ES2853375T3 - Sales novedosas y composiciones farmacéuticas de las mismas para el tratamiento de trastornos inflamatorios - Google Patents
Sales novedosas y composiciones farmacéuticas de las mismas para el tratamiento de trastornos inflamatorios Download PDFInfo
- Publication number
- ES2853375T3 ES2853375T3 ES15704974T ES15704974T ES2853375T3 ES 2853375 T3 ES2853375 T3 ES 2853375T3 ES 15704974 T ES15704974 T ES 15704974T ES 15704974 T ES15704974 T ES 15704974T ES 2853375 T3 ES2853375 T3 ES 2853375T3
- Authority
- ES
- Spain
- Prior art keywords
- salt
- compound
- disease
- hcl
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000003839 salts Chemical class 0.000 title claims abstract description 241
- 238000011282 treatment Methods 0.000 title description 103
- 239000008194 pharmaceutical composition Substances 0.000 title description 62
- 208000027866 inflammatory disease Diseases 0.000 title description 17
- 150000001875 compounds Chemical class 0.000 claims abstract description 239
- 239000012458 free base Substances 0.000 claims abstract description 18
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 133
- 239000007787 solid Substances 0.000 claims description 107
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 91
- 238000000034 method Methods 0.000 claims description 61
- 238000000634 powder X-ray diffraction Methods 0.000 claims description 47
- 238000003756 stirring Methods 0.000 claims description 25
- 238000001914 filtration Methods 0.000 claims description 22
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 claims description 19
- 239000012074 organic phase Substances 0.000 claims description 19
- 238000002360 preparation method Methods 0.000 claims description 14
- 238000001035 drying Methods 0.000 claims description 11
- 235000019253 formic acid Nutrition 0.000 claims description 10
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 claims description 9
- 230000008569 process Effects 0.000 claims description 8
- 238000002156 mixing Methods 0.000 claims description 7
- JEGUKCSWCFPDGT-UHFFFAOYSA-N h2o hydrate Chemical compound O.O JEGUKCSWCFPDGT-UHFFFAOYSA-N 0.000 claims 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 150
- 201000010099 disease Diseases 0.000 description 137
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 72
- 238000011321 prophylaxis Methods 0.000 description 68
- 239000000203 mixture Substances 0.000 description 60
- 208000006673 asthma Diseases 0.000 description 56
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 51
- 210000000845 cartilage Anatomy 0.000 description 51
- 239000003814 drug Substances 0.000 description 51
- 239000000243 solution Substances 0.000 description 51
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 42
- 239000002904 solvent Substances 0.000 description 41
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 39
- 230000002062 proliferating effect Effects 0.000 description 37
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 36
- 208000023275 Autoimmune disease Diseases 0.000 description 32
- 206010020751 Hypersensitivity Diseases 0.000 description 32
- 230000007815 allergy Effects 0.000 description 30
- 206010028980 Neoplasm Diseases 0.000 description 29
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 28
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 28
- 201000004681 Psoriasis Diseases 0.000 description 28
- 239000003795 chemical substances by application Substances 0.000 description 28
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 27
- 108010050904 Interferons Proteins 0.000 description 27
- 102000014150 Interferons Human genes 0.000 description 27
- 102000004889 Interleukin-6 Human genes 0.000 description 27
- 108090001005 Interleukin-6 Proteins 0.000 description 27
- 238000003556 assay Methods 0.000 description 27
- 230000000694 effects Effects 0.000 description 27
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 27
- 229940047124 interferons Drugs 0.000 description 26
- 206010010356 Congenital anomaly Diseases 0.000 description 25
- 208000026935 allergic disease Diseases 0.000 description 25
- 230000036244 malformation Effects 0.000 description 25
- 230000015556 catabolic process Effects 0.000 description 24
- 238000006731 degradation reaction Methods 0.000 description 24
- 230000013632 homeostatic process Effects 0.000 description 24
- 206010039073 rheumatoid arthritis Diseases 0.000 description 24
- 206010052779 Transplant rejections Diseases 0.000 description 22
- 201000011510 cancer Diseases 0.000 description 22
- 210000004027 cell Anatomy 0.000 description 22
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 21
- 238000004458 analytical method Methods 0.000 description 21
- 208000010668 atopic eczema Diseases 0.000 description 21
- 101000997835 Homo sapiens Tyrosine-protein kinase JAK1 Proteins 0.000 description 20
- 238000006243 chemical reaction Methods 0.000 description 20
- 238000004519 manufacturing process Methods 0.000 description 20
- 239000000725 suspension Substances 0.000 description 20
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 19
- 102100033438 Tyrosine-protein kinase JAK1 Human genes 0.000 description 19
- 229940079593 drug Drugs 0.000 description 19
- 239000003981 vehicle Substances 0.000 description 19
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 18
- 208000011231 Crohn disease Diseases 0.000 description 18
- 230000001684 chronic effect Effects 0.000 description 18
- 201000008482 osteoarthritis Diseases 0.000 description 18
- 206010009900 Colitis ulcerative Diseases 0.000 description 17
- 102000042838 JAK family Human genes 0.000 description 17
- 108091082332 JAK family Proteins 0.000 description 17
- 201000006704 Ulcerative Colitis Diseases 0.000 description 17
- 239000002253 acid Substances 0.000 description 17
- 230000004968 inflammatory condition Effects 0.000 description 17
- 230000005764 inhibitory process Effects 0.000 description 17
- 238000012360 testing method Methods 0.000 description 17
- 239000003112 inhibitor Substances 0.000 description 16
- 229940124597 therapeutic agent Drugs 0.000 description 16
- -1 ATG Chemical compound 0.000 description 15
- 208000027207 Whipple disease Diseases 0.000 description 15
- 206010009887 colitis Diseases 0.000 description 15
- 239000000843 powder Substances 0.000 description 15
- 101000997832 Homo sapiens Tyrosine-protein kinase JAK2 Proteins 0.000 description 14
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 14
- 108091000080 Phosphotransferase Proteins 0.000 description 14
- 238000002441 X-ray diffraction Methods 0.000 description 14
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 14
- 238000009472 formulation Methods 0.000 description 14
- 208000032839 leukemia Diseases 0.000 description 14
- 102000020233 phosphotransferase Human genes 0.000 description 14
- 239000013641 positive control Substances 0.000 description 14
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 13
- 102100033444 Tyrosine-protein kinase JAK2 Human genes 0.000 description 13
- 238000010790 dilution Methods 0.000 description 13
- 239000012895 dilution Substances 0.000 description 13
- 208000035475 disorder Diseases 0.000 description 13
- 239000012453 solvate Substances 0.000 description 13
- 238000003828 vacuum filtration Methods 0.000 description 13
- 101000934996 Homo sapiens Tyrosine-protein kinase JAK3 Proteins 0.000 description 12
- 241000124008 Mammalia Species 0.000 description 12
- 239000002775 capsule Substances 0.000 description 12
- 239000000758 substrate Substances 0.000 description 12
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 11
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 11
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 11
- 102100025387 Tyrosine-protein kinase JAK3 Human genes 0.000 description 11
- 206010003246 arthritis Diseases 0.000 description 11
- 201000004624 Dermatitis Diseases 0.000 description 10
- 206010012438 Dermatitis atopic Diseases 0.000 description 10
- 208000001640 Fibromyalgia Diseases 0.000 description 10
- 208000030836 Hashimoto thyroiditis Diseases 0.000 description 10
- 101000844245 Homo sapiens Non-receptor tyrosine-protein kinase TYK2 Proteins 0.000 description 10
- 208000004575 Infectious Arthritis Diseases 0.000 description 10
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 10
- 208000034578 Multiple myelomas Diseases 0.000 description 10
- 206010035226 Plasma cell myeloma Diseases 0.000 description 10
- 206010060862 Prostate cancer Diseases 0.000 description 10
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 10
- 208000021386 Sjogren Syndrome Diseases 0.000 description 10
- 201000008937 atopic dermatitis Diseases 0.000 description 10
- 230000015572 biosynthetic process Effects 0.000 description 10
- 230000000052 comparative effect Effects 0.000 description 10
- 208000004921 cutaneous lupus erythematosus Diseases 0.000 description 10
- 201000001981 dermatomyositis Diseases 0.000 description 10
- 229910052757 nitrogen Inorganic materials 0.000 description 10
- 239000000047 product Substances 0.000 description 10
- 201000001223 septic arthritis Diseases 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- 229940122245 Janus kinase inhibitor Drugs 0.000 description 9
- 208000005777 Lupus Nephritis Diseases 0.000 description 9
- 102100032028 Non-receptor tyrosine-protein kinase TYK2 Human genes 0.000 description 9
- 206010033128 Ovarian cancer Diseases 0.000 description 9
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 9
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 9
- 230000001976 improved effect Effects 0.000 description 9
- CUGZEDSDRBMZMY-UHFFFAOYSA-N trihydrate;hydrochloride Chemical compound O.O.O.Cl CUGZEDSDRBMZMY-UHFFFAOYSA-N 0.000 description 9
- 208000003456 Juvenile Arthritis Diseases 0.000 description 8
- 206010059176 Juvenile idiopathic arthritis Diseases 0.000 description 8
- 206010061535 Ovarian neoplasm Diseases 0.000 description 8
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 8
- 239000002585 base Substances 0.000 description 8
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 8
- 235000019439 ethyl acetate Nutrition 0.000 description 8
- 201000002215 juvenile rheumatoid arthritis Diseases 0.000 description 8
- 239000002953 phosphate buffered saline Substances 0.000 description 8
- 239000003643 water by type Substances 0.000 description 8
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 7
- 206010006187 Breast cancer Diseases 0.000 description 7
- 208000026310 Breast neoplasm Diseases 0.000 description 7
- 241000282472 Canis lupus familiaris Species 0.000 description 7
- 102100027995 Collagenase 3 Human genes 0.000 description 7
- 101000577887 Homo sapiens Collagenase 3 Proteins 0.000 description 7
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical group CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 7
- 208000007766 Kaposi sarcoma Diseases 0.000 description 7
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 7
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 7
- 230000000172 allergic effect Effects 0.000 description 7
- 229960002170 azathioprine Drugs 0.000 description 7
- LMEKQMALGUDUQG-UHFFFAOYSA-N azathioprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC=NC2=C1NC=N2 LMEKQMALGUDUQG-UHFFFAOYSA-N 0.000 description 7
- 239000000428 dust Substances 0.000 description 7
- 238000010348 incorporation Methods 0.000 description 7
- 229910001629 magnesium chloride Inorganic materials 0.000 description 7
- 238000000746 purification Methods 0.000 description 7
- 230000002285 radioactive effect Effects 0.000 description 7
- 206010039083 rhinitis Diseases 0.000 description 7
- 210000001519 tissue Anatomy 0.000 description 7
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 6
- 206010014733 Endometrial cancer Diseases 0.000 description 6
- 206010014759 Endometrial neoplasm Diseases 0.000 description 6
- 206010018364 Glomerulonephritis Diseases 0.000 description 6
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 6
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 6
- 239000004480 active ingredient Substances 0.000 description 6
- 208000028004 allergic respiratory disease Diseases 0.000 description 6
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 6
- 239000013078 crystal Substances 0.000 description 6
- 230000007850 degeneration Effects 0.000 description 6
- 238000004090 dissolution Methods 0.000 description 6
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 6
- 229940011051 isopropyl acetate Drugs 0.000 description 6
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical compound CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 6
- 201000007270 liver cancer Diseases 0.000 description 6
- 208000014018 liver neoplasm Diseases 0.000 description 6
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 6
- 239000011976 maleic acid Substances 0.000 description 6
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 229960000485 methotrexate Drugs 0.000 description 6
- 201000006417 multiple sclerosis Diseases 0.000 description 6
- 201000002528 pancreatic cancer Diseases 0.000 description 6
- 208000008443 pancreatic carcinoma Diseases 0.000 description 6
- 230000009885 systemic effect Effects 0.000 description 6
- 238000002560 therapeutic procedure Methods 0.000 description 6
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 6
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 5
- 206010002654 Anotia Diseases 0.000 description 5
- 241001383249 Anotia Species 0.000 description 5
- 206010053555 Arthritis bacterial Diseases 0.000 description 5
- 206010003267 Arthritis reactive Diseases 0.000 description 5
- 208000036487 Arthropathies Diseases 0.000 description 5
- 201000001320 Atherosclerosis Diseases 0.000 description 5
- 206010008342 Cervix carcinoma Diseases 0.000 description 5
- 206010008685 Chondritis Diseases 0.000 description 5
- 206010008723 Chondrodystrophy Diseases 0.000 description 5
- 206010058112 Chondrolysis Diseases 0.000 description 5
- 208000013586 Complex regional pain syndrome type 1 Diseases 0.000 description 5
- 208000005831 Congenital Microtia Diseases 0.000 description 5
- 206010011219 Costochondritis Diseases 0.000 description 5
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 5
- 108010036949 Cyclosporine Proteins 0.000 description 5
- 206010012442 Dermatitis contact Diseases 0.000 description 5
- 208000003556 Dry Eye Syndromes Diseases 0.000 description 5
- 206010016207 Familial Mediterranean fever Diseases 0.000 description 5
- 208000004262 Food Hypersensitivity Diseases 0.000 description 5
- 201000005569 Gout Diseases 0.000 description 5
- 206010018634 Gouty Arthritis Diseases 0.000 description 5
- 206010061218 Inflammation Diseases 0.000 description 5
- 108010002350 Interleukin-2 Proteins 0.000 description 5
- 102000000588 Interleukin-2 Human genes 0.000 description 5
- 208000012659 Joint disease Diseases 0.000 description 5
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 5
- 241001237732 Microtia Species 0.000 description 5
- 238000005481 NMR spectroscopy Methods 0.000 description 5
- 108090000630 Oncostatin M Proteins 0.000 description 5
- 208000010191 Osteitis Deformans Diseases 0.000 description 5
- 208000002804 Osteochondritis Diseases 0.000 description 5
- 201000009859 Osteochondrosis Diseases 0.000 description 5
- 208000027868 Paget disease Diseases 0.000 description 5
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 5
- 201000001947 Reflex Sympathetic Dystrophy Diseases 0.000 description 5
- 208000018569 Respiratory Tract disease Diseases 0.000 description 5
- 201000009594 Systemic Scleroderma Diseases 0.000 description 5
- 206010042953 Systemic sclerosis Diseases 0.000 description 5
- 208000026317 Tietze syndrome Diseases 0.000 description 5
- 208000024780 Urticaria Diseases 0.000 description 5
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 5
- 208000008919 achondroplasia Diseases 0.000 description 5
- 230000004913 activation Effects 0.000 description 5
- 206010006451 bronchitis Diseases 0.000 description 5
- 238000004364 calculation method Methods 0.000 description 5
- 201000010881 cervical cancer Diseases 0.000 description 5
- 239000003153 chemical reaction reagent Substances 0.000 description 5
- 208000029771 childhood onset asthma Diseases 0.000 description 5
- 208000017568 chondrodysplasia Diseases 0.000 description 5
- 208000023819 chronic asthma Diseases 0.000 description 5
- 208000019069 chronic childhood arthritis Diseases 0.000 description 5
- 208000010247 contact dermatitis Diseases 0.000 description 5
- 231100000673 dose–response relationship Toxicity 0.000 description 5
- 230000002357 endometrial effect Effects 0.000 description 5
- 208000024711 extrinsic asthma Diseases 0.000 description 5
- 235000020932 food allergy Nutrition 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 230000002650 habitual effect Effects 0.000 description 5
- 230000004047 hyperresponsiveness Effects 0.000 description 5
- 239000012442 inert solvent Substances 0.000 description 5
- 230000004054 inflammatory process Effects 0.000 description 5
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 5
- 239000002919 insect venom Substances 0.000 description 5
- 201000010659 intrinsic asthma Diseases 0.000 description 5
- 230000000155 isotopic effect Effects 0.000 description 5
- 210000004072 lung Anatomy 0.000 description 5
- 201000005202 lung cancer Diseases 0.000 description 5
- 208000020816 lung neoplasm Diseases 0.000 description 5
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 5
- 235000019341 magnesium sulphate Nutrition 0.000 description 5
- 208000027202 mammary Paget disease Diseases 0.000 description 5
- 208000015625 metaphyseal chondrodysplasia Diseases 0.000 description 5
- 206010027555 microtia Diseases 0.000 description 5
- 201000005962 mycosis fungoides Diseases 0.000 description 5
- 230000001272 neurogenic effect Effects 0.000 description 5
- 230000002981 neuropathic effect Effects 0.000 description 5
- AICOOMRHRUFYCM-ZRRPKQBOSA-N oxazine, 1 Chemical compound C([C@@H]1[C@H](C(C[C@]2(C)[C@@H]([C@H](C)N(C)C)[C@H](O)C[C@]21C)=O)CC1=CC2)C[C@H]1[C@@]1(C)[C@H]2N=C(C(C)C)OC1 AICOOMRHRUFYCM-ZRRPKQBOSA-N 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 208000002574 reactive arthritis Diseases 0.000 description 5
- 201000000306 sarcoidosis Diseases 0.000 description 5
- 230000011664 signaling Effects 0.000 description 5
- 201000009890 sinusitis Diseases 0.000 description 5
- 206010043778 thyroiditis Diseases 0.000 description 5
- 231100000611 venom Toxicity 0.000 description 5
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 4
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 4
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 4
- 102000004127 Cytokines Human genes 0.000 description 4
- 108090000695 Cytokines Proteins 0.000 description 4
- 208000002249 Diabetes Complications Diseases 0.000 description 4
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 4
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 4
- 241000282414 Homo sapiens Species 0.000 description 4
- 108010024121 Janus Kinases Proteins 0.000 description 4
- 102000015617 Janus Kinases Human genes 0.000 description 4
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 4
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 4
- 208000014767 Myeloproliferative disease Diseases 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 4
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 4
- 239000004743 Polypropylene Substances 0.000 description 4
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 description 4
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 description 4
- 150000001413 amino acids Chemical class 0.000 description 4
- 125000004429 atom Chemical group 0.000 description 4
- 230000003197 catalytic effect Effects 0.000 description 4
- 229960001265 ciclosporin Drugs 0.000 description 4
- 229960004397 cyclophosphamide Drugs 0.000 description 4
- 229930182912 cyclosporin Natural products 0.000 description 4
- 229940104302 cytosine Drugs 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 239000000706 filtrate Substances 0.000 description 4
- 230000002496 gastric effect Effects 0.000 description 4
- 239000003862 glucocorticoid Substances 0.000 description 4
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 4
- 239000001257 hydrogen Substances 0.000 description 4
- 229910052739 hydrogen Inorganic materials 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 238000001990 intravenous administration Methods 0.000 description 4
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 4
- 201000010901 lateral sclerosis Diseases 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 4
- 230000001404 mediated effect Effects 0.000 description 4
- HPNSFSBZBAHARI-UHFFFAOYSA-N micophenolic acid Natural products OC1=C(CC=C(C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-UHFFFAOYSA-N 0.000 description 4
- 208000005264 motor neuron disease Diseases 0.000 description 4
- HPNSFSBZBAHARI-RUDMXATFSA-N mycophenolic acid Chemical compound OC1=C(C\C=C(/C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-RUDMXATFSA-N 0.000 description 4
- 239000002674 ointment Substances 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- 210000002381 plasma Anatomy 0.000 description 4
- 229920001155 polypropylene Polymers 0.000 description 4
- 229920000136 polysorbate Polymers 0.000 description 4
- 229960004618 prednisone Drugs 0.000 description 4
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 4
- 230000002035 prolonged effect Effects 0.000 description 4
- 239000011535 reaction buffer Substances 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 229960004641 rituximab Drugs 0.000 description 4
- 229960002052 salbutamol Drugs 0.000 description 4
- 239000007858 starting material Substances 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 229940037128 systemic glucocorticoids Drugs 0.000 description 4
- ZFXYFBGIUFBOJW-UHFFFAOYSA-N theophylline Chemical compound O=C1N(C)C(=O)N(C)C2=C1NC=N2 ZFXYFBGIUFBOJW-UHFFFAOYSA-N 0.000 description 4
- IEQAICDLOKRSRL-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-dodecoxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound CCCCCCCCCCCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO IEQAICDLOKRSRL-UHFFFAOYSA-N 0.000 description 3
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 3
- 208000017667 Chronic Disease Diseases 0.000 description 3
- 229930105110 Cyclosporin A Natural products 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- 108010008165 Etanercept Proteins 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 108010002352 Interleukin-1 Proteins 0.000 description 3
- 102000015696 Interleukins Human genes 0.000 description 3
- 108010063738 Interleukins Proteins 0.000 description 3
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 3
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 3
- 206010025323 Lymphomas Diseases 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 3
- 102000002063 Non-Receptor Type 2 Protein Tyrosine Phosphatase Human genes 0.000 description 3
- 108010015832 Non-Receptor Type 2 Protein Tyrosine Phosphatase Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 3
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 3
- 206010039491 Sarcoma Diseases 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 3
- 208000031673 T-Cell Cutaneous Lymphoma Diseases 0.000 description 3
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 229960002964 adalimumab Drugs 0.000 description 3
- 229940065524 anticholinergics inhalants for obstructive airway diseases Drugs 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 239000000872 buffer Substances 0.000 description 3
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 description 3
- 239000000812 cholinergic antagonist Substances 0.000 description 3
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 3
- 239000003246 corticosteroid Substances 0.000 description 3
- 229960001334 corticosteroids Drugs 0.000 description 3
- 239000006071 cream Substances 0.000 description 3
- 201000007241 cutaneous T cell lymphoma Diseases 0.000 description 3
- YMGUBTXCNDTFJI-UHFFFAOYSA-N cyclopropanecarboxylic acid Chemical compound OC(=O)C1CC1 YMGUBTXCNDTFJI-UHFFFAOYSA-N 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 229960003957 dexamethasone Drugs 0.000 description 3
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- FKKRGXZJQLLGGN-UHFFFAOYSA-N ethyl n-[(6-bromopyridin-2-yl)carbamothioyl]carbamate Chemical compound CCOC(=O)NC(=S)NC1=CC=CC(Br)=N1 FKKRGXZJQLLGGN-UHFFFAOYSA-N 0.000 description 3
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 3
- 238000001704 evaporation Methods 0.000 description 3
- 230000008020 evaporation Effects 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 3
- 150000004677 hydrates Chemical class 0.000 description 3
- 150000003840 hydrochlorides Chemical class 0.000 description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 3
- XXSMGPRMXLTPCZ-UHFFFAOYSA-N hydroxychloroquine Chemical compound ClC1=CC=C2C(NC(C)CCCN(CCO)CC)=CC=NC2=C1 XXSMGPRMXLTPCZ-UHFFFAOYSA-N 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 229960000598 infliximab Drugs 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 238000011835 investigation Methods 0.000 description 3
- ZXEKIIBDNHEJCQ-UHFFFAOYSA-N isobutanol Chemical compound CC(C)CO ZXEKIIBDNHEJCQ-UHFFFAOYSA-N 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 210000001503 joint Anatomy 0.000 description 3
- 210000003734 kidney Anatomy 0.000 description 3
- 210000000265 leukocyte Anatomy 0.000 description 3
- 210000004185 liver Anatomy 0.000 description 3
- 239000000314 lubricant Substances 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 3
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 3
- XLBCMNCPMMPNHH-UHFFFAOYSA-N n-(5-bromo-[1,2,4]triazolo[1,5-a]pyridin-2-yl)cyclopropanecarboxamide Chemical compound N=1N2C(Br)=CC=CC2=NC=1NC(=O)C1CC1 XLBCMNCPMMPNHH-UHFFFAOYSA-N 0.000 description 3
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 3
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 3
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 3
- 238000001139 pH measurement Methods 0.000 description 3
- 210000000496 pancreas Anatomy 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 229960005205 prednisolone Drugs 0.000 description 3
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 3
- 208000025638 primary cutaneous T-cell non-Hodgkin lymphoma Diseases 0.000 description 3
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 3
- 230000019491 signal transduction Effects 0.000 description 3
- 210000003491 skin Anatomy 0.000 description 3
- KZKGKUREPCFQIU-UHFFFAOYSA-N sodium;triazinane-4,5,6-trithione Chemical compound [Na].[Na].[Na].S=C1NNNC(=S)C1=S KZKGKUREPCFQIU-UHFFFAOYSA-N 0.000 description 3
- 230000006641 stabilisation Effects 0.000 description 3
- 238000011105 stabilization Methods 0.000 description 3
- 150000003431 steroids Chemical class 0.000 description 3
- 210000002784 stomach Anatomy 0.000 description 3
- 229960001940 sulfasalazine Drugs 0.000 description 3
- NCEXYHBECQHGNR-QZQOTICOSA-N sulfasalazine Chemical compound C1=C(O)C(C(=O)O)=CC(\N=N\C=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-QZQOTICOSA-N 0.000 description 3
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- 229960001967 tacrolimus Drugs 0.000 description 3
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 150000004684 trihydrates Chemical class 0.000 description 3
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 3
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 3
- UCTWMZQNUQWSLP-VIFPVBQESA-N (R)-adrenaline Chemical compound CNC[C@H](O)C1=CC=C(O)C(O)=C1 UCTWMZQNUQWSLP-VIFPVBQESA-N 0.000 description 2
- 229930182837 (R)-adrenaline Natural products 0.000 description 2
- WHTVZRBIWZFKQO-AWEZNQCLSA-N (S)-chloroquine Chemical compound ClC1=CC=C2C(N[C@@H](C)CCCN(CC)CC)=CC=NC2=C1 WHTVZRBIWZFKQO-AWEZNQCLSA-N 0.000 description 2
- GNENVASJJIUNER-UHFFFAOYSA-N 2,4,6-tricyclohexyloxy-1,3,5,2,4,6-trioxatriborinane Chemical compound C1CCCCC1OB1OB(OC2CCCCC2)OB(OC2CCCCC2)O1 GNENVASJJIUNER-UHFFFAOYSA-N 0.000 description 2
- CNIIGCLFLJGOGP-UHFFFAOYSA-N 2-(1-naphthalenylmethyl)-4,5-dihydro-1H-imidazole Chemical compound C=1C=CC2=CC=CC=C2C=1CC1=NCCN1 CNIIGCLFLJGOGP-UHFFFAOYSA-N 0.000 description 2
- ZNOVTXRBGFNYRX-UHFFFAOYSA-N 2-[[4-[(2-amino-5-methyl-4-oxo-1,6,7,8-tetrahydropteridin-6-yl)methylamino]benzoyl]amino]pentanedioic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C)C1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 ZNOVTXRBGFNYRX-UHFFFAOYSA-N 0.000 description 2
- ICSNLGPSRYBMBD-UHFFFAOYSA-N 2-aminopyridine Chemical compound NC1=CC=CC=N1 ICSNLGPSRYBMBD-UHFFFAOYSA-N 0.000 description 2
- PZWLWAYUUJLSJL-UHFFFAOYSA-N 4-[[4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)phenyl]methyl]-1,4-thiazinane 1,1-dioxide Chemical compound O1C(C)(C)C(C)(C)OB1C(C=C1)=CC=C1CN1CCS(=O)(=O)CC1 PZWLWAYUUJLSJL-UHFFFAOYSA-N 0.000 description 2
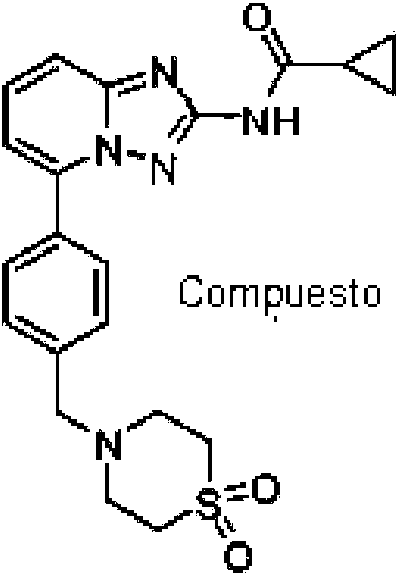
- BYWJAVQGRJEEHH-UHFFFAOYSA-N 5-[4-[(1,1-dioxo-1,4-thiazinan-4-yl)methyl]phenyl]-[1,2,4]triazolo[1,5-a]pyridin-2-amine Chemical compound N12N=C(N)N=C2C=CC=C1C(C=C1)=CC=C1CN1CCS(=O)(=O)CC1 BYWJAVQGRJEEHH-UHFFFAOYSA-N 0.000 description 2
- BKLJUYPLUWUEOQ-UHFFFAOYSA-N 6-bromopyridin-2-amine Chemical compound NC1=CC=CC(Br)=N1 BKLJUYPLUWUEOQ-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- PDBXHPORMXSXKO-UHFFFAOYSA-N 8-benzyl-7-[2-[ethyl(2-hydroxyethyl)amino]ethyl]-1,3-dimethylpurine-2,6-dione;hydron;chloride Chemical class Cl.N=1C=2N(C)C(=O)N(C)C(=O)C=2N(CCN(CCO)CC)C=1CC1=CC=CC=C1 PDBXHPORMXSXKO-UHFFFAOYSA-N 0.000 description 2
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 2
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 2
- 206010005003 Bladder cancer Diseases 0.000 description 2
- 108010006654 Bleomycin Proteins 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 208000003174 Brain Neoplasms Diseases 0.000 description 2
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 2
- 206010013710 Drug interaction Diseases 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 102100031939 Erythropoietin Human genes 0.000 description 2
- 208000006168 Ewing Sarcoma Diseases 0.000 description 2
- 206010016654 Fibrosis Diseases 0.000 description 2
- 238000005033 Fourier transform infrared spectroscopy Methods 0.000 description 2
- 108010044091 Globulins Proteins 0.000 description 2
- 102000006395 Globulins Human genes 0.000 description 2
- 208000009329 Graft vs Host Disease Diseases 0.000 description 2
- 101000617830 Homo sapiens Sterol O-acyltransferase 1 Proteins 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 2
- WTDHULULXKLSOZ-UHFFFAOYSA-N Hydroxylamine hydrochloride Chemical compound Cl.ON WTDHULULXKLSOZ-UHFFFAOYSA-N 0.000 description 2
- 230000035986 JAK-STAT signaling Effects 0.000 description 2
- 208000008839 Kidney Neoplasms Diseases 0.000 description 2
- 239000005089 Luciferase Substances 0.000 description 2
- 239000007993 MOPS buffer Substances 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 2
- UCHDWCPVSPXUMX-TZIWLTJVSA-N Montelukast Chemical compound CC(C)(O)C1=CC=CC=C1CC[C@H](C=1C=C(\C=C\C=2N=C3C=C(Cl)C=CC3=CC=2)C=CC=1)SCC1(CC(O)=O)CC1 UCHDWCPVSPXUMX-TZIWLTJVSA-N 0.000 description 2
- 208000003445 Mouth Neoplasms Diseases 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- AMQJEAYHLZJPGS-UHFFFAOYSA-N N-Pentanol Chemical compound CCCCCO AMQJEAYHLZJPGS-UHFFFAOYSA-N 0.000 description 2
- 229910020700 Na3VO4 Inorganic materials 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- 208000007641 Pinealoma Diseases 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 2
- 206010038389 Renal cancer Diseases 0.000 description 2
- 201000000582 Retinoblastoma Diseases 0.000 description 2
- 208000009359 Sezary Syndrome Diseases 0.000 description 2
- 208000021388 Sezary disease Diseases 0.000 description 2
- 206010041067 Small cell lung cancer Diseases 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 102100021993 Sterol O-acyltransferase 1 Human genes 0.000 description 2
- 101000697584 Streptomyces lavendulae Streptothricin acetyltransferase Proteins 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 206010042971 T-cell lymphoma Diseases 0.000 description 2
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 2
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 2
- 206010046799 Uterine leiomyosarcoma Diseases 0.000 description 2
- 208000033559 Waldenström macroglobulinemia Diseases 0.000 description 2
- HUCJFAOMUPXHDK-UHFFFAOYSA-N Xylometazoline Chemical compound CC1=CC(C(C)(C)C)=CC(C)=C1CC1=NCCN1 HUCJFAOMUPXHDK-UHFFFAOYSA-N 0.000 description 2
- YEEZWCHGZNKEEK-UHFFFAOYSA-N Zafirlukast Chemical compound COC1=CC(C(=O)NS(=O)(=O)C=2C(=CC=CC=2)C)=CC=C1CC(C1=C2)=CN(C)C1=CC=C2NC(=O)OC1CCCC1 YEEZWCHGZNKEEK-UHFFFAOYSA-N 0.000 description 2
- WFIHKLWVLPBMIQ-UHFFFAOYSA-N [1,3]thiazolo[5,4-b]pyridine Chemical class C1=CN=C2SC=NC2=C1 WFIHKLWVLPBMIQ-UHFFFAOYSA-N 0.000 description 2
- 229960003697 abatacept Drugs 0.000 description 2
- RXSUFCOOZSGWSW-UHFFFAOYSA-M acetyloxy-(4-aminophenyl)mercury Chemical compound CC(=O)O[Hg]C1=CC=C(N)C=C1 RXSUFCOOZSGWSW-UHFFFAOYSA-M 0.000 description 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 2
- 230000001154 acute effect Effects 0.000 description 2
- 239000000556 agonist Substances 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 229940035676 analgesics Drugs 0.000 description 2
- 239000000730 antalgic agent Substances 0.000 description 2
- NUZWLKWWNNJHPT-UHFFFAOYSA-N anthralin Chemical compound C1C2=CC=CC(O)=C2C(=O)C2=C1C=CC=C2O NUZWLKWWNNJHPT-UHFFFAOYSA-N 0.000 description 2
- 229940125715 antihistaminic agent Drugs 0.000 description 2
- 239000000739 antihistaminic agent Substances 0.000 description 2
- 239000003430 antimalarial agent Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 239000012455 biphasic mixture Substances 0.000 description 2
- 229960001561 bleomycin Drugs 0.000 description 2
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 210000001185 bone marrow Anatomy 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 239000013592 cell lysate Substances 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 229960003677 chloroquine Drugs 0.000 description 2
- WHTVZRBIWZFKQO-UHFFFAOYSA-N chloroquine Natural products ClC1=CC=C2C(NC(C)CCCN(CC)CC)=CC=NC2=C1 WHTVZRBIWZFKQO-UHFFFAOYSA-N 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- ZOOSILUVXHVRJE-UHFFFAOYSA-N cyclopropanecarbonyl chloride Chemical compound ClC(=O)C1CC1 ZOOSILUVXHVRJE-UHFFFAOYSA-N 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- VWVSBHGCDBMOOT-IIEHVVJPSA-N desoximetasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@H](C(=O)CO)[C@@]1(C)C[C@@H]2O VWVSBHGCDBMOOT-IIEHVVJPSA-N 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 229960002311 dithranol Drugs 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 239000002158 endotoxin Substances 0.000 description 2
- 238000006911 enzymatic reaction Methods 0.000 description 2
- 229960005139 epinephrine Drugs 0.000 description 2
- 229960000403 etanercept Drugs 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- RWTNPBWLLIMQHL-UHFFFAOYSA-N fexofenadine Chemical compound C1=CC(C(C)(C(O)=O)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 RWTNPBWLLIMQHL-UHFFFAOYSA-N 0.000 description 2
- 229960003592 fexofenadine Drugs 0.000 description 2
- 230000004761 fibrosis Effects 0.000 description 2
- 235000019634 flavors Nutrition 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- DHCLVCXQIBBOPH-UHFFFAOYSA-L glycerol 2-phosphate(2-) Chemical compound OCC(CO)OP([O-])([O-])=O DHCLVCXQIBBOPH-UHFFFAOYSA-L 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229960000890 hydrocortisone Drugs 0.000 description 2
- 229960004171 hydroxychloroquine Drugs 0.000 description 2
- 230000002519 immonomodulatory effect Effects 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 230000000495 immunoinflammatory effect Effects 0.000 description 2
- 239000003018 immunosuppressive agent Substances 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 210000000936 intestine Anatomy 0.000 description 2
- 230000031146 intracellular signal transduction Effects 0.000 description 2
- 210000004153 islets of langerhan Anatomy 0.000 description 2
- PHTQWCKDNZKARW-UHFFFAOYSA-N isoamylol Chemical compound CC(C)CCO PHTQWCKDNZKARW-UHFFFAOYSA-N 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 201000010982 kidney cancer Diseases 0.000 description 2
- 229960000681 leflunomide Drugs 0.000 description 2
- VHOGYURTWQBHIL-UHFFFAOYSA-N leflunomide Chemical compound O1N=CC(C(=O)NC=2C=CC(=CC=2)C(F)(F)F)=C1C VHOGYURTWQBHIL-UHFFFAOYSA-N 0.000 description 2
- 235000019359 magnesium stearate Nutrition 0.000 description 2
- 201000004792 malaria Diseases 0.000 description 2
- 230000003211 malignant effect Effects 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 201000001441 melanoma Diseases 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 229960001428 mercaptopurine Drugs 0.000 description 2
- 239000002207 metabolite Substances 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 239000008108 microcrystalline cellulose Substances 0.000 description 2
- 229940016286 microcrystalline cellulose Drugs 0.000 description 2
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 229960005127 montelukast Drugs 0.000 description 2
- 229940014456 mycophenolate Drugs 0.000 description 2
- 229960000951 mycophenolic acid Drugs 0.000 description 2
- 208000025113 myeloid leukemia Diseases 0.000 description 2
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- LQNUZADURLCDLV-UHFFFAOYSA-N nitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC=C1 LQNUZADURLCDLV-UHFFFAOYSA-N 0.000 description 2
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 201000008968 osteosarcoma Diseases 0.000 description 2
- 235000006408 oxalic acid Nutrition 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- WYWIFABBXFUGLM-UHFFFAOYSA-N oxymetazoline Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C)=C1CC1=NCCN1 WYWIFABBXFUGLM-UHFFFAOYSA-N 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- XNLICIUVMPYHGG-UHFFFAOYSA-N pentan-2-one Chemical compound CCCC(C)=O XNLICIUVMPYHGG-UHFFFAOYSA-N 0.000 description 2
- 239000008024 pharmaceutical diluent Substances 0.000 description 2
- 238000001126 phototherapy Methods 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 238000012877 positron emission topography Methods 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 208000029340 primitive neuroectodermal tumor Diseases 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 210000002307 prostate Anatomy 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- ZCCUUQDIBDJBTK-UHFFFAOYSA-N psoralen Chemical compound C1=C2OC(=O)C=CC2=CC2=C1OC=C2 ZCCUUQDIBDJBTK-UHFFFAOYSA-N 0.000 description 2
- 239000000700 radioactive tracer Substances 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 239000013557 residual solvent Substances 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 2
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 2
- 208000000587 small cell lung carcinoma Diseases 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 238000001228 spectrum Methods 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 201000008205 supratentorial primitive neuroectodermal tumor Diseases 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- 238000013268 sustained release Methods 0.000 description 2
- 229960000278 theophylline Drugs 0.000 description 2
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea Chemical compound NC(N)=S UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 description 2
- 208000008732 thymoma Diseases 0.000 description 2
- 238000004448 titration Methods 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 238000001890 transfection Methods 0.000 description 2
- 238000011269 treatment regimen Methods 0.000 description 2
- 230000001960 triggered effect Effects 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- IHIXIJGXTJIKRB-UHFFFAOYSA-N trisodium vanadate Chemical compound [Na+].[Na+].[Na+].[O-][V]([O-])([O-])=O IHIXIJGXTJIKRB-UHFFFAOYSA-N 0.000 description 2
- 201000005112 urinary bladder cancer Diseases 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- 229960004764 zafirlukast Drugs 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- XWTYSIMOBUGWOL-UHFFFAOYSA-N (+-)-Terbutaline Chemical compound CC(C)(C)NCC(O)C1=CC(O)=CC(O)=C1 XWTYSIMOBUGWOL-UHFFFAOYSA-N 0.000 description 1
- LJRDOKAZOAKLDU-UDXJMMFXSA-N (2s,3s,4r,5r,6r)-5-amino-2-(aminomethyl)-6-[(2r,3s,4r,5s)-5-[(1r,2r,3s,5r,6s)-3,5-diamino-2-[(2s,3r,4r,5s,6r)-3-amino-4,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-6-hydroxycyclohexyl]oxy-4-hydroxy-2-(hydroxymethyl)oxolan-3-yl]oxyoxane-3,4-diol;sulfuric ac Chemical compound OS(O)(=O)=O.N[C@@H]1[C@@H](O)[C@H](O)[C@H](CN)O[C@@H]1O[C@H]1[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](N)C[C@@H](N)[C@@H]2O)O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)N)O[C@@H]1CO LJRDOKAZOAKLDU-UDXJMMFXSA-N 0.000 description 1
- SXXFNENRGADUMK-ILYOTBPNSA-N (6z,9z,12z)-15-iodo-16-pentyl-1-oxacyclohexadeca-6,9,12-trien-2-one Chemical compound CCCCCC1OC(=O)CCC\C=C/C\C=C/C\C=C/CC1I SXXFNENRGADUMK-ILYOTBPNSA-N 0.000 description 1
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 description 1
- NDAUXUAQIAJITI-LBPRGKRZSA-N (R)-salbutamol Chemical compound CC(C)(C)NC[C@H](O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-LBPRGKRZSA-N 0.000 description 1
- ZZIKIHCNFWXKDY-FMIVXFBMSA-N (e)-2-amino-3,4-dihydroxy-2-(hydroxymethyl)-14-oxoicos-6-enoic acid Chemical compound CCCCCCC(=O)CCCCCC\C=C\CC(O)C(O)C(N)(CO)C(O)=O ZZIKIHCNFWXKDY-FMIVXFBMSA-N 0.000 description 1
- VSNHCAURESNICA-NJFSPNSNSA-N 1-oxidanylurea Chemical compound N[14C](=O)NO VSNHCAURESNICA-NJFSPNSNSA-N 0.000 description 1
- XNWFRZJHXBZDAG-UHFFFAOYSA-N 2-METHOXYETHANOL Chemical compound COCCO XNWFRZJHXBZDAG-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- QQZOPKMRPOGIEB-UHFFFAOYSA-N 2-Oxohexane Chemical compound CCCCC(C)=O QQZOPKMRPOGIEB-UHFFFAOYSA-N 0.000 description 1
- ZKLPARSLTMPFCP-OAQYLSRUSA-N 2-[2-[4-[(R)-(4-chlorophenyl)-phenylmethyl]-1-piperazinyl]ethoxy]acetic acid Chemical compound C1CN(CCOCC(=O)O)CCN1[C@@H](C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-OAQYLSRUSA-N 0.000 description 1
- CBUOGMOTDGNEAW-UHFFFAOYSA-N 2-[4-(bromomethyl)phenyl]-4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(CBr)C=C1 CBUOGMOTDGNEAW-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- SPCKHVPPRJWQRZ-UHFFFAOYSA-N 2-benzhydryloxy-n,n-dimethylethanamine;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1C(OCCN(C)C)C1=CC=CC=C1 SPCKHVPPRJWQRZ-UHFFFAOYSA-N 0.000 description 1
- ZNQVEEAIQZEUHB-UHFFFAOYSA-N 2-ethoxyethanol Chemical compound CCOCCO ZNQVEEAIQZEUHB-UHFFFAOYSA-N 0.000 description 1
- 229940093475 2-ethoxyethanol Drugs 0.000 description 1
- KUWPCJHYPSUOFW-YBXAARCKSA-N 2-nitrophenyl beta-D-galactoside Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1OC1=CC=CC=C1[N+]([O-])=O KUWPCJHYPSUOFW-YBXAARCKSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- VXGRJERITKFWPL-UHFFFAOYSA-N 4',5'-Dihydropsoralen Natural products C1=C2OC(=O)C=CC2=CC2=C1OCC2 VXGRJERITKFWPL-UHFFFAOYSA-N 0.000 description 1
- WNWVKZTYMQWFHE-UHFFFAOYSA-N 4-ethylmorpholine Chemical compound [CH2]CN1CCOCC1 WNWVKZTYMQWFHE-UHFFFAOYSA-N 0.000 description 1
- TVGFHUIJNZRKFW-UHFFFAOYSA-N 5-bromo-[1,2,4]triazolo[1,5-a]pyridin-2-amine Chemical compound C1=CC=C(Br)N2N=C(N)N=C21 TVGFHUIJNZRKFW-UHFFFAOYSA-N 0.000 description 1
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 1
- MJZJYWCQPMNPRM-UHFFFAOYSA-N 6,6-dimethyl-1-[3-(2,4,5-trichlorophenoxy)propoxy]-1,6-dihydro-1,3,5-triazine-2,4-diamine Chemical compound CC1(C)N=C(N)N=C(N)N1OCCCOC1=CC(Cl)=C(Cl)C=C1Cl MJZJYWCQPMNPRM-UHFFFAOYSA-N 0.000 description 1
- USSIQXCVUWKGNF-UHFFFAOYSA-N 6-(dimethylamino)-4,4-diphenylheptan-3-one Chemical compound C=1C=CC=CC=1C(CC(C)N(C)C)(C(=O)CC)C1=CC=CC=C1 USSIQXCVUWKGNF-UHFFFAOYSA-N 0.000 description 1
- WYWHKKSPHMUBEB-UHFFFAOYSA-N 6-Mercaptoguanine Natural products N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 1
- RTAPDZBZLSXHQQ-UHFFFAOYSA-N 8-methyl-3,7-dihydropurine-2,6-dione Chemical class N1C(=O)NC(=O)C2=C1N=C(C)N2 RTAPDZBZLSXHQQ-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-OUBTZVSYSA-N Ammonia-15N Chemical compound [15NH3] QGZKDVFQNNGYKY-OUBTZVSYSA-N 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- 206010061424 Anal cancer Diseases 0.000 description 1
- 208000007860 Anus Neoplasms Diseases 0.000 description 1
- 206010073360 Appendix cancer Diseases 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 206010003571 Astrocytoma Diseases 0.000 description 1
- 201000008271 Atypical teratoid rhabdoid tumor Diseases 0.000 description 1
- 206010004146 Basal cell carcinoma Diseases 0.000 description 1
- 206010004593 Bile duct cancer Diseases 0.000 description 1
- 206010005949 Bone cancer Diseases 0.000 description 1
- 208000018084 Bone neoplasm Diseases 0.000 description 1
- 206010006143 Brain stem glioma Diseases 0.000 description 1
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 1
- PJFHZKIDENOSJB-UHFFFAOYSA-N Budesonide/formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1.C1CC2=CC(=O)C=CC2(C)C2C1C1CC3OC(CCC)OC3(C(=O)CO)C1(C)CC2O PJFHZKIDENOSJB-UHFFFAOYSA-N 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- DQQBLZJZTHPZIT-UHFFFAOYSA-N C1CC1(C2=NN3C(=N2)C=CC=C3C4=CC=C(C=C4)CO)C(=O)N Chemical compound C1CC1(C2=NN3C(=N2)C=CC=C3C4=CC=C(C=C4)CO)C(=O)N DQQBLZJZTHPZIT-UHFFFAOYSA-N 0.000 description 1
- JGLMVXWAHNTPRF-CMDGGOBGSA-N CCN1N=C(C)C=C1C(=O)NC1=NC2=CC(=CC(OC)=C2N1C\C=C\CN1C(NC(=O)C2=CC(C)=NN2CC)=NC2=CC(=CC(OCCCN3CCOCC3)=C12)C(N)=O)C(N)=O Chemical compound CCN1N=C(C)C=C1C(=O)NC1=NC2=CC(=CC(OC)=C2N1C\C=C\CN1C(NC(=O)C2=CC(C)=NN2CC)=NC2=CC(=CC(OCCCN3CCOCC3)=C12)C(N)=O)C(N)=O JGLMVXWAHNTPRF-CMDGGOBGSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 description 1
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-OUBTZVSYSA-N Carbon-13 Chemical compound [13C] OKTJSMMVPCPJKN-OUBTZVSYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-NJFSPNSNSA-N Carbon-14 Chemical compound [14C] OKTJSMMVPCPJKN-NJFSPNSNSA-N 0.000 description 1
- 206010007279 Carcinoid tumour of the gastrointestinal tract Diseases 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 206010007558 Cardiac failure chronic Diseases 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 208000005024 Castleman disease Diseases 0.000 description 1
- ZKLPARSLTMPFCP-UHFFFAOYSA-N Cetirizine Chemical compound C1CN(CCOCC(=O)O)CCN1C(C=1C=CC(Cl)=CC=1)C1=CC=CC=C1 ZKLPARSLTMPFCP-UHFFFAOYSA-N 0.000 description 1
- 108010005939 Ciliary Neurotrophic Factor Proteins 0.000 description 1
- 102100031614 Ciliary neurotrophic factor Human genes 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 206010014476 Elevated cholesterol Diseases 0.000 description 1
- 201000008228 Ependymoblastoma Diseases 0.000 description 1
- 206010014967 Ependymoma Diseases 0.000 description 1
- 206010014968 Ependymoma malignant Diseases 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 1
- 208000032027 Essential Thrombocythemia Diseases 0.000 description 1
- HKVAMNSJSFKALM-GKUWKFKPSA-N Everolimus Chemical compound C1C[C@@H](OCCO)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 HKVAMNSJSFKALM-GKUWKFKPSA-N 0.000 description 1
- 201000008808 Fibrosarcoma Diseases 0.000 description 1
- WJOHZNCJWYWUJD-IUGZLZTKSA-N Fluocinonide Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@H]3OC(C)(C)O[C@@]3(C(=O)COC(=O)C)[C@@]2(C)C[C@@H]1O WJOHZNCJWYWUJD-IUGZLZTKSA-N 0.000 description 1
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical class OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- 208000022072 Gallbladder Neoplasms Diseases 0.000 description 1
- 201000003741 Gastrointestinal carcinoma Diseases 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- VPNYRYCIDCJBOM-UHFFFAOYSA-M Glycopyrronium bromide Chemical compound [Br-].C1[N+](C)(C)CCC1OC(=O)C(O)(C=1C=CC=CC=1)C1CCCC1 VPNYRYCIDCJBOM-UHFFFAOYSA-M 0.000 description 1
- BLCLNMBMMGCOAS-URPVMXJPSA-N Goserelin Chemical compound C([C@@H](C(=O)N[C@H](COC(C)(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NNC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 BLCLNMBMMGCOAS-URPVMXJPSA-N 0.000 description 1
- 108010069236 Goserelin Proteins 0.000 description 1
- 102000009465 Growth Factor Receptors Human genes 0.000 description 1
- 108010009202 Growth Factor Receptors Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 208000032843 Hemorrhage Diseases 0.000 description 1
- 206010073069 Hepatic cancer Diseases 0.000 description 1
- 208000017604 Hodgkin disease Diseases 0.000 description 1
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 1
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 1
- 101001109689 Homo sapiens Nuclear receptor subfamily 4 group A member 3 Proteins 0.000 description 1
- 101000992170 Homo sapiens Oncostatin-M Proteins 0.000 description 1
- 208000035150 Hypercholesterolemia Diseases 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- 102000003816 Interleukin-13 Human genes 0.000 description 1
- 108090000176 Interleukin-13 Proteins 0.000 description 1
- 102000010789 Interleukin-2 Receptors Human genes 0.000 description 1
- 108010038453 Interleukin-2 Receptors Proteins 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 102000004388 Interleukin-4 Human genes 0.000 description 1
- 108010002616 Interleukin-5 Proteins 0.000 description 1
- 102000000743 Interleukin-5 Human genes 0.000 description 1
- 206010061252 Intraocular melanoma Diseases 0.000 description 1
- 208000009164 Islet Cell Adenoma Diseases 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- 229940116839 Janus kinase 1 inhibitor Drugs 0.000 description 1
- 206010072206 Janus kinase 2 mutation Diseases 0.000 description 1
- 206010023203 Joint destruction Diseases 0.000 description 1
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 1
- ZCVMWBYGMWKGHF-UHFFFAOYSA-N Ketotifene Chemical compound C1CN(C)CCC1=C1C2=CC=CC=C2CC(=O)C2=C1C=CS2 ZCVMWBYGMWKGHF-UHFFFAOYSA-N 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- 239000005517 L01XE01 - Imatinib Substances 0.000 description 1
- 239000005551 L01XE03 - Erlotinib Substances 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 201000005099 Langerhans cell histiocytosis Diseases 0.000 description 1
- 206010023825 Laryngeal cancer Diseases 0.000 description 1
- 208000018142 Leiomyosarcoma Diseases 0.000 description 1
- 108090000581 Leukemia inhibitory factor Proteins 0.000 description 1
- 206010061523 Lip and/or oral cavity cancer Diseases 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 208000006644 Malignant Fibrous Histiocytoma Diseases 0.000 description 1
- 208000032271 Malignant tumor of penis Diseases 0.000 description 1
- 208000000172 Medulloblastoma Diseases 0.000 description 1
- 235000006679 Mentha X verticillata Nutrition 0.000 description 1
- 235000002899 Mentha suaveolens Nutrition 0.000 description 1
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 1
- 206010027406 Mesothelioma Diseases 0.000 description 1
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 1
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 1
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 description 1
- 239000004909 Moisturizer Substances 0.000 description 1
- 201000002481 Myositis Diseases 0.000 description 1
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 1
- 206010029216 Nervousness Diseases 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 1
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 1
- 206010030216 Oesophagitis Diseases 0.000 description 1
- 206010031096 Oropharyngeal cancer Diseases 0.000 description 1
- 206010057444 Oropharyngeal neoplasm Diseases 0.000 description 1
- 208000007571 Ovarian Epithelial Carcinoma Diseases 0.000 description 1
- BRUQQQPBMZOVGD-XFKAJCMBSA-N Oxycodone Chemical compound O=C([C@@H]1O2)CC[C@@]3(O)[C@H]4CC5=CC=C(OC)C2=C5[C@@]13CCN4C BRUQQQPBMZOVGD-XFKAJCMBSA-N 0.000 description 1
- 238000013494 PH determination Methods 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 208000000821 Parathyroid Neoplasms Diseases 0.000 description 1
- 208000002471 Penile Neoplasms Diseases 0.000 description 1
- 206010034299 Penile cancer Diseases 0.000 description 1
- 239000004264 Petrolatum Substances 0.000 description 1
- 208000009565 Pharyngeal Neoplasms Diseases 0.000 description 1
- 206010034811 Pharyngeal cancer Diseases 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 206010050487 Pinealoblastoma Diseases 0.000 description 1
- 201000008199 Pleuropulmonary blastoma Diseases 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 229940079156 Proteasome inhibitor Drugs 0.000 description 1
- 206010065874 Psoriatic conditions Diseases 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 208000015634 Rectal Neoplasms Diseases 0.000 description 1
- 102000007078 STAT Transcription Factors Human genes 0.000 description 1
- 108010072819 STAT Transcription Factors Proteins 0.000 description 1
- 208000004337 Salivary Gland Neoplasms Diseases 0.000 description 1
- 206010061934 Salivary gland cancer Diseases 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- GIIZNNXWQWCKIB-UHFFFAOYSA-N Serevent Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1 GIIZNNXWQWCKIB-UHFFFAOYSA-N 0.000 description 1
- 208000000453 Skin Neoplasms Diseases 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 208000021712 Soft tissue sarcoma Diseases 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 108700012920 TNF Proteins 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- 206010057644 Testis cancer Diseases 0.000 description 1
- 206010043515 Throat cancer Diseases 0.000 description 1
- 102000036693 Thrombopoietin Human genes 0.000 description 1
- 102100034195 Thrombopoietin Human genes 0.000 description 1
- 108010041111 Thrombopoietin Proteins 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 201000009365 Thymic carcinoma Diseases 0.000 description 1
- 208000024770 Thyroid neoplasm Diseases 0.000 description 1
- 239000004012 Tofacitinib Substances 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 102000000887 Transcription factor STAT Human genes 0.000 description 1
- 108050007918 Transcription factor STAT Proteins 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 208000015778 Undifferentiated pleomorphic sarcoma Diseases 0.000 description 1
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Natural products NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 1
- 206010046431 Urethral cancer Diseases 0.000 description 1
- 206010046458 Urethral neoplasms Diseases 0.000 description 1
- 208000002495 Uterine Neoplasms Diseases 0.000 description 1
- 201000005969 Uveal melanoma Diseases 0.000 description 1
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 1
- 208000008383 Wilms tumor Diseases 0.000 description 1
- OGQICQVSFDPSEI-UHFFFAOYSA-N Zorac Chemical compound N1=CC(C(=O)OCC)=CC=C1C#CC1=CC=C(SCCC2(C)C)C2=C1 OGQICQVSFDPSEI-UHFFFAOYSA-N 0.000 description 1
- YYAZJTUGSQOFHG-IAVNQIGZSA-N [(6s,8s,10s,11s,13s,14s,16r,17r)-6,9-difluoro-17-(fluoromethylsulfanylcarbonyl)-11-hydroxy-10,13,16-trimethyl-3-oxo-6,7,8,11,12,14,15,16-octahydrocyclopenta[a]phenanthren-17-yl] propanoate;2-(hydroxymethyl)-4-[1-hydroxy-2-[6-(4-phenylbutoxy)hexylamino]eth Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1.C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)C1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(OC(=O)CC)[C@@]2(C)C[C@@H]1O YYAZJTUGSQOFHG-IAVNQIGZSA-N 0.000 description 1
- PZRPBPMLSSNFOM-UHFFFAOYSA-N [4-(hydroxymethyl)phenyl]boronic acid Chemical compound OCC1=CC=C(B(O)O)C=C1 PZRPBPMLSSNFOM-UHFFFAOYSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 229960005339 acitretin Drugs 0.000 description 1
- 208000017733 acquired polycythemia vera Diseases 0.000 description 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000011149 active material Substances 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 208000020990 adrenal cortex carcinoma Diseases 0.000 description 1
- 208000007128 adrenocortical carcinoma Diseases 0.000 description 1
- 229940009456 adriamycin Drugs 0.000 description 1
- 230000032683 aging Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- IHUNBGSDBOWDMA-AQFIFDHZSA-N all-trans-acitretin Chemical compound COC1=CC(C)=C(\C=C\C(\C)=C\C=C\C(\C)=C\C(O)=O)C(C)=C1C IHUNBGSDBOWDMA-AQFIFDHZSA-N 0.000 description 1
- 208000030961 allergic reaction Diseases 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 229960003556 aminophylline Drugs 0.000 description 1
- PECIYKGSSMCNHN-UHFFFAOYSA-N aminophylline Chemical compound NCCN.O=C1N(C)C(=O)N(C)C2=NC=N[C]21.O=C1N(C)C(=O)N(C)C2=NC=N[C]21 PECIYKGSSMCNHN-UHFFFAOYSA-N 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 1
- YBBLVLTVTVSKRW-UHFFFAOYSA-N anastrozole Chemical compound N#CC(C)(C)C1=CC(C(C)(C#N)C)=CC(CN2N=CN=C2)=C1 YBBLVLTVTVSKRW-UHFFFAOYSA-N 0.000 description 1
- 229960002932 anastrozole Drugs 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 229940045799 anthracyclines and related substance Drugs 0.000 description 1
- 230000001078 anti-cholinergic effect Effects 0.000 description 1
- 230000002590 anti-leukotriene effect Effects 0.000 description 1
- 230000000781 anti-lymphocytic effect Effects 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 230000001494 anti-thymocyte effect Effects 0.000 description 1
- 229940033495 antimalarials Drugs 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 229940045719 antineoplastic alkylating agent nitrosoureas Drugs 0.000 description 1
- 239000003972 antineoplastic antibiotic Substances 0.000 description 1
- 239000003435 antirheumatic agent Substances 0.000 description 1
- 201000011165 anus cancer Diseases 0.000 description 1
- 208000021780 appendiceal neoplasm Diseases 0.000 description 1
- 239000011260 aqueous acid Substances 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 239000008135 aqueous vehicle Substances 0.000 description 1
- 239000010478 argan oil Substances 0.000 description 1
- 229940092117 atgam Drugs 0.000 description 1
- 229960005207 auranofin Drugs 0.000 description 1
- AUJRCFUBUPVWSZ-XTZHGVARSA-M auranofin Chemical compound CCP(CC)(CC)=[Au]S[C@@H]1O[C@H](COC(C)=O)[C@@H](OC(C)=O)[C@H](OC(C)=O)[C@H]1OC(C)=O AUJRCFUBUPVWSZ-XTZHGVARSA-M 0.000 description 1
- 229940120638 avastin Drugs 0.000 description 1
- CBHOOMGKXCMKIR-UHFFFAOYSA-N azane;methanol Chemical compound N.OC CBHOOMGKXCMKIR-UHFFFAOYSA-N 0.000 description 1
- 229960003060 bambuterol Drugs 0.000 description 1
- ANZXOIAKUNOVQU-UHFFFAOYSA-N bambuterol Chemical compound CN(C)C(=O)OC1=CC(OC(=O)N(C)C)=CC(C(O)CNC(C)(C)C)=C1 ANZXOIAKUNOVQU-UHFFFAOYSA-N 0.000 description 1
- 229960005176 bamifylline Drugs 0.000 description 1
- VVUYEFBRTFASAH-UHFFFAOYSA-N bamifylline Chemical compound N=1C=2N(C)C(=O)N(C)C(=O)C=2N(CCN(CCO)CC)C=1CC1=CC=CC=C1 VVUYEFBRTFASAH-UHFFFAOYSA-N 0.000 description 1
- 229950000971 baricitinib Drugs 0.000 description 1
- XUZMWHLSFXCVMG-UHFFFAOYSA-N baricitinib Chemical compound C1N(S(=O)(=O)CC)CC1(CC#N)N1N=CC(C=2C=3C=CNC=3N=CN=2)=C1 XUZMWHLSFXCVMG-UHFFFAOYSA-N 0.000 description 1
- 229960004669 basiliximab Drugs 0.000 description 1
- NBMKJKDGKREAPL-DVTGEIKXSA-N beclomethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O NBMKJKDGKREAPL-DVTGEIKXSA-N 0.000 description 1
- 229940092705 beclomethasone Drugs 0.000 description 1
- 229960003270 belimumab Drugs 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229940022836 benlysta Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 229940125388 beta agonist Drugs 0.000 description 1
- 229960002537 betamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-DVTGEIKXSA-N betamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-DVTGEIKXSA-N 0.000 description 1
- 208000026900 bile duct neoplasm Diseases 0.000 description 1
- 108091008324 binding proteins Proteins 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 238000010256 biochemical assay Methods 0.000 description 1
- 239000003139 biocide Substances 0.000 description 1
- 229960000074 biopharmaceutical Drugs 0.000 description 1
- 229960004620 bitolterol Drugs 0.000 description 1
- FZGVEKPRDOIXJY-UHFFFAOYSA-N bitolterol Chemical compound C1=CC(C)=CC=C1C(=O)OC1=CC=C(C(O)CNC(C)(C)C)C=C1OC(=O)C1=CC=C(C)C=C1 FZGVEKPRDOIXJY-UHFFFAOYSA-N 0.000 description 1
- 208000034158 bleeding Diseases 0.000 description 1
- 230000000740 bleeding effect Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 229940000031 blood and blood forming organ drug Drugs 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 238000010241 blood sampling Methods 0.000 description 1
- 208000012172 borderline epithelial tumor of ovary Diseases 0.000 description 1
- GXJABQQUPOEUTA-RDJZCZTQSA-N bortezomib Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)B(O)O)NC(=O)C=1N=CC=NC=1)C1=CC=CC=C1 GXJABQQUPOEUTA-RDJZCZTQSA-N 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 229940124630 bronchodilator Drugs 0.000 description 1
- 229960004436 budesonide Drugs 0.000 description 1
- 229940080593 budesonide / formoterol Drugs 0.000 description 1
- 229940046731 calcineurin inhibitors Drugs 0.000 description 1
- LWQQLNNNIPYSNX-UROSTWAQSA-N calcipotriol Chemical compound C1([C@H](O)/C=C/[C@@H](C)[C@@H]2[C@]3(CCCC(/[C@@H]3CC2)=C\C=C\2C([C@@H](O)C[C@H](O)C/2)=C)C)CC1 LWQQLNNNIPYSNX-UROSTWAQSA-N 0.000 description 1
- 229960002882 calcipotriol Drugs 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 235000011148 calcium chloride Nutrition 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 238000011088 calibration curve Methods 0.000 description 1
- 229960004117 capecitabine Drugs 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 238000000423 cell based assay Methods 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000001516 cell proliferation assay Methods 0.000 description 1
- 229960001803 cetirizine Drugs 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 208000006990 cholangiocarcinoma Diseases 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- DERZBLKQOCDDDZ-JLHYYAGUSA-N cinnarizine Chemical compound C1CN(C(C=2C=CC=CC=2)C=2C=CC=CC=2)CCN1C\C=C\C1=CC=CC=C1 DERZBLKQOCDDDZ-JLHYYAGUSA-N 0.000 description 1
- 229960000876 cinnarizine Drugs 0.000 description 1
- ZCZQDTUCMRSEAS-CCLYOLAMSA-N co-codamol Chemical compound OP(O)(O)=O.CC(=O)NC1=CC=C(O)C=C1.C([C@H]1[C@H](N(CC[C@@]112)C)C3)=C[C@H](O)[C@@H]1OC1=C2C3=CC=C1OC ZCZQDTUCMRSEAS-CCLYOLAMSA-N 0.000 description 1
- 239000011280 coal tar Substances 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 239000003636 conditioned culture medium Substances 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- 229940109248 cromoglycate Drugs 0.000 description 1
- IMZMKUWMOSJXDT-UHFFFAOYSA-N cromoglycic acid Chemical compound O1C(C(O)=O)=CC(=O)C2=C1C=CC=C2OCC(O)COC1=CC=CC2=C1C(=O)C=C(C(O)=O)O2 IMZMKUWMOSJXDT-UHFFFAOYSA-N 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 239000012228 culture supernatant Substances 0.000 description 1
- 238000011461 current therapy Methods 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 239000000824 cytostatic agent Substances 0.000 description 1
- 229960002806 daclizumab Drugs 0.000 description 1
- 229960000640 dactinomycin Drugs 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 239000000850 decongestant Substances 0.000 description 1
- 229940124581 decongestants Drugs 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000003412 degenerative effect Effects 0.000 description 1
- CFCUWKMKBJTWLW-UHFFFAOYSA-N deoliosyl-3C-alpha-L-digitoxosyl-MTM Natural products CC=1C(O)=C2C(O)=C3C(=O)C(OC4OC(C)C(O)C(OC5OC(C)C(O)C(OC6OC(C)C(O)C(C)(O)C6)C5)C4)C(C(OC)C(=O)C(O)C(C)O)CC3=CC2=CC=1OC(OC(C)C1O)CC1OC1CC(O)C(O)C(C)O1 CFCUWKMKBJTWLW-UHFFFAOYSA-N 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 231100000223 dermal penetration Toxicity 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229960002593 desoximetasone Drugs 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 229960004193 dextropropoxyphene Drugs 0.000 description 1
- XLMALTXPSGQGBX-GCJKJVERSA-N dextropropoxyphene Chemical compound C([C@](OC(=O)CC)([C@H](C)CN(C)C)C=1C=CC=CC=1)C1=CC=CC=C1 XLMALTXPSGQGBX-GCJKJVERSA-N 0.000 description 1
- 238000000113 differential scanning calorimetry Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- XYYVYLMBEZUESM-UHFFFAOYSA-N dihydrocodeine Natural products C1C(N(CCC234)C)C2C=CC(=O)C3OC2=C4C1=CC=C2OC XYYVYLMBEZUESM-UHFFFAOYSA-N 0.000 description 1
- IJKVHSBPTUYDLN-UHFFFAOYSA-N dihydroxy(oxo)silane Chemical compound O[Si](O)=O IJKVHSBPTUYDLN-UHFFFAOYSA-N 0.000 description 1
- 125000000532 dioxanyl group Chemical group 0.000 description 1
- 229960000520 diphenhydramine Drugs 0.000 description 1
- FSRXIRGQJIHEFB-UHFFFAOYSA-N diphenylphosphane;ethane Chemical compound CC.C=1C=CC=CC=1PC1=CC=CC=C1 FSRXIRGQJIHEFB-UHFFFAOYSA-N 0.000 description 1
- VXIHRIQNJCRFQX-UHFFFAOYSA-K disodium aurothiomalate Chemical compound [Na+].[Na+].[O-]C(=O)CC(S[Au])C([O-])=O VXIHRIQNJCRFQX-UHFFFAOYSA-K 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 229910000397 disodium phosphate Inorganic materials 0.000 description 1
- 235000019800 disodium phosphate Nutrition 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 229960003668 docetaxel Drugs 0.000 description 1
- 238000011143 downstream manufacturing Methods 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 229940099191 duragesic Drugs 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 208000014616 embryonal neoplasm Diseases 0.000 description 1
- 231100001129 embryonic lethality Toxicity 0.000 description 1
- 229940073621 enbrel Drugs 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 229960000305 enflurane Drugs 0.000 description 1
- JPGQOUSTVILISH-UHFFFAOYSA-N enflurane Chemical compound FC(F)OC(F)(F)C(F)Cl JPGQOUSTVILISH-UHFFFAOYSA-N 0.000 description 1
- 150000002085 enols Chemical class 0.000 description 1
- 230000002327 eosinophilic effect Effects 0.000 description 1
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 1
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 1
- 229940082789 erbitux Drugs 0.000 description 1
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 description 1
- 230000010437 erythropoiesis Effects 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- 201000004101 esophageal cancer Diseases 0.000 description 1
- 208000028299 esophageal disease Diseases 0.000 description 1
- 208000006881 esophagitis Diseases 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- AFAXGSQYZLGZPG-UHFFFAOYSA-N ethanedisulfonic acid Chemical compound OS(=O)(=O)CCS(O)(=O)=O AFAXGSQYZLGZPG-UHFFFAOYSA-N 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- BDTDECDAHYOJRO-UHFFFAOYSA-N ethyl n-(sulfanylidenemethylidene)carbamate Chemical compound CCOC(=O)N=C=S BDTDECDAHYOJRO-UHFFFAOYSA-N 0.000 description 1
- HQMNCQVAMBCHCO-DJRRULDNSA-N etretinate Chemical compound CCOC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)C=C(OC)C(C)=C1C HQMNCQVAMBCHCO-DJRRULDNSA-N 0.000 description 1
- 229960002199 etretinate Drugs 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 229960005167 everolimus Drugs 0.000 description 1
- 238000013265 extended release Methods 0.000 description 1
- 238000013213 extrapolation Methods 0.000 description 1
- 208000024519 eye neoplasm Diseases 0.000 description 1
- PJMPHNIQZUBGLI-UHFFFAOYSA-N fentanyl Chemical compound C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 PJMPHNIQZUBGLI-UHFFFAOYSA-N 0.000 description 1
- 229960002428 fentanyl Drugs 0.000 description 1
- IVLVTNPOHDFFCJ-UHFFFAOYSA-N fentanyl citrate Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1N(C(=O)CC)C(CC1)CCN1CCC1=CC=CC=C1 IVLVTNPOHDFFCJ-UHFFFAOYSA-N 0.000 description 1
- 239000012065 filter cake Substances 0.000 description 1
- 229960000556 fingolimod Drugs 0.000 description 1
- KKGQTZUTZRNORY-UHFFFAOYSA-N fingolimod Chemical compound CCCCCCCCC1=CC=C(CCC(N)(CO)CO)C=C1 KKGQTZUTZRNORY-UHFFFAOYSA-N 0.000 description 1
- 238000003818 flash chromatography Methods 0.000 description 1
- 229960000785 fluocinonide Drugs 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- 229940114006 fluticasone / salmeterol Drugs 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- WBJINCZRORDGAQ-UHFFFAOYSA-N formic acid ethyl ester Natural products CCOC=O WBJINCZRORDGAQ-UHFFFAOYSA-N 0.000 description 1
- 229960002848 formoterol Drugs 0.000 description 1
- BPZSYCZIITTYBL-UHFFFAOYSA-N formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1 BPZSYCZIITTYBL-UHFFFAOYSA-N 0.000 description 1
- 201000010175 gallbladder cancer Diseases 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 201000011243 gastrointestinal stromal tumor Diseases 0.000 description 1
- 230000014509 gene expression Effects 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 208000005017 glioblastoma Diseases 0.000 description 1
- 229940015042 glycopyrrolate Drugs 0.000 description 1
- 229960002913 goserelin Drugs 0.000 description 1
- 208000024908 graft versus host disease Diseases 0.000 description 1
- 208000035474 group of disease Diseases 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 229960003132 halothane Drugs 0.000 description 1
- BCQZXOMGPXTTIC-UHFFFAOYSA-N halothane Chemical compound FC(F)(F)C(Cl)Br BCQZXOMGPXTTIC-UHFFFAOYSA-N 0.000 description 1
- 201000010536 head and neck cancer Diseases 0.000 description 1
- 208000014829 head and neck neoplasm Diseases 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 239000003481 heat shock protein 90 inhibitor Substances 0.000 description 1
- 239000001307 helium Substances 0.000 description 1
- 229910052734 helium Inorganic materials 0.000 description 1
- 229960001626 helium Drugs 0.000 description 1
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 1
- 229940022353 herceptin Drugs 0.000 description 1
- 210000003630 histaminocyte Anatomy 0.000 description 1
- 102000049918 human JAK1 Human genes 0.000 description 1
- 102000049921 human JAK2 Human genes 0.000 description 1
- 102000049912 human JAK3 Human genes 0.000 description 1
- 102000047217 human NR4A3 Human genes 0.000 description 1
- 102000043703 human OSM Human genes 0.000 description 1
- 102000047536 human TYK2 Human genes 0.000 description 1
- 210000005104 human peripheral blood lymphocyte Anatomy 0.000 description 1
- 229940048921 humira Drugs 0.000 description 1
- LLPOLZWFYMWNKH-CMKMFDCUSA-N hydrocodone Chemical compound C([C@H]1[C@H](N(CC[C@@]112)C)C3)CC(=O)[C@@H]1OC1=C2C3=CC=C1OC LLPOLZWFYMWNKH-CMKMFDCUSA-N 0.000 description 1
- 229960000240 hydrocodone Drugs 0.000 description 1
- OROGSEYTTFOCAN-UHFFFAOYSA-N hydrocodone Natural products C1C(N(CCC234)C)C2C=CC(O)C3OC2=C4C1=CC=C2OC OROGSEYTTFOCAN-UHFFFAOYSA-N 0.000 description 1
- 239000008309 hydrophilic cream Substances 0.000 description 1
- 230000009610 hypersensitivity Effects 0.000 description 1
- YLMAHDNUQAMNNX-UHFFFAOYSA-N imatinib methanesulfonate Chemical compound CS(O)(=O)=O.C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 YLMAHDNUQAMNNX-UHFFFAOYSA-N 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 230000004957 immunoregulator effect Effects 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 229940124589 immunosuppressive drug Drugs 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 239000003983 inhalation anesthetic agent Substances 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- 201000002313 intestinal cancer Diseases 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 150000008040 ionic compounds Chemical class 0.000 description 1
- OEXHQOGQTVQTAT-JRNQLAHRSA-N ipratropium Chemical compound O([C@H]1C[C@H]2CC[C@@H](C1)[N@@+]2(C)C(C)C)C(=O)C(CO)C1=CC=CC=C1 OEXHQOGQTVQTAT-JRNQLAHRSA-N 0.000 description 1
- 229960001888 ipratropium Drugs 0.000 description 1
- 229960001361 ipratropium bromide Drugs 0.000 description 1
- KEWHKYJURDBRMN-ZEODDXGYSA-M ipratropium bromide hydrate Chemical compound O.[Br-].O([C@H]1C[C@H]2CC[C@@H](C1)[N@@+]2(C)C(C)C)C(=O)C(CO)C1=CC=CC=C1 KEWHKYJURDBRMN-ZEODDXGYSA-M 0.000 description 1
- GJRQTCIYDGXPES-UHFFFAOYSA-N iso-butyl acetate Natural products CC(C)COC(C)=O GJRQTCIYDGXPES-UHFFFAOYSA-N 0.000 description 1
- FGKJLKRYENPLQH-UHFFFAOYSA-M isocaproate Chemical compound CC(C)CCC([O-])=O FGKJLKRYENPLQH-UHFFFAOYSA-M 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- OQAGVSWESNCJJT-UHFFFAOYSA-N isovaleric acid methyl ester Natural products COC(=O)CC(C)C OQAGVSWESNCJJT-UHFFFAOYSA-N 0.000 description 1
- 230000008407 joint function Effects 0.000 description 1
- 210000004731 jugular vein Anatomy 0.000 description 1
- 229960003299 ketamine Drugs 0.000 description 1
- 229960004958 ketotifen Drugs 0.000 description 1
- 238000011813 knockout mouse model Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 206010023841 laryngeal neoplasm Diseases 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 150000002617 leukotrienes Chemical class 0.000 description 1
- 229960001508 levocetirizine Drugs 0.000 description 1
- 229950008204 levosalbutamol Drugs 0.000 description 1
- 208000012987 lip and oral cavity carcinoma Diseases 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 239000003509 long acting drug Substances 0.000 description 1
- 229940125386 long-acting bronchodilator Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000003055 low molecular weight heparin Substances 0.000 description 1
- 229940127215 low-molecular weight heparin Drugs 0.000 description 1
- 206010025135 lupus erythematosus Diseases 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 229940124302 mTOR inhibitor Drugs 0.000 description 1
- 208000026045 malignant tumor of parathyroid gland Diseases 0.000 description 1
- 239000003628 mammalian target of rapamycin inhibitor Substances 0.000 description 1
- 201000006512 mast cell neoplasm Diseases 0.000 description 1
- 208000006971 mastocytoma Diseases 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 229940126601 medicinal product Drugs 0.000 description 1
- 201000008203 medulloepithelioma Diseases 0.000 description 1
- RQZAXGRLVPAYTJ-GQFGMJRRSA-N megestrol acetate Chemical compound C1=C(C)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 RQZAXGRLVPAYTJ-GQFGMJRRSA-N 0.000 description 1
- 229960004296 megestrol acetate Drugs 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 108020004084 membrane receptors Proteins 0.000 description 1
- 102000006240 membrane receptors Human genes 0.000 description 1
- KBOPZPXVLCULAV-UHFFFAOYSA-N mesalamine Chemical compound NC1=CC=C(O)C(C(O)=O)=C1 KBOPZPXVLCULAV-UHFFFAOYSA-N 0.000 description 1
- 229960004963 mesalazine Drugs 0.000 description 1
- LMOINURANNBYCM-UHFFFAOYSA-N metaproterenol Chemical compound CC(C)NCC(O)C1=CC(O)=CC(O)=C1 LMOINURANNBYCM-UHFFFAOYSA-N 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 229960001797 methadone Drugs 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- GBMDVOWEEQVZKZ-UHFFFAOYSA-N methanol;hydrate Chemical compound O.OC GBMDVOWEEQVZKZ-UHFFFAOYSA-N 0.000 description 1
- 229940043265 methyl isobutyl ketone Drugs 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- CFCUWKMKBJTWLW-BKHRDMLASA-N mithramycin Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@H]1O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1C)O[C@@H]1O[C@H](C)[C@@H](O)[C@H](O[C@@H]2O[C@H](C)[C@H](O)[C@H](O[C@@H]3O[C@H](C)[C@@H](O)[C@@](C)(O)C3)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@H]1C[C@@H](O)[C@H](O)[C@@H](C)O1 CFCUWKMKBJTWLW-BKHRDMLASA-N 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 229950007856 mofetil Drugs 0.000 description 1
- 230000001333 moisturizer Effects 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 235000019799 monosodium phosphate Nutrition 0.000 description 1
- 229960003816 muromonab-cd3 Drugs 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- RTGDFNSFWBGLEC-SYZQJQIISA-N mycophenolate mofetil Chemical compound COC1=C(C)C=2COC(=O)C=2C(O)=C1C\C=C(/C)CCC(=O)OCCN1CCOCC1 RTGDFNSFWBGLEC-SYZQJQIISA-N 0.000 description 1
- 229960004866 mycophenolate mofetil Drugs 0.000 description 1
- 206010028537 myelofibrosis Diseases 0.000 description 1
- 229930183907 myrocin Natural products 0.000 description 1
- YKYONYBAUNKHLG-UHFFFAOYSA-N n-Propyl acetate Natural products CCCOC(C)=O YKYONYBAUNKHLG-UHFFFAOYSA-N 0.000 description 1
- UPSFMJHZUCSEHU-JYGUBCOQSA-N n-[(2s,3r,4r,5s,6r)-2-[(2r,3s,4r,5r,6s)-5-acetamido-4-hydroxy-2-(hydroxymethyl)-6-(4-methyl-2-oxochromen-7-yl)oxyoxan-3-yl]oxy-4,5-dihydroxy-6-(hydroxymethyl)oxan-3-yl]acetamide Chemical compound CC(=O)N[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@H]1[C@H](O)[C@@H](NC(C)=O)[C@H](OC=2C=C3OC(=O)C=C(C)C3=CC=2)O[C@@H]1CO UPSFMJHZUCSEHU-JYGUBCOQSA-N 0.000 description 1
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 1
- NEOZIFRQXFFBFZ-UHFFFAOYSA-N n-[5-[4-(bromomethyl)phenyl]-[1,2,4]triazolo[1,5-a]pyridin-2-yl]cyclopropanecarboxamide Chemical compound C1=CC(CBr)=CC=C1C1=CC=CC2=NC(NC(=O)C3CC3)=NN12 NEOZIFRQXFFBFZ-UHFFFAOYSA-N 0.000 description 1
- GOQYKNQRPGWPLP-UHFFFAOYSA-N n-heptadecyl alcohol Natural products CCCCCCCCCCCCCCCCCO GOQYKNQRPGWPLP-UHFFFAOYSA-N 0.000 description 1
- 229960005016 naphazoline Drugs 0.000 description 1
- UFWIBTONFRDIAS-UHFFFAOYSA-N naphthalene-acid Natural products C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 1
- 230000001613 neoplastic effect Effects 0.000 description 1
- 201000008383 nephritis Diseases 0.000 description 1
- 201000008026 nephroblastoma Diseases 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- VLZLOWPYUQHHCG-UHFFFAOYSA-N nitromethylbenzene Chemical compound [O-][N+](=O)CC1=CC=CC=C1 VLZLOWPYUQHHCG-UHFFFAOYSA-N 0.000 description 1
- 239000002687 nonaqueous vehicle Substances 0.000 description 1
- 238000010606 normalization Methods 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- 201000008106 ocular cancer Diseases 0.000 description 1
- 201000002575 ocular melanoma Diseases 0.000 description 1
- 229960000470 omalizumab Drugs 0.000 description 1
- 229940127240 opiate Drugs 0.000 description 1
- 229940005483 opioid analgesics Drugs 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 229960002657 orciprenaline Drugs 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 201000006958 oropharynx cancer Diseases 0.000 description 1
- 208000021284 ovarian germ cell tumor Diseases 0.000 description 1
- 229960002085 oxycodone Drugs 0.000 description 1
- 229960001528 oxymetazoline Drugs 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- 208000022102 pancreatic neuroendocrine neoplasm Diseases 0.000 description 1
- 208000003154 papilloma Diseases 0.000 description 1
- 208000029211 papillomatosis Diseases 0.000 description 1
- 229960005489 paracetamol Drugs 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 229960001639 penicillamine Drugs 0.000 description 1
- 230000009984 peri-natal effect Effects 0.000 description 1
- 229940066842 petrolatum Drugs 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 238000011170 pharmaceutical development Methods 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- IPNPIHIZVLFAFP-UHFFFAOYSA-N phosphorus tribromide Chemical compound BrP(Br)Br IPNPIHIZVLFAFP-UHFFFAOYSA-N 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 201000003113 pineoblastoma Diseases 0.000 description 1
- 208000010916 pituitary tumor Diseases 0.000 description 1
- 229940072689 plaquenil Drugs 0.000 description 1
- 208000010626 plasma cell neoplasm Diseases 0.000 description 1
- 150000003057 platinum Chemical class 0.000 description 1
- 229960003171 plicamycin Drugs 0.000 description 1
- 208000037244 polycythemia vera Diseases 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 235000015320 potassium carbonate Nutrition 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 238000004313 potentiometry Methods 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 230000036316 preload Effects 0.000 description 1
- 238000004886 process control Methods 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 230000008741 proinflammatory signaling process Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 229940090181 propyl acetate Drugs 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 239000003207 proteasome inhibitor Substances 0.000 description 1
- 230000006920 protein precipitation Effects 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 238000003908 quality control method Methods 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 206010038038 rectal cancer Diseases 0.000 description 1
- 201000001275 rectum cancer Diseases 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 229940116176 remicade Drugs 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 208000037803 restenosis Diseases 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 229960004017 salmeterol Drugs 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- 235000020183 skimmed milk Nutrition 0.000 description 1
- 201000000849 skin cancer Diseases 0.000 description 1
- 210000004927 skin cell Anatomy 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 229960001315 sodium aurothiomalate Drugs 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- AJPJDKMHJJGVTQ-UHFFFAOYSA-M sodium dihydrogen phosphate Chemical compound [Na+].OP(O)([O-])=O AJPJDKMHJJGVTQ-UHFFFAOYSA-M 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 159000000000 sodium salts Chemical group 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 238000003797 solvolysis reaction Methods 0.000 description 1
- 206010062261 spinal cord neoplasm Diseases 0.000 description 1
- 206010041823 squamous cell carcinoma Diseases 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 210000002536 stromal cell Anatomy 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 229960001603 tamoxifen Drugs 0.000 description 1
- AYUNIORJHRXIBJ-TXHRRWQRSA-N tanespimycin Chemical compound N1C(=O)\C(C)=C\C=C/[C@H](OC)[C@@H](OC(N)=O)\C(C)=C\[C@H](C)[C@@H](O)[C@@H](OC)C[C@H](C)CC2=C(NCC=C)C(=O)C=C1C2=O AYUNIORJHRXIBJ-TXHRRWQRSA-N 0.000 description 1
- 229950007866 tanespimycin Drugs 0.000 description 1
- 229940120982 tarceva Drugs 0.000 description 1
- 238000003419 tautomerization reaction Methods 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- 229960000565 tazarotene Drugs 0.000 description 1
- 229960000195 terbutaline Drugs 0.000 description 1
- FBWNMEQMRUMQSO-UHFFFAOYSA-N tergitol NP-9 Chemical compound CCCCCCCCCC1=CC=C(OCCOCCOCCOCCOCCOCCOCCOCCOCCO)C=C1 FBWNMEQMRUMQSO-UHFFFAOYSA-N 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 201000002510 thyroid cancer Diseases 0.000 description 1
- 229960003087 tioguanine Drugs 0.000 description 1
- MNRILEROXIRVNJ-UHFFFAOYSA-N tioguanine Chemical compound N1C(N)=NC(=S)C2=NC=N[C]21 MNRILEROXIRVNJ-UHFFFAOYSA-N 0.000 description 1
- 229960001350 tofacitinib Drugs 0.000 description 1
- UJLAWZDWDVHWOW-YPMHNXCESA-N tofacitinib Chemical compound C[C@@H]1CCN(C(=O)CC#N)C[C@@H]1N(C)C1=NC=NC2=C1C=CN2 UJLAWZDWDVHWOW-YPMHNXCESA-N 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 229940100611 topical cream Drugs 0.000 description 1
- 229940100615 topical ointment Drugs 0.000 description 1
- 229940035306 topicort Drugs 0.000 description 1
- XFCLJVABOIYOMF-QPLCGJKRSA-N toremifene Chemical compound C1=CC(OCCN(C)C)=CC=C1C(\C=1C=CC=CC=1)=C(\CCCl)C1=CC=CC=C1 XFCLJVABOIYOMF-QPLCGJKRSA-N 0.000 description 1
- 229960005026 toremifene Drugs 0.000 description 1
- 239000011573 trace mineral Substances 0.000 description 1
- 235000013619 trace mineral Nutrition 0.000 description 1
- 210000003437 trachea Anatomy 0.000 description 1
- 229960001262 tramazoline Drugs 0.000 description 1
- QQJLHRRUATVHED-UHFFFAOYSA-N tramazoline Chemical compound N1CCN=C1NC1=CC=CC2=C1CCCC2 QQJLHRRUATVHED-UHFFFAOYSA-N 0.000 description 1
- LLPOLZWFYMWNKH-UHFFFAOYSA-N trans-dihydrocodeinone Natural products C1C(N(CCC234)C)C2CCC(=O)C3OC2=C4C1=CC=C2OC LLPOLZWFYMWNKH-UHFFFAOYSA-N 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 239000012096 transfection reagent Substances 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- CDMIYIVDILNBIJ-UHFFFAOYSA-N triazinane-4,5,6-trithione Chemical compound SC1=NN=NC(S)=C1S CDMIYIVDILNBIJ-UHFFFAOYSA-N 0.000 description 1
- LZKAPHHZFJPLII-UHFFFAOYSA-N triazolo[4,5-b]pyridin-2-amine Chemical compound C1=CC=NC2=NN(N)N=C21 LZKAPHHZFJPLII-UHFFFAOYSA-N 0.000 description 1
- HRXKRNGNAMMEHJ-UHFFFAOYSA-K trisodium citrate Chemical compound [Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O HRXKRNGNAMMEHJ-UHFFFAOYSA-K 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 1
- 238000001665 trituration Methods 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 238000000870 ultraviolet spectroscopy Methods 0.000 description 1
- 229960003824 ustekinumab Drugs 0.000 description 1
- 206010046766 uterine cancer Diseases 0.000 description 1
- 208000037965 uterine sarcoma Diseases 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 238000007738 vacuum evaporation Methods 0.000 description 1
- 206010046885 vaginal cancer Diseases 0.000 description 1
- 208000013139 vaginal neoplasm Diseases 0.000 description 1
- NQPDZGIKBAWPEJ-UHFFFAOYSA-N valeric acid Chemical compound CCCCC(O)=O NQPDZGIKBAWPEJ-UHFFFAOYSA-N 0.000 description 1
- 239000002525 vasculotropin inhibitor Substances 0.000 description 1
- 239000005526 vasoconstrictor agent Substances 0.000 description 1
- 229940099039 velcade Drugs 0.000 description 1
- 229960003048 vinblastine Drugs 0.000 description 1
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 1
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 1
- 229960004528 vincristine Drugs 0.000 description 1
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 1
- GBABOYUKABKIAF-GHYRFKGUSA-N vinorelbine Chemical compound C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC([C@]23[C@H]([C@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC GBABOYUKABKIAF-GHYRFKGUSA-N 0.000 description 1
- 229960002066 vinorelbine Drugs 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- QYSXJUFSXHHAJI-YRZJJWOYSA-N vitamin D3 Chemical class C1(/[C@@H]2CC[C@@H]([C@]2(CCC1)C)[C@H](C)CCCC(C)C)=C\C=C1\C[C@@H](O)CCC1=C QYSXJUFSXHHAJI-YRZJJWOYSA-N 0.000 description 1
- 239000003039 volatile agent Substances 0.000 description 1
- 230000002087 whitening effect Effects 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 229960000833 xylometazoline Drugs 0.000 description 1
- MWLSOWXNZPKENC-SSDOTTSWSA-N zileuton Chemical compound C1=CC=C2SC([C@H](N(O)C(N)=O)C)=CC2=C1 MWLSOWXNZPKENC-SSDOTTSWSA-N 0.000 description 1
- 229960005332 zileuton Drugs 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
- A61K31/541—Non-condensed thiazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04L—TRANSMISSION OF DIGITAL INFORMATION, e.g. TELEGRAPHIC COMMUNICATION
- H04L63/00—Network architectures or network communication protocols for network security
- H04L63/04—Network architectures or network communication protocols for network security for providing a confidential data exchange among entities communicating through data packet networks
- H04L63/0428—Network architectures or network communication protocols for network security for providing a confidential data exchange among entities communicating through data packet networks wherein the data content is protected, e.g. by encrypting or encapsulating the payload
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04L—TRANSMISSION OF DIGITAL INFORMATION, e.g. TELEGRAPHIC COMMUNICATION
- H04L63/00—Network architectures or network communication protocols for network security
- H04L63/06—Network architectures or network communication protocols for network security for supporting key management in a packet data network
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04L—TRANSMISSION OF DIGITAL INFORMATION, e.g. TELEGRAPHIC COMMUNICATION
- H04L63/00—Network architectures or network communication protocols for network security
- H04L63/08—Network architectures or network communication protocols for network security for authentication of entities
- H04L63/0861—Network architectures or network communication protocols for network security for authentication of entities using biometrical features, e.g. fingerprint, retina-scan
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04L—TRANSMISSION OF DIGITAL INFORMATION, e.g. TELEGRAPHIC COMMUNICATION
- H04L63/00—Network architectures or network communication protocols for network security
- H04L63/20—Network architectures or network communication protocols for network security for managing network security; network security policies in general
- H04L63/205—Network architectures or network communication protocols for network security for managing network security; network security policies in general involving negotiation or determination of the one or more network security mechanisms to be used, e.g. by negotiation between the client and the server or between peers or by selection according to the capabilities of the entities involved
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04L—TRANSMISSION OF DIGITAL INFORMATION, e.g. TELEGRAPHIC COMMUNICATION
- H04L67/00—Network arrangements or protocols for supporting network services or applications
- H04L67/01—Protocols
- H04L67/10—Protocols in which an application is distributed across nodes in the network
- H04L67/104—Peer-to-peer [P2P] networks
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04L—TRANSMISSION OF DIGITAL INFORMATION, e.g. TELEGRAPHIC COMMUNICATION
- H04L67/00—Network arrangements or protocols for supporting network services or applications
- H04L67/50—Network services
- H04L67/51—Discovery or management thereof, e.g. service location protocol [SLP] or web services
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04W—WIRELESS COMMUNICATION NETWORKS
- H04W4/00—Services specially adapted for wireless communication networks; Facilities therefor
- H04W4/80—Services using short range communication, e.g. near-field communication [NFC], radio-frequency identification [RFID] or low energy communication
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04W—WIRELESS COMMUNICATION NETWORKS
- H04W8/00—Network data management
- H04W8/22—Processing or transfer of terminal data, e.g. status or physical capabilities
- H04W8/24—Transfer of terminal data
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
-
- H—ELECTRICITY
- H04—ELECTRIC COMMUNICATION TECHNIQUE
- H04W—WIRELESS COMMUNICATION NETWORKS
- H04W92/00—Interfaces specially adapted for wireless communication networks
- H04W92/16—Interfaces between hierarchically similar devices
- H04W92/18—Interfaces between hierarchically similar devices between terminal devices
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Computer Networks & Wireless Communication (AREA)
- Signal Processing (AREA)
- Computer Security & Cryptography (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- General Engineering & Computer Science (AREA)
- Computing Systems (AREA)
- Computer Hardware Design (AREA)
- Rheumatology (AREA)
- Physical Education & Sports Medicine (AREA)
- Databases & Information Systems (AREA)
- Biomedical Technology (AREA)
- Pulmonology (AREA)
- Pain & Pain Management (AREA)
- Transplantation (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Peptides Or Proteins (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Una sal aceptable para uso farmacéutico de un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** en la que la sal es un aducto Base Libre/HCl/ H2O 1:1:3.
Description
DESCRIPCIÓN
Sales novedosas y composiciones farmacéuticas de las mismas para el tratamiento de trastornos inflamatorios
Campo de la invención
La presente invención se refiere a las formas salinas y cristalinas de un compuesto de acuerdo con la Fórmula I, útiles en la profilaxis y/o el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones. En particular, la sal de la invención inhibe JAK, una familia de quinasas de la tirosina, y más particularmente JAK1. La presente invención también proporciona composiciones farmacéuticas que comprenden la sal de la invención.
Antecedentes de la invención
Las terapias actuales para tratar afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones, en particular artritis reumatoide, están lejos de lo satisfactorio y aún permanece vigente una necesidad de identificar nuevos agentes terapéuticos que pueden ser de uso en su tratamiento. Estas afecciones son afecciones crónicas que requieren terapia prolongada, y la ingesta repetida del fármaco. El tratamiento prolongado puede ser una carga pesada sobre el paciente y el médico por igual, ya que el paciente puede ser, o puede convertirse en, intolerante al fármaco, y además, la posología elevada, o la frecuencia posológica alta pueden resultar en efectos colaterales incómodos, y/o bajo cumplimiento del paciente, en los que el paciente puede, ocasionalmente, deliberadamente o accidentalmente, perder una dosis. El impacto de la falta de adherencia varía entre enfermedades crónicas y oscila de mínima a muy significativa (Ingersoll & Cohen, 2008). Por consiguiente, existe una necesidad de identificar nuevos agentes para reforzar el arsenal del médico, y compuestos con régimen de posología de frecuencia baja para mejorar la vida de los pacientes.
Las quinasas Janus (JAK) son quinasas de tirosina citoplasmáticas que transducen la señalización de citosina de los receptores de membrana a los factores de transcripción de STAT. Se describen cuatro miembros de la familia JAK, JAK1, JAK2, JAK3 y TYK2. Tras la unión de la citosina a su receptor, los miembros de la familia JAK se auto- y/o transforsoforilan entre sí, seguido de fosforilación de STAT que luego migran al núcleo para modular la transcripción. La transducción de la señal intracelular de JAK-STAT sirve a los interferones, la mayoría de las interleucinas, así como una variedad de citosinas y factores endócrinos tales como EPO, TPO, GH, OSM, LIF, CNTF, GM-c Sf y PRL (Vainchenker, Dusa, & Constantinescu, 2008).
La combinación de modelos genéticos y la investigación del inhibidor JAK de molécula pequeña revelaron el potencial terapéutico de varias JAK.
JAK1 es una diana en el área de enfermedad inmuno-inflamatoria. JAK1 se heterodimeriza con otros JAK para transducir la señalización proinflamatoria accionada por citosinas. Por consiguiente, la inhibición de JAK1 es de interés para enfermedades inmunoinflamatorias con citosinas asociadas con una patología que usan la señalización de JAK1, tal como IL-2, IL-6, IL-4, IL-5, IL-13, o IFNgamma, así como otras enfermedades accionadas por transducción de la señal mediada por JAK.
En los roles de los miembros de la familia JAK, existe cierta superposición, ya que la mayoría de las vías de señalización incluyen más de un JAK, sin embargo, para algunos factores de crecimiento tales como eritropoyetina y trombopoyetina, solo está involucrado JAK2.
JAK3 cumple una función principal en el bloqueo de la función inmune mediante la transmisión de señales generadas por interleucina (IL)-2.
Por otro lado, TYK2 funcionaría en combinación con JAK2 con el fin de transducir la señalización de citosinas tales como IL-12 y IL-23.
La función de las enzimas JAK se ha estudiado principalmente usando ratones en los que cada uno de los miembros de la familia JAK se ha eliminado. Los ratones knockout de JAK1 exhiben un fenotipo letal perinatal y también tienen desarrollo y función linfoide defectuosos como resultado de la señalización defectuosa de las citosinas a través de JAK1. La deficiencia de JAK2 resulta en letalidad embrionaria el día 12 como resultado de una insuficiencia en la eritropoyesis definitiva. Los ratones con deficiencia de JAK3 tienen fenotipo de inmununodeficiencia combinado (SCID) pero no tienen defectos inmunes (Vertovsek, 2009).
Según se ha observado con los inhibidores JAK compatibles, la inhibición no selectiva puede estar relacionada con efectos colaterales tal como anemia, una tasa aumentada de infecciones, recuentos más bajos de neutrófilos y linfocitos, una reducción en la hemoglobina, y niveles elevados de colesterol (Dolgin, 2011).
Por consiguiente, el desarrollo de un inhibidor de JAK selectivo sería beneficioso para minimizar dichos efectos colaterales.
La degeneración del cartílago es un hito de varias enfermedades, entre las que la artritis reumatoide y la osteoartritis son las más prominentes. La artritis reumatoide (RA) es una enfermedad degenerativa crónica de las articulaciones, caracterizada por la inflamación y destrucción de las estructuras articulares. Cuando la enfermedad no se trata, puede conducir a discapacidad y dolor sustancial debido a la pérdida de la función de las articulaciones y resultar en menor expectativa de vida. El objetivo de una terapia de RA, por lo tanto, no solo es ralentizar la enfermedad sino lograr la remisión para detener la destrucción de las articulaciones y mejorar la calidad de vida. Además de la severidad de la evolución de la enfermedad, la alta prevalencia de RA (~ 0,8% de los adultos están afectados a nivel mundial) significa un alto impacto socio-económico (Smolen & Steiner, 2003) (O'Dell, 2004). JAK1 está implicada en una transducción de señal intracelular para muchas citosinas y hormonas. Las patologías asociadas con cualquiera de estas citosinas y hormonas pueden aliviarse mediante inhibidores de JAK1. Por consiguiente, varis trastornos alérgicos, inflamatorios y autoinmunes podrían beneficiarse a partir del tratamiento con compuestos descritos en esta invención incluyendo artritis reumatoide, lupus eritematoso sistémico, artritis idiopática juvenil, osteoartritis, asma, enfermedad pulmonar obstructiva crónica (EPOC), fibrosis de tejidos, inflamación eosinofílica, esofagitis, enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, colitis ulcerativa), trasplante, enfermedad de injerto contra huésped, psoriasis, miositis, artritis psoriásica, espondilitis anquilosante, artritis idiopática juvenil y esclerosis múltiple. (Kopf, Bachmann, & Marsland, 2010)
La psoriasis es una enfermedad que puede afectar la piel. La causa de psoriasis no se comprende totalmente pero se presume que es una enfermedad relacionada mediada de manera inmune relacionada con la liberación de las citosinas, en particular el TNFa, que produce inflamación y rápida reproducción de las células cutáneas. Esta hipótesis se ha corroborado mediante la observación de que la medicación inmunosupresora puede aclarar las placas de psoriasis. (Zenz, et al., 2005) La psoriasis también puede causar inflamación de las articulaciones, lo que se conoce como artritis psoriásica. Entre el 10-30% de todas las personas con psoriasis también tienen artritis psoriásica. ((CHMP), 18 de noviembre de 2004). Debido a su naturaleza recurrente crónica, la psoriasis es un desafío para tratar. Se ha demostrado recientemente que la inhibición de JAK podría resultar en la mejora exitosa de la condición psoriásica (Punwani, et al., 2012).
La enfermedad inflamatoria intestinal (IBD) es un grupo de afecciones inflamatorias del colon y el intestino delgado. Los tipos principales de IBD son enfermedad de Crohn y colitis ulcerativa. Recientemente, se ha encontrado a través de estudios de asociación de amplitud del genoma (GWAS) que la fosfatasa de tirosina la proteína de células T (TCPTP) es un JAK/STAT y la fosfatasa del receptor del factor de crecimiento que se haya relacionado con la patogénesis de la diabetes tipo 1, artritis reumatoide, y enfermedad de Crohn por GWAS. (Zikherman & Weiss, 2011). Por consiguiente, la inhibición de la vía de JAK puede proporcionar un modo de tratamiento de la IBD.
Los miembros de la familia JAK se han implicado en afecciones adicionales incluyendo trastornos mieloproliferativos (O’Sullivan, Liongue, Lewis, Stephenson, & Ward, 2007), en los que se han identificado mutaciones en JAK2. Esto indica que los inhibidores de JAK en particular JAK2 también pueden ser de utilidad en el tratamiento de trastornos mieloproliferativos. Además, la familia JAK, en particular JAK1, JAK2 y JAK3, se ha relacionado con los cánceres, en particular leucemias (por ej., leucemia mieloide aguda (O’Sullivan, Liongue, Lewis, Stephenson, & Ward, 2007) (Xiang, et al., 2008) y leucemia linfoblástica aguda (Mullighan, 2009)), linfoma de células T cutáneas (Zhang, 1996) o tumores sólidos, por ej., leiomiosarcoma uterino (Constantinescu, Girardot, & Pecquet, 2007), cáncer de próstata (Tam, McGlynn, Traynor, Mukherjee, Bartlett, & Edwards, 2007) y cáncer de mama (Berishaj, et al., 2007). Estos resultados indican que los inhibidores de JAK, en particular JAK1 también pueden tener utilidad en el tratamiento de cánceres (leucemias y tumores sólidos, por ej., liomiosarcoma uterino, cáncer de próstata, cánceres pancreáticos).
Además, la enfermedad de Castleman, mieloma múltiple, glomerulonefritis proliferativo mesangial, psoriasis y sarcoma de Kaposi probablemente se deben a la hipersecreción de la citosina IL-6, cuyos efectos biológicos están mediados por señalización de JAK-STAT intracelular (Naka, Nishimoto, & Kishimoto, 2002). Este resultado muestra que los inhibidores de JAK, también pueden encontrar utilidad en el tratamiento de dichas enfermedades.
De este modo, los compuestos que son potentes inhibidores de JAK ofrecerían el potencial de tratamiento de una amplia variedad de enfermedades y afecciones descritas con anterioridad.
El compuesto {5-[4-(1,1-dioxo-tiomorfolin-4-ilmetil)-fenil]-[1,2,4]triazolo[1,5-a]piridin-2-il}-amida del ácido ciclopropancarboxílico (Compuesto I), que tiene la estructura química:
se describe en nuestra solicitud anterior WO 2010/149769 (Menet C. J., 2010) como un inhibidor de JAK y útil en el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativa, alergia, rechazo al trasplante, enfermedades que involucran deterioro de la producción de cartílago, malformaciones congénitas de cartílagos, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones. En adelante este compuesto se denomina Compuesto I. Los datos presentados en el documento WO 2010/149769 demuestran que a pesar de las actividades in vitro similares, el Compuesto I tiene potencia in vivo inesperadamente alta comparado con compuestos estructuralmente similares.
Una característica importante de varias sustancias bioactivas (por ejemplo pero sin limitación, productos farmacéuticos, medicinas y biocidas, normalmente referidos como fármacos) es su ''biodisponibilidad'' o concentración activa en una forma que puede ser absorbida y utilizada por un órgano u organismo diana. En muchos casos, la biodisponibilidad se relaciona con la solubilidad del fármaco en agua.
Para ser de utilidad como agente terapéutico, el fármaco debe ser soluble en un intervalo de concentración adecuado para el período de tiempo requerido. Se encuentran disponibles varias opciones para lograr estas propiedades, incluyendo formulación del fármaco como una píldora, cápsulas, soluciones, u otras formulaciones similares. Son de particular interés los fármacos de "liberación de orden cero", en los que la tasa de liberación del fármaco es constante. Sin embargo, desarrollar estos sistemas puede ser complicado y costoso.
Con frecuencia, los fármacos en su forma de base libre son escasamente solubles en agua, pero la presencia de sitios ácidos (por ejemplo, ácidos carboxílicos, fenoles, ácidos sulfónicos) o sitios alcalinos (por ejemplo grupos amino, centros alcalinos de nitrógeno) pueden usarse ventajosamente para producir las sales del fármaco. Los compuestos iónicos resultantes se tornan mucho más solubles en agua en virtud de su carácter iónico y mejor energía de disolución, y de este modo mejoran la biodisponibilidad. Una pauta de 50 pg/ml para solubilidad acuosa se proporciona en el texto de Lipinsky etal. (Lipinski, Lombardo, Dominy, & Feeney, 2001).
Los agentes formadores de sales están disponibles en un número extenso, y la selección de sales debe diseñarse cuidadosamente. El objetivo de la selección de sales es identificar la mejor forma de sal adecuada para desarrollo, y se basa principalmente en cuatro criterios principales: solubilidad acuosa a varios pH, alto grado de cristalinidad, baja higroscopicidad y estabilidad química óptima (Handbook of Pharmaceutical Salts: Properties, Selection and Use, Stahl, P.H. and Wermuth, C.G. Eds. Wiley-VCH, Weinheim, Germany, 2002).
Si una sal adecuada de un fármaco puede identificarse, se requieren investigaciones adicionales para identificar si hay formas cristalinas alternativas. La disponibilidad de dichas formas alternativas es altamente impredecible y puede requerir una combinación de intuición, diseño empírico cuidadoso, perseverancia y casualidad. En la parte más alta de los desafíos asociados con incluso hallar una o más formas cristalinas definidas, las propiedades de cualquier forma cristalina descubierta de este modo necesita evaluarse cuidadosamente para ver si una o más de ellas es realmente adecuada para desarrollo farmacéutico. De hecho, en un primer aspecto, la cristalinidad de los fármacos afecta, entre otras propiedades físicas y mecánicas, la solubilidad, la tasa de disolución, la fluidez, la dureza, la capacidad de compresión y el punto de fusión. En un segundo aspecto, una forma cristalina puede tener ventajas sobre la forma amorfa, por ejemplo, la purificación al alto grado de pureza requerida por la mayoría de las autoridades regulatorias es más eficiente y por consiguiente cuesta menos para que se forme la forma cristalina que el sólido amorfo. Además, la manipulación de la forma cristalina se mejora sobre la forma amorfa, la cual tiende a ser oleosa, o pegajosa, y en la práctica, el secado de un material cristalino que tiene una temperatura de secado y desolvación bien definida es más fácilmente controlada, que para el sólido amorfo, que tiene una mayor afinidad por los solventes orgánicos y las temperaturas de secado variables. Finalmente el procesamiento corriente abajo del fármaco cristalino permite el control de proceso mejorado. En un tercer aspecto, la estabilidad física y química, y por consiguiente la vida útil también mejoró para las formas cristalinas por sobre las formas amorfas.
Finalmente, las propiedades farmacocinéticas y farmacodinámicas de un fármaco pueden relacionarse con una forma estructural cristalina particular, y es fundamental para producir y retener la misma forma desde la producción hasta la administración al paciente. Por consiguiente, la obtención de sales y/o formas cristalinas por sobre materiales amorfos
es altamente deseable (Hilfiker, Blatter, & von Raumer, 2006).
De este modo, el objetivo de esta invención es divulgar formas de sales y polimorfos de las sales de la invención, que tienen propiedades farmacológicas deseables, y que muestren mejoras en su perfil farmacéutico comparado con la forma de base libre y/o la forma amorfa de la sal de la invención, en particular exposición mejorada in vivo.
Descripción de los dibujos
La Figura 1 muestra el difractograma de XRPD del Compuesto I patrón 1.
La Figura 2 muestra el difractograma de XRPD del Compuesto I patrón 3.
La Figura 3 muestra el difractograma de XRPD del Compuesto I patrón 4.
La Figura 4 (comparativa) muestra el difractograma de XRPD del Compuesto I. HCl.
La Figura 5 muestra el difractograma de XRPD del Compuesto I. HCl.3H2O.
La Figura 6 muestra el análisis de DVS del Compuesto I. HCl.3H2O.
La Figura 7 muestra oligoelementos de DSC del Compuesto I. HCl.3H2O.
La Figura 8 (comparativa) muestra el difractograma de XRPD del Compuesto I. HCl.MeOH.
La Figura 9 muestra el difractograma de XRPD del Compuesto I.HCl.1,5HCO2H.
La Figura 10 (incluyendo los ejemplos comparativos) muestra la exposición del Compuesto I indistintamente como base libre o como una sal de HCl.3H2O tras dosificación po diaria.
La Figura 11 muestra la estructura de cristal del Compuesto I. HCl.3H2O.
Sumario de la invención
La presente invención se basa en la identificación de sales y formas cristalinas novedosas del Compuesto I, útiles en el tratamiento y/o la profilaxis de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones. En particular, las sales de la invención pueden actuar como inhibidores de JAK, y más particularmente de JAK1. La presente invención proporciona también procedimientos para la producción de estas sales y composiciones farmacéuticas que comprenden estas sales.
Por consiguiente, en un aspecto la presente invención proporciona una sal de un compuesto de acuerdo con la Fórmula (I) que sigue (en adelante también denominada Compuesto I):
en la que dicha sal es 1:1:3 de sal de Base Libre/HCl/ H2O.
En otro aspecto de la invención, la sal de la invención es un aducto [Compuesto I.HCL3H2O] en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en cualquiera de una o más de las siguientes posiciones: 7,3, 8,4, 8,8, 10,7, 12,0, 12,2, 13,2, 13,7, 14,5, 16,3, 16,7, 17,6, 19,3, 20,2, 20,6, 21,0, 21,4, 21,8, 22,8, 23,4, 23,9, 24,5, 25,2, 25,7, 25,9, 26,4, 27,2, 27,7, 28,3, 28,6, 28,9, 29,2, 29,6, 7 y 32,7° 20± 0,2° 20. En un aspecto particular de la invención, la sal de la invención exhibe solubilidad y exposición mejoradas por sobre la base libre, lo que puede resultar en una eficacia mejorada y una dosis más baja de fármaco administrada. A su vez, la reducción del nivel de posología de la dosis puede potencialmente reducir la toxicidad que puede ocurrir a través
de la interacción medicamentosa.
En un aspecto particular, las sales de la invención se proporcionan para uso en la profilaxis y/o el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones.
En un aspecto adicional, la presente invención proporciona composiciones farmacéuticas que comprenden una sal de la invención, y un portador, excipiente o diluyente farmacéuticos. En un aspecto particular, la composición farmacéutica puede comprender, además, principios terapéuticamente activos adicionales, adecuados para uso en combinación con las sales de la invención. En un aspecto más particular, el principio terapéuticamente activo es un agente para el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones.
Más aún, las sales de la invención, útiles en las composiciones farmacéuticas y en los procedimientos de tratamiento divulgados en la presente memoria, son aceptables para uso farmacéutico como se preparan y se usan.
En un aspecto adicional de la invención, esta invención proporciona un procedimiento de tratamiento de un mamífero, en particular seres humanos, afectados con una condición seleccionada de entre las mencionadas en la presente memoria, y particularmente afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo a los trasplantes, enfermedades que implican degradación y/o interrupción de la homeóstasis de cartílagos, malformaciones congénitas de cartílagos, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones, cuyo procedimiento comprende administrar una cantidad efectiva de la composición farmacéutica o las sales de la invención como se describe en la presente memoria.
La presente invención proporciona también composiciones farmacéuticas que comprenden una sal de la invención, y un portador, excipiente o diluyente farmacéutico adecuado para uso en medicina. En un aspecto particular, la composición farmacéutica es para uso en la profilaxis y/o el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones.
En aspectos adicionales, la invención proporciona procedimientos para sintetizar la sal de la invención, con protocolos de síntesis representativos y vías divulgadas más adelante en la presente memoria.
Otros objetivos y otras ventajas resultarán evidentes para aquellos expertos en la técnica a partir de una consideración de la descripción detallada resultante.
Se apreciará que las sales de la invención pueden metabolizarse para producir metabolitos biológicamente activos.
Descripción detallada de la invención
Definiciones
Se pretende que los siguientes términos tengan los significados presentados con estos a continuación y sean útiles en la comprensión de la descripción y el alcance buscado de la presente invención.
Cuando se describe la invención, que puede incluir compuestos, composiciones farmacéuticas que contienen dichos compuestos y procedimientos de uso de dichos compuestos y dichas composiciones, los siguientes términos, si están presentes, tienen los siguientes significados, a menos que se indique de otro modo. Se deberá comprender también que cuando se describe en la presente memoria, cualquiera de las fracciones definidas a continuación puede ser sustituida con una variedad de sustituyentes, y que las definiciones respectivas pretenden incluir dichas fracciones sustituidas dentro de su alcance como se establece a continuación. A menos que se indique de otro modo, el término 'sustituido' se deberá definir como se indica a continuación. Además, debe comprenderse que los términos 'grupos' y 'radicales' pueden considerarse sinónimos cuando se usan en la presente memoria.
Los artículos "un" y "una" pueden usarse en la presente memoria para referir a uno o a más de uno (es decir al menos a uno) de los objetos gramaticales del artículo. A modo de ejemplo, 'un análogo' significa un análogo o más de un análogo.
“Sales de la invención”, y expresiones equivalentes, pretenden abarcar las sales del compuesto de acuerdo con la Fórmula (I) (Compuesto I) como se describe en la presente memoria, cuya expresión incluye las sales aceptables para uso farmacéutico, y los solvatos, por ej., hidratos, y los solvatos de las sales aceptables para uso farmacéutico cuando lo permita el contexto.
“Aceptable para uso farmacéutico” significa aprobado o susceptible de aprobarse por una agencia regulatoria del gobierno federal o estatal o la agencia correspondiente en países fuera de los Estados Unidos, o que aparece en la lista de la Farmacopea de los EE. UU. u otra farmacopea generalmente reconocida para uso en animales, y más
particularmente, en seres humanos.
“Vehículo aceptable para uso farmacéutico” se refiere a un diluyente, adyuvante, excipiente o portador con el que se administra una sal de la invención.
“Solvato” se refiere a formas del compuesto que están asociadas con un disolvente, normalmente por una reacción de solvólisis. Esta asociación física incluye unión de hidrógeno. Los solventes convencionales incluyen agua, etanol, ácido acético y similares. Las sales de la invención pueden prepararse, por ej., en forma cristalina y pueden ser solvatadas o hidratadas. Los solvatos adecuados incluyen solvatos aceptables para uso farmacéutico, tales como hidratos, e incluyen, además, tanto solvatos estequimétricos como solvatos no estequimétricos. En ciertas instancias, el solvato será capaz de aislamiento, por ejemplo, cuando una o más moléculas de disolvente se incorporan en el retículo de cristal del sólido cristalino. “Solvato” abarca tanto los solvatos en fase de solución como aislables. Los solvatos representativos incluyen hidratos, etanolatos y metanolatos.
“Individuo” incluye seres humanos. Los términos “ser humano”, “paciente” e “individuo” se utilizan en la presente memoria como sinónimos.
“Cantidad efectiva” significa la cantidad de una sal de la invención que, cuando se administra a un individuo para tratar una enfermedad, es suficiente para efectuar dicho tratamiento para la enfermedad. La “cantidad efectiva” puede variar dependiendo del compuesto, la enfermedad y su severidad, y la edad, el peso, etc., del individuo que se tratará.
“Prevenir” o “prevención” se refiere a una reducción en el riesgo de adquirir o desarrollar una enfermedad o un trastorno (es decir, causar que al menos uno de los síntomas clínicos de la enfermedad no se desarrolle en un individuo que pueda estar expuesto a un agente causante de la enfermedad, o predispuesto a la enfermedad antes de la aparición de la enfermedad.
El término “profilaxis” se relaciona con “prevención”, y se refiere a una medida o procedimiento cuya finalidad es prevenir, en lugar de tratar o curar una enfermedad. Ejemplos no limitativos de medidas profilácticas pueden incluir la administración de vacunas; la administración de heparina de bajo peso molecular a pacientes hospitalarios en riesgo de trombosis debido a, por ejemplo, inmovilización; y la administración de un agente anti malaria tal como cloroquina, antes de una visita a una región geográfica donde la malaria es endémica o el riesgo de contraer malaria es alto.
“Tratar” o “tratamiento” de cualquier enfermedad o trastorno se refiere, en una realización, a aliviar la enfermedad o el trastorno (es decir, detener la enfermedad o reducir la manifestación, extensión o severidad de al menos uno de sus síntomas clínicos). En otra realización “tratar” o “tratamiento” se refieren a aliviar al menos un parámetro físico, que puede no ser discernible para el individuo. Incluso en otra realización, “tratar” o “tratamiento” se refiere a modular la enfermedad o el trastorno, ya sea físicamente (por ej., estabilización de un síntoma discernible), fisiológicamente (por ej., estabilización de un parámetro físico), o ambos. En una realización adicional, “tratar” o “tratamiento” se refiere a hacer más lenta la progresión de la enfermedad.
Como se usa en la presente memoria, el término “enfermedades inflamatorias” se refiere al grupo de afecciones que incluyen, artritis reumatoide, osteoartritis, artritis idiopática juvenil, psoriasis, artritis psoriásica, enfermedad alérgica de las vías aéreas (por ej. asma, rinitis), enfermedad pulmonar obstructiva crónica (EPOC), enfermedades inflamatorias intestinales (por ej. enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis), estados patológicos accionados por endotoxinas (por ej. complicaciones posteriores a una cirugía de bypass o estados crónicos de endotoxinas que contribuyen por ej. a insuficiencia cardíaca crónica), y enfermedades relacionadas que incluyen los cartílagos, tales como las de las articulaciones. Particularmente, el término se refiere a artritis reumatoide, osteoartritis, enfermedad alérgica de las vías aéreas (por ej., asma) enfermedad pulmonar obstructiva crónica (EPOC) y enfermedades inflamatorias intestinales. Más particularmente, el término se refiere a artritis reumatoide, y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis).
Como se usa en la presente memoria, el término “enfermedad(es) autoinmune(s)” se refiere al grupo de enfermedades que incluyen enfermedad obstructiva de las vías aéreas, incluyendo afecciones tal como EPOC, asma (por ej., asma intrínseco, asma extrínseco, asma por el polvo, asma infantil) particularmente asma crónico o asma habitual (por ejemplo, asma tardío e híper respuesta de las vías aéreas), bronquitis, incluyendo asma bronquial, lupus eritematoso sistémico (SLE), lupus eritematoso cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, esclerosis múltiple, psoriasis, enfermedad del ojo seco, diabetes mellitus tipo I, y complicaciones asociadas con ésta, eczema atópico (dermatitis atópica) tiroiditis (tiroiditis de Hashimoto y autoinmune), dermatitis de contacto y dermatitis eczematosa adicional, enfermedad inflamatoria intestinal (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis), ateroesclerosis y esclerosis lateral amiotrófica. Particularmente el término se refiere a EPOC, asma, lupus eritematoso sistémico, diabetes mellitus tipo I y enfermedad inflamatoria intestinal.
Como se usa en la presente memoria, el término “enfermedad(es) proliferativa(s)” se refiere a afecciones tales como el cáncer (por ej., leiomiosarcoma o cáncer de próstata), trastornos mieloproliferativos (por ej., policitemia vera, trombocitosis esencial y mielofibrosis), leucemia (por ej., leucemia mieloide aguda, leucemia linfoblástica aguda y crónica), mieloma múltiple, psoriasis, restenosis, escleroderma o fibrosis. En particular el término se refiere a cáncer, leucemia, mieloma múltiple y psoriasis.
Como se usa en la presente memoria, el término “cáncer” se refiere a un crecimiento maligno o benigno de células en la piel o en los órganos corporales, por ejemplo, pero sin limitación, mama, próstata, pulmón, riñón, páncreas, estómago o intestino. Un cáncer tiende a infiltrarse en el tejido adyacente y esparcirse (hacer metástasis) a órganos distantes, por ejemplo, a los huesos, al hígado, a los pulmones o al cerebro. Como se usa en la presente memoria, el término cáncer incluye tanto los tipos de células tumorales con metástasis (tales como, pero sin limitación, melanoma, linfoma, leucemia, fibrosarcoma, rabdomiosarcoma y mastocitoma) como los tipos de carcinoma de tejidos (tales como, pero sin limitación, cáncer colorectal, cáncer de próstata, cáncer de pulmón de células pequeñas y cáncer de pulmón de células no pequeñas, cáncer de mama, cáncer de páncreas, cáncer de vejiga, cáncer renal, cáncer gástrico, glioblastoma, cáncer primario de hígado, cáncer de ovario, cáncer de próstata y leiomiosarcoma uterino). En particular, el término “cáncer” se refiere a leucemia linfoblástica aguda, leucemia mielodie, carcinoma adrenocortical, cáncer anal, cáncer de apéndice, astrocitomas, tumor teratoide/rabdoide atípico, carcinoma de células basales, cáncer del conducto biliar, cáncer de vejiga, cáncer de huesos (osteosarcoma e histiocitoma fibroso maligno), glioma del tronco encefálico, tumores de cerebro, tumores del cerebro y la médula espinal, leucemia linfocítica crónica, leucemia mielógena crónica, linfoma de células T cutáneas, tumores embrionarios, cáncer de endometrio, ependimoblastoma, ependimoma, cáncer de esófago, familia de tumores del sarcoma de Ewing, cáncer de ojo, retinoblastoma, cáncer de vesícula biliar, cáncer gástrico (estómago), tumor carcinoide gastrointestinal, tumor estromal gastrointestinal (GIST), tumor de células estromales gastrointestinales, tumor de células germinales, glioma, leucemia de células capilares, cáncer de cabeza y cuello, cáncer hepatocelular (hígado), cáncer hipofaríngeo, melanoma intraocular, tumores de células islote (páncreas endócrino), sarcoma de Kaposi, cáncer de riñón, histiocitosis de células de Langerhans, cáncer laríngeo, leucemia, leucemia linfoblástica aguda, leucemia mieloide aguda, leucemia linfocítica crónica, leucemia mielógena crónica, leucemia de células capilares, cáncer de hígado, cáncer de pulmón de células no pequeñas, cáncer de pulmón de células pequeñas, linfoma de Burkitt, linfoma de células T cutáneas, linfoma de Hodgkin, linfoma no de Hodgkin, linfoma, macroglobulinemia de Waldenstrom, meduloblastoma, meduloepitelioma, melanoma, mesotelioma, cáncer de boca, leucemia mielógena crónica, leucemia mieloide, mieloma múltiple, cáncer asofaríngeo, neuroblastoma, cáncer de pulmón de células no pequeñas, cáncer bucal, cáncer orofaríngeo, osteosarcoma, histocitoma fibroso maligno de huesos, cáncer de ovario, cáncer epitelial de ovario, tumor de células germinales de ovario, tumor potencial maligno bajo de ovario, cáncer de páncreas, papilomatosis, cáncer de paratiroides, cáncer de pene, cáncer de faringe, tumores parenquimales pineales de diferenciación intermedia, pineoblastoma y tumores neuroectodérmicos primitivos supratentoriales, tumor de la glándula pituitaria, mieloma múltiple/neoplasma de células plasmáticas, blastoma pleuropulmonar, linfoma del sistema nervioso central primario, cáncer de próstata, cáncer rectal, cáncer de (riñón) de célula renal, retinoblastoma, rabdomiosarcoma, cáncer de glándulas salivales, sarcoma, familia de tumores de sarcoma de Ewing, sarcoma, síndrome de Sezary, cáncer de piel, cáncer de pulmón de células pequeñas, cáncer de intestino delgado, sarcoma de tejido blando, carcinoma de células escamosas, cáncer de estómago (gástrico), tumores neuroectodérmicos primitivos supratentoriales, linfoma de células T, cáncer testicular, cáncer de garganta, carcinoma de timoma y tímico, cáncer de tiroides, cáncer de uretra, cáncer de útero, sarcoma uterino, cáncer vaginal, cáncer vulvar, macroglobulinemia de Waldenstrom, y tumor de Wilms. Más particularmente, el cáncer se selecciona de cáncer de mama, cáncer de endometrio y cervical, cáncer de pulmón, cáncer de ovario, cáncer de próstata, cáncer hepático, y cáncer pancreático.
Como se usa en la presente memoria, el término “leucemia” se refiere a enfermedades neoplásicas de la sangre y órganos que forman la sangre. Dichas enfermedades pueden causar disfunción de la médula ósea y del sistema inmune, lo cual torna al huésped altamente sensible a infección y sangrado. En particular, el término leucemia se refiere a leucemia mieloide aguda (AML), y leucemia linfoblástica aguda (ALL) y leucemia linfoblástica aguda (CLL).
Como se usa en la presente memoria, el término “alergia” se refiere al grupo de afecciones caracterizadas por un trastorno de hipersensibilidad del sistema inmune que incluye enfermedad alérgica de las vías respiratorias (por ej., asma, rinitis), sinusitis, eczema y urticaria, así como alergias a los alimentos o alergias al veneno de los insectos.
Como se usa en la presente memoria, el término “asma” como se usa en la presente memoria se refiere a cualquier trastorno de los pulmones caracterizado por variaciones en el flujo de gases pulmonares asociados con constricción de las vías aéreas de cualquier causa (intrínseca, extrínseca, o ambas; alérgica o no alérgica). El término asma puede usarse con uno o más adjetivos para indicar la causa.
Como se usa en la presente memoria, el término “rechazo a trasplantes” se refiere a rechazo agudo o crónico a alo- o xenoinjertos de células, tejido, u órganos sólidos de (por ej., islotes pancreáticos, mastocitos, médula ósea, piel, músculo, tejido corneal, tejido neuronal, corazón, pulmón, corazón-pulmón combinados, riñón, hígado, intestino, páncreas, tráquea o esófago, o enfermedades de injerto contra huésped.
Como se usa en la presente memoria, el término “enfermedades que incluyen la degradación y/o interrupción de la homeóstasis de cartílagos” incluye afecciones tal como osteoartritis, artritis psoriásica, artritis reumatoide juvenil, artritis por gota, artritis séptica o infecciosa, artritis reactiva, distrofia simpática refleja, algositrofia, acondroplasia, enfermedad de Paget, síndrome de Tietze o condritis costal, fibromialgia, osteocondritis, artritis neurogénica o neuropática, artropatía, sarcoidosis, amilosis, hidartrosis, enfermedad periódica, espondilitis reumatoide, formas endémicas de artritis como osteoartritis deformante endémica, enfermedad de Mseleni y enfermedad de Handigodu; degeneración resultante de fibromialgia, lupus eritematoso sistémico, escleroderma y espondilitis anquilosante.
Como se usa en la presente memoria, “malformaciones congénitas de cartílagos” incluye afecciones tales como condrólisis hereditaria, condrodisplasias y pseudocondrodisplasias, en particular, pero sin limitación, microtia, anotia, condrodisplasia metafisaria y trastornos relacionados.
Como se usa en la presente memoria, el término “enfermedades asociadas con la hipersecreción de IL6” incluye afecciones tal como la enfermedad de Castelman, mieloma múltiple, psoriasis, sarcoma de Kaposi y/o glomerulonefritis proliferativa mesangial.
Como se usa en la presente memoria, el término “enfermedades asociadas con la hipersecreción de interferones” incluye afecciones tal como lupus eritematoso sistémico y cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, psoriasis, artritis reumatoide.
Cuando se hace referencia en la presente memoria a intervalos, por ejemplo, pero sin limitación, alquilo Ci-8, la mención de un intervalo debe considerarse una representación de cada miembro de dicho intervalo.
Como se usa en la presente memoria, el término “variante isotópica” se refiere a un compuesto que contiene proporciones no naturales de isotopos en uno o más de los átomos que constituyen dicho compuesto. Por ejemplo, una “variante isotópica” de un compuesto puede contener uno o más isotopos no radiactivos, tal como, por ejemplo, deuterio (2H o D), carbono-13 (13C), nitrógeno-15 (15N), o similares. Se comprenderá que, en un compuesto en el que se realiza dicha sustitución isotópica, los siguientes átomos, donde están presentes, pueden variar, de modo tal que, por ejemplo, cualquier hidrógeno puede ser 2H/D, cualquier carbono puede ser 13C, o cualquier hidrógeno puede ser 15N, y que la presencia y la colocación de dichos átomos puede ser determinada dentro de las habilidades en la técnica. Del mismo modo, la invención puede incluir la preparación de variantes isotópicas con radioisótopos, en la instancia, por ejemplo, en la que los compuestos resultantes pueden usarse para estudios de distribución de tejidos en sustrato y/o fármaco. Los isotopos radiactivos tritio, es decir, 3H, y carbono 14, es decir, 14C, son particularmente útiles para este fin en vista de la facilidad de incorporación y los medios fáciles de detección. Además, pueden prepararse compuestos que estén sustituidos con isotopos de emisión de positrones, tal como 11C, 18F, 15O y 13N, y serían útiles en los estudios de Topografía por Emisión de Positrones (PET) para examinar la ocupación del receptor en el sustrato.
Todas las variantes isotópicas de los compuestos proporcionados en la presente memoria, ya sean radiactivos o no, pretenden estar abarcados dentro del alcance de la invención.
“Tautómeros” se refiere a los compuestos que son formas intercambiables de una estructura de compuesto particular, y que varían en el desplazamiento de los átomos de hidrógeno y electrones. De este modo, dos estructuras pueden estar en equilibrio a través del movimiento de electrones n y un átomo (normalmente H). Por ejemplo, los enoles y las cetonas son tautómeros porque se interconvierten rápidamente por tratamiento indistintamente con ácido o base. Otro ejemplo de tautomerismo es las formas ácido y nitro de fenilnitrometano, que se forman del mismo modo por tratamiento con ácido o base.
Las formas tautoméricas pueden ser relevantes para el logro de la reactividad química óptima y la actividad biológica de un compuesto de interés.
Se apreciará que las sales de la invención pueden metabolizarse para producir metabolitos biológicamente activos.
La invención
La presente invención se refiere a una sal 1:1:3 de Base Libre/HCl/H2O del compuesto {5-[4-(1,1-dioxo-tiomorfolin-4-ilmetil)-fenil]-[1,2,4]triazolo[1,5-a]piridin-2-il}-amida del ácido ciclopropancarboxílico (Compuesto I), y procedimientos para la preparación de la sal, que es útil en la profilaxis y/o el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones. En particular, las sales de la invención inhiben JAK, una familia de quinasas de la tirosina, y más particularmente JAK1.
La presente invención también proporciona procedimientos para la profilaxis y/o el tratamiento de enfermedades que incluyen afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones por administración de una sal de la invención, o una composición farmacéutica que contiene dicha sal.
De esta manera, en un aspecto la presente invención proporciona una sal de un compuesto de acuerdo con la Fórmula (I) (Compuesto I) a continuación:
en la que dicha sal es sal 1:1:3 de Base Libre/HCl/hbO.
En una realización, la sal de la invención es aquella formada con un agente formador de sal seleccionado de ácido clorhídrico.
En una realización, la sal de la invención es un solvato. En una realización particular, la sal de la invención es un trisolvato. En una realización mucho más particular, la sal de la invención es un trisolvato.
En una realización, la sal de la invención es un hidrato. En una realización más particular, la sal de la invención es un trihidrato. En una realización mucho más particular, la sal de la invención es un trihidrato.
En una realización, la sal de la divulgación es un aducto [Compuesto I:agente formador de sal:disolvente]. En una realización particular, la sal de la divulgación es un aducto [Compuesto I:agente formador de sal:disolvente] de 1:1:0 a 1:1:4. En una realización más particular, la sal de la divulgación es un aducto [Compuesto I:agente formador de sal:disolvente] 1:1:0, 1:1:1, 1:1:1.5, 1:1:2, o 1:1:3. En una realización mucho más particular, la sal de la invención es un aducto [Compuesto I:agente formador de sal:disolvente] 1:1:3.
En otra realización particular, la sal de la divulgación es un aducto [Compuesto I:HCl:disolvente]. En una realización particular, la sal de la divulgación es un aducto [Compuesto I:HCl:disolvente] de 1:1:0 a 1:1:4. En una realización más particular, la sal de la invención es un aducto [Compuesto I:HCl:disolvente] 1:1:0, 1:1:1, 1:1:1.5, 1:1:2, o 1:1:3. En una realización mucho más particular, la sal de la invención es un aducto [Compuesto I:HCl:disolvente] 1:1:3. En una realización mucho más particular adicional, el disolvente se selecciona de H2O
En otra realización, la sal de la divulgación es un aducto [Compuesto I:HCl:H2O]. En una realización particular, la sal de la invención es un aducto [Compuesto I:HCl:H2O] de 1:1:0 a 1:1:4. En una realización más particular, la sal de la divulgación es un aducto [Compuesto I:HCl:H2O] 1:1:0, 1:1:1, 1:1:1.5, 1:1:2, o 1:1:3. En una realización mucho más particular, la sal de la invención es un aducto [Compuesto I:HCl:H2O] 1:1:3.
En una realización, la sal de la invención exhibe picos en un espectro de XRPD.
En una realización, la sal de la invención está en una forma cristalina.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:H2O] 1:1:0 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en cualquiera de una o más de las siguientes posiciones: 7,4, 8,9, 12,4, 14,8, 15,1, 16,9, 17,6, 19,4, 20,7, 21,1, 22,8, 24,9, 26,0, 28,6, 29,8, y 32,6° 20 ± 0,2° 20.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:H2O] 1:1:0 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo al menos en 5, 10, 15, o más de las siguientes posiciones: 7,4, 8,9, 12,4, 14,8, 15,1, 16,9, 17,6, 19,4, 20,7, 21,1, 22,8, 24,9, 26,0, 28,6, 29,8, y 32,6° 20 ± 0,2° 20.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:H2O] 1:1:0 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en todas las siguientes posiciones: 7,4, 8,9, 12,4, 14,8, 15,1, 16,9, 17,6, 19,4, 20,7, 21,1, 22,8, 24,9, 26,0, 28,6, 29,8, y 32,6° 20 ± 0,2° 20. En una realización particular, la sal de la invención está caracterizada por el Patrón XRPD expresado en términos de ángulos 2 theta según lo mostrado en la Figura 4.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:H2O] 1:1:3 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en cualquiera de una o más de las siguientes posiciones: 7,3, 8,4, 8,8, 10,7, 12,0, 12,2, 13,2, 13,7, 14,5, 16,3, 16,7, 17,6, 19,3, 20,2, 20,6, 21,0, 21,4, 21,8, 22,8, 23,4, 23,9, 24,5, 25,2, 25,7, 25,9, 26,4, 27,2, 27,7, 28,3, 28,6, 28,9, 29,2, 29,6, y 32,7° 20 ± 0,2° 20.
En una realización particular, la sal de la invención es un aducto [Compuesto I:HCl:H2O] 1:1:3 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo al menos en 5, 10, 15, 20, 25, 30 o más de las siguientes posiciones: 7,3, 8,4, 8,8, 10,7, 12,0, 12,2, 13,2, 13,7, 14,5, 16,3, 16,7, 17,6, 19.3, 20,2, 20,6, 21,0, 21,4, 21,8, 22,8, 23,4, 23,9, 24,5, 25,2, 25,7, 25,9, 26,4, 27,2, 27,7, 28,3, 28,6, 28,9, 29,2, 29,6, y 32,7° 20 ± 0,2° 20.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:H2O] 1:1:3 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en todas las siguientes posiciones: 7.3, 8,4, 8,8, 10,7, 12,0, 12,2, 13,2, 13,7, 14,5, 16,3, 16,7, 17,6, 19,3, 20,2, 20,6, 21,0, 21,4, 21,8, 22,8, 23,4, 23,9, 24,5, 25,2, 25,7, 25,9, 26,4, 27,2, 27,7, 28,3, 28,6, 28,9, 29,2, 29,6, y 32,7° 20 ± 0,2° 20. En una realización particular, la sal de la invención está caracterizada por el Patrón XRPD expresado en términos de ángulos 2 theta según lo mostrado en la Figura 5.
En una realización, el aducto [Compuesto I:HCl:H2O] 1:1:3 en una forma cristalina sólida tiene un tamaño de las partículas de menos de 1000 pM, según lo medido por difracción del láser (Tabla II). En una realización particular, el aducto [Compuesto I:HCl:H2O] 1:1:3 en una forma sólida cristalina tiene un tamaño de partícula entre 50 pm y 800 pm. En una realización más particular, el aducto [Compuesto I:HCl:H2O] 1:1:3 en una forma sólida cristalina tiene un tamaño de partícula entre 200 pm y 600 pm.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:MeOH] 1:1:1 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en cualquiera de una o más de las siguientes posiciones: 7,1, 14,4, 16,6, 17,3, 18,9, 23,4, 24,8, y 29,0° 20 ± 0,2° 20.
En una realización particular, la sal de la invención es un aducto [Compuesto I:HCl:MeOH] 1:1:1 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo al menos en 3, 5, 7 o más de las siguientes posiciones: 7,1, 14,4, 16,6, 17,3, 18,9, 23,4, 24,8, y 29,0° 20 ± 0,2° 20.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:MeOH] 1:1:1 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en todas las siguientes posiciones: 7,1, 14,4, 16,6, 17,3, 18,9, 23,4, 24,8, y 29,0° 20 ± 0,2° 20. En una realización particular, la sal de la invención está caracterizada por el Patrón XRPD expresado en términos de ángulos 2 theta según lo mostrado en la Figura 8.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:HCO2H] 1:1:1,5 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en cualquiera de una o más de las siguientes posiciones: 7,1, 14,4, 14,8, 16,4, 17,4, 18,6, 20,8, 23,4, 24,5, 24,9, y 29,0° 20 ± 0,2° 20.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:HCO2H] 1:1:1,5 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo al menos en 3, 5, 7, 9 o más de las siguientes posiciones: 7,1, 14,4, 14,8, 16,4, 17,4, 18,6, 20,8, 23,4, 24,5, 24,9, y 29,0° 20 ± 0,2° 20.
En una realización, la sal de la invención es un aducto [Compuesto I:HCl:HCO2H] 1:1:1,5 en forma cristalina sólida, en la que la forma cristalina se caracteriza por un pico de difracción por rayos X del polvo en todas las siguientes posiciones: 7,1, 14,4, 14,8, 16,4, 17,4, 18,6, 20,8, 23,4, 24,5, 24,9, y 29,0° 20 ± 0,2° 20. En una realización particular, la sal de la invención está caracterizada por el Patrón XRPD expresado en términos de ángulos 2 theta según lo mostrado en la Figura 9.
En una realización, una sal de la invención se obtiene por combinación del Compuesto I, con un ácido seleccionado de ácido bromhídrico, ácido sulfúrico, ácido toluensulfónico, ácido bencensulfónico, ácido oxálico, ácido maleico, ácido naftalen-2-sulfónico, ácido naftalen-1,5-disulfónico, ácido 1-2-etan disulfónico, ácido metansulfónico, ácido 2-hidroxi etansulfónico, ácido fosfórico, ácido etansulfónico, ácido malónico, ácido 2-5-dihidroxibenzoico, y ácido L-tartárico, en un disolvente inerte, y la precipitación de dicha sal de dicho disolvente. En una realización particular, la sal de la invención se obtiene por el agregado del Compuesto I y un agente formador de sal en un disolvente adecuado para lograr la disolución completa, seguido de una evaporación controlada del disolvente, para lograr la supersaturación, y de este modo la cristalización de la correspondiente sal.
En una realización, la sal de la invención se obtiene mediante la mezcla del Compuesto I, y un ácido en una relación molar de entre 5:1 y 1:5 del Compuesto I: ácido. En una realización particular, la sal de la invención se obtiene mediante la mezcla del Compuesto I, y un ácido en una relación molar de entre 2:1 y 1:2 del Compuesto I: ácido. En una realización, la sal de la invención se obtiene mediante la mezcla de un Compuesto I y un ácido en una relación molar de 1:1.
En otra realización particular, el disolvente para la preparación de la sal de la invención se selecciona de cetonas, alcoholes, ésteres, alquilo C1-10, cicloalquilo C3-7, arilo C6-10 monocíclico o fusionado, sulfóxido, alquilnitrilo C1-10, éteres C1-10 lineales, ramificados o cíclicos, y haloalquilo C1-10. En una realización particular, el disolvente para la preparación de la sal de la invención se selecciona de acetona, anisol, butanol, acetato de butilo, TBME, DMSO, etanol, acetato de etilo, heptano, acetato de isopropilo, MEK, acetato de isopropilo, MeCN, ciclohexano, DCM, dioxano, metanol, nitrometano, THF, THF de metilo, tolueno, agua, acetona acuosa al 10%, THF acuoso al 10%, y metanol al 10%. En una realización particular, el disolvente para la preparación de la sal de la invención se selecciona de dioxano, THF,
acetona, DCM, y MeOH.
En otro aspecto se proporciona un procedimiento de preparación de la sal de la invención que comprende las etapas de:
i) hacer reaccionar el Compuesto I, con un ácido seleccionado de ácido clorhídrico,
en un disolvente inerte; y
ii) precipitar la sal mencionada a partir del disolvente mencionado.
En un aspecto adicional, se proporciona una sal de la invención que se obtiene por, o se obtiene mediante, el procedimiento mencionado con anterioridad.
En una realización, con respecto a la preparación de la sal de la invención, el disolvente inerte se selecciona de dioxano, THF, acetona, Dc M, y MeOH.
En una realización, con respecto a la preparación de la sal de la invención, el disolvente inerte es DCM.
En una realización, con respecto a la preparación de la sal de la invención, el disolvente inerte se selecciona de iPrOH/agua, iPrOH, iBuOH, y tBuOH.
En una realización se proporciona un procedimiento de preparación de un aducto [Compuesto I: HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) Agitar el Compuesto I con agua,
ii) Añadir HCl acuoso,
iii) Agitar, además, la mezcla obtenida en la etapa ii),
iv) Enfriar la mezcla de la etapa iii) hasta 15°C,
v) Continuar agitando durante un máximo de 24h a 15°C,
vi) Separar el sólido resultante por filtración obtenida en la etapa v) previo, y
vii) Secar bajo nitrógeno durante al menos 4h dicho sólido resultante obtenido en la etapa previa vi). En una realización particular se proporciona un procedimiento de preparación de un aducto [Compuesto I: HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) Agitar el Compuesto I con agua a 50°C,
ii) Añadir HCl acuoso,
iii) Agitar la mezcla obtenida en la etapa ii) en forma adicional a 50°C durante 15 min,
iv) Enfriar la mezcla de la etapa iii) hasta 15°C,
v) Continuar agitando durante 12h a 24h a 15°C,
vi) Separar el sólido resultante por filtración obtenida en la etapa previa v), y
vii) Secar bajo nitrógeno durante al menos 4h dicho sólido resultante obtenido en la etapa previa vi). En otra realización se proporciona un procedimiento de preparación de un aducto [Compuesto I: HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) Mezclar el Compuesto I suspendido en DCM, con MeOH,
ii) Añadir agua bajo agitación,
iii) Separar la fase orgánica,
iv) Añadir una solución de HCl a la fase orgánica obtenida en la etapa previa iii),
v) Separar el sólido resultante por filtración obtenida en la etapa previa iv),
vi) Secar dicho sólido resultante obtenido en la etapa previa v),
vii) Añadir el sólido obtenido en la etapa previa vi) a una solución de ácido fórmico/agua, bajo agitación,
viii) Añadir agua a la solución obtenida en la etapa previa vii),
ix) Separar por filtración el sólido resultante obtenido en la etapa previa viii), y
x) Secar el sólido resultante obtenido en la etapa previa ix),
En otra realización se proporciona un procedimiento de preparación de un aducto [Compuesto I: HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) Mezclar el Compuesto I suspendido en DCM, con MeOH a 35°C,
ii) Añadir agua bajo agitación a 35°C durante al menos 15 min,
iii) Separar la fase orgánica,
iv) Añadir una solución p/p al 10% de HCl en MeOH a la fase orgánica obtenida en la etapa previa iii), v) Separar el sólido resultante por filtración obtenida en la etapa previq iv),
vi) Secar dicho sólido resultante obtenido en la etapa previq v),
vii) Añadir el sólido obtenido en la etapa previa vi) a una solución 1,6/0,4 de ácido fórmico/agua, bajo agitación a 55°C
viii) Añadir agua a la solución obtenida en la etapa previq vii),
ix) Separar por filtración el sólido resultante obtenido en la etapa previq viii), y
x) Secar el sólido resultante obtenido en la etapa previq ix),
En otra realización se proporciona un procedimiento de preparación de un aducto [Compuesto I: HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) Hacer reaccionar el Compuesto I suspendido en DCM, con MeOH y trimercaptotriazina de trisodio, ii) Filtrar la suspensión resultante,
iii) Añadir agua bajo agitación,
iv) Separar la fase orgánica,
v) Añadir una solución de HCl a la fase orgánica obtenida en la etapa iv),
vi) Separar el sólido resultante por filtración obtenida en la etapa v),
vii) Secar dicho sólido resultante obtenido en la etapa vi),
viii) Añadir el sólido obtenido en la etapa vii) a una solución de ácido fórmico/agua, bajo agitación, ix) Añadir agua a la solución de la etapa viii),
x) Separar por filtración el sólido resultante obtenido en la etapa ix), y
xi) Secar el sólido resultante obtenido en la etapa x),
En otro aspecto se proporciona un procedimiento de preparación de un aducto [Compuesto I: HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) Hacer reaccionar el Compuesto I suspendido en DCM, con MeOH y trimercaptotriazina de trisodio a 35°C durante al menos 5h,
ii) Filtrar la suspensión resultante,
iii) Añadir agua bajo agitación a 35°C durante al menos 15 min,
iv) Separar la fase orgánica,
v) Añadir una solución p/p al 10% de HCl en MeOH a la fase orgánica obtenida en la etapa iv), vi) Separar el sólido resultante por filtración obtenida en la etapa v),
vii) Secar dicho sólido resultante obtenido en la etapa vi),
viii) Añadir el sólido obtenido en la etapa vii) a una solución 1,6/0,4 de ácido fórmico/agua, bajo agitación a 55°C
ix) Añadir agua a la solución de la etapa viii),
x) Separar por filtración el sólido resultante obtenido en la etapa ix), y
xi) Secar el sólido resultante obtenido en la etapa x),
Alternativamente, la ejecución de una o más de las variables especificadas de un grupo o una realización, o combinaciones de los anteriores también se contemplan en la presente invención.
Composiciones farmacéuticas
Cuando se emplea como producto farmacéutico, la sal de la invención se administra normalmente en la forma de una composición farmacéutica. Dichas composiciones pueden prepararse en un modo muy conocido en la técnica farmacéutica y comprenden al menos una sal activa de la invención.
Generalmente, una sal de la invención se administra en una cantidad farmacéuticamente efectiva. Un médico normalmente determinará la cantidad de la sal de la invención realmente administrada, en vista de las circunstancias relevantes, que incluyen la afección a tratar, la vía de administración elegida, la sal de la invención administrada en realidad, la edad, el peso y la respuesta del paciente individual, la severidad de los síntomas del paciente y similares.
La composición farmacéutica de esta invención puede administrarse por una variedad de vías que incluyen la vía oral, rectal, transdérmica, subcutánea, intraarticular, intravenosa, intramuscular e intranasal. Dependiendo de la vía de administración final, una sal de la invención se formula preferentemente como composiciones inyectables u orales o como ungüentos, lociones, o como parches, todos para administración transdérmica.
Las composiciones para administración oral pueden tener la forma de soluciones o suspensiones líquidas a granel, o polvos a granel. Más comúnmente, sin embargo, las composiciones se presentan en formas farmacéuticas unitarias para facilitar la administración exacta de la dosis. El término "formas farmacéuticas unitarias" se refiere a unidades físicamente separables adecuadas como formas farmacéuticas unitarias para seres humanos y otros mamíferos, en las que cada unidad contiene una cantidad predeterminada de material activo calculada para producir el efecto terapéutico deseado en asociación con un excipiente farmacéutico, vehículo o portador adecuados. Las formas farmacéuticas unitarias típicas incluyen las ampollas o jeringas pre llenadas, pre medidas de composiciones líquidas, o las píldoras, los comprimidos, las cápsulas o similares, en el caso de las composiciones sólidas. En dichas composiciones, la sal de la invención normalmente es un componente menor (de aproximadamente 0,1 a aproximadamente 50% en peso o preferentemente de aproximadamente 1 a aproximadamente 40% en peso) en la que el resto son varios vehículos o portadores y auxiliares de procesamiento útiles para formar la forma farmacéutica deseada.
Las formas líquidas adecuadas para administración oral pueden incluir un vehículo acuoso o no acuoso adecuado con tampones, agentes de suspensión y dispersión, colorantes, sabores y similares. Las formas sólidas incluyen, por ejemplo, cualquiera de los siguientes ingredientes, o sales de la invención de una naturaleza similar: un aglutinante tal como celulosa microcristalina, goma tragacanto o gelatina; un excipiente tal como almidón o lactosa, un agente desintegrante tal como ácido algínico, Primogel o almidón de maíz; un lubricante tal como estearato de magnesio; un deslizante tal como dióxido de silicio coloidal; un agente edulcorante tal como sacarosa o sacarina; o un agente saborizante tal como saborizante de menta o naranja.
Las composiciones inyectables normalmente se basan en solución salina estéril inyectable o solución salina tamponada con fosfato u otros portadores inyectables conocidos en la técnica. Como antes, la sal activa de la invención de acuerdo con la Fórmula I en dichas composiciones es normalmente un componente menor, con frecuencia de aproximadamente 0,05 a 10% en peso en el que el resto es el portador inyectable y similares.
Las composiciones transdérmicas están formuladas normalmente como ungüento o crema tópicos que contienen el(los) principio(s) activo(s), generalmente en una cantidad que oscila de aproximadamente 0,01 a aproximadamente 20% en peso, preferentemente de aproximadamente 0,1 a aproximadamente 20% en peso, preferentemente de aproximadamente 0,1 a aproximadamente 10% en peso, y más preferentemente de aproximadamente 0,5 a aproximadamente 15% en peso. Cuando se formulan como ungüento, los principios activos normalmente se combinan con una base indistintamente parafínica o un ungüento soluble en agua. Alternativamente, los principios activos pueden estar formulados en una crema con, por ejemplo, una base de crema de aceite en agua. Dichas formulaciones transdérmicas son muy conocidas en la técnica y generalmente incluyen ingredientes adicionales para mejorar la penetración dérmica de estabilidad de los principios activos o la formulación. Todos dichos ingredientes y formulaciones transdérmicas conocidos se incluyen dentro del alcance de la invención.
Una sal de la invención puede ser administrada por un dispositivo transdérmico. De esta manera, la administración transdérmica puede lograrse usando un parche, indistintamente del tipo reservorio o membrana porosa, o de una variedad de matriz sólida.
Los componentes descritos más arriba para las composiciones para administración oral, inyectable o tópica son simplemente representativos. Otros materiales, además de las técnicas de procesamiento y similares, se establecen en la Parte 8 de Remington’s Pharmaceutical Sciences, 17th edition, 1985, Mack Publishing Company, Easton, Pennsylvania, la cual se incorpora a la presente a modo de referencia.
Una sal de la invención también pueden administrarse en formas de liberación sostenida o a partir de sistemas de administración de liberación sostenida de fármacos. Una descripción de los materiales de liberación sostenida representativos pueden encontrarse en Remington’s Pharmaceutical Sciences.
Los siguientes ejemplos de formulación incluyen composiciones farmacéuticas representativas que pueden prepararse de acuerdo con esta invención. La presente invención, sin embargo, no está limitada a las siguientes composiciones farmacéuticas.
Formulación 1 - Comprimidos
Una sal de la invención puede mezclarse como polvo seco con un aglutinante de gelatina seca en una relación en peso de aproximadamente 1:2. Una cantidad menor de estearato de magnesio puede añadirse como lubricante. La mezcla puede formarse en comprimidos de 240-270 mg (80-90 mg de sal activa de la invención por comprimido) en una prensa para comprimidos.
Formulación 2 - Cápsulas
Una sal de la invención puede mezclarse como polvo seco con un diluyente de almidón en una relación en peso de aproximadamente 1:1. La mezcla puede llenarse en cápsulas de 250 mg (125 mg de sal activa de la invención por cápsula).
Formulación 3 - Líquido
Una sal de la invención (125 mg), puede mezclarse con sacarosa (1,75 g) y goma xántica (4 mg) y la mezcla resultante puede mezclarse, pasarse a través de un tamiz U.S. malla Nro. 10, y luego mezclarse con una solución realizada previamente de celulosa microcristalina y carboximetilcelulosa de sodio (11:89, 50 mg) en agua. Pueden diluirse benzoato de sodio (10 mg), sabor y color con agua y añadirse con agitación. Luego puede añadirse suficiente agua con agitación. Además, luego puede añadirse suficiente agua para producir un volumen total de 5 ml.
Formulación 4 - Comprimidos
Una sal de la invención puede mezclarse como polvo seco con un aglutinante de gelatina seca en una relación en peso de aproximadamente 1:2. Una cantidad menor de lubritab puede añadirse como lubricante. La mezcla puede formarse en comprimidos de 25-900 mg (8-300 mg de sal activa de la invención) en una prensa para comprimidos.
Formulación 5 - Inyección
Una sal de la invención puede disolverse o suspenderse en un medio acuoso inyectable de solución salina tamponada con fosfato hasta una concentración de aproximadamente 5 mg/ml.
Formulación 6 - Tópica
Alcohol estearílico (250 g) y una vaselina (250 g) pueden fundirse a aproximadamente 75°C y luego una mezcla de una sal de la invención (50 g) metil parabeno (0,25 g), propilparabeno (0,15 g), lauril sulfato de sodio (10 g), y propilenglicol (120 g) disuelto en agua (aproximadamente 370 g) puede añadirse y la mezcla resultante puede agitarse hasta que se congela.
Procedimientos de tratamiento
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en medicina. En una realización particular, la presente invención proporciona sales de la invención o composiciones farmacéuticas que comprenden una sal de la invención para uso en la profilaxis y/o el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención en medicina. En una realización particular, la presente invención proporciona sales de la invención o composiciones farmacéuticas que comprenden una sal de la invención para uso en la profilaxis y/o el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones.
En otra realización, la presente invención proporciona sales de la invención o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que implican la degradación y/o interrupción de la homeóstasis de cartílagos, malformaciones congénitas de cartílagos, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición.
En una realización, la presente invención proporciona composiciones farmacéuticas que comprenden una sal de la invención, y otro agente terapéutico. En una realización particular, otro agente terapéutico es un agente para el tratamiento de afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo al trasplante, enfermedades que incluyen degradación y/o interrupción de la homeostasis de cartílago, malformaciones congénitas de cartílago, y/o enfermedades asociadas con la hipersecreción de IL6 o interferones.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de enfermedades inflamatorias. En una realización particular, la enfermedad inflamatoria se selecciona de artritis reumatoide, osteoartritis, enfermedad alérgica de las vías respiratorias (por ej., asma) enfermedad pulmonar obstructiva crónica (EPOC) y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica, o colitis). Más particularmente, la enfermedad inflamatoria se selecciona de artritis reumatoide, y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis).
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de enfermedades inflamatorias. En una realización particular, la enfermedad inflamatoria se selecciona de artritis reumatoide, osteoartritis, enfermedad alérgica de las vías respiratorias (por ej., asma) enfermedad pulmonar obstructiva crónica (EPOC) y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica, o colitis). Más particularmente, la enfermedad inflamatoria se selecciona de artritis reumatoide, y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis).
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de enfermedades inflamatorias. En una realización particular, la enfermedad inflamatoria se selecciona de artritis reumatoide, osteoartritis, enfermedad alérgica de las vías respiratorias (por ej., asma) enfermedad pulmonar obstructiva crónica (EPOC) y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica, o colitis). Más particularmente, la enfermedad inflamatoria se selecciona de artritis reumatoide, y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis).
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre enfermedades inflamatorias, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, la enfermedad inflamatoria se selecciona de artritis reumatoide, osteoartritis, enfermedad alérgica de las vías respiratorias (por ej., asma) enfermedad pulmonar obstructiva crónica (EPOC) y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica, o colitis). Más particularmente, la enfermedad inflamatoria se selecciona de artritis reumatoide, y enfermedades inflamatorias intestinales (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis).
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de enfermedades autoinmunes. En una realización particular, la enfermedad autoinmune se selecciona de EPOC, asma (por ej., asma intrínseco, asma extrínseco, asma por el polvo, asma infantil) particularmente asma crónico o asma habitual (por ejemplo, asma tardío e híper respuesta de las vías aéreas), bronquitis, incluyendo asma bronquial, lupus eritematoso sistémico (SLE), lupus eritematoso cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, esclerosis múltiple, psoriasis, enfermedad del ojo seco, diabetes mellitus tipo I, y complicaciones asociadas con ésta, eczema atópico (dermatitis atópica) tiroiditis (tiroiditis de Hashimoto y autoinmune), dermatitis de contacto y dermatitis eczematosa adicional, enfermedad inflamatoria intestinal (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis), ateroesclerosis y esclerosis lateral amiotrófica. Particularmente, la enfermedad autoinmune se selecciona de EPOC, asma, lupus eritematoso sistémico, diabetes mellitus tipo I y enfermedad inflamatoria intestinal.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de enfermedades autoinmunes. En una realización particular, la enfermedad autoinmune se selecciona de EPOC, asma (por ej., asma intrínseco, asma extrínseco, asma por el polvo, asma infantil) particularmente asma crónico o asma habitual (por ejemplo, asma tardío e híper respuesta de las vías aéreas), bronquitis, incluyendo asma bronquial, lupus eritematoso sistémico (SLE), lupus eritematoso cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, esclerosis múltiple, psoriasis, enfermedad del ojo seco, diabetes mellitus tipo I, y complicaciones asociadas con ésta, eczema atópico (dermatitis atópica) tiroiditis (tiroiditis de Hashimoto y autoinmune), dermatitis de contacto y dermatitis eczematosa adicional, enfermedad inflamatoria intestinal (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis), ateroesclerosis y esclerosis lateral amiotrófica. Particularmente, la enfermedad autoinmune se selecciona de EPOC, asma, lupus eritematoso sistémico, diabetes mellitus tipo I y enfermedad inflamatoria intestinal.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de enfermedades autoinmunes. En una realización particular, la enfermedad autoinmune se selecciona de EPOC, asma (por ej., asma intrínseco, asma extrínseco, asma por el polvo, asma infantil) particularmente asma crónico o asma habitual (por ejemplo, asma tardío e híper respuesta de las vías aéreas), bronquitis, incluyendo asma bronquial, lupus eritematoso sistémico (SLE), lupus eritematoso cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, esclerosis múltiple, psoriasis, enfermedad del ojo seco, diabetes mellitus tipo I, y complicaciones asociadas con ésta, eczema atópico (dermatitis atópica) tiroiditis (tiroiditis de Hashimoto y autoinmune), dermatitis de contacto y dermatitis eczematosa adicional, enfermedad inflamatoria intestinal (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis), ateroesclerosis y esclerosis lateral amiotrófica. Particularmente, la enfermedad autoinmune se selecciona de EPOC, asma, lupus eritematoso sistémico, diabetes mellitus tipo I y enfermedad inflamatoria intestinal.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre enfermedades autoinmunes, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, la enfermedad autoinmune se selecciona de EPOC, asma (por ej., asma intrínseco, asma extrínseco, asma por el polvo, asma infantil) particularmente asma crónico o asma habitual (por ejemplo, asma tardío e híper respuesta de las vías aéreas), bronquitis, incluyendo asma bronquial, lupus eritematoso sistémico (SLE), lupus eritematoso cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, esclerosis múltiple, psoriasis, enfermedad del ojo seco, diabetes mellitus tipo I, y complicaciones asociadas con ésta, eczema atópico (dermatitis atópica) tiroiditis (tiroiditis de Hashimoto y autoinmune), dermatitis de contacto y dermatitis eczematosa adicional, enfermedad inflamatoria intestinal (por ej., enfermedad de Crohn, Whipple, colitis ulcerativa crónica o colitis), ateroesclerosis y esclerosis lateral amiotrófica. Particularmente, la enfermedad autoinmune se selecciona de EPOC, asma, lupus eritematoso sistémico, diabetes mellitus tipo I y enfermedad inflamatoria intestinal.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de enfermedades proliferativas. En una realización particular, la enfermedad proliferativa se selecciona de cáncer y leucemia. En una realización más particular, la enfermedad proliferativa se selecciona de cáncer de mama, cáncer de endometrio y cervical, cáncer de pulmón, cáncer de ovario, cáncer de próstata, cáncer hepático, y cáncer pancreático.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de enfermedades proliferativas. En una realización particular, la enfermedad proliferativa se selecciona de cáncer y leucemia. En una realización más particular, la enfermedad proliferativa se selecciona de cáncer de mama, cáncer de endometrio y cervical, cáncer de pulmón, cáncer de ovario, cáncer de próstata, cáncer hepático, y cáncer pancreático.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de enfermedades proliferativas. En una realización particular, la enfermedad proliferativa se selecciona de cáncer y leucemia. En una realización más particular, la enfermedad proliferativa se selecciona de cáncer de mama, cáncer de endometrio y cervical, cáncer de pulmón, cáncer de ovario, cáncer de próstata, cáncer hepático, y cáncer pancreático.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre enfermedades proliferativas, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, la enfermedad proliferativa se selecciona de cáncer y leucemia. En una realización más particular, la enfermedad proliferativa se selecciona de cáncer de mama, cáncer de endometrio y cervical, cáncer de pulmón, cáncer de ovario, cáncer de próstata, cáncer hepático, y cáncer pancreático.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de alergias. En una realización particular, la alergia se selecciona de enfermedad alérgica de las vías respiratorias (por ej., asma, rinitis), sinusitis, eczema y urticaria, así como alergias a los alimentos o alergias al veneno de insectos.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de la alergia. En una realización particular, la alergia se selecciona de enfermedad alérgica de las vías respiratorias (por ej., asma, rinitis), sinusitis, eczema y urticaria, así como alergias a los alimentos o alergias al veneno de insectos.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de la alergia. En una realización particular, la alergia se selecciona de enfermedad alérgica de las vías respiratorias (por ej., asma, rinitis), sinusitis, eczema y urticaria, así como alergias a los alimentos o alergias al veneno de insectos.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre alergia, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, la alergia se selecciona de enfermedad alérgica de las vías respiratorias (por ej., asma, rinitis), sinusitis, eczema y urticaria, así como alergias a los alimentos o alergias al veneno de insectos.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de rechazo a los trasplantes.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de la rechazo a los trasplantes.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento del rechazo a los trasplantes.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre rechazo a los trasplantes, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de enfermedades que implican degradación y/o interrupción de la homeóstasis de cartílagos. En una realización particular, las enfermedades que incluyen la degradación y/o interrupción de la homeóstasis de cartílagos se selecciona de osteoartritis, artritis psoriásica, artritis reumatoide juvenil, artritis por gota, artritis séptica o infecciosa, artritis reactiva, distrofia simpática refleja, algositrofia, acondroplasia, enfermedad de Paget, síndrome de Tietze o condritis costal, fibromialgia, osteocondritis, artritis neurogénica o neuropática, artropatía, sarcoidosis, amilosis, hidartrosis, enfermedad periódica, espondilitis reumatoide, formas endémicas de artritis como osteoartritis deformante endémica, enfermedad de Mseleni y enfermedad de Handigodu; degeneración resultante de fibromialgia, lupus eritematoso sistémico, escleroderma y espondilitis anquilosante.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de enfermedades que incluyen la degradación y/o interrupción de la homeóstasis de cartílagos. En una realización particular, las enfermedades que incluyen la degradación y/o interrupción de la homeóstasis de cartílagos se selecciona de osteoartritis, artritis psoriásica, artritis reumatoide juvenil, artritis por gota, artritis séptica o infecciosa, artritis reactiva, distrofia simpática refleja, algositrofia, acondroplasia, enfermedad de Paget, síndrome de Tietze o condritis costal, fibromialgia, osteocondritis, artritis neurogénica o neuropática, artropatía, sarcoidosis, amilosis, hidartrosis, enfermedad periódica, espondilitis reumatoide, formas endémicas de artritis como osteoartritis deformante endémica, enfermedad de Mseleni y enfermedad de Handigodu; degeneración resultante de fibromialgia, lupus eritematoso sistémico, escleroderma y espondilitis anquilosante.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de enfermedades que implican degradación y/o interrupción de la homeóstasis de cartílagos. En una realización particular, las enfermedades que incluyen la degradación y/o interrupción de la homeóstasis de cartílagos se selecciona de osteoartritis, artritis psoriásica, artritis reumatoide juvenil, artritis por gota, artritis séptica o infecciosa, artritis reactiva, distrofia simpática refleja, algositrofia, acondroplasia, enfermedad de Paget, síndrome de Tietze o condritis costal, fibromialgia, osteocondritis, artritis neurogénica o neuropática, artropatía, sarcoidosis, amilosis, hidartrosis, enfermedad periódica, espondilitis reumatoide, formas endémicas de artritis como osteoartritis deformante
endémica, enfermedad de Mseleni y enfermedad de Handigodu; degeneración resultante de fibromialgia, lupus eritematoso sistémico, escleroderma y espondilitis anquilosante.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre enfermedades que incluyen la degradación y/o interrupción de la homeóstasis de cartílagos, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, las enfermedades que incluyen la degradación y/o interrupción de la homeóstasis de cartílagos se selecciona de osteoartritis, artritis psoriásica, artritis reumatoide juvenil, artritis por gota, artritis séptica o infecciosa, artritis reactiva, distrofia simpática refleja, algositrofia, acondroplasia, enfermedad de Paget, síndrome de Tietze o condritis costal, fibromialgia, osteocondritis, artritis neurogénica o neuropática, artropatía, sarcoidosis, amilosis, hidartrosis, enfermedad periódica, espondilitis reumatoide, formas endémicas de artritis como osteoartritis deformante endémica, enfermedad de Mseleni y enfermedad de Handigodu; degeneración resultante de fibromialgia, lupus eritematoso sistémico, escleroderma y espondilitis anquilosante.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de malformación(es) congénitas de cartílagos. En una realización particular, la(s) malformaciones congénitas de cartílagos se seleccionan de condrólisis hereditaria, condrodisplasias y pseudocondrodisplasias, en particular, pero sin limitación, microtia, anotia, condrodisplasia metafisaria y trastornos relacionados.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de malformación(es) congénitas de cartílagos. En una realización particular, la(s) malformaciones congénitas de cartílagos se seleccionan de condrólisis hereditaria, condrodisplasias y pseudocondrodisplasias, en particular, pero sin limitación, microtia, anotia, condrodisplasia metafisaria y trastornos relacionados.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de malformación(es) congénitas de cartílagos. En una realización particular, la(s) malformaciones congénitas de cartílagos se seleccionan de condrólisis hereditaria, condrodisplasias y pseudocondrodisplasias, en particular, pero sin limitación, microtia, anotia, condrodisplasia metafisaria y trastornos relacionados.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre malformación(es) congénitas de cartílagos, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, la(s) malformaciones congénitas de cartílagos se seleccionan de condrólisis hereditaria, condrodisplasias y pseudocondrodisplasias, en particular, pero sin limitación, microtia, anotia, condrodisplasia metafisaria y trastornos relacionados.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de enfermedades asociadas con la hipersecreción de IL6. En una realización particular, las enfermedades asociadas con la hipersecreción de IL6” se selecciona(n) de la enfermedad de Castelman, mieloma múltiple, psoriasis, sarcoma de Kaposi y/o glomerulonefritis proliferativa mesangial.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de enfermedades asociadas con la hipersecreción de IL6. En una realización particular, las enfermedades asociadas con la hipersecreción de IL6” se selecciona(n) de la enfermedad de Castelman, mieloma múltiple, psoriasis, sarcoma de Kaposi y/o glomerulonefritis proliferativa mesangial.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de enfermedades asociadas con la hipersecreción de IL6. En una realización particular, las enfermedades asociadas con la hipersecreción de IL6” se selecciona(n) de la enfermedad de Castelman, mieloma múltiple, psoriasis, sarcoma de Kaposi y/o glomerulonefritis proliferativa mesangial.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre enfermedades asociadas con la hipersecreción de IL6, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, las enfermedades asociadas con la hipersecreción de IL6” se selecciona(n) de la enfermedad de Castelman, mieloma múltiple, psoriasis, sarcoma de Kaposi y/o glomerulonefritis proliferativa mesangial.
En una realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, para uso en la profilaxis y/o el tratamiento de enfermedades asociadas con la
hipersecreción de interferones. En una realización particular, la enfermedad asociada con hipersecreción de interferones se selecciona de lupus eritematoso sistémico y cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, psoriasis y artritis reumatoide.
En una realización, la presente invención proporciona el uso de una sal de la invención, o composiciones farmacéuticas que comprenden una sal de la invención, en la profilaxis y/o el tratamiento de enfermedades asociadas con la hipersecreción de interferones. En una realización particular, la enfermedad asociada con hipersecreción de interferones se selecciona de lupus eritematoso sistémico y cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, psoriasis y artritis reumatoide.
En otra realización, la presente invención proporciona sales de la invención, o composiciones farmacéuticas que comprenden una sal de la invención para uso en la fabricación de un medicamento para uso en la profilaxis y/o el tratamiento de enfermedades asociadas con la hipersecreción de interferones. En una realización particular, la enfermedad asociada con hipersecreción de interferones se selecciona de lupus eritematoso sistémico y cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, psoriasis y artritis reumatoide.
En un procedimiento adicional de aspectos de tratamiento esta invención proporciona procedimientos de profilaxis y/o tratamiento de un mamífero que sufre enfermedades asociadas con la hipersecreción de interferones, cuyos procedimientos comprenden la administración de una cantidad efectiva de una sal de la invención o una o más de las composiciones farmacéuticas descritas en la presente memoria para el tratamiento o la profilaxis de dicha condición. En una realización particular, la enfermedad asociada con hipersecreción de interferones se selecciona de lupus eritematoso sistémico y cutáneo, nefritis por lupus, dermatomiositis, síndrome de Sjogren, psoriasis y artritis reumatoide.
Un régimen particular de la presente invención comprende la administración a un individuo que sufre afecciones inflamatorias, enfermedades autoinmunes, enfermedades proliferativas, alergia, rechazo a los trasplantes, enfermedades que implican la degradación y/o interrupción de la homeóstasis de cartílagos, malformaciones congénitas y/o enfermedades asociadas con la hipersecreción de IL6 o interferones, de una cantidad efectiva de una sal de la invención durante un período de tiempo suficiente para reducir el nivel de las enfermedades antes mencionadas en el individuo, y preferentemente terminar los procesos responsables para dichos procesos.
Por el uso de estos patrones de dosificación, cada dosis proporciona de aproximadamente 1 a aproximadamente 500 mg de la sal de la invención, en las que cada dosis particular proporciona de aproximadamente 10 a aproximadamente 300 mg, más particularmente aproximadamente 25 a aproximadamente 250 mg, y especialmente 10 mg, 20 mg, 25 mg, 50 mg, 75 mg, 100 mg, 150 mg, 200 mg, 250 mg o 300 mg.
Los niveles de dosis para inyección oscilan de aproximadamente 0,1 mg/kg/h a al menos 10 mg/kg/h, en total durante de aproximadamente 1 a aproximadamente 120 h y especialmente 24 a 96 h. También puede administrarse un bolo de precarga de aproximadamente 0,1 mg/kg a aproximadamente 10 mg/kg o más para lograr niveles adecuados en estado estacionario. No se espera que la dosis máxima total exceda aproximadamente 1 g/día para un paciente humano de 40 a 80 kg.
Para la profilaxis y/o el tratamiento de afecciones prolongadas, tal como las afecciones degenerativas, el régimen para tratamiento normalmente se prolonga durante muchos meses o años de modo tal que se prefiere la administración oral para conveniencia y tolerancia del paciente. Con la administración oral, de una a cuatro (1 -4) dosis regulares por día, especialmente de una a tres (1-3) dosis regulares por día, normalmente una a dos (1-2) dosis regulares por día, y mucho más normalmente una (1) dosis regular por día son regímenes representativos. Alternativamente para fármacos de efecto prolongado, con la administración oral, una vez cada semana por medio, una vez por semana y una vez por día son regímenes representativos. En particular, el régimen de administración puede ser cada 1 -14 días, más particularmente, 1-10 días, incluso más particularmente 1-7, y mucho más particularmente 1-3 días.
Por el uso de estos patrones de dosificación, cada dosis proporciona de aproximadamente 1 a aproximadamente 500 mg de la sal de la invención, en las que cada dosis particular proporciona de aproximadamente 10 a aproximadamente 300 mg, más particularmente aproximadamente 25 a aproximadamente 250 mg, y especialmente 10 mg, 20 mg, 25 mg, 50 mg, 75 mg, 100 mg, 150 mg, 200 mg, 250 mg o 300 mg.
Las dosis transdérmicas generalmente se seleccionan para proporcionar niveles en sangre similares o más bajos que los logrados usando dosis inyectables.
Cuando se usa para prevenir la aparición de una condición, una sal de la invención se administrará a un paciente que presente riesgo de desarrollar la afección, normalmente tras el consejo y bajo la supervisión de un médico, a los niveles posológicos descritos más arriba. Los pacientes en riesgo de desarrollar una afección particular generalmente incluyen aquellos que tienen antecedentes familiares de la afección, o aquellos que según la identificación realizada por análisis o determinación genética sean particularmente susceptibles a desarrollar la afección.
Una sal de la invención puede administrarse como principio activo solo o puede administrarse en combinación con otros agentes terapéuticos, incluyendo otras sales de la invención que demuestran la misma actividad terapéutica, o una similar, y que se determine que son seguras y eficaces para dicha administración combinada. En una realización
específica, la administración concomitante de dos (o más) agentes permite el uso de dosis significativamente más bajas, reduciendo de esta manera los efectos colaterales observados.
En una realización, una sal de la invención, o una composición farmacéutica que comprende una sal de la invención se administra como medicamento. En una realización específica, dicha composición farmacéutica comprende, además, un principio activo adicional.
En una realización, una sal de la invención se administra de manera concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de una enfermedad que implica inflamación, los agentes particulares incluyen, pero sin limitación, agentes inmuno reguladores, por ej., azatioprina, corticosteroides (por ej., prednisolona o dexametasona), ciclofosfamida, ciclosporina A, tacrolimo, micofenolato, mofetilo, muromonab-CD3 (OKT3, por ej., Orthocolone®), ATG, aspirina, paracetamol, ibuprofeno, naproxeno y piroxicam.
En una realización, una sal de la invención se administra en forma concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de la artritis (por ej., artritis reumatoide), los agentes particulares incluyen, pero sin limitación, analgésicos, fármacos antiinflamatorios no esteroides (AINE), esteroides DMARDS sintéticos (por ejemplo, pero sin limitación metotrexato, leflunomida, sulfasalazina, auranofina, aurotiomalato de sodio, penicilamina, cloroquina, hidroxicloroquina, azatioprina, tofacitinib, baricitinib, fostamatinib, y ciclosporina), y DMARDS biológicos (por ejemplo, pero sin limitación infliximab, etanercept, adalimumab, rituximab y abatacept).
En una realización, una sal de la invención se administra de manera concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de trastornos proliferativos, los agentes particulares incluyen, pero sin limitación: metotrexato, leukovorina, adriamicina, prednisona, bleomicina, ciclofosfamida, 5- fluorouracilo, paclitaxel, docetaxel, vincristina, vinblastina, vinorelbina, doxorubicina, tamoxifeno, toremifeno, acetato de megestrol, anastrozol, goserelina, anticuerpo monoclonal anti-HER2 (por ej., Herceptin™), capecitabina, clorhidrato de raloxifeno, inhibidores de EGFR (por ej., lressa®, Tarceva™, Erbitux™), inhibidores de VEGF (por ej., Avastin™), inhibidores de proteasoma (por ej., Velcade™), Glivec® e inhibidores de hsp90 (por ej., 17-AAG). Además, la sal de la invención de acuerdo con la Fórmula I puede administrarse en combinación con otras terapias que incluyen, pero sin limitación, radioterapia o cirugía. En una realización específica, el trastorno proliferativo se selecciona de cáncer, enfermedad mieloproliferativa o leucemia.
En una realización, una sal de la invención se administra de manera concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de enfermedades autoinmunes, los agentes particulares incluyen, pero sin limitación: glucocorticoides, agentes citostáticos (por ej., análogos de purina), agentes de alquilación, (por ej., mostazas de nitrógeno (ciclofosfamida), nitrosoureas, sales de platino de la invención y otros), antimetabolitos (porej., metotrexato, azatioprina y mercaptopurina), antibióticos citotóxicos (por ej., dactinomicina antraciclinas, mitomicina C, bleomicina y mitramicina), anticuerpos (por ej., anticuerpos monoclonales anti-CD20, anti-CD25 o anti-CD3 (OTK3), Atgam® y Thymoglobuline®), ciclosporina, tacrolimo, rapamicina (sirolimo), interferones (por ej., IFN-P), proteínas que se unen al TNF (porej., infliximab, etanercept, o adalimumab), micofenolato, fingolimod y miriocina.
En una realización, una sal de la invención se administra de manera concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de rechazo a los trasplantes, los agentes particulares incluyen, pero sin limitación: inhibidores de calcineurina (por ej., ciclosporina o tacrolimo (FK506)), inhibidores de mTOR (por ej., sirolimo, everolimo), anti-proliferativos (por ej., azatioprina, ácido micofenólico), corticosteroides (por ej., prednisolona, hidrocortisona), anticuerpos (por ej., anticuerpos monoclonales del receptor anti-IL-2Ra, basiliximab, daclizumab), anticuerpos policlonales anti-células T (porej., globulina anti-timocito (ATG), globulina anti-linfocito (ALG)).
En una realización, una sal de la invención se administra en forma concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de asma y/o rinitis y/o EPOC, los agentes particulares incluyen, pero sin limitación: agonistas adrecoceptores beta2 (por ej., salbutamol, levalbuterol, terbtalina y bitolterol), epinefrina (inhalada o comprimidos), anticolinérgicos (por ej., bromuro de ipratropio), glucocorticoides (orales o inhalados). Los agonistas p2 de acción prolongada (por ej., salmeterol, formoterol, bambuterol, y albuterol oral de liberación prolongada), combinaciones de esteroides inhalados y broncodilatadores de acción prolongada (por ej., fluticasona/salmeterol, budesonida/formoterol), antagonistas e inhibidores de la síntesis de leucotrieno (por ej., montelukast, zafirlukast y zileuton), inhibidores de liberación de mediadores (por ej., cromoglicato y cetotifeno), reguladores biológicos de la respuesta de IgE (porej., omalizumab), antihistaminas (porej., ceterizina, cinarizina, fexofenadina) y vasoconstrictores (por ej., oximetazolina, xilometazolina, nafazolina y tramazolina).
Además, una sal de la invención puede administrarse en combinación con las terapias de emergencia para el asma y/o EPOC, dichas terapias incluyen administración de oxígeno o helio, salbutamol o terbutalina nebulizados (opcionalmente combinados con un anticolinérgico (por ej., ipratropio), esteroides sistémicos (orales o intravenosos, por ej., prednisona, prednisolona, metilprednisolona, dexametasona o hidrocortisona), salbutamol intravenoso, beta agonistas no específicos, metaproterenol), anticolinérgicos (IV o negulizados, por ej., glicopirrolato, atropina, ipratropio), metilxantinas (teofilina, aminofilina, bamifilina), anestésicos por inhalación que tienen un efecto broncodilatador (por ej., isoflurano, halotano, enflurano), cetamina y sulfato de magnesio intravenoso.
En una realización, una sal de la invención se administra en forma concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de enfermedad inflamatoria de intestino (IBD), los agentes particulares incluyen, pero sin limitación: glucocorticoides (por ej., prednisona, budesonida) agentes inmunomoduladores, sintéticos, modificadores de la enfermedad (por ej., metotrexato, leflunomida, sulfasalazina, mesalazina, azatioprina, 6- mercaptopurina y ciclosporina) agentes inmunomoduladores, biológicos, modificadores de la enfermedad (infliximab, adalimumab, rituximab, y abatacept).
En una realización, una sal de la invención se administra en forma concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de SLE, los agentes particulares incluyen, pero sin limitación: anticuerpos monoclonales humanos (belimumab (Benlysta)), fármacos antirreumáticos modificadores de la enfermedad (DMARD) tal como antimaláricos (por ej., plaquenil, hidroxicloroquina), inmunosupresores (por ej., metotrexato y azatioprina), ciclofosfamida y ácido micofenólico, fármacos inmunosupresores y analgésicos, tal como fármacos antiinflamatorios no esteroides, opiatos (por ej., dextropropoxifeno y co-codamol), opioides (porej., hidrocodona, oxicodona, MS Contin, o metadona) y el parche transdérmico duragésico de fentanilo.
En una realización, una sal de la invención se administra en forma concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de la psoriasis, los agentes particulares incluyen, pero sin limitación: tratamientos tópicos tal como soluciones para el baño, humectantes, cremas y ungüentos medicados que contienen alquitrán de carbón, ditranol (antralina), corticosteroides como desoximetasona (Topicort™), fluocinonida, análogos de vitamina D3 (por ejemplo calcipotriol), aceite de argán y retinoides (etretinato, acitretina, tazaroteno), tratamientos sistémicos tal como metotrexato, ciclosporina, retinoides, tioguanina, hidroxiurea, sulfasalazina, micofenolato mofetilo, azatioprina, tacrolimo, ésteres de ácido fumárico o biologías tal como Amevive™, Enbrel™, Humira™, Remicade™, Raptiva™ y ustekinumab (un bloqueador de IL 12 y IL-23). Además, una sal de la invención puede administrarse en combinación con otras terapias que incluyen, pero sin limitación, fototerapia o fotoquimioterapia (por ej., psoralen y fototerapia ultravioleta A (PUVA)).
En una realización, una sal de la invención se administra en forma concomitante con otro agente terapéutico para el tratamiento y/o la profilaxis de una reacción alérgica, los agentes particulares incluyen, pero sin limitación: antihistaminas (por ej., cetirizina, difenhidramina, fexofenadina, levocetirizina), glucocorticoides (por ej., prednisona, betametasona, beclometasona, dexametasona), epinefrina, teofilina o antileucotrienos (por ej., montelukast o zafirlukast), anti-colinérgicos y descongestivos.
Por administración concomitante se incluye cualquier medio de administración de dos o más agentes terapéuticos al paciente como parte del mismo régimen de tratamiento, como será evidente para los expertos en la técnica. Mientras que dos o más agentes pueden administrarse simultáneamente en una sola formulación, es decir, como una composición farmacéutica individual, esto no es esencial. Los agentes pueden administrarse en diferentes formulaciones y en diferentes momentos.
Procedimientos de síntesis química
General
El compuesto de acuerdo con la Fórmula I, y la sal de 1:1:3 Base Libre/HCl/H2O de la invención pueden prepararse a partir de materiales de partida ampliamente disponibles con el uso de los siguientes procedimientos y procedimientos generales. Se apreciará que donde se presenten las afecciones de los procesos preferidos o típicos (es decir, temperaturas de reacción, tiempos, proporciones en moles de reactivos, disolventes, presiones, etc.), también pueden usarse otras afecciones de proceso a menos que se indique de otro modo. Las afecciones de reacción óptimas pueden variar con los reactivos particulares o el disolvente usado, pero una persona experta en la técnica puede determinar dichas afecciones mediante procedimientos de optimización de rutina.
Además, como resultará evidente para aquellas personas con experiencia en la técnica, puede ser necesario el uso de grupos protectores convencionales para evitar que ciertos grupos funcionales sufran reacciones no deseadas. La elección de un grupo protector adecuado para un grupo funcional particular así como las afecciones adecuadas para la protección y desprotección son muy conocidas en la técnica (Greene, T W; Wuts, P G M;, 1991).
Los siguientes procedimientos se presentan con detalles respecto de la preparación de una sal de la invención como se define anteriormente en la presente memoria y en los ejemplos comparativos. Una sal de la invención puede prepararse a partir de materiales de partida y reactivos comercialmente disponibles o conocidos por una persona capacitada en la técnica de la síntesis orgánica.
Todos los reactivos son de grado comercial y se usan como se recibe sin purificación adicional, a menos que se indique de otro modo. Los solventes anhidros disponibles en el mercado se usan para reacciones conducidas bajo atmósfera inerte. Los solventes de grado reactivo se usan en todos los otros casos, a menos que se especifique de otro modo. La cromatografía en columna se realiza sobre gel de sílice 60 (35-70 gm). La cromatografía de fase delgada se lleva a cabo con el uso de placas F-254 de gel de sílice pre-revestidas (espesor 0,25 mm). Los espectros 1H RMN se registran en un espectrómetro Broker DPX 400 RMN (400 MHz o un espectrómetro Broker Advance 300 RMN (300 MHz). Las desviaciones químicas (5) para los espectros de 1H RMN se informan en partes por millón (ppm) con relación a tetrametilsilano (5 0.00) o el pico del disolvente residual apropiado, es decir CHCl3 (5 7,27), como
referencia interna. Las multiplicidades se expresan como singulete (s), duplete (d), triplete (t), cuarteto (q), quintuplete (quin), multiplete (m) y amplio (br). Los espectros de electroaspersión MS se obtienen sobre u espectrómetro LC/MS de la plataforma Waters o con UPLC Waters Acquity H-Class acoplado a un espetrómetro 3100 detector de Masa Waters. Columnas usadas: Waters Acquity UPLC BEH C18 1,7 gm, 2,1mm ID x 50mm L, Waters Acquity UPLC BEH C18 1,7 gm, 2,1mm ID x 30 mm L, o Waters Xterra MS 5gm C18, 100 x 4,6mm. Los procedimientos utilizan indistintamente gradientes MeCN/H2O (H2O contiene cualquiera de 0,1% TFA o 0,1% NH3) o gradientes MeOH /H2O (H2O contiene 0,05% TFA). El calentamiento en microondas se realiza con un iniciador Biotage.
Tabla I. Lista de abreviaturas usadas en la sección experimental:
Tabla II. Aparato del estudio de sal
Preparación sintética de la sal de la invención
Ejemplo 1. Preparación del Compuesto I
1.1. Vía 1
1.1.1. 4-[4-(4,4,5,5-Tetrametil-[1,3,2]dioxaborolan-2-il)-bencil]-tiomorfolin-1,1-dióxido
Se disuelven 2-(4-Bromometil-fenil)-4,4,5,5-tetrametil-[1,3,2]dioxaborolano (1 eq.) y DIPEA (2 eq.) en DCM/MeOH (5:1 v:v) bajo N2 y 1, 1 -dióxido de tiomorfolino (2 eq.) en porciones. La solución resultante se agitó a temperatura ambiente durante 16h. Después de este tiempo, la reacción está completa. El disolvente se evapora. El compuesto se extrae con EtOAc y agua, se lava con salmuera y se seca sobre MgSO4. Las capas orgánicas se filtran y se evaporan. El compuesto final se aísla sin purificación adicional.
1.1.2. (5-bromo-[1,2,4]triazolo[1,5-a]piridin-2-il)-amida del ácido ciclopropanocarboxílico
1.1.2.1. Etapa i): 1-(6-Bromo-piridin-2-il)-3-carboetoxi-tiourea
A una solución de 2-amino-6-bromopiridina (1) (253,8 g, 1,467 mol) en DCM (2,5 L) enfriada hasta 5°C se añade isotiocianato de etoxicarbonilo (173,0 ml, 1,467 mol) gota a gota durante 15 min. La mezcla de reacción se deja entibiar hasta la temperatura ambiente. (20 °C) y se agita durante 16 h. La evaporación al vacío da un sólido que puede recolectarse por filtración, lavarse minuciosamente con petróleo (3 x 600 ml) y secarse al aire para producir el producto deseado. La tiourea puede usarse como tal para la próxima etapa sin ninguna purificación. 1H (400 MHz, CDCh) 5 12,03 (1H, br s), 8,81 (1H, d), 8,15 (1H, br s), 7,60 (1H, t), 7,32 (1H, dd), 4,31 (2H, q), 1,35 (3H, t).
1.1.2.2. Etapa ii): 5-Bromo-[1,2,4]t
riazolo[1,5-a]piridin-2-ilamina
A una suspensión de clorhidrato de hidroxilamina (101,8 g, 1,465 mol) en EtOH/MeOH (1:1, 900 ml) se añade N,N-diisopropilctilamina (145,3 ml, 0,879 mol) y la mezcla se agita a temperatura ambiente (20 °C) durante 1 h. 1-(6-Bromopiridin-2-il)-3-carboetoxi-tiourea (2) (89,0 g, 0,293 mol) se añade luego y la mezcla se calienta lentamente hasta reflujo (Nota: se requiere rascador blanqueador para desactivar el H2S evolucionado). Después de 3h a reflujo, la mezcla se deja enfriar y se filtra para recolectar el sólido precipitado. El producto adicional se recolecta por evaporación al vacío del filtrado, incorporación de H2O (250 ml) y filtración. Los sólidos combinados se lavan consecutivamente con H2O (250 ml), EtOH/MeOH (1:1,250 ml) y Et2O (250 ml) luego se seca al vacío para producir el derivado tiazolopiridina (3) como un sólido. El compuesto puede usarse como tal para la próxima etapa sin ninguna purificación. 1H (400 MHz, DMSO-d6) 57,43-7,34 (2H, m, 2 x H aromático), 7,24 (1H, dd, J 6,8 y 1,8 Hz, H aromático), 6,30 (2H, br, NH2); m/z 213/215 (1:1, M+H+ , 100%).
1.1.2.3. Etapa (iii): (5-bromo-[1,2,4]triazolo[1,5-a]piridin-2-il)-amida del ácido ciclopropancarboxílico
A una solución de la 2-amino-triazolopiridina obtenida en la etapa previa (7,10 g, 33,3 mmol) en MeCN anhidro (150 ml) a 5°C se añade Et3N (11,6 ml, 83,3 mmol) seguido de cloruro de ciclopropancarboxílico (83,3 mmol). La mezcla de reacción se deja enfriar luego hasta la temperatura ambiente y se agita hasta que se consume todo el material de partida. Si se requiere, se añade Et3N (4,64 ml, 33,3 mmol) y cloruro de ciclopropancarbonilo (33,3 mmol) adicional para asegurar la reacción completa. Después de la evaporación del disolvente al vacío el residuo resultante se trata con solución de amoníaco metanólico 7 N (50 ml) y se agita a temperatura ambiente (durante 1-16 h) para hidrolizar cualquier producto bis-acilado. El aislamiento del producto se realiza por remoción de los volátiles al vacío seguido de trituración con Et2O (50 ml). Los sólidos se recolectan por filtración, se lavan con H2O (2x50ml), acetona (50 ml) y Et2O (50 ml), luego se secan al vacío para dar el compuesto deseado.
1.1.3. Compuesto I
Se añade 4-[4-(4,4,5,5-tetrametil-[1,3,2]dioxaborolan-2-il)-benzil]-tiomorfolin-1,1-dióxido (1,1 eq.) a una solución de (5-bromo-[1,2,4]triazolo[1,5-a]piridin-2-il)-amida del ácido ciclopropanocarboxílico en 1,4-dioxano/agua (4:1). K2CO3 (2 eq.) y PdCbdppf (0,03 eq.) se añaden a la solución. La mezcla resultante se calienta luego en un baño de aceite a 90°C durante 16h bajo N2. Se añade agua y la solución se extrae con acetato de etilo. Las fases orgánicas se secan sobre MgSO4 anhidro y se evaporan al vacío.
El compuesto final se obtiene después de purificación por cromatografía flash.
Alternativamente, una vez completa la reacción, un depurador de paladio, tal como 1,2-bis(difenilfosfin)etano, se añade, la mezcla de reacción se deja enfriar y se realiza una filtración. La torta del filtro se reemulsiona en un disolvente adecuado (por ej., acetona), el sólido se separa por filtración, se lava con más acetona, y se seca. El sólido resultante se resuspende en agua, se añade HCl acuoso y después de agitar a temperatura ambiente la solución resultante se filtra sobre celite (Celpure P300). Luego se añade NaOH acuoso al filtrado y la suspensión resultante se agita a temperatura ambiente, el sólido se separa por filtración, se lava con agua y se seca por succión. Finalmente, la torta se solubiliza nuevamente en una mezcla de THF/H2O, se trata con un depurador de paladio (por ej., SMOPEX 234) a 50°C, la suspensión se filtra, los solventes orgánicos se retiran por evaporación y la emulsión resultante se lava con agua y metanol, se seca y se tamiza, para obtener el compuesto deseado como la base libre.
1.2. Vía 2
1.2.1. Etapa 1: [5-(4-hidroximetil-fenil)-[1,2,4-triazolo[1,5-a]-piridin-2-il]-amida del ácido ciclopropancarboxílico
Se añade ácido 4-(hidroximetil)fenilborónico (1,1 eq.) a una solución de (5-bromo-[1,2,4]triazolo[1,5-a]piridin-2-il)-amida del ácido ciclopropanocarboxílico en 1,4-dioxano/agua (4:1). K2CO3 (2 eq.) y PdChdppf (0,03 eq.) se añaden a la solución. La mezcla resultante se calienta luego en un baño de aceite a 90°C durante 16h bajo N2. Se añade agua y la solución se extrae con acetato de etilo. Las fases orgánicas se secan sobre MgSO4 anhidro y se evaporan al vacío. La mezcla resultante se usa sin purificación adicional.
1.2.2. Etapa 2: [5-(4-bromometil-fenil)-[1,2,4]triazolo[1,5-a]piridin-2-il]-amida del ácido cidopropancarboxílico
A una solución de [5-(4-hidroximeti-fenil)-[1,2,4]-triazolo-[1,5-a]piridin-2-il]amida del ácido ciclopropancarboxílico (1,0 eq.) en cloroformo se añade lentamente tribromuro de fósforo (1,0 eq.). La mezcla de reacción se agita a temperatura ambiente durante 20 horas, se desactiva con hielo y agua (20 ml) y se extrae con diclorometano. La fase orgánica se seca sobre MgSO4 anhidro, se filtra y se concentra hasta la sequedad. El residuo blanco resultante se tritura con diclorometano/éter dietílico 2:1 para producir el producto deseado.
1.2.3. Etapa 3:
Se disuelven [5-(4-bromometil-fenil)-[1,2,4]-triazolo-[1,5-a]piridin-2-il]amida del ácido ciclopropancarboxílico (1 eq.) y DIPEA (2 eq.) en DCM/MeOH (5:1 v:v) bajo N2 y se añade gota a gota 1,1- dióxido de tiomorfolina (1,1 eq.). La solución resultante se agitó a temperatura ambiente durante 16h. Después de este tiempo, la reacción está completa. El disolvente se evapora. El compuesto se disuelve en DCM, se lava con agua y se seca sobre MgSO4 anhidro. Las fases orgánicas se filtran y se evaporan. El compuesto final se aísla por cromatografía en columna usando EtOAc para producir el producto deseado.
Ejemplo 2. Preparación de las sales del Compuesto I.
2.1. Protocolo 1
El disolvente se añade a las muestras del Compuesto I (aproximadamente 5 mg) en porciones relativas en volumen de 10, 15 y 20 volúmenes, y después de cada incorporación las muestras se agitan a 50°C en un agitador durante 20 min para alentar la disolución, antes de enfriar hasta la temperatura ambiente para la siguiente incorporación de disolvente. El disolvente se selecciona de isopropanol, etanol, metanol, acetato de isopropilo, THF, TBME, acetona, metil etil cetona, DCM y MeCN.
En estas condiciones, casi la disolución completa del Compuesto I solo ocurre en DCM.
Después de la incorporación de 20 volúmenes relativos de disolvente, se añade HCl (solución 1 M en THF) (12 gl ~ 1 eq.) a cada muestra y se realizan observaciones. Las muestras se almacenan en un agitador sobre un ciclo de calor -frío (50°C / temperatura ambiente, 4 h a cada temperatura) durante 16 h. Los sólidos resultantes se aíslan por filtración al vacío, se secan bajo succión y se analizan por XRPD.
La formación de sal de HCl se observa solamente en etanol, metanol, THF, acetona, metil etil cetona y MeCN.
2.2. Protocolo 2 (incluyendo ejemplos comparativos)
El Compuesto I (~20mg) se trata con 400 gl (20 volúmenes) de disolvente (THF, acetona) y se trata con soluciones de ácido acuosas a temperatura ambiente (véase Tabla III a continuación). Los experimentos se colocan en una cámara de maduración que se cicla entre la temperatura ambiente y 50°C con cuatro horas transcurridas bajo cada condición. Después de tres días los sólidos se aíslan por filtración y cualquier solución se deja evaporar. Cualquier sólido formado se aísla, o los sólidos remanentes se tratan con EtOAc y se colocan nuevamente en la cámara de maduración durante cuatro días. Cualquier sólido adicional se aísla por filtración.
Los sólidos se analizan por XRPD.
Cuando se somete a este protocolo, las sales solo se forman en ácido sulfúrico, pTSA, ácido 1,2-etan disulfónico, ácido 2-hidroxietansulfónico, ácido naftalen2-sulfónico, y ácido maleico.
Tabla III Ácidos usados en el Protocolo 2
2.3. Protocolo 3 (incluyendo los ejemplos comparativos)
A una suspensión del Compuesto I (~25 mg) y disolvente (MeOH, THF, Acetona o DCM) (20 volúmenes relativos) a aproximadamente 40°C se añade 1,05 o 2,1 eq. del ácido (HCl, HBr, H2SO4 , PH-SO3H, ácido oxálico, ácido maleico, o pTSA.H2O), y se realizan observaciones visuales. Las muestras se almacenan en un agitador a 26°C durante 14 h. Se toma una alícuota y el sólido se aísla por filtración al vacío, se seca bajo succión y se analiza por XRPD. Luego las mezclas se almacenan en un agitador a 26°C durante un adicional de 31 h. El sólido remanente de aquellas muestras que exhiben patrones de XRPD cristalinos diferentes a la base libre se aíslan por filtración al vacío y se realiza análisis adicional (DSC, RMN, Estabilidad).
El resto de cada muestra se almacena en un agitador sobre un ciclo de calor / frío (50°C / temperatura ambiente, 4 h a cada temperatura) durante 136 h. Nuevamente, una alícuota de cada muestra se toma y el sólido se aísla por filtración al vacío, se secan bajo succión y se analizan por XRPD. El sólido remanente de aquellas muestras que exhiben patrones de XRPD cristalinos diferentes a la base libre se aíslan por filtración al vacío y se emprende análisis adicional (DSC, RMN, Estabilidad).
Las muestras que permanecen en aislamiento se dejan evaporar lentamente en condiciones ambiente hasta que el disolvente se ha evaporado, y cualquier sólido formado se aísla y se analiza por XRPD.
Cuando se somete a este protocolo, las sales solo se forman en HBr, HCl, ácido sulfúrico, pTSA y ácido maleico.
2.4 Protocolo 4 (incluyendo los ejemplos comparativos)
2.4.1. HCl
HCl (solución 1 M en THF) (655 pL, 0,65 mmol, 1,1 eq.) se añade a una suspensión agitada de Compuesto I (252,6 mg, 0,59 mmol, 1 eq.) y metanol (5,05 ml, 20 vol.) a 50°C. La mezcla se enfría hasta 25°C a 1 °C/min y se agita a 25°C durante 22 h.
El sólido se aísla por filtración al vacío y se seca bajo succión.
El análisis de XRPD confirmó la formación de una sal no higroscópica estable, que contiene 4-5% de agua, que tiene una solubilidad acuosa medida a 1,9 mg/ml.
2.4.2. Ácido maleico (comparativo)
El Compuesto I (246,4 mg, 0,58 mmol, 1 eq.) se suspende en 5 % agua en acetona (4,95 ml, 20 vol.) a 25°C y la muestra se entibia hasta 50°C. Se añade ácido maleico (solución 1 M en THF) (1,2 ml, 1,22 mmol, 2,1 eq.) a la suspensión agitada a 50°C. La mezcla se enfría hasta 25°C a 1°C/min y se agita a 25°C durante 22 h.
El sólido se aisló por filtración al vacío y se seca bajo succión.
El análisis de XRPD confirmó la formación de una sal no higroscópica estable, que tiene una estabilidad acuosa medida a 0,4 mg/ml.
2.4.3. pTSA (comparativo)
pTSA (solución 1 M en EtOH) (1,3 ml, 1,3 mmol, 2,2 eq.) se añade a una suspensión agitada de Compuesto I (250,7 mg, 0,59 mmol, 1 eq.) y THF (5 ml, 20 vol.) a 50°C. La mezcla se enfría hasta 25°C a 1 °C/min y se agita a 25°C durante 22 h.
El sólido se aísla por filtración al vacío y se seca bajo succión.
El análisis de XRPD confirmó la formación de una sal, que resultó ser inestable.
2.5. Análisis de sal complementaria
Los sólidos recuperados de este protocolo también se someten a evaluación de pureza, equivalente de sal (IC), RMN (disolvente residual), DSC, TGA (solvatos) y estabilidad (1 semana a 40°C / Humedad relativa 75%).
2.5.1. Determinación de pKa
Los datos se recolectan en un instrumento Siriuis GIpKa con un accesorio D-PAS. Se realizan las mediciones a 25 °C en solución acuosa por UV y en mezclas de agua y metanol por potenciometría. El medio de titulación fue ajustado en su potencia iónica con KCl 0,15 M (ac.). Los valores encontrados en las mezclas de metanol y agua se corrigen a 0% de co-disolvente por medio de extrapolación de Yasuda-Shedlovsky.
Los datos se refinan usando el software Refinement Pro.
Después de este procedimiento, se obtienen los siguientes valores: 1,58 ± 0,01,3,68 ± 0,02, y 12,02 ±0,01.
2.5.2. Determinación del pH
Las mediciones de pH se realizan sobre el material experimental como emulsión. Normalmente, 1 ml de agua desmineralizada se añade hasta aproximadamente 300 mg del material analizado y la suspensión luego se somete a vórtice. Si se encuentra disponible sólido insuficiente o la viscosidad es demasiado alta para la medición del pH con el uso de un electrodo de pH, la cantidad de agua aumenta hasta que es posible realizar una medición en incrementos de 1 ml. El electrodo de pH se calibró con el uso de una calibración de tres puntos.
Finalmente, el pYH se registra al inicio (= después de 2 min para permitir una medición relativamente estable del pH).
2.5.3. Estudio de solubilidad.
2.5.3.1. Protocolo
La solubilidad de un compuesto se determina en diferentes solventes por equilibrio de un exceso de producto durante al menos 24 h a 20°C en un agitador giratorio. La solución súper saturada luego se filtra y la concentración del producto en el filtrado se determina con el uso de espectrometría UV.
En agua, la influencia del pH se ajusta hasta un pH 2, pH 7 y pH 9. Se usan HCl y NaOH para ajustar el pH.
2.5.3.2. Resultados
Por ejemplo, cuando se somete a este protocolo, la solubilidad de la base libre y la correspondiente medición de sal de HCl se informan en la tabla IV a continuación. Inesperadamente, ir del Compuesto I al Compuesto I. HCl.3H2O no resulta sistemáticamente en una solubilidad mejorada.
Tabla IV Solubilidad del Compuesto I como base libre y la correspondiente sal de HCl en varios solventes
2.5.4. Conclusiones
Como se demostró con anterioridad, la solubilidad del Compuesto I varía en gran medida dependiendo del disolvente usado, y la formación de sal no ocurre inevitablemente con cada ácido, ilustrando la dificultad en seleccionar una combinación satisfactoria de disolvente y ácido, lo que es específico para el Compuesto I.
Ejemplo 3. Estudio de polimorfismo
3.1. Compuesto I
3.1.1. Formación del Compuesto I amorfo
El Compuesto I (38 mg) se calienta en un instrumento de DSC bajo nitrógeno de acuerdo con el siguiente procedimiento: 1) Se calentó desde 30°C hasta 250°C a 10°C/min; 2) Se mantuvo isotérmico durante 1 min; 3) Se enfrió de 250°C a 30°C a 100°C/min; y 4) Se mantuvo isotérmico durante 4 min.
El sólido resultante se confirma como amorfo por análisis de XRPD.
3.1.2. Estudio de polimorfismo
El compuesto amorfo se sometió a cuarenta solventes diferentes (formiato de etilo, TBME, acetona, acetato de metilo, metanol, tetrahidrofurano, éter diisopropílico, acetato de etilo, etanol, metil etil cetona, acetonitrilo, t-BuOH, 2-Propanol, 1-2-Dimetoxietano, Acetato de isopropilo, 1-Propanol, 2-Butanol, nitrometano, 1-4-Dioxano, acetato de propilo, 2-Pentanona, 2-Metil-1-Propanol, Tolueno, Acetato de isobutilo, Metilisobutil cetona, 1-Butanol, 2-Metoxietanol, Acetato de butilo, metil butil cetona, 3-Metil-1-Butanol, 2-Etoxietanol, 1-Pentanol, Anisol, Benzonitrilo, nitrobenceno, IPA 5% agua, EtOH 5% agua, MeCN 5% agua, THF 5% agua, y acetona 5% agua) y se cicla térmicamente entre la temperatura ambiente y 50°C con cuatro horas transcurridas entre cada condición. Después de cinco días, los sólidos se recolectan por filtración y se analizan inicialmente por XRPD.
3.1.3. Resultados de polimorfismo del Compuesto I
Cuando se somete a este protocolo, los sólidos obtenidos se analizaron por XRPD, y los siguientes patrones más estables se informan en la Tabla V, Tabla VI, y Tabla VII a continuación.
Tabla V. Compuesto I Patrón 1 Patrón XRPD (Figura 1)
Tabla VI Compuesto I Patrón 3 Patrón XRPD (Figura 2)
Tabla VII Compuesto I Patrón 4 Patrón XRPD (Figura 3)
3.2 Polimorfismo de las sales de HCI del Compuesto I y sus solvatos
3.2.1 Formación de sales de HCl amorfas del Compuesto I
El Compuesto I (25,47 mg) se mezcla con agua (70 ml, -2750 volúmenes relativos) y se agita a temperatura ambiente durante 30 min. La mezcla resultante se filtra a través de un filtro de jeringa con membrana de PVDF de 0,45 mm y se congela en un baño a -78 °C. El disolvente se remueve usando un liofilizador para producir la sal de mono-HCl amorfa del Compuesto I (confirmada por XRPD, transición del vidrio a 149°C (análisis de DSC modulado))
3.2.2. Protocolos de estudio
Los volúmenes de 25 solventes diferentes (Acetona, anisol, butanol, acetato de butilo, TBME, DMSO, etanol, acetato de etilo, heptano, acetato de isopropilo, MEK, acetato de isopropilo, MeCN, ciclohexano, DCM, dioxano, metanol, nitrometano, THF, THF de metilo, tolueno, agua, acetona acuosa al 10%, THF acuoso al 10% y metanol al 10%), se añaden a la sal de mono-HCl amorfa del Compuesto I, dichos volúmenes oscilan de 125 pL (5 vol rel) a 1 ml (40 vol. Rel.), o hasta que se observa una suspensión móvil o disolución casi completa. La muestra se almacena en un agitador en un ciclo de calor / frío (50°C / temperatura ambiente, 4h) durante 23h.
Después de 23 h, donde se ha formado el sólido, se toma una alícuota y el sólido se aísla por filtración al vacío, mientras que la suspensión remanente se mantiene en un agitador en un ciclo de calor / frío (50°C / temperatura ambiente, 4 h). El sólido de la alícuota se seca bajo succión durante 30 min y se analiza por XRPD, luego se seca de manera adicional en un horno de vacío a 30 °C y 0,0005 Mpa (5 mbar) durante 34 h, y se analiza nuevamente por XRPD. Finalmente, la muestra secada se almacena a 40°C / 75 % HR durante 72 h y se analiza nuevamente por XRPD.
Después de 47 h, donde se ha formado el sólido en la suspensión, se toma una alícuota y el sólido se aísla por filtración al vacío, mientras que la suspensión remanente se mantiene en un agitador en un ciclo de calor / frío (50°C / temperatura ambiente, 4 h). El sólido de la alícuota se almacena bajo condiciones ambiente durante 72 h y 14 d con análisis por XRPD en cada momento de medición. El sólido, que se ha almacenado bajo condiciones ambiente durante 14 d, se almacena a 40 °C / 75 % HR durante 43 h y se analiza nuevamente por XRPD.
Después de 143h, donde se ha formado el sólido, se toma una alícuota de la suspensión remanente analizada en un agitador en un ciclo de calor / frío (50°C / temperatura ambiente, 4 h) y el sólido se aísla por filtración al vacío, se seca bajo succión durante 2 h, luego se analiza por XRPD. El sólido aislado se seca en un horno de vacío a 30°C y 0,0005 Mpa (5 mbar) durante 20 h, y se analiza nuevamente por XRPD. La muestra secada se almacena a 40°C / 75 % HR durante 114 h y se analiza nuevamente por XRPD.
3.2.3. Resultados
Además de este estudio, se identifican dos formas estables.
3.2.3.1. Compuesto I. HCl (comparativo)
HCl (solución 3,6 M en dioxano) (2,5 ml, 9,05 mmol 1,1 eq.) se añade en porciones a una suspensión agitada de Compuesto I amorfo (3,499 g, 8,22 mmol, 1 eq.) y metanol (70 ml, 20 volúmenes relativos) a 50 °C durante un período de 2 min. La mezcla se enfría hasta 20°C a 0,1°/min y se agita a 20°C durante un adicional de 10 h. La mezcla se enfría hasta 15°C a 0,5°C/min y se agita durante 30 min. El sólido resultante se aísla por filtración al vacío, se lava con
metanol (2 x 3,5 ml, 1x7 ml) y se seca bajo succión para producir el Compuesto l. HCl.
3.2.3.2. Compuesto I. HCI.3 H2O
HCl (solución 1 M en THF) (250 pL, 0,25 mmol, 1,05 eq.) se añade a una suspensión de Compuesto I amorfo (100,37 mg, 0,24 mmol, 1 eq.) y DCM (2 ml, 20 volúmenes relativos) a 40°C. La mezcla se almacena en un agitador en un ciclo de calor / frío (40°C / temperatura ambiente, 4 h) durante 70 h. El sólido se aísla por filtración al vacío y se seca bajo succión para producir el Compuesto l. HCL3H2O.
3.2.3.3. Análisis
Los patrones de difracción por rayos X se divulgan en la Tabla VIII y en la Tabla IX a continuación.
Tabla VIII Compuesto I. Patrón XRPD de HCl (Figura 4)
Tabla IX Compuesto I. Patrón HRPD de HCL3H2O (Figura 5)
3.2.3.4. Difracción por rayos X del cristal simple del Compuesto I. HCI.3 H2O (Figura 11)
El Compuesto I. HCL3H2O se recristaliza a partir de acetona:agua (1:1). Los resultados se muestran en la Tabla X a continuación.
Tabla X. Estructura individual de cristal del Compuesto I. HCI.3H2O
El procedimiento de refinamiento se basa en los menos cuadrados de la matriz completa sobre F2. R [F2 > 2o(F2)] = 0,0377 y wR(F2) = 0,0837. Bondad de ajuste (S) = 1,109. El procedimiento de refinamiento usó 5649 reflejos, 339 parámetros y 0 limitaciones. Todas las posiciones de hidrógeno se identificaron usando el mapa de diferencia y aquellas unidas a átomos C y átomos N se colocaron luego en posiciones calculadas y se refinaron usando un modelo de conducción. Aquellos hidrógenos unidos al oxígeno y nitrógeno del agua se refinaron libremente. El Apmax final = 0,314 y Á y Apmin = -0,368 e Á.
La estructura de cristal del Compuesto I. HCl.3H2Ü (Figura 11) muestra la inclusión inesperada de las moléculas de agua en el retículo de cristal, lo que puede proporcionar estabilización adicional del sistema.
Ejemplo 4. Formación a gran escala del Compuesto I . HCI.3 H2O
4.1. Protocolo 1
Al Compuesto I (44 kg, 1,0 eq.) bajo atmósfera inerte, se añade agua (15 vol. rel., 1000 L), y la mezcla se agita a 50°C. Se añaden 3,5 eq. de HCl ac. (5 vol. rel.) durante 10-15 min, a una temperatura máxima de 55°C. Tras la compleción de la adición, se continúa con la agitación a 50°C durante 15 min, y la reacción luego se enfría hasta 15°C y se agita a esa temperatura durante al menos 12h aunque no más de 24h.
El sólido resultante se separa por filtración, y la torta se lava con agua (2,0 vol. rel.) y la torta se seca bajo nitrógeno durante al menos 4h para producir el producto deseado.
4.2. Protocolo 2
Al Compuesto I (45g, 106 mmol, 1 eq.) bajo atmósfera inerte se añade DCM (675 ml) y metanol (225 ml). La suspensión resultante se calienta hasta 35°C bajo agitación, y se añade sal de trisodio de trimercaptotriazina 15% en agua (22,5 g, 14 mmol, 0,13 eq.), y la solución resultante se agita durante 5h, después de lo cual la solución se filtra en un papel de 0,45 pm bajo presión de nitrógeno.
Al filtrado se añade agua (50 ml), y la mezcla bifásica resultante se agita a 35°C durante 15 min, después de cuyo período las fases se separan, y la fase orgánica se deja enfriar hasta 20°C, y se lava dos veces con 50 ml de agua.
La fase orgánica se enfría hasta 15-20°C, luego se añade HCl 10% en metanol (42,4 g, 116mmol, 1,10 eq.) durante 30 min, causando la precipitación de un sólido. La suspensión se agita de manera adicional a 20°C durante 3h, luego el precipitado se aísla por filtración, la torta se lava con metanol (2x50 ml) para producir el compuesto deseado, que se seca al vacío a 45°C durante 3 h. La torta luego se resuspende en agua (220 ml) y se agita durante 6 h a 50°C, y luego se enfría hasta 15-20°C. El sólido resultante se separa por filtración y la torta se lava con agua (2 x 30 ml), y se seca a 45°C durante 3h para producir el producto deseado.
4.3. Protocolo 3
4.3.1. Etapa 1: Compuesto I. HCl.MeOH
Al Compuesto I (100g, 235 mmol, 1 eq.) suspendido en DCM (1,5 L), se añade MeOH (0,5 L), y la solución resultante se calienta hasta 35°C. Se añade trimercaptotriazina de trisodio 85% (8,7 g, 3 mmol, 0,13 eq.) en agua (42 ml) y la mezcla resultante se agita a 35°C durante al menos 5h. La solución luego se filtra sobre un filtro de papel de 0,45 gm bajo presión de nitrógeno.
A la solución resultante se añade agua (150 g), se agita a 35°C durante 15 a 30 min, y se separa la mezcla bifásica. La fase orgánica se lava nuevamente con agua (2 x 150 g).
Finalmente, se añade una solución de HCl en MeOH (10% p/p) (141 g), y la suspensión se agita a 20°C durante 3h, y el sólido resultante se separa por filtración, la torta se lava con MeOH (2 x 118g), se seca al vacío durante 3h a 45°C, para producir el Compuesto l. HCl.MeOH que se analiza por XRPD. (Tabla XI).
4.3.2. Etapa 2: Compuesto I. HCl.3H2O
A ácido fórmico (200g, 1,6 eq.) en agua (36g, 0,4 eq.) se añade Compuesto l. HCl.MeOH (100 g, 1 eq.) obtenido en la etapa 1 anterior. La mezcla resultante se calienta hasta 55°C bajo agitación y la solución se filtra a través de un cartucho de filtro de 0,45 gm. Se añade ácido fórmico 85% ac. (200 g), y la mezcla se enfría hasta 28-32°C bajo suave agitación.
Luego se añade agua (100g) seguido de Compuesto I. HCl.3H2O (1g) causando la precipitación del Compuesto I.HCI.1,5HCO2H, que se analiza por XRPD (Tabla XII).
Bajo agitación a 28-32°C, se añade agua (2L) en porciones en 8 porciones de 100ml, 1 porción de 200 ml, y 2 porciones de 500 ml.
La suspensión acuosa luego se filtra, la torta se lava con agua (2x100 ml) y se seca a 30-35°C para producir el Compuesto l. HCl.3H2O, que se analiza por XRPD y DSC. (Figura 5 y Figura 7)
Tabla XI Compuesto I. Patrón XRPD de HCl:MeOH (Figura 8)
Tabla XII Compuesto I. Patrón XRPD de HCl.HCOOH (Figura 9)
Ejemplo 5. Compuesto I. Estudio de estabilidad de HCL3 H2O.
5.1. Estudio de estabilidad acelerada
5.1.1. Protocolo
Muestras del Compuesto I. HCL3H2O se almacenan en afecciones para evaluar la estabilidad química y la estabilidad física como se describe en la Tabla XIII.
Tabla XIII Condiciones de estabilidad
Las muestras se toman a T0, luego cada mes hasta 3 meses, y se analizan por FT-IR, DSC, y XRPD.
5.2. Estudio de Estabilidad extendida
5.2.1. Protocolo
Las muestras de los compuestos de prueba se almacenan en afecciones para evaluar la estabilidad química y la estabilidad física como se describe en la Tabla XIV que sigue:
Tabla XIV Condiciones de estabilidad
Se toman muestras en el T0, luego cada mes hasta 12 meses, luego a los 18, 24 y 36 meses; y cada una de las alícuotas luego se analiza por HPLC, titulación por Karl-Fisher, FT-IR, DSC, y XRPD.
5.3. Análisis de GVS del Compuesto l. HCI.3 H2O
El análisis de GVS se llevó a cabo para evaluar la estabilidad del Compuesto I. HCL3H2O y se presenta en la Figura 6. La evolución del material se sigue por medio de XPRD en varios momentos de medición.
No se observó cambio en la forma a HR elevada. El Compuesto I. HCL3H2O se deshidrata al Compuesto I.HCl anhidro tras calentar por encima de 60°C o a menos de 10 % HR. La rehidratación del Compuesto I. HCL3H2O ocurre tras enfriar hasta la temperatura ambiente o por exposición al 20 % o más de humedad relativa.
5.3.1 Conclusiones
Inesperadamente, el Compuesto I. HCL3H2O puede deshidratarse en el Compuesto I.HCl, pero se convierte nuevamente en la forma de trihidrato más estable del Compuesto l. HCL3H2O en afecciones normales. Esto no pudo haber sido previsto por los expertos en la técnica.
Ejemplos biológicos
Ejemplo 6. Ensayos in vitro
6.1. Ensayo de inhibición de JAK 1
El dominio catalítico de JAK1 humana recombinante (aminoácidos 850-1154; número de catálogo 08-144) se adquiere de Carna Biosciences. 10 gg de JAK1 se incuba con 12,5 gg de sustrato polyGT (número de catálogo de Sigma P0275) en tampón de reacción de quinasa (15 mM Tris-HCl pH 7,5, 1 mM Dt T, 0,01% Tween-20, 10 mM MgCl2, 2 gM ATP no radiactivo, 0,25 gCi 33P-gamma-ATP (GE Healthcare, número de catálogo AH9968) concentraciones finales) con o sin 5gL que contiene compuesto de prueba o vehículo (DMSO, 1 % concentración final), en un volumen total de 25 gL, en una placa de polipropileno de 96 pocillos (Greiner, base V). Después de 45 min a 30°C, las reacciones se detienen por el agregado de 25 gl/pocillo de ácido fosfórico 150 mM. La totalidad de la reacción de quinasa terminada se transfiere a placas de filtro de 96 pocillos previamente lavadas (ácido fosfórico 75 mM) (número de catálogo de Perkin Elmer 6005177) usando un cosechador de células (Perkin Elmer). Las placas se lavan 6 veces con 300 gl por pocillo de una solución 75 mM de ácido fosfórico y la base de las placas se sella. Se añaden 40 gl/pocillo de Microscint-20,
la parte superior de las placas se sella y se realiza la lectura usando el Topcount (Perkin Elmer). La actividad de quinasa se calcula restando recuentos por minuto (cpm) obtenidos en presencia de un inhibidor de control positivo (10 pM esturosporina) de cpm obtenido en presencia de vehículo. La capacidad que tiene un compuesto de prueba de inhibir su actividad se determina como:
Porcentaje de inhibición = ((cpm determinado para la muestra con el compuesto de prueba presente - cpm determinado para la muestra con inhibidor de control positivo) dividido por (cpm determinado en presencia de vehículo - cpm determinado para la muestra con inhibidor de control positivo)) * 100.
Las series de dilución de la dosis se preparan para los compuestos, permitiendo el análisis de los efectos de respuesta a la dosis en el ensayo de JAK1 y el cálculo de la IC50 para cada compuesto. Cada compuesto se analiza como rutina a la concentración de 20pM seguido de una dilución serial 1/3, 8 puntos (20pM - 6,67pM - 2,22pM - 740nM - 247nM -82nM - 27nM - 9nM) en una concentración final de 1% DMSO. Cuando la potencia de la serie de compuestos aumenta, se preparan más diluciones y/o la concentración superior se reduce (por ej., 5 pM, 1 pM).
Los siguientes compuestos se han analizado para determinar su actividad contra JAK1 y los valores de IC50, según lo determinado usando los ensayos descritos en la presente memoria, se dan a continuación en la Tabla XV.
Tabla XV Valores de los compuestos JAK1 IC50
6.2. Ensayo de determinación de Ki de JAK1
Para la determinación de Ki, se mezclan diferentes cantidades de compuesto con la enzima y la reacción enzimática se sigue como función de la concentración de ATP. La Ki se determina por medio de gráfico doble recíproco de Km contra concentración del compuesto (gráfico de Lineweaver-Burk). 1 pg de JAK1 (Invitrogen, PV4774) se usa en este ensayo. El sustrato es 50nM Ulight-jAK-1 (Tyrl023) Péptido (Perkin Elmer, TRF0121) La reacción se realiza en 25mM MOPS pH 6,8, 0,01%, 2 mM DTT, 5 mM MgCl2 Brij-35 con concentraciones variables de ATP y compuesto. El sustrato fosforilado se mide usando un anticuerpo anti-fosfotirosina marcado Eu PT66 (Perkin Elmer, AD0068). La lectura se realiza en el envision (Perkin Elmer) con excitación a 320 nm y emisión seguido a 615 nm y 665 nm. Por ejemplo, cuando el Compuesto I se analiza en este ensayo, se mide un valor de Ki de 39 nM.
6.3. Ensayo de inhibición de JAK2
El dominio catalítico de JAK2 humana recombinante (aminoácidos 808-1132; número de catálogo PV4210) se adquiere de Invitrogen. 0.025mU de JAK2 se incuba con 2,5 pg de sustrato polyGT (número de catálogo de Sigma P0275) en tampón de reacción de quinasa (5 mM MOPS pH 7,5, 9 mM MgAc, 0.3mM EDTA, 0,06% Brij y 0,6 mM DTT, 1 pM ATP no radiactivo, 0,25 pCi 33P-gamma-ATP (GE Healthcare, número de catálogo AH9968) concentraciones finales) con o sin 5pL que contiene compuesto de prueba o vehículo (DMSO, 1 % concentración final), en un volumen total de 25 pL, en una placa de polipropileno de 96 pocillos (Greiner, base V). Después de 90 min a 30°C, las reacciones se detienen por el agregado de 25 pl/pocillo de ácido fosfórico 150 mM. La totalidad de la reacción de quinasa terminada se transfiere a placas de filtro de 96 pocillos previamente lavadas (ácido fosfórico 75 mM) (número de catálogo de Perkin Elmer 6005177) usando un cosechador de células (Perkin Elmer). Las placas se lavan 6 veces con 300 pl por pocillo de una solución 75 mM de ácido fosfórico y la base de las placas se sella. Se añaden 40 pl/pocillo de Microscint-20, la parte superior de las placas se sella y se realiza la lectura usando el Topcount (Perkin Elmer). La actividad de quinasa se calcula restando recuentos por minuto (cpm) obtenidos en presencia de un inhibidor de control positivo (10 pM esturosporina) de cpm obtenido en presencia de vehículo. La capacidad que tiene un compuesto de prueba de inhibir su actividad se determina como:
Porcentaje de inhibición = ((cpm determinado para la muestra con el compuesto de prueba presente - cpm determinado para la muestra con inhibidor de control positivo) dividido por (cpm determinado en presencia de vehículo - cpm determinado para la muestra con inhibidor de control positivo)) * 100.
Las series de dilución de la dosis se preparan para los compuestos, permitiendo el análisis de los efectos de respuesta a la dosis en el ensayo de JAK2 y el cálculo de la IC50 para cada compuesto. Cada compuesto se analiza como rutina a la concentración de 20pM seguido de una dilución serial 1/3, 8 puntos (20 pM - 6.67 pM - 2.22 pM - 740 nM - 247 nM - 82 nM - 27 nM - 9 nM) en una concentración final de 1% DMSO. Cuando la potencia de la serie de compuestos aumenta, se preparan más diluciones y/o la concentración superior se reduce (por ej., 5 pM, 1 pM).
Los siguientes compuestos se han analizado para determinar su actividad contra JAK2 y los valores de IC50, según lo determinado usando los ensayos descritos en la presente memoria, se dan a continuación en la Tabla XVI.
Tabla XVI Valores de los compuestos JAK2 IC50
6.4. Ensayo de determinación de Kd de JAK2
JAK2 (Invitrogen, PV4210) se usa a una concentración final de 5 nM. El experimento de unión se realiza en 50mM Hepes pH 7,5, 0,01% Brij-35, 10mM MgCl2, 1 mM EGTA usando 25nM rastreador de quinasa 236 (Invitrogen, PV5592) y 2 nM Eu-anti-GST (Invitrogen, PV5594) con concentraciones variadas de compuesto. La detección del rastreador se realiza de acuerdo con el procedimiento de los fabricantes.
Por ejemplo, cuando el Compuesto I se analiza en este ensayo, se mide un valor de Kd de 205 nM.
6.5. Ensayo de inhibición de JAK3
El dominio catalítico de JAK3 humana recombinante (aminoácidos 781-1124; número de catálogo PV3855) se adquiere de Invitrogen. 0.025mU de JAK3 se incuba con 2,5 gg de sustrato polyGT (número de catálogo de Sigma P0275) en tampón de reacción de quinasa (25 mM Tris pH 7,5, 0,5 mM EGTA, 0,5 mM Na3VO4, 5 mM b-glicerolfosfato, 0,01% Triton X-100, 1 pM ATP no radiactivo, 0,25 gCi 33P-gamma-ATP (GE Healthcare, número de catálogo AH9968) concentraciones finales) con o sin 5pL que contiene compuesto de prueba o vehículo (DMSO, 1 % concentración final), en un volumen total de 25 pL, en una placa de polipropileno de 96 pocillos (Greiner, base V). Después de 105 min a 30°C, las reacciones se detienen por el agregado de 25 pl/pocillo de ácido fosfórico 150 mM. La totalidad de la reacción de quinasa terminada se transfiere a placas de filtro de 96 pocillos previamente lavadas (ácido fosfórico 75 mM) (número de catálogo de Perkin Elmer 6005177) usando un cosechador de células (Perkin Elmer). Las placas se lavan 6 veces con 300 pl por pocillo de una solución 75 mM de ácido fosfórico y la base de las placas se sella. Se añaden 40 pl/pocillo de Microscint-20, la parte superior de las placas se sella y se realiza la lectura usando el Topcount (Perkin Elmer). La actividad de quinasa se calcula restando recuentos por minuto (cpm) obtenidos en presencia de un inhibidor de control positivo (10 pM esturosporina) de cpm obtenido en presencia de vehículo. La capacidad que tiene un compuesto de prueba de inhibir su actividad se determina como:
Porcentaje de inhibición = ((cpm determinado para la muestra con el compuesto de prueba presente - cpm determinado para la muestra con inhibidor de control positivo) dividido por (cpm determinado en presencia de vehículo - cpm determinado para la muestra con inhibidor de control positivo)) * 100.
Las series de dilución de la dosis se preparan para los compuestos, permitiendo el análisis de los efectos de respuesta a la dosis en el ensayo de JAK3 y el cálculo de la IC50 para cada compuesto. Cada compuesto se analiza como rutina a la concentración de 20pM seguido de una dilución serial 1/3, 8 puntos (20pM - 6,67pM - 2,22pM - 740nM - 247nM -82nM - 27nM - 9nM) en una concentración final de 1% DMSO. Cuando la potencia de la serie de compuestos aumenta, se preparan más diluciones y/o la concentración superior se reduce (por ej., 5 pM, 1 pM).
Los siguientes compuestos se han analizado para determinar su actividad contra JAK3 y los valores de IC50, según lo determinado usando los ensayos descritos en la presente memoria, se dan a continuación en la Tabla XVII.
Tabla XVII Valores de los compuestos JAK3 IC50
6.6. Ensayo de determinación de Ki de JAK3
Para la determinación de Ki, se mezclan diferentes cantidades de compuesto con la enzima y la reacción enzimática se sigue como función de la concentración de ATP. La Ki se determina por medio de gráfico doble recíproco de Km contra concentración del compuesto (gráfico de Lineweaver-Burk). JAK3 (Carna Biosciences, 09CBS-0625B) se usa a una concentración final de 10 ng/ml. El sustrato es sal de sodio Poly(Glu,Tyr) (4:1) , MW 20000 - 50 000 (Sigma, P0275) La reacción se realiza en 25mM Tris pH 7,5,0,01% Triton X-100, 0,5mM Eg Ta , 2,5mM DTT, 0,5mM Na3VO4, 5mM b- glicerolfosfato, 10mM MgCl2 con concentraciones variadas de ATP y compuesto y se detiene por la incorporación de 150 mM ácido fosfórico. La medición de fosfato incorporado en el sustrato polyGT se realiza por la carga de las muestras en una placa de filtro (usando un cosechador, Perkin Elmer) y posterior lavado. El 33P incorporado en polyGT se mide en un contador de centelleo Topcount después de la incorporación de líquido para centelleo a las placas del filtro (Perkin Elmer).
Por ejemplo, cuando el Compuesto I se analiza en este ensayo, se mide un valor de Ki de 353 nM.
6.7. Ensayo de inhibición de TYK2
El dominio catalítico de TYK2 humana recombinante (aminoácidos 871-1187; número de catálogo 08-147) se adquiere de Carna Biosciences. 5 ng de TYK2 se incuba con 12,5 gg de sustrato polyGT (número de catálogo de Sigma P0275) en tampón de reacción de quinasa (25 mM Hepes pH 7,5, 100 mM NaCl, 0,2 mM Na3VÜ4, 0,1% NP-40, 0,1 gM ATP no radiactivo, 0,125 gCi 33P-gamma-ATP (GE Healthcare, número de catálogo AH9968) concentraciones finales) con o sin 5gL que contiene compuesto de prueba o vehículo (DMSO, 1% concentración final), en un volumen total de 25 gL, en una placa de polipropileno de 96 pocillos (Greiner, base V). Después de 90 min a 30°C, las reacciones se detienen por el agregado de 25 gl/pocillo de ácido fosfórico 150 mM. La totalidad de la reacción de quinasa terminada se transfiere a placas de filtro de 96 pocillos previamente lavadas (ácido fosfórico 75 mM) (número de catálogo de Perkin Elmer 6005177) usando un cosechador de células (Perkin Elmer). Las placas se lavan 6 veces con 300 gl por pocillo de una solución 75 mM de ácido fosfórico y la base de las placas se sella. Se añaden 40 gl/pocillo de Microscint-20, la parte superior de las placas se sella y se realiza la lectura usando el Topcount (Perkin Elmer). La actividad de quinasa se calcula restando recuentos por minuto (cpm) obtenidos en presencia de un inhibidor de control positivo (10 gM esturosporina) de cpm obtenido en presencia de vehículo. La capacidad que tiene un compuesto de prueba de inhibir su actividad se determina de la siguiente manera:
Porcentaje de inhibición = ((cpm determinado para la muestra con el compuesto de prueba presente - cpm determinado para la muestra con inhibidor de control positivo) dividido por (cpm determinado en presencia de vehículo - cpm determinado para la muestra con inhibidor de control positivo)) * 100.
Las series de dilución de la dosis se preparan para los compuestos, permitiendo el análisis de los efectos de respuesta a la dosis en el ensayo de TYK2 y el cálculo de la IC50 para cada compuesto. Cada compuesto se analiza como rutina a la concentración de 20gM seguido de una dilución serial 1/3, 8 puntos (20gM - 6,67gM - 2,22gM - 740nM - 247nM -82nM - 27nM - 9nM) en una concentración final de 1% DMSO. Cuando la potencia de la serie de compuestos aumenta, se preparan más diluciones y/o la concentración superior se reduce (por ej., 5 gM, 1 gM).
Los siguientes compuestos se han analizado para determinar su actividad contra TYK2 y los valores de IC50, según lo determinado usando los ensayos descritos en la presente memoria, se dan a continuación en la Tabla XVIII.
Tabla XVIII Valores de los compuestos TYK2 IC50
6.8. Ensayo de determinación de Kd de TYK2
TYK2 (Carna Biosciences, 09CBS-0983D) se usa a una concentración final de 5 nM. El experimento de unión se realiza en 50mM Hepes pH 7,5, 0,01% Brij-35, 10mM MgCl2, 1mM EGTA usando 50nM rastreador de quinasa 236 (Invitrogen, PV5592) y 2 nM Eu-anti-GST (Invitrogen, PV5594) con concentraciones variadas de compuesto. La detección del rastreador se realiza de acuerdo con el procedimiento de los fabricantes.
Por ejemplo, cuando el Compuesto I se analiza en este ensayo, se mide un valor de Kd de 376 nM.
Ejemplo 7. Ensayos celulares
7.1. Ensayo de señalización de JAK-STAT
Se mantienen células HeLa en medio de Eagle Modificado de Dulbecco (DMEM) que contiene 10% suero de ternero fetal inactivado por calor, 100 U/ml de penicilina y 100 gg/ml de estreptomicina. Se usan células HeLa al 70 % de confluencia para transfección. 20.000 células en 87 gl de medio de cultivo se transfectan transitoriamente con 40 gg de informante pSTAT 1 (2)-luciferasa (Panomics), 8 gg de informante LacZ como informante de control interno y 52 gg de pBSK usando 0,32 gL de Jet-PEI (Polyplus) como reactivo de transfección por en formato de placa de 96 pocillos. Después de la incubación durante la noche, a 37°C, 10% de CO2, se retira el medio de transfección. Se añaden 75 gl de DMEM 1,5% de suero de ternero fetal inactivado con calor. 15 gl de compuesto a concentración 6,7 x se añade durante 60 min y luego 10 gl de OSM humano (Peprotech) a 33 gg/ml de concentración final.
Todos los compuestos se analizan por duplicado comenzando con 20 gM seguido de una dilución serial 1/3, 8 dosis en total (20 gM - 6.6 gM - 2.2 gM - 740 nM - 250 nM - 82 nM - 27 nM - 9 nM) en una concentración final de 0,2% DMSO.
Después de la incubación durante la noche a 37°C, 10% células de CO2 se lisan en 100 gl de tampón de lisis/pocillo (PBS, 0,9 mM CaCl2, 0,5 mM MgCl2, 5% Trehalosa, 0,025% Tergitol NP9, 0,15% BSA). 40 gL de lisado celular se usa para leer la actividad de p-galactosidasa mediante el agregado de 180 gl de solución de p-Gal (30gl de ONPG 4mg/ml 150 gl de tampón de p-Galactosidasa (0,06 M Na2HPO4, 0,04 M NaH2PO4, 1 mM MgCl2)) durante 20 min. La reacción se detiene por la adición de 50 gl de Na2CO31 M. La absorbancia se lee a 405 nm.
La actividad de luciferasa se mide usando 40 pl de lisado celular más 40 pl de Steadylite® como se describe por el fabricante (Perkin Elmer), en el Envision (Perkin Elmer). 10 pM de un inhibidor de pan-JAK se usa como control positivo (100% de inhibición). Como control negativo se usa 0,5% DMSO (0% de inhibición). Los controles positivo y negativo se usan para calcular los valores de z” y “porcentaje de inhibición” (PIN).
Porcentaje de inhibición = ((fluorescencia determinada en presencia de vehículo - fluorescencia determinada para la muestra con compuesto experimental presente) dividido por (fluorescencia determinada en presencia de vehículo -fluorescencia determinada para la muestra sin activación)) * 100.
Los valores PIN se grafican para compuestos analizados en dosis-respuesta, los valores de EC50 se derivan y se divulgan en la Tabla XIX que sigue.
Tabla XIX Valores de JAK-STAT EC50
7.2. Ensayo de señalización de OSM/IL-W
Se muestra que OSM e IL-1 p regulan de manera ascendente sinergísticamente los niveles de MMP13 en la línea celular de condrosarcoma humana SW1353. Las células se siembran en placas de 96 pocillos a 15.000 células/pocillo en un volumen de 120 pL de DMEM (Invitrogen) que contiene 10% (v/v) FBS y 1% penicilina/estreptomicina (InVitrogen) incubada a 37°C / 5% CO2. Las células se incuban previamente con 15 pl de compuesto en medio M199 con 2% DMSO 1 hr antes de activar con 15 pl OSM e IL-1 p para alcanzar 25 pg/ml de OSM and 1 pg/ml de IL-1 p, y los niveles de MMP13 se miden en medio acondicionado 48 h después de activar. La actividad de MMP13 se mide usando un ensayo de captura de anticuerpos. Para este fin, placas de 384 pocillos (NUNC, 460518, MaxiSorb negras) se recubren con 35 pl de 1,5 pg/ml solución de anticuerpo MMP13 anti-humano (R&D Systems, MAB511) durante 24 hrs a 4°C. Después de lavar los pocillos 2 veces con PBS 0,05% Tween, los sitios de unión remanentes se bloquean con 100 pL de leche descremada en polvo al 5% (Santa Cruz, sc-2325, Blotto) en PBS durante 24 hr a 4°C. Luego, los pocillos se lavan dos veces con PBS 0,05% Tween y 35 pL de dilución 1/10 de sobrenadante de cultivo que contiene MMP13 en tampón de bloqueo diluido 100 veces se añade y se incuba durante 4 hr a temperatura ambiente. A continuación los pocillos se lavan dos veces con PBS 0,05% Tween seguido de activación de MMP13 por la adición de 35 pl de una solución 1,5 mM de acetato 4-aminofenilmercúrico (APMA) (Sigma, A9563) e incubación a 37°C durante 1 hr. Los pocillos se lavan nuevamente con PBS 0,05% Tween y se añade 35 pl de sustrato MMP13 (Biomol, P-126, OmniMMP sustrato fluorogénico). Después de la incubación durante 24 hrs a 37°C la fluorescencia del sustrato convertido se mide en un lector Perkin Elmer Wallac EnVision 2102 Multilabel (excitación de longitud de onda: 320 nm, emisión de longitud de onda: 405 nm).
Porcentaje de inhibición = ((fluorescencia determinada en presencia de vehículo - fluorescencia determinada para la muestra con compuesto experimental presente) dividido por (fluorescencia determinada en presencia de vehículo -fluorescencia determinada para la muestra sin activación)) * 100.
Por ejemplo, cuando el Compuesto I se analiza en este ensayo, se mide un valor de EC50 de 2242,5 (± 1098,5) nM.
7.3. Ensayo de proliferación de PBL
Linfocitos de sangre periférica humana PBL) se estimulan con IL-2 y la proliferación se mide usando un ensayo de incorporación. Los PBL se estimulan primero durante 72 hrs con PHA para inducir el receptor de IL-2, luego se dejan en ayuno durante 24 hrs para detener la proliferación celular seguido de estimulación de IL-2 durante otras 72 hrs (incluyendo 24hr de marcado de BrdU). Las células se preincuban con compuestos de prueba 1 hora antes de la adición de IL-2. Las células se cultivan en RPMI 1640 que contiene 10% (v/v) FBS.
Ejemplo 8. Ensayos in vivo
8.1. Estudio de PK/PD
8.1.1. Estudio de biodisponibilidad en perros
8.1.1.1. Ajuste experimental
El objetivo de este experimento es comparar la PK en perros beagle macho sanos (3 perros por grupo) después de una sola administración oral de Compuesto I o como Compuesto I. HCL3H2O formulado como cápsulas de dos potencias diferentes (25 y 100 mg).
Los perros no se ponen en ayuno antes de la administración, y tienen libre acceso a agua. Cada día del tratamiento, se proporciona media ración de alimento después de la toma de muestra de sangre T0, 8 a 17 min antes del tratamiento, y la segunda media ración se administra inmediatamente después de la administración o 1h después del
tratamiento para el período 2. Un período de eliminación de 3 días se asegura entre tratamientos.
Compuesto I o Compuesto I. HCL3H2O se administra a una dosis diana de 10 mg/kg en cápsulas (indistintamente 4 x 25 mg, o 1 cápsula x 100 mg). La composición de la cápsula se describe a continuación en la Tabla XX.
Tabla XX Composición de las cápsulas de 25 y 100 mg
Las cápsulas se administran oralmente con agua (5-10 ml), para proporcionar buen tránsito esofágico. Cada animal se controla al menos una vez por día.
Se recolecta sangre de la vena yugular en tubos heparinizados de litio en el T0 (antes de la administración de comida) y luego a las 1 h, 2h, 4h, 6h, 8h, 10h, y 24h después del tratamiento.
Luego se obtiene el plasma de sangre por centrifugado (2500 g durante 10 min a 4°C), y se almacena a -20°C hasta el análisis.
8.1.1.2, Análisis de plasma
Las alícuotas representativas de plasma se diluyen con plasma de perro de control según la necesidad para asegurar que las concentraciones presentes están dentro del intervalo de la curva de calibración, y se extraen por precipitación de proteínas con 2 volúmenes de acetonitrilo acidificado (con 0,1% ácido fórmico) que contiene Compuesto I deuterado como estándar interno (a 150 gg/ml).
Después de mezclado en vórtice y centrifugado a 4°C, los sobrenadantes se diluyen con un volumen de 0,5 de agua grado HPLC en una placa midi-eppendorf de 96 pocillos. La placa se sella y se agita para asegurar la homogeneidad de la muestra antes del análisis. Las muestras se analizan para el Compuesto I por LC-MS/MS usando un espectrómetro de masa Waters TQS, contra una serie de estándares de calibración coincidentes y control de calidad. El procedimiento de Waters TQS tiene un intervalo de curva estándar de 1,00 gg/ml (límite inferior de cuantificación para muestras no diluidas), hasta un máximo de 4000 gg/ml para el Compuesto I.
El análisis de farmacocinética se realiza usando el software WinNonlin™ versión 5.3, usando concentraciones de animales individuales. El análisis no compartimental se aplica para determinar los parámetros de PK (Cmax, Tmax„ ABCü.iast, t1/2, etc...)
Las concentraciones por debajo del límite de detección se ajustan a cero para la estadística descriptiva y los cálculos de parámetros de PK.
Las dosis reales de Compuesto I administrado a cada perro se usan para normalización de la dosis de los parámetros de PK (Cmax y ABC). Los resultados se presentan en la Tabla a continuación y en la Figura 10.
Tabla XXI Resultados del estudio de biodisponibilidad en perros
El Compuesto I (como base libre) se toma por vía oral y por consiguiente pasa a través de la vía gástrica ácida que contiene HCl, en la que el Compuesto I.HCl debe formarse. La persona experta debe esperar, por consiguiente no ver diferencia entre las dos formas administradas.
Sin embargo, como se ilustra en la Figura 10, en promedio y en las 2 potencias de cápsula, el Compuesto I. HCI.3H2O se absorbe más rápidamente, y muestra exposición mejorada in vivo sobre el Compuesto I, lo que puede resultar en el régimen de administración inferior, y por consiguiente cumplimiento mejorado del paciente, y potencialmente menor toxicidad, o problemas de interacción medicamentosa.
Comentarios finales
Los expertos en la técnica apreciarán que las descripciones que anteceden son ejemplificativas y explicativas en su naturaleza, y pretenden ilustrar la invención y sus realizaciones preferidas. A través de experimentación de rutina, un experto reconocerá modificaciones y variaciones evidentes que pueden realizarse sin alejarse de la invención. Todas dichas modificaciones que entran dentro del alcance de las reivindicaciones anexas pretenden incluirse en ellas. De este modo, la invención tiene como finalidad definirse no por la descripción que antecede, sino por las siguientes realizaciones y sus equivalentes.
Se deberá comprender que factores tal como la capacidad diferencial de penetración celular de los varios compuestos puede contribuir a discrepancias entre la actividad de los compuestos en los ensayos celulares y bioquímicos in vitro.
Al menos algunos de los nombres químicos de la sal de la invención según se dan y se establecen en esta solicitud, pueden generase en una base automatizada por el uso de un programa de software de nomenclatura química disponible en el mercado, y no se han verificado independientemente. Los programas representativos que realizan esta función incluyen la herramienta de nomenclatura Lexichem vendida por Open Eye Software, Inc. y la herramienta Autonom Software comercializada por MDL, Inc. En la instancia en la que el nombre químico indicado y la estructura representada difieran, regirá la estructura representada.
Referencias
(CHMP), C. f. (18 November 2004). Guideline on Clinical Investigation of Medicinal Products indicated for the treatment of Psoriasis.
Berishaj, M., Gao, S. P., Ahmed, S., Leslie, K., Al-Ahmadie, H., Gerald, W. L., et al. (2007). Stat3 is tyrosinephosphorylated through the interleukin-6/glycoprotein 130/Janus kinase pathway in breast cancer. Breast Cancer Research, 9(3), 1-9.
Constantinescu, S. N., Girardot, M., & Pecquet, C. (2007). Mining for JAK-STAT mutations in cancer. Trends in Biochemical Sciences, 33(3), 122-131.
Dolgin, E. (2011). Companies hope for kinase inhibitor JAKpot. Nat Rev Drug Discov, 10(10), 717-8.
Greene, T W; Wuts, P G M;. (1991). Protecting Groups in Organic Synthesis, Second Edition. New York: Wiley. Hilfiker, R., Blatter, F., & von Raumer, M. (2006). Relevance of Solid-state Properties. In Polymorphism: in the Pharmaceutical Industry (pp. 1-20). Weinheim: WILEY-VCH Verlag GmbH & Co. KGaA.
Ingersoll, K. S., & Cohen, J. (2008). The impact of medication regimen factors on adherence to chronic. J Behav Med, 31(3), 213-224.
Kopf, M., Bachmann, M. F., & Marsland, B. J. (2010). Averting inflammation by targeting the cytokine environment. Nat Rev: Drug Disc, 9, 703-718.
Lipinski, C. A., Lombardo, F., Dominy, B. W., & Feeney, P. J. (2001). Experimental and computational approaches to estimate. Advanced Drug Delivery Reviews solubility andpermeability in drug discovery and development settings, 46, 3-26.
Menet, C. J. (2010). Patent No. WO2010/149769. PCT.
Mullighan, C. G. (2009). JAK mutations in high-risk childhood acute lymphoblastic leukemia. Proc. Natl. Acad. Sci., 106(23), 9414-9418.
Naka, T., Nishimoto, N., & Kishimoto, T. (2002). The paradigm of IL-6: from basic science to medicine. Arthritis Res, 4 (suppl 3), S233-S242.
O'Sullivan, L. A., Liongue, C., Lewis, R. S., Stephenson, S. E., & Ward, A. C. (2007). Cytokine receptor signaling through the Jak-Stat-Socs pathway in disease. Mol Immuno, 44(10), 2497-506.
O'Dell, J. R. (2004). Therapeutic Strategies for Rheumatoid Arthritis. N Engl J Med, 350, 2591-602.
Punwani, N., Scherle, P., Flores, R., Shi, J., Liang, J., Yeleswaram, S., et al. (2012). Preliminary clinical activity of a topical JAK1/2 inhibitor in the treatment of psoriasis. J Am Acad Dermatol, 67, 658- 64.
Smolen, J. S., & Steiner, G. (2003). Therapeutic strategies for rheumatoid arthritis. Nat Rev: Drug Disc, 2, 473-488. Tam, L., McGlynn, L. M., Traynor, P., Mukheijee, R., Bartlett, J. M., & Edwards, J. (2007). Expression levels of the JAK/STAT pathway in the transition from hormone-sensitive to hormone-refractory prostate cancer. British Journal of Cancer, 97, 378 - 383.
Vainchenker, W., Dusa, A., & Constantinescu, S. N. (2008). JAKs in pathology: Role of Janus kinases in hematopoietic malignancies and immunodeficiencies. Seminars in Cell & Developmental Biology, 19, 385-393.
Verstovsek, S. (2009). Therapeutic potential of JAK2 inhibitors. Hematology Am Soc Hematol Educ Program, 636-42. Xiang, Z., Zhao, Y., Mitaksov, V., Fremont, D. FL, Kasai, Y., Molitoris, A., et al. (2008). Identification of somatic JAK1 mutations in patients with acute myeloid leukemia. Blood, 111, 4809-4812.
Zenz, R., Eferl, R., Florin, L., Hummerich, L., Mehic, D., Scheuch, H., et al. (2005). Psoriasis-like skin disease and arthritis caused by inducible epidermal deletion of Jun proteins. Nature, 437(7057), 369-75.
Zhang, Q. (1996). Activation of JAK/STAT proteins involved in signal transduction pathway mediated by receptor for interleukin 2 in malignant T lymphocytes derived from cutaneous anaplastic large T-cell lymphoma and Sezary syndrome. Proc. Natl. Acad. Sci., 93, 9148-9153.
Zikherman, j., & Weiss, A. (2011). Unraveling the functional implications of GWAS: how T cell protein tyrosine phosphatase drives autoimmune disease. J Clin Invest, 121 (12), 4618-21.
Claims (5)
2. Una sal aceptable para uso farmacéutico o hidrato aceptable para uso farmacéutico de una sal de acuerdo con la reivindicación 1, en la que el hidrato de la sal está en forma cristalina.
3. Un hidrato aceptable para uso farmacéutico de una sal de acuerdo con la reivindicación 2,
en el que el hidrato Base Libre/HCl/H2O 1:1:3 de la sal se caracteriza al menos por un pico de difracción de rayos X en polvo en una cualquiera o más de las siguientes posiciones: 7,25, 8,31, 8,78, 10,69, 11,96, 12,25, 13,17, 13,74, 16,23, 16,71,19,26, 19,64, 20,15, 20,57, 20,95, 21,38, 21,69, 22,77, 23,37, 25,14, 25,71, 25,89, 27,66, 28,57, 28,81, 29,17, 29,58, 30,63, 30,94, 32,06, 32,63, 34,14, 36,22, 36,67 y 37,12° 20 ± 0,2° 20.
4. Un hidrato aceptable para uso farmacéutico de una sal de acuerdo con la reivindicación 2, en el que el hidrato Base Libre/HCl/H2O 1:1:3 de la sal se caracteriza por los siguientes parámetros de difracción:
5. Un procedimiento de preparación de un aducto [Compuesto de acuerdo con la Fórmula I:HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) mezclar el compuesto de Fórmula I suspendido en DCM, con MeOH a 35°C,
ii) añadir agua bajo agitación a 35°C durante al menos 15 min,
iii) separar la fase orgánica,
iv) añadir una solución p/p al 10% de HCl en MeOH a la fase orgánica obtenida en la etapa previa iii), v) separar el sólido resultante por filtración obtenida en la etapa previa iv),
vi) secar dicho sólido resultante obtenido en la etapa previa v),
vii) añadir el sólido obtenido en la etapa previa vi) a una solución 1,6/0,4 de ácido fórmico/agua, bajo agitación a 55°C,
viii) añadir agua a la solución obtenida en la etapa previa vii),
ix) separar por filtración el sólido resultante obtenido en la etapa previa viii), y
secar el sólido resultante obtenido en la etapa previa ix).
5. Un procedimiento de preparación de un aducto [Compuesto de acuerdo con la Fórmula I:HCl:3H2O] en una forma sólida cristalina que comprende las etapas de:
i) mezclar el compuesto de Fórmula I suspendido en DCM, con MeOH a 35°C,
ii) añadir agua bajo agitación a 35°C durante al menos 15 min,
iii) separar la fase orgánica,
iv) añadir una solución p/p al 10% de HCl en MeOH a la fase orgánica obtenida en la etapa previa iii), v) separar el sólido resultante por filtración obtenida en la etapa previa iv),
vi) secar dicho sólido resultante obtenido en la etapa previa v),
vii) añadir el sólido obtenido en la etapa previa vi) a una solución 1,6/0,4 de ácido fórmico/agua, bajo agitación a 55°C,
viii) añadir agua a la solución obtenida en la etapa previa vii),
ix) separar por filtración el sólido resultante obtenido en la etapa previa viii), y
secar el sólido resultante obtenido en la etapa previa ix).
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB1402071.3A GB201402071D0 (en) | 2014-02-07 | 2014-02-07 | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| PCT/EP2015/052242 WO2015117981A1 (en) | 2014-02-07 | 2015-02-04 | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2853375T3 true ES2853375T3 (es) | 2021-09-15 |
Family
ID=50390572
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15704974T Active ES2853375T3 (es) | 2014-02-07 | 2015-02-04 | Sales novedosas y composiciones farmacéuticas de las mismas para el tratamiento de trastornos inflamatorios |
Country Status (28)
| Country | Link |
|---|---|
| US (7) | US9382247B2 (es) |
| EP (2) | EP3842432A1 (es) |
| JP (2) | JP2017505329A (es) |
| KR (1) | KR102478614B1 (es) |
| CN (2) | CN105960407A (es) |
| AR (1) | AR099307A1 (es) |
| AU (4) | AU2015215045B2 (es) |
| CA (1) | CA2938219C (es) |
| CY (1) | CY1124349T1 (es) |
| DK (1) | DK3102575T3 (es) |
| EA (2) | EA201990330A1 (es) |
| ES (1) | ES2853375T3 (es) |
| GB (1) | GB201402071D0 (es) |
| HR (1) | HRP20210194T1 (es) |
| HU (1) | HUE053309T2 (es) |
| IL (1) | IL246833B (es) |
| LT (1) | LT3102575T (es) |
| MX (2) | MX395415B (es) |
| NZ (1) | NZ722603A (es) |
| PL (1) | PL3102575T3 (es) |
| PT (1) | PT3102575T (es) |
| RS (1) | RS61450B1 (es) |
| SG (2) | SG10202013187PA (es) |
| SI (1) | SI3102575T1 (es) |
| SM (1) | SMT202100060T1 (es) |
| TW (2) | TWI767878B (es) |
| UY (1) | UY35984A (es) |
| WO (1) | WO2015117981A1 (es) |
Families Citing this family (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI462920B (zh) | 2009-06-26 | 2014-12-01 | 葛萊伯格有限公司 | 用於治療退化性及發炎疾病之新穎化合物 |
| GB201402071D0 (en) | 2014-02-07 | 2014-03-26 | Galapagos Nv | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| GB201402070D0 (en) * | 2014-02-07 | 2014-03-26 | Galapagos Nv | Pharmaceutical compositions for the treatment of inflammatory disorders |
| CA2982630A1 (en) * | 2015-04-13 | 2016-10-20 | Galapagos Nv | Methods for the treatment of inflammatory disorders |
| RS64677B1 (sr) * | 2015-04-13 | 2023-11-30 | Galapagos Nv | Metode lečenja kardiovaskularnih poremećaja |
| AU2016278040B2 (en) | 2015-06-16 | 2019-07-04 | Nanophagix LLC | Drug delivery and imaging chemical conjugate, formulations and methods of use thereof |
| CN105198880B (zh) * | 2015-09-18 | 2017-07-25 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物a晶型及其制备方法 |
| CN105198876B (zh) * | 2015-09-18 | 2017-09-29 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物h晶型及其制备方法 |
| CN105111206B (zh) * | 2015-09-18 | 2017-07-25 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物e晶型及其制备方法 |
| CN105218539B (zh) * | 2015-09-18 | 2017-07-25 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物b晶型及其制备方法 |
| CN105198879B (zh) * | 2015-09-18 | 2017-09-22 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物c晶型及其制备方法 |
| CN105198878B (zh) * | 2015-09-18 | 2017-07-25 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物f晶型及其制备方法 |
| CN105198877B (zh) * | 2015-09-18 | 2017-09-22 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物g晶型及其制备方法 |
| CN105111207B (zh) * | 2015-09-18 | 2017-07-25 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物d晶型及其制备方法 |
| WO2017106568A1 (en) | 2015-12-17 | 2017-06-22 | Gilead Sciences, Inc. | Combination of a jak inhibitor and a bromodomain inhibitor for treating cancer |
| US20170173034A1 (en) | 2015-12-17 | 2017-06-22 | Gilead Sciences, Inc. | Combination of a jak inhibitor and a syk inhibitor for treating cancers and inflammatory disorders |
| US20170174788A1 (en) | 2015-12-17 | 2017-06-22 | Gilead Sciences, Inc. | Combination of a jak inhibitor and an mmp9 binding protein for treating inflammatory disorders |
| CN105669669A (zh) * | 2016-03-04 | 2016-06-15 | 上海宣创生物科技有限公司 | 一种环丙烷甲酰胺衍生物的a晶型、b晶型、d晶型、g晶型和m晶型及其制备方法 |
| EP3434675A4 (en) * | 2016-03-21 | 2019-03-06 | Crystal Pharmatech Co., Ltd | HYDROCHLORIDE SALT CREAM OF A MEDICAMENT FOR TREATING OR PREVENTING JAC-ASSOCIATED DISEASES AND METHOD OF PRODUCTION THEREOF |
| CN109476662A (zh) * | 2016-08-03 | 2019-03-15 | 苏州科睿思制药有限公司 | 一种jak1选择性抑制剂的新晶型及其制备方法和用途 |
| JP2019534304A (ja) | 2016-11-10 | 2019-11-28 | ガラパゴス・ナムローゼ・フェンノートシャップGalapagos N.V. | 炎症性疾患の治療のための化合物及びその医薬組成物 |
| GB201702603D0 (en) | 2017-02-17 | 2017-04-05 | Galápagos Nv | Novel compositions and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| PL3595667T3 (pl) * | 2017-03-14 | 2024-03-18 | Galapagos Nv | Kompozycje farmaceutyczne zawierające inhibitor jak |
| GB201808575D0 (en) | 2018-05-24 | 2018-07-11 | Galapagos Nv | Methods for the treatment of psoriatic arthrits |
| US10815227B2 (en) | 2018-08-27 | 2020-10-27 | Cadila Healthcare Limited | Processes for the preparation of filgotinib |
| WO2020092245A1 (en) * | 2018-10-29 | 2020-05-07 | Zorday IP, LLC | Network-enabled electronic cigarette |
| WO2020177705A1 (zh) * | 2019-03-05 | 2020-09-10 | 苏州科睿思制药有限公司 | Filgotinib的马来酸盐晶型CSI及其制备方法和用途 |
| EA202192389A1 (ru) * | 2019-03-30 | 2022-01-21 | Юникем Лабораторис Лимитед | Новый способ получения филготиниба и его промежуточных соединений |
| WO2021044327A1 (en) * | 2019-09-03 | 2021-03-11 | Dr. Reddy's Laboratories Limited | Solid forms of filgotinib maleate and processes thereof |
| CN114075188A (zh) * | 2020-08-11 | 2022-02-22 | 南京柯菲平盛辉制药有限公司 | 芳香杂环酰胺类化合物及其制备方法和医药用途 |
| EP4259150A4 (en) * | 2020-12-09 | 2024-12-25 | Servatus Ltd | COMBINATION THERAPY FOR INFLAMMATORY JOINT DISEASES |
| CN113773322B (zh) * | 2021-11-10 | 2022-02-11 | 奥锐特药业(天津)有限公司 | 一种Filgotinib的制备方法 |
| WO2026027676A1 (en) | 2024-07-31 | 2026-02-05 | Alfasigma S.P.A. | Biomarkers for determining treatment of ulcerative colitis with filgotinib |
| WO2026027669A1 (en) | 2024-07-31 | 2026-02-05 | Alfasigma S.P.A. | Biomarkers for determining treatment of ulcerative colitis with filgotinib |
Family Cites Families (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2549632B2 (ja) * | 1986-08-20 | 1996-10-30 | 三井石油化学工業株式会社 | オレフインの重合方法 |
| WO2000044722A1 (en) | 1999-01-29 | 2000-08-03 | Chugai Seiyaku Kabushiki Kaisha | Chondrongenesis promotors and indolin-2-one derivatives |
| US20040138285A1 (en) | 2001-04-27 | 2004-07-15 | Makoto Okazaki | Chondrogenesis promoters |
| US6514989B1 (en) | 2001-07-20 | 2003-02-04 | Hoffmann-La Roche Inc. | Aromatic and heteroaromatic substituted 1,2,4-triazolo pyridine derivatives |
| JPWO2004039816A1 (ja) * | 2002-10-29 | 2006-03-02 | 塩野義製薬株式会社 | セフェム化合物の無機酸塩の結晶 |
| CA2515190A1 (en) | 2003-02-14 | 2004-08-26 | Pfizer Products Inc. | Triazolo-pyridines as anti-inflammatory compounds |
| US20050222171A1 (en) | 2004-01-22 | 2005-10-06 | Guido Bold | Organic compounds |
| US20070004658A1 (en) | 2004-06-21 | 2007-01-04 | Nick Vandeghinste | Method and means for treatment of osteoarthritis |
| EP1786811A2 (en) | 2004-08-18 | 2007-05-23 | Pharmacia & Upjohn Company LLC | Triazolopyridine compounds |
| WO2006038116A2 (en) | 2004-10-07 | 2006-04-13 | Warner-Lambert Company Llc | Triazolopyridine derivatives as antibacterial agents |
| GB0515026D0 (en) | 2005-07-21 | 2005-08-31 | Novartis Ag | Organic compounds |
| JP5336375B2 (ja) | 2006-08-30 | 2013-11-06 | セルゾーム リミテッド | キナーゼ阻害剤としてのトリアゾール誘導体 |
| CL2008001626A1 (es) | 2007-06-05 | 2009-06-05 | Takeda Pharmaceuticals Co | Compuestos derivados de heterociclos fusionados, agente farmaceutico que los comprende y su uso en la profilaxis y tratamiento del cancer. |
| US8053574B2 (en) | 2007-07-18 | 2011-11-08 | Novartis Ag | Organic compounds |
| WO2009017954A1 (en) | 2007-08-01 | 2009-02-05 | Phenomix Corporation | Inhibitors of jak2 kinase |
| CA2691448A1 (en) | 2007-08-31 | 2009-03-05 | Dominique Swinnen | Triazolopyridine compounds and their use as ask inhibitors |
| GB0719803D0 (en) | 2007-10-10 | 2007-11-21 | Cancer Rec Tech Ltd | Therapeutic compounds and their use |
| BRPI0909945A2 (pt) | 2008-06-20 | 2015-07-28 | Genentech Inc | "composto, composição farmacêutica, método para tratar ou atenuar a gravidade de uma doença ou condição responsiva à inibição da atividade jak2 quinase em um paciente, kit para o tratamento de uma doença ou distúrbio responsivo à inibição da jak quinase" |
| WO2010010184A1 (en) | 2008-07-25 | 2010-01-28 | Galapagos Nv | [1, 2, 4] triazolo [1, 5-a] pyridines as jak inhibitors |
| WO2010010186A1 (en) | 2008-07-25 | 2010-01-28 | Galapagos Nv | Novel compounds useful for the treatment of degenerative and inflammatory diseases |
| WO2010010188A1 (en) | 2008-07-25 | 2010-01-28 | Galapagos Nv | Novel compounds useful for the treatment of degenerative and inflammatory diseases. |
| JO3041B1 (ar) * | 2008-07-25 | 2016-09-05 | Galapagos Nv | مركبات جديدة مفيدة لمعالجة الأمراض التنكسية والالتهابية |
| WO2010010189A1 (en) | 2008-07-25 | 2010-01-28 | Galapagos Nv | Novel compounds useful for the treatment of degenerative and inflammatory diseases |
| WO2010010187A1 (en) | 2008-07-25 | 2010-01-28 | Galapagos Nv | Novel compounds useful for the treatment of degenerative and inflammatory diseases |
| WO2010013768A1 (ja) * | 2008-07-31 | 2010-02-04 | 第一三共株式会社 | チアゾリジンジオン化合物の結晶及びその製造方法 |
| CN102459258B (zh) | 2009-06-05 | 2015-11-25 | 赛福伦公司 | 1,2,4-三唑并[1,5a]吡啶衍生物的制备和用途 |
| TWI462920B (zh) | 2009-06-26 | 2014-12-01 | 葛萊伯格有限公司 | 用於治療退化性及發炎疾病之新穎化合物 |
| JO3030B1 (ar) | 2009-06-26 | 2016-09-05 | Galapagos Nv | مركب جديد مفيد لمعالجة الامراض التنكسية والالتهابات |
| JPWO2011036895A1 (ja) | 2009-09-25 | 2013-02-14 | 杏林製薬株式会社 | マレイン酸塩およびその結晶 |
| CN102146082A (zh) | 2010-02-04 | 2011-08-10 | 江苏恒瑞医药股份有限公司 | 吡咯并n杂环类衍生物的可药用的盐、其制备方法及其在医药上的应用 |
| JP2013049632A (ja) * | 2011-08-30 | 2013-03-14 | Kowa Co | ベンゾチアジン化合物のモノマレイン酸塩を有効成分とするアレルギー疾患の予防及び/又は治療剤 |
| SA112330992B1 (ar) * | 2011-11-10 | 2015-09-13 | كيورين فارماسوتيكال كو.، ليمتد | صورة متبلرة من 7-{(s4، s3)-3-[(سيكلو بروبيل أمينو) ميثيل]-4-فلورو بيروليدين-1-يل}-6-فلورو-1-(2-فلورو إيثيل)- 8-ميثوكسي-4-أوكسو-1، 4-داي هيدرو كينولين-3- حمض كربوكسيلي |
| US20130310340A1 (en) | 2012-05-16 | 2013-11-21 | Rigel Pharmaceuticals, Inc. | Method of treating muscular degradation |
| AU2013279597B2 (en) | 2012-06-22 | 2017-04-20 | Alfasigma S.P.A. | Aminotriazolopyridine for use in the treatment of inflammation, and pharmaceutical compositions thereof |
| GB201402070D0 (en) | 2014-02-07 | 2014-03-26 | Galapagos Nv | Pharmaceutical compositions for the treatment of inflammatory disorders |
| GB201402071D0 (en) | 2014-02-07 | 2014-03-26 | Galapagos Nv | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| CA2982630A1 (en) | 2015-04-13 | 2016-10-20 | Galapagos Nv | Methods for the treatment of inflammatory disorders |
| RS64677B1 (sr) | 2015-04-13 | 2023-11-30 | Galapagos Nv | Metode lečenja kardiovaskularnih poremećaja |
| US20170173034A1 (en) | 2015-12-17 | 2017-06-22 | Gilead Sciences, Inc. | Combination of a jak inhibitor and a syk inhibitor for treating cancers and inflammatory disorders |
| PL3595667T3 (pl) | 2017-03-14 | 2024-03-18 | Galapagos Nv | Kompozycje farmaceutyczne zawierające inhibitor jak |
| GB201808575D0 (en) | 2018-05-24 | 2018-07-11 | Galapagos Nv | Methods for the treatment of psoriatic arthrits |
-
2014
- 2014-02-07 GB GBGB1402071.3A patent/GB201402071D0/en not_active Ceased
-
2015
- 2015-02-04 EP EP20211405.4A patent/EP3842432A1/en not_active Withdrawn
- 2015-02-04 JP JP2016550633A patent/JP2017505329A/ja active Pending
- 2015-02-04 IL IL246833A patent/IL246833B/en unknown
- 2015-02-04 AU AU2015215045A patent/AU2015215045B2/en active Active
- 2015-02-04 RS RS20210134A patent/RS61450B1/sr unknown
- 2015-02-04 CN CN201580006893.3A patent/CN105960407A/zh active Pending
- 2015-02-04 PT PT157049743T patent/PT3102575T/pt unknown
- 2015-02-04 SG SG10202013187PA patent/SG10202013187PA/en unknown
- 2015-02-04 EA EA201990330A patent/EA201990330A1/ru unknown
- 2015-02-04 SI SI201531491T patent/SI3102575T1/sl unknown
- 2015-02-04 WO PCT/EP2015/052242 patent/WO2015117981A1/en not_active Ceased
- 2015-02-04 SM SM20210060T patent/SMT202100060T1/it unknown
- 2015-02-04 MX MX2020003368A patent/MX395415B/es unknown
- 2015-02-04 SG SG11201606433PA patent/SG11201606433PA/en unknown
- 2015-02-04 HU HUE15704974A patent/HUE053309T2/hu unknown
- 2015-02-04 CA CA2938219A patent/CA2938219C/en active Active
- 2015-02-04 EA EA201691584A patent/EA032596B1/ru unknown
- 2015-02-04 LT LTEP15704974.3T patent/LT3102575T/lt unknown
- 2015-02-04 PL PL15704974T patent/PL3102575T3/pl unknown
- 2015-02-04 DK DK15704974.3T patent/DK3102575T3/da active
- 2015-02-04 EP EP15704974.3A patent/EP3102575B1/en active Active
- 2015-02-04 US US14/614,396 patent/US9382247B2/en active Active
- 2015-02-04 MX MX2016010068A patent/MX376000B/es active IP Right Grant
- 2015-02-04 CN CN202010324636.7A patent/CN111499630A/zh active Pending
- 2015-02-04 KR KR1020167023807A patent/KR102478614B1/ko active Active
- 2015-02-04 ES ES15704974T patent/ES2853375T3/es active Active
- 2015-02-04 HR HRP20210194TT patent/HRP20210194T1/hr unknown
- 2015-02-04 NZ NZ722603A patent/NZ722603A/en unknown
- 2015-02-06 UY UY0001035984A patent/UY35984A/es not_active Application Discontinuation
- 2015-02-06 AR ARP150100351A patent/AR099307A1/es unknown
- 2015-02-06 TW TW104104160A patent/TWI767878B/zh active
- 2015-02-06 TW TW110136599A patent/TWI792593B/zh active
-
2016
- 2016-07-01 US US15/200,228 patent/US20160376269A1/en not_active Abandoned
-
2017
- 2017-07-10 US US15/645,308 patent/US10708263B2/en active Active
-
2019
- 2019-04-08 AU AU2019202441A patent/AU2019202441B2/en active Active
- 2019-09-30 US US16/588,207 patent/US10919890B2/en active Active
-
2020
- 2020-01-28 JP JP2020011555A patent/JP2020097595A/ja active Pending
- 2020-10-26 AU AU2020260391A patent/AU2020260391B2/en active Active
-
2021
- 2021-01-08 US US17/144,788 patent/US11667633B2/en active Active
- 2021-02-01 CY CY20211100080T patent/CY1124349T1/el unknown
-
2022
- 2022-09-23 AU AU2022235624A patent/AU2022235624B2/en active Active
-
2023
- 2023-04-25 US US18/306,867 patent/US12234235B2/en active Active
-
2025
- 2025-01-22 US US19/033,986 patent/US20250289816A1/en active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2853375T3 (es) | Sales novedosas y composiciones farmacéuticas de las mismas para el tratamiento de trastornos inflamatorios | |
| ES2788671T3 (es) | Composiciones farmacéuticas para el tratamiento de afecciones inflamatorias | |
| JP2014221825A (ja) | JAK阻害剤としての5−フェニル−[1,2,4]トリアゾロ[1,5−a]ピリジン−2−イルカルボキサミド | |
| PT2346864E (pt) | Novos compostos úteis para o tratamento de doenças degenerativas e inflamatórias | |
| CN112851682B (zh) | 一种取代的吡啶酰胺类化合物及其应用 | |
| ES2693019T3 (es) | Derivados de bencimidazol y composiciones farmacéuticas de los mismos para el tratamiento de enfermedades inflamatorias | |
| HK1231859B (en) | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders | |
| HK1231859A1 (en) | Novel salts and pharmaceutical compositions thereof for the treatment of inflammatory disorders | |
| EA041895B1 (ru) | Новые соли и их фармацевтические композиции для лечения воспалительных заболеваний |