ES2872531T3 - Composición farmacéutica que comprende Atomoxetina y método para su preparación - Google Patents
Composición farmacéutica que comprende Atomoxetina y método para su preparación Download PDFInfo
- Publication number
- ES2872531T3 ES2872531T3 ES16728613T ES16728613T ES2872531T3 ES 2872531 T3 ES2872531 T3 ES 2872531T3 ES 16728613 T ES16728613 T ES 16728613T ES 16728613 T ES16728613 T ES 16728613T ES 2872531 T3 ES2872531 T3 ES 2872531T3
- Authority
- ES
- Spain
- Prior art keywords
- atomoxetine
- pharmaceutical composition
- pharmaceutically acceptable
- silicon dioxide
- composition according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/485—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/135—Amines having aromatic rings, e.g. ketamine, nortriptyline
- A61K31/138—Aryloxyalkylamines, e.g. propranolol, tamoxifen, phenoxybenzamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1611—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4808—Preparations in capsules, e.g. of gelatin, of chocolate characterised by the form of the capsule or the structure of the filling; Capsules containing small tablets; Capsules with outer layer for immediate drug release
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Una composición farmacéutica en forma de cápsula de gelatina dura para administración oral que comprende Atomoxetina o una de sus sales o polimorfos farmacéuticamente aceptables como principio activo y una cantidad de 2% a 4% p/p de dióxido de silicio que actúa como agente de suspensión, en donde la cápsula de gelatina dura no contiene SLS.
Description
DESCRIPCIÓN
Composición farmacéutica que comprende Atomoxetina y método para su preparación
Campo técnico de la invención
La presente invención se refiere a una formulación farmacéutica estable para administración oral que contiene una cantidad terapéuticamente eficaz de Atomoxetina o de su sal o polimorfo y a un método para la preparación.
Antecedentes de la invención
La Atomoxetina (nombre comercial: Strattera) es un inhibidor de la reabsorción de noradrenalina aprobado para el tratamiento del trastorno por hiperactividad con déficit de atención (THDA). Clasificado como inhibidor de la reabsorción de noradrenalina (noradrenalina), la Atomoxetina está aprobada para su uso en niños, adolescentes y adultos. Sin embargo, no se ha estudiado su eficacia en niños menores de seis años. Su principal ventaja sobre los tratamientos estimulantes habituales para el THDA es que no es posible la adicción. Los efectos terapéuticos iniciales de la Atomoxetina suelen tardar de 2 a 4 semanas en manifestarse. Pueden ser necesarias de 2 a 4 semanas más para que se vean los efectos terapéuticos completos. Su eficacia puede ser menor que la de los medicamentos estimulantes. A diferencia de los agonistas de los adrenorreceptores a2 como la guanfacina y la clonidina, el uso de Atomoxetina se puede interrumpir bruscamente sin que se observen efectos de abstinencia significativos.
La Atomoxetina no es un psicoestimulante ni un derivado de la anfetamina. En un estudio aleatorio, con doble anonimato, controlado con placebo, con posible adicción en adultos que comparó los efectos de la Atomoxetina y el placebo, la Atomoxetina no se asoció con un patrón de respuesta que sugiriera propiedades estimulantes o euforizantes.
La farmacocinética de la Atomoxetina en niños y adolescentes es similar a la de los adultos. La Atomoxetina se absorbe rápida y casi completamente después de la administración oral, alcanzando la concentración plasmática máxima media observada (Cmax) aproximadamente 1 a 2 horas después de la administración. La biodisponibilidad absoluta de la Atomoxetina después de la administración oral osciló entre el 63% y el 94%, dependiendo de las diferencias interindividuales en el modesto metabolismo de primer paso. La Atomoxetina se puede administrar con o sin alimentos. La Atomoxetina se distribuye ampliamente y se une extensamente (98%) a las proteínas plasmáticas, principalmente a la albúmina.
En los adultos, se debe confirmar la presencia de síntomas de THDA que existían previamente en la infancia. Es deseable la corroboración de terceros y STRATTERA no debe iniciarse cuando la verificación de los síntomas del THDA infantil es incierta. El diagnóstico no se puede hacer únicamente por la presencia de uno o más síntomas de THDA. Según el criterio clínico, los pacientes deben tener un THDA de gravedad al menos moderada, como el indicado por un deterioro funcional al menos moderado en 2 o más entornos (por ejemplo, funcionamiento social, académico y/o ocupacional), que afecte varios aspectos de la vida de un individuo.
Se han descrito casos de comportamiento relacionado con el suicidio (intentos de suicidio e ideas suicidas) en pacientes tratados con Atomoxetina. En los ensayos clínicos dobles a ciegas, los comportamientos relacionados con el suicidio fueron poco frecuentes, pero se observaron con mayor frecuencia entre los niños y adolescentes tratados con Atomoxetina en comparación con los tratados con placebo, donde no hubo episodios. En los ensayos clínicos dobles a ciegas con adultos no hubo diferencia en la frecuencia de comportamiento relacionado con el suicidio entre Atomoxetina y placebo. En los pacientes que están en tratamiento del THDA debe supervisarse minuciosamente la aparición o el empeoramiento de un comportamiento suicida.
La Atomoxetina pertenece a la categoría terapéutica de antidepresivos y es un polvo blanco o casi blanco. Es soluble en agua en todas las proporciones, soluble en etanol anhidro y prácticamente insoluble en heptano. La sal Atomoxetina HCl se designa químicamente hidrocloruro de (3, R)-N-metil-3-(2-metilfenoxi)-3-fenilpropan-1 -amina.
Se ha administrado en forma de cápsula de gelatina dura de tamaño, aspecto, peso de llenado y carga de fármaco variables, desde 10 mg hasta 100 mg en monodosis.
La patente EP 1379 492 B1 describe formulaciones de Atomoxetina en forma de cápsulas duras que comprenden almidón y un lubricante de aceite de silicona.
Se han descrito otros intentos como en las patentes EP 1 715 856 B1 y EP 1 758 557 B1 para formulaciones farmacéuticas alternativas de Atomoxetina que tienen unas características de liberación, un mecanismo de liberación del fármaco y un proceso de fabricación diferentes.
Aunque cada una de las patentes anteriores representa composiciones farmacéuticas adecuadas para administrar Atomoxetina, todavía hay necesidad de composiciones farmacéuticas estables alternativas.
Compendio de la invención
Por lo tanto, un objeto de la presente invención consiste en proporcionar una formulación farmacéutica sólida estable alternativa para administración oral que contenga Atomoxetina o una sal o polimorfo farmacéuticamente aceptable de la misma, como principio activo.
Un objeto principal de la presente invención es proporcionar una formulación farmacéutica sólida oral que comprende Atomoxetina, que puede formularse en formas farmacéuticas de diferentes concentraciones ajustando proporcionalmente las cantidades de los excipientes farmacéuticamente aceptables, así como el compuesto farmacéuticamente activo. Las formas farmacéuticas de la presente invención se caracterizan por una linealidad farmacotécnica, sin tener ningún efecto sobre las características de disolución y biodisponibilidad de dicho fármaco.
Un planteamiento adicional de la presente invención es proporcionar un método para la preparación de dichas formas farmacéuticas para administración oral que contengan Atomoxetina que sea fácil de fabricar, de manera rápida y económica.
De acuerdo con los objetos anteriores de la presente invención, se proporciona una composición farmacéutica de liberación inmediata para administración oral que comprende Atomoxetina o una de sus sales o polimorfos farmacéuticamente aceptables como principio activo y una cantidad eficaz de un agente de suspensión farmacéuticamente aceptable.
Otros objetos y ventajas de la presente invención resultarán evidentes para los expertos en la técnica a la vista de la siguiente descripción detallada.
Descripción detallada de la invención
Para los propósitos de la presente invención, una composición farmacéutica que comprende un principio activo farmacéutico se considera "estable" si dicho principio se degrada menos o más lentamente que por sí solo y/o en composiciones farmacéuticas conocidas.
Es bien sabido que durante el desarrollo de cualquier forma farmacéutica, las impurezas deben mantenerse en límites muy bajos, ya que dichas impurezas pueden ser tóxicas y dañinas para los seres humanos. Además, las impurezas disminuyen la potencia de las composiciones farmacéuticas durante el almacenamiento. También pueden actuar como catalizadores o intermediarios en reacciones químicas y cambiar el fármaco a otra forma. Por lo tanto, hay necesidad de desarrollar una formulación que sea estable y no favorezca la degradación del principio farmacéutico activo.
Un parámetro muy importante para la industria farmacéutica es el logro de la linealidad entre la concentración y el peso de la forma farmacéutica. La presente invención proporciona formas farmacéuticas sólidas que presentan linealidad entre la concentración de la formulación del fármaco y la masa total de la formulación, mediante el aumento proporcional de las cantidades del fármaco y los excipientes en la formulación. Dicho planteamiento proporciona la capacidad de realizar un estudio de bioequivalencia a una sola concentración y extrapolar los resultados a otras concentraciones de la forma farmacéutica, proporcionando así una solución mucho más económica.
Otra realización de la presente invención es el uso de un proceso rentable para la preparación de formas farmacéuticas sólidas. Se eligieron cápsulas de gelatina dura como forma farmacéutica en la presente invención. Las cápsulas de gelatina dura se utilizan ampliamente porque a) la deglución es muy fácil, b) las carcasas no tienen sabor y pueden administrarse medicamentos que no tienen sabor y olor agradables, c) se pueden fabricar en diferentes colores y d) el medicamento se liberará fácilmente ya que no hay compactación. Por lo general, no se utilizan para los compuestos que son muy solubles porque el fármaco se liberará de una vez. Cuando se toma una decisión al final de la fase II en una línea de producción, cuya forma farmacéutica se desarrollará para el mercado, generalmente se asumen altos costos de producción de los productos en cápsulas de gelatina dura. Esta suposición es válida si los costos de producción se limitan a la comparación de los costos del excipiente únicamente. Cuando se tienen en cuenta los costos totales de fabricación, que incluyen los costos ocultos provenientes del equipo de proceso, el espacio GMP requerido, el tiempo total de producción, los controles en proceso, el trabajo analítico, de limpieza y de validación, la comparación resulta normalmente a favor de la formulación de la cápsula.
En la presente invención motivada por la tendencia del mercado a proporcionar formas farmacéuticas que comprenden excipientes naturales, se decidió utilizar cápsulas de gelatina dura sin SLS a diferencia de las utilizadas para el producto que ya se encuentra en el mercado. Sorprendentemente, se encontró que la cubierta de la cápsula tiene un impacto sobre las características de disolución de la forma farmacéutica específica.
El producto comercializado utiliza una gran cantidad de almidón pregelatinizado. Dicho excipiente es conocido por sus propiedades de hinchamiento. Esta propiedad en relación con la cantidad utilizada atrapa el principio activo en la capa de gel que se forma, por lo que provoca un retraso en la liberación. Para el producto comercializado esto se soluciona con el tipo de cubierta de cápsula. En la presente invención, el uso de cápsulas sin SLS, para lograr las características deseadas, hizo necesario el uso de un agente de suspensión.
Se probaron varios agentes de suspensión, como lactosa, almidón glicolato de sodio, croscarmelosa de sodio, lauril sulfato de sodio y varios tipos de dióxido de silicio.
El dióxido de silicio coloidal (Aerosil) tiene un uso bien conocido en la industria farmacéutica como fluidificantes en composiciones. Sin embargo, en la presente invención se demostró que funciona como un agente de suspensión que ayuda a que el principio farmacéuticamente activo no quede atrapado dentro del gel formado por el almidón pregelatinizado. Se añadió en una cantidad de menos del 5% p/p, preferiblemente del 4% p/p o menos y más preferiblemente del 2% p/p o menos.
De igual manera, se encontró que el material Syloid® 244 FP era funcional para la presente invención. Es una sílice amorfa sintética que aparece como un polvo blanco suelto. Cumple con los requisitos de prueba para el dióxido de silicio como se describe en la última edición de la Farmacopea de los Estados Unidos/Formulario Nacional (USP/NF), para la sílice, tipo dental como se describe en la última edición de la Farmacopea Europea (EP), y para los dióxidos de silicio como se describe en la última edición de Japanese Pharmaceutical Excipients. Es un gel de sílice de alto volumen de poros con una gran superficie interna. Tiene una fuerte afinidad por la humedad y los líquidos orgánicos. La sílice Syloid® 244 FP puede adsorber hasta 1,6 ml de líquido por gramo y se recomienda especialmente como fluidificante, auxiliar de formación de comprimidos y vehículo para productos farmacéuticos y de cuidado personal.
Además, las composiciones farmacéuticas de la presente invención también pueden contener uno o más excipientes de formulación adicionales tales como diluyentes, disgregadores, aglutinantes, lubricantes, fluidificantes y agentes aromatizantes, siempre que sean compatibles con el principio activo de la composición, de modo que no interfieran con él en la composición y para aumentar la estabilidad del fármaco y la vida útil del producto farmacéutico.
Los diluyentes pueden ser, por ejemplo, celulosa microcristalina, dextratos, dextrosa, fructosa, manitol, sorbitol, sacarosa, xilitol, maltosa, maltodextrina, maltitol.
Los disgregadores pueden seleccionarse de ácido algínico, dióxido de carbono, goma guar, metilcelulosa, polacrilina potásica, poloxámero, alginato de sodio.
Los aglutinantes pueden ser, por ejemplo, ácido algínico, carbómero, etilcelulosa, gelatina, glucosa líquida, goma guar, hidroxietilcelulosa, metilcelulosa, polidextrosa, óxido de polietileno.
Además, se incorpora al menos un lubricante en la formulación. Los lubricantes pueden ser, por ejemplo, talco, estearato de magnesio, estearato de calcio, behenato de glicerilo, aceite de ricino hidrogenado, ácido esteárico, dimeticona.
Se utilizan fluidificantes para favorecer la fluidez del polvo al reducir la fricción y la cohesión entre partículas. Estos se utilizan en combinación con lubricantes ya que no tienen la capacidad de reducir la fricción de la pared del molde. Los fluidificantes pueden ser, por ejemplo, dimeticona, silicato cálcico, fosfato cálcico tribásico.
Se utilizan agentes aromatizantes para enmascarar posibles principios activos de sabor desagradable y mejorar la probabilidad de que el paciente complete un ciclo de medicación. Dichos agentes son particularmente útiles en el caso de comprimidos bucodispersables, masticables y sublinguales. Los agentes aromatizantes pueden ser, por ejemplo, polvo de menta, mentol, vainillina, aspartamo, acesulfamo de potasio, sacarina.
Según la presente invención, se utilizó la granulación en seco como proceso para la preparación de formas farmacéuticas de Atomoxetina. Es uno de los métodos más económicos, ya que solo se utiliza equipo habitual y el producto suele caracterizarse por una resistencia física satisfactoria sin necesidad de envases especiales.
Las principales ventajas de dicho proceso son que se requiere menos equipo y espacio. Además, dicho proceso elimina la necesidad de una solución aglutinante, equipo pesado de mezclado y la costosa y lenta etapa de secado requerida para la granulación húmeda.
El proceso se caracteriza por las siguientes etapas:
- Pesaje de principio activo y excipientes;
- Tamizado de todos los excipientes y mezcla en seco con el principio activo;
- Mezclado de la mezcla anterior con fluidificantes;
- Clasificación por tamaño de la masa para eliminar grumos;
- Encapsulado
Los siguientes ejemplos ilustran realizaciones preferidas según la presente invención.
Ejemplos
Ejemplo de referencia 1:
Tabla 1: Ensayos de formulación 1-6
Todos los ensayos de composición se fabricaron con el siguiente procedimiento:
- Pesaje de principio activo y excipientes
- Tamizado de todos los excipientes y mezcla en seco con el principio activo
- Mezclado de la mezcla anterior con Dimeticona
- Clasificación por tamaño de la masa para eliminar los grumos.
- Encapsulado en cápsulas sin SLS
Se fabricó una primera composición (ensayo 1) que tenía los mismos excipientes que el producto comercializado con la diferencia de que se encapsuló en una cápsula de gelatina dura sin SLS.
Las características de disolución obtenidas (tabla 2) se desviaron seriamente en los primeros 10-15 minutos de las del producto comercializado. Con el fin de mejorar la liberación del principio activo de la forma farmacéutica, se incorporó una serie de activadores de disolución conocidos en la formulación, tal como los presentados en la tabla 1 anterior para los ensayos de formulación 2 a 6. En los ensayos 2 y 3 se reemplazó el almidón 1500, en parte y totalmente respectivamente, por lactosa para evitar el hinchamiento del almidón. En los ensayos 4 y 5 se añadieron disgregadores conocidos, almidón glicolato de sodio y croscarmelosa de sodio para mejorar la disolución. Por último, se agregó SLS en la composición por razones similares. Como se puede ver en la tabla 2, ninguno de los excipientes utilizados logró abordar el problema.
A pesar de que, SLS se probó como parte de la composición real, a diferencia del producto comercializado donde se encuentra en la cubierta de la cápsula, no tuvo el efecto deseado.
Tabla 2: Características de disolución de Strattera® y ensayos 1 a 6 en HCl 0,1 N como medio de disolución.
Ejemplo 2:
Tabla 3: Ensayos de formulación 7-10
Las composiciones de los ensayos 7 a 10 se prepararon todas según el procedimiento descrito en el ejemplo 1 y sus características de disolución se midieron en las mismas condiciones (tabla 4).
Tabla 4: Características de disolución de los ensayos 7 a 10 en HCl 0,1 N como medio de disolución.
Es evidente a partir de los resultados que Aerosil mejoró la velocidad de disolución de la Atomoxetina al evitar que el fármaco quede atrapado en el gel formado. Se puede observar que hay un aumento de la velocidad de disolución cuando se aumenta la concentración de Aerosil y la cantidad de Dimeticona es baja. Por otra parte, cuando la cantidad de dimeticona está en la concentración más alta seleccionada, no hay ningún efecto representado por el aumento de Aerosil. En general, las cuatro composiciones fueron aceptables, sin embargo, vale la pena mencionar que los ensayos 9 y 10 tuvieron una mejor fluidez de los gránulos, lo cual es una ventaja adicional en la producción a gran escala y aún más, el ensayo 10 tuvo un volumen ligeramente más compacto que conduce a una encapsulación más rápida y fácil . Ejemplo 3:
Además, se investigó otro tipo de sílice, a saber, Syloid® 244FP y una reducción de peso del contenido de la cápsula (tabla 5).
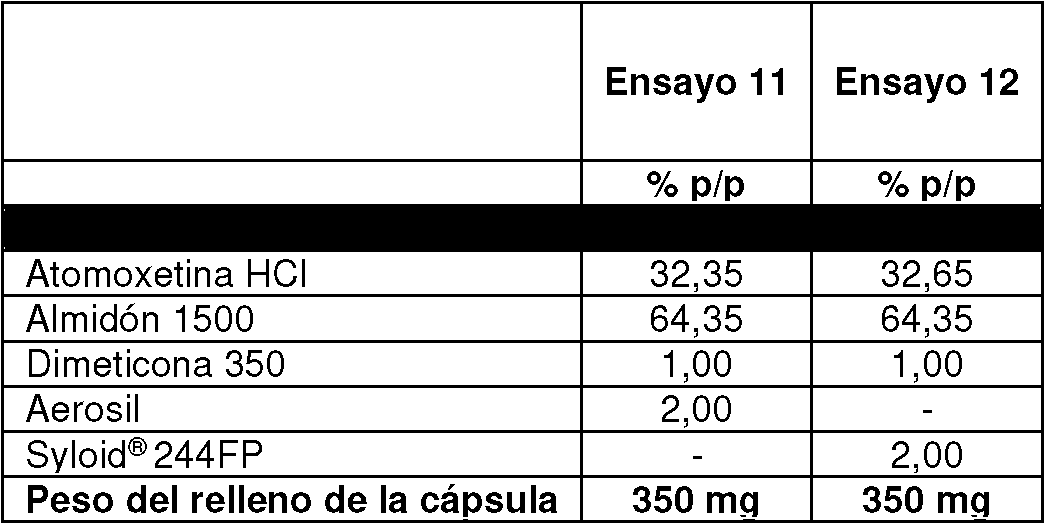
Tabla 5: Ensayos de formulación 11-12
El procedimiento de fabricación fue el mismo que en los ejemplos anteriores, así como las condiciones de las características de disolución.
Tabla 6: Características de disolución de los ensayos 11 y 12 en HCl 0,1 N como medio de disolución.
Es evidente a partir de lo anterior que la reducción del peso del relleno de la cápsula mejoró significativamente la liberación de disolución de Atomoxetina y que el empleo de Syloid® 244FP cumple ligeramente las normas de la presente invención.
Los ensayos de las formulaciones 1 y 11 se cargaron en cámaras de estabilidad. Los datos de estabilidad tras el almacenamiento en el momento cero y 6 meses en condiciones de almacenamiento a largo plazo (25°C/60% HR), intermedias (30°C/60% HR) y aceleradas (40°C/75% HR) se presentan en la tabla siguiente.
Tabla 7: Resultados de estabilidad de los ensayos 1 y 11
Lo que puede verse sorprendentemente en la tabla 7 anterior es que el uso de dióxido de silicio coloidal proporciona un efecto estabilizador. Los resultados anteriores muestran una buena estabilidad del producto de la presente invención, así como una buena compatibilidad entre el fármaco y los excipientes propuestos por la presente invención. Además, los buenos resultados en cuanto a las características fisicoquímicas, la excelente estabilidad del fármaco, así como el procedimiento de fabricación particular seguido, indican las ventajas de la presente invención.
La composición del ensayo 11 se preparó para un contenido de principio activo de 10, 18, 25, 40, 60, 80 y 100 mg con un peso total de relleno de cápsula de 35, 63, 87,5, 140, 210, 280 y 350 mg, respectivamente. Los resultados de las características de disolución fueron excelentes y directamente comparables con los del producto comercializado que no sigue este aumento lineal del contenido activo en peso. Así, para la composición que se propone aquí, se logra el importante aspecto de linealidad que corresponde a los beneficios económicos para cualquier empresa.
Si bien la presente invención se ha descrito con respecto a las realizaciones particulares, será evidente para los expertos en la técnica que se pueden realizar varios cambios y modificaciones en la invención.
Claims (6)
1. Una composición farmacéutica en forma de cápsula de gelatina dura para administración oral que comprende Atomoxetina o una de sus sales o polimorfos farmacéuticamente aceptables como principio activo y una cantidad de 2% a 4% p/p de dióxido de silicio que actúa como agente de suspensión, en donde la cápsula de gelatina dura no contiene SLS.
2. La composición farmacéutica según la reivindicación 1, en la que la Atomoxetina o una de sus sales o polimorfos farmacéuticamente aceptables está en una cantidad del 25% al 40% p/p.
3. Composición farmacéutica según la reivindicación 1, en la que el dióxido de silicio es un dióxido de silicio coloidal o un dióxido de silicio amorfo.
4. La composición farmacéutica según cualquiera de las reivindicaciones anteriores, en donde además comprende al menos un excipiente farmacéuticamente aceptable seleccionado entre agentes diluyentes, lubricantes, fluidificantes y aromatizantes.
5. La composición farmacéutica según cualquier reivindicación anterior, en la que dicha composición comprende además almidón pregelatinizado y dimeticona.
6. Un procedimiento para la preparación de una composición farmacéutica según la reivindicación 1, que comprende las etapas siguientes:
- Pesaje de Atomoxetina o una de sus sales o polimorfos farmacéuticamente aceptables como principio activo, el dióxido de silicio en una cantidad del 2% al 4% p/p y cualquier excipiente opcional farmacéuticamente aceptable; - Tamizado de todos los excipientes y mezcla en seco con el principio activo;
- Mezclado de la mezcla anterior con un lubricante;
- Clasificación por tamaño de la masa para eliminar los grumos;
- Encapsulado en cápsulas de gelatina dura sin SLS.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GR20150100240A GR1008819B (el) | 2015-05-22 | 2015-05-22 | Φαρμακευτικο σκευασμα που περιλαμβανει ατομοξετινη και μεθοδος παρασκευης αυτου |
| PCT/EP2016/000831 WO2016188623A1 (en) | 2015-05-22 | 2016-05-19 | Pharmaceutical composition comprising atomoxetine and method for the preparation thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2872531T3 true ES2872531T3 (es) | 2021-11-02 |
Family
ID=56119443
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16728613T Active ES2872531T3 (es) | 2015-05-22 | 2016-05-19 | Composición farmacéutica que comprende Atomoxetina y método para su preparación |
Country Status (4)
| Country | Link |
|---|---|
| EP (1) | EP3297612B1 (es) |
| ES (1) | ES2872531T3 (es) |
| GR (1) | GR1008819B (es) |
| WO (1) | WO2016188623A1 (es) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109160759B (zh) * | 2018-10-12 | 2021-04-20 | 中水电第十一工程局(郑州)有限公司 | 一种硅粉悬浮液的制备方法 |
| WO2020086065A1 (en) | 2018-10-23 | 2020-04-30 | Halliburton Energy Services, Inc. | Position measurement system for correlation array |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH695982A5 (de) | 2001-03-06 | 2006-11-15 | Lilly Co Eli | Inhibitor der Monaminaufnahme. |
| AU2004312059A1 (en) | 2003-12-31 | 2005-07-21 | Actavis Group Hf | Atomoxetine formulations |
| ATE516019T1 (de) | 2004-05-11 | 2011-07-15 | Egalet Ltd | Quellbare dosierform mit gellan-gummit |
| GR1006879B (el) * | 2005-09-14 | 2010-07-13 | "Φαρματεν" Φαρμακευτικη Βιομηχανικη Εμπορικη Α.Ε., | Βελτιωμενες φαρμακευτικες συνθεσεις που περιεχουν αναστολεις της αναγωγασης του 3-υδροξυ-3-μεθυλογλουταρυλοσυνενζυμου α (hmg-coa) και μεθοδος παρασκευης αυτων |
| KR102090784B1 (ko) * | 2013-06-28 | 2020-03-18 | 한미약품 주식회사 | 빠른 용출률을 나타내는 아토목세틴을 포함하는 경구용 약학 제제 및 이의 제조방법 |
-
2015
- 2015-05-22 GR GR20150100240A patent/GR1008819B/el active IP Right Grant
-
2016
- 2016-05-19 WO PCT/EP2016/000831 patent/WO2016188623A1/en not_active Ceased
- 2016-05-19 ES ES16728613T patent/ES2872531T3/es active Active
- 2016-05-19 EP EP16728613.7A patent/EP3297612B1/en not_active Not-in-force
Also Published As
| Publication number | Publication date |
|---|---|
| EP3297612A1 (en) | 2018-03-28 |
| WO2016188623A1 (en) | 2016-12-01 |
| GR1008819B (el) | 2016-08-01 |
| EP3297612B1 (en) | 2021-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2393640T3 (es) | Comprimidos bucodisgregables | |
| ES2354688T3 (es) | Formulaciones para la administración oral de compuestos activos. | |
| ES2326167T3 (es) | Comprimidos dispersables de deferasirox. | |
| US8642649B2 (en) | Orally dispersible tablet | |
| KR101099176B1 (ko) | 구강내 속붕성 정제 | |
| BRPI0617208A2 (pt) | preparação farmacêutica contendo meloxicam | |
| PT2018158E (pt) | Nova forma de administração de racecadotril | |
| WO2011027009A1 (es) | Composición farmacéutica de ibuprofeno, tramadol y un aminoácido básico, procedimiento para su preparación y utilización de la misma | |
| CN102630162B (zh) | 4-甲基吡唑制剂 | |
| ES2872531T3 (es) | Composición farmacéutica que comprende Atomoxetina y método para su preparación | |
| CN1172669C (zh) | 沙利度坦在制造治疗或预防主要抑郁性病症的药物中的应用 | |
| PT1474152E (pt) | Formulação farmacêutica oralmente dispersável contendo ivabradina | |
| ES2241777T3 (es) | Composiciones farmaceuticas que contienen terbinafina. | |
| CA2853117C (en) | Sublingual pharmaceutical composition containing an antihistamine agent and method for the preparation thereof | |
| BR112015014430B1 (pt) | Composição em comprimido | |
| JP6061924B2 (ja) | 口腔内分散性製剤 | |
| ES2314440T3 (es) | Composicion farmaceutica bucodispersable de un compuesto antitrombotico. | |
| ES2953126T3 (es) | Un método para fabricar una composición farmacéutica que comprende Nefopam y Acetaminofén, y la composición farmacéutica obtenida de esta manera | |
| WO2016054240A1 (en) | Fixed dose combinations for the treatment of viral diseases | |
| ES2862209T3 (es) | Composiciones orales sólidas de liberación prolongada no pulsátil que contienen betahistina | |
| JP2019515045A (ja) | 甲状腺ホルモン又はそのアナログを提供する組成物及び方法 | |
| US20260069569A1 (en) | Ebselen containing oral dosage forms | |
| JP4500051B2 (ja) | ピリベジルの口内分散性薬剤組成物 | |
| ES2960057T3 (es) | Comprimido de molsidomina de liberación prolongada | |
| Lodhi et al. | Review Study on Fast Dissolving Tablets Formulation of Antiemetic Medication |