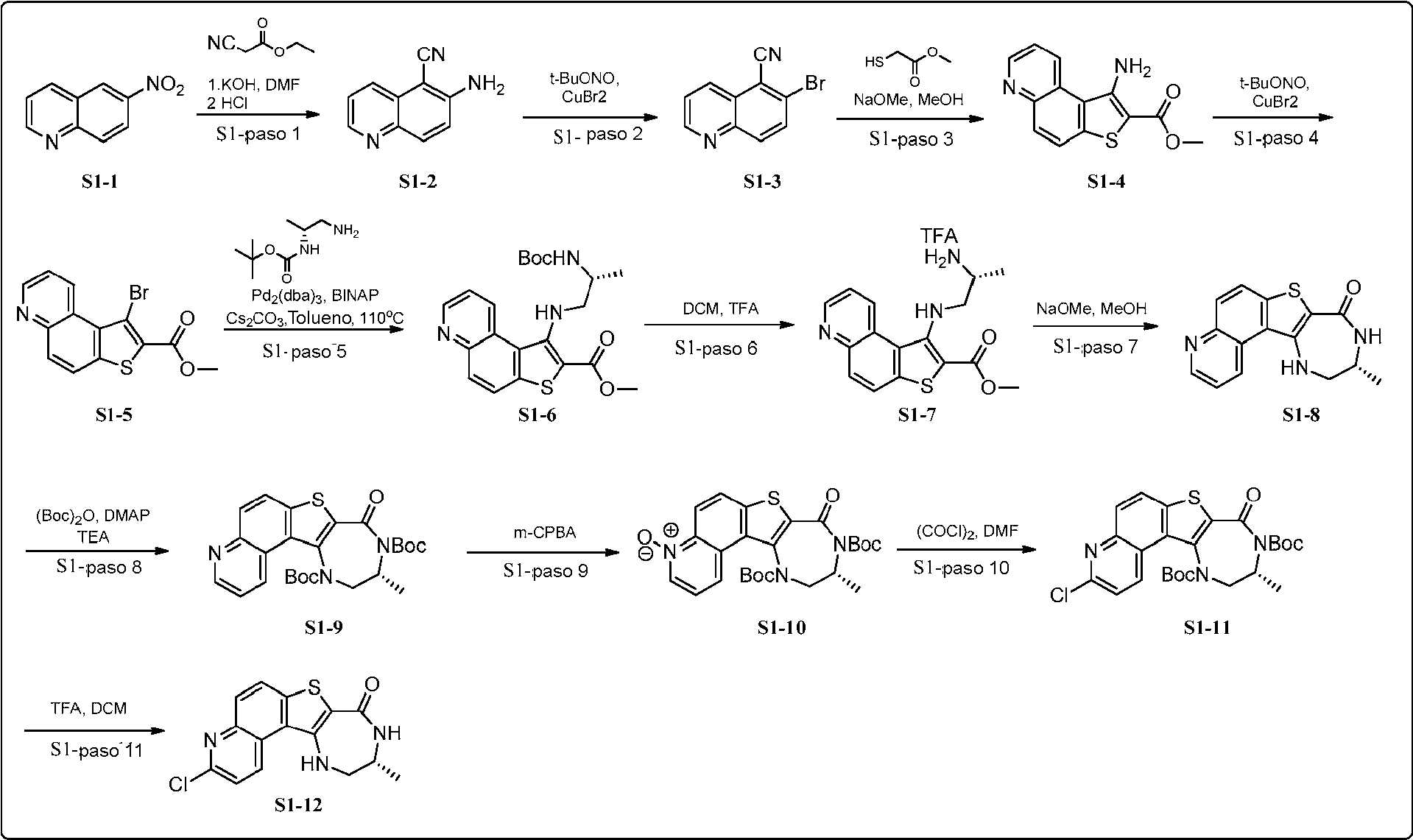
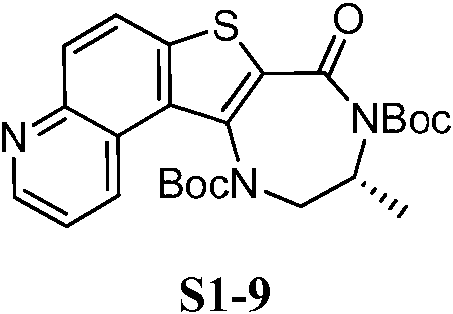
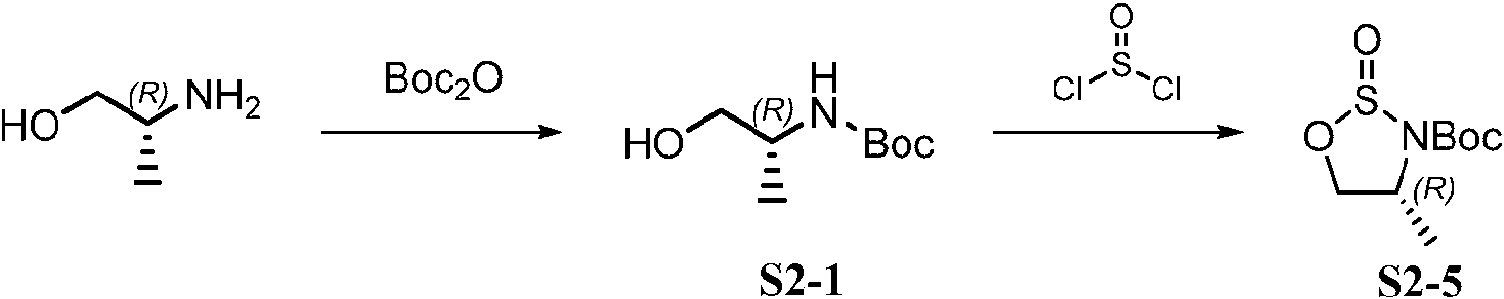
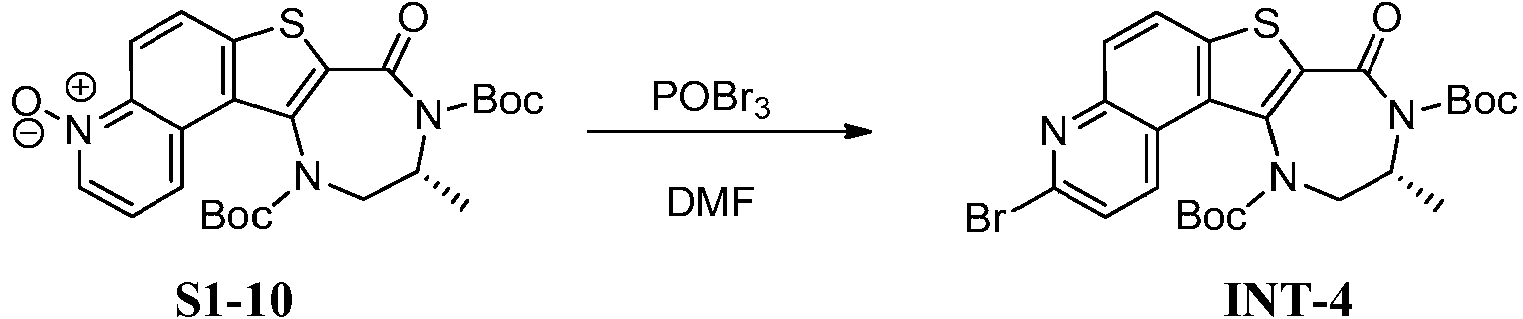
ES2874561T3 - Inhibidores de MK2 y usos de los mismos - Google Patents
Inhibidores de MK2 y usos de los mismos Download PDFInfo
- Publication number
- ES2874561T3 ES2874561T3 ES15842903T ES15842903T ES2874561T3 ES 2874561 T3 ES2874561 T3 ES 2874561T3 ES 15842903 T ES15842903 T ES 15842903T ES 15842903 T ES15842903 T ES 15842903T ES 2874561 T3 ES2874561 T3 ES 2874561T3
- Authority
- ES
- Spain
- Prior art keywords
- mmol
- int
- methyl
- synthesis
- stirred
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229940124789 MK2 inhibitor Drugs 0.000 title description 8
- 150000001875 compounds Chemical class 0.000 claims abstract description 381
- 150000003839 salts Chemical class 0.000 claims abstract description 31
- 239000000203 mixture Substances 0.000 claims description 165
- 239000003981 vehicle Substances 0.000 claims description 14
- 239000002671 adjuvant Substances 0.000 claims description 13
- 239000003937 drug carrier Substances 0.000 claims description 13
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 392
- 239000000243 solution Substances 0.000 description 260
- 230000015572 biosynthetic process Effects 0.000 description 243
- 238000003786 synthesis reaction Methods 0.000 description 241
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 235
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 223
- 239000007787 solid Substances 0.000 description 223
- 239000011541 reaction mixture Substances 0.000 description 216
- 238000001819 mass spectrum Methods 0.000 description 206
- 238000005160 1H NMR spectroscopy Methods 0.000 description 160
- 239000012044 organic layer Substances 0.000 description 153
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 152
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 144
- 238000006243 chemical reaction Methods 0.000 description 137
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 136
- 235000019439 ethyl acetate Nutrition 0.000 description 132
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 130
- 230000002829 reductive effect Effects 0.000 description 129
- RSWJZQPZLNLWGF-UHFFFAOYSA-N 2H-thieno[3,2-f]quinolin-8-one Chemical compound C=1CSC=2C=1C1=CC(C=NC1=CC=2)=O RSWJZQPZLNLWGF-UHFFFAOYSA-N 0.000 description 98
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 82
- -1 digluconate Chemical class 0.000 description 77
- GXJQFSNHEKKWLN-UHFFFAOYSA-N 7h-quinolin-8-one Chemical compound C1=CN=C2C(=O)CC=CC2=C1 GXJQFSNHEKKWLN-UHFFFAOYSA-N 0.000 description 72
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 65
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 64
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 64
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 61
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 59
- 239000013058 crude material Substances 0.000 description 57
- 239000012267 brine Substances 0.000 description 56
- 239000000725 suspension Substances 0.000 description 55
- 238000002953 preparative HPLC Methods 0.000 description 51
- 238000000746 purification Methods 0.000 description 47
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 46
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 41
- 238000000034 method Methods 0.000 description 39
- 239000010410 layer Substances 0.000 description 38
- 208000035475 disorder Diseases 0.000 description 35
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 35
- 239000011734 sodium Substances 0.000 description 34
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 32
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 30
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 30
- 201000010099 disease Diseases 0.000 description 29
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 27
- 108090000623 proteins and genes Proteins 0.000 description 26
- 235000002639 sodium chloride Nutrition 0.000 description 26
- 239000000047 product Substances 0.000 description 25
- 210000004027 cell Anatomy 0.000 description 24
- 102000004169 proteins and genes Human genes 0.000 description 23
- 238000010898 silica gel chromatography Methods 0.000 description 23
- 239000006196 drop Substances 0.000 description 22
- VLKZOEOYAKHREP-UHFFFAOYSA-N hexane Substances CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 22
- 239000007788 liquid Substances 0.000 description 22
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 22
- 229910052938 sodium sulfate Inorganic materials 0.000 description 22
- 235000011152 sodium sulphate Nutrition 0.000 description 22
- 238000012360 testing method Methods 0.000 description 22
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 21
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 21
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 21
- 108091000080 Phosphotransferase Proteins 0.000 description 20
- 102000020233 phosphotransferase Human genes 0.000 description 20
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 19
- 102000001253 Protein Kinase Human genes 0.000 description 19
- 108060006633 protein kinase Proteins 0.000 description 19
- 238000005481 NMR spectroscopy Methods 0.000 description 18
- 238000003756 stirring Methods 0.000 description 18
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 17
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 17
- 239000003112 inhibitor Substances 0.000 description 17
- QDXGKRWDQCEABB-UHFFFAOYSA-N pyrimidine-5-carboxamide Chemical compound NC(=O)C1=CN=CN=C1 QDXGKRWDQCEABB-UHFFFAOYSA-N 0.000 description 17
- 230000000694 effects Effects 0.000 description 16
- 239000005457 ice water Substances 0.000 description 16
- 239000000741 silica gel Substances 0.000 description 16
- 229910002027 silica gel Inorganic materials 0.000 description 16
- JZSYSXZDIQUOGP-UHFFFAOYSA-N 2,4-difluoropyrimidine Chemical compound FC1=CC=NC(F)=N1 JZSYSXZDIQUOGP-UHFFFAOYSA-N 0.000 description 15
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 15
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 15
- 238000004440 column chromatography Methods 0.000 description 15
- 229910052757 nitrogen Inorganic materials 0.000 description 15
- 229910000027 potassium carbonate Inorganic materials 0.000 description 15
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 15
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 14
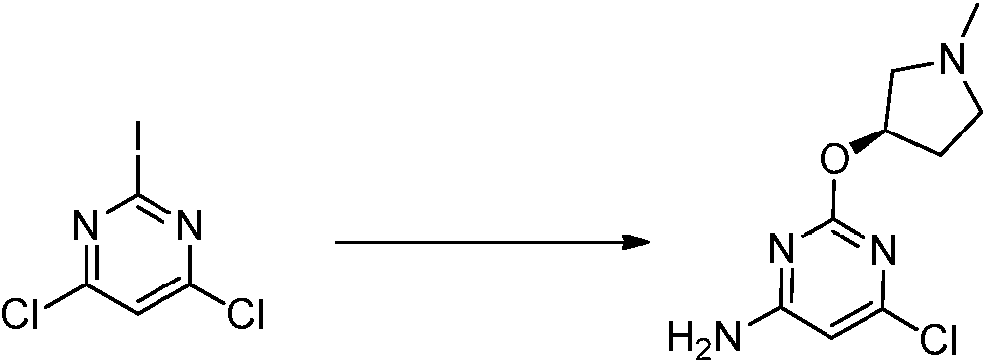
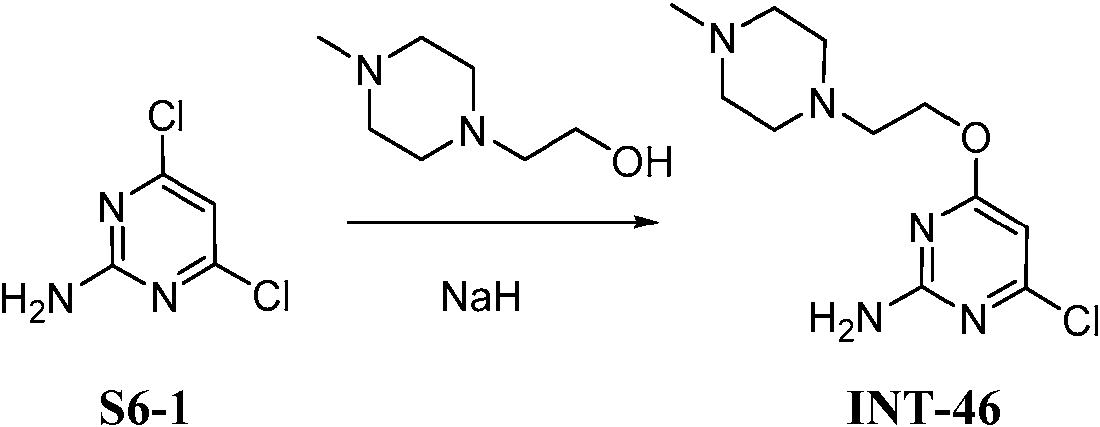
- QCTQVQBBOBTFRE-UHFFFAOYSA-N ClC1=CC(=NC(=N1)OC1CN(CCC1)C)N Chemical compound ClC1=CC(=NC(=N1)OC1CN(CCC1)C)N QCTQVQBBOBTFRE-UHFFFAOYSA-N 0.000 description 14
- 230000001404 mediated effect Effects 0.000 description 14
- 239000012071 phase Substances 0.000 description 14
- 235000018102 proteins Nutrition 0.000 description 14
- 230000002441 reversible effect Effects 0.000 description 14
- 229910000104 sodium hydride Inorganic materials 0.000 description 14
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 13
- YEJAJYAHJQIWNU-UHFFFAOYSA-N azelastine hydrochloride Chemical compound Cl.C1CN(C)CCCC1N1C(=O)C2=CC=CC=C2C(CC=2C=CC(Cl)=CC=2)=N1 YEJAJYAHJQIWNU-UHFFFAOYSA-N 0.000 description 13
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 13
- 229910000024 caesium carbonate Inorganic materials 0.000 description 13
- 239000000706 filtrate Substances 0.000 description 13
- 238000004007 reversed phase HPLC Methods 0.000 description 13
- DYJLMFCOEDXHFK-UHFFFAOYSA-N 11-thia-6,14,15-triazatetracyclo[8.8.0.02,7.012,18]octadeca-1(10),2(7),3,5,8,12(18),14,16-octaen-13-one Chemical compound C1=CC=NC=2C=CC3=C(C1=2)C1=C(S3)C(N=NC=C1)=O DYJLMFCOEDXHFK-UHFFFAOYSA-N 0.000 description 12
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 12
- 102000004190 Enzymes Human genes 0.000 description 12
- 108090000790 Enzymes Proteins 0.000 description 12
- 102000008016 Eukaryotic Initiation Factor-3 Human genes 0.000 description 12
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 12
- 239000000284 extract Substances 0.000 description 12
- 230000002401 inhibitory effect Effects 0.000 description 12
- 230000005764 inhibitory process Effects 0.000 description 12
- 238000012746 preparative thin layer chromatography Methods 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- CXNIUSPIQKWYAI-UHFFFAOYSA-N xantphos Chemical compound C=12OC3=C(P(C=4C=CC=CC=4)C=4C=CC=CC=4)C=CC=C3C(C)(C)C2=CC=CC=1P(C=1C=CC=CC=1)C1=CC=CC=C1 CXNIUSPIQKWYAI-UHFFFAOYSA-N 0.000 description 12
- NFTNYEQPGPAENQ-UHFFFAOYSA-N CN(CCOC1=NC(=CC(=N1)N)F)C Chemical compound CN(CCOC1=NC(=CC(=N1)N)F)C NFTNYEQPGPAENQ-UHFFFAOYSA-N 0.000 description 11
- 238000003556 assay Methods 0.000 description 11
- 239000012043 crude product Substances 0.000 description 11
- 239000002552 dosage form Substances 0.000 description 11
- 239000002244 precipitate Substances 0.000 description 11
- 229920006395 saturated elastomer Polymers 0.000 description 11
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 10
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 10
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 10
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 10
- 125000004548 quinolin-3-yl group Chemical group N1=CC(=CC2=CC=CC=C12)* 0.000 description 10
- 239000012312 sodium hydride Substances 0.000 description 10
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 9
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 9
- DFPAKSUCGFBDDF-UHFFFAOYSA-N Nicotinamide Chemical compound NC(=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-UHFFFAOYSA-N 0.000 description 9
- 235000011114 ammonium hydroxide Nutrition 0.000 description 9
- 239000012472 biological sample Substances 0.000 description 9
- 238000001914 filtration Methods 0.000 description 9
- 238000003818 flash chromatography Methods 0.000 description 9
- 238000009472 formulation Methods 0.000 description 9
- 239000002609 medium Substances 0.000 description 9
- 239000003208 petroleum Substances 0.000 description 9
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 9
- 239000000126 substance Substances 0.000 description 9
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 8
- 101000810330 Arabidopsis thaliana Eukaryotic translation initiation factor 3 subunit E Proteins 0.000 description 8
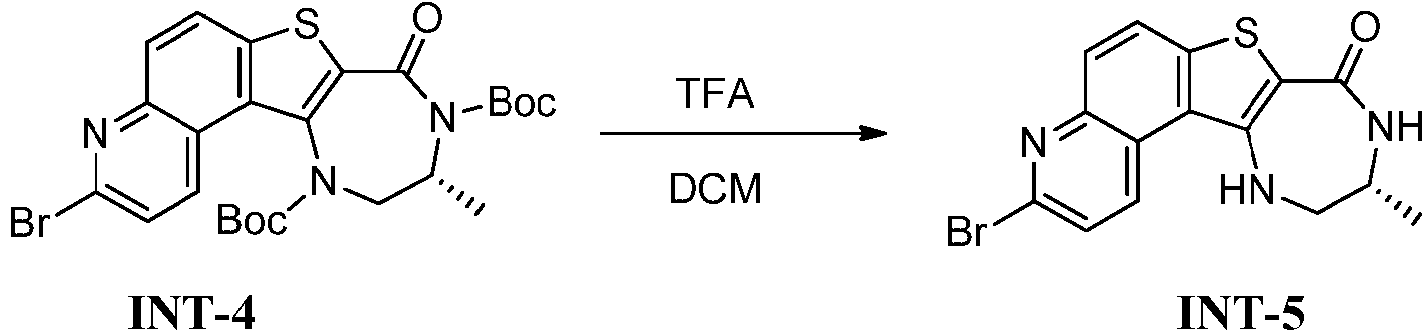
- DLDGRXKBNNQTBD-SSDOTTSWSA-N BrC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound BrC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O DLDGRXKBNNQTBD-SSDOTTSWSA-N 0.000 description 8
- 108010045100 HSP27 Heat-Shock Proteins Proteins 0.000 description 8
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- 239000002585 base Substances 0.000 description 8
- 239000002775 capsule Substances 0.000 description 8
- 239000003814 drug Substances 0.000 description 8
- 235000019441 ethanol Nutrition 0.000 description 8
- 239000003921 oil Substances 0.000 description 8
- 235000019198 oils Nutrition 0.000 description 8
- 229920001223 polyethylene glycol Polymers 0.000 description 8
- 208000024891 symptom Diseases 0.000 description 8
- 208000011580 syndromic disease Diseases 0.000 description 8
- 239000003826 tablet Substances 0.000 description 8
- HNDGEYCCZGRMTN-UHFFFAOYSA-N thieno[3,2-f:4,5-f]bis[1]benzothiophene Chemical compound S1C2=CC=3SC=CC=3C=C2C2=C1C=C(SC=C1)C1=C2 HNDGEYCCZGRMTN-UHFFFAOYSA-N 0.000 description 8
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 8
- PEDMFCHWOVJDNW-UHFFFAOYSA-N 5-fluoro-2-nitroaniline Chemical compound NC1=CC(F)=CC=C1[N+]([O-])=O PEDMFCHWOVJDNW-UHFFFAOYSA-N 0.000 description 7
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 7
- ZATNFORFELDNSM-GFCCVEGCSA-N C(C)(C)(C)OC(=O)N[C@@H](CNC1=C(SC=2C1=C1C=CC=NC1=CC=2)C(=O)OC)C Chemical compound C(C)(C)(C)OC(=O)N[C@@H](CNC1=C(SC=2C1=C1C=CC=NC1=CC=2)C(=O)OC)C ZATNFORFELDNSM-GFCCVEGCSA-N 0.000 description 7
- 102100039165 Heat shock protein beta-1 Human genes 0.000 description 7
- 206010028980 Neoplasm Diseases 0.000 description 7
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 7
- 229960000583 acetic acid Drugs 0.000 description 7
- 150000001413 amino acids Chemical class 0.000 description 7
- 229910052786 argon Inorganic materials 0.000 description 7
- 230000001363 autoimmune Effects 0.000 description 7
- XYOVOXDWRFGKEX-UHFFFAOYSA-N azepine Chemical compound N1C=CC=CC=C1 XYOVOXDWRFGKEX-UHFFFAOYSA-N 0.000 description 7
- 238000010438 heat treatment Methods 0.000 description 7
- 229910052739 hydrogen Inorganic materials 0.000 description 7
- 239000000377 silicon dioxide Substances 0.000 description 7
- 239000007858 starting material Substances 0.000 description 7
- GZPHSAQLYPIAIN-UHFFFAOYSA-N 3-pyridinecarbonitrile Chemical compound N#CC1=CC=CN=C1 GZPHSAQLYPIAIN-UHFFFAOYSA-N 0.000 description 6
- VITWKLCJAFIUGR-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)F)CI Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)F)CI VITWKLCJAFIUGR-UHFFFAOYSA-N 0.000 description 6
- SKNKZKXDWPKKFO-CQSZACIVSA-N ClC1=NC=C(C(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C(=O)NCC1=CC=C(C=C1)OC Chemical compound ClC1=NC=C(C(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C(=O)NCC1=CC=C(C=C1)OC SKNKZKXDWPKKFO-CQSZACIVSA-N 0.000 description 6
- WSPZDDYKUFPBGO-UHFFFAOYSA-N FC1=CC(=NC(=N1)OC1CN(CCC1)C)N Chemical compound FC1=CC(=NC(=N1)OC1CN(CCC1)C)N WSPZDDYKUFPBGO-UHFFFAOYSA-N 0.000 description 6
- GDCCWBXPPAQDOH-UHFFFAOYSA-N NC1=C(SC=2C1=C1C=CC=NC1=CC=2)C(=O)OC Chemical compound NC1=C(SC=2C1=C1C=CC=NC1=CC=2)C(=O)OC GDCCWBXPPAQDOH-UHFFFAOYSA-N 0.000 description 6
- 239000007832 Na2SO4 Substances 0.000 description 6
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 101000767160 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Intracellular protein transport protein USO1 Proteins 0.000 description 6
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 6
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 6
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 6
- 241001130469 Tila Species 0.000 description 6
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 6
- 150000001412 amines Chemical class 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 238000001816 cooling Methods 0.000 description 6
- 239000003480 eluent Substances 0.000 description 6
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 6
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 6
- 239000008101 lactose Substances 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 6
- 239000012074 organic phase Substances 0.000 description 6
- 102000002574 p38 Mitogen-Activated Protein Kinases Human genes 0.000 description 6
- 108010068338 p38 Mitogen-Activated Protein Kinases Proteins 0.000 description 6
- 239000000546 pharmaceutical excipient Substances 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- 239000000523 sample Substances 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- PDMMBPHJODEJQV-UHFFFAOYSA-N 2,6-dichloro-n-[(4-methoxyphenyl)methyl]pyrimidin-4-amine Chemical compound C1=CC(OC)=CC=C1CNC1=CC(Cl)=NC(Cl)=N1 PDMMBPHJODEJQV-UHFFFAOYSA-N 0.000 description 5
- BXYZFBZFOPCYGD-UHFFFAOYSA-N 3-[[3-[3-benzoyl-8-(trifluoromethyl)quinolin-4-yl]phenoxy]methyl]benzoic acid Chemical compound OC(=O)C1=CC=CC(COC=2C=C(C=CC=2)C=2C3=CC=CC(=C3N=CC=2C(=O)C=2C=CC=CC=2)C(F)(F)F)=C1 BXYZFBZFOPCYGD-UHFFFAOYSA-N 0.000 description 5
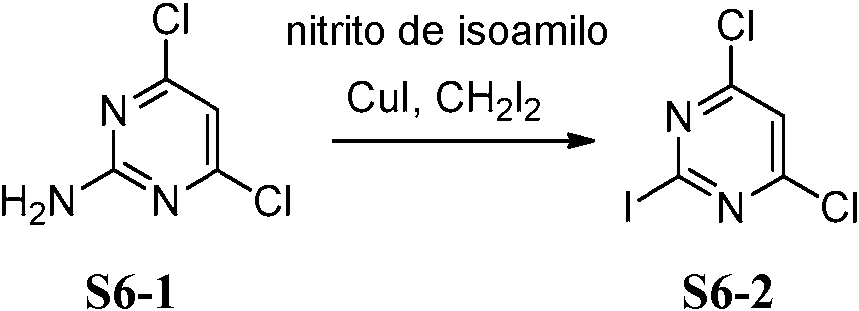
- YMVNHXZFDQSCRK-UHFFFAOYSA-N 4,6-dichloro-2-iodopyrimidine Chemical compound ClC1=CC(Cl)=NC(I)=N1 YMVNHXZFDQSCRK-UHFFFAOYSA-N 0.000 description 5
- UHEDQSRQDTVBPY-UHFFFAOYSA-N 4-chloro-6-(4-methylpiperazin-1-yl)-1,3,5-triazin-2-amine Chemical compound C1CN(C)CCN1C1=NC(N)=NC(Cl)=N1 UHEDQSRQDTVBPY-UHFFFAOYSA-N 0.000 description 5
- 125000004217 4-methoxybenzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1OC([H])([H])[H])C([H])([H])* 0.000 description 5
- PYCIBXGKTGBHHF-UHFFFAOYSA-N 6-aminoquinoline-5-carbonitrile Chemical compound N1=CC=CC2=C(C#N)C(N)=CC=C21 PYCIBXGKTGBHHF-UHFFFAOYSA-N 0.000 description 5
- DTWHKRFZYKUTHB-UHFFFAOYSA-N 6-bromoquinoline-5-carbonitrile Chemical compound N1=CC=CC2=C(C#N)C(Br)=CC=C21 DTWHKRFZYKUTHB-UHFFFAOYSA-N 0.000 description 5
- 208000023275 Autoimmune disease Diseases 0.000 description 5
- JAKDAWYJWRNELA-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)Cl)I Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)Cl)I JAKDAWYJWRNELA-UHFFFAOYSA-N 0.000 description 5
- QNXSIFUWJWKTTA-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)Cl)OC1CN(CCC1)C Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)Cl)OC1CN(CCC1)C QNXSIFUWJWKTTA-UHFFFAOYSA-N 0.000 description 5
- VKEIGYSQABRPMW-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)F)C(=O)OC Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)F)C(=O)OC VKEIGYSQABRPMW-UHFFFAOYSA-N 0.000 description 5
- JOCFQUCSEWKBKG-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)F)CO Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)F)CO JOCFQUCSEWKBKG-UHFFFAOYSA-N 0.000 description 5
- ITOPAZWZNWXZGO-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)F)I Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)F)I ITOPAZWZNWXZGO-UHFFFAOYSA-N 0.000 description 5
- VMCALTJFFMUSQV-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)F)N Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)F)N VMCALTJFFMUSQV-UHFFFAOYSA-N 0.000 description 5
- WXGQUFSFDDYUOZ-UHFFFAOYSA-N ClC1=CC(=NC(=N1)I)NCC1=CC=C(C=C1)OC Chemical compound ClC1=CC(=NC(=N1)I)NCC1=CC=C(C=C1)OC WXGQUFSFDDYUOZ-UHFFFAOYSA-N 0.000 description 5
- XQFWFUOFJZOHBO-UHFFFAOYSA-N ClC1=CC(=NC(=N1)OCCOC)NCC1=CC=C(C=C1)OC Chemical compound ClC1=CC(=NC(=N1)OCCOC)NCC1=CC=C(C=C1)OC XQFWFUOFJZOHBO-UHFFFAOYSA-N 0.000 description 5
- VYJQBTBISGWCMB-UHFFFAOYSA-N ClC1=NC(=NC(=C1)NCC1=CC=C(C=C1)OC)C(=O)OC Chemical compound ClC1=NC(=NC(=C1)NCC1=CC=C(C=C1)OC)C(=O)OC VYJQBTBISGWCMB-UHFFFAOYSA-N 0.000 description 5
- OOXNZRSYNLEPIS-UHFFFAOYSA-N FC1=CC(=NC(=N1)CN1CCCCC1)N Chemical compound FC1=CC(=NC(=N1)CN1CCCCC1)N OOXNZRSYNLEPIS-UHFFFAOYSA-N 0.000 description 5
- HHNVLXOWTGBYPT-RXMQYKEDSA-N FC1=NC(=NC(=C1)F)O[C@H]1COCC1 Chemical compound FC1=NC(=NC(=C1)F)O[C@H]1COCC1 HHNVLXOWTGBYPT-RXMQYKEDSA-N 0.000 description 5
- TYQFCXKEJPCFOQ-UHFFFAOYSA-N N-(6-fluoropyrimidin-4-yl)-N',N'-dimethylethane-1,2-diamine Chemical compound CN(C)CCNC1=CC(F)=NC=N1 TYQFCXKEJPCFOQ-UHFFFAOYSA-N 0.000 description 5
- MUHAUXCKZWLACN-SSDOTTSWSA-N OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O MUHAUXCKZWLACN-SSDOTTSWSA-N 0.000 description 5
- NLKBUJQLMRHSKP-SSDOTTSWSA-N [(2r)-2-[(2-methylpropan-2-yl)oxycarbonylamino]propyl] methanesulfonate Chemical compound CS(=O)(=O)OC[C@@H](C)NC(=O)OC(C)(C)C NLKBUJQLMRHSKP-SSDOTTSWSA-N 0.000 description 5
- 230000001154 acute effect Effects 0.000 description 5
- 239000000969 carrier Substances 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 208000019425 cirrhosis of liver Diseases 0.000 description 5
- 238000000576 coating method Methods 0.000 description 5
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 5
- 235000018417 cysteine Nutrition 0.000 description 5
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 5
- 230000003176 fibrotic effect Effects 0.000 description 5
- 210000001035 gastrointestinal tract Anatomy 0.000 description 5
- 208000027866 inflammatory disease Diseases 0.000 description 5
- 230000002427 irreversible effect Effects 0.000 description 5
- 230000004048 modification Effects 0.000 description 5
- 238000012986 modification Methods 0.000 description 5
- 239000006187 pill Substances 0.000 description 5
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- ZFCHNZDUMIOWFV-UHFFFAOYSA-M pyrimidine-2-carboxylate Chemical compound [O-]C(=O)C1=NC=CC=N1 ZFCHNZDUMIOWFV-UHFFFAOYSA-M 0.000 description 5
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 5
- 235000017557 sodium bicarbonate Nutrition 0.000 description 5
- 239000007909 solid dosage form Substances 0.000 description 5
- 230000000699 topical effect Effects 0.000 description 5
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 5
- 239000001993 wax Substances 0.000 description 5
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 4
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 4
- ALOCUZOKRULSAA-UHFFFAOYSA-N 1-methylpiperidin-4-amine Chemical compound CN1CCC(N)CC1 ALOCUZOKRULSAA-UHFFFAOYSA-N 0.000 description 4
- NTSYSQNAPGMSIH-UHFFFAOYSA-N 2,4,6-trifluoropyrimidine Chemical compound FC1=CC(F)=NC(F)=N1 NTSYSQNAPGMSIH-UHFFFAOYSA-N 0.000 description 4
- ZEMZPXWZVTUONV-UHFFFAOYSA-N 2-(2-dicyclohexylphosphanylphenyl)-n,n-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 ZEMZPXWZVTUONV-UHFFFAOYSA-N 0.000 description 4
- JPZOAVGMSDSWSW-UHFFFAOYSA-N 4,6-dichloropyrimidin-2-amine Chemical compound NC1=NC(Cl)=CC(Cl)=N1 JPZOAVGMSDSWSW-UHFFFAOYSA-N 0.000 description 4
- PPUIVMHRKBEYCR-UHFFFAOYSA-N 6-fluoropyrimidin-4-amine Chemical class NC1=CC(F)=NC=N1 PPUIVMHRKBEYCR-UHFFFAOYSA-N 0.000 description 4
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 4
- UAJOQWQMIDQIRX-UHFFFAOYSA-N C(C)(C)(C)NC1=NC(=NC(=C1)F)CN1CCCCC1 Chemical compound C(C)(C)(C)NC1=NC(=NC(=C1)F)CN1CCCCC1 UAJOQWQMIDQIRX-UHFFFAOYSA-N 0.000 description 4
- 208000024172 Cardiovascular disease Diseases 0.000 description 4
- BOBUBXHCKDDIDY-UHFFFAOYSA-N ClC1=CC(=NC(=N1)OCCN1CCN(CC1)C)N Chemical compound ClC1=CC(=NC(=N1)OCCN1CCN(CC1)C)N BOBUBXHCKDDIDY-UHFFFAOYSA-N 0.000 description 4
- 108010089790 Eukaryotic Initiation Factor-3 Proteins 0.000 description 4
- CKHXGVLZMBYEJF-UHFFFAOYSA-N FC1=NC(=CC(=N1)F)OCCOC Chemical compound FC1=NC(=CC(=N1)F)OCCOC CKHXGVLZMBYEJF-UHFFFAOYSA-N 0.000 description 4
- ZAGZXJFSNYXWPH-UHFFFAOYSA-N FC1=NC(=NC(=C1)F)OCC1(COC1)C Chemical compound FC1=NC(=NC(=C1)F)OCC1(COC1)C ZAGZXJFSNYXWPH-UHFFFAOYSA-N 0.000 description 4
- 206010016654 Fibrosis Diseases 0.000 description 4
- OUBORTRIKPEZMG-UHFFFAOYSA-N INT-2 Chemical compound Nc1c(ncn1-c1ccc(F)cc1)C(=N)C#N OUBORTRIKPEZMG-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 241000283891 Kobus Species 0.000 description 4
- 102100034069 MAP kinase-activated protein kinase 2 Human genes 0.000 description 4
- 108010041955 MAP-kinase-activated kinase 2 Proteins 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- 101100348848 Mus musculus Notch4 gene Proteins 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- CNZPGLOLJYMTJW-SBSPUUFOSA-N OC(=O)C(F)(F)F.COC(=O)c1sc2ccc3ncccc3c2c1NC[C@@H](C)N Chemical compound OC(=O)C(F)(F)F.COC(=O)c1sc2ccc3ncccc3c2c1NC[C@@H](C)N CNZPGLOLJYMTJW-SBSPUUFOSA-N 0.000 description 4
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- 108010029485 Protein Isoforms Proteins 0.000 description 4
- 102000001708 Protein Isoforms Human genes 0.000 description 4
- 206010040070 Septic Shock Diseases 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 4
- 101001060278 Xenopus laevis Fibroblast growth factor 3 Proteins 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- 125000004202 aminomethyl group Chemical group [H]N([H])C([H])([H])* 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 230000001908 autoinhibitory effect Effects 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 239000012230 colorless oil Substances 0.000 description 4
- QTMDXZNDVAMKGV-UHFFFAOYSA-L copper(ii) bromide Chemical compound [Cu+2].[Br-].[Br-] QTMDXZNDVAMKGV-UHFFFAOYSA-L 0.000 description 4
- 208000022993 cryopyrin-associated periodic syndrome Diseases 0.000 description 4
- MGNCLNQXLYJVJD-UHFFFAOYSA-N cyanuric chloride Chemical compound ClC1=NC(Cl)=NC(Cl)=N1 MGNCLNQXLYJVJD-UHFFFAOYSA-N 0.000 description 4
- 239000002270 dispersing agent Substances 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 239000003995 emulsifying agent Substances 0.000 description 4
- 239000002158 endotoxin Substances 0.000 description 4
- QINRQIZOBCQKAZ-UHFFFAOYSA-N ethyl 4-amino-2-methylsulfanylpyrimidine-5-carboxylate Chemical compound CCOC(=O)C1=CN=C(SC)N=C1N QINRQIZOBCQKAZ-UHFFFAOYSA-N 0.000 description 4
- 239000003701 inert diluent Substances 0.000 description 4
- 239000000543 intermediate Substances 0.000 description 4
- 150000002500 ions Chemical class 0.000 description 4
- 239000013038 irreversible inhibitor Substances 0.000 description 4
- 229940043355 kinase inhibitor Drugs 0.000 description 4
- 229920006008 lipopolysaccharide Polymers 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 208000030159 metabolic disease Diseases 0.000 description 4
- SRVUVLBNPDRACT-UHFFFAOYSA-N methyl 1-bromothieno[3,2-f]quinoline-2-carboxylate Chemical compound N1=CC=CC2=C(C(=C(C(=O)OC)S3)Br)C3=CC=C21 SRVUVLBNPDRACT-UHFFFAOYSA-N 0.000 description 4
- 231100000252 nontoxic Toxicity 0.000 description 4
- 230000003000 nontoxic effect Effects 0.000 description 4
- 230000026731 phosphorylation Effects 0.000 description 4
- 238000006366 phosphorylation reaction Methods 0.000 description 4
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 4
- JQXZBJAAOLPTKP-ZCFIWIBFSA-N tert-butyl n-[(2r)-1-aminopropan-2-yl]carbamate Chemical compound NC[C@@H](C)NC(=O)OC(C)(C)C JQXZBJAAOLPTKP-ZCFIWIBFSA-N 0.000 description 4
- QNBSOZHFBNUGCB-LURJTMIESA-N tert-butyl n-[(2s)-1-azidopropan-2-yl]carbamate Chemical compound [N-]=[N+]=NC[C@H](C)NC(=O)OC(C)(C)C QNBSOZHFBNUGCB-LURJTMIESA-N 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- 238000004809 thin layer chromatography Methods 0.000 description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 4
- 239000011534 wash buffer Substances 0.000 description 4
- NLQMSBJFLQPLIJ-UHFFFAOYSA-N (3-methyloxetan-3-yl)methanol Chemical group OCC1(C)COC1 NLQMSBJFLQPLIJ-UHFFFAOYSA-N 0.000 description 3
- UKANCZCEGQDKGF-UHFFFAOYSA-N 1-methylpiperidin-3-ol Chemical compound CN1CCCC(O)C1 UKANCZCEGQDKGF-UHFFFAOYSA-N 0.000 description 3
- RZVUFAWKJMGXSK-UHFFFAOYSA-N 2,4-dichloro-5-(ethoxymethyl)pyrimidine Chemical compound CCOCC1=CN=C(Cl)N=C1Cl RZVUFAWKJMGXSK-UHFFFAOYSA-N 0.000 description 3
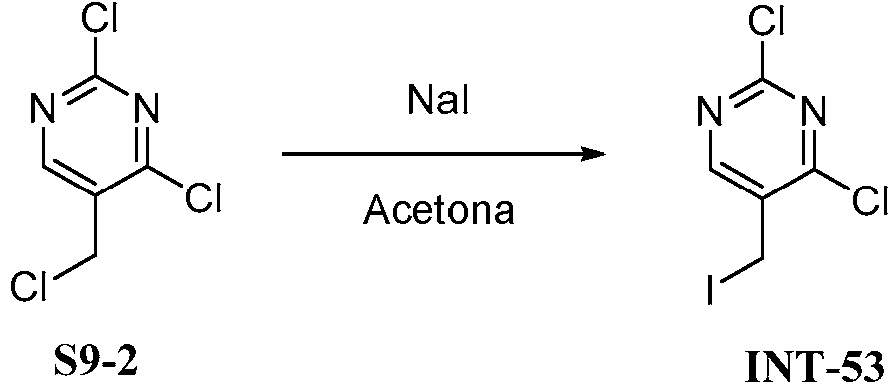
- NEIMQFSSWKAYTR-UHFFFAOYSA-N 2,4-dichloro-5-(iodomethyl)pyrimidine Chemical compound ClC1=NC=C(CI)C(Cl)=N1 NEIMQFSSWKAYTR-UHFFFAOYSA-N 0.000 description 3
- QHTUMQYGZQYEOZ-UHFFFAOYSA-N 2-(4-methylpiperazin-1-yl)ethanol Chemical group CN1CCN(CCO)CC1 QHTUMQYGZQYEOZ-UHFFFAOYSA-N 0.000 description 3
- XNWFRZJHXBZDAG-UHFFFAOYSA-N 2-METHOXYETHANOL Chemical compound COCCO XNWFRZJHXBZDAG-UHFFFAOYSA-N 0.000 description 3
- MCLDVUCSDZGNRR-UHFFFAOYSA-N 4,6-difluoropyrimidine Chemical compound FC1=CC(F)=NC=N1 MCLDVUCSDZGNRR-UHFFFAOYSA-N 0.000 description 3
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 3
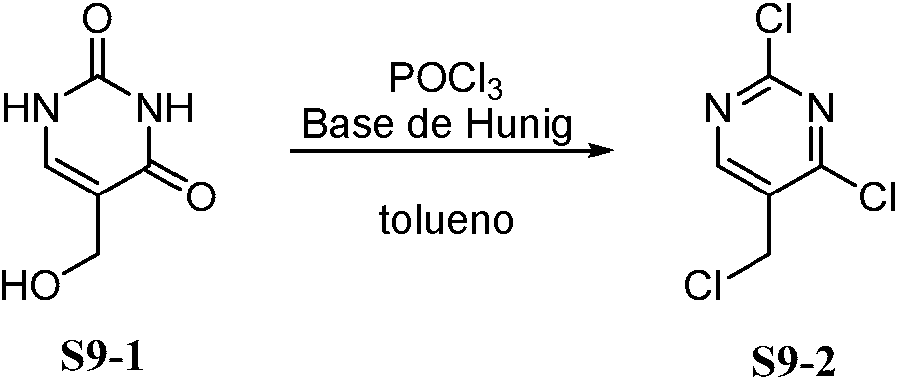
- JDBGXEHEIRGOBU-UHFFFAOYSA-N 5-hydroxymethyluracil Chemical compound OCC1=CNC(=O)NC1=O JDBGXEHEIRGOBU-UHFFFAOYSA-N 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- CELVMQZHFSJQJV-UHFFFAOYSA-N BrCC=1C(=NC=NC=1)Cl Chemical compound BrCC=1C(=NC=NC=1)Cl CELVMQZHFSJQJV-UHFFFAOYSA-N 0.000 description 3
- MTQHOWKZZNFZGT-GFCCVEGCSA-N C(C)(C)(C)NCC=1C(=NC(=NC=1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound C(C)(C)(C)NCC=1C(=NC(=NC=1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O MTQHOWKZZNFZGT-GFCCVEGCSA-N 0.000 description 3
- HDBVIMRLICNIHN-MRXNPFEDSA-N C(C)(C)(C)OC1CCN(CC1)CC=1C(=NC(=NC=1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound C(C)(C)(C)OC1CCN(CC1)CC=1C(=NC(=NC=1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O HDBVIMRLICNIHN-MRXNPFEDSA-N 0.000 description 3
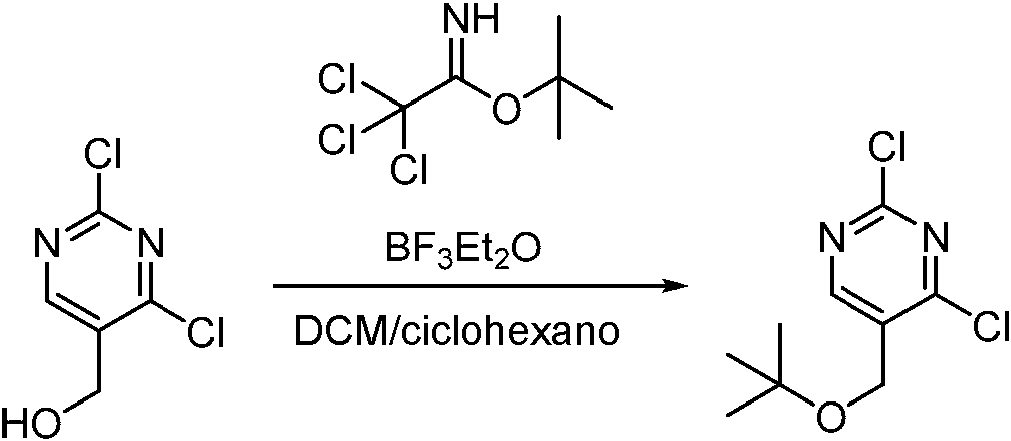
- XOACFSGKRSKQFZ-UHFFFAOYSA-N C(C)(C)(C)OCC=1C(=NC(=NC=1)Cl)Cl Chemical compound C(C)(C)(C)OCC=1C(=NC(=NC=1)Cl)Cl XOACFSGKRSKQFZ-UHFFFAOYSA-N 0.000 description 3
- ZNZAUCLAOHGMFG-NSHDSACASA-N CN(C)C[C@H]1NC(C2=C(C=3C=4C=CC(=NC=4C=CC=3S2)NC2=NC=NC(=C2)F)NC1)=O Chemical compound CN(C)C[C@H]1NC(C2=C(C=3C=4C=CC(=NC=4C=CC=3S2)NC2=NC=NC(=C2)F)NC1)=O ZNZAUCLAOHGMFG-NSHDSACASA-N 0.000 description 3
- KAWXGOCFLLRCOO-CYBMUJFWSA-N CN(CCN(C1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C1=NC=NC(=C1)F)C Chemical compound CN(CCN(C1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C1=NC=NC(=C1)F)C KAWXGOCFLLRCOO-CYBMUJFWSA-N 0.000 description 3
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 3
- MLOSZSZAOFIOHD-SECBINFHSA-N ClC1=CC(=NC(=N1)C)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=CC(=NC(=N1)C)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O MLOSZSZAOFIOHD-SECBINFHSA-N 0.000 description 3
- LDIVPNQIWIPVKY-SNVBAGLBSA-N ClC1=CC(=NC(=N1)COC)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=CC(=NC(=N1)COC)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O LDIVPNQIWIPVKY-SNVBAGLBSA-N 0.000 description 3
- BRCRRBUUZKIITM-UHFFFAOYSA-N ClC1=CC(=NC(=N1)OCCOC)N Chemical compound ClC1=CC(=NC(=N1)OCCOC)N BRCRRBUUZKIITM-UHFFFAOYSA-N 0.000 description 3
- XPDGEIMRHLXWBJ-CHWSQXEVSA-N ClC1=CC(=NC(=N1)O[C@H]1CN(CC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=CC(=NC(=N1)O[C@H]1CN(CC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O XPDGEIMRHLXWBJ-CHWSQXEVSA-N 0.000 description 3
- NOFJNUKFUPIGMZ-SECBINFHSA-N ClC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O NOFJNUKFUPIGMZ-SECBINFHSA-N 0.000 description 3
- SGXSWXXFRJOOBI-SECBINFHSA-N ClC1=CN=CC(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=CN=CC(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O SGXSWXXFRJOOBI-SECBINFHSA-N 0.000 description 3
- PHYXZHOULJWQGV-SECBINFHSA-N ClC1=NC(=CC(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CO Chemical compound ClC1=NC(=CC(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CO PHYXZHOULJWQGV-SECBINFHSA-N 0.000 description 3
- CPPDSBJOGLXXGW-OAHLLOKOSA-N ClC1=NC(=NC(=C1)OCCN1CCN(CC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC(=NC(=C1)OCCN1CCN(CC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O CPPDSBJOGLXXGW-OAHLLOKOSA-N 0.000 description 3
- QFWPZRYSEPLDPE-SECBINFHSA-N ClC1=NC(=NC=C1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC(=NC=C1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O QFWPZRYSEPLDPE-SECBINFHSA-N 0.000 description 3
- NTYSYYAFTJAFSZ-MRVPVSSYSA-N ClC1=NC=C(C(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C(=O)O Chemical compound ClC1=NC=C(C(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C(=O)O NTYSYYAFTJAFSZ-MRVPVSSYSA-N 0.000 description 3
- WZZFAHNHSXLEDK-GFCCVEGCSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1C=NC=CC=1 Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1C=NC=CC=1 WZZFAHNHSXLEDK-GFCCVEGCSA-N 0.000 description 3
- SDDLMLXRFFIOCS-OAHLLOKOSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN(C)C1CCCCC1 Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN(C)C1CCCCC1 SDDLMLXRFFIOCS-OAHLLOKOSA-N 0.000 description 3
- PYOQIOLRFIRRSO-LLVKDONJSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COCC Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COCC PYOQIOLRFIRRSO-LLVKDONJSA-N 0.000 description 3
- UPUFEYJEHMSMAU-GFCCVEGCSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COCCOC Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COCCOC UPUFEYJEHMSMAU-GFCCVEGCSA-N 0.000 description 3
- CNYJSZLEHVVWIM-SNVBAGLBSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CS(=O)(=O)C Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CS(=O)(=O)C CNYJSZLEHVVWIM-SNVBAGLBSA-N 0.000 description 3
- BOKXDPGNOCYZTM-SECBINFHSA-N ClC1=NC=CC(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC=CC(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O BOKXDPGNOCYZTM-SECBINFHSA-N 0.000 description 3
- PIIXTPQYNGPGDH-SECBINFHSA-N ClC1=NC=CC(=N1)SC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC=CC(=N1)SC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O PIIXTPQYNGPGDH-SECBINFHSA-N 0.000 description 3
- JVHOZUXGNLRJCA-LLVKDONJSA-N ClC=1N=C(C2=C(N=1)CCN(C2)C)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC=1N=C(C2=C(N=1)CCN(C2)C)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O JVHOZUXGNLRJCA-LLVKDONJSA-N 0.000 description 3
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 3
- VTCVFPKTUDXVRA-CQSZACIVSA-N FC1=CC(=NC(=N1)CN1CCN(CC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound FC1=CC(=NC(=N1)CN1CCN(CC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O VTCVFPKTUDXVRA-CQSZACIVSA-N 0.000 description 3
- DHKPTQDGFDWNEM-SNVBAGLBSA-N FC1=CC(=NC(=N1)OC1COC1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound FC1=CC(=NC(=N1)OC1COC1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O DHKPTQDGFDWNEM-SNVBAGLBSA-N 0.000 description 3
- KEZJJQMWYOAKCG-UHFFFAOYSA-N FC1=CC(=NC(=N1)OCCOC)N Chemical compound FC1=CC(=NC(=N1)OCCOC)N KEZJJQMWYOAKCG-UHFFFAOYSA-N 0.000 description 3
- NLVJBERCYZLYJC-SNVBAGLBSA-N FC1=CC(=NC=N1)N(C1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C Chemical compound FC1=CC(=NC=N1)N(C1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C NLVJBERCYZLYJC-SNVBAGLBSA-N 0.000 description 3
- JSRPHVISXUBQJD-GFCCVEGCSA-N FC1=CC(=NC=N1)N(C1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CCOC Chemical compound FC1=CC(=NC=N1)N(C1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CCOC JSRPHVISXUBQJD-GFCCVEGCSA-N 0.000 description 3
- RRCPUMPDKMAEEW-SECBINFHSA-N FC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound FC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O RRCPUMPDKMAEEW-SECBINFHSA-N 0.000 description 3
- OSCGIKXSEZMPLR-SNVBAGLBSA-N FC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)CNC)=O Chemical compound FC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)CNC)=O OSCGIKXSEZMPLR-SNVBAGLBSA-N 0.000 description 3
- ZFDIHXOMOVDUKM-SECBINFHSA-N FC1=CC(=NC=N1)SC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound FC1=CC(=NC=N1)SC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O ZFDIHXOMOVDUKM-SECBINFHSA-N 0.000 description 3
- LVDVOJSHQJZHHJ-RXMQYKEDSA-N FC1=NC(=CC(=N1)F)O[C@H]1COCC1 Chemical compound FC1=NC(=CC(=N1)F)O[C@H]1COCC1 LVDVOJSHQJZHHJ-RXMQYKEDSA-N 0.000 description 3
- HHNVLXOWTGBYPT-YFKPBYRVSA-N FC1=NC(=NC(=C1)F)O[C@@H]1COCC1 Chemical compound FC1=NC(=NC(=C1)F)O[C@@H]1COCC1 HHNVLXOWTGBYPT-YFKPBYRVSA-N 0.000 description 3
- 206010025323 Lymphomas Diseases 0.000 description 3
- 101710141394 MAP kinase-activated protein kinase 2 Proteins 0.000 description 3
- 241000124008 Mammalia Species 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 101100317378 Mus musculus Wnt3 gene Proteins 0.000 description 3
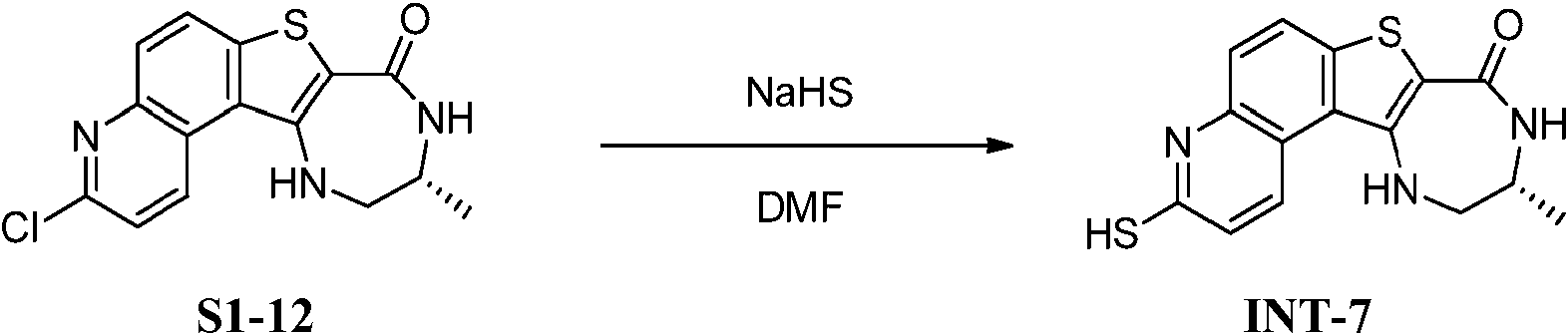
- DUBGTLWCQIHABF-SSDOTTSWSA-N NC[C@H]1NC(C2=C(C=3C=4C=CC(=NC=4C=CC=3S2)Cl)NC1)=O Chemical compound NC[C@H]1NC(C2=C(C=3C=4C=CC(=NC=4C=CC=3S2)Cl)NC1)=O DUBGTLWCQIHABF-SSDOTTSWSA-N 0.000 description 3
- 108010066154 Nuclear Export Signals Proteins 0.000 description 3
- 108010077850 Nuclear Localization Signals Proteins 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- 208000002193 Pain Diseases 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- 229930006000 Sucrose Natural products 0.000 description 3
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 3
- 206010052779 Transplant rejections Diseases 0.000 description 3
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 3
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 3
- 206010047115 Vasculitis Diseases 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- MJBWDEQAUQTVKK-IAGOWNOFSA-N aflatoxin M1 Chemical compound C=1([C@]2(O)C=CO[C@@H]2OC=1C=C(C1=2)OC)C=2OC(=O)C2=C1CCC2=O MJBWDEQAUQTVKK-IAGOWNOFSA-N 0.000 description 3
- 235000010443 alginic acid Nutrition 0.000 description 3
- 229920000615 alginic acid Chemical class 0.000 description 3
- 235000001014 amino acid Nutrition 0.000 description 3
- 229940024606 amino acid Drugs 0.000 description 3
- 229910021529 ammonia Inorganic materials 0.000 description 3
- 235000019270 ammonium chloride Nutrition 0.000 description 3
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 3
- MUALRAIOVNYAIW-UHFFFAOYSA-N binap Chemical compound C1=CC=CC=C1P(C=1C(=C2C=CC=CC2=CC=1)C=1C2=CC=CC=C2C=CC=1P(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 MUALRAIOVNYAIW-UHFFFAOYSA-N 0.000 description 3
- 210000004899 c-terminal region Anatomy 0.000 description 3
- 239000001768 carboxy methyl cellulose Substances 0.000 description 3
- 230000003197 catalytic effect Effects 0.000 description 3
- 230000036755 cellular response Effects 0.000 description 3
- 208000026106 cerebrovascular disease Diseases 0.000 description 3
- 238000004587 chromatography analysis Methods 0.000 description 3
- 230000001684 chronic effect Effects 0.000 description 3
- 210000000805 cytoplasm Anatomy 0.000 description 3
- 230000003111 delayed effect Effects 0.000 description 3
- 235000014113 dietary fatty acids Nutrition 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 125000005745 ethoxymethyl group Chemical group [H]C([H])([H])C([H])([H])OC([H])([H])* 0.000 description 3
- 239000000194 fatty acid Substances 0.000 description 3
- 229930195729 fatty acid Natural products 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 239000012065 filter cake Substances 0.000 description 3
- 235000013305 food Nutrition 0.000 description 3
- 235000019253 formic acid Nutrition 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 239000008187 granular material Substances 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- 238000000099 in vitro assay Methods 0.000 description 3
- 230000002779 inactivation Effects 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 230000002757 inflammatory effect Effects 0.000 description 3
- 239000000314 lubricant Substances 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 238000004949 mass spectrometry Methods 0.000 description 3
- JOJUSJUMORAJNN-UHFFFAOYSA-N methyl 4-amino-6-chloropyrimidine-2-carboxylate Chemical compound NC1=NC(=NC(=C1)Cl)C(=O)OC JOJUSJUMORAJNN-UHFFFAOYSA-N 0.000 description 3
- 239000002480 mineral oil Substances 0.000 description 3
- 235000010446 mineral oil Nutrition 0.000 description 3
- 108091005573 modified proteins Proteins 0.000 description 3
- 102000035118 modified proteins Human genes 0.000 description 3
- 235000005152 nicotinamide Nutrition 0.000 description 3
- 239000011570 nicotinamide Substances 0.000 description 3
- 229960003966 nicotinamide Drugs 0.000 description 3
- 239000002674 ointment Substances 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 3
- 239000008194 pharmaceutical composition Substances 0.000 description 3
- 235000021317 phosphate Nutrition 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 210000000664 rectum Anatomy 0.000 description 3
- 230000037390 scarring Effects 0.000 description 3
- 210000003491 skin Anatomy 0.000 description 3
- QDRKDTQENPPHOJ-LUIAAVAXSA-N sodium 1,1,2,2,2-pentadeuterioethanolate Chemical compound C(C([2H])([2H])[2H])([O-])([2H])[2H].[Na+] QDRKDTQENPPHOJ-LUIAAVAXSA-N 0.000 description 3
- 235000009518 sodium iodide Nutrition 0.000 description 3
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 3
- 239000008247 solid mixture Substances 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 239000005720 sucrose Substances 0.000 description 3
- 239000000829 suppository Substances 0.000 description 3
- 239000000375 suspending agent Substances 0.000 description 3
- YBRBMKDOPFTVDT-UHFFFAOYSA-N tert-butylamine Chemical compound CC(C)(C)N YBRBMKDOPFTVDT-UHFFFAOYSA-N 0.000 description 3
- DBAKEZYZWPGPHH-UHFFFAOYSA-N thieno[3,2-f]quinoline Chemical compound C1=CC=C2C(C=CS3)=C3C=CC2=N1 DBAKEZYZWPGPHH-UHFFFAOYSA-N 0.000 description 3
- GKTQKQTXHNUFSP-UHFFFAOYSA-N thieno[3,4-c]pyrrole-4,6-dione Chemical compound S1C=C2C(=O)NC(=O)C2=C1 GKTQKQTXHNUFSP-UHFFFAOYSA-N 0.000 description 3
- 210000001519 tissue Anatomy 0.000 description 3
- 239000000080 wetting agent Substances 0.000 description 3
- FLVFPAIGVBQGET-RXMQYKEDSA-N (3r)-1-methylpyrrolidin-3-ol Chemical group CN1CC[C@@H](O)C1 FLVFPAIGVBQGET-RXMQYKEDSA-N 0.000 description 2
- IDPURXSQCKYKIJ-UHFFFAOYSA-N 1-(4-methoxyphenyl)methanamine Chemical compound COC1=CC=C(CN)C=C1 IDPURXSQCKYKIJ-UHFFFAOYSA-N 0.000 description 2
- PVOAHINGSUIXLS-UHFFFAOYSA-N 1-Methylpiperazine Chemical group CN1CCNCC1 PVOAHINGSUIXLS-UHFFFAOYSA-N 0.000 description 2
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 2
- VLOODHWTRPYFIS-UHFFFAOYSA-N 2,4-dichloro-5-(chloromethyl)pyrimidine Chemical compound ClCC1=CN=C(Cl)N=C1Cl VLOODHWTRPYFIS-UHFFFAOYSA-N 0.000 description 2
- JKAPWXKZLYJQJJ-UHFFFAOYSA-N 2,4-dichloro-6-methoxy-1,3,5-triazine Chemical compound COC1=NC(Cl)=NC(Cl)=N1 JKAPWXKZLYJQJJ-UHFFFAOYSA-N 0.000 description 2
- MUEJUOUFUTUSED-UHFFFAOYSA-N 2,4-dichloro-6-piperidin-1-yl-1,3,5-triazine Chemical compound ClC1=NC(Cl)=NC(N2CCCCC2)=N1 MUEJUOUFUTUSED-UHFFFAOYSA-N 0.000 description 2
- BHWWVJLPSHEQBF-UHFFFAOYSA-N 2,4-dichloro-6-pyrrolidin-1-yl-1,3,5-triazine Chemical compound ClC1=NC(Cl)=NC(N2CCCC2)=N1 BHWWVJLPSHEQBF-UHFFFAOYSA-N 0.000 description 2
- BTTNYQZNBZNDOR-UHFFFAOYSA-N 2,4-dichloropyrimidine Chemical group ClC1=CC=NC(Cl)=N1 BTTNYQZNBZNDOR-UHFFFAOYSA-N 0.000 description 2
- QTMPYFZNWHQZAZ-UHFFFAOYSA-N 2-(methoxymethyl)pyrrolidine;hydrochloride Chemical compound Cl.COCC1CCCN1 QTMPYFZNWHQZAZ-UHFFFAOYSA-N 0.000 description 2
- JSAKBYXSHKYFQU-UHFFFAOYSA-N 2-fluoropyridin-4-amine Chemical compound NC1=CC=NC(F)=C1 JSAKBYXSHKYFQU-UHFFFAOYSA-N 0.000 description 2
- LEHHIPIDKQVNEV-UHFFFAOYSA-N 3,3-difluoropiperidine;hydrochloride Chemical group Cl.FC1(F)CCCNC1 LEHHIPIDKQVNEV-UHFFFAOYSA-N 0.000 description 2
- MTJGVAJYTOXFJH-UHFFFAOYSA-N 3-aminonaphthalene-1,5-disulfonic acid Chemical compound C1=CC=C(S(O)(=O)=O)C2=CC(N)=CC(S(O)(=O)=O)=C21 MTJGVAJYTOXFJH-UHFFFAOYSA-N 0.000 description 2
- DHDPUVPGALXWOL-UHFFFAOYSA-N 3-methyloxetan-3-ol Chemical compound CC1(O)COC1 DHDPUVPGALXWOL-UHFFFAOYSA-N 0.000 description 2
- ITRGRVVBODKGCW-UHFFFAOYSA-N 4,6-dichloro-n,n-dimethyl-1,3,5-triazin-2-amine Chemical compound CN(C)C1=NC(Cl)=NC(Cl)=N1 ITRGRVVBODKGCW-UHFFFAOYSA-N 0.000 description 2
- UQAMDAUJTXFNAD-UHFFFAOYSA-N 4-(4,6-dichloro-1,3,5-triazin-2-yl)morpholine Chemical compound ClC1=NC(Cl)=NC(N2CCOCC2)=N1 UQAMDAUJTXFNAD-UHFFFAOYSA-N 0.000 description 2
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 2
- PSLFYIQTJUMHSA-UHFFFAOYSA-N 4-chloro-6-(2-methoxyethoxy)pyrimidin-2-amine Chemical compound COCCOC1=CC(Cl)=NC(N)=N1 PSLFYIQTJUMHSA-UHFFFAOYSA-N 0.000 description 2
- TVHRQDVVPKXZOZ-UHFFFAOYSA-N 6-chloro-4-iodopyridine-3-carbonitrile Chemical compound ClC1=CC(I)=C(C#N)C=N1 TVHRQDVVPKXZOZ-UHFFFAOYSA-N 0.000 description 2
- DUKKRSPKJMHASP-UHFFFAOYSA-N 6-chloropyrimidin-4-amine Chemical group NC1=CC(Cl)=NC=N1 DUKKRSPKJMHASP-UHFFFAOYSA-N 0.000 description 2
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 2
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 2
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 description 2
- 208000024827 Alzheimer disease Diseases 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical class [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical class OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 201000001320 Atherosclerosis Diseases 0.000 description 2
- 208000008439 Biliary Liver Cirrhosis Diseases 0.000 description 2
- 208000033222 Biliary cirrhosis primary Diseases 0.000 description 2
- 208000020084 Bone disease Diseases 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- YHZFUHUOOZQFRM-MRVPVSSYSA-N BrC=1C(=NC(=NC=1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound BrC=1C(=NC(=NC=1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O YHZFUHUOOZQFRM-MRVPVSSYSA-N 0.000 description 2
- XAMXPLHGOXKZFT-CYBMUJFWSA-N C(C)(C)(C)N(C)CC1=CC(=NC(=N1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound C(C)(C)(C)N(C)CC1=CC(=NC(=N1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O XAMXPLHGOXKZFT-CYBMUJFWSA-N 0.000 description 2
- KGHQIDGOBDBPCV-CYBMUJFWSA-N C(C)(C)(C)N(C)CC=1C(=NC(=NC=1)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound C(C)(C)(C)N(C)CC=1C(=NC(=NC=1)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O KGHQIDGOBDBPCV-CYBMUJFWSA-N 0.000 description 2
- RBIYSEAHGKWJDG-GFCCVEGCSA-N C(C)(C)(C)NCC1=CC(=NC(=N1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound C(C)(C)(C)NCC1=CC(=NC(=N1)Cl)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O RBIYSEAHGKWJDG-GFCCVEGCSA-N 0.000 description 2
- NZIGRCNEXPKYBO-UHFFFAOYSA-N C(C)(C)(C)OC1CCN(CC1)CC=1C(=NC(=NC=1)Cl)Cl Chemical compound C(C)(C)(C)OC1CCN(CC1)CC=1C(=NC(=NC=1)Cl)Cl NZIGRCNEXPKYBO-UHFFFAOYSA-N 0.000 description 2
- UJGAASKGPUZGIA-LLVKDONJSA-N C(C)OCC=1C(=NC(=NC=1)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound C(C)OCC=1C(=NC(=NC=1)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O UJGAASKGPUZGIA-LLVKDONJSA-N 0.000 description 2
- LBLVYDSCHIARCI-GFCCVEGCSA-N CN(CCOC1=NC(=CC(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)F)C Chemical compound CN(CCOC1=NC(=CC(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)F)C LBLVYDSCHIARCI-GFCCVEGCSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 2
- CJRFNAZXQXTXRS-ZCFIWIBFSA-N ClC1=CC(=NC(=N1)O[C@H]1CN(CC1)C)N Chemical compound ClC1=CC(=NC(=N1)O[C@H]1CN(CC1)C)N CJRFNAZXQXTXRS-ZCFIWIBFSA-N 0.000 description 2
- DTQNXEBTPZTFFY-VIFPVBQESA-N ClC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)CO)=O Chemical compound ClC1=CC(=NC=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)CO)=O DTQNXEBTPZTFFY-VIFPVBQESA-N 0.000 description 2
- WYBPKJAEUICHHC-SNVBAGLBSA-N ClC1=NC(=NC(=N1)N1CC(CC1)(F)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC(=NC(=N1)N1CC(CC1)(F)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O WYBPKJAEUICHHC-SNVBAGLBSA-N 0.000 description 2
- LNZPJJIETFUYFU-LLVKDONJSA-N ClC1=NC(=NC(=N1)N1CC(CCC1)(F)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC(=NC(=N1)N1CC(CCC1)(F)F)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O LNZPJJIETFUYFU-LLVKDONJSA-N 0.000 description 2
- JQWJACJTSFCQKI-LLVKDONJSA-N ClC1=NC(=NC(=N1)N1CCCC1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC(=NC(=N1)N1CCCC1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O JQWJACJTSFCQKI-LLVKDONJSA-N 0.000 description 2
- RQRVGVOXRWJDCU-LLVKDONJSA-N ClC1=NC(=NC(=N1)N1CCOCC1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC(=NC(=N1)N1CCOCC1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O RQRVGVOXRWJDCU-LLVKDONJSA-N 0.000 description 2
- DHAOQLQJIZSIJI-MRVPVSSYSA-N ClC1=NC(=NC(=N1)OC)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC(=NC(=N1)OC)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O DHAOQLQJIZSIJI-MRVPVSSYSA-N 0.000 description 2
- TZRBRFDJTHETEI-ZETCQYMHSA-N ClC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)CO)=O Chemical compound ClC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)CO)=O TZRBRFDJTHETEI-ZETCQYMHSA-N 0.000 description 2
- NZZNEILQTNHBBX-LLVKDONJSA-N ClC1=NC=2CCCCC=2C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC=2CCCCC=2C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O NZZNEILQTNHBBX-LLVKDONJSA-N 0.000 description 2
- OUWILTNPMMHZLG-UHFFFAOYSA-N ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OC(C)C Chemical compound ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OC(C)C OUWILTNPMMHZLG-UHFFFAOYSA-N 0.000 description 2
- BEVGUJPCQQWNEZ-FIBGUPNXSA-N ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OC([2H])([2H])[2H] Chemical compound ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OC([2H])([2H])[2H] BEVGUJPCQQWNEZ-FIBGUPNXSA-N 0.000 description 2
- DDQSQZOFOWEZJS-UHFFFAOYSA-N ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OCCO Chemical compound ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OCCO DDQSQZOFOWEZJS-UHFFFAOYSA-N 0.000 description 2
- CTYBMGRKOQKYBU-UHFFFAOYSA-N ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OCCOC Chemical compound ClC1=NC=C(C(=N1)Cl)CN1CCC(CC1)OCCOC CTYBMGRKOQKYBU-UHFFFAOYSA-N 0.000 description 2
- RZVUFAWKJMGXSK-ZBJDZAJPSA-N ClC1=NC=C(C(=N1)Cl)COC(C([2H])([2H])[2H])([2H])[2H] Chemical compound ClC1=NC=C(C(=N1)Cl)COC(C([2H])([2H])[2H])([2H])[2H] RZVUFAWKJMGXSK-ZBJDZAJPSA-N 0.000 description 2
- PXLNZVUGYJIUBK-UHFFFAOYSA-N ClC1=NC=C(C(=N1)Cl)COC(F)F Chemical compound ClC1=NC=C(C(=N1)Cl)COC(F)F PXLNZVUGYJIUBK-UHFFFAOYSA-N 0.000 description 2
- NACNPDUPSRAROD-UHFFFAOYSA-N ClC1=NC=C(C(=N1)Cl)CS(=O)(=O)C Chemical compound ClC1=NC=C(C(=N1)Cl)CS(=O)(=O)C NACNPDUPSRAROD-UHFFFAOYSA-N 0.000 description 2
- OCJLUCCJOUHBMA-ZIAGYGMSSA-N ClC1=NC=C(C(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C(=O)N1C[C@@H](CC1)N(C)C Chemical compound ClC1=NC=C(C(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C(=O)N1C[C@@H](CC1)N(C)C OCJLUCCJOUHBMA-ZIAGYGMSSA-N 0.000 description 2
- GGRVHLKSLQGTLJ-CYBMUJFWSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1CCN(CC=1)C Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1CCN(CC=1)C GGRVHLKSLQGTLJ-CYBMUJFWSA-N 0.000 description 2
- LGKGLONKFKWJLR-GFCCVEGCSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1CCNCC=1 Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1CCNCC=1 LGKGLONKFKWJLR-GFCCVEGCSA-N 0.000 description 2
- OUTSQWFHNHRBCJ-GFCCVEGCSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1CCOCC=1 Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)C=1CCOCC=1 OUTSQWFHNHRBCJ-GFCCVEGCSA-N 0.000 description 2
- GIPBOZMOWOAZDM-CYBMUJFWSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN(C)C(C)C Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN(C)C(C)C GIPBOZMOWOAZDM-CYBMUJFWSA-N 0.000 description 2
- BVEMSYVDIREACR-CQSZACIVSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN(C)CCOCC Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN(C)CCOCC BVEMSYVDIREACR-CQSZACIVSA-N 0.000 description 2
- JVXBEOTZJXTVEE-IURRXHLWSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1C(CCC1)COC Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1C(CCC1)COC JVXBEOTZJXTVEE-IURRXHLWSA-N 0.000 description 2
- LSHMLZHKOMGAGQ-CQSZACIVSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1CCC(CC1)OC Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1CCC(CC1)OC LSHMLZHKOMGAGQ-CQSZACIVSA-N 0.000 description 2
- DIZIEKQMCRPZBZ-OAHLLOKOSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1CCC(CC1)OCCF Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1CCC(CC1)OCCF DIZIEKQMCRPZBZ-OAHLLOKOSA-N 0.000 description 2
- SMHCFHCHCNRWPY-OAHLLOKOSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1CCN(CC1)CC Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1CCN(CC1)CC SMHCFHCHCNRWPY-OAHLLOKOSA-N 0.000 description 2
- HJVGCIZMOXPWEC-GDBMZVCRSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1C[C@@H](CCC1)OC Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CN1C[C@@H](CCC1)OC HJVGCIZMOXPWEC-GDBMZVCRSA-N 0.000 description 2
- PJUGIHAOHKLRPM-SECBINFHSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CO Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)CO PJUGIHAOHKLRPM-SECBINFHSA-N 0.000 description 2
- OAWIWQKQAJPDRU-GFCCVEGCSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COC1(COC1)C Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COC1(COC1)C OAWIWQKQAJPDRU-GFCCVEGCSA-N 0.000 description 2
- NZEBXRUNHXMTRL-SNVBAGLBSA-N ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COCC(F)F Chemical compound ClC1=NC=C(C(=N1)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)COCC(F)F NZEBXRUNHXMTRL-SNVBAGLBSA-N 0.000 description 2
- QJZDJDAKEDVGHV-SECBINFHSA-N ClC1=NC=CC(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC=CC(=N1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O QJZDJDAKEDVGHV-SECBINFHSA-N 0.000 description 2
- DRJYNMIMWHMTKP-UHFFFAOYSA-N ClC1=NC=NC=C1CN(C(C)(C)C)C Chemical compound ClC1=NC=NC=C1CN(C(C)(C)C)C DRJYNMIMWHMTKP-UHFFFAOYSA-N 0.000 description 2
- PHEDXBVPIONUQT-UHFFFAOYSA-N Cocarcinogen A1 Natural products CCCCCCCCCCCCCC(=O)OC1C(C)C2(O)C3C=C(C)C(=O)C3(O)CC(CO)=CC2C2C1(OC(C)=O)C2(C)C PHEDXBVPIONUQT-UHFFFAOYSA-N 0.000 description 2
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 2
- 229910021590 Copper(II) bromide Inorganic materials 0.000 description 2
- 229920002261 Corn starch Polymers 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- QLVXRVVIOFDQDX-UHFFFAOYSA-N FC1(F)CCCN(C1)C1=NC(Cl)=NC(Cl)=N1 Chemical compound FC1(F)CCCN(C1)C1=NC(Cl)=NC(Cl)=N1 QLVXRVVIOFDQDX-UHFFFAOYSA-N 0.000 description 2
- FTNYJYIJPYLOHR-UHFFFAOYSA-N FC1(F)CCN(C1)C1=NC(Cl)=NC(Cl)=N1 Chemical compound FC1(F)CCN(C1)C1=NC(Cl)=NC(Cl)=N1 FTNYJYIJPYLOHR-UHFFFAOYSA-N 0.000 description 2
- LKYDLVYHHTVZPA-UHFFFAOYSA-N FC1=CC(=NC(=N1)CN1CCN(CC1)C)N Chemical compound FC1=CC(=NC(=N1)CN1CCN(CC1)C)N LKYDLVYHHTVZPA-UHFFFAOYSA-N 0.000 description 2
- SDCOHVYOCKQZPG-UHFFFAOYSA-N FC1=CC(=NC(=N1)OC1COC1)N Chemical compound FC1=CC(=NC(=N1)OC1COC1)N SDCOHVYOCKQZPG-UHFFFAOYSA-N 0.000 description 2
- JWWUUHYQISHKGO-UHFFFAOYSA-N FC1=CC(=NC(=N1)OCC1(COC1)C)N Chemical compound FC1=CC(=NC(=N1)OCC1(COC1)C)N JWWUUHYQISHKGO-UHFFFAOYSA-N 0.000 description 2
- KLTJZNSGAGNMIR-YFKPBYRVSA-N FC1=CC(=NC(=N1)O[C@@H]1COCC1)N Chemical compound FC1=CC(=NC(=N1)O[C@@H]1COCC1)N KLTJZNSGAGNMIR-YFKPBYRVSA-N 0.000 description 2
- BZNBGRZOZXDDPU-ZCFIWIBFSA-N FC1=CC(=NC(=N1)O[C@H]1CN(CC1)C)N Chemical compound FC1=CC(=NC(=N1)O[C@H]1CN(CC1)C)N BZNBGRZOZXDDPU-ZCFIWIBFSA-N 0.000 description 2
- PWLFMHFCKGVOMR-UHFFFAOYSA-N FC1=NC(=CC(=N1)F)OCC1(COC1)C Chemical compound FC1=NC(=CC(=N1)F)OCC1(COC1)C PWLFMHFCKGVOMR-UHFFFAOYSA-N 0.000 description 2
- LVDVOJSHQJZHHJ-YFKPBYRVSA-N FC1=NC(=CC(=N1)F)O[C@@H]1COCC1 Chemical compound FC1=NC(=CC(=N1)F)O[C@@H]1COCC1 LVDVOJSHQJZHHJ-YFKPBYRVSA-N 0.000 description 2
- VUBZZMPJLPVTTE-UHFFFAOYSA-N FC1=NC(=CC(=N1)OCCN(C)C)F Chemical compound FC1=NC(=CC(=N1)OCCN(C)C)F VUBZZMPJLPVTTE-UHFFFAOYSA-N 0.000 description 2
- NFTUSOXNNNJSRB-UHFFFAOYSA-N FC1=NC(=NC(=C1)F)OCCN(C)C Chemical compound FC1=NC(=NC(=C1)F)OCCN(C)C NFTUSOXNNNJSRB-UHFFFAOYSA-N 0.000 description 2
- WRQAPBWDQDEZIS-UHFFFAOYSA-N FC1=NC(=NC(=C1)F)OCCOC Chemical compound FC1=NC(=NC(=C1)F)OCCOC WRQAPBWDQDEZIS-UHFFFAOYSA-N 0.000 description 2
- NKANYCPCMZPNTO-UHFFFAOYSA-N FC1=NC(=NC(=C1)OC1COC1)N Chemical compound FC1=NC(=NC(=C1)OC1COC1)N NKANYCPCMZPNTO-UHFFFAOYSA-N 0.000 description 2
- UZQNKULUNUVSCZ-UHFFFAOYSA-N FC1=NC(=NC(=C1)OCC1(COC1)C)N Chemical compound FC1=NC(=NC(=C1)OCC1(COC1)C)N UZQNKULUNUVSCZ-UHFFFAOYSA-N 0.000 description 2
- XHFJSSYFRSWSMH-UHFFFAOYSA-N FC1=NC(=NC(=C1)OCCOC)N Chemical compound FC1=NC(=NC(=C1)OCCOC)N XHFJSSYFRSWSMH-UHFFFAOYSA-N 0.000 description 2
- JQLIRMSINVJPEJ-YFKPBYRVSA-N FC1=NC(=NC(=C1)O[C@@H]1COCC1)N Chemical compound FC1=NC(=NC(=C1)O[C@@H]1COCC1)N JQLIRMSINVJPEJ-YFKPBYRVSA-N 0.000 description 2
- QKTDVOFUQDXANO-VXGBXAGGSA-N FC1=NC(=NC(=C1)O[C@H]1COCC1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound FC1=NC(=NC(=C1)O[C@H]1COCC1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O QKTDVOFUQDXANO-VXGBXAGGSA-N 0.000 description 2
- 201000008808 Fibrosarcoma Diseases 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical class OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- 208000007465 Giant cell arteritis Diseases 0.000 description 2
- 208000032612 Glial tumor Diseases 0.000 description 2
- 206010018338 Glioma Diseases 0.000 description 2
- 206010018364 Glomerulonephritis Diseases 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 208000017604 Hodgkin disease Diseases 0.000 description 2
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- 201000009794 Idiopathic Pulmonary Fibrosis Diseases 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- 102000004889 Interleukin-6 Human genes 0.000 description 2
- 108090001005 Interleukin-6 Proteins 0.000 description 2
- 206010059176 Juvenile idiopathic arthritis Diseases 0.000 description 2
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 2
- GTNDXUXKZFKVRN-SECBINFHSA-N NC[C@H]1NC(C2=C(C=3C=4C=CC(=NC=4C=CC=3S2)NC2=NC=NC(=C2)Cl)NC1)=O Chemical compound NC[C@H]1NC(C2=C(C=3C=4C=CC(=NC=4C=CC=3S2)NC2=NC=NC(=C2)Cl)NC1)=O GTNDXUXKZFKVRN-SECBINFHSA-N 0.000 description 2
- 229910002651 NO3 Inorganic materials 0.000 description 2
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 206010035664 Pneumonia Diseases 0.000 description 2
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 2
- 208000012654 Primary biliary cholangitis Diseases 0.000 description 2
- 101710092489 Protein kinase 2 Proteins 0.000 description 2
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 description 2
- 206010040047 Sepsis Diseases 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 2
- 201000009594 Systemic Scleroderma Diseases 0.000 description 2
- 206010042953 Systemic sclerosis Diseases 0.000 description 2
- 206010044248 Toxic shock syndrome Diseases 0.000 description 2
- 231100000650 Toxic shock syndrome Toxicity 0.000 description 2
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 2
- PYOQIOLRFIRRSO-CAURYLKOSA-N [2H]C([2H])([2H])C([2H])([2H])OCC1=C(OC2=CC=C3C4=C(SC5=C4NC[C@@H](C)NC5=O)C=CC3=N2)N=C(Cl)N=C1 Chemical compound [2H]C([2H])([2H])C([2H])([2H])OCC1=C(OC2=CC=C3C4=C(SC5=C4NC[C@@H](C)NC5=O)C=CC3=N2)N=C(Cl)N=C1 PYOQIOLRFIRRSO-CAURYLKOSA-N 0.000 description 2
- LSHMLZHKOMGAGQ-ROXCVRLESA-N [2H]C([2H])([2H])OC1CCN(CC2=C(OC3=CC=C4C5=C(SC6=C5NC[C@@H](C)NC6=O)C=CC4=N3)N=C(Cl)N=C2)CC1 Chemical compound [2H]C([2H])([2H])OC1CCN(CC2=C(OC3=CC=C4C5=C(SC6=C5NC[C@@H](C)NC6=O)C=CC4=N3)N=C(Cl)N=C2)CC1 LSHMLZHKOMGAGQ-ROXCVRLESA-N 0.000 description 2
- 230000002159 abnormal effect Effects 0.000 description 2
- 201000000028 adult respiratory distress syndrome Diseases 0.000 description 2
- 230000001476 alcoholic effect Effects 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- XXROGKLTLUQVRX-UHFFFAOYSA-N allyl alcohol Chemical compound OCC=C XXROGKLTLUQVRX-UHFFFAOYSA-N 0.000 description 2
- 239000000908 ammonium hydroxide Substances 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000012911 assay medium Substances 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 230000005784 autoimmunity Effects 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- SESFRYSPDFLNCH-UHFFFAOYSA-N benzyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1=CC=CC=C1 SESFRYSPDFLNCH-UHFFFAOYSA-N 0.000 description 2
- 229920002988 biodegradable polymer Polymers 0.000 description 2
- 239000004621 biodegradable polymer Substances 0.000 description 2
- 239000012455 biphasic mixture Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 239000006172 buffering agent Substances 0.000 description 2
- 235000019437 butane-1,3-diol Nutrition 0.000 description 2
- 239000006227 byproduct Substances 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 239000004359 castor oil Substances 0.000 description 2
- 230000007882 cirrhosis Effects 0.000 description 2
- 229940110456 cocoa butter Drugs 0.000 description 2
- 235000019868 cocoa butter Nutrition 0.000 description 2
- 239000013068 control sample Substances 0.000 description 2
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 2
- 239000008120 corn starch Substances 0.000 description 2
- 229940099112 cornstarch Drugs 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 201000001981 dermatomyositis Diseases 0.000 description 2
- 238000003795 desorption Methods 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- RAABOESOVLLHRU-UHFFFAOYSA-N diazene Chemical compound N=N RAABOESOVLLHRU-UHFFFAOYSA-N 0.000 description 2
- 229910000071 diazene Inorganic materials 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical class CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 2
- 229940043264 dodecyl sulfate Drugs 0.000 description 2
- 239000008298 dragée Substances 0.000 description 2
- 230000002526 effect on cardiovascular system Effects 0.000 description 2
- 230000001804 emulsifying effect Effects 0.000 description 2
- 238000003821 enantio-separation Methods 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 239000002702 enteric coating Substances 0.000 description 2
- 238000009505 enteric coating Methods 0.000 description 2
- VFRSADQPWYCXDG-LEUCUCNGSA-N ethyl (2s,5s)-5-methylpyrrolidine-2-carboxylate;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.CCOC(=O)[C@@H]1CC[C@H](C)N1 VFRSADQPWYCXDG-LEUCUCNGSA-N 0.000 description 2
- SRJBDGLSCPDXBL-UHFFFAOYSA-N ethyl 2,4-dichloropyrimidine-5-carboxylate Chemical compound CCOC(=O)C1=CN=C(Cl)N=C1Cl SRJBDGLSCPDXBL-UHFFFAOYSA-N 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- 206010016629 fibroma Diseases 0.000 description 2
- 230000004761 fibrosis Effects 0.000 description 2
- 238000011049 filling Methods 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 239000012458 free base Substances 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 230000002496 gastric effect Effects 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 238000007429 general method Methods 0.000 description 2
- 239000012362 glacial acetic acid Substances 0.000 description 2
- 125000005456 glyceride group Chemical group 0.000 description 2
- 208000024908 graft versus host disease Diseases 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 229940093915 gynecological organic acid Drugs 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 239000007972 injectable composition Substances 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- 229940100601 interleukin-6 Drugs 0.000 description 2
- 208000036971 interstitial lung disease 2 Diseases 0.000 description 2
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 2
- OWFXIOWLTKNBAP-UHFFFAOYSA-N isoamyl nitrite Chemical compound CC(C)CCON=O OWFXIOWLTKNBAP-UHFFFAOYSA-N 0.000 description 2
- 208000017169 kidney disease Diseases 0.000 description 2
- 239000008297 liquid dosage form Substances 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 238000000816 matrix-assisted laser desorption--ionisation Methods 0.000 description 2
- 201000001441 melanoma Diseases 0.000 description 2
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 2
- 239000004530 micro-emulsion Substances 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- DXASQZJWWGZNSF-UHFFFAOYSA-N n,n-dimethylmethanamine;sulfur trioxide Chemical group CN(C)C.O=S(=O)=O DXASQZJWWGZNSF-UHFFFAOYSA-N 0.000 description 2
- 210000003739 neck Anatomy 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 231100000344 non-irritating Toxicity 0.000 description 2
- 239000000346 nonvolatile oil Substances 0.000 description 2
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 2
- 239000004006 olive oil Substances 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 description 2
- 230000000737 periodic effect Effects 0.000 description 2
- 206010034674 peritonitis Diseases 0.000 description 2
- 235000019271 petrolatum Nutrition 0.000 description 2
- 210000003800 pharynx Anatomy 0.000 description 2
- PHEDXBVPIONUQT-RGYGYFBISA-N phorbol 13-acetate 12-myristate Chemical compound C([C@]1(O)C(=O)C(C)=C[C@H]1[C@@]1(O)[C@H](C)[C@H]2OC(=O)CCCCCCCCCCCCC)C(CO)=C[C@H]1[C@H]1[C@]2(OC(C)=O)C1(C)C PHEDXBVPIONUQT-RGYGYFBISA-N 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- FVSKHRXBFJPNKK-UHFFFAOYSA-N propionitrile Chemical compound CCC#N FVSKHRXBFJPNKK-UHFFFAOYSA-N 0.000 description 2
- 229960004063 propylene glycol Drugs 0.000 description 2
- 210000002307 prostate Anatomy 0.000 description 2
- 125000004528 pyrimidin-5-yl group Chemical group N1=CN=CC(=C1)* 0.000 description 2
- YPOXGDJGKBXRFP-UHFFFAOYSA-M pyrimidine-4-carboxylate Chemical compound [O-]C(=O)C1=CC=NC=N1 YPOXGDJGKBXRFP-UHFFFAOYSA-M 0.000 description 2
- XVIAPHVAGFEFFN-UHFFFAOYSA-N pyrimidine-5-carbonitrile Chemical compound N#CC1=CN=CN=C1 XVIAPHVAGFEFFN-UHFFFAOYSA-N 0.000 description 2
- 208000002574 reactive arthritis Diseases 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 201000009410 rhabdomyosarcoma Diseases 0.000 description 2
- 206010039073 rheumatoid arthritis Diseases 0.000 description 2
- 238000002390 rotary evaporation Methods 0.000 description 2
- 201000000306 sarcoidosis Diseases 0.000 description 2
- PCMORTLOPMLEFB-ONEGZZNKSA-N sinapic acid Chemical compound COC1=CC(\C=C\C(O)=O)=CC(OC)=C1O PCMORTLOPMLEFB-ONEGZZNKSA-N 0.000 description 2
- PCMORTLOPMLEFB-UHFFFAOYSA-N sinapinic acid Natural products COC1=CC(C=CC(O)=O)=CC(OC)=C1O PCMORTLOPMLEFB-UHFFFAOYSA-N 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000012279 sodium borohydride Substances 0.000 description 2
- 229910000033 sodium borohydride Inorganic materials 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- 238000000527 sonication Methods 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 208000020431 spinal cord injury Diseases 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 239000011550 stock solution Substances 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N succinic acid Chemical compound OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- 239000003765 sweetening agent Substances 0.000 description 2
- 206010043207 temporal arteritis Diseases 0.000 description 2
- IOGXOCVLYRDXLW-UHFFFAOYSA-N tert-butyl nitrite Chemical compound CC(C)(C)ON=O IOGXOCVLYRDXLW-UHFFFAOYSA-N 0.000 description 2
- 239000012414 tert-butyl nitrite Substances 0.000 description 2
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 2
- 230000001960 triggered effect Effects 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- LSPHULWDVZXLIL-UHFFFAOYSA-N (+/-)-Camphoric acid Chemical class CC1(C)C(C(O)=O)CCC1(C)C(O)=O LSPHULWDVZXLIL-UHFFFAOYSA-N 0.000 description 1
- VCGRFBXVSFAGGA-UHFFFAOYSA-N (1,1-dioxo-1,4-thiazinan-4-yl)-[6-[[3-(4-fluorophenyl)-5-methyl-1,2-oxazol-4-yl]methoxy]pyridin-3-yl]methanone Chemical compound CC=1ON=C(C=2C=CC(F)=CC=2)C=1COC(N=C1)=CC=C1C(=O)N1CCS(=O)(=O)CC1 VCGRFBXVSFAGGA-UHFFFAOYSA-N 0.000 description 1
- MXZROAOUCUVNHX-GSVOUGTGSA-N (1r)-1-aminopropan-1-ol Chemical compound CC[C@H](N)O MXZROAOUCUVNHX-GSVOUGTGSA-N 0.000 description 1
- YFWAJBZGZRKMJQ-UHFFFAOYSA-N (2,4-dichloropyrimidin-5-yl)methanol Chemical compound OCC1=CN=C(Cl)N=C1Cl YFWAJBZGZRKMJQ-UHFFFAOYSA-N 0.000 description 1
- SSCSSDNTQJGTJT-UHFFFAOYSA-N (3,6-dihydroxy-1-methyl-2,3-dihydroindol-5-yl)iminourea Chemical compound CN1CC(O)C2=CC(N=NC(N)=O)=C(O)C=C12 SSCSSDNTQJGTJT-UHFFFAOYSA-N 0.000 description 1
- AVAWMINJNRAQFS-ZCFIWIBFSA-N (3r)-n,n-dimethylpyrrolidin-3-amine Chemical compound CN(C)[C@@H]1CCNC1 AVAWMINJNRAQFS-ZCFIWIBFSA-N 0.000 description 1
- XDPCNPCKDGQBAN-SCSAIBSYSA-N (3r)-oxolan-3-ol Chemical group O[C@@H]1CCOC1 XDPCNPCKDGQBAN-SCSAIBSYSA-N 0.000 description 1
- XDPCNPCKDGQBAN-BYPYZUCNSA-N (3s)-oxolan-3-ol Chemical group O[C@H]1CCOC1 XDPCNPCKDGQBAN-BYPYZUCNSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- DQXKOHDUMJLXKH-PHEQNACWSA-N (e)-n-[2-[2-[[(e)-oct-2-enoyl]amino]ethyldisulfanyl]ethyl]oct-2-enamide Chemical compound CCCCC\C=C\C(=O)NCCSSCCNC(=O)\C=C\CCCCC DQXKOHDUMJLXKH-PHEQNACWSA-N 0.000 description 1
- MOWXJLUYGFNTAL-DEOSSOPVSA-N (s)-[2-chloro-4-fluoro-5-(7-morpholin-4-ylquinazolin-4-yl)phenyl]-(6-methoxypyridazin-3-yl)methanol Chemical compound N1=NC(OC)=CC=C1[C@@H](O)C1=CC(C=2C3=CC=C(C=C3N=CN=2)N2CCOCC2)=C(F)C=C1Cl MOWXJLUYGFNTAL-DEOSSOPVSA-N 0.000 description 1
- LRANPJDWHYRCER-UHFFFAOYSA-N 1,2-diazepine Chemical compound N1C=CC=CC=N1 LRANPJDWHYRCER-UHFFFAOYSA-N 0.000 description 1
- 229940058015 1,3-butylene glycol Drugs 0.000 description 1
- ABDDQTDRAHXHOC-QMMMGPOBSA-N 1-[(7s)-5,7-dihydro-4h-thieno[2,3-c]pyran-7-yl]-n-methylmethanamine Chemical compound CNC[C@@H]1OCCC2=C1SC=C2 ABDDQTDRAHXHOC-QMMMGPOBSA-N 0.000 description 1
- JOHXQRCYGMOSFR-UHFFFAOYSA-N 1-azidopropan-2-ylcarbamic acid Chemical compound OC(=O)NC(C)CN=[N+]=[N-] JOHXQRCYGMOSFR-UHFFFAOYSA-N 0.000 description 1
- CZZCIUKNDIAFKX-UHFFFAOYSA-N 1-hydroxypropan-2-ylcarbamic acid Chemical compound OCC(C)NC(O)=O CZZCIUKNDIAFKX-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- POXWDTQUDZUOGP-UHFFFAOYSA-N 1h-1,4-diazepine Chemical compound N1C=CC=NC=C1 POXWDTQUDZUOGP-UHFFFAOYSA-N 0.000 description 1
- VYDQUABHDFWIIX-UHFFFAOYSA-N 2,2-difluoro-2-fluorosulfonylacetic acid Chemical compound OC(=O)C(F)(F)S(F)(=O)=O VYDQUABHDFWIIX-UHFFFAOYSA-N 0.000 description 1
- DPVIABCMTHHTGB-UHFFFAOYSA-N 2,4,6-trichloropyrimidine Chemical compound ClC1=CC(Cl)=NC(Cl)=N1 DPVIABCMTHHTGB-UHFFFAOYSA-N 0.000 description 1
- 239000005631 2,4-Dichlorophenoxyacetic acid Substances 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- KBAXPKVNVXMVKV-UHFFFAOYSA-N 2,4-dichloro-5,6,7,8-tetrahydroquinazoline Chemical compound C1CCCC2=NC(Cl)=NC(Cl)=C21 KBAXPKVNVXMVKV-UHFFFAOYSA-N 0.000 description 1
- WRAAHQVXMZLMQR-UHFFFAOYSA-N 2,4-dichloro-5,7-dihydrofuro[3,4-d]pyrimidine Chemical compound ClC1=NC(Cl)=NC2=C1COC2 WRAAHQVXMZLMQR-UHFFFAOYSA-N 0.000 description 1
- IHJDGIDSEZWIQT-UHFFFAOYSA-N 2,4-dichloro-7,8-dihydro-5h-thiopyrano[4,3-d]pyrimidine Chemical compound C1SCCC2=NC(Cl)=NC(Cl)=C21 IHJDGIDSEZWIQT-UHFFFAOYSA-N 0.000 description 1
- CQCDGPMCNAANOQ-UHFFFAOYSA-N 2,4-dichloro-n-[(4-methoxyphenyl)methyl]pyrimidine-5-carboxamide Chemical compound C1=CC(OC)=CC=C1CNC(=O)C1=CN=C(Cl)N=C1Cl CQCDGPMCNAANOQ-UHFFFAOYSA-N 0.000 description 1
- KMHSUNDEGHRBNV-UHFFFAOYSA-N 2,4-dichloropyrimidine-5-carbonitrile Chemical group ClC1=NC=C(C#N)C(Cl)=N1 KMHSUNDEGHRBNV-UHFFFAOYSA-N 0.000 description 1
- LSEAAPGIZCDEEH-UHFFFAOYSA-N 2,6-dichloropyrazine Chemical compound ClC1=CN=CC(Cl)=N1 LSEAAPGIZCDEEH-UHFFFAOYSA-N 0.000 description 1
- OWXBXLGJIFPPMS-UHFFFAOYSA-N 2,6-difluoropyridin-4-amine Chemical compound NC1=CC(F)=NC(F)=C1 OWXBXLGJIFPPMS-UHFFFAOYSA-N 0.000 description 1
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 1
- DOSGEBYQRMBTGS-UHFFFAOYSA-N 2-(3,6-dihydro-2h-pyran-4-yl)-4,4,5,5-tetramethyl-1,3,2-dioxaborolane Chemical compound O1C(C)(C)C(C)(C)OB1C1=CCOCC1 DOSGEBYQRMBTGS-UHFFFAOYSA-N 0.000 description 1
- WPNNIQKFJQWIKI-UHFFFAOYSA-N 2-[(3-methyloxetan-3-yl)methoxy]pyrimidin-4-amine Chemical compound N=1C=CC(N)=NC=1OCC1(C)COC1 WPNNIQKFJQWIKI-UHFFFAOYSA-N 0.000 description 1
- OTLLEIBWKHEHGU-UHFFFAOYSA-N 2-[5-[[5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolan-2-yl]methoxy]-3,4-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-3,5-dihydroxy-4-phosphonooxyhexanedioic acid Chemical compound C1=NC=2C(N)=NC=NC=2N1C(C(C1O)O)OC1COC1C(CO)OC(OC(C(O)C(OP(O)(O)=O)C(O)C(O)=O)C(O)=O)C(O)C1O OTLLEIBWKHEHGU-UHFFFAOYSA-N 0.000 description 1
- ZNQVEEAIQZEUHB-UHFFFAOYSA-N 2-ethoxyethanol Chemical compound CCOCCO ZNQVEEAIQZEUHB-UHFFFAOYSA-N 0.000 description 1
- 229940093475 2-ethoxyethanol Drugs 0.000 description 1
- SPWJNWKKNZWCPA-UHFFFAOYSA-N 2-fluoropyrimidin-4-amine Chemical compound NC1=CC=NC(F)=N1 SPWJNWKKNZWCPA-UHFFFAOYSA-N 0.000 description 1
- 229940080296 2-naphthalenesulfonate Drugs 0.000 description 1
- LEACJMVNYZDSKR-UHFFFAOYSA-N 2-octyldodecan-1-ol Chemical compound CCCCCCCCCCC(CO)CCCCCCCC LEACJMVNYZDSKR-UHFFFAOYSA-N 0.000 description 1
- VAIHBHWKPBXNLR-UHFFFAOYSA-N 2-piperidin-4-yloxyethanol Chemical compound OCCOC1CCNCC1 VAIHBHWKPBXNLR-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- KVTUSMPNLUCCQO-UHFFFAOYSA-N 3,3-difluoropyrrolidine Chemical compound FC1(F)CCNC1 KVTUSMPNLUCCQO-UHFFFAOYSA-N 0.000 description 1
- JZSAUQMXKHBZEO-UHFFFAOYSA-N 3,5-dichloropyridazine Chemical compound ClC1=CN=NC(Cl)=C1 JZSAUQMXKHBZEO-UHFFFAOYSA-N 0.000 description 1
- HCDMJFOHIXMBOV-UHFFFAOYSA-N 3-(2,6-difluoro-3,5-dimethoxyphenyl)-1-ethyl-8-(morpholin-4-ylmethyl)-4,7-dihydropyrrolo[4,5]pyrido[1,2-d]pyrimidin-2-one Chemical compound C=1C2=C3N(CC)C(=O)N(C=4C(=C(OC)C=C(OC)C=4F)F)CC3=CN=C2NC=1CN1CCOCC1 HCDMJFOHIXMBOV-UHFFFAOYSA-N 0.000 description 1
- XEMDFESAXKSEGI-UHFFFAOYSA-N 3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=CN=C1 XEMDFESAXKSEGI-UHFFFAOYSA-N 0.000 description 1
- WNEODWDFDXWOLU-QHCPKHFHSA-N 3-[3-(hydroxymethyl)-4-[1-methyl-5-[[5-[(2s)-2-methyl-4-(oxetan-3-yl)piperazin-1-yl]pyridin-2-yl]amino]-6-oxopyridin-3-yl]pyridin-2-yl]-7,7-dimethyl-1,2,6,8-tetrahydrocyclopenta[3,4]pyrrolo[3,5-b]pyrazin-4-one Chemical compound C([C@@H](N(CC1)C=2C=NC(NC=3C(N(C)C=C(C=3)C=3C(=C(N4C(C5=CC=6CC(C)(C)CC=6N5CC4)=O)N=CC=3)CO)=O)=CC=2)C)N1C1COC1 WNEODWDFDXWOLU-QHCPKHFHSA-N 0.000 description 1
- AJZDHLHTTJRNQJ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-[2-(tetrazol-1-yl)ethyl]benzamide Chemical compound N1(N=NN=C1)CCNC(C1=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)=O AJZDHLHTTJRNQJ-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 1
- ZRPLANDPDWYOMZ-UHFFFAOYSA-N 3-cyclopentylpropionic acid Chemical class OC(=O)CCC1CCCC1 ZRPLANDPDWYOMZ-UHFFFAOYSA-N 0.000 description 1
- MCLXKFUCPVGZEN-UHFFFAOYSA-N 4,6-dichloro-1,3,5-triazin-2-amine Chemical compound NC1=NC(Cl)=NC(Cl)=N1 MCLXKFUCPVGZEN-UHFFFAOYSA-N 0.000 description 1
- JEGIGVNQAHMOII-UHFFFAOYSA-N 4,6-dichloro-2-(methoxymethyl)pyrimidine Chemical compound COCC1=NC(Cl)=CC(Cl)=N1 JEGIGVNQAHMOII-UHFFFAOYSA-N 0.000 description 1
- FIMUTBLUWQGTIJ-UHFFFAOYSA-N 4,6-dichloro-2-methylpyrimidine Chemical compound CC1=NC(Cl)=CC(Cl)=N1 FIMUTBLUWQGTIJ-UHFFFAOYSA-N 0.000 description 1
- XJPZKYIHCLDXST-UHFFFAOYSA-N 4,6-dichloropyrimidine Chemical compound ClC1=CC(Cl)=NC=N1 XJPZKYIHCLDXST-UHFFFAOYSA-N 0.000 description 1
- KJFMZGRMRFLJQR-UHFFFAOYSA-N 4,6-difluoropyrimidin-2-amine Chemical compound NC1=NC(F)=CC(F)=N1 KJFMZGRMRFLJQR-UHFFFAOYSA-N 0.000 description 1
- KTXVOCUROHMWQP-UHFFFAOYSA-N 4-(2-methoxyethoxy)piperidine Chemical compound COCCOC1CCNCC1 KTXVOCUROHMWQP-UHFFFAOYSA-N 0.000 description 1
- BLBDTBCGPHPIJK-UHFFFAOYSA-N 4-Amino-2-chloropyridine Chemical group NC1=CC=NC(Cl)=C1 BLBDTBCGPHPIJK-UHFFFAOYSA-N 0.000 description 1
- FOANNJQFHJONSC-UHFFFAOYSA-N 4-[(2-methylpropan-2-yl)oxy]piperidine Chemical compound CC(C)(C)OC1CCNCC1 FOANNJQFHJONSC-UHFFFAOYSA-N 0.000 description 1
- KVCQTKNUUQOELD-UHFFFAOYSA-N 4-amino-n-[1-(3-chloro-2-fluoroanilino)-6-methylisoquinolin-5-yl]thieno[3,2-d]pyrimidine-7-carboxamide Chemical compound N=1C=CC2=C(NC(=O)C=3C4=NC=NC(N)=C4SC=3)C(C)=CC=C2C=1NC1=CC=CC(Cl)=C1F KVCQTKNUUQOELD-UHFFFAOYSA-N 0.000 description 1
- RPDVPWWBNQKLAS-UHFFFAOYSA-N 4-chloro-5-methylpyrimidine Chemical compound CC1=CN=CN=C1Cl RPDVPWWBNQKLAS-UHFFFAOYSA-N 0.000 description 1
- RKGXJBAAWCGBQA-UHFFFAOYSA-N 4-propan-2-yloxypiperidine Chemical compound CC(C)OC1CCNCC1 RKGXJBAAWCGBQA-UHFFFAOYSA-N 0.000 description 1
- SIKXIUWKPGWBBF-UHFFFAOYSA-N 5-bromo-2,4-dichloropyrimidine Chemical compound ClC1=NC=C(Br)C(Cl)=N1 SIKXIUWKPGWBBF-UHFFFAOYSA-N 0.000 description 1
- JEOBFTOIMFEXNK-UHFFFAOYSA-N 6-chloro-2-(methoxymethyl)pyrimidin-4-amine Chemical compound COCC1=NC(N)=CC(Cl)=N1 JEOBFTOIMFEXNK-UHFFFAOYSA-N 0.000 description 1
- QEHWAQITIOWIEX-UHFFFAOYSA-N 6-chloro-2-n,2-n,4-n,4-n-tetramethyl-1,3,5-triazine-2,4-diamine Chemical compound CN(C)C1=NC(Cl)=NC(N(C)C)=N1 QEHWAQITIOWIEX-UHFFFAOYSA-N 0.000 description 1
- AALZEWSKCRJZID-UHFFFAOYSA-N 6-fluoro-N-(2-methoxyethyl)pyrimidin-4-amine Chemical compound FC1=CC(=NC=N1)NCCOC AALZEWSKCRJZID-UHFFFAOYSA-N 0.000 description 1
- OGIDDUSIUCSNAK-UHFFFAOYSA-N 6-fluoro-N-methylpyrimidin-4-amine Chemical compound FC1=CC(=NC=N1)NC OGIDDUSIUCSNAK-UHFFFAOYSA-N 0.000 description 1
- SMHPLBXIVNQFBA-UHFFFAOYSA-N 6-nitroquinoline Chemical compound N1=CC=CC2=CC([N+](=O)[O-])=CC=C21 SMHPLBXIVNQFBA-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical class O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- CYJRNFFLTBEQSQ-UHFFFAOYSA-N 8-(3-methyl-1-benzothiophen-5-yl)-N-(4-methylsulfonylpyridin-3-yl)quinoxalin-6-amine Chemical compound CS(=O)(=O)C1=C(C=NC=C1)NC=1C=C2N=CC=NC2=C(C=1)C=1C=CC2=C(C(=CS2)C)C=1 CYJRNFFLTBEQSQ-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- OZAIFHULBGXAKX-VAWYXSNFSA-N AIBN Substances N#CC(C)(C)\N=N\C(C)(C)C#N OZAIFHULBGXAKX-VAWYXSNFSA-N 0.000 description 1
- 108091006112 ATPases Proteins 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 208000004476 Acute Coronary Syndrome Diseases 0.000 description 1
- 208000030090 Acute Disease Diseases 0.000 description 1
- 206010033646 Acute and chronic pancreatitis Diseases 0.000 description 1
- 206010000871 Acute monocytic leukaemia Diseases 0.000 description 1
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 1
- 208000036762 Acute promyelocytic leukaemia Diseases 0.000 description 1
- 208000026872 Addison Disease Diseases 0.000 description 1
- 102000057290 Adenosine Triphosphatases Human genes 0.000 description 1
- 206010001324 Adrenal atrophy Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 208000035285 Allergic Seasonal Rhinitis Diseases 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 206010002198 Anaphylactic reaction Diseases 0.000 description 1
- 235000017060 Arachis glabrata Nutrition 0.000 description 1
- 244000105624 Arachis hypogaea Species 0.000 description 1
- 235000010777 Arachis hypogaea Nutrition 0.000 description 1
- 235000018262 Arachis monticola Nutrition 0.000 description 1
- 200000000007 Arterial disease Diseases 0.000 description 1
- 206010003267 Arthritis reactive Diseases 0.000 description 1
- 206010003571 Astrocytoma Diseases 0.000 description 1
- 208000031212 Autoimmune polyendocrinopathy Diseases 0.000 description 1
- 206010050245 Autoimmune thrombocytopenia Diseases 0.000 description 1
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 1
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 1
- 206010004664 Biliary fibrosis Diseases 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 206010005949 Bone cancer Diseases 0.000 description 1
- 208000018084 Bone neoplasm Diseases 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical class [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-M Butyrate Chemical class CCCC([O-])=O FERIUCNNQQJTOY-UHFFFAOYSA-M 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Chemical class CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- 201000003274 CINCA syndrome Diseases 0.000 description 1
- 101100021281 Caenorhabditis elegans lin-8 gene Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 206010008609 Cholangitis sclerosing Diseases 0.000 description 1
- 208000000094 Chronic Pain Diseases 0.000 description 1
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical class [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- IZHKDGWJPPJCRN-SECBINFHSA-N ClC1=CC(=NC(=N1)CO)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=CC(=NC(=N1)CO)OC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O IZHKDGWJPPJCRN-SECBINFHSA-N 0.000 description 1
- BOFAWQFEHDOBEY-KWCCSABGSA-N ClC1=CC(=NC(=N1)OC1CN(CCC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=CC(=NC(=N1)OC1CN(CCC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O BOFAWQFEHDOBEY-KWCCSABGSA-N 0.000 description 1
- KRXUHTWAFIYLPJ-UHFFFAOYSA-N ClC1=NC(=NC(=C1)OCCN1CCN(CC1)C)N Chemical compound ClC1=NC(=NC(=C1)OCCN1CCN(CC1)C)N KRXUHTWAFIYLPJ-UHFFFAOYSA-N 0.000 description 1
- XQFLIKNPXOZOEM-UHFFFAOYSA-N ClC1=NC=C(C(=N1)Cl)CN1C(CCC1)COC Chemical compound ClC1=NC=C(C(=N1)Cl)CN1C(CCC1)COC XQFLIKNPXOZOEM-UHFFFAOYSA-N 0.000 description 1
- ISOYCIWOHJKMJG-OAHLLOKOSA-N ClC1=NC=C(C(=O)NCC2=CC=C(C=C2)OC)C(=C1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound ClC1=NC=C(C(=O)NCC2=CC=C(C=C2)OC)C(=C1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O ISOYCIWOHJKMJG-OAHLLOKOSA-N 0.000 description 1
- 208000015943 Coeliac disease Diseases 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 206010056489 Coronary artery restenosis Diseases 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- VMQMZMRVKUZKQL-UHFFFAOYSA-N Cu+ Chemical compound [Cu+] VMQMZMRVKUZKQL-UHFFFAOYSA-N 0.000 description 1
- 208000014311 Cushing syndrome Diseases 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 206010011878 Deafness Diseases 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- 208000007342 Diabetic Nephropathies Diseases 0.000 description 1
- 206010012689 Diabetic retinopathy Diseases 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- 101100339887 Drosophila melanogaster Hsp27 gene Proteins 0.000 description 1
- 101100291385 Drosophila melanogaster p38a gene Proteins 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- 206010014824 Endotoxic shock Diseases 0.000 description 1
- 241000792859 Enema Species 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 206010015943 Eye inflammation Diseases 0.000 description 1
- LCCRSNAYYXQSJN-KWCCSABGSA-N FC1=CC(=NC(=N1)OC1CN(CCC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O Chemical compound FC1=CC(=NC(=N1)OC1CN(CCC1)C)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O LCCRSNAYYXQSJN-KWCCSABGSA-N 0.000 description 1
- ZZGDBINXVJXNRE-UHFFFAOYSA-N FC1=CC(=NC(=N1)OCCN1CCN(CC1)C)N Chemical compound FC1=CC(=NC(=N1)OCCN1CCN(CC1)C)N ZZGDBINXVJXNRE-UHFFFAOYSA-N 0.000 description 1
- KLTJZNSGAGNMIR-RXMQYKEDSA-N FC1=CC(=NC(=N1)O[C@H]1COCC1)N Chemical compound FC1=CC(=NC(=N1)O[C@H]1COCC1)N KLTJZNSGAGNMIR-RXMQYKEDSA-N 0.000 description 1
- DXTNKQUELUESFQ-SECBINFHSA-N FC1=NC(=CC(=C1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)F Chemical compound FC1=NC(=CC(=C1)NC1=NC=2C=CC3=C(C=2C=C1)C1=C(S3)C(N[C@@H](CN1)C)=O)F DXTNKQUELUESFQ-SECBINFHSA-N 0.000 description 1
- JQLIRMSINVJPEJ-RXMQYKEDSA-N FC1=NC(=NC(=C1)O[C@H]1COCC1)N Chemical compound FC1=NC(=NC(=C1)O[C@H]1COCC1)N JQLIRMSINVJPEJ-RXMQYKEDSA-N 0.000 description 1
- AUCHYEHQIYWOBU-UHFFFAOYSA-N FC1=NC=C(C#N)C(=C1)I Chemical group FC1=NC=C(C#N)C(=C1)I AUCHYEHQIYWOBU-UHFFFAOYSA-N 0.000 description 1
- 206010016207 Familial Mediterranean fever Diseases 0.000 description 1
- 208000035690 Familial cold urticaria Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 208000007659 Fibroadenoma Diseases 0.000 description 1
- 208000001640 Fibromyalgia Diseases 0.000 description 1
- 239000004606 Fillers/Extenders Substances 0.000 description 1
- 206010016935 Follicular thyroid cancer Diseases 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical class [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- 208000007882 Gastritis Diseases 0.000 description 1
- 241000206672 Gelidium Species 0.000 description 1
- 201000010915 Glioblastoma multiforme Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 208000002705 Glucose Intolerance Diseases 0.000 description 1
- 206010018429 Glucose tolerance impaired Diseases 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Polymers OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 1
- 208000024869 Goodpasture syndrome Diseases 0.000 description 1
- 201000005569 Gout Diseases 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 206010072579 Granulomatosis with polyangiitis Diseases 0.000 description 1
- 208000003807 Graves Disease Diseases 0.000 description 1
- 208000015023 Graves' disease Diseases 0.000 description 1
- 239000007821 HATU Substances 0.000 description 1
- 101150096895 HSPB1 gene Proteins 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- 239000004705 High-molecular-weight polyethylene Substances 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- 206010058490 Hyperoxia Diseases 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 206010062767 Hypophysitis Diseases 0.000 description 1
- 206010021245 Idiopathic thrombocytopenic purpura Diseases 0.000 description 1
- 208000024934 IgG4-related mediastinitis Diseases 0.000 description 1
- 208000014919 IgG4-related retroperitoneal fibrosis Diseases 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 208000005615 Interstitial Cystitis Diseases 0.000 description 1
- 208000003456 Juvenile Arthritis Diseases 0.000 description 1
- 208000007766 Kaposi sarcoma Diseases 0.000 description 1
- 208000002260 Keloid Diseases 0.000 description 1
- 206010023330 Keloid scar Diseases 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical class OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 125000002842 L-seryl group Chemical group O=C([*])[C@](N([H])[H])([H])C([H])([H])O[H] 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 208000004852 Lung Injury Diseases 0.000 description 1
- 208000005777 Lupus Nephritis Diseases 0.000 description 1
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 1
- 102000043136 MAP kinase family Human genes 0.000 description 1
- 108091054455 MAP kinase family Proteins 0.000 description 1
- 102220517763 MAP kinase-activated protein kinase 2_D207A_mutation Human genes 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-L Malonate Chemical compound [O-]C(=O)CC([O-])=O OFOBLEOULBTSOW-UHFFFAOYSA-L 0.000 description 1
- 240000003183 Manihot esculenta Species 0.000 description 1
- 235000016735 Manihot esculenta subsp esculenta Nutrition 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 description 1
- 208000002805 Mediastinal fibrosis Diseases 0.000 description 1
- 201000009906 Meningitis Diseases 0.000 description 1
- 208000001145 Metabolic Syndrome Diseases 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 208000035489 Monocytic Acute Leukemia Diseases 0.000 description 1
- 201000002795 Muckle-Wells syndrome Diseases 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 208000000112 Myalgia Diseases 0.000 description 1
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 1
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 1
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 1
- 208000009525 Myocarditis Diseases 0.000 description 1
- 201000002481 Myositis Diseases 0.000 description 1
- AYCPARAPKDAOEN-LJQANCHMSA-N N-[(1S)-2-(dimethylamino)-1-phenylethyl]-6,6-dimethyl-3-[(2-methyl-4-thieno[3,2-d]pyrimidinyl)amino]-1,4-dihydropyrrolo[3,4-c]pyrazole-5-carboxamide Chemical compound C1([C@H](NC(=O)N2C(C=3NN=C(NC=4C=5SC=CC=5N=C(C)N=4)C=3C2)(C)C)CN(C)C)=CC=CC=C1 AYCPARAPKDAOEN-LJQANCHMSA-N 0.000 description 1
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 1
- 208000003510 Nephrogenic Fibrosing Dermopathy Diseases 0.000 description 1
- 206010067467 Nephrogenic systemic fibrosis Diseases 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- 206010030216 Oesophagitis Diseases 0.000 description 1
- 240000007817 Olea europaea Species 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 208000003435 Optic Neuritis Diseases 0.000 description 1
- 206010033307 Overweight Diseases 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 101150003085 Pdcl gene Proteins 0.000 description 1
- 241000721454 Pemphigus Species 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 208000031845 Pernicious anaemia Diseases 0.000 description 1
- 208000037581 Persistent Infection Diseases 0.000 description 1
- 239000004264 Petrolatum Substances 0.000 description 1
- 108010089430 Phosphoproteins Proteins 0.000 description 1
- 102000007982 Phosphoproteins Human genes 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 229920002732 Polyanhydride Polymers 0.000 description 1
- 206010065159 Polychondritis Diseases 0.000 description 1
- 229920000954 Polyglycolide Polymers 0.000 description 1
- 229920001710 Polyorthoester Polymers 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 206010036805 Progressive massive fibrosis Diseases 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 208000033826 Promyelocytic Acute Leukemia Diseases 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 102000007327 Protamines Human genes 0.000 description 1
- 108010007568 Protamines Proteins 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 208000032056 Radiation Fibrosis Syndrome Diseases 0.000 description 1
- 208000003782 Raynaud disease Diseases 0.000 description 1
- 208000012322 Raynaud phenomenon Diseases 0.000 description 1
- 208000033464 Reiter syndrome Diseases 0.000 description 1
- 206010063837 Reperfusion injury Diseases 0.000 description 1
- 206010038748 Restrictive cardiomyopathy Diseases 0.000 description 1
- 206010038979 Retroperitoneal fibrosis Diseases 0.000 description 1
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 1
- 235000004443 Ricinus communis Nutrition 0.000 description 1
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 1
- 240000000984 Sauvagesia erecta Species 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 206010048908 Seasonal allergy Diseases 0.000 description 1
- 201000010208 Seminoma Diseases 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- 206010041067 Small cell lung cancer Diseases 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 244000061456 Solanum tuberosum Species 0.000 description 1
- 235000002595 Solanum tuberosum Nutrition 0.000 description 1
- HVUMOYIDDBPOLL-XWVZOOPGSA-N Sorbitan monostearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O HVUMOYIDDBPOLL-XWVZOOPGSA-N 0.000 description 1
- SSZBUIDZHHWXNJ-UHFFFAOYSA-N Stearinsaeure-hexadecylester Natural products CCCCCCCCCCCCCCCCCC(=O)OCCCCCCCCCCCCCCCC SSZBUIDZHHWXNJ-UHFFFAOYSA-N 0.000 description 1
- 206010042971 T-cell lymphoma Diseases 0.000 description 1
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 208000001106 Takayasu Arteritis Diseases 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 206010043276 Teratoma Diseases 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 208000031981 Thrombocytopenic Idiopathic Purpura Diseases 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 208000030886 Traumatic Brain injury Diseases 0.000 description 1
- 206010069363 Traumatic lung injury Diseases 0.000 description 1
- OKJPEAGHQZHRQV-UHFFFAOYSA-N Triiodomethane Natural products IC(I)I OKJPEAGHQZHRQV-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 102100031638 Tuberin Human genes 0.000 description 1
- 108050009309 Tuberin Proteins 0.000 description 1
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 208000025865 Ulcer Diseases 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- 206010046851 Uveitis Diseases 0.000 description 1
- 206010047642 Vitiligo Diseases 0.000 description 1
- 208000000208 Wet Macular Degeneration Diseases 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- LXRZVMYMQHNYJB-UNXOBOICSA-N [(1R,2S,4R)-4-[[5-[4-[(1R)-7-chloro-1,2,3,4-tetrahydroisoquinolin-1-yl]-5-methylthiophene-2-carbonyl]pyrimidin-4-yl]amino]-2-hydroxycyclopentyl]methyl sulfamate Chemical compound CC1=C(C=C(S1)C(=O)C1=C(N[C@H]2C[C@H](O)[C@@H](COS(N)(=O)=O)C2)N=CN=C1)[C@@H]1NCCC2=C1C=C(Cl)C=C2 LXRZVMYMQHNYJB-UNXOBOICSA-N 0.000 description 1
- 239000001089 [(2R)-oxolan-2-yl]methanol Substances 0.000 description 1
- REAYFGLASQTHKB-UHFFFAOYSA-N [2-[3-(1H-pyrazol-4-yl)phenoxy]-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound N1N=CC(=C1)C=1C=C(OC2=NC(=CC(=C2)CN)C(F)(F)F)C=CC=1 REAYFGLASQTHKB-UHFFFAOYSA-N 0.000 description 1
- ZEYSHALLPAKUHG-FIBGUPNXSA-N [2H]C([2H])([2H])OC1CCNCC1 Chemical compound [2H]C([2H])([2H])OC1CCNCC1 ZEYSHALLPAKUHG-FIBGUPNXSA-N 0.000 description 1
- BYWBCSRCPLBDFU-CYBMUJFWSA-N [3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxyphenyl]-[(3R)-3-aminopyrrolidin-1-yl]methanone Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C=CC=1)C(=O)N1C[C@@H](CC1)N BYWBCSRCPLBDFU-CYBMUJFWSA-N 0.000 description 1
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 239000003655 absorption accelerator Substances 0.000 description 1
- 229940124532 absorption promoter Drugs 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 1
- 239000012346 acetyl chloride Substances 0.000 description 1
- 206010069351 acute lung injury Diseases 0.000 description 1
- 208000005298 acute pain Diseases 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical class [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 150000008055 alkyl aryl sulfonates Chemical class 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 150000008052 alkyl sulfonates Chemical class 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 125000005336 allyloxy group Chemical group 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- CEGOLXSVJUTHNZ-UHFFFAOYSA-K aluminium tristearate Chemical compound [Al+3].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CEGOLXSVJUTHNZ-UHFFFAOYSA-K 0.000 description 1
- 229940063655 aluminum stearate Drugs 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 1
- 230000036783 anaphylactic response Effects 0.000 description 1
- 208000003455 anaphylaxis Diseases 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 229940045988 antineoplastic drug protein kinase inhibitors Drugs 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 208000028922 artery disease Diseases 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 229940072107 ascorbate Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Chemical class 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 238000003149 assay kit Methods 0.000 description 1
- 230000003143 atherosclerotic effect Effects 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 230000001746 atrial effect Effects 0.000 description 1
- 201000004339 autoimmune neuropathy Diseases 0.000 description 1
- 201000003710 autoimmune thrombocytopenic purpura Diseases 0.000 description 1
- 238000010533 azeotropic distillation Methods 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical class [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical class OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 229960002903 benzyl benzoate Drugs 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 238000004166 bioassay Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000008512 biological response Effects 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- SIPUZPBQZHNSDW-UHFFFAOYSA-N bis(2-methylpropyl)aluminum Chemical compound CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 208000029028 brain injury Diseases 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 206010006451 bronchitis Diseases 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 235000010216 calcium carbonate Nutrition 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- MIOPJNTWMNEORI-UHFFFAOYSA-N camphorsulfonic acid Chemical class C1CC2(CS(O)(=O)=O)C(=O)CC1C2(C)C MIOPJNTWMNEORI-UHFFFAOYSA-N 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 208000035269 cancer or benign tumor Diseases 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 230000009787 cardiac fibrosis Effects 0.000 description 1
- 239000012876 carrier material Substances 0.000 description 1
- 235000019438 castor oil Nutrition 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000033077 cellular process Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 210000003679 cervix uteri Anatomy 0.000 description 1
- 229940081733 cetearyl alcohol Drugs 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- OVJIHFBAXJKTRF-SSDOTTSWSA-N chembl556392 Chemical compound O=C1N[C@H](C)CNC2=C1SC1=CC=C(N=C(Cl)C=C3)C3=C21 OVJIHFBAXJKTRF-SSDOTTSWSA-N 0.000 description 1
- 229910052729 chemical element Inorganic materials 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 208000003167 cholangitis Diseases 0.000 description 1
- 208000037976 chronic inflammation Diseases 0.000 description 1
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 1
- 208000020832 chronic kidney disease Diseases 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- 239000004927 clay Substances 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000010835 comparative analysis Methods 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 208000018631 connective tissue disease Diseases 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- USVZFSNDGFNNJT-UHFFFAOYSA-N cyclopenta-1,4-dien-1-yl(diphenyl)phosphane (2,3-dichlorocyclopenta-1,4-dien-1-yl)-diphenylphosphane iron(2+) Chemical compound [Fe++].c1cc[c-](c1)P(c1ccccc1)c1ccccc1.Clc1c(cc[c-]1Cl)P(c1ccccc1)c1ccccc1 USVZFSNDGFNNJT-UHFFFAOYSA-N 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 231100000895 deafness Toxicity 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 208000033679 diabetic kidney disease Diseases 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- 239000002027 dichloromethane extract Substances 0.000 description 1
- WGLUMOCWFMKWIL-UHFFFAOYSA-N dichloromethane;methanol Chemical compound OC.ClCCl WGLUMOCWFMKWIL-UHFFFAOYSA-N 0.000 description 1
- BSHICDXRSZQYBP-UHFFFAOYSA-N dichloromethane;palladium(2+) Chemical compound [Pd+2].ClCCl BSHICDXRSZQYBP-UHFFFAOYSA-N 0.000 description 1
- LCSNDSFWVKMJCT-UHFFFAOYSA-N dicyclohexyl-(2-phenylphenyl)phosphane Chemical group C1CCCCC1P(C=1C(=CC=CC=1)C=1C=CC=CC=1)C1CCCCC1 LCSNDSFWVKMJCT-UHFFFAOYSA-N 0.000 description 1
- MXFYYFVVIIWKFE-UHFFFAOYSA-N dicyclohexyl-[2-[2,6-di(propan-2-yloxy)phenyl]phenyl]phosphane Chemical compound CC(C)OC1=CC=CC(OC(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 MXFYYFVVIIWKFE-UHFFFAOYSA-N 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- CSJLBAMHHLJAAS-UHFFFAOYSA-N diethylaminosulfur trifluoride Substances CCN(CC)S(F)(F)F CSJLBAMHHLJAAS-UHFFFAOYSA-N 0.000 description 1
- NZZFYRREKKOMAT-UHFFFAOYSA-N diiodomethane Chemical compound ICI NZZFYRREKKOMAT-UHFFFAOYSA-N 0.000 description 1
- GXGAKHNRMVGRPK-UHFFFAOYSA-N dimagnesium;dioxido-bis[[oxido(oxo)silyl]oxy]silane Chemical compound [Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O GXGAKHNRMVGRPK-UHFFFAOYSA-N 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 1
- 229910000396 dipotassium phosphate Inorganic materials 0.000 description 1
- 235000019797 dipotassium phosphate Nutrition 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- LNGNZSMIUVQZOX-UHFFFAOYSA-L disodium;dioxido(sulfanylidene)-$l^{4}-sulfane Chemical class [Na+].[Na+].[O-]S([O-])=S LNGNZSMIUVQZOX-UHFFFAOYSA-L 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- POULHZVOKOAJMA-UHFFFAOYSA-M dodecanoate Chemical compound CCCCCCCCCCCC([O-])=O POULHZVOKOAJMA-UHFFFAOYSA-M 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000003596 drug target Substances 0.000 description 1
- 208000011325 dry age related macular degeneration Diseases 0.000 description 1
- 239000003221 ear drop Substances 0.000 description 1
- 229940047652 ear drops Drugs 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- 239000012060 enantioenriched intermediate Substances 0.000 description 1
- 206010014599 encephalitis Diseases 0.000 description 1
- 201000010048 endomyocardial fibrosis Diseases 0.000 description 1
- 239000007920 enema Substances 0.000 description 1
- 229940095399 enema Drugs 0.000 description 1
- 208000010227 enterocolitis Diseases 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 208000006881 esophagitis Diseases 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical class CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- QQXMRTNJTHNBJF-UHFFFAOYSA-N ethyl 2-amino-4-chloropyrimidine-5-carboxylate Chemical group CCOC(=O)C1=CN=C(N)N=C1Cl QQXMRTNJTHNBJF-UHFFFAOYSA-N 0.000 description 1
- ZIUSEGSNTOUIPT-UHFFFAOYSA-N ethyl 2-cyanoacetate Chemical compound CCOC(=O)CC#N ZIUSEGSNTOUIPT-UHFFFAOYSA-N 0.000 description 1
- SNNHLSHDDGJVDM-UHFFFAOYSA-N ethyl 4-chloro-2-methylsulfanylpyrimidine-5-carboxylate Chemical compound CCOC(=O)C1=CN=C(SC)N=C1Cl SNNHLSHDDGJVDM-UHFFFAOYSA-N 0.000 description 1
- DEQYTNZJHKPYEZ-UHFFFAOYSA-N ethyl acetate;heptane Chemical compound CCOC(C)=O.CCCCCCC DEQYTNZJHKPYEZ-UHFFFAOYSA-N 0.000 description 1
- UREBWPXBXRYXRJ-UHFFFAOYSA-N ethyl acetate;methanol Chemical compound OC.CCOC(C)=O UREBWPXBXRYXRJ-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000029142 excretion Effects 0.000 description 1
- 239000002095 exotoxin Substances 0.000 description 1
- 231100000776 exotoxin Toxicity 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000011536 extraction buffer Substances 0.000 description 1
- 239000003889 eye drop Substances 0.000 description 1
- 229940012356 eye drops Drugs 0.000 description 1
- 206010064570 familial cold autoinflammatory syndrome Diseases 0.000 description 1
- 208000010706 fatty liver disease Diseases 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 210000000232 gallbladder Anatomy 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 208000007565 gingivitis Diseases 0.000 description 1
- 208000005017 glioblastoma Diseases 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- YQEMORVAKMFKLG-UHFFFAOYSA-N glycerine monostearate Natural products CCCCCCCCCCCCCCCCCC(=O)OC(CO)CO YQEMORVAKMFKLG-UHFFFAOYSA-N 0.000 description 1
- SVUQHVRAGMNPLW-UHFFFAOYSA-N glycerol monostearate Natural products CCCCCCCCCCCCCCCCC(=O)OCC(O)CO SVUQHVRAGMNPLW-UHFFFAOYSA-N 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 210000003128 head Anatomy 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000016354 hearing loss disease Diseases 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 230000002949 hemolytic effect Effects 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 1
- MNWFXJYAOYHMED-UHFFFAOYSA-N heptanoic acid Chemical compound CCCCCCC(O)=O MNWFXJYAOYHMED-UHFFFAOYSA-N 0.000 description 1
- 239000008241 heterogeneous mixture Substances 0.000 description 1
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-M hexadecanoate Chemical compound CCCCCCCCCCCCCCCC([O-])=O IPCSVZSSVZVIGE-UHFFFAOYSA-M 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N hydrogen thiocyanate Natural products SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical class OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 230000000222 hyperoxic effect Effects 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 229940102223 injectable solution Drugs 0.000 description 1
- 229940102213 injectable suspension Drugs 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 230000031146 intracellular signal transduction Effects 0.000 description 1
- 238000007917 intracranial administration Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007919 intrasynovial administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 201000002215 juvenile rheumatoid arthritis Diseases 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 210000001117 keloid Anatomy 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 238000000021 kinase assay Methods 0.000 description 1
- 238000012933 kinetic analysis Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 229940001447 lactate Drugs 0.000 description 1
- 229940099584 lactobionate Drugs 0.000 description 1
- JYTUSYBCFIZPBE-AMTLMPIISA-N lactobionic acid Chemical compound OC(=O)[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O JYTUSYBCFIZPBE-AMTLMPIISA-N 0.000 description 1
- 235000019388 lanolin Nutrition 0.000 description 1
- 210000000867 larynx Anatomy 0.000 description 1
- 229940070765 laurate Drugs 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 1
- 150000002642 lithium compounds Chemical class 0.000 description 1
- 231100000515 lung injury Toxicity 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 229940049920 malate Drugs 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 201000006512 mast cell neoplasm Diseases 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- GRWIABMEEKERFV-UHFFFAOYSA-N methanol;oxolane Chemical compound OC.C1CCOC1 GRWIABMEEKERFV-UHFFFAOYSA-N 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- DQNQNLWKAGZNIT-UHFFFAOYSA-N methyl 2,6-dichloropyrimidine-4-carboxylate Chemical compound COC(=O)C1=CC(Cl)=NC(Cl)=N1 DQNQNLWKAGZNIT-UHFFFAOYSA-N 0.000 description 1
- PQIIRUIULSNZCL-UHFFFAOYSA-N methyl 4,6-dichloropyrimidine-2-carboxylate Chemical group COC(=O)C1=NC(Cl)=CC(Cl)=N1 PQIIRUIULSNZCL-UHFFFAOYSA-N 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 229940042472 mineral oil Drugs 0.000 description 1
- 230000000116 mitigating effect Effects 0.000 description 1
- CQDGTJPVBWZJAZ-UHFFFAOYSA-N monoethyl carbonate Chemical compound CCOC(O)=O CQDGTJPVBWZJAZ-UHFFFAOYSA-N 0.000 description 1
- 108091005763 multidomain proteins Proteins 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 206010028537 myelofibrosis Diseases 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- DILRJUIACXKSQE-UHFFFAOYSA-N n',n'-dimethylethane-1,2-diamine Chemical compound CN(C)CCN DILRJUIACXKSQE-UHFFFAOYSA-N 0.000 description 1
- ZQGJEUVBUVKZKS-UHFFFAOYSA-N n,2-dimethylpropan-2-amine Chemical compound CNC(C)(C)C ZQGJEUVBUVKZKS-UHFFFAOYSA-N 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-M naphthalene-2-sulfonate Chemical compound C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-M 0.000 description 1
- 229940097496 nasal spray Drugs 0.000 description 1
- 239000007922 nasal spray Substances 0.000 description 1
- 230000027405 negative regulation of phosphorylation Effects 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 208000004296 neuralgia Diseases 0.000 description 1
- 208000007538 neurilemmoma Diseases 0.000 description 1
- 230000004770 neurodegeneration Effects 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 208000021722 neuropathic pain Diseases 0.000 description 1
- 235000001968 nicotinic acid Nutrition 0.000 description 1
- 239000011664 nicotinic acid Substances 0.000 description 1
- 208000008338 non-alcoholic fatty liver disease Diseases 0.000 description 1
- 206010053219 non-alcoholic steatohepatitis Diseases 0.000 description 1
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 1
- 230000030147 nuclear export Effects 0.000 description 1
- 150000007523 nucleic acids Chemical group 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- 229940049964 oleate Drugs 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 201000005737 orchitis Diseases 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 201000008968 osteosarcoma Diseases 0.000 description 1
- 201000004535 ovarian dysfunction Diseases 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 235000020232 peanut Nutrition 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 201000001245 periodontitis Diseases 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- JRKICGRDRMAZLK-UHFFFAOYSA-L peroxydisulfate Chemical compound [O-]S(=O)(=O)OOS([O-])(=O)=O JRKICGRDRMAZLK-UHFFFAOYSA-L 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 229940066842 petrolatum Drugs 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- DYUMLJSJISTVPV-UHFFFAOYSA-N phenyl propanoate Chemical compound CCC(=O)OC1=CC=CC=C1 DYUMLJSJISTVPV-UHFFFAOYSA-N 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- UXCDUFKZSUBXGM-UHFFFAOYSA-N phosphoric tribromide Chemical compound BrP(Br)(Br)=O UXCDUFKZSUBXGM-UHFFFAOYSA-N 0.000 description 1
- 229950010765 pivalate Drugs 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 201000006292 polyarteritis nodosa Diseases 0.000 description 1
- 239000001818 polyoxyethylene sorbitan monostearate Substances 0.000 description 1
- 235000010989 polyoxyethylene sorbitan monostearate Nutrition 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229940113124 polysorbate 60 Drugs 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- 239000012041 precatalyst Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 201000009395 primary hyperaldosteronism Diseases 0.000 description 1
- 201000000742 primary sclerosing cholangitis Diseases 0.000 description 1
- 125000001500 prolyl group Chemical group [H]N1C([H])(C(=O)[*])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 1
- 229950008679 protamine sulfate Drugs 0.000 description 1
- 239000003909 protein kinase inhibitor Substances 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 208000005069 pulmonary fibrosis Diseases 0.000 description 1
- IIVUJUOJERNGQX-UHFFFAOYSA-N pyrimidine-5-carboxylic acid Chemical compound OC(=O)C1=CN=CN=C1 IIVUJUOJERNGQX-UHFFFAOYSA-N 0.000 description 1
- 150000003856 quaternary ammonium compounds Chemical class 0.000 description 1
- 125000001453 quaternary ammonium group Chemical group 0.000 description 1
- LOAUVZALPPNFOQ-UHFFFAOYSA-M quinaldate Chemical compound C1=CC=CC2=NC(C(=O)[O-])=CC=C21 LOAUVZALPPNFOQ-UHFFFAOYSA-M 0.000 description 1
- 238000000163 radioactive labelling Methods 0.000 description 1
- 239000002287 radioligand Substances 0.000 description 1
- 239000011535 reaction buffer Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 229940100618 rectal suppository Drugs 0.000 description 1
- 239000006215 rectal suppository Substances 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 230000025053 regulation of cell proliferation Effects 0.000 description 1
- 230000014493 regulation of gene expression Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 208000009169 relapsing polychondritis Diseases 0.000 description 1
- 201000002793 renal fibrosis Diseases 0.000 description 1
- 239000013557 residual solvent Substances 0.000 description 1
- 230000003938 response to stress Effects 0.000 description 1
- 208000037803 restenosis Diseases 0.000 description 1
- 239000003340 retarding agent Substances 0.000 description 1
- 239000013037 reversible inhibitor Substances 0.000 description 1
- 230000000630 rising effect Effects 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 208000010157 sclerosing cholangitis Diseases 0.000 description 1
- 210000000582 semen Anatomy 0.000 description 1
- 230000036303 septic shock Effects 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- XGVXKJKTISMIOW-ZDUSSCGKSA-N simurosertib Chemical compound N1N=CC(C=2SC=3C(=O)NC(=NC=3C=2)[C@H]2N3CCC(CC3)C2)=C1C XGVXKJKTISMIOW-ZDUSSCGKSA-N 0.000 description 1
- 201000009890 sinusitis Diseases 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 208000000587 small cell lung carcinoma Diseases 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- HYHCSLBZRBJJCH-UHFFFAOYSA-M sodium hydrosulfide Chemical compound [Na+].[SH-] HYHCSLBZRBJJCH-UHFFFAOYSA-M 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- JQWHASGSAFIOCM-UHFFFAOYSA-M sodium periodate Chemical compound [Na+].[O-]I(=O)(=O)=O JQWHASGSAFIOCM-UHFFFAOYSA-M 0.000 description 1
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical compound [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 1
- 235000010265 sodium sulphite Nutrition 0.000 description 1
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 1
- LYPGDCWPTHTUDO-UHFFFAOYSA-M sodium;methanesulfinate Chemical compound [Na+].CS([O-])=O LYPGDCWPTHTUDO-UHFFFAOYSA-M 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000001587 sorbitan monostearate Substances 0.000 description 1
- 235000011076 sorbitan monostearate Nutrition 0.000 description 1
- 229940035048 sorbitan monostearate Drugs 0.000 description 1
- VNFWTIYUKDMAOP-UHFFFAOYSA-N sphos Chemical compound COC1=CC=CC(OC)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 VNFWTIYUKDMAOP-UHFFFAOYSA-N 0.000 description 1
- 230000007863 steatosis Effects 0.000 description 1
- 231100000240 steatosis hepatitis Toxicity 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 239000003206 sterilizing agent Substances 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 230000035882 stress Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 239000001384 succinic acid Substances 0.000 description 1
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 1
- HHVIBTZHLRERCL-UHFFFAOYSA-N sulfonyldimethane Chemical compound CS(C)(=O)=O HHVIBTZHLRERCL-UHFFFAOYSA-N 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 210000001138 tear Anatomy 0.000 description 1
- 230000002123 temporal effect Effects 0.000 description 1
- 208000001608 teratocarcinoma Diseases 0.000 description 1
- PCVMBAOWKUKBRU-QMMMGPOBSA-N tert-butyl (4s)-4-(aminomethyl)-2,2-dimethyl-1,3-oxazolidine-3-carboxylate Chemical group CC(C)(C)OC(=O)N1[C@@H](CN)COC1(C)C PCVMBAOWKUKBRU-QMMMGPOBSA-N 0.000 description 1
- YPTQBCCFRRAECZ-UHFFFAOYSA-N tert-butyl 2,4-dichloro-7,8-dihydro-5h-pyrido[4,3-d]pyrimidine-6-carboxylate Chemical compound ClC1=NC(Cl)=C2CN(C(=O)OC(C)(C)C)CCC2=N1 YPTQBCCFRRAECZ-UHFFFAOYSA-N 0.000 description 1
- RBOGBIZGALIITO-UHFFFAOYSA-N tert-butyl 2,6-dimethylpiperazine-1-carboxylate Chemical compound CC1CNCC(C)N1C(=O)OC(C)(C)C RBOGBIZGALIITO-UHFFFAOYSA-N 0.000 description 1
- VVDCRJGWILREQH-UHFFFAOYSA-N tert-butyl 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-3,6-dihydro-2h-pyridine-1-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CCC(B2OC(C)(C)C(C)(C)O2)=C1 VVDCRJGWILREQH-UHFFFAOYSA-N 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- BSYVTEYKTMYBMK-UHFFFAOYSA-N tetrahydrofurfuryl alcohol Chemical compound OCC1CCCO1 BSYVTEYKTMYBMK-UHFFFAOYSA-N 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 230000002446 thrombocytic effect Effects 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 208000030901 thyroid gland follicular carcinoma Diseases 0.000 description 1
- 206010043778 thyroiditis Diseases 0.000 description 1
- 208000037816 tissue injury Diseases 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 230000009529 traumatic brain injury Effects 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- SZCZSKMCTGEJKI-UHFFFAOYSA-N tuberin Natural products COC1=CC=C(C=CNC=O)C=C1 SZCZSKMCTGEJKI-UHFFFAOYSA-N 0.000 description 1
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 1
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 1
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 210000004291 uterus Anatomy 0.000 description 1
- 229940070710 valerate Drugs 0.000 description 1
- NQPDZGIKBAWPEJ-UHFFFAOYSA-N valeric acid Chemical compound CCCCC(O)=O NQPDZGIKBAWPEJ-UHFFFAOYSA-N 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 239000003039 volatile agent Substances 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000010497 wheat germ oil Substances 0.000 description 1
- 239000003871 white petrolatum Substances 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D495/14—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/55—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole
- A61K31/551—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having seven-membered rings, e.g. azelastine, pentylenetetrazole having two nitrogen atoms, e.g. dilazep
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Enzymes And Modification Thereof (AREA)
Abstract
Un compuesto seleccionado de: **(Ver fórmula)** o **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo.
Description
DESCRIPCIÓN
Inhibidores de MK2 y usos de los mismos
CAMPO TÉCNICO DE LA INVENCIÓN
La presente invención se refiere a compuestos útiles como inhibidores de quinasas MK2. La invención también proporciona composiciones farmacéuticamente aceptables que comprenden compuestos de la presente invención. Se divulgan métodos para usar dichas composiciones en el tratamiento de varios trastornos.
ANTECEDENTES DE LA INVENCIÓN
La búsqueda de nuevos agentes terapéuticos se ha visto muy favorecida en los últimos años por una mejor comprensión de la estructura de las enzimas y otras biomoléculas asociadas con enfermedades. Una clase importante de enzimas que ha sido objeto de extensos estudios son las proteínas quinasas.
Las proteínas quinasas constituyen una gran familia de enzimas relacionadas estructuralmente que son responsables del control de una variedad de procesos de transducción de señales dentro de la célula. Se piensa que las proteínas quinasas han evolucionado a partir de un gen ancestral común debido a la conservación de su estructura y función catalítica. Casi todas las quinasas contienen un dominio catalítico similar de 250-300 aminoácidos. Las quinasas pueden clasificarse en familias por los sustratos que fosforilan (por ejemplo, proteínatirosina, proteína-serina/treonina, lípidos, etc.).
La proteína quinasa 2 activada por proteína quinasa activada por mitógenos (MAPKAP K2 o MK2) media múltiples respuestas celulares dependientes de p38 MAPK. MK2 es un importante regulador intracelular de la producción de citoquinas, como el factor de necrosis tumoral alfa (TNF-a), la interleucina 6 (IL-6) y el interferón gamma (IFNy), que están implicados en muchas enfermedades inflamatorias agudas y crónicas, por ejemplo artritis reumatoide y enfermedad inflamatoria intestinal. MK2 reside en el núcleo de células no estimuladas y tras la estimulación, se trasloca al citoplasma y fosforila y activa la tuberina y HSP27. MK2 también está implicada en insuficiencia cardíaca, lesión isquémica cerebral, regulación de la resistencia al estrés y producción de TNF-a. (ver Deak et al., EMBO. 17:4426-4441 (1998); Shi et al., Biol. Chem. 383:1519-1536 (2002); Staklatvala., Curr. Opin. Pharmacol. 4:372-377 (2004), and Shiroto et al., J. Mol. Cardiol. 38:93-97 (2005)).
Muchas enfermedades están asociadas con respuestas celulares anormales desencadenadas por eventos mediados por proteína quinasas como se ha descrito anteriormente. Estas enfermedades incluyen, pero no se limitan a, enfermedades autoinmunes, enfermedades inflamatorias, enfermedades óseas, enfermedades metabólicas, enfermedades neurológicas y neurodegenerativas, cáncer, enfermedades cardiovasculares, alergias y asma, enfermedad de Alzheimer y enfermedades relacionadas con hormonas. Por consiguiente, sigue habiendo una necesidad de encontrar inhibidores de las proteína quinasas útiles como agentes terapéuticos.
SUMARIO DE LA INVENCIÓN
El alcance de la invención está definido por las reivindicaciones adjuntas. Cualquier ejemplo o realización que no esté dentro del alcance de las reivindicaciones adjuntas se describe con propósitos de referencia.
Ahora se ha descubierto que los compuestos de esta invención, y composiciones farmacéuticamente aceptables de los mismos, son eficaces como inhibidores de MK2. La invención proporciona compuestos seleccionados de:
o una sal farmacéuticamente aceptable de los mismos.
La invención también proporciona composiciones farmacéuticamente aceptables que comprenden los compuestos anteriores de la invención y un portador, adyuvante o vehículo farmacéuticamente aceptable.
Los compuestos de la presente invención, y las composiciones farmacéuticamente aceptables de los mismos, son útiles para tratar una variedad de enfermedades, trastornos o afecciones, asociados con respuestas celulares anormales desencadenadas por eventos mediados por proteína quinasas. Tales enfermedades, trastornos o afecciones incluyen las descritas en la presente.
Los compuestos proporcionados por esta invención también son útiles para el estudio de quinasas en fenómenos biológicos y patológicos; el estudio de las vías de transducción de señales intracelulares mediadas por tales quinasas; y la evaluación comparativa de nuevos inhibidores de quinasas.
DESCRIPCIÓN DETALLADA DE CIERTAS REALIZACIONES
1. D escripción g en e ra l de los com p uestos de la invención:
En ciertas realizaciones, la presente invención proporciona inhibidores irreversibles de MK2. En algunas realizaciones, tales compuestos incluyen los de las fórmulas descritas en la presente, o una sal farmacéuticamente aceptable de los mismos.
En algunas realizaciones, la presente invención proporciona compuestos seleccionados de:
o una sal farmacéuticamente aceptable de los mismos.
2. C om puestos y d efin ic iones:
Como se usan en la presente, se aplicarán las siguientes definiciones a menos que se indique lo contrario. Para los propósitos de esta invención, los elementos químicos se identifican de acuerdo con la Tabla Periódica de los Elementos, versión CAS, Handbook of Chemistry Handbook of Chemistry and Physics, 75a Ed. Además, los principios generales de química orgánica se describen en "Organic Chemistry", Thomas Sorrell, University Science
Books, Sausalito: 1999, y "March’s Advanced Organic Chemistry", 5a Ed., Ed.: Smith, M.B. and March, J., John Wiley & Sons, New York: 2001.
Como se usa en la presente, el término "sal farmacéuticamente aceptable" se refiere a aquellas sales que, dentro del alcance del buen juicio médico, son adecuadas para su uso en contacto con los tejidos de humanos y animales inferiores sin toxicidad, irritación, respuesta alérgica y similares indebidas, y están en consonancia con una relación beneficio/riesgo razonable. Las sales farmacéuticamente aceptables son bien conocidas en la técnica. Por ejemplo, S.M. Berge et al., describen sales farmacéuticamente aceptables en detalle en J. Pharmaceutical Sciences, 1977, 66, 1-19. Las sales farmacéuticamente aceptables de los compuestos de esta invención incluyen las derivadas de ácidos y bases inorgánicos y orgánicos adecuados. Ejemplos de sales de adición de ácido no tóxicas farmacéuticamente aceptables son sales de un grupo amino formado con ácidos inorgánicos como ácido clorhídrico, ácido bromhídrico, ácido fosfórico, ácido sulfúrico y ácido perclórico o con ácidos orgánicos como ácido acético, ácido oxálico, ácido maleico, ácido tartárico, ácido cítrico, ácido succínico o ácido malónico o usando otros métodos usados en la técnica como intercambio iónico. Otras sales farmacéuticamente aceptables incluyen sales de adipato, alginato, ascorbato, aspartato, bencenosulfonato, benzoato, bisulfato, borato, butirato, canforato, canforsulfonato, citrato, ciclopentanopropionato, digluconato, dodecilsulfato, etanosulfonato, formiato, fumarato, glucoheptonato, glicerofosfato, gluconato, hemisulfato, heptanoato, hexanoato, hidroyoduro, 2-hidroxietanosulfonato, lactobionato, lactato, laurato, lauril sulfato, malato, maleato, malonato, metanosulfonato, 2-naftalenosulfonato, nicotinato, nitrato, oleato, oxalato, palmitato, pamoato, pectinato, persulfato, 3-fenilpropionato, fosfato, pivalato, propionato, estearato, succinato, sulfato, tartrato, tiocianato, p-toluenosulfonato, undecanoato, valerato y similares.
Las sales derivadas de bases apropiadas incluyen sales de metales alcalinos, metales alcalinotérreos, amonio y N+(alquilo C1-4K Las sales de metales alcalinos o alcalinotérreos representativas incluyen sodio, litio, potasio, calcio, magnesio y similares. Otras sales farmacéuticamente aceptables incluyen, cuando sea apropiado, cationes de amonio, amonio cuaternario y amina no tóxicos formados usando contraiones como haluro, hidróxido, carboxilato, sulfato, fosfato, nitrato, sulfonato de alquilo inferior y arilsulfonato.
A menos que se indique lo contrario, también se pretende que las estructuras representadas en la presente incluyan todas las formas isoméricas (por ejemplo, enantioméricas, diastereoméricas y geométricas (o conformacionales)) de la estructura; por ejemplo, las configuraciones R y S para cada centro asimétrico, isómeros de doble enlace Z y E, e isómeros conformacionales Z y E. Por lo tanto, los isómeros estereoquímicos individuales así como las mezclas enantioméricas, diastereoméricas y geométricas (o conformacionales) de los presentes compuestos están dentro del alcance de la invención. Además, a menos que se indique lo contrario, todas las formas tautoméricas de los compuestos de la invención están dentro del alcance de la invención. Además, a menos que se indique lo contrario, también se pretende que las estructuras representadas en la presente incluyan compuestos que difieren solo en la presencia de uno o más átomos enriquecidos isotópicamente. Por ejemplo, los compuestos que tienen las presentes estructuras que incluyen el reemplazo de hidrógeno pr deuterio o tritio, o el reemplazo de un carbono por 13C- o 14C- están dentro del alcance de esta invención. Tales compuestos son útiles, por ejemplo, como herramientas analíticas, como sondas en ensayos biológicos o como agentes terapéuticos de acuerdo con la presente invención.
Las combinaciones de sustituyentes y variables contempladas por esta invención son solo aquellas que dan como resultado la formación de compuestos estables. El término "estable", como se usa en la presente, se refiere a compuestos que poseen estabilidad suficiente para permitir la fabricación y que mantienen la integridad del compuesto durante un período de tiempo suficiente para ser útil para los propósitos detallados en la presente (por ejemplo, administración terapéutica o profiláctica a un sujeto).
La enumeración de una lista de grupos químicos en cualquier definición de una variable en la presente incluye definiciones de esa variable como cualquier grupo individual o combinación de grupos enumerados. La enumeración de una realización para una variable en la presente incluye esa realización como una realización individual o en combinación con cualquier otra realización o partes de la misma.
El término "muestra biológica", como se usa en la presente, incluye, sin limitación, cultivos celulares o extractos de los mismos; material de biopsia obtenido de un mamífero o extractos del mismo; y sangre, saliva, orina, heces, semen, lágrimas u otros fluidos corporales o extractos de los mismos. La inhibición de la actividad de una proteína quinasa, por ejemplo, MK2 o un mutante de la misma, en una muestra biológica es útil para una variedad de propósitos que son conocidos por los expertos en la técnica. Los ejemplos de tales propósitos incluyen, pero no se limitan a, transfusión de sangre, trasplante de órganos, almacenamiento de especímenes biológicos y ensayos biológicos.
Como se usa en la presente, una "enfermedad o trastorno asociado con MK2" o, alternativamente, "una enfermedad o trastorno mediado por MK2" significa cualquier enfermedad u otra afección perjudicial en la que se sabe o se sospecha que MK2, o un mutante del mismo, desempeña un papel.
El término "sujeto", como se usa en la presente, significa un mamífero e incluye sujetos humanos y
animales, como animales domésticos (por ejemplo, caballos, perros, gatos, etc.). Los términos "sujeto" y "paciente" se usan indistintamente. En algunas realizaciones, el "paciente" o "sujeto" significa un animal, preferiblemente un mamífero, y lo más preferiblemente un humano.
El término "portador, adyuvante o vehículo farmacéuticamente aceptable" se refiere a un portador, adyuvante o vehículo no tóxico que no destruye la actividad farmacológica del compuesto con el que está formulado. Los portadores, adyuvantes o vehículos farmacéuticamente aceptables que pueden usarse en las composiciones de esta invención incluyen, pero no se limitan a, intercambiadores de iones, alúmina, estearato de aluminio, lecitina, proteínas del suero, como albúmina de suero humano, sustancias tampón como fosfatos, glicina, ácido sórbico, sorbato de potasio, mezclas de glicéridos parciales de ácidos grasos vegetales saturados, agua, sales o electrolitos, como sulfato de protamina, hidrogenofosfato de disodio, hidrogenofosfato de potasio, cloruro de sodio, sales de zinc, sílice coloidal, trisilicato de magnesio, polivinilpirrolidona, sustancias a base de celulosa, polietilenglicol, carboximetilcelulosa de sodio, poliacrilatos, ceras, polímeros de bloque de polietilenopolioxipropileno, polietilenglicol y grasa de lana. La cantidad de compuestos de la presente invención que pueden combinarse con los materiales portadores para producir una composición en una forma de dosificación individual variará dependiendo del huésped tratado, el modo particular de administración, etc. Preferiblemente, las composiciones proporcionadas se formulan de tal manera que pueda administrarse una dosificación de entre 0,01 y aproximadamente 100 mg/kg, o de aproximadamente 0,1 mg/kg a aproximadamente 50 mg/kg, y preferiblemente de aproximadamente 1 mg/kg a aproximadamente 25 mg/kg, del peso corporal del sujeto/día del inhibidor a un paciente que recibe estas composiciones para obtener el efecto terapéutico deseado. La cantidad de un compuesto de la presente invención en la composición también dependerá del compuesto particular en la composición.
La expresión "forma de dosificación unitaria" como se usa en la presente se refiere a una unidad físicamente discreta de un compuesto proporcionado y/o composiciones del mismo apropiadas para el sujeto a tratar. Se entenderá, sin embargo, que el uso diario total del agente activo (es decir, compuestos y composiciones de la presente invención) será decidida por el médico tratante dentro del alcance del buen juicio médico. El nivel de dosis eficaz específico para cualquier sujeto (es decir, paciente) u organismo particulares dependerá de una variedad de factores que incluyen el trastorno que se está tratando y la gravedad del trastorno; la actividad del agente activo específico empleado; la composición específica empleada; edad, peso corporal, salud general, sexo y dieta del sujeto; momento de administración, vía de administración y tasa de excreción del agente activo específico empleado; duración del tratamiento; y factores similares bien conocidos en las técnicas médicas.
El término "parenteral", como se usa en la presente, incluye técnicas de inyección o infusión subcutánea, intravenosa, intramuscular, intraarticular, intrasinovial, intraesternal, intratecal, intrahepática, intralesional e intracraneal.
Como se usa en la presente, una "cantidad terapéuticamente eficaz" significa una cantidad de una sustancia (por ejemplo, un agente terapéutico, composición y/o formulación) que provoca una respuesta biológica deseada. En algunas realizaciones, una cantidad terapéuticamente eficaz de una sustancia es una cantidad que es suficiente, cuando se administra como parte de un régimen de dosificación a un sujeto que padece o es susceptible a una enfermedad, trastorno y/o afección, para tratar, diagnosticar, prevenir y/o retrasar la aparición de la enfermedad, trastorno y/o afección. Como apreciarán los expertos en esta técnica, la cantidad eficaz de una sustancia puede variar dependiendo de factores como el criterio de valoración biológico deseado, la sustancia a administrar, la célula o tejido objetivo, etc. Por ejemplo, la cantidad eficaz de un compuesto proporcionado en una formulación para tratar una enfermedad, trastorno, y/o condición es la cantidad que alivia, mejora, mitiga, inhibe, previene, retrasa el inicio, reduce la gravedad y/o reduce la incidencia de uno o más síntomas o características de la enfermedad, trastorno y/o afección. En algunas realizaciones, una "cantidad terapéuticamente eficaz" es por lo menos una cantidad mínima de un compuesto proporcionado, o una composición que contiene un compuesto proporcionado, que es suficiente para tratar uno o más síntomas de una enfermedad o trastorno mediado por MK2.
Como se usa en la presente, los términos "tratamiento", "tratar" y "tratando" se refieren a aliviar, inhibir, retrasar el inicio, prevenir, mejorar y/o mitigar parcial o completamente un trastorno o afección, o uno o más síntomas del trastorno o afección, como se describe en la presente. En algunas realizaciones, el tratamiento puede administrarse después de que se hayan desarrollado uno o más síntomas. En algunas realizaciones, el término "tratar" incluye prevenir o detener la progresión de una enfermedad o trastorno. En otras realizaciones, el tratamiento puede administrarse en ausencia de síntomas. Por ejemplo, el tratamiento puede administrarse a un individuo susceptible antes de la aparición de los síntomas (por ejemplo, a la luz de un historial de síntomas y/o a la luz de factores genéticos u otros factores de susceptibilidad). El tratamiento también puede continuarse después de que los síntomas hayan desaparecido, por ejemplo, para prevenir o retrasar su reaparición. Por tanto, en algunas realizaciones, el término "tratar" incluye prevenir la recaída o la reaparición de una enfermedad o trastorno.
Como se usa en la presente, el término "inhibidor" se define como un compuesto que se une a y/o inhibe la proteína quinasa objetivo, MK2, con afinidad medible. En ciertas realizaciones, un inhibidor tiene una IC50 y/o constante de unión de menos de aproximadamente 50 pM, menos de aproximadamente 1 pM, menos de aproximadamente 500 nM, menos de aproximadamente 100 nM, o menos de aproximadamente 10 nM.
Los términos "afinidad medible" e "inhibir mediblemente", como se usan en la presente, significan un cambio medible en la actividad de MK2 entre una muestra que comprende un compuesto de la presente invención, o composición del mismo, y MK2, y una muestra equivalente que comprende MK2, en ausencia de dicho compuesto, o composición del mismo.
Como se usa en la presente, el término "irreversible" o "inhibidor irreversible" se refiere a un inhibidor (es decir, un compuesto) que puede unirse covalentemente a una quinasa de una manera sustancialmente no reversible. Es decir, mientras que un inhibidor reversible puede unirse (pero generalmente no puede formar un enlace covalente con) una quinasa y, por lo tanto, puede disociarse de la quinasa, un inhibidor irreversible permanecerá sustancialmente unido a una quinasa una vez que se haya producido el enlace covalente. Los inhibidores irreversibles muestran habitualmente dependencia del tiempo, por lo que el grado de inhibición aumenta con el tiempo con el que el inhibidor está en contacto con la enzima. En ciertas realizaciones, un inhibidor irreversible permanecerá sustancialmente unido a una quinasa una vez que se haya producido el enlace covalente y permanecerá unido durante un periodo de tiempo que es mayor que la vida de la proteína.
Los métodos para identificar si un compuesto actúa como inhibidor irreversible son conocidos por los expertos en la técnica. Tales métodos incluyen, pero no se limitan a, análisis cinético enzimático del perfil de inhibición del compuesto con una quinasa, el uso de espectrometría de masas del objetivo de fármaco proteíco modificado en presencia del compuesto inhibidor, exposición discontinua, también conocida como “lavado”, experimentos, y el uso de marcado, como un inhibidor radiomarcado, para mostrar la modificación covalente de la enzima, así como otros métodos conocidos por un experto en la técnica.
Como se usa en la presente, el término "resistencia a fármacos" se refiere a cambios en la secuencia de ácidos nucleicos de tipo salvaje que codifica una proteína objetivo, y/o la secuencia de aminoácidos de la proteína objetivo, y/o la secuencia de aminoácidos de otra proteína, tales cambios disminuyen o anulan el efecto inhibidor del inhibidor sobre la proteína objetivo. Sin desear estar limitado por ninguna teoría en particular, se cree que ciertos compuestos de la presente invención, es decir, compuestos que son inhibidores irreversibles de quinasas, pueden ser inhibidores efectivos de formas de proteína quinasas resistentes a fármacos.
3. D escripción de rea lizac iones e jem plares:
Como se describe en la presente, la presente invención proporciona inhibidores irreversibles de la quinasa MK2. Sin desear estar limitados por ninguna teoría particular, se cree que los compuestos de la invención comprenden un fracción capaz de unirse covalentemente a un residuo de cisteína clave en el dominio de unión de la quinasa MK2. A Tal fracción se hace referencia en la presente como una "fracción reactiva". Un experto en la técnica apreciará que la quinasa MK2, y los mutantes de la misma, tienen un residuo de cisteína en el dominio de unión. Sin desear estar limitados a ninguna teoría en particular, se cree que la proximidad de una fracción reactiva, presente en un inhibidor de MK2 proporcionado, a la cisteína de interés facilita la modificación covalente de esa cisteína por la fracción reactiva.
Los residuos de cisteína de interés también pueden describirse mediante una porción de identificación de la secuencia de aminoácidos de la quinasa MK2 que incluye la cisteína de interés. Por tanto, en ciertas realizaciones, Cys140 de MK2 se caracteriza porque Cys140 es la cisteína incorporada en la siguiente secuencia de aminoácidos de MK2:
SEQ ID NO. 1:
MLSNSQGQSPPVPFPAPAPPPQPPTPALPHPPAQPPPPPPQQFPQFHVKSGLQIKKNA
IIDDYKVTSOVLGLGINGKVLQIFNKRTQEKFALKMLQDCPKARREVELHWRASQ
CPHIVRIVDVYENLYAGRKCLLIVMECLDGGELFSRIQDRGDQAFTEREASEIMKSI
GEAIQYLHSINIAHRDVKPENLLYTSKRPNAILKLTDFGFAKETTSHNSLTTPCYTPY
YVAPEVLGPEKYDKSCDMWSLGVIMYILLCGYPPFYSNHGLAISPGMKTRIRMGQ
YEFPNPEWSEVSEEVKMLIRNLLKTEPTQRMTITEFMNHPWIMQSTKVPQTPLHTS
RVLKEDKERWEDVKEEMTSALATMRVDYEQIKIKKIEDASNPLLLKRRKKARALE
AAALAH.
Para mayor claridad, Cys140 se proporciona en la secuencia de aminoácidos abreviada a continuación: SEQ ID NO. 2:
NLYAGRKCLLIVMEC(140)LDGGELFSRIQDR.
En ambas SEQ ID NO. 1 y 2, la cisteína 140 está resaltada en negrita con subrayado.
En algunas realizaciones, los compuestos de la presente invención incluyen una fracción reactiva caracterizada porque los compuestos proporcionados modifican covalentemente Cys140 de MK2.
En ciertas realizaciones, los compuestos de la presente invención incluyen una fracción reactiva caracterizada porque un compuesto modifica covalentemente un objetivo de Cys140 de MK2, inhibiendo de este modo irreversiblemente la quinasa.
Por tanto, en algunas realizaciones, una fracción reactiva presente en un compuesto inhibidor de MK2 proporcionado es capaz de unirse covalentemente a un residuo de cisteína inhibiendo de este modo irreversiblemente la enzima. En algunas realizaciones, el residuo de cisteína es Cys140 de MK2. Un experto en la técnica reconocerá que una variedad de fracciones reactivas, como se define en la presente, son adecuadas para tal enlace covalente. Tales fracciones reactivas incluyen, pero no se limitan a, las descritos en la presente y representadas a continuación.
De acuerdo con un aspecto, la presente invención proporciona compuestos seleccionados de:
o
o una sal farmacéuticamente aceptable de los mismos.
Como se ha descrito anteriormente, y como se expone en las reivindicaciones adjuntas, la invención proporciona compuestos específicos (compuestos 1-82, 1-96, 1-97, I-100, 1-121, 1-127 y1 -135), y sales farmacéuticamente aceptables de los mismos. Los compuestos de la invención se representan en la Tabla 1, a continuación, junto con otros compuestos divulgados.
Tabla 1
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
(continuación)
continuación
Ĩcontinuación)
Ĩcontinuación)
Ĩcontinuación)
Ĩcontinuación)
Ĩcontinuación)
continuación
Ĩcontinuación)
Ĩcontinuación)
continuación
(continuación)
(continuación)
(continuación)
continuación
continuación
continuación
continuación
continuación
continuación
En algunas realizaciones, la presente invención proporciona un compuesto de la invención (uno de los compuestos I-82, I-96, 1-97, I-100, I-121, I 127 and 1-135), representados en la Tabla 1, o una sal farmacéuticamente aceptable del mismo.
4. Usos, form ulación y adm in istrac ión :
C om posic iones farm acéuticam ente aceptab les
De acuerdo con otra realización, la invención proporciona una composición que comprende un compuesto de esta invención o una sal farmacéuticamente aceptable del mismo y un portador, adyuvante o vehículo farmacéuticamente aceptable. En ciertas realizaciones, la cantidad de compuesto en las composiciones de esta invención es tal que es eficaz para inhibir de forma medible MK2, o un mutante del mismo, en una muestra biológica o en un paciente. En ciertas realizaciones, se formula una composición de esta invención para su administración a un paciente con necesidad de dicha composición. En algunas realizaciones, se formula una composición de esta invención para la administración oral a un paciente.
Los compuestos y composiciones, de acuerdo con el método divulgado en la presente, se administran usando cualquier cantidad y cualquier vía de administración eficaz para tratar o disminuir la gravedad de un trastorno proporcionado en la presente (es decir, una enfermedad o trastorno mediado por MK2). La cantidad exacta requerida variará de un sujeto a otro, dependiendo de la especie, la edad y el estado general del sujeto, la gravedad de la infección, el agente particular, su modo de administración y similares. Los compuestos de la invención se formulan preferiblemente en forma de dosificación unitaria para facilitar la administración y la uniformidad de dosificación.
Las composiciones de la presente invención pueden administrarse por vía oral, parenteral, por pulverización por inhalación, por vía tópica, rectal, nasal, bucal, vaginal, intraperitoneal, intracisternal o mediante un depósito implantado. En algunas divulgaciones, las composiciones se administran por vía oral, intraperitoneal o intravenosa.
Las formas inyectables estériles de las composiciones de esta invención pueden ser una suspensión acuosa u oleaginosa. Estas suspensiones pueden formularse de acuerdo con técnicas conocidas en la técnica usando agentes dispersantes o humectantes y agentes de suspensión adecuados. La preparación inyectable estéril también puede ser una solución o suspensión inyectable estéril en un diluyente o solvente parenteralmente aceptable no tóxico, por ejemplo como una solución en 1,3-butanodiol. Entre los vehículos y solventes aceptables que pueden emplearse se encuentran el agua, la solución de Ringer y solución isotónica de cloruro de sodio. Además, los aceites fijos estériles se emplean convencionalmente como solvente o medio de suspensión.
Para este propósito, puede emplearse cualquier aceite fijo insípido incluyendo mono o diglicéridos sintéticos. Los ácidos grasos, como el ácido oleico y sus derivados glicéridos, son útiles en la preparación de inyectables, al igual que los aceites naturales farmacéuticamente aceptables, como el aceite de oliva o el aceite de ricino, especialmente en sus versiones polioxietiladas. Estas soluciones o suspensiones oleosas también pueden contener un diluyente o dispersante de alcohol de cadena larga, como carboximetilcelulosa o agentes dispersantes similares que se usan comúnmente en la formulación de formas de dosificación farmacéuticamente aceptables, incluyendo emulsiones y suspensiones. También pueden usarse otros surfactantes comúnmente usados, como Tweens, Spans y otros agentes emulsionantes o potenciadores de biodisponibilidad que se usan comúnmente en la fabricación de formas de dosificación sólidas, líquidas, u otras para propósitos de formulación.
Las formulaciones inyectables pueden esterilizarse, por ejemplo, mediante filtración a través de un filtro de retención bacteriano o incorporando agentes esterilizantes en forma de composiciones sólidas estériles que pueden disolverse o dispersarse en agua estéril u otro medio inyectable estéril antes de su uso.
Para prolongar el efecto de un compuesto de la presente invención, a menudo es deseable ralentizar la absorción del compuesto por inyección subcutánea o intramuscular. Esto puede lograrse mediante el uso de una suspensión líquida de material cristalino o amorfo con poca solubilidad en agua. La velocidad de absorción del compuesto depende entonces de su velocidad de disolución que, a su vez, puede depender del tamaño del cristal y de la forma cristalina. Alternativamente, la absorción retardada de una forma de compuesto administrada por vía parenteral se logra disolviendo o suspendiendo el compuesto en un vehículo oleoso. Las formas de depósito inyectables se preparan formando matrices microencapsuladas del compuesto en polímeros biodegradables como polilactida-poliglicólido. Dependiendo de la relación de compuesto a polímero y la naturaleza del polímero particular empleado, puede controlarse la velocidad de liberación del compuesto. Ejemplos de otros polímeros biodegradables incluyen poli(ortoésteres) y poli(anhídridos). Las formulaciones inyectables de depósito también se preparan atrapando el compuesto en liposomas o microemulsiones que son compatibles con los tejidos corporales.
En algunas realizaciones, se formulan composiciones farmacéuticamente aceptables para administración oral. Tales formulaciones pueden administrarse con o sin alimentos. En algunas divulgaciones, las composiciones farmacéuticamente aceptables de esta invención se administran sin alimentos. En otras divulgaciones, las composiciones farmacéuticamente aceptables de esta invención se administran con alimentos. Las composiciones farmacéuticamente aceptables de esta invención pueden administrarse por vía oral en cualquier forma de dosificación aceptable por vía oral, incluyendo pero no limitado a, cápsulas, comprimidos, suspensiones o soluciones acuosas. En el caso de comprimidos para uso oral, los portadores comúnmente usados incluyen lactosa y almidón de maíz. También se añaden típicamente agentes lubricantes, como estearato de magnesio. Para administración oral en forma de cápsula, los diluyentes útiles incluyen lactosa y almidón de maíz seco. Cuando se requieren suspensiones acuosas para uso oral, el ingrediente activo se combina con agentes emulsionantes y de suspensión. Si se desea, también pueden añadirse ciertos agentes edulcorantes, aromatizantes o colorantes.
Las formas de dosificación sólidas para administración oral incluyen cápsulas, comprimidos, píldoras, polvos y gránulos. En tales formas de dosificación sólidas, el compuesto activo se mezcla con por lo menos un excipiente o portador inerte farmacéuticamente aceptable, como citrato de sodio o fosfato dicálcico y/o a) cargas o extensores como almidones, lactosa, sacarosa, glucosa, manitol y ácido silícico, b) aglutinantes como, por ejemplo, carboximetilcelulosa, alginatos, gelatina, polivinilpirrolidinona, sacarosa y goma arábiga, c) humectantes como glicerol, d) agentes disgregantes como agar-agar, carbonato de calcio, almidón de patata o tapioca, ácido algínico, ciertos silicatos y carbonato de sodio, e) agentes retardantes de la solución como parafina, f) aceleradores de la absorción como compuestos de amonio cuaternario, g) agentes humectantes como, por ejemplo, alcohol cetílico y monoestearato de glicerol, h) absorbentes como caolín y arcilla bentonita, y/o i) lubricantes como talco, estearato de calcio, estearato de magnesio, polietilenglicoles sólidos, lauril sulfato de sodio y mezclas de los mismos. En el caso de cápsulas, comprimidos y píldoras, la forma de dosificación también puede comprender agentes tamponadores.
También pueden emplearse composiciones sólidas de un tipo similar como cargas en cápsulas de gelatina rellenas blandas y duras usando excipientes como lactosa o azúcar de leche, así como polietilenglicoles de alto peso
molecular y similares. Las formas de dosificación sólidas de comprimidos, grageas, cápsulas, píldoras y gránulos pueden prepararse con recubrimientos y cubiertas como recubrimientos entéricos y otros recubrimientos bien conocidos en la técnica de formulación farmacéutica. Pueden contener opcionalmente agentes opacificantes y también pueden ser de una composición que liberen el ingrediente o los ingredientes activos solo, o preferentemente, en una cierta parte del tracto intestinal, opcionalmente, de manera retardada. Los ejemplos de composiciones de inclusión que pueden usarse incluyen sustancias poliméricas y ceras. También pueden emplearse composiciones sólidas de un tipo similar como cargas en cápsulas rellenas de gelatina blandas y duras usando tales excipientes como lactosa o azúcar de la leche así como polietilenglicoles de alto peso molecular y similares.
Los compuestos activos también pueden estar en forma microencapsulada con uno o más excipientes como se ha indicado anteriormente. Las formas de dosificación sólidas de comprimidos, grageas, cápsulas, píldoras y gránulos pueden prepararse con recubrimientos y cubiertas como recubrimientos entéricos, recubrimientos de control de liberación y otros recubrimientos bien conocidos en la técnica de formulación farmacéutica. En tales formas de dosificación sólidas, el compuesto activo puede mezclarse con por lo menos un diluyente inerte, como sacarosa, lactosa o almidón. Tales formas de dosificación también pueden comprender, como es práctica normal, sustancias adicionales distintas de los diluyentes inertes, por ejemplo, lubricantes para comprimidos y otros coadyuvantes para formar comprimidos como estearato de magnesio y celulosa microcristalina. En el caso de cápsulas, comprimidos y píldoras, las formas de dosificación también pueden comprender agentes tamponadores. Pueden contener opcionalmente agentes opacificantes y también pueden ser de una composición tal que liberen el ingrediente o los ingredientes activos solamente, o preferentemente, en una determinada parte del tracto intestinal, opcionalmente, de manera retardada. Los ejemplos de composiciones de inclusión que pueden usarse incluyen sustancias poliméricas y ceras.
Las formas de dosificación líquidas para administración oral incluyen, pero no se limitan a, emulsiones, microemulsiones, soluciones, suspensiones, jarabes y elixires farmacéuticamente aceptables. Además de los compuestos activos, las formas de dosificación líquidas pueden contener diluyentes inertes usados comúnmente en la técnica como, por ejemplo, agua u otros solventes, agentes solubilizantes y emulsionantes como alcohol etílico, alcohol isopropílico, carbonato de etilo, acetato de etilo, alcohol bencílico, benzoato de bencilo, propilenglicol, 1,3-butilenglicol, dimetilformamida, aceites (en particular, aceites de semilla de algodón, cacahuete, maíz, germen de trigo, oliva, ricino y sésamo), glicerol, alcohol tetrahidrofurfurílico, polietilenglicoles y ésteres de ácidos grasos de sorbitán y mezclas de los mismos. Además de diluyentes inertes, las composiciones orales también pueden incluir adyuvantes como agentes humectantes, agentes emulsionantes y de suspensión, agentes edulcorantes, aromatizantes y perfumantes.
Alternativamente, las composiciones farmacéuticamente aceptables de esta invención pueden administrarse en forma de supositorios para administración rectal. Estos pueden prepararse mezclando el agente con un excipiente no irritante adecuado que sea sólido a temperatura ambiente pero líquido a temperatura rectal y, por lo tanto, se derretirá en el recto para liberar el fármaco. Tales materiales incluyen manteca de cacao, cera de abejas y polietilenglicoles.
Las composiciones para administración rectal o vaginal son preferiblemente supositorios que pueden prepararse mezclando los compuestos de esta invención con excipientes o portadores no irritantes adecuados como manteca de cacao, polietilenglicol o una cera para supositorios que son sólidos a temperatura ambiente pero líquidos a temperatura corporal y por lo tanto se funden en el recto o la cavidad vaginal y liberan el compuesto activo.
Las composiciones farmacéuticamente aceptables de esta invención también pueden administrarse por vía tópica, especialmente cuando el objetivo del tratamiento incluye áreas u órganos fácilmente accesibles mediante aplicación tópica, incluyendo enfermedades de los ojos, la piel o el tracto intestinal inferior. Las formulaciones tópicas adecuadas se preparan fácilmente para cada una de estas áreas u órganos.
La aplicación tópica para el tracto intestinal inferior puede efectuarse en una formulación de supositorio rectal (ver más arriba) o en una formulación de enema adecuada. También pueden usarse parches tópicamente transdérmicos.
Para aplicaciones tópicas, las composiciones farmacéuticamente proporcionadas pueden formularse en una pomada adecuada que contenga el componente activo suspendido o disuelto en uno o más portadores. Los portadores para la administración tópica de los compuestos de esta invención incluyen, pero no se limitan a, aceite mineral, vaselina líquida, vaselina blanca, propilenglicol, polioxietileno, compuesto de polioxipropileno, cera emulsionante y agua. Alternativamente, las composiciones farmacéuticamente aceptables proporcionadas pueden formularse en una loción o crema adecuada que contenga los componentes activos suspendidos o disueltos en uno o más portadores farmacéuticamente aceptables. Los portadores adecuados incluyen, pero no se limitan a, aceite mineral, monoestearato de sorbitán, polisorbato 60, cera de ésteres cetílicos, alcohol cetearílico, 2-octildodecanol, alcohol bencílico y agua.
Para uso oftálmico, las composiciones farmacéuticamente aceptables proporcionadas pueden formularse
como suspensiones micronizadas en solución salina estéril con pH ajustado isotónica o, preferiblemente, como soluciones en solución salina estéril con pH ajustado isotónica, con o sin un conservante como cloruro de bencilalconio. Alternativamente, para usos oftálmicos, las composiciones farmacéuticamente aceptables pueden formularse en una pomada como vaselina.
Las composiciones farmacéuticamente aceptables de esta invención también pueden administrarse mediante aerosol nasal o inhalación. Tales composiciones se preparan de acuerdo con técnicas bien conocidas en la técnica de la formulación farmacéutica y pueden prepararse como soluciones en solución salina, empleando alcohol bencílico u otros conservantes adecuados, promotores de la absorción para mejorar la biodisponibilidad, fluorocarbonos y/u otros agentes solubilizantes o dispersantes convencionales.
Las formas de dosificación para la administración tópica o transdérmica de un compuesto de esta invención incluyen pomadas, pastas, cremas, lociones, geles, polvos, soluciones, espráis, inhalantes o parches. El componente activo se mezcla en condiciones estériles con un portador farmacéuticamente aceptable y cualquier conservante o tampón necesario, según se requiera. La formulación oftálmica, las gotas para los oídos y las gotas para los ojos también se contemplan dentro del alcance de esta invención. Además, la presente invención contempla el uso de parches transdérmicos, que tienen la ventaja adicional de proporcionar una administración controlada de un compuesto al cuerpo. Tales formas de dosificación pueden elaborarse disolviendo o dispersando el compuesto en el medio apropiado. También pueden usarse potenciadores de la absorción para aumentar el flujo del compuesto a través de la piel. La velocidad puede controlarse proporcionando una membrana de control de la velocidad o dispersando el compuesto en una matriz de polímero o gel.
Usos de com p uestos y com p osic iones farm acéuticam ente aceptab les
Los compuestos y composiciones descritos en la presente son generalmente útiles para la inhibición de la actividad de quinasas de una o más enzimas. Ejemplos de quinasas que son inhibidas por los compuestos y composiciones descritos en la presente y contra las cuales son útiles los métodos descritos en la presente incluyen MK2, o un mutante de la misma.
La actividad de un compuesto utilizado en esta invención como inhibidor de una quinasa MK2, o un mutante de la misma, puede ensayarse in vitro, in vivo o en una línea celular. Los ensayos in vitro incluyen ensayos que determinan la inhibición de la actividad de fosforilación y/o las consecuencias funcionales posteriores, o la actividad de ATPasa de la quinasa MK2 activada, o un mutante de la misma. Los ensayos in vitro alternativos cuantifican la capacidad del compuesto de prueba para unirse a MK2. La unión del inhibidor puede medirse radiomarcando el compuesto de prueba antes de la unión, aislando el complejo compuesto de prueba/MK2 y determinando la cantidad de radiomarcado unido. Alternativamente, la unión del inhibidor puede determinarse realizando un experimento de competición en el que los compuestos de prueba se incuban con la quinasa MK2 unida a radioligandos conocidos. Las condiciones detalladas para ensayar un compuesto utilizado en esta invención como inhibidor de MK2, o un mutante de la misma, se exponen en los Ejemplos a continuación.
De acuerdo con una divulgación, se describe un método para inhibir la actividad de la proteína quinasa en una muestra biológica que comprende el paso de poner en contacto dicha muestra biológica con un compuesto de esta invención, o una composición que comprende dicho compuesto.
De acuerdo con otra divulgación, se proporciona un método para inhibir la actividad de la quinasa MK2, o un mutante de la misma, en una muestra biológica que comprende el paso de poner en contacto dicha muestra biológica con un compuesto de esta invención, o una composición que comprende dicho compuesto. En ciertas divulgaciones, se describe un método para inhibir irreversiblemente la actividad de la quinasa MK2, o un mutante de la misma, en una muestra biológica que comprende el paso de poner en contacto dicha muestra biológica con un compuesto de esta invención, o una composición que comprende dicho compuesto.
De acuerdo con otra divulgación, se proporciona un método para inhibir la actividad de la quinasa MK2, o un mutante de la misma, en un paciente que comprende el paso de administrar a dicho paciente un compuesto de la presente invención, o una composición que comprende dicho compuesto. De acuerdo con ciertas divulgaciones, se proporciona un método para inhibir irreversiblemente la actividad de la quinasa MK2, o un mutante de la misma, en un paciente que comprende el paso de administrar a dicho paciente un compuesto de la presente invención, o una composición que comprende dicho compuesto. En otras divulgaciones, se proporciona un método para tratar una enfermedad o trastorno mediado por MK2, en un paciente con necesidad de ello, que comprende el paso de administrar a dicho paciente un compuesto de acuerdo con la presente invención o una composición farmacéuticamente aceptable del mismo. Tales trastornos se describen con detalle en la presente.
Q uinasa M K 2
La proteína quinasa 2 activada por MAP quinasa (“MK2”) es una enzima que en los humanos está codificada por el gen MAPKAPK2. Este gen codifica un miembro de la familia de las proteínas quinasas
Ser/Thr. Esta quinasa está regulada a través de la fosforilación directa por la p38 MAP quinasa. Junto con la p38 MAP quinasa, se sabe que esta quinasa está implicada en muchos procesos celulares, incluyendo respuestas inflamatorias y al estrés, exportación nuclear, regulación de la expresión génica y proliferación celular. Se ha demostrado que la proteína de choque térmico HSP27 es uno de los sustratos de esta quinasa in vivo. Se han encontrado dos variantes de transcripción que codifican dos isoformas diferentes para este gen.
MK2 es una proteína de múltiples dominios que consta de un dominio rico en prolina N-terminal, un dominio catalítico, un dominio autoinhibidor y en el extremo C-terminal una señal de exportación nuclear (NES) y una señal de localización nuclear (NLS). Se han caracterizado dos isoformas de MK2 humana. Una isoforma consiste de 400 aminoácidos y la otra isoforma de 370 residuos que se cree que es una variante de corte y empalme que carece del NLS C-terminal. MK2 se localiza en el núcleo de la célula y tras la unión y fosforilación por p38, la MK2 NES se vuelve funcional y ambas quinasas se cotransportan fuera del núcleo al citoplasma. Curiosamente, el transporte del complejo MK2/p38 no requiere MK2 catalíticamente activa, ya que el mutante del sitio activo, Asp207Ala, todavía se transporta al citoplasma. Se cree que la fosforilación de MK2 humana por p38 en los residuos T222, S272 y T334 activa la enzima induciendo un cambio conformacional del dominio autoinhibidor, exponiendo por tanto el sitio activo para la unión del sustrato. Las mutaciones de dos residuos de dominio autoinhibidor W332A y K326E en MK2 murino demuestran un aumento en la actividad basal y una deleción C-terminal del dominio autoinhibidor hace que la enzima sea constitutivamente activa, proporcionando evidencia adicional del papel de este dominio en la inhibición de la actividad de MK2.
Las enfermedades o trastornos asociados con MK2 que se tratan con compuestos de la presente invención incluyen trastornos autoinmunes, trastornos inflamatorios crónicos, trastornos inflamatorios agudos, trastornos autoinflamatorios, trastornos fibróticos, trastornos metabólicos, neoplasias o trastornos cardiovasculares o cerebrovasculares. Por tanto, en algunas divulgaciones, se proporciona un método para tratar una enfermedad o trastorno mediado por MK2 en un paciente con necesidad de ello, en donde dicho método comprende administrar a dicho paciente una cantidad terapéuticamente eficaz de un compuesto proporcionado o una composición del mismo. Tales enfermedades o trastornos mediados por MK2 incluyen, pero no se limitan a, los descritos en la presente.
En algunas divulgaciones, la enfermedad o trastorno mediado por MK2 es un trastorno autoinmune, un trastorno inflamatorio crónico y/o agudo, y/o un trastorno autoinflamatorio. Los trastornos autoinmunes y/o inflamatorios y/o autoinflamatorios ejemplares incluyen: enfermedades inflamatorias del intestino (por ejemplo, colitis ulcerosa o enfermedad de Crohn), esclerosis múltiple, psoriasis, artritis, artritis reumatoide, osteoartritis, artritis juvenil, artritis psoriásica, artritis reactiva, espondilitis anquilosante, síndromes periódicos asociados con criopirina, síndrome de Muckle-Wells, síndrome autoinflamatorio por frío familiar, enfermedad inflamatoria multisistémica de inicio neonatal, sindroma periódico asociado al receptor de TNF, pancreatitis aguda y crónica, aterosclerosis, gota, espondilitis anquilosante, trastornos fibróticos (por ejemplo, fibrosis hepática o fibrosis pulmonar idiopática), nefropatía, sarcoidosis, esclerodermia, anafilaxia, diabetes (por ejemplo, diabetes mellitus tipo 1 o diabetes mellitus tipo 2), retinopatía diabética, enfermedad de Still, vasculitis, sarcoidosis, inflamación pulmonar, síndrome de dificultad respiratoria aguda, degeneración macular húmeda y seca relacionada con la edad, síndromes hemolíticos autoinmunes, hepatitis autoinmune e inflamatoria, neuropatía autoinmune, insuficiencia ovárica autoinmune, orquitis autoinmune, trombocitopenia autoinmune, enfermedad autoinmune asociada a implantes de silicona, síndrome de Sjogren, fiebre mediterránea familiar, lupus eritematoso sistémico, síndromes de vasculitis (por ejemplo, arteritis temporal, de Takayasu y de células gigantes, enfermedad de Behget o granulomatosis de Wegener), vitiligo, manifestación hematológica secundaria de enfermedades autoinmunes (por ejemplo, anemias), autoinmunidad inducida por fármacos, tiroiditis de Hashimoto, hipofisitis, pupura trombocítica idiopática, autoinmunidad inducida por metales, miastenia grave, pénfigo, sordera autoinmune (por ejemplo, enfermedad de Menier), síndrome de Goodpasture, enfermedad de Graves, síndromes autoinmunes relacionados con HW, enfermedad de Gullain-Barre, enfermedad de Addison, síndrome antifosfolípido, asma, dermatitis atópica, enfermedad celíaca, síndrome de Cushing, dermatomiositis, atrofia suprarrenal idiopática, trombocitopenia idiopática, síndrome de Kawasaki, síndrome de Lambert-Eatnicon, anemia perniciosa, polinosis, poliarteritis nodosa, cirrosis biliar primaria, colangitis esclerosante primaria, síndrome de Raynaud, síndrome de Reiter, policondritis recidivante, síndrome de Schmidt, tirotoxidosis, sepsis, choque séptico, choque endotóxico, choque tóxico inducido por exotoxinas, sepsis gramnegativa, síndrome de choque tóxico, glomerulonefritis, peritonitis, cistitis intersticial, inflamaciones inducidas por hiperoxia, enfermedad pulmonar obstructiva crónica (EPOC), vasculitis, reacción de injerto contra huésped (por ejemplo, enfermedad de injerto contra huésped), rechazos de aloinjerto (por ejemplo, rechazo agudo de aloinjerto o rechazo crónico de aloinjerto), rechazo temprano de trasplante (por ejemplo, rechazo agudo de aloinjerto), lesión por reperfusión, dolor (por ejemplo, dolor agudo, dolor crónico, dolor neuropático o fibromialgia), infecciones crónicas, meningitis, encefalitis, miocarditis, gingivitis, trauma posquirúrgico, lesión tisular, lesión cerebral traumática, enterocolitis, sinusitis, uveítis, inflamación ocular, neuritis óptica, úlceras gástricas, esofagitis, peritonitis, periodontitis, dermatomiositis, gastritis, miositis, polimialgia, neumonía y bronquitis.
En algunas divulgaciones, la enfermedad o trastorno mediado por MK2 es un trastorno fibrótico. Los trastornos fibróticos ejemplares incluyen esclerosis/esclerodermia sistémica, nefritis lúpica, enfermedad del tejido conectivo, curación de heridas, cicatrización quirúrgica, lesión de la médula espinal, cicatrización del SNC, lesión
pulmonar aguda, fibrosis pulmonar (por ejemplo, fibrosis pulmonar idiopática o fibrosis quística), enfermedad pulmonar obstructiva crónica, síndrome de dificultad respiratoria del adulto, lesión pulmonar aguda, lesión pulmonar inducida por fármacos, glomerulonefritis, enfermedad renal crónica (por ejemplo, nefropatía diabética), nefropatía inducida por hipertensión, fibrosis del tracto alimentario o gastrointestinal, fibrosis renal, fibrosis hepática o biliar, fibrosis hepática (por ejemplo, esteatohepatitis no alcohólica, hepatitis C o carcinoma hepatocelular), cirrosis (por ejemplo, cirrosis biliar primaria o cirrosis debida a enfermedad del hígado graso (por ejemplo, esteatosis alcohólica y no alcohólica)), fibrosis inducida por radiación (por ejemplo, cabeza y cuello, gastrointestinal o pulmonar), colangitis esclerosante primaria, reestenosis, fibrosis cardíaca (por ejemplo, fibrosis endomiocárdica o fibrosis auricular), cicatrización oftálmica, fibroesclerosis, cánceres fibróticos, fibromas, fibroma, fibroadenomas, fibrosarcomas, arteriopatía de trasplante, queloide, fibrosis mediastínica, mielofibrosis, fibrosis retroperitoneal, fibrosis masiva progresiva, y fibrosis sistémica nefrogénica.
En algunas divulgaciones, la enfermedad o trastorno mediado por MK2 es un trastorno metabólico. Los trastornos metabólicos ejemplares incluyen obesidad, resistencia a los esteroides, intolerancia a la glucosa y síndrome metabólico.
En algunas divulgaciones, la enfermedad o trastorno mediado por MK2 es una neoplasia. Las neoplasias ejemplares incluyen cánceres. En algunas realizaciones, las neoplasias ejemplares incluyen trastornos de angiogénesis, mieloma múltiple, leucemias (por ejemplo, leucemia linfocítica aguda, leucemia mielógena aguda y crónica, leucemia linfocítica crónica, leucemia linfoblástica aguda o leucemia promielocítica), linfomas (por ejemplo, linfoma de células B), linfoma de células T, linfoma de células del manto, linfoma de células pilosas, linfoma de Burkitt, tumores de mastocitos, enfermedad de Hodgkin o enfermedad no de Hodgkin), síndrome mielodisplásico, fibrosarcoma, rabdomiosarcoma; astrocitoma, neuroblastoma, glioma y schwannomas; melanoma, seminoma, teratocarcinoma, osteosarcoma, xenoderma pigmentoso, queratoctantoma, cáncer folicular de tiroides, sarcoma de Kaposi, melanoma, teratoma, rabdomiosarcoma, trastornos metastásicos y óseos, así como cáncer de hueso, boca/faringe, esófago, laringe, estómago, intestino, colon, recto, pulmón (por ejemplo, cáncer de pulmón de células no pequeñas o cáncer de pulmón de células pequeñas), hígado, páncreas, nervios, cerebro (por ejemplo, glioma o glioblastoma multiforme), cabeza y cuello, garganta, ovario, útero, próstata, testículos, vejiga, riñón, mama, vesícula biliar, cuello uterino, tiroides, próstata y piel.
En algunas divulgaciones, el trastorno mediado por MK2 es un trastorno cardiovascular o cerebrovascular. Los trastornos cardiovasculares ejemplares incluyen aterosclerosis, reestenosis de una arteria coronaria aterosclerótica, síndrome coronario agudo, infarto de miocardio, vasculopatía por aloinjerto cardíaco y derrame cerebral. Las enfermedades cerebrovasculares ejemplares incluyen trastornos del sistema nervioso central con un componente inflamatorio o apoptótico, enfermedad de Alzheimer, enfermedad de Parkinson, enfermedad de Huntington, esclerosis lateral amiotrófica, lesión de la médula espinal, isquemia neuronal y neuropatía periférica. EJEMPLIFICACIÓN
Como se representa en los Ejemplos a continuación, en ciertas realizaciones ejemplares, los compuestos se preparan de acuerdo con los siguientes procedimientos generales. Se apreciará que, aunque los métodos generales representan la síntesis de ciertos compuestos de la presente invención, los siguientes métodos generales y otros métodos conocidos por un experto en la técnica, pueden aplicarse a todos los compuestos y subclases y especies de cada uno de estos compuestos, como se describe en la presente.
El alcance de la invención se define en las reivindicaciones adjuntas. Cualquiera de los siguientes ejemplos que no entre dentro del alcance de las reivindicaciones adjuntas se describe con propósitos de referencia.
Los compuestos enantioenriquecidos de la invención se prepararon en forma enantioenriquecida usando materiales de partida quirales, o se separaron después de la reacción con un material de partida racémico, usando cromatografía quiral. Para compuestos preparados como mezclas racémicas o diastereoméricas, los isómeros individuales pueden prepararse en forma ópticamente pura empleando materiales de partida quirales o realizando cromatografía quiral.
En los ejemplos ilustrativos que siguen, las reacciones se llevaron a cabo a temperatura ambiente, en el intervalo de 18-25° C a menos que se indique lo contrario. Las soluciones orgánicas se secaron sobre sulfato de magnesio anhidro o sulfato de sodio y se llevó a cabo la evaporación del solvente usando un evaporador rotatorio a presión reducida. En general, los cursos de las reacciones fueron seguidos por TLC o LCMS y los tiempos de reacción son representativos. Los rendimientos se dan solo con propósitos de ilustración y no son necesariamente los que pueden obtenerse mediante el desarrollo diligente del proceso.
Las reacciones de microondas se realizaron en un sistema de microondas de reacción Biotage Explorer. Los datos de 1H NMR están en valores delta para los principales protones de diagnóstico, expresados en partes por millón (ppm) con respecto al tetrametilsilano (TMS) o el solvente residual. Los espectros de 1H NMR se determinaron a 400 MHz. Las proporciones de solventes se dan en términos de volumen: volumen (v/v). Los datos
de espectros de masas (MS) se generaron en un sistema LCMS en el que el componente de HPLC comprendía generalmente o un instrumento Agilent o Shimadzu LCMS-2020 y se realizaron en una columna Sepax BR-C18 (4,6 x 50 mm, 3 pm) o similar, eluyendo con eluyente ácido (por ejemplo, usando un gradiente entre el 0-95% de agua/acetonitrilo con 0,1% de ácido fórmico o ácido trifluoroacético). Los cromatogramas fueron en electropulverización (ESI) positiva, negativa y/o UV. Los valores de LCMS para m/z se proporcionan en todas partes y generalmente, solo se informan los iones que indican la masa original. A menos que se indique lo contrario, el valor indicado es (M+H) o (M+1) para el modo de iones positivos. La HPLC preparativa se realizó en sílice de fase inversa C18 usando mezclas cada vez menos polares como eluyente, por ejemplo, mezclas cada vez menos polares de agua y acetonitrilo que contenía un 1% de ácido trifluoroacético.
Los compuestos finales y los productos intermedios enantioenriquecidos se sintetizaron usando materiales quirales disponibles comercialmente y su estereoquímica como se registra es absoluta. A menos que se especifique lo contrario, los materiales de partida estaban disponibles comercialmente o se sintetizaron de acuerdo con métodos conocidos.
Tabla de abreviaturas
Los números de los compuestos utilizados en los Ejemplos a continuación corresponden a los números de los compuestos indicados en la Tabla 1, supra.
Síntesis de productos intermedios comunes
Esquema 1A
S1-Paso 1: Síntesis de 6-aminoquinolina-5-carbonitrilo (S1-2)
A una solución de 6-nitroquinolina (100 g, 0,57 mol) en dimetilformamida (1 l), se le añadieron hidróxido de potasio (96,4 g, 1,7 mol) y cianoacetato de etilo (183,3 ml, 1,7 mmol) y la reacción se agitó a temperatura ambiente. durante 48 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. Al residuo resultante, se le añadió HCl al 30% (1,0 l) y se agitó a 100° C durante 3 h. La mezcla de la reacción se enfrió a 0° C y se basificó con una solución de hidróxido de sodio 2N (800 g) y se formó un sólido. El sólido se filtró y se lavó con agua. Luego se disolvió en 20 volúmenes de acetato de etilo y se calentó a 60° C y se trató con carbón vegetal (20,0 g) durante 1 h. La mezcla de la reacción se filtró a través de celite y se concentró a presión reducida. El sólido amarillo obtenido se secó para proporcionar el compuesto del título S1-2 (55,0 g, 56%). 1H NMR (400 MHz, DMSO-d6) 56.84 (br s, 2H), 7.26 (d, J=9.3 Hz, 1H), 7.51 (dd, J=4.2 Hz, 8.3 Hz, 1H), 7.90 (d, J=9.3 Hz, 1H), 8.03 (d, J=8.3 Hz, 1H), 8.60 (d, J=4.2 Hz, 1H). MS m/z (M+H): 170.1.
S1-Paso 2: Síntesis de 6-bromoquinolina-5-carbonitrilo (S1-3)
A una solución de 6-aminoquinolin-5-carbonitrilo (S1-2) (55,0 g, 325 mmol) en acetonitrilo (1,3 l), se le añadió nitrito de terc-butilo (102 ml, 858,5 mmol) a 0° C. La mezcla de la reacción se agitó a 0° C durante 1 h. Luego
se añadió bromuro de cobre (II) (115 g, 520 mmol) a 0° C y se agitó y luego se calentó a 60° C durante 12 h. Luego, la mezcla de la reacción se enfrió a temperatura ambiente y se añadió agua (2,5 l). Esta mezcla se extrajo con cloroformo al 2% en metanol (2,5 l). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El sólido que se había formado mientras se concentraba se filtró y se secó para proporcionar el compuesto del título S1-3 (45,0 g, 62%) como un sólido marrón. 1H NMR (400 MHz, DMSO-d6): 57.85 (dd, J=4.2 Hz, 8.5 Hz, 1H), 8.15 (d, J=9.1 Hz, 1H), 8.28 (d, J=9.0 Hz, 1H), 8.48 (d, J=8.5 Hz, 1H), 9.10 (d, J=3.6 Hz, 1H) MS m/z (M+H): 233.2.
S1-Paso 3: Síntesis de 1-aminotieno[3,2-f]quinolin-2-carboxilato de metilo (S1-4)
A una solución de 6-bromoquinolina-5-carbonitrilo (S1-3) (45,0 g, 193 mmol) en metanol (500 ml), se le añadió metóxido de sodio (20,8 g, 386 mmol) seguido de tioglicolato de metilo (30,7 g, 289,6 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 90° C durante 4 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El residuo obtenido se diluyó con agua y se agitó durante 15 min a temperatura ambiente, tras lo cual se formó un sólido. El sólido se filtró y se secó para proporcionar el compuesto del título S1-4 (40 g, 80%) como un sólido de color amarillo. 1H NMR (400 MHz, DMsO-d6) 5 3.84 (s, 3H), 7.09 (br s, 2H), 7.68 (dd, J=4.2 Hz, 8.5 Hz, 1H), 8.03 (d, J=8.9 Hz, 1H), 8.15 (d, J=8.9 Hz, 1H), 8.93 (d, J=3.5 Hz, 1H), 9.12 (d, J=8.5 Hz, 1H). MS m/z (M+H): 259.0
S1-Paso 4: Síntesis de 1-bromotieno[3,2-f]quinolin-2-carboxilato de metilo (S1-5)
A una solución de 1-aminotieno[3,2-f]quinolin-2-carboxilato de metilo (S1-4) (40 g, 154,8 mmol) en acetonitrilo (1000 ml), nitrito de terc-butilo (27,6 ml, 232 mmol) se añadió gota a gota a 0° C y se agitó durante 1 h a 0° C.A la mezcla resultante, se le añadió bromuro de cobre (II) (41,5 g, 185,8 mmol) en porciones a 0° C y se agitó a temperatura ambiente durante 3 h. Una vez completada, la mezcla de la reacción se diluyó con agua (3,0 l) y se extrajo con metanol al 2% en cloroformo (3,0 l). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para proporcionar el compuesto del título S1-5 (20 g, 40%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-ds) 53.93 (s, 3H), 7.77 (dd, J=4.2 Hz, 8.7 Hz, 1H), 8.14 (d, J=9.0 Hz, 1H), 8.40 (d, J=9.0 Hz, 1H), 9.02 (d, J=3.1 Hz, 1H), 10.10 (d, J=8.8 Hz, 1H). MS m/z (M+H): 323.9.
S1-Paso 5: Síntesis de 1-[[(2R)-2-(terc-butoxicarbonilamino)propil]amino]tieno[3,2-f]quinolin-2-carboxilato de metilo (S1-6)
A una solución de 1-bromotieno [3,2-f] quinolin-2-carboxilato de metilo (S1-5) (14 g, 43,4 mmol) en tolueno (140 ml), se le añadieron carbonato de cesio (28,3 g, 86,9 mmol) y 1-aminopropan-2-ilcarbamato de (R)-terc-butilo (11,3 g, 65,0 mmol, preparado como se describe en el Esquema 2, a continuación) a temperatura ambiente y se desgasificaron durante 15 min. A la mezcla resultante, se le añadió BINAP (2,7 g, 4,3 mmol) y Pd2(dba)3 (3,9 g, 4,3
mmol) a temperatura ambiente y se desgasificó de nuevo durante 10 min. La mezcla de la reacción resultante se agitó a 110° C durante 16 h. Una vez completada, la mezcla de la reacción se filtró a través de celite y se lavó con acetato de etilo y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar el compuesto del título S1-6 (12 g, 66%) como un sólido blanquecino. 1H NMR (400 MHz, DMSO-d6): 5 1.01 (d, J=6.5 Hz, 3H), 1.34 (s, 9H), 3.12 (m, 2H), 3.63 (m, 1H), 3.88 (s, 3H), 6.55 (t, J=7.0 Hz, 1H), 6.71 (br s, 1H), 7.70 (dd, J=4.2 Hz, 8.3 Hz, 1H), 8.04 (d, J=9.0 Hz, 1H), 8.21 (d, J=9.0 Hz, 1H), 8.94 (d, J=3.9 Hz, 1H), 9.04 (d, J=8.3 Hz, 1H). MS m/z (M+H): 416.1.
S1-Paso 6: Síntesis de 1-[[(2R)-2-aminopropil]amino]tieno[3,2-f]quinolin-2-carboxilato trifluoroacetato de metilo (S1-7)
A una solución de 1-[[(2R)-2-(terc-butoxicarbonilamino)propil]amino]tieno[3,2-f]quinolin-2-carboxilato de metilo (S1-6) (11 g, 26,0 mmol) en diclorometano (120 ml), se le añadió ácido trifluoroacético (24,0 g, 211,8 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 25° C durante 2 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida, se co-destiló con diclorometano (3 x 20 ml) para proporcionar el compuesto del título S1-7 (9,0 g, bruto) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-ds): 5 1.26 (d, J=6.2 Hz, 3H), 3.16-3.19 (m, 1H), 3.36-3.49 (m, 2H), 3.92 (s, 3H), 6.39 (br s, 1H), 7.76 (dd, J=4.2 Hz, 8.5 Hz, 1H), 7.86 (br s, 2H), 8.09 (d, J=9.0 Hz, 1H), 8.27 (d, J=9.0 Hz, 1H), 8.99 (d, J=4.2 Hz, 1H), 9.10 (d, J=8.5 Hz, 1H). MS m/z (M+H): 316.1.
S1-Paso 7: Síntesis de (14R)-14-Metil-20-tia-16,17,18-triazatetraciclooctadeca-2(6),3(8),4,9(16),10,12-hexaen-15-ona (S1-8)
A una solución de sal de trifluoroacetato de 1-[[(2R)-2-aminopropil]amino]tieno[3,2-f]quinolin-2-carboxilato de metilo (S1-7) (9,0 g, 28,5 mmol) en metanol (640 ml), se le añadió metóxido de sodio (7,7 g, 142,7 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 90° C durante 12 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El residuo obtenido se diluyó con agua y se agitó durante 15 min, tiempo durante el cual se formó un sólido. El sólido se filtró y se secó al vacío para proporcionar el compuesto del título S1-8 (4,5 g, 55%) como un sólido verde. 1H NMR (400 MHz, DMSO-d6): 5 1.18 (d, J=6.7 Hz, 3H), 3.46 (d, J=2.4 Hz, 2H), 3.59-3.61 (m, 1H), 7.06 (br s, 1H), 7.64 (dd, J=4.2 Hz, 8.5 Hz, 1H), 7.94 (d, J=8.8 Hz, 1H), 8.00 (br s, 1H), 8.09 (d, J=8.9 Hz, 1H), 8.89 (d, J=4.0 Hz, 1H), 9.15 (d, J=8.5 Hz, 1H). MS m/z (M+H): 284.1.
S1-Paso 8: Síntesis de (20R)-20-metil-21-oxo-34-tia-26,27,28-triazatetraciclooctadeca-8(12),9(14),10,15(26),16,18-hexano-27,28-dicarboxilato de di-terc-butilo (S1-9)
A una solución de (14R)-14-metil-20-tia-16,17,18-triazatetraciclooctadeca-2(6),3(8),4,9(16),10,12-hexaen-15-ona (S1-8) (4,5 g, 15,9 mmol) en diclorometano (100 ml), se le añadieron 4-dimetilaminopiridina (0,5 g, 4,0 mmol) y trietilamina (5,5 ml, 39,7 mmol) a temperatura ambiente. La reacción se agitó durante 10 min, luego se añadió
dicarbonato de di-terc-butilo (15,5 ml, 67,5 mmol) a temperatura ambiente y se continuó agitando durante 4 h. Una vez completada, la mezcla de la reacción se diluyó con diclorometano y se lavó con agua. La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar el compuesto del título S1-9 (6,8 g, 88%) como un sólido blanco. MS m/z (M+H): 484.2.
S1-Paso 9: Síntesis de (20R)-20-metil-26-oxido-21-oxo-35-tia-27,28-diaza-26-azoniatetraciclooctadeca-8(12),9(14),10,15(26),16,18-hexano-27,28-dicarboxilato de di-terc-butilo (S1-10)
A una solución de (20R)-20-metil-21-oxo-34-tia-26,27,28-triazatetraciclooctadeca-8(12),9(14),10,15(26),16,18-hexano-27,28-dicarboxilato de di-terc-butilo (S1-9) (6,8 g, 14,0 mmol) en diclorometano (200 ml), se le añadió ácido m-cloroperoxibenzoico (3,6 g, 21,0 mmol) en porciones a 0° C. la mezcla de la reacción resultante se agitó a 30° C durante 3 h. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo y se extrajo con diclorometano. La capa de diclorometano se lavó con una solución de bicarbonato de sodio, se secó sobre sulfato de sodio, se filtró y se concentró a presión reducida. El residuo obtenido se trituró con éter dietílico para proporcionar el compuesto del título S1-10 (6,5 g, 92%) como un sólido amarillo pálido. MS m/z (M+H): 500.1.
S1-Paso 10: Síntesis de (20R)-16-cloro-20-metil-21-oxo-34-tia-26,27,28-triazatetraciclooctadeca-8(13),9,11(16),14(26),15(17),18-hexano-27,28-dicarboxilato de di-terc-butilo (S1-11)
A una solución de (20R)-20-metil-26-oxido-21-oxo-35-tia-27,28-diaza-26-azoniatetraciclooctadeca-8(12),9(14),10,15(26),16,18-hexano-27,28-dicarboxilato de di-terc-butilo (S1-10) (4,0 g, 8,0 mmol) en dimetilformamida (100 ml), se le añadió cloruro de oxalilo (1,03 ml, 12,0 mmol) gota a gota a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El residuo obtenido se diluyó con agua y se agitó durante 5 min, durante ese tiempo se formó un sólido. El sólido se aisló por filtración y se lavó con éter de petróleo para proporcionar el compuesto del título S1-11 (3,9 g, 93%) como un sólido blanquecino. MS m/z (M+H): 518.1.
S1-Paso 11: Síntesis de (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12)
A una solución de (20R)-16-cloro-20-metil-21-oxo-34-tia-26,27,28-triazatetraciclooctadeca-8(13),9,11(16),14(26),15(17),18-hexano-27,28-dicarboxilato de di-terc-butilo (S1-11) (3,0 g, 5,8 mmol) en diclorometano (30,0 ml), se le añadió gota a gota ácido trifluoroacético (3,3 g, 28,9 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida y se co-destiló con diclorometano tres veces. El residuo obtenido se basificó con solución saturada de bicarbonato de sodio (pH ~8) y se formó un sólido. El sólido se filtró y se secó para proporcionar el compuesto del título S1-12 (1,8 g, 96%) como un sólido amarillo. H NMR (400 m Hz, DMSO-d6): 5 1.18 (d, J=6.7 Hz, 3H), 3.44 (m, 2H), 3.59 (m, 1H), 7.07 (br s, 1H), 7.72 (d, J=8.9 Hz, 1H), 7.89 (d, J=8.9 Hz, 1H),
8.10 (d, J=4.1 Hz, 1H), 8.20 (d, J=8.9 Hz, 1H), 9.21 (d, J=8.9 Hz, 1H). MS m/z (M+H): 318.2.
Una solución del compuesto S1-4 (200 g, 775 mmol) en DMF (7,75 l) se enfrió a 0° C bajo nitrógeno. Se añadió NaH (37,2 g, 930 mmol, 60% en mineral) en porciones durante 0,5 h. La mezcla se agitó a 0° C durante otras 0,5 horas y se añadió el compuesto S2-6 (185,5 g, 783 mmol) en porciones durante 0,5 horas. Una vez completada la adición, el análisis de TLC mostró que el material de partida estaba casi consumido. Se añadió lentamente agua (4 l) y la mezcla se agitó durante 10 min. Luego se añadió HCl acuoso (4 l, 1 N) y la mezcla se agitó a temperatura ambiente durante 1 h. Se añadió Na2CÜ3 para ajustar el pH 8 y el sólido resultante se recogió por filtración, se lavó con agua y luego se disolvió en DCM (2,0 l). La fase orgánica se separó, se secó sobre sulfato de sodio anhidro y se concentró. El residuo se suspendió en acetato de etilo (2,0 l) durante 1 hora y luego se filtró. La torta de filtración se secó al vacío para proporcionar el compuesto S1-6 (196 g, rendimiento del 61%) como un sólido blanco. H NMR (400 MHz, DMSO-d6): 51.01 (d, J=6.5 Hz, 3H), 1.34 (s, 9H), 3.12 (m, 2H), 3.63 (m, 1H), 3.88 (s, 3H), 6.55 (t, J=7.0 Hz, 1H), 6.71 (br, 1H), 7.70 (dd, J=4.2 Hz, 8.3 Hz, 1H), 8.04 (d, J=9.0 Hz, 1H), 8.21 (d, J=9.0 Hz, 1H), 8.94 (d, J=3.9 Hz, 1H), 9.04 (d, J=8.3 Hz, 1H). MS m/z (M+H): 416.1.
Una solución del compuesto S1-6 (450 g, 1,08 mol) en DCM (5,4 l) se enfrió a 0° C. Se añadió gota a gota TFA (989 g, 8,67 mol) y la mezcla de la reacción se agitó a temperatura ambiente durante la noche. La mezcla se vertió en NaHCO3 acuoso (1,0 kg en 10,0 l de H2O) con agitación. Se separaron dos fases y la fase acuosa se
extrajo con DCM. Las fases orgánicas se combinaron, se lavaron con agua, se secaron sobre sulfato de sodio anhidro y se concentraron para producir el compuesto S1-7 como base libre (330 g, rendimiento del 96%) como un aceite marrón. 1H NMR (400 MHz, DMSO-d6): 51.07 (d, J=6.4 Hz, 3H), 3.08 (m, 1H), 3.12 (m, 2H), 3.95 (s, 3H), 6.67 (t, J=6.0 Hz), 7.52 (m, 1H), 7.92 (d, 8.8 Hz, 1H), 8.06 (d, 8.8 Hz, 1H), 8.92 (m, 1H), 9.15 (d, J=8.4 Hz, 1H).
A una solución de base libre S1-7 (170 g, 0,54 mol) en metanol (9 l) se le añadió metóxido de sodio (29 g, 0,54 mol). La mezcla de la reacción se agitó a 70° C durante la noche y luego se concentró. Se añadió agua (7,0 l) y la mezcla resultante se agitó durante 20 min y se filtró. La torta del filtro se lavó con agua, se secó al vacío y luego se suspendió en DCM (3,0 l) durante 1 h. La mezcla se filtró y la torta del filtro se lavó con DCM y se secó al vacío para proporcionar el compuesto S1-8 (274 g, rendimiento del 90%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5 1.18 (d, J=6.7 Hz, 3H), 3.46 (d, J=2.4 Hz, 2H), 3.59-3.61 (m, 1H), 7.06 (br s, 1H), 7.64 (dd, J=4.2 Hz, 8.5 Hz, 1H), 7.94 (d, J=8.8 Hz, 1H), 8.00 (br s, 1H), 8.09 (d, J=8.9 Hz, 1H), 8.89 (d, J=4.0 Hz, 1H), 9.15 (d, J=8.5 Hz, 1H). MS m/z (M+H): 284.1.
S2-Paso 1: Síntesis de (R)-2-(terc-butoxicarbonilamino)propil metanosulfonato (S2-2)
A una solución agitada de 1-hidroxipropan-2-ilcarbamato de (R)-terc-butilo (S2-1) (10,0 g, 57 mmol) en diclorometano (100 ml), se le añadieron gota a gota trietilamina (8,65 g, 86 mmol) y cloruro de metanosulfonilo disueltos en diclorometano (5 ml, 63 mmol) a 0° C. La solución resultante se agitó durante 2 h, después de lo cual la mezcla de la reacción se repartió entre diclorometano (200 ml) y agua (100 ml). La fase orgánica se lavó con una solución de HCl 0,1 M (50 ml), una solución de bicarbonato de sodio (50 ml) y salmuera (50 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para obtener el compuesto del título S2-2 (12 g, 83%) como un sólido amarillo claro. 1H NMR (400 MHz, DMSO-d6) 5 1.06 (d, J=6.6 Hz, 3h), 1.37 (s, 9H), 3.15 (s, 3H), 3.73 (m, 1H), 4.03 (d, J=5.8 Hz, 2H), 6.92 (d, J=7.6 Hz, 1H).
m / ^ N H B oc
n 3 y
S2-3
S2-Paso 2: Síntesis de 1-azidopropan-2-ilcarbamato de (S)-terc-butilo (S2-3)
A una solución de (R)-2-(terc-butoxicarbonilamino)propil metanosulfonato (S2-2) (12 g, 47 mmol) en dimetilsulfóxido (75,0 ml), se añadió lentamente azida sódica (3,7 g, 57 mmol) a temperatura ambiente. La mezcla resultante se calentó a 45° C durante 24 horas. Después, la mezcla de la reacción se repartió entre diclorometano (200 ml) y agua con hielo (100 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para obtener el compuesto del título S2-3 (6,0 g, 64%) como un aceite amarillo claro. 1H NMR (400 MHz, DMSO-d6) 51.02 (d, J=6.0 Hz, 3H), 1.37 (s, 9H), 3.20 (d, J=6.0 Hz, 2H), 3.64 (m, 1H), 6.84 (br s, 1H).
S2-Paso 3: Síntesis de 1-aminopropan-2-ilcarbamato de (R)-terc-butilo (S2-4)
A una solución agitada de 1-azidopropan-2-ilcarbamato de (S)-terc-butilo (S2-3) (6,0 g, 30 mmol) en acetato de etilo (50,0 ml), se le añadió Pd/C al 10% (2,3 g). La mezcla de la reacción se agitó en una atmósfera de hidrógeno (1 atm) durante 15 h a temperatura ambiente. La mezcla de la reacción se filtró a través de celite, el celite se lavó con acetato de etilo y el filtrado se concentró a presión reducida para obtener el compuesto del título S2-4 (4,8 g, 92%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-d6) ó 0.95 (d, J=6.6 Hz, 3H), 1.36 (s, 9H), 2.49 (m, 2H), 3.32 (m, 1H), 6.49 (br s, 1H).
Esquema 2B
Una solución de (R)-aminopropan-1-ol (100 g, 1,33 mol) en metanol (1,0 l) se enfrió a 0° C. Se añadieron TEA (278 ml, 2,0 mol) y Boc2O (320 g, 1,47 mol). La mezcla de la reacción se calentó a temperatura ambiente y se agitó durante 1 h. La mezcla se concentró y el residuo se disolvió en DCM (1,0 l). La solución resultante se lavó con NH4Cl acuoso saturado. La fase acuosa se volvió a extraer con DCM (0,2 l). Las fases orgánicas se combinaron, se lavaron con NH4Cl acuoso saturado, se secaron sobre sulfato de sodio anhidro y se concentraron para proporcionar el compuesto S2-1 como un aceite viscoso (240 g), que se usó en el paso siguiente sin purificación adicional.
Se enfrió una solución de imidazol (562 g, 8,26 mol) en DCM (5,5 l) a 0° C. A esta solución se le añadió una solución de cloruro de tionilo (180 ml, 2,48 mol) en DCM (1,9 l) gota a gota durante 0,5 h. Se retiró el baño de enfriamiento y la mezcla se agitó a temperatura ambiente durante 1 h. La mezcla se enfrió a -10° C y se añadió gota a gota una solución del compuesto S2-1 (obtenido en el paso anterior) en DCM (2,6 l). Se retiró el baño de enfriamiento y la mezcla de la reacción se agitó a temperatura ambiente durante 10 min. Se añadió ácido cítrico acuoso (7,2 l, 10%) y la mezcla resultante se agitó durante 15 min. La fase orgánica se separó, se lavó con salmuera (10 l), se secó sobre sulfato de sodio anhidro y se concentró para proporcionar el compuesto S2-5 como una mezcla de diastereómeros, que se usó en el paso siguiente sin purificación adicional. 1H NMR (400 MHz, DMSO-d6) ó 1.29 (d, J=6.4 Hz, 1.6H), 1.50 (d, J=6.0 Hz, 1.5H), 1.53 (s, 9H), 4.06 (m, 0.5H), 4.31 (m, 1H), 4.68 (t, J=9.6 Hz, 0.5H), 4.79 (t, J=9.2 Hz, 0.5H), 5.02 (m, 0.5H).
O Nal04
S RuCI3 (0.05% mol)
O ' "NBoc -------------------------------
S2-5
A una solución de compuesto S2-5 bruto (320 g) en acetonitrilo (5,0 l) se le añadió RuCh (150 mg, 0,725 mmol) seguido de una solución de NaIO4 (310 g, 1,45 mol) en agua (3,3 l). La mezcla de la reacción se agitó a temperatura ambiente durante 40 min y luego se diluyó mediante la adición de DCM (5,0 l) y agua (5,0 l). La fase orgánica se separó, se lavó con salmuera, se secó sobre sulfato de sodio anhidro y se concentró para proporcionar el compuesto S2-6 (218 g) como un sólido marrón. 1H NMR (400 MHz, DMSO-d6) ó 1.51 (d, J=6.4 Hz, 3H), 1.56 (s, 9H), 4.20 (dd, J=9.2 Hz, 6.4 Hz, 1H), 4.42 (m, 1H), 4.67 (dd, J=8.8 Hz, 6.0 Hz, 1H).
Síntesis de (S)-3-cloro-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-1)
El compuesto del título se sintetizó de la misma manera que (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12), sustituyendo 4-(aminometil)-2,2-dimetiloxazolidin-3-carboxilato de (S)-terc-butilo por (1-aminopropan-2-il)carbamato de (R)-terc-butilo. Esto dio el compuesto del título INT-1. Ver Anderson, D.; Meyers, M. et al. Bioorganic & Medicinal Chemistry Letters 19 (2009) 4878-4881.
Síntesis de 3-amino-10-metil-8-oxo-10,11-dihidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-12(9H)-carboxilatode (R)-terc-butilo (INT-2)
Una solución de 3-cloro-10-metil-8-oxo-10,11-dihidro-8H-[1,4]diazepino-[5',6':4,5]tieno[3,2-f]quinolina-9,12-dicarboxilato de (R)-di-terc-butilo (S1-11) (400 mg, 0,7 mmol) en THF se trató con Pd2(dba)3 (76 mg, 0,07 mmol) y 2-(diciclohexilfosfino)bifenilo (65 mg, 0,18 mmol) en un tubo sellado. La solución resultante se desgasificó brevemente aplicando vacío y luego se lavó con nitrógeno tres veces. Luego se añadió hexametildisilazida de litio (1,0 M en THF) (1,9 ml, 1,9 mmol) a temperatura ambiente. La mezcla de la reacción se agitó a 65° C durante 1 h. Una vez completada, la mezcla de la reacción se inactivó con agua fría (10,0 ml) y se extrajo con acetato de etilo (3 x 15 ml). Las capas orgánicas combinadas se secaron sobre sulfato de sodio anhidro y se concentraron a presión reducida. El material bruto obtenido se purificó mediante cromatografía en gel de sílice para proporcionar el compuesto del título INT-2 (180 mg, 58%) como un sólido marrón. MS m/z (M+H): 399.1.
Síntesis de (R)-3-amino-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-8-ona (INT-3)
Se disolvió 3-amino-10-metil-8-oxo-10,11 -dihidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-12(9H)-carboxilato de (R)-terc-butilo (INT-2) (8,0 mg, 0,02 mmol) en diclorometano (1 ml) y se agitó a temperatura ambiente. A esta solución se le añadió ácido trifluoroacético (0,5 ml, 6,49 mmol). La reacción se agitó a temperatura ambiente durante una hora, después de lo cual se eliminaron los volátiles a presión reducida. El residuo resultante se volvió a disolver en diclorometano, se concentró sobre gel de sílice y se purificó mediante cromatografía en gel de sílice (8:1 MeOH/NH4OH en diclorometano (0-10%) para proporcionar el compuesto del título INT-3 (4,0 mg, 67% de rendimiento). MS: m/z 299.0 (M+H) 1H NMR (400 MHz, DMSO-ds): 59.01 (d, 1H), 8.04 (d, 1H), 7.88 (d, 1H), 6.96 (d, 1H), 6.45 (m, 1H), 3.68 (m, 2H), 3.52 (m, 1H), 1.36 (d, 3H).
Síntesis de 3-bromo-10-metil-8-oxo-10,11-dihidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-9,12-dicarboxilato de (R)-di-terc-butilo (INT-4)
A una solución de (R)-9,12-bis(terc-butoxicarbonil)-10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina4-óxido (S1-10) (2,5 g, 5,0 mmol) en dimetilformamida (70,0 ml), se añadió oxibromuro de fósforo (2,15 g, 7,5 mmol) en porciones a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida. El residuo obtenido se diluyó con agua y se agitó durante 5 min y se formó un sólido. El sólido obtenido se filtró y se lavó con éter de petróleo para proporcionar el compuesto del título INT-4 (2,4 g, 78%) como un sólido blanquecino. MS m/z (M+H): 562.1.
Síntesis de (R)-3-bromo-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-8-ona (INT-5)
A una solución de 3-bromo-10-metil-8-oxo-10,11-dihidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-9,12-dicarboxilato de (R)-di-terc-butilo (INT-4) (1,4 g, 2,5 mmol) en diclorometano (90,0 ml), se le añadió ácido trifluoroacético (36,0 ml, 12,4 mmol) a 0° C La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida y se co destiló con diclorometano tres veces. El sólido bruto obtenido se diluyó con solución saturada de bicarbonato de sodio a 0° C hasta pH ~8 y se agitó durante 10 min. En este tiempo se formó un sólido. El sólido se filtró y se secó para proporcionar el compuesto del título INT-5 (830 mg, 88%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 5 1.18 (d, J=6.7 Hz, 3H), 3.44 (s, 2H), 3.60 (br s, 1H), 7.05 (br s, 1H), 7.81 (d, J=8.9 Hz, 1H), 7.90 (d, J=8.9 Hz, 1H), 8.06 (d, J=3.16 Hz, 1H), 8.19 (d, J=8.9 Hz, 1H), 9.10 (d, J=8.9 Hz, 1H). MS m/z (M+H): 362.0.
Síntesis de (R)-3-hidroxi-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino-[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-6)
En un vial de microondas de 10 ml se suspendió (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona, sintetizada en el Esquema (S1-12) (0,1 g, 0,315 mmol) en 3 ml de ácido acético glacial con 1 ml de H2O. El vial se selló y se irradió a 130° C durante 3 h en un reactor de microondas Biotage Explorer. La reacción se enfrió, el precipitado formado se aisló por filtración, se lavó 3 veces con agua y se secó a vacío alto. El filtrado se concentró sobre gel de sílice y se cromatografió con MeOH/NH4OH 8:1 en diclorometano (0-10%). El precipitado y el producto aislado por cromatografía se combinaron para proporcionar el compuesto del título INT-6 (0,080 g, 0,267 mmol, 85% de rendimiento) como un polvo amarillo.
Síntesis a gran escala de (R)-3-h¡drox¡-10-metil-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no-[5',6':4,5]t¡eno[3,2-f]quinolin-8-ona (INT-6)
Se suspendió (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12, 40 g, 0,126 mol) en 300 ml de ácido acético glacial con 100 ml de H2O. La mezcla se agitó a 110° C durante 4 d y luego se enfrió y se concentró hasta la sequedad. Se añadió hidróxido de amonio (28-30% ac) (200 ml) al residuo y la mezcla resultante se agitó a temperatura ambiente durante 30 min y luego se filtró. La torta se lavó con agua y se secó al vacío. El producto bruto se suspendió en acetato de etilo (350 ml) durante 1 h y luego se filtró. La torta se secó al vacío para proporcionar INT-6 como un sólido amarillo (33 g, 87,6%). 1H NMR (400 MHz, DMSO-d6): 5 1.16 (d, J=6.8 Hz, 3H), 3.40 (br, 2H), 3.56 (br, 1H), 6.61 (d, J=10.0 Hz, 1H), 6.88 (br, 1H), 7.44 (d, J=8.8 Hz, 1H), 7.94 (d, J=8.8 Hz, 1H), 8.12 (d, J=4.0 Hz, 1H), 8.81 (d, J=10 Hz, 1H) 11.99 (br, 1H). MS m/z (M+H): 300.1.
Síntesis de ((R)-3-mercapto-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-7)
A una solución de S1-12 (150 mg, 0,5 mmol), en dimetilformamida (2,0 ml), se le añadió hidrosulfuro de sodio (30% p/v, 52,9 mg, 0,9 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 100° C durante 5 h. Una vez completada, la mezcla de la reacción se inactivó con agua y se acidificó con HCl 1N (pH ~2), después de lo cual se formó un sólido. El sólido se filtró y se secó al vacío para proporcionar el compuesto del título INT-7 (100 mg, 55%) como un sólido de color amarillo. 1H NMR (400 MHz, DMSO-d6): 51.16 (d, J=6.6 Hz, 3H), 3.39 (br s, 2H), 3.56 (br s, 1H), 6.91 (br s, 1H), 7.36 (d, J=9.3 Hz, 1H), 7.72 (d, J=8.9 Hz, 1H), 8.04 (d, J=8.9 Hz, 1H), 8.07 (br s, 1H), 8.66 (d, J=9.4 Hz, 1H), 13.87 (br s, 1H). MS m/z (M+H): 316.2.
Síntesis de 4-amino-2-(metiltio)pirimidina-5-carboxilato de etilo (INT-8)
En un vial de 15 ml, se disolvió 4-cloro-2-(metiltio)pirimidina-5-carboxilato de etilo (1,00 g, 4,30 mmol) en THF (10 ml) y se añadió trietilamina (2,00 ml, 14,35 mmol), seguido de amoniaco (2 ml, 4,30 mmol). La mezcla resultante se agitó durante la noche a temperatura ambiente. Una vez completada la reacción, los solventes se evaporaron y la mezcla bruta se purificó por cromatografía en gel de sílice usando hexano/acetato de etilo (0-40%) como eluyente para dar el compuesto del título INT-8 (0,72 g, 3,38 mmol, 79% de rendimiento) como un sólido. 1H NMR (400 MHz, DMSO-d6): 58.55 (s, 1H), 8.02 (br s, 1H), 7.64 (br s, 1H), 4.24 (q, 2H), 2.44 (s, 3H), 1.27 (t, 3H).
Síntesis de 2-((4,6-difluoropirimidin-2-il)oxi)-N,N-dimetiletanamina (S3-2a) y 2-((2,6-difluoropirimidin-4-il)oxi)-N,N-dimetiletanamina (S3-2b)
En un matraz de fondo redondo de 20 ml se disolvió 2,4,6-trifluoropirimidina (S3-1) (0,370 ml, 4,48 mmol) en tetrahidrofurano (8 ml) para dar una solución incolora. Se añadió 2-(dimetilamino)etanol (0,450 ml, 4,48 mmol) a -78° C y la reacción se calentó a temperatura ambiente y se agitó durante 1 h. Una vez completada, la reacción se concentró sobre gel de sílice y se cromatografió con MeOH/NH4OH 8:1 en diclorometano (0-10%). Las fracciones que contenían el producto se recogieron y concentraron para producir los compuestos del título (S3-2a) (0,500 g, 2,462 mmol, 55% de rendimiento) y (S3-2b) (0,045 g, 0,224 mmol, 5% de rendimiento) como una mezcla inseparable. Esta mezcla se usó tal cual en los pasos posteriores.
Síntesis de 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina (S3-3a)
Se añadió amoniaco 7N en MeOH (0,352 ml, 2,461 mmol) a una solución de 2-((4,6-difluoropirimidin-2-il)oxi)-N,N-dimetiletanamina (S3-2a) (0,5 g, 2,461 mmol)) y 2-((2,6-difluoropirimidin-4-il)oxi)-N,N-dimetiletanamina (S3-2b) (0,045 g, 0,221 mmol) en metanol (3 ml). Luego, la reacción se calentó a 70° C. Después de 30 min de calentamiento se formó un precipitado blanco. La reacción se enfrió, se diluyó con diclorometano y se lavó con bicarbonato de sodio saturado (ac.). La capa orgánica se separó y la capa acuosa se extrajo 3 veces adicionales con diclorometano. Las capas orgánicas combinadas se secaron sobre sulfato de sodio y se concentraron para proporcionar un sólido blanco que se recristalizó a partir de acetato de etilo y heptano para proporcionar el compuesto del título S3-3a (0,246 g, 1,230 mmol, rendimiento del 50%).
Síntesis de 6-fluoro-2-(oxetan-3-iloxi)pirimidin-4-amina (INT-9a) y 4-fluoro-6-(oxetan-3-iloxi)pirimidin-2-amina (INT-9b)
El compuesto del título se sintetizó de la misma manera que 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina (S3-3a) sustituyendo oxetan-3-ol por 2-(dimetilamino)etanol. La mezcla de la reacción se calentó a 45° C y el producto se aisló mediante cromatografía en gel de sílice proporcionando el compuesto del título INT-9a (0,266 g, 1,437 mmol, rendimiento del 62%). También se aisló como subproducto una pequeña cantidad de 4-fluoro-6-(oxetan-3-iloxi)pirimidin-2-amina (INT-9b).
Síntesis de (rac)-6-fluoro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina (INT-10)
El compuesto del título se sintetizó de la misma manera que 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina (S3-3a) sustituyendo 1 -metilpiperidin-3-ol por 2-(dimetilamino)etanol. La mezcla de la reacción se calentó a 45° C y el producto se aisló mediante cromatografía en gel de sílice, proporcionando el compuesto del título INT-10 (20 mg, rendimiento del 41%) como un aceite incoloro. MS m/z (M+H): 227.0.
S3-1 INT-11
Síntesis de 6-fluoro-2-(2-(4-metilpiperazin-1-il)etoxi)pirimidin-4-amina (INT-11)
El compuesto del título se sintetizó de la misma manera que 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina (S3-3a) sustituyendo 2-(4-metilpiperazin-1-il)etanol por 2-(dimetilamino)etanol. La mezcla de la reacción se calentó a 45° C y el producto se aisló mediante cromatografía en gel de sílice, proporcionando el compuesto del título INT-11 (60 mg, 51,6%) como un sólido pegajoso incoloro. 1H NMR (400 m Hz, DMSO-d6): 52.34 (s, 3H), 2.34 2.36 (m, 1H), 2.50-2.54 (m, 6H), 2.55-2.65 (m, 3H), 4.25 (t, J=5.6 Hz, 2H), 5.63 (s, 1H), 7.19 (br s, 2H). MS m/z (M+H): 256.2.
S3-1 INT-12
Síntesis de (R)-6-fluoro-2-((1-metilpirrolidin-3-il)oxi)pirimidin-4-amina (INT-12)
El compuesto del título se sintetizó de la misma manera que 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina (S3-3a) sustituyendo (R)-1-metilpirrolidin-3-ol por 2-(dimetilamino)etanol. La mezcla de la reacción se calentó a 45° C y el producto se aisló mediante cromatografía en gel de sílice, proporcionando el compuesto del título INT-12 (60 mg, 51,6%) (140 mg, 70%) como un sólido blanco. MS m/z (M+H): 2l3.1.
Síntesis de 4,6-difluoro-2-((3-metiloxetan-3-il)metoxi)pirimidina (INT-13) y 2,4-difluoro-6-((3-metiloxetan-3-il)metoxi)pirimidina (INT-14)
En un vial de 20 ml se disolvieron (3-metiloxetan-3-il)metanol (0,744 ml, 7,46 mmol), carbonato de cesio (2,430 g, 7,46 mmol) y 2,4,6-trifluoropirimidina (S3-1) (1 g, 7,46 mmol) en 10 ml de THF seco para dar una suspensión incolora. La reacción se agitó a temperatura ambiente durante 1 hora, se vertió en bicarbonato de sodio saturado (ac.) y se extrajo 3 veces con diclorometano. Las capas orgánicas combinadas se secaron sobre sulfato de sodio, se decantaron, se concentraron sobre gel de sílice y se purificaron por cromatografía (acetato de etilo al 0-100% en heptano) para dar una mezcla inseparable 1,3:1 de isómeros INT-13 e INT-14, favoreciendo 4,6-difluoro-2-((3-metiloxetan-3-il)metoxi)pirimidina INT-13. La mezcla se usó tal cual para los pasos posteriores.
Síntesis de 6-fluoro-2-((3-metiloxetan-3-il)metoxi)pirimidin-4-amina (INT-15a) y 4-fluoro-6-((3-metiloxetan-3-il)metoxi)pirimidina-2-amina (INT-15b)
En un vial de 20 ml, la mezcla aislada anterior se calentó a 40° C durante la noche en 10 ml de NH37N en metanol. Una vez completada, la reacción se enfrió y se concentró sobre gel de sílice a presión reducida. Se aisló 6-fluoro-2-((3-metiloxetan-3-il)metoxi)pirimidin-4-amina (INT-15a) mediante cromatografía en gel de sílice (acetato de etilo al 0-100% en heptano) como la fracción más polar (0,557 g, 2,6 mmol, rendimiento del 35,0%). También se aisló como subproducto una pequeña cantidad de 4-fluoro-6-((3-metiloxetan-3-il)metoxi)pirimidin-2-amina (INT-15b).
Síntesis de 4,6-difluoro-2-(2-metoxietoxi)pirimidina (INT-16) y 2,4-difluoro-6-(2-metoxietoxi)pirimidina (INT-17) El compuesto del título se sintetizó de la misma manera que 4,6-difluoro-2-((3-metiloxetan-3-il)metoxi)pirimidina (INT-13) sustituyendo 2-metoxietanol por (3-metiloxetan-3-il)metanol. Esto dio una mezcla inseparable (1:1) de los compuestos del título INT-17 e INT-16 como un líquido incoloro. 1H NMR (400 MHz, CDCh): 5 6.24 (s, 1H), 6.15 (s, 1H), 4.50 (m, 2H), 4.48 (m, 2H), 3.71 (m, 4H), 3.39 (s, 6H).
Síntesis de 4-fluoro-6-(2-metoxietoxi)pirimidin-2-amina (INT-18) y 6-fluoro-2-(2-metoxietoxi)pirimidin-4-amina (INT-19)
En un vial de 20 ml, se calentó luego una mezcla (1:1) de 2,4-difluoro-6-(2-metoxietoxi)pirimidina (INT-17) y 4,6-difluoro-2-(2-metoxietoxi)pirimidina (INT-16) a 65° C en 10 ml de NH3 al 30% en agua. Una vez completada, la reacción se enfrió, se extrajo tres veces con diclorometano y los extractos orgánicos combinados se secaron sobre sulfato de sodio. Luego, la fracción orgánica se concentró sobre gel de sílice y se purificó por cromatografía en gel de sílice (0-100% de acetato de etilo en heptano) para dar los compuestos del título INT-181H NMR (400 MHz, DMSO-d6): 55.62 (1H), 5.09 (br s, 2H), 4.40 (m, 2H), 3.69 (m, 2H), 3.39 (s, 3H) y INT-191H NMR (400 MHz, DMSO-d6): 55.67 (1H), 5.10 (br s, 2 H), 4.42 (m, 2H), 3.67 (m, 2H), 3.40 (s, 3H) como fracciones separadas.
Síntesis de (S)-2,4-difluoro-6-((tetrahidrofuran-3-il)oxi)pirimidina (INT-20) y (S)-4,6-difluoro-2-((tetrahidrofuran-3-il)oxi)pirimidina (iNt-21) (1,00: 0,77)
Los compuestos del título se sintetizaron de la misma manera que 4,6-difluoro-2-((3-metiloxetan-3-il)metoxi)irimidina (INT-13) sustituyendo (S)-tetrahidrofuran-3-ol por (3-metiloxetan-3-il)metanol. Se aisló una mezcla inseparable de (S)-2,4-difluoro-6-((tetrahidrofuran-3-il)oxi)pirimidina (INT-20) y (S)-4,6-difluoro-2-((tetrahidrofuran-3-il)oxi)pirimidina (INT-21) (1,00: 0,77) y se usó directamente en el paso siguiente. 1H NMR (400 MHz, CDCh): 56.19 (s, 1H), 6.17 (s, 1H), 5.60 (m, 1H), 5.47 (m, 1H), 3.98 (m, 4H), 3.91 (m, 4H), 2.27 (m, 2H), 2.24 (m, 2H).
Síntesis de (S)-4-fluoro-6-((tetrahidrofuran-3-il)oxi)pirimidin-2-amina (INT-22) y (S)-6-fluoro-2-((tetrahidrofuran-3-il)oxi)pirimidin-4-amina (INT-23) (1,00:0,77)
El compuesto del título se sintetizó de la misma manera que 4-fluoro-6-(2-metox¡etox¡)p¡rim¡d¡n-2-am¡na (INT-18) y 6-fluoro-2-(2-metoxietoxi)pirimidin-4-amina (INT-19) para dar una mezcla de los compuestos del título INT-22 1H NMR (400 MHz, DMSO-d6): 57.04 (br s, 2H), 5.66 (s, 1H), 5.44 (m, 1H), 3.84-3.72 (m, 4H), 2.20-2.15 (m, 1H), 1.97-1.95 (m, 1H) y INT-231H NMR (400 MHz, DMSO-d6): 57.23 (br s, 2H), 5.63 (s, 1H), 5.31 (m, 1H), 3.83-3.71 (m, 4H), 2.17-2.12 (m, 1H), 1.95-1.92 (m, 1H) que se separaron por cromatografía en gel de sílice (0-100% acetato de etilo en heptano).
Síntesis de (R)-2,4-difluoro-6-((tetrahidrofuran-3-il)oxi)pirimidina (INT-24) y (R)-4,6-difluoro-2-((tetrahidrofuran-3-ilo)oxi)pirimidina (INT-25) (1.3:1)
Los compuestos del título se sintetizaron de la misma manera que 4,6-difluoro-2-((3-metiloxetan-3-il)metoxi)pirimidina (INT-13) sustituyendo (R)-tetrahidrofuran-3-ol por (3-metiloxetan-3-il)metanol. Se aisló una mezcla inseparable de (R)-2,4-difluoro-6-((tetrahidrofuran-3-il)oxi)pirimidina (INT-24) y (R)-4,6-difluoro-2-((tetrahidrofuran-3-il)oxi)pirimidina (INT-25) (1,3:1) y se usó directamente en el siguiente paso. 1H NMR (400 MHz, CDCla): 56.19 (s, 1H), 6.17 (s, 1H), 5.60 (m, 1H), 5.48 (m, 1H), 3.98 (m, 4H), 3.91 (m, 4H), 2.30 (m, 2H), 2.20 (m, 2H).
Síntesis de (R)-4-fluoro-6-((tetrahidrofuran-3-il)oxi)pirimidin-2-amina y (R)-6-fluoro-2-((tetrahidrofuran-3-il)oxi)pirimidin-4-amina (1.3: 1)
El compuesto del título se sintetizó de la misma manera que 4-fluoro-6-(2-metoxietoxi)pirimidin-2-amina (INT-18) y 6-fluoro-2-(2-metoxietoxi)pirimidin-4-amina (INT-19), partiendo de una mezcla de (R)-2,4-difluoro-6-((tetrahidrofuran-3-il)oxi)pirimidina (INT-24) y (R)-4,6-difluoro-2-((tetrahidrofuran-3-il)oxi)pirimidina (INT-25) para dar una mezcla de los compuestos del título iNT-261H NMR (400 MHz, CDCl3): 55.64 (s, 1H), 5.43 (m, 1H), 5.13 (br s, 2H), 4.05-3.88 (m, 4H), 2.18-2.16 (m, 2H) y INT-271H NMR (400 MHz, CDCla): 55.61 (s, 1H), 5.49 (m, 1H), 5.10 (br s, 2H), 3.96-3.86 (m, 4H), 2.21 -2.11 (m, 2H) que se separaron por cromatografía en gel de sílice (acetato de etilo al 0-100% en heptano).
S4-Paso 1: Síntesis de N-terc-butil-6-cloro-2-yodo-pirimidin-4-amina (S4-2)
A una solución agitada de hidruro de sodio (122 mg, 5,1 mmol) y 2-metilpropan-2-amina (399 mg, 5,4 mmol) en tetrahidrofurano (15,0 ml), se le añadió 4,6-dicloro-2-yodo-pirimidina (S4-1) (1,0 g, 3,6 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 5 h. Una vez completada, la mezcla de la reacción se diluyó con acetato de etilo y se lavó con agua. La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en gel de sílice (mesh 100-200) usando 2-5% de acetato de etilo/éter de petróleo para proporcionar el compuesto del título S4-2 (480 mg, 42,3%) como un sólido amarillo pálido. MS m/z (M+H): 312.0.
S4-Paso 2: Síntesis de (rac)-N-terc-butil-6-cloro-2-[(1-metil-3-piperidil)oxi]pirimidin-4-amina (S4-3)
A una solución de hidruro de sodio (18 mg, 0,7 mmol) en tetrahidrofurano (10,0 ml) se le añadieron (rac)-1-metilpiperidin-3-ol (85 mg, 0,7 mmol) y N-terc-butil-6-cloro-2-yodo-pirimidin-4-amina (S4-2) (200 mg, 0,6 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 24 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se purificó mediante cromatografía en columna de gel de sílice usando metanol al 5% en diclorometano para proporcionar el compuesto del título S4-3 (100 mg, 52%) como un líquido gomoso. EM: m/z 299.1 (M+H).
S4-Paso 3: Síntesis de (rac)-6-cloro-2-[(1-metil-3-piperidil)oxi]pirimidin-4-amina (S4-4)
A una solución agitada de (rac)-N-terc-butil-6-cloro-2-[(1-metil-3-piperidil)oxi]pirimidin-4-amina (S4-3) (25 mg, 0,1 mmol) en diclorometano (6,0 ml), se le añadió ácido sulfúrico (4,1 mg, 0,04 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 60° C durante 1 h. Una vez completada, la mezcla de la reacción se basificó con una solución acuosa de amoniaco y se extrajo con diclorometano. La capa orgánica se lavó con agua, solución de salmuera, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para proporcionar el compuesto del título S4-4 (10 mg, 49%) como un sólido blanquecino. 1H NMR (400 MHz, DMSO-d6): 51.33-1.34 (m, 2H), 1.42 1.51 (m, 1 H), 1.67-1.71 (m, 1H), 1.87-1.89 (m, 1H), 1.99-2.02 (m, 2H), 2.15 (s, 3H), 2.75-2.81 (m, 1H), 4.81-4.87 (m, 1H), 6.08 (s, 1H), 7.12 (br s, 2H). MS: m/z 243.1 (M+H).
S4-1 INT-28
Síntesis de (R)-6-cloro-2-((1-metilpirrolidin-3-il)oxi)pirimidin-4-amina (INT-28)
El compuesto del título se sintetizó de la misma manera que (rac)-6-cloro-2-[(1-metil-3-piperidil)oxi]pirimidin-4-amina (S4-4) sustituyendo (R)-1 -metilpirrolidina -3-ol por (rac)-1-metilpiperidin-3-ol en el Paso 2 de la síntesis de S4-4 para dar el compuesto del título INT-28 (90 mg, 58%) como un sólido blanquecino. 1H NMR (400 MHz, DMSO-ds): 5 1.76-1.80 (m, 1H), 2.20-2.27 (m, 1H), 2.31 (s, 3H), 2.43-2.45 (m, 1H), 2.62-2.65 (m, 1H), 2.71-2.75 (m, 1H), 2.83-2.88 (m, 1H), 5.19-5.22 (m, 1H), 6.10 (s, 1H), 7.13 (br s, 2H). MS m/z (M+H): 229.1.
S5-Paso 1: Síntesis de 2,6-dicloro-N-(4-metoxibencil)pirimidin-4-amina (S5-2)
A una solución de 2,4,6-tricloropirimidina (2,0 g, 0,01 mol mmol) en t-butanol (5,0 ml), se le añadieron trietilamina (2,2 g, 0,02 mol) y p-metoxibencil amina (1,6 g, 0,012 mol) a 0° C. La mezcla de la reacción resultante se agitó a 75° C durante 4 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto obtenido se diluyó con diclorometano y se lavó con agua y salmuera. La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El sólido obtenido se purificó mediante cromatografía en columna con acetato de etilo al 1-10% en éter de petróleo para proporcionar el compuesto del título S5-2 (650 mg, 17%) como un sólido blanquecino. 1H NMR: (400 MHz, DMSO-d6): 5 3.72 (s, 3H), 4.42 (d, J=4.8 Hz, 2H), 6.54 (s, 1H), 6.89 (d, J=8.8 Hz, 2H), 7.23 (d J=8.8 Hz, 2H), 8.51 (br s, 1H). MS m/z (M+H): 284.3.
S5-Paso 2: Síntesis de 6-cloro-N-(4-metoxibencil)-2-(2-metoxietoxi)pirimidin-4-amina (S5-3)
A una solución de 2,6-dicloro-N-(4-metoxibencil)pirimidin-4-amina (S5-2) (750 mg, 2,6 mmol) en tetrahidrofurano (15,0 ml), se añadió hidruro de sodio (76,02 mg, 3,2 mmol) a 0° C y se agitó durante 10 min. A la mezcla resultante, se añadió 2-etoxietanol (241,01 mg, 3,2 mmol) a 0° C. La reacción se dejó calentar a 25° C y se agitó durante 12 h. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo (30,0 ml) y se extrajo con acetato de etilo (2 x 50 ml). La capa orgánica se lavó con una solución de salmuera (50,0 ml), se secó sobre sulfato de sodio anhidro, se filtró y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna con 20% de acetato de etilo en hexano para proporcionar el compuesto del título S5-3 (550 mg, 64%) como un sólido blanco. 1H NMR (400 MHz, DMSO-ds): 53.26 (s, 3H), 3.57 (t, J=4.7 Hz, 2H), 3.72 (s, 3H), 4.29 (t, J=4.6 Hz, 2H), 4.42 (br s, 2H), 6.20 (s, 1H), 6.89 (d, J=8.5 Hz, 2H), 7.23 (d, J=8.5 Hz, 2H), 8.09 (br s, 1H). MS m/z (M+H): 324.1.
S5-Paso 3: Síntesis de 6-cloro-2-(2-metoxietoxi)pirimidin-4-amina (S5-4)
Se enfrió a 0° una solución de 6-cloro-N-(4-metoxibencil)-2-(2-metoxietoxi) pirimidin-4-amina (S5-3) (350 mg, 1,1 mmol) en diclorometano (10,0 ml). C y se añadió ácido sulfúrico (212,05 mg, 2,1 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 30 min. Una vez completada, la mezcla de la reacción se inactivó con una solución de amoniaco y se extrajo con diclorometano (2 x 100 ml). La capa orgánica se lavó con 2 x 50 ml de agua, seguido de 20 ml de solución de salmuera saturada. La capa orgánica se secó sobre sulfato de magnesio anhidro, se filtró y se concentró a presión reducida. El material bruto obtenido se purificó mediante TLC preparativa para proporcionar el compuesto del título S5-4 (200 mg, 89%) como un sólido blanco. MS m/z (M+H): 204.1.
Síntesis de 6-cloro-2-(2-(4-metilpiperazin-1-il)etoxi)pirimidin-4-amina (INT-29)
El compuesto del título se sintetizó de la misma manera que 6-cloro-2-(2-metox¡etox¡)p¡rim¡d¡n-4-am¡na (S5-4) sustituyendo 2-(4-metilpiperazin-1-il)etanol por 2-metoxietanol en S5-Paso 2 para dar 6-cloro-2-(2-(4-metilpiperazin-1-il)etoxi)pirimidin-4-amina INT-29 (120 mg, 57%) como un sólido blanco. MS m/z (M+H): 272.3.
S6-paso 1: Síntesis de 4,6-dicloro-2-yodo-pirimidina (S6-2)
A una solución de 4,6-dicloropirimidin-2-amina (S6-1) (5,0 g, 30,5 mmol) en tetrahidrofurano (40,0 ml), se le añadieron yoduro de cobre (I) (5,8 g, 30,5 mmol), yodometano (41,6 g, 155,5 mmol) y nitrito de isoamilo (10,7 g, 91,4 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 80° C durante 3 h. Una vez completada, se filtró a través de un lecho de celite y el filtrado se concentró a presión reducida. El material bruto obtenido se disolvió en acetato de etilo (60 ml) y se lavó con agua (2 x 30 ml) seguido de solución de salmuera (30 ml). La capa orgánica se secó sobre sulfato de sodio anhidro, se filtró y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna de gel de sílice con acetato de etilo al 10% en hexano para proporcionar el compuesto del título S6-2 (4,2 g, 50%) como un sólido amarillo pálido. 1H NMR (400 MHz, CDCh): 57.38 (s, 1H).
S6-Paso 2: Síntesis de 6-cloro-2-yodo-N-(4-metoxibencil)pirimidin-4-amina (S6-3)
A una solución de 4,6-dicloro-2-yodo-pirimidina (S6-2) (2,0 g, 7,3 mmol) en t-butanol (20,0 ml), trietilamina (1,47 g, 14,5 mmol) y p-metoxibencil amina (1,0 g, 7,3 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 70° C durante 2 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El residuo obtenido se disolvió en acetato de etilo (20,0 ml) y la capa orgánica se lavó con agua (2 x 10 ml) seguido de solución de salmuera saturada (1 x 10 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró a presión reducida. El material bruto se purificó mediante cromatografía en columna ultrarrápida con acetato de etilo al 10% en hexano para proporcionar el compuesto del título S6-3 (1,8 g, 65%) como un sólido
blanquecino. MS m/z (M+H): 376.1.
S6-Paso 3: Síntesis de 4-cloro-6-((4-metoxibencil)amino)pirimidina-2-carboxilato de metilo (S6-4)
A una solución de 6-cloro-2-yodo-N-(4-metoxibencil)pirimidin-4-amina (S6-3) (1,0 g, 2,6 mmol) en metanol (8,0 ml), se le añadieron trietilamina (1,1 ml, 8,0 mmol)) y complejo de dicloro[1,1'-bis(difenilfosfino)ferroceno]paladio (II) diclorometano (108,6 mg, 0,1 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 80° C en atmósfera de CO(g) durante 5 h. Una vez completada, la reacción se filtró a través de celite y el filtrado se concentró a presión reducida. El residuo obtenido se disolvió en acetato de etilo (20,0 ml) y la capa orgánica se lavó con agua (2 x 10 ml) seguido de una solución de salmuera (1 x 10 ml). La capa orgánica se secó sobre sulfato de sodio y se concentró a presión reducida. El material bruto se purificó mediante cromatografía en columna ultrarrápida eluyendo en acetato de etilo al 5% en hexano para proporcionar el compuesto del título S6-4 (800 mg, 97%) como un líquido marrón. MS m/z (M+H): 308.2.
S6-Paso 4: Síntesis de 4-amino-6-cloropirimidina-2-carboxilato de metilo (S6-5)
Se enfrió 4-cloro-6-((4-metoxibencil)amino)pirimidina-2-carboxilato de metilo (S6-4) (400 mg, 1,3 mmol) a 0° C y se añadieron ácido trifluoroacético (0,2 ml, 6,5 mmol) y ácido trifluorometanosulfónico (0,2 ml, 6,5 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 30 min. Una vez completada, la reacción se concentró a presión reducida. El residuo obtenido se diluyó con solución saturada de bicarbonato de sodio y se extrajo con diclorometano (20,0 ml). La capa orgánica se lavó con 2 x 10 ml de agua seguido de 10 ml de solución de salmuera saturada. Luego, la capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró a presión reducida. El material bruto se purificó mediante cromatografía en columna ultrarrápida con metanol al 1% en cloroformo para proporcionar el compuesto del título S6-5 (110 mg, 45%) como un sólido marrón. 1H NMR (400 MHz, DMSO-d6): 63.81 (s, 3H), 6.51 (s, 1H), 7.57 (br s, 2H).
E squem a 7
S7-Paso 1: Síntesis de N4-terc-butil-6-fluoro-pirimidina-2,4-diamina (S7-2)
En un tubo sellable, se añadieron una solución de 4,6-difluoropirimidin-2-amina (1,0 g, 7,6 mmol) en 1,4-dioxano/dimetilformamida (20,0 ml, 1:1), carbonato de potasio (1,6 g, 11,9 mmol) y terc-butilamina (1,7 g, 23,0 mmol). La mezcla de la reacción resultante se agitó a temperatura ambiente durante 48 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se diluyó con agua fría (10,0 ml) después de lo cual se formó un sólido. El sólido se filtró y se secó al aire para proporcionar el compuesto del título S7-2 (1,2 g, 85%) como un sólido blanquecino. MS m/z (M+H): 185.1.
S7-Paso 2: Síntesis de N-terc-butil-6-fluoro-2-yodo-pirimidin-4-amina (S7-3)
A una solución de N4 -terc-butil-6-fluoro-pirimidina-2,4-diamina (S7-2) (2,1 g, 11,4 mmol) en tetrahidrofurano (10,0 ml), se le añadieron yoduro de cobre (I) (3,0 g 15,7 mmol), diyodometano (3,16 ml, 39,2 mmol) y nitrito de isoamilo (5,0 ml, 34,2 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 70° C durante 2 h. Una vez completada, la mezcla de la reacción se filtró a través de celite y luego se concentró a presión reducida. El material bruto se purificó mediante cromatografía en columna de gel de sílice para proporcionar el compuesto del título S7-3 (1,5 g, 45%) como un líquido aceitoso marrón. MS m/z (M+H): 296.0.
S7-Paso 3: Síntesis de 4-(terc-butilamino)-6-fluoropirimidina-2-carboxilato de metilo (S7-4)
A una solución de N-terc-butil-6-fluoro-2-yodo-pirimidin-4-amina (S7-3) (1,5 g, 5,1 mmol) en metanol (20,0 ml), se le añadieron PdCl2(dppf) (0,33 g, 0,4 mmol) y trietilamina (0,8 g, 7,6 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 20 psi CO durante 4 h. Una vez completada, la mezcla de la reacción se filtró a través de celite y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna de gel de sílice para proporcionar el compuesto del título S7-4 (800 mg, 69%) como un líquido marrón. 1H NMR (400 MHz, DMSO-d6): 5 1.39 (s, 9H), 3.83 (s, 3H), 6.20 (s, 1H), 7.72 (br s, 1H). MS m/z (M+H): 228.1.
S7-Paso 4: Síntesis de (4-(terc-butilamino)-6-fluoropirimidin-2-il)metanol (S7-5)
A una solución de 4-(terc-butilamino)-6-fluoropirimidin-2-carboxilato de metilo (S7-4) (800 mg, 3,5 mmol) en metanol (20,0 ml), se le añadió borohidruro de sodio (1,3 g, 35,2 mmol) a temperatura ambiente y la reacción se agitó durante 3 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se disolvió en agua (10,0 ml) y se extrajo con acetato de etilo (2 x 10,0 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para proporcionar el compuesto del título S7-5 (600 mg, 86%) como un líquido blanquecino. MS m/z (M+H): 200.1.
S7-Paso 5: Síntesis de N-(terc-butil)-6-fluoro-2-(yodometil)pirimidin-4-amina (S7-6)
A una solución de (4-(terc-butilamino)-6-fluoropirimidin-2-il)metanol (S7-5) (600 mg, 3,0 mmol) en diclorometano (20,0 ml), se le añadieron imidazol (512 mg, 7,5 mmol) y trifenilfosfina (1,6 g, 6,0 mmol) seguido de la adición en porciones de yodo (382 mg, 1,5 mmol) a 25° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 1 h. Una vez completada, la mezcla de la reacción se inactivó con una solución saturada de tiosulfito de sodio (3,0 ml) y se extrajo con diclorometano (2 x 10 ml). La capa orgánica se secó sobre sulfato de sodio anhidro, se filtró y se concentró a presión reducida. El material bruto se purificó mediante cromatografía en gel de sílice para proporcionar el compuesto del título S7-6 (400 mg, 43%) como un sólido viscoso.
1H NMR (400 MHz, DMSO-d6): 51.39 (s, 9H), 4.22 (s, 2H), 5.89 (s, 1H), 7.45 (br s, 1H).
S7-Paso 6: Síntesis de N-(terc-butil)-6-fluoro-2-(piperidin-1-ilmetil)pirimidin-4-amina (S7-7)
A una solución de piperidina (82,6 mg, 0,97 mmol) en acetonitrilo (5,0 ml), se le añadió carbonato de potasio (220 mg, 1,6 mmol) seguido de la adición de N-(terc-butil)-6-fluoro-2-(yodometil)pirimidin-4-amina (S7-6) (250 mg, 0,8 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 30 min. Una vez completada, la mezcla de la reacción se diluyó con agua (10,0 ml) y se extrajo con acetato de etilo (2 x 10 ml). La capa orgánica se separó, se secó sobre sulfato de sodio anhidro, se filtró y se concentró a presión reducida. El material bruto se purificó mediante TLC preparativa para proporcionar el compuesto del título S7-7 (170
mg, 79%) como un líquido verde pálido. 1H NMR (400 MHz, DMSO-d6): 5 1.33-1.36 (m, 2H), 1.38 (s, 9H), 1.44-1.50 (m, 4H), 2.44-2.46 (m, 4H), 3.37 (s, 2H), 5.90 (s, 1H), 7.26 (br s, 1H).
S7-Paso 7: 6-fluoro-2-(p¡per¡d¡n-1-¡lmet¡l)p¡r¡m¡d¡n-4-am¡na (S7-8)
A una solución de N-(terc-butil)-6-fluoro-2-(yodometil)pirimidin-4-amina (S7-7) (170 mg, 0,6 mmol) en diclorometano (15,0 ml), se le añadió H2SO4 concentrado (0,3 ml) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, se decantó el diclorometano y al sólido gomoso resultante se le añadieron unas pocas gotas de solución de NH3 seguido de destilación azeotrópica usando tolueno (2 x 5 ml) para producir el producto bruto. El sólido se trituró con metanol al 10% en cloroformo (4 x 5 ml). La capa orgánica se separó, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para proporcionar el compuesto del título S7-8 (120 mg, 95%) como un sólido blanquecino. MS m/z (M+H): 211.1.
Esquema 8
S8-2
S8-Paso 1: Síntes¡s de metanosulfonato de (S)-(3-cloro-8-oxo-9,10,11,12-tetrah¡dro-8H-[1.4] d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-10-¡l)met¡lo (S8-2)
A una solución agitada de S)-3-cloro-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-1) (50 mg, 0,1 mmol) en diclorometano (5,0 ml) se le añadió trietilamina (0,86 ml, 0,4 mmol) seguido de cloruro de metanosulfonilo (0,24 ml, 0,2 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 10 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto resultante se diluyó con agua con hielo y se formó un sólido. El sólido se filtró y se secó para proporcionar el compuesto S8-2 (50 mg, 81%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 53.18 (s, 3H), 3.42-3.43 (m, 1H), 3.85-3.90 (m, 2H), 4.09-4.13 (m, 1H), 4.28-4.32 (m, 1H), 7.13 (br s, 1H), 7.72 (d, J=8.8 Hz, 1H), 7.90 (d, J=8.8 Hz, 1H), 8.21 (d, J=8.8 Hz, 1H), 8.34 (d, J=5.2 Hz, 1H), 9.16 (d, J=8.8
Hz, 1H). MS m/z (M+H): 412.2.
S8-Paso 2: Síntesis de (S)-10-(azidometil)-3-cloro-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S8-3)
A una solución agitada de metanosulfonato de (S)-(3-cloro-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-10-il)metilo (S8-2) (50,0 mg, 0,1 mmol) en dimetilformamida (2,0 ml), se le añadió azida sódica (15,78 mg, 0,2 mmol) a 0° C. La mezcla de la reacción se agitó a 50° C durante 10 h. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida. El bruto se diluyó con agua con hielo, después de lo cual se formaron sólidos. Los sólidos obtenidos se filtraron y se secaron para proporcionar el compuesto S8-3 (30 mg, 69%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-d6): 53.37-3.51 (m, 2H), 3.63-3.66 (m, 1H), 3.74-3.79 (m, 1H), 7.15 (br s, 1H), 7.72 (d, J=8.8 Hz, 1H), 7.90 (d, J=9.2 Hz, 1H), 8.20 (d, J=8.8 Hz, 1H), 8.33 (d, J=5.2 Hz, 1H), 9.17 (d, J=8.8 Hz, 1H). MS m/z (M+H): 359.1.
S8-Paso 3: Síntesis de (S)-10-(azidometil)-3-((6-fluoropirimidin-4-il)amino)-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S8-4)
Se desgasificó brevemente una solución de (S)-10-(azidometil)-3-cloro-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S8-3) (200 mg, 0,5 mmol) en 1,4-dioxano (6,0 ml) aplicando vacío y luego se enjuagó abundantemente con nitrógeno. A esta 6-fluoropirimidin-4-amina (75,4 mg, 0,7 mmol), se le añadieron secuencialmente Pd2(dba)3 (50,9 mg, 0,06 mmol), Xantphos (32,1 mg, 0,06 mmol) y carbonato de cesio (541,9 mg, 1,6 mmol) a temperatura ambiente. La mezcla se desgasificó de nuevo y se agitó a 90° C durante 10 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se lavó con agua, seguido de metanol al 5% en diclorometano para proporcionar el compuesto S8-4 (80 mg, 32%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-ds): 53.42-3.55 (m, 2H), 3.63-3.66 (m, 1H), 3.76-3.80 (m, 1H), 7.07 (br s, 1H), 7.69 (d, J=8.8 Hz, 1H), 7.90 (d, J=9.2 Hz, 1H), 8.06 (d, J=9.2 Hz, 1H), 8.17 (br s, 1H), 8.26 (d, J=5.2 Hz, 1H), 8.58 (br s, 1H), 9.07 (d, J=8.8 Hz, 1H), 10.92 (br s, 1H).
S8-Paso 4: Síntesis de ((3-((6-fluoropirimidin-4-il)amino)-8-oxo-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-10-il)metil)carbamato de (S)-terc-butilo (S8-5)
A una solución agitada de (S)-10-(azidometil)-3-((6-fluoropirimidin-4-il)amino)-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S8-4) (150 mg, 0,3 mmol) en tetrahidrofurano/agua (2:1) (6,0 ml) se le añadió trifenilfosfina (270 mg, 1,0 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a
85° C durante 16 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se lavó con éter dietílico seguido de metanol al 5% en diclorometano para proporcionar (R)-10-(aminometil)-3-((6-fluoropirimidin-4-il)amino)-9,10,11,12bruto.-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (100 mg) como un sólido amarillo pálido. El material bruto aislado se disolvió en dimetilformamida (5,0 ml) y se añadieron trietilamina (86 mg, 0,7 mmol) y dicarbonato de di-terc-butilo (106 mg, 0,4 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 10 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se purificó mediante HPLC preparativa para proporcionar el compuesto S8-5 (20 mg, 11% después de 2 pasos) como un sólido amarillo. MS m/z (M+H): 510.1.
Síntesis de 6-fluoro-2-((4-metilpiperazin-1-il)metil)pirimidin-4-amina (INT-30)
El compuesto del título se sintetizó de la misma manera que 6-fluoro-2-(piperidin-1-ilmetil)pirimidin-4-amina (S7-8) sustituyendo piperidina por 1-metilpiperazina en S7-Paso 6 para dar el compuesto del título INT-30 (120 mg, 88%) como un sólido blanquecino. 1H NMR (400 MHz, DMSO-d6) (D2O Exchange): 52.29 (s, 3H), 2.52-2.65 (m, 8H), 3.36 (s, 2H), 5.90 (s, 1H), 7.12 (br s, 2H). MS m/z (M+H): 226.2.
Síntesis de 4-cloro-6-(4-metilpiperazin-1-il)-1,3,5-triazin-2-amina (INT-31)
En un matraz de fondo redondo de 10 ml se disolvieron 4,6-dicloro-1,3,5-triazin-2-amina (0,047 g, 0,285 mmol) y 1-metilpiperazina (0,032 ml, 0,285 mmol) en tetrahidrofurano (5 ml) para dar una solución incolora. La reacción se calentó a 65° C y después de una hora la reacción se volvió turbia. La reacción se enfrió y se concentró sobre gel de sílice y se cromatografió con MeOH/NH4OH 8:1 en diclorometano (0-10%) para proporcionar el compuesto del título INT-31 (0,057 g, 0,251 mmol, 88% de rendimiento).
Síntesis de N1-(6-fluoropirimidin-4-il)-N2,N2-dimetiletano-1,2-diamina (INT-32)
En un matraz de fondo redondo de 10 ml, se añadieron 4,6-difluoropirimidina (0,305 g, 2,63 mmol) y K2CO3 (0,363 g, 2,63 mmol) a 1,4-dioxano (5 ml) para dar una suspensión incolora. A esto se añadió N1,N1-dimetiletano-1,2-diamina (0,287 ml, 2,63 mmol) y la reacción se agitó a temperatura ambiente. Después de una hora, la reacción se concentró sobre sílice y gel y se cromatografió con MeOH/NH4OH 8:1 en diclorometano (0-10%) para proporcionar el compuesto del título INT-32 (0,290 g, 1,577 mmol, rendimiento del 60%).
Síntesis de 6-fluoro-N-(2-metoxietil)pirimidin-4-amina (INT-33)
En un m a tra z de fo n d o red on do de 10 ml, se d iso lv ie ro n 4 ,6 -d iflu o ro p ir im id in a (0 ,35 ml, 4 ,13 m m ol) y base de H ün ig (0 ,722 ml, 4 ,13 m m ol) en te tra h id ro fu ra n o (5 m l) p a ra d a r un a so lu c ió n in co lo ra . La re a cc ión se e n frió a 0° C y se añ ad ió 2 -m e to x ie ta n a m in a (0 ,322 ml, 4 ,13 m m ol). S e d e jó c a le n ta r la rea cc ión a te m p e ra tu ra a m b ie n te y se ag itó d u ra n te 3 ho ras. U n a ve z c o m p le ta d a , la rea cc ión se c o n c e n tró so b re ge l de s ílic e p u rifica d o p o r c ro m a to g ra fía (a ce ta to de e tilo al 0 -100 % en h e p tan o) p a ra d a r el c o m p u e s to de l t ítu lo INT-33 (0 ,318 g, 1 ,859 m m ol, 45 % de re n d im ie n to ).
Síntesis de 2,4-dicloro-6-(pirrolidin-1-il)-1,3,5-triazina (INT-34)
A 2 ,4 ,6 -tr ic lo ro -1 ,3 ,5 -tr ia z in a (662 m g, 3 ,59 m m ol) en 4 m l de T H F a 0° C se le a ñ a d ió ba se de H ün ig (732 pl, 4 ,19 m m ol) se g u id a de p irro lid in a (100 pl, 1 ,197 m m ol) en 2 ml de T H F g o ta a go ta . La rea cc ión se ag itó a 0° C. La LC M S d e sp u é s de 1 h m o stró la m a sa d e s e a d a co m o el p ico p rin c ip a l y u n a p e q u e ñ a c a n tid a d de a d uc to de dip irro lid in a . La m e zc la b ru ta se filtró , se c o n c e n tró y se pu rificó m e d ia n te c ro m a to g ra fía en ge l de s ílic e (0 -25% de a ce ta to de e tilo /h e p ta n o s ) p a ra d a r el c o m p u e s to de l t ítu lo INT-34 (223 m g, 1 ,018 m m ol, re n d im ie n to de l 85 % ) co m o un só lido b lanco . M s m /z: 219.1 [M H ].
Síntesis de 4-(4,6-dicloro-1,3,5-triazin-2-il)morfolina (INT-35)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e 2 ,4 -d ic lo ro -6 -(p irro lid in -1 - il)-1 ,3 ,5 -tria z in a (INT-34) s u s titu y e n d o p irro lid in a p o r m o rfo lin a p a ra d a r el c o m p u e s to de l t ítu lo INT-35 co m o un s ó lid o b lanco . EM: m /z 235. [M H ].
Síntesis de 2,4-dicloro-6-(piperidin-1-il)-1,3,5-triazina (INT-36)
A 2,4,6-tricloro-1,3,5-triazina (300 mg, 1,627 mmol) y carbonato de sodio (259 mg, 2,440 mmol) se le añadió tetrahidrofurano (8 ml) a 0° C, seguido de piperdina (163 gl, 1,627 mmol). La mezcla de la reacción se volvió turbia en unos pocos minutos. La LCMS después de 1 h mostró la masa deseada como el producto principal y algún aducto de di-adición como el producto secundario. El material bruto se filtró, se concentró y se purificó mediante cromatografía en gel de sílice (0-20% de acetato de etilo/heptanos) para producir una mezcla del compuesto del título (INT-36, principal) y di-aducto (secundario). LCMS m/z: 233.0 [M+H].
INT-37
Síntesis de 4,6-dicloro-N,N-dimetil-1,3,5-triazin-2-amina (INT-37)
A 2,4,6-tricloro-1,3,5-triazina (300 mg, 1,627 mmol) y carbonato de cesio (689 mg, 2,115 mmol) en tetrahidrofurano (8 ml) se le añadió dimetilamina (1 M en THF (813 gl, 1,627 mmol)) gota a gota a 0° C. Después de 45 min, la LCMS mostró la masa deseada como producto principal y una cantidad menor de aducto de di-adición. La mezcla bruta se filtró y se purificó mediante cromatografía en gel de sílice (0-20% de acetato de etilo/heptanos) para obtener 144 mg de mezcla de principalmente el compuesto del título INT-37 y algo de 6-cloro-N2,N2,N4,N4-tetrametil-1,3,5-triazina-2,4-diamina no deseado. La mezcla se usó en el paso siguiente sin más purificación.
INT-38
Síntesis de 2,4-dicloro-6-metoxi-1,3,5-triazina (INT-38)
A 2,4,6-tricloro-1,3,5-triazina (300 mg, 1,627 mmol) en MeOH (32,500 ml) se le añadió bicarbonato de sodio (137 mg, 1,627 mmol) y la mezcla se agitó a temperatura ambiente durante 45 minutos. Luego, la mezcla se diluyó con agua y se extrajo con diclorometano, se lavó con NaCl saturado (ac.), se secó sobre sulfato de sodio, se filtró y se concentró para dar el compuesto del título INT-38 (271 mg, 1,506 mmol, rendimiento del 93%) como un sólido blanco. 1H-NMR (400 MHz, CDCla): 54.14 (s, 3H).
Síntesis de 2,4-dicloro-6-(3,3-difluoropirrolidin-1-il)-1,3,5-triazina (INT-39)
A 2,4,6-tricloro-1,3,5-triazina (150 mg, 0,813 mmol) y carbonato de cesio (583 mg, 1,789 mmol) en THF (8 ml) a 0° C se le añadió clorhidrato de 3,3-difluoropirrolidina (120 mg, 0,813 mmol) en una porción. A esto se le añadieron 2,2 eq (313 gl) de base de Hünig. La LCMS después de 2 h mostró la masa deseada como el pico principal. La mezcla de la reacción se filtró, se concentró y se purificó mediante cromatografía en gel de sílice (0-10% de acetato de etilo/heptanos) para dar el compuesto del título INT-39 (123 mg, 0,482 mmol, 59,3% de rendimiento) como un sólido blanco. MS m/z: 254.8 [M+H].
Síntesis de 2,4-dicloro-6-(3,3-difluoropiperidin-1-il)-1,3,5-triazina (INT-40)
El compuesto del título se sintetizó de la misma manera que la 2,4-dicloro-6-(3,3-d¡fluorop¡rrolid¡n-1 -il)-1,3,5-triazina (INT-39) sustituyendo el clorhidrato de 3,3-difluoropiperidina por clorhidrato de 3,3-difluoropirrolidina para dar el compuesto del título INT-40. MS: m/z 268.9 [M+H].
Síntesis de ácido (R) -2-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidin-5-carboxílico (INT-41)
En un vial de 20 ml se añadió 2-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6',4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidin-5-carboxilato de (R)-etilo (1-18) (0,112 g, 0,232 mmol) a 5 ml de solución de metanol/agua 4:1. Se añadió LiOH (0,371 ml, 0,371 mmol) y la reacción se calentó a 35° C. Una vez completada, se añadió HCl (0,371 ml, 0,371 mmol) y el producto precipitó de la solución. La reacción se filtró y los sólidos se enjuagaron con agua fría y se secaron al vacío para proporcionar el compuesto INT-41 (0,103 g, 0,226 mmol, rendimiento del 98%).
Síntesis de 10-metil-3-((2-(metilsulfonil)pirimidin-4-il)amino)-8-oxo-10,11-dihidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-12(9H)-carboxilato de (R)-terc-butilo (INT-42)
A una solución de 3-amino-10-metil-8-oxo-10,11-dihidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-12(9H)-carboxilato de (R)-terc-butilo (INT-2) (100,0 mg, 0,2 mmol) en 1,4-dioxano (2,0 ml), se le añadieron 4-cloro-2-metilsulfonilpirimidina (58,0 mg, 0,3 mmol) y carbonato de potasio (102,4 mg, 0,7 mmol), a temperatura ambiente. La solución resultante se desgasificó brevemente aplicando vacío y luego se enjuagó con nitrógeno tres veces. Finalmente, se añadieron Pd2(dba)3(45,9 mg, 0,05 mmol) y DavePhos (2,5 mg, 0,01 mmol) a temperatura ambiente y la mezcla se desgasificó adicionalmente. Se dejó agitar la mezcla de la reacción a 100° C durante 3 h. Una vez completada la reacción, la mezcla de la reacción se diluyó con agua (10,0 ml) y se extrajo con acetato de etilo (2 veces, 10,0 ml). Las capas orgánicas combinadas se secaron sobre sulfato de sodio anhidro y se concentraron a presión reducida. El material bruto obtenido se purificó mediante preparativo para proporcionar el compuesto INT-42 (45 mg, 32%) como un sólido marrón. MS m/z: 555.2 (M+H).
Síntesis de 4-amino-2-cloro-N-(4-metoxibencil)pirimidina-5-carboxamida (INT-43b)
A una solución agitada de 2,4-dicloro-N-[(4-metoxifenil)metil]pirimidina-5-carboxamida (INT-43a, 500 mg, 1,6 mmol, preparada de acuerdo con el procedimiento descrito en la WO 2011/090760 A1) en THF (5 ml) se le añadió amoniaco (1 ml, 24,03 mmol) a 0° C y se agitó a temperatura ambiente durante 30 min. Una vez completada, la mezcla de la reacción se diluyó con agua y se extrajo con acetato de etilo. La capa orgánica combinada se lavó con agua seguido de solución de salmuera, se secó sobre Na2SO4 anhidro y se concentró a presión reducida para proporcionar 1 (440 mg, 85% de rendimiento) como un sólido blanquecino. 1H NMR (400 MHz, DMSO-d6): 53.71 (s, 3H), 4.35 (d, J=6 Hz, 2H), 6.88 (d, J=8.6 Hz, 2H), 7.23 (d, J=8.5 Hz, 2H), 8.22 (s, br, 2H), 8.54 (s, 1H), 9.09 (d, J=5.7 Hz, 1H).
Síntesis de (R)-2-cloro-N-(4-metoxibencil)-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-5-carboxamida (INT-43)
El compuesto del título se sintetizó de la misma manera que I-1 sustituyendo INT-43b por 5-fluoro-2-nitroanilina y (R)-3-bromo-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-5) por (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona. El calentamiento se realizó de forma convencional a 100° C durante 6 h (en lugar de mediante irradiación con microondas). Esto dio (R)-2-cloro-N-(4-metoxibencil)-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidin-5-carboxamida INT-43 (141 mg, 88%) como un sólido amarillo. MS m/z (M+H): 574.1.
Síntesis de (R)-2-cloro-N-(4-metoxibencil)-4-(metil(10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-5-carboxamida (INT-44)
A una solución agitada de (R)-2-cloro-N-(4-metoxibencil)-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1.4] )diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-5-carboxamida (INT-43) (180 mg, 0,3 mmol) en dimetilformamida (2,0 ml) se le añadieron carbonato de potasio (86,66 mg, 0,6 mmol), yoduro de potasio (10,4 mg,
0,06 mmol) y yoduro de metilo (66,7 mg, 0,5 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 75° C durante 1 h. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida. El producto bruto se diluyó con agua y los sólidos formados se filtraron y lavaron con agua y luego se secaron al vacío para proporcionar el compuesto INT-44 (120 mg, 53%) como un sólido amarillo. MS m/z (M+H): 588.4.
Síntesis de 4-cloro-6-(2-metoxietoxi)pirimidin-2-amina (INT-45)
A una solución de 4,6-dicloropirimidin-2-amina (1,0 g, 6,1 mmol) en tetrahidrofurano (20,0 ml), se le añadió hidruro de sodio (175,6 mg, 7,3 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 0° C durante 10 min. A la mezcla de la reacción se le añadió 2-metoxietanol (556,8 mg, 7,3 mmol) a 0° C y se agitó a temperatura ambiente durante 4 h. Una vez completada, la mezcla de la reacción se inactivó con agua con hielo (50 ml), se extrajo con acetato de etilo (2 x 50 ml) y se lavó con salmuera (50,0 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para producir 1 (900 mg, 68%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-ds): 5 3.27 (s, 3H), 3.58-3.61 (m, 2H), 4.33-4.35 (m, 2H), 6.08 (s, 1H), 6.96 (br s, 2H). MS m/z (M+H): 204.1.
Síntesis de 4-cloro-6-[2-(4-metilpiperazin-1-il)etoxi]pirimidin-2-amina (INT-46)
A una suspensión de hidruro de sodio (13,4 mg, 0,3 mmol) en tetrahidrofurano (5,0 ml) se le añadió 2-(4-metilpiperazin-1-il)etanol (43,9 mg, 0,3 mmol) a 0° C. La mezcla de la reacción se agitó a temperatura ambiente durante 30 min. Se añadió una solución de 4,6-dicloropirimidin-2-amina (50 mg, 0,3 mmol) en dimetilformamida (0,5 ml) a la mezcla de la reacción a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 3 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El residuo obtenido se lavó con éter dietílico para proporcionar el compuesto 1 (20 mg, 24%) como un sólido marrón. 1H NMR (400 MHz, DMSO-d6): 5 2.11 (s, 3H), 2.26 (br s, 4H), 2.41 (br s, 4H), 2.58-2.61 (t, J=5.8 Hz, 2H), 4.29-4.32 (t, J=5.9 Hz, 2H), 6.06 (d, J=3.1 Hz, 1H), 6.99 (br s, 2H). MS m/z (M+H): 272.1.
Síntesis de (R)-10-(aminometil)-3-cloro-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-8-ona (INT-47)
A una solución agitada de (S)-10-(azidometil)-3-cloro-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[Ala3,2-f]quinolin-8-ona (S8-3) (50 mg, 0,1 mmol) en agua/tetrahidrofurano (1:3, 4,0 ml)
se le añadió trifenilfosfina (146 mg, 0,4 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 85° C durante 16 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se lavó con éter dietílico para proporcionar el compuesto INT-47 (35 mg, 76%) como un sólido amarillo pálido. MS m/z (M+H): 333.2.
Síntesis de (S)-3-cloro-10-((dimetilamino)metil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-48)
A una solución de (R)-10-(aminometil)-3-cloro-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (10,0 mg, 0,03 mmol) (INT-47) en metanol (4,0 ml) se le añadió formaldehído (0,01 ml, 0,6 mmol) y la reacción se agitó durante 10 min. a temperatura ambiente. Se añadieron ácido acético (1,0 gl) y cianoborohidruro de sodio (1,9 mg, 0,03 mmol) y se continuó agitando a 25° C durante 1 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se diluyó con agua y se extrajo con acetato de etilo. La capa orgánica se lavó con agua seguido de salmuera. La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El material bruto se purificó mediante cromatografía en gel de sílice usando metanol al 5% en diclorometano como eluyente para proporcionar el compuesto INT-48 (7,0 mg, 64%) como un sólido amarillo.
1H NMR (400 MHz, DMSO-ds): 52.21 (s, 6H), 2.33-2.35 (m, 2H), 3.37-3.45 (m, 1H), 3.53-3.62 (m, 1H), 3.63-3.70 (m, 1H), 7.07 (t, J=4.8 Hz, 1H), 7.62 (br s, 1H), 7.70 (d, J=8.8 Hz, 1H), 7.89 (d, J=8.8 Hz, 1H), 8.19 (d, J=8.8 Hz, 1H), 9.19 (d, J=9.2 Hz, 1H). MS m/z (M+H): 361.3.
Síntesis de (S)-3-cloro-10-(yodometil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-8-ona (INT-49)
A una solución agitada de metanosulfonato de (S)-(3-cloro-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-10-il)metilo (S8-2) (140 mg, 0,3 mmol) en acetona (5,0 ml) se le añadió yoduro de sodio (506,46 mg, 3,4 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 60° C durante 16 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se diluyó con agua con hielo, después de lo cual se formaron sólidos. Los sólidos se filtraron y se secaron para proporcionar el compuesto INT-49 (135 mg, 90%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-d6): 5 3.20-3.24 (m, 1H), 3.31-3.35 (m, 1H), 3.42-3.45 (m, 1H), 3.68-3.71 (m, 1H), 3.86-3.89 (m, 1H), 7.18 (br s, 1H), 7.74 (d, J=9.2 Hz, 1H), 7.89 (d, J=8.8 Hz, 1H), 8.20 (d, J=8.8 Hz, 1H), 8.33 (d, J=4.8 Hz, 1H), 9.18 (d, J=8.8 Hz, 1H). MS m/z (M+H): 444.2.
Síntesis de (R)-3-cloro-10-((metilamino)metil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-50)
Se agitó una mezcla de (S)-3-cloro-10-(yodometil)-9,10,11,12-tetrahidro-8H
[1 ,4 ]d ia z e p in o [5 ',6 ':4 ,5 ]tie n o [3 ,2 -f]q u in o lin -8 -o n a (INT-49) (20 m g, 0 ,05 m m ol) y m e tila m in a (2 M en T H F ) (1,8 m l, 4 m m ol) a 90° C d u ra n te 3 h. D e spu és , la m e zc la de la rea cc ión se co n c e n tró a p re s ión red uc id a . El m a te ria l b ru to o b te n id o se p u rificó m e d ia n te T L C p re p a ra tiv a p a ra p ro p o rc io n a r el c o m p u e s to INT-50 (6 ,0 m g, 40 % ) co m o un só lido a m a rillo . 1H N M R (400 M H z, D M S O -d6): 5 2.25 (s, 3H ), 2.52 -2.54 (m , 2H ), 3.22 -3.25 (m, 1H ), 3.32 -3.35 (m, 1H), 3.5 5 -3.60 (m , 1H), 7.14 (t, J= 5.6 Hz, 1H ), 7.70 (d, J = 9.2 Hz, 1H), 7.89 (d, J= 8.8 Hz, 1H), 8.19 (d, J= 8.8 Hz, 1H ), 8.23 (b r s, 1H), 9.24 (d, J= 9.2 Hz, 1H). M S m /z (M H ): 347.1.
Síntesis de (R)-6-cloro-N-(4-metoxibencil)-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)nicotinamida (iNt-51)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e 1-1 s u s titu y e n d o 4 -a m in o -6 -c lo ro -N -(4 -m e to x ib e n c il)n ic o tin a m id a p o r 5 -f lu o ro -2 -n itro a n ilin a . El ca le n ta m ie n to se re a lizó de fo rm a co n v e n c io n a l a 100° C d u ra n te 3 h (en lu g a r de m ed ia n te irra d ia c ió n con m ic ro o n d a s ) p a ra p ro p o rc io n a r el c o m p u e s to INT-51 (15 m g, re n d im ie n to de l 47 % ) co m o un só lido am a rillo . EM : m /z 573.2 (M h ).
Síntesis de (S)-2-cloro-4-((10-(hidroximetil)-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)-N-(4-metoxibencil)pirimidina-5-carboxamida (INT-52)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e 1-17 s u s titu y e n d o 4 -a m in o -2 -c lo ro -N -(4 -m e to x ib e n c il)p ir im id in a -5 -c a rb o x a m id a p o r 6 -flu o ro p ir im id in -4 -a m in a p a ra p ro p o rc io n a r el c o m p u e s to INT-52 (22 mg, 14% ) co m o un só lido am a rillo p á lid o . M S m /z (M H ): 590.3.
Síntesis de 5-(hidroximetil)pirimidina-2,4(1H,3H)-diona (S9-1)
A una mezcla de 1H-pirimidina-2,4-diona (20 g, 178,4 mmol) en una solución acuosa de hidróxido de potasio (8,0 g, 142,7 mmol) en agua (160,0 ml), se le añadió paraformaldehído (6,96 g, 231,9 mmol) en porciones a 0° C. La mezcla de la reacción resultante se agitó a 55° C durante 36 h. Una vez completada, la reacción se enfrió a temperatura ambiente y se concentró a 1/3° del volumen a presión reducida para obtener una masa espesa blanca. El residuo se diluyó con acetona (150 ml) y se agitó a 25° C durante 15 min, momento en el que se formó un precipitado. El sólido se filtró y se lavó con acetona (3 x 50 ml) y se secó al vacío para producir S9-1 (25 g, 98%) como un sólido blanco. MS m/z (M-H): 140.9.
Síntesis de 2,4-dicloro-5-(clorometil)pirimidina (S9-2)
A una suspensión de S9-1 (25 g, 175,9 mmol) en tolueno (50,0 ml), se le añadió oxicloruro de fósforo (134,87 g, 879,6 mmol) a 0° C y se continuó agitando durante 15 min. A la mezcla de la reacción, se le añadió gota a gota DIPEA (68,1 g, 527,7 mmol) mientras se mantenía la temperatura a 0° C. La mezcla de la reacción resultante se agitó a 120° C durante 7 h. Una vez completada la reacción, la mezcla de la reacción se enfrió a temperatura ambiente y se vertió en una mezcla bifásica agitada de acetato de etilo y agua (150 ml/150 ml) a 0° C durante un período de 45 min y se agitó a la misma temperatura. temperatura durante otras 1,5 h. Después, la mezcla de la reacción se extrajo con acetato de etilo al 25% en tolueno (4 x 150 ml). La capa orgánica combinada se lavó con agua (2 x 500 ml) y una solución de salmuera saturada (1 x 500 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para proporcionar S9-2 (28 g, 81%) como un líquido marrón que se usó sin purificación adicional. 1H NMR (400 MHz, DMSO-d6): 58.96 (s, 1H), 4.84 (s, 2H).
Síntesis de 2,4-dicloro-5-(yodometil)pirimidina (INT-53)
A una solución de yoduro de sodio (23,4 g, 156,0 mmol) en acetona seca (150 ml), se le añadió S9-2 (28,0 g, 141,8 mmol) a temperatura ambiente y se agitó durante 30 min. La mezcla de la reacción resultante se calentó a 65° C durante 20 min. Una vez completada, la mezcla de la reacción se enfrió a temperatura ambiente, se filtró y se lavó con acetona (2 x 50 ml). El filtrado combinado se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna ultrarrápida (gel de sílice 60-120, acetona al 10% en éter de petróleo) para producir INT-53 (21 g, 48%) como un sólido amarillo claro. 1H NMR (400 MHz, DMSO-d6): 58.95 (s, 1H), 4.53 (s, 2H). MS m/z (M+H): 287.9.
Síntesis de 2,4-dicloro-5-((metilsulfonil)metil)pirimidina (INT-54)
Se disolvió INT-53 (0,3 g, 1,038 mmol) en 10 ml de DCM con 2 ml de DMSO. Se añadió metanosulfinato de sodio (0,106 g, 1,038 mmol) y la reacción se calentó a 50° C. Después de 3 h, la reacción se diluyó con heptano, se filtró y se concentró para dar INT-54 en DMSO que se usó directamente para el siguiente paso. MS m/z (M+H): 241.0, 243.0.
Síntesis de 2,4-dicloro-5-((difluorometoxi)metil)pirimidina (INT-55)
A una solución agitada de (2,4-dicloropirimidin-5-il)metanol (400 mg, 2,23 mmol) en CH3CN (16 ml) se le añadió yoduro de cobre (I) (45,6 mg, 0,24 mmol) a temperatura ambiente bajo atmósfera inerte seguid de agitación a 60° C durante 10 min. Se añadió gota a gota ácido 2,2-difluoro-2-(fluorosulfonil)acético (2,39 g, 14,4 mmol) y la mezcla de la reacción se mantuvo a 60° C durante otras 4 h. La mezcla de la reacción se inactivó mediante la adición de agua con hielo (30 ml) y se extrajo con acetato de etilo (2 x 50 ml). La capa orgánica combinada se lavó con salmuera (50 ml), se secó sobre Na2SO4 anhidro.y se concentró a presión reducida para obtener el material bruto. La purificación mediante cromatografía en columna sobre gel de sílice (eluyente: EtOAc/hexanos al 15%) para proporcionar el compuesto INT-55 (200 mg, 0,55 mmol, 24,5%) como un aceite incoloro. MS m/z (M+H): 229.0.
Síntesis de 5-(terc-butoximetil)-2,4-dicloropirimidina (INT-56)
A una solución agitada de (2,4-dicloropirimidin-5-il)metanol (200 mg, 1,12 mmol) en una mezcla de DCM (2 ml) y ciclohexano (2 ml) se le añadió 2,2,2-tricloroetanimidato de terc-butilo (268,56 mg, 1,23 mmol) y BF3Et2O (50 ul) a temperatura ambiente. La reacción se agitó a temperatura ambiente durante 15 h. El producto bruto se purificó mediante TLC preparativa (hexano/acetato de etilo, 5:1) para obtener INT-56 (200 mg, 76,1%) como un sólido blanquecino. 1H NMR (400 MHz, CDCla) 58.71 (s, 1H), 4.52 (s, 2H), 1.33 (s, 9H).
reflujo/4 h
INT-57
Síntesis de 5-(bromometil)-4-cloropirimidina (INT-57)
A una solución agitada de 4-cloro-5-metil-pirimidina (1,2 g, 9,33 mmol) en CCl4 (30 ml) se le añadió 1-bromopirrolidina-2,5-diona (2,66 g, 14,9 mmol) y AIBN (0,31 g, 1,87 mmol) a temperatura ambiente y se agitó a 80° C durante 4 h. La reacción se detuvo mediante la adición de Na2SO3 acuoso saturado (40 ml). La capa orgánica se separó y la capa acuosa se extrajo con diclorometano (2 x 30 ml). La capa orgánica combinada se lavó con salmuera (100 ml), se filtró y se concentró a presión reducida para dar el material bruto. La purificación por cromatografía en columna (éter de petróleo: acetato de etilo = 10:1) proporcionó INT-57 (500 mg, 25,8%) como un aceite incoloro.
Síntesis de N-((4-cloropirimidin-5-il)metil)-N,2-dimetilpropan-2-amina (INT-58)
A una solución agitada de 5-(bromometil)-4-cloro-pirimidina (300,0 mg, 1,45 mmol) en MeCN (20 ml) se le añadió N, 2-dimetilpropan-2-amina (113,4 mg, 1,3 mmol) y K2CO3 (393,3 mg, 2,9 mmol) a 0° C y se agitó a esta temperatura durante 1,5 h. La mezcla de la reacción se filtró a través de una almohadilla de Celite® y el filtrado se concentró a presión reducida para dar el material bruto. La purificación por cromatografía en columna (éter de petróleo: acetato de etilo = 15:1) proporcionó INT-58 (140 mg, 45,3%) como un aceite incoloro.
5-(Aliloximetil)-2,4-dicloropirimidina (INT-59)
A una solución de alcohol alílico (0,08 ml, 1,25 mmol) en tetrahidrofurano (3,0 ml), se le añadió tercbutóxido de potasio (174,8 mg, 1,56 mmol) a 0° C y se agitó durante 30 min seguido de la adición de INT-53 (300 mg, 1,0 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 0° C durante 15 min. Una vez completada, se añadió agua con hielo (5,0 ml) a la mezcla de la reacción y luego se extrajo con acetato de etilo (10,0 ml). La capa orgánica se lavó con agua (10,0 ml) seguido de una solución de salmuera saturada (10,0 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para obtener un residuo bruto (300 mg). El residuo se purificó mediante TLC preparativa para proporcionar INT-59 (50 mg, 10%) como un líquido marrón. MS /z
(M+H): 219.1
2,4-D¡cloro-5-(etoximet¡l)p¡r¡m¡d¡na (INT-60): Método A
Se agitó una solución de hidruro de sodio (o KOtBu, 8,3 mmol) (199,4 mg, 8,3 mmol) en etanol (15,0 ml) a 50° C durante 45 min. A la mezcla, se añadió INT-53 (3,0 g, 10,4 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 10 min. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo (50,0 ml), se extrajo con acetato de etilo (2 x 100 ml) y se lavó con solución de salmuera (50 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida (2,8 g). El material bruto obtenido se purificó mediante TLC preparativa para producir INT-60 (402 mg, 19%) como un líquido incoloro. 1H NMR (400 MHz, CDCl3) 58.66 (s, 1H), 4.56 (s, 2H), 3.69-3.64 ((m, 2H), 1.30 (t, J=7.2 Hz, 3H). MS m/z (M+H): 207.1.
Síntesis alternativa de 2,4-dicloro-5-(etoximetil)pirimidina (INT-60): Método B
A una solución de etanol (20 ml) se le añadió cloruro de acetilo (0,55 g, 7,04 mmol). La mezcla se agitó a temperatura ambiente durante 10 min y luego se añadió S9-1 (1,0 g, 7,04 mmol). La mezcla se calentó a 75-80° C durante la noche, se enfrió y luego se concentró para proporcionar 5-(etoximet¡l)p¡r¡m¡dina-2,4(1H,3H)-d¡ona (1,15 g, 96%) bruta como un sólido blanco, que se usó para el siguiente paso sin purificación adicional.
A una suspensión de 5-(etoximet¡l)p¡r¡m¡dina-2,4(1H,3H)-d¡ona (0,5 g, 2,94 mmol) en tolueno (1 ml), se le añadió oxicloruro de fósforo (0,67, 7,35 mmol) a 0° C. y se agitó durante 15 min. A la mezcla de la reacción, se le añadió gota a gota base de Hünig (0,77 ml, 4,41 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 120° C durante 1 h, luego se enfrió a temperatura ambiente y se vertió en una mezcla bifásica agitada de acetato de etilo y agua (1/1, v/v) a 0° C durante un período de 45 min. Se continuó la agitación a la misma temperatura durante 1,5 h más. Luego, la mezcla de la reacción se extrajo con acetato de etilo. La capa orgánica combinada se lavó con agua y salmuera, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para proporcionar INT-60 (0,40 g, 65%) como un líquido marrón. El producto bruto se purificó adicionalmente mediante cromatografía en gel de sílice (éter de petróleo/acetato de etilo, 30/1 a 30/1). 1H NMR (400 MHz, CDCh): 58.67 (s, 1H), 4.56 (s, 2H), 3.66 (q, J=7.2 Hz, 2H), 1.30 (t, J=7.2 Hz, 3H).
Método C
A una suspensión de NaH (79,75 mg, 3,32 mmol) en THF anhidro (50 ml) a 0° C en atmósfera de nitrógeno se le añadió 3-metiloxetan-3-ol (268,39 mg, 3,05 mmol). Después de agitar durante 30 min a 0° C, la mezcla de la reacción se transfirió mediante una cánula a una solución de INT-53 (800 mg, 2,77 mmol) en THF anhidro (50 ml). Después de agitar durante 2 h más a 0° C, se añadió NH4Cl (saturado acuoso) y la reacción se extrajo con acetato de etilo (3 x 50 ml). Los extractos orgánicos combinados se secaron sobre MgSÜ4, se concentraron a presión reducida y el residuo resultante se purificó mediante cromatografía en columna de sílice eluyendo con una mezcla de éter de petróleo: acetato de etilo (1/1). Se obtuvo INT-61 (350 mg, 51%) como un sólido marrón. 1H NMR (400 MHz, CDCl3): 58.71 (s, 1H), 4.77-4.75 (d, J=6.8 Hz, 2H), 4.53 (s, 2H), 4.48-4.46 (d, J=7.2 Hz, 2H), 1.66 (s, 3H). MS m/z (M+H): 249.1.
Los siguientes productos intermedios se sintetizaron mediante uno o más del Método A, Método B o Método C como se ha descrito anteriormente, reemplazando el etanol o 3-metiloxetan-3-ol de esos métodos con el alcohol respectivo en la columna marcada como "Alcohol" para dar los compuestos que se muestran en la columna "producto" de la tabla a continuación.
Métodos A y C
Método B
(continuación)
Síntesis de rac-2,4-dicloro-5-((2-(metoximetil)pirrolidin-1-il)metil)pirimidina
A una suspensión agitada de INT-53 (500,0 mg, 1,73 mmol) en CH3CN anhidro (20 ml, DMF también es un solvente aceptable para esta transformación) se le añadió carbonato de potasio (358,3 mg, 2,6 mmol) y clorhidrato de rac-2-(metoximetil)pirrolidina (262,4 mg, 1,73 mmol) a 0° C para dar una solución marrón. La solución se agitó durante 3 h. La mezcla de la reacción se diluyó con cloroformo y se concentró. La purificación por TLC preparativa (hexano: acetato de etilo 3/1) proporcionó INT-69 (160 mg, 33,4%) MS m/z (M+H): 276,2.
Los siguientes productos intermedios se sintetizaron por el mismo método que INT-69 reemplazando el clorhidrato de rac-2-(metoximetil) pirrolidina con la amina respectiva en la columna marcada como “Amina” usando el procedimiento anterior para dar los compuestos mostrados en la columna de producto.
(continuación)
continuación
continuación
continuación
(continuación)
Síntesis de 2-cloro-6-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)oxi)pirimidina-4-carboxilato de (R)-metilo (INT-91)
Se añadió INT-6 (0,3 g, 1,002 mmol) a 15 ml de DMF seca y se sonicó. A la solución resultante, se le
añadió K2CO3 (1,385 g, 10,02 mmol) y la reacción se calentó a 90° C durante 10 min. Luego, la reacción se enfrió y se añadió 2,6-dicloropirimidin-4-carboxilato de metilo (0,270 g, 1,303 mmol). La reacción se lavó abundantemente con argón y se calentó de nuevo a 90° C durante 3 h. Una vez que se consideró que se hubo completado la reacción, la reacción se enfrió, se filtró y se vertió en agua. El precipitado amarillo que se desarrolló se aisló por filtración, se trituró con EtOAc y se secó al vacío durante la noche. El polvo resultante, INT-91 (0,373 g, 0,794 mmol, rendimiento del 79%) se usó sin purificación adicional para transformaciones posteriores. MS m/z (M+H): 470.0.
Síntesis de (R)-3-((2-cloro-6-(hidroximetil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-92)
Se disolvió INT-91 (0,373 g, 0,794 mmol) en DCM (6 ml) con MeOH (1,2 ml) y se enfrió a 0° C. Se añadió borohidruro de sodio (0,120 g, 3,18 mmol) en dos porciones en el transcurso de 30 min. Se dejó agitar la reacción durante dos horas, después de lo cual se diluyó con 5 ml de metanol y se concentró sobre gel de sílice. Luego se purificó mediante cromatografía ultrarrápida usando un gradiente de MeOH al 0-10% en DCM para producir INT-92 (0,141 g, 0,319 mmol, rendimiento del 40,2%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5 9.35 (d, J=9.2 Hz, 1H), 8.17 (d, J=9.2 Hz, 1H), 8.14 (d, J=5.2 Hz, 1H), 7.83 (d, J=8.7 Hz, 1H), 7.62 (d, J=8.7 Hz, 1H), 7.25 (s, 1H), 7.15 (br, 1H), 4.56 (s, 2H), 3.59 (m, 1H), 3.44 (m, 2H), 1.16 (d, J=6.4 Hz, 3H). MS m/z (M+H): 442.1.
Síntesis de (R)-3-((2-cloro-6-(clorometil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-93)
En un vial de 20 ml, se agitaron CCL (0,277 ml, 2,87 mmol) y trifenilfosfina (753 mg, 2,87 mmol) a temperatura ambiente en 5 ml de DCM durante 15 min. La solución mencionada anteriormente se transfirió luego a un vial que contenía INT-92 (141 mg, 0,319 mmol). Se añadieron 2 ml de DMF seca para ayudar a solubilizar el material de partida y la reacción se calentó a 50° C durante la noche. A la mañana siguiente se consideró que la reacción se había completado, se concentró sobre gel de sílice y se purificó mediante cromatografía ultrarrápida usando un gradiente de MeOH al 0-10% en DCM para producir INT-93 (137 mg, 0,298 mmol, rendimiento del 93%). MS m/z (M+H): 460,0; 462.0.
Síntesis de 4-(2-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6' :4,5]tieno[3,2-f]quinolin-3-il)oxi)pirimidin-5-il)-5,6-dihidropiridin-1(2H)-carboxilato de (R)-terc-butilo (iNt-94)
Se desgasificaron 1-116 (240 mg, 0,489 mmol), 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-5,6dihidropiridina-1 (2H)-carboxilato de terc-butilo (227 mg, 0,734 mmol), carbonato de potasio (203 mg, 1,467 mmol) y PdCÍ2(dppf) (35,8 mg, 0,049 mmol) en DMF (8,0 ml) mediante evacuación/sonicación (3x), rellenando cada vez con N2. La mezcla de la reacción se calentó a 85° C con agitación. Después de 3 h, la mezcla se diluyó con agua y se extrajo con DCM (5x). Las capas orgánicas combinadas se lavaron con salmuera, se secaron sobre Na2SÜ4, se filtraron y se concentraron. La purificación por HPLC (10-95% de MeCN/agua, 0,1% de TFA) dio INT-94 (54 mg, 0,091 mmol, 19% de rendimiento) como un sólido amarillo.
Síntesis de (R)-3-((2-cloro-5-(1,2,3,6-tetrahidropiridin-4-il)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-95)
Se disolvió INT-94 (54 mg, 0,091 mmol) en TFA (1,0 ml) para dar una solución roja. Después de 3 min, la UPLC muestra una reacción completa. El TFA se eliminó mediante evaporación rotatoria y el residuo rojo oscuro resultante se trató con hidróxido de amonio (~2 ml, con cuidado, gota a gota). El color cambió de rojo oscuro a amarillo y se formó un precipitado. La mezcla se sonicó para formar una suspensión que se concentró por evaporación rotatoria para dar un residuo sólido amarillo que se usó directamente sin purificación adicional.
Síntesis de (R)-3-((5-((aliloxi)metil)-2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-96)
A una solución de INT-6 (50 mg, 0,2 mmol) en dimetilformamida (1,0 ml), se le añadió terc-butóxido de potasio (37,2 mg, 0,3 mmol) a 0° C y se agitó durante 10 min seguido de la adición de INT-59 (72,7 mg, 0,3 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 1 h. Una vez completada, la mezcla de la reacción se inactivó con agua (5,0 ml) y se extrajo con 10% de metanol/diclorometano (2 x 10 ml). La capa orgánica se lavó con agua (10 ml) seguido de una solución de salmuera saturada (10 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El material bruto obtenido (50 mg) se purificó mediante TLC preparativa para producir INT-96 (5 mg, 6%) como un sólido amarillo pálido. MS m/z (M+H): 482.1.
Síntesis de 2,4-dicloro-5-((4-(2-metoxietoxi)piperidin-1-il)metil)pirimidina (INT-99)
A una suspensión agitada de K2CO3 (539,0 mg, 3,9 mmol) e INT-53 (750 mg, 2,6 mmol) en CH3CN (25,0 ml) se le añadió clorhidrato de 4-(2-metoxietoxi)piperidina (250,0 mg, 1,3 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se filtró a través de una almohadilla de Celite® y el filtrado se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar INT-99 (152,0 mg, 36,5%) como un líquido incoloro.
1H NMR (400 MHz, CDCh) 5 8.66 (s, 1H), 3.62-3.53 (m, 6H), 3.45-3.37 (m, 4H), 2.85-2.72 (m, 2H), 2.35-2.22 (m, 2H), 2.00-1.82 (m, 2H), 1.72-1.55 (m, 2H). MS m/z (M+H): 320.1.
Síntesis de 2,4-dicloro-5-((4-(2-fluoroetoxi)piperidin-1-il)metil) (INT-100)
A una suspensión agitada de K2CO3 (602,0 mg, 4,4 mmol) e INT-53 (1,6 g, 5,5 mmol) en CH3CN (25,0 ml) se añadió clorhidrato de 2-(piperidin-4-iloxi)etanol (604,0 mg, 2,2 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se filtró a través de una almohadilla de Celite® y el filtrado se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar 2-((1-((2,4-dicloropirimidin-5-il)metil)piperidin-4-il)oxi)etan-1-ol (304,0 mg, 45%) como líquido incoloro. MS m/z (M+H): 302.1.
A una solución agitada de 2-((1-((2,4-dicloropirimidin-5-il)metil)piperidin-4-il)oxi)etan-1-ol (304,0 mg, 1,0 mmol) en CH2Cl2 (8,0 ml) se añadió DAST (322,0 mg, 2,0 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar INT-100 (70,0 mg, 23%) como un líquido incoloro. MS m/z (M+H): 308.2.
Síntesis de 2,4-dicloro-5-((4-(metoxi-d3)piperidin-1-il)metil)pirimidina (INT-101)
A una suspensión agitada de K2CO3 (539,0 mg, 3,9 mmol) e INT-53 (750 mg, 2,6 mmol) en CH3CN (25,0 ml) se le añadió clorhidrato de 4-(metoxi-d3)piperidina (250,0 mg, 1,3 mmol) a 0° C. La mezcla de la reacción
resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se filtró a través de una almohadilla de Celite® y el filtrado se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar INT-101 (167,0 mg, 46%) como un líquido incoloro.
1H NMR (400 MHz, CDCla) 5 8.65 (s, 1H), 3.57 (s, 2H), 3.31-3.20 (m, 1H), 2.78-2.65 (m, 2H), 2.38-2.22 (m, 2H), 1.95-1.82 (m, 2H), 1.70-1.54 (m, 2H). MS m/z (M+H): 279.1.
Síntesis de 2,4-dicloro-5-((4-isopropoxipiperidin-1-il)metil)pirimidina (INT-102)
A una suspensión agitada de K2CO3 (1,45 g, 10,5 mmol) e INT-53 (2,0 g, 6,9 mmol) en CH3CN (50 ml) se le añadió clorhidrato de 4-isopropoxipiperidina (623 mg, 3,5 mmol) a 0° C en porciones. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se filtró a través de una almohadilla de Celite® y el filtrado se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar INT-102 (547 mg, 51,5%) como un líquido incoloro.
1H NMR (400 MHz, CDCla) 5 8.66 (s, 1H), 3.72-3.66 (m, 1H), 3.61-3.54 (m, 2H), 3.47-3.38 (m, 1H), 2.81-2.69 (m, 2H), 2.35-2.22 (m, 2H), 1.93-1.79 (m, 2H), 1.68-1.54 (m, 2H), 1.14 (d, J=4.0 Hz, 6H). MS m/z (M+H): 304.2.
Síntesis de 5-((4-(terc-butoxi)piperidin-1-il)metil)-2,4-dicloropirimidina (INT-103)
A una suspensión agitada de K2CO3 (478,0 mg, 3,5 mmol) e INT-53 (500,0 mg, 1,7 mmol) en CH3CN (15,0 ml) se le añadió clorhidrato de 4-terc-butoxipiperidina (200,0 mg, 1,0 mmol). a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante la noche. Una vez completada, la mezcla de la reacción se filtró a través de una almohadilla de Celite® y el filtrado se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía en columna para proporcionar INT-103 (168 mg, 53%) como un líquido incoloro. 1H NMR (400 MHz, CDCla) 58.67 (s, 1H), 3.58 (s, 2H), 3.53-3.47 (m, 1H), 2.80-2.76 (m, 2H), 2.35-2.20 (m, 2H), 1.83 1.69 (m, 2H), 1.66-1.54 (m, 2H), 1.20 (s, 9H). MS m/z (M+H): 318.0.
Síntesis de 2,4-dicloro-5-((etoxi-d5)metil)pirimidina (INT-104)
Se preparó etan-1-olato-d5 de sodio (0,969 mmol) en 3,0 ml de THF como sigue. A una suspensión de hidruro de sodio (60% en aceite mineral, 44,3 mg, 1,108 mmol) en THF (3,0 ml) a 0° C se le añadió etan-1,1,2,2,2-ds-1 -ol-d (0,057 ml, 0,969 mmol). Se retiró el baño de enfriamiento y la mezcla resultante se agitó a temperatura ambiente durante 40 min.
Una primera porción de etan-1-olato-d5 de sodio en THF (3,0 ml;. 0,969 mmol) se preparó de acuerdo con el procedimiento anterior y se enfrió a 0° C. A la solución enfriada de etan-1-olato-d5 de sodio en THF se le añadió una solución de INT-53 (400 mg, 1,385 mmol) en THF (3,0 ml). Después de 2 h, se preparó una segunda porción de etan-1-olato-d5 de sodio en THF (3,0 ml; 0,969 mmol) de acuerdo con el procedimiento anterior, se enfrió a 0° C y se añadió a la mezcla de la reacción. Después de 14 h, la mezcla de la reacción se diluyó con solución saturada de cloruro de amonio (5,0 ml), se extrajo con acetato de etilo (2 x 20 ml) y se lavó con solución de salmuera (5 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El material bruto obtenido se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con un gradiente de EtOAc-heptano del 5% al 20% para proporcionar INT-104 (99 mg, rendimiento del 34%) como un líquido incoloro. 1H NMR (400 MHz, DMSO-d6) 58.76 (s, 1H), 4.53 (s, 2H). MS m/z (M+H): 212.1.
Ejemplo 1
Síntesis de 2-cloro-4-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-3-il)amino)pirimidina-5-carboxilato de (R)-et¡lo (1-18)
En un vial de 20 ml, se añadieron (R)-3-amino-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-3) (0,095 g, 0,318 mmol), 2,4-dicloropirimidina-5-carboxilato de etilo (0,084 g, 0,382 mmol) y base de Hünig (0,111 ml, 0,637 mmol) a 5 ml de i-PrOH. El vial se selló y la suspensión se calentó a 95° C durante 24 horas. Una vez que se determinó que estaba completa, la reacción se enfrió y se formó un precipitado. Se añadieron 5 ml de éter etílico, el vial se sonicó brevemente y el producto se aisló por filtración para proporcionar el compuesto I-18 (0,112 g, 0,232 mmol, 72,8% de rendimiento). 1H NMR (400 MHz, DMSO-ds): 5 1.18 (d, J=6.7 Hz, 3H), 1.35 (t, J=7 Hz, 3H), 3.42-3.46 (m, 2H), 3.60 (m, 1H), 4.39 (q, J=7 Hz, 2H), 7.08 (br s, 1H), 7.81 (d, J=9.0 Hz, 1H), 8.06 (d, J=4 Hz, 1H), 8.10 (d, J=9.0 Hz, 1H), 8.54 (d, J=9.2 Hz, 1H), 8.93 (s, 1H), 9.27 (d, J=9.3 Hz, 1H), 10.99 (s, 1H). MS m/z (M+H): 483.29.
Ejemplo 2
Síntesis de (R)-2-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-5-carbonitrilo (1-16)
El compuesto del título se sintetizó de la misma manera que I-18 sustituyendo 2,4-dicloropirimidina-5-carbonitrilo en lugar de 2,4-dicloropirimidina-5-carboxilato de etilo para proporcionar el compuesto I-16 (13 mg,
rendimiento del 11%) como sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5 1.17 (d, J=6.5 Hz, 3H), 3.40-3.44 (m, 2H), 3.56-3.60 (m, 1H), 7.08 (br s, 1H), 7.84 (d, J=8.8 Hz, 1H), 7.89 (s, 1H), 8.09 (s, 1H), 8.13 (d, J=8.6 Hz, 1H), 8.81 (br s, 1H), 9.20 (d, J=9.4 Hz, 1H), 11.14 (s, 1H). MS m/z (M+H): 436.27.
Ejemplo 3
Síntesis de (R)-2-cloro-4-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no-[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-3-¡l)am¡no)-N-(1-met¡lp¡per¡d¡n-4-¡l)p¡r¡mid¡n-5-carboxam¡da (1-19)
En un vial de 4 dram, se añadió DMF (0,5 ml) a la mezcla de ácido (R)-2-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-J]quinolin-3-il)amino)pirimidina-5-carboxílico (INT-41) (10 mg, 0,022 mmol) y HATU (9,19 mg, 0,024 mmol). La mezcla resultante se enfrió a 0° C usando un baño de enfriamiento con hielo y metanol. Luego, se añadieron lentamente 1-metilpiperidin-4-amina premezclada (2.51 mg, 0.022 mmol) y DIPEA (0,012 ml, 0,066 mmol) en 0.5 ml de DMF (0,5 ml) a la mezcla anterior, y la reacción se agitó mientras se calentaba a temperatura ambiente durante 30 minutos. Después de que se hubo completado la reacción, la mezcla en bruto se purificó en HPLC preparativa usando acetonitrilo/H2O (01% de TFA) para proporcionar el compuesto I-19 (4 mg, 7,26 mol, 33,0% de rendimiento) como un sólido. 1H NMR (400 MHz, D m S O -d6): 59.20-9.04 (m, 3H), 8.38-8.09 (m, 4H), 7.40 (d, 1H), 7.13 (br s, 1H), 3.52-3.36 (m, 4H), 3.05-3.01 (m, 2H), 2.73 (m, 3H), 2.17-1.71 (m, 4H), 1.17 (d, 3H). MS m/z: 514.9 (M-36+).
Ejemplo 4
Síntes¡s de (R)-2-cloro-N-c¡cloprop¡l-4-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]diazepino[5,,6,:4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-5-carboxamida (1-21)
El compuesto del título se sintetizó de la misma manera que 1-19 usando cicloproilamina en lugar de 1-metilpiperidin-4-amina para proporcionar el compuesto 1-21 como un sólido. MS m/z: 457.9 (M-36).
Ejemplo 5
Síntesis de (R)-2-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)-N-(oxetan-3-il)pirimidin-5-carboxamida (1-20)
El compuesto del título se sintetizó de la misma manera que I-19 usando oxetan-3-amina en lugar de 1-metilpiperidin-4-amina para proporcionar el compuesto I-20, aislado como un sólido. MS m/z: 473.9 (M-36).
Ejemplo 6
Síntesis de (R)-3-((2-cloro-5-((R)-3-(dimetilamino)pirrolidina-1-carbonil)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-24)
El compuesto del título se sintetizó de la misma manera que I-19 usando (R) -N,N-dimetilpirrolidin-3-amina en lugar de 1-metilpiperidin-4-amina para proporcionar el compuesto I-24, aislado como un sólido. 1H NMR (400 MHz, DMSO-d6): 59.90 (br s, 1H), 9.24 (d, 1H), 9.20 (d, 1H), 9.04 (d, 1H), 8.20 (m 1H), 8.19 (d, 1H), 7.34 (m, 1H), 7.11 (br t, 1H), 4.07-3.30 (m, 5 h , parcialmente superpuesto por agua), 2.87 (br s, 6H), 2.49-2.15 (m, 2H, parcialmente fusionado con el pico de los solventes), 1.17 (d, 3H).
Ejemplo 7
Síntesis de (R)-6-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)nicotinonitrilo (I-25)
A una solución de (R)-3-amino-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-3) (60 mg, 0,2 mmol) en 1,4-dioxano (3,0 ml), se añadieron 6-cloro-4-yodonicotinonitrilo (63,8 mg, 0,2 mmol) y carbonato de potasio (55,6 mg, 0,4 mmol) a temperatura ambiente. La mezcla de la reacción se desgasificó durante 5 minutos seguido de la adición de Pd2(dba)3 (9,1 mg, 0,01 mmol) y Xantphos (19,2 mg, 0,03 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 100° C durante 8 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El residuo obtenido se diluyó con agua (7,0 ml), dando lugar a la formación de un precipitado sólido. Los sólidos se filtraron y se secaron al aire, luego se cristalizaron a partir de dimetilsulfóxido/agua para proporcionar el compuesto I-25 (40 mg, 43%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 5 1.19 (d, J=6.6 Hz, 3H), 3.45 (br s, 2H), 3.59 (br s, 1H), 7.01 (br s, 1H), 7.64 (d, J=9.2 Hz, 1H), 7.79 (d, J=8.9 Hz, 1H), 8.03-8.08 (m, 2H), 8.68 (s, 1H), 8.83 (s, 1H), 9.13 (d, J=9.3 Hz, 1H), 10.1 (br s, 1H). MS m/z (M+H): 435.2.
Ejemplo 8
Síntesis de (R)-6-fluoro-4-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]tieno[3,2-f]qu¡nol¡n-3-¡l)am¡no)n¡cotinon¡tr¡lo (I-27)
El compuesto del título se sintetizó de la misma manera que I-25, sustituyendo 6-fluoro-4-yodonicotinonitrilo por 6-cloro-4-yodonicotinonitrilo para proporcionar el compuesto I-27 (40 mg, 28%), aislado como un sólido amarillo.
1H NMR (400 MHz, DMSO-ds): 5 1.19 (d, J=6.7 Hz, 3H), 3.45 (br s, 2H), 3.55 (br s, 1H), 7.01 (br s, 1H), 7.67 (d, J=9.1 Hz, 1H), 7.86 (d, J=8.7 Hz, 1H), 8.03-8.07 (m, 2H), 8.51 (s, 1H), 8.61 (s, 1H), 9.14 (d, J=9.0 Hz, 1H), 10.1 (br s, 1H). MS m/z (M+H): 419.3.
Ejemplo 9
Síntes¡s de (R)-6-fluoro-4-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-3-il)amino)nicotinamida (1-29)
Se trató (R)-6-fluoro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)nicotinonitrilo (I-27) (30 mg, 0,1 mmol) con H2SO4 conc. (0,5 ml) a 0° C. La mezcla de la reacción resultante se agitó a 60° C durante 1 h. Una vez completada la reacción, la mezcla de la reacción se inactivó con agua fría (1,0 ml), después de lo cual se formaron sólidos. Los sólidos obtenidos se filtraron y se secaron al aire para obtener el producto bruto. El producto bruto se disolvió en dimetilsulfóxido (1,0 ml) y se calentó a 80° C y luego se filtró para eliminar las partículas no disueltas. Se añadió agua (1,0 ml) al filtrado. Los sólidos formados se filtraron y se secaron al aire para proporcionar el compuesto I-29 (6,0 mg, 17%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-de): 5 1.19 (d, J=6.7 Hz, 3H), 3.44 (br s, 2H), 3.58-3.59 (m, 1H), 7.01 (br s, 1H), 7.28 (d, J=6.7 Hz, 1H), 7.85 (br s, 1H), 7.88 (d, J=8.8 Hz, 1H), 8.02 (br s, 1H), 8.06 (d, J=8.8 Hz, 1H), 8.42 (br s, 1H), 8.63 (s, 1H), 8.85 (s, 1H), 9.11 (d, J=8.9 Hz, 1H), 12.08 (s, 1H). MS m/z (M+H): 437.2.
Ejemplo 10
Síntesis de (R)-10-met¡l-3-((2-(met¡lsulfon¡l)p¡r¡m¡d¡n-4-¡l)am¡no)-9,10,11,12-tetrah¡dro-8H-[1.4] d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-8-ona (I-14)
A una solución de 10-metil-3-((2-(metilsulfonil)pirimidin-4-il)amino)-8-oxo-10,11 -dihidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolina-12(9H)-carboxilato de (R)-terc-butilo (INT-42) (15,0 mg, 0,03 mmol) en diclorometano (2,0 ml), se añadió ácido trifluoroacético (2,0 ml) a 0° C. Se dejó agitar la mezcla de la reacción resultante a 0° C durante 20 min. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida y se destiló azeotrópicamente con cloroformo (2 x 10 ml). El residuo obtenido se diluyó con solución saturada de bicarbonato de sodio (10 ml) y se extrajo con acetato de etilo (2 x 10 ml). Las capas orgánicas combinadas se secaron sobre sulfato de sodio anhidro y se concentraron a presión reducida. El producto bruto obtenido se purificó mediante TLC preparativa para proporcionar el compuesto I-14 (6,0 mg, 49%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5 1.18 (d, J=6.7 Hz, 3H), 3.39 (s, 3H), 3.45 (br s, 2H), 3.59 (br s, 1H), 7.02 (br s, 1H), 7.88 (d, J=8.9 Hz, 1H), 7.93 (br s, 1H), 8.03 (d, J=4.1 Hz, 1H), 8.45 (br s, 1H), 8.09 (d, J=8.9 Hz, 1H), 8.70 (d, J=5.9 Hz, 1H), 9.15 (d, J=9.3 Hz, 1H), 11.19 (br s, 1H). MS: m/z 455.3 (M+H).
Ejemplo 11
Síntes¡s de (R)-3-((5-fluoro-2-n¡trofen¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-1)
Se trató (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolina-8-ona (S1-12) (120 mg, 0,4 mmol) en 1,4-dioxano (5 ml) con 5-fluoro-2-nitroanilina (70 mg, 0,4 mmol). La solución resultante se desgasificó brevemente aplicando vacío y luego se lavó abundantemente con nitrógeno. Se añadieron carbonato de cesio (246 mg, 0,7 mmol), Pd2(dba)3 (17 mg, 0,01 mmol) y Xantphos (43 mg, 0,07 mmol) y la mezcla se desgasificó adicionalmente como se ha descrito anteriormente. La mezcla de la reacción se agitó con irradiación de microondas a 130° C durante 1 h. Una vez completada la reacción, la mezcla de la reacción se filtró a través de celite, se lavó con acetato de etilo y se concentró a presión reducida. El residuo resultante se trituró con éter dietílico y se purificó adicionalmente mediante HPLC preparativa para proporcionar el compuesto I-1 (16 mg, 10%) como un sólido marrón pálido. 1H NMR (400 MHz, DMSO-d6): 5 1.18 (d, J=6.7 Hz, 3H), 3.44 (br s, 2H), 3.58 (br s, 1H), 7.00 7.04 (m, 2H), 7.47 (d, J=9.1 Hz, 1H), 7.73 (d, J=8.9 Hz, 1H), 8.01-8.03 (m, 2H), 8.24 (dd, J=6.1, 9.2 Hz, 1H), 8.73 (dd, J=2.6, 12.1 Hz, 1H), 9.07 (d, J=9.1 Hz, 1H), 10.26 (s, 1H). MS: m/z (M+H): 438.22 (M+H).
Ejemplo 12
Síntesis de (R)-4-fluoro-2-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)benzonitrilo (1-2)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra qu e I-1 s u s titu y e n d o 2 -a m in o -4 -flu o ro b e n z o n ¡tr ilo p o r 5 -flu o ro -2 -n itro a n ilin a pa ra p ro p o rc io n a r el co m p u e s to I-2, o b te n id o co m o un só lid o a m a rillo . 1H N M R (400 M H z, D M S O -d6): 5: 1.18 (d, J= 6.7 Hz, 3H ), 3.44 (s, 2H ), 3.57 -3.59 (m , 1H ), 6.97 (t, J= 5 Hz, 1H), 7.03 (dt, J= 2.5 , 8.4 Hz, 1H), 7.45 (d, J= 9 Hz, 1H), 7.70 (d, J= 9 Hz, 1H), 7.86 (dd, J= 6.4 , 8.7 Hz, 1H), 7.98 (d, J = 8.8 Hz, 1H), 8.02 (d, J= 4.3 Hz, 1H), 8.35 (dd, J= 2.5 , 12 Hz, 1H), 9.03 (d, J= 9 Hz, 1H), 9.61 (s, 1H). M S: m /z 418.1 (M H ).
Ejemplo 13
Síntesis de (R)-3-((2-cloropirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-5)
El co m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e I-1 s u s titu y e n d o 2 -c lo ro p ir im id in -4 -a m in a p o r 5-flu o ro -2 -n itro a n ilin a p a ra p ro p o rc io n a r el co m p u e s to I-5, o b te n id o c o m o un só lid o a m a rillo p á lid o . 1H N M R (400 M H z, D M S O -d6): 5 1.17 (d, J = 6.7 Hz, 3H ), 3.44 (b r s, 2H ), 3.58 -3.59 (m , 1 H), 7.07 (d, J= 5 Hz, 1H), 7.76 (d, J= 8.6 Hz, 1 H), 7.8 5 (d, J= 9 Hz, 1H), 8.03 -8.08 (m , 2H ), 8.33 (b r s, 1H), 8.45 (d, J= 6 Hz, 1H ), 9.15 (d, J= 9.2 Hz, 1H), 10.99 (s, 1H). M S: m /z 411.1 (M H ).
Ejemplo 14
[1,4]d¡azep¡no[5',6':4,5]tieno[3,2-f]qu¡nol¡n-8-ona (I-8)
El compuesto del título se sintetizó de la misma manera que I-1 sustituyendo 2-fluorop¡rim¡d¡n-4-am¡na por 5-fluoro-2-nitroanil¡na. El calentamiento se realizó de manera convencional a 90° C durante 16 h (en lugar de mediante irradiación con microondas) para proporcionar el compuesto I-8 (8 mg, rendimiento del 11%), obtenido como un sólido blanquecino. 1H NMR (400 MHz, DMSO-d6): 5: 1.17 (d, J=6.7 Hz, 3H), 3.44 (s, 2H), 3.58 (s, 1H), 7.05 (br s, 1H), 7.80 (d, J=8.8 Hz, 1H), 7.86 (d, J=9.0 Hz, 1H), 8.04 (d, J=4.2 Hz, 1H), 8.07 (d, J=8.8 Hz, 1H), 8.21 (br s, 1H), 8.46 (d, J=4.7 Hz, 1H), 9.15 (d, J=9.2 Hz, 1H), 10.98 (s, 1H). MS: m/z 395.32 (M+H).
Ejemplo 15
Síntesis de 4-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-3-il)am¡no)-2-(metiltio)pirimidina-5-carboxilato de (R)-et¡lo (1-12)
En un vial de 15 ml, se añadió 1,4-dioxano a (R) -3-bromo-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-5) (10 mg, 0,028 mmol) y 4-amino-2-(metiltio)pirimidina-5-carboxilato de etilo (INT-8 ) (8,83 mg, 0,041 mmol) seguido de NaOt-Bu (7,96 mg, 0,083 mmol) y precatalizador BrettPhos-G1 (4,00 mg, 0,552 gmol). La mezcla heterogénea resultante se purgó con argón durante 3 minutos y se calentó a 80° C durante la noche. Una vez que se hubo completado, la reacción se purificó por HPLC preparativa usando acetonitrilo/H2O (0,1% de TFA) para proporcionar el compuesto I-12 (6 mg, 0,012 mmol, 43,9% de rendimiento) como un sólido. 1H NMR (400 MHz, DMSO-d6): 511.01 (s, 1H), 9.23 (d, 1H), 8.86 (d, 1H), 8.69 (d, 1H), 8.10 (m, 2H), 7.81 (d, 1H), 7.10 (br.s, 1H), 4.38 (q, 2H), 3.60 (m, 1H), 3.45 (m, 2H), 2.66 (s, 3H), 1.35 (d, 3H), 1.18 (t, 3H). MS m/z: 494.9 (M+H).
Ejemplo 16
Síntesis de (R)-2-cloro-4-(metil(10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]diazep¡no[5',6':4,5]t¡eno[3,2-f]quinolin-3-il)amino)pirimidina-5-carboxamida (1-34)
A una solución agitada de (R)-2-cloro-N-(4-metoxibencil)-4-(metil(10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidin-5-carboxamida (INT-44) (60 mg, 0,1 mmol) en diclorometano (1,0 ml) se añadieron ácido trifluoroacético (1,0 ml, 0,1 mmol) y ácido trifluorometanosulfónico (153,12 mg, 1,0 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 25° C durante 1 h. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida. El residuo se diluyó con agua y los sólidos
formados se filtraron y lavaron con agua y luego se secaron al vacío. El producto bruto se purificó mediante TLC preparativa eluyendo con metanol al 5% en diclorometano para proporcionar el compuesto I-34 (6,0 mg, 12%) como un sólido naranja. 1H NMR (400 MHz, DMSO-d6): 5 1.17 (d, J=6.7 Hz, 3H), 3.42 (m, 2H), 3.57 (m, 1H), 4.14 (s, 3H), 7.09 (t, J=5.5 Hz, 1H), 7.76 (br s, 1H), 7.84 (d, J=9.9 Hz, 1H), 8.05 (d, J=9.2 Hz, 1H), 8.15 (d, J=3.8 Hz, 1H), 8.26 (d, J=9.2 Hz, 1H), 8.79 (s, 1H), 8.85 (br s, 1H), 9.10 (d, J=9.9 Hz, 1H). MS m/z (M+H): 468.4.
Ejemplo 17
Síntesis de (R)-2-cloro-4-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]tieno[3,2-f]qu¡nol¡n-3-il)amino)pirimidina-5-carboxamida (1-9)
A una solución agitada de (R)-2-cloro-N-(4-metoxibencil)-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4])diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidin-5-carboxamida (INT-43) (20 mg, 0,03 mmol) en diclorometano (1,0 ml) se añadieron ácido trifluoroacético (1 ml) y ácido trifluorometanosulfónico (0,03 ml, 0,3 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 25° C durante 1 h. Una vez completada la reacción, la mezcla de la reacción se diluyó con agua y los sólidos formados se filtraron, se lavaron con diclorometano y se secaron. El polvo resultante se purificó mediante TLC preparativa eluyendo con MeOH al 5% en diclorometano para proporcionar el compuesto I-9 (11 mg, 68%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 51.18 (d, J=6.7 Hz, 3H), 3.46 (m, 2H), 3.60 (m, 1H), 7.06 (br s, 1H), 7.82 (d, J=8.9 Hz, 1H), 8.01 (br s, 1H), 8.07-8.09 (m, 2H), 8.51 (br s, 1H), 8.61 (d, J=9.4 Hz, 1H), 8.90 (s, 1H), 9.26 (d, J=9.5 Hz, 1H), 12.11 (br s, 1H). MS: m/z 454.3 (M+H).
Ejemplo 18
Síntesis de (R)-3-((6-fluoropirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-11)
El compuesto del título se sintetizó de la misma manera que I-1 sustituyendo 6-fluoropirimidin-4-amina por 5-fluoro-2-nitroanilina. El calentamiento se realizó de forma convencional a 100° C durante 16 h (en lugar de mediante irradiación con microondas) para proporcionar el compuesto I-11 como un sólido marrón. 1H NMR (400 MHz, DMSO-ds): 5: 1.17 (d, J=6.7 Hz, 3H), 3.44 (s, 2H), 3.59-3.60 (m, 1H), 6.99 (t, J=5 Hz, 1H), 7.68 (d, J=9.2 Hz, 1H), 7.89 (d, J=9 Hz, 1H), 8.03 (s, 1H), 8.06 (d, J=9 Hz, 1H), 8.17 (s, 1H), 8.59 (d, J=2 Hz, 1H), 9.10 (d, J=9 Hz, 1H), 10.93 (s, 1H). MS: m/z 395.1 (M+H).
Ejemplo 19
Síntesis de (R)-3-((6-cloropirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-7)
El compuesto del título se sintetizó de la misma manera que I-1 sustituyendo 6-clorop¡r¡mid¡n-4-am¡na por 5-fluoro-2-nitroanilina. El calentamiento se realizó de forma convencional a 100° C durante 16 h (en lugar de mediante irradiación con microondas) para proporcionar el compuesto I-7 como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5 1.17 (d, J=6.7 Hz, 3H), 3.47 (br s, 2H), 3.58 (br s, 1H), 7.00 (br s, 1H), 7.76 (d, J=9.0 Hz, 1H), 7.84 (d, J=9.0 Hz, 1H), 8.04-8.08 (m, 2H), 8.46 (s, 1H), 8.64 (s, 1), 9.11 (d, J=9.3 Hz, 1H), 10.88 (s, 1H). MS m/z (M+H): 411.3. Ejemplo 20
Síntesis de (R)-3-((6-fluoropirimidin-4-il)(metil)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-38)
El compuesto del título se sintetizó de la misma manera que I-1 sustituyendo 6-fluoro-N-metilpirimidin-4-amina por 5-fluoro-2-nitroanilina. El calentamiento se realizó de forma convencional a 90° C durante 16 h (en lugar de mediante irradiación con microondas) para proporcionar el compuesto I-38 como un sólido amarillo claro. 1H NMR (400 MHz, DMSO-ds): 51.18 (d, J=6.7 Hz, 3H), 3.44-3.46 (m, 2H), 3.59-3.60 (m, 1H), 3.68 (s, 3H), 6.88 (s, 1H), 7.10 (t, J=5.4 Hz, 1H), 7.80 (d, J=9.0 Hz, 1H), 7.85 (d, J=8.9 Hz, 1H), 8.05 (d, J=4.3 Hz, 1H), 8.11 (d, J=8.9 Hz, 1H), 8.49 (d, J=2.2 Hz, 1H), 9.18 (d, J=9.1 Hz, 1H). MS: m/z 409.3 (M+H).
Ejemplo 21
Síntesis de (R)-6-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)nicotinamida (I-15)
A una solución agitada de (R)-6-cloro-N-(4-metoxibencil)-4-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4])diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)nicotinamida (INT-51) (20 mg, 0,04 mmol) en diclorometano: ácido trifluoroacético (2 ml, proporción 1:1), se añadió ácido trifluorometanosulfónico (52 mg, 0,34 mmol) a 0° C y se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida y se añadió solución de NaHCÜ3 acuosa saturada (3 ml) a 0° C y se agitó durante 20 min. El sólido formado se filtró y se lavó con agua y el compuesto bruto se purificó mediante HPLC preparativa para proporcionar el compuesto 1-15 (8 mg, rendimiento 61) como un sólido amarillo. 1H NMR (400 MHz, DMSO-D6): 5: 1.20 (d, J=6.7 Hz, 3H), 3.44-3.49 (m, 2H), 3.58 (d, J=3.1 Hz, 1H), 7.04 (, J=5.4 Hz, 1H), 7.29 (d, J=9.2 Hz, 1H), 7.83 (d, J=9 Hz, 1H), 7.93 (br s, 1H), 8.08 (d, J=9 Hz, 2H), 8.48 (br s, 1H), 8.72 (s, 1H), 9.10 (d, J=9.3 Hz, 1H), 9.27 (s, 1H), 11.97 (s, 1H). MS: m/z 453.28 (M+H).
Ejemplo 22
Síntesis de 4-cloro-2-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-5-carboxilato de (R)-etilo (I-23)
El compuesto del título se sintetizó de la misma manera que I-1 sustituyendo 2-amino-4-cloro-pirimidin-5-carboxilato de etilo por 5-fluoro-2-nitroanilina y (R)-3-bromo-10-metil-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-5) por (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12). El compuesto del título I-23 se obtuvo como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 5 1.18 (d, J=6.7 Hz, 3H), 1.32 (t, J=7.0 Hz, 3H), 3.45 (br s, 2H), 3.60 (br s, 1H), 4.32 (q, J=7.0 Hz, 2H), 4.29-4.34 (m, 2H), 7.07 (t, J=5.0 Hz, 1H), 7.80 (d, J=8.9 Hz, 1H), 8.03 (d, J=4.0 Hz, 1H), 8.06 (d, J=8.8 Hz, 1H), 8.40 (d, J=9.3 Hz, 1H), 8.96 (s, 1H), 9.19 (d, J=9.3 Hz, 1H), 11.2 (br s, 1H). MS m/z (M+H): 483.1.
Ejemplo 23
Síntesis de (R)-3-((2,6-difluoropiridin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-6)
Una solución de (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12) (50 mg, 0,16 mmol), 2,6-difluoropiridin-4-amina (40,9 mg, 0,3 mmol) y carbonato de cesio (154 mg, 0,5
mmol) en 1,4-dioxano (5 ml) se desgasificó con argón durante 10 min. Se añadieron BINAP (9,8 mg, 0,02 mmol) y Pd2(dba)3 (14,4 mg, 0,02 mmol), la solución se desgasificó de nuevo con argón durante 5 min y luego se calentó a 100° C durante 16 h. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida. El compuesto bruto resultante se purificó mediante cromatografía en columna (malla de sílice 100-200, metanol al 10% en diclorometano como eluyente) seguido de concentración de las fracciones relevantes y purificación adicional por HPLC de fase inversa para proporcionar el compuesto 1-6 (7 mg, rendimiento del 10%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5: 1.17 (d, J=6.7 Hz, 3H), 3.43 (s, 2H), 3.59 (d, J=4 Hz, 1H), 6.98 (d, J=5.3 Hz, 1H), 7.24 (d, J=9 Hz, 1H), 7.59 (s, 2H), 7.87 (d, J=9 Hz, 1H), 8.03-8.06 (m, 2H), 9.09 (d, J=9 Hz, 1H), 10.51 (s, 1H). MS: m/z 412.1 (M+H).
Ejemplo 24
Síntesis de (R)-3-((2-fluorop¡r¡d¡n-4-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1.4] diazep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-8-ona(I-3)
En un vial de microondas de 10 ml, se disolvieron Pd2(dba)3 (21,61 mg, 0,024 mmol), carbonato de cesio (77 mg, 0,236 mmol), 2-diciclohexilfosfino-2 '-(N,N-dimetilamino)-bifenilo (DavePhos, 18,58 mg, 0,047 mmol), 4-amino-2-fluoropiridina (8,82 mg, 0,079 mmol) y (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12) (25 mg, 0,079 mmol) en 0,5 ml de t-BuOH seco. La reacción se puso al vacío y luego se volvió a llenar con nitrógeno. La reacción se calentó a 100° C durante la noche, luego se enfrió, se filtró y se concentró hasta la sequedad. El residuo se volvió a disolver en DMSO y se purificó por HPLC de fase inversa con 95%-5% de H2O (que contiene TFA al 0,5% v/v)/acetonitrilo para proporcionar el compuesto I-3 (0,004 g, 7,8 pmol, rendimiento del 10,0%). MS: m/z 393.6 (M+H), 391.7 (M-H). 1H NMR (400 MHz, DMSO-ds): 5 1.13 (d, 3H), 3.39 (m, 2H), 3.55 (m, 1H), 6.94 (br s, 1H), 7.20 (d, 1H), 7.81 (d, 1H), 7.99 (m, 4H), 9.02 (d, 1H), 10.21 (s, 1H).
Ejemplo 25
Síntes¡s de (R)-3-((2-clorop¡r¡d¡n-4-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-4)
El compuesto del título se sintetizó de la misma manera que I-3 sustituyendo 4-amino-2-cloro piridina por 4-amino-2-fluoropiridina para proporcionar el compuesto I-4 (0,003 g, 5,7 pmol, 7,3% de rendimiento). MS: m/z 409.7 (M+H), 407.8 (M-H). 1H NMR (400 MHz, DMSO-ds): 5 1.13 (d, 3H), 3.38 (br s, 2H), 3.55 (m, 1H), 6.95 (br s, 1H), 7.17 (d, 1H), 7.72 (d, 1H), 7.78 (d, 1H), 8.01 (m, 2H), 8.16 (d, 1H), 9.03 (d, 1H).
Ejemplo 26
Síntesis de (R)-3-((2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (1-32)
En un vial de microondas de 5 ml, se suspendieron (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12) (0,04 g, 0,126 mmol), BINAP (7,84 mg, 0,013 mmol), Pd(OAc)2 (8,48 mg, 0,013 mmol), carbonato de cesio (0,082 g, 0,252 mmol) y 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina (S3-3a) (0,028 g, 0,138 mmol) en 3 ml de 1,4-dioxano. La reacción se puso al vacío, se sonicó y luego se volvió a llenar con nitrógeno. La reacción se irradió en un microondas Biotage Explorer a 130° C durante 1 h. La reacción se enfrió, se filtró y se concentró hasta la sequedad. El residuo se volvió a disolver en DMSO y se purificó por HPLC de fase inversa con 95%-5% de H2O (que contenía TFA al 0,5% v/v)/acetonitrilo para proporcionar el compuesto I-32 (0,017 g, 0,035 mmol, rendimiento del 28,0%). MS: m/z 466.1 (M+H), 463.8 (M-H). 1H NMR (400 MHz, DMSO-ds): 51.18 (d, 3H), 2.88 (s, 6H), 3.43 (m, 2H), 3.59 (m, 3H), 4.67 (m, 2H), 7.04 (m, 1H), 7.78 (br s, 1H), 7.88 (d, 1H), 8.08 (d, 1H), 9.14 (d, 1H), 9.89 (br s, 1H), 10.93 (s, 1H).
Ejemplo 27
Síntesis de (R)-3-((6-fluoro-2-(oxetan-3-iloxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-37)
El compuesto del título se sintetizó de la misma manera que I-32 sustituyendo 6-fluoro-2-(oxetan-3-iloxi)pirimidin-4-amina (INT-9a) por 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina para proporcionar el compuesto I-37 (0,0033 g, 7,07 pmol, 5,6% de rendimiento). MS: m/z 467.1 (M+H), 464.6(M-H).
Ejemplo 28
Síntesis de (R)-3-((6-fluoro-2-((3-metiloxetan-3-il)metoxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-39)
El compuesto del título se sintetizó de la misma manera que I-32 sustituyendo 6-fluoro-2-((3-metiloxetan-3-il)metoxi)pirimidin-4-amina (INT-15a) por 2-(2-(dimetilamino))etoxi)-6-fluoropirimidin-4-amina (S3-3a) para proporcionar el compuesto I-39 (0,01 g, 0,02 mmol, 12,9% de rendimiento). m S: m/z 495.0 (M+H). 1H n M r (400 MHz, DMSO-ds): 51.18 (d, 3H), 1.38 (s, 3H), 3.55 (m, 3H), 4.33 (d, 2H), 4.42 (s, 2H), 4.51 (d, 2H), 7.03 (t, 1H), 7.75
(br s, 1H), 7.88 (d, 1H), 8.07 (m, 2H), 9.12 (d, 1H), 10.91 (s, 1H).
Ejemplo 29
Síntesis de (R)-3-((4-fluoro-6-(oxetan-3-¡lox¡)p¡r¡m¡d¡n-2-il)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-42)
El compuesto del título se sintetizó de la misma manera que I-32 sustituyendo 4-fluoro-6-(oxetan-3-¡lox¡)p¡rim¡d¡n-2-am¡na (INT-9b) por 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina (S3-3a). Esto proporcionó el compuesto I-42 (0,02 g, 0,04 mmol, rendimiento del 26,7%). MS: m/z 467.1 (M+H). 1H NMR (400 MHz, DMSO-d6): 5 1.20 (d, 3H), 3.47 (m, 2H), 3.62 (m, 1H), 4.64 (m, 2H), 4.97 (m, 2H), 5.67 (m, 1H), 6.28 (sm 1H), 7.08 (br s, 1H), 7.77 (d, 1H), 8.07 (d, 1H), 8.29 (d, 1H), 9.18 (d, 1H), 10.66 (s, 1H).
Ejemplo 30
Síntes¡s de (R)-3-((4-fluoro-6-((3-met¡loxetan-3-¡l)metox¡)p¡r¡m¡d¡n-2-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-43)
El compuesto del título se sintetizó de la misma manera que I-32 sustituyendo 4-fluoro-6-((3-metiloxetan-3-il)metoxi)pirimidin-2-amina (INT-15b) por 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina. Esto produjo el compuesto I-43 (0,01 g, 0,02 mmol, rendimiento del 13,8%). MS: m/z 495.1 (M+H). 1H NMR (400 MHz, DMSO-d6): 5 1.18 (d, 3H), 1.38 (s, 3H), 3.46 (br s, 2H), 3.61 (m, 1H), 4.33 (d, 2H), 4.52 (m, 4H), 6.25 (s, 1H), 7.17 (s, 1H), 7.77 (d, 1H), 8.07 (d, 1H), 8.40 (d, 1H), 9.17 (d, 1H), 10.64 (s, 1H).
Ejemplo 31
Síntes¡s de (R)-3-((6-fluoro-2-(((S)-tetrah¡drofuran-3-¡l)ox¡)p¡r¡m¡d¡n-4-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-40)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e I-32 s u s titu ye n d o (S )-6 -flu o ro -2 -(( te tra h ¡d ro fu ra n -3 -¡l)o x ¡)p ¡r im ¡d ¡n -4 -a m ¡n a (INT-23) p o r 2 -(2 -(d im e tila m in o )e to x i)-6 -flu o ro p ir im id in -4 -a m in a pa ra p ro p o rc io n a r el c o m p u e s to I-40 co m o un só lido . 1H N M R (400 M H z, D M S O -d 6 ): 5 10.82 (s, 1H), 9.11 (d, 1H), 8.06 (d, 2H ), 7.84 (d, 2H ), 7.53 (b r s, 1H), 7.01 (s, 1H), 5.47 (t, 1H ), 3.95 -3.78 (m, 4H ), 3.78 -3.30 (m, 4H ), 2.27-2.01 (m, 2H ), 1.17 (d, 3H ). M S m /z: 480.8 (M H ).
Ejemplo 32
Síntesis de (R)-3-((4-fluoro-6-(((S)-tetrah¡drofuran-3-¡l)ox¡)p¡r¡m¡d¡n-2-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-50)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e I-32 s u s titu ye n d o (S )-4 -flu o ro -6 -((te tra h id ro fu ra n -3 - il)o x i)p ir im id in -2 -a m in a (INT-22) p o r 2- (2 -(d im e tila m in o )e to x i)-6 -flu o ro p ir im id in -4 -a m in a pa ra p ro p o rc io n a r el c o m p u e s to I-50 co m o un só lido . 1H n M r (400 M H z, D M S O -d 6 ): 5 10.61 (s, 1 H), 9.15 (d, 1H), 8.36 (d, 1H), 8.05 (d, 2H ), 7.76 (d, 1H), 7.05 (s, 1H), 6.19 (s, 1H), 4.01 -3.83 (m, 4H ), 3.60 -3.45 (m, 3H ), 2.48-2.01 (m, 2H ), 1.18 (d, 3H ). M S m /z: 480.8 (M H ).
Ejemplo 33
Síntes¡s de (R)-3-((6-fluoro-2-(((R)-tetrah¡drofuran-3-¡l)ox¡)p¡r¡m¡d¡n-4-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-41)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e I-32 s u s titu y e n d o (R )-6 -flu o ro -2 -((te tra h id ro fu ra n -3 - il)o x i)p ir im id in -4 -a m in a (INT-27) p o r 2 -(2 -(d im e tila m in o )e to x i)-6 -flu o ro p ir im id in -4 -a m in a pa ra p ro p o rc io n a r el c o m p u e s to I-41 co m o un só lido . 1H N m R (400 M H z, D M S O -d 6 ): 5 10.83 (s, 1 H), 9.11 (d, 1H), 8.05 (d, 2H ), 7.84 (d, 2H ), 7.65 (b r s, 1H), 7.01 (s, 1H), 5.48 (t, 1H ), 3.95 -3.82 (m, 4H ), 3.51 (m , 1H), 3.43 (m, 2H ), 2.30 -2.06 (m , 2H ), 1.17 (d, 3H ). M S m /z: 481.0 (M H ).
Ejemplo 34
Síntesis de (R)-3-((6-fluoro-2-(2-metoxietoxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-J]quinolin-8-ona (I-44)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e I-32 s u s titu y e n d o 6 -flu o ro -2 -(2 -m e to x ¡e to x ¡)p ¡rim ¡d ¡n -4 -a m ¡n a (INT-19) p o r 2 -(2 -(d im e tila m in o )e to x i)-6 -flu o ro p ir im id in a -4 -a m in a p a ra p ro p o rc io n a r el c o m p u e s to I-44 (18 m g, 0 ,038 m m ol, re n d im ie n to de l 27 ,2% ) en fo rm a de só lido . 1H N M R (400 M H z, D M S O -d 6 ): 5 10.82 (s, 1H), 9.10 (d, 1H), 8.05 (m , 2H ), 7.84 (m, 2H ), 7.01 (b r s, 1H), 4.42 (t, 2H ), 3.67 (m, 2H ), 3.58 (m, 1H), 3.42 (m, 2H ), 3.30 (s, 3H ), 1.16 (d, 3H ). M S m /z: 469.0 (M H ).
Ejemplo 35
Síntesis de (R)-3-((4-fluoro-6-(((R)-tetrahidrofuran-3-il)oxi)pirimidin-2-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-46)
El c o m p u e s to de l t ítu lo se s in te tizó de la m ism a m a n e ra q u e I-32 s u s titu y e n d o (R )-4 -flu o ro -6 -((te tra h id ro fu ra n -3 - il)o x i)p ir im id in -2 -a m in a (INT-26) p o r 2 -(2 -(d im e tila m in o )e to x i)-6 -flu o ro p ir im id in -4 -a m in a pa ra p ro p o rc io n a r el c o m p u e s to I-46 co m o un só lido . 1H N m R (400 M H z, D M S O -d 6 ): 5 10.61 (s, 1 H), 9.14 (d, 1H), 8.35 (d, 1H), 8.04 (d, 2H ), 7.75 (d, 1H), 7.04 (s, 1H), 6.18 (s, 1H), 5.57 (t, 1H ), 3.98 (m, 1H), 3.87 -3.77 (m, 3H ), 3.61 (m, 1H), 3.44 (m, 2H ), 2.31 (m, 1H), 2.04 (m, 1H), 1.17 (d, 3H ). M S m /z: 481.0 (M H ).
Ejemplo 36
Síntesis de (R)-3-((4-fluoro-6-(2-metoxietoxi)pirimidin-2-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-45)
El compuesto del título se sintetizó de la misma manera que I-32 sustituyendo 4-fluoro-6-(2-metox¡etox¡)p¡rim¡d¡n-2-am¡na (INT-18) por 2-(2-(dimetilamino)etoxi)-6-fluoropirimidina-4-amina para proporcionar el compuesto I-45 como un sólido. 1H NMR (400 MHz, DMSO-d6): 5 10.62 (s, 1H), 9.15 (d, 1H), 8.37 (d, 1H), 8.07 (m, 2H), 7.76 (d, 1H), 7.05 (br s, 1H), 6.20 (s, 1H), 4.52 (t, 2H), 3.69 (t, 2H), 3.59 (m, 1H), 3.44 (m, 2H), 3.30 (s, 3H), 1.17 (d, 3H). MS m/z: 469.0 (M+H).
Ejemplo 37
Síntesis de (R)-3-((6-cloro-2-(metoximetil)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-51)
El compuesto del título se sintetizó de la misma manera que I-32 sustituyendo 6-cloro-2-(metoximetil)pirimidin-4-amina por 2-(2-(dimetilamino)etoxi)-6-fluoropirimidin-4-amina. Esto produjo el compuesto I-51 (0,025 g, 0,06 mmol, rendimiento del 10,7%). MS: m/z 454.9 (M+H). 1H NMR (400 MHz, DMSO-ds): 5 1.18 (d, 3H), 3.41 (s, 3H), 3.44 (m, 3H), 4.49 (s, 2H), 7.05 (br s, 1H), 7.85 (d, 1H), 8.08 (m, 2H), 9.12 (d, 1H), 10.99, (s, 1H). Ejemplo 38
Síntesis de (10R)-3-((6-fluoro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (mezcla 1:1 de diastereómeros) (I-47)
Una solución de (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5,,6,:4,5]tieno[3,2-f]quinolin-8-ona (S1-12) (150 mg, 0,47 mmol) y (rac)-6-fluoro-2-[(1-metil-3-piperidil)oxi]pirimidin-4-amina (INT-10) (128,1 mg, 0,56 mmol) disuelta en 1,4-dioxano (6,0 ml) se desgasificó brevemente aplicando vacío y luego se lavó abundantemente con nitrógeno tres veces. A la solución anterior se le añadió carbonato de cesio (461,3 mg, 1,41 mmol), Pd2(dba)3(43,2 mg, 0,05 mmol) y Xantphos (27,3 mg, 0,05 mmol) a temperatura ambiente y la solución se desgasificó de nuevo durante 5 minutos. La mezcla de la reacción resultante se agitó a 100° C durante 6 h. Una vez completada la reacción, la mezcla de la reacción se concentró a presión reducida, tras lo cual se formaron sólidos. Los sólidos obtenidos se lavaron con agua, éter dietílico y acetona para proporcionar el compuesto I-47 (30 mg, 12%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSo-d6): 51.18 (d, J=6.6 Hz, 3H), 1.43-1.57 (m, 2H), 1.73 (m, 1H), 1.97-2.15 (m, 2H), 2.19 (s, 4H), 2.5 (m, 1H), 2.88 (d, J=9.4 Hz, 1H), 3.44-3.49 (m, 2H), 3.55-3.59 (m, 1H), 4.99 (m, 1H), 6.99 (s, 1H), 7.69 (s, br, 1H), 7.79 (d, J=7.2 Hz, 1H), 7.86 (d, J=8.9 Hz, 1H), 8.01-8.06 (m, 2H), 9.10 (d, J=9.1 Hz, 1H), 10.76 (s, br, 1H). MS m/z (M+H): 508.3.
Ejemplo 39
Síntesis de (R)-3-((6-fluoro-2-(2-(4-met¡lp¡peraz¡n-1-¡l)etox¡)p¡rim¡d¡n-4-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (l-48)
El compuesto del título se sintetizó de la misma manera que I-47 sustituyendo 6-fluoro-2-(2-(4-met¡lp¡peraz¡n-1-¡l)etox¡)p¡r¡mid¡n-4-am¡na (INT-11) por (rac)-6-fluoro-2-[(1-metil-3-piperidil)oxi]pirimidin-4-amina (INT-10) para proporcionar el compuesto I-48 como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-d6): 5 1.18 (d, J=6.4 Hz, 3H), 2.12 (s, 3H), 2.29 (br s, 4H), 2.49 (br s, 4H), 2.68 (br s, 2H), 3.43 (br s, 2H), 3.58 (br s, 1H), 4.41 (s, 2H), 6.99 (s, 1H), 7.58 (br s, 1H), 7.78-7.85 (m, 2H), 8.00-8.05 (m, 2H), 9.12 (d, J=9.1 Hz, 1H), 10.39 (br s, 1H). MS m/z (M+H): 537.2.
Ejemplo 40
Síntes¡s de (R)-3-((6-fluoro-2-(((R)-1-met¡lp¡rrol¡d¡n-3-¡l)ox¡)p¡r¡m¡d¡n-4-¡l)am¡no)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-49)
El compuesto del título se sintetizó de la misma manera que I-47 sustituyendo (R)-6-fluoro-2-((1-metilpirrolidin-3-il)oxi)pirimidin-4-amina (INT-12) por (rac)-6-fluoro-2-[(1-metil-3-piperidil)oxi]pirimidin-4-amina (INT-10) al compuesto I-49 (8,0 mg, 16%) como un sólido amarillo claro. 1H NMR (400 MHz, DMSo-d6): 5 1.19 (d, J=6.7 Hz, 3H), 2.27 (s, 3H), 2.31-2.40 (m, 2H), 2.61-2.68 (m, 3H), 2.82-2.84 (m, 1H), 3.44 (br s, 2H), 3.59 (br s, 1H), 5.33 (br s, 1H), 6.99 (br s, 1H), 7.49 (br s, 1H), 7.83-7.85 (m, 2H), 8.01 (br s, 1H), 8.05 (d, J=8.8 Hz, 1H), 9.13 (d, J=9.3 Hz, 1H), 10.75 (br s, 1H). MS m/z (M+H): 494.5.
Ejemplo 41
Síntesis de (10R)-3-((6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (mezcla 1:1 de diastereómeros) (I-59)
Se desgasificó brevemente una solución de (R)-3-bromo-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-5) (100 mg, 0,3 mmol) y (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina (S4-4) (67 mg, 0,3 mmol) disuelto en 1,4-dioxano (5,0 ml) aplicando vacío y luego se lavó con nitrógeno tres veces. A la solución anterior se le añadió carbonato de cesio (269,8 mg, 0,8 mmol), Pd2(dba)3 (25,3 mg, 0,03 mmol) y xantfos (15,9 mg, 0,03 mmol) a temperatura ambiente. La mezcla resultante se desgasificó adicionalmente y se agitó a 100° C durante 6 h. Una vez completada, la mezcla de la reacción se concentró y se formó un sólido. El sólido obtenido se lavó con agua, diclorometano y se purificó mediante HPLC preparativa para proporcionar el compuesto I-59 (13 mg, 9%) como un sólido rojo. 1H NMR (400 MHz, CD3OD): 5 1.35 (d, J=6.8 Hz, 3H), 1.88-1.97 (m, 2H), 2.19-2.30 (m, 2H), 2.94 (s, 3H), 3.07-3.15 (m, 2H), 3.51-3.60 (m, 3H), 3.70-3.79 (m, 1H), 3.88-3.91 (m, 1H), 5.57 (br s, 1H), 7.54 (d, J=9.2 Hz, 1H), 7.86 (d, J=8.8 Hz, 1H), 8.00 (d, J=8.8 Hz, 1H), 8.18 (s, 1H), 9.08 (d, J=9.2 Hz, 1H). MS m/z (M+H): 524.6.
Ejemplo 42
Síntesis de (R)-3-((6-cloro-2-(((R)-1-metilpirrolidin-3-il)oxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-60)
El compuesto del título se sintetizó de la misma manera que I-59 sustituyendo (R)-6-cloro-2-((1-metilpirrolidin-3-il)oxi)pirimidin-4-amina (INT-28) por (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina para proporcionar el compuesto I-60 (10,0 mg, 7%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-d6): 51.19 (d, J=6.5 Hz, 3H), 2.27 (s, 3H), 2.32-2.36 (m, 2H), 2.66-2.68 (m, 3H), 2.83-2.87 (m, 1H), 3.45 (br s, 2H), 3.60 (br s, 1H), 5.34 (br s, 1H), 6.98 (br s, 1H), 7.72-7.74 (m, 1H), 7.81 (d, J=8.8 Hz, 1H), 7.91 -7.97 (m, 2H), 8.06 (d, J=8.9 Hz, 1H), 9.14 (d, J=9.3 Hz, 1H), 10.7 (br s, 1H). MS m/z (M+H): 510.4.
Ejemplo 43
Síntesis de (R)-3-((6-cloro-2-(2-metoxietoxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-67)
El compuesto del título se sintetizó de la misma manera que I-59 sustituyendo 2-cloro-6-(2-metox¡etox¡)p¡rim¡d¡n-4-am¡na (S5-4) por (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina para dar el compuesto I-67 (25 mg, 18%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 51.19 (d, J=6.6 Hz, 3H), 3.34 (s, 3H), 3.45 (br s, 2H), 3.60 (br s, 1H), 3.68 (t, J=4.4 Hz, 2H), 4.44 (t, J=4.4 Hz, 2H), 6.98 (br s, 1H), 7.79-7.82 (m, 2H), 7.97-7.98 (m, 2H), 8.06 (d, J=8.8 Hz, 1H), 9.14 (d, J=9.3 Hz, 1H), 10.73 (br s, 1H). MS m/z (M+H): 485.4.
Ejemplo 44
Síntesis de (R)-3-((6-cloro-2-(2-(4-metilpiperazin-1-il)etoxi)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-66)
El compuesto del título se sintetizó de la misma manera que I-59 sustituyendo 6-cloro-2-(2-(4-metilpiperazin-1-il)etoxi)pirimidin-4-amina (INT-29) por 6-cloro-2-(2-(4-metilpiperazin-1-il)etoxi)pirimidin-4-amina para dar el compuesto I-66 (10 mg, 4,1%) como un sólido amarillo claro. 1H NMR (400 MHz, DMSO-d6): 5 1.19 (d, J=6.7 Hz, 3H), 1.88 (s, 1H), 2.13 (s, 3H), 2.30 (br s, 4H), 2.50 (br s, 4H), 2.67-2.70 (t, J=5.7 Hz, 2H), 3.45 (br s, 2H), 3.60 (br s, 1H), 4.41-4.43 (t, J=5.6 Hz, 2H), 7.80-7.91 (br m, 3H), 7.98 (d, J=3.7 Hz, 1H), 8.06 (d, J=8.9 Hz, 1H), 9.13 (d, J=9.3 Hz, 1H), 10.72 (br s, 1H). MS m/z (M+H): 553.1.
Ejemplo 45
Síntesis de (R)-3-((4-cloro-6-(2-(4-metilpiperazin-1-il)etoxi)pirimidin-2-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-61)
El compuesto del título se sintetizó de la misma manera que I-59 sustituyendo 6-cloro-2-(2-(4-met¡lp¡peraz¡n-1-¡l)etox¡)p¡r¡mid¡n-4-am¡na (INT-46) por (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina para proporcionar el compuesto I-61 (14 mg, 14,6%) como un sólido amarillo claro. 1H NMR (400 MHz, DMSO-d6): 51.19 (d, J=6.6 Hz, 3H), 2.11 (s, 3H), 2.27 (br s, 4H), 2.49 (br s, 4H), 2.67-2.70 (t, J=5.6 Hz, 2H), 3.45 (br s, 2H), 3.60 (br s, 1 H), 4.49-4.52 (t, J=5.6 Hz, 2H), 6.54 (s, 1H), 7.01 (br s, 1H), 7.76 (d, J=8.8 Hz, 1H), 7.97 (d, J=3.2 Hz, 1H), 8.04 (d, J=8.9 Hz, 1H), 8.39 (d, J=9.2 Hz, 1H), 9.15 (d, J=9.3 Hz, 1H), 10.39 (br s, 1H). MS m/z (M+H): 553.2.
Ejemplo 46
Síntesis de (R)-3-((4-cloro-6-(2-metoxietoxi)pirimidin-2-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-69)
El compuesto del título se sintetizó de la misma manera que I-59 sustituyendo 4-cloro-6-(2-metoxietoxi)pirimidin-2-amina (INT-45) por (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina para dar el compuesto I-69 (8,0 mg, 12%) como un sólido amarillo. 1H n Mr (400 MHz, DMsO-ds): 51.19 (d, J=6.7 Hz, 3H), 3.30 (s, 3H), 3.45 (s, 2H), 3.59-3.60 (br m, 1H), 3.70 (t, J=4.5 Hz, 2H), 4.52 (t, J=4.3 Hz, 2H), 6.57 (s, 1H), 7.00 (br s, 1H), 7.76 (d, J=8.9 Hz, 1H), 7.96 (br s, 1H), 8.03 (d, J=8.9 Hz, 1H), 8.40 (d, J=9.3 Hz, 1H), 9.15 (d, J=9.4 Hz, 1H), 10.41 (br s, 1H). MS m/z (M+H): 485.1.
Ejemplo 47
Síntesis de 4-cloro-6-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-2-carboxilato de (R)-metilo (1-70)
El compuesto del título se sintetizó de la misma manera que 1-59 sustituyendo 4-amino-6-cloropirimidin-2-carboxilatodemetilo (S6-5) por (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina para dar el compuesto 1-70 (10,0 mg, 11%) como un sólido amarillo pálido. 1H NMR (400 MHz, DMSO-d6): 5 1.19 (d, J=6.7 Hz, 3H), 3.45 (br s, 2H), 3.60 (br s, 1H), 3.92 (s, 3H), 6.98 (br s, 1H), 7.80 (br s, 1H), 7.87 (d, J=8.9 Hz, 1H), 7.98 (br s, 1H), 8.08 (d, J=8.9 Hz, 1H), 8.67 (br s, 1H), 9.14 (d, J=9.2 Hz, 1H), 11.23 (br s, 1H). MS m/z (M+H): 469.0.
Ejemplo 48
El compuesto del título se sintetizó de la misma manera que 1-59 sustituyendo 6-fluoro-2-(piperidin-1-ilmetil)pirimidin-4-amina (S7-8) por (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina para dar el compuesto 1-74 (44 mg, 29%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 5 1.18 (d, J=6.8 Hz, 3H), 1.38 (m, 2H), 1.51 (m, 4H), 2.45-2.48 (m, 4H), 3.44 (m, 2H), 3.52 (s, 2H), 3.59 (m, 1H), 6.96 (m, 1H), 7.71 (d, J=8.8 Hz, 1H), 7.87 (d, J=8.8 Hz, 1H), 7.96 (m, 1H), 8.03-8.05 (m, 2H), 9.08 (d, J=9.2 Hz, 1H), 10.89 (br s, 1H). MS m/z (M+H): 492.4. Ejemplo 49
Síntesis de (R)-3-((6-fluoro-2-((4-metilpiperazin-1-il)metil)pirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-73)
El compuesto del título se sintetizó de la misma manera que I-59 sustituyendo 6-fluoro-2-((4-metilpiperazin-1-¡l)met¡l)p¡r¡mid¡n-4-am¡na (INT-30) por (rac)-6-cloro-2-((1-metilpiperidin-3-il)oxi)pirimidin-4-amina para dar el compuesto I-73 (40 mg, 39%) como un sólido amarillo. 1H NMR (400 MHz, DMSo-ds): 51.18 (d, J=6.8 Hz, 3H), 2.14 (s, 3H), 2.32-2.40 (m, 4H), 2.52-2.58 (m, 4H), 3.44 (m, 2H), 3.55 (s, 2H), 3.59-3.65 (m, 1H), 6.96 (m, 1H), 7.72 (d, J=9.2 Hz, 1H), 7.87 (d, J=8.8 Hz, 1H), 7.97 (m, 1H), 8.03-8.05 (m, 2H), 9.09 (d, J=9.6 Hz, 1H), 10.89 (br s, 1H). MS m/z (M+H): 507.5.
Ejemplo 50
Síntesis de (R)-3-((4-cloro-6-(4-metilpiperazin-1-il)-1,3,5-triazin-2-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-10)
En un matraz de fondo redondo de 10 ml había (R)-3-bromo-10-metil-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-31) (0,03 g, 0,083 mmol), 4-cloro-6-(4-metilpiperazin-1-il)-1,3,5-triazin-2-amina (0,019 g, 0,083 mmol, ver la sección "síntesis de productos intermedios" para la síntesis) y K2CO3 (0,034 g, 0,248 mmol) en 1,4-dioxano (5 ml) para dar una suspensión amarilla. Se añadieron Pd2(dba)3 (7,58 mg, 8,28 gmol) y 2'-(diciclohexilfosfino)-N,N-dimetil-[1,1'-bifenil]-2-amina (DavePhos 6,52 mg, 0,017 mmol) y la reacción se calentó a reflujo bajo nitrógeno durante 4 horas. Después, la reacción se enfrió, se filtró sobre una almohadilla de sílice y se concentró. El residuo resultante se volvió a disolver en 1 ml de DMSO y se purificó mediante HPLC de fase inversa con 95%-5% de H2O (que contenía TFA al 0,5% v/v)/acetonitrilo para proporcionar el compuesto I-10 (0,0027 g, 5,29 gmol, rendimiento del 6,39%). MS: m/z 510.1 (M+H), 507.7 (M-H).
Ejemplo 51
Síntesis de (R)-3-((4-cloropirimidin-2-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-13)
El compuesto del título se sintetizó de la misma manera que I-10 sustituyendo 4-clorop¡r¡mid¡n-2-am¡na por 4-cloro-6-(4-met¡lp¡peraz¡n-1-¡l)-1,3,5-triaz¡n-2-am¡na para proporcionar el compuesto I-13 (0,0018 g, 4,38 gmol, rendimiento del 5,29%). MS: m/z 410.2 (M+H).
Ejemplo 52
Síntesis de (R)-3-((2-(dimetilamino)etil)(6-fluoropirimidin-4-il)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-33)
En un vial de microondas de 10 ml se disolvieron Pd2(dba)3 (7,20 mg, 7,87 gmol), carbonato de cesio (0,051 g, 0,157 mmol), diciclohexil(2',6'-diisopropoxi-[1,1'-bifenil]-2-il)fosfina (SPhos, 7,34 mg, 0,016 mmol), N1-(6-fluoropirimidin-4-il)-N2,N2-dimetiletano-1,2-diamina (INT-32) (0,017 g, 0,094 mmol) y (R)-3-cloro-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S1-12) (0,025 g, 0,079 mmol) en 5 ml de 1,4-dioxano seco. La reacción se puso al vacío, se sonicó y se volvió a llenar con nitrógeno. La reacción se irradió en un microondas Biotage Explorer a 130° C durante 3 horas. La reacción se enfrió, se filtró y se concentró hasta la sequedad. El residuo se volvió a disolver en DMSO y se purificó por HPLC de fase inversa con 95%-5% de H2O (que contenía TFA al 0,5% v/v)/acetonitrilo para proporcionar el compuesto I-33 (0,0066 g, 0,014 mmol, rendimiento del 18,02%). 1H NMR (400 MHz, DMSO-ds): 5 1.18 (d, 3H), 2.99 (s, 6H), 3.48 (m, 6H), 3.60 (m, 2H), 4.61 (m, 2H), 7.17 (t, 1H), 7.85 (d, 1H), 7.96 (d, 1H), 7.18 (m, 2H), 8.61 (s, 1H), 9.24 (d, 1H), 9.58 (br s, 1H).
Ejemplo 53
Síntesis de (R)-3-((6-fluoropirimidin-4-il)(2-metoxietil)amino)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-36)
El compuesto del título se sintetizó de la misma manera que I-33 sustituyendo 6-fluoro-N-(2-metox¡et¡l)p¡rim¡d¡n-4-am¡na (INT-33) por N1-(6-fluoropirimidin-4-il)-N2,N2-dimetiletano-1,2-diamina para proporcionar el compuesto I-36 (0,0019 g, 4,20 gmol, rendimiento del 3,34%). MS: m/z 453.0 (M+H), 450.8 (M-H).
Ejemplo 54
Síntesis de (R)-3-((2-fluoropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-52)
En un vial de 20 ml se suspendió (R)-3-hidroxi-10-metil-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-6) (0,072 g, 0,241 mmol) en 3 ml de DMF seca. Se añadió hidruro de sodio (60% en peso en aceite de dispersión, 9,62 mg, 0,241 mmol) y la reacción se calentó a 90° C. El material de partida se disuelve lentamente en la solución a medida que se libera gas y el color se vuelve ámbar oscuro. Después de 10 min de calentamiento, la reacción se enfría a 0° C y se añade gota a gota 2,4-difluoropirimidina (0,028 g, 0,241 mmol). La reacción se agitó a temperatura ambiente o se calentó a 50° C. Una vez completada, la reacción se inactivó con NH4Cl saturado (ac.) y se vierte en agua. La reacción se extrajo tres veces con diclorometano y los extractos orgánicos se combinaron, se secaron sobre sulfato de sodio y se concentraron al vacío. El residuo resultante se volvió a disolver en DMSO y se purificó por HPLC de fase inversa con 95%-5% de H2O (que contenía TFA al 0,5% v/v)/acetonitrilo para proporcionar el compuesto I-52 (0,036 g, 0,091 mmol, rendimiento del 37,9%). MS: m/z 395.9 (M+H), 393.7 (M-H). 1H NMR (400 MHz, DMSO-ds): 51.17 (d, 3H), 3.43 (m, 2H), 3.59 (m, 1H), 5.72 (s, 1H), 7.14 (t, 1H) 7.39 (m, 1H), 7.64 (d, 1H), 7.84 (d, 1H), 8.15 (m, 2H), 8.77 (m, 1H), 9.36 (d, 1H).
Ejemplo 55
Síntesis de (R)-3-((6-cloro-2-metilpirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-58)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 4,6-d¡cloro-2-met¡lp¡r¡m¡dina por 2,4-difluoropirimidina para proporcionar el compuesto I-58 (0,005 g, 0,01 mmol, rendimiento del 16,9%). MS: m/z 425.9 (M+H), 423.6 (M-H). 1H NMR (400 MHz, DMSO-d6): 5 1.42 (d, 3H), 3.59 (m, 1H), 3.75 (d, 1H), 3.84 (m, 1H), 5.36 (br s, 1H), 7.07 (br s, 1H), 7.13 (s, 1H), 7.26 (s, 1H), 7.36 (d, 1H), 7.92 (d, 2H), 7.99 (d, 1H) 9.00 (d, 1H).
Ejemplo 56
Síntesis de (R)-3-((6-cloro-2-(metoximetil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-57)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 4,6-dicloro-2-(metoximetil)pirimidina por 2,4-difluoropirimidina para proporcionar el compuesto I-57 (0,025 g, 0,055 mmol, rendimiento del 11%) MS: m/z 455.8 (M+H), 453.6 (M-H). 1H NMR (400 MHz, DMSO-ds): 5 1.18 (d, 3H), 3.27 (s, 3H), 3.61 (m, 3H), 4.42 (s, 2H), 7.15 (br s, 1H), 7.55 (s, 1H), 7.60 (d, 1H), 7.83 (d, 1H), 8.16 (m, 2H), 9.35 (d, 1H). Ejemplo 57
Síntesis de (R)-3-((6-cloropirazin-2-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-55)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 2,6-dicloropirazina por 2,4-difluoropirimidina para proporcionar el compuesto I-55 (2,4 mg, 4,51 pmol, rendimiento del 9,01%) como un sólido amarillo. LCMS m/z: 411.8 [M+H].
Ejemplo 58
Síntesis de (R)-3-((6-clorop¡r¡m¡d¡n-4-¡l)oxi)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]quinolin-8-ona (I-56)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 4,6-dicloropirimidina por 2,4-difluoropirimidina para proporcionar el compuesto I-56. MS m/z: 411.8 [M+H]. 1H-NMR (400 MHz, CDCh): 59.02 (d, 1H), 8.65 (s, 1H), 8.04-7.92 (m, 2H), 7.39 (d, 1H), 7.30 (s, 1H), 3.86 (m, 1H), 3.80-3.72 (m, 1H), 3.60 (m, 1H), 1.44 (d, 3H).
Ejemplo 59
Síntesis de (R)-3-((2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-53)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 2,4-dicloropirimidina por 2,4-difluoropirimidina para proporcionar el compuesto I-53 (30 mg, 20%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5 1.20 (d, J=6.6 Hz, 3H), 3.46 (br s, 2H), 3.60 (br s, 1H), 7.10 (br s, 1H), 7.42 (d, J=5.6 Hz, 1H), 7.61 (d, J=9.0 Hz, 1H), 7.84 (d, J=8.9 Hz, 1H), 8.04 (br s, 1H), 8.17 (d, J=8.8 Hz, 1H), 8.74 (d, J=5.6 Hz, 1H), 9.37 (d, J=9.0
Hz, 1H). MS m/z (M+H): 412.3.
Ejemplo 60
Síntesis de (R)-3-((6-fluoro-2-met¡lp¡r¡m¡d¡n-4-il)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-65)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 4,6-d¡fluoro-2-met¡lp¡rim¡d¡na por 2,4-difluoropirimidina para proporcionar el compuesto I-65 como un sólido. 1H NMR (400 MHz, DMSO-d6): d 9.33 (d, 1H), 8.15 (m, 2H), 7.82 (m, 1H), 7.56 (d, 1H), 7.13 (br s, 1H), 7.03 (s, 1H), 3.58-3.43 (m, 3H), 2.40 (s, 3H), 1.17 (d, 3H). MS m/z: 409.9 (M+H).
Ejemplo 61
Síntes¡s de (R)-met¡l4-cloro-6-((10-met¡l-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]quinolin-3-il)oxi)pirimidina-2-carboxilato (I-71)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 4,6-dicloropirimidina-2-carboxilato de metilo por 2,4-difluoropirimidina para proporcionar el compuesto I-71 (16 mg, 11,3%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 5 1.20 (d, J=6.6 Hz, 3H), 3.46 (br s, 2H), 3.61 (br s, 1H), 3.82 (s, 3H), 7.10 (br s, 1H), 7.61 (d, J=9.1 Hz, 1H), 7.82 (d, J=8.8 Hz, 1H), 7.86 (s, 1H), 8.05 (br s, 1H), 8.17 (d, J=8.9 Hz, 1H), 9.37 (d, J=9.1 Hz, 1H). MS m/z (M+H): 470.1.
Ejemplo 62
Síntesis de (R)-3-((6-cloro-2-(hidroximetil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-68)
A una solución de 4-cloro-6-((10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6'):4,5]tieno[3,2-f]quinolin-3-il)oxi)pirimidin-2-carboxilato de (R)-metilo (I-71) (30 mg, 0,06 mmol) en tetrahidrofurano (3,0 ml), se le añadió hidruro de diisobutilaluminio (1 M) (72,6 mg, 0,50 ml, 0,5 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se inactivó con una solución saturada de cloruro de amonio (5 ml) y se extrajo con acetato de etilo (2 x 15 ml). La capa orgánica se lavó con (2 x 10 ml) agua seguido de salmuera (1 x 10 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El producto bruto se purificó mediante TLC preparativa para proporcionar el compuesto I-68 (6,0 mg, 18%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 51.19 (d, J=6.6 Hz, 3H), 3.46 (br s, 2H), 3.60 (br s, 1H), 4.43 (d, J=6.6 Hz, 2H), 5.34 (t, J=6.2 Hz, 1H), 7.09 (br s, 1H), 7.44 (s, 1H), 7.57 (d, J=9.0 Hz, 1H), 7.82 (d, J=8.9 Hz, 1H), 8.04 (br s, 1H), 8.15 (d, J=8.8 Hz, 1H), 9.35 (d, J=9.1 Hz, 1H). MS m/z (M+H): 442.4. Ejemplo 63
Síntesis de (R)-3-((4-cloro-6-(pirrolidin-1-il)-1,3,5-triazin-2-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-62)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 2,4-dicloro-6-(pirrolidin-1-il)-1,3,5-triazina (INT-34) por 2,4-difluoropirimidina para proporcionar el compuesto I-62. MS: m/z: 481.9 [M+1]. 1H-NMR (400 MHz, CDCla): 58.98 (d, 1H), 7.99-7.88 (m, 2H), 7.32 (d, 1H), 6.12 (s, 1H), 5.28 (t, 1H), 3.87-3.79 (m, 1H), 3.76 3.69 (m, 1H), 3.63 (t, 2H), 3.60-3.52 (m, 1H), 3.44 (t, 2H), 2.02-1.89 (m, 4H), 1.40 (d, 3H).
Ejemplo 64
Síntesis de (R)-3-((4-cloro-6-morfolino-1,3,5-triazin-2-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-63)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 4-(4,6-dicloro-1,3,5-triazin-2-il)morfolina (INT-35) por 2,4-difluoropirimidina para proporcionar el compuesto I-63. MS: m/z 497.9 [M+H]. 1H-NMR (400 MHz, DMSO-d6): 59.33 (d, 1H), 8.20-8.13 (m, 2H), 7.87 (d, 1H), 7.62 (d, 1H), 7.15 (s, 1H), 3.80-3.70 (m, 3H), 3.68-3.62 (t, 2H), 3.59-3.53 (m, 4H), 3.45 (m, 2H), 1.199d, 3H).
Ejemplo 65
Síntesis de (R)-3-((4-cloro-6-(p¡per¡d¡n-1-¡l)-1,3,5-tr¡az¡n-2-il)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-64)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 2,4-dicloro-6-(piperidin-1 -il)-1,3,5-triazina (INT-36) por 2,4-difluoropirimidina para producir compuesto I-64. MS: m/z: 495.8 [M+H].
Ejemplo 66
Síntes¡s de (R)-3-((4-cloro-6-(d¡met¡lam¡no)-1,3,5-tr¡az¡n-2-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-75)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 4,6-dicloro-N,N-dimetil-1,3,5-triazin-2-amina (INT-37) por 2,4-difluoropirimidina para proporcionar el compuesto I-75. MS: m/z 455.8 [M+H]. 1H-NMR (400 MHz, DMSO-d6): 59.33 (d, 1H), 8.21-8.14 (m, 2H), 7.889d, 1H), 7.63 (d, 1H), 7.15 (s, 1H), 3.65-3.57 (m, 1H), 3.50-3.44 (m, 2H), 3.12 (s, 3H0, 2.96 (s, 3H), 1.199d, 3H).
Ejemplo 67
Síntesis de (R)-3-((4-cloro-6-metoxi-1,3,5-triazin-2-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-76)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 2,4-dicloro-6-metoxi-1,3,5-triazina (INT-38) por 2,4-difluoropirimidina para proporcionar el compuesto I-76. MS: m/z 442.7 [M+H]. 1H-NMR (400 MHz, DMSO-d6): 59.38 (d, 1H), 8.24-8.14 (m, 2H), 7.92-7.87 (m, 1H), 7.71-7.66 (m, 1H), 7.17 (s, 1H), 3.96 (s, 3H), 3.66-3.56 (m, 1H), 3.50-3.40 (m, 2H), 1.19 (d, 3H).
Ejemplo 68
Síntesis de (R)-3-((4-cloro-6-(3,3-difluoropirrolidin-1-il)-1,3,5-triazin-2-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-77)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 2,4-dicloro-6-(3,3-difluoropirrolidin-1 -il)-1,3,5-triazina (INT-39) por 2,4-difluoropirimidina para proporcionar el compuesto I-77. MS: m/z 517.8 [M+H].
Ejemplo 69
Síntesis de (R)-3-((4-cloro-6-(3,3-difluoropiperidin-1-il)-1,3,5-triazin-2-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-78)
El compuesto del título se sintetizó de la misma manera que I-52 sustituyendo 2,4-dicloro-6-(3,3-difluoropiperidin-1 -il)-1,3,5-triazina (INT-40) por 2,4 -difluoropirimidina para proporcionar el compuesto I-78. MS: m/z 531.8 [M+H]. 1H-NMR (400 MHz, DMSO-d6): 5 9.34 (dd, 1H), 8.20 (dd, 1H), 8.16 (d, 1H), 7.88 (dd, 1H), 7.66 (dd, 1H), 7.16 (s, 1H), 4.15 (t, 1H), 3.97 (t, 2H), 3.84 (t, 3H), 3.65 (m, 2H), 2.12 (m, 2H), 1.78-1.60 (m, 2H), 1.19 (d, 3H).
Ejemplo 70
Síntesis de (R)-3-((6-cloropiridazin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-J]quinolin-8-ona
En un vial de microondas, se añadió NaH (26,7 mg, 0,668 mmol) a INT-6 (50 mg, 0,167 mmol) en DMF (4 ml) y se calentó convencionalmente a 55° C durante una hora. Luego, la mezcla de la reacción se enfrió a 0° C y se añadió 3,5-dicloropiridazina (49,8 mg, 0,334 mmol) en 0,5 ml de DMF. La mezcla resultante se irradió a 100° C durante 1 h 45 min. Una vez completada la reacción, la mezcla bruta se purificó directamente mediante HPLC preparativa usando CH3CN/H2O (ácido fórmico al 0,1%) como eluyentes para proporcionar I-79 (15 mg, 0,036 mmol, rendimiento del 21,80%) como un sólido. 1H NMR (400 MHz, DMSO-d6): 59.43 (s, 1H), 9.34 (d, 1H), 8.14-8.07 (m, 3H), 7.74 (d, 1H), 7.56 (d, 1H), 7.10 (br t, 1H), 3.44-3.30 (m, 3H, fusionado con DMSO-H2O pico), 1.16 (d, 3H). MS m/z=411.8 (M+1+).
Ejemplo 71
Síntesis de (R)-3-((6-fluoropirimidin-4-il)tio)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-54)
A una suspensión de hidruro de sodio (22,83 mg, 0,9 mmol) en dimetilformamida (1,0 ml), se añadieron ((R)-3-mercapto-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6' :4,5]tieno[3,2-f]quinolin-8-ona (iNt-7) (100 mg, 0,3 mmol) y 4,6-difluoropirimidina (73,6 mg, 0,6 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 90° C durante 2 h. Una vez completada la reacción, la mezcla de la reacción se inactivó con agua y se extrajo con metanol al 5% en diclorometano (3 x 5 ml). La capa se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El material bruto obtenido se purificó mediante TLC preparativa para proporcionar el compuesto I-54 (15 mg, 10%) como un sólido amarillo. 1H n M r (400 MHz, DMSO-d6): 5 1.19 (d, J=6.7 Hz, 3H), 3.46 (br s, 2H), 3.61 (br s, 1H), 7.11 (br s, 1H), 7.48 (s, 1H), 7.92-7.96 (m, 2H), 8.05 (br s, 1H), 8.20 (d, J=8.9 Hz, 1H), 8.78 (br s, 1H), 9.25 (d, J=9.0 Hz, 1H). MS: m/z 412.3 (M+H).
Ejemplo 72
Síntesis de (R)-3-((2-cloropirimidin-4-il)tio)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-72)
El compuesto del título se sintetizó de la misma manera que I-54 sustituyendo 2,4-dicloropirimidina por 4,6-difluoropirimidina para proporcionar el compuesto I-72 (25 mg, 18%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 5 1.19 (d, J=6.6 Hz, 3H), 3.45 (br m, 2H), 3.60 (br m, 1H), 7.12 (br s, 1H), 7.57 (d, J=5.4 Hz, 1H), 77.95 7.97 (m, 2H), 8.07 (br s, 1H), 8.21 (d, J=8.9 Hz, 1H), 8.53 (d, J=5.4 Hz, 1H), 9.26 (d, J=8.9 Hz, 1H). MS m/z (M+H): 428.3.
Ejemplo 73
Síntesis de (S)-3-((6-fluoropirimidin-4-il)amino)-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-17)
A una solución agitada de (S)-3-cloro-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-1) (50 mg, 0,15 mol) 6-fluoropirimidin-4-amina (33,9 mg, 0,3 mmol) en 1,4-dioxano (10 ml) se le añadió carbonato de cesio (146,42 mg, 0,45 mmol) y la solución se desgasificó con argón durante 10 min. A la solución anterior se le añadió Xantphos (8,6 mg, 0,015 mmol) seguido de Pd2(dba)3 (14 mg, 0,015 mmol) y la solución se desgasificó de nuevo durante 5 min con argón y se agitó a 100° C durante 16 h. Una vez completada, se añadieron agua con hielo (5 ml) y diclorometano (10 ml) a la mezcla de la reacción y se agitó durante 30 min. Se formó un sólido y se recogió por filtración y se lavó con agua (5 ml) seguido de metanol (5 ml) para proporcionar el compuesto I-17 (40 mg, rendimiento del 63%) como un sólido marrón. 1H NMR (400 MHz, DMSO-ds): 53.43-3.59 (m, 5H), 4.95 (t, J=5 Hz, 1H), 6.96 (t, J=4.8 Hz, 1H), 7.68 (d, J=9 Hz, 1H), 7.84 (s, 1H), 7.89 (d, J=9 Hz, 1H), 8.05 (d, J=9 Hz, 1H), 8.17 (s, 1H), 8.58 (s, 1H), 9.09 (d, J=9 Hz, 1H), 10.92 (s, 1H). MS m/z (M+H): 411.2.
Ejemplo 74
Síntesis de (S)-3-((6-cloropirimidin-4-il)amino)-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-22)
El compuesto del título se sintetizó de la misma manera que I-17 sustituyendo 6-clorop¡r¡mid¡n-4-am¡na por 6-fluorop¡rim¡d¡n-4-am¡na para proporcionar el compuesto 1-22 (20 mg) como un sólido amarillo. 1H NMR (400 MHz, DMSO-D6): 5: 3.43-3.59 (m, 5H), 4.95 (t, J=5 Hz, 1H), 6.96 (t, J=4.8 Hz, 1H), 7.75 (d, J=9 Hz, 1H), 7.82 (s, 1H), 7.85 (s, 1H), 8.06 (d, J=9 Hz, 1H), 8.46 (br s, 1H), 8.63 (s, 1H), 9.10 (d, J=9.3 Hz, 1H), 10.86 (s, 1H). MS m/z (M+H): 427.37.
Ejemplo 75
Síntesis de (S)-2-cloro-4-((10-(hidroximetil)-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)amino)pirimidina-5-carboxamida (I-30)
A una solución de (S)-2-cloro-4-((10-(hidroximetil)-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6'4,5]tieno[3,2-f]quinolin-3-il)amino)-N-(4-metoxibencil)pirimidin-5-carboxamida (INT-52) (22 mg, 0,04 mmol) en diclorometano (2,0 ml) se añadieron ácido trifluoroacético (0,5 ml, 0,04 mmol) seguido de ácido trifluorometanosulfónico (55,9 mg, 0,4 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 1 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida y se co-destiló con diclorometano (2 x 10 ml). El material bruto obtenido se diluyó con solución saturada de bicarbonato de sodio (10 ml) y se agitó durante 10 min. después de lo cual se formó un precipitado. El precipitado se filtró y se lavó con agua seguido de metanol al 2% en diclorometano y se secó para proporcionar el compuesto I-30 (11 mg, 52%) como un sólido marrón. 1H NMR (400 MHz, DMSO-d6): 3.42-3.50 (m, 3H), 3.55-3.58 (m, 2 h ), 4.95 (br s, 1H), 7.04 (br s, 1H), 7.82 (d, J=8.9 Hz, 1H), 7.85 (br s, 1H), 8.07-8.09 (m, 2H), 8.52 (s, 1H), 8.61 (d, J=9.3 Hz, 1H), 8.90 (s, 1H), 9.25 (d, J=9.5 Hz, 1H), 12.12 (s, 1H). MS m/z (M+H): 470.2.
Ejemplo 76
Síntesis de (R)-10-(aminometil)-3-((6-fluoropirimidin-4-il)amino)-9,10,11,12-tetrahidro-8H-[1.4] diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (S8-6 , I-26)
A una solución agitada de ((3-((6-fluoropirimidin-4-il)amino)-8-oxo-9,10,11,12-tetrahidro-8H-[1.4] Seañadiódiazepino[5',6':4,5]tieno[3,2-f]quinolin-l0-il)metil)carbamato de (S)-terc-butilo (S8-5) (16,0 mg, 0,03 mmol) en diclorometano (2,0 ml) se le añadió ácido trifluoroacético (1,1 ml) a temperatura ambiente. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 1 h. Una vez completada, la mezcla de la reacción se concentró a presión reducida. El material bruto se trituró con éter dietílico para producir la sal de trifluoroacetato del compuesto I-26 (14 mg) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 52.81-2.88 (m, 1H), 2.97-3.02 (m, 1H), 3.78-3.80 (m, 1H), 3.80-3.88 (m, 2H), 7.05 (br s, 1H), 7.72 (d, J=9.3 Hz, 1H), 7.83 (br s, 2H), 7.93 (d, J=8.9 Hz, 1H), 8.07-8.10 (m, 2H), 8.17 (s, 1H), 8.59 (s, 1H), 9.07 (d, J=9.1 Hz, 1H), 10.94 (br s, 1H). MS m/z (M+H): 410.3. Ejemplo 77
Síntesis de (R)-10-(aminometil)-3-((6-cloropirimidin-4-il)amino)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (1-28)
El compuesto del título se sintetizó de la misma manera que 1-17 sustituyendo 6-cloropirimidin-4-amina por 6-fluoropirimidin-4-amina y (R)-10-(aminometil)-3-cloro-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-47) por (S)-3-cloro-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-1) para proporcionar el compuesto I-28 como un sólido naranja. 1H NMR (400 MHz, DMSO-d6): 5 2.79-2.80 (m, 1H), 2.98-3.01 (m, 2H), 3.07-3.10 (m, 1H), 3.69-3.79 (m, 2H), 3.82-3.88 (m, 1H), 7.78-7.88 (m, 3H), 8.08-8.10 (m, 2H), 8.45 (br s, 1H), 8.64 (s, 1H), 9.08 (d, J=9.1 Hz, 1H), 10.89 (br s, 1H). MS m/z (M+H): 426.3.
Ejemplo 78
Síntesis de (S)-10-((dimetilamino)metil)-3-((6-fluoropirimidin-4-il)amino)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-31)
El compuesto del título se sintetizó de la misma manera que I-17 sustituyendo (S)-3-cloro-10-((dimetilamino)metil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-48 ) por (S)-3-cloro-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (InT-1 ), para proporcionar el compuesto I-31 (6,0 mg, 40%) como un sólido amarillo. 1H N m R (400 MHz, DMSO-d6): 5 2.25 (s, 3H), 2.52-2.54 (m, 2H), 3.22-3.25 (m, 1H), 3.32-3.35 (m, 1H), 3.55-3.60 (m, 1H), 7.14 (t, J=5.6 Hz, 1H), 7.70 (d, J=9.2 Hz, 1H), 7.89 (d, J=8.8 Hz, 1H), 8.19 (d, J=8.8 Hz, 1H), 8.23 (br s, 1H), 9.24 (d, J=9.2 Hz, 1H). MS m/z (M+H): 347.1. Ejemplo 79
Síntesis de (R)-3-((6-fluoropirimidin-4-il)amino)-10-((metilamino)metil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-35)
El compuesto del título se sintetizó de la misma manera que I-17 sustituyendo (R)-3-cloro-10-((metilamino)met¡l)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (INT-50) por (S)-3-cloro-10-(hidroximetil)-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (iNt-1 ) para proporcionar el compuesto I-35 (17 mg, 14%) como un sólido marrón claro. 1H NMR (400 MHz, DMSO-d6): 52.26 (s, 3H), 2.31-2.33 (m, 1H), 2.40-2.50 (m, 1H), 3.22-3.25 (m, 1H), 3.55 (m, 2H), 7.05 (m, 1H), 7.69 (d, J=9.0 Hz, 1H), 7.90 (d, J=8.8 Hz, 1H), 8.06 (d, J=8.9 Hz, 1H), 8.17 (d, J=9.5 Hz, 2H), 8.58 (s, 1H), 9.14 (d, J=9.1 Hz, 1H), 10.9 (br s, 1H). MS m/z (M+H): 424.2.
Ejemplo 80
Síntesis de (R)-3-((5-((terc-butil(metil)amino)metil)-2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-80)
A una suspensión agitada de INT-6 (75 mg, 0,2 mmol) en DMF anhidra (5 ml) se le añadió t-BuOK (28,1 mg, 0,25 mmol) a 0° C para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-90 (93,2 mg, 0,4 mmol) en DMF (2 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (20 ml) y agua (30 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). La capa orgánica combinada se lavó con salmuera (50 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó el producto deseado I-80 (24 mg, 18%) como un sólido amarillo. (400 MHz, DMSo-d6): 59.34 (d, J=9.2 Hz, 1H), 8.70 (s, 1H), 8.15 (d, J=8.8 Hz, 1H), 8.03 (br, 1H), 7.82 (d, J=9.2 Hz, 1H), 7.56 (d, J=8.8 Hz, 1H), 7.10-7.11 (m, 1H), 3.66 (s, 2H), 3.61 (br, 1H), 3.46 (br, 2H), 2.17 (s, 3H), 1.19 (d, J=6.8 Hz, 3H), 1.10 (s, 9H). MS m/z (M+H): 511.3.
Ejemplo 81
Síntesis de (R)-3-((2-cloro-5-((2-metoxietoxi)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-81)
En un matraz de fondo redondo de 100 ml, purgado y mantenido con una atmósfera inerte de nitrógeno, se disolvió INT-6 (115,9 mg, 0,39 mmol) en DMF (10 ml). Se añadió lentamente t-BuOK (1 M en THF) (0,64 ml, 0,64 mmol) mediante una jeringuilla a la solución a 0° C y la reacción cambió a marrón claro. La solución resultante se agitó durante 20 min a 0° C. Después de estos 20 min, se añadió gota a gota INT-64 (137 mg, 0,58 mmol) en DMF (2 ml) con agitación a 0° C. La solución resultante se calentó a temperatura ambiente y se agitó durante la noche. La LCMS confirmó la formación del producto deseado. La reacción se concentró hasta la sequedad y el residuo se diluyó con EtOAc (300 ml) y se lavó con 2 x 300 ml de agua y luego 1 x 300 ml de solución de salmuera saturada. A continuación, el extracto orgánico se secó sobre sulfato de sodio, se filtró y se concentró a sequedad. Luego, el material bruto se purificó mediante cromatografía en columna (DCM: MeOH = 30:1). Las fracciones deseadas se concentraron hasta la sequedad al vacío y se purificaron adicionalmente mediante HPLC preparativa para obtener (I-81) (536,7 mg, 28,5%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.37 (d, J=9.2 Hz, 1H), 8.72 (s, 1H), 8.20 (d, J=9.2 Hz, 1H), 8.15 (d, J=4.4 Hz, 1H), 7.87 (d, J=9.2 Hz, 1H), 7.63 (d, J=8.8 Hz, 1H), 7.19-7.16 (m, 1H), 4.71 (s, 2H), 3.73-3.71 (m, 2H), 3.63-3.61 (m, 1H), 3.55-3.54 (m, 2H), 3.51-3.44 (m, 2H), 3.28 (s, 3H), 1.20 (d, J=6.8 Hz, 3H). MS m/z (M+H): 500.0.
Ejemplo 82
Síntesis de (R)-3-((2-cloro-5-(etoximetil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-82)
A una solución de INT-6 (270 mg, 0,9 mmol) en DMA (o DMF) (3,0 ml) se le añadió terc-butóxido de potasio (202,4 mg, 1,8 mmol) a 0° C y se agitó durante 10 min. A la mezcla resultante se le añadió INT-60 (280,1 mg, 1,4 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 25° C durante 30 min. Una vez completada, la mezcla de la reacción se diluyó con agua (20,0 ml), después de lo cual se formó un sólido. El sólido se filtró y se secó al vacío produciendo 250 mg. El bruto se purificó mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) para producir I-82 (80 mg, 19%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.35 (d, J=9.2 Hz, 1H), 8.70 (br, 1H), 8.17 (d, J=9.2 Hz, 1H), 8.11 (d, J=4.0 Hz, 1H), 7.84 (d, J=8.8 Hz, 1H), 7.61 (d, J=8.8 Hz,
1H), 7.14 (t, J=4.8 Hz, 1H), 4.64 (s, 2H), 3.60-3.64 (m, 2H), 3.58 (br, 1H), 1.17-1.20 (m, 6H). MS m/z (M+H): 470.5. Ejemplo 83
Síntesis de ((10R)-3-((5-((3-azab¡c¡clo[3.1.0]hexan-3-¡l)met¡l)-2-clorop¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]tieno[3,2-f]qu¡nol¡n-8-ona (I-83)
A una suspensión agitada de INT-6 (130 mg, 0,43 mmol) en DMF anhidra (15 ml) se le añadió t-BuOK (1 M en THF, 0,87 ml, 0,87 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 h a esta temperatura. Se añadió gota a gota I-75 (110 mg, 0,45 mmol) en DMF (3 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (50 ml) y agua (20 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 50 ml). Los extractos orgánicos combinados se lavaron con salmuera (30 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó el producto deseado I-83 (57,7 mg, 26,5%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.36 (d, J=9.2 Hz, 1H), 8.64 (s, 1H), 8.20-8.14 (m, 2H), 7.85 (d, J=9.2 Hz, 1H), 7.60 (d, J=9.2 Hz, 1H), 7.18-7.16 (m, 1H), 3.77 (s, 2H), 3.63-3.43 (m, 3H), 2.98 (d, J=8.4 Hz, 2H), 2.46 (d, J=8.0 Hz, 2H), 1.40-1.38 (m, 2H), 1.20 (d, J=6.8 Hz, 3H), 0.68 0.65 (m, 1H), 0.36-0.29 (m, 1H).
Ejemplo 84
Sintes¡s de ((R)-3-((2-cloro-5-((((S)-tetrah¡drofuran-3-¡l)ox¡)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,41]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-84)
A una solución agitada de INT-6 (207 mg, 0,690 mmol) en DMF (15 ml) se le añadió t-BuOK (155,19 mg,
1,38 mmol) a 0° C y la reacción se agitó durante 10 min. Luego se añadió una solución de INT-66 (189,47 mg, 0,76 mmol) en DMF (5 ml) a 0° C y la reacción se agitó a temperatura ambiente durante la noche. La mezcla de la reacción se repartió entre acetato de etilo (50 ml) y agua (20 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 50 ml). Los extractos orgánicos combinados se lavaron con salmuera (30 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó el producto deseado I-84 (63,3 mg, 18%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.34 (d, J=8.0 Hz, 1H), 8.71 (s, 1H), 8.19-8.12 (m, 2H), 7.84 (d, J=8.8 Hz, 1H), 7.61 (d, J=8.8 Hz, 1H), 7.16-7.14 (m, 1H), 4.70-4.63 (m, 2H), 4.36-4.32 (m, 1H), 3.80-3.77 (m, 2H), 3.75-3.67 (m, 2H), 3.61-3.60 (m, 1H), 3.47-3.46 (m, 2H), 2.02-1.97 (m, 2H), 1.22-1.17 (m, 3H). MS m/z (M+H): 511.9.
Ejemplo 85
Síntesis de (R)-3-((5-((3-azab¡c¡clo[3.1.1]heptan-3-¡l)met¡l)-2-clorop¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]tieno[3,2-f]qu¡nol¡n-8-ona (I-85)
A una suspensión agitada de INT-6 (100 mg, 0,33 mmol) en DMF anhidra (10 ml), se le añadió t-BuOK (1 M en THF, 0,67 ml, 0,67 mmol) a 0° C para dar una solución marrón. La solución resultante se agitó durante 0,5 h a esta temperatura. Se añadió gota a gota INT-76 (110 mg, 0,40 mmol) en DMF (3 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (50 ml) y agua (20 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 50 ml). La capa orgánica combinada se lavó con salmuera (30 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó el producto deseado I-85 (43,7 mg, 24,7%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds) 59.36 (d, J=9.2 Hz, 1H), 8.73 (s, 1H), 8.19-8.13 (m, 2H), 7.84 (d, J=8.8 Hz, 1H), 7.59 (d, J=8.8 Hz, 1H), 7.18-7.15 (m, 1H), 3.84 (s, 2H), 3.62-3.42 (m, 3H), 2.91 (s, 4H), 2.32-2.30 (m, 2H), 1.97-1.92 (m, 2H), 1.50-1.46 (m, 2H), 1.22 (d, J=11.2 Hz, 3H).
Ejemplo 86
Síntes¡s de (R)-3-((2-cloro-5,7-d¡h¡drofuro[3,4-d]p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-86)
En un vial de 20 ml, se añadió INT-6 (0,05 g, 0,167 mmol) a 3 ml de DMF seca y se sonicó brevemente. A esto, se le añadió K2CO3 (0,231 g, 1,670 mmol) y la reacción se calentó a 90° C durante 10 min. Luego, la reacción se enfrió a temperatura ambiente y se añadió 2,4-dicloro-5,7-dihidrofuro[3,4-d]pirimidina (0,055 g, 0,288 mmol) y posteriormente se calentó a 90° C durante 2 h. Una vez completada, la reacción se enfrió, se filtró para eliminar cualquier carbonato de potasio no disuelto y la mezcla de la reacción bruta se purificó directamente mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) para producir I-86 (0,052 g, 0,114 mmol, rendimiento del 68%) como un sólido amarillo después de la liofilización. 1H NMR (400 MHz, DMSO-d6): 59.31 (d, J=9.2 Hz, 1H), 8.13 (d, J=8.7 Hz, 1H), 8.10 (d, J=4.6 Hz, 1H), 7.79 (d, J=8.7 Hz, 1H), 7.58 (d, J=9.2 Hz, 1H), 7.11 (br, 1H), 4.98 (s, 4H), 3.55 (m, 1H), 3.39 (m, 2H), 1.12 (d, J=6.9 Hz, 3H) MS m/z (M+H): 453.8.
Ejemplo 87
Síntesis de (R)-3-((2-cloro-5-((d¡¡soprop¡lam¡no)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-87)
A una suspensión de INT-6 (128 mg, 0,429 mmol) en DMF (3 ml) a temperatura ambiente se le añadió hidruro de sodio (60% en aceite) (20,59 mg, 0,515 mmol). El color de la reacción cambió de amarillo verdoso a marrón oscuro y en 10 minutos la reacción se volvió homogénea. Después de 20 min, la mezcla de la reacción se enfrió a 0° C y se añadió gota a gota una solución de INT-89 (135 mg, 0,515 mmol) en DMF (1,5 ml) durante 2 min. La reacción se agitó durante la noche y a la mañana siguiente la reacción se enfrió a 0° C, se inactivó con NH4Cl acuoso saturado (~1 ml, inicialmente gota a gota, precaución: desprendimiento de gas) y agua ~3 ml. Se retiró el baño de enfriamiento y se continuó agitando a RT durante 10 min para dar una suspensión amarilla. La reacción se extrajo con DCM (5 x 10 ml), la emulsión era persistente. Los extractos orgánicos se filtraron a través de Na2SO4 y se concentraron. El producto bruto se purificó mediante HPLC preparativa (10-95% de MeCN/agua, 0,1% de TFA). Se obtuvo I-87 (133 mg, 0,253 mmol, rendimiento del 59,0%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.36 (d, J=9.2 Hz, 1H), 8.88 (br, 2H), 8.17 (d, J=9.2 Hz, 1H), 8.13 (d, J=4.6 Hz, 1H), 7.83 (d, J=9.2 Hz, 1H), 7.63 (d, J=9.2 Hz, 1H), 7.14 (br, 1H), 4.51 (d, J=5.0 Hz, 2H) 3.82 (m, 2H), 3.57 (m, 1H), 3.42 (m, 2H), 1.40 (d, J=6.4 Hz, 6H), 1.34 (d, J=6.4 Hz, 6H), 1.14 (d, J=6.9 Hz, 3H). MS m/z (M+H): 524.8.
Ejemplo I-88
Síntesis de (R)-3-((2-cloro-5-((diisobutilamino)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-88)
A una suspensión agitada de INT-6 (31,3 mg, 0,1 mmol) en DMF anhidro (4 ml) se le añadió t-BuOK (1 M en THF, 0,2 ml, 0,2 mmol) a 0° C gota a gota para dar una solución marrón y la solución resultante se agitó durante 0,5 horas adicionales a esta temperatura. Se añadió gota a gota INT-77 (60,2 mg, 0,2 mmol) en DMF (1 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (5 ml) y agua (5 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 5 ml). La capa orgánica combinada se lavó con salmuera (10 ml) y la capa orgánica se separó, se secó sobre Na2SO4., se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-88 (8,5 mg, 13,8%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.37 (d, J=9.2 Hz, 1H), 8.72 (s, 1H), 8.19-8.15 (m, 2H), 7.83 (d, J=8.8 Hz, 1H), 7.55 (d, J=9.2 Hz, 1H), 7.17-7.15 (m, 1H), 3.66-3.61 (m, 3H), 3.61-3.48 (m, 2H), 2.19 2.17 (m, 4H), 1.84-1.77 (m, 1H), 1.23-1.18 (m, 3H), 0.86-0.82 (m, 12H). MS m/z (M+H): 553.1.
Ejemplo 89
Síntesis de (10R)-3-((2-cloro-5-((2-(metoximetil)pirrolidin-1-il)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-89)
A una suspensión agitada de INT-6 (100 mg, 0,3 mmol) en DMF anhidra (10 ml) se añadió t-BuOK (1 M en THF, 0,7 ml, 0,7 mmol) a 0° C, gota a gota, para dar una solución marrón. La solución resultante se agitó durante 10
min más a temperatura ambiente. Se añadió gota a gota INT-78 (184 mg, 0,6 mmol) en DMF (2 ml) a la solución anterior y se agitó 4 h a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4., se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-89 (72,5 mg, 38,6%) como una mezcla 1:1 de diastereómeros. 1H NMR (400 MHz, DMSO-d6) 59.35 (d, J=9.1 Hz, 1H), 8.70 (s, 1H), 8.25 8.09 (m, 2H), 7.84 (d, J=8.8 Hz, 1H), 7.59 (d, J=9.2 Hz, 1H), 7.16 (t, J=5.2 Hz, 1H), 4.17 (d, J=14.8 Hz, 1H), 3.70 3.55 (m, 2H), 3.52-3.34 (m, 3H), 3.30-3.17 (m, 4H), 3.10-2.95 (m, 1H), 2.90-2.75 (m, 1H), 2.50-2.25 (m, 1H), 2.00 1.80 (m, 1H), 1.75-1.59 (m, 2H), 1.57-1.40 (m, 1H), 1.19 (d, J=6.8 Hz, 3H) MS m/z (M+H): 539.2.
Ejemplo 90
Síntesis de (R)-3-((2-cloro-5-(((2-metox¡et¡l)(met¡l)am¡no)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-90)
A una suspensión agitada de INT-6 (72 mg, 0,24 mmol) en DMF anhidra (5 ml) se le añadió t-BuOK (1 M en THF, 0,48 ml, 0,48 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-79 (120 mg, 0,48 mmol) en DMF (1 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (20 ml) y agua (30 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). La capa orgánica combinada se lavó con salmuera (50 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-90 (36,9 mg, 28,4%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6) 59.35 (d, J=9.0 Hz, 1H), 8.71 (s, 1H), 8.19-8.13 (m, 2H), 7.84 (d, J=9.0 Hz, 1H), 7.60 (d, J=9.0 Hz, 1H), 7.17-7.13 (m, 1H), 3.71 (s, 2H), 3.51-3.49 (m, 1H), 3.48-3.46 (m, 4H), 3.23 (s, 3H), 2.74-2.59 (m, 2H), 2.30 (s, 3H), 1.19 (d, J=6.6 Hz, 3H). MS m/z (M+H): 513.0.
Ejemplo 91
Síntesis de (R)-3-((2-cloro-5-((isopropil(metil)amino)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-91)
A una suspensión agitada de INT-6 (39,9 mg, 0,13 mmol) en DMF anhidra (4 ml) se le añadió t-BuOK (1 M en THF, 0,26 ml, 0,26 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-70 (62 mg, 0,26 mmol) en DMF (1 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (5 ml) y agua (5 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 5 ml). Las capas orgánicas combinadas se lavaron con salmuera (10 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-91 (19 mg, 29%) como un sólido amarillo. 1H-NMR (400 MHz, DMSO-d6): 59.36 (d, J=9.2 Hz, 1H), 8.68 (s, 1H), 8.19-8.14 (m, 2H), 7.85 (d, J=8.8 Hz, 1H), 7.60 (d, J=9.2 Hz, 1H), 7.17-7.15 (m, 1H), 3.65-3.61 (m, 3H), 3.48-3.46 (m, 2H), 2.94-2.87 (m, 1H), 2.18 (s, 3H), 1.19 (d, J=6.8 Hz, 3H), 1.03 (d, J=6.4 Hz, 6H). MS m/z (M+H): 497.0.
Ejemplo 92
Síntesis de (R)-3-((2-cloro-5-((ciclohexil(metil)amino)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-92)
A una suspensión agitada de INT-6 (198 mg, 0,66 mmol) en DMF anhidra (15 ml) se le añadió t-BuOK (1 M en THF, 1,3 ml, 1,32 mmol) a 0° C gota a gota para dar una solución marrón y la solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-72 (199,5 mg, 0,73 mmol) en DMF (5 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (20 ml) y agua (30 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). La capa orgánica combinada se lavó con salmuera (50 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó el producto deseado I-92 (19,4 mg, 9,7%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.35 (d, J=8.0 Hz, 1H), 8.67 (s, 1H), 8.19-8.14 (m, 2H), 7.84 (d, J=8.8 Hz, 1H), 7.59 (d, J=8.8 Hz, 1H), 7.18-7.15 (m, 1H), 3.71 (s, 2H), 3.62-3.61 (m, 1H), 3.48-3.47 (m, 2H), 2.46-2.44 (m, 1H), 2.24 (s, 3H), 1.81 -1.71 (m, 4H), 1.32-1.15 (m, 9H). MS m/z (M+H): 537.4. Ejemplo 93
Síntesis de (R)-3-((2-cloro-5-((4-metoxipiperidin-1-il)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-93)
A una suspensión agitada de INT-6 (90 mg, 0,3 mmol) en DMF anhidra (9 ml) se le añadió t-BuOK (1 M en THF, 0,6 ml, 0,6 mmol) a 0° C gota a gota para dar una solución marrón y la solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-73 (166,1 mg, 0,6 mmol) en DMF (2 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-93 (43,5 mg, 26,2%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6) 59.35 (d, J=9.0 Hz, 1H), 8.69 (s, 1H), 8.19-8.14 (m, 2H), 7.84 (d, J=9.0 Hz, 1H), 7.60 (d, J=9.0 Hz, 1H), 7.18-7.15 (m, 1H), 3.64 (s, 3H), 3.61-3.46 (m, 2H), 3.22-3.15 (m, 4H), 2.77-2.75 (m, 2H), 2.27-2.20 (m, 2H), 1.86-1.72 (m, 2H), 1.51-1.40 (m, 2H), 1.20 (d, J=6.6 Hz, 3H). MS m/z (M+H): 539.0.
Ejemplo 94
Síntesis de (R)-3-((2-cloro-5-((4-etilpiperazin-1-il)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-94)
A una suspensión agitada de INT-6 (80 mg, 0,27 mmol) en DMF anhidra (8 ml) se le añadió t-BuOK (1 M en THF, 0,54 ml, 0,54 mmol) a 0° C gota a gota para dar una solución marrón y la solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-74 (147,1 mg, 0,54 mmol) en DMF (2 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de
etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-94 (38,9 mg, 26,7%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6) 59.31 (d, J=9.0 Hz, 1H), 8.69 (s, 1H), 8.20-8.14 (m, 2H), 7.84 (d, J=9.0 Hz, 1H), 7.61 (d, J=9.0 Hz, 1H), 7.18-7.16 (m, 1H), 3.66-3.62 (m, 2H), 3.47-3.45 (m, 2H), 2.49 2.27 (m, 10H), 1.19 (d, J=6.6 Hz, 3H), 0.99 (br s, 3H). MS m/z (M+H): 538.1.
Ejemplo 95
Síntesis de (R)-3-((2-cloro-5-((3,3-d¡met¡lp¡per¡d¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-95)
A una suspensión agitada de INT-6 (115 mg, 0,38 mmol) en DMF anhidra (15 ml) se le añadió t-BuOK (1 M en THF, 0,76 ml, 0,76 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-80 (115,8 mg, 0,42 mmol) en DMF (5 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-95 (33,5 mg, 29,1%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.33 (d, J=9.2 Hz, 1H), 8.67 (s, 1H), 8.17-8.12 (m, 2H), 7.82 (d, J=8.8 Hz, 1H), 7.56 (d, J=9.2 Hz, 1H), 7.15-7.13 (m, 1H), 3.60-3.58 (m, 3H), 3.58-3.41 (m, 2H), 2.39-2.31 (m, 2H), 2.14-2.06 (m, 2H), 1.56-1.52 (m, 2H), 1.20-1.13 (m, 5H), 0.90 (s, 6H). MS m/z (M+H): 537.0. Ejemplo 96
Síntes¡s de (R)-3-((2-cloro-5-(metox¡met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-96)
A una suspensión agitada de INT-6 (203,3 mg, 0,68 mmol) en DMF anhidra (17 ml) se le añadió t-BuOK (1 M en THF, 1,36 ml, 1,36 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó
durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-63 (262,2 mg, 1,36 mmol) en DMF (3 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (40 ml) y agua (50 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 40 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-96 (110,4 mg, 35,5%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.37 (d, J=9.2 Hz, 1H), 8.72 (s, 1H), 8.19 (d, J=8.8 Hz, 1H), 8.14 (d, J=4.4 Hz, 1H), 7.87 (d, J=8.8 Hz, 1H), 7.64 (d, J=9.2 Hz, 1H), 7.18-7.16 (m, 1H), 4.62 (s, 2H), 3.62-3.61 (m, 1H), 3.51 -3.47 (m, 2H), 3.42 (s, 3H), 1.19 (d, J=6.8 Hz, 3H). MS m/z (M+H): 455.9.
Ejemplo 97
Síntesis de (R)-3-((5-(terc-butox¡met¡l)-2-clorop¡r¡m¡d¡n-4-il)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-97)
A una solución agitada de INT-6 (100 mg, 0,3 mmol) en DMF (10 ml) se le añadió t-BuOK (1 M en THF, 0,7 ml, 0,7 mmol) a 0° C gota a gota para dar una solución marrón que se agitó durante 10 min. Se añadió gota a gota INT-56 (157 mg, 0,7 mmol) en DMF (2 ml) a la solución anterior y se agitó durante 2 h a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (50 ml) y agua (50 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 50 ml). Las capas orgánicas combinadas se lavaron con salmuera (100 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-97 (70,4 mg, 42,2%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 5 9.35 (d, J=9.2 Hz, 1H), 8.69 (s, 1H), 8.21-8.10 (m, 2H), 7.85 (d, J=8.8 Hz, 1H), 7.61 (d, J=9.2 Hz, 1H), 7.17-7.14 (m, 1H), 4.59 (s, 2H), 3.70-3.55 (m, 1H), 3.54-3.38 (m, 2H), 1.25 (s, 9H), 1.18 (d, J=6.8 Hz, 3H). MS m/z (M+H): 498.1. Ejemplo 98
Síntes¡s de (R)-3-((2-cloro-5-(((tetrah¡dro-2H-p¡ran-4-¡l)ox¡)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-98)
A una suspensión agitada de INT-6 (170 mg, 0,57 mmol) en DMF anhidra (17 ml) se le añadió t-BuOK (1 M en THF, 1,14 ml, 1,14 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-67 (179,3 mg, 0,68 mmol) en DMF (2 ml) a la
solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (40 ml) y agua (50 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 40 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-98 (78,9 mg, 26,1%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.37 (d, J=9.0 Hz, 1H), 8.75 (s, 1H), 8.20 8.14 (m, 2H), 7.86 (d, J=9.0 Hz, 1H), 7.63 (d, J=9.0 Hz, 1H), 7.18-7.16 (m, 1H), 4.73 (s, 2H), 3.86-3.81 (m, 2H), 3.74 3.70 (m, 1H), 3.63-3.61 (m, 1H), 3.49-3.47 (m, 2H), 3.38-3.34 (m, 2H), 1.96-1.92 (m, 2H), 1.55-1.46 (m, 2H), 1.20 (d, J=6.6 Hz, 3H). MS m/z (M+H): 526.2.
Ejemplo 99
Síntesis de (R)-3-((2-cloro-5-(((R)-2-met¡lp¡rrol¡d¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-99)
A una solución agitada de INT-6 (100 mg, 0,3 mmol) en DMF (10 ml) se le añadió t-BuOK (1 M en THF, 0,7 ml, 0,7 mmol) a 0° C gota a gota para dar una solución marrón y la reacción se agitó durante 10 min. Se añadió gota a gota INT-81 (90 mg, 0,4 mmol) en DMF (2 ml) a la solución anterior y la reacción se agitó 4 h a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (20 ml) y agua (50 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-99 (16,5 mg, 9,3%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds) 59.33 (d, J=9.1 Hz, 1H), 8.67 (s, 1H), 8.23-8.09 (m, 2H), 7.83 (d, J=9.2 Hz, 1H), 7.68-7.55 (m, 1H), 7.20 7.10 (m, 1H), 4.02 (d, J=14.8 Hz, 1H), 3.70-3.55 (m, 1H), 3.54-3.38 (m, 3H), 3.05-2.90 (m, 1H), 2.56-2.50 (m, 1H), 2.30-2.15 (m, 1H), 2.00-1.85 (m, 1H), 1.70-1.55 (m, 2H), 1.40-1.22 (m, 1H), 1.18 (d, J=6.8 Hz, 3H), 1.09 (d, J=6.0 Hz, 3H) MS m/z (M+H): 509.1.
Ejemplo 100
Síntes¡s de (R)-3-((2-cloro-5-((2-fluoroetox¡)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-100)
A una suspensión agitada de INT-6 (444. mg, 1,48 mmol) en DMF anhidra (40 ml) se le añadió t-BuOK (1 M en THF, 3 ml, 3 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-65 (400,6 mg, 1,8 mmol) en DMF (2 ml) a la solución anterior y la reacción se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (60 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (60 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-100 (187,5 mg, 25,9%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6) 59.37 (d, J=9.0 Hz, 1H), 8.74 (s, 1H), 8.21-8.11 (m, 2H), 7.86 (d, J=9.0 Hz, 1H), 7.63 (d, J=9.0 Hz, 1H), 7.18-7.14 (m, 1H), 4.75 (s, 2H), 4.70 (t, J=3.9 Hz, 1H), 4.54 (t, J=3.9 Hz, 1H), 3.90 (t, J=3.9 Hz, 1H), 3.80 (t, J=3.9 Hz, 1H), 3.62-3.46 (m, 3H), 1.19 (d, J=6.6 Hz, 3H). MS m/z (M+H): 488.0.
Ejemplo 101
Síntesis de (R)-3-((2-cloro-5-(((S)-2-met¡lp¡rrol¡d¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]diazep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-8-ona (I-101)
A una solución agitada de INT-6 (100 mg, 0,3 mmol) en DMF (10 ml) se le añadió t-BuOK (1 M en THF, 0,7 ml, 0,7 mmol) a 0° C gota a gota para dar una solución marrón y la reacción se agitó durante 10 min. Se añadió gota a gota INT-82 (164 mg, 0,6 mmol) en DMF (2 ml) a la solución anterior y se agitó 4 h a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (20 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). Las capas orgánicas combinadas se lavaron con salmuera (100 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-101 (32,0 mg, 18,1%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 5 9.33 (d, J=9.1 Hz, 1H), 8.67 (s, 1H), 8.23-8.09 (m, 2H), 7.83 (d, J=8.8 Hz, 1H), 7.68-7.55 (m, 1H), 7.20-7.10 (m, 1H), 4.02 (d, J=14.4 Hz, 1H), 3.68-3.55 (m, 1H), 3.54-3.37 (m, 3H), 3.05-2.90 (m, 1H), 2.56-2.50 (m, 1H), 2.30-2.15 (m, 1H), 2.00-1.85 (m, 1H), 1.71-1.55 (m, 2H), 1.40-1.22 (m, 1H), 1.18 (d, J=6.8 Hz, 3H), 1.09 (d, J=6.0 Hz, 3H) MS m/z (M+H): 509.1.
Ejemplo 102
Síntesis de (R)-3-((5-((terc-butilamino)metil)-2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-102)
A una suspensión de INT-6 (77 mg, 0,256 mmol) en DMF (5 ml) a temperatura ambiente se le añadió carbonato de potasio (283 mg, 2,050 mmol). La mezcla se desgasificó por evacuación y se volvió a llenar con N2 (3x). La mezcla se calentó a 90° C durante 10 min y luego se añadió mediante una jeringuilla una solución de INT-88 (78 mg, 0,333 mmol) en DMF (2 ml). Después de 1 h a 90° C se completó la reacción. La mezcla de la reacción se filtró y se diluyó con agua y toda la masa de reacción se purificó directamente mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) para dar I-102 (136 mg, 0,223 mmol, 87% de rendimiento) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.41 (d, J=9.2 Hz, 1H), 8.96 (br, 2H), 8.85 (s, 1H), 8.23 (d, J=8.7 Hz, 1H), 8.18 (d, J=4.6 Hz, 1H), 7.87 (d, J=8.7 Hz, 1H), 7.64 (d, J=9.2 Hz, 1H), 7.18 (br, 1H), 4.36 (br, 2H) 3.80-3.48 (m, 4H), 1.42 (s, 9H), 1.19 (d, J=6.9 Hz, 3H). MS m/z (M+H): 497.1.
Ejemplo 103
Síntesis de (R)-3-((2-cloro-5-(((3-metiloxetan-3-il)oxi)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-103)
A una suspensión agitada de INT-6 (251 mg, 0,84 mmol) en DMF anhidra (15 ml) se le añadió t-BuOK (1 M en THF, 1,68 ml, 1,68 mmol) a 0° C gota a gota para dar una solución marrón y la solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-61 (190 mg, 0,76 mmol) en DMF (5 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-103 (53,1 mg, 27,9%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6): 59.37 (d, J=9.0 Hz, 1H), 8.79 (s, 1H), 8.21-8.13 (m, 2H), 7.87 (d, J=9.0 Hz, 1H), 7.64 (d, J=9.0 Hz, 1H), 7.18-7.15 (m, 1H), 4.67-4.65 (m, 4H), 4.37 (d, J=6.0 Hz, 2H), 3.62-3.61 (m, 1H), 3.47-3.46 (m, 2H), 1.59 (s, 3H), 1.24-1.18 (m, 3H). MS m/z (M+H): 512.1.
Ejemplo 104
Síntesis de (R)-3-((5-((terc-but¡l(met¡l)am¡no)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]diazep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-8-ona (I-104)
A una solución agitada de INT-6 (100 mg, 0,3 mmol) en DMF (10 ml) se le añadió NaH (33 mg, 0,8 mmol) a 0° C y se agitó durante 2 h. Se añadió gota a gota INT-58 (86 mg, 0,4 mmol) en DMF (2 ml) a la solución anterior y luego se calentó a 135° C durante 70 min con irradiación de microondas. La mezcla de la reacción se enfrió y se repartió entre acetato de etilo (50 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 50 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml), se secaron sobre Na2SÜ4, se filtraron y se concentraron a presión reducida. La purificación por HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) proporcionó I-104 (21,4 mg, 13,3%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.31 (d, J=9.2 Hz, 1H), 8.76 (s, 1H), 8.68 (s, 1H), 8.20-8.09 (m, 2H), 7.78 (d, J=8.8 Hz, 1H), 7.49 (d, J=9.2 Hz, 1H), 7.13-7.11 (m, 1H), 3.70-3.52 (m, 3H), 3.50-3.38 (s, 2H), 2.25-2.13 (m, 5H), 1.90-1.75 (m, 1H), 1.18 (d, J=6.8 Hz, 3H), 0.85 (d, J=6.4 Hz, 6H). MS m/z (M+H): 477.2.
Ejemplo 105
Síntes¡s de (R)-3-((2-cloro-6,6-d¡óx¡do-7,8-d¡h¡dro-5H-t¡op¡rano[4,3-d]p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-105)
Se suspendió INT-6 (50 mg, 0,167 mmol) en 10 ml de DMF seca y el recipiente se enjuagó abundantemente con nitrógeno. Se añadió carbonato de potasio (0,231 g, 1,670 mmol) y la reacción se calentó a 90° C durante 10 min. A esta mezcla, se le añadió 6 ,6-dióxido de 2,4-dicloro-7,8-dihidro-5H-tiopirano[4,3-d]pirimidina (51
mg, 0,200 mmol) y la reacción se agitó durante 1 hora más a 90° C. La reacción se consideró completa por LC/MS, se vertió en NH4Cl saturado (ac.) y se extrajo 3 veces con DCM. El DCM combinado se secó sobre sulfato de sodio, se filtró y se concentró. Luego, el material bruto se purificó mediante HPLC de fase inversa para proporcionar I-105 (4 mg, 7,75 pmol, rendimiento del 4,64%). 1H NMR (400 MHz, DMSO-d6): 59.31 (d, J=9.2 Hz, 1H), 8.14 (d, J=8.4 Hz, 1H), 8.09 (d, J=4.5 Hz, 1H), 7.80 (d, J=8.7 Hz, 1H), 7.57 (d, J=8.7 Hz, 1H), 3.62 (t, J=6.9 Hz, 2H), 3.57 (m, 1H), 3.38 (m, 4H), 1.12 (d, J=6.9 Hz, 3H). MS m/z (M+H): 516.0.
Ejemplo 106
Síntesis de (R)-3-((2-cloro-5-(((S)-3-metox¡p¡per¡d¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-il)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]diazep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-8-ona (I-106)
A una suspensión agitada de INT-6 (90 mg, 0,3 mmol) en DMF anhidra (9 ml) se le añadió t-BuOK (1 M en THF, 0,6 ml, 0,6 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 h más a esta temperatura. Se añadió gota a gota INT-85 (166 mg, 0,6 mmol) en DMF (2 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-106 (4,0 mg, 2,5%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds) 59.34 (d, J=9.2 Hz, 1H), 8.67 (s, 1H), 8.17-8.12 (m, 2H), 7.82 (d, J=8.8 Hz, 1H), 7.58 (d, J=9.2 Hz, 1H), 7.16-7.14 (m, 1H), 3.66-3.52 (m, 3H), 3.47-3.44 (m, 2H), 3.23-3.20 (m, 4H), 2.98-2.95 (m, 1H), 2.70-2.67 (m, 1H), 2.11-2.06 (m, 1H), 2.01-1.96 (m, 1H), 1.86-1.89 (m, 1H), 1.67-1.62 (m, 1H), 1.45-1.36 (m, 1H), 1.21-1.12 (m, 4H). MS m/z (M+H): 539.2.
Ejemplo 107
Síntesis de (R)-3-((2-cloro-5-(((R)-3-metoxipiperidin-1-il)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-107)
A una suspensión agitada de INT-6 (90 mg, 0,3 mmol) en DMF anhidra (9 ml) se le añadió t-BuOK (1 M en THF, 0,6 ml, 0,6 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 h adicionales a esta temperatura. Se añadió gota a gota INT-86 (166 mg, 0,6 mmol) en DMF (2 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-107 (56,3 mg, 33,6%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.34 (d, J=9.2 Hz, 1H), 8.68 (s, 1H), 8.17-8.12 (m, 2H), 7.82 (d, J=8.8 Hz, 1H), 7.58 (d, J=9.2 Hz, 1H), 7.16-7.14 (m, 1H), 3.66 (s, 1H), 3.62-3.57 (m, 3H), 3.47-3.44 (m, 2H), 3.23-3.20 (m, 4H), 2.98-2.95 (m, 1H), 2.70-2.67 (m, 1H), 2.11-2.06 (m, 1H), 2.01-1.96 (m, 1H), 1.86-1.89 (m, 1H), 1.67-1.62 (m, 1H), 1.45-1.36 (m, 1H), 1.21-1.12 (m, 4H). MS m/z (M+H): 539.1.
Ejemplo 108
Síntesis de (R)-3-((2-cloro-5-(((2-etoxietil)(metil)amino)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-108)
A una suspensión agitada de INT-6 (400 mg, 1,34 mmol) en DMF anhidra (35 ml) se le añadió t-BuOK (1 M en THF, 2,67 ml, 2,67 mmol) a 0° C para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-87 (271,4 mg, 1,34 mmol) en DMF (5 ml) a la solución anterior y la reacción se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-108 (36,9 mg, 13,6%) como un sólido amarillo.1H NMR (400 MHz, DMSO-d6): 59.33 (d, J=9.2 Hz, 1H), 8.17-8.11 (m, 2H), 7.83 (d, J=8.8 Hz, 1H), 7.58 (d, J=9.2 Hz, 1H), 7.16-7.13 (m, 1H), 3.60-3.59 (m, 1H), 3.50-3.40 (m, 2H), 2.80-2.79 (m, 2H), 2.74-2.71 (m, 2H), 1.84-1.83 (m, 4H), 1.17 (d, J=9.2 Hz, 3H). MS m/z (M+H): 466.0.
Ejemplo 109
Síntesis de (R)-3-((2-cloro-5,6,7,8-tetrahidroquinazolin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-109)
A una suspensión agitada de INT-6 (339 mg, 1,13 mmol) en DMF anhidra (25 ml) se le añadió t-BuOK (1 M en THF, 2,26 ml, 2,26 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota 2,4-dicloro-5,6,7,8-tetrahidroquinazolina (299,1 mg, 1,13 mmol) en DMF (5 ml) a la solución anterior y la reacción se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-109 (87,4 mg, 29,2%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.34 (d, J=9.2 Hz, 1H), 8.71 (s, 1H), 8.18-8.11 (m, 2H), 7.83 (d, J=9.2 Hz, 1H), 7.58 (d, J=9.2 Hz, 1H), 7.10-7.20 (m, 1H), 3.70 (s, 2H), 3.60-3.50 (m, 1H), 3.52-3.36 (m, 6H), 2.63-2.60 (m, 2H), 2.29 (s, 3H), 1.17 (d, J=7.8 Hz, 3H), 1.06 (t, J=7.8 Hz, 3H). MS m/z (M+H): 527.0.
Ejemplo 110
Síntesis de (R)-3-((2-cloro-5-((2,2-difluoroetoxi)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-110)
A una suspensión agitada de INT-6 (154,4 mg, 0,52 mmol) en DMF anhidra (30 ml) se le añadió t-BuOK (1 M en THF, 0,5 ml, 0,88 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-62 (150,4 mg, 0,62 mmol) en DMF (2 ml) a la solución anterior y la reacción se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (20 ml) y agua (30 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). Las capas orgánicas combinadas se lavaron con salmuera (40 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-110 (70,0 mg, 26,8%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6): 59.37 (br d, J=9.0 Hz, 1H), 8.74 (s, 1H), 8.19 (d, J=9.0 Hz, 1H), 8.13 (d, J=4.2 Hz, 1H), 7.86 (d, J=9.0 Hz, 1H), 7.62 (d, J=9.0 Hz, 1H), 7.16 (br t, J=4.8 Hz, 1H), 6.45-6.42 (m, 1H), 4.82 (s, 2H), 3.96-3.84 (m, 2H), 3.65-3.56 (m, 1H), 3.47 (t, J=4.5 Hz, 2H), 1.19 (d, J=6.6 Hz, 3H). MS m/z (M+H): 506.0.
Ejemplo 111
Síntesis de (R)-3-((2-cloro-4-((10-metil-8-oxo-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]quinolin-3-il)oxi)pirimidin-5-il)metoxi)propanonitrilo (I-111)
A una suspensión agitada de INT-6 (120 mg, 0,4 mmol) en DMF anhidra (12 ml) se le añadió t-BuOK (1M en THF, 0,8 ml, 0,8 mmol) gota a gota a 0° C para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-68 (186 mg, 0,8 mmol) en DMF (2 ml) a la solución anterior y la reacción se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 30 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-111 (55,9 mg, 27,6%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.35 (d, J=9.0 Hz, 1H), 8.73 (s, 1H), 8.19 8.12 (m, 2H), 7.85 (d, J=8.8 Hz, 1H), 7.62 (d, J=9.0 Hz, 1H), 7.16-7.14 (m, 1H), 4.75 (s, 2H), 3.77 (t, J=6.0 Hz, 2H)), 3.60-3.59 (m, 1H), 3.49-3.45 (m, 2H), 2.88-2.85 (m, 2H), 1.18 (d, J=6.8 Hz, 3H). MS m/z (M+H): 495.1.
Ejemplo 112
Síntesis de (R)-3-((2-cloro-5-((metilsulfonil)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-112)
Se disolvió INT-6 (0,207 g, 0,692 mmol) en 2 ml de DMF seca y se añadió K2CO3 (0,956 g, 6,92 mmol). La reacción se calentó a 90° C durante 5 min, se enfrió y se añadió INT-54 (0,250 g, 1,038 mmol) en DMSO. La reacción se agitó a 90° C durante 3 h, momento en el que se determinó que la reacción se había completado. Se enfrió la reacción y se filtró el exceso de base. La mezcla de la reacción bruta se purificó mediante HPLC de fase inversa para dar I-112 (0,105 g, 0,208 mmol, 30% de rendimiento). 1H NMR (400 MHz, DMSO-d6): 59.34 (d, J=8.2 Hz, 1H), 8.75 (s, 1H), 8.18 (d, J=8.7 Hz, 1H), 8.14 (d, J=2.8 Hz, 1H), 7.85 (d, J=8.7 Hz, 1H), 7.58 (d, J=9.2 Hz, 1H), 7.16 (t, J=5.5 Hz, 1H), 4.75 (s, 2H), 3.59 (m, 1H), 3.44 (m, 2H), 3.17 (s, 3H), 1.16 (d, J=6.9 Hz, 3H). MS m/z (M+H):
504.0.
Ejemplo 113
Síntesis de (R)-3-((2-cloro-5-((d¡fluorometox¡)met¡l)p¡rim¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-113)
A una suspensión agitada de INT-6 (109,0 mg, 0,36 mmol) en DMF anhidra (10 ml) se le añadió t-BuOK (1 M en THF, 0,62 ml, 0,62 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-55 (100,1 mg, 0,42 mmol) en DMF (2 ml) a la solución anterior y la reacción se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (10 ml) y agua (10 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 10 ml). Las capas orgánicas combinadas se lavaron con salmuera (10 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. El bruto se pasó a través de gel de sílice (DCM/MeOH 30:1) para producir I-113 (13,4 mg, 7,48%) como un sólido amarillo. 1H NmR (400 MHz, DMSO-d6): 5 9.34 (d, J=8.7 Hz, 1H), 8.78 (s, 1H), 8.18-8.09 (m, 2H), 7.84 (d, J=9.0 Hz, 1H), 7.59 (d, J=9.0 Hz, 1H), 7.13-6.62 (m, 2H), 5.09 (s, 2H), 3.57-3.56 (m, 1H), 3.50-3.49 (m, 2H), 1.15 (d, J=6.0 Hz, 3H). MS m/z (M+H): 492.2.
Ejemplo 114
Síntes¡s de (R)-3-((5-((3-oxa-8-azab¡c¡clo[3.2.1]octan-8-¡l)met¡l)-2-clorop¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-114)
A una suspensión agitada de INT-6 (120,0 mg, 0,40 mmol) en DMF anhidra (12 ml) se le añadió t-BuOK (1 M en THF, 0,8 ml, 0,8 mmol) gota a gota a 0° C para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-83 (131,9 mg, 0,48 mmol) en DMF (3 ml) a la solución anterior y la reacción se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (30 ml) y agua (40 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 40 ml). Las capas orgánicas combinadas se lavaron con salmuera (80 ml) y la capa orgánica se
separó, se secó sobre Na2SÜ4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-114 (40,9 mg, 19%) como una mezcla de diastereoisómeros. 1H NMR (300 MHz, DMSO-d6) 59.31 (d, J=9.0 Hz, 1H), 8.80 (s, 1H), 8.15-8.08 (m, 2H), 7.80 (d, J=9.0 Hz, 1H), 7.57 (d, J=9.0 Hz, 1H), 7.12-7.09 (m, 1H), 3.58-3.54 (m, 5H), 3.45-3.39 (m, 4H), 3.11-3.09 (m, 2H), 1.94-1.90 (m, 2H), 1.76-1.72 (m, 2H), 1.15 (d, J=6.6 Hz, 3H). MS m/z (M+H): 537.0.
Ejemplo 115
Síntesis de (R)-3-((2-cloro-5-(((3R,5S)-3,5-d¡met¡lp¡peraz¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]tieno[3,2-f]qu¡nol¡n-8-ona (I-115)
A una solución agitada de INT-6 (215,37 mg, 0,720 mmol) en DMF (30 ml) se le añadió t-BuOK (1 M en THF) (0,96 ml, 0,960 mmol) a 0° C y la reacción se agitó a esta temperatura durante 20 minutos para dar una solución marrón. Luego se añadió INT-84 (360 mg, 0,96 mmol) a la mezcla de la reacción a 0° C, se calentó a temperatura ambiente y se dejó en agitación durante la noche. La mezcla de la reacción se diluyó con agua, la capa acuosa se extrajo con acetato de etilo (3 x 50 ml) y el extracto orgánico se lavó con 2 x 20 ml de solución de salmuera saturada. La capa orgánica se secó sobre sulfato de sodio, se filtró y luego se concentró. El material bruto se filtró a través de gel de sílice eluyendo con acetato de etilo para obtener (2R,6S)-4-((2-cloro-4-(((R)-10-metil-8-oxo-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-3-il)oxi)pirimidin-5-il)metil)-2,6-dimetilpiperazin-1-carboxilato de terc-butilo (180 mg, 29%) como un sólido amarillo. A este material (100,0 mg, 0,16 mmol) disuelto en DCM, se le añadió TFA (1,0 ml, 0,16 mmol) y la reacción se agitó a temperatura ambiente durante 1 minuto. La mezcla se inactivó con NaHCO3 acuoso saturado (10 ml) seguido de extracción con acetato de etilo (3 x 30 ml). Los extractos orgánicos combinados se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron al vacío. La purificación adicional mediante TLC preparativa sobre gel de sílice (DCM: MeOH = 4:1) proporcionó I-115 (67 mg, 65,5%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.35 (d, J=9.0 Hz, 1H), 8.71 (s, 1H), 8.20-8.12 (m, 2H), 7.82 (d, J=8.8 Hz, 1H), 7.58 (d, J=9.2 Hz, 1H), 7.16-7.14 (m, 1H), 3.66-3.52 (m, 3H), 3.49-3.41 (m, 2H), 3.11-2.79 (m, 4H), 1.91-1.75 (m, 2H), 1.22-1.17 (m, 4H), 1.02 (d, J=5.6 Hz, 6H). MS m/z (M+H): 538.1.
Ejemplo 116
Síntesis de (R)-3-((5-bromo-2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-116)
Se suspendió INT-6 (1,6 g, 5,34 mmol) en 20 ml de DMF seca. Se añadió K2CO3 (7,39 g, 53,4 mmol) y la reacción se lavó abundantemente con nitrógeno. La reacción se calentó a 90° C durante 10 minutos, se enfrió y se añadió 5-bromo-2,4-dicloropirimidina (1,583 g, 6,95 mmol). La reacción se calentó de nuevo a 90° C durante 4 h más. La reacción se enfrió, se filtró para eliminar cualquier base no disuelta y luego se vertió en agua (200 ml). El precipitado resultante se recogió por filtración y se secó a presión reducida para proporcionar I-116 (1,922 g, 3,92 mmol, 73,3% de rendimiento) como un sólido amarillo. 1H NMR (400 MHz, DMsO-d6): 59.39 (d, J=9.6 Hz, 1H), 9.03 (s, 1H), 8.21 (d, J=8.7 Hz, 1H), 8.16 (d, J=4.1 Hz, 1H), 7.87 (d, J=9.2 Hz, 1H), 7.71 (d, J=9.2 Hz, 1H), 7.18 (t, J=5.5 Hz, 1H), 3.61 (m, 1H), 3.46 (m, 2H), 1.19 (d, J=6.9 Hz, 3H).
Ejemplo 117
Síntesis de (R)-3-((6-((terc-butilamino)metil)-2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-117)
Se disolvieron t-butilamina (0,019 ml, 0,363 mmol), yoduro de sodio (0,272 g, 1,814 mmol) y (R)-INT-93 (0,167 g, 0,363 mmol) en 3 ml de DMF seca. La reacción se agitó a temperatura ambiente durante 8 horas. Una vez completada, la reacción se filtró para eliminar el exceso de sales y se purificó directamente mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) para dar I-117. 1H NMR (400 MHz, DMSO-d6): 5 9.40 (d, J=9.2 Hz, 1H), 9.10 (t, J=6.0 Hz, 1H), 8.20 (d, J=9.2 Hz, 1H), 8.16 (d, J=4.1 Hz, 1H), 7.82 (d, J=9.2 Hz, 1H), 7.63 (d, J=9.2 Hz, 1H), 7.51 (s, 1H), 7.16 (m, 1H), 4.39 (t, J=4.0 Hz, 2H), 3.59 (m, 1H), 3.44 (m, 2H), 1.33 (s, 9H), 1.17 (d, J=6.9 Hz). MS m/z (M+H): 484.1.
Ejemplo 118
Síntesis de (R)-3-((6-((terc-butil(metil)amino)metil)-2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-118)
Se disolvieron 1-117 (0,025 g, 0,050 mmol) y formaldehído (37% ac.) (0,011 ml, 0,151 mmol) en 3 ml de THF, 1 ml de MeOH y 0,1 ml de ácido acético. A esta mezcla se le añadió triacetoxiborohidruro de sodio (0,053 g, 0,252 mmol). La reacción se agitó durante 2 h a temperatura ambiente, se concentró hasta la sequedad y se volvió a disolver en 3 ml de DMSO con 1 ml de H2O y se purificó directamente mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1%de TFA) para dar I-118. 1H NMR (400 MHz, DMSO-d6): 59.62 (br, 1H), 9.40 (d, J=9.2 Hz, 1H), 8.20 (d, J=8.7 Hz), 8.16 (d, J=4.1 Hz, 1H), 7.83 (d, J=9.2 Hz, 1H), 7.63 (d, J=9.2 Hz, 1H), 7.59 (s, 1H), 7.17 (br, 1H), 4.69 (d, J=15.1 Hz, 1H), 4.27 (dd, J=13.3 Hz, 8.7 Hz, 1H), 3.60 (m, 1H), 3.45 (m, 2H), 2.72 (d, J=5.0 Hz, 3H), 1.41 (s, 9H), 1.17 (d, J=6.9 Hz, 3H). MS m/z (M+H): 511.1.
Ejemplo 119
Síntesis de (R)-3-((2-fluoro-5,7-dihidrofuro[3,4-d]pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-8-ona (I-119)
A una solución de I-86 (302 mg, 0,66 mmol) en DMSO (15 ml), se le añadió KF (383,3 mg, 6,6 mmol) a temperatura ambiente. La mezcla resultante se agitó a 110° C durante 2 h. La reacción se repartió entre acetato de etilo (20 ml) y agua (30 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). Las capas orgánicas combinadas se lavaron con salmuera (50 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) proporcionó el producto deseado I-119 (24,4 mg, 8,4%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-ds): 59.38 (d, J=9.3 Hz, 1H), 8.20 (d, J=9.0 Hz, 1H), 8.14-8.12 (m, 1H), 7.86 (d, J=8.7 Hz, 1H), 7.65 (d, J=8.7 Hz, 1H), 7.15-7.10 (m, 1H), 5.04 (s, 4H), 3.68-3.55 (m, 1H), 3.47-3.42 (m, 2H), 1.19 (d, J=6.6 Hz, 1H). MS m/z (M+H): 438.1.
Ejemplo 120
Síntesis de (R)-3-((5-((terc-butil(metil)amino)metil)-2-fluoropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-120)
A una solución de I-80 (80,0 mg, 0,16 mmol) en DMSO (6 ml), se añadió KF (90,8 mg, 1,57 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 110° C durante 2 h. La reacción se enfrió y luego se repartió entre acetato de etilo (20 ml) y agua (30 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). La capa orgánica combinada se lavó con salmuera (50 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) proporcionó el producto deseado, I-120 (10,4 mg, 12,8%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6): 59.35 (d, J=9.3 Hz, 1H), 8.70 (s, 1H), 8.18 (d, J=9.0 Hz, 1H), 8.15-8.11 (m, 1H), 7.84 (d, J=9.0 Hz, 1H), 7.61 (d, J=8.7 Hz, 1H), 7.17-7.15 (m, 1H), 3.70-3.65 (m, 3H), 3.47 3.41 (m, 2H), 2.18 (s, 3H), 1.19 (d, J=6.3 Hz, 3H), 1.13 (s, 9H). MS m/z (M+H): 495.2.
Ejemplo 121
Síntesis de (R)-3-((5-(etoximetil)-2-fluoropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-121)
A una solución de I-82 (180 mg, 0,38 mmol) en DMSO (15 ml), se le añadió KF (222,2 mg, 3,8 mmol) a temperatura ambiente. La mezcla de la reacción resultante se agitó a 110° C durante 2 h. La mezcla de la reacción se repartió entre acetato de etilo (20 ml) y agua (30 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 20 ml). La capa orgánica combinada se lavó con salmuera (50 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,1% de TFA) proporcionó el producto deseado, I-121 (49,2 mg, 26,9%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6): 59.33 (d, J=9.3 Hz, 1H), 8.72 (s, 1H), 8.19 (d, J=8.7 Hz, 1H), 8.09 8.07 (m, 1H), 7.86 (d, J=9.3 Hz, 1H), 7.64 (d, J=8.7 Hz, 1H), 7.14-7.05 (m, 1H), 4.67 (s, 1H), 3.64-3.62 (m, 3H), 3.47 3.41 (m, 2H), 1.23-1.18 (m, 6H). MS m/z (M+H): 454.1.
Ejemplo 122
Síntesis de (R)-3-((2-cloro-5-(1-metil-1,2,3,6-tetrahidropiridin-4-il)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-122)
A una solución de INT-95 en THF (2 ml) y metanol (1 ml) se le añadió ácido acético (10,45 pl, 0,183 mmol) y formaldehído (0,068 ml, 0,913 mmol) (37% en agua). Después de agitar durante 10 min, se añadió triacetoxiborohidruro de sodio (58,0 mg, 0,274 mmol). Después de 40 min, la mezcla de la reacción se enfrió a 0° C, se inactivó con NaHCO3 saturado acuoso, se extrajo con DCM-MeOH (4x, 9:1). Las capas orgánicas combinadas se secaron sobre Na2SO4, se filtraron y se concentraron. La purificación por HPLC (10-95% de MeCN/agua, 0,1% de TFA) dio I-122 (9,0 mg, 0,018 mmol, 19% de rendimiento). 1H NMR (400 MHz, DMSO-d6): 59.90 (br, 1H), 9.38 (d, J=9.2 Hz, 1H), 8.72 (s, 1H), 8.22-8.17 (m, 2H), 7.86 (d, J=9.2 Hz, 1H), 7.67 (d, J=9.2 Hz, 1H), 7.18 (t, J=5.3 Hz, 1H), 6.38 (s, 1H), 4.10-3.74 (m, 2H), 3.62-3.28 (m, 5H), 2.97-2.81 (m, 5H), 1.19 (d, J=6.9 Hz, 3H). MS m/z (M+H): 507.0.
Ejemplo 123
Síntesis de (R)-3-((2-cloro-5-(piridin-3-il)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-123)
A una suspensión de I-116 (30,1 mg, 0,062 mmol) en 1,4-dioxano anhidro (1,5 ml) se le añadió Pd(dppf)Cl2-CH2CI2 (0,12 ml, 5% en moles, 0,025 M en 1,4-dioxano anhidro) a temperatura ambiente para dar una solución en lechada marrón claro. Se añadió 3-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)piridina (15,2 mg, 0,074 mmol) en 1,4-dioxano anhidro (0,2 ml) a la solución resultante seguido de la adición de Cs2CO3 (0,1 ml, 1,0 M en agua). La mezcla resultante se desgasificó con nitrógeno y se agitó a 80° C en un agitador durante la noche. Después de enfriar a temperatura ambiente y eliminar los solventes, el residuo se disolvió en DMSO (3,0 ml) y se filtró. La solución filtrada se purificó mediante HPLC de fase inversa (ácido fórmico al 0,01% en agua-CH3CN) para proporcionar el producto deseado I-123 (6,1 mg, 20,6%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6) 59.34 (d, J=8.7 Hz, 1H), 8.97 (d, J=1.8 Hz, 1H), 8.94 (s, 1H), 8.66 (dd, J=4.8, 1.8 Hz, 1H), 8.21 (m, 1H), 8.16 (d, J=8.7 Hz, 1H), 8.13-8.14 (br, 1H), 7.82 (d, J=8.7 Hz, 1H), 7.71 (d, J=8.7 Hz, 1H), 7.58 (dd, J=8.2, 1.0 Hz, 1H), 7.17 (t, J=5.7 Hz), 3.57-3.60 (m, 1H), 3.45-3.46 (m, 2H), 1.19 (d, J=6.6 Hz, 3H). MS m/z (M+H): 489.4.
Ejemplo 124
Síntesis de (R)-3-((2-cloro-5-(3,6-dihidro-2H-piran-4-il)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (1-124)
Se disolvieron I-116 (180 mg, 0,367 mmol), 2-(3,6-dihidro-2H-piran-4-il)-4,4,5,5-tetrametil-1,3,2-dioxaborolano (154 mg, 0,733 mmol), PdCb(dppf) (0,027 g, 0,037 mmol) y carbonato de potasio (152 mg, 1,100 mmol) en 8 ml de DMF seca y se desgasificaron mediante evacuación/sonicación (2x) rellenando cada vez con argón. Luego, la reacción se calentó a 85° C con agitación. Una vez que se determinó que se hubo completado la reacción por LC/MS, la mezcla se enfrió, se vertió en agua y se extrajo 3 veces con DCM. Las capas orgánicas combinadas se secaron sobre sulfato de sodio, se filtraron y se concentraron. El residuo resultante se purificó mediante HPLC de fase inversa para proporcionar I-124 (16 mg, 0,032 mmol, rendimiento del 8,84%). 1H NMR (400 MHz, DMSO-ds) 59.34 (d, J=9.6 Hz, 1H), 8.69 (s, 1H), 8.17 (d, J=9.2 Hz, 1H), 9.34 (m, 1H), 7.84 (d, J=9.6 Hz, 1H), 7.65 (d, J=11 Hz, 1H), 7.17 (br, 1H), 6.43 (s, 1H), 4.23 (m, 1H), 4.06 (m, 1H), 3.79 (t, J=6.0 Hz, 1H), 3.60 (t, J=5.5 Hz, 1H), 3.45 (m, 1H), 2.03 (m, 1H), 1.19 (d, J=6.6 Hz, 3H).
Ejemplo 125
Síntesis de (R)-3-((2-cloro-5,6,7,8-tetrahidropirido[4,3-d]pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-125)
Se suspendió INT-6 (50 mg, 0,167 mmol) en 10 ml de DMF seca y se enjuagó con nitrógeno. Se añadió carbonato de potasio (0,231 g, 1,670 mmol) y la reacción se agitó a 90° C durante 10 min. A esta mezcla, se le añadió 2,4-dicloro-7,8-dihidropirido[4,3-d]pirimidin-6(5H)-carboxilato de terc-butilo (61 mg, 0,200 mmol) y la reacción se agitó 1 hora a 90° C. Una vez que la reacción se consideró completa por LC/MS, la mezcla se vertió en NH4Cl saturado, extraído 3x con DCM. Los extractos de DCM combinados se secaron sobre sulfato de sodio, se filtraron y se concentraron sobre sílice. Luego, el material bruto se purificó mediante cromatografía ultrarrápida usando un gradiente de MeOH al 0-30% en EtOAc. Las fracciones que contenían el producto se combinaron, se concentraron y luego el residuo resultante se disolvió en TFA (1,162 ml, 15,08 mmol) y se agitó durante 1 h a temperatura ambiente. Una vez completada, la reacción se concentró, se trató con 3 ml de NH4OH (ac.) y el sólido resultante se aisló por filtración, se lavó con agua y se secó a alto vacío para dar I-125 como un sólido amarillo (68 mg, 87 % producir). 1H NMR (400 MHz, DMSO-d6): 59.40 (d, J=8.0 Hz, 1H), 9.53 (br, 1H), 8.22 (d, J=9.2 Hz, 1H), 8.18 (d, J=4.1 Hz, 1H), 7.85 (d, J=9.2 Hz, 1H) 7.18 (br, 1H), 4.45 (br, 1H), 3.62 (m, 1H), 3.56 (m, 2H), 3.46 (m, 2H), 3.12 (t, J=6.4 Hz, 1H), 2.54 (s, 3H), 1.19 (d, 6.4 Hz, 3H). MS m/z (M+H): 466.6.
Ejemplo 126
Síntesis de (R)-3-((2-cloro-6-metil-5,6,7,8-tetrahidropirido[4,3-d]pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-126)
Se disolvió I-125 (0,1 g, 0,214 mmol) en 3 ml de una mezcla 1:2 de MeOH-THF. Se añadieron ácido acético (0,025 ml, 0,428 mmol) y formaldehído (0,080 ml, 1,071 mmol) y la reacción se agitó durante 10 min y luego se añadió triacetoxiborohidruro de sodio (0,136 g, 0,642 mmol). Se dejó agitar la reacción durante una hora más a temperatura ambiente. Una vez completada, la reacción se diluyó con 1 ml de agua, se concentró y el residuo resultante se disolvió en 4 ml de DMSO y se purificó directamente mediante HPLC preparativa de fase inversa (10-95% de MeCN/Agua, 0,1% de TFA) para dar I-126 (0,05 g, 49% de rendimiento). 1H NMR (400 MHz, DMSO-d6): 5 9.36 (d, J=11.4 Hz, 1H), 8.09 (d, J=8.7 Hz, 1H), 7.83 (d, J=8.7 Hz, 1H), 7.52 (d, J=9.2 Hz, 1H), 4.65 (br, 2H), 3.75 (m, 3H), 3.59 (m, 2H), 3.20 (s, 3H), 1.32 (d, J=6.9 Hz, 3H). MS m/z (M+H): 480.8.
Ejemplo 127
Síntesis de (R)-3-((2-cloro-5-(hidroximetil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (1 -127)
A una solución de INT-96 (60 mg, 0,1 mmol) en dimetilformamida (2,0 ml), se le añadieron tetraquis(trifenilfosfina)paladio (0) (14,4 mg, 0,01 mmol) y trietilsilano (72,4 mg, 0,6 mmol) a 0° C. La mezcla de la reacción resultante se agitó a temperatura ambiente durante 2 h. Una vez completada, la mezcla de la reacción se diluyó con agua (4,0 ml) y se extrajo con 10% de metanol/diclorometano (2 x 10 ml). La capa orgánica se lavó con agua (5 ml) seguido de una solución de salmuera saturada (5 ml). La capa orgánica se secó sobre sulfato de sodio anhidro y se concentró a presión reducida. El material bruto obtenido se purificó mediante HPLC preparativa para proporcionar I-127 (22 mg, 40%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 51.18 (d, J=6.8 Hz, 3H), 3.46 (br s, 1H), 3.60 (br s, 1H), 4.68 (s, 2H), 5.66 (br s, 1H), 7.15 (t, J=5.2 Hz, 1H), 7.60 (d, J=9.2 Hz, 1H), 7.84 (d, J=9.2 Hz, 1H), 8.11 (d, J=4.4 Hz, 1H), 8.17 (d, J=8.8 Hz, 1H), 8.69 (s, 1H), 9.35 (d, J=8.8 Hz, 1H). MS m/z (M+H): 442.4.
Ejemplo 128
Síntesis de (R)-3-((2-cloro-5-((4-h¡drox¡p¡per¡d¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-128)
A una suspensión agitada de INT-6 (150,0 mg, 0,5 mmol) en DMF anhidra (7,5 ml) se le añadió t-BuOK (1 M en THF, 0,6 ml, 0,6 mmol) gota a gota a 0° C para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-97 (144,5 mg, 0,55 mmol) en DMF (2 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (10 ml) y agua (20 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 10 ml). La capa orgánica combinada se lavó con salmuera (30 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-128 (30 mg, 11,4%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6): 59.35 (d, J=9.0 Hz, 1H), 8.68 (s, 1H), 8.19-8.12 (m, 2H), 7.84 (d, J=9.0 Hz, 1H), 7.59 (d, J=9.3 Hz, 1H), 7.15 (t, J=2.4 Hz, 1H), 4.56 (d, J=4.2 Hz, 1H), 3.63 (s, 3H), 3.47 3.45 (m, 3H), 2.81-2.71 (m, 2H), 2.30-2.11 (m, 2H), 1.75-1.65 (m, 2H), 1.46-1.40 (m, 2H), 1.19 (d, J=6.6 Hz, 3H). MS m/z (M+H): 525.0.
Ejemplo 129
(R)-3-((2-cloro-5-((4-etox¡p¡per¡d¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-il)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nolin-8-ona (1-129)
A una suspensión agitada de INT-6 (131,0 mg, 0,44 mmol) en DMF anhidra (11 ml) se le añadió t-BuOK (1 M en THF, 0,72 ml, 0,72 mmol) a 0° C gota a gota para dar una solución marrón. La solución resultante se agitó durante 0,5 horas más a esta temperatura. Se añadió gota a gota INT-98 (128,0 mg, 0,44 mmol) en DMF (1 ml) a la solución anterior y se agitó durante la noche a temperatura ambiente. La mezcla de la reacción se repartió entre acetato de etilo (15 ml) y agua (15 ml), la capa orgánica se separó y la capa acuosa se extrajo con acetato de etilo (2 x 15 ml). La capa orgánica combinada se lavó con salmuera (30 ml) y la capa orgánica se separó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. La purificación por HPLC preparativa proporcionó I-129 (49,8 mg, 20,4%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-d6): 59.89 (brs, 1H), 9.39 (d, J=4.5 Hz, 1H), 8.88 (s, 1H), 8.23-8.14 (m, 2H), 7.88 (d, J=4.4 Hz, 1H), 7.66 (d, J=9.0 Hz, 1H), 7.20-7.05 (m, 1H), 4.68-4.43 (m, 2H), 3.80 3.63 (m, 2H), 3.60-3.44 (m, 6H), 3.26-3.03 (m, 2H), 2.27-2.17 (m, 1H), 2.16-1.88 (m, 2H), 1.76-1.56 (m, 1H), 1.21 (d, J=6.0 Hz, 3H), 1.19-1.02 (m, 3H). MS m/z (M+H): 553.
Ejemplo 130
Síntes¡s de (R)-3-((2-cloro-5-((4-(2-metox¡etox¡)p¡per¡d¡n-1-¡l)met¡l)p¡r¡m¡d¡n-4-¡l)ox¡)-10-met¡l-9,10,11,12-tetrah¡dro-8H-[1,4]d¡azep¡no[5',6':4,5]t¡eno[3,2-f]qu¡nol¡n-8-ona (I-130)
A una solución de INT-6 (135,6 mg, 0,4 mmol) en DMF (20 ml) se le añadió carbonato potásico (625,9 mg, 4,5 mmol) a temperatura ambiente y se agitó a 90° C durante 10 min. A la mezcla resultante, se le añadió INT-99 (145,0 mg, 0,4 mmol) a 90° C. La mezcla de la reacción resultante se agitó a 90° C durante 1 h. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo (15,0 ml), se extrajo con acetato de etilo (2 x 10 ml) y se lavó con solución de salmuera (30 ml). La capa orgánica se separó, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para dar material bruto. El bruto se purificó mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,05% de NH4HCO3) para proporcionar I-130 (14,5 mg, 6%) como un sólido amarillo. 1H NMR (300 MHz, DMSO-ds) 59.35 (d, J=9.0 Hz, 1H), 8.69 (s, 1H), 8.18 (d, J=9.0 Hz, 1H), 8.12-8.08 (m,
1H), 7.84 (d, J=9.0 Hz, 1H), 7.59 (d, J=9.0 Hz, 1H), 7.15 (t, J=5.4 Hz, 1H), 3.63-3.52 (m, 3H), 3.52-3.39 (m, 7H), 3.23 (s, 3H), 2.78-2.74 (m, 2H), 2.26-2.19 (m, 2H), 1.84-1.81 (m, 2H), 1.50-1.44 (m, 2H), 1.20 (d, J=5.4 Hz, 3H). MS m/z (M+H): 583.4.
Ejemplo 131
Síntesis de (R)-3-((2-cloro-5-((4-(2-fluoroetoxi)piperidin-1-il)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-131)
A una solución INT-6 (54,4 mg, 0,2 mmol) en DMF) (10 ml) se le añadió terc-butóxido de potasio (1 M en THF, 0,4 ml, 0,4 mmol) a 0° C y se agitó durante 10 min. A la mezcla resultante, se añadió INT-100 (56,0 mg, 0,2 mmol) a 0° C. La mezcla de la reacción resultante se agitó a 25° C durante la noche. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo (15,0 ml), se extrajo con acetato de etilo (2 x 10 ml) y se lavó con solución de salmuera (30 ml). La capa orgánica se separó, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para dar material bruto. El bruto se purificó mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,05% de NH4HCO3) para proporcionar I-131 (19,3 mg, 19%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.35 (d, J=9.0 Hz, 1H), 8.69 (s, 1H), 8.18 (d, J=9.0 Hz, 1H), 8.12-8.08 (m, 1H), 7.84 (d, J=9.0 Hz, 1H), 7.59 (d, J=9.0 Hz, 1H), 7.15 (t, J=5.4 Hz, 1H), 4.57 (t, J=3.9 Hz, 1H), 4.41 (t, J=3.9 Hz, 1H), 3.68 (t, J=4.2 Hz, 1H), 3.64 (s, 3H), 3.58 (t, J=4.2 Hz, 1H), 3.47-3.43 (m, 2H), 3.36-3.33 (m, 1H), 2.78-2.75 (m, 2H), 2.27-2.20 (m, 2H), 1.87-1.83 (m, 2H), 1.50-1.47 (m, 2H), 1.20 (d, J=6.6 Hz, 3H). MS m/z (M+H): 571.0.
Ejemplo 132
Síntesis de (R)-3-((2-cloro-5-((4-(metoxi-d3)piperidin-1-il)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-132)
A una solución de INT-6 (107,2 mg, 0,4 mmol) en DMF (15 ml) se le añadió carbonato potásico (495,0 mg, 3,6 mmol) a temperatura ambiente y se agitó a 90° C durante 10 min. A la mezcla resultante se le añadió INT-101 (100,0 mg, 0,4 mmol) a 90° C. La mezcla de la reacción resultante se agitó a 90° C durante 1 h. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo (30,0 ml), se extrajo con acetato de etilo (2 x 20 ml) y se lavó con solución de salmuera (50 ml). La capa orgánica se separó, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para dar material bruto. El bruto se purificó mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,05% de NH4HCO3) para proporcionar I-132 (7,6 mg, 4%) como un sólido amarillo.
1H NMR (400 MHz, DMSO-ds): 59.35 (d, J=9.0 Hz, 1H), 8.69 (s, 1H), 8.18 (d, J=9.0 Hz, 1H), 8.12-8.08 (m, 1H), 7.84
(d, J=9.0 Hz, 1H), 7.59 (d, J=9.0 Hz, 1H), 7.15 (t, J=5.4 Hz, 1H), 3.64-3.53 (m, 3H), 3.47-3.40 (m, 2H), 3.28-3.17 (m, 1H), 2.76-2.73 (m, 2H), 2.27-2.24 (m, 2H), 1.87-1.83 (m, 2H), 1.47-1.44 (m, 2H), 1.20 (d, J=6.6 Hz, 3H). MS m/z (M+H): 542.0.
Ejemplo 133
Síntesis de (R)-3-((2-cloro-5-((4-isopropoxipiperidin-1-il)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-133)
A una solución de INT-6 (147,6 mg, 0,5 mmol) en DMF (30,0 ml) se le añadió carbonato potásico (681,5 mg, 5,0 mmol) a temperatura ambiente y se agitó a 90° C durante 10 min. A la mezcla resultante se le añadió INT-102 (150,0 mg, 0,5 mmol) a 90° C. La mezcla de la reacción resultante se agitó a 90° C durante 1 h. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo (30,0 ml), se extrajo con acetato de etilo (2 x 20 ml) y se lavó con solución de salmuera (50 ml). La capa orgánica se separó, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para dar material bruto. El bruto se purificó mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,05% de NH4HCO3) para proporcionar I-133 (24,2 mg, 10,2%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 59.35 (d, J=9.3 Hz, 1H), 8.67 (br, 1H), 8.17 (d, J=9.0 Hz, 1H), 8.12-8.08 (m, 1H), 7.84 (d, J=9.0 Hz, 1H), 7.59 (d, J=9.0 Hz, 1H), 7.15 (t, J=4.8 Hz, 1H), 3.70-3.63 (m, 4H), 3.53-3.47 (m, 2H), 3.41-3.36 (m, 1H), 2.78-2.74 (m, 2H), 2.26-2.19 (m, 2H), 1.79-1.63 (m, 2H), 1.44-1.41 (m, 2H), 1.20 (d, J=6.6 Hz, 3H), 1.05 (d, J=6.0 Hz, 6H). MS m/z (M+H): 567.1.
Ejemplo 134
Síntesis de (R)-3-((5-((4-(terc-butoxi)piperidin-1-il)metil)-2-cloropirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (I-134)
A una solución de INT-6 (158,0 mg, 0,5 mmol) en DMF (20 ml) se le añadió carbonato de potasio (828,0 mg, 6,0 mmol) a 90° C y se agitó durante 10 min. A la mezcla resultante, se le añadió INT-103 (168,0 mg, 0,5 mmol) y se agitó a 90° C durante 1 h. Una vez completada, la mezcla de la reacción se diluyó con agua con hielo (30,0 ml), se extrajo con acetato de etilo (2 x 20 ml) y se lavó con solución de salmuera (50 ml). La capa orgánica se separó, se secó sobre sulfato de sodio anhidro y se concentró a presión reducida para dar material bruto. El bruto se purificó mediante HPLC preparativa de fase inversa (10-95% de MeCN/agua, 0,05% de NH4HCO3) para producir I-134 (11,7
mg, 4%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-d6): 59.35 (d, J=9.3 Hz, 1H), 8.68 (s, 1H), 8.18 (d, J=8.7 Hz, 1H), 8.12-8.08 (m, 1H), 7.84 (d, J=9.0 Hz, 1H), 7.60 (d, J=9.0 Hz, 1H), 7.15 (t, J=4.8 Hz, 1H), 3.68-3.55 (m, 3H), 3.54-3.40 (m, 3H), 2.76-2.73 (m, 2H), 2.27-2.24 (m, 2H), 1.69-1.63 (m, 2H), 1.44-1.41 (m, 2H), 1.20 (d, J=6.6 Hz, 3H), 1.13 (s, 9H). MS m/z (M+H): 581.2.
Ejemplo 135
Síntesis de (R)-3-((2-cloro-5-((etoxi-d5)metil)pirimidin-4-il)oxi)-10-metil-9,10,11,12-tetrahidro-8H-[1,4]diazepino[5',6':4,5]tieno[3,2-f]quinolin-8-ona (1-135)
A una suspensión de INT-6 (66 mg, 0,220 mmol) en DMF (3,0 ml) se le añadió carbonato de potasio (274 mg, 1,980 mmol) y la mezcla resultante se agitó a 90° C durante 10 min. Se añadió una solución de INT-104 (56 mg, 0,264 mmol) en DMF (2,0 ml). La mezcla de la reacción resultante se agitó a 90° C durante 4 h. Una vez completada, la mezcla de la reacción se filtró y los filtrados se concentraron a presión reducida. El material bruto obtenido se purificó mediante cromatografía ultrarrápida en una columna de gel de sílice eluyendo con un gradiente de MeOH-EtOAc del 1% al 15% para producir I-135 (68 mg, rendimiento del 65%) como un sólido amarillo. 1H NMR (400 MHz, DMSO-ds): 59.34 (d, J=9.2 Hz, 1H), 8.69 (s, 1H), 8.17 (d, J=9.2 Hz, 1H), 8.14 (d, J=4.6 Hz, 1H), 7.84 (d, J=9.2 Hz, 1H), 7.61 (d, J=9.2 Hz, 1H), 7.16 (t, J=5.0 Hz, 1H), 4.63 (s, 2H), 3.56-3.60 (m, 1H), 3.40-3.47 (m, 2H), 1.16 (d, J=6.9 Hz, 3H). MS m/z (M+H): 475.1.
Ejemplos biológicos
A continuación se describen ensayos in vitro usados para medir la actividad biológica de los compuestos proporcionados como inhibidores selectivos de MK2.
EJEMPLO 136
Ensayo Omnia® de proteína quinasa 2 activada por proteína quinasa activada por mitógenos para la evaluación de la potencia de compuestos
El siguiente protocolo describe un ensayo de quinasa de lectura continua optimizado para medir la potencia de los compuestos contra la enzima proteína quinasa 2 activada por proteína quinasa activada por mitógeno activada por p38a (MAPKAP-K2 o MK2). Detalles adicionales de este ensayo se describen por Life Technologies, Carlsbad, CA en su sitio web en la siguiente URL: http://tools.lifetechnologies.com/content/sfs/manuals/omnia_kinase_assay_man.pdf.
[Reactivo] usado:
[MK-2] = 0,4 nM,
[ATP] = 10 |jM y
[ST3-Sox] = 10 jM (ATPappKM = 10 jM)
Brevemente, se prepararon soluciones madre 10X de MK2 (PV3317, de Life Technologies), 1,13x ATP (AS001A) y sustrato peptídico conjugado con Sox, S/T3-Sox, (KZN1031) en tampón de reacción de quinasa 1X que consiste de 20 mM Tris, pH 7,5, MgCl25 mM, EGTA 1 mM, p-glicerofosfato 5 mM, glicerol al 5% (10X stock, KB001A) y DTT 0,2 mM (DS001A). Se añadió solución enzimática (5 jl) a cada uno de DMSO (5 jl) o compuestos de prueba diluidos en serie preparados en DMSO en una placa de microtitulación de superficie sin unión, blanca, de 384 pocillos Corning (N° 3574) (Corning, NY). Las reacciones de quinasa se iniciaron con la adición de 45 jl de la mezcla de sustrato ATP-péptido S/T3-Sox y se monitorizaron cada 71 segundos durante 120 minutos a Aex360/Aem485 en un lector de placas Synergy H4 de BioTek (Winooski, VT) a temperatura ambiente.
Las señales de fondo de los pocilios de control sin enzimas se restaron de todas las curvas de progreso. Las porciones lineales iniciales de las curvas de progreso neto se ajustaron de acuerdo con una ecuación lineal para producir la pendiente y el porcentaje de inhibición (% de inhibición) en cada concentración de compuesto. Las curvas de progreso neto obtenidas durante las dos primeras horas de reacciones también se ajustaron de acuerdo con una ecuación ascendente exponencial simple (Ec. 1) para producir valores de kobs en cada concentración de compuesto. Los gráficos de % de inhibición frente a las concentraciones de inhibidor se ajustaron de acuerdo con una ecuación de dosis-respuesta (Ec. 2) para generar valores de IC50 y pendiente de Hill, mientras que los gráficos de kobs frente a la concentración de inhibidor se ajustaron de acuerdo con la Ecuación 3 (Ec.3) para generar valores kinact/KI aparente usando el software GraphPad PRISM (Versión 6.00; GraphPad San Diego, CA).
donde F es la intensidad de fluorescencia del lector de placas, V0 es una constante que refleja la relación entre la lectura del instrumento y la concentración de producto, t es el tiempo, e es el número de Euler y kobs es la constante de velocidad de inactivación observada.
donde el % de inhibición es porcentaje de inhibición, de IC50 es la concentración inhibidora máxima media, [I] es la concentración de inhibidor, y n es la pendiente de Hill.
donde kobs es la constante de velocidad de inactivación observada, kinact es la constante de velocidad de inactivación aparente, KI es la constante de inhibición aparente y [I] es la concentración de inhibidor. Los resultados de este ensayo, que muestran IC50 (es decir, la concentración a la que un de compuesto de prueba inhibe el 50% de fosforilación del péptido sustrato) se informan en nanomolar. Los resultados de potencia de los compuestos probados se muestran en la Tabla A en la columna titulada "MK2 IC5 0".
EJEMPLO 137
Ensayo de espectrometría de masas para detectar el nivel de modificación covalente de MK2
Los compuestos I-1 a I-50 de la invención se probaron en un ensayo de espectrometría de masas para medir su capacidad para modificar covalentemente la proteína MK2. A continuación se describe el procedimiento para este ensayo. La proteína MK2 intacta (Invitrogen, N° de cat. PR5320A) se incubó durante 60 minutos a temperatura ambiente con un exceso de 10 veces del compuesto de prueba con respecto a la proteína. Se diluyeron alícuotas de la mezcla resultante (6 gl cada una) con ácido trifluoroacético (TFA, 10 gl) al 0,2% antes de micro C4 ZipTipping directamente sobre el objetivo MALDI usando ácido sinapínico como matriz de desorción (10 mg/ml en TFA al 0,1%: acetonitrilo 50:50, v/v). La masa del centroide de la proteína objetivo en la muestra de control se comparó con la masa del centroide de la proteína objetivo incubada con el compuesto. Un cambio en la masa del centroide de la proteína tratada en comparación con la proteína no tratada se dividió por el peso molecular del compuesto. Este número corresponde al porcentaje de proteína modificada (una medida de la proporción de proteína objetivo total unida covalentemente al compuesto de prueba) después de una hora de incubación. Los resultados de este ensayo se informan en la Tabla A bajo la columna “Modificación de Masa”.
Los compuestos I-51 a I-129 se probaron en un ensayo de espectrometría de masas de perlas magnéticas para medir su capacidad para modificar covalentemente la proteína MK2. A continuación se describe el procedimiento para este ensayo. La proteína MK2 (Invitrogen, N° de Cat. PR5320A) se incubó durante 60 minutos a temperatura ambiente con un exceso de 10 veces de compuesto de prueba a proteína. Se añadieron 3 gl de perlas magnéticas de Ni-NTA a las alícuotas de 6 gl de muestra, se lavaron, se eluyeron con ácido trifluoroacético (TFA, 2 gl) al 0,2% y se colocaron directamente sobre el objetivo MALDI usando ácido sinapínico como matriz de desorción (10 mg/ml en TFA al 0,1%: acetonitrilo 50:50, v/v). La masa del centroide de la proteína objetivo en la muestra de control se comparó con la masa del centroide de la proteína objetivo incubada con el compuesto. Un cambio en la masa del centroide de la proteína tratada en comparación con la proteína no tratada se dividió por el peso molecular del compuesto. Este número corresponde al porcentaje de proteína modificada (una medida de la proporción de proteína objetivo total unida covalentemente al compuesto de prueba) después de una hora de incubación. Los
resultados de este ensayo se informan en la Tabla A bajo la columna “Modificación de Masa”.
EJEMPLO 138
Ensayo Celular de MK2 - Detección de Hsp27 total y fosfo (Serina 78) por MSD ELISA (Thp1)
Los compuestos de la invención se probaron en células de leucemia monocítica aguda humana Thp-1 para medir la inhibición de la actividad MK2. Se cultivaron células Thp-1 en medio de cultivo que contenía RPMI/FBS (suero bovino fetal) al 10%/2-mercaptoetanol 0,05 mM.72 horas antes del ensayo, se sembraron 8 x 104 células por pocillo en una placa de 96 pocillos de fondo plano junto con 10 ng/ml de forbol 12-miristato 13-acetato (PMA). Las células se cultivaron en una incubadora a 37° C hasta que se necesitaron para el ensayo. El medio de la placa celular se reemplazó con medio de cultivo justo antes del ensayo mientras se realizaban las diluciones del compuesto.
Se prepararon soluciones madre del compuesto de prueba, 1 mM en DMSO. Se añadieron 0,9 pl de compuesto de prueba a 300 pl de medio celular para una concentración de partida de 3000 nM. Se realizaron diluciones en serie de tres veces (1:3) en medio de ensayo celular hasta la concentración final de 0,15 nM. Se descartó el medio de la placa celular, seguido de la adición de 100 pl del medio que contenía el compuesto. La preparación resultante se incubó a 37° C durante 1 hora.
Se eliminó el medio de ensayo celular que contenía el compuesto de prueba y las células se lavaron una vez con medio de ensayo celular. Se añadió medio de ensayo celular que contenía 50 ng/ml de LPS (lipopolisacárido) a cada pocillo y se incubó durante 45 minutos. Después de la incubación con LPS, las células se lavaron una vez con PBS (solución salina tamponada con fosfato) y se lisaron con 60 pl de tampón de extracción celular (Invitrogen N° FNN0011) más inhibidores de proteasa y fosfatasa. Luego, la placa se almacenó a -80° C hasta su análisis posterior.
Se adquirió el kit de ensayo ELISA MULTI-SPOT Phospho(Ser78)/Total HSP27 de Meso Scale Delivery (MSD; N° de catálogo K15128D). MSD proporciona una placa que ha sido prerrevestida con anticuerpos de captura para phosphor-HSP27 (Ser78) y HSP27 total. La placa MSD prerrecubierta se bloqueó con 150 pl/pocillo de bSa al 3% en tampón de lavado MSD. La preparación se colocó en un agitador a temperatura ambiente durante una hora. Mientras se bloqueaba la placa ELISA, la placa de ensayo celular almacenada a -80° C se colocó en un agitador a 4° C durante 1 hora para descongelar.
La placa MSD bloqueada se lavó en un lavador de placas, extrayendo el último bit de solución de lavado, seguido de la adición de 30 pl del lisado de la placa de ensayo celular. La preparación se cubrió y se incubó durante 1 hora a temperatura ambiente. Se eliminó el lisado, se lavó la placa 3 veces en un lavador de placas y se extrajo el último bit de tampón de lavado y se reemplazó con 25 pl/anticuerpo de detección de pocillo (anti-HSP27 total conjugado con un compuesto electroquimioluminiscente, etiqueta MSD SULFO-TAG, suministrado en el kit) elaborado en tampón de lavado BSA/MSD al 1%. La placa se incubó durante 1 hora a temperatura ambiente en un agitador, seguido de 3 lavados. Se extrajo el último bit de tampón de lavado. Se añadieron 150 pl/pocillo de tampón de lectura 1x MSD (tampón de lectura 4x suministrado con el kit) y la placa se analizó en el MSD SECTOR® Imager para su análisis. El SECTOR® Imager mide la intensidad de la luz emitida para proporcionar una medida cuantitativa de HSP27 fosforilada (Ser78) y HSP27 total presente en la muestra. El porcentaje relativo de fosfoproteína en una muestra se calcula dividiendo la intensidad de la señal de Fosfo-HSP27 entre la intensidad de la señal de HSP27 total medida en cada pocillo. Se realizó un análisis de ajuste de curva usando el software Graph Pad Prism para generar una EC50 basada en las respuestas inhibidoras de la relación de señal p-HSP27/HSP27 total inducida por LPS normalizada a los controles tratados con DMSO (ajustado al 100% de intensidad de señal). Los resultados de este ensayo, que muestran la EC50 (es decir, la concentración a la que un compuesto de prueba inhibe la fosforilación de Hsp27 en el 50%) se presentan en nanomolar. Los resultados de este ensayo se informan en la Tabla A bajo la columna "EC50 de señalización de pHSP27 ".
La Tabla A muestra datos para compuestos seleccionados en varios ensayos. Los compuestos que tienen una actividad designada como "A" proporcionaron una EC50/IC50<100 nM; los compuestos que tienen una actividad designada como "B" proporcionaron una EC50/IC50 de 101-500 nM; los compuestos que tienen una actividad designada como "C" proporcionaron una EC50/IC50 de 501-999 nM; los compuestos que tienen una actividad designada como "D" proporcionaron un EC50/IC50 de >1000 nM. Los compuestos que tienen una actividad designada como "E" proporcionaron una modificación en masa de >70%; los compuestos que tienen una actividad designada como "F" proporcionaron una modificación en masa del 31-69%; los compuestos que tienen una actividad designada como "G" proporcionaron una modificación de masa de <30%.
Tabla A.
continuación
continuación
continuación
Aunque hemos descrito una serie de realizaciones de esta invención, es evidente que nuestros ejemplos básicos pueden modificarse para proporcionar otras realizaciones que utilicen los compuestos de esta invención. Por lo tanto, se apreciará que el alcance de esta invención se define por las reivindicaciones adjuntas en lugar de por las realizaciones específicas que se han representado a modo de ejemplo.
Claims (1)
- REIVINDICACIONES1. Un compuesto seleccionado de:o una sal farmacéuticamente aceptable del mismo.2. El compuesto de la reivindicación 1, donde el compuesto es:o una sal farmacéuticamente aceptable del mismo.3. El compuesto de la reivindicación 1, donde el compuesto es:o una sal farmacéuticamente aceptable del mismo.4. El compuesto de la reivindicación 1, donde el compuesto es:o una sal farmacéuticamente aceptable del mismo.5. El compuesto de la reivindicación 1, donde el compuesto es:o una sal farmacéuticamente aceptable del mismo.6. El compuesto de la reivindicación 1, donde el compuesto es:o una sal farmacéuticamente aceptable del mismo.7. El compuesto de la reivindicación 1, donde el compuesto es:o una sal farmacéuticamente aceptable del mismo.8. El compuesto de la reivindicación 1, donde el compuesto es:o una sal farmacéuticamente aceptable del mismo.9. Una composición farmacéuticamente aceptable que comprende el compuesto de acuerdo con la reivindicación 2 y un portador, adyuvante o vehículo farmacéuticamente aceptable.10. Una composición farmacéuticamente aceptable que comprende el compuesto de acuerdo con la reivindicación 3 y un portador, adyuvante o vehículo farmacéuticamente aceptable.11. Una composición farmacéuticamente aceptable que comprende el compuesto de acuerdo con la reivindicación 4 y un portador, adyuvante o vehículo farmacéuticamente aceptable.12. Una composición farmacéuticamente aceptable que comprende el compuesto de acuerdo con la reivindicación 5 y un portador, adyuvante o vehículo farmacéuticamente aceptable.13. Una composición farmacéuticamente aceptable que comprende el compuesto de acuerdo con la reivindicación 6 y un portador, adyuvante o vehículo farmacéuticamente aceptable.14. Una composición farmacéuticamente aceptable que comprende el compuesto de acuerdo con la reivindicación 7 y un portador, adyuvante o vehículo farmacéuticamente aceptable.15. Una composición farmacéuticamente aceptable que comprende el compuesto de acuerdo con la reivindicación 8 y un portador, adyuvante o vehículo farmacéuticamente aceptable.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462051788P | 2014-09-17 | 2014-09-17 | |
| US201562199927P | 2015-07-31 | 2015-07-31 | |
| PCT/US2015/050495 WO2016044463A2 (en) | 2014-09-17 | 2015-09-16 | Mk2 inhibitors and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2874561T3 true ES2874561T3 (es) | 2021-11-05 |
Family
ID=55454109
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15842903T Active ES2874561T3 (es) | 2014-09-17 | 2015-09-16 | Inhibidores de MK2 y usos de los mismos |
Country Status (30)
| Country | Link |
|---|---|
| US (5) | US9458175B2 (es) |
| EP (2) | EP3912981A1 (es) |
| JP (3) | JP6556225B2 (es) |
| KR (1) | KR102457848B1 (es) |
| CN (1) | CN106998692B (es) |
| AU (1) | AU2015317741B2 (es) |
| BR (1) | BR112017005266B1 (es) |
| CA (1) | CA2961607C (es) |
| CL (1) | CL2017000576A1 (es) |
| CO (1) | CO2017003279A2 (es) |
| CY (1) | CY1124215T1 (es) |
| DK (1) | DK3193611T3 (es) |
| EA (1) | EA037299B1 (es) |
| EC (1) | ECSP17023281A (es) |
| ES (1) | ES2874561T3 (es) |
| HR (1) | HRP20210529T1 (es) |
| HU (1) | HUE054347T2 (es) |
| IL (1) | IL251051B (es) |
| LT (1) | LT3193611T (es) |
| MA (1) | MA40534B1 (es) |
| MX (2) | MX373341B (es) |
| PL (1) | PL3193611T3 (es) |
| PT (1) | PT3193611T (es) |
| RS (1) | RS62017B1 (es) |
| SA (1) | SA517381115B1 (es) |
| SG (2) | SG11201701861RA (es) |
| SI (1) | SI3193611T1 (es) |
| SM (1) | SMT202100311T1 (es) |
| TW (1) | TWI744217B (es) |
| WO (1) | WO2016044463A2 (es) |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016518316A (ja) | 2013-03-15 | 2016-06-23 | セルジーン アビロミクス リサーチ, インコーポレイテッド | Mk2阻害剤およびそれらの使用 |
| RS62017B1 (sr) | 2014-09-17 | 2021-07-30 | Celgene Car Llc | Mk2 inhibitori i njihova upotreba |
| CN106632077B (zh) * | 2016-10-10 | 2019-01-22 | 上海再启生物技术有限公司 | 一种2-氨基-4-溴嘧啶的制备方法 |
| US10882867B2 (en) * | 2017-03-16 | 2021-01-05 | Celgene Car Llc | Forms and compositions of a MK2 inhibitor |
| US11230551B2 (en) | 2017-03-16 | 2022-01-25 | Celgene Car Llc | Deuterated analogs of MK2 inhibitors and uses thereof |
| JP7282039B2 (ja) * | 2017-03-16 | 2023-05-26 | セルジーン シーエーアール エルエルシー | Mk2阻害剤、その合成、およびそれに至るまでの中間体 |
| WO2018170204A1 (en) * | 2017-03-16 | 2018-09-20 | Celgene Car Llc | 9,10,11,12-tetrahydro-8h-[1,4]diazepino[5',6':4,5]thieno[3,2-f]quinolin-8-one compounds and uses thereof |
| JP7200120B2 (ja) | 2017-03-16 | 2023-01-06 | セルジーン シーエーアール エルエルシー | Mk2阻害剤として有用なヘテロアリール化合物 |
| CN107058259A (zh) * | 2017-05-18 | 2017-08-18 | 南京中医药大学 | 分子标志物mk2基因及其应用 |
| CA3114883A1 (en) | 2018-10-02 | 2020-04-09 | Disc Medicine, Inc. | Matriptase 2 inhibitors and uses thereof |
| CN114364681A (zh) * | 2019-05-17 | 2022-04-15 | 西建卡尔有限责任公司 | 治疗mk2介导的病症的方法 |
| KR20220153582A (ko) | 2020-02-14 | 2022-11-18 | 솔크 인스티튜트 포 바이올로지칼 스터디즈 | 마크로시클릭 ulk1/2 억제제 |
| JP2023513797A (ja) * | 2020-02-14 | 2023-04-03 | ソーク インスティテュート フォー バイオロジカル スタディーズ | Ulk1/2阻害剤による単剤療法および併用療法 |
| US20230087078A1 (en) * | 2020-03-02 | 2023-03-23 | Washington University | Compositions and methods for the treatment of pancreatic cancer |
| US20230255979A1 (en) * | 2020-07-24 | 2023-08-17 | Bristol-Myers Squibb Company | Methods of treating acute respiratory disorders |
| US20230414575A1 (en) * | 2020-11-12 | 2023-12-28 | Akttyva Therapeutics, Inc. | Mk2 activating compounds for use in treating vascular leak and endothelial barrier disorders |
| KR20230142529A (ko) * | 2021-02-01 | 2023-10-11 | 셀진 코포레이션 | Mk2 억제제, 이의 합성, 및 이의 중간체 |
| EP4079855A1 (en) * | 2021-04-20 | 2022-10-26 | Eberhard Karls Universität Tübingen Medizinische Fakultät | Compound and method for the prophylaxis and treatment of leukemia |
| TW202328141A (zh) * | 2021-08-27 | 2023-07-16 | 大陸商瑞石生物醫藥有限公司 | 喹啉并呋喃衍生物及其用途 |
| MX2024008704A (es) | 2022-01-14 | 2024-07-22 | Shanghai Hansoh Biomedical Co Ltd | Derivado policiclico que contiene piridina, y metodo de preparacion de este y uso de este. |
| WO2024044731A1 (en) * | 2022-08-26 | 2024-02-29 | Matchpoint Therapeutics Inc. | Diazepino-thieno-quinoxaline compounds and their use in therapy |
| EP4608401A2 (en) * | 2022-10-27 | 2025-09-03 | Bristol-Myers Squibb Company | Mk2 inhibitors and uses thereof |
| US20260109708A1 (en) * | 2023-02-07 | 2026-04-23 | Celgene Corporation | Compounds and compositions useful as degraders of mk2 kinase |
| WO2024229401A2 (en) * | 2023-05-04 | 2024-11-07 | Matchpoint Therapeutics Inc. | Diazepino-thieno-quinoxaline compounds and their use in therapy |
| CN121368484A (zh) * | 2023-06-26 | 2026-01-20 | 深圳信立泰药业股份有限公司 | 一种mk2抑制剂在制备预防和/或治疗疾病药物中的应用 |
Family Cites Families (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5015778A (en) | 1989-12-18 | 1991-05-14 | The Dow Chemical Company | Catalytic method to produce hydroxy substituted arylophenones |
| CN1087725C (zh) | 1994-03-25 | 2002-07-17 | 同位素技术有限公司 | 用氘代方法增强药物效果 |
| US5441946A (en) | 1994-04-14 | 1995-08-15 | Rhone-Poulenc-Rorer Pharmaceuticals, Inc. | Phosphonate derivatives of lipophilic amines |
| GB9828511D0 (en) * | 1998-12-24 | 1999-02-17 | Zeneca Ltd | Chemical compounds |
| US6861440B2 (en) * | 2001-10-26 | 2005-03-01 | Hoffmann-La Roche Inc. | DPP IV inhibitors |
| TW200413273A (en) | 2002-11-15 | 2004-08-01 | Wako Pure Chem Ind Ltd | Heavy hydrogenation method of heterocyclic rings |
| CN1747949A (zh) | 2002-12-20 | 2006-03-15 | 法马西亚公司 | 无环吡唑化合物 |
| EP1663204B1 (en) | 2003-08-29 | 2014-05-07 | Exelixis, Inc. | C-kit modulators and methods of use |
| WO2005105814A1 (en) | 2004-04-28 | 2005-11-10 | Incyte Corporation | Tetracyclic inhibitors of janus kinases |
| MX2007009388A (es) | 2005-02-04 | 2007-09-25 | Senomyx Inc | Compuestos que comprenden porciones heteroarilo unidas y su uso como modificadores del sabor unami, saborizantes y mejoradores del sabor para composiciones comestibles. |
| EP1849781A1 (en) | 2006-04-28 | 2007-10-31 | Laboratorios del Dr. Esteve S.A. | Substituted 3-Amino-4-hydroxy pyrrolidines compounds, their preparation and use as medicaments |
| EP2223925A1 (en) | 2006-10-09 | 2010-09-01 | Takeda Pharmaceutical Company Limited | Kinase inhibitors |
| CN101687869A (zh) | 2007-07-16 | 2010-03-31 | 诺瓦提斯公司 | 作为mk2抑制剂的四环内酰胺衍生物 |
| CN101910151A (zh) | 2007-10-22 | 2010-12-08 | 先灵公司 | 双环杂环衍生物及其作为gpr119活性调节剂的用途 |
| TWI546290B (zh) | 2008-06-27 | 2016-08-21 | 賽基艾維洛米斯研究股份有限公司 | 雜芳基化合物及其用途 |
| US8338439B2 (en) | 2008-06-27 | 2012-12-25 | Celgene Avilomics Research, Inc. | 2,4-disubstituted pyrimidines useful as kinase inhibitors |
| WO2010048149A2 (en) | 2008-10-20 | 2010-04-29 | Kalypsys, Inc. | Heterocyclic modulators of gpr119 for treatment of disease |
| US20110269744A1 (en) * | 2010-03-12 | 2011-11-03 | Astellas Pharma Inc. | Benzazepine Compound |
| WO2011153553A2 (en) * | 2010-06-04 | 2011-12-08 | The Regents Of The University Of California | Methods and compositions for kinase inhibition |
| EP2508511A1 (en) * | 2011-04-07 | 2012-10-10 | Laboratoire Biodim | Inhibitors of viral replication, their process of preparation and their therapeutical uses |
| ES2742261T3 (es) * | 2011-04-15 | 2020-02-13 | Hivih | Inhibidores de la replicación viral, su proceso de preparación y sus usos terapéuticos |
| KR102251706B1 (ko) | 2012-02-22 | 2021-05-14 | 메르크 파텐트 게엠베하 | 액정 매질 |
| EP2832734A4 (en) * | 2012-03-28 | 2015-08-26 | Takeda Pharmaceutical | HETEROCYCLIC COMPOUND |
| TW201406758A (zh) * | 2012-06-28 | 2014-02-16 | Daiichi Sankyo Co Ltd | 三環性化合物 |
| HK1210696A1 (en) * | 2012-07-11 | 2016-05-06 | Nimbus Iris, Inc. | Irak inhibitors and uses thereof |
| BR112015006418A2 (pt) * | 2012-09-24 | 2017-07-04 | Speede Claremont | método para apagar dados iniciados por um dispositivo de usuário de remetente remoto; e sistema de armazenamento de entrega de dados entre um dispositivo de usuário remetente e um dispositivo de usuário de destino |
| TW201417817A (zh) * | 2012-09-25 | 2014-05-16 | Daiichi Sankyo Co Ltd | Gsk3抑制劑與抗dr5抗體之組合 |
| WO2014139144A1 (en) | 2013-03-15 | 2014-09-18 | Agios Pharmaceuticals, Inc. | Therapeutic compounds and compositions |
| JP2016518316A (ja) * | 2013-03-15 | 2016-06-23 | セルジーン アビロミクス リサーチ, インコーポレイテッド | Mk2阻害剤およびそれらの使用 |
| WO2015050957A2 (en) | 2013-10-02 | 2015-04-09 | Treatments For Systemic Lupus Erythematosus | Treatments for systemic lupus erythematosus |
| WO2016032882A1 (en) | 2014-08-25 | 2016-03-03 | Stc.Unm | Inhibition of mk2 in the treatment of cancer |
| RS62017B1 (sr) | 2014-09-17 | 2021-07-30 | Celgene Car Llc | Mk2 inhibitori i njihova upotreba |
| WO2016112292A1 (en) | 2015-01-08 | 2016-07-14 | Moerae Matrix, Inc. | Formulation of mk2 inhibitor peptides |
| WO2018170204A1 (en) | 2017-03-16 | 2018-09-20 | Celgene Car Llc | 9,10,11,12-tetrahydro-8h-[1,4]diazepino[5',6':4,5]thieno[3,2-f]quinolin-8-one compounds and uses thereof |
| US10882867B2 (en) | 2017-03-16 | 2021-01-05 | Celgene Car Llc | Forms and compositions of a MK2 inhibitor |
| US11230551B2 (en) | 2017-03-16 | 2022-01-25 | Celgene Car Llc | Deuterated analogs of MK2 inhibitors and uses thereof |
| JP7282039B2 (ja) | 2017-03-16 | 2023-05-26 | セルジーン シーエーアール エルエルシー | Mk2阻害剤、その合成、およびそれに至るまでの中間体 |
| JP7200120B2 (ja) | 2017-03-16 | 2023-01-06 | セルジーン シーエーアール エルエルシー | Mk2阻害剤として有用なヘテロアリール化合物 |
| CN114364681A (zh) | 2019-05-17 | 2022-04-15 | 西建卡尔有限责任公司 | 治疗mk2介导的病症的方法 |
| US20230255979A1 (en) | 2020-07-24 | 2023-08-17 | Bristol-Myers Squibb Company | Methods of treating acute respiratory disorders |
-
2015
- 2015-09-16 RS RS20210725A patent/RS62017B1/sr unknown
- 2015-09-16 EP EP21164056.0A patent/EP3912981A1/en active Pending
- 2015-09-16 HU HUE15842903A patent/HUE054347T2/hu unknown
- 2015-09-16 KR KR1020177010439A patent/KR102457848B1/ko active Active
- 2015-09-16 US US14/856,311 patent/US9458175B2/en active Active
- 2015-09-16 CA CA2961607A patent/CA2961607C/en active Active
- 2015-09-16 ES ES15842903T patent/ES2874561T3/es active Active
- 2015-09-16 BR BR112017005266-0A patent/BR112017005266B1/pt active IP Right Grant
- 2015-09-16 TW TW104130645A patent/TWI744217B/zh active
- 2015-09-16 SM SM20210311T patent/SMT202100311T1/it unknown
- 2015-09-16 MX MX2017003359A patent/MX373341B/es active IP Right Grant
- 2015-09-16 EA EA201790380A patent/EA037299B1/ru not_active IP Right Cessation
- 2015-09-16 PL PL15842903T patent/PL3193611T3/pl unknown
- 2015-09-16 LT LTEP15842903.5T patent/LT3193611T/lt unknown
- 2015-09-16 DK DK15842903.5T patent/DK3193611T3/da active
- 2015-09-16 WO PCT/US2015/050495 patent/WO2016044463A2/en not_active Ceased
- 2015-09-16 SI SI201531617T patent/SI3193611T1/sl unknown
- 2015-09-16 CN CN201580058026.4A patent/CN106998692B/zh active Active
- 2015-09-16 JP JP2017515845A patent/JP6556225B2/ja active Active
- 2015-09-16 SG SG11201701861RA patent/SG11201701861RA/en unknown
- 2015-09-16 EP EP15842903.5A patent/EP3193611B1/en active Active
- 2015-09-16 SG SG10201902326XA patent/SG10201902326XA/en unknown
- 2015-09-16 AU AU2015317741A patent/AU2015317741B2/en active Active
- 2015-09-16 HR HRP20210529TT patent/HRP20210529T1/hr unknown
- 2015-09-16 PT PT158429035T patent/PT3193611T/pt unknown
- 2015-09-16 MA MA40534A patent/MA40534B1/fr unknown
-
2016
- 2016-09-29 US US15/280,157 patent/US9790235B2/en active Active
-
2017
- 2017-03-09 CL CL2017000576A patent/CL2017000576A1/es unknown
- 2017-03-09 IL IL25105117A patent/IL251051B/en active IP Right Grant
- 2017-03-14 MX MX2020005213A patent/MX2020005213A/es unknown
- 2017-03-16 SA SA517381115A patent/SA517381115B1/ar unknown
- 2017-04-04 CO CONC2017/0003279A patent/CO2017003279A2/es unknown
- 2017-04-13 EC ECIEPI201723281A patent/ECSP17023281A/es unknown
- 2017-10-13 US US15/782,995 patent/US10253040B1/en active Active
-
2019
- 2019-04-04 US US16/375,317 patent/US10577380B2/en active Active
- 2019-07-09 JP JP2019127476A patent/JP2019194236A/ja active Pending
-
2020
- 2020-02-27 US US16/802,654 patent/US11584757B2/en active Active
-
2021
- 2021-06-09 CY CY20211100504T patent/CY1124215T1/el unknown
-
2022
- 2022-03-16 JP JP2022041396A patent/JP7375072B2/ja active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2874561T3 (es) | Inhibidores de MK2 y usos de los mismos | |
| JP7022131B2 (ja) | ブルトン型チロシンキナーゼのイミダゾピラジン阻害剤 | |
| TW202417455A (zh) | 新穎三雜環化合物及藥學組成物 | |
| AU2005322855B2 (en) | Pyrimidine derivatives as kinase modulators and method of use | |
| US11098057B2 (en) | 9,10,11,12-tetrahydro-8H-[1,4]diazepino[5′,6′:4,5]thieno[3,2-F]quinolin-8-one compounds and uses thereof | |
| AU2017296338A1 (en) | Novel pyrimidine carboxamides as inhibitors of vanin-1 enzyme | |
| WO2016090079A1 (en) | Heteroaryl compounds and uses thereof | |
| CN113227100A (zh) | 噻吩并吡啶酮化合物 | |
| HK1241225A1 (en) | Mk2 inhibitors and uses thereof | |
| HK1241225B (en) | Mk2 inhibitors and uses thereof | |
| WO2024092115A2 (en) | Mk2 inhibitors and uses thereof | |
| CN117940433A (zh) | 喹啉并呋喃衍生物及其用途 |