ES2904676T3 - Compuestos de amino indol útiles como inhibidores de TLR - Google Patents
Compuestos de amino indol útiles como inhibidores de TLR Download PDFInfo
- Publication number
- ES2904676T3 ES2904676T3 ES18833773T ES18833773T ES2904676T3 ES 2904676 T3 ES2904676 T3 ES 2904676T3 ES 18833773 T ES18833773 T ES 18833773T ES 18833773 T ES18833773 T ES 18833773T ES 2904676 T3 ES2904676 T3 ES 2904676T3
- Authority
- ES
- Spain
- Prior art keywords
- dimethoxyphenyl
- isopropyl
- indol
- indole
- piperazin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000003112 inhibitor Substances 0.000 title description 11
- IHWDSEPNZDYMNF-UHFFFAOYSA-N 1H-indol-2-amine Chemical class C1=CC=C2NC(N)=CC2=C1 IHWDSEPNZDYMNF-UHFFFAOYSA-N 0.000 title description 5
- -1 -OH Chemical group 0.000 claims abstract description 257
- 150000001875 compounds Chemical class 0.000 claims abstract description 153
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims abstract description 72
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 claims abstract description 60
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims abstract description 60
- 125000000719 pyrrolidinyl group Chemical group 0.000 claims abstract description 60
- 150000003839 salts Chemical class 0.000 claims abstract description 49
- 239000012453 solvate Substances 0.000 claims abstract description 45
- 125000002757 morpholinyl group Chemical group 0.000 claims abstract description 40
- 125000004076 pyridyl group Chemical group 0.000 claims abstract description 36
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims abstract description 35
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 32
- 125000003709 fluoroalkyl group Chemical group 0.000 claims abstract description 32
- 125000004193 piperazinyl group Chemical group 0.000 claims abstract description 32
- 150000001204 N-oxides Chemical class 0.000 claims abstract description 31
- 125000001424 substituent group Chemical group 0.000 claims abstract description 31
- 125000003386 piperidinyl group Chemical group 0.000 claims abstract description 30
- 229910052801 chlorine Inorganic materials 0.000 claims abstract description 28
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 28
- 125000000623 heterocyclic group Chemical group 0.000 claims abstract description 26
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims abstract description 23
- 229910052731 fluorine Inorganic materials 0.000 claims abstract description 19
- 125000003944 tolyl group Chemical group 0.000 claims abstract description 17
- 125000002853 C1-C4 hydroxyalkyl group Chemical group 0.000 claims abstract description 16
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims abstract description 15
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 14
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 14
- 125000002393 azetidinyl group Chemical group 0.000 claims abstract description 13
- 125000004103 aminoalkyl group Chemical group 0.000 claims abstract description 12
- 125000005959 diazepanyl group Chemical group 0.000 claims abstract description 12
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims abstract description 12
- 125000004966 cyanoalkyl group Chemical group 0.000 claims abstract description 11
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims abstract description 10
- 125000002883 imidazolyl group Chemical group 0.000 claims abstract description 10
- 125000003039 tetrahydroisoquinolinyl group Chemical group C1(NCCC2=CC=CC=C12)* 0.000 claims abstract description 10
- 125000001412 tetrahydropyranyl group Chemical group 0.000 claims abstract description 10
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims abstract description 10
- 125000004433 nitrogen atom Chemical group N* 0.000 claims abstract description 9
- 125000000168 pyrrolyl group Chemical group 0.000 claims abstract description 9
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 claims abstract description 9
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 8
- 125000005843 halogen group Chemical group 0.000 claims abstract description 7
- 125000001544 thienyl group Chemical group 0.000 claims abstract description 7
- 125000003226 pyrazolyl group Chemical group 0.000 claims abstract description 4
- 125000001425 triazolyl group Chemical group 0.000 claims abstract description 4
- 125000006577 C1-C6 hydroxyalkyl group Chemical group 0.000 claims abstract description 3
- 125000004428 fluoroalkoxy group Chemical group 0.000 claims abstract description 3
- 125000000714 pyrimidinyl group Chemical group 0.000 claims abstract description 3
- 125000000335 thiazolyl group Chemical group 0.000 claims abstract description 3
- 125000003566 oxetanyl group Chemical group 0.000 claims abstract 3
- 201000006417 multiple sclerosis Diseases 0.000 claims description 56
- 239000008194 pharmaceutical composition Substances 0.000 claims description 25
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 16
- 208000023275 Autoimmune disease Diseases 0.000 claims description 15
- 239000003937 drug carrier Substances 0.000 claims description 13
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 13
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 12
- JFNPNEAIJKWMSX-CYBMUJFWSA-N (3R)-N-[3-propan-2-yl-2-(1H-pyrazolo[3,4-b]pyridin-4-yl)-1H-indol-5-yl]pyrrolidine-3-carboxamide Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)NC(=O)[C@H]1CNCC1)C1=C2C(=NC=C1)NN=C2 JFNPNEAIJKWMSX-CYBMUJFWSA-N 0.000 claims description 9
- IULCIEBFFRMCDW-UHFFFAOYSA-N 1-[3-propan-2-yl-2-(1H-pyrazolo[3,4-b]pyridin-4-yl)-1H-indol-5-yl]imidazolidin-2-one Chemical compound CC(C)C1=C(NC2=CC=C(C=C12)N1CCNC1=O)C1=CC=NC2=C1C=NN2 IULCIEBFFRMCDW-UHFFFAOYSA-N 0.000 claims description 8
- YVLSNBJPFWCAGY-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-(1-propan-2-ylazepan-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCN(CC1)C1CCN(CCC1)C(C)C YVLSNBJPFWCAGY-UHFFFAOYSA-N 0.000 claims description 8
- KLBOVSWEOGCQSU-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N,3-diethyl-N-[1-(1-methylpiperidin-4-yl)piperidin-4-yl]-1H-indol-5-amine Chemical compound N1(CCC(N2CCC(N(C3=CC=C4NC(C5=CC(=C(C=C5)OC)OC)=C(C4=C3)CC)CC)CC2)CC1)C KLBOVSWEOGCQSU-UHFFFAOYSA-N 0.000 claims description 8
- LMTRLPVOFZQABZ-UHFFFAOYSA-N 3-[2-(methylamino)ethylamino]-1-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]pyrrolidin-2-one Chemical compound CNCCNC1CCN(C1=O)C1=CC=C2NC(=C(C(C)C)C2=C1)C1=CC(C)=NC=C1 LMTRLPVOFZQABZ-UHFFFAOYSA-N 0.000 claims description 8
- MNTFXNKPNNEWTE-UHFFFAOYSA-N 3-[2-aminoethyl(methyl)amino]-1-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]pyrrolidin-2-one Chemical compound NCCN(C1C(N(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=NC=C1)C)C(C)C)=O)C MNTFXNKPNNEWTE-UHFFFAOYSA-N 0.000 claims description 8
- VGQLXVMGALOXAO-UHFFFAOYSA-N 5-[4-(1,4-diazepan-1-yl)piperidin-1-yl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indole Chemical compound N1(CCNCCC1)C1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C VGQLXVMGALOXAO-UHFFFAOYSA-N 0.000 claims description 8
- OQOYWPNIKQCROM-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-piperazin-1-yl-3-propan-2-yl-1H-indole Chemical class COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCNCC1 OQOYWPNIKQCROM-UHFFFAOYSA-N 0.000 claims description 7
- SPTACRJNTPNJSV-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-(1,2,2,6,6-pentamethylpiperidin-4-yl)-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CC(N(C(C1)(C)C)C)(C)C SPTACRJNTPNJSV-UHFFFAOYSA-N 0.000 claims description 7
- ONXJEHLNFWIHQB-UHFFFAOYSA-N 5-[3-(1,4-diazepan-1-yl)azetidin-1-yl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indole Chemical compound N1(CCNCCC1)C1CN(C1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C ONXJEHLNFWIHQB-UHFFFAOYSA-N 0.000 claims description 7
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 7
- 201000000596 systemic lupus erythematosus Diseases 0.000 claims description 7
- JFNPNEAIJKWMSX-ZDUSSCGKSA-N (3S)-N-[3-propan-2-yl-2-(1H-pyrazolo[3,4-b]pyridin-4-yl)-1H-indol-5-yl]pyrrolidine-3-carboxamide Chemical compound N1C[C@H](CC1)C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=C2C(=NC=C1)NN=C2)C(C)C JFNPNEAIJKWMSX-ZDUSSCGKSA-N 0.000 claims description 6
- QXSBICPTEHJGIA-UHFFFAOYSA-N 1-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]imidazolidin-2-one Chemical compound CC(C)C1=C(NC2=CC=C(C=C12)N1CCNC1=O)C1=CC(C)=NC=C1 QXSBICPTEHJGIA-UHFFFAOYSA-N 0.000 claims description 6
- YWILYONFCMXQFM-UHFFFAOYSA-N 2-[4-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperazin-1-yl]-N-methylethanamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCN(CC1)CCNC YWILYONFCMXQFM-UHFFFAOYSA-N 0.000 claims description 6
- 125000004200 2-methoxyethyl group Chemical group [H]C([H])([H])OC([H])([H])C([H])([H])* 0.000 claims description 6
- WUJWTRGTVWUNAL-UHFFFAOYSA-N 3-[2-(dimethylamino)ethoxy]-1-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]pyrrolidin-2-one Chemical compound CN(CCOC1C(N(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=NC=C1)C)C(C)C)=O)C WUJWTRGTVWUNAL-UHFFFAOYSA-N 0.000 claims description 6
- 125000004183 alkoxy alkyl group Chemical group 0.000 claims description 6
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 claims description 6
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 6
- AHWHTNPWLYWPPW-UHFFFAOYSA-N 1-[2-(2,6-dimethylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]-3-(4-propan-2-ylpiperazin-1-yl)pyrrolidin-2-one Chemical compound CC(C)N1CCN(CC1)C1CCN(C1=O)C1=CC=C2NC(=C(C(C)C)C2=C1)C1=CC(C)=NC(C)=C1 AHWHTNPWLYWPPW-UHFFFAOYSA-N 0.000 claims description 5
- BVQUXCZEYVUIKZ-UHFFFAOYSA-N 4-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-1-N-[2-(methylamino)ethyl]cyclohexane-1,4-diamine Chemical compound C(NC1CCC(NC2=CC=C3C(C(C(C)C)=C(C4=CC=C(C(OC)=C4)OC)N3)=C2)CC1)CNC BVQUXCZEYVUIKZ-UHFFFAOYSA-N 0.000 claims description 5
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 5
- DXQNCFSAOZWIEG-QUCCMNQESA-N (1R,2S)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]cyclohexane-1-carboxamide Chemical compound N[C@@H]1[C@@H](CCCC1)C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C DXQNCFSAOZWIEG-QUCCMNQESA-N 0.000 claims description 4
- UDSXCVPQTLSVMG-LJQANCHMSA-N (2R)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-4-methylpentanamide Chemical compound N[C@@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CC(C)C UDSXCVPQTLSVMG-LJQANCHMSA-N 0.000 claims description 4
- ABYHZDBTSWTEII-MRXNPFEDSA-N (2R)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]butanediamide Chemical compound N[C@@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CC(=O)N ABYHZDBTSWTEII-MRXNPFEDSA-N 0.000 claims description 4
- WOGDXMCPXVFJGM-GOSISDBHSA-N (2R)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]pentanamide Chemical compound N[C@@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CCC WOGDXMCPXVFJGM-GOSISDBHSA-N 0.000 claims description 4
- JIMHNMYQDVBFGA-QGZVFWFLSA-N (2R)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]pentanediamide Chemical compound N[C@@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CCC(=O)N JIMHNMYQDVBFGA-QGZVFWFLSA-N 0.000 claims description 4
- SOBYKXHXFDDVKA-IQMFZBJNSA-N (2R,3R)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-3-methylpentanamide Chemical compound N[C@@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)[C@@H](CC)C SOBYKXHXFDDVKA-IQMFZBJNSA-N 0.000 claims description 4
- FOQVDMQAUAMYQU-SFHVURJKSA-N (2S)-2,5-diamino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]pentanamide Chemical compound N[C@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CCCN FOQVDMQAUAMYQU-SFHVURJKSA-N 0.000 claims description 4
- QMSCMHHNQWMYJJ-IBGZPJMESA-N (2S)-2,6-diamino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]hexanamide Chemical compound N[C@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CCCCN QMSCMHHNQWMYJJ-IBGZPJMESA-N 0.000 claims description 4
- DKTWBTAHWFDCKY-VWLOTQADSA-N (2S)-2-amino-2-cyclohexyl-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]acetamide Chemical compound N[C@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)C1CCCCC1 DKTWBTAHWFDCKY-VWLOTQADSA-N 0.000 claims description 4
- SCSASTCUJSMKTR-VWLOTQADSA-N (2S)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-2-phenylacetamide Chemical compound N[C@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)C1=CC=CC=C1 SCSASTCUJSMKTR-VWLOTQADSA-N 0.000 claims description 4
- ABYHZDBTSWTEII-INIZCTEOSA-N (2S)-2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]butanediamide Chemical compound N[C@H](C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CC(=O)N ABYHZDBTSWTEII-INIZCTEOSA-N 0.000 claims description 4
- BVNWMNFUZIOOCE-KRWDZBQOSA-N (4S)-4-amino-5-[[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]amino]-5-oxopentanoic acid Chemical compound N[C@@H](CCC(=O)O)C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C BVNWMNFUZIOOCE-KRWDZBQOSA-N 0.000 claims description 4
- HDHMFENXTUDGIU-UHFFFAOYSA-N 1-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-4-N-[2-(dimethylamino)ethyl]-4-N-methylcyclohexane-1,4-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N(C)CCN(C)C HDHMFENXTUDGIU-UHFFFAOYSA-N 0.000 claims description 4
- CPUGOFHESYXJFN-UHFFFAOYSA-N 1-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-4-hydroxypyrrolidin-2-one Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)N1CC(O)CC1=O CPUGOFHESYXJFN-UHFFFAOYSA-N 0.000 claims description 4
- RPZPVYMWEXBLOZ-UHFFFAOYSA-N 1-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-N,N-dimethylpiperidin-4-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCC(CC1)N(C)C RPZPVYMWEXBLOZ-UHFFFAOYSA-N 0.000 claims description 4
- XJCDJLUUGLGAIL-UHFFFAOYSA-N 1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-4-[2-(dimethylamino)ethyl]-1,4-diazepan-5-one Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCN(CCN(C)C)C(=O)CC1 XJCDJLUUGLGAIL-UHFFFAOYSA-N 0.000 claims description 4
- DUGTVRQGEMFRRM-UHFFFAOYSA-N 1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-N,N-dimethylpiperidin-4-amine Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)N(C)C DUGTVRQGEMFRRM-UHFFFAOYSA-N 0.000 claims description 4
- UIYZRMBWFPHGNR-UHFFFAOYSA-N 1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-N,N-dimethylpyrrolidin-3-amine Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(C1)N(C)C UIYZRMBWFPHGNR-UHFFFAOYSA-N 0.000 claims description 4
- DFUNYFUTZTYIRD-UHFFFAOYSA-N 1-[4-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-1,4-diazepan-1-yl]ethanone Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)N1CCCN(CC1)C(C)=O DFUNYFUTZTYIRD-UHFFFAOYSA-N 0.000 claims description 4
- CFPBZGSPMQMLOU-UHFFFAOYSA-N 1-[4-[[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]amino]piperidin-1-yl]ethanone Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)NC1CCN(CC1)C(C)=O CFPBZGSPMQMLOU-UHFFFAOYSA-N 0.000 claims description 4
- KFFUZFWIRNYSOD-UHFFFAOYSA-N 2-(2,6-dimethoxypyridin-4-yl)-3-ethyl-5-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC1=NC(=CC(=C1)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)C1CCN(CC1)C)OC KFFUZFWIRNYSOD-UHFFFAOYSA-N 0.000 claims description 4
- HQTCHVFKSGUEBN-UHFFFAOYSA-N 2-(2,6-dimethoxypyridin-4-yl)-3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC1=NC(=CC(=C1)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)C1CCN(CC1)C(C)C)OC HQTCHVFKSGUEBN-UHFFFAOYSA-N 0.000 claims description 4
- AZMVEVBDSIBVAR-UHFFFAOYSA-N 2-(2,6-dimethoxypyridin-4-yl)-3-ethyl-5-piperazin-1-yl-1H-indole Chemical compound COC1=NC(=CC(=C1)C=1NC2=CC=C(C=C2C=1CC)N1CCNCC1)OC AZMVEVBDSIBVAR-UHFFFAOYSA-N 0.000 claims description 4
- IFMAKTASOPSASH-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-(4-piperidin-4-yloxypiperidin-1-yl)-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCC(CC1)OC1CCNCC1 IFMAKTASOPSASH-UHFFFAOYSA-N 0.000 claims description 4
- MMXZWEJCPTVPEN-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-(4-piperidin-4-ylpiperidin-1-yl)-1H-indole Chemical compound N1(CCC(CC1)C1CCNCC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)CC MMXZWEJCPTVPEN-UHFFFAOYSA-N 0.000 claims description 4
- UVSWLDHEJBSRBG-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-ethylpiperidin-4-yl)oxypiperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCC(CC1)OC1CCN(CC1)CC UVSWLDHEJBSRBG-UHFFFAOYSA-N 0.000 claims description 4
- OSCCDFKDDWGOBU-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-ethylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)C1CCN(CC1)CC OSCCDFKDDWGOBU-UHFFFAOYSA-N 0.000 claims description 4
- GTEKYZATQIXIJN-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-methylpiperidin-4-yl)-1,4-diazepan-1-yl]-1H-indole Chemical compound CCC1=C(NC2=CC=C(C=C12)N1CCCN(CC1)C1CCN(C)CC1)C1=CC(OC)=C(OC)C=C1 GTEKYZATQIXIJN-UHFFFAOYSA-N 0.000 claims description 4
- XNYBXVRQVWSJFO-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-methylpiperidin-4-yl)oxypiperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCC(CC1)OC1CCN(CC1)C XNYBXVRQVWSJFO-UHFFFAOYSA-N 0.000 claims description 4
- CLHONIBDKRCCQH-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)C1CCN(CC1)C CLHONIBDKRCCQH-UHFFFAOYSA-N 0.000 claims description 4
- QGHDVTPYLSMEHS-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-6-propan-2-yl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC(=C(C=C2C=1CC)N1CCN(CC1)C1CCN(CC1)C(C)C)C(C)C QGHDVTPYLSMEHS-UHFFFAOYSA-N 0.000 claims description 4
- BMAPVHRSOMHGSN-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-N-[(7-propan-2-yl-7-azaspiro[3.5]nonan-2-yl)methyl]-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)NCC1CC2(C1)CCN(CC2)C(C)C BMAPVHRSOMHGSN-UHFFFAOYSA-N 0.000 claims description 4
- ATFRWASMPMMYRS-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-methyl-5-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C)N1CCN(CC1)C1CCN(CC1)C ATFRWASMPMMYRS-UHFFFAOYSA-N 0.000 claims description 4
- SJJIKRNAIVFGJK-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-methyl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C)N1CCN(CC1)C1CCN(CC1)C(C)C SJJIKRNAIVFGJK-UHFFFAOYSA-N 0.000 claims description 4
- BLYJCPRXQCWACV-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-methyl-5-[4-(2,2,6,6-tetramethylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C)N1CCN(CC1)C1CC(NC(C1)(C)C)(C)C BLYJCPRXQCWACV-UHFFFAOYSA-N 0.000 claims description 4
- IPKIKRNHZGLXBZ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-(2-pyridin-4-ylpiperidin-1-yl)-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1C(CCCC1)C1=CC=NC=C1 IPKIKRNHZGLXBZ-UHFFFAOYSA-N 0.000 claims description 4
- JNGGYHZLBMEVTN-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-(4-pyrrolidin-1-ylpiperidin-1-yl)-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCCC1 JNGGYHZLBMEVTN-UHFFFAOYSA-N 0.000 claims description 4
- ISMNWLFIPFTWHA-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-(2-pyrrolidin-1-ylethyl)piperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)CCN1CCCC1 ISMNWLFIPFTWHA-UHFFFAOYSA-N 0.000 claims description 4
- GYCWJUNAPGRGMS-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-(4-propan-2-ylpiperazin-1-yl)piperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)C(C)C GYCWJUNAPGRGMS-UHFFFAOYSA-N 0.000 claims description 4
- QYSRMSLQMCNKDI-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-[1-(thiophen-3-ylmethyl)piperidin-4-yl]piperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)C1CCN(CC1)CC1=CSC=C1 QYSRMSLQMCNKDI-UHFFFAOYSA-N 0.000 claims description 4
- BAIUOFWVXVDOJU-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-[4-(2-pyrrolidin-1-ylethyl)piperazin-1-yl]piperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)CCN1CCCC1 BAIUOFWVXVDOJU-UHFFFAOYSA-N 0.000 claims description 4
- WUSRHWQSQRRPGK-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-[4-(3-pyrrolidin-1-ylpropyl)piperazin-1-yl]piperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)CCCN1CCCC1 WUSRHWQSQRRPGK-UHFFFAOYSA-N 0.000 claims description 4
- SJZADSJVYQSAOF-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-N-[4-(2-pyrrolidin-1-ylethoxy)phenyl]-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1=CC=C(C=C1)OCCN1CCCC1 SJZADSJVYQSAOF-UHFFFAOYSA-N 0.000 claims description 4
- KHLAPUOWADPBAQ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-(4-pent-4-ynylpiperazin-1-yl)-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCN(CC1)CCCC#C KHLAPUOWADPBAQ-UHFFFAOYSA-N 0.000 claims description 4
- CZZJXLBWWSKXLE-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-(4-piperazin-1-ylpiperidin-1-yl)-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCNCC1 CZZJXLBWWSKXLE-UHFFFAOYSA-N 0.000 claims description 4
- LGVUYPAIZXMFAU-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-(4-piperidin-4-yloxypiperidin-1-yl)-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)OC1CCNCC1 LGVUYPAIZXMFAU-UHFFFAOYSA-N 0.000 claims description 4
- HINAMZSJQBQVCU-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[2,2-dimethyl-4-(1-methylpiperidin-4-yl)piperazin-1-yl]-3-ethyl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1C(CN(CC1)C1CCN(CC1)C)(C)C HINAMZSJQBQVCU-UHFFFAOYSA-N 0.000 claims description 4
- WQYCXWFRPLUFEN-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-(1-ethylpiperidin-4-yl)oxypiperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)OC1CCN(CC1)CC WQYCXWFRPLUFEN-UHFFFAOYSA-N 0.000 claims description 4
- SKZIGKICGLPZAD-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCN(CC1)C1CCN(CC1)C SKZIGKICGLPZAD-UHFFFAOYSA-N 0.000 claims description 4
- ZKTCMJKPJULXTE-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-(4-ethyl-1,4-diazepan-1-yl)piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound CCN1CCCN(CC1)C1CCN(CC1)C1=CC=C2NC(=C(C(C)C)C2=C1)C1=CC(OC)=C(OC)C=C1 ZKTCMJKPJULXTE-UHFFFAOYSA-N 0.000 claims description 4
- DYDUDOOZLCWSSQ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-(4-ethylpiperazin-1-yl)piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)CC DYDUDOOZLCWSSQ-UHFFFAOYSA-N 0.000 claims description 4
- AYUXKSXAYMXHID-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-(4-methyl-1,4-diazepan-1-yl)piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)N1CCCN(C)CC1 AYUXKSXAYMXHID-UHFFFAOYSA-N 0.000 claims description 4
- CRYBHYLNEGTEME-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-(4-methylpiperazin-1-yl)piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)C CRYBHYLNEGTEME-UHFFFAOYSA-N 0.000 claims description 4
- GXCMIKPGQYSUOZ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-[1-[(1-methylpyrrol-2-yl)methyl]piperidin-4-yl]piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)C1CCN(CC1)CC=1N(C=CC=1)C GXCMIKPGQYSUOZ-UHFFFAOYSA-N 0.000 claims description 4
- KSZIVRDHGRAQPK-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)N1CCN(CC1)C1CCN(C)CC1 KSZIVRDHGRAQPK-UHFFFAOYSA-N 0.000 claims description 4
- KZFBCELDMWCEPK-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-[4-(2-methoxyethyl)piperazin-1-yl]piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)CCOC KZFBCELDMWCEPK-UHFFFAOYSA-N 0.000 claims description 4
- MBTMIYNIMJRIKS-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-[4-(2-methylpropyl)piperazin-1-yl]piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)CC(C)C MBTMIYNIMJRIKS-UHFFFAOYSA-N 0.000 claims description 4
- XTCPDZBJSAILAS-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-[4-[(4-methylphenyl)methyl]piperazin-1-yl]piperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)CC1=CC=C(C=C1)C XTCPDZBJSAILAS-UHFFFAOYSA-N 0.000 claims description 4
- COTGPCSSYBATNV-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-(4-ethylpiperazin-1-yl)cyclohexyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)CC COTGPCSSYBATNV-UHFFFAOYSA-N 0.000 claims description 4
- WWTTVEHMQBRIFH-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-(4-methylpiperazin-1-yl)cyclohexyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)C WWTTVEHMQBRIFH-UHFFFAOYSA-N 0.000 claims description 4
- YFMSLXZRIBJPPQ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-[2-(ethylamino)ethoxy]phenyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1=CC=C(C=C1)OCCNCC YFMSLXZRIBJPPQ-UHFFFAOYSA-N 0.000 claims description 4
- MFIDLUYDBMAOSE-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-[4-(2-methylpropyl)piperazin-1-yl]cyclohexyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)CC(C)C MFIDLUYDBMAOSE-UHFFFAOYSA-N 0.000 claims description 4
- FGVNHBLGLHUWHY-UHFFFAOYSA-N 2-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-4-(methylamino)piperidin-4-yl]acetonitrile Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)(NC)CC#N FGVNHBLGLHUWHY-UHFFFAOYSA-N 0.000 claims description 4
- MIFQUJMWAKIMNO-UHFFFAOYSA-N 2-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-N,N-dimethylethanamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)CCN(C)C MIFQUJMWAKIMNO-UHFFFAOYSA-N 0.000 claims description 4
- VHXSJLCFKKHTJR-UHFFFAOYSA-N 2-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]oxy-N,N-dimethylethanamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)OCCN(C)C VHXSJLCFKKHTJR-UHFFFAOYSA-N 0.000 claims description 4
- YWYFBJLUAVNFPO-UHFFFAOYSA-N 2-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]propan-2-ol Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)C(C)(C)O YWYFBJLUAVNFPO-UHFFFAOYSA-N 0.000 claims description 4
- PXDCCYXZQZOZHH-UHFFFAOYSA-N 2-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-2,8-diazaspiro[3.5]nonane Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CC2(C1)CNCCC2 PXDCCYXZQZOZHH-UHFFFAOYSA-N 0.000 claims description 4
- FJPQVELXVROIFY-UHFFFAOYSA-N 2-[4-[2-(3,4-dimethoxyphenyl)-3-ethyl-1H-indol-5-yl]-1,4-diazepan-1-yl]-N-methylethanamine Chemical compound CCC1=C(NC2=CC=C(C=C12)N1CCCN(CCNC)CC1)C1=CC(OC)=C(OC)C=C1 FJPQVELXVROIFY-UHFFFAOYSA-N 0.000 claims description 4
- STXAQTYPHFMICB-UHFFFAOYSA-N 2-[4-[2-(3,4-dimethoxyphenyl)-3-ethyl-1H-indol-5-yl]-3,3-dimethylpiperazin-1-yl]-N-methylethanamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1C(CN(CC1)CCNC)(C)C STXAQTYPHFMICB-UHFFFAOYSA-N 0.000 claims description 4
- OOWYMSSXUQRNCR-UHFFFAOYSA-N 2-[4-[2-(3,4-dimethoxyphenyl)-3-ethyl-1H-indol-5-yl]piperazin-1-yl]-N-methylethanamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)CCNC OOWYMSSXUQRNCR-UHFFFAOYSA-N 0.000 claims description 4
- RYDYPOMRKOSKLM-UHFFFAOYSA-N 2-[4-[2-(3,4-dimethoxyphenyl)-3-ethyl-6-methyl-1H-indol-5-yl]piperazin-1-yl]-N-methylethanamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC(=C(C=C2C=1CC)N1CCN(CC1)CCNC)C RYDYPOMRKOSKLM-UHFFFAOYSA-N 0.000 claims description 4
- QSULZFNIDGLZDG-UHFFFAOYSA-N 2-[4-[3-ethyl-2-(2-methoxypyridin-4-yl)-1H-indol-5-yl]piperazin-1-yl]-N-methylethanamine Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)CCNC)C1=CC(=NC=C1)OC QSULZFNIDGLZDG-UHFFFAOYSA-N 0.000 claims description 4
- POQYOYUIIUTPKF-UHFFFAOYSA-N 2-[4-amino-1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]acetonitrile Chemical compound NC1(CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C)CC#N POQYOYUIIUTPKF-UHFFFAOYSA-N 0.000 claims description 4
- QFJIKIYXEYNKPW-UHFFFAOYSA-N 2-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]acetamide Chemical compound NCC(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C QFJIKIYXEYNKPW-UHFFFAOYSA-N 0.000 claims description 4
- LDYJPANMXWGCOB-UHFFFAOYSA-N 3-[3-methyl-2-(1H-pyrrolo[2,3-b]pyridin-4-yl)-1H-indol-5-yl]-9-[(1-methylpyrrol-2-yl)methyl]-3,9-diazaspiro[5.5]undecane Chemical compound CN1C(=CC=C1)CN1CCC2(CC1)CCN(CC2)C=1C=C2C(=C(NC2=CC=1)C1=C2C(=NC=C1)NC=C2)C LDYJPANMXWGCOB-UHFFFAOYSA-N 0.000 claims description 4
- FOPYIVSTCKLVKC-UHFFFAOYSA-N 3-ethyl-2-(2-methoxypyridin-4-yl)-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C1=CC(=NC=C1)OC FOPYIVSTCKLVKC-UHFFFAOYSA-N 0.000 claims description 4
- AKDYQPPUUGPRHH-UHFFFAOYSA-N 3-ethyl-2-(2-methoxypyridin-4-yl)-5-[4-(2,2,6,6-tetramethylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CC(NC(C1)(C)C)(C)C)C1=CC(=NC=C1)OC AKDYQPPUUGPRHH-UHFFFAOYSA-N 0.000 claims description 4
- IVIGHFJYEQPZHY-UHFFFAOYSA-N 3-ethyl-2-(2-methoxypyridin-4-yl)-5-[4-[1-(2-methylpropyl)piperidin-4-yl]piperazin-1-yl]-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)CC(C)C)C1=CC(=NC=C1)OC IVIGHFJYEQPZHY-UHFFFAOYSA-N 0.000 claims description 4
- PGQGOPTXXNEQGH-UHFFFAOYSA-N 3-ethyl-2-(2-methylpyridin-4-yl)-5-[4-(1-propan-2-ylpiperidin-4-yl)oxypiperidin-1-yl]-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCC(CC1)OC1CCN(CC1)C(C)C)C1=CC(=NC=C1)C PGQGOPTXXNEQGH-UHFFFAOYSA-N 0.000 claims description 4
- IXGXHASSZKKWHK-UHFFFAOYSA-N 3-ethyl-2-(2-methylpyridin-4-yl)-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C1=CC(=NC=C1)C IXGXHASSZKKWHK-UHFFFAOYSA-N 0.000 claims description 4
- WUDFGSDZTGSPPA-UHFFFAOYSA-N 3-ethyl-5-[4-(1-ethylpiperidin-4-yl)piperazin-1-yl]-2-(2-methylpyridin-4-yl)-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)CC)C1=CC(=NC=C1)C WUDFGSDZTGSPPA-UHFFFAOYSA-N 0.000 claims description 4
- NOSAVOGVQJRDRK-UHFFFAOYSA-N 3-ethyl-5-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]-2-(2-methylpyridin-4-yl)-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C)C1=CC(=NC=C1)C NOSAVOGVQJRDRK-UHFFFAOYSA-N 0.000 claims description 4
- OYNNQZJEDMSRNZ-UHFFFAOYSA-N 3-ethyl-5-[4-[1-(2-methylpropyl)piperidin-4-yl]piperazin-1-yl]-2-(2-methylpyridin-4-yl)-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)CC(C)C)C1=CC(=NC=C1)C OYNNQZJEDMSRNZ-UHFFFAOYSA-N 0.000 claims description 4
- WTXIIDWGMONECA-UHFFFAOYSA-N 4-(5-piperazin-1-yl-3-propan-2-yl-1H-indol-2-yl)-1H-pyrrolo[2,3-b]pyridine Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)N1CCNCC1)C1=C2C(=NC=C1)NC=C2 WTXIIDWGMONECA-UHFFFAOYSA-N 0.000 claims description 4
- QCHKPCIFYABBKH-UHFFFAOYSA-N 4-(6-methyl-5-piperazin-1-yl-3-propan-2-yl-1H-indol-2-yl)-1H-pyrazolo[3,4-b]pyridine Chemical compound C(C)(C)C1=C(NC2=CC(=C(C=C12)N1CCNCC1)C)C1=C2C(=NC=C1)NN=C2 QCHKPCIFYABBKH-UHFFFAOYSA-N 0.000 claims description 4
- OAENJRGHZSPYQO-UHFFFAOYSA-N 4-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-1-N-(1-methylpiperidin-4-yl)cyclohexane-1,4-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NC1CCN(CC1)C OAENJRGHZSPYQO-UHFFFAOYSA-N 0.000 claims description 4
- MDNKNVDTRYTIFI-UHFFFAOYSA-N 4-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-1-N-[2-(dimethylamino)ethyl]cyclohexane-1,4-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCN(C)C MDNKNVDTRYTIFI-UHFFFAOYSA-N 0.000 claims description 4
- CNBSAWWNUVFIFB-UHFFFAOYSA-N 4-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-1-N-[3-(dimethylamino)propyl]cyclohexane-1,4-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCCN(C)C CNBSAWWNUVFIFB-UHFFFAOYSA-N 0.000 claims description 4
- KZVIFXTYRVAYIQ-UHFFFAOYSA-N 4-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-4-methylpiperidin-4-yl]morpholine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)(C)N1CCOCC1 KZVIFXTYRVAYIQ-UHFFFAOYSA-N 0.000 claims description 4
- WDPXSIVBYXZZOX-UHFFFAOYSA-N 4-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-2,6-dimethylmorpholine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CC(OC(C1)C)C WDPXSIVBYXZZOX-UHFFFAOYSA-N 0.000 claims description 4
- RNOPURFUARYPSZ-UHFFFAOYSA-N 4-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]morpholine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCOCC1 RNOPURFUARYPSZ-UHFFFAOYSA-N 0.000 claims description 4
- GSYCVAHROAOHNE-UHFFFAOYSA-N 4-[3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indol-2-yl]-1-methylpyrrolo[2,3-b]pyridine Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C1=C2C(=NC=C1)N(C=C2)C GSYCVAHROAOHNE-UHFFFAOYSA-N 0.000 claims description 4
- CZFYDCCFZHBZKU-UHFFFAOYSA-N 4-[3-propan-2-yl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indol-2-yl]-1H-pyrazolo[3,4-b]pyridine Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C1=C2C(=NC=C1)NN=C2 CZFYDCCFZHBZKU-UHFFFAOYSA-N 0.000 claims description 4
- GUHUEKAFBYARBK-UHFFFAOYSA-N 4-amino-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]butanamide Chemical compound NCCCC(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C GUHUEKAFBYARBK-UHFFFAOYSA-N 0.000 claims description 4
- XDHVOWMWFUUYCB-UHFFFAOYSA-N 5-[4-(4-tert-butylpiperazin-1-yl)piperidin-1-yl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indole Chemical compound C(C)(C)(C)N1CCN(CC1)C1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C XDHVOWMWFUUYCB-UHFFFAOYSA-N 0.000 claims description 4
- MVWFJHGLUMEWQD-UHFFFAOYSA-N 9-[2-(3,4-dimethoxyphenyl)-3-ethyl-1H-indol-5-yl]-3-propan-2-yl-3,9-diazaspiro[5.5]undecane Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCC2(CC1)CCN(CC2)C(C)C MVWFJHGLUMEWQD-UHFFFAOYSA-N 0.000 claims description 4
- LGVITJPTAFLUQQ-UHFFFAOYSA-N COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)NCCN1CCOCC1 Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)NCCN1CCOCC1 LGVITJPTAFLUQQ-UHFFFAOYSA-N 0.000 claims description 4
- RSCNQNFSLZQSDP-UHFFFAOYSA-N COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C)N1CCN(CC1)C1CCN(CC1)CC Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C)N1CCN(CC1)C1CCN(CC1)CC RSCNQNFSLZQSDP-UHFFFAOYSA-N 0.000 claims description 4
- SZMWGZWWZHFZLS-UHFFFAOYSA-N N-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-1,2,2,6,6-pentamethylpiperidin-4-amine Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)NC1CC(C)(C)N(C)C(C)(C)C1 SZMWGZWWZHFZLS-UHFFFAOYSA-N 0.000 claims description 4
- VKEPPKQLYCDZJQ-UHFFFAOYSA-N N-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-1-methylpiperidin-4-amine Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)NC1CCN(C)CC1 VKEPPKQLYCDZJQ-UHFFFAOYSA-N 0.000 claims description 4
- MLJZCUPOVOIQJF-UHFFFAOYSA-N N-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-N',N'-dimethylethane-1,2-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)NCCN(C)C MLJZCUPOVOIQJF-UHFFFAOYSA-N 0.000 claims description 4
- AIJGAZPLVMWYMP-UHFFFAOYSA-N N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]morpholine-2-carboxamide Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC(=O)C1CNCCO1 AIJGAZPLVMWYMP-UHFFFAOYSA-N 0.000 claims description 4
- NOROBUNWFGKTIL-UHFFFAOYSA-N N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]pyrrolidine-3-carboxamide Chemical compound N1CC(CC1)C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C NOROBUNWFGKTIL-UHFFFAOYSA-N 0.000 claims description 4
- WGIXADJTARJXOG-UHFFFAOYSA-N N-[4-(4-tert-butylpiperazin-1-yl)cyclohexyl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-amine Chemical compound C(C)(C)(C)N1CCN(CC1)C1CCC(CC1)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C WGIXADJTARJXOG-UHFFFAOYSA-N 0.000 claims description 4
- GJVHXACVXVRBPN-UHFFFAOYSA-N N-methyl-2-[4-[3-propan-2-yl-2-(1H-pyrrolo[2,3-b]pyridin-4-yl)-1H-indol-5-yl]piperazin-1-yl]ethanamine Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)CCNC)C1=C2C(=NC=C1)NC=C2 GJVHXACVXVRBPN-UHFFFAOYSA-N 0.000 claims description 4
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 4
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 4
- VQLJAGPSKAQRSD-UHFFFAOYSA-N 1-N-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-4-N-[3-(dimethylamino)propyl]-4-N-methylcyclohexane-1,4-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N(C)CCCN(C)C VQLJAGPSKAQRSD-UHFFFAOYSA-N 0.000 claims description 3
- IFGVYMZTDLYUAZ-UHFFFAOYSA-N 1-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-2-methyl-3,4-dihydro-1H-isoquinoline Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)C1N(C)CCC2=C1C=CC=C2 IFGVYMZTDLYUAZ-UHFFFAOYSA-N 0.000 claims description 3
- NLEFAIZNEZZBEX-UHFFFAOYSA-N 1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-3-(dimethylamino)pyrrolidin-2-one Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1C(C(CC1)N(C)C)=O NLEFAIZNEZZBEX-UHFFFAOYSA-N 0.000 claims description 3
- 208000037976 chronic inflammation Diseases 0.000 claims description 3
- 208000037893 chronic inflammatory disorder Diseases 0.000 claims description 3
- 125000002632 imidazolidinyl group Chemical group 0.000 claims description 3
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims description 3
- 238000002560 therapeutic procedure Methods 0.000 claims description 3
- HVOSVHKJGADUCT-UHFFFAOYSA-N 1-[4-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]piperazin-1-yl]ethanone Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N1CCN(CC1)C(C)=O HVOSVHKJGADUCT-UHFFFAOYSA-N 0.000 claims description 2
- JMIQDZRJADWZKR-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-N-[1-(1-methylpiperidin-4-yl)piperidin-4-yl]-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)NC1CCN(CC1)C1CCN(CC1)C JMIQDZRJADWZKR-UHFFFAOYSA-N 0.000 claims description 2
- WRLJSMPPEWRHCK-UHFFFAOYSA-N 4-[3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indol-2-yl]-1H-pyrazolo[3,4-b]pyridine Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C1=C2C(=NC=C1)NN=C2 WRLJSMPPEWRHCK-UHFFFAOYSA-N 0.000 claims description 2
- VKQMLNRCMCZRLT-UHFFFAOYSA-N 4-[3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indol-2-yl]-1H-pyrrolo[2,3-b]pyridine Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C1=C2C(=NC=C1)NC=C2 VKQMLNRCMCZRLT-UHFFFAOYSA-N 0.000 claims description 2
- JAVOJIDANFTHBB-UHFFFAOYSA-N 4-[3-methyl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indol-2-yl]-1H-pyrrolo[2,3-b]pyridine Chemical compound C(C)(C)N1CCC(CC1)N1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=C2C(=NC=C1)NC=C2)C JAVOJIDANFTHBB-UHFFFAOYSA-N 0.000 claims description 2
- QKBQZZSXGPNXPB-UHFFFAOYSA-N 4-[3-methyl-5-[4-[1-(2-methylpropyl)piperidin-4-yl]piperazin-1-yl]-1H-indol-2-yl]-1H-pyrrolo[2,3-b]pyridine Chemical compound C(C(C)C)N1CCC(CC1)N1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=C2C(=NC=C1)NC=C2)C QKBQZZSXGPNXPB-UHFFFAOYSA-N 0.000 claims description 2
- VFYGBAOTGCHXHQ-UHFFFAOYSA-N 4-[3-propan-2-yl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indol-2-yl]-1H-pyrrolo[2,3-b]pyridine Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C1=C2C(=NC=C1)NC=C2 VFYGBAOTGCHXHQ-UHFFFAOYSA-N 0.000 claims description 2
- IFFWQFQPRKNIID-UHFFFAOYSA-N 4-[5-[4-(1-ethylpiperidin-4-yl)piperazin-1-yl]-3-methyl-1H-indol-2-yl]-1H-pyrrolo[2,3-b]pyridine Chemical compound C(C)N1CCC(CC1)N1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=C2C(=NC=C1)NC=C2)C IFFWQFQPRKNIID-UHFFFAOYSA-N 0.000 claims description 2
- RESRMRJOGRPGTD-UHFFFAOYSA-N CC1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C)C1=C2C(=NC=C1)NC=C2 Chemical compound CC1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)C)C1=C2C(=NC=C1)NC=C2 RESRMRJOGRPGTD-UHFFFAOYSA-N 0.000 claims description 2
- LAGBDBBYZMTYOO-UHFFFAOYSA-N N'-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-N,N,N'-trimethylpropane-1,3-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)N(CCCN(C)C)C LAGBDBBYZMTYOO-UHFFFAOYSA-N 0.000 claims description 2
- YVUUPQVRSUQODP-UHFFFAOYSA-N N-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-N',N'-dimethylpropane-1,3-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)NCCCN(C)C YVUUPQVRSUQODP-UHFFFAOYSA-N 0.000 claims description 2
- 208000021386 Sjogren Syndrome Diseases 0.000 claims description 2
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 claims description 2
- 125000004194 piperazin-1-yl group Chemical group [H]N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 claims description 2
- IVAJRYGUNZIMEY-UHFFFAOYSA-N 1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-N-(1-propan-2-ylpiperidin-4-yl)piperidin-4-amine Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)NC1CCN(CC1)C(C)C IVAJRYGUNZIMEY-UHFFFAOYSA-N 0.000 claims 2
- SGCYRZDGEZNDHE-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)-1,4-diazepan-1-yl]-1H-indole Chemical compound CCC1=C(NC2=CC=C(C=C12)N1CCCN(CC1)C1CCN(CC1)C(C)C)C1=CC(OC)=C(OC)C=C1 SGCYRZDGEZNDHE-UHFFFAOYSA-N 0.000 claims 2
- UIRUFGURZDZFAE-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)oxypiperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCC(CC1)OC1CCN(CC1)C(C)C UIRUFGURZDZFAE-UHFFFAOYSA-N 0.000 claims 2
- OETQUHWBCQUZFO-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)C1CCN(CC1)C(C)C OETQUHWBCQUZFO-UHFFFAOYSA-N 0.000 claims 2
- JGJDQYFFEUEGRG-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-(2,2,6,6-tetramethylpiperidin-4-yl)piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)C1CC(NC(C1)(C)C)(C)C JGJDQYFFEUEGRG-UHFFFAOYSA-N 0.000 claims 2
- OTLXKVTWKZKZOQ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-[1-(2-methylpropyl)piperidin-4-yl]piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCN(CC1)C1CCN(CC1)CC(C)C OTLXKVTWKZKZOQ-UHFFFAOYSA-N 0.000 claims 2
- QBJWLMAYASCFLI-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-methyl-5-[4-[1-(2-methylpropyl)piperidin-4-yl]piperazin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C)N1CCN(CC1)C1CCN(CC1)CC(C)C QBJWLMAYASCFLI-UHFFFAOYSA-N 0.000 claims 2
- LXAPXNIEHHDQDG-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-[1-(3,3,3-trifluoropropyl)piperidin-4-yl]piperidin-1-yl]-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)C1CCN(CC1)CCC(F)(F)F LXAPXNIEHHDQDG-UHFFFAOYSA-N 0.000 claims 2
- WSNMJSKNBFOIFG-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-[4-(1-methylpiperidin-4-yl)oxypiperidin-1-yl]-3-propan-2-yl-1H-indole Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)OC1CCN(CC1)C WSNMJSKNBFOIFG-UHFFFAOYSA-N 0.000 claims 2
- LBRLPFJJVKGVIP-UHFFFAOYSA-N 3-[2-(3,4-dimethoxyphenyl)-3-ethyl-1H-indol-5-yl]-9-methyl-3,9-diazaspiro[5.5]undecane Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N1CCC2(CC1)CCN(CC2)C LBRLPFJJVKGVIP-UHFFFAOYSA-N 0.000 claims 2
- GDGZWLOHRXAXHK-UHFFFAOYSA-N 4-[3-ethyl-5-[4-(1-propan-2-ylpiperidin-4-yl)oxypiperidin-1-yl]-1H-indol-2-yl]-1H-pyrazolo[3,4-b]pyridine Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCC(CC1)OC1CCN(CC1)C(C)C)C1=C2C(=NC=C1)NN=C2 GDGZWLOHRXAXHK-UHFFFAOYSA-N 0.000 claims 2
- PUZGILYGSVNZCV-UHFFFAOYSA-N 4-[6-methyl-3-propan-2-yl-5-[4-(1-propan-2-ylpiperidin-4-yl)piperazin-1-yl]-1H-indol-2-yl]-1H-pyrazolo[3,4-b]pyridine Chemical compound C(C)(C)C1=C(NC2=CC(=C(C=C12)N1CCN(CC1)C1CCN(CC1)C(C)C)C)C1=C2C(=NC=C1)NN=C2 PUZGILYGSVNZCV-UHFFFAOYSA-N 0.000 claims 2
- HSKPHCQIERBIFV-UHFFFAOYSA-N 5-[4-(4-cyclopentylpiperazin-1-yl)piperidin-1-yl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indole Chemical compound C1(CCCC1)N1CCN(CC1)C1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C HSKPHCQIERBIFV-UHFFFAOYSA-N 0.000 claims 2
- ZAIUIHWPSGWFNF-UHFFFAOYSA-N 5-[4-[4-(cyclopropylmethyl)piperazin-1-yl]piperidin-1-yl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indole Chemical compound C1(CC1)CN1CCN(CC1)C1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C ZAIUIHWPSGWFNF-UHFFFAOYSA-N 0.000 claims 2
- GVVBYNQWZFXXSR-UHFFFAOYSA-N 6-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-1,2,3,4,4a,5,7,7a-octahydropyrrolo[3,4-b]pyridine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CC2NCCCC2C1 GVVBYNQWZFXXSR-UHFFFAOYSA-N 0.000 claims 2
- UQJHWEAJOPRLSU-UHFFFAOYSA-N 6-benzyl-1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]-3,4,4a,5,7,7a-hexahydro-2H-pyrrolo[3,4-b]pyridine Chemical compound C(C1=CC=CC=C1)N1CC2N(CCCC2C1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C UQJHWEAJOPRLSU-UHFFFAOYSA-N 0.000 claims 2
- DSUJSRJAASRMCS-UHFFFAOYSA-N 9-[2-(3,4-dimethoxyphenyl)-3-ethyl-6-methyl-1H-indol-5-yl]-3-propan-2-yl-3,9-diazaspiro[5.5]undecane Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC(=C(C=C2C=1CC)N1CCC2(CC1)CCN(CC2)C(C)C)C DSUJSRJAASRMCS-UHFFFAOYSA-N 0.000 claims 2
- BDCMWPYONXMUTO-UHFFFAOYSA-N N'-[1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-yl]-N-methylethane-1,2-diamine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)NCCNC BDCMWPYONXMUTO-UHFFFAOYSA-N 0.000 claims 2
- NJDLTTOXNNHOAJ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-ethyl-5-[4-[1-(2,2,6,6-tetramethylpiperidin-4-yl)piperidin-4-yl]oxypiperidin-1-yl]-1H-indole Chemical compound CCC1=C(NC2=CC=C(C=C12)N1CCC(CC1)OC1CCN(CC1)C1CC(C)(C)NC(C)(C)C1)C1=CC(OC)=C(OC)C=C1 NJDLTTOXNNHOAJ-UHFFFAOYSA-N 0.000 claims 1
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical compound CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 claims 1
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 108
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 75
- YMWUJEATGCHHMB-UHFFFAOYSA-N methylene chloride Substances ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 55
- 239000000203 mixture Substances 0.000 description 53
- 238000000034 method Methods 0.000 description 51
- 239000012071 phase Substances 0.000 description 51
- 230000014759 maintenance of location Effects 0.000 description 49
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 48
- 239000011541 reaction mixture Substances 0.000 description 43
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical class OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 40
- 238000006243 chemical reaction Methods 0.000 description 39
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 39
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 38
- 239000000243 solution Substances 0.000 description 38
- 235000002639 sodium chloride Nutrition 0.000 description 34
- 201000010099 disease Diseases 0.000 description 32
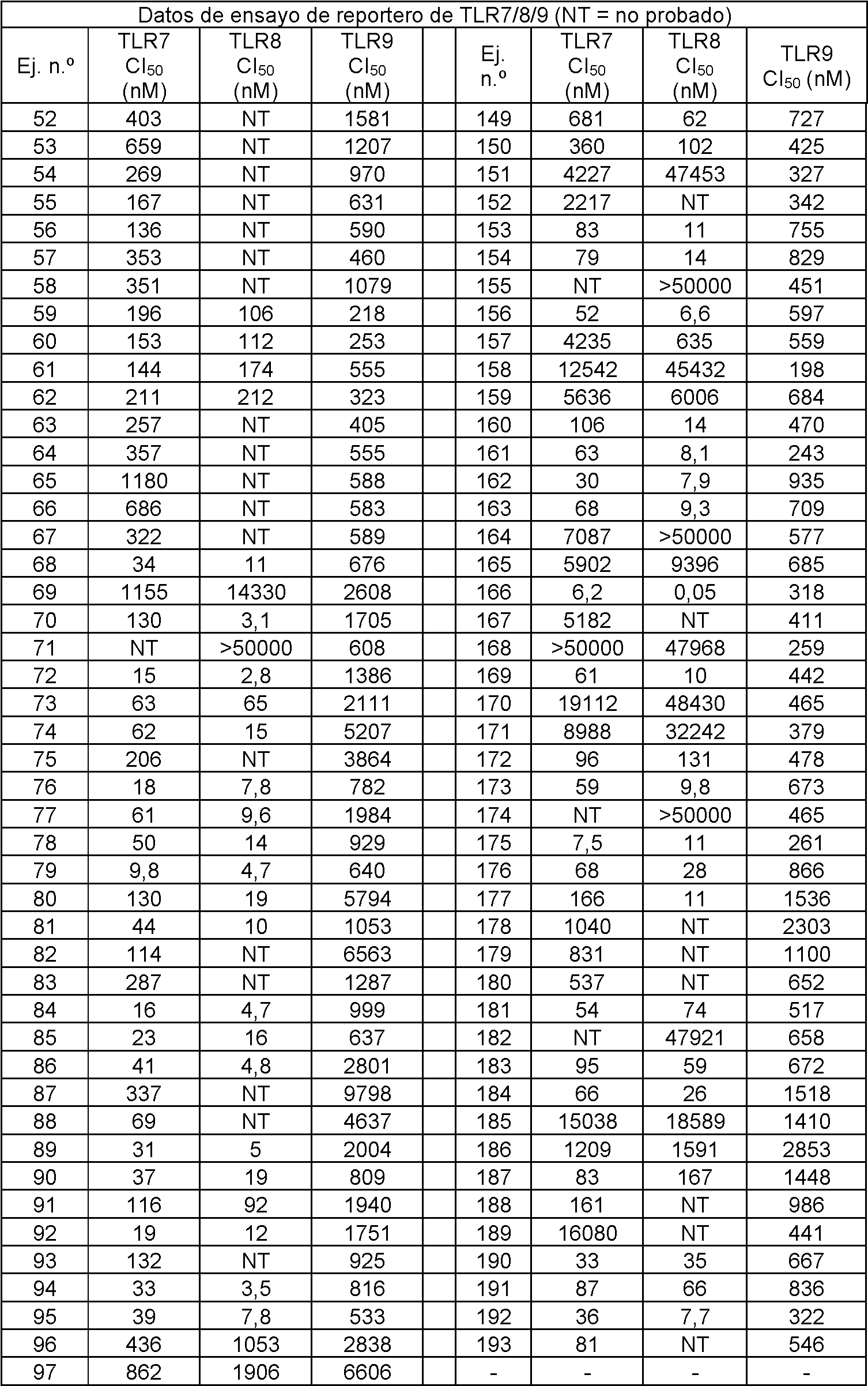
- 102100039390 Toll-like receptor 7 Human genes 0.000 description 30
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 29
- 239000000543 intermediate Substances 0.000 description 29
- 239000007787 solid Substances 0.000 description 27
- 101000669402 Homo sapiens Toll-like receptor 7 Proteins 0.000 description 25
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Chemical class OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 24
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 22
- 102100033110 Toll-like receptor 8 Human genes 0.000 description 20
- 102000008235 Toll-Like Receptor 9 Human genes 0.000 description 19
- 108010060818 Toll-Like Receptor 9 Proteins 0.000 description 19
- 229910001873 dinitrogen Inorganic materials 0.000 description 19
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 18
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 18
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 18
- 239000002904 solvent Substances 0.000 description 18
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 17
- 238000001514 detection method Methods 0.000 description 17
- 235000019439 ethyl acetate Nutrition 0.000 description 17
- 238000004128 high performance liquid chromatography Methods 0.000 description 17
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 16
- 239000003643 water by type Substances 0.000 description 16
- 125000004093 cyano group Chemical group *C#N 0.000 description 15
- 238000005160 1H NMR spectroscopy Methods 0.000 description 14
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 14
- 238000002360 preparation method Methods 0.000 description 14
- 229910052938 sodium sulfate Inorganic materials 0.000 description 14
- 235000011152 sodium sulphate Nutrition 0.000 description 14
- 101000800483 Homo sapiens Toll-like receptor 8 Proteins 0.000 description 13
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 13
- 238000004519 manufacturing process Methods 0.000 description 13
- 239000000725 suspension Substances 0.000 description 13
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- 239000000872 buffer Substances 0.000 description 12
- 239000012043 crude product Substances 0.000 description 12
- 239000003814 drug Substances 0.000 description 12
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 11
- 241000124008 Mammalia Species 0.000 description 11
- 102000002689 Toll-like receptor Human genes 0.000 description 11
- 108020000411 Toll-like receptor Proteins 0.000 description 11
- 239000005695 Ammonium acetate Substances 0.000 description 10
- 235000019257 ammonium acetate Nutrition 0.000 description 10
- 229940043376 ammonium acetate Drugs 0.000 description 10
- 239000013058 crude material Substances 0.000 description 10
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 10
- 239000003921 oil Substances 0.000 description 10
- 235000019198 oils Nutrition 0.000 description 10
- 239000002245 particle Substances 0.000 description 10
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 9
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 9
- 239000002671 adjuvant Substances 0.000 description 9
- 125000004432 carbon atom Chemical group C* 0.000 description 9
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 8
- 229910000024 caesium carbonate Inorganic materials 0.000 description 8
- 239000003995 emulsifying agent Substances 0.000 description 8
- 238000009472 formulation Methods 0.000 description 8
- 239000000463 material Substances 0.000 description 8
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 8
- 238000002953 preparative HPLC Methods 0.000 description 8
- 239000000377 silicon dioxide Substances 0.000 description 8
- 239000003826 tablet Substances 0.000 description 8
- 229940124597 therapeutic agent Drugs 0.000 description 8
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 8
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 7
- 108010060752 Toll-Like Receptor 8 Proteins 0.000 description 7
- 239000004480 active ingredient Substances 0.000 description 7
- 239000012267 brine Substances 0.000 description 7
- 239000003795 chemical substances by application Substances 0.000 description 7
- 238000004440 column chromatography Methods 0.000 description 7
- 235000014113 dietary fatty acids Nutrition 0.000 description 7
- 208000035475 disorder Diseases 0.000 description 7
- 239000000194 fatty acid Substances 0.000 description 7
- 229930195729 fatty acid Natural products 0.000 description 7
- 239000000796 flavoring agent Substances 0.000 description 7
- 239000003755 preservative agent Substances 0.000 description 7
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 7
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 7
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 108010060825 Toll-Like Receptor 7 Proteins 0.000 description 6
- VZTDIZULWFCMLS-UHFFFAOYSA-N ammonium formate Chemical compound [NH4+].[O-]C=O VZTDIZULWFCMLS-UHFFFAOYSA-N 0.000 description 6
- 239000000969 carrier Substances 0.000 description 6
- 239000003153 chemical reaction reagent Substances 0.000 description 6
- 239000003085 diluting agent Substances 0.000 description 6
- 150000002148 esters Chemical class 0.000 description 6
- 150000004665 fatty acids Chemical class 0.000 description 6
- 208000027866 inflammatory disease Diseases 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 239000012044 organic layer Substances 0.000 description 6
- 230000036961 partial effect Effects 0.000 description 6
- 239000000546 pharmaceutical excipient Substances 0.000 description 6
- 102000005962 receptors Human genes 0.000 description 6
- 108020003175 receptors Proteins 0.000 description 6
- 238000010898 silica gel chromatography Methods 0.000 description 6
- 239000003765 sweetening agent Substances 0.000 description 6
- 239000000080 wetting agent Substances 0.000 description 6
- 229920000858 Cyclodextrin Polymers 0.000 description 5
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 5
- 239000007900 aqueous suspension Substances 0.000 description 5
- 239000002775 capsule Substances 0.000 description 5
- 210000004027 cell Anatomy 0.000 description 5
- 239000007859 condensation product Substances 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 239000000839 emulsion Substances 0.000 description 5
- 235000019197 fats Nutrition 0.000 description 5
- 235000013355 food flavoring agent Nutrition 0.000 description 5
- 235000003599 food sweetener Nutrition 0.000 description 5
- 208000015181 infectious disease Diseases 0.000 description 5
- 239000003446 ligand Substances 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 231100000252 nontoxic Toxicity 0.000 description 5
- 230000003000 nontoxic effect Effects 0.000 description 5
- 230000011664 signaling Effects 0.000 description 5
- 239000003381 stabilizer Substances 0.000 description 5
- 239000003981 vehicle Substances 0.000 description 5
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 4
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 4
- KVNWQLSSEYAXKE-UHFFFAOYSA-N 4-(5-bromo-3-propan-2-yl-1H-indol-2-yl)-1-tritylpyrazolo[3,4-b]pyridine Chemical compound BrC=1C=C2C(=C(NC2=CC=1)C1=C2C(=NC=C1)N(N=C2)C(C1=CC=CC=C1)(C1=CC=CC=C1)C1=CC=CC=C1)C(C)C KVNWQLSSEYAXKE-UHFFFAOYSA-N 0.000 description 4
- LALIORMAUQIDCI-UHFFFAOYSA-N 5-bromo-2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indole Chemical compound BrC=1C=C2C(=C(NC2=CC=1)C1=CC(=NC=C1)C)C(C)C LALIORMAUQIDCI-UHFFFAOYSA-N 0.000 description 4
- OJIJONZBYJVFFF-UHFFFAOYSA-N 5-bromo-2-iodo-3-propan-2-yl-1H-indole Chemical compound BrC=1C=C2C(=C(NC2=CC=1)I)C(C)C OJIJONZBYJVFFF-UHFFFAOYSA-N 0.000 description 4
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 4
- RVWDEOHMEBDIEL-UHFFFAOYSA-N ClC=1C=C2C(=C(N(C2=CC=1)C(=O)OC(C)(C)C)C1=CC(=C(C=C1)OC)OC)C(C)C Chemical compound ClC=1C=C2C(=C(N(C2=CC=1)C(=O)OC(C)(C)C)C1=CC(=C(C=C1)OC)OC)C(C)C RVWDEOHMEBDIEL-UHFFFAOYSA-N 0.000 description 4
- 206010009900 Colitis ulcerative Diseases 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical class CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical class CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 208000034578 Multiple myelomas Diseases 0.000 description 4
- 206010028980 Neoplasm Diseases 0.000 description 4
- 208000002193 Pain Diseases 0.000 description 4
- 206010035226 Plasma cell myeloma Diseases 0.000 description 4
- 239000002202 Polyethylene glycol Substances 0.000 description 4
- 102100038280 Prostaglandin G/H synthase 2 Human genes 0.000 description 4
- 206010063837 Reperfusion injury Diseases 0.000 description 4
- 201000006704 Ulcerative Colitis Diseases 0.000 description 4
- 239000013543 active substance Substances 0.000 description 4
- 125000003545 alkoxy group Chemical group 0.000 description 4
- 208000026935 allergic disease Diseases 0.000 description 4
- 239000003963 antioxidant agent Substances 0.000 description 4
- 235000006708 antioxidants Nutrition 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 239000002270 dispersing agent Substances 0.000 description 4
- 239000008187 granular material Substances 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 239000010410 layer Substances 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 230000036407 pain Effects 0.000 description 4
- 229920003023 plastic Polymers 0.000 description 4
- 239000004033 plastic Substances 0.000 description 4
- 229920001223 polyethylene glycol Polymers 0.000 description 4
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 4
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 4
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 4
- 229910000027 potassium carbonate Inorganic materials 0.000 description 4
- 235000015320 potassium carbonate Nutrition 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 239000012041 precatalyst Substances 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 230000002062 proliferating effect Effects 0.000 description 4
- 238000002390 rotary evaporation Methods 0.000 description 4
- 239000000375 suspending agent Substances 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- WYURNTSHIVDZCO-UHFFFAOYSA-N tetrahydrofuran Substances C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- UGOMMVLRQDMAQQ-UHFFFAOYSA-N xphos Chemical compound CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 UGOMMVLRQDMAQQ-UHFFFAOYSA-N 0.000 description 4
- ZAILJGQNFGUOIU-UHFFFAOYSA-N 1-[2-(2,6-dimethylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]-3-piperazin-1-ylpyrrolidin-2-one Chemical compound CC(C)C1=C(NC2=CC=C(C=C12)N1CCC(N2CCNCC2)C1=O)C1=CC(C)=NC(C)=C1 ZAILJGQNFGUOIU-UHFFFAOYSA-N 0.000 description 3
- JGNPXTDWINWLQP-UHFFFAOYSA-N 1-[3-propan-2-yl-2-(1-tritylpyrazolo[3,4-b]pyridin-4-yl)-1H-indol-5-yl]imidazolidin-2-one Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)N1C(NCC1)=O)C1=C2C(=NC=C1)N(N=C2)C(C1=CC=CC=C1)(C1=CC=CC=C1)C1=CC=CC=C1 JGNPXTDWINWLQP-UHFFFAOYSA-N 0.000 description 3
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 3
- USQMPYFHBFLRKT-UHFFFAOYSA-N 2,4-dibromo-N-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]butanamide Chemical compound BrC(C(=O)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=NC=C1)C)C(C)C)CCBr USQMPYFHBFLRKT-UHFFFAOYSA-N 0.000 description 3
- DFCJIHLQJGFKIW-UHFFFAOYSA-N 2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-amine Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)N)C1=CC(=NC=C1)C DFCJIHLQJGFKIW-UHFFFAOYSA-N 0.000 description 3
- KKXINILIYQBCRB-UHFFFAOYSA-N 3-bromo-1-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]pyrrolidin-2-one Chemical compound BrC1C(N(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=NC=C1)C)C(C)C)=O KKXINILIYQBCRB-UHFFFAOYSA-N 0.000 description 3
- WHANOPMZBUMSDB-UHFFFAOYSA-N 3-hydroxy-1-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]pyrrolidin-2-one Chemical compound OC1C(N(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=NC=C1)C)C(C)C)=O WHANOPMZBUMSDB-UHFFFAOYSA-N 0.000 description 3
- YVEPRAAAPQFQDH-UHFFFAOYSA-N 3-propan-2-yl-2-(1H-pyrazolo[3,4-b]pyridin-4-yl)-1H-indol-5-amine Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)N)C1=C2C(=NC=C1)NN=C2 YVEPRAAAPQFQDH-UHFFFAOYSA-N 0.000 description 3
- GDASLEYMRAIZOG-UHFFFAOYSA-N 5-[4-(azepan-4-yl)piperazin-1-yl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indole Chemical compound N1CCC(CCC1)N1CCN(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C GDASLEYMRAIZOG-UHFFFAOYSA-N 0.000 description 3
- FBNRLQRIMLEPOY-UHFFFAOYSA-N 5-bromo-3-propan-2-yl-1h-indole Chemical compound C1=C(Br)C=C2C(C(C)C)=CNC2=C1 FBNRLQRIMLEPOY-UHFFFAOYSA-N 0.000 description 3
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 3
- 201000006474 Brain Ischemia Diseases 0.000 description 3
- 206010008120 Cerebral ischaemia Diseases 0.000 description 3
- 208000011231 Crohn disease Diseases 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- WMONLBJNOJLQJB-UHFFFAOYSA-N FC(C(=O)O)(F)F.COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N(C1CCNCC1)CC Chemical compound FC(C(=O)O)(F)F.COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1CC)N(C1CCNCC1)CC WMONLBJNOJLQJB-UHFFFAOYSA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 201000005569 Gout Diseases 0.000 description 3
- 206010061218 Inflammation Diseases 0.000 description 3
- 102000019223 Interleukin-1 receptor Human genes 0.000 description 3
- 108050006617 Interleukin-1 receptor Proteins 0.000 description 3
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 201000004681 Psoriasis Diseases 0.000 description 3
- 206010040070 Septic Shock Diseases 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 3
- 208000006011 Stroke Diseases 0.000 description 3
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 description 3
- 241000700605 Viruses Species 0.000 description 3
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 230000002491 angiogenic effect Effects 0.000 description 3
- 125000003725 azepanyl group Chemical group 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000037396 body weight Effects 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 206010008118 cerebral infarction Diseases 0.000 description 3
- 239000003086 colorant Substances 0.000 description 3
- 239000006184 cosolvent Substances 0.000 description 3
- 229940079593 drug Drugs 0.000 description 3
- 125000001153 fluoro group Chemical group F* 0.000 description 3
- 239000007903 gelatin capsule Substances 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 3
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 3
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 3
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 230000004054 inflammatory process Effects 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 239000008101 lactose Substances 0.000 description 3
- 235000010445 lecithin Nutrition 0.000 description 3
- 239000000787 lecithin Substances 0.000 description 3
- 229940067606 lecithin Drugs 0.000 description 3
- 229940057995 liquid paraffin Drugs 0.000 description 3
- 206010025135 lupus erythematosus Diseases 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 239000004530 micro-emulsion Substances 0.000 description 3
- 208000010125 myocardial infarction Diseases 0.000 description 3
- 230000004770 neurodegeneration Effects 0.000 description 3
- 208000015122 neurodegenerative disease Diseases 0.000 description 3
- 239000000346 nonvolatile oil Substances 0.000 description 3
- 239000004006 olive oil Substances 0.000 description 3
- 235000008390 olive oil Nutrition 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 239000000123 paper Substances 0.000 description 3
- 239000003208 petroleum Substances 0.000 description 3
- 230000002335 preservative effect Effects 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 229920006395 saturated elastomer Polymers 0.000 description 3
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 3
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 239000001993 wax Substances 0.000 description 3
- UFYBTLOLWSABAU-UHFFFAOYSA-N (2-methylpyridin-4-yl)boronic acid Chemical compound CC1=CC(B(O)O)=CC=N1 UFYBTLOLWSABAU-UHFFFAOYSA-N 0.000 description 2
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 2
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 2
- TVUDGCLAPGUZEC-UHFFFAOYSA-N 1-[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]piperidin-4-one Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCC(CC1)=O TVUDGCLAPGUZEC-UHFFFAOYSA-N 0.000 description 2
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 2
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 2
- ISWYMTFOZAZEIC-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-5-[4-(4-pyridin-4-ylpiperazin-1-yl)piperidin-1-yl]-1H-indole Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(=CC=C2N1)N1CCC(CC1)N1CCN(CC1)C1=CC=NC=C1 ISWYMTFOZAZEIC-UHFFFAOYSA-N 0.000 description 2
- IQQBZTQHCIIERA-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-N-[4-(4-pyridin-4-ylpiperazin-1-yl)cyclohexyl]-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)C1=CC=NC=C1 IQQBZTQHCIIERA-UHFFFAOYSA-N 0.000 description 2
- YLDMZXJBBXKIFI-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-N-[4-[4-(2-pyrrolidin-1-ylethyl)piperazin-1-yl]cyclohexyl]-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)CCN1CCCC1 YLDMZXJBBXKIFI-UHFFFAOYSA-N 0.000 description 2
- JNWRGDQAEYJJQO-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-3-propan-2-yl-N-[4-[4-(3-pyrrolidin-1-ylpropyl)piperazin-1-yl]cyclohexyl]-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)CCCN1CCCC1 JNWRGDQAEYJJQO-UHFFFAOYSA-N 0.000 description 2
- OMVQISRHLPDLIJ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-(1,4-dioxaspiro[4.5]decan-8-yl)-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC2(OCCO2)CC1 OMVQISRHLPDLIJ-UHFFFAOYSA-N 0.000 description 2
- SMOITQSTVVHUPE-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-[4-(2-methoxyethyl)piperazin-1-yl]cyclohexyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)CCOC SMOITQSTVVHUPE-UHFFFAOYSA-N 0.000 description 2
- WHJLHRMDHTVSRV-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-[4-(dimethylamino)piperidin-1-yl]cyclohexyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCC(CC1)N(C)C WHJLHRMDHTVSRV-UHFFFAOYSA-N 0.000 description 2
- KGHRRBIWCCLROW-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-[4-[(4-methylphenyl)methyl]piperazin-1-yl]cyclohexyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)CC1=CC=C(C=C1)C KGHRRBIWCCLROW-UHFFFAOYSA-N 0.000 description 2
- VVSZHJMTMRRXAU-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-methyl-N-[(1-methylpyrrolidin-2-yl)methyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N(CC1N(CCC1)C)C VVSZHJMTMRRXAU-UHFFFAOYSA-N 0.000 description 2
- IZHVBANLECCAGF-UHFFFAOYSA-N 2-hydroxy-3-(octadecanoyloxy)propyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)COC(=O)CCCCCCCCCCCCCCCCC IZHVBANLECCAGF-UHFFFAOYSA-N 0.000 description 2
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 2
- NFGADJHVZXHYHE-UHFFFAOYSA-N 3-ethyl-5-[4-(1-ethylpiperidin-4-yl)piperazin-1-yl]-2-(2-methoxypyridin-4-yl)-1H-indole Chemical compound C(C)C1=C(NC2=CC=C(C=C12)N1CCN(CC1)C1CCN(CC1)CC)C1=CC(=NC=C1)OC NFGADJHVZXHYHE-UHFFFAOYSA-N 0.000 description 2
- SLSFBNQTXUTOMH-UHFFFAOYSA-N 4-[[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]amino]cyclohexan-1-one Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)=O SLSFBNQTXUTOMH-UHFFFAOYSA-N 0.000 description 2
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- 244000215068 Acacia senegal Species 0.000 description 2
- 235000006491 Acacia senegal Nutrition 0.000 description 2
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 2
- 208000024827 Alzheimer disease Diseases 0.000 description 2
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 2
- 235000003911 Arachis Nutrition 0.000 description 2
- 244000105624 Arachis hypogaea Species 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 241000416162 Astragalus gummifer Species 0.000 description 2
- 201000001320 Atherosclerosis Diseases 0.000 description 2
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 2
- 208000004429 Bacillary Dysentery Diseases 0.000 description 2
- 208000023328 Basedow disease Diseases 0.000 description 2
- 208000020084 Bone disease Diseases 0.000 description 2
- ZEACBGOYDLWRJT-UHFFFAOYSA-N COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCCN1CCOCC1 Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCCN1CCOCC1 ZEACBGOYDLWRJT-UHFFFAOYSA-N 0.000 description 2
- ZCBUUXLLMZTDRW-UHFFFAOYSA-N COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCN1CCOCC1 Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCN1CCOCC1 ZCBUUXLLMZTDRW-UHFFFAOYSA-N 0.000 description 2
- 206010006895 Cachexia Diseases 0.000 description 2
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 2
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 2
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 2
- 108010037462 Cyclooxygenase 2 Proteins 0.000 description 2
- 206010048843 Cytomegalovirus chorioretinitis Diseases 0.000 description 2
- 206010016207 Familial Mediterranean fever Diseases 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N Formic acid Chemical compound OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 206010018634 Gouty Arthritis Diseases 0.000 description 2
- 208000009329 Graft vs Host Disease Diseases 0.000 description 2
- 208000015023 Graves' disease Diseases 0.000 description 2
- 229920000084 Gum arabic Polymers 0.000 description 2
- 208000031886 HIV Infections Diseases 0.000 description 2
- 208000037357 HIV infectious disease Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- 208000007766 Kaposi sarcoma Diseases 0.000 description 2
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 description 2
- 208000005777 Lupus Nephritis Diseases 0.000 description 2
- 206010027480 Metastatic malignant melanoma Diseases 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 2
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 2
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 2
- 102000010168 Myeloid Differentiation Factor 88 Human genes 0.000 description 2
- 108010077432 Myeloid Differentiation Factor 88 Proteins 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- OLIQWDZCVIUPRQ-UHFFFAOYSA-N N-[4-(4-cyclopentylpiperazin-1-yl)cyclohexyl]-2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-amine Chemical compound C1(CCCC1)N1CCN(CC1)C1CCC(CC1)NC=1C=C2C(=C(NC2=CC=1)C1=CC(=C(C=C1)OC)OC)C(C)C OLIQWDZCVIUPRQ-UHFFFAOYSA-N 0.000 description 2
- UEEJHVSXFDXPFK-UHFFFAOYSA-N N-dimethylaminoethanol Chemical compound CN(C)CCO UEEJHVSXFDXPFK-UHFFFAOYSA-N 0.000 description 2
- AHVYPIQETPWLSZ-UHFFFAOYSA-N N-methyl-pyrrolidine Natural products CN1CC=CC1 AHVYPIQETPWLSZ-UHFFFAOYSA-N 0.000 description 2
- 102000003945 NF-kappa B Human genes 0.000 description 2
- 108010057466 NF-kappa B Proteins 0.000 description 2
- 206010029113 Neovascularisation Diseases 0.000 description 2
- MWUXSHHQAYIFBG-UHFFFAOYSA-N Nitric oxide Chemical compound O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 description 2
- 239000005642 Oleic acid Substances 0.000 description 2
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 2
- 208000001132 Osteoporosis Diseases 0.000 description 2
- 208000018737 Parkinson disease Diseases 0.000 description 2
- 235000019483 Peanut oil Nutrition 0.000 description 2
- 108050003267 Prostaglandin G/H synthase 2 Proteins 0.000 description 2
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 2
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 2
- 206010037660 Pyrexia Diseases 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- 206010040047 Sepsis Diseases 0.000 description 2
- 206010040550 Shigella infections Diseases 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 229920001615 Tragacanth Polymers 0.000 description 2
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 2
- 208000033559 Waldenström macroglobulinemia Diseases 0.000 description 2
- QRAYLCXKNWIKMX-UHFFFAOYSA-N [1-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]-2-oxopyrrolidin-3-yl] trifluoromethanesulfonate Chemical compound CC(C)C1=C(NC2=CC=C(C=C12)N1CCC(OS(=O)(=O)C(F)(F)F)C1=O)C1=CC(C)=NC=C1 QRAYLCXKNWIKMX-UHFFFAOYSA-N 0.000 description 2
- 235000010489 acacia gum Nutrition 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 235000010443 alginic acid Nutrition 0.000 description 2
- 239000000783 alginic acid Substances 0.000 description 2
- 229920000615 alginic acid Polymers 0.000 description 2
- 229960001126 alginic acid Drugs 0.000 description 2
- 150000004781 alginic acids Chemical class 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 230000003078 antioxidant effect Effects 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 206010003246 arthritis Diseases 0.000 description 2
- 208000006673 asthma Diseases 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- 230000001363 autoimmune Effects 0.000 description 2
- 208000037979 autoimmune inflammatory disease Diseases 0.000 description 2
- 235000010290 biphenyl Nutrition 0.000 description 2
- 239000004305 biphenyl Substances 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 229910000019 calcium carbonate Inorganic materials 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 229910000389 calcium phosphate Inorganic materials 0.000 description 2
- 235000011010 calcium phosphates Nutrition 0.000 description 2
- 201000011510 cancer Diseases 0.000 description 2
- 208000001969 capillary hemangioma Diseases 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 239000011111 cardboard Substances 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- NMMPMZWIIQCZBA-UHFFFAOYSA-M chloropalladium(1+);dicyclohexyl-[2-[2,4,6-tri(propan-2-yl)phenyl]phenyl]phosphane;2-phenylethanamine Chemical compound [Pd+]Cl.NCCC1=CC=CC=[C-]1.CC(C)C1=CC(C(C)C)=CC(C(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 NMMPMZWIIQCZBA-UHFFFAOYSA-M 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 208000022993 cryopyrin-associated periodic syndrome Diseases 0.000 description 2
- 229940097362 cyclodextrins Drugs 0.000 description 2
- 208000001763 cytomegalovirus retinitis Diseases 0.000 description 2
- 230000001086 cytosolic effect Effects 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 235000019441 ethanol Nutrition 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 239000003292 glue Substances 0.000 description 2
- 208000024908 graft versus host disease Diseases 0.000 description 2
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 2
- FBPFZTCFMRRESA-UHFFFAOYSA-N hexane-1,2,3,4,5,6-hexol Chemical compound OCC(O)C(O)C(O)C(O)CO FBPFZTCFMRRESA-UHFFFAOYSA-N 0.000 description 2
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 230000002757 inflammatory effect Effects 0.000 description 2
- 230000028709 inflammatory response Effects 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 2
- 239000000314 lubricant Substances 0.000 description 2
- 208000030159 metabolic disease Diseases 0.000 description 2
- 208000021039 metastatic melanoma Diseases 0.000 description 2
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 2
- 239000008108 microcrystalline cellulose Substances 0.000 description 2
- 229940016286 microcrystalline cellulose Drugs 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 239000001788 mono and diglycerides of fatty acids Substances 0.000 description 2
- 208000031225 myocardial ischemia Diseases 0.000 description 2
- KVKFRMCSXWQSNT-UHFFFAOYSA-N n,n'-dimethylethane-1,2-diamine Chemical compound CNCCNC KVKFRMCSXWQSNT-UHFFFAOYSA-N 0.000 description 2
- XBXCNNQPRYLIDE-UHFFFAOYSA-M n-tert-butylcarbamate Chemical compound CC(C)(C)NC([O-])=O XBXCNNQPRYLIDE-UHFFFAOYSA-M 0.000 description 2
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 2
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 2
- 201000008482 osteoarthritis Diseases 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 244000045947 parasite Species 0.000 description 2
- 239000000312 peanut oil Substances 0.000 description 2
- 239000008389 polyethoxylated castor oil Substances 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 238000000524 positive electrospray ionisation mass spectrometry Methods 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000036303 septic shock Effects 0.000 description 2
- 239000008159 sesame oil Substances 0.000 description 2
- 235000011803 sesame oil Nutrition 0.000 description 2
- 201000005113 shigellosis Diseases 0.000 description 2
- 229960002930 sirolimus Drugs 0.000 description 2
- 235000010413 sodium alginate Nutrition 0.000 description 2
- 239000000661 sodium alginate Substances 0.000 description 2
- 229940005550 sodium alginate Drugs 0.000 description 2
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 2
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 2
- 230000007928 solubilization Effects 0.000 description 2
- 238000005063 solubilization Methods 0.000 description 2
- 235000011069 sorbitan monooleate Nutrition 0.000 description 2
- 239000001593 sorbitan monooleate Substances 0.000 description 2
- 229940035049 sorbitan monooleate Drugs 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 238000004808 supercritical fluid chromatography Methods 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- WJSQHYKNVQZONT-UHFFFAOYSA-N tert-butyl 5-chloro-2-(3,4-dimethoxyphenyl)-3-ethylindole-1-carboxylate Chemical compound ClC=1C=C2C(=C(N(C2=CC=1)C(=O)OC(C)(C)C)C1=CC(=C(C=C1)OC)OC)CC WJSQHYKNVQZONT-UHFFFAOYSA-N 0.000 description 2
- PYJQGFCHEHXPNV-UHFFFAOYSA-N tert-butyl N-[2-(2-methylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]carbamate Chemical compound C1(N[C]2C(=C1C(C)C)C=C(NC(=O)OC(C)(C)C)C=C2)=C1C=C(C)N=C[CH]1 PYJQGFCHEHXPNV-UHFFFAOYSA-N 0.000 description 2
- YBDHLOMWBRDZIS-UHFFFAOYSA-N tert-butyl N-[3-propan-2-yl-2-(1-tritylpyrazolo[3,4-b]pyridin-4-yl)-1H-indol-5-yl]carbamate Chemical compound C(C)(C)C1=C(NC2=CC=C(C=C12)NC(OC(C)(C)C)=O)C1=C2C(=NC=C1)N(N=C2)C(C1=CC=CC=C1)(C1=CC=CC=C1)C1=CC=CC=C1 YBDHLOMWBRDZIS-UHFFFAOYSA-N 0.000 description 2
- OWPIFQXNMLDXKW-UHFFFAOYSA-N tert-butyl indole-1-carboxylate Chemical compound C1=CC=C2N(C(=O)OC(C)(C)C)C=CC2=C1 OWPIFQXNMLDXKW-UHFFFAOYSA-N 0.000 description 2
- CWXPZXBSDSIRCS-UHFFFAOYSA-N tert-butyl piperazine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCNCC1 CWXPZXBSDSIRCS-UHFFFAOYSA-N 0.000 description 2
- HLZKNKRTKFSKGZ-UHFFFAOYSA-N tetradecan-1-ol Chemical compound CCCCCCCCCCCCCCO HLZKNKRTKFSKGZ-UHFFFAOYSA-N 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 230000008736 traumatic injury Effects 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 2
- WJKHJLXJJJATHN-UHFFFAOYSA-N triflic anhydride Chemical compound FC(F)(F)S(=O)(=O)OS(=O)(=O)C(F)(F)F WJKHJLXJJJATHN-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000008158 vegetable oil Substances 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- 239000003039 volatile agent Substances 0.000 description 2
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 2
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 1
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 1
- HRMRQBJUFWFQLX-SSDOTTSWSA-N (3r)-1-[(2-methylpropan-2-yl)oxycarbonyl]pyrrolidine-3-carboxylic acid Chemical compound CC(C)(C)OC(=O)N1CC[C@@H](C(O)=O)C1 HRMRQBJUFWFQLX-SSDOTTSWSA-N 0.000 description 1
- 125000006274 (C1-C3)alkoxy group Chemical group 0.000 description 1
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 1
- CGXOAAMIQPDTPE-UHFFFAOYSA-N 1,2,2,6,6-pentamethylpiperidin-4-amine Chemical compound CN1C(C)(C)CC(N)CC1(C)C CGXOAAMIQPDTPE-UHFFFAOYSA-N 0.000 description 1
- QACMXJJLQXUOPQ-UHFFFAOYSA-N 1,2-dichloroethane;3-(ethyliminomethylideneamino)-n,n-dimethylpropan-1-amine Chemical compound ClCCCl.CCN=C=NCCCN(C)C QACMXJJLQXUOPQ-UHFFFAOYSA-N 0.000 description 1
- KPKNTUUIEVXMOH-UHFFFAOYSA-N 1,4-dioxa-8-azaspiro[4.5]decane Chemical compound O1CCOC11CCNCC1 KPKNTUUIEVXMOH-UHFFFAOYSA-N 0.000 description 1
- KDAFVGCPLFJMHY-UHFFFAOYSA-N 1,4-dioxaspiro[4.5]decan-8-amine Chemical compound C1CC(N)CCC21OCCO2 KDAFVGCPLFJMHY-UHFFFAOYSA-N 0.000 description 1
- IGGAGOBKENGEDX-UHFFFAOYSA-N 1-[4-[4-[[2-(3,4-dimethoxyphenyl)-3-propan-2-yl-1H-indol-5-yl]amino]cyclohexyl]piperazin-1-yl]ethanone Chemical compound COC1=C(OC)C=C(C=C1)C1=C(C(C)C)C2=CC(NC3CCC(CC3)N3CCN(CC3)C(C)=O)=CC=C2N1 IGGAGOBKENGEDX-UHFFFAOYSA-N 0.000 description 1
- FHJATBIERQTCTN-UHFFFAOYSA-N 1-[4-amino-2-(ethylaminomethyl)imidazo[4,5-c]quinolin-1-yl]-2-methylpropan-2-ol Chemical compound C1=CC=CC2=C(N(C(CNCC)=N3)CC(C)(C)O)C3=C(N)N=C21 FHJATBIERQTCTN-UHFFFAOYSA-N 0.000 description 1
- XXJGBENTLXFVFI-UHFFFAOYSA-N 1-amino-methylene Chemical compound N[CH2] XXJGBENTLXFVFI-UHFFFAOYSA-N 0.000 description 1
- MICMHFIQSAMEJG-UHFFFAOYSA-N 1-bromopyrrolidine-2,5-dione Chemical compound BrN1C(=O)CCC1=O.BrN1C(=O)CCC1=O MICMHFIQSAMEJG-UHFFFAOYSA-N 0.000 description 1
- PZNPLUBHRSSFHT-RRHRGVEJSA-N 1-hexadecanoyl-2-octadecanoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCCCC(=O)O[C@@H](COP([O-])(=O)OCC[N+](C)(C)C)COC(=O)CCCCCCCCCCCCCCC PZNPLUBHRSSFHT-RRHRGVEJSA-N 0.000 description 1
- HUUPVABNAQUEJW-UHFFFAOYSA-N 1-methylpiperidin-4-one Chemical compound CN1CCC(=O)CC1 HUUPVABNAQUEJW-UHFFFAOYSA-N 0.000 description 1
- AVFZOVWCLRSYKC-UHFFFAOYSA-N 1-methylpyrrolidine Chemical compound CN1CCCC1 AVFZOVWCLRSYKC-UHFFFAOYSA-N 0.000 description 1
- SRSKXJVMVSSSHB-UHFFFAOYSA-N 1h-pyrrolo[3,2-c]pyridine Chemical class N1=CC=C2NC=CC2=C1 SRSKXJVMVSSSHB-UHFFFAOYSA-N 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- CHHHXKFHOYLYRE-UHFFFAOYSA-M 2,4-Hexadienoic acid, potassium salt (1:1), (2E,4E)- Chemical compound [K+].CC=CC=CC([O-])=O CHHHXKFHOYLYRE-UHFFFAOYSA-M 0.000 description 1
- ZADFHMVJXSWMNZ-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-N-[4-[4-(1-methylpiperidin-4-yl)piperazin-1-yl]cyclohexyl]-3-propan-2-yl-1H-indol-5-amine Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)N1CCN(CC1)C1CCN(CC1)C ZADFHMVJXSWMNZ-UHFFFAOYSA-N 0.000 description 1
- 125000006176 2-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- 125000005916 2-methylpentyl group Chemical group 0.000 description 1
- HCDMJFOHIXMBOV-UHFFFAOYSA-N 3-(2,6-difluoro-3,5-dimethoxyphenyl)-1-ethyl-8-(morpholin-4-ylmethyl)-4,7-dihydropyrrolo[4,5]pyrido[1,2-d]pyrimidin-2-one Chemical compound C=1C2=C3N(CC)C(=O)N(C=4C(=C(OC)C=C(OC)C=4F)F)CC3=CN=C2NC=1CN1CCOCC1 HCDMJFOHIXMBOV-UHFFFAOYSA-N 0.000 description 1
- VHFFWODMKVZPOH-UHFFFAOYSA-N 3-bromo-1-[2-(2,6-dimethylpyridin-4-yl)-3-propan-2-yl-1H-indol-5-yl]pyrrolidin-2-one Chemical compound BrC1C(N(CC1)C=1C=C2C(=C(NC2=CC=1)C1=CC(=NC(=C1)C)C)C(C)C)=O VHFFWODMKVZPOH-UHFFFAOYSA-N 0.000 description 1
- FRKGSNOMLIYPSH-UHFFFAOYSA-N 3-hydroxypyrrolidin-2-one Chemical compound OC1CCNC1=O FRKGSNOMLIYPSH-UHFFFAOYSA-N 0.000 description 1
- 125000005917 3-methylpentyl group Chemical group 0.000 description 1
- KGFFQIJSWJUKBR-UHFFFAOYSA-N 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1-tritylpyrazolo[3,4-b]pyridine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=NC2=C1C=NN2C(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 KGFFQIJSWJUKBR-UHFFFAOYSA-N 0.000 description 1
- VXWVFZFZYXOBTA-UHFFFAOYSA-N 5-bromo-1h-indole Chemical compound BrC1=CC=C2NC=CC2=C1 VXWVFZFZYXOBTA-UHFFFAOYSA-N 0.000 description 1
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 description 1
- 229920001450 Alpha-Cyclodextrin Polymers 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 206010055128 Autoimmune neutropenia Diseases 0.000 description 1
- 208000011594 Autoinflammatory disease Diseases 0.000 description 1
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 1
- 208000003950 B-cell lymphoma Diseases 0.000 description 1
- 230000003844 B-cell-activation Effects 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 241000713704 Bovine immunodeficiency virus Species 0.000 description 1
- 239000004255 Butylated hydroxyanisole Substances 0.000 description 1
- KWGUDCLJRRLNTP-UHFFFAOYSA-N COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCNCC1.FC(C(=O)O)(F)F Chemical compound COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCNCC1.FC(C(=O)O)(F)F KWGUDCLJRRLNTP-UHFFFAOYSA-N 0.000 description 1
- 206010058019 Cancer Pain Diseases 0.000 description 1
- 241000282465 Canis Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 206010007572 Cardiac hypertrophy Diseases 0.000 description 1
- 208000006029 Cardiomegaly Diseases 0.000 description 1
- 206010007953 Central nervous system lymphoma Diseases 0.000 description 1
- 206010063094 Cerebral malaria Diseases 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 206010008909 Chronic Hepatitis Diseases 0.000 description 1
- 208000035473 Communicable disease Diseases 0.000 description 1
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 229920002785 Croscarmellose sodium Polymers 0.000 description 1
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- 206010012438 Dermatitis atopic Diseases 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- 206010013911 Dysgeusia Diseases 0.000 description 1
- 208000037487 Endotoxemia Diseases 0.000 description 1
- 241000713730 Equine infectious anemia virus Species 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- OSYIYHYZFXLUSH-UHFFFAOYSA-N FC(S(=O)(=O)O)(F)F.C(C)(C)C1=C(NC2=CC=C(C=C12)N1C(CCC1)=O)C1=CC(=NC=C1)C Chemical compound FC(S(=O)(=O)O)(F)F.C(C)(C)C1=C(NC2=CC=C(C=C12)N1C(CCC1)=O)C1=CC(=NC=C1)C OSYIYHYZFXLUSH-UHFFFAOYSA-N 0.000 description 1
- 241000713800 Feline immunodeficiency virus Species 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 208000018522 Gastrointestinal disease Diseases 0.000 description 1
- 206010018364 Glomerulonephritis Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 239000007821 HATU Substances 0.000 description 1
- 229910004373 HOAc Inorganic materials 0.000 description 1
- 208000030836 Hashimoto thyroiditis Diseases 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- 208000035186 Hemolytic Autoimmune Anemia Diseases 0.000 description 1
- 208000005176 Hepatitis C Diseases 0.000 description 1
- 206010019755 Hepatitis chronic active Diseases 0.000 description 1
- 101000831496 Homo sapiens Toll-like receptor 3 Proteins 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010021143 Hypoxia Diseases 0.000 description 1
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 1
- 108091069196 IL-1 family Proteins 0.000 description 1
- 102000039996 IL-1 family Human genes 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 206010061598 Immunodeficiency Diseases 0.000 description 1
- 208000029462 Immunodeficiency disease Diseases 0.000 description 1
- 102000000589 Interleukin-1 Human genes 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- 102000003814 Interleukin-10 Human genes 0.000 description 1
- 108090000174 Interleukin-10 Proteins 0.000 description 1
- 206010059176 Juvenile idiopathic arthritis Diseases 0.000 description 1
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 208000019693 Lung disease Diseases 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 101000574441 Mus musculus Alkaline phosphatase, germ cell type Proteins 0.000 description 1
- 206010028289 Muscle atrophy Diseases 0.000 description 1
- 208000000112 Myalgia Diseases 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- HEGVTKDWTUCLGW-UHFFFAOYSA-N N1C=CC2=CC=CC=C12.COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCN(CC1)CCNC Chemical compound N1C=CC2=CC=CC=C12.COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)N1CCN(CC1)CCNC HEGVTKDWTUCLGW-UHFFFAOYSA-N 0.000 description 1
- FEOMRSQLSODKNJ-UHFFFAOYSA-N N1C=CC2=CC=CC=C12.COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCNC Chemical compound N1C=CC2=CC=CC=C12.COC=1C=C(C=CC=1OC)C=1NC2=CC=C(C=C2C=1C(C)C)NC1CCC(CC1)NCCNC FEOMRSQLSODKNJ-UHFFFAOYSA-N 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 206010033645 Pancreatitis Diseases 0.000 description 1
- 229910002666 PdCl2 Inorganic materials 0.000 description 1
- 201000011152 Pemphigus Diseases 0.000 description 1
- 241000721454 Pemphigus Species 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 102000007327 Protamines Human genes 0.000 description 1
- 108010007568 Protamines Proteins 0.000 description 1
- 208000033464 Reiter syndrome Diseases 0.000 description 1
- 108700008625 Reporter Genes Proteins 0.000 description 1
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 description 1
- 208000005074 Retroviridae Infections Diseases 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 229940124639 Selective inhibitor Drugs 0.000 description 1
- 201000010001 Silicosis Diseases 0.000 description 1
- 108020004682 Single-Stranded DNA Proteins 0.000 description 1
- NWGKJDSIEKMTRX-AAZCQSIUSA-N Sorbitan monooleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@@H](O)[C@H]1OC[C@H](O)[C@H]1O NWGKJDSIEKMTRX-AAZCQSIUSA-N 0.000 description 1
- 108090000190 Thrombin Proteins 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 206010043781 Thyroiditis chronic Diseases 0.000 description 1
- 102100024324 Toll-like receptor 3 Human genes 0.000 description 1
- 206010044248 Toxic shock syndrome Diseases 0.000 description 1
- 231100000650 Toxic shock syndrome Toxicity 0.000 description 1
- 206010048873 Traumatic arthritis Diseases 0.000 description 1
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- WERKSKAQRVDLDW-ANOHMWSOSA-N [(2s,3r,4r,5r)-2,3,4,5,6-pentahydroxyhexyl] (z)-octadec-9-enoate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO WERKSKAQRVDLDW-ANOHMWSOSA-N 0.000 description 1
- MCGSCOLBFJQGHM-SCZZXKLOSA-N abacavir Chemical compound C=12N=CN([C@H]3C=C[C@@H](CO)C3)C2=NC(N)=NC=1NC1CC1 MCGSCOLBFJQGHM-SCZZXKLOSA-N 0.000 description 1
- 229960004748 abacavir Drugs 0.000 description 1
- 230000001594 aberrant effect Effects 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- YBCVMFKXIKNREZ-UHFFFAOYSA-N acoh acetic acid Chemical compound CC(O)=O.CC(O)=O YBCVMFKXIKNREZ-UHFFFAOYSA-N 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 231100000354 acute hepatitis Toxicity 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 description 1
- 201000000028 adult respiratory distress syndrome Diseases 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 229920013820 alkyl cellulose Chemical class 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 229940087168 alpha tocopherol Drugs 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- CEGOLXSVJUTHNZ-UHFFFAOYSA-K aluminium tristearate Chemical compound [Al+3].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CEGOLXSVJUTHNZ-UHFFFAOYSA-K 0.000 description 1
- 229940063655 aluminum stearate Drugs 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 230000036592 analgesia Effects 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 239000003430 antimalarial agent Substances 0.000 description 1
- 229940033495 antimalarials Drugs 0.000 description 1
- 239000003443 antiviral agent Substances 0.000 description 1
- 230000002917 arthritic effect Effects 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 201000008937 atopic dermatitis Diseases 0.000 description 1
- 201000005000 autoimmune gastritis Diseases 0.000 description 1
- 201000000448 autoimmune hemolytic anemia Diseases 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 235000013871 bee wax Nutrition 0.000 description 1
- 239000012166 beeswax Substances 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- WHGYBXFWUBPSRW-FOUAGVGXSA-N beta-cyclodextrin Chemical compound OC[C@H]([C@H]([C@@H]([C@H]1O)O)O[C@H]2O[C@@H]([C@@H](O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O[C@H]3O[C@H](CO)[C@H]([C@@H]([C@H]3O)O)O3)[C@H](O)[C@H]2O)CO)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@@H]3O[C@@H]1CO WHGYBXFWUBPSRW-FOUAGVGXSA-N 0.000 description 1
- 229960004853 betadex Drugs 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 208000019664 bone resorption disease Diseases 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 1
- 229940043253 butylated hydroxyanisole Drugs 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 229930194791 calphostin Natural products 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 125000002843 carboxylic acid group Chemical group 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 229960000590 celecoxib Drugs 0.000 description 1
- RZEKVGVHFLEQIL-UHFFFAOYSA-N celecoxib Chemical compound C1=CC(C)=CC=C1C1=CC(C(F)(F)F)=NN1C1=CC=C(S(N)(=O)=O)C=C1 RZEKVGVHFLEQIL-UHFFFAOYSA-N 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920006217 cellulose acetate butyrate Polymers 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 229940082500 cetostearyl alcohol Drugs 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- 238000004296 chiral HPLC Methods 0.000 description 1
- CZKMPDNXOGQMFW-UHFFFAOYSA-N chloro(triethyl)germane Chemical compound CC[Ge](Cl)(CC)CC CZKMPDNXOGQMFW-UHFFFAOYSA-N 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 239000008119 colloidal silica Substances 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 229960001681 croscarmellose sodium Drugs 0.000 description 1
- 229960000913 crospovidone Drugs 0.000 description 1
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- GCUVBACNBHGZRS-UHFFFAOYSA-N cyclopenta-1,3-diene cyclopenta-2,4-dien-1-yl(diphenyl)phosphane iron(2+) Chemical compound [Fe++].c1cc[cH-]c1.c1cc[c-](c1)P(c1ccccc1)c1ccccc1 GCUVBACNBHGZRS-UHFFFAOYSA-N 0.000 description 1
- 229960004397 cyclophosphamide Drugs 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- DEZRYPDIMOWBDS-UHFFFAOYSA-N dcm dichloromethane Chemical compound ClCCl.ClCCl DEZRYPDIMOWBDS-UHFFFAOYSA-N 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 230000001066 destructive effect Effects 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 208000010643 digestive system disease Diseases 0.000 description 1
- FSBVERYRVPGNGG-UHFFFAOYSA-N dimagnesium dioxido-bis[[oxido(oxo)silyl]oxy]silane hydrate Chemical compound O.[Mg+2].[Mg+2].[O-][Si](=O)O[Si]([O-])([O-])O[Si]([O-])=O FSBVERYRVPGNGG-UHFFFAOYSA-N 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- UXGNZZKBCMGWAZ-UHFFFAOYSA-N dimethylformamide dmf Chemical compound CN(C)C=O.CN(C)C=O UXGNZZKBCMGWAZ-UHFFFAOYSA-N 0.000 description 1
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 1
- 229910000396 dipotassium phosphate Inorganic materials 0.000 description 1
- 235000019797 dipotassium phosphate Nutrition 0.000 description 1
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- CETRZFQIITUQQL-UHFFFAOYSA-N dmso dimethylsulfoxide Chemical compound CS(C)=O.CS(C)=O CETRZFQIITUQQL-UHFFFAOYSA-N 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 201000006549 dyspepsia Diseases 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 230000001804 emulsifying effect Effects 0.000 description 1
- 239000008387 emulsifying waxe Substances 0.000 description 1
- 238000003821 enantio-separation Methods 0.000 description 1
- 239000002158 endotoxin Substances 0.000 description 1
- 239000002702 enteric coating Substances 0.000 description 1
- 238000009505 enteric coating Methods 0.000 description 1
- OCLXJTCGWSSVOE-UHFFFAOYSA-N ethanol etoh Chemical compound CCO.CCO OCLXJTCGWSSVOE-UHFFFAOYSA-N 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 125000005745 ethoxymethyl group Chemical group [H]C([H])([H])C([H])([H])OC([H])([H])* 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- OJCSPXHYDFONPU-UHFFFAOYSA-N etoac etoac Chemical compound CCOC(C)=O.CCOC(C)=O OJCSPXHYDFONPU-UHFFFAOYSA-N 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 201000007249 familial juvenile hyperuricemic nephropathy Diseases 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 229940124670 gardiquimod Drugs 0.000 description 1
- 208000018685 gastrointestinal system disease Diseases 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 230000014509 gene expression Effects 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 229940074045 glyceryl distearate Drugs 0.000 description 1
- 229940075507 glyceryl monostearate Drugs 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 239000007902 hard capsule Substances 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- 208000024798 heartburn Diseases 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 208000005252 hepatitis A Diseases 0.000 description 1
- 208000002672 hepatitis B Diseases 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- UBHWBODXJBSFLH-UHFFFAOYSA-N hexadecan-1-ol;octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO.CCCCCCCCCCCCCCCCCCO UBHWBODXJBSFLH-UHFFFAOYSA-N 0.000 description 1
- 102000045715 human TLR7 Human genes 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- XXSMGPRMXLTPCZ-UHFFFAOYSA-N hydroxychloroquine Chemical compound ClC1=CC=C2C(NC(C)CCCN(CCO)CC)=CC=NC2=C1 XXSMGPRMXLTPCZ-UHFFFAOYSA-N 0.000 description 1
- 229960004171 hydroxychloroquine Drugs 0.000 description 1
- CBOIHMRHGLHBPB-UHFFFAOYSA-N hydroxymethyl Chemical compound O[CH2] CBOIHMRHGLHBPB-UHFFFAOYSA-N 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 206010020718 hyperplasia Diseases 0.000 description 1
- 230000007954 hypoxia Effects 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- YAMHXTCMCPHKLN-UHFFFAOYSA-N imidazolidin-2-one Chemical compound O=C1NCCN1 YAMHXTCMCPHKLN-UHFFFAOYSA-N 0.000 description 1
- 230000007813 immunodeficiency Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 239000003701 inert diluent Substances 0.000 description 1
- 230000002458 infectious effect Effects 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 206010022000 influenza Diseases 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229940102223 injectable solution Drugs 0.000 description 1
- 229940102213 injectable suspension Drugs 0.000 description 1
- 108091005434 innate immune receptors Proteins 0.000 description 1
- 229940076144 interleukin-10 Drugs 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 230000004068 intracellular signaling Effects 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- HVTICUPFWKNHNG-UHFFFAOYSA-N iodoethane Chemical compound CCI HVTICUPFWKNHNG-UHFFFAOYSA-N 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 208000002551 irritable bowel syndrome Diseases 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 208000012947 ischemia reperfusion injury Diseases 0.000 description 1
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 208000011379 keloid formation Diseases 0.000 description 1
- VHOGYURTWQBHIL-UHFFFAOYSA-N leflunomide Chemical compound O1N=CC(C(=O)NC=2C=CC(=CC=2)C(F)(F)F)=C1C VHOGYURTWQBHIL-UHFFFAOYSA-N 0.000 description 1
- 229960000681 leflunomide Drugs 0.000 description 1
- 208000021601 lentivirus infection Diseases 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- 239000000391 magnesium silicate Substances 0.000 description 1
- 229910000386 magnesium trisilicate Inorganic materials 0.000 description 1
- 235000019793 magnesium trisilicate Nutrition 0.000 description 1
- 229940099273 magnesium trisilicate Drugs 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- COTNUBDHGSIOTA-UHFFFAOYSA-N meoh methanol Chemical compound OC.OC COTNUBDHGSIOTA-UHFFFAOYSA-N 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 229960000485 methotrexate Drugs 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 229940043348 myristyl alcohol Drugs 0.000 description 1
- KFIGICHILYTCJF-UHFFFAOYSA-N n'-methylethane-1,2-diamine Chemical compound CNCCN KFIGICHILYTCJF-UHFFFAOYSA-N 0.000 description 1
- LLYKPZOWCPVRPD-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine;n,n-dimethylpyridin-4-amine Chemical compound CN(C)C1=CC=NC=C1.CN(C)C1=CC=CC=N1 LLYKPZOWCPVRPD-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000002232 neuromuscular Effects 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 230000005937 nuclear translocation Effects 0.000 description 1
- GYCKQBWUSACYIF-UHFFFAOYSA-N o-hydroxybenzoic acid ethyl ester Natural products CCOC(=O)C1=CC=CC=C1O GYCKQBWUSACYIF-UHFFFAOYSA-N 0.000 description 1
- 239000007764 o/w emulsion Substances 0.000 description 1
- KDWFDOFTPHDNJL-TUBOTVQJSA-N odn-2006 Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](COP(O)(=O)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)O[C@H]2[C@H]([C@@H](O[C@@H]2COP(O)(=S)O[C@H]2[C@H]([C@@H](O[C@@H]2COP(O)(=O)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)O[C@H]2[C@H]([C@@H](O[C@@H]2COP(O)(=O)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=O)O[C@H]2[C@H]([C@@H](O[C@@H]2COP(O)(=S)O[C@H]2[C@H]([C@@H](O[C@@H]2COP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(NC(=O)C(C)=C2)=O)OP(O)(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(NC(=O)C(C)=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(NC(=O)C(C)=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(NC(=O)C(C)=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(NC(=O)C(C)=C2)=O)OP(O)(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C3=C(C(NC(N)=N3)=O)N=C2)OP(S)(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C(N=C(N)C=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(NC(=O)C(C)=C2)=O)OP(O)(=O)OC[C@@H]2[C@H](C[C@@H](O2)N2C(NC(=O)C(C)=C2)=O)O)N2C3=C(C(NC(N)=N3)=O)N=C2)O)N2C(N=C(N)C=C2)=O)O)N2C3=C(C(NC(N)=N3)=O)N=C2)O)N2C3=C(C(NC(N)=N3)=O)N=C2)O)N2C(N=C(N)C=C2)=O)O)[C@@H](O)C1 KDWFDOFTPHDNJL-TUBOTVQJSA-N 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 239000003883 ointment base Substances 0.000 description 1
- 230000000771 oncological effect Effects 0.000 description 1
- 239000006186 oral dosage form Substances 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 229940046781 other immunosuppressants in atc Drugs 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 102000007863 pattern recognition receptors Human genes 0.000 description 1
- 108010089193 pattern recognition receptors Proteins 0.000 description 1
- 201000001976 pemphigus vulgaris Diseases 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- BCIIMDOZSUCSEN-UHFFFAOYSA-N piperidin-4-amine Chemical compound NC1CCNCC1 BCIIMDOZSUCSEN-UHFFFAOYSA-N 0.000 description 1
- 125000004482 piperidin-4-yl group Chemical group N1CCC(CC1)* 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229940113116 polyethylene glycol 1000 Drugs 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000013809 polyvinylpolypyrrolidone Nutrition 0.000 description 1
- 229920000523 polyvinylpolypyrrolidone Polymers 0.000 description 1
- 235000010241 potassium sorbate Nutrition 0.000 description 1
- 239000004302 potassium sorbate Substances 0.000 description 1
- 229940069338 potassium sorbate Drugs 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 208000016800 primary central nervous system lymphoma Diseases 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 229940072288 prograf Drugs 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 229950008679 protamine sulfate Drugs 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 201000003651 pulmonary sarcoidosis Diseases 0.000 description 1
- 238000005086 pumping Methods 0.000 description 1
- 238000010926 purge Methods 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 229940099538 rapamune Drugs 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 208000002574 reactive arthritis Diseases 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000008844 regulatory mechanism Effects 0.000 description 1
- 229960000371 rofecoxib Drugs 0.000 description 1
- RZJQGNCSTQAWON-UHFFFAOYSA-N rofecoxib Chemical compound C1=CC(S(=O)(=O)C)=CC=C1C1=C(C=2C=CC=CC=2)C(=O)OC1 RZJQGNCSTQAWON-UHFFFAOYSA-N 0.000 description 1
- HJORMJIFDVBMOB-UHFFFAOYSA-N rolipram Chemical compound COC1=CC=C(C2CC(=O)NC2)C=C1OC1CCCC1 HJORMJIFDVBMOB-UHFFFAOYSA-N 0.000 description 1
- 229950005741 rolipram Drugs 0.000 description 1
- 201000005404 rubella Diseases 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 150000003873 salicylate salts Chemical class 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 239000008299 semisolid dosage form Substances 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910001467 sodium calcium phosphate Inorganic materials 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 239000007901 soft capsule Substances 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 238000007614 solvation Methods 0.000 description 1
- 239000011877 solvent mixture Substances 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 239000008347 soybean phospholipid Substances 0.000 description 1
- 208000010110 spontaneous platelet aggregation Diseases 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 150000003431 steroids Chemical class 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid group Chemical class S(O)(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 201000004595 synovitis Diseases 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 229940037128 systemic glucocorticoids Drugs 0.000 description 1
- 208000020408 systemic-onset juvenile idiopathic arthritis Diseases 0.000 description 1
- 229960001967 tacrolimus Drugs 0.000 description 1
- WDPWEXWMQDRXAL-UHFFFAOYSA-N tert-butyl 1,4-diazepane-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCCNCC1 WDPWEXWMQDRXAL-UHFFFAOYSA-N 0.000 description 1
- VDCSUVVWZCJDRG-UHFFFAOYSA-N tert-butyl 2-(3,4-dimethoxyphenyl)-5-(1,4-dioxaspiro[4.5]decan-8-ylamino)-3-propan-2-ylindole-1-carboxylate Chemical compound O1CCOC11CCC(CC1)NC=1C=C2C(=C(N(C2=CC=1)C(=O)OC(C)(C)C)C1=CC(=C(C=C1)OC)OC)C(C)C VDCSUVVWZCJDRG-UHFFFAOYSA-N 0.000 description 1
- UDLZCTCCTFKPFF-UHFFFAOYSA-N tert-butyl 2-(3,4-dimethoxyphenyl)-5-[4-[(2-methylpropan-2-yl)oxycarbonyl]piperazin-1-yl]-3-propan-2-ylindole-1-carboxylate Chemical compound C(C)(C)(C)OC(=O)N1CCN(CC1)C=1C=C2C(=C(N(C2=CC=1)C(=O)OC(C)(C)C)C1=CC(=C(C=C1)OC)OC)C(C)C UDLZCTCCTFKPFF-UHFFFAOYSA-N 0.000 description 1
- DSYICRCIJQILLE-UHFFFAOYSA-N tert-butyl 4-(azetidin-3-yl)-1,4-diazepane-1-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCCN1C1CNC1 DSYICRCIJQILLE-UHFFFAOYSA-N 0.000 description 1
- LZRDHSFPLUWYAX-UHFFFAOYSA-N tert-butyl 4-aminopiperidine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCC(N)CC1 LZRDHSFPLUWYAX-UHFFFAOYSA-N 0.000 description 1
- PMLBUVZPRKXMOX-UHFFFAOYSA-N tert-butyl 4-oxoazepane-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCCC(=O)CC1 PMLBUVZPRKXMOX-UHFFFAOYSA-N 0.000 description 1
- QYJVBVKFXDHFPQ-UHFFFAOYSA-N tert-butyl n-(2-aminoethyl)-n-methylcarbamate Chemical compound NCCN(C)C(=O)OC(C)(C)C QYJVBVKFXDHFPQ-UHFFFAOYSA-N 0.000 description 1
- MSWTVSDFEYSRMQ-UHFFFAOYSA-N tert-butyl n-methyl-n-(2-oxoethyl)carbamate Chemical compound O=CCN(C)C(=O)OC(C)(C)C MSWTVSDFEYSRMQ-UHFFFAOYSA-N 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- WHRNULOCNSKMGB-UHFFFAOYSA-N tetrahydrofuran thf Chemical compound C1CCOC1.C1CCOC1 WHRNULOCNSKMGB-UHFFFAOYSA-N 0.000 description 1
- OULAJFUGPPVRBK-UHFFFAOYSA-N tetratriacontyl alcohol Natural products CCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCCO OULAJFUGPPVRBK-UHFFFAOYSA-N 0.000 description 1
- 150000003536 tetrazoles Chemical class 0.000 description 1
- WROMPOXWARCANT-UHFFFAOYSA-N tfa trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC(=O)C(F)(F)F WROMPOXWARCANT-UHFFFAOYSA-N 0.000 description 1
- 231100001274 therapeutic index Toxicity 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 229960004072 thrombin Drugs 0.000 description 1
- 206010043554 thrombocytopenia Diseases 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- VXUYXOFXAQZZMF-UHFFFAOYSA-N titanium(IV) isopropoxide Chemical compound CC(C)O[Ti](OC(C)C)(OC(C)C)OC(C)C VXUYXOFXAQZZMF-UHFFFAOYSA-N 0.000 description 1
- 229960000984 tocofersolan Drugs 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 1
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 201000008827 tuberculosis Diseases 0.000 description 1
- 229940046728 tumor necrosis factor alpha inhibitor Drugs 0.000 description 1
- 239000002452 tumor necrosis factor alpha inhibitor Substances 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 230000010472 type I IFN response Effects 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- 210000002268 wool Anatomy 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- 239000002076 α-tocopherol Substances 0.000 description 1
- 235000004835 α-tocopherol Nutrition 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/12—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/12—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains three hetero rings
- C07D491/20—Spiro-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Rheumatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Pain & Pain Management (AREA)
- Physical Education & Sports Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Indole Compounds (AREA)
Abstract
Un compuesto de Fórmula (I) **(Ver fórmula)** N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en la que: G es: (i) **(Ver fórmula)** (ii) **(Ver fórmula)** (iii) **(Ver fórmula)** (iv) un anillo heterocíclico de 9 miembros seleccionado de: **(Ver fórmula)** o (v) anillo heterocíclico de 10 miembros seleccionado de: **(Ver fórmula)** R1 es H, Cl, -CN, alquilo C1-4, fluoroalquilo C1-3, hidroxialquilo C1-3, hidroxi-fluoroalquilo C1-3, -CRv=CH2, cicloalquilo C3-6, -CH2(cicloalquilo C3-6), -C(O)O(alquilo C1-3), o tetrahidropiranilo; cada R2 es independientemente halo, -CN, -OH, -NO2, alquilo C1-4, fluoroalquilo C1-2, cianoalquilo C1-2, hidroxialquilo C1-3, aminoalquilo C1-3, -O(CH2)1-2OH, -(CH2)0-4O(alquilo C1-4), fluoroalcoxi C1-3, -(CH2)1-4O(alquilo C1-3), -O(CH2)1-2OC(O)(alquilo C1-3), -O(CH2)1-2NRxRx, -C(O)O(alquilo C1-3), -(CH2)0-2C(O)NRyRy, - C(O)NRx(hidroxialquilo C1-5), -C(O)NRx(alcoxialquilo C2-6), -C(O)NRx(cicloalquilo C3-6), -NRyRy, -NRy(fluoroalquilo C1-3), -NRy(hidroxialquilo C1-4), -NRxCH2(fenilo), -NRxS(O)2(cicloalquilo C3-6), -NRxC(O)(alquilo C1-3), - NRxCH2(cicloalquilo C3-6), -(CH2)0-2S(O)2(alquilo C1-3), -(CH2)0-2(cicloalquilo C3-6), -(CH2)0-2(fenilo), morfolinilo, dioxotiomorfolinilo, dimetil pirazolilo, metilpiperidinilo, metilpiperazinilo, amino-oxadiazolilo, imidazolilo, triazolilo o - C(O)(tiazolilo); R2a es alquilo C1-6, fluoroalquilo C1-3, hidroxialquilo C1-6, aminoalquilo C1-3, -(CH2)0-4O(alquilo C1-3), cicloalquilo C3- 6, -(CH2)1-3C(O)NRxRx, -CH2(cicloalquilo C3-6), -CH2(fenilo), tetrahidrofuranilo, tetrahidropiranilo, o fenilo; cada R2b es independientemente H, halo, -CN, -NRxRx, alquilo C1-6, fluoroalquilo C1-3, hidroxialquilo C1-3, fluoroalcoxi C1-3, -(CH2)0-2O(alquilo C1-3), -(CH2)0-3C(O)NRxRx, -(CH2)1-3(cicloalquilo C3-6), -C(O)O(alquilo C1-3), - C(O)NRx(C1-3 alquilo), -CRx=CRxRx, o -CRx=CH(cicloalquilo C3-6); R2c es R2a o R2b; R2d es R2a o R2b; siempre y cuando uno de R2c y R2d es R2a, y el otro de R2c y R2 es R2b; cada R5 es independientemente F, Cl, -CN, alquilo C1-3, fluoroalquilo C1-2, o -OCH3; R7 es: (i) R7a, -CH2R7a, -C(O)R7a, -C(O)CH(NH2)R7a, -C(O)(CH2)1-3NH2, -C(O)CH(NH2)(alquilo C1-4), - C(O)CH(NH2)(CH2)1-2C(O)OH, -C(O)CH(NH2)(CH2)2-4NH2 o -C(O)CH(NH2)(CH2)1-3C(O)NH2; o (ii) cicloalquilo C3-6 sustituido con un sustituyente seleccionado de -NRx(CH2)2-3NRyRy, -NRx(metilpiperidinilo), - NRx(CH2)2-3(morfolinilo), dimetilamino piperidinilo y piperazinilo sustituido con un sustituyente seleccionado de alquilo C1-4, -C(O)CH3, -(CH2)1-2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), cicloalquilo C3-6, piridinilo y metilpiperidinilo; R7a es azaespiro[3.5]nonanilo, cicloalquilo C3-6, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, diazepanonilo, diazepanilo, morfolinilo, fenilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo, o pirrolilo, cada uno sustituido con cero a 1 sustituyente seleccionado de alquilo C1-3, -NH2, metilpiperidinilo, metilpirrolidinilo, - OCH2CH2(pirrolidinilo), y -OCH2CH2NHCH2CH3; y cero a 4 sustituyentes seleccionados de -CH3; R7b es: (i) alquilo C1-4, hidroxialquilo C1-3, -(CH2)2-3CºCH, -(CH2)1-2O(alquilo C1-2), -(CH2)1-2S(O)2(alquilo C1-2), -(CH2)0- 3NRxRy, -CH2C(O)NRxRx, -NRx(hidroxialquilo C1-4), -NRy(cianoalquilo C1-2), -NRx(fluoroalquilo C1-2), -NRx(C2-4 hidroxifluoroalquilo), -NRx(CH2)1-2C(O)NRxRx, -NRx(CH2)1-3NRxRx, -NRxCH2CH2NRxRx, -NRxC(O)(CH2)1- 2NRxRx, -O(CH2)1-3NRxRx, -C(O)CH2NRxRx, -(CH2)1-2R7d, -NHR7d, -NH(CH2)1-2R7d o -OR7d; o (ii) azepanilo, azetidinilo, diazepanilo, dioxotiomorfolinilo, morfolinilo, oxaazaespiro[3,3]heptanilo, oxetanilo, piperazinonilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b; cada R7c es independientemente F, Cl, -CN, alquilo C1-2, -CF3, o -CH2CN; R7d es azaespiro[3.5]nonanilo, biciclo[1.1.1]pentanilo, cicloalquilo C3-6, morfolinilo, oxetanilo, fenilo, piperidinilo, pirazolilo, pirrolidinilo, tetrahidrofuranilo o tetrahidropiranilo, cada uno sustituido con cero a 1 sustituyente seleccionado de alquilo C1-3, -NRxRx, -C(O)CH3, metilpiperidinilo, metilpirrolidinilo, tetrametilpiperidinilo, - OCH2CH2(pirrolidinilo), y -OCH2CH2NHCH2CH3; y cero a 4 sustituyentes seleccionados de -CH3; R8 es H o alquilo C1-3; o R7 y R8 junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo y pirrolilo, en donde dicho anillo heterocíclico está sustituido con cero a 1 R7b y cero a 2 R7c; R8a es -OH, alquilo C1-6, fluoroalquilo C1-4, hidroxialquilo C1-4, -(CH2)1-2O(alquilo C1-3), -C(O)(alquilo C1-3), -(CH2)1- 2(cicloalquilo C3-6), -(CH2)1-3(metil fenilo), -(CH2)1-3(pirrolidinilo), -(CH2)1-3(metilpirazolilo), -(CH2)1-3(tiofenilo), - NRxRx, cicloalquilo C3-6, metilpiperidinilo, piridinilo o pirimidinilo; cada R8b es independientemente F, Cl, -CN, alquilo C1-3, o -CF3; Rv es H, alquilo C1-2 o fluoroalquilo C1-2; cada Rx es independientemente H o -CH3; cada Ry es independientemente H o alquilo C1-6; n es cero, 1, o 2; y p es cero, 1, 2, 3, o 4.
Description
DESCRIPCIÓN
Compuestos de amino indol útiles como inhibidores de TLR
La presente invención se refiere generalmente a compuestos de amino indol útiles como inhibidores de la señalización a través de los receptores 7, 8 o 9 tipo Toll (TLR7, TLR8, TLR9) o combinaciones de los mismos. En el presente documento se proporcionan compuestos de amino indol, composiciones que comprenden tales compuestos y usos de los mismos. La invención se refiere además a composiciones farmacéuticas que contienen al menos un compuesto de acuerdo con la invención que son útiles para el tratamiento de afecciones relacionadas con la modulación de TLR, tales como enfermedades inflamatorias y autoinmunes, y para inhibir la actividad de TLR en un mamífero.
Los miembros de la familia de receptores Toll/IL-1 son reguladores importantes de la inflamación y la resistencia del anfitrión. La familia de receptores tipo Toll reconoce patrones moleculares derivados de organismos infecciosos que incluyen bacterias, hongos, parásitos y virus (revisado en Kawai, T. et al., Nature Immunol., 11:373-384 (2010)). La unión del ligando al receptor induce la dimerización y el reclutamiento de moléculas adaptadoras a un motivo citoplasmático conservado en el receptor denominado dominio del receptor Toll/IL-1 (TIR). Con la excepción de TLR3, todos los TLRs reclutan la molécula adaptadora MyD88. La familia de receptores de IL-1 también contiene un motivo TIR citoplasmático y recluta MyD88 luego de la unión a ligando (revisado en Sims, J.E. et al., Nature Rev. Immunol., 10:89-102 (2010)).
Los receptores tipo Toll (TLR, por sus siglas en inglés) son una familia de receptores inmunes innatos transmembrana conservados evolutivamente que participan en la defensa de primera línea. Como receptores de reconocimiento de patrones, los TLRs protegen contra moléculas extrañas, activadas por patrones moleculares asociados a patógenos (PAMPs), o de tejido dañado, activados por patrones moleculares asociados a peligros (DAMPs). Se han identificado un total de 13 miembros de la familia TLR, 10 en humanos, que abarcan la superficie celular o el compartimento endosómico. TLR7/8/9 se encuentra entre el conjunto que se localiza endosómicamente y responde al ARN monocatenario (TLR7 y TLR8) o al ADN monocatenario no metilado que contiene motivos de citosina-fosfato-guanina (CpG) (TLR9).
La activación de TLR7/8/9 puede iniciar varias respuestas inflamatorias (producción de citocinas, activación de células B y producción de IgG, respuesta de interferón tipo I). En el caso de los trastornos autoinmunes, la activación sostenida aberrante de TLR7/8/9 conduce al empeoramiento de los estados de enfermedad. Aunque se ha demostrado que la sobreexpresión de TLR7 en ratones exacerba la enfermedad autoinmune, se descubrió que la eliminación de TLR7 en ratones es protectora contra la enfermedad en ratones MRL/lpr propensos a lupus. La doble eliminación de TLR7 y 9 mostró una mayor protección mejorada.
Como numerosas afecciones pueden beneficiarse del tratamiento que implica la modulación de las citocinas, la producción de IFN y la actividad de las células B, es inmediatamente evidente que los nuevos compuestos capaces de modular TLR7 y/o TLR8 y/o TLR9 y los métodos para usar estos compuestos podrían proporcionar beneficios terapéuticos sustanciales Una amplia variedad de pacientes.
El documento US 201H0008885 desvela derivados de pirrolo[3,2-C]piridina como inhibidores de TLR.
La presente invención se refiere a una nueva clase de compuestos de amino indol que resultan ser inhibidores efectivos de la señalización a través de TLR7/8/9. Estos compuestos se proporcionan para ser útiles como productos farmacéuticos con estabilidad deseable, biodisponibilidad, índice terapéutico y valores de toxicidad que son importantes para su capacidad de carga.
Descripción detallada
La presente invención proporciona compuestos de la Fórmula (I) que son útiles como inhibidores de la señalización a través del receptor 7, 8 o 9 tipo Toll y son útiles para el tratamiento de enfermedades proliferativas, enfermedades alérgicas, enfermedades autoinmunes y enfermedades inflamatorias, o estereoisómeros, N-óxido, tautómeros, sales farmacéuticamente aceptables o solvatos de los mismos.
La presente invención también proporciona composiciones farmacéuticas que comprenden un portador farmacéuticamente aceptable y al menos uno de los compuestos de la presente invención o estereoisómeros, tautómeros, sales farmacéuticamente aceptables o solvatos de los mismos.
La presente invención también proporciona al menos uno de los compuestos de la presente invención o estereoisómeros, tautómeros, sales farmacéuticamente aceptables o solvatos de los mismos para su uso en la inhibición del receptor 7, 8 o 9 de tipo Toll en un huésped que necesite tal tratamiento.
La presente invención también al menos uno de los compuestos de la presente invención o estereoisómeros, tautómeros, sales farmacéuticamente aceptables o solvatos de los mismos para su uso en el tratamiento de enfermedades proliferativas, metabólicas, alérgicas, autoinmunes e inflamatorias, en un huésped que necesite tal
tratamiento.
La presente invención también proporciona al menos uno de los compuestos de Fórmula (I) o sales y solvatos de los mismos para su uso en el tratamiento de una enfermedad o trastorno asociado a la actividad del receptor 7, 8 o 9 tipo Toll, en un mamífero que lo necesite.
La presente invención también proporciona procesos e intermediarios para preparar los compuestos de la Fórmula (I) incluyendo sales y solvatos de los mismos.
La presente invención también proporciona al menos uno de los compuestos de la Fórmula (I) o sales y solvatos de los mismos, para uso en terapia.
El compuesto de la Fórmula (I) y las composiciones que comprenden los compuestos de la Fórmula (I) se pueden usar para tratar, prevenir o curar diversas afecciones relacionadas con los receptores 7, 8 o 9 de tipo Toll. Las composiciones farmacéuticas que comprenden estos compuestos son útiles para tratar, prevenir o retrasar la progresión de enfermedades o trastornos en varias áreas terapéuticas, tales como enfermedades alérgicas, enfermedades autoinmunes, enfermedades inflamatorias y enfermedades proliferativas.
Estas y otras características de la invención se expondrán en forma expandida a medida que continúa la invención.
Descripción Detallada
El primer aspecto de la presente invención proporciona al menos un compuesto de la Fórmula (I):
N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde:
G es:
(i)
(ii)
(iii)
(iv) un anillo heterocíclico de 9 miembros seleccionado de:
Ċ
(v) anillo heterocíclico de 10 miembros seleccionado de:
Ri es H, Cl, -CN, alquilo C1-4, fluoroalquilo C1-3, hidroxialquilo C1-3, C1-3 hidroxi-fluoroalquilo, -CRv=CH2, cicloalquilo C3-6, -CH2(cicloalquilo C3-6), -C(O)O(alquilo C1-3), o tetrahidropiranilo;
cada R2 es independientemente halo, -CN, -OH, -NO2, alquilo C1-4, fluoroalquilo C1-2, cianoalquilo C1-2, hidroxialquilo C1-3, aminoalquilo C1-3, -O(CH2)1-2OH, -(CH2)0-4O(alquilo C1-4), fluoroalcoxi C1-3, -(CH2)1-4O(alquilo C1-3), -O(CH2)1-2OC(O)(alquilo C1-3), -O(CH2)1-2NRxRx, -C(O)O(alquilo C1-3), -(CH2)0-2C(O)NRyRy, -C(O)NRx(hidroxialquilo C1-5), -C(O)NRx(alcoxialquilo C2-6), -C(O)NRx(cicloalquilo C3-6), -NRyRy, -NRy(fluoroalquilo C1-3), -NRy(hidroxialquilo C1-4), -NRxCH2(fenilo), -NRxS(O)2(cicloalquilo C3-6), -NRxC(O)(alquilo C1-3), -NRxCH2(cicloalquilo C3-6), -(CH2)0-2S(O)2(alquilo C1-3), -(CH2)0-2(cicloalquilo C3- 3), -(CH2)0-2(fenilo), morfolinilo, dioxotiomorfolinilo, dimetil pirazolilo, metilpiperidinilo, metilpiperazinilo, amino-oxadiazolilo, imidazolilo, triazolilo, o -C(O)(tiazolilo);
R2a es alquilo C1-6, fluoroalquilo C1-3, hidroxialquilo C1-6, aminoalquilo C1-3, -(CH2)0-4O(alquilo C1-3), cicloalquilo C3-6, -(CH2)1-3C(O)NRxRx, -CH2(cicloalquilo C3-6), -CH2(fenilo), tetrahidrofuranilo, tetrahidropiranilo, o fenilo; cada R2b es independientemente H, halo, -CN, -NRxRx, alquilo C1-6, fluoroalquilo C1-3, hidroxialquilo C1-3, fluoroalcoxi C1-3, -(CH2)0-2O(alquilo C1-3), -(CH2)0-3C(O)NRxRx, -(CH2)1-3(cicloalquilo C3-6), -C(O)O(alquilo C1-3), -C(O)NRx(C1-3 alquilo), -CRx=CRxRx, o -CRx=CH(cicloalquilo C3-6);
R2c es R2a o R2b;
R2d es R2a o R2b; siempre y cuando uno de R2c y R2d sea R2a, y el otro de R2c y R2d sea R2b;
cada R5 es independientemente F, Cl, -CN, alquilo C1-3, fluoroalquilo C1-2, o -OCH3;
R7 es:
(i) R7a, -CH2R7a, -C(O)R7a, -C(O)CH(NH2)R7a, -C(O)(CH2)1-3NH2, -C(O)CH(NH2)(alquilo C1-4), -C(O)CH(NH2)(CH2)1-2C(O)OH, -C(O)CH(NH2)(CH2)2-4NH2, o -C(O)CH(NH2)(CH2)1-3C(O)NH2; o
(ii) cicloalquilo C3-6 sustituido con un sustituyente seleccionado de -NRx(CH2)2-3NRyRy, -NRx(metilpiperidinilo), -NRx(CH2)2-3(morfolinilo), dimetilamino piperidinilo, y piperazinilo sustituido con un sustituyente seleccionado de alquilo C1-4, -C(O)CH3, -(CH2K 2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), cicloalquilo C3-6, piridinilo, y metilpiperidinilo;
R7a es azaespiro[3.5]nonanilo, cicloalquilo C3-6, diazaeespiro[3.5]nonanilo, diazaeespiro[5,5]undecanilo, diazepanonilo, diazepanilo, morfolinilo, fenilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo, o pirrolilo, cada uno sustituido con cero a 1 sustituyente seleccionado de alquilo C1-3, -NH2, metilpiperidinilo, metilpirrolidinilo, -OCH2CH2(pirrolidinilo), y -OCH2CH2NHCH2CH3; y cero a 4 sustituyentes seleccionados de -CH3;
R7b es:
(i) alquilo C1-4, hidroxialquilo C1-3, -(CH2)2-3C=CH, -(CH2)1-2O(alquilo C1-2), -(CH2)1-2S(O)2(alquilo C1-2), -(CH2V 3NRxRy, -CH2C(O)NRxRx, -NRx(hidroxialquilo C1-4), -NRy(cianoalquilo C1-2), -NRx(fluoroalquilo C1-2), -NRx(C2-4 hidroxifluoroalquilo), -NRx(CH2)1-2C(O)NRxRx, -NRx(CH2)1-3NRxRx, -NRxCH2CH2NRxRx, -NRxC(O)(CH2)1-2NRxRx, -O(CH2)1-3NRxRx, -C(O)CH2NRxRx, -(CH2)1-2R7d, -NHR7d, -NH(CH2)1-2R7d, o -OR7d; o
(ii) azepanilo, azetidinilo, diazepanilo, dioxotiomorfolinilo, morfolinilo, oxaazaeespiro[3,3]heptanilo, oxetanilo, piperazinonilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo, otetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b;
cada R7c es independientemente F, Cl, -CN, alquilo C1-2, -CF3, o -CH2CN;
R7d es azaeespiro[3.5]nonanilo, biciclo[1.1.1]pentanilo, cicloalquilo C3-6, morfolinilo, oxetanilo, fenilo, piperidinilo,
pirazolilo, pirrolidinilo, tetrahidrofuranilo, o tetrahidropiranilo, cada uno sustituido con cero a 1 sustituyente seleccionado de alquilo C1-3, -NRxRx, -C(O)CH3, metilpiperidinilo, metilpirrolidinilo, tetrametilpiperidinilo, -OCH2CH2(pirrolidinilo), y -OCH2CH2NHCH2CH3; y cero a 4 sustituyentes seleccionados de -CH3;
R8 es H o alquilo C1-3;
o R7 y Ra junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo, y pirrolilo, en donde el anillo heterocíclico es sustituido con cero a 1 R7b y cero a 2 R7c;
Raa es -OH, alquilo C1-6, fluoroalquilo C1-4, hidroxialquilo C1-4, -(CH2)1-2O(alquilo C1-3), -C(O)(alquilo 2(cicloalquilo C3-6), -(CH2)1-3(metilfenilo), -(CH2)1-3(pirrolidinilo), -(CH2)1-3(metilpirazolilo), -(CH2)1-3(tiofenilo), -NRxRx, cicloalquilo C3-6, metilpiperidinilo, piridinilo, o pirimidinilo;
cada Rab es independientemente F, Cl, -CN, alquilo C1-3, o -CF3;
Rv es H, alquilo C1-2, o fluoroalquilo C1-2;
cada Rx es independientemente H o -CH3;
cada Ry es independientemente H o alquilo C1-6;
n es cero, 1, o 2; y
p es cero, 1, 2, 3, o 4.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo o una sal del mismo en donde
G es:
y R1, R5, R7, Ra, y n se definen en el primer aspecto.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde G es:
y R1, R2, R5, R7, Ra, n, y p se definen en el primer aspecto.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde G es
y R1, R2a, R2b, R2c, R2d, R5, R7, Ra, n, y p se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales R2a es alquilo C1-4, fluoroalquilo C1-2, hidroxialquilo C1-4, -(CH2)1-3OCH3, cicloalquilo C3-6, -CH2C(O)NRxRx, -CH2(cicloalquilo C3-6), -CH2(fenilo), tetrahidrofuranilo, o fenilo; y cada R2b es independientemente H, F, Cl, -CN, -NRxRx, alquilo C1-6, fluoroalquilo C1-2, hidroxialquilo C1-3, -(CH2)o-2O(alquilo C1-2), -(CH2)o-2C(O)NRxRx, -(CH2)1-3(ciclopropilo), -C(O)O(alquilo C1-2), -C(O)NRx(alquilo C1-3), -CRx=CH2, o -CH=CH(cicloalquilo C3-6). En esta modalidad también se incluyen compuestos en los cuales R2a es -CH3; y cada R2b es independientemente H, Cl, o -CH3.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde G es un anillo heterocíclico de 9 miembros seleccionado de:
a
y Ri, R2, R5, R7, R8, n, y p se definen en el primer aspecto.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde G es un anillo heterocíclico de 10 miembros seleccionado de:
y R1, R2, R5, R7, R8, n, y p se definen en el primer aspecto.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde G es:
y Ri, R2, R2a, R2b, R5, R7, R8, n, y p se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales R1 es -CH3, -CH2CH3, o -CH(CH3)2; cada R2 es independientemente Cl, -CH3, o -OCH3; R2a es -CH3; cada R2b es independientemente H, Cl, o -CH3; R7 es: (i) -CH2(isopropilazaespiro[3.5]nonanilo), -CH2(metilpirrolidinilo), -C(O)(CH2)1-3NH2, -C(O)CH(NH2)CH2CH2CH3, -C(O)CH(NH2)CH2CH(CH3)2, -C(O)CH(NH2)CH(CH3)CH2CH3, -C(O)CH(NH2)CH2CH2C(O)OH, -C(O)CH(NH2)(CH2)3-4NH2, -C(O)CH(NH2)(CH2)1-2C(O)NH2, -C(O)CH(NH2)(ciclohexilo), -C(O)CH(NH2)(fenilo), -C(O)(aminociclohexilo), -C(O)(morfolinilo), -C(O)(pirrolidinilo), pentametilpiperidinilo, metilpiperidinil-piperidinilo, metilpirrolidinil-pirrolidinilo, o fenilo sustituido con -OCH2CH2(pirrolidinilo) o -OCH2CH2NHCH2CH3; o (ii) ciclohexilo sustituido con -NRx(CH2)2-3N(CH3)2, -NHCH2CH2NHCH3, -NH(metilpiperidinilo), -NH(CH2)2-3(morfolinilo), dimetilamino piperidinilo, o piperazinilo sustituido con -CH3, -CH2CH3, -C(CH3)3, -CH2CH(CH3)2, -C(O)CH3, -CH2CH2OCH3, -CH2(metilfenilo), -(CH2)2-s(pirrolidinilo), ciclopentilo, piridinilo, o metilpiperidinilo; R8 es H, -CH3 o -CH2CH3; o R7 y R8 junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, y pirrolidinilo, en donde el anillo heterocíclico es sustituido con cero a 1 R7b y cero a 2 R7c; R7b es: (i) -CH3, -CH(CH3)2, -C(CH^OH, -CH2CH2CH2C=CH, -CH2CH2NH(CH3), -CH2CH2N(CH3)2, -NRxRx, -NHCH2CH2NH(CH3), -NHCH2CH2N(CH3)2, -N(CH3)CH2CH2NH2, -NRxCH2CH2CH2N(CH3)2, -OCH2CH2N(CH3)2, -CH2(fenilo), -CH2(metil pirazolilo), -CH2CH2(pirrolidinilo), -NH(metilpiperidinilo), -NH(isopropilpiperidinilo), -NH(pentametilpiperidinilo), -NH(acetilpiperidinilo), -NHCH2CH2(morfolinilo), -O(piperidinilo), -O(metilpiperidinilo), -O(etilpiperidinilo), -O(isopropilpiperidinilo), o -O(piperidinil)-(tetrametilpiperidinilo); o (ii) azepanilo, diazepanilo, morfolinilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo, o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b; cada R7c es independientemente -CH3 o -CH2CN; R8a es -OH, -CH3, -CH2CH3, -CH(CH3)2, -C(CH3)3, -CH2CH(CH3)2, -CH2CH2OCH3, -CH2CH2CF3, -C(O)CH3, -CH2(ciclopropilo), -CH2(metil fenilo), -(CH2)2-3(pirrolidinilo), -CH2(metilpirazolilo), -CH2(tiofenilo), -NRxRx, ciclopentilo, metilpiperidinilo, o piridinilo; cada R8b es -CH3; cada R5 es independientemente -CH3 o -CH(CH3)2; cada Rx es independientemente H o -CH3; n es cero o 1; y p es cero, 1, 2, o 3.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde R1 es H, Cl, -CN, alquilo C1-4, C1-3 fluoroalquilo, hidroxialquilo
C1-3, hidroxi-fluoroalquilo C1-3, cicloalquilo C3-6, -CH2(cicloalquilo C3-6), o -C(O)O(alquilo C1-3); y G, R5, R7, definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales R1 es H, Cl, -CN, alquilo C1-4,
C1-2 fluoroalquilo, hidroxialquilo C1-2, o -C(O)O(alquilo C1-2). En esta modalidad también se incluyen compuestos en los cuales R1 es -CH3, -CH2CH3, o -CH(CH3)2.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde cada R2 es independientemente F, Cl, Br, -CN, -OH, -NO2, alquilo C1-4, fluoroalquilo C1-2, cianoalquilo C1-2, hidroxialquilo C1-3, aminoalquilo C1-3, -OCH2OH, -(CH2)0-2O(alquilo
C1-4), fluoroalcoxi C1-2, -(CH2)1-2O(alquilo C1-3), -O(CH2)1-2OC(O)(alquilo C1-2), -O(CH2)1-2NRxRx, -C(O)O(alquilo C1-2), -C(O)NRyRy, -C(O)NRx(hidroxialquilo C1-5), -C(O)NRx(alcoxialquilo C2-6), -C(O)NRx(cicloalquilo C3-6), -NRyRy, -NRy(fluoroalquilo C1-3), -NRy(hidroxialquilo C1-4), -NRxC(O)(alquilo C1-3), -S(O)2(alquilo C1-3), cicloalquilo C3-6, fenilo, morfolinilo, dioxotiomorfolinilo, dimetil pirazolilo, metilpiperidinilo, metilpiperazinilo, amino-oxadiazolilo, imidazolilo, o triazolilo; y G, R1, R5, R7, R8, Rx, Ry, n, y p se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales cada R2 es independientemente F, Cl, -CN, -OH, alquilo C1-4, fluoroalquilo C1-2, cianoalquilo C1-2, hidroxialquilo C1-3, aminoalquilo C1-3, C1-4 alcoxi, -NRyRy, -C(O)NRyRy, -C(O)NRx(hidroxialquilo C1-4), -C(O)NRx(alcoxialquilo C2-4), -C(O)NRx(cicloalquilo C3-6), -S(O)2(alquilo C1-3), cicloalquilo C3-6, morfolinilo, fenilo, o dimetil pirazolilo. En esta modalidad también se incluyen compuestos en los cuales cada R2 es independientemente
Cl, -CH3, o -OCH3. Además, en esta modalidad están compuestos en los que cada R2 es independientemente Cl, -CH3, o -OCH3; y p es cero, 1, 2, o 3.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una
sal farmacéuticamente aceptable del mismo en donde R7 es -CH2R7a, -C(O)(CH2)i-3NH2, -C(O)CH(NH2)(alquilo C1-4), -C(O)CH(NH2)(CH2)i -2C(O)OH, -C(O)CH(NH2)(CH2)2-4NH2, -C(O)CH(NH2)(CH2)1-3C(O)NH2, -C(O)CH(NH2)R7a, -C(O)R7a, o R7ai R8 es H o alquilo C1-3; yG , R1, R5, R7a, y n se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales R7 es -CH2R7a, -C(O)(CH2)1-3NH2, -C(O)CH(NH2)(alquilo C1-4), -C(O)CH(NH2)(CH2)1-2C(O)OH, -C(O)CH(NH2)(CH2)2-4NH2, -C(O)CH(NH2)(CH2)1-3C(O)NH2, -C(O)CH(NH2)R7a, -C(O)R7a, o R7a. En esta modalidad también se incluyen compuestos en los cuales R7 es -CH2(isopropil azaespiro[3.5]nonanilo), -CH2(metilpirrolidinilo), -C(O)(CH2)1-3NH2, -C(O)CH(NH2)CH2CH2CH3, -C(O)CH(NH2)CH2CH(CH3)2, -C(O)CH(NH2)CH(CH3)CH2CH3, -C(O)CH(NH2)CH2CH2C(O)OH, -C(O)CH(NH2)(CH2)3-4NH2, -C(O)CH(NH2)(CH2)1-2C(O)NH2, -C(O)CH(NH2)(ciclohexilo), -C(O)CH(NH2)(fenilo), -C(O)(aminociclohexilo), -C(O)(morfolinilo), -C(O)(pirrolidinilo), pentametilpiperidinilo, metilpiperidinil-piperidinilo, metilpirrolidinil-pirrolidinilo, o fenilo sustituido con -OCH2CH2(pirrolidinilo) o -OCH2CH2NHCH2CH3; y R8 es H o alquilo C1-2.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde R7 es cicloalquilo C3-6 sustituido con un sustituyente seleccionado de -NRx(CH2)2-3NRyRy, -NRx(metilpiperidinilo), -NRx(CH2)2-3(morfolinilo), dimetilamino piperidinilo, y piperazinilo sustituido con un sustituyente seleccionado de alquilo C1-4, -C(O)CH3, -(CH2)1-2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), cicloalquilo C3-6, piridinilo, y metilpiperidinilo; R8 es H o alquilo C1-3; y G, R1, R5, Rx, Ry, y n se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales cicloalquilo C3-6 sustituido con un sustituyente seleccionado de -NRx(CH2)2-3NRxRx, -NH(CH2)2-3NHCH3, -NH(metilpiperidinilo), -NH(CH2)2-3(morfolinilo), dimetilamino piperidinilo, y piperazinilo sustituido con un sustituyente seleccionado de alquilo C1-4, -C(O)CH3, -(CH2)1-2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), cicloalquilo C3-6, piridinilo, y metilpiperidinilo. En esta modalidad también se incluyen compuestos en los cuales R8 es ciclohexilo sustituido con -NRx(CH2)2-3N(CH3)2, -NHCH2CH2NHCH3, -NH(metilpiperidinilo), -NH(CH2)2-3(morfolinilo), dimetilamino piperidinilo, o piperazinilo sustituido con -CH3, -CH2CH3, -C(CH3)3, -CH2CH(CH3)2, -C(O)CH3, -CH2CH2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), ciclopentilo, piridinilo, o metilpiperidinilo; y R8 es H o alquilo C1-2.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde R7 y R8 junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo, y pirrolilo, en donde el anillo heterocíclico es sustituido con cero a 1 R7b y cero a 2 R7c; y G, R1, R5, R7b, R7c, y n se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales R7 y R8 junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, y pirrolidinilo, en donde el anillo heterocíclico es sustituido con cero a 1 R7b y cero a 2 R7c. En esta modalidad también se incluyen compuestos en los cuales R7b es: (i) -CH3, -CH(CH3)2, -C(CH3)2OH, -CH2CH2CH2C=CH, -CH2CH2NH(CH3), -CH2CH2N(CH3)2, -NRxRx, -NHCH2CH2NH(CH3), -NHCH2CH2N(CH3)2, -N(CH3)CH2CH2NH2, -NRxCH2CH2CH2N(CH3)2, -OCH2CH2N(CH3)2, -CH2(fenilo), -CH2(metil pirazolilo), -CH2CH2(pirrolidinilo), -NH(metilpiperidinilo), -NH(isopropilpiperidinilo), -NH(pentametilpiperidinilo), -NH(acetilpiperidinilo), -NHCH2CH2(morfolinilo), -O(piperidinilo), -O(metilpiperidinilo), -O(etilpiperidinilo), -O(isopropilpiperidinilo), o -O(piperidinil)-(tetrametilpiperidinilo); o (ii) azepanilo, diazepanilo, morfolinilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo, o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b; y cada R7c es independientemente -CH3 o -CH2CN; y Rx, R8a, y R8b se definen en el primer aspecto.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde R7b es alquilo C1-4, hidroxialquilo C1-3, -(CH2)2-3C=CH, -(CH2)ü-3NRxRx, -NRx(CH2)1-3NRxRx, -N(CH3)CH2CH2NH2, -O(CH2)1-3NRxRx, -(CH2)1-2R7d, -NRxR7d, -NRx(CH2)1-2R7d, o -OR7d; y G, R1, R5, R7, R8, R7d, Rx, y n se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales R7b es alquilo C1-4, hidroxialquilo C1-3, -(CH2)2-3C=CH, -(CH2)0-3NRxRx, -NRx(CH2)1-3NRxRx, -N(CH3)CH2CH2NH2, -O(CH2)1-3NRxRx, -(CH2)1-2R7d, -NHR7d, -NH(CH2)1-2R7d, o -OR7d. En esta modalidad también se incluyen compuestos en los cuales R7b es -CH3, -CH(CH3)2, -C(CH3)2OH, -CH2CH2CH2C=CH, -CH2CH2NH(CH3), -CH2CH2N(CH3)2, -NRxRx, -NHCH2CH2NH(CH3), -NHCH2CH2N(CH3)2, -N(CH3)CH2CH2NH2, -NRxCH2CH2CH2N(CH3)2, -OCH2CH2N(CH3)2, -CH2(fenilo), -CH2(metil pirazolilo), -CH2CH2(pirrolidinilo), -NH(metilpiperidinilo), -NH(isopropilpiperidinilo), -NH(pentametilpiperidinilo), -NH(acetilpiperidinilo), -NHCH2CH2(morfolinilo), -O(piperidinilo), -O(metilpiperidinilo), -O(etilpiperidinilo), -O(isopropilpiperidinilo), o -O(piperidinil)-(tetrametilpiperidinilo).
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde R7b es azepanilo, diazepanilo, morfolinilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo, o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b; cada R7c es independientemente F, Cl, -CN, alquilo C1-2, -CF3, o -CH2CN; y G, R1, R5, R7, R8, y n se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales R7b es azepanilo, diazepanilo, morfolinilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo, o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b; R8a es -OH, alquilo C1-4, fluoroalquilo C1-3, -(CH2)1-2O(alquilo C1-2), -C(O)(alquilo C1-2), -CH2(cicloalquilo C3-6), -(CH2)1-2(metil fenilo), -(CH2)1-3(pirrolidinilo), -(CH2)1-2(metilpirazolilo), -(CH2)1-2(tiofenilo), -NRxRx, cicloalquilo C3-6, metilpiperidinilo, o piridinilo; cada R8b es independientemente F o -CH3; y cada Rx es
independientemente H o -CH3. En esta modalidad también se incluyen compuestos en los cuales en donde R7b es azepanilo, diazepanilo, morfolinilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo, o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8ay cero a 3 R8b.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde cada R5 es independientemente F, Cl, -CN, alquilo C1-3, -CF3, o -OCH3; n es cero, 1, o 2; y G, R1, R7, R8, y n se definen en el primer aspecto. En esta modalidad se incluyen compuestos en los cuales cada R5 es independientemente F, Cl, alquilo C1-3, -CF3, o -OCH3. En esta modalidad también se incluyen compuestos en los cuales cada R5 es independientemente -CH3 o -CH(CH3)2. This embodiment also includes compounds in which n es cero o 1.
Una modalidad proporciona un compuesto de la Fórmula (I), N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo en donde el compuesto es (R)-N-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4- il)-1H-indol-5-il)pirrolidin-3-carboxamida (9); (S)-N-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)pirrolidin-3-carboxamida (10); 2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)acetamida (11); 4-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)butanamida (12); N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pirrolidin-3-carboxamida (13); (R)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pentanamida (14); N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)morfolin-2-carboxamida (15); (R)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-metilpentanamida (16); (2R,3R)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-3-metilpentanamida (17); (S)-2-amino-N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)succinamida (18); (R)-2-amino-N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)succinamida (19); (S)-2,5-diamino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pentanamida (20); (1R,2S)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)ciclohexano-1-carboxamida (21); (R)-2-amino-N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pentandiamida (22); (S)-2,6-diamino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)hexanamida (23); ácido (S)-4-amino-5-((2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)amino)-5-oxopentanoico (24); (S)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-2-fenilacetamida (25); (S)-2-amino-2-ciclohexil-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)acetamida (26); 2-(3,4-dimetoxifenil)-N,3-dietil-N-(1'-metil-1,4'-bipiperidin-4-il)-1H-indol-5-amina (28); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-(metilamino)etil)ciclohexano-1,4-diamina (30-31); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-(dimetilamino)etil)ciclohexano-1,4-diamina (32-33); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-metilpiperazin-1-il)ciclohexil)-1H-indol-5-amina (34); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5- il)-N4-(2-(dimetilamino)etil)-N4-metilciclohexano-1,4-diamina (35); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(3-(dimetilamino)propil)ciclohexano-1,4-diamina (36-37); 2-(3,4-dimetoxifenil)-N-(4-(4-etilpiperazin-1-il)ciclohexil)-3-isopropil-1H-indol-5-amina (38-39); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(1-metilpiperidin-4-il)ciclohexano-1,4-diamina (40-41); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(3-(dimetilamino)propil)-N4-metilciclohexano-1,4-diamina (42-43); 1-(4-(4-((2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)amino) ciclohexil)piperazin-1-il)etan-1-ona (44-45); 2-(3,4-dimetoxifenil)-N-(4-(4-(dimetilamino)piperidin-1-il)ciclohexil)-3-isopropil-1H-indol-5-amina (46); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-morfolinoetil)ciclohexano-1,4-diamina (47-48); N-(4-(4-(terc-butil)piperazin-1-il)ciclohexil)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-amina (49-50); 2-(3,4-dimetoxifenil)-N-(4-(4-isobutilpiperazin-1-il)ciclohexil)-3-isopropil-1H-indol-5-amina (51-53); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(2-metoxietil)piperazin-1-il)ciclohexil)-1H-indol-5-amina (54); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(3-morfolinopropil)ciclohexano-1,4-diamina (55-56); N-(4-(4-ciclopentilpiperazin-1-il)ciclohexil)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-amina (57-58); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(piridin-4-il)piperazin-1-il)ciclohexil)-1H-indol-5-amina (59-60); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(1-metilpiperidin-4-il)piperazin-1-il)ciclohexil)-1H-indol-5-amina (61-62); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(2-(pirrolidin-1-il)etil)piperazin-1-il)ciclohexil)-1H-indol-5-amina (63-64); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(4-metilbencil)piperazin-1-il)ciclohexil)-1H-indol-5-amina (65-66); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(3-(pirrolidin-1-il)propil)piperazin-1-il)ciclohexil)-1H-indol-5-amina (67); 2-(3,4-dimetoxifenil)-3-isopropil-N-(1,2,2,6,6-pentametilpiperidin-4-il)-1H-indol-5-amina (103); 2-(3,4-dimetoxifenil)-3-isopropil-N-metil-N-((1-metilpirrolidin-2-il)metil)-1H-indol-5-amina (104); 2-(3,4-dimetoxifenil)-N-(4-(2-(etilamino)etoxi)fenil)-3-isopropil-1H-indol-5-amina (105); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(2-(pirrolidin-1-il)etoxi)fenil)-1H-indol-5-amina (106); 2-(3,4-dimetoxifenil)-3-etil-N-((7-isopropil-7-azaespiro[3.5]nonan-2-il)metil)-1H-indol-5-amina (124); o 2-(3,4-dimetoxifenil)-3-etil-N-(1'-metil-[1,4'-bipiperidin]-4-il)-1H-indol-5-amina (125).
En una modalidad, se proporciona un compuesto de la Fórmula (I) o una sal del mismo en donde el compuesto es 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)-3-((2-(metilamino)etil)amino)pirrolidin-2-ona (1); 3-((2-aminoetil)(metil)amino)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (2); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-3-(dimetilamino)pirrolidin-2-ona (3-4); 1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(4-isopropilpiperazin-1 -il)pirrolidin-2-ona (5-6); 3-(2-(dimetilamino)etoxi)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (7); 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)imidazolidin-2-ona (8); 1-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)imidazolidin-2-ona (27); 5-(3-(1,4-diazepan-1-il)azetidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (29); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(2,2,6,6-tetrametil-1l2-piperidin-4-il)piperazin-1-il)-1H-indol (68); 2-(3,4-dimetoxifenil)-3-etil-6-isopropil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol (69); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(pirrolidin-1-il)piperidin-1-il)-1H-indol (70); 2-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N,N-dimetiletan-1-amina (71);N1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N2-metiletan-1,2-diamina (72); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(piperazin-1-il)piperidin-1-il)-1H-indol (73); 4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)morfolina (74); N1-(1-(2-(3,4-dimetoxifenil)3-isopropil-1H-indol-5-il)piperidin-4-il)-N2,N2-dimetiletan-1,2-diamina (75); N1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N3,N3-dimetilpropan-1,3-diamina (76-77); 2-(3,4-dimetoxifenil)-5-(4-(4-etilpiperazin-1-il)piperidin-1-il)-3-isopropil-1H-indol (78); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N-(1-metilpiperidin-4-il)piperidin-4-amina (79); 4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-2,6-dimetilmorfolina (80); N1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N1,N3,N3-trimetilpropan-1,3-diamina (81); 1-(4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)piperazin-1-il)etan-1-ona (82); 1'-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N,N-dimetil-[1,4'-bipiperidin]-4-amina (83); 2-(3,4-dimetoxifenil)-5-(4-(4-etil-1,4-diazepan-1-il)piperidin-1-il)-3-isopropil-1H-indol (84); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-isopropilpiperazin-1-il)piperidin-1-il)-1H-indol (85); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N-(2-morfolinoetil)piperidin-4-amina (86); 5-(4-(4-(cidopropylmetil)piperazin-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (87); 1-(4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-1,4-diazepan-1-il)etan-1-ona (88); 1-(4-((1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)amino)piperidin-1-il)etan-1-ona (89); 5-(4-(4-(terc-butil)piperazin-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (90); 2-(3,4-dimetoxifenil)-5-(4-(4-isobutilpiperazin-1-il)piperidin-1-il)-3-isopropil-1H-indol (91); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(2-metoxietil)piperazin-1-il)piperidin-1-il)-1H-indol (92); 5-(4-(4-ddopentilpiperazin-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (93); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(piridin-4-il)piperazin-1-il)piperidin-1-il)-1H-indol (94); N-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-1,2,2,6,6-pentametilpiperidin-4-amina (95); 2-(3,4-dimetoxifenil)-3-isopropil-5-(1'-((1-metil-1H-pirrol-2- il)metil)-[4,4'-bipiperidin]-1-il)-1H-indol (96); 2-(3,4-dimetoxifenil)-3-isopropil-5-(1'-(3,3,3-tnfluoropropil)-[4,4'-bipiperidin]-1-il)-1H-indol (97); 2-(3,4-dimetoxifenil)-3-isopropil-5-(1'-(tiofen-3-ylmetil)-[4,4'-bipiperidin]-1-il)-1H-indol (98); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(1-metilpiperidin-4-il)piperazin-1-il)piperidin-1-il)-1H-indol (99); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(2-(pirrolidin-1-il)etil)piperazin-1-il)piperidin-1-il)-1H-indol (100); 2-(3,4-dimetoxifenil)-3- isopropil-5-(4-(4-(4-metilbencil)piperazin-1-il)piperidin-1-il)-1H-indol (101); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(3-(pirrolidin-1-il)propil)piperazin-1-il)piperidin-1-il)-1H-indol (102); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-(2-(dimetilamino)etil)-1,4-diazepan-5-ona (107); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N,N-dimetilpiperidin-4- amina (108); 2-(4-amino-1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)acetonitrilo (109); 2-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)propan-2-ol (110); 3-doro-5-(5-(4-(dimetilamino)piperidin-1-il)-3-isopropil-1H-indol-2-il)-1,4-dimetil-1l4,2l5-piridin-2-ona (111); 2-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-(metilamino)piperidin-4-il)acetonitrilo (112); 2-(3,4-dimetoxifenil)-3-isopropil-5-(2-(piridin-4-il)piperidin-1-il)-1H-indol (113); 2-((1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)oxi)-N,N-dimetiletan-1-amina (114); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(2-(pirrolidin-1-il)etil)piperidin-1-il)-1H-indol (115); 1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-4-hidroxipirrolidin-2-ona (116); 4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-metilpiperidin-4-il)morfolina (117); 6-bendl-1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)odahidro-1H-pirrolo[3,4-b]piridina (118); 1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-2-metil-1,2,3,4-tetrahidroisoquinolina (119); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N,N-dimetilpirrolidin-3-amina (120); 5-(4-(1,4-diazepan-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (121); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(1-isopropilazepan-4-il)piperazin-1-il)-1H-indol (122); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-metil-1,4-diazepan-1-il)piperidin-1-il)-1H-indol (123); 2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol, sal TFA (126); 2-(4-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperazin-1-il)-N-metiletanamina (127); 4-(3-isopropil-5-(piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (128); 2-(2,6-dimetoxipiridin-4-il)-3-etil-5-(piperazin-1-il)-1H-indol (129); 4-(3-isopropil-6-metil-5-(piperazin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (130); 5-([4,4'-bipiperidin]-1-il)-2-(3,4-dimetoxifenil)-3-etil-1H-indol (131); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(piperidin-4-iloxi)piperidin-1-il)-1H-indol (132); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(piperidin-4-iloxi)piperidin-1-il)-1H-indol (133); 2-(3,4-dimetoxifenil)-3-etil-5-(4-((1-metilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol (134); 6-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)odahidro-1H-pirrolo[3,4-b]piridina (135); 2-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-2,6-diazaespiro[3.5]nonane (136); 2-(4-(3-etil-2-(2-metoxipiridin-4-il)-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (137); 2-(4-(3-isopropil-2-(1H-pirrolo[2,3-b]piridin-4-il)-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (138); 3-etil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (139); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (140); 4-(3-metil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (141); 3-etil-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (142); 3-etil-2-(2-metoxipiridin-4-il)-5-(4-(1-metilpipendin-4-il)piperazin-1-il)-1H-indol (143); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-6-metil-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (144); 4-(5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (145); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(pent-4-in-1-il)piperazin-1-il)-1H-indol (146); 3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (147); 3-etil-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-2-(2-metoxipiridin-4-il)-1H-indol (148); 2-(3,4-dimetoxifenil)-3-metil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (149); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)-3,3-dimetilpiperazin-1-il)-N-metiletan-1-amina (150); 4-(5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (151); 3-etil-5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (152); 3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-2-(2-metoxipiridin-4-il)-1H-indol (153); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (154); 2-(3,4-dimetoxifenil)-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol (155); 2-(2,6-dimetoxipiridin-4-il)-3-etil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (156); 4-(3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (157); 4-(5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (158); 4-(3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (159); 3-etil-5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-2-(2-metoxipiridin-4-il)-1H-indol (160); 3-etil-2-(2-metoxipiridin-4-il)-5-(4-(2,2,6,6-tetrametilpiperidin-4-il)piperazin-1-il)-1H-indol (161); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (162); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-1H-indol (163); 2-(3,4-dimetoxifenil)-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol (164); 4-(3-etil-5-(4-(1isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1-metil-1H-pirrolo[2,3-b]piridina (165); 4-(3-isopropil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (166); 4-(3-isopropil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (167-168); 2-(3,4-dimetoxifenil)-3-etN-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol (169); 2-(3,4-dimetoxifenN)-5-(4-(1-isobutNpiperidin-4-N)piperazin-1-N)-3- metil-1H-indol (170); 2-(3,4-dimetoxifenil)-3-metil-5-(4-(2,2,6,6-tetrametilpiperidin-4-il)piperazin-1-il)-1H-indol (171); 2-(3,4-dimetoxifenil)-5-(2,2-dimetil-4-(1-metilpiperidin-4-il)piperazin-1-il)-3-etil-1H-indol (172); 2-(2,6-dimetoxipiridin-4-il)-3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol (173-174); 4-(3-isopropN-5-(4-(1-isopropNpiperidin-4-il)piperazin-1-il)-6-metil-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (175); 2-(3,4-dimetoxifenil)-3-etN-5-(4-(2,2,6,6-tetrametilpiperidin-4-il)piperazin-1-il)-1H-indol (176); 2-(3,4-dimetoxifenN)-3-etN-5-(4-(1-isobutNpiperidin-4-N)piperazin-1-il)-1H-indol (177); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)-1,4-diazepan-1-il)-N-metiletan-1-amina (178); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-metilpiperidin-4-il)-1,4-diazepan-1-il)-1H-indol (179); 2-(3,4-dimetoxifenil)-3-etN-5-(4-(1-isopropilpiperidin-4-il)-1,4-diazepan-1-il)-1H-indol (180); 3-(2-(3,4-dimetoxifenN)-3-etil-1H-indol-5-N)-9-metN-3,9-diazaespiro[5,5]undecano (181); 3-etil-5-(4-((1-isopropilpiperidin-4-il)oxi)piperidin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (182); 3-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)-9-isopropil-3,9-diazaespiro[5,5]undecano (183); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-metilpiperazin-1-il)piperidin-1-il)-1H-indol (184); 4-(3-etN-5-(4-((1-isopropNpiperidin-4-il)oxi)piperidin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (185); 3-(2-(3,4-dimetoxifenN)-3-etN-6-metil-1H-indol-5-N)-9-isopropil-3,9-diazaespiro[5,5]undecano (186); 2-(3,4-dimetoxifenN)-3-isopropN-5-(4-((1-metNpiperidin-4-N)oxi)piperidin-1-il)-1H-indol (187); 2-(3,4-dimetoxifenil)-3-etil-5-(4-((1-etilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol (188); 3-((1-metil-1H-pirrol-2-il)metil)-9-(3-metil-2-(1H-pirrolo[2,3-b]piridin-4-il)-1H-indol-5-il)-3,9-diazaespiro[5,5]undecano (189); 2-(3,4-dimetoxifenil)-5-(4-((1-etilpiperidin-4-il)oxi)piperidin-1-il)-3-isopropil-1H-indol (190); 2-(3,4-dimetoxifenil)-3-etN-5-(4-((1-isopropilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol (191); 1-(2-(3,4-dimetoxifenN)-3-isopropil-1H-indol-5-N)-N-(1-isopropilpiperidin-4-il)piperidin-4-amina (192); o 2-(3,4-dimetoxifenil)-3-etil-5-(4-((2',2,,6,,6'-tetr âmetil-[1,4,-bipiperidin]-4- il)oxi)piperidin-1-il)-1H-indol (193).
La presente invención puede materializarse de otras formas específicas. La invención abarca todas las combinaciones de los aspectos y/o modalidades de la invención indicados aquí. Se entiende que cualquiera y todas las modalidades de la presente invención pueden tomarse junto con cualquier otra modalidad o modalidades para describir modalidades adicionales. También debe entenderse que cada elemento individual de las modalidades está destinado a combinarse con cualquiera y todos los demás elementos de cualquier modalidad para describir una modalidad adicional.
Definiciones
Las características y ventajas de la invención pueden entenderse más fácilmente por los expertos en la materia al leer la siguiente descripción detallada. Debe apreciarse que ciertas características de la invención que, por razones de claridad, se describen arriba y abajo en el contexto de modalidades separadas, también se pueden combinar para formar una sola modalidad. Por el contrario, varias características de la invención que, por razones de brevedad, se describen en el contexto de una sola modalidad, también se pueden combinar para formar subcombinaciones de las mismas. Las modalidades identificadas aquí como a modo de ejemplo o preferidas pretenden ser ilustrativas y no limitantes.
A menos que se indique específicamente lo contrario en el presente documento, las referencias hechas en singular también pueden incluir el plural. Por ejemplo, "un" y "una" pueden referirse a uno, o uno o más.
Como se usa en el presente documento, la frase "compuestos" se refiere a por lo menos un compuesto. Por ejemplo, un compuesto de la Fórmula (I) incluye un compuesto de la Fórmula (I) y dos o más compuestos de la Fórmula (I).
A menos que se indique lo contrario, se supone que cualquier heteroátomo con valencias insatisfechas tiene átomos de hidrógeno suficientes para satisfacer las valencias.
Las definiciones establecidas en este documento tienen prioridad sobre las definiciones establecidas en cualquier patente, solicitud de patente y/o publicación de solicitud de patente incorporada aquí como referencia.
A continuación se enumeran definiciones de varios términos usados para describir la presente invención. Estas definiciones se aplican a los términos, ya que se usan en toda la especificación (a menos que estén limitados en casos específicos), ya sea individualmente o como parte de un grupo más grande.
A lo largo de la descripción, un experto en la materia puede elegir grupos y sustituyentes de los mismos para proporcionar restos y compuestos estables.
De acuerdo con una convención usada en la técnica,
se usa en las fórmulas estructurales de este documento para representar el enlace que es el punto de unión del resto o sustituyente al núcleo o estructura de la cadena principal.
Los términos "halo" y "halógeno", como se usan en este documento, se refieren a F, Cl, Br e I.
El término "ciano" se refiere al grupo CN.
El término "amino" se refiere al grupo NH2.
El término "oxo" se refiere al grupo =O.
El término "alquilo", como se usa en el presente documento, se refiere a grupos hidrocarbonados alifáticos saturados de cadena lineal y ramificada que contienen, por ejemplo, de 1 a 12 átomos de carbono, de 1 a 6 átomos de carbono y de 1 a 4 átomos de carbono. Ejemplos de grupos alquilo incluyen, pero no se limitan a, metilo (Me), etilo (Et), propilo (por ejemplo, n-propilo e i-propilo), butilo (por ejemplo, n-butilo, i-butilo, sec-butilo y t-butilo) y pentilo (por ejemplo, npentilo, isopentilo, neopentilo), n-hexilo, 2-metilpentilo, 2-etilbutilo, 3-metilpentilo y 4-metilpentilo. Cuando los números aparecen en un subíndice después del símbolo "C", el subíndice defina con más especificidad el número de átomos de carbono que puede contener un grupo en particular. Por ejemplo, "alquilo de C1-6" denota grupos alquilo de cadena lineal y ramificada con uno a seis átomos de carbono.
El término "fluoroalquilo" como se usa en el presente documento pretende incluir grupos hidrocarbonados alifáticos saturados de cadena lineal y ramificada sustituidos con uno o más átomos de flúor. Por ejemplo, "fluoroalquilo de C1-4" pretende incluir grupos alquilo de C1, C2, C3 y C4 sustituidos con uno o más átomos de flúor. Los ejemplos representativos de grupos fluoroalquilo incluyen, pero sin limitación, CF3 y CH2CF3.
El término "cianoalquilo" incluye grupos alquilo saturados de cadena lineal y ramificada sustituidos con uno o más grupos ciano. Por ejemplo, "cianoalquilo" incluye CH2CN, CH2CH2CN y cianoalquilo de C1-4.
El término "aminoalquilo" incluye grupos alquilo saturados de cadena lineal y ramificada sustituidos con uno o más grupos amino. Por ejemplo, "aminoalquilo" incluye CH2NH2, CH2CH2NH2 y aminoalquilo de C1-4.
El término "hidroxialquilo" incluye grupos alquilo saturados de cadena ramificada y lineal sustituidos con uno o más grupos hidroxilo. Por ejemplo, "hidroxialquilo" incluye CH2OH, CH2CH2OH e hidroxialquilo de C1-4.
El término "hidroxifluoroalquilo" incluye grupos alquilo saturados de cadena ramificada y lineal sustituidos con uno o más grupos hidroxilo y uno o más átomos de flúor. Por ejemplo, "hidroxifluoroalquilo" incluye CHFCH2OH, CH2CHFC (CH3)2OH e hidroxifluoroalquilo de C1-4.
El término "cicloalquilo", como se usa en el presente documento, se refiere a un grupo derivado de una molécula de hidrocarburo monocíclico o policíclico no aromático mediante la eliminación de un átomo de hidrógeno de un átomo de carbono del anillo saturado. Ejemplos representativos de grupos cicloalquilo incluyen, pero sin limitación, ciclopropilo, ciclopentilo y ciclohexilo. Cuando los números aparecen en un subíndice después del símbolo "C", el subíndice defina con más especificidad el número de átomos de carbono que puede contener un grupo cicloalquilo en particular. Por ejemplo, "cicloalquilo de C3-C6" denota grupos cicloalquilo con tres a seis átomos de carbono.
El término "alcoxi", como se usa en el presente documento, se refiere a un grupo alquilo unido al resto molecular de origen a través de un átomo de oxígeno, por ejemplo, grupo metoxi (OCH3). Por ejemplo, "alcoxi de C1-3" denota grupos alcoxi con uno a tres átomos de carbono.
El término "alcoxialquilo", como se usa en el presente documento, se refiere a un grupo alcoxi unido a través de su átomo de oxígeno a un grupo alquilo, que está unido al resto molecular original, por ejemplo, grupo metoximetilo (CH2OCH3). Por ejemplo, "alcoxialquilo de C2-4" denota grupos alcoxialquilo con dos a cuatro átomos de carbono, tales como -CH2OCH3, -CH2CH2OCH3, -CH2OCH2CH3 y -CH2CH2OCH2CH3.
La frase "farmacéuticamente aceptable" se emplea en el presente documento para referirse a aquellos compuestos, materiales, composiciones y/o formas de dosificación que, dentro del alcance del buen juicio médico, son adecuados para su uso en contacto con los tejidos de seres humanos y animales sin excesivo toxicidad, irritación, respuesta alérgica u otro problema o complicación, proporcional a una relación beneficio/riesgo razonable.
Los compuestos de la Fórmula (I) se pueden proporcionar como sólidos amorfos o sólidos cristalinos. La liofilización se puede emplear para proporcionar los compuestos de la Fórmula (I) como sólidos amorfos.
Debe entenderse además que los solvatos (por ejemplo, hidratos) de los compuestos de la Fórmula (I) también están dentro del alcance de la presente invención. El término "solvato" significa una asociación física de un compuesto de la Fórmula (I) a una o más moléculas disolventes, ya sean orgánicas o inorgánicas. Esta asociación física incluye enlaces de hidrógeno. En ciertos casos, el solvato podrá aislarse, por ejemplo, cuando se incorporan una o más
moléculas de Solvente en la red cristalina del sólido cristalino. "Solvato" abarca tanto la fase de solución como los solvatos aislables. Los solvatos a modo de ejemplo incluyen hidratos, etanolatos, metanolatos, isopropanolatos, solvatos de acetonitrilo y solvatos de acetato de etilo. Los métodos de solvatación son conocidos en la técnica.
Además, los compuestos de la Fórmula (I), después de su preparación, pueden aislarse y purificarse para obtener una composición que contenga una cantidad en peso igual o superior al 99% de un compuesto de la Fórmula (I) ("sustancialmente puro"), que luego se usa o formula como se describe aquí. Tales compuestos "sustancialmente puros" de la Fórmula (I) también se contemplan aquí como parte de la presente invención.
"Compuesto estable" y "estructura estable" están destinados a indicar un compuesto que es suficientemente robusto para sobrevivir al aislamiento hasta un grado útil de pureza a partir de una mezcla de reacción y formulación en un agente terapéutico eficaz. La presente invención está destinada a incorporar compuestos estables.
"Cantidad terapéuticamente eficaz" pretende incluir una cantidad de un compuesto de la presente invención solo o una cantidad de la combinación de compuestos reivindicados o una cantidad de un compuesto de la presente invención en combinación con otros ingredientes activos efectivos para actuar como un inhibidor de TLR7/8/9, o eficaz para tratar o prevenir estados de enfermedades autoinmunes y/o inflamatorias, como LES, EII, esclerosis múltiple (EM) y síndrome de Sjogren y artritis reumatoide.
Como se usa en el presente documento, "tratar" o "tratamiento" cubre el tratamiento de un estado de enfermedad en un mamífero, particularmente en un ser humano, e incluye: (a) evitar que el estado de enfermedad ocurra en un mamífero, en particular, cuando el mamífero esté predispuesto al estado de la enfermedad pero aún no se le ha diagnosticado que lo tenga; (b) inhibir el estado de enfermedad, es decir, detener su desarrollo; y/o (c) aliviar el estado de la enfermedad, es decir, provocar la regresión del estado de la enfermedad.
Los compuestos de la presente invención están destinados a incluir todos los isótopos de átomos que se encuentren en los presentes compuestos. Los isótopos incluyen aquellos átomos que tienen el mismo número atómico pero diferentes números de masa. A modo de ejemplo general y sin limitación, los isótopos de hidrógeno incluyen deuterio (D) y tritio (T). Los isótopos de carbono incluyen 13C y 14C. Los compuestos de la invención marcados isotópicamente pueden prepararse generalmente mediante técnicas convencionales conocidas por los expertos en la técnica o mediante procesos análogos a los descritos en este documento, usando un reactivo marcado isotópicamente apropiado en lugar del reactivo no marcado empleado de otro modo. Por ejemplo, metilo (-CH3) también incluye grupos metilo deuterados como -CD3.
Utilidad
El sistema inmune humano ha evolucionado para defender al cuerpo de microorganismos, virus y parásitos que pueden causar infección, enfermedad o muerte. Los mecanismos reguladores complejos aseguran que los diversos componentes celulares del sistema inmune se dirijan a las sustancias u organismos extraños, sin causar daños permanentes o significativos al individuo. Si bien los eventos iniciadores no se entienden bien en este momento, en los estados de enfermedades autoinmunes, el sistema inmunitario dirige su respuesta inflamatoria a los órganos diana en el individuo afectado. Las diferentes enfermedades autoinmunes se caracterizan normalmente por el órgano o tejido objetivo predominante o inicial afectado; como la articulación en el caso de la artritis reumatoide, la glándula tiroides en el caso de la tiroiditis de Hashimoto, el sistema nervioso central en el caso de la esclerosis múltiple, el páncreas en el caso de la diabetes tipo I y el intestino en el caso de la inflamación enfermedad gastrointestinal.
Los compuestos de la invención inhiben la señalización a través del receptor 7, u 8, o 9 tipo Toll (TLR7, TLR8, TLR9) o combinaciones de los mismos. En consecuencia, los compuestos de la Fórmula (I) tienen utilidad en el tratamiento de afecciones asociadas a la inhibición de la señalización a través de uno o más de TLR7, TLR8 o TLR9. Las afecciones incluyen enfermedades asociadas al receptor de TLR7, TLR8 o TLR9 en las que los niveles de citocinas se modulan como consecuencia de la señalización intracelular.
Como se usa en el presente documento, los términos "tratar" o "tratamiento" abarcan el tratamiento de un estado de enfermedad en un mamífero, particularmente en un ser humano, e incluyen: (a) prevenir o retrasar la aparición del estado de enfermedad en un mamífero, en particular, cuando el mamífero esté predispuesto al estado de la enfermedad pero aún no se le haya diagnosticado que lo tenga; (b) inhibir el estado de la enfermedad, es decir, detener su desarrollo; y/o (c) lograr una reducción total o parcial de los síntomas o el estado de la enfermedad, y/o aliviar, mejorar, disminuir o curar la enfermedad o trastorno y/o sus síntomas.
En vista de su actividad como inhibidores selectivos de TLR7, TLR8 o TLR9, los compuestos de la Fórmula (I) son útiles en el tratamiento de enfermedades asociadas a los receptores de la familia TLR7, TLR8 o TLR9, pero no se limitan a enfermedades inflamatorias como la enfermedad de Crohn, ulcerosa colitis, asma, enfermedad de injerto contra hospedero, rechazo de aloinjerto, enfermedad pulmonar obstructiva crónica; enfermedades autoinmunes tales como la enfermedad de Graves, artritis reumatoide, lupus eritematoso sistémico, nefritis lúpica, lupus cutáneo, psoriasis; enfermedades autoinflamatorias, incluidos los síndromes periódicos asociados a la criopirina (CAPS), el síndrome periódico asociado al receptor de TNF (TRAPS), la fiebre mediterránea familiar (FMF), las fijaciones en
adultos, la artritis idiopática juvenil de inicio sistémico, la gota y la artritis gotosa; enfermedades metabólicas que incluyen diabetes tipo 2, aterosclerosis, infarto de miocardio; trastornos óseos destructivos tales como enfermedad de resorción ósea, osteoartritis, osteoporosis, trastorno óseo relacionado con mieloma múltiple; trastornos proliferativos tales como leucemia mielógena aguda, leucemia mielógena crónica; trastornos angiogénicos tales como trastornos angiogénicos que incluyen tumores sólidos, neovascularización ocular y hemangiomas infantiles; enfermedades infecciosas como sepsis, shock séptico y shigelosis; enfermedades neurodegenerativas como la enfermedad de Alzheimer, la enfermedad de Parkinson, isquemias cerebrales o enfermedades neurodegenerativas causadas por lesiones traumáticas, enfermedades oncológicas y virales como melanoma metastásico, sarcoma de Kaposi, mieloma múltiple e infección por VIH y retinitis por CMV, SIDA, respectivamente.
Más particularmente, las afecciones o enfermedades específicas que pueden tratarse con los compuestos de la invención incluyen, sin limitación, pancreatitis (aguda o crónica), asma, alergias, síndrome de dificultad respiratoria del adulto, enfermedad pulmonar obstructiva crónica, glomerulonefritis, artritis reumatoide, lupus eritematoso sistémico, esclerodermia, tiroiditis crónica, enfermedad de Graves, gastritis autoinmune, diabetes, anemia hemolítica autoinmune, neutropenia autoinmune, trombocitopenia, dermatitis atópica, hepatitis crónica activa, miastenia grave, esclerosis múltiple, enfermedad inflamatoria intestinal, colitis ulcerosa, enfermedad de Crohn, psoriasis, enfermedad de injerto vs hospedero, reacción inflamatoria inducida por endotoxina, tuberculosis, aterosclerosis, degeneración muscular, caquexia, artritis psoriásica, síndrome de Reiter, gota, artritis traumática, artritis de rubéola, sinovitis aguda, enfermedad de células p pancreáticas; enfermedades caracterizadas por infiltración masiva de neutrófilos; espondilitis reumatoide, artritis gotosa y otras afecciones artríticas, malaria cerebral, enfermedad inflamatoria pulmonar crónica, silicosis, sarcoidosis pulmonar, enfermedad de resorción ósea, rechazo de aloinjertos, fiebre y mialgias debido a infección, caquexia secundaria a infección, formación de queloides, formación de tejido cicatricial, ulcerativo colitis, pirosis, gripe, osteoporosis, osteoartritis, leucemia mielógena aguda, leucemia mielógena crónica, melanoma metastásico, sarcoma de Kaposi, mieloma múltiple, sepsis, shock séptico y shigelosis; enfermedad de Alzheimer, enfermedad de Parkinson, isquemias cerebrales o enfermedad neurodegenerativa causada por una lesión traumática; trastornos angiogénicos que incluyen tumores sólidos, neovascularización ocular y hemangiomas infantiles; enfermedades virales, incluyendo infección aguda por hepatitis (incluyendo hepatitis A, hepatitis B y hepatitis C), infección por VIH y retinitis por CMV, SIDA, ARC o neoplasia maligna y herpes; accidente cerebrovascular, isquemia miocárdica, isquemia en ataques cardíacos por accidente cerebrovascular, hipoxia orgánica, hiperplasia vascular, lesión por reperfusión cardíaca y renal, trombosis, hipertrofia cardíaca, agregación plaquetaria inducida por trombina, endotoxemia y/o síndrome de shock tóxico, afecciones asociadas a prostaglandina endoperoxidasa sindasa-2 y pénfigo vulgar. En esta invención se incluyen modalidades en las que la afección se selecciona entre lupus, incluyendo nefritis lúpica y lupus eritematoso sistémico (LES), enfermedad de Crohn, colitis ulcerosa, rechazo de aloinjerto, artritis reumatoide, psoriasis, espondilitis anquilosante, artritis psoriásica y pénfigo vulgar. También se incluyen modalidades en las que la afección se selecciona entre lesión por reperfusión de isquemia, incluida la lesión por reperfusión de isquemia cerebral derivada de accidente cerebrovascular y lesión por reperfusión de isquemia cardíaca derivada de infarto de miocardio. Otra modalidad es uno en el que la condición es mieloma múltiple.
En una modalidad, los compuestos de la Fórmula (I) son útiles en el tratamiento del cáncer, incluida la macroglobulinemia de Waldenstrom (WM), el linfoma difuso de células B grandes (DLBCL), la leucemia linfocítica crónica (CLL), el linfoma cutáneo difuso de células B grandes y el linfoma primario del SNC.
Además, los inhibidores de TLR7, TLR8 o TLR9 de la presente invención inhiben la expresión de proteínas proinflamatorias inducibles como la prostaglandina endoperóxido sintasa-2 (PGHS-2), también denominada ciclooxigenasa-2 (COX-2), IL-1, IL-6, IL-18, quimiocinas. En consecuencia, las condiciones adicionales asociadas a TLR7/8/9 incluyen edema, analgesia, fiebre y dolor, como dolor neuromuscular, dolor de cabeza, dolor causado por cáncer, dolor dental y dolor de artritis. Los compuestos de la invención también pueden usarse para tratar infecciones virales veterinarias, tales como infecciones por lentivirus, que incluyen, pero no se limitan a, virus de anemia infecciosa equina; o infecciones por retrovirus, que incluyen virus de inmunodeficiencia felina, virus de inmunodeficiencia bovina y virus de inmunodeficiencia canina.
Por lo tanto, la presente invención proporciona al menos un compuesto de Fórmula (I) o una sal del mismo para su uso en el tratamiento de tales afecciones, en un sujeto que lo necesita. "Cantidad terapéuticamente efectiva o eficaz" pretende incluir una cantidad de un compuesto de la presente invención que es efectiva cuando se administra sola o en combinación para inhibir la enfermedad autoinmune o la enfermedad inflamatoria crónica.
Las modalidades para tratar afecciones asociadas a TLR7, TLR8 o TLR9 pueden comprender administrar compuestos de la Fórmula (I) solos o en combinación entre sí y/u otros agentes terapéuticos adecuados útiles en el tratamiento de tales afecciones. En consecuencia, "cantidad terapéuticamente efectiva o eficaz" también pretende incluir una cantidad de la combinación de compuestos reivindicados que es efectiva para inhibir TLR7, TLR8 o TLR9 y/o tratar enfermedades asociadas a TLR7, TLR8 o TLR9.
Ejemplos de tales otros agentes terapéuticos incluyen corticosteroides, rolipram, calfostina, fármacos antiinflamatorios supresores de citocinas (CSAIDs), interleucina-10, glucocorticoides, salicilatos, óxido nítrico y otros inmunosupresores; inhibidores de la translocación nuclear, como la desoxiespergualina (DSG); medicamentos antiinflamatorios no esteroideos (AINEs) tales como ibuprofeno, celecoxib y rofecoxib; esteroides tales como
prednisona o dexametasona; agentes antivirales tales como abacavir; agentes antiproliferativos tales como metotrexato, leflunomida, FK506 (tacrolimus, PROGRAF®); antipalúdicos tales como hidroxicloroquina; fármacos citotóxicos como azatiprina y ciclofosfamida; Inhibidores de TNF-a tales como tenidap, anticuerpos anti-TNF o receptor soluble de TNF y rapamicina (sirolimus o RAPAMUNE®) o derivados de los mismos.
Los otros agentes terapéuticos anteriores, cuando se emplean en combinación con los compuestos de la presente invención, se pueden usar, por ejemplo, en las cantidades indicadas en la Physician’s Desk Reference (PDR) o según lo determine un experto en la materia. En las modalidades de la presente invención, los otros agentes terapéuticos se pueden administrar antes, simultáneamente o después de la administración de los compuestos de la invención. La presente invención también proporciona composiciones farmacéuticas capaces de tratar afecciones asociadas al receptor de TLR7/8/9, incluyendo enfermedades mediadas por el receptor de la familia IL-1 como las descritas anteriormente.
Las composiciones de la invención pueden contener otros agentes terapéuticos como los descritos anteriormente y pueden formularse, por ejemplo, empleando vehículos o diluyentes sólidos o líquidos convencionales, así como aditivos farmacéuticos de un tipo apropiado para el modo de administración deseado (por ejemplo, excipientes, aglutinantes, conservadores, estabilizantes, sabores, etc.) de acuerdo con técnicas tales como las bien conocidas en la técnica de formulación farmacéutica.
En consecuencia, la presente invención incluye además composiciones que comprenden uno o más compuestos de la Fórmula (I) y un portador farmacéuticamente aceptable.
Un "portador farmacéuticamente aceptable" se refiere a medios generalmente aceptados en la técnica para el suministro de agentes biológicamente activos a animales, en particular, mamíferos. Los portadores farmacéuticamente aceptables se formulan de acuerdo con una serie de factores que están dentro del alcance de los expertos en la materia. Estos incluyen, entre otros, el tipo y la naturaleza del agente activo que se está formulando; el sujeto al que se administrará la composición que contiene el agente; la ruta prevista de administración de la composición; y, la indicación terapéutica dirigida. Los portadores farmacéuticamente aceptables incluyen medios líquidos tanto acuosos como no acuosos, así como varias formas de dosificación sólidas y semisólidas. los portadores pueden incluir una cantidad de ingredientes y aditivos diferentes además del agente activo, tales ingredientes adicionales se incluyen en la formulación por varias razones, por ejemplo, estabilización del agente activo, aglutinantes, etc., bien conocidos por aquellos de habilidad ordinaria en el arte. Las descripciones de portadores farmacéuticamente aceptables adecuados y los factores que intervienen en su selección se encuentran en varias fuentes fácilmente disponibles, como, por ejemplo, Remington's Pharmaceutical Sciences, 17a edición (1985), que se incorpora aquí como referencia en su totalidad.
Los compuestos de acuerdo con la Fórmula (I) pueden administrarse por cualquier medio adecuado para la afección a tratar, que puede depender de la necesidad de un tratamiento específico del sitio o la cantidad de compuesto de la Fórmula (I) a administrar.
También se incluye dentro de esta invención una clase de composiciones farmacéuticas que comprenden un compuesto de la Fórmula (I) y uno o más portadores y/o diluyentes y/o adyuvantes no tóxicos, farmacéuticamente aceptables (denominados colectivamente en este documento como materiales "portadores") y, si se desea, otros ingredientes activos. Los compuestos de la Fórmula (I) pueden administrarse por cualquier ruta adecuada, preferiblemente en forma de una composición farmacéutica adaptada a la ruta, y en una dosis eficaz para el tratamiento pretendido. Los compuestos y composiciones de la presente invención pueden, por ejemplo, administrarse por vía oral, mucosa o parenteral, incluyendo intravascularmente, intravenosamente, intraperitonealmente, subcutáneamente, intramuscularmente e intraesternalmente en formulaciones de unidades de dosificación que contengan portadores, adyuvantes y vehículos farmacéuticamente aceptables convencionales. Por ejemplo, el portador farmacéutico puede contener una mezcla de manitol o lactosa y celulosa microcristalina. La mezcla puede contener componentes adicionales tales como un agente lubricante, por ejemplo, estearato de magnesio y un agente desintegrante tal como crospovidona. La mezcla portadora puede llenarse en una cápsula de gelatina o comprimirse como una tableta. La composición farmacéutica puede administrarse como una forma de dosificación oral o una infusión, por ejemplo.
Para la administración oral, la composición farmacéutica puede estar en forma de, por ejemplo, una tableta, cápsula, cápsula líquida, suspensión o líquido. La composición farmacéutica se prepara preferiblemente en forma de una unidad de dosificación que contiene una cantidad particular del ingrediente activo. Por ejemplo, la composición farmacéutica puede proporcionarse como una tableta o cápsula que comprende una cantidad de ingrediente activo en el intervalo de aproximadamente 0,1 a 1000 mg, preferiblemente de aproximadamente 0,25 a 250 mg, y más preferiblemente de aproximadamente 0,5 a 100 mg. Una dosis diaria adecuada para un humano u otro mamífero puede variar ampliamente dependiendo de la condición del paciente y otros factores, pero puede determinarse usando métodos de rutina.
Cualquier composición farmacéutica contemplada en el presente documento puede, por ejemplo, administrarse por vía oral a través de cualquier preparación oral aceptable y adecuada. Las preparaciones orales a modo de ejemplo incluyen, pero no se limitan a, por ejemplo, tabletas, grageas, pastillas, suspensiones acuosas y aceitosas, polvos o
gránulos dispersables, emulsiones, cápsulas duras y blandas, cápsulas líquidas, jarabes y elixires. Las composiciones farmacéuticas destinadas a la administración oral se pueden preparar de acuerdo con cualquier método conocido en la técnica para fabricar composiciones farmacéuticas destinadas a la administración oral. Para proporcionar preparaciones farmacéuticamente sabrosas, una composición farmacéutica de acuerdo con la invención puede contener al menos un agente seleccionado de agentes edulcorantes, agentes saborizantes, agentes colorantes, demulcentes, antioxidantes y agentes conservadores.
Una tableta puede, por ejemplo, prepararse mezclando al menos un compuesto de la Fórmula (I) con al menos un excipiente no tóxico farmacéuticamente aceptable adecuado para la fabricación de tabletas. Los excipientes a modo de ejemplo incluyen, pero no se limitan a, por ejemplo, diluyentes inertes, tales como, por ejemplo, carbonato de calcio, carbonato de sodio, lactosa, fosfato de calcio y fosfato de sodio; agentes de granulación y desintegración, tales como, por ejemplo, celulosa microcristalina, croscarmelosa de sodio, almidón de maíz y ácido algínico; agentes aglutinantes, tales como, por ejemplo, almidón, gelatina, polivinilpirrolidona y acacia; y agentes lubricantes, tales como, por ejemplo, estearato de magnesio, ácido esteárico y talco. Además, una tableta puede no estar recubierta o recubierta por técnicas conocidas para enmascarar el mal sabor de un fármaco de sabor desagradable o retrasar la desintegración y absorción del ingrediente activo en el tracto gastrointestinal, manteniendo así los efectos del ingrediente activo durante un período más largo. Ejemplos de materiales de enmascaramiento del sabor solubles en agua incluyen, pero no se limitan a, hidroxipropilmetilcelulosa e hidroxipropilcelulosa. Ejemplos de materiales de retardo de tiempo incluyen, pero sin limitación, etilcelulosa y butirato de acetato de celulosa.
Las cápsulas de gelatina dura se pueden preparar, por ejemplo, mezclando al menos un compuesto de la Fórmula (I) con al menos un diluyente sólido inerte, tal como, por ejemplo, carbonato de calcio; fosfato de calcio; y caolín.
Las cápsulas de gelatina blanda se pueden preparar, por ejemplo, mezclando al menos un compuesto de la Fórmula (I) con al menos un portador soluble en agua, tal como, por ejemplo, polietilenglicol; y al menos un medio oleoso, tal como, por ejemplo, aceite de maní, parafina líquida y aceite de oliva.
Se puede preparar una suspensión acuosa, por ejemplo, mezclando al menos un compuesto de la Fórmula (I) con al menos un excipiente adecuado para la fabricación de una suspensión acuosa. Los excipientes a modo de ejemplo adecuados para la fabricación de una suspensión acuosa incluyen, pero no se limitan a, por ejemplo, agentes de suspensión, tales como, por ejemplo, carboximetilcelulosa de sodio, metilcelulosa, hidroxipropilmetilcelulosa, alginato de sodio, ácido algínico, polivinilpirrolidona, goma de tragacanto y goma de acacia; agentes dispersantes o humectantes, tales como, por ejemplo, un fosfátido natural, por ejemplo, lecitina; productos de condensación de óxido de alquileno con ácidos grasos, tales como, por ejemplo, estearato de polioxietileno; productos de condensación de óxido de etileno con alcoholes alifáticos de cadena larga, tales como, por ejemplo, heptadecaetileno-oxicetanol; productos de condensación de óxido de etileno con ésteres parciales derivados de ácidos grasos y hexitol, tales como, por ejemplo, monooleato de polioxietilen sorbitol; y productos de condensación de óxido de etileno con ésteres parciales derivados de ácidos grasos y anhídridos de hexitol, tales como, por ejemplo, monooleato de polietilen sorbitano. Una suspensión acuosa también puede contener al menos un conservador, tal como, por ejemplo, phidroxibenzoato de etilo y n-propilo; al menos un agente colorante; al menos un agente aromatizante; y/o al menos un agente edulcorante, que incluye pero no se limita a, por ejemplo, sacarosa, sacarina y aspartame.
Las suspensiones oleosas pueden, por ejemplo, prepararse suspendiendo al menos un compuesto de la Fórmula (I) en un aceite vegetal, tal como, por ejemplo, aceite de araquís; aceite de oliva; aceite de ajonjolí; y aceite de coco; o en aceite mineral, como, por ejemplo, parafina líquida. Una suspensión oleosa también puede contener al menos un agente espesante, como, por ejemplo, cera de abejas; parafina dura y alcohol cetílico. Para proporcionar una suspensión aceitosa agradable al paladar, se puede agregar al menos uno de los agentes edulcorantes ya descritos anteriormente, y/o al menos un agente saborizante a la suspensión aceitosa. Una suspensión aceitosa puede contener además al menos un conservador, que incluye, pero no se limita a, por ejemplo, un antioxidante, tal como, por ejemplo, hidroxianisol butilado y alfa-tocoferol.
Los polvos y gránulos dispersables se pueden preparar, por ejemplo, mezclando al menos un compuesto de la Fórmula (I) con al menos un agente dispersante y/o humectante; al menos un agente de suspensión; y/o al menos un conservador. Los agentes dispersantes, agentes humectantes y agentes de suspensión adecuados son como ya se han descrito anteriormente. Los conservadores a modo de ejemplo incluyen, pero no se limitan a, por ejemplo, antioxidantes, por ejemplo, ácido ascórbico. Además, los polvos y gránulos dispersables también pueden contener al menos un excipiente, que incluye, pero no se limita a, por ejemplo, agentes edulcorantes; agentes saborizantes; y agentes colorantes.
Una emulsión de al menos un compuesto de la Fórmula (I) del mismo puede, por ejemplo, prepararse como una emulsión de aceite en agua. La fase oleosa de las emulsiones que comprenden compuestos de la Fórmula (I) puede estar constituida por ingredientes conocidos de una manera conocida. La fase oleosa puede proporcionarse, pero no se limita a, por ejemplo, un aceite vegetal, tal como, por ejemplo, aceite de oliva y aceite de araquís; un aceite mineral, tal como, por ejemplo, parafina líquida; y mezclas de los mismos. Si bien la fase puede comprender simplemente un emulsionante, puede comprender una mezcla de al menos un emulsionante con una grasa o un aceite o con una grasa y un aceite. Los agentes emulsionantes adecuados incluyen, pero no se limitan a, por ejemplo, fosfátidos naturales,
por ejemplo, lecitina de soja; ésteres o ésteres parciales derivados de ácidos grasos y anhídridos de hexitol, tales como, por ejemplo, monooleato de sorbitán; y productos de condensación de ésteres parciales con óxido de etileno, tales como, por ejemplo, monooleato de polioxietilensorbitán. Preferiblemente, se incluye un emulsionante hidrofílico junto con un emulsionante lipofílico que actúa como estabilizador. También se prefiere incluir tanto un aceite como una grasa. Juntos, el (los) emulsionante (s) con o sin estabilizador (es) forman la denominada cera emulsionante, y la cera junto con el aceite y la grasa forman la denominada base de ungüento emulsionante que forma la fase oleosa dispersa de la formulaciones de crema. Una emulsión también puede contener un agente edulcorante, un agente aromatizante, un conservador y/o un antioxidante. Los emulsionantes y estabilizadores de emulsión adecuados para usar en la formulación de la presente invención incluyen Tween 60, Span 80, alcohol cetoestearílico, alcohol miristílico, monoestearato de glicerilo, laurilsulfato de sodio, diestearato de glicerilo solo o con cera u otros materiales bien conocidos en la técnica.
Los compuestos de la Fórmula (I) pueden, por ejemplo, también administrarse por vía intravenosa, subcutánea y/o intramuscular a través de cualquier forma inyectable farmacéuticamente aceptable y adecuada. Las formas inyectables a modo de ejemplo incluyen, pero no se limitan a, por ejemplo, soluciones acuosas estériles que comprenden portadores y disolventes aceptables, tales como, por ejemplo, agua, solución de Ringer y solución isotónica de cloruro de sodio; microemulsiones estériles de aceite en agua; y suspensiones acuosas u oleaginosas.
Las formulaciones para administración parenteral pueden estar en forma de soluciones o suspensiones de inyección estériles isotónicas acuosas o no acuosas. Estas soluciones y suspensiones pueden prepararse a partir de polvos o gránulos estériles usando uno o más de los portadores o diluyentes mencionados para usar en las formulaciones para administración oral o usando otros agentes dispersantes o humectantes y agentes de suspensión adecuados. Los compuestos se pueden disolver en agua, polietilenglicol, propilenglicol, etanol, aceite de maíz, aceite de semilla de algodón, aceite de cacahuate, aceite de ajonjolí, alcohol bencílico, solución de cloruro de sodio, goma de tragacanto y/o varios amortiguadores. Otros adyuvantes y modos de administración son bien conocidos en la técnica farmacéutica. El ingrediente activo también se puede administrar mediante inyección como una composición con portadores adecuados que incluyen solución salina, dextrosa o agua, o con ciclodextrina (es decir, Captisol), solubilización codisolvente (es decir, propilenglicol) o solubilización micelar (es decir, Tween 80).
La preparación inyectable estéril también puede ser una solución o suspensión inyectable estéril en un diluyente o disolvente parenteralmente aceptable no tóxico, por ejemplo, como una solución en 1,3-butanodiol. Entre los vehículos y disolventes aceptables que pueden emplearse están el agua, la solución de Ringer y la solución isotónica de cloruro de sodio. Además, los aceites fijos estériles se emplean convencionalmente como disolvente o medio de suspensión. Para este propósito, se puede emplear cualquier aceite fijo suave, incluyendo mono o diglicéridos sintéticos. Además, los ácidos grasos como el ácido oleico encuentran uso en la preparación de inyectables.
Una microemulsión de aceite en agua inyectable estéril puede, por ejemplo, prepararse 1) disolviendo al menos un compuesto de la Fórmula (I) en una fase oleosa, tal como, por ejemplo, una mezcla de aceite de soja y lecitina; 2) combinar la Fórmula (I) que contiene la fase oleosa con una mezcla de agua y glicerol; y 3) procesar la combinación para formar una microemulsión.
Se puede preparar una suspensión acuosa u oleaginosa estéril de acuerdo con métodos ya conocidos en la técnica. Por ejemplo, se puede preparar una solución o suspensión acuosa estéril con un diluyente o disolvente parenteralmente aceptable no tóxico, tal como, por ejemplo, 1,3-butanodiol; y una suspensión oleaginosa estéril se puede preparar con un disolvente o medio de suspensión aceptable no tóxico estéril, tal como, por ejemplo, aceites fijos estériles, por ejemplo, mono o diglicéridos sintéticos; y ácidos grasos, tales como, por ejemplo, ácido oleico.
Los portadores, adyuvantes y vehículos farmacéuticamente aceptables que pueden usarse en las composiciones farmacéuticas de esta invención incluyen, pero no se limitan a, intercambiadores de iones, alúmina, estearato de aluminio, lecitina, sistemas de administración de fármacos autoemulsionantes (SEDDS) tales como succinato de dalfa-tocoferol polietilenglicol 1000, tensioactivos usados en formas de dosificación farmacéutica tales como Tweens, aceite de ricino polietoxilado como el tensioactivo CREMOPHOR (BASF) u otras matrices de suministro polimérico similares, proteínas séricas, como la albúmina de suero humano, sustancias amortiguadoras como los fosfatos, glicina, ácido sórbico, sorbato de potasio, mezclas parciales de glicéridos de ácidos grasos vegetales saturados, agua, sales o electrolitos, como sulfato de protamina, fosfato ácido disódico, fosfato ácido de potasio, cloruro de sodio, sales de zinc, sílice coloidal, trisilicato de magnesio, polivinilpirrolidona, sustancias a base de celulosa, polietilenglicol, carboximetilcelulosa de sodio, poliacrilatos, ceras, polímeros en bloque de polietileno-polioxipropileno, polietilenglicol y grasa de lana. Las ciclodextrinas tales como alfa, beta y gamma-ciclodextrina, o derivados químicamente modificados como las hidroxialquilciclodextrinas, incluidas las 2 y 3-hidroxipropil-ciclodextrinas, u otros derivados solubilizados también pueden usarse ventajosamente para mejorar la administración de los compuestos de las fórmulas descritas en la presente.
Los compuestos farmacéuticamente activos de esta invención pueden procesarse de acuerdo con métodos convencionales de farmacia para producir agentes medicinales para la administración a pacientes, incluidos humanos y otros mamíferos. Las composiciones farmacéuticas pueden someterse a operaciones farmacéuticas convencionales tales como esterilización y/o pueden contener adyuvantes convencionales, tales como conservadores, estabilizantes,
agentes humectantes, emulsionantes, amortiguadores, etc. Las tabletas y píldoras pueden prepararse adicionalmente con recubrimientos entéricos. Las composiciones también pueden comprender adyuvantes, tales como agentes humectantes, edulcorantes, saborizantes y perfumantes.
Las cantidades de compuestos que se administran y el régimen de dosificación para tratar una condición de enfermedad con los compuestos y/o composiciones de esta invención depende de varios factores, que incluyen la edad, el peso, el sexo, la condición médica del sujeto, el tipo de la enfermedad, la gravedad de la enfermedad, la ruta y la frecuencia de administración y el compuesto particular empleado. Por lo tanto, el régimen de dosificación puede variar ampliamente, pero puede determinarse rutinariamente usando métodos estándar. Puede ser apropiada una dosis diaria de aproximadamente 0,001 a 100 mg/kg de peso corporal, preferiblemente entre aproximadamente 0,0025 y aproximadamente 50 mg/kg de peso corporal y lo más preferiblemente entre aproximadamente 0,005 a 10 mg/kg de peso corporal. La dosis diaria se puede administrar en una a cuatro dosis por día. Otros programas de dosificación incluyen una dosis por semana y una dosis por ciclo de dos días.
Para fines terapéuticos, los compuestos activos de esta invención se combinan normalmente con uno o más adyuvantes apropiados para la ruta de administración indicada. Si se administran por vía oral, los compuestos pueden mezclarse con lactosa, sacarosa, almidón en polvo, ésteres de celulosa de ácidos alcanoicos, ésteres de alquilcelulosa, talco, ácido esteárico, estearato de magnesio, óxido de magnesio, sales de sodio y calcio de ácidos fosfórico y sulfúrico, gelatina, goma de acacia, alginato de sodio, polivinilpirrolidona y/o alcohol polivinílico, y luego en tabletas o encapsulados para una administración conveniente. Las cápsulas o tabletas pueden contener una formulación de liberación controlada que se puede proporcionar en una dispersión de compuesto activo en hidroxipropilmetilcelulosa.
Las composiciones farmacéuticas de esta invención comprenden al menos un compuesto de la Fórmula (I) y opcionalmente un agente adicional seleccionado de cualquier portador, adyuvante y vehículo farmacéuticamente aceptable. Las composiciones alternativas de esta invención comprenden un compuesto de la Fórmula (I) descrita en este documento, o un profármaco del mismo, y un portador, adyuvante o vehículo farmacéuticamente aceptable.
La presente invención también abarca un artículo de fabricación. Como se usa en este documento, el artículo de fabricación está destinado a incluir, entre otros, kits y paquetes. El artículo de fabricación de la presente invención comprende: (a) un primer recipiente; (b) una composición farmacéutica ubicada dentro del primer recipiente, en donde la composición comprende: un primer agente terapéutico, que comprende: un compuesto de la presente invención o una forma de sal farmacéuticamente aceptable del mismo; y (c) un prospecto que indica que la composición farmacéutica puede usarse para el tratamiento de un trastorno inflamatorio y/o una enfermedad autoinmune (como se definió anteriormente). En otra modalidad, el prospecto establece que la composición farmacéutica puede usarse en combinación (como se definió previamente) con un segundo agente terapéutico para tratar un trastorno inflamatorio y/o una enfermedad autoinmune. El artículo de fabricación puede comprender además: (d) un segundo contenedor, en donde los componentes (a) y (b) están ubicados dentro del segundo contenedor y el componente (c) está ubicado dentro o fuera del segundo contenedor. Ubicado dentro del primer y segundo contenedor significa que el contenedor respectivo contiene el artículo dentro de sus límites.
El primer recipiente es un receptáculo usado para contener una composición farmacéutica. Este contenedor puede ser para fabricación, almacenamiento, envío y/o venta individual/a granel. El primer contenedor está destinado a cubrir una botella, frasco, vial, matraz, jeringa, tubo (por ejemplo, para una preparación de crema) o cualquier otro contenedor usado para fabricar, mantener, almacenar o distribuir un producto farmacéutico.
El segundo contenedor es uno usado para contener el primer contenedor y, opcionalmente, el inserto del paquete. Ejemplos del segundo contenedor incluyen, entre otros, cajas (por ejemplo, cartón o plástico), cajas, cartones, bolsas (por ejemplo, bolsas de papel o plástico), bolsas y sacos. El inserto del paquete se puede unir físicamente al exterior del primer contenedor a través de cinta, pegamento, grapas u otro método de fijación, o puede descansar dentro del segundo contenedor sin ningún medio físico de fijación al primer contenedor. Como alternativa, el inserto del paquete se encuentra en el exterior del segundo contenedor. Cuando se encuentra en el exterior del segundo contenedor, es preferible que el inserto del paquete se adhiera físicamente mediante cinta, pegamento, grapas u otro método de fijación. Como alternativa, puede estar adyacente o tocar el exterior del segundo contenedor sin estar físicamente unido.
El prospecto es un indicador, etiqueta, marcador, etc. que menciona información relacionada con la composición farmacéutica ubicada dentro del primer recipiente. La información recitada generalmente será determinada por la agencia reguladora que gobierna el área en la que se venderá el artículo de fabricación (por ejemplo, la administración de alimentos y medicamentos de los Estados Unidos). En una modalidad, el prospecto enumera específicamente las indicaciones para las cuales se ha aprobado la composición farmacéutica. El inserto del paquete puede estar hecho de cualquier material en el que una persona pueda leer la información contenida en el mismo o en el mismo. Por ejemplo, el inserto del paquete es un material imprimible (por ejemplo, papel, plástico, cartón, papel de aluminio, papel con respaldo adhesivo o plástico, etc.) sobre el cual se ha formado la información deseada (por ejemplo, impresa o aplicada).
Métodos de preparación
Los compuestos de la presente invención se pueden preparar de varias maneras bien conocidas por un experto en la técnica de síntesis orgánica. Los compuestos de la presente invención se pueden sintetizar usando los métodos descritos a continuación, junto con métodos de síntesis conocidos en la técnica de la química orgánica sintética, o variaciones al respecto, tal como aprecian los expertos en la materia. Los métodos preferidos incluyen, pero no se limitan a, los descritos a continuación. Todas las referencias citadas en este documento se incorporan en su totalidad por referencia.
Los compuestos de esta invención pueden prepararse usando las reacciones y técnicas descritas en esta sección. Las reacciones se llevan a cabo en Solventes apropiados para los reactivos y materiales empleados y son adecuados para las transformaciones que se efectúan. Además, en la descripción de los métodos de síntesis descritos a continuación, debe entenderse que todas las condiciones de reacción propuestas, incluida la elección del Solvente, la atmósfera de reacción, la temperatura de reacción, la duración del experimento y los procedimientos de elaboración, se eligen como condiciones estándar para esa reacción, que debería ser fácilmente reconocida por un experto en la materia. Un experto en la técnica de la síntesis orgánica entiende que la funcionalidad presente en diversas porciones de la molécula debe ser compatible con los reactivos y las reacciones propuestas. Las restricciones a los sustituyentes que son compatibles con las condiciones de reacción serán fácilmente evidentes para un experto en la técnica y luego se deben usar métodos alternativos. Esto a veces requerirá un juicio para modificar el orden de los pasos de síntesis o seleccionar un esquema de proceso particular sobre otro para obtener un compuesto deseado de la invención. También se reconocerá que otra consideración importante en la planificación de cualquier ruta de síntesis en este campo es la elección juiciosa del grupo protector usado para la protección de los grupos funcionales reactivos presentes en los compuestos descritos en esta invención. Una descripción autorizada que detalla las muchas alternativas al profesional capacitado es Greene y Wuts (Protective Groups in Organic Synthesis, tercera edición, Wiley y Sons, 1999).
Ejemplos
Los siguientes ejemplos ilustran las modalidades particulares y preferidas de la presente invención y no limitan el alcance de la presente invención. Las abreviaturas y símbolos químicos, así como las abreviaturas y símbolos científicos tienen sus significados habituales y habituales, a menos que se especifique lo contrario. Las abreviaturas adicionales empleadas en los Ejemplos y en otras partes de esta solicitud se definen anteriormente. Los intermediarios comunes son generalmente útiles para la preparación de más de un Ejemplo y se identifican secuencialmente (por ejemplo, Intermediario 1, Intermediario 2, etc.) y se abrevian como Int. 1 o I1, Int. 2 o I2, etc. Los compuestos de los Ejemplos se identifican por el ejemplo y el paso en el que se prepararon (por ejemplo, "1-A" denota el Ejemplo 1, paso A), o por el ejemplo solo cuando el compuesto es el título compuesto del ejemplo (por ejemplo, "1" denota el compuesto del título del Ejemplo 1). En algunos casos se describen preparaciones alternativas de intermediarios o ejemplos. Con frecuencia, los químicos expertos en la técnica de la síntesis pueden idear preparaciones alternativas que pueden ser deseables con base en una o más consideraciones tales como un tiempo de reacción más corto, materiales de partida menos costosos, facilidad de operación o aislamiento, rendimiento mejorado, susceptible de catálisis, evitación de reactivos tóxicos, accesibilidad de instrumentación especializada y disminución del número de pasos lineales, etc. La intención de describir preparaciones alternativas es permitir aún más la preparación de los ejemplos de esta invención. En algunos casos, algunos grupos funcionales en los ejemplos y reivindicaciones resumidos pueden reemplazarse por reemplazos bioisostéricos bien conocidos que se conocen bien en la técnica, por ejemplo, el reemplazo de un grupo ácido carboxílico con un resto tetrazol o fosfato.
Abreviaturas
Ac acetilo
ACN acetonitrilo
AcOH ácido acético
anhid. anhidro
ac. acuoso
Bn bencilo
Bu butilo
Boc terc-butoxicarbonilo
CV volúmenes de columna
DCE dicloroetano
DCM diclorometano
DMAP dimetilaminopiridina
DMF dimetilformamida
DMSO sulfóxido de dimetilo
EDC clorhidrato de 1-(3-dimetilaminopropil)-3-etilcarbodiimida
EtOAc acetato de etilo
Et etilo
EtOH etanol
H o H2 hidrógeno
h, hr o hrs hora (s)
HCTU hexafluorofosfato de 0-(6-clorobenzotriazol-1-il)-W,W,W'W-tetrametiluronio
hex hexano
i iso
IPA alcohol isopropílico
HOAc ácido acético
HCl ácido clorhídrico
HPLC cromatografía líquida de alta presión
LC cromatografía líquida
M molar
mM milimolar
Me metilo
MeOH metanol
MHz megahercios
min. minuto(s)
mins minuto(s)
M+1(M+H)+
MS espectrometría de masas
n o N normal
NBS n-bromosuccinimida
nm nanómetro
nM nanomolar
NMP N-metilpirrolidina
Pd/C paladio sobre carbono
PdCl2(dppf)2 [1,1'- 6/s(difenilfosfino)ferroceno]-dicloropalladio (II)
Pd(PPha)4 tetraquis(trifenilfosfina)-paladio
Ph fenilo
PPha trifenilfosfina
Pr propilo
PSI libras por pulgada cuadrada
PyBOP hexafluorofosfato de bromotripirrolidinofosfonio
Tiempo de ret. Tiempo de retención
sat. saturado
SFC cromatografía de fluidos supercríticos
TEA trietilamina
TFA ácido trifluoroacético
THF tetrahidrofurano
Condiciones analíticas y preparativas de HPLC:
QC-ACN-AA-XB: Columna: Waters Acquity UPLC BEH C18, 2,1 x 50 mm, partículas de 1,7 pm; Fase móvil A: 5:95 de acetonitrilo:agua con acetato de amonio 10 mM; Fase móvil B: 95:5 de acetonitrilo:agua con acetato de amonio 10 mM; Temperatura: 50 °C; Gradiente: 0-100 % de B durante 3 minutos, luego una retención de 0,75 minutos al 100 % de B; Flujo: 1,0 ml/min; Detección: UV a 220 nm.
QC-ACN-TFA-XB: Columna: Waters Acquity UPLC BEH C18, 2,1 x 50 mm, partículas de 1,7 pm; Fase móvil A: 5:95 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Fase móvil B: 95:5 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Temperatura: 50 °C; Gradiente: 0-100 % de B durante 3 minutos, luego una retención de 0,75 minutos al 100 % de B; Flujo: 1,0 ml/min; Detección: UV a 220 nm.
Método A1: L3 Acquity: Columna: (CLEM) UPLC BEH C18, 2,1 x 50 mm, partículas de 1,7 pm; Fase móvil: (A) agua; (B) acetonitrilo; Amortiguador: 0,05 % de TFA; Intervalo de gradiente: 2 %-98 % B (0 a 1 min) 98 % B (a 1.5 min) 98 %-2 % B (a 1,6 min); Tiempo de gradiente: 1,6 min; Velocidad de flujo: 0,8 ml/min; Tiempo de análisis: 2,2 min; Detección: Detector 1: UV a 220 nm; Detector 2: EM (IEN+).
Método B1: L2 Aquity; Columna: (CLEM) UPLC BEH C18, 2,1 x 50 mm, partículas de 1,7 pm; Fase móvil: (A) agua; (B) acetonitrilo; Amortiguador: 0,05 % de TFA; Intervalo de gradiente: 2 %-98 % B (0 a 1 min), 98 %-2 % B (a 1.5 min); Tiempo de gradiente: 1,8 min; Velocidad de flujo: 0,8 ml/min; Tiempo de análisis: 2,2 min; Detección: Detector 1: UV a 220 nm; Detector 2: EM (IEN+).
Método C1 SCP: Columna: Waters Acquity UPLC BEH C18, 2,1 x 50 mm, partículas de 1,7 pm; Fase móvil A: 5:95 de acetonitrilo:agua con acetato de amonio 10 mM; Fase móvil B: 95:5 de acetonitrilo:agua con acetato de amonio 10 mM. Temperatura: 50 °C; Gradiente: 0-100 % de B durante 3 minutos, luego una retención de 0,75 minutos al 100 % de B; Flujo: 1,11 ml/min; Detección: UV a 220 nm.
Método D1 SCP: Columna: Waters Acquity UPLC BEH C18, 2,1 x 50 mm, partículas de 1,7 pm; Fase móvil A: 5:95 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Fase móvil B: 95:5 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Temperatura: 50 °C; Gradiente: 0-100 % de B durante 3 minutos, luego una retención de 0,75 minutos al 100 % de B; Flujo: 1,11 ml/min; Detección: UV a 220 nm.
Método D2 SCP: Columna: XBridge C18, 19 x 200 mm, partículas de 5 pm;
Fase móvil A: 5:95 de acetonitrilo:agua con acetato de amonio 10 mM; Fase móvil B: 95:5 de acetonitrilo:agua con acetato de amonio 10 mM; Gradiente: 10-50 % de B durante 20 minutos, luego una retención de 5 minutos al 100 % de B; Flujo: 20 ml/min. Detección: UV a 220 nm.
Método D3 SCP: Columna: XBridge C18, 19 x 200 mm, partículas de 5 pm; Fase móvil A: 5:95 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Fase móvil B: 95:5 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Gradiente: 6-46 % de B durante 20 minutos, luego una retención de 4 minutos al 100 % de B; Flujo: 20 ml/min. Detección: UV a 220 nm.
Método E1 iPAC: Columna: Waters Xbridge C18 4,6 x 50 mm 5 pm partículas; Fase móvil A: 5:95 de acetonitrilo:agua con acetato de amonio 10 mM; Fase móvil B: 95:5 de acetonitrilo:agua con acetato de amonio 10 mM. Temperatura: 50 °C; Gradiente: 0-100 % B durante 1 minuto; Flujo: 4 ml/min; Detección: UV a 220 nm.
Método F1 iPAC: Columna: Waters Acquity BEH C18 2,1x50 mm 1,7 pm partículas; Fase móvil A: 5:95 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Fase móvil B: 95:5 de acetonitrilo:agua con ácido trifluoroacético al 0,1 %; Temperatura: 50 °C; Gradiente: 0-100 % de B durante 2,20 minutos; Flujo: 0,800 ml/min; Detección: UV a 220 nm.
(A) : Columna-Ascentis Express C18 (50 x 2,1 mm-2,7 pm) Mphase A: 10 mM NH4COOH en agua: ACN (98:02); Fase B: NH4COOH 10 mM en agua: ACN (02:98), Gradiente: 0-100 % B durante 3 minutos, Flujo = 1 ml/min. (B) : Waters Acquity BEH C18 (2,1 x 50 mm) 1,7 micras; Amortiguador: acetato de amonio 5 mM pH 5 ajustado con HCOOH, Solvente A: Amortiguador: ACN (95: 5), Solvente B: Amortiguador: ACN (5:95), Método:% B: 0 min-5 %: 1,1 min - 95 %: 1,7 min-95 %, flujo: 0,8 ml/min.
(C) : Columna-Ascentis Express C18 (50 x 2,1 mm-2,7 pm) Fase móvil A: 0,1 % de HCOOH en agua; Fase móvil B: ACN. Temperatura: 50 °C; Gradiente: 0-100 % B durante 3 minutos; Velocidad de flujo: 1,0 ml/min. (D) : Kinetex XB-C18 (75 x 3 mm) 2,6 micras; Solvente A: formiato de amonio 10 mM en agua: acetonitrilo (98:02); Fase móvil B: formiato de amonio 10 mM en agua: acetonitrilo (02:98); Temperatura: 50 °C; Gradiente: 0-100 % B durante 3 minutos; Velocidad de flujo: 1,1 ml/min; Detección: UV a 220 nm.
(E) : Columna: Ascentis Express C18 (50 x 2,1) mm, 2,7 pm; Fase móvil A: 5:95 de acetonitrilo:agua con NH4OAc 10 mM; Fase móvil B: 95:5 de acetonitrilo:agua con 10 mM de NH4OAc; Temperatura: 50 °C; Gradiente: 0-100 % B durante 3 minutos; Flujo: 1,1 ml/min.
(F) : Columna: Ascentis Express C18 (50 x 2,1) mm, 2,7 pm; Fase móvil A: 5:95 acetonitrilo: agua con 0,1 % de TfA; Fase móvil B: 95:5 de acetonitrilo:agua con 0,1 % de TFA; Temperatura: 50 °C; Gradiente: 0-100 % B durante 3 minutos; Flujo: 1,1 ml/min.
(G) : Columna: Waters Acquity UPLC BEH C18 (2,1 x 50 mm), 1,7 micras; Solvente A = 100 % de agua con 0,05 % de TFA; Solvente B = acetonitrilo al 100 % con TFA al 0,05 %; gradiente = 2-98 % de B durante 1 minuto, luego una retención de 0,5 minutos a 98 % de B; Velocidad de flujo: 0,8 ml/min; Detección: UV a 220 nm.
(H) : Columna: Acentis Express C18 (50 x 2,1 mm) 1,7 pm, Acentis C8 NH4COOH 5 min. M, Fase móvil A: -10 mM de formato de amonio: ACN (98: 2), Fase móvil B: -10 mM de formato de amonio: ACN (2:98), gradiente: 20 %-100 % B (0-4 min); 100 % de B (4-4,6 min); Flujo: 1 ml/min.
(I) Columna: Sunfire C18 (4,6 x 150) mm, 3,5 pm; Fase móvil A: 5:95 de acetonitrilo:agua con 0,05 % de TFA; Fase móvil B: 95:5 de acetonitrilo:agua con 0,05 % de TFA; Temperatura: 50 °C; Gradiente: 10-100 % de B durante 12 minutos; Flujo: 1 ml/min.
(J) Columna: Sunfire C18 (4,6 x 150) mm, 3,5 pm; Fase móvil A: 5:95 de acetonitrilo:agua con 0,05 % de TFA; Fase móvil B: 95:5 de acetonitrilo:agua con 0,05 % de TFA.
(K) Waters Acquity SDS, Fase móvil: A: agua B: ACN; 5 %-95 % de B en 1 min; Intervalo de gradiente: 50 %-98% B (0-0,5 min); 98% de B (0,5 min-1 min); 98 %-2 % de B (1-1,1 min); Tiempo de ejecución: 1,2 min; Velocidad de flujo: 0,7 ml/min; Tiempo de análisis: 1,7 min; Detección: Detector 1: UV a 220 nm; Detector 2: EM (ES+).
(L) Accuity UPLC BEH C18 (3,0 x 50 mm) 1,7 pm. Amortiguador: acetato de amonio 5 mM, Fase móvil A: Amortiguador: ACN (95: 5); Fase móvil B: Amortiguador: ACN (5:95) Método:% B: 0 min-20 %: 1,1 min -90 %: 1,7 min-90 %. Tiempo de ejecución: 2,25 min; Velocidad de flujo: 0,7 ml/min; Detección: Detector 1: UV a 220 nm; Detector 2: EM (ES+).
(M) : Kinetex SBC18 (4,6 x 50 mm) 5 micras; Solvente A: formiato de amonio 10 mM en agua: acetonitrilo (98:02); Fase móvil B: formiato de amonio 10 mM en agua: acetonitrilo (02:98); Temperatura: 50 °C; Gradiente: 30-100 % B (0-4 min), 100 % B (4-4,6 min), 100-30 % B (4,6-4,7 min), 30 % B (4,7-5,0 min); Velocidad de flujo: 1,5 ml/min; Detección: UV a 220 nm.
(N) : Columna-Ascentis Express C18 (50 x 2,1 mm-2,7 pm) Mphase A: NH4COOH 10 mM en agua: ACN (98:02); Mphase B: NH4COOH 10 mM en agua: ACN (02:98), Gradiente: 0-100% B (0-1,7 minutos); 100 % B (1,7-3,4 minutos). Flujo = 1 ml/min.
(O) Waters Acquity SDS Column BEH C18 (2,1 x 50 mm) 1,7 pm. Fase A: amortiguador en agua; fase móvil B: amortiguador en Ac N, gradiente: 20-98 % de B (0-1,25 minutos); 98 % de B (1,25-1,70 minutos); 98 % -2 % B (1,70-1,75 minutos); Flujo = 0,8 ml/min.
MODELO 1
5-bromo-3-isopropil-1H-indol
Un matraz de fondo redondo de 250 ml se cargó con trietilsilano (8,90 g, 77 mmol), ácido tricloroacético (6,25 g, 38,3 mmol) y tolueno (50 ml). La solución se calentó a 70 °C. Se añadió por goteo una solución de 5-bromo-1H-indol (5,0 g, 25,5 mmol) y acetona (2,247 ml, 30,6 mmol) en tolueno (30 ml) a través de un embudo de adición. La solución de color pardo resultante se calentó a 70 °C durante 1,5 h. La solución se enfrió a 10 °C. La reacción se interrumpió con la adición de bicarbonato de sodio al 10 %. La solución se diluyó con éter dietílico. La capa orgánica se separó, se secó y se concentró al vacío para proporcionar el compuesto en bruto. El material en bruto se purificó usando cromatografía sobre gel de sílice eluyendo con acetato de etilo al 5 % en hexanos para proporcionar 5-bromo-3-isopropil-1H-indol (5,5 g, 23,10 mmol, 95 % de rendimiento) en forma de un aceite. Tiempo de retención de LC 1,42 min [D]. EM m/z: 238,2 (M+H). RMN 1H (400 MHz, DMSO-da) 811,03-10,90 (m, 1H), 7,75-7,64 (m, 1H), 7,33-7,28 (m, 1H), 7,19-7,13 (m, 2H), 3,19-3,04 (m, 1H), 1,31-1,26 (m, 6H).
MODELO 2
5-bromo-2-yodo-3-isopropil-1H-indol
A una solución agitada de 5-bromo-3-isopropil-1H-indol (500 mg, 2,100 mmol) en THF (10 ml) se le añadió trifluorometanosulfonato de plata (647 mg, 2,52 mmol). La solución se agitó o 2 minutos. A continuación, se añadió I2 (533 mg, 2,100 mmol) en t Hf (10 ml) y la mezcla de reacción se agitó a temperatura ambiente durante 30 minutos. La reacción se interrumpió con la adición de solución acuosa de Na2S2O3. La solución se extrajo con EtOAc, se secó sobre sulfato de sodio y se concentró para obtener material en bruto. La masa en bruto se purificó por cromatografía en columna de gel de sílice para proporcionar 5-bromo-2-yodo-3-isopropil-1H-indol (500 mg, 1,374 mmol, 65,4 % de rendimiento). Tiempo de retención de CLEM 1,62 min [B]. Rm N 1H (400 MHz, DMSO-d6) 8 ppm 11,6 (s, 1H), 7,77 (s a 1H), 7,2-7,3 (m, 1H), 7,1-7,2 (m, 1H), 3,33 (s a, 3H), 2,50 (s a, 6H).
MODELO 3
5-bromo-3-isopropil-2-(2-metilpiridin-4-il)-1H-indol
A un vial de 14,78 ml (4 dram) con un tabique de alivio de presión se le añadieron ácido 5-bromo-2-yodo-3-isopropil-1H-indol (100 mg, 0,275 mmol), ácido (2-metilpiridin-4-il)borónico (37,6 mg, 0,275 mmol), aducto de PdCh(dppf)-CH2Cl2 (22,43 mg, 0,027 mmol) y THF (1 ml). El vial se evacuó y se purgó con N2 varias veces. A continuación, se añadió fosfato de potasio, tribásico (0,275 ml, 0,824 mmol). El vial se evacuó y purgó varias veces con N2 y se calentó a 65 °C. Después de 3 horas, la CLEM indicó que el material de partida estaba presente. La reacción continuó durante la noche a temperatura ambiente. La CLEM indicó que la reacción fue incompleta. Se añadieron ácido (2-metilpiridin-4-il)borónico (37,6 mg, 0,275 mmol) y aducto de PdCh(dppf)-CH2Cl2 (22,43 mg, 0,027 mmol) adicionales, y la mezcla de reacción se calentó a 90 °C. Después de 3 horas, c LEm indicó que la reacción se había completado. La mezcla de reacción se diluyó con agua y se extrajo con EtOAc (3x15 ml). Las fases orgánicas se combinaron, se secaron sobre sulfato de sodio, se filtraron y se concentraron para dar un aceite de color amarillo, que se purificó por cromatografía en gel de sílice sobre (Isco 12 g de sílice, 100 % de hexanos -100 % de EtOAc). Las fracciones similares se combinaron y concentraron para proporcionar 5-bromo-3-isopropil-2-(2-metilpiridin-4-il)-1H-indol (45 mg, 0,137 mmol, 49,8 % de rendimiento). Tiempo de retención de CLEM 0,83 min [b 1 ]. EM m/z: 329. 331 (M+H).
MODELO 4
3-bromo-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona
Intermediario T-4A: (3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)carbamato de ferc-butilo
A una solución de 5-bromo-3-isopropil-2-(2-metilpiridin-4-il)-1H-indol (0,5 g, 1,519 mmol) y carbamato de ferc-butilo (0,213 g, 1,822 mmol) en tolueno (15 ml) se le añadió ferc-butóxido de sodio (0,292 g, 3,04 mmol) a temperatura ambiente. La mezcla se desgasificó durante 10 minutos con nitrógeno, y se añadió Pd2(dba)3 (0,139 g, 0,152 mmol), seguido de la adición de 2-(di-ferc-butilfosfino)bifenilo (0,023 g, 0,076 mmol) y se desgasificó adicionalmente durante 5 min. La mezcla resultante se agitó a 90 °C durante 3 h. La mezcla de reacción se diluyó con acetato de etilo (100 ml), se lavó con agua (2 x 50 ml), salmuera (20 ml), se secó sobre sulfato de sodio y se concentró para obtener el producto en bruto. El material en bruto se purificó por cromatografía en columna usando una columna de sílice de 40 g, el compuesto se eluyó con metanol al 4 % en cloroformo, las fracciones se recolectaron, se concentraron para proporcionar (3-isopropil-2-(2-metilpiridin-4-il))-1H-indol-5-il)carbamato de ferc-butilo (0,3 g, 0,821 mmol, 54% de rendimiento) en forma de un sólido de color amarillo. Tiempo de retención de CLEM 3,55 min [D]. EM m/z: 366,2 (M+H).
Intermediario T-4B: 3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-amina
A una solución de (3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)carbamato de ferc-butilo (0,3 g, 0,821 mmol) en DCM (2 ml) se le añadió HCl 4 M en dioxano (1,231 ml, 4,93 mmol) a temperatura ambiente. La mezcla se agitó a la misma temperatura durante 3 h. La mezcla de reacción se concentró para proporcionar 3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-amina (0,21 g, 96 % de rendimiento) en forma de un sólido de color amarillo pálido. Tiempo de retención de CLEM 1,75 min [D]. EM m/z: 266,1 (M+H).
Intermediario T-4C: 2,4-dibromo-N-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)butanamida
A una solución de 3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-amina (0,21 g, 0,791 mmol) en DCM (5 ml) se le añadió cloruro de 2,4-dibromobutanoilo (0,105 ml, 0,791 mmol) a 0 °C por goteo. La mezcla de reacción se agitó a temperatura ambiente durante 4 h. La masa de reacción se diluyó con DCM (50 ml), se lavó con agua (50 ml), se secó sobre sulfato de sodio y se concentró para obtener el producto en bruto. El material en bruto se purificó por cromatografía en columna usando 24 g de columna de sílice. El producto se eluyó con MeOH al 4,5 % en cloroformo, las fracciones se recolectaron y se concentraron para proporcionar 2,4-dibromo-N-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)butanamida (0,28 g, 0,568 mmol, 72 % de rendimiento) en forma de un sólido de color amarillo. Tiempo de retención de CLEM 2,83 min [D]. EM m/z: 492,2 (M+2H).
Modelo 4:
A una solución de 2,4-dibromo-N-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)butanamida (0,28 g, 0,568 mmol) en DCM (10 ml) se le añadió por goteo NaOH acuoso (0,091 g, 2,271 mmol) (solución al 50 % en agua). La mezcla se agitó a temperatura ambiente durante 2 h. La reacción se interrumpió con agua con hielo (50 ml). La masa de reacción se extrajo con DCM (2 X 50 ml). La capa orgánica se secó sobre sulfato de sodio y se concentró para obtener el producto en bruto. El material en bruto se purificó por cromatografía en columna usando 24 g de columna de sílice. El producto se eluyó con acetato de etilo al 60-80 % en éter de petróleo, las fracciones se recolectaron y se concentraron para proporcionar 3-bromo-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (0,15 g, 0,364 mmol, 64 % de rendimiento) en forma de un sólido de color amarillo. Tiempo de retención de CLEM 2,38 min [D]. EM m/z: 412,2 (M+2H).
Los siguientes modelos se prepararon de acuerdo con los procedimientos generales descritos en los Modelos 1-4:
Tabla 1
EJEMPLOS 1 Y 2
1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)-3-((2-(metilamino)etil)amino)pirrolidin-2-ona (1) y 3-((2-aminoetil)(metil)amino)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (2)
A una solución de 3-bromo-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (0,1 g, 0,243 mmol) y K2CO3 (0,034 g, 0,243 mmol) en t Hf (1 ml) y agua (0,1 ml) se le añadió N1-metiletano-1,2-diamina (0,018 g, 0,243 mmol). La mezcla de reacción resultante se calentó a 90 °C durante 24 h. La masa de reacción se concentró al vacío para obtener el producto en bruto. La muestra en bruto se purificó por cromatografía quiral usando una columna: Chiralpak-IC (250 x 4,6 mm), volumen de inyección de 5 |jm: 10, 0,2 % de DEA en metanol como codisolvente. Las fracciones se recolectaron, se concentraron y se liofilizaron para proporcionar 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)-3-((2-(metilamino)etil)amino)pirrolidin-2-ona (7 mg, 7 % de rendimiento) y 3-((2-aminoetil)(metil)amino)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (7 mg, 7 % de rendimiento) como sólidos pálidos.
Ejemplo 1: tiempo de retención de CLEM 1,25 min [C1]. EM m/z: 406,2 (M+H). RMN 1H (400 MHz, DMSO-da) 8 ppm 11,83 (s, 1H), 8,94 (d, J = 5,6 Hz, 1H), 8,35 (d, J =1,7 Hz, 1H), 7,95-7,84 (m, 1H), 7,76-7,67 (m, 2H), 7,53 7,23 (m, 1H), 4,27-4,20 (m, 2H), 3,72-3,66 (m, 3H), 3,54 (d, J = 6,4 Hz, 3H), 2,96-2,90 (m, 6 H), 2,88-2,83 (m, 3H), 2,48 (d, J =10,3 Hz, 2H), 1,72 (dd, J = 7,1. 5,4 Hz, 6 H).
Ejemplo 2: tiempo de retención de CLEM 1,32 min [C1]. EM m/z: 406,2 (M+H). RMN 1H (400 MHz, DMSO-d6) 8 ppm 11,96 (s, 1H), 9,00 (d, J = 5,9 Hz, 1H), 8,33 (s, 1H), 8,23 (s a, 2H), 8,07 (s, 1H), 8,02 (d, J = 5,9 Hz, 1H), 7,78 7,69 (m, 2H), 7,58-7,30 (m, 1H), 4,19-4,13 (m, 3H), 3,71 (dt, J = 14,0. 7,1 Hz, 2H), 3,38 (s a, 4H), 3,02-2,97 (m, 3H), 2,93 (s a, 3H), 2,72-2,65 (m, 1H), 2,54-2,44 (m, 2H), 1,73 (dd, J =7,1. 2,7 Hz, 6H).
Los siguientes ejemplos se prepararon de acuerdo con el procedimiento general usado en la preparación de los ejemplos 1 y 2.
Tabla 2
EJEMPLOS 5 Y 6
1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(4-isopropilpiperazin-1-il)pirrolidin-2-ona (5-6)
Intermediario 5A: 4-(1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-2-oxopirrolidin-3-il)piperazin-1 -carboxilato de ferc-butilo
A una solución de 3-bromo-1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)pirrolidin-2-ona (0,15 g, 0,352 mmol) y K2CO3 (0,049 g, 0,352 mmol) en THF (3 ml) y agua (0,5 ml) se le añadió piperazin-1-carboxilato de ferc-butilo (0,066 g, 0,352 mmol). La mezcla de reacción resultante se calentó a 90 °C durante 24 h. La masa de reacción se inactivó con agua (20 ml) y se extrajo con acetato de etilo (3 X 10 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 4-(1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-2-oxopirrolidin-3-il)piperazin-1-carboxilato de ferc-butilo (0,14 g, 75 %) en forma de un sólido de color pardo. Tiempo de retención de CLEM 1,33 min [F], EM m/z: 532,2 (M+H).
Intermediario 5B: 1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(piperazin-1-il)pirrolidin-2-ona
A una solución de 4-(1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-2-oxopirrolidin-3-il)piperazin-1 -carboxilato de ferc-butilo (0,12 g, 0,226 mmol) en d Cm (2 ml) se le añadió HCl 4 M en dioxano (0,339 ml, 1,354 mmol) a temperatura ambiente. La mezcla se agitó a la misma temperatura durante 3 h. La mezcla de reacción se concentró para proporcionar 1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(piperazin-1-il)pirrolidin-2-ona (0,095 g, 97% de rendimiento) en forma de un sólido de color amarillo pálido. Tiempo de retención de CLEM 2,99 min [F]. EM m/z: 432,4 (M+H).
Ejemplos 5 y 6 :
A una solución de 1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(piperazin-1-il)pirrolidin-2-ona (0,095 g, 0,220 mmol) y acetona (0,048 ml, 0,660 mmol) en metanol (4 ml) se le añadió isopropóxido de titanio (IV) (0,077 ml, 0,264 mmol) por goteo. La solución de color amarillo claro resultante se agitó en nitrógeno a 25 °C durante 4 h. A continuación, se le añadió ciano borohidruro de sodio (0,014 g, 0,220 mmol) y la mezcla se agitó a temperatura ambiente durante 12 h. La masa de reacción se inactivó con agua (10 ml) y se extrajo con DCM (2 X 10 ml). La capa orgánica separada se secó sobre sulfato de sodio, se filtró y se concentró. La muestra en bruto se purificó por cromatografía quiral HPLC usando Columna: Luxcellulose-4 (250 X 4,6) mm, 5 p, volumen de inyección: 10, 0,2 % DEA en metanol como codisolvente para proporcionar 1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(4-isopropilpiperazin-1 -il)pirrolidin-2-ona (0,012 g, 12 %) (RT quiral: 5,72) en forma de un sólido de color amarillo pálido y 1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(4-isopropilpiperazin-1-il)pirrolidin-2-ona (0,011 g, 11 %)(RT quiral: 11,97) en forma de un sólido de color amarillo pálido.
Ejemplo 5: tiempo de retención de CLEM 1,62 min [E]. EM m/z: 474,4 (M+H). RT quiral: 5,72 min. RMN 1H (400 MHz, DMSO-d6) 8 ppm 11,18 (s, 1H), 7,95 (s., 1H), 7,34 (s, 2H), 7,16 (s, 2H), 3,78-3,52 (m, 2H), 3,50 (s, 3H), 2,87 (m, 3H), 2,66 (s, 2H), 2,59-2,53 (m, 6 ), 2,33 (s, 1H), 2,07 (s, 2H), 1,79 (m, 2H), 1,42-1,39 (m, 6 H), 0,97-0,95 (m, 6 H)
Ejemplo 6 : tiempo de retención de CLEM 1,62 min [E]. EM m/z: 474,4 (M+H). RT quiral: 11,97 min. RMN 1H (400M Hz, DMSO-d6) 8 ppm 11,18 (s, 1H), 7,95 (s., 1H), 7,34 (s, 2H), 7,16 (s, 2H), 3,78-3,52 (m, 2H), 3,50 (s, 3H), 2,87 (m, 3H), 2,66 (s, 2H), 2,59-2,53 (m, 6 ), 2,33 (s, 1H), 2,07 (s, 2H), 1,79 (m, 2H), 1,42-1,39 (m, 6 H), 0,97-0,95 (m, 6 H).
3-(2-(dimetilamino)etoxi)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona
Intermediario 7A: 3-hidroxi-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona
Una solución de 5-bromo-3-isopropil-2-(2-metilpiridin-4-il)-1H-indol (0,5 g, 1,519 mmol), 3-hidroxipirrolidin-2-ona (0,184 g, 1,822 mmol), carbonato de cesio (1,237 g, 3,80 mmol) y N,N'-dimetiletilendiamina (0,054 g, 0,607 mmol) en disolvente de dioxano (5 ml) se desgasificó y se calentó a 130 °C durante 18 h. La masa de reacción se diluyó con DCM (50 ml), se lavó con agua (50 ml), se secó sobre sulfato de sodio y se concentró para obtener el producto en bruto. El material en bruto se purificó por cromatografía en columna usando 24 g de columna de sílice. El compuesto se eluyó con MeOH al 4 % en cloroformo, las fracciones se recolectaron y se concentraron para proporcionar 3-hidroxi-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (0,4 g, 1,145 mmol, 75 % de rendimiento) en forma de un sólido de color pardo. Tiempo de retención de CLEM 1,58 min [D]. EM m/z: 350,2 (M+H).
Intermediario 7B: trifluorometansulfonato de 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)-2-oxopirrolidin-3-ilo
A una solución de 3-hidroxi-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (0,05 g, 0,143 mmol) en DCM (2 ml) se le añadió piridina (0,012 ml, 0,143 mmol) seguida de la adición de anhídrido tríflico (0,024 ml, 0,143 mmol) a 0 °C. La mezcla de reacción se agitó a 25 °C durante 2 h. La TLC mostró formación de manchas no polares y ausencia de material de partida. La masa de reacción se inactivó con agua (20 ml) y se extrajo con acetato de etilo (3 X 20 ml). La capa orgánica se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar trifluorometansulfonato de 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)-2-oxopirrolidin-3-ilo (0,04 g, 58%) en forma de un sólido de color amarillo.
Ejemplo 7:
Una solución de trifluorometansulfonato de 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)-2-oxopirrolidin-3-ilo (0,04 g, 0,083 mmol), 2-(dimetilamino)etanol (0,022 g, 0,249 mmol) y K2CO3 (0,011 g, 0,083 mmol) en acetonitrilo (2 ml) de disolvente se agitó a temperatura ambiente durante 12 h. La reacción se detuvo con agua (10 ml). La mezcla de reacción se extrajo con acetato de etilo (3 x 10 ml). La capa orgánica separada se secó sobre sulfato de sodio, se filtró y se concentró para obtener el producto en bruto. El material en bruto se purificó por CLEM de preparación con las siguientes condiciones: Waters Xbridge C18,19x150 mm, 5 pm; Columna de protección: Waters XBridge C18, 19x10 mm, 5 pm; Fase móvil A: 5:95 de metanol:agua con NH4OAc 10 mM; Fase móvil B: 95:5 de metanol:agua con 10 mM NH4OAc; Gradiente: 15-65 % de B durante 25 minutos, seguido de una retención de 10 minutos al 65 % de B y una retención de 5 minutos al 100 % de B; Flujo: 15 ml/min. Las fracciones se recolectaron, se concentraron y se liofilizaron para proporcionar 3-(2-(dimetilamino)etoxi)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (11,1 mg, 32 %) en forma de un sólido de color amarillo pálido. Tiempo de retención de CLEM 1,27 min [E]. EM m/z: 421,1 (M+H). RMN 1H (400 MHz, DMSO-da) 8 ppm 11,67 (s, 1H), 8,82 (d, J = 5,1 Hz, 1H), 8,28 (d, J =1,7 Hz, 1H), 7,67 (t, J = 8,4 Hz, 2H), 7,62-7,55 (m, 2H), 5,17 (t, J = 9,7 Hz, 1H), 4,25-4,13 (m, 4H), 4,05-4,00 (m, 3H), 3,55 (s, 4H), 2,82 (s, 4H), 1,84 (s, 2H), 1,70 (dd, J = 7,0, 4,3 Hz, 6H).
EJEMPLO 8
1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)imidazolidin-2-ona
El ejemplo 8 se preparó de acuerdo con el método general descrito en el intermediario 7A. Tiempo de retención de CLEM 1,50 min [E]. EM m/z: 335,3 (M+H).
EJEMPLO 9
(R)-N-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)pirrolidin-3-carboxamida
Intermediario 9A: 4-(5-bromo-3-isopropil-1H-indol-2-il)-1-tritil-1H-pirazolo[3,4-b]piridina:
Una solución de 5-bromo-2-yodo-3-isopropil-1H-indol (2,0 g, 5,49 mmol), K2CO3 (3,50 g, 16,48 mmol) y 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1-tritil-1H-pirazolo[3,4-b]piridina (2,68 g, 5,49 mmol) en THF (80 ml) y agua (10 ml) como mezcla de disolvente se desgasificó durante 5 min con nitrógeno. A continuación, se añadió aducto de PdCh(dppf)-CH2Cl2 (0,449 g, 0,549 mmol) y la mezcla de reacción resultante se agitó a 80 °C durante 6 h. La masa de reacción se diluyó con exceso de acetato de etilo, se lavó con agua, salmuera, se secó sobre sulfato de sodio y se concentró para obtener el producto en bruto. El material en bruto se purificó por cromatografía en columna usando 40 g de columna de sílice, el compuesto se eluyó con acetato de etilo al 80 % en éter de petróleo, las fracciones se recolectaron y se concentraron para proporcionar 4-(5-bromo-3-isopropil-1H-indol-2-il)-1-tritil-1H-pirazolo [3,4-b]piridina (2,2 g, 3,68 mmol, 67,0 % de rendimiento) en forma de un sólido de color pardo claro. Tiempo de retención de CLEM 4,423 min [D], EM m/z: 597,2 (M+H).
Intermediario 9B: (3-isopropil-2-(1-tritil-1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)carbamato de ferc-butilo
A una solución de 4-(5-bromo-3-isopropil-1H-indol-2-il)-1-tritil-1H-pirazolo[3,4-b]piridina (1,5 g, 2,51 mmol) y carbamato de ferc-butilo (0,353 g, 3,01 mmol) en tolueno (15 ml) se le añadió NaOtBu (0,482 g, 5,02 mmol) a temperatura ambiente. La mezcla se desgasificó durante 10 minutos con nitrógeno. A continuación, se añadió Pd2dba3 (0,230 g, 0,251 mmol) seguido de la adición de 2-(di-ferc-butilfosfino)bifenilo (0,037 g, 0,126 mmol). La solución se desgasificó nuevamente durante 5 min. La mezcla resultante se agitó a 90 °C durante 3 h. La mezcla de reacción se diluyó con acetato de etilo (100 ml), se lavó con agua (2 x 50 ml), salmuera (20 ml), se secó sobre sulfato de sodio y se concentró para obtener el producto en bruto. El material en bruto se purificó por cromatografía en columna usando
40 g de columna de sílice, el compuesto se eluyó con acetato de etilo al 14 % en hexano, las fracciones se recolectaron y se concentraron para proporcionar (3-isopropil-2-(1-tritil-1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)carbamato de tere-butilo (1,5 g, 2,51 mmol, 94 % de rendimiento) en forma de un sólido de color amarillo. Tiempo de retención de CLEM 1,63 min [D]. EM m/z: 634,2 (M+H).
Intermediario 9C: 3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-amina
A una solución de (3-isopropil-2-(1-tritil-1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)carbamato de tere-butilo (1,5 g, 2,367 mmol) en DCM (5 ml) se le añadió HCl 4 M en dioxano (3,55 ml, 14,20 mmol) a temperatura ambiente. La mezcla se agitó a la misma temperatura durante 3 h. La mezcla de reacción se concentró para proporcionar 3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-amina (0,67 mg, 99% de rendimiento) en forma de un sólido de color amarillo pálido. Tiempo de retención de CLEM 1,46 min [E]. EM m/z: 291,1 (M+H).
Intermediario 9D: 3-((3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)carbamoil)pirrolidin-1-carboxilato de (R)-tere-butilo
A una solución de 3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-amina (0,025 g, 0,086 mmol) y ácido (R)-1-(tere-butoxicarbonil)pirrolidin-3-carboxílico (0,020 g, 0,094 mmol) en DMF (2 ml) se le añadieron DIPEA (0,045 ml, 0,257 mmol) y HATU (0,065 g, 0,172 mmol) a temperatura ambiente. La mezcla de reacción se agitó a la misma temperatura durante 3 h. La masa de reacción se diluyó con DCM (10 ml), se lavó con agua (10 ml), se secó sobre sulfato de sodio y se concentró para proporcionar 3-((3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)carbamoil)pirrolidin-1-carboxilato de (R)-tere-butilo (0,03 g, 0,061 mmol) en forma de un sólido de color amarillo. Tiempo de retención de CLEM 2,29 min [D]. EM m/z: 489,2 (M+H).
Ejemplo 9:
A una solución de 3-((3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il) carbamoil)pirrolidin-1-carboxilato de (R) -tere-butilo (0,03 g, 0,061 mmol) en DCM (2 ml) ácido clorhídrico 4 M en dioxano (0,090 ml, 0,368 mmol) a temperatura ambiente. La mezcla de reacción se agitó a la misma temperatura durante 1 h. La masa de reacción se concentró para obtener el producto en bruto. El producto se purificó por CLEM prep. con las siguientes condiciones: Waters Xbridge C18, 19x150 mm, 5 pm; Columna de protección: Waters XBridge C18, 19x10 mm, 5 pm; Fase móvil A: 5:95 de metanol:agua con NH4OAc 10 mM; Fase móvil B: 95:5 de metanol:agua con 10 mM NH4OAc; Gradiente: 15-65 % de B durante 25 minutos, seguido de una retención de 10 minutos al 65 % de B y una retención de 5 minutos al 100 % de B; Flujo: 15 ml/min. La fracción se recolectó, se concentró y se liofilizó para proporcionar (R)-N-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)pirrolidin-3-carboxamida (4,5 mg, 19 %) en forma de un sólido de color amarillo pálido. Tiempo de retención de CLEM 1,14 min [C1]. EM m/z: 389,1 (M+H); RMN 1H (400 MHz, DMSO-d6) 8 ppm 13,80 (s a, 1H), 11,27 (s, 1H), 10,09 (s, 1H), 8,65-8,56 (m, 1H), 8,26 (d, J =1,5 Hz, 1H), 8,18-8,11 (m, 1H), 7,42 7,28 (m, 2H), 7,22 (d, J = 4,5 Hz, 1H), 3,27-3,14 (m, 4H), 2,89 (s, 1H), 2,28-2,19 (m, 2H), 2,15-2,05 (m, 1H), 1,51-1,39 (m, 6H).
EJEMPLO 10
(S) -N-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)pirrolidin-3-carboxamida
El ejemplo 10 se preparó de acuerdo con el procedimiento general descrito en el ejemplo 9. Tiempo de retención de CLEM 2,29 min [D]. EM m/z: 489,2 (M+H).
Los siguientes ejemplos se prepararon de acuerdo con el procedimiento general descrito en el Ejemplo 9:
Tabla 3
(continuación)
EJEMPLO 27
1-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il) imidazolidin-2-ona
Intermediario 27A: 1-(3-isopropil-2-(1-tritil-1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)imidazolidin-2-ona
Una solución de 4-(5-bromo-3-isopropil-1H-indol-2-il)-1-tritil-1H-pirazolo[3,4-b]piridina (0,500 g, 0,837 mmol), imidazolidin-2-ona (0,108 g, 1,255 mmol) y CS2CO3 (0,545 g, 1,674 mmol) en dioxano (25 ml) se desgasificó durante 3 min. A continuación, se añadieron yoduro de cobre (I) (0,080 g, 0,418 mmol) y N,N'-dimetiletilendiamina (0,074 g, 0,837 mmol). La mezcla de reacción resultante se calentó a 130 °C durante 16 h. La masa de reacción se diluyó con DCM (100 ml), se lavó con agua (50 ml), se secó sobre sulfato de sodio y se concentró para obtener el producto en bruto. El material en bruto se purificó por cromatografía en columna usando una columna de sílice de 24 g, el compuesto se eluyó con acetato de etilo al 45 % en éter de petróleo, las fracciones se recolectaron y se concentraron para proporcionar 1-(3-isopropil-2-(1-tritil-1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)imidazolidin-2-ona (0,270 g, 0,448 mmol, 53,5% de rendimiento) en forma de un sólido de color amarillo claro. Tiempo de retención de CLEM 1,10 min. [D], EM m/z: 603,3 (M+H).
Intermediario 27B: 1-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)imidazolidin-2-ona
A una solución de 1-(3-isopropil-2-(1-tritil-1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il) imidazolidin-2-ona (0,050 g, 0,083 mmol) en dioxano (2,0 ml) se le añadió HCl 4 M en dioxano (0,518 ml, 2,074 mmol) a 10 °C. La mezcla se agitó a la misma temperatura durante 4 h. La masa de la mezcla de reacción se concentró para obtener el producto en bruto. El producto en bruto se purificó por CLEM prep. con las siguientes condiciones: Waters Xbridge C18, 19x150 mm, 5 |jm; Columna de protección: Waters XBridge C18, 19x10 mm, 5 jm ; Fase móvil A: 5:95 de acetonitrilo:agua con NH4OAc 10 mM; Fase móvil B: 95:5 de acetonitrilo:agua con 10 mM de NH4OAc; Gradiente: 10-30 % de B durante 25 minutos, seguido de una retención de 10 minutos a 30 % de B y una retención de 5 minutos a 100 % de B; Flujo: 15 ml/min. Las fracciones que contenían el producto se combinaron y se secaron usando un evaporador centrífugo Genevac para proporcionar 1-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)imidazolidin-2-ona (6,9 mg, 23 %) en forma de un sólido de color amarillo pálido. Tiempo de retención de CLEM 1,381 min [E]. EM m/z: 361,1 (M+H); RMN 1H (400 MHz, DMSO-d6) 8 ppm 14,13-13,99 (m, 1H), 11,59-11,35 (m, 1H), 8,86 (d, J = 4,9 Hz, 1H), 8,41 (s, 1H), 8,14 -8,01 (m, 1H), 7,86-7,61 (m, 2H), 7,47 (s, 1H), 7,10-6,91 (m, 1H), 4,29-4,11 (m, 2H), 3,74-3,59 (m, 3H), 1,70 (d, J = 7,1 Hz, 6 H).
EJEMPLO 28
2-(3,4-dimetoxifenil)-N,3-dietil-N-(1'-metil-1,4'-bipiperidin-4-il)-1H-indol-5-amina
Intermediario 28A: 5-(1-(ferc-butoxicarbonil)piperidin-4-ilamino)-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de ferc-butilo
A un vial de reacción de 7,39 ml (2 dram) se le añadieron 5-cloro-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de ferc-butilo (0,100 g, 0,240 mmol), carbonato de cesio (0,235 g, 0,721 mmol), precatalizador XPhos de segunda generación (0,019 g, 0,024 mmol) y 4-aminopiperidin-1-carboxilato de ferc-butilo (0,144 g, 0,721 mmol) en dioxano (2 ml). El vial se tapó con una tapa revestida de teflón y se bombeó/purgó con gas nitrógeno tres veces. La mezcla se puso a calentar a 100 °C durante 2 horas. La mezcla de reacción se enfrió a temperatura ambiente, se concentró a sequedad en una corriente de gas nitrógeno y se diluyó con acetato de etilo y agua. El contenido se transfirió a un embudo separador y las capas se separaron. Los orgánicos se lavaron con salmuera, se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron mediante evaporación rotatoria. El residuo se purificó por cromatografía sobre gel de sílice y después de la concentración de fracciones similares, se recolectó 5-((1-(fercbutoxicarbonil)piperidin-4-il)amino)-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de ferc-butilo (0,106 g, 0,183 mmol, 76 % de rendimiento) en forma de un sólido de color pardo. Tiempo de retención de CLEM 1,05 min [F1]. EM m/z: 580,4 (M+H).
Intermediario 28B: 5-((1-(ferc-butoxicarbonil)piperidin-4-il)(etil)amino)-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de ferc-butilo
A un vial de 7,39 ml (2 dram) se le añadieron 5-((1-(ferc-butoxicarbonil)piperidin-4-il)amino)-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de ferc-butilo (0,029 g, 0,050 mmol), carbonato de cesio (0,049 g, 0,150 mmol), acetona (1 ml) y yodoetano (0,078 g, 0,500 mmol). La mezcla de reacción se agitó a temperatura ambiente durante 2 horas, luego, se filtró a través de Celite y se enjuagó con acetona. Los volátiles se retiraron en una corriente de nitrógeno y se recolectó 5-((1-(ferc-butoxicarbonil)piperidin-4-il)(etil)amino)-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de fercbutilo (0,03 g, 0,050 mmol, 99 % de rendimiento). Tiempo de retención de CLe M 1,24 min [B]. EM m/z: 608,4 (M+H).
Intermediario 28C: 2,2,2-trifluoroacetato de 2-(3,4-dimetoxifenil)-N,3-dietil-N-(piperidin-4-il)-1H-indol-5-amina
A un vial de 7,39 ml (2 dram) se le añadieron 5-((1-(ferc-butoxicarbonil)piperidin-4-il)(etil)amino)-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de ferc-butilo (0,03 g, 0,050 mmol), DCM (0,5 ml) y ácido 2,2,2-trifluoroacético (0,057 g, 0,500 mmol). La mezcla de reacción se agitó durante 20 minutos a temperatura ambiente y se concentró a sequedad. Se recolectó 2,2,2-trifluoroacetato de 2-(3,4-dimetoxifenil)-N,3-dietil-N-(piperidin-4-il)-1H-indol-5-amina. Tiempo de retención de CLEM 0,73 min [B]. EM m/z: 408,2 (M+H).
Ejemplo 28:
A 2,2,2-trifluoroacetato de 2-(3,4-dimetoxifenil)-N,3-dietil-N-(piperidin-4-il)-1H-indol-5-amina (0,025 g) se le añadieron DMF (1,0 ml), TEA (0,035 ml, 0,250 mmol), ácido acético (0,01 ml) y 1-metilpiperidin-4-ona (0,017 g, 0,150 mmol). Después de agitar durante 15 minutos a temperatura ambiente, se le añadió cianoborohidruro de sodio (9,43 mg, 0,150 mmol) y la mezcla se agitó durante 14 horas. Se añadió MeOH (0,5 ml) y la mezcla se concentró en una corriente de nitrógeno gaseoso. Este residuo se diluyó con DMF (2,0 ml), se filtró a través de un filtro de jeringa y se purificó por HPLC preparativa para proporcionar 2-(3,4-dimetoxifenil)-N,3-dietil-N-(1'-metil-1,4'-bipiperidin-4-il)-1H-indol-5-amina. Tiempo de retención de HPLC 1,46 min [Método C]. EM m/z. 505,4 (M+H). Tiempo de retención de HPLC 1,00 min
[Método D]. EM m/z: 505,3 (M+H). RMN 1H (500 MHz, DMSO-da) 511,71-11,39 (m, 1H), 7,94 (s, 1H), 7,75 (s a, 1H), 7,52 (d, J = 8,8 Hz, 1H), 7,32 (s, 1H), 7,28-7,07 (m, 2H), 3,99 (s a, 1H), 3,83 (d, J =11,8 Hz, 8H), 3,76 (d a, J = 4,0 Hz, 1H), 3,66-3,49 (m, 1H), 3,37 (s a, 1H), 3,13-2,93 (m, 2H), 2,92-2,81 (m, 4H), 2,74 (d a, J =12,5 Hz, 5H), 2,22 (d a, J = 11,1 Hz, 2H), 1,83 (d a, J =11,1 Hz, 4H), 1,27 (t, J = 7,6 Hz, 4H), 1,00 (t a, J = 6,9 Hz, 4H).
EJEMPLO 29
5-(3-(1,4-diazepan-1-il)azetidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol
En un tubo de reacción en un Bohdan Miniblock XT se disolvió 5-cloro-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de ferc-butilo (13,5 mg, 0,031 mmol) en dioxano (0,550 ml). Se añadieron carbonato de cesio (30,7 mg, 0,094 mmol) y precatalizador XPhos de segunda generación (0,0024 mg, 0,0031 mmol). A continuación, se añadió 4-(azetidin-3-il)-1,4-diazepano-1-carboxilato de ferc-butilo (0,012 g, 0,047 mmol). El tubo de reacción se tapó y se desgasificó mediante bombeo/purgado con gas nitrógeno. La mezcla de reacción se calentó a 100 °C durante 2 horas. La mezcla de reacción se enfrió a temperatura ambiente, se concentró a sequedad en una corriente de gas nitrógeno. La mezcla se diluyó con HCl 4 M en dioxano (0,5 ml), se agitó durante 1 hora a temperatura ambiente y se concentró a través de una corriente de gas nitrógeno. El residuo se purificó por HPLC preparativa para proporcionar 5-(3-(1,4-diazepan-1 -il)azetidin-1 -il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (0,106 g, 0,183 mmol, 76% de rendimiento). Tiempo de retención de Hp LC 1,36 min [Método C]. e M m/z: 449,4 (M+H). Tiempo de retención de HPLC 1,11 min [Método D]. EM m/z: 449,4 (M+H). RMN 1H (500 MHz, DMSO-d6) 510,79-10,62 (m, 1H), 7,96 (s, 1H), 7,22 (d, J = 8,8 Hz, 1H), 7,16-6,95 (m, 3H), 6,43 (d a, J = 8,4 Hz, 1H), 4,14-4,03 (m, 2H), 3,88-3,71 (m, 7H), 3,40-3,18 (m, 3H), 3,09 2,98 (m, 1H), 2,90 (s, 4H), 2,74 (s, 4H), 2,03 (s a, 2H), 1,48-1,34 (m, 6H).
EJEMPLO 30
N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-(metilamino)etil)ciclohexano-1,4-diamina
Intermediario 30A: 2-(3,4-dimetoxifenil)-3-isopropil-N-(1,4-dioxaespiro[4,5]decan-8-il)-1H-indol-5-amina
A un vial de reacción de 7,39 ml (2 dram) se le añadieron 5-cloro-2-(3,4-dimetoxifenil)-3-etil-1H-indol-1-carboxilato de ferc-butilo (0,310 g, 0,721 mmol), carbonato de cesio (0,705 g, 2,16 mmol), precatalizador XPhos de segunda generación (0,057 g, 0,072 mmol) y 1,4-dioxaespiro[4,5]decan-8-amina (227 mg, 1,442 mmol) en dioxano (3 ml). El vial se tapó con una tapa revestida de teflón y se bombeó/purgó con gas nitrógeno tres veces. La mezcla se calentó a 100 °C durante 16 horas. La mezcla de reacción se enfrió a temperatura ambiente, se concentró a sequedad en una corriente de gas nitrógeno y se diluyó con DCM y agua. El contenido se transfirió a un embudo separador y las capas se separaron. Los orgánicos se lavaron con salmuera, se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron mediante evaporación rotatoria. El residuo se purificó por cromatografía sobre gel de sílice y después de la concentración de fracciones similares, se recolectó 2-(3,4-dimetoxifenil)-3-isopropil-N-(1,4-dioxaespiro[4,5]decan-8-il)-1H-indol-5-amina (0,200 g, 0,363 mmol, 50% de rendimiento). Tiempo de retención de CLEM 1,20 min [F1]. EM m/z: 450,4 (M+H).
Intermediario 30B: 4-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-ilamino)cidohexanona
A 5-(1,4-dioxaespiro[4,5]decan-8-ilamino)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de ferc-butilo (0,053 g, 0,096 mmol) en DCM (0,5 ml) se le añadió TFA (1000 pl, 12,98 mmol). El vial de reacción se tapó. La mezcla de reacción se agitó a 90 °C durante 7 horas. Los volátiles se retiraron en una corriente de gas nitrógeno para proporcionar 4-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-ilamino)ciclohexanona (0,040 g, 0,099 mmol, 100% de rendimiento). Tiempo de retención de CLEM 0,988 min [F1]. EM m/z: 407,4 (M+H).
Ejemplo 30:
A 4-((2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)amino)ciclohexanona (0,018 g, 0,044 mmol) en un vial de reacción se le añadieron DCM (1 ml), (2-aminoetil)(metil)carbamato de ferc-butilo (0,023 g, 0,133 mmol) y ácido acético (2,53 pl, 0,044 mmol). La mezcla de reacción se agitó a temperatura ambiente durante 15 minutos, luego se le añadió cianoborohidruro de sodio (8,35 mg, 0,133 mmol). La agitación continuó a la misma temperatura durante 1 hora. La muestra se concentró hasta la sequedad, y luego se añadieron DCM (1 ml) y TFA (1 ml). La mezcla de reacción se agitó durante 15 minutos y se concentró a sequedad. El residuo se diluyó con DMF y se purificó por HPLC preparativa para proporcionar N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-(metilamino)etil)ciclohexano-1,4-diamina indol (0,0013 g, 0,0015 mmol, 3,50 % de rendimiento). Tiempo de retención de HPLC 1,21 min [Método C]. EM m/z: 465,4 (M+H). Tiempo de retención de HPLC 0,95 min [Método D]. EM m/z: 465,3 (M+H). RMN 1H (500 MHz, DMSO-da). Desplazamiento 11,49-11,31 (m, 1H), 7,82 (s a, 1H), 7,48 (d, J = 8,4 Hz, 1H), 7,25-7,00 (m, 4H), 3,83 (d, J = 7,7 Hz, 6 H), 3,58-3,42 (m, 1H), 3,41-3,31 (m, 1H), 3,24 (d a, J = 9,8 Hz, 4H), 3,13 (s a, 1H), 2,64 (s, 3H), 2,20-2,00 (m, 4H), 1,55 (d a, J =12,8 Hz, 2H), 1,47-1,34 (m, 8H).
Los siguientes ejemplos se prepararon de acuerdo con los procesos generales descritos en los ejemplos anteriores:
Tabla 4
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
EJEMPLO 103
2-(3,4-dimetoxifenil)-3-isopropil-N-(1,2,2,6,6-pentametilpiperidin-4-il)-1H-indol-5-amina
A un vial de reacción de 7,39 ml (2 dram) se le añadieron 5-cloro-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de ferc-butilo (0,018 g, 0,042 mmol), carbonato de cesio (0,041 g, 0,126 mmol), precatalizador Xphos de segunda generación (3,29 mg, 4,19 |jmol), 1,2,2,6,6-pentametilpiperidin-4-amina (7,13 mg, 0,042 mmol) y dioxano (1 ml). La mezcla se tapó con una tapa revestida de teflón y se bombeó/purgó con nitrógeno gaseoso tres veces. La mezcla se puso a calentar a 100 °C durante 2 horas. Al enfriar a temperatura ambiente, la mezcla se concentró, se diluyó con DCM/MeOH (3,0 ml) y se filtró a través de un filtro de jeringa. El filtrado se concentró hasta un residuo parduzco. Al residuo se le añadió HCl 4 M/dioxano (1,0 ml). La mezcla de reacción se agitó durante 1 hora a temperatura ambiente. La mezcla se concentró a sequedad en una corriente de gas nitrógeno, luego se diluyó con DMSO (2,0 ml) y se purificó por HPLC preparativa para proporcionar 2-(3,4-dimetoxifenil)-3-isopropil-N-(1,2,2,6,6-pentametilpiperidin-4-il)-1H-indol-5-amina (0,0029 g, 0,0060 mmol, 14,3% de rendimiento). Tiempo de retención de HPLC 1,44 min [Método C]. EM m/z: 464,4 (M+H). Tiempo de retención de HPLC 1,14 min [Método D]. EM m/z: 464,5 (M+H). RMN 1H (500 MHz, DMSO-d6) 811,05-10,72 (m, 1H), 8,48-8,17 (m, 1H), 7,96 (s, 1H), 7,37-7,19 (m, 1H), 7,16 6,96 (m, 4H), 4,05-3,93 (m, 1H), 3,82 (d, J = 8,8 Hz, 3H), 3,49-3,40 (m, 1H), 3,37-3,26 (m, 1H), 2,90 (s, 2H), 2,80-2,68 (m, 4H), 2,56 (t, J = 5,6 Hz, 2H), 2,14 (d a, J =12,1 Hz, 2H), 1,73 (s a, 2H), 1,50-1,17 (m, 15H).
Los ejemplos en la Tabla 5 se prepararon de acuerdo con el procedimiento general descrito en el Ejemplo 103.
Tabla 5
continuación
continuación
continuación
EJEMPLO 121
5-(4-(1,4-diazepan-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol
Intermediario 121A: 2-(3,4-dimetoxifenil)-3-isopropil-5-(1,4-dioxa-8-azaespiro[4,5]decan-8-il)-1H-indol-1-carboxilato de ferc-butilo
A 5-cloro-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de ferc-butilo (1,040 g, 2,419 mmol), carbonato de cesio (2,364 g, 7,26 mmol) en dioxano (10 ml) se le añadieron precatalizador Xphos de segunda generación (0,190 g, 0,242 mmol) y 1,4-dioxa-8-azaespiro[4,5]decano (0,693 g, 4,84 mmol). El recipiente de reacción se tapó con una tapa revestida de teflón y se bombeó/purgó con gas nitrógeno tres veces. La mezcla de reacción se calentó a 100 °C durante 1 hora. La mezcla de reacción se enfrió a temperatura ambiente, se concentró a sequedad en una corriente de gas nitrógeno y se diluyó con DCM y agua. El contenido se transfirió a un embudo separador y las capas se separaron. Los orgánicos se lavaron con salmuera, se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron mediante evaporación rotatoria para proporcionar 2-(3,4-dimetoxifenil)-3-isopropil-5-(1,4-dioxa-8-azaespiro[4,5]decan-8-il)-1H-indol-1-carboxilato de ferc-butilo (1,30 g, 2,422 mmol, 100 % de rendimiento). Tiempo de retención de CLEM 1,205 min [F1]. EM m/z: 537,5 (M+H).
Intermediario 121B: 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-ona
A un vial de reacción de 7,39 ml (2 dram) se le añadieron 2-(3,4-dimetoxifenil)-3-isopropil-5-(1,4-dioxa-8-azaespiro[4,5]decan-8-il)-1H-indol-1-carboxilato de ferc-butilo (0,175 g, 0,326 mmol), DCM (2,0 ml) y TFA (4000 pl, 51,9 mmol). El vial se tapó y la mezcla de reacción se agitó a 90 °C durante 7 horas. La mezcla se enfrió a temperatura ambiente y se concentró a sequedad en una corriente de gas nitrógeno para proporcionar 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-ona en bruto (0,135 g, 0,344 mmol, 100 % de rendimiento). Tiempo de retención de CLEM 0,995 min [F1]. EM m/z: 393,0 (M+H).
Ejemplo 121:
A 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-ona (0,025 g, 0,064 mmol) en un vial de reacción se le añadieron DCM (1 ml), 1,4-diazepano-1-carboxilato de ferc-butilo (0,038 g, 0,191 mmol) y ácido acético (3,63 pl, 0,064 mmol). La mezcla de reacción se agitó a temperatura ambiente durante 15 minutos, luego se añadió cianoborohidruro de sodio (0,012 g, 0,191 mmol). La agitación continuó a la misma temperatura durante 1 hora. La muestra se concentró a sequedad. Luego, se añadieron DCM (1 ml) y TFA (1 ml). La mezcla de reacción se agitó durante 15 minutos y se concentró a sequedad. El residuo se diluyó con DMF y se purificó por HPLC preparativa para proporcionar 5-(4-(1,4-diazepan-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (0,0043 g, 0,009 mmol, 14% de rendimiento). Tiempo de retención de Hp LC 1,36 min [Método C]. EM (E-) m/z. 477,3 (M+H). Tiempo de retención de HPLC 0,98 min [Método D]. EM m/z: 477,3 (M+H). RMN 1H (500 MHz, DMSO-d6) 811,24-11,01 (m, 1H), 7,65 (s a, 1H), 7,38 (d a, J =8,8 Hz, 1H), 7,28 (s, 1H), 7,21-7,00 (m, 4H), 3,83 (d, J = 8,1 Hz, 8H), 3,71 (d a, J =11,4 Hz, 3H), 3,58-3,43 (m, 1H), 3,39-3,25 (m, 3H), 3,18 (s, 1H), 2,27-1,97 (m, 7H), 1,42 (d a, J = 6,7 Hz, 8H), 0,84-0,84 (m, 1H).
EJEMPLO 122
2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(1-isopropilazepan-4-il)piperazin-1-il)-1H-indol
Intermediario 122A: 5-(4-(ferc-butoxicarbonil)piperazin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de ferc-butilo
A un vial de 7,39 ml (2 dram) se le añadieron 5-cloro-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de fercbutilo (0,215 g, 0,500 mmol), carbonato de cesio (0,489 g, 1,500 mmol), precatalizador XPhos de segunda generación (0,039 g, 0,050 mmol) y piperazin-1-carboxilato de ferc-butilo (0,279 g, 1,500 mmol) en dioxano (3,0 ml). La mezcla se tapó con una tapa revestida de teflón y se bombeó/purgó con nitrógeno gaseoso tres veces. La mezcla se calentó a 100 °C durante 48 horas. La mezcla de reacción se enfrió a temperatura ambiente, se concentró a sequedad en una corriente de gas nitrógeno y se diluyó con acetato de etilo y agua. Los contenidos se transfirieron a un embudo separador y las capas se separaron. Los orgánicos se lavaron con salmuera, se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron mediante evaporación rotatoria. El residuo se purificó por cromatografía en gel de sílice y después de la concentración de fracciones similares, se recolectó 5-(4-(ferc-butoxicarbonil)piperazin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de ferc-butilo (0,225 g, 0,322 mmol, 78% de rendimiento). Tiempo de retención de CLEM 1,10 min [B1]. EM m/z: 580,4 (M+H).
Intermediario 122B: 2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol, sal de TFA
A un vial de reacción de 7,39 ml (2 dram) se le añadieron 5-(4-(terc-butoxicarbonil)piperazin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de terc-butilo (0,055 g, 0,095 mmol), DCM (0,5 ml) y TFA (0,073 ml, 0,949 mmol). La mezcla de reacción se agitó a temperatura ambiente durante 30 minutos, luego se concentró en una corriente de gas nitrógeno para proporcionar 2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol, sal TFA (0,045 g, 0,95 mmol, 100 % de rendimiento) como un residuo amarillento. Tiempo de retención de CLEM 1,16 min [D]. EM m/z: 380,3 (M+H).
Intermediario 122C: 5-(4-(azepan-4-il)piperazin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol, 2 TFA
A un vial de 7,39 ml (2 dram) se le añadieron 2,2,2-trifluoroacetato de 2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol (0,030 g, 0,061 mmol) y DMF (1 ml). A continuación, se añadieron TEA (0,042 ml, 0,304 mmol), 4-oxoazepano-1-carboxilato de terc-butilo (0,026 g, 0,122 mmol) y ácido acético (0,010 ml). La mezcla de reacción se agitó durante 1 hora a temperatura ambiente y se le añadió cianoborohidruro de sodio (0,011 g, 0,182 mmol). La mezcla de reacción se agitó durante 16 horas a temperatura ambiente, luego se diluyó con agua (0,5 ml) y se concentró. Se añadieron DCM (0,5 ml) y TFA (0,5 ml) y se agitó durante 20 minutos. Esto se concentró y el residuo amarillento resultante, 5-(4-(azepan-4-il)piperazin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol, 2 TFA. Tiempo de retención de CLEM 1,09 min [C]. EM m/z: 477,4 (M+H).
Ejemplo 122:
A un vial de 7,39 ml (2 dram) se le añadieron bis(2,2,2 -trifluoroacetato) de 5-(4-(azepan-4-il)piperazin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (0,020 g, 0,028 mmol) y DMF (1 ml). A continuación, se añadieron TEA (0,020 ml, 0,142 mmol), propan-2-ona (4,95 mg, 0,085 mmol) y ácido acético (0,010 ml). La mezcla de reacción se agitó durante 1 hora a temperatura ambiente y se le añadió cianoborohidruro de sodio (5,35 mg, 0,085 mmol). La mezcla de reacción se agitó durante 16 horas a temperatura ambiente y se diluyó con agua (0,1 ml) y MeOH (1,0 ml). Los sólidos se separaron por filtración y la solución resultante se purificó por HPLC preparativa para proporcionar 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(1-isopropilazepan-4-il)piperazin-1-il)-1H-indol (0,0042 g, 0,0077 mmol, 27% de rendimiento). Tiempo de retención de HPLC 1,39 min [Método C]. EM m/z: 519,4 (M+H). Tiempo de retención de HPLC 1,14 min [Método D]. EM m/z: 519,5 (M+H). RMN 1H (500 MHz, DMSO-d6) 8 10,71 (s a, 1H), 7,18 (d a, J = 8,4 Hz, 1H), 7,10 (s a, 1H), 7,04-6,90 (m, 3H), 6,81 (d a, J = 8,1 Hz, 1H), 3,75 (d, J = 9,1 Hz, 8H), 3,38 (s a, 1H), 3,32-3,21 (m, 1H), 3,20-3,01 (m, 3H), 2,83 (s, 2H), 2,67 (s, 2H), 2,25-1,58 (m, 8H), 1,34 (d a, J = 7,1 Hz, 6H), 1,18 (d a, J = 5,7 Hz, 8H).
Los ejemplos en la Tabla 6 se prepararon de acuerdo con el procedimiento general descrito en los ejemplos anteriores.
Tabla 6
(continuación)
EJEMPLO 126
2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol, sal de TFA
A un vial de reacción de 7,39 ml (2 dram) se le añadieron 5-(4-(terc-butoxicarbonil)piperazin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-1-carboxilato de terc-butilo (0,055 g, 0,095 mmol), DCM (0,5 ml) y TFA (0,073 ml, 0,949 mmol). La mezcla de reacción se agitó a temperatura ambiente durante 30 minutos, luego se concentró en una corriente de gas nitrógeno para producir un residuo amarillento. El residuo se diluyó con DMF y se purificó por HPLC preparativa para proporcionar 2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol (0,0076 g, 0,019 mmol, 20% de rendimiento). Tiempo de retención de HPLC 1,17 min [Método C]. EM m/z: 380,3 (M+H). Tiempo de retención de HPLC 1,16 min [Método D]. EM m/z: 380,3 (M+H). RMN 1H (500 MHz, DMSO-da) 810,86-10,74 (m, 1H), 8,73 (s a, 1H), 7,95 (s, 1H), 7,27 (d, J = 8,8 Hz, 1H), 7,19 (s, 1H), 7,12-6,98 (m, 3H), 6,88 (d a, J = 8,8 Hz, 1H), 3,82 (d, J = 8,8 Hz, 6 H), 3,57-3,44 (m, 2H), 3,38-3,20 (m, 3H), 2,89 (s, 2H), 2,74 (s, 2H), 1,41 (d a, J =7,1 Hz, 6 H).
EJEMPLO 127
2-(4-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperazin-1-il)-N-metiletanamina
A un vial de reacción de 7,39 ml (2 dram) se le añadieron 2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol, 2,2,2-trifluoroacetato (0,015 g, 0,030 mmol) y DMF (1 ml). A continuación, se añadieron TEA (0,021 ml, 0,152 mmol), metil(2-oxoetil)carbamato de terc-butilo (0,011 g, 0,061 mmol) y ácido acético (0,010 ml). La mezcla de reacción se agitó durante 1 hora a temperatura ambiente y se añadió cianoborohidruro de sodio (5,73 mg, 0,091 mmol). La mezcla
de reacción se agitó durante la noche a temperatura ambiente. La mezcla de reacción se diluyó con agua (0,5 ml) y se concentró en una corriente de nitrógeno gaseoso. Este residuo se diluyó con DCM (0,5 ml) y TFA (0,5 ml) y se agitó durante 30 minutos a temperatura ambiente. La muestra se concentró, se diluyó con DMF (2,0 ml), se filtró y se purificó por HPLC preparativa para proporcionar 2-(4-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperazin-1-il)-N-metiletanamina indol (0,013 g, 0,0080 mmol, 27 % de rendimiento). Tiempo de retención de HPLC 1,62 min [Método C]. EM m/z: 519,4 (M+H). Tiempo de retención de HPLC 1,15 min [Método D]. EM m/z: 519,5 (M+H). RMN 1H (500 MHz, DMSO-d6) 6 11,06-10,85 (m, 1H), 7,31 (d a, J = 8,4 Hz, 1H), 7,27 (s, 1H), 7,13-6,95 (m, 4H), 3,82 (d, J = 8,4 Hz, 6H), 3,46 (s a, 1H), 3,51-3,40 (m, 1H), 3,37-3,28 (m, 1H), 3,23 (s a, 2H), 3,14-2,93 (m, 3H), 2,90 (s, 1H), 2,74 (s, 1H), 2,64 (s, 4H), 1,71-1,47 (m, 1H), 1,48-1,18 (m, 7H), 1,37-1,18 (m, 1H))
Los ejemplos en la Tabla 7 se prepararon de acuerdo con el mismo procedimiento descrito en los ejemplos anteriores.
Tabla 7
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
continuación
Ensayos biológicos
Las propiedades farmacológicas de los compuestos de esta invención pueden confirmarse mediante varios ensayos biológicos. Los ensayos biológicos ejemplificados, que siguen, se han llevado a cabo con compuestos de la invención.
Ensayos de reportero de inhibición de TLR7/8/9
Se usaron células HEK-Blue™ (Invivogen) que sobreexpresaban receptores TLR7, TLR8 o TLR9 humanos para detectar inhibidores de estos receptores usando un gen reportero SEAP (fosfatasa alcalina embrionaria secretada) inducible bajo el control del promotor mínimo IFN-p fusionado a cinco sitios de unión a NF-kB y AP-1. Brevemente, las células se siembran en placas Greiner de 384 pocillos (15000 células por pocillo para TLR7, 20,000 para TLR8 y 25,000 para TLR9) y luego se tratan con compuestos de prueba en DMSO para producir un intervalo de concentración de respuesta a la dosis final de 0,05 nM - 50 pM. Después de un pretratamiento compuesto de 30 minutos a temperatura ambiente, las células se estimulan con un ligando TLR7 (gardiquimod a una concentración final de 7,5 pM), ligando TLR8 (R848 a una concentración final de 15,9 pM) o ligando TLR9 (ODN2006 a una concentración final de 5 nM) para activar NF-kB y AP-1 que inducen la producción de SEAP. Después de una incubación de 22 horas a 37 °C, 5 % de CO2, los niveles de SEAP se determinan con la adición del reactivo de detección HEK-Blue™ (Invivogen), un medio de cultivo celular que permite la detección de SEAP, de acuerdo con las especificaciones del fabricante. El porcentaje de inhibición se determina como el porcentaje de reducción en la señal de HEK-Blue presente
en los pozos tratados con agonista más DMSO solo en comparación con los pozos tratados con un inhibidor conocido.
TABLA 8
(continuación)
Claims (13)
1. Un compuesto de Fórmula (I)
N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en la que: G es:
(i)
(ii)
(iii)
(iv) un anillo heterocíclico de 9 miembros seleccionado de:
o
(v) anillo heterocíclico de 10 miembros seleccionado de:
Ri es H, Cl, -CN, alquilo C1-4, fluoroalquilo C1-3, hidroxialquilo C1-3, hidroxi-fluoroalquilo C1-3, -CRv=CH2, cicloalquilo C3-6, -CH2(cicloalquilo C3-6), -C(O)O(alquilo C1-3), o tetrahidropiranilo;
cada R2 es independientemente halo, -CN, -OH, -NO2, alquilo C1-4, fluoroalquilo C1-2, cianoalquilo C1-2, hidroxialquilo C1-3, aminoalquilo C1-3, -O(CH2)1-2OH, -(CH2)o-4O(alquilo C1-4), fluoroalcoxi C1-3, -(CH2)1-4O(alquilo C1-3), -O(CH2)1-2OC(O)(alquilo C1-3), -O(CH2)1-2NRxRx, -C(O)O(alquilo C1-3), -(CH2)o-2C(O)NRyRy, -C(O)NRx(hidroxialquilo C1-5), -C(O)NRx(alcoxialquilo C2-6), -C(O)NRx(cicloalquilo C3-6), -NRyRy, -NRy(fluoroalquilo C1-3), -NRy(hidroxialquilo C1-4), -NRxCH2(fenilo), -NRxS(O)2(cicloalquilo C3-6), -NRxC(O)(alquilo C1-3), -NRxCH2(cicloalquilo C3-6), -(CH2)o-2S(O)2(alquilo C1-3), -(CH2)o-2(cicloalquilo C3-6), -(CH2)o-2(fenilo), morfolinilo, dioxotiomorfolinilo, dimetil pirazolilo, metilpiperidinilo, metilpiperazinilo, amino-oxadiazolilo, imidazolilo, triazolilo o -C(O)(tiazolilo);
R2a es alquilo C1-6, fluoroalquilo C1-3, hidroxialquilo C1-6, aminoalquilo C1-3, -(CH2)o-4O(alquilo C1-3), cicloalquilo C3-6, -(CH2)1-3C(O)NRxRx, -CH2(cicloalquilo C3-6), -CH2(fenilo), tetrahidrofuranilo, tetrahidropiranilo, o fenilo;
cada R2b es independientemente H, halo, -CN, -NRxRx, alquilo C1-6, fluoroalquilo C1-3, hidroxialquilo C1-3, fluoroalcoxi C1-3, -(CH2)0-2O(alquilo C1-3), -(CH2)0-3C(O)NRxRx, -(CH2)1-3(cicloalquilo C3-6), -C(O)O(alquilo C1-3), -C(O)NRx(C1-3 alquilo), -CRx=CRxRx, o -CRx=CH(cicloalquilo C3-6);
R2c es R2a o R2b;
R2d es R2a o R2b; siempre y cuando uno de R2c y R2d es R2a, y el otro de R2c y R2 es R2b;
cada R5 es independientemente F, Cl, -CN, alquilo C1-3, fluoroalquilo C1-2, o -OCH3;
R7 es:
(i) R7a, -CH2R7a, -C(O)R7a, -C(O)CH(NH2)R7a, -C(O)(CH2)1-3NH2, -C(O)CH(NH2)(alquilo C1-4), -C(O)CH(NH2)(CH2)1-2C(O)OH, -C(O)CH(NH2)(CH2)2-4NH2 o -C(O)CH(NH2)(CH2)1-3C(O)NH2; o
(ii) cicloalquilo C3-6 sustituido con un sustituyente seleccionado de -NRx(CH2)2-3NRyRy, -NRx(metilpiperidinilo), -NRx(CH2)2-3(morfolinilo), dimetilamino piperidinilo y piperazinilo sustituido con un sustituyente seleccionado de alquilo C1-4, -C(O)CH3, -(CH2)1-2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), cicloalquilo C3-6, piridinilo y metilpiperidinilo;
R7a es azaespiro[3.5]nonanilo, cicloalquilo C3-6, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, diazepanonilo, diazepanilo, morfolinilo, fenilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo, o pirrolilo, cada uno sustituido con cero a 1 sustituyente seleccionado de alquilo C1-3, -NH2, metilpiperidinilo, metilpirrolidinilo, -OCH2CH2(pirrolidinilo), y -OCH2CH2NHCH2CH3; y cero a 4 sustituyentes seleccionados de -CH3;
R7b es:
(i) alquilo C1-4, hidroxialquilo C1-3, -(CH2)2-3C=CH, -(CH2)1-2O(alquilo C1-2), -(CH2)1-2S(O)2(alquilo C1-2), -(CH2)0-3NRxRy, -CH2C(O)NRxRx, -NRx(hidroxialquilo C1-4), -NRy(cianoalquilo C1-2), -NRx(fluoroalquilo C1-2), -NRx(C2-4 hidroxifluoroalquilo), -NRx(CH2)1-2C(O)NRxRx, -NRx(CH2)1-3NRxRx, -NRxCH2CH2NRxRx, -NRxC(O)(CH2)1-2NRxRx, -O(CH2)1-3NRxRx, -C(O)CH2NRxRx, -(CH2)1-2R7d, -NHR7d, -NH(CH2)1-2R7d o -OR7d; o
(ii) azepanilo, azetidinilo, diazepanilo, dioxotiomorfolinilo, morfolinilo, oxaazaespiro[3,3]heptanilo, oxetanilo, piperazinonilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b;
cada R7c es independientemente F, Cl, -CN, alquilo C1-2, -CF3, o -CH2CN;
R7d es azaespiro[3.5]nonanilo, biciclo[1.1.1]pentanilo, cicloalquilo C3-6, morfolinilo, oxetanilo, fenilo, piperidinilo, pirazolilo, pirrolidinilo, tetrahidrofuranilo o tetrahidropiranilo, cada uno sustituido con cero a 1 sustituyente seleccionado de alquilo C1-3, -NRxRx, -C(O)CH3, metilpiperidinilo, metilpirrolidinilo, tetrametilpiperidinilo, -OCH2CH2(pirrolidinilo), y -OCH2CH2NHCH2CH3; y cero a 4 sustituyentes seleccionados de -CH3;
R8 es H o alquilo C1-3;
o R7 y R8 junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo y pirrolilo, en donde dicho anillo heterocíclico está sustituido con cero a 1 R7b y cero a 2 R7c;
R8a es -OH, alquilo C1-6, fluoroalquilo C1-4, hidroxialquilo C1-4, -(CH2)1-2O(alquilo C1-3), -C(O)(alquilo C1-3), -(CH2)1-2(cicloalquilo C3-6), -(CH2)1-3(metil fenilo), -(CH2)1-3(pirrolidinilo), -(CH2)1-3(metilpirazolilo), -(CH2)1-3(tiofenilo), -NRxRx, cicloalquilo C3-6, metilpiperidinilo, piridinilo o pirimidinilo;
cada R8b es independientemente F, Cl, -CN, alquilo C1-3, o -CF3;
Rv es H, alquilo C1-2 o fluoroalquilo C1-2;
cada Rx es independientemente H o -CH3;
cada Ry es independientemente H o alquilo C1-6;
n es cero, 1, o 2; y
p es cero, 1, 2, 3, o 4.
2. El compuesto de acuerdo con la reivindicación 1, N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde:
R1 es H, Cl, -CN, alquilo C1-4, fluoroalquilo C1-2, hidroxialquilo C1-2, o -C(O)O(alquilo C1-2);
cada R2 es independientemente F, Cl, -CN, -OH, alquilo C1-4, fluoroalquilo C1-2, cianoalquilo C1-2, hidroxialquilo C1-3, aminoalquilo C1-3, -(CH2)0-2O(alquilo C1-4), -NRyRy, -(CH2)0-2C(O)NRyRy, -C(O)NRx(hidroxialquilo C1-4), -C(O)NRx(C2-4 alcoxialquilo), -C(O)NRx(cicloalquilo C3-6), -(CH2)0-2S(O)2(alquilo C1-3), -(c H2)0-1 (cicloalquilo C3-6), morfolinilo, -(CH2)0-1(fenilo) o dimetil pirazolilo;
R2a es alquilo C1-4, fluoroalquilo C1-2, hidroxialquilo C1-4, -(CH2)1-3OCH3, cicloalquilo C3-6, -CH2C(O)NRxRx, -CH2(cicloalquilo C3-6), -CH2(fenilo), tetrahidrofuranilo o fenilo;
cada R2b es independientemente H, F, Cl, -CN, -NRxRx, alquilo C1-6, fluoroalquilo C1-2, hidroxialquilo C1-3, -(CH2)0-2O(alquilo C1-2), -(CH2)0-2C(O)NRxRx, -(CH2)1-3(ciclopropilo), -C(O)O(alquilo C1-2), -C(O)NRx(alquilo C1-3), -CRx=CH2 o -CH=CH(cicloalquilo C3-6);
cada R5 es independientemente F, Cl, -CN, alquilo C1-2, o -OCH3;
R7 es:
(i) R7a, -CH2R7a, -C(O)R7a, -C(O)CH(NH2)R7a, -C(O)(CH2)1-3NH2, -C(O)CH(NH2)(alquilo C1-4), C(O)CH(NH2)(CH2) i-2C(O)OH> -C(O)CH(NH2)(CH2)2-4NH2 o -C(O)CH(NH2)(CH2)i-3C(O)NH2; o
(ii) cicloalquilo C3-6 sustituido con un sustituyente seleccionado de -NRx(CH2)2-3NRxRx, -NH(CH2)2-3NHCH3, -NH(metilpiperidinilo), -NH(CH2)2-3(morfolinilo), dimetilamino piperidinilo y piperazinilo sustituido con un sustituyente seleccionado de alquilo C1-4, -C(O)CH3, -(CH2)1-2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), cicloalquilo C3-6, piridinilo y metilpiperidinilo;
R/b es:
(i) alquilo C1-4, hidroxialquilo C1-3, -(CH2)2-3C=CH, -(CH2)1-2O(alquilo C1-2), -(CH2)1-2S(O)2(alquilo C1-2), -(CH2)o-3NRxRy, -CH2C(O)NRxRx, -NRx(hidroxialquilo C1-4), -NRy(cianoalquilo C1-2), -NRx(fluoroalquilo C1-2), -NRx(C2-4 hidroxifluoroalquilo), -NRx(CH2)1-2C(O)NRxRx, -NRx(CH2)1-3NRxRx, -NRxCH2CH2NRxRx, -NRxC(O)(CH2)1-2NRxRx, -O(CH2)1-3NRxRx, -C(O)CH2NRxRx, -(C H ^ R /d , -NHR/d, -N ^ C H ^ R /d o -OR/d; o
(ii) azepanilo, azetidinilo, diazepanilo, dioxotiomorfolinilo, morfolinilo, oxaazaespiro[3,3]heptanilo, oxetanilo, piperazinonilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8a y cero a 3 R8b;
cada R/c es independientemente F, -CH3 o -CH2CN;
R/d es azaespiro[3.5]nonanilo, biciclo[1.1.1]pentanilo, cicloalquilo C3-6, morfolinilo, oxetanilo, fenilo, piperidinilo, pirazolilo, pirrolidinilo, tetrahidrofuranilo o tetrahidropiranilo, cada uno sustituido con cero a 1 sustituyente seleccionado de alquilo C1-3, -NH2, -C(O)CH3, metilpiperidinilo, metilpirrolidinilo, tetrametilpiperidinilo, -OCH2CH2(pirrolidinilo) y -OCH2CH2NHCH2CH3; y cero a 4 sustituyentes seleccionados de -CH3;
R8 es H o alquilo C1-2;
o R7 y Ra junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo y pirrolilo, en donde el anillo heterocíclico está sustituido con cero a 1 R/b y cero a 2 R/c;
Raa es -OH, alquilo C1-4, fluoroalquilo C1-3, -(CH2)1-2O(alquilo C1-2), -C(O)(alquilo C1-2), -CH2(cicloalquilo (CH2)1-2(metil fenilo), -(CH2)1-3(pirrolidinilo), -(CH2)1-2(metilpirazolilo), -(CH2)1-2(tiofenilo), -NRxRx, cicloalquilo C3-6, metilpiperidinilo o piridinilo; y
cada Rab es independientemente F o -CH3.
4. El compuesto de acuerdo con la reivindicación 1, N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde:
G es:
(i)
(ii)
(iii)
o
(iv)
R1 es -CH3, -CH2CH3, o -CH(CH3)2;
cada R2 es independientemente Cl, -CH3, o -OCH3;
R2a es -CH3;
cada R2b es independientemente H, Cl, o -CH3;
cada R5 es independientemente -CH3 o -CH(CH3)2;
R7 es:
(i) -CH2(isopropil azaespiro[3.5]nonanilo), -CH2(metilpirrolidinilo), -C(O)(CH2)1-3NH2, -C(O)CH(NH2)CH2CH2CH3, -C(O)CH(NH2)CH2CH(CH3)2, -C(O)CH(NH2)CH(CH3)CH2CH3, -C(O)CH(NH2)CH2CH2C(O)OH, -C(O)CH(NH2)(CH2)3-4NH2, -C(O)CH(NH2)(CH2)1-2C(O)NH2, -C(O)CH(NH2)(ciclohexilo), -C(O)CH(NH2)(fenilo), -C(O)(aminociclohexilo), -C(O)(morfolinilo), -C(O)(pirrolidinilo), pentametilpiperidinilo, metilpiperidinil-piperidinilo, metilpirrolidinil-pirrolidinilo o fenilo sustituido con -OCH2CH2(pirrolidinilo) o -OCH2CH2NHCH2CH3; o
(ii) ciclohexilo sustituido con -NRx(CH2)2-3N(CH3)2, -NHCH2CH2NHCH3, -NH(metilpiperidinilo), -NH(CH2)2-3(morfolinilo), dimetilamino piperidinilo o piperazinilo sustituido con -CH3, -CH2CH3, -C(CH3)3, -CH2CH(CH3)2,
C(O)CH3, -CH2CH2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), ciclopentilo, piridinilo o metilpiperidinilo;
R8 es H, -CH3 o -CH2CH3;
o R7 y R* junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo y pirrolidinilo, en donde dicho anillo heterocíclico es sustituido con cero a 1 R7b y cero a 2 R7c;
R7b es:
(i) -CH3, -CH(CH3)2, -C(CH3)2OH, -CH2CH2CH2C=CH, -CH2CH2NH(CH3), -CH2CH2N(CH3)2, -NRxRx, -NHCH2CH2NH(CH3), -NHCH2CH2N(CH3)2, -N(CH3)CH2CH2NH2, -NRxCH2CH2CH2N(CH3)2, -OCH2CH2N(CH3)2, -CH2(fenilo), -CH2(metil pirazolilo), -CH2CH2(pirrolidinilo), -NH(metilpiperidinilo), -NH(isopropilpiperidinilo), -NH(pentametilpiperidinilo), -NH(acetilpiperidinilo), -NHCH2CH2(morfolinilo), -O(piperidinilo), -O(metilpiperidinilo), -O(etilpiperidinilo), -O(isopropilpiperidinilo) o -O(piperidinil)-(tetrametilpiperidinilo); o (ii) azepanilo, diazepanilo, morfolinilo, piperazinilo, piperidinilo, piridinilo, pirrolidinonilo, pirrolidinilo o tetrahidroisoquinolinilo, cada uno sustituido con cero a 1 R8ay cero a 3 R8b;
cada R7c es independientemente -CH3 o -CH2CN;
R8a es -OH, -CH3, -CH2CH3, -CH(CH3)2, -C(CH3)3, -CH2CH(CH3)2, -CH2CH2OCH3, -CH2CH2CF3, -C(O)CH3, -CH2(ciclopropilo), -CH2(metil fenilo), -(CH2)2-3(pirrolidinilo), -CH2(metilpirazolilo), -CH2(tiofenilo), -NRxRx, ciclopentilo, metilpiperidinilo o piridinilo;
cada R8b es -CH3;
cada Rx es independientemente H o -CH3;
n es cero o 1; y
p es cero, 1, 2, o 3.
5. El compuesto de acuerdo con la reivindicación 1, N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde R7 es -CH2R7a, -C(O)(CH2)1-3NH2, -C(O)CH(NH2)(alquilo C1-4), -C(O)CH(NH2)(CH2)1-2C(O)OH, -C(O)CH(NH2)(CH2)2-4NH2, -C(O)CH(NH2)(CH2)1-3C(O)NH2, -C(O)CH(NH2)R7a, -C(O)R7a o R7a.
6. El compuesto de acuerdo con la reivindicación 1, N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde R7 es cicloalquilo C3-6 sustituido con un sustituyente seleccionado de -NRx(CH2)2-3NRyRy, -NRx(metilpiperidinilo), -NRx(CH2)2-3(morfolinilo), dimetilamino piperidinilo, y piperazinilo sustituido con un sustituyente seleccionado de alquilo C1-4, -C(O)CH3, -(CH2)1-2OCH3, -CH2(metilfenilo), -(CH2)2-3(pirrolidinilo), cicloalquilo C3-6, piridinilo y metilpiperidinilo.
7. El compuesto de acuerdo con la reivindicación 1, N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde R7 y R8 junto con el átomo de nitrógeno al cual están unidos forman un anillo heterocíclico seleccionado de azetidinilo, diazepanonilo, diazepanilo, diazaespiro[3.5]nonanilo, diazaespiro[5,5]undecanilo, imidazolilo, imidazolidinonilo, octahidro-1H-pirrolo[3,4-b]piridinilo, piperazinilo, piperidinilo, pirrolidinonilo, pirrolidinilo y pirrolilo, en donde el anillo heterocíclico está sustituido con cero a 1 R7b y cero a 2 R7c.
8. El compuesto de acuerdo con la reivindicación 1, N-óxido, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde dicho compuesto es: (R)-N-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)pirrolidin-3-carboxamida (9); (S)-N-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)pirrolidin-3-carboxamida (10); 2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)acetamida (11); 4-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)butanamida (12); N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pirrolidin-3-carboxamida (13); (R)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pentanamida (14); N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)morfolin-2-carboxamida (15); (R)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-metilpentanamida (16); (2R,3R)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-3-metilpentanamida (17); (S)-2-amino-N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)succinamida (18); (R)-2-amino-N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)succinamida (19); (S)-2,5-diamino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pentanamida (20); (1R,2S)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)ciclohexano-1-carboxamida (21); (R)-2-amino-N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)pentandiamida (22); (S)-2,6-diamino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)hexanamida (23); ácido (S)-4-amino-5-((2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)amino)-5-oxopentanoico (24); (S)-2-amino-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-2-fenilacetamida (25); (S)-2-amino-2-ciclohexil-N-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)acetamida (26); 2-(3,4-dimetoxifenil)-N,3-dietil-N-(1'-metil-1,4'-bipiperidin-4-il)-1H-indol-5-amina (28); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-(metilamino)etil)ciclohexano-1,4-diamina (30-31); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-(dimetilamino)etil)ciclohexano-1,4-diamina (32-33); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-metilpiperazin-1-il)ciclohexil)-1H-indol-5-amina (34); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-(dimetilamino)etil)-N4-metilciclohexano-1,4-diamina (35); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(3-(dimetilamino)propil)ciclohexano-1,4-diamina (36-37); 2-(3,4-dimetoxifenil)-N-(4-(4-etilpiperazin-1-il)ciclohexil)-3-isopropil-1H-indol-5-amina (38-39); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(1-metilpiperidin-4-il)ciclohexano-1,4-diamina (40-41); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(3(dimetilamino)propil)-N4-metilcidohexano-1,4-diamina (42-43); 1-(4-(4-((2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)amino)cidohexil)piperazin-1-il)etan-1-ona (44-45); 2-(3,4-dimetoxifenil)-N-(4-(4-(dimetilaiT iino)pipendin-1-il)cidohexil)-3-isopropil-1H-indol-5-amina (46); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(2-morfolinoetil)cidohexano-1,4-diamina (47-48); N-(4-(4-(terc-butil)piperazin-1-il)ciclohexil)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-amina (49-50); 2-(3,4-dimetoxifenil)-N-(4-(4-isobutilpiperazin-1-il)ciclohexil)-3-isopropil-1H-indol-5-amina (51-53); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(2-metoxietil)piperazin-1-il)cidohexil)-1H-indol-5-amina (54); N1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N4-(3-morfolinopropil)cidohexano-1,4-diamina (55-56); N-(4-(4-cidopentilpiperazin-1-il)cidohexil)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-amina (57-58); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(piridin-4-il)piperazin-1-il)cidohexil)-1H-indol-5-amina (59-60); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(l-metilpiperidin-4-il)piperazin-1-il)cidohexil)-1H-indol-5-amina (61-62); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(2-(pirrolidin-1-il)etil)piperazin-1-il)cidohexil)-1H-indol-5-amina (63-64); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(4-metilbencil)piperazin-1-il)cidohexil)-1H-indol-5-amina (65-66); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(4-(3-(pirrolidin-1-il)propil)piperazin-1-il)cidohexil)-lH-indol-5-amina (67); 2-(3,4-dimetoxifenil)-3-isopropil-N-(1,2,2,6,6-pentametilpiperidin-4-il)-1H-indol-5-amina (103); 2-(3,4-dimetoxifeml)-3-isopropil-N-metil-N-((1-iT ietilpirrolidin-2-il)metil)-1H-indol-5-amina (104); 2-(3,4-dimetoxifenil)-N-(4-(2-(etilamino)etoxi)fenil)-3-isopropil-1H-indol-5-amina (105); 2-(3,4-dimetoxifenil)-3-isopropil-N-(4-(2-(pirrolidin-1-il)etoxi)fenil)-1H-indol-5-amina (106); 2-(3,4-dimetoxifenil)-3-etil-N-((7-isopropil-7-azaespiro[3.5]nonan-2-il)metil)-1H-indol-5-amina (124); o 2-(3,4-dimetoxifenil)-3-etil-N-(1'-metil-[1,4'-bipiperidin]-4-il)-1H-indol-5-amina (125).
9. El compuesto de acuerdo con la reivindicación 1, N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, en donde dicho compuesto es: 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)-3-((2-(metilamino)etil)amino)pirrolidin-2-ona (1); 3-((2-aminoetil)(metil)amino)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (2); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-3-(dimetilamino)pirrolidin-2-ona (3 4); 1-(2-(2,6-dimetilpiridin-4-il)-3-isopropil-1H-indol-5-il)-3-(4-isopropilpiperazin-1-il)pirrolidin-2-ona (5-6); 3-(2-(dimetilamino)etoxi)-1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)pirrolidin-2-ona (7); 1-(3-isopropil-2-(2-metilpiridin-4-il)-1H-indol-5-il)imidazolidin-2-ona (8); 1-(3-isopropil-2-(1H-pirazolo[3,4-b]piridin-4-il)-1H-indol-5-il)imidazolidin-2-ona (27); 5-(3-(1,4-diazepan-1-il)azetidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (29); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(2,2,6,6-tetrametil-1l2-piperidin-4-il)piperazin-1-il)-1H-indol (68); 2-(3,4-dimetoxifenil)-3-etil-6-isopropil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol (69); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(pirrolidin-1-il)piperidin-1-il)-1H-indol (70); 2-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N,N-dimetiletan-1-amina (71); N1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N2-metiletan-1,2-diamina (72); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(piperazin-1-il)piperidin-1-il)-1H-indol (73); 4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)morfolina (74); N1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N2,N2-dimetiletan-1,2-diamina (75); N1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N3,N3-dimetilpropan-1,3-diamina (76-77); 2-(3,4-dimetoxifenil)-5-(4-(4-etilpiperazin-1-il)piperidin-1-il)-3-isopropil-1H-indol (78); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N-(1-metilpiperidin-4-il)piperidin-4-amina (79); 4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-2,6-dimetilmorfolina (80); N1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-N1,N3,N3-trimetilpropan-1,3-diamina (81); 1-(4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)piperazin-1-il)etan-1-ona (82); 1'-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N,N-dimetil-[1,4'-bipiperidin]-4-amina (83); 2-(3,4-dimetoxifenil)-5-(4-(4-etil-1,4-diazepan-1-il)piperidin-1-il)-3-isopropil-1H-indol (84); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-isopropilpiperazin-1-il)piperidin-1-il)-1H-indol (85); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N-(2-morfolinoetil)piperidin-4-amina (86); 5-(4-(4-(ciclopropilmetil)piperazin-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (87); 1-(4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-1,4-diazepan-1-il)etan-1-ona (88); 1-(4-((1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)amino)piperidin-1-il)etan-1-ona (89); 5-(4-(4-(terc-butil)piperazin-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (90); 2-(3,4-dimetoxifenil)-5-(4-(4-isobutilpiperazin-1-il)piperidin-1-il)-3-isopropil-1H-indol (91); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(2-metoxietil)piperazin-1-il)piperidin-1-il)-1H-indol (92); 5-(4-(4-ciclopentilpiperazin-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (93); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(piridin-4-il)piperazin-1-ií)piperidin-1-il)-1H-indol (94); N-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-1,2,2,6,6-pentametilpiperidin-4-amina (95); 2-(3,4-dimetoxifenil)-3-isopropil-5-(1'-((1-metil-1H-pirrol-2-il)metil)-[4,4'-bipiperidin]-1-il)-1H-indol (96); 2-(3,4-dimetoxifenil)-3-isopropil-5-(1'-(3,3,3-trifluoropropil)-[4,4'-bipiperidin]-1-il)-1H-indol (97); 2-(3,4-dimetoxifenil)-3-isopropil-5-(1'-(tiofen-3-ilmetil)-[4,4'-bipiperidin]-1-il)-1H-indol (98); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(1-metilpiperidin-4-il)piperazin-1-il)piperidin-1-il)-1H-indol (99); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(2-(pirrolidin-1-il)etil)piperazin-1-il)piperidin-1-il)-1H-indol (100); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(4-metilbencil)piperazin-1-il)piperidin-1-il)-1H-indol (101); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-(3-(pirrolidin-1-il)propil)piperazin-1-il)piperidin-1-il)-1H-indol (102); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-(2-(dimetilamino)etil)-1,4-diazepan-5-ona (107); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N,N-dimetilpiperidin-4-amina (108); 2-(4-amino-1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)acetonitrilo (109); 2-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)propan-2-ol (110); 3-cloro-5-(5-(4-(dimetilamino)piperidin-1-il)-3-isopropil-1H-indol-2-il)-1,4-dimetil-1l4,2l5-piridin-2-ona (111); 2-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-(metilamino)piperidin-4-il)acetonitrilo (112); 2-(3,4-dimetoxifenil)-3-isopropil-5-(2-(piridin-4-il)piperidin-1-il)-1H-indol (113); 2-((1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)oxi)-N,N-dimetiletan-1-amina (114); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(2-(pirrolidin-1-il)etil)piperidin-1-il)-1H-indol (115); 1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-4-hidroxipirrolidin-2-ona (116); 4-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-4-metilpiperidin-4-il)morfolina (117); 6-bencil-1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)octahidro-1H-pirrolo[3,4-b]piridina (118); 1-(1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperidin-4-il)-2-metil-1,2,3,4-tetrahidroisoquinolina
(119); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N,N-dimetilpirrolidin-3-amina (120); 5-(4-(1,4-diazepan-1-il)piperidin-1-il)-2-(3,4-dimetoxifenil)-3-isopropil-1H-indol (121); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(1-isopropilazepan-4-il)piperazin-1-il)-1H-indol (122); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-metil-1,4-diazepan-1-il)piperidin-1-il)-1H-indol (123); 2-(3,4-dimetoxifenil)-3-isopropil-5-(piperazin-1-il)-1H-indol, sal TFA (126); 2-(4-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)piperazin-1-il)-N-metiletanamina (127); 4-(3-isopropil-5-(piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (128); 2-(2,6-dimetoxipiridin-4-il)-3-etil-5-(piperazin-1-il)-1H-indol (129); 4-(3-isopropil-6-metil-5-(piperazin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (13o); 5-([4,4'-bipiperidin]-1-il)-2-(3,4-dimetoxifenil)-3-etil-1H-indol (131); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(piperidin-4-iloxi)piperidin-1-il)-1H-indol (132); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(piperidin-4-iloxi)piperidin-1-il)-1H-indol (133); 2-(3,4-dimetoxifenil)-3-etil-5-(4-((1-metilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol (134); 6-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)octahidro-1H-pirrolo[3,4-b]piridina (135); 2-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-2,6-diazaespiro[3.5]nonane (136); 2-(4-(3-etil-2-(2-metoxipiridin-4-il)-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (137); 2-(4-(3-isopropil-2-(1H-pirrolo[2,3-b]piridin-4-il)-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (138); 3-etil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (139); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (140); 4-(3-metil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (141); 3-etil-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (142); 3-etil-2-(2-metoxipiridin-4-il)-5-(4-(1-metilpipendin-4-il)piperazin-1-il)-1H-indol (143); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-6-metil-1H-indol-5-il)piperazin-1-il)-N-metiletan-1-amina (144); 4-(5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (145); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(pent-4-in-1-il)piperazin-1-il)-1H-indol (146); 3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (147); 3-etil-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-2-(2-metoxipindin-4-il)-1H-indol (148); 2-(3,4-dimetoxifenil)-3-metil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (149); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)-3,3-dimetilpiperazin-1-il)-N-metiletan-1-amina (150); 4-(5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (151); 3-etil-5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-2- (2-metilpiridin-4-il)-1H-indol (152); 3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-2-(2-metoxipiridin-4-il)-1H-indol (153); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (154); 2-(3,4-dimetoxifenil)-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol (155); 2-(2,6-dimetoxipiridin-4-il)-3-etil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (156); 4-(3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (157); 4-(5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (158); 4-(3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (159); 3-etil-5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-2-(2-metoxipiridin-4-il)-1H-indol (160); 3-etil-2-(2-metoxipiridin-4-il)-5-(4-(2,2,6,6-tetrametilpiperidin-4-il)piperazin-1-il)-1H-indol (161); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(1-metilpiperidin-4-il)piperazin-1-il)-1H-indol (162); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-etilpiperidin-4-il)piperazin-1-il)-1H-indol (163); 2-(3,4-dimetoxifenil)-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-3-metil-1H-indol (164); 4-(3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1-metil-1H-pirrolo[2,3-b]piridina (165); 4-(3-isopropil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirrolo[2,3-b]piridina (166); 4-(3-isopropil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (167-168); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol (169); 2-(3,4-dimetoxifenil)-5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-3- metil-1H-indol (170); 2-(3,4-dimetoxifenil)-3-metil-5-(4-(2,2,6,6-tetrametilpiperidin-4-il)piperazin-1-il)-1H-indol (171); 2-(3,4-dimetoxifenil)-5-(2,2-dimetil-4-(1-metilpiperidin-4-il)piperazin-1-il)-3-etil-1H-indol (172); 2-(2,6-dimetoxipiridin-4-il)-3-etil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-1H-indol (173-174); 4-(3-isopropil-5-(4-(1-isopropilpiperidin-4-il)piperazin-1-il)-6-metil-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (175); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(2,2,6,6-tetrametilpiperidin-4-il)piperazin-1-il)-1H-indol (176); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-isobutilpiperidin-4-il)piperazin-1-il)-1H-indol (177); 2-(4-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)-1,4-diazepan-1-il)-N-metiletan-1-amina (178); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1-metilpiperidin-4-il)-1,4-diazepan-1-il)-1H-indol (179); 2-(3,4-dimetoxifenil)-3-etil-5-(4-(1 -isopropilpiperidin-4-il)-1,4-diazepan-1-il)-1H-indol (180); 3-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)-9-metil-3,9-diazaespiro[5,5]undecano (181); 3-etil-5-(4-((1-isopropilpiperidin-4-il)oxi)piperidin-1-il)-2-(2-metilpiridin-4-il)-1H-indol (182); 3-(2-(3,4-dimetoxifenil)-3-etil-1H-indol-5-il)-9-isopropil-3,9-diazaespiro[5,5]undecano (183); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-(4-metilpiperazin-1-il)piperidin-1-il)-1H-indol (184); 4-(3-etil-5-(4-((1-isopropilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol-2-il)-1H-pirazolo[3,4-b]piridina (185); 3-(2-(3,4-dimetoxifenil)-3-etil-6-metil-1H-indol-5-il)-9-isopropil-3,9-diazaespiro[5,5]undecano (186); 2-(3,4-dimetoxifenil)-3-isopropil-5-(4-((1-metilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol (187); 2-(3,4-dimetoxifenil)-3-etil-5-(4-((1-etilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol (188); 3-((1-metil-1H-pirrol-2-il)metil)-9-(3-metil-2-(1H-pirrolo[2,3-b]piridin-4-il)-1H-indol-5-il)-3,9-diazaespiro[5,5]undecano (189); 2-(3,4-dimetoxifenil)-5-(4-((1-etilpiperidin-4-il)oxi)piperidin-1-il)-3-isopropil-1H-indol (190); 2-(3,4-dimetoxifenil)-3-etil-5-(4-((1-isopropilpiperidin-4-il)oxi)piperidin-1-il)-1H-indol (191); 1-(2-(3,4-dimetoxifenil)-3-isopropil-1H-indol-5-il)-N-(1-isopropilpiperidin-4-il)piperidin-4-amina (192); o 2-(3,4-dimetoxifenil)-3-etil-5-(4-((2',2',6',6'-tetrametil-[1,4'-bipiperidin]-4- il)oxi)piperidin-1-il)-1H-indol (193).
10. Una composición farmacéutica que comprende un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-9, N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo; y un vehículo farmacéuticamente aceptable.
11. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-9, N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable de los mismos, para uso en terapia.
12. El compuesto de acuerdo con una cualquiera de las reivindicaciones 1-9, N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo, para uso en terapia para tratar enfermedades autoinmunes
o enfermedades inflamatorias crónicas.
13. El compuesto, N-óxidos, estereoisómeros, tautómeros, solvatos o una sal farmacéuticamente aceptable del mismo para su uso de acuerdo con la reivindicación 12, en donde dichas enfermedad autoinmune o enfermedad inflamatoria crónica se seleccionan de lupus eritematoso sistémico (LES), artritis reumatoide, esclerosis múltiple (EM) y síndrome de Sjogren.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762608032P | 2017-12-20 | 2017-12-20 | |
| PCT/US2018/066344 WO2019126242A1 (en) | 2017-12-20 | 2018-12-19 | Amino indole compounds useful as tlr inhibitors |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2904676T3 true ES2904676T3 (es) | 2022-04-05 |
Family
ID=65019594
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18833773T Active ES2904676T3 (es) | 2017-12-20 | 2018-12-19 | Compuestos de amino indol útiles como inhibidores de TLR |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US11306092B2 (es) |
| EP (1) | EP3728218B1 (es) |
| JP (1) | JP7287967B2 (es) |
| KR (1) | KR102714788B1 (es) |
| CN (1) | CN111491929B (es) |
| AU (1) | AU2018390610A1 (es) |
| BR (1) | BR112020011984A2 (es) |
| CA (1) | CA3086431A1 (es) |
| EA (1) | EA202091480A1 (es) |
| ES (1) | ES2904676T3 (es) |
| IL (1) | IL275504A (es) |
| MX (1) | MX2020005513A (es) |
| SG (1) | SG11202005694RA (es) |
| WO (1) | WO2019126242A1 (es) |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10071079B2 (en) | 2016-06-29 | 2018-09-11 | Bristol-Myers Squibb Company | [1,2,4]triazolo[1,5-a]pyridinyl substituted indole compounds |
| EP3728218B1 (en) | 2017-12-20 | 2021-12-01 | Bristol-Myers Squibb Company | Amino indole compounds useful as tlr inhibitors |
| KR102730859B1 (ko) * | 2017-12-20 | 2024-11-15 | 브리스톨-마이어스 스큅 컴퍼니 | 아릴 및 헤테로아릴 치환된 인돌 화합물 |
| JP7328977B2 (ja) | 2018-02-12 | 2023-08-17 | エフ. ホフマン-ラ ロシュ アーゲー | ウイルス感染の処置および予防のための新規のスルホン化合物および誘導体 |
| EP3802539B1 (en) | 2018-06-05 | 2023-09-20 | F. Hoffmann-La Roche AG | Tetrahydro-1h-pyrazino[2,1-a]isoindolylquinoline compounds for the treatment of autoimmune disease |
| EP3807270B1 (en) | 2018-06-12 | 2023-09-13 | F. Hoffmann-La Roche AG | Novel heteroaryl heterocyclyl compounds for the treatment of autoimmune disease |
| CN112584903B (zh) | 2018-07-23 | 2025-12-23 | 豪夫迈·罗氏有限公司 | 用于自身免疫性疾病治疗的哌嗪化合物 |
| EP3847169A1 (en) | 2018-09-04 | 2021-07-14 | F. Hoffmann-La Roche AG | Benzothiazole compounds for the treatment of autoimmune diseases |
| EP3847173B1 (en) | 2018-09-06 | 2023-04-12 | F. Hoffmann-La Roche AG | Novel pyrazolopyridine compounds for the treatment of autoimmune disease |
| US11548884B2 (en) | 2018-09-06 | 2023-01-10 | Hoffmann-La Roche Inc. | Cyclic amidine compounds for the treatment of autoimmune disease |
| WO2021084022A1 (en) | 2019-10-31 | 2021-05-06 | F. Hoffmann-La Roche Ag | Hydropyrazino[1,2-d][1,4]diazepine compounds for the treatment of autoimmune disease |
| CN114728976B (zh) | 2019-11-19 | 2024-08-16 | 豪夫迈·罗氏有限公司 | 用于治疗自身免疫性疾病的氢-1H-吡咯并[1,2-a]吡嗪化合物 |
| WO2021099406A1 (en) | 2019-11-20 | 2021-05-27 | F. Hoffmann-La Roche Ag | Spiro(isobenzofuranazetidine) compounds for the treatment of autoimmune disease |
| US20240317735A1 (en) * | 2020-07-14 | 2024-09-26 | Hoffmann-La Roche Inc. | Hydroisoquinoline or hydronaphthyridine compounds for the treatment of autoimmune disease |
| CN116075510A (zh) | 2020-08-19 | 2023-05-05 | 百时美施贵宝公司 | 1H-苯并[d]咪唑衍生物作为TLR9抑制剂用于治疗纤维化 |
| AU2021328575A1 (en) | 2020-08-19 | 2023-03-16 | Bristol-Myers Squibb Company | Imidazo(1,2-a)pyridine and (1,2,4)triazolo(1,5-a)pyridine derivatives as TLR9 inhibitors for the treatment of fibrosis |
| WO2022040267A1 (en) | 2020-08-19 | 2022-02-24 | Bristol-Myers Squibb Company | 1h-pyrrolo[3,2-c]pyridine and 1h-pyrrolo[2,3-c]pyridine derivatives as tlr9 inhibitors for the treatment of fibrosis |
| CN116783202A (zh) * | 2021-02-09 | 2023-09-19 | 吉利德科学公司 | 噻吩并吡咯化合物 |
| CR20230478A (es) | 2021-04-16 | 2023-11-30 | Gilead Sciences Inc | Compuestos de tienopirrol. |
| DE102021207925A1 (de) | 2021-07-23 | 2023-01-26 | Continental Reifen Deutschland Gmbh | Verbindung, Verfahren zu deren Herstellung sowie Verwendung der Verbindung als Alterungsschutzmittel und/oder Ozonschutzmittel und/oder Farbstoff |
| DE102021207926A1 (de) | 2021-07-23 | 2023-01-26 | Continental Reifen Deutschland Gmbh | Verbindung, Verfahren zu deren Herstellung sowie Verwendung der Verbindung als Alterungsschutzmittel und/oder Ozonschutzmittel und/oder Farbstoff |
| KR20240056747A (ko) | 2021-09-10 | 2024-04-30 | 길리애드 사이언시즈, 인코포레이티드 | 티에노피롤 화합물 |
| CN114591339B (zh) * | 2022-05-10 | 2022-08-02 | 上海维申医药有限公司 | 一类Toll样受体抑制剂及其制备和应用 |
Family Cites Families (45)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6187777B1 (en) | 1998-02-06 | 2001-02-13 | Amgen Inc. | Compounds and methods which modulate feeding behavior and related diseases |
| WO2000035886A2 (en) | 1998-12-18 | 2000-06-22 | Axys Pharmaceuticals, Inc. | (hetero)aryl-bicyclic heteroaryl derivatives, their preparation and their use as protease inhibitors |
| HRP20020349A2 (en) | 1999-10-19 | 2004-02-29 | Merck & Co Inc | Tyrosine kinase inhibitors |
| AU2003235741B8 (en) | 2002-01-07 | 2009-01-15 | Eisai R&D Management Co., Ltd. | Deazapurines and uses thereof |
| BRPI0411514A (pt) | 2003-06-20 | 2006-08-01 | Coley Pharm Gmbh | antagonistas de receptor toll-like de molécula pequena |
| WO2006113458A1 (en) | 2005-04-15 | 2006-10-26 | Bristol-Myers Squibb Company | Heterocyclic inhibitors of protein arginine methyl transferases |
| CA2648652A1 (en) | 2006-04-04 | 2007-10-11 | Myriad Genetics, Inc. | Compounds for diseases and disorders |
| DE102006033109A1 (de) | 2006-07-18 | 2008-01-31 | Grünenthal GmbH | Substituierte Heteroaryl-Derivate |
| US8027888B2 (en) | 2006-08-31 | 2011-09-27 | Experian Interactive Innovation Center, Llc | Online credit card prescreen systems and methods |
| JP2010511018A (ja) | 2006-12-01 | 2010-04-08 | ガラパゴス・ナムローゼ・フェンノートシャップ | 変性疾患及び炎症性疾患の治療に有用なトリアゾロピリジン化合物 |
| WO2008152471A1 (en) | 2007-06-12 | 2008-12-18 | Coley Pharmaceutical Group, Inc. | Quinazoline derivative useful as toll-like receptor antagonist |
| WO2009030996A1 (en) | 2007-09-05 | 2009-03-12 | Coley Pharmaceutical Group, Inc. | Triazole compounds as toll-like receptor (tlr) agonists |
| EP2205085A1 (en) | 2007-09-25 | 2010-07-14 | Merck Sharp & Dohme Corp. | 2-aryl or heteroaryl indole derivatives |
| WO2010036905A1 (en) | 2008-09-26 | 2010-04-01 | Eisai R & D Management Co., Ltd. | Benzoxazole compounds and methods of use |
| US8785489B2 (en) | 2008-10-17 | 2014-07-22 | Boehringer Ingelheim International Gmbh | Heteroaryl substituted indole compounds useful as MMP-13 inhibitors |
| TWI462920B (zh) | 2009-06-26 | 2014-12-01 | 葛萊伯格有限公司 | 用於治療退化性及發炎疾病之新穎化合物 |
| JP5864417B2 (ja) | 2009-07-16 | 2016-02-17 | マリンクロッド エルエルシー | トール様受容体9のアンタゴニストとしての(+)−モルフィナンおよびその治療的使用 |
| RU2012116207A (ru) | 2009-09-24 | 2013-10-27 | Ф.Хоффманн-Ля Рош Аг | Производные индола в качестве модуляторов crac |
| MX2012004792A (es) * | 2009-10-22 | 2013-02-01 | Vertex Pharma | Composiciones para el tratamiento de fibrosis quistica y otras enfermedades cronicas. |
| WO2012054862A2 (en) | 2010-10-21 | 2012-04-26 | The Brigham And Women's Hospital, Inc. | Agents, compositions, and methods for treating pruritis and related skin conditions |
| CN103562201B (zh) | 2011-01-12 | 2016-10-19 | 帆德制药股份有限公司 | 作为toll样受体调节剂的取代的苯并氮杂卓 |
| DK2663550T3 (en) | 2011-01-12 | 2017-03-27 | Ventirx Pharmaceuticals Inc | SUBSTITUTED BENZOAZEPINS AS MODULATORS OF TOLL-LIKE RECEPTORS |
| KR102052215B1 (ko) | 2011-06-01 | 2019-12-04 | 야누스 바이오테라퓨틱스, 인크. | 신규한 면역 시스템 조절제 |
| WO2012167053A1 (en) | 2011-06-01 | 2012-12-06 | Janus Biotherapeutics, Inc. | Novel immune system modulators |
| KR101913619B1 (ko) | 2011-06-09 | 2018-12-28 | 리젠 파마슈티컬스 소시에떼 아노님 | Gpr-119의 조절제로서의 신규한 화합물 |
| KR101913135B1 (ko) | 2011-07-15 | 2018-10-30 | 얀센 파마슈티칼즈, 인코포레이티드 | 감마 세크레타제 조절 인자로서의 신규의 치환 인돌 유도체 |
| WO2013052550A2 (en) | 2011-10-04 | 2013-04-11 | Janus Biotherapeutics, Inc. | Novel imidazole quinoline-based immune system modulators |
| TWI619704B (zh) | 2012-05-18 | 2018-04-01 | 大日本住友製藥股份有限公司 | 羧酸化合物 |
| JO3407B1 (ar) | 2012-05-31 | 2019-10-20 | Eisai R&D Man Co Ltd | مركبات رباعي هيدرو بيرازولو بيريميدين |
| EP2738172A1 (en) | 2012-11-28 | 2014-06-04 | Almirall, S.A. | New bicyclic compounds as crac channel modulators |
| JP6223563B2 (ja) | 2013-10-14 | 2017-11-01 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | 選択的に置換されたキノリン化合物 |
| CN105992766A (zh) * | 2013-12-13 | 2016-10-05 | 武田药品工业株式会社 | 作为tlr抑制剂的吡咯并[3,2-c]吡啶衍生物 |
| HUE054672T2 (hu) | 2014-08-15 | 2021-09-28 | Chia Tai Tianqing Pharmaceutical Group Co Ltd | TLR7 agonistaként alkalmazott pirrolopirimidin vegyületek |
| EP3398948A3 (en) | 2014-08-22 | 2018-12-05 | Janus Biotherapeutics, Inc. | 2,4,6,7-tetrasubstituted pteridine compounds and methods of synthesis and use thereof |
| US10071079B2 (en) | 2016-06-29 | 2018-09-11 | Bristol-Myers Squibb Company | [1,2,4]triazolo[1,5-a]pyridinyl substituted indole compounds |
| BR112019001270A2 (pt) * | 2016-07-30 | 2019-04-30 | Bristol-Myers Squibb Company | compostos indol substituídos com dimetoxifenila como inibidores de tlr7, tlr8 ou tlr9 |
| JP7028861B2 (ja) * | 2016-09-09 | 2022-03-02 | ブリストル-マイヤーズ スクイブ カンパニー | ピリジル置換のインドール化合物 |
| JP7265554B2 (ja) | 2017-11-14 | 2023-04-26 | ブリストル-マイヤーズ スクイブ カンパニー | 置換インドール化合物 |
| EA202091484A1 (ru) | 2017-12-18 | 2021-03-25 | Бристол-Маерс Сквибб Компани | 4-азаиндольные соединения |
| WO2019126081A1 (en) | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Amide substituted indole compounds useful as tlr inhibitors |
| MX2020005462A (es) | 2017-12-19 | 2020-09-07 | Bristol Myers Squibb Co | Compuestos de indol sustituidos utiles como inhibidores de receptores tipo toll (tlr). |
| JP7304352B2 (ja) | 2017-12-19 | 2023-07-06 | ブリストル-マイヤーズ スクイブ カンパニー | 6-アザインドール化合物 |
| EP3728218B1 (en) | 2017-12-20 | 2021-12-01 | Bristol-Myers Squibb Company | Amino indole compounds useful as tlr inhibitors |
| SG11202005733QA (en) | 2017-12-20 | 2020-07-29 | Bristol Myers Squibb Co | Diazaindole compounds |
| KR102730859B1 (ko) | 2017-12-20 | 2024-11-15 | 브리스톨-마이어스 스큅 컴퍼니 | 아릴 및 헤테로아릴 치환된 인돌 화합물 |
-
2018
- 2018-12-19 EP EP18833773.7A patent/EP3728218B1/en active Active
- 2018-12-19 SG SG11202005694RA patent/SG11202005694RA/en unknown
- 2018-12-19 CA CA3086431A patent/CA3086431A1/en active Pending
- 2018-12-19 MX MX2020005513A patent/MX2020005513A/es unknown
- 2018-12-19 KR KR1020207020526A patent/KR102714788B1/ko active Active
- 2018-12-19 EA EA202091480A patent/EA202091480A1/ru unknown
- 2018-12-19 CN CN201880081662.2A patent/CN111491929B/zh active Active
- 2018-12-19 US US16/955,166 patent/US11306092B2/en active Active
- 2018-12-19 AU AU2018390610A patent/AU2018390610A1/en not_active Abandoned
- 2018-12-19 WO PCT/US2018/066344 patent/WO2019126242A1/en not_active Ceased
- 2018-12-19 BR BR112020011984-9A patent/BR112020011984A2/pt not_active Application Discontinuation
- 2018-12-19 JP JP2020534859A patent/JP7287967B2/ja active Active
- 2018-12-19 ES ES18833773T patent/ES2904676T3/es active Active
-
2020
- 2020-06-18 IL IL275504A patent/IL275504A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP7287967B2 (ja) | 2023-06-06 |
| EP3728218A1 (en) | 2020-10-28 |
| EP3728218B1 (en) | 2021-12-01 |
| KR20200101399A (ko) | 2020-08-27 |
| CN111491929B (zh) | 2023-11-28 |
| US20200339581A1 (en) | 2020-10-29 |
| AU2018390610A1 (en) | 2020-08-06 |
| KR102714788B1 (ko) | 2024-10-08 |
| JP2021507918A (ja) | 2021-02-25 |
| MX2020005513A (es) | 2020-09-03 |
| IL275504A (en) | 2020-08-31 |
| BR112020011984A2 (pt) | 2020-11-17 |
| SG11202005694RA (en) | 2020-07-29 |
| EA202091480A1 (ru) | 2020-11-06 |
| CA3086431A1 (en) | 2019-06-27 |
| US11306092B2 (en) | 2022-04-19 |
| WO2019126242A1 (en) | 2019-06-27 |
| CN111491929A (zh) | 2020-08-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2904676T3 (es) | Compuestos de amino indol útiles como inhibidores de TLR | |
| ES2922174T3 (es) | Compuestos de indol sustituidos con amida útiles como inhibidores de TLR | |
| ES2927960T3 (es) | Compuestos de indol éter sustituidos | |
| ES2977657T3 (es) | Compuestos de 6-azaindol | |
| ES2965182T3 (es) | Compuestos de indol sustituidos con arilo y heteroarilo | |
| ES2921020T3 (es) | Compuestos de indol sustituidos con [1,2,4]triazolo[4,3-a]piridinilo | |
| ES2932361T3 (es) | Compuestos de indol sustituidos útiles como inhibidores de TLR | |
| ES2886964T3 (es) | Compuestos de indol sustituidos con [1,2,4]triazolo[1,5-a]piridinilo | |
| ES2960411T3 (es) | Compuestos de 4-azaindol | |
| ES2863474T3 (es) | Compuestos de indol sustituidos con dimetoxifenilo como inhibidores de TLR7, TLR8 o TLR9 | |
| ES2902504T3 (es) | Compuestos de indol sustituidos con piridilo | |
| ES2904773T3 (es) | Compuestos de diazaindol | |
| ES2965164T3 (es) | Compuestos de carbazol sustituidos | |
| KR102911861B1 (ko) | 치환된 인돌 이량체 화합물 | |
| BR112018077119B1 (pt) | COMPOSTOS INDÓIS SUBSTITUÍDOS COM [1,2,4]TRIAZOL[1,5-a]PIRIDINILA, USO DOS MESMOS, E COMPOSIÇÃO FARMACÊUTICA |