ES2906754T3 - Uso de laminina 2 para el diagnóstico de carcinoma hepatocelular y cáncer de páncreas - Google Patents
Uso de laminina 2 para el diagnóstico de carcinoma hepatocelular y cáncer de páncreas Download PDFInfo
- Publication number
- ES2906754T3 ES2906754T3 ES19219313T ES19219313T ES2906754T3 ES 2906754 T3 ES2906754 T3 ES 2906754T3 ES 19219313 T ES19219313 T ES 19219313T ES 19219313 T ES19219313 T ES 19219313T ES 2906754 T3 ES2906754 T3 ES 2906754T3
- Authority
- ES
- Spain
- Prior art keywords
- monomer
- laminin gamma
- cea
- laminin
- pancreatic cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54313—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals the carrier being characterised by its particulate form
- G01N33/54326—Magnetic particles
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57525—Immunoassay; Biospecific binding assay; Materials therefor for cancer of the liver or pancreas
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/577—Immunoassay; Biospecific binding assay; Materials therefor involving monoclonal antibodies binding reaction mechanisms characterised by the use of monoclonal antibodies
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/78—Connective tissue peptides, e.g. collagen, elastin, laminin, fibronectin, vitronectin, cold insoluble globulin [CIG]
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/50—Determining the risk of developing a disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/56—Staging of a disease; Further complications associated with the disease
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Food Science & Technology (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Biotechnology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Microbiology (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Gastroenterology & Hepatology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
Un método para diagnosticar cáncer de páncreas en un sujeto con necesidad de ello, que comprende: (a) determinar los niveles de monómero de laminina gamma 2, antígeno carcinoembrionario (CEA) y antígeno carbohidrato 19-9 (CA19-9) en una muestra biológica obtenida del sujeto; (b) comparar los niveles de monómero de laminina gamma 2, CEA y CA19-9 con los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9, respectivamente; y (c) identificar que el sujeto tiene cáncer de páncreas cuando los niveles de monómero de laminina gamma 2, CEA y CA19-9 son mayores que los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9, respectivamente.
Description
DESCRIPCIÓN
Uso de laminina 2 para el diagnóstico de carcinoma hepatocelular y cáncer de páncreas
CAMPO TÉCNICO
Esta invención se refiere a métodos para determinar un diagnóstico de cáncer de páncreas en un paciente mediante la detección de biomarcadores en el paciente, así como para determinar las cantidades del mismo. Los biomarcadores se usan para identificar a un paciente con cáncer de páncreas, así como determinar un diagnóstico. ANTECEDENTES DE LA TÉCNICA
El cáncer es una enfermedad que se produce de muchas formas, por ejemplo, carcinoma hepatocelular y cáncer de páncreas.
El cáncer de páncreas es una de las principales causas de muerte por cáncer porque es difícil de detectar en las primeras etapas y se propaga rápidamente. Por consiguiente, la detección del cáncer de páncreas típicamente no se produce hasta que aparecen los síntomas en las etapas avanzadas del cáncer.
Katayama et al (2005) Cancer Letters 225(1): 167-176 se refiere a aumentos en el nivel circulante del fragmento de la cadena y2 de laminina en pacientes con adenocarcinomas de células ductales pancreáticas metastásicos. Chan et al (2014) Clinical Cancer Research 20(22): 5787-5795 se refiere a la validación de biomarcadores que complementan CA19.9 en la detección temprana del cáncer de páncreas. La US 2015/072349 se refiere a un método para evaluar una probabilidad de que un sujeto tenga un cáncer, diagnosticar un cáncer y/o monitorizar la progresión del cáncer que comprende medir una cantidad de un biomarcador y comparar la cantidad medida con un control.
Por consiguiente, hay una necesidad en la técnica para la identificación de métodos que proporcionen una detección más temprana y/o más precisa del cáncer pancreático.
SUMARIO DE LA INVENCIÓN
La invención se define en las reivindicaciones adjuntas.
La presente invención está dirigida a un método para diagnosticar cáncer de páncreas en un sujeto con necesidad de ello, el método comprendiendo: (a) determinar los niveles de monómero de laminina gamma 2, antígeno carcinoembrionario (CEA) y antígeno carbohidrato 19-9 (CA19- 9) en una muestra biológica obtenida del sujeto; (b) comparar los niveles de monómero de laminina gamma 2, CEA y CA19-9 con los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9, respectivamente; y (c) identificar al sujeto con cáncer de páncreas cuando los niveles de monómero de laminina gamma 2, CEA y CA19-9 son mayores que los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9, respectivamente.
En otro aspecto, la presente invención está dirigida a un kit para detectar cáncer de páncreas en un sujeto con necesidad de ello, el kit comprendiendo: (a) uno o más anticuerpos que se unen cada uno específicamente al monómero de laminina gamma 2; (b) uno o más anticuerpos que se unen cada uno específicamente a CEA; y (c) uno o más anticuerpos que se unen cada uno específicamente a CA19-9, en donde cada uno de (a), (b) y (c) se proporcionan en recipientes separados.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
La FIG. 1 muestra gráficos que representan la concentración de monómero de laminina gamma 2 (pg/ml) frente a unidades de luz relativas (RLU). Específicamente, cada gráfico representa una curva de calibración representativa para el inmunoensayo descrito en el Ejemplo 2. Para el gráfico de la izquierda, la concentración de monómero de laminina gamma 2 fue de 0 pg/ml a 20.000 pg/ml. Para el gráfico de la derecha, la concentración de monómero de laminina gamma 2 fue de 0 pg/ml a 100 pg/ml. Cada curva de calibración se deriva de tres réplicas.
La FIG. 2 A muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua representa la concentración sérica media (pg/ml) de monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa la media más 2 desviaciones estándar (media 2SD) para el grupo de sujetos donantes sanos, que fue de 81,3 pg/ml.
La FIG. 2B muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua representa la concentración sérica media (pg/ml) de
monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa la media más 2 desviaciones estándar (media 2SD) para el grupo de sujetos donantes sanos, que era de 79,5 pg/ml. Las flechas identifican los sujetos para las concentraciones de AFP y CA19-9 especificadas.
La FIG. 2C muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua representa la concentración sérica media (pg/ml) de monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa el valor de corte derivado del análisis ROC, que fue de 75,9 pg/ml.
La FIG. 2D muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua representa la concentración sérica media (pg/ml) de monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa el valor de corte derivado del análisis ROC, que fue de 75,9 pg/ml. Las flechas identifican los sujetos para las concentraciones de AFP y CA19-9 especificadas.
La FIG. 3A muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Las designaciones "I", "II", "III" y "IV" representan los grupos de sujetos que tienen HCC en etapa I, HCC en etapa II, HCC en etapa III y HCC en etapa IV, respectivamente. "LC" representa cirrosis hepática y "CH" representa hepatitis. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua representa la concentración sérica media (pg/ml) de monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa la media más 2 desviaciones estándar (media 2SD) para el grupo de sujetos donantes sanos, que fue de 79,5 pg/ml. Las flechas identifican a los sujetos para las concentraciones de AFP especificadas.
La FIG. 3B muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Las designaciones "I", "II", "III" y "IV" representan los grupos de sujetos que tienen HCC en etapa I, HCC en etapa II, HCC en etapa III y HCC en etapa IV, respectivamente. "LC" representa cirrosis hepática y "CH" representa hepatitis. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua representa la concentración sérica media (pg/ml) de monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa el valor de corte derivado del análisis ROC, que fue de 75,9 pg/ml. Las flechas identifican a los sujetos para las concentraciones de AFP especificadas.
La FIG. 4A muestra un gráfico de características operativas del receptor (ROC) para los marcadores monómero de laminina gamma 2 (Ln-Y2), PIVKA-II y AFP, en el que los sujetos que tienen HCC se compararon con cirrosis hepática (LC), hepatitis (CH) y sujetos donantes sanos.
La FIG. 4B muestra un gráfico de características operativas del receptor (ROC) para los marcadores monómero de laminina gamma 2 (Ln-Y2), PIVKA-II y AFP, en el que los sujetos que tienen HCC se compararon con sujetos donantes sanos.
La FIG. 4C muestra un gráfico de características operativas del receptor (ROC) para los marcadores monómero de laminina gamma 2 (Ln-Y2), PIVKA-II y AFP, en el que los sujetos que tienen HCC se compararon con hepatitis hepática (CH).
La FIG. 5A muestra un diagrama de Venn de sujetos que tienen HCC y niveles elevados de monómero de laminina gamma 2 (Ln-Y2), AFP y/o PIVKA-II en comparación con el valor de corte (79,5 pg/ml, media del grupo de donantes sanos 2SD). Cada valor de porcentaje representa el porcentaje de sujetos con HCC que tenían un nivel elevado del marcador indicado en comparación con cada valor de corte.
La FIG. 5B muestra un diagrama de Venn de sujetos que tienen HCC y niveles elevados de monómero de laminina gamma 2 (Ln-Y2), AFP y/o PIVKA-II en comparación con el valor de corte (75,9 pg/ml, derivado del análisis ROC). Cada valor de porcentaje representa el porcentaje de sujetos con HCC que tenían un nivel elevado del marcador indicado en comparación con cada valor de corte.
La FIG. 5C muestra un diagrama de Venn de sujetos que tienen HCC y niveles elevados de monómero de laminina gamma 2 (Ln-Y2), AFP y/o PIVKA-II en comparación con el valor de corte (116,6 pg/ml, el valor de corte óptimo para distinguir el HCC de enfermedad hepática crónica no maligna). Cada valor de porcentaje representa el porcentaje de sujetos con HCC que tenían un nivel elevado del marcador indicado en comparación con cada valor de corte.
La FIG. 6A muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Las designaciones "III" y "IV" representan los grupos de sujetos que tienen cáncer de páncreas en etapa III y cáncer de páncreas en etapa IV, respectivamente. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua representa la concentración sérica media (pg/ml) de monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa la media más 2 desviaciones estándar (media 2SD) para el grupo de sujetos donantes sanos, que fue de 79,5 pg/ml.
La FIG. 6B muestra un gráfico que representa el grupo de sujetos frente a la concentración sérica (pg/ml) de monómero de laminina gamma 2. Las designaciones "III" y "IV" representan los grupos de sujetos que tienen cáncer de páncreas en etapa III y cáncer de páncreas en etapa IV, respectivamente. Para cada grupo de sujetos, el número entre paréntesis representa el número de sujetos en el grupo y la línea continua
representa la concentración sérica media (pg/ml) de monómero de laminina gamma 2 para el grupo. La línea continua que se extiende a lo largo del eje x representa el valor de corte derivado del análisis ROC, que fue de 75,9 pg/ml.
La FIG. 7 muestra un gráfico de características operativas del receptor (ROC) para los marcadores monómero de laminina gamma 2 (Ln-Y2), CEA y CA19-9, en el que los sujetos que tienen cáncer de páncreas se compararon con los sujetos que tenían pancreatitis y sujetos donantes sanos.
La FIG. 8 muestra un diagrama de Venn de sujetos que tienen cáncer de páncreas y niveles elevados de monómero de laminina gamma 2 (Ln-Y2), CEA y/o CA19-9 en comparación con el valor de corte. Cada valor porcentual representa el porcentaje de sujetos con cáncer de páncreas que tenían un nivel elevado del marcador indicado en comparación con cada valor de corte.
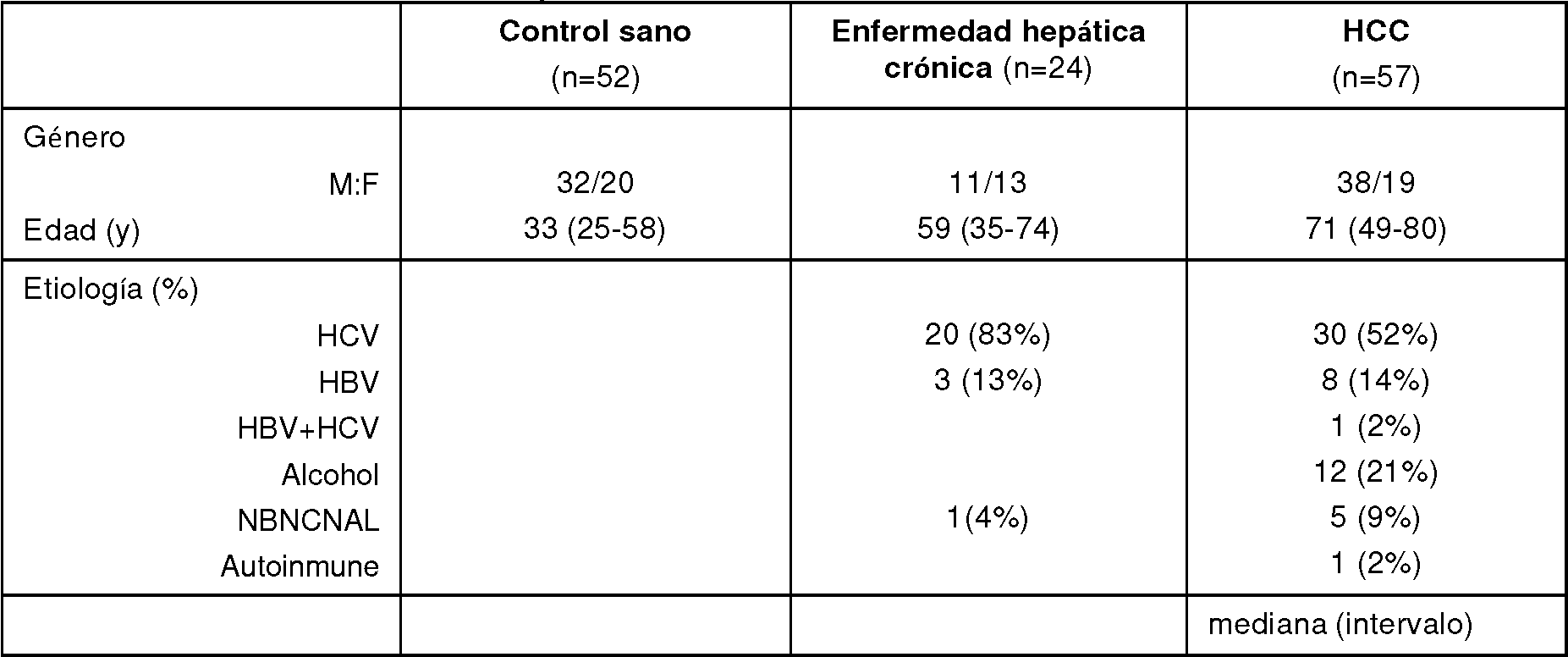
La FIG. 9 muestra un diagrama de dispersión de las concentraciones séricas de Ln-Y2 determinadas en muestras de suero de sujetos normales (Control) (n = 52), pacientes con enfermedad hepática crónica (CLD) (n = 24) y pacientes con HCC (n = 57) Las líneas horizontales representan concentraciones medias. Abreviaturas: Ln-Y2, laminina y2.
La FIG. 10 muestra un diagrama de dispersión de las concentraciones de AFP en suero determinadas en muestras de suero de sujetos normales (Control) (n = 52), pacientes con enfermedad hepática crónica (n = 24) y pacientes con HCC (n = 57). Abreviaturas: CLD, enfermedad hepática crónica; HCC, carcinoma hepatocelular; AFP, alfa-fetoproteína; PIVKA-II, protrombina inducida por la ausencia II de vitamina K; SE, error estándar.
La FIG. 11 muestra un diagrama de dispersión de las concentraciones séricas de PIVKA-II determinadas en muestras de suero de sujetos normales (Control) (n = 52), pacientes con enfermedad hepática crónica (n = 24) y pacientes con HCC (n = 57). Las líneas horizontales representan concentraciones medias. Abreviaturas: CLD, enfermedad hepática crónica; HCC, carcinoma hepatocelular; AFP, alfafetoproteína; PIVKA-II, protrombina inducida por la ausencia II de vitamina K; SE, error estándar.
La FIG. 12 muestra los valores de Ln-Y2 de acuerdo con la estadificación tumoral basada en la clasificación TNM. Las líneas horizontales representan concentraciones medias. Abreviaturas: CLD, enfermedad hepática crónica.
La FIG. 13 muestra los valores de AFP de acuerdo con la estadificación tumoral basada en la clasificación TNM. Las líneas horizontales representan concentraciones medias. Abreviaturas: CLD, enfermedad hepática crónica.
La FIG. 14 muestra los valores de PIVKA-II de acuerdo con la estadificación tumoral basada en la clasificación TNM. Las líneas horizontales representan concentraciones medias. Abreviaturas: CLD, enfermedad hepática crónica.
DESCRIPCIÓN DETALLADA
La presente divulgación se refiere a biomarcadores para detectar cáncer de páncreas. La presente divulgación está dirigida a analizar o cuantificar los niveles de monómero de laminina gamma 2, CEA y CA19-9 para diagnosticar cáncer de páncreas en un sujeto.
La presente divulgación divulga métodos en los que el biomarcador monómero de laminina gamma 2 puede usarse para identificar o diagnosticar, lo que incluye ayudar a identificar o diagnosticar, a un paciente con cáncer de páncreas, para identificar o ayudar a identificar si un paciente padece cáncer de páncreas, para clasificar el riesgo de un paciente de desarrollar cáncer de páncreas, así como para determinar o ayudar a determinar un diagnóstico, pronóstico o régimen de tratamiento. El nivel de monómero de laminina gamma 2 es mayor en un sujeto que padece o está en riesgo de padecer cáncer de páncreas en comparación con un sujeto que no padece o tiene riesgo de padecer cáncer de páncreas. El nivel de monómero de laminina gamma 2 puede aumentar con las etapas avanzadas del cáncer de páncreas. Los métodos descritos en la presente pueden usarse junto con otros biomarcadores, como PIVKA-II, AFP, CEA, CA19-9 o combinaciones de los mismos, para identificar y diagnosticar, lo que incluye ayudar a identificar o diagnosticar, pacientes que padecen de cáncer de páncreas.
Los encabezados de sección como se usan en esta sección y toda la divulgación de la presente son meramente para propósitos de organización y no se pretende que sean limitativos.
1. Definiciones
A menos que se defina lo contrario, todos los términos técnicos y científicos usados en la presente tienen el mismo significado que el entendido comúnmente por un experto en la técnica. En caso de conflicto, prevalecerá el presente documento, incluyendo las definiciones. Los métodos y materiales preferidos se describen a continuación, aunque pueden usarse métodos y materiales similares o equivalentes a los descritos en la presente en la puesta en práctica o las pruebas de la presente invención. Los materiales, métodos y ejemplos divulgados en la presente son solo ilustrativos y no se pretenden que sean limitativos.
Se pretende que los términos "comprende", "incluye", "teniendo", "tiene", "puede", "contiene" y las variantes de los mismos, como se usan en la presente, sean frases términos o palabras de transición abiertas, que no
excluyen la posibilidad de actos o estructuras adicionales. Las formas singulares "un", "uno" y "el" incluyen referencias plurales a menos que el contexto indique claramente lo contrario. La presente divulgación también contempla otras realizaciones que "comprenden", “consisten de” y "consisten esencialmente de", las realizaciones o elementos presentados en la presente, ya se expongan explícitamente o no.
Para la enumeración de intervalos numéricos en la presente, se contempla explícitamente cada número intermedio entre ellos con el mismo grado de precisión. Por ejemplo, para el intervalo de 6-9, se contemplan los números 7 y 8 además de 6 y 9, y para el intervalo 6,0-7,0, se contemplan explícitamente los números 6,0, 6,1, 6,2, 6,3, 6,4, 6,5, 6,6, 6,7, 6,8, 6,9 y 7,0.
El "área bajo curva" o "AUC" se refiere al área bajo una curva ROC. La AUC bajo una curva ROC es una medida de precisión. Un área de 1 representa una prueba perfecta, mientras que un área de 0,5 representa una prueba insignificante. Una AUC preferida puede ser por lo menos de aproximadamente 0,700, por lo menos de aproximadamente 0,750, por lo menos de aproximadamente 0,800, por lo menos de aproximadamente 0,850, por lo menos de aproximadamente 0,900, por lo menos de aproximadamente 0,910, por lo menos de aproximadamente 0,920, por lo menos de aproximadamente 0,930, por lo menos de aproximadamente 0,940, por lo menos de aproximadamente 0,950, por lo menos de aproximadamente 0,960, por lo menos de aproximadamente 0,970, por lo menos de aproximadamente 0,980, por lo menos de aproximadamente 0,990, o por lo menos de aproximadamente 0,995.
"Cáncer", como se usa en la presente, se refiere al crecimiento no controlado y no regulado de células anormales en el cuerpo. Las células cancerosas también se denominan células malignas. El cáncer puede invadir partes cercanas del cuerpo y también puede extenderse a partes más distantes del cuerpo a través del sistema linfático o el torrente sanguíneo. Los cánceres pueden incluir, pero no están limitados a, carcinoma adrenocortical, cáncer anal, cáncer de vejiga, tumor cerebral, cáncer de mama, tumor carcinoide, gastrointestinal, carcinoma de primario desconocido, cáncer de cuello uterino, cáncer de colon, cáncer de endometrio, cáncer de esófago, cáncer de conducto biliar extrahepático, familia de tumores de Ewings (PNET), tumor de células germinales extracraneal, melanoma intraocular, cáncer de ojo, cáncer de vesícula biliar, cáncer gástrico (estómago), tumor de células germinales extragonadal, tumor trofoblástico gestacional, cáncer de cabeza y cuello, cáncer hipofaríngeo, carcinoma de células de los islotes, cáncer de riñón (cáncer de células renales), cáncer de laringe, leucemia linfoblástica aguda, leucemia, mieloide aguda, leucemia linfocítica crónica, leucemia mielógena crónica, leucemia de células pilosas, cáncer de labio y cavidad oral, cáncer de hígado (incluyendo el carcinoma hepatocelular), cáncer de pulmón de células no pequeñas, cáncer de pulmón de células pequeñas, linfoma relacionado con el SIDA, linfoma del sistema nervioso central (primario), linfoma de células T cutáneo, linfoma de la enfermedad de Hodgkin, linfoma no de la enfermedad de Hodgkin, mesotelioma maligno, melanoma, carcinoma de células de Merkel, cáncer de cuello escamoso metastásico con neoplasias primarias ocultas, mieloma múltiple y otras neoplasias de células plasmáticas, micosis fungoides, síndrome mielodisplásico, trastornos mieloproliferativos, cáncer nasofaríngeo, euroblastoma, cáncer oral, cáncer orofaríngeo, osteosarcoma, cáncer epitelial de ovario, tumor de células germinales de ovario, cáncer de páncreas, exocrino, cáncer de páncreas, carcinoma de células de los islotes, cáncer de seno paranasal y de cavidad nasal, cáncer de paratiroides, cáncer de pene, cáncer de pituitaria, neoplasia de células plasmáticas, cáncer de próstata, rabdomiosarcoma, cáncer rectal, cáncer de células renales (cáncer de riñón), células renales de transición pelvis y uretra, cáncer de glándulas salivales, síndrome de Sezary, cáncer de piel, cáncer del intestino delgado, sarcoma de tejido blando, cáncer de testículo, timoma maligno, cáncer de tiroides, cáncer de uretra, cáncer de útero, cáncer inusual de la infancia, cáncer vaginal, cáncer de vulva y tumor de Wilms.
"Componente", "componentes" o "por lo menos un componente" se refieren de manera general a un anticuerpo de captura, una detección o conjugan un calibrador, un control, un panel de sensibilidad, un recipiente, un tampón, un diluyente, una sal, una enzima, un cofactor para una enzima, un reactivo de detección, un reactivo/solución de pretratamiento, un sustrato (por ejemplo, como solución), una solución de parada y similares que pueden incluirse en un kit para el análisis de una muestra de prueba, como una muestra de orina, suero o plasma de un paciente, de acuerdo con los métodos descritos en la presente y otros métodos conocidos en la técnica. Algunos componentes pueden estar en solución o liofilizados para su reconstitución para su uso en un ensayo.
"Sujeto de control", como se usa en la presente, se refiere a un sujeto sano, es decir, un sujeto que no tiene signos o síntomas clínicos de carcinoma hepatocelular, cáncer de páncreas o cáncer distinto del carcinoma hepatocelular o cáncer de páncreas. El sujeto de control se evalúa clínicamente para detectar signos o síntomas no detectados de otra manera de carcinoma hepatocelular, cáncer de páncreas o cáncer que no sea carcinoma hepatocelular o cáncer de páncreas, tal evaluación puede incluir un examen físico rutinario y/o pruebas de laboratorio.
El "grupo de control" como se usa en la presente se refiere a un grupo de sujetos de control o sujetos sanos, es decir, un grupo de sujetos que no tienen signos o síntomas clínicos de carcinoma hepatocelular, cáncer de páncreas o cáncer distinto del carcinoma hepatocelular o cáncer de páncreas.
"Marcador" y "marcador detectable", como se usa en la presente, se refiere a una fracción unida a un anticuerpo o un analito para hacer que la reacción entre el anticuerpo y el analito sea detectable, y el anticuerpo o analito así marcado es referido como "detectablemente marcado." Un marcador puede producir una señal que es detectable por medios visuales o instrumentales. Varios marcadores incluyen sustancias que producen señales, como cromagenes, compuestos fluorescentes, compuestos quimioluminiscentes, compuestos radiactivos y similares. Los ejemplos representativos de marcadores incluyen fracciones que producen luz, por ejemplo, compuestos de acridinio, y fracciones que producen fluorescencia, por ejemplo, fluoresceína. Otros marcadores se describen en la presente. A este respecto, la fracción en sí misma puede no ser detectable pero puede volverse detectable tras la reacción con otra fracción más. Se pretende que el uso del término "marcado detectablemente" abarque dicho marcado.
Puede usarse cualquier marcador detectable adecuado como se conoce en la técnica. Por ejemplo, el marcador detectable puede ser un marcador radioactivo (como 3H, 14C, 32P, 33P, 35S, 90Y, 99Tc, 111ln, 1251, 1311, 177Lu, 166Ho y 153Sm), un marcador enzimático (como peroxidasa de rábano picante, peroxidasa alcalina, glucosa 6-fosfato deshidrogenasa y similares), un marcador quimioluminiscente (como ésteres de acridinio, tioésteres o sulfonamidas; ésteres de luminol, isoluminol, fenantridinio y similares), un marcador fluorescente (como fluoresceína (por ejemplo, 5-fluoresceína, 6-carboxifluoresceína, 3'6-carboxifluoresceína, 5(6)-carboxifluoresceína, 6-hexacloro-fluoresceína, 6-tetraclorofluoresceína, isotiocianato de fluoresceína y similares), rodamina, ficobiliproteínas, R-ficoeritrina, puntos cuánticos (por ejemplo, seleniuro de cadmio con cubierta de sulfuro de zinc), un marcador termométrico, o un marcador de reacción en cadena de inmuno-polimerasa. En Polak y Van Noorden, Introduction to Immunocytochemistry, 2a ed., Springer Verlag, NY (1997), y en Haugland, Handbook of Fluorescent Probes and Research Chemicals (1996), se encuentra una introducción a los marcadores, los procedimientos de marcado y la detección de marcadores, que es un manual combinado y un catálogo publicado por Molecular Probes, Inc., Eugene, Oregon. Puede usarse un marcador fluorescente en FPIA (ver, por ejemplo, las Patentes de Estados Unidos N° 5.593.896, 5.573.904, 5.496.925, 5.359.093 y 5.352.803). Puede usarse un compuesto de acridinio como marcador detectable en un ensayo quimioluminiscente homogéneo (ver, por ejemplo, Adamczyk et al., Bioorg. Med. Chem. Lett. 16: 1324-1328 (2006); Adamczyk et al., Bioorg. Med. Chem. Lett. 4: 2313-2317 (2004); Adamczyk et al., Biorg. Med. Chem. Lett. 14: 3917-3921 (2004); y Adamczyk et al., Org. Lett. 5: 3779-3782 (2003)).
En un aspecto, el compuesto de acridinio es una acridinio-9-carboxamida. Los métodos para preparar 9-carboxamidas de acridinio se describen en Mattingly, J. Biolumin. Chemilumin. 6: 107-114 (1991); Adamczyk et al., J. Org. Chem. 63: 5636-5639 (1998); Adamczyk et al., Tetrahedron 55: 10899-10914 (1999); Adamczyk et al., Org. Lett. 1: 779-781 (1999); Adamczyk et al., Bioconjugate Chem. 11: 714-724 (2000); Mattingly et al., In Luminescence Biotechnology: Instruments and Applications; Dyke, K. V. Ed.; CRC Press: Boca Raton, pp. 77-105 (2002); Adamczyk et al., Org. Lett. 5: 3779-3782 (2003); y las Patentes de Estados Unidos N° 5.468.646, 5.543.524 y 5.783.69.
Otro ejemplo de un compuesto de acridinio es un éster de arilo de acridinio-9-carboxilato. Un ejemplo de un éster de arilo de acridinio-9-carboxilato de fórmula II es el fluorosulfonato de 10-metil-9-(fenoxicarbonil)acridinio (disponible de Cayman Chemical, Ann Arbor, MI). Los métodos para preparar ésteres de arilo de acridinio 9-carboxilato se describen en McCapra et al., Photochem. Photobiol. 4: 1111-21 (1965); Razavi y col., Luminescence 15: 245-249 (2000); Razavi et al., Luminescence 15: 239-244 (2000); y la Patente de Estados Unidos N° 5.241.070. Tales ésteres de arilo de acridinio-9-carboxilato son indicadores quimioluminiscentes eficientes para el peróxido de hidrógeno producido en la oxidación de un analito por al menos una oxidasa en términos de la intensidad de la señal y/o la rapidez de la señal. El curso de la emisión quimioluminiscente para el éster de arilo de acridinio-9-carboxilato se completa rápidamente, es decir, en menos de 1 segundo, mientras que la emisión quimioluminiscente de la acridinio-9-carboxamida se extiende durante 2 segundos. El éster de arilo de acridinio-9-carboxilato, sin embargo, pierde sus propiedades quimioluminiscentes en presencia de proteínas. Por lo tanto, su uso requiere la ausencia de proteínas durante la generación y detección de señales. Los métodos para separar o eliminar proteínas en la muestra son bien conocidos por los expertos en la técnica e incluyen, pero no están limitados a, ultrafiltración, extracción, precipitación, diálisis, cromatografía y/o digestión (ver, por ejemplo, Wells, High Throughput Bioanalytical Sample Preparation. Methods and Automation Strategies, Elsevier (2003)). La cantidad de proteína eliminada o separada de la muestra de prueba puede ser de aproximadamente el 40%, aproximadamente el 45%, aproximadamente el 50%, aproximadamente el 55%, aproximadamente el 60%, aproximadamente el 65%, aproximadamente el 70%, aproximadamente el 75%, aproximadamente el 80%, aproximadamente el 85%, aproximadamente el 90% o aproximadamente el 95%. Más detalles sobre el éster de arilo de acridinio-9-carboxilato y su uso se exponen en la Solicitud de Patente de Estados Unidos N° 11/697.835, presentada el 9 de abril de 2007. Los ésteres de arilo de acridinio-9-carboxilato pueden disolverse en cualquier solvente adecuado, como N,N-dimetilformamida (DMF) anhidra desgasificada o colato de sodio acuoso.
"Neoplasia", como se usa en la presente, se refiere a un crecimiento anormal de tejido. La neoplasia se conoce comúnmente como tumor. El crecimiento anormal habitualmente, pero no siempre, forma una masa.
"Control normal" o "control sano" como se usa en la presente significa una muestra o espécimen tomado de un sujeto, o un sujeto real que no tiene carcinoma hepatocelular, cáncer de páncreas o ningún cáncer, o que no está
en riesgo de desarrollar cáncer.
"Normal", "sano" y "control", como se usa en la presente, se refieren indistintamente a muestras tomadas de sujetos o sujetos que no tienen carcinoma hepatocelular, cáncer de páncreas o ningún cáncer, o que no están en riesgo de desarrollar cáncer.
"Enfermedad pancreática benigna" y "enfermedad pancreática", como se usan en la presente, se refieren indistintamente a enfermedad pancreática que no es cáncer o se ha convertido en cáncer. La enfermedad pancreática benigna incluye pancreatitis, varios tipos de quistes y tumores, neoplasia intraepitelial pancreática (PanIN) y neoplasias mucinosas papilares intraductales (IPMN) y neoplasias quísticas mucinosas (MCN).
"Cáncer de páncreas en estadio temprano", como se usa en la presente, se refiere a cáncer de páncreas que está limitado al páncreas, fuera del páncreas o ganglios linfáticos cercanos, pero que no se ha expandido a vasos sanguíneos o nervios importantes cercanos u órganos distantes. El cáncer de páncreas en estadio temprano incluye cánceres de páncreas en estadio 0, estadio I y estadio II. Ver Yachida et al. (2010) Nature 467:1114-1119; ver también las Directrices de la National Comprehensive Cancer Network (NCCN) Versión 2.2012 Adenocarcinoma de páncreas.
"Cáncer de páncreas en estadio avanzado", como se usa en la presente, se refiere a cáncer de páncreas que se ha expandido a los vasos sanguíneos importantes cercanos, nervios u órganos distantes. El cáncer de páncreas en estadio avanzado incluye el cáncer de páncreas en estadio III o IV.
"Cáncer de páncreas en estadio 0", como se usa en la presente, se refiere a cáncer de páncreas limitado a una sola capa de células en el páncreas. El cáncer de páncreas no es visible en las pruebas de imagenología ni a simple vista. El tumor está confinado a las capas superiores de las células del conducto pancreático y no ha invadido tejidos más profundos ni se ha extendido fuera del páncreas. Los tumores en estadio 0 a veces se denominan carcinoma pancreático in situ o neoplasia intraepitelial pancreática III (PanIn III).
"Cáncer de páncreas en estadio I", como se usa en la presente, se refiere a un cáncer confinado o limitado al páncreas y que no se ha propagado a los ganglios linfáticos cercanos. El "estadio IA" se refiere a un tumor confinado al páncreas y que mide menos de 2 cm. "Estadio IB" se refiere a un tumor confinado al páncreas y tiene un tamaño mayor de 2 cm.
"Cáncer de páncreas en estadio II", como se usa en la presente, se refiere a un cáncer de diseminación local que ha crecido fuera del páncreas o se ha propagado a los ganglios linfáticos cercanos. "Estadio I IA" se refiere a un tumor que crece fuera del páncreas pero no en vasos sanguíneos grandes, ganglios linfáticos cercanos o sitios distantes. El "estadio IIB" se refiere a un tumor o confinado al páncreas o que crece fuera del páncreas, pero que no se ha propagado a los vasos sanguíneos grandes ni a los nervios principales cercanos. El estadio IIB puede propagarse a los ganglios linfáticos cercanos, pero no a sitios distantes.
"Cáncer de páncreas en estadio III", como se usa en la presente, se refiere a un cáncer de propagación más amplia que se ha expandido a los vasos sanguíneos o nervios principales cercanos pero que no ha hecho metástasis. El tumor crece fuera del páncreas hacia los vasos sanguíneos grandes cercanos o los nervios principales y puede o no haberse propagado a los ganglios linfáticos cercanos. No se ha propagado a sitios distantes.
"Cáncer de páncreas en estadio IV", como se usa en la presente, se refiere a un cáncer de propagación confirmado que se ha propagado a órganos o sitios distantes. El cáncer de páncreas en estadio IVA está confinado localmente, pero implica órganos o vasos sanguíneos adyacentes, lo que dificulta la extirpación quirúrgica. El cáncer de páncreas en estadio IVA también se conoce como localizado o localmente avanzado. El cáncer de páncreas en estadio IVB se ha propagado a órganos distantes, más comúnmente al hígado. El cáncer de páncreas en estadio IVB también se denomina metastásico.
"Límite predeterminado" y "nivel predeterminado", como se usan en la presente, se refieren a un valor límite de ensayo que se usa para evaluar resultados de eficacia diagnóstica, pronóstica o terapéutica comparando los resultados del ensayo con el límite/nivel predeterminado, donde el límite/nivel predeterminado ya se ha vinculado o asociado con varios parámetros clínicos (por ejemplo, presencia de enfermedad, estadio de la enfermedad, gravedad de la enfermedad, progresión, no progresión o mejora de la enfermedad, etc.) La divulgación proporciona niveles predeterminados ejemplares. Sin embargo, es bien conocido que los valores límite pueden variar dependiendo de la naturaleza del inmunoensayo (por ejemplo, anticuerpos empleados, condiciones de reacción, pureza de la muestra, etc.). Además, está dentro de los conocimientos habituales de un experto en la técnica adaptar la divulgación en la presente para otros inmunoensayos para obtener valores límite específicos de inmunoensayos para esos otros inmunoensayos basados en la descripción proporcionada por esta divulgación. Mientras que el valor exacto del límite/nivel predeterminado puede variar entre ensayos, las correlaciones descritas en la presente deberían ser de aplicación general.
"Reactivo de pretratamiento", por ejemplo, reactivo de lisis, precipitación y/o solubilización, como se usa en un ensayo de diagnóstico como se describe en la presente, es uno que lisa cualquier célula y/o solubiliza cualquier analito que esté presente en una muestra de prueba. El pretratamiento no es necesario para todas las muestras, como se describe más adelante en la presente. Entre otras cosas, solubilizar el analito (es decir, monómero de laminina gamma 2, PIKVA-II, AFP, CEA y/o CA19-9, fragmentos de monómero de laminina gamma 2, PIVKA-II, AFP, CEA y/o CA19-9, variantes del monómero de laminina gamma 2, PIVKA-II, AFP, CEA y/o CA19-9, o cualquier combinación de los mismos) implica la liberación del analito de cualquier proteína de unión endógena presente en la muestra. Un reactivo de pretratamiento puede ser homogéneo (que no requiera un paso de separación) o heterogéneo (que requiera un paso de separación). Con el uso de un reactivo de pretratamiento heterogéneo, se eliminan las proteínas de unión al analito precipitadas de la muestra de prueba antes de pasar al siguiente paso del ensayo. El reactivo de pretratamiento opcionalmente puede comprender: (a) uno o más solventes y sal, (b) uno o más solventes, sal y detergente, (c) detergente, (d) detergente y sal, o (e) cualquier reactivo o combinación de reactivos apropiados para la lisis celular y/o solubilización del analito.
Los "reactivos de control de calidad" en el contexto de inmunoensayos y kits descritos en la presente incluyen, pero no están limitados a, calibradores, controles y paneles de sensibilidad. Típicamente se usa un "calibrador" o "estándar" (por ejemplo, uno o más, como una pluralidad) para establecer curvas de calibración (estándar) para la interpolación de la concentración de un analito, como un anticuerpo o un analito. Alternativamente, puede usarse un único calibrador, que está cerca de un valor de corte positivo/negativo predeterminado. Pueden usarse múltiples calibradores (es decir, más de un calibrador o una cantidad variable de calibradores) en conjunto para comprender un "panel de sensibilidad".
"Evaluación de riesgos", "clasificación de riesgos", "identificación de riesgos" o "estratificación de riesgos" de sujetos (por ejemplo, pacientes) como se usa en la presente se refiere a la evaluación de factores que incluyen biomarcadores, para predecir el riesgo de ocurrencia de eventos futuros, que incluyen el inicio de la enfermedad o la progresión de la enfermedad, de tal manera que pueden tomarse las decisiones de tratamiento con respecto al sujeto sobre una base más informada.
"Muestra", "muestra biológica", "muestra de prueba", "espécimen", "muestra de un sujeto", "muestra obtenida de un sujeto" y "muestra del paciente" como se usan en la presente pueden usarse indistintamente y pueden ser una muestra de sangre, tejido, orina, suero, plasma, líquido amniótico, líquido cefalorraquídeo, células o tejidos placentarios, células endoteliales, leucocitos o monocitos. La muestra puede usarse directamente como se obtiene de un paciente o puede pretratarse como por filtración, destilación, extracción, concentración, centrifugación, inactivación de componentes interferentes, adición de reactivos y similares, para modificar el carácter de la muestra de alguna manera como se analiza en la presente o de otra manera como se conoce en la técnica.
Puede utilizarse cualquier tipo de célula, tejido o fluido corporal para obtener una muestra. Dichos tipos de células, tejidos y fluidos pueden incluir secciones de tejidos como biopsias y muestras de autopsias, secciones congeladas tomadas con propósitos histológicos, sangre (como sangre completa), plasma, suero, esputo, heces, lágrimas, moco, saliva, fluido de lavado broncoalveolar (BAL), cabello, piel, glóbulos rojos, plaquetas, líquido intersticial, líquido de lentes oculares, líquido cefalorraquídeo, sudor, líquido nasal, líquido sinovial, menstruación, líquido amniótico, semen, etc. Los tipos de células y tejidos también pueden incluyen líquido linfático, líquido ascético, líquido ginecológico, orina, líquido peritoneal, líquido cefalorraquídeo, un líquido recogido por enjuague vaginal o un líquido recogido por limpieza vaginal. Puede proporcionarse un tipo de tejido o célula mediante la extracción de una muestra de células de un animal, pero también puede lograrse mediante el uso de células previamente aisladas (por ejemplo, aisladas por otra persona, en otro momento y/o para otro propósito). También pueden usarse tejidos de archivo, como los que tienen tratamiento o antecedentes de resultados. El aislamiento y/o purificación de proteínas o nucleótidos puede no ser necesario.
En la puesta en práctica de la presente divulgación se usan métodos bien conocidos en la técnica para recoger, manipular y procesar orina, sangre, suero y plasma, y otros fluidos corporales. La muestra de prueba puede comprender fracciones adicionales además del analito de interés como anticuerpos, antígenos, haptenos, hormonas, fármacos, enzimas, receptores, proteínas, péptidos, polipéptidos, oligonucleótidos o polinucleótidos. Por ejemplo, la muestra puede ser una muestra de sangre completa obtenida de un sujeto. Puede ser necesario o desearse que una muestra de prueba, particularmente sangre completa, sea tratada antes del inmunoensayo como se describe en la presente, por ejemplo, con un reactivo de pretratamiento. Incluso en los casos en que el pretratamiento no es necesario (por ejemplo, la mayoría de las muestras de orina, una muestra archivada preprocesada, etc.), el pretratamiento de la muestra es una opción que puede realizarse por mera conveniencia (por ejemplo, como parte de un protocolo en una plataforma comercial). La muestra puede usarse directamente como se obtiene del sujeto o después del pretratamiento para modificar una característica de la muestra. El pretratamiento puede incluir extracción, concentración, inactivación de componentes interferentes y/o la adición de reactivos.
El término "sensibilidad" como se usa en la presente se refiere al número de positivos verdaderos dividido por el número de positivos verdaderos más el número de falsos negativos, donde la sensibilidad ("sens") puede estar
dentro del intervalo de 0<sens<1. Idealmente, los métodos divulgados en la presente tienen el número de falsos negativos igual a cero o casi igual a cero, de tal manera que no se identifica erróneamente que ningún sujeto no tenga cáncer de páncreas cuando de hecho tiene cáncer de páncreas. Al contrario, a menudo se realiza una evaluación de la capacidad de un algoritmo de predicción para clasificar los negativos correctamente, una medición complementaria de la sensibilidad.
El término "especificidad" como se usa en la presente se refiere al número de negativos verdaderos dividido por el número de negativos verdaderos más el número de falsos positivos, donde la especificidad ("spec") puede estar dentro del intervalo de 0 <spec<1. Idealmente, los métodos descritos en la presente tienen el número de falsos positivos igual a cero o casi igual a cero, de tal manera que no se identifica erróneamente que un sujeto tenga adenoma cuando en realidad no tiene cáncer de páncreas. Por lo tanto, se prefiere un método que tenga tanto sensibilidad como especificidad igual a uno, o 100%.
"Serie de composiciones de calibración" se refiere a una pluralidad de composiciones que comprenden una concentración conocida de monómero de laminina gamma 2, PIVKA-II, AFP, CEA y/o CA19-9, en donde cada una de las composiciones difiere de las otras composiciones en la serie por la concentración de monómero de laminina gamma 2, PIVKA-II, AFP, CEA y/o CA19-9.
El término "sujeto", "paciente" o "sujeto en el método" como se usa en la presente indistintamente, significa cualquier vertebrado, incluyendo, pero no limitados a, un mamífero (por ejemplo, vaca, cerdo, camello, llama, caballo, cabra, conejo, oveja, hámsteres, conejillo de indias, gato, perro, rata y ratón, un primate no humano (por ejemplo, un mono, como un mono cynomolgous o rhesus, chimpancé, etc.) y un humano. En algunas realizaciones, el sujeto o sujeto puede ser humano o no humano. En algunas realizaciones, el sujeto puede ser un sujeto humano en riesgo o que se sospecha que está en riesgo de desarrollar o de tener ya cáncer de páncreas, o un cáncer que no sea cáncer de páncreas.
Los términos "tratar", "tratado" o "tratando", como se usan en la presente, se refieren a un agente terapéutico en el que el objeto es ralentizar (disminuir) una afección, trastorno o enfermedad fisiológica no deseada, u obtener resultados clínicos beneficiosos o deseados. Para los propósitos de esta invención, los resultados clínicos beneficiosos o deseados incluyen, pero no están limitados a, alivio de los síntomas; disminución de la extensión de la afección, trastorno o enfermedad; estabilización (es decir, no empeoramiento) del estado de la afección, trastorno o enfermedad; retraso en el inicio o desaceleración de la progresión de la afección, trastorno o enfermedad; mejora de la afección, trastorno o estado de la enfermedad; y remisión (ya sea parcial o total), ya sea detectable o indetectable, o mejora de la afección, trastorno o enfermedad. El tratamiento también incluye prolongar la supervivencia en comparación con la supervivencia esperada si no recibe tratamiento.
"Variante" como se usa en la presente con respecto a un ácido nucleico significa (i) una parte o fragmento de una secuencia de nucleótidos referenciada; (ii) el complemento de una secuencia de nucleótidos referenciada o una parte de la misma; (iii) un ácido nucleico que es sustancialmente idéntico a un ácido nucleico referenciado o al complemento del mismo; o (iv) un ácido nucleico que hibrida en condiciones estrictas con el ácido nucleico referenciado, el complemento del mismo, o una secuencia sustancialmente idéntica al mismo.
La variante puede definirse adicionalmente como un péptido o polipéptido que difiere en la secuencia de aminoácidos por la inserción, deleción o sustitución conservadora de aminoácidos, pero retiene por lo menos una actividad biológica. Los ejemplos representativos de "actividad biológica" incluyen la capacidad de unirse a un anticuerpo específico o de promover una respuesta inmune. La variante también se usa en la presente para describir una proteína con una secuencia de aminoácidos que es sustancialmente idéntica a una proteína referenciada con una secuencia de aminoácidos que retiene por lo menos una actividad biológica. En la técnica se reconoce que una sustitución conservadora de un aminoácido, es decir, reemplazar un aminoácido con un aminoácido diferente de propiedades similares (por ejemplo, hidrofilia, grado y distribución de regiones cargadas) implica típicamente un cambio menor. Estos cambios menores pueden identificarse, en parte, considerando el índice hidropático de los aminoácidos, como se entiende en la técnica. Kyte yet al., J. Mol. Biol. 157:105-132 (1982). El índice hidropático de un aminoácido se basa en una consideración de su hidrofobicidad y carga. Se sabe en la técnica que los aminoácidos de índices hidropáticos similares pueden sustituirse y retener aun la función proteica. En un aspecto, los aminoácidos que tienen índices hidropáticos de ± 2 están sustituidos. La hidrofilia de los aminoácidos también puede usarse para revelar sustituciones que darían como resultado que las proteínas retengan la función biológica. Una consideración de la hidrofilia de los aminoácidos en el contexto de un péptido permite el cálculo de la mayor hidrofilia media local de ese péptido, una medida útil que se ha informado que se correlaciona bien con la antigenicidad y la inmunogenicidad. Patente de Estados Unidos N° 4.554.10. La sustitución de aminoácidos que tienen valores de hidrofilia similares puede dar como resultado que los péptidos retengan actividad biológica, por ejemplo inmunogenicidad, como se entiende en la técnica. Las sustituciones pueden realizarse con aminoácidos que tienen valores de hidrofilia dentro de ± 2 entre sí. Tanto el índice de hidrofobicidad como el valor de hidrofilia de los aminoácidos están influenciados por la cadena lateral particular de ese aminoácido. De acuerdo con esa observación, se entiende que las sustituciones de aminoácidos que son compatibles con la función biológica dependen de la similitud relativa de los aminoácidos, y particularmente de las cadenas laterales de esos
aminoácidos, como lo revela la hidrofobicidad, hidrofilia, carga, tamaño y otras propiedades. "Variante" también puede usarse para describir un polipéptido o un fragmento del mismo que ha sido procesado diferencialmente como por proteólisis, fosforilación u otra modificación postraduccional, pero que conserva su reactividad antigénica.
Una variante puede ser una secuencia de ácidos nucleicos que es sustancialmente idéntica en toda la longitud de la secuencia génica completa o un fragmento de la misma. La secuencia de ácido nucleico puede ser un 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, o 100% idéntica en toda la longitud de la secuencia génica o un fragmento de la misma. Una variante puede ser una secuencia de aminoácidos que es sustancialmente idéntica en toda la longitud de la secuencia de aminoácidos o fragmento de la misma. La secuencia de aminoácidos puede ser un 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% o 100% idénticos en toda la longitud de la secuencia de aminoácidos o un fragmento de la misma.
2. Métodos para diagnosticar una enfermedad usando monómero de laminina gamma 2
En la presente se proporciona un método para diagnosticar cáncer de páncreas en un sujeto con necesidad de ello como se define en las reivindicaciones.
El método de diagnóstico incluye determinar los niveles de monómero de laminina gamma 2, CEA y CA19-9, en una muestra obtenida del sujeto y comparar los niveles del monómero de laminina gamma 2, CEA y CA19-9 en la muestra con los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9, respectivamente. Un aumento en los niveles de monómero de laminina gamma 2, CEA y CA19-9 indica que el sujeto padece o corre el riesgo de padecer la enfermedad.
a. Monómero de laminina gamma 2
El método para diagnosticar una enfermedad, como el cáncer de páncreas, incluye medir los niveles de monómero de laminina gamma 2 en una muestra de un sujeto. El monómero de laminina gamma 2 (también referido en la presente como "laminina gamma 2" o "Ln-y2") es un miembro de la familia de proteínas laminina, que son glicoproteínas de la matriz extracelular y constituyentes de las membranas basales. Cada laminina heterotrimérica está compuesta por tres cadenas no idénticas: laminina alfa, laminina beta y laminina gamma. Pueden combinarse diferentes isómeros de cadena alfa, beta y gamma para dar lugar a diferentes isoformas de laminina heterotriméricas. La laminina gamma 2 es un isómero de la cadena gamma y junto con la laminina alfa 3 y la laminina beta 3 forma la laminina 5. La laminina 5 se localiza predominantemente en la lámina basal y la membrana basal. En humanos, el monómero de laminina gamma 2 está codificado por el gen LAMC2, que está localizado en el brazo largo (q) del cromosoma 1 humano entre las posiciones 25 y 31 (1q25-1q31). El monómero de laminina gamma 2 humana puede ser una proteína precursora, que incluye el péptido señal, o la proteína secretada, en la que el péptido señal se ha eliminado por escisión.
b. Antígeno carcinoembrionario (CEA)
El método para diagnosticar una enfermedad puede incluir medir los niveles de monómero de laminina gamma 2 y los niveles de antígeno carcinoembrionario (CEA). El CEA está implicado en la adhesión celular y es una glicoproteína anclada a la superficie de la célula glicosil fosfatidil inositol (GPI) cuyas glicoformas sialofucosiladas especializadas sirven como ligandos de L-selectina y E-selectina de carcinoma de colon funcionales. El CEA es un antígeno asociado a tumores que se caracteriza por una glicoproteína de aproximadamente 200 kDa de tamaño. El CEA está aprobado por la FDA y está destinado a ser usado como una ayuda en el pronóstico y el manejo de pacientes con cáncer con concentraciones cambiantes de CEA.
Adicionalmente, el CEA es un marcador relacionado con el cáncer colorrectal (CCR) y ha sido aprobado clínicamente para monitorizar cánceres gastrointestinales (GI), incluyendo el CRC. Se ha caracterizado su rendimiento para detectar algunos CRC. La relevancia clínica se ha demostrado en cánceres colorrectal, gástrico, de pulmón, de próstata, de páncreas y de ovario (Abbott ARCHITECT CEA Package Insert 34-4067/R4). El CEA puede detectarse y cuantificarse usando Abbott ARCHITECT® CEA.
c. Antígeno de carbohidratos 19-9 (CA19-9)
El método para diagnosticar una enfermedad puede incluir medir los niveles de monómero de laminina gamma 2 y los niveles de antígeno de carbohidratos 19-9 (CA19-9 o CA 19-9). El CA19-9 es una glicoproteína mucina derivada de una línea celular de carcinoma colorrectal humano y está relacionada con la proteína del grupo sanguíneo Lewis. Específicamente, CA19-9 pertenece al antígeno del grupo sanguíneo Lewis sialilado y puede ser indetectable en individuos que son negativos al antígeno de Lewis. Adicionalmente, el CA19-9 está presente en el tejido epitelial del estómago, la vesícula biliar, el páncreas y la próstata.
El CA19-9 ha sido aprobado por la FDA para su uso como ayuda en el tratamiento del cáncer de páncreas
y se pretende que se use junto con otra información de diagnóstico como tomografía computarizada (CT) y procedimientos de imágenes de resonancia magnética (MRI). El CA19-9 en suero también puede ser elevado en pacientes con afecciones no malignas como la pancreatitis y otros trastornos gastrointestinales (Abbott ARCHITECT CA19-9 XR Package Insert 015-550 11/05). Los niveles elevados de CA19-9 pueden ser informativos para algunos cánceres colorrectales (CRC). El CA19-9 puede detectarse y cuantificarse usando Abbott ARCHITECT® CA19-9 XR. d. Combinaciones de monómero de laminina gamma 2 y biomarcadores adicionales
El método de diagnóstico detecta niveles de monómero de laminina gamma 2, CEA y CA19-9 en la muestra obtenida del sujeto. Un aumento en los niveles de monómero de laminina gamma 2, CEA y CA19-9 con respecto al nivel de referencia indica que el sujeto padece o está en riesgo de padecer cáncer de páncreas.
e. Enfermedad
El método proporcionado en la presente se usa para proporcionar un diagnóstico de un sujeto que tiene cáncer de páncreas. El cáncer de páncreas es un cáncer que se origina en el páncreas. El cáncer de páncreas puede incluir, pero no se limita a, cáncer de páncreas exocrino, como adenocarcinoma de páncreas, carcinoma de células acinares, adenocarcinoma, carcinoma adenoescamoso, tumor de células gigantes, cistadenocarcinoma mucinoso, pancreatoblastoma, cistoadenocarcinoma seroso, tumores sólidos y pseudopilares, y neoplasias quísticas papilares, cáncer de páncreas endocrino, como tumores neuroendocrinos pancreáticos (NET), tumores de células de los islotes, carcinoma de células de los islotes, carcinoide pancreático, tumor endocrino pancreático (PET), gastrinoma (síndrome de Zollinger-Ellison), glucagonoma, insulinoma, tumor de células de los islotes no funcional, somatostatinoma, y tumor liberador de péptidos intestinal vasoactivo (VIPoma o síndrome de Verner-Morrison) y linfoma del páncreas. El adenocarcinoma puede desarrollarse a partir de una neoplasia papilar-mucinosa intraductal benigna (IPMN).
El método de diagnóstico mide los niveles de monómero de laminina gamma 2, CEA y CA19-9 en la muestra obtenida del sujeto. Un aumento en los niveles de monómero de laminina gamma 2, CEA y CA19-9 con respecto al nivel de referencia indica que el sujeto padece o está en riesgo de padecer cáncer de páncreas.
(a) Estadio del cáncer de páncreas
El método descrito en la presente puede usarse para proporcionar un diagnóstico de un sujeto que tiene cáncer de páncreas en un estadio particular. La enfermedad puede ser cáncer de páncreas en estadio 0, cáncer de páncreas en estadio I, cáncer de páncreas en estadio II, cáncer de páncreas en estadio III o cáncer de páncreas en estadio IV. El nivel del monómero de laminina gamma 2 puede aumentar con el estadio del cáncer de páncreas. Por ejemplo, el nivel de monómero de laminina gamma 2 puede ser más alto en el cáncer de páncreas en estadio IV que el nivel de monómero de laminina gamma 2 en el cáncer de páncreas en estadio III. Por consiguiente, los niveles crecientes de monómero de laminina gamma 2 pueden indicar que el cáncer de páncreas está progresando de un estadio a otro en el sujeto.
F. Inmunoensayo para determinar el monómero de laminina gamma 2 y/o el por lo menos un nivel adicional de biomarcadores
El método de diagnóstico puede emplear un inmunoensayo para determinar los niveles de monómero de laminina gamma 2 y/o por lo menos uno de los biomarcadores adicionales CEA y CA19-9 en una muestra obtenida del sujeto. El inmunoensayo puede cuantificar los niveles de monómero de laminina gamma 2 y/o por lo menos uno de los biomarcadores adicionales.
La presencia o cantidad de monómero de laminina gamma 2 y/o el por lo menos uno de los biomarcadores adicionales puede determinarse usando anticuerpos que se unen específicamente a cada biomarcador (es decir, monómero de laminina gamma 2, CEA y/o CA19-9 así como cualquier analito adicional si se usan tales analitos adicionales). Los ejemplos de anticuerpos que pueden usarse incluyen un anticuerpo policlonal, un anticuerpo monoclonal, un anticuerpo humano, una molécula de inmunoglobulina, un Fv enlazado a disulfuro, un anticuerpo monoclonal, un afinidad madurada, un scFv, un anticuerpo quimérico, un anticuerpo de dominio único, un anticuerpo injertado con CDR, un diacuerpo, un anticuerpo humanizado, un anticuerpo multiespecífico, un Fab, un anticuerpo de doble especificidad, un DVD, un Fab', un anticuerpo biespecífico, un F(ab')2 , un Fv y combinaciones de los mismos.
Por ejemplo, el método inmunológico puede incluir (a) medir el nivel de monómero de laminina gamma 2: (i) poniendo en contacto la muestra de prueba con por lo menos un anticuerpo de captura, en donde el anticuerpo de captura se une a un epítopo en el monómero de laminina gamma 2 o un fragmento de monómero de laminina gamma 2 para formar un complejo de anticuerpo de captura-monómero de laminina gamma 2; (ii) poniendo en contacto el complejo de anticuerpo de captura-monómero de laminina gamma 2 con por lo menos un anticuerpo de detección que comprende un marcador detectable, en donde el anticuerpo de detección se une a un epítopo en el
monómero de laminina gamma 2 que no está unido por el anticuerpo de captura y forma un complejo anticuerpo de captura-monómero de laminina gamma 2-anticuerpo de detección; y (iii) determinando el nivel de monómero de laminina gamma 2 en la muestra de prueba en base a la señal generada por el marcador detectable en el complejo de anticuerpo de captura-monómero de laminina gamma 2-anticuerpo de detección formado en (a) (ii); (b) medir el nivel del por lo menos un biomarcador adicional: (i) poniendo en contacto la muestra de prueba con por lo menos un anticuerpo de captura, en donde el anticuerpo de captura se une a un epítopo en el por lo menos un biomarcador adicional o un fragmento del por lo menos un biomarcador adicional para formar un complejo de anticuerpo de captura-por lo menos un biomarcador adicional; (ii) poniendo en contacto el complejo de anticuerpo de captura-por lo menos un biomarcador adicional con por lo menos un anticuerpo de detección que comprende un marcador detectable, en donde el anticuerpo de detección se une a un epítopo en el por lo menos un biomarcador adicional al que no se ha unido el anticuerpo de captura y forma un complejo de anticuerpo de captura-por lo menos un biomarcador adicional-anticuerpo de detección y (iii) determinando el nivel del por lo menos un biomarcador adicional en la muestra de prueba en base a la señal generada por el marcador detectable en el complejo de anticuerpo de captura-por lo menos un biomarcador adicional-anticuerpo de detección formado en (b)(ii); o una combinación de los mismos.
Puede utilizarse cualquier inmunoensayo. El inmunoensayo puede ser un inmunoensayo ligado a enzimas (ELISA), un radioinmunoensayo (RIA), un ensayo de inhibición competitiva, como ensayos de inhibición competitiva directa o inversa, un ensayo de polarización de fluorescencia o un ensayo de unión competitiva, por ejemplo. El ELISA puede ser un ELISA sándwich. La unión inmunológica específica del anticuerpo con el marcador puede detectarse mediante marcadores directos, como marcadores fluorescentes o luminiscentes, metales y radionucleidos unidos al anticuerpo o mediante marcadores indirectos, como fosfatasa alcalina o peroxidasa de rábano picante.
Puede incorporarse en el inmunoensayo el uso de anticuerpos inmovilizados o fragmentos de los mismos. Los anticuerpos pueden inmovilizarse sobre una variedad de soportes, como partículas de matriz magnéticas o cromatográficas, la superficie de una placa de ensayo (como pocillos de microtitulación), piezas de un material de sustrato sólido y similares. Se puede preparar una tira de ensayo recubriendo el anticuerpo o la pluralidad de anticuerpos en una matriz sobre un soporte sólido. Esta tira puede sumergirse luego en la muestra biológica de prueba y luego procesarse rápidamente a través de lavados y pasos de detección para generar una señal medible, como una mancha coloreada.
El ELISA sándwich mide la cantidad de antígeno entre dos capas de anticuerpos (es decir, un anticuerpo de captura y un anticuerpo de detección (que puede estar marcado con un marcador detectable)). El monómero de laminina gamma 2 y/o por lo menos un biomarcador adicional, es decir, PIVKA-II, AFP, CEA y/o CA19-9, a medir, puede contener por lo menos dos sitios antigénicos capaces de unirse al anticuerpo. Pueden usarse anticuerpos monoclonales o policlonales como los anticuerpos de captura y detección en el ELISA sándwich.
Generalmente, se emplean por lo menos dos anticuerpos para separar y cuantificar el monómero de laminina gamma 2 o el por lo menos un biomarcador adicional, es decir, CEA y/o CA19-9 (así como cualquier analito adicional), en una muestra de prueba o biológica. Más específicamente, los por lo menos dos anticuerpos se unen a ciertos epítopos de monómero de laminina gamma 2 o el por lo menos un biomarcador adicional que forman un complejo inmune que se denomina "sándwich". Pueden usarse uno o más anticuerpos para capturar el monómero de laminina gamma 2 o el por lo menos un biomarcador adicional en la muestra de prueba (estos anticuerpos son referidos frecuentemente como anticuerpo de "captura" o anticuerpos de "captura") y se usan uno o más anticuerpos para unir un marcador detectable (concretamente, cuantificable) al sándwich (estos anticuerpos son referidos frecuentemente como anticuerpo de "detección" o anticuerpos de "detección"). En un ensayo sándwich, ambos anticuerpos que se unen a su epítopo pueden no verse disminuidos por la unión de cualquier otro anticuerpo en el ensayo a su epítopo respectivo. En otras palabras, los anticuerpos pueden seleccionarse de tal manera que uno o más de los primeros anticuerpos puestos en contacto con una muestra de prueba sospechosa de contener monómero de laminina gamma 2 o el por lo menos un biomarcador adicional no se unan a todo o parte de un epítopo reconocido por el segundo anticuerpo o anticuerpos posteriores, interfiriendo de este modo con la capacidad del uno o más segundos anticuerpos de detección para unirse con el monómero de laminina gamma 2 o el por lo menos un biomarcador adicional.
En una realización preferida, puede ponerse en contacto una muestra de prueba o biológica que se sospecha que contiene monómero de laminina gamma 2 y/o por lo menos un biomarcador adicional, es decir, CEA y/o CA19-9, con por lo menos un primer anticuerpo de captura (o anticuerpos) y por lo menos un segundo anticuerpo de detección ya sea simultánea o secuencialmente. En el formato de ensayo sándwich, una muestra de prueba que se sospechosa que contiene monómero de laminina gamma 2 y/o por lo menos un biomarcador adicional se pone en contacto con el por lo menos un primer anticuerpo de captura que se une específicamente a un epítopo particular en condiciones que permiten formación de un complejo de primer anticuerpo-monómero de laminina gamma 2 o -por lo menos un biomarcador adicional. Si se usa más de un anticuerpo de captura, se forma un complejo primer de anticuerpo de captura múltiple-monómero de laminina gamma 2 o -por lo menos un biomarcador adicional. En un ensayo sándwich, los anticuerpos, preferiblemente, el por lo menos un anticuerpo de captura, se usan en cantidades molares en exceso de la cantidad máxima de monómero de laminina gamma 2 o el por lo menos un biomarcador
adicional esperado en la muestra de prueba.
Opcionalmente, antes de poner en contacto la muestra de prueba con el por lo menos un primer anticuerpo de captura, el por lo menos un primer anticuerpo de captura puede unirse a un soporte sólido que facilite la separación del complejo de primer anticuerpo-monómero de laminina gamma 2 o -por lo menos un biomarcador adicional de la muestra de prueba. Puede usarse cualquier soporte sólido conocido en la técnica, incluyendo pero no limitado a, soportes sólidos hechos de materiales poliméricos en forma de pocillos, tubos o perlas. El anticuerpo (o anticuerpos) puede unirse al soporte sólido por adsorción, por unión covalente usando un agente de acoplamiento químico o por otros medios conocidos en la técnica, siempre que dicha unión no interfiera con la capacidad del anticuerpo para unirse al marcador. Además, si es necesario, el soporte sólido puede derivatizarse para permitir la reactividad con varios grupos funcionales en el anticuerpo. Dicha derivatización requiere el uso de ciertos agentes de acoplamiento como, pero no limitado a, anhídrido maleico, N-hidroxisuccinimida y 1-etil-3-(3-dimetilaminopropil)carbodiimida.
Después de que la muestra de prueba que se sospecha que contiene monómero de laminina gamma 2 y/o por lo menos un biomarcador adicional se pone en contacto con el por lo menos un primer anticuerpo de captura, la muestra de prueba se incuba para permitir la formación de un complejo de primer anticuerpo de captura (o anticuerpo múltiple)- monómero de laminina gamma 2 o -por lo menos un biomarcador adicional. La incubación se puede llevar a cabo a un pH de aproximadamente 4,5 a aproximadamente 10,0, a una temperatura de aproximadamente 2° C a aproximadamente 45° C, y durante un período de por lo menos aproximadamente un (1) minuto a aproximadamente dieciocho (18) horas, de aproximadamente 2-6 minutos, o de aproximadamente 3-4 minutos.
Después de la formación del complejo de primer/múltiple anticuerpo de captura-monómero de laminina gamma 2 o por lo menos un complejo biomarcador adicional, el complejo se pone en contacto con por lo menos un segundo anticuerpo de detección (en condiciones que permiten la formación de un complejo de primer/múltiple anticuerpo-monómero de laminina gamma 2 o -por lo menos un biomarcador adicional-segundo anticuerpo). Si el complejo de primer anticuerpo-monómero de laminina gamma 2 o -por lo menos un biomarcador adicional se pone en contacto con más de un anticuerpo de detección, se forma entonces un complejo de detección de anticuerpos múltiple de primer/múltiple anticuerpo de captura-monómero de laminina gamma 2 o -por lo menos un biomarcador adicional. Como con el primer anticuerpo, cuando el por lo menos un segundo (y subsiguientes) anticuerpo se pone en contacto con el complejo de primer anticuerpo-monómero de laminina gamma 2 o -por lo menos un biomarcador adicional, se requiere un período de incubación en condiciones similares a las descritas anteriormente para la formación del complejo de primer/múltiple anticuerpo-monómero de laminina gamma 2 o -por lo menos un biomarcador/anticuerpo múltiple adicional. Por lo menos un segundo anticuerpo contiene un marcador detectable. El marcador detectable puede unirse al por lo menos un segundo anticuerpo antes, simultáneamente o después de la formación del complejo de primer/múltiple anticuerpo-monómero de laminina gamma 2 o -por lo menos un biomarcador/anticuerpo múltiple adicional. Puede usarse cualquier marcador detectable conocido en la técnica.
g. Nivel de referencia
El método de diagnóstico proporcionado en la presente usa los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9 para identificar y determinar si un sujeto padece o corre el riesgo de padecer la enfermedad o no. Los niveles de monómero de laminina gamma 2, CEA y CA19-9 medidos en la muestra obtenida del sujeto y mayores que los niveles de referencia respectivos identifican al sujeto como que padece o corre el riesgo de padecer la enfermedad. Los niveles de monómero de laminina gamma 2 y/o el por lo menos un biomarcador adicional menores o iguales a los niveles de referencia respectivos pueden identificar que el sujeto no padece o no está en riesgo de padecer la enfermedad.
(1) Niveles de referencia para monómero de laminina gamma 2, CEA y/o CA19-9
Generalmente, pueden emplearse niveles predeterminados o de referencia como punto de referencia para evaluar los resultados obtenidos tras analizar una muestra de prueba para el monómero de laminina gamma 2, CEA y CA19-9. Generalmente, al hacer tal comparación, los niveles predeterminados se obtienen ejecutando un ensayo particular un número suficiente de veces y en condiciones apropiadas de tal manera que un enlace o asociación de la presencia, cantidad o concentración del analito con un estadio o criterio de valoración particular de la enfermedad con indicaciones particulares. Típicamente, los niveles predeterminados se obtienen con ensayos de sujetos de referencia (o poblaciones de sujetos). El sujeto de referencia puede ser un sujeto de control. La población de referencia o el grupo de referencia puede ser un grupo de control. El monómero de laminina gamma 2, CEA y CA19-9 medidos pueden incluir el monómero de laminina gamma 2, CEA, y CA19-9, fragmentos de los mismos, productos de degradación de los mismos, y/o productos de escisión enzimática de los mismos.
En particular, con respecto a los niveles predeterminados empleados para controlar la progresión de la enfermedad y/o el tratamiento, la cantidad o concentración de fragmentos de monómero de laminina gamma 2,
PIVKA-II, AFP, CEA y/o CA19-9 pueden ser "sin cambios", "favorable" (o "alterado favorablemente"), o
"desfavorable" (o "alterado desfavorablemente"). "Elevado" o "aumentado" se refiere a una cantidad o una
concentración en una muestra de prueba que es más alta o mayor que un nivel o intervalo típico o normal (por
ejemplo, nivel predeterminado), como un nivel típico o normal encontrado en un grupo de control o muestra de
control, o es más alto o mayor que otro nivel o intervalo de referencia (por ejemplo, muestra anterior o de referencia).
El término "disminuido" o "reducido" se refiere a una cantidad o una concentración en una muestra de prueba que es
inferior o menor a un nivel o intervalo típico o normal (por ejemplo, nivel predeterminado), como un nivel típico o
normal encontrado en un grupo de control o muestra de control, o es inferior o menor que otro nivel o intervalo de
referencia (por ejemplo, muestra anterior o de referencia). El término "alterado" se refiere a una cantidad o una
concentración en una muestra que está alterada (aumentada o disminuida) sobre un nivel o intervalo típico o normal
(por ejemplo, nivel predeterminado), como un nivel típico o normal encontrado en un grupo de control o muestra de
control, o sobre otro nivel o intervalo de referencia (por ejemplo, muestra anterior o de referencia).
Los niveles o intervalos típicos o normales para el monómero de laminina gamma 2, CEA y CA19-9 se
definen de acuerdo con la práctica estándar. Se puede considerar que se ha producido un denominado nivel alterado
o alteración cuando hay algún cambio neto en comparación con el nivel o intervalo típico o normal, o el nivel o
intervalo de referencia que no puede explicarse por un error experimental o variación de la muestra. En algunas
realizaciones, el nivel medido en una muestra particular se comparará con el nivel o intervalo de niveles
determinados en muestras similares de un sujeto llamado normal, es decir, un sujeto de control. En este contexto, un
sujeto "normal" (a veces denominado "control" o "sano") es un individuo sin cáncer de páncreas detectable, y un
paciente o población "normal" es uno o unos que no presentan cáncer de páncreas detectable, por ejemplo. Un
"sujeto aparentemente normal" es aquel en el que el monómero de laminina gamma 2, CEA y CA19-9 no se ha
evaluado o se está evaluando. Se dice que el nivel de un analito está "elevado" cuando el analito es normalmente
indetectable (por ejemplo, el nivel normal es cero, o dentro de un intervalo de aproximadamente 25 a
aproximadamente 75 percentiles de poblaciones normales), pero se detecta en una muestra de prueba, así como
cuando el analito está presente en la muestra de prueba a un nivel superior al normal.
En una realización, el nivel de referencia para CEA puede ser de aproximadamente 5,0 ng/ml. En otra
realización, el nivel de referencia para CEA en suero puede ser 5,0 ng/ml. En otras realizaciones, el nivel de
referencia para CEA en suero puede ser de aproximadamente 1,0 ng/ml, 1,5 ng/ml, 2,0 ng/ml, 2,5 ng/ml, 3,0 ng/ml,
3.5 ng/ml, 4,0 ng/ml, 4,5 ng/ml, 5,0 ng/ml, 5,5 ng/ml, 6,0 ng/ml, 6,5 ng/ml, 7,0 ng/ml, 7,5 ng/ml, 8,0 ng/ml, 8,5 ng/ml,
9.0 ng/ml, 9,5 ng ml, o 10,0 ng/ml.
Los valores de corte (o valores de corte predeterminados) pueden determinarse mediante la metodología
del Modelo de Índice Adaptativo (AIM). Los valores de corte (o valores de corte predeterminados) pueden
determinarse mediante un análisis de curva operativa del receptor (ROC) a partir de muestras biológicas del grupo
de pacientes. El análisis ROC, como se conoce generalmente en las técnicas biológicas, es una determinación de la
capacidad de una prueba para discriminar una condición de otra, por ejemplo, para determinar el rendimiento de
cada marcador en la identificación de un paciente que tiene CRC. Una descripción del análisis ROC tal como se
aplica de acuerdo con la presente divulgación se proporciona en P.J. Heagerty et al., Time-dependent ROC curves
for censored survival data and a diagnostic marker, Biometrics 56:337-44(2000).
Alternativamente, los valores de corte pueden determinarse mediante un análisis de cuartil de muestras biológicas de un grupo de pacientes. Por ejemplo, un valor de corte puede determinarse seleccionando un valor que corresponda a cualquier valor en el intervalo del percentil 25-75, preferiblemente un valor que corresponda al percentil 25, el percentil 50 o el percentil 75, y más preferiblemente el percentil 75.
Estos análisis estadísticos pueden realizarse usando cualquier método conocido en la técnica y pueden implementarse mediante cualquier número de paquetes de software disponibles comercialmente (por ejemplo, de Analyse-it Software Ltd., Leeds, UK; StataCorp Lp , College Station, TX; sAs Institute Inc., Cary, NC.).
3. Método de monitorización de la progresión de la enfermedad.
También se divulga en la presente un método para monitorizar la progresión de la enfermedad en un sujeto con necesidad de ello. El método de monitorización puede aplicar el método de diagnóstico descrito anteriormente para determinar si la enfermedad ha progresado o no en el sujeto.
El método de monitorización puede incluir obtener una primera muestra biológica del sujeto y una segunda muestra biológica del sujeto. La primera muestra biológica puede obtenerse del sujeto por lo menos aproximadamente día, 2 días, 3 días, 4 días, 5 días, 6 días, 7 días, 8 días, 9 días, 10 días, 11 días, 12 días, 13 días, 14 días, 15 días, 16 días, 17 días, 18 días, 19 días, 20 días, 21 días, 22 días, 23 días, 24 días, 25 días, 26 días, 27 días, 28 días, 29 días, 30 días, 31 días, 32 días, 33 días, 34 días, 35 días, 36 días, 37 días, 38 días, 39 días, 40 días, 41 días, 42 días, 43 días, 44 días, 45 días, 46 días, 47 días, 48 días, 49 días, 50 días, 51 días, 52 días, 53 días, 54 días, 55 días, 56 días, 57 días, 58 días, 59 días, 60 días, 1 semana, 2 semanas, 3 semanas, 4 semanas, 5 semanas, 6 semanas, 7 semanas, 8 semanas, 9 semanas, 10 semanas, 11 semanas, 12 semanas, 13 semanas, 14 semanas, 15 semanas, 16 semanas, 17 semanas, 18 semanas, 19 semanas, 20 semanas, 21 semanas, 22 semanas, 23 semanas, 24 semanas, 25 semanas, 26 semanas, 27 semanas, 28 semanas, 29 semanas, 30 semanas, 31 semanas, 32 semanas, 33 semanas, 34 semanas, 35 semanas, 36 semanas, 37 semanas, 38 semanas, 39 semanas, 40 semanas, 41 semanas, 42 semanas, 43 semanas, 44 semanas, 45 semanas, 46 semanas, 47 semanas, 48 semanas, 49 semanas, 50 semanas, 51 semanas, 52 semanas, 1 mes, 2 meses, 3 meses, 4 meses, 5 meses, 6 meses, 7 meses, 8 meses, 9 meses, 10 meses, 11 meses, 12 meses, 13 meses, 14 meses, 15 meses, 16 meses, 17 meses, 18 meses, 19 meses, 20 meses, 21 meses, 22 meses, 23 meses, 24 meses, 1 año, 2 años, 3 años, 4 años, o 5 años antes de que se obtenga la segunda muestra biológica del sujeto.
El método de monitorización también puede incluir medir un primer nivel de monómero de laminina gamma 2 en la primera muestra biológica y un segundo nivel de monómero de laminina gamma 2 en la segunda muestra biológica. El método de monitorización puede incluir además comparar el primer y el segundo niveles de monómero de laminina gamma 2 y determinar que (i) la enfermedad ha progresado en el sujeto cuando el segundo nivel de monómero de laminina gamma 2 es mayor que el primer nivel de monómero de laminina gamma 2 o (ii) la enfermedad no ha progresado en el sujeto cuando el segundo nivel de monómero de laminina gamma 2 es equivalente o menor que el primer nivel de monómero de laminina gamma 2.
El método de monitorización puede incluir además medir un primer nivel del por lo menos un biomarcador adicional en la primera muestra biológica y un segundo nivel del por lo menos un biomarcador adicional en la segunda muestra biológica y comparar el primer y el segundo nivel del por lo menos un biomarcador adicional. El método de monitorización también puede determinar que la enfermedad ha progresado en el sujeto cuando el segundo nivel de monómero de laminina gamma 2 y el por lo menos un biomarcador adicional es mayor que el primer nivel de monómero de laminina gamma 2 y el por lo menos un biomarcador adicional, respectivamente, o la enfermedad no ha progresado en el sujeto cuando el segundo nivel de monómero de laminina gamma 2 y el por lo menos un biomarcador adicional es equivalente o menor que el primer nivel de monómero de laminina gamma 2 y el por lo menos un biomarcador adicional, respectivamente.
4. Kit
También se proporciona en la presente un kit como se define en las reivindicaciones. El kit puede incluir instrucciones para detectar el monómero de laminina gamma 2 y/o por lo menos un biomarcador adicional. Las instrucciones incluidas en el kit pueden adherirse al material de embalaje o pueden incluirse como prospecto. Las instrucciones pueden ser materiales impresos o escritos, pero no se limitan a ellos. Esta divulgación contempla cualquier medio capaz de almacenar tales instrucciones y comunicarlas a un usuario final. Tales medios incluyen, pero no se limitan a, medios de almacenamiento electrónicos (por ejemplo, discos magnéticos, cintas, cartuchos, chips), medios ópticos (por ejemplo, CD ROM) y similares. Como se usa en la presente, el término "instrucciones" puede incluir la dirección de un sitio de Internet que proporciona las instrucciones.
El kit también comprende uno o más recipientes, como viales o botellas, con cada uno de los anticuerpos proporcionados en recipientes separados.
Por ejemplo, el kit puede comprender Instrucciones para analizar la muestra de prueba para determinar el monómero de laminina gamma 2, CEA y CA19-9 mediante inmunoensayo, por ejemplo, inmunoensayo de micropartículas quimioluminiscentes. Las instrucciones pueden estar en papel o en formato legible por ordenador, como un disco, CD, DVD o similar. El kit contiene por lo menos un anticuerpo de captura que se une específicamente al monómero de laminina gamma 2, por lo menos un anticuerpo de captura que se une específicamente a CEA y por lo menos un anticuerpo de captura que se une específicamente a CA19-9. El kit también puede contener un anticuerpo conjugado (como un anticuerpo marcado con un marcador detectable) para cada anticuerpo de captura (es decir, un anticuerpo conjugado para cada uno de los anticuerpos de captura que se unen específicamente al monómero de laminina gamma 2, CEA y CA19-9, respectivamente). Alternativa o adicionalmente, el kit puede comprender un calibrador o control, por ejemplo, purificado y opcionalmente liofilizado (por ejemplo, monómero de laminina gamma 2, CEA y/o CA19-9) y/o por lo menos un recipiente (por ejemplo, tubo, placas de microtitulación o tiras, que ya pueden estar recubiertas con un anticuerpo monoclonal de monómero gamma 2, CEA y/o CA19-9 anti-laminina) para realizar el ensayo, y/o un tampón, como un tampón de ensayo o un tampón de lavado, cualquiera de los cuales puede proporcionarse como una solución concentrada, una solución de sustrato para el marcador detectable (por ejemplo, un marcador enzimático) o una solución de parada. Preferiblemente, el kit comprende todos los componentes, es decir, reactivos, estándares, tampones, diluyentes, etc., que son necesarios para realizar el ensayo. Las instrucciones también pueden incluir instrucciones para generar una curva estándar o un estándar de referencia con el propósito de cuantificar el monómero de laminina gamma 2 y/o los biomarcadores adicionales (es decir, CEA y CA19-9).
Como se ha mencionado anteriormente, cualquier anticuerpo que se proporcione en el kit, como los anticuerpos recombinantes específicos para el monómero de laminina gamma 2 y los biomarcadores adicionales (es decir, CEA y CA19-9) pueden incorporar un marcador detectable, como un fluoróforo, una fracción radiactiva, una enzima, un marcador de biotina/avidina, un cromóforo, un marcador quimioluminiscente o similares, o el kit puede incluir reactivos para marcar los anticuerpos o reactivos para detectar los anticuerpos (por ejemplo, anticuerpos de detección) y/o para marcar los analitos o reactivos para detectar el analito. Los anticuerpos, calibradores y/o controles pueden proporcionarse en recipientes separados o pre-dispensarse en un formato de ensayo apropiado, por ejemplo, en placas de microtitulación.
Opcionalmente, el kit incluye componentes de control de calidad (por ejemplo, paneles de sensibilidad, calibradores y controles positivos). La preparación de reactivos de control de calidad es bien conocida en la técnica y se describe en hojas de inserción para una variedad de productos de inmunodiagnóstico. Los miembros del panel de sensibilidad se usan opcionalmente para establecer las características de rendimiento del ensayo, y además opcionalmente son indicadores útiles de la integridad de los reactivos del kit de inmunoensayo, y la estandarización de los ensayos.
El kit también puede incluir opcionalmente otros reactivos necesarios para realizar un ensayo de diagnóstico o facilitar evaluaciones de control de calidad, como tampones, sales, enzimas, cofactores enzimáticos, sustratos, reactivos de detección y similares. También pueden incluirse en el kit otros componentes, como tampones y soluciones para el aislamiento y/o el tratamiento de una muestra de prueba (por ejemplo, reactivos de pretratamiento). El kit puede incluir adicionalmente uno o más controles adicionales. Uno o más de los componentes del kit pueden estar liofilizados, en cuyo caso el kit puede comprender además reactivos adecuados para la reconstitución de los componentes liofilizados.
Los varios componentes del kit se proporcionan opcionalmente en recipientes adecuados según sea necesario, por ejemplo, una placa de microtitulación. El kit puede incluir además recipientes para contener o almacenar una muestra (por ejemplo, un recipiente o cartucho para una muestra sanguínea). Cuando sea apropiado, el kit también puede contener opcionalmente recipientes de reacción, recipientes de mezclado y otros componentes que facilitan la preparación de reactivos o la muestra de prueba. El kit también puede incluir uno o más instrumentos para ayudar a obtener una muestra de prueba, como una jeringuilla, pipeta, fórceps, cuchara medidora o similares.
Si el marcador detectable es por lo menos un compuesto de acridinio, el kit puede comprender por lo menos una acridinio-9-carboxamida, por lo menos un éster de arilo de acridinio-9-carboxilato, o cualquier combinación de los mismos. Si el marcador detectable es por lo menos un compuesto de acridinio, el kit también puede comprender una fuente de peróxido de hidrógeno, como un tampón, una solución y/o por lo menos una solución básica.
Si se desea, el kit puede contener una fase sólida, como una partícula magnética, perla, tubo de ensayo, placa de microtitulación, cubeta, membrana, molécula de andamiaje, película, papel de filtro, un cristal de cuarzo, disco o chip. El kit también puede incluir un marcador detectable que puede estar o está conjugado con un anticuerpo, tal como un anticuerpo que funciona como un anticuerpo de detección. El marcador detectable puede ser, por ejemplo, un marcador directo, que puede ser una enzima, oligonucleótido, nanopartícula, quimioluminóforo, fluoróforo, neutralizador de fluorescencia, neutralizador de quimioluminiscencia, o biotina. Los kits pueden incluir opcionalmente cualquier reactivo adicional necesario para detectar el marcador.
Si se desea, el kit puede comprender además uno o más componentes, solos o en combinación adicional con instrucciones, para analizar la muestra de prueba para otro analito, que puede ser un biomarcador, como un biomarcador del cáncer. Los ejemplos de analitos incluyen, pero no están limitados a, PIVKA-II, AFP, y fragmentos de PIVKA-II, AFP, así como otros analitos y biomarcadores analizados en la presente, o conocidos de otro modo en la técnica. En algunos casos, uno o más componentes para analizar una muestra de prueba para monómero de laminina gamma 2, CEA y CA19-9 permiten la determinación de la presencia, cantidad o concentración del monómero de laminina gamma 2, CEA y CA19-9. También puede analizarse una muestra, como una muestra de suero, para el monómero de laminina gamma 2, CEA y/o CA19-9 usando TOF-MS y un estándar interno.
El kit (o componentes del mismo), así como los métodos descritos anteriormente, que detectan la concentración de monómero de laminina gamma 2 y/o los biomarcadores adicionales (es decir, CEA y CA19 -9) en una muestra de prueba mediante un inmunoensayo como se describe en la presente, puede adaptarse para su uso en una variedad de sistemas automatizados y semiautomatizados (incluyendo aquellos en los que la fase sólida comprende una micropartícula), como se describe, por ejemplo, en las Patentes de Estados Unidos N° 5.089.424 y 5.006.309, y comercializado, por ejemplo, por Abbott Laboratories (Abbott Park, IL) como ARCHITECT®.
Algunas de las diferencias entre un sistema automatizado o semiautomatizado en comparación con un sistema no automatizado (por ejemplo, ELISA) incluyen el sustrato al que está unido el primer compañero de unión específico (por ejemplo, anticuerpo de analito o anticuerpo de captura) (que puede afectar la formación de sándwich y la reactividad del analito), y la duración y el momento de la captura, detección y/o cualquier paso de lavado opcional. Mientras que un formato no automatizado, como un ELISA, puede requerir un tiempo de incubación relativamente más largo con la muestra y el reactivo de captura (por ejemplo, aproximadamente 2 horas), un formato automatizado o semiautomatizado (por ejemplo, ARCHITECT® y cualquier plataforma sucesora, Abbott Laboratories) puede tener un tiempo de incubación relativamente más corto (por ejemplo, aproximadamente 18 minutos para ARCHITECT®). De manera similar, mientras que un formato no automatizado como un ELISA puede incubar un anticuerpo de detección como el reactivo conjugado durante un tiempo de incubación relativamente más largo (por ejemplo, aproximadamente 2 horas), un formato automatizado o semiautomatizado (por ejemplo, ARCHITECT® y cualquier plataforma sucesora) puede tener un tiempo de incubación relativamente más corto (por ejemplo, aproximadamente 4 minutos para ARCHITECT® y cualquier plataforma sucesora).
Otras plataformas disponibles de Abbott Laboratories incluyen, pero no están limitadas a, AxSYM®, IMx® (ver, por ejemplo, la Patente de Estados Unidos N° 5.294.404, PRISm®, EIA (perla y Quantum™ II, así como otras plataformas. Además, los ensayos, los kits y los componentes del kit pueden emplearse en otros formatos, por ejemplo, en sistemas electroquímicos u otros sistemas de análisis portátiles o de punto de atención. La presente divulgación es, por ejemplo, aplicable al sistema de inmunoensayo electroquímico comercial Abbott Point of Care (i-STAT®, Abbott Laboratories) que realiza inmunoensayos tipo sándwich. Los inmunosensores y sus métodos de fabricación y funcionamiento en dispositivos de prueba de un solo uso se describen, por ejemplo, en la Patente de Estados Unidos N° 5.063.081, Publicación de Solicitud de Patente de Estados Unidos N° 2003/0170881, Publicación de Solicitud de Patente de Estados Unidos N° 2004/0018577, Publicación de Solicitud de Patente de Estados Unidos N° 2005/0054078, y la Publicación de Solicitud de Patente de Estados Unidos N° No. 2006/0160164.
En particular, con respecto a la adaptación de un ensayo al sistema I-STAT®, se prefiere la siguiente configuración. Se fabrica un chip de silicio microfabricado con un par de electrodos de trabajo amperométricos de oro y un electrodo de referencia de cloruro de plata-plata. En uno de los electrodos de trabajo, se adhieren las perlas de poliestireno (0,2 mm de diámetro) con anticuerpo de captura inmovilizado a un recubrimiento de polímero de alcohol polivinílico estampado sobre el electrodo. Este chip se monta en un cartucho I-STAT® con un formato de fluidos adecuado para inmunoensayo. En una parte de la pared de la cámara de retención de muestras del cartucho hay una capa que comprende el anticuerpo de detección marcado con fosfatasa alcalina (u otro marcador). Dentro de la bolsa de fluido del cartucho hay un reactivo acuoso que incluye fosfato de p-aminofenol.
En funcionamiento, una muestra sospechosa de contener monómero de laminina gamma 2 y/o el por lo menos un biomarcador adicional se añade a la cámara de retención del cartucho de prueba y el cartucho se inserta en el lector I-STAT®. Después de que el segundo anticuerpo (anticuerpo de detección) se haya disuelto en la muestra, un elemento de bomba dentro del cartucho fuerza a la muestra a un conducto que contiene el chip. Aquí se oscila para promover la formación del sándwich entre el primer anticuerpo de captura y el segundo anticuerpo de detección marcado. En el penúltimo paso del ensayo, el fluido se expulsa de la bolsa y hacia el conducto para lavar la muestra del chip y hacia una cámara de desechos. En el paso final del ensayo, el marcador de fosfatasa alcalina reacciona con fosfato de p-aminofenol para escindir el grupo fosfato y permitir que el p-aminofenol liberado se oxide electroquímicamente en el electrodo de trabajo. En base a la corriente medida, el lector es capaz de calcular la cantidad de monómero de laminina gamma 2 y/o por lo menos un biomarcador adicional (por ejemplo, PIVKA-II, AFP, CEA y/o CA19-9) en la muestra por medio de un algoritmo incorporado y la curva de calibración determinada de fábrica.
La presente invención se ilustra por los siguientes ejemplos no limitativos.
5. Ejemplos
Ejemplo 1 - Ejemplo de referencia
Métodos y materiales
Anticuerpos y antígenos. La proteína monomérica recombinante Ln-y2 se purificó del medio de cultivo de transfectantes de células de riñón canino Madin-Darby. El heterotrimérico recombinante Ln-332 se adquirió de Oriental Yeast Co., Ltd. (Tokio, Japón). Para CLIA y transferencia Western, se preparó un anticuerpo monoclonal anti-Ln-y2 (2H2) y un anticuerpo policlonal anti-Ln-y2 de dominio III, como se describe en el Ejemplo 2. Se adquirió un anticuerpo monoclonal anti-Ln-a3 de ratón de Oriental Yeast Co., Ltd.
Análisis de marcadores tumorales para HCC. El nivel de AFP en suero se midió usando el sistema ARCHITECT y el nivel de PIVKA-II se midió usando LUMIPULSE (Fujirebio, Inc., Tokio, Japón) en SRL Tokyo Laboratories, Inc. (Tokio, Japón).
Análisis estadístico. Los niveles de Ln-y2 en suero se informaron como media ± desviación estándar (SD) y mediana: intervalo. Los niveles de AFP y PIVKA-II en suero se informaron como mediana:intervalo. La transformación logarítmica se usó en los valores de AFP y PIVKA-II para tener en cuenta el amplio intervalo de valores para ambos marcadores entre los pacientes con HCC. La prueba de Mann-Whitney se usó para datos continuos, Los valores p inferiores a 0,05 se consideraron significativos. Se usaron el software Graph Pad Prism 6 (San Diego, CA, USA) y el software Analyze-it (FIGS. 2-6 y 9-14) para generar los gráficos de dispersión, las curvas de características operativas del receptor (ROC) y el cálculo de área bajo las curvas ROC (AUC). El punto de corte óptimo incluía el punto en la curva ROC más cercano al (0, 1).
Ejemplo 2
Inmunoensayo de monómero de laminina gamma 2
Se estableció un inmunoensayo que detectó específicamente el monómero de laminina gamma 2.
Inmunoensayo quimioluminiscente totalmente automatizado (CLIA). Se midió la concentración de proteína Ln-y2 humana mediante un ensayo sándwich de dos pasos usando micropartículas paramagnéticas recubiertas con anticuerpo 2H2 (Nakagawa M et al., manuscrito en preparación) y anticuerpo policlonal de conejo marcado con acridinio. El método de ensayo se ajustó para su aplicación a una máquina de detección totalmente automatizada (ARCHITECT de Abbott Laboratories, Chicago, IL, USA).
Generación de anticuerpo policlonal dirigido contra monómero de laminina gamma 2. Se generó un anticuerpo policlonal dirigido contra el monómero de laminina gamma 2 inmunizando un conejo con dominio purificado III (aminoácidos 383-608) del monómero de laminina gamma 2 humano. Este dominio III recombinante se expresó y se purificó a partir de E. coli. Específicamente, el dominio III se expresó como una proteína de fusión GST usando la tecnología Gateway (Invitrogen). Los sueros de conejo se purificaron usando una columna de proteína A. La purificación adicional del anticuerpo policlonal se realizó con una agarosa magnética de anticuerpo monoclonal anti-His-tag (MBL) conjugada con el dominio III por diclorhidrato de dimetil pimelimidato (DMP). También se concentró el anticuerpo policlonal purificado.
Anticuerpo monoclonal 2H2. El mAb 2H2 era un anticuerpo monoclonal de ratón descrito en N. Koshikawa et al., Cancer Research (2008) 68(2):530-536. El mAb 2H2 se purificó del sobrenadante del hibridoma cultivado mediante una columna de proteína G.
Generación de monómero de laminina gamma 2 recombinante. El gen que codifica el monómero de laminina gamma 2 de longitud completa se introdujo en células MDCK para generar células MDCK transfectadas que expresan el monómero de laminina gamma 2. Las células MDCK que expresan altos niveles de monómero de laminina gamma 2 se seleccionaron mediante dilución limitante y se cultivaron en DMEM libre de suero (Invitrogen). El monómero de laminina gamma 2 se purificó usando una columna de anticuerpo monoclonal 2H2 (mAb 2H2) y se concentró mediante precipitación con sulfato de amonio.
Inmunoensayo. El mAb 2H2 se inmovilizó en micropartículas paramagnéticas. Específicamente, las micropartículas se lavaron con tampón MES (pH 5,5) y se añadieron N-(3-dimetilaminopropil)-N'-etilcarbodiimidaclorhidrato (Sigma-Aldrich) y N-hidroxi-succinimida (Sigma-Aldrich) a las micropartículas lavadas. Después de una incubación de 30 minutos a temperatura ambiente, las micropartículas se lavaron y se añadieron mAb 2H2 diluidos en tampón MES a las micropartículas lavadas. Después de 2 horas de incubación a temperatura ambiente, las micropartículas se lavaron con TBS, Tween al 1% y luego se almacenaron.
El tampón de dilución de micropartículas era un tampón TBS que contenía EDTA 20 mM, 1% de BSA, 0,2% de leche desnatada, 0,1% de Tween-20, 0,2 mg/ml de HBR, 0,2 mg/ml de IgG de ratón, 0,1% de ProClin300 y 100 ppm. Foamaway, pH 7,4. Las micropartículas se diluyeron en el tampón de dilución de micropartículas a una concentración de sólidos final de 0,05%.
El anticuerpo policlonal de conejo descrito anteriormente dirigido contra el dominio III del monómero de laminina gamma 2 humano se utilizó como un anticuerpo de detección. Específicamente, este anticuerpo policlonal se conjugó con acridinio en tampón PBS que contiene 0,5% de CHAPS. El exceso de acridinio se eliminó mediante la columna de centrifugación Zeba Micro Desalt (Thermo). El anticuerpo marcado con acridinio resultante se disolvió en tampón MES que contenía NaCl 0,15 M, 1,09% de TritonX405, 2,0 mg/ml de gammaglobulina bovina, 5% de BSA, 2% de Tween-20, 0,1% de ProClin300 y Foamaway a 100 ppm, pH 6,3..
La solución de dilución de inmunoensayo era tampón TBS que contenía 1% de BSA, 16,1% de sacarosa, 0,075% de azida sódica, 0,1% de ProClin950 y 100 ppm de Foamaway, pH 8,0. El diluyente de muestra era tampón PBS con 1% de BSA y 0,1% de Tween-20. El calibrador para el inmunoensayo era monómero de laminina gamma 2 recombinante diluido en el diluyente de muestra. Específicamente, el calibrador para monómero de laminina gamma 2 varió de 0 ng/ml y 20 ng/ml. Las cantidades específicas fueron 0,00, 0,01, 0,02, 0,05, 0,10, 1,00, 10,00 y 20,00 ng/ml.
El inmunoensayo se realizó en un instrumento de inmunoensayo, concretamente el analizador i2000 ARCHITECT. Se generó una curva de calibración para el monómero de laminina gamma 2 usando el calibrador. Las curvas de calibración ejemplares se muestran en la FIG. 1.
Ejemplo 3
Detección de monómero de laminina gamma 2 en especímenes
El inmunoensayo descrito anteriormente en el Ejemplo 2 se usó para detectar concentraciones séricas de monómero de laminina gamma 2 en varios especímenes. Se recogieron muestras de suero de los especímenes y se diluyeron en el diluyente de muestra descrito anteriormente.
Especímenes. Los especímenes eran especímenes de carcinoma hepatocelular (HCC), especímenes de cáncer de páncreas, especímenes de cáncer colorrectal (CRC), especímenes de cáncer de estómago, especímenes de cirrosis hepática (LC), especímenes de hepatitis, especímenes de pancreatitis/colangitis, especímenes de cáncer múltiple/metástasis, especímenes de insuficiencia hepática, especímenes benignos, especímenes de donantes sanos y otros especímenes de cáncer. Los especímenes se recogieron en fueron recolectadas en St. Marianna University School of Medicine. Para los controles normales, se recogieron especímenes de donantes sanos de voluntarios sanos sin antecedentes de enfermedad hepática, consumo de alcohol de menos de 40 g/semana y sin factores de riesgo de hepatitis viral. Para establecer el valor de corte para Ln-y2, se analizaron sueros de control de 52 voluntarios japoneses sanos. Las características demográficas y clínicas de voluntarios sanos y pacientes con enfermedad hepática crónica o HCC se muestran en la Tabla 1. Los niveles de Ln-y2 en suero medios y medianos de voluntarios sanos fueron 44,3 ± 17,6 pg/ml (media ± SD) y 41,1 pg/ml (intervalo: 10,9-79,0 pg/ml), respectivamente.
Tabla 1 Información demográfica y etiología de enfermedades hepáticas. Todos los datos se ex resaron como mediana: intervalo.
Resultados. Las FIGS. 2A y 2B muestran gráficos de puntos de la concentración sérica (pg/ml) de monómero de laminina gamma 2 para las muestras indicadas. Cada espécimen fue representado por un círculo sólido. La concentración sérica media para cada grupo de especímenes se representó mediante una línea continua. La media más 2 desviaciones estándar (media 2SD) de donantes sanos (HD) también se mostró con una línea continua que se extiende a lo largo del eje x y fue de 79,5 pg/ml. Las FIGS. 2C y 2D muestran gráficos de puntos de la concentración sérica (pg/ml) de monómero de laminina gamma 2 para los especímenes indicados. Cada espécimen se representó por un círculo sólido (FIGS. 2C y 2D). La concentración sérica media para cada grupo de especímenes se representó mediante una línea continua. El valor de corte derivado del análisis ROC de HCC en comparación con donantes sanos (HD) también se mostró con una línea continua que se extiende a lo largo del eje x y fue de 75,9 pg/ml. La concentración sérica del monómero de laminina gamma 2 fue mayor en los especímenes de HCC y de cáncer de páncreas en comparación con los especímenes de donantes sanos y los especímenes con otros carcinomas digestivos (es decir, cáncer colorrectal y cáncer de estómago).
Adicionalmente, la concentración sérica de monómero de laminina gamma 2 fue mayor en especímenes de HCC y cáncer de páncreas en comparación con especímenes de cirrosis hepática, especímenes de CH y especímenes de pancreatitis/colangitis. Sin embargo, un espécimen de cirrosis hepática con una concentración sérica más alta de monómero de laminina gamma 2 tenía un nivel de proteína alfa fetal (AFP) de 39,9 ng/ml (FIGS.
2B y 2D). Un espécimen de CH con una concentración sérica más alta de monómero de laminina gamma 2 tenía un nivel de proteína alfa fetal (AFP) de 39,0 ng/ml (FIGS. 2B y 2D). Un espécimen de pancreatitis/colangitis con una concentración sérica más alta de monómero de laminina gamma 2 tenía un nivel de antígeno de carbohidratos 19-9 (CA19-9) de 79,0 U/ml. Por consiguiente, los especímenes distintos de HCC y cáncer pancreático que tenían concentraciones séricas más altas de monómero de laminina gamma 2 tenían niveles anormales de otros marcadores de cáncer como AFP y CA19-9.
Ejemplo 4 - Ejemplo de referencia
Concentración sérica de monómero de laminina gamma 2 en etapas I-IV de HCC
Como se describe en el Ejemplo 3, la concentración sérica del monómero de laminina gamma 2 fue mayor en especímenes de HCC. Los especímenes de HCC se examinaron adicionalmente con respecto a la concentración sérica de monómero de laminina gamma 2 en diferentes etapas de HCC. Específicamente, el inmunoensayo descrito anteriormente en el Ejemplo 2 se usó para detectar concentraciones séricas de monómero de laminina gamma 2 de especímenes de etapa I de HCC, etapa II de HCC II, etapa III de HCC y etapa IV de HCC, así como de cirrosis hepática (LC), hepatitis (CH), y especímenes de donantes sanos. Se recogieron muestras de suero de los especímenes y se diluyeron en el diluyente de muestra descrito anteriormente.
Resultados. Los resultados de estos estudios se muestran en las FIGS. 3A-3B, que muestran la concentración sérica (pg/ml) de monómero de laminina gamma 2 para cada grupo de especímenes indicados. Cada espécimen se representó con un círculo sólido. La concentración sérica media de monómero de laminina gamma 2 para cada grupo de especímenes se indicó con una línea continua. La línea continua que se extiende a lo largo del eje x indica la media más 2 desviaciones estándar (media 2SD) para los especímenes de donantes sanos, que fue de 79,5 pg/ml en la FIG. 3A. La línea continua que se extiende a lo largo del eje x indica que el valor de corte derivado del análisis ROC de HCC en comparación con donantes sanos (HD) también se mostró con una línea continua que se extiende a lo largo del eje x y fue de 75,9 pg/ml en la FIG. 3B.
Como se muestra en las FIGS. 3A-3B, se observaron concentraciones séricas elevadas de monómero de laminina gamma 2 en especímenes de etapa I de HCC, etapa II de HCC II, etapa III de HCC y etapa IV de HCC en comparación con especímenes de LC, CH y de donantes sanos. Los especímenes de LC y CH con concentraciones séricas más altas de monómero de laminina gamma 2 tenían niveles anormales de proteína alfa fetal marcadora de cáncer (AFP), es decir, 39,9 ng/ml y 39,0 ng/ml. Por consiguiente, estos resultados indicaron que el monómero de laminina gamma 2 se detectó en suero de especímenes de HCC en etapa temprana y que los niveles de monómero de laminina gamma 2 en suero aumentaron con la etapa de HCC (es decir, aumentaron de manera dependiente de la etapa para HCC).
De acuerdo con la clasificación TNM, 10 pacientes fueron diagnosticados con etapa I, 18 con etapa II, 21 con etapa III y 8 con tumores de etapa IV. Los niveles de Ln-y2 aumentaron de la etapa I a la etapa IV con niveles medianos (intervalo) de 114,3 pg/ml (intervalo: 65,3-323,6 pg/ml), 184,3 pg/ml (intervalo: 39,5-549,1 pg/ml), 174,6 pg/ml (intervalo: 32,4-985,8 pg/ml) y 248,1 pg/ml (intervalo: 59,8-529,4 pg/ml), respectivamente (Fig. 12). Los valores de AFP correspondientes fueron de 5,3 ng/ml (intervalo: 2,2-44,6 ng/ml), 16,2 ng/ml (intervalo: 1,5-899 ng/ml), 72,5 ng/ml (intervalo: 3,2-2364 ng/ml), y 1116 ng/ml (intervalo: 5,3-417198 ng/ml) ng/ml para los HCC en etapa I, II, III y IV, respectivamente (Fig. 13). Los valores correspondientes de PIVKA-II fueron 55,0 mAU/ml (intervalo: 14,0-302 mAU/ml), 47,5 mAU/ml (intervalo: 13,0-5380) mAU/ml, 162 mAU/ml (intervalo: 11,0-20779), y 683 mAU/ml (intervalo: 32,0-75000 mAU/ml) para los HCC de etapa I, II, III y IV HCC, respectivamente (Fig. 14). Entre los pacientes con HCC en etapa temprana (T1 o T2), las tasas de positividad para Ln-y2, AFP y PIVKA-II fueron 17/28 (61%), 11/28
(39%) y 16/28 (57% ), respectivamente.
Ejemplo 5 - Ejemplo de referencia
Especificidad y sensibilidad de monómero de laminina gamma 2 como un marcador para HCC
Se examinaron la especificidad y la sensibilidad del monómero de laminina gamma 2, la proteína alfa fetal (AFP) y el antagonista II de la vitamina K inducido por proteínas (PIVKA-II) como marcadores de HCC. Específicamente, el nivel de cada marcador se examinó en 57 especímenes de HCC y 76 especímenes de donantes sanos, cirrosis hepática (LC) o hepatitis (CH), para un total de 133 especímenes.
Se generó un gráfico de características operativas del receptor (ROC) trazando la tasa de positivos verdaderos observada de monómero de laminina gamma 2, AFP y PIVKA-II en los especímenes de HCC frente a la tasa de falsos positivos observada del monómero de laminina gamma 2, AFP, y PIVKA-II en especímenes de donantes sanos, LC y CH. Por consiguiente, el gráfico ROC era un gráfico de sensibilidad (frecuencia de positivos verdaderos (TPF)) contra especificidad (frecuencia de falsos positivos (FPF)). Un valor de 1,000 representaba el 100% de sensibilidad y el 100% de especificidad. Este gráfico ROC se muestra en la FIG. 4A y el área bajo la curva (AUC) para cada uno de monómero de laminina gamma 2, AFP y PIVKA-II se muestra en la Tabla 2.
Tabla 2
Se examinaron la especificidad y la sensibilidad del monómero de laminina gamma 2, la proteína alfa fetal (AFP) y el antagonista II de la vitamina K inducido por proteínas (PIVKA-II) como marcadores de HCC. Específicamente, el nivel de cada marcador se examinó en 57 especímenes de HCC y 52 donantes sanos, para un total de 109 especímenes. Los niveles séricos de Ln-y2 se midieron en 24 pacientes con enfermedad hepática crónica y 57 pacientes con HCC (Fig. 9). La infección con HCV fue el factor etiológico más común entre los dos grupos de sujetos con enfermedad hepática. Las concentraciones de Ln-y2 medianas fueron de 76,7 pg/ml, con un intervalo entre 38,7 y 215,9 pg/ml (pacientes con enfermedad hepática crónica) y 173,2 pg/ml, con un intervalo entre 32,4 y 986 pg/ml (pacientes con HCC). Se observó un aumento significativo en los niveles de Ln-Y2 en pacientes con HCC en comparación con pacientes con enfermedad hepática crónica y voluntarios sanos (p <0,01).
Se generó un gráfico de características operativas del receptor (ROC) trazando la tasa de positivos verdaderos observada de monómero de laminina gamma 2, AFP y PIVKA-II en las muestras de HCC frente a la tasa de falsos positivos observada de monómero de laminina gamma 2, AFP, y PIVKA-II en especímenes de donantes sanos. Por consiguiente, el gráfico ROC era un gráfico de sensibilidad (frecuencia de positivos verdaderos (TPF)) frente a especificidad (frecuencia de falsos positivos (FPF)). Un valor de 1,000 representaba el 100% de sensibilidad y el 100% de especificidad. Este gráfico ROC se muestra en la FIG. 4B y el área bajo la curva (AUC) para cada uno del monómero de laminina gamma 2, AFP y PIVKA-II se muestran en la Tabla 3.
Tabla 3
Cuando el valor de corte se estableció en 75,9 pg/ml, la sensibilidad y la especificidad fueron del 86% (intervalo de confianza [IC] del 95%, 74-94%) y 98% (IC del 95%, 90-99%), respectivamente. La capacidad discriminativa de Ln-Y2 (AUC de curva ROC = 0,952; IC 95%, 91-99%) superó significativamente la de PIVKA-II (AUC de curva ROC = 0,825; IC del 95%, 73-92%, p <0,05 ) y fue tan eficaz como AFP (AUC de curva ROC = 0,929; IC del 95%, 88-98%) al comparar voluntarios sanos y pacientes con HCC. Cuando se compararon voluntarios sanos con pacientes con enfermedad hepática crónica no maligna, este valor de corte produjo una capacidad discriminativa para Ln-Y2 (AUC de curva ROC = 0,819; IC del 95%, 72-92%) con una sensibilidad y especificidad del 50% (IC del 95%, 29-71%) y 96% (IC del 95%, 87-99%), respectivamente. Con este valor de corte, se encontró positividad de LnY2 en 1 (2%), 12 (50%) y 50 (86%) sujetos entre voluntarios sanos, pacientes con enfermedad hepática crónica y pacientes con HCC, respectivamente. Estos resultados indican que este valor de corte (>75,9 pg/ml) es útil para distinguir pacientes con enfermedad hepática crónica, con o sin HCC, de sujetos sanos.
Se examinaron la especificidad y la sensibilidad del monómero de laminina gamma 2, la proteína alfa fetal (AFP) y el antagonista II de la vitamina K inducido por proteínas (PIVKA-II) como marcadores de HCC. Específicamente, el nivel de cada marcador se examinó en 57 especímenes de HCC y 24 especímenes de hepatitis (CH), para un total de 81 especímenes.
Se generó un gráfico de características operativas del receptor (ROC) representando la tasa de positivos verdaderos observada de monómero de laminina gamma 2, AFP y PIVKA-II en los especímenes de HCC frente a la tasa de falsos positivos observada del monómero de laminina gamma 2, AFP, y PIVKA-II en especímenes de CH. Por consiguiente, el gráfico ROC era un gráfico de sensibilidad (frecuencia de positivos verdaderos (TPF)) contra especificidad (frecuencia de falsos positivos (FPF)). Un valor de 1,000 representaba el 100% de sensibilidad y el 100% de especificidad. Este gráfico ROC se muestra en la FIG. 4C y el área bajo la curva (AUC) para cada uno del monómero de laminina gamma 2, AFP y PIVKA-II se muestran en la Tabla 4
Tabla 4
El valor de corte óptimo para distinguir el HCC de la enfermedad hepática crónica no maligna fue 116,6 pg/ml (Fig. 4C), con una sensibilidad y especificidad del 63% (IC del 95%, 49-76%) y 83% (IC del 95%, 63-95%), respectivamente. Al distinguir pacientes con enfermedad hepática crónica de aquellos con HCC, PIVKA-II (AUC de curva ROC = 0,845; IC del 95%, 76-93%) superó a Ln-Y2 (AUC de curva ROC = 0,793; IC del 95%, 69-89%; las diferencias no fueron estadísticamente significativas) y AFP (AUC de curva ROC = 0,788; IC del 95%, 69-89%). Se observó positividad de Ln-Y2 (>116,6 pg/ml) en 0/52 (0%), 4/24 (17%) y 36/57 (63%) sujetos entre voluntarios sanos, pacientes con enfermedad hepática crónica y pacientes con HCC, respectivamente. La positividad de AFP (>20 ng/ml; el límite superior normal informado en sujetos japoneses) (6) se observó en 0/52 (0%), 4/24 (17%) y 30/57 (53%) sujetos entre voluntarios sanos, pacientes con enfermedad hepática crónica y pacientes con HCC, respectivamente. Las concentraciones medianas (intervalo) de AFP fueron 2,3 ng/ml (controles sanos, intervalo: 0,9 8,2 ng/ml), 3,8 ng/ml (pacientes con enfermedad hepática crónica, intervalo: 1,2-109,7 ng/ml) y 24,4 ng/ml (pacientes con HCC, intervalo: 1,5-417199 ng/ml) (Fig. 10). La positividad de PIVKA-II (>40 mAU/ml, el límite superior normal informado en sujetos japoneses) (6) se observó en 1/52 (1,9%), 1/24 (4,2%) y 39/57 (68%) sujetos entre voluntarios sanos, pacientes con enfermedad hepática crónica y pacientes con HCC, respectivamente. Las concentraciones medianas (intervalo) de PIVKA-II fueron 24,5 mAU/ml (controles sanos, intervalo: 15,0-45,0 mAU/ml), 21,0 mAU/ml (pacientes con enfermedad hepática crónica, intervalo: 12,0-58,0 mAU/ml), y 103 mAU/ml (pacientes con HCC, intervalo: 11,0-75000 mAU/ml) (Fig. 11). Se encontró que los niveles de Ln-Y2, AFP y PIVKA-II eran significativamente elevados (p <0,001) en sueros de pacientes con HCC en comparación con sueros de tanto voluntarios sanos como pacientes con enfermedad hepática crónica. Se encontró que los niveles de Ln-Y2 y AFP eran significativamente elevados (p <0,01) en sueros de pacientes con enfermedad hepática crónica en comparación con sueros de voluntarios sanos.
Estos resultados indicaron que el monómero de laminina gamma 2 mostró mayor sensibilidad y especificidad como marcador para HCC que AFP y PIVKA-II, y por tanto, fue un marcador más preciso para HCC que AFP y PIVKA-II.
Además, la FIG. 5 A y la Tabla 5 muestran la tasa positiva de detección de HCC para monómero de laminina gamma 2, PIVKA-II, AFP y combinaciones de los mismos. El valor de corte del monómero de laminina gamma 2 fue la media más 2 desviaciones estándar (media 2SD) para las muestras de donantes sanos, que fue de 79,5 pg/ml. Tres muestras de HCC fueron negativas para los tres de monómero de laminina gamma 2, PIVKA-II y AFP.
Tabla 5
Estos resultados indicaron que el monómero de laminina gamma 2 tenía una tasa positiva más alta de detección de HCC que PIVKA-II o a Fp . La tasa positiva de detección de HCC fue la misma para el monómero de laminina gamma 2 y la combinación de AFP y PIVKA-II, es decir, 80%.
La tasa positiva de detección de HCC aumentó cuando se combinó el monómero laminina gamma 2 con PIVKA-II o AFP en comparación con el monómero de laminina gamma 2 solo, es decir, 93,0% o 86,0% frente a 77,2%. Sin embargo, la combinación de los tres marcadores proporcionó una tasa positiva de detección de HCC (94.7%) que fue equivalente a la tasa positiva de detección de Hc C proporcionada por la combinación de monómero de laminina gamma 2 y PIVKA-II (93.0%). Por consiguiente, la adición de AFP a la combinación de monómero de laminina gamma 2 y PIVKA-II no aumentó más la tasa positiva de detección de HCC.
La FIG. 5B y la Tabla 6 muestran la tasa positiva de detección de HCC para el monómero de laminina gamma 2, PIVKA-II, AFP y combinaciones de los mismos. El valor de corte del monómero de laminina gamma 2 se calculó a partir del análisis ROC de HCC en comparación con donantes sanos (HD), que fue de 75,9 pg/ml. Tres especímenes de HCC fueron negativos para los tres de monómero de laminina gamma 2, PIVKA-II y AFP.
Tabla 6
Estos resultados indicaron que el monómero de laminina gamma 2 tenía una tasa positiva más alta de detección de HCC que PIVKA-II o AFp . La tasa positiva de detección de HCC fue la misma para el monómero de laminina gamma 2 y la combinación de AFP y PIVKA-II, es decir, 80%.
La tasa positiva de detección de HCC aumentó cuando se combinó el monómero de laminina gamma 2 con PIVKA-II o AFP en comparación con el monómero de laminina gamma 2 solo, es decir, 84,2% o 94,7% frente a 87,7%. Sin embargo, la combinación de los tres marcadores proporcionó una tasa positiva de detección de HCC (94,7%) que fue equivalente a la tasa positiva de detección de HCC proporcionada por la combinación de monómero de laminina gamma 2 y PIVKA-II (94,7%). Por consiguiente, la adición de AFP a la combinación de monómero de laminina gamma 2 y PIVKA-II no aumentó más la tasa positiva de detección de HCC.
La FIG. 5C y la Tabla 7 muestran la tasa positiva de detección de HCC para monómero de laminina gamma 2 (>116,6 pg/ml), PIVKA-II (>40 mAU/ml), AFP (>20 ng/ml) y combinaciones de los mismos. El valor de corte del monómero de laminina gamma 2 se calculó a partir del análisis ROC de HCC en comparación con los especímenes de hepatitis (CH), que fue de 116,6 pg/ml. Mientras que la combinación de Ln-Y2 y PIVKA-II se detectó en 51/57
pacientes (89,5%), la combinación de Ln-Y2 y AFP se detectó en 46/57 (80,7%) y la combinación de PIVKA-II y AFP en 47/57 (82,5%). La combinación de los 3 marcadores se detectó en 54/57 pacientes (94,7%). Curiosamente, el 67% (12/18) de los pacientes que fueron negativos para PIVKA-II mostraron positividad para Ln-Y2. Tres especímenes de HCC fueron negativos para los tres de monómero de laminina gamma 2, PIVKA-II y AFP.
Tabla 7
Estos resultados indicaron que el monómero de laminina gamma 2 tenía una tasa positiva más alta de detección de HCC que PIVKA-II o a Fp . La tasa positiva de detección de HCC fue la misma para el monómero de laminina gamma 2 y la combinación de AFP y PIVKA-II, es decir, 80%.
La tasa positiva de detección de HCC aumentó cuando se combinó el monómero de laminina gamma 2 con PIVKA-II o AFP en comparación con el monómero de laminina gamma 2 solo, es decir, 63,2% o 89,5% frente a 80,7%. Sin embargo, la combinación de los tres marcadores proporcionó una tasa positiva de detección de HCC (94.7%) que fue equivalente a la tasa positiva de detección de HCC proporcionada por la combinación de monómero de laminina gamma 2 y PIVKA-II (89,5%). Por consiguiente, la adición de AFP a la combinación de monómero de laminina gamma 2 y PIVKA-II no aumentó más la tasa positiva de detección de HCC.
Ejemplo 6
Concentración sérica de monómero de laminina gamma 2 en las etapas III y IV del cáncer de páncreas Como se describe en el Ejemplo 3, la concentración sérica de monómero de laminina gamma 2 fue mayor en especímenes de cáncer de páncreas. Los especímenes de cáncer de páncreas se examinaron adicionalmente con respecto a la concentración sérica de monómero de laminina gamma 2 en diferentes etapas de cáncer de páncreas. Específicamente, se usó el inmunoensayo descrito en el Ejemplo 2 para detectar concentraciones séricas de monómero de laminina gamma 2 de especímenes de cáncer de páncreas en etapa III y de cáncer de páncreas en etapa IV, así como pancreatitis y especímenes de donantes sanos. Se recogieron muestras de suero de los especímenes y se diluyeron en el diluyente de muestra descrito anteriormente.
Resultados. Los resultados de estos estudios se muestran en la FIG. 6A y 6B, que muestran la concentración sérica (pg/ml) de monómero de laminina gamma 2 para cada grupo de especímenes indicados. Cada espécimen fue representado con un cuadrado sólido. La concentración sérica media de monómero de laminina gamma 2 para cada grupo de especímenes se indicó con una línea continua. La línea continua que se extiende a lo largo del eje x indica la media más 2 desviaciones estándar (media 2SD) para los especímenes de donantes sanos, que fue de 79,5 pg/ml en la FIG. 6A. La línea continua que se extiende a lo largo del eje x representa el valor de corte derivado del análisis ROC, que fue de 75,9 pg/ml en la FIG. 6B.
Como se muestra en la FIG. 6A y 6B, se observaron concentraciones séricas elevadas de monómero de laminina gamma 2 en el cáncer de páncreas en etapa III y en el cáncer de páncreas en etapa IV en comparación con pancreatitis y especímenes de donantes sanos. Por consiguiente, estos resultados indicaron que los niveles de monómero de laminina gamma 2 en suero aumentaron con la etapa del cáncer de páncreas (es decir, aumentaron de manera dependiente de la etapa).
Ejemplo 7
Especificidad y sensibilidad de monómero de laminina gamma 2 como marcador para cáncer de páncreas Se examinaron la especificidad y la sensibilidad del monómero de laminina gamma 2, el carcinoembrionario (CEA) y el antígeno de carbohidratos 19-9 (CA19-9) como marcadores de cáncer de páncreas. Específicamente, el nivel de cada marcador se examinó en 20 especímenes de cáncer de páncreas y 60 especímenes de pancreatitis o
de donantes sanos, para un total de 80 especímenes. Se generó un gráfico de características operativas del receptor (ROC) trazando la tasa de positivos verdaderos observada de monómero de laminina gamma 2, CEA y CA19-9 en los especímenes de cáncer de páncreas frente a la tasa de falsos positivos observada de monómero de laminina gamma 2, CEA y CA19 -9 en los especímenes de donantes sanos y pancreatitis. Por consiguiente, el gráfico ROC era un gráfico de sensibilidad (frecuencia de positivos verdaderos (TPF)) frente a especificidad (frecuencia de falsos positivos (FPF)). Un valor de 1,000 representaba el 100% de sensibilidad y el 100% de especificidad. Este gráfico ROC se muestra en la FIG. 7 y el área bajo la curva (AUC) para cada uno de los monómeros de laminina gamma 2, CEA y CA19-9 se muestra en la Tabla 8.
Tabla 8
Estos resultados indicaron que el monómero de laminina gamma 2 mostró mayor sensibilidad y especificidad como marcador para el cáncer de páncreas que CA19-9 y, por tanto, fue un marcador más preciso para el cáncer de páncreas que CA19-9.
Además, la FIG. 8 y la Tabla 9 muestran la tasa positiva de detección de cáncer de páncreas para monómero de laminina gamma 2, CEA y CA19-9, y combinaciones de los mismos. Un espécimen de cáncer de páncreas fue negativo para los tres de monómero de laminina gamma 2, CEA y CA19-9
Tabla 9
Estos resultados indicaron que el monómero de laminina gamma 2 era un marcador para el diagnóstico de cáncer de páncreas. Además, la tasa positiva de detección de cáncer de páncreas fue mayor para las combinaciones de monómero de laminina gamma 2, CEA y CA19-9 en comparación con la tasa positiva de detección de cáncer de páncreas para cada uno de monómero de laminina gamma 2, CEA y CA19-9.
Se entiende que la descripción detallada anterior y los ejemplos que la acompañan son meramente ilustrativos y no deben tomarse como limitaciones sobre el alcance de la invención, que se define únicamente por las reivindicaciones adjuntas y sus equivalentes.
Para los expertos en la técnica serán evidentes varios cambios y modificaciones a los casos divulgados.
Claims (10)
1. Un método para diagnosticar cáncer de páncreas en un sujeto con necesidad de ello, que comprende:
(a) determinar los niveles de monómero de laminina gamma 2, antígeno carcinoembrionario (CEA) y antígeno carbohidrato 19-9 (CA19-9) en una muestra biológica obtenida del sujeto;
(b) comparar los niveles de monómero de laminina gamma 2, CEA y CA19-9 con los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9, respectivamente; y
(c) identificar que el sujeto tiene cáncer de páncreas cuando los niveles de monómero de laminina gamma 2, CEA y CA19-9 son mayores que los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9, respectivamente.
2. El método de la reivindicación 1, en el que la muestra biológica es una muestra de sangre completa, una muestra de plasma o una muestra de suero.
3. El método de las reivindicaciones 1 o 2, en el que los niveles de monómero de laminina gamma 2, CEA y CA19-9 en la muestra biológica se determinan usando un inmunoensayo.
4. El método de cualquiera de las reivindicaciones 1-3, en el que los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9 son niveles de monómero de laminina gamma 2, CEA y CA19-9, respectivamente, en una muestra de control.
5. El método de cualquiera de las reivindicaciones 1-4, en el que los niveles de referencia de monómero de laminina gamma 2, CEA y CA19-9 son niveles de punto de corte.
6. El método de la reivindicación 5, en el que los niveles de punto de corte se determinan mediante un análisis de media más 2 desviación estándar de múltiples muestras de control.
7. El método de cualquiera de las reivindicaciones 1-6, en el que el nivel de referencia de monómero de laminina gamma 2 es un nivel de monómero de laminina gamma 2 en un calibrador.
8. El método de cualquiera de las reivindicaciones 1-7, en el que el nivel de monómero de laminina gamma 2 se determina usando un anticuerpo 2H2, que se une específicamente al monómero de laminina gamma 2.
9. Un kit para detectar cáncer de páncreas en un sujeto con necesidad de ello, el kit comprendiendo:
(a) uno o más anticuerpos, cada uno de los cuales se une específicamente al monómero de laminina gamma 2; (b) uno o más anticuerpos cada uno de los cuales se une específicamente a CEA; y
(c) uno o más anticuerpos cada uno de los cuales se une específicamente a CA19-9,
en donde cada uno de (a), (b) y (c) se proporciona en recipientes separados.
10. El kit de la reivindicación 9, que comprende un anticuerpo 2H2, que se une específicamente al monómero de laminina gamma 2.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562233745P | 2015-09-28 | 2015-09-28 | |
| US201662295607P | 2016-02-16 | 2016-02-16 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2906754T3 true ES2906754T3 (es) | 2022-04-20 |
Family
ID=57211551
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19219313T Active ES2906754T3 (es) | 2015-09-28 | 2016-09-28 | Uso de laminina 2 para el diagnóstico de carcinoma hepatocelular y cáncer de páncreas |
| ES16788569T Active ES2784369T3 (es) | 2015-09-28 | 2016-09-28 | Uso de laminina 2 para el diagnóstico de carcinoma hepatocelular y cáncer de páncreas |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16788569T Active ES2784369T3 (es) | 2015-09-28 | 2016-09-28 | Uso de laminina 2 para el diagnóstico de carcinoma hepatocelular y cáncer de páncreas |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US20170089905A1 (es) |
| EP (2) | EP3657174B1 (es) |
| JP (2) | JP6829445B2 (es) |
| CN (2) | CN108603882A (es) |
| ES (2) | ES2906754T3 (es) |
| WO (1) | WO2017057778A2 (es) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20170089905A1 (en) | 2015-09-28 | 2017-03-30 | Abbott Japan Co., Ltd. | Methods of diagnosing hepatocellular carcinoma and pancreatic cancer |
| WO2017156594A1 (en) * | 2016-03-18 | 2017-09-21 | University Of Melbourne | Use of laminins as biomarkers for cancer diagnosis and prognosis |
| CN109444429A (zh) * | 2018-12-13 | 2019-03-08 | 郑州安图生物工程股份有限公司 | 利用化学发光免疫技术测定层粘连蛋白的试剂盒 |
| EP4354143A4 (en) * | 2021-06-10 | 2025-04-23 | The Kitasato Institute | Kit for diagnosis of cancer and use thereof |
| JP7745210B2 (ja) * | 2021-07-26 | 2025-09-29 | 国立大学法人 東京大学 | 細胆管増生を伴う肝細胞を検出するためのバイオマーカー |
| CN113970638B (zh) | 2021-10-24 | 2023-02-03 | 清华大学 | 确定胃癌极早期发生风险及评估胃癌前病变进展风险的分子标志及其在诊断试剂盒中的应用 |
| CN121511407A (zh) * | 2023-04-28 | 2026-02-10 | 雅培实验室 | 晚期肝细胞癌的诊断 |
| WO2025193825A1 (en) | 2024-03-13 | 2025-09-18 | Abbott Laboratories | Diagnosis and monitoring of liver disease |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4554101A (en) | 1981-01-09 | 1985-11-19 | New York Blood Center, Inc. | Identification and preparation of epitopes on antigens and allergens on the basis of hydrophilicity |
| EP0273115B1 (en) | 1986-10-22 | 1994-09-07 | Abbott Laboratories | Chemiluminescent acridinium and phenanthridinium salts |
| US5006309A (en) | 1988-04-22 | 1991-04-09 | Abbott Laboratories | Immunoassay device with liquid transfer between wells by washing |
| US5089424A (en) | 1988-06-14 | 1992-02-18 | Abbott Laboratories | Method and apparatus for heterogeneous chemiluminescence assay |
| US5241070A (en) | 1988-09-26 | 1993-08-31 | Ciba Corning Diagnostics Corp. | Nucleophilic polysubstituted aryl acridinium esters and uses thereof |
| US5063081A (en) | 1988-11-14 | 1991-11-05 | I-Stat Corporation | Method of manufacturing a plurality of uniform microfabricated sensing devices having an immobilized ligand receptor |
| CA2069530A1 (en) | 1991-06-03 | 1992-12-04 | Cass J. Grandone | Reagent pack for immunoassays |
| WO1993020442A1 (en) | 1992-03-30 | 1993-10-14 | Abbott Laboratories | Reagents and methods for the detection and quantification of thyroxine in fluid samples |
| US5352803A (en) | 1992-03-30 | 1994-10-04 | Abbott Laboratories | 5(6)-methyl substituted fluorescein derivatives |
| US7419821B2 (en) | 2002-03-05 | 2008-09-02 | I-Stat Corporation | Apparatus and methods for analyte measurement and immunoassay |
| US20040018577A1 (en) | 2002-07-29 | 2004-01-29 | Emerson Campbell John Lewis | Multiple hybrid immunoassay |
| US7682833B2 (en) | 2003-09-10 | 2010-03-23 | Abbott Point Of Care Inc. | Immunoassay device with improved sample closure |
| US7723099B2 (en) | 2003-09-10 | 2010-05-25 | Abbott Point Of Care Inc. | Immunoassay device with immuno-reference electrode |
| US7906293B2 (en) | 2007-04-09 | 2011-03-15 | Abbott Laboratories | Acridinium phenyl esters useful in the analysis of biological |
| KR101192297B1 (ko) * | 2008-12-10 | 2012-10-17 | 한국생명공학연구원 | 간암에 대한 신규 바이오마커 및 그의 용도 |
| US8283162B2 (en) * | 2009-03-10 | 2012-10-09 | Abbott Laboratories | Antibodies relating to PIVKAII and uses thereof |
| US9120862B2 (en) * | 2010-07-26 | 2015-09-01 | Abbott Laboratories | Antibodies relating to PIVKA-II and uses thereof |
| CN107102135A (zh) * | 2011-05-20 | 2017-08-29 | 阿波特日本有限公司 | 用于减少非特异性结合的免疫检验方法和试剂 |
| KR20140057361A (ko) * | 2011-08-31 | 2014-05-12 | 온코사이트 코포레이션 | 암의 치료 및 진단을 위한 방법 및 조성물 |
| US20150072349A1 (en) * | 2012-03-16 | 2015-03-12 | University Health Network | Cancer Biomarkers and Methods of Use |
| US20140045196A1 (en) * | 2012-08-13 | 2014-02-13 | University Of Tokyo | Methods of prognosis and diagnosis of cancer |
| US20140271621A1 (en) * | 2013-03-14 | 2014-09-18 | Abbott Laboratories | Methods of prognosis and diagnosis of pancreatic cancer |
| CN104391122B (zh) * | 2014-12-05 | 2016-03-30 | 重庆乾德生物技术有限公司 | 一种afp、pivka-ⅱ联合检测试剂盒 |
| US20170089905A1 (en) | 2015-09-28 | 2017-03-30 | Abbott Japan Co., Ltd. | Methods of diagnosing hepatocellular carcinoma and pancreatic cancer |
-
2016
- 2016-09-27 US US15/277,871 patent/US20170089905A1/en not_active Abandoned
- 2016-09-28 JP JP2018516096A patent/JP6829445B2/ja active Active
- 2016-09-28 ES ES19219313T patent/ES2906754T3/es active Active
- 2016-09-28 WO PCT/JP2016/079711 patent/WO2017057778A2/en not_active Ceased
- 2016-09-28 CN CN201680069426.XA patent/CN108603882A/zh active Pending
- 2016-09-28 EP EP19219313.4A patent/EP3657174B1/en active Active
- 2016-09-28 ES ES16788569T patent/ES2784369T3/es active Active
- 2016-09-28 EP EP16788569.8A patent/EP3356828B1/en active Active
- 2016-09-28 CN CN202210131434.XA patent/CN114563560A/zh active Pending
-
2019
- 2019-04-18 US US16/388,251 patent/US11340229B2/en active Active
-
2021
- 2021-01-05 JP JP2021000357A patent/JP7174385B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021060418A (ja) | 2021-04-15 |
| EP3657174A1 (en) | 2020-05-27 |
| JP2018533724A (ja) | 2018-11-15 |
| US20170089905A1 (en) | 2017-03-30 |
| US20190242899A1 (en) | 2019-08-08 |
| CN114563560A (zh) | 2022-05-31 |
| WO2017057778A3 (en) | 2017-05-11 |
| EP3356828A2 (en) | 2018-08-08 |
| JP6829445B2 (ja) | 2021-02-10 |
| EP3356828B1 (en) | 2020-02-12 |
| WO2017057778A2 (en) | 2017-04-06 |
| US11340229B2 (en) | 2022-05-24 |
| ES2784369T3 (es) | 2020-09-24 |
| JP7174385B2 (ja) | 2022-11-17 |
| EP3657174B1 (en) | 2021-12-01 |
| CN108603882A (zh) | 2018-09-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2906754T3 (es) | Uso de laminina 2 para el diagnóstico de carcinoma hepatocelular y cáncer de páncreas | |
| ES2780192T3 (es) | Folato receptor alfa como marcador diagnóstico y de pronóstico para cánceres que expresan folato receptor alfa | |
| CN104755935B (zh) | 癌症的预后和诊断方法 | |
| WO2022083673A1 (zh) | 食管癌的生物标志物及其应用 | |
| US20140271621A1 (en) | Methods of prognosis and diagnosis of pancreatic cancer | |
| ES2634629T3 (es) | Integrina alfa-V-beta 6 para el diagnóstico/pronóstico del carcinoma colorrectal | |
| WO2010136629A9 (es) | Métodos para el diagnóstico o pronóstico del cáncer colorrectal | |
| HK40030145B (en) | Use of laminin 2 for diagnosing hepatocellular carcinoma and pancreatic cancer | |
| HK40030145A (en) | Use of laminin 2 for diagnosing hepatocellular carcinoma and pancreatic cancer | |
| KR101130842B1 (ko) | 폐암 진단용 Xage-1d 마커 및 이를 이용한 진단 키트 | |
| US20130330745A1 (en) | Methods of prognosis and diagnosis in sepsis | |
| HK1259462A1 (en) | Use of laminin 2 for diagnosing hepatocellular carcinoma and pancreatic cancer | |
| HK1259462B (en) | Use of laminin 2 for diagnosing hepatocellular carcinoma and pancreatic cancer | |
| US20230305010A1 (en) | Timp1 as a marker for cholangiocarcinoma | |
| WO2019221245A1 (ja) | 新規肝癌マーカー | |
| JP2008122276A (ja) | コラーゲン特異的分子シャペロンhsp47の測定方法 | |
| HK1211345B (en) | Methods of prognosis and diagnosis of cancer | |
| WO2016005639A1 (es) | Método de diagnóstico de cáncer de páncreas |