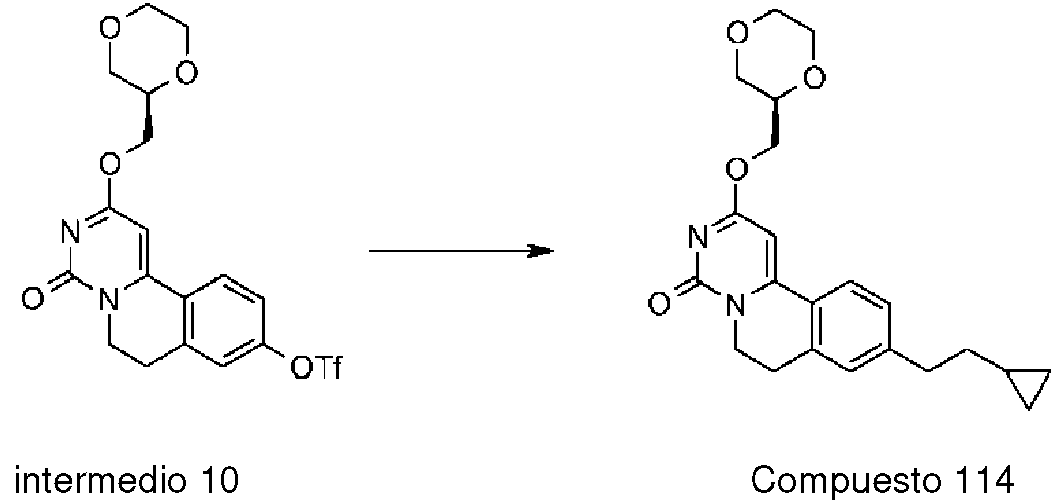
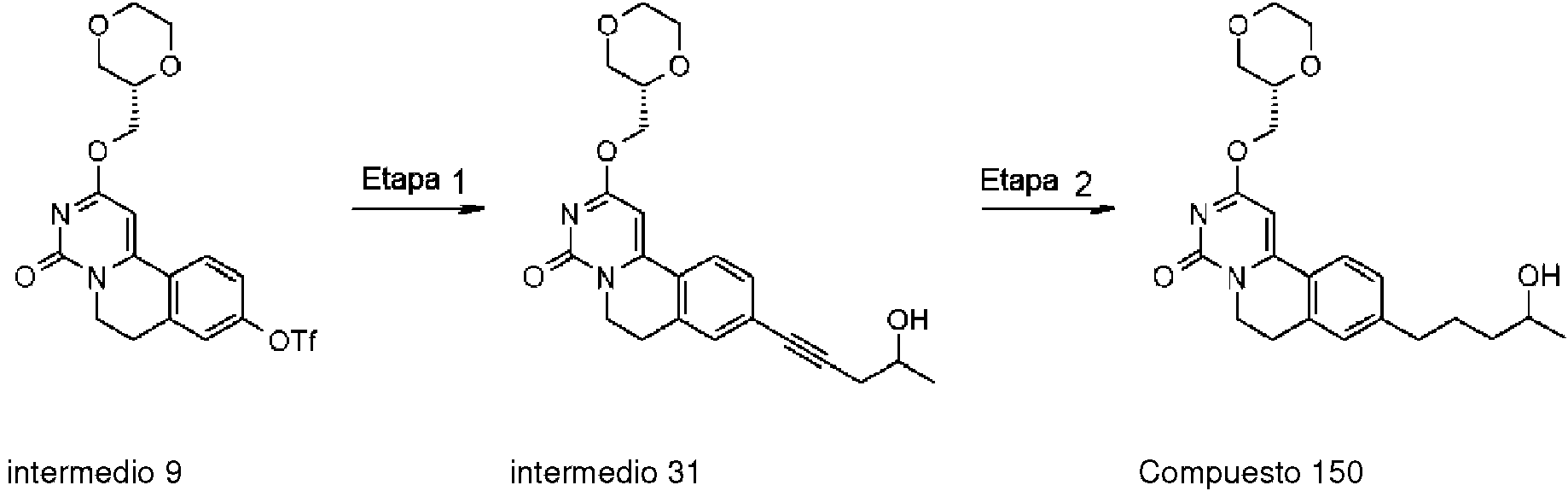
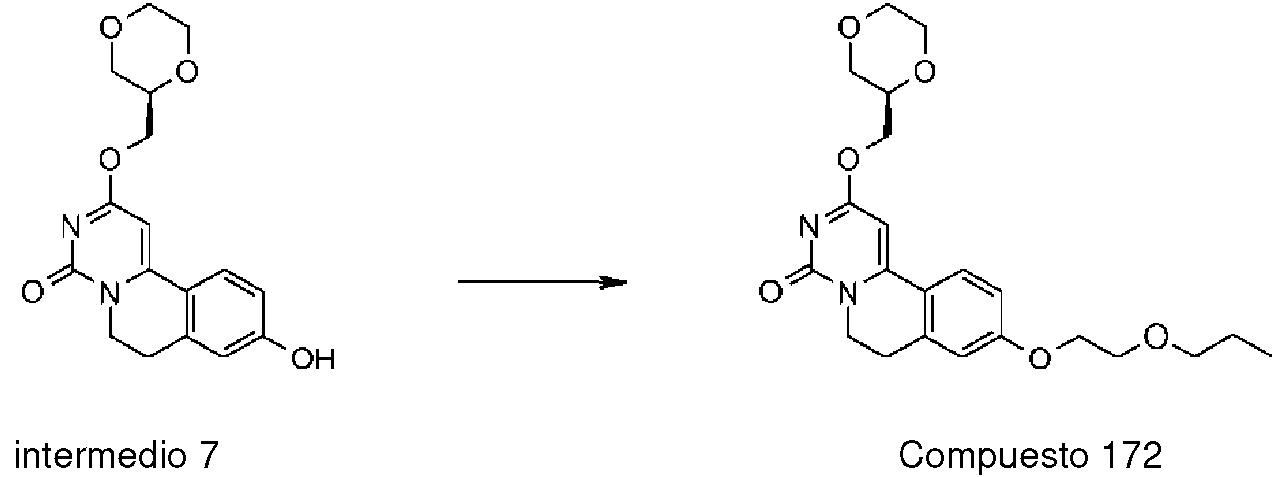
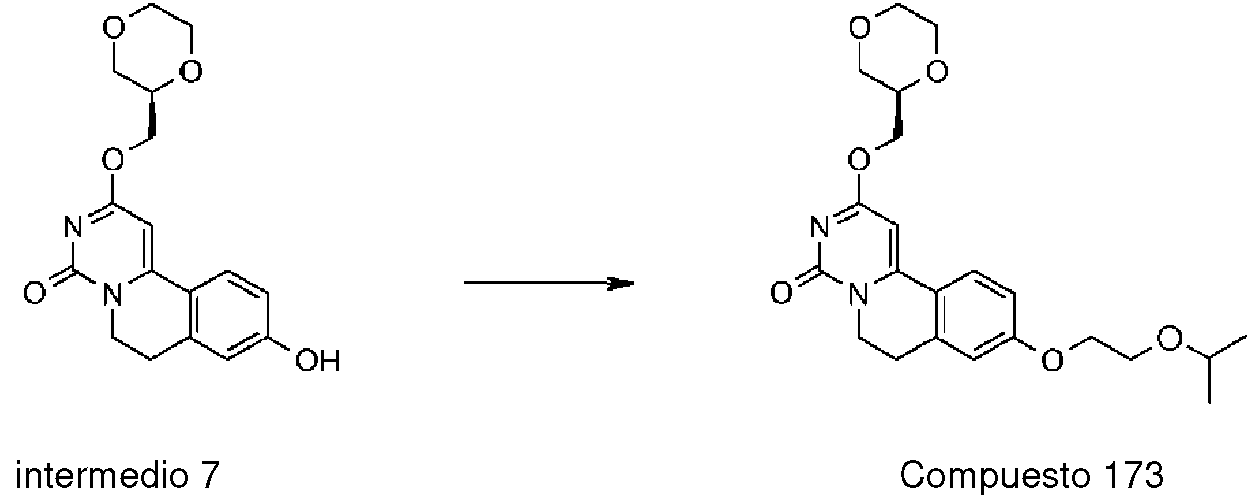
ES2911449T3 - Dihidropirimidinoisoquinolinonas y sus composiciones farmacéuticas para el tratamiento de la esclerosis múltiple - Google Patents
Dihidropirimidinoisoquinolinonas y sus composiciones farmacéuticas para el tratamiento de la esclerosis múltiple Download PDFInfo
- Publication number
- ES2911449T3 ES2911449T3 ES17184834T ES17184834T ES2911449T3 ES 2911449 T3 ES2911449 T3 ES 2911449T3 ES 17184834 T ES17184834 T ES 17184834T ES 17184834 T ES17184834 T ES 17184834T ES 2911449 T3 ES2911449 T3 ES 2911449T3
- Authority
- ES
- Spain
- Prior art keywords
- ylmethoxy
- dihydro
- dioxan
- pyrimido
- isoquinolin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000011282 treatment Methods 0.000 title claims abstract description 35
- 201000006417 multiple sclerosis Diseases 0.000 title claims abstract description 25
- 239000008194 pharmaceutical composition Substances 0.000 title claims description 13
- 150000001875 compounds Chemical class 0.000 claims abstract description 502
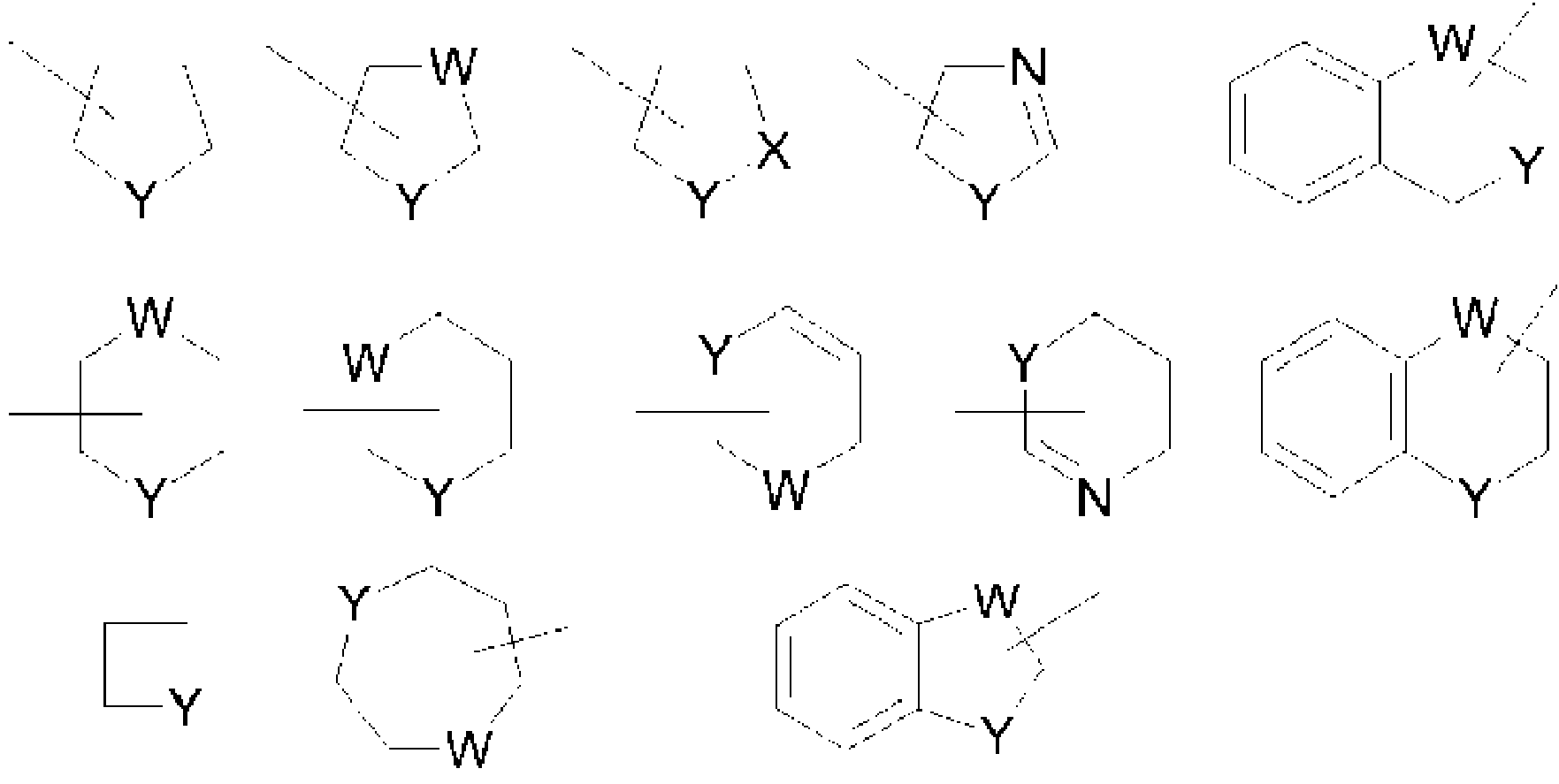
- 125000005842 heteroatom Chemical group 0.000 claims abstract description 94
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 87
- 229910052717 sulfur Inorganic materials 0.000 claims abstract description 84
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 51
- -1 - -NO2 Chemical group 0.000 claims abstract description 50
- 125000005843 halogen group Chemical group 0.000 claims abstract description 50
- 150000003839 salts Chemical class 0.000 claims abstract description 34
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 claims abstract description 31
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims abstract description 25
- 239000012453 solvate Substances 0.000 claims abstract description 17
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims abstract description 10
- 125000004450 alkenylene group Chemical group 0.000 claims abstract description 9
- 125000002947 alkylene group Chemical group 0.000 claims abstract description 9
- 125000004419 alkynylene group Chemical group 0.000 claims abstract description 9
- 125000000392 cycloalkenyl group Chemical group 0.000 claims abstract description 5
- 125000004366 heterocycloalkenyl group Chemical group 0.000 claims abstract description 5
- 229910052739 hydrogen Inorganic materials 0.000 claims description 76
- 125000000217 alkyl group Chemical group 0.000 claims description 59
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 50
- 125000003118 aryl group Chemical group 0.000 claims description 36
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 claims description 28
- 125000003545 alkoxy group Chemical group 0.000 claims description 24
- 229910052799 carbon Inorganic materials 0.000 claims description 17
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 17
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 10
- 125000006568 (C4-C7) heterocycloalkyl group Chemical group 0.000 claims description 7
- 239000003814 drug Substances 0.000 claims description 5
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 claims description 4
- VBOGBNPLAJEBNR-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-pyrazin-2-ylethyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(CCC=4N=CC=NC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 VBOGBNPLAJEBNR-UHFFFAOYSA-N 0.000 claims description 4
- RIDUIZFRYDXCCD-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-methoxy-4-methylpent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(OC)C(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 RIDUIZFRYDXCCD-UHFFFAOYSA-N 0.000 claims description 4
- UCKMDBYAIBGKDN-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-pyridin-3-yl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=NC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 UCKMDBYAIBGKDN-UHFFFAOYSA-N 0.000 claims description 4
- ZKHKSLQAUALGNN-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-methoxypropyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCCOC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 ZKHKSLQAUALGNN-KRWDZBQOSA-N 0.000 claims description 4
- FXENJTMDNMCZIQ-IBGZPJMESA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-[2-(1-hydroxycyclopentyl)ethyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C(C=2N(C(N=C(OC[C@H]3OCCOC3)C=2)=O)CC2)C2=CC=1CCC1(O)CCCC1 FXENJTMDNMCZIQ-IBGZPJMESA-N 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 4
- FUKDWBZBOLZEPO-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1,3-oxazol-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC=4OC=CN=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 FUKDWBZBOLZEPO-UHFFFAOYSA-N 0.000 claims description 3
- GHTUWHMYNSQWBE-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1h-indazol-5-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=C5C=NNC5=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 GHTUWHMYNSQWBE-UHFFFAOYSA-N 0.000 claims description 3
- NFUONRNKWZXWKG-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1h-indol-5-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=C5C=CNC5=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 NFUONRNKWZXWKG-UHFFFAOYSA-N 0.000 claims description 3
- IOEBVXSFJUYZAS-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-ethoxypyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound CCOC1=NC=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 IOEBVXSFJUYZAS-UHFFFAOYSA-N 0.000 claims description 3
- IIOUXJJBJJESOH-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-methoxyphenyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=CC=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 IIOUXJJBJJESOH-UHFFFAOYSA-N 0.000 claims description 3
- CMMVXNAUFZNASV-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-pyridin-2-ylethyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(CCC=4N=CC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 CMMVXNAUFZNASV-UHFFFAOYSA-N 0.000 claims description 3
- RORQQZAQQRNVCC-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-pyrimidin-2-ylethynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC=4N=CC=CN=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 RORQQZAQQRNVCC-UHFFFAOYSA-N 0.000 claims description 3
- UHBVJNATYAFKGG-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-pyrrolidin-1-ylpyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C(=NC=CC=4)N4CCCC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 UHBVJNATYAFKGG-UHFFFAOYSA-N 0.000 claims description 3
- QOACGHRYBVFGBR-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxy-3-pyridin-3-ylprop-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=CN=CC=1C(O)C#CC(C=1)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 QOACGHRYBVFGBR-UHFFFAOYSA-N 0.000 claims description 3
- DKAOVRWVJAWHND-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxy-3-pyridin-3-ylpropyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=CN=CC=1C(O)CCC(C=1)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 DKAOVRWVJAWHND-UHFFFAOYSA-N 0.000 claims description 3
- LQTVLMJGKMGMCX-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-imidazol-1-ylprop-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CCN4C=NC=C4)C=C3CCN2C(=O)N=C1OCC1COCCO1 LQTVLMJGKMGMCX-UHFFFAOYSA-N 0.000 claims description 3
- KDECCZNQCUZKMM-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(4-methoxyphenyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=CC(OC)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 KDECCZNQCUZKMM-UHFFFAOYSA-N 0.000 claims description 3
- MBCWUPQNTZIPCF-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(5-methoxypyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=CN=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 MBCWUPQNTZIPCF-UHFFFAOYSA-N 0.000 claims description 3
- RTDPLTPARBVFOC-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(6-pyrrolidin-1-ylpyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=NC(=CC=4)N4CCCC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 RTDPLTPARBVFOC-UHFFFAOYSA-N 0.000 claims description 3
- WMUHITDTZXIXDX-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(2-methylpropan-2-yl)oxymethyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(COC(C)(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 WMUHITDTZXIXDX-UHFFFAOYSA-N 0.000 claims description 3
- XKTDLLOBRXQBKU-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(5-ethyl-1,2,4-oxadiazol-3-yl)methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound O1C(CC)=NC(COC=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=N1 XKTDLLOBRXQBKU-UHFFFAOYSA-N 0.000 claims description 3
- MZEXYPXWKJZIAA-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(5-methyl-1,2,4-oxadiazol-3-yl)methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound O1C(C)=NC(COC=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=N1 MZEXYPXWKJZIAA-UHFFFAOYSA-N 0.000 claims description 3
- QWVGYCGJYBKYSC-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(5-phenyl-1,3-oxazol-2-yl)methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC=4OC(=CN=4)C=4C=CC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 QWVGYCGJYBKYSC-UHFFFAOYSA-N 0.000 claims description 3
- BPFWZVHBOZPPJX-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[2-(1-hydroxycyclopentyl)ethynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C(C=2N(C(N=C(OCC3OCCOC3)C=2)=O)CC2)C2=CC=1C#CC1(O)CCCC1 BPFWZVHBOZPPJX-UHFFFAOYSA-N 0.000 claims description 3
- UDEWBHZYVLSYNN-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-ethynyl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#C)C=C3CCN2C(=O)N=C1OCC1COCCO1 UDEWBHZYVLSYNN-UHFFFAOYSA-N 0.000 claims description 3
- KFLOTFVSWTXWOA-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-methoxy-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 KFLOTFVSWTXWOA-UHFFFAOYSA-N 0.000 claims description 3
- RDXHLXPVIQVMJC-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-pyridin-4-yl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=CN=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 RDXHLXPVIQVMJC-UHFFFAOYSA-N 0.000 claims description 3
- GBEMSGJRHUHGQM-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-pyrimidin-5-yl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=NC=NC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 GBEMSGJRHUHGQM-UHFFFAOYSA-N 0.000 claims description 3
- ZKHKSLQAUALGNN-QGZVFWFLSA-N 2-[[(2r)-1,4-dioxan-2-yl]methoxy]-9-(3-methoxypropyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCCOC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@H]1COCCO1 ZKHKSLQAUALGNN-QGZVFWFLSA-N 0.000 claims description 3
- FXENJTMDNMCZIQ-LJQANCHMSA-N 2-[[(2r)-1,4-dioxan-2-yl]methoxy]-9-[2-(1-hydroxycyclopentyl)ethyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C(C=2N(C(N=C(OC[C@@H]3OCCOC3)C=2)=O)CC2)C2=CC=1CCC1(O)CCCC1 FXENJTMDNMCZIQ-LJQANCHMSA-N 0.000 claims description 3
- LGDSFSUAFPMIIJ-LJQANCHMSA-N 2-[[(2r)-1,4-dioxan-2-yl]methoxy]-9-[2-(4-hydroxyoxan-4-yl)ethynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C(C=2N(C(N=C(OC[C@@H]3OCCOC3)C=2)=O)CC2)C2=CC=1C#CC1(O)CCOCC1 LGDSFSUAFPMIIJ-LJQANCHMSA-N 0.000 claims description 3
- WCHQRUYPBWMRFP-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(2-propan-2-yloxyethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCOC(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 WCHQRUYPBWMRFP-SFHVURJKSA-N 0.000 claims description 3
- XTFGTMPOQSBSFP-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(2-propoxyethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCOCCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 XTFGTMPOQSBSFP-SFHVURJKSA-N 0.000 claims description 3
- ZYKSMEXRFQZAAW-IBGZPJMESA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-ethyl-3-hydroxypentyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(O)(CC)CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 ZYKSMEXRFQZAAW-IBGZPJMESA-N 0.000 claims description 3
- FUQAHVVPRZZLSA-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxy-3-methylbutyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(C)(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 FUQAHVVPRZZLSA-KRWDZBQOSA-N 0.000 claims description 3
- LACCZGDYHGONEM-YMXDCFFPSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxy-4,4-dimethylpentyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(O)C(C)(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 LACCZGDYHGONEM-YMXDCFFPSA-N 0.000 claims description 3
- DPDKIIHUMBDOHL-JRZJBTRGSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxybutyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 DPDKIIHUMBDOHL-JRZJBTRGSA-N 0.000 claims description 3
- ARXUTZULCOVLEU-ZVAWYAOSSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxypentyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(O)CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 ARXUTZULCOVLEU-ZVAWYAOSSA-N 0.000 claims description 3
- FRYSOWASMQOUDH-YDNXMHBPSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-methoxy-4-methylpentyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(OC)C(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 FRYSOWASMQOUDH-YDNXMHBPSA-N 0.000 claims description 3
- ZKGGBGUHHLWFKC-PKHIMPSTSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-methoxybutyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(C)OC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 ZKGGBGUHHLWFKC-PKHIMPSTSA-N 0.000 claims description 3
- DOHKQKMAJBATQH-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-methylbut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 DOHKQKMAJBATQH-SFHVURJKSA-N 0.000 claims description 3
- NSCFDDAIAZZOIZ-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(4-hydroxy-4-methylpentyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCCC(C)(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 NSCFDDAIAZZOIZ-SFHVURJKSA-N 0.000 claims description 3
- VFYZBZNEAMFLHG-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(4-hydroxybutyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCCCO)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 VFYZBZNEAMFLHG-KRWDZBQOSA-N 0.000 claims description 3
- RUKXQQIDEBYETE-PKHIMPSTSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(4-hydroxypentyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCCC(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 RUKXQQIDEBYETE-PKHIMPSTSA-N 0.000 claims description 3
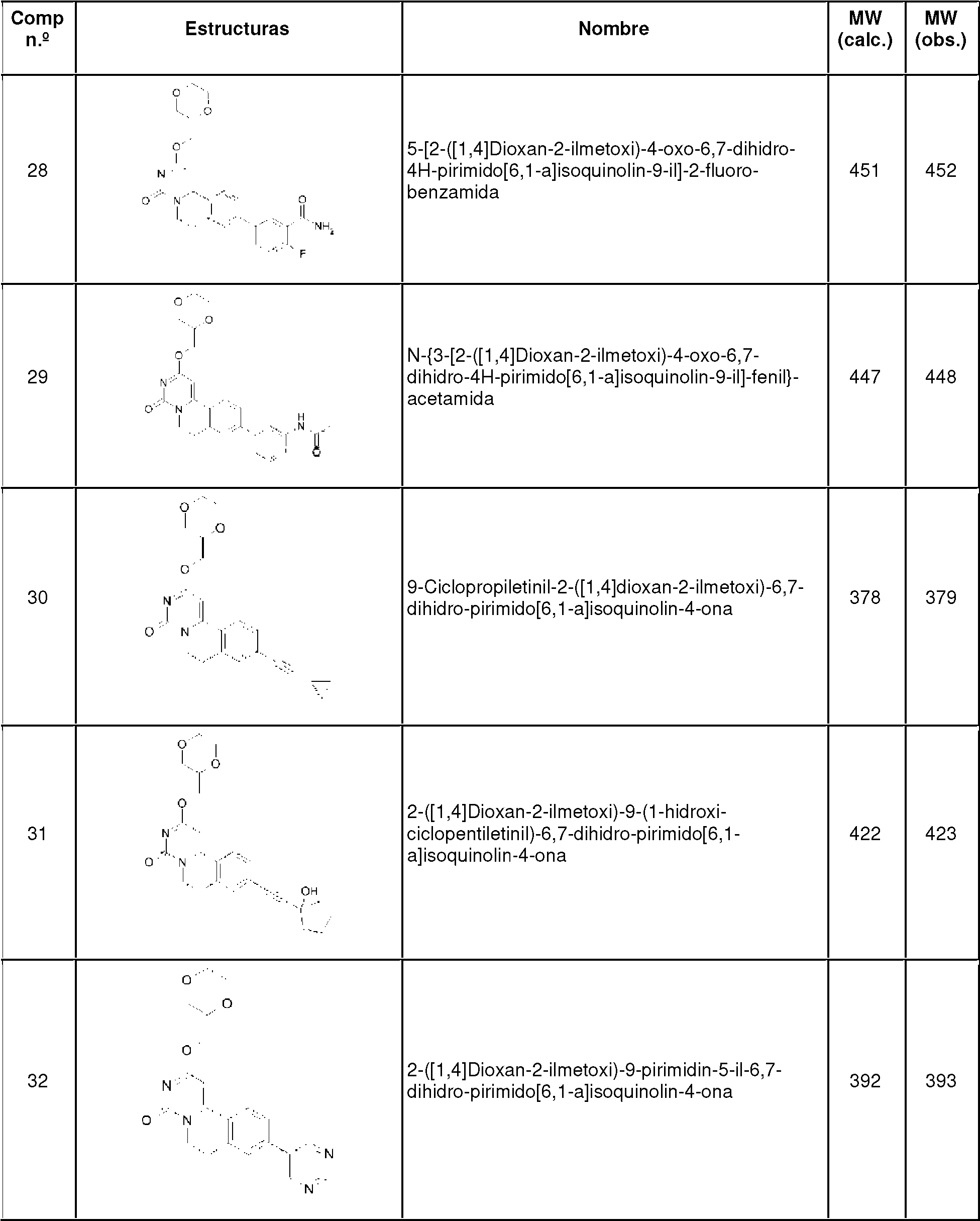
- YDRDGVRBICOWFX-UHFFFAOYSA-N 3-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]benzamide Chemical compound NC(=O)C1=CC=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 YDRDGVRBICOWFX-UHFFFAOYSA-N 0.000 claims description 3
- MOTGLUMBOMRAEA-UHFFFAOYSA-N 4-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]pyridine-3-carbonitrile Chemical compound C1=C2C3=CC=C(C=4C(=CN=CC=4)C#N)C=C3CCN2C(=O)N=C1OCC1COCCO1 MOTGLUMBOMRAEA-UHFFFAOYSA-N 0.000 claims description 3
- KIMZPIYRCIUCII-UHFFFAOYSA-N 5-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]-2-fluorobenzamide Chemical compound C1=C(F)C(C(=O)N)=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 KIMZPIYRCIUCII-UHFFFAOYSA-N 0.000 claims description 3
- URZPEGGUMAIOJZ-KRWDZBQOSA-N 9-(2,2-dimethylpropoxy)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCC(C)(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 URZPEGGUMAIOJZ-KRWDZBQOSA-N 0.000 claims description 3
- YWPOGCYNFZSDEW-UHFFFAOYSA-N 9-(2,6-dimethoxypyridin-3-yl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=NC(OC)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 YWPOGCYNFZSDEW-UHFFFAOYSA-N 0.000 claims description 3
- IRBAWVGZNJIROV-UHFFFAOYSA-N 9-(2-cyclopropylethynyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC4CC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 IRBAWVGZNJIROV-UHFFFAOYSA-N 0.000 claims description 3
- IRBAWVGZNJIROV-GOSISDBHSA-N 9-(2-cyclopropylethynyl)-2-[[(2r)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC4CC4)C=C3CCN2C(=O)N=C1OC[C@H]1COCCO1 IRBAWVGZNJIROV-GOSISDBHSA-N 0.000 claims description 3
- YHSONAVIPVCZDX-UHFFFAOYSA-N 9-(3-anilinoprop-1-ynyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CCNC=4C=CC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 YHSONAVIPVCZDX-UHFFFAOYSA-N 0.000 claims description 3
- LCNCDLIVLWJDTQ-QFIPXVFZSA-N 9-(3-anilinopropyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(CCCNC=4C=CC=CC=4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 LCNCDLIVLWJDTQ-QFIPXVFZSA-N 0.000 claims description 3
- YJRYAOMRRMQDAV-UHFFFAOYSA-N 9-(cyclopentyloxymethyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COC4CCCC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 YJRYAOMRRMQDAV-UHFFFAOYSA-N 0.000 claims description 3
- UWACCCXIIBRQDS-UHFFFAOYSA-N 9-[(5-cyclopropyl-1,2,4-oxadiazol-3-yl)methoxy]-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC=4N=C(ON=4)C4CC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 UWACCCXIIBRQDS-UHFFFAOYSA-N 0.000 claims description 3
- SVTUOYWRUDSQLS-UHFFFAOYSA-N 9-[(5-tert-butyl-1,3-oxazol-2-yl)methoxy]-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound O1C(C(C)(C)C)=CN=C1COC1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 SVTUOYWRUDSQLS-UHFFFAOYSA-N 0.000 claims description 3
- ZSUKDKDFDYRWSI-UHFFFAOYSA-N n-[3-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]phenyl]acetamide Chemical compound CC(=O)NC1=CC=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 ZSUKDKDFDYRWSI-UHFFFAOYSA-N 0.000 claims description 3
- 229940124597 therapeutic agent Drugs 0.000 claims description 3
- UFXFBYILWDOVNC-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1-methylindol-5-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C2N(C)C=CC2=CC=1C(C=1)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 UFXFBYILWDOVNC-UHFFFAOYSA-N 0.000 claims description 2
- JUURNCDFTFERJD-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1-propylpyrazol-4-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NN(CCC)C=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 JUURNCDFTFERJD-UHFFFAOYSA-N 0.000 claims description 2
- LXEDZWSAQCWVOW-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1h-indol-2-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4NC5=CC=CC=C5C=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 LXEDZWSAQCWVOW-UHFFFAOYSA-N 0.000 claims description 2
- UBAOKCMYALUHJA-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1h-pyrazol-4-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C4=CNN=C4)C=C3CCN2C(=O)N=C1OCC1COCCO1 UBAOKCMYALUHJA-UHFFFAOYSA-N 0.000 claims description 2
- OJUGVILFVLNQIN-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-pyridin-2-ylethynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC=4N=CC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 OJUGVILFVLNQIN-UHFFFAOYSA-N 0.000 claims description 2
- FQYOAZIPVGMPMX-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxy-4-methylpent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)C(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 FQYOAZIPVGMPMX-UHFFFAOYSA-N 0.000 claims description 2
- XYEJBVUGGUZHMQ-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxy-5-methylhex-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)CC(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 XYEJBVUGGUZHMQ-UHFFFAOYSA-N 0.000 claims description 2
- FMUHXPKLGMHDNM-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxybut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 FMUHXPKLGMHDNM-UHFFFAOYSA-N 0.000 claims description 2
- QUXJSJPUEFPUAX-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxypent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 QUXJSJPUEFPUAX-UHFFFAOYSA-N 0.000 claims description 2
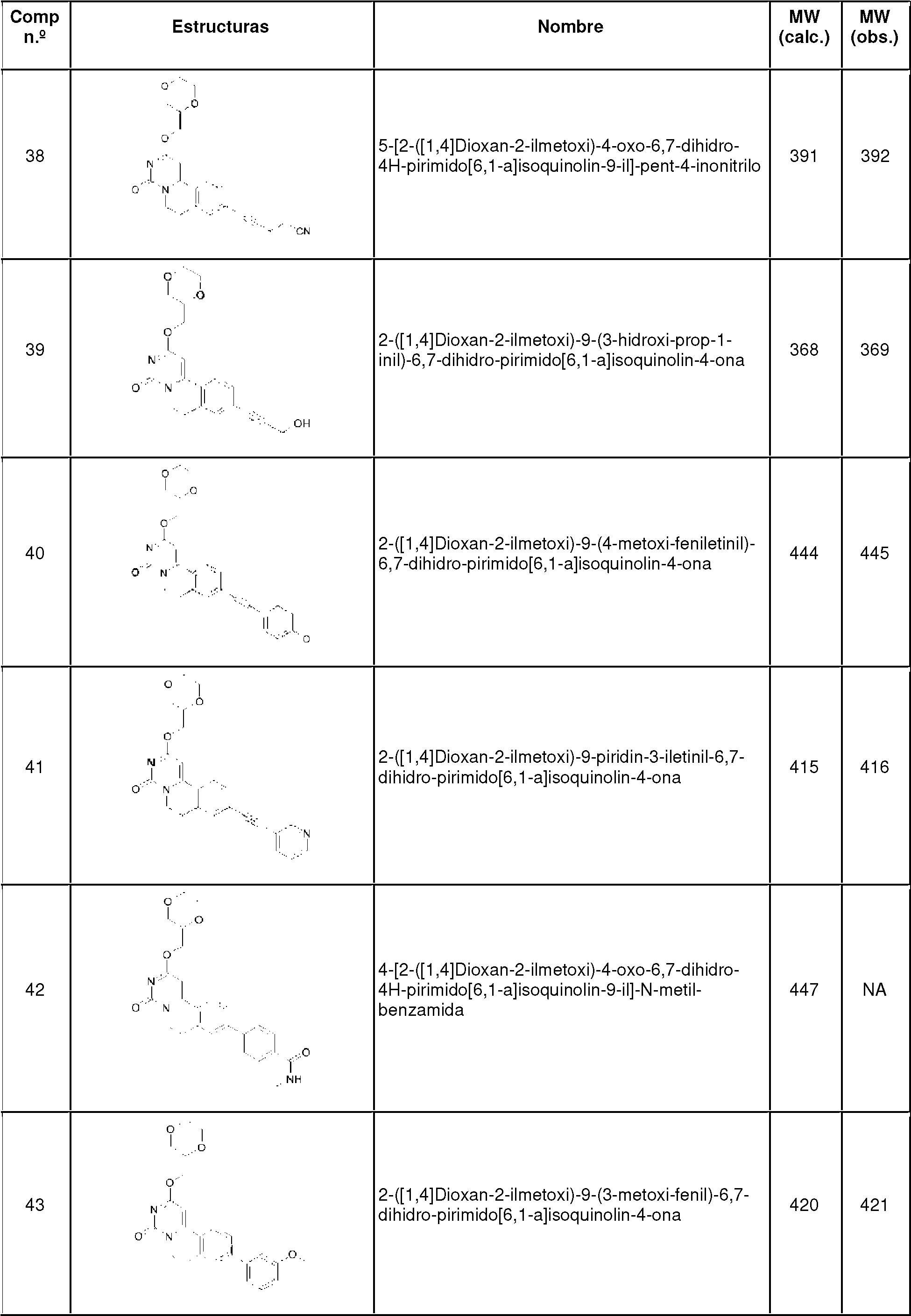
- ZGJBNCCPCLGHNI-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxyprop-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCO)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 ZGJBNCCPCLGHNI-UHFFFAOYSA-N 0.000 claims description 2
- HLAQLEHDEDDXKD-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-methoxyprop-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCOC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 HLAQLEHDEDDXKD-UHFFFAOYSA-N 0.000 claims description 2
- DOHKQKMAJBATQH-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-methylbut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 DOHKQKMAJBATQH-UHFFFAOYSA-N 0.000 claims description 2
- YDYBKRUWQDWECH-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(6-methoxypyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NC(OC)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 YDYBKRUWQDWECH-UHFFFAOYSA-N 0.000 claims description 2
- FKDTXJMMDQIQOI-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(6-methylpyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NC(C)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 FKDTXJMMDQIQOI-UHFFFAOYSA-N 0.000 claims description 2
- JACDZXYQWMDVHD-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(6-piperidin-1-ylpyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=NC(=CC=4)N4CCCCC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 JACDZXYQWMDVHD-UHFFFAOYSA-N 0.000 claims description 2
- KSGKMLVYIUJQMZ-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(pyridin-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC=4N=CC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 KSGKMLVYIUJQMZ-UHFFFAOYSA-N 0.000 claims description 2
- NHIUBSCZOIMDJS-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(5-propan-2-yl-1,2,4-oxadiazol-3-yl)methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound O1C(C(C)C)=NC(COC=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=N1 NHIUBSCZOIMDJS-UHFFFAOYSA-N 0.000 claims description 2
- JZZYQXJKGTXYCE-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[2-(3-methylimidazol-4-yl)ethynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound CN1C=NC=C1C#CC1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 JZZYQXJKGTXYCE-UHFFFAOYSA-N 0.000 claims description 2
- KDZIDRHAOFIRCJ-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[3-(pyridin-3-ylmethylamino)prop-1-ynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CCNCC=4C=NC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 KDZIDRHAOFIRCJ-UHFFFAOYSA-N 0.000 claims description 2
- MWUKVCCBFVEQTL-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[6-(trifluoromethyl)pyridin-3-yl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NC(C(F)(F)F)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 MWUKVCCBFVEQTL-UHFFFAOYSA-N 0.000 claims description 2
- FYDLWSDXHIOKMI-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-hex-1-ynyl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCCCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 FYDLWSDXHIOKMI-UHFFFAOYSA-N 0.000 claims description 2
- BDMWQQBSFVLOPB-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-pent-1-ynyl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 BDMWQQBSFVLOPB-UHFFFAOYSA-N 0.000 claims description 2
- YYMRQEAZLNSZOV-UHFFFAOYSA-N 2-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]benzonitrile Chemical compound C1=C2C3=CC=C(C=4C(=CC=CC=4)C#N)C=C3CCN2C(=O)N=C1OCC1COCCO1 YYMRQEAZLNSZOV-UHFFFAOYSA-N 0.000 claims description 2
- YYMRQEAZLNSZOV-LJQANCHMSA-N 2-[2-[[(2r)-1,4-dioxan-2-yl]methoxy]-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]benzonitrile Chemical compound C1=C2C3=CC=C(C=4C(=CC=CC=4)C#N)C=C3CCN2C(=O)N=C1OC[C@H]1COCCO1 YYMRQEAZLNSZOV-LJQANCHMSA-N 0.000 claims description 2
- YYMRQEAZLNSZOV-IBGZPJMESA-N 2-[2-[[(2s)-1,4-dioxan-2-yl]methoxy]-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]benzonitrile Chemical compound C1=C2C3=CC=C(C=4C(=CC=CC=4)C#N)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 YYMRQEAZLNSZOV-IBGZPJMESA-N 0.000 claims description 2
- WCHQRUYPBWMRFP-GOSISDBHSA-N 2-[[(2r)-1,4-dioxan-2-yl]methoxy]-9-(2-propan-2-yloxyethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCOC(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@H]1COCCO1 WCHQRUYPBWMRFP-GOSISDBHSA-N 0.000 claims description 2
- XTFGTMPOQSBSFP-GOSISDBHSA-N 2-[[(2r)-1,4-dioxan-2-yl]methoxy]-9-(2-propoxyethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCOCCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@H]1COCCO1 XTFGTMPOQSBSFP-GOSISDBHSA-N 0.000 claims description 2
- CLGGBTXQLRICFB-LJQANCHMSA-N 2-[[(2r)-1,4-dioxan-2-yl]methoxy]-9-(oxan-4-yloxymethyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COC4CCOCC4)C=C3CCN2C(=O)N=C1OC[C@H]1COCCO1 CLGGBTXQLRICFB-LJQANCHMSA-N 0.000 claims description 2
- FKTFVDHBAYCXFO-GGYWPGCISA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(oxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC4OCCCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 FKTFVDHBAYCXFO-GGYWPGCISA-N 0.000 claims description 2
- NWHHOSIUJNIWBU-IBGZPJMESA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(oxan-4-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC4CCOCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 NWHHOSIUJNIWBU-IBGZPJMESA-N 0.000 claims description 2
- FDBUJVHYUALRBC-FQEVSTJZSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(oxan-4-ylmethoxymethyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COCC4CCOCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 FDBUJVHYUALRBC-FQEVSTJZSA-N 0.000 claims description 2
- VBMLIXPOHJZPOV-IBGZPJMESA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(oxan-4-ylmethylamino)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(NCC4CCOCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 VBMLIXPOHJZPOV-IBGZPJMESA-N 0.000 claims description 2
- SUTVBPGMNVGUEY-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(oxetan-3-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC4COC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 SUTVBPGMNVGUEY-KRWDZBQOSA-N 0.000 claims description 2
- QPMSMEGRSPIYCY-UHFFFAOYSA-N 2-[[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]oxy]acetonitrile Chemical compound C1=C2C3=CC=C(OCC#N)C=C3CCN2C(=O)N=C1OCC1COCCO1 QPMSMEGRSPIYCY-UHFFFAOYSA-N 0.000 claims description 2
- KXXDHPDMCWWMPD-UHFFFAOYSA-N 3-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]benzonitrile Chemical compound C1=C2C3=CC=C(C=4C=C(C=CC=4)C#N)C=C3CCN2C(=O)N=C1OCC1COCCO1 KXXDHPDMCWWMPD-UHFFFAOYSA-N 0.000 claims description 2
- UCJBLOVGSXNIMZ-UHFFFAOYSA-N 4-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]benzonitrile Chemical compound C1=C2C3=CC=C(C=4C=CC(=CC=4)C#N)C=C3CCN2C(=O)N=C1OCC1COCCO1 UCJBLOVGSXNIMZ-UHFFFAOYSA-N 0.000 claims description 2
- MWFFRLNSJQASOR-UHFFFAOYSA-N 5-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]pyridine-2-carboxylic acid Chemical compound O1C(COCC1)COC1=NC(N2C(C3=CC=C(C=C3CC2)C=2C=CC(=NC=2)C(=O)O)=C1)=O MWFFRLNSJQASOR-UHFFFAOYSA-N 0.000 claims description 2
- GOABXHRYGPVPPU-UHFFFAOYSA-N 9-(2-cyclohexylethynyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC4CCCCC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 GOABXHRYGPVPPU-UHFFFAOYSA-N 0.000 claims description 2
- CGLMQSKTQZSXCH-GOSISDBHSA-N 9-(2-cyclopropylethyl)-2-[[(2r)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(CCC4CC4)C=C3CCN2C(=O)N=C1OC[C@H]1COCCO1 CGLMQSKTQZSXCH-GOSISDBHSA-N 0.000 claims description 2
- JYBKRGIWCQSOHN-UHFFFAOYSA-N 9-(3,5-dichlorophenyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound ClC1=CC(Cl)=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 JYBKRGIWCQSOHN-UHFFFAOYSA-N 0.000 claims description 2
- YKKXXDAPUOFZDC-LJQANCHMSA-N 9-(3-cyclopropylpropoxy)-2-[[(2r)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCCCC4CC4)C=C3CCN2C(=O)N=C1OC[C@H]1COCCO1 YKKXXDAPUOFZDC-LJQANCHMSA-N 0.000 claims description 2
- YKKXXDAPUOFZDC-IBGZPJMESA-N 9-(3-cyclopropylpropoxy)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCCCC4CC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 YKKXXDAPUOFZDC-IBGZPJMESA-N 0.000 claims description 2
- BUJAVCYRADIVPH-IBGZPJMESA-N 9-(4,4-dimethylpentoxy)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCCC(C)(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 BUJAVCYRADIVPH-IBGZPJMESA-N 0.000 claims description 2
- HVVOJEOEPSKBIY-UHFFFAOYSA-N 9-(cyclohexen-1-yl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4CCCCC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 HVVOJEOEPSKBIY-UHFFFAOYSA-N 0.000 claims description 2
- QJUIYCMYFUURCZ-IBGZPJMESA-N 9-(cyclohexylamino)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(NC4CCCCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 QJUIYCMYFUURCZ-IBGZPJMESA-N 0.000 claims description 2
- NOKFUPIFXYMEMG-FQEVSTJZSA-N 9-(cyclohexylmethylamino)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(NCC4CCCCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 NOKFUPIFXYMEMG-FQEVSTJZSA-N 0.000 claims description 2
- WKKMOSLPKTZYHE-FQEVSTJZSA-N 9-(cyclopentylmethoxymethyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COCC4CCCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 WKKMOSLPKTZYHE-FQEVSTJZSA-N 0.000 claims description 2
- YJRYAOMRRMQDAV-LJQANCHMSA-N 9-(cyclopentyloxymethyl)-2-[[(2r)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COC4CCCC4)C=C3CCN2C(=O)N=C1OC[C@H]1COCCO1 YJRYAOMRRMQDAV-LJQANCHMSA-N 0.000 claims description 2
- UWACCCXIIBRQDS-QGZVFWFLSA-N 9-[(5-cyclopropyl-1,2,4-oxadiazol-3-yl)methoxy]-2-[[(2r)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC=4N=C(ON=4)C4CC4)C=C3CCN2C(=O)N=C1OC[C@H]1COCCO1 UWACCCXIIBRQDS-QGZVFWFLSA-N 0.000 claims description 2
- WVXXBOGIESBOAV-UHFFFAOYSA-N 9-[(5-tert-butyl-1,2,4-oxadiazol-3-yl)methoxy]-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound O1C(C(C)(C)C)=NC(COC=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=N1 WVXXBOGIESBOAV-UHFFFAOYSA-N 0.000 claims description 2
- OQPXEVMRXYMSCF-UHFFFAOYSA-N 9-[3-[benzyl(methyl)amino]prop-1-ynyl]-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=CC=CC=1CN(C)CC#CC(C=1)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 OQPXEVMRXYMSCF-UHFFFAOYSA-N 0.000 claims description 2
- DJFFTHUKYSGWTP-FQEVSTJZSA-N 9-[cyclohexyl(methyl)amino]-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C(C=2N(C(N=C(OC[C@H]3OCCOC3)C=2)=O)CC2)C2=CC=1N(C)C1CCCCC1 DJFFTHUKYSGWTP-FQEVSTJZSA-N 0.000 claims description 2
- ZSYGTUKDHOKEBC-UHFFFAOYSA-N 9-cyclopropyl-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C4CC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 ZSYGTUKDHOKEBC-UHFFFAOYSA-N 0.000 claims description 2
- FQFILJKFZCVHNH-UHFFFAOYSA-N tert-butyl n-[3-[(5-bromo-2-chloropyrimidin-4-yl)amino]propyl]carbamate Chemical compound CC(C)(C)OC(=O)NCCCNC1=NC(Cl)=NC=C1Br FQFILJKFZCVHNH-UHFFFAOYSA-N 0.000 claims description 2
- RFTGHRMNRSHWBL-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=CC=C3CCN2C(=O)N=C1OCC1COCCO1 RFTGHRMNRSHWBL-UHFFFAOYSA-N 0.000 claims 1
- FOLJWRCFTUIJDT-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-methoxypyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=NC=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 FOLJWRCFTUIJDT-UHFFFAOYSA-N 0.000 claims 1
- BCFJWOVDPHJBTF-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-methylpyridin-4-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NC(C)=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 BCFJWOVDPHJBTF-UHFFFAOYSA-N 0.000 claims 1
- HPNCYWFFYIFFCB-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-pyridin-3-ylethynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC=4C=NC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 HPNCYWFFYIFFCB-UHFFFAOYSA-N 0.000 claims 1
- JWIVRAVRGYCFQU-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(2-pyridin-4-ylethynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC=4C=CN=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 JWIVRAVRGYCFQU-UHFFFAOYSA-N 0.000 claims 1
- DJLCKRYRNSUXLI-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxy-3-methylbut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(C)(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 DJLCKRYRNSUXLI-UHFFFAOYSA-N 0.000 claims 1
- AOYPYDSFTKKNAR-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-methoxyphenyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=CC=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 AOYPYDSFTKKNAR-UHFFFAOYSA-N 0.000 claims 1
- GITIKJVOXNTBIV-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(4-hydroxybut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCCO)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 GITIKJVOXNTBIV-UHFFFAOYSA-N 0.000 claims 1
- QKGNRHGIXBMVIU-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(4-morpholin-4-ylphenyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=CC(=CC=4)N4CCOCC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 QKGNRHGIXBMVIU-UHFFFAOYSA-N 0.000 claims 1
- AXUGDRKDFNZHBY-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(6-ethoxypyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NC(OCC)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 AXUGDRKDFNZHBY-UHFFFAOYSA-N 0.000 claims 1
- KWHDRSJRWXRARR-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(6-morpholin-4-ylpyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4C=NC(=CC=4)N4CCOCC4)C=C3CCN2C(=O)N=C1OCC1COCCO1 KWHDRSJRWXRARR-UHFFFAOYSA-N 0.000 claims 1
- WDXDBZNLHDATCD-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(6-propan-2-yloxypyridin-3-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NC(OC(C)C)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 WDXDBZNLHDATCD-UHFFFAOYSA-N 0.000 claims 1
- HYVQFMCVFHCARC-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(1-methylpyrazol-3-yl)methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound CN1C=CC(COC=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=N1 HYVQFMCVFHCARC-UHFFFAOYSA-N 0.000 claims 1
- BSSVGTOJDBSHHZ-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(3-methyl-1,2,4-oxadiazol-5-yl)methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound CC1=NOC(COC=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=N1 BSSVGTOJDBSHHZ-UHFFFAOYSA-N 0.000 claims 1
- LJIYHSOKPSIAOS-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[(3-methyl-1,2-oxazol-5-yl)methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound O1N=C(C)C=C1COC1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 LJIYHSOKPSIAOS-UHFFFAOYSA-N 0.000 claims 1
- NIDXRAREIYMXAW-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[2-(4-methoxyphenyl)ethynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=CC(OC)=CC=C1C#CC1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 NIDXRAREIYMXAW-UHFFFAOYSA-N 0.000 claims 1
- ZOPUGIAXQNDWQJ-UHFFFAOYSA-N 3-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]-4-fluorobenzamide Chemical compound NC(=O)C1=CC=C(F)C(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 ZOPUGIAXQNDWQJ-UHFFFAOYSA-N 0.000 claims 1
- XHQGJPXVKBSGHO-UHFFFAOYSA-N 3-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]-5-fluorobenzamide Chemical compound NC(=O)C1=CC(F)=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 XHQGJPXVKBSGHO-UHFFFAOYSA-N 0.000 claims 1
- YHYPVCLQMAAXSH-UHFFFAOYSA-N 3-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]pyridine-4-carbonitrile Chemical compound C1=C2C3=CC=C(C=4C(=CC=NC=4)C#N)C=C3CCN2C(=O)N=C1OCC1COCCO1 YHYPVCLQMAAXSH-UHFFFAOYSA-N 0.000 claims 1
- LGNHTQPLDMLJSM-UHFFFAOYSA-N 4-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]-n-methylbenzamide Chemical compound C1=CC(C(=O)NC)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 LGNHTQPLDMLJSM-UHFFFAOYSA-N 0.000 claims 1
- USOKHCCWUACLRD-UHFFFAOYSA-N 5-[2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl]pyridine-2-carbonitrile Chemical compound C1=C2C3=CC=C(C=4C=NC(=CC=4)C#N)C=C3CCN2C(=O)N=C1OCC1COCCO1 USOKHCCWUACLRD-UHFFFAOYSA-N 0.000 claims 1
- NVXCVOSFBURWAP-UHFFFAOYSA-N 9-(2,3-dimethoxyphenyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=CC=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1OC NVXCVOSFBURWAP-UHFFFAOYSA-N 0.000 claims 1
- RYKVFDPZZFYMCH-UHFFFAOYSA-N 9-(2,5-dimethoxyphenyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=CC=C(OC)C(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1 RYKVFDPZZFYMCH-UHFFFAOYSA-N 0.000 claims 1
- QKGNXXBOQFMEJH-UHFFFAOYSA-N 9-(2-chlorophenyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound ClC1=CC=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 QKGNXXBOQFMEJH-UHFFFAOYSA-N 0.000 claims 1
- XUUMONIOFNJCFP-UHFFFAOYSA-N 9-(3,3-dimethylbut-1-ynyl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(C)(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 XUUMONIOFNJCFP-UHFFFAOYSA-N 0.000 claims 1
- LMVWRWNWERGULV-UHFFFAOYSA-N 9-(3,6-dihydro-2h-pyran-4-yl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C=4CCOCC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 LMVWRWNWERGULV-UHFFFAOYSA-N 0.000 claims 1
- GKJJFXZUNPOFRS-UHFFFAOYSA-N 9-(3-chloro-2-methoxypyridin-4-yl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound COC1=NC=CC(C=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=C1Cl GKJJFXZUNPOFRS-UHFFFAOYSA-N 0.000 claims 1
- LDEXEZSXQFUIEE-UHFFFAOYSA-N 9-[(1,5-dimethylpyrazol-3-yl)methoxy]-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound CN1C(C)=CC(COC=2C=C3C(C=4N(C(N=C(OCC5OCCOC5)C=4)=O)CC3)=CC=2)=N1 LDEXEZSXQFUIEE-UHFFFAOYSA-N 0.000 claims 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 abstract description 12
- 125000001475 halogen functional group Chemical group 0.000 abstract 2
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 abstract 1
- 239000000543 intermediate Substances 0.000 description 347
- 238000007429 general method Methods 0.000 description 197
- 239000000203 mixture Substances 0.000 description 87
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical class OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 85
- 238000006243 chemical reaction Methods 0.000 description 79
- 239000000243 solution Substances 0.000 description 57
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 54
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 46
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 44
- 102100033864 G-protein coupled receptor 84 Human genes 0.000 description 44
- 101710107771 G-protein coupled receptor 84 Proteins 0.000 description 43
- 239000011541 reaction mixture Substances 0.000 description 39
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 38
- 239000002904 solvent Substances 0.000 description 37
- 210000004027 cell Anatomy 0.000 description 34
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 29
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 29
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 27
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 26
- 238000000034 method Methods 0.000 description 26
- 150000002148 esters Chemical class 0.000 description 25
- 125000004076 pyridyl group Chemical group 0.000 description 25
- 239000012043 crude product Substances 0.000 description 24
- 239000000741 silica gel Substances 0.000 description 24
- 229910002027 silica gel Inorganic materials 0.000 description 24
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 24
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 23
- 125000004432 carbon atom Chemical group C* 0.000 description 23
- 210000000440 neutrophil Anatomy 0.000 description 23
- 238000012360 testing method Methods 0.000 description 23
- 235000019439 ethyl acetate Nutrition 0.000 description 22
- 201000010099 disease Diseases 0.000 description 21
- 241000282414 Homo sapiens Species 0.000 description 20
- 238000003818 flash chromatography Methods 0.000 description 20
- 229910052731 fluorine Inorganic materials 0.000 description 20
- 239000002253 acid Substances 0.000 description 19
- 239000002585 base Substances 0.000 description 19
- 229910052801 chlorine Inorganic materials 0.000 description 19
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 19
- 235000019341 magnesium sulphate Nutrition 0.000 description 19
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 18
- 239000000523 sample Substances 0.000 description 18
- 238000003786 synthesis reaction Methods 0.000 description 18
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 17
- 239000012044 organic layer Substances 0.000 description 17
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- 239000002131 composite material Substances 0.000 description 16
- 125000002883 imidazolyl group Chemical group 0.000 description 16
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 16
- 125000002971 oxazolyl group Chemical group 0.000 description 16
- 125000003373 pyrazinyl group Chemical group 0.000 description 16
- 125000000714 pyrimidinyl group Chemical group 0.000 description 16
- 125000000335 thiazolyl group Chemical group 0.000 description 16
- 125000001425 triazolyl group Chemical group 0.000 description 16
- 125000001072 heteroaryl group Chemical group 0.000 description 15
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 15
- 238000003556 assay Methods 0.000 description 14
- 230000015572 biosynthetic process Effects 0.000 description 14
- 239000012267 brine Substances 0.000 description 14
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 14
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 14
- 230000000694 effects Effects 0.000 description 14
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 14
- 238000011534 incubation Methods 0.000 description 13
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 13
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 13
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 12
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 12
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 12
- 241000700159 Rattus Species 0.000 description 12
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 12
- 239000000872 buffer Substances 0.000 description 12
- 238000009472 formulation Methods 0.000 description 12
- 125000002541 furyl group Chemical group 0.000 description 12
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 12
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 12
- 125000001715 oxadiazolyl group Chemical group 0.000 description 12
- 238000000746 purification Methods 0.000 description 12
- 230000004044 response Effects 0.000 description 12
- 125000001113 thiadiazolyl group Chemical group 0.000 description 12
- 125000001544 thienyl group Chemical group 0.000 description 12
- 230000014509 gene expression Effects 0.000 description 11
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 11
- 230000005764 inhibitory process Effects 0.000 description 11
- 238000001294 liquid chromatography-tandem mass spectrometry Methods 0.000 description 11
- 229940002612 prodrug Drugs 0.000 description 11
- 239000000651 prodrug Substances 0.000 description 11
- 239000000047 product Substances 0.000 description 11
- 239000006228 supernatant Substances 0.000 description 11
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 10
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 10
- 230000035605 chemotaxis Effects 0.000 description 10
- IRSFLDGTOHBADP-UHFFFAOYSA-N embelin Chemical compound CCCCCCCCCCCC1=C(O)C(=O)C=C(O)C1=O IRSFLDGTOHBADP-UHFFFAOYSA-N 0.000 description 10
- 238000002474 experimental method Methods 0.000 description 10
- 239000000706 filtrate Substances 0.000 description 10
- VVWRJUBEIPHGQF-MDZDMXLPSA-N propan-2-yl (ne)-n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)\N=N\C(=O)OC(C)C VVWRJUBEIPHGQF-MDZDMXLPSA-N 0.000 description 10
- 239000000758 substrate Substances 0.000 description 10
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 9
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 9
- 208000006673 asthma Diseases 0.000 description 9
- 239000003153 chemical reaction reagent Substances 0.000 description 9
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 9
- 239000010410 layer Substances 0.000 description 9
- 238000012746 preparative thin layer chromatography Methods 0.000 description 9
- 239000007787 solid Substances 0.000 description 9
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 8
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 8
- 206010061218 Inflammation Diseases 0.000 description 8
- 241000699670 Mus sp. Species 0.000 description 8
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 8
- 239000000556 agonist Substances 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 8
- 239000003795 chemical substances by application Substances 0.000 description 8
- 238000010790 dilution Methods 0.000 description 8
- 239000012895 dilution Substances 0.000 description 8
- 235000019253 formic acid Nutrition 0.000 description 8
- 230000004054 inflammatory process Effects 0.000 description 8
- 210000001853 liver microsome Anatomy 0.000 description 8
- 239000012528 membrane Substances 0.000 description 8
- 238000010992 reflux Methods 0.000 description 8
- 239000000725 suspension Substances 0.000 description 8
- YNTJKQDWYXUTLZ-UHFFFAOYSA-N 2-(3-chlorophenoxy)propanoic acid Chemical compound OC(=O)C(C)OC1=CC=CC(Cl)=C1 YNTJKQDWYXUTLZ-UHFFFAOYSA-N 0.000 description 7
- 201000009794 Idiopathic Pulmonary Fibrosis Diseases 0.000 description 7
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 7
- 125000004429 atom Chemical group 0.000 description 7
- 239000006285 cell suspension Substances 0.000 description 7
- 125000000623 heterocyclic group Chemical group 0.000 description 7
- 208000036971 interstitial lung disease 2 Diseases 0.000 description 7
- DLBFLQKQABVKGT-UHFFFAOYSA-L lucifer yellow dye Chemical compound [Li+].[Li+].[O-]S(=O)(=O)C1=CC(C(N(C(=O)NN)C2=O)=O)=C3C2=CC(S([O-])(=O)=O)=CC3=C1N DLBFLQKQABVKGT-UHFFFAOYSA-L 0.000 description 7
- 239000002480 mineral oil Substances 0.000 description 7
- 235000010446 mineral oil Nutrition 0.000 description 7
- 230000008569 process Effects 0.000 description 7
- 239000011734 sodium Substances 0.000 description 7
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 7
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 7
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 6
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 6
- VFTRKSBEFQDZKX-UHFFFAOYSA-N 3,3'-diindolylmethane Chemical compound C1=CC=C2C(CC=3C4=CC=CC=C4NC=3)=CNC2=C1 VFTRKSBEFQDZKX-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 6
- 239000007995 HEPES buffer Substances 0.000 description 6
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 229910052796 boron Inorganic materials 0.000 description 6
- 238000005119 centrifugation Methods 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 229920003045 dextran sodium sulfate Polymers 0.000 description 6
- 230000004968 inflammatory condition Effects 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 230000005012 migration Effects 0.000 description 6
- 238000013508 migration Methods 0.000 description 6
- 125000002950 monocyclic group Chemical group 0.000 description 6
- 125000002757 morpholinyl group Chemical group 0.000 description 6
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 6
- 239000008188 pellet Substances 0.000 description 6
- 125000003386 piperidinyl group Chemical group 0.000 description 6
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 6
- 239000002244 precipitate Substances 0.000 description 6
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 6
- 238000003908 quality control method Methods 0.000 description 6
- 102000005962 receptors Human genes 0.000 description 6
- 108020003175 receptors Proteins 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- 125000001424 substituent group Chemical group 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- 125000005309 thioalkoxy group Chemical group 0.000 description 6
- 239000003981 vehicle Substances 0.000 description 6
- 239000003039 volatile agent Substances 0.000 description 6
- OZFAFGSSMRRTDW-UHFFFAOYSA-N (2,4-dichlorophenyl) benzenesulfonate Chemical compound ClC1=CC(Cl)=CC=C1OS(=O)(=O)C1=CC=CC=C1 OZFAFGSSMRRTDW-UHFFFAOYSA-N 0.000 description 5
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 5
- IRBAWVGZNJIROV-SFHVURJKSA-N 9-(2-cyclopropylethynyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC4CC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 IRBAWVGZNJIROV-SFHVURJKSA-N 0.000 description 5
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 5
- 239000012591 Dulbecco’s Phosphate Buffered Saline Substances 0.000 description 5
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 5
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 5
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 5
- 206010047115 Vasculitis Diseases 0.000 description 5
- XJLXINKUBYWONI-DQQFMEOOSA-N [[(2r,3r,4r,5r)-5-(6-aminopurin-9-yl)-3-hydroxy-4-phosphonooxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [(2s,3r,4s,5s)-5-(3-carbamoylpyridin-1-ium-1-yl)-3,4-dihydroxyoxolan-2-yl]methyl phosphate Chemical compound NC(=O)C1=CC=C[N+]([C@@H]2[C@H]([C@@H](O)[C@H](COP([O-])(=O)OP(O)(=O)OC[C@@H]3[C@H]([C@@H](OP(O)(O)=O)[C@@H](O3)N3C4=NC=NC(N)=C4N=C3)O)O2)O)=C1 XJLXINKUBYWONI-DQQFMEOOSA-N 0.000 description 5
- 239000004480 active ingredient Substances 0.000 description 5
- 150000008064 anhydrides Chemical class 0.000 description 5
- 125000002619 bicyclic group Chemical group 0.000 description 5
- 229910000024 caesium carbonate Inorganic materials 0.000 description 5
- 125000000753 cycloalkyl group Chemical group 0.000 description 5
- GHVNFZFCNZKVNT-UHFFFAOYSA-N decanoic acid Chemical compound CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 5
- 208000035475 disorder Diseases 0.000 description 5
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 5
- 210000002865 immune cell Anatomy 0.000 description 5
- 230000000155 isotopic effect Effects 0.000 description 5
- 208000030159 metabolic disease Diseases 0.000 description 5
- 230000004060 metabolic process Effects 0.000 description 5
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 5
- 238000010232 migration assay Methods 0.000 description 5
- 125000004433 nitrogen atom Chemical group N* 0.000 description 5
- 229910052700 potassium Inorganic materials 0.000 description 5
- 239000011591 potassium Substances 0.000 description 5
- 125000006239 protecting group Chemical group 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- 206010039073 rheumatoid arthritis Diseases 0.000 description 5
- 229910052708 sodium Inorganic materials 0.000 description 5
- 238000003756 stirring Methods 0.000 description 5
- 239000011550 stock solution Substances 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 5
- 239000003643 water by type Substances 0.000 description 5
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 4
- CMEPUAROFJSGJN-UHFFFAOYSA-N 1,4-dioxan-2-ylmethanol Chemical compound OCC1COCCO1 CMEPUAROFJSGJN-UHFFFAOYSA-N 0.000 description 4
- CEBKHWWANWSNTI-UHFFFAOYSA-N 2-methylbut-3-yn-2-ol Chemical compound CC(C)(O)C#C CEBKHWWANWSNTI-UHFFFAOYSA-N 0.000 description 4
- YACFFSVYSPMSGS-UHFFFAOYSA-N 3-methoxyprop-1-yne Chemical compound COCC#C YACFFSVYSPMSGS-UHFFFAOYSA-N 0.000 description 4
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- 208000035473 Communicable disease Diseases 0.000 description 4
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical compound NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 4
- 208000029523 Interstitial Lung disease Diseases 0.000 description 4
- 238000005481 NMR spectroscopy Methods 0.000 description 4
- 229920002565 Polyethylene Glycol 400 Polymers 0.000 description 4
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 4
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 4
- 210000001744 T-lymphocyte Anatomy 0.000 description 4
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 description 4
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 4
- QBYJBZPUGVGKQQ-SJJAEHHWSA-N aldrin Chemical compound C1[C@H]2C=C[C@@H]1[C@H]1[C@@](C3(Cl)Cl)(Cl)C(Cl)=C(Cl)[C@@]3(Cl)[C@H]12 QBYJBZPUGVGKQQ-SJJAEHHWSA-N 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 239000005557 antagonist Substances 0.000 description 4
- 239000007864 aqueous solution Substances 0.000 description 4
- 206010003246 arthritis Diseases 0.000 description 4
- 210000003719 b-lymphocyte Anatomy 0.000 description 4
- MUALRAIOVNYAIW-UHFFFAOYSA-N binap Chemical compound C1=CC=CC=C1P(C=1C(=C2C=CC=CC2=CC=1)C=1C2=CC=CC=C2C=CC=1P(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 MUALRAIOVNYAIW-UHFFFAOYSA-N 0.000 description 4
- 239000002775 capsule Substances 0.000 description 4
- 229960000623 carbamazepine Drugs 0.000 description 4
- FFGPTBGBLSHEPO-UHFFFAOYSA-N carbamazepine Chemical compound C1=CC2=CC=CC=C2N(C(=O)N)C2=CC=CC=C21 FFGPTBGBLSHEPO-UHFFFAOYSA-N 0.000 description 4
- 230000001684 chronic effect Effects 0.000 description 4
- 229940125904 compound 1 Drugs 0.000 description 4
- 229940125782 compound 2 Drugs 0.000 description 4
- 238000013461 design Methods 0.000 description 4
- 239000002552 dosage form Substances 0.000 description 4
- 230000002124 endocrine Effects 0.000 description 4
- 208000030172 endocrine system disease Diseases 0.000 description 4
- 239000002158 endotoxin Substances 0.000 description 4
- 238000011049 filling Methods 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- UEXQBEVWFZKHNB-UHFFFAOYSA-N intermediate 29 Natural products C1=CC(N)=CC=C1NC1=NC=CC=N1 UEXQBEVWFZKHNB-UHFFFAOYSA-N 0.000 description 4
- 239000011777 magnesium Substances 0.000 description 4
- 229920000609 methyl cellulose Polymers 0.000 description 4
- 239000001923 methylcellulose Substances 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- UQPUONNXJVWHRM-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 UQPUONNXJVWHRM-UHFFFAOYSA-N 0.000 description 4
- JLFNLZLINWHATN-UHFFFAOYSA-N pentaethylene glycol Chemical compound OCCOCCOCCOCCOCCO JLFNLZLINWHATN-UHFFFAOYSA-N 0.000 description 4
- 239000000546 pharmaceutical excipient Substances 0.000 description 4
- 239000002953 phosphate buffered saline Substances 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- AQHHHDLHHXJYJD-UHFFFAOYSA-N propranolol Chemical compound C1=CC=C2C(OCC(O)CNC(C)C)=CC=CC2=C1 AQHHHDLHHXJYJD-UHFFFAOYSA-N 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- KSAVQLQVUXSOCR-UHFFFAOYSA-M sodium lauroyl sarcosinate Chemical compound [Na+].CCCCCCCCCCCC(=O)N(C)CC([O-])=O KSAVQLQVUXSOCR-UHFFFAOYSA-M 0.000 description 4
- 239000012134 supernatant fraction Substances 0.000 description 4
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- 230000036962 time dependent Effects 0.000 description 4
- 229920002554 vinyl polymer Polymers 0.000 description 4
- NPLZNDDFVCGRAG-UHFFFAOYSA-N (2-cyanophenyl)boronic acid Chemical compound OB(O)C1=CC=CC=C1C#N NPLZNDDFVCGRAG-UHFFFAOYSA-N 0.000 description 3
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 3
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 3
- KAESVJOAVNADME-UHFFFAOYSA-N 1H-pyrrole Natural products C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 3
- PVKCAQKXTLCSBC-UHFFFAOYSA-N 1h-isoquinolin-4-one Chemical compound C1=CC=C2C(=O)C=NCC2=C1 PVKCAQKXTLCSBC-UHFFFAOYSA-N 0.000 description 3
- RIYFONBSYWACFF-UHFFFAOYSA-N 2-bromoethylcyclopropane Chemical compound BrCCC1CC1 RIYFONBSYWACFF-UHFFFAOYSA-N 0.000 description 3
- IJRKLHTZAIFUTB-UHFFFAOYSA-N 5-nitro-2-(2-phenylethylamino)benzoic acid Chemical compound OC(=O)C1=CC([N+]([O-])=O)=CC=C1NCCC1=CC=CC=C1 IJRKLHTZAIFUTB-UHFFFAOYSA-N 0.000 description 3
- XUKUURHRXDUEBC-KAYWLYCHSA-N Atorvastatin Chemical compound C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CC[C@@H](O)C[C@@H](O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-KAYWLYCHSA-N 0.000 description 3
- XUKUURHRXDUEBC-UHFFFAOYSA-N Atorvastatin Natural products C=1C=CC=CC=1C1=C(C=2C=CC(F)=CC=2)N(CCC(O)CC(O)CC(O)=O)C(C(C)C)=C1C(=O)NC1=CC=CC=C1 XUKUURHRXDUEBC-UHFFFAOYSA-N 0.000 description 3
- 208000023275 Autoimmune disease Diseases 0.000 description 3
- BGGALFIXXQOTPY-NRFANRHFSA-N C1(=C(C2=C(C=C1)N(C(C#N)=C2)C[C@@H](N1CCN(CC1)S(=O)(=O)C)C)C)CN1CCC(CC1)NC1=NC(=NC2=C1C=C(S2)CC(F)(F)F)NC Chemical compound C1(=C(C2=C(C=C1)N(C(C#N)=C2)C[C@@H](N1CCN(CC1)S(=O)(=O)C)C)C)CN1CCC(CC1)NC1=NC(=NC2=C1C=C(S2)CC(F)(F)F)NC BGGALFIXXQOTPY-NRFANRHFSA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- 108010081668 Cytochrome P-450 CYP3A Proteins 0.000 description 3
- 102100039205 Cytochrome P450 3A4 Human genes 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- 208000037487 Endotoxemia Diseases 0.000 description 3
- 208000009386 Experimental Arthritis Diseases 0.000 description 3
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- 102000013462 Interleukin-12 Human genes 0.000 description 3
- 108010065805 Interleukin-12 Proteins 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- LIMFPAAAIVQRRD-BCGVJQADSA-N N-[2-[(3S,4R)-3-fluoro-4-methoxypiperidin-1-yl]pyrimidin-4-yl]-8-[(2R,3S)-2-methyl-3-(methylsulfonylmethyl)azetidin-1-yl]-5-propan-2-ylisoquinolin-3-amine Chemical compound F[C@H]1CN(CC[C@H]1OC)C1=NC=CC(=N1)NC=1N=CC2=C(C=CC(=C2C=1)C(C)C)N1[C@@H]([C@H](C1)CS(=O)(=O)C)C LIMFPAAAIVQRRD-BCGVJQADSA-N 0.000 description 3
- POFVJRKJJBFPII-UHFFFAOYSA-N N-cyclopentyl-5-[2-[[5-[(4-ethylpiperazin-1-yl)methyl]pyridin-2-yl]amino]-5-fluoropyrimidin-4-yl]-4-methyl-1,3-thiazol-2-amine Chemical compound C1(CCCC1)NC=1SC(=C(N=1)C)C1=NC(=NC=C1F)NC1=NC=C(C=C1)CN1CCN(CC1)CC POFVJRKJJBFPII-UHFFFAOYSA-N 0.000 description 3
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 3
- 239000004743 Polypropylene Substances 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 201000004681 Psoriasis Diseases 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 3
- 108700012920 TNF Proteins 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 239000002168 alkylating agent Substances 0.000 description 3
- 229940100198 alkylating agent Drugs 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- 229960005370 atorvastatin Drugs 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 229910002091 carbon monoxide Inorganic materials 0.000 description 3
- 230000003915 cell function Effects 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- 229940126142 compound 16 Drugs 0.000 description 3
- 229940125810 compound 20 Drugs 0.000 description 3
- 229940126086 compound 21 Drugs 0.000 description 3
- 230000009089 cytolysis Effects 0.000 description 3
- 230000002354 daily effect Effects 0.000 description 3
- MXFYYFVVIIWKFE-UHFFFAOYSA-N dicyclohexyl-[2-[2,6-di(propan-2-yloxy)phenyl]phenyl]phosphane Chemical compound CC(C)OC1=CC=CC(OC(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 MXFYYFVVIIWKFE-UHFFFAOYSA-N 0.000 description 3
- 231100000673 dose–response relationship Toxicity 0.000 description 3
- 210000003743 erythrocyte Anatomy 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- NPTDXPDGUHAFKC-UHFFFAOYSA-N ethynylcyclopropane Chemical compound C#CC1CC1 NPTDXPDGUHAFKC-UHFFFAOYSA-N 0.000 description 3
- 239000000796 flavoring agent Substances 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 3
- 210000003494 hepatocyte Anatomy 0.000 description 3
- 150000004677 hydrates Chemical class 0.000 description 3
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 3
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 150000002500 ions Chemical class 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 3
- 239000000314 lubricant Substances 0.000 description 3
- 238000004020 luminiscence type Methods 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 210000001589 microsome Anatomy 0.000 description 3
- 230000002314 neuroinflammatory effect Effects 0.000 description 3
- 229930027945 nicotinamide-adenine dinucleotide Natural products 0.000 description 3
- HYIMSNHJOBLJNT-UHFFFAOYSA-N nifedipine Chemical compound COC(=O)C1=C(C)NC(C)=C(C(=O)OC)C1C1=CC=CC=C1[N+]([O-])=O HYIMSNHJOBLJNT-UHFFFAOYSA-N 0.000 description 3
- 229960001597 nifedipine Drugs 0.000 description 3
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 230000035699 permeability Effects 0.000 description 3
- 239000008363 phosphate buffer Substances 0.000 description 3
- 239000011148 porous material Substances 0.000 description 3
- 238000011533 pre-incubation Methods 0.000 description 3
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 3
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 238000013222 sprague-dawley male rat Methods 0.000 description 3
- 238000004544 sputter deposition Methods 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 3
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 3
- 201000008827 tuberculosis Diseases 0.000 description 3
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 2
- DIOHEXPTUTVCNX-UHFFFAOYSA-N 1,1,1-trifluoro-n-phenyl-n-(trifluoromethylsulfonyl)methanesulfonamide Chemical compound FC(F)(F)S(=O)(=O)N(S(=O)(=O)C(F)(F)F)C1=CC=CC=C1 DIOHEXPTUTVCNX-UHFFFAOYSA-N 0.000 description 2
- APQIUTYORBAGEZ-UHFFFAOYSA-N 1,1-dibromoethane Chemical compound CC(Br)Br APQIUTYORBAGEZ-UHFFFAOYSA-N 0.000 description 2
- KBFFXDRANASBGL-UHFFFAOYSA-N 1-[2-(3-methoxyphenyl)ethyl]-1,3-diazinane-2,4,6-trione Chemical compound COC1=CC=CC(CCN2C(NC(=O)CC2=O)=O)=C1 KBFFXDRANASBGL-UHFFFAOYSA-N 0.000 description 2
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 2
- MMYKTRPLXXWLBC-UHFFFAOYSA-N 1-bromo-2-ethoxyethane Chemical compound CCOCCBr MMYKTRPLXXWLBC-UHFFFAOYSA-N 0.000 description 2
- JTLAIKFGRHDNQM-UHFFFAOYSA-N 1-bromo-2-fluoroethane Chemical compound FCCBr JTLAIKFGRHDNQM-UHFFFAOYSA-N 0.000 description 2
- YZUPZGFPHUVJKC-UHFFFAOYSA-N 1-bromo-2-methoxyethane Chemical compound COCCBr YZUPZGFPHUVJKC-UHFFFAOYSA-N 0.000 description 2
- LQMDOONLLAJAPZ-UHFFFAOYSA-N 1-ethynylcyclopentan-1-ol Chemical compound C#CC1(O)CCCC1 LQMDOONLLAJAPZ-UHFFFAOYSA-N 0.000 description 2
- CJTZXIJETZZARD-UHFFFAOYSA-N 1-iodo-2,2-dimethylpropane Chemical compound CC(C)(C)CI CJTZXIJETZZARD-UHFFFAOYSA-N 0.000 description 2
- PAMIQIKDUOTOBW-UHFFFAOYSA-N 1-methylpiperidine Chemical compound CN1CCCCC1 PAMIQIKDUOTOBW-UHFFFAOYSA-N 0.000 description 2
- XTBAPWCYTNCZTO-UHFFFAOYSA-N 1H-isoindolone Natural products C1=CC=C2C(=O)N=CC2=C1 XTBAPWCYTNCZTO-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- HXNYJZAEGHSVKR-YMXDCFFPSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxy-4-methylpentyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCC(O)C(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 HXNYJZAEGHSVKR-YMXDCFFPSA-N 0.000 description 2
- RPRAXVBIKFVDNO-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(4-hydroxy-4-methylpent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCC(C)(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 RPRAXVBIKFVDNO-SFHVURJKSA-N 0.000 description 2
- KZBSTXQYMUCJLA-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(4-methoxybutyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCCCOC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 KZBSTXQYMUCJLA-SFHVURJKSA-N 0.000 description 2
- BPFWZVHBOZPPJX-IBGZPJMESA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-[2-(1-hydroxycyclopentyl)ethynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C(C=2N(C(N=C(OC[C@H]3OCCOC3)C=2)=O)CC2)C2=CC=1C#CC1(O)CCCC1 BPFWZVHBOZPPJX-IBGZPJMESA-N 0.000 description 2
- XVEMVXXDOOBYHB-IBGZPJMESA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-[3-(2-methoxyethoxy)prop-1-ynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCOCCOC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 XVEMVXXDOOBYHB-IBGZPJMESA-N 0.000 description 2
- HCGFUIQPSOCUHI-UHFFFAOYSA-N 2-propan-2-yloxyethanol Chemical compound CC(C)OCCO HCGFUIQPSOCUHI-UHFFFAOYSA-N 0.000 description 2
- YEYKMVJDLWJFOA-UHFFFAOYSA-N 2-propoxyethanol Chemical compound CCCOCCO YEYKMVJDLWJFOA-UHFFFAOYSA-N 0.000 description 2
- KGIGUEBEKRSTEW-UHFFFAOYSA-N 2-vinylpyridine Chemical compound C=CC1=CC=CC=N1 KGIGUEBEKRSTEW-UHFFFAOYSA-N 0.000 description 2
- MGADZUXDNSDTHW-UHFFFAOYSA-N 2H-pyran Chemical compound C1OC=CC=C1 MGADZUXDNSDTHW-UHFFFAOYSA-N 0.000 description 2
- VIIBOHRJBXNITD-UHFFFAOYSA-N 3-(chloromethyl)-5-cyclopropyl-1,2,4-oxadiazole Chemical compound ClCC1=NOC(C2CC2)=N1 VIIBOHRJBXNITD-UHFFFAOYSA-N 0.000 description 2
- PUNRPAWKFTXZIW-UHFFFAOYSA-N 3-ethylpent-1-yn-3-ol Chemical compound CCC(O)(CC)C#C PUNRPAWKFTXZIW-UHFFFAOYSA-N 0.000 description 2
- USCSRAJGJYMJFZ-UHFFFAOYSA-N 3-methyl-1-butyne Chemical compound CC(C)C#C USCSRAJGJYMJFZ-UHFFFAOYSA-N 0.000 description 2
- XMIIGOLPHOKFCH-UHFFFAOYSA-N 3-phenylpropionic acid Chemical compound OC(=O)CCC1=CC=CC=C1 XMIIGOLPHOKFCH-UHFFFAOYSA-N 0.000 description 2
- OWCNPTHAWPMOJU-UHFFFAOYSA-N 4,4-dimethylpentan-1-ol Chemical compound CC(C)(C)CCCO OWCNPTHAWPMOJU-UHFFFAOYSA-N 0.000 description 2
- HSHNITRMYYLLCV-UHFFFAOYSA-N 4-methylumbelliferone Chemical compound C1=C(O)C=CC2=C1OC(=O)C=C2C HSHNITRMYYLLCV-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- BGXQHNQYMRFIGL-SFHVURJKSA-N 9-(2,2-dimethylbutylamino)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(NCC(C)(C)CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 BGXQHNQYMRFIGL-SFHVURJKSA-N 0.000 description 2
- KJVMULZFHGUNRH-ZOWNYOTGSA-N 9-amino-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one;hydrochloride Chemical compound Cl.C=1C(N)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 KJVMULZFHGUNRH-ZOWNYOTGSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- 125000000041 C6-C10 aryl group Chemical group 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 239000005632 Capric acid (CAS 334-48-5) Substances 0.000 description 2
- 206010009900 Colitis ulcerative Diseases 0.000 description 2
- 208000011231 Crohn disease Diseases 0.000 description 2
- 102000002004 Cytochrome P-450 Enzyme System Human genes 0.000 description 2
- 108010015742 Cytochrome P-450 Enzyme System Proteins 0.000 description 2
- NBSCHQHZLSJFNQ-GASJEMHNSA-N D-Glucose 6-phosphate Chemical compound OC1O[C@H](COP(O)(O)=O)[C@@H](O)[C@H](O)[C@H]1O NBSCHQHZLSJFNQ-GASJEMHNSA-N 0.000 description 2
- RGHNJXZEOKUKBD-SQOUGZDYSA-N D-gluconic acid Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O RGHNJXZEOKUKBD-SQOUGZDYSA-N 0.000 description 2
- 206010012438 Dermatitis atopic Diseases 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 208000017701 Endocrine disease Diseases 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- VFRROHXSMXFLSN-UHFFFAOYSA-N Glc6P Natural products OP(=O)(O)OCC(O)C(O)C(O)C(O)C=O VFRROHXSMXFLSN-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 229920002527 Glycogen Polymers 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 201000005569 Gout Diseases 0.000 description 2
- 208000035895 Guillain-Barré syndrome Diseases 0.000 description 2
- 239000012981 Hank's balanced salt solution Substances 0.000 description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 2
- 102000004890 Interleukin-8 Human genes 0.000 description 2
- 108090001007 Interleukin-8 Proteins 0.000 description 2
- 239000005639 Lauric acid Substances 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- 208000019693 Lung disease Diseases 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 2
- 206010049567 Miller Fisher syndrome Diseases 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- CHJJGSNFBQVOTG-UHFFFAOYSA-N N-methyl-guanidine Natural products CNC(N)=N CHJJGSNFBQVOTG-UHFFFAOYSA-N 0.000 description 2
- 239000007832 Na2SO4 Substances 0.000 description 2
- 244000061176 Nicotiana tabacum Species 0.000 description 2
- 235000002637 Nicotiana tabacum Nutrition 0.000 description 2
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 2
- 208000018737 Parkinson disease Diseases 0.000 description 2
- 101150003085 Pdcl gene Proteins 0.000 description 2
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 108010029485 Protein Isoforms Proteins 0.000 description 2
- 102000001708 Protein Isoforms Human genes 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- 239000012980 RPMI-1640 medium Substances 0.000 description 2
- 238000010240 RT-PCR analysis Methods 0.000 description 2
- 241000219061 Rheum Species 0.000 description 2
- 206010040047 Sepsis Diseases 0.000 description 2
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 206010051379 Systemic Inflammatory Response Syndrome Diseases 0.000 description 2
- 201000006704 Ulcerative Colitis Diseases 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 2
- CMEPUAROFJSGJN-RXMQYKEDSA-N [(2r)-1,4-dioxan-2-yl]methanol Chemical compound OC[C@@H]1COCCO1 CMEPUAROFJSGJN-RXMQYKEDSA-N 0.000 description 2
- CMEPUAROFJSGJN-YFKPBYRVSA-N [(2s)-1,4-dioxan-2-yl]methanol Chemical compound OC[C@H]1COCCO1 CMEPUAROFJSGJN-YFKPBYRVSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 208000036981 active tuberculosis Diseases 0.000 description 2
- 125000004423 acyloxy group Chemical group 0.000 description 2
- 210000001789 adipocyte Anatomy 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 150000001345 alkine derivatives Chemical class 0.000 description 2
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 2
- 208000028004 allergic respiratory disease Diseases 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 239000003146 anticoagulant agent Substances 0.000 description 2
- 229940127219 anticoagulant drug Drugs 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 201000008937 atopic dermatitis Diseases 0.000 description 2
- 208000010668 atopic eczema Diseases 0.000 description 2
- 208000022362 bacterial infectious disease Diseases 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- IANQTJSKSUMEQM-UHFFFAOYSA-N benzofuran Natural products C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 2
- OTJZCIYGRUNXTP-UHFFFAOYSA-N but-3-yn-1-ol Chemical compound OCCC#C OTJZCIYGRUNXTP-UHFFFAOYSA-N 0.000 description 2
- UADYIMLSJBHNHU-UHFFFAOYSA-N but-3-yn-2-ol Chemical compound [CH2]C(O)C#C UADYIMLSJBHNHU-UHFFFAOYSA-N 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000004202 carbamide Substances 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- 238000000423 cell based assay Methods 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 239000013592 cell lysate Substances 0.000 description 2
- 230000003399 chemotactic effect Effects 0.000 description 2
- 125000001309 chloro group Chemical group Cl* 0.000 description 2
- VZWXIQHBIQLMPN-UHFFFAOYSA-N chromane Chemical compound C1=CC=C2CCCOC2=C1 VZWXIQHBIQLMPN-UHFFFAOYSA-N 0.000 description 2
- WCZVZNOTHYJIEI-UHFFFAOYSA-N cinnoline Chemical compound N1=NC=CC2=CC=CC=C21 WCZVZNOTHYJIEI-UHFFFAOYSA-N 0.000 description 2
- 239000007979 citrate buffer Substances 0.000 description 2
- CBGUOGMQLZIXBE-XGQKBEPLSA-N clobetasol propionate Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CCl)(OC(=O)CC)[C@@]1(C)C[C@@H]2O CBGUOGMQLZIXBE-XGQKBEPLSA-N 0.000 description 2
- 238000011260 co-administration Methods 0.000 description 2
- 206010009887 colitis Diseases 0.000 description 2
- 229940125797 compound 12 Drugs 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- KVFDZFBHBWTVID-UHFFFAOYSA-N cyclohexanecarbaldehyde Chemical compound O=CC1CCCCC1 KVFDZFBHBWTVID-UHFFFAOYSA-N 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- 230000006735 deficit Effects 0.000 description 2
- 230000003111 delayed effect Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 206010012601 diabetes mellitus Diseases 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- SWSQBOPZIKWTGO-UHFFFAOYSA-N dimethylaminoamidine Natural products CN(C)C(N)=N SWSQBOPZIKWTGO-UHFFFAOYSA-N 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 239000003651 drinking water Substances 0.000 description 2
- 235000020188 drinking water Nutrition 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 238000007876 drug discovery Methods 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 201000002491 encephalomyelitis Diseases 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 235000019634 flavors Nutrition 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 239000012458 free base Substances 0.000 description 2
- 235000021588 free fatty acids Nutrition 0.000 description 2
- 208000015707 frontal fibrosing alopecia Diseases 0.000 description 2
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 2
- 229940096919 glycogen Drugs 0.000 description 2
- 210000000224 granular leucocyte Anatomy 0.000 description 2
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 2
- 229960002897 heparin Drugs 0.000 description 2
- 229920000669 heparin Polymers 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 125000001183 hydrocarbyl group Chemical group 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 239000007928 intraperitoneal injection Substances 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 201000004792 malaria Diseases 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 239000008108 microcrystalline cellulose Substances 0.000 description 2
- 229940016286 microcrystalline cellulose Drugs 0.000 description 2
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 2
- 210000000274 microglia Anatomy 0.000 description 2
- 230000003228 microsomal effect Effects 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 210000001616 monocyte Anatomy 0.000 description 2
- TXXHDPDFNKHHGW-UHFFFAOYSA-N muconic acid Chemical compound OC(=O)C=CC=CC(O)=O TXXHDPDFNKHHGW-UHFFFAOYSA-N 0.000 description 2
- LPOIGVZLNWEGJG-UHFFFAOYSA-N n-benzyl-5-(4-methylpiperazin-1-yl)-2-nitroaniline Chemical compound C1CN(C)CCN1C1=CC=C([N+]([O-])=O)C(NCC=2C=CC=CC=2)=C1 LPOIGVZLNWEGJG-UHFFFAOYSA-N 0.000 description 2
- IZKIWEYIOKPHLF-UHFFFAOYSA-N n-prop-2-ynylaniline Chemical compound C#CCNC1=CC=CC=C1 IZKIWEYIOKPHLF-UHFFFAOYSA-N 0.000 description 2
- 210000004498 neuroglial cell Anatomy 0.000 description 2
- 230000011242 neutrophil chemotaxis Effects 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- 231100000062 no-observed-adverse-effect level Toxicity 0.000 description 2
- 231100000252 nontoxic Toxicity 0.000 description 2
- 230000003000 nontoxic effect Effects 0.000 description 2
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- LBSKEFWQPNVWTP-UHFFFAOYSA-N pent-1-yn-3-ol Chemical compound CCC(O)C#C LBSKEFWQPNVWTP-UHFFFAOYSA-N 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 239000004417 polycarbonate Substances 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- 238000012877 positron emission topography Methods 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 230000037452 priming Effects 0.000 description 2
- 230000000770 proinflammatory effect Effects 0.000 description 2
- TVDSBUOJIPERQY-UHFFFAOYSA-N prop-2-yn-1-ol Chemical compound OCC#C TVDSBUOJIPERQY-UHFFFAOYSA-N 0.000 description 2
- 229960003712 propranolol Drugs 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 230000007115 recruitment Effects 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 238000013207 serial dilution Methods 0.000 description 2
- 239000000779 smoke Substances 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 2
- YEENEYXBHNNNGV-XEHWZWQGSA-M sodium;3-acetamido-5-[acetyl(methyl)amino]-2,4,6-triiodobenzoate;(2r,3r,4s,5s,6r)-2-[(2r,3s,4s,5r)-3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound [Na+].CC(=O)N(C)C1=C(I)C(NC(C)=O)=C(I)C(C([O-])=O)=C1I.O[C@H]1[C@H](O)[C@@H](CO)O[C@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 YEENEYXBHNNNGV-XEHWZWQGSA-M 0.000 description 2
- FIWQZURFGYXCEO-UHFFFAOYSA-M sodium;decanoate Chemical compound [Na+].CCCCCCCCCC([O-])=O FIWQZURFGYXCEO-UHFFFAOYSA-M 0.000 description 2
- 238000003797 solvolysis reaction Methods 0.000 description 2
- 230000006641 stabilisation Effects 0.000 description 2
- 238000011105 stabilization Methods 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000007858 starting material Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 238000013268 sustained release Methods 0.000 description 2
- 229960003604 testosterone Drugs 0.000 description 2
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 2
- BRNULMACUQOKMR-UHFFFAOYSA-N thiomorpholine Chemical compound C1CSCCN1 BRNULMACUQOKMR-UHFFFAOYSA-N 0.000 description 2
- 229930192474 thiophene Natural products 0.000 description 2
- 231100000607 toxicokinetics Toxicity 0.000 description 2
- 230000002103 transcriptional effect Effects 0.000 description 2
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 2
- PBIMIGNDTBRRPI-UHFFFAOYSA-N trifluoro borate Chemical compound FOB(OF)OF PBIMIGNDTBRRPI-UHFFFAOYSA-N 0.000 description 2
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 2
- 210000003462 vein Anatomy 0.000 description 2
- 229960003048 vinblastine Drugs 0.000 description 2
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 2
- IIBSDEGSGLVNOY-UHFFFAOYSA-N (1-ethylpyrazol-4-yl)boronic acid Chemical compound CCN1C=C(B(O)O)C=N1 IIBSDEGSGLVNOY-UHFFFAOYSA-N 0.000 description 1
- SYWDZJWBRYIJJB-UHFFFAOYSA-N (1-methylindol-5-yl)boronic acid Chemical compound OB(O)C1=CC=C2N(C)C=CC2=C1 SYWDZJWBRYIJJB-UHFFFAOYSA-N 0.000 description 1
- WRPVRKKWSXLHKX-UHFFFAOYSA-N (1-propylpyrazol-4-yl)boronic acid Chemical compound CCCN1C=C(B(O)O)C=N1 WRPVRKKWSXLHKX-UHFFFAOYSA-N 0.000 description 1
- ASGMFNBUXDJWJJ-JLCFBVMHSA-N (1R,3R)-3-[[3-bromo-1-[4-(5-methyl-1,3,4-thiadiazol-2-yl)phenyl]pyrazolo[3,4-d]pyrimidin-6-yl]amino]-N,1-dimethylcyclopentane-1-carboxamide Chemical compound BrC1=NN(C2=NC(=NC=C21)N[C@H]1C[C@@](CC1)(C(=O)NC)C)C1=CC=C(C=C1)C=1SC(=NN=1)C ASGMFNBUXDJWJJ-JLCFBVMHSA-N 0.000 description 1
- UAOUIVVJBYDFKD-XKCDOFEDSA-N (1R,9R,10S,11R,12R,15S,18S,21R)-10,11,21-trihydroxy-8,8-dimethyl-14-methylidene-4-(prop-2-enylamino)-20-oxa-5-thia-3-azahexacyclo[9.7.2.112,15.01,9.02,6.012,18]henicosa-2(6),3-dien-13-one Chemical compound C([C@@H]1[C@@H](O)[C@@]23C(C1=C)=O)C[C@H]2[C@]12C(N=C(NCC=C)S4)=C4CC(C)(C)[C@H]1[C@H](O)[C@]3(O)OC2 UAOUIVVJBYDFKD-XKCDOFEDSA-N 0.000 description 1
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 1
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 description 1
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 1
- VREWSCMOGIXMDQ-UHFFFAOYSA-N (2,3-dimethoxyphenyl)boronic acid Chemical compound COC1=CC=CC(B(O)O)=C1OC VREWSCMOGIXMDQ-UHFFFAOYSA-N 0.000 description 1
- QOZLFNQLIKOGDR-UHFFFAOYSA-N (2,5-dimethoxyphenyl)boronic acid Chemical compound COC1=CC=C(OC)C(B(O)O)=C1 QOZLFNQLIKOGDR-UHFFFAOYSA-N 0.000 description 1
- ADGHSWFUZUADDH-UHFFFAOYSA-N (2,6-dimethoxypyridin-3-yl)boronic acid Chemical compound COC1=CC=C(B(O)O)C(OC)=N1 ADGHSWFUZUADDH-UHFFFAOYSA-N 0.000 description 1
- RRCMGJCFMJBHQC-UHFFFAOYSA-N (2-chlorophenyl)boronic acid Chemical compound OB(O)C1=CC=CC=C1Cl RRCMGJCFMJBHQC-UHFFFAOYSA-N 0.000 description 1
- FXUMKSCYKPOZOO-UHFFFAOYSA-N (2-ethoxypyridin-3-yl)boronic acid Chemical compound CCOC1=NC=CC=C1B(O)O FXUMKSCYKPOZOO-UHFFFAOYSA-N 0.000 description 1
- ROEQGIFOWRQYHD-UHFFFAOYSA-N (2-methoxyphenyl)boronic acid Chemical compound COC1=CC=CC=C1B(O)O ROEQGIFOWRQYHD-UHFFFAOYSA-N 0.000 description 1
- NVOLYUXUHWBCRJ-UHFFFAOYSA-N (2-methoxypyridin-3-yl)boronic acid Chemical compound COC1=NC=CC=C1B(O)O NVOLYUXUHWBCRJ-UHFFFAOYSA-N 0.000 description 1
- UFYBTLOLWSABAU-UHFFFAOYSA-N (2-methylpyridin-4-yl)boronic acid Chemical compound CC1=CC(B(O)O)=CC=N1 UFYBTLOLWSABAU-UHFFFAOYSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- GCTFTMWXZFLTRR-GFCCVEGCSA-N (2r)-2-amino-n-[3-(difluoromethoxy)-4-(1,3-oxazol-5-yl)phenyl]-4-methylpentanamide Chemical compound FC(F)OC1=CC(NC(=O)[C@H](N)CC(C)C)=CC=C1C1=CN=CO1 GCTFTMWXZFLTRR-GFCCVEGCSA-N 0.000 description 1
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 1
- YJLIKUSWRSEPSM-WGQQHEPDSA-N (2r,3r,4s,5r)-2-[6-amino-8-[(4-phenylphenyl)methylamino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1CNC1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O YJLIKUSWRSEPSM-WGQQHEPDSA-N 0.000 description 1
- VIJSPAIQWVPKQZ-BLECARSGSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-acetamido-5-(diaminomethylideneamino)pentanoyl]amino]-4-methylpentanoyl]amino]-4,4-dimethylpentanoyl]amino]-4-methylpentanoyl]amino]propanoyl]amino]-5-(diaminomethylideneamino)pentanoic acid Chemical compound NC(=N)NCCC[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(C)=O VIJSPAIQWVPKQZ-BLECARSGSA-N 0.000 description 1
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 1
- DKYRKAIKWFHQHM-UHFFFAOYSA-N (3,5-dichlorophenyl)boronic acid Chemical compound OB(O)C1=CC(Cl)=CC(Cl)=C1 DKYRKAIKWFHQHM-UHFFFAOYSA-N 0.000 description 1
- YABZNRCHCVTPDV-UHFFFAOYSA-N (3,5-dimethyl-1h-pyrazol-4-yl)boronic acid Chemical compound CC1=NNC(C)=C1B(O)O YABZNRCHCVTPDV-UHFFFAOYSA-N 0.000 description 1
- IBTSWKLSEOGJGJ-UHFFFAOYSA-N (3-acetamidophenyl)boronic acid Chemical compound CC(=O)NC1=CC=CC(B(O)O)=C1 IBTSWKLSEOGJGJ-UHFFFAOYSA-N 0.000 description 1
- RNNYXSWJFLHIRC-UHFFFAOYSA-N (3-carbamoyl-4-fluorophenyl)boronic acid Chemical compound NC(=O)C1=CC(B(O)O)=CC=C1F RNNYXSWJFLHIRC-UHFFFAOYSA-N 0.000 description 1
- FTMWTTRIUYYHDE-UHFFFAOYSA-N (3-carbamoyl-5-fluorophenyl)boronic acid Chemical compound NC(=O)C1=CC(F)=CC(B(O)O)=C1 FTMWTTRIUYYHDE-UHFFFAOYSA-N 0.000 description 1
- WDGWHKRJEBENCE-UHFFFAOYSA-N (3-carbamoylphenyl)boronic acid Chemical compound NC(=O)C1=CC=CC(B(O)O)=C1 WDGWHKRJEBENCE-UHFFFAOYSA-N 0.000 description 1
- YQNAXOGPSUVHNU-UHFFFAOYSA-N (3-chloro-2-methoxypyridin-4-yl)boronic acid Chemical compound COC1=NC=CC(B(O)O)=C1Cl YQNAXOGPSUVHNU-UHFFFAOYSA-N 0.000 description 1
- XDBHWPLGGBLUHH-UHFFFAOYSA-N (3-cyanophenyl)boronic acid Chemical compound OB(O)C1=CC=CC(C#N)=C1 XDBHWPLGGBLUHH-UHFFFAOYSA-N 0.000 description 1
- BIFLCXDWWOPWRD-UHFFFAOYSA-N (3-cyanopyridin-4-yl)boronic acid Chemical compound OB(O)C1=CC=NC=C1C#N BIFLCXDWWOPWRD-UHFFFAOYSA-N 0.000 description 1
- NLLGFYPSWCMUIV-UHFFFAOYSA-N (3-methoxyphenyl)boronic acid Chemical compound COC1=CC=CC(B(O)O)=C1 NLLGFYPSWCMUIV-UHFFFAOYSA-N 0.000 description 1
- NLQMSBJFLQPLIJ-UHFFFAOYSA-N (3-methyloxetan-3-yl)methanol Chemical compound OCC1(C)COC1 NLQMSBJFLQPLIJ-UHFFFAOYSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- FNHHVPPSBFQMEL-KQHDFZBMSA-N (3S)-5-N-[(1S,5R)-3-hydroxy-6-bicyclo[3.1.0]hexanyl]-7-N,3-dimethyl-3-phenyl-2H-1-benzofuran-5,7-dicarboxamide Chemical compound CNC(=O)c1cc(cc2c1OC[C@@]2(C)c1ccccc1)C(=O)NC1[C@H]2CC(O)C[C@@H]12 FNHHVPPSBFQMEL-KQHDFZBMSA-N 0.000 description 1
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 1
- UDQTXCHQKHIQMH-KYGLGHNPSA-N (3ar,5s,6s,7r,7ar)-5-(difluoromethyl)-2-(ethylamino)-5,6,7,7a-tetrahydro-3ah-pyrano[3,2-d][1,3]thiazole-6,7-diol Chemical compound S1C(NCC)=N[C@H]2[C@@H]1O[C@H](C(F)F)[C@@H](O)[C@@H]2O UDQTXCHQKHIQMH-KYGLGHNPSA-N 0.000 description 1
- OQANPHBRHBJGNZ-FYJGNVAPSA-N (3e)-6-oxo-3-[[4-(pyridin-2-ylsulfamoyl)phenyl]hydrazinylidene]cyclohexa-1,4-diene-1-carboxylic acid Chemical compound C1=CC(=O)C(C(=O)O)=C\C1=N\NC1=CC=C(S(=O)(=O)NC=2N=CC=CC=2)C=C1 OQANPHBRHBJGNZ-FYJGNVAPSA-N 0.000 description 1
- OOKAZRDERJMRCJ-KOUAFAAESA-N (3r)-7-[(1s,2s,4ar,6s,8s)-2,6-dimethyl-8-[(2s)-2-methylbutanoyl]oxy-1,2,4a,5,6,7,8,8a-octahydronaphthalen-1-yl]-3-hydroxy-5-oxoheptanoic acid Chemical compound C1=C[C@H](C)[C@H](CCC(=O)C[C@@H](O)CC(O)=O)C2[C@@H](OC(=O)[C@@H](C)CC)C[C@@H](C)C[C@@H]21 OOKAZRDERJMRCJ-KOUAFAAESA-N 0.000 description 1
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 1
- MPDDTAJMJCESGV-CTUHWIOQSA-M (3r,5r)-7-[2-(4-fluorophenyl)-5-[methyl-[(1r)-1-phenylethyl]carbamoyl]-4-propan-2-ylpyrazol-3-yl]-3,5-dihydroxyheptanoate Chemical compound C1([C@@H](C)N(C)C(=O)C2=NN(C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C2C(C)C)C=2C=CC(F)=CC=2)=CC=CC=C1 MPDDTAJMJCESGV-CTUHWIOQSA-M 0.000 description 1
- CEBAHYWORUOILU-UHFFFAOYSA-N (4-cyanophenyl)boronic acid Chemical compound OB(O)C1=CC=C(C#N)C=C1 CEBAHYWORUOILU-UHFFFAOYSA-N 0.000 description 1
- BHHPDDMECQZQNL-UHFFFAOYSA-N (4-cyanopyridin-3-yl)boronic acid Chemical compound OB(O)C1=CN=CC=C1C#N BHHPDDMECQZQNL-UHFFFAOYSA-N 0.000 description 1
- VOAAEKKFGLPLLU-UHFFFAOYSA-N (4-methoxyphenyl)boronic acid Chemical compound COC1=CC=C(B(O)O)C=C1 VOAAEKKFGLPLLU-UHFFFAOYSA-N 0.000 description 1
- WHDIUBHAKZDSJL-UHFFFAOYSA-N (4-morpholin-4-ylphenyl)boronic acid Chemical compound C1=CC(B(O)O)=CC=C1N1CCOCC1 WHDIUBHAKZDSJL-UHFFFAOYSA-N 0.000 description 1
- YQOLEILXOBUDMU-KRWDZBQOSA-N (4R)-5-[(6-bromo-3-methyl-2-pyrrolidin-1-ylquinoline-4-carbonyl)amino]-4-(2-chlorophenyl)pentanoic acid Chemical compound CC1=C(C2=C(C=CC(=C2)Br)N=C1N3CCCC3)C(=O)NC[C@H](CCC(=O)O)C4=CC=CC=C4Cl YQOLEILXOBUDMU-KRWDZBQOSA-N 0.000 description 1
- NDVPMVJEURRBQM-UHFFFAOYSA-N (5-carbamoyl-2-fluorophenyl)boronic acid Chemical compound NC(=O)C1=CC=C(F)C(B(O)O)=C1 NDVPMVJEURRBQM-UHFFFAOYSA-N 0.000 description 1
- ISDFOFZTZUILPE-UHFFFAOYSA-N (5-methoxypyridin-3-yl)boronic acid Chemical compound COC1=CN=CC(B(O)O)=C1 ISDFOFZTZUILPE-UHFFFAOYSA-N 0.000 description 1
- LMJIDBVSSSPRII-UHFFFAOYSA-N (5-methylfuran-2-yl)boronic acid Chemical compound CC1=CC=C(B(O)O)O1 LMJIDBVSSSPRII-UHFFFAOYSA-N 0.000 description 1
- OIIOPWHTJZYKIL-PMACEKPBSA-N (5S)-5-[[[5-[2-chloro-3-[2-chloro-3-[6-methoxy-5-[[[(2S)-5-oxopyrrolidin-2-yl]methylamino]methyl]pyrazin-2-yl]phenyl]phenyl]-3-methoxypyrazin-2-yl]methylamino]methyl]pyrrolidin-2-one Chemical compound C1(=C(N=C(C2=C(C(C3=CC=CC(=C3Cl)C3=NC(OC)=C(N=C3)CNC[C@H]3NC(=O)CC3)=CC=C2)Cl)C=N1)OC)CNC[C@H]1NC(=O)CC1 OIIOPWHTJZYKIL-PMACEKPBSA-N 0.000 description 1
- IOQORVDNYPOZPL-VQTJNVASSA-N (5S,6R)-5-(4-chlorophenyl)-6-cyclopropyl-3-[6-methoxy-5-(4-methylimidazol-1-yl)pyridin-2-yl]-5,6-dihydro-2H-1,2,4-oxadiazine Chemical compound ClC1=CC=C(C=C1)[C@@H]1NC(=NO[C@@H]1C1CC1)C1=NC(=C(C=C1)N1C=NC(=C1)C)OC IOQORVDNYPOZPL-VQTJNVASSA-N 0.000 description 1
- JRWBBVDYZMMZOH-UHFFFAOYSA-N (6-cyanopyridin-3-yl)boronic acid Chemical compound OB(O)C1=CC=C(C#N)N=C1 JRWBBVDYZMMZOH-UHFFFAOYSA-N 0.000 description 1
- UONCERAQKBPLML-UHFFFAOYSA-N (6-ethoxypyridin-3-yl)boronic acid Chemical compound CCOC1=CC=C(B(O)O)C=N1 UONCERAQKBPLML-UHFFFAOYSA-N 0.000 description 1
- DHADXDMPEUWEAS-UHFFFAOYSA-N (6-methoxypyridin-3-yl)boronic acid Chemical compound COC1=CC=C(B(O)O)C=N1 DHADXDMPEUWEAS-UHFFFAOYSA-N 0.000 description 1
- MZUSCPDSQJSBSY-UHFFFAOYSA-N (6-methylpyridin-3-yl)boronic acid Chemical compound CC1=CC=C(B(O)O)C=N1 MZUSCPDSQJSBSY-UHFFFAOYSA-N 0.000 description 1
- SGEOBUJTURUUJE-UHFFFAOYSA-N (6-propan-2-yloxypyridin-3-yl)boronic acid Chemical compound CC(C)OC1=CC=C(B(O)O)C=N1 SGEOBUJTURUUJE-UHFFFAOYSA-N 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- WHTVZRBIWZFKQO-AWEZNQCLSA-N (S)-chloroquine Chemical compound ClC1=CC=C2C(N[C@@H](C)CCCN(CC)CC)=CC=NC2=C1 WHTVZRBIWZFKQO-AWEZNQCLSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- SRKGZXIJDGWVAI-GVAVTCRGSA-M (e,3r)-7-[6-tert-butyl-4-(4-fluorophenyl)-2-propan-2-ylpyridin-3-yl]-3,5-dihydroxyhept-6-enoate Chemical compound CC(C)C1=NC(C(C)(C)C)=CC(C=2C=CC(F)=CC=2)=C1\C=C\C(O)C[C@@H](O)CC([O-])=O SRKGZXIJDGWVAI-GVAVTCRGSA-M 0.000 description 1
- DEVSOMFAQLZNKR-RJRFIUFISA-N (z)-3-[3-[3,5-bis(trifluoromethyl)phenyl]-1,2,4-triazol-1-yl]-n'-pyrazin-2-ylprop-2-enehydrazide Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(C2=NN(\C=C/C(=O)NNC=3N=CC=NC=3)C=N2)=C1 DEVSOMFAQLZNKR-RJRFIUFISA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- CSNIZNHTOVFARY-UHFFFAOYSA-N 1,2-benzothiazole Chemical compound C1=CC=C2C=NSC2=C1 CSNIZNHTOVFARY-UHFFFAOYSA-N 0.000 description 1
- KTZQTRPPVKQPFO-UHFFFAOYSA-N 1,2-benzoxazole Chemical compound C1=CC=C2C=NOC2=C1 KTZQTRPPVKQPFO-UHFFFAOYSA-N 0.000 description 1
- 125000005918 1,2-dimethylbutyl group Chemical group 0.000 description 1
- 125000005926 1,2-dimethylbutyloxy group Chemical group 0.000 description 1
- FTNJQNQLEGKTGD-UHFFFAOYSA-N 1,3-benzodioxole Chemical compound C1=CC=C2OCOC2=C1 FTNJQNQLEGKTGD-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- KKHFRAFPESRGGD-UHFFFAOYSA-N 1,3-dimethyl-7-[3-(n-methylanilino)propyl]purine-2,6-dione Chemical compound C1=NC=2N(C)C(=O)N(C)C(=O)C=2N1CCCN(C)C1=CC=CC=C1 KKHFRAFPESRGGD-UHFFFAOYSA-N 0.000 description 1
- VMLKTERJLVWEJJ-UHFFFAOYSA-N 1,5-naphthyridine Chemical compound C1=CC=NC2=CC=CN=C21 VMLKTERJLVWEJJ-UHFFFAOYSA-N 0.000 description 1
- FLBAYUMRQUHISI-UHFFFAOYSA-N 1,8-naphthyridine Chemical compound N1=CC=CC2=CC=CN=C21 FLBAYUMRQUHISI-UHFFFAOYSA-N 0.000 description 1
- MHSLDASSAFCCDO-UHFFFAOYSA-N 1-(5-tert-butyl-2-methylpyrazol-3-yl)-3-(4-pyridin-4-yloxyphenyl)urea Chemical compound CN1N=C(C(C)(C)C)C=C1NC(=O)NC(C=C1)=CC=C1OC1=CC=NC=C1 MHSLDASSAFCCDO-UHFFFAOYSA-N 0.000 description 1
- PVOAHINGSUIXLS-UHFFFAOYSA-N 1-Methylpiperazine Chemical compound CN1CCNCC1 PVOAHINGSUIXLS-UHFFFAOYSA-N 0.000 description 1
- KQZLRWGGWXJPOS-NLFPWZOASA-N 1-[(1R)-1-(2,4-dichlorophenyl)ethyl]-6-[(4S,5R)-4-[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylcyclohexen-1-yl]pyrazolo[3,4-b]pyrazine-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)Cl)[C@@H](C)N1N=C(C=2C1=NC(=CN=2)C1=CC[C@@H]([C@@H](C1)C)N1[C@@H](CCC1)CO)C#N KQZLRWGGWXJPOS-NLFPWZOASA-N 0.000 description 1
- WZZBNLYBHUDSHF-DHLKQENFSA-N 1-[(3s,4s)-4-[8-(2-chloro-4-pyrimidin-2-yloxyphenyl)-7-fluoro-2-methylimidazo[4,5-c]quinolin-1-yl]-3-fluoropiperidin-1-yl]-2-hydroxyethanone Chemical compound CC1=NC2=CN=C3C=C(F)C(C=4C(=CC(OC=5N=CC=CN=5)=CC=4)Cl)=CC3=C2N1[C@H]1CCN(C(=O)CO)C[C@@H]1F WZZBNLYBHUDSHF-DHLKQENFSA-N 0.000 description 1
- PKRRNTJIHGOMRC-UHFFFAOYSA-N 1-benzofuran-2-ylboronic acid Chemical compound C1=CC=C2OC(B(O)O)=CC2=C1 PKRRNTJIHGOMRC-UHFFFAOYSA-N 0.000 description 1
- CEVMYGZHEJSOHZ-UHFFFAOYSA-N 1-bromo-3-methoxypropane Chemical compound COCCCBr CEVMYGZHEJSOHZ-UHFFFAOYSA-N 0.000 description 1
- KBIAVTUACPKPFJ-UHFFFAOYSA-N 1-ethynyl-4-methoxybenzene Chemical compound COC1=CC=C(C#C)C=C1 KBIAVTUACPKPFJ-UHFFFAOYSA-N 0.000 description 1
- CGHIBGNXEGJPQZ-UHFFFAOYSA-N 1-hexyne Chemical compound CCCCC#C CGHIBGNXEGJPQZ-UHFFFAOYSA-N 0.000 description 1
- AMMPLVWPWSYRDR-UHFFFAOYSA-N 1-methylbicyclo[2.2.2]oct-2-ene-4-carboxylic acid Chemical compound C1CC2(C(O)=O)CCC1(C)C=C2 AMMPLVWPWSYRDR-UHFFFAOYSA-N 0.000 description 1
- IBXNCJKFFQIKKY-UHFFFAOYSA-N 1-pentyne Chemical compound CCCC#C IBXNCJKFFQIKKY-UHFFFAOYSA-N 0.000 description 1
- UGOQKSGJGCADAG-UHFFFAOYSA-N 1-prop-2-ynylimidazole Chemical compound C#CCN1C=CN=C1 UGOQKSGJGCADAG-UHFFFAOYSA-N 0.000 description 1
- YQEHAHXOJGYJDW-UHFFFAOYSA-N 1-pyridin-3-ylprop-2-yn-1-ol Chemical compound C#CC(O)C1=CC=CN=C1 YQEHAHXOJGYJDW-UHFFFAOYSA-N 0.000 description 1
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- ABEXEQSGABRUHS-UHFFFAOYSA-N 16-methylheptadecyl 16-methylheptadecanoate Chemical compound CC(C)CCCCCCCCCCCCCCCOC(=O)CCCCCCCCCCCCCCC(C)C ABEXEQSGABRUHS-UHFFFAOYSA-N 0.000 description 1
- 238000004293 19F NMR spectroscopy Methods 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- MFJCPDOGFAYSTF-UHFFFAOYSA-N 1H-isochromene Chemical compound C1=CC=C2COC=CC2=C1 MFJCPDOGFAYSTF-UHFFFAOYSA-N 0.000 description 1
- CLVPGJWAMIADSY-UHFFFAOYSA-N 1h-indazol-5-ylboronic acid Chemical compound OB(O)C1=CC=C2NN=CC2=C1 CLVPGJWAMIADSY-UHFFFAOYSA-N 0.000 description 1
- VHADYSUJZAPXOW-UHFFFAOYSA-N 1h-indol-5-ylboronic acid Chemical compound OB(O)C1=CC=C2NC=CC2=C1 VHADYSUJZAPXOW-UHFFFAOYSA-N 0.000 description 1
- KEZNMOUMHOZFRA-UHFFFAOYSA-N 1h-pyrazol-4-ylboronic acid Chemical compound OB(O)C=1C=NNC=1 KEZNMOUMHOZFRA-UHFFFAOYSA-N 0.000 description 1
- AMFYRKOUWBAGHV-UHFFFAOYSA-N 1h-pyrazolo[4,3-b]pyridine Chemical compound C1=CN=C2C=NNC2=C1 AMFYRKOUWBAGHV-UHFFFAOYSA-N 0.000 description 1
- LTMRRSWNXVJMBA-UHFFFAOYSA-L 2,2-diethylpropanedioate Chemical compound CCC(CC)(C([O-])=O)C([O-])=O LTMRRSWNXVJMBA-UHFFFAOYSA-L 0.000 description 1
- QYPLKDUOPJZROX-UHFFFAOYSA-N 2,2-dimethylbutanal Chemical compound CCC(C)(C)C=O QYPLKDUOPJZROX-UHFFFAOYSA-N 0.000 description 1
- OXBLVCZKDOZZOJ-UHFFFAOYSA-N 2,3-Dihydrothiophene Chemical compound C1CC=CS1 OXBLVCZKDOZZOJ-UHFFFAOYSA-N 0.000 description 1
- OYJGEOAXBALSMM-UHFFFAOYSA-N 2,3-dihydro-1,3-thiazole Chemical compound C1NC=CS1 OYJGEOAXBALSMM-UHFFFAOYSA-N 0.000 description 1
- JKTCBAGSMQIFNL-UHFFFAOYSA-N 2,3-dihydrofuran Chemical compound C1CC=CO1 JKTCBAGSMQIFNL-UHFFFAOYSA-N 0.000 description 1
- WGFNXGPBPIJYLI-UHFFFAOYSA-N 2,6-difluoro-3-[(3-fluorophenyl)sulfonylamino]-n-(3-methoxy-1h-pyrazolo[3,4-b]pyridin-5-yl)benzamide Chemical compound C1=C2C(OC)=NNC2=NC=C1NC(=O)C(C=1F)=C(F)C=CC=1NS(=O)(=O)C1=CC=CC(F)=C1 WGFNXGPBPIJYLI-UHFFFAOYSA-N 0.000 description 1
- JRFGYWSBNKDLGZ-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(1-ethylpyrazol-4-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NN(CC)C=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 JRFGYWSBNKDLGZ-UHFFFAOYSA-N 0.000 description 1
- OEPJEARHYWJBCU-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-ethyl-3-hydroxypent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)(CC)CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 OEPJEARHYWJBCU-UHFFFAOYSA-N 0.000 description 1
- YLALDPZXHDFNQM-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxy-3-phenylbut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=CC=CC=1C(O)(C)C#CC(C=1)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 YLALDPZXHDFNQM-UHFFFAOYSA-N 0.000 description 1
- VUIPUKDNNNJULW-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(3-hydroxyhex-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)CCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 VUIPUKDNNNJULW-UHFFFAOYSA-N 0.000 description 1
- JFJQSOXFJBIMOJ-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(5-methylfuran-2-yl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound O1C(C)=CC=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 JFJQSOXFJBIMOJ-UHFFFAOYSA-N 0.000 description 1
- KEYIADWBIYGSQO-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-(furan-2-ylmethylamino)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(NCC=4OC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 KEYIADWBIYGSQO-UHFFFAOYSA-N 0.000 description 1
- RJWYVPVVMDCLSE-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[1-(3-methylbutyl)pyrazol-4-yl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=NN(CCC(C)C)C=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 RJWYVPVVMDCLSE-UHFFFAOYSA-N 0.000 description 1
- MFLNNZYQRZBWIP-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-[2-(1-methylimidazol-2-yl)ethynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound CN1C=CN=C1C#CC1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 MFLNNZYQRZBWIP-UHFFFAOYSA-N 0.000 description 1
- RHAOSQPRANZJHK-UHFFFAOYSA-N 2-(1,4-dioxan-2-ylmethoxy)-9-prop-1-ynyl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 RHAOSQPRANZJHK-UHFFFAOYSA-N 0.000 description 1
- FQMZXMVHHKXGTM-UHFFFAOYSA-N 2-(1-adamantyl)-n-[2-[2-(2-hydroxyethylamino)ethylamino]quinolin-5-yl]acetamide Chemical compound C1C(C2)CC(C3)CC2CC13CC(=O)NC1=CC=CC2=NC(NCCNCCO)=CC=C21 FQMZXMVHHKXGTM-UHFFFAOYSA-N 0.000 description 1
- VCUXVXLUOHDHKK-UHFFFAOYSA-N 2-(2-aminopyrimidin-4-yl)-4-(2-chloro-4-methoxyphenyl)-1,3-thiazole-5-carboxamide Chemical compound ClC1=CC(OC)=CC=C1C1=C(C(N)=O)SC(C=2N=C(N)N=CC=2)=N1 VCUXVXLUOHDHKK-UHFFFAOYSA-N 0.000 description 1
- QEBYEVQKHRUYPE-UHFFFAOYSA-N 2-(2-chlorophenyl)-5-[(1-methylpyrazol-3-yl)methyl]-4-[[methyl(pyridin-3-ylmethyl)amino]methyl]-1h-pyrazolo[4,3-c]pyridine-3,6-dione Chemical compound C1=CN(C)N=C1CN1C(=O)C=C2NN(C=3C(=CC=CC=3)Cl)C(=O)C2=C1CN(C)CC1=CC=CN=C1 QEBYEVQKHRUYPE-UHFFFAOYSA-N 0.000 description 1
- OKJKIWMQIZJLFG-UHFFFAOYSA-N 2-(3-hydroxyphenyl)ethylurea Chemical compound NC(=O)NCCC1=CC=CC(O)=C1 OKJKIWMQIZJLFG-UHFFFAOYSA-N 0.000 description 1
- WJBMRZAHTUFBGE-UHFFFAOYSA-N 2-(3-methoxyphenyl)ethanamine Chemical compound COC1=CC=CC(CCN)=C1 WJBMRZAHTUFBGE-UHFFFAOYSA-N 0.000 description 1
- SFUNVKXTODHDQY-UHFFFAOYSA-N 2-(3-methoxyphenyl)ethylurea Chemical compound COC1=CC=CC(CCNC(N)=O)=C1 SFUNVKXTODHDQY-UHFFFAOYSA-N 0.000 description 1
- XMGJGSKRRWXOIF-UHFFFAOYSA-N 2-(azepan-1-yl)ethyl 2-cyclohexyl-2-thiophen-3-ylacetate;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C1CCCCC1C(C1=CSC=C1)C(=O)OCCN1CCCCCC1 XMGJGSKRRWXOIF-UHFFFAOYSA-N 0.000 description 1
- MHNWCBOXPOLLIB-UHFFFAOYSA-N 2-(bromomethyl)oxane Chemical compound BrCC1CCCCO1 MHNWCBOXPOLLIB-UHFFFAOYSA-N 0.000 description 1
- NAOPGVBLRHCPHI-UHFFFAOYSA-N 2-(chloromethyl)-1,3-oxazole Chemical compound ClCC1=NC=CO1 NAOPGVBLRHCPHI-UHFFFAOYSA-N 0.000 description 1
- UCLTZKFBJAFGCD-UHFFFAOYSA-N 2-(chloromethyl)-5-phenyl-1,3-oxazole Chemical compound O1C(CCl)=NC=C1C1=CC=CC=C1 UCLTZKFBJAFGCD-UHFFFAOYSA-N 0.000 description 1
- IMSODMZESSGVBE-UHFFFAOYSA-N 2-Oxazoline Chemical compound C1CN=CO1 IMSODMZESSGVBE-UHFFFAOYSA-N 0.000 description 1
- PYRKKGOKRMZEIT-UHFFFAOYSA-N 2-[6-(2-cyclopropylethoxy)-9-(2-hydroxy-2-methylpropyl)-1h-phenanthro[9,10-d]imidazol-2-yl]-5-fluorobenzene-1,3-dicarbonitrile Chemical compound C1=C2C3=CC(CC(C)(O)C)=CC=C3C=3NC(C=4C(=CC(F)=CC=4C#N)C#N)=NC=3C2=CC=C1OCCC1CC1 PYRKKGOKRMZEIT-UHFFFAOYSA-N 0.000 description 1
- PXLDABOJDRUBRB-GOSISDBHSA-N 2-[[(2r)-1,4-dioxan-2-yl]methoxy]-9-pentyl-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(CCCCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@H]1COCCO1 PXLDABOJDRUBRB-GOSISDBHSA-N 0.000 description 1
- PEFSAXPTEDRHFK-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(2-ethoxyethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCOCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 PEFSAXPTEDRHFK-KRWDZBQOSA-N 0.000 description 1
- ALSNCWKOUFIJHW-ZYZRXSCRSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(2-ethylhexylamino)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(NCC(CC)CCCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 ALSNCWKOUFIJHW-ZYZRXSCRSA-N 0.000 description 1
- HDGSQKHLTYKQFN-HNNXBMFYSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(2-fluoroethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCF)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 HDGSQKHLTYKQFN-HNNXBMFYSA-N 0.000 description 1
- VFPRXDIPJDALBQ-INIZCTEOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(2-methoxyethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OCCOC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 VFPRXDIPJDALBQ-INIZCTEOSA-N 0.000 description 1
- OEPJEARHYWJBCU-IBGZPJMESA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-ethyl-3-hydroxypent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)(CC)CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 OEPJEARHYWJBCU-IBGZPJMESA-N 0.000 description 1
- DJLCKRYRNSUXLI-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxy-3-methylbut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(C)(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 DJLCKRYRNSUXLI-KRWDZBQOSA-N 0.000 description 1
- LTUBGODGYMWGBU-YMXDCFFPSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxy-4,4-dimethylpent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)C(C)(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 LTUBGODGYMWGBU-YMXDCFFPSA-N 0.000 description 1
- FQYOAZIPVGMPMX-YMXDCFFPSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxy-4-methylpent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)C(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 FQYOAZIPVGMPMX-YMXDCFFPSA-N 0.000 description 1
- FMUHXPKLGMHDNM-JRZJBTRGSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxybut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 FMUHXPKLGMHDNM-JRZJBTRGSA-N 0.000 description 1
- QUXJSJPUEFPUAX-ZVAWYAOSSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxypent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(O)CC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 QUXJSJPUEFPUAX-ZVAWYAOSSA-N 0.000 description 1
- ZGJBNCCPCLGHNI-INIZCTEOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-hydroxyprop-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCO)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 ZGJBNCCPCLGHNI-INIZCTEOSA-N 0.000 description 1
- RIDUIZFRYDXCCD-YDNXMHBPSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-methoxy-4-methylpent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(OC)C(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 RIDUIZFRYDXCCD-YDNXMHBPSA-N 0.000 description 1
- HVTMZNQMPHTIHA-PKHIMPSTSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-methoxybut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CC(C)OC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 HVTMZNQMPHTIHA-PKHIMPSTSA-N 0.000 description 1
- HLAQLEHDEDDXKD-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(3-methoxyprop-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCOC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 HLAQLEHDEDDXKD-KRWDZBQOSA-N 0.000 description 1
- GITIKJVOXNTBIV-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(4-hydroxybut-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCCO)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 GITIKJVOXNTBIV-KRWDZBQOSA-N 0.000 description 1
- XZELLAGAOATKHG-PKHIMPSTSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(4-hydroxypent-1-ynyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCC(O)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 XZELLAGAOATKHG-PKHIMPSTSA-N 0.000 description 1
- MJIQIOIDMFDDBI-KRWDZBQOSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-(oxetan-3-yloxymethyl)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COC4COC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 MJIQIOIDMFDDBI-KRWDZBQOSA-N 0.000 description 1
- VHYAHDGHXLDCRL-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-[(3-methyloxetan-3-yl)methoxymethyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C=C(C=2N(C(N=C(OC[C@H]3OCCOC3)C=2)=O)CC2)C2=CC=1COCC1(C)COC1 VHYAHDGHXLDCRL-SFHVURJKSA-N 0.000 description 1
- JYCHUBYLKOFCRG-FQEVSTJZSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-[3-(2-ethoxyethoxy)prop-1-ynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCOCCOCC)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 JYCHUBYLKOFCRG-FQEVSTJZSA-N 0.000 description 1
- KPCFQZWDXFNIFC-SFHVURJKSA-N 2-[[(2s)-1,4-dioxan-2-yl]methoxy]-9-[3-(2-fluoroethoxy)prop-1-ynyl]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(C#CCOCCF)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 KPCFQZWDXFNIFC-SFHVURJKSA-N 0.000 description 1
- FMKGJQHNYMWDFJ-CVEARBPZSA-N 2-[[4-(2,2-difluoropropoxy)pyrimidin-5-yl]methylamino]-4-[[(1R,4S)-4-hydroxy-3,3-dimethylcyclohexyl]amino]pyrimidine-5-carbonitrile Chemical compound FC(COC1=NC=NC=C1CNC1=NC=C(C(=N1)N[C@H]1CC([C@H](CC1)O)(C)C)C#N)(C)F FMKGJQHNYMWDFJ-CVEARBPZSA-N 0.000 description 1
- PAYROHWFGZADBR-UHFFFAOYSA-N 2-[[4-amino-5-(5-iodo-4-methoxy-2-propan-2-ylphenoxy)pyrimidin-2-yl]amino]propane-1,3-diol Chemical compound C1=C(I)C(OC)=CC(C(C)C)=C1OC1=CN=C(NC(CO)CO)N=C1N PAYROHWFGZADBR-UHFFFAOYSA-N 0.000 description 1
- VVCMGAUPZIKYTH-VGHSCWAPSA-N 2-acetyloxybenzoic acid;[(2s,3r)-4-(dimethylamino)-3-methyl-1,2-diphenylbutan-2-yl] propanoate;1,3,7-trimethylpurine-2,6-dione Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O.CN1C(=O)N(C)C(=O)C2=C1N=CN2C.C([C@](OC(=O)CC)([C@H](C)CN(C)C)C=1C=CC=CC=1)C1=CC=CC=C1 VVCMGAUPZIKYTH-VGHSCWAPSA-N 0.000 description 1
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 1
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 1
- UXGVMFHEKMGWMA-UHFFFAOYSA-N 2-benzofuran Chemical compound C1=CC=CC2=COC=C21 UXGVMFHEKMGWMA-UHFFFAOYSA-N 0.000 description 1
- REXUYBKPWIPONM-UHFFFAOYSA-N 2-bromoacetonitrile Chemical compound BrCC#N REXUYBKPWIPONM-UHFFFAOYSA-N 0.000 description 1
- NXMYLLIQRKHHHH-UHFFFAOYSA-N 2-chloro-9-methoxy-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(OC)=CC=C2C=1CCN1C2=CC(Cl)=NC1=O NXMYLLIQRKHHHH-UHFFFAOYSA-N 0.000 description 1
- LGYNIFWIKSEESD-UHFFFAOYSA-N 2-ethylhexanal Chemical compound CCCCC(CC)C=O LGYNIFWIKSEESD-UHFFFAOYSA-N 0.000 description 1
- NHUBNHMFXQNNMV-UHFFFAOYSA-N 2-ethynylpyridine Chemical compound C#CC1=CC=CC=N1 NHUBNHMFXQNNMV-UHFFFAOYSA-N 0.000 description 1
- UPHOPMSGKZNELG-UHFFFAOYSA-N 2-hydroxynaphthalene-1-carboxylic acid Chemical compound C1=CC=C2C(C(=O)O)=C(O)C=CC2=C1 UPHOPMSGKZNELG-UHFFFAOYSA-N 0.000 description 1
- LFOIDLOIBZFWDO-UHFFFAOYSA-N 2-methoxy-6-[6-methoxy-4-[(3-phenylmethoxyphenyl)methoxy]-1-benzofuran-2-yl]imidazo[2,1-b][1,3,4]thiadiazole Chemical compound N1=C2SC(OC)=NN2C=C1C(OC1=CC(OC)=C2)=CC1=C2OCC(C=1)=CC=CC=1OCC1=CC=CC=C1 LFOIDLOIBZFWDO-UHFFFAOYSA-N 0.000 description 1
- KDIUHXUETKEUNL-UHFFFAOYSA-N 2-methyl-5-trimethylsilylpent-4-yn-2-ol Chemical compound CC(C)(O)CC#C[Si](C)(C)C KDIUHXUETKEUNL-UHFFFAOYSA-N 0.000 description 1
- KSLSOBUAIFEGLT-UHFFFAOYSA-N 2-phenylbut-3-yn-2-ol Chemical compound C#CC(O)(C)C1=CC=CC=C1 KSLSOBUAIFEGLT-UHFFFAOYSA-N 0.000 description 1
- MLJZIQHWAUYAPA-UHFFFAOYSA-N 2-piperidin-1-yl-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(N2CCCCC2)N=C1 MLJZIQHWAUYAPA-UHFFFAOYSA-N 0.000 description 1
- RKTXCUGUPDEZHR-UHFFFAOYSA-N 2-pyrrolidin-1-yl-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=CN=C1N1CCCC1 RKTXCUGUPDEZHR-UHFFFAOYSA-N 0.000 description 1
- HGBBKKWVSQBIMM-UHFFFAOYSA-N 2-pyrrolidin-1-yl-5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(N2CCCC2)N=C1 HGBBKKWVSQBIMM-UHFFFAOYSA-N 0.000 description 1
- 125000004485 2-pyrrolidinyl group Chemical group [H]N1C([H])([H])C([H])([H])C([H])([H])C1([H])* 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- CMLFRMDBDNHMRA-UHFFFAOYSA-N 2h-1,2-benzoxazine Chemical compound C1=CC=C2C=CNOC2=C1 CMLFRMDBDNHMRA-UHFFFAOYSA-N 0.000 description 1
- UMZCLZPXPCNKML-UHFFFAOYSA-N 2h-imidazo[4,5-d][1,3]thiazole Chemical compound C1=NC2=NCSC2=N1 UMZCLZPXPCNKML-UHFFFAOYSA-N 0.000 description 1
- 229940093768 3,3'-diindolylmethane Drugs 0.000 description 1
- 235000010045 3,3'-diindolylmethane Nutrition 0.000 description 1
- PPWNCLVNXGCGAF-UHFFFAOYSA-N 3,3-dimethylbut-1-yne Chemical compound CC(C)(C)C#C PPWNCLVNXGCGAF-UHFFFAOYSA-N 0.000 description 1
- MLMQPDHYNJCQAO-UHFFFAOYSA-N 3,3-dimethylbutyric acid Chemical compound CC(C)(C)CC(O)=O MLMQPDHYNJCQAO-UHFFFAOYSA-N 0.000 description 1
- WPWNEKFMGCWNPR-UHFFFAOYSA-N 3,4-dihydro-2h-thiochromene Chemical compound C1=CC=C2CCCSC2=C1 WPWNEKFMGCWNPR-UHFFFAOYSA-N 0.000 description 1
- YVWATSXVUOJOIG-UHFFFAOYSA-N 3,6-dihydro-2h-pyran-4-ylboronic acid Chemical compound OB(O)C1=CCOCC1 YVWATSXVUOJOIG-UHFFFAOYSA-N 0.000 description 1
- DFRAKBCRUYUFNT-UHFFFAOYSA-N 3,8-dicyclohexyl-2,4,7,9-tetrahydro-[1,3]oxazino[5,6-h][1,3]benzoxazine Chemical compound C1CCCCC1N1CC(C=CC2=C3OCN(C2)C2CCCCC2)=C3OC1 DFRAKBCRUYUFNT-UHFFFAOYSA-N 0.000 description 1
- XLZYKTYMLBOINK-UHFFFAOYSA-N 3-(4-hydroxybenzoyl)benzoic acid Chemical compound OC(=O)C1=CC=CC(C(=O)C=2C=CC(O)=CC=2)=C1 XLZYKTYMLBOINK-UHFFFAOYSA-N 0.000 description 1
- BXDLNPSUWNWPNY-UHFFFAOYSA-N 3-(chloromethyl)-1,5-dimethylpyrazole Chemical compound CC1=CC(CCl)=NN1C BXDLNPSUWNWPNY-UHFFFAOYSA-N 0.000 description 1
- PGYXLMWYFOXGGN-UHFFFAOYSA-N 3-(chloromethyl)-5-ethyl-1,2,4-oxadiazole Chemical compound CCC1=NC(CCl)=NO1 PGYXLMWYFOXGGN-UHFFFAOYSA-N 0.000 description 1
- ZFYVXZGJPJTIPQ-UHFFFAOYSA-N 3-(chloromethyl)-5-methyl-1,2,4-oxadiazole Chemical compound CC1=NC(CCl)=NO1 ZFYVXZGJPJTIPQ-UHFFFAOYSA-N 0.000 description 1
- CHNMYSFXOVDDFY-UHFFFAOYSA-N 3-(chloromethyl)-5-propan-2-yl-1,2,4-oxadiazole Chemical compound CC(C)C1=NC(CCl)=NO1 CHNMYSFXOVDDFY-UHFFFAOYSA-N 0.000 description 1
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 1
- WFOVEDJTASPCIR-UHFFFAOYSA-N 3-[(4-methyl-5-pyridin-4-yl-1,2,4-triazol-3-yl)methylamino]-n-[[2-(trifluoromethyl)phenyl]methyl]benzamide Chemical compound N=1N=C(C=2C=CN=CC=2)N(C)C=1CNC(C=1)=CC=CC=1C(=O)NCC1=CC=CC=C1C(F)(F)F WFOVEDJTASPCIR-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- UETNOXJRYZSQRA-UHFFFAOYSA-N 3-chloro-1,4-dimethylpyrazole Chemical compound CC1=CN(C)N=C1Cl UETNOXJRYZSQRA-UHFFFAOYSA-N 0.000 description 1
- ZRPLANDPDWYOMZ-UHFFFAOYSA-N 3-cyclopentylpropionic acid Chemical compound OC(=O)CCC1CCCC1 ZRPLANDPDWYOMZ-UHFFFAOYSA-N 0.000 description 1
- ISBNDFWSSCIEHO-UHFFFAOYSA-N 3-cyclopropylpropan-1-ol Chemical compound OCCCC1CC1 ISBNDFWSSCIEHO-UHFFFAOYSA-N 0.000 description 1
- CLRPXACRDTXENY-UHFFFAOYSA-N 3-ethynylpyridine Chemical compound C#CC1=CC=CN=C1 CLRPXACRDTXENY-UHFFFAOYSA-N 0.000 description 1
- 125000004575 3-pyrrolidinyl group Chemical group [H]N1C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- MCGBIXXDQFWVDW-UHFFFAOYSA-N 4,5-dihydro-1h-pyrazole Chemical compound C1CC=NN1 MCGBIXXDQFWVDW-UHFFFAOYSA-N 0.000 description 1
- ZGDLVKWIZHHWIR-UHFFFAOYSA-N 4-[5-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridin-2-yl]morpholine Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=C(N2CCOCC2)N=C1 ZGDLVKWIZHHWIR-UHFFFAOYSA-N 0.000 description 1
- WYFCZWSWFGJODV-MIANJLSGSA-N 4-[[(1s)-2-[(e)-3-[3-chloro-2-fluoro-6-(tetrazol-1-yl)phenyl]prop-2-enoyl]-5-(4-methyl-2-oxopiperazin-1-yl)-3,4-dihydro-1h-isoquinoline-1-carbonyl]amino]benzoic acid Chemical compound O=C1CN(C)CCN1C1=CC=CC2=C1CCN(C(=O)\C=C\C=1C(=CC=C(Cl)C=1F)N1N=NN=C1)[C@@H]2C(=O)NC1=CC=C(C(O)=O)C=C1 WYFCZWSWFGJODV-MIANJLSGSA-N 0.000 description 1
- MPMKMQHJHDHPBE-RUZDIDTESA-N 4-[[(2r)-1-(1-benzothiophene-3-carbonyl)-2-methylazetidine-2-carbonyl]-[(3-chlorophenyl)methyl]amino]butanoic acid Chemical compound O=C([C@@]1(N(CC1)C(=O)C=1C2=CC=CC=C2SC=1)C)N(CCCC(O)=O)CC1=CC=CC(Cl)=C1 MPMKMQHJHDHPBE-RUZDIDTESA-N 0.000 description 1
- GSDQYSSLIKJJOG-UHFFFAOYSA-N 4-chloro-2-(3-chloroanilino)benzoic acid Chemical compound OC(=O)C1=CC=C(Cl)C=C1NC1=CC=CC(Cl)=C1 GSDQYSSLIKJJOG-UHFFFAOYSA-N 0.000 description 1
- RJWBTWIBUIGANW-UHFFFAOYSA-N 4-chlorobenzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=C(Cl)C=C1 RJWBTWIBUIGANW-UHFFFAOYSA-N 0.000 description 1
- DQAZPZIYEOGZAF-UHFFFAOYSA-N 4-ethyl-n-[4-(3-ethynylanilino)-7-methoxyquinazolin-6-yl]piperazine-1-carboxamide Chemical compound C1CN(CC)CCN1C(=O)NC(C(=CC1=NC=N2)OC)=CC1=C2NC1=CC=CC(C#C)=C1 DQAZPZIYEOGZAF-UHFFFAOYSA-N 0.000 description 1
- SWJWVPMUAUALKX-UHFFFAOYSA-N 4-ethynyloxan-4-ol Chemical compound C#CC1(O)CCOCC1 SWJWVPMUAUALKX-UHFFFAOYSA-N 0.000 description 1
- FDEDJRHULYIJOR-UHFFFAOYSA-N 4-ethynylpyridine Chemical compound C#CC1=CC=NC=C1 FDEDJRHULYIJOR-UHFFFAOYSA-N 0.000 description 1
- UTIFIONYBLSHIL-UHFFFAOYSA-N 4-methylpent-1-yn-3-ol Chemical compound CC(C)C(O)C#C UTIFIONYBLSHIL-UHFFFAOYSA-N 0.000 description 1
- 125000004487 4-tetrahydropyranyl group Chemical group [H]C1([H])OC([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- MRUWJENAYHTDQG-UHFFFAOYSA-N 4H-pyran Chemical compound C1C=COC=C1 MRUWJENAYHTDQG-UHFFFAOYSA-N 0.000 description 1
- GDRVFDDBLLKWRI-UHFFFAOYSA-N 4H-quinolizine Chemical compound C1=CC=CN2CC=CC=C21 GDRVFDDBLLKWRI-UHFFFAOYSA-N 0.000 description 1
- FYDQQEVRVKAASZ-UHFFFAOYSA-N 5-(chloromethyl)-3-methyl-1,2,4-oxadiazole Chemical compound CC1=NOC(CCl)=N1 FYDQQEVRVKAASZ-UHFFFAOYSA-N 0.000 description 1
- ZWBJJNWJUXXFNP-UHFFFAOYSA-N 5-(chloromethyl)-3-methyl-1,2-oxazole Chemical compound CC=1C=C(CCl)ON=1 ZWBJJNWJUXXFNP-UHFFFAOYSA-N 0.000 description 1
- VKLKXFOZNHEBSW-UHFFFAOYSA-N 5-[[3-[(4-morpholin-4-ylbenzoyl)amino]phenyl]methoxy]pyridine-3-carboxamide Chemical compound O1CCN(CC1)C1=CC=C(C(=O)NC=2C=C(COC=3C=NC=C(C(=O)N)C=3)C=CC=2)C=C1 VKLKXFOZNHEBSW-UHFFFAOYSA-N 0.000 description 1
- GYCPLYCTMDTEPU-UHFFFAOYSA-N 5-bromopyrimidine Chemical compound BrC1=CN=CN=C1 GYCPLYCTMDTEPU-UHFFFAOYSA-N 0.000 description 1
- XFJBGINZIMNZBW-CRAIPNDOSA-N 5-chloro-2-[4-[(1r,2s)-2-[2-(5-methylsulfonylpyridin-2-yl)oxyethyl]cyclopropyl]piperidin-1-yl]pyrimidine Chemical compound N1=CC(S(=O)(=O)C)=CC=C1OCC[C@H]1[C@@H](C2CCN(CC2)C=2N=CC(Cl)=CN=2)C1 XFJBGINZIMNZBW-CRAIPNDOSA-N 0.000 description 1
- JFOSWQQRTHDTGG-UHFFFAOYSA-N 5-ethynyl-1-methylimidazole Chemical compound CN1C=NC=C1C#C JFOSWQQRTHDTGG-UHFFFAOYSA-N 0.000 description 1
- NTNUBJHPRAMQPC-UHFFFAOYSA-N 5-methylhex-1-yn-3-ol Chemical compound CC(C)CC(O)C#C NTNUBJHPRAMQPC-UHFFFAOYSA-N 0.000 description 1
- LUGZUJZYTRPEDY-UHFFFAOYSA-N 5-tert-butyl-2-(chloromethyl)-1,3-oxazole Chemical compound CC(C)(C)C1=CN=C(CCl)O1 LUGZUJZYTRPEDY-UHFFFAOYSA-N 0.000 description 1
- AIVSLDAXUIRICJ-UHFFFAOYSA-N 5-tert-butyl-3-(chloromethyl)-1,2,4-oxadiazole Chemical compound CC(C)(C)C1=NC(CCl)=NO1 AIVSLDAXUIRICJ-UHFFFAOYSA-N 0.000 description 1
- HZVHOILAWGOYKI-UHFFFAOYSA-N 6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=CC=C2CCN3C(=O)N=CC=C3C2=C1 HZVHOILAWGOYKI-UHFFFAOYSA-N 0.000 description 1
- RSIWALKZYXPAGW-NSHDSACASA-N 6-(3-fluorophenyl)-3-methyl-7-[(1s)-1-(7h-purin-6-ylamino)ethyl]-[1,3]thiazolo[3,2-a]pyrimidin-5-one Chemical compound C=1([C@@H](NC=2C=3N=CNC=3N=CN=2)C)N=C2SC=C(C)N2C(=O)C=1C1=CC=CC(F)=C1 RSIWALKZYXPAGW-NSHDSACASA-N 0.000 description 1
- GDUANFXPOZTYKS-UHFFFAOYSA-N 6-bromo-8-[(2,6-difluoro-4-methoxybenzoyl)amino]-4-oxochromene-2-carboxylic acid Chemical compound FC1=CC(OC)=CC(F)=C1C(=O)NC1=CC(Br)=CC2=C1OC(C(O)=O)=CC2=O GDUANFXPOZTYKS-UHFFFAOYSA-N 0.000 description 1
- 102100031126 6-phosphogluconolactonase Human genes 0.000 description 1
- 108010029731 6-phosphogluconolactonase Proteins 0.000 description 1
- HCCNBKFJYUWLEX-UHFFFAOYSA-N 7-(6-methoxypyridin-3-yl)-1-(2-propoxyethyl)-3-(pyrazin-2-ylmethylamino)pyrido[3,4-b]pyrazin-2-one Chemical compound O=C1N(CCOCCC)C2=CC(C=3C=NC(OC)=CC=3)=NC=C2N=C1NCC1=CN=CC=N1 HCCNBKFJYUWLEX-UHFFFAOYSA-N 0.000 description 1
- XASOHFCUIQARJT-UHFFFAOYSA-N 8-methoxy-6-[7-(2-morpholin-4-ylethoxy)imidazo[1,2-a]pyridin-3-yl]-2-(2,2,2-trifluoroethyl)-3,4-dihydroisoquinolin-1-one Chemical compound C(N1C(=O)C2=C(OC)C=C(C=3N4C(=NC=3)C=C(C=C4)OCCN3CCOCC3)C=C2CC1)C(F)(F)F XASOHFCUIQARJT-UHFFFAOYSA-N 0.000 description 1
- DFIYXVFBAYHFHF-SFHVURJKSA-N 9-(2,2-dimethylpropoxymethyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C=1C(COCC(C)(C)C)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OC[C@@H]1COCCO1 DFIYXVFBAYHFHF-SFHVURJKSA-N 0.000 description 1
- CGLMQSKTQZSXCH-SFHVURJKSA-N 9-(2-cyclopropylethyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(CCC4CC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 CGLMQSKTQZSXCH-SFHVURJKSA-N 0.000 description 1
- QYUIEQFTTNJTMS-UHFFFAOYSA-N 9-(3,5-dimethyl-1h-pyrazol-4-yl)-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound CC1=NNC(C)=C1C1=CC=C2C3=CC(OCC4OCCOC4)=NC(=O)N3CCC2=C1 QYUIEQFTTNJTMS-UHFFFAOYSA-N 0.000 description 1
- YHSONAVIPVCZDX-QFIPXVFZSA-N 9-(3-anilinoprop-1-ynyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CCNC=4C=CC=CC=4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 YHSONAVIPVCZDX-QFIPXVFZSA-N 0.000 description 1
- XIWIBKWGVWDVAZ-FQEVSTJZSA-N 9-(cyclohexyloxymethyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COC4CCCCC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 XIWIBKWGVWDVAZ-FQEVSTJZSA-N 0.000 description 1
- XFWPJCXTBXFACX-KRWDZBQOSA-N 9-(cyclopropylmethoxy)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(OCC4CC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 XFWPJCXTBXFACX-KRWDZBQOSA-N 0.000 description 1
- ABVVTAOXKDJPMY-SFHVURJKSA-N 9-(cyclopropylmethoxymethyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(COCC4CC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 ABVVTAOXKDJPMY-SFHVURJKSA-N 0.000 description 1
- RNGJWXRTLWVRTL-UHFFFAOYSA-N 9-[3-(benzylamino)prop-1-ynyl]-2-(1,4-dioxan-2-ylmethoxy)-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CCNCC=4C=CC=CC=4)C=C3CCN2C(=O)N=C1OCC1COCCO1 RNGJWXRTLWVRTL-UHFFFAOYSA-N 0.000 description 1
- 230000035502 ADME Effects 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 208000026872 Addison Disease Diseases 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 208000005676 Adrenogenital syndrome Diseases 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-OUBTZVSYSA-N Ammonia-15N Chemical compound [15NH3] QGZKDVFQNNGYKY-OUBTZVSYSA-N 0.000 description 1
- 206010003559 Asthma late onset Diseases 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 201000001320 Atherosclerosis Diseases 0.000 description 1
- 208000032116 Autoimmune Experimental Encephalomyelitis Diseases 0.000 description 1
- 238000011725 BALB/c mouse Methods 0.000 description 1
- IYHHRZBKXXKDDY-UHFFFAOYSA-N BI-605906 Chemical compound N=1C=2SC(C(N)=O)=C(N)C=2C(C(F)(F)CC)=CC=1N1CCC(S(C)(=O)=O)CC1 IYHHRZBKXXKDDY-UHFFFAOYSA-N 0.000 description 1
- 208000035143 Bacterial infection Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 206010051728 Bone erosion Diseases 0.000 description 1
- JQUCWIWWWKZNCS-LESHARBVSA-N C(C1=CC=CC=C1)(=O)NC=1SC[C@H]2[C@@](N1)(CO[C@H](C2)C)C=2SC=C(N2)NC(=O)C2=NC=C(C=C2)OC(F)F Chemical compound C(C1=CC=CC=C1)(=O)NC=1SC[C@H]2[C@@](N1)(CO[C@H](C2)C)C=2SC=C(N2)NC(=O)C2=NC=C(C=C2)OC(F)F JQUCWIWWWKZNCS-LESHARBVSA-N 0.000 description 1
- 125000004648 C2-C8 alkenyl group Chemical group 0.000 description 1
- UHNRLQRZRNKOKU-UHFFFAOYSA-N CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O Chemical compound CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O UHNRLQRZRNKOKU-UHFFFAOYSA-N 0.000 description 1
- BQXUPNKLZNSUMC-YUQWMIPFSA-N CCN(CCCCCOCC(=O)N[C@H](C(=O)N1C[C@H](O)C[C@H]1C(=O)N[C@@H](C)c1ccc(cc1)-c1scnc1C)C(C)(C)C)CCOc1ccc(cc1)C(=O)c1c(sc2cc(O)ccc12)-c1ccc(O)cc1 Chemical compound CCN(CCCCCOCC(=O)N[C@H](C(=O)N1C[C@H](O)C[C@H]1C(=O)N[C@@H](C)c1ccc(cc1)-c1scnc1C)C(C)(C)C)CCOc1ccc(cc1)C(=O)c1c(sc2cc(O)ccc12)-c1ccc(O)cc1 BQXUPNKLZNSUMC-YUQWMIPFSA-N 0.000 description 1
- JGLMVXWAHNTPRF-CMDGGOBGSA-N CCN1N=C(C)C=C1C(=O)NC1=NC2=CC(=CC(OC)=C2N1C\C=C\CN1C(NC(=O)C2=CC(C)=NN2CC)=NC2=CC(=CC(OCCCN3CCOCC3)=C12)C(N)=O)C(N)=O Chemical compound CCN1N=C(C)C=C1C(=O)NC1=NC2=CC(=CC(OC)=C2N1C\C=C\CN1C(NC(=O)C2=CC(C)=NN2CC)=NC2=CC(=CC(OCCCN3CCOCC3)=C12)C(N)=O)C(N)=O JGLMVXWAHNTPRF-CMDGGOBGSA-N 0.000 description 1
- PKMUHQIDVVOXHQ-HXUWFJFHSA-N C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O Chemical compound C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O PKMUHQIDVVOXHQ-HXUWFJFHSA-N 0.000 description 1
- WWZKQHOCKIZLMA-UHFFFAOYSA-N Caprylic acid Natural products CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-OUBTZVSYSA-N Carbon-13 Chemical compound [13C] OKTJSMMVPCPJKN-OUBTZVSYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-NJFSPNSNSA-N Carbon-14 Chemical compound [14C] OKTJSMMVPCPJKN-NJFSPNSNSA-N 0.000 description 1
- 206010007558 Cardiac failure chronic Diseases 0.000 description 1
- 102000009410 Chemokine receptor Human genes 0.000 description 1
- 108050000299 Chemokine receptor Proteins 0.000 description 1
- 241000606161 Chlamydia Species 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 229940126657 Compound 17 Drugs 0.000 description 1
- 229940126639 Compound 33 Drugs 0.000 description 1
- 229940127007 Compound 39 Drugs 0.000 description 1
- 208000008448 Congenital adrenal hyperplasia Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 208000014311 Cushing syndrome Diseases 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- 108010074922 Cytochrome P-450 CYP1A2 Proteins 0.000 description 1
- RGHNJXZEOKUKBD-UHFFFAOYSA-N D-gluconic acid Natural products OCC(O)C(O)C(O)C(O)C(O)=O RGHNJXZEOKUKBD-UHFFFAOYSA-N 0.000 description 1
- 208000016192 Demyelinating disease Diseases 0.000 description 1
- 206010012305 Demyelination Diseases 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 206010012442 Dermatitis contact Diseases 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- BUDQDWGNQVEFAC-UHFFFAOYSA-N Dihydropyran Chemical compound C1COC=CC1 BUDQDWGNQVEFAC-UHFFFAOYSA-N 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- 101150104316 Dnase2b gene Proteins 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 208000004232 Enteritis Diseases 0.000 description 1
- 241000588921 Enterobacteriaceae Species 0.000 description 1
- 108010008165 Etanercept Proteins 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Substances 0.000 description 1
- 108091060211 Expressed sequence tag Proteins 0.000 description 1
- 108091006027 G proteins Proteins 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- 102000030782 GTP binding Human genes 0.000 description 1
- 108091000058 GTP-Binding Proteins 0.000 description 1
- 208000007882 Gastritis Diseases 0.000 description 1
- 108010018962 Glucosephosphate Dehydrogenase Proteins 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101001069589 Homo sapiens G-protein coupled receptor 84 Proteins 0.000 description 1
- LELOWRISYMNNSU-UHFFFAOYSA-N Hydrocyanic acid Natural products N#C LELOWRISYMNNSU-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 208000031226 Hyperlipidaemia Diseases 0.000 description 1
- 102000003816 Interleukin-13 Human genes 0.000 description 1
- 108090000176 Interleukin-13 Proteins 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 102000004388 Interleukin-4 Human genes 0.000 description 1
- 102000000743 Interleukin-5 Human genes 0.000 description 1
- 108010002616 Interleukin-5 Proteins 0.000 description 1
- 241000764238 Isis Species 0.000 description 1
- 108010044467 Isoenzymes Proteins 0.000 description 1
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 1
- 208000003456 Juvenile Arthritis Diseases 0.000 description 1
- 206010059176 Juvenile idiopathic arthritis Diseases 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 235000006679 Mentha X verticillata Nutrition 0.000 description 1
- 235000002899 Mentha suaveolens Nutrition 0.000 description 1
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 1
- TXXHDPDFNKHHGW-CCAGOZQPSA-N Muconic acid Natural products OC(=O)\C=C/C=C\C(O)=O TXXHDPDFNKHHGW-CCAGOZQPSA-N 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- LVDRREOUMKACNJ-BKMJKUGQSA-N N-[(2R,3S)-2-(4-chlorophenyl)-1-(1,4-dimethyl-2-oxoquinolin-7-yl)-6-oxopiperidin-3-yl]-2-methylpropane-1-sulfonamide Chemical compound CC(C)CS(=O)(=O)N[C@H]1CCC(=O)N([C@@H]1c1ccc(Cl)cc1)c1ccc2c(C)cc(=O)n(C)c2c1 LVDRREOUMKACNJ-BKMJKUGQSA-N 0.000 description 1
- AVYVHIKSFXVDBG-UHFFFAOYSA-N N-benzyl-N-hydroxy-2,2-dimethylbutanamide Chemical compound C(C1=CC=CC=C1)N(C(C(CC)(C)C)=O)O AVYVHIKSFXVDBG-UHFFFAOYSA-N 0.000 description 1
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 1
- QOVYHDHLFPKQQG-NDEPHWFRSA-N N[C@@H](CCC(=O)N1CCC(CC1)NC1=C2C=CC=CC2=NC(NCC2=CN(CCCNCCCNC3CCCCC3)N=N2)=N1)C(O)=O Chemical compound N[C@@H](CCC(=O)N1CCC(CC1)NC1=C2C=CC=CC2=NC(NCC2=CN(CCCNCCCNC3CCCCC3)N=N2)=N1)C(O)=O QOVYHDHLFPKQQG-NDEPHWFRSA-N 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- JCXJVPUVTGWSNB-UHFFFAOYSA-N Nitrogen dioxide Chemical compound O=[N]=O JCXJVPUVTGWSNB-UHFFFAOYSA-N 0.000 description 1
- 206010058667 Oral toxicity Diseases 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 229910019213 POCl3 Inorganic materials 0.000 description 1
- DPWPWRLQFGFJFI-UHFFFAOYSA-N Pargyline Chemical compound C#CCN(C)CC1=CC=CC=C1 DPWPWRLQFGFJFI-UHFFFAOYSA-N 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N Pd(PPh3)4 Substances [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- 241000009328 Perro Species 0.000 description 1
- 201000011252 Phenylketonuria Diseases 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 229920000604 Polyethylene Glycol 200 Polymers 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 206010038063 Rectal haemorrhage Diseases 0.000 description 1
- 208000002200 Respiratory Hypersensitivity Diseases 0.000 description 1
- 229910005965 SO 2 Inorganic materials 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 241000607768 Shigella Species 0.000 description 1
- PNUZDKCDAWUEGK-CYZMBNFOSA-N Sitafloxacin Chemical compound C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 PNUZDKCDAWUEGK-CYZMBNFOSA-N 0.000 description 1
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical class [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- 230000024932 T cell mediated immunity Effects 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 description 1
- 210000000447 Th1 cell Anatomy 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 241000607734 Yersinia <bacteria> Species 0.000 description 1
- LJOOWESTVASNOG-UFJKPHDISA-N [(1s,3r,4ar,7s,8s,8as)-3-hydroxy-8-[2-[(4r)-4-hydroxy-6-oxooxan-2-yl]ethyl]-7-methyl-1,2,3,4,4a,7,8,8a-octahydronaphthalen-1-yl] (2s)-2-methylbutanoate Chemical compound C([C@H]1[C@@H](C)C=C[C@H]2C[C@@H](O)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)CC1C[C@@H](O)CC(=O)O1 LJOOWESTVASNOG-UFJKPHDISA-N 0.000 description 1
- SPXSEZMVRJLHQG-XMMPIXPASA-N [(2R)-1-[[4-[(3-phenylmethoxyphenoxy)methyl]phenyl]methyl]pyrrolidin-2-yl]methanol Chemical compound C(C1=CC=CC=C1)OC=1C=C(OCC2=CC=C(CN3[C@H](CCC3)CO)C=C2)C=CC=1 SPXSEZMVRJLHQG-XMMPIXPASA-N 0.000 description 1
- MXZNUGFCDVAXLG-CHWSQXEVSA-N [(2S)-1-[(2R)-3-methyl-2-(pyridine-4-carbonylamino)butanoyl]pyrrolidin-2-yl]boronic acid Chemical compound CC(C)[C@@H](NC(=O)c1ccncc1)C(=O)N1CCC[C@@H]1B(O)O MXZNUGFCDVAXLG-CHWSQXEVSA-N 0.000 description 1
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 1
- PSLUFJFHTBIXMW-WYEYVKMPSA-N [(3r,4ar,5s,6s,6as,10s,10ar,10bs)-3-ethenyl-10,10b-dihydroxy-3,4a,7,7,10a-pentamethyl-1-oxo-6-(2-pyridin-2-ylethylcarbamoyloxy)-5,6,6a,8,9,10-hexahydro-2h-benzo[f]chromen-5-yl] acetate Chemical compound O([C@@H]1[C@@H]([C@]2(O[C@](C)(CC(=O)[C@]2(O)[C@@]2(C)[C@@H](O)CCC(C)(C)[C@@H]21)C=C)C)OC(=O)C)C(=O)NCCC1=CC=CC=N1 PSLUFJFHTBIXMW-WYEYVKMPSA-N 0.000 description 1
- RLRIZHLAYQLYCO-UHFFFAOYSA-N [2-(1,4-dioxan-2-ylmethoxy)-4-oxo-6,7-dihydropyrimido[6,1-a]isoquinolin-9-yl] trifluoromethanesulfonate Chemical compound C=1C(OS(=O)(=O)C(F)(F)F)=CC=C2C=1CCN(C(N=1)=O)C2=CC=1OCC1COCCO1 RLRIZHLAYQLYCO-UHFFFAOYSA-N 0.000 description 1
- UWKSYZHFTGONHY-UHFFFAOYSA-N [4-(methylcarbamoyl)phenyl]boronic acid Chemical compound CNC(=O)C1=CC=C(B(O)O)C=C1 UWKSYZHFTGONHY-UHFFFAOYSA-N 0.000 description 1
- MWDGTPAHKOWCSY-UHFFFAOYSA-N [6-(methylcarbamoyl)pyridin-3-yl]boronic acid Chemical compound CNC(=O)C1=CC=C(B(O)O)C=N1 MWDGTPAHKOWCSY-UHFFFAOYSA-N 0.000 description 1
- BNTIPMNMTIAWIW-UHFFFAOYSA-N [6-(trifluoromethyl)pyridin-3-yl]boronic acid Chemical compound OB(O)C1=CC=C(C(F)(F)F)N=C1 BNTIPMNMTIAWIW-UHFFFAOYSA-N 0.000 description 1
- UKRKJOQTJHREDX-UHFFFAOYSA-M [Br-].[Mg+]CCC1CC1 Chemical compound [Br-].[Mg+]CCC1CC1 UKRKJOQTJHREDX-UHFFFAOYSA-M 0.000 description 1
- COERJHDMQUPDCV-UHFFFAOYSA-N [K].FB(F)F Chemical compound [K].FB(F)F COERJHDMQUPDCV-UHFFFAOYSA-N 0.000 description 1
- SMNRFWMNPDABKZ-WVALLCKVSA-N [[(2R,3S,4R,5S)-5-(2,6-dioxo-3H-pyridin-3-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [[[(2R,3S,4S,5R,6R)-4-fluoro-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl] hydrogen phosphate Chemical compound OC[C@H]1O[C@H](OP(O)(=O)OP(O)(=O)OP(O)(=O)OP(O)(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)C2C=CC(=O)NC2=O)[C@H](O)[C@@H](F)[C@@H]1O SMNRFWMNPDABKZ-WVALLCKVSA-N 0.000 description 1
- WREOTYWODABZMH-DTZQCDIJSA-N [[(2r,3s,4r,5r)-3,4-dihydroxy-5-[2-oxo-4-(2-phenylethoxyamino)pyrimidin-1-yl]oxolan-2-yl]methoxy-hydroxyphosphoryl] phosphono hydrogen phosphate Chemical compound O[C@@H]1[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OP(O)(O)=O)O[C@H]1N(C=C\1)C(=O)NC/1=N\OCCC1=CC=CC=C1 WREOTYWODABZMH-DTZQCDIJSA-N 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000011149 active material Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 208000025368 adrenal gland disease Diseases 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 230000010085 airway hyperresponsiveness Effects 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 229910001420 alkaline earth metal ion Inorganic materials 0.000 description 1
- BHELZAPQIKSEDF-UHFFFAOYSA-N allyl bromide Chemical compound BrCC=C BHELZAPQIKSEDF-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 239000003430 antimalarial agent Substances 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000008135 aqueous vehicle Substances 0.000 description 1
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 description 1
- 125000003710 aryl alkyl group Chemical group 0.000 description 1
- 239000012131 assay buffer Substances 0.000 description 1
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 230000007844 axonal damage Effects 0.000 description 1
- 230000003376 axonal effect Effects 0.000 description 1
- AAMATCKFMHVIDO-UHFFFAOYSA-N azane;1h-pyrrole Chemical compound N.C=1C=CNC=1 AAMATCKFMHVIDO-UHFFFAOYSA-N 0.000 description 1
- HONIICLYMWZJFZ-UHFFFAOYSA-N azetidine Chemical compound C1CNC1 HONIICLYMWZJFZ-UHFFFAOYSA-N 0.000 description 1
- 244000052616 bacterial pathogen Species 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- RFRXIWQYSOIBDI-UHFFFAOYSA-N benzarone Chemical compound CCC=1OC2=CC=CC=C2C=1C(=O)C1=CC=C(O)C=C1 RFRXIWQYSOIBDI-UHFFFAOYSA-N 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- GONOPSZTUGRENK-UHFFFAOYSA-N benzyl(trichloro)silane Chemical compound Cl[Si](Cl)(Cl)CC1=CC=CC=C1 GONOPSZTUGRENK-UHFFFAOYSA-N 0.000 description 1
- 230000002457 bidirectional effect Effects 0.000 description 1
- 238000010256 biochemical assay Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 1
- 208000029028 brain injury Diseases 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- AEILLAXRDHDKDY-UHFFFAOYSA-N bromomethylcyclopropane Chemical compound BrCC1CC1 AEILLAXRDHDKDY-UHFFFAOYSA-N 0.000 description 1
- 206010006451 bronchitis Diseases 0.000 description 1
- 239000007975 buffered saline Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- OGEBRHQLRGFBNV-RZDIXWSQSA-N chembl2036808 Chemical compound C12=NC(NCCCC)=NC=C2C(C=2C=CC(F)=CC=2)=NN1C[C@H]1CC[C@H](N)CC1 OGEBRHQLRGFBNV-RZDIXWSQSA-N 0.000 description 1
- 208000029771 childhood onset asthma Diseases 0.000 description 1
- 229960003677 chloroquine Drugs 0.000 description 1
- WHTVZRBIWZFKQO-UHFFFAOYSA-N chloroquine Natural products ClC1=CC=C2C(NC(C)CCCN(CC)CC)=CC=NC2=C1 WHTVZRBIWZFKQO-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- QZHPTGXQGDFGEN-UHFFFAOYSA-N chromene Chemical compound C1=CC=C2C=C[CH]OC2=C1 QZHPTGXQGDFGEN-UHFFFAOYSA-N 0.000 description 1
- 208000025302 chronic primary adrenal insufficiency Diseases 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940126543 compound 14 Drugs 0.000 description 1
- 229940125758 compound 15 Drugs 0.000 description 1
- 229940126208 compound 22 Drugs 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 229940125961 compound 24 Drugs 0.000 description 1
- 229940125846 compound 25 Drugs 0.000 description 1
- 229940125851 compound 27 Drugs 0.000 description 1
- 229940127204 compound 29 Drugs 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 229940125877 compound 31 Drugs 0.000 description 1
- 229940125878 compound 36 Drugs 0.000 description 1
- 229940125807 compound 37 Drugs 0.000 description 1
- 229940127573 compound 38 Drugs 0.000 description 1
- 229940126540 compound 41 Drugs 0.000 description 1
- 229940125936 compound 42 Drugs 0.000 description 1
- 229940125844 compound 46 Drugs 0.000 description 1
- 229940127271 compound 49 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 229940126545 compound 53 Drugs 0.000 description 1
- 229940127113 compound 57 Drugs 0.000 description 1
- 229940125900 compound 59 Drugs 0.000 description 1
- 229940126179 compound 72 Drugs 0.000 description 1
- 208000010247 contact dermatitis Diseases 0.000 description 1
- 229910001850 copernicium Inorganic materials 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- XZWQKJXJNKYMAP-UHFFFAOYSA-N cyclohexen-1-ylboronic acid Chemical compound OB(O)C1=CCCCC1 XZWQKJXJNKYMAP-UHFFFAOYSA-N 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- ISQVBYGGNVVVHB-UHFFFAOYSA-N cyclopentylmethanol Chemical compound OCC1CCCC1 ISQVBYGGNVVVHB-UHFFFAOYSA-N 0.000 description 1
- GUDMZGLFZNLYEY-UHFFFAOYSA-N cyclopropylmethanol Chemical compound OCC1CC1 GUDMZGLFZNLYEY-UHFFFAOYSA-N 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 238000007418 data mining Methods 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 238000010511 deprotection reaction Methods 0.000 description 1
- 231100000223 dermal penetration Toxicity 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 125000005043 dihydropyranyl group Chemical group O1C(CCC=C1)* 0.000 description 1
- IJKVHSBPTUYDLN-UHFFFAOYSA-N dihydroxy(oxo)silane Chemical compound O[Si](O)=O IJKVHSBPTUYDLN-UHFFFAOYSA-N 0.000 description 1
- MQIZSSSBYFJIJF-UHFFFAOYSA-N dimethyl hexadecanedioate Chemical compound COC(=O)CCCCCCCCCCCCCCC(=O)OC MQIZSSSBYFJIJF-UHFFFAOYSA-N 0.000 description 1
- SXZIXHOMFPUIRK-UHFFFAOYSA-N diphenylmethanimine Chemical compound C=1C=CC=CC=1C(=N)C1=CC=CC=C1 SXZIXHOMFPUIRK-UHFFFAOYSA-N 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 230000009266 disease activity Effects 0.000 description 1
- 208000016097 disease of metabolism Diseases 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 210000004921 distal colon Anatomy 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 229940073621 enbrel Drugs 0.000 description 1
- 150000002085 enols Chemical class 0.000 description 1
- BJXYHBKEQFQVES-NWDGAFQWSA-N enpatoran Chemical compound N[C@H]1CN(C[C@H](C1)C(F)(F)F)C1=C2C=CC=NC2=C(C=C1)C#N BJXYHBKEQFQVES-NWDGAFQWSA-N 0.000 description 1
- 208000010227 enterocolitis Diseases 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-N ethanesulfonic acid Chemical compound CCS(O)(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-N 0.000 description 1
- GWNFQAKCJYEJEW-UHFFFAOYSA-N ethyl 3-[8-[[4-methyl-5-[(3-methyl-4-oxophthalazin-1-yl)methyl]-1,2,4-triazol-3-yl]sulfanyl]octanoylamino]benzoate Chemical compound CCOC(=O)C1=CC(NC(=O)CCCCCCCSC2=NN=C(CC3=NN(C)C(=O)C4=CC=CC=C34)N2C)=CC=C1 GWNFQAKCJYEJEW-UHFFFAOYSA-N 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- UKFXDFUAPNAMPJ-UHFFFAOYSA-N ethylmalonic acid Chemical compound CCC(C(O)=O)C(O)=O UKFXDFUAPNAMPJ-UHFFFAOYSA-N 0.000 description 1
- SSDZYLQUYMOSAK-UHFFFAOYSA-N ethynylcyclohexane Chemical compound C#CC1CCCCC1 SSDZYLQUYMOSAK-UHFFFAOYSA-N 0.000 description 1
- TXVJSWLZYQMWPC-UHFFFAOYSA-N ethynylcyclopentane Chemical compound C#CC1CCCC1 TXVJSWLZYQMWPC-UHFFFAOYSA-N 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 230000000763 evoking effect Effects 0.000 description 1
- 208000012997 experimental autoimmune encephalomyelitis Diseases 0.000 description 1
- 208000024711 extrinsic asthma Diseases 0.000 description 1
- 238000013230 female C57BL/6J mice Methods 0.000 description 1
- 238000013100 final test Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- JKFAIQOWCVVSKC-UHFFFAOYSA-N furazan Chemical compound C=1C=NON=1 JKFAIQOWCVVSKC-UHFFFAOYSA-N 0.000 description 1
- DDRPCXLAQZKBJP-UHFFFAOYSA-N furfurylamine Chemical compound NCC1=CC=CO1 DDRPCXLAQZKBJP-UHFFFAOYSA-N 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 229940050410 gluconate Drugs 0.000 description 1
- 239000000174 gluconic acid Substances 0.000 description 1
- 235000012208 gluconic acid Nutrition 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 208000035474 group of disease Diseases 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000004404 heteroalkyl group Chemical group 0.000 description 1
- LTFTWJYRQNTCHI-UHFFFAOYSA-N hex-1-yn-3-ol Chemical compound CCCC(O)C#C LTFTWJYRQNTCHI-UHFFFAOYSA-N 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 239000008309 hydrophilic cream Substances 0.000 description 1
- RCCPEORTSYDPMB-UHFFFAOYSA-N hydroxy benzenecarboximidothioate Chemical compound OSC(=N)C1=CC=CC=C1 RCCPEORTSYDPMB-UHFFFAOYSA-N 0.000 description 1
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 1
- 208000003532 hypothyroidism Diseases 0.000 description 1
- 230000002989 hypothyroidism Effects 0.000 description 1
- 238000005417 image-selected in vivo spectroscopy Methods 0.000 description 1
- CQQJSOXDEFZGFG-UHFFFAOYSA-N imidazo[4,5-d]imidazole Chemical compound C1=NC2=NC=NC2=N1 CQQJSOXDEFZGFG-UHFFFAOYSA-N 0.000 description 1
- YAMHXTCMCPHKLN-UHFFFAOYSA-N imidazolidin-2-one Chemical compound O=C1NCCN1 YAMHXTCMCPHKLN-UHFFFAOYSA-N 0.000 description 1
- MTNDZQHUAFNZQY-UHFFFAOYSA-N imidazoline Chemical compound C1CN=CN1 MTNDZQHUAFNZQY-UHFFFAOYSA-N 0.000 description 1
- 239000012642 immune effector Substances 0.000 description 1
- 230000008105 immune reaction Effects 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- HOBCFUWDNJPFHB-UHFFFAOYSA-N indolizine Chemical compound C1=CC=CN2C=CC=C21 HOBCFUWDNJPFHB-UHFFFAOYSA-N 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 238000012739 integrated shape imaging system Methods 0.000 description 1
- 229940117681 interleukin-12 Drugs 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 201000010659 intrinsic asthma Diseases 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 235000013847 iso-butane Nutrition 0.000 description 1
- HEBMCVBCEDMUOF-UHFFFAOYSA-N isochromane Chemical compound C1=CC=C2COCCC2=C1 HEBMCVBCEDMUOF-UHFFFAOYSA-N 0.000 description 1
- GWVMLCQWXVFZCN-UHFFFAOYSA-N isoindoline Chemical compound C1=CC=C2CNCC2=C1 GWVMLCQWXVFZCN-UHFFFAOYSA-N 0.000 description 1
- VDBNYAPERZTOOF-UHFFFAOYSA-N isoquinolin-1(2H)-one Chemical compound C1=CC=C2C(=O)NC=CC2=C1 VDBNYAPERZTOOF-UHFFFAOYSA-N 0.000 description 1
- ZLTPDFXIESTBQG-UHFFFAOYSA-N isothiazole Chemical compound C=1C=NSC=1 ZLTPDFXIESTBQG-UHFFFAOYSA-N 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 210000004731 jugular vein Anatomy 0.000 description 1
- 201000002215 juvenile rheumatoid arthritis Diseases 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- XMGQYMWWDOXHJM-UHFFFAOYSA-N limonene Chemical compound CC(=C)C1CCC(C)=CC1 XMGQYMWWDOXHJM-UHFFFAOYSA-N 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000003055 low molecular weight heparin Substances 0.000 description 1
- 229940127215 low-molecular weight heparin Drugs 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- YADSQVVJGJHEMZ-UHFFFAOYSA-M magnesium;1-methoxypropane;bromide Chemical compound [Mg+2].[Br-].COCC[CH2-] YADSQVVJGJHEMZ-UHFFFAOYSA-M 0.000 description 1
- 238000003760 magnetic stirring Methods 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- 229960001047 methyl salicylate Drugs 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- DDLIGBOFAVUZHB-UHFFFAOYSA-N midazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NC=C2CN=C1C1=CC=CC=C1F DDLIGBOFAVUZHB-UHFFFAOYSA-N 0.000 description 1
- 229960003793 midazolam Drugs 0.000 description 1
- 239000003226 mitogen Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- AFKRXFQDBKTGKZ-UHFFFAOYSA-N n-(pyridin-3-ylmethyl)prop-2-yn-1-amine Chemical compound C#CCNCC1=CC=CN=C1 AFKRXFQDBKTGKZ-UHFFFAOYSA-N 0.000 description 1
- YGBMCLDVRUGXOV-UHFFFAOYSA-N n-[6-[6-chloro-5-[(4-fluorophenyl)sulfonylamino]pyridin-3-yl]-1,3-benzothiazol-2-yl]acetamide Chemical compound C1=C2SC(NC(=O)C)=NC2=CC=C1C(C=1)=CN=C(Cl)C=1NS(=O)(=O)C1=CC=C(F)C=C1 YGBMCLDVRUGXOV-UHFFFAOYSA-N 0.000 description 1
- LDYBFSGEBHSTOQ-UHFFFAOYSA-N n-benzylprop-2-yn-1-amine Chemical compound C#CCNCC1=CC=CC=C1 LDYBFSGEBHSTOQ-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- GOQYKNQRPGWPLP-UHFFFAOYSA-N n-heptadecyl alcohol Natural products CCCCCCCCCCCCCCCCCO GOQYKNQRPGWPLP-UHFFFAOYSA-N 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N n-hexanoic acid Natural products CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- KVBGVZZKJNLNJU-UHFFFAOYSA-N naphthalene-2-sulfonic acid Chemical compound C1=CC=CC2=CC(S(=O)(=O)O)=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- IOMMMLWIABWRKL-WUTDNEBXSA-N nazartinib Chemical compound C1N(C(=O)/C=C/CN(C)C)CCCC[C@H]1N1C2=C(Cl)C=CC=C2N=C1NC(=O)C1=CC=NC(C)=C1 IOMMMLWIABWRKL-WUTDNEBXSA-N 0.000 description 1
- KPSSIOMAKSHJJG-UHFFFAOYSA-N neopentyl alcohol Chemical compound CC(C)(C)CO KPSSIOMAKSHJJG-UHFFFAOYSA-N 0.000 description 1
- 230000003959 neuroinflammation Effects 0.000 description 1
- 230000007971 neurological deficit Effects 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- VLZLOWPYUQHHCG-UHFFFAOYSA-N nitromethylbenzene Chemical compound [O-][N+](=O)CC1=CC=CC=C1 VLZLOWPYUQHHCG-UHFFFAOYSA-N 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 239000002687 nonaqueous vehicle Substances 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000003883 ointment base Substances 0.000 description 1
- PIDFDZJZLOTZTM-KHVQSSSXSA-N ombitasvir Chemical compound COC(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@H]1C(=O)NC1=CC=C([C@H]2N([C@@H](CC2)C=2C=CC(NC(=O)[C@H]3N(CCC3)C(=O)[C@@H](NC(=O)OC)C(C)C)=CC=2)C=2C=CC(=CC=2)C(C)(C)C)C=C1 PIDFDZJZLOTZTM-KHVQSSSXSA-N 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 231100000418 oral toxicity Toxicity 0.000 description 1
- 239000007968 orange flavor Substances 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 108091008880 orphan GPCRs Proteins 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 208000015124 ovarian disease Diseases 0.000 description 1
- 201000004535 ovarian dysfunction Diseases 0.000 description 1
- 231100000543 ovarian dysfunction Toxicity 0.000 description 1
- 238000012261 overproduction Methods 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical compound C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- LMYJGUNNJIDROI-UHFFFAOYSA-N oxan-4-ol Chemical compound OC1CCOCC1 LMYJGUNNJIDROI-UHFFFAOYSA-N 0.000 description 1
- HJZXNSXKMBRTJZ-UHFFFAOYSA-N oxan-4-ylmethyl methanesulfonate Chemical compound CS(=O)(=O)OCC1CCOCC1 HJZXNSXKMBRTJZ-UHFFFAOYSA-N 0.000 description 1
- CXLGNJCMPWUZKM-UHFFFAOYSA-N oxane-4-carbaldehyde Chemical compound O=CC1CCOCC1 CXLGNJCMPWUZKM-UHFFFAOYSA-N 0.000 description 1
- CQDAMYNQINDRQC-UHFFFAOYSA-N oxatriazole Chemical compound C1=NN=NO1 CQDAMYNQINDRQC-UHFFFAOYSA-N 0.000 description 1
- AICOOMRHRUFYCM-ZRRPKQBOSA-N oxazine, 1 Chemical compound C([C@@H]1[C@H](C(C[C@]2(C)[C@@H]([C@H](C)N(C)C)[C@H](O)C[C@]21C)=O)CC1=CC2)C[C@H]1[C@@]1(C)[C@H]2N=C(C(C)C)OC1 AICOOMRHRUFYCM-ZRRPKQBOSA-N 0.000 description 1
- QMLWSAXEQSBAAQ-UHFFFAOYSA-N oxetan-3-ol Chemical compound OC1COC1 QMLWSAXEQSBAAQ-UHFFFAOYSA-N 0.000 description 1
- NJDNNGVASRCMGO-UHFFFAOYSA-N oxetan-3-ylmethyl methanesulfonate Chemical compound CS(=O)(=O)OCC1COC1 NJDNNGVASRCMGO-UHFFFAOYSA-N 0.000 description 1
- 125000003566 oxetanyl group Chemical group 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 208000022560 parathyroid gland disease Diseases 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 230000007903 penetration ability Effects 0.000 description 1
- JTHLRRZARWSHBE-UHFFFAOYSA-N pent-4-yn-2-ol Chemical compound CC(O)CC#C JTHLRRZARWSHBE-UHFFFAOYSA-N 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 239000008024 pharmaceutical diluent Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- RLOWWWKZYUNIDI-UHFFFAOYSA-N phosphinic chloride Chemical compound ClP=O RLOWWWKZYUNIDI-UHFFFAOYSA-N 0.000 description 1
- LFSXCDWNBUNEEM-UHFFFAOYSA-N phthalazine Chemical compound C1=NN=CC2=CC=CC=C21 LFSXCDWNBUNEEM-UHFFFAOYSA-N 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- IWELDVXSEVIIGI-UHFFFAOYSA-N piperazin-2-one Chemical compound O=C1CNCCN1 IWELDVXSEVIIGI-UHFFFAOYSA-N 0.000 description 1
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- XUWHAWMETYGRKB-UHFFFAOYSA-N piperidin-2-one Chemical compound O=C1CCCCN1 XUWHAWMETYGRKB-UHFFFAOYSA-N 0.000 description 1
- 125000004483 piperidin-3-yl group Chemical group N1CC(CCC1)* 0.000 description 1
- 125000004482 piperidin-4-yl group Chemical group N1CCC(CC1)* 0.000 description 1
- LYKMMUBOEFYJQG-UHFFFAOYSA-N piperoxan Chemical compound C1OC2=CC=CC=C2OC1CN1CCCCC1 LYKMMUBOEFYJQG-UHFFFAOYSA-N 0.000 description 1
- IUGYQRQAERSCNH-UHFFFAOYSA-N pivalic acid Chemical compound CC(C)(C)C(O)=O IUGYQRQAERSCNH-UHFFFAOYSA-N 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 201000010065 polycystic ovary syndrome Diseases 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 235000015320 potassium carbonate Nutrition 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 239000008057 potassium phosphate buffer Substances 0.000 description 1
- WSHYKIAQCMIPTB-UHFFFAOYSA-M potassium;2-oxo-3-(3-oxo-1-phenylbutyl)chromen-4-olate Chemical compound [K+].[O-]C=1C2=CC=CC=C2OC(=O)C=1C(CC(=O)C)C1=CC=CC=C1 WSHYKIAQCMIPTB-UHFFFAOYSA-M 0.000 description 1
- 230000036515 potency Effects 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000036316 preload Effects 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 201000009395 primary hyperaldosteronism Diseases 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 238000003672 processing method Methods 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- CPNGPNLZQNNVQM-UHFFFAOYSA-N pteridine Chemical compound N1=CN=CC2=NC=CN=C21 CPNGPNLZQNNVQM-UHFFFAOYSA-N 0.000 description 1
- 208000005069 pulmonary fibrosis Diseases 0.000 description 1
- USPWKWBDZOARPV-UHFFFAOYSA-N pyrazolidine Chemical compound C1CNNC1 USPWKWBDZOARPV-UHFFFAOYSA-N 0.000 description 1
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 description 1
- GSOOLIFIQJUSFP-UHFFFAOYSA-N pyridin-2-ylmethanol;hydrochloride Chemical compound [Cl-].OCC1=CC=CC=[NH+]1 GSOOLIFIQJUSFP-UHFFFAOYSA-N 0.000 description 1
- ABMYEXAYWZJVOV-UHFFFAOYSA-N pyridin-3-ylboronic acid Chemical compound OB(O)C1=CC=CN=C1 ABMYEXAYWZJVOV-UHFFFAOYSA-N 0.000 description 1
- QLULGIRFKAWHOJ-UHFFFAOYSA-N pyridin-4-ylboronic acid Chemical compound OB(O)C1=CC=NC=C1 QLULGIRFKAWHOJ-UHFFFAOYSA-N 0.000 description 1
- HZFPPBMKGYINDF-UHFFFAOYSA-N pyrimidin-5-ylboronic acid Chemical compound OB(O)C1=CN=CN=C1 HZFPPBMKGYINDF-UHFFFAOYSA-N 0.000 description 1
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 239000001397 quillaja saponaria molina bark Substances 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 239000013074 reference sample Substances 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 239000013557 residual solvent Substances 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 230000006965 reversible inhibition Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 206010039083 rhinitis Diseases 0.000 description 1
- MYFATKRONKHHQL-UHFFFAOYSA-N rhodamine 123 Chemical compound [Cl-].COC(=O)C1=CC=CC=C1C1=C2C=CC(=[NH2+])C=C2OC2=CC(N)=CC=C21 MYFATKRONKHHQL-UHFFFAOYSA-N 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 208000007442 rickets Diseases 0.000 description 1
- MNDBXUUTURYVHR-UHFFFAOYSA-N roflumilast Chemical compound FC(F)OC1=CC=C(C(=O)NC=2C(=CN=CC=2Cl)Cl)C=C1OCC1CC1 MNDBXUUTURYVHR-UHFFFAOYSA-N 0.000 description 1
- 229960002586 roflumilast Drugs 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229930182490 saponin Natural products 0.000 description 1
- 150000007949 saponins Chemical class 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 208000013223 septicemia Diseases 0.000 description 1
- 238000012163 sequencing technique Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 229960001940 sulfasalazine Drugs 0.000 description 1
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 238000004885 tandem mass spectrometry Methods 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 238000003419 tautomerization reaction Methods 0.000 description 1
- 125000005207 tetraalkylammonium group Chemical group 0.000 description 1
- 125000001712 tetrahydronaphthyl group Chemical group C1(CCCC2=CC=CC=C12)* 0.000 description 1
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical compound C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 150000003536 tetrazoles Chemical group 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- CBDKQYKMCICBOF-UHFFFAOYSA-N thiazoline Chemical compound C1CN=CS1 CBDKQYKMCICBOF-UHFFFAOYSA-N 0.000 description 1
- 238000004809 thin layer chromatography Methods 0.000 description 1
- 150000003573 thiols Chemical class 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 229940100611 topical cream Drugs 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 229940100615 topical ointment Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000041 toxicology testing Toxicity 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- YWBFPKPWMSWWEA-UHFFFAOYSA-O triazolopyrimidine Chemical compound BrC1=CC=CC(C=2N=C3N=CN[N+]3=C(NCC=3C=CN=CC=3)C=2)=C1 YWBFPKPWMSWWEA-UHFFFAOYSA-O 0.000 description 1
- CWMFRHBXRUITQE-UHFFFAOYSA-N trimethylsilylacetylene Chemical compound C[Si](C)(C)C#C CWMFRHBXRUITQE-UHFFFAOYSA-N 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 238000001665 trituration Methods 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- PJVWKTKQMONHTI-UHFFFAOYSA-N warfarin Chemical compound OC=1C2=CC=CC=C2OC(=O)C=1C(CC(=O)C)C1=CC=CC=C1 PJVWKTKQMONHTI-UHFFFAOYSA-N 0.000 description 1
- 229960005080 warfarin Drugs 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 239000003871 white petrolatum Substances 0.000 description 1
- 238000013389 whole blood assay Methods 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 229920001285 xanthan gum Polymers 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 244000000190 yeast pathogen Species 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Diabetes (AREA)
- Pulmonology (AREA)
- Hematology (AREA)
- Rheumatology (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Vascular Medicine (AREA)
- Urology & Nephrology (AREA)
- Dermatology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Obesity (AREA)
- Endocrinology (AREA)
- Transplantation (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Un compuesto de acuerdo con la fórmula Ia: **(Ver fórmula)** en donde R1 es H, Me o halo; L1 está ausente o es -O-, -S- o -NR4a-; G es R2, -W-L2-R2, o -W-L3-R3; W es alquileno C1-4, alquenileno C2-4 que tiene un enlace doble o alquinileno C2-4 que tiene un enlace triple; L2 está ausente o es -O-; R2 es - H, - alquilo C1-8, opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de - OH, -halo, - CN, - alcoxi C1-6, - cicloalquilo C3-7, - heterocicloalquilo de 4-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O, - heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, y - fenilo, - cicloalquenilo C4-7 que comprende un enlace doble, - heterocicloalquenilo de 5-7 miembros que comprende un enlace doble y uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S, - cicloalquilo C3-7 opcionalmente sustituido con uno o varios grupos R5 seleccionados, de modo independiente, - heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O, opcionalmente sustituido con uno a tres grupos R5 seleccionados de modo independiente, - heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno a tres grupos R6 seleccionados de modo independiente, o - arilo C6-10 opcionalmente sustituido con uno o varios grupos R6 seleccionados de modo independiente; L3 es -NR4b-; R3 es - alquilo C1-4 sustituido con - arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o - heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios R, grupos R7 seleccionados de modo independiente, - heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o - arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente; Cada R4a y R4b se selecciona, de modo independiente, de H, alquilo C1-4 y cicloalquilo C3-7; R5 es oxo o R6; R6 es - OH, - halo, - -NO2, - alquilo C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH, - alcoxi C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH, - cicloalquilo C3-7, - -C(=O)OR8, - -C(=O)NR9R10, - -NHC(=O)-alquilo C1-4, - -CN, - fenilo, - -O-fenilo, - heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S, o - heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S, opcionalmente sustituido con uno o varios alquilo C1-4, alcoxi C1-4, CN, halo y - C(=O)OR11 seleccionados de modo independiente; R7 es alquilo C1-4 o halo; y cada uno de R8, R9, R10 y R11 se selecciona, de modo independiente, de H y alquilo C1-4, o una de sus sales o solvatos farmacéuticamente aceptables o un solvato de la sal farmacéuticamente aceptable, para su uso en el tratamiento de la esclerosis múltiple.
Description
DESCRIPCIÓN
Dihidropirimidinoisoquinolinonas y sus composiciones farmacéuticas para el tratamiento de la esclerosis múltiple
Campo de la invención
La presente invención se refiere nuevos compuestos y composiciones farmacéuticas de los mismos que antagonizan GPR84, para el tratamiento de la esclerosis múltiple.
Antecedentes de la invención
GPR84 se aisló recientemente y se caracterizó a partir de células B humanas (Wittenberger et al., 2001, J Mol Biol, 307, 799-813) como resultado de una estrategia de minería de datos de marca de secuencia expresada, y también usando un método de reacción en cadena polimerasa-transcriptasa inversa de cebador degenerado (RT-PCR) con el objetivo de identificar nuevos receptores de quimioquinas expresados en neutrófilos (Yousefi S et al. 2001 J Leukoc Biol; 69, 1045-52).
GPR84 (también conocido como EX33) permaneció un GPCR huérfano hasta la identificación de FFA de cadena media con longitudes de cadena de carbono de 9-14 como ligandos para este receptor (Wang et al. (2006) J. Biol. Chem. 281:3457-64). Se describió que GPR84 es activado por ácido cáprico (C10: 0), ácido undecanoico (C11: 0) y ácido láurico (C12: 0) con potencias de 5 pM, 9 pM y 11 pM, respectivamente. También se describió que dos moléculas pequeñas tenían cierta actividad agonista de GPR84: 3,3'-di-indolilmetano (DIM) (Wang et al. (2006) J. Biol. Chem.
281:3457-64) y embelina (WO 2007/027661).
Se ha demostrado que la expresión de GPR84 se expresa en células inmunitarias al menos, aunque sin limitación, en leucocitos polimorfonucleares (PMN), neutrófilos, monocitos, células T, células B. Wang et al., 2006, The Journal of Biological Chemistry, 281, 45, 3457-3464, Yousefi et al., 2001, Journal of Leukocyte Biology, 69, 1045 1052, Venkataraman and Kuo, 2005, Immunology Letters, 101, 144-153, WO2007/027661 A2). Se midieron niveles más altos de GPR84 en neutrófilos y eosinófilos que en las células T y células B. Se demostró que la expresión de GPR84 en tejidos puede cumplir un papel en la propagación de la respuesta inflamatoria tal como pulmón, bazo, médula ósea.
Por ejemplo, en una revisión reciente, Du Bois informó sobre el estado actual de los terapias para las enfermedades intersticiales pulmonares, tales como la fibrosis pulmonar idiopática (IPF). Hay casi 300 causas de daño o inflamación distintas de la enfermedad pulmonar intersticial que pueden producir cicatrices pulmonares difusas, y muy probablemente las etapas iniciales de la patología del IPF que involucran inflamación (Du Bois, 2010, Nat Rev, Drug Discovery, 9, 129), y se pueden usar ventajosamente terapias de combinación que implican el tratamiento antiinflamatorio.
La expresión de GPR84 estaba altamente regulada por aumento en monocitos/macrófagos después de la estimulación con LPS (Wang et al., 2006, The Journal of Biological Chemistry, 281,45, 3457-3464).
Los ratones knock-out GPR84 (KO) son viables e indistinguibles de los controles de camada de tipo salvaje (Venkataraman and Kuo, 2005, Immunology Letters, 101, 144-153). Se informa que la proliferación de células T y B en respuesta a varios mitógenos que es normal en ratones deficientes en GPR84 (Venkataraman and Kuo, 2005, Immunology Letters, 101, 144-153). Las células T diferenciadas T auxiliares 2 (Th2) de GPR84 KO secretaron niveles más altos de IL4, IL5, IL13, las 3 citoquinas Th2 principales, en comparación con los controles de camada de tipo salvaje. Por el contrario, la producción de la citoquina Th1, INFy, fue similar en células T diferenciadas Th1 de GPR84 KO y camada de tipo salvaje (Venkataraman and Kuo, 2005, Immunology Letters, 101, 144-153).
Además, el ácido cáprico, ácido undecanoico y ácido láurico aumentaron de forma dependiente de la dosis la secreción de la subunidad p40 de la interleuquina-12 (IL-12 p40) a partir de células tipo macrófago murino RAW264.7 estimuladas con LPS. La citoquina pro-inflamatoria IL-12 cumple un papel fundamental en la promoción de la inmunidad mediada por células para erradicar los patógenos mediante la inducción y el mantenimiento de respuestas T auxiliar 1 (Th1) y la inhibición de las respuestas T auxiliar 2 (Th2). Los FFA de cadena media, a través de sus acciones directas en GPR84, pueden afectar el equilibrio Th1/Th2.
Berry et al. identificaron un motivo distintivo transcripcional del gen 393 de sangre entera para la tuberculosis activa (TB) (Berry et al., 2010, Nature, 466, 973-979). GPR84 fue parte de este motivo distintivo transcripcional del gen 393 para la TB activa, lo que indica un papel potencial de GPR84 en las enfermedades infecciosas.
La expresión de GPR84 también se describió en microglia, las células efectoras inmunitarias primarias del sistema nervioso central (SNC) de origen mieloide-monocítico (Bouchard et al., 2007, Glia, 55: 790-800). Como se observó en células inmunitarias periféricas, la expresión de GPR84 en la microglia fue altamente inducible en afecciones inflamatorias tales como tratamiento con TNFa e IL1, pero también notablemente endotoxemia y encefalomielitis autoinmune experimental (EAE), lo que sugiere un papel en procesos neuroinflamatorios. Estos resultados sugieren que GPR84 puede ser regulador por aumento en el SNC no solo durante la endotoxemia y la esclerosis múltiple, sino
también en todas las condiciones neurológicas en las que se producen citoquinas proinflamatorias de TNFa o IL1b, incluyendo lesión cerebral, infección, enfermedad de Alzheimer, enfermedad de Parkinson (PD).
La expresión de GPR84 también se observó en adipocitos y se demostró que está potenciada por estímulos inflamatorios (Nagasaki et al., 2012). Los resultados sugieren que GPR84 emerge en los adipocitos en respuesta al TNFa a partir de macrófagos infiltrantes y exacerba el ciclo vicioso entre adiposidad y diabesidad, y por lo tanto la inhibición de la actividad GPR84 puede ser beneficiosa para el tratamiento de enfermedades endocrinas y/o metabólicas.
Compendio de la invención
Por consiguiente, en un primer aspecto de la invención, se describe un compuesto de la invención que tiene una fórmula Ia:
R1 es H, Me o halo;
L1 está ausente o es -O-, -S- o -NR4a-;
G es
R2,
-W-L2-R2 , o
-W-L3-R3 ;
W es alquileno C1-4, alquenileno C2-4 que tiene un enlace doble o alquinileno C2-4 que tiene un enlace triple; L2 está ausente o es -O-;
R2 es
• H,
• alquilo C1 -8, opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de o OH,
° halo,
o CN,
o alcoxi C1-6,
o cicloalquilo C3-7,
o heterocicloalquilo de 4-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O,
o heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, y
° fenilo,
• cicloalquenilo C4-7 que comprende un enlace doble,
• heterocicloalquenilo de 5-7 miembros que comprende un enlace doble y uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S,
• cicloalquilo C3-7 opcionalmente sustituido con uno o varios grupos R5 seleccionados de modo independiente,
• heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O, opcionalmente sustituido con uno a tres grupos R5 seleccionados de modo independiente,
• heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno a tres grupos R6 seleccionados de modo independiente, o
• arilo C6-10 opcionalmente sustituido con uno o varios grupos R6 seleccionados de modo independiente; L3 es -NR4b-;
R3 es
• alquilo C1-4 sustituido con
° arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o
° heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente,
• heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o
• arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente;
Cada R4a y R4b se selecciona, de modo independiente, de H, alquilo C1-4 y cicloalquilo C3-7;
R5 es oxo o R6;
R6 es
OH,
• halo,
-NO2,
alquilo C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH,
alcoxi C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH,
cicloalquilo C3-7,
-C(=O)OR8,
-C(=O)NR9R10,
-NHC(=O)-alquilo C1-4,
-CN,
fenilo,
• -O-fenilo,
• heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S, o
• heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S; opcionalmente sustituido con uno o varios alquilo C1-4, alcoxi C1-4, CN, halo y -C(=O)OR11 seleccionados de modo independiente;
R7 es alquilo C1-4 o halo, y
cada uno de R8, R9, R10 y R11 se selecciona, de modo independiente, de H y alquilo C1-4 para su uso en el tratamiento de la esclerosis múltiple.
En un aspecto adicional, la presente invención proporciona composiciones farmacéuticas que comprenden un compuesto de la invención, y un portador, excipiente o diluyente farmacéutico para el tratamiento de la esclerosis múltiple. La composición puede comprender adicionalmente otros ingredientes activos adecuados para su uso en combinación con un compuesto de la invención.
En aspectos adicionales, esta descripción proporciona métodos para sintetizar un compuesto de la invención, con protocolos y vías de síntesis representativos que se describen en la presente memoria.
Otros objetos y ventajas resultarán evidentes para los expertos en la técnica a partir de la consideración de la siguiente descripción detallada.
Descripción detallada de la invención
Definiciones
Se considera que los siguientes términos tienen los significados que se presentan a continuación y son útiles para comprender la descripción y el alcance pretendido de la presente invención.
Cuando se describe la invención, los siguientes términos, si están presentes, tienen los siguientes significados a menos que se indique lo contrario. También se debe entender que cuando se describe en la presente cualquiera de los restos definidos más adelante puede estar sustituido con una diversidad de sustituyentes, y se considera que las respectivas definiciones incluyen tales restos sustituidos dentro de su alcance como se expone a continuación. A menos que se indique lo contrario, el término 'sustituido» se define como se indica a continuación. Además se debe entender que los términos 'grupos' y 'radicales' se pueden considerar intercambiables cuando se usan en la presente.
Los artículos 'un' y 'una' se pueden usar en la presente para referirse a uno o más de uno (es decir, al menos uno) de los objetos gramaticales del artículo. A modo de ejemplo, 'un análogo' significa un análogo o más de un análogo.
'Alquilo' significa hidrocarburo alifático lineal o ramificado que tiene la cantidad especificada de átomos de carbono. Los grupos alquilo particulares tienen 1 a 6 átomos de carbono o 1 a 4 átomos de carbono. Ramificado significa que uno o varios grupos alquilo tales como metilo, etilo o propilo están unidos a una cadena de alquilo lineal. Los grupos alquilo particulares son metilo, etilo, n-propilo, isopropilo, n-butilo, ter-butilo, sec-butilo, n-pentilo, n-hexilo y 1,2-dimetilbutilo. Los grupos alquilo particulares tienen entre 1 y 4 átomos de carbono.
'Alquileno' se refiere a grupos radicales alcano divalentes que tienen la cantidad de átomos de carbono especificados, en particular 1 a 6 átomos de carbono y más en particular, 1 a 4 átomos de carbono que pueden ser de cadena lineal o ramificada. Este término se ejemplifica por medio de grupos tales como metileno (-CH2-), etileno (-CH2-CH2-), isómeros de propileno (por ejemplo, -CH2-CH2-CH2- y -CH(CH3)-CH2-).
'Alquenileno' se refiere a grupos de radicales alqueno divalentes que tienen la cantidad de átomos de carbono y la cantidad de enlaces dobles especificadas, en particular 2 a 6 átomos de carbono y más en particular, 2 a 4 átomos de carbono que pueden ser de cadena lineal o ramificada. Este término se ejemplifica por grupos tales como -CH=CH-, -CH2-CH=CH-, -C(CH3)=CH-, -C(CH3)=CH-CH2-, -C(CH3)=C(CH3)- y -CH2-C(CH3)=CH-.
'Alquinileno' se refiere a grupos de radicales alquino divalentes que tiene una cantidad de átomos de carbono y la cantidad de enlaces triples especificadas, en particular 2 a 6 átomos de carbono y más en particular, 2 a 4 átomos de carbono que puede ser de cadena lineal o ramificada. Este término se ejemplifica por grupos tales como -C=C-, -CH2-CeC- y -C(CH3)H-CeCH-.
'Alcoxi' se refiere al grupo O-alquilo, donde el grupo alquilo tiene la cantidad de átomos de carbono especificada. En particular, el término se refiere al grupo -O-alquilo C1-C6. Los grupos alcoxi particulares son metoxi, etoxi, n-propoxi, isopropoxi, n-butoxi, ter-butoxi, sec-butoxi, n-pentoxi, n-hexoxi y 1,2-dimetilbutoxi. Los grupos alcoxi particulares son alcoxi inferior, es decir, con 1 a 6 átomos de carbono. Otros grupos alcoxi particulares tienen entre 1 y 4 átomos de carbono.
'Amino' se refiere al radical -NH2.
'Arilo' se refiere a un grupo hidrocarbonado aromático monovalente derivado por remoción de un átomo de hidrógeno de un átomo de carbono simple de un sistema de anillos aromáticos principal. En particular, el arilo se refiere a una estructura de anillos aromáticos, monocíclicos o policíclicos que incluyen la cantidad de miembros del anillo especificada. Los grupos arilo particulares tienen de 6 a 10 miembros del anillo. Cuando el grupo arilo es un sistema de anillos monocíclicos, contiene preferiblemente 6 átomos de carbono. Los grupos arilo particulares incluyen fenilo, naftilo, indenilo y tetrahidronaftilo.
'Carboxi' se refiere al radical -C(O)OH.
'Cicloalquilo' se refiere a grupos hidrocarbilo no aromáticos cíclicos que tienen la cantidad de átomos de carbono especificada. Los grupos cicloalquilo particulares tienen de 3 a 7 átomos de carbono. Estos grupos cicloalquilo incluyen, a modo de ejemplo, estructuras de anillos simples tales como ciclobutilo, ciclopentilo, ciclohexilo y cicloheptilo.
'Ciano' se refiere al radical -CN.
'Halo' o 'halógeno' se refiere a fluoro (F), cloro (Cl), bromo (Br) y yodo (I). Los grupos halo particulares son fluoro o cloro.
'Hetero' cuando se usa para describir un compuesto o un grupo presente en un compuesto significa que uno o varios átomos de carbono en el compuesto o grupo fueron reemplazados por un heteroátomo de nitrógeno, oxígeno o azufre. Hetero se puede aplicar a cualquiera de los grupos hidrocarbilo descritos con anterioridad tales como alquilo, por ejemplo heteroalquilo, cicloalquilo, por ejemplo heterocicloalquilo, arilo, por ejemplo heteroarilo, que tienen de 1 a 5 y en particular, de 1 a 3 heteroátomos.
'Heteroarilo' significa una estructura de anillos aromáticos, monocíclicos o policíclicos que incluye uno o varios heteroátomos y la cantidad de miembros del anillo especificada. Los grupos heterarilo particulares tienen 5 a 10 miembros del anillo o 5 a 6 miembros del anillo. El grupo heteroarilo puede ser, por ejemplo, un anillo monocíclico de cinco miembros o de seis miembros o una estructura bicíclica formada por anillos de cinco o seis miembros fusionados o dos anillos de seis miembros fusionados o, a modo de otro ejemplo, dos anillos de cinco miembros fusionados. Cada anillo puede contener hasta cuatro heteroátomos normalmente seleccionados de nitrógeno, azufre y oxígeno. Normalmente, el anillo heteroarilo contendrá hasta 4 heteroátomos, más normalmente, hasta 3 heteroátomos, más usualmente hasta 2, por ejemplo, un único heteroátomo. En una realización, el anillo heteroarilo contiene al menos un átomo de nitrógeno del anillo. Los átomos de nitrógeno en los anillos heteroarilo pueden ser básicos, como en el caso de un imidazol o piridina o esencialmente no básicos como en el caso de un nitrógeno de indol o de pirrol. En general, la cantidad de átomos de nitrógeno básicos presentes en el grupo heteroarilo, incluyendo cualquier sustituyente del grupo amino del anillo, será menor que cinco. Los ejemplos de grupos heteroarilo monocíclicos de cinco miembros incluyen, pero sin limitación, grupos pirrol, furano, tiofeno, imidazol, furazano, oxazol, oxadiazol, oxatriazol, isoxazol, tiazol, isotiazol, pirazol, triazol y tetrazol. Los ejemplos de grupos heteroarilo monocíclicos de seis miembros incluyen, pero sin limitación, piridina, pirazina, piridazina, pirimidina y triazina. Los ejemplos particulares de grupos heteroarilo bicíclicos que contienen un anillo de cinco miembros fusionado con otro anillo de cinco miembros incluyen, pero sin limitación, imidazotiazol y imidazoimidazol. Los ejemplos particulares de grupos heteroarilo bicíclicos que contienen un anillo de seis miembros fusionado con un anillo de cinco miembros incluyen, pero sin limitación, grupos benzfurano, benztiofeno, bencimidazol, benzoxazol, isobenzoxazol, bencisoxazol, benztiazol, bencisotiazol, isobenzofurano, indol, isoindol, isoindolona, indolizina, indolina, isoindolina, purina (por ejemplo, adenina, guanina), indazol, pirazolopirimidina, triazolopirimidina, benzodioxol y pirazolopiridina. Los ejemplos particulares de grupos heteroarilo bicíclicos que contienen dos anillos de seis miembros incluyen, pero sin limitación, grupos quinolina, isoquinolina, cromano, tiocromano, cromeno, isocromeno, cromano, isocromano, benzodioxano, quinolizina, benzoxazina, benzodiazina, piridopiridina, quinoxalina, quinazolina, cinnolina, ftalazina, naftiridina y pteridina. Los grupos heteroarilo particulares son aquellos derivados de tiofeno, pirrol, benzotiofeno, benzofurano, indol, piridina, quinolina, imidazol, oxazol y pirazina.
Los ejemplos de heteroarilos representativos incluyen los siguientes:
en donde cada Y se selecciona de >C=O, NH, O y S.
Como se usa en la presente, el término 'heterocicloalquilo' se refiere a un anillo y/o anillos no aromáticos heterocíclicos estables que contienen uno o varios heteroátomos seleccionados, de modo independiente, de N, O y S, fusionados, en donde el grupo contiene la cantidad de miembros del anillo especificada. Los grupos heterocicloalquilo particulares tienen 4-10 miembros del anillo o 5 a 7 miembros del anillo o 5 a 6 miembros del anillo. El grupo heterocicloalquilo puede ser, por ejemplo, un anillo monocíclico de cinco miembros o de seis miembros o una estructura bicíclica formada por anillos fusionados de cinco y seis miembros o dos anillos fusionados de seis miembros o, a modo de otro ejemplo, dos anillos fusionados de cinco miembros. Cada anillo puede contener hasta cuatro heteroátomos normalmente seleccionados de nitrógeno, azufre y oxígeno. Normalmente, el anillo heterocicloalquilo contendrá hasta 4 heteroátomos, más normalmente hasta 3 heteroátomos, más usualmente hasta 2, por ejemplo, un único heteroátomo. En una realización, el anillo heterocicloalquilo contiene al menos un átomo de nitrógeno del anillo. Un sistema de anillos heterocíclicos fusionados puede incluir anillos carbocíclicos y necesitan incluir únicamente un anillo heterocíclico. Los ejemplos de anillos heterocíclicos incluyen, pero sin limitación, morfolina, piperidina (por ejemplo 1-piperidinilo, 2-piperidinilo, 3-piperidinilo y 4-piperidinilo), pirrolidina (por ejemplo 1 -pirrolidinilo, 2-pirrolidinilo y 3 pirrolidinilo), pirrolidona, pirano (2H-pirano o 4H-pirano), dihidrotiofeno, dihidropirano, dihidrofurano, dihidrotiazol, tetrahidrofurano, tetrahidrotiofeno, dioxano, tetrahidropirano (por ejemplo 4-tetrahidropiranilo), imidazolina, imidazolidinona, oxazolina, tiazolina, 2-pirazolina, pirazolidina, piperazina y N-alquilpiperazinas tales como N-metilpiperazina. Otros ejemplos incluyen tiomorfolina y su S-óxido y S,S-dióxido (en particular tiomorfolina). Otros ejemplos más incluyen azetidina, piperidona, piperazona y N-alquilpiperidinas tales como N-metilpiperidina. Los ejemplos particulares de grupos heterocicloalquilo se muestran en los siguientes ejemplos ilustrativos:
en donde cada W se selecciona de CH2 , NH, O y S; y cada Y se selecciona de NH, O, CO, SO2 y S.
'Hidroxi' se refiere al radical -OH.
'Nitro' se refiere al radical -NO2.
'Sustituido’ se refiere a un grupo, en el que uno o varios átomos de hidrógeno se reemplazan cada uno, de modo independiente, con el mismo o con diferentes sustituyentes.
'Tiol' se refiere al grupo -SH.
'Tioalcoxi' se refiere al grupo -SR10 donde R10 es un grupo alquilo con la cantidad de átomos de carbono especificada. En particular, los grupos tioalcoxi donde R10 es un alquilo C1-C6. Los grupos tioalcoxi particulares son tiometoxi, tioetoxi, n-tiopropoxi, tioisopropoxi, n-tiobutoxi, ter-tiobutoxi, sec-tiobutoxi, n-tiopentoxi, n-tiohexoxi y 1,2-dimetiltiobutoxi. Los grupos tioalcoxi particulares son tioalcoxi inferior, es decir, con 1 a 6 átomos de carbono. Otros grupos tioalcoxi particulares tienen entre 1 y 4 átomos de carbono.
Como se usa en la presente, el término 'sustituido con uno o varios' se refiere a uno a cuatro sustituyentes. En una realización, se refiere a uno a tres sustituyentes. En otras realizaciones, se refiere a uno o dos sustituyentes. En otra realización más, se refiere a un sustituyente.
Un experto en la técnica de síntesis orgánica reconocerá que el número máximo de heteroátomos en un anillo heterocíclico estable, químicamente factible, ya sea aromático o no aromático, está determinado por el tamaño del
anillo, el grado de insaturación y la valencia de los heteroátomos. En general, un anillo heterocíclico puede tener de uno a cuatro heteroátomos siempre que el anillo heteroaromático sea químicamente factible y estable.
"Farmacéuticamente aceptable" significa aprobado o aprobable por una agencia regulatoria del gobierno federal o estatal o la agencia correspondiente en países que no sean los Estados Unidos, o que se encuentra en la Farmacopea de los Estados Unidos u otra farmacopea generalmente reconocida para uso en animales, y más particularmente, en seres humanos.
'Sal farmacéuticamente aceptable' se refiere a una sal de un compuesto que es farmacéuticamente aceptable y que posee la actividad farmacológica deseada del compuesto original. En particular, tales sales son no tóxicas, pueden ser sales de adición de ácidos inorgánicos u orgánicos y sales de adición de base. Específicamente, tales sales incluyen: (1) sales de adición de ácido, formadas con ácidos inorgánicos tales como ácido clorhídrico, ácido bromhídrico, ácido sulfúrico, ácido nítrico, ácido fosfórico; o formados con ácidos orgánicos tales como ácido acético, ácido propiónico, ácido hexanoico, ácido ciclopentanpropiónico, ácido glicólico, ácido pirúvico, ácido láctico, ácido malónico, ácido succínico, ácido málico, ácido maleico, ácido fumárico, ácido tartárico, ácido cítrico, ácido benzoico, ácido 3-(4-hidroxibenzoil)benzoico, ácido cinámico, ácido mandélico, ácido metansulfónico, ácido etansulfónico, ácido 1,2-etandisulfónico, ácido 2-hidroxietansulfónico, ácido bencensulfónico, ácido 4-clorobencensulfónico, ácido 2-naftalensulfónico, ácido 4-toluensulfónico, ácido alcanforsulfónico, ácido 4-metilbiciclo[2.2.2]-oct-2-eno-1-carboxílico, ácido glucoheptonico, ácido 3-fenilpropiónico, ácido trimetilacético, ácido ter-butilacético, ácido laurilsulfúrico, ácido glucónico, ácido glutámico, ácido hidroxinaftoico, ácido salicílico, ácido esteárico, ácido mucónico; o (2) sales formadas cuando un protón ácido presente en el compuesto precursor se reemplaza con un ion metálico, por ejemplo, un ión de metal alcalino, un ion de metal alcalinotérreo o un ion de aluminio; o se coordina con una base orgánica tal como etanolamina, dietanolamina, trietanolamina, N-metilglucamina. Las sales además incluyen, solo a modo de ejemplo, sodio, potasio, calcio, magnesio, amonio, tetraalquilamonio; y cuando el compuesto contiene una funcionalidad básica, sales de ácidos orgánicos o inorgánicos no tóxicos, tales como clorhidrato, bromhidrato, tartrato, mesilato, acetato, maleato, oxalato. El término 'catión farmacéuticamente aceptable' se refiere a un contraión catiónicp iónico aceptable de un grupo funcional ácido. Tales cationes se ejemplifican con cationes de sodio, potasio, calcio, magnesio, amonio, tetraalquilamonio.
'Vehículo farmacéuticamente aceptable' se refiere a un diluyente, adyuvante, excipiente o portador con el que se administra un compuesto de la invención.
'Solvato' se refiere a formas del compuesto que están asociadas con un solvente, usualmente por una reacción de solvólisis. Esta asociación física incluye enlaces de hidrógeno. Los solventes convencionales incluyen agua, etanol, ácido acético. Los compuestos de la invención se pueden preparar, por ejemplo, en forma cristalina y puede estar solvatados o hidratados. Los solvatos adecuados incluyen solvatos farmacéuticamente aceptables, tales como hidratos, e incluyen además tanto solvatos estequiométricos como solvatos no estequiométricos. En ciertos casos, el solvato será capaz de aislarse, por ejemplo cuando se incorporan una o más moléculas de solvente en la red cristalina del sólido cristalino. 'Solvato' abarca tanto solvatos en fase de solución como aislables. Los solvatos representativos incluyen hidratos, etanolatos y metanolatos.
'Sujeto' incluye a los seres humanos. Los términos "humano", "paciente" y "sujeto" se usan indistintamente en la presente.
Por 'cantidad efectiva' se entiende la cantidad de compuesto de la invención que, cuando se administra a un sujeto para tratar una enfermedad, es suficiente para efectuar dicho tratamiento para la enfermedad. La 'cantidad efectiva' puede variar de acuerdo con el compuesto, la enfermedad y su gravedad, y la edad, peso, etc., del sujeto para tratar.
'Prevención' o 'prevenir' se refiere a la reducción del riesgo de adquirir o desarrollar una enfermedad o trastorno (es decir, causar que al menos uno de los síntomas clínicos de la enfermedad no se desarrolle en un sujeto que puede estar expuesto a un agente causante de la enfermedad, o predispuestos a la enfermedad antes de la aparición de la enfermedad.
El término 'profilaxis' está relacionado con la 'prevención', y se refiere a una medida o procedimiento cuyo propósito es prevenir, más que tratar o curar una enfermedad. Los ejemplos no limitantes de las medidas profilácticas pueden incluir la administración de vacunas; la administración de heparina de bajo peso molecular a pacientes hospitalarios con riesgo de trombosis, debida, por ejemplo, a la inmovilización; y la administración de un agente antipalúdico tal como cloroquina, antes de una visita a una región geográfica donde la malaria es endémica o el riesgo de contraer la malaria es alto.
'Tratar' o 'tratamiento' de cualquier enfermedad o trastorno se refiere, en una realización, a mejorar la enfermedad o trastorno (es decir, detener la enfermedad o reducir la manifestación, extensión o gravedad de al menos uno de sus síntomas clínicos). En otra realización, 'tratar' o 'tratamiento' se refiere a la mejora de al menos un parámetro físico, que puede no ser discernible por el sujeto. En otra realización más, 'tratar' o 'tratamiento' se refiere a la modulación de la enfermedad o trastorno, ya sea físicamente (por ejemplo, estabilización de un síntoma discernible), fisiológicamente (por ejemplo, estabilización de un parámetro físico) o ambos. En una realización adicional, 'tratar' o 'tratamiento' se refiere a retardar la progresión de la enfermedad.
Como se usa en la presente, el término 'afecciones inflamatorios' se refiere al grupo de afecciones que incluyen, artritis reumatoidea, osteoartritis, artritis idiopática juvenil, vasculitis, psoriasis, gota, enfermedad alérgica de las vías respiratorias (por ejemplo, asma, rinitis) enfermedades inflamatorias intestinales (por ejemplo, enfermedad de Crohn, colitis ulcerosa), y estados de enfermedad producidos por endotoxina (por ejemplo, complicaciones después de cirugía de bypass o estados endotoxínicos crónicos que contribuyen a, por ejemplo, insuficiencia cardíaca crónica). Particularmente el término se refiere a artritis reumatoidea, enfermedad alérgica de las vías respiratorias (por ejemplo, asma) y enfermedades inflamatorias intestinales.
Como se usa en la presente, el término 'enfermedades infecciosas' se refiere a enfermedades infecciosas bacterianas e incluye, pero sin limitación, afecciones tales como sepsis, septicemia, endotoxemia, síndrome de respuesta inflamatoria sistémica (SIRS), gastritis, enteritis, enterocolitis, tuberculosis y otras infecciones que implican, por ejemplo, Yersinia, Salmonella, Chlamydia, Shigella o enterobacterias.
Como se usa en la presente el término 'enfermedades autoinmunes' se refiere al grupo de enfermedades que incluyen enfermedades obstructivas de las vías respiratorias (incluyendo afecciones tales como EPOC (enfermedad pulmonar obstructiva crónica)), psoriasis, asma (por ejemplo, asma intrínseca, asma extrínseca, asma de polvo, asma infantil), particularmente asma crónico o inveterado (por ejemplo, asma tardío e hiperreactividad de las vías respiratorias), bronquitis, que incluyen asma bronquial, lupus eritematoso sistémico (SLE), esclerosis múltiple, diabetes mellitus tipo I y complicaciones asociadas con ella, eccema atópico (dermatitis atópica), dermatitis de contacto y otras dermatitis eczematosa, vasculitis, enfermedad inflamatoria intestinal (por ejemplo, enfermedad de Crohn y colitis ulcerosa), aterosclerosis y esclerosis lateral amiotrófica. En particular, el término se refiere a EPOC, asma, psoriasis, lupus eritematoso sistémico, diabetes mellitus tipo I, vasculitis y enfermedad inflamatoria intestinal.
Como se usa en la presente, la expresión 'enfermedad endocrina y/o metabólica' se refiere al grupo de afecciones que implican la sobre-producción o la subproducción de ciertas hormonas corporales, mientras que los trastornos metabólicos afectan la capacidad del cuerpo para procesar ciertos nutrientes y vitaminas. Los trastornos endocrinos incluyen hipotiroidismo, hiperplasia adrenal congénita, enfermedades de la glándula paratiroidea, diabetes mellitus, enfermedades de las glándulas suprarrenales (que incluyes síndrome de Cushing y enfermedad de Addison) y disfunción ovárica (que incluye síndrome del ovario poliquístico), entre otros. Algunos ejemplos de trastornos metabólicos incluyen fibrosis quística, fenilcetonuria (PKU), diabetes, hiperlipidemia, gota y raquitismo.
Como se usa en la presente, el término 'enfermedades que implican deterioro de las funciones de las células inmunitarias' incluye afecciones con síntomas tales como infecciones virales y bacterianas recurrentes y prolongadas, y recuperación lenta. Otros síntomas invisibles pueden ser la incapacidad para matar parásitos, levaduras y patógenos bacterianos en los intestinos o en todo el cuerpo.
Como se usa en la presente, el término 'afecciones neuroinflamatorias' se refiere a enfermedades o trastornos caracterizados por déficits neurológicos abruptos asociados con inflamación, desmielinización y daño axonal, e incluye pero sin limitación afecciones tales como síndrome de Guillain-Barré (GBS), esclerosis múltiple, degeneración axonal, encefalomielitis autoinmune.
Se entiende que los 'compuestos de la invención' y expresiones equivalentes abarcan los compuestos de fórmula, como se describe en la presente, expresión que incluye las sales farmacéuticamente aceptables y los solvatos, por ejemplo, los hidratos y los solvatos de las sales farmacéuticamente aceptables cuando el contexto así lo permita. De manera similar, la referencia a los intermedios, independientemente de que se reivindiquen o no ellos mismos, se entiende que abarca sus sales y solvatos, cuando el contexto lo permita.
Cuando se hace referencia en la presente a rangos, por ejemplo, pero sin limitación, alquilo C1-6 , la cita de un rango se debe considerar una representación de cada miembro de dicho rango.
Otros derivados referenciales de los compuestos de esta invención tienen actividad tanto en sus formas de ácido como de derivados de ácido, pero en la forma sensible al ácido a menudo ofrece ventajas de solubilidad, compatibilidad de tejidos o liberación retardada en el organismo de mamífero (ver Bundgard, H., Design de Prodrugs, pp. 7-9, 21-24, Elsevier, Ámsterdam 1985). Los profármacos como los compuestos referenciales incluyen derivados ácidos bien conocidos por los expertos en la técnica, tales como, por ejemplo, ésteres preparados por la reacción del ácido original con un alcohol adecuado, o amidas preparadas por reacción del compuesto ácido original con una amina sustituida o no sustituida, o anhídridos ácidos o anhídridos mixtos. Los ésteres, amidas y anhídridos alifáticos o aromáticos simples derivados de grupos ácidos laterales de los compuestos de esta invención son profármacos referenciales particularmente útiles. En algunos casos es deseable preparar profármacos de tipo éster doble tales como ésteres de (aciloxi)alquilo o ésteres de ((alcoxicarbonil)oxi)alquilo. Particularmente, tales profármacos referenciales son los alquilo C1 a Cs, y arilo C6-10 sustituido o no sustituido, de los compuestos de la invención.
Como se usa en la presente, el término 'variante isotópica' se refiere a un compuesto que contiene proporciones no naturales de isótopos en uno o más de los átomos que constituyen dicho compuesto. Por ejemplo, una 'variante isotópica' de un compuesto puede contener uno o más isótopos no radiactivos, tales como por ejemplo, deuterio (2H o D), carbono-13 (13C), nitrógeno-15 (15N), o similares. Se comprenderá que, en un compuesto donde se realiza dicha sustitución isotópica, los siguientes átomos, cuando están presentes, pueden variar, de manera que por ejemplo,
cualquier hidrógeno puede ser 2H/D, cualquier carbono puede ser 13C o cualquier nitrógeno puede ser 15N, y que la presencia y la colocación de tales átomos se puede determinarse dentro de la técnica. Asimismo, la invención puede incluir la preparación de variantes isotópicas con radioisótopos, en el caso por ejemplo, donde los compuestos resultantes se pueden usar para estudios de distribución tisular de fármacos y/o sustrato. Los isótopos radioactivos tritio, es decir 3H, y carbono 14, es decir, 14C, son particularmente útiles para este propósito en vista de su facilidad de incorporación y medios de detección rápidos. Además, se pueden preparar compuestos que están sustituidos con isótopos emisores de positrones, tales como 11C, 18F, 15O y 13N, y pueden ser útiles en estudios de topografía de emisión de positrones (PET) para examinar la ocupación del receptor de sustrato.
También se debe entender que los compuestos que tienen la misma fórmula molecular pero difieren en la naturaleza o secuencia de unión de sus átomos o en la disposición de sus átomos en el espacio se denominan 'isómeros'. Los isómeros que difieren en la disposición de sus átomos en el espacio se denominan 'estereoisómeros'.
Los estereoisómeros que no son imágenes especulares entre sí se denominan 'diastereómeros' y los que son imágenes especulares no superponibles entre sí se denominan 'enantiómeros'. Cuando un compuesto tiene un centro asimétrico, por ejemplo, está unido a cuatro grupos diferentes, es posible un par de enantiómeros. Un enantiómero se puede caracterizar por la configuración absoluta de su centro asimétrico y está descrito por las reglas de secuenciación R y S de Cahn y Prelog, o por la manera en la que la molécula gira el plano de luz polarizada y se designa como dextrorrotatorio o levorrotatorio (es decir, como isómeros (+) o (-), respectivamente). Un compuesto quiral puede existir como enantiómero individual o como una mezcla de estos. Una mezcla que contiene proporciones iguales de los enantiómeros se denomina 'mezcla racémica'.
Los 'tautómeros' se refieren a compuestos que son formas intercambiables de una estructura de compuesto particular, y que varían en el desplazamiento de los átomos de hidrógeno y electrones. En consecuencia, dos estructuras pueden estar en equilibrio a través del movimiento de electrones n y un átomo (generalmente H). Por ejemplo, los enoles y cetonas son tautómeros porque se interconvierten rápidamente por tratamiento con ácido o base. Otro ejemplo de tautomerismo son las formas aci- y nitro de fenilnitrometano, que se forman igualmente por tratamiento con ácido o base.
Las formas tautoméricas pueden ser relevantes para el logro de la reactividad química óptima y la actividad biológica de un compuesto de interés.
Los compuestos de la invención pueden poseer uno o más centros asimétricos; por lo tanto, tales compuestos se pueden producir como (R) - o (S) -estereoisómeros individuales o como mezclas de estos.
A menos que se indique lo contrario, la descripción o designación de un compuesto particular en la memoria descriptiva y en las reivindicaciones pretende incluir tanto enantiómeros individuales como mezclas, racémicas o no, de estos. Los métodos para la determinación de estereoquímica y la separación de estereoisómeros son bien conocidos en la técnica.
Se apreciará que los compuestos de la invención se pueden metabolizar para producir metabolitos biológicamente activos.
LOS COMPUESTOS
En esta memoria se describen nuevos compuestos que antagonizan GPR84 y que pueden ser útiles para el tratamiento de afecciones inflamatorias (por ejemplo, enfermedades intestinales inflamatorias (IBD), artritis reumatoidea, vasculitis, enfermedades pulmonares (por ejemplo, enfermedad pulmonar obstructiva crónica (EPOC), y enfermedades pulmonares intersticiales (por ejemplo, fibrosis pulmonar idiopática (IPF)), afecciones neuroinflamatorias, enfermedades infecciosas, enfermedades autoinmunes, enfermedades endocrinas y/o metabólicas, y/o enfermedades que implican el deterioro de las funciones de las células inmunitarias.
En esta memoria también se describen métodos para la producción de los compuestos de la invención, composiciones farmacéuticas que comprenden los compuestos de la invención y métodos para tratar enfermedades que involucran afecciones inflamatorias (por ejemplo, enfermedades intestinales inflamatorias (IBD), artritis reumatoidea, vasculitis, enfermedades pulmonares (por ejemplo, enfermedad pulmonar obstructiva crónica (EPOC), y enfermedades pulmonares intersticiales (por ejemplo, fibrosis pulmonar idiopática (IPF)), afecciones neuroinflamatorias, enfermedades infecciosas, enfermedades autoinmunes, enfermedades endocrinas y/o metabólicas, y/o enfermedades que implican el deterioro de las funciones de las células inmunitarias mediante la administración de un compuesto de la invención. Un compuesto de la invención es un inhibidor de GPR84.
Por consiguiente, un primer aspecto de la descripción es un compuesto que tiene una fórmula la:
R1 es H, Me o halo;
L1 está ausente o es -O-, -S- o -NR4a-;
G es
R2,
-W-L2-R2 , o
-W-L3-R3 ;
W es alquileno C1-4, alquenileno C2-4 que tiene un enlace doble o alquinileno C2-4 que tiene un enlace triple; L2 está ausente o es -O-;
R2 es
• H,
• alquilo C1-8, opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de o OH,
° halo,
o CN,
o alcoxi C1-6,
o cicloalquilo C3-7,
o heterocicloalquilo de 4-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O,
o heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, y
o fenilo,
• cicloalquenilo C4-7 que comprende un enlace doble,
• heterocicloalquenilo de 5-7 miembros que comprende un enlace doble y uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S,
• cicloalquilo C3-7 opcionalmente sustituido con uno o varios grupos R5 seleccionados de modo independiente,
• heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O, opcionalmente sustituido con uno a tres grupos R5 seleccionados de modo independiente,
• heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno a tres grupos R6 seleccionados de modo independiente, o
• arilo C6-10 opcionalmente sustituido con uno o varios grupos R6 seleccionados de modo independiente; L3 es -NR4b-;
R3 es
• alquilo C1-4 sustituido con
° arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o
° heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente,
• heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o
• arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente; Cada R4a y R4b se selecciona, de modo independiente, de H, alquilo C1-4 y cicloalquilo C3-7;
R5 es oxo o R6;
R6 es
OH,
• halo,
-NO2,
alquilo C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH,
alcoxi C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH,
cicloalquilo C3-7,
-C(=O)OR8,
-C(=O)NR9R10,
-NHC(=O)-alquilo C1-4,
-CN,
fenilo,
-O-fenilo,
heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S, o
heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S; opcionalmente sustituido con uno o varios alquilo C1-4, alcoxi C1-4, CN, halo y -C(=O)OR11 seleccionados de modo independiente;
R7 es alquilo C1-4 o halo; y
cada uno de R8, R9, R10 y R11 se selecciona, de modo independiente, de H y alquilo C1-4.
En una realización, el compuesto es según la Fórmula la, en la que R1 es H.
En una realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-IVc, en donde L1 está ausente o es -O-. En una realización preferida, L1 está ausente.
En otra realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-IVc, en donde L1 es -NR4a-, en donde R4a es como se describió previamente. En una realización preferida, R4a es H, Me, Et o ciclopropilo. En una realización de mayor preferencia, R4a es H.
En una realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IVc, en donde W es alquileno C1-4. En una realización preferida, W es -CH2-, -CH2-CH2-, -CH2-CH2-CH(CH3)-, -CH2-CH(-CH2-CH3)-, -CH2-C(CH3)2-o -CH2-CH2-CH2-. En una realización de mayor preferencia, W es -CH2-. En otra realización de mayor preferencia, W es -CH2-CH2-.
En una realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IVc, en donde W es alquenileno C2-4 que tiene un enlace doble. En una realización preferida, W es -CH=CH-, -CH2-CH=CH- o -CH=CH-CH2-. En una realización de mayor preferencia, W es -CH=CH-. En otra realización de mayor preferencia, W es -CH2-CH=CH-.
En una realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IVc, en donde W es alquinileno C2-4 que tiene un enlace triple. En una realización preferida, W es -CeC-, - CH2-CEC- o -CEC-CH2-. En una realización de mayor preferencia, W es -CeC-. En otra realización de mayor preferencia, W es -CH2-CEC-.
En una realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IIIc, en donde L2 está ausente. En otra realización, L2 es -O-.
En una realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IIIc, en donde L1 está ausente o es -O-, W es alquileno C1-4; y L2 y R2 son como se describió previamente. En una realización preferida, W es -CH2-, -CH2-CH2- o -CH2-CH2-CH2-. En una realización de mayor preferencia, W es - CH2-. En otra realización preferida, W es -CH2-CH2-.
En otra realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IIIc, en donde L1 está ausente o es -O-, W es alquenileno C2-4 que tiene un enlace doble; y L2 y R2 son como se describió previamente. En una realización preferida, W es -CH=CH-, -CH2-CH=CH- o -CH=CH-CH2-. En una realización de mayor preferencia, W es -CH=CH-. En otra realización de mayor preferencia, W es -CH2-CH=CH-.
En otra realización más, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IIIc, en donde L1 está ausente, W es alquinileno C2-4 que tiene un enlace triple; y L2 y R2 son como se describió previamente. En una realización preferida, W es -CeC-, -CH2-CEC- o -CEC-CH2-. En una realización de mayor preferencia, W es -CeC-. En otra realización de mayor preferencia, W es -CH2-CEC-.
En una realización, el compuesto es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IIIc, en donde L1 y L2 están ausentes, W es alquileno C1-4; y R2 es como se describió previamente. En una realización preferida, W es -CH2-, -CH2-CH2- o -CH2-CH2-CH2-. En una realización de mayor preferencia, W es -CH2-. En otra realización de mayor preferencia, W es -CH2-CH2-.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IIIc, en donde L1 y L2 están ausentes, W es alquenileno C2-4 que tiene un enlace doble; y R2 es como se describió previamente. En una realización preferida, W es -CH=CH-, -CH2-CH=CH- o -CH=CH-CH2-. En una realización de mayor preferencia, W es -CH=CH-. En otra realización de mayor preferencia, W es -CH2-CH=CH-.
En otra realización más, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic o IIIa-IIIc, en donde L1 y L2 están ausentes, W es alquinileno C2-4 que tiene un enlace triple; y R2 es como se describió previamente. En una realización preferida, W es -CeC-, -CH2-CEC- o -CEC-CH2-. En una realización de mayor preferencia, W es -CeC-. En otra realización de mayor preferencia, W es -CH2-CEC-.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es H.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es alquilo C1-8. En una realización preferida, R2 es Me, Et, n-Pr, i-Pr, /'-Bu o f-Bu. En una realización de mayor preferencia, R2 es Me, Et, /-Pr o f-Bu. En una realización de mayor preferencia, R2 es f-Bu.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es alquilo C1-8 sustituido con uno a tres grupos seleccionados de OH, halo, CN, alcoxi C1-6, cicloalquilo C3-7, heterocicloalquilo de 4-6 miembros (que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O), heteroarilo de 5-6 miembros (que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O) y fenilo. En una realización preferida, R2 es Me, Et, n-Pr, /-Pr, /-Bu o f-Bu sustituido con uno a tres grupos seleccionados de OH, halo, CN, alcoxi C1-6, cicloalquilo C3-7, heterocicloalquilo de 4-6 miembros
(que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O), heteroarilo de 5-6 miembros (que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O) y fenilo. En otra realización preferida, es alquilo C1-8 sustituido con uno a tres grupos seleccionados de OH, F, Cl, Cn , -OMe, -OEt, O/'-Pr, ciclopropilo, ciclobutilo, oxetanilo, tetrahidrofuranilo, tetrahidropiranilo, pirralolilo, imidazolilo, triazolilo, oxazolilo, tiazolilo, piridinilo, pirimidinilo, pirazinilo y fenilo. En una realización de mayor preferencia, R2 es Me, Et, n-Pr, /-Pr, /-Bu o t-Bu sustituido con uno a tres grupos seleccionados de OH, F, Cl, CN, - OMe, -OEt, -O/-Pr, ciclopropilo, ciclobutilo, oxetanilo, tetrahidrofuranilo, tetrahidropiranilo, pirralolilo, imidazolilo, triazolilo, oxazolilo, tiazolilo, piridinilo, pirimidinilo, pirazinilo y fenilo.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es alquilo C1-8 sustituido con un grupo seleccionado de OH, halo, CN, alcoxi C1-6 , cicloalquilo C3-7 , heterocicloalquilo de 4-6 miembros (que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O), heteroarilo de 5-6 miembros (que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O) y fenilo. En una realización preferida, R2 es Me, Et, n-Pr, /-Pr, /-Bu o t-Bu sustituido con un grupo seleccionado de OH, halo, CN, alcoxi C1-6 , cicloalquilo C3-7, heterocicloalquilo de 4-6 miembros (que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O), heteroarilo de 5-6 miembros (que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O) y fenilo. En otra realización preferida, es alquilo C1-8 sustituido con un grupo seleccionado de OH, F, Cl, CN, -OMe, -OEt, - O/-Pr, ciclopropilo, ciclobutilo, oxetanilo, tetrahidrofuranilo, tetrahidropiranilo, pirralolilo, imidazolilo, triazolilo, oxazolilo, tiazolilo, piridinilo, pirimidinilo, pirazinilo y fenilo. En una realización de mayor preferencia, R2 es Me, Et, n-Pr, /-Pr, /-Bu o t-Bu sustituido con un grupo seleccionado de OH, F, Cl, CN, -OMe, -OEt, - O/-Pr, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, oxetanilo, tetrahidrofuranilo, tetrahidropiranilo, pirralolilo, imidazolilo, triazolilo, oxazolilo, tiazolilo, piridinilo, pirimidinilo, pirazinilo y fenilo. En una realización de máxima preferencia, R2 es -CH2-OH, -C(c H3)2-OH, -Ch (OH)Ch 3, -CH(o H)-C2H5, -CH(OH)-C3H7, - C(OH)(C2Hs)2 , -C(OH)H-CH(CH3)2, -C(OH)H-CH2-CH(CH3)2, -C(OH)H-C(CH3)3, -CH2-CN, -CH2-OCH3 , - CH2-CH2-OCH3 , -CH(OCH3)-CH3, -C(OCH3)H-CH(CH3)2, -CH2-F, -CH2-CH2-F, -CH2-ciclopropilo, -CH2-ciclopentilo, -CH2-oxetanilo, -CH2-tetrahidrofuranilo o -CH2-tetrahidropiranilo.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es cicloalquenilo C4-7 que comprende un enlace doble. En una realización preferida, R2 es ciclohexenilo.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es heterocicloalquenilo de 5-7 miembros que comprende un enlace doble y uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S. En una realización preferida, R2 es dihidropiranilo.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es cicloalquilo C3-7. En una realización preferida, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo. En una realización de mayor preferencia, R2 es ciclopropilo.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es cicloalquilo C3-7 sustituido con uno a tres grupos R5 seleccionados de modo independiente. En una realización preferida, R2 es cicloalquilo C3-7 sustituido con un grupo R5. En una realización de mayor preferencia, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5. En otra realización de mayor preferencia, R2 es cicloalquilo C3-7 sustituido con un grupo R5, en donde R5 es oxo o R6 en donde R6 se selecciona de OH o alquilo C1-6. En una realización de máxima preferencia, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5, en donde R5 es oxo o R6 en donde R6 se selecciona de OH o alquilo C1-6. En otra realización de máxima preferencia, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5, en donde R5 es R6 y R6 se selecciona de OH.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, en donde R2 es heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O. En una realización preferida, R2 es oxetanilo, tetrahidrofuranilo, tetrahidropiranilo o dioxanilo.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, R2 es heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O sustituido con uno a tres grupos R5 seleccionados de modo independiente. En una realización preferida, R2 es heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O sustituido con un grupo R5. En una realización de mayor preferencia, R2 es heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O sustituido con un grupo R5, en donde R5 se selecciona de oxo o R6, en donde R6 se selecciona de OH y alquilo C1-6. En otra realización de mayor preferencia, R2 es oxetanilo, tetrahidrofuranilo, tetrahidropiranilo o dioxanilo, cada uno de los cuales está sustituido con un grupo R5. En una realización de máxima preferencia, R2 es oxetanilo, tetrahidrofuranilo, tetrahidropiranilo o dioxanilo, cada uno de los cuales está sustituido con un grupo R5, en donde R5 se selecciona de oxo o R6 en donde R6 se selecciona de OH y alquilo C1-6 ,
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O. En
una realización preferida, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno a tres grupos R6 seleccionados de modo independiente. En una realización preferida, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente. En una realización de mayor preferencia, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, sustituido con uno o dos grupos R6 seleccionados de modo independiente. En otra realización de mayor preferencia, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, halo, alquilo C1-6, alquilo C1-6 sustituido con uno o varios halo, alcoxi C1-6, -CN, cicloalquilo C3-7, heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S y fenilo. En la realización de máxima preferencia, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, cada uno de los cuales está sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, halo, alquilo C1-6, alquilo C1-6 sustituido con uno o varios halo, alcoxi C1-6, -CN, cicloalquilo C3-7, heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S y fenilo. En otra realización de máxima preferencia, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, F, Cl, Me, Et, Pr, /'-Pr, f-Bu, -CF3 , -OMe, -OEt, O/'-Pr, -CN, ciclopropilo, pirrolidinilo, morfolinilo, piperidinilo o fenilo. En otra realización de máxima preferencia, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, cada uno de los cuales está sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, F, Cl, Me, Et, Pr, /-Pr, f-Bu, -CF3 , -OMe, -OEt, -O/-Pr, -CN, ciclopropilo, pirrolidinilo, morfolinilo, piperidinilo y fenilo.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, R2 es arilo C6-10. En una realización preferida, R2 es fenilo.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-IIIc, R2 es arilo C6-10 sustituido con uno o varios grupos R6 seleccionados de modo independiente. En una realización preferida, R2 es arilo C6-10 sustituido con uno o dos grupos R6 seleccionados de modo independiente. En una realización de mayor preferencia, R2 es arilo C6-10 sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de halo, CN, alquilo C1-6, alcoxi C1-6 o -NHC(=O)-alquilo C1-4. En otra realización de mayor preferencia, R2 es arilo C6-10 sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de -C(=O)NR9R10 y cada R9 y R10 se selecciona, de modo independiente, de H y alquilo C1-4. En otra realización más de mayor preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente. En una realización de máxima preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de halo, CN, alquilo C1-6, alcoxi C1-6 y -NHC(=O)-alquilo C1-4. En otra realización de máxima preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de -C(=O)NR9R10 y cada R9 y R10 se selecciona, de modo independiente, de H y alquilo C1-4. En otra realización de máxima preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de F, Cl, CN, Me, -OMe, -OEt y -NHC(=O)Me. En otra realización de máxima preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de - C(=O)NH2 y -C(=O)NHMe.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic, IVa, IVb o IVc, en donde L3 es -NR4b- y R4b es como se describió previamente. En una realización preferida, R4b es H, Me, Et o ciclopropilo. En una realización de mayor preferencia, R4a es H.
En otra realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic, IVa, IVb o IVc, en donde R3 es alquilo C1-4 sustituido con arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente o heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente. En una realización preferida, R3 es Me o Et, cada uno de los cuales está sustituido con arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente) o heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente. En otra realización preferida, R3 es alquilo C1-4 sustituido con fenilo o piridilo, cada uno de los cuales está opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente. En una realización de mayor preferencia, R3 es alquilo C1-4 sustituido con fenilo o piridilo. En una realización de mayor preferencia, R3 es alquilo C1-4 sustituido con fenilo o piridilo, cada uno de los cuales está sustituido con Me, Et, F o Cl. En una realización de máxima preferencia, R3 es Me o Et, cada uno de los cuales está sustituido con fenilo o piridilo. En una realización de mayor preferencia, R3 es Me o
Et, cada uno de los cuales está sustituido con fenilo o piridilo, cada uno de los cuales está sustituido con Me, Et, F o Cl.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic, IVa, IVb o IVc, en donde R3 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O. En una realización preferida, R3 es piridilo.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic, IVa, IVb o IVc, en donde R3 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 es como se describió previamente. En una realización preferida, R3 es piridilo, sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 es como se describió previamente. En otra realización preferida, R3 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 se selecciona de Me, Et, F y Cl. En una realización de mayor preferencia, R3 es piridilo sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 se selecciona de Me, Et, F y Cl. En una realización de máxima preferencia, R3 es piridilo sustituido con un grupo R7 seleccionado de Me, Et, F y Cl.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic, IVa, IVb o IVc, en donde R3 es arilo C6-10. En una realización preferida, R3 es fenilo.
En una realización, el compuesto de la invención es de acuerdo con cualquiera de las fórmulas Ia-Ic, IVa, IVb o IVc, en donde R3 es arilo C6-10 sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 es como se describió previamente. En una realización preferida, R3 es fenilo, sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 es como se describió previamente. En otra realización preferida, R3 es arilo C6-10 sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 se selecciona de Me, Et, F y Cl. En una realización de mayor preferencia, R3 es fenilo sustituido con uno o varios grupos R7 seleccionados de modo independiente, en donde cada grupo R7 se selecciona de Me, Et, F y Cl. En una realización de máxima preferencia, R3 es fenilo sustituido con un grupo R7 seleccionado de Me, Et, F y Cl.
En una realización, el compuesto de la invención es de acuerdo con la fórmula Va, Vb, Vc o Vd:
en donde R2 es como se describió previamente.
En otra realización, el compuesto de la invención no es de acuerdo con la fórmula Va, Vb, Vc o Vd.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula VIa, VIb, VIc o VId:
en donde R2 es como se describió previamente.
En otra realización, el compuesto de la invención no es de acuerdo con la fórmula Via, VIb, VIc o VId.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Viia, Viib, Viic o VI Id:
en donde R2 es como se describió previamente.
En una realización, el compuesto de la invención es de acuerdo con la fórmula Va, Vb, Via, VIb, Viia o Viib, en donde R2 es cicloalquilo C3-7. En una realización preferida, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo. En una realización de mayor preferencia, R2 es ciclopropilo.
En una realización, el compuesto de la invención es de acuerdo con la fórmula Va, Vb, Via, VIb, Viia o Viib, en donde R2 no es cicloalquilo C3-7. En una realización preferida, R2 no es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo. En una realización de mayor preferencia, R2 no es ciclopropilo.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Va, Vb, Via, VIb, Viia o Viib, en donde R2 es cicloalquilo C3-7 sustituido con uno a tres grupos R5 seleccionados de modo independiente. En una realización preferida, R2 es cicloalquilo C3-7 sustituido con un grupo R5. En una realización de mayor preferencia, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5. En otra realización más preferida, R2 es cicloalquilo C3-7 sustituido con un grupo R5, en donde R5 es oxo o R6 en donde R6 se selecciona de OH o alquilo C1-6. En una realización de máxima preferencia, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5, en donde R5 es oxo o R6 en donde R6 se selecciona de OH y alquilo C1-6. En otra realización de máxima preferencia, R2 es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5, en donde R5 es OH.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Va, Vb, Via, VIb, Viia o Viib, en donde R2 no es cicloalquilo C3-7 sustituido con uno a tres grupos R5 seleccionados de modo independiente. En una realización preferida, R2 no es cicloalquilo C3-7 sustituido con un grupo R5. En una realización de mayor preferencia, R2 no es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5. En otra realización más preferida, R2 no es cicloalquilo C3-7 sustituido con un grupo R5, en donde R5 es oxo o R6 en donde R6 se selecciona de OH y alquilo C1-6. En una realización de máxima preferencia, R2 no es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5, en donde R5 es oxo o R6 en donde R6 se selecciona de OH y alquilo C1-6. En otra realización de máxima preferencia, R2 no es ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo, cada uno de los cuales está sustituido con un grupo R5, en donde R5 es OH.
En una realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc, Vid, Viic o VI Id, en donde R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O. En una realización preferida, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo.
En una realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc, Vid, Viic o VI Id, en donde R2 no es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O. En una realización preferida, R2 no es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc, Vid, Viic o VI Id, en donde R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno a tres grupos R6 seleccionados de modo independiente. En una realización preferida, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente. En una realización de mayor preferencia, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, sustituido con uno o dos grupos R6 seleccionados de modo independiente. En otra realización de mayor preferencia, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, halo, alquilo C1-6, alquilo C1-6
sustituido con uno o varios halo, alcoxi Ci-6, -CN, cicloalquilo C3-7, heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S y fenilo. En una realización de máxima preferencia, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, cada uno de los cuales está sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, halo, alquilo C1-6, alquilo C1-6 sustituido con uno o varios halo, alcoxi C1-6, -CN, cicloalquilo C3-7, heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S y fenilo. En otra realización de máxima preferencia, R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, F, Cl, Me, Et, Pr, /'-Pr, f-Bu, -CF3 , -OMe, -OEt, O/'-Pr, -CN, ciclopropilo, pirrolidinilo, morfolinilo, piperidinilo y fenilo. En otra realización de máxima preferencia, R2 es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, cada uno de los cuales está sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, F, Cl, Me, Et, Pr, /-Pr, f-Bu, -CF3 , -OMe, -OEt, -O/-Pr, -CN, ciclopropilo, pirrolidinilo, morfolinilo, piperidinilo y fenilo.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc, VId, VI Ic o VI Id, en donde R2 no es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno a tres grupos R6 seleccionados de modo independiente. En una realización preferida, R2 no es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente. En una realización de mayor preferencia, R2 no es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, sustituido con uno o dos grupos R6 seleccionados de modo independiente. En otra realización de mayor preferencia, R2 no es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, halo, alquilo C1-6, alquilo C1-6 sustituido con uno o varios halo, alcoxi C1-6, -CN, cicloalquilo C3-7, heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S y fenilo. En una realización de máxima preferencia, R2 no es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, cada uno de los cuales está sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, halo, alquilo C1-6, alquilo C1-6 sustituido con uno o varios halo, alcoxi C1-6, -CN, cicloalquilo C3-7, heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S y fenilo. En otra realización de máxima preferencia, R2 no es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, F, Cl, Me, Et, Pr, /-Pr, f-Bu, -CF3 , -OMe, -OEt, O/-Pr, -CN, ciclopropilo, pirrolidinilo, morfolinilo, piperidinilo y fenilo. En otra realización de máxima preferencia, R2 no es furanilo, tienilo, oxazolilo, tiazolilo, oxadiazolilo, tiadiazolilo, imidazolilo, triazolilo, piridinilo, pirazinilo, pirimidinilo, indanilo o indazolilo, cada uno de los cuales está sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada R6 se selecciona, de modo independiente, de OH, F, Cl, Me, Et, Pr, /-Pr, f-Bu, -CF3 , -OMe, -OEt, -O/-Pr, -CN, ciclopropilo, pirrolidinilo, morfolinilo, piperidinilo y fenilo.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc, VId, VI Ic o VI Id, en donde R2 es arilo C6-10. En una realización preferida, R2 es fenilo.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc o VId, en donde R2 no es arilo C6-10. En una realización preferida, R2 no es fenilo.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc, VId, VI Ic o VI Id, en donde R2 es arilo C6-10 sustituido con uno o varios grupos R6 seleccionados de modo independiente. En una realización preferida, R2 es arilo C6-10 sustituido con uno o dos grupos R6 seleccionados de modo independiente. En una realización de mayor preferencia, R2 es arilo C6-10 sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de halo, CN, alquilo C1-6, alcoxi C1-6 y -NHC(=O)-alquilo C1-4. En otra realización de mayor preferencia, R2 es arilo C6-10 sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de -C(=O)NR9R10 y cada R9 y R10 se selecciona, de modo independiente, de H y alquilo C1-4. En otra realización de mayor preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente. En una realización de máxima preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de halo, CN, alquilo C1-6, alcoxi C1-6 y -NHC(=O)-alquilo C1-4. En otra realización de máxima preferencia, R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de -C(=O)NR9R10 y cada R9 y R10 se selecciona, de modo independiente, de H y alquilo C1-4. En otra realización de máxima preferencia R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de F, Cl, CN, Me, -OMe, -OEt, - y -NHC(=O)Me. En otra realización de máxima preferencia R2 es fenilo sustituido con uno o dos grupos R6 seleccionados de modo independiente, en donde cada grupo R6 se selecciona de C(=O)NH2 y -C(=O)NHMe.
En otra realización, el compuesto de la invención es de acuerdo con la fórmula Vc, Vd, VIc, VId, VIIc o VIId, en donde R2 no es arilo C6-10 sustituido con uno o varios grupos R6 seleccionados de modo independiente.
En una realización, el compuesto se selecciona de:
9-Aliloxi-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-piridin-3-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-piridin-4-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo,
3- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo,
4- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo,
[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-iloxi]-acetonitrilo,
2-([1,4]Dioxan-2-ilmetoxi)-9-(oxazol-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(piridin-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(3,5-Dicloro-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Benzofuran-2-il-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
éster ter-butílico del ácido 2-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-indol-1-carboxílico,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-indol-2-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(6-metoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(6-trifluorometil-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-3H-imidazol-4-iletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(5-ter-Butil-[1,2,4]oxadiazol-3-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
metilamida del ácido 5-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-piridin-2-carboxílico,
2-([1,4]Dioxan-2-ilmetoxi)-9-pent-1 -inil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-piridin-2-il-etil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-pirazin-2-il-etil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-indol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(5-metoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-indazol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2- ([1,4]Dioxan-2-ilmetoxi)-9-(4-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
3- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzamida,
5- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-2-fluoro-benzamida, N-{3-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-fenil}-acetamida, 9-Ciclopropiletinil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1-hidroxi-ciclopentiletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-pirimidin-5-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-Ciclohex-1-enil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-([1,4]Dioxan-2-ilmetoxi)-9-(1-metil-1 H-indol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(6-metil-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-piridin-2-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-([1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-pent-4-inonitrilo, -([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(4-metoxi-feniletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-piridin-3-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-N-metil-benzamida, -([1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-(2-cloro-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-([1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-(1,5-Dimetil-1 H-pirazol-3-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(1-metil-1 H-pirazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-[1,2,4]oxadiazol-5-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, - ([1,4]Dioxan-2-ilmetoxi)-9-(4-morfolin-4-il-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-4-fluoro-benzamida, -[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-5-fluoro-benzamida, -(3,3-Dimetil-but-1-inil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-piridin-4-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-isoxazol-5-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-metil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(2-metoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-(3,6-Dihidro-2H-piran-4-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, - [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-piridin-2-carbonitrilo, -([1,4]Dioxan-2-ilmetoxi)-9-(6-isopropoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(6-etoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(6-morfolin-4-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -(2,3-Dimetoxi-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
-(3-cloro-2-metoxi-piridin-4-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, - ([1,4]Dioxan-2-ilmetoxi)-9-(2-metil-piridin-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-isonicotinonitrilo, -(2,5-Dimetoxi-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, -([1,4]Dioxan-2-ilmetoxi)-9-(3,4,5,6-tetrahidro-2H-[1,2']bipiridinil-5'-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-- ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-etoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2,6-Dimetoxi-piridin-3-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
4-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-nicotinonitrilo,
9-ter-Butoximetil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-pirrolidin-1-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(6-pirrolidin-1-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(5-fenil-oxazol-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(5-ter-Butil-oxazol-2-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(5-Ciclopropil-[1,2,4]oxadiazol-3-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(5-etil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(5-metil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(5-isopropil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopentiletinil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclohexiletinil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-hex-1-inil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-[3-(Bencil-metil-amino)-prop-1-inil]-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-5-metil-hex-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-etil-3-hidroxi-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-fenil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(3-Bencilamino-prop-1-inil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-[(furan-2-ilmetil)-amino]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1-etil-1 H-pirazol-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-[1 -(3-metil-butil)-1 H-pirazol-4-il]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(5-metil-furan-2-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-hex-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(3,5-Dimetil-1 H-pirazol-4-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-pirazol-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1-propil-1 H-pirazol-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-[2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo, 2-[2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo,
9-(5-Ciclopropil-[1,2,4]oxadiazol-3-ilmetoxi)-2-((R)-1 -[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-etinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-pirimidin-2-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-fenilamino-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4] Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-piridin-3-il-prop-1 -inil)-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona, 9-Ciclopentiloximetil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclopropiletinil-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-(3-metil-but-1 -inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-imidazol-1 -il-prop-1 -inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(2-Ciclopropil-etil)-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopentiloximetil-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-piridin-3-il-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Aliloxi-2-((R)-1 -[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Aliloxi-2-((S)-1 -[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-4-iloximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-{3-[(piridin-3-ilmetil)-amino]-prop-1-inil}-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1 -[1,4]Dioxan-2-ilmetoxi)-9-pentil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropiletinil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2-Ciclopropil-etil)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(oxetan-3-iloximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metil-oxetan-3-ilmetoximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2,2-Dimetil-butilamino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-etil-hexilamino)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-metoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-etoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropilmetoxi-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-fluoro-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[3-(2-metoxi-etoxi)-prop-1 -inil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-[3-(2-etoxi-etoxi)-prop-1-inil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[3-(2-fluoro-etoxi)-prop-1 -inil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(2,2-Dimetil-propoximetil)-2-((S)-1 -[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclohexiloximetil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropilmetoximetil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(4,4-Dimetil-pentiloxi)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(3-Ciclopropil-propoxi)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclohexilamino-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4,4-dimetil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclopentilmetoximetil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-fenilamino-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(Ciclohexil-metil-amino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(Ciclohexilmetil-amino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-[(tetrahidro-piran-4-ilmetil)-amino]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-etil-3-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-metil-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2,2-Dimetil-propoxi)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-4-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-4-ilmetoximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-metoxi-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(oxetan-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(3-Ciclopropil-propoxi)-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[2-(1 -hidroxi-ciclopentil)-etil]-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona, 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-tetrahidro-piran-4-iletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
En una realización, el compuesto de la invención se selecciona de:
2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[2-(1 -hidroxi-ciclopentil)-etil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-propoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-isopropoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-propoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-isopropoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, and
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-metoxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
En una realización, el compuesto de la invención es 9-ciclopropiletinil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidropirimido[6,1-a]isoquinolin-4-ona.
En otra realización, el compuesto de la invención no es 9-ciclopropiletinil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidropirimido[6,1-a]isoquinolin-4-ona.
En una realización, un compuesto de la invención no es una variante isotópica.
En un aspecto, un compuesto de la invención está presente como la base libre.
En un aspecto, un compuesto de la invención es una sal farmacéuticamente aceptable.
En un aspecto un compuesto de la invención está presente como la base libre o una sal farmacéuticamente aceptable.
En un aspecto, un compuesto de la invención es un solvato.
En un aspecto, un compuesto de la invención es un solvato de una sal farmacéuticamente aceptable del compuesto.
En determinados aspectos, se proporcionan profármacos y derivados referenciales de un compuesto de la invención de acuerdo con la fórmula anterior. Los profármacos son derivados referenciales de un compuesto de la invención, que tienen grupos metabólicamente escindibles y por solvólisis o en condiciones fisiológicas, se vuelven los compuestos de la invención, que son farmacéuticamente activos, in vivo. Estos ejemplos incluyen, pero sin limitación, derivados de éster de colina, éster de N-alquilmorfolina.
Otros derivados de los compuestos de esta invención tienen actividad tanto en sus formas ácidas como de derivados ácidos, pero la forma ácida sensible a menudo ofrece ventajas de solubilidad, compatibilidad tisular o^ liberación demorada en el organismo de mamífero (ver Bundgard, H. Design of Prodrugs, pp. 7-9, 21-24, Elsevier, Ámsterdam 1985). Los profármacos como compuestos referenciales incluyen derivados ácidos bien conocidos por los expertos en la técnica tales como, por ejemplo, ésteres preparados por reacción del ácido principal con un alcohol apropiado o amidas preparadas por reacción del compuesto ácido principal con una amina no sustituida o anhídridos de ácido o anhídridos mixtos. Los ésteres alifáticos o aromáticos simples, amidas y anhídridos derivados de grupos ácidos pendientes de los compuestos de esta invención son profármacos referenciales preferidos. En algunos casos, es deseable preparar profármacos referenciales de tipo éster doble tales como ésteres de (aciloxi)alquilo o ésteres de ((alcoxicarbonil)oxi)alquilo. Son particularmente útiles el alquilo C1 a C8, alquenilo C2-C8 , arilo, arilo C7-C12 sustituido y ésteres de arilalquilo C7-C12 de los compuestos de la invención.
COMPOSICIONES FARMACÉUTICAS
Cuando se emplea como un producto farmacéutico, un compuesto de la invención se administra típicamente en forma de una composición farmacéutica. Tales composiciones se pueden preparar de una manera bien conocida en la técnica farmacéutica y comprenden al menos un compuesto activo. Generalmente, se administra un compuesto de la invención en una cantidad farmacéuticamente efectiva. La cantidad de un compuesto administrado realmente será determinada por un médico, a la luz de las circunstancias relevantes, que incluye la afección para tratar, la vía de administración elegida, el compuesto real administrado, la edad, el peso y la respuesta del paciente individual, la gravedad de los síntomas del paciente.
Las composiciones farmacéuticas de la invención se pueden administrar por una variedad de vías que incluyen oral, rectal, transdérmica, subcutánea, intraarticular, intravenosa, intramuscular, intranasal e inhalación. De acuerdo con la vía de administración deseada un compuesto de esta invención con preferencia se formula como composiciones inyectables u orales o como pomadas, como lociones o como parches, todos para administración transdérmica.
Las composiciones para administración oral pueden adoptar la forma de soluciones o suspensiones líquidas a granel, o polvos a granel. Más comúnmente, sin embargo, las composiciones se presentan en formas de dosis unitarias para facilitar una dosificación precisa. El término "formas de dosis unitarias" se refiere a unidades físicamente discretas adecuadas como dosis unitarias para sujetos humanos y otros mamíferos, cada unidad contiene una cantidad predeterminada de material activo calculada para producir el efecto terapéutico deseado, en asociación con un excipiente, vehículo o portador farmacéutico adecuado. Las formas de dosis unitarias típicas incluyen ampollas o jeringas premedidas, precargadas de las composiciones líquidas o pastillas, comprimidos, cápsulas o similares en el caso de composiciones sólidas. En tales composiciones, un compuesto de la invención es usualmente un componente menor (de aproximadamente 0,1 a aproximadamente 50% en peso o con preferencia de aproximadamente 1 a aproximadamente 40% en peso) con el resto que es varios vehículos o portadores y auxiliares de procesamiento útiles para formar la forma de dosis deseada.
Las formas líquidas adecuadas para la administración oral pueden incluir un vehículo acuoso o no acuoso adecuado con tampones, agentes de suspensión y dispensación, colorantes, sabores. Las formas sólidas pueden incluir, por ejemplo, cualquiera de los siguientes ingredientes o compuestos de naturaleza similar: un aglutinante tal como celulosa microcristalina, goma de tragacanto o gelatina; un excipiente tal como almidón o lactosa, un agente desintegrante tal
como ácido algínico, Primogel o almidón de maíz; un lubricante tal como estearato de magnesio; un deslizante tal como dióxido de silicio coloidal; un agente edulcorante tal como sacarosa o sacarina; o un agente saborizante tal como menta, salicilato de metilo o sabor a naranja.
Las composiciones inyectables se basan normalmente en solución salina estéril inyectable o solución salina tamponada con fosfato u otros portadores inyectables conocidos en la técnica. Como antes, el compuesto activo en tales composiciones es típicamente un componente menor, que es a menudo de aproximadamente 0,05 a 10% en peso, el resto es el portador inyectable.
Las composiciones transdérmicas se formulan típicamente como un ungüento o crema tópico que contiene el ingrediente activos, generalmente en una cantidad que varía de aproximadamente 0,01 a aproximadamente 20% en peso, con preferencia de aproximadamente 0,1 a aproximadamente 20% en peso, con preferencia de aproximadamente 0,1 a aproximadamente 10% en peso, y con más preferencia de aproximadamente 0,5 a aproximadamente 15% en peso. Cuando se formulan como ungüento, los ingredientes activos se combinarán típicamente con una base de ungüento parafínico o miscible con agua. Alternativamente, los ingredientes activos se pueden formular en una crema con, por ejemplo, una base de crema de aceite en agua. Tales formulaciones transdérmicas son bien conocidas en la técnica y generalmente incluyen ingredientes adicionales para mejorar la penetración dérmica o estabilidad de los ingredientes activos o la formulación. Todas estas formulaciones transdérmicas e ingredientes conocidos se incluyen dentro del alcance de esta invención.
También se puede administrar un compuesto de la invención mediante un dispositivo transdérmico. Por consiguiente, la administración transdérmica se puede llevar a cabo usando un parche del tipo de reservorio o membrana porosa, o de una variedad de matriz sólida.
Los componentes descritos anteriormente para las composiciones administrables por vía oral, inyectables o administrables por vía tópica son meramente representativos. Otros materiales así como las técnicas de procesamiento se exponen en la Parte 8 de Remington's Pharmaceutical Sciences, 17a edición, 1985, Mack Publishing Company, Easton, Pensilvania.
También se puede administrar un compuesto de la invención en formas de liberación sostenida o en sistemas de administración de fármacos de liberación sostenida. Se puede encontrar una descripción de materiales de liberación sostenida representativos en Remington's Pharmaceutical Sciences.
Los siguientes ejemplos de formulación ilustran composiciones farmacéuticas representativas que se pueden preparar de acuerdo con esta invención. La presente invención, sin embargo, no está limitada a las siguientes composiciones farmacéuticas.
Formulación 1 - Comprimidos
Un compuesto de la invención se puede mezclar como un polvo seco con un aglutinante de gelatina seca en una relación en peso aproximada de 1:2. Se puede añadir una menor cantidad de estearato de magnesio como un lubricante. La mezcla se puede formar en comprimidos de 240-270 mg (80-90 mg de compuesto de amida activo por comprimido) en una prensa de comprimidos.
Formulación 2 - Cápsulas
Un compuesto de la invención se puede mezclar como un polvo seco con un diluyente de almidón en una relación en peso aproximada de 1:1. La mezcla se puede llenar en cápsulas de 250 mg (125 mg de compuesto de amida activo por cápsula).
Formulación 3 - Líquido
Un compuesto de la invención (125 mg) se puede mezclar con sacarosa (1,75 g) y goma de xantano (4 mg) y la mezcla resultante se puede combinar, pasar a través de un tamiz U.S. de malla N.° 10 y luego se puede mezclar con una solución hecha previamente de celulosa microcristalina y carboximetilcelulosa sódica (11:89, 50 mg) en agua. Benzoato de sodio (10 mg), saborizante y colorante se pueden diluir luego con agua y añadir con agitación. Luego se puede añadir suficiente agua con agitación. Luego se puede añadir suficiente agua para producir un volumen total de 5 mL.
Formulación 4 - Comprimidos
Un compuesto de la invención se puede mezclar como un polvo seco con un aglutinate de gelatina seca en una relación en peso aproximada de 1:2. Se puede añadir una menor cantidad de estearato de magnesio como un lubricante. La mezcla se forma en comprimidos de 450-900 mg (150-300 mg de compuesto de amida activo) en una prensa de comprimidos.
Formulación 5 - Inyección
Un compuesto de la invención se puede disolver o suspender en un medio acuoso inyectable de solución salina estéril tamponada hasta una concentración de aproximadamente 5 mg/mL.
Formulación 6 - Tópico
Alcohol estearílico (250 g) y petrolato blanco (250 g) se puede fundir a aproximadamente 75 °C y luego se puede añadir una mezcla de un compuesto de la invención (50 g) metilparabeno (0,25 g), propilparabeno (0,15 g), laurilsulfato sódico (10 g) y propilenglicol (120 g) disuelto en agua (aproximadamente 370 g) y la mezcla resultante se puede agitar hasta que se congela.
En un aspecto, la presente invención proporciona el compuesto de la invención, o una composición farmacéutica que comprende el compuesto de la invención para usar en el tratamiento de la esclerosis múltiple.
Un régimen particular del presente método comprende la administración a un sujeto que sufre de una afección inflamatoria, de una cantidad efectiva de un compuesto de la invención durante un periodo de tiempo suficiente para reducir el nivel de inflamación en el sujeto, y con preferencia terminar, los procesos responsables de dicha inflamación. Una realización especial del método comprende la administración de una cantidad efectiva de un compuesto de la invención a un sujeto que sufre de o es susceptible al desarrollo de una afección inflamatoria, durante un período de tiempo suficiente para reducir o prevenir, respectivamente, la inflamación de dicho paciente, y con preferencia terminar, los procesos responsables de dicha inflamación.
Los niveles de dosis de inyección varían de aproximadamente 0,1 mg/kg/h hasta al menos 10 mg/kg/h, todos desde aproximadamente 1 a aproximadamente 120 h y especialmente de 24 a 96 h. También se puede administrar un bolo de precarga de aproximadamente 0,1 mg/kg a aproximadamente 10 mg/kg más para alcanzar niveles adecuados de estado estacionario. No se espera que la dosis total máxima exceda aproximadamente 2 g/día para un paciente humano de 40 a 80 kg.
Las dosis transdérmicas se seleccionan generalmente para proporcionar niveles sanguíneos similares o inferiores a los obtenidos usando dosis de inyección.
Cuando se usa para evitar el inicio de una afección, se administrará un compuesto de la invención a un paciente en riesgo de desarrollar la afección, típicamente bajo asesoramiento y supervisión de un médico, en los niveles de dosis descritos anteriormente. Los pacientes con riesgo de desarrollar una condición en particular generalmente incluyen aquellos que tienen antecedentes familiares de la afección, o los que han sido identificados por pruebas o análisis genéticos como particularmente susceptibles a desarrollar la afección.
A compuesto de la invención se puede administrar como el único agente activo o se puede administrar en combinación con otros agentes terapéuticos, que incluyen otros compuestos que demuestren la misma actividad terapéutica o similar y que se determina que son seguros y eficaces para dicha administración combinada. En una realización específica, la coadministración de dos (o más) agentes permite la utilización de dosis significativamente menores de cada uno, de este modo se reducen los efectos secundarios observados.
Por coadministración se incluye cualquier medio para suministrar dos o más agentes terapéuticos al paciente como parte del mismo régimen de tratamiento, como será evidente para los expertos en la técnica. Aunque los dos o más agentes se pueden administrar simultáneamente en una formulación única, esto no es esencial. Los agentes se pueden administrar en diferentes formulaciones y en diferentes momentos.
PROCEDIMIENTOS DE SÍNTESIS GENERALES
General
Se puede preparar un compuesto de la invención a partir de materiales de partida fácilmente disponibles usando los siguientes métodos y procedimientos generales. Se apreciará que cuando se dan condiciones de proceso típicas o preferidas (es decir, temperaturas de reacción, tiempos, relaciones molares de reactivos, solventes, presiones, etc.), pueden usarse otras condiciones del proceso a menos que se indique lo contrario. Las condiciones óptimas de reacción pueden variar con los reactivos o solventes particulares usados, pero tales condiciones pueden ser determinadas por un experto en la técnica mediante procedimientos de optimización de rutina.
Adicionalmente, como será evidente para los expertos en la técnica, pueden ser necesarios grupos protectores convencionales para evitar que ciertos grupos funcionales experimenten reacciones no deseadas. La elección de un grupo protector adecuado para un grupo funcional particular así como las condiciones adecuadas para la protección y desprotección son bien conocidas en la técnica. Por ejemplo, se describen numerosos grupos protectores, y su introducción y eliminación, en T. W. Greene y P. G. M. Wuts, Protecting Groups in Organic Synthesis, Wiley-Blackwell; 4a edición revisada (2006), y las referencias allí citadas.
Los siguientes métodos se presentan con detalles en cuanto a la preparación de 6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona representativa que se han enumerado anteriormente en la presente. Un compuesto de la invención se puede preparar a partir de materiales de partida y reactivos conocidos por un experto en la técnica de síntesis orgánica.
Todos los reactivos fueron de calidad comercial y se usaron tal como se recibieron sin purificación adicional, a menos que se indique lo contrario. Se usaron solventes anhidros comercialmente disponibles para las reacciones realizadas bajo atmósfera inerte. Se utilizaron solventes de grado reactivo en todos los demás casos, a menos que se especifique lo contrario. La cromatografía en columna se realizó sobre un estándar de sílice (30-70 gm). La cromatografía en capa fina se llevó a cabo usando placas de gel de sílice 60 F-254 pre-recubiertas (espesor 0,25 mm). Los espectros de 1H RMN se registraron en un espectrómetro Bruker Advance 400 RMN (400 MHz) o un espectrómetro Bruker Advance 300 NMR (300 MHz). Los desplazamientos químicos (5) para los espectros de 1H RMN se indican en partes por millón (ppm) con respecto al tetrametilsilano (5 0,00) o el pico de solvente residual apropiado como referencia interna. Las multiplicidades se dan como singlete (s), doblete (d), doblete de doblete (dd), triplete (t), cuarteto (q), multiplete (m) y ancho (br). Los espectros de MS electroaspersión se obtuvieron en un espectrómetro LC/MS de plataforma Waters o en un Lc /m SD Agilent Serie 1100. LCMS analítico: Columnas usadas, UPLC Waters Acquity BEH C18 1,7 gm, 2,1 mm ID x 50 mm L o UPLC Waters Acquity BEH C18 1,7 gm, 2,1 mm ID x 30 mm L o Waters XBridge C183,5 gm, 2,1 mm ID x 50 mm L. Todas los métodos están usando gradientes de MeCN/H2O. MeCN y H2O contienen ácido fórmico 0,1% o NH3 (10 mM). LCMS preparativa: Columna utilizada, Waters XBridge Prep C185 gm ODB 30 mm ID x 100 mm L. Todos los métodos están usando gradientes MeOH/H2O o MeCN/H2O. MeOH, MeCN y H2O contienen ácido fórmico 0,1% o dietilamina 0,1%. Quiral analítico LC: Columna utilizada, Chiralpak IA 5 gm 250 x 4,6 mm. El calentamiento por microondas se realizó con un iniciador Biotage.
Tabla I: Listado de las abreviaturas usadas en la sección experimental:
MÉTODO DE SÍNTESIS GENERAL
Intermedios
Los intermedios para preparar los compuestos de acuerdo con la invención se pueden producir de acuerdo con los siguientes esquemas.
Intermediario 1 Intermediario 2
Intermedio 1: [2-(3-metox¡-fenil)-et¡l]-urea
Una solución de 3-metoxifenetilamina (100 g, 661,3 mmol, 1 eq.), urea (157,3 g, 2619,0 mmol, 4 eq.), AcOH (36 mL) y HCl ac. (12 mL) en H2O (800 mL) se calentó a reflujo durante 5 días. La mezcla de reacción se enfrió a temperatura ambiente, el sólido se filtró, se lavó con agua y se secó para obtener el intermedio 1.
(1H, CDCh) 5 (ppm): 7,24 (1H, t), 6,82-6,77 (3H, m), 5,10 (1H, br s), 4,52 (2H, br), 3,81 (1H, s), 3,42 (2H, br t), 2,80 (2H, t)
Intermedio 2: [2-(3-hidroxi-fenil)-etil]-urea
Una solución del intermedio 1 (72 g, 370,7 mmol) en HBr concentrado (500 mL) se calentó a reflujo durante la noche. La mezcla de reacción se llevó a pH básico por adición de NaHCO3 y se extrajo con EtOAc. La capa orgánica se secó sobre MgSO4 y se concentró al vacío para obtener el intermedio 2.
(1H, MeOD-d4) 5 (ppm): 7,15 (1H, t), 6,76-6,68 (3H, m), 3,40-3,36 (2H, t), 2,77-2,74 (2H, t)
Intermedio 3: [2-(3-aliloxi-fenil)-etil]-urea
A una solución del intermedio 2 (45 g, 249,7 mmol, 1 eq.) y K2CO3 (103,5 g, 749,1 mmol, 3 eq.) en DMF anhidra (300 mL) bajo una atmósfera de nitrógeno, se añadió bromuro de alilo (50,5 mL, 499,4 mmol, 2 eq.). La mezcla de reacción se agitó durante 2,5 días, luego DMF se evaporó hasta sequedad. El residuo se disolvió en EtOAc, se lavó con Na2CO3 saturado, salmuera, se secó sobre MgSO4 y se concentró al vacío para obtener el intermedio 3.
(1H, MeOD-d4) 5 (ppm): 7,24 (1H, t), 6,87-6,81 (3H, m), 6,16-6,06 (1H, m), 5,45 (1H, dd), 5,29 (1H, dd), 4,59-4,57 (2H, m), 3,38 (2H, t), 2,80 (2H, t)
Intermedio 4: 1 -[2-(3-aliloxi-fenil)-etil]-pirimidin-2,4,6-triona
Sodio (20,06 g, 872 mmol, 1 eq.) se disolvió en EtOH (1,4 L). Malonato de dietilo (132,4 mL, 872 mmol, 1 eq.) se añadió y la mezcla de reacción se calentó a reflujo durante 1 h. El intermedio 3 (96 g, 436 mmol, 0,5 eq.) en EtOH (300 mL) se añadió y la mezcla de reacción se calentó a reflujo durante 12 h. La reacción se enfrió a temperatura ambiente, HCl ac. 1 N se añadió y el precipitado se filtró, se lavó con agua y se secó para obtener el intermedio 4. (1H, CDCla) 5 (ppm): 8,40 (1H, br s), 7,25 (1H, t), 6,88-6,82 (3H, m), 6,14-6,04 (1H, m), 5,45 (1H, dd), 5,32 (1H, dd), 4,58-4,56 (2H, m), 4,13 (2H, t), 3,64 (2H, s), 2,92 (2H, t)
MW (calc.): 288,3; MW (obs.): 289,3 (M 1)
Intermedio 5: 9-aliloxi-2-cloro-6,7-dihidro-pirimido[6,1-a]isoquinotin-4-ona
Una solución del intermedio 4 (20 g, 69,4 mmol, 1 eq.) en POCh (150 mL) se agitó a 50 °C durante 3 días. POCl3 se evaporó al vacío y el residuo se disolvió en DCM y se neutralizó con NaHCO3 saturado. La capa orgánica se lavó con agua, se secó sobre MgSO4 y se concentró para obtener el intermedio 5.
(1H, CDCla) 5 (ppm): 7,71 (2H, d), 6,97 (1H, dd), 6,86 (1H, d), 6,71 (1H, s), 6,13-6,04 (1H, m), 5,47 (1H, dd), 5,36 (1H, dd), 4,67-4,65 (2H, m), 4,27 (2H, t), 3,05 (2H, t)
MW (calc.): 288,7; MW (obs.): 289,3 (M+1)
Métodos generales
Método general A:
A una solución de NaH (2 eq., 60% en aceite mineral) en DCM anhidra a 0 °C, se añade 2-hidroximetil-[1,4]dioxano (2 eq.) con la quiralidad apropiada, después de 15 min, el intermedio 5 (1 eq.) se añade a 0 °C y la reacción se agita a temperatura ambiente hasta completar. NH4Cl saturado se añade a la mezcla de reacción, la capa orgánica se lava con agua, se seca sobre MgSO4 y se concentra. El producto deseado se purifica por cromatografía flash en gel de sílice.
2-Hidroximetil-[1,4]dioxano, (R) 2-hidroximetil-[1,4]dioxano y (S) 2-hidroximetil-[1,4]dioxano son asequibles en comercios o se pueden preparar con facilidad [Young Kim et al; Bioorganic & Medicinal Chemistry 15 (2007) 2667 2679].
Síntesis ilustrativa del método general A:
Compuesto 118: 9-aliloxi-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona Una solución de (R) 2-hidroximetil-[1,4]dioxano (56,6 g, 479 mmol, 2 eq.) y NaH (19,9 g, 479 mmol, 2 eq., 60% en aceite mineral) en DCM anhidra (300 mL) se agitó durante 30 min a 0 °C. El intermedio 5 (69,2 g, 240 mmol, 1 eq.) en solución en DCM anhidra (700 mL) se añadió a 0 °C. La mezcla de reacción se agitó durante 2 h. Saturated NH4Cl se añadió, la capa orgánica se lavó con agua, se secó sobre MgSO4 y se evaporó hasta sequedad. El producto crudo se purificó por cromatografía flash en gel de sílice (MeOH/DCM) para obtener el compuesto 118.
(1H, CDCI3) 5 (ppm): 7,66 (1H, d), 6,94 (1H, dd), 6,83 (1H, d), 6,32 (1H, s), 6,15-6,03 (1H, m), 5,47 (1H, dd), 5,37 (1H, dd), 4,65-4,63 (2H, m), 4,51-4,39 (2H, m), 4,23 (2H,t), 4,06-3,98 (1H, m), 3,92-3,47 (6H, m), 3,01 (2H, t) Compuesto 1: 9-al¡lox¡-2-(-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
El compuesto 1 se preparó usando el método general A a partir de 2-hidroximetil-[1,4]dioxano.
(1H, CDCla) 5 (ppm): 7,66 (1H, d), 6,94 (1H, dd), 6,83 (1H, d), 6,32 (1H, s), 6,11-6,04 (1H, m), 5,47 (1H, dd), 5,35 (1H, dd), 4,65-4,63 (2H, m), 4,491 -4,40 (2H, m), 4,22 (2H, t), 4,02-3,99 (1H, m), 3,90-3,46 (6H, m), 3,00 (2H, t)
MW (calc.): 370,4; MW (obs.): 371,4 (M+1)
Compuesto 117: 9-all¡tox¡-2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona El compuesto 117 se preparó usando el método general A a partir de (S) 2-hidroximetil-[1,4]dioxano.
(1H, CDCla) 5 (ppm): 7,66 (1H, d), 6,94 (1H, dd), 6,83 (1H, d), 6,31 (1H, s), 6,12-6,04 (1H, m), 5,49 (1H, dd), 5,36 (1H, dd), 4,65-4,63 (2H, m), 4,50-4,42 (2H, m), 4,23 (2H, t), 4,04-4,00 (1H, m), 3,91-3,50 (6H, m), 3,01 (2H, t)
MW (calc.): 370,4; MW (obs.): 371,2 (M+1)
Método general B:
A una suspensión del compuesto 1, 117 ó 118 (1 eq.) en una mezcla de DCM/MeOH (1/1) se añade K2CO3 (2 eq.) y Pd(PPha)4 (0,05 eq.). La mezcla de reacción se desgasifica antes de agitar a temperatura ambiente. Después de completar, se añade agua a la mezcla de reacción y la capa acuosa se separa. El pH de la solución acuosa se ajusta hasta pH 1 con HCl acuoso 2 M. El precipitado se filtra, se lava con agua y se seca para obtener el intermedio 6, 7 u 8.
Síntesis ilustrativa del método general B:
Intermed¡o 6: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-h¡drox¡-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
A una suspensión del compuesto 118 (31,15 g, 84,2 mmol, 1 eq.) en una mezcla de DCM/MeOH (1/1, 800 mL) se añadió feC03 (23,2 g, 138,2 mmol, 2 eq.) y Pd(PPh3)4(4,86 g, 4,21 mmol, 0,05 eq.). La mezcla de reacción se agitó a temperatura ambiente durante 2 h. Agua (800 mL) se añadió y la capa acuosa se separó. El pH de la solución acuosa se ajusta hasta pH 1 con HCl acuoso 2 M. El precipitado se filtró, se lavó con agua y se secó para obtener el intermedio 6.
(1H, DMS0-d6) 5 (ppm): 7,84 (1H, d), 6,77 (1H, dd), 6,74 (1H, d), 6,45 (1H, s), 4,25-4,23 (2H, m), 3,99 (2H, t), 3,87 3,75 (3H, m), 3,68-3,58 (2H, m), 3,52-3,46 (1H, m), 3,40-3,30 (1H, m), 2,91 (2H, t)
MW (calc.): 330,4; MW (obs.): 331,3 (M+1)
Intermed¡o 7: 2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-h¡drox¡-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
El intermedio 7 se preparó usando el método general B a partir del compuesto 117.
(1H, DMS0-d6) 5 (ppm): 7,83 (1H, d), 6,77 (1H, dd), 6,74 (1H, d), 6,44 (1H, s), 4,27-4,20 (2H, m), 3,98 (2H, t), 3,87 3,74 (3H, m), 3,68-3,57 (2H, m), 3,52-3,46 (1H, m), 3,40-3,34 (1H, m), 2,91 (2H, t)
Intermedio 8: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-h¡drox¡-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soquinol¡n-4-ona El intermedio 8 se preparó usando el método general B a partir del compuesto 1.
(1H, DMSO-d6) 5 (ppm): 7,84 (1H, d), 6,77 (1H, dd), 6,74 (1H, d), 6,45 (1H, s), 4,27-4,20 (2H, m); 3,99 (2H, t), 3,88 3,73 (3H, m), 3,68-3,58 (2H, m), 3,52-3,46 (1H, m), 3,40-3,34 (1H, m), 2,91 (2H, t)
MW (calc.): 330,4; MW (obs.): 331,0 (M+1)
Método general C:
Una solución del intermedio 6, 7 u 8 (1 eq.), N-fenil-bis(trifluorometansulfonimida) (1,2 eq.) y Et3N (1,3 eq.) en DCM bajo nitrógeno se agita a temperatura ambiente hasta completar. La mezcla de reacción se concentra y el producto crudo se purifica por cristalización en /'PrOH para obtener el intermedio 9, 10 u 11.
Síntesis ilustrativa del método general C:
Intermed¡o 9: éster 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-ílico del ácido trifluoro-metansulfónico
Una solución del intermedio 6, (24 g, 72,7 mmol, 1 eq.), N-fenil-bis(trifluorometansulfonimida) (31,15 g, 87,2 mmol, 1,2 eq.) y Et3N (13,2 mL, 94,4 mmol, 1,3 eq.) en DCM (700 mL) bajo una atmósfera de nitrógeno se agita a temperatura ambiente durante la noche. La mezcla de reacción se concentra. El producto crudo se extrae en /PrOH (75 mL) calentado a reflujo y se enfría a temperatura ambiente. Después de dos días a temperatura ambiente, el sólido se filtra y se seca para obtener el intermedio 9.
(1H, CDCh) 5 (ppm): 7,83 (1H, d), 7,35 (1H, dd), 7,29 (1H, d), 6,41 (1H, s), 4,51-4,42 (2H, m), 4,28 (2H, t), 4,06-4,01 (1H, m), 3,89-3,69 (5H, m), 3,52 (1H, m), 3,11 (2H, t)
Intermedio 10: éster 2-((R)-1-[1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-ílico del ácido trifluoro-metansulfónico
El intermedio 10 se preparó usando el método general C a partir del intermedio 7.
(1H, CDCh) 5 (ppm): 7,83 (1H, d), 7,34 (1H, dd), 7,29 (1H, d), 6,41 (1H, s), 4,51-4,41 (2H, m), 4,28 (2H, t), 4,05-4,00 (1H, m), 3,91-3,66 (5H, m), 3,52 (1H, t), 3,11 (2H, t)
Intermedio 11: éster 2-([1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-ílico del ácido trifluoro-metansulfónico
El intermedio 11 se preparó usando el método general C a partir del intermedio 8.
(1H, DMSO-d6) 5 (ppm): 8,21 (1H, d), 7,65 (1H, d), 7,54 (1H, dd), 6,75 (1H, s), 4,28-4,26 (2H, m), 4,04 (2H, t), 3,90 3,84 (1H, m), 3,81-3,75 (2H, m), 3,68-3,58 (2H, m), 3,53-3,47 (1H, m), 3,41-3,36 (1H, m), 3,10 (t, 2H)
MW (calc.): 462,4; MW (obs.): 463,3 (M+1)
Intermedio 13: clorhidrato de 9-amino-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
Etapa 1: 9-(Benzhidriliden-amino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 12)
Una solución del intermedio 9 (1 g, 2,16 mmol, 1 eq.), Pd(OAc)2 (24 mg, 0,11 mmol 0,05 eq.), Cs2CO3 (2,11 g, 6,48 mmol, 3 eq.) BINAP (134 mg, 0,21 mmol, 0,1 eq.) y benzofenonimina (587 mg, 3,24 mmol, 1,5 eq.) en tolueno (20 mL)
se calentó a 150 °C en un microondas durante 45 min. El solvente se evaporó hasta sequedad y la mezcla cruda se extrajo en agua y se extrajo con EtOAc. La capa orgánica se secó sobre MgSO4 y se concentró al vacío. El intermedio 9-(Benzhidriliden-amino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona 12 se obtuvo después de la purificación por cromatografía flash en gel de sílice y se usó de inmediato en la siguiente etapa. Etapa 2: clorhidrato de 9-amino-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (intermedio 13)
A una solución del intermedio 12 en un mínimo de DCM/ Et2O se añadió HCl 2 N en Et2O (4 mL). El precipitado se filtró y se secó para obtener el intermedio 13.
(1H, DMSO-d6) 5 (ppm): 7,82 (1H, d), 7,45 (3H, br), 6,68 (1H, d), 6,67 (1H, s), 6,51 (1H, s), 4,32 (2H, d), 3,99 (2H, t), 3,90-3,84 (1H, m), 3,82-3,35 (6H, m), 2,88 (2H, t)
MW (calc.): 329,4; MW (obs.): 330,2 (M+1)
Método general D:
^O H Brw BF,K _____ „ . 0 . .BF,K
El alcohol correspondiente (2 eq.) se añade a una solución de NaH (2 eq., 60% en aceite mineral) en THF a 0 °C. La reacción se calienta a temperatura ambiente durante 30 min, luego se enfría otra vez a 0 °C. Metiltrifluoroborato de boro (1 eq.) se añade a la reacción en una porción y la mezcla se agita a temperatura ambiente desde algunas horas hasta 3 días (controlado por 19F-RMN). La reacción se neutraliza con una solución de KHF2 (1,5 M, 3 eq.) y la mezcla se evapora hasta sequedad. El residuo se suspende en acetona, las capas inorgánicas se filtran y el filtrado se evapora hasta sequedad. El residuo se suspende en una cantidad mínima de acetona, se añade Et2O y el producto se obtiene por filtración.
Síntesis ilustrativa del método general D:
Intermedio 14: trifluoroborato de tetrahidro-2H-piran-4-ol-metilo
intermedio 14
Tetrahidro-piran-4-ol (152 mg, 1,49 mmol, 2 eq.) se añadió a una solución de NaH (60 mg, 1,49 mmol, 2 eq., 60% en aceite mineral) en THF (4 mL) a 0 °C. La reacción se calentó a temperatura ambiente durante 30 min, luego se volvió a enfriar otra vez a 0 °C. Metiltrifluoroborato de bromo (150 mg, 0,75 mmol, 1 eq.) se añadió a la reacción en una porción y la mezcla se agitó a temperatura ambiente durante 1 día (controlado por 19F-RMN). La reacción se neutralizó con una solución de KHF2 (1,5 mL, 1,5 M, 3 eq.) y la mezcla se evaporó hasta sequedad. El residuo se suspendió en acetona, las capas inorgánicas se filtraron y el filtrado se evaporó hasta sequedad. El residuo se suspendió en una cantidad mínima de acetona (1,5 mL) y Et2O (6 mL) se añadió. El intermedio 14 se obtuvo por filtración.
(1H, DMSO-ds) 5 ppm 3,78 (2 H, d), 3,31 - 3,21 (2 H, m), 3,18 - 3,08 (1 H, m), 2,50 - 2,45 (2 H, m), 1,86 - 1,74 (2 H, m), 1,34 - 1,19 (2 H, m)
Intermedio 15: 3-oxi-oxetanmetiltrifluoroborato de potasio
intermedio 15
El intermedio 15 se preparó por medio del método general D con oxetan-3-ol (el reactivo de trifluoroborato se recuperó con las capas inorgánicas más que el filtrado).
(1H, DMSO-ds) 5 ppm 4,56 (2 H, s), 4,32 (3 H, d), 2,40 (2 H, d)
Intermedio 16: (3-metil-3-met¡lox¡-oxetan-met¡ltr¡fluoroborato de potasio
intermedio 16
Intermedio 16 se preparó por medio del método general D con (3-metiloxetan-3-il)metanol (el reactivo de trifluoroborato se recuperó con las capas inorgánicas más que el filtrado).
(1H, DMSO-afe) 5 ppm 4,34 (2 H, d), 4,14 (2 H, d), 3,26 (2 H, s), 2,59 - 2,52 (2 H, m), 1,19 (3 H, s)
Intermedio 17: 2,2-dimetil-propiloxi-metiltrifluoroborato de potasio
intermedio 17
El intermedio 17 se preparó por medio del método general D con 2,2-dimetil-propan-1-ol.
(1H, DMSO-afe) 5 ppm 2,88 (2 H, s), 2,51 - 2,45 (2 H, m), 0,83 (9 H, s)
Intermedio 18: ciclopropilmetoxi-metiltrifluoroborato de potasio
intermedio 18
El intermedio 18 se preparó por medio del método general D con ciclopropil-metanol.
(1H, DMSO-afe) 5 ppm 3,00 (2 H, d), 2,46 (2 H, d), 1,00 - 0,82 (1 H, m), 0,46 - 0,31 (2 H, m), 0,13 - 0,00 (2 H, m) Intermedio 19: ciclopentilmetoxi-metiltrifluoroborato
intermedio 19
El intermedio 19 se preparó por medio del método general D con ciclopentil-metanol.
(1H, DMSO-afe) 5 ppm 3,04 (2 H, d), 2,46 (2 H, d), 2,08 - 1,94 (1 H, m), 1,47 (6 H, br. s.), 1,07 - 1,22 (2 H, m) Intermedio 20: 2-ciclopropil-etil-trifluoroborato de potasio
intermedio 20
Un recipiente de base redonda de 2 bocas equipado con un condensador de reflujo y un embudo de adición se cargó con Mg (193 mg, 8,05 mmol, 3 eq.) y Et2O (1 mL) bajo N2. Una gota de (2-bromo-etil)-ciclopropano puro se añadió seguido por dos gotas de dibromoetano. Una vez que aparecieron las primeras burbujas, (2-bromoetil)-ciclopropano (400 mg, 2,68 mmol, 1 eq.) en Et2O (5 mL) se añadió gota a gota. Después de completar la adición, la suspensión
resultante se agitó a temperatura ambiente durante 1 h. En un recipiente separado, purgad con N2 , una solución hecha de B(OMe)3 (0,45 mL, 4,02 mmol, 1,5 eq.) en THF (6 mL) se enfrió hasta -78 °C. A esta solución, la suspensión de bromuro de 2-ciclopropil-etilmagnesio se añadió gota a gota por medio de una aguja de doble extremo. La mezcla se dejó agitar durante 1 h a -78 °C y luego se calentó a temperatura ambiente durante 1 h. Después de enfriar la mezcla hasta 0 °C, una solución acuosa saturada de KHF2 (2,5 mL, 4,5 M, 4,1 eq.) se añadió gota a gota y la mezcla de reacción se dejó calentar a temperatura ambiente. Después de 30 min, la solución se concentró al vacío. Los sólidos secos se trituraron con acetona caliente y se filtró para remover sales inorgánicas. El filtrado resultante se concentró y el residuo sólido se trituró con Et2O. 2-ciclopropil-etil-trifluoroborato de potasio se filtró y se secó al vacío.
(1H, DMSO-afe) 5 ppm 1,07 - 0,92 (2 H, m), 0,66 - 0,53 (1 H, m), 0,27 - 0,21 (2 H, m), 0,067 - -0,07 (2 H, m), -0,117 - -0,17 (2 H, m)
Método general E:
intermedio 9, 10, 11
Un vial se carga con el intermedio 9, 10 u 11 (1 eq.), el ácido borónico apropiado, éster borónico o trifluoroborato de potasio (4,4 eq.), Cs2CO3 (2,6 eq.), (DPPF)PdCh.DCM (0,05 eq.), en 1,4-dioxano/H2O (10/1, v/v) y la mezcla se desgasifica con N2. El vial se sella y se calienta hasta 80 °C. Cuando la reacción se completa, el vial se enfría a temperatura ambiente y la reacción se elabora o las sustancias volátiles se evaporan al vacío. El producto luego se obtiene después de la purificación por cromatografía flash en gel de sílice, TLC preparativa o HPLC-MS preparativa.
Síntesis ilustrativa del método general E:
Compuesto 2: 2-([1,4]dioxan-2-ilmetoxi)-9-piridin-3-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
intermedio 11 Compuesto 2
Un vial se cargó con el intermedio 11 (84 mg, 0,074 mmol, 1 eq.), ácido piridin-3-borónico (40 mg, 0,327 mmol, 4,4 eq.), Cs2CO3 (62 mg, 0,190 mmol, 2,6 eq.), (DPPF)PdCl2.DCM (3,3 mg, 0,004 mmol, 0,05 eq.), en 1,4-dioxano (1 mL) y H2O (0,1 mL) y la mezcla se desgasificó con N2. El vial se selló y se calentó hasta 80 °C. Después de 1 h, el vial se enfrió a temperatura ambiente y las sustancias volátiles se evaporaron al vacío. El residuo luego se purificó por cromatografía flash en gel de sílice, eluyendo con 7,5% de MeOH/DCM para obtener el compuesto 2.
(1H, CDCla) 5 ppm 8,89 (1 H, s), 8,67 (1 H, d), 7,93 (1 H, d), 7,82 (1 H, d), 7,61 (1 H, d), 7,53 (1 H, s), 7,43 (1 H, dd), 6,43 (1 H, s), 4,51 - 4,37 (2 H, m), 4,26 (2 H, t), 3,99 (1 H, m), 3,92 - 3,60 (5 H, m), 3,49 (1 H, m), 3,10 (2 H, t)
Método general F:
Una solución del intermedio 6, 7 u 8 (1 eq.), el agente alquilante apropiado (1,5 eq.), K2CO3 (2 eq.), KI (1 eq.) en MEK se calienta a 80 °C. Cuando la reacción se completa, los compuestos volátiles se evaporan hasta sequedad y el residuo se purifica por cromatografía flash en gel de sílice para dar el producto deseado.
Síntesis ilustrativa del método general F:
Compuesto 8: 2-([1,4]dioxan-2-ilmetoxi)-9-(oxazol-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
intermedio 8 Compuesto 8
Una solución del intermedio 8 (40 mg, 0,12 mmol, 1 eq.), 2-clorometiloxazol (21 mg, 0,18 mmol, 1,5 eq.), K2CO3 (33 mg, 0,24 mmol, 2 eq.), KI (20 mg, 0,12 mmol, 1 eq.) en MEK (2 mL) se calentó a 80 °C durante 16 h. La reacción se evaporó hasta sequedad y el residuo se purificó por cromatografía flash en gel de sílice, eluyendo con 4% de MeOH/DCM para dar el compuesto 8.
(1H, CDCh) 5 ppm 7,72 (1 H, d), 7,68 - 7,60 (1 H, m), 7,18 (1 H, d), 7,02 (1 H, dd), 6,93 (1 H, d), 6,28 (1 H, s), 5,23 (2 H, s), 4,49 - 4,33 (2 H, m), 4,19 (2 H, t), 4,02 - 3,94 (1 H, m), 3,89 - 3,61 (5 H, m), 3,48 (1 H, dd), 2,98 (2 H, t) MW (calc.): 411,4; MW (obs.): 412,4 (M+1)
Método general G:
El intermedio 9, 10, 11 (1 eq.) se disuelve en DMF, el alquino apropiado (3 eq.) se añade seguido por TEA (3,5 eq.) y la mezcla se desgasifica. Pd(PPh3)3Cl2 (0,05 eq.) se añade con CuI (0,2 eq.) y la mezcla de reacción se calienta a 80 °C. Cuando la reacción se completa, se enfría a temperatura ambiente y o bien se elabora o las sustancias volátiles
se evaporan hasta sequedad. El producto luego se obtiene después de la purificación por cromatografía flash en gel de sílice, TLC preparativa o HPLC-MS preparativa.
Síntesis ilustrativa del método general G:
Compuesto 16: 2-([1,4]dioxan-2-ilmetoxi)-9-(1-metil-1H-imidazol-2-iletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
El intermedio 11 (1,4 g, 3,03 mmol, 1 eq.) se disolvió en DMF (20 mL), 5-etinil-1 -metil-1 H-imidazol (0,92 mL, 9,09 mmol, 3 eq.) se añadió seguido por TEA (1,48 mL, 10,61 mmol, 3,5 eq.). La mezcla se desgasificó y Pd(PPh3)3Cl2 (106 mg, 0,15 mmol, 0,05 eq.) se añadió con CuI (115 mg, 0,61 mmol, 0,2 eq.). La mezcla de reacción se calentó a 80 °C durante 16 h. La reacción se enfrió a temperatura ambiente y se neutralizó con salmuera, la mezcla luego se extrajo con EtOAc. La capa orgánica se secó sobre MgSO4 y el solvente se evaporó al vacío. El producto crudo luego se purificó por cromatografía flash en gel de sílice, eluyendo del 0 al 5% de MeOH/DCM para dar el compuesto 16. (1H, CDCl3) 5 ppm 7,73 (1 H, d), 7,57 - 7,50 (2 H, m), 7,48 - 7,45 (1 H, m), 7,42 (1 H, d), 6,42 (1 H, s), 4,53 - 4,39 (2 H, m), 4,28 - 4,23 (2 H, m), 4,07 - 3,97 (1 H, m), 3,94 - 3,64 (8 H, m), 3,52 (1 H, dd), 3,06 (2 H, t)
MW (calc.): 418,4; MW (obs.): 419,4 (M+1)
Método general H:
tBuOK (3 eq.) se añade a una solución del correspondiente alcohol acetilénico (1 eq.) en THF, luego se añade MeI (10 eq.) y la reacción se agita a temperatura ambiente. Cuando la reacción se completó, la mezcla de reacción se filtra y el filtrado se evapora hasta sequedad. El producto se obtiene después de la purificación por TLC preparativa. Síntesis ilustrativa del método general H:
Compuesto 110: 2-([1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pent-1-inil)-6,7-dihidropirimido[6,1-a]isoquinolin-4-ona
Compuesto 91 Compuesto 110
tBuOK (5,19 mg, 0,046 mmol, 0,95 eq.) se añadió a una solución del compuesto 90 (20 mg, 0,049 mmol, 1 eq.) en THF (2 mL), MeI (0,030 mL, 0,487 mmol, 10 eq.) luego se añadió y la reacción se agitó a temperatura ambiente durante 16 h. Algo más de tBuOK (11 mg, 0,097 mmol, 2 eq.) se añadió y la reacción se agitó durante un día extra. La mezcla de reacción se filtró y el filtrado se evaporó hasta sequedad. El producto crudo se purificó por TLC preparativa eluyendo con el 2% de MeOH/DCM para obtener el compuesto 110.
(1H, CDCla) 5 ppm 7,70 - 7,60 (1 H, d), 7,50 - 7,42 (1 H, d), 7,39 (1 H, s), 6,37 (1 H, s), 4,50 - 4,35 (2 H, m), 4,25 - 4,15 (2 H, m), 4,05 - 3,95 (2 H, m), 3,92 - 3,60 (5 H, m), 3,56 - 3,45 (4 H, m), 3,05 - 3,95 (2 H, m), 2,15 - 1,95 (1 H, m), 1,15 - 1 (6 H, t)
MW (calc.): 424,5; MW (obs.): 425,2 (M+1)
Método general I:
Un vial se carga con Pd/C (10% p/p) y una solución del alquino apropiado (1 eq.) en MeOH se añade. El sistema se purga con N2 antes de llenar con H2 , luego la reacción se agita a temperatura ambiente hasta completar. La reacción se filtra a través de Celite y el filtrado se evapora hasta sequedad. El producto limpio se obtiene después de la purificación por cromatografía flash en gel de sílice, TLC preparativa o HPLC-MS preparativa.
Síntesis ilustrativa del método general I:
Compuesto 116: 2-([1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-3-piridin-3-il-propil)-6,7-dihidropirimido[6,1-a]isoquinolin-4-ona
Un vial se cargó con Pd/C (9 mg, 10% p/p) y una solución del compuesto 108 (87 mg 0,20 mmol, 1 eq.) en MeOH (10 mL) se añadió. El sistema se purgó con N2 antes de llenar con H2 , luego la reacción se agitó durante 16 h a temperatura ambiente. La reacción se filtró a través de Celite y el filtrado se evaporó hasta sequedad. El producto crudo se purificó por HPLC-MS preparativa para dar el compuesto 116.
(1H, CDCla) 5 ppm 8,60 - 8,48 (2 H, m), 7,73 (1 H, d), 7,61 (1 H, d), 7,30 (1 H, dd), 7,20 (1 H, d), 7,12 (1 H, s), 6,35 (1 H, s), 4,77 (1 H, dd), 4,47 - 4,33 (2 H, m), 4,18 (2 H, t), 3,97 (1 H, m), 3,90 - 3,60 (5 H, m), 3,48 (1 H, t), 2,96 (2 H, t), 2,90 - 2,70 (2 H, m), 2,15 (1 H, m), 2,10 - 1,98 (1 H, m), 1,38 (1 H, t)
MW (calc.): 449,5; MW (obs.): 450,1 (M+1)
Método general J:
El intermedio 13 (1 eq.) se disuelve en DMF, el aldehído apropiado (4 eq.) se añade seguido por KOH (1 eq.). La reacción se agita durante 15 min a temperatura ambiente antes de añadir STAB (10 eq.), la mezcla luego se agita a temperatura ambiente hasta completar la reacción. La mezcla luego se neutraliza con salmuera, se extrae con EtOAc, la capa orgánica se seca sobre MgSO4 y se evapora hasta sequedad. La purificación por HPLC-MS preparativa da como resultado el correspondiente producto.
Síntesis ilustrativa del método general J:
Compuesto 126: 9-(2,2-dimetil-butilamino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
intermedio 13 Compuesto 126
El intermedio 13 (50 mg, 0,14 mmol, 1 eq.) se disolvió en DMF (2 mL), 2,2-dimetilbutanal (56 mg, 0,56 mmol, 4 eq.) se añadió seguido por KOH (8 mg, 0,14 mmol, 1 eq.). La reacción se agitó durante 15 min a temperatura ambiente antes de añadir STAB (297 mg, 1,40 mmol, 10 eq.), la mezcla luego se agitó durante 2 días a temperatura ambiente. La reacción se neutralizó con salmuera y la mezcla se extrajo con EtOAc. La capa orgánica se secó sobre MgSO4 y se evaporó hasta sequedad. El producto crudo se purificó por HPLC-MS preparativa para dar el compuesto 126.
(1H, CDCla) 5 ppm 7,50 (1 H, d), 6,63 (1 H, dd), 6,48 (1 H, s), 6,21 (1 H, s), 4,47 - 4,34 (2 H, m), 4,21 - 4,14 (2 H, m), 4,01 - 3,91 (1 H, m), 3,89 - 3,60 (5 H, m), 3,48 (1 H, dd), 2,98 (2 H, s), 2,90 (2 H, t), 1,36 (2 H, dd), 0,96 (6 H, s), 0,87 (3 H, t)
MW (calc.): 413,5; MW (obs.): 414,4 (M+1)
Método general K:
Intermedio 9 intermedio 15
Etapa 1: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 15)
El intermedio 152-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona se sintetizó por medio del método general E con el intermedio 9 y prop-2-in-1-ol.
Etapa 2:
El intermedio 15 (1 eq.) se disuelve en una mezcla de THF/DMF (1/1), NaH (1,1 eq., 60% en aceite mineral) se añade seguido por el agente alquilante apropiado (1 eq.) y la reacción se agita a 70 °C. Cuando la reacción se completó, la mezcla se elabora con salmuera y EtOAc, la capa orgánica se seca sobre MgSO4 y se evapora hasta sequedad. La purificación por HPLC-MS preparativa proporciona el correspondiente producto.
Síntesis ilustrativa del método general K:
Compuesto 133: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-[3-(2-metoxi-etoxi)-prop-1-inil]-6,7-dihidropirimido[6,1-a]isoquinolin-4-ona
intermedio 15 Compuesto 133
El intermedio 15 (92 mg, 0,25 mmol, 1 eq.) se disolvió en una mezcla de THF/DMF (6 mL, 1/1), NaH (11 mg, 0,275 mmol, 1,1 eq., 60% en aceite mineral) se añadió seguido por 1-bromo-2-metoxi-etano (35 mg, 0,25 mmol, 1 eq.) y la reacción se agitó a temperatura ambiente durante 16 h, luego a 70 °C durante 1 día. La mezcla se elaboró con salmuera y EtOAc, la capa orgánica se secó sobre MgSO4 y se evaporó hasta sequedad. El producto crudo se purificó por HPLC-MS preparativa para proporcionar el compuesto 133.
(1H, CDCh) 5 ppm 7,64 (1 H, s), 7,48 - 7,40 (1 H, m), 7,40 - 7,35 (1 H, m), 6,40 - 6,34 (1 H, m), 4,47 (4 H, s), 4,28 -4,15 (1 H, m), 3,93 - 3,56 (10 H, m), 3,43 (5 H, s), 3,06 - 2,95 (2 H, m)
MW (calc.): 426,5; MW (obs.): 427,4 (M+1)
Método general L:
A una solución de tBuOK (2,2 eq.) en DMF se añade gota a gota una solución del intermedio 6 (1 eq.) en DMF a 0 °C y la mezcla se agita durante 1 h. Una solución del agente alquilante apropiado (10 eq.) en DMF se añade gota a gota a la solución previa a 0 °C, luego la reacción se agita a 80 °C. Cuando la reacción se completó, la mezcla se enfría a temperatura ambiente, se neutralizó con agua y se extrajo con EtOAc. Las capas orgánicas combinadas se secan sobre Na2SO4 y se evaporan hasta sequedad. El producto se aísla por purificación por TLC preparativa.
Síntesis ilustrativa del método general L:
Compuesto 158: 9-(2,2-dimetil-propoxi)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
A una solución de tBuOK (19 mg, 0,166 mmol, 1,1 eq.) en DMF (2 mL) se añadió gota a gota una solución del intermedio 6 (50 mg, 0,151 mmol, 1 eq.) en DMF (2 mL) a 0 °C y la mezcla se agitó durante 1 h. Una solución de 1-yodo-2,2-dimetil-propano (0,021 mL, 0,159 mmol, 1,05 eq.) en DMF (2 mL) se añadió gota a gota a la solución previa a 0 °C, luego la reacción se agitó a 80 °C durante 1 día. Se añadieron reactivos extra, 1-yodo-2,2-dimetil-propano (0,4 mL, 10 eq.) y tBuOK (19 mg, 0,166 mmol, 1,1 eq.) y la reacción se agitó a 80 °C durante un día más. La mezcla se enfrió a temperatura ambiente, se neutralizó con agua y se extrajo con EtOAc. Las capas orgánicas combinadas se lavaron con salmuera, se secaron sobre Na2SO4 y se evaporó hasta sequedad. El compuesto 158 se obtuvo por purificación con TLC preparativa [DCM/MeOH, 98/2].
(1H, CDCl3) 5 ppm 7,70 - 7,56 (1 H, d), 6,95 - 6,85 (1 H, d), 6,80 (1 H, s), 6,28 (1 H, s), 4,50 - 4,35 (2 H, m), 4,25 - 4,10 (2 H, m), 4,05 - 3,92 (1 H, m), 3,10 - 3,57 (8 H, m), 3,55 - 3,40 (1 H, m), 3,05 - 2,90 (2 H, m), 1,05 (9H, s).
MW (calc.): 400,5; MW (obs.): 401,2 (M+1)
Compuestos de la invención
Los compuestos de acuerdo con la invención se pueden producir como se describe más abajo.
Compuesto 1: 9-Aliloxi-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 2: 2-([1,4]dioxan-2-ilmetoxi)-9-piridin-3-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 3: 2-([1,4]dioxan-2-ilmetoxi)-9-piridin-4-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido piridin-4-borónico.
Compuesto 4: 2-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nolin-9-¡l]-benzon¡tr¡lo. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2-cianofenilborónico. Compuesto 5: 3-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-benzon¡tr¡lo. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 3-cianofenilborónico. Compuesto 6: 4-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-benzon¡tr¡lo. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 4-cianofenilborónico. Compuesto 7: [2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡lox¡]-aceton¡tr¡lo. Este compuesto se prepara por medio del método general F usando el intermedio 8 y bromo-acetonitrilo, KI no se usó en el experimento.
Compuesto 8: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(oxazol-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Síntesis completamente descrita con anterioridad.
Compuesto 9: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(p¡r¡d¡n-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general F usando el intermedio 8 y clorhidrato de piridin-2-il-metanol. Compuesto 10: 9-(3,5-d¡cloro-fen¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 3,5-diclorofenilborónico. Compuesto 11: 9-benzofuran-2-¡l-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y 1-benzofuran-2-ilborónico. Compuesto 12: 2-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-¡ndol-1-carboxíl¡co ter-but¡lo ester.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y 1 -(ter-butoxicarbonil)-1 H-indol-2-ilborónico.
Compuesto 13: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(1H-¡ndol-2-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
El compuesto 12 (57 mg, 0,11 mmol) se disolvió en una mezcla de DCM/TFA (1/1, 2 mL) y la reacción se agitó a temperatura ambiente durante 6 h. La mezcla se evaporó hasta sequedad para recuperar el compuesto 13 en forma de una sal de TFA.
(1H DMSO-afe) 5 ppm 8,11 (1 H, d), 7,95 - 7,86 (2 H, m), 7,57 (1 H, d), 7,43 (1 H, d), 7,15 (1 H, t), 7,10 (1 H, d), 6,71 (1 H, s), 4,31 - 4,25 (2 H, m), 4,09 (2 H, t), 3,92 - 3,84 (1 H, m), 3,79 (2 H, td), 3,71 - 3,57 (2 H, m), 3,55 - 3,46 (1 H, m), 3,40 (1 H, dd), 3,08 (2 H, t)
MW (calc.): 429,5 MW (obs.): 430,5 (M+1)
Compuesto 14: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(6-metox¡-p¡r¡d¡n-3-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2-metoxi-5-piridinborónico.
Compuesto 15: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(6-tr¡fluoromet¡l-p¡r¡d¡n-3-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4- ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2-(trifluorometil) piridin-5- borónico.
Compuesto 16: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-met¡l-3H-¡m¡dazol-4-¡let¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 17: 9-(5-ter-but¡l-[1,2,4]oxad¡azol-3-¡lmetox¡)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 5-(ter-butil)-3-(clorometil)-1,2,4-oxadiazol.
Compuesto 18: met¡lam¡da de ác¡do 5-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-p¡r¡d¡n-2-carboxíl¡co.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 2-(N-metilaminocarbonil) piridin-5-borónico.
Compuesto 19: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-pent-1-¡n¡l-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y pent-1-ino.
Compuesto 20: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(2-p¡r¡d¡n-2-¡l-et¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 11 intermedio 22 Compuesto 20
Etapa 1: 2-([1,4]dioxan-2-ilmetoxi)-9-((E)-2-piridin-2-il-vinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (intermedio 22).
Un recipiente de base redonda se cargó con el intermedio 11 (50 mg, 0,11 mmol, 1 eq.), 2-vinil-piridina (0,014 mL, 0,13 mmol, 1,2 eq.), (DPPF)PdCl2.DCM (4,4 mg, 0,0054 mmol, 0,05 eq.) y TEA (0,03 mL, 0,22 mmol, 2 eq.) bajo N2 , luego el recipiente se desgasificó. DMF (2 mL) luego se añadió y la reacción se agitó a 100 °C durante 16 h. La reacción se enfrió a temperatura ambiente y se evaporó hasta sequedad, el residuo luego se purificó por cromatografía flash en gel de sílice, eluyendo del 0 al 3% de MeOH/DCM para dar el intermedio 222-([1,4]dioxan-2-ilmetoxi)-9-((E)-2-piridin-2-il-vinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
(1H, CDCla) 5 ppm 8,66 - 8,59 (1 H, m), 7,74 - 7,53 (4 H, m), 7,46 (1 H, s), 7,39 (1 H, d), 7,30 - 7,15 (2 H, m), 6,37 (1 H, s), 4,48 - 4,34 (2 H, m), 4,21 (2 H, t), 4,02 - 3,93 (1 H, m), 3,89 - 3,59 (5 H, m), 3,53 - 3,42 (1 H, m), 3,03 (2 H, m) MW (calc.): 417,5; MW (obs.): 418,4 (M+1)
Etapa 2: 2-([ 1,4]dioxan-2-ilmetoxi)-9-(2-piridin-2-il-etil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 20).
Un recipiente de base redonda se cargó con el intermedio 22 (45 mg, 0,11 mmol, 1 eq.), PtÜ2 (6 mg, 0,025 mmol, 0,23 eq.) y THF (2 mL) se añadió. El sistema se purgó con N2 antes de llenar con H2 , luego la reacción se agitó durante 16 h a temperatura ambiente. La mezcla de reacción se filtró a través de un cartucho de SPE guanidina y el solvente se evaporó hasta sequedad. El producto crudo se purificó por cromatografía flash en gel de sílice, eluyendo del 1 al 10% de MeOH/DCM para dar el compuesto 20.
(1H, CDCl3) 5 ppm 8,58 (1 H, dd), 7,66 - 7,56 (2 H, m), 7,22 (1 H, dd), 7,19 - 7,09 (3 H, m), 6,36 (1 H, s), 4,50 - 4,36 (2 H, m), 4,25 - 4,17 (2 H, m), 4,04 - 3,95 (1 H, m), 3,91 - 3,62 (5 H, m), 3,50 (1 H, dd), 3,14 (4 H, s), 2,98 (2 H, t) MW (calc.): 419,5; MW (obs.): 420,5 (M+1)
Compuesto 21: 2-([1,4]dioxan-2-ilmetoxi)-9-(2-pirazin-2-il-etil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
intermedio 11 intermedio 23 Compuesto 21
Etapa 1: 2-([1,4]dioxan-2-ilmetoxi)-9-((E)-2-pirazin-2-il-vinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (intermedio 23).
Un recipiente de base redonda se cargó con el intermedio 11 (50 mg, 0,11 mmol, 1 eq.), 2-vinil-piridina (0,014 mL, 0,13 mmol, 1,2 eq.), (DPPF)PdCh.DCM (4,4 mg, 0,0054 mmol, 0,05 eq.) y TEA (0,03 mL, 0,22 mmol, 2 eq.) bajo N2 , luego el recipiente se desgasificó. DMF (2 mL) luego se añadió y la reacción se agitó a 100 °C durante 16 h. La reacción se enfrió a temperatura ambiente y se evaporó hasta sequedad, el residuo luego se purificó por cromatografía flash en gel de sílice, eluyendo del 0 al 4% de MeOH/DCM para dar el intermedio 232-([1,4]dioxan-2-ilmetoxi)-9-((E)-2-pirazin-2-il-vinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
(1H, CDCla) 5 ppm 8,69 (1 H, m), 8,63 - 8,58 (1 H, m), 8,49 (1 H, m), 7,84 - 7,71 (2 H, m), 7,63 (1 H, d), 7,53 (1 H, s), 7,31 (1 H, s), 6,42 (1 H, s), 4,52 - 4,39 (2 H, m), 4,30 - 4,22 (2 H, m), 4,02 (1 H, dd), 3,93 - 3,63 (5 H, m), 3,52 (1 H, dd), 3,08 (2 H, m)
MW (calc.): 418,5; MW (obs.): 419,4 (M+1)
Etapa 2: 2-([ 1,4]dioxan-2-ilmetoxi)-9-(2-pirazin-2-il-etil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 21).
Un recipiente de base redonda se cargó con el intermedio 23 (38 mg, 0,09 mmol, 1 eq.), PtO2 (5 mg, 0,021 mmol, 0,23 eq.) y THF (2 mL) se añadió. El sistema se purgó con N2 antes de llenar con H2 ten la reacción se agitó durante 16 h a temperatura ambiente. La mezcla de reacción se filtró a través de un cartucho de SPE guanidina y el solvente se evaporó hasta sequedad. El producto crudo se purificó por cromatografía flash en gel de sílice, eluyendo del 1 a 10% de MeOH/DCM para dar el compuesto 21.
(1H, CDCla) 5 ppm 8,55 (1 H, dd), 8,44 (2 H, dd), 7,63 (1 H, d), 7,22 (1 H, dd), 7,15 (1 H, s), 6,36 (1 H, s), 4,36 - 4,53 (2 H, m), 4,17 - 4,26 (2 H, m), 3,95 - 4,07 (1 H, m), 3,61 - 3,93 (5 H, m), 3,51 (1 H, dd), 3,17 (4 H, s), 2,99 (2 H, t) MW (calc.): 420,5; MW (obs.): 421,5 (M+1)
Compuesto 22: 2-([1,4]dioxan-2-ilmetoxi)-9-(1H-indol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E intermedio 11 y usando ácido 5-indolilborónico.
Compuesto 23: 2-([1,4]dioxan-2-ilmetoxi)-9-(2-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2-metoxifenilborónico. Compuesto 24: 2-([1,4]dioxan-2-ilmetoxi)-9-(5-metoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 3-metoxi-5-piridinborónico.
Compuesto 25: 2-([1,4]dioxan-2-ilmetoxi)-9-(1H-indazol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 1H-indazol-5-borónico. Compuesto 26: 2-([1,4]dioxan-2-ilmetoxi)-9-(4-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 4-metoxifenilborónico. Compuesto 27: 3-[2-([1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzamida. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 3-aminocarbonilfenilborónico.
Compuesto 28: 5-[2-([1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-2-fluorobenzamida.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 3-(aminocarbonil)-4-fluorobencenborónico.
Compuesto 29: N-{3-[2-([1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-fenil}-acetamida.
Este compuesto se prepara por medio del método general E intermedio 11 y usando ácido 3-acetamidofenilborónico. Compuesto 30: 9-ciclopropiletinil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general G intermedio 11 y usando etinil-ciclopropano.
Compuesto 31: 2-([1,4]dioxan-2-ilmetoxi)-9-(1-hidroxi-ciclopentiletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G intermedio 11 y usando 1-etinil-ciclopentanol.
Compuesto 32: 2-([1,4]dioxan-2-ilmetoxi)-9-pirimidin-5-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E intermedio 11 y usando ácido 5-pirimidinilborónico. Compuesto 33: 9-ciclohex-1-enil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido ciclohexen-1 -borónico.
Compuesto 34: 2-([1,4]dioxan-2-ilmetoxi)-9-(1-metil-1H-indol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 1-metilindol-5-borónico.
Compuesto 35: 2-([1,4]dioxan-2-ilmetoxi)-9-(6-metil-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 6-metilpiridin-3-ilborónico. Compuesto 36: 2-([1,4]dioxan-2-ilmetoxi)-9-piridin-2-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y 2-etinil-piridina.
Compuesto 37: 2-([1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y 3-metoxi-propino.
Compuesto 38: 5-[2-([1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-pent-4-innitrilo.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y pent-4-inonitrilo.
Compuesto 39: 2-([1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y prop-2-in-1-ol. Compuesto 40: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(4-metox¡-fen¡let¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y 1-etinil-4-metoxi-benceno. Compuesto 41: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-p¡r¡d¡n-3-¡let¡n¡l-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y 3-etinil-piridina Compuesto 42: 4-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-N-met¡lbenzam¡da.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 4-(N-metilaminocarbonil)fenilborónico.
Compuesto 43: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-metox¡-fen¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 3-metoxifenilborónico. Compuesto 44: 9-(2-cloro-fen¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2-clorofenilborónico. Compuesto 45: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(4-h¡drox¡-but-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y but-3-in-1-ol.
Compuesto 46: 9-(1,5-d¡met¡l-1H-p¡razol-3-¡lmetox¡)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 3-clorometil-1,5-dimetil-1H-pirazol.
Compuesto 47: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(1-met¡l-1H-p¡razol-3-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do [6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 3-clorometil-1 -metil-1 H-pirazol. Compuesto 48: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-met¡l-[1,2,4]oxad¡azol-5-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 5-clorometil-3-metil-[1,2,4]oxadiazol.
Compuesto 49: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(4-morfol¡n-4-¡l-fen¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 4-morfolinofenilborónico, con CsF como base y DMF como disolvente.
Compuesto 50: 3-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-4-fluorobenzam¡da.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 5-carbamoil-2-fluorobencenborónico, con CsF como base y DMF como disolvente.
Compuesto 51: 3-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-5-fluorobenzam¡da.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 3-(aminocarbonil)-5-fluorobencenborónico, con CsF como base y DMF como disolvente.
Compuesto 52: 9-(3,3-D¡met¡l-but-1-¡n¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 3,3-dimetil-but-1-ino.
Compuesto 53: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-p¡r¡d¡n-4-¡let¡n¡l-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y 4-etinil-piridina.
Compuesto 54: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-met¡l-¡soxazol-5-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 5-clorometil-3-metil-isoxazol. Compuesto 55: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-3-met¡l-but-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 2-metil-but-3-in-2-ol.
Compuesto 56: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(2-metox¡-p¡r¡d¡n-3-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2-metoxi-3-piridinilborónico.
Compuesto 57: 2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y (cianometil) trifluoroborato de potasio.
Compuesto 58: 9-(3,6-d¡h¡dro-2H-p¡ran-4-¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 3,6-dihidro-2H-piran-4-borónico.
Compuesto 59: 5-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-p¡r¡d¡n-2-carbon¡tr¡lo.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 2-cianopiridin-5-borónico.
Compuesto 60: 2-([1,4]D¡oxan-2-¡lmetox¡)-9-(6-¡sopropox¡-p¡r¡d¡n-3-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 6-isopropoxipiridin-3-borónico.
Compuesto 61: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(6-etox¡-p¡r¡d¡n-3-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 6-etoxipiridin-3-borónico. Compuesto 62: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(6-morfol¡n-4-¡l-p¡r¡d¡n-3-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y 4-[5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2-piridinil]morfolina.
Compuesto 63: 9-(2,3-d¡metox¡-fen¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2,3-dimetoxifenilborónico. Compuesto 64: 9-(3-cloro-2-metox¡-p¡r¡d¡n-4-¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 3-cloro-2-metoxipiridin-4-borónico.
Compuesto 65: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(2-met¡l-p¡r¡d¡n-4-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 2-metilpiridin-4-borónico.
Compuesto 66: 3-[2-([1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-¡son¡cot¡non¡tr¡lo.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 4-cianopiridin-3- borónico.
Compuesto 67: 9-(2,5-d¡metox¡-fen¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2,5-dimetoxifenilborónico. Compuesto 68: 2-([1,4]dioxan-2-ilmetoxi)-9-(3,4,5,6-tetrahidro-2H-[1,2']bipiridinil-5'-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y 1-[5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-2-piridinil]piperidina.
Compuesto 69: 2-([1,4]dioxan-2-ilmetoxi)-9-(2-etoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2-etoxipiridin-3-borónico. Compuesto 70: 9-(2,6-dimetoxi-piridin-3-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ácido 2,6-dimetoxi-3-piridinborónico.
Compuesto 71: 4-[2-([1,4]dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-nicotinonitrilo.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 3-cianopiridin-4-borónico.
Compuesto 72: 9-ter-butoximetil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ter-butoximetiltrifluoroborato de potasio.
Compuesto 73: 2-([1,4]dioxan-2-ilmetoxi)-9-(2-pirrolidin-1-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y 2-(pirrolidin-1-il)-3-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)piridina.
Compuesto 74: 2-([1,4]dioxan-2-ilmetoxi)-9-(6-pirrolidin-1-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y 2-(1-pirrolidinil)-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)piridina.
Compuesto 75: 2-([1,4]dioxan-2-ilmetoxi)-9-(5-fenil-oxazol-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 2-clorometil-5-fenil-oxazol. Compuesto 76: 9-(5-ter-butil-oxazol-2-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 5-ter-butil-2-clorometil-oxazol. Compuesto 77: 9-(5-ciclopropil-[1,2,4]oxadiazol-3-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 3-clorometil-5-ciclopropil-[1,2,4] oxadiazol.
Compuesto 78: 2-([1,4]dioxan-2-ilmetoxi)-9-(5-etil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 3-clorometil-5-etil-[1,2,4] oxadiazol.
Compuesto 79: 2-([1,4]dioxan-2-ilmetoxi)-9-(5-metil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 3-clorometil-5-metil-[1,2,4]oxadiazol.
Compuesto 80: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(5-¡soprop¡l-[1,2,4]oxad¡azol-3-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 8 y 3-clorometil-5-isopropil-[1,2,4]oxadiazol.
Compuesto 81: 9-c¡clopent¡let¡n¡l-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y etinil-ciclopentano.
Compuesto 82: 9-c¡clohex¡let¡n¡l-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y etinil-ciclohexano.
Compuesto 83: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-met¡l-but-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y 3-metil-but-1-ino.
Compuesto 84: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-hex-1-¡n¡l-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y hex-1-ino.
Compuesto 85: 9-[3-(benc¡l-met¡l-am¡no)-prop-1-¡n¡l]-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y bencil-metil-prop-2-inil-amina. Compuesto 86: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-5-met¡l-hex-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 5-metil-hex-1-in-3-ol, con iPr2NH como base y THF como disolvente.
Compuesto 87: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-but-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y but-3-in-2-ol, con iPr2NH como base y THF como disolvente.
Compuesto 88: 9-c¡cloprop¡l-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y ciclopropiltrifluoroborato de potasio.
Compuesto 89: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-pent-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y pent-1 -in-3-ol con iPr2NH como base y THF como disolvente.
Compuesto 90: 2-([1,4]D¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-4-met¡l-pent-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 4-metil-pent-1-in-3-ol con iPr2NH como base y THF como disolvente.
Compuesto 91: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-et¡l-3-h¡drox¡-pent-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 3-etil-pent-1 -in-3-ol con iPr2NH como base y THF como disolvente.
Compuesto 92: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-3-fen¡l-but-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 2-fenil-but-3-in-2-ol con Cs2CO3 como base y MeCN como disolvente a reflujo.
Compuesto 93: 9-(3-benc¡lam¡no-prop-1-¡n¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y bencil-prop-2-inil-amina con Cs2COa como base y MeCN como disolvente a reflujo.
Compuesto 94: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-[(furan-2-¡lmet¡l)-am¡no]-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Una suspensión de intermedio 11 (200 mg, 0,433 mmol, 1 eq.), furan-2-ilmetanamina (0,038 mL, 0,433 mmol, 1 eq.) y CS2CO3 (0,17 g, 0,519 mmol, 1,2 eq.) en tolueno (4 mL) se desgasificó con Ar durante 30 min antes de añadir BINAP (+/-) (16 mg, 0,026 mmol, 0,06 eq.) y Pd(OAc)2 (3,88 mg, 0,017 mmol, 0,04 eq.). La reacción se calentó hasta 65 °C durante 16 h. La reacción se enfrió a temperatura ambiente, se añadieron BINAp (+/-) (16 mg, 0,026 mmol, 0,06 eq.) y Pd(OAc)2 (3,88 mg, 0,017 mmol, 0,04 eq.) y la reacción se desgasificó. La reacción se calentó hasta 80 °C durante 1 día extra. La reacción se enfrió a temperatura ambiente, se añadieron BINAP (+/-) (16 mg, 0,026 mmol, 0,06 eq.) y Pd(OAc)2 (3,88 mg, 0,017 mmol, 0,04 eq.) y la reacción se desgasificó. La reacción se calentó hasta 80 °C durante 1 día extra. La reacción se enfrió a temperatura ambiente y se diluyó con DCM y se lavó con KHSO4 acuoso 0,5 N. La capa acuosa se extrajo con DCM, las capas orgánicas combinadas se secaron sobre Na2SO4 y se evaporaron hasta sequedad. El producto crudo se purificó por HPLC-MS preparativa [H2O (98— ^2): MeCN (2— 98) / 0,1% de HCO2H] para dar el compuesto 94.
(1H, CDCla) 5 ppm 7,57 - 7,48 (1 H, d), 7,38 (1 H, s), 6,68 - 6,55 (1 H, d), 6,49 (1 H, s), 6,35 (1 H, s), 6,28 (1 H, s), 6,20 (1 H, s), 4,60 - 4,50 (1 H, m), 4,38 - 4,30 (4 H, m), 4,22 - 4,15 (2 H, m), 4,03 - 3,93 (1 H, m), 3,95 - 3,60 (5 H, m), 3,55 -3,40 (1 H, t), 2,98 - 2,85 (2 H, m)
MW (calc.): 409,4; MW (obs.): 410,2 (M+1)
Compuesto 95: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(1-et¡l-1H-p¡razol-4-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 1-etil-1 H-pirazol-4-borónico.
Compuesto 96: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-[1-(3-met¡l-but¡l)-1H-p¡razol-4-¡l]-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 1 -(3-metilbutil)-1 H-pirazol-4-borónico.
Compuesto 97: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(5-met¡l-furan-2-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 2-metilfuran-5-borónico.
Compuesto 98: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-hex-1-¡n¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general G usando el intermedio 11 y hex-1-in-3-ol, Cs2CO3 como base y MeCN como disolvente a reflujo.
Compuesto 99: 9-(3,5-d¡met¡l-1H-p¡razol-4-¡l)-2-([1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 3,5-dimetilpirazol-4-borónico.
Compuesto 100: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(1H-p¡razol-4-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido pirazol-4-borónico.
Compuesto 101: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(1-prop¡l-1H-p¡razol-4-¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 11 y éster pinacólico de ácido 1-propil-1 H-pirazol-4-borónico.
Compuesto 102: 2-[2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-benzon¡tr¡lo.
Este compuesto se prepara por medio del método general E usando el intermedio 10 y éster pinacólico de ácido 2-cianofenilborónico.
Compuesto 103: 2-[2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-4-oxo-6,7-d¡h¡dro-4H-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-9-¡l]-benzon¡tr¡lo.
Este compuesto se prepara por medio del método general E usando el intermedio 9 y éster pinacólico de ácido 2-cianofenilborónico.
Compuesto 104: 9-(5-c¡cloprop¡l-[1,2,4]oxad¡azol-3-¡lmetox¡)-2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡drop¡r¡m¡do[6,1 -a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 7 y 3-clorometil-5-ciclopropil-[1,2,4]oxadiazol.
Compuesto 105: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-et¡n¡l-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 11 intermedio 24 Compuesto 105
Etapa 1:2-([ 1,4]dioxan-2-ilmetoxi)-9-prop-1-inil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 24).
El intermedio 242-([1,4]dioxan-2-ilmetoxi)-9-prop-1-inil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona se sintetiza por medio del método general E con el intermedio 11 y etinil-trimetil-silano.
(1H, CDCh) 5 ppm 7,66 - 7,61 (1 H, m), 7,47 - 7,43 (1 H, m), 7,42 - 7,38 (1 H, m), 6,37 (1 H, s), 4,50 - 4,36 (2 H, m), 4,23 - 4,16 (2 H, m), 4,04 - 3,93 (1 H, m), 3,90 - 3,60 (4 H, m), 3,53 - 3,44 (1 H, m), 3,02 - 2,97 (1 H, m), 0,27 (7 H, s) MW (calc.): 410,5; MW (obs.): 411,4 (M+1)
Etapa 2 :2-([1,4]dioxan-2-ilmetoxi)-9-etinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 105). TBAF (4,06 mL, 4,06 mmol, 1,2 eq.) se añadió gota a gota a una solución del intermedio 24 (1,39 g, 3,39 mmol, 1 eq.) en THF (40 mL) a 0 °C y la reacción se agitó durante 1 h a 0 °C. La reacción luego se evaporó hasta sequedad y el residuo se redisolvió en HCl 1 N. La fase acuosa se extrajo con DCM, las capas orgánicas combinadas se secaron sobre MgSO4 y el solvente se evaporó al vacío. El producto crudo se purificó por cromatografía flash en gel de sílice, eluyendo del 0 al 5% de MeOH/DCM para obtener el compuesto 105.
(1H, CDCla) 5 ppm 7,65 (1 H, s), 7,51 - 7,46 (1 H, m), 7,45 - 7,41 (1 H, m), 6,37 (1 H, s), 4,49 - 4,36 (2 H, m), 4,21 (2 H, s), 4,04 - 3,94 (1 H, m), 3,90 - 3,61 (5 H, m), 3,53 - 3,44 (1 H, m), 3,25 (1 H, s), 3,00 (2 H, s) MW (calc.): 330,3; MW (obs.): 331
Compuesto 106: 2-([1,4]dioxan-2-ilmetoxi)-9-pirimidin-2-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
El compuesto 105 (50 mg, 0,15 mmol, 1 eq.) se disolvió en DMF (3 mL), 5-bromo-pirimidina (47 mg, 0,30 mmol, 2 eq.) se añadió seguido por TEA (0,062 mL, 0,44 mmol, 3 eq.) y la mezcla se desgasificó. Pd(PPh3)3Cl2 (5 mg, 0,0074 mmol, 0,05 eq.) se añadió con CuI (6 mg, 0,029 mmol, 0,2 eq.) y la mezcla de reacción se calentó a 80 °C durante 16 h. Las sustancias volátiles se evaporaron hasta sequedad y el producto crudo se purificó por cromatografía flash en gel de sílice, eluyendo del 0 al 5% de MeOH/DCM para dar el compuesto 106.
Compuesto 107: 2-([1,4]dioxan-2-ilmetoxi)-9-(3-fenilamino-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y fenil-prop-2-inil-amina con iPr2NH como base y THF como disolvente.
Compuesto 108: 2-([1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-3-piridin-3-il-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 1-piridin-3-il-prop-2-in-1-ol. Compuesto 109: 9-ciclopentiloximetil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona. Este compuesto se prepara por medio del método general E usando el intermedio 11 y ciclopentoximetiltrifluoroborato de potasio.
Compuesto 110: 2-([1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 111: 9-ciclopropiletinil-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 10 y etinil-ciclopropano.
Compuesto 112: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-metil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 9 y 3-metil-but-1-ino.
Compuesto 113: 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-imidazol-1-il-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y 1 -prop-2-inil-1 H-imidazol.
Compuesto 114: 9-(2-c¡cloprop¡l-et¡l)-2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Un recipiente de base redonda se cargó con el intermedio 10 (2 g, 4,33 mmol, 1 eq.), intermedio 20 (1,1 g, 6,5 mmol, 1,5 eq.), K2CO3 (1,8 g, 13 mmol, 3 eq.), Pd(OAc)2 (19 mg, 0,087 mmol, 0,02 eq.), RuPhos (81 mg, 0,173 mmol, 0,04 eq.), tolueno (30 mL) y H2O (3 mL). La mezcla se desgasificó con N2 y se calentó a 80 °C durante 16 h. La reacción se enfrió a temperatura ambiente, se neutralizó con salmuera y se extrajo con EtOAc. La capa orgánica se secó sobre MgSO4 y se evaporó hasta sequedad. El producto crudo se purificó por cromatografía flash en gel de sílice, eluyendo del 70 al 90% EtOAc/H para dar el compuesto 114.
(1H, CDCla) 5 ppm 7,64 - 7,58 (1 H, m), 7,24 - 7,19 (1 H, m), 7,13 (1 H, s), 6,35 (1 H, s), 4,49 - 4,36 (2 H, m), 4,25 -4,17 (2 H, m), 4,03 - 3,95 (1 H, m), 3,90 - 3,61 (5 H, m), 3,54 - 3,45 (1 H, m), 3,02 - 2,95 (2 H, m), 2,81 - 2,72 (2 H, m), 1,59 - 1,49 (2 H, m), 0,77 - 0,64 (1 H, m), 0,49 - 0,42 (2 H, m), 0,10 - 0,02 (2 H, m) MW (calc.): 382,5; MW (obs.): 383,4 (M+1)
Compuesto 115: 9-c¡clopent¡lox¡met¡l-2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 10 y ciclopentoximetiltrifluoroborato de potasio.
Compuesto 116: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-3-p¡r¡d¡n-3-¡l-prop¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 117: 9-al¡lox¡-2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 118: 9-al¡lox¡-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 119: 2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(tetrah¡dro-p¡ran-4-¡lox¡met¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 10 y el intermedio 14.
Compuesto 120: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-{3-[(p¡r¡d¡n-3-¡lmet¡l)-am¡no]-prop-1-¡n¡l}-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 11 y prop-2-in-1-il(piridin-3-ilmetil)amina.
Compuesto 121: 2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-pent¡l-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general I usando el compuesto 111.
Compuesto 122: 9-c¡cloprop¡let¡n¡l-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
El intermedio 9 (13,5 g, 29,20 mmol, 1 eq.) se disolvió en DMF desgasificado (1000 mL) bajo una atmósfera de nitrógeno, etinilciclopropano (3,5 g, 53,00 mmol, 1,8 eq.) se añadió seguido por Pd(PPh3)3Cl2 (1,11 g, 1,58 mmol, 0,05 eq.), CuI (1,9 g, 9,98 mmol, 0,34 eq.) y TEA (12,5 mL, 89,7 mmol, 3,1 eq.). La mezcla de reacción se agitó durante 3 h a 80 °C y 15 h a temperatura ambiente. La reacción se concentró al vacío. El producto crudo luego se purificó por trituración en /'PrOH caliente para obtener el compuesto 122.
(1H, CDCla) 5 ppm 7,63 (1 H, d), 7,39 (1 H, dd), 7,31 (1 H, s), 6,36 (1 H, s), 4,50 - 4,39 (2 H, m), 4,20 (2 H, t), 4,02 -3,98 (1 H, m), 3,89 - 3,66 (5 H, m), 3,49 (1 H, t), 2,96 (2 H, t), 1,59 - 1,48 (1 H, m), 0,98 - 0,81 (4 H, m)
MW (calc.): 378,4; MW (obs.): 379,4
ee = 98,3%
Compuesto 123: 9-(2-c¡cloprop¡l-et¡l)-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡drop¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Un recipiente de base redonda se cargó con el intermedio 9 (2,08 g, 4,51 mmol, 1 eq.), intermedio 20 (1,35 g, 7,67 mmol, 1,7 eq.), K2CO3 (1,87 g, 13,53 mmol, 3 eq.), Pd(OAc)2 (20 mg, 0,09 mmol, 0,02 eq.), RuPhos (84 mg, 0,18 mmol, 0,04 eq.), tolueno (30 mL) y H2O (3 mL). La mezcla se desgasificó con N2 y se calentó a 80 °C durante 1,5 días.
La reacción se enfrió a temperatura ambiente y algunos reactivos más se añadieron, 2-ciclopropil-etil-trifluoroborato de potasio (0,3 eq.), Pd(OAc)2 (0,02 eq.), RuPhos (0,04 eq.), la reacción se desgasificó y la reacción se calentó a 80 °C durante 16 h. La reacción se enfrió a temperatura ambiente, se neutralizó con H2O y se extrajo con EtOAc. La capa orgánica se secó sobre MgSO4 y se evaporó hasta sequedad. El producto crudo se purificó por cromatografía flash en gel de sílice, eluyendo del 80 al 90% EtOAc/H en el compuesto 123.
(1H, CDCla) 5 ppm 7,64 - 7,58 (1 H, m), 7,24 - 7,19 (1 H, m), 7,13 (1 H, s), 6,35 (1 H, s), 4,49 - 4,36 (2 H, m), 4,24 -4,17 (2 H, m), 4,03 - 3,95 (1 H, m), 3,91 - 3,62 (5 H, m), 3,49 (1 H, dd), 3,03 - 2,95 (2 H, m), 2,81 - 2,73 (2 H, m), 1,59 - 1,50 (2 H, m), 0,71 (1 H, s), 0,49 - 0,42 (2 H, m), 0,09 - 0,03 (2 H, m)
MW (calc.): 382,5; MW (obs.): 383,4
Compuesto 124: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(oxetan-3-¡lox¡met¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 9 y el intermedio 15.
Compuesto 125: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-met¡l-oxetan-3-¡lmetox¡met¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 9 y el intermedio 16.
Compuesto 126: 9-(2,2-d¡met¡l-but¡lam¡no)-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 127: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-4-met¡l-pent¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 25)
Intermedio 25 se prepara por medio del método general G usando el intermedio 9, 4-Metil-pent-1 -in-3-ol, /Pr2NH como base y THF como disolvente.
(1H, CDCta) 5 ppm 7,65 - 7,60 (1 H, d), 7,48 - 7,40 (1 H, m), 7,37 (1 H, s), 6,36 (1 H, s), 4,50 - 4,30 (3 H, m), 4,25 - 4,15 (2 H, m), 4,05 - 3,95 (1 H, m), 3,92 - 3,60 (6 H, m), 3,68 - 3,40 (1 H, m), 3,05 - 2,92 (2 H, m), 2,10 - 1,95 (1 H, m), 1,93 1,80 (1 H, m), 1,15-1,00 (6 H,m)
MW (calc.): 410,5; MW (obs.): 411,2 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 127)
Compuesto 127 se prepara por medio del método general I usando el intermedio 25.
Compuesto 128: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(2-et¡l-hex¡lam¡no)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general J usando el intermedio 13 y 2-etil-hexanal.
Compuesto 129: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(2-metox¡-etox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 6 y 1-bromo-2-metoxi-etano, KI no se usó en este experimento.
Compuesto 130: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(2-etox¡-etox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general F usando el intermedio 6 y 1 -bromo-2-etoxi-etano, KI no se usó en este experimento.
Compuesto 131: 9-c¡cloprop¡lmetox¡-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 6 y bromometil-ciclopropano, KI no se usó en este experimento.
Compuesto 132: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(2-fluoro-etox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona. Este compuesto se prepara por medio del método general F usando el intermedio 6 y 1-bromo-2-fluoro-etano, KI no se usó en este experimento.
Compuesto 133: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-[3-(2-metox¡-etox¡)-prop-1-¡n¡l]-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 134: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-[3-(2-etox¡-etox¡)-prop-1-¡n¡l]-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general K usando el intermedio 21 y 1-bromo-2-etoxi-etano.
Compuesto 135: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-[3-(2-fluoro-etox¡)-prop-1-¡n¡l]-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general K usando el intermedio 21 y 1-bromo-2-fluoroetano. Compuesto 136: 9-(2,2-d¡met¡l-propox¡met¡l)-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 9, en una mezcla de DME/H2O (2/1), en un microondas a 120 °C durante 20 min y el intermedio 17.
Compuesto 137: 9-c¡clohex¡lox¡met¡l-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 9 y ciclohexiloximetiltrifluoroborato de potasio en una mezcla de DME/H2O (2/1), en un microondas a 120 °C durante 20 min.
Compuesto 138: 9-c¡cloprop¡lmetox¡met¡l-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 9, en una mezcla de DME/H2O (2/1), en un microondas a 120 °C durante 20 min y el intermedio 18.
Compuesto 139: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(tetrah¡dro-p¡ran-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general F usando el intermedio 6 y 2-bromometil-tetrahidro-pirano, KI no se usó en este experimento.
Compuesto 140: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-but¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 9 intermedio 26 Compuesto 140
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 26).
El intermedio 26 se preparó por medio del método general G usando el intermedio 9 y but-3-in-2-ol, el producto crudo se usó en la siguiente etapa sin caracterización.
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 140).
El compuesto 140 se preparó por medio del método general I usando el intermedio 26.
Compuesto 141: 9-(4,4-d¡met¡l-pent¡lox¡)-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 6 Compuesto 141
El intermedio 6 (0,1 g, 0,303 mmol, 1 eq.), 4,4-dimetil-pentan-1-ol (35 mg, 0,303 mmol, 1 eq.) y PPh3 (95 mg, 0,363 mmol, 1,2 eq.) se suspendieron en 1,4-dioxano (5 mL) y la mezcla se desgasificó con N2. DIAD (0,065 mL, 0,333 mmol, 1,1 eq.) se añadió gota a gota y la reacción se agitó a temperatura ambiente durante 2 h. La mezcla de reacción se evaporó hasta sequedad y el residuo se purificó por TLC preparativa eluyendo con EtOAc para dar el compuesto 141. (1H, CDCla) 5 ppm 7,70 - 7,58 (1 H, d), 6,95 - 6,82 (1 H, d), 6,77 (1 H, s), 6,27 (1 H, s), 4,50 - 4,32 (2 H, m), 4,38- 4,15 (2 H, m), 4,05 - 3,92 (3 H, m), 3,92 - 3,60 (5 H, m), 3,55 - 3,42 (1 H, t), 3,05 - 2,92 (2 H, m), 1,85 - 1,70 (2 H, m), 1,40 - 1,30 (2 H, m), 0,92 (9 H, s)
MW (calc.): 428,5; MW (obs.): 429,2 (M+1)
Compuesto 142: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-metox¡-4-met¡l-pent¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 27)
El intermedio 27 se prepara por medio del método general H usando el intermedio 25. MW (calc.): 424,5; MW (obs.): 425,2 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 142).
El compuesto 142 se prepara por medio del método general I usando el intermedio 27.
Compuesto 143: 9-(3-c¡cloprop¡l-propox¡)-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 6 Compuesto 143
El intermedio 6 (2,12 g, 2,42 mmol, 1 eq.), 4,4-dimetil-pentan-1-ol (0,77 g, 7,71 mmol, 1,2 eq.) y PPh3 (2,02 g, 7,71 mmol, 1,2 eq.) se suspendieron en 1,4-dioxano (50 mL) y la mezcla se desgasificó con N2. DIAD (1,56 mL, 7,71 mmol, 1,1 eq.) se añadió gota a gota y la reacción se agitó a temperatura ambiente durante 2 h. La mezcla de reacción se neutralizó con salmuera y se extrajo con EtOAc, la fase orgánica se secó sobre MgSO4 y se evaporó hasta sequedad. El compuesto 143 se obtuvo por purificación por cromatografía flash en gel de sílice, eluyendo del 60 al 100% EtOAc/H. (1H, CDCh) 5 ppm 7,66 - 7,60 (1 H, m), 6,91 - 6,86 (1 H, m), 6,80 - 6,76 (1 H, m), 6,28 (1 H, s), 4,48 - 4,35 (2H, m),4,24-4,17 (2H, m), 4,11 - 4,04 (2 H, m), 4,02 - 3,95 (1 H, m), 3,91 - 3,61 (5 H, m), 3,54 - 3,45 (1 H, m), 3,03 - 2,94 (2 H, m), 1,98 - 1,88 (2 H, m), 1,45 - 1,36 (2 H, m), 0,78 - 0,66 (1 H, m), 0,50 - 0,43 (2 H, m), 0,09 - 0,03 (2 H, m)
MW (calc.): 412,5; MW (obs.): 413,5
Compuesto 145: 9-c¡clohex¡lam¡no-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general J usando el intermedio 13 y ciclohexanona.
Compuesto 146: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-4,4-d¡met¡l-pent¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4,4-dimetil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 28).
El intermedio 28 se prepara por medio del método general G usando el intermedio 9. MW (calc.): 424,5; MW (obs.): 425,4 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-4,4-dimetil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 146).
El compuesto 146 se prepara por medio del método general I usando el intermedio 28.
Compuesto 147: 9-c¡clopent¡lmetox¡met¡l-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 9, en una mezcla de DME/H2 O (2/1), en un microondas a 120 °C durante 20 min y el intermedio 19.
Compuesto 148: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-metox¡-but¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 26 intermedio 29 Compuesto 148
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 29)
El intermedio 29 se prepara por medio del método general H usando el intermedio 26.
MW (calc.): 396,4; MW (obs.): 397,2 (M+1)
Etapa 1: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 148)
El compuesto 148 se prepara por medio del método general I usando el intermedio 29.
Compuesto 149: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-fen¡lam¡no-prop¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
intermedio 9 intermedio 30 Compuesto 149
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-fenilamino-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 30)
El intermedio 30 se prepara por medio del método general G usando el intermedio 9 y fenil-prop-2-inil-amina.
MW (calc.): 443,5; MW (obs.): 444,2 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-fenilamino-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 149)
Compuesto 149 se prepara por medio del método general I usando el intermedio 30.
Compuesto 150: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(4-h¡drox¡-pent¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Etapa 1 :2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 31)
El intermedio 31 se preparó por medio del método general G usando el intermedio 9, pent-4-in-2-ol, iPr2NH como base y THF como disolvente.
MW (calc.): 396,4; MW (obs.): 397,2 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(4-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 150)
El compuesto 150 se preparó por medio del método general I usando el intermedio 31.
Compuesto 151: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(4-h¡drox¡-but¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 32)
Intermedio 32 se preparó por medio del método general G usando el intermedio 9, but-3-in-1-ol, iPr2NH como base y THF como disolvente.
(1H, CDCla) 5 ppm 7,70 - 7,65 (1 H, m), 7,45 - 7,35 (1 H, m), 7,34 (1 H, s), 6,35 (1 H, s), 4,50 - 4,32 (2 H, m), 4,28 -4,10 (2 H, m), 4,05 - 3,90 (1 H, m), 3,95 - 3,60 (7 H, m), 3,55 - 3,40 (1 H, m), 3,05 - 2,90 (2 H, m), 2,80 - 2,65 (2 H, m), 2,00 - 1,80 (1 H, m)
MW (calc.): 382,4; MW (obs.): 383,2 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(4-hidroxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 151).
El compuesto 151 se preparó por medio del método general I usando el intermedio 32.
Compuesto 152: 9-(c¡clohex¡l-met¡l-am¡no)-2-((S)-1-[1,4]d¡oxan-2-ilmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]isoquinolin-4-ona.
Compuesto 147 Compuesto 152
Mel (0,007 mg, 0,11 mmol, 1,2 eq.) se añadió al compuesto 147 (38 mg, 0,092 mmol, 1 eq.) y NaH (6 mg, 0,15 mmol, 1,6 eq.) en DMF (5 mL) y la reacción se agitó a temperatura ambiente durante 16 h. Algo más de NaH (6 mg, 0,15 mmol, 1,6 eq.) y MeI (0,07 mg, 0,11 mmol, 1,2 eq.) se añadieron a la mezcla de reacción y se agitó durante otros 2 días. La mezcla se neutralizó con salmuera y se extrajo con EtOAc. Las capas orgánicas se secaron sobre MgSO4 y se evaporaron hasta sequedad. El residuo se purificó por HPLC-MS preparativa para proporcionar el compuesto 152. (1H, CDCl3) 5 ppm 7,57 - 7,50 (1 H, m), 6,71 (1 H, d), 6,53 (1 H, br. s.), 6,21 (1 H, s), 4,51 - 4,33 (2 H, m), 4,26 - 4,14 (2 H, m), 4,06 - 3,93 (1 H, m), 3,92 - 3,56 (6 H, m), 3,56 - 3,41 (1 H, m), 3,00 - 2,90 (2 H, m), 2,88 (3 H, s), 2,04 -1,63 (2 H, m), 1,60 - 1,31 (5 H, m), 1,28 - 1,08 (1 H, m)
MW (calc.): 425,5; MW (obs.): 426,4
Compuesto 153: 9-(c¡clohex¡lmet¡l-amino)-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general J usando el intermedio 13 y ciclohexanocarbaldehído. Compuesto 154: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-[(tetrah¡dro-piran-4-¡lmet¡l)-am¡no]-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general J usando el intermedio 13 y tetrahidro-piran-4-carbaldehído. Compuesto 155: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-etil-3-h¡drox¡-pent¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 9 intermedio 33 Compuesto 155
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-etil-3-hidroxi-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 33)
El intermedio 33 se prepara por medio del método general G usando el intermedio 9 y 3-etil-pent-1 -in-3-ol.
(1H, CDCla) 5 ppm 7,51 - 7,46 (1 H, m), 7,28 - 7,24 (1 H, m), 7,22 - 7,19 (1 H, m), 6,20 (1 H, s), 4,30 - 4,19 (2 H, m), 4,08 - 4,00 (2 H, m), 3,87 - 3,79 (1 H, m), 3,75 - 3,47 (5 H, m), 3,39 - 3,30 (1 H, m), 3,03 (1 H, br. S), 2,88 - 2,80 (2 H, m), 1,746 - 1,56 (4 H, m), 0,97 (6 H, s)
MW (calc.): 424,5; MW (obs.): 425,5 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-etil-3-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 155).
El compuesto 155 se prepara por medio del método general I usando el intermedio 33.
Compuesto 156: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-3-met¡l-but¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
intermedio 9 intermedio 34 Compuesto 156
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-metil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 34)
El intermedio 34 se prepara por medio del método general G usando el intermedio 9 y 2-metil-but-3-in-2-ol.
(1H, CDCta) 5 ppm 7,58 (1 H, d), 7,38 - 7,33 (1 H, m), 7,32 - 7,29 (1 H, m), 6,32 (1 H, s), 4,43 - 4,32 (2 H, m), 4,18 -4,12 (2 H, m), 3,99 - 3,91 (1 H, m), 3,87 - 3,58 (5 H, m), 3,50 - 3,42 (1 H, m), 2,97 - 2,90 (2 H, m), 1,60 (6 H, s) MW (calc.): 396,4; MW (obs.): 397,3 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-3-metil-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 156)
Compuesto 156 se prepara por medio del método general I usando el intermedio 34.
Compuesto 157: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(3-h¡drox¡-pent¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 9 intermedio 35 Compuesto 157
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 35)
El intermedio 35 se prepara por medio del método general G usando el intermedio 9 y pent-1 -in-3-ol.
(1H, CDCI3) 5 ppm 7,62 - 7,57 (1 H, m), 7,41 - 7,35 (1 H, m), 7,33 (1 H, s), 6,34 (1 H, s), 4,60 - 4,53 (1 H, m), 4,45 -4,33 (2 H, m), 4,20 - 4,14 (2 H, m), 4,00 - 3,92 (1 H, m), 3,88 - 3,59 (5 H, m), 3,51 - 3,42 (1 H, m), 2,99 - 2,90 (2 H, m), 1,90 - 1,74 (2 H, m), 1,07 (3 H, t)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 157)
El compuesto 157 se prepara por medio del método general I usando el intermedio 35.
Compuesto 158: 9-(2,2-d¡met¡l-propox¡)-2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡dro-p¡rim¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Síntesis completamente descrita con anterioridad.
Compuesto 159: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(tetrah¡dro-p¡ran-4-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general L con el intermedio 6 y éster tetrahidro-piran-4-ilmetílico de ácido metansulfónico.
Compuesto 160: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(4-h¡drox¡-4-met¡l-pent¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
intermedio 9 intermedio 36 Compuesto 160
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (intermedio 36)
Un vial se cargó con el intermedio 9 (0,15 g, 0,324 mmol, 1 eq.), 2-metil-5-trimetilsilanil-pent-4-in-2-ol (66 mg, 0,389 mmol, 1,2 eq), CuI (2,5 mg, 0,013 mmol, 0,04 eq.), iPr2NH (0,41 mL, 2,92 mmol, 9 eq.) y THF (2 mL). La solución se purgó con Ar durante 15 min. y Pd(PPh3)Cl2 (11 mg, 0,016 mmol, 0,05 eq.) se añadió con TBAF (0,39 mL, 0,39 mmol, 1,2 eq., 1 M en THF). El vial se selló y la reacción se calentó hasta 80 °C durante 16 h. La mezcla de reacción se evaporó hasta sequedad y el producto crudo se purificó por TLC preparativa [DCM/MeOH, 98/2] para obtener el intermedio 36 2-((S)-1 -[1,4]dioxan-2-ilmetoxi)-9-(4-hidroxi-4-metil-pent-1 -inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
(1H, CDCla) 5 ppm 7,70 - 7,58 (1 H, m), 7,45 - 7,38 (1 H, m), 7,35 (1 H, s), 6,37 (1H, s), 4,50 - 4,30 (2 H, m), 4,28 - 4,15 (2 H, m), 4,05 - 3,95 (1 H, m), 3,95 - 3,55 (5 H, m), 3,55 - 3,40 (1 H, m), 3,05 - 2,95 (2 H, m), 2,62 (2 H, s),1,39 (6 H, s) MW (calc.): 410,5; MW (obs.): 411,4
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(4-hidroxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 160)
El compuesto 160 se prepara por medio del método general I usando el intermedio 36.
Compuesto 161: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(tetrah¡dro-p¡ran-4-¡lmetox¡met¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general E usando el intermedio 9 y 4-(tetrahidropiranilmetoxi)metiltrifluoroborato de potasio.
Compuesto 162: 2-([1,4]d¡oxan-2-¡lmetox¡)-9-metox¡-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Intermediario 37
Compuesto 162 Intermediario 38
Etapa 1 :1-[2-(3-metoxi-fenil)-etil]-pirimidin-2,4,6-triona (intermedio 37)
Sodio (236 mg, 10,2 mmol, 2 eq.) se añadió a EtOH desgasificado (18 mL), cuando el sodio se disolvió por completo, malonato de etilo (1,56 mL, 10,2 mmol, 2 eq.) se añadió y la reacción se calentó a reflujo durante 1 h. El intermedio 1 (995 mg, 5,12 mmol, 1 eq.) en EtOH (4 mL) luego se añadió y la reacción se calentó a reflujo durante 1 día. El intermedio 37 deseado 1 -[2-(3-metoxi-fenil)-etil]-pirimidin-2,4,6-triona se precipitó después de la adición de HCl acuoso 2 N, se filtró y se lavó con H2O y, finalmente, se secó.
(1H, DMSO-cfe) 5 ppm 7,27 - 7,18 (1 H, m), 6,84 - 6,72 (3 H, m), 3,92 - 3,83 (2 H, m), 3,75 (3 H, s), 3,62 (2 H, s), 2,80 - 2,70 (2 H, m)
MW (calc.): 262,3; MW (obs.): 263,3 (M+1)
Etapa 2 :2-cloro-9-metoxi-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (intermedio 38)
El intermedio 37 (920 mg, 3,51 mmol, 1 eq.) se calentó en POCl3 (5 mL) a 50 °C durante 2 días. Las sustancias volátiles se evaporaron al vacío, el residuo se disolvió en DCM y se lavó con una solución acuosa saturada de NaHCO3, antes de secar sobre MgSO4. La evaporación de la fase orgánica dio el intermedio 382-cloro-9-metoxi-6,7-dihidropirimido[6,1-a]isoquinolin-4-ona, que se usó en la siguiente etapa sin ulterior purificación.
(1H, CDCh) 5 ppm 7,73 - 7,66 (1 H, m), 6,98 - 6,90 (1 H, m), 6,85 - 6,80 (1 H, m), 6,69 (1 H, s), 4,00 - 4,20 (2 H, m), 3,91 (3 H, s), 3,04 (2 H, m)
Etapa 3 :2-([1,4]dioxan-2-ilmetoxi)-9-metoxi-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (compuesto 162) El [1,4]dioxan-2-il-metanol (42 mg, 0,36 mmol, 2 eq.) se disolvió en DCM (3 mL) con NaH (14 mg, 0,36 mmol, 2 eq., 60% en aceite mineral). Después de 30 min, el intermedio 38 (50 mg, 0,18 mmol, 1 eq.) se añadió a la mezcla y la reacción se agitó a temperatura ambiente durante 16 h. La mezcla de reacción se evaporó hasta sequedad y el producto crudo se purificó por HPLC-MS preparativa para proporcionar el compuesto 162.
(1H, CDCl3) 5 ppm 7,68 - 7,62 (1 H, m), 6,95 - 6,87 (1 H, m), 6,82 - 6,77 (1 H, m), 6,29 (1 H, s), 4,51 - 4,35 (2 H, m), 4,26 - 4,17 (2 H, m), 4,05 - 3,92 (1 H, m), 3,91 - 3,60 (8 H, m), 3,55 - 3,44 (1 H, m), 3,04 - 2,94 (2 H,m)
MW (calc.): 344,4; MW (obs.): 345,0
Compuesto 163: 2-((S)-1-[1,4]d¡oxan-2-¡lmetox¡)-9-(oxetan-3-¡lmetox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Este compuesto se prepara por medio del método general L usando el intermedio 6 y éster oxetan-3-ilmetílico de ácido metansulfónico.
Compuesto 164: 9-(3-c¡cloprop¡l-propox¡)-2-((R)-1-[1,4]d¡oxan-2-¡lmetox¡)-6,7-d¡h¡drop¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona.
Una solución del intermedio 6 (1,15 g, 3,48 mmol, 1 eq.) y 3-ciclopropan-1-ol (0,349 g, 3,48 mmol, 1eq.) en 1,4-dioxano se desgasificó con argón durante 10 min. PPh3 (1,096 g, 4,18 mmol, 1,2 eq.) se añadió y la mezcla de reacción se
desgasificó con argón durante 5 min más. DIAD (0,745 mL, 3,83 mmol, 1,1 eq.) se añadió gota a gota a 0 °C. La mezcla de reacción se agitó a temperatura ambiente durante 16 h. 3-Ciclopropilpropan-1-ol (0,150 mg, 1,49 mmol, 0,43 eq.) y PPh3 (0,30 g, 1,14 mmol, 0,33 eq.) se añadieron. La mezcla de reacción se enfrió hasta 0 °C y DIAD (0,350 mL, 1,80 mmol, 5,2 eq.) se añadió. Después de 1 h a temperatura ambiente, la mezcla de reacción se concentró al vacío y el producto crudo se purificó por cromatografía flash en gel de sílice para obtener el compuesto 164.
(1H, DMSO-afe) 5 ppm 7,93 (1H, d), 6,97-6,92 (2 H, m), 6,53 (1H, s), 4,24-4,23 (2H, m), 4,08 (2H, t), 4,00 (2H, t), 3,98 3,74 (3H, m), 3,68-3,57 (2H, m), 3,51-3,48 (1H, m), 3,37 (1H, t), 2,96 (2H, t), 1,84-1,80 (2H, m), 1,36-1,30 (2H, m), 0,81-0,63 (1H, m), 0,42-0,39 (2H, m), 0,04-0,02 (2H, m) MW (calc.): 412,5; MW (obs.): 413,0 (M+1) Compuesto 165: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
intermedio 9 intermedio 39 Compuesto 165
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 39)
El intermedio 39 se preparó por medio del método general G usando el intermedio 9 y 3-metoxi-propino.
(1H, CDCla) 5 ppm 7,68 (1 H, d), 7,48 (1 H, d), 7,42 (1 H, s), 6,40 (1 H, s), 4,50 - 4,41 (2 H, m), 4,38 (2 H, s), 4,23 (2 H, t), 4,05 - 3,98 (1 H, m), 3,89 - 3,70 (5 H, m), 3,55 - 3,50 (4 H, m), 3,03 (2 H, t)
MW (calc.): 382,4; MW (obs.): 383,4 (M+1)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 165)
El compuesto 165 se preparó por medio del método general I usando el intermedio 39.
Compuesto 166: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-[2-(1-hidroxi-ciclopentil)-etil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
intermedio 9 intermedio 40 Compuesto 166
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(1-hidroxi-ciclopentiletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 40)
El intermedio 40 se prepara por medio del método general G usando el intermedio 9 y 3-metoxi-propino. (1H, CDCI3) 5 ppm 7,54 (1 H, d), 7,31 (1 H, d), 7,26 (1 H, s), 6,28 (1 H, s), 4,39 - 4,30 (2 H, m), 4,12 (2 H, t), 3,95 - 3,91 (1 H, m), 3,82 - 3,58 (5 H, m), 3,50 (1 H, m), 3,16 (1 H, s), 2,89 (2 H, t), 2,05 - 1,98 (4 H, m), 1,90 - 1,70 (4H, m)
Etapa 2: 2-((S)-1-[1,4]dioxan-2-ilmetoxi)-9-[2-(1-hidroxi-ciclopentil)-etil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 166)
El compuesto 166 se preparó por medio del método general I usando el intermedio 40.
Compuesto 167: 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-tetrahidro-piran-4-iletinil)-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona.
Este compuesto se prepara por medio del método general G usando el intermedio 10 y 4-etinil-tetrahidropiran-4-ol. Compuesto 168: 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
intermedio 10 intermedio 41 Compuesto 168
Etapa 1: 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 40)
El intermedio 41 se prepara por medio del método general G usando el intermedio 10 y 3-metoxi-propino.
(1H, CDCla) 5 ppm 7,56 (1 H, d), 7,48 (1 H, d), 7,33 (1 H, s), 6,27 (1 H, s), 4,32 - 4,27 (2 H, m), 4,23 (2 H, s), 4,08 (2 H, t), 3,88 - 3,85 (1 H, m), 3,76 - 3,49 (5 H, m), 3,40 - 3,34 (4 H, m), 2,90 (2 H, t)
Etapa 2: 2-((R)-1-[1,4]dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 165)
El compuesto 168 se prepara por medio del método general I usando el intermedio 41.
Compuesto 169: 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-[2-(1-hidroxi-ciclopentil)-etil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
intermedio 10 intermedio 42 Compuesto 169
Etapa 1: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(1-hidroxi-ciclopentiletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Intermedio 42)
El intermedio 42 se prepara por medio del método general G usando el intermedio 10 y 1-Etinil-ciclopentanol.
(1H, CDCl3) 5 ppm 7,47 (1 H, d), 7,25 (1 H, d), 7,20 (1 H, s), 6,22 (1 H, s), 4,32 - 4,24 (2 H, m), 4,05 (2 H, t), 3,88 - 3,85 (1H, m), 3,77 - 3,52 (5 H, m), 3,38 (1H, t), 2,83 (2 H, t), 2,02 - 1,90 (4H, m), 1,85 - 1,67 (4H, m)
Etapa 2: 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(1-hidroxi-ciclopentiletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona (Compuesto 169)
El compuesto 169 se prepara por medio del método general I usando el intermedio 42.
Compuesto 170: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-propoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
El intermedio 6 (0,15 g, 0,45 mmol, 1 eq.), 2-propoxi-etanol (63 pL, 0,55 mmol, 1,2 eq.) y PPh3 (144 mg, 0,55 mmol, 1,2 eq.) se suspendieron en 1,4-dioxano (5 mL) y la mezcla se desgasificó con N2. d Ia D (0,108 mL, 0,55 mmol, 1,2 eq.) se añadió y la reacción se agitó a temperatura ambiente durante la noche. 0,5 eq. de DIAD y PPh3 se añadieron y la mezcla de reacción se agitó a temperatura ambiente durante 2 h extra. La mezcla de reacción se diluyó con salmuera, se extrajo con EtOAc, se secó sobre MgSÜ4 y se concentró. El producto crudo se purificó en columna de gel de sílice para dar el compuesto 170.
Compuesto 171: 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-isopropoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona
intermedio 6 Compuesto 171
El intermedio 6 (0,15 g, 0,45 mmol, 1 eq.), 2-isopropoxi-etanol (63 pL, 0,55 mmol, 1,2 eq.) y PPh3 (144 mg, 0,55 mmol, 1,2 eq.) se suspendieron en 1,4-dioxano (5 mL) y la mezcla se desgasificó con N2. DlAD (0,108 mL, 0,55 mmol, 1,2 eq.) se añadió y la reacción se agitó a temperatura ambiente durante 5 h. 0,5 eq. de DIAD y PPh3 se añadieron y la mezcla de reacción se agitó a temperatura ambiente durante la noche. La mezcla de reacción se diluyó con salmuera, se extrajo con EtOAc, se secó sobre MgSO4 y se concentró. El producto crudo se purificó en columna de gel de sílice para dar el compuesto 171.
Compuesto 172: 2-((R)-1-[1,4]D¡oxan-2-¡lmetox¡)-9-(2-propox¡-etox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
El intermedio 7 (0,25 g, 0,76 mmol, 1 eq.), 2-propoxi-etanol (105 pL, 0,91 mmol, 1,2 eq.) y PPh3 (238 mg, 0,91 mmol, 1,2 eq.) se suspendieron en 1,4-dioxano (10 mL) y la mezcla se desgasificó con N2. DIAD (0,180 mL, 0,91 mmol, 1,2 eq.) se añadió y la reacción se agitó a temperatura ambiente durante la noche. 0,3 eq. de DIAD y PPh3 se añadieron y la mezcla de reacción se agitó a temperatura ambiente durante 24 h extra. La mezcla de reacción se diluyó con salmuera, se extrajo con EtOAc, se secó sobre MgSÜ4 y se concentró. El producto crudo se purificó en columna de gel de sílice para dar el compuesto 172.
Compuesto 173: 2-((R)-1-[1,4]D¡oxan-2-¡lmetox¡)-9-(2-¡sopropox¡-etox¡)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
El intermedio 7 (0,25 g, 0,76 mmol, 1 eq.), 2-isopropoxi-etanol (105 pL, 0,91 mmol, 1,2 eq.) y PPh3 (238 mg, 0,91 mmol, 1,2 eq.) se suspendieron en 1,4-dioxano (10 mL) y la mezcla se desgasificó con N2. DIAD (0,180 mL, 0,91 mmol, 1,2 eq.) se añadió y la reacción se agitó a temperatura ambiente durante 5 h. 0,3 eq. de DIAD y PPh3 se añadieron y la mezcla de reacción se agitó a temperatura ambiente durante la noche. La mezcla de reacción se diluyó con salmuera, se extrajo con EtOAc, se secó sobre MgSO4 y se concentró. El producto crudo se purificó en columna de gel de sílice para dar el compuesto 173.
Compuesto 174: 2-((S)-1-[1,4]D¡oxan-2-¡lmetox¡)-9-(4-metox¡-but¡l)-6,7-d¡h¡dro-p¡r¡m¡do[6,1-a]¡soqu¡nol¡n-4-ona
Etapa 1 :3-metoxi-propil-trifluoroborato de potasio
intermedio 43
En un recipiente de base redonda de 2 bocas equipado con un condensador de reflujo y un embudo de adición se cargó con Mg (471 mg, 19,20 mmol, 3 eq.) y Et2O (2 mL) bajo N2. Una gota de (2-bromo-etil)-ciclopropano puro se añadió seguido por dos gotas de dibromoetano. Una vez que las primeras burbujas aparecieron, se añadió 1-bromo-3-metoxi-propano (1 g, 6,54 mmol, 1 eq.) en Et2O (10 mL) gota a gota. Después de completar la adición, la suspensión resultante se agitó a temperatura ambiente durante 1 h. En un recipiente separado, purgado con N2, una solución hecha de B(OMe)3 (1,1 mL, 9,81 mmol, 1,5 eq.) en THF (12 mL) se enfrió hasta -78 °C. A esta solución, la suspensión de bromuro de 3-metoxi-propilmagnesio se añadió gota a gota por medio de una aguja de doble extremo. La mezcla se dejó agitar durante 1 h a -78 °C y luego se calentó a temperatura ambiente durante 1 h. Después de enfriar la mezcla hasta 0 °C, una solución acuosa saturada de KHF2 (5,8 mL, 4,5 M, 4,1 eq.) se añadió gota a gota y la mezcla de reacción se dejó calentar a temperatura ambiente. Después de 30 min, la solución se concentró al vacío. Los sólidos secos se trituraron con acetona caliente y se filtraron para remover sales inorgánicas. El filtrado resultante se concentró
y el residuo sólido se trituró con Et2Ü. 3-metoxi-propil-trifluoroborato de potasio, intermedio 43, se filtró y se secó al vacío.
(1H, DMSO-afe) 5 ppm 3,19 - 3,13 (5 H, m), 1,38 - 1,29 (2 H, m), -0,1 - 0,19 (2 H, m)
Etapa 2 :2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-metoxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona El compuesto 174 se prepara por medio del método general E usando los intermedios 9 y 43.
Tabla II: Datos de espectros de masa de los compuestos de la invención
MW: Peso molecular
calc.: calculado
obs.: observado
Tabla III: Datos de RMN de los compuestos de la invención
(2 H,
Ejemplos biológicos
1. Ensayos i n v i t r o
1 . 1 . E n s a y o b a s a d o e n c é l u l a s : E n s a y o d e u n i ó n G T p - y S .
El siguiente ensayo se puede usar para la determinación de la activación de GPR84. El ensayo de unión de [35S]GTPyS mide el nivel de activación de la proteína G después de la ocupación agonista de un GPCR, mediante la determinación de la unión del análogo no hidrolizable [35S] GTPyS a las subunidades Ga.
El ensayo se realiza en una placa de 96 pocillos en la que se añaden los reactivos siguientes. Primero se añaden 50 gL de compuesto a la placa de ensayo, seguido de la adición de 20 gL de 3,3'-diindolilmetano a una concentración de EC80 (concentración que da 80% de la actividad de GPR84). En una última etapa se añaden 30 gl de una mezcla que consiste en perlas de membranas-GTPYS-SpA [la mezcla consiste en membranas de 20 gg/pocillo derivadas de una línea celular estable que sobreexpresa GPR84 (las membranas se preincuban con 0,1 gM de GDP durante 15 min a 4 ° C), 0,1 nM de perlas [35S]GTPyS (Perkin Elmer, NEG030) y 0,5 mg/pocillo de perlas Pv T-WGA SpA (Perkin Elmer, RPNQ0001)]. Todos los componentes se diluyen en tampón de ensayo que contiene HEPES 20 mM pH 7,4; MgCl25 mM; NaCl 250 mM; BSA 0,05%; saponina 75 ug/mL. Las reacciones se incuban durante 90 minutos a temperatura ambiente seguido por centrifugación a 2000 rpm durante 15 min. Las placas se leen en un lector Topcount (Perkin Elmer) inmediatamente después de la centrifugación (tiempo de lectura, 1 min/pocillo).
TABLA IV: IC50 de GTPyS (nM) para el ensayo GPR84 de compuestos de la invención seleccionados
na: no activos
* > 1001 nM
* * 501-1000 nM
* * * 101-500 nM
* ***0.01 - 100 nM
2. Ensayos celulares
2.1. Ensayo de migración de neutrófilos humanos
Los autores han establecido los agonistas GPR84 (MCFA tal como el decanoato de sodio, 3,3'-di-indol¡lmetano y Embelina inducen la quimiotaxis de neutrófilos y que los antagonistas de GPR84 pueden bloquear la quimiotaxis inducida por agonistas GPR84 pero no la quimiotaxis inducida por IL8, lo que indica que el receptor acoplado a proteína G-84 (GPR84) es un actor esencial en el proceso de reclutamiento de neutrófilos.
Por lo tanto, el efecto de los agonistas o antagonistas para GPR84 se puede analizar en una prueba de migración de neutrófilos. En el ensayo de migración de neutrófilos, los neutrófilos, recién aislados de las capas leucocitarias de voluntarios humanos, se tratan con un compuesto durante 30 minutos. Posteriormente, los neutrófilos se transfieren a los pocillos superiores de un sistema de soporte permeable a transwell 96 de Corning HTS, cuyos pocillos inferiores se llenan con una solución de embelina a ECso (concentración que da 80% de la actividad de GPR84). Después de 1
h de incubación, la migración de los neutrófilos hacia la embelina en el compartimiento inferior se puede cuantificar mediante la medición del contenido de ATP de los pocillos inferiores usando el sistema de ensayo de detección de ATP de luminiscencia ATPlite (Perkin Elmer, Núm. De catálogo: 436110).
2.1.1 Aislamiento de neutrófilos de capa leucocitaria humana
Se diluye una capa leucocitaria humana con un volumen igual de DPBS enfriado con hielo. Se mezclan suavemente 20 ml de la capa leucocitaria diluida con 4 ml de tampón ACD (ácido cítrico 140 mM, citrato de sodio 200 mM y dextrosa 220 mM). A continuación, se añaden a la mezcla 12 ml de la solución de dextranol 6%/NaCl 0,9% (15 g de dextrano T2000 y 2,25 g de NaCl disuelto en 250 ml de H2O) y las muestras se invierten suavemente hasta 20 veces. El volumen total se transfirió a un nuevo recipiente y se incubó a temperatura ambiente durante 1 h para que se produjera la separación completa de las dos fases. El sobrenadante amarillento luego se transfiere a un tubo de centrifugación limpio y se centrifuga durante 12 minutos a 1300 rpm y 4 °C. Después de la centrifugación, el sobrenadante se descarta y el sedimento celular restante se resuspende rápidamente en 12 ml de H2O helada para que se produzca la lisis de los eritrocitos. Después de 20 segundos, se añadieron 4 ml de KCl 0,6 M enfriado con hielo. Las muestras se mezclan cuidadosamente y se centrifugan durante 6 minutos a 1300 rpm, 4°C. El sobrenadante se descarta y el procedimiento de lisis de los eritrocitos se repite una vez más. Posteriormente, el sedimento celular se resuspende en 4 ml de DPBS y se coloca en capa sobre 5 ml de Lymphoprep (Nycomed Pharma, Núm. Cat .: 1114545) en un tubo de centrífuga de 15 ml. Después de la centrifugación durante 12 min a 1300 rpm, 4 °C, el sobrenadante se retira y el sedimento celular, que contiene los neutrófilos, se resuspende en 25 ml de tampón de quimiotaxis (medio RPMI 1640, suplementado con HEPES 10 mM, recién hecho para cada experimento)
2.1.2 Ensayo de migración
Se prepara una suspensión celular de 8,9x106 células por mililitro. Se añaden 20 gl de solución de compuesto en tampón de quimiotaxis a 180 gl de suspensión celular. La mezcla se incuba a 37 °C durante 30 minutos con resuspensión intermedia de las células después de 15 minutos. Después de esto, se transfieren 70 gl de suspensión de células al compartimiento superior de un sistema de soporte permeable de transwell 96 de Corning HTS con membrana de policarbonato de tamaño de poro de 5,0 gm (Corning, catálogo N.°: 3387). El pocillo receptor del sistema transwell luego se llena con 200 gL de tampón de quimiotaxis que contiene compuesto y agente quimiotáctico (embelina). Después de la incubación a 37 °C en CO25% durante 1 h, la placa superior del sistema transwell se retira y la suspensión celular de la placa receptora se transfiere a una placa de parte inferior en V de 96 pocillos. Se añaden 50 gl de DPBS a la placa receptora para evitar que las células restantes se sequen. La placa de parte inferior en V se centrifuga durante 6 minutos a 1500 rpm. El sobrenadante se retira y las células se resuspenden en 50 gL de DPBS. Las células luego se transfieren de nuevo a la placa receptora del sistema transwell. Después de esto, se añadieron 100 gL de solución de ATPlite (Perkin Elmer, n° de cat.: 436110) a las células. La placa se incuba durante 10 minutos en la oscuridad, mientras se agita. Luego se transfieren 170 gl de lisado celular a una placa de 96 pocillos blanca y se mide la luminiscencia. La señal luminiscente detectada se considera linealmente relacionada con el número de células que han migrado del pocillo superior al pocillo receptor.
TABLA VII: inhibición de la migración de neutrófilos humanos
*>1001 nM
*** íojteSTObM
****0,01-100 nM
2.2. Ensayo de migración de neutrófilos de rata
Los autores han establecido los agonistas GPR84 (MCFA tal como el decanoato de sodio, 3,3'-di-indolilmetano y Embelina inducen la quimiotaxis de neutrófilos y que los antagonistas de GPR84 pueden bloquear la quimiotaxis inducida por agonistas GPR84 pero no la quimiotaxis inducida por IL8, lo que indica que el receptor acoplado a proteína G-84 (GPR84) es un actor esencial en el proceso de reclutamiento de neutrófilos.
Por lo tanto, el efecto de los agonistas o antagonistas para GPR84 se puede analizar en una prueba de migración de neutrófilos. En el ensayo de migración de neutrófilos de rata, los neutrófilos, recién aislados de la rata después de la inyección intraperitoneal de glucógeno (0,1%, w/v), se tratan con un compuesto durante 30 minutos. Posteriormente, los neutrófilos se transfieren a los pocillos superiores de un sistema de soporte permeable a transwell 96 de Corning HTS, cuyos pocillos inferiores se llenan con una solución de embelina a EC80 (concentración que da 80% de la actividad de GPR84). Después de 1 h de incubación, la migración de los neutrófilos hacia la embelina en el compartimiento inferior se puede cuantificar mediante la medición del contenido de ATP de los pocillos inferiores usando el sistema de ensayo de sustrato Cell Titer Glow (Promega, Cat.N°.: G755B).
2.2.1. Aislamiento de neutrófilos de ratas
24 h después de la inyección intraperitoneal de glucógeno (0,1%, p/v), las células se recolectan mediante lavado peritoneal con 25 ml de HBSS y luego se centrifugan durante 12 minutos a 1300 rpm y 4 °C. Después de la centrifugación, el sobrenadante se descarta y el sedimento celular restante se resuspende rápidamente en 12 ml de H2O helada para que se produzca la lisis de los eritrocitos. Después de 20 segundos, se añadieron 4 ml de KCl 0,6 M enfriado con hielo. Las muestras se mezclan cuidadosamente y se centrifugan durante 6 minutos a 1300 rpm, 4 °C. El sobrenadante se descarta y el sedimento celular se resuspende en 4 ml de DPBS y se coloca en capa sobre 5 ml de Lymphoprep (Axis Shield, Cat N.°: 1114544) en un tubo de centrífuga de 15 ml. Después de la centrifugación durante 30 minutos a 1500 rpm, 4 °C, el sobrenadante se retira y el sedimento celular, que contiene los neutrófilos, se resuspende en 5 ml de tampón de quimiotaxis (medio RPMI 1640, suplementado con HEPES 10 mM, recién preparado para cada experimento).
2.2.2. Ensayo de migración
Se prepara una suspensión celular de 8,9x106 células por mililitro. Se añaden 10 pl de solución de compuesto en tampón de quimiotaxis a 90 pl de suspensión celular. La mezcla se incuba a 37 °C durante 30 minutos con resuspensión intermedia de las células después de 15 minutos. Después de esto, se transfieren 75 pl de suspensión de células al compartimiento superior de un sistema de soporte permeable de transwell 96 de Corning HTS con membrana de policarbonato de tamaño de poro de 5,0 pm (Corning, catálogo N.°: 3387). El pocillo receptor del sistema transwell luego se llena con 200 pL de tampón de quimiotaxis que contiene compuesto y agente quimiotáctico (embelina). Después de la incubación a 37 °C en CO25% durante 1 h, la placa superior del sistema transwell se retira y se añaden 70 pl de sustrato Cell Titer Glow (Promega, n° cat.: G755B) a la placa receptora. La placa receptora se incuba durante 10 minutos en la oscuridad, mientras se agita. Luego se transfieren 180 p l de lisado celular a una placa de 96 pocillos blanco y se mide la luminiscencia. La señal luminiscente detectada se considera linealmente relacionada con el número de células que han migrado del pocillo superior al pocillo receptor.
3. Modelos de ADME, PK y seguridad
3.1 Solubilidad acuosa
A partir de un patrón de 10 mM en DMSO, se prepara una dilución seriada del compuesto en DMSO. La serie de dilución se transfiere a una placa 96 NUNC Maxisorb de parte inferior F y se añade tampón de fosfato 0,1 M pH 7,4 o tampón de citrato 0,1 M pH 3,0 a temperatura ambiente.
Las concentraciones finales varían de 18,75 a 300 pM en 5 etapas de dilución iguales. La concentración final de DMSO no excede 3%.
Se añaden 200 pM de pireno a los puntos de esquina de cada placa de 96 pocillos y sirve como punto de referencia para la calibración del eje Z en el microscopio.
Las placas de ensayo se sellan y se incuban durante 1 h a 37 °C mientras se agitan a 230 rpm. A continuación, las placas se escanean bajo un microscopio de luz blanca, que produce imágenes individuales del precipitado por concentración. El precipitado se analiza y convierte en un número por una herramienta de software desarrollada a la medida. La primera concentración a la que el compuesto parece estar completamente disuelto es la concentración indicada, sin embargo la concentración verdadera se encuentra entre esta concentración y una etapa de dilución más alta.
Los valores de solubilidad se informan en pM y en pg/mL.
3.2. Solubilidad termodinámica
Se preparan dos soluciones individuales de 2 mg/ml de compuesto en un tampón de fosfato 0,1 M, pH 7,4, o un tampón de citrato 0,1 M, pH 3,0, a temperatura ambiente, en un vial de vidrio de 2 ml.
Después de la adición de una agitación magnética, las muestras se agitan a temperatura ambiente durante 24 h.
Después de 24 h, los viales se centrifugan 10 min a 1400 rpm. El sobrenadante de la muestra se transfiere a continuación a una placa de solubilidad MultiscreenR (Millipore, MSSLBPC50) y se filtra (10-12 "Hg) con la ayuda de un colector de vacío en una placa limpia de 96 pocillos de parte inferior en V de polipropileno Greiner. Por muestra, se realizan dos diluciones (factor 10 y 100) en DMSO. Se pueden realizar otras diluciones si el área de pico adquirida no está dentro de la curva estándar.
Un patrón de DMSO 10 mM, hecho de materia seca, se usa para hacer un patrón de trabajo de 200 pg/mL. La curva estándar para el compuesto se prepara en DMSO a partir del patrón de trabajo de 200pg/mL. Se realizan ocho concentraciones y dos muestras de control de calidad (QC) en tubos de 2 ml. Las primeras 3 concentraciones (50, 35 y 15 pg/ml) y la primera muestra QC (20 pg/ml) se realizan a partir del patrón de trabajo de 200 pg/ml. La 4a concentración (5 pg/ml) se hace con la solución de 50 pg/ml y la 5a concentración (1 pg/ml) con la solución de 15
|jg/ml. Las últimas tres concentraciones (0,2, 0,1 y 0,05 jg/ml) se hacen con la solución 1 jg/m l. La segunda muestra QC (0,5 jg/m l) se hace con la primera muestra QC.
De cada etapa de la dilución seriada, las diluciones del control de calidad y muestras, se transfiere un volumen a una placa Deepwell de 96 pocillos. Las muestras se inyectan en un sistema LC-MS/MS (API2000 de Applied Biosystems).
Las muestras se analizan en LC-MS/MS con un caudal de flujo de 0,5 ml/min. El solvente A es ácido fórmico 0,1% en agua y el solvente B es ácido fórmico 0,1% en metanol. La muestra se corre bajo pulverización de ion positivo sobre una columna Pursuit 5 C18 2,0 mm (Varian). El gradiente de solvente tiene un tiempo de corrida total de 1,4 minutos y varía de 10% de B a 100% de B.
Las muestras de solubilidad termodinámica se analizan con la ayuda del software QuanLynx. Para la curva estándar se puede utilizar una curva lineal o cuadrática en el análisis. Se excluyen las muestras de la curva estándar que tienen más de un 15% de desviación; las concentraciones más bajas de la curva pueden variar hasta un 20%. Las áreas de pico de las muestras se trazan contra la curva estándar para obtener la solubilidad del compuesto.
Los valores de solubilidad se informan en jM o jg/mL.
3.3 Estabilidad microsómica
Una solución madre 10 mM de compuesto en DMSO se diluyó 1,668 veces en un tampón de fosfato 105 mM pH 7,4. De esta dilución compuesta, se transfieren 50 j l en dos placas de 96 ensayos: una para el punto de tiempo 0 min (placa T0) y una para el punto de tiempo 30 min (placa T30) y precalentada a 37 °C.
En la muestra de referencia de tiempo cero (placa T0), se añaden 100 jL de MeOH (1: 1) a los pocillos. En cada placa de ensayo (T0 y T30 min), se añaden luego 50 j l de mezcla microsómica.
Las concentraciones de reacción finales son: 3 jM de compuesto, 0,5 mg/mL de microsomas, 0,4 U/mL de GDPDH, 3.3 mM de MgCL, 3,3 mM de glucosa-6-fosfato y 1,3 mM de NADP+.
La placa T30 se incuba a 37 °C, 300 rpm y después de 30 minutos de incubación la reacción se detiene con MeOH (1: 1). Las muestras se mezclan, se centrifugan y el sobrenadante se recolecta para análisis en LC-MS/MS (API2000 de Applied Biosystems).
Las muestras se analizan en LC-MS/MS con un caudal de flujo de 0,5 ml/min. El solvente A es ácido fórmico 0,1% en agua y el solvente B es ácido fórmico al 0,1% en metanol. La muestra se corre bajo pulverización de ion positivo sobre una columna Pursuit 5 C18 2,0 mm (Varian). El gradiente de solvente tiene un tiempo de corrida total de 1,4 minutos y varía de 10% de B a 100% de B. El área del pico del compuesto original en el tiempo 0 se considera que es 100% restante. El porcentaje restante después de 30 minutos de incubación se calcula a partir del tiempo 0. La solubilidad del compuesto en la concentración final del ensayo en el tampón se inspecciona por microscopio y también se informan los resultados.
3.4 Estabilidad de los hepatocitos
Los compuestos de ensayo (concentración inicial 1 gM, n = 2) se incuban en medio E de Williams, que contiene 4 mM de L-glutamina y 2 mM de sulfato de magnesio, con hepatocitos criopreservados mezclados (Celsis International) en suspensión a densidades celulares de 0,25-0,5 millones células viables/ml. Las incubaciones se realizan a 37 °C en un baño de agua con agitación con 100 gL de muestras tomadas de la incubación a 0, 10, 20, 45 y 90 minutos, y las reacciones terminadas por adición de 100 gL de acetonitrilo que contiene carbamazepina como estándar interno analítico. Las muestras se centrifugan y las fracciones sobrenadantes se analizan por LC-MS/MS. Las respuestas del instrumento (es decir, las alturas de los picos) se hacen referencia a las muestras de punto de tiempo cero (como 100%) para determinar el porcentaje de compuesto que queda. Se usan gráficos de Ln del % restante para cada compuesto para determinar la vida media de las incubaciones de hepatocitos. Los valores de vida media se calculan a partir de la relación: T1/2 (min) = -0,693/A,, donde A es la pendiente de la curva de concentración Ln versus tiempo. Los compuestos estándar testosterona, midazolam, y 4-metilumbeliferona se incluyen en el diseño del ensayo.
3.5 Unión de proteína plasmática (Diálisis de equilibrio)
Una solución patrón de 10 mM del compuesto en DMSO se diluye con un factor 10 en DMSO. Esta solución se diluye adicionalmente en plasma humano, rata, ratón o perro recién descongelado (BioReclamation INC) con una concentración final de 5 gM y concentración final de DMSO de 0,5%.
Se prepara una placa Pierce Red Device con insertos (ThermoScientific) y se llena con 450 j l de PBS en la cámara de tampón y 300 j l del plasma enriquecido en la cámara de plasma. La placa se incuba durante 4 h a 37 °C mientras se agita a 100 rpm. Después de la incubación, se transfirieron 120 j l de ambas cámaras a 480 j l de metanol en una placa de pocillos profundos PP, de fodon redondo y 96 pocillos (Nunc) y se sella con una tapa de lámina de aluminio. Las muestras se mezclan y se centrifugan inmediatamente 30 min a 1400 rcf a 4 °C y el sobrenadante se transfiere a una placa de PP de 96 de parte inferior en V (Greiner, 651201) para análisis en Lc -MS/MS (API2000 de Applied Biosystems).
Las muestras se analizan en LC-MS/MS con un caudal de flujo de 0,5 ml/min. El solvente A es ácido fórmico 0,1% en agua y el solvente B es ácido fórmico 0,1% en metanol. La muestra se corre bajo pulverización de ion positivo sobre una columna Pursuit 5 C18 2,0 mm (Varian). El gradiente de solvente tiene un tiempo de corrida total de 1,4 minutos y varía de 10% de B a 100% de B.
El área de pico del compuesto en la cámara de tampón y la cámara de plasma se considera que es compuesto al 100%. El porcentaje unido al plasma se deriva de estos resultados y se indica como porcentaje unido al plasma. La solubilidad del compuesto en la concentración de ensayo final en PBS se inspecciona por microscopio para indicar si se observa o no la precipitación.
3.6 Permeabilidad de Caco2
Los ensayos de Caco-2 bidireccionales se realizan como se describe a continuación. Las células Caco-2 se obtienen de European Collection of Cell Cultures (ECACC, catálogo 86010202) y se usan después de un cultivo celular de 21 días en placas Transwell de 24 pocillos (Corning, área de crecimiento celular: 0,33 cm2 , tamaño de poro de membrana: 0,4 gM, diámetro de membrana: 6,5 mm).
Se siembran 2x105 células/pocillo en medio de siembra consistente en DMEM GlutaMAX™-I 1 NEAA 1% FBS 10% (FetalClone II) Pen/strip 1%. El medio se cambia cada 2 - 3 días.
Los compuestos de referencia y ensayo (propanolol y rodamina 12 A {3} o vinblastina, todos adquiridos de Sigma) se preparan en una solución salina equilibrada de Hanks que contiene HEPES 25 mM (pH 7,4) y se añade a las cámaras apicales (125 gL) o basolaterales (600 gl) del ensamblaje de placa Transwell a una concentración de 10 gM con una concentración final de DMSO 0,25%.
Se añade 50 gM de Amarillo Lucifer (Sigma) se añade al tampón donante en todos los pocillos para evaluar la integridad de las capas celulares mediante el control de la permeación de Amarillo Lucifer. Como Amarillo Lucifer (LY) no puede penetrar libremente las barreras lipófilas, un alto grado de transporte LY indica una mala integridad de la capa celular.
Después de una incubación de 1 h a 37 °C mientras se agita en un agitador orbital a 150 rpm, se toman alícuotas de 70gL de ambas cámaras apicales (A) y basales (B) y añadidas a 100 gL de solución de acetonitrilo: agua 50:50 que contiene un estándar interno analítico (carbamazepina 0,5 gM) en una placa de 96 pocillos.
El amarillo Lucifer se mide con un Spectramax Gemini XS (Ex 426nm y Em 538nm) en una placa limpia de 96 pocillos que contiene 150 gl de líquido desde el lado apical y basolateral.
Las concentraciones del compuesto en las muestras se miden por cromatografía líquida de alta resolución/espectroscopia de masas (LC-MS/MS).
Los valores de permeabilidad aparente (Papp) se calculan a partir de la relación:
Papp = |CO m pueS tO ] aceptorfinal x V aceptor / ( [CO m pUSSÍO jdona1te inlcla|-* V donanlc1 /T |nc x V donamc/á re a superficial X 60 X 10 1 cm/s
V = volumen de la cámara
Tinc = tiempo de incubación.
Área de superficie = 0,33 cm2
Las relaciones Efflux, como una indicación del eflujo activo de la superficie celular apical, se calculan utilizando la relación Papp B> A/Papp A> B.
Se utilizan los siguientes criterios de aceptación del ensayo:
Propranolol: valor Papp (A>B) > 20(x10-6 cm/s)
Rodamina 123 o Vinblastina: Valor Papp (A>B) < 5 (x10-6 cm/s) con relación de eflujo >5.
Permeabilidad de amarillo Lucifer: <100 nm/s
3.7 Responsabilidad por la prolongación del intervalo QT
El potencial para la prolongación de QT se evalúa en el ensayo de pinzamiento clonal manual de hERG.
3.7.1 Pinzamiento clonal de célula entera convencional
Los registros de pinzamiento clonal de células enteras se realizan usando un amplificador EPC10 controlado por el software Pulse v8.77 (HEKA). La resistencia de la serie es típicamente inferior a 10 MQ y compensada por más del 60%, los registros no se restan fugas. Los electrodos se fabrican a partir de vidrio de pipeta GC150TF (Harvard). La solución de baño externa contiene: NaCl 135 mM, KCl 5 mM, CaCl2 1,8 mM, Glucosa 5 mM, HEPES 10 mM, pH 7,4.
La solución de pipeta zonal interna contiene: Kgluconato 100 mM, KCl 20 mM, CaCl2 1 mM, MgCl2 1 mM, Na2ATP 5 mM, Glutatión 2 mM, EGTA 11 mM, HEPES 10 mM, pH 7,2.
Los fármacos se perfunden usando un sistema de perfusión rápida Biologic MEV-9/EVH-9.
Todos los registros se realizan en células HEK293 que expresan de forma estable canales hERG. Las células se cultivan en cubreobjetos redondos de 12 mm (vidrio alemán, Bellco) anclados en la cámara de registro usando dos varillas de platino (Goodfellow). Las corrientes hERG se evocan usando un pulso de activación de 40 mV durante 1000 ms seguido de un impulso de corriente de cola a -50 mV durante 2000 ms, el potencial de retención es de -80 mV. Los pulsos se aplican cada 20s y todos los experimentos se realizan a temperatura ambiente.
3.7.2 Análisis de datos
Los valores de IC50 se calculan para cada compuesto analizado. Se calcula la diferencia del nivel entre la IC50 en el pinzamiento clonal hERG manual y la IC50 no unida en el ensayo de sangre entera.
Para las curvas de respuesta de concentración, se mide la amplitud de corriente de cola de pico durante la etapa de voltaje a -50 mV. El ajuste de curvas de datos de concentración-respuesta se realiza usando la ecuación:
y = a [( b - a )/ (1+ 10a ( ( logc-x) d )]
donde a es la respuesta mínima, b es la respuesta máxima y d es la pendiente de Hill, esta ecuación se puede usar para calcular tanto IC50 (donde y = 50 y c es el valor IC50) e IC20 (donde y = 20 y c es el valor IC20). El software GraphPad® Prism® (Graphpad® Software Inc.) se utiliza para el total del ajuste de curva. Una diferencia de 100 veces o mayor indica un bajo potencial para la prolongación QT.
3.8 Estudio farmacocinético
3.8.1 Estudio farmacocinético de dosis única en ratas
Los compuestos se formulan en PEG200/mezclas fisiológicas salinas para la vía intravenosa y en PEG400 /metilcelulosa 0,5% (10/90 v/v) para la vía oral. Los compuestos de ensayo se dosifican oralmente como una cebadura esofágica única a 5-10 mg/kg y dosificados por vía intravenosa como un bolo a través de la vena caudal a razón de 1 mg/kg a ratas Sprague-Dawley macho. Cada grupo consiste en 3 ratas. Las muestras de sangre se recolectan a través de la vena yugular usando ratas canuladas o en el seno retro-orbital con heparina de litio como anticoagulante en los puntos de tiempo en el rango siguiente: 0,05 a 8 h (vía intravenosa) y 0,25 a 6 ó 24 h (vía oral). Las muestras de sangre entera se centrifugan a 5000 rpm durante 10 min y las muestras de plasma resultantes se almacenan a -20 °C hasta efectuar el análisis.
3.8.2 Estudio farmacocinético de dosis múltiple en ratas
Los compuestos se formulan en PEG400/metilcelulosa 0,5% (10/90 v/v) para la vía oral. Los compuestos de ensayo se dosifican oralmente como una cebadura esofágica diaria a 30 ó 300 mg/kg a ratas Sprague-Dawley macho durante 14 días. Cada grupo consiste en 3 ratas. Las muestras de sangre se recolectan a través de la vena de la cola con heparina de litio como anticoagulante en los siguientes puntos de tiempo el día 1, 7 y 14: 0,25, 1, 4, 8 y 24 h. Además, en el día 2 se toman muestras de sangre a 0,25, 1 y 4 h y en el día 4 y 11 a 0,25 h. Las muestras de sangre entera se centrifugan a 5000 rpm durante 10 min y las muestras de plasma resultantes se almacenan a -20 ° C hasta efectuar el análisis.
3.8.3 Cuantificación de los niveles del compuesto en plasma
Las concentraciones plasmáticas de cada compuesto de ensayo se determinan mediante un método LC-MS/MS en el que el espectrómetro de masas se opera en modo de electroaspersión positivo o negativo.
3.8.4 Determinación de parámetros farmacocinéticos
Los parámetros farmacocinéticos se calculan usando Winnonlin® (Pharsight®, US).
3.9 Estudio de toxicidad de rata de 7 días
Se realiza un estudio de toxicidad oral de 7 días con compuestos de ensayo en ratas macho Sprague-Dawley para evaluar su toxicidad y toxicocinética tóxica, a dosis diarias de 100, 300 y 1000 mg/kg/día, por cebadura, con el volumen de dosis constante de 10 ml/kg/día.
Los compuestos de ensayo se formulan en PEG400/metilcelulosa 0,5% (10/90, v/v). Cada grupo incluye 6 ratas machos principales así como 3 animales satélites para toxicocinética. Un cuarto grupo se administra PEG400/metilcelulosa 0,5% (10/90, v/v) solamente, a la misma frecuencia, volumen de dosis y por la misma vía de administración, y actúa como el grupo de control del vehículo.
El objetivo del estudio es determinar la dosis más baja que produce eventos adversos identificados (sin nivel de efecto adverso observable - NOAEL).
3.10 Inhibición de citocromo P450
La inhibición del CYP reversible y la inhibición del CYP3A4 dependiente del tiempo se determinan en los microsomas del hígado humano y sustratos de sonda específicos.
3.10.1 Inhibición de P450 en microsomas hepáticos humanos, inhibición reversible
El potencial inhibidor de un compuesto de ensayo se evalúa para las isoenzimas del citocromo P450 humano CYP1A2, 2C8, 2C9, 2C19, 2D6 y 3A4.
Se prepara una solución patrón de 10 mM del compuesto de ensayo en DMSO, se diluye en serie en tampón de Tris (100 mM, pH 7,4) y se añade a microsomas hepáticos (Xenotech LLC) y NADPH a 37 °C en un baño de agua con agitación. Se obtienen siete concentraciones diferentes de compuestos de ensayo (0,05 a 100 pM), DMSO 1% y NADPH 1 mM para reaccionar.
Después de 15 o 30 minutos las reacciones se terminan por la adición de 100 pl de acetonitrilo que contiene carbamazepina como estándar interno analítico. Las muestras se centrifugan y las fracciones del sobrenadante se analizan por LC-MS/MS. Para cada isoforma, se hace referencia a las respuestas del instrumento (alturas de pico) a las de los controles DMSO (consideradas como 100%) para determinar el porcentaje de reducción en el metabolismo de sonda, usando imidazolam y testosterona como sustrato de sonda. El porcentaje de inhibición del metabolismo de sonda y Log [concentración del compuesto de ensayo] se representan gráficamente usando el software Graphpad Prism. El modelo de respuesta a la dosis sigmoidal se ajusta a los datos para determinar la IC50.
La inhibición de CYP3A4 usando nifedipina y atorvastatina como sustrato de sonda se lleva a cabo de la siguiente manera.
Se prepara una solución patrón 1,67 mM del compuesto de ensayo en metanol, se diluye en forma seriada 1: 3 en tampón de fosfato de potasio 50 mM pH 7,4 y se añade a los microsomas hepáticos humanos (BD Gentest) y sustrato de sona. Siete diferentes concentraciones de compuestos de ensayo (0,045 - 33,3 pM), metanol 2%, microsomas 0,1 mg/ml, atorvastatina 10 pM o nifedipina 5 pM. Después de un calentamiento previo de 5 minutos a 37 °C, se inició la reacción mediante la adición del la mezcla de cofactor (7,65 mg/ml de glucosa-6-fosfato, 1,7 mg/ml de NADP, 6 U/ml de glucosa-6-fosfato deshidrogenasa).
Después de 5 min (nifedipina) o 10 min (atorvastatina) a 37°C, la reacción (50 pL) se termina con 150 pL de solución de acetonitrilo:metanol (2:1) con un estándar interno (warfarina). Las muestras se centrifugan y las fracciones del sobrenadante se analizan por LC-MS/MS. Las respuestas del instrumento (relación de las áreas pico dell compuesto de ensayo /estándar interno) hacen referencia a las de los controles del solvente (asumidas como 100%) con el fin de determinar el porcentaje de reducción en el metabolismo de la sonda. Los gráficos de porcentaje de la actividad de control versus concentración se generan y se ajustan usando el software GraphPad Prism para generar IC50.
3.10.2 Inhibición de CYP3A4 en microsomas hepáticos humanos, dependiente del tiempo
El potencial inhibidor dependiente del tiempo de un compuesto de ensayo se evalúa para determinar la isoenzima 3A4 del citocromo P450 humano. El compuesto se preincuba con los microsomas hepáticos humanos antes de la adición de los sustratos de sonda. El resultado se compara con la condición en la que el compuesto no se preincuba con los microsomas hepáticos humanos para ver si existe un cambio en la IC50, lo que indica la inhibición dependiente del tiempo.
Se prepara una solución patrón de 10 mM del compuesto de ensayo en DMSO y se diluye 1:20 con tampón de Tris (100 mM pH 7,4) y también se diluye en forma seriada en tampón de T ris/DMSO 5%.
El cofactor, NADPH, y cada dilución del compuesto de ensayo se mezcla en dos placas separadas durante 0 y 30 min de preincubación. Se añaden microsomas hepáticos humanos (Xenotech LLC) solo a la placa "30 minutos de preincubación" y ambas placas se incuban a continuación durante 30 minutos a 37 °C en un baño de agua con agitación. Después de la preincubación, se añaden microsomas a la placa de "0 minutos" y se añaden sustratos de
sonda apropiados (en DMSO 0,5%) a ambas placas. Las placas luego se devuelven al baño de agua para una incubación adicional.
En total, se evalúan seis concentraciones diferentes de compuesto de ensayo (1,6 a 50 pM). Las reacciones se terminan con 100 pl de acetonitrilo que contiene carbamazepina como estándar analítico interno. Las muestras se centrifugan y las fracciones del sobrenadante se analizan por LC-MS/MS. Para cada isoforma, las respuestas del instrumento (relación de altura de pico con patrón interno) se hacen con referencia a las de los controles de DMSO (consideradas como 100%) con el fin de determinar el porcentaje de reducción en el metabolismo de la sonda. El porcentaje de inhibición del metabolismo de la sonda y Log [Concentración del compuesto de ensayo] se representan gráficamente utilizando el software Graphpad Prism. El modelo de respuesta a la dosis sigmoidal se ajusta los datos para determinar la IC50.
4. Estudios in vivo
La actividad in vivo de los compuestos de la invención puede demostrarse en los siguientes modelos de inflamación de eficacia in vivo.
4.1 Enfermedades intestinales inflamatorias (ratones)
El modelo de enfermedades intestinales inflamatorias (DII) inducido por DSS crónica de ratón es un modelo de enfermedad bien validado para las enfermedades intestinales inflamatorias (Wirtz S. et al., 2007 Nature Protocols 2, 541-546; Sina C. et al., 2009 J. Immunol. 1837514-7522).
Para inducir una colitis crónica, los ratones BALB/c hembras se alimentan con sulfato de sodio de dextrano 4% (DSS) disuelto en agua potable durante 4 días, seguido de 3 días de agua potable regular. Este ciclo se repite tres veces. Este protocolo permite inducir una colitis fuerte al mismo tiempo que se evitan altas tasas de mortalidad. Los animales se dividen en varios grupos:
a. agua intacta; vehículo solo, n=10),
b. enfermo (DSS; vehículo solo, n=10),
c. sulfasalazina usada ocmo referencia (DSS; 20 mg/kg/día, p.o., n=10) y
d. el compuesto analizado (DSS; 1,3, 10, 30 mg/kg/día, p.o., n=10).
Los parámetros clínicos se miden cada dos días. El índice de actividad de la enfermedad (DAI) es una medida compuesta que combina las puntuaciones individuales para la pérdida de peso, consistencia de las heces y sangrado rectal. Los ratones se sacrifican en el día 20 del experimento de acuerdo con el protocolo introducido por Sina et al. (2009). En el momento del sacrificio, se extrae el colon completo y se lava con PBS estéril. Los segmentos del colon distal se diseccionan para el análisis histológico, la expresión génica y la medición del nivel de proteína.
4.2 Artritis inducida por colágeno (ratones).
La artritis inducida por colágeno de ratón (CIA) es el modelo de artritis reumatoide de referencia (Brand, et al., 2007 Nature Protocols 2, 1269 - 1275, Lin et al., 2007 Br J Pharmacol 1, 829 - 831). Los ratones DBA1 // J machos se inyectan con una solución de colágeno II (adyuvante de Freund completo). La reacción inmunitaria se refuerza con una segunda inyección (adyuvante de Freund incompleto) 21 días después. Al día 31, la artritis se califica de acuerdo con el método de Khachigian et al. (Khachigian et al., 2006 Nature Protocols 1,2512-2516) y los animales se asignan aleatoriamente para alcanzar una puntuación clínica media de 2 por grupo. Los animales se dividen en varios grupos: intacto (sin tratamiento, n = 5), enfermo (vehículo solo, n = 10), Enbrel® como referencia (10 mg/kg, 3 x semana, ip, n = 10) y el compuesto analizado (3, 10 ó 30 mg/kg/día, p.o., n=10). La dosificación terapéutica duró desde el día 31 hasta el día 46 y la artritis se calificó todos los días. Los ratones se sacrifican al día 46, se toman fotos de rayos X de las patas traseras de cada animal individual y la gravedad de la erosión ósea se clasifica con la puntuación radiológica de Larsen (Salvemini y col., 2001 Arthritis Rheum 44, 2909-2921).
4.3 Modelo de humo de tabaco (ratones)
Las exposiciones diarias de ratones C57BL/6J hembra endogámicos al humo del tabaco (TS) durante 11 días consecutivos producen inflamación pulmonar, como lo indica un aumento en el número total de células recuperadas en el lavado broncoalveolar (BAL), en comparación con grupo expuesto al aire tratado de forma similar, 24 h después de la exposición final. El período de exposición a TS se incrementa inicialmente de 25 minutos al comienzo del estudio (día 1) hasta un máximo de 45 minutos en el día 3 hasta el día 11. Los animales se dividen en varios grupos: intacto (sin tratamiento, n = 5), enfermo (vehículo solo, n = 10), Roflumilast como referencia (5 mg/kg/día po, n = 10), y los compuestos analizados (10 ó 30 mg/kg/bid, po, n = 10). Al final de 11 días, se cuentan los números de macrófagos, células epiteliales, neutrófilos y linfocitos en el BAL. BAL se analiza además para la expresión génica y nivel de proteína. El tejido pulmonar se disecciona para el análisis histológico, la expresión génica y la medición del nivel de proteína.
Los expertos en la técnica apreciarán que las descripciones anteriores son ejemplificativas y de naturaleza explicativa, y se considera que ilustran la invención y sus realizaciones preferidas. A través de la experimentación de rutina, un profesional reconocerá las modificaciones y variaciones evidentes que se pueden realizar. Todas estas modificaciones que entran dentro del alcance de las reivindicaciones adjuntas están destinadas a ser incluidas en el mismo. Por lo tanto, se considera que la invención se define no por la descripción anterior, sino por las siguientes reivindicaciones. Todas las publicaciones citadas en esta memoria descriptiva se citan como referencias.
Se debe entender que factores tales como la capacidad de penetración celular diferencial de los diversos compuestos pueden contribuir a discrepancias entre la actividad de los compuestos en los ensayos bioquímicos y celulares in vitro. Al menos algunos de los nombres químicos del compuesto de la invención dado y expuesto en esta solicitud se pueden haber generado de forma automatizada mediante el uso de un programa de software de nomenclatura química comercialmente disponible, y no se han verificado de forma independiente. Los programas representativos que realizan esta función incluyen la herramienta de nomenclatura Lexichem vendida por Open Eye Software, Inc. y la herramienta Autonom Software vendida por MDL, Inc. En el caso en que el nombre químico indicado y la estructura representada difieran, regirá la estructura representada.
Las estructuras químicas mostradas en la presente se prepararon usando ChemDraw® o ISIS®/DRAW. Cualquier valencia abierta que aparece en un átomo de carbono, oxígeno o nitrógeno en las estructuras de la presente indica la presencia de un átomo de hidrógeno. Cuando existe un centro quiral en una estructura pero no se muestra estereoquímica específica para el centro quiral, ambos enantiómeros asociados con la estructura quiral están abarcados por la estructura.
REFERENCIAS
Wittenberger et al., 2001 J Mol Biol, 307, 799-813
Yousefi S et al., 2001 J Leukoc Biol, 69, 1045-52
Wang et al., 2006 The Journal of Biological Chemistry, 281,45, 34457-34464
Venkataraman et al., 2005, Immunology Letters, 101, 144-153
WO2007/027661 A2
Berry et al., 2010, Nature, 466, 973-979
Bouchard et al., 2007, Glia, 55:790-800
Bundgard, H., 1985 Design of Prodrugs, pp. 7-9, 21-24, Elsevier, Amsterdam 1985
Part 8 of Remington's Pharmaceutical Sciences, 17th edition, 1985, Mack Publishing Company, Easton, Pennsylvania T. W. Greene and P. G. M. Wuts, 2006 Protecting Groups in Organic Synthesis, Wiley-Blackwell; 4th Revised edition Young Kim et al., 2007 Bioorganic & Medicinal Chemistry 15, 2667-2679
Le Pouls et al., 2003, The Journal of Biological Chemistry, 278, 28, 25481-25489
Brown et al., 2003, The Journal of Biological Chemistry, 278, 13, 11312-11319
Stoddart et al., 2008, Pharmacological Reviews, 60, 405-417
Wirtz S. et al., 2007 Nature Protocols 2, 541-546
Sina C. et al., 2009 J. Immunol. 1837514-7522
Brand, et al., 2007 Nature Protocols 2, 1269-1275
Lin et al., 2007 Br J Pharmacol 1,862-872
Khachigian et al., 2006 Nature Protocols 1,2512-2516
Salvemini et al., 2001 Arthritis Rheum 44, 2909-2921
Du Bois, 2010, Nat Rev, Drug Discovery, 9, 129
Nagasaki et. al., 2012, FEBS Letters, 586, 368-372
Claims (15)
1. Un compuesto de acuerdo con la fórmula la:
R1 es H, Me o halo;
L1 está ausente o es -O-, -S- o -NR4a-;
G es
R2,
-W-L2-R2 , o
-W-L3-R3;
W es alquileno C1-4, alquenileno C2-4 que tiene un enlace doble o alquinileno C2-4 que tiene un enlace triple; L2 está ausente o es -O-;
R2 es
- H,
- alquilo C1-8, opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de o OH,
° halo,
o CN,
o alcoxi C1-6,
o cicloalquilo C3-7,
o heterocicloalquilo de 4-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O,
o heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, y
o fenilo,
- cicloalquenilo C4-7 que comprende un enlace doble,
- heterocicloalquenilo de 5-7 miembros que comprende un enlace doble y uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S,
- cicloalquilo C3-7 opcionalmente sustituido con uno o varios grupos R5 seleccionados, de modo independiente,
- heterocicloalquilo de 4-10 miembros que comprende uno a dos heteroátomos seleccionados, de modo independiente, de S y O, opcionalmente sustituido con uno a tres grupos R5 seleccionados de modo independiente,
- heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno a tres grupos R6 seleccionados de modo independiente, o
- arilo C6-10 opcionalmente sustituido con uno o varios grupos R6 seleccionados de modo independiente; L3 es -NR4b-;
R3 es
- alquilo C1-4 sustituido con
° arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o
° heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios R, grupos R7 seleccionados de modo independiente,
- heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente, o
- arilo C6-10 opcionalmente sustituido con uno o varios grupos R7 seleccionados de modo independiente; Cada R4a y R4b se selecciona, de modo independiente, de H, alquilo C1-4 y cicloalquilo C3-7;
R5 es oxo o R6;
R6 es
- OH,
- halo,
- -NO2 ,
- alquilo C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH,
- alcoxi C1-6 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de halo y OH,
- cicloalquilo C3-7,
- -C(=O)OR8,
- -C(=O)NR9R10,
- -NHC(=O)-alquilo C1-4,
- -CN,
- fenilo,
- -O-fenilo,
- heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S, o
- heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S, opcionalmente sustituido con uno o varios alquilo C1-4, alcoxi C1-4, CN, halo y -C(=O)OR11 seleccionados de modo independiente;
R7 es alquilo C1-4 o halo; y
cada uno de R8, R9, R10 y R11 se selecciona, de modo independiente, de H y alquilo C1-4,
o una de sus sales o solvatos farmacéuticamente aceptables o un solvato de la sal farmacéuticamente aceptable, para su uso en el tratamiento de la esclerosis múltiple.
2. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 1, en donde R1 es H.
4. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 3, en donde el compuesto es de acuerdo con la fórmula IIa y L1 está ausente.
5. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 3, en donde el compuesto es de acuerdo con la fórmula IIIa y L1 está ausente o es -O-; W es alquileno C1-4 o alquenileno C2-4 que tiene un enlace doble.
6. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 3, en donde el compuesto es de acuerdo con la fórmula IIIa y L1 está ausente; W es alquinileno C2-4 que tiene un enlace triple; y L2 y R2 son como se describe en la reivindicación 1.
7. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 5 ó 6, en donde L2 está ausente.
8. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 3, en donde el compuesto es de acuerdo con la fórmula IIIa, en donde L1 y L2 están ausentes, W es -CH2-CH2-, -CH=CH- o -CeC- y R2 es como se describe en la reivindicación 1.
9. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con cualquiera de las reivindicaciones 3-8, en donde R2 es heteroarilo de 5-10 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O, opcionalmente sustituido con uno a tres grupos R6 seleccionados de modo independiente.
10. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 9, en donde R6 se selecciona de OH, halo, alquilo C1-6 , alquilo C1-6 sustituido con uno o varios halo, alcoxi C1-6 , -CN, cicloalquilo C3-7 , heterocicloalquilo de 4-7 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, O y S y fenilo.
11. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con cualquiera de las reivindicaciones 3-8 en donde R2 es alquilo C1-8 opcionalmente sustituido con uno a tres grupos seleccionados, de modo independiente, de OH, halo, CN, alcoxi C1-6, cicloalquilo C3-7 , heterocicloalquilo de 4-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de S y O, heteroarilo de 5-6 miembros que comprende uno a tres heteroátomos seleccionados, de modo independiente, de N, S y O y fenilo.
12. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con cualquiera de las reivindicaciones 3-8, en donde R2 es cicloalquilo C3-7.
13. Un compuesto o su sal farmacéuticamente aceptable para su uso en el tratamiento de la esclerosis múltiple, de acuerdo con la reivindicación 1, en donde el compuesto se selecciona de:
9-Aliloxi-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-piridin-3-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-piridin-4-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo,
3- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo,
4- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo,
[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-iloxi]-acetonitrilo,
2-([1,4]Dioxan-2-ilmetoxi)-9-(oxazol-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(piridin-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(3,5-Dicloro-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Benzofuran-2-il-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
éster ter-butílico del ácido 2-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-indol-1-carboxílico,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-indol-2-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(6-metoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(6-trifluorometil-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-3H-imidazol-4-iletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(5-ter-Butil-[1,2,4]oxadiazol-3-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
metilamida del ácido 5-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-piridin-2-carboxílico,
2-([1,4]Dioxan-2-ilmetoxi)-9-pent-1 -inil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-piridin-2-il-etil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-pirazin-2-il-etil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-indol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(5-metoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-indazol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2- ([1,4]Dioxan-2-ilmetoxi)-9-(4-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
3- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzamida,
5- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-2-fluoro-benzamida, N-{3-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-fenil}-acetamida, 9-Ciclopropiletinil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1-hidroxi-ciclopentiletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-pirimidin-5-il-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclohex-1-enil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1-metil-1 H-indol-5-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(6-metil-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4] Dioxan-2-ilmetoxi)-9-piridin-2-iletinil-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
5-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-pent-4-inonitrilo,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(4-metoxi-feniletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4] Dioxan-2-ilmetoxi)-9-piridin-3-iletinil-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona,
4- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-N-metil-benzamida, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2-cloro-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(1,5-Dimetil-1 H-pirazol-3-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(1-metil-1 H-pirazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-[1,2,4]oxadiazol-5-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2- ([1,4]Dioxan-2-ilmetoxi)-9-(4-morfolin-4-il-fenil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
3- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-4-fluoro-benzamida, 3-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-5-fluoro-benzamida, 9-(3,3-Dimetil-but-1-inil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-piridin-4-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-isoxazol-5-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-metil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(2-metoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(3,6-Dihidro-2H-piran-4-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 5- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-piridin-2-carbonitrilo, 2-([1,4]Dioxan-2-ilmetoxi)-9-(6-isopropoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(6-etoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(6-morfolin-4-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(2,3-Dimetoxi-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(3-cloro-2-metoxi-piridin-4-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2- ([1,4]Dioxan-2-ilmetoxi)-9-(2-metil-piridin-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
3- [2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-isonicotinonitrilo, 9-(2,5-Dimetoxi-fenil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3,4,5,6-tetrahidro-2H-[1,2']bipiridinil-5'-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4- ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-etoxi-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2,6-Dimetoxi-piridin-3-il)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
4-[2-([1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-nicotinonitrilo,
9-ter-Butoximetil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(2-pirrolidin-1-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(6-pirrolidin-1-il-piridin-3-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(5-fenil-oxazol-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(5-ter-Butil-oxazol-2-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(5-Ciclopropil-[1,2,4]oxadiazol-3-ilmetoxi)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(5-etil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(5-metil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(5-isopropil-[1,2,4]oxadiazol-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopentiletinil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclohexiletinil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-hex-1 -inil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-[3-(Bencil-metil-amino)-prop-1-inil]-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-5-metil-hex-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-etil-3-hidroxi-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-fenil-but-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(3-Bencilamino-prop-1-inil)-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-[(furan-2-ilmetil)-amino]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1-etil-1 H-pirazol-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-[1 -(3-metil-butil)-1 H-pirazol-4-il]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(5-metil-furan-2-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-hex-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(3,5-Dimetil-1 H-pirazol-4-il)-2-([1,4]]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-(1H-pirazol-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(1-propil-1 H-pirazol-4-il)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-[2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo, 2-[2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-4-oxo-6,7-dihidro-4H-pirimido[6,1-a]isoquinolin-9-il]-benzonitrilo, 9-(5-Ciclopropil-[1,2,4]oxadiazol-3-ilmetoxi)-2-((R)-1 -[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-etinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-pirimidin-2-iletinil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-fenilamino-prop-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4] Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-piridin-3-il-prop-1 -inil)-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona, 9-Ciclopentiloximetil-2-([1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pent-1-inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclopropiletinil-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-(3-metil-but-1 -inil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-imidazol-1 -il-prop-1 -inil)-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona, 9-(2-Ciclopropil-etil)-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopentiloximetil-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-piridin-3-il-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Aliloxi-2-((R)-1 -[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Aliloxi-2-((S)-1 -[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-4-iloximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-([1,4]Dioxan-2-ilmetoxi)-9-{3-[(piridin-3-ilmetil)-amino]-prop-1-inil}-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1 -[1,4]Dioxan-2-ilmetoxi)-9-pentil-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropiletinil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2-Ciclopropil-etil)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(oxetan-3-iloximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metil-oxetan-3-ilmetoximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2,2-Dimetil-butilamino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-etil-hexilamino)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-metoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-etoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropilmetoxi-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-fluoro-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[3-(2-metoxi-etoxi)-prop-1 -inil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-[3-(2-etoxi-etoxi)-prop-1-inil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[3-(2-fluoro-etoxi)-prop-1 -inil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(2,2-Dimetil-propoximetil)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclohexiloximetil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-Ciclopropilmetoximetil-2-((S)-1-[1,4]]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(4,4-Dimetil-pentiloxi)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(3-Ciclopropil-propoxi)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclohexilamino-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-4,4-dimetil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-Ciclopentilmetoximetil-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-fenilamino-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(Ciclohexil-metil-amino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 9-(Ciclohexilmetil-amino)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-[(tetrahidro-piran-4-ilmetil)-amino]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-etil-3-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-3-metil-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-hidroxi-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(2,2-Dimetil-propoxi)-2-((S)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-4-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-4-metil-pentil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(tetrahidro-piran-4-ilmetoximetil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-([1,4]Dioxan-2-ilmetoxi)-9-metoxi-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(oxetan-3-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
9-(3-Ciclopropil-propoxi)-2-((R)-1-[1,4]dioxan-2-ilmetoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[2-(1 -hidroxi-ciclopentil)-etil]-6,7-dihidro-pirimido[6,1 -a]isoquinolin-4-ona, 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(4-hidroxi-tetrahidro-piran-4-iletinil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(3-metoxi-propil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1 -[1,4]Dioxan-2-ilmetoxi)-9-[2-(1 -hidroxi-ciclopentil)-etil]-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-propoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((S)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-isopropoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, 2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-propoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona,
2-((R)-1-[1,4]Dioxan-2-ilmetoxi)-9-(2-isopropoxi-etoxi)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona, and 2-((S)-1-[1,4]Dioxan-2-ihnetoxi)-9-(4-metoxi-butil)-6,7-dihidro-pirimido[6,1-a]isoquinolin-4-ona.
14. Una composición farmacéutica para su uso en el tratamiento de la esclerosis múltiple que comprende un compuesto o su sal farmacéuticamente aceptable, de acuerdo con cualquiera de las reivindicaciones 1-13 y un portador farmacéuticamente aceptable.
15. La composición farmacéutica para su uso en el tratamiento de la esclerosis múltiple de acuerdo con la reivindicación 14 que comprende otro agente terapéutico.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161578979P | 2011-12-22 | 2011-12-22 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2911449T3 true ES2911449T3 (es) | 2022-05-19 |
Family
ID=47520068
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12812237.1T Active ES2643379T3 (es) | 2011-12-22 | 2012-12-20 | Nuevas dihidropirimidinoisoquinolinonas y sus composiciones farmacéuticas para el tratamiento de trastornos inflamatorios |
| ES17184834T Active ES2911449T3 (es) | 2011-12-22 | 2012-12-20 | Dihidropirimidinoisoquinolinonas y sus composiciones farmacéuticas para el tratamiento de la esclerosis múltiple |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES12812237.1T Active ES2643379T3 (es) | 2011-12-22 | 2012-12-20 | Nuevas dihidropirimidinoisoquinolinonas y sus composiciones farmacéuticas para el tratamiento de trastornos inflamatorios |
Country Status (34)
| Country | Link |
|---|---|
| US (5) | US8927543B2 (es) |
| EP (3) | EP3378862B1 (es) |
| JP (1) | JP6062453B2 (es) |
| KR (1) | KR102012268B1 (es) |
| CN (1) | CN103998448B (es) |
| AR (1) | AR089284A1 (es) |
| AU (1) | AU2012357067B2 (es) |
| BR (1) | BR112014015142B1 (es) |
| CA (1) | CA2859578C (es) |
| CL (1) | CL2014001664A1 (es) |
| CO (1) | CO7010835A2 (es) |
| CR (1) | CR20140305A (es) |
| CY (2) | CY1119434T1 (es) |
| DK (2) | DK2794604T3 (es) |
| EA (1) | EA023826B1 (es) |
| ES (2) | ES2643379T3 (es) |
| HR (2) | HRP20171404T1 (es) |
| HU (1) | HUE12812237T4 (es) |
| IL (2) | IL233212B (es) |
| IN (1) | IN2014MN01033A (es) |
| LT (2) | LT2794604T (es) |
| MX (1) | MX351681B (es) |
| NI (1) | NI201400060A (es) |
| PE (1) | PE20141685A1 (es) |
| PH (1) | PH12014501178A1 (es) |
| PL (2) | PL2794604T3 (es) |
| PT (2) | PT3378862T (es) |
| SG (1) | SG11201403169PA (es) |
| SI (2) | SI3378862T1 (es) |
| TW (1) | TWI567073B (es) |
| UA (1) | UA111767C2 (es) |
| UY (1) | UY34545A (es) |
| WO (1) | WO2013092791A1 (es) |
| ZA (1) | ZA201404607B (es) |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UA117095C2 (uk) | 2011-12-22 | 2018-06-25 | Аліос Біофарма, Інк. | Нуклеозидна сполука або її фармацевтично прийнятна сіль |
| AR089284A1 (es) | 2011-12-22 | 2014-08-13 | Galapagos Nv | Dihidropirimidinoisoquinolinonas y composiciones farmaceuticas de las mismas para el tratamiento de trastornos inflamatorios |
| USRE48171E1 (en) | 2012-03-21 | 2020-08-25 | Janssen Biopharma, Inc. | Substituted nucleosides, nucleotides and analogs thereof |
| US9441007B2 (en) | 2012-03-21 | 2016-09-13 | Alios Biopharma, Inc. | Substituted nucleosides, nucleotides and analogs thereof |
| EP2935262B1 (en) | 2012-12-20 | 2017-03-15 | Galapagos NV | Novel dihydropyrimidinoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders (gpr84 antagonists) |
| GB201319677D0 (en) * | 2013-11-07 | 2013-12-25 | Eth Z Rich | Cyclopropanation |
| GB201411241D0 (en) * | 2014-06-25 | 2014-08-06 | Galapagos Nv | Novel dihydropyridoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| GB201506894D0 (en) * | 2015-04-23 | 2015-06-10 | Galapagos Nv | Novel dihydropyridoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders |
| CN108530480B (zh) * | 2017-03-06 | 2022-06-28 | 中国科学院上海药物研究所 | Gpr84受体拮抗剂及其应用 |
| EP3403649A1 (en) | 2017-05-16 | 2018-11-21 | Bayer Pharma Aktiengesellschaft | Inhibitors and antagonists of gpr84 for the treatment of endometriosis |
| CN111343986A (zh) | 2017-11-15 | 2020-06-26 | 加拉帕戈斯股份有限公司 | 用于治疗纤维化疾病的化合物及其药物组合物 |
| CR20220291A (es) | 2019-12-19 | 2022-08-10 | Bayer Ag | Derivados de furoindazol |
| WO2021123394A1 (en) | 2019-12-20 | 2021-06-24 | University Of Copenhagen | G protein-coupled receptor modulators and a pharmaceutical composition |
| WO2022112186A1 (en) | 2020-11-24 | 2022-06-02 | Galapagos Nv | Compound for use in and methods of treatment of fibrotic diseases |
| JP2024506858A (ja) | 2021-02-02 | 2024-02-15 | リミナル・バイオサイエンシーズ・リミテッド | Gpr84アンタゴニストおよびその使用 |
| CA3211437A1 (en) | 2021-02-23 | 2022-09-01 | Bayer Aktiengesellschaft | Furoindazole derivatives as gpr84 antagonists |
| WO2022194267A1 (zh) * | 2021-03-18 | 2022-09-22 | 武汉人福创新药物研发中心有限公司 | 一种gpr84拮抗剂及其制备方法和用途 |
| WO2022218372A1 (zh) * | 2021-04-14 | 2022-10-20 | 武汉人福创新药物研发中心有限公司 | 一种二氢嘧啶并异喹啉酮类衍生物及用途 |
| CA3218018A1 (en) | 2021-04-29 | 2022-11-03 | Bayer Aktiengesellschaft | Furoindazole derivatives as antagonists or inhibitors of gpr84 |
| US20250066335A1 (en) | 2021-06-18 | 2025-02-27 | University Of Copenhagen | Polysubstituted 4-hydroxypyridine and 4-hydroxyquinoline derivatives as gpr84 antagonists |
| JP7705966B2 (ja) * | 2021-06-21 | 2025-07-10 | 武漢人福創新薬物研発中心有限公司 | Gpr84アンタゴニストとしての三環式化合物 |
| CN115611944A (zh) | 2021-07-15 | 2023-01-17 | 中国科学院上海药物研究所 | 不对称gpr84拮抗剂及其用途 |
| WO2023076668A1 (en) * | 2021-10-29 | 2023-05-04 | Board Of Supervisors Of Louisiana State University And Agricultural And Mechanical College | Compositions and methods for treatment of cancer |
| GB202202297D0 (en) | 2022-02-21 | 2022-04-06 | Verona Pharma Plc | Formulation production process |
| WO2024083705A1 (en) | 2022-10-18 | 2024-04-25 | Bayer Aktiengesellschaft | Furoindazole derivatives for the treatment of pain |
| CN120569392A (zh) * | 2022-12-30 | 2025-08-29 | 广州市联瑞制药有限公司 | 三环类化合物及其制备方法和应用 |
| WO2024220480A2 (en) * | 2023-04-17 | 2024-10-24 | The Board Of Trustees Of The Leland Stanford Junior University | Method for detecting innate immune action in vivo using gpr84-pet |
| CN121620356A (zh) | 2023-06-26 | 2026-03-06 | 维罗纳制药公司 | 包含恩塞芬汀的颗粒组合物 |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2720085A1 (de) | 1977-05-05 | 1978-11-16 | Hoechst Ag | Pyrimido(6,1-a)isochinolin-2-on- derivate |
| AU744986B2 (en) * | 1997-07-12 | 2002-03-07 | Cancer Research Technology Limited | Cyclin dependent kinase inhibiting purine derivatives |
| JP2002543046A (ja) * | 1999-03-31 | 2002-12-17 | バーナリス・リミテッド | ピリミド[6,1−a]イソキノリン−4−オン誘導体 |
| US7501512B2 (en) * | 2003-07-08 | 2009-03-10 | Smithkline Beecham Corporation | Chemical compounds |
| WO2005050225A2 (en) | 2003-10-31 | 2005-06-02 | Bayer Healthcare Ag | Diagnostics and therapeutics for diseases associated with g protein-coupled receptor 84 (gpr84) |
| CA2621144A1 (en) | 2005-09-02 | 2007-03-08 | Arena Pharmaceuticals, Inc. | Human g protein-coupled receptor and modulators thereof for the treatment of atherosclerosis and atherosclerotic disease and for the treatment of conditions related to mcp-1 expression |
| US7989461B2 (en) | 2005-12-23 | 2011-08-02 | Amgen Inc. | Substituted quinazolinamine compounds for the treatment of cancer |
| US8217177B2 (en) * | 2006-07-14 | 2012-07-10 | Amgen Inc. | Fused heterocyclic derivatives and methods of use |
| AR073354A1 (es) | 2008-07-31 | 2010-11-03 | Genentech Inc | Compuestos de pirimidina, composiciones farmaceuticas y su uso en el tratamiento del cancer. |
| JP2011088847A (ja) * | 2009-10-21 | 2011-05-06 | Takeda Chem Ind Ltd | 三環性化合物およびその用途 |
| BR112014015298B1 (pt) | 2011-12-22 | 2021-06-15 | Connexios Life Sciences Pvt. Ltd | Composto derivado de aza-adamantano, composição farmacêutica e uso do composto |
| AR089284A1 (es) | 2011-12-22 | 2014-08-13 | Galapagos Nv | Dihidropirimidinoisoquinolinonas y composiciones farmaceuticas de las mismas para el tratamiento de trastornos inflamatorios |
| RU2669695C2 (ru) | 2011-12-22 | 2018-10-15 | Конекшис Лайф Сайенсиз Пвт. Лтд. | Циклические амидные производные как ингибиторы 11-бета-гидроксистероид-дегидрогеназы и их применение |
| JP5903499B2 (ja) | 2011-12-22 | 2016-04-13 | ノバルティス アーゲー | ジヒドロ−ベンゾ−オキサジンおよびジヒドロ−ピリド−オキサジン誘導体 |
| EP2935262B1 (en) | 2012-12-20 | 2017-03-15 | Galapagos NV | Novel dihydropyrimidinoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders (gpr84 antagonists) |
-
2012
- 2012-12-17 AR ARP120104774A patent/AR089284A1/es active IP Right Grant
- 2012-12-20 TW TW101148765A patent/TWI567073B/zh not_active IP Right Cessation
- 2012-12-20 HU HUE12812237A patent/HUE12812237T4/hu unknown
- 2012-12-20 PT PT171848344T patent/PT3378862T/pt unknown
- 2012-12-20 ES ES12812237.1T patent/ES2643379T3/es active Active
- 2012-12-20 WO PCT/EP2012/076275 patent/WO2013092791A1/en not_active Ceased
- 2012-12-20 PE PE2014000988A patent/PE20141685A1/es active IP Right Grant
- 2012-12-20 PL PL12812237T patent/PL2794604T3/pl unknown
- 2012-12-20 US US13/721,788 patent/US8927543B2/en active Active
- 2012-12-20 IN IN1033MUN2014 patent/IN2014MN01033A/en unknown
- 2012-12-20 AU AU2012357067A patent/AU2012357067B2/en not_active Ceased
- 2012-12-20 ES ES17184834T patent/ES2911449T3/es active Active
- 2012-12-20 BR BR112014015142-3A patent/BR112014015142B1/pt not_active IP Right Cessation
- 2012-12-20 HR HRP20171404TT patent/HRP20171404T1/hr unknown
- 2012-12-20 SI SI201231991T patent/SI3378862T1/sl unknown
- 2012-12-20 MX MX2014007363A patent/MX351681B/es active IP Right Grant
- 2012-12-20 LT LTEP12812237.1T patent/LT2794604T/lt unknown
- 2012-12-20 DK DK12812237.1T patent/DK2794604T3/da active
- 2012-12-20 EP EP17184834.4A patent/EP3378862B1/en active Active
- 2012-12-20 DK DK17184834.4T patent/DK3378862T3/da active
- 2012-12-20 JP JP2014547997A patent/JP6062453B2/ja not_active Expired - Fee Related
- 2012-12-20 EP EP12812237.1A patent/EP2794604B1/en active Active
- 2012-12-20 CN CN201280061536.3A patent/CN103998448B/zh not_active Expired - Fee Related
- 2012-12-20 EA EA201491245A patent/EA023826B1/ru not_active IP Right Cessation
- 2012-12-20 CA CA2859578A patent/CA2859578C/en active Active
- 2012-12-20 PL PL17184834T patent/PL3378862T3/pl unknown
- 2012-12-20 SI SI201231087T patent/SI2794604T1/sl unknown
- 2012-12-20 KR KR1020147020306A patent/KR102012268B1/ko not_active Expired - Fee Related
- 2012-12-20 EP EP22155038.7A patent/EP4019519A1/en not_active Withdrawn
- 2012-12-20 UA UAA201408294A patent/UA111767C2/uk unknown
- 2012-12-20 LT LTEP17184834.4T patent/LT3378862T/lt unknown
- 2012-12-20 SG SG11201403169PA patent/SG11201403169PA/en unknown
- 2012-12-20 HR HRP20220456TT patent/HRP20220456T1/hr unknown
- 2012-12-20 PT PT128122371T patent/PT2794604T/pt unknown
- 2012-12-21 UY UY0001034545A patent/UY34545A/es unknown
-
2014
- 2014-01-06 US US14/148,057 patent/US9255095B2/en active Active
- 2014-05-26 PH PH12014501178A patent/PH12014501178A1/en unknown
- 2014-06-18 IL IL233212A patent/IL233212B/en active IP Right Grant
- 2014-06-19 NI NI201400060A patent/NI201400060A/es unknown
- 2014-06-20 CL CL2014001664A patent/CL2014001664A1/es unknown
- 2014-06-23 ZA ZA2014/04607A patent/ZA201404607B/en unknown
- 2014-06-24 CR CR20140305A patent/CR20140305A/es unknown
- 2014-07-22 CO CO14158655A patent/CO7010835A2/es unknown
-
2015
- 2015-12-11 US US14/966,879 patent/US10047083B2/en active Active
-
2017
- 2017-10-11 CY CY20171101053T patent/CY1119434T1/el unknown
-
2018
- 2018-02-18 IL IL257581A patent/IL257581A/en unknown
- 2018-05-04 US US15/971,245 patent/US11220499B2/en active Active
-
2021
- 2021-11-12 US US17/454,712 patent/US20220227751A1/en not_active Abandoned
-
2022
- 2022-04-18 CY CY20221100292T patent/CY1125167T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2911449T3 (es) | Dihidropirimidinoisoquinolinonas y sus composiciones farmacéuticas para el tratamiento de la esclerosis múltiple | |
| EP2935262B1 (en) | Novel dihydropyrimidinoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders (gpr84 antagonists) | |
| CA2824460A1 (en) | Azetidine derivatives useful for the treatment of metabolic and inflammatory diseases | |
| WO2015197550A1 (en) | Novel dihydropyridoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders | |
| ES2963409T3 (es) | Derivados de pirazolopiridina como inhibidores de PASK | |
| HK1201528B (en) | Novel dihydropyrimidinoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders | |
| NZ626473B2 (en) | Novel dihydropyrimidinoisoquinolinones and pharmaceutical compositions thereof for the treatment of inflammatory disorders |