ES2929206T3 - Derivados de triazolo quinoxalina sustituidos - Google Patents
Derivados de triazolo quinoxalina sustituidos Download PDFInfo
- Publication number
- ES2929206T3 ES2929206T3 ES19742596T ES19742596T ES2929206T3 ES 2929206 T3 ES2929206 T3 ES 2929206T3 ES 19742596 T ES19742596 T ES 19742596T ES 19742596 T ES19742596 T ES 19742596T ES 2929206 T3 ES2929206 T3 ES 2929206T3
- Authority
- ES
- Spain
- Prior art keywords
- triazolo
- fluoro
- quinoxaline
- indol
- trimethyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- XSJMOLCRLLDSFM-UHFFFAOYSA-N 2h-triazolo[4,5-f]quinoxaline Chemical class C1=CC2=NC=CN=C2C2=NNN=C21 XSJMOLCRLLDSFM-UHFFFAOYSA-N 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 126
- 238000011282 treatment Methods 0.000 claims abstract description 12
- 238000011321 prophylaxis Methods 0.000 claims abstract description 7
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 178
- -1 Fluoro-1,4,4,9-tetramethyl-8-(3-prop-1-ynyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound 0.000 claims description 156
- OKKJLVBELUTLKV-UHFFFAOYSA-N methanol Substances OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 141
- 125000000217 alkyl group Chemical group 0.000 claims description 98
- PDOPFYRTIVSUKL-UHFFFAOYSA-N 4-(azepan-1-yl)-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1CCCCCN1C1=NC2=CC=CC=C2N2C1=NN=C2 PDOPFYRTIVSUKL-UHFFFAOYSA-N 0.000 claims description 82
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 68
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 claims description 52
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 49
- 125000001424 substituent group Chemical group 0.000 claims description 41
- XSCHRSMBECNVNS-UHFFFAOYSA-N quinoxaline Chemical compound N1=CC=NC2=CC=CC=C21 XSCHRSMBECNVNS-UHFFFAOYSA-N 0.000 claims description 34
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 claims description 30
- 125000003118 aryl group Chemical group 0.000 claims description 28
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 28
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 26
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 25
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 23
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 20
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 18
- 125000003161 (C1-C6) alkylene group Chemical group 0.000 claims description 18
- 229920006395 saturated elastomer Polymers 0.000 claims description 18
- 125000001072 heteroaryl group Chemical group 0.000 claims description 17
- 239000002253 acid Substances 0.000 claims description 15
- 125000002947 alkylene group Chemical group 0.000 claims description 15
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 claims description 12
- 229910052757 nitrogen Inorganic materials 0.000 claims description 12
- 150000003839 salts Chemical class 0.000 claims description 11
- 150000004702 methyl esters Chemical class 0.000 claims description 7
- 239000002552 dosage form Substances 0.000 claims description 6
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 5
- UHCBBWUQDAVSMS-UHFFFAOYSA-N fluoroethane Chemical compound CCF UHCBBWUQDAVSMS-UHFFFAOYSA-N 0.000 claims description 5
- INWFZHYGKKDJMD-UHFFFAOYSA-N 7-fluoro-8-(1H-indol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC=CC=2NC=CC1=2)F)C)C INWFZHYGKKDJMD-UHFFFAOYSA-N 0.000 claims description 4
- AZTQBZUSWRWEPP-UHFFFAOYSA-N 7-fluoro-8-(1H-indol-7-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=CC=CC=3C=CNC1=3)C)C(C)=NN=2)(C)C AZTQBZUSWRWEPP-UHFFFAOYSA-N 0.000 claims description 4
- UVLLFBVUNMLPPH-UHFFFAOYSA-N 8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4,9-tetramethyl-7-(trifluoromethoxy)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2C(=CNC2=C(C=1)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)OC(F)(F)F)C UVLLFBVUNMLPPH-UHFFFAOYSA-N 0.000 claims description 4
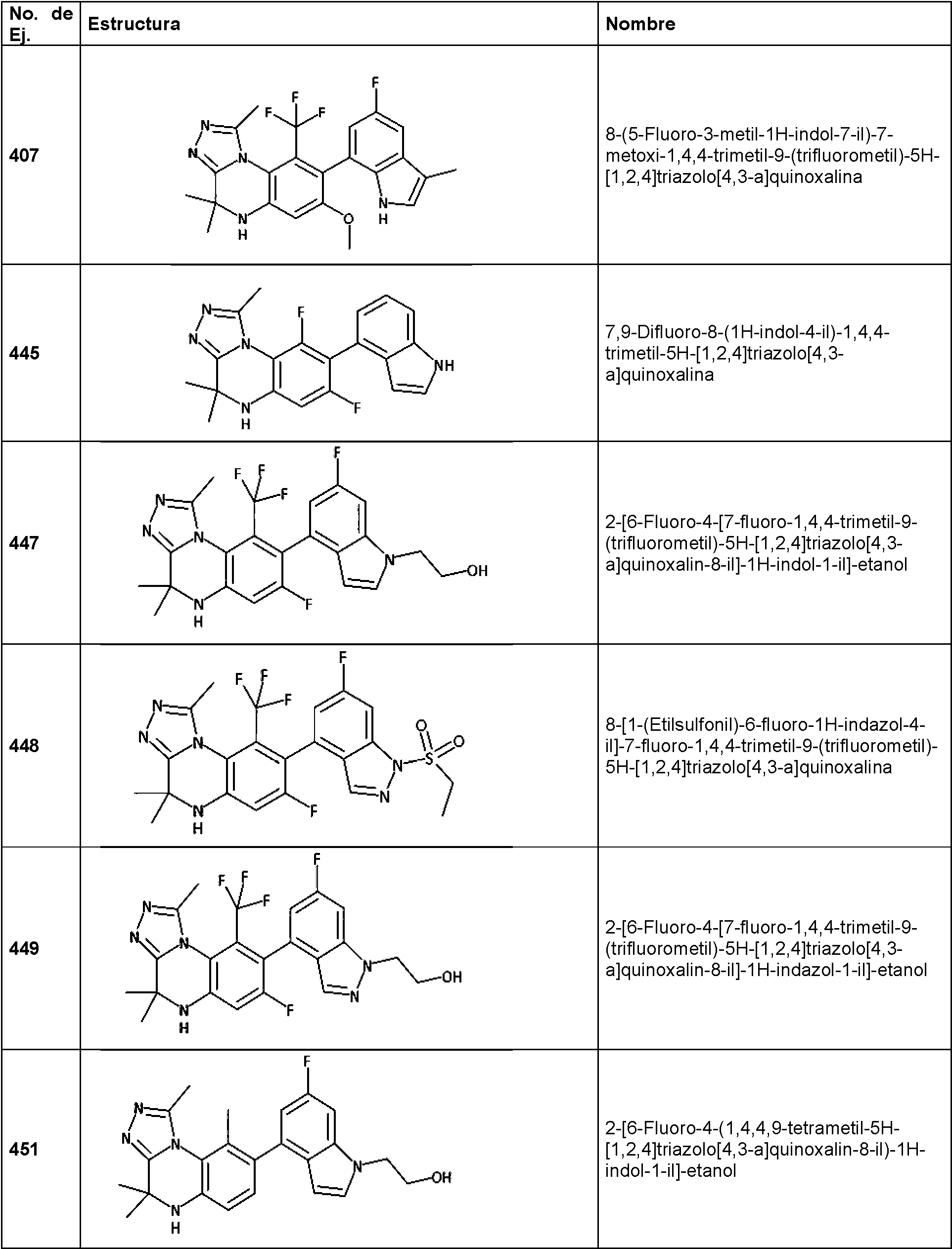
- FYTMPTPLTDTQOD-UHFFFAOYSA-N 8-(5-fluoro-3-methyl-1H-indol-7-yl)-7-methoxy-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2C(=CNC2=C(C=1)C1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)OC)C FYTMPTPLTDTQOD-UHFFFAOYSA-N 0.000 claims description 4
- 206010061218 Inflammation Diseases 0.000 claims description 4
- 229910052739 hydrogen Inorganic materials 0.000 claims description 4
- 230000004054 inflammatory process Effects 0.000 claims description 4
- PFFMOLTYNNYPFR-UHFFFAOYSA-N 1-but-2-ynyl-7,9-difluoro-4,4-dimethyl-8-(3-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC=CC=2C(C)=CNC1=2)F)CC#CC)C PFFMOLTYNNYPFR-UHFFFAOYSA-N 0.000 claims description 3
- JKFOPSAHHVMFHS-UHFFFAOYSA-N 1-but-2-ynyl-7,9-difluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C#CC)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=C(C=C2C(=CNC=12)C)F)F JKFOPSAHHVMFHS-UHFFFAOYSA-N 0.000 claims description 3
- BVOPULMOVZEKMM-UHFFFAOYSA-N 4-[7-(7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-1H-indol-3-yl]-2-methylbut-3-yn-2-ol Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC=CC=2C(C#CC(O)(C)C)=CNC1=2)F)C)C BVOPULMOVZEKMM-UHFFFAOYSA-N 0.000 claims description 3
- ITHKXUVZAPFRAH-UHFFFAOYSA-N 7-chloro-8-(6-fluoro-1-methylindol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)C)C)C(=NN=3)C)(C)C ITHKXUVZAPFRAH-UHFFFAOYSA-N 0.000 claims description 3
- XMBTZSXWWLRYFT-UHFFFAOYSA-N 7-fluoro-1,4,4-trimethyl-8-(1-methylsulfonylindazol-4-yl)-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C(F)(F)F)C1=C2C(=CC=C1)N(N=C2)S(=O)(=O)C)F)C)C XMBTZSXWWLRYFT-UHFFFAOYSA-N 0.000 claims description 3
- IFZPDQZDSFRCOH-UHFFFAOYSA-N 7-fluoro-8-(1H-indol-7-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=CC=CC=3C=CNC1=3)C(F)(F)F)C(C)=NN=2)(C)C IFZPDQZDSFRCOH-UHFFFAOYSA-N 0.000 claims description 3
- CASKFGCVJDUTQY-UHFFFAOYSA-N 7-fluoro-8-(6-fluoro-1-methylsulfonylindol-4-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C(F)(F)F)C1=CC(F)=CC=2N(C=CC1=2)S(=O)(=O)C)F)C)C CASKFGCVJDUTQY-UHFFFAOYSA-N 0.000 claims description 3
- UGTHSLSUEBYAFJ-UHFFFAOYSA-N 7-fluoro-8-[5-fluoro-3-(2,2,2-trifluoroethyl)-1H-indol-7-yl]-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC(F)=CC=2C(CC(F)(F)F)=CNC1=2)F)C)C UGTHSLSUEBYAFJ-UHFFFAOYSA-N 0.000 claims description 3
- AOWXXHMFVGURDO-UHFFFAOYSA-N 9-(difluoromethyl)-1,4,4-trimethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=CC=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)F AOWXXHMFVGURDO-UHFFFAOYSA-N 0.000 claims description 3
- NDFHFDRIDNWHFL-UHFFFAOYSA-N 9-fluoro-8-(6-fluoro-1-methylindol-4-yl)-1,4,4,7-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C1=C2C=CN(C2=CC(=C1)F)C NDFHFDRIDNWHFL-UHFFFAOYSA-N 0.000 claims description 3
- 206010065390 Inflammatory pain Diseases 0.000 claims description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 3
- 208000002193 Pain Diseases 0.000 claims description 3
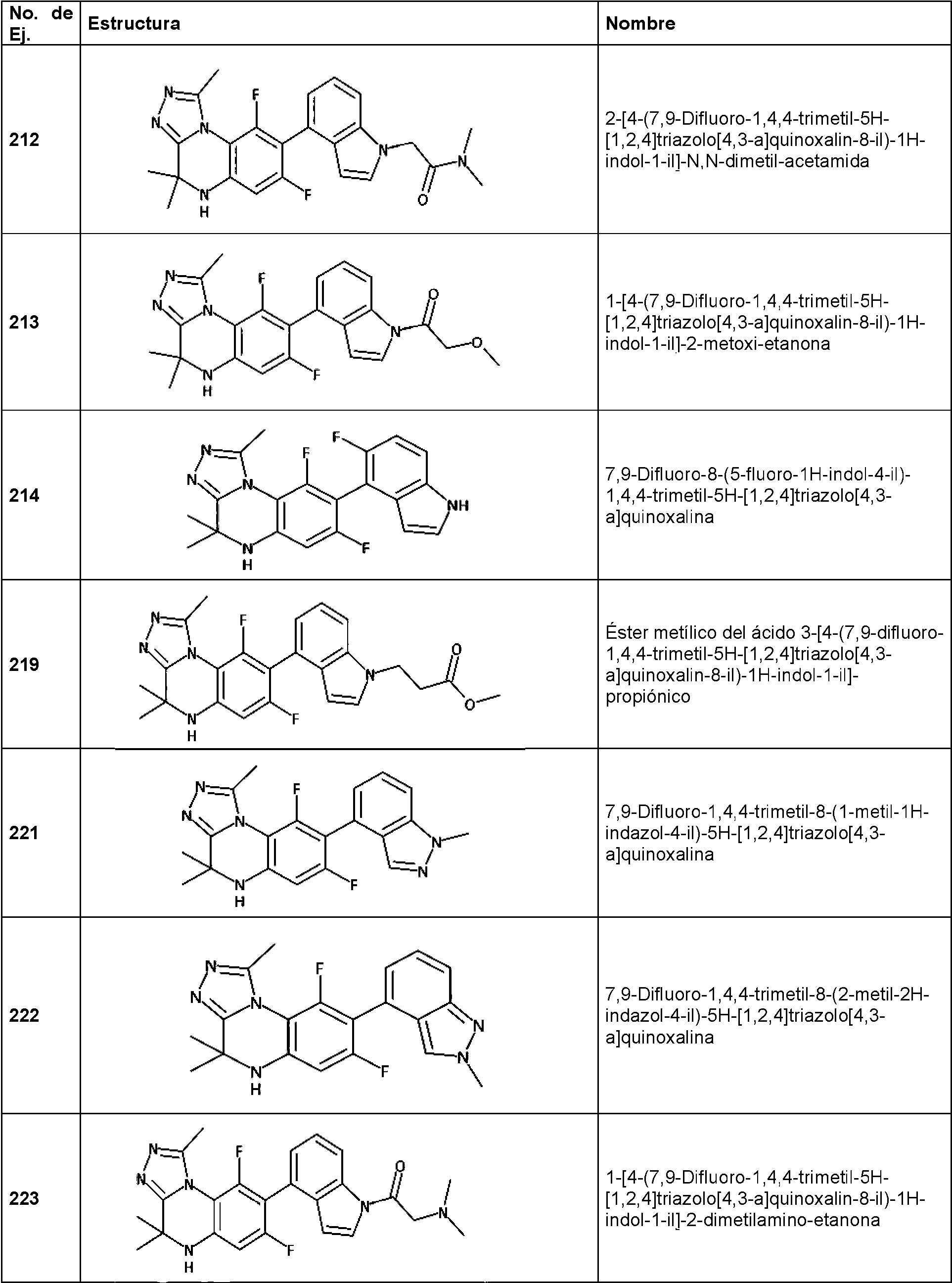
- UMDLNPURWLZZAQ-UHFFFAOYSA-N 1-[4-(7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-6-fluoroindol-1-yl]ethanone Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)C(C)=O)F)C(=NN=3)C)(C)C UMDLNPURWLZZAQ-UHFFFAOYSA-N 0.000 claims description 2
- YPAFHBISENSOSL-UHFFFAOYSA-N 1-[4-(7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indol-1-yl]-2-methoxyethanone Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)C(COC)=O)F)C(=NN=3)C)(C)C YPAFHBISENSOSL-UHFFFAOYSA-N 0.000 claims description 2
- MMWIJZXJRWUJBN-UHFFFAOYSA-N 1-[7-fluoro-8-(5-fluoro-3-prop-1-ynyl-1H-indol-7-yl)-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-1-yl]ethanol Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=C3C(=CC(F)=C1)C(C#CC)=CN3)C)C(C(C)O)=NN=2)(C)C MMWIJZXJRWUJBN-UHFFFAOYSA-N 0.000 claims description 2
- HOTOHRAPAHXXOT-UHFFFAOYSA-N 1-ethyl-7-fluoro-4,4,9-trimethyl-8-(1-methylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C1=C2C=NN(C2=CC=C1)C)C HOTOHRAPAHXXOT-UHFFFAOYSA-N 0.000 claims description 2
- PWEIPSGCRJGDES-UHFFFAOYSA-N 1-ethyl-7-fluoro-4,4,9-trimethyl-8-(1-methylsulfonylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C1=C2C=NN(C2=CC=C1)S(=O)(=O)C)C PWEIPSGCRJGDES-UHFFFAOYSA-N 0.000 claims description 2
- DWFKOJRYTWSMBJ-UHFFFAOYSA-N 1-ethyl-7-fluoro-4,4,9-trimethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)C DWFKOJRYTWSMBJ-UHFFFAOYSA-N 0.000 claims description 2
- NRQWTSPDSRUSRO-UHFFFAOYSA-N 1-ethyl-7-fluoro-8-(6-fluoro-1-methylsulfonylindazol-4-yl)-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C)C NRQWTSPDSRUSRO-UHFFFAOYSA-N 0.000 claims description 2
- XOLNGWPPLLSCBI-UHFFFAOYSA-N 1-ethyl-7-fluoro-8-(6-fluoro-1H-indol-4-yl)-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC(F)=CC=2NC=CC1=2)F)CC)C XOLNGWPPLLSCBI-UHFFFAOYSA-N 0.000 claims description 2
- FRACBGCOQMRESM-UHFFFAOYSA-N 1-ethyl-7-fluoro-8-[6-fluoro-1-(2-methoxyethyl)indol-4-yl]-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC(F)=CC=2N(C=CC1=2)CCOC)F)CC)C FRACBGCOQMRESM-UHFFFAOYSA-N 0.000 claims description 2
- KCHQKCZEFDWQFE-UHFFFAOYSA-N 2-[4-(7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indazol-1-yl]ethanol Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)CCO)F)C(=NN=3)C)(C)C KCHQKCZEFDWQFE-UHFFFAOYSA-N 0.000 claims description 2
- SGLOAKWZNYILLP-UHFFFAOYSA-N 2-[4-(7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indol-1-yl]-N,N-dimethylacetamide Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CC(=O)N(C)C)F)C(=NN=3)C)(C)C SGLOAKWZNYILLP-UHFFFAOYSA-N 0.000 claims description 2
- DVIXVDCNQZUFPD-UHFFFAOYSA-N 2-[4-(7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indol-1-yl]-N,N-dimethylethanamine Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCN(C)C)F)C(=NN=3)C)(C)C DVIXVDCNQZUFPD-UHFFFAOYSA-N 0.000 claims description 2
- LTJZROZNILLMKV-UHFFFAOYSA-N 2-[4-(9-ethyl-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-6-fluoroindazol-1-yl]ethanol Chemical compound C(C)C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=NN(C2=CC(=C1)F)CCO LTJZROZNILLMKV-UHFFFAOYSA-N 0.000 claims description 2
- MBPAHYHLIRTEQE-UHFFFAOYSA-N 2-[4-(9-ethyl-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-6-fluoroindol-1-yl]ethanol Chemical compound C(C)C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC(=C1)F)CCO MBPAHYHLIRTEQE-UHFFFAOYSA-N 0.000 claims description 2
- CAESTCZFKPVOQV-UHFFFAOYSA-N 2-[4-[7-(difluoromethoxy)-9-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]-6-fluoroindol-1-yl]ethanol Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)CCO)F)C(=NN=3)C)(C)C)F CAESTCZFKPVOQV-UHFFFAOYSA-N 0.000 claims description 2
- ZZOZJKJXJTYQRP-UHFFFAOYSA-N 2-[4-[7-(difluoromethyl)-9-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]-6-fluoroindol-1-yl]ethanol Chemical compound FC(C=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)CCO)F)C(=NN=3)C)(C)C)F ZZOZJKJXJTYQRP-UHFFFAOYSA-N 0.000 claims description 2
- HVFQDONVCXPTBJ-UHFFFAOYSA-N 2-[4-[7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]indol-1-yl]ethanol Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCO)C(F)(F)F)C(=NN=3)C)(C)C HVFQDONVCXPTBJ-UHFFFAOYSA-N 0.000 claims description 2
- GIHQZRBCTMWMPY-UHFFFAOYSA-N 2-[6-fluoro-4-(7-fluoro-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indol-1-yl]ethanol Chemical compound FC1=CC(=C2C=CN(C2=C1)CCO)C1=C(C=C2NC(C=3N(C2=C1OC)C(=NN=3)C)(C)C)F GIHQZRBCTMWMPY-UHFFFAOYSA-N 0.000 claims description 2
- VDWMLUPLAPBFKF-UHFFFAOYSA-N 2-[6-fluoro-4-(9-fluoro-7-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indol-1-yl]ethanol Chemical compound FC1=CC(=C2C=CN(C2=C1)CCO)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)OC VDWMLUPLAPBFKF-UHFFFAOYSA-N 0.000 claims description 2
- UPXLMSPVOIBCNB-UHFFFAOYSA-N 2-[6-fluoro-4-[1,4,4,9-tetramethyl-7-(trifluoromethoxy)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]indol-1-yl]ethanol Chemical compound FC1=CC(=C2C=CN(C2=C1)CCO)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)OC(F)(F)F UPXLMSPVOIBCNB-UHFFFAOYSA-N 0.000 claims description 2
- KPESPBZXUMMNLK-UHFFFAOYSA-N 2-[6-fluoro-4-[7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]indazol-1-yl]ethanol Chemical compound FC1=CC(=C2C=NN(C2=C1)CCO)C1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)F KPESPBZXUMMNLK-UHFFFAOYSA-N 0.000 claims description 2
- QCROBHCYSWTYSG-UHFFFAOYSA-N 2-[6-fluoro-4-[7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]indol-1-yl]ethanol Chemical compound FC1=CC(=C2C=CN(C2=C1)CCO)C1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)F QCROBHCYSWTYSG-UHFFFAOYSA-N 0.000 claims description 2
- VVMVIRPFSBHRKH-UHFFFAOYSA-N 4-(7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-1H-indole-6-carbonitrile Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC(=C1)C#N)C)C(=NN=3)C)(C)C VVMVIRPFSBHRKH-UHFFFAOYSA-N 0.000 claims description 2
- CIYAMRONXPXNJM-UHFFFAOYSA-N 4-(7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-1H-indole-7-carbonitrile Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=C(C=C1)C#N)C)C(=NN=3)C)(C)C CIYAMRONXPXNJM-UHFFFAOYSA-N 0.000 claims description 2
- YIYGSTAHTBASCT-UHFFFAOYSA-N 4-[7-(7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-1H-indol-3-yl]-2-methylbut-3-yn-2-amine Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC=CC=2C(C#CC(N)(C)C)=CNC1=2)F)C)C YIYGSTAHTBASCT-UHFFFAOYSA-N 0.000 claims description 2
- URIZLDXDPRASFO-UHFFFAOYSA-N 4-[7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]-1H-indole-6-carbonitrile Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC(=C1)C#N)C(F)(F)F)C(=NN=3)C)(C)C URIZLDXDPRASFO-UHFFFAOYSA-N 0.000 claims description 2
- KWJLZCAVYBTANP-UHFFFAOYSA-N 4-[7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]-1H-indole-7-carbonitrile Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=C(C=C1)C#N)C(F)(F)F)C(=NN=3)C)(C)C KWJLZCAVYBTANP-UHFFFAOYSA-N 0.000 claims description 2
- WLEJAFLOXYNGFO-UHFFFAOYSA-N 7,9-difluoro-8-(6-fluoro-1H-indol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C)C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC(F)=CC=2NC=CC1=2)F)C WLEJAFLOXYNGFO-UHFFFAOYSA-N 0.000 claims description 2
- ZZFJRKZOFBOLJO-UHFFFAOYSA-N 7-(difluoromethoxy)-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)C)C(=NN=3)C)(C)C)F ZZFJRKZOFBOLJO-UHFFFAOYSA-N 0.000 claims description 2
- CRRMMCSCIRRLLC-UHFFFAOYSA-N 7-(difluoromethoxy)-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)C)C(=NN=3)C)(C)C)F CRRMMCSCIRRLLC-UHFFFAOYSA-N 0.000 claims description 2
- LQLAOQYBFWKMKA-UHFFFAOYSA-N 7-(difluoromethoxy)-9-fluoro-1,4,4-trimethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)F)C(=NN=3)C)(C)C)F LQLAOQYBFWKMKA-UHFFFAOYSA-N 0.000 claims description 2
- KLJFOCMMISVJQG-UHFFFAOYSA-N 7-(difluoromethoxy)-9-fluoro-1,4,4-trimethyl-8-(3-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C=1C=CC=C2C(=CNC=12)C)F)C(=NN=3)C)(C)C)F KLJFOCMMISVJQG-UHFFFAOYSA-N 0.000 claims description 2
- NYTIUDQEHYGBHW-UHFFFAOYSA-N 7-(difluoromethoxy)-9-fluoro-1,4,4-trimethyl-8-[2-(trifluoromethyl)-1H-indol-4-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=C(NC2=CC=C1)C(F)(F)F)F)C(=NN=3)C)(C)C)F NYTIUDQEHYGBHW-UHFFFAOYSA-N 0.000 claims description 2
- NDBGKVZQWAGMGI-UHFFFAOYSA-N 7-(difluoromethoxy)-9-fluoro-8-(1H-indol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC=C1)F)C(=NN=3)C)(C)C)F NDBGKVZQWAGMGI-UHFFFAOYSA-N 0.000 claims description 2
- IPWGVLRMDUGSBN-UHFFFAOYSA-N 7-(difluoromethoxy)-9-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)F)C(=NN=3)C)(C)C)F IPWGVLRMDUGSBN-UHFFFAOYSA-N 0.000 claims description 2
- IAFJHOIBWJODRF-UHFFFAOYSA-N 7-(difluoromethyl)-9-fluoro-1,4,4-trimethyl-8-(1-methylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)C)F)C(=NN=3)C)(C)C)F IAFJHOIBWJODRF-UHFFFAOYSA-N 0.000 claims description 2
- GCQBNLJGIKDNIW-UHFFFAOYSA-N 7-(difluoromethyl)-9-fluoro-1,4,4-trimethyl-8-(3-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C=C2NC(C=3N(C2=C(C=1C=1C=CC=C2C(=CNC=12)C)F)C(=NN=3)C)(C)C)F GCQBNLJGIKDNIW-UHFFFAOYSA-N 0.000 claims description 2
- GYPFKWYOSRWGQM-UHFFFAOYSA-N 7-(difluoromethyl)-9-fluoro-8-(1H-indol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC=C1)F)C(=NN=3)C)(C)C)F GYPFKWYOSRWGQM-UHFFFAOYSA-N 0.000 claims description 2
- HPKHYMJESFVFIT-UHFFFAOYSA-N 7-(difluoromethyl)-9-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)F)C(=NN=3)C)(C)C)F HPKHYMJESFVFIT-UHFFFAOYSA-N 0.000 claims description 2
- QOPMBRQYLWHBJZ-UHFFFAOYSA-N 7-(difluoromethyl)-9-fluoro-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)F)C(=NN=3)C)(C)C)F QOPMBRQYLWHBJZ-UHFFFAOYSA-N 0.000 claims description 2
- UGQXQVTUNWOTCV-UHFFFAOYSA-N 7-[7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl]-1H-indole-3-carbonitrile Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C(F)(F)F)C1=C2C(=CC=C1)C(C#N)=CN2)F)C)C UGQXQVTUNWOTCV-UHFFFAOYSA-N 0.000 claims description 2
- JCVCYWIEZPXQIJ-UHFFFAOYSA-N 7-chloro-1,4,4,9-tetramethyl-8-(1-methylsulfonylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)S(=O)(=O)C)C)C(=NN=3)C)(C)C JCVCYWIEZPXQIJ-UHFFFAOYSA-N 0.000 claims description 2
- SXNOFVPQLWHFEM-UHFFFAOYSA-N 7-chloro-1,4,4,9-tetramethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)C)C(=NN=3)C)(C)C SXNOFVPQLWHFEM-UHFFFAOYSA-N 0.000 claims description 2
- UTOOFAOJYVVKQQ-UHFFFAOYSA-N 7-chloro-1,4,4,9-tetramethyl-8-(3-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C=1C=CC=C2C(=CNC=12)C)C)C(=NN=3)C)(C)C UTOOFAOJYVVKQQ-UHFFFAOYSA-N 0.000 claims description 2
- UTSGGSUGOYZQGL-UHFFFAOYSA-N 7-chloro-1,4,4,9-tetramethyl-8-(3-methyl-2H-indazol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C=1C=CC=C2C(=NNC=12)C)C)C(=NN=3)C)(C)C UTSGGSUGOYZQGL-UHFFFAOYSA-N 0.000 claims description 2
- VHQYDXYKVGPVOY-UHFFFAOYSA-N 7-chloro-1,4,4,9-tetramethyl-8-(6-methyl-1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)C)S(=O)(=O)C)C)C(=NN=3)C)(C)C VHQYDXYKVGPVOY-UHFFFAOYSA-N 0.000 claims description 2
- WCLAQKNLSXCADD-UHFFFAOYSA-N 7-chloro-1,4,4,9-tetramethyl-8-[6-(trifluoromethyl)-1H-indol-4-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC(=C1)C(F)(F)F)C)C(=NN=3)C)(C)C WCLAQKNLSXCADD-UHFFFAOYSA-N 0.000 claims description 2
- YEOUOGZJXWSHTJ-UHFFFAOYSA-N 7-chloro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)C)C(=NN=3)C)(C)C YEOUOGZJXWSHTJ-UHFFFAOYSA-N 0.000 claims description 2
- WDALKXCDDPHQFB-UHFFFAOYSA-N 7-chloro-8-(6-fluoro-1-methylsulfonylindol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C)C)C(=NN=3)C)(C)C WDALKXCDDPHQFB-UHFFFAOYSA-N 0.000 claims description 2
- ZWJVWPOKIULOCV-UHFFFAOYSA-N 7-chloro-8-(7-fluoro-1H-indol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=C(C=C1)F)C)C(=NN=3)C)(C)C ZWJVWPOKIULOCV-UHFFFAOYSA-N 0.000 claims description 2
- FYTFSUYHVWZFIA-UHFFFAOYSA-N 7-chloro-8-[1-(2,2-difluoroethyl)indol-4-yl]-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CC(F)F)C)C(=NN=3)C)(C)C FYTFSUYHVWZFIA-UHFFFAOYSA-N 0.000 claims description 2
- VFYLWXJBQCVIOM-UHFFFAOYSA-N 7-chloro-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)C)C(=NN=3)C)(C)C VFYLWXJBQCVIOM-UHFFFAOYSA-N 0.000 claims description 2
- IPJLEIFLACMGRT-UHFFFAOYSA-N 7-chloro-9-fluoro-1,4,4-trimethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)F)C(=NN=3)C)(C)C IPJLEIFLACMGRT-UHFFFAOYSA-N 0.000 claims description 2
- NDZXNNYTXNVEPI-UHFFFAOYSA-N 7-chloro-9-fluoro-1,4,4-trimethyl-8-(3-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C=1C=CC=C2C(=CNC=12)C)F)C(=NN=3)C)(C)C NDZXNNYTXNVEPI-UHFFFAOYSA-N 0.000 claims description 2
- FKKRQRMBDWXKJZ-UHFFFAOYSA-N 7-chloro-9-fluoro-1,4,4-trimethyl-8-[2-(trifluoromethyl)-1H-indol-4-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=C(NC2=CC=C1)C(F)(F)F)F)C(=NN=3)C)(C)C FKKRQRMBDWXKJZ-UHFFFAOYSA-N 0.000 claims description 2
- RXZORSKXDOTXTI-UHFFFAOYSA-N 7-chloro-9-fluoro-8-(1H-indol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC=C1)F)C(=NN=3)C)(C)C RXZORSKXDOTXTI-UHFFFAOYSA-N 0.000 claims description 2
- NQRCVSJNAYCFGG-UHFFFAOYSA-N 7-chloro-9-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)F)C(=NN=3)C)(C)C NQRCVSJNAYCFGG-UHFFFAOYSA-N 0.000 claims description 2
- FSPIHUGJEMWSRF-UHFFFAOYSA-N 7-chloro-9-fluoro-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)F)C(=NN=3)C)(C)C FSPIHUGJEMWSRF-UHFFFAOYSA-N 0.000 claims description 2
- RVKHRQOXVACKHD-UHFFFAOYSA-N 7-fluoro-1,4,4,9-tetramethyl-8-(1-methylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)C)C)C(=NN=3)C)(C)C RVKHRQOXVACKHD-UHFFFAOYSA-N 0.000 claims description 2
- ZIOZHVBDQNUXBD-UHFFFAOYSA-N 7-fluoro-1,4,4,9-tetramethyl-8-(6-methyl-1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)C)S(=O)(=O)C)C)C(=NN=3)C)(C)C ZIOZHVBDQNUXBD-UHFFFAOYSA-N 0.000 claims description 2
- ASVKCZOBWZKBRO-UHFFFAOYSA-N 7-fluoro-1,4,4,9-tetramethyl-8-[3-(2,2,2-trifluoroethyl)-1H-indol-7-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC=CC=2C(CC(F)(F)F)=CNC1=2)F)C)C ASVKCZOBWZKBRO-UHFFFAOYSA-N 0.000 claims description 2
- XVCFEDGOOQQGCV-UHFFFAOYSA-N 7-fluoro-1,4,4,9-tetramethyl-8-[3-(oxolan-3-yl)-1H-indol-7-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC=CC=2C(C3CCOC3)=CNC1=2)F)C)C XVCFEDGOOQQGCV-UHFFFAOYSA-N 0.000 claims description 2
- DNBLXLNAFONOTK-UHFFFAOYSA-N 7-fluoro-1,4,4,9-tetramethyl-8-[6-(trifluoromethyl)-1H-indol-4-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC(=C1)C(F)(F)F)C)C(=NN=3)C)(C)C DNBLXLNAFONOTK-UHFFFAOYSA-N 0.000 claims description 2
- VUXSKUFLFHPHCI-UHFFFAOYSA-N 7-fluoro-1,4,4-trimethyl-8-(3-methyl-1H-indol-7-yl)-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=C3C(=CC=C1)C(C)=CN3)C(F)(F)F)C(C)=NN=2)(C)C VUXSKUFLFHPHCI-UHFFFAOYSA-N 0.000 claims description 2
- PNEWFODHBFBBIN-UHFFFAOYSA-N 7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-8-[6-(trifluoromethyl)-1H-indol-4-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC(=C1)C(F)(F)F)C(F)(F)F)C(=NN=3)C)(C)C PNEWFODHBFBBIN-UHFFFAOYSA-N 0.000 claims description 2
- OFOXHIILHXYAAG-UHFFFAOYSA-N 7-fluoro-8-(1H-indazol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NNC2=CC=C1)C)C(=NN=3)C)(C)C OFOXHIILHXYAAG-UHFFFAOYSA-N 0.000 claims description 2
- LIULEWNYTPZZMK-UHFFFAOYSA-N 7-fluoro-8-(1H-indazol-4-yl)-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NNC2=CC=C1)OC)C(=NN=3)C)(C)C LIULEWNYTPZZMK-UHFFFAOYSA-N 0.000 claims description 2
- DRYWYIUFLXCDPL-UHFFFAOYSA-N 7-fluoro-8-(5-fluoro-1H-indol-7-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C=CNC=12)F)C(F)(F)F)C(=NN=3)C)(C)C DRYWYIUFLXCDPL-UHFFFAOYSA-N 0.000 claims description 2
- ZEFPETGOBPDSRD-UHFFFAOYSA-N 7-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)OC)C(=NN=3)C)(C)C ZEFPETGOBPDSRD-UHFFFAOYSA-N 0.000 claims description 2
- WWLJGGIERAKYOZ-UHFFFAOYSA-N 7-fluoro-8-(6-fluoro-1-methylsulfonylindazol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C)C)C(=NN=3)C)(C)C WWLJGGIERAKYOZ-UHFFFAOYSA-N 0.000 claims description 2
- XLJMEDJQRKQBAP-UHFFFAOYSA-N 7-fluoro-8-(6-fluoro-1-methylsulfonylindol-4-yl)-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C)OC)C(=NN=3)C)(C)C XLJMEDJQRKQBAP-UHFFFAOYSA-N 0.000 claims description 2
- LAKWGLPARHJBLS-UHFFFAOYSA-N 7-fluoro-8-(6-fluoro-1H-indol-4-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC(=C1)F)C(F)(F)F)C(=NN=3)C)(C)C LAKWGLPARHJBLS-UHFFFAOYSA-N 0.000 claims description 2
- CFCOTMZSBAPBPT-UHFFFAOYSA-N 7-fluoro-8-(7-fluoro-1H-indazol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NNC2=C(C=C1)F)C)C(=NN=3)C)(C)C CFCOTMZSBAPBPT-UHFFFAOYSA-N 0.000 claims description 2
- PYLFIAKHUAUUPJ-UHFFFAOYSA-N 7-fluoro-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)C)C(=NN=3)C)(C)C PYLFIAKHUAUUPJ-UHFFFAOYSA-N 0.000 claims description 2
- SULNKCLEDBXGEB-UHFFFAOYSA-N 7-fluoro-8-[6-fluoro-1-(2-methoxyethyl)indol-4-yl]-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)CCOC)OC)C(=NN=3)C)(C)C SULNKCLEDBXGEB-UHFFFAOYSA-N 0.000 claims description 2
- RXACLNMVVSIYKV-UHFFFAOYSA-N 7-fluoro-9-methoxy-1,4,4-trimethyl-8-(1-methylsulfonylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)S(=O)(=O)C)OC)C(=NN=3)C)(C)C RXACLNMVVSIYKV-UHFFFAOYSA-N 0.000 claims description 2
- XDQPROMGPUUYHI-UHFFFAOYSA-N 7-fluoro-9-methoxy-1,4,4-trimethyl-8-(3-methyl-2H-indazol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C=1C=CC=C2C(=NNC=12)C)OC)C(=NN=3)C)(C)C XDQPROMGPUUYHI-UHFFFAOYSA-N 0.000 claims description 2
- OQVQKAIGDYBLRB-UHFFFAOYSA-N 7-fluoro-9-methoxy-1,4,4-trimethyl-8-[6-(trifluoromethyl)-1H-indol-4-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=CC(=C1)C(F)(F)F)OC)C(=NN=3)C)(C)C OQVQKAIGDYBLRB-UHFFFAOYSA-N 0.000 claims description 2
- FXDVAGXYKMLXON-UHFFFAOYSA-N 7-fluoro-9-methoxy-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)OC)C(=NN=3)C)(C)C FXDVAGXYKMLXON-UHFFFAOYSA-N 0.000 claims description 2
- ILMLGBDHGGJINR-UHFFFAOYSA-N 7-methoxy-1,4,4-trimethyl-8-(1-methylindol-4-yl)-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound COC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)C)C(F)(F)F)C(=NN=3)C)(C)C ILMLGBDHGGJINR-UHFFFAOYSA-N 0.000 claims description 2
- WYLZMLHPNPYZML-UHFFFAOYSA-N 7-methoxy-1,4,4-trimethyl-8-(1-methylsulfonylindazol-4-yl)-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound COC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)S(=O)(=O)C)C(F)(F)F)C(=NN=3)C)(C)C WYLZMLHPNPYZML-UHFFFAOYSA-N 0.000 claims description 2
- PELANMNKCSNRQF-UHFFFAOYSA-N 7-methoxy-1,4,4-trimethyl-8-(1-methylsulfonylindol-4-yl)-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound COC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)C(F)(F)F)C(=NN=3)C)(C)C PELANMNKCSNRQF-UHFFFAOYSA-N 0.000 claims description 2
- PIBTXXCDVGULEX-UHFFFAOYSA-N 7-methoxy-1,4,4-trimethyl-8-(3-methyl-1H-indol-7-yl)-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound COC=1C=C2NC(C=3N(C2=C(C=1C=1C=CC=C2C(=CNC=12)C)C(F)(F)F)C(=NN=3)C)(C)C PIBTXXCDVGULEX-UHFFFAOYSA-N 0.000 claims description 2
- UWVOEHUYWOCTHN-UHFFFAOYSA-N 7-methoxy-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound COC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)C)C(=NN=3)C)(C)C UWVOEHUYWOCTHN-UHFFFAOYSA-N 0.000 claims description 2
- YSMJYDIKIGSBHV-UHFFFAOYSA-N 8-(1-cyclopropyl-6-fluoroindol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC(F)=CC=2N(C=CC1=2)C1CC1)F)C)C YSMJYDIKIGSBHV-UHFFFAOYSA-N 0.000 claims description 2
- RACYVPPWOLOFKU-UHFFFAOYSA-N 8-(1-cyclopropylindazol-4-yl)-1-ethyl-7-fluoro-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)N1N=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)CC)(C)C)F RACYVPPWOLOFKU-UHFFFAOYSA-N 0.000 claims description 2
- MVWQXJVLIDHVLO-UHFFFAOYSA-N 8-(1-cyclopropylsulfonylindol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)S(=O)(=O)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F MVWQXJVLIDHVLO-UHFFFAOYSA-N 0.000 claims description 2
- VOUSVQMMCBABPE-UHFFFAOYSA-N 8-(1-ethylindazol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)N1N=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F VOUSVQMMCBABPE-UHFFFAOYSA-N 0.000 claims description 2
- PDRYJLOPOYHNFJ-UHFFFAOYSA-N 8-(1-ethylsulfonyl-6-fluoroindol-4-yl)-7-fluoro-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)S(=O)(=O)N1C=CC2=C(C=C(C=C12)F)C1=C(C=C2NC(C=3N(C2=C1OC)C(=NN=3)C)(C)C)F PDRYJLOPOYHNFJ-UHFFFAOYSA-N 0.000 claims description 2
- LYYULBDJGAEAIA-UHFFFAOYSA-N 8-(1-ethylsulfonylindol-4-yl)-7-methoxy-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)S(=O)(=O)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)OC LYYULBDJGAEAIA-UHFFFAOYSA-N 0.000 claims description 2
- HRLOOFLYYAXOHL-UHFFFAOYSA-N 8-(2-ethylindazol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)N1N=C2C=CC=C(C2=C1)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F HRLOOFLYYAXOHL-UHFFFAOYSA-N 0.000 claims description 2
- UFPVNEDKTCDKDD-UHFFFAOYSA-N 8-(3-cyclopropyl-5-fluoro-1H-indol-7-yl)-7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)C1=CNC2=C(C=C(C=C12)F)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F UFPVNEDKTCDKDD-UHFFFAOYSA-N 0.000 claims description 2
- CPUULSGMKRDAKC-UHFFFAOYSA-N 8-(3-ethyl-5-fluoro-1H-indol-7-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC(F)=CC=2C(CC)=CNC1=2)F)C)C CPUULSGMKRDAKC-UHFFFAOYSA-N 0.000 claims description 2
- OMOBHOCEQHVTSM-UHFFFAOYSA-N 8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4,7,9-pentamethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2C(=CNC2=C(C=1)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C)C OMOBHOCEQHVTSM-UHFFFAOYSA-N 0.000 claims description 2
- ISWCMFLPXMBWNK-UHFFFAOYSA-N 8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2C(=CNC2=C(C=1)C1=CC=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)C ISWCMFLPXMBWNK-UHFFFAOYSA-N 0.000 claims description 2
- PXQMUNRNUKOTJB-UHFFFAOYSA-N 8-(6-chloro-1H-indol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC1=CC(=C2C=CNC2=C1)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F PXQMUNRNUKOTJB-UHFFFAOYSA-N 0.000 claims description 2
- VMQWDLBWOUGOSI-UHFFFAOYSA-N 8-(6-chloro-1H-indol-4-yl)-7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC1=CC(=C2C=CNC2=C1)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F VMQWDLBWOUGOSI-UHFFFAOYSA-N 0.000 claims description 2
- IBEQSZAUTLSLGN-UHFFFAOYSA-N 8-(6-fluoro-1-methylindol-4-yl)-7-methoxy-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC1=CC(=C2C=CN(C2=C1)C)C1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)OC IBEQSZAUTLSLGN-UHFFFAOYSA-N 0.000 claims description 2
- NDLQCFCMTDRUJL-UHFFFAOYSA-N 8-(6-fluoro-1-methylsulfonylindazol-4-yl)-1,4,4,7,9-pentamethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC1=CC(=C2C=NN(C2=C1)S(=O)(=O)C)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C NDLQCFCMTDRUJL-UHFFFAOYSA-N 0.000 claims description 2
- FNVCERRMIPAMCN-UHFFFAOYSA-N 8-(6-fluoro-1-methylsulfonylindol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC1=CC(=C2C=CN(C2=C1)S(=O)(=O)C)C1=CC=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C FNVCERRMIPAMCN-UHFFFAOYSA-N 0.000 claims description 2
- IDNYBGMZOPFPFG-UHFFFAOYSA-N 8-(6-fluoro-1-methylsulfonylindol-4-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC1=CC(=C2C=CN(C2=C1)S(=O)(=O)C)C1=CC=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C IDNYBGMZOPFPFG-UHFFFAOYSA-N 0.000 claims description 2
- LDCBAHGPUOFKCX-UHFFFAOYSA-N 8-(7-chloro-1-methylsulfonylindol-4-yl)-7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=CC(=C2C=CN(C=12)S(=O)(=O)C)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F LDCBAHGPUOFKCX-UHFFFAOYSA-N 0.000 claims description 2
- RFWUHZSCGHJVIX-UHFFFAOYSA-N 8-(7-chloro-1H-indol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=CC(=C2C=CNC=12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F RFWUHZSCGHJVIX-UHFFFAOYSA-N 0.000 claims description 2
- WDEFFLQICXPPBF-UHFFFAOYSA-N 8-(7-chloro-1H-indol-4-yl)-7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=CC(=C2C=CNC=12)C1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)F WDEFFLQICXPPBF-UHFFFAOYSA-N 0.000 claims description 2
- GSEADXXGVWBCJK-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)-6-fluoroindazol-4-yl]-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1N=CC2=C(C=C(C=C12)F)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F)F GSEADXXGVWBCJK-UHFFFAOYSA-N 0.000 claims description 2
- ZQAMZTIVENRYFG-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)indol-4-yl]-1,4,4,7,9-pentamethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C)F ZQAMZTIVENRYFG-UHFFFAOYSA-N 0.000 claims description 2
- IWXBQGFJWDNMSR-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)indol-4-yl]-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F)F IWXBQGFJWDNMSR-UHFFFAOYSA-N 0.000 claims description 2
- XKSNUWLJBSKMKS-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)indol-4-yl]-7-fluoro-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1OC)C(=NN=3)C)(C)C)F)F XKSNUWLJBSKMKS-UHFFFAOYSA-N 0.000 claims description 2
- CXUYPVYZUCFMGA-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)indol-4-yl]-7-methoxy-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)OC)F CXUYPVYZUCFMGA-UHFFFAOYSA-N 0.000 claims description 2
- AMCXJILYWBMUMX-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)indol-4-yl]-9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C(F)F)C(=NN=3)C)(C)C)F)F AMCXJILYWBMUMX-UHFFFAOYSA-N 0.000 claims description 2
- KJZYUWSDWUPODL-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)indol-4-yl]-9-fluoro-1,4,4,7-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)C)F KJZYUWSDWUPODL-UHFFFAOYSA-N 0.000 claims description 2
- ZPABFZAUZCYEKI-UHFFFAOYSA-N 8-[1-(2,2-difluoroethyl)indol-4-yl]-9-fluoro-7-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)OC)F ZPABFZAUZCYEKI-UHFFFAOYSA-N 0.000 claims description 2
- JKXKYFPWCNZIPK-UHFFFAOYSA-N 8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4,7,9-pentamethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound COCCN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C JKXKYFPWCNZIPK-UHFFFAOYSA-N 0.000 claims description 2
- VFDBFRGASGUERO-UHFFFAOYSA-N 8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4,9-tetramethyl-7-(trifluoromethoxy)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound COCCN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)OC(F)(F)F VFDBFRGASGUERO-UHFFFAOYSA-N 0.000 claims description 2
- IYILYSPNWUNRAA-UHFFFAOYSA-N 8-[1-(cyclopropylmethyl)indol-4-yl]-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F IYILYSPNWUNRAA-UHFFFAOYSA-N 0.000 claims description 2
- YXXGSLUCDNNCPS-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-8-(1-methylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=NN(C2=CC=C1)C)F YXXGSLUCDNNCPS-UHFFFAOYSA-N 0.000 claims description 2
- IJARHRSDYJIMNN-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-8-(1-methylsulfonylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=NN(C2=CC=C1)S(=O)(=O)C)F IJARHRSDYJIMNN-UHFFFAOYSA-N 0.000 claims description 2
- RQLZNVQUTOQYKX-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)F RQLZNVQUTOQYKX-UHFFFAOYSA-N 0.000 claims description 2
- YQBBQFUJBWOUEW-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-8-(1-propan-2-ylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC=C1)S(=O)(=O)C(C)C)F YQBBQFUJBWOUEW-UHFFFAOYSA-N 0.000 claims description 2
- APUKHLBYTXCFAT-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-8-(3-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C=1C=CC=C2C(=CNC=12)C)F APUKHLBYTXCFAT-UHFFFAOYSA-N 0.000 claims description 2
- HGFNTWMKMXWDPP-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-8-(3-methyl-2H-indazol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C=1C=CC=C2C(=NNC=12)C)F HGFNTWMKMXWDPP-UHFFFAOYSA-N 0.000 claims description 2
- ANSAHXHDNYZYSD-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-8-(5-fluoro-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C=1C=C(C=C2C=CNC=12)F)F ANSAHXHDNYZYSD-UHFFFAOYSA-N 0.000 claims description 2
- PTEMBDFSTHUZPG-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C=1C=C(C=C2C(=CNC=12)C)F)F PTEMBDFSTHUZPG-UHFFFAOYSA-N 0.000 claims description 2
- FZZHQMXUWORPEB-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-8-(6-fluoro-1-methylindol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC(=C1)F)C)F FZZHQMXUWORPEB-UHFFFAOYSA-N 0.000 claims description 2
- XMVZQQMVJFUHEL-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-8-(6-fluoro-1H-indol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CNC2=CC(=C1)F)F XMVZQQMVJFUHEL-UHFFFAOYSA-N 0.000 claims description 2
- GYVOKTXJIMDNRO-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-8-(7-fluoro-1H-indol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CNC2=C(C=C1)F)F GYVOKTXJIMDNRO-UHFFFAOYSA-N 0.000 claims description 2
- XTOQKOVDAHBRKK-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC=C1)CCOC)F XTOQKOVDAHBRKK-UHFFFAOYSA-N 0.000 claims description 2
- RUEJSDLPVPWKAP-UHFFFAOYSA-N 9-(difluoromethyl)-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=CC=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C=1C=C(C=C2C(=CNC=12)C)F)F RUEJSDLPVPWKAP-UHFFFAOYSA-N 0.000 claims description 2
- ODNASHVVOPOJSN-UHFFFAOYSA-N 9-(difluoromethyl)-8-(6-fluoro-1-methylsulfonylindol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=CC=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C)F ODNASHVVOPOJSN-UHFFFAOYSA-N 0.000 claims description 2
- GLXSEDZMQMSNTJ-UHFFFAOYSA-N 9-chloro-7-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(NC2=C(N3C1=NN=C3C)C(=C(C(F)=C2)C1=CC(F)=CC=2C(C)=CNC1=2)Cl)(C)C GLXSEDZMQMSNTJ-UHFFFAOYSA-N 0.000 claims description 2
- FPLLQZOSVLTCJJ-UHFFFAOYSA-N 9-ethyl-7-fluoro-1,4,4-trimethyl-8-(1-methylsulfonylindazol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=NN(C2=CC=C1)S(=O)(=O)C FPLLQZOSVLTCJJ-UHFFFAOYSA-N 0.000 claims description 2
- UAAFJFNEVSFVQK-UHFFFAOYSA-N 9-ethyl-7-fluoro-1,4,4-trimethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC=C1)S(=O)(=O)C UAAFJFNEVSFVQK-UHFFFAOYSA-N 0.000 claims description 2
- FUYJNMLMYJJOHZ-UHFFFAOYSA-N 9-ethyl-7-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C=1C=C(C=C2C(=CNC=12)C)F FUYJNMLMYJJOHZ-UHFFFAOYSA-N 0.000 claims description 2
- SNXNAJLJKHHYPX-UHFFFAOYSA-N 9-ethyl-7-fluoro-8-(6-fluoro-1-methylsulfonylindazol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C SNXNAJLJKHHYPX-UHFFFAOYSA-N 0.000 claims description 2
- KEFVDNMBNJLUJK-UHFFFAOYSA-N 9-ethyl-7-fluoro-8-(6-fluoro-1-methylsulfonylindol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C KEFVDNMBNJLUJK-UHFFFAOYSA-N 0.000 claims description 2
- HCPBTJNRCWWKMR-UHFFFAOYSA-N 9-fluoro-1,4,4,7-tetramethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C1=C2C=CN(C2=CC=C1)S(=O)(=O)C HCPBTJNRCWWKMR-UHFFFAOYSA-N 0.000 claims description 2
- WZZXYUSDYMEGHU-UHFFFAOYSA-N 9-fluoro-1,4,4,7-tetramethyl-8-(3-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C=1C=CC=C2C(=CNC=12)C WZZXYUSDYMEGHU-UHFFFAOYSA-N 0.000 claims description 2
- UXSVLFNBCCYXPS-UHFFFAOYSA-N 9-fluoro-7-methoxy-1,4,4-trimethyl-8-(1-methylsulfonylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C1=C2C=CN(C2=CC=C1)S(=O)(=O)C UXSVLFNBCCYXPS-UHFFFAOYSA-N 0.000 claims description 2
- PERNENJNJJWCBN-UHFFFAOYSA-N 9-fluoro-7-methoxy-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C1=C2C=CN(C2=CC=C1)CCOC PERNENJNJJWCBN-UHFFFAOYSA-N 0.000 claims description 2
- MRJMDECGTKMOMS-UHFFFAOYSA-N 9-fluoro-8-(1H-indol-4-yl)-7-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C1=C2C=CNC2=CC=C1 MRJMDECGTKMOMS-UHFFFAOYSA-N 0.000 claims description 2
- WITUHSIEULTPFT-UHFFFAOYSA-N 9-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=CC=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C=1C=C(C=C2C(=CNC=12)C)F WITUHSIEULTPFT-UHFFFAOYSA-N 0.000 claims description 2
- LVGOKZNHKIFEJH-UHFFFAOYSA-N 9-fluoro-8-(5-fluoro-3-methyl-1H-indol-7-yl)-7-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C=1C=C(C=C2C(=CNC=12)C)F LVGOKZNHKIFEJH-UHFFFAOYSA-N 0.000 claims description 2
- MLORFLNLJGDRPH-UHFFFAOYSA-N 9-fluoro-8-(6-fluoro-1-methylsulfonylindol-4-yl)-7-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C MLORFLNLJGDRPH-UHFFFAOYSA-N 0.000 claims description 2
- QIXLHUWSRFQFRU-UHFFFAOYSA-N 9-fluoro-8-[1-(2-methoxyethyl)indol-4-yl]-1,4,4,7-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C1=C2C=CN(C2=CC=C1)CCOC QIXLHUWSRFQFRU-UHFFFAOYSA-N 0.000 claims description 2
- IBTQMOQCFNBIOM-UHFFFAOYSA-N C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C1=C2C=CN(C2=CC=C1)CCOC)C Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C1=C2C=CN(C2=CC=C1)CCOC)C IBTQMOQCFNBIOM-UHFFFAOYSA-N 0.000 claims description 2
- WGIRJWURRCKKSK-UHFFFAOYSA-N C(C)S(=O)(=O)N1C=CC2=C(C=C(C=C12)F)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F Chemical compound C(C)S(=O)(=O)N1C=CC2=C(C=C(C=C12)F)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F WGIRJWURRCKKSK-UHFFFAOYSA-N 0.000 claims description 2
- FKMBGHLSGBCLBL-UHFFFAOYSA-N C(C)S(=O)(=O)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F Chemical compound C(C)S(=O)(=O)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F FKMBGHLSGBCLBL-UHFFFAOYSA-N 0.000 claims description 2
- KGNGHYWQKYCILF-UHFFFAOYSA-N C(C1=CC=CC=C1)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=CC=C2C(=CNC=12)C)F Chemical compound C(C1=CC=CC=C1)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=CC=C2C(=CNC=12)C)F KGNGHYWQKYCILF-UHFFFAOYSA-N 0.000 claims description 2
- VUWXHFYXGDESCQ-UHFFFAOYSA-N ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)CCOC)F)C(=NN=3)C)(C)C Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)CCOC)F)C(=NN=3)C)(C)C VUWXHFYXGDESCQ-UHFFFAOYSA-N 0.000 claims description 2
- NZYHLHNPURJZFB-UHFFFAOYSA-N FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC=C1)S(=O)(=O)CC)F Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC=C1)S(=O)(=O)CC)F NZYHLHNPURJZFB-UHFFFAOYSA-N 0.000 claims description 2
- HBYVLSVOTQVKKC-UHFFFAOYSA-N FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F)F Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F)F HBYVLSVOTQVKKC-UHFFFAOYSA-N 0.000 claims description 2
- CKDYPHOUMCIBDY-UHFFFAOYSA-N FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)OC(F)F)F Chemical compound FC(CN1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)OC(F)F)F CKDYPHOUMCIBDY-UHFFFAOYSA-N 0.000 claims description 2
- GGCYQSWPPIVVKN-UHFFFAOYSA-N FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)F)C(=NN=3)C)(C)C)F Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)F)C(=NN=3)C)(C)C)F GGCYQSWPPIVVKN-UHFFFAOYSA-N 0.000 claims description 2
- SRQOGDBCXOSWJP-UHFFFAOYSA-N FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)C)C(=NN=3)C)(C)C)F Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)C)C(=NN=3)C)(C)C)F SRQOGDBCXOSWJP-UHFFFAOYSA-N 0.000 claims description 2
- HSOWPWRQYDIBTK-UHFFFAOYSA-N FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)C)F)C(=NN=3)C)(C)C)F Chemical compound FC(OC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)C)F)C(=NN=3)C)(C)C)F HSOWPWRQYDIBTK-UHFFFAOYSA-N 0.000 claims description 2
- OIBLWONMIBXFDT-UHFFFAOYSA-N FC1=CC(=C2C=CN(C2=C1)S(=O)(=O)C)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C Chemical compound FC1=CC(=C2C=CN(C2=C1)S(=O)(=O)C)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C OIBLWONMIBXFDT-UHFFFAOYSA-N 0.000 claims description 2
- CYEPCSOYYMDTFO-UHFFFAOYSA-N FC1=CC(=C2C=CN(C2=C1)S(=O)(=O)C)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C(F)(F)F Chemical compound FC1=CC(=C2C=CN(C2=C1)S(=O)(=O)C)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C(F)(F)F CYEPCSOYYMDTFO-UHFFFAOYSA-N 0.000 claims description 2
- ZNCISQCBTSOVGL-UHFFFAOYSA-N FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C ZNCISQCBTSOVGL-UHFFFAOYSA-N 0.000 claims description 2
- OXEPKWOCVGBLIG-UHFFFAOYSA-N FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C=1C=C(C=C2C(=CNC=12)C)F Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)C)C=1C=C(C=C2C(=CNC=12)C)F OXEPKWOCVGBLIG-UHFFFAOYSA-N 0.000 claims description 2
- LIJDNPNIGFNSBT-UHFFFAOYSA-N FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C1=C2C=CN(C2=CC(=C1)F)CCOC Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C1=C2C=CN(C2=CC(=C1)F)CCOC LIJDNPNIGFNSBT-UHFFFAOYSA-N 0.000 claims description 2
- NRCZWXZKAVMVQJ-UHFFFAOYSA-N FC=1C=C2C(=CNC2=C(C=1)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)OC)C Chemical compound FC=1C=C2C(=CNC2=C(C=1)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)OC)C NRCZWXZKAVMVQJ-UHFFFAOYSA-N 0.000 claims description 2
- RVLFZUZLOXGAKJ-UHFFFAOYSA-N FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)C)S(=O)(=O)C)OC)C(=NN=3)C)(C)C Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)C)S(=O)(=O)C)OC)C(=NN=3)C)(C)C RVLFZUZLOXGAKJ-UHFFFAOYSA-N 0.000 claims description 2
- SHWGYROXGMWEGE-UHFFFAOYSA-N FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)C)C)C(=NN=3)C)(C)C Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)C)C)C(=NN=3)C)(C)C SHWGYROXGMWEGE-UHFFFAOYSA-N 0.000 claims description 2
- WUOKSDHEMJAMET-UHFFFAOYSA-N FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)OC)S(=O)(=O)C)C)C(=NN=3)C)(C)C Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)OC)S(=O)(=O)C)C)C(=NN=3)C)(C)C WUOKSDHEMJAMET-UHFFFAOYSA-N 0.000 claims description 2
- VCEYCSQGTZUYDZ-UHFFFAOYSA-N FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)OC)C(=NN=3)C)(C)C Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)S(=O)(=O)C)OC)C(=NN=3)C)(C)C VCEYCSQGTZUYDZ-UHFFFAOYSA-N 0.000 claims description 2
- CVGFSNTWZCPBDS-UHFFFAOYSA-N FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C)OC)C(=NN=3)C)(C)C Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C)OC)C(=NN=3)C)(C)C CVGFSNTWZCPBDS-UHFFFAOYSA-N 0.000 claims description 2
- UWRIQPMGPQVDHJ-UHFFFAOYSA-N FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)S(=O)(=O)C)C)C(=NN=3)C)(C)C Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC=C1)S(=O)(=O)C)C)C(=NN=3)C)(C)C UWRIQPMGPQVDHJ-UHFFFAOYSA-N 0.000 claims description 2
- FQFILJKFZCVHNH-UHFFFAOYSA-N tert-butyl n-[3-[(5-bromo-2-chloropyrimidin-4-yl)amino]propyl]carbamate Chemical compound CC(C)(C)OC(=O)NCCCNC1=NC(Cl)=NC=C1Br FQFILJKFZCVHNH-UHFFFAOYSA-N 0.000 claims description 2
- YPQVWGWNCYQFFL-UHFFFAOYSA-N 1,4,4-trimethyl-8-(3-methyl-1H-indol-7-yl)-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1=NN=C2N1C1=C(C(=CC=C1NC2(C)C)C=1C=CC=C2C(=CNC=12)C)C(F)(F)F YPQVWGWNCYQFFL-UHFFFAOYSA-N 0.000 claims 1
- QGSPPQJNWNCAGK-UHFFFAOYSA-N 1-[4-(7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indol-1-yl]ethanone Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)C(C)=O)F)C(=NN=3)C)(C)C QGSPPQJNWNCAGK-UHFFFAOYSA-N 0.000 claims 1
- AIERWJVBSRXFAU-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-4,4-dimethyl-8-(3-prop-1-ynyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=CC=CC=3C(C#CC)=CNC1=3)F)C(CC)=NN=2)(C)C AIERWJVBSRXFAU-UHFFFAOYSA-N 0.000 claims 1
- ALTDIQTZZPHEQN-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-8-(5-fluoro-1H-indol-7-yl)-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=CC(F)=CC=3C=CNC1=3)F)C(CC)=NN=2)(C)C ALTDIQTZZPHEQN-UHFFFAOYSA-N 0.000 claims 1
- HRFGPUKMHFDAQT-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-8-(5-fluoro-3-prop-1-ynyl-1H-indol-7-yl)-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC(F)=CC=2C(C#CC)=CNC1=2)F)CC)C HRFGPUKMHFDAQT-UHFFFAOYSA-N 0.000 claims 1
- SSHWFGVQVPVZAR-UHFFFAOYSA-N 7,9-difluoro-8-(1H-indazol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NNC2=CC=C1)F)C(=NN=3)C)(C)C SSHWFGVQVPVZAR-UHFFFAOYSA-N 0.000 claims 1
- HIHUZRVWTAMSLU-UHFFFAOYSA-N 7-(1-ethyl-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-1H-indole-3-carbonitrile Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=CC=C2C(=CNC=12)C#N)F HIHUZRVWTAMSLU-UHFFFAOYSA-N 0.000 claims 1
- ILHIRHYRBDIUQC-UHFFFAOYSA-N 7-chloro-8-(3-cyclopropyl-5-fluoro-1H-indol-7-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C=1C=C(C=C2C(=CNC=12)C1CC1)F)C)C(=NN=3)C)(C)C ILHIRHYRBDIUQC-UHFFFAOYSA-N 0.000 claims 1
- MULSPABIBHMIAS-UHFFFAOYSA-N 7-fluoro-8-(7-fluoro-1H-indazol-4-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NNC2=C(C=C1)F)C(F)(F)F)C(=NN=3)C)(C)C MULSPABIBHMIAS-UHFFFAOYSA-N 0.000 claims 1
- KLVZJCMDGAHNSX-UHFFFAOYSA-N 7-fluoro-8-(7-fluoro-1H-indol-4-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CNC2=C(C=C1)F)C)C(=NN=3)C)(C)C KLVZJCMDGAHNSX-UHFFFAOYSA-N 0.000 claims 1
- BPOMNLPHHGLRSO-UHFFFAOYSA-N 8-(1-cyclopropylindol-4-yl)-7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F BPOMNLPHHGLRSO-UHFFFAOYSA-N 0.000 claims 1
- KOSDPVDTWSMZBW-UHFFFAOYSA-N 8-(1-cyclopropylsulfonyl-6-fluoroindol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=C2C(=CC(F)=C1)N(C=C2)S(=O)(=O)C1CC1)F)C)C KOSDPVDTWSMZBW-UHFFFAOYSA-N 0.000 claims 1
- SHCBFUASFJLUJK-UHFFFAOYSA-N 8-(1-cyclopropylsulfonylindazol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)S(=O)(=O)N1N=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F SHCBFUASFJLUJK-UHFFFAOYSA-N 0.000 claims 1
- SGUYSGKIQHZWKO-UHFFFAOYSA-N 8-(1-ethylsulfonyl-6-fluoroindol-4-yl)-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC(F)=CC=2N(C=CC1=2)S(=O)(=O)CC)F)C)C SGUYSGKIQHZWKO-UHFFFAOYSA-N 0.000 claims 1
- KNTXDXXQRTYCCK-UHFFFAOYSA-N 8-(3-cyclopropyl-5-fluoro-1H-indol-7-yl)-7-fluoro-9-methoxy-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)C1=CNC2=C(C=C(C=C12)F)C1=C(C=C2NC(C=3N(C2=C1OC)C(=NN=3)C)(C)C)F KNTXDXXQRTYCCK-UHFFFAOYSA-N 0.000 claims 1
- TUTFBIBZOHHOLQ-UHFFFAOYSA-N 8-(6-fluoro-1-methylindol-4-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC1=CC(=C2C=CN(C2=C1)C)C1=CC=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C TUTFBIBZOHHOLQ-UHFFFAOYSA-N 0.000 claims 1
- XFQMABGOCQSRRV-UHFFFAOYSA-N 8-[1-(cyclopropylmethyl)-6-fluoroindol-4-yl]-1-ethyl-7-fluoro-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2C)C1=CC(F)=CC=2N(CC3CC3)C=CC1=2)F)CC)C XFQMABGOCQSRRV-UHFFFAOYSA-N 0.000 claims 1
- NOHDLZHNSADHSF-UHFFFAOYSA-N 8-[1-(cyclopropylmethyl)indazol-4-yl]-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)CN1N=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F NOHDLZHNSADHSF-UHFFFAOYSA-N 0.000 claims 1
- DMBDWXLOMIPIHV-UHFFFAOYSA-N 8-[1-(cyclopropylmethylsulfonyl)indazol-4-yl]-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)CS(=O)(=O)N1N=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F DMBDWXLOMIPIHV-UHFFFAOYSA-N 0.000 claims 1
- TWNGRBRUWRTUDQ-UHFFFAOYSA-N 8-[1-(cyclopropylmethylsulfonyl)indol-4-yl]-7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)CS(=O)(=O)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)F TWNGRBRUWRTUDQ-UHFFFAOYSA-N 0.000 claims 1
- YAUSPUDDQWIJFB-UHFFFAOYSA-N 9-chloro-8-(3-cyclobutyl-1H-indol-7-yl)-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C)C2=NN=C(N2C2=C(N1)C=C(C(=C2Cl)C1=CC=CC=2C(C3CCC3)=CNC1=2)F)C YAUSPUDDQWIJFB-UHFFFAOYSA-N 0.000 claims 1
- ICXWBIVZTRCUDZ-UHFFFAOYSA-N ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C)F)C(=NN=3)C)(C)C Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)C)F)C(=NN=3)C)(C)C ICXWBIVZTRCUDZ-UHFFFAOYSA-N 0.000 claims 1
- XLOJGFDALABKFD-UHFFFAOYSA-N N-[2-[4-(7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)indol-1-yl]ethyl]-2,2-difluoropropanamide Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCNC(C(C)(F)F)=O)F)C(=NN=3)C)(C)C XLOJGFDALABKFD-UHFFFAOYSA-N 0.000 claims 1
- 102000003676 Glucocorticoid Receptors Human genes 0.000 abstract description 39
- 108090000079 Glucocorticoid Receptors Proteins 0.000 abstract description 39
- 229940117965 Glucocorticoid receptor modulator Drugs 0.000 abstract description 9
- 230000001404 mediated effect Effects 0.000 abstract description 9
- 239000011541 reaction mixture Substances 0.000 description 437
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 361
- 239000000243 solution Substances 0.000 description 235
- 239000007787 solid Substances 0.000 description 186
- 235000019439 ethyl acetate Nutrition 0.000 description 179
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 163
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 155
- 239000012267 brine Substances 0.000 description 155
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 155
- 229910052938 sodium sulfate Inorganic materials 0.000 description 153
- 235000011152 sodium sulphate Nutrition 0.000 description 153
- 239000007832 Na2SO4 Substances 0.000 description 152
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 149
- 239000012044 organic layer Substances 0.000 description 147
- 239000012043 crude product Substances 0.000 description 123
- 238000004440 column chromatography Methods 0.000 description 122
- 239000000543 intermediate Substances 0.000 description 119
- 238000006243 chemical reaction Methods 0.000 description 116
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 116
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 111
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 109
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 99
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 82
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 81
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 71
- 239000002904 solvent Substances 0.000 description 70
- 230000015572 biosynthetic process Effects 0.000 description 56
- 239000000203 mixture Substances 0.000 description 54
- 239000000741 silica gel Substances 0.000 description 52
- 229910002027 silica gel Inorganic materials 0.000 description 52
- 238000003786 synthesis reaction Methods 0.000 description 52
- 239000013058 crude material Substances 0.000 description 50
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 47
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 46
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 45
- 239000000706 filtrate Substances 0.000 description 44
- 238000003756 stirring Methods 0.000 description 42
- 238000005160 1H NMR spectroscopy Methods 0.000 description 41
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 40
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 40
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 36
- 239000000725 suspension Substances 0.000 description 34
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 32
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 29
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 27
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 27
- 239000010410 layer Substances 0.000 description 24
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 22
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 20
- 239000007788 liquid Substances 0.000 description 20
- 238000000034 method Methods 0.000 description 20
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 18
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 18
- 235000011056 potassium acetate Nutrition 0.000 description 18
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 17
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 17
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 17
- AUZONCFQVSMFAP-UHFFFAOYSA-N disulfiram Chemical compound CCN(CC)C(=S)SSC(=S)N(CC)CC AUZONCFQVSMFAP-UHFFFAOYSA-N 0.000 description 16
- 238000003818 flash chromatography Methods 0.000 description 16
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 16
- 239000003480 eluent Substances 0.000 description 15
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 15
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 15
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 15
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 14
- OAYLNYINCPYISS-UHFFFAOYSA-N ethyl acetate;hexane Chemical compound CCCCCC.CCOC(C)=O OAYLNYINCPYISS-UHFFFAOYSA-N 0.000 description 14
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 14
- NWZSZGALRFJKBT-KNIFDHDWSA-N (2s)-2,6-diaminohexanoic acid;(2s)-2-hydroxybutanedioic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O.NCCCC[C@H](N)C(O)=O NWZSZGALRFJKBT-KNIFDHDWSA-N 0.000 description 13
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 13
- 238000005481 NMR spectroscopy Methods 0.000 description 13
- NFHFRUOZVGFOOS-UHFFFAOYSA-N Pd(PPh3)4 Substances [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- IKDUDTNKRLTJSI-UHFFFAOYSA-N hydrazine monohydrate Substances O.NN IKDUDTNKRLTJSI-UHFFFAOYSA-N 0.000 description 13
- 238000002953 preparative HPLC Methods 0.000 description 13
- 229910000104 sodium hydride Inorganic materials 0.000 description 13
- 239000007858 starting material Substances 0.000 description 13
- WLPUWLXVBWGYMZ-UHFFFAOYSA-N tricyclohexylphosphine Chemical compound C1CCCCC1P(C1CCCCC1)C1CCCCC1 WLPUWLXVBWGYMZ-UHFFFAOYSA-N 0.000 description 13
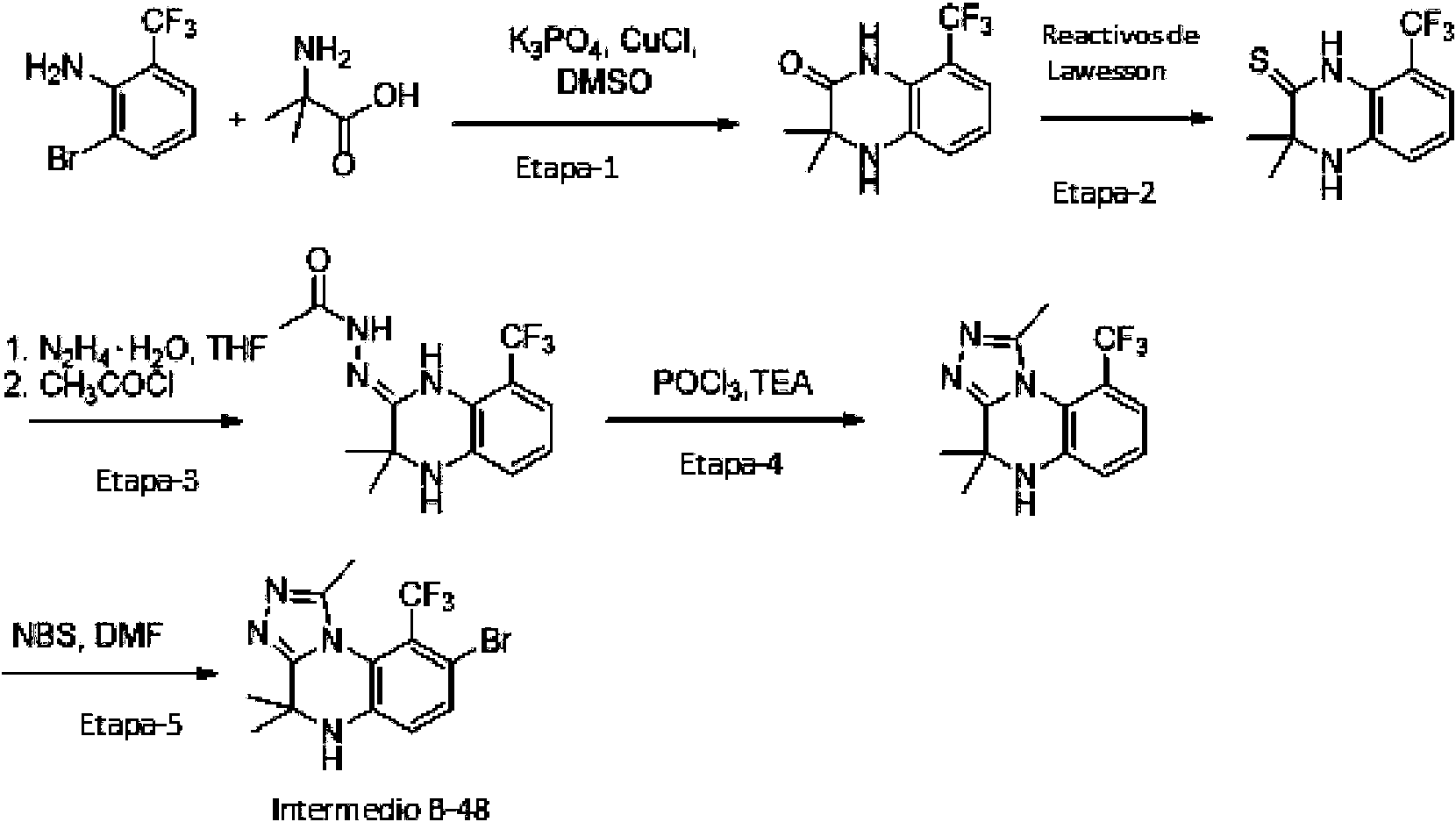
- FUOOLUPWFVMBKG-UHFFFAOYSA-N 2-Aminoisobutyric acid Chemical compound CC(C)(N)C(O)=O FUOOLUPWFVMBKG-UHFFFAOYSA-N 0.000 description 12
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 12
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 12
- 125000003566 oxetanyl group Chemical group 0.000 description 12
- 229910000029 sodium carbonate Inorganic materials 0.000 description 12
- 239000012312 sodium hydride Substances 0.000 description 12
- 125000000530 1-propynyl group Chemical group [H]C([H])([H])C#C* 0.000 description 11
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 11
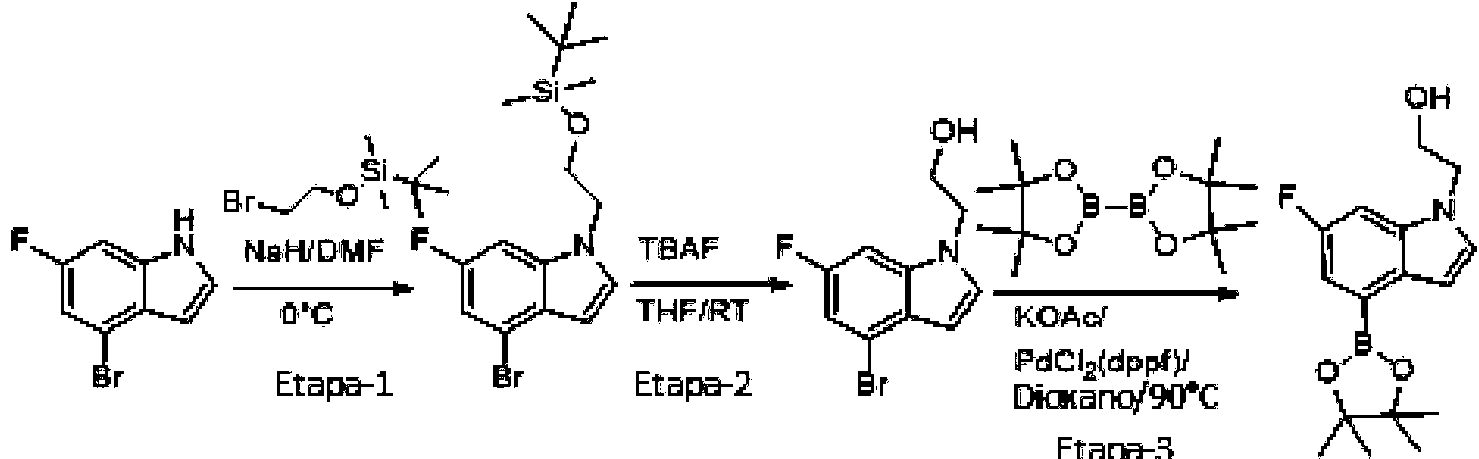
- DMOWKZSCECYXSE-UHFFFAOYSA-N 4-bromo-6-fluoro-1h-indole Chemical compound FC1=CC(Br)=C2C=CNC2=C1 DMOWKZSCECYXSE-UHFFFAOYSA-N 0.000 description 11
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 11
- 229960000583 acetic acid Drugs 0.000 description 11
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 11
- 239000012346 acetyl chloride Substances 0.000 description 11
- 210000004027 cell Anatomy 0.000 description 11
- 239000005457 ice water Substances 0.000 description 11
- CFHGBZLNZZVTAY-UHFFFAOYSA-N lawesson's reagent Chemical compound C1=CC(OC)=CC=C1P1(=S)SP(=S)(C=2C=CC(OC)=CC=2)S1 CFHGBZLNZZVTAY-UHFFFAOYSA-N 0.000 description 11
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Natural products C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 11
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 11
- 238000010992 reflux Methods 0.000 description 11
- 235000017550 sodium carbonate Nutrition 0.000 description 11
- 102100039556 Galectin-4 Human genes 0.000 description 10
- 101000608765 Homo sapiens Galectin-4 Proteins 0.000 description 10
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 10
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 10
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 10
- 238000000746 purification Methods 0.000 description 10
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 9
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 9
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 9
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 9
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 9
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 9
- 235000011114 ammonium hydroxide Nutrition 0.000 description 9
- 229910052799 carbon Inorganic materials 0.000 description 9
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 9
- WGLUMOCWFMKWIL-UHFFFAOYSA-N dichloromethane;methanol Chemical compound OC.ClCCl WGLUMOCWFMKWIL-UHFFFAOYSA-N 0.000 description 9
- 229910052740 iodine Inorganic materials 0.000 description 9
- 239000011630 iodine Substances 0.000 description 9
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 9
- 125000006023 1-pentenyl group Chemical group 0.000 description 8
- 125000006024 2-pentenyl group Chemical group 0.000 description 8
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 8
- 238000003556 assay Methods 0.000 description 8
- 125000004432 carbon atom Chemical group C* 0.000 description 8
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 8
- 239000012299 nitrogen atmosphere Substances 0.000 description 8
- 238000010898 silica gel chromatography Methods 0.000 description 8
- 238000006467 substitution reaction Methods 0.000 description 8
- 229920002554 vinyl polymer Polymers 0.000 description 8
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 7
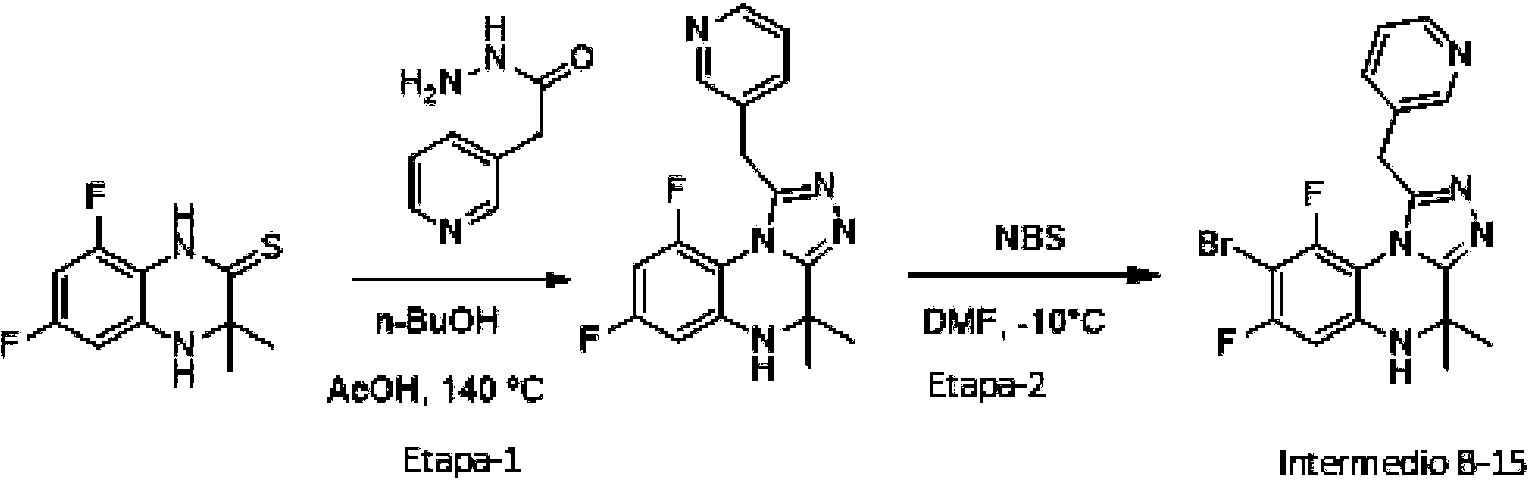
- PEGKLIWRAQMCAC-UHFFFAOYSA-N 6,8-difluoro-3,3-dimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound FC=1C=C2NC(C(NC2=C(C=1)F)=S)(C)C PEGKLIWRAQMCAC-UHFFFAOYSA-N 0.000 description 7
- CFODBBYXRORSGP-UHFFFAOYSA-N 6-fluoro-3,3,8-trimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C)=S)(C)C CFODBBYXRORSGP-UHFFFAOYSA-N 0.000 description 7
- 239000000556 agonist Substances 0.000 description 7
- 125000004122 cyclic group Chemical group 0.000 description 7
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 7
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 7
- 238000000605 extraction Methods 0.000 description 7
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 7
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 7
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 7
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 7
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 7
- 125000006238 prop-1-en-1-yl group Chemical group [H]\C(*)=C(/[H])C([H])([H])[H] 0.000 description 7
- 235000011121 sodium hydroxide Nutrition 0.000 description 7
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 6
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 6
- 239000005557 antagonist Substances 0.000 description 6
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 6
- 238000005859 coupling reaction Methods 0.000 description 6
- WLVKDFJTYKELLQ-UHFFFAOYSA-N cyclopropylboronic acid Chemical compound OB(O)C1CC1 WLVKDFJTYKELLQ-UHFFFAOYSA-N 0.000 description 6
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 6
- 208000035475 disorder Diseases 0.000 description 6
- 239000007789 gas Substances 0.000 description 6
- 239000003862 glucocorticoid Substances 0.000 description 6
- PHTQWCKDNZKARW-UHFFFAOYSA-N isoamylol Chemical compound CC(C)CCO PHTQWCKDNZKARW-UHFFFAOYSA-N 0.000 description 6
- ZCSHNCUQKCANBX-UHFFFAOYSA-N lithium diisopropylamide Chemical compound [Li+].CC(C)[N-]C(C)C ZCSHNCUQKCANBX-UHFFFAOYSA-N 0.000 description 6
- 125000000466 oxiranyl group Chemical group 0.000 description 6
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 6
- MWWATHDPGQKSAR-UHFFFAOYSA-N propyne Chemical compound CC#C MWWATHDPGQKSAR-UHFFFAOYSA-N 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 6
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 6
- CXNIUSPIQKWYAI-UHFFFAOYSA-N xantphos Chemical compound C=12OC3=C(P(C=4C=CC=CC=4)C=4C=CC=CC=4)C=CC=C3C(C)(C)C2=CC=CC=1P(C=1C=CC=CC=1)C1=CC=CC=C1 CXNIUSPIQKWYAI-UHFFFAOYSA-N 0.000 description 6
- CYPYTURSJDMMMP-WVCUSYJESA-N (1e,4e)-1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1.C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 CYPYTURSJDMMMP-WVCUSYJESA-N 0.000 description 5
- CRAMGGHZYOROQI-UHFFFAOYSA-N 5-fluoro-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound FC=1C=C2C=CNC2=C(C=1)B1OC(C(O1)(C)C)(C)C CRAMGGHZYOROQI-UHFFFAOYSA-N 0.000 description 5
- 230000004568 DNA-binding Effects 0.000 description 5
- SLXYJZJXBKWTLN-UHFFFAOYSA-N N-(2-cyclopropyl-4-fluorophenyl)acetamide Chemical compound C1(CC1)C1=C(C=CC(=C1)F)NC(C)=O SLXYJZJXBKWTLN-UHFFFAOYSA-N 0.000 description 5
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 5
- 101150118680 aflR gene Proteins 0.000 description 5
- NBMKJKDGKREAPL-DVTGEIKXSA-N beclomethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(Cl)[C@@H]1[C@@H]1C[C@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O NBMKJKDGKREAPL-DVTGEIKXSA-N 0.000 description 5
- 229940092705 beclomethasone Drugs 0.000 description 5
- 239000010949 copper Substances 0.000 description 5
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 5
- 125000005842 heteroatom Chemical group 0.000 description 5
- 239000003446 ligand Substances 0.000 description 5
- 238000004020 luminiscence type Methods 0.000 description 5
- 229910052698 phosphorus Inorganic materials 0.000 description 5
- 239000011574 phosphorus Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 229940037128 systemic glucocorticoids Drugs 0.000 description 5
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- KDVXWYQULOXLRP-UHFFFAOYSA-N 1-methylsulfonyl-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indole Chemical compound CS(=O)(=O)N1C=CC2=C(C=CC=C12)B1OC(C(O1)(C)C)(C)C KDVXWYQULOXLRP-UHFFFAOYSA-N 0.000 description 4
- 125000005916 2-methylpentyl group Chemical group 0.000 description 4
- 125000005917 3-methylpentyl group Chemical group 0.000 description 4
- ULVDSUCFEQPJSB-UHFFFAOYSA-N 6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1h-indole Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC(F)=CC2=C1C=CN2 ULVDSUCFEQPJSB-UHFFFAOYSA-N 0.000 description 4
- RDSVSEFWZUWZHW-UHFFFAOYSA-N 7-bromo-1h-indole Chemical compound BrC1=CC=CC2=C1NC=C2 RDSVSEFWZUWZHW-UHFFFAOYSA-N 0.000 description 4
- XOMFQRPHXMTJSG-UHFFFAOYSA-N 7-bromo-5-fluoro-1h-indole Chemical compound FC1=CC(Br)=C2NC=CC2=C1 XOMFQRPHXMTJSG-UHFFFAOYSA-N 0.000 description 4
- JBRDBGCBGWURDW-UHFFFAOYSA-N 7-bromo-6,8-difluoro-3,3-dimethyl-1,4-dihydroquinoxalin-2-one Chemical compound BrC1=C(C=C2NC(C(NC2=C1F)=O)(C)C)F JBRDBGCBGWURDW-UHFFFAOYSA-N 0.000 description 4
- QPGBVXASSFHGGP-UHFFFAOYSA-N 7-fluoro-8-(3-iodo-1H-indol-7-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=CC=CC=3C(I)=CNC1=3)C)C(C)=NN=2)(C)C QPGBVXASSFHGGP-UHFFFAOYSA-N 0.000 description 4
- CIECBFLZLFPFRB-UHFFFAOYSA-N 8-bromo-7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1C(F)(F)F)C(=NN=3)C)(C)C)F CIECBFLZLFPFRB-UHFFFAOYSA-N 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 4
- 239000005089 Luciferase Substances 0.000 description 4
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 4
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 4
- 239000012124 Opti-MEM Substances 0.000 description 4
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 4
- 229940045803 cuprous chloride Drugs 0.000 description 4
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 4
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 4
- CSJLBAMHHLJAAS-UHFFFAOYSA-N diethylaminosulfur trifluoride Substances CCN(CC)S(F)(F)F CSJLBAMHHLJAAS-UHFFFAOYSA-N 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 230000014509 gene expression Effects 0.000 description 4
- 208000027866 inflammatory disease Diseases 0.000 description 4
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 4
- 108020001756 ligand binding domains Proteins 0.000 description 4
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 4
- 125000002757 morpholinyl group Chemical group 0.000 description 4
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 4
- 238000001665 trituration Methods 0.000 description 4
- ZBLBNIWXWPMMNO-UHFFFAOYSA-N 1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=CC=C2C(F)(F)F)C)C ZBLBNIWXWPMMNO-UHFFFAOYSA-N 0.000 description 3
- SWXYUHJASGRVLD-UHFFFAOYSA-N 1-methylsulfonyl-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indazole Chemical compound CS(=O)(=O)N1N=CC2=C(C=CC=C12)B1OC(C(O1)(C)C)(C)C SWXYUHJASGRVLD-UHFFFAOYSA-N 0.000 description 3
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 3
- JHZJSKGFAVLZTG-UHFFFAOYSA-N 3-(oxolan-3-yl)-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound C1(C)(OB(OC1(C)C)C1=CC=CC=2C(C3CCOC3)=CNC1=2)C JHZJSKGFAVLZTG-UHFFFAOYSA-N 0.000 description 3
- NWENNJXUXPYQBH-UHFFFAOYSA-N 3-cyclopropyl-5-fluoro-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound C1(CC1)C1=CNC2=C(C=C(C=C12)F)B1OC(C(O1)(C)C)(C)C NWENNJXUXPYQBH-UHFFFAOYSA-N 0.000 description 3
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 3
- KNIACCNVZRPXJD-UHFFFAOYSA-N 5-fluoro-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-3-(2,2,2-trifluoroethyl)-1H-indole Chemical compound FC=1C=C2C(=CNC2=C(C=1)B1OC(C(O1)(C)C)(C)C)CC(F)(F)F KNIACCNVZRPXJD-UHFFFAOYSA-N 0.000 description 3
- KWTAWEJZVCKGHT-UHFFFAOYSA-N 6,8-difluoro-3,3-dimethyl-1,4-dihydroquinoxalin-2-one Chemical compound FC1=CC(F)=C2NC(=O)C(C)(C)NC2=C1 KWTAWEJZVCKGHT-UHFFFAOYSA-N 0.000 description 3
- DAEJZSZMAITTBJ-UHFFFAOYSA-N 6,8-difluoro-3,3-dimethyl-7-(3-methyl-1H-indol-7-yl)-1,4-dihydroquinoxaline-2-thione Chemical compound FC=1C=C2NC(C(NC2=C(C=1C=1C=CC=C2C(=CNC=12)C)F)=S)(C)C DAEJZSZMAITTBJ-UHFFFAOYSA-N 0.000 description 3
- OLQFSGYKJGLXAB-UHFFFAOYSA-N 6,8-difluoro-7-(5-fluoro-3-methyl-1H-indol-7-yl)-3,3-dimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound FC=1C=C2NC(C(NC2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)F)=S)(C)C OLQFSGYKJGLXAB-UHFFFAOYSA-N 0.000 description 3
- RZADCELTGJDOTF-UHFFFAOYSA-N 6-fluoro-1-methylsulfonyl-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indole Chemical compound FC1=CC(=C2C=CN(C2=C1)S(=O)(=O)C)B1OC(C(O1)(C)C)(C)C RZADCELTGJDOTF-UHFFFAOYSA-N 0.000 description 3
- JGHILWPRCUHDLB-UHFFFAOYSA-N 6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1-(2,2,2-trifluoroethyl)indole Chemical compound FC1=CC(=C2C=CN(C2=C1)CC(F)(F)F)B1OC(C(O1)(C)C)(C)C JGHILWPRCUHDLB-UHFFFAOYSA-N 0.000 description 3
- AUBJCFXRCSDESH-UHFFFAOYSA-N 7-bromo-6,8-difluoro-3,3-dimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound BrC1=C(C=C2NC(C(NC2=C1F)=S)(C)C)F AUBJCFXRCSDESH-UHFFFAOYSA-N 0.000 description 3
- XFEBMTWVNOWQRT-UHFFFAOYSA-N 8-bromo-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline-9-carbaldehyde Chemical compound BrC1=CC=C2NC(C=3N(C2=C1C=O)C(=NN=3)C)(C)C XFEBMTWVNOWQRT-UHFFFAOYSA-N 0.000 description 3
- LEGGFLQKONQTAE-UHFFFAOYSA-N CC(=O)n1ccc2c(cccc12)B1OC(C)(C)C(C)(C)O1 Chemical compound CC(=O)n1ccc2c(cccc12)B1OC(C)(C)C(C)(C)O1 LEGGFLQKONQTAE-UHFFFAOYSA-N 0.000 description 3
- 241000699802 Cricetulus griseus Species 0.000 description 3
- 241000400611 Eucalyptus deanei Species 0.000 description 3
- 108090000331 Firefly luciferases Proteins 0.000 description 3
- 108060001084 Luciferase Proteins 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- 230000002411 adverse Effects 0.000 description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-N ammonia Natural products N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 125000002393 azetidinyl group Chemical group 0.000 description 3
- 125000004069 aziridinyl group Chemical group 0.000 description 3
- 125000002619 bicyclic group Chemical group 0.000 description 3
- 229910052794 bromium Inorganic materials 0.000 description 3
- 229910000024 caesium carbonate Inorganic materials 0.000 description 3
- 230000001413 cellular effect Effects 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 3
- DXGPLGPVXNBIQZ-UHFFFAOYSA-L copper;2-hydroxybenzoate;methyl n-(1h-benzimidazol-2-yl)carbamate;6-methyl-n-phenyl-2,3-dihydro-1,4-oxathiine-5-carboxamide;quinolin-8-olate Chemical compound [Cu+2].OC1=CC=CC=C1C([O-])=O.C1=CN=C2C([O-])=CC=CC2=C1.C1=CC=C2NC(NC(=O)OC)=NC2=C1.S1CCOC(C)=C1C(=O)NC1=CC=CC=C1 DXGPLGPVXNBIQZ-UHFFFAOYSA-L 0.000 description 3
- 230000008878 coupling Effects 0.000 description 3
- 238000010168 coupling process Methods 0.000 description 3
- 238000007872 degassing Methods 0.000 description 3
- 125000004852 dihydrofuranyl group Chemical group O1C(CC=C1)* 0.000 description 3
- 125000004611 dihydroisoindolyl group Chemical group C1(NCC2=CC=CC=C12)* 0.000 description 3
- 125000005048 dihydroisoxazolyl group Chemical group O1N(CC=C1)* 0.000 description 3
- 125000005050 dihydrooxazolyl group Chemical group O1C(NC=C1)* 0.000 description 3
- 125000004655 dihydropyridinyl group Chemical group N1(CC=CC=C1)* 0.000 description 3
- 125000005054 dihydropyrrolyl group Chemical group [H]C1=C([H])C([H])([H])C([H])([H])N1* 0.000 description 3
- 125000000532 dioxanyl group Chemical group 0.000 description 3
- 125000005879 dioxolanyl group Chemical group 0.000 description 3
- 125000005411 dithiolanyl group Chemical group S1SC(CC1)* 0.000 description 3
- 231100000673 dose–response relationship Toxicity 0.000 description 3
- 102000037865 fusion proteins Human genes 0.000 description 3
- 108020001507 fusion proteins Proteins 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 125000002632 imidazolidinyl group Chemical group 0.000 description 3
- 125000003965 isoxazolidinyl group Chemical group 0.000 description 3
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 3
- MZRVEZGGRBJDDB-UHFFFAOYSA-N n-Butyllithium Substances [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 3
- 210000001672 ovary Anatomy 0.000 description 3
- 125000000160 oxazolidinyl group Chemical group 0.000 description 3
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 3
- 230000037361 pathway Effects 0.000 description 3
- 125000004193 piperazinyl group Chemical group 0.000 description 3
- 125000003386 piperidinyl group Chemical group 0.000 description 3
- 125000003367 polycyclic group Chemical group 0.000 description 3
- 230000023603 positive regulation of transcription initiation, DNA-dependent Effects 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 3
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 3
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 3
- 235000017557 sodium bicarbonate Nutrition 0.000 description 3
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 125000004853 tetrahydropyridinyl group Chemical group N1(CCCC=C1)* 0.000 description 3
- 125000003554 tetrahydropyrrolyl group Chemical group 0.000 description 3
- 125000003507 tetrahydrothiofenyl group Chemical group 0.000 description 3
- 125000001984 thiazolidinyl group Chemical group 0.000 description 3
- 125000004568 thiomorpholinyl group Chemical group 0.000 description 3
- 230000035903 transrepression Effects 0.000 description 3
- 229940086542 triethylamine Drugs 0.000 description 3
- 238000010626 work up procedure Methods 0.000 description 3
- NBOZWQRTCRJKSC-UHFFFAOYSA-N (1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-9-yl)methanol Chemical compound CC1=NN=C2N1C1=C(C=CC=C1NC2(C)C)CO NBOZWQRTCRJKSC-UHFFFAOYSA-N 0.000 description 2
- MAUMSNABMVEOGP-UHFFFAOYSA-N (methyl-$l^{2}-azanyl)methane Chemical compound C[N]C MAUMSNABMVEOGP-UHFFFAOYSA-N 0.000 description 2
- PDWQYOPXBHPSCA-UHFFFAOYSA-N 1,2-dichloroethane;oxolane Chemical compound ClCCCl.C1CCOC1 PDWQYOPXBHPSCA-UHFFFAOYSA-N 0.000 description 2
- HBHRVYSYHVJDPC-UHFFFAOYSA-N 1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1=NN=C2N1C1=C(C=CC=C1NC2(C)C)C HBHRVYSYHVJDPC-UHFFFAOYSA-N 0.000 description 2
- RTHBJEKDDKPIJZ-UHFFFAOYSA-N 1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline-9-carbaldehyde Chemical compound CC1=NN=C2N1C1=C(C=CC=C1NC2(C)C)C=O RTHBJEKDDKPIJZ-UHFFFAOYSA-N 0.000 description 2
- OUGDCAIKFIWDFM-UHFFFAOYSA-N 1-(4-bromoindol-1-yl)ethanone Chemical compound CC(=O)n1ccc2c(Br)cccc12 OUGDCAIKFIWDFM-UHFFFAOYSA-N 0.000 description 2
- VSRNEXNTFNUVLN-UHFFFAOYSA-N 1-(7-bromo-5-fluoro-1H-indol-3-yl)ethanol Chemical compound BrC=1C=C(C=C2C(=CNC=12)C(C)O)F VSRNEXNTFNUVLN-UHFFFAOYSA-N 0.000 description 2
- RVFSNQWYGVPRCP-UHFFFAOYSA-N 1-(benzenesulfonyl)-4-bromo-6-fluoro-2-methylindole Chemical compound BrC1=C2C=C(N(C2=CC(=C1)F)S(=O)(=O)C1=CC=CC=C1)C RVFSNQWYGVPRCP-UHFFFAOYSA-N 0.000 description 2
- CZEXVNDQUSHRPL-UHFFFAOYSA-N 1-(benzenesulfonyl)-4-bromo-6-fluoroindole Chemical compound C12=CC(F)=CC(Br)=C2C=CN1S(=O)(=O)C1=CC=CC=C1 CZEXVNDQUSHRPL-UHFFFAOYSA-N 0.000 description 2
- NKKBVCVCRYYFRF-UHFFFAOYSA-N 1-benzyl-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C1=CC=CC=C1)C1=NN=C2N1C1=C(C=C(C=C1NC2(C)C)F)F NKKBVCVCRYYFRF-UHFFFAOYSA-N 0.000 description 2
- BEAJAJLXMMUIMT-UHFFFAOYSA-N 1-benzyl-8-bromo-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C1=CC=CC=C1)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)Br)F BEAJAJLXMMUIMT-UHFFFAOYSA-N 0.000 description 2
- YZUPZGFPHUVJKC-UHFFFAOYSA-N 1-bromo-2-methoxyethane Chemical compound COCCBr YZUPZGFPHUVJKC-UHFFFAOYSA-N 0.000 description 2
- ZRTVDCQQSGZXRW-UHFFFAOYSA-N 1-cyclopropyl-6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indole Chemical compound C1(CC1)N1C=CC2=C(C=C(C=C12)F)B1OC(C(O1)(C)C)(C)C ZRTVDCQQSGZXRW-UHFFFAOYSA-N 0.000 description 2
- XXUBVKVWLBBLPC-UHFFFAOYSA-N 1-cyclopropylsulfonyl-6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indole Chemical compound C1(CC1)S(=O)(=O)N1C=CC2=C(C=C(C=C12)F)B1OC(C(O1)(C)C)(C)C XXUBVKVWLBBLPC-UHFFFAOYSA-N 0.000 description 2
- LIABWLXKKNYEFF-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C1=NN=C2N1C1=C(C=C(C=C1NC2(C)C)F)F LIABWLXKKNYEFF-UHFFFAOYSA-N 0.000 description 2
- RQPLIPSBMIYFAL-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-4,4-dimethyl-8-(5-methyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=C(C=C2C=CNC=12)C)F RQPLIPSBMIYFAL-UHFFFAOYSA-N 0.000 description 2
- NAIFNSWLQJCIED-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-8-(3-iodo-5-methyl-1H-indol-7-yl)-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=C(C=C2C(=CNC=12)I)C)F NAIFNSWLQJCIED-UHFFFAOYSA-N 0.000 description 2
- AXAWEEJUCADOIJ-UHFFFAOYSA-N 1-ethyl-7-fluoro-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C=C(F)C=C13)C)C(CC)=NN=2)(C)C AXAWEEJUCADOIJ-UHFFFAOYSA-N 0.000 description 2
- JUZCZYTYEDZNFQ-UHFFFAOYSA-N 1-ethylsulfonyl-6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indole Chemical compound C(C)S(=O)(=O)N1C=CC2=C(C=C(C=C12)F)B1OC(C(O1)(C)C)(C)C JUZCZYTYEDZNFQ-UHFFFAOYSA-N 0.000 description 2
- CHIFTAQVXHNVRW-UHFFFAOYSA-N 1h-indole-3-carbonitrile Chemical compound C1=CC=C2C(C#N)=CNC2=C1 CHIFTAQVXHNVRW-UHFFFAOYSA-N 0.000 description 2
- 125000004793 2,2,2-trifluoroethoxy group Chemical group FC(CO*)(F)F 0.000 description 2
- UWKQJZCTQGMHKD-UHFFFAOYSA-N 2,6-di-tert-butylpyridine Chemical compound CC(C)(C)C1=CC=CC(C(C)(C)C)=N1 UWKQJZCTQGMHKD-UHFFFAOYSA-N 0.000 description 2
- YNTJKQDWYXUTLZ-UHFFFAOYSA-N 2-(3-chlorophenoxy)propanoic acid Chemical compound OC(=O)C(C)OC1=CC=CC(Cl)=C1 YNTJKQDWYXUTLZ-UHFFFAOYSA-N 0.000 description 2
- REIYJGPPNKKCNB-UHFFFAOYSA-N 2-(4-bromo-6-fluoroindazol-1-yl)ethanol Chemical compound BrC1=C2C=NN(C2=CC(=C1)F)CCO REIYJGPPNKKCNB-UHFFFAOYSA-N 0.000 description 2
- NRTUHSWDROVIEN-UHFFFAOYSA-N 2-(4-bromo-6-fluoroindol-1-yl)ethoxy-tert-butyl-dimethylsilane Chemical compound BrC1=C2C=CN(C2=CC(=C1)F)CCO[Si](C)(C)C(C)(C)C NRTUHSWDROVIEN-UHFFFAOYSA-N 0.000 description 2
- ADBUIWGABVQONJ-UHFFFAOYSA-N 2-(difluoromethyl)-4-fluoro-1-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=C(F)C=C1C(F)F ADBUIWGABVQONJ-UHFFFAOYSA-N 0.000 description 2
- GMOKYLWICVYFLS-UHFFFAOYSA-N 2-(difluoromethyl)-4-fluoroaniline Chemical compound NC1=CC=C(F)C=C1C(F)F GMOKYLWICVYFLS-UHFFFAOYSA-N 0.000 description 2
- VGYVBEJDXIPSDL-UHFFFAOYSA-N 2-bromo-4-fluoro-1-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=C(F)C=C1Br VGYVBEJDXIPSDL-UHFFFAOYSA-N 0.000 description 2
- OTYCOVZULSPPPW-UHFFFAOYSA-N 2-bromo-4-fluoro-6-(trifluoromethyl)aniline Chemical compound NC1=C(Br)C=C(F)C=C1C(F)(F)F OTYCOVZULSPPPW-UHFFFAOYSA-N 0.000 description 2
- ZWWPWHUAFDKNCB-UHFFFAOYSA-N 2-bromo-6-(difluoromethyl)-4-fluoroaniline Chemical compound BrC1=C(C(=CC(=C1)F)C(F)F)N ZWWPWHUAFDKNCB-UHFFFAOYSA-N 0.000 description 2
- MHACZOOLIFPIHE-UHFFFAOYSA-N 2-bromo-6-ethyl-4-fluoroaniline Chemical compound CCC1=CC(F)=CC(Br)=C1N MHACZOOLIFPIHE-UHFFFAOYSA-N 0.000 description 2
- JBKINHFZTVLNEM-UHFFFAOYSA-N 2-bromoethoxy-tert-butyl-dimethylsilane Chemical compound CC(C)(C)[Si](C)(C)OCCBr JBKINHFZTVLNEM-UHFFFAOYSA-N 0.000 description 2
- VYZFBDMDLZPLCQ-UHFFFAOYSA-N 2-cyclopropyl-4-fluoroaniline Chemical compound NC1=CC=C(F)C=C1C1CC1 VYZFBDMDLZPLCQ-UHFFFAOYSA-N 0.000 description 2
- RKFMDUVMPSAXRJ-UHFFFAOYSA-N 2-ethenyl-4-fluoro-1-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=C(F)C=C1C=C RKFMDUVMPSAXRJ-UHFFFAOYSA-N 0.000 description 2
- AFCGCODEEUFDAF-UHFFFAOYSA-N 2-ethyl-4-fluoroaniline Chemical compound CCC1=CC(F)=CC=C1N AFCGCODEEUFDAF-UHFFFAOYSA-N 0.000 description 2
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 2
- CEBKHWWANWSNTI-UHFFFAOYSA-N 2-methylbut-3-yn-2-ol Chemical compound CC(C)(O)C#C CEBKHWWANWSNTI-UHFFFAOYSA-N 0.000 description 2
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 2
- LWIYBOCPCVPJRS-UHFFFAOYSA-N 3,3,8-trimethyl-1,4-dihydroquinoxalin-2-one Chemical compound N1C(C)(C)C(=O)NC2=C1C=CC=C2C LWIYBOCPCVPJRS-UHFFFAOYSA-N 0.000 description 2
- LZZLDOLIITUADP-UHFFFAOYSA-N 3,3,8-trimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound CC1(C(NC2=C(C=CC=C2N1)C)=S)C LZZLDOLIITUADP-UHFFFAOYSA-N 0.000 description 2
- PFGCUTKHSCDCMD-UHFFFAOYSA-N 3,3-dimethyl-8-(trifluoromethyl)-1,4-dihydroquinoxalin-2-one Chemical compound CC1(C)Nc2cccc(c2NC1=O)C(F)(F)F PFGCUTKHSCDCMD-UHFFFAOYSA-N 0.000 description 2
- KEILIKTWFFSANO-UHFFFAOYSA-N 3,3-dimethyl-8-(trifluoromethyl)-1,4-dihydroquinoxaline-2-thione Chemical compound CC1(C(NC2=C(C=CC=C2N1)C(F)(F)F)=S)C KEILIKTWFFSANO-UHFFFAOYSA-N 0.000 description 2
- QOXOZONBQWIKDA-UHFFFAOYSA-N 3-hydroxypropyl Chemical compound [CH2]CCO QOXOZONBQWIKDA-UHFFFAOYSA-N 0.000 description 2
- BMBWYAHYJLTCPP-UHFFFAOYSA-N 3-methyl-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1h-indole Chemical compound C1=CC=C2C(C)=CNC2=C1B1OC(C)(C)C(C)(C)O1 BMBWYAHYJLTCPP-UHFFFAOYSA-N 0.000 description 2
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 2
- PCHRHKUFYHUJBZ-UHFFFAOYSA-N 4-bromo-1-(2,2-difluoroethyl)-6-fluoroindole Chemical compound BrC1=C2C=CN(C2=CC(=C1)F)CC(F)F PCHRHKUFYHUJBZ-UHFFFAOYSA-N 0.000 description 2
- NXKQAFKTMQXQEM-UHFFFAOYSA-N 4-bromo-1-cyclopropyl-6-fluoroindole Chemical compound BrC1=C2C=CN(C2=CC(=C1)F)C1CC1 NXKQAFKTMQXQEM-UHFFFAOYSA-N 0.000 description 2
- ZEJIPOITFAKAOV-UHFFFAOYSA-N 4-bromo-1-cyclopropylsulfonyl-6-fluoroindole Chemical compound C1(=CC(F)=CC=2N(C=CC1=2)S(=O)(=O)C1CC1)Br ZEJIPOITFAKAOV-UHFFFAOYSA-N 0.000 description 2
- YCRSMIGCDBHLRR-UHFFFAOYSA-N 4-bromo-1-ethylsulfonyl-6-fluoroindole Chemical compound BrC1=C2C=CN(C2=CC(=C1)F)S(=O)(=O)CC YCRSMIGCDBHLRR-UHFFFAOYSA-N 0.000 description 2
- JFBLMHVEFLSUAW-UHFFFAOYSA-N 4-bromo-1-methylsulfonylindazole Chemical compound BrC1=C2C=NN(C2=CC=C1)S(=O)(=O)C JFBLMHVEFLSUAW-UHFFFAOYSA-N 0.000 description 2
- NASJIRWIVQLEQL-UHFFFAOYSA-N 4-bromo-1-methylsulfonylindole Chemical compound BrC1=C2C=CN(C2=CC=C1)S(=O)(=O)C NASJIRWIVQLEQL-UHFFFAOYSA-N 0.000 description 2
- GRJZJFUBQYULKL-UHFFFAOYSA-N 4-bromo-1h-indole Chemical compound BrC1=CC=CC2=C1C=CN2 GRJZJFUBQYULKL-UHFFFAOYSA-N 0.000 description 2
- INOLHLMHAZZHNC-UHFFFAOYSA-N 4-bromo-6-fluoro-1-(2,2,2-trifluoroethyl)indole Chemical compound BrC1=C2C=CN(C2=CC(=C1)F)CC(F)(F)F INOLHLMHAZZHNC-UHFFFAOYSA-N 0.000 description 2
- ZWNWZLXYXCKMBA-UHFFFAOYSA-N 4-bromo-6-fluoro-1-(2-methoxyethyl)indole Chemical compound C1=C(F)C=C2N(CCOC)C=CC2=C1Br ZWNWZLXYXCKMBA-UHFFFAOYSA-N 0.000 description 2
- NPJQSCIXDWNCKY-UHFFFAOYSA-N 4-bromo-6-fluoro-1-methylsulfonylindazole Chemical compound BrC1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C NPJQSCIXDWNCKY-UHFFFAOYSA-N 0.000 description 2
- BPIWPHSYLXYURY-UHFFFAOYSA-N 4-bromo-6-fluoro-1-methylsulfonylindole Chemical compound CS(=O)(=O)n1ccc2c(Br)cc(F)cc12 BPIWPHSYLXYURY-UHFFFAOYSA-N 0.000 description 2
- MVXYHEQEDIYGJN-UHFFFAOYSA-N 4-bromo-6-fluoro-1H-indole-2-carbonitrile Chemical compound Fc1cc(Br)c2cc([nH]c2c1)C#N MVXYHEQEDIYGJN-UHFFFAOYSA-N 0.000 description 2
- HBFJMBJKIVHKRN-UHFFFAOYSA-N 4-bromo-6-fluoro-1H-indole-2-carboxamide Chemical compound BrC1=C2C=C(NC2=CC(=C1)F)C(=O)N HBFJMBJKIVHKRN-UHFFFAOYSA-N 0.000 description 2
- VUKKRGQLFZMXNZ-UHFFFAOYSA-N 4-bromo-6-fluoro-1h-indazole Chemical compound FC1=CC(Br)=C2C=NNC2=C1 VUKKRGQLFZMXNZ-UHFFFAOYSA-N 0.000 description 2
- QLXJQHDHMHTMAL-UHFFFAOYSA-N 4-bromo-6-fluoro-1h-indole-2-carboxylic acid Chemical compound C1=C(F)C=C2NC(C(=O)O)=CC2=C1Br QLXJQHDHMHTMAL-UHFFFAOYSA-N 0.000 description 2
- KWOXFTXDNBBHFX-UHFFFAOYSA-N 4-bromo-6-fluoro-2-methyl-1H-indole Chemical compound Cc1cc2c(Br)cc(F)cc2[nH]1 KWOXFTXDNBBHFX-UHFFFAOYSA-N 0.000 description 2
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 2
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 description 2
- XCKPEIWHNXQMAD-UHFFFAOYSA-N 5-fluoro-3-methyl-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound FC=1C=C2C(=CNC2=C(C=1)B1OC(C(O1)(C)C)(C)C)C XCKPEIWHNXQMAD-UHFFFAOYSA-N 0.000 description 2
- ZJLJKDMKVPOUHW-UHFFFAOYSA-N 5-methyl-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound Cc1cc(B2OC(C)(C)C(C)(C)O2)c2[nH]ccc2c1 ZJLJKDMKVPOUHW-UHFFFAOYSA-N 0.000 description 2
- QQWHUALCHHURHK-UHFFFAOYSA-N 6,8-difluoro-3,3-dimethyl-7-(3-methyl-1H-indol-7-yl)-1,4-dihydroquinoxalin-2-one Chemical compound FC=1C=C2NC(C(NC2=C(C=1C=1C=CC=C2C(=CNC=12)C)F)=O)(C)C QQWHUALCHHURHK-UHFFFAOYSA-N 0.000 description 2
- XQDQRTCZRQUOPV-UHFFFAOYSA-N 6,8-difluoro-7-(5-fluoro-3-methyl-1H-indol-7-yl)-3,3-dimethyl-1,4-dihydroquinoxalin-2-one Chemical compound FC=1C=C2NC(C(NC2=C(C=1C=1C=C(C=C2C(=CNC=12)C)F)F)=O)(C)C XQDQRTCZRQUOPV-UHFFFAOYSA-N 0.000 description 2
- YKSCTXZAXYCEGL-UHFFFAOYSA-N 6-fluoro-1-(2-methoxyethyl)-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indole Chemical compound FC1=CC(=C2C=CN(C2=C1)CCOC)B1OC(C(O1)(C)C)(C)C YKSCTXZAXYCEGL-UHFFFAOYSA-N 0.000 description 2
- FQJIYIBGBZWQLI-UHFFFAOYSA-N 6-fluoro-1-methylsulfonyl-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indazole Chemical compound FC1=CC(=C2C=NN(C2=C1)S(=O)(=O)C)B1OC(C(O1)(C)C)(C)C FQJIYIBGBZWQLI-UHFFFAOYSA-N 0.000 description 2
- LTHIUKJMNPDQBE-UHFFFAOYSA-N 6-fluoro-3,3,8-trimethyl-1,4-dihydroquinoxalin-2-one Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C)=O)(C)C LTHIUKJMNPDQBE-UHFFFAOYSA-N 0.000 description 2
- NISFHCQMWLFLKP-UHFFFAOYSA-N 6-fluoro-3,3-dimethyl-8-(trifluoromethyl)-1,4-dihydroquinoxalin-2-one Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C(F)(F)F)=O)(C)C NISFHCQMWLFLKP-UHFFFAOYSA-N 0.000 description 2
- AGXUEQQUCZAXGT-UHFFFAOYSA-N 6-fluoro-3,3-dimethyl-8-(trifluoromethyl)-1,4-dihydroquinoxaline-2-thione Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C(F)(F)F)=S)(C)C AGXUEQQUCZAXGT-UHFFFAOYSA-N 0.000 description 2
- JYZILZPNIHWXOJ-UHFFFAOYSA-N 7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1)F)C(=NN=3)C)(C)C JYZILZPNIHWXOJ-UHFFFAOYSA-N 0.000 description 2
- MQIUUSJELALAFF-UHFFFAOYSA-N 7,9-difluoro-4,4-dimethyl-1-(pyridin-2-ylmethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1)F)C(=NN=3)CC1=NC=CC=C1)(C)C MQIUUSJELALAFF-UHFFFAOYSA-N 0.000 description 2
- YGHVMOKOKSJOJN-UHFFFAOYSA-N 7,9-difluoro-4,4-dimethyl-1-(pyridin-3-ylmethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C=C(F)C=C13)F)C(CC1=CN=CC=C1)=NN=2)(C)C YGHVMOKOKSJOJN-UHFFFAOYSA-N 0.000 description 2
- ORJJDUXNTHTYEL-UHFFFAOYSA-N 7,9-difluoro-4,4-dimethyl-1-(pyridin-4-ylmethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C=C(F)C=C13)F)C(CC1=CC=NC=C1)=NN=2)(C)C ORJJDUXNTHTYEL-UHFFFAOYSA-N 0.000 description 2
- UEGUNKFGPNFPOD-UHFFFAOYSA-N 7,9-difluoro-8-(3-iodo-1H-indol-7-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC=CC=2C(I)=CNC1=2)F)C)C UEGUNKFGPNFPOD-UHFFFAOYSA-N 0.000 description 2
- PQZSMXNNENEWGS-UHFFFAOYSA-N 7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-3-(2,2,2-trifluoroethyl)-1H-indole Chemical compound CC1(OB(OC1(C)C)C=1C=CC=C2C(=CNC=12)CC(F)(F)F)C PQZSMXNNENEWGS-UHFFFAOYSA-N 0.000 description 2
- JXFZRNILTXIQHS-UHFFFAOYSA-N 7-bromo-3-(2,2,2-trifluoroethyl)-1H-indole Chemical compound BrC=1C=CC=C2C(=CNC=12)CC(F)(F)F JXFZRNILTXIQHS-UHFFFAOYSA-N 0.000 description 2
- BHZLCQBNPKEHTN-UHFFFAOYSA-N 7-bromo-3-(oxolan-3-yl)-1H-indole Chemical compound BrC=1C=CC=C2C(=CNC=12)C1COCC1 BHZLCQBNPKEHTN-UHFFFAOYSA-N 0.000 description 2
- JNBXMKSEWNJSIR-UHFFFAOYSA-N 7-bromo-3-cyclobutyl-1H-indole Chemical compound Brc1cccc2c(c[nH]c12)C1CCC1 JNBXMKSEWNJSIR-UHFFFAOYSA-N 0.000 description 2
- KQMPYFSSPFWEMV-UHFFFAOYSA-N 7-bromo-3-cyclopropyl-5-fluoro-1-(methoxymethyl)indole Chemical compound BrC=1C=C(C=C2C(=CN(C=12)COC)C1CC1)F KQMPYFSSPFWEMV-UHFFFAOYSA-N 0.000 description 2
- WZUVJLURLZPVIB-UHFFFAOYSA-N 7-bromo-3-cyclopropyl-5-fluoro-1H-indole Chemical compound Fc1cc(Br)c2[nH]cc(C3CC3)c2c1 WZUVJLURLZPVIB-UHFFFAOYSA-N 0.000 description 2
- PMWADUVPZWTPJQ-UHFFFAOYSA-N 7-bromo-3-ethyl-5-fluoro-1H-indole Chemical compound CCc1c[nH]c2c(Br)cc(F)cc12 PMWADUVPZWTPJQ-UHFFFAOYSA-N 0.000 description 2
- ZSQGHQWPOHETSW-UHFFFAOYSA-N 7-bromo-5-fluoro-1h-indole-3-carbaldehyde Chemical compound FC1=CC(Br)=C2NC=C(C=O)C2=C1 ZSQGHQWPOHETSW-UHFFFAOYSA-N 0.000 description 2
- IWLZHMUZDOTSRL-UHFFFAOYSA-N 7-bromo-5-fluoro-3-(2,2,2-trifluoroethyl)-1H-indole Chemical compound BrC=1C=C(C=C2C(=CNC=12)CC(F)(F)F)F IWLZHMUZDOTSRL-UHFFFAOYSA-N 0.000 description 2
- WBGJCCIVCWRGGY-UHFFFAOYSA-N 7-bromo-5-fluoro-3-iodo-1-(methoxymethyl)indole Chemical compound BrC=1C=C(C=C2C(=CN(C=12)COC)I)F WBGJCCIVCWRGGY-UHFFFAOYSA-N 0.000 description 2
- CQYDSEUYZTYLEQ-UHFFFAOYSA-N 7-bromo-5-fluoro-3-iodo-1H-indole Chemical compound BrC=1C=C(C=C2C(=CNC=12)I)F CQYDSEUYZTYLEQ-UHFFFAOYSA-N 0.000 description 2
- RIPHXXHZNPGTMV-UHFFFAOYSA-N 7-bromo-5-fluoro-3-methyl-1h-indole Chemical compound C1=C(F)C=C2C(C)=CNC2=C1Br RIPHXXHZNPGTMV-UHFFFAOYSA-N 0.000 description 2
- DCPYEEKBRKJUCY-UHFFFAOYSA-N 7-bromo-5-methyl-1h-indole Chemical compound CC1=CC(Br)=C2NC=CC2=C1 DCPYEEKBRKJUCY-UHFFFAOYSA-N 0.000 description 2
- SWLFDQWZQJMRIV-UHFFFAOYSA-N 7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1)C)C(=NN=3)C)(C)C SWLFDQWZQJMRIV-UHFFFAOYSA-N 0.000 description 2
- PXLRXIQNKPIWBP-UHFFFAOYSA-N 7-fluoro-1,4,4,9-tetramethyl-8-(3-prop-1-ynyl-1H-indol-7-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=C3C(=CC=C1)C(C#CC)=CN3)C)C(C)=NN=2)(C)C PXLRXIQNKPIWBP-UHFFFAOYSA-N 0.000 description 2
- DGBXVFRYTUIOPJ-UHFFFAOYSA-N 7-fluoro-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1)C(F)(F)F)C(=NN=3)C)(C)C DGBXVFRYTUIOPJ-UHFFFAOYSA-N 0.000 description 2
- KSTBHQSWGOYXTJ-UHFFFAOYSA-N 7-fluoro-4,4,9-trimethyl-1-(1-phenylmethoxyethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C1=CC=CC=C1)OC(C)C1=NN=C2N1C1=C(C=C(C=C1NC2(C)C)F)C KSTBHQSWGOYXTJ-UHFFFAOYSA-N 0.000 description 2
- QCMUPVGOZYKCPA-UHFFFAOYSA-N 8-(difluoromethyl)-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxalin-2-one Chemical compound FC(C=1C=C(C=C2NC(C(NC=12)=O)(C)C)F)F QCMUPVGOZYKCPA-UHFFFAOYSA-N 0.000 description 2
- OAPPHIJDYBRYHW-UHFFFAOYSA-N 8-(difluoromethyl)-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound FC(C=1C=C(C=C2NC(C(NC=12)=S)(C)C)F)F OAPPHIJDYBRYHW-UHFFFAOYSA-N 0.000 description 2
- UGMUMUHBCIANPY-UHFFFAOYSA-N 8-bromo-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=CC=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C UGMUMUHBCIANPY-UHFFFAOYSA-N 0.000 description 2
- IXSBOLFTHISFIB-UHFFFAOYSA-N 8-bromo-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=CC(=C2C(F)(F)F)Br)C)C IXSBOLFTHISFIB-UHFFFAOYSA-N 0.000 description 2
- PGTMDMPABWWMCP-UHFFFAOYSA-N 8-bromo-1-(cyclopropylmethyl)-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)Br)F)C(CC1CC1)=NN=2)(C)C PGTMDMPABWWMCP-UHFFFAOYSA-N 0.000 description 2
- SNYZURCCLDCBFF-UHFFFAOYSA-N 8-bromo-1-ethyl-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)CC)(C)C)F SNYZURCCLDCBFF-UHFFFAOYSA-N 0.000 description 2
- HMCAQJZOFINNTI-UHFFFAOYSA-N 8-bromo-1-ethyl-7-fluoro-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)Br)C)C(CC)=NN=2)(C)C HMCAQJZOFINNTI-UHFFFAOYSA-N 0.000 description 2
- BVZRTNZVRWDIML-UHFFFAOYSA-N 8-bromo-7,9-difluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)Br)F)C(C)=NN=2)(C)C BVZRTNZVRWDIML-UHFFFAOYSA-N 0.000 description 2
- MWZHYTSLVDQSOE-UHFFFAOYSA-N 8-bromo-7,9-difluoro-4,4-dimethyl-1-(pyridin-2-ylmethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)CC1=NC=CC=C1)(C)C)F MWZHYTSLVDQSOE-UHFFFAOYSA-N 0.000 description 2
- MMBAKCJENDFPKZ-UHFFFAOYSA-N 8-bromo-7,9-difluoro-4,4-dimethyl-1-(pyridin-3-ylmethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(NC2=C(N3C1=NN=C3CC1=CC=CN=C1)C(=C(C(F)=C2)Br)F)(C)C MMBAKCJENDFPKZ-UHFFFAOYSA-N 0.000 description 2
- KGPHSPAPHGKENR-UHFFFAOYSA-N 8-bromo-7,9-difluoro-4,4-dimethyl-1-(pyridin-4-ylmethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)CC1=CC=NC=C1)(C)C)F KGPHSPAPHGKENR-UHFFFAOYSA-N 0.000 description 2
- QJNLWUYRWHXLBJ-UHFFFAOYSA-N 8-bromo-7-fluoro-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)Br)C)C(C)=NN=2)(C)C QJNLWUYRWHXLBJ-UHFFFAOYSA-N 0.000 description 2
- UABAESXJQIVZSO-UHFFFAOYSA-N 8-bromo-9-(difluoromethyl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=CC=C2NC(C=3N(C2=C1C(F)F)C(=NN=3)C)(C)C UABAESXJQIVZSO-UHFFFAOYSA-N 0.000 description 2
- NBDVSJQBABIOTL-UHFFFAOYSA-N 8-bromo-9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1C(F)F)C(=NN=3)C)(C)C)F NBDVSJQBABIOTL-UHFFFAOYSA-N 0.000 description 2
- MJPZVRIZDHIMRL-UHFFFAOYSA-N 8-bromo-9-chloro-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1Cl)C(=NN=3)C)(C)C)F MJPZVRIZDHIMRL-UHFFFAOYSA-N 0.000 description 2
- QIGCRMIFXVFHKK-UHFFFAOYSA-N 8-bromo-9-ethyl-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1CC)C(=NN=3)C)(C)C)F QIGCRMIFXVFHKK-UHFFFAOYSA-N 0.000 description 2
- VDEXKCKDDPVVKH-UHFFFAOYSA-N 8-chloro-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxalin-2-one Chemical compound ClC=1C=C(C=C2NC(C(NC=12)=O)(C)C)F VDEXKCKDDPVVKH-UHFFFAOYSA-N 0.000 description 2
- JMZHHTJVJNHFNF-UHFFFAOYSA-N 8-chloro-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound ClC=1C=C(C=C2NC(C(NC=12)=S)(C)C)F JMZHHTJVJNHFNF-UHFFFAOYSA-N 0.000 description 2
- NPKIMYZJJSSESP-UHFFFAOYSA-N 8-cyclopropyl-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound C1(CC1)C=1C=C(C=C2NC(C(NC=12)=S)(C)C)F NPKIMYZJJSSESP-UHFFFAOYSA-N 0.000 description 2
- NHMQPXBMHFBBRT-UHFFFAOYSA-N 8-ethyl-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxalin-2-one Chemical compound C(C)C=1C=C(C=C2NC(C(NC=12)=O)(C)C)F NHMQPXBMHFBBRT-UHFFFAOYSA-N 0.000 description 2
- SUVSTFOJZIERRZ-UHFFFAOYSA-N 8-ethyl-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxaline-2-thione Chemical compound C(C)C=1C=C(C=C2NC(C(NC=12)=S)(C)C)F SUVSTFOJZIERRZ-UHFFFAOYSA-N 0.000 description 2
- RASOGCYPEUFXSJ-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)F RASOGCYPEUFXSJ-UHFFFAOYSA-N 0.000 description 2
- LGKLYPBYUKUWLG-UHFFFAOYSA-N 9-chloro-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound ClC=1C=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F LGKLYPBYUKUWLG-UHFFFAOYSA-N 0.000 description 2
- QSHKPFUXIHQOBA-UHFFFAOYSA-N 9-ethyl-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C(C)C=1C=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F QSHKPFUXIHQOBA-UHFFFAOYSA-N 0.000 description 2
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical compound CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 description 2
- 206010001382 Adrenal suppression Diseases 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical group [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- ROFVEXUMMXZLPA-UHFFFAOYSA-N Bipyridyl Chemical compound N1=CC=CC=C1C1=CC=CC=N1 ROFVEXUMMXZLPA-UHFFFAOYSA-N 0.000 description 2
- NXLVEJUJGSYGNK-UHFFFAOYSA-N BrC1=C(C(=CC(=C1)F)C1CC1)N Chemical compound BrC1=C(C(=CC(=C1)F)C1CC1)N NXLVEJUJGSYGNK-UHFFFAOYSA-N 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 2
- 239000005977 Ethylene Substances 0.000 description 2
- PTKUHYKOQXQADM-UHFFFAOYSA-N FC1=CC(=C2C=C(NC2=C1)C)B1OC(C(O1)(C)C)(C)C Chemical compound FC1=CC(=C2C=C(NC2=C1)C)B1OC(C(O1)(C)C)(C)C PTKUHYKOQXQADM-UHFFFAOYSA-N 0.000 description 2
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- CVKRFZCSHKOSBM-UHFFFAOYSA-N N'-(3,3,8-trimethyl-4H-quinoxalin-2-yl)acetohydrazide Chemical compound CC1(C(NC2=C(C=CC=C2N1)C)=NNC(C)=O)C CVKRFZCSHKOSBM-UHFFFAOYSA-N 0.000 description 2
- NBFFNPQUWQXTIK-UHFFFAOYSA-N N'-(6-fluoro-3,3,8-trimethyl-4H-quinoxalin-2-yl)-2-phenylmethoxypropanehydrazide Chemical compound C(C1=CC=CC=C1)OC(C(=O)NN=C1NC2=C(C=C(C=C2NC1(C)C)F)C)C NBFFNPQUWQXTIK-UHFFFAOYSA-N 0.000 description 2
- HHACKFZCOCSOPX-UHFFFAOYSA-N N'-(6-fluoro-3,3,8-trimethyl-4H-quinoxalin-2-yl)-3-methoxypropanehydrazide Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C)=NNC(CCOC)=O)(C)C HHACKFZCOCSOPX-UHFFFAOYSA-N 0.000 description 2
- WEPGRRJMCYHGSU-UHFFFAOYSA-N N'-(6-fluoro-3,3,8-trimethyl-4H-quinoxalin-2-yl)acetohydrazide Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C)=NNC(C)=O)(C)C WEPGRRJMCYHGSU-UHFFFAOYSA-N 0.000 description 2
- XKMLISXGKFCKJV-UHFFFAOYSA-N N'-(8-chloro-6-fluoro-3,3-dimethyl-4H-quinoxalin-2-yl)acetohydrazide Chemical compound ClC=1C=C(C=C2NC(C(NC=12)=NNC(C)=O)(C)C)F XKMLISXGKFCKJV-UHFFFAOYSA-N 0.000 description 2
- YCRWUPDGXVAVAE-UHFFFAOYSA-N N'-(8-ethyl-6-fluoro-3,3-dimethyl-4H-quinoxalin-2-yl)acetohydrazide Chemical compound C(C)C=1C=C(C=C2NC(C(NC=12)=NNC(C)=O)(C)C)F YCRWUPDGXVAVAE-UHFFFAOYSA-N 0.000 description 2
- ZSXGLVDWWRXATF-UHFFFAOYSA-N N,N-dimethylformamide dimethyl acetal Chemical compound COC(OC)N(C)C ZSXGLVDWWRXATF-UHFFFAOYSA-N 0.000 description 2
- 208000001132 Osteoporosis Diseases 0.000 description 2
- 229910002666 PdCl2 Inorganic materials 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- 101100054666 Streptomyces halstedii sch3 gene Proteins 0.000 description 2
- 208000007271 Substance Withdrawal Syndrome Diseases 0.000 description 2
- SPEUIVXLLWOEMJ-UHFFFAOYSA-N acetaldehyde dimethyl acetal Natural products COC(C)OC SPEUIVXLLWOEMJ-UHFFFAOYSA-N 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 239000000443 aerosol Substances 0.000 description 2
- QWCKQJZIFLGMSD-UHFFFAOYSA-N alpha-aminobutyric acid Chemical compound CCC(N)C(O)=O QWCKQJZIFLGMSD-UHFFFAOYSA-N 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 238000005893 bromination reaction Methods 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 229910002091 carbon monoxide Inorganic materials 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 238000000423 cell based assay Methods 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- DOBRDRYODQBAMW-UHFFFAOYSA-N copper(i) cyanide Chemical compound [Cu+].N#[C-] DOBRDRYODQBAMW-UHFFFAOYSA-N 0.000 description 2
- 238000006880 cross-coupling reaction Methods 0.000 description 2
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 2
- 206010012601 diabetes mellitus Diseases 0.000 description 2
- 125000004786 difluoromethoxy group Chemical group [H]C(F)(F)O* 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- IPZJQDSFZGZEOY-UHFFFAOYSA-N dimethylmethylene Chemical compound C[C]C IPZJQDSFZGZEOY-UHFFFAOYSA-N 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 125000004785 fluoromethoxy group Chemical group [H]C([H])(F)O* 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 239000012362 glacial acetic acid Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- IZZWJPQHPPRVLP-UHFFFAOYSA-N hexane;2-methoxy-2-methylpropane Chemical compound CCCCCC.COC(C)(C)C IZZWJPQHPPRVLP-UHFFFAOYSA-N 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- CBOIHMRHGLHBPB-UHFFFAOYSA-N hydroxymethyl Chemical compound O[CH2] CBOIHMRHGLHBPB-UHFFFAOYSA-N 0.000 description 2
- 230000002757 inflammatory effect Effects 0.000 description 2
- HEBMCVBCEDMUOF-UHFFFAOYSA-N isochromane Chemical compound C1=CC=C2COCCC2=C1 HEBMCVBCEDMUOF-UHFFFAOYSA-N 0.000 description 2
- 230000000155 isotopic effect Effects 0.000 description 2
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 2
- NUJOXMJBOLGQSY-UHFFFAOYSA-N manganese dioxide Chemical compound O=[Mn]=O NUJOXMJBOLGQSY-UHFFFAOYSA-N 0.000 description 2
- XUTPWROKESSNOG-UHFFFAOYSA-N methyl 2,2-dimethyl-3-oxo-1,4-dihydroquinoxaline-5-carboxylate Chemical compound COC(=O)C=1C=CC=C2NC(C(NC=12)=O)(C)C XUTPWROKESSNOG-UHFFFAOYSA-N 0.000 description 2
- FGSIUBWPZRBMOC-UHFFFAOYSA-N methyl 2-amino-3-bromobenzoate Chemical compound COC(=O)C1=CC=CC(Br)=C1N FGSIUBWPZRBMOC-UHFFFAOYSA-N 0.000 description 2
- HNNBQGUXGDZKOH-UHFFFAOYSA-N methyl 4-bromo-6-fluoro-1h-indole-2-carboxylate Chemical compound C1=C(F)C=C2NC(C(=O)OC)=CC2=C1Br HNNBQGUXGDZKOH-UHFFFAOYSA-N 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- VMWJCFLUSKZZDX-UHFFFAOYSA-N n,n-dimethylmethanamine Chemical compound [CH2]N(C)C VMWJCFLUSKZZDX-UHFFFAOYSA-N 0.000 description 2
- JAVSBNOXENOHEI-UHFFFAOYSA-N n-(2-bromo-4-fluorophenyl)acetamide Chemical compound CC(=O)NC1=CC=C(F)C=C1Br JAVSBNOXENOHEI-UHFFFAOYSA-N 0.000 description 2
- MUJIDPITZJWBSW-UHFFFAOYSA-N palladium(2+) Chemical compound [Pd+2] MUJIDPITZJWBSW-UHFFFAOYSA-N 0.000 description 2
- UQPUONNXJVWHRM-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 UQPUONNXJVWHRM-UHFFFAOYSA-N 0.000 description 2
- NIZKVZYBUGUDTI-UHFFFAOYSA-N pent-3-ynoic acid Chemical compound CC#CCC(O)=O NIZKVZYBUGUDTI-UHFFFAOYSA-N 0.000 description 2
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 2
- 125000004076 pyridyl group Chemical group 0.000 description 2
- 238000007363 ring formation reaction Methods 0.000 description 2
- 238000005245 sintering Methods 0.000 description 2
- DAEPDZWVDSPTHF-UHFFFAOYSA-M sodium pyruvate Chemical compound [Na+].CC(=O)C([O-])=O DAEPDZWVDSPTHF-UHFFFAOYSA-M 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- PCZOZSATUTWXIC-UHFFFAOYSA-N tetraethylazanium;cyanide Chemical compound N#[C-].CC[N+](CC)(CC)CC PCZOZSATUTWXIC-UHFFFAOYSA-N 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- YNJBWRMUSHSURL-UHFFFAOYSA-N trichloroacetic acid Chemical compound OC(=O)C(Cl)(Cl)Cl YNJBWRMUSHSURL-UHFFFAOYSA-N 0.000 description 2
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 description 1
- RKOUFQLNMRAACI-UHFFFAOYSA-N 1,1,1-trifluoro-2-iodoethane Chemical compound FC(F)(F)CI RKOUFQLNMRAACI-UHFFFAOYSA-N 0.000 description 1
- KEZRUCVOEDIMPK-UHFFFAOYSA-N 1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline-9-carboxylic acid Chemical compound CC1=NN=C2N1C3=C(C=CC=C3NC2(C)C)C(=O)O KEZRUCVOEDIMPK-UHFFFAOYSA-N 0.000 description 1
- LESFWGACIWWTQG-UHFFFAOYSA-N 1-(2,2-difluoroethyl)-6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indole Chemical compound FC(CN1C=CC2=C(C=C(C=C12)F)B1OC(C(O1)(C)C)(C)C)F LESFWGACIWWTQG-UHFFFAOYSA-N 0.000 description 1
- TVKBBBYDBRQYBR-UHFFFAOYSA-N 1-(7-fluoro-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-1-yl)ethanol Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1)C)C(=NN=3)C(C)O)(C)C TVKBBBYDBRQYBR-UHFFFAOYSA-N 0.000 description 1
- DXKCONYFNXBJLY-UHFFFAOYSA-N 1-(8-bromo-7-fluoro-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-1-yl)ethanol Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C(C)O)(C)C)F DXKCONYFNXBJLY-UHFFFAOYSA-N 0.000 description 1
- XXJGBENTLXFVFI-UHFFFAOYSA-N 1-amino-methylene Chemical compound N[CH2] XXJGBENTLXFVFI-UHFFFAOYSA-N 0.000 description 1
- ZVDFTBJXUXQPAU-UHFFFAOYSA-N 1-bromo-5-fluoro-2-methyl-3-nitrobenzene Chemical compound CC1=C(Br)C=C(F)C=C1[N+]([O-])=O ZVDFTBJXUXQPAU-UHFFFAOYSA-N 0.000 description 1
- HFGMJLTZCUZABK-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-8-(1H-indol-7-yl)-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC=CC=2C=CNC1=2)F)CC)C HFGMJLTZCUZABK-UHFFFAOYSA-N 0.000 description 1
- LGIHCIFCDONZBK-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-8-(3-iodo-1H-indol-7-yl)-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(NC2=C(N3C1=NN=C3CC)C(=C(C(F)=C2)C1=CC=CC=2C(I)=CNC1=2)F)(C)C LGIHCIFCDONZBK-UHFFFAOYSA-N 0.000 description 1
- JDIBCIRKYFYCKT-UHFFFAOYSA-N 1-ethyl-7,9-difluoro-8-(5-fluoro-3-iodo-1H-indol-7-yl)-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=C3C(=CC(F)=C1)C(I)=CN3)F)C(CC)=NN=2)(C)C JDIBCIRKYFYCKT-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- 238000004229 14N NMR spectroscopy Methods 0.000 description 1
- 238000005451 15N solid-state nuclear magnetic resonance spectroscopy Methods 0.000 description 1
- HABOMNOJYJNVHE-UHFFFAOYSA-N 1h-indol-7-ylboronic acid Chemical compound OB(O)C1=CC=CC2=C1NC=C2 HABOMNOJYJNVHE-UHFFFAOYSA-N 0.000 description 1
- YDZWSZWUNZWCOK-UHFFFAOYSA-M 2,2,2-trifluoroethyl-(2,4,6-trimethylphenyl)iodanium trifluoromethanesulfonate Chemical compound FC(S(=O)(=O)[O-])(F)F.FC(C[I+]C1=C(C=C(C=C1C)C)C)(F)F YDZWSZWUNZWCOK-UHFFFAOYSA-M 0.000 description 1
- ZUBSOOAAXYCXMN-UHFFFAOYSA-N 2,2-difluoroethyl 4-methylbenzenesulfonate Chemical compound CC1=CC=C(S(=O)(=O)OCC(F)F)C=C1 ZUBSOOAAXYCXMN-UHFFFAOYSA-N 0.000 description 1
- YZGUDTWQNMJMNL-UHFFFAOYSA-N 2,2-dimethyl-3-oxo-1,4-dihydroquinoxaline-5-carboxylic acid Chemical compound CC1(C)Nc2cccc(C(O)=O)c2NC1=O YZGUDTWQNMJMNL-UHFFFAOYSA-N 0.000 description 1
- CSFVISOIQMHABM-UHFFFAOYSA-N 2-(4,5-dihydro-1H-imidazol-2-yl)phenol Chemical compound OC1=CC=CC=C1C1=NCCN1 CSFVISOIQMHABM-UHFFFAOYSA-N 0.000 description 1
- MFVCEAAJFALISW-UHFFFAOYSA-N 2-(4-bromo-6-fluoroindol-1-yl)ethanol Chemical compound BrC1=C2C=CN(C2=CC(=C1)F)CCO MFVCEAAJFALISW-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- KMLPAXUOFJGCSY-UHFFFAOYSA-N 2-[6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indazol-1-yl]ethanol Chemical compound FC1=CC(=C2C=NN(C2=C1)CCO)B1OC(C(O1)(C)C)(C)C KMLPAXUOFJGCSY-UHFFFAOYSA-N 0.000 description 1
- QCBZRAFZZDYLDX-UHFFFAOYSA-N 2-[6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)indol-1-yl]ethanol Chemical compound FC1=CC(=C2C=CN(C2=C1)CCO)B1OC(C(O1)(C)C)(C)C QCBZRAFZZDYLDX-UHFFFAOYSA-N 0.000 description 1
- SRIZNTFPBWRGPB-UHFFFAOYSA-N 2-amino-3-bromobenzoic acid Chemical compound NC1=C(Br)C=CC=C1C(O)=O SRIZNTFPBWRGPB-UHFFFAOYSA-N 0.000 description 1
- WUJKFVGKLTWVSQ-UHFFFAOYSA-N 2-bromo-4,6-difluoroaniline Chemical compound NC1=C(F)C=C(F)C=C1Br WUJKFVGKLTWVSQ-UHFFFAOYSA-N 0.000 description 1
- VTWSBILIFIFEFG-UHFFFAOYSA-N 2-bromo-4-fluoro-6-methylaniline Chemical compound CC1=CC(F)=CC(Br)=C1N VTWSBILIFIFEFG-UHFFFAOYSA-N 0.000 description 1
- YLMFXCIATJJKQL-UHFFFAOYSA-N 2-bromo-4-fluoroaniline Chemical compound NC1=CC=C(F)C=C1Br YLMFXCIATJJKQL-UHFFFAOYSA-N 0.000 description 1
- OPZDXMCOWFPQPE-UHFFFAOYSA-N 2-bromo-4-fluorobenzaldehyde Chemical compound FC1=CC=C(C=O)C(Br)=C1 OPZDXMCOWFPQPE-UHFFFAOYSA-N 0.000 description 1
- JXNZCXHQQAUHBJ-UHFFFAOYSA-N 2-bromo-4-methyl-1-nitrobenzene Chemical compound CC1=CC=C([N+]([O-])=O)C(Br)=C1 JXNZCXHQQAUHBJ-UHFFFAOYSA-N 0.000 description 1
- BQSYRDIUPNIUGC-UHFFFAOYSA-N 2-bromo-6-(trifluoromethyl)aniline Chemical compound NC1=C(Br)C=CC=C1C(F)(F)F BQSYRDIUPNIUGC-UHFFFAOYSA-N 0.000 description 1
- LIBGMUMMWYKJSC-UHFFFAOYSA-N 2-bromo-6-chloro-4-fluoroaniline Chemical compound NC1=C(Cl)C=C(F)C=C1Br LIBGMUMMWYKJSC-UHFFFAOYSA-N 0.000 description 1
- UKDQALCDSBOTRX-UHFFFAOYSA-N 2-bromo-6-methyl-4-(trifluoromethyl)aniline Chemical compound CC1=CC(C(F)(F)F)=CC(Br)=C1N UKDQALCDSBOTRX-UHFFFAOYSA-N 0.000 description 1
- LDUCMSVRKKDATH-UHFFFAOYSA-N 2-bromo-6-methylaniline Chemical compound CC1=CC=CC(Br)=C1N LDUCMSVRKKDATH-UHFFFAOYSA-N 0.000 description 1
- LDLCZOVUSADOIV-UHFFFAOYSA-N 2-bromoethanol Chemical compound OCCBr LDLCZOVUSADOIV-UHFFFAOYSA-N 0.000 description 1
- GVPVKNZZLIICEQ-UHFFFAOYSA-N 2-cyclopropylacetohydrazide Chemical compound NNC(=O)CC1CC1 GVPVKNZZLIICEQ-UHFFFAOYSA-N 0.000 description 1
- LIUCWHQVLKSECA-UHFFFAOYSA-N 2-hydroxyacetohydrazide Chemical compound NNC(=O)CO LIUCWHQVLKSECA-UHFFFAOYSA-N 0.000 description 1
- XEPXDMNZXBUSOI-UHFFFAOYSA-N 2-methoxyacetohydrazide Chemical compound COCC(=O)NN XEPXDMNZXBUSOI-UHFFFAOYSA-N 0.000 description 1
- VUGCBIWQHSRQBZ-UHFFFAOYSA-N 2-methylbut-3-yn-2-amine Chemical compound CC(C)(N)C#C VUGCBIWQHSRQBZ-UHFFFAOYSA-N 0.000 description 1
- MSXVEPNJUHWQHW-UHFFFAOYSA-N 2-methylbutan-2-ol Chemical compound CCC(C)(C)O MSXVEPNJUHWQHW-UHFFFAOYSA-N 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- FPTCVTJCJMVIDV-UHFFFAOYSA-N 2-phenylacetohydrazide Chemical compound NNC(=O)CC1=CC=CC=C1 FPTCVTJCJMVIDV-UHFFFAOYSA-N 0.000 description 1
- XMTKNMQAPNHLJP-UHFFFAOYSA-N 2-phenylmethoxypropanoyl chloride Chemical compound ClC(=O)C(C)OCC1=CC=CC=C1 XMTKNMQAPNHLJP-UHFFFAOYSA-N 0.000 description 1
- BUCTVILECOJXIB-UHFFFAOYSA-N 2-pyridin-4-ylacetohydrazide Chemical compound NNC(=O)CC1=CC=NC=C1 BUCTVILECOJXIB-UHFFFAOYSA-N 0.000 description 1
- UKTOCZJHSPZPBK-UHFFFAOYSA-N 3-cyclobutyl-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound CC1(OB(OC1(C)C)C1=CC=CC=2C(C3CCC3)=CNC1=2)C UKTOCZJHSPZPBK-UHFFFAOYSA-N 0.000 description 1
- PGHWWHYGEGVEOH-UHFFFAOYSA-N 3-cyclopropyl-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound C1(CC1)C1=CNC2=C(C=CC=C12)B1OC(C(O1)(C)C)(C)C PGHWWHYGEGVEOH-UHFFFAOYSA-N 0.000 description 1
- KKBFIMLNUJDLCL-UHFFFAOYSA-N 3-ethyl-5-fluoro-7-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole Chemical compound C(C)C1=CNC2=C(C=C(C=C12)F)B1OC(C(O1)(C)C)(C)C KKBFIMLNUJDLCL-UHFFFAOYSA-N 0.000 description 1
- JSMDUOFOPDSKIQ-UHFFFAOYSA-N 3-methoxypropanoyl chloride Chemical compound COCCC(Cl)=O JSMDUOFOPDSKIQ-UHFFFAOYSA-N 0.000 description 1
- QDCIXBBEUHMLDN-UHFFFAOYSA-N 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1h-indole Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=CC2=C1C=CN2 QDCIXBBEUHMLDN-UHFFFAOYSA-N 0.000 description 1
- MYZTXGAFWDGFHM-UHFFFAOYSA-N 4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1h-indole-2-carbonitrile Chemical compound O1C(C)(C)C(C)(C)OB1C1=CC=CC2=C1C=C(C#N)N2 MYZTXGAFWDGFHM-UHFFFAOYSA-N 0.000 description 1
- KJIODOACRIRBPB-UHFFFAOYSA-N 4-bromo-1h-indazole Chemical compound BrC1=CC=CC2=C1C=NN2 KJIODOACRIRBPB-UHFFFAOYSA-N 0.000 description 1
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 1
- LRCQLCWUUBSUOY-UHFFFAOYSA-N 4-fluoro-2-(trifluoromethyl)aniline Chemical compound NC1=CC=C(F)C=C1C(F)(F)F LRCQLCWUUBSUOY-UHFFFAOYSA-N 0.000 description 1
- UZFMOKQJFYMBGY-UHFFFAOYSA-N 4-hydroxy-TEMPO Chemical compound CC1(C)CC(O)CC(C)(C)N1[O] UZFMOKQJFYMBGY-UHFFFAOYSA-N 0.000 description 1
- KKAFVHUJZPVWND-UHFFFAOYSA-N 5-fluoro-2-nitrobenzaldehyde Chemical compound [O-][N+](=O)C1=CC=C(F)C=C1C=O KKAFVHUJZPVWND-UHFFFAOYSA-N 0.000 description 1
- 125000006163 5-membered heteroaryl group Chemical group 0.000 description 1
- ONPGOSVDVDPBCY-CQSZACIVSA-N 6-amino-5-[(1r)-1-(2,6-dichloro-3-fluorophenyl)ethoxy]-n-[4-(4-methylpiperazine-1-carbonyl)phenyl]pyridazine-3-carboxamide Chemical compound O([C@H](C)C=1C(=C(F)C=CC=1Cl)Cl)C(C(=NN=1)N)=CC=1C(=O)NC(C=C1)=CC=C1C(=O)N1CCN(C)CC1 ONPGOSVDVDPBCY-CQSZACIVSA-N 0.000 description 1
- XEGWHPKPVKOZKW-UHFFFAOYSA-N 6-fluoro-4-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-1H-indole-2-carbonitrile Chemical compound FC1=CC(=C2C=C(NC2=C1)C#N)B1OC(C(O1)(C)C)(C)C XEGWHPKPVKOZKW-UHFFFAOYSA-N 0.000 description 1
- IKAVGNWBTRDIPL-UHFFFAOYSA-N 7,9-difluoro-1,4,4-trimethyl-8-[3-(trifluoromethyl)-1H-indol-7-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC=CC=2C(C(F)(F)F)=CNC1=2)F)C)C IKAVGNWBTRDIPL-UHFFFAOYSA-N 0.000 description 1
- FRQDOCYSQHHNMB-UHFFFAOYSA-N 7,9-difluoro-8-[6-fluoro-1-(2,2,2-trifluoroethyl)indol-4-yl]-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC(F)=CC=2N(C=CC1=2)CC(F)(F)F)F)C)C FRQDOCYSQHHNMB-UHFFFAOYSA-N 0.000 description 1
- SOOVNNMPIUCBRT-UHFFFAOYSA-N 7-(1-ethyl-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-5-fluoro-1H-indole-3-carbonitrile Chemical compound CC1(C2=NN=C(N2C2=C(N1)C=C(C(=C2F)C1=CC(F)=CC=2C(C#N)=CNC1=2)F)CC)C SOOVNNMPIUCBRT-UHFFFAOYSA-N 0.000 description 1
- SOIFTGWZCNZAHR-UHFFFAOYSA-N 7-(1-ethyl-7,9-difluoro-4,4-dimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-yl)-5-methyl-1H-indole-3-carbonitrile Chemical compound C(C)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=C(C=C2C(=CNC=12)C#N)C)F SOIFTGWZCNZAHR-UHFFFAOYSA-N 0.000 description 1
- DXQTXSMLFFSQIM-UHFFFAOYSA-N 7-fluoro-1-(methoxymethyl)-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C=C(F)C=C13)C)C(COC)=NN=2)(C)C DXQTXSMLFFSQIM-UHFFFAOYSA-N 0.000 description 1
- HLIVQNCFPNZWIQ-UHFFFAOYSA-N 7-fluoro-8-(5-fluoro-1H-indol-7-yl)-1-(methoxymethyl)-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=CC(F)=CC=3C=CNC1=3)C)C(COC)=NN=2)(C)C HLIVQNCFPNZWIQ-UHFFFAOYSA-N 0.000 description 1
- JCHRQTGGPIOEDS-UHFFFAOYSA-N 7-fluoro-8-(5-fluoro-3-iodo-1H-indol-7-yl)-1-(methoxymethyl)-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound N1C(C=2N(C3=C(C(=C(F)C=C13)C1=CC(F)=CC=3C(I)=CNC1=3)C)C(COC)=NN=2)(C)C JCHRQTGGPIOEDS-UHFFFAOYSA-N 0.000 description 1
- YQYWOLAVJDCRRW-UHFFFAOYSA-N 7-fluoro-8-(6-fluoro-1-methylindol-4-yl)-1,4,4-trimethyl-9-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)F)C)C(F)(F)F)C(=NN=3)C)(C)C YQYWOLAVJDCRRW-UHFFFAOYSA-N 0.000 description 1
- TUJARNLBMMNCEU-UHFFFAOYSA-N 8-(5-fluoro-3-methyl-1H-indol-7-yl)-1,4,4,9-tetramethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C=C2C(=CNC2=C(C=1)C1=CC=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C TUJARNLBMMNCEU-UHFFFAOYSA-N 0.000 description 1
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 1
- YMCQHGRXXSALDN-UHFFFAOYSA-N 8-bromo-1,4,4,9-tetramethyl-7-(trifluoromethyl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound BrC1=C(C=C2NC(C=3N(C2=C1C)C(=NN=3)C)(C)C)C(F)(F)F YMCQHGRXXSALDN-UHFFFAOYSA-N 0.000 description 1
- PQXODTNPNPXXJD-UHFFFAOYSA-N 8-bromo-7-fluoro-1-(methoxymethyl)-4,4,9-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound CC1(NC2=C(N3C1=NN=C3COC)C(=C(C(F)=C2)Br)C)C PQXODTNPNPXXJD-UHFFFAOYSA-N 0.000 description 1
- WICJCYUOTYOOSF-UHFFFAOYSA-N 8-bromo-9-cyclopropyl-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(C)(C2=NN=C(N2C2=C(N1)C=C(C(=C2C1CC1)Br)F)C)C WICJCYUOTYOOSF-UHFFFAOYSA-N 0.000 description 1
- ZNTZBZMABHWBMO-UHFFFAOYSA-N 8-cyclopropyl-6-fluoro-3,3-dimethyl-1,4-dihydroquinoxalin-2-one Chemical compound C1(CC1)C=1C=C(C=C2NC(C(NC=12)=O)(C)C)F ZNTZBZMABHWBMO-UHFFFAOYSA-N 0.000 description 1
- RWYMQKDGBSLLAS-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-1,4,4-trimethyl-8-(1-methylindol-4-yl)-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CN(C2=CC=C1)C)F RWYMQKDGBSLLAS-UHFFFAOYSA-N 0.000 description 1
- CDLZCZJYFMZDOT-UHFFFAOYSA-N 9-(difluoromethyl)-7-fluoro-8-(1H-indol-4-yl)-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC(C=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F)C1=C2C=CNC2=CC=C1)F CDLZCZJYFMZDOT-UHFFFAOYSA-N 0.000 description 1
- SCRPYPRVXHLISF-UHFFFAOYSA-N 9-cyclopropyl-7-fluoro-1,4,4-trimethyl-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound C1(CC1)C=1C=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)F SCRPYPRVXHLISF-UHFFFAOYSA-N 0.000 description 1
- RDBFUKSNHPDOOB-UHFFFAOYSA-N 9-fluoro-7-methoxy-1,4,4-trimethyl-8-[2-(trifluoromethyl)-1H-indol-4-yl]-5H-[1,2,4]triazolo[4,3-a]quinoxaline Chemical compound FC=1C(=C(C=C2NC(C=3N(C=12)C(=NN=3)C)(C)C)OC)C1=C2C=C(NC2=CC=C1)C(F)(F)F RDBFUKSNHPDOOB-UHFFFAOYSA-N 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- GQCGQHZRHRUTAF-UHFFFAOYSA-N C(C1=CC=CC=C1)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=C(C=C2C(=CNC=12)C)F)F Chemical compound C(C1=CC=CC=C1)C1=NN=C2N1C1=C(C(=C(C=C1NC2(C)C)F)C=1C=C(C=C2C(=CNC=12)C)F)F GQCGQHZRHRUTAF-UHFFFAOYSA-N 0.000 description 1
- FQFXGHHRTLAIPN-UHFFFAOYSA-N C1(CC1)CS(=O)(=O)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F Chemical compound C1(CC1)CS(=O)(=O)N1C=CC2=C(C=CC=C12)C1=C(C=C2NC(C=3N(C2=C1F)C(=NN=3)C)(C)C)F FQFXGHHRTLAIPN-UHFFFAOYSA-N 0.000 description 1
- XKIQUDPFKKFURP-UHFFFAOYSA-N COC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)C(F)(F)F)C(=NN=3)C)(C)C Chemical compound COC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC=C1)CCOC)C(F)(F)F)C(=NN=3)C)(C)C XKIQUDPFKKFURP-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- XJUZRXYOEPSWMB-UHFFFAOYSA-N Chloromethyl methyl ether Chemical compound COCCl XJUZRXYOEPSWMB-UHFFFAOYSA-N 0.000 description 1
- GCSWEQZAUPGXDX-UHFFFAOYSA-N ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C)C)C(=NN=3)C)(C)C Chemical compound ClC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=NN(C2=CC(=C1)F)S(=O)(=O)C)C)C(=NN=3)C)(C)C GCSWEQZAUPGXDX-UHFFFAOYSA-N 0.000 description 1
- 229910021595 Copper(I) iodide Inorganic materials 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 1
- CYCGRDQQIOGCKX-UHFFFAOYSA-N Dehydro-luciferin Natural products OC(=O)C1=CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 CYCGRDQQIOGCKX-UHFFFAOYSA-N 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 244000166102 Eucalyptus leucoxylon Species 0.000 description 1
- 235000004694 Eucalyptus leucoxylon Nutrition 0.000 description 1
- JSSORRNOFJWUCG-UHFFFAOYSA-N FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)OC)S(=O)(=O)C)C(F)(F)F)C(=NN=3)C)(C)C Chemical compound FC=1C=C2NC(C=3N(C2=C(C=1C1=C2C=CN(C2=CC(=C1)OC)S(=O)(=O)C)C(F)(F)F)C(=NN=3)C)(C)C JSSORRNOFJWUCG-UHFFFAOYSA-N 0.000 description 1
- GISRWBROCYNDME-PELMWDNLSA-N F[C@H]1[C@H]([C@H](NC1=O)COC1=NC=CC2=CC(=C(C=C12)OC)C(=O)N)C Chemical compound F[C@H]1[C@H]([C@H](NC1=O)COC1=NC=CC2=CC(=C(C=C12)OC)C(=O)N)C GISRWBROCYNDME-PELMWDNLSA-N 0.000 description 1
- BJGNCJDXODQBOB-UHFFFAOYSA-N Fivefly Luciferin Natural products OC(=O)C1CSC(C=2SC3=CC(O)=CC=C3N=2)=N1 BJGNCJDXODQBOB-UHFFFAOYSA-N 0.000 description 1
- 208000010412 Glaucoma Diseases 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 206010022489 Insulin Resistance Diseases 0.000 description 1
- DDWFXDSYGUXRAY-UHFFFAOYSA-N Luciferin Natural products CCc1c(C)c(CC2NC(=O)C(=C2C=C)C)[nH]c1Cc3[nH]c4C(=C5/NC(CC(=O)O)C(C)C5CC(=O)O)CC(=O)c4c3C DDWFXDSYGUXRAY-UHFFFAOYSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 206010028289 Muscle atrophy Diseases 0.000 description 1
- HHBXBCWNVDDGIF-UHFFFAOYSA-N N'-(6-fluoro-3,3,8-trimethyl-4H-quinoxalin-2-yl)propanehydrazide Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C)=NNC(CC)=O)(C)C HHBXBCWNVDDGIF-UHFFFAOYSA-N 0.000 description 1
- ADKFVCYWEPIRIO-UHFFFAOYSA-N N'-[3,3-dimethyl-8-(trifluoromethyl)-4H-quinoxalin-2-yl]acetohydrazide Chemical compound CC1(C(NC2=C(C=CC=C2N1)C(F)(F)F)=NNC(C)=O)C ADKFVCYWEPIRIO-UHFFFAOYSA-N 0.000 description 1
- RQQLYKYRFNNDBZ-UHFFFAOYSA-N N'-[6-fluoro-3,3-dimethyl-8-(trifluoromethyl)-4H-quinoxalin-2-yl]acetohydrazide Chemical compound FC=1C=C2NC(C(NC2=C(C=1)C(F)(F)F)=NNC(C)=O)(C)C RQQLYKYRFNNDBZ-UHFFFAOYSA-N 0.000 description 1
- FDUUKNRTIRKXGQ-UHFFFAOYSA-N N'-[8-(difluoromethyl)-6-fluoro-3,3-dimethyl-4H-quinoxalin-2-yl]acetohydrazide Chemical compound FC(C=1C=C(C=C2NC(C(NC=12)=NNC(C)=O)(C)C)F)F FDUUKNRTIRKXGQ-UHFFFAOYSA-N 0.000 description 1
- KWYHDKDOAIKMQN-UHFFFAOYSA-N N,N,N',N'-tetramethylethylenediamine Chemical compound CN(C)CCN(C)C KWYHDKDOAIKMQN-UHFFFAOYSA-N 0.000 description 1
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 108010052090 Renilla Luciferases Proteins 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- 108010084455 Zeocin Proteins 0.000 description 1
- MCRWZBYTLVCCJJ-DKALBXGISA-N [(1s,3r)-3-[[(3s,4s)-3-methoxyoxan-4-yl]amino]-1-propan-2-ylcyclopentyl]-[(1s,4s)-5-[6-(trifluoromethyl)pyrimidin-4-yl]-2,5-diazabicyclo[2.2.1]heptan-2-yl]methanone Chemical compound C([C@]1(N(C[C@]2([H])C1)C(=O)[C@@]1(C[C@@H](CC1)N[C@@H]1[C@@H](COCC1)OC)C(C)C)[H])N2C1=CC(C(F)(F)F)=NC=N1 MCRWZBYTLVCCJJ-DKALBXGISA-N 0.000 description 1
- ITHXHGFXUPNKMX-UHFFFAOYSA-N [6,8-difluoro-3,3-dimethyl-7-(3-methyl-1H-indol-7-yl)-4H-quinoxalin-2-yl]hydrazine Chemical compound FC1=C2NC(C(NC2=CC(=C1C=1C=CC=C2C(=CNC=12)C)F)(C)C)=NN ITHXHGFXUPNKMX-UHFFFAOYSA-N 0.000 description 1
- GZBWAPOSMYJENZ-UHFFFAOYSA-N [6,8-difluoro-7-(5-fluoro-3-methyl-1H-indol-7-yl)-3,3-dimethyl-4H-quinoxalin-2-yl]hydrazine Chemical compound FC1=C2NC(C(NC2=CC(=C1C=1C=C(C=C2C(=CNC=12)C)F)F)(C)C)=NN GZBWAPOSMYJENZ-UHFFFAOYSA-N 0.000 description 1
- OFLXLNCGODUUOT-UHFFFAOYSA-N acetohydrazide Chemical compound C\C(O)=N\N OFLXLNCGODUUOT-UHFFFAOYSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000001270 agonistic effect Effects 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 230000000947 anti-immunosuppressive effect Effects 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 239000012131 assay buffer Substances 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 125000003725 azepanyl group Chemical group 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000005874 benzothiadiazolyl group Chemical group 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 230000027455 binding Effects 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 230000031709 bromination Effects 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- AEILLAXRDHDKDY-UHFFFAOYSA-N bromomethylcyclopropane Chemical compound BrCC1CC1 AEILLAXRDHDKDY-UHFFFAOYSA-N 0.000 description 1
- 230000006037 cell lysis Effects 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- LSXDOTMGLUJQCM-UHFFFAOYSA-M copper(i) iodide Chemical compound I[Cu] LSXDOTMGLUJQCM-UHFFFAOYSA-M 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 125000006448 cycloalkyl cycloalkyl group Chemical group 0.000 description 1
- SHQSVMDWKBRBGB-UHFFFAOYSA-N cyclobutanone Chemical compound O=C1CCC1 SHQSVMDWKBRBGB-UHFFFAOYSA-N 0.000 description 1
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000006547 cyclononyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 1
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- JFYKIEHOOZWARC-UHFFFAOYSA-N cyclopropanecarbohydrazide Chemical compound NNC(=O)C1CC1 JFYKIEHOOZWARC-UHFFFAOYSA-N 0.000 description 1
- PFWWSGFPICCWGU-UHFFFAOYSA-N cyclopropanesulfonyl chloride Chemical compound ClS(=O)(=O)C1CC1 PFWWSGFPICCWGU-UHFFFAOYSA-N 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 125000005959 diazepanyl group Chemical group 0.000 description 1
- WMKGGPCROCCUDY-PHEQNACWSA-N dibenzylideneacetone Chemical compound C=1C=CC=CC=1\C=C\C(=O)\C=C\C1=CC=CC=C1 WMKGGPCROCCUDY-PHEQNACWSA-N 0.000 description 1
- 125000005045 dihydroisoquinolinyl group Chemical group C1(NC=CC2=CC=CC=C12)* 0.000 description 1
- 125000005044 dihydroquinolinyl group Chemical group N1(CC=CC2=CC=CC=C12)* 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- YHEBUXDOUNWVNZ-UHFFFAOYSA-M diphenyl(trifluoromethyl)sulfanium;trifluoromethanesulfonate Chemical compound [O-]S(=O)(=O)C(F)(F)F.C=1C=CC=CC=1[S+](C(F)(F)F)C1=CC=CC=C1 YHEBUXDOUNWVNZ-UHFFFAOYSA-M 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- FRYHCSODNHYDPU-UHFFFAOYSA-N ethanesulfonyl chloride Chemical compound CCS(Cl)(=O)=O FRYHCSODNHYDPU-UHFFFAOYSA-N 0.000 description 1
- UCZLBERYFYDXOM-UHFFFAOYSA-N ethenyltin Chemical compound [Sn]C=C UCZLBERYFYDXOM-UHFFFAOYSA-N 0.000 description 1
- DLLJVQNYBYOKGS-UHFFFAOYSA-N ethoxyethane;pentane Chemical compound CCCCC.CCOCC DLLJVQNYBYOKGS-UHFFFAOYSA-N 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- ZZUFCTLCJUWOSV-UHFFFAOYSA-N furosemide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(C(O)=O)=C1NCC1=CC=CO1 ZZUFCTLCJUWOSV-UHFFFAOYSA-N 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 230000008297 genomic mechanism Effects 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- BHEPBYXIRTUNPN-UHFFFAOYSA-N hydridophosphorus(.) (triplet) Chemical compound [PH] BHEPBYXIRTUNPN-UHFFFAOYSA-N 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- SHFJWMWCIHQNCP-UHFFFAOYSA-M hydron;tetrabutylazanium;sulfate Chemical compound OS([O-])(=O)=O.CCCC[N+](CCCC)(CCCC)CCCC SHFJWMWCIHQNCP-UHFFFAOYSA-M 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- UTWGRMYWDUMKNY-UHFFFAOYSA-N indole-1-carboxylic acid Chemical compound C1=CC=C2N(C(=O)O)C=CC2=C1 UTWGRMYWDUMKNY-UHFFFAOYSA-N 0.000 description 1
- 150000002475 indoles Chemical group 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- MGFYSGNNHQQTJW-UHFFFAOYSA-N iodonium Chemical compound [IH2+] MGFYSGNNHQQTJW-UHFFFAOYSA-N 0.000 description 1
- SVSZHSMOMDNMLS-UHFFFAOYSA-N isoquinolin-7-ylboronic acid Chemical group C1=CN=CC2=CC(B(O)O)=CC=C21 SVSZHSMOMDNMLS-UHFFFAOYSA-N 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- NXPHGHWWQRMDIA-UHFFFAOYSA-M magnesium;carbanide;bromide Chemical compound [CH3-].[Mg+2].[Br-] NXPHGHWWQRMDIA-UHFFFAOYSA-M 0.000 description 1
- RMGJCSHZTFKPNO-UHFFFAOYSA-M magnesium;ethene;bromide Chemical compound [Mg+2].[Br-].[CH-]=C RMGJCSHZTFKPNO-UHFFFAOYSA-M 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- GIIGKSLSTHEBBS-UHFFFAOYSA-N methyl 2,2-dimethyl-3-sulfanylidene-1,4-dihydroquinoxaline-5-carboxylate Chemical compound COC(=O)C=1C=2NC(C(NC=2C=CC=1)(C)C)=S GIIGKSLSTHEBBS-UHFFFAOYSA-N 0.000 description 1
- RXYCUKSOYJWGPE-UHFFFAOYSA-N methyl 2-azidoacetate Chemical compound COC(=O)CN=[N+]=[N-] RXYCUKSOYJWGPE-UHFFFAOYSA-N 0.000 description 1
- UJVBOZXJIAIJAM-UHFFFAOYSA-N methyl 3-(2-acetylhydrazinyl)-2,2-dimethyl-1H-quinoxaline-5-carboxylate Chemical compound COC(=O)C=1C=2NC(C(NC=2C=CC=1)(C)C)=NNC(C)=O UJVBOZXJIAIJAM-UHFFFAOYSA-N 0.000 description 1
- XUCUNBZVJXDMIA-UHFFFAOYSA-N methyl 5-acetyl-1,4,4-trimethyl-[1,2,4]triazolo[4,3-a]quinoxaline-9-carboxylate Chemical compound COC(=O)C=1C=CC=C2N(C(C=3N(C=12)C(=NN=3)C)(C)C)C(C)=O XUCUNBZVJXDMIA-UHFFFAOYSA-N 0.000 description 1
- 230000009149 molecular binding Effects 0.000 description 1
- 238000003032 molecular docking Methods 0.000 description 1
- 201000000585 muscular atrophy Diseases 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 239000005416 organic matter Substances 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 125000005961 oxazepanyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- JLPJFSCQKHRSQR-UHFFFAOYSA-N oxolan-3-one Chemical compound O=C1CCOC1 JLPJFSCQKHRSQR-UHFFFAOYSA-N 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 238000010651 palladium-catalyzed cross coupling reaction Methods 0.000 description 1
- 239000004031 partial agonist Substances 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 125000004817 pentamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- 239000002831 pharmacologic agent Substances 0.000 description 1
- CWCMIVBLVUHDHK-ZSNHEYEWSA-N phleomycin D1 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC[C@@H](N=1)C=1SC=C(N=1)C(=O)NCCCCNC(N)=N)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C CWCMIVBLVUHDHK-ZSNHEYEWSA-N 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000000634 powder X-ray diffraction Methods 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- DXGIRFAFSFKYCF-UHFFFAOYSA-N propanehydrazide Chemical compound CCC(=O)NN DXGIRFAFSFKYCF-UHFFFAOYSA-N 0.000 description 1
- RZWZRACFZGVKFM-UHFFFAOYSA-N propanoyl chloride Chemical compound CCC(Cl)=O RZWZRACFZGVKFM-UHFFFAOYSA-N 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 230000005588 protonation Effects 0.000 description 1
- 229950010131 puromycin Drugs 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000004526 pyridazin-2-yl group Chemical group N1N(C=CC=C1)* 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 150000003252 quinoxalines Chemical class 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- 229940054269 sodium pyruvate Drugs 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- 238000011895 specific detection Methods 0.000 description 1
- 238000003153 stable transfection Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 125000003039 tetrahydroisoquinolinyl group Chemical group C1(NCCC2=CC=CC=C12)* 0.000 description 1
- 125000000147 tetrahydroquinolinyl group Chemical group N1(CCCC2=CC=CC=C12)* 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- CMQCNTNASCDNGR-UHFFFAOYSA-N toluene;hydrate Chemical compound O.CC1=CC=CC=C1 CMQCNTNASCDNGR-UHFFFAOYSA-N 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 1
- 125000003258 trimethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- GPRLSGONYQIRFK-MNYXATJNSA-N triton Chemical compound [3H+] GPRLSGONYQIRFK-MNYXATJNSA-N 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Pain & Pain Management (AREA)
- Rheumatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
La presente invención se refiere a compuestos según la fórmula general (I) que actúan como moduladores del receptor de glucocorticoides y pueden usarse en el tratamiento y/o profilaxis de trastornos que están mediados al menos parcialmente por el receptor de glucocorticoides. (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Derivados de triazolo quinoxalina sustituidos
La presente invención se refiere a compuestos según la fórmula general (I)
que actúan como moduladores del receptor de glucocorticoides y que se pueden usar en el tratamiento y/o la profilaxis de trastornos que están mediados al menos parcialmente por el receptor de glucocorticoides.
Los glucocorticoides (GC) ejercen fuertes efectos terapéuticos antiinflamatorios, inmunosupresores y que modifican la enfermedad mediados por el receptor de glucocorticoides (GR). Durante décadas, han sido muy usados para tratar enfermedades inflamatorias e inmunes y aún representan la terapia más eficaz para esas afecciones. Sin embargo, el tratamiento crónico con GC de enfermedades inflamatorias está obstaculizado por los efectos adversos asociados a los GC. Estos efectos secundarios no deseados incluyen la resistencia a la insulina, diabetes, hipertensión, glaucoma, depresión, osteoporosis, supresión adrenal y desgaste muscular, siendo la osteoporosis y diabetes las enfermedades más graves desde el punto de vista del médico (Hapgood JP. et al., Pharmacol Ther. 2016 sep; 165: 93-113; Buttgereit F. el al, Clin Exp Rheumatol. 2015 jul-ago;33(4 Supl 92):S29-33; Hartmann K. et al, Physiol Rev. 2016 abr;96(2):409-47).
Un ejemplo de un glucocorticoide oral es la prednisona, que se receta con frecuencia para el tratamiento de varios trastornos inflamatorios (De Bosscher K et al., Trends Pharmacol Sci. 2016 ene;37(1):4-16; Buttgereit F. et al., JAMA.
2016;315(22):2442-2458). Debido a que los GC causan supresión adrenal, los síntomas de abstinencia de prednisolona pueden ser graves si el fármaco se interrumpe abruptamente cuando todos los signos de la enfermedad han desaparecido. Por lo tanto, la disminución gradual del GC a dosis fisiológicas es a menudo parte de los protocolos de tratamiento para reducir el riesgo de recaídas y otros síntomas de abstinencia (Liu D. et al., Allergy Asthma Clin Immunol. 2013 ago 15;9(1):30). Por lo tanto, existe una gran necesidad médica de nuevos fármacos antiinflamatorios potentes con menos efectos adversos.
La investigación reciente se ha centrado en el desarrollo de agonistas parciales o moduladores selectivos del receptor de glucocorticoides que activan las vías para inhibir la inflamación, pero evitan dirigirse a las vías que conducen a los efectos adversos asociados a los GC. Se ha demostrado que la mayoría de estos efectos están mediados por diferentes mecanismos genómicos dependientes del GR denominados transactivación y transrepresión. Las acciones antiinflamatorias de los GC se pueden atribuir principalmente a la transrepresión de los genes inflamatorios, mientras que determinados efectos secundarios están mediados predominantemente por la transactivación de varios genes. Según la naturaleza de un ligando, el GR puede modularse selectivamente en una conformación específica que favorezca la transrepresión sobre la transactivación, lo que origina un beneficio terapéutico mejorado (De Bosscher K et al., Trends Pharmacol Sci. 2016 ene;37(1):4-16). El concepto de tales ligandos disociadores ya se definió hace aproximadamente dos décadas y se han identificado varios compuestos que se evaluaron en pruebas preclínicas y clínicas, pero ninguno de ellos ha sido todavía aprobado para su uso clínico.
Los compuestos que son activos como moduladores del receptor de glucocorticoides son también conocidos a partir de los documentos WO 2009/035067 y WO 2017/034006.
Un objeto de la presente invención fue proporcionar compuestos nuevos que sean moduladores del receptor de glucocorticoides y que preferiblemente tengan ventajas sobre los compuestos de la técnica anterior. Los compuestos nuevos deberían ser adecuados en particular para su uso en el tratamiento y/o la profilaxis de trastornos o enfermedades que están mediadas, al menos parcialmente, por el receptor de glucocorticoides.
Se ha alcanzado este objeto mediante el contenido de las reivindicaciones de la patente.
Sorprendentemente, se descubrió que los compuestos según la invención son moduladores muy potentes del receptor de glucocorticoides.
La presente invención se refiere a un compuesto según la fórmula general (I),
en donde
R1 representa H; alquilo-C1-10; cidoalquilo-C3-10; heterocicloalquilo de 3 a 7 miembros; arilo; o heteroarilo de 5 o 6 miembros; en donde cicloalquilo-C3-10, heterocicloalquilo de 3 a 7 miembros, arilo y heteroarilo de 5 o 6 miembros se pueden puentear opcionalmente mediante alquileno-C1-6;
R2 representa H; F; Cl; Br; I; CN; alquilo-C1-10; cicloalquilo-C3-10; O-alquilo-C1-10; N(H)(alquilo-C1-10), N(alquilo-C1-10)2 ; C(O)-alquilo-C1-10; C(O)-O-alquilo-C1-10; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-10); C(O)-N(alquilo-C1-10)2 ; O-cicloalquilo-C3-10; N(H)(cicloalquilo-C3-10), N(alquilo-C1-10)(cicloalquilo-C3-10); C(O)-cicloalquilo-C3-10; C(O)-O-cicloalquilo-C3-10; C(O)-N(H)(cicloalquilo-C3-10) o C(O)-N(alquilo-C1-10)(cicloalquilo-C3-10); en donde el cicloalquilo-C3-10 se puede puentear opcionalmente mediante alquileno-C1-6;
R3 representa H; F; Cl; Br; I; CN; alquilo-C1-10; cicloalquilo-C3-10; O-alquilo-C1-10; N(H)(alquilo-C1-10); N(alquilo-C1-10)2 ; C(O)-alquilo-C1-10; C(O)-O-alquilo-C1-10; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-10); C(O)-N(alquilo-C1-10)2 ; O-cicloalquilo-C3-10; N(H)(cicloalquilo-C3-10), N(alquilo-C1-10)(cicloalquilo-C3-10); C(O)-cicloalquilo-C3-10; C(O)-O-cicloalquilo-C3-10; C(O)-N(H)(cicloalquilo-C3-10) o C(O)-N(alquilo-C1-10)(cicloalquilo-C3-10); en donde el cicloalquilo-C3-10 se puede puentear opcionalmente mediante alquileno-C1-6;
R5 y R6 representan independientemente uno de otro H o alquilo-C1-4 no sustituido;
X representa N o NR7;
Z representa N, NR7 o CR9; con la condición de que cuando X representa NR7, Z representa N o CR9; cuando X representa N, Z representa NR7;
R7 representa H o L-R8; en donde
L representa un enlace; S(O); S(O)2 ; alquileno-C1-6; C(O); alquileno-C1-6-C(O); C(O)-O; alquileno-C1-6-C(O)-O; alquileno-C1-6-N(H)-C(O); alquileno-C1-6-N(alquilo-C1-10)-C(O); alquileno-C1-6-N(H)-C(O)-O; alquileno-C1-6-N(alquilo-C1-10)-C(O)-O; O; NH o N(alquilo-C1-10);
R8 representa alquilo-C1-10; cicloalquilo-C3-10 o heterocicloalquilo de 3 a 7 miembros; en donde el cicloalquilo-C3-10 y el heterocicloalquilo de 3 a 7 miembros se pueden puentear opcionalmente mediante alquileno-C1-6;
R9 y R10 representan independientemente uno de otro H; F; Cl; Br; I; CN; alquilo-C1-10; cicloalquilo-C3-10; heterocicloalquilo de 3 a 7 miembros; S(O)-(alquilo-C1-10); S(O)-(cicloalquilo-C3-10); S(O)-(heterocicloalquilo de 3 a 7 miembros); S(O)2-(alquilo-C1-10); S(O)2-(cicloalquilo-C3-10); S(O)2-(heterocicloalquilo de 3 a 7 miembros); P(O)-(alquilo-C1-10)2 ; P(O)(alquilo-C1-10)(cicloalquilo-C3-10); P(O)(alquilo-C1-10)(heterocicloalquilo de 3 a 7 miembros); P(O)-(O-alquilo-C1-10)2 ; P(O)(O-alquilo-C1-10)(O-cicloalquilo-C3-10); P(O)(O-alquilo-C1-10)(O-(heterocicloalquilo de 3 a 7 miembros)); O-alquilo-C1-10; S-alquilo-C1-10; N(H)(alquilo-C1-10), N(alquilo-C1-10)2 ; C(O)-alquilo-C1-10; C(O)-O-alquilo-C1-10; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-10); C(O)-N(alquilo-C1-10)2 ; O-cicloalquilo-C3-10; N(H)(cicloalquilo-C3-10), N(alquilo-C1-10)(cicloalquilo-C3-10); C(O)-cicloalquilo-C3-10; C(O)-O-cicloalquilo-C3-10; C(O)-N(H)(cicloalquilo-C3-10); C(O)-N(alquilo-C1-10)(cicloalquilo-C3-10); O-heterocicloalquilo de 3 a 7 miembros; N(H)(heterocicloalquilo de 3 a 7 miembros), N(alquilo-C1-10)(heterocicloalquilo de 3 a 7 miembros); C(O)-heterocicloalquilo de 3 a 7 miembros; C(O)-O-(heterocicloalquilo de 3 a 7 miembros); C(O)-N(H)(heterocicloalquilo de 3 a 7 miembros) o C(O)-N(alquilo-C1-10)(heterocicloalquilo de 3 a 7 miembros); en donde el cicloalquilo-C3-10 y el heterocicloalquilo de 3 a 7 miembros se pueden puentear opcionalmente mediante alquileno-C1-6;
R11 representa F; Cl; Br; I; CN; CN; alquilo-C1-10; O-alquilo-C1-10; NO2 ; OH, NH2; cicloalquilo-C3-10;
heterocicloalquilo de 3 a 7 miembros; S(O)-(alquilo-C1-1o); S(O)-(cicloalquilo-C3-1o); S(O)-(heterocicloalquilo de 3 a 7 miembros); s(O)2-(alquilo-Ci-io); S(O)2-(cicloalquilo-C3-1o); S(O)2-(heterocicloalquilo de 3 a 7 miembros); P(O)-(alquilo-Ci-io)2 ; P(O)(alquilo-C1-10)(cicloalquilo-C3-10); P(O)(alquilo-C1-10)(heterocicloalquilo de 3 a 7 miembros); P(O)-(O-alquilo-C1-10)2 ; P(O)(O-alquilo-C1-1o)(O-cicloalquilo-C3-1o); P(O)(O-alquilo-C1-1o)(O-(heterocicloalquilo de 3 a 7 miembros)); O-alquilo-C1-1o; N(H)(alquilo-C1-1o), N(alquilo-C1-1o)2 ; C(O)-alquilo-C1-1o; C(O)-O-alquilo-C1-1o; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-1o); C(O)-N(alquilo-C1-1o)2 ; O-cicloalquilo-C3-1o; N(H)(cicloalquilo-C3-1o), N(alquilo-C1-1o)(cicloalquilo-C3-1o); C(O)-cicloalquilo-C3-1o; C(O)-O-cicloalquilo-C3-1o; C(O)-N(H)(cicloalquilo-C3-1o); C(O)-N(alquilo-C1-1o)(cicloalquilo-C3-1o); O-heterocicloalquilo de 3 a 7 miembros; N(H)(heterocicloalquilo de 3 a 7 miembros), N(alquilo-C1-1o)(heterocicloalquilo de 3 a 7 miembros); C(O)-heterocicloalquilo de 3 a 7 miembros; C(O)-O-(heterocicloalquilo de 3 a 7 miembros); C(O)-N(H)(heterocicloalquilo de 3 a 7 miembros) o C(O)-N(alquilo-C1-1o)(heterocicloalquilo de 3 a 7 miembros); en donde el cicloalquilo-C3-1o y el heterocicloalquilo de 3 a 7 miembros se pueden puentear opcionalmente mediante alquileno-C1-6;
n representa 0, 1,2 o 3;
en donde alquilo-C1-1o, alquilo-C1-4 y alquileno-C1-6 en cada caso independientemente uno de otro, son lineales o ramificados, saturados o insaturados;
en donde alquilo-C1-1o, alquilo-C1-4, alquileno-C1-6, cicloalquilo-C3-1o y heterocicloalquilo de 3 a 7 miembros en cada caso independientemente uno de otro, no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-C1-6; CF3 ; CF2H; CFH2 ; CF2C CFCb; C(O)-alquilo-C1-6; C(O)-OH; C(O)-Oalquilo-C1-6; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; OH; =O; OCF3 ; OCF2H; OCFH2 ; OCF2Cl; OCFCb; O-alquilo-C1-6; O-C(O)-alquilo-C1-6; O-C(O)-O-alquilo-C1-6; O-(CO)-N(H)(alquilo-C1-6); O-C(O)-N(alquilo-C1-6)2 ; O-S(O)2-NH2 ; O-S(O)2-N(H)(alquilo-C1-6); O-S(O)2-N(alquilo-C1-6)2 ; NH2 ; N(H)(alquilo-C1-6); N(alquilo-C1-6)2 ; N(H)-C(O)-alquilo-C1-6; N(H)-C(O)-O-alquilo-C1-6; N(H)-C(O)-NH2 ; N(H)-C(O)-N(H)(alquilo-C1-6); N(H)-C(O)-N(alquilo-C1-6)2 ; N(alquilo-C1-6)-C(O)-alquilo-C1-6; N(alquilo-C1-6)-C(O)-O-alquilo-C1-6; N(alquilo-C1-6)-C(O)-NH2 ; N(alquilo-C1-6)-C(O)-N(H)(alquilo-C1-6); N(alquilo-C1-6)-C(O)-N(alquilo-C1-6)2 ; N(H)-S(O)2OH; N(H)-S(O)2-alquilo-C1-6; N(H)-S(O)2-O-alquilo-C1-6; N(H)-S(O)2-NH2 ; N(H)-S(O)2-N(H)(alquilo-C1-6); N(H)-S(O)2N(alquilo-C1-6)2 ; N(alquilo-C1-6)-S(O)2-OH; N(alquilo-C1-6)-S(O)2-alquilo-C1-6; N(alquilo-C1-6)-S(O)2-O-alquilo-C1-6; N(alquilo-C1-6)-S(O)2-NH2 ; N(alquilo-C1-6)-S(O)2-N(H)(alquilo-C1-6); N(alquilo-C1-6)-S(O)2-N(alquilo-C1-6)2 ; SCF3 ; SCF2H; SCFH2 ; S-alquilo-C1-6; S(O)-alquilo-C1-6; s (o )2-alquilo-C1-6; S(O)2-OH; S(O)2-O-alquilo-C1-6; S(O)2-NH2 ; S(O)2-N(H)(alquilo-C1-6); S(O)2-N(alquilo-C1-6)2 ; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo; heteroarilo de 5 o 6 miembros; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); O-fenilo; O-(heteroarilo de 5 o 6 miembros); C(O)-cicloalquilo-C3-6; C(O)-(heterocicloalquilo de 3 a 6 miembros); C(O)-fenilo; C(O)-(heteroarilo de 5 o 6 miembros); S(O)2-(cicloalquilo-C3-6); S(O)2-(heterocicloalquilo de 3 a 6 miembros); S(O)2-fenilo o S(O)2-(heteroarilo de 5 o 6 miembros);
en donde arilo y heteroarilo de 5 o 6 miembros en cada caso independientemente uno de otro, no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-C1-6; CF3; CF2H; CFH2 ; CF2Cl; CFCb; alquileno-C1-4-CF3; alquileno-C1-4-CF2H; alquileno-C1-4-CFH2; C(O)-alquilo-C1-6; C(O)-OH; C(O)-Oalquilo-C1-6; C(O)-N(H)(OH); C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; OH; OCF3 ; OCF2H; OCFH2 ; OCF2Cl; OCFCl2 ; O-alquilo-C1-6; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); NH2 ; N(H)(alquilo-C1-6); N(alquilo-C1-6)2 ; N(H)-C(O)-alquilo-C1-6; N(alquilo-C1-6)-C(O)-alquilo-C1-6; N(H)-C(O)-NH2 ; N(H)-C(O)-N(H)(alquilo-C1-6); N(H)-C(O)-N(alquilo-C1-6)2 ; N(alquilo-C1-6)-C(O)-N(H)(alquilo-C1-6); N(alquilo-C1-6)-C(O)-N(alquilo-C1-6)2 ; N(H)-S(O)2-alquilo-C1-6; SCF3 ; S-alquilo-C1-6; S(O)-alquilo-C1-6; S(O)2-alquilo-C1-6; S(O)2-NH2 ; S(O)2-N(H)(alquilo-C1-6); S(O)2-N(alquilo-C1-6)2 ; cicloalquilo-C3-6; alquileno-C1-4-cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; alquileno-C1-4-(heterocicloalquilo de 3 a 6 miembros); fenilo o heteroarilo de 5 o 6 miembros;
en la forma del compuesto libre o una sal fisiológicamente aceptable del mismo.
En una realización preferida, el compuesto según la presente invención está presente en forma de compuesto libre. Para el propósito de la memoria descriptiva, "compuesto libre" significa preferiblemente que el compuesto según la presente invención no está presente en forma de una sal. Los métodos para determinar si una sustancia química está presente como compuesto libre o como una sal son conocidos por el experto en la técnica, tales como RMN de estado sólido de 14N o 15N, difracción de rayos X, difracción de rayos X en polvo, IR, Raman, XPS. La 1H-RMN registrada en solución también se puede usar para considerar la presencia de protonación.
En otra realización preferida, el compuesto según la presente invención está presente en forma de una sal fisiológicamente aceptable. Para los propósitos de esta memoria descriptiva, la expresión "sal fisiológicamente aceptable" se refiere preferiblemente a una sal obtenida a partir de un compuesto según la presente invención y a un ácido o base fisiológicamente aceptable.
Según la presente invención, el compuesto según la presente invención puede estar presente en cualquier forma posible, incluidos solvatos, cocristales y polimorfos. Para los propósitos de esta memoria descriptiva, el término "solvato" se refiere preferiblemente a un aducto de (i) un compuesto según la presente invención y/o a una sal fisiológicamente aceptable del mismo con (ii) equivalentes moleculares distintos de uno o más disolventes.
Además, el compuesto según la presente invención puede estar presente en forma de racemato, enantiómeros, diastereómeros, tautómeros o cualquier mezcla de los mismos.
La presente invención también incluye isómeros isotópicos de un compuesto de la invención, en donde al menos un átomo del compuesto se reemplaza por un isótopo del átomo respectivo, que es diferente del isótopo que se produce predominantemente de forma natural, así como cualquier mezcla de isómeros isotópicos de dicho compuesto. Los isótopos preferidos son 2H (deuterio), 3H (tritio), 13C y 14C. Los isómeros isotópicos de un compuesto de la invención generalmente pueden prepararse mediante procedimientos convencionales conocidos por el experto en la técnica.
Según la presente invención, los términos "alquilo-C1-10", "alquilo-CW, "alquilo-CW y "alquilo-CW significan preferiblemente residuos de hidrocarburos alifáticos acíclicos saturados o no saturados (es decir, no aromáticos), que pueden ser lineales (es decir, no ramificados) o ramificados y que pueden no estar sustituidos o estar mono o polisustituidos (por ejemplo, di o trisustituidos) y que contienen de 1 a 10 (es decir, 1, 2, 3, 4, 5, 6, 7, 8, 9 o 10), 1 a 8 (es decir, 1, 2, 3, 4, 5, 6, 7 u 8), 1 a 6 (es decir, 1, 2, 3, 4, 5 o 6) y 1 a 4 (es decir, 1, 2, 3 o 4) átomos de carbono, respectivamente. En una realización preferida, el alquilo-C1-10, alquilo-C1-8, alquilo-C1-6 y alquilo-C1-4 están saturados. En otra realización preferida, el alquilo-C1-10, alquilo-C1-8, alquilo-C1-6 y alquilo-C1-4 no están saturados. Según esta realización, el alquilo-C1-10, alquilo-C1-8, alquilo-C1-6 y alquilo-C1-4 comprenden al menos un doble enlace C-C (un enlace C=C) o al menos un triple enlace C-C (un enlace CeC). Incluso en otra realización preferida, el alquilo-C1-10, alquilo-C1-8, alquilo-C1-6 y alquilo-C1-4 están (i) saturados o (ii) no saturados, en done el alquilo-C1-10, alquilo-C1-8, alquilo-C1-6 y alquilo-C1-4 comprenden al menos uno, preferiblemente un triple enlace C-C (un enlace CeC). Los grupos alquilo-C1-10 preferidos se seleccionan de metilo, etilo, etenilo (vinilo), n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), n-butilo, 1-butinilo, 2-butinilo, 1-butenilo, 2-butenilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, 2-pentilo, 3-pentilo, 1-pentenilo, 2-pentenilo, 1-pentinilo, 2-pentinilo, 2-metilbutilo, 3-metilbutilo, 3-metilbut-2-ilo, 2-metilbut-2-ilo, 3-metilbut-1-inilo, 2,2-dimetilpropilo, n-hexilo, 2-hexilo, 3-hexilo, 2-metilpentilo, 4-metilpentilo, 4-metilpent-2-ilo, 2-metilpent-2-ilo, 3,3-dimetilbutilo, 3,3-dimetilbut-2-ilo, 3-metilpentilo, 3-metilpent-2-ilo y 3-metilpent-3-ilo; más preferiblemente metilo, etilo, n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), n-butilo, 1-butinilo, 2-butinilo, 1-butenilo, 2-butenilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, 2-pentilo, 3-pentilo, 1-pentenilo, 2-pentenilo, 1-pentenilo, 2-pentenilo, 2-metibutilo, 3-metibutilo, 3-metilbut-2-ilo, 2-metilbut-2-ilo, 3-metilbut-1-inilo, 2,2-dimetilpropilo, n-hexilo, n-heptilo, n-octilo, n-nonilo y n-decilo. Los grupos alquilo-C1-8 preferidos se seleccionan de metilo, etilo, etenilo (vinilo), n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), n-butilo, 1-butinilo, 2-butinilo, 1-butenilo, 2- butenilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, 2-pentilo, 3-pentilo, 1-pentenilo, 2-pentenilo, 1-pentinilo, 2-pentinilo, 2-metilbutilo, 3-metilbutilo, 3-metilbut-2-ilo, 2-metilbut-2-ilo, 3-metilbut-1-inilo, 2,2-dimetilpropilo, n-hexilo, 2-hexilo, 3-hexilo, 2-metilpentilo, 4-metilpentilo, 4-metilpent-2-ilo, 2-metilpent-2-ilo, 3,3-dimetilbutilo, 3,3-dimetilbut-2-ilo, 3- metilpentilo, 3-metilpent-2-ilo y 3-metilpent-3-ilo; más preferiblemente metilo, etilo, n-propilo, 2-propilo, 1-propinilo, 2- propinilo, propenilo (-CH2CH=CH2 , -Ch =CH-CH3, -C(=CH2)-CH3), n-butilo, 1-butinilo, 2-butinilo, 1-butenilo, 2-butenilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, 2-pentilo, 3-pentilo, 1-pentenilo, 2-pentenilo, 1-pentenilo, 2-pentenilo, 2-metibutilo, 3-metibutilo, 3-metilbut-2-ilo, 2-metilbut-2-ilo, 3-metilbut-1-inilo, 2,2-dimetilpropilo, n-hexilo, nheptilo, n-octilo, n-nonilo y n-decilo. Los grupos alquilo-C1-6 preferidos se seleccionan de metilo, etilo, etenilo (vinilo), n-propilo, 2-propilo, n-butilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, 2-pentilo, 3-pentilo, 2-metilbutilo, 3-metilbutilo, 3- metilbut-2-ilo, 2-metilbut-2-ilo, 2,2-dimetilpropilo, n-hexilo, 2-hexilo, 3-hexilo, 2-metilpentilo, 4-metilpentilo, 4-metilpent-2-ilo, 2-metilpent-2-ilo, 3,3-dimetilbutilo, 3,3-dimetilbut-2-ilo, 3-metilpentilo, 3-metilpent-2-ilo y 3-metilpent-3-ilo; más preferiblemente metilo, etilo, n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), n-butilo, 1-butinilo, 2-butinilo, 1-butenilo, 2-butenilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, 2-pentilo, 3-pentilo, 1-pentenilo, 2-pentenilo, 1-pentenilo, 2-pentenilo, 2-metibutilo, 3-metibutilo, 3-metilbut-2-ilo, 2-metilbut-2-ilo, 3-metilbut-1-inilo, 2,2-dimetilpropilo, n-hexilo. Los grupos alquilo-C1-6 particularmente preferidos se seleccionan de los grupos alquilo-C1-4. Los grupos alquilo-C1-4 preferidos se seleccionan de metilo, etilo, etenilo (vinilo), n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), nbutilo, 1-butinilo, 2-butinilo, 1-butenilo, 2-butenilo, isobutilo, sec-butilo, terc-butilo y 3-metilbut-1-inilo.
Además, según la presente invención, los términos “alquileno-CW; “alquileno-CW y “alquileno-C1-2” se refieren a residuos alifáticos lineales o ramificados, preferiblemente lineales, y preferiblemente saturados, que se seleccionan preferiblemente del grupo que consiste en metileno (-CH2-), etileno (-CH2CH2-), propileno (-CH2CH2CH2- o -C(CH3)2-), butileno (-CH2CH2CH2CH2-), pentileno (-CH2CH2CH2CH2CH2-) y hexileno (-CH2CH2CH2CH2CH2CH2-); más preferiblemente metileno (-CH2-) y etileno (-CH2CH2-) y lo más preferiblemente metileno (-CH2-). Preferiblemente, el alquileno-C1-6 se selecciona de alquileno-C1-4, más preferiblemente de alquileno-C1-2.
Además, según la presente invención, los términos “cicloalquilo-C3-1o” y “cicloalquilo-C3-6” significan preferiblemente hidrocarburos alifáticos cíclicos que contienen 3, 4, 5, 6, 7, 8, 9 o 10 átomos de carbono y 3, 4, 5 o 6 átomos de carbono, respectivamente, en donde los hidrocarburos en cada caso pueden ser saturados o insaturados (pero no aromáticos), no sustituidos o mono o polisustituidos. Preferiblemente, el cicloalquilo-C3-10 y el cicloalquilo-C3-6 son saturados. El cicloalquilo-C3-10 y el cicloalquilo-C3-6 se pueden unir a la estructura general respectiva superior a través de cualquier miembro del anillo deseado y posible del grupo cicloalquilo. Los grupos cicloalquilo-C3-10 y cicloalquilo-C3-6 también se pueden condensar con otros sistemas anulares saturados, (parcialmente) insaturados, (hetero)cíclicos, aromáticos o heteroaromáticos, es decir, con residuos de cicloalquilo, heterociclilo, arilo o heteroarilo, que en cada caso pueden a su vez estar no sustituidos o mono o polisustituidos. Además, el cicloalquilo-C3-10 y el
cidoalquilo-C3-6 se pueden puentear individualmente o en multiplicidad, tal como, por ejemplo, en el caso de adamantilo, biciclo[2.2.1]heptilo o biciclo[2.2.2]octilo. Sin embargo, preferiblemente, el cicloalquilo-C3-10 y el cicloalquilo-C3-6 no se condensan con otros sistemas anulares ni puenteados. Más preferiblemente, el cicloalquilo-C3-10 y el cicloalquilo-C3-6 no se condensan con otros sistemas anulares ni se puentean y están saturados. Los grupos cicloalquilo-C3-10 preferidos se seleccionan del grupo que consiste en ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, ciclopentenilo, ciclohexenilo, cicloheptilo, ciclooctilo, ciclononilo, ciclodecilo, adamantilo, ciclopentenilo, ciclohexenilo, cicloheptenilo, ciclooctenilo, biciclo[2.2.1]heptilo y biciclo[2.2.2]octilo. Los grupos cicloalquilo-C3-10 particularmente preferidos se seleccionan de los grupos cicloalquilo-C3-6. Los grupos cicloalquilo-C3-6 preferidos se seleccionan del grupo que consiste en ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, ciclopentenilo y ciclohexenilo. Los grupos cicloalquilo-C3-6 particularmente preferidos se seleccionan del grupo que consiste en ciclopropilo, ciclobutilo, ciclopentilo y ciclohexilo, lo más preferiblemente ciclopropilo.
Según la presente invención, los términos "heterocicloalquilo de 3 a 7 miembros" y "heterocicloalquilo de 3 a 6 miembros" significan preferiblemente residuos heterocicloalifáticos saturados o no saturados (pero no aromáticos) que tienen de 3 a 7, es decir, 3, 4, 5, 6 o 7 miembros en el anillo y 3 a 6, es decir, 3, 4, 5 o 6 miembros en el anillo, respectivamente, en donde en cada caso al menos uno, si es apropiado también dos o tres átomos de carbono se reemplazan por un heteroátomo o un grupo de heteroátomos seleccionados cada uno independientemente uno de otro del grupo que consiste en O, S, S(=O), S(=O)2 , N, NH y N(alquilo-C1-4) como N(CH3), en donde los átomos de carbono del anillo pueden estar no sustituidos o mono o polisustituidos. Preferiblemente, el heterocicloalquilo de 3 a 7 miembros y heterocicloalquilo de 3 a 6 miembros están saturados. Los grupos heterocicloalquilo de 3 a 7 miembros y heterocicloalquilo de 3 a 6 miembros también pueden condensarse con otros sistemas anulares aromáticos o heteroaromáticos, saturados o (parcialmente) insaturados de cicloalquilo o heterociclilo. Sin embargo, más preferiblemente, el heterocicloalquilo de 3 a 7 miembros y el heterocicloalquilo de 3 a 6 miembros no se condensan con otros sistemas anulares. Incluso más preferiblemente, el heterocicloalquilo de 3 a 7 miembros y el heterocicloalquilo de 3 a 6 miembros no se condensan con otros sistemas anulares y están saturados. El grupo heterocicloalquilo de 3 a 7 miembros y heterocicloalquilo de 3 a 6 miembros pueden unirse a la estructura general de orden superior a través de cualquier miembro anular deseado y posible del residuo heterocicloalifático si no se indica lo contrario. En una realización preferida, el heterocicloalquilo de 3 a 7 miembros y el heterocicloalquilo de 3 a 6 miembros están unidos a la estructura general de orden superior a través de un átomo de carbono.
Los grupos heterocicloalquilo de 3 a 7 miembros preferidos se seleccionan del grupo que consiste en azepanilo, dioxepanilo, oxazepanilo, diazepanilo, tiazolidinilo, tetrahidrotiofenilo, tetrahidropiridinilo, tiomorfolinilo, tetrahidropiranilo, oxetanilo, oxiranilo, tetrahidrofuranilo, morfolinilo, pirrolidinilo, 4-metilpiperazinilo, morfolinonilo, azetidinilo, aziridinilo, ditiolanilo, dihidropirrolilo, dioxanilo, dioxolanilo, dihidropiridinilo, dihidrofuranilo, dihidroisoxazolilo, dihidrooxazolilo, imidazolidinilo, isoxazolidinilo, oxazolidinilo, piperazinilo, piperidinilo, pirazolidinilo, piranilo; tetrahidropirrolilo, dihidroquinolinilo, dihidroisoquinolinilo, dihidroindolinilo, dihidroisoindolilo, tetrahidroquinolinilo, tetrahidroisoquinolinilo y tetrahidroindolinilo. Los grupos heterocicloalquilo de 3 a 7 miembros particularmente preferidos se seleccionan de grupos heterocicloalquilo de 3 a 6 miembros. Los grupos heterocicloalquilo de 3 a 6 miembros preferidos se seleccionan del grupo que consiste en tetrahidropiranilo, oxetanilo, oxiranilo, tetrahidrofuranilo, tiazolidinilo, tetrahidrotiofenilo, tetrahidropiridinilo, tiomorfolinilo, morfolinilo, pirrolidinilo, 4-metilpiperazinilo, morfolinilo, azetidinilo, aziridinilo, ditiolanilo, dihidropirrolilo, dioxanilo, dioxolanilo, dihidropiridinilo, dihidrofuranilo, dihidroisoxazolilo, dihidrooxazolilo, imidazolidinilo, isoxazolidinilo, oxazolidinilo, piperazinilo, piperidinilo, pirazolidinilo, piranilo, tetrahidropirrolilo, dihidroindolinilo, dihidroisoindolilo y tetrahidroindolinilo. Los grupos heterocicloalquilo de 3 a 6 miembros particularmente preferidos se seleccionan del grupo que consiste en tetrahidropiranilo, oxetanilo, oxiranilo y tetrahidrofuranilo.
Según la presente invención, el término "arilo" significa preferiblemente hidrocarburos aromáticos que tienen de 6 a 14, es decir, 6, 7, 8, 9, 10, 11, 12, 13 o 14 miembros en el anillo, preferiblemente que tienen de 6 a 10, es decir 6, 7, 8, 9 o 10 miembros en el anillo, incluidos fenilos y naftilos. Cada residuo de arilo puede no estar sustituido o estar mono o polisustituido. El arilo se puede unir a la estructura general de orden superior a través de cualquier miembro del anillo deseado y posible del residuo de arilo. Los residuos de arilo también se pueden condensar con otros sistemas anulares cicloalquilo o heterocicloalquilo saturados o (parcialmente) insaturados, aromáticos o heteroaromáticos, que a su vez pueden no estar sustituidos o estar mono o polisustituidos. En una realización preferida, el arilo se condensa con un sistema anular adicional. Los ejemplos de residuos de arilo condensados son 2H-benzo[b][1,4]oxazin-3(4H)-onilo, 1H-benzo[d]imidazolilo, 2,3-dihidro-1H-indenilo, tetrahidronaftalenilo, isocromano, 1,3-dihidroisobenzofuranilo, benzodioxolanilo y benzodioxanilo. Preferiblemente, el arilo se selecciona del grupo que consiste en fenilo, 1H-benzo[d]imidazolilo, 2H-benzo[b][1,4]oxazin-3(4H)-onilo, 2,3-dihidro-1H-indenilo, tetrahidronaftalenilo, isocromano, 1,3-dihidroisobenzofuranilo, 1-naftilo, 2-naftilo, fluorenilo y antracenilo, cada uno de los cuales puede estar, respectivamente, no sustituido o mono o polisustituido. En otra realización preferida, el arilo no se condensa con ningún sistema anular adicional. Un arilo particularmente preferido es fenilo, no sustituido o mono o polisustituido.
Según la presente invención, el término "heteroarilo de 5 a 6 miembros" significa preferiblemente un residuo aromático cíclico de 5 o 6 miembros que contiene al menos 1, si es apropiado también 2, 3, 4 o 5 heteroátomos, en donde los heteroátomos se seleccionan cada uno independientemente uno de otro del grupo S, N y O y el residuo heteroarilo puede no estar sustituido o estar mono o polisustituido, si no se indica lo contrario. En el caso de sustitución en el heteroarilo, los sustituyentes pueden ser iguales o diferentes y estar en cualquier posición deseada y posible del
heteroarilo. La unión a la estructura general de orden superior se puede llevar a cabo a través de cualquier miembro del anillo deseado y posible del residuo heteroarilo, si no se indica lo contrario. Preferiblemente, el heteroarilo de 5 a 6 miembros está unido a la estructura general de orden superior a través de un átomo de carbono del heterociclo. El heteroarilo también puede ser parte de un sistema bicíclico o policíclico que tenga hasta 14 miembros en el anillo, en donde el sistema anular se puede formar con otros cicloalquilo o heterocicloalquilo saturados o (parcialmente) insaturados, sistemas anulares aromáticos o heteroaromáticos, que a su vez pueden no estar sustituidos o estar mono o polisustituidos, si no se indica lo contrario. En una realización preferida, el heteroarilo de 5 a 6 miembros es parte de un sistema bi o policíclico, preferiblemente bicíclico. En otra realización preferida, el heteroarilo de 5 a 6 miembros no es parte de un sistema bi o policíclico. Preferiblemente, el heteroarilo de 5 a 6 miembros se selecciona del grupo que consiste en piridilo (es decir, 2-piridilo, 3-piridilo, 4-piridilo), pirimidinilo, piridazinilo, pirazinilo, pirrolilo, imidazolilo, pirazolilo, oxazolilo, isoxazolilo, tiazolilo, isotiazolilo, furanilo, tienilo (tiofenilo), triazolilo, tiadiazolilo, 4,5,6,7-tetrahidro-2H-indazolilo, 2,4,5,6-tetrahidrociclopenta[c]pirazolilo, benzofuranilo, benzoimidazolilo, benzotienilo, benzotiadiazolilo, benzotiazolilo, benzotriazolilo, benzooxazolilo, benzooxadiazolilo, quinazolinilo, quinoxalinilo, carbazolilo, quinolinilo, dibenzofuranilo, dibenzotienilo, imidazotiazolilo, indazolilo, indolizinilo, indolilo, isoquinolinilo, naftiridinilo, oxazolilo, oxadiazolilo, fenazinilo, fenotiazinilo, ftalazinilo, purinilo, fenazinilo, tetrazolilo y triazinilo. Los heteroarilos de 5 a 6 miembros particularmente preferidos se seleccionan del grupo que consiste en piridilo (es decir, 2-piridilo, 3-piridilo, 4-piridilo).
Los compuestos según la presente invención se definen por sustituyentes, por ejemplo, por R1, R2 y R3 (sustituyentes de 1a generación) que pueden estar en sí mismos sustituidos opcionalmente por su parte (sustituyentes de 2a generación). Dependiendo de la definición, esos sustituyentes de los sustituyentes pueden estar opcionalmente resustituidos por su parte (sustituyentes de 3a generación). Si, por ejemplo, R1 = un alquilo-Ci-10 (sustituyente de ia generación), luego el alquilo-C1-10 puede, por su parte, estar sustituido, por ejemplo con un N(H)(alquilo C1-6) (sustituyente de 2a generación). Esto produce el grupo funcional R1 = (alquilo-C1-10-NH-alquilo-C1-6). El NH-alquilo-C1-6 puede, a su vez por su parte resustituirse, por ejemplo, con Cl (sustituyente de 3 a generación). En general, esto produce el grupo funcional R1 = alquilo-C1-10-NH-alquilo-C1-6, en donde el alquilo-C1-6 del NH-alquilo-C1-6 está sustituido con Cl. Sin embargo, en una realización preferida, los sustituyentes de 3 a generación pueden no estar resustituidos, es decir, no hay entonces sustituyentes de 4 a generación. Más preferiblemente, los sustituyentes de 2a generación pueden no estar resustituidos, es decir, no hay sustituyentes de 3 a generación.
Si un residuo aparece de forma múltiple en una molécula, entonces este residuo puede tener respectivamente diferentes significados para varios sustituyentes: si, por ejemplo, tanto R2 como R3 denotan alquilo-C1-6, entonces alquilo-C1-6 puede por ejemplo representar etilo para R2 y puede representar metilo para R3.
En relación con los términos "alquilo-C1-10", "alquilo-CW, "alquilo-CW, "cicloalquilo-C3-10", "cicloalquilo-C3-6", "heterocicloalquilo de 3 a 7 miembros", "heterocicloalquilo de 3 a 6 miembros", "alquileno-CW, "alquileno C1-4" y "alquileno C1-2", el término "sustituido" se refiere en el sentido de la presente invención, con respecto a los residuos o grupos correspondientes, a la sustitución individual (monosustitución) o a la sustitución múltiple (polisustitución), por ejemplo disustitución o trisustitución; más preferiblemente a monosustitución o disustitución; de uno o más átomos de hidrógeno cada uno independientemente uno del otro con al menos un sustituyente. En el caso de una sustitución múltiple, es decir, en el caso de residuos polisustituidos, tales como residuos di o trisustituidos, estos residuos pueden estar polisustituidos en átomos diferentes o en los mismos, por ejemplo, trisustituidos en el mismo átomo de carbono, como en el caso de CF3 , CH2CF3 o disustituidos como en el caso de 1,1-difluorociclohexilo, o en diversos puntos, como en el caso de CH(OH)-CH=CH-CHCl2 o 1-cloro-3-fluorociclohexilo. La sustitución múltiple puede llevarse a cabo utilizando el mismo o diferentes sustituyentes.
En relación con los términos "arilo", "fenilo", "heteroarilo" y "heteroarilo de 5 a 6 miembros", el término "sustituido" se refiere en el sentido de esta invención a la sustitución individual (monosustitución) o a la sustitución múltiple (polisustitución), por ejemplo, disustitución o trisustitución, de uno o más átomos de hidrógeno, cada uno independientemente uno del otro con al menos un sustituyente. La sustitución múltiple puede llevarse a cabo utilizando el mismo o diferentes sustituyentes.
Según la presente invención, preferiblemente alquilo-C1-10, alquilo-C1-6, alquilo-C1-4, cicloalquilo-C3-10, cicloalquilo-C3-6, heterocicloalquilo de 3 a 7 miembros, heterocicloalquilo de 3 a 6 miembros, alquileno-C1-6, alquileno-C1-4 y alquileno-C1-2 en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-C1-6; CF3 ; CF2H; CFH2 ; CF2Cl; CFCb; C(O)-alquilo-C1-6; C(O)-OH; C(O)-Oalquilo-C1-6; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; OH; =O; OCF3; OCF2H; OCFH2 ; OCF2Cl; OCFCb; O-alquilo-C1-6; O-C(O)-alquilo-C1-6; O-C(O)-O-alquilo-C1-6; O-(CO)-N(H)(alquilo-C1-6); O-C(O)-N(alquilo-C1-6)2 ; O-S(O)2-NH2 ; O-S(O)2-N(H)(alquilo-C1-6); O-S(O)2-N(alquilo-C1-6)2 ; NH2 ; N(H)(alquilo-C1-6); N(alquilo-C1-6)2 ; N(H)-C(O)-alquilo-C1-6; N(H)-C(O)-O-alquilo-C1-6; N(H)-C(O)-NH2 ; N(H)-C(O)-N(H)(alquilo-C1-6); N(H)-C(O)-N(alquilo-C1-6)2 ; N(alquilo-C1-6)-C(O)-alquilo-C1-6; N(alquilo-C1-6)-C(O)-O-alquilo-C1-6; N(alquilo-C1-6)-C(O)-NH2 ; N(alquilo-C1-6)-C(O)-N(H)(alquilo-C1-6); N(alquilo-C1-6)-C(O)-N(alquilo-C1-6)2 ; N(H)-S(O)2OH; N(H)-S(O)2-alquilo-C1-6; N(H)-S(O)2-O-alquilo-C1-6; N(H)-S(O)2-NH2 ; N(H)-S(O)2-N(H)(alquilo-C1-6); N(H)-S(O)2N(alquilo-C1-6)2 ; N(alquilo-C1-6)-S(o )2-Oh ; N(alquilo-C1-6)-S(O)2-alquilo-C1-6; N(alquilo-C1-6)-S(O)2-O-alquilo-C1-6; N(alquilo-C1-6)-S(O)2-NH2 ; N(alquilo-C1-6)-S(O)2-N(H)(alquilo-C1-6); N(alquilo-C1-6)-S(O)2-N(alquilo-C1-6)2 ; SCF3; SCF2H; SCFH2 ; S-alquilo-C1-6; S(O)-alquilo-C1-6; S(O)2-alquilo-C1-6; S(O)2-OH; S(O)2-O-alquilo-C1-6; S(O)2-NH2 ; S(O)2-N(H)(alquilo-C1-6); S(O)2-N(alquiloCi-a)2 i cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo; heteroarilo de 5 o 6 miembros; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); O-fenilo; O-(heteroarilo de 5 o 6 miembros); C(O)-cicloalquilo-C3-6; C(O)-(heterocicloalquilo de 3 a 6 miembros); C(O)-fenilo; C(O)-(heteroarilo de 5 o 6 miembros); S(O)2-(cicloalquilo-C3-6); S(O)2-(heterocicloalquilo de 3 a 6 miembros); S(O)2-fenilo y S(O)2-(heteroarilo de 5 o 6 miembros);
Los sustituyentes preferidos de alquilo-C1-10, alquilo-C1-6, alquilo-C1-4, cicloalquilo-C3-10, cicloalquilo-C3-6, heterocicloalquilo de 3 a 7 miembros, heterocicloalquilo de 3 a 6 miembros, alquileno-C1-6 y alquileno-Ci-4 se seleccionan del grupo que consiste en F; Cl; Br; I; CN; alquilo-C1-6; CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-C1-6)2 ; OH; OCF3; OCF2H; OCFH2; O-alquilo-C1-6; NH2 ; N(H)(alquilo-C1-6); N(alquilo-C1-6)2 ; SCF3 ; SCF2H; SCFH2 ; S-alquilo-C1-6; S(O)-alquilo-C1-6; S(O)2-alquilo-C1-6; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo y heteroarilo de 5 o 6 miembros; y de manera particularmente preferente F, CN, CH3 , CH2CH3 , CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(CH3); C(O)-N(CH3)2; OH, NH2 , OCH3 , SCH3 , S(O)2(CH3), S(O)(CH3), N(CH3)2, ciclopropilo y oxetanilo. Según esta realización, el alquilo-01 - 10 , alquilo-C1-6, alquilo-C1-4, cicloalquilo-C3-10, cicloalquilo-C3-6, heterocicloalquilo de 3 a 7 miembros, heterocicloalquilo de 3 a 6 miembros están preferiblemente de manera independiente uno de otro no sustituidos, mono o trisustituidos, más preferiblemente no sustituidos o monosustituidos o disustituidos con un sustituyente seleccionado del grupo que consiste en F; Cl; Br; I; CN; alquilo-Ci-6; CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci-6)2 ; OH; OCF3 ; OCF2H; OCFH2 ; O-alquilo-Ci-6; NH2 ; N(H)(alquilo-Ci-6); N(alquilo-Ci-6)2 ; SCF3 ; SCF2H; SCFH2 ; S-alquilo-Ci-6; S(O)-alquilo-Ci-6; S(O)2-alquilo-Ci-6; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo y heteroarilo de 5 o 6 miembros. Preferiblemente, los grupos alquileno-Ci-6 y los grupos alquileno-Ci-4 no están sustituidos.
Según la presente invención, preferiblemente el arilo, el fenilo y el heteroarilo de 5 o 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-Ci-6; CF3 ; CF2H; CFH2 ; CF2Cl; c Fc I2 ; alquileno-Ci-4-CF3; alquileno-Ci-4-CF2H; alquileno-Ci-4-CFH2; C(O)-alquilo-Ci-6; C(O)-OH; C(O)-Oalquilo-Ci-6; C(O)-N(H)(OH); C(O)-NH2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci-6)2 ; OH; OCF3 ; OCF2H; OCFH2 ; OCF2CI; OCFCI2 ; O-alquilo-Ci-6; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); NH2 ; N(H)(alquilo-Ci-6); N(alquilo-Ci-6)2 ; N(H)-C(O)-alquilo-Ci-6; N(alquilo-Ci-6)-C(O)-alquilo-Ci-6; N(H)-C(O)-NH2 ; N(H)-C(O)-N(H)(alquilo-Ci-6); N(H)-C(O)-N(alquilo-Ci-6)2 ; N(alquilo-Ci-6)-C(O)-N(H)(alquilo-Ci-6); N(alquilo-Ci-6)-C(O)-N(alquilo-Ci-6)2 ; N(H)-S(O)2-alquilo-Ci-6; SCF3 ; S-alquilo-Ci-6; S(O)-alquilo-Ci-6; S(O)2-alquilo-Ci-6; S(O)2-NH2 ; S(O)2-N(H)(alquilo-Ci-6); s(O)2-N(alquilo-Ci-6)2 ; cicloalquilo-C3-6; alquileno-Ci-4-cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; alquileno-Ci-4-(heterocicloalquilo de 3 a 6 miembros); fenilo o heteroarilo de 5 o 6 miembros.
Los sustituyentes preferidos de arilo, fenilo y heteroarilo de 5 o 6 miembros se seleccionan del grupo que consiste en F; Cl; Br; I; CN; alquilo-Ci-6; CF3 ; CF2H; CFH2; alquileno-Ci-4-CF3; alquileno-Ci-4-CF2H; alquileno-Ci-4-CFH2; OH; OCF3 ; OCF2H; OCFH2 ; O-alquilo-Ci-6; O-cicloalquilo-C3-6 y cicloalquilo-C3-6; y particularmente de manera preferida en F; Cl; Br; CN; CH3 ; CH2CH3 ; CF3 ; CF2H; CFH2; CH2-CF3 ; OH; OCF3 ; OCF2H; OCFH2 ; O-CH3 ; O-ciclopropilo y ciclopropilo. Según esta realización, arilo, fenilo y heteroarilo de 5 o 6 miembros están preferiblemente cada uno independientemente uno de otro no sustituidos, mono o trisustituidos, más preferiblemente no sustituidos o monosustituidos o disustituidos con un sustituyente seleccionado del grupo que consiste en F; Cl; Br; I; CN; alquilo-Ci-6; CF3 ; CF2H; CFH2 ; alquileno-Ci-4-CF3; alquileno-Ci-4-CF2H; alquileno-Ci-4-CFH2; OH; OCF3 ; OCF2H; OCFH2; O-alquilo-Ci-6; O-cicloalquilo-C3-6 y cicloalquilo-C3-6.
En una realización preferida, el compuesto según la presente invención es según la fórmula general (II) o (III)
En una realización preferida, X representa NR7 y Z representa N o CR9. Más preferiblemente, X representa NR7 y Z representa CR9. En otra realización preferida, X representa N y Z representa NR7.
Más preferiblemente, el compuesto según la presente invención es según la fórmula general (II) en donde X representa NR7 y Z representa N o CR9, más preferiblemente CR9.
En una realización preferida, Ri representa H; alquilo-Ci-6; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros;
fenilo; o heteroarilo de 5 o 6 miembros; en donde cicloalquilo-C3-6, heterocicloalquilo de 3 a 6 miembros, fenilo y heteroarilo de 5 o 6 miembros pueden puentearse opcionalmente a través de alquileno-Ci-4. Según esta realización, preferiblemente el alquilo-Ci-6; cicloalquilo-C3-6; alquileno-Ci-4 y heterocicloalquilo de 3 a 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono, di o trisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-Ci-6; CF3 ; CF2H; CFH2 ; CF2Cl; CFCb; C(O)-NH2 ; C(O)-N(H)(alquilo-Ci-6);
C(O)-N(alquilo-Ci-6)2 ; OH; ; OCF3 ; OCF2H; OCFH2 ; O-alquilo-Ci-6; O-C(O)-alquilo-Ci-6; NH2 ; N(H)(alquilo-Ci-6);
N(alquilo-Ci-6)2 ; N(H)-C(O)-alquilo-Ci-6; N(H)-C(O)-O-alquilo-Ci-6; SCF3 ; SCF2H; SCFH2 ; S-alquilo-Ci-6; S(O)-alquilo-Ci-6; S(O)2-alquilo-Ci-6; S(O)2-O-alquilo-Ci-6; S(O)2-NH2 ; S(O)2-N(H)(alquilo-Ci-6); S(O)2-N(alquilo-Ci-6)2 ; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo; heteroarilo de 5 o 6 miembros; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); O-fenilo; O-(heteroarilo de 5 o 6 miembros); C(O)-cicloalquilo-C3-6; C(O)-(heterocicloalquilo de 3 a 6 miembros); C(O)-fenilo; C(O)-(heteroarilo de 5 o 6 miembros); S(O)2-(cicloalquilo-C3-6);
S(O)2-(heterocicloalquilo de 3 a 6 miembros); S(O)2-fenilo o S(O)2-(heteroarilo de 5 o 6 miembros); más preferiblemente F; Cl; Br; I; CN; alquilo-Ci-6; CF3; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci-6)2 ; OH; OCF3 ; OCF2H; OCFH2 ; O-alquilo-Ci-6; NH2 ; N(H)(alquilo-Ci-6); N(alquilo-Ci-6)2 ; SCF3 ; SCF2H; SCFH2 ; S-alquilo-Ci-6; S(O)-alquilo-Ci-6; S(O)2-alquilo-Ci-6; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo y heteroarilo de 5 o 6 miembros; y de manera particularmente preferente F, CN, CH3 , CH2CH3 , CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(CH3); C(O)-N(CH3)2; OH, NH2 , OCH3 , SCH3 , S(O)2(CH3), S(O)(CH3), N(CH3)2, ciclopropilo y oxetanilo;
y preferiblemente fenilo y heteroarilo de 5 o 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono; di o trisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-Ci-6; CF3 ; CF2H; CFH2 ; alquileno-Ci-4-CF3; alquileno-Ci-4-CF2H; alquileno-Ci-4-CFH2; C(O)-alquilo-Ci-6; C(O)-OCi-6-alquilo; C(O)-; C(O)-NH2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci-6)2 ; OH; OCF3; OCF2H; OCFH2 ; O-alquilo-Ci-6; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); NH2 ; N(H)(alquilo-Ci-6); N(alquilo-Ci-6)2 ; SCF3; S-alquilo-Ci-6; S(O)-alquilo-Ci-6; S(O)2-alquilo-Ci-6; cicloalquilo-C3-6; alquileno-Ci-4-cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; alquileno-Ci-4-(heterocicloalquilo de 3 a 6 miembros); fenilo o heteroarilo de 5 o 6 miembros; más preferiblemente F; Cl; Br; I; CN; alquilo-Ci-6; CF3 ; CF2H; CFH2; alquileno-Ci-4-CF3; alquileno-Ci-4-CF2H; alquileno-Ci-4-CFH2 ; OH; OCF3 ; OCF2H; OCFH2 ; O-alquilo-Ci-6; O-cicloalquilo-C3-6 y cicloalquilo-C3-6; y particularmente de manera preferida F; Cl; Br; CN; CH3 ; CH2CH3 ; CF3 ; CF2H; CFH2 ; CH2-CF3 ; OH; OCF3 ; OCF2H; OCFH2 ; O-CH3 ; O-ciclopropilo y ciclopropilo.
En otra realización preferida, R1 representa H; alquilo-Ci-4; cicloalquilo-C3-6, puenteado opcionalmente a través de alquileno-Ci-2; heterocicloalquilo de 3 a 6 miembros, puenteado opcionalmente a través de alquileno-Ci-2; fenilo, puenteado opcionalmente a través de alquileno-Ci-2; o heteroarilo de 5 o 6 miembros, puenteado opcionalmente a través de alquileno-Ci-2;
preferiblemente en donde
alquilo-Ci-4, cicloalquilo-C3-6 y heterocicloalquilo de 3 a 6 miembros en cada caso independientemente uno de otro, no están sustituidos, están mono, di o trisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F, CN, CH3, CH2CH3, CF3; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(CH3); C(O)-N(CH3)2; OH, NH2 , OCH3, SCH3, S(O)2(CH3), S(O)(CH3), N(CH3)2, ciclopropilo y oxetanilo; y
alquileno-Ci-2 no está sustituido; y
fenilo y heteroarilo de 5 o 6 miembros en cada caso independientemente uno de otro, no están sustituidos, o está mono, di o trisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F; Cl; Br; CN; CH3 ;
CH2CH3 ; CF3 ; CF2H; CFH2 ; CH2-CF3 ; OH; OCF3 ; OCF2H; OCFH2 ; O-CH3 ; O-ciclopropilo y ciclopropilo.
En otra realización más, R1 representa H; CH3 , CF3 , CF2H; CFH2 ; etilo, n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), n-butilo, 1-butinilo, 2-butinilo, 1-butenilo, 2-butenilo, isobutilo, sec-butilo; terc-butilo; (CH2K 2OCH3 ; (CH2)i-2OH; (CH2)o-2C(H)(OH)-(CH2)o-2CH3; (CH2)i-2SCH3; (CH2)i-2N(CH3)2;
(CH2)i-2S(O)CH3; (CH2)i-2S(O)2CH3; (CH2)i-2CN; (CH2)o-2C(H)(CN)-(CH2)o-2CH3; (CH2)o-2-ciclopropilo, (CH2)o-2-ciclobutilo, (CH2)o-2-ciclopentilo y (CH2)o-2-ciclohexilo; (CH2 )o-2-tetrahidropiranilo, (CH2)o-2-oxetanilo, (CH2)o-2-oxiranilo, (CH2)o-2-tetrahidrofuranilo; (CH2)o-2-fenilo; (CH2)o-2-piridilo, (CH2)o-2-pirimidinilo, (CH2)o-2-piridazinilo, (CH2)o-2-tienilo, (CH2)o-2-oxazolilo o (CH2)o-2-tiazolilo.
Preferiblemente, R2 representa H; F; Cl; Br; CN; alquilo-Ci-6; cicloalquilo-C3-6; O-alquilo-Ci-6; N(H)(alquilo-Ci-6), N(alquilo-Ci-6)2 ; C(O)-alquilo-Ci-6; C(O)-O-alquilo-Ci-6; C(O)-NH2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci-6)2 ; O-cicloalquilo-C3-6; N(H)(cicloalquilo-C3-6), N(alquilo-Ci-6)(cicloalquilo-C3-6); C(O)-cicloalquilo-C3-6; C(O)-O-cicloalquilo-C3-6; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-Ci-6)(cicloalquilo-C3-6); en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-Ci-4.
En una realización preferida, R2 representa H; F; Cl; Br; CN; alquilo-Ci-6; cicloalquilo-C3-6; O-alquilo-Ci-6; C(O)-NH2 ;
C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci-6)2 ; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-Ci-6)(cicloalquilo-C3-6); en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-Ci-4;
preferiblemente en donde
alquilo-Ci-6 y cidoalquilo-C3-6 en cada caso independientemente uno de otro no están sustituidos, están mono, di o trisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F, CN, CH3 , CH2CH3 , CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(CH3); C(O)-N(CH3)2; OH, NH2 , OCH3 , SCH3 , S(O)2(CH3), S(O)(CH3), N(CH3)2, ciclopropilo y oxetanilo; y
alquileno-C1-4 no está sustituido.
En una realización particularmente preferida, R2 representa H; F; Cl; Br; CN; metilo; etilo; etenilo (vinilo); n-propilo; 2-propilo; 1-propinilo; 2-propinilo; propenilo (-CH2CH=CH2 ; -CH=CH-CH3; -C(=CH2)-CH3); n-butilo; isobutilo; sec-butilo; terc-butilo; CF3 ; CH2CF3 ; CHF2 ; CH2CHF2 ; CH2F; CH2CH2F; OCH3 ; OCH2CH3 ; OC(H)(CH3)2; OCH2CH2CH3;O-C(CH3)3; OCF3; OCH2CF3; OCHF2; OCH2CHF2; OCH2F; OCH2CH2F; CH2OH; CH2CH2OH; CH2C(H)(OH)CH3; CH2CH2CH2OH; CH2CH2CH2CH2OH; C(CH3)2CH2OH; C(O)-CH3; C(O)-CH2CH3; C(O)-C(H)(CH3)2 C(O)-CH2CH2CH3; C(O)-C(CH3)3; ciclopropilo; ciclobutilo; ciclopentilo; ciclohexilo; CH2-ciclopropilo; CH2-ciclobutilo; CH2-ciclopentilo; CH2-ciclohexilo; O-ciclopropilo; O-ciclobutilo; O-ciclopentilo; O-ciclohexilo; C(O)-ciclopropilo; C(O)-ciclobutilo; C(O)-ciclopentilo; C(O)-ciclohexilo o C(O)-NH2.
Preferiblemente, R3 representa H; F; Cl; Br; CN; alquilo-C1-6; cicloalquilo-C3-6; O-alquilo- C1-6; N(H)(alquilo-C1-6), N(alquilo-C1-6)2 ; C(O)-alquilo-C1-6; C(O)-O-alquilo-C1-6; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; O-cicloalquilo-C3-6; N(H)(cicloalquilo-C3-6), N(alquilo-C1-6)(cicloalquilo-C3-6); C(O)-cicloalquilo-C3-6; C(O)-O-cicloalquilo-C3-6; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-C1-6)(cicloalquilo-C3-6); en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-C1-4.
En una realización preferida, R3 representa H; F; Cl; Br; CN; alquilo-C1-6; cicloalquilo-C3-6; O-alquilo-C1-6; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-C1-6)(cicloalquilo-C3-6); en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-C1-4;
preferiblemente en donde
alquilo-C1-6 y cicloalquilo-C3-6 en cada caso independientemente uno de otro no están sustituidos, están mono, di o trisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F, CN, CH3 , CH2CH3 , CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(CH3); C(O)-N(CH3)2; OH, NH2 , OCH3, SCH3, S(O)2(CH3), S(O)(CH3), N(CH3)2, ciclopropilo y oxetanilo; y
alquileno-C1-4 no está sustituido.
En una realización particularmente preferida, R3 representa H; F; Cl; Br; CN; metilo; etilo; etenilo (vinilo); n-propilo; 2-propilo; 1-propinilo; 2-propinilo; propenilo (-CH2CH=CH2 ; -CH=CH-CH3; -C(=CH2)-CH3); n-butilo; isobutilo; sec-butilo; terc-butilo; CF3 ; CH2CF3 ; CHF2 ; CH2CHF2 ; CH2F; CH2CH2F; OCH3 ; OCH2CH3 ; OC(H)(CH3)2; OCH2CH2CH3;O-C(CH3)3; OCF3; OCH2CF3; OCHF2; OCH2CHF2; OCH2F; OCH2CH2F; CH2OH; CH2CH2OH; CH2C(H)(OH)CH3; CH2CH2CH2OH; CH2CH2CH2CH2OH; C(CH3)2CH2OH; C(O)-CH3; C(O)-CH2CH3; C(O)-C(H)(CH3)2 C(O)-CH2CH2CH3; C(O)-C(CH3)3; ciclopropilo; ciclobutilo; ciclopentilo; ciclohexilo; CH2-ciclopropilo; CH2-ciclobutilo; CH2-ciclopentilo; CH2-ciclohexilo; O-ciclopropilo; O-ciclobutilo; O-ciclopentilo; O-ciclohexilo; C(O)-ciclopropilo; C(O)-ciclobutilo; C(O)-ciclopentilo; C(O)-ciclohexilo, C(O)-NH2.
En una realización preferida,
R2 representa H; F; Cl; Br; CN; alquilo-C1-6; cicloalquilo-C3-6; O-alquilo-C1-6; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-C1-6)(cicloalquilo-C3-6); en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-C1-4; y/o
R3 representa H; F; Cl; Br; CN; alquilo-C1-6; cicloalquilo-C3-6; O-alquilo-C1-6; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-C1-6)(cicloalquilo-C3-6);
en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-C1-4.
Según la presente invención, R5 y R6 representan independientemente uno de otro H o alquilo-C1-4 no sustituido. Preferiblemente, R5 y R6 representan independientemente uno de otro H, CH3 , CH2CH3 ; CH2CH2CH3 , CH(CH3)2 o CH2CH2CH2CH3 , más preferiblemente H, CH3 , CH2CH3 o CH2CH2CH3 ; incluso más preferiblemente H, CH3 o CH2CH3 ; lo más preferiblemente H o CH3. En una realización particularmente preferida, ambos R5 y R6 representan CH3.
En una realización particularmente preferida, el compuesto según la presente invención es según la fórmula general (II) o (III), en donde X representa NR7 y Z representa N o CR9, más preferiblemente CR9, y en donde ambos R5 y R6 representan CH3.
En una realización preferida, al menos uno de R1, R2, R3, R5 y R6 no es H. Más preferiblemente, ambos R5 y R6 no son H y al menos uno de R1, R2 y R3 no es H. En una realización preferida, ambos R5 y R6 no son H y uno de R1, R2 y R3 no es H. En otra realización preferida, ambos R5 y R6 no son H y dos de R1, R2 y R3 no son H. En otra realización preferida más, R1, R2, R3, R5 y R6 no son H.
En una realización particularmente preferida,
- el compuesto según la presente invención es según la fórmula general (II) o (III); y/o
- X representa NR7 y Z representa N o CR9; y/o
- R5 y R6 ambos representan metilo; y/o
- al menos uno de R1, R2 y R3 no es H.
Según la presente invención, R7 representa H o L-R8.
En una realización preferida, R7 representa H. Según esta realización, preferiblemente X representa NH y Z representa N o CR9; o X representa N y Z representa NH. Más preferiblemente, X representa NH y Z representa CR9.
Incluso según esta realización, preferiblemente el compuesto según la presente invención es según la fórmula general (II) o (III), en donde X representa NH y Z representa N o CR9, más preferiblemente CR9.
En otra realización preferida, R7 no es H. Según esta realización preferida, R7 representa L-R8.
En una realización preferida, L representa un enlace; S(O); S(O)2 ; alquileno-C1-4; C(O); alquileno-C1-4-C(O); C(O)-O; alquileno-C1-4-C(O)-O; alquileno-C1-4-N(H)-C(O); alquileno-C1-4-N(alquilo-C1-6)-C(O); alquileno-C1-4-N(H)-C(O)-O o alquileno-C1-4-N(alquilo-C1-6)-C(O)-O. Según esta realización, el alquileno-C1-4 y el alquilo-C1-6 preferiblemente no están sustituidos.
Más preferiblemente, L representa un enlace; S(O); S(O)2 ; alquileno-C1-4; C(O); alquileno-C1-4-C(O); C(O)-O; alquileno-C1-4-C(O)-O; alquileno-C1-4-N(H)-C(O) o alquileno-C1-4-N(H)-C(O)-O; incluso más preferiblemente un enlace; S(O); S(O)2; CH2; CH2CH2; C(CH3)2; CH2CH2CH2; C(O); CH2-C(O); CH2CH2-C(O); CH2CH2CH2-C(O); C(CH3)2-C(O); C(O)-O; CH2-C(O)-O; CH2CH2-C(O)-O; CH2CH2CH2-C(O)-O; C(CH3)2-C(O)-O; CH2-N(H)-C(O); CH2CH2-N(H)-C(O); C(CH3)2-N(H)-C(O); CH2CH2CH2-N(H)-C(O); CH2-N(H)-C(O)-O; CH2CH2-N(H)-C(O)-O; C(CH3)2-N(H)-C(O)-O o CH2CH2CH2-N(H)-C(O)-O; lo más preferiblemente un enlace; S(O)2 ; CH2 ; C(O); C(O)-O; CH2-C(O)-O; CH2CH2-C(O)-O; CH2CH2-N(H)-C(O) o CH2CH2-N(H)-C(O)-O.
En una realización preferida, R8 representa alquilo-C1-6; cicloalquilo-C3-6 o heterocicloalquilo de 3 a 6 miembros; en donde el cicloalquilo-C3-6 y el heterocicloalquilo de 3 a 6 miembros se pueden puentear opcionalmente mediante alquileno-C1-4; y preferiblemente en donde el alquilo-C1-6; cicloalquilo-C3-6 y heterocicloalquilo de 3 a 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F; Cl; Br; I; CN; alquilo-C1-6; CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; OH; OCF3; OCF2H; OCFH2 ; O-alquilo-C1-6; NH2 ; N(H)(alquilo-C1-6); N(alquilo-C1-6)2 ; SCF3 ; SCF2H; SCFH2 ; S-alquilo-C1-6; S(O)-alquilo-C1-6; S(O)2-alquilo-C1-6; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo y heteroarilo de 5 o 6 miembros.
Más preferiblemente R8 representa
alquilo-C1-6 que se selecciona del grupo que consiste en metilo, etilo, etenilo (vinilo), n-propilo, 2-propilo, n-butilo, isobutilo, sec-butilo, terc-butilo, n-pentilo, 2-pentilo, 3-pentilo, 2-metilbutilo, 3-metilbutilo, 3-metilbut-2-ilo, 2-metilbut-2-ilo, 2,2-dimetilpropilo, n-hexilo, 2-hexilo, 3-hexilo, 2-metilpentilo, 4-metilpentilo, 4-metilpent-2-ilo, 2-metilpent-2-ilo, 3,3-dimetilbutilo, 3,3-dimetilbut-2-ilo, 3-metilpentilo, 3-metilpent-2-ilo y 3-metilpent-3-ilo; preferiblemente metilo, etilo, etenilo (vinilo),n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), nbutilo, 1-butinilo, 2-butinilo, 1-butenilo, 2-butenilo, isobutilo, sec-butilo y terc-butilo;
cicloalquilo-C3-6, que se selecciona del grupo que consiste en ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, ciclopentenilo y ciclohexenilo; preferiblemente ciclopropilo, ciclobutilo, ciclopentilo y ciclohexilo;
o
heterocicloalquilo de 3 a 6 miembros, que se selecciona del grupo que consiste en tetrahidropiranilo, oxetanilo, oxiranilo, tetrahidrofuranilo, tiazolidinilo, tetrahidrotiofenilo, tetrahidropiridinilo, tiomorfolinilo, morfolinilo, pirrolidinilo, 4-metilpiperazinilo, morfolinonilo, azetidinilo, aziridinilo, ditiolanilo, dihidropirrolilo, dioxanilo, dioxolanilo, dihidropiridinilo, dihidrofuranilo, dihidroisoxazolilo, dihidrooxazolilo, imidazolidinilo, isoxazolidinilo, oxazolidinilo, piperazinilo, piperidinilo, pirazolidinilo, piranilo, tetrahidropirrolilo, dihidroindolinilo, dihidroisoindolilo y tetrahidroindolinilo;
preferiblemente tetrahidropiranilo, oxetanilo, oxiranilo y tetrahidrofuranilo;
en donde el cidoalquilo-C3-6 y el heterocicloalquilo de 3 a 6 miembros se pueden puentear opcionalmente mediante alquileno-C1-4; y
en donde el alquilo-C1-6, cicloalquilo-C3-6 y el heterocicloalquilo de 3 a 6 miembros en cada caso independientemente uno de otro, no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F, CN, CH3 , CH2CH3 , CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(CH3); C(O)-N(CH3)2; OH, NH2 , OCH3 , SCH3 , S(O)2(CH3), S(O)(CH3), N(CH3)2, ciclopropilo y oxetanilo.
Más preferiblemente R8 representa metilo, etilo, n-propilo, 2-propilo, n-butilo, isobutilo, sec-butilo, terc-butilo, CF3 , CHF2 , CH2F, CH2CF3 , CH2CHF2 , CH2CH2F, CHFCH3 , CHFCH2F, CHFCHF2 , CHFCF3 , CF2CH3 , CF2CH2F, CF2CHF2 , CF2CF3 , CH2CH2CF3 , CH2CH2CHF2 , CH2CH2CH2F, CH2CHFCH3 , CH2CHFCH2F, CH2CHFCHF2 , CH2CHFCF3 , CH2CF2CH3 , CH2CF2CH2F, CH2CF2CHF2 , CH2CF2CF3 , CH2OH, CH2CH2OH, C(H)(OH)CH3, CH2CH2CH2OH, C(CH3)2OH, C(H)(OH)CH2CH3, C(H)(CH3)-CH2OH, CH2C(H)(OH)-CH3, CH2CH2CH2CH2OH, CH2CH2C(H)(OH)CH3, CH2C(H)(OH)CH2CH3, C(H)(OH)CH2CH2CH3, CH2-C(CH3)2-OH, C(CH3)2CH2OH, C(H)(OH)CH2CF3, C(H)(OH)CH2CHF2 , C(H)(OH)CH2CH2F, CH2C(H)(OH)-CF3, CH2C(H)(OH)-CHF2 , CH2C(H)(OH)-CH2F, CH2OCH3 , CH2CH2OCH3 , C(H)(CH3)-OCH3, CH2CH2CH2OCH3 , C(CH3)2OCH3, C(H)(OCH3)CH2CH3, C(H)(CH3)-CH2OCH3, CH2C(H)(OCH3)-CH3, CH2CH2CH2CH2OCH3 , CH2CH2C(H)(OCH3)CH3, CH2C(H)(OCH3)CH2CH3, C(H)(OCH3)CH2CH2CH3, CH2-C(CH3)2-OCH3, C(CH3)2CH2OCH3, CH2NH2 , CH2CH2NH2 , CH2CH2CH2NH2 , C(CH3)2NH2, C(H)(NH2)CH2CH3, C(H)(CH3)-CH2NH2, CH2C(H)(NH2)-CH3, CH2CH2CH2CH2NH2 , CH2CH2C(H)(NH2)CH3, CH2C(H)(NH2)CH2CH3, C(H)(NH2)CH2CH2CH3, CH2-C(CH3)2-NH2, C(CH3)2CH2NH2, CH2N(CH3)2, CH2CH2N(CH3)2, CH2CH2CH2N(CH3)2, C(CH3)2N(CH3)2, C(H)(N(CH3)2)CH2CH3, C(H)(CH3)-CH2N(CH3)2, CH2C(H)(N(CH3)2)-CH3, CH2CH2CH2CH2N(CH3)2, CH2CH2C(H)(N(CH3)2)CH3, CH2C(H)(N(CH3)2)CH2CH3, C(H)(N(CH3)2)CH2CH2CH3, CH2-C(CH3)2-N(CH3)2, C(CH3)2CH2N(CH3)2, CH2-C(O)N(CH3)2, CH2CH2-C(O)N(CH3)2, CH2CH2CH2-C(O)N(CH3)2, C(CH3)2-C(O)N(CH3)2, C(H)(C(O)N(CH3)2)CH2CH3, C(H)(CH3)-CH2-C(O)N(CH3)2, CH2C(H)(C(O)N(CH3)2)-CH3, CH2CH2CH2CH2-C(O)N(CH3)2, CH2CH2C(H)(C(O)N(CH3)2)CH3, CH2C(H)(C(O)N(CH3)2)CH2CH3, C(H)(C(O)N(CH3)2)CH2CH2CH3, CH2-C(CH3)2-C(O)N(CH3)2, C(CH3)2CH2-C(O)N(CH3)2, (CH2)0-2-ciclopropilo, (CH2)0-2-ciclobutilo, (CH2)0-2-ciclopentilo, (CH2)0-2-ciclohexilo, (CH2)0-2-tetrahidropiranilo, (CH2)0-2-oxetanilo, (CH2)0-2-oxiranilo o (CH2)0-2-tetrahidrofuranilo.
Las realizaciones preferidas (E1 a E45) abarcan aquellas en donde L y R8 tienen el significado que se proporciona en la tabla a continuación:
Preferiblemente,
L representa un enlace; S(O); S(O)2 ; alquileno-Ci-4; C(O); alquileno-Ci-4-C(O); C(O)-O; alquileno-Ci-4-C(O)-O; alquileno-Ci-4-N(H)-C(O); alquileno-C1-4-N(alquilo-C1-6)-C(O); alquileno-C1-4-N(H)-C(O)-O; o alquileno-C1-4-N(alquilo-C1-a)-C(O)-O; y
R8 representa alquilo-C1-a; cicloalquilo-C3-a o heterocicloalquilo de 3 a a miembros; en donde el cicloalquilo-C3-a y el heterocicloalquilo de 3 a a miembros se pueden puentear opcionalmente mediante alquileno-C1-4.
En una realización particularmente preferida,
L representa un enlace; S(O); S(O)2 ; alquileno-C1-4; C(O); alquileno-C1-4-C(O); C(O)-O; alquileno-C1-4-C(O)-O; alquileno-C1-4-N(H)-C(O) o alquileno-C1-4-N(H)-C(O)-O;
R8 representa alquilo-C1-a; cicloalquilo-C3-a o heterocicloalquilo de 3 a a miembros; en donde el cicloalquilo-C3-a y el heterocicloalquilo de 3 a a miembros se pueden puentear opcionalmente mediante alquileno-C1-4.
Más preferiblemente,
L representa un enlace; S(O); S(O)2 ; alquileno-C1-4; C(O); alquileno-C1-4-C(O); C(O)-O; alquileno-C1-4-C(O)-O; alquileno-C1-4-N(H)-C(O) o alquileno-C1-4-N(H)-C(O)-O; incluso más preferiblemente un enlace; S(O); S(O)2 ; CH2 ; CH2CH2 ; C(CH3)2; CH2CH2CH2 ; C(O); CH2-C(O); CH2CH2-C(O); CH2CH2CH2-C(O); C(CH3)2-C(O); C(O)-O; CH2-C(O)-O; CH2CH2-C(O)-O; CH2CH2CH2-C(O)-O; C(CH3)2-C(O)-O; CH2-N(H)-C(O); CH2CH2-N(H)-C(O); C(CH3)2-N(H)-C(O); CH2CH2CH2-N(H)-C(O); CH2-N(H)-C(O)-O; CH2CH2-N(H)-C(O)-O; C(CH3)2-N(H)-C(O)-O o CH2CH2CH2-N(H)-C(O)-O; lo más preferiblemente un enlace; S(O)2 ; CH2 ; C(O); C(O)-O; CH2-C(O)-O; CH2CH2-C(O)-O; CH2CH2-N(H)-C(O) o CH2CH2-N(H)-C(O)-O; y
R8 representa alquilo-C1-a; cicloalquilo-C3-a o heterocicloalquilo de 3 a a miembros; en donde el cicloalquilo-C3-a y el heterocicloalquilo de 3 a a miembros se pueden puentear opcionalmente mediante alquileno-C1-4; y preferiblemente en donde el alquilo-C1-a; cicloalquilo-C3-a y el heterocicloalquilo de 3 a a miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F; Cl; Br; I; CN; alquilo-C1-a; CF3 ; CF2H; CFH2; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-a); C(O)-N(alquilo-C1-a)2 ; OH; OCF3 ; OCF2H; OCFH2 ; O-alquilo-C1-a; NH2 ; N(H)(alquilo-C1-a); N(alquilo-C1-a)2 ; SCF3 ; SCF2H; SCFH2 ; S-alquilo-C1-a; S(O)-alquilo-C1-a; S(O)2-alquilo-C1-a; cicloalquilo-C3-a; heterocicloalquilo de 3 a a miembros; fenilo y heteroarilo de 5 o a miembros.
Preferiblemente, R9 representa H; F; Cl; Br; I; CN; alquilo-C1-a; cicloalquilo-C3-a, heterocicloalquilo de 3 a a miembros; S(O)-(alquilo-C1-a); S(O)-(cicloalquilo-C3-a); S(O)-(heterocicloalquilo de 3 a a miembros); S(O)2-(alquilo-C1-a); S(O)2-(cicloalquilo-C3-a); S(O)2-(heterocicloalquilo de 3 a a miembros); P(O)-(alquilo-C1-a)2 ; P(O)(alquilo-C1-a)(cicloalquilo-C3-a); P(O)(alquilo-C1-a)(heterocicloalquilo de 3 a a miembros); P(O)-(O-alquilo-C1-a)2 ; P(O)(O-alquilo-C1-a)(O-cicloalquilo-C3-a); P(O)(O-alquilo-C1-a)(O-(heterocicloalquilo de 3 a a miembros)); O-alquilo-C1-a; S-alquilo-C1-a; N(H)(alquilo-C1-a), N(alquilo-C1-a)2 ; C(O)-alquilo-C1-a; C(O)-O-alquilo-C1-a; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-a); C(O)-N(alquilo-C1-a)2 ; O-cicloalquilo-C3-a; N(H)(cicloalquilo-C3-a), N(alquilo-C1-a)(cicloalquilo-C3-a); C(O)-cicloalquilo-C3-a; C(O)-O-cicloalquilo-C3-a; C(O)-N(H)(cicloalquilo-C3-a); C(O)-N(alquilo-C1-a)(cicloalquilo-C3-a); O-(heterocicloalquilo de 3 a a miembros); N(H)(heterocicloalquilo de 3 a a miembros), N(alquilo-C1-a)(heterocicloalquilo de 3 a a miembros); C(O)-heterocicloalquilo de 3 a a miembros; C(O)-O-(heterocicloalquilo de 3 a a miembros); C(O)-N(H)(heterocicloalquilo de 3 a a miembros) o C(O)-N(alquilo-C1-a)(heterocicloalquilo de 3 a a miembros);
en donde el cidoalquilo-C3-6 y el heterocicloalquilo de 3 a 6 miembros se pueden puentear opcionalmente mediante alquileno-Ci-4; preferiblemente en donde el alquilo-C1-6, cicloalquilo-C3-6 y el heterocicloalquilo de 3 a 6 miembros en cada caso no están sustituidos.
Más preferiblemente, R9 representa H; F; Cl; Br; I; CN; metilo, etilo, n-propilo, 2-propilo, n-butilo, isobutilo, sec-butilo, terc-butilo, CF3 , CHF2 , CH2F, CH2CF3 , CH2CHF2 , CH2CH2F, ciclopropilo, ciclobutilo, tetrahidropiranilo, oxetanilo, oxiranilo, tetrahidrofuranilo, S(O)-(CH3); S(O)-(CH2CH3); S(O)-((CH2)0-2-ciclopropilo); S(O)-((CH2)0-2-ciclobutilo); S(O)-((CH2)0-2-ciclopentilo); S(O)-((CH2)0-2-ciclohexilo); S(O)-((CH2)0-2-tetrahidropiranilo), S(O)-((CH2)0-2-oxetanilo), s (o )-((CH2)0-2-oxiranilo), S(O)-((CH2)0-2-tetrahidrofuranilo), S(O)2-(CH3); S(O)2-(CH2CH3); S(O)2-((CH2)0-2-ciclopropilo); S(O)2-((CH2)0-2-ciclobutilo); S(O)2-((CH2)0-2-ciclopentilo); S(O)2-((CH2)0-2-ciclohexilo); S(O)2-((CH2)0-2-tetrahidropiranilo), S(O)2-((CH2)0-2-oxetanilo), S(O)2-((CH2)0-2-oxiranilo), S(O)2-((CH2)0-2-tetrahidrofuranilo), O-CH3 , O-CH2CH3 , O-CH2CH2CH3 , O-C(H)(CH3)2, N(H)(CH3), N(H)(CH2CH3), N(CH3)2 o N(CH3)(CH2CH3).
En una realización particularmente preferida, R9 representa H; F; CN; metilo; etilo; n-propilo; 2-propilo; CF3 ; CH2CF3 ; CHF2 ; CH2CHF2 ; CH2F; CH2CH2F; S(O)-CH3; S(O)-CH2CH3; S(O)-CH2CH2CH3; S(O)-CH(CH3)2; S(O)2-CH3; S(O)2-CH2CH3 ; S(O)2-CH2CH2CH3 o S(O)2-CH(CH3)2.
Preferiblemente, R10 representa H; F; Cl; Br; I; CN; alquilo-C1-6; cicloalquilo-C3-6, heterocicloalquilo de 3 a 6 miembros; S(O)-(alquilo-C1-6); S(O)-(cicloalquilo-C3-6); S(O)-(heterocicloalquilo de 3 a 6 miembros); S(O)2-(alquilo-C1-6); S(O)2-(cicloalquilo-C3-6); S(O)2-(heterocicloalquilo de 3 a 6 miembros); P(O)-(alquilo-C1-6)2 ; P(O)(alquilo-C1-6)(cicloalquilo-C3-6); P(O)(alquilo-C1-6)(heterocicloalquilo de 3 a 6 miembros); P(O)-(O-alquilo-C1-6)2 ; P(O)(O-alquilo-C1-6)(O-cicloalquilo-C3-6); P(O)(O-alquilo-C1-6)(O-(heterocicloalquilo de 3 a 6 miembros)); O-alquilo-C1-6; S-alquilo-C1-6; N(H)(alquilo-C1-6), N(alquilo-C1-6)2 ; C(O)-alquilo-C1-6; C(O)-O-alquilo-C1-6; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; O-cicloalquilo-C3-6; N(H)(cicloalquilo-C3-6), N(alquilo-C1-6)(cicloalquilo-C3-6); C(O)-cicloalquilo-C3-6; C(O)-O-cicloalquilo-C3-6; C(O)-N(H)(cicloalquilo-C3-6); C(O)-N(alquilo-C1-6)(cicloalquilo-C3-6); O-(heterocicloalquilo de 3 a 6 miembros); N(H)(heterocicloalquilo de 3 a 6 miembros), N(alquilo-C1-6)(heterocicloalquilo de 3 a 6 miembros); C(O)-heterocicloalquilo de 3 a 6 miembros; C(O)-O-(heterocicloalquilo de 3 a 6 miembros); C(O)-N(H)(heterocicloalquilo de 3 a 6 miembros) o C(O)-N(alquilo-C1-6)(heterocicloalquilo de 3 a 6 miembros);
en donde el cicloalquilo-C3-6 y el heterocicloalquilo de 3 a 6 miembros se pueden puentear opcionalmente mediante alquileno-C1-4; y preferiblemente en donde el alquilo-C1-6; cicloalquilo-C3-6 y heterocicloalquilo de 3 a 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F; Cl; Br; I; CN; alquilo-C1-6; CF3 ; CF2H; CFH2 ; C(O)-NH2 ; C(O)-N(H)(alquilo-C1-6); C(O)-N(alquilo-C1-6)2 ; OH; OCF3; OCF2H; OCFH2 ; O-alquilo-C1-6; NH2 ; N(H)(alquilo-C1-6); N(alquilo-C1-6)2 ; SCF3 ; SCF2H; SCFH2 ; S-alquilo-C1-6; S(O)-alquilo-C1-6; S(O)2-alquilo-C1-6; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo y heteroarilo de 5 o 6 miembros.
En otra realización preferida, R10 representa H; F; Cl; Br; CN; alquilo-C1-6; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; P(O)-(alquilo-C1-6)2 ; P(O)(alquilo-C1-6)(cicloalquilo-C3-6); P(O)(alquilo-C1-6)(heterocicloalquilo de 3 a 6 miembros) P(O)-(O-alquilo-C1-6)2 ; P(O)(O-alquilo-C1-6)(O-cicloalquilo-C3-6); P(O)(O-alquilo-C1-6)(O-(heterocicloalquilo de 3 a 6 miembros));
preferiblemente en donde el alquilo-C1-6; cicloalquilo-C3-6 y heterocicloalquilo de 3 a 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F; Cl; Br; I; CN; alquilo-C1-4; CF3 ; CF2H; CFH2 ; OH; OCF3 ; OCF2H; OCFH2 ; O-alquilo-C1-4; NH2 ; N(H)(alquilo-C1-4); N(alquilo-C1-4)2; S-alquilo-C1-4; S(O)-alquilo-C1-4 y S(O)2-alquilo-C1-4; más preferiblemente F, Cl, Br, CF3 , OCH3 , OCF3 , OCHF2 , OCH2F, OH y NH2.
Más preferiblemente, R10 representa H; F; Cl; Br; I; CN; metilo, etilo, n-propilo, 2-propilo, 1-propinilo, 2-propinilo, propenilo (-CH2CH=CH2 , -CH=CH-CH3, -C(=CH2)-CH3), n-butilo, 1-butinilo, 2-butinilo, 1 -butenilo, 2-butenilo, 3-metil-1-butinilo, n-butilo, isobutilo, sec-butilo, terc-butilo, CF3 , CHF2 , CH2F, CH2CF3 , CH2CHF2 , CH2CH2F, CH2CHFCH3 , CH2CHFCH2F, CH2CHFCHF2 , CH2CHFCF3 , CH2CF2CH3 , CH2CF2CH2F, CH2CF2CHF2 , CH2CF2CF3 , CH2OH, CH2CH2OH, C(H)(OH)CH3, CH2CH2CH2OH, C(CH3)2OH, C(H)(OH)CH2CH3, C(H)(CH3)-CH2OH, CH2C(H)(OH)-CH3, CH2CH2CH2CH2OH, CH2CH2C(H)(OH)CH3, CH2C(H)(OH)CH2CH3, C(H)(OH)CH2CH2CH3, CH2-C(CH3)2-OH, C(CH3)2CH2OH, CEC-C(H)(OH)CH3, C(H)(OH)-CEC-CH3, CEC-C(CH3)(OH)CH3, C(CH3)(OH)-CEC-CH3, C(H)(OH)CH2CF3, C(H)(OH)CH2CHF2, C(H)(OH)CH2CH2F, CH2C(H)(OH)-CF3, CH2C(H)(OH)-CHF2, CH2C(H)(OH)-CH2F, CH2OCH3 , CH2CH2OCH3 , C(H)(CH3)-OCH3, CH2CH2CH2OCH3 , C(CH3)2OCH3, C(H)(OCH3)CH2CH3, C(H)(CH3)-CH2OCH3, CH2C(H)(OCH3)-CH3, CH2CH2CH2CH2OCH3 , CH2CH2C(H)(OCH3)CH3, CH2C(H)(OCH3)CH2CH3, C(H)(OCH3)CH2CH2CH3, CH2-C(CH3)2-OCH3, C(CH3)2CH2OCH3, CH2NH2 , CH2CH2NH2 , CH2CH2CH2NH2 , C(CH3)2NH2, C(H)(NH2)CH2CH3, C(H)(CH3)-CH2NH2, CH2C(H)(NH2)-CH3, CH2CH2CH2CH2NH2 , CH2CH2C(H)(NH2)CH3, CH2C(H)(NH2)CH2CH3, C(H)(NH2)CH2CH2CH3, CH2-C(CH3)2-NH2, C(CH3)2CH2NH2, c e c -C(H)(NH2)CH3, C(H)(NH2)-CEC-CH3, CEC-C(CH3)(NH2)CH3, C(CH3)(NH2)-CEC-CH3, CH2N(CH3)2, CH2CH2N(CH3)2, CH2CH2CH2N(CH3)2, C(CH3)2N(CH3)2, C(H)(N(CH3)2)CH2CH3, C(H)(CH3)-CH2N(CH3)2, CH2C(H)(N(CH3)2)-CH3, CH2CH2CH2CH2N(CH3)2, CH2CH2C(H)(N(CH3)2)CH3, CH2C(H)(N(CH3)2)CH2CH3, C(H)(N(CH3)2)CH2CH2CH3, CH2-C(CH3)2-N(CH3)2, C(CH3)2CH2N(CH3)2, S(O)-CH3, S(O)-CH2CH3, S(O)-((CH2)0-2-ciclopropilo), S(O)-((CH2)0-2
ciclobutilo), S(OM(CH2)o-2-cidopentNo), S(O)-((CH2)o-2-cidohexilo), S(O)2-CHa, S(O)2-CH2CHa, S(O)2-((CH2)o-2-ciclopropilo), s (o )2-((CH2)o-2-ciclobutilo), S(O)2-((cH 2)o-2-ciclopentilo), S(O)2-((CH2)o-2-ciclohexilo), P(O)-(CHa)2 , P(O)-(CHa)(CH2CHa), P(O)-(CHa)((CH2)o-2-ciclopropilo), P(O)-(CHa)((CH2)o-2-ciclobutilo), P(O)-(CHa)((CH2)o-2-ciclopentilo), P(O)-(CHa)((CH2)o-2-ciclohexilo), (CH2)o-2-ciclopropilo, (CH2)o-2-ciclobutilo, (CH2)o-2-tetrahidropiranilo, (CH2)o-2-oxetanilo, (CH2 )o-2-oxiranilo, (CH2)o-2-tetrahidrofuranilo, O-CHa, O-CH2CHa, O-CH2CH2CHa, O-C(H)(CHa)2 , N(H)(CHa), N(H)(CH2CHa), N(CHa)2 o N(CHa)(CH2CHa).
En una realización preferida, al menos uno de R9 y R1° es H.
Según la presente invención, n representa o, 1,2 o a. En una realización preferida, n representa o. En otra realización preferida, n representa 1. Incluso en otra realización preferida, n representa 2. Incluso en otra realización preferida, n representa a. Más preferiblemente, n representa 1 o 2, lo más preferiblemente 1.
Preferiblemente, R11 representa F; Cl; Br; I; CN; alquilo-C1-6; O-alquilo-C1-6; NO2 ; OH, NH2 ; cicloalquilo-Ca-6; heterocicloalquilo de a a 6 miembros; S(O)-(alquilo-C1-6); S(O)2-(alquilo-C1-6); P(O)-(alquilo-C1-6)2 ; O-alquilo-C1-6; N(H)(alquilo-C1-a), N(alquilo-C1-6)2 ;
preferiblemente en donde el alquilo-C1-6; cicloalquilo-Ca-6 y heterocicloalquilo de a a 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados del grupo que consiste en F; Cl; Br; I; CN; alquilo-C1-4; CFa; CF2H; CFH2 ; OH; OCFa; OCF2H; OCFH2 ; O-alquilo-C1-4; NH2 ; N(H)(alquilo-C1-4); N(alquilo-C1-4)2; S-alquilo-C1-4; S(O)-alquilo-C1-4 y S(O)2-alquilo-C1-4; más preferiblemente F, Cl, Br, CFa, OCHa, OCFa, OCHF2 , OCH2F, OH y NH2.
En una realización particularmente preferida, R11 representa F; Cl; Br; I; CN; alquilo-C1-6 u O-alquilo-C1-6;
preferiblemente, en donde el alquilo-C1-6 en cada caso independientemente uno de otro no está sustituido o está mono o polisustituido con uno o más sustituyentes seleccionados del grupo que consiste en F y CFa.
Más preferiblemente, R11 representa F; Cl; Br; I; CN; CHa, CH2CHa, O-CHa u O-CH2CHa.
En una realización particularmente preferida, R11 representa F; Cl; Br; I; CN; alquilo-C1-6 u O-alquilo-C1-6; y/o n representa o, 1 o 2.
En una realización preferida, el compuesto según la presente invención se selecciona del grupo que consiste en
1 7.9- Difluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalina
2 8-(1-Ciclopropil-6-fluoro-1H-indol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,aa]quinoxalina
3 7.9- Difluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,aa]quinoxalina
4 1-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalin-8-il)-6-fluoro-1H-indol-1-il]-etanona
5 7.9- Difluoro-8-(6-fluoro-2-metil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalina 6 4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalin-8-il)-6-fluoro-1H-indol-2-carbonitrilo
9 7.9- Difluoro-8-(1 H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalina
10 7.9- Difluoro-1,4,4-trimetil-8-[a-(trifluorometil)-1H-indol-7-il]-5H-[1,2,4]triazolo[4,a-a]quinoxalina 11 1-Etil-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalina
12 7-(1-Etil-7,9-difluoro-4,4-dimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalin-8-il)-1H-indol-a-carbonitrilo
13 1-Etil-7,9-difluoro-4,4-dimetil-8-(a-prop-1-inil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,a-a]quinoxalina
14 1-Etil-7,9-difluoro-8-(5-fluoro-1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalina
15 7-(1-Etil-7,9-difluoro-4,4-dimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalin-8-il)-5-fluoro-1H-indol-acarbonitrilo
16 1-Etil-7,9-difluoro-8-(5-fluoro-a-prop-1-inil-1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,aa]quinoxalina
17 7- (1-Etil-7,9-difluoro-4,4-dimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalin-8-il)-5-metil-1H-indol-acarbonitrilo
18 8- [1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,aa]quinoxalina
19 8-[1-(Ciclopropilsulfonil)-6-fluoro-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,aa]quinoxalina
20 1-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,a-a]quinoxalin-8-il)-1H-indol-1-il]-etanona
7.9- Difluoro-8-[6-fluoro-1-(2,2,2-trifluoro-etil)-1H-indol^-il]-1,4,4-trimetM-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-[5-fluoro-3-(2,2,2-trifluoro-etil)-1H-indol-7-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4,9-tetrametil-8-[3-(2,2,2-trifluoro-etil)-1H-indol-7-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-8-(1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (1-Cidopropil-1H-indol-4-il)-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-1,4,4,9-tetrametil-8-(3-prop-1-inil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Cloro-7-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(5-fluoro-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (3-CidopropN-5-fluoro-1H-mdol-7-N)-7-fluoro-1,4,4,9-tetraiTietN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-8-(6-fluoro-1H-indol-4-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(Cidopropil-metil)-6-fluoro-1H-indol-4-il]-1-etil-7-fluoro-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1- Etil-7-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
4-[7-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-3-il]-2-metil-but-3-in-2-ol
[3-[7-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-3-il]-1,1-dimetilprop-2-inil]-amina
9- Cloro-8-(3-cidobutil-1H-indol-7-il)-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-1,4,4,9-tetrametil-8-(3-tetrahidro-furan-3-il-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (3-Etil-5-fluoro-1H-indol-7-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 2- [4-(9-Etil-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-6-fluoro-1H-indol-1-il]-etanol
2-[4-(9-Etil-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-6-fluoro-1H-indazol-1-il]-etanol
9- Etil-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Etil-7-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Etil-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Etil-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Etil-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Bencil-7,9-difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Bencil-7,9-difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-But-2-inil-7,9-difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-But-2-inil-7,9-difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-1-(piridin-4-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-1-(piridin-4-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-1-(piridin-3-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-1-(piridin-2-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-4,4-dimetN-8-(3-metil-1H-indol-7-N)-1-(piridin-2-N-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(5-fluoro-3-prop-1-iniMH-indol-7-N)-1-(metoximetN)-4,4,9-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
[7-Fluoro-8-(5-fluoro-3-prop-1-inil-1H-indol-7-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-1-il]-MeOH
1-[7-Fluoro-8-(5-fluoro-3-prop-1-inil-1H-indol-7-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-1-il]-etanol
7- Fluoro-8-(5-fluoro-3-prop-1-iniMH-indol-7-N)-1-(2-metoxi-etN)-4,4,9-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
1-(Cidopropil-metil)-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1- Cidopropil-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (3-CidopropiMH-indol-7-N)-1,4,4,9-tetrametN-7-(trifluorometN)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-7-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-7-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Cloro-8-(3-cidopropil-1H-indol-7-il)-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (3-CidopropN-5-fluoro-1H-indol-7-N)-7-fluoro-1,4,4-trimetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-(1-CidopropN-6-fluoro-1H-indol-4-N)-7-fluoro-1,4,4-trimetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- [7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-3-carbonitrilo
7.9- Difluoro-8-[1-(isopropilsulfonil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(CidopentNsulfonN)-1H-indol-4-N]-7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Ciclopropil-metil)-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-1,4,4-trimetil-8-[1-(tetrahidro-piran-4-ilsulfonil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(Ciclopropilsulfonil)-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Ciclopropil-metilsulfonil)-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2- [4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-N,N-dimetilacetamida
1-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-2-metoxietanona
7.9- Difluoro-8-(5-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
Éster metílico del ácido 3-[4-(7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8-N)-1H-indol-1-il]-propiónico
7.9- Difluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-(2-metil-2H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1- [4-(7,9-Difluoro-1,4,4-trimetM-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-2-dimetilamino-etanona
7.9- Difluoro-8-(5-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-[2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina Éster terc-butílico del ácido N-[2-[4-(7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1 H-indol-1 -il]-etil]-carbámico
N-[2-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-M)-1H-indol-1-il]-etM]-2,2-difluoro-propionamida
2- [4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etil-amina 7.9- Difluoro-8-(1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-[1-(2-metoxi-etil)-1H-indazol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(CidopropilsulfonN)-1H-mdazol-4-N]-7,9-difluoro-1,4,4-tniTietN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Cidopropil-irietN)-1H-mdazol-4-N]-7,9-difluoro-1,4,4-tniTietN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(1-Etil-1H-indazol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(2-Etil-2H-indazol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
Éster terc-butílico del ácido 4-(7,9-difluoro-1,4,4-triirietN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8-N)-1H-indazol-1-carboxílico
8-[1-(Cidopropil-metilsulfonil)-1H-indazol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-4,4,9-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-Etil-7-fluoro-4,4,9-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(1-Ciclopropil-1H-indazol-4-il)-1-etil-7-fluoro-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (1-Ciclopropil-1H-indazol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-Etil-7-fluoro-8-(5-fluoro-1H-indol-4-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1- Etil-7-fluoro-4,4,9-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(5-fluoro-3-metil-1 H-indol-7-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Fluoro-8-(5-fluoro-3-metil-1 H-indol-7-il)-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- (Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-[2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-9-fluoro-1,4,4-trimetil-8-[2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-(1H-indol-4-il)-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-7-metoxi-1,4,4-trimetil-8-[2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2- [4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indazol-1-il]-etanol 7- (Difluoro-metoxi)-9-fluoro-8-[1-(2-metoxi-etil)-2-(trifluorometil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
Éster terc-butílico del ácido 4-(7-fluoro-9-metoxM,4,4-triirietN-5H-[1,2,4]triazolo[4,3-a]qumoxalm-8- il)-1 H-indol-1 -carboxílico
9- Fluoro-7-metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Fluoro-7-metoxi-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metoxi)-9-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
9-Fluoro-7-metoxi-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-9-metoxi-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-1,4,4-trimetil-8-[1-metilsulfonil-2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3
a]quinoxalina
7-Cloro-9-fluoro-8-(6-fluoro-1-metNsulfoml-1H-indol-4-N)-1,4,4-trimetN-5H-[1,2,4]tnazolo[4,3-a]quinoxalina
7-Fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-8-[1-(2-metoxi-etil)-1 H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-9-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-9-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(1H-indol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-7-metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-[1-(2-metoxi-etil)-2-(trifluorometil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-(Difluoro-metil)-7-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metN)-9-fluoro-8-(6-fluoro-1-metNsulfoml-1H-indol-4-N)-1,4,4-tnmetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-(Difluoro-metil)-7-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.7.9- Pentametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-CidopropN-2-(trifluorometN)-1H-indol-4-N]-7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Cloro-8-[1-(2,2-difluoro-etM)-1H-indol^-il]-9-fluoro-1,4,4-trimetM-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-9-fluoro-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1 H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- (Difluoro-metoxi)-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metil)-7-fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-(Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-1,4,4,7-tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Cloro-8-[1-(2,2-difluoro-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(6-Fluoro-1-metilsulfonil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-[1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(2-Metoxi-etil)-1H-indol-4-il]-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (5-Fluoro-3-metil-1H-indol-7-il)-7-metoxi-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- (Difluoro-metil)-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Cloro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1.4.4.7.9- Pentametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Metoxi-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-1,4,4,7-tetrametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-1,4,4,9-tetrametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-1,4,4,9-tetrametil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7-fluoro-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- Fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metoxi)-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Cloro-1,4,4,9-tetrametil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-[1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Etilsulfonil)-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Etilsulfonil)-1H-indol-4-il]-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(6-Fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (6-Fluoro-1-metilsulfonil-1H-indazol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 2-[6-Fluoro-4-(9-fluoro-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etanol
2-[6-Fluoro-4-(7-fluoro-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etanol
7- Fluoro-9-metoxi-1,4,4-trimetil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- (Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
[2-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etil]-dimetilamina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-(difluoro-metoxi)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[4-[7-(Difluoro-metil)-9-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-6-fluoro-1H-indol-1-il]-etanol
7-Cloro-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.7.9- Pentametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- (Difluoro-metil)-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-9-fluoro-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-(difluoro-metoxi)-9-fluoro-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
2-[4-[7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-6-fluoro-1H-indol-1-il]-etanol
7- (Difluoro-metil)-9-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-fluoro-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-9-(difluoro-metil)-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-8-(1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-8-[1-(isopropilsulfonil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(Cidopropilsulfonil)-1H-indol-4-il]-9-(difluoro-metil)-7-fluoro-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-(6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- Cloro-9-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.9- Tetrametil-8-(3-metil-1H-indol-7-il)-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(5-Fluoro-3-metil-1H-indol-7-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(1 H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[6-Fluoro-4-[7-fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-1-il]-etanol
8-[1-(EtNsulfonN)-6-fluoro-1H-indazol-4-N]-7-fluoro-1,4,4-trimetN-9-(tnfluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
2-[6-Fluoro-4-[7-fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indazol-1-il]-etanol
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 2-[6-Fluoro-4-(1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etanol 8-(5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(6-fluoro-1-metNsulfomMH-indazol-4-N)-1,4,4-trimetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8- [1-(EtilsulfonM)-1H-indol-4-M]-7-fluoro-1,4,4-trimetM-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[4-[7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-1-il]-etanol
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(5-Fluoro-3-metil-1H-indol-7-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2-Metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-8-[1-(etilsulfonil)-1H-indol-4-il]-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-CidopropN-7-fluoro-1,4,4-trimetN-8-(1-metNsulfomMH-indol-4-N)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Cidopropil-7-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metil)-7-fluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(6-fluoro-1H-indol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(2,2-Difluoro-etN)-6-fluoro-1H-indazol-4-N]-1,4,4,9-tetrametN-7-(trifluorometNoxi)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- Fluoro-1,4,4,9-tetrametil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina 2-[6-Fluoro-4-[1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-1-il]-etanol
8- [1-(2,2-Difluoro-etN)-6-fluoro-1H-mdazol-4-N]-9-(difluoro-metN)-7-fluoro-1,4,4-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-1,4,4-trimetil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-1,4,4-tnmetN-8-(6-metiM-metNsulfonil-1H-indol-4-N)-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- Fluoro-9-metoxi-1,4,4-trimetil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metN)-7-fluoro-1,4,4-trimetN-8-(6-metiM-metNsulfoniMH-indol-4-N)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
4-[7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-6-carbonitrilo
8- [6-Fluoro-1-(2-metoxi-etN)-1H-indazol-4-N]-1,4,4,9-tetrametN-7-(trifluorometNoxi)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(1-metil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(3-Cidopropil-5-fluoro-1H-indol-7-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H
[1.2.4] triazolo[4,3-a]quinoxalina
8-(3-CidopropN-5-fluoro-1H-indol-7-N)-7-fluoro-9-iTietoxM,4,4-triiTietN-5H-[1,2,4]tnazolo[4,3-a]quinoxalina
7-Fluoro-8-(7-fluoro-1-iTietNsulfomMH-indol-4-N)-1,4,4-tniTietN-9-(trifluoroiTietN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Cloro-8-(3-cidopropil-5-fluoro-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4,9-tetrametil-8-(1-metil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Cloro-1,4,4,9-tetrametil-8-(1-metil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-6-fluoro-1H-indazol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(1H-indazol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-1,4,4,9-tetrametil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
4-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-6-carbonitrilo 8- [1-(CidopropN-iTietNsulfoml)-1H-indol-4-N]-7-fluoro-1,4,4,9-tetraiTietN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1.4.4- Trimetil-8-(1-metilsulfonil-1H-indol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(7-fluoro-1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(CidopropN-irietNsulfoml)-1H-indol-4-N]-9-(difluoro-iTietN)-7-fluoro-1,4,4-tniTietN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
1.4.4- Trimetil-8-(3-metil-1H-indol-7-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4-trimetM-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Cloro-8-(7-fluoro-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (5-Fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-8-[1-(2,2-difluoro-etil)-6-fluoro-1H-indazol-4-il]-9-fluoro-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Metoxi-1,4,4-trimetil-8-(1-metil-1H-indol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-8-(1H-indazol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (6-Cloro-1H-indol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(7-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-(6-Cloro-1H-indol-4-il)-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (1-Cidopropil-1H-indol-4-il)-9-(difluoro-metil)-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-8-(5-fluoro-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-8-(5-fluoro-1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (6-Fluoro-1-metil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
519 7- Cloro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 520 9-Fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 521 9-(Difluoro-metil)-7-fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
522 8- (6-Fluoro-1-metil-1H-indol-4-M)-1,4,4-trimetM-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
523 8-(1-Cidopropil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
524 7- Fluoro-8-(7-fluoro-1H-indazol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
525 8- (7-Cloro-1-metilsulfonil-1H-indol-4-il)-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
526 9- (Difluoro-metil)-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
527 9-(Difluoro-metil)-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
528 9-(Difluoro-metil)-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 529 8-(7-Cloro-1H-indol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
530 8-(7-Cloro-1H-indol-4-il)-7-fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
531 4-[7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-7-carbonitrilo
532 7-Fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
533 7-Cloro-8-(1-cidopropil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
534 4-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-7-carbonitrilo
535 7-Fluoro-8-(7-fluoro-1H-indazol-4-il)-1,4,4-tnmetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
536 7-Fluoro-8-(6-metoxi-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
537 7-Fluoro-8-(6-metoxi-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
en la forma del compuesto libre o una sal fisiológicamente aceptable del mismo.
Los compuestos según la presente invención se pueden sintetizar mediante reacciones estándar en el campo de la química orgánica conocidas por el experto en la técnica o de la manera como se describe en la presente memoria (véase el Esquema de Reacción 1 a continuación) o análogamente. Las condiciones de reacción en las rutas de síntesis descritas en la presente memoria son conocidas por el experto en la técnica y, en algunos casos, también se ejemplifican en los Ejemplos descritos en la presente memoria.
Esquema de reacción 1:
Se puede introducir un resto indol/indazol sustituido en compuestos de la fórmula (VII) sometiendo un compuesto de la fórmula (IV) en una reacción de acoplamiento C-C catalizada por metal. Las reacciones de acoplamiento C-C catalizadas por metal son conocidas en la técnica (véase Metal Catalyzed Cross-Coupling Reactions and More, 3 Volúmen Set Wiley, 2014; Angew. Chem. Int. Ed., 2012, 51, 5062 - 5085). Las reacciones de acoplamiento C-C favorables son reacciones de acoplamiento cruzado catalizadas por paladio (véase, por ejemplo, Angew. Chem., 2005, 117, 4516 - 4563). La ciclación de triazolo del compuesto (II) brinda acceso a los compuestos de la fórmula general (III). La formación de triazolo en quinoxalinas se conoce en la técnica (véase Heterocycles, 1992, 34, 771 - 780; Biological and Pharmaceutical Bulletin, 2005, 28, 1216 - 1220). La bromación aromática electrofílica del compuesto (III) proporciona el compuesto (IV). Las reacciones de bromación de compuestos aromáticos son generalmente conocidas (véase Science of Synthesis, Compounds with One Saturated Carbon-Heteroatom Bond, Volúmen 35, Houben-Weyl, 2007). Si se desea, el compuesto de la fórmula (II) se puede bromar al compuesto (V) que puede experimentar una reacción de acoplamiento cruzado catalizada por metal para proporcionar el compuesto (VI). La formación de triazol conduce a una ruta alternativa para los compuestos de la fórmula general (VII). La ciclación de quinoxalina mediada por cobre del compuesto (I) al compuesto (II) se conoce en la técnica (véase, Adv. Synth. Catal., 2010, 352, 2531 - 2537). Los compuestos de la fórmula (I) están disponibles comercialmente o se pueden preparar según métodos conocidos en la técnica.
Los compuestos según la presente invención se pueden producir de la manera descrita en el presente o de manera análoga.
En una realización preferida, los compuestos según la presente invención son moduladores del receptor de glucocorticoides. En el sentido de la presente invención, la expresión "modulador selectivo del receptor de glucocorticoides (modulador del receptor de glucocorticoides)" preferiblemente significa que el compuesto respectivo exhibe en un ensayo de acoplamiento a la diana celular para potencia agonista o antagonista en el receptor de glucocorticoides un valor de CE50 o CI50 en el receptor de glucocorticoides de como máximo 15 pM (10-10'6 moles/L); o como máximo 10 pM; más preferiblemente como máximo 1 pM; incluso más preferiblemente como máximo 500 nM (10‘9 moles/L); incluso más preferiblemente como máximo 300 nM; incluso más preferiblemente como máximo 100 nM; lo más preferiblemente como máximo 10 nM; y en particular como máximo 1 nM.
El experto en la técnica sabe cómo ensayar los compuestos para la modulación (agonista o antagonista) de la actividad del receptor de glucocorticoides. Los ensayos de acoplamiento a la diana preferidos para ensayar los compuestos para determinar su potencia agonista o antagonista (CE50, CI50) en el receptor de glucocorticoides se describen a continuación en la presente memoria:
Ensayos basados en células del receptor de glucocorticoides
Los moduladores potenciales selectivos del receptor de glucocorticoides de esta intervención pueden analizarse para determinar la modulación de la actividad del receptor de glucocorticoides usando ensayos basados en células. Estos ensayos implican una línea celular de ovario de hámster chino (CHO) que contiene fragmentos del receptor de glucocorticoides, así como proteínas de fusión. Los fragmentos del receptor de glucocorticoides utilizados pueden unirse al ligando (por ejemplo, beclometasona) para identificar moléculas que compiten por la unión con ligandos del receptor de glucocorticoides. En más detalle, el dominio de unión al ligando del receptor de glucocorticoides se fusiona al dominio de unión al ADN (DBD) del factor de transcripción GAL4 (GAL4 DBD-GR) y se integra de forma estable en una línea celular CHO que contiene una construcción informadora GAL4-UAS-Luciferasa. Para identificar los moduladores selectivos del receptor de glucocorticoides, la línea celular informadora se incuba con las moléculas mediante el uso de una curva de dilución del compuesto semilogarítmica de 8 puntos durante varias horas. Después de la lisis celular, se detecta la luminiscencia producida por la luciferasa después de la adición del sustrato y se pueden calcular los valores de CE50 o CI50. El acoplamiento de moléculas que inducen la expresión de genes a través del receptor de glucocorticoides que se une al ADN conduce a la expresión del gen de la luciferasa bajo el control de la proteína de fusión GAL4 DBD-GR y, por lo tanto, a un aumento dependiente de la dosis de la señal de luminiscencia. La unión de moléculas que reprimen la expresión génica inducida por beclometasona del gen de la luciferasa bajo el control de la proteína de fusión GAL4 d BD-GR conduce a una reducción dependiente de la dosis de la señal de luminiscencia.
En una realización preferida, el compuesto según la presente invención exhibe en un ensayo de acoplamiento a la diana celular para potencia agonista o antagonista en el receptor de glucocorticoides un valor de CE50 o CI50 en el receptor de glucocorticoides de como máximo 1 pM (10-6 moles/L); incluso más preferiblemente como máximo 500 nM (10-9 moles/L); incluso más preferiblemente como máximo 300 nM; incluso más preferiblemente como máximo 100 nM; lo más preferiblemente como máximo 50 nM; y en particular como máximo 10 nM, o como máximo 1 nM.
En una realización preferida, el compuesto según la presente invención exhibe en un ensayo de acoplamiento a la diana celular para potencia agonista o antagonista en el receptor de glucocorticoides un valor de CE50 o CI50 en el receptor de glucocorticoides en el intervalo de 0,1 nM (10-9 moles/L) a 1.000 nM; incluso más preferiblemente 1 nM a 800 nM; aún más preferiblemente de 1 nM a 500 nM; incluso más preferiblemente de 1 nM a 300 nM; lo más preferiblemente 1 nM a 100 nM; y en particular de 1 nM a 80 nM.
Preferiblemente, los compuestos según la presente invención son útiles como moduladores selectivos del receptor de glucocorticoides.
Por lo tanto, los compuestos según la presente invención son preferiblemente útiles para el tratamiento o la prevención in vivo de enfermedades en las que está implicada la participación del receptor de glucocorticoides.
La presente invención por lo tanto se refiere además a un compuesto según la presente invención para su uso en la modulación de la actividad del receptor de glucocorticoides.
Por lo tanto, otro aspecto de la presente invención se refiere a un compuesto según la presente invención para su uso en el tratamiento y/o profilaxis de un trastorno que está mediado, al menos en parte, por el receptor de glucocorticoides. Incluso otro aspecto de la presente invención se refiere a un método de tratamiento de un trastorno que está mediado, al menos en parte, por el receptor de glucocorticoides que comprende la administración de una cantidad terapéuticamente eficaz de un compuesto según la presente invención a un sujeto que lo necesita, preferiblemente un ser humano.
Un aspecto adicional de la invención se refiere al uso de un compuesto según la presente invención como un medicamento.
Otro aspecto de la presente invención se refiere a una forma de dosificación farmacéutica que comprende un compuesto según la presente invención. Preferiblemente, la forma de dosificación farmacéutica comprende un compuesto según la presente invención y uno o más excipientes farmacéuticos tales como vehículos aditivos y/o sustancias auxiliares fisiológicamente aceptables; y opcionalmente uno o más ingredientes farmacológicamente activos adicionales. Los ejemplos de vehículos aditivos y/o sustancias auxiliares fisiológicamente aceptables adecuados son rellenos, disolventes, diluyentes, colorantes y/o aglutinantes. Estas sustancias son conocidas por el experto en la técnica (véase H. P. Fiedler, Lexikon der Hilfsstoffe fur Pharmazie, Kosmetik und angrenzende Gebiete, Editio Cantor Aulendoff).
La forma de dosificación farmacéutica según la presente invención es preferiblemente para administración sistémica, tópica o local, preferiblemente para la administración oral. Por lo tanto, la forma de dosificación farmacéutica puede estar en forma de un líquido, semisólido o sólido, por ejemplo, en forma de soluciones inyectables, gotas, jugos, jarabes, aerosoles, suspensiones, comprimidos, parches, películas, cápsulas, emplastos, supositorios, ungüentos, cremas, lociones, geles, emulsiones, aerosoles o en forma de multipartículas, por ejemplo, en la forma de granulados o gránulos, si es necesario prensados en comprimidos, decantados en cápsulas o suspendidos en un líquido, y también se pueden administrar como tales.
La forma de dosificación farmacéutica según la presente invención se prepara preferiblemente con la ayuda de medios, dispositivos, métodos y procesos convencionales conocidos en la técnica. La cantidad del compuesto según la presente invención que se administrará al paciente puede variar y depende, por ejemplo, del peso o la edad del paciente y también del tipo de administración, la indicación y la gravedad del trastorno. Preferiblemente, se administran de 0,001 a 100 mg/kg, más preferiblemente de 0,05 a 75 mg/kg, lo más preferiblemente de 0,05 a 50 mg de un compuesto según la presente invención por kg de peso corporal del paciente.
Se cree que el receptor de glucocorticoides tiene potencial para modificar una variedad de enfermedades o trastornos en mamíferos como los seres humanos. Éstas incluyen, en particular, enfermedades inflamatorias.
Otro aspecto de la presente invención se refiere a un compuesto según la presente invención para su uso en el tratamiento y/o la profilaxis del dolor y/o la inflamación; más preferiblemente dolor inflamatorio.
Un aspecto adicional de la presente invención se refiere a un método para el tratamiento del dolor y/o la inflamación; más preferiblemente dolor inflamatorio.
Ejemplos
Las siguientes abreviaturas se usan en las descripciones de los experimentos:
AcOH = ácido acético; Ac = grupo acetilo; Attaphos = bis(di-ferc-butil(4 dimetilaminofenil)fosfina)dicloropaladio(II); Ar = argón; BISPIN (o Bis-Pin) = bis(pinacolato)diborano ; dba = dibencilidenacetona; DCM = diclorometano; DIPEA = N,N-diisopropiletilamina; d Ma Dm F = N,N-dimetilformamida dimetilacetal; DMAP = 4-(dimetilamino)-piridina; DMF = N,N-dimetilformamida; DMSO = dimetilsulfóxido; dppf = 1,1'; bis(difenilfosfanil)ferroceno; EtOAc = acetato de etilo; EtOH = etanol; h = hora; LDA = diisopropilamida de litio; LiHMDS = bis(trimetilsilil)amida de litio; MeOH = metanol; min = minuto; n-BuLi = n-butillitio; RT = temperatura ambiente; Rt = tiempo de retención; terc = terciario; TEA = trietilamina; THF = tetrahidrofurano; p-TSA = ácido para-tolueno sulfónico; TMSCl = cloruro de trimetilsililo; X-Phos = 2-diciclohexilfosfino-2',4',6'-triisopropilbifenilo.
Síntesis de 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-1)
d qkW H D 'C
In te rm ed io A-1
Eraps- 2
Etapa 1: A una solución en agitación de 2-bromo-4-fluoro-6-nitrotolueno (4,69 g, 20 mmoles, 1 eq) en 1,4-dioxano (25 ml) se añadió lentamente N,N-dimetilformamida dimetilacetal (13,3 mL, 100 mmoles, 5 eq) y pirrolidina (1,47 mL, 20 mmoles, 1 eq). Luego, la mezcla de reacción se agitó durante 18 horas 100 °C. La mezcla de reacción se concentró hasta obtener un residuo oscuro. A este residuo se añadió AcOH (30 mL) y polvo de hierro (11 g, 200 mmoles, 10 eq) y luego la mezcla de reacción se calentó a reflujo durante 1 hora. La mezcla de reacción luego se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se neutralizó con una solución de hidróxido de sodio al 50 % y luego se extrajo con EtOAc (2 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y se evaporaron para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 4-bromo-6-fluoro-1H-indol (1,3 g, 30 %) como un líquido marrón.
Etapa 2: Una suspensión en agitación de 4-bromo-6-fluoro-1 H-indol (1,1 g, 5,1 mmoles, 1 eq), bis(pinacolato)diborano (2,6 g, 10,2 mmoles, 2 eq) y acetato de potasio (2,0 g, 20,4 mmoles, 4 eq) en 1,4-dioxano (20 mL) se desoxigenó con Ar durante 10 minutos. Después se añadió Pd2(dba)3 (0,07 g, 0,07 mmoles, 0,015 eq) y triciclohexilfosfina (0,102 g, 0,36 mmoles, 0,07 eq) a la mezcla de reacción y nuevamente se desoxigenó con Ar durante 10 minutos. Luego, la mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción luego se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (1,1 g, 82 %) como un sólido amarillo claro.
Síntesis de 6-fluoro-1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-2)
E:apa triciclohexitfosfina Intermedio A-2
dioxanc.'nffl-C
E:apa-2
Etapa 1: A una solución en agitación de 4-bromo-6-fluoro-1H-indol (0,18 g, 0,841 mmoles, 1 eq) en DMF (5 mL) se añadió hidruro de sodio por partes (60 %, 0,07 g, 1,68 mmoles, 2 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió cloruro de metanosulfonilo (0,114 ml, 1,26 mmoles, 1,5 eq) a la mezcla de reacción a 0 °C. La mezcla de reacción se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con EtOAc (50 mL). Las capas orgánicas combinadas se lavaron con agua (5 x 10 mL), salmuera (10 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 4-bromo-6-fluoro-1-(metilsulfonil)-1H-indol (0,1 g, 41 %) como un sólido blanquecino.
Etapa 2: A una suspensión en agitación de 4-bromo-6-fluoro-1-(metilsulfonil)-1H-indol (1,2 g, 3,53 mmoles, 1 eq) en 1,4-dioxano (20 mL), se añadió bis-pinacolato diborano (1,79 g, 7,06 mmoles, 2 eq) y acetato de potasio (1,39 g, 10,62 mmoles, 4 eq) y la mezcla se desoxigenó con Ar durante 10 minutos. Luego, se añadieron Pd2(dba)3 (0,048 g, 0,052 mmoles, 0,015 eq) y triciclohexilfosfina (0,071 g, 0,25 mmoles, 0,07 eq) a la mezcla de reacción y nuevamente se desoxigenó con Ar durante 10 minutos. La mezcla de reacción se agitó durante 14 horas 110 °C. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 6-fluoro-1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan- 2-il)-1H-indol (1,0 g, 80 %) como un sólido amarillo claro.
Síntesis de 6-fluoro-2-metil-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-3)
o-B'o
Ai
ln te rm ed ioA -3
Etapa 1: A una solución en agitación de 4-bromo-6-fluoroindol (3,4 g, 15,88 mmoles, 1 eq) en THF (80 mL) se añadió hidruro de sodio por partes (suspensión al 60 %) (0,95 g, 23,8 mmoles, 1,5 eq) a 0 °C. La mezcla de reacción se agitó durante 30 minutos a RT. Después, se añadió cloruro de p-toluenosulfonilo (3,36 g, 19,06 mmoles, 1,2 eq) a la mezcla de reacción a 0 °C. La mezcla de reacción se agitó durante 2 horas a RT. La mezcla de reacción se inactivó con hielo (20 g). La capa orgánica se separó y la capa acuosa se extrajo mediante EtOAc (2 x 30 mL). La capa orgánica combinada se lavó con salmuera (50 mL), se secó sobre Na2SO4, se concentró a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 4-bromo-6-fluoro-1-(fenilsulfonil)-1 H- indol (2,1 g, 38 %) como un sólido blanco.
Etapa 2: A una solución en agitación de 4-bromo-6-fluoro-1-(fenilsulfonil)-1H-indol (2,0 g, 5,43 mmoles, 1 eq) en THF (26 mL) se añadió gota a gota LDA (11,96 ml, 11,96 mmoles, 2,2 eq) a 0 °C. La mezcla de reacción luego se agitó durante 20 minutos a 0 °C. Luego, se añadió yoduro de metilo (1,96 g, 11,96 mmoles, 2,2 eq) a la mezcla de reacción y se agitó durante 16 horas a RT. La mezcla de reacción se inactivó con la adición de una solución saturada de cloruro
de amonio (30 mL). La capa orgánica se separó y la capa acuosa se extrajo con EtOAc (2 x 50 mL). La capa orgánica combinada se lavó con salmuera (50 mL), se secó sobre Na2SO4, se concentró a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 4-bromo-6-fluoro-2-metil-1-(fenilsulfonil)-1 H-indol (1,8 g, 90 %) como un sólido blanco.
Etapa 3: A una solución en agitación de 4-bromo-6-fluoro-2-metil-1-(fenilsulfonil)-1H-indol (0,2 g, 0,53 mmoles, 1 eq) en una mezcla de THF, MeOH y agua (2 mL, 1 mL, 0,5 mL) se añadió hidróxido de sodio (0,08 g, 2,11 mmoles, 4 eq). La mezcla de reacción luego se agitó durante 4 horas a RT. Los disolventes se evaporaron y se añadió agua al residuo y se formó un precipitado que se recogió por filtración y se secó en vacío para obtener el 4-bromo-6-fluoro-2-metil-1H-indol (0,1 g, 83 %) como un sólido blanco.
Etapa 4: A una suspensión en agitación de 4-bromo-6-fluoro-2-metil-1H-indol (0,5 g, 2,19 mmoles, 1 eq), bis(pinacolato)diborano (0,67 g, 4,39 mmoles, 2 eq) y acetato de potasio (0,86 g, 8,8 mmoles, 4 eq) en 1,4-dioxano (20 mL) se desoxigenó con Ar durante 10 minutos. Después, se añadieron Pd2(dba)3 (0,11 g, 1,09 mmoles, 0,05 eq) y triciclohexilfosfina (0,05 g, 0,17 mmoles, 0,08 eq) a la mezcla de reacción y nuevamente se desoxigenó con Ar durante 10 minutos. Luego, la mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción luego se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 6-fluoro-2-metil-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan- 2-il)-1 H-indol (0,4 g, 66 %) como un sólido amarillo claro.
Síntesis de 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1 H-indol-2-carbonitrilo (intermedio A-4)
dloxano/reflujo
Intermedio A-4
Etapa 1: A una solución agitada de 2-bromo-4-fluoro-benzaldehído (0,6 g, 2,95 mmoles, 1 eq) en MeOH (5 mL) se añadió acetato de metilazido (1,35 g, 11,22 mmoles, 4 eq) y se enfrió hasta -15 °C. Luego, se añadió NaOMe al 25 % (2,7 ml, 11,82 mmoles, 4 eq) y la mezcla se agitó durante 4 horas a la misma temperatura. Luego, la mezcla de reacción se vertió en hielo, el sólido resultante se filtró y se secó. A este sólido se añadió xileno y se calentó a reflujo durante 16 horas. A continuación, la masa de reacción se evaporó y el producto crudo se recogió en EtOAc (20 mL), se lavó con salmuera (10 mL), se secó sobre Na2SO4 y se concentró. El producto crudo se purificó mediante cromatografía en columna para proporcionar 4-bromo-6-fluoro-1H-indol-2-carboxilato de metilo (0,35 g, 41 %) como un sólido blanco.
Etapa 2: A una solución agitada de 4-bromo-6-fluoro-1H-indol-2-carboxilato de metilo (3 g, 11,03 mmoles, 1 eq) se añadió THF (8 mL), MeOH (4 mL), H2O (4 mL) seguido de LiOH (1,3 g, 33,08 mmoles, 3 eq) y se agitó durante 16 horas a RT. Luego, la masa de reacción se evaporó y el producto crudo se recogió en H2O y se acidificó con HCl 2N y se extrajo con EtOAc (2 x 50 mL), se lavó con H2O (20 mL) y salmuera (20 mL), se secó sobre Na2SO4 y se concentró para proporcionar ácido 4-bromo-6-fluoro-1H-indol-2-carboxílico (1,2 g, 43 %) como un sólido blanquecino.
Etapa 3: A una solución agitada de ácido 4-bromo-6-fluoro-1H-indol-2-carboxílico (1 g, 3,87 mmoles, 1 eq) en DCM (20 mL) se añadió cloruro de oxalilo (0,6 ml, 7,75 mmoles, 2 eq) a 0 °C y se agitó durante 2 horas. Luego, el disolvente se evaporó bajo N2 , el producto crudo se enfrió hasta 0 °C y luego se añadió una solución acuosa de NH3 y la mezcla se agitó durante 20 minutos. Luego, la masa de reacción se extrajo con EtOAc (2 x 30 mL), se lavó con salmuera (20
mL), se secó sobre Na2SO4 y se concentró. El producto crudo se purificó mediante cromatografía en columna para proporcionar 4-bromo-6-fluoro-1H-indol-2-carboxamida (0,5 g, 50 %) como un sólido blanco.
Etapa 4: A una solución agitada de 4-bromo-6-fluoro-1H-indol-2-carboxamida (0,15 g, 0,58 mmoles, 1 eq) en tolueno (10 mL) se añadió POCb (0,27 mL, 2,91 mmoles, 5 eq) y se calentó a reflujo durante 3 horas. Luego, el disolvente se evaporó y el producto crudo se enfrió y basificó con solución saturada de NaHCO3 y se extrajo con EtOAc (2 x 15 mL), se lavó con H2O (10 mL), salmuera (10 mL), se secó sobre Na2SO4 y se concentró. El producto crudo se purificó mediante cromatografía en columna para proporcionar 4-bromo-6-fluoro-1H-indol-2-carbonitrilo (0,08 g, 58 %) como masa pegajosa.
Etapa 5. A una solución agitada de 4-bromo-6-fluoro-1H-indol-2-carbonitrilo (0,08 g, 0,33 mmoles, 1 eq.) en 1,4-dioxano se añadió KOAc (0,07 g, 0,67 mmoles, 2 eq) y Bispinacolatodiborano (0,17 g, 0,67 mmoles, 2 eq) y se desgasificó con Ar durante 10 minutos. Luego, se añadió Pd2(dba)3 (0,03 g, 0,03 mmoles, 0,1 eq), P(Cy)3 (0,01 g, 0,03 mmoles, 0,1 eq) y la mezcla se calentó a reflujo durante 16 horas. Luego, la masa de reacción se filtró sobre lecho de celite, se lavó con EtOAc, el filtrado se lavó con H2O (10 mL), salmuera (10 mL), se secó sobre Na2SO4 y se concentró para proporcionar 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol-2-carbonitrilo crudo (0,08 g) que se usó para la siguiente etapa sin purificación adicional.
Síntesis de 5-metil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-7)
dim ane/1 l ( r c
E:apa-2 Intermedio A-7
Etapa 1: A una solución de 2-bromo-4-metil-1-nitrobenceno (1,0 g, 4,63 mmoles, 1 eq.) en THF (30 mL) se añadió bromuro de vinilmagnesio (18,5 mL, 18,5 mmoles, 4 eq. solución 1,0 M en THF) a -60 °C en atmósfera de nitrógeno. Luego, la mezcla de reacción se agitó a la misma temperatura durante 4 horas. La reacción se inactivó con una solución saturada de cloruro de amonio a -60 °C. Luego, la mezcla resultante se extrajo con EtOAc (2 x 50 mL), se lavó con solución de salmuera y se concentró a presión reducida para dar el producto crudo que se purificó mediante cromatografía instantánea en columna para proporcionar 7-bromo-5-metil-1H-indol (0,5 g, 52 %) como líquido amarillo denso.
Etapa 2: A una solución de 7-bromo-5-metil-1H-indol (0,5 g, 2,38 mmoles, 1 eq.) en 1,4-dioxano (10 mL) se añadieron KOAc (0,932 g, 9,52 mmoles, 4 eq.), bis-pinacolatodiborano (1,2 g, 4,76 mmoles, 2 eq.) y la mezcla de reacción se desoxigenó con Ar durante 15 minutos. Luego, se añadieron Pd2dba3 (0,032 g, 0,0375 mmoles, 0,015 eq.) y triciclohexilfosfina (0,48 g, 0,171 mmoles, 0,072 eq.) y la mezcla se desoxigenó con Ar durante 10 minutos. La mezcla de reacción se puso a reflujo durante 16 horas. Luego, la mezcla de reacción se enfría hasta RT y se filtra a través de celite y se concentra a presión reducida. La masa concentrada se purificó mediante cromatografía instantánea en columna para proporcionar 5-metil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (0,5 g, 81,7 %) de un sólido amarillo.
Síntesis de 1-(etilsulfonil)-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-8)
reentre
E:apa Intermedio A-S
Etapa 1: A una solución en agitación de 4-bromo-6-fluoro-1H-indol (1,0 g, 4,67 mimóles, 1 eq) en DMF (24 mL) se añadió hidruro de sodio por partes (60 %, 0,224 g, 9,34 mimóles, 2 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió cloruro de etanosulfonilo (0,604 mL, 7 mmoles, 1,5 eq) a la mezcla de reacción a 0 °C. La mezcla de reacción luego se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con EtOAc (200 mL). Las capas orgánicas combinadas se lavaron con agua (5 x 30 mL), salmuera (30 mL), se secaron sobre Na2SO4 anhidro y se evaporaron a presión reducida. El producto en crudo se purificó mediante cromatografía en columna para proporcionar 4-bromo-1-(etilsulfonil)-6-fluoro-1H-indol (0,513 g, 36 %) como un sólido blanquecino.
Etapa 2: Una suspensión en agitación de 4-bromo-1-(etilsulfonil)-6-fluoro-1H-indol (0,51 g, 1,6 mmoles, 1 eq), bis(pinacolato)diborano (0,843 g, 3,2 mmoles, 2 eq) y acetato de potasio (0,653 g, 6,4 mmoles, 4 eq) en 1,4-dioxano (15 mL) se desoxigenó con Ar durante 10 minutos. Después, se añadió Pd2(dba)3 (0,023 g, 0,025 mmoles, 0,015 eq) y triciclohexilfosfina (0,036 g, 0,12 mmoles, 0,072 eq) a la mezcla de reacción y nuevamente se desoxigenó con Ar durante 10 minutos. Luego, la mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 1-(etilsulfonil)-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan- 2-il)-1 H-indol (0,212 g, 38 %) como un sólido blanquecino.
Síntesis de 1-(ciclopropilsulfonil)-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-9)
E:apa-2 Intermedio A-9
Etapa 1: A una solución agitada de 4-bromo-6-fluoro-1H-indol (1,0 g, 4,67 mmoles, 1 eq) en DMF (24 mL) se añadió hidruro de sodio (60 %) (0,467 g, 11,68 mmoles, 2,5 eq) a 0 °C y la mezcla se agitó a r T durante 30 minutos. Luego, se añadió cloruro de ciclopropanosulfonilo (1,3 g, 9,34 mmoles, 2,0 eq) a la mezcla de reacción y se agitó de nuevo durante otras 2 horas. Una vez completada la reacción, la mezcla de reacción se inactivó con agua y se extrajo con EtOAc (2 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 4-bromo-1-(ciclopropilsulfonil)-6-fluoro-1H-indol (0,6 g, 40 %) como un sólido blanco.
Etapa 2: A una solución agitada de 4-bromo-1-(ciclopropilsulfonil)-6-fluoro-1H-indol (0,5 g, 1,57 mmoles, 1 eq), se añadió bis(pinacolato)diborano (0,790 g, 3,14 mmoles, 2 eq) y acetato de potasio (0,46 g, 4,71 mmoles, 3 eq) en 1,4-dioxano (20 mL) y la mezcla se desoxigenó con Ar durante 10 minutos. Luego, se añadió PdCh(dppf)DCM (0,128 g, 0,157 mmoles, 0,1 eq) y la mezcla se agitó a 90 °C durante otras 16 horas. Una vez completada la reacción, la mezcla de reacción se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 1-(ciclopropilsulfonil)-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (0,600 g, 76 %) como un sólido amarillo claro.
Síntesis de 1-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol-1-il)etanona (intermedio A-10)
Etapa 1: A una solución agitada de 4-bromo-1H-indol (0,5 g, 2,55 mimóles, 1 eq) en THF (25 mL) se añadió hidruro de sodio (60 %) (0,122 g, 3,06 mimóles, 1,2 eq) a 0 °C y se continuó agitando a RT durante 30 minutos. Luego, se añadió cloruro de acetilo (0,02 mL, 3,06 mmoles, 1,2 eq) a la mezcla de reacción y se agitó de nuevo durante otras 2 horas. La mezcla de reacción se inactivó con agua y se extrajo con EtOAc (2 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 1-(4-bromo-1H-indol-1-il)etanona (0,55 g, 91 %) como un líquido marrón.
Etapa 2: Una solución agitada de 1-(4-bromo-1H-indol-1-il)etanona (0,55 g, 2,31 mmoles, 1 eq), bis(pinacolato)diborano (0,707 g, 4,62 mmoles, 2 eq) y acetato de potasio (0,680 g, 6,93 mmoles, 3 eq) en 1,4-dioxano (20 mL) se desoxigenó mediante Ar durante 10 minutos y luego se le añadió Pd2(dba)3 (0,106 g, 0,1155 mmoles, 0,08 eq) y Cy3P (0,052 g, 0,1848 mmoles, 0,08 eq) a la mezcla de reacción y se puso a reflujo a 90 °C durante otras 16 horas. La mezcla de reacción se enfrió hasta RT y se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 1-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol-1-il)etanona (0,600 g, 92 %) como un líquido marrón.
Síntesis de 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1-(2,2,2-trifluoroetil)-1H-indol (intermedio A-11)
E:apa-2 Intermedio A - l l
Etapa 1: A una solución de 4-bromo-6-fluoro-1H-indol (2,0 g, 9,345 mmoles, 1 eq.) en DMF (25 mL) se le añadió Cs2CO3 (15,18 g, 46,72 mmoles, 5 eq.) y 1,1,1-trifluoro-2-yodoetano (5,8 g, 28,037 mmoles, 3,0 eq) en un tubo sellado. La mezcla de reacción se puso a reflujo a 50 °C durante 24 horas. La mezcla de reacción se filtró a través de sinterización y el filtrado se diluyó con EtOAc (100 mL). La capa orgánica se lavó con agua fría (3 x 50 mL), salmuera (25 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar una mezcla que se purificó adicionalmente por HPLC Prep. para proporcionar 4-bromo-6-fluoro-1-(2,2,2-trifluoroetil)-1H-indol (0,400 g, 14 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 4-bromo-6-fluoro-1-(2,2,2-trifluoroetil)-1H-indol (0,450 g, 1,52 mmoles, 1 eq), bis(pinacolato)diborano (0,461 g, 1,824 mmoles, 1,2 eq) y acetato de potasio (0,446 g, 4,56 mmoles, 3 eq) en 1,4-dioxano (20 mL) se desoxigenó mediante Ar durante 10 minutos y luego se añadió PdCl2(dppf)DCM (0,124 g, 0,152 mmoles, 0,1 eq) a la mezcla de reacción y se agitó a 90 °C durante otras 16 horas. La mezcla de reacción se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1-(2,2,2-trifluoroetilo)-1H-indol crudo que se usó en la siguiente etapa sin purificación adicional.
Síntesis de 1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-12)
Etapa 1: A una solución en agitación de 4-bromo-1H-indol (1,0 g, 5,1 mimóles, 1 eq) en DMF (20 ml) se añadió hidruro de sodio por partes (60 %, 0,245 g, 10,2 mimóles, 2 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió cloruro de metanosulfonilo (0,584 ml, 7,6 mmoles, 1,5 eq) a la mezcla de reacción a 0 °C. La mezcla de reacción se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con EtOAc (100 mL). Las capas orgánicas combinadas se lavaron con agua (5 x 20 mL), salmuera (20 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 4-bromo-1-(metilsulfonil)-1H-indol (0,532 g, 38 %) como un sólido blanquecino.
Etapa 2: Una suspensión en agitación de 4-bromo-1-(metilsulfonil)-1H-indol (0,36 g, 1,31 mmoles, 1 eq), bis(pinacolato)diborano (0,66 g, 2,62 mmoles, 2 eq) y acetato de potasio (0,57 g, 5,25 mmoles, 4 eq) en 1,4-dioxano (10 L1) se desoxigenó mediante Ar durante 10 minutos. Después, se añadió Pd2(dba)3 (0,018g, 0,019 mmoles, 0,015 eq) y triciclohexilfosfina (0,027 g, 0,094 mmoles, 0,072 eq) a la mezcla de reacción y nuevamente se desoxigenó mediante Ar durante 10 minutos. Luego, la mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción luego se enfrió hasta RT y después se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan- 2-il)-1H-indol (0,31 g, 73 %) como un sólido blanquecino.
Síntesis de 5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-3-(2,2,2-trifluoroetil)-1 H-indol (intermedio A-13)
«ano s
E:apa Intermedio ñ
13
Etapa 1: A una solución de 7-bromo-5-fluoro-1H-indol (0,5 g, 2,336 mmoles, 1 eq.) en DCM (25 mL) se añadió 2,6-diterc-butilpiridina (0,893 g, 4,672 mmoles, 2 eq.) y la mezcla se agitó durante 10 minutos a RT. Se añadió trifluorometanosulfonato de 2,2,2-trifluoroetil(2,4,6-trimetilfenil)yodonio (1,45 g, 3,063 mmoles, 1,3 eq) y la mezcla se agitó durante 2 horas a RT. El disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar 7-bromo-5-fluoro-3-(2,2,2-trifluoroetil)-1H-indol (0,300 g, 43 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 7-bromo-5-fluoro-3-(2,2,2-trifluoroetil)-1H-indol (0,9 g, 3,04 mmoles, 1 eq), bis(pinacolato)diborano (1,53 g, 6,081 mmoles, 2 eq) y acetato de potasio (0,893 g, 9,121 mmoles, 3 eq) en 1,4-dioxano (20 mL) se desoxigenó mediante Ar durante 10 minutos. Luego, se añadió PdCl2(dppf)DCM (0,215 g, 0,304 mmoles, 0,1 eq) a la mezcla de reacción y la mezcla se agitó a 90 °C durante otras 16 horas. La mezcla de reacción se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea a 5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-3-(2,2,2-trifluoroetil)-1H-indol (0,600 g, 58 %) como un líquido gomoso.
S ín te s is d e 7 -(4 ,4 ,5 ,5 - te t ra m e t i l -1 ,3 ,2 -d io x a b o ro la n -2 - i l) -3 -(2 ,2 ,2 - tr i f lu o ro e t i l) -1 H - in d o l ( in te rm e d io A -14 )
Etapa 1: A una solución de 7-bromo-1H-indol (0,264 g, 1,346 mimóles, 1 eq.) en DCM (25 mL) se añadió 2,6-di-tercbutilpiridina (0,515 g, 2,694 mimóles, 2 eq.) y la mezcla se agitó durante 10 minutos a RT. Se añadió trifluorometanosulfonato de 2,2,2-trifluoroetil(2,4,6-trimetilfenM)yodonio (1,4 g, 1,7509 mimóles, 1,3 eq) y se continuó la agitación durante 2 horas a RT. El disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar 7-bromo-3-(2,2,2-trifluoroetil)-1H-indol (0,300 g, 81 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 7-bromo-3-(2,2,2-trifluoroetil)-1H-indol (0,15 g, 0,539 mmoles, 1 eq), bis(pinacolato)diborano (273 g, 1,079 mmoles, 2 eq) y acetato de potasio (0,158 g, 1,617 mmoles, 3 eq) en 1,4-dioxano (20 mL) se desoxigenó mediante Ar durante 10 minutos. Luego, se añadió PdCh(dppf)DCM (0,044 g, 0,054 mmoles, 0,1 eq) a la mezcla de reacción y se agitó a 90 °C durante otras 16 horas. La mezcla de reacción se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar 7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-3-(2,2,2-trifluoroetil)-1 H-indol (0,100 g, 57 %) como un líquido gomoso.
Síntesis de 5-fluoro-3-metil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-15)
Etapa 1: A una solución de 2-bromo-4-fluoro-1-nitrobenceno (0,5 g, 2,27 mmoles, 1 eq.) en THF (20 mL) se añadió bromuro de (E)-prop-1-en-1-ilmagnesio (0,5 M en THF) (13,6 mL, 6,818 mmoles, 3 eq) a -60 °C bajo atmósfera de nitrógeno. Luego, la mezcla de reacción se agitó a la misma temperatura durante 4 horas. La reacción se inactivó con una solución saturada de cloruro de amonio a -60 °C. Luego, la mezcla resultante se extrajo con EtOAc (2 x 100 mL), se lavó con solución de salmuera y se concentró a presión reducida para dar el producto crudo que se purificó mediante cromatografía instantánea en columna para proporcionar 7-bromo-5-fluoro-3-metil-1H-indol (0,3 g, 58 %) como líquido amarillo denso.
Etapa 2: A una solución de 7-bromo-5-fluoro-3-metil-1H-indol (0,8 g, 3,669 mmoles, 1 eq) en 1,4-dioxano (15,0 mL) se añadió KOAC (1,43 g, 14,67 mmoles, 4 eq) y bispincolatediborano (1,12 g, 7,33 mmoles, 2 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd2(dba)3 (0,16 g, 0,183 mmoles, 0,05 eq) y Cy3P (0,082 g, 0,293 mmoles, 0,08 eq). La mezcla de reacción se puso a reflujo durante 16 horas. Una vez completada la reacción (monitorizada mediante TLC), el disolvente se evaporó a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 5-fluoro-3-metil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (0,7 g, 70 %), como un sólido marrón.
Síntesis de 3-ciclopropil-5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-16)
Intermedio A-16
Etapa 1: A una solución en agitación de 7-bromo-5-fluoroindol (7,0 g, 32,7 mimóles, 1 eq) en DMF (175 mL) se añadió hidróxido de potasio en polvo (4,56 g, 81,77 mimóles, 2,5 eq). Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (12,46 g, 49,06 mmoles, 1,5 eq) a la mezcla de reacción y finalmente se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con EtOAc (1.000 mL) y se lavó con agua (5 x 100 mL) seguido de salmuera (100 mL). La capa orgánica se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 7-bromo-5-fluoro-3-yodo-1H-indol (6,2, 56 %) como un sólido marrón.
Etapa 2: A una solución en agitación de 7-bromo-5-fluoro-3-yodo-1H-indol (6,2 g, 18,23 mmoles, 1 eq) en THF (109 mL) se añadió gota a gota LiHMDS (1 M) (91,15 ml, 91,15 mmoles, 5 eq) a -78 °C en atmósfera inerte. La mezcla de reacción se agitó durante 30 minutos en la misma condición. Luego, se añadió MOMCl (5,83 g, 72,94 mmoles, 4 eq) a la mezcla de reacción a -78 °C. La mezcla de reacción se dejó calentar hasta RT y luego se agitó durante 16 horas. La mezcla de reacción se inactivó mediante la adición de una solución saturada de cloruro de amonio (100 mL). La capa orgánica se separó y la capa acuosa se extrajo con EtOAc (100 mL). Las capas orgánicas combinadas se lavaron con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 7-bromo-5-fluoro-3-yodo-1-(metoximetil)-1H-indol (5,4 g, 57 %) como un sólido blanquecino.
Etapa 3: Una suspensión agitada de 7-bromo-5-fluoro-3-yodo-1-(metoximetil)-1H-indol (2,7 g, 7,03 mmoles, 1 eq), ácido ciclopropilborónico (1,84 g, 2,03 mmoles, 3 eq) y K3PO4 (4,5 g, 21,05 mmoles, 3 eq) en 1,4-dioxano (45 mL) se desoxigenó mediante Ar durante 10 minutos. Luego, se añadió Pd(OAc)2 (0,08 g, 0,3525 mmoles, 0,05 eq) y xantphos (0,407 g, 0,713 mmoles, 0,1 eq) a la mezcla de reacción y nuevamente se desoxigenó durante 10 minutos. Finalmente, la mezcla de reacción se agitó a 100 °C durante 16 horas. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 7-bromo-3-ciclopropil-5-fluoro-1-(metoximetil)-1H-indol (0,65 g, 31 %) como un sólido blanquecino.
Etapa 4: A una solución en agitación de 7-bromo-3-ciclopropil-5-fluoro-1-(metoximetil)-1H-indol (1,25 g, 4,19 mmoles, 1 eq) en una mezcla de MeOH y agua (3:1) (66 mL) se añadió ácido oxálico (1,13 g, 12,58 mmoles, 3 eq). Luego, la mezcla de reacción se agitó a 90 °C durante 18 horas. La mezcla de reacción se enfrió hasta RT y se concentró a presión reducida para obtener el residuo. El residuo se diluyó con EtOAc (100 mL) y se lavó con agua (2 x 40 mL) y salmuera (40 mL). La capa orgánica se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 7-bromo-3-ciclopropil-5-fluoro-1H-indol (0,57 g, 54 %) como un líquido incoloro.
Etapa 5. Una suspensión en agitación de 7-bromo-3-ciclopropil-5-fluoro-1H-indol (0,57 g, 2,24 mmoles, 1 eq), bispinacolatodiborano (1,7 g, 6,73 mmoles, 3 eq) y acetato de potasio (0,66 g, 6,73 mmoles, 3 eq) en 1,4-dioxano (20 mL) se desoxigenó con Ar durante 10 minutos. Después, se añadió Pd2(dba)3 (0,031g, 0,033 mmoles, 0,015 eq) y triciclohexilfosfina (0,047 g, 0,168 mmoles, 0,075 eq) a la mezcla de reacción y nuevamente se desoxigenó con Ar durante 10 minutos. Luego, la mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción luego se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 3-ciclopropil-5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan- 2-il)-1H-indol (0,35 g, 52 %) como un sólido blanquecino.
S ín te s is d e 3 -c ic lo b u t i l- 7 -(4 ,4 ,5 ,5 - te t ra m e t i l -1 ,3 ,2 -d io x a b o ro la n -2 - i l) -1 H - in d o l ( in te rm e d io A -17 )
Intermedio 17
Etapa 1: A una solución en agitación de ácido 2,2,2-tricloroacético (9,97 g, 61,22 mimóles, 1,5 eq) y trietilsilano (19,7 mL, 122,4 mimóles, 3,0 eq) en tolueno (20 mL) se añadieron 7-bromo-1H-indol (8,0 g, 40,81 mmol) y ciclobutanona (3,37 ml, 44,89 mmoles, 1,1 eq) en tolueno (20 mL) y la mezcla se agitó a 70 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se enfrió hasta 10 °C, se inactivó con solución acuosa saturada de NaHCO3, se extrajo con EtOAc (2 x 300 mL), la capa orgánica se lavó con salmuera (50 mL), se secó sobre Na2SO4 anhidro, se filtró y el disolvente se evaporó a presión reducida para obtener el producto crudo que se purificó mediante columna combiflash para proporcionar 7-bromo-3-ciclobutil-1H-indol (5,0 g, 49 %) como un sólido blanco.
Etapa 2: A una solución de 7-bromo-3-ciclobutil-1H-indol (1,0 g, 4,0 mmoles, 1 eq) en 1,4-dioxano (30 mL) se añadieron KOAC (1,17 g, 12,0 mmoles, 3,0 eq) y bis-pincolato de diborano (2,03 g, 8,0 mmoles, 2 eq). La solución se desgasificó con Ar durante 20 min, seguido de la adición de PdCb.dppfDCM (0,16 g, 0,2 mmoles, 0,05 eq). La mezcla de reacción se agitó a 90 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se evaporó a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 3-ciclobutil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (1,1 g, 93 %), como un sólido blanquecino.
Síntesis de 3-(tetrahidrofuran-3-il)-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1 H-indol (intermedio A-18)
Etapa 1: A una solución en agitación de ácido 2,2,2-tricloroacético (7,48 g, 45,91 mmoles, 1,5 eq) y trietilsilano (14,8 ml, 91,83 mmoles, 3,0 eq) en tolueno (15 mL) se añadieron 7-bromoindol (6,0 g, 30,611 mmoles) y dihidrofuran-3-ona (2,58 mL, 33,67 mmoles, 1,1 eq) en tolueno (15 mL) a 70 °C y se agitó durante 24 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se enfrió hasta 10 °C, se inactivó con solución acuosa saturada de NaHCO3, se extrajo con EtOAc (2 x 300 mL), la capa orgánica se lavó con salmuera (50 mL), se secó sobre Na2SO4 anhidro, se filtró y se evaporó a presión reducida para obtener el producto crudo que se purificó mediante columna combiflash para proporcionar 7-bromo-3-(tetrahidrofuran-3-il)-1H-indol (1,1 g, 14 %) como un sólido pegajoso.
Etapa 2: A una solución de 7-bromo-3-(tetrahidrofuran-3-il)-1H-indol (1,0 g, 3,75 mmoles, 1 eq) en 1,4-dioxano (30 mL) se añadieron KOAC (1,1 g, 11,27 mmoles, 3,0 eq) y bis-pincolatediborano (1,9 g, 7,51 mmoles, 2 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de PdCb.dppfDCM (0,15 g, 0,18 mmoles, 0,05 eq). La mezcla de reacción se agitó a 90 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), el disolvente se evaporó a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 3-(tetrahidrofuran-3-il)-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (1,0 g, 85 %), como un sólido blanquecino.
S ín te s is d e 3 -e t i l- 5 - f lu o ro -7 -(4 ,4 ,5 ,5 - te t ra m e t i l-1 ,3 ,2 -d io x a b o ro la n -2 - i l) -1 H - in d o l ( in te rm e d io A -19 )
Interm edio A -13 DMF.'&^C
E^apa--
Etapa 1: Al DMF (10 mL), se añadió POCI3 (0,22 mL, 2,412 mimóles, 1,1 eq) a 0 °C. A esta solución se añadió gota a gota 7-bromo-5-fluoro-1H-indol (0,5 g, 2,192 mimóles, 1 eq) y la mezcla se agitó a 0 °C durante 1 hora. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se basificó con NaOH y se acidificó de nuevo con HCl. Precipitó un sólido que se filtró, se lavó con agua y se secó a presión reducida para proporcionar 7-bromo-5-fluoro-1H-indol-3-carbaldehído (0,23 g, 43 %) como un sólido blanco.
Etapa 2: A una solución de 7-bromo-5-fluoro-1H-indol-3-carbaldehído (0,23 g, 0,95 mmoles, 1 eq.) en THF (10 mL) se añadió bromuro de metilmagnesio (3,0 M en THF) (1,1 mL, 3,33 mmoles, 3,5 eq) a -78 °C bajo atmósfera de nitrógeno. Luego, la mezcla de reacción se agitó a la misma temperatura durante 4 horas. La reacción se inactivó con una solución saturada de cloruro de amonio a -78 °C. Luego, la mezcla resultante se extrajo con EtOAc (2 x 20 mL), se lavó con solución de salmuera y se concentró a presión reducida para proporcionar 1-(7-bromo-5-fluoro-1H-indol-3-il)etanol crudo (0,12, g, 50 %) como un líquido amarillo denso, que se usó para la siguiente etapa sin purificación adicional.
Etapa 3: A una solución de 1-(7-bromo-5-fluoro-1H-indol-3-il)etanol (0,12 g, 0,465 mmoles, 1 eq.) en THF (5 mL) se añadió LAH (0,045 g, 1,162 mmoles, 2,5 eq) a 0 °C en atmósfera de nitrógeno. La mezcla de reacción se agitó a RT durante 1 hora. Una vez completada la reacción (controlada por TLC), la reacción se inactivó con la técnica de tratamiento de Fisher. Luego, la mezcla resultante se filtró a través de sinterización y el filtrado se evaporó a presión reducida para proporcionar el producto crudo que se purificó mediante cromatografía en columna para proporcionar 7-bromo-3-etil-5-fluoro-1H-indol (0,07 g, 63 %) como una goma marrón.
Etapa 4: Una suspensión en agitación de 7-bromo-3-etil-5-fluoro-1H-indol (0,4 g, 1,652 mmoles, 1 eq), bis(pinacolato)diborano (0,46 g, 1,818 mmoles, 1,1 eq) y acetato de potasio (0,485 g, 4,956 mmoles, 3 eq) en 1,4-dioxano (25 ml) se desoxigenó con Ar durante 10 minutos. Después, se añadió PdCb(dppf)DCM (0,13 g, 0,165 mmol.
0,1 eq) a la mezcla de reacción y nuevamente se desoxigenó mediante Ar durante 10 minutos. Luego, la mezcla de reacción se agitó durante 16 horas a 110 °C. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna para proporcionar 3-etil-5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (0,36 g, 75 %) como una goma amarilla clara.
Síntesis de 2-(6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol-1-il)etanol (intermedio A-20)
Intermedio A-20
Etapa 1: A una solución de 4-bromo-6-fluoro-1H-indol (0,5 g, 2,34 mimóles, 1 eq.) en DMF (5 mL) se añadió hidruro de sodio (0,130 g, 2,80 mimóles, 1,2 eq) a 0 °C. La solución se agitó a RT durante 30 minutos seguido de la adición de (2-bromoetoxi) (terc-butil)dimetilsilano (1,17 g, 4,67 mmoles, 2,0 eq) y la mezcla de reacción se agitó a RT durante 2 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con EtOAc (20 mL) y la capa orgánica se lavó con agua fría (5 x 10 mL), salmuera (10 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 4-bromo-1-(2-((terc-butildimetilsilil)oxi)etil)-6-fluoro-1H-indol (0,85 g, 98 %) como un líquido marrón que tenía (2-bromoetoxi)(terc-butil)dimetilsilano como impureza.
Etapa 2: A una solución agitada de 4-bromo-1-(2-((terc-butildimetilsilil)oxi)etil)-6-fluoro-1H-indol (1,3 g, 3,49 mmoles, 1 eq.) en THF (15 mL) se añadió TBAF (3,49 mL) (1 M) a RT y la mezcla se agitó durante 16 horas. Después de completar la reacción (controlada por LCMS y TLC), la mezcla de reacción se diluyó con EtOAc (20 mL) y la capa orgánica se lavó con agua fría (5 x 10 mL), salmuera (10 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 2-(4-bromo-6-fluoro-1H-indol-1-il) (0,55 g, 61 %) como un líquido marrón.
Etapa 3: Una solución agitada de 2-(4-bromo-6-fluoro-1H-indol-1-il)etanol (0,55 g, 2,13 mmoles, 1 eq), bis(pinacolato)diborano (0,647 g, 2,55 mmoles, 1,2 eq) y acetato de potasio (0,626 g, 6,393 mmoles, 3 eq) en 1,4-dioxano (20 mL) se desoxigenó mediante Ar durante 10 minutos. Luego, se añadió PdCb(dppf)DCM (0,173 g, 0,213 mmoles, 0,1 eq) a la mezcla de reacción y la mezcla se agitó a 90 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el producto crudo que se usó en la siguiente etapa sin purificación adicional.
Síntesis de 2-(6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indazol-1-il)etanol (intermedio A-21)
Etapa 1: A una solución agitada de 4-bromo-6-fluoro-1H-indazol (0,2 g, 0,93 mmoles, 1 eq) en DMF (5 mL) se añadió K2CO3 (0,38 g, 2,79 mmoles, 3,0 eq) a RT y la mezcla se agitó durante 20 minutos. Luego, se añadió 2-bromo-etanol (0,07 mL, 0,93 mmoles, 1 eq) y la mezcla se agitó durante 16 horas a 50 °C. Una vez completada la reacción (controlada por TLC), la masa de reacción se inactivó con agua helada y se extrajo con EtOAc (3 x 20 mL), se lavó con H2O (3 x 20 mL) y salmuera (25 mL), se secó sobre Na2SO4 y se concentró. El producto crudo se purificó mediante cromatografía en columna para proporcionar 2-(4-bromo-6-fluoro-1H-indazol-1-il)etanol (0,12 g, 50 %) como un sólido blanco.
Etapa 2: A una solución de 2-(4-bromo-6-fluoro-1H-indazol-1-il)etanol (0,9 g, 3,473 mmoles, 1 eq) en 1,4-dioxano (60,0 mL) se añadieron KOAc (1,02 g, 10,419 mmoles, 3 eq) y bispincolatodiborano (1,76 g, 6,947 mmoles, 2,0 eq). La
solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd2(dba)3 (0,17 g, 0,173 mimóles, 0,05 eq) y Cy3P (0,077 g, 0,277 mmoles, 0,08 eq). La mezcla de reacción se puso a reflujo durante 16 horas. Una vez completada la reacción (controlada por t Lc ), el disolvente se evaporó a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar -(6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol-1-il)etanol (0,95 g, 89 %) como un sólido marrón.
Síntesis de 1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indazol (intermedio A-22)
Etapa 1: A una solución en agitación de 4-bromo-1H-indazol (1,0 g, 5,07 mmoles, 1 eq) en DMF (25 ml) se añadió hidruro de sodio por partes (60 %, 0,406 g, 10,152 mmoles, 2 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Se añadió cloruro de metanosulfonilo (0,59 mL, 7,6 mmoles, 1,5 eq) a la mezcla de reacción a 0 °C. La mezcla de reacción se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con EtOAc (150 mL). Las capas orgánicas combinadas se lavaron con agua (5 x 30 mL), salmuera (30 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 10 %/hexano; valor Rf-0,5) para proporcionar 4-bromo-1-(metilsulfonil)-1H-indazol (0,95 g, 69 %) como un sólido amarillo claro.
Etapa 2: Una suspensión en agitación de 4-bromo-1-(metilsulfonil)-1H-indazol (0,95, 3,45 mmoles, 1 eq), bis(pinacolato)diborano (1,75 g, 6,91 mmoles, 2 eq) y acetato de potasio (1,01 g, 10,36 mmoles, 3 eq) en 1,4-dioxano (35 mL) se desoxigenó mediante Ar durante 10 minutos. Después, se añadió Pd(dppf)CbDCM (0,141 g, 0,1727 mmoles, 0,05 eq) a la mezcla de reacción y nuevamente se desoxigenó mediante Ar durante 10 minutos. La mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 10 %/hexano; valor Rf-0,45) para proporcionar 1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indazol (0,9 g, 85,4 %) como un sólido blanquecino.
Síntesis de 6-fluoro-1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indazol (intermedio A-23)
Etapa 1: A una solución en agitación de 4-bromo-6-fluoro-1H-indazol (1,2 g, 5,58 mmoles, 1 eq) en DMF (30 mL) se añadió hidruro de sodio por partes (60 %, 0,446 g, 11,16 mmoles, 2 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 30 minutos a r T. Se añadió cloruro de metanosulfonilo (0,65 ml, 8,37 mmoles, 1,5 eq) a la mezcla de reacción a 0 °C. La mezcla de reacción se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con EtOAc (150 mL). Las capas orgánicas combinadas se lavaron con agua (5 x 30 mL), salmuera (30 mL), se secaron sobre Na2SO4 anhidro y se evaporaron a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 10 %/hexano; valor Rf-0,5) para proporcionar 4-bromo-6-fluoro-1-(metilsulfonil)-1H-indazol (1,3 g, 80 %) como un sólido amarillo claro.
Etapa 2: Una suspensión en agitación de 4-bromo-6-fluoro-1-(metilsulfonil)-1H-indazol (1,3, 4,43 mmoles, 1 eq), bis(pinacolato)diborano (2,25 g, 8,87 mmoles, 2 eq) y acetato de potasio (1,3 g, 13,3 mmoles, 3 eq) en 1,4-dioxano
(45 mL) se desoxigenó mediante Ar durante 10 minutos. Luego, se añadió Pd(dppf)CbDCM (0,18 g, 0,22 mimóles, 0,05 eq) a la mezcla de reacción y nuevamente se desoxigenó mediante Ar durante 10 minutos. La mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 10 %/hexano; valor Rf-0,45) para proporcionar 6-fluoro-1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indazol (1,1 g, 73 %) como un sólido blanquecino.
Síntesis de 6-fluoro-1-(2-metoxietil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-24)
Etapa 1: A una solución en agitación de 4-bromo-6-fluoro-1H-indol (0,5 g, 2,34 mmoles, 1 eq) en DMF (5 mL) se añadió hidruro de sodio por partes (0,112 g, 2,8 mmoles, 1,2 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió 1-bromo-2-metoxietano (0,812 mL, 5,84 mmoles, 2,5 eq) a la mezcla de reacción a 0 °C. La mezcla de reacción se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con EtOAc (50 mL). Las capas orgánicas combinadas se lavaron con agua (5 x 10 mL), salmuera (10 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 20 %/hexano; valor Rf-0,6) para proporcionar 4-bromo-6-fluoro-1-(2-metoxietil)-1H-indol (0,63 g, 99 %) como una goma marrón.
Etapa 2: Una suspensión en agitación de 4-bromo-6-fluoro-1-(2-metoxietil)-1H-indol (0,8 g, 2,94 mmoles, 1 eq), bispinacolatodiborano (1,2 g, 4,4 mmoles, 1,5 eq.) y acetato de potasio (0,865 g, 8,823 mmoles, 3 eq.) en 1,4-dioxano (20 mL) se desoxigenó mediante Ar durante 10 minutos. Luego, se añadió PdCb(dppf)DCM (0,239 g, 0,29 mmoles, 0,01 eq) q) y la mezcla de reacción se agitó durante 14 horas a 90 °C. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 5 %/hexano; valor Rf-0,6) para proporcionar 6-fluoro-1-(2-metoxietil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (0,93 g, 99 %) como un sólido gomoso marrón claro.
Síntesis de 1-(2,2-difluoroetil)-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-25)
Etapa 1: A una solución agitada de 4-bromo-6-fluoro-1H-indol (0,1 g, 0,469 mmoles, 1 eq) en DMF (25 ml) se añadió Cs2COa (0,457 g, 1,407 mmoles, 3 eq) seguido de LiBr (86,84 g, 0,469 mmoles, 1 eq) y la mezcla se agitó a RT durante 10 minutos. Luego, se añadió 4-metilbencenosulfonato de 2,2-difluoroetilo (0,133 g, 0,563 mmoles, 1,2 eq) a la mezcla de reacción y se calentó a 80 °C durante 3 horas (TLC). La mezcla de reacción se diluyó luego con agua (10 mL) y EtOAc (15 mL). La capa orgánica se lavó con agua fría (3 x 10 mL), salmuera (10 mL), se secó sobre Na2SO4 anhidro y se concentró a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 100-200, sistema TLC: EtoAc/Hexano (3:7); valor Rf-0,5) para proporcionar 4-bromo-1-(2,2-difluoroetil)-6-fluoro-1H-indol (0,75 g, 58 %).
Etapa 2: Una suspensión de 4-bromo-1-(2,2-difluoroetil)-6-fluoro-1H-indol (0,2 g, 0,722 mmoles, 1 eq), bis(pinacolato)diboro (0,275 g, 1,083 mmoles, 1,5 eq) y acetato de potasio (0,212 g, 2,166 mmoles, 3 eq) en 1,4-dioxano (10 mL) se desoxigenó bien mediante Ar durante 10 minutos. Luego, se añadió complejo de dicloruro de 1,1'Bis(difenilfosfino)ferroceno paladio(II) DCM (0,03 g, 0,0361 mimóles, 0,05 eq) a la mezcla de reacción y la mezcla de reacción se calentó a 100 °C durante 16 horas (LCMS). La mezcla de reacción se enfrió luego hasta RT, se filtró a través de una almohadilla de celite y el filtrado se concentró a presión reducida para obtener 1 -(2,2-difluoroetil)-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol crudo que se usó en la siguiente etapa sin purificación adicional (Rendimiento ~ 49 % en LCMS).
Síntesis de 3-ciclopropil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-26)
A partir de 7-bromo-1H-indol, el intermedio A-26 se sintetizó en analogía con la síntesis descrita para el intermedio A-16.
Síntesis de 1-ciclopropil-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-27)
Cu(OAcefe ,
F rd n a/65- Intermedio A-27
E:apa-1 E:apa-2
Etapa 1: A una solución en agitación de 4-bromo-6-fluoro-1H-indol (5,4 g, 25,23 mmoles, 1 eq) en tolueno (45 mL) se añadieron ácido ciclopropilborónico (4,33 g, 50,46 mmoles, 2 eq), Cu(OAc)2 (0,46 g, 2,52 mmoles, 0,1 eq), 2-(4,5-dihidro-1H-imidazol-2-il)fenol (0,41 g, 2,52 mmoles, 0,1 eq) y piridina (6,0 g, 75,7 mmoles, 3 eq). La mezcla de reacción se agitó durante 24 horas a 65 °C. El disolvente se eliminó a presión reducida y se azeotropó mediante MeOH dos veces. El residuo se purificó mediante cromatografía en columna (gel de sílice malla 230-400, EtOAc al 10 %/hexano, valor Rf-0,6) para proporcionar 4-bromo-1-ciclopropil-6-fluoro-1H-indol (0,85 g, 13 %) como un líquido marrón.
Etapa 2: Una suspensión en agitación de 4-bromo-1-ciclopropil-6-fluoro-1H-indol (0,85 g, 3,35 mmoles, 1 eq), bis(pinacolato)diborano (1,7 g, 6,7 mmoles, 2 eq) y acetato de potasio (1,31 g, 13,38 mmoles, 4 eq) en 1,4-dioxano (20 mL) se desoxigenó mediante Ar durante 10 minutos. Después, se añadió Pd2(dba)3 (0,046 g, 0,05 mmoles, 0,015 eq) y triciclohexilfosfina (0,067 g, 0,24 mmoles, 0,072 eq) a la mezcla de reacción y nuevamente se desoxigenó mediante Ar durante 10 minutos. La mezcla de reacción se agitó durante 14 horas a 110 °C. La mezcla de reacción se enfrió hasta RT y luego se filtró a través de un lecho de celite. El filtrado se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 20 %/hexano; valor Rf-0,6) para proporcionar 1-ciclopropil-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol
(0,61 g, 61 %) como un sólido amarillo claro.
1H-RMN (400 MHz; DMSO-D6, 20 °C): 87,45 (dd, 1H), 7,35 (d, 1H), 7,15 (dd, 1H), 6,67 (d, 1H), 3,41 (m, 1H), 1,32 (12H), 1,03-1,08 (2H), 0,82-0,92 (2H).
Síntesis de 5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-71)
Una mezcla de 7-bromo-5-fluoro-1H-indol (1 g, 4,7 mmoles, 1 eq), bis(pinacolato)diborano (2,02 g, 7,9 mmoles, 1,7 eq), acetato de potasio (917 mg, 9,4 mmoles, 2 eq), complejo de dicloruro de 1,1'-Bis(difenilfosfino)ferroceno paladio(II) DCM (382 mg, 0,467 mmoles, 0,1 eq) en 1,4-dioxano (13 mL) se desgasificó con nitrógeno y la mezcla de reacción se agitó a 60 °C. Una vez completada la reacción (controlada por LCMS), se añadió una solución saturada de bicarbonato de sodio a la mezcla de reacción, que luego se extrajo con EtOAc (2 x). Las capas orgánicas combinadas se lavaron con salmuera, se secaron sobre MgSO4 anhidro y se evaporaron a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice, EtOAc/ciclohexano como eluyente) para proporcionar 5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (940 mg, 77 %).
Los intermedios de la Tabla 1 se sintetizaron en analogía con el Intermedio A-1 al Intermedio A-27.
Los intermedios de la Tabla 2 están disponibles comercialmente:
Síntesis de 8-bromo-7,9-difluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-1):
Etapa 1: En un tubo de ensayo sellado, se desoxigenó una suspensión de 2-bromo-4,6-difluoroanilina (25 g, 120,19 mimóles, 1 eq.), ácido 2-amino-2-metilpropanoico (24,75 g, 240,38 mmoles, 2 eq.), K3PO4 (50,96 g, 240,38 mmoles, 2 eq.) y Cul (2,29 g, 12,02 mmoles, 0,1 eq.) en DMSO seco (375 mL) con Ar durante 20 minutos. La mezcla de reacción se agitó después a 125 °C durante 16 horas. Una vez completada la reacción, se filtró a través de un lecho de celite y se lavó con EtOAc (100 mL). El filtrado se diluyó con EtOAc (500 mL) y se lavó con agua (3 x 150 mL), salmuera (200 mL), se secó sobre Na2SO4 anhidro y se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (34,0 g, 67 %) como un sólido marrón.
Etapa 2: A una solución de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (34,0 g, 160 mmoles, 1 eq.) en tolueno (650 mL) se añadió reactivo de Lawesson (97,3 g, 240 mmoles, 1,5 eq.) a RT y la mezcla de reacción se puso a reflujo a 120 °C durante 40 minutos. Una vez completada la reacción, la mezcla de reacción se inactivó con solución saturada de NaHCO3 (250 mL) seguido de extracción con EtOAc (3 x 150 mL). Las capas orgánicas combinadas se lavaron con agua (300 mL), salmuera (200 mL), se secaron sobre Na2SO4 anhidro y se evaporaron para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (26 g, 66 %) como un sólido amarillo.
Etapa 3: A una solución de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (5,0 g, 21,9 mmoles, 1 eq.) en n-BuOH (60 mL) se le añade acetohidrazida (5,35 g, 72,3 mmoles, 3,3 eq) seguido de la adición de AcOH (6 mL) y luego la mezcla de reacción se agita a 140 °C durante 16 horas. Una vez completada la reacción, la mezcla de reacción se concentra y el residuo se diluye con EtOAc (150 mL). Las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y se evaporaron para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 7,9-difluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (4,5 g, 82 %) como un sólido blanquecino.
Etapa 4: A la solución agitada de 7,9-difluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (4,5 g, 18 mmoles, 1 eq.) en DMF (40 mL) se añadió N-bromosuccinimida (3,5 g, 19,8 mmoles, 1,1 eq) por partes. La mezcla de reacción se dejó calentar hasta RT y se agitó durante 2 horas. La mezcla de reacción se diluyó con EtOAc (300 mL). Las capas orgánicas combinadas se lavaron con agua (5 x 50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y se evaporaron a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 8-bromo-7,9-difluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (4,0 g, 61 %) como un sólido marrón.
Síntesis de 8-bromo-1-etil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-2):
Etapa 1: A una solución de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (7,0 g, 30,7 mimóles, 1 eq.) en n-BuOH (84 mL) se le añadió propionohidrazida (8,92 g, 101,3 mimóles, 3,3 eq) seguido de la adición de ácido acético (8,4 mL) y luego la mezcla de reacción se agitó a 140 °C durante 16 horas. Una vez completada la reacción, la mezcla de reacción se concentró y el residuo se diluyó con EtOAc (150 mL). Las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y se evaporaron para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 1 -etil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (6,0 g, 74 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 1-etil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (5,5 g, 20,8 mmoles, 1 eq.) en DMF (50 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (3,89 g, 21,8 mmoles, 1,05 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1,5 horas. Una vez completada la reacción, la mezcla de reacción se diluyó con EtOAc (300 mL) y las capas orgánicas se lavaron con agua (5 x 50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 8-bromo-1-etil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (4,4 g, 62 %) como un sólido blanquecino.
Síntesis de 8-bromo-7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-3):
Etapa 1: Una suspensión de 2-bromo-4-fluoro-6-metil anilina (5 g, 24,5 mmoles, 1 eq.), ácido 2-aminoisobutárico (5,05 g, 49 mmoles, 2 eq.), Cs2CO3 (15,92 g, 49 mmoles, 2 eq.) y yoduro cuproso (0,466 g, 2,45 mmoles, 0,1 eq.) en DMSO seco (75 mL) en un tubo sellado se desoxigenó con Ar durante 20 minutos. Luego, la mezcla de reacción se agitó a 125 °C durante 16 horas. La mezcla de reacción se filtró a través de un lecho de celite y se lavó con EtOAc (100 mL). El filtrado se diluyó con EtOAc (200 mL) y se lavó con agua (3 x 100 mL), salmuera (100 mL), se secó sobre Na2SO4 anhidro y se evaporó a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-ona (3,0 g, 59 %) como un sólido marrón.
Etapa 2: A una solución de 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-ona (3,66 g, 17,6 mmoles, 1 eq.) en tolueno (75 mL) se añadió reactivo de Lawesson (10,67 g, 26,2 mmoles, 1,5 eq.) a RT y la mezcla de reacción se agitó a 120 °C durante 40 minutos. La mezcla de reacción se inactivó con solución saturada de NaHCO3 (100 mL) seguido de extracción con EtOAc (2 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (2,8 g, 71 %) como un sólido amarillo.
Etapa 3: A una solución en agitación de 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (5,50 g, 24,55 mmoles, 1 eq) en THF (30 mL) se añadió gota a gota hidrato de hidrazina (5,17 mL, 122,76 mmoles, 5 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 16 horas a RT. Se añadió TEA (16,7 ml, 122,76 mmoles, 5 eq) a la mezcla de reacción y se agitó durante otros 10 minutos. Se añadió cloruro de acetilo (5,78 g, 73,65 mmoles, 3 eq) a la mezcla de reacción muy lentamente a 0 °C y luego se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con agua (50 mL) y se extrajo con DCM (5 x 100 mL). Las capas orgánicas combinadas se lavaron con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se lavó con éter dietílico para proporcionar N'-(6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-iliden)acetohidrazida (5,5 g, 85 %) como un sólido blanco.
Etapa 4: Se tomó N'-(6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-iliden)acetohidrazida (5,5 g, 20,8 mmoles, 1 eq) en un matraz de fondo redondo (50 mL) y luego se enfrió hasta -10 °C. Luego, se añadió oxicloruro de fósforo (18,4 ml, 197,6 mmoles, 9,5 eq) gota a gota al compuesto seguido de la adición gota a gota de TEA (2,9 ml, 20,8 mmoles, 1 eq). Después de eso, la mezcla de reacción se agitó a -10 °C durante 10 minutos y luego 10 minutos a RT
y finalmente se calentó a reflujo durante 4 horas. La mezcla de reacción se enfrió hasta 0 °C y luego se añadió gota a gota hielo triturado con agitación constante. A esta parte acuosa luego se le añadió lentamente una solución fría de amonio (100 mL). La capa acuosa se extrajo con DCM (2 x 100 mL). Las capas orgánicas combinadas se lavaron con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4, anhidro, se concentró a presión reducida para obtener el material crudo. El producto crudo se purificó mediante cromatografía en columna para proporcionar 7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (3,0 g, 59 %) como un sólido amarillo.
Etapa 5: Una solución agitada de 7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a] quinoxalina (4,0 g, 16,2 mmoles, 1 eq) en DMF (40 mL) a -10 °C se trata por partes durante 10 minutos con N-bromosuccinimida sólida (3,1 g, 17,1 mmoles, 1,05 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1,5 horas. La mezcla de reacción se diluyó con EtOAc (300 mL) y las capas orgánicas se lavaron con agua (5 x 50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna para proporcionar 8-bromo-7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (3,3 g, 63 %) como un sólido blanquecino.
Síntesis de 8-bromo-7-fluoro-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-4):
Etapa 1: A una solución de 4-fluoro-2-trifluorometil-fenilamina (50 g, 0,279 moles) en DCM (550 mL) se añadió una solución de Br2 (15,1 ml, 0,29 moles) en DCM (100 mL) gota a gota a 0 °C y la mezcla de reacción resultante se agitó a 0 °C durante 2 horas. La mezcla de reacción se diluyó con agua (1.000 mL) y se extrajo con EtOAc (2 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (2 x 500 mL) seguido de salmuera (250 mL), se secaron sobre Na2SO4 anhidro y se concentraron para proporcionar el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 2-bromo-4-fluoro-6-trifluorometil-fenilamina (50 g, 69,4 %) como un líquido marrón.
Etapa 2: A la suspensión agitada de 2-bromo-4-fluoro-6-trifluorometil-fenilamina (25 g, 0,097 moles) en DMSO seco (375 mL) se añadió ácido 2-amino-2-metil-propiónico (20 g, 0,194 moles) seguido de K3PO4 (41,1 g, 0,194 moles) a RT. La mezcla de reacción resultante se desgasificó con nitrógeno durante 30 minutos, luego se añadió CuCl (0,96 g, 0,0097 moles) y la mezcla de reacción se agitó a 140 °C durante 16 horas. La mezcla de reacción se enfrió hasta RT y se filtró a través de celite. El lecho de celite se lavó con EtOAc (500 mL). El filtrado resultante se vertió en agua helada (1.000 mL). La capa acuosa resultante se extrajo con EtOAc (2 x 250 mL). La parte orgánica total se lavó con agua (2 x 500 mL), salmuera (250 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida para proporcionar el producto crudo que se purificó mediante cromatografía en columna para proporcionar 6-fluoro-3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalin-2-ona (16 g, 63 %) como un sólido marrón.
Etapa 3: A una solución de 6-fluoro-3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalin-2-ona (26 g, 0,0992 moles) en tolueno (390 mL) se añadió reactivo de Lawesson (60,14 g, 0,1488 moles) a RT y la mezcla de reacción se puso a reflujo a 120 °C durante 2 horas. La mezcla de reacción se concentró. El residuo sólido obtenido se inactivó con solución saturada de NaHCO3 (1.500 mL) y la capa acuosa resultante se extrajo con EtOAc (3 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (1.000 mL), salmuera (1.000 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo. El producto crudo obtenido se purificó mediante cromatografía en columna para proporcionar 6-fluoro-3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalina-2-tiona (26 g, 94,3 %) como un sólido amarillo.
Etapa 4: A una solución en agitación de 6-fluoro-3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalina-2-tiona (29,5 g, 0,106 moles) en THF (750 mL) se añadió gota a gota hidrato de hidrazina (15,91 g, 0,318 moles) a 0 °C. La mezcla de reacción se agitó a RT durante 16 horas. Posteriormente, se añadieron TEA (101,19 mL, 0,742 moles) y cloruro de acetilo (30,14 ml, 0,424 moles) a la mezcla de reacción gota a gota a 0 °C y la mezcla se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con agua (500 mL) y se extrajo con MeOH-DCM al 10 % (5 x 500 mL). La parte
orgánica total se lavó con salmuera (250 mL), se secó sobre Na2SO4 y se concentró a presión reducida para proporcionar (6-fluoro-3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalin-2-ilideno)-hidrazida de ácido acético (30 g, 88,9 %) como un sólido blanquecino.
Etapa 5. Se tomó (6-fluoro-3,3-dimetil-8-trifluorometil-3,4-dihidro-1 H-quinoxalin-2-iliden)-hidrazida de ácido acético (17 g, 0,053 moles) en un matraz de fondo redondo y luego se enfrió hasta -10 °C. Luego, se añadió oxalilcloruro de fósforo (24,7 mL, 0,265 moles) gota a gota al compuesto, seguido de la adición gota a gota de TEA (7,36 ml, 0,053 moles). Después de eso, la mezcla de reacción se agitó a -10 °C durante 10 minutos y luego durante 10 minutos a RT y finalmente la mezcla se calentó a reflujo durante 4 horas. La mezcla de reacción se enfrió hasta 0 °C y se inactivó con agua helada triturada (250 mL). La parte acuosa se basificó luego usando solución de amonio fría (250 mL) gota a gota. La capa acuosa básica resultante se extrajo luego con EtOAc (3 x 500 mL). La parte orgánica total se lavó con salmuera (250 mL), se secó sobre Na2SO4 anhidro y se concentró a presión reducida para proporcionar el producto crudo. El producto crudo obtenido se purificó por trituración usando MTBE para proporcionar 7-fluoro-1,4,4-trimetil-9-trifluorometil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (8,5 g, 53 %) como un sólido amarillo.
Etapa 6: A una solución de 7-fluoro-1,4,4-trimetil-9-trifluorometil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (5,9 g, 19,64 mmoles) en DMF (177 mL) se añadió NBS (3,84 g, 21,61 moles) en partes a -10 °C. La mezcla de reacción resultante se agitó a RT durante 16 horas. La mezcla de reacción se diluyó con agua (500 mL) y se extrajo con EtOAc (2 x 750 mL). Las capas orgánicas combinadas se lavaron con agua (750 mL) seguido de salmuera (400 mL), se secaron sobre Na2SO4 anhidro y se concentraron para proporcionar el producto crudo. El producto crudo obtenido se purificó mediante cromatografía en columna para proporcionar 8-bromo-7-fluoro-1,4,4-trimetil-9-trifluorometil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (3 g, 40 %) como un sólido blanquecino.
Síntesis de 8-bromo-9-cloro-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-5):
Etapa 1: A la suspensión agitada de 2-bromo-6-cloro-4-fluoro-fenilamina (75 g, 0,334 moles) en DMSO seco (1.125 mL) se añadió ácido 2-amino-2-metil-propiónico (68,8 g, 0,668 moles) seguido de K3PO4 (141,8 g, 0,668 moles) a RT. La mezcla de reacción resultante se desgasificó con nitrógeno durante 30 minutos, luego se añadió CuCl (6,36 g, 0,0334 moles) y la mezcla de reacción se calentó a 140 °C durante 6 horas. La mezcla de reacción se enfrió hasta RT y se filtró a través de celite. El lecho de celite se lavó con EtOAc (1.500 mL). El filtrado resultante se vertió en agua helada (2.000 mL). La fase acuosa resultante se extrajo con EtOAc (2 x 750 mL). La parte orgánica total se lavó con agua (2 x 1.500 mL), seguido de salmuera (750 mL), se secó sobre Na2SO4 anhidro y se evaporó a presión reducida para proporcionar el producto crudo. El producto crudo se purificó mediante cromatografía en columna para proporcionar 8-cloro-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-ona (40 g, 52,4 %) como un sólido marrón.
Etapa 2: A una solución de 8-cloro-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-ona (25 g, 0,109 moles) en tolueno (375 mL) se añadió reactivo de Lawesson (66,26 g, 0,1639 moles) a Rt y la mezcla de reacción se puso a reflujo a 120 °C durante 2 horas. La mezcla de reacción se concentró. El residuo sólido obtenido se inactivó con solución saturada de NaHCO3 (1.500 mL) y la capa acuosa resultante se extrajo con EtOAc (3 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (750 mL), salmuera (750 mL), se secaron sobre Na2SO4 anhidro y se evaporaron para obtener el producto crudo. El producto crudo obtenido se purificó mediante cromatografía en columna para proporcionar 8-cloro-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalina-2-tiona (24 g, 89,7 %) como un sólido amarillo.
Etapa 3: A una solución agitada de 8-cloro-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalina-2-tiona (28,8 g, 0,118 moles) en THF (750 mL) se añadió gota a gota hidrato de hidrazina (17,7 g, 0,354 moles) a 0 °C. La mezcla de reacción se agitó a RT durante 16 horas. Se añadió TEA (82,4 mL, 0,59 moles) seguido de cloruro de acetilo (25,16 mL, 0,354 moles) a la mezcla de reacción gota a gota a 0 °C y se agitó durante 2 horas a RT. Después de completar el material de partida (controlado por LCMS), la mezcla de reacción se diluyó con agua (500 mL) y se extrajo con MeOH-DCM al 10 % (5 x 500 mL). La parte orgánica total se lavó con salmuera (250 mL), se secó sobre Na2SO4 y se concentró a
presión reducida para proporcionar (8-cloro-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida de ácido acético (30 g, 90 %) como un sólido blanco.
Etapa 4: Se tomó (8-cloro-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida de ácido acético (15 g, 0,052 moles) en un matraz de fondo redondo (500 mL) y luego se enfrió hasta -10 °C. Después, se añadió cloruro de oxalilo de fósforo (24,23 ml, 0,26 moles) gota a gota al compuesto seguido de la adición gota a gota de TEA (7,22 mL, 0,052 moles). Después de eso, la mezcla de reacción se agitó a -10 °C durante 10 minutos y luego durante 10 minutos a RT y finalmente en condiciones de reflujo durante 1,5 horas. Después de completar el material de partida (controlado por LCMS) la mezcla de reacción se enfrió hasta 0 °C y se inactivó con agua helada triturada (250 mL). La parte acuosa se basificó luego usando solución de amonio fría (250 mL) gota a gota. La capa acuosa básica resultante se extrajo luego con EtOAc (3 x 500 mL). La parte orgánica total se lavó con salmuera (250 mL), se secó sobre Na2SO4 anhidro y se concentró a presión reducida para proporcionar el compuesto crudo. El producto crudo obtenido se purificó por trituración usando MTBE para proporcionar 9-cloro-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (8,6 g, 61 %) como un sólido blanquecino.
Etapa 5. A una solución de 9-cloro-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (15 g, 0,056 moles) en DMF (450 mL) se añadió NBS (10,9 g, 0,0616 moles) por partes a -10 °C. La mezcla de reacción resultante se agitó a RT durante 16 horas. Después de completar el material de partida (controlado por LCMS), la mezcla de reacción se diluyó con agua (800 mL) y se extrajo con EtOAc (2 x 750 mL). Las capas orgánicas combinadas se lavaron con agua (2 x 750 mL) seguido de salmuera (400 mL), se secaron sobre Na2SO4 anhidro y se concentraron para proporcionar el compuesto crudo. El producto crudo obtenido se purificó mediante cromatografía en columna para proporcionar 8-bromo-9-cloro-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (12,1 g, 62 %) como un sólido blanquecino.
Síntesis de 8-bromo-1-etil-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-6):
Etapa 1: A una solución en agitación de 6-fluoro-3,3,8-trimetil-3,4-dihidro-1H-quinoxalina-2-tiona (10 g, 0,0445 moles) en THF (250 mL) se añadió gota a gota hidrato de hidrazina (6,69 g, 0,1337 moles) a 0 °C. La mezcla de reacción se agitó a RT durante 16 horas. Se añadió TEA (30,98 mL, 0,2229 moles) seguido de la adición gota a gota de cloruro de propionilo (11,67 mL, 0,1337 moles) a 0 °C y la mezcla se agitó durante 2 horas a RT. Después de completar el material de partida (controlado por LCMS), la mezcla de reacción se diluyó con agua (250 mL) y se extrajo con MeOH-DCM al 10 % (5 x 250 mL). La parte orgánica total se lavó con salmuera (250 mL), se secó sobre Na2SO4 y se concentró a presión reducida para proporcionar (6-fluoro-3,3,8-trimetil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida de ácido propiónico (12 g, 96,7 %) como un sólido blanquecino.
Etapa 2: Se tomó (6-fluoro-3,3,8-trimetil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida de ácido propiónico (12 g, 0,0431 moles) en un matraz de fondo redondo y luego se enfrió hasta -10 °C. Luego, se añadió oxalilcloruro de fósforo (20,1 mL, 0,2158 moles) gota a gota al compuesto, seguido de la adición gota a gota de TEA (6 mL, 0,0431 moles). Después de eso, la mezcla de reacción se agitó a -10 °C durante 10 minutos y luego durante 10 minutos a RT y finalmente en condiciones de reflujo durante 4 horas. Después de completar el material de partida (controlado por LCMS), la mezcla de reacción se enfrió hasta 0 °C y se inactivó con agua helada triturada (250 mL). La parte acuosa se basificó luego usando solución de amonio fría (250 mL) gota a gota. La capa acuosa básica resultante se extrajo luego con EtOAc (3 x 500 mL). La parte orgánica total se lavó con salmuera (250 mL), se secó sobre Na2SO4 anhidro y se concentró a presión reducida para proporcionar el compuesto crudo. El producto crudo obtenido se purificó por trituración usando MTBE para proporcionar 1-etil-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (6,5 g, 58 %) como un sólido blanquecino.
Etapa 3: A una solución de 1-etil-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (7,5 g, 0,0288 moles) en DMF (180 mL) se añadió NBS (5,3 g, 0,0302 moles) por partes a -10 °C. La mezcla de reacción resultante se agitó a RT durante 4 horas. Después de completar el material de partida (controlado por LCMS), la mezcla de reacción se diluyó con agua (500 mL) y se extrajo con EtOAc (2 x 250 mL). Las capas orgánicas combinadas se lavaron con agua (500 mL) seguido de salmuera (400 mL), se secaron sobre Na2SO4 anhidro y se concentraron para proporcionar el compuesto crudo. El producto crudo obtenido se purificó mediante cromatografía en columna para proporcionar 8-bromo-1-etil-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (3,8 g, 38 %) como un sólido blanquecino.
Síntesis de 8-bromo-9-etil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-8):
apa-: -.-
NBS/DMF
u C
Etapa 1: La solución agitada de 2-bromo-4-fluoro-1-nitrobenceno (5,0 g, 22,52 mimóles, 1 eq) en tolueno (110 mL) se desgasificó con Ar durante 20 minutos. A la solución anterior, se añadió butilo terciario de vinil estaño (7,8 g, 24,77 mimóles, 1,1 eq) y Pd(PPh3)4 (0,832 ml, 0,72 mmoles, 0,05 eq), luego se agitó durante 48 horas a 90 °C y 24 horas a RT. El disolvente se evaporó y el residuo se disolvió en EtOAc (500 mL). La capa orgánica se lavó con agua y luego con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400 EtOAc al 5 %/hexano; valor Rf-0,4) para proporcionar 4-fluoro-1-nitro-2-vinilbenceno (3,5 g, 93 %) como un sólido marrón que aún incluía algunos reactivos y material de partida de estaño (no se eliminaron por completo).
Etapa 2: La solución agitada de 4-fluoro-1-nitro-2-vinilbenceno (6,0 g) en EtOH (400 mL) se desgasificó con Ar durante 20 minutos. A la solución anterior se añadió Pd/C (50 % de humedad) (1,0 g, 20 %), se purgó con hidrógeno en agitador Parr a 60 psi durante 1 hora. El disolvente se evaporó y el residuo se disolvió en EtOAc (500 mL). La capa orgánica se lavó con agua muchas veces y luego con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400; EtoAc al 10 %/hexano; valor Rf-0,4) para proporcionar 2-etil-4-fluoroanilina (2,0 g, 99 %) como un sólido marrón claro que aún incluía un poco de material de partida.
Etapa 3: Una solución agitada de 2-etil-4-fluoroanilina (0,6 g, 4,314 mmoles, 1 eq) en DCM (40 mL) a -10 °C se trató por partes con N-bromosuccinimida sólida (0,844 g, 4,745 mmoles, 1,1 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1,5 horas. La mezcla de reacción se diluyó con DCM (100 mL) y la capa orgánica se lavó con agua (2 x 50 mL), salmuera (50 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna de gel de sílice (230-400) (EtOAc al 5 %/hexano, valor Rf-0,4)) para proporcionar 2-bromo-6-etil-4-fluoroanilina (0,875 g, 93 %) como un líquido de color rojo.
Etapa 4: Una suspensión de 2-bromo-6-etil-4-fluoroanilina (0,2 g, 0,917 mmoles, 1 eq.), ácido 2-amino-2-metilpropanoico (0,19 g, 1,834 mmoles, 2 eq.), K3PO4 (0,39 g, 1,834 mmoles, 2 eq.) y cloruro cuproso (0,01 g, 0,092 mmoles, 0,1 eq.) en DMSO seco (10 mL) en un tubo sellado se desoxigenaron con Ar durante 20 minutos. Luego, la mezcla de reacción se agitó a 100 °C durante 16 horas. La mezcla de reacción se filtró a través de un lecho de celite y se lavó con EtOAc (50 mL). El filtrado se diluyó con EtOAc (50 mL) y se lavó con agua (3 x 50 mL), salmuera (100 mL), se secó sobre Na2SO4 anhidro y se evaporó a presión reducida para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400; EtOAc al 20 %/hexano; valor Rf-0,4) para proporcionar 8-etil-6-fluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (0,1 g, 49 %) como un sólido marrón.
Etapa 5. A una solución del compuesto 8-etil-6-fluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (1,5 g, 6,76 mmoles, 1 eq.) en tolueno (25 mL) se añadió reactivo de Lawesson (2,7 g, 6,76 mmoles, 1,0 eq.) a RT y la mezcla de reacción se puso a reflujo a 120 °C durante 40 minutos. La mezcla de reacción se inactivó con solución saturada de NaHCO3 (100 mL) seguido de extracción con EtOAc (2 x 100 mL). La capa orgánica combinada se lavó con agua (100 mL), salmuera (100 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400; EtOAc al 20 %/hexano; valor Rf-0,4) para
proporcionar 8-etil-6-fluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (1,5 g, 93 %) como un sólido amarillo.
Etapa 6: A una solución en agitación de 8-etil-6-fluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (0,5 g, 2,1 mmoles, 1 eq) en THF (30 mL) se añadió gota a gota hidrato de hidrazina (1 mL, 31,2 mmoles, 14 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 16 horas a RT. Luego, se añadió TEA (1,5 mL, 10,50 mmoles, 5 eq) a la mezcla de reacción y se agitó durante otros 10 minutos. Se añadió cloruro de acetilo (0,85 mL, 10,50 mmoles, 5 eq) a la mezcla de reacción muy lentamente a 0 °C y luego se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con agua (50 mL) y se extrajo con DCM (5 x 100 mL). La capa orgánica combinada se lavó con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se purificó mediante lavado con éter dietílico para proporcionar N'-(8-etil-6-fluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-iliden)acetohidrazida (1,55 g, 89 %) como un sólido blanco.
Etapa 7: A N'-(8-etil-6-fluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-iliden)acetohidrazida (2,05 g, 7,37 mmoles, 1 eq.) se añadió POCb (7,1 mL) a 0 °C. A la mezcla se añadió TEA (1,0 mL) y se agitó durante 5 minutos a 0 °C. La mezcla de reacción se llevó gradualmente a RT y luego se puso a reflujo durante la noche. Una vez completada la reacción, la mezcla de reacción se enfrió hasta 0 °C y se añadió por partes a una solución acuosa de amoniaco enfriada (0 °C) con agitación vigorosa. Después de la neutralización, se extrajo con DCM (3 x 100 mL). La capa orgánica combinada se lavó con agua (2 x 25 mL), salmuera (25 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 100-200, EtOAc, valor Rf-0,4) para proporcionar 9-etil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1 g, 52 %) como un sólido amarillo.
Etapa 8: Una solución agitada de 9-etil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,1 g, 3,84 mmoles, 1 eq.) en DMF (20 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (0,684 g, 0,47 mmoles, 1 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1 hora. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con EtOAc (50 mL) y la capa orgánica se lavó con agua (5 x 10 mL), salmuera (20 mL), se secó sobre Na2SO4 anhidro y se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 230-400; MeOH al 5 %/DCM; valor Rf-0,3) para proporcionar 8-bromo-9-etil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1,2 g, 93 %) como un sólido blanquecino.
1H-RMN (400 MHz; DMSO-D6, 20 °C): 86,93 (s, 1H), 6,78-6,81 (1H), 2,80-2,93 (2H), 2,38 (s, 3H), 1,43 (bs, 6H), 0,95 0,98 (3H).
Síntesis de 1-bencil-8-bromo-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-13):
Etapa 1: A una solución de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (1,5 g, 6,571 mmoles, 1 eq) en n-BuOH (25 mL) se añadió 2-fenilacetohidrazida (3,25 g, 21,685 mmoles, 3,3 eq) seguido de la adición de ácido acético (2,5 mL) y luego la mezcla de reacción se agitó a 140 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (50 mL) y se extrajo con EtOAc (2 x 50 mL). Las capas orgánicas combinadas se lavaron con agua (50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna combiflash (MeOH al 7 %/DCM; valor Rf-0,3) para proporcionar 1-bencil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1 g, 47 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 1-bencil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1,0 g, 3,067 mmoles, 1 eq.) en DMF (8 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (0,573 g, 3,22 mmoles, 1,05 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1,5 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con EtOAc (100 mL) y las capas orgánicas se lavaron con agua (5 x 20 mL), salmuera (20 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna combiflash (MeOH al 5
%/DCM; valor Rf-0,3) para proporcionar 1-bencil-8-bromo-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,8 g, 64,5 %) como un sólido blanquecino.
1H-RMN (400 MHz; DMSO-D6, 20 °C): 87,15-7,26 (4H), 7,03-7,06 (2H), 6,72 (d, 1H), 4,36 (d, 2H), 1,48 (s, 6H).
Síntesis de 8-bromo-7,9-difluoro-4,4-dimetil-1-(piridin-4-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-14):
Etapa 1: A una solución de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (1,5 g, 6,5 mmoles, 1 eq.) en n-BuOH (50 mL) se añadió hidrazida de ácido piridin-4-il-acético (3,27 g, 21 mmoles, 3,3 eq) seguido de la adición de ácido acético (5 mL) y luego la mezcla de reacción se agitó a 140 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (100 mL) y se extrajo con EtOAc (2 x 100 mL), las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 100-200, MeOH al 10 %/DCM, valor Rf-0,5) para proporcionar 7,9-difluoro-4,4-dimetil-1-(piridin-4-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1 g, 47 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 7,9-difluoro-4,4-dimetil-1-(piridin-4-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1 g, 3,05 mmoles, 1 eq.) en DMF (30 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (0,598 g, 3,36 mmoles, 1,1 eq.). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (100 mL) y se extrajo con EtOAc (3 x 50 mL). Las capas orgánicas combinadas se lavaron con agua (50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 100-200, MeOH/DCM al 10 %; valor Rf-0,4) para proporcionar 8-bromo-7,9-difluoro-4,4-dimetil-1-(piridin-4-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,48 g, 39 %) como un sólido marrón.
1H-RMN (400 MHz; DMSO-D6, 20 °C): 88,38-8,41 (2H), 7,55 (d, 1H), 7,55 (d, 1H), 7,29 (dd, 1H), 7,24 (s, 1H), 6,77 (d, 1H), 4,34-4,36 (2H), 1,49 (s, 6H).
Síntesis de 8-bromo-7,9-difluoro-4,4-dimetil-1-(piridin-3-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-15):
Etapa 1: A una solución de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (1,5 g, 6,5 mmoles, 1 eq.) en n-BuOH (50 mL) se añadió el compuesto hidrazida de ácido piridin-3-il-acético (3,27 g, 21 mmoles, 3,3 eq) seguido de
la adición de ácido acético (5 mL) y luego la mezcla de reacción se agitó a 140 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (100 mL) y se extrajo con EtOAc (2 x 100 mL), la capa orgánica combinada se lavó con agua (100 mL), salmuera (100 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 100-200, MeOH al 10 %/DCM, valor Rf-0,5) para proporcionar 7,9-difluoro-4,4-dimetil-1-(piridin-3-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,3 g, 47 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 7,9-difluoro-4,4-dimetil-1-(piridin-3-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1 g, 3,05 mmoles, 1 eq.) en DMF (30 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (0,598 g, 3,36 mmoles, 1,1 eq.). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (100 mL) y se extrajo con EtOAc (3 x 50 mL). Las capas orgánicas combinadas se lavaron con agua (50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y se evaporaron a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 100-200, MeOH al 10 %/DCM valor Rf-0,4) para proporcionar 8-bromo-7,9-difluoro-4,4-dimetil-1-(piridin-3-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,8 g, 65 %) como un sólido marrón.
1H-RMN (400 MHz; DMSO-D6, 20 °C): 88,44 (d, 1H), 7,25 (s, 1H), 7,14 (d, 2H), 6,76 (d, 1H), 4,37-4,39 (2H), 1,49 (s, 6H), 1,123 (s, 3H).
Síntesis de 8-bromo-7,9-difluoro-4,4-dimetil-1-(piridin-2-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-16):
Etapa 1: A una solución de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (1,5 g, 6,5 mmoles, 1 eq.) en n-BuOH (50 mL) se añadió el compuesto hidrazida de ácido piridin-2-il-acético (3,27 g, 21 mmoles, 3,3 eq) seguido de la adición de ácido acético (5 mL) y luego la mezcla de reacción se agitó a 140 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (100 mL) y se extrajo con EtOAc (2 x 100 mL), la capa orgánica combinada se lavó con agua (100 mL), salmuera (100 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 100-200, MeOH al 10%/DCM, valor Rf-0,5) para proporcionar 7,9-difluoro-4,4-dimetil-1-(piridin-2-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,3 g, 14 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 7,9-difluoro-4,4-dimetil-1-(piridin-2-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1 g, 3,05 mmoles, 1 eq.) en DMF (30 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (0,598 g, 3,36 mmoles, 1,1 eq.). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (100 mL) y se extrajo con EtOAc (3 x 50 mL). Las capas orgánicas combinadas se lavaron con agua (50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 100-200, MeOH al 10 %/DCM valor Rf-0,4) para proporcionar 8-bromo-7,9-difluoro-4,4-dimetil-1-(piridin-2-ilmetil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,3 g, 56 %) como un sólido marrón.
Síntesis de 8-bromo-7-fluoro-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-17):
Etapa 1: A una solución en agitación de 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (4,5 g, 20,09 mimóles, 1 eq) en ciclohexanol (20 mL) se añadió 2-metoxiacetohidrazida (2,5 g, 24,10 mimóles, 1,2 eq). Luego, la mezcla de reacción se agitó a 160 °C durante 6 horas. La mezcla de reacción se enfrió hasta RT, se diluyó con EtOAc (100 mL) y se lavó con agua (2 x 50 mL) seguido de salmuera (50 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna de gel de sílice (230-400) (MeOH al 5 %/DCM, valor Rf-0,4) para proporcionar 7-fluoro-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalina (1,1 g, 20 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de 7-fluoro-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1,1 g, 3,96 mmoles, 1 eq) en DMF (12 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (0,744 g, 4,18 mmoles, 1,05 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1,5 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con EtOAc (100 mL) y las capas orgánicas se lavaron con agua (5 x 30 mL), salmuera (30 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna de gel de sílice (230 400) (MeOH al 5 %/DCM, valor Rf-0,3) para proporcionar 8-bromo-7-fluoro-1-(metoximetil)-4,4,9-trimetilo-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalina (1,0 g, 71 %) como un sólido blanquecino.
Síntesis de (8-bromo-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-1-il)MeOH (intermedio B-18):
Etapa 1: A una solución en agitación de 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (véase el ejemplo 69 para la síntesis) (7,7 g, 34,37 mmoles, 1 eq) en ciclohexanol (34,4 mL) se añadió 2-hidroxiacetohidrazida (3,77 g, 42,25 mmoles, 1,2 eq). La mezcla de reacción se agitó a 160 °C durante 6 horas. La mezcla de reacción se enfrió hasta RT, se diluyó con EtOAc (34,4 mL) y se lavó con agua (2 x 50 mL) seguido de salmuera (50 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna de gel de sílice (230-400) (MeOH al 5 %/DCM, valor Rf-0,3) para proporcionar (7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-1-il)MeOH (0,95 g, 11 %) como un sólido blanquecino.
Etapa 2: Una solución agitada de (7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-1-il)MeOH (1,745 g, 6,66 mmoles, 1 eq) en DMF (25 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (1,24 g, 6,99 mmoles, 1,05 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1,5 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con EtOAc (150 mL) y las capas orgánicas se lavaron con agua (5 x 30 mL), salmuera (30 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna de gel de sílice (230 400) (MeOH al 5 %/DCM, valor Rf-0,3) para proporcionar (8-bromo-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-1-il)MeOH (1,45 g, 63,8 %) como un sólido blanquecino.
S ín te s is d e 1 -(8 -b ro m o -7 - f lu o ro -4 ,4 ,9 - t r im e t i l -4 ,5 -d ih id ro -[1 ,2 ,4 ] t r ia z o lo [4 ,3 -a ]q u in o x a lin -1 - i l) e ta n o l ( in te rm e d io B -19 ) :
Etapa 1: A una solución en agitación de 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (6,5 g, 29 mimóles, 1 eq) en THF (36 mL) se añadió gota a gota hidrato de hidrazina (7,25 mL, 145 mimóles, 5 eq) a 0 °C. La mezcla de reacción se agitó durante 16 horas a RT. Se añadió TEA (19,73 mL, 145 mmoles, 5 eq) a la mezcla de reacción y se agitó durante otros 10 minutos. Se añadió cloruro de 2-(benciloxi)propanoilo (7,5 mL, 72,5 mmoles, 2,5 eq) a la mezcla de reacción muy lentamente a 0 °C y luego se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con agua (50 mL) y se extrajo con DCM (3 x 100 mL). Las capas orgánicas combinadas se lavaron con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se purificó mediante lavado con éter dietílico para proporcionar 2-(benciloxi)-N'-(6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-iliden)propanohidrazida (7,5 g, 67 %) como un sólido blanquecino.
Etapa 2: Se tomó 2-(benciloxi)-N'-(6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-iliden)propanohidrazida (2,5 g, 6,51 mmoles, 1 eq) en un matraz de fondo redondo (50 mL) y luego se enfrió hasta -10 °C. Luego, se añadió oxicloruro de fósforo (6,23 mL, 65,1 mmoles, 10 eq) gota a gota al compuesto seguido de la adición gota a gota de TEA (0,903 mL, 6,51 mmoles, 1 eq). Después de eso, la mezcla de reacción se agitó a -10 ° C durante 10 minutos y luego 10 minutos a RT y finalmente en condiciones de reflujo durante 4 horas. La mezcla de reacción se enfrió hasta 0 °C y luego se añadió gota a gota a hielo triturado con agitación constante. A esta parte acuosa se le añadió lentamente una solución fría de amonio (100 mL). La parte acuosa se extrajo con DCM (2 x 100 mL). Las capas orgánicas combinadas se lavaron con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400, MeOH al 5 %/DCM, valor Rf-0,4) para proporcionar 1-(1-(benciloxi)etil)-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1,0 g, 42 %) como un sólido amarillo.
Etapa 3: Una solución en agitación de 1-(1-(benciloxi)etil)-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (2,5 g, 6,83 mmoles, 1 eq) en MeOH (250 mL) se desoxigenó bien con Ar durante 10 minutos. Se añadió Pd/C (0,5 g) a la mezcla de reacción y la mezcla se desoxigenó de nuevo durante 10 minutos. Finalmente, la mezcla de reacción se colocó en un aparato par. La mezcla de reacción se agitó a RT durante 24 horas bajo atmósfera de hidrógeno a 50 psi. La mezcla de reacción se filtró a través de un lecho de celite y se lavó con MeOH (100 mL), el filtrado se concentró a presión reducida para obtener 1-(7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-1-il)etanol puro (1,0 g, 53 %) como un sólido blanco.
Etapa 4: Una solución agitada de 1-(7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-1-il)etanol (1,0 g, 3,8 mmoles, 1 eq) en DMF (15 mL) a -10 °C se trató por partes durante 10 minutos con N-bromosuccinimida sólida (0,71 g, 3,99 mmoles, 1,05 eq). La mezcla de reacción se dejó calentar hasta RT y se agitó durante 1,5 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con EtOAc (100 mL) y las capas orgánicas se lavaron con agua (5 x 30 mL), salmuera (30 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna de gel de sílice (230 400) (MeOH al 5 %/DCM, valor Rf-0,3) para proporcionar 1-(8-bromo-7-fluoro-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-1-il)etanol (0,95 g, 70 %) como un sólido blanquecino.
S ín te s is d e 8 -b ro m o -7 - f lu o ro -1 -(2 -m e to x ie t i l) -4 ,4 ,9 - t r im e t i l -4 ,5 -d ih id ro -[1 ,2 ,4 ] t r ia z o lo [4 ,3 -a ]q u in o x a lin a (in te rm e d io B -20 ) :
Etapa 1: A una solución en agitación de 6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (3,0 g, 13,5 mimóles, 1 eq) en THF (18 mL) se añadió gota a gota hidrato de hidrazina (3 mL, 67,56 mimóles, 5 eq) a 0 °C. Luego, la mezcla de reacción se agitó durante 16 horas a RT. Se añadió TEA (15 mL, 94,57 mmoles, 7 eq) a la mezcla de reacción y se agitó durante otros 10 minutos. Se añadió cloruro de 3-metoxipropanoilo (4,9 g, 40,5 mmoles, 3 eq) muy lentamente a 0 °C y luego se agitó durante 2 horas a RT. La mezcla de reacción se diluyó con agua (50 mL) y se extrajo con DCM (3 x 100 mL). Las capas orgánicas combinadas se lavaron con salmuera (100 mL). La capa orgánica se secó sobre Na2SO4, se concentró a presión reducida para obtener el material crudo que se purificó mediante lavado con éter dietílico para proporcionar N'-(6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-iliden)-3-metoxipropanohidrazida (2,5 g, 60 %) como un sólido blanquecino.
Etapa 2 y Etapa 3: N'-(6-fluoro-3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-iliden)-3-metoxipropanohidrazida se convirtió en el intermedio B-20 siguiendo la ruta sintética general descrita para el intermedio B-12 (etapa 2 y etapa 3).
1H-RMN (400 MHz; DMSO-D6, 20 °C): 86,81-6,87 (2H), 3,60 (m, 2H), 3,15 (s, 3H), 2,37 (s, 3H), 1,20-1,65 (8H).
Síntesis de 8-bromo-1-(ciclopropilmetil)-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-21):
Etapa 1: A una solución de 7-bromo-6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (4 g, 13,79 mmoles, 1 eq.) en tolueno (50 mL) se añadió reactivo de Lawesson (8,36 g, 20,69 mmoles, 1,5 eq.) a RT y la mezcla de reacción se puso a reflujo a 120 °C durante 40 minutos. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se inactivó con solución saturada de NaHCO3 (50 mL) seguido de extracción con EtOAc (3 x 75 mL). Las capas orgánicas combinadas se lavaron con agua (100 mL), salmuera (100 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 100-200; EtOAc al 15 %/hexano; valor Rf-0,3) para proporcionar 7-bromo-6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (3,1 g, 73 %) como un sólido amarillo.
Etapa 2: A una solución de 7-bromo-6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (0,5 g, 1,63 mmoles, 1 eq) en n-BuOH (10 mL) se añadió 2-ciclopropilacetohidrazida (0,614 g, 5,39 mmoles, 3,3 eq) seguido de la adición de ácido acético (1 mL) y luego la mezcla de reacción se agitó a 140 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluyó con agua (20 mL) y se extrajo con EtOAc (3 x 30 mL). Las capas orgánicas combinadas se lavaron con agua (30 mL), salmuera (30 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 100-200; EtOAc; valor Rf-0,2) para proporcionar 8-bromo-1-(ciclopropilmetil)-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,35 g, 79 %) como un sólido blanco.
S ín te s is d e 8 -b ro m o -1 -c ic lo p ro p il-7 ,9 -d if lu o ro -4 ,4 -d im e t i l- 4 ,5 -d ih id ro -[1 ,2 ,4 ] t r ia z o lo [4 ,3 -a ]q u in o x a lin a ( in te rm e d io B-22 ) :
A partir de 7-bromo-6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona y ciclopropanocarbohidrazida, se sintetizó el Intermedio B-22 en analogía con la síntesis descrita para el Intermedio B-21 (Etapa 2).
Síntesis de 8-bromo-1,4,4,9-tetrametil-7-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-23):
A partir de 2-bromo-6-metil-4-(trifluorometil)anilina, se sintetizó el intermedio B-23 en analogía con la síntesis descrita para el intermedio B-4 (etapa 2 a etapa 6).
Los intermedios de la Tabla 3 se sintetizaron en analogía con la síntesis representada en el Esquema de Reacción 1:
Síntesis de 8-bromo-9-(difluorometil)-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-28):
Etapa 1: A una solución agitada de 5-fluoro-2-nitro-benzaldehído (20,0 g, 118,27 mimóles) en DCM (600 mL) se añadió DAST (23,3 ml, 177,51 mimóles) a 0 °C. La mezcla de reacción se agitó a temperatura ambiente durante 4 horas. Una vez completada la reacción, la mezcla de reacción se inactivó con solución saturada de NaHCO3 y se extrajo con DCM (2 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (500 mL) seguido de salmuera (500 mL), luego se secaron sobre Na2SO4 anhidro y se concentraron. El material crudo se purificó mediante cromatografía en columna usando EtOAc al 2-3 %/hexano para proporcionar 2-difluorometil-4-fluoro-1-nitro-benceno (22,0 g, 88 %) como un líquido amarillo.
Etapa 2: A una solución agitada de 2-difluorometil-4-fluoro-1-nitro-benceno (22,0 g, 115,16 mmoles) en etanol (372 mL) se añadió SnCb-2 H2O (103,7 g, 460,46 mmoles) seguido de HCI concentrado (76 mL) a 0 oC. La mezcla de reacción se agitó a temperatura ambiente durante 2 horas. Una vez completada la reacción, la mezcla de reacción se concentró, el residuo se basificó con solución de NaOH 5N y se extrajo con MTBE (2 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (500 mL) seguido de salmuera (500 mL), se secaron sobre Na2SO4 anhidro y se concentraron. El material crudo se purificó mediante cromatografía en columna usando EtOAc al 2-3 %/hexano para proporcionar 2-difluorometil-4-fluoro-fenilamina (12,5 g, 41 %) como un líquido amarillo gomoso.
Etapa 3: A una solución de 2-difluorometil-4-fluoro-fenilamina (8,0 g, 49,64 mmoles) en DCM (150 mL) se añadió una solución de bromo (3,84 mL, 74,47 mmoles) en DCM (100 mL) gota a gota a 0 °C. La mezcla de reacción resultante se agitó a temperatura ambiente durante 16 horas. Una vez completada la reacción (controlada por TLC en EA al 10 %- Hexano, Rf= 0,7), la mezcla de reacción se inactivó con una solución saturada de NaHCO3. Las dos capas se separaron, la capa acuosa se extrajo luego con DCM (2 x 200 mL). Las capas orgánicas combinadas se lavaron con agua (2 x 500 ml) y salmuera (250 ml) y luego se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida. Tres lotes de esta reacción se realizaron en paralelo, que luego se combinaron para proporcionar el compuesto crudo. Este material crudo combinado se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y EtOAc al 5 %/hexano como eluyente) para proporcionar 2-bromo-6-difluorometil-4-fluoro-fenilamina (18,0 g, 51 %) como un sólido blanco.
Etapa 4: A la suspensión agitada de 2-bromo-6-difluorometil-4-fluoro-fenilamina (18,0 g, 73,77 mmoles) en DMSO seco (270 mL) se añadió ácido 2-amino-2-metil-propiónico (15,2 g, 147,54 mmoles) seguido de K3PO4 (31,31 g, 147,54 mmoles) a temperatura ambiente. La mezcla de reacción resultante se desgasificó con nitrógeno durante 30 minutos, luego se añadió cloruro cuproso (730 mg, 7,37 mmoles) y la mezcla de reacción se calentó a 125 °C durante 16 horas. Una vez completada la reacción (controlada por TLC, Ea al 20 %-Hexano, Rf 0,4), la mezcla de reacción se enfrió hasta temperatura ambiente y se filtró a través de celite. El lecho de celite se lavó con EtOAc (2 x 200 mL). El filtrado resultante se vertió en agua helada (500 mL). La capa acuosa resultante se extrajo con EtOAc (2 x 250 mL). Las capas orgánicas combinadas se lavaron con agua (3 x 200 mL) y salmuera (400 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida para proporcionar la mezcla cruda. La mezcla cruda se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y EtOAc al 15 %/hexano como eluyente) para proporcionar 8-difluorometil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-ona (9,0 g, 50 %) como un sólido marrón.
Etapa 5: A una solución agitada de 8-difluorometil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-ona (9,0 g, 36,88 mmoles) en tolueno (300 ml) se añadió reactivo de Lawesson (22,39 g, 55,32 mmoles) a temperatura ambiente y la mezcla de reacción se calentó luego a 120 °C durante 3 horas. Una vez completada la reacción (controlada por TLC en EA al 20 %-Hexano, Rf 0,6), la mezcla de reacción se enfrió hasta temperatura ambiente y luego se concentró a
presión reducida. El residuo obtenido se inactivó con solución saturada de NaHCO3 (500 ml) y la capa acuosa resultante se extrajo con EtOAc (3 x 250 ml). Las capas orgánicas combinadas se lavaron con agua (500 ml) y salmuera (250 ml), se secaron sobre Na2SO4 anhidro y luego se evaporaron a sequedad a presión reducida. El material crudo se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y EtOAc al 20 %/hexano como eluyente) para proporcionar 8-difluorometil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalina-2-tiona (9,0 g, 94 %) como un sólido amarillo.
Etapa 6: A una solución agitada de 8-difluorometil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalina-2-tiona (9,0 g, 34,57 mmoles) en THF (60 ml) se añadió gota a gota hidrato de hidrazina (5,19 g, 103,73 mmoles) a 0 °C. La mezcla de reacción se agitó a temperatura ambiente durante 16 horas. Se añadió TEA (24,2 ml, 172,89 mmoles) seguido de cloruro de acetilo (7,4 ml, 103,73 mmoles) a la mezcla de reacción gota a gota a 0 °C y la mezcla de reacción resultante se agitó luego durante 2 horas a temperatura ambiente. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua y se extrajo con MeOH al 10 %-DCM (5 x 100 ml). Las capas orgánicas combinadas se lavaron con salmuera, se secaron sobre Na2SO4 y se concentraron a presión reducida para proporcionar (8-difluorometil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida del ácido acético (9,0 g, 87 %, en crudo) como un sólido amarillo pálido.
Etapa 7: Se enfrió (8-difluorometil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida del ácido acético (9,0 g, 30 mmoles) en un matraz de fondo redondo hasta -10 °C. Se añadió oxalilcloruro de fósforo (13,98 ml, 150 mmoles) gota a gota, seguido de la adición gota a gota de trietil amina (4,2 ml, 30 mmoles). La mezcla de reacción se agitó a -10 °C durante 10 minutos y luego durante 10 minutos a RT y finalmente a reflujo durante 2 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se enfrió hasta 0 °C y se inactivó con hielo picado en agua (200 ml). La parte acuosa se basificó luego añadiendo solución acuosa de amoníaco fría (500 ml) gota a gota. La capa acuosa básica resultante se extrajo luego con EtOAc (3 x 250 ml). Las capas orgánicas combinadas se lavaron con salmuera, se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para proporcionar el compuesto crudo. El producto crudo obtenido se codestiló con MTBE dos veces, luego se trituró con hexano y se secó para proporcionar 9-difluorometil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (4,5 g, 53 %) como un sólido amarillo pálido.
Etapa 8: A una solución de 9-difluorometil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (11,0 g, 39,0 mmoles) en DMF (180 mL) se añadió NBS (7,2 g, 40,2 mmoles) por partes a 0 °C. La mezcla de reacción resultante se agitó a 0 °C durante 1 hora. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua (400 mL) y se extrajo con EtOAc (2 x 400 mL). Las capas orgánicas combinadas se lavaron con agua (2 x 200 mL) y salmuera, se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y MeOH al 5 %/DCM como eluyente) para proporcionar 8-bromo-9-difluorometil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (7,2 g, 65 %) como un sólido blanquecino.
1H-RMN (400 MHz, DMSO-d6): 8 = 6,91-6,64 (m, 2H), 4,58 (s, 1H), 2,56 (s, 3H), 1,58 (brs, 3H), 1,24 (brs, 3H).
Síntesis de 8-bromo-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-40):
ntermedio EI-4D
Etapa 1: Una suspensión de 2-bromo-6-metilanilina (1,0 g, 54,0 mmoles, 1,0 eq) y ácido 2-aminobutírico (1,1 g, 10,8 mmoles, 2,0 eq) en DMSO (10 ml) en un tubo sellado se desoxigenó con Ar durante 20 minutos. Luego, se añadieron K3PO4 (2,3 g, 10,8 mmoles, 2,0 eq) y CuCl (53,0 mg, 5,4 mmoles, 0,1 eq). La mezcla de reacción se agitó luego a 140 °C durante 16 horas. Una vez completada la reacción, la mezcla de reacción se filtró a través de un lecho de celite y el lecho de celite se lavó con EtOAc (100 ml). El filtrado se diluyó con EtOAc (100 ml) y se lavó con agua (3 x 150 ml) y salmuera (200 ml), se secó sobre Na2SO4 anhidro y luego se evaporó a presión reducida para obtener el compuesto crudo, que se purificó mediante cromatografía en columna (gel de sílice de malla 100-200; EtOAc al 30 %/hexano; valor Rf-0,4) para proporcionar 3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-ona (0,6 g, 60 %).
Etapa 2: A una solución de 3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-ona (7,0 g, 36,0 mimóles, 1,0 eq) en tolueno (75 ml) se añadió reactivo de Lawesson (22,0 g, 55 mimóles, 1,5 eq.) a temperatura ambiente y luego la mezcla de reacción se puso a reflujo a 120 °C durante 40 minutos. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se inactivó con solución saturada de NaHCO3 (100 ml) seguido de extracción con EtOAc (2 x 100 ml). Las capas orgánicas combinadas se lavaron con agua (100 ml) y salmuera (100 ml), se secaron sobre Na2SO4 anhidro y se evaporaron a presión reducida para obtener el compuesto crudo que se purificó mediante cromatografía en columna (gel de sílice malla 230-400; EtOAc al 20 %/hexano; valor Rf-0,4) para proporcionar 3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (5,0 g, 66 %) como un sólido amarillo.
Etapa 3: A una solución en agitación del compuesto 3,3,8-trimetil-3,4-dihidroquinoxalina-2(1H)-tiona (5,0 g, 62,4 mmoles, 1 eq) en THF (30 ml) se añadió gota a gota hidrato de hidracina (6,0 ml, 121,0 mmoles, 5 eq) a 0 °C. La mezcla de reacción se agitó luego durante 16 horas a temperatura ambiente. Luego, se añadió TEA (16,5 ml, 122,7 mmoles, 5 eq) a la mezcla de reacción y la mezcla de reacción se agitó durante otros 10 minutos. Luego, se añadió cloruro de acetilo (5,65 g, 73,65 mmoles, 3 eq) a la mezcla de reacción muy lentamente a 0 °C y la mezcla de reacción resultante se agitó luego durante 2 horas a temperatura ambiente. La mezcla de reacción se diluyó luego con agua (50 ml) y se extrajo con DCM (5 x 100 ml). Las capas orgánicas combinadas se lavaron con salmuera (100 ml), se secaron sobre Na2SO4 y se concentraron a presión reducida para obtener el material crudo que se purificó mediante lavado con éter dietílico para proporcionar N'-(3,3,8-trimetil-3,4-dihidroquinoxalin-2(1 H)-iliden)acetohidrazida (2,0 g, 34 %) como un sólido blanco.
Etapa 4: Se recogió N'-(3,3,8-trimetil-3,4-dihidroquinoxalin-2(1H)-iliden)acetohidrazida (6,0 g, 24 mmoles, 1 eq) en un matraz de fondo redondo (50 ml) y se luego se enfrió hasta -10 ° C. Luego, se añadió oxicloruro de fósforo (23,0 ml, 243 mmoles, 10 eq) gota a gota al compuesto seguido de la adición gota a gota de TEA (3,5 ml, 24 mmoles, 1 eq). Después de eso, la mezcla de reacción se agitó a -10 °C durante 10 minutos y luego 10 minutos a temperatura ambiente y finalmente a reflujo durante 4 horas. Luego, la mezcla de reacción se enfrió hasta 0 °C y luego se añadió gota a gota en hielo triturado en agua bajo agitación constante. A esto se añadió lentamente una solución fría de amoníaco (100 ml). La parte acuosa se extrajo luego con DCM (2 x 100 mL). Las capas orgánicas combinadas se lavaron con salmuera (100 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para obtener el compuesto crudo, que se purificó mediante cromatografía en columna (gel de sílice malla 230-400, MeOH al 5 %/Dc M; valor Rf-0,4) para proporcionar 1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (3,2 g, 58,6 %) como un sólido amarillo.
Etapa 5: Una solución agitada de 1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (3,2 g, 14 mmoles, 1,00 eq) en DMF (40 ml) a -10 °C se trata con N-bromosuccinimida sólida (2,7 g, 15 mmoles, 1,05 eq) por partes durante 10 minutos. La mezcla de reacción se dejó calentar hasta temperatura ambiente y luego se agitó durante 1,5 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con EtOAc (300 ml) y se lavó con agua (5 x 50 ml) y salmuera (50 ml), se secó sobre Na2SO4 anhidro y se evaporó a presión reducida para obtener el compuesto crudo, que se purificó mediante cromatografía en columna de gel de sílice (230-400) (MeOH al 5 %/DCM, valor Rf- 0,3) para proporcionar 8-bromo-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (2,0 g, 48 %) como un sólido blanquecino.
Síntesis de 8-bromo-9-ciclopropil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-44):
nre rned io El-44
Etapa 1: Se disolvió 2-bromo-4-fluoro-fenilamina (20,0 g, 0,105 moles) en anhídrido acético (10 mL) a 10 °C y se agitó a temperatura ambiente durante 3 horas. Una vez completada la reacción (controlada por TLC, acetato de etilo al 10 %/hexano), la masa de reacción espesa se diluyó con n-hexano y se filtró. El material sólido se lavó con n-hexano y luego se secó en vacío para proporcionar N-(2-bromo-4-fluoro-fenil)-acetamida (20,0 g, 82 %) como un sólido blanquecino.
Etapa 2: A una solución agitada de N-(2-bromo-4-fluoro-fenil)-acetamida (65,0 g, 0,28 moles) en una mezcla de tolueno-agua (1:1, 1,3 L) se añadió triciclohexil fosfina (7,85 g, 0,03 moles) seguido de la adición de K3PO4 (208,2 g, 0,98 moles) a temperatura ambiente. Esta mezcla se desgasificó luego con Ar durante 30 minutos. Se añadió ácido ciclopropil borónico (31,2 g, 0,37 moles) seguido de Pd(OAc)2 (3,2 g, 0,01 moles) y la mezcla de reacción se calentó a 100 °C durante 16 horas. Después de consumir el material de partida (controlado por TLC, EA al 20 %-Hexano, Rf 0,4), la mezcla de reacción se enfrió hasta temperatura ambiente, se diluyó con EtOAc (1 L), se lavó con agua (2 x 500 ml) seguido de salmuera (500 ml) y luego se secó sobre Na2SO4 anhidro y se concentró a presión reducida para proporcionar el compuesto crudo. El compuesto crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y EtOAc al 15-20 %/hexano como eluyente) para proporcionar N-(2-ciclopropil-4-fluoro-fenil)-acetamida (51,5 g, 95 %) como un sólido marronáceo.
Etapa 3: Una suspensión agitada de N-(2-ciclopropil-4-fluoro-fenil)-acetamida (4) (52,0 g, 0,269 moles) en HCl (2,1 L, 2M) se calentó hasta 90 °C durante 16 horas. Una vez completada la reacción (controlada por TLC, EA al 20 %-Hexano, Rf 0,6), se enfrió hasta temperatura ambiente y se basificó a pH ~13-14 con solución de NaOH (2M). La mezcla se extrajo con EtOAc (1 L). La capa orgánica se lavó luego con agua (2 x 500 ml) y salmuera (500 ml), se secó sobre Na2SO4 anhidro y se concentró a presión reducida para proporcionar 2-ciclopropil-4-fluoro-fenilamina (40,0 g, crudo) como un líquido marrón oscuro.
Etapa 4: A una solución agitada de 2-ciclopropil-4-fluoro-fenilamina (20,0 g, 0,132 moles) en DMF (350 ml) se añadió NBS (85,0 g, 0,477 moles) por partes a -10 °C. La mezcla de reacción resultante se agitó a 0 °C durante 1 hora. Una vez completada la reacción (controlada por TLC, EtOAc al 20 %/ hex), la mezcla de reacción se diluyó con agua (1 L) y se extrajo con MTBE (2 x 750 ml). Las capas orgánicas combinadas se lavaron con salmuera fría (3 x 500 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida. El material crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y EtOAc al 5-10 %/hexano como eluyente) para proporcionar 2-bromo-6-ciclopropil-4-fluoro-fenilamina (20,2 g, 65 % en dos etapas) como un líquido marronáceo.
Etapa 5: A una suspensión agitada de 2-bromo-6-ciclopropil-4-fluoro-fenilamina (20,0 g, 86,88 mmoles) en DMSO seco (300 mL) se añadió ácido 2-amino-2-metil-propiónico (17,9 g, 173,94 mmoles) seguido de K3PO4 (36,9 g, 173,94 mmoles) a temperatura ambiente. La mezcla de reacción resultante se desgasificó con Ar durante 30 minutos. Luego, se añadió CuCl (860 mg, 8,69 mmoles) y la mezcla de reacción se calentó hasta 140 °C durante 16 horas. Después del consumo del material de partida (controlado por TLC, EA al 30 %-Hexano, Rf 0,4), la mezcla de reacción se enfrió hasta temperatura ambiente y se filtró a través de un lecho de celite. El lecho de celite se lavó con EtOAc (500 ml). Las capas orgánicas se lavaron con agua (2 x 750 ml) y salmuera (500 ml), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida para proporcionar el material crudo. El material crudo obtenido se purificó mediante cromatografía en columna usando EtOAc al 15-20 %-hexano para proporcionar 8-ciclopropil-6-fluoro-3,3
dimetil-3,4-dihidro-1H-quinoxalin-2-ona (10,1 g, 50 %) como un sólido marrón.
Etapa 6: A una solución de 8-cidopropil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-2-ona (10,0 g, 42,7 mmoles) en tolueno (200 ml) se añadió reactivo de Lawesson (25,9 g, 64,1 mmoles) a temperatura ambiente y la mezcla de reacción se puso a reflujo a 120 °C durante 1 hora. Una vez completada la reacción (controlada por TLC en EA al 20 %-Hexano, Rf 0,7), la masa de reacción se enfrió hasta temperatura ambiente y se inactivó con una solución saturada de NaHCO3 (35 ml). La capa acuosa resultante se extrajo con EtOAc (3 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (500 ml) seguido de salmuera (500 ml), se secaron sobre Na2SO4 anhidro y se concentraron para proporcionar el material crudo. El material crudo obtenido se purificó mediante cromatografía en columna (usando sílice malla 100-200 y EtOAc al 5- 10 %/hexano) para proporcionar 8-ciclopropil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalina-2-tiona (9,5 g, 89 %) como un sólido amarillo.
Etapa 7: A una solución agitada de 8-ciclopropil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalina-2-tiona (9,0 g, 36,0 mmoles) en THF (216 ml) se añadió hidrato de hidrazina (5,3 ml, 108 mmoles) gota a gota a 0 °C. La mezcla de reacción se agitó luego a temperatura ambiente durante 16 horas. Luego, se añadió TEA (30,2 ml, 216,0 mmoles) seguido de cloruro de acetilo (10,3 ml, 144,0 mmoles) a la mezcla de reacción gota a gota a 0 °C y la mezcla de reacción se agitó durante 2 horas a temperatura ambiente. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua (300 ml) y se extrajo con EtOAc (2 x 500 ml). Las capas orgánicas combinadas se lavaron con salmuera (300 ml), se secaron sobre Na2SO4 y se concentraron a presión reducida para proporcionar [8-ciclopropil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-(2E)-iliden]-hidrazida de ácido acético (9,0 g, crudo) como un sólido amarillo pálido.
Etapa 8: Se recogió [8-ciclopropil-6-fluoro-3,3-dimetil-3,4-dihidro-1H-quinoxalin-(2E)-iliden]-hidrazida de ácido acético (6,0 g, 20,66 mmoles) en un matraz de fondo redondo y se enfrió hasta -10 °C. Se añadió oxalilcloruro de fósforo (9,7 ml, 103,32 mmoles) y la mezcla se agitó a -10 °C durante 15 minutos. Se añadió lentamente TEA (2,9 ml, 20,66 mmoles) a la mezcla de reacción a -10 °C y la mezcla se agitó durante 15 minutos. La mezcla de reacción se agitó a continuación a temperatura ambiente durante 15 minutos, seguido de calentamiento a 120 °C durante 1,5 h. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se enfrió hasta temperatura ambiente, se vertió en hielo triturado en agua y se basificó (pH~8-9) usando una solución acuosa de amoníaco. La capa acuosa básica resultante se extrajo con EtOAc (2 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (500 ml) seguido de salmuera (500 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida. El residuo se trituró con MTBE al 50 %-Hexano (50 mL x 2) para proporcionar 9-ciclopropil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalina (5,0 g, crudo) como un sólido amarillo pálido.
Etapa 9: A una solución agitada de 9-ciclopropil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (5,0 g, 18,36 mmoles) en DMF (80 mL) se añadió NBS (3,4 g, 18,91 moles) por partes a -10 °C. La mezcla de reacción resultante se agitó a 0 °C durante 1 hora. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua (250 ml) y se extrajo con EtOAc (2 x 250 ml). Las capas orgánicas combinadas se lavaron con salmuera fría (3 x 250 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida. El material crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y acetona al 30-35 %/hexano como eluyente) para proporcionar 8-bromo-9-ciclopropil-7-fluoro-1,4,4-trimetil-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalina (1,2 g, 17 % en tres etapas) como un sólido blanquecino.
1H-RMN (400 MHz, DMSO-d6): 8 = 6,89 (s, 1H), 6,81-6,79 (t, 1H), 2,50-2,47 (d, 3H), 2,08 (t, 1H), 1,67 (s, 3H), 1,37(bs,1H), 1,10(s,3H), 0,92(b,1H) 0,82 (bs, 1H), 0,01 (bs, 1H).
Síntesis de 8-bromo-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-48):
Etapa 1: A una suspensión agitada de 2-bromo-6-trifluorometil-fenilamina (25,0 g, 0,104 moles) en DMSO seco (375 ml) se añadió ácido 2-amino-2-metil-propiónico (21,5 g, 0,208 moles) seguido de K3PO4 (44,2 g, 0,208 moles) a temperatura ambiente. La mezcla de reacción resultante se desgasificó con nitrógeno durante 30 minutos, luego se añadió cloruro cuproso (1,03 g, 0,010 moles) y la mezcla de reacción se calentó hasta 140 °C durante 6 horas. Una vez completado el material de partida (controlado por TLC, EA al 20 %-Hexano, Rf 0,4), la mezcla de reacción se enfrió hasta temperatura ambiente y se filtró a través de celite. El lecho de celite se lavó con EtOAc (2 x 250 ml). El filtrado resultante se vertió en agua helada (800 ml). La capa acuosa resultante se extrajo con EtOAc (2 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (2 x 650 ml) y salmuera (650 ml), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida para proporcionar el material crudo. El material crudo obtenido se trituró con MTBE-Hexano para proporcionar 3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalin-2-ona (17,0 g, 66 %) como un sólido marrón.
Etapa 2: A una solución de 3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalin-2-ona (17,0 g, 0,07 moles) en tolueno (300 ml) se añadió reactivo de Lawesson (42,6 g, 0,105 moles) a temperatura ambiente y la mezcla de reacción se puso a reflujo a 120 °C durante 2 horas. Una vez completada la reacción (controlada por TLC en EA al 20 %-Hexano, Rf 0,6), la mezcla de reacción se inactivó con solución saturada de NaHCO3 (450 ml) y la capa acuosa resultante se extrajeron con EtOAc (2 x 300 ml). Las capas orgánicas combinadas se lavaron con agua (400 ml) y salmuera (200 ml), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el compuesto crudo. El producto crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 100-200 y EtOAc al 10 %/hexano como eluyente) para proporcionar 3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalina-2-tiona (17,0 g, 94 %) como un sólido amarillo.
Etapa 3: A una solución agitada de 3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalina-2-tiona (17,0 g, 0,065 moles) en THF (500 ml) se añadió hidrato de hidrazina (9,8 g, 0,195 moles) gota a gota a 0 °C. La mezcla de reacción luego se agitó a temperatura ambiente durante 4 horas. Luego, se añadió TEA (63,7 ml, 0,455 moles) seguido de cloruro de acetilo (20,4 g, 0,260 moles) a la mezcla de reacción gota a gota a 0 °C y la mezcla resultante se agitó durante 16 horas a temperatura ambiente. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua (300 ml) y se extrajo con MeOH-DCM al 10% (2 x 300 ml). Las capas orgánicas combinadas se lavaron con salmuera (350 ml), se secaron sobre Na2SO4 y se concentraron a presión reducida para proporcionar (3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida del ácido acético (16,0 g, crudo) como un sólido blanquecino.
Etapa 4: Se recogió (3,3-dimetil-8-trifluorometil-3,4-dihidro-1H-quinoxalin-2-iliden)-hidrazida del ácido acético (16,0 g, 0,053 moles) en un matraz de fondo redondo y luego se enfrió hasta -10 °C. Luego, se añadió oxalilcloruro de fósforo (24,7 ml, 0,265 moles) gota a gota seguido de la adición gota a gota de trietil amina (7,34 ml, 0,053 moles). Después de eso, la mezcla de reacción se agitó a -10 °C durante 10 minutos, luego se dejó con agitación a temperatura ambiente durante 10 minutos y luego se calentó a reflujo durante 4 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se enfrió hasta 0 °C y luego se inactivó con hielo triturado en agua (300 ml). La parte acuosa luego se basificó añadiendo solución de amoniaco fría (150 ml) gota a gota. La capa acuosa básica resultante se extrajo luego con EtOAc (3 x 150 ml). Las capas orgánicas combinadas se lavaron con salmuera (250 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para proporcionar el compuesto crudo. El
producto crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 230-400 y MeOH al 5 %/DCM como eluyente) para proporcionar 1,4,4-trimetil-9-trifluorometil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (5,0 g, 27 % en dos etapas) como un sólido blanquecino.
Etapa 5: A una solución de 1,4,4-trimetil-9-trifluorometil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (4,8 g, 0,017 moles) en DMF (120 ml) se añadió NBS (3,3 g, 0,019 moles) por partes a 0 °C. La mezcla de reacción resultante se agitó a temperatura ambiente durante 16 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua (250 ml) y se extrajo con EtOAc (2 x 150 ml). Las capas orgánicas combinadas se lavaron con agua (2 x 180 ml) y salmuera (200 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para proporcionar el compuesto crudo. El compuesto crudo obtenido se combinó con otro lote de la misma reacción (usando 5,0 g de 1,4,4-trimetil-9-trifluorometil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina) y luego se purificó mediante cromatografía en columna (gel de sílice malla 230-400 y MeOH al 5 %/d CM como eluyente) para proporcionar 8-bromo-1,4,4-trimetil-9-trifluorometil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (5,3 g, 42 % de rendimiento total) como un sólido blanquecino.
1H-RMN (400 MHz, DMSO-d6): 8 = 7,66-7,64 (d, 1H), 7,31 (s, 1H), 7,14-7,12 (d, 1H), 2,34 (s, 3H), 1,70 (s, 3H), 1,21 (s, 3H).
Síntesis de 8-bromo-9-(difluorometil)-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-52):
Etapa 1: A una solución en agitación de ácido 2-amino-3-bromo-benzoico (100,0 g, 0,465 moles) en MeOH (1 L) se añadió H2SO4 concentrado (100 ml) a 0 °C y la mezcla se calentó hasta 80 °C durante 48 horas. Una vez completada la reacción (controlada por TLC, EA al 5 %-Hexano, Rf 0,4), la mezcla de reacción se enfrió hasta temperatura ambiente. La mezcla de reacción luego se concentró a presión reducida, el residuo obtenido se basificó con solución saturada de NaHCO3 (a pH~8-9) y luego se extrajo con EtOAc (2 x 500 ml). Las capas orgánicas combinadas se lavaron con agua (250 ml) y salmuera (250 ml), luego se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para proporcionar éster metílico del ácido 2-amino-3-bromo-benzoico (80,0 g, 75 %) como un sólido marronáceo.
Etapa 2: A una suspensión en agitación de éster metílico del ácido 2-amino-3-bromo-benzoico (30,0 g, 0,131 moles) en DMSO seco (450 ml) se añadió ácido 2-amino-2-metil-propiónico (27,1 g, 0,262 moles) seguido de K3PO4 (55,6 g, 0,262 moles) a temperatura ambiente. La mezcla de reacción resultante se desgasificó con nitrógeno durante 30 minutos, luego se añadió cloruro cuproso (1,29 g, 0,01 moles) y la mezcla de reacción se calentó hasta 140 °C durante 4-5 horas. Una vez completada la reacción (controlada por t Lc , EA al 20 %-Hexano, Rf 0,4), la mezcla de reacción se enfrió hasta temperatura ambiente y se filtró a través de celite. El lecho de celite se lavó con EtOAc (2 x 250 ml). El filtrado resultante se vertió en agua helada (800 ml). La capa acuosa se extrajo con EtOAc (2 x 500 mL). Las capas orgánicas combinadas se lavaron con agua (2 x 650 ml) y salmuera (650 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para proporcionar 2,2-dimetil-3-oxo-1,2,3,4-tetrahidroquinoxalina-5-carboxilato de metilo (3,0 g, crudo). La capa acuosa se acidificó con HCl concentrado (pH~2-3) y luego se extrajo con EtOAc (2 x 500 ml). Las capas orgánicas combinadas se lavaron con salmuera (500 ml), se secaron sobre Na2SO4 anhidro y se evaporaron a presión reducida para producir ácido 2,2-dimetil-3-oxo-1,2,3,4-tetrahidroquinoxalina-5-carboxílico (15,0 g). Este material se disolvió en MeOH (150 ml), seguido de la adición lenta de H2SO4 concentrado (15 ml) a 0 °C. La mezcla de reacción resultante se agitó luego a 90 °C durante 50 horas. La mezcla de reacción se concentró y el residuo obtenido se basificó con solución saturada de NaHCO3 (pH~8-9) y luego se extrajo con EtOAc (2 x 250 ml). Las capas orgánicas combinadas se lavaron con agua (150 ml) y salmuera (150 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para obtener 2,2-dimetil-3-oxo-1,2,3,4-tetrahidroquinoxalina-5-carboxilato de metilo (~13 g, crudo). Los lotes combinados de 2,2-dimetil-3-oxo-1,2,3,4-tetrahidroquinoxalina-5-carboxilato de metilo se trituraron con hexano para proporcionar éster metílico del ácido 2,2-dimetil-3-oxo-1,2,3,4-tetrahidro-quinoxalina-5-carboxílico (13,1 g, 43 %) como un sólido marronáceo.
Etapa 3: A una solución en agitación de éster metílico del ácido 2,2-dimetil-3-oxo-1,2,3,4-tetrahidro-quinoxalina-5-carboxílico (20,0 g, 85,47 mmoles) en tolueno (430 ml) se añadió reactivo de Lawesson (51,9 g, 128,21 mmoles) a temperatura ambiente y luego la mezcla de reacción se calentó a reflujo hasta 120 °C durante 2 horas. Una vez completada la reacción (controlada por TLC en EA al 20 %-Hexano, Rf 0,6), la mezcla de reacción se inactivó con solución saturada de NaHCO3 (500 ml) y la capa acuosa resultante se extrajeron con EtOAc (2 x 400 ml). Las capas orgánicas combinadas se lavaron con agua (500 ml) y salmuera (300 ml), se secaron sobre Na2SO4 anhidro y se concentraron a presión reducida para obtener el compuesto crudo. El producto crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 100-200, EtOAc al 7-8 % en hexano como eluyente) para proporcionar éster metílico del ácido 2,2-dimetil-3-tioxo-1,2,3,4-tetrahidro-quinoxalina-5-carboxílico (16,0 g, 75 %) como un sólido amarillo.
Etapa 4: A una solución en agitación de éster metílico del ácido 2,2-dimetil-3-tioxo-1,2,3,4-tetrahidro-quinoxalina-5-carboxílico (30,0 g, 0,12 moles) en THF (800 ml) se añadió hidrato de hidrazina (10,6 ml, 0,22 moles) gota a gota a 0 °C y la mezcla se agitó luego a temperatura ambiente durante 10 horas. A la mezcla de reacción se añadió luego TEA (60,3 ml, 0,43 moles) gota a gota a 0 °C, seguido de cloruro de acetilo (23,1 ml, 0,32 moles), y la mezcla resultante se agitó durante 4 horas a temperatura ambiente. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua (500 ml) y se extrajo con MeOH-DCM al 10 % (2 x 300 ml). Las capas orgánicas combinadas se lavaron luego con salmuera (350 ml), se secaron sobre Na2SO4 y se concentraron a presión reducida. El compuesto obtenido se purificó luego mediante cromatografía en columna (gel de sílice malla 100-200 y MeOH al 1,5-2 % en DCM como eluyente) para proporcionar éster metílico del ácido 3-(acetil-hidrazono)-2,2-dimetil-1,2,3,4-tetrahidro-quinoxalina-5-carboxílico (20,1 g, 58 %) como un sólido blanquecino.
Etapa 5: Al éster metílico del ácido 3-(acetil-hidrazono)-2,2-dimetil-1,2,3,4-tetrahidro-quinoxalina-5-carboxílico (12,0 g, 41,35 mmoles) se añadió anhídrido acético (200 ml) y la mezcla resultante se calentó hasta 140 °C durante 8 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se concentró a presión reducida. El residuo se diluyó con EtOAc, se lavó con una solución saturada de NaHCO3, se secó sobre Na2SO4 y se concentró a presión reducida. El material crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 100 200 y MeOH al 1,5-2 % en DCM como eluyente) para proporcionar éster metílico del ácido 5-acetil-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carboxílico (5,5 g, 42 %) como un sólido blanquecino.
Etapa 6: Una solución en agitación de éster metílico del ácido 5-acetil-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carboxílico (5,4 g, 0,12 moles) en HCl 6N (200 ml) se calentó hasta 80 °C durante 6 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se concentró, el residuo se sometió a destilación azeotrópica con tolueno (cuatro veces) seguido de trituración con éter-pentano para proporcionar la sal dihidrocloruro del éster metílico del ácido 1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carboxílico (5,2 g, crudo) como un sólido verdoso.
Etapa 7: A una solución en agitación de la sal dihidrocloruro del éster metílico del ácido 1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carboxílico (2,5 g, 7,25 mmoles) en THF (70 ml) se añadió lentamente hidruro de litio y aluminio (18,12 ml, 18,12 mmoles, 2M en THF) a 0 °C y la mezcla de reacción resultante se agitó a temperatura ambiente durante 16 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se inactivó con Na2SO4 saturado y luego se filtró a través de un lecho de celite. El lecho de celite se lavó luego con THF caliente (3 x 50 ml). Los filtrados combinados se concentraron a presión reducida y luego se sometieron a destilación azeotrópica con tolueno (3 x 50 ml) para proporcionar (1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-9-il) metanol (1,9 g, crudo) como un sólido marronáceo.
Etapa 8: Se disolvió (1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-9-il)metanol (2,2 g, 9,01 mimóles) en THF-DCE (1:1, 65 ml). Se añadió dióxido de manganeso (4,7 g, 54,06 mimóles) y la mezcla de reacción resultante se agitó a 80-90 °C durante 48 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se filtró a través de un lecho de celite y el lecho de celite se lavó con THF-DCE (1:1,25 ml). El filtrado combinado se concentró a presión reducida y el material crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 100 200, MeOH al 2-2,5 %-DCM como eluyente) para proporcionar 1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carbaldehído (1,74 g, 80 %) como un sólido blanquecino.
Etapa 9: A una solución en agitación de 1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carbaldehído (2,0 g, 8,25 mmoles) en DMF (30 ml) se añadió NBS (1,5 g, 8,50 mmoles) por partes a 0 °C y la mezcla de reacción resultante se agitó luego a esa temperatura durante 1 hora. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con agua (250 ml) y se extrajo con EtOAc (2 x 150 ml). Las capas orgánicas combinadas se lavaron con agua (2 x 180 ml), se secaron sobre Na2SO4 anhidro y luego se concentraron a presión reducida. El material crudo obtenido se purificó mediante cromatografía en columna (gel de sílice malla 230-400, MeOH al 2-3 % en DCM como eluyente) para proporcionar 8-bromo-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carbaldehído (1,1 g, 42 %) como un sólido marronáceo.
Etapa 10: Se disolvió 8-bromo-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carbaldehído (1,0 g, 3,12 mmoles) en DCM (10 ml) y se enfrió hasta 0 °C. Se añadió DAST (0,61 ml, 1,5 eq) y la mezcla de reacción se agitó a 10-15 °C durante 6 horas. La mezcla de reacción se mantuvo a -20 °C durante 16 horas. La mezcla de reacción se calentó luego hasta 0 °C. Se añadió DAST (0,61 ml, 1,5 eq) y la mezcla de reacción se agitó durante tres horas. Luego, se añadió DAST (0,61 ml, 1,5 eq) y la mezcla de reacción se agitó durante otras tres horas. La mezcla de reacción se inactivó luego con solución saturada de NaHCO3 (pH~8-9) a 0 °C y se extrajo con DCM (50 mL x 2). Las capas orgánicas combinadas se lavaron con agua fría (30 ml) y salmuera (30 ml), se secaron sobre sulfato de sodio y luego se concentraron a presión reducida para obtener el compuesto crudo. La reacción descrita se realizó en cuatro lotes en paralelo, utilizando cada uno 1,0 g (3,12 mmoles) de 8-bromo-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina-9-carbaldehído. Los lotes combinados de los compuestos crudos se purificaron por cromatografía en columna (gel de sílice malla 230-400, acetona al 30-35 % en hexano como eluyente) para proporcionar 8-bromo-9-difluorometil-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1,4 g, 33 %) como un sólido blanquecino.
1H-RMN (400 MHz, DMSO-d6): 8 = 7,57-7,54 (d, 1H), 7,27-7,06 (t, 1H), 7,04-7,03 (m, 2H), 2,41 (s, 3H), 1,68 (brs, 3H), 1,19 (brs, 3H).
Cualquiera de los intermedios-A se puede acoplar a cualquiera de los intermedios-B en reacciones químicas estándar que son conocidas por el experto en la técnica, por ejemplo, aquellas que se describen a continuación en la presente memoria.
Ejemplo 1: 7.9-d¡fluoro-8-(6-fluoro-1H-¡ndol-4-¡l)-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
A una solución de 8-bromo-7,9-d¡fluoro-1,4,4-tr¡met¡l-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]quinoxal¡na (intermedio B-1) (0,5 g, 1,52 mmoles, 1 eq.) en tolueno: EtOH (2: 1) (9 mL) se añadió solución de Na2CO3 al 10 % (1,5 mL) y 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-1) (0,40 g, 1,52 mmoles, 1 eq) en un tubo sellado. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,09 g, 0,08 mmoles, 0,05 eq). La mezcla de reacción se puso a reflujo a 130 °C durante 16 horas. Una vez completada la reacción, la mezcla de reacción se evaporó a sequedad y el residuo se diluyó con EtOAc (50 mL) y se lavó con agua (2 x 25 mL), salmuera (25 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar 7,9-difluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-4,5-dih¡dro-[1,2,4]tr¡azolo[4,3-a]qu¡noxalina (0,35 g, 60 %) como un sólido amarillo claro.
1H-RMN (400 MHz; DMSO-D6, 20 °C): 8 11,3 (s, 1H), 7,39-7,41 (1H), 7,25-7,29 (1H), 7,18 (s, 1H), 6,96-7,00 (1H), 6,78-6,81 (1H), 5,75 (s, 1H), 2,48 (s, 3H), 1,16-1,57 (6H).
LC MS: [M+H]+ encontrado: 384.
Ejemplo 2: 8-(1-c¡cloprop¡l-6-fluoro-1H-¡ndol-4-¡l)-7.9-d¡fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
Una solución en agitación de 7,9-difluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-triimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (ejemplo 1) (0,2 g, 0,52 mimóles, 1 eq), ácido ciclopropilborónico (0,09 g, 1,05 mimóles, 2 eq) y Na2CO3 (0,11 g, 1,04 mmoles, 2 eq) en DCM (4 mL) se desoxigenó bien mediante Ar. Se añadió una suspensión caliente de Cu(OAc) (0,95 g, 0,52 mml, 1 eq) y bipiridina (0,71 g, 0,522 mmoles, 1 eq) en DCM (4 mL) a la mezcla de reacción. La mezcla de reacción se agitó luego durante 16 horas a 70 °C. La mezcla de reacción se filtró a través de un lecho de celite y se lavó con DCM (30 mL). La capa orgánica se lavó con agua (2 x 25 mL), salmuera (25 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna instantánea para producir el compuesto 8-(1-ciclopropil-6-fluoro-1H-indol-4-il)-7,9-difluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,045 g, 20 %) como un sólido blanquecino.
1H-RMN (400 MHz; DMSO-D6, 20 °C): 87,43 (d, 1H, J = 9,2 Hz), 7,38(d, 1H, J = 2,8 Hz), 7,19 (s, 1H), 7,04(d, 1H, J = 9,6 Hz), 6,78 (d, 1H, J = 10,8Hz), 6,25 (s, 1H), 3,45 (m, 1H), 2,5 (s, 3H), 1,56 (s, 3H), 1,48 (s, 3H), 1,05-0,98 (m, 4H).
LC MS: [M+H]+ encontrado: 424.
Ejemplo_____3 _____7.9-d¡fluoro-8-(6-fluoro-1-(met¡lsulfon¡l)-1H-¡ndol-4-¡l)-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-alquinoxalina
A una solución de 8-broimo-7,9-d¡fluoro-1,4,4-tr¡imet¡l-4,5-dih¡dro-[1,2,4]tr¡azolo[4,3-a]qu¡noxal¡na (intermedio B-1) (0,8 g, 2,43 mmoles, 1 eq.) en tolueno: EtOH (2:1) (15 mL) se añadió solución de Na2Co3 al 10 % (2 mL) y 6-fluoro-1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-2) (0,99 g, 2,92 mmoles, 1,2 eq) en un tubo sellado. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,14 g, 0,12 mmoles, 0,05 eq). La mezcla de reacción se puso a reflujo a 130 °C durante 16 horas. Una vez completada la reacción, el disolvente se eliminó a presión reducida y el residuo se diluyó con EtOAc (50 mL) y se lavó con agua (2 x 25 mL), salmuera (25 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna instantánea para proporcionar el compuesto 7,9-difluoro-8-(6-fluoro-1-(metilsulfonil)-1H-indol-4-il)-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a1quinoxalina (0,12 g, 12 %) como un sólido blanco.
1H-RMN (400 MHz; DMSO-D6, 200C): 87,71 (d, 1H, J = 9,2 Hz), 7,66 (d, 1H, J = 3,2 Hz), 7,35 (d, 1H, J = 9,6 Hz), 7,27(s, 1H), 6,81 (d, 1H, J = 10,8 Hz), 6,72 (s, 1H), 3,58 (s, 3H), 2,74 (s, 3H), 1,56 (s, 3H), 1,50 (s, 3H).
LC MS: [M+H]+ encontrado: 461,8.
Ejemplo 4: 1-(4-(7.9-d¡fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1quinoxal¡n-8-¡l)-6-fluoro-1H-¡ndol-1-il)etanona
A una solución en agitación de 7,9-difluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (ejemplo 1) (0,4 g, 1,044 mmoles, 1 eq) se añadió hidróxido de sodio en polvo (0,105 g, 2,61 mmoles, 2,5 eq) e hidrógenosulfato de tetrabutilamonio (0,071 g, 0,21 mmoles, 0,02 eq) en DCM (8 mL). Se añadió una solución de cloruro de acetilo (0,123 g, 1,55 mmoles, 1,5 eq) en DCM (4 mL) a la mezcla de reacción. La mezcla de reacción se agitó luego durante 4 horas a RT. La mezcla de reacción se diluyó con DCM (50 mL) y se lavó con agua (2 x 20 mL), salmuera (20 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar 1-(4-(7,9-difluoro-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-6-fluoro-1H-indol-1-il)etanona (0,065 g, 15 %) como un sólido blanco.
1H-RMN (400 MHz; DMSO-Da, 20 °C): 88,17 (d, 1H, J = 8,4 Hz), 7,94 (d, 1H, J = 3,6 Hz), 7,30 (d, 1H, J = 9,6Hz), 7,26 (s, 1H), 6,81 (d, 1H, J = 10,4Hz), 6,64 (s, 1H), 2,67 (s, 3H), 2,5 (s, 3H), 1,57 (s, 3H), 1,49 (s, 3H) .
LC MS: [M+H]+ encontrado: 426,1.
Ejemplo 5: 7.9-d¡fluoro-8-(6-fluoro-2-met¡l-1H-¡ndol-4-¡l)-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
Etapa 1: A una soluc¡ón ag¡tada de 7,9-d¡fluoro-8-(1H-¡ndol-7-¡l)-1,4,4-tr¡met¡l-4,5-d¡h¡dro-[1,2,41 tr¡azolo[4,3-a1qu¡noxal¡na (ejemplo 9) (1,4 g, 3,83 mmoles, 1 eq) en DMF (4 mL) se añad¡ó h¡dróx¡do de potas¡o en polvo (0,537
g, 9,5 mimóles, 2,5 eq). Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (0,487 g, 3,83 mmoles, 1 eq) y la mezcla de reacción se agitó durante 4 horas. La mezcla de reacción se vertió luego en agua helada y se formó un precipitado. El precipitado se recogió luego por filtración y se secó para proporcionar 7,9-difluoro-8-(3-yodo-1H-indol-7-il)-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,5 g, 27 %) como un sólido marrón.
Etapa 2: Una suspensión de 7,9-difluoro-8-(3-yodo-1H-indol-7-il)-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1,0 g, 2,04 mmoles, 1 eq) y trifluorometanosulfonato de difenil(trifluorometil)sulfonio (1,645 g, 4,07 mmoles, 2 eq) en DMF (20 mL) se desoxigenó mediante Ar durante 10 minutos. Luego, se añadió polvo de cobre (0,388 mg, 6,11 mmoles, 3 eq) a la mezcla de reacción. La mezcla de reacción se agitó luego a 100 °C durante 24 horas. La mezcla de reacción se filtró a través de un lecho de celite y el filtrado se diluyó con EtOAc (150 mL). La capa orgánica se lavó luego con agua (5 x 30 mL) y salmuera (30 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar 7,9-difluoro-1,4,4-trimetil-8-(3-(trifluorometil)-1H-indol-7-il)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,12 g, 14 %) como un sólido blanco.
1H-RMN (400 MHz; DMSO-D6, 200C): 811,86 (s, 1H), 7,99 (s, 1H), 7,68 (m, 1H), 7,3 (d, 2H, J = 4,04 Hz), 7,2 (s, 1H), 6,81 (d, 1H, J = 10,28 Hz), 2,5 (s, 3H), 1,55 (d, 6H, J = 4,72 Hz).
LC MS: [M+H]+ encontrado: 434,2.
Ejemplo 11: 1-et¡l-7.9-d¡fluoro-8-(1H-¡ndol-7-¡l)-4.4-d¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4,3-a1qu¡noxal¡na
A una solución de 8-bromo-1-et¡l-7,9-d¡fluoro-4,4-d¡met¡l-4,5-d¡h¡dro-[1,2,4]triazolo[4,3-a]qu¡noxal¡na (intermedio B- 2) (1,0 g, 2,91 mmoles, 1 eq) en tolueno: EtOH (2:1) (10 mL) se añadieron solución de Na2CO3 al 10 % (2 mL) y ácido (1H-indol-7-il)borónico (1,06 g, 4,37 mmoles, 1,5 eq) en un tubo sellado. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,168 g, 0,145 mmoles, 0,05 eq). La mezcla de reacción se puso a reflujo a 110 °C durante 16 horas. Una vez completada la reacción, el disolvente se evaporó y el residuo se diluyó con EtOAc (150 mL). La capa orgánica se lavó con agua (2 x 50 mL), salmuera (30 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 1-etil-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a1quinoxalina (0,93 g, 84 %) como un sólido blanquecino.
1H-RMN (400 MHz; DMSO-D6, 20 0C): 8 10,99 (s, 1H), 7,61-7,63 (1H), 7,35 (s, 1H), 7,08-7,12 (3H), 6,79-6,82 (1H, 6,52 (s, 1H), 2,80-2,92 (2H), 1,55 (s, 6H), 1,17-1,23 (3H).
LC MS: [M+H]+ encontrado: 380,2.
Ejemplo 12: 7-(1-et¡l-7.9-d¡fluoro-4.4-d¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡n-8-il)-1H-¡ndol-3-carbon¡tr¡lo
Etapa 1: A una solución agitada de 1-etil-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (ejemplo 11) (0,50 g, 1,32 mmoles, 1 eq) en DMF (10 mL) se añadió hidróxido de potasio en polvo (0,185 g, 3,3 mmoles, 2,5 eq). Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (0,402 g, 1,58 mmoles, 1,2 eq) a la mezcla de reacción y se agitó durante 4 horas. La mezcla de reacción se diluyó luego con EtOAc (80 mL) y se lavó con agua (5 x 20 mL y salmuera (30 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 1-etil-7,9-difluoro-8-(3-yodo-1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3a]quinoxalina (0,25 g, 38 %) como un sólido marrón claro.
Etapa 2: Una suspensión en agitación de 1-etil-7,9-difluoro-8-(3-yodo-1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,25 g, 0,495 mmoles, 1 eq), CuCN (0,088 g, 0,99 mmoles, 2 eq) y cianuro de tetraetilamonio (0,038 g, 0,247 mmoles, 0,5 eq) en DMF y THF (1:1) (8 mL) se desoxigenó bien mediante Ar durante 10 minutos. Luego, se añadió Pd2dba3 (0,022 g, 0,0247 mmoles, 0,05 eq) y dppf (0,041 g, 0,0742 mmoles, 0,15 eq) a la mezcla de reacción y se desoxigenó de nuevo mediante Ar durante 10 minutos. Finalmente, la mezcla de reacción se agitó durante 18 horas a 110 °C. La mezcla de reacción se filtró a través de lecho de celite y el filtrado se diluyó con EtOAc (30 mL). La capa orgánica se lavó con agua (5 x 20 mL) y salmuera (20 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 7-(7,9-difluoro-1,4,4-trimetil-4,5-dihidro-[1,2,41triazolo[4,3-a1quinoxalin-8-il)-1H-indol-3-carbonitrilo (0,08 g, 40 %) como un sólido blanquecino.
Ejemplo_____ 13: 1-et¡l-7.9-d¡fluoro-4.4-d¡met¡l-8-(3-(prop-1-¡n-1-¡l)-1H-¡ndol-7-¡l)-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-alquinoxalina
Una solución de 1-et¡l-7,9-d¡fluoro-8-(3-yodo-1H-¡ndol-7-¡l)-4,4-d¡metil-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]qu¡noxal¡na (0,5 g, 0,99 mmoles, 1 eq) en THF y TEA (1:1) (8 mL) se desoxigenó mediante Ar durante 10 minutos en un tubo sellado. Luego, se añadió Pd(Pph3)2Cl2 (0,035 g, 0,0455 mmoles, 0,05 eq) y Cul (0,038 g, 0,198 mmoles, 0,2 eq) a la mezcla de reacción y se desoxigenó de nuevo mediante Ar durante 10 minutos a -78 °C. En el tubo de ensayo, el gas de prop-1-ino se condensó en TEA (4 mL) a -78 °C. El volumen se elevó a 5 mL. El gas de prop-1-ino condensado se vertió instantáneamente en la mezcla de reacción a -78 ° C. La mezcla de reacción se agitó luego durante 2 horas a -78 °C y 14 horas a RT. La mezcla de reacción se diluyó mediante DCM (50 mL). La capa orgánica se lavó con agua (2 x 20 mL) y salmuera (20 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 1-etil-7,9-difluoro-4,4-dimetil-8-(3-(prop-1-in-1-il)-1H-indol-7-il)-4,5-dihidro-[1,2,4]triazolo[4,3-a1quinoxalina (0,09 g, 22 %) como un sólido blanquecino.
1H-RMN (400 MHz, DMSO-da): 8 11,27(s, 1H), 7,62-7,60 (m, 1H), 7,56 (d, J = 2,48 Hz, 1H), 7,20-7,13 (m, 3 H), 6,80 (d, J = 10,24 Hz, 1H), 2,90-2,81 (m, 2H), 2,10 (s, 3 H), 1,56 (s, 3H), 1,53 (s, 3H), 1,21 (t, J = 7,44 Hz, 3H)
Ejemplo 14: 1-et¡l-7.9-d¡fluoro-8-(5-fluoro-1H-¡ndol-7-¡l)-4.4-d¡met¡l-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
El ejemplo 14 se sintetizó en analogía con el procedimiento descrito para el ejemplo 11 usando 5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol y el intermedio B-2.
1H-RMN (400 MHz, DMSO-d6): 8 11,2 (s, 1H), 7,40-7,44 (2H), 7,19 (s, 1H), 7,00-7,03 (1H), 6,80-6,83 (1H), 6,51 (s, 1H), 2,85-2,90 (2H), 1,55 (s, 6H), 1,20-1,24 (3H).
Ejemplo 15: 7-(1-et¡l-7.9-d¡fluoro-4.4-d¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1quinoxal¡n-8-¡l)-5-fluoro-1H-¡ndol-3-carbonitrilo
Etapa 1: A una solución agitada de 1 -etil-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetM-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (ejemplo 14) (1,2 g, 3,0 mmoles, 1 eq) en DMF (25 mL) se añadió hidróxido de potasio en polvo (0,425 g, 7,5 mmoles, 2,5 eq). Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (1,14 g, 4,5 mmoles, 1,5 eq) a la mezcla de reacción y se agitó durante 4 horas. La mezcla de reacción se diluyó luego con EtOAc (200 mL) y se lavó con agua (5 x 20 mL) y salmuera (30 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 1-etil-7.9-difluoro-8-(5-fluoro-3-yodo-1H-indol-7-il)-4.4-dimetil-4.5-dihidro-[1.2.41tnazolo[4.3-a]quinoxalina (1,0 g, 64 %) como un sólido marrón claro.
Etapa 2: Una suspensión en agitación de 1-etil-7,9-difluoro-8-(5-fluoro-3-yodo-1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,4 g, 0,764 mmoles, 1 eq), CuCN (0,137 g, 1,53 mmoles, 2 eq) y cianuro de tetraetilamonio (0,06 g, 0,382 mmoles, 0,5 eq) en DMF y THF (1:1) (14 mL) se desoxigenó bien mediante Ar durante 10 minutos. Luego, se añadió Pd2dba3 (0,035 g, 0,038 mmoles, 0,05 eq) y dppf (0,063 g, 0,114 mmoles, 0,15 eq) a la mezcla de reacción y se desoxigenó de nuevo mediante Ar durante 10 minutos. Finalmente, la mezcla de reacción se agitó durante 18 horas a 110 °C. La mezcla de reacción se filtró a través de un lecho de celite y el filtrado se diluyó con EtOAc (30 mL). La capa orgánica se lavó con agua (5 x 20 mL) y salmuera (20 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 7-(1-etil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-5-fluoro-1H-indol-3-carbonitrilo (0,110 g, 34 %) como un sólido blanquecino.
1H RMN (400 MHz, DMSO-d6): 812,28 (s, 1H), 8,37 (s, 1H), 7,56-7,53 (m, 1H), 7,30-7,26 (m, 2H), 6,82 (d, J = 10,36 Hz, 1H), 2,89-2,82 (m, 2H), 1,57 (s, 3H), 1,53 (s, 3H), 1,22 (t, J = 7,32Hz, 3H).
Ejemplo 16: 1-et¡l-7.9-d¡fluoro-8-(5-fluoro-3-(prop-1-¡n-1-¡l)-1H-¡ndol-7-il)-4.4-d¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-alquinoxalina
El Ejemplo 16 se sintetizó en analogía con el procedimiento descrito para el Ejemplo 13 a partir de 1-etil-7.9-difluoro-8-(5-fluoro-3-yodo-1H-¡ndol-7-N)-4,4-d¡met¡l-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]qu¡noxal¡na.
1H RMN (400 MHz. DMSO-d6): 8 11,37 (s. 1H). 7,65 (d. J = 1,96Hz, 1H). 7,33 (t. J = 1,68 Hz. 1H). 7,20 (s. 1H). 7,10 (d. J = 8,76 Hz. 1H). 6,80 (d. J = 10,4 Hz. 1H). 2,88-2,84 (m. 2H). 2,09 (s. 3H). 1,56 (s. 3H). 1,53 (s. 3H). 1,21 (t. J = 7,28 Hz, 3H).
Ejemplo 17: 7-(1-et¡l-7.9-d¡fluoro-4.4-d¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1quinoxal¡n-8-¡l)-5-met¡l-1H-¡ndol-3-carbonitrilo
Etapa 1: A una solución del intermedio B-2 (0,65 g, 1,77 mimóles, 1 eq) en tolueno: EtOH (2:1) (9 mL) se añadió solución de Na2CO3 al 10 % (1,0 mL) e intermedio A-7 (0,548 g, 2,13 mimóles, 1,2 eq) en un tubo sellado. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,102 g, 0,0885 mmoles, 0,05 eq). La mezcla de reacción se puso a reflujo a 110 °C durante 16 horas. Una vez completada la reacción, la mezcla de reacción se evaporó a sequedad y el residuo se diluyó con EtOAc (50 mL). La capa orgánica se lavó con agua (2 x 30 mL), salmuera (30 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 1 -etil-7,9-difluoro-4,4-dimetil-8-(5-metil-1H-indol-7-il)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,61 g, 88 %) como un sólido blanquecino.
Etapa 2: A una solución agitada de 1-etil-7,9-difluoro-4,4-dimetil-8-(5-metil-1H-indol-7-il)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,6 g, 1,52 mmoles, 1 eq) en DMF (10 mL) se añadió hidróxido de potasio en polvo (0,213 g, 3,816 mmoles, 2,5 eq). Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (0,387 g, 3,052 mmoles, 2 eq) a la mezcla de reacción y se agitó durante 4 horas. La mezcla de reacción se diluyó luego con EtOAc (100 mL) y se lavó con agua (5 x 20 mL) y salmuera (30 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 1-etil-7,9-difluoro-8-(3-yodo-5-metil-1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,35 g, 44 %) como un sólido marrón claro.
Etapa 3: Una suspensión en agitación de 1-etil-7,9-difluoro-8-(3-yodo-5-metil-1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,15 g, 0,308 mmoles, 1 eq), Zn(CN)2 (0,036 g, 0,308 mmoles, 1 eq) y TMEDA (0,014 mL, 0,0929 mmoles, 0,3 eq) en DMA (3 mL) se desoxigenó bien mediante Ar durante 10 minutos. Luego, se añadió Pd2dba3 (0,028 g, 0,0308 mmoles, 0,1 eq) y xantphos (0,018 g, 0,0308 mmoles, 0,1 eq) a la mezcla de reacción y nuevamente se desoxigenó mediante Ar durante 10 minutos. Finalmente, la mezcla de reacción se agitó durante 14 horas a 90 °C. La mezcla de reacción se filtró a través de lecho de celite y el filtrado se diluyó con EtOAc (30 mL). La capa orgánica se lavó con agua (5 x 20 mL) y salmuera (20 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 7-(1-etil-7,9-difluoro-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-5-metil-1H-indol-3-carbonitrilo (0,08 g, 63 %) como un sólido blanquecino.
1H RMN (400 MHz, DMSO-d6): 812,04 (s, 1H), 8,22 (s, 1H), 7,51 (s, 1H), 7,22 (s, 1H), 7,14 (s, 1H), 6,82 (d, J = 9,48 Hz, 1H), 2,94-2,82 (m, 2H), 2,47 (s, 3H), 1,56 (s, 3H), 1,53 (s, 3H), 1,21 (t, J = 7,4Hz, 3H)
Ejemplo_____ 18:_____ 8-(1-(et¡lsulfon¡l)-6-fluoro-1H-¡ndol-4-¡l)-7.9-d¡fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-alquinoxalina
El ejemplo 18 se sintetizó en analogía con el procedimiento descrito para el ejemplo 3 usando 1-(etilsulfonil)-6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H.-indol (intermedio A-8) y el intermedio B-1.
1H RMN (400 MHz, DMSO-d6): 87,72-7,67 (m, 2H), 7,36 (d, J = 9,92 Hz, 1H), 7,27 (s, 1H), 6,81 (d, J = 10,64 Hz, 1H), 6,72 (s, 1H), 3,74 (q, J = 7,28 Hz, 2H), 2,25 (s, 3H), 1,56 (s, 3H), 1,5 (s, 3H), 1,12 (t, J = 7,28 Hz, 3H).
Ejemplo 19: 8-(1-(c¡cloprop¡lsulfon¡l)-6-fluoro-1H-¡ndol-4-¡l)-7.9-d¡fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolof4.3-alquinoxalina
A una solución de 8-bromo-7,9-d¡fluoro-1,4,4-tr¡metil-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]qu¡noxal¡na (intermedio B-1) (0,5 g, 1,57 mmoles, 1 eq.) en dioxano: alcohol isoamílico (2:1) (9 mL) se añadieron solución de K2CO3 (0,725 g, 5,25 mmoles, 3 eq.) y 1-(4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol-1-il)etanona (intermedio A-10) (0,634 g, 1,929 mmoles, 1,1 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Attaphos (0,061 g, 0,087 mmoles, 0,05 eq). La mezcla de reacción se puso a reflujo a 100 °C durante 16 horas. El disolvente se evaporó a sequedad y el residuo se diluyó con EtOAc (50 mL) y se lavó con agua (2 x 25 mL), salmuera (25 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó por HPLC preparativa para proporcionar 1-(4-(7,9-d¡fluoro-1,4,4-tr¡met¡l-4,5-d¡h¡dro-[1,2,4]triazolo[4,3-a]qu¡noxal¡n-8-¡l)-1H-¡ndol-1-¡l)etanona (0,160 g, 22 %) como un sólido blanco.
1H RMN (400 MHz, DMSO-d6): 88,41 (d, J = 8 Hz, 1H), 7,92 (d, J = 3,6 Hz,1H), 7,43 (t, J = 8,0 Hz, 1H), 7,33 (d, J = 7,6 Hz, 1H), 7,19 (s, 1H), 6,81 (d, J = 10,4 Hz, 1H), 6,62 (bs, 1H), 2,67 (s, 3H), 1,57 (s, 3H),1,49 (s, 3H).
Ejemplo 21: 7.9-d¡fluoro-8-í6-fluoro-1-í2.2.2-tr¡fluoroet¡l)-1H-¡ndol-4-¡l)-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
A una solución de 6-fluoro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1-(2,2,2-trifluoroetil)-1H-indol (intermedio A-11) (0,4 g, 1,166 mmoles, 1 eq.) en tolueno: EtOH (2:1) (9 mL) se añadieron solución de Na2CO3 al 10 % (0,4 mL) e intermedio B-1 (0,307 g, 0,932 mmoles, 0,8 eq) en un tubo sellado. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,067 g, 0,058 mmoles, 0,05 eq). La mezcla de reacción se puso a reflujo a 90 °C durante 16 horas. La mezcla de reacción se filtró a través de un lecho de celite. El filtrado se concentró a
presión reducida para obtener el producto crudo que se purificó mediante HPLC preparativa para producir el compuesto 7,9-difluoro-8-(6-fluoro-1-(2,2,2-trifluoroetil)-1H-indol-4-il)-1,4,4-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,055 g, 10 %) como un sólido blanquecino.
RMN (400 MHz, DMSO-d6): 87,65 (d, J = 10 Hz, 1H), 7,46 (d, J = 3,2 Hz, 1H), 7,21 (s, 1H), 7,09 (d, J = 9,6 Hz, 1H), 6,80 (d, J = 10,4 Hz, 1H), 6,43 (s, 1H), 6,81 (d, J = 10,0 Hz, 1H), 5,24 (q, J = 8,8 Hz, 2H), 5,86 (bs, 6H).
Ejemplo 22: 7.9-d¡fluoro-1.4.4-tr¡met¡l-8-(1-(met¡lsulfon¡l)-1H-¡ndol-4-¡l)-4.5-d¡h¡dro-[1.2.41tr¡azolo[4,3-a1qu¡noxal¡na
El ejemplo 22 se sintetizó en analogía con el procedimiento descrito para el ejemplo 3 usando 1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-12) y el intermedio B-1.
RMN (400 MHz, DMSO-d6): 7,93 (d, J = 8,28 Hz, 1H), 7,64 (d, J = 3,64 Hz, 1H), 7,49 (t, J = 7,68 Hz, 1H), 7,38 (d, J = 7,24 Hz, 1H), 7,21 (s, 1H), 6,81 (d, J = 10,16 Hz, 1H), 6,71 (s, 1H), 3,52 (s, 3H), 1,57 (s, 3H), 1,5 (s, 3H).
Ejemplo 23: 7-fluoro-8-(5-fluoro-3-(2.2.2-tr¡fluoroet¡l)-1H-¡ndol-7-¡l)-1.4.4.9-tetramet¡l-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-alquinoxalina
A una solución de 5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-3-(2,2,2-trifluoroetil)-1H-indol (intermedio A-13) (0,600 g, 1,749 mmoles, 1,0 eq.) en dioxano: alcohol isoamílico (2:1) (25 mL) se añadieron solución de K2CO3 (0,724 g, 5,247 mmoles, 3 eq.) y 8-bromo-7-fluoro-1,4,4,9-tetramet¡l-4,5-d¡h¡dro-[1,2,4]triazolo[4,3-a]qu¡noxal¡na (intermedio B-3) (0,284 g, 0,874 mmoles, 0,5 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Attaphos (0,062 g, 0,087 mmoles, 0,05 eq.). La mezcla de reacción se agitó a 100 °C durante 16 horas. El disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea y por HPLc preparativa para proporcionar 7-fluoro-8-(5-fluoro-3-(2,2,2-trifluoroetil)-1 H-indol-7-il)-1,4,4,9-tetramet¡l-4,5-d¡hidro-[1,2,4]tr¡azolo[4,3-a]qu¡noxal¡na (0,200 g, 25 %) como un sólido blanco.
1H RMN (400 MHz, DMSO-d6): 811,10 (s, 1H), 7,45- 7,40 (m, 2H), 6,97 (d, J = 8,8, 1H), 6,80 (s, 2H), 3,76 (q, J = 10,8 Hz, 2H), 2,50 (s, 3H), 1,96 (s, 3H), 1,53 (s, 3H), 1,44 (s, 3H).
Ejemplo_____ 24______7-fluoro-1.4.4.9-tetramet¡l-8-(3-(2.2.2-tr¡fluoroet¡l)-1H-¡ndol-7-¡l)-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
El ejemplo 24 se sintetizó en analogía con el procedimiento descrito para el ejemplo 3 usando 7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-3-(2,2,2-trifluoroetil)-1H-indol (intermedio A-14) y el intermedio C.
RMN (400 MHz, DMSO-d6): 8 10,97 (s, 1H), 7,64 (d, J = 7,2 Hz, 1H), 7,32 (s, 1H), 7,13 (d, J = 6,8, 1H), 7,04 (d, J = 6,4, 1H), 6,80 (d, J = 10.1H), 6,74 (s, 1H), 3,76 (q, J = 12 Hz, 2H), 2,49 (s, 3H), 1,93 (s, 3H), 1,55 (s, 3H), 1,43 (s, 3H).
E je m p lo 25 : 7 - f lu o ro -8 -(1 H -¡n d o l-7 -¡ l) -1.4.4.9 - te tra m e t¡ l-4.5 -d ¡h ¡d ro -[1.2.41 tr ¡a z o lo [4.3 -a 1 q u ¡n o x a l¡n a
A una solución del intermedio B-3 (1,2 g, 3,69 mimóles, 1 eq) en tolueno: EtOH (2:1) (15 mL) se añadieron solución de Na2CO3 al 10 % (2 mL) y ácido (1H-indol-7-M)borónico (1,07 g, 4,43 mmoles, 1,2 eq) en un tubo sellado. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,213 g, 0,1845 mmoles, 0,05 eq). La mezcla de reacción se agitó a 110 °C durante 16 horas. El disolvente se evaporó a sequedad y el residuo se diluyó con EtOAc (150 mL). La capa orgánica se lavó con agua (2 x 50 mL), salmuera (30 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 7-fluoro-8-(1H-indol-7-il)-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,85 g, 64 %) como un sólido blanquecino.
1H RMN (400 MHz, DMSO-d6): 810,88 (s, 1H), 7,58-7,60 (1H), 7,30 (s, 1H), 7,06-7,11 (1H), 6,98-7,00 (1H), 6,78-6,81 (1H), 6,73 (s, 1H), 6,50 (s, 1H), 2,47 (s, 3H), 1,94 (s, 3H), 1,56 (s, 3H), 1,43 (s, 3H).
Ejemplo 26: 7-fluoro-8-(1H-¡ndol-4-¡l)-1.4.4.9-tetramet¡l-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
El ejemplo 26 se sintetizó en analogía con el procedimiento descrito para el ejemplo 1 usando 4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol y el intermedio B-3.
1H RMN (400 MHz, DMSO-d6): 811,21 (s, 1H), 7,44-7,46 (1H), 7,37 (s, 1H), 7,17-7,20 (1H), 6,96-6,98 (1H), 6,77-6,79 (1H), 6,69 (s, 1H), 6,09 (s, 1H), 2,44 (s, 3H), 1,98 (s, 3H), 1,54 (s, 3H), 1,44 (s, 3H).
Ejemplo 27: 8-(1-c¡cloprop¡l-1H-¡ndol-4-¡l)-7-fluoro-1.4.4.9-tetramet¡l-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
Una solución en agitación de 7-fluoro-8-(1H-¡ndol-4-¡l)-1,4,4,9-tetramet¡l-4,5-d¡h¡dro-[1,2,4]triazolo[4,3-a]qu¡noxal¡na (ejemplo 26) (0,2 g, 0,554 mmoles, 1 eq), ácido ciclopropilborónico (0,095 g, 1,1 mmoles, 2 eq) y Na2CO3 (0,12 g, 1,1 mmoles, 2 eq) en DCM (4 mL) se desoxigenó mediante Ar. Se añadió una suspensión caliente de Cu(OAc) (0,1 g, 0,554 mml, 1 eq) y bipiridina (0,86 g, 0,554 mmoles, 1 eq) en DCM (4 mL) a la mezcla de reacción. La mezcla de reacción se agitó luego durante 16 horas a 70 °C. La mezcla de reacción se filtró a través de un lecho de celite y se lavó con DCM (30 mL). La capa orgánica se lavó con agua (2 x 25 mL), salmuera (25 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea para proporcionar 8-(1-ciclopropil-1H-indol-4-il)-7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a1quinoxalina (0,07 g, 32 %) como un sólido blanquecino.
RMN (400 MHz, DMSO-d6): 87,60 (d, J = 8,16 Hz, 1H), 7,35 (d, J = 2,96 Hz, 1H), 7,26 (t, J = 7,56 Hz, 1H), 7,02 (d, J = 7,08 Hz, 1H), 6,76 (d, J = 10,12 Hz, 1H), 6,71 (s, 1H), 6,05 (s, 1H), 3,49-3,48 (m, 1H), 2,42 (s, 3H), 1,98 (s, 3H), 1,52 (s, 3H), 1,42 (s, 3H), 1,08-0,99 (m, 4H).
Ejemplo 28: 7-fluoro-1.4.4.9-tetramet¡l-8-(3-(prop-1-¡n-1-¡l)-1H-¡ndol-7-¡l)-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
Etapa 1: A una solución agitada de 7-fluoro-8-(1H-indol-7-il)-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (ejemplo 25) (0,85 g, 2,35 mimóles, 1 eq) en DMF (20 mL) se añadió hidróxido de potasio en polvo (0,329 g, 5,87 mmoles, 2,5 eq). Luego, la mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (0,897 g, 3,53 mmoles, 1,5 eq) a la mezcla de reacción y se agitó durante 4 horas. La mezcla de reacción se diluyó luego con EtOAc (100 mL) y se lavó con agua (5 x 20 mL) y salmuera (30 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 7-fluoro-8-(3-yodo-1H-indol-7-il)-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,27 g, 24 %) como un sólido marrón claro.
Etapa 2: Una solución de 7-fluoro-8-(3-yodo-1H-indol-7-il)-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,48 g, 0,98 mmoles, 1 eq) en THF y TEA (1:1) (8 mL) se desoxigenó mediante Ar durante 10 minutos en un tubo sellado. Luego, se añadió Pd(PPh3)2Ch (0,035 g, 0,049 mmoles, 0,05 eq) y Cul (0,038 g, 0,197 mmoles, 0,2 eq) a la mezcla de reacción y se desoxigenó de nuevo mediante Ar durante 10 minutos a -78 °C. En el tubo de ensayo, el gas de prop-1-ino se condensó en TEA (3 mL) a -78 °C. El volumen se elevó a 5 mL. El gas de prop-1-ino condensado se vertió instantáneamente en la mezcla de reacción a -78 ° C. La mezcla de reacción se agitó luego durante 2 horas a -78 °C y 14 horas a RT. La mezcla de reacción se diluyó con DCM (50 mL). La capa orgánica se lavó con agua (2 x 20 mL) y salmuera (20 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna para proporcionar 7-fluoro-1,4,4,9-tetrametil-8-(3-(prop-1-in-1-il)-1H-indol-7-il)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,08 g, 20 %) como un sólido blanquecino.
RMN (400 MHz, DMSO-da): 811,12 (s, 1H), 7,58 (d, J = 7,56 Hz, 1H), 7,50 (s, 1H),7,17 (t, J = 7,56Hz, 1H), 7,07 (d, J = 7,32 Hz, 1H), 6,79 (d, J = 10,16Hz, 1H), 6,74 (s, 1H), 2,10 (s, 3H), 2,07 (s, 3H), 1,92 (s, 3H), 1,53 (s, 3H), 1,43 (s, 3H).
Ejemplo 29: 7-fluoro-1.4.4-tr¡met¡l-8-(3-met¡l-1H-¡ndol-7-¡l)-9-(tr¡fluoromet¡l)-4.5-d¡h¡dro-[1.2.41tr¡azolo[4,3-a1qu¡noxal¡na
A una solución de 3-metil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (0,25 g, 0,579 mmoles, 1 eq) en tolueno: EtOH (2:1) (10 mL), se añadió 8-bromo-7-fluoro-1,4,4-tr¡metil-9-(tr¡fluoromet¡l)-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]quinoxalina (intermedio B-4) (0,223 g, 0,254 mmoles, 1,5 eq) y Na2CO3 al 10 % (0,5 mL) a RT. Después de desgasificar la mezcla de reacción, se añadió Pd(PPh3)4 (0,038 g, 0,028 mmoles, 0,05 eq) a RT y la mezcla de reacción se agitó a 90 °C durante otras 16 horas. La mezcla de reacción se filtró a través de sinterización y se diluyó con agua (20 mL). La capa acuosa se extrajo con EtOAc (3 x 50 mL). Las capas orgánicas combinadas se lavaron con agua (50 mL), salmuera (50 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo que se purificó mediante cromatografía en columna para proporcionar 7-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-9-(trifluoromet¡l)-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]qu¡noxal¡na (0,042 g, 17 %) como un sólido blanco.
RMN (400 MHz, DMSO-d6, T=100 °C): 810,29 (s, 1H), 7,55 (d, J = 8,0 Hz, 1H), 7,13-7,04 (m, 4H), 2,45 (s, 3H), 2,28 (s, 3H), 1,75 (s, 3H), 1,31 (bs, 3H).
E je m p lo 30 : 9 -c lo ro -7 - f lu o ro -8 -(5 - f lu o ro -3 -m e t¡ l-1 H -¡n d o l-7 -¡ l) -1.4.4 - tr ¡m e t¡ l-4.5 -d ¡h ¡d ro -[1.2.41 tr ¡a z o lo [4.3 -a 1 q u ¡n o x a l¡n a
en analogía con el procedimiento descrito para el ejemplo 29 usando 5-fluoro-3-metil-7-xaborolan-2-il)-1H-indol (intermedio A-15) y el intermedio B-5.
: 810,71 (s, 1H), 7,29 (d, J = 9,6Hz, 1H), 7,15 (s, 1H), 7,1 (s, 1H), 6,90 (d, J = 10,0 Hz, 2H), 52 (s, 3H),1,45 (s, 3H).
oro-3-met¡l-1H-¡ndol-7-¡l)-1.4.4.9-tetramet¡l-4.5-d¡h¡dro-f1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
en analogía con el procedimiento descrito para el ejemplo 29 usando 5-fluoro-3-metil-7-xaborolan-2-il)-1H-indol (intermedio A-15) y el intermedio B-3.
: 810,65 (s, 1H), 7,28 (d, J = 10,0 Hz, 1H), 7,15 (s, 1H), 6,90 (d, J = 8,2 Hz, 1H), 6,77-6,80 (s, 3H), 1,95 (s, 3H), 1,53 (s, 3H), 1,43 (s, 3H).
El ejemplo 32 se sintetizó en analogía con el procedimiento descrito para el ejemplo 29 usando 5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol y el intermedio B-3.
1H RMN (400 MHz, DMSO-d6): 8 11,0 (s, 1H), 7,35-7,38 (2H), 6,91-6,93 (1H), 6,77-6,81 (2H), 6,50 (s, 1H), 2,47 (s, 3H), 1,96 (s, 3H), 1,54 (s, 3H), 1,44 (s, 3H).
Ejemplo_____ 33_____ 8-(3-ciclopropil-5-fluoro-1H-indol-7-il)-7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-H,2,41triazolor4,3-alquinoxalina
Etapa 1: A una solución agitada de 7-fluoro-8-(5-fluoro-1H-indol-7-il)-1,4,4,9-tetrametil-4,5-dihidro-[1,2,41triazolo[4,3-a]quinoxalina (ejemplo 32) (0,7 g, 1,846 mmoles, 1 eq) en DMF (6 mL) a -10 °C se añadió por partes durante 10 minutos N-bromosuccinimida sólida (0,338 g, 1,902 mmoles, 1,03 eq). La mezcla de reacción se dejó calentar hasya RT y se agitó durante 1,5 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se diluyó con EtOAc (30 mL) y las capas orgánicas se lavaron con agua (5 x 25 mL) y salmuera (25 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida para obtener el producto crudo que se purificó mediante lavado con éter para proporcionar 8-(3-bromo-5-fluoro-1H-indol-7-il)-7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalina (0,8 g, 95 %) como un sólido blanquecino.
Etapa 2: A una solución de 8-(3-bromo-5-fluoro-1H-indol-7-il)-7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,41triazolo[4,3-a]quinoxalina (22,0 g, 48,034 mmoles, 1 eq) en THF (400 mL), se añadió NaH (6,72 g, 168,11 mmoles, 3,5 eq) a RT. Después de 15 minutos de agitación, se añadió (BOC)2O (15,4 mL, 75,052 mmoles, 1,5 eq) a RT. La reacción se puso a reflujo durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se inactivó con hielo y se extrajo con EtOAc. La capa orgánica se lavó con agua, salmuera, se secó sobre Na2SO4, se filtró y el disolvente se evaporó a presión reducida para obtener el producto crudo. El producto crudo se purificó mediante cromatografía en columna para proporcionar 3-bromo-5-fluoro-7-(7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-carboxilato de terc-butilo (17,0 g, 63 %) como un sólido marrón.
Etapa 3: A una solución de 3-bromo-5-fluoro-7-(7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,41triazolo[4,3-a1quinoxalin-8-il)-1 H-indol-1 -carboxilato de terc-butilo (0,35 g, 0,627 mmoles, 1 eq) en tolueno: EtOH (2:1) (10,0 ml), se añadió Cs2CO3 (0,611 g, 1,881 mmoles, 3 eq) y ácido ciclopropilborónico (0,108 g, 1,254 mmoles, 2 eq) a RT. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(OAc)2 (0,014 g, 0,062 mmoles, 0,1 eq) y Fosfina de Adamentilo (0,019 g, 0,062 mmoles, 0,1 eq) a RT y la mezcla de reacción se agitó a 110 °C durante 16 horas. Una vez completada la reacción (controlada por LCMS), el disolvente se evaporó y el residuo se diluyó con EtOAc (150 mL). La capa orgánica se lavó con agua (2 x 50 mL), salmuera (30 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener 3-ciclopropil-5-fluoro-7-(7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1 H-indol-1-carboxilato de terc-butilo crudo (0,15 g, 46 %), como una goma marrón, que se usó para la siguiente etapa sin purificación adicional.
Etapa 4: A una solución de 3-ciclopropil-5-fluoro-7-(7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-carboxilato de terc-butilo (0,5 g, 0,96 mmoles, 1 eq) en MeOH (12,0 mL) y H2O (4,0 mL), se añadió K2CO3 (0,4 g, 2,884 mmoles, 3 eq) a RT. La mezcla de reacción se calentó luego a 90 °C durante 24 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se filtró a través de sinterización y el disolvente se evaporó a presión reducida. El producto crudo se purificó por HPLC preparativa para producir 8-(3-ciclopropil-5-fluoro-1H-indol-7-il)-7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,18 g, 45 %) como un sólido blanco.
RMN (400 MHz, DMSO-d6): 810,67 (s, 1H), 7,37 (d, J = 9,2 Hz, 1H), 7,06 (s, 1H), 6,90 (d, J = 9,6 Hz, 1H), 6,76-6,79 (m, 2H), 1,95 (s, 4H), 1,43-1,53 (m, 6H), 0,85 (d, J = 8,8 Hz, 2H), 0,61 (s, 2H); (CH3- omitido por DMSO).
Ejemplo 34: 1-et¡l-7-fluoro-8-(6-fluoro-1H-¡ndol-4-¡l)-4.4.9-tr¡met¡l-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
El ejemplo 34 se sintetizó en analogía con el procedimiento descrito para el ejemplo 29 usando 6-fluoro-4-(4.4.5.5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol y el intermedio B-6.
LC MS: [M+H]+ encontrado: 394.
Ejemplo 35: 8-(1-(c¡cloprop¡lmet¡l)-6-fluoro-1H-¡ndol-4-¡l)-1-et¡l-7-fluoro-4.4.9-tr¡met¡l-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-alquinoxalina
A una solución de 1-etil-7-fluoro-8-(6-fluoro-1H-indol-4-il)-4.4.9-trimetil-4.5-dihidro-[1.2.41triazolo[4.3-a1quinoxalina (ejemplo 34) (0.1 g. 0.254 mmoles. 1 eq.) en DMF (5 mL) se añadió hidruro de sodio (0.022 g. 0.508 mmoles. 2 eq) a 0 °C. La solución se agitó a RT durante 30 minutos seguido de la adición de bromometil-ciclopropano (0.02 g. 0.152 mmoles. 0.6 eq) y la mezcla de reacción se agitó a RT durante 2 horas. Una vez completada la reacción (controlada por LCMS). la mezcla de reacción se diluye con EtOAc (20 mL) y la capa orgánica se lavó con agua fría (5 x 10 mL). salmuera (10 mL). se secó sobre Na2SO4 anhidro y se evaporó a presión reducida. El producto crudo se purificó por HPLC preparativa para proporcionar 8-(1-(ciclopropilmetil)-6-fluoro-1H-indol-4-il)-1-etil-7-fluoro-4.4.9-trimetil-4.5-dihidro-[1.2.41triazolo[4.3-a1quinoxalina (0.03 g. 27 %) como un sólido blanquecino.
RMN (400 MHz. DMSO-d6): 87.47 (d. J = 9.2 Hz. 2H). 6.89 (s. 1H). 6.77 (t. J = 10.1 Hz. J = 8.4 Hz. 1H). 6.06 (s. 1H).
4.04 (s. 2H). 2.78 (bs. 2H). 1.99 (s. 3H). 1.47 (bs. 6H). 1.25 (t. J = 7.08 Hz. 3H). 0.53 (d. J = 7.08 Hz. 2H). 0.42 (s. 2H).
Ejemplo 36: 1-et¡l-7-fluoro-8-(6-fluoro-1-(2-metox¡et¡l)-1H-¡ndol-4-¡l)-4.4.9-tr¡met¡l-4.5-dih¡dro-[1.2.41tr¡azolo[4.3-a1quinoxalina
A una solución de 1-etil-7-fluoro-8-(6-fluoro-1H-indol-4-il)-4.4.9-trimetil-4.5-dihidro-[1.2.41triazolo[4.3-a1quinoxalina (ejemplo 34) (0.1 g. 0.254 mmoles. 1 eq.) en DMF (5 mL) se añadió hidruro de sodio (0.022 g. 0.508 mmoles. 2 eq) a 0 °C. La solución se agitó a RT durante 30 minutos seguido de la adición de 1-bromo-2-metoxi-etano (0.022 g. 0.152 mmoles. 0.6 eq) y la mezcla de reacción se agitó a RT durante 2 horas. Una vez completada la reacción (controlada por LCMS). la mezcla de reacción se diluyó con EtOAc (20 mL) y la capa orgánica se lavó con agua fría (5 x 10 mL). salmuera (10 mL). se secó sobre Na2SO4 anhidro y el disolvente se evaporó a presión reducida. El producto crudo se purificó por HPLC preparativa para proporcionar 1-etil-7-fluoro-8-(6-fluoro-1-(2-metoxietil)-1H-indol-4-il)-4.4.9-trimetil-4.5-dihidro-[1.2.41triazolo[4.3-a1quinoxalina (0.08 g. 70 %) como un sólido blanquecino.
RMN (400 MHz. DMSO-d6): 87.48 (d. J =9.4 Hz. 1H). 7.39 (s. 1H). 6.9 (bs. 1H). 6.79 (d. J = 8.4 Hz. 1H). 6.05 (s. 1H).
4.34 (s. 2H). 3.68 (s. 2H). 3.24 (s. 3H). 2.67 (bs. 2H). 1.98 (s. 3H).1.46 (bs. 6H). 1.24 (t. J = 7.2 Hz. 3H).
E je m p lo ________ 37 _________7 -f lu o ro -8 -(6 - f lu o ro -1 -(m e t¡ ls u lfo n ¡ l) -1 H - ¡n d o l-4 - ¡ l) -1.4.4 - tr ¡m e t¡ l-9 -( t r if lu o ro m e t¡ l) -4.5 -d ¡h ¡d ro -[1.2.41 tr ia z o lo [4.3 -a 1 q u ¡n o x a l¡n a
Una suspensión de 8-bromo-7-fluoro-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-4) (0,5 g, 1,32 mimóles, 1 eq), 6-fluoro-1-(imetilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-2) (0,536 g, 1,58 mimóles, 1,2 eq) y K2CO3 (0,55 g, 3,96 mimóles, 3 eq) en alcohol isoamílico y agua (2:1) (15 mL) se desgasificó con Ar durante 20 minutos seguido de la adición de Attaphos (0,047 g, 0,066 mmoles, 0,05 eq). La mezcla de reacción se agitó a 110 °C durante 16 horas en un tubo sellado. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se evapora a sequedad y el residuo se diluyó con EtOAc (50 mL). La capa orgánica se lavó con agua (2 x 30 mL), salmuera (30 mL), se secó sobre Na2SO4 anhidro y se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna para proporcionar 7-fluoro-8-(6-fluoro-1-(metilsulfonil)-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,055 g, 8 %) como un sólido blanquecino.
RMN (400 MHz, DMSO-d6, T=100 °C): 87,73 (d, J = 9,44 Hz, 1H), 7,60 (d, J = 3,64 Hz, 1H), 7,24 (bs, 2H), 7,17 (d, J = 10Hz, 1H), 6,51 (bs, 1H), 3,49 (s, 3H), 2,46 (s, 3H), 1,75 (bs, 3H), 1,38 (bs, 3H).
Ejemplo_____ 38:_____ 8-(3-c¡cloprop¡l-5-fluoro-1H-¡ndol-7-¡l)-6-fluoro-1.4.4.9-tetramet¡l-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-alquinoxalina
El ejemplo 38 se sintetizó en analogía con el procedimiento descrito para el ejemplo 29 usando 3-ciclopropil-5-fluoro-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-16) y el intermedio B-7.
RMN (400 MHz, DMSO-d6): 810,64 (s, 1H), 7,36 (d, J = 7,76 Hz, 1H), 7,17 (d, J = 10,64 Hz, 1H), 7,08 (s, 1H), 6,9 (d, J = 9,8 Hz, 1H), 6,49 (s, 1H), 2,5 (s, 3H), 1,98 (s, 3H), 1,93-1,9 (m, 1H), 1,53-1,48 (m, 6H), 0,85 (d, J = 8,08 Hz, 2H), 0,60 (d, J = 3,32 Hz, 2H).
Ejemplo 39: 4-(7-(7-fluoro-1.4.4.9-tetramet¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1quinoxal¡n-8-¡l)-1H-¡ndol-3-¡l)-2-met¡lbut-3-in-2-ol
Etapa 1: A una solución agitada de 7-fluoro-8-(1H-indol-7-il)-1,4,4,9-tetraimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (ejemplo 25) (3,7 g, 10,24 mmoles, 1 eq) en DMF (25 mL), se añadieron KOH (1,43 g, 25,62 mmoles, 2,5 eq) y yodo (2,6 g, 10,24 mmoles, 1,0 eq) en DMF (20 mL) a 0 °C y la mezcla de reacción resultante se agitó durante 1 hora a 0 °C. La mezcla de reacción se diluyó con EtOAc (800 mL), se lavó con metabisulfito de sodio acuoso (2 x 300 mL), agua (4 x 300 mL), solución de salmuera (300 mL), se secó (Na2SO4), se filtró y se concentró a presión reducida para proporcionar 7-fluoro-8-(3-yodo-1 H-indol-7-il)-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (3,0 g, 61 %).
Etapa 2: Una solución de 7-fluoro-8-(3-yodo-1H-indol-7-il)-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,3 g, 0,61 mmoles, 1,0 eq.) en DMF (5 mL) y TEA (5 mL) se desgasificó con Ar durante 20 minutos seguido de la adición de Cul (2,9 mg, 0,015 mmoles, 0,025 eq.), PdCb(PPh)3 (21,5 g, 0,03 mmoles, 0,05 eq.) y 2-metilbut-3-in-2-ol (0,077 g, 0,92 mmoles, 1,5 eq). La mezcla de reacción se agitó a RT durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se filtró a través de un lecho de celite y el filtrado
se concentró para obtener el producto crudo, que se purificó por HPLC preparativa para proporcionar 4-(7-(7-fluoro-1,4,4,9-tetrametil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1 H-indol-3-il)-2-metilbut-3-in-2-ol (0,08 g, 30 %) como un sólido blanco.
1H RMN (400 MHz, DMSO-da): 811,2 (s, 1H), 7,59 (d, J = 8,0 Hz, 1H), 7,54 (s, 1H), 7,20 (t, J = 7,6 Hz, 1H), 7,09 (d, J = 6,8 Hz, 1H), 6,79 (d, J = 10 HZ, 1H), 6,75 (s,1H), 5,37 (s, 1H), 2,46 (s, 3H), 1,92 (s, 3H) 1,44-1,51 (m,12H).
Ejemplo 40: 4-(7-(7-fluoro-1.4.4.9-tetramet¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1quinoxal¡n-8-¡l)-1H-¡ndol-3-¡l)-2-met¡lbut-3-in-2-amina
Una solución de 7-fluoro-8-(3-yodo-1H-¡ndol-7-¡l)-1,4,4,9-tetraiTiet¡l-4,5-d¡h¡dro-[1,2,4]tnazolo[4,3-a]qu¡noxal¡na (0,3 g, 0,61 mmoles, 1,0 eq.) en Dm F (1,8 mL) y TEA (0,17 mL, 1,23 mmoles, 2,0 eq) se desgasificó con Ar durante 20 minutos seguido de la adición de Cul (2,9 mg, 0,015 mmoles, 0,025 eq.), PdCb(Pph)3 (21,5 g, 0,03 mmoles, 0,05 eq.) y 2-metilbut-3-in-2-amina (0,103 g, 1,23 mmoles, 2,0 eq). La mezcla de reacción se agitó a RT durante 2 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se filtró a través de un lecho de celite y el filtrado se concentró para obtener el producto crudo, que se purificó por HPLC preparativa para proporcionar 4-(7-(7-fluoro-1,4,4,9-tetramet¡l-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]qu¡noxal¡n-8-¡l)-1H-¡ndol-3-¡l)-2-met¡lbut-3-¡n-2-am¡na (0,15 g, 55 %) como un sólido blanquecino.
iH RMN (400 MHz, DMSO-d6): 811,15 (s, 1H), 7,59 (d, J = 7,8 Hz, 1H), 7,48 (s, 1H), 7,19 (t, J = 7,4 Hz, 1H), 7,07 (d, J = 6,8 Hz, 1H), 6,79 (d, J = 10 HZ, 1H), 6,74 (s,1H), 2,46 (s, 3H), 2,05 (s, 1H), 1,92 (s, 3H) 1,42-1,53 (m,12H).
Ejemplo 41: 9-cloro-8-(3-c¡clobut¡l-1H-¡ndol-7-¡l)-7-fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
El ejemplo 42 se sintetizó en analogía con el procedimiento descrito para el ejemplo 37 usando 3-(tetrahidrofuran-3-il)-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-18) y el intermedio B-3.
iH RMN (400 MHz, DMSO-d6): 810,67 (s, 1H), 7,61 (d, J = 8,0 Hz, 1H), 7,15 (s, 1H), 7,08 (t, J = 7,6 Hz, 1H), 6,99 (d, J = 7,2 Hz, 1H), 6,78 (d, J = 10 Hz, 1H), 6,72 (s, 1H), 4,12-4,15 (m, 1H), 3,92-3,97 (m, 1H), 3,84 (q, J = 7,6 Hz, J = 15,6 Hz, 1H), 3,59-3,69 (m, 2H), 2,46 (s, 3H), 2,33-2,37 (m, 1H), 2,04-2,10 (m, 1H), 1,93 (s, 3H), 1,55 (s, 3H), 1,42 (s,
3H).
Ejemplo 43: 8-(3-et¡l-5-fluoro-1 H-¡ndol-7-¡l)-7.9-d¡fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
El ejemplo 43 se s¡ntet¡zó en analogía con el proced¡m¡ento descr¡to para el ejemplo 1 usando 3-et¡l-5-fluoro-7-(4.4.5.5-tetramet¡l-1.3.2-d¡oxaborolan-2-¡l)-1H-¡ndol (intermedio A-19) y el intermedio B-1.
1H RMN (400 MHz. DMSO-da): 8 10.81 (bs. 1H). 7.36 (d. J = 8.8 Hz. 1H). 7.20 (s. 2H). 6.99 (d. J = 7.2 Hz. 1H). 6.80 (d. J = 9.6 Hz. 1H). 2.69-2.71 (m. 2H). 1.54 (bs. 6H). 1.27 (bs. 3H); (CHs- om¡t¡do por DMSO).
Ejemplo 44: 2-(4-(9-et¡l-7-fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-f1.2.41tr¡azolof4.3-a1qu¡noxal¡n-8-¡l)-6-fluoro-1H-¡ndol-1-¡l)etanol
A una soluc¡ón ag¡tada del intermedio B-8 (0.14 g. 0.413 mmoles. 1 eq.) en 1.4-d¡oxano (10 mL) se añad¡eron CsF (0.19 g. 1.24 mmoles. 3 eq.) y el compuesto intermedio A-20 (0.138 g. 0.45 mmoles. 1.1 eq) en un tubo sellado. La soluc¡ón se desgas¡f¡có con Ar durante 20 m¡nutos segu¡do de la ad¡c¡ón de Pd(PPh3)4 (0.023 g. 0.021 mmoles. 0.05 eq). La mezcla de reacc¡ón se puso a reflujo a 90 °C durante 16 horas. Una vez completada la reacc¡ón (controlada por TLC). la mezcla de reacc¡ón se f¡ltró a través de un lecho de cel¡te. El f¡ltrado se concentró a pres¡ón reduc¡da para obtener el producto crudo que se pur¡f¡có med¡ante cromatografía en columna (MeOH al 5 %/DCM. Rf-0.3) segu¡do de HPLC preparat¡va para proporc¡onar 2-(4-(9-et¡l-7-fluoro-1.4.4-tr¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡n-8-¡l)-6-fluoro-1H-¡ndol-1-¡l)etanol (0.1 g. 56 %) como un sól¡do blanquec¡no.
1H RMN (400 MHz. DMSO-d6): 87.45-7.39 (m. 2H). 6.95 (d. J = 10 Hz. 1H). 6.83 (s. 1H). 6.75 (d. J = 10.1 Hz. 1H).
6.13 (s. 1H). 4.92 (s. 1H). 4.22 (d. J = 5.6 Hz. 2H). 3.75 (d. J = 4.8 Hz. 2H). 2.68-2.62 (m. 1H). 1.54-1.18 (m. 6H). 0.51 (s. 3H).
Ejemplo 69: 1-(but-2-¡n-1-¡l)-7.9-d¡fluoro-8-(5-fluoro-3-met¡l-1H-¡ndol-7-¡l)-4.4-d¡met¡l-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
Etapa 1: Una solución agitada de 6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (3,43 g, 16,18 mimóles, 1 eq.) en DMF (30 mL) a 0 °C se trató por partes durante 10 minutos con N-bromosuccinimida (3,02 g, 16,99 mimóles, 1,05 eq.). La mezcla de reacción se agitó a 0 °C durante 1 hora y a RT durante 30 minutos. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se diluye con agua (100 mL) y se extrae con EtOAc (3 x 100 mL). La capa orgánica combinada se lavó con agua (4 x 50 mL), salmuera (50 mL), se secó sobre Na2SO4 anhidro y se evaporó a presión reducida. El producto crudo se purificó mediante cromatografía en columna (gel de sílice malla 100-200, EtOAc al 30 %/hexano, valor Rf-0,5) para proporcionar 7-bromo-6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (4,0 g, 85 %) como un sólido marrón.
Etapa 2: A una solución de 7-bromo-6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (1,0 g, 3,44 mmoles, 1 eq.) en tolueno: EtOH (2:1) (20 mL) se añadieron una solución acuosa de Na2CO3 al 10 % (5,5 mL) y el intermedio A-15 (1,42 g, 5,16 mmoles, 1,5 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,199 g, 0,17 mmoles, 0,05 eq). La desgasificación continuó durante otros 10 minutos y la mezcla de reacción se calentó a 110 °C durante 16 horas en un tubo sellado. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se evaporó, el residuo se diluyó con agua (25 mL) y se extrajo con EtOAc (3 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (25 mL), salmuera (25 mL), se secaron sobre Na2SO4 anhidro y se evaporaron para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea (gel de sílice malla 100-200; EtOAc al 50 %/hexano; valor Rf-0,3) para proporcionar 6,8-difluoro-7-(5-fluoro-3-metil-1H-indol-7-il)-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (0,510 g, 41 %) como un sólido marrón.
Etapa 3: A una solución de 6,8-difluoro-7-(5-fluoro-3-metil-1H-indol-7-il)-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (0,500 g, 1,4 mmoles, 1 eq.) en tolueno (10 mL) se añadió reactivo de Lawesson (0,848 g, 2,1 mmoles, 1,5 eq.) a RT y la mezcla de reacción se puso a reflujo a 120 °C durante 30 minutos. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se enfrió, se inactivó con solución saturada de NaHCO3 (50 mL) seguido de extracción con EtOAc (3 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (25 mL), salmuera (25 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna (gel de sílice malla 100-200; EtOAc al 10 %/hexano; valor Rf-0,6) para proporcionar 6,8-difluoro-7-(5-fluoro-3-metil-1H-indol-7-il)-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (0,480 g, 91 %) como un sólido amarillo.
Etapa 4: A una solución de 6,8-difluoro-7-(5-fluoro-3-metil-1H-indol-7-il)-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona (0,240 g, 0,64 mmoles, 1 eq) en THF (6 mL) se añadió hidrato de hidrazina (0,11 mL, 2,32 mmoles, 3 eq) y la mezcla se agitó durante la noche a RT. La terminación de la formación de 5,7-difluoro-6-(5-fluoro-3-metil-1 H-indol-7-il)-3-hidrazono-2,2-dimetil-1,2,3,4-tetrahidroquinoxalina se controló mediante TLC y LCMS, (EtOAc; valor Rf-0,1). Esta mezcla de reacción se usó para la siguiente etapa sin procesamiento y purificación.
Etapa 5. A una solución de ácido pent-3-inoico (0,376 g, 3,84 mmoles, 6 eq) en benceno (8 mL) se añadió cloruro de oxalilo (0,8 mL) a 0 °C y la mezcla se calentó a 50 °C durante 1 hora bajo atmósfera de nitrógeno. La mezcla de reacción se concentró a presión reducida en atmósfera de nitrógeno a 25 °C. El residuo se disolvió en THF (5 mL) y la solución resultante se añadió gota a gota a la solución de 5,7-difluoro-6-(5-fluoro-3-metil-1H-indol-7-il)-3-hidrazono-2,2-dimetil-1,2,3,4-tetrahidroquinoxalina ya preparada (mencionada anteriormente) a 0 °C. Se añadió TEA (0,6 mL, 3,84 mmoles, 6 eq) a la mezcla y se agitó durante 1,5 horas a RT. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se inactivó con agua (5 mL) y se extrajo con EtOAc (3 x 20 mL). Las capas orgánicas combinadas se lavaron con salmuera (10 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener N'-(6,8-difluoro-7-(5-fluoro-3-metil-1H-indol-7-il)-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-iliden)pent-3-inohidrazida cruda (0,285 g) (EtOAc al 50 %-hexano; valor Rf-0,5) que se usó para la siguiente etapa sin purificación
adicional.
Etapa 6: A una solución de N'-(6,8-difluoro-7-(5-fluoro-3-metil-1H-indol-7-il)-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-iliden)pent-3-inohidrazida (0,280, 0,62 mimóles) en n-butanol (8 mL) se añadió ácido acético glacial (cantidad catalítica, 2 gotas con tubo capilar) y la mezcla se calentó a 140 °C durante 3 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se concentró a presión reducida. El residuo se diluyó con agua (25 mL) y se extrajo con EtOAc (3 x 50 mL). La parte orgánica combinada se lavó con salmuera (10 mL), se secó (Na2SO4 anhidro) y se concentró a presión reducida hasta una masa pegajosa que se purificó por HPLC preparativa (MeOH al 5 %-DCM; valor Rf-0,35) para obtener 1 -(but-2-in-1-il)-7,9-difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (57 mg, 10 % en tres etapas) como un sólido blanquecino [otra reacción a escala de 240 mg a partir de 6,8-difluoro-7-(5-fluoro-3-metil-1H-indol-7-il)-3,3-dimetil-3,4-dihidroquinoxalina-2(1H)-tiona se ha preparado y el rendimiento mencionado aquí es el rendimiento combinado].
1H RMN (400 MHz, DMSO-d6): 8 10,74 (s, 1H), 7,34 (dd, 1H), 7,21 (s, 2H), 6,94 (dd, 1H), 6,78 (d, 1H), 3,91 (s, 2H), 2,26 (s, 3H), 1,60 (s, 6H), 1,51 (bs, 3H).
Ejemplo______70:______1-(but-2-¡n-1-¡l)-7.9-d¡fluoro-4.4-d¡met¡l-8-(3-met¡l-1H-¡ndol-7-¡l)-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-alquinoxalina
Etapa 1: A una solución de 7-bromo-6,8-difluoro-3,3-dimetil-3,4-dihidroquinoxalin-2(1H)-ona (1,32 g, 4,53 mmoles, 1 eq.) en tolueno: EtOH (2:1) (15 mL) se añadieron solución acuosa de Na2CO3 al 10 % (7,3 mL) y 3-metil-7-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (1,75 g, 6,8 mmoles, 1,5 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,262 g, 0,23 mmoles, 0,05 eq). La desgasificación continuó durante otros 10 minutos y la mezcla de reacción se calentó a 110 °C durante 16 horas en un tubo sellado. Una vez completada la reacción (controlada por TLC), el disolvente se evaporó, el residuo se diluyó con agua (25 mL) y se extrajo con EtOAc (3 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (25 mL), salmuera (25 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna instantánea (gel de sílice malla 100-200; EtOAc al 50 %/hexano; valor Rf-0,3) para proporcionar 6,8-difluoro-3,3-dimetil-7-(3-metil-1H-indol-7-il)-3,4-dihidroquinoxalin-2(1H)-ona (0,55 g, 35 %) como un sólido marrón.
Etapa 2: A una solución de 6,8-difluoro-3,3-dimetil-7-(3-metil-1H-indol-7-il)-3,4-dihidroquinoxalin-2(1H)-ona (0,55 g,
1,61 mimóles, 1 eq.) en tolueno (10 mL) se añadió reactivo de Lawesson (0,975 g, 2,41 mimóles, 1,5 eq.) a RT y la mezcla de reacción se puso a reflujo a 120 °C durante 30 minutos. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se enfrió, inactivó con solución saturada de NaHCO3 (50 mL) seguido de extracción con EtOAc (3 x 100 mL). Las capas orgánicas combinadas se lavaron con agua (25 mL), salmuera (25 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna (gel de sílice malla 100-200; EtOAc al 10 %/hexano; valor Rf-0,7) para proporcionar 6,8-difluoro-3,3-dimetil-7-(3-metil-1H-indol-7-il)-3,4-dihidroquinoxalina-2(1H)-tiona (0,503 g, 87 %) como un sólido amarillo.
Etapa 3: A una solución de 6,8-difluoro-3,3-dimetil-7-(3-metil-1H-indol-7-il)-3,4-dihidroquinoxalina-2(1H)-tiona (0,400 g, 1,12 mmoles, 1 eq) en THF (8 mL) se añadió hidrato de hidrazina (0,16 mL, 3,36 mmoles, 3 eq) y la mezcla se agitó durante la noche a RT. La terminación de la formación de 5,7-difluoro-3-hidrazono-2,2-dimetil-6-(3-metil-1H-indol-7-il)-1,2,3,4-tetrahidroquinoxalina se controló mediante TLC y LCMS, (EtOAc; valor Rf-0,1). Esta mezcla de reacción se usó para la siguiente etapa sin procesamiento y purificación.
Etapa 4: A una solución de ácido pent-3-inoico (0,658 g, 6,72 mmoles, 6 eq) en benceno (10 mL) se añadió cloruro de oxalilo (1,4 mL) a 0 °C y la mezcla se calentó a 50 °C durante 1 hora bajo atmósfera de nitrógeno. La mezcla de reacción se concentró a presión reducida en atmósfera de nitrógeno a 25 °C. El residuo se disolvió en THF (5 mL) y la solución resultante se añadió gota a gota a la solución de 5,7-difluoro-3-hidrazono-2,2-dimetil-6-(3-metil-1H-indol-7-il)-1,2,3,4-tetrahidroquinoxalina ya preparada (mencionada anteriormente) a 0 °C. Se añadió TEA (1 mL, 6,72 mmoles, 6 eq) a la mezcla y se agitó durante 1,5 horas a RT. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se inactivó con agua (5 mL) y se extrajo con EtOAc (3 x 20 mL). Las capas orgánicas combinadas se lavaron con salmuera (10 mL), se secaron sobre Na2SO4 anhidro y el disolvente se evaporó para obtener N'-(6,8-difluoro-3,3-dimetil-7-(3-metil-1 H-indol-7-il)-3,4-dihidroquinoxalin-2(1H)-iliden)pent-3-inohidrazida cruda (0,450 g) (EtOAc al 50 %-hexano; valor Rf-0,5) que se usó para la siguiente etapa sin purificación adicional.
Etapa 5. A una solución de N'-(6,8-difluoro-3,3-dimetil-7-(3-metil-1H-indol-7-il)-3,4-dihidroquinoxalin-2(1H)-iliden)pent-3-inohidrazida (0,450 g, 1,03 mmoles) en n-butanol (8 mL) se añadió ácido acético glacial (cantidad catalítica, 2 gotas con tubo capilar) y la mezcla se calentó a 140 °C durante 3 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se concentró a presión reducida. El residuo se diluyó con agua (25 mL) y se extrajo con EtOAc (3 x 50 mL). La parte orgánica combinada se lavó con salmuera (10 mL), se secó (Na2SO4 anhidro) y se concentró a presión reducida hasta una masa pegajosa que se purificó por HPLC preparativa (MeOH al 5 %-DCM; valor Rf-0,35) para obtener 1 -(but-2-in-1-il)-7,9-difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (76 mg, 11 % en tres etapas) como un sólido blanquecino [otra reacción a escala de 200 mg a partir de 6,8-difluoro-3,3-dimetil-7-(3-metil-1H-indol-7-il)-3,4-dihidroquinoxalina-2(1H)-tiona se ha preparado y el rendimiento mencionado aquí es el rendimiento combinado].
1H RMN (400 MHz, DMSO-d6): 810,60 (s, 1H), 7,56 (d, 1H), 7,06-7,15 (4H), 6,77 (d, 1H), 3,90 (s, 2H), 2,29 (s, 3H), 1,60 (s, 6H), 1,51 (s, 3H).
Ejemplo______ 76______ 7-fluoro-8-(5-fluoro-3-(prop-1-in-1-il)-1H-indol-7-il)-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1.2.41tr¡azolo[4,3-a1qu¡noxal¡na
Etapa-3
Etapa 1: A una solución del intermedio B-17 (1,0, 2,82 mimóles, 1 eq) en tolueno: etanol (2:1) (15 mL) se añadió solución de Na2CO3 al 10 % (2 mL) y 5-fluoro-7-(tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (1,1 g, 4,22 mmoles, 1,5 eq) en un tubo sellado. La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,162 g, 0,14 mmoles, 0,05 eq). La mezcla de reacción se puso a reflujo a 110 °C durante 16 horas. Una vez completada la reacción (controlada por LCMS), la mezcla de reacción se evapora a sequedad y el residuo se diluyó con EtOAc (100 mL). La capa orgánica se lavó con agua (2 x 30 mL), salmuera (30 mL), se secó sobre Na2SO4 anhidro y el disolvente se evaporó para obtener el producto crudo, que se purificó mediante cromatografía en columna combiflash (MeOH al 5 %/DCM; valor Rf-0,4) para proporcionar 7-fluoro-8-(5-fluoro-1H-indol-7-il)-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (1,1 g, 96 %) como un sólido blanquecino.
Etapa 2: A una solución agitada de 7-fluoro-8-(5-fluoro-1H-indol-7-il)-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalina (1,1 g, 2,68 mmoles, 1 eq) en DMF (20 mL) se añadió hidróxido de potasio en polvo (0,39 g, 6,95 mmoles, 2,5 eq). La mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (1,06g, 4,18 mmoles, 1,5 eq) a la mezcla de reacción y se agitó durante 4 horas. La mezcla de reacción se diluyó con EtOAc (150 mL) y se lavó con agua (5 x 30 mL) y salmuera (30 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna de gel de sílice (230-400) (MeOH al 5 %/DCM, valor Rf-0,4) para proporcionar 7-fluoro-8-(5-fluoro-3-yodo-1H-indol-7-il)-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,26 g, 18 %) como un sólido marrón claro.
Etapa 3: Una solución de 7-fluoro-8-(5-fluoro-3-yodo-1H-indol-7-il)-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1.2.4] triazolo[4,3-a]quinoxalina (0,26 g, 0,49 mmoles, 1 eq) en THF y TEA (1:1) (6 mL) se desoxigenó mediante Ar durante 10 minutos en un tubo sellado. Se añadió Pd(PPh3)2Cl2 (0,017 g, 0,024 mmoles, 0,05 eq) y Cul (0,019 g, 0,097 mmoles, 0,1 eq) a la mezcla de reacción y se desoxigenó de nuevo mediante Ar durante 10 minutos a -78 °C. En el tubo de ensayo, el gas de propino se condensó en TEA (3 mL) a -78°C. El volumen se elevó a 5 mL. El gas de propino condensado se vertió instantáneamente en la mezcla de reacción a -78°C. La mezcla de reacción se agitó durante 2 horas a -78 °C y 14 horas a RT. La mezcla de reacción se diluyó con DCM (50 mL). La capa orgánica se lavó con agua (2 x 20 mL) y salmuera (20 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna de gel de sílice (230-400) (MeOH al 5 %/DCM, valor Rf-0,4) para proporcionar 7-fluoro-8-(5-fluoro-3-(prop-1-in-1-il)-1H-indol-7-il)-1-(metoximetil)-4,4,9-trimetil-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,055 g, 25 %) como un sólido blanquecino.
1H RMN (400 MHz, DMSO-d6): 811,21 (s, 1H), 7,59 (d, J = 2,28 Hz, 1H), 7,28 (dd, J = 1,96 Hz, J = 6,96 Hz, 1H), 6,96 (dd, J = 2,24Hz, J = 7,56 Hz, 1H), 6,83 (s, 1H), 6,78 (d, J = 10,08 Hz, 1H), 4,69 (d, J = 13,32 Hz, 1H), 4,61 (d, J = 13,32 Hz, 1H), 3,25 (s, 3H), 2,09 (s, 3H), 1,98 (s, 3H), 1,52 (s, 3H), 1,5 (s, 3H).
Ejemplo_____ 77_____ (7-fluoro-8-(5-fluoro-3-(prop-1-¡n-1-¡l)-1H-¡ndol-7-¡l)-4.4.9-tr¡met¡l-4.5-d¡h¡dro-[1,2.41tr¡azolo[4.3-a1quinoxal¡n-1-¡l)metanol
El Ejemplo 77 se sintetizó a partir del intermedio B-18 siguiendo una ruta sintética similar a la descrita para el Ejemplo 76.
1H RMN (400 MHz, DMSO-d6): 811,14 (s, 1H), 7,59 (s, 1H), 7,28 (d, J = 7,28 Hz 1H), 6,98 (d, J = 9,6 Hz, 1H), 6,78 (t, J = 6,96 Hz, 2H), 5,53 (d, J = 5,48 Hz, 1H), 4,73 (d, J = 5,4 Hz, 2H), 2,08 (d, J = 9,28 Hz, 3H), 2,03(s, 3H), 1,53 (s, 3H), 1,48 (s, 3H).
Ejemplo 78: 1-(7-fluoro-8-(5-fluoro-3-(prop-1-¡n-1-¡l)-1H-¡ndol-7-¡l)-4.4.9-tr¡met¡l-4.5-d¡h¡dro-H.2.41tr¡azolor4.3-a1qu¡noxal¡n-1-¡l)etanol
El Ejemplo 78 se s¡ntet¡zó a part¡r del intermedio B-19 s¡gu¡endo una ruta s¡ntét¡ca s¡m¡lar a la descr¡ta para el Ejemplo 76.
1H RMN (400 MHz. DMSO-d6): 611.25 (s. 1H). 10.9 (bs. 2H). 7.59 (t. J = 2.56Hz. 2H). 7.28 (d. J = 9.04 Hz. 2H). 7.06 (d. J = 9.72 Hz. 1H). 6.96 (dd. J = 2.32 Hz. J = 7.6 Hz. 2H). 6.77-6.71 (m. 4H). 5.5 (d. J = 7.04Hz. 1H). 5.36 (bs. 1H).
5.03-4.95 (m. 2H). 2.08 (t. J = 6.6Hz. 10H). 1.55 (bs. 17H).
Ejemplo______ 79______ 7-fluoro-8-(5-fluoro-3-(prop-1-¡n-1-¡l)-1H-¡ndol-7-¡l)-1-(2-metox¡et¡l)-4.4.9-tr¡met¡l-4.5-d¡h¡dror1.2.4ltr¡azolor4.3-alqu¡noxal¡na
El Ejemplo 79 se s¡ntet¡zó a part¡r del intermedio B-20 s¡gu¡endo una ruta s¡ntét¡ca s¡m¡lar a la descr¡ta para el Ejemplo 76.
1H RMN (400 MHz. DMSO-d6): 6 11.29 (s. 1H). 7.59 (d. J = 2.52 Hz. 1H). 7.28 (dd. J = 1.6 Hz. J = 6.8 Hz 1H). 7.01 (bs. 1H). 6.81 (s. 1H). 6.79 (s. 1H). 3.74 (t. J = 6.56 Hz. 2H). 3.2 (s. 3H). 3.07 (bs. 1H). 2.97 (bs. 1H). 2.08 (d. J = 9.48 Hz. 3H). 1.95 (s. 3H). 1.48 (bs. 6H).
Ejemplo 87: 8-(3-c¡cloprop¡l-1 H-¡ndol-7-¡l)-7-fluoro-1.4.4-tr¡met¡l-9-(tr¡fluoromet¡l)-4.5-d¡h¡dro-[1.2.4ltr¡azolo[4.3-a1qu¡noxal¡na
A partir de 7-fluoro-8-(1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (= Ejemplo 86), se sintetizó el ejemplo 87 en analogía con la síntesis descrita para el ejemplo 33.
1H RMN (400 MHz, DMSO-da): 810,58-10,6 (1H), 7,66 (d, J = 8,0 Hz, 1H), 7,36-7,40 (1H), 7,15-6,99 (m, 4H), 2,44 (s, 3H), 1,94 (m, 1H), 1,75 (s, 3H), 1,31-1,34 (3H), 0,85 (d, J = 7,96 Hz, 2H), 0,63 (m, 2H).
Ejemplo 89: 7-(7-fluoro-1.4.4-tr¡met¡l-9-(tr¡fluoromet¡l)-4.5-d¡h¡dro-[1.2.41tr¡azolo[4,3-a1qu¡noxal¡n-8-¡l)-1H-¡ndol-3-carbonitrilo
Etapa 1: A una solución agitada de 7-fluoro-8-(1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1.2.4] tnazolo[4,3-a]quinoxal¡na (=Ejemplo 86) (0,4 g, 1,04 mmoles, 1 eq) en DMF (12 mL) se añadió polvo de KOH (0,147 g, 2,62 mmoles, 2,5 eq). La mezcla de reacción se agitó durante 30 minutos a RT. Luego, se añadió yodo (0,264 g, 2,08 mmoles, 2 eq) a la mezcla de reacción y se agitó durante 4 horas. La mezcla de reacción se diluyó con EtOAc (80 mL) y se lavó con agua (5 x 20 mL) y salmuera (30 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo, que se purificó mediante cromatografía en columna de gel de sílice (230-400) (MeoH al 5 %/DCM, valor Rf-0,4) para proporcionar 7-fluoro-8-(3-yodo-1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a1quinoxalina (0,400 g, 66 %) como un sólido marrón claro.
Etapa 2: Una suspensión en agitación de 7-fluoro-8-(3-yodo-1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1.2.4] triazolo[4,3-a]qu¡noxal¡na (0,2 g, 0,369 mmoles, 1 eq), Zn(CN)2 (0,043 g, 0,369 mmoles, 1 eq) y t Me DA (0,016 mL, 0,110 mmoles, 0,3 eq) en DMA (3 mL) se desoxigenó bien con Ar durante 10 minutos. Se añadió Pd2dba3 (0,033 g, 0,0369 mmoles, 0,1 eq) y Xantphos (0,021 g, 0,0369 mmoles, 0,1 eq) a la mezcla de reacción y de nuevo se desoxigenó con Ar durante 10 minutos. Finalmente, la mezcla de reacción se agitó durante 14 horas a 90 °C. La mezcla de reacción se filtró a través de un lecho de celite y el filtrado se diluyó con EtOAc (30 mL). La capa orgánica se lavó con agua (5 x 20 mL) y salmuera (20 mL). La capa orgánica se secó sobre Na2SO4 anhidro, se concentró a presión reducida para obtener el material crudo que se purificó mediante cromatografía en columna de gel de sílice (230-400) (MeOH al 5 %/DCM, valor Rf-0,4) para proporcionar 7-(7-fluoro-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,41triazolo[4,3-a]quinoxalin-8-il)-1 H-indol-3-carbonitrilo (0,072 g, 44 %) como un sólido blanquecino.
1H RMN (400 MHz, DMSO-d6): 812,10-12,19 (1H), 8,28 (d, J = 2,7 Hz, 1H), 7,72 (d, J = 6,8 Hz, 1H), 7,46-7,51 (1H), 7,34-7,25 (m, 2H), 7,19-7,12 (m, 1H), 2,45 (s, 3H), 1,76 (s, 3H), 1,32-1,36 (3H).
Ejemplo 446: 7-fluoro-1.4.4-tr¡met¡l-8-(1-(met¡lsulfon¡l)-1H-¡ndazol-4-¡l)-9-(tr¡fluoromet¡l)-4.5-d¡h¡dro-[1.2.41tr¡azolo[4.3-a1qu¡noxal¡na
A una solución de 8-bromo-7-fluoro-1,4,4-trimetil-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (intermedio B-4) (0,3 g, 0,7912 mimóles, 1 eq.) en alcohol t-amílico: dioxano (2:1) (15,0-7,0 ml) se añadió solución de K2CO32M (1,0 ml) y 1-(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indazol (intermedio A-22) (0,48 g, 1,5824 mmoles, 2,0 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Attaphos (0,028 g, 0,0395 mmoles, 0,05 eq). La mezcla de reacción se calentó a 90 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se filtró a través de una almohadilla de celite y se lavó con EtOAc. La capa orgánica combinada se evaporó para obtener el producto crudo que se purificó mediante HPLC preparativa (valor Rf-0,3: MeOH al 5 %/DCM) para proporcionar 7-fluoro-1,4,4-trimetil-8-(1-(metilsulfonil)-1H-indazol-4-il)-9-(trifluorometil)-4,5-dihidro-[1,2,4]triazolo[4,3-a]quinoxalina (0,065 g, 17 %) como un sólido blanco.
1H RMN (400 MHz, DMSO-d6): 88,34 (s, 1H), 8,09 (d, 1H), 7,73 (t, 1H), 7,45 (bs, 1H), 7,27 (s, 1H), 7,19 (d, 1H), 3,50 (s, 3H), 2,49 (s, 3H), 1,66-1,78 (bs, 3H), 1,23-1,52 (bs, 3H).
Ejemplo 450: 1.4.4.9-tetramet¡l-8-(1-(met¡lsulfon¡l)-1H-¡ndol-4-¡l)-4.5-d¡h¡dro-[1.2,41tr¡azolo[4.3-a1qu¡noxal¡na
A una solución de 8-bromo-1,4,4,9-tetrametil-4,5-d¡h¡dro-[1,2,4]tr¡azolo[4,3-a]alqu¡noxal¡na (intermedio B-40) (0,15 g, 0,488 mmoles, 1 eq) en dioxano: agua (10:1) (22 ml) se añadió CsF (0,222 g, 1,464 mmoles, 3 eq) y 1 -(metilsulfonil)-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)-1H-indol (intermedio A-12) (0,313 g, 0,977 mmoles, 2 eq). La solución se desgasificó con Ar durante 20 minutos seguido de la adición de Pd(PPh3)4 (0,028 g, 0,024 mmoles, 0,05 eq). La mezcla de reacción se calentó a 90 °C durante 16 horas. Una vez completada la reacción (controlada por TLC), la mezcla de reacción se filtró a través de una almohadilla de celite y se lavó con EtOAc. La capa orgánica combinada se evaporó para obtener el producto crudo que se purificó por HPLc preparativa para proporcionar 1,4,4,9-tetrametil-8-(1-(metilsulfonil)-1H-indol-4-il)-4,5-dihidro-[1,2,4]triazolo[4,3-a1quinoxalina (0,085 g, 41 %) como un sólido blanco.
1H RMN (400 MHz, dmso-d6): 87,88-7,85 (m, 1H), 7,62 (d, 1H), 7,48 (t, 1H), 7,28 (d, 1H), 7,13-7,11 (m, 1H), 6,97 6,95 (m, 1H), 6,53 (s, 2H), 3,49 (s, 3H), 2,03 (s, 3H), 1,46 (bs, 6H).
En las siguientes tablas 4, 5, 6 y 7 se resume cómo se han obtenido los ejemplos restantes.
Tabla 4:
Los ejemplos en la Tabla 5 se sintetizaron en analogía con el Ejemplo 1.
Los ejemplos en la Tabla 6 se sintetizaron en reacciones químicas estándar que son conocidas por el experto en la técnica:
Tabla 7:
Las estructuras moleculares y los nombres químicos de los Ejemplos resumidos en las Tablas 4, 5, 6 y 7 se proporcionan en la Tabla 8 a continuación:
metil-
Modo de acción agonista en el receptor de glucocorticoides
La línea celular informadora CHO-Gal4/GR consistía en una línea celular de ovario de hámster chino (CHO) (Leibniz
Institute D SM Z - Germán Collection of Microorganisms and Cell Cultures GmbH: ACC-110) que contiene un gen de luciferasa de luciérnaga bajo el control del dominio de unión a ligando de GR fusionado al dominio de unión al ADN (DBD) de GAL4 (GAL4 DBD-GR) integrado de forma estable en células CHO. Esta línea celular se estableció por transfección estable de células CHO con una construcción informadora G,AL4-UAS-Luciferasa. En una etapa posterior, se transfectó el dominio de unión a ligando de GR clonado en pIRES2-EGFP-GAL4 que contiene el dominio de unión a ADN de GAL4 de pFA-AT2. Esta construcción de fusión activó la expresión de la luciferasa de luciérnaga bajo el control de una secuencia de activación de GAL4 en 5' multimerizada (UAS). La señal de la luminiscencia emitida fue registrada por FLIPRTETRA. Esto permitió la detección específica de la activación inducida por ligando del GR y, por lo tanto, la identificación de compuestos con propiedades agonistas. El informador GAL4/UAS se mezcló previamente con un vector que expresaba constitutivamente luciferasa de Renilla, que funcionó como un control positivo interno para la eficiencia de la transfección.
El medio de cultivo completo para el ensayo fue:
• MEZCLA DMEM F-12 (1:1) (LONZA No. de cat.: BE04-687F/U1) 500mL
• 5 mL de Piruvato de Sodio 100 mM (LONZA No. de cat.: BE12-115E)
• 25 mL de Bicarbonato de Sodio al 7,5 % (LONZA No. de cat.: BE17-613E)
• 6,5 mL de Hepes 1 M (LONZA No. de cat.: BE17-737E)
• 5 mL de Penicilina/Estreptomicina 100X (LONZA No. de cat.: DE17-602E)
• 50 mL de Suero Bovino Fetal (Euroclone No. de cat.: ECS 0180L)
• 0,25 mL de 10mg/mL de Puromicina (InvivoGen cat.: ant-pr-1)
• 0,5 mL de 100 mg/mL de Zeocina (InvivoGen cat.: ant-zn-1)
Se suspendieron células CHO-Gal4/GR crioconservadas en medio completo y se sembraron 5.000 células/25 pl/pocillo en los pocillos de placas de ensayo de poliestireno de 384 pocillos (Thermo Scientific, No. de cat. 4332) y se cultivaron a 37 °C, CO2 al 5 % y 95 % de humedad. Después de 24 horas, se eliminó cuidadosamente el medio de crecimiento y se reemplazó por 30 pl de Opti-MEM (GIBCO, No. de cat. 31985062) como tampón de ensayo. Para ensayar los compuestos, se generó una curva de dilución del compuesto semilogarítmica de 8 puntos en DMSO al 100 % a partir de una preparación madre 2 mM y los compuestos luego se diluyeron a 1:50 en Opti-MEM. Luego, se añadieron 10 pl de los compuestos a los pocillos que contenían 30 pl de Opti-MEM dando como resultado un rango de concentración de ensayo final de 10 pM a 0,003 pM en DMSO al 0,5 %. Los compuestos se ensayaron a 8 concentraciones en puntos de datos por cuadruplicado. Las células se incubaron durante 6 horas con compuestos y beclometasona (Sigma, No. de cat. Y0000351) como compuesto de control a 37 °C, CO2 al 5 % y 95 % de humedad en un volumen total de 40 pl. Finalmente, las células se lisaron con 20 pl de solución de Tritón/Luciferina y la señal de la luminiscencia emitida se registró en FLIPRTETRA durante 2 minutos.
La eficacia relativa de un compuesto (% de efecto) se calculó en función del efecto completo del agonista beclometasona:
% de efecto= ((compuesto- mín)/(máx - mín)) x 100
[mín=Opti-MEM solo, máx=beclometasona]
Para calcular la CE50, máx, mín y el factor de pendiente para cada compuesto, se ajustó una curva de respuesta a la concentración representando el % de efecto frente a la concentración del compuesto usando una ecuación logística de 4 parámetros:
y = A (B-A)/(1+((10C)/x)D)
[A=mín y, B=máx y, C=logCE50, D=pendiente]
Modo de acción antagonista en el receptor de glucocorticoides
La línea celular informadora CHO-Gal4/GR consistía en una línea celular de ovario de hámster chino (CHO) (Leibniz Institute D SM Z - German Collection of Microorganisms and Cell Cultures GmbH: ACC-110) que contiene un gen de luciferasa de luciérnaga bajo el control del dominio de unión a ligando de GR fusionado al dominio de unión al ADN (DBD) de GAL4 (GAL4 DBD-GR) integrado de forma estable en células CHO. Esta línea celular se estableció por transfección estable de células CHO con una construcción informadora G^L4-UAS-Luciferasa. En una etapa posterior, se transfectó el dominio de unión a ligando de GR clonado en pIRES2-EGFP-GAL4 que contiene el dominio de unión
a ADN de GAL4 de pFA-AT2. Esta construcción de fusión activó la expresión de la luciferasa de luciérnaga bajo el control de una secuencia de activación de GAL4 en 5' multimerizada (UAS). La señal de la luminiscencia emitida se registró por FLIPRTETRA Esto permitió la detección específica de las propiedades antagonistas de los compuestos al medir la inhibición inducida por ligando de GR activado con beclometasona. El informador GAL4/UAS se mezcló previamente con un vector que expresaba constitutivamente luciferasa de Renilla, que funcionó como un control positivo interno para la eficiencia de la transfección.
El medio de cultivo completo para el ensayo fue:
MEZCLA DMEM F-12 (1:1) (LONZA No. de cat.: BE04-687F/U1) 500mL
5 mL de Piruvato de Sodio 100 mM (LONZA No. de cat.: BE12-115E)
25 mL de Bicarbonato de Sodio al 7,5 % (LONZA No. de cat.: BE17-613E)
6,5 mL de Hepes 1 M (LONZA No. de cat.: BE17-737E)
5 mL de Penicilina/Estreptomicina 100X (LONZA No. de cat.: DE17-602E)
50 mL de Suero Bovino Fetal (Euroclone No. de cat.: ECS 0180L)
0,25 mL de 10mg/mL de Puromicina (InvivoGen cat.: ant-pr-1)
0,5 mL de 100 mg/mL de Zeocina (InvivoGen cat.: ant-zn-1)
Se suspendieron células CHO-Gal4/GR crioconservadas en medio completo y se sembraron 5.000 células/25 pl/pocillo en los pocillos de placas de ensayo de poliestireno de 384 pocillos (Thermo Scientific, No. de cat.4332) y se cultivaron a 37 °C, CO 2 al 5 % y 95 % de humedad. Después de 24 horas, se eliminó cuidadosamente el medio de crecimiento y se reemplazó por 20 pl de Opti-MEM (GIBCO, No. de cat. 31985062) como tampón de ensayo. Para ensayar los compuestos, se generó una curva de dilución del compuesto semilogarítmica de 8 puntos en DMSO al 100 % a partir de una preparación madre 2 mM y los compuestos luego se diluyeron a 1:50 en Opti-MEM. Para ensayar los compuestos en el modo antagonista, se añadieron 10 pl de compuestos a los pocillos que contenían 20 pl de Opti-MEM y se incubaron durante 10 minutos. Después de esta preincubación, se añadieron 10 pl del agonista de referencia beclometasona (Sigma, No. de cat. Y0000351) a una CE50 de 2,5 nM, lo que dio como resultado un rango de concentración de ensayo final de 10 pM a 0,003 pM en DMSO al 0,5 % en un volumen total de 40 pl. Los compuestos se ensayaron a 8 concentraciones en puntos de datos por cuadruplicado. Las células se incubaron durante 6 horas con compuestos y mifepristona como compuesto de control (Sigma, No. de cat. M8046) a 37 °C, CO 2 al 5 % y 95 % de humedad. Finalmente, las células se lisaron con 20 pl de solución de Tritón/Luciferina y la señal de la luminiscencia emitida se registró en FLIPRTETRA durante 2 minutos.
La eficacia relativa de un compuesto (% de efecto) se calculó en función del efecto completo del antagonista mifepristona:
% de efecto= ((compuesto- mín)/(máx - mín)) x -100
[mín=Opti-MEM solo, máx=mifepristona]
Para calcular la CI
50
, máxi, mín y el factor de pendiente para cada compuesto, se ajustó una curva de respuesta a la concentración representando el % de efecto frente a la concentración del compuesto usando una ecuación logística de 4 parámetros:
y = A (B-A)/(1+((10C)/x)D)
[A=mín y, B=máx y, C=logCl50, D=pendiente]
En la Tabla 9 a continuación, se resumen los rangos de CI50 o CE50 de los Ejemplos que se observaron en el ensayo agonista o el ensayo antagonista descritos anteriormente.
Tabla 9 (A < 100nM; B = 100nM-1pM; C = 1pM-15pM; n.d. = no determinado):
Claims (15)
1. Un compuesto según la fórmula general (I),
en donde
R1 representa H; alquilo-C
1
-
10
; ddoalquilo-C3-10; heterocicloalquilo de 3 a 7 miembros; arilo; o heteroarilo de 5 o 6 miembros;
en donde cicloalquilo-C3-10, heterocicloalquilo de 3 a 7 miembros, arilo y heteroarilo de 5 o 6 miembros se pueden puentear opcionalmente mediante alquileno-C 1-6 ;
R2 representa H; F; Cl; Br; I; CN; alquilo-C 1-10 ; cicloalquilo-C3-10; O-alquilo-C 1-10 ; N(H)(alquilo-C 1-10 ), N(alquilo-C 1-10 ) 2 ; C(O)-alquilo-C 1-10 ; C(O)-O-alquilo-C 1-10 ; C(O)-NH 2 ; C(O)-N(H)(alquilo-C 1-10 ); C(O)-N(alquilo-C 1-10 ) 2 ; O-cicloalquilo-C3-10 ; N(H)(cicloalquilo-C3-10), N(alquilo-C1-10)(cicloalquilo-C3-10); C(O)-cicloalquilo-C3-10; C(O)-O-cicloalquilo-C3-10; C(O)-N(H)(cicloalquilo-C3-10) o C(O)-N(alquilo-C1-10)(cicloalquilo-C3-10);
en donde el cicloalquilo-C3-10 se puede puentear opcionalmente mediante alquileno-C 1-6 ;
R3 representa H; F; Cl; Br; I; CN; alquilo-C 1-10 ; cicloalquilo-C3-10; O-alquilo-C 1-10 ; N(H)(alquilo-C 1-10 ); N(alquilo-C 1-10 ) 2 ; C(O)-alquilo-C 1-10 ; C(O)-O-alquilo-C 1-10 ; C(O)-NH 2 ; C(O)-N(H)(alquilo-C 1-10 ); C(O)-N(alquilo-C 1-10 ) 2 ; O-cicloalquilo-C3-10 ; N(H)(cicloalquilo-C3-10), N(alquilo-C1-10)(cicloalquilo-C3-10); C(O)-cicloalquilo-C3-10; C(O)-O-cicloalquilo-C3-10; C(O)-N(H)(cicloalquilo-C3-10) o C(O)-N(alquilo-C1-10)(cicloalquilo-C3-10);
en donde el cicloalquilo-C3-10 se puede puentear opcionalmente mediante alquileno-C 1-6 ;
R5 y R6 representan independientemente uno de otro H o alquilo-C1-4 no sustituido;
X representa N o NR7;
Z representa N, NR7 o CR9;
con la condición de que
cuando X representa NR7, Z representa N o CR9;
cuando X representa N, Z representa NR7;
R7 representa H o L-R8; en donde
L representa un enlace; S(O); S(O)
2
; alquileno-C
1-6
; C(O); alquileno-C
1-6
-C(O); C(O)-O; alquileno-C
1-6
-C(O)-O; alquileno-C
1-6
-N(H)-C(O); alquileno-C
1-6
-N(alquilo-C
1-10
)-C(O); alquileno-C
1-6
-N(H)-C(O)-O; alquileno-C
1-6
-N(alquilo-C
1-10
)-C(O)-O; O; NH o N(alquilo-C
1-10
);
R8 representa alquilo-C 1-10 ; cicloalquilo-C3-10 o heterocicloalquilo de 3 a 7 miembros; en donde el cicloalquilo-C3-10 y el heterocicloalquilo de 3 a 7 miembros se pueden puentear opcionalmente mediante alquileno-C 1-6 ;
R9 y R10 representan independientemente uno de otro H; F; Cl; Br; I; CN; alquilo-C 1-10 ; cicloalquilo-C3-10; heterocicloalquilo de 3 a 7 miembros; S(O)-(alquilo-C 1-10 ); S(O)-(cicloalquilo-C3-10); S(O)-(heterocicloalquilo de 3 a 7 miembros); S(O) 2 -(alquilo-C 1-10 ); S(O)2-(cicloalquilo-C3-10); S(O) 2 -(heterocicloalquilo de 3 a 7 miembros); P(O)-(alquilo-C 1-10 ) 2 ; P(O)(alquilo-C1-10)(cicloalquilo-C3-10); P(O)(alquilo-C 1-10 )(heterocicloalquilo de 3 a 7 miembros); P(O)-(O-alquilo-C 1-10 ) 2 ; P(O)(O-alquilo-C1-10)(O-cicloalquilo-C3-10); P(O)(O-alquilo-C 1-10 )(O-(heterocicloalquilo de 3 a 7 miembros)); O-alquilo-Ci -10 ; S-alquilo-Ci -10 ; N(H)(alquilo-Ci-io), N(alquilo-Ci-io) 2 ; C(O)-alquilo-Ci-io; C(O)-O-alquilo-Ciio; C(O)-NH 2 ; C(O)-N(H)(alquilo-Ci-io); C(O)-N(alquilo-Ci-io) 2 ; O-cicloalquilo-C3-io; N(H)(cicloalquilo-C3-io), N(alquilo-Ci-io)(cicloalquilo-C3-io); C(O)-cicloalquilo-C3-io; C(O)-O-cicloalquilo-Ca-io; C(O)-N(H)(cicloalquilo-C3-io); C(O)-N(alquilo-Ci-io)(cicloalquilo-C3-io); O-heterocicloalquilo de 3 a 7 miembros; N(H)(heterocicloalquilo de 3 a 7 miembros), N(alquilo-Ci-io)(heterocicloalquilo de 3 a 7 miembros); C(O)-heterocicloalquilo de 3 a 7 miembros; C(O)-O-(heterocicloalquilo de 3 a 7 miembros); C(O)-N(H)(heterocicloalquilo de 3 a 7 miembros) o C(O)-N(alquilo-Ciio)(heterocicloalquilo de 3 a 7 miembros); en donde el cicloalquilo-C3-io y el heterocicloalquilo de 3 a 7 miembros se pueden puentear opcionalmente mediante alquileno-Ci-6;
R11 representa F; Cl; Br; I; CN; CN; alquilo-Ci-io; O-alquilo-Ci-io; NO 2 ; OH, NH 2 ; cicloalquilo-C3-io; heterocicloalquilo de 3 a 7 miembros; S(O)-(alquilo-Ci-io); S(O)-(cicloalquilo-C3-io); S(O)-(heterocicloalquilo de 3 a 7 miembros); S(O) 2 -(alquilo-Ci -10 ); S(O)2-(cicloalquilo-C3-io); S(O) 2 -(heterocicloalquilo de 3 a 7 miembros); P(O)-(alquilo-Ci-io) 2 ; P(O)(alquilo-Ci-io)(cicloalquilo-C3-io); P(O)(alquilo-Ci-io)(heterocicloalquilo de 3 a 7 miembros); P(O)-(O-alquilo-Ci-io) 2 ; P(O)(O-alquilo-Ci-io)(O-cicloalquilo-C3-io); P(O)(O-alquilo-Ci-io)(O-(heterocicloalquilo de 3 a 7 miembros)); O-alquilo-C 1-10 ; N(H)(alquilo-Ci-io), N(alquilo-Ci-io) 2 ; C(O)-alquilo-Ci-io; C(O)-O-alquilo-Ci-io; C(O)-NH 2 ; C(O)-N(H)(alquilo-Ci-io); C(O)-N(alquilo-Ci-io) 2 ; O-cicloalquilo-C3-io; N(H)(cicloalquilo-C3-io), N(alquilo-Ci-io)(cicloalquilo-C3-io); C(O)-cicloalquilo-C3-io; C(O)-O-cicloalquilo-C3-io; C(O)-N(H)(cicloalquilo-C3-io); C(O)-N(alquilo-Ci-io)(cicloalquilo-C3-io); O-heterocicloalquilo de 3 a 7 miembros; N(H)(heterocicloalquilo de 3 a 7 miembros), N(alquilo-Ci-io)(heterocicloalquilo de 3 a 7 miembros); C(O)-heterocicloalquilo de 3 a 7 miembros; C(O)-O-(heterocicloalquilo de 3 a 7 miembros); C(O)-N(H)(heterocicloalquilo de 3 a 7 miembros) o C(O)-N(alquilo-Ci-io)(heterocicloalquilo de 3 a 7 miembros); en donde el cicloalquilo-C3-io y el heterocicloalquilo de 3 a 7 miembros se pueden puentear opcionalmente mediante alquileno-Ci-6;
n representa 0, 1, 2 o 3;
en donde el alquilo-Ci-io, alquilo-Ci-4 y alquileno-Ci-6 en cada caso independientemente uno de otro es lineal o ramificado, saturado o insaturado;
en donde el alquilo-Ci -10 , alquilo-Ci-4, alquileno-Ci-6, cicloalquilo-C3-io y heterocicloalquilo de 3 a 7 miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-Ci-6; CF 3 ; CF 2 H; CFH 2 ; CF 2 Cl; CFCl 2 ; C(O)-alquilo-Ci-6; C(O)-OH; C(O)-Oalquilo-Ci-6; C(O)-NH 2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci -6 ) 2 ; OH; =O; OCF 3 ; OCF 2 H; OCFH 2 ; OCF 2 Cl; OCFCl 2 ; O-alquilo-Ci-6; O-C(O)-alquilo-Ci-6; O-C(O)-O-alquilo-Ci-6; O-(CO)-N(H)(alquilo-Ci-6); O-C(O)-N(alquilo-Ci -6 ) 2 ; O-S(O) 2 -NH 2 ; O-S(O) 2 -N(H)(alquilo-Ci -6 ); O-S(O) 2 -N(alquilo-Ci -6 ) 2 ; NH 2 ; N(H)(alquilo-Ci-6); N(alquilo-Ci -6 ) 2 ; N(H)-C(O)-alquilo-Ci-6; N(H)-C(O)-O-alquilo-Ci-6; N(H)-C(O)-NH 2 ; N(H)-C(O)-N(H)(alquilo-Ci-6); N(H)-C(O)-N(alquilo-Ci -6 ) 2 ; N(alquilo-Ci-6)-C(O)-alquilo-Ci-6; N(alquilo-Ci-6)-C(O)-O-alquilo-Ci-6; N(alquilo-Ci -6 )-C(O)-NH 2 ; N(alquilo-Ci-6)-C(O)-N(H)(alquilo-Ci-6); N(alquilo-Ci -6 )-C(O)-N(alquilo-Ci -6 ) 2 ; N(H)-S(O) 2 OH; N(H)-S(O) 2 -alquilo-Ci -6 ; N(H)-S(O) 2 -O-alquilo-C 1-6 ; N(H)-S(O) 2 -NH 2 ; N(H)-S(O) 2 -N(H)(alquilo-Ci -6 ); N(H)-S(O) 2 N(alquilo-Ci -6 ) 2 ; N(alquilo-Ci -6 )-S(O) 2 -OH; N(alquilo-Ci -6 )-S(O) 2 -alquilo-Ci -6 ; N(alquilo-Ci -6 )-S(O) 2 -O-alquilo-Ci -6 ; N(alquilo-Ci -6 )-S(O) 2 -NH 2 ; N(alquilo-Ci -6 )-s(O) 2 -N(H)(alquilo-Ci-6); N(alquilo-Ci -6 )-S(O) 2 -N(alquilo-Ci -6 ) 2 ; SCF 3 ; SCF 2 H; SCFH 2 ; S-alquilo-Ci-6; S(O)-alquilo-Ci-6; s (o )2-alquilo-Ci-6; S(O) 2 -OH; S(O) 2 -O-alquilo-Ci -6 ; S(O) 2 -NH 2 ; S(O) 2 -N(H)(alquilo-Ci -6 ); S(O) 2 -N(alquilo-Ci -6 ) 2 ; cicloalquilo-C 3-6 ; heterocicloalquilo de 3 a 6 miembros; fenilo; heteroarilo de 5 o 6 miembros; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); O-fenilo; O-(heteroarilo de 5 o 6 miembros); C(O)-cicloalquilo-C3-6; C(O)-(heterocicloalquilo de 3 a 6 miembros); C(O)-fenilo; C(O)-(heteroarilo de 5 o 6 miembros); S(O)2-(cicloalquilo-C3-6); S(O) 2 -(heterocicloalquilo de 3 a 6 miembros); S(O) 2 -fenilo o S(O) 2 -(heteroarilo de 5 o 6 miembros);
en donde el arilo y el heteroarilo de 5 o 6 miembros en cada caso independientemente uno de otro no están sustituidos o están mono o polisustituidos con uno o más sustituyentes seleccionados de F; Cl; Br; I; CN; alquilo-Ci-6; CF 3 ; CF 2 H; CFH 2 ; CF 2 Cl; CFCb; alquileno-Ci-4-CF3; alquileno-Ci-4-CF2H; alquileno-Ci-4-CFH2; C(O)-alquilo-Ci-6; C(O)-OH; C(O)-Oalquilo-Ci-6; C(O)-N(H)(OH); C(O)-NH 2 ; C(O)-N(H)(alquilo-Ci-6); C(O)-N(alquilo-Ci -6 ) 2 ; OH; OCF 3 ; OCF 2 H; OCFH 2 ; OCF 2 Cl; OCFCl 2 ; O-alquilo-Ci-e; O-cicloalquilo-C3-6; O-(heterocicloalquilo de 3 a 6 miembros); NH 2 ; N(H)(alquilo-Ci-6); N(alquilo-Ci -6 ) 2 ; N(H)-C(O)-alquilo-Ci-6; N(alquilo-Ci-6)-C(O)-alquilo-Ci-6; N(H)-C(O)-NH 2 ; N(H)-C(O)-N(H)(alquilo-Ci-6); N(H)-C(O)-N(alquilo-Ci -6 ) 2 ; N(alquilo-Ci-6)-C(O)-N(H)(alquilo-Ci-6); N(alquilo-Ci -6 )-C(O)-N(alquilo-Ci -6 ) 2 ; N(H)-s(O) 2 -alquilo-Ci -6 ; SCF 3 ; S-alquilo-Ci-6; S(O)-alquilo-Ci-6; S(O) 2 -alquilo-Ci -6 ; S(O) 2 -NH 2 ; S(O) 2 -N(H)(alquilo-Ci -6 ); S(O) 2 -N(alquilo-Ci -6 ) 2 ; cicloalquilo-C3-6; alquileno-Ci-4-cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; alquileno-Ci-4-(heterocicloalquilo de 3 a 6 miembros); fenilo o heteroarilo de 5 o 6 miembros;
en la forma del compuesto libre o una sal fisiológicamente aceptable del mismo.
2. El compuesto según la reivindicación 1, en donde R5 y R6 representan ambos CH 3 .
4. El compuesto según cualquiera de las reivindicaciones anteriores, en donde X representa NR7 y Z representa N o CR9.
5. El compuesto según cualquiera de las reivindicaciones anteriores, en donde
R1 representa H; alquilo-C 1-6 ; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; fenilo; o heteroarilo de 5 o 6 miembros; en donde cicloalquilo-C3-6, heterocicloalquilo de 3 a 6 miembros, fenilo y heteroarilo de 5 o 6 miembros se pueden puentear opcionalmente mediante alquileno-C1-4.
6. El compuesto según cualquiera de las reivindicaciones anteriores, en donde
R2 representa H; F; Cl; Br; CN; alquilo-C 1-6 ; cicloalquilo-C3-6; O-alquilo-C 1-6 ; C(O)-NH 2 ; C(O)-N(H)(alquilo-C 1-6 ); C(O)-N(alquilo-C 1-6 ) 2 ; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-C1-6)(cicloalquilo-C3-6); en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-C1-4; y/o
R3 representa H; F; Cl; Br; CN; alquilo-C 1-6 ; cicloalquilo-C3-6; O-alquilo-C 1-6 ; C(O)-NH 2 ; C(O)-N(H)(alquilo-C 1-6 ); C(O)-N(alquilo-C 1-6 ) 2 ; C(O)-N(H)(cicloalquilo-C3-6) o C(O)-N(alquilo-C1-6)(cicloalquilo-C3-6); en donde el cicloalquilo-C3-6 se puede puentear opcionalmente mediante alquileno-C1-4.
7. El compuesto según cualquiera de las reivindicaciones anteriores, en donde R7 representa H.
8. El compuesto según cualquiera de las reivindicaciones 1 a 6, en donde R7 representa L-R8; en donde
L representa un enlace; S(O); S(O) 2 ; alquileno-C1-4; C(O); alquileno-C1-4-C(O); C(O)-O; alquileno-C1-4-C(O)-O; alquileno-C1-4-N(H)-C(O) o alquileno-C1-4-N(H)-C(O)-O;
R8 representa alquilo-C 1-6 ; cicloalquilo-C3-6 o heterocicloalquilo de 3 a 6 miembros; en donde el cicloalquilo-C3-6 y el heterocicloalquilo de 3 a 6 miembros se pueden puentear opcionalmente mediante alquileno-C1-4.
9. El compuesto según cualquiera de las reivindicaciones anteriores, en donde
R9 representa H; F; CN; metilo; etilo; n-propilo; 2-propilo; CF 3 ; CH 2 CF 3 ; CHF 2 ; CH 2 CHF 2 ; CH 2 F; CH 2 CH 2 F; S(O)-CH3; S(O)-CH2CH3; S(O)-CH2CH2CH3; S(O)-CH(CH3)2; S(O)2-CH3; S(O)2-CH2CH3; S(O)2-CH2CH2CH3 o S(O)2-CH(CH3)2.
10. El compuesto según cualquiera de las reivindicaciones anteriores, en donde
R10 representa H; F; Cl; Br; CN; alquilo-C 1-6 ; cicloalquilo-C3-6; heterocicloalquilo de 3 a 6 miembros; P(O)-(alquilo-C 1-6 ) 2 ; P(O)(alquilo-C1-6)(cicloalquilo-C3-6); P(O)(alquilo-C 1-6 )(heterocicloalquilo de 3 a 6 miembros) P(O)-(O-alquilo-C 1-6 ) 2 ; P(O)(O-alquilo-C1-6)(O-cicloalquilo-C3-6); P(O)(O-alquilo-C 1-6 )(O-(heterocicloalquilo de 3 a 6 miembros)).
11. El compuesto según cualquiera de las reivindicaciones anteriores, en donde
R11 representa F; Cl; Br; I; CN; alquilo-C
1 -6
u O-alquilo-C
1
-
6
; y/o
n representa 0, 1 o 2.
12. El compuesto según cualquiera de las reivindicaciones anteriores seleccionado del grupo que consiste en 1 7,9-Difluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2 8-(1-Ciclopropil-6-fluoro-1H-indol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(6-fluoro-1-irietNsuf:oml-1H-indol-4-N)-1,4,4-triiTietN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-6-fluoro-1H-indol-1-il]-etanona
7.9- Difluoro-8-(6-fluoro-2-metil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 4-(7,9-Difluoro-1,4,4-triiTietN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8-N)-6-fluoro-1H-mdol-2-carbonitrilo
7.9- Difluoro-8-(1 H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-[3-(trifluorometil)-1H-indol-7-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-Etil-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(1-Etil-7,9-difluoro-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-3-carbonitrilo 1-Etil-7,9-difluoro-4,4-dimetil-8-(3-prop-1-inil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-Etil-7,9-difluoro-8-(5-fluoro-1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(1-EtN-7,9-difluoro-4,4-diiTietN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8-N)-5-fluoro-1H-mdol-3-carbonitrilo
1-Etil-7,9-difluoro-8-(5-fluoro-3-prop-1-inil-1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- (1-EtN-7,9-difluoro-4,4-diiTietN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8-N)-5-iTietiMH-indol-3-carbonitrilo
8- [1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Ciclopropilsulfonil)-6-fluoro-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etanona 7.9- Difluoro-8-[6-fluoro-1-(2,2,2-trifluoro-etil)-1H-indol^-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-[5-fluoro-3-(2,2,2-trifluoro-etil)-1H-indol-7-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4,9-tetrametil-8-[3-(2,2,2-trifluoro-etil)-1H-indol-7-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-8-(1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (1-Ciclopropil-1H-indol-4-il)-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-1,4,4,9-tetrametil-8-(3-prop-1-inil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Cloro-7-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(5-fluoro-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (3-Ciclopropil-5-fluoro-1H-indol-7-il)-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-8-(6-fluoro-1H-indol-4-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(Ciclopropil-metil)-6-fluoro-1H-indol-4-il]-1-etil-7-fluoro-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
4-[7-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-3-il]-2-metil-but-3-in-2-ol
[3-[7-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-3-il]-1,1-dimetilprop-2-inil]-amina
9- Cloro-8-(3-ciclobutil-1H-indol-7-il)-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-1,4,4,9-tetrametil-8-(3-tetrahidro-furan-3-il-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (3-Etil-5-fluoro-1H-indol-7-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[4-(9-Etil-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-6-fluoro-1H-indol-1-il]-etanol
2-[4-(9-Etil-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-6-fluoro-1H-indazol-1-il]-etanol
9-Etil-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Etil-7-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Etil-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Etil-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Etil-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Bendl-7,9-difluoro-8-(5-fluoro-3-metiMH-indol-7-N)-4,4-dimetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Bencil-7,9-difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-But-2-inil-7,9-difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-But-2-inil-7,9-difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-1-(piridin-4-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-1-(piridin-4-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-1-(piridin-3-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-4,4-dimetil-1-(piridin-2-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-4,4-dimetil-8-(3-metil-1H-indol-7-il)-1-(piridin-2-il-metil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(5-fluoro-3-prop-1-imMH-mdol-7-N)-1-(metoximetN)-4,4,9-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
[7-Fluoro-8-(5-fluoro-3-prop-1-inil-1H-indol-7-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-1-il]-MeOH
1-[7-Fluoro-8-(5-fluoro-3-prop-1-inil-1H-indol-7-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-1-il]-etanol
7- Fluoro-8-(5-fluoro-3-prop-1-imMH-indol-7-N)-1-(2-metoxi-etN)-4,4,9-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
1-(Cidopropil-metil)-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-Cidopropil-7,9-difluoro-8-(1H-indol-7-il)-4,4-dimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (3-CidopropiMH-indol-7-N)-1,4,4,9-tetrametN-7-(trifluorometN)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-7-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-7-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Cloro-8-(3-cidopropil-1H-indol-7-il)-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (3-CidopropN-5-fluoro-1H-mdol-7-N)-7-fluoro-1,4,4-trimetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-(1-CidopropN-6-fluoro-1H-mdol-4-N)-7-fluoro-1,4,4-trimetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- [7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-3-carbonitrilo
7.9- Difluoro-8-[1-(isopropilsulfonil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(CidopentNsufomN)-1H-mdol-4-N]-7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Ciclopropil-metil)-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-1,4,4-trimetil-8-[1-(tetrahidro-piran^-ilsulfonM)-1H-indol^-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(Ciclopropilsulfonil)-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(CidopropN-metNsulfonN)-1H-indol-4-N]-7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-N,N-dimetilacetamida
1-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-2-metoxietanona
7.9- Difluoro-8-(5-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina Éster metílico del ácido 3-[4-(7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8-N)-1H-indol-1-il]-propiónico
7.9- Difluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-1,4,4-trimetil-8-(2-metil-2H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1- [4-(7,9-Difluoro-1,4,4-trimetM-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-2-dimetilamino-etanona
7.9- Difluoro-8-(5-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-[2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina Éster terc-butílico del ácido N-[2-[4-(7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8-il)-1 H-indol-1 -il]-etil]-carbámico
N-[2-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etil]-2,2-difluoro-propionamida
2- [4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etil-amina 7.9- Difluoro-8-(1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-[1-(2-metoxi-etil)-1H-indazol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(Ciclopropilsulfonil)-1H-indazol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Ciclopropil-metil)-1H-indazol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(1-Etil-1H-indazol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(2-Etil-2H-indazol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
Éster terc-butílico del ácido 4-(7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indazol-1-carboxílico
8-[1-(Ciclopropil-metilsulfonil)-1H-indazol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-4,4,9-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-Etil-7-fluoro-4,4,9-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(1-Ciclopropil-1H-indazol-4-il)-1-etil-7-fluoro-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (1-Ciclopropil-1H-indazol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1-Etil-7-fluoro-8-(5-fluoro-1H-indol-4-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-4,4,9-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(5-fluoro-3-metil-1 H-indol-7-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Fluoro-8-(5-fluoro-3-metil-1 H-indol-7-il)-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- (Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-[2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-9-fluoro-1,4,4-trimetil-8-[2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-(1H-indol-4-il)-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Fluoro-7-metoxi-1,4,4-tnmetN-8-[2-(trifluorometN)-1H-indol-4-N]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indazol-1-il]-etanol 7- (Difluoro-metoxi)-9-fluoro-8-[1-(2-metoxi-etil)-2-(trifluorometil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
Éster terc-butílico del ácido 4-(7-fluoro-9-metoxi-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxaNn-8- il)-1 H-indol-1 -carboxílico
9- Fluoro-7-metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-Fluoro-7-metoxi-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metoxi)-9-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-(6-fluoro-1-metNsulfonil-1H-indol-4-N)-1,4,4-tnmetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
9-Fluoro-7-metoxi-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-9-metoxi-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7.9- Difluoro-1,4,4-trimetil-8-[1-metilsulfonil-2-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-8-[1-(2-metoxi-etil)-1 H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-9-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-9-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(1H-indol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-7-metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-[1-(2-metoxi-etil)-2-(trifluorometil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-(Difluoro-metil)-7-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-9-fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metil)-9-fluoro-8-(6-fluoro-1-metilsulfonil-1 H-indol^-il)-1,4,4-trimetil-5H-
[1.2.4] triazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9-(Difluoro-metil)-7-fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1,4,4,7,9-metilsulfonil-1 H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-CidopropN-2-(trifluorometN)-1H-indol-4-N]-7,9-difluoro-1,4,4-trimetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Cloro-8-[1-(2,2-difluoro-etM)-1H-indol^-il]-9-fluoro-1,4,4-trimetM-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-9-fluoro-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1 H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- (Difluoro-metoxi)-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metN)-7-fluoro-8-(1H-mdol-4-N)-1,4,4-tnmetN-5H-[1,2,4]triazolo[4,3-a]quinoxaNna 9-(Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-1,4,4,7-tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metil)-9-fluoro-1,4,4-trimetil-8-(1-metil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Cloro-8-[1-(2,2-difluoro-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(6-Fluoro-1-metilsulfonil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-[1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(2-Metoxi-etil)-1H-indol-4-il]-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Cloro-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metil)-9-fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Metoxi-8-[1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (5-Fluoro-3-metil-1H-indol-7-il)-7-metoxi-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- (Difluoro-metN)-7-fluoro-8-(6-fluoro-1-metNsulfoml-1H-mdazol-4-N)-1,4,4-tnmetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Cloro-8-(6-fluoro-1-metNsulfoml-1H-indazol-4-N)-1,4,4,9-tetrametN-5H-[1,2,4]tnazolo[4,3-a]quinoxalina
1-Etil-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indazol-4-il)-4,4,9-trimetil-5H-[1,2,4]triazolo[4,3-
a]quinoxalina
7-Fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-1,4,4-trimetil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1.4.4.7.9- Pentametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Metoxi-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Fluoro-1,4,4,7-tetrametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-1,4,4,9-tetrametil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-1,4,4,9-tetrametil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7-fluoro-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- Fluoro-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-(Difluoro-metoxi)-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Cloro-1,4,4,9-tetrametil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-[1-(Etilsulfonil)-6-fluoro-1H-indol-4-il]-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Etilsulfonil)-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(Etilsulfonil)-1H-indol-4-il]-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(6-Fluoro-1-metilsulfonil-1H-indazol-4-il)-1,4,4,7,9-pentametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- (6-Fluoro-1-metilsulfonil-1H-indazol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 2-[6-Fluoro-4-(9-fluoro-7-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etanol
2-[6-Fluoro-4-(7-fluoro-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etanol
7- Fluoro-9-metoxi-1,4,4-trimetil-8-(3-metil-1H-indazol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- (Difluoro-metil)-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
[2-[4-(7,9-Difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etil]-dimetilamina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-(difluoro-metoxi)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[4-[7-(Difluoro-metil)-9-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-6-fluoro-1H-indol-1-il]-etanol
7-Cloro-1,4,4,9-tetrametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Metoxi-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.7.9- Pentametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 9- (Difluoro-metil)-7-fluoro-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-9-fluoro-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-(difluoro-metoxi)-9-fluoro-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-(Difluoro-metoxi)-9-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1.2.4] triazolo[4,3-a]quinoxalina
2-[4-[7-(Difluoro-metoxi)-9-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-6-fluoro-1H-indol-1-il]-etanol
7- (Difluoro-metN)-9-fluoro-8-[6-fluoro-1-(2-metoxi-etN)-1H-indol-4-N]-1,4,4-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-fluoro-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2,2-Difluoro-etil)-1H-indol-4-il]-9-(difluoro-metil)-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-8-(1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-8-[1-(isopropilsulfonil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(CidopropNsulfonN)-1H-mdol-4-N]-9-(difluoro-metN)-7-fluoro-1,4,4-tnmetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
9- (Difluoro-metN)-7-fluoro-8-[6-fluoro-1-(2-metoxi-etN)-1H-indol-4-N]-1,4,4-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-(6-Fluoro-1-metNsulfonN-1H-indol-4-N)-1,4,4,9-tetrametN-7-(trifluorometNoxi)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- Cloro-9-fluoro-8-[6-fluoro-1-(2-metoxi-etil)-1H-indol-4-il]-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.9- Tetrametil-8-(3-metil-1H-indol-7-il)-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- (5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(5-Fluoro-3-metil-1H-indol-7-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(1 H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indazol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[6-Fluoro-4-[7-fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-1-il]-etanol
8- [1-(EtNsulfonN)-6-fluoro-1H-mdazol-4-N]-7-fluoro-1,4,4-tnmetN-9-(tnfluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
2-[6-Fluoro-4-[7-fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indazol-1-il]-etanol
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[6-Fluoro-4-(1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-1-il]-etanol 8-(5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(6-fluoro-1-metNsulfoml-1H-indazol-4-N)-1,4,4-tnmetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8- [1-(EtilsulfonM)-1H-indol-4-M]-7-fluoro-1,4,4-trimetM-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
2-[4-[7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-1-il]-etanol
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indazol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(5-Fluoro-3-metil-1H-indol-7-il)-1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(5-Fluoro-3-metil-1H-indol-7-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8- [1-(2-Metoxi-etil)-1H-indol-4-il]-1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-8-[1-(etilsulfonil)-1H-indol-4-il]-7-fluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Cidopropil-7-fluoro-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-Cidopropil-7-fluoro-1,4,4-trimetil-8-(3-metil-1H-indol-7-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
1.4.4.9- Tetrametil-8-(1-metilsulfonil-1H-indol-4-il)-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9-(Difluoro-metil)-7-fluoro-8-(6-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Fluoro-8-(6-fluoro-1H-indol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(2,2-Difluoro-etN)-6-fluoro-1H-indazol-4-N]-1,4,4,9-tetrametN-7-(trifluorometiloxi)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- Fluoro-1,4,4,9-tetrametil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina 2-[6-Fluoro-4-[1,4,4,9-tetrametil-7-(trifluorometiloxi)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-1-il]-etanol
8- [1-(2,2-Difluoro-etN)-6-fluoro-1H-indazol-4-N]-9-(difluoro-metN)-7-fluoro-1,4,4-tnmetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-1,4,4-trimetil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-[6-(trifluorometil)-1H-indol-4-il]-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7-Fluoro-1,4,4-tnmetN-8-(6-metiM-metNsulfonil-1H-indol-4-N)-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7- Fluoro-9-metoxi-1,4,4-trimetil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metN)-7-fluoro-1,4,4-tnmetN-8-(6-metiM-metNsulfoniMH-indol-4-N)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
4-[7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-6-carbonitrilo
8- [6-Fluoro-1-(2-metoxi-etN)-1H-indazol-4-N]-1,4,4,9-tetrametN-7-(tnfluorometNoxi)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-1,4,4-trimetM-8-(1-metM-1H-indol-4-M)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-(3-CidopropN-5-fluoro-1H-indol-7-N)-7-metoxi-1,4,4-tnmetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
8-(3-Ciclopropil-5-fluoro-1H-indol-7-il)-7-fluoro-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(7-fluoro-1-metNsulfonil-1H-indol-4-N)-1,4,4-tnmetN-9-(trifluorometN)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
7-Cloro-8-(3-ciclopropil-5-fluoro-1H-indol-7-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-1,4,4,9-tetrametil-8-(1-metil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-9-metoxi-1,4,4-trimetil-8-(1-metil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 7- Cloro-1,4,4,9-tetrametil-8-(1-metil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8- [1-(2,2-Difluoro-etil)-6-fluoro-1H-indazol-4-il]-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Fluoro-8-(1H-indazol-4-il)-9-metoxi-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7-Cloro-1,4,4,9-tetrametil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- dDfluoro-1,4,4-trimetil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7- Fluoro-1,4,4,9-tetrametil-8-(6-metil-1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
4-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-6-carbonitrilo 8- [1-(Ciclopropil-metilsulfonil)-1H-indol-4-il]-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
9- (Difluoro-metil)-7-fluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 1,4,4-Trimetil-8-(1-metilsulfonil-1H-indol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-(6-Fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
8-[1-(2,2-Difluoro-etil)-1H-indol-4-il]-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
7.9- Difluoro-8-(7-fluoro-1H-indazol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 8-[1-(CidopropN-metNsulfonN)-1H-indol-4-N]-9-(difluoro-metil)-7-fluoro-1,4,4-tnmetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
503 1,4,4-Trimetil-8-(3-metil-1H-indol-7-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 504 7-Fluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 505 7-Fluoro-8-(7-fluoro-1H-indol-4-il)-1,4,4-trimetM-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
506 7- Cloro-8-(7-fluoro-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 507 8- (5-Fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
508 7-Cloro-8-[1-(2,2-difluoro-etN)-6-fluoro-1H-indazol-4-N]-9-fluoro-1,4,4-trimetN-5H-[1.2.4] triazolo[4,3-a]quinoxalina
509 7-Metoxi-1,4,4-trimetil-8-(1-metil-1H-indol-4-il)-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
510 7- Fluoro-8-(1H-indazol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
511 8- (6-Cloro-1H-indol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 512 9- (Difluoro-metN)-7-fluoro-1,4,4-trimetN-8-(7-metiM-metNsulfoniMH-indol-4-N)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
513 8-(6-Cloro-1H-indol-4-il)-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
514 8- (1-CidopropiMH-indol-4-N)-9-(difluoro-metN)-7-fluoro-1,4,4-tnmetN-5H-[1,2,4]triazolo[4,3-a]quinoxalina
515 9- (Difluoro-metil)-7-fluoro-8-(5-fluoro-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
516 7- Fluoro-8-(5-fluoro-1H-indol-7-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
517 8- (6-Fluoro-1-metil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
518 7-Fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 519 7- Cloro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 520 9- Fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4,7-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 521 9-(Difluoro-metil)-7-fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
522 8- (6-Fluoro-1-metil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
523 8-(1-Cidopropil-1H-indol-4-il)-7-metoxi-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
524 7- Fluoro-8-(7-fluoro-1H-indazol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 525 8- (7-Cloro-1-metilsulfonil-1H-indol-4-il)-7-fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
526 9- (Difluoro-metil)-8-(6-fluoro-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
527 9-(Difluoro-metil)-8-(5-fluoro-3-metil-1H-indol-7-il)-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
528 9-(Difluoro-metil)-1,4,4-trimetil-8-(1-metilsulfonil-1H-indol-4-il)-5H-[1,2,4]triazolo[4,3-a]quinoxalina 529 8-(7-Cloro-1H-indol-4-il)-7,9-difluoro-1,4,4-trimetil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
530 8-(7-Cloro-1H-indol-4-il)-7-fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
531 4-[7-Fluoro-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il]-1H-indol-7-carbonitrilo
532 7-Fluoro-8-(6-fluoro-1-metil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
533 7-Cloro-8-(1-cidopropil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina 534 4-(7-Fluoro-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalin-8-il)-1H-indol-7-carbonitrilo 535 7-Fluoro-8-(7-fluoro-1H-indazol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1,2,4]triazolo[4,3-a]quinoxalina
536 7-Fluoro-8-(6-metoxi-1-metilsulfonil-1H-indol-4-il)-1,4,4-trimetil-9-(trifluorometil)-5H-[1.2.4] triazolo[4,3-a]quinoxalina
537 7-Fluoro-8-(6-metoxi-1-metilsulfonil-1H-indol-4-il)-1,4,4,9-tetrametil-5H-[1,2,4]triazolo[4,3-a]quinoxalina
en la forma del compuesto libre o una sal fisiológicamente aceptable del mismo.
13. Una forma de dosificación farmacéutica que comprende un compuesto según cualquiera de las reivindicaciones 1 a 12.
14. El compuesto según cualquiera de las reivindicaciones 1 a 12 para su uso en el tratamiento y/o la profilaxis del dolor y/o inflamación.
15. El compuesto según la reivindicación 14 para su uso en el tratamiento y/o la profilaxis del dolor inflamatorio.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18184613 | 2018-07-20 | ||
| PCT/EP2019/069611 WO2020016453A1 (en) | 2018-07-20 | 2019-07-22 | Substituted triazolo quinoxaline derivatives |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2929206T3 true ES2929206T3 (es) | 2022-11-25 |
Family
ID=63014350
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19742596T Active ES2929206T3 (es) | 2018-07-20 | 2019-07-22 | Derivados de triazolo quinoxalina sustituidos |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US12110293B2 (es) |
| EP (1) | EP3823971B1 (es) |
| JP (1) | JP7336506B2 (es) |
| CN (1) | CN112673009B (es) |
| AU (1) | AU2019304532B2 (es) |
| BR (1) | BR112021000950A2 (es) |
| CA (1) | CA3106752A1 (es) |
| DK (1) | DK3823971T3 (es) |
| EA (1) | EA202190271A1 (es) |
| ES (1) | ES2929206T3 (es) |
| HR (1) | HRP20221020T1 (es) |
| HU (1) | HUE059430T2 (es) |
| IL (1) | IL280212B2 (es) |
| LT (1) | LT3823971T (es) |
| MX (1) | MX2021000762A (es) |
| PL (1) | PL3823971T3 (es) |
| PT (1) | PT3823971T (es) |
| RS (1) | RS63671B1 (es) |
| SI (1) | SI3823971T1 (es) |
| WO (1) | WO2020016453A1 (es) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI811400B (zh) | 2018-07-20 | 2023-08-11 | 德商歌林達有限公司 | 經進一步取代之三唑并喹噁啉衍生物 |
| IL280212B2 (en) | 2018-07-20 | 2023-09-01 | Gruenenthal Chemie | Transmuted triazoloquinoxaline histories |
| ES3025970T3 (en) * | 2020-01-17 | 2025-06-10 | Gruenenthal Gmbh | Quinoxaline derivatives as modulators of the glucocorticoid receptor |
| WO2021144439A1 (en) * | 2020-01-17 | 2021-07-22 | Grünenthal GmbH | Quinoxaline derivatives |
| CN115124471B (zh) * | 2021-03-24 | 2024-02-13 | 中国工程物理研究院化工材料研究所 | 一类具有高能和低熔点特性的吡唑环类炸药及其合成方法 |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1994026746A1 (en) * | 1993-05-06 | 1994-11-24 | Novo Nordisk A/S | [1,2,4]TRIAZOLO[4,3-a]QUINOXALINE COMPOUNDS, THEIR PREPARATION AND USE |
| JP3601219B2 (ja) | 1996-11-13 | 2004-12-15 | 松下電器産業株式会社 | 光ピックアップ用の平行プリズム |
| US7277744B2 (en) | 1999-03-22 | 2007-10-02 | Schaefer Allan L | Early detection of inflammation and infection using infrared thermography |
| BRPI0407926A (pt) * | 2003-03-27 | 2006-02-21 | Pfizer Prod Inc | 4-amino[1,2,4]triazol[4,3-a]quinoxalinas substituìdas |
| US7662846B2 (en) * | 2003-04-23 | 2010-02-16 | Merck Sharp & Dohme Corp. | Selective spirocyclic glucocorticoid receptor modulators |
| BRPI0513119A (pt) | 2004-07-14 | 2008-04-29 | Ligand Pharm Inc | compostos e métodos modulares de receptores intracelulares |
| EP1995242B1 (en) | 2006-03-14 | 2012-11-07 | Santen Pharmaceutical Co., Ltd | Novel 1,2,3,4-tetrahydroquinoxaline derivative having glucocorticoid receptor binding activity |
| TWI410422B (zh) | 2007-01-15 | 2013-10-01 | Mitsubishi Tanabe Pharma Corp | 縮合四氫喹啉衍生物及其醫藥用途 |
| ES2419239T3 (es) * | 2007-05-29 | 2013-08-20 | Santen Pharmaceutical Co., Ltd | Nuevo derivado de 1,2,3,4-tetrahidroquinoxalina que tiene como sustituyente un grupo fenilo con una estructura de éster de ácido sulfónico o una estructura de amida de ácido sulfónico introducida en el mismo y que tienen una actividad de unión al receptor de glucocorticoides |
| WO2009003567A1 (fr) | 2007-06-29 | 2009-01-08 | Johnson Controls Technology Company | Procede de montage d'un composant electrique sur un element de support et dispositif de raccordement electrique |
| JP2009046435A (ja) | 2007-08-21 | 2009-03-05 | Mitsubishi Tanabe Pharma Corp | グルココルチコイド受容体モジュレーター |
| WO2009035067A1 (ja) | 2007-09-13 | 2009-03-19 | Santen Pharmaceutical Co., Ltd. | 1,3,3-トリメチル-7-フェニル-3,4-ジヒドロ-1h-キノキサリン-2-オン誘導体からなるグルココルチコイド受容体アゴニスト |
| WO2009103007A2 (en) | 2008-02-13 | 2009-08-20 | Ligand Pharmaceuticals Incorporated | Steroid hormone receptor modulator compounds and methods |
| WO2013034755A1 (en) | 2011-09-09 | 2013-03-14 | H. Lundbeck A/S | Triazolopyrazine derivatives and their use for treating neurological and psychiatric disorders |
| KR20150007352A (ko) | 2012-06-15 | 2015-01-20 | 화이자 인코포레이티드 | Kat ii 억제제로서 삼환 화합물 |
| CN107922356A (zh) | 2015-08-25 | 2018-04-17 | 参天制药株式会社 | [4‑(1,3,3‑三甲基‑2‑氧代‑3,4‑二氢‑1h‑喹喔啉‑7‑基)苯氧基]乙基氧基化合物或其盐 |
| EP3567041B1 (en) | 2017-01-09 | 2023-12-27 | Impact Therapeutics (Shanghai), Inc | Substituted fused heteroaryl compound serving as a kinase inhibitor, and applications thereof |
| TWI811400B (zh) * | 2018-07-20 | 2023-08-11 | 德商歌林達有限公司 | 經進一步取代之三唑并喹噁啉衍生物 |
| IL280212B2 (en) | 2018-07-20 | 2023-09-01 | Gruenenthal Chemie | Transmuted triazoloquinoxaline histories |
-
2019
- 2019-07-22 IL IL280212A patent/IL280212B2/en unknown
- 2019-07-22 EP EP19742596.0A patent/EP3823971B1/en active Active
- 2019-07-22 JP JP2021503034A patent/JP7336506B2/ja active Active
- 2019-07-22 BR BR112021000950-7A patent/BR112021000950A2/pt unknown
- 2019-07-22 PT PT197425960T patent/PT3823971T/pt unknown
- 2019-07-22 LT LTEPPCT/EP2019/069611T patent/LT3823971T/lt unknown
- 2019-07-22 MX MX2021000762A patent/MX2021000762A/es unknown
- 2019-07-22 RS RS20220977A patent/RS63671B1/sr unknown
- 2019-07-22 PL PL19742596.0T patent/PL3823971T3/pl unknown
- 2019-07-22 SI SI201930309T patent/SI3823971T1/sl unknown
- 2019-07-22 CN CN201980048220.2A patent/CN112673009B/zh active Active
- 2019-07-22 CA CA3106752A patent/CA3106752A1/en active Pending
- 2019-07-22 ES ES19742596T patent/ES2929206T3/es active Active
- 2019-07-22 DK DK19742596.0T patent/DK3823971T3/da active
- 2019-07-22 EA EA202190271A patent/EA202190271A1/ru unknown
- 2019-07-22 WO PCT/EP2019/069611 patent/WO2020016453A1/en not_active Ceased
- 2019-07-22 HU HUE19742596A patent/HUE059430T2/hu unknown
- 2019-07-22 HR HRP20221020TT patent/HRP20221020T1/hr unknown
- 2019-07-22 AU AU2019304532A patent/AU2019304532B2/en active Active
-
2021
- 2021-01-20 US US17/152,930 patent/US12110293B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021532103A (ja) | 2021-11-25 |
| DK3823971T3 (da) | 2022-09-05 |
| CN112673009B (zh) | 2023-09-19 |
| WO2020016453A1 (en) | 2020-01-23 |
| JP7336506B2 (ja) | 2023-08-31 |
| CN112673009A (zh) | 2021-04-16 |
| CA3106752A1 (en) | 2020-01-23 |
| EP3823971B1 (en) | 2022-07-27 |
| BR112021000950A2 (pt) | 2021-04-20 |
| PT3823971T (pt) | 2022-10-26 |
| EA202190271A1 (ru) | 2021-06-07 |
| HUE059430T2 (hu) | 2022-11-28 |
| PL3823971T3 (pl) | 2023-01-09 |
| IL280212B2 (en) | 2023-09-01 |
| HRP20221020T1 (hr) | 2022-11-11 |
| EP3823971A1 (en) | 2021-05-26 |
| US12110293B2 (en) | 2024-10-08 |
| RS63671B1 (sr) | 2022-11-30 |
| LT3823971T (lt) | 2022-09-12 |
| IL280212B1 (en) | 2023-05-01 |
| US20210139488A1 (en) | 2021-05-13 |
| AU2019304532A1 (en) | 2021-03-18 |
| SI3823971T1 (sl) | 2022-10-28 |
| MX2021000762A (es) | 2021-03-29 |
| AU2019304532B2 (en) | 2024-08-29 |
| IL280212A (en) | 2021-03-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2929206T3 (es) | Derivados de triazolo quinoxalina sustituidos | |
| TWI714567B (zh) | 作為lsd1抑制劑之雜環化合物 | |
| CN103492376B (zh) | 双环杂环化合物及其治疗用途 | |
| ES2973525T3 (es) | Derivados de triazolo quinoxalina adicionalmente sustituidos | |
| CN109384790B (zh) | 成纤维细胞生长因子受体抑制剂及其用途 | |
| ES2976780T3 (es) | Derivados de quinoxalina | |
| ES3025970T3 (en) | Quinoxaline derivatives as modulators of the glucocorticoid receptor | |
| HK40048161B (en) | Substituted triazolo quinoxaline derivatives | |
| HK40048161A (en) | Substituted triazolo quinoxaline derivatives | |
| HK40048159A (en) | Further substituted triazolo quinoxaline derivatives | |
| HK40048159B (en) | Further substituted triazolo quinoxaline derivatives | |
| EA043276B1 (ru) | Замещенные триазолохиноксалиновые производные | |
| EA045285B1 (ru) | Дополнительно замещенные производные триазоло-хиноксалина |