ES2951983T3 - Método de obtención de secoiridoides de tipo oleaceína y oleomisional y de producción de preparados farmacéuticos respectivos - Google Patents
Método de obtención de secoiridoides de tipo oleaceína y oleomisional y de producción de preparados farmacéuticos respectivos Download PDFInfo
- Publication number
- ES2951983T3 ES2951983T3 ES20713080T ES20713080T ES2951983T3 ES 2951983 T3 ES2951983 T3 ES 2951983T3 ES 20713080 T ES20713080 T ES 20713080T ES 20713080 T ES20713080 T ES 20713080T ES 2951983 T3 ES2951983 T3 ES 2951983T3
- Authority
- ES
- Spain
- Prior art keywords
- obtaining
- solution
- secairidoids
- water
- substance
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/30—Preparation of carboxylic acid esters by modifying the acid moiety of the ester, such modification not being an introduction of an ester group
- C07C67/31—Preparation of carboxylic acid esters by modifying the acid moiety of the ester, such modification not being an introduction of an ester group by introduction of functional groups containing oxygen only in singly bound form
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
- A61K31/222—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin with compounds having aromatic groups, e.g. dipivefrine, ibopamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/25—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids with polyoxyalkylated alcohols, e.g. esters of polyethylene glycol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C67/00—Preparation of carboxylic acid esters
- C07C67/48—Separation; Purification; Stabilisation; Use of additives
- C07C67/56—Separation; Purification; Stabilisation; Use of additives by solid-liquid treatment; by chemisorption
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C69/00—Esters of carboxylic acids; Esters of carbonic or haloformic acids
- C07C69/66—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety
- C07C69/73—Esters of carboxylic acids having esterified carboxylic groups bound to acyclic carbon atoms and having any of the groups OH, O—metal, —CHO, keto, ether, acyloxy, groups, groups, or in the acid moiety of unsaturated acids
- C07C69/738—Esters of keto-carboxylic acids or aldehydo-carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/62—Carboxylic acid esters
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Neurosurgery (AREA)
- Zoology (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Emergency Medicine (AREA)
- Wood Science & Technology (AREA)
- Mycology (AREA)
- Polymers & Plastics (AREA)
- Food Science & Technology (AREA)
- Nutrition Science (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Hospice & Palliative Care (AREA)
- Vascular Medicine (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Genetics & Genomics (AREA)
- Urology & Nephrology (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Psychiatry (AREA)
Abstract
La presente invención se refiere a un método para la obtención en forma pura o en mezcla de oleaceína y sustancias oleomisionales de frutos y hojas de olivo y ciertos derivados de los mismos, las formas dioles bioactivas, mediante extracción selectiva de hojas o frutos especialmente seleccionados con agua o disolventes orgánicos. . También se refiere a preparaciones farmacéuticas que contienen las sustancias anteriores en diversas combinaciones y a las propiedades terapéuticas de estas preparaciones para el tratamiento del cáncer, enfermedades degenerativas del sistema nervioso central, diabetes, hiperlipidemia, enfermedades inflamatorias y la prevención de la formación de placas y trombos ateroscleróticos. . (Traducción automática con Google Translate, sin valor legal)
Description
DESCRIPCIÓN
Método de obtención de secoiridoides de tipo oleaceína y oleomisional y de producción de preparados farmacéuticos respectivos
CAMPO DE LA TÉCNICA
La solicitud se refiere a un método de obtención de ciertos secoiridoides de frutos u hojas del olivo, a preparados farmacéuticos que contienen algunos de ellos y a las propiedades terapéuticas de estos preparados. La solicitud se refiere al campo de la medicina, la farmacia y a la ciencia de los alimentos.
ESTADO DE LA TÉCNICA
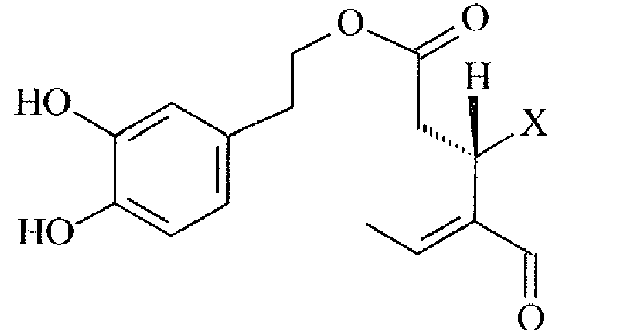
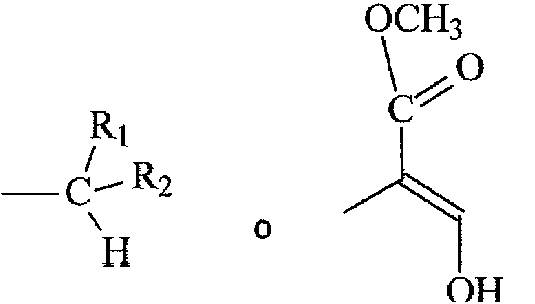
Los secoiridoides del siguiente tipo general
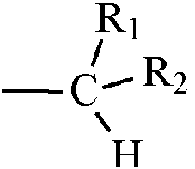
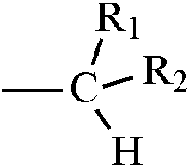
en donde X =
y R1 = H o COOCH3, R2 = CHO
son componentes importantes del aceite de oliva. Específicamente, la S-(E)-oleaceína (1) y el S-(E)-oleomisional (2) son sustancias fenólicas presentes en la mayoría de las variedades de aceite de oliva en concentraciones que varían desde 0 hasta 1000 mg/kg (Journal of Agricultural and Food Chemistry 2014, 62(3), 600-607, OLIVAE 2015, 122, 22-35). La sustancia (2) está en equilibrio con las formas dialdehídicas (2a, b) correspondientes. Para todas esas sustancias existen varios métodos publicados referentes a su aislamiento de fuentes naturales o a su síntesis química y además para todas ellas existen numerosas propiedades biológicas y farmacéuticas publicadas (antiinflamatorias, antineoplásicas, antidiabéticas, neuroprotectoras, antioxidantes).
Sin embargo, los inventores, basándose en los experimentos que han llevado a cabo, son conscientes de que estas sustancias no son las verdaderas formas activas biodisponibles. En realidad, las sustancias (1), (2), cuando se ponen en contacto con líquidos biológicos humanos, reaccionan químicamente con el agua a una velocidad relativamente lenta, diferente para cada sustancia, y se convierten gradualmente en las formas activas de 5S-(E)-oleaceinodiol (3), 5S-(E)-oleomisionadiol (4) que presentan elevada actividad y solubilidad enormemente elevada en agua con respecto a las sustancias (1), (2).
Es, por tanto, muy importante desarrollar métodos que permitan la producción de las sustancias (3), (4) en forma pura y preparados farmacéuticas o suplementos nutricionales o cosméticos que contengan las formas biodisponibles (3), (4) individualmente o en mezcla, por lo que no necesitan activarse al entrar en el cuerpo humano. Al mismo tiempo, es muy importante encontrar nuevos métodos que conducirán a la producción de las sustancias (1), (2) con un mayor rendimiento que los métodos existentes y sin usar cromatografía de líquidos para purificarlas.
Hasta la fecha, la estructura de la sustancia (3) nunca se ha dilucidado completa ni correctamente, ni se ha descrito un método industrialmente utilizable de producción selectiva o en forma de una mezcla de sustancias (3) y (4). Se han descrito los datos espectroscópicos de la sustancia (4) (J. Chem. Soc., Perkin trans. 1995, 1, 1519-1523) después de la hidrólisis enzimática de oleuropeína pura, mientras que la sustancia (4) se ha producido en rendimientos muy bajos, en mezclas con otras sustancias que no se pueden utilizar, de extractos del fruto del olivo (Food Res. Intl. 2000, 33: 475-485).
Se debe mencionar que existen referencias en la bibliografía referentes al uso de plantas de la especie Phillyrea que se han usado para producir el isómero S-(Z)-oleaceinodiol, en mezcla con otras sustancias no utilizables en
rendimiento muy bajo (Phytochemistry Letters 8 (2014) 163-170). Además, las sustancias isoméricas S-(Z)-oleaceinodiol y 5S-(Z)-oleomisionadiol parecen ser producidas con rendimientos muy bajos, en mezclas con otras sustancias que no se pueden utilizar, cuando se extrae aceite de oliva con una mezcla de agua y metanol (J. Agric. Food Chem. 2015, 66, 6053-6063).
Es muy importante tener en cuenta que las sustancias (1), (2) tienen diferentes grupos funcionales y en particular dos grupos aldehído cada uno de los cuales puede reaccionar con agua en una forma diferente y en condiciones diferentes (pH, temperatura, tiempo), siendo, por lo tanto, la asociación de las estructuras específicas (3), (4) con acciones terapéuticas específicas no obvias y teniendo una naturaleza inventiva.
Un elemento de innovación importante en la presente invención es el uso de alcoholes hidrófilos poliméricos como solubilizantes. Los alcoholes propuestos son biocompatibles y pueden solubilizar completamente las sustancias (1), (2) y al mismo tiempo cuando se ponen en contacto con agua, pueden liberar las formas activas (3), (4).
Se debe observar que existen referencias en la bibliografía referentes al uso de plantas de la especie Ligustrum que se han usado para la producción de oleaceína (1) con rendimiento muy bajo, en mezclas con otras sustancias y con procedimientos de purificación complejos (Journal of Ethnopharmacology 120 (2008) 220-225).
Las estructuras químicas de las sustancias descritas en la presente invención son las siguientes:
DESCRIPCIÓN DETALLADA DE REALIZACIONES PREFERIDAS
1. Principio del método de obtención de oleaceinodiol (3) y oleaceína (1):
El oleaceinodiol (3) se produce mediante la reacción de la oleaceína (1) con agua. La oleaceína se produce biosintéticamente a partir de la sustancia precursora oleuropeína bajo la acción de p-glucosidasa, seguido por una reacción de desmetilación y descarboxilación. Los inventores saben que la fuente más abundante de la oleuropeína es u hojas frescas de olivo (Olea europaea L. y todas las subespecies y cultivares) u hojas parcialmente secadas en las que se mantiene la actividad de glucosidasa y desmetilasa. Las enzimas se mantienen en compartimentos celulares separados de la sustancia precursora, de manera que no tiene lugar ninguna reacción cuando la hoja está intacta. Si las enzimas de la planta se ponen en contacto con el precursor en presencia de agua durante la trituración de las hojas, entonces la conversión de la oleuropeína en oleaceína se logra a un rendimiento que puede alcanzar el 1 % en peso de la hoja fresca. Se indica específicamente que, si las hojas se cortan en ausencia de agua, entonces el rendimiento de esta reacción es muy bajo (<0,1 %), no teniendo utilidad práctica. Por tanto, la reacción no ocurre si la temperatura del agua es distinta de 15-40 °C. Estudios previos realizados por extracción de hojas de olivo con agua a una temperatura más alta de, por ejemplo, 100 °C o incluso superior (Procopio et al. J. Agric. Food.
Chem. 2009, 57, 11161-11167 o Conde et al., Food Chem. 2008, 114, 806- 812) indican que los extractos obtenidos solo contienen oleuropeína o productos de descomposición de la misma, tales como hidroxitirosol, pero no oleaceína debido al hecho de que a temperaturas más altas la glucosidasa se desactiva y, por lo tanto, no puede reaccionar con la oleuropeína.
Además, los inventores, basándose en experimentos que han realizado, han encontrado que el oleaceinodiol cuando se pone en contacto con un disolvente orgánico no polar, tal como diclorometano o acetato de etilo, se extrae cuantitativamente y selectivamente en la fase orgánica, liberando una molécula de agua y volviendo a la forma lipófila aldehídica. Los inventores, utilizando todo el conocimiento anterior que han obtenido de sus experimentos, desarrollaron el siguiente método de producción de una disolución de oleaceinodiol puro:
1ai. Hojas frescas de olivo de la especie Olea europaea L., que incluye todas las subespecies y cultivares (u hojas con un contenido de humedad de 0,1-10 %), se cortan en presencia de agua a una relación (hojas: agua p/p) desde 1:1 hasta 1:20 hasta 15-40 °C y se dejan en contacto durante un periodo de tiempo que varía desde 30 minutos hasta 12 horas (mezcla A).
1aii. Alternativamente, frutos frescos intactos de Olea europaea L., que incluyen todas las subespecies y cultivares, o frutos congelados se ponen en contacto con agua a una relación que varía desde 1:1 hasta 1:20 a 15-40 °C durante un periodo de tiempo que varía desde 30 minutos hasta 12 horas. El rendimiento es mayor si el fruto está congelado, ya que durante el proceso de descongelación las células se rompen y se logra el contacto instantáneo del sustrato (oleuropeína) con las enzimas de desglucosilación y desmetilación.
lb. La mezcla acuosa A resultante de 1 ai o 1aii se filtra y se obtiene la fase acuosa. Esta disolución contiene oleaceinodiol mezclado con azúcares y otros fenoles solubles en agua.
lc. La disolución acuosa de la etapa 1b se extrae con un disolvente orgánico inmiscible con agua en una relación que varía desde 1:10 hasta 10:1 (por ejemplo, diclorometano o acetato de etilo o dióxido de carbono supercrítico) y se obtiene la fase orgánica.
ld. La fase orgánica de la etapa 1c se evapora y se obtiene el producto B, que contiene oleaceína del 95 % pureza, sin la necesidad de purificación cromatográfica adicional, a diferencia de todos los métodos conocidos hasta la fecha para la producción de oleaceína.
le. El producto B (oleaceína) se mezcla con agua desionizada y destilada, con agitación vigorosa, a una temperatura de 15-40 °C durante un periodo que varía desde 5 minutos hasta 24 horas, y durante la reacción química con agua se convierte en una disolución de oleacinodiol con un contenido de hasta el 2 % (disolución C). Se debe prestar especial atención al pH del agua, que debe ser neutro (6,9-7,1)
lf. Alternativamente, el producto B (oleaceína de la etapa 1d) se puede mezclar con polietilenglicol PEG200 a 400 (disolución F) y convertir en un hemiacetal de polietilenglicol estable (5) con un tamaño de cadena, como se muestra en la fórmula, que es n = 4-9.
lg. La disolución F se puede diluir con agua a una relación PEG200 (o 400): agua que varía desde 1:10 hasta 1:20 o 1:100, etc., dando la disolución G y convirtiendo el hemiacetal de polietilenglicol de oleaceína (5) en oleaceinodiol (3). La disolución G se puede usar para la administración directa a seres humanos por vía oral (jarabes, disoluciones, suspensiones), inyectable o transdérmica (incorporada en cremas o geles).
lh. La disolución C o F o G se puede usar a una concentración apropiada para preparar supositorios después de mezclar con una base adecuada (base de supositorio) o para preparar comprimidos después de mezclar con excipientes (por ejemplo, lactosa), secado en lecho fluido y compresión. Se debe observar que, en la preparación de comprimidos, usar un excipiente adecuado y ajustar los niveles de humedad durante el secado permite que la sustancia permanezca en forma de diol. Esto se confirma por la disolución instantánea del comprimido en agua que no habría ocurrido si la sustancia estuviera en la forma aldehídica lipófila.
Como se puede apreciar del examen espectroscópico de la disolución C usando espectroscopía de RMN en agua deuterada (D2O) (Figura 1), esto es una disolución verdadera de la forma de diol y no una emulsión de la forma dialdehídica en la fase acuosa, que está presente en una cantidad muy pequeña.
Propiedades farmacéuticas del oleaceinodiol:
li. La disolución C o F o G mostró una potente actividad antioxidante inhibiendo la peroxidación de lípidos a una concentración de 1 μM.
1k. Un estudio de la actividad citotóxica de la disolución C o F o G mostró que el oleaceinodiol a una concentración de 5 μM podría conducir a la muerte del 50 % de las células cancerosas HeLa y MCF-7 y, por lo tanto, la disolución C o F o G y cualquier preparado farmacéutico derivado de la misma se podrían usar para
tratar cáncer.
ll. La disolución C o F o G a una concentración de 50 μM de oleaceinodiol mostró el 65 % de inhibición de la enzima COX-2 y, por lo tanto, la disolución C o F o G y cualquier preparado farmacéutico derivado de la misma se pueden usar para tratar enfermedades inflamatorias.
lm. Por extensión de los casos 1 i-1l, las disoluciones C o F o G tienen las mismas propiedades terapéuticas (neuroprotectoras, antidiabéticas, antitrombóticas) que se conocen para la oleaceína ya que en todos los casos la oleaceína se convierte al menos parcialmente en oleaceinodiol en el medio acuoso en el que se realizan experimentos para medir sus actividades biológicas.
Ejemplo 1
Se cortan hojas secadas de olivo de la variedad Kalamata (10 kg) con 1 % de humedad en presencia de agua (100 l) a 25 °C y se dejan en contacto durante 30 min. La mezcla se filtra y la fase acuosa se obtiene. La disolución acuosa se extrae con diclorometano (80 l) y la fase de diclorometano se obtiene y se evapora a vacío a 30 °C. El residuo (100 g) está constituido por oleaceína con una pureza del 95 %. La oleaceína se mezcla con agua (10 l) bajo agitación vigorosa durante 30 min y se transforma en una disolución pura de oleaceinodiol. Alternativamente, la oleaceína (1 g) se mezcla con PEG200 o PEG 400 (5 ml) y se convierte en el hemiacetal estable de polietilenglicol. Esta disolución es estable a temperatura ambiente durante 12 meses. Esta disolución se puede diluir hasta 100 ml con una disolución saturada de azúcar, dando un jarabe que contiene 1 % de oleaceinodiol, estable durante 15-30 días con uso antiinflamatorio.
Ejemplo 2
Se disponen frutos intactos del olivo (200 g) en el congelador (-20 °C) durante 24 horas y luego se dejan durante 24 horas en contacto con agua (500 ml) a 25 °C. La mezcla se filtra y la fase acuosa se obtiene. La disolución acuosa se extrae con diclorometano (250 ml) y la fase de diclorometano se evapora a vacío. El residuo (1 g) está constituido por oleaceína con una pureza del 95 %. La oleaceína se mezcla con agua (100 ml) con agitación durante 30 min y se convierte en una disolución de oleaceinodiol puro. Alternativamente, la oleaceína (1 g) se mezcla con PEG200 o PEG 400 (5 ml) y se convierte en el hemiacetal estable de polietilenglicol. Se mezclan 100 μl de la disolución de polietilenglicol con base de supositorio fundido (2 g) y se deja que se enfríe dando supositorios de 100 mg.
2. Principio del método de obtención de oleomisionadiol (4) y oleomisional (2)
Los inventores, basándose en experimentos que han realizado, han encontrado que, si las hojas del olivo o los frutos del olivo verdes no maduros intactos se ponen en contacto con un disolvente orgánico lipófilo sin ser triturado el material vegetal, entonces solo tiene lugar la primera etapa de la desglucosilación, no ocurriendo la segunda etapa de la desmetilación. De esta forma, la sustancia precursora oleuropeína se convierte selectivamente en oleomisional.
Esta sustancia, después de retirar el disolvente orgánico, se puede poner en contacto con una disolución acuosa y reaccionar muy lentamente con el agua y convertirse en oleomisionadiol soluble en agua (4). De esta forma se puede separar de los terpenos insolubles en agua que se extraen en la primera etapa con el disolvente orgánico. La disolución pura de oleomisionadiol se obtiene por filtración.
La evaporación de la disolución acuosa puede proporcionar oleomisional puro (2), ya que ocurre una reacción de deshidratación y la forma de aldehído / enol se restaura gradualmente. En esta etapa, el oleomisional coexiste con los dos oleuropeinodiales estereoisoméricos (2a, b).
Los inventores, utilizando todo el conocimiento anterior, derivado de sus experimentos, desarrollaron el siguiente método de obtención de una disolución de oleomisionadiol puro:
2a. Hojas frescas de olivo o frutos del olivo intactos frescos sin ser triturados se ponen en contacto con un disolvente orgánico inmiscible con agua (por ejemplo, diclorometano o acetato de etilo o dióxido de carbono supercrítico) en una relación que varía desde 1:1 hasta 1:20 a 15-40 °C y se dejan en contacto durante un periodo de tiempo que varía desde 30 minutos hasta 12 horas (mezcla A).
2b. La mezcla se filtra y se obtiene la fase orgánica. Esta disolución contiene oleomisional en mezcla con terpenos (principalmente ácido oleanólico y maslínico).
2c. La disolución se evapora a presión reducida y a 30 °C y el residuo se obtiene.
2d. El residuo se disuelve en agua (con un pH de no más de 7) con agitación durante 1 a 24 horas a 15-35 °C y durante la reacción química con agua el oleomisional (y sus isómeros) se convierte en una disolución de oleomisionadiol, mientras que todos los otros componentes siguen siendo insolubles. Los componentes
insolubles se retiran por filtración, y se obtiene la disolución acuosa D que contiene oleomisionadiol puro (4). 2e. La disolución se evapora y se obtiene el producto E, que contiene oleomisional (en equilibrio con sus isómeros) con una pureza total de > 95 % en forma de un líquido viscoso.
2f. El producto E se disuelve en PEG200 o 400 y se convierte en una disolución H que contiene el hemiacetal estable de polietilenglicol de oleomisional (6).
2g. La disolución H se puede diluir con agua en una relación de PEG200 (o 400): agua = 1:10 o 1:20 o 1:100, etc., dando una disolución J en la que el hemiacetal de polietilenglicol de oleomisionadiol (6) se convierte en oleomisionadiol (4). La disolución J se puede usar para la administración directa a los seres humanos por vía oral (jarabes, disoluciones, suspensiones), inyectable o transdérmica (incorporada en cremas o geles).
2h. La disolución D o H o J se puede usar a una concentración apropiada para preparar supositorios después de mezclar con una base adecuada (base de supositorio) o para preparar comprimidos después de mezclar con excipientes (por ejemplo, lactosa), secado en lecho fluido y compresión. Se debe observar que, en la preparación de los comprimidos, el uso de un excipiente adecuado y el ajuste de los niveles de humedad durante el secado permite a la sustancia seguir en la forma de diol.
Como se puede apreciar del examen espectroscópico de la disolución D usando espectroscopía de RMN (Figura 2), esta es una disolución verdadera de la forma de diol que existe en dos formas diaestereoméricas y no una emulsión de la forma dialdehídica.
Propiedades farmacéuticas del oleomisionadiol:
2h. La disolución D o H o J mostró una potente actividad antioxidante, inhibiendo la peroxidación de lípidos a una concentración de 1 μM.
2i. Un estudio de la actividad citotóxica de la disolución D o H o J mostró que el oleomisionadiol a una concentración de 50 μM podría conducir a la muerte celular del 50 % de las células cancerosas HeLa y MCF-7 y, por lo tanto, la disolución D o H o J y cualquier preparado farmacéutico derivado de la misma se pueden usar para tratar cáncer.
2j. La disolución D o H o J a una concentración de oleaceinodiol a 40 μM mostró una inhibición del 62 % de la enzima C0X-2 y, por lo tanto, las disoluciones D o H o J y cualquier preparado farmacéutico derivado de las mismas se pueden usar para tratar enfermedades inflamatorias.
Ejemplo 3
Se dejan hojas frescas de olivo de la variedad Koroneiki (100 g) en contact con diclorometano (500 g) a 25 °C durante 30 min. La mezcla se filtra y la fase orgánica se evapora a vacío. El residuo se disuelve en agua desionizada y destilada a pH = 6 (100 ml) con agitación durante 24 horas, se filtra y se obtiene una disolución de oleomisional puro. La disolución se evapora o liofiliza y se obtiene oleomisional (160 mg) con una pureza de > 95 %. Alternativamente, se mezcla oleomisional (160 mg) con PEG200 o PEG 400 (5 ml) y se convierte en el hemiacetal estable de polietilenglicol. La disolución resultante se puede diluir hasta 100 ml con una disolución saturada de azúcar, dando un jarabe que contiene 0,16 % de oleomisional estable durante 15-30 días con actividad antiinflamatoria.
Ejemplo 4
Se dejan aceitunas intactas frescas de la variedad Koroneiki (200 g) en contacto con diclorometano (500 g) a temperatura ambiente durante 30 min. La mezcla se filtra y la fase orgánica se evapora a vacío. El residuo se disuelve entonces en agua desionizada y destilada a pH = 6 (100 ml) con agitación durante 24 horas, se filtra y se obtiene una disolución de oleomisionadiol puro. La disolución se evapora o liofiliza y se obtiene olieomisional (200 mg) con una pureza de > 95 %. Alternativamente, el oleomisional (1 g) se mezcla con PEG200 o PEG 400 (5 ml) y se convierte en el hemiacetal estable de polietilenglicol de oleomisional.
Claims (14)
1. Un método de obtención de secoiridoides de tipo
en donde
X =
y R1 = H o COOCHa,
R2 = CH(OH)2 o
según el cual:
material vegetal de las especies Olea europaea L., que incluye todas las subespecies y cultivares, se pone en contacto con un disolvente en una relación que varía desde 1:1 hasta 1:20 a una temperatura de 15-40 °C, se deja en contacto durante un periodo de tiempo que varía desde 30 minutos hasta 12 horas, para activar a dicha temperatura una reacción de una enzima con oleuropeína, estando presentes dicha enzima y oleuropeína en dicho material vegetal, y generar una mezcla (A).
2. El método de obtención de secoiridoides según la reivindicación 1, donde el material vegetal es hojas frescas o secadas con humedad que varía desde el 0,1 % hasta el 10 %, que han sido previamente trituradas en el interior de una disolución acuosa o frutos frescos intactos o frutos que han sido refrigerados (a 2-8 °C) o congelados (a -18 a -24 °C) durante al menos 24 horas y el disolvente es agua, que incluye además: filtración de la mezcla (A), obtención de la fase acuosa, extracción de la misma con un disolvente orgánico inmiscible en agua, seleccionado de un grupo de disolventes que consiste en diclorometano o acetato de etilo o dióxido de carbono supercrítico a una relación que varía desde 10:1 hasta 1:10, obtención y evaporación de la fase orgánica, dando un producto (B), que contiene la sustancia donde:
X =
y R1 = H y R2 = CHO
3. El método de obtención de secoiridoides según la reivindicación 2, que incluye además mezclar el producto (B) con agua desionizada y destilada con pH = 6,9-7,1 a una relación de hasta el 2 % p/p y temperatura 15-40 °C durante un periodo de tiempo que varía desde 5 min hasta 24 horas, dando una disolución (C) que contiene la sustancia con:
X =
y R1 = H y R2 = CH(OH)2
4. El método de obtención de secoiridoides según la reivindicación 1, donde el material vegetal está constituido de hojas o frutos frescos intactos, el disolvente es un disolvente orgánico inmiscible en agua, seleccionado de un grupo de disolventes que consiste en diclorometano o acetato de etilo o dióxido de carbono supercrítico y además incluye: filtración de la mezcla (A), obtención de la fase orgánica, evaporación de la misma, obtención del residuo, dilución del mismo en agua desionizada y destilada con pH =≤7 con agitación a una relación de hasta el 2 % p/p y temperatura 15-35 °C durante un periodo de tiempo que varía desde 1 hasta 24 horas, retirada de los componentes insolubles por filtración y obtención de la disolución (D), que contiene la sustancia con:
X =
y R1 = COOCHa y R2 = CH(OH)2,
12. Uso de secoiridoides como en cualquiera de las reivindicaciones 10 u 11 mezclados con excipientes apropiados para producir preparados farmacéuticos para administración ya sea por vía oral, o por vía transdérmica o disoluciones inyectables o supositorios o comprimidos producidos después del secado y compresión.
13. Uso de secoiridoides como en cualquiera de las reivindicaciones 10 u 11 mezclados con excipientes apropiados para la producción de suplementos nutricionales.
14. Los preparados farmacéuticos de la reivindicación 12 para su uso en terapia del cáncer, enfermedades neurodegenerativas, diabetes, hiperlipidemia, enfermedades inflamatorias y para prevenir la creación de placas ateroscleróticas y trombos.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GR20190100075A GR20190100075A (el) | 2019-02-13 | 2019-02-13 | Μεθοδος παραλαβης σεκοϊριδοειδων τυπου ελαιασινης και ελαιομισσιοναλης και παραγωγης των αντιστοιχων φαρμακευτικων παρασκευασματων τους |
| PCT/GR2020/000014 WO2020165613A1 (en) | 2019-02-13 | 2020-02-11 | Method for obtaining oleacein and oleomissional type secoiridoids and for producing respective pharmaceutical preparations |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2951983T3 true ES2951983T3 (es) | 2023-10-26 |
Family
ID=68172228
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES20713080T Active ES2951983T3 (es) | 2019-02-13 | 2020-02-11 | Método de obtención de secoiridoides de tipo oleaceína y oleomisional y de producción de preparados farmacéuticos respectivos |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US12466779B2 (es) |
| EP (1) | EP3924326B1 (es) |
| JP (1) | JP7641904B2 (es) |
| AU (1) | AU2020221684B2 (es) |
| ES (1) | ES2951983T3 (es) |
| GR (1) | GR20190100075A (es) |
| WO (1) | WO2020165613A1 (es) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GR1010545B (el) * | 2019-02-13 | 2023-09-25 | Προκοπιος Παναγιωτη Μαγιατης | Μεθοδος παραλαβης σεκοϊριδοειδων τυπου ελαιοκανθαλης και παραγωγης των αντιστοιχων φαρμακευτικων παρασκευασματων |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5264269B2 (ja) * | 2008-04-28 | 2013-08-14 | 株式会社J−オイルミルズ | 性ホルモン誘発剤及びそれを用いたタンパク代謝改善、体質改善方法 |
| PL227843B1 (pl) * | 2012-07-14 | 2018-01-31 | Warszawski Uniwersytet Medyczny | Zastosowanie Ligustrum vulgare L. do wytwarzania preparatu zawierającego oleaceinę |
| WO2017077134A1 (en) * | 2015-11-05 | 2017-05-11 | Institut D'investigació Biomèdica De Girona | Compounds for the treatment of cancer and/or cancer treatment resistance by inhibition of cancer stem cells |
| PL423146A1 (pl) * | 2017-10-12 | 2019-04-23 | Warszawski Univ Medyczny | Oleaceina do zastosowanie w prewencji miażdżycy |
| GR1010545B (el) | 2019-02-13 | 2023-09-25 | Προκοπιος Παναγιωτη Μαγιατης | Μεθοδος παραλαβης σεκοϊριδοειδων τυπου ελαιοκανθαλης και παραγωγης των αντιστοιχων φαρμακευτικων παρασκευασματων |
-
2019
- 2019-02-13 GR GR20190100075A patent/GR20190100075A/el unknown
-
2020
- 2020-02-11 ES ES20713080T patent/ES2951983T3/es active Active
- 2020-02-11 AU AU2020221684A patent/AU2020221684B2/en active Active
- 2020-02-11 JP JP2021547333A patent/JP7641904B2/ja active Active
- 2020-02-11 US US17/430,467 patent/US12466779B2/en active Active
- 2020-02-11 EP EP20713080.8A patent/EP3924326B1/en active Active
- 2020-02-11 WO PCT/GR2020/000014 patent/WO2020165613A1/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| EP3924326A1 (en) | 2021-12-22 |
| EP3924326B1 (en) | 2023-06-07 |
| EP3924326C0 (en) | 2023-06-07 |
| US20220119335A1 (en) | 2022-04-21 |
| GR20190100075A (el) | 2020-09-16 |
| AU2020221684A1 (en) | 2021-09-23 |
| JP2022521065A (ja) | 2022-04-05 |
| JP7641904B2 (ja) | 2025-03-07 |
| AU2020221684B2 (en) | 2024-12-19 |
| WO2020165613A1 (en) | 2020-08-20 |
| US12466779B2 (en) | 2025-11-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2873449T3 (es) | Composición rica en hidroxitirosol a partir de agua de vegetación de aceitunas y método de uso del mismo | |
| ES2438003T3 (es) | Nuevo extracto de cardo lechero, método para su preparación y empleo | |
| BRPI0708826A2 (pt) | extratos e mÉtodos que compreendem espÉcies de canela | |
| ES2843640T3 (es) | Procedimiento de preparación de un extracto de matriz vegetal con un compuesto anfifílico no iónico como adyuvante de extracción en medio acuoso | |
| PT810222E (pt) | Processo de extraccao de polifenois catequicos a partir de potentilhas extracto obtido e sua utilizacao | |
| JP6985139B2 (ja) | ボスウェリア属の植物に由来する抽出物、並びに関連する生成物及び使用 | |
| ES2951983T3 (es) | Método de obtención de secoiridoides de tipo oleaceína y oleomisional y de producción de preparados farmacéuticos respectivos | |
| AU2025242225A1 (en) | Method for obtaining oleocanthal type secoiridoids and for producing respective pharmaceutical preparations | |
| WO2020097721A1 (en) | Preparation of extracts and compositions comprising extracts | |
| ES3023858T3 (en) | Pharmaceutical products based on cannabinoid acid esters | |
| Galović et al. | Potential of Helicrysum italicum cultivated in urban environment: SCCO2 extract cytotoxicity & NF-kB activation in HeLa, MCF-7 and MRC-5 cells | |
| WO2020256570A2 (es) | Extracto antioxidante y anticancerigeno de la caña de azucar y su manufactura | |
| ES2989459T3 (es) | Proceso para la preparación de un extracto de Epilobium spp. con alto contenido de oenoteína B | |
| Westcott et al. | Medicinal Lignans from Flaxseed: Isolation and | |
| Mshengu | Chemical constituents from Elytropappus rhinocerotis and Rhoicissus tridentata: Structural and Activity Studies | |
| Jelisa | Flavonoid Compound from Rambutan Bark (Nephelium lappaceum L.) | |
| KR100197866B1 (ko) | 신규의 제리쿠드라닌 화합물 및 그의 제조방법 | |
| Putri et al. | Optimization Parameters of Natural Deep Eutectic Solvent Based on Choline Chloride and Fructose for Extraction of Polyphenol from Jotang (Spilanthes acmella) Stem | |
| EP3009132B1 (en) | Method of producing purified stilbene compounds | |
| JP6294259B2 (ja) | β−アルブチンの製造方法 | |
| SU709091A1 (ru) | "Способ получени суммы полифенольных соединений, обладающих желчегонным действием | |
| Wealth | Phytochemistry: A Multifunctional Ecological Heritage and a Rewarding | |
| PL249157B1 (pl) | Sposób wytwarzania preparatu inhibującęgo acetylocholinoesterazę otrzymanego z owoców żurawiny wielkoowocowej | |
| KR100659696B1 (ko) | 산화질소 합성 억제제로서 유용한 스코폴레틴 화합물의 분리방법 | |
| HK1219899B (en) | Method of producing purified stilbene compounds |