KR20140136005A - 지속성 조성물 - Google Patents
지속성 조성물 Download PDFInfo
- Publication number
- KR20140136005A KR20140136005A KR1020147026646A KR20147026646A KR20140136005A KR 20140136005 A KR20140136005 A KR 20140136005A KR 1020147026646 A KR1020147026646 A KR 1020147026646A KR 20147026646 A KR20147026646 A KR 20147026646A KR 20140136005 A KR20140136005 A KR 20140136005A
- Authority
- KR
- South Korea
- Prior art keywords
- composition
- oil
- cyclic amide
- present
- active agent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 114
- 239000002904 solvent Substances 0.000 claims abstract description 37
- 239000004359 castor oil Substances 0.000 claims abstract description 31
- 235000019438 castor oil Nutrition 0.000 claims abstract description 31
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 claims abstract description 31
- 150000003950 cyclic amides Chemical class 0.000 claims abstract description 30
- 241001465754 Metazoa Species 0.000 claims abstract description 26
- 230000002459 sustained effect Effects 0.000 claims abstract description 12
- 239000008365 aqueous carrier Substances 0.000 claims abstract description 10
- 239000013543 active substance Substances 0.000 claims description 47
- 238000000034 method Methods 0.000 claims description 33
- 238000011282 treatment Methods 0.000 claims description 25
- 238000013268 sustained release Methods 0.000 claims description 17
- 239000012730 sustained-release form Substances 0.000 claims description 17
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 claims description 15
- 239000003963 antioxidant agent Substances 0.000 claims description 15
- 230000003078 antioxidant effect Effects 0.000 claims description 13
- 238000004519 manufacturing process Methods 0.000 claims description 11
- 239000005660 Abamectin Substances 0.000 claims description 10
- YZBLFMPOMVTDJY-CBYMMZEQSA-N moxidectin Chemical compound O1[C@H](C(\C)=C\C(C)C)[C@@H](C)C(=N/OC)\C[C@@]11O[C@H](C\C=C(C)\C[C@@H](C)\C=C\C=C/2[C@]3([C@H](C(=O)O4)C=C(C)[C@@H](O)[C@H]3OC\2)O)C[C@H]4C1 YZBLFMPOMVTDJY-CBYMMZEQSA-N 0.000 claims description 9
- 239000005871 repellent Substances 0.000 claims description 9
- 230000002940 repellent Effects 0.000 claims description 9
- -1 epinomectin Chemical compound 0.000 claims description 8
- 239000004322 Butylated hydroxytoluene Substances 0.000 claims description 7
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical group CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 claims description 7
- RRZXIRBKKLTSOM-XPNPUAGNSA-N avermectin B1a Chemical compound C1=C[C@H](C)[C@@H]([C@@H](C)CC)O[C@]11O[C@H](C\C=C(C)\[C@@H](O[C@@H]2O[C@@H](C)[C@H](O[C@@H]3O[C@@H](C)[C@H](O)[C@@H](OC)C3)[C@@H](OC)C2)[C@@H](C)\C=C\C=C/2[C@]3([C@H](C(=O)O4)C=C(C)[C@@H](O)[C@H]3OC\2)O)C[C@H]4C1 RRZXIRBKKLTSOM-XPNPUAGNSA-N 0.000 claims description 7
- 235000010354 butylated hydroxytoluene Nutrition 0.000 claims description 7
- 229940095259 butylated hydroxytoluene Drugs 0.000 claims description 7
- 239000000077 insect repellent Substances 0.000 claims description 7
- 150000001875 compounds Chemical class 0.000 claims description 6
- QLFZZSKTJWDQOS-YDBLARSUSA-N doramectin Chemical compound O1[C@@H](C)[C@H](O)[C@@H](OC)C[C@@H]1O[C@@H]1[C@@H](OC)C[C@H](O[C@@H]2C(=C/C[C@@H]3C[C@@H](C[C@@]4(O3)C=C[C@H](C)[C@@H](C3CCCCC3)O4)OC(=O)[C@@H]3C=C(C)[C@@H](O)[C@H]4OC\C([C@@]34O)=C/C=C/[C@@H]2C)/C)O[C@H]1C QLFZZSKTJWDQOS-YDBLARSUSA-N 0.000 claims description 6
- 229960003997 doramectin Drugs 0.000 claims description 6
- 235000012424 soybean oil Nutrition 0.000 claims description 6
- 239000003549 soybean oil Substances 0.000 claims description 6
- 208000030852 Parasitic disease Diseases 0.000 claims description 5
- 229960004816 moxidectin Drugs 0.000 claims description 5
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 claims description 5
- 235000012343 cottonseed oil Nutrition 0.000 claims description 4
- 239000002385 cottonseed oil Substances 0.000 claims description 4
- FXWHFKOXMBTCMP-WMEDONTMSA-N milbemycin Natural products COC1C2OCC3=C/C=C/C(C)CC(=CCC4CC(CC5(O4)OC(C)C(C)C(OC(=O)C(C)CC(C)C)C5O)OC(=O)C(C=C1C)C23O)C FXWHFKOXMBTCMP-WMEDONTMSA-N 0.000 claims description 4
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical group O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 claims description 4
- LDVVTQMJQSCDMK-UHFFFAOYSA-N 1,3-dihydroxypropan-2-yl formate Chemical compound OCC(CO)OC=O LDVVTQMJQSCDMK-UHFFFAOYSA-N 0.000 claims description 3
- AZSNMRSAGSSBNP-UHFFFAOYSA-N 22,23-dihydroavermectin B1a Natural products C1CC(C)C(C(C)CC)OC21OC(CC=C(C)C(OC1OC(C)C(OC3OC(C)C(O)C(OC)C3)C(OC)C1)C(C)C=CC=C1C3(C(C(=O)O4)C=C(C)C(O)C3OC1)O)CC4C2 AZSNMRSAGSSBNP-UHFFFAOYSA-N 0.000 claims description 3
- SPBDXSGPUHCETR-JFUDTMANSA-N 8883yp2r6d Chemical compound O1[C@@H](C)[C@H](O)[C@@H](OC)C[C@@H]1O[C@@H]1[C@@H](OC)C[C@H](O[C@@H]2C(=C/C[C@@H]3C[C@@H](C[C@@]4(O[C@@H]([C@@H](C)CC4)C(C)C)O3)OC(=O)[C@@H]3C=C(C)[C@@H](O)[C@H]4OC\C([C@@]34O)=C/C=C/[C@@H]2C)/C)O[C@H]1C.C1C[C@H](C)[C@@H]([C@@H](C)CC)O[C@@]21O[C@H](C\C=C(C)\[C@@H](O[C@@H]1O[C@@H](C)[C@H](O[C@@H]3O[C@@H](C)[C@H](O)[C@@H](OC)C3)[C@@H](OC)C1)[C@@H](C)\C=C\C=C/1[C@]3([C@H](C(=O)O4)C=C(C)[C@@H](O)[C@H]3OC\1)O)C[C@H]4C2 SPBDXSGPUHCETR-JFUDTMANSA-N 0.000 claims description 3
- 201000010099 disease Diseases 0.000 claims description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 3
- 229960002418 ivermectin Drugs 0.000 claims description 3
- 239000008159 sesame oil Substances 0.000 claims description 3
- 235000011803 sesame oil Nutrition 0.000 claims description 3
- IBSREHMXUMOFBB-JFUDTMANSA-N 5u8924t11h Chemical compound O1[C@@H](C)[C@H](O)[C@@H](OC)C[C@@H]1O[C@@H]1[C@@H](OC)C[C@H](O[C@@H]2C(=C/C[C@@H]3C[C@@H](C[C@@]4(O3)C=C[C@H](C)[C@@H](C(C)C)O4)OC(=O)[C@@H]3C=C(C)[C@@H](O)[C@H]4OC\C([C@@]34O)=C/C=C/[C@@H]2C)/C)O[C@H]1C.C1=C[C@H](C)[C@@H]([C@@H](C)CC)O[C@]11O[C@H](C\C=C(C)\[C@@H](O[C@@H]2O[C@@H](C)[C@H](O[C@@H]3O[C@@H](C)[C@H](O)[C@@H](OC)C3)[C@@H](OC)C2)[C@@H](C)\C=C\C=C/2[C@]3([C@H](C(=O)O4)C=C(C)[C@@H](O)[C@H]3OC\2)O)C[C@H]4C1 IBSREHMXUMOFBB-JFUDTMANSA-N 0.000 claims description 2
- 235000019482 Palm oil Nutrition 0.000 claims description 2
- 235000019483 Peanut oil Nutrition 0.000 claims description 2
- 235000019485 Safflower oil Nutrition 0.000 claims description 2
- 235000019486 Sunflower oil Nutrition 0.000 claims description 2
- 229950008167 abamectin Drugs 0.000 claims description 2
- 239000000828 canola oil Substances 0.000 claims description 2
- 235000019519 canola oil Nutrition 0.000 claims description 2
- 239000003240 coconut oil Substances 0.000 claims description 2
- 235000019864 coconut oil Nutrition 0.000 claims description 2
- 235000005687 corn oil Nutrition 0.000 claims description 2
- 239000002285 corn oil Substances 0.000 claims description 2
- 239000007972 injectable composition Substances 0.000 claims description 2
- 239000004006 olive oil Substances 0.000 claims description 2
- 235000008390 olive oil Nutrition 0.000 claims description 2
- 239000002540 palm oil Substances 0.000 claims description 2
- 239000000312 peanut oil Substances 0.000 claims description 2
- 238000011321 prophylaxis Methods 0.000 claims description 2
- 235000005713 safflower oil Nutrition 0.000 claims description 2
- 239000003813 safflower oil Substances 0.000 claims description 2
- AFJYYKSVHJGXSN-KAJWKRCWSA-N selamectin Chemical compound O1[C@@H](C)[C@H](O)[C@@H](OC)C[C@@H]1O[C@@H]1C(/C)=C/C[C@@H](O[C@]2(O[C@@H]([C@@H](C)CC2)C2CCCCC2)C2)C[C@@H]2OC(=O)[C@@H]([C@]23O)C=C(C)C(=N\O)/[C@H]3OC\C2=C/C=C/[C@@H]1C AFJYYKSVHJGXSN-KAJWKRCWSA-N 0.000 claims description 2
- 229960002245 selamectin Drugs 0.000 claims description 2
- 239000002600 sunflower oil Substances 0.000 claims description 2
- 230000001225 therapeutic effect Effects 0.000 claims description 2
- 239000012190 activator Substances 0.000 claims 1
- JXGHTEWKHUPUSU-UHFFFAOYSA-N butanedioic acid;methanesulfonic acid Chemical compound CS(O)(=O)=O.OC(=O)CCC(O)=O JXGHTEWKHUPUSU-UHFFFAOYSA-N 0.000 claims 1
- 230000001681 protective effect Effects 0.000 claims 1
- 239000012867 bioactive agent Substances 0.000 abstract description 9
- 238000002347 injection Methods 0.000 description 28
- 239000007924 injection Substances 0.000 description 28
- 238000009472 formulation Methods 0.000 description 24
- 230000000694 effects Effects 0.000 description 20
- 239000004480 active ingredient Substances 0.000 description 17
- 230000002688 persistence Effects 0.000 description 16
- 238000003197 gene knockdown Methods 0.000 description 15
- 244000045947 parasite Species 0.000 description 12
- 230000002085 persistent effect Effects 0.000 description 11
- 239000000546 pharmaceutical excipient Substances 0.000 description 11
- SESFRYSPDFLNCH-UHFFFAOYSA-N benzyl benzoate Chemical compound C=1C=CC=CC=1C(=O)OCC1=CC=CC=C1 SESFRYSPDFLNCH-UHFFFAOYSA-N 0.000 description 10
- 230000008901 benefit Effects 0.000 description 9
- 235000013601 eggs Nutrition 0.000 description 9
- 238000003860 storage Methods 0.000 description 8
- 230000007774 longterm Effects 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 150000002596 lactones Chemical class 0.000 description 6
- 239000003921 oil Substances 0.000 description 6
- 235000019198 oils Nutrition 0.000 description 6
- 229960002903 benzyl benzoate Drugs 0.000 description 5
- 229940000188 cydectin Drugs 0.000 description 5
- 230000002550 fecal effect Effects 0.000 description 5
- 230000001418 larval effect Effects 0.000 description 5
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 4
- 210000000577 adipose tissue Anatomy 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 4
- 229940093471 ethyl oleate Drugs 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- URAYPUMNDPQOKB-UHFFFAOYSA-N triacetin Chemical compound CC(=O)OCC(OC(C)=O)COC(C)=O URAYPUMNDPQOKB-UHFFFAOYSA-N 0.000 description 4
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 239000006184 cosolvent Substances 0.000 description 3
- 238000003682 fluorination reaction Methods 0.000 description 3
- 239000002917 insecticide Substances 0.000 description 3
- 238000011068 loading method Methods 0.000 description 3
- WWZKQHOCKIZLMA-UHFFFAOYSA-N octanoic acid Chemical compound CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 description 3
- 238000012856 packing Methods 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 238000003307 slaughter Methods 0.000 description 3
- 239000004094 surface-active agent Substances 0.000 description 3
- 241000893172 Chabertia Species 0.000 description 2
- GHVNFZFCNZKVNT-UHFFFAOYSA-N Decanoic acid Natural products CCCCCCCCCC(O)=O GHVNFZFCNZKVNT-UHFFFAOYSA-N 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 241000243795 Ostertagia Species 0.000 description 2
- 241001494479 Pecora Species 0.000 description 2
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 description 2
- 239000011149 active material Substances 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000000975 bioactive effect Effects 0.000 description 2
- 230000000740 bleeding effect Effects 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 235000019197 fats Nutrition 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 239000001087 glyceryl triacetate Substances 0.000 description 2
- 235000013773 glyceryl triacetate Nutrition 0.000 description 2
- 230000012447 hatching Effects 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 244000000053 intestinal parasite Species 0.000 description 2
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 2
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 2
- 230000002265 prevention Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- 229960002622 triacetin Drugs 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 241000238876 Acari Species 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- 244000291564 Allium cepa Species 0.000 description 1
- 235000002732 Allium cepa var. cepa Nutrition 0.000 description 1
- 241000239290 Araneae Species 0.000 description 1
- 241000244203 Caenorhabditis elegans Species 0.000 description 1
- 241000202814 Cochliomyia hominivorax Species 0.000 description 1
- 208000003322 Coinfection Diseases 0.000 description 1
- 241001126268 Cooperia Species 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 241000255925 Diptera Species 0.000 description 1
- 241000283087 Equus Species 0.000 description 1
- 239000004348 Glyceryl diacetate Substances 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 241000243976 Haemonchus Species 0.000 description 1
- 241000243974 Haemonchus contortus Species 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- HLFSDGLLUJUHTE-SNVBAGLBSA-N Levamisole Chemical compound C1([C@H]2CN3CCSC3=N2)=CC=CC=C1 HLFSDGLLUJUHTE-SNVBAGLBSA-N 0.000 description 1
- 206010024769 Local reaction Diseases 0.000 description 1
- 241001137882 Nematodirus Species 0.000 description 1
- 241000510960 Oesophagostomum Species 0.000 description 1
- 208000035415 Reinfection Diseases 0.000 description 1
- 241000244174 Strongyloides Species 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- 241001051525 Tortus Species 0.000 description 1
- 241000243797 Trichostrongylus Species 0.000 description 1
- 241000243796 Trichostrongylus colubriformis Species 0.000 description 1
- 241001489151 Trichuris Species 0.000 description 1
- 241001127743 Trilobodrilus axi Species 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- 244000098338 Triticum aestivum Species 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 230000002924 anti-infective effect Effects 0.000 description 1
- 239000003096 antiparasitic agent Substances 0.000 description 1
- 229940125687 antiparasitic agent Drugs 0.000 description 1
- 229960004217 benzyl alcohol Drugs 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- 244000309466 calf Species 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000005018 casein Substances 0.000 description 1
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 1
- 235000021240 caseins Nutrition 0.000 description 1
- 230000000112 colonic effect Effects 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 150000005676 cyclic carbonates Chemical class 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- WPNHOHPRXXCPRA-TVXIRPTOSA-N eprinomectin Chemical compound O1[C@@H](C)[C@@H](NC(C)=O)[C@H](OC)C[C@@H]1O[C@H]1[C@@H](OC)C[C@H](O[C@@H]2C(=C/C[C@@H]3C[C@@H](C[C@@]4(O3)C=C[C@H](C)[C@@H](C(C)C)O4)OC(=O)[C@@H]3C=C(C)[C@@H](O)[C@H]4OC\C([C@@]34O)=C\C=C/[C@@H]2C)\C)O[C@H]1C WPNHOHPRXXCPRA-TVXIRPTOSA-N 0.000 description 1
- 229960002346 eprinomectin Drugs 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229940074076 glycerol formal Drugs 0.000 description 1
- 235000019443 glyceryl diacetate Nutrition 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 150000003278 haem Chemical class 0.000 description 1
- 239000012051 hydrophobic carrier Substances 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000000749 insecticidal effect Effects 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 230000000366 juvenile effect Effects 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 229960001614 levamisole Drugs 0.000 description 1
- HBOQXIRUPVQLKX-UHFFFAOYSA-N linoleic acid triglyceride Natural products CCCCCC=CCC=CCCCCCCCC(=O)OCC(OC(=O)CCCCCCCC=CCC=CCCCCC)COC(=O)CCCCCCCC=CCC=CCCCCC HBOQXIRUPVQLKX-UHFFFAOYSA-N 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000005923 long-lasting effect Effects 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 238000005374 membrane filtration Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000003071 parasitic effect Effects 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000011076 safety test Methods 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 239000013049 sediment Substances 0.000 description 1
- 210000000813 small intestine Anatomy 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000004544 spot-on Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 229960003604 testosterone Drugs 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 239000007143 thioglycolate medium Substances 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000816 toxic dose Toxicity 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- LADGBHLMCUINGV-UHFFFAOYSA-N tricaprin Chemical compound CCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCC)COC(=O)CCCCCCCCC LADGBHLMCUINGV-UHFFFAOYSA-N 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 230000003442 weekly effect Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7042—Compounds having saccharide radicals and heterocyclic rings
- A61K31/7048—Compounds having saccharide radicals and heterocyclic rings having oxygen as a ring hetero atom, e.g. leucoglucosan, hesperidin, erythromycin, nystatin, digitoxin or digoxin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/22—Heterocyclic compounds, e.g. ascorbic acid, tocopherol or pyrrolidones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/44—Oils, fats or waxes according to two or more groups of A61K47/02-A61K47/42; Natural or modified natural oils, fats or waxes, e.g. castor oil, polyethoxylated castor oil, montan wax, lignite, shellac, rosin, beeswax or lanolin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/10—Anthelmintics
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Dermatology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Tropical Medicine & Parasitology (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Plant Substances (AREA)
Abstract
본 발명은 치료적으로 유효한 양의 생리활성제를 포함하는, 이를 필요로 하는 동물을 치료하기 위한 지속성 조성물에 있어서, 상기 조성물이 비수성 담체; 및 피마자유, 적어도 하나의 사이클릭 아미드를 포함하는 용매 시스템;을 포함하는 것을 특징으로 하는 지속성 조성물에 관한 것이다.
Description
본 발명은 생리활성제를 포함하는 지속성 조성물 및 특히, 이에 제한되지 않지만, 동물 내에 또는 동물상의 기생충 감염의 치료 또는 예방용 조성물에 관한 것이다.
의료 및 수의학 분야에서는 개선된 지속성 조성물을 제공할 필요가 있고 또한 오랫동안 필요를 느껴왔다. 지속성 조성물을 이용하는 현저한 이점은 덜 빈번하게 상기 조성물을 투여할 수 있다는 것이다. 이것은 환자 또는 동물에게만 아니라 간병인에게 스트레스, 시간 및 고생이 더 적다는 것에 해당한다. 현저한 이점을 제공하면서, 상기 조성물의 더 적은 소모 및 저장이 또한 필요하다.
이미 사용중인 많은 알려진 생리 활성제가 있지만, 이 경우에 지속성 전달 프로파일을 포함하는 양호한 약물동태학적 특성을 가진 조성물에서 이들을 제공하는 것이 흔히 어려울 수 있다.
문제는 흔히 투여 후 활성제의 불량한 안정성 또는 용해성, 조절되지 않거나 원치않는 방출 프로파일, 불량한 녹다운 효과 또는 원치않는 부작용이 지속된다는 것이다.
예를 들면, 수의학 분야에서, 구충제는 내부 및 외부 기생충을 제어하거나 치료하는데 사용된다. 이러한 기생충을 치료할 때 사용하는 광범위한 다른 구충제 및 유도체가 있다. 그러나, 마크로사이클릭 락톤과 같은 많은 구충제는, 통상적인 용매에 난용성이다. 그들은 일반적으로 외부 및 내부 기생충에 대한 지속성 보호를 위해 사용되는 주사 형태로 투여하는 것이 특히 어렵다.
마크로사이클릭 락톤화합물 예를 들어 아버멕틴(avermectin), 이버멕틴(ivermectin), 도라멕틴(doramectin), 밀버마이신(milbemycin) 및 모시덱틴(moxidectin)은 수성 조성물에 쉽게 분해할 수 있다.
이 문제에 대응하기 위한 시도로서, 제제 화학자는 이러한 활성제를 글리콜 용매, 글리세롤 포르말 및/또는 계면활성제 등의 부형제와 함께 포함시켰다.
그러나, 많은 구충 조성물과 관련하여 직면하는 추가적인 중요한 문제는, 상기 조성물의 대부분에 대해 장기 지속성을 제공하려고 시도했지만, 마크로사이클릭 락톤이 동물 내에서 너무 빠르게 방출된다는 것이다. 이것은 더욱 정기적으로 재투여를 요하는 활성제로부터 보호기간 단축을 초래한다는 점에서 불리하다.
또한 높은 농도의 생리 활성제 (예를 들어, 마크로사이클릭 락톤)에 노출되는 동물, 특히 10주령 미만의 송아지와 같은 어린 동물에게는 매우 위험할 수 있다. 따라서 또 다른 문제는 독성 결과를 회피하기 위해 활성제의 조절되지 않는 방출 프로파일을 회피하려고 시도되고 있다.
더욱이, 흔히 기생충의 시체를 제거하는데 도움이 되는 초기 "녹다운 효과"(knockdown effect)를 제공하기 위하여 활성제의 조절된 "파열"(burst)을 제공하는 것이 유리할 수 있다. 다음에 이러한 조절된 파열은 기생충이 완전히 제거되는 것을 보장하거나, 또는 장기간 보호를 제공하기 위해 구충제의 장기 지속성 느린 방출을 수반할 수 있다.
이와 같은 조절된 프로파일 방출은 특히 하나의 지속성 조성물에서 달성하기 어려울 수 있다. 이것은 구충제와 같은 불안정한 활성물질에 특히 사실이다. 이러한 방출이 달성된다고 하더라도, 그것은 종종 부형제의 복잡한 조합, 제조 과정의 노동 증가, 상기 조성물을 제조하는데 장치 또는 다른 자원을 훼손하면서 실현된다.
주사용 조성물은 지속성 조성물로서 제형화하는데 특히 곤란할 수 있다. 예를 들어, 폴리머, 글리콜, 알코올계 용매 등의 사용되는 부형제의 대부분은 바늘을 통하여 투여하기 어려울 수 있는 조성물에서 높은 점도와 같은 원치 않는 특성들을 초래할 수 있다. 마찬가지로, 지속성 주사제에 사용되는 부형제의 일부는 주사에 대한 부위 반응 증가를 초래할 수 있다. 또한, 일부 조성물은 불량한 저장특성을 가질 수 있다. 더욱이, 활성물질의 지속성 방출 및 따라서 보호의 지속성을 제공하기 위한 시도에도 불구하고, 많은 것이 이러한 목표에 미치지 못하였다.
국제출원 공보 WO 97/11709 (Harvey)는 벤질 알코올과 같은 4개 이상의 탄소 원자를 갖는 알코올로부터 선택된 공용매 및 식물성유를 포함하는 구충성 락톤 조성물을 기술하고 있다.
미국특허 제6,552,002호(Steber)는 계면활성제 (소르비탄 에스테르로서 기술됨), 용매 및 공용매와 함께 고농도(5~30% w/w)로 마크로사이클릭 락톤 화합물을 포함하는 서방성 조성물을 기술하고 있다.
Steber는 일반적으로 사용되는 것 이상으로 상기 활성농도를 증가시킴으로써, 활성물질의 지속적 방출이 가능하다는 것을 논의하고 있다. 그러나 활성물질의 높은 로딩(loading)은 앞서 논의한 바와 같이 독성 문제로 인하여 위험할 수 있다.
더욱이, Steber에서 지속적 방출 프로파일을 제공하기 위해 필요한 활성물질의 농도가 더 높으면 부형제들의 복잡한 조합을 필요로 한다. 이러한 필요에도 불구하고, 활성물질의 높은 로딩은 본질적으로 상기 조성물에 스트레스를 유도하고, 감소된 수명을 유도할 가능성이 있다. 다른 단점은 아마도 더 높은 제조비용 및/또는 전달에 대한 더 큰 부위반응을 포함한다.
미국특허 제6,174,540호 (Williams)는 수소화 피마자유, 소수성 담체 (트리아세틴, 벤질벤조에이트, 또는 에틸 올리에이트), 및 아실화 모노글리세라이드, 프로필디카프릴레이트/디카프레이트의 하나, 또는 카프릴릭/카프릭산 트리글리세라이드와 함께 치료제 (예를 들어 살충제, 구충제, NSAIDs 등)를 포함하는 지속성 주사용 제형을 기술하고 있다. Williams는 확인된 부형제들의 조합이, 예상대로, 다양한 생리활성제에 지속성 방출 프로파일을 제공할 수 있는 능력을 가지고 있다는 것을 밝혀냈다.
NZ 332224 (Grosse-Bley)도 또한 일가- 또는 다가 알코올, 지방족 또는 방향족 알코올, 또는 환상 카보네이트의 지방산 에스테르로부터 선택된 추가적인 공용매와 함께 피마자유를 포함하는 아버멕틴(avermectin) 및 미베마이신(mibemycins)을 포함하는 주사용 제제를 기술하고 있다.
국제출원공보 WO 2007/024719 (Soll)는 추가적인 임의의 부형제와 함께, 생리활성제, 피하 휘발성 용매, 생물학적으로 허용가능한 폴리머를 포함하는, 외부 기생충과 내부 기생충을 치료하기 위한 지속성 주사용 제형을 기술하고 있다. 폴리머의 사용은 특히 방출 프로필을 42일까지 연장 가능한 것으로 논의했다.
EP 393890 (Wicks)는 아버멕틴 화합물에 대한 용매로서 에틸 올리에이트 (지방산 에스테르) 및 참기름의 조합물의 사용을 기술하고 있다. 이들 제제는 주사로 투여시 내약성이 좋은 것으로 밝혀졌다. 그러나 이들은 저장 안정성이 부족하며, 침전물은 4?에서 저장시 며칠 후에 형성된다.
국제출원공보 WO 2010116267 (Costa)는 면실유 및 벤질 벤조에이트의 담체 중에 3.5%에서 도라멕틴(doramectin)의 고농도 주사용 제제를 기술하고 있다. 비교예는 40% v/v 피마자유 및 60% v/v 에틸 올리에이트의 담체 중에 3% 도라멕틴을 함유하는 NZ 332224 (Grosse-Bley)로부터의 제형이다. Costa는 기술된 면실유/벤질 벤조에이트 조성물과 Grosse-Bley에서 비교용 피마자유 조성물 사이에 나선구더기(구더기증 원인 파리 코클리오미아 호미니보락스(Cochliomyia hominivorax)의 유충)를 치료하는데 있어서 효능의 비교를 제공한다. 결과는 피마자유 제제로부터 활성제의 방출이 지연되거나 또는 비교적 느려서 유효한 전신 농도가 면실유/벤질벤조에이트 제형보다 현저하게 더 느리게 도달한다는 것을 보여주었다. 도라멕틴과 같은 아버멕틴에 대한 피마자유의 높은 친화성은 담체로부터 약물의 방출을 유리하지 않게 느리다는 것이 제안되었다.
현재 시판중인 제품인 양(Sheep)의 사이덱틴®(Cydectin®) 지속성 주사제는 모시덱틴(moxidectin)을 함유하는 장기 지속성 제제로서 판매되고 있다. 이 제품은 단일 투여 후 91일 동안 헤몬쿠스 콘토르투스(Haemonchus contortus), 112일 동안 오스테르기아 서컴신타(Ostergia circumcincta), 및 42일 동안 트리코스트론길루스 콜루브리포미스(Trichostrongylus colubriformis)에 의한 재감염을 방지하는 것을 나타낸다. 본 발명자들에 의해 수행된 예비연구는 배설물 샘플에서 부화한 난자에서 유충 카운트를 분석하였다. 이 연구는 사이덱틴®(Cydectin®) 장기 지속성이 약 100일까지 감소된 난자 카운트를 제공하였다는 것을 발견하였다.
(http://cydectin.co.nz/discover-cydectin/cydectin-long-action-injection-for-sheep.aspx)
더욱이, 사이덱틴은 투여 후 동물 내에 주사 부위에서 부위반응 (예를 들어, 붓기 및 염증)으로 이어질 수 있다.
사이덱틴®과 같은 현재 시판중인 조성물보다 더 긴 기간 동안 기생충에 대한 보호를 제공할 수 있는 안정한 지속성 제형을 제공할 필요성이 오래도록 있어왔다.
더욱더, 빠르게 더욱 조절된 "출혈"(bleed)이 동물 내의 증상을 빠르게 조절하기 위한 양호한 초기 녹다운 효과를 제공한 다음, 상기 동물에 더 긴 지속성 보호를 제공하는 치료를 제공하는 제제를 제공할 필요가 있다.
당해 분야에서 지속성 조성물을 제형화하기 위한 여러 시도에도 불구하고, 상술한 문제점들은 계속 지속되고 있다.
본 발명의 목적은 전술한 문제점들을 다루거나 또는 공중에게 유용한 선택을 제공하는 것이다.
본 명세서에 인용된 임의의 특허 또는 특허출원을 포함한 모든 참조문헌들은 본명세서에서 참고로 인용된다. 임의의 참조문헌이 선행기술을 구성하는 것으로 인정하는 것은 아니다. 참조문헌들의 논의는 그의 저자가 주장하는 것을 언급하고, 또한 출원인은 인용된 문서들의 정확성 및 적절성에 이의를 제기할 수 있는 권리를 보유한다. 다수의 선행기술 공보들이 본 명세서에서 인용되어 있지만, 이러한 인용이 이들 문서중의 임의의 것이 뉴질랜드에서 또는 다른 임의의 국가에서 당업계의 일반지식의 일부를 구성함을 인정하는 것은 아니다는 것을 명확하게 이해될 것이다.
본 명세서 전반에 걸쳐, 단어 "~들을 포함한다"(comprise), 또는 "~을 포함한다"(comprises) 또는 "포함하는"(comprising)과 같은 그의 변형은 언급된 구성요소, 정수 또는 단계, 또는 구성요소, 정수 또는 단계의 그룹을 포함하고, 구성요소, 정수 또는 단계, 또는 구성요소, 정수 또는 단계의 그룹을 배제하지 않음을 암시하는 것으로 이해될 것이다.
본 발명의 추가 양상들 및 이점들은 단지 예시적으로 제공되는 다음의 설명으로부터 명백해질 것이다.
본 발명의 한 양상에 따르면, 이를 필요로 하는 동물을 치료하기 위한, 생리활성제를 포함하는 지속성 조성물에 있어서, 상기 조성물이 비수성 담체 및 피마자유 및 적어도 하나의 사이클릭 아미드를 포함하는 용매 시스템을 포함하는 것을 특징으로 하는 지속성 조성물이 제공된다.
본 명세서 전반을 통하여, 용어 "지속성"(long acting)은 초기 투여 후에 유효하며 또한 장기간에 걸쳐 그 효과를 유지하는 의미로 간주되어야 한다.
바람직하게는, 상기 조성물의 지속성 성질이란 용어는 초기 투여 후에 40일 이상 허용 가능하고 적절한 효능을 제공한다.
본 발명의 장점
본 발명자들은 놀랍게도 본 발명의 조성물이, 동물에게 전달되는 경우, 본 조성물의 급속한 녹다운 및 우수한 지속성 특성을 제공한다는 것을 밝혀냈다.
이론으로 제한받고 싶지 않지만, 본 발명자들은 본 발명의 급속한 녹다운 및 양호한 장기 지속성이란 유리한 특성들이 적어도 하나의 사이클릭아미드 용매와 피마자유의 조합에 의해 제공될 수 있다고 생각한다.
본 발명자들은 사이클릭 아미드 용매가 단기간내에 생리활성제의 초기 방출을 가능하게 하고, 피마자유가 장기간에 걸쳐 생리활성제의 더 긴 방출을 유지한다고 생각한다. 즉, 상기 피마자유 및 사이클릭 아미드 용매는 시간 경과에 따라 주사 부위로부터 활성제의 이상성 방출(biphasic release)을 제공하며, 이는 함께 상승적으로 작용하여 상기 활성제의 입증된 방출 프로파일을 제공하는 것으로 생각된다.
이러한 이상성 방출은 본 발명이 가장 바람직하게는 모시덱틴과 같은 구충제를 사용함에도 불구하고 실질적으로 임의의 생리활성제와 함께 사용될 때 나타나는 것으로 예상된다.
본 발명자들은 본 조성물이 또한 전달 후에 생리활성 방출의 조절된 단기간 "파열"을 제공하여 초기 녹다운 효과에 이어서 상기 생리활성제의 장기간 전달을 제공하는데 사용될 수 있다고 예견하였다. 이것은 동물을 빠르게 안정화시키거나 치료하기 위해 단기간내에 더 높은 수준으로, 단 장기간에 걸쳐 더 낮은 수준으로(예를 들면 증상의 심각도가 줄어들면) 상기 생리활성제가 필요한 더욱 급성 증상을 치료하는데 매우 유용할 수 있다. 이러한 유리한 방출 프로파일 없이, 간병인은 동일한 결과를 달성하기 위해 동시에 또는 연속적으로 투여된 두 가지 치료를 별도로 전달해야 할 수 있다.
요약하면, 본 발명의 몇몇 이점들은 다음을 포함할 수 있다:
- 동물에게 별도의 처리 스트레스를 회피하기 위해 반복투여와는 대조적으로 단일 투여량의 허용;
- 전달 후 단기간 및 장기간에 걸쳐 생리활성제의 지속된 방출 프로파일;
- 그렇지 않으면 활성제의 조절되지 않은 방출로 인해 발생할 수 있는 독성문제의 회피;
- 상업적으로 시판중인 사이덱틴®과 같은 지속성 조성물에 비하여 개선된 지속성 및 녹다운 효과 (아래 참조);
- Steber등이 교시한 바와 같이 더 긴 지속성을 달성하기 위해 활성제의 높은 로딩을 회피하고 따라서 본 조성물의 잠재적인 부작용 또는 불안정선 등을 감소시킴;
- 장기간 저장 안정성;
- 제조 공정의 효율성;
- 전달시 부위 반응이 적거나 없음. 저투여량 시험은 부위 반응(site reaction)을 나타내지 않았다. 고투여량 시험(아래에 설명)은 사이덱틴®과 유사한 최소한의 부위반응을 나타냈다. 이것은 본 발명의 조성물이 주사 부위에서 느린 방을 제공하는 것으로 보이기 때문에 예기치 않은 것이며, 따라서 사이덱틴®보다 더 높은 부위반응이 기대되었다.
사이덱틴과
비교:
본 발명의 예시적인 조성물을 사이덱틴®과 비교한 경우 (지속성 모시덱틴 주사) 예비결과는 사이덱틴®의 지속기간에 비하여 90일 후에 피하지방에서 상당히 높은 잔류물을 나타냈다. 이것은 본 발명의 조성물에 의해 제공되는 더 큰 지속성을 강력하게 뒷받침한다. 본 연구들은 동일한 활성성분(모시덱틴) 및 농도가 사이덱틴®에 존재하는 시험 조성물에서 사용되었다는 것을 보장하기 위해 설정되었다.
이들 연구는 모시덱틴이 사이덱틴®에서 나타나는 것보다 더욱 효과적으로 지방조직 내에 흡수될 수 있다는 것을 제안한다. 지방 조직내에 모시덱틴 흡수율이 혈중 농도와 상관 없이, 최대 한계를 가지고 있다는 것이 가능하다. 따라서, 본 발명에 의해 제공되는 주사 부위로부터 잠재적으로 더 느린 방출은 실제로 상당량의 활성제를 지방 내로 흡수시킬 수 있다.
일단 지방조직에서, 모시덱틴은 다른 조직내로 서서히 방출되는 것으로 생각된다.
사이덱틴®에서 더 빠르게 방출되는 활성제는 간과 같은 다른 수단에 의해 혈류 및/또는 주사 부위로부터 제거되며, 따라서 지방조직으로 유효한 전이를 방지하는 것이 가능하다.
또한 활성제의 높은 투여량은 예시된 지속성을 달성하는데 도움이 될 수 있으며, 이것은 주사부위로부터 느린 방출에 의해 도움이 될 수 있다. 그러나 사이덱틴®이 시험제제로서 2% w/w의 동일한 복용량을 포함한 경우, 높은 수준의 모시덱틴이 보는 바와 같이 개선된 결과에 대한 유일한 이유가 될 수 없는 것으로 생각된다.
본 발명의 추가 양상들은 첨부된 도면과 관련하여 단지 예시적으로 제공되는 다음의 설명으로부터 명백해질 것이다.
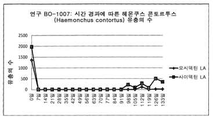
도 1: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 헤몬쿠스 콘토르투스(Haemonchus contortus) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 2: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 트리코스트론길루스(Trichostrongylus) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 3: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 쿠우퍼리아(Cooperia) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 4: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 오에소파고스토뭄/샤베르티아(Oesophagostomum / Chabertia) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 5: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 오스테르타기아(Ostertagia) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 1: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 헤몬쿠스 콘토르투스(Haemonchus contortus) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 2: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 트리코스트론길루스(Trichostrongylus) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 3: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 쿠우퍼리아(Cooperia) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 4: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 오에소파고스토뭄/샤베르티아(Oesophagostomum / Chabertia) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
도 5: 지속성 및 녹다운 효과에 대하여 부화한 난자로부터 오스테르타기아(Ostertagia) 유충 카운트의 파일럿 비-도살연구 (제형 1과 사이덱틴® LA 주사제의 비교).
바람직한 실시형태
바람직하게, 본 조성물은 비경 주사를 위해 구성된다.
본 조성물의 중요한 이점은 사용된 부형제가 용이한 주사를 위해 양호한 일관성을 허용한다는 것이다. 현재 이용가능한 유사한 조성물, 예를 들면 사이덱틴®은 매우 점성일 수 있으며, 이것은 주사를 어렵게 할 수 있으며, 특히 동물에게 잠재적으로 고통스럽거나 또는 해로울 수 있다. 예를 들어, 사이덱틴®은 그의 점도 요구 사항 때문에 사용되는 특수한 주사기를 필요로 한다. 예비 연구에서, 본 발명의 시제품은 사이덱틴®보다 투여하기에 더 용이한 것으로 보였다.
그러나, 유익한 지속성 방출 프로파일을 제공할 수 있는 본 조성물의 능력은 당업계에서 일반적으로 사용되는 공지된 부형제를 사용하여, 다른 투여경로에 용이하게 적합할 수 있다. 이러한 전달 양상은 국소 (예를 들면 스폿(spot-on) 또는 스프레이(spray-on)에 적합한 조성물), 또는 경구 (예를 들면 정제 또는 음약에 적합한 조성물) 또는 내부 (예를 들면 덩어리로서 적합한 조성물)를 포함할 수 있다.
바람직하게는, 상기 생리활성제는 구충제 화합물이다.
상기 구충제는 상기 조성물중에 0.005 내지 30% w/v의 농도로 존재할 수 있다.
바람직하게는, 상기 구충제는 상기 조성물 중에 0.005 내지 5% w/v의 농도로 존재한다.
본 발명의 중요한 이점은, 원하는 방출 프로파일이 구충제의 정상적 및 안전한 양을 사용하여 달성될 수 있다는 것이다. 이것은 잠재적으로 활성제의 독성투여량의 위험을 무릎쓰고 동물을 두고, 적합한 방출 프로파일을 달성하기 위해 활성 농도를 5-30%로 증가시킬 필요성을 논의하는 미국특허 제6,552,002호(Steber)와는 다르다.
명확하게는, 대안적인 생리활성제가 사용되는 경우, 생리활성제의 양은 임상적 및 약물동력학적 요구사항에 맞도록 조절될 수 있다.
그러나, 본 발명자들은 생리활성제는 대안적으로 본 발명의 범위를 벗어나지 않고 살충제, 구충제, 성장촉진제, 항감염 또는 NSAID와 같은 임의의 생리활성제일 수 있다는 것을 인정한다. 합리적으로는, 사이클릭 아미드 용매와 함께 오일의 본 발명 조합물이 상술한 바와 같은 지속성 방출 프로파일을 필요로 하는 임의의 생리 활성제와 함께 사용될 수 있는 것으로 예상할 것이다. 이것은 부형제들의 조합물이 아직 여전히 원하는 결과를 제공하는 다양한 생리활성제와 함께 사용될 수 있다는 것을 확인하는 미국특허 제6,174,540호 (Williams)의 기술내용에 의해 뒷받침된다.
본 발명자들은 특히 본 발명이 실질적으로 임의의 마크로사이클릭 락톤 화합물, 예를 들면 아버멕틴 및 밀버마이신과 함께 잘 작용한다고 생각한다.
바람직하게, 상기 구충제는 아버멕틴(avermectin), 모시덱틴(moxidectin), 밀버마이신(milbemycin), 이버멕틴(ivermectin), 아바멕틴(abamectin), 도라멕틴(doramectin), 에프리노멕틴(eprinomectin) 및 셀라멕틴(selamectin)으로 이루어진 군으로부터 선택된다.
바람직하게는, 상기 구충제는 모시덱틴이다.
모시덱틴은 사이덱틴®에 의해 예시되는 바와 같이 장기간 동안 치료수준으로 알려진 지속성을 가지기 때문에 가장 바람직한 활성제이다. 모시덱틴은 또한 높은 수준의 효능, 광범위한 활성을 가지며 또한 사용하기에 비교적 안전하다.
관계없이, 본 발명이 그의 범위를 벗어나지 않고 다른 유형의 활성제 및 상기 활성제를 포함하는 조성물의 용도를 확장하는 것으로 이해하여야 한다.
피마자유는 상기 활성제의 용매시스템의 일부로서 유용하고, 상기 활성제의 지속된 방출을 제공하는데 특히 유익한 것으로 발견되었다.
상기 피마자유는 상기 조성물 중에 1 내지 70% w/v의 농도로 존재할 수 있다.
바람직하게는, 피마자유는 상기 조성물중에 1 내지 20% w/v로 존재한다.
더욱 바람직하게는, 상기 피마자유는 본 조성물 중에 1 내지 15% w/v로 존재한다.
본 발명자들은 대략 7% w/v 피마자유의 농도가 특히 효과적으로 작용한다는 것을 발견하였다. 이러한 양의 피마자유는 주사 부위에서의 최적 비율로 상승적으로 방출되는 활성제를 생기게 하는 경향이 있었다.
본 조성물은 비-수성 담체를 포함한다.
바람직하게 상기 비-수성 담체는 투여되었을 때 적합한 점도 및 내약성 등 본 조성물에 적합한 물리적 특성을 제공하도록 선택된다.
바람직하게 상기 비-수성 담체는 오일 등의 소수성 매개체이다.
바람직하게는, 상기 오일은 식물성, 동물성 또는 합성 기원이다.
더욱 바람직하게는, 상기 담체는 카놀라유, 옥수수유, 면실유, 올리브유, 땅콩유, 참기름, 대두유, 잇꽃유, 코코넛유, 해바라기유, 팜유, 모노글리세라이드, 디글리세라이드 및 트리글리세라이드, 중간사슬 숙신산 트리글리세라이드, 카프릴 릭/카프릭 트리글리세라이드, 카프릴릭/카프릭/리놀레익 트리글리세라이드, 카프릴 릭/카프릭/숙신 트리글리세라이드로 구성된 그룹으로부터 선택된다.
가장 바람직하게는, 상기 담체는 대두유이다.
바람직하게는 상기 활성제는 용매 시스템의 존재없이 상기 비수성 담체 중에 불용성이거나 비교적 불용성이다.
본 발명자들은 담체로서 대두유 및 용매 시스템으로부터 피마자유의 조합이 특히 유용한 방출 특성들을 제공한다는 것을 밝혀냈다. 이것은 대두유 때문에 용매시스템에 의해 가용화된 활성성분을 투여하기 위한 매개체로서 작용하는 비교적 불활성 담체인 것으로 생각된다.
상기 사이클릭 아미드 용매는 상기 조성물중에 1 내지 50% w/v의 농도로 존재할 수 있다.
바람직하게는, 상기 사이클릭 아미드 용매는 상기 조성물중에 약 15% w/v의 농도로 존재한다.
본 발명자들은 상기 지속성 조성물 중에 사이클릭 아미드 용매를 사용하면 상기 조성물의 상기 지속성 방출이 잔류 오일에 의해 조절되기 전에 생리활성 성분의 초기 "출혈"을 허용한다는 것을 확인하였다. 용매로서 피마자유를 사용하여, 특히 아버멕틴 및 밀베마이신을 사용하여 선행기술에서 확인된 현저한 단점은 활성성분과 피마자유 사이의 친화성이 너무 낮으면 활성성분의 방출이 너무 느릴 수 있다는 것이다. 이것은 활성성분의 효과를 지연시키고, 활성성분이 완전히 효과적인 것을 방지하고 및/또는 내성 발전 가능성을 증가시킬 수 있다. 상기 용매 시스템으로서 피마자유와 조합하여 사이클릭 아미드를 사용하면 이러한 문제를 놀랍게도 해결한다.
이론으로 제한받고 싶지 않지만, 본 발명자들은 사이클릭아미드 용매가 활성성분과의 복합체를 형성할 수 있으며, 이것은 동물내에 투여된 조성물로부터 활성성분의 일부를 빠르게 방출한다고 생각한다. 다음에 활성성분의 나머지는 상기 조성물로부터 더욱 느리게 방출할 수 있으며, 지속성 효과를 가능하게 한다.
그 외에, 상기 사이클릭아미드 용매 및 피마자유의 조합은 종래기술에 비하여 피마자유의 요구조건을 낮추는 것을 도울 수있다. 이것은 유리하게 방출 속도/지속성 효과를 제어할 수 있는 더 큰 능력을 제공할 수 있다.
더욱이, 본 발명자들은 사이클릭 아미드 용매의 농도를 조절하면 초기 "출혈"의 속도의 주의 깊은 조절을 허용할 수 있다는 것을 확인하였다. 이것은 동물에서 증상의 심각도 또는 치료하고자 하는 증상에 따라 상기 조성물의 초기 방출 프로파일을 조심스럽게 변경할 수 있는 능력을 제공할 수 있다. 이것은 흔히 활성성분의 조절되지 않은 초기 방출과 함께 악명스러울 정도로 조절하기 힘들 수 있기 때문에 유리할 수 있다.
바람직하게는, 상기 사이클릭 아미드 용매는 피롤리돈이다.
더욱 바람직하게는, 상기 피롤리돈은 1-메틸-2-피롤리디논(NMP), 2-피롤리돈 및 이들의 조합으로 이루어진 군으로부터 선택된다.
가장 바람직하게는, 상기 사이클릭아미드 용매는 NMP이다. NMP의 이점은 그것이 제약 업계에서 통상 사용되고 있다는 것이고, 내성이 좋고 또한 비교적 저렴하다는 것이다.
특히 바람직한 조성물은 피마자유와 NMP의 조합물과 함께, 생리활성제로서 모시덱틴을 포함한다.
본 조성물은 항산화제를 포함 할 수 있다. 실질적으로 임의의 항산화제가 사용될 수 있다. 그러나, 본 발명자들은 특히 유용한 항산화제가 부틸화 하이드록시아니솔(BHA), 부틸화 하이드록시톨루엔(BHT) 또는 이들의 조합일 수 있다고 생각한다.
상기 문헌에서, 항산화제들은 조성물 중의 마크로사이클릭 락톤을 안정화시키는데 사용되었다. 그러나, 마크로사이클릭 락톤 화합물을 다른 활성성분과 함께 조합하는 경우에, 상기 항산화제는 흔히 상기 조성물을 안정화시키는데 충분하지 않다. 본 발명의 조성물은 다수의 활성성분 (예를 들어 마크로사이클릭 락톤 및 레바미솔)을 함께 조합시킬 수 있으며, 또한 상기 항산화제를 그의 통상의 항산화제 기능을 수행하고 및/또는 상기 제제를 안정화하기 위해 존재할 수 있다.
전형적으로, 상기 항산화제는 상기 제제중에 0.005 내지 10% w/v로 존재할 수 있다.
바람직하게, 상기 항산화제는 BHT이고 상기 조성물중에 대략 0.05% w/v의 농도로 존재한다.
다른 담체 또는 부형제는 다음 성분들중의 하나를 포함할 수 있다: 아세틴 (모노, 디 및 트리아세틴), 에틸 올리에이트 및 벤질 벤조에이트.
치료 방법
상기 논의한 바와 같은 조성물로 이를 필요로 하는 동물을 치료하는 방법이며, 상기 동물에게 상기 조성물을 전달하여 증상 또는 질병에 대하여 지속성 보호 및 이들의 치료를 제공하는 단계를 포함하는 방법.
바람직한 실시형태에서, 상기 방법은 내부 또는 외부 기생충 감염의 보호 또는 치료 방법이다. 예를 들어, 상기 방법은 사상충 또는 장내 기생충의 보호 또는 치료를 위한 것일 수 있다. 이 실시형태에서, 상기 조성물중에 사용되는 상기 생리활성제는 모시덱틴과 같은 적어도 하나의 구충제를 포함한다.
본 조성물은 적어도 50일 이상 동안 상기 생리활성제의 지속적 전달을 제공하도록 구성될 수 있다. 초기 연구(최선의 양태 참조)는 상기 지속성 제제가 초기 투여 후 133 이상 효과적일 수 있다고 지적했다. 이것은 사이덱틴®과 같은 현재 사용가능한 제제의 중요한 이점이다.
기생충 감염에 대한 예방 또는 치료를 위해, 상기 조성물 중의 적어도 하나의 생리활성제가 구충제인, 실질적으로 상술한 바와 같은 조성물의 제조에서의 사용.
바람직하게는, 상기 사용은 사상충 또는 장내 기생충에 대한 지속성 예방 또는 치료를 위한 것이다.
제조 방법
적어도 하나의 오일 및 적어도 하나의 사이클릭 아미드 용매를 생리활성제에 첨가하는 단계를 특징으로 하는, 생리활성제를 포함하는 지속성 조성물의 제조방법.
바람직하게, 상기 방법은 다음 단계를 포함한다:
a) 제조용기에 상기 사이클릭 아미드 용매를 첨가하는 단계;
b) 상기 사이클릭 아미드 용매에 상기 생리활성제를 첨가하는 단계;
c) 상기 혼합물에 상기 피마자유를 첨가하는 단계; 및
d) 비수성 담체를 용적까지 첨가하는 단계.
바람직하게는, 상기 사이클릭 아미드 용매는 b) 단계 이전에 약 40 내지 50 ?로 가열된다.
바람직하게는, 상기 생리활성제는 단계 c) 이전에 사이클릭 아미드 용매 중에 용해된다.
바람직하게는, 항산화제는 단계 b) 이전에 첨가된다. 본 발명자들은 이것이 상기 조성물의 전반적인 효과/안정성을 향상시키는 중요한 단계였다는 것을 발견했다. 이것은 특히 사이클릭아미드 용매가 바람직하게 가열되는 경우인 것으로 밝혀졌다.
발명을 실시하기
위한 최선의 양태
실시예 1 : 제제 1
| 모시덱틴 주사 LA | |||
| SI 번호 | 성분들 | %w/v | 기능 |
| 1 | 모시덱틴** | 2.1 | 활성성분 |
| 2 | BHT(부틸화된 하이드록시톨루엔) | 0.05 | 항산화제 |
| 3 | NMP(Pharmasolve) | 15 | 용매 |
| 4 | 피마자유 | 7 | 용매 |
| 5 | 대두유 | 적량 | 담체 |
** 임의의 미량을 채우기 위해 첨가된 5% 과량은 안정성을 손실하고 제조과정 중에 손실된다.
| 제제 1의 시험 | 설명서 |
| 설명 | 투명한 황색, 약간 점성 용액 |
| 상대 밀도 | 0.920 - 0.980 @ 20℃ |
| 활성성분: 모시덱틴 | 1.96 - 2.20% w/v (제조시) 1.80 - 2.30% w/v (종료시) |
| 무균성 | 막여과법(BP방법)에 의함 30-35℃에서 14일(최소)배양 후 유동 티오글리콜레이트 배지에서 성장 없음 20-25℃에서 14일(최소)배양 후 대두 카제인 소화 배지에서 성장 없음 |
실시예 2: 안전성 시험
배치 번호: T1782, 배치 크기: 3.5L
저장 조건: 25℃/60% RH
포장: 100mL flexipack 감마+불소화
| 초기 | 3개월 | 6개월 | 9개월 | 18개월 | |
| 설명 | 적합 | 적합 | 적합 | 적합 | 적합 |
| 상대밀도 | 0.944 | 0.942 | 0.943 | 0.941 | 0.943 |
| 활성성분: 모시덱틴 |
2.10 | 2.11 | 2.10 | 2.10 | 2.05 |
| 무균성 | 적합 | 적합 | 적합 | 적합 | 적합 |
배치 번호: T1782, 배치 크기: 3.5L
저장 조건: 30℃/65% RH
포장: 100mL flexipack 감마+불소화
| 초기 | 3개월 | 6개월 | 9개월 | 18개월 | |
| 설명 | 적합 | 적합 | 적합 | 적합 | 적합 |
| 상대밀도 | 0.944 | 0.942 | 0.939 | 0.941 | 0.942 |
| 활성성분: 모시덱틴 |
2.10 | 2.11 | 2.11 | 2.09 | 2.02 |
| 무균성 | 적합 | 적합 | 적합 | 적합 | 적합 |
배치 번호: T1782, 배치 크기: 3.5L
저장 조건: 40℃/75% RH
포장: 100mL flexipack 감마+불소화
| 초기 | 3개월 | 6개월 | 9개월 | |
| 설명 | 적합 | 적합 | 적합 | 적합 |
| 상대밀도 | 0.944 | 0.942 | 0.940 | 0.940 |
| 활성성분: 모시덱틴 |
2.10 | 2.08 | 2.05 | 2.03 |
| 무균성 | 적합 | 적합 | 적합 | - |
실시예 3
지속성 및 녹다운 효과 분석에 대하여 배설물 샘플로부터 부화한 난자로부터 유충 카운트의 파일럿 비-도살 연구 (결과는 도 1-5에 도시되며, 여기서 제형 1은 모시덱틴 LA로 표시됨).
상기 처리군은 시린지 (0.2mL 증가분으로 측정할 수 있음)를 사용하여 투여하였으며, 각각의 동물에 투여될 수 있는 용량은 그의 생체중을 기준으로 하였으며, 이것은 처리 일(0 일)에 결정하였다. 시험 제제 및 참조제품의 투여량 (양에 대한 사이덱틴 지속성 주사)는 1mL/20kg (1mg/kg)이었다. 이러한 용량은 귀 바로 아래의 목 쪽에 피하주사로 투여하였다.
배설물 샘플은 19주 동안 대략 주 간격으로 처리 후 수집하였다. 이들 샘플은 직장으로부터 직접 수집하고 최소 2g으로 평량하였다. 배설물 난자 카운트는 각각의 샘플에 대해 수행하였으며 또한 정량적 유충 배양은 각각의 샘플링 시간에서 각각의 처리 군으로부터 모아진 샘플에 대해 수행하였다.
파일럿 연구는 2% w/v 모시덱틴을 함유하는, 양(sheep)에 대한 사이덱틴® 지속성(LA) 주사에 비하여 시험된 모든 실시예에서 제제 1의 개선된 지속효능을 예시하였다.
일반적 경향은 유충 카운트가 상승하기 시작함에 따라 사이덱틴®이 100일 이하로 지속성을 상실하기 시작하였다는 것을 보여주었다. 일부의 경우에 이러한 상승은 점차적이었으며 (도 1), 또 다른 경우에 상기 상승은 급격하였다 (예를 들면 도 4 및 5 참조).
그러나 모든 경우에 제제 1은 100일 마크 이후 감소된 유충 카운트를 보여주었다. 이것은 시판중인 사이덱틴®에 비하여 본 발명의 개선된 지속성을 예시한다.
그 외에, 제제 1은 사이덱틴®에 비하여 시험 기간 전반에 걸쳐 전체적으로 양호한 효능을 나타냈다. 도 1-5의 각각에서 제제 1은 기선(base line)에 근접되게 잔류하였으며, 반면 사이덱틴®은 흔히 도 2, 3, 4 및 5에 도시된 바와 같이 기선으로부터 편차을 나타냈다.
실시예 4
사이덱틴® LA 주사제에 비하여 추천된 최소 투여량으로 투여하였을 때 양에서 회충의 자연 혼합 감염에 대하여, 실시예 1에서와 같이 제제 1의 녹다운 효능을 평가하기 위한 파일럿 도살 효능 연구.이 연구는 처리 후 7일 및 13일에 배설물 유충 배양 데이터와 함께 처리군의 투여 후 13일에 도살하였을 때 총 기생충 카운트(worm counts)의 결정을 포함하였다.
처리 후 7일 및 13일에 배설물 샘플 유충 배양 데이터를 기본으로 하는 효능은 하기 표 6에 나타낸다. 처리 후 13일에 제사위, 소장 및 대장 분석으로부터 총 성인 기생충 카운트를 기본으로 하는 효능은 하기 표 7에 나타낸다.
이들 초기 결과는 제제 1과 사이덱틴® LA 대조예의 효능 사이의 현저한 차이를 나타내지 않았다. 이것은 제제 1이 시판중인 사이덱틴® 제품에 비하여 적절한 녹다운 효과를 유지한다는 것을 예시한다.
표 6. 미처리 대조군에 비하여 또한 배설물 유충 배양 데이터를 기본으로 하여 모시덱틴 LA 주사 또는 사이덱틴 지속성 주사로 처리 후 7일 및 13일에 각각의 기생충 종의 수 및 제어 수준(%).
| 기생충 종 | 처리 후 일 | |||||
| 7 | 13 | |||||
| 투여된 제품 | 투여된 제품 | |||||
| 모시덱틴 LA 주사 | 사이덱틴 LA | 미처리 | 모시덱틴 LA 주사 | 사이덱틴 | 미처리 | |
| 헤몬쿠스 | 100% (0) |
100% (0) |
10800 | 100% (0) |
100% (0) |
5200 |
| 오스테르타기아 | 95.8% (275) |
95.8% (271) |
6480 | 99.6% (14) |
98.4% (53) |
3380 |
| 트리코스트론길루스 | 82.1% (155) |
63.1% (319) |
864 | 95.1% (64) |
96.8% (41) |
1300 |
| 쿠우퍼리아 | 100% (0) |
100% (0) |
2160 | 100% (0) |
100% (0) |
2340 |
| 오에소파고스토뭄/샤베르티아 | 100% (0) |
100% (0) |
1296 | 100% (0) |
100% (0) |
780 |
(괄호안의 수는 발견된 유충의 실제 수를 나타낸다)
표 7. 미처리 대조군과 비교하여 총 기생충 카운트을 기준으로 하여 처리 후 13일 5단계 (성인) 기생충에 대하여 시험 및 참조 제품의 효능(%)
| 제품 | 제사위 | 소장 | 대장 | |||||||
| Haem | Ost | T. axei | Nem | Trich | Coop | Strong | Oes | Chab | Trichu | |
| 모시덱틴 LA | >99.9 | >99.9 | >99.9 | 99.9 | 90.6 | 99.9 | 87.8 | >99.9 | >99.9 | >99.9 |
| 사이덱틴 LA | >99.9 | >99.9 | >99.9 | 99.9 | 95.7 | >99.9 | 96.6 | >99.9 | >99.9 | >99.9 |
1미처리 대조 동물에 비하여 기하평균의 감소(%)를 기준
Heam = 헤몬쿠스 콘토르투스,
Ost = 오소테르타기아 서컴신타,
Nem = 네마토디루스 sp.(Nematodirus sp),
Trich = 트리코스트론길루스 sp.,
Coop = 쿠우퍼리아 spp.,
Strong = 스트론길로이데스(Strongyloides),
Oes = 오에소파고스토뭄 sp.,
Chab = 샤베르티아 (Chabertia), 및
Trichu = 트리쿠리스 sp.(Trichuris sp)
본 발명의 양상들은 단지 실시예에 의거하여 설명하였으며 또한 첨부된 특허청구범위에 정의된 바와 같은 본 발명의 범위를 벗어나지 않고 변형 및 추가가 이루어질 수 있는 것을 이해되어야 한다.
Claims (26)
- 치료적으로 유효한 양의 생리활성제를 포함하고,
비수성 담체; 및 피마자유, 및 적어도 하나의 사이클릭 아미드를 포함하는 용매 시스템;을 포함하는 것을 특징으로 하는, 치료가 필요한 동물의 치료용 지속작용성 조성물. - 청구항 1에 있어서,
상기 사이클릭 아미드가 피롤리돈인 조성물. - 청구항 1 또는 청구항 2에 있어서,
상기 조성물 중의 상기 적어도 하나의 사이클릭 아미드가 N-메틸피롤리돈(NMP)인 조성물. - 청구항 1 내지 청구항 3 중 어느 한 항에 있어서,
상기 사이클릭 아미드가 상기 조성물 중에 1 내지 50% w/v의 양으로 존재하는 조성물. - 청구항 1 내지 청구항 4 중 어느 한 항에 있어서,
상기 피마자유가 상기 조성물 중에 1 내지 20% w/v의 양으로 존재하는 조성물. - 청구항 1 내지 청구항 5 중 어느 한 항에 있어서,
상기 조성물이 주사용 조성물인 조성물. - 청구항 1 내지 청구항 6 중 어느 한 항에 있어서,
상기 생리활성제가 구충제 화합물인 조성물. - 청구항 7에 있어서,
상기 구충제가 아버멕틴(avermectin), 모시덱틴(moxidectin), 밀버마이신(milbemycin), 이버멕틴(ivermectin), 아바멕틴(abamectin), 도라멕틴(doramectin), 에피노멕틴(epinomectin) 및 셀라멕틴(selamectin)으로 이루어진 군으로부터 선택되는 조성물. - 청구항 7 또는 청구항 8에 있어서,
상기 구충제 화합물이 상기 조성물 중에 0.005 내지 5% w/v의 양으로 존재하는 조성물. - 청구항 7 내지 청구항 9 중 어느 한 항에 있어서,
상기 구충제 화합물이 모시덱틴인 조성물. - 청구항 1 내지 청구항 10 중 어느 한 항에 있어서,
상기 비수성 담체가 카놀라유, 옥수수유, 면실유, 올리브유, 땅콩유, 참기름, 대두유, 잇꽃유, 코코넛유, 해바라기유, 팜유, 모노글리세라이드, 디글리세라이드 및 트리글리세라이드 중간사슬 숙신산 트리글리세라이드로 이루어진 그룹으로부터 선택되는 오일을 포함하는 조성물. - 청구항 1 내지 청구항 11 중 어느 한 항에 있어서,
상기 사이클릭 아미드 용매가 상기 조성물 중에 대략 15% w/v로 존재하는 조성물. - 청구항 1 내지 청구항 12 중 어느 한 항에 있어서,
상기 피마자유가 상기 조성물 중에 대략 7% w/v로 존재하는 조성물. - 청구항 1 내지 청구항 13 중 어느 한 항에 있어서,
상기 조성물이 항산화제를 포함하는 조성물. - 청구항 14에 있어서,
상기 항산화제가 부틸화 하이드록시톨루엔(BHT)인 조성물. - 청구항 14 또는 청구항 15에 있어서,
상기 항산화제가 상기 조성물 중에 0.001 내지 10% w/v로 존재하는 조성물. - 청구항 14 내지 청구항 16 중 어느 한 항에 있어서,
상기 항산화제가 상기 조성물 중에 대략 0.05% w/v로 존재하는 조성물. - 청구항 1 내지 청구항 17 중 어느 한 항의 조성물을 치료가 필요한 동물에게 전달하여, 소정의 증상 또는 질환에 대하여 지속 작용하는 보호 또는 치료를 제공하는 단계를 포함하는, 동물의 치료 방법.
- 청구항 18에 있어서, 상기 증상이 동물 내 또는 동물상의 기생충 감염인 방법.
- 청구항 18 또는 청구항 19에 있어서,
상기 증상 또는 질환에 대한 보호 또는 치료가 상기 조성물의 전달 후 적어도 50일 동안 지속되는 방법. - 상기 기생충 감염에 대해 지속 작용하는 치료 또는 예방을 위한, 청구항 1 내지 청구항 17항 중 어느 한 항에 따른 조성물의 제조에서의 용도.
- 피마자유 및 적어도 하나의 사이클릭 아미드 용매를, 생리활성제에 첨가하는 단계를 특징으로 하는, 생리활성제를 포함하는 지속작용성 조성물의 제조방법.
- 청구항 22에 있어서, 상기 단계가,
a) 제조용기에 상기 사이클릭 아미드 용매를 첨가하는 단계;
b) 상기 사이클릭 아미드 용매에 상기 생리활성제를 첨가하는 단계;
c) 상기 활성제/사이클릭 아미드 혼합물에 상기 피마자유를 첨가하는 단계; 및
d) 비수성 담체를 용적까지 첨가하는 단계;를 포함하는 방법. - 첨부된 도면 및 최선의 양태 부분에서 실시예와 관련하여 본 명세서에 기술된 바와 같은 지속작용성 조성물.
- 첨부된 도면 및 본 명세서에서의 실시예와 관련하여 청구항 1의 지속작용성 조성물로 치료가 필요한 동물을 치료하는 방법.
- 첨부된 도면 및 최선의 양태 부분에서 실시예와 관련하여 본 명세서에 기술된 바와 같은 지속작용성 조성물을 제조하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| NZ59875712 | 2012-03-13 | ||
| NZ598757 | 2012-03-13 | ||
| PCT/NZ2013/000036 WO2013137748A1 (en) | 2012-03-13 | 2013-03-13 | Long acting compositions |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140136005A true KR20140136005A (ko) | 2014-11-27 |
Family
ID=49161532
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020147026646A Withdrawn KR20140136005A (ko) | 2012-03-13 | 2013-03-13 | 지속성 조성물 |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US9616044B2 (ko) |
| EP (1) | EP2825154A4 (ko) |
| JP (1) | JP6273252B2 (ko) |
| KR (1) | KR20140136005A (ko) |
| CN (1) | CN104168886A (ko) |
| AU (1) | AU2013201479C1 (ko) |
| CA (1) | CA2867079A1 (ko) |
| CL (1) | CL2014002401A1 (ko) |
| CO (1) | CO7071132A2 (ko) |
| CR (1) | CR20140423A (ko) |
| DO (1) | DOP2014000207A (ko) |
| IL (1) | IL234597A0 (ko) |
| MX (1) | MX354966B (ko) |
| NI (1) | NI201400106A (ko) |
| PE (1) | PE20142279A1 (ko) |
| PH (1) | PH12014502016A1 (ko) |
| RU (1) | RU2014141088A (ko) |
| SV (1) | SV2014004804A (ko) |
| WO (1) | WO2013137748A1 (ko) |
| ZA (1) | ZA201406753B (ko) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ITUB20153652A1 (it) | 2015-09-16 | 2017-03-16 | Fatro Spa | Microsfere contenenti lattoni macrociclici antielminitici |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5169846A (en) | 1989-10-12 | 1992-12-08 | Crooks Michael J | Non-aqueous micellar solutions of anthelmintic benzimidazoles, closantel, or phenothiazine, and insect growth regulators |
| ES2131515T3 (es) * | 1991-09-30 | 1999-08-01 | Merck & Co Inc | Formulados inyectables de accion prolongada que contienen aceite de ricino hidrogenado. |
| DE19520275A1 (de) | 1995-06-02 | 1996-12-05 | Bayer Ag | Endoparasitizide Mittel |
| KR100277287B1 (ko) | 1995-09-25 | 2001-01-15 | 맨슨 하비 콜린 | 거대환 락톤 구충제 조성물 |
| DE19613972A1 (de) | 1996-04-09 | 1997-10-16 | Bayer Ag | Injektionsformulierungen von Avermectinen und Milbemycinen auf Basis von Rizinusöl |
| DE19638045A1 (de) * | 1996-09-18 | 1998-03-19 | Bayer Ag | Injektionsformulierungen von Avermectinen und Milbemycinen |
| US6998131B2 (en) * | 1996-09-19 | 2006-02-14 | Merial Limited | Spot-on formulations for combating parasites |
| GB9815801D0 (en) * | 1998-07-21 | 1998-09-16 | Merck & Co Inc | Liquid polymeric compositions for controlled released bioactive substances |
| CN1130990C (zh) | 1999-11-02 | 2003-12-17 | 王毅远 | 一种纯天然方便食品及其制造方法 |
| US6340672B1 (en) | 2000-02-16 | 2002-01-22 | Phoenix Scientific, Inc. | Parasiticidal formulation and a method of making this formulation |
| AU781682B2 (en) | 2000-03-20 | 2005-06-09 | Zoetis Services Llc | Sustained-release compositions for parenteral administration |
| CN1383821A (zh) | 2001-03-16 | 2002-12-11 | 王玉万 | 一种含丙硫苯咪唑亚砜或其盐类的兽用注射剂 |
| AU2002100152B4 (en) * | 2002-02-28 | 2002-04-11 | Jurox Pty Ltd | Parasiticide composition |
| US7001889B2 (en) * | 2002-06-21 | 2006-02-21 | Merial Limited | Anthelmintic oral homogeneous veterinary pastes |
| US6653288B1 (en) * | 2002-09-30 | 2003-11-25 | Virbac S.A. | Injectable anthelmintic compositions and methods for using same |
| CN1490009A (zh) * | 2002-10-17 | 2004-04-21 | 王玉万 | 含抗球虫药物的缓释注射剂 |
| US20060257440A1 (en) * | 2003-05-19 | 2006-11-16 | Makoto Asai | Insecticidal composition |
| NZ535644A (en) | 2003-07-25 | 2007-05-31 | Ashmont Holdings Ltd | Anthelmintic formulations |
| CN1293921C (zh) | 2003-08-18 | 2007-01-10 | 王玉万 | 含乙基纤维素和脂肪酸酯类的长效注射剂 |
| CN1867341B (zh) | 2003-10-17 | 2010-06-16 | 英特威国际有限公司 | 用于控制寄生虫的包括阿巴克丁与伊维菌素的组合的组合物 |
| AU2005100403B4 (en) | 2005-05-13 | 2005-09-01 | Jurox Pty Ltd | Parasiticide Composition |
| BRPI0800259A2 (pt) * | 2008-02-27 | 2011-05-31 | Noxon Do Brasil Quimica E Farmaceutica Ltda | formulações veterinárias compreendendo lactonas macrocìclicas e minerais, seus usos na preparação de produtos veterinários e métodos de ganho de produtividade e tratamento e/ou profilaxia de doenças causadas por agentes biológicos nocivos à saúde animal |
| US20100022469A1 (en) | 2008-06-24 | 2010-01-28 | Majid Razzak | Anthelminthic formulations |
| MX2009001235A (es) * | 2008-09-19 | 2010-04-29 | Agrovet Market S A | Composicion y uso de un gel oral endoparasiticida bioadhesivo de larga accion a base de doramectina. |
| DK2396006T3 (da) * | 2009-02-16 | 2013-02-11 | Ah Usa 42 Llc | Doramectinformulering med høj dosis |
| CN101703776B (zh) * | 2009-09-28 | 2012-07-11 | 洛阳惠中兽药有限公司 | 一种抗感染剂长效注射液的制备方法 |
| BRPI1001224A2 (pt) | 2010-04-07 | 2011-03-15 | Clarion Biociencias Ltda | processo de fabricação de formulação injetável a base de fluazuron associado a avermectinas para o controle e prevenção de endo e ectoparasitas em animais domésticos |
| FI2658541T4 (fi) * | 2010-12-27 | 2026-03-12 | Intervet Int Bv | Paikallisesti rajoitetulle alueelle käytettävä glykofurolia käsittävä isoksatsoliiniformulaatio |
-
2013
- 2013-03-13 EP EP13760308.0A patent/EP2825154A4/en not_active Withdrawn
- 2013-03-13 MX MX2014010957A patent/MX354966B/es active IP Right Grant
- 2013-03-13 JP JP2015500382A patent/JP6273252B2/ja not_active Expired - Fee Related
- 2013-03-13 US US14/384,308 patent/US9616044B2/en not_active Expired - Fee Related
- 2013-03-13 KR KR1020147026646A patent/KR20140136005A/ko not_active Withdrawn
- 2013-03-13 WO PCT/NZ2013/000036 patent/WO2013137748A1/en not_active Ceased
- 2013-03-13 RU RU2014141088A patent/RU2014141088A/ru unknown
- 2013-03-13 PE PE2014001416A patent/PE20142279A1/es not_active Application Discontinuation
- 2013-03-13 CN CN201380014128.7A patent/CN104168886A/zh active Pending
- 2013-03-13 AU AU2013201479A patent/AU2013201479C1/en active Active
- 2013-03-13 CA CA2867079A patent/CA2867079A1/en not_active Abandoned
-
2014
- 2014-09-09 PH PH12014502016A patent/PH12014502016A1/en unknown
- 2014-09-10 SV SV2014004804A patent/SV2014004804A/es unknown
- 2014-09-11 IL IL234597A patent/IL234597A0/en unknown
- 2014-09-11 NI NI201400106A patent/NI201400106A/es unknown
- 2014-09-11 CL CL2014002401A patent/CL2014002401A1/es unknown
- 2014-09-11 DO DO2014000207A patent/DOP2014000207A/es unknown
- 2014-09-15 ZA ZA2014/06753A patent/ZA201406753B/en unknown
- 2014-09-15 CO CO14203983A patent/CO7071132A2/es unknown
- 2014-09-16 CR CR20140423A patent/CR20140423A/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| CO7071132A2 (es) | 2014-09-30 |
| EP2825154A1 (en) | 2015-01-21 |
| CA2867079A1 (en) | 2013-09-19 |
| RU2014141088A (ru) | 2016-05-10 |
| PH12014502016B1 (en) | 2014-11-24 |
| DOP2014000207A (es) | 2014-11-30 |
| AU2013201479B2 (en) | 2015-07-02 |
| CN104168886A (zh) | 2014-11-26 |
| SV2014004804A (es) | 2017-04-20 |
| MX2014010957A (es) | 2014-10-13 |
| JP2015509978A (ja) | 2015-04-02 |
| AU2013201479A1 (en) | 2013-10-03 |
| PH12014502016A1 (en) | 2014-11-24 |
| EP2825154A4 (en) | 2015-11-11 |
| US20150038565A1 (en) | 2015-02-05 |
| ZA201406753B (en) | 2015-12-23 |
| JP6273252B2 (ja) | 2018-01-31 |
| US9616044B2 (en) | 2017-04-11 |
| WO2013137748A1 (en) | 2013-09-19 |
| AU2013201479C1 (en) | 2017-11-09 |
| CR20140423A (es) | 2014-10-20 |
| MX354966B (es) | 2018-03-27 |
| IL234597A0 (en) | 2014-11-30 |
| NI201400106A (es) | 2015-01-14 |
| PE20142279A1 (es) | 2015-01-25 |
| CL2014002401A1 (es) | 2015-04-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6653288B1 (en) | Injectable anthelmintic compositions and methods for using same | |
| KR20220004158A (ko) | 주사가능한 제약 조성물 및 그의 용도 | |
| CA2341281C (en) | Sustained-release anti-parasitic compositions comprising macrolides | |
| AU2007332222C1 (en) | Pour on formulation | |
| JPH0672108B2 (ja) | 水素化ひまし油を含む長期持続性注射製剤 | |
| CA2630458C (en) | Benzimidazole non-aqueous compositions | |
| EP1259244B1 (en) | Veterinary compositions for the treatment of parasitic diseases | |
| CN1822880B (zh) | 杀灭寄生物的组合物 | |
| KR20140136005A (ko) | 지속성 조성물 | |
| AU1069900A (en) | Doramectin formulations | |
| EA002628B1 (ru) | Водно-дисперсная лекарственная форма ивермектина для лечения экто- и эндопаразитозов | |
| NZ608177B2 (en) | Long acting compositions | |
| NZ608177A (en) | Long acting compositions | |
| WO2026041786A1 (en) | Injectable veterinary composition and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20140923 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |