KR20170052655A - 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 - Google Patents
혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 Download PDFInfo
- Publication number
- KR20170052655A KR20170052655A KR1020177009620A KR20177009620A KR20170052655A KR 20170052655 A KR20170052655 A KR 20170052655A KR 1020177009620 A KR1020177009620 A KR 1020177009620A KR 20177009620 A KR20177009620 A KR 20177009620A KR 20170052655 A KR20170052655 A KR 20170052655A
- Authority
- KR
- South Korea
- Prior art keywords
- seq
- amino acid
- acid sequence
- variable region
- chain variable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/16—Hydrolases (3) acting on ester bonds (3.1)
- C12N9/18—Carboxylic ester hydrolases (3.1.1)
- C12N9/20—Triglyceride splitting, e.g. by means of lipase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y301/00—Hydrolases acting on ester bonds (3.1)
- C12Y301/01—Carboxylic ester hydrolases (3.1.1)
- C12Y301/01003—Triacylglycerol lipase (3.1.1.3)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/54—F(ab')2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/624—Disulfide-stabilized antibody (dsFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/626—Diabody or triabody
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/16—Hydrolases (3) acting on ester bonds (3.1)
- C12N9/18—Carboxylic ester hydrolases (3.1.1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/99—Enzyme inactivation by chemical treatment
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y301/00—Hydrolases acting on ester bonds (3.1)
- C12Y301/01—Carboxylic ester hydrolases (3.1.1)
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Wood Science & Technology (AREA)
- Microbiology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Epidemiology (AREA)
- Mycology (AREA)
- General Chemical & Material Sciences (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Physics & Mathematics (AREA)
- Endocrinology (AREA)
- Plant Pathology (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
Description
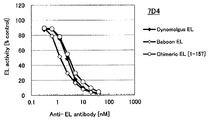
도 1b는 7D4 항체의 필리핀 원숭이 EL, 비비 EL 및 인간(1-157) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
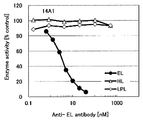
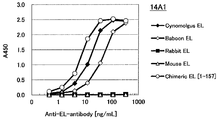
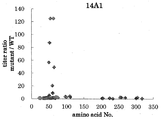
도 1c는 14A1 항체의 필리핀 원숭이 EL, 비비 EL 및 인간(1-157) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
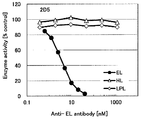
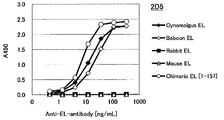
도 1d는 2D5 항체의 필리핀 원숭이 EL, 비비 EL 및 인간(1-157) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
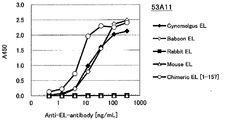
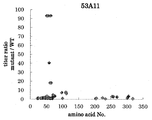
도 1e는 53A11 항체의 필리핀 원숭이 EL, 비비 EL 및 인간(1-157) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
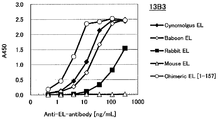
도 1f는 13B3 항체의 필리핀 원숭이, 비비, 토끼, 인간(1-157) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
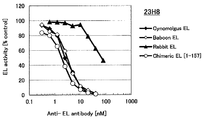
도 1g는 23H8 항체의 필리핀 원숭이, 비비, 토끼 및 인간(1-157) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
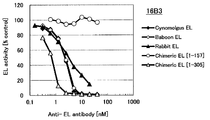
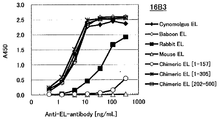
도 1h는 16B3 항체의 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 인간(1-157) 마우스 키메라 EL 및 인간(1-305) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
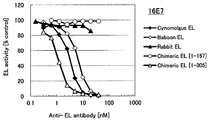
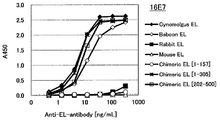
도 1i는 16E7 항체의 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 인간(1-157) 마우스 키메라 EL 및 인간(1-305) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
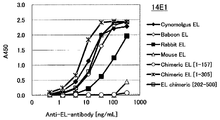
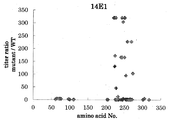
도 1j는 14E1 항체의 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 인간(1-157) 마우스 키메라 EL 및 인간(1-305) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
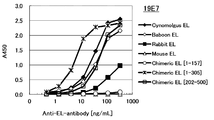
도 1k는 19E7 항체의 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 인간(1-157) 마우스 키메라 EL 및 인간(1-305) 마우스 키메라 EL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
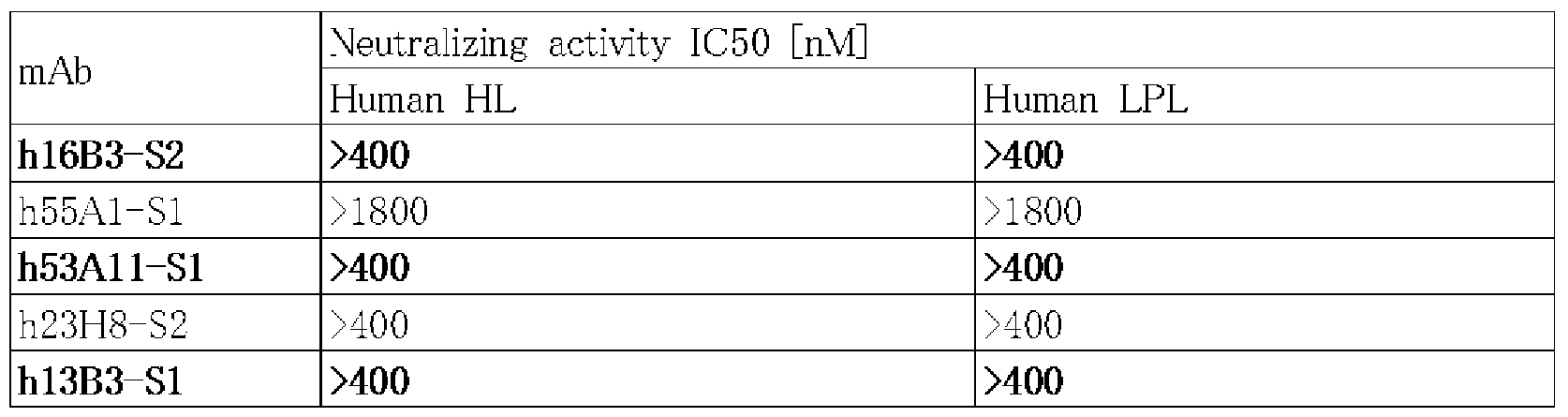
도 2a는 55A1 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2b는 7D4 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2c는 14A1 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2d는 2D5 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2e는 53A11 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2f는 13B3 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2g는 23H8 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2h는 16B3 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2i는 16E7 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2j는 14E1 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2k는 19E7 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
도 2l은 16F6 항체의, 인간 HL 및 인간 LPL에 대한 효소 활성 저해능을 측정한 결과를 나타낸다.
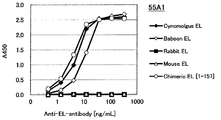
도 3a는 55A1 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL 및 인간(1-157) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
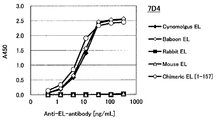
도 3b는 7D4 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL 및 인간(1-157) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3c는 14A1 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL 및 인간(1-157) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3d는 2D5 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL 및 인간(1-157) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3e는 53A11 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL 및 인간(1-157) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3f는 13B3 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL 및 인간(1-157) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3g는 23H8 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL 및 인간(1-157) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3h는 16B3 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL, 인간(1-157) 마우스 키메라 EL, 인간(1-305) 마우스 키메라 EL 및 인간(202-500) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3i는 16E7 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL, 인간(1-157) 마우스 키메라 EL, 인간(1-305) 마우스 키메라 EL 및 인간(202-500) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3j는 14E1 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL, 인간(1-157) 마우스 키메라 EL, 인간(1-305) 마우스 키메라 EL 및 인간(202-500) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3k는 19E7 항체의, 필리핀 원숭이 EL, 비비 EL, 토끼 EL, 마우스 EL, 인간(1-157) 마우스 키메라 EL, 인간(1-305) 마우스 키메라 EL 및 인간(202-500) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 3l은 16F6 항체의, 비비 EL, 인간(1-305) 마우스 키메라 EL 및 인간(187-500) 마우스 키메라 EL에 대한 결합성을 측정한 결과를 나타낸다.
도 4a는 55A1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4b는 7D4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4c는 14A1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4d는 2D5 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4e는 53A11 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4f는 13B3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4g는 23H8 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4h는 16B3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4i는 16E7 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4j는 14E1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4k는 19E7 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 4l은 16F6 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 5a는 55A1 항체, 7D4 항체, 14A1 항체 및 2D5 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 5b는 55A1 항체, 7D4 항체, 14A1 항체 및 2D5 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 5c는 53A11 항체, 13B3 항체 및 23H8 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 5d는 53A11 항체, 13B3 항체 및 23H8 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 6a는 16B3 항체 및 16E7 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 6b는 16B3 항체 및 16E7 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 6c는 14E1 항체 및 19E1 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 6d는 14E1 항체 및 19E1 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 7a는 변이를 도입한 비비 EL에 대한 55A1 항체의 결합성을 나타낸다.
도 7b는 변이를 도입한 비비 EL에 대한 7D4 항체의 결합성을 나타낸다.
도 7c는 변이를 도입한 비비 EL에 대한 14A1 항체의 결합성을 나타낸다.
도 7d는 변이를 도입한 비비 EL에 대한 2D5 항체의 결합성을 나타낸다.
도 7e는 변이를 도입한 비비 EL에 대한 53A11 항체의 결합성을 나타낸다.
도 7f는 변이를 도입한 비비 EL에 대한 13B3 항체의 결합성을 나타낸다.
도 7g는 변이를 도입한 비비 EL에 대한 23H8 항체의 결합성을 나타낸다.
도 7h는 변이를 도입한 비비 EL에 대한 16B3 항체의 결합성을 나타낸다.
도 7i는 변이를 도입한 비비 EL에 대한 16E7 항체의 결합성을 나타낸다.
도 7j는 변이를 도입한 비비 EL에 대한 14E1 항체의 결합성을 나타낸다.
도 7k는 변이를 도입한 비비 EL에 대한 19E7 항체의 결합성을 나타낸다.
도 7l은 변이를 도입한 비비 EL에 대한 16F6 항체의 결합성을 나타낸다.
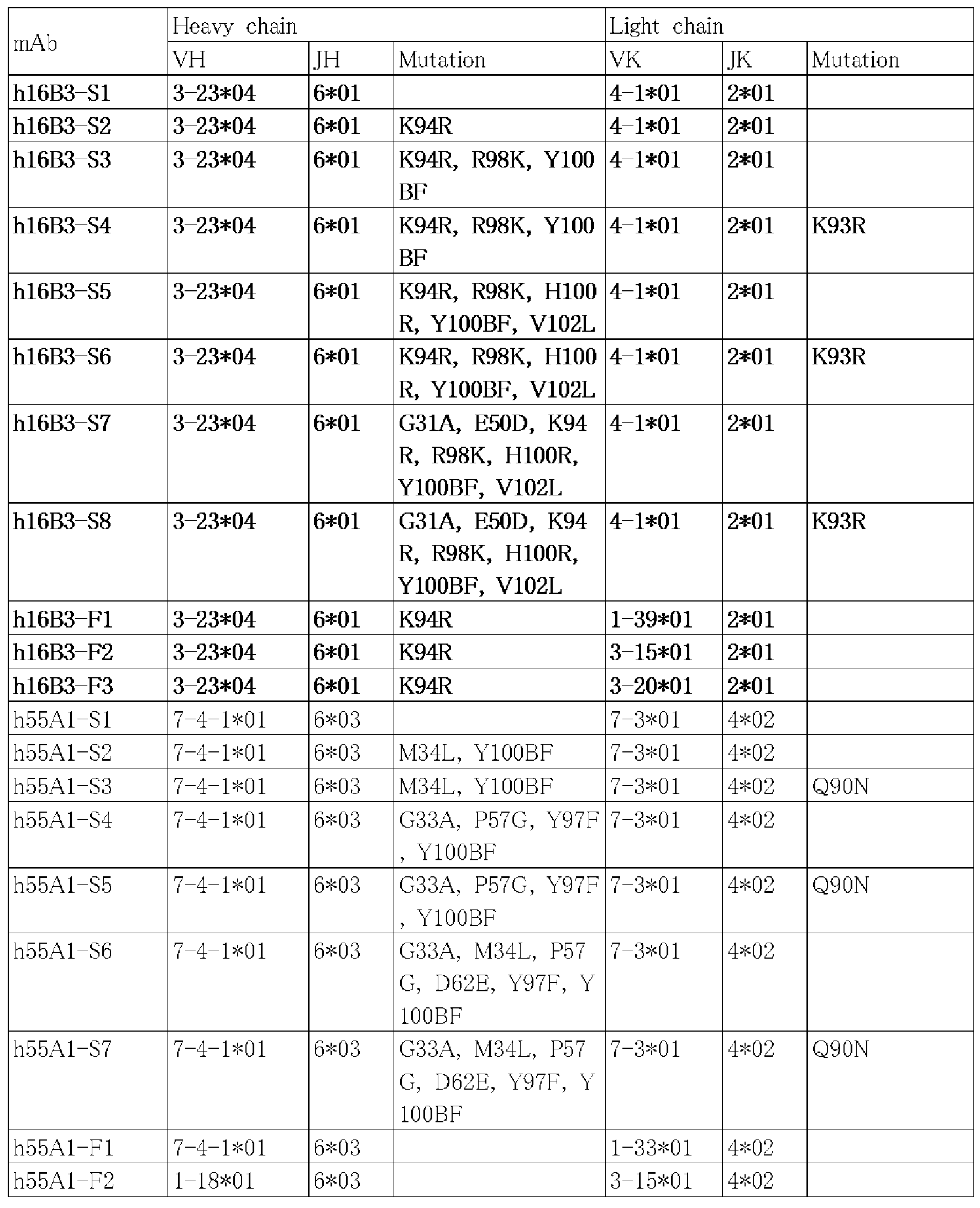
도 8a는 h16B3-S1∼S7 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 8b는 h16B3-S1∼S7 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 8c는 h16B3-F1∼F3 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 8d는 h16B3-F1∼F3 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 9a는 h55A1-S1∼S7 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 9b는 h55A1-S1∼S7 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 9c는 h55A1-F1∼F6 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 9d는 h55A1-F1∼F6 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 10a는 h53A11-S1∼S4 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 10b는 h53A11-S1∼S4 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 11a는 h23H8-S1∼S3 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 11b는 h23H8-S1∼S3 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 12a는 h13B3-S1∼S4 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 12b는 h13B3-S1∼S4 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 13a는 h12B10-S1∼S4 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 13b는 h12B10-S1∼S4 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 14a는 h16F6-S1∼S5 항체의 중쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
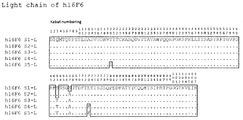
도 14b는 h16F6-S1∼S5 항체의 경쇄 가변 영역의 아미노산 서열의 얼라인먼트를 나타낸다.
도 15a는 h16B3-S1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15b는 h16B3-S2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15c는 h16B3-S3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15d는 h16B3-S4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15e는 h16B3-S5 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15f는 h16B3-S6 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15g는 h16B3-S7 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15h는 h16B3-S8 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15i는 h16B3-F1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15j는 h16B3-F2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 15k는 h16B3-F3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16a는 h55A1-S1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16b는 h55A1-S2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16c는 h55A1-S3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16d는 h55A1-S4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16e는 h55A1-S5 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16f는 h55A1-S6 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16g는 h55A1-S7 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16h는 h55A1-F1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16i는 h55A1-F2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16j는 h55A1-F3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16k는 h55A1-F4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16l은 h55A1-F5 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 16m은 h55A1-F6 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 17a는 h53A11-S1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 17b는 h53A11-S2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 17c는 h53A11-S3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 17d는 h53A11-S4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 18a는 h23H8-S1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 18b는 h23H8-S2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 18c는 h23H8-S3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 19a는 h13B3-S1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 19b는 h13B3-S2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 19c는 h13B3-S3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 19d는 h13B3-S4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 20a는 h12B10-S1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 20b는 h12B10-S2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 20c는 h12B10-S3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 20d는 h12B10-S4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 21a는 h16F6-S1 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 21b는 h16F6-S2 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 21c는 h16F6-S3 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 21d는 h16F6-S4 항체의 가변 영역의 아미노산 서열을 나타낸다.
도 21e는 h16F6-S5 항체의 가변 영역의 아미노산 서열을 나타낸다.
Claims (19)
- 서열번호 1로 표시되는 아미노산 서열의 1위 내지 157위를 인식하는, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편.
- 제 1 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 50위 내지 100위를 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 1 항 또는 제 2 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 50위의 아르기닌, 52위의 아스파라긴, 54위의 아르기닌, 58위의 아스파트산, 60위의 글루탐산, 61위의 히스티딘, 63위의 글리신, 65위의 타이로신 또는 100위의 아스파라긴을 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 1 항 또는 제 2 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 50위의 아르기닌, 60위의 글루탐산, 61위의 히스티딘, 65위의 타이로신 또는 100위의 아스파라긴을 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 1 항 또는 제 2 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 65위의 타이로신을 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 서열번호 1로 표시되는 아미노산 서열의 202위 내지 305위를 인식하는, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편.
- 제 6 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 220위 내지 273위를 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 6 항 또는 제 7 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 220위의 히스티딘, 221위의 트레오닌, 222위의 타이로신, 223위의 트레오닌, 224위의 아르기닌, 226위의 페닐알라닌, 227위의 글리신, 231위의 글리신, 232위의 아이소류신, 233위의 글루타민, 234위의 메싸이오닌, 240위의 아스파트산, 242위의 타이로신, 243위의 프롤린, 244위의 아스파라긴, 246위의 글리신, 249위의 글루타민, 250위의 프롤린, 251위의 글리신, 254위의 류신, 258위의 류신, 263위의 타이로신, 269위의 발린 또는 273위의 글루탐산을 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 6 항 또는 제 7 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 220위의 히스티딘, 221위의 트레오닌, 240위의 아스파트산, 242위의 타이로신, 243위의 프롤린, 244위의 아스파라긴, 246위의 글리신, 249위의 글루타민, 250위의 프롤린 또는 251위의 글리신을 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 6 항 또는 제 7 항에 있어서,
서열번호 1로 표시되는 아미노산 서열의 220위의 히스티딘, 221위의 트레오닌, 240위의 아스파트산, 242위의 타이로신, 243위의 프롤린, 244위의 아스파라긴, 246위의 글리신, 249위의 글루타민, 250위의 프롤린 및 251위의 글리신을 인식하는, 인간화 모노클로널 항체 또는 그의 항체 단편. - 1) 서열번호 2, 서열번호 3 및 서열번호 4의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
2) 서열번호 2, 서열번호 3 및 서열번호 4의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
3) 서열번호 2, 서열번호 3 및 서열번호 4의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
4) 서열번호 2, 서열번호 3 및 서열번호 4의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
5) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
6) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
7) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
8) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
9) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
10) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
11) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
12) 서열번호 2, 서열번호 3 및 서열번호 8의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
13) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
14) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
15) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
16) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
17) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
18) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
19) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
20) 서열번호 2, 서열번호 3 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
21) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
22) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
23) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
24) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 7의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
25) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
26) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
27) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
28) 서열번호 11, 서열번호 12 및 서열번호 10의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 5, 서열번호 6 및 서열번호 9의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
29) 서열번호 13, 서열번호 14 및 서열번호 15의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
30) 서열번호 13, 서열번호 14 및 서열번호 15의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
31) 서열번호 13, 서열번호 14 및 서열번호 15의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
32) 서열번호 13, 서열번호 14 및 서열번호 15의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
33) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
34) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
35) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
36) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
37) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
38) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
39) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
40) 서열번호 19, 서열번호 14 및 서열번호 20의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
41) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
42) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
43) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
44) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
45) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
46) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
47) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
48) 서열번호 22, 서열번호 23 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
49) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
50) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
51) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
52) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 18의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
53) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
54) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
55) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
56) 서열번호 25, 서열번호 106 및 서열번호 24의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 16, 서열번호 17 및 서열번호 21의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
57) 서열번호 26, 서열번호 27 및 서열번호 28의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 29, 서열번호 30 및 서열번호 31의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
58) 서열번호 26, 서열번호 27 및 서열번호 28의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 29, 서열번호 30 및 서열번호 31의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
59) 서열번호 26, 서열번호 27 및 서열번호 28의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 29, 서열번호 30 및 서열번호 31의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
60) 서열번호 26, 서열번호 27 및 서열번호 28의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 29, 서열번호 30 및 서열번호 31의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
61) 서열번호 32, 서열번호 33 및 서열번호 34의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 35, 서열번호 36 및 서열번호 37의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
62) 서열번호 32, 서열번호 33 및 서열번호 34의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 35, 서열번호 36 및 서열번호 37의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
63) 서열번호 32, 서열번호 33 및 서열번호 34의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 35, 서열번호 36 및 서열번호 37의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
64) 서열번호 32, 서열번호 33 및 서열번호 34의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 35, 서열번호 36 및 서열번호 37의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
65) 서열번호 38, 서열번호 39 및 서열번호 40의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 41, 서열번호 42 및 서열번호 43의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
66) 서열번호 38, 서열번호 39 및 서열번호 40의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 41, 서열번호 42 및 서열번호 43의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
67) 서열번호 38, 서열번호 39 및 서열번호 40의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 41, 서열번호 42 및 서열번호 43의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
68) 서열번호 38, 서열번호 39 및 서열번호 40의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 41, 서열번호 42 및 서열번호 43의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
69) 서열번호 44, 서열번호 45 및 서열번호 46의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
70) 서열번호 44, 서열번호 45 및 서열번호 46의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
71) 서열번호 44, 서열번호 45 및 서열번호 46의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
72) 서열번호 44, 서열번호 45 및 서열번호 46의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
73) 서열번호 44, 서열번호 45 및 서열번호 50의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
74) 서열번호 44, 서열번호 45 및 서열번호 50의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
75) 서열번호 44, 서열번호 45 및 서열번호 50의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
76) 서열번호 44, 서열번호 45 및 서열번호 50의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
77) 서열번호 44, 서열번호 45 및 서열번호 51의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
78) 서열번호 44, 서열번호 45 및 서열번호 51의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
79) 서열번호 44, 서열번호 45 및 서열번호 51의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
80) 서열번호 44, 서열번호 45 및 서열번호 51의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
81) 서열번호 52, 서열번호 45 및 서열번호 53의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
82) 서열번호 52, 서열번호 45 및 서열번호 53의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
83) 서열번호 52, 서열번호 45 및 서열번호 53의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
84) 서열번호 52, 서열번호 45 및 서열번호 53의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 47, 서열번호 48 및 서열번호 49의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
85) 서열번호 54, 서열번호 55 및 서열번호 56의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 57, 서열번호 58 및 서열번호 59의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
86) 서열번호 54, 서열번호 55 및 서열번호 56의 아미노산 서열을 갖는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 57, 서열번호 58 및 서열번호 59의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
87) 서열번호 54, 서열번호 55 및 서열번호 56의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 57, 서열번호 58 및 서열번호 59의 아미노산 서열을 갖는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
88) 서열번호 54, 서열번호 55 및 서열번호 56의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 중쇄 가변 영역, 및
서열번호 57, 서열번호 58 및 서열번호 59의 아미노산 서열을 갖는 3개의 CDR 중 하나 이상의 CDR에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산 서열로 이루어지는 3개의 CDR을 포함하는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편
으로 이루어지는 군으로부터 선택되는 인간화 모노클로널 항체 또는 그의 항체 단편. - 1) 서열번호 60의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
2) 서열번호 60의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
3) 서열번호 60의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
4) 서열번호 60의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
5) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
6) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
7) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
8) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
9) 서열번호 63의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
10) 서열번호 63의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
11) 서열번호 63의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
12) 서열번호 63의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
13) 서열번호 63의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
14) 서열번호 63의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
15) 서열번호 63의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
16) 서열번호 63의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
17) 서열번호 65의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
18) 서열번호 65의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
19) 서열번호 65의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
20) 서열번호 65의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
21) 서열번호 65의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
22) 서열번호 65의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
23) 서열번호 65의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
24) 서열번호 65의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
25) 서열번호 66의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
26) 서열번호 66의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
27) 서열번호 66의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
28) 서열번호 66의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 61의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
29) 서열번호 66의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
30) 서열번호 66의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
31) 서열번호 66의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
32) 서열번호 66의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
33) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
34) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
35) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
36) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
37) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
38) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
39) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
40) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
41) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
42) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
43) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
44) 서열번호 62의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
45) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
46) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
47) 서열번호 70의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
48) 서열번호 70의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
49) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
50) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
51) 서열번호 72의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
52) 서열번호 72의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
53) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
54) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
55) 서열번호 72의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
56) 서열번호 72의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
57) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
58) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
59) 서열번호 74의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
60) 서열번호 74의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
61) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
62) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
63) 서열번호 74의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
64) 서열번호 74의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
65) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
66) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
67) 서열번호 75의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
68) 서열번호 75의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
69) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
70) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
71) 서열번호 75의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
72) 서열번호 75의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
73) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
74) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
75) 서열번호 70의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
76) 서열번호 70의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
77) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
78) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
79) 서열번호 77의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
80) 서열번호 77의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
81) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
82) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
83) 서열번호 77의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
84) 서열번호 77의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
85) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
86) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
87) 서열번호 77의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
88) 서열번호 77의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
89) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
90) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
91) 서열번호 81의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
92) 서열번호 81의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
93) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
94) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
95) 서열번호 81의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
96) 서열번호 81의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
97) 서열번호 82의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 83의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
98) 서열번호 82의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 83의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
99) 서열번호 82의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 83의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
100) 서열번호 82의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 83의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
101) 서열번호 82의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 84의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
102) 서열번호 82의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 84의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
103) 서열번호 82의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 84의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
104) 서열번호 82의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 84의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
105) 서열번호 82의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
106) 서열번호 82의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
107) 서열번호 82의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
108) 서열번호 82의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
109) 서열번호 86의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
110) 서열번호 86의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
111) 서열번호 86의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
112) 서열번호 86의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 85의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
113) 서열번호 87의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 88의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
114) 서열번호 87의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 88의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
115) 서열번호 87의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 88의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
116) 서열번호 87의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 88의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
117) 서열번호 87의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 89의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
118) 서열번호 87의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 89의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
119) 서열번호 87의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 89의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
120) 서열번호 87의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 89의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
121) 서열번호 87의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 90의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
122) 서열번호 87의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 90의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
123) 서열번호 87의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 90의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
124) 서열번호 87의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 90의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
125) 서열번호 91의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
126) 서열번호 91의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
127) 서열번호 91의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
128) 서열번호 91의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
129) 서열번호 93의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
130) 서열번호 93의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
131) 서열번호 93의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
132) 서열번호 93의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 92의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
133) 서열번호 91의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
134) 서열번호 91의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
135) 서열번호 91의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
136) 서열번호 91의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
137) 서열번호 93의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
138) 서열번호 93의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
139) 서열번호 93의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
140) 서열번호 93의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 94의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
141) 서열번호 95의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
142) 서열번호 95의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
143) 서열번호 95의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
144) 서열번호 95의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
145) 서열번호 97의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
146) 서열번호 97의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
147) 서열번호 97의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
148) 서열번호 97의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
149) 서열번호 98의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
150) 서열번호 98의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
151) 서열번호 98의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
152) 서열번호 98의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
153) 서열번호 99의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
154) 서열번호 99의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
155) 서열번호 99의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
156) 서열번호 99의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 96의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
157) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 101의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
158) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 101의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
159) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 101의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
160) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 101의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
161) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 102의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
162) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 102의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
163) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 102의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
164) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 102의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
165) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 103의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
166) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 103의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
167) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 103의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
168) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 103의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
169) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 104의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
170) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 104의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
171) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 104의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
172) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 104의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
173) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 105의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
174) 서열번호 100의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 105의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
175) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 105의 아미노산 서열을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편,
176) 서열번호 100의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 중쇄 가변 영역, 및
서열번호 105의 아미노산 서열에 있어서 1 또는 수개의 아미노산이 결실, 치환 또는 부가된 아미노산을 갖는 경쇄 가변 영역을 갖고, 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 또는 그의 항체 단편
으로 이루어지는 군으로부터 선택되는 인간화 모노클로널 항체 또는 그의 항체 단편. - 1) 서열번호 60의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
2) 서열번호 60의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
3) 서열번호 60의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
4) 서열번호 60의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
5) 서열번호 62의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 64의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
6) 서열번호 63의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
7) 서열번호 63의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
8) 서열번호 63의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
9) 서열번호 65의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
10) 서열번호 65의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
11) 서열번호 65의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
12) 서열번호 66의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 67의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
13) 서열번호 66의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 68의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
14) 서열번호 66의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 69의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
15) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
16) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
17) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
18) 서열번호 70의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
19) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
20) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
21) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
22) 서열번호 72의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
23) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
24) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
25) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
26) 서열번호 74의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
27) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
28) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 78의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
29) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 79의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
30) 서열번호 75의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
31) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
32) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
33) 서열번호 77의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
34) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 71의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
35) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 73의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
36) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 76의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
37) 서열번호 81의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 80의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
38) 서열번호 86의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 83의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편,
39) 서열번호 86의 아미노산 서열을 갖는 중쇄 가변 영역, 및
서열번호 84의 아미노산 서열을 갖는 경쇄 가변 영역을 갖는 인간화 모노클로널 항체 또는 그의 항체 단편
으로 이루어지는 군으로부터 선택되는 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 1 항 내지 제 13 항 중 어느 한 항에 기재된 인간화 모노클로널 항체 또는 그의 항체 단편을 함유하는, 혈관내피 리파제가 관련되는 질환의 치료 또는 예방을 위한 의약 조성물.
- 제 14 항에 있어서,
혈관내피 리파제가 관련되는 질환이 지질대사이상증인 의약 조성물. - 제 1 항 내지 제 13 항 중 어느 한 항에 있어서,
혈관내피 리파제가 관련되는 질환의 치료 또는 예방을 위한, 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 16 항에 있어서,
혈관내피 리파제가 관련되는 질환이 지질대사이상증인 인간화 모노클로널 항체 또는 그의 항체 단편. - 제 1 항 내지 제 13 항 중 어느 한 항에 기재된 인간화 모노클로널 항체 또는 그의 항체 단편을 투여하는 것을 특징으로 하는, 혈관내피 리파제가 관련되는 질환의 예방 또는 치료 방법.
- 제 18 항에 있어서,
혈관내피 리파제가 관련되는 질환이 지질대사이상증인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014184710 | 2014-09-11 | ||
| JPJP-P-2014-184710 | 2014-09-11 | ||
| PCT/JP2015/075668 WO2016039402A1 (ja) | 2014-09-11 | 2015-09-10 | 血管内皮リパーゼの酵素活性を阻害するヒト化モノクローナル抗体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20170052655A true KR20170052655A (ko) | 2017-05-12 |
| KR102520286B1 KR102520286B1 (ko) | 2023-04-10 |
Family
ID=55459146
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177009620A Active KR102520286B1 (ko) | 2014-09-11 | 2015-09-10 | 혈관내피 리파제의 효소 활성을 저해하는 인간화 모노클로널 항체 |
Country Status (18)
| Country | Link |
|---|---|
| US (2) | US10570215B2 (ko) |
| EP (1) | EP3192813A4 (ko) |
| JP (2) | JP6635599B2 (ko) |
| KR (1) | KR102520286B1 (ko) |
| CN (1) | CN107074963B (ko) |
| AR (1) | AR101811A1 (ko) |
| AU (1) | AU2015313179B2 (ko) |
| CA (1) | CA2960994C (ko) |
| CL (1) | CL2017000595A1 (ko) |
| EA (1) | EA036324B1 (ko) |
| IL (1) | IL250981B (ko) |
| MX (1) | MX388559B (ko) |
| MY (1) | MY181835A (ko) |
| PH (1) | PH12017500461B1 (ko) |
| SG (2) | SG10201900605SA (ko) |
| TW (2) | TWI734410B (ko) |
| WO (1) | WO2016039402A1 (ko) |
| ZA (1) | ZA201702489B (ko) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PT3316909T (pt) * | 2015-06-30 | 2023-11-22 | Seattle Genetics Inc | Anticorpos anti-ntb-a e composições e métodos relacionados |
| AU2018298676A1 (en) * | 2017-07-10 | 2019-12-19 | Innate Pharma | Siglec-9-neutralizing antibodies |
| WO2019091449A1 (zh) * | 2017-11-10 | 2019-05-16 | 江苏恒瑞医药股份有限公司 | Cd96抗体、其抗原结合片段及医药用途 |
| JP7692411B2 (ja) * | 2019-11-07 | 2025-06-13 | メディミューン,エルエルシー | 心血管疾患の治療用の内皮リパーゼ抗体 |
| EP4110290A4 (en) * | 2020-02-24 | 2024-06-05 | Medimmune, LLC | ANTI-ENDOTHELIAL LIPASE ANTIBODY FORMULATIONS |
| US20240092897A1 (en) * | 2020-11-05 | 2024-03-21 | Shanghai Jmt-Bio Technology Co., Ltd. | Anti-siglec-15 antibody and application thereof in preparing drug |
| WO2025111317A1 (en) * | 2023-11-21 | 2025-05-30 | The Brigham And Women's Hospital, Inc. | Klrb1 binding agents and methods of use thereof |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999032611A1 (en) * | 1997-12-19 | 1999-07-01 | Progenitor, Inc. | A lipase expressed in endothelial cells and methods for its use |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH062075B2 (ja) * | 1988-04-30 | 1994-01-12 | 大日本製薬株式会社 | 抗ヒトポストヘパリンプラズマ由来リポ蛋白リパーゼモノクローナル抗体およびその製造方法 |
| ATE291080T1 (de) * | 1996-12-06 | 2005-04-15 | Aventis Pharma Inc | Von humanem lipase-ähnlichem gen kodierte polypeptide, sowie zusammensetzungen und methoden |
| NZ531180A (en) | 1999-03-26 | 2005-06-24 | Aventis Pharma Inc | Compositions and methods for effecting the levels of cholesterol using the LIPG polypeptide |
| US9296825B2 (en) * | 2011-10-12 | 2016-03-29 | Shionogi & Co., Ltd. | Monoclonal antibody against EL which inhibits enzyme activity of EL |
| WO2014142182A1 (ja) * | 2013-03-14 | 2014-09-18 | 塩野義製薬株式会社 | 血管内皮リパーゼの酵素活性を阻害するモノクローナル抗体 |
-
2015
- 2015-09-07 TW TW109108293A patent/TWI734410B/zh active
- 2015-09-07 TW TW104129560A patent/TWI688575B/zh active
- 2015-09-10 WO PCT/JP2015/075668 patent/WO2016039402A1/ja not_active Ceased
- 2015-09-10 EP EP15840346.9A patent/EP3192813A4/en not_active Withdrawn
- 2015-09-10 EA EA201790590A patent/EA036324B1/ru not_active IP Right Cessation
- 2015-09-10 SG SG10201900605SA patent/SG10201900605SA/en unknown
- 2015-09-10 CN CN201580059706.8A patent/CN107074963B/zh active Active
- 2015-09-10 CA CA2960994A patent/CA2960994C/en active Active
- 2015-09-10 PH PH1/2017/500461A patent/PH12017500461B1/en unknown
- 2015-09-10 JP JP2016547492A patent/JP6635599B2/ja active Active
- 2015-09-10 AU AU2015313179A patent/AU2015313179B2/en active Active
- 2015-09-10 MY MYPI2017700661A patent/MY181835A/en unknown
- 2015-09-10 MX MX2017002968A patent/MX388559B/es unknown
- 2015-09-10 KR KR1020177009620A patent/KR102520286B1/ko active Active
- 2015-09-10 AR ARP150102894A patent/AR101811A1/es not_active Application Discontinuation
- 2015-09-10 SG SG11201701762VA patent/SG11201701762VA/en unknown
-
2017
- 2017-03-07 IL IL250981A patent/IL250981B/en active IP Right Grant
- 2017-03-10 US US15/456,041 patent/US10570215B2/en active Active
- 2017-03-10 CL CL2017000595A patent/CL2017000595A1/es unknown
- 2017-04-07 ZA ZA2017/02489A patent/ZA201702489B/en unknown
-
2019
- 2019-11-18 US US16/687,272 patent/US11136411B2/en active Active
- 2019-12-16 JP JP2019226429A patent/JP6827255B2/ja active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999032611A1 (en) * | 1997-12-19 | 1999-07-01 | Progenitor, Inc. | A lipase expressed in endothelial cells and methods for its use |
Non-Patent Citations (6)
| Title |
|---|
| Cardiovascular Research, 2010, 제87권, 페이지 385-393* * |
| J Clin Invest, 2003년, 제111권 3호, 357페이지 |
| J. Clin. Invest., 2003, 제111권, 제3호, 페이지 357-362 * |
| Nature Genetics, 1999년, 제21권, 424페이지 |
| TCM, 제14권, 제5호, 2004년, p. 202-206 |
| The Journal of Biological Chemistry Vol. 279, No. 43, 22, 45085-45092, 2004 |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6827255B2 (ja) | 血管内皮リパーゼの酵素活性を阻害するヒト化モノクローナル抗体 | |
| JP6040943B2 (ja) | 新規抗ヒトctgf抗体 | |
| US10745491B2 (en) | Method of inhibiting the enzymatic activity of vascular endothelial lipase with a monoclonal antibody | |
| JP6195306B2 (ja) | Elの酵素活性を阻害するelに対するモノクローナル抗体 | |
| TW202325739A (zh) | 新穎Nav1.7單株抗體 | |
| JP2022523750A (ja) | 抗-fgf19抗体 | |
| BR112017004429B1 (pt) | Anticorpo monoclonal humanizado, que inibe a atividade enzimática da lipase endotelial vascular, composição farmacêutica e uso do mesmo |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| U11 | Full renewal or maintenance fee paid |
Free format text: ST27 STATUS EVENT CODE: A-4-4-U10-U11-OTH-PR1001 (AS PROVIDED BY THE NATIONAL OFFICE) Year of fee payment: 4 |