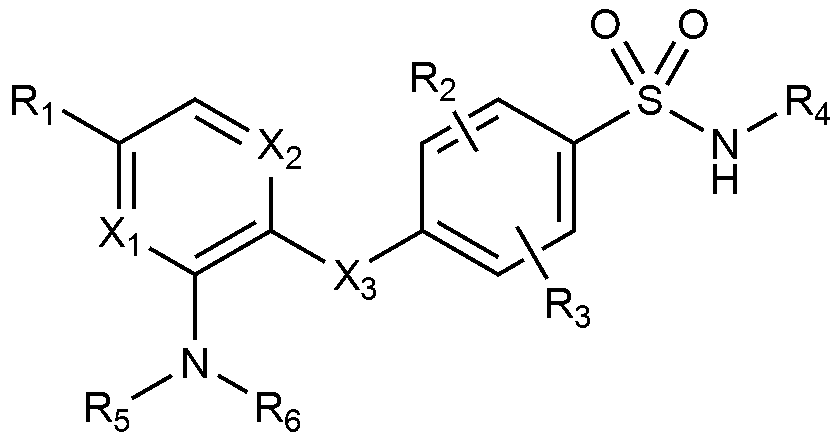
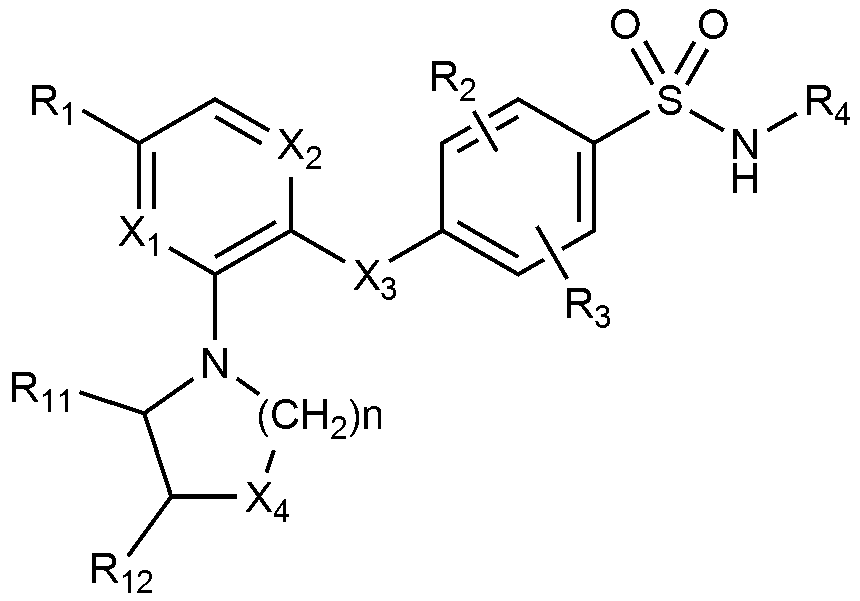
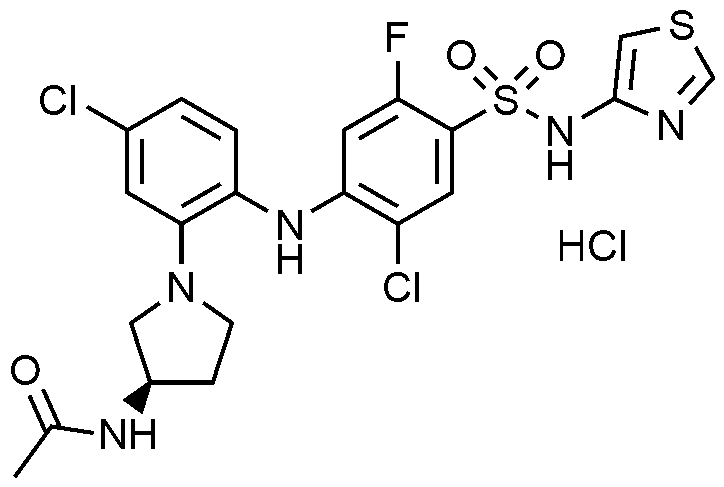
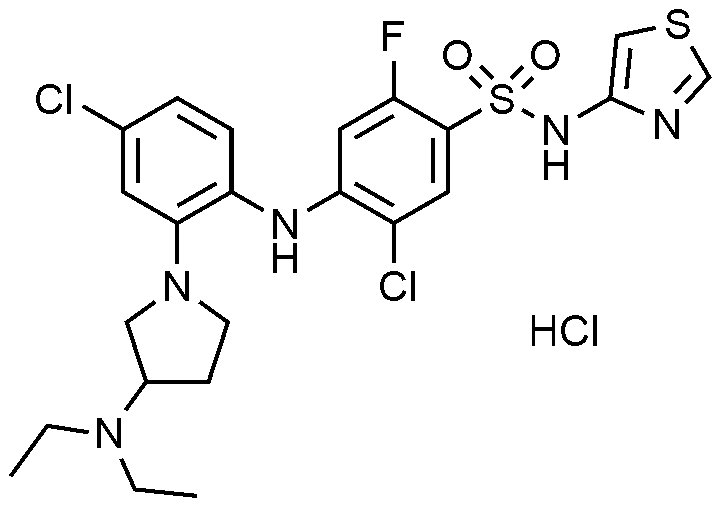
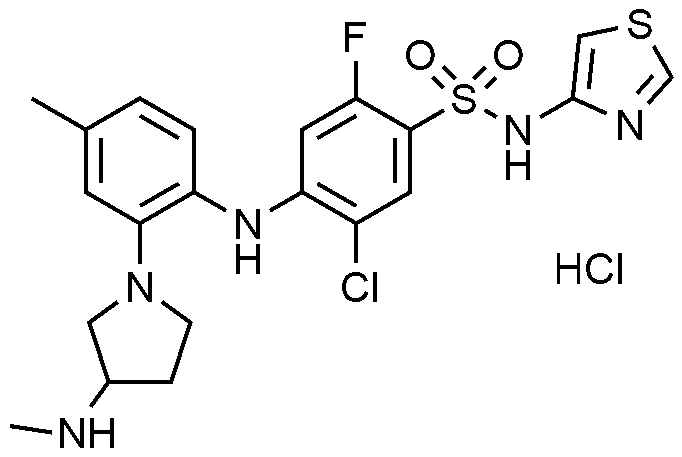
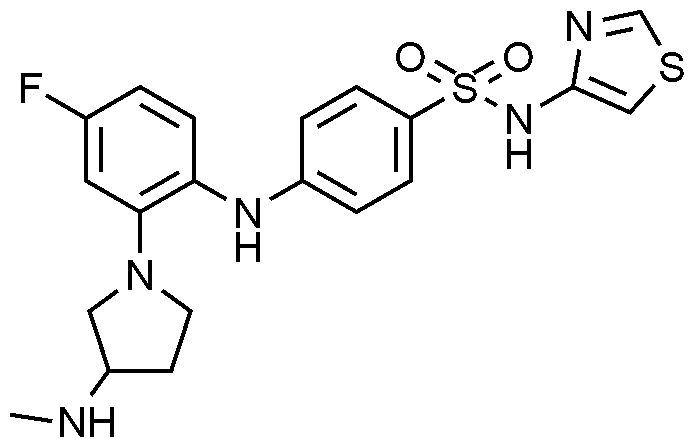
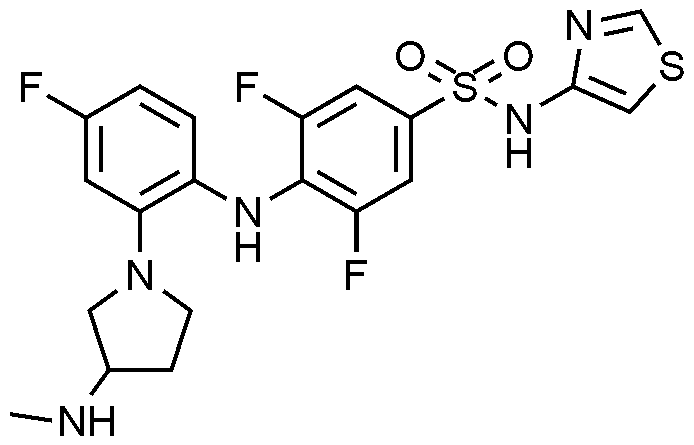
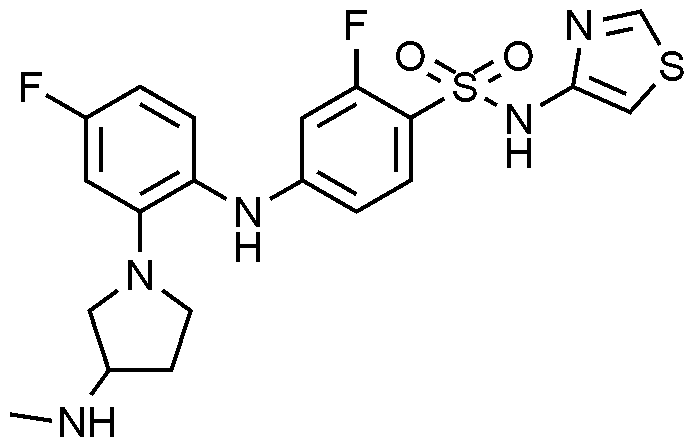
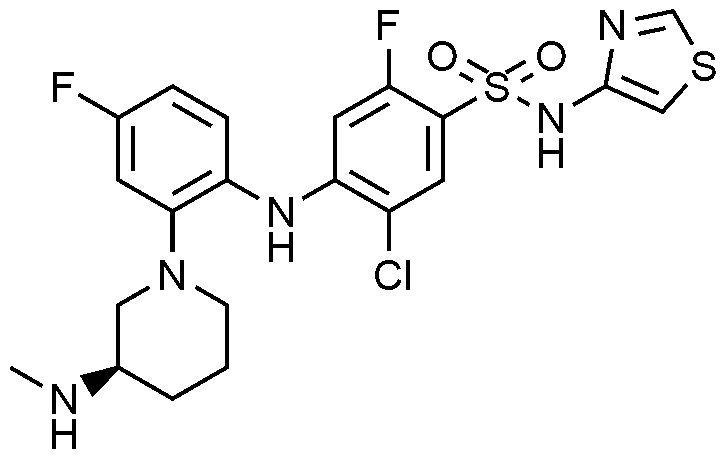
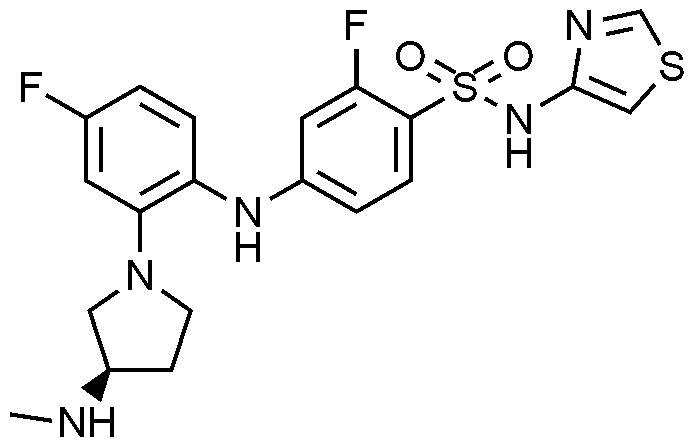
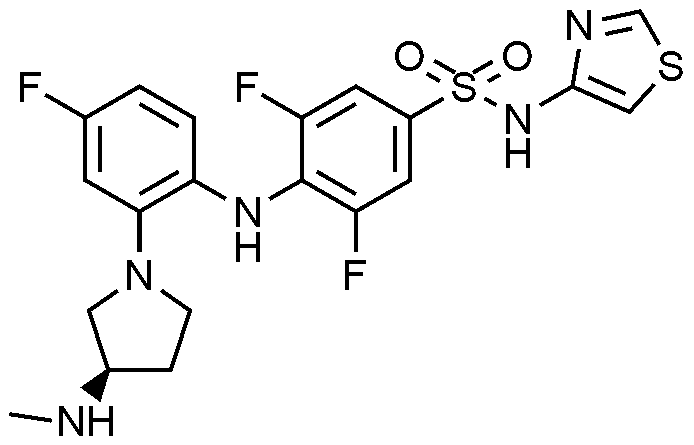
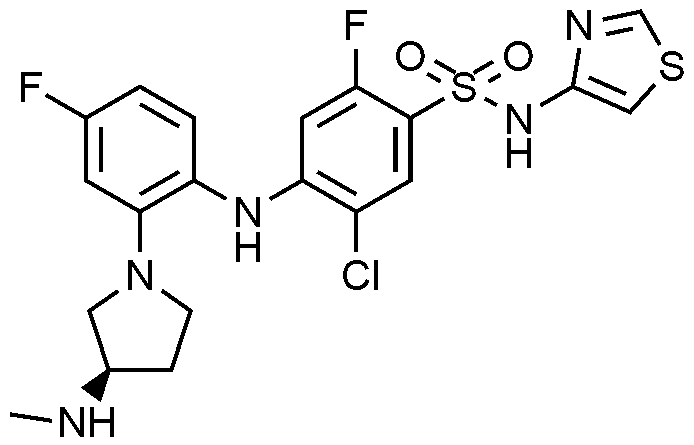
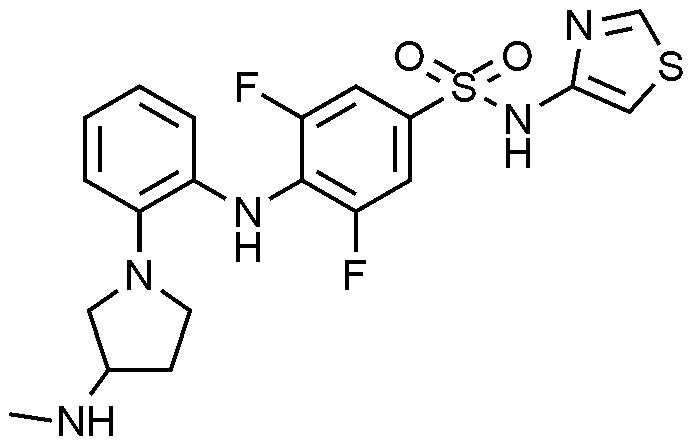
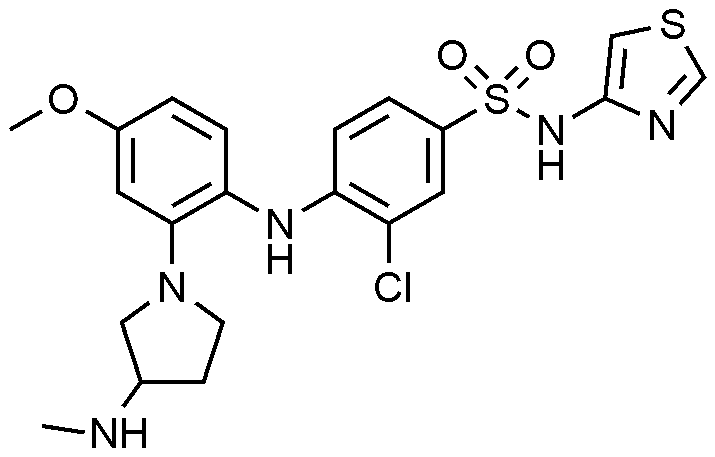
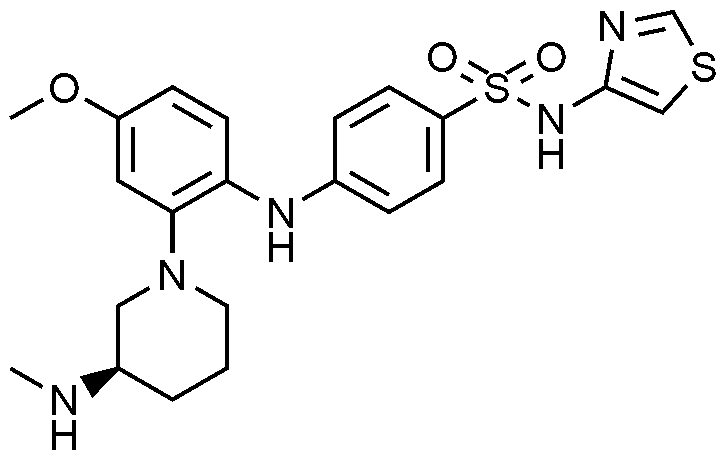
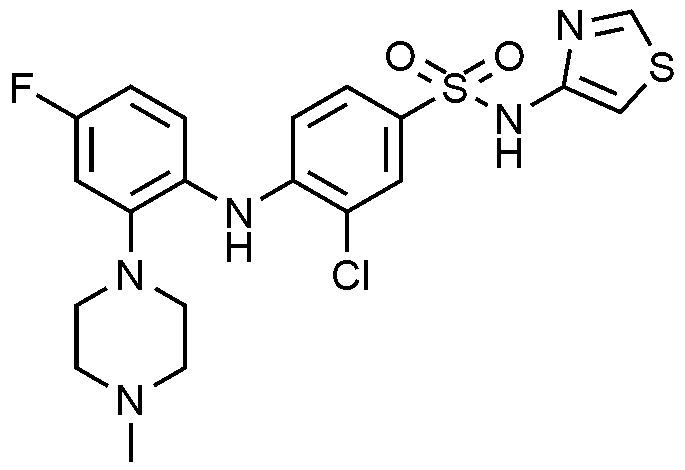
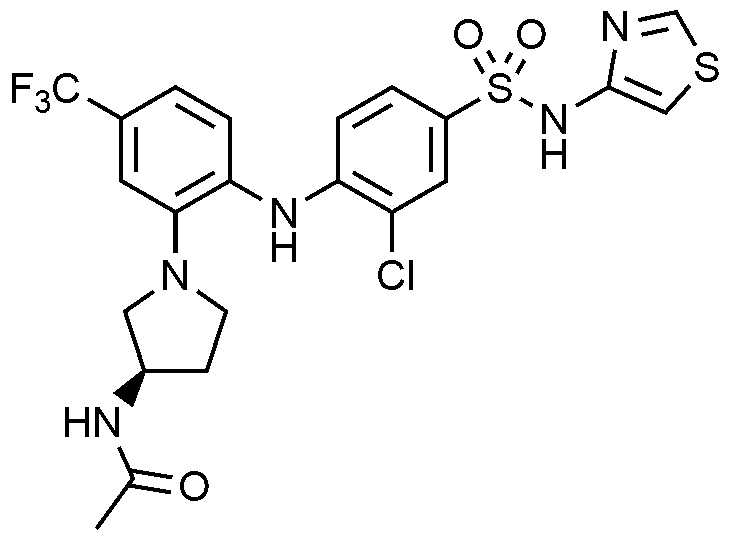
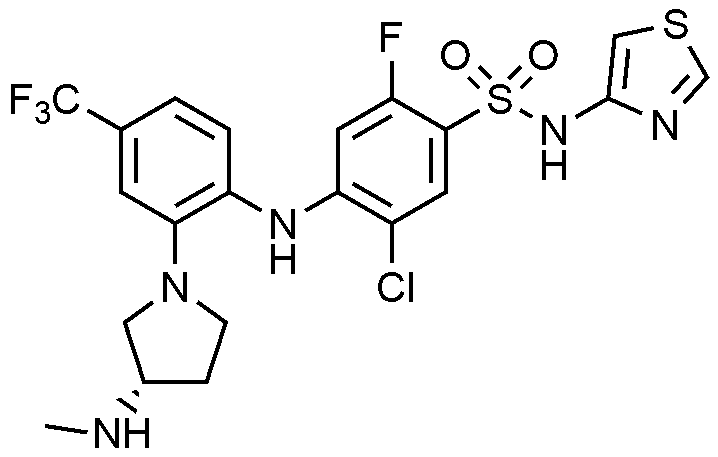
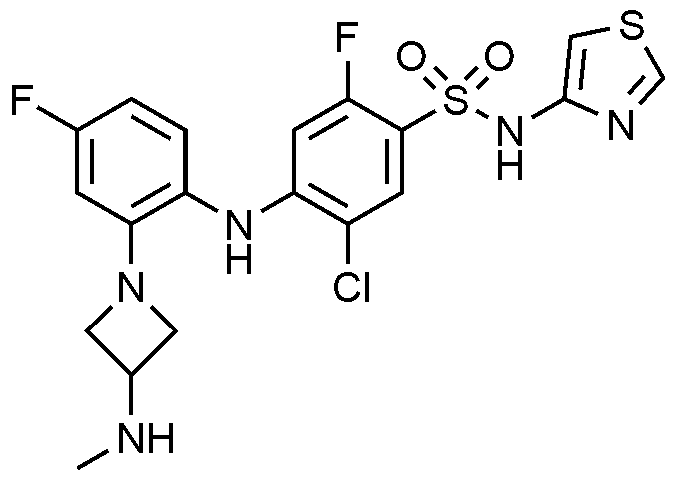
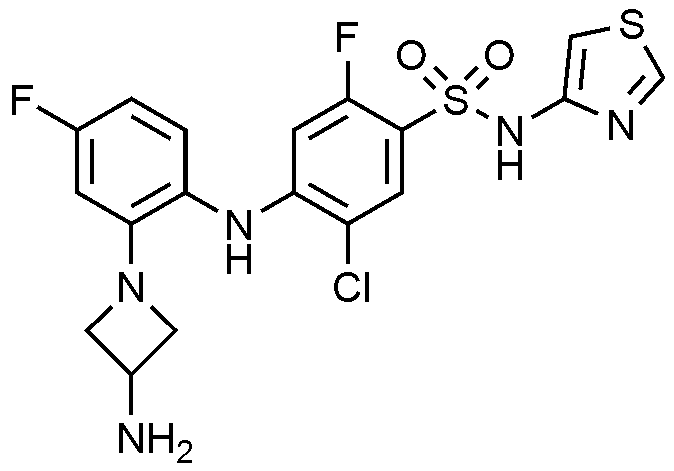
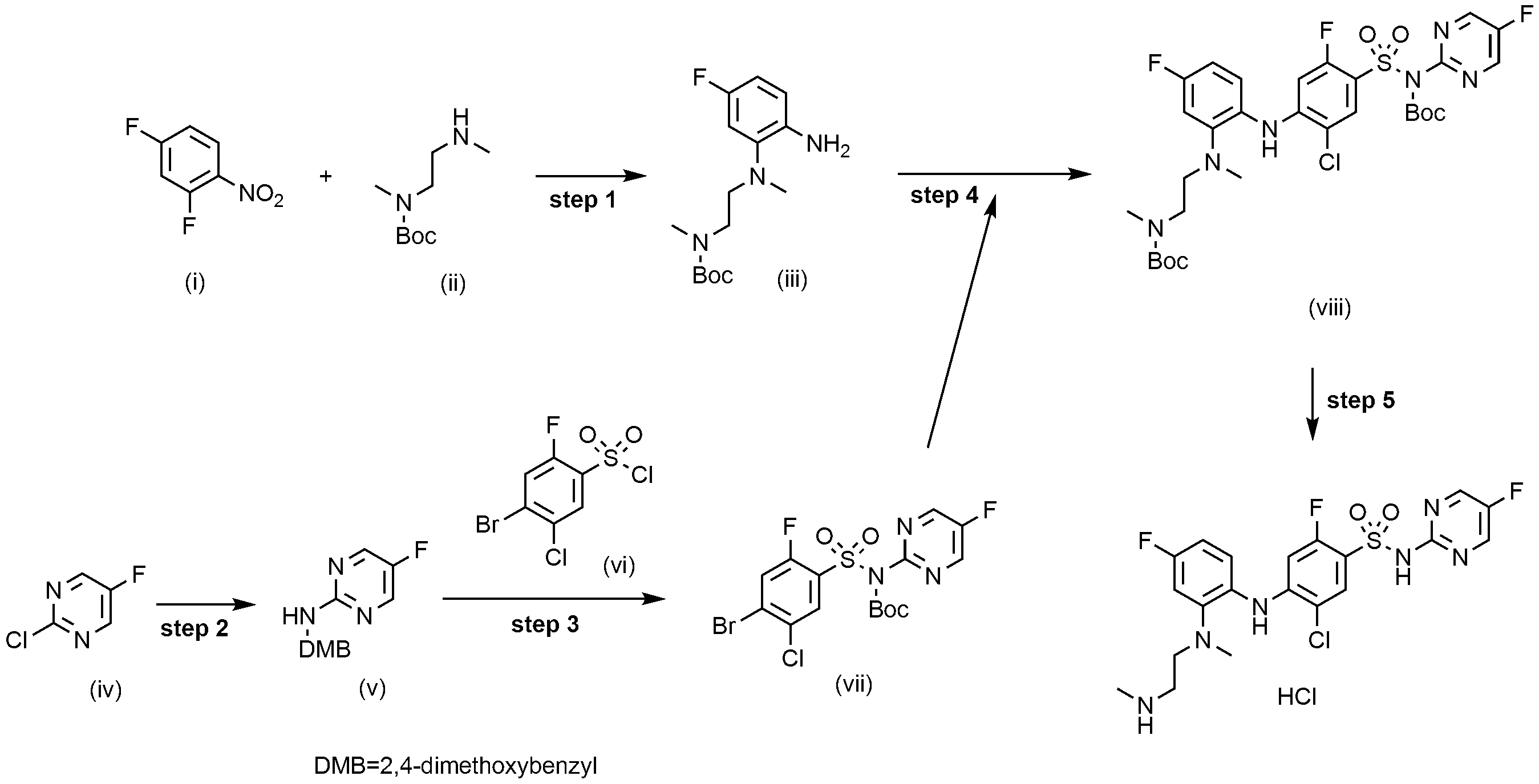
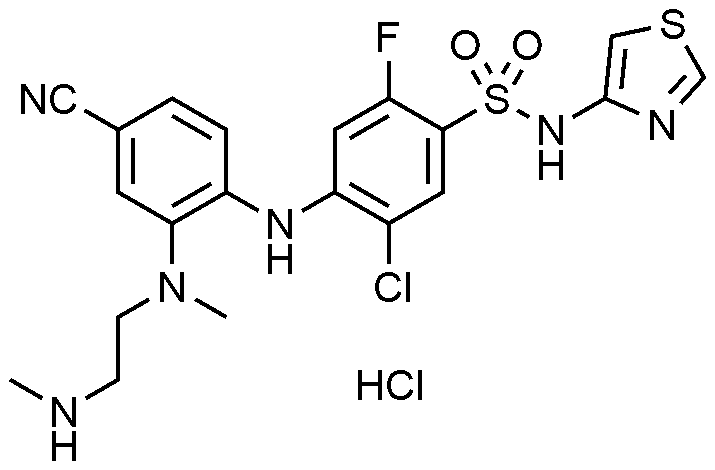
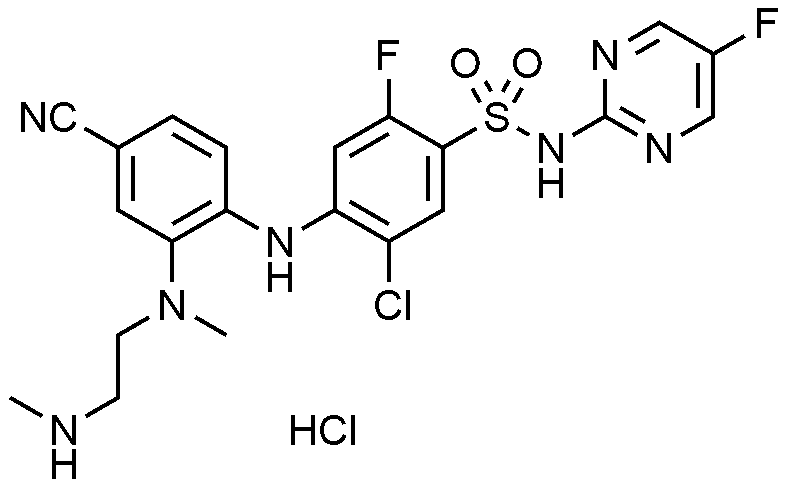
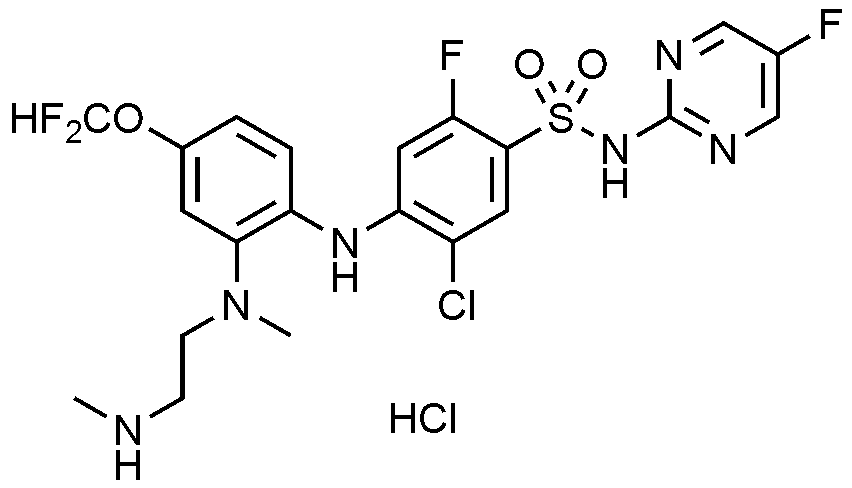
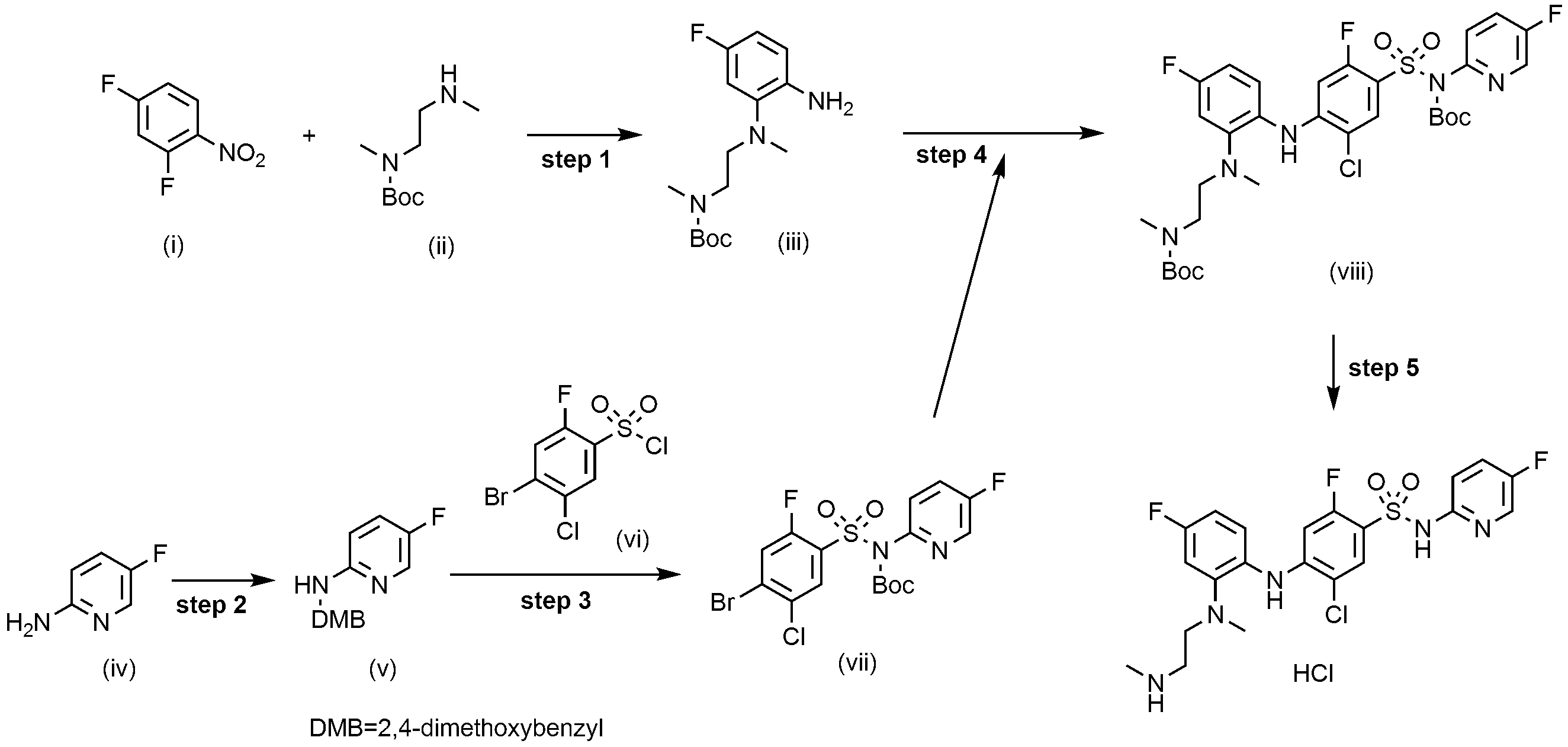
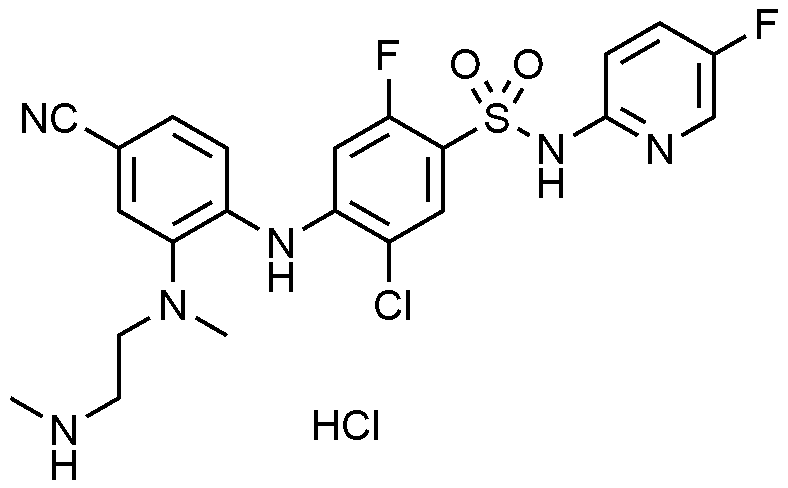
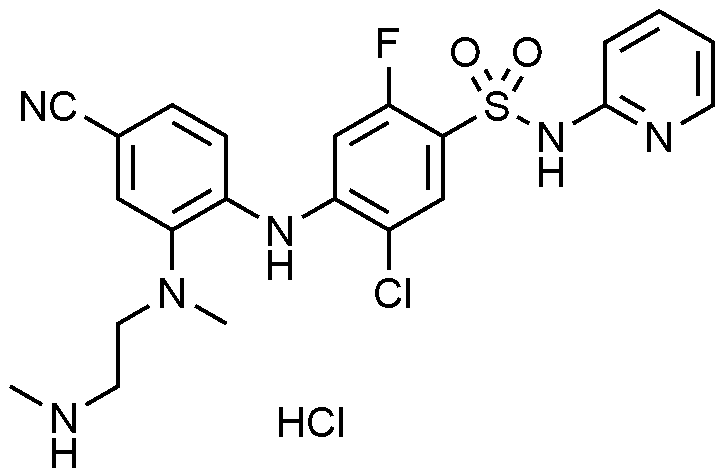
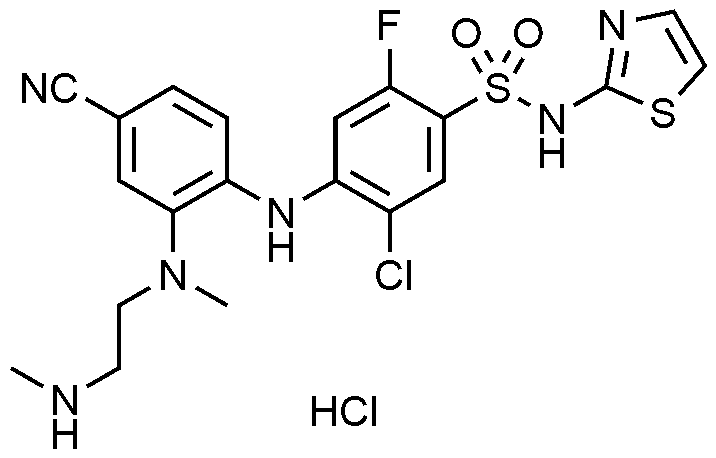
이하, 하기 실시예에 의하여 본 발명을 더욱 상세하게 설명하고자 한다. 단, 하기 실시예는 본 발명을 예시하기 위한 것일 뿐, 본 발명의 범위가 이들만으로 한정되는 것은 아니다.
실시예
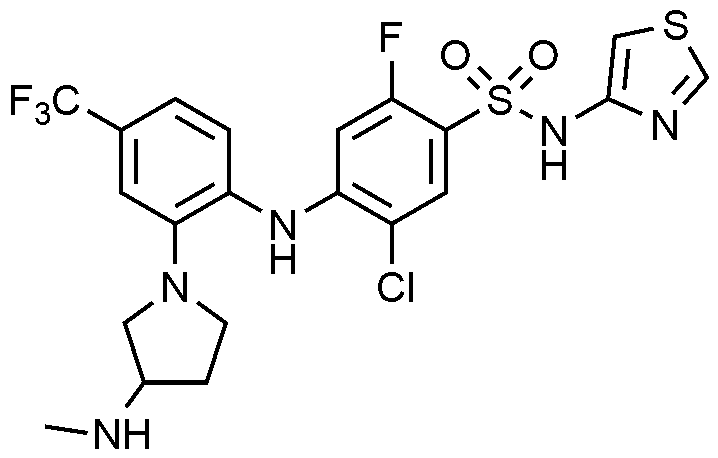
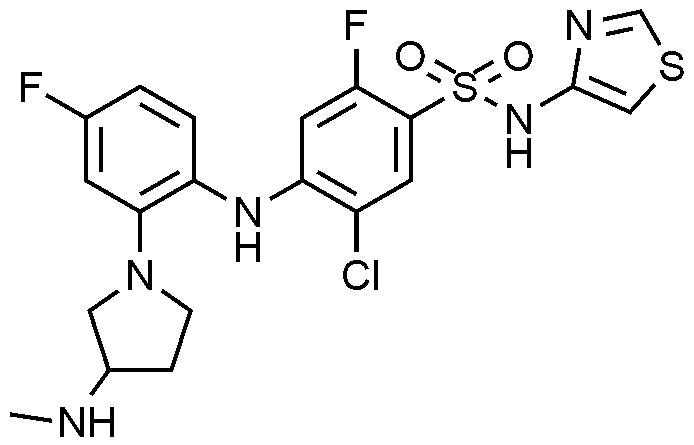
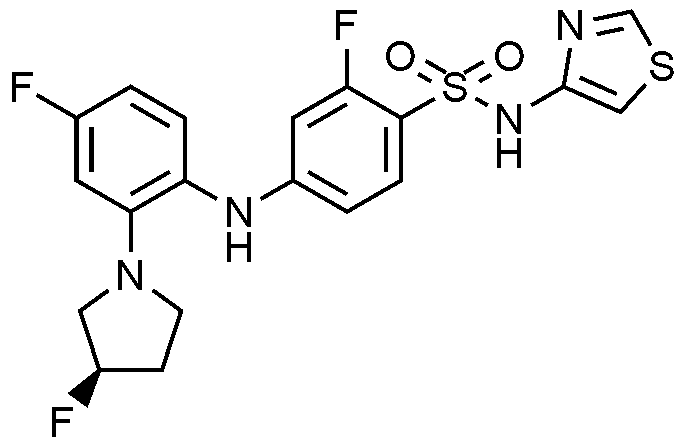
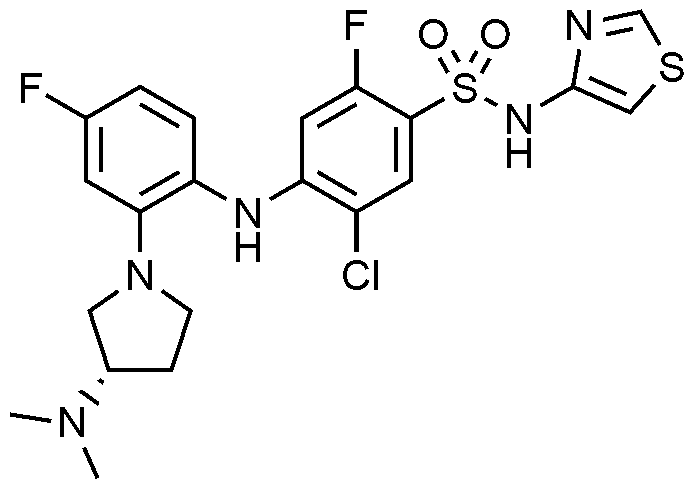
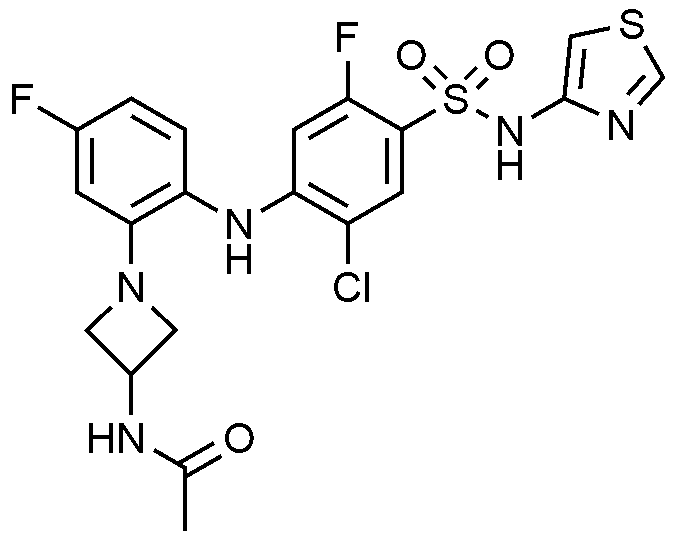
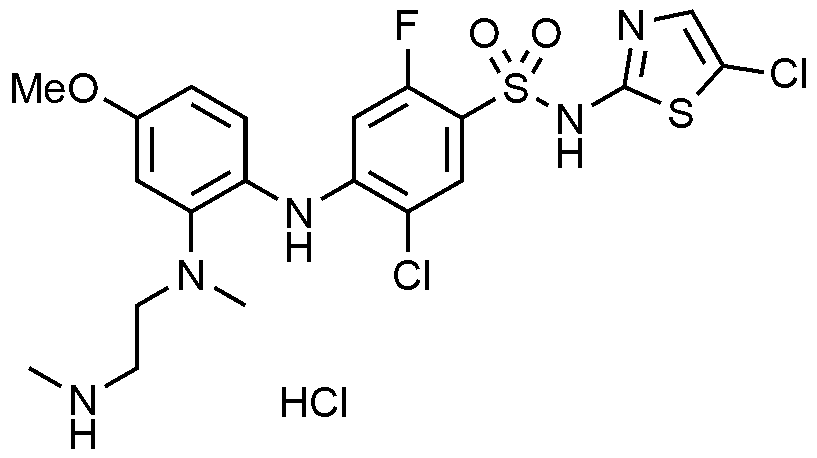
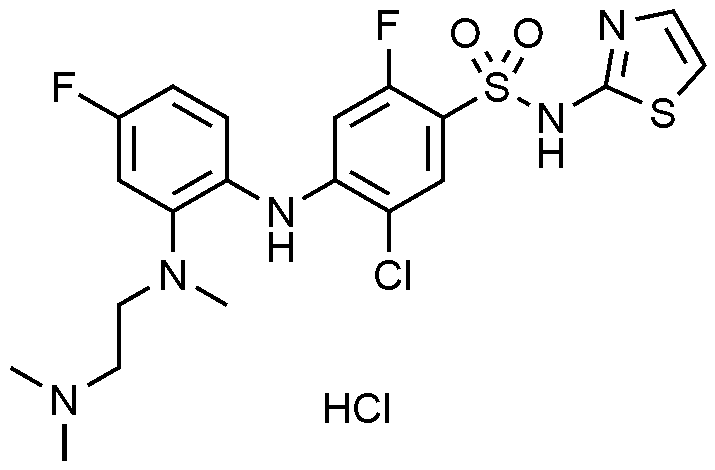
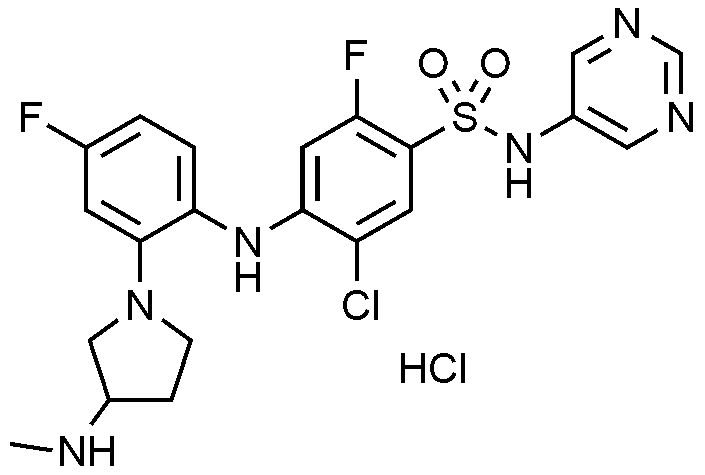
1: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
단계 1)
터트
-부틸 (1-(2-아미노-5-
플루오로페닐
)
피롤리딘
-3-일)(
메틸
)
카바
메이트의 제조
2,4-디플루오로-1-니트로벤젠(2.0 g, 12.6 mmol)과 터트-부틸 메틸(피롤리딘-3-일)카바메이트(2.5 g, 1.0 eq.)을 DMF(20 mL)에 용해한 후 K2CO3(2.6 g, 1.5 eq.)을 넣어주었다. 내부 온도를 60~70℃로 유지하며, 2시간 동안 교반한 후 반응액이 진한 노란색을 띄게 되면 TLC로 반응 종결을 확인하였다. 실온으로 냉각 후 에틸아세테이트(EA)/H2O을 넣고, 교반한 후 층 분리하였다. 분리된 유기층에 MgSO4을 넣고 교반하여 건조 후 여과하였다. 여과액을 감압 농축한 후 잔사를 EtOH(10 mL)과 증류수(10 mL)에 용해한 후 Na2S2O4(13.0 g, 6 eq.) 를 넣었다. 내부 온도 60~70℃을 유지하며, 2시간 교반 후 반응액의 노란색이 옅어져 거의 무색이 되면 TLC로 반응 종결을 확인하였다. 실온으로 냉각 후 증류수(50 mL)을 넣고 EA(100 mL)로 2회 추출하였다. 유기층에 MgSO4을 넣고 교반하여 건조 후 여과하였다. 여과액을 감압 농축하여 얻어진 잔사를 컬럼 크로마토그라피(n-Hexane/EA = 3/1)로 분리하여 표제 화합물(2.0 g, 51.1%)을 얻었다.
1H NMR (MeOD): 6.73(m, 1H), 6.57(t, 1H), 3.23(m, 1H), 3.10(m, 2H), 2.94(m, 1H), 2.91(s, 3H), 2.25(m, 1H), 1.99(m, 1H)
단계 2)
터트
-부틸
싸이아졸
-4-
일카바메이트의
제조
싸이아졸-4-카르복시산(5.0 g, 38.8 mmol)을 t-BuOH(100 mL)에 용해한 후 TEA(8.1 mL, 1.5 eq.)과 DPPA(7.1 mL, 1.5 eq.)를 넣어주었다. 내부 온도를 90~100℃로 유지하며, 3일 동안 교반한 후 TLC로 반응 종결을 확인하였다. 생성물을 감압 농축한 후 증류수(50 mL)을 넣고 EA(100 mL)로 2회 추출하였다. 유기층에 MgSO4을 넣고 교반하여 건조 후 여과하였다. 여과액을 감압 농축한 후 잔사를 소량의 EA에 넣고 슬러리화하고, 생성된 고체를 여과하여 흰색의 표제 화합물(4.0 g, 51.5%)을 얻었다.
1H NMR (MeOD): 8.73(s, 1H), 7.24(s, 1H), 1.52(s, 9H)
단계 3)
터트
-부틸 ((4-
브로모
-5-
클로로
-2-
플루오로페닐
)술포닐)(
싸이아졸
-4-일)카바메이트의 제조
단계 2)에서 제조한 터트-부틸 싸이아졸-4-일카바메이트(4.0 g, 20.0 mmol)를 반응 용기에 담고 질소 가스로 내부를 치환시켰다. THF(32 mL)에 용해한 후 dry ice-acetone을 이용하여 -78℃로 냉각시켰다. 냉각 후 LiHMDS(22.4 mL, 1.5 eq.)를 천천히 넣어주고 반응물을 30분 동안 교반시켰다. 4-브로모-5-클로로-2-플루오로벤젠술포닐 클로라이드(6.0 g, 1.0 eq.)를 THF(10 mL)에 용해한 후 반응액에 천천히 넣어주었다. 반응물을 밤새 교반시키고 TLC로 반응 종결을 확인하였다. 증류수(50 mL)를 넣고 EA(100 mL)로 2회 추출하였다. 유기층에 MgSO4을 넣고 교반하여 건조 후 여과하였다. 여과액을 감압 농축한 후 잔사를 THF/n-Hexane으로 결정화하여 표제 화합물(4.4 g, 59.0%)을 얻었다.
1H NMR (MeOD): 9.00(s, 1H), 8.22(d, 1H), 7.90(d, 1H), 7.78(s, 1H), 1.35(s, 9H)
단계 4)
터트
-부틸 (1-(2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트의 제조
단계 1)에서 제조한 터트-부틸 (1-(2-아미노-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(0.5 g, 1.1 mmol)과 단계 3)에서 제조한 터트-부틸 ((4-브로모-5-클로로-2-플루오로페닐)술포닐)(싸이아졸-4-일)카바메이트(0.9 g, 1.2 eq.)을 1,4-다이옥산(10 mL)에 용해하였다. 상기 반응 용액에 Pd(OAc)2(0.03 g, 0.1 eq), rac-BINAP(0.19 g, 0.2 eq.), Cs2CO3(1.5 g, 3.0 eq.)을 넣었다. Microwave initiator를 이용하여 120℃에서 30분 동안 반응시킨 후 TLC로 반응 종결을 확인하였다. 증류수(50 mL)을 넣고 EA(100 mL)로 2회 추출하였다. 유기층에 MgSO4을 넣고 교반한 후, 여과 및 건조하였다. 여과액을 감압 농축한 후 잔사를 컬럼 크로마토그라피(EA/n-Hexane = 1/1)로 분리하고, 이를 2번 반복하여 표제 화합물(2.0 g, 88.2%)을 얻었다.
1H NMR (MeOD): 8.95(s, 1H), 7.94(d, 1H), 7.65(s, 1H), 7.14(t, 1H), 6.70(d, 1H), 6.64(t, 1H), 6.07(d, 1H), 3.40(m, 1H), 3.28(m, 2H), 3.16(m, 1H), 2.64(s, 3H), 2.06(m, 1H), 1.89(m, 1H), 1.41(s, 9H), 1.36(s, 9H)
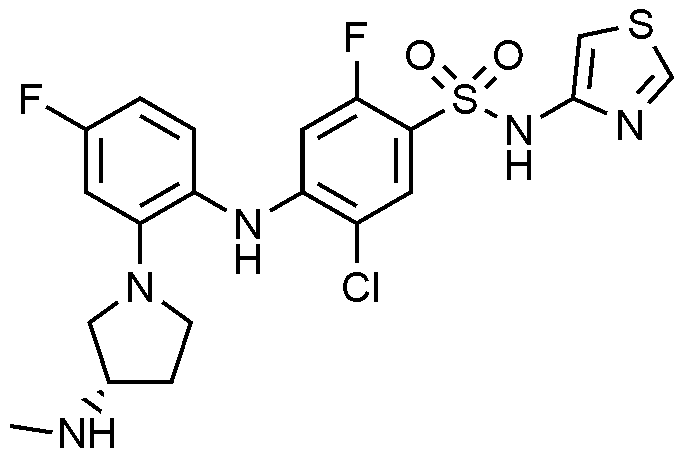
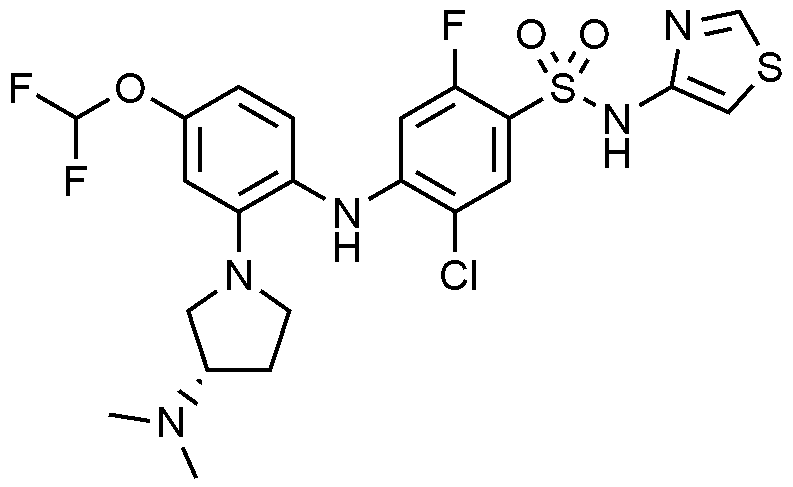
단계 5) 5-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
단계 4)에서 제조한 터트-부틸 (1-(2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(2.0 g, 2.9 mmol)에 1.25 M HCl in MeOH(15 mL)를 넣었다. 40~50℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 생성물을 농축하여 얻어진 잔사에 메틸렌클로라이드(15 mL)를 넣고 1시간 동안 교반시켜 생성된 고체를 여과하여 표제 화합물(0.9 g, 58.8%)을 얻었다.
1H NMR (MeOD): 8.73(s, 1H), 7.75(d, 1H), 7.12(t, 1H), 7.00(s, 1H), 6.69(d, 1H), 6.67(t, 1H), 6.05(d, 1H), 3.73(m, 1H), 3.54(m, 1H), 3.45(m, 1H), 3.38(m, 1H), 3.26(m, 1H), 2.63(s, 3H), 2.31(m, 1H), 1.96(m, 1H)
이하, 실시예 2 내지 9는 상기 실시예 1과 동일한 방법으로 제조하되, 제조하고자 하는 화합물의 구조에 상응하는 반응물을 사용하여 각각 제조하였다.
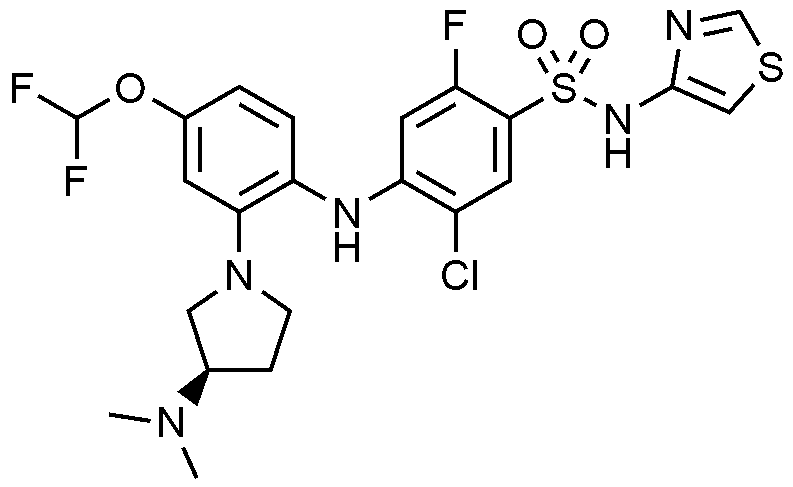
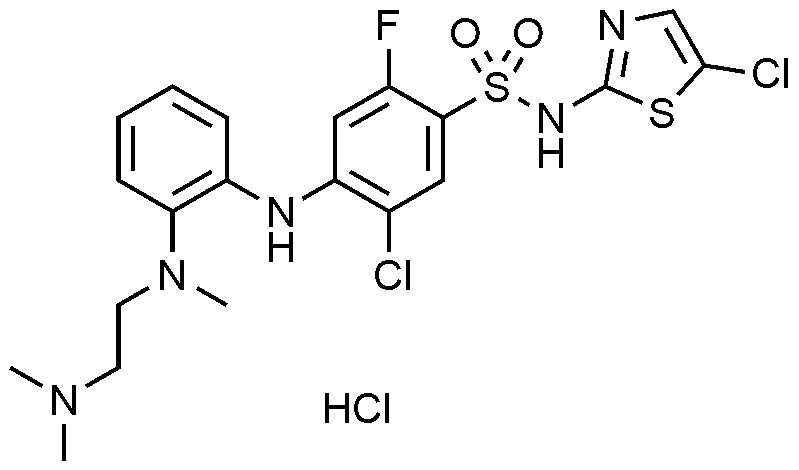
실시예
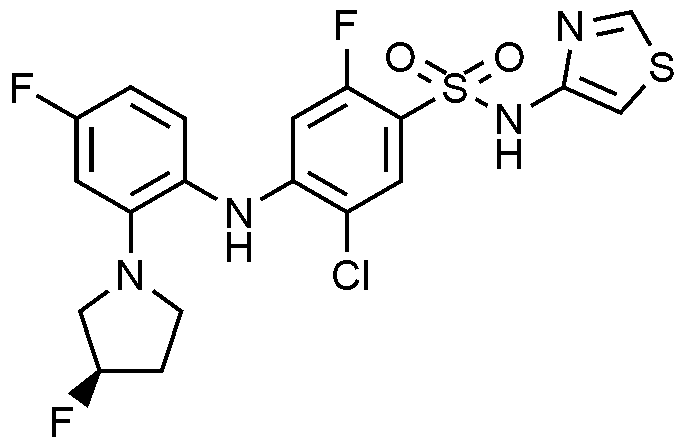
2: 5
-
클로로
-4-((4-
클로로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
1H NMR (500 MHz, MeOD): 8.79(s, 1H), 7.74(d, 1H), 7.09(d, 1H), 7.02(s, 1H), 6.98(s, 1H), 6.92(d, 1H), 6.13(d, 1H), 3.76(m, 1H), 3.53(m, 3H), 2.64(s, 3H), 2.31(m, 1H), 2.01(m, 1H), 1.27(m, 1H)
실시예
3: (R)-5-
클로로
-4-((4-
클로로
-2-(2-
메틸피페라진
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
1H NMR (500 MHz, MeOD): 8.73(d, 1H), 7.84(d, 1H), 7.38(d, 1H), 7.30(d, 1H), 7.28(d, 1H), 7.04(d, 1H), 6.99(d, 1H), 3.40(m, 3H), 3.15(m, 2H), 3.07(m, 1H), 2.86(m, 1H), 0.93(m, 3H)
실시예
4: (R)-5-
클로로
-4-((4-
클로로
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
1H NMR (500 MHz, MeOD): 8.75(d, 1H), 7.80(d, 1H), 7.28(d, 1H), 7.20(d, 1H), 7.17(m, 1H), 7.03(d, 1H), 6.58(d, 1H), 3.44(m, 1H), 3.02(m, 1H), 2.94(m, 1H), 2.78(m, 1H), 2.67(s ,3H), 2.08(m, 1H), 1.79(m, 1H), 1.50(m, 1H), 1.41(m, 1H), 0.87(m, 1H)
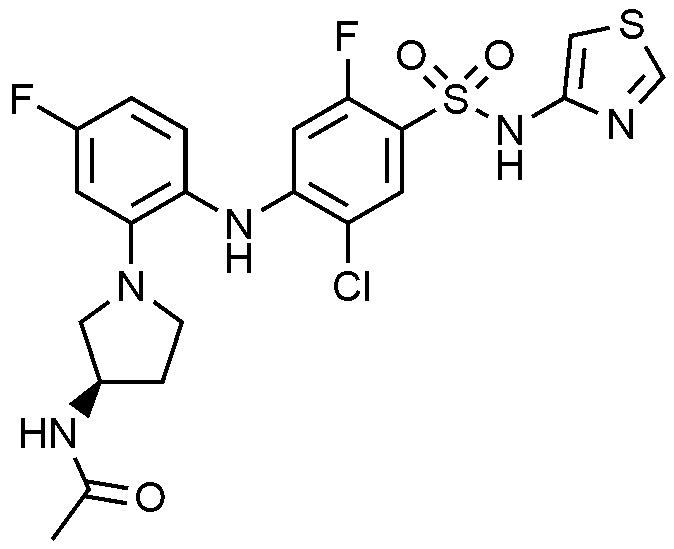
실시예
5: (R)-N-(1-(5-
클로로
-2-((2-
클로로
-5-
플루오로
-4-(N-(
싸이아졸
-4-일)술파모일)페닐)아미노)페닐)피롤리딘-3-일)아세트아미드
하이드로클로라이드의
제조
1H NMR (500 MHz, MeOD): 8.78(m, 1H), 7.76(d, 1H), 7.17(d, 1H), 7.08(m, 1H), 7.02(s, 1H), 6.92(m, 1H), 6.15(t, 1H), 4.26(m, 1H), 3.55(m, 1H), 3.35(m, 1H), 3.25(m, 1H), 2.27(m, 1H), 1.93(m, 1H), 1.90(s, 3H)
실시예
6: 5
-
클로로
-4-((4-
클로로
-2-(3-(
디에틸아미노
)
피롤리딘
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
1H NMR (500 MHz, MeOD): 8.78(d, 1H), 7.77(d, 1H), 7.12(d, 1H), 7.03(m, 1H), 6.99(dd, 1H), 6.03(d, 1H), 4.08(m, 1H), 3.52(m, 3H), 3.17(m, 4H), 3.05(m, 1H), 2.39(m, 1H), 2.01(m, 1H), 1.26(m, 6H)
실시예
7: 4
-((2-([1,3'-
비피롤리딘
]-1'-일)-4-
클로로페닐
)아미노)-5-
클로로
-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
1H NMR (500 MHz, MeOD): 8.76(d, 1H), 7.77(d, 1H), 7.11(d, 1H), 7.02(m, 2H), 6.97(m, 1H), 6.07(d, 1H), 3.91(m, 1H), 3.50(m, 5H), 3.22(m, 1H), 3.05(m, 2H), 2.36(m, 1H), 1.97(m, 5H)
실시예
8: 5
-
클로로
-2-
플루오로
-4-((4-
메틸
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
1H NMR (500 MHz, MeOD): 8.76(d, 1H), 7.74(d, 1H), 7.02(m, 2H), 6.91(s, 1H), 6.85(d, 1H), 6.16(d, 1H), 3.78(m, 1H), 3.45(m, 3H), 3.23(m, 1H), 2.65(s, 3H), 2.35(s, 3H), 2.34(m, 1H), 2.01(m, 1H)
실시예
9: (S)-5-
클로로
-4-((4-
클로로
-2-(3-
메틸피페라진
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
1H NMR (500 MHz, MeOD): 8.73(d, 1H), 7.79(d, 1H), 7.29(d, 1H), 7.20(m, 2H), 7.03(d, 1H), 6.54(d, 1H), 3.88(m, 1H), 3.44(s, 3H), 3.04(m, 1H), 2.97(m, 1H), 2.80(m, 1H), 1.27(m, 3H)
실시예
10: 4
-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
상기 실시예 1의 단계 3에서, 4-브로모-5-클로로-2-플루오로벤젠술포닐 클로라이드 대신 4-브로모벤젠술포닐 클로라이드를 사용하는 것을 제외하고는 실시예 1의 단계 1 내지 4와 동일한 방법으로 중간체인 터트-부틸 (1-(2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트를 제조하였다.
얻어진 중간체에 1.25 M HCl in MeOH(15 mL)를 넣었다. 40~50℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 생성물을 농축하여 얻어진 잔사를 PLC로 분리 및 정제하여 목적 화합물 0.05 g(수율 48%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.57(d, 2H), 7.07(t, 1H), 6.92(s, 1H), 6.66-6.54(m, 4H), 3.42-3.30(m, 4H), 3.14-3.13(m, 1H), 2.42(s, 3H), 2.18-2.16(m, 1H), 1.84-1.40(m, 1H)
이하, 실시예 11 내지 91는 상기 실시예 10과 동일한 방법으로 제조하되, 제조하고자 하는 화합물의 구조에 상응하는 반응물을 사용하여 각각 제조하였다.
실시예
11: 3
-
클로로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.74(s, 1H), 7.47(d, 1H), 7.05(t, 1H), 6.93(s, 1H), 6.63(d, 1H), 6.54(t, 1H), 6.33(d, 1H), 3.40-3.37(m, 2H), 3.17-3.11(m, 3H), 2.31(s, 3H), 2.08-2.00(m, 1H), 1.72-1.68(m, 1H)
실시예
12: 3
,5-
디플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.73(s, 1H), 7.43(d, 2H), 7.04(s, 1H), 6.63(t, 1H), 6.75(d, 1H), 6.60(t, 1H), 3.66-3.63(m, 1H), 3.49-3.35(m, 3H), 3.08-3.04(m, 1H), 2.63(s, 3H), 2.31-2.28(m, 1H), 1.96-1.93(m, 1H)
실시예
13: 2
-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.56(t, 1H), 7.03(t, 1H), 6.84(s, 1H), 6.63(d, 1H), 6.55(t, 1H), 6.40(d, 1H), 6.23(d, 1H), 3.35-3.30(m, 3H), 3.18-3.16(m, 2H), 2.36(s, 3H), 2.11-2.05(m, 1H), 1.78-1.75(m, 1H)
실시예
14: 4
-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(
트리플루오로메톡시
)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.60(d, 2H), 7.16(d, 1H), 6.92(s, 1H),6.77-6.68(m, 4H), 3.38-3.61(m, 1H), 3.35-3.33(m, 2H), 3.28-3.27(m 1H), 3.09-3.06(m, 1H), 2.36(s, 3H), 2.36-2.35(m, 1H), 1.85-1.83(m, 1H)
실시예
15: 3
,5-
디플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(
트리플
루오로메톡시)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.62(s, 1H), 7.41(d, 2H), 6.87(s, 1H), 6.76-6.75(m, 1H), 6.69-6.67(m, 2H), 3.59(s, 1H), 3.49-3.47(m, 2H), 3.25-3.23(m, 1H), 2.99-2.98(m, 1H), 2.59(s, 3H), 2.29-2.27(m, 1H), 1.99-1.97(m, 1H)
실시예
16: 2
-
플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(
트리플루오
로메톡시)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.58(t, 1H), 7.16(d, 1H), 6.84(s, 1H), 6.84-6.83(m, 2H), 6.49(d, 1H), 6.35(d, 1H), 3.38-3.34(m, 3H), 3.23-3.21(m, 1H), 3.12-3.10(m, 1H), 2.41(s, 3H), 2.18-2.16(m, 1H), 1.85-1.83(m, 1H)
실시예
17: 5
-
클로로
-2-
플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(트리플루오로메톡시)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.74(d, 1H), 7.15(d, 1H), 6.85(s, 1H), 6.75-6.74(m, 2H), 6.04(d, 1H), 3.45-3.38(m, 3H), 3.19-3.17(m, 2H), 2.40(s, 3H), 2.13-2.12(m, 1H), 1.80-1.79(m, 1H)
실시예
18: 5
-
클로로
-4-((5-
클로로
-3-(3-(
메틸아미노
)
피롤리딘
-1-일)피리딘-2-일)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(d, 1H), 8.30(d, 1H), 7.96(d, 1H), 7.84(d, 1H), 7.53(d, 1H), 6.87(d, 1H), 3.44(m, 3H), 3.10(m, 2H), 2.50(s, 3H), 2.36(m, 1H), 1.95(m, 1H)
실시예
19: 5
-
클로로
-4-((6-
클로로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)피리딘-3-일)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.76(s, 1H), 7.34(s, 1H), 6.90(m, 2H), 6.70(s, 1H), 6.01(d, 1H), 3.45(m, 3H), 2.99(m, 2H), 2.49(s,3H), 2.11(m, 2H)
실시예
20: 5
-
클로로
-2-
플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(트리플루오로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.67(d, 1H), 7.78(d, 1H), 7.26(d, 1H), 7.16(m, 2H), 6.81(d, 1H), 6.21(d, 1H), 3.39(m, 3H), 3.17(m, 2H), 2.43(s, 3H), 2.13(m, 1H), 1.94(m, 1H)
실시예
21: 5
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.63(d, 1H), 7.73(d, 1H), 7.07(d, 1H), 6.70(t, 2H), 6.62(t, 2H), 6.03(d, 1H), 3.40(m, 3H), 3.23(m, 2H), 2.42(s, 3H), 2.11(m, 1H), 1.83(m, 1H)
실시예
22: (R)-4-((4-
플루오로
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.61(d, 2H), 7.17(t, 1H), 6.89(s, 1H), 6.77-6.75(m, 3H), 6.74-6.73(m, 1H), 3.34-3.30(m, 1H), 2.88-2.59(m, 4H), 2.32(s, 3H), 1.82-1.70(m, 2H), 1.45-1.44(m, 2H)
실시예
23: (R)-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.61(t, 1H), 7.20(t, 1H), 6.87(d, 1H), 6.85-6.81(m, 2H), 6.78(d, 1H), 6.67(d, 1H), 3.34(s, 1H), 2.92-2.79(m, 4H), 2.48(s, 3H), 1.89-1.87(m, 2H), 1.79-1.78(m, 1H), 1.47-1.46(m, 1H)
실시예
24: (R)-3-
클로로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.80(s, 1H), 7.54(s, 1H), 7.24-7.21(m, 1H), 6.89-6.77(m, 4H), 3.01-2,97(m, 1H), 2.68-2.41(m, 3H), 2.30(s, 3H), 1.86-1.84(m, 1H), 1.68-1.66(m, 1H), 1.40-1.35(m, 2H)
실시예
25: (R)-3,5-
디플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.64(s, 1H), 7.41(d, 2H), 6.85(d, 1H), 6.75-6.66(m, 3H), 3.26-3.24(m, 1H), 2.88-2.78(m, 4H), 2.55(s, 3H), 1.87-1.86(m, 1H) 1.85-1.83(m, 1H), 1.74-1.72(m, 1H), 1.37-1.35(m, 1H)
실시예
26: (R)-5-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.66(s, 1H), 7.77(d, 1H), 7.22(t, 1H), 6.89-6.84(m, 2H), 6.81(s, 1H), 6.35(d, 1H), 3.38-3.36(m, 1H), 3.03-3.01(m, 1H), 2.63-2.61(m, 1H), 2.48-2.44(m, 2H), 2.37(s, 3H), 1.89-1.87(m, 1H), 1.68-1.66(m, 1H), 1.32-1.32(m, 2H)
실시예
27: (R)-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.56(d, 2H), 7.04(t, 1H), 6.92(s, 1H), 6.63-6.53(m, 4H), 3.24-3.21(m, 3H), 3.14-3.10(m, 2H), 2.31(s, 3H), 2.11-2.08(m, 1H), 1.73-1.70(m, 1H)
실시예
28: (R)-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.57-7.53(m, 1H), 7.05-7.03(m, 1H), 6.83(s, 1H), 6.62(d, 1H), 6.55-6.53(m, 1H), 6.40(d, 1H), 6.23(d, 1H), 3.34-3.30(m, 2H), 3.28-3.27(m, 1H), 3.18-3.15(m, 2H), 2.36(s, 3H), 2.13-2.10(m, 1H), 1.76-1.74(m, 1H)
실시예
29: (R)-3-
클로로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.75(s, 1H), 7.47-7.45(m, 1H), 7.06-7.04(m, 1H), 6.92(s, 1H), 6.62(d, 1H), 6.54(d, 1H), 6.32(d, 1H), 3.40-3.37(m, 2H), 3.17-3.11(m, 3H), 2.33(s, 3H), 2.08-2.05(m, 1H), 1.72-1.69(m, 1H)
실시예
30: (R)-3,5-
디플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.65(s, 1H), 7.37(d, 2H), 6.77-6.74(m, 2H), 6.69(d, 1H), 6.56-6.52(m, 1H), 3.41-3.26(m, 3H), 3.26-3.24(m, 1H), 3.05-3.02(m, 1H), 2.48(s, 3H), 2.20-2.18(m, 1H), 1.83-1.81(m, 1H)
실시예
31: (R)-5-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤
리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.67(s, 1H), 7.72(d, 1H), 7.04(t, 1H), 6.81(d, 1H), 6.62(t, 1H), 5.98(d, 1H), 5.48(s, 1H), 3.43-3.36(m, 2H), 3.39-3.36(m, 1H), 3.30-3.26(m, 2H), 2.36(s, 3H), 2.36-2.10(m, 1H), 1.77-1.73(m, 1H)
실시예
32: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.73(d, 1H), 7.06(t, 1H), 6.83(s, 1H), 6.64(d, 1H), 6.57(t, 1H), 6.01(d, 1H), 3.50-3.40(m, 3H), 3.28-3.23(m, 2H), 2.48(s, 3H), 2.20-2.19(m, 1H), 1.95-1.93(m, 1H)
실시예
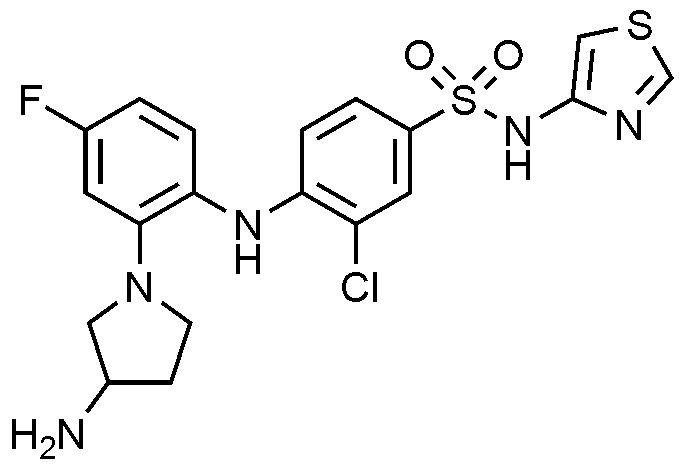
33: 4
-((2-(3-
아미노피롤리딘
-1-일)-4-
플루오로페닐
)아미노)-2-
플루
오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.72(s, 1H), 7.58(t, 1H), 7.10(t, 1H), 6.93(m, 1H), 6.68(d, 1H), 6.62(d, 1H), 6.45(d, 1H), 6.33(d, 1H), 3.79(m, 1H), 3.50(m, 2H), 3.30(m, 1H), 3.20(m, 1H), 2.29(m, 1H), 1.95(m, 1H)
실시예
34: 4
-((2-(3-
아미노피롤리딘
-1-일)-4-
플루오로페닐
)아미노)-3-
클로
로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.70(d, 1H), 7.75(s, 1H), 7.47(d, 1H), 7.07(t, 1H), 7.07(t, 1H), 6.64(d, 1H), 6.58(t, 1H), 6.37(d, 1H), 3.71(m, 1H), 3.59(m, 2H), 3.25(m, 1H), 3.13(m, 1H), 2.13(m, 1H), 1.77(m, 1H)
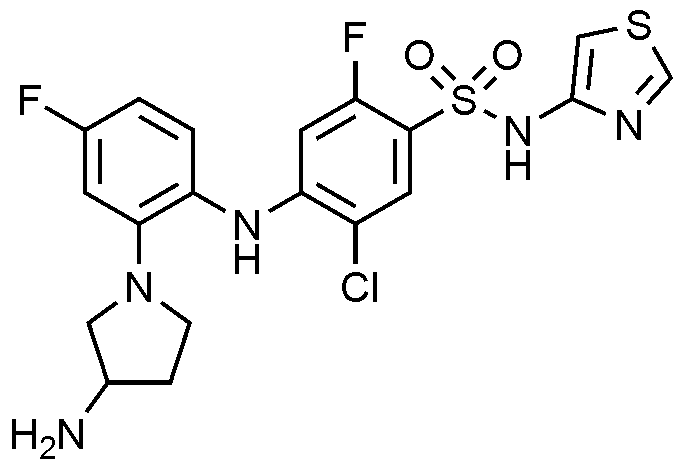
실시예
35: 4
-((2-(3-
아미노피롤리딘
-1-일)-4-
플루오로페닐
)아미노)-5-
클로
로-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.72(s, 1H), 7.74(d, 1H), 7.10(t, 1H), 6.98(d, 1H), 6.68(d, 1H), 6.63(t, 1H), 6.06(d, 1H), 3.73(m, 1H), 3.53(m, 2H), 3.24(m, 2H), 2.23(m, 1H), 1.87(m, 1H)
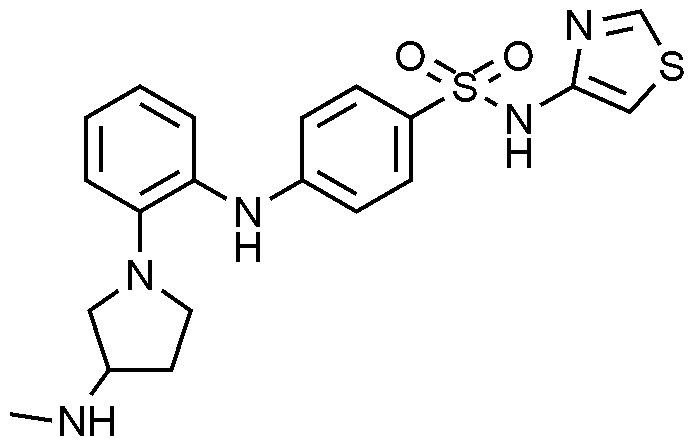
실시예
36: 4
-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(
싸이아졸
-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.58(d, 2H), 7.14(d, 1H), 7.05(t, 1H), 6.96(d, 1H), 6.91-6.87(m, 2H), 6.75(d, 2H), 3.34-3.30(m, 2H), 3.18-3.15(m, 2H), 3.00-2.97(m, 1H), 2.35(s, 3H), 2.15-2.12(m, 1H), 1.75-1.71(m, 1H)
실시예
37: 2
-
플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(
트리플루오
로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(d, 1H), 7.65(t, 1H), 7.35(d, 1H), 7.20(m, 2H), 6.87(d, 1H), 6.74(d, 1H), 6.66(d, 1H), 3.65(m, 1H), 3.47(m, 1H), 3.37(m, 2H), 3.03(m, 1H), 2.60(s, 3H), 2.30(m, 1H), 2.02(m, 1H)
실시예
38: 3
-
클로로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(
트리플루오로
메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.67(d, 1H), 7.80(d, 1H), 7.53(d, 1H), 7.25(d, 1H), 7.17(s, 1H), 7.13(d, 1H), 6.89(d, 1H), 6.59(d, 1H), 3.35(m, 2H), 3.28(m, 1H), 3.12(m, 2H), 2.37(s, 3H), 2.11(m, 1H), 1.75(m, 1H)
실시예
39: 4
-((4-(
디플루오로메톡시
)-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.58(t, 1H), 7.12(d, 1H), 6.70(t, 1H), 6.66(m, 2H), 6.50(d, 1H), 6.38(d, 1H), 3.59(m, 1H), 3.41(m, 2H), 3.32(m, 1H), 3.12(m, 1H), 2.54(s, 3H), 2.24(m, 1H), 1.93(m, 1H)
실시예
40: 3
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.76(s, 1H), 7.47(d, 1H), 7.09(d, 1H), 6.81(t, 2H), 6.65(m, 2H), 6.39(d, 1H), 3.40(m, 3H), 3.18(m, 2H), 2.44(s, 3H), 2.15(m, 1H), 1.81(m, 1H)
실시예
41: (R)-4-((4-
플루오로
-2-(3-
플루오로피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.54(d, 2H), 7.02(t, 1H), 6.92(s, 1H), 6.60(d, 1H), 6.52-6.49(m, 3H), 3.57-3.53(m, 1H), 3.49-3.46(m, 1H), 3.26-3.21(m, 3H), 2.10-2.06(m, 1H), 2.00-1.94(m, 1H)
실시예
42: (R)-2-
플루오로
-4-((4-
플루오로
-2-(3-
플루오로피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.54(t, 1H), 7.01(t, 1H), 6.90(d, 1H), 6.59(t, 1H), 6.50(d, 1H), 6.32(d, 1H), 6.17(d, 1H), 3.43-3.41(m, 2H), 3.26-3.21(m, 2H), 2.21-1.94(m, 3H)
실시예
43: (R)-3-
클로로
-4-((4-
플루오로
-2-(3-
플루오로피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8,69(s, 1H), 7.73(s, 1H), 7.44(d, 1H), 7.04(t, 1H), 6.92(s, 1H), 6.61(d, 1H), 6.53(t, 1H), 6.28(d, 1H), 3.47-3.41(m, 3H), 3.26-3.24(m, 2H), 2.12-1.97(m, 2H)
실시예
44: (R)-3,5-
디플루오로
-4-((4-
플루오로
-2-(3-
플루오로피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.73(s, 1H), 7.34(d, 2H), 7.04(s, 1H), 6.92(t, 1H), 6.57(d, 1H), 6.47(t, 1H), 3.56-3.25(m, 4H), 3.13-3.11(m, 1H), 2.04-1.99(m, 2H)
실시예
45: (R)-5-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-
플루오로피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.70(s, 1H), 7.70(d, 1H), 7.04(t, 1H), 6.96(d, 1H), 6.65(d, 1H), 6.55(t, 1H), 5.92(d, 1H), 3.46-3.40(m, 3H), 3.37-3.33(m, 2H), 2.15-1.96(m, 2H)
실시예
46: 2
-
플루오로
-4-((3-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(d, 1H), 7.65(t, 1H), 7.08(lm, 2H), 6.88(m, 3H), 6.74(m, 1H), 3.56(m, 1H), 3.37(m, 2H), 3.34(m, 1H), 3.17(m, 1H), 3.16(s, 3H), 2.35(m, 1H), 2.05(m, 1H)
실시예
47: 3
-
클로로
-4-((3-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.67(d, 1H), 7.84(d, 1H), 7.63(d, 1H), 7.19(d, 1H), 7.05(m, 2H), 6.87(s, 1H), 6.79(m, 1H), 3.60(m, 1H), 3.52(m, 1H), 3.33(m, 1H), 3.26(m, 1H), 3.20(m, 1H), 2.56(s, 3H), 2.27(m, 1H), 1.90(m, 1H)
실시예
48: 5
-
클로로
-2-
플루오로
-4-((3-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.65(s, 1H), 7.81(d, 1H), 7.10(m, 1H), 7.05(m, 1H), 6.84(m, 3H), 3.53(m, 3H), 3.25(m, 2H), 2.56(s, 3H), 2.26(m, 1H), 1.91(m, 1H)
실시예
49: 2
-
플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.57(t, 1H), 7.14-7.09(m, 2H), 6.97(d, 1H), 6.92-6.90(m, 1H), 6.84(s, 1H), 6.55(d, 1H), 6.40(d, 1H), 3.42-3.41(m, 1H), 3.34-3.30(m, 1H), 3.26-3.21(m, 2H), 3.04-3.02(m, 1H), 2.42(s, 3H), 2.20-2.17(m, 1H), 1.85-1.81(m, 1H)
실시예
50: 3
-
클로로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.66(s, 1H), 7.76(s, 1H), 7.48(d, 1H), 7.15-7.10(m, 2H), 6.96(d, 1H), 6.89-6.86(m, 1H), 6.83(s, 1H), 6.52(d 1H), 3.30-3.25(m, 3H), 3.11-3.07(m, 2H), 2.34(s, 3H), 2.10-2.07(m, 1H), 1.73-1.69(m, 1H)
실시예
51: 3
,5-
디플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.65(s, 1H), 7.43(d, 2H), 7.04(d, 1H), 6.93-6.87(m, 2H), 6.75(s, 1H), 6.64(d, 1H), 3.63-3.60(m, 1H), 3.45-3.43(m, 2H), 3.19-3.17(m, 1H), 2.96-2.92(m, 1H), 2.61(s, 3H), 2.32-2.28(m, 1H), 1.98-1.95(m, 1H)
실시예
52: 5
-
클로로
-2-
플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.66(s, 1H), 7.74(d, 1H), 7.20(t, 1H), 7.12(d, 1H), 6.96(d, 1H), 6.92-6.89(m, 1H), 6.79(s, 1H), 6.12(d, 1H), 3.30(s, 3H), 3.16-3.11(m, 2H), 2.40(s, 3H), 2.15-2.12(m, 1H), 1.79-1.78(m, 1H)
실시예
53: 2
-
플루오로
-4-((4-
메톡시
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.71(s, 1H), 7.55(t, 1H), 7.02(d, 1H), 6.89(s, 1H), 6.49(m, 3H), 6.33(d, 1H), 3.78(s, 3H), 3.67(m, 1H), 3.42(m, 1H), 3.38(m, 2H), 3.10(m, 1H), 2.58(s, 3H), 2.27(m, 1H), 1.99(m, 1H)
실시예
54: 3
-
클로로
-4-((4-
메톡시
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.70(d, 1H), 7.74(d, 1H), 7.45(d, 1H), 7.00(d, 1H), 6.94(d, 1H), 6.49(m, 2H), 6.37(d, 1H), 3.78(s, 3H), 3.47(m, 1H), 3.38(m, 2H), 3.27(m, 1H), 3.16(m, 1H), 2.46(s, 3H), 2.17(m, 1H), 1.83(m, 1H)
실시예
55: 5
-
클로로
-2-
플루오로
-4-((4-
메톡시
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.71(d, 1H), 7.72(d, 1H), 7.01(d, 1H), 6.89(d, 1H), 6.51(m, 2H), 6.48(d, 1H), 3.81(s, 3H), 3.67(m, 1H), 3.45(m, 3H), 3.20(m, 1H), 2.59(s, 3H), 2.27(m, 1H), 1.96(m, 1H)
실시예
56: (R)-4-((4-
메톡시
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.59(d, 2H), 7.13(d, 1H), 6.93(s, 1H), 6.78(d, 2H), 6.62(d, 2H), 3.77(s, 3H), 3.25(m, 1H), 2.87-2.65(m, 4H), 2.39(s, 3H), 1.85(m, 1H), 1.70(m, 1H), 1.54(m, 2H)
실시예
57: (R)-2-
플루오로
-4-((4-
메톡시
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.70(s, 1H), 7.58(t, 1H), 7.12(d, 1H), 6.88(s, 1H), 6.65-6.58(m, 3H), 6.49(d, 1H), 3.78(s, 3H), 3.25(m, 1H), 2.89-2.77(m, 4H), 2.47(s, 3H), 1.88(m, 2H), 1.46(m, 2H)
실시예
58: (R)-3-
클로로
-4-((4-
메톡시
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.77(s, 1H), 7.51(d, 1H), 7.17(d, 1H), 6.90(s, 1H), 6.72(d, 1H), 6.67(d, 2H), 3.78(s, 3H), 2.96-2.94(m, 1H), 2.70-2.45(m, 3H), 2.33(s, 3H), 1.88(m, 1H), 1.68(m, 1H), 1.44-1.37(m, 3H)
실시예
59: (R)-3,5-
디플루오로
-4-((4-
메톡시
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.40(d, 2H), 6.80(t, 2H), 6.63(s, 1H), 6.56(d, 1H), 3.74(s, 3H), 2.90-2.70(m, 4H), 2.53(s, 3H), 1.86-1.28(m, 5H)
실시예
60: (R)-5-
클로로
-2-
플루오로
-4-((4-
메톡시
-2-(3-(
메틸아미노
)피페리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.68(s, 1H), 7.74(d, 1H), 7.15(d, 1H), 6.81(s, 1H), 6.69(d, 2H), 6.31(d, 1H), 3.79(s, 3H), 2.99(m, 1H), 2.67-2.49(m, 3H), 2.39(s, 3H), 1.88(m, 1H), 1.68(m, 1H), 1.35-1.28(m, 3H)
실시예
61: 3
-
클로로
-4-((4-
플루오로
-2-(4-
메틸피페라진
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.70(s, 1H), 7.81(s, 1H), 7.54(d, 1H), 7.24(d, 1H), 7.00(s, 1H), 6.89-6.79(m, 3H), 2.98-2.92(m, 4H), 2.37(m, 4H), 2.20(s, 3H)
실시예
62: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(4-
메틸피페라진
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.71(s, 1H), 7.77(d, 1H), 7.24(t, 1H), 6.98(s, 1H), 6.91-6.82(m, 2H), 6.40(d, 1H), 2.96(m, 4H), 2.36(m, 4H), 2.15(s, 3H)
실시예
63: (S)-5-
클로로
-4-((2-(3-(디메틸아미노)
피롤리딘
-1-일)-4-
플루오
로페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.62(d, 1H), 7.79(d, 1H), 6.98(m, 2H), 6.52(m, 2H), 6.23(m, 2H), 3.22(m, 3H), 3.14(m, 1H), 2.70(m, 1H), 2.23(s, 6H), 1.78(m, 2H)
실시예
64: (S)-5-
클로로
-4-((2-(3-(디메틸아미노)
피롤리딘
-1-일)-4-(
트리플
루오로메틸)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.63(s, 1H), 7.83(d, 1H), 7.17(m, 3H), 6.99(s, 1H), 6.64(s, 1H), 6.56(d, 1H), 3.25(m, 4H), 2.81(m, 1H), 2.24(s, 6H), 1.85(m, 2H)
실시예
65: 5
-
클로로
-2-
플루오로
-4-((2-(4-
메틸피페라진
-1-일)-4-(
트리플루
오로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.71(s, 1H), 7.72(d, 1H), 7.28(m, 3H), 6.06(s, 1H), 6.06(d, 1H), 3.37(m, 4H), 2.66(m, 4H), 2.37(s, 3H)
실시예
66: 5
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(4-
메틸피페라진
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.72(s, 1H), 7.78(s, 1H), 7.28(d, 1H), 6.98-6.82(m, 4H), 6.49(d, 1H), 3.39-3.30(m, 4H), 2.97(m, 4H), 2.25(s, 3H)
실시예
67: 5
-
클로로
-2-
플루오로
-4-((2-(4-
메틸피페라진
-1-일)-4-(
트리플루
오로메톡시)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.71(s, 1H), 7.81(d, 1H), 7.35(d, 1H), 7.03-6.98(m, 3H), 6.59(d, 1H), 4.09(d, 1H), 2.97(m, 4H), 2.42(m, 4H), 2.22(s, 3H)
실시예
68: (S)-3-
클로로
-4-((2-(3-(디메틸아미노)
피롤리딘
-1-일)-4-(
트리플
루오로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.66(d, 1H), 7.80(d, 1H), 7.52(dd, 1H), 7.28(s, 1H), 7.14(m, 2H), 7.05(d, 1H), 6.89(d, 1H), 6.64(s, 1H), 3.22(m, 2H), 3.16(m, 2H), 2.79(m, 1H), 2.23(s, 6H), 2.10(m, 1H), 2.06(m, 1H)
실시예
69: (S)-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.70(d, 1H), 7.56(t, 1H), 7.06(t, 1H), 6.90(d, 1H), 6.65(d, 1H), 6.57(t, 1H), 6.43(d, 1H), 6.30(d, 1H), 3.37(m, 3H),l 3.24(m, 1H), 3.13(m, 1H), 2.44(S, 3H), 2.18(m, 1H), 2.00(m, 1H)
실시예
70: (S)-5-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤
리딘-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.71(s, 1H), 7.73(d, 1H), 7.07(t, 1H), 6.92(s, 1H), 6.67(d, 1H), 6.59(t, 1H), 6.01(d, 1H), 3.45(m, 3H), 3.23(m, 2H), 2.46(s, 3H), 2.17(m ,1H), 1.83(m, 1H)
실시예
71: (S)-5-
클로로
-4-((2-(3-(디메틸아미노)
피롤리딘
-1-일)-4-
메톡시
페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.58(d, 1H), 7.76(d, 1H), 6.99(m, 2H), 6.37(m, 2H), 6.26(m, 2H), 3.80(s, 3H), 3.25-3.21(m, 5H), 2.76(m, 1H), 2.21(s, 6H), 2.05(m, 1H)
실시예
72: (S)-5-
클로로
-4-((4-(
디플루오로메톡시
)-2-(3-(디메틸아미노)
피
롤리딘-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.63(d, 1H), 7.79(d, 1H), 7.04(m, 1H), 6.96(d, 1H), 6.57(m, 2H), 6.50(d, 1H), 6.29(m, 2H), 3.22(m, 4H), 2.75(m, 1H), 2.22(s, 6H), 2.05(m, 1H), 1.78(m, 1H)
실시예
73: (R)-5-
클로로
-4-((2-(3-(디메틸아미노)
피롤리딘
-1-일)-4-
플루오
로페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.64(s, 1H), 7.79(d, 1H), 7.01(t, 1H), 6.98(s, 1H), 6.51(m, 2H), 6.23(m, 2H), 3.24(m, 5H), 2.71(m, 1H), 2.20(s, 6H), 1.77(m, 1H)
실시예
74: (R)-5-
클로로
-4-((2-(3-(디메틸아미노)
피롤리딘
-1-일)-4-(
트리플
루오로메틸)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.64(d, 1H), 7.84(d, 1H), 7.24(d, 1H), 7.12(m, 2H), 6.98(d, 1H), 6.66(s, 1H), 6.54(d, 1H), 3.23(m, 4H), 2.83(m, 1H), 2.23(s, 6H), 1.90(m, 2H)
실시예
75: (R)-5-
클로로
-4-((4-(
디플루오로메톡시
)-2-(3-(디메틸아미노)
피
롤리딘-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 8.62(d, 1H), 7.79(d, 1H), 7.05(d, 1H), 6.98(d, 1H), 6.57(s, 1H), 6.50(t, 1H), 6.31(m, 2H), 3.24(m, 3H), 3.15(m, 1H), 2.74(m, 1H), 2.21(s, 6H), 1.77(m, 2H)
실시예
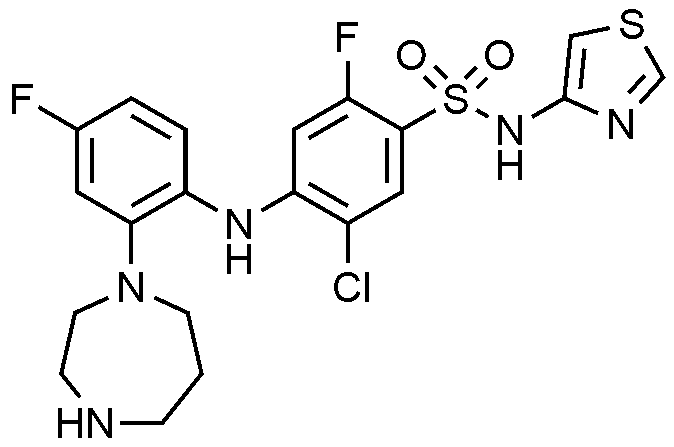
76: 4
-((2-(1,4-
디아제판
-1-일)-4-
플루오로페닐
)아미노)-5-
클로로
-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.76(d, 1H), 7.20(m, 1H), 6.97(d, 1H), 6.92(s, 1H), 6.82(t, 1H), 6.22(d, 1H), 3.30(m, 2H), 3.20(t, 2H), 3.10(m, 4H), 1.95(m, 2H)
실시예
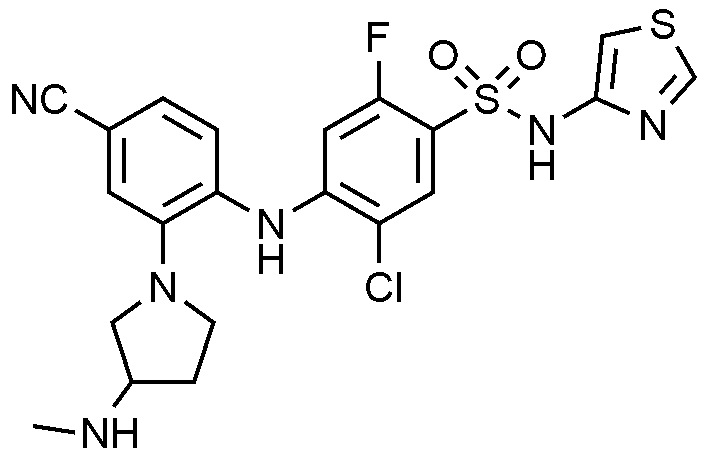
77: 5
-
클로로
-4-((4-
시아노
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.69(s, 1H), 7.80(d, 1H), 7.29(s, 1H), 7.24(m, 2H), 6.90(s, 1H), 6.33(d, 1H), 3.42(m, 3H), 3.16(m, 2H), 2.47(s, 3H), 2.18(m, 1H), 1.85(m, 1H)
실시예
78: (R)-N-(1-(2-((2-
클로로
-5-
플루오로
-4-(N-(
싸이아졸
-4-일)
술파모
일)페닐)아미노)-5-(트리플루오로메틸)페닐)피롤리딘-3-일)아세트아미드의 제조
1H NMR (500 MHz, CDCl3): 9.25(broad, 1H), 8.64(d, 1H), 7.84(d, 1H), 7.18(m, 2H), 7.02(d, 1H), 6.69(s, 1H), 6.52(d, 1H), 5.60(d, 1H), 4.50(m, 1H), 3.37(m, 1H), 3.27(m, 1H), 3.09(m, 2H), 2.27(m, 1H), 1.95(s, 3H), 1.77(m, 1H)
실시예
79: (R)-N-(1-(2-((2-
클로로
-4-(N-(
싸이아졸
-4-일)
술파모일
)페닐)아미노)-5-(트리플루오로메틸)페닐)피롤리딘-3-일)아세트아미드의 제조
1H NMR (500 MHz, CDCl3): 9.34(s, 1H), 8.69(d, 1H), 7.79(d, 1H), 7.52(d, 1H), 7.28(d, 1H), 7.18(m, 2H), 7.07(s, 1H), 6.86(d, 1H), 6.69(s, 1H), 5.59(d, 1H), 4.51(m, 1H), 3.49(s, 3H), 3.33(m, 1H), 3.26(m, 1H), 3.06(m, 2H), 2.27(m, 1H), 1.94(s, 3H), 1.75(m, 1H)
실시예
80: (S)-3-
클로로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(
트리플루
오로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.70(s, 1H), 7.82(s, 1H), 7.55(d, 1H), 7.23(m, 3H), 6.95(s, 1H), 6.69(d, 1H), 3.60(m, 1H), 3.44(m, 2H), 3.30(m, 1H), 3.15(m, 1H), 2.57(s, 3H), 2.24(m, 1H), 1.94(m, 1H)
실시예
81: (S)-5-
클로로
-2-
플루오로
-4-((2-(3-(
메틸아미노
)
피롤리딘
-1-일)-4-(트리플루오로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.65(s, 1H), 7.77(d, 1H), 7.24(d, 1H), 7.19(s, 1H), 7.16(d, 1H), 6.74s, 1H), 6.24(d, 1H), 3.57(m, 1H), 3.45(m, 2H), 3.30(m, 1H), 3.17(m, 1H), 2.54(s, 3H), 2.22(m, 1H), 1.93(m, 1H)
실시예
82: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
아제티딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.86(s, 1H), 8.17(s, 1H), 7.07(d, 1H), 6.84(d, 1H), 6.79(d, 1H), 6.40(m, 1H), 6.33(s, 1H), 3.93-3.70 (m, 4H), 3.35(m, 1H), 3.23(s, 3H)
실시예
83: 4
-((2-(3-
아미노아제티딘
-1-일)-4-
플루오로페닐
)아미노)-5-
클로
로-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.84(s, 1H), 8.07(s, 1H), 7.11(d, 1H), 6.85(d, 1H), 6.81(d, 1H), 6.40(m, 1H), 6.33(s, 1H), 4.03-3.82 (m, 4H), 3.42(m, 1H)
실시예
84: 5
-
클로로
-4-((2-(3-(디메틸아미노)
아제티딘
-1-일)-4-
플루오로페
닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, MeOD): 8.76(s, 1H), 8.10(s, 1H), 7.07(d, 1H), 6.84(d, 1H), 6.79(d, 1H), 6.40(m, 1H), 6.33(s, 1H), 3.99-3.65 (m, 4H), 3.33(m, 1H), 3.12(s, 6H)
실시예
85: N-(1-(2-((2-
클로로
-5-
플루오로
-4-(N-(
싸이아졸
-4-일)
술파모일
)페닐)아미노)-5-플루오로페닐)아제티딘-3-일)아세트아미드의 제조
1H NMR (500 MHz, MeOD): 8.56(s, 1H), 8.00(s, 1H), 7.00(d, 1H), 6.77(d, 1H), 6.71(d, 1H), 6.30(m, 1H), 6.29(s, 1H), 3.91-3.55 (m, 4H), 3.35(m, 1H), 2.13(s, 3H)
실시예
86: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-
메톡시피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 10.93(s, 1H), 8.74(d, 1H), 7.81(d, 1H), 6.99(t, 1H), 6.50(m, 2H), 6.24(m, 2H), 3.92(t, 1H), 3.32(m, 2H), 3.26(s, 3H), 3.11(m, 2H), 2.01(m, 1H), 1.92(m, 1H), 1.69(m, 1H)
실시예
87: 5
-
클로로
-2-
플루오로
-4-((2-(3-
메톡시피롤리딘
-1-일)-4-(
트리플
루오로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 10.79(s, 1H), 8.74(d, 1H), 7.85(d, 1H), 7.25(m, 2H), 7.15(s, 1H), 7.11(d, 1H), 6.94(d, 1H), 6.66(s, 1H), 6.56(d, 1H), 3.97(t, 1H), 3.31(m, 2H), 3.30(s, 3H), 3.12(m, 2H), 2.04(m, 2H)
실시예
88: (R)-N-(1-(2-((2-
클로로
-5-
플루오로
-4-(N-(
싸이아졸
-4-일)
술파모
일)페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)아세트아미드의 제조
1H NMR (500 MHz, CDCl3): 10.63(s, 1H), 8.70(d, 1H), 7.78(d, 1H), 7.01(m, 1H), 6.94(d, 1H), 6.51(m, 2H), 6.30(s, 1H), 6.17(d, 1H), 5.78(d, 1H), 4.44(m, 1H), 3.38(m, 1H), 3.27(m, 1H), 3.10(m, 1H), 3.03(m, 1H), 2.15(m, 1H), 1.90(s, 3H), 1.75(m, 1H)
실시예
89: 3
-
클로로
-4-((4-
플루오로
-2-(3-
메톡시피롤리딘
-1-일)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 10.74(s, 1H), 8.77(s, 1H), 7.72(s, 1H), 7.42(d, 1H), 7.01(m, 2H), 6.53(m, 3H), 6.18(s, 1H), 3.90(s, 1H), 3.34(m, 2H), 3.25(s, 3H), 3.12(m, 2H), 1.99(m, 1H), 1.89(m, 1H)
실시예
90: 3
-
클로로
-4-((2-(3-
메톡시피롤리딘
-1-일)-4-(
트리플루오로메틸
)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
1H NMR (500 MHz, CDCl3): 10.38(s, 1H), 8.76(s, 1H), 7.78(s, 1H), 7.50(d, 1H), 7.26(d, 1H), 7.14(m, 2H), 7.02(s, 1H), 6.91(d, 1H), 6.65(s, 1H), 3.97(s, 1H), 3.33(m, 5H), 3.12(m, 2H), 2.03(m, 2H)
실시예
91: (R)-N-(1-(2-((2-
클로로
-4-(N-(
싸이아졸
-4-일)
술파모일
)페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)아세트아미드의 제조
1H NMR (500 MHz, CDCl3): 10.43(broad, 1H), 8.76(s, 1H), 7.71(s 1H), 7.41(s, 1H), 7.03(s, 2H), 6.54(m, 3H), 6.25(s, 1H), 5.90(s, 1H), 4.40(s, 1H), 3.28(m, 2H), 2.98(m, 3H), 2.15(m, 1H), 2.03-1.74(m, 3H)
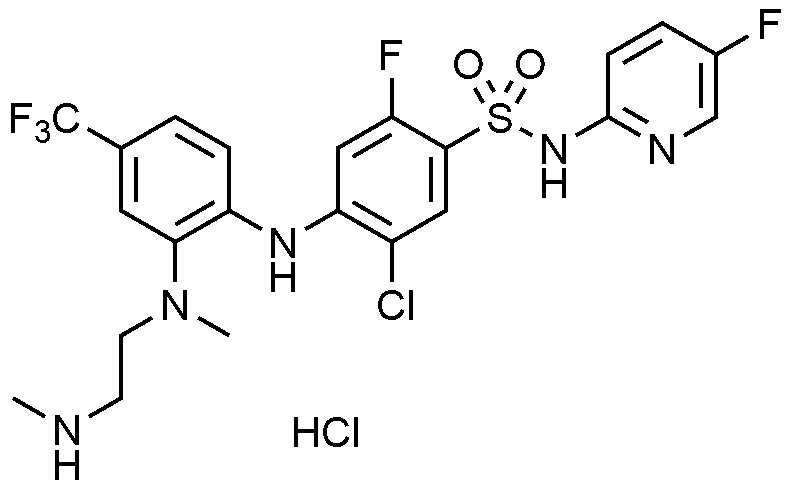
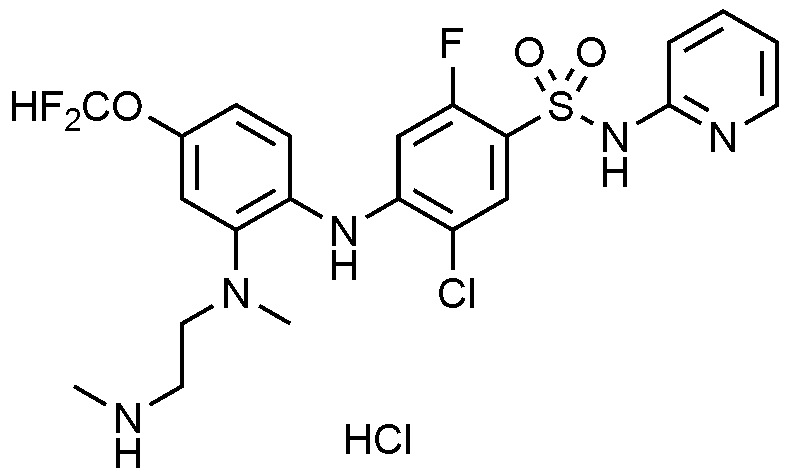
실시예
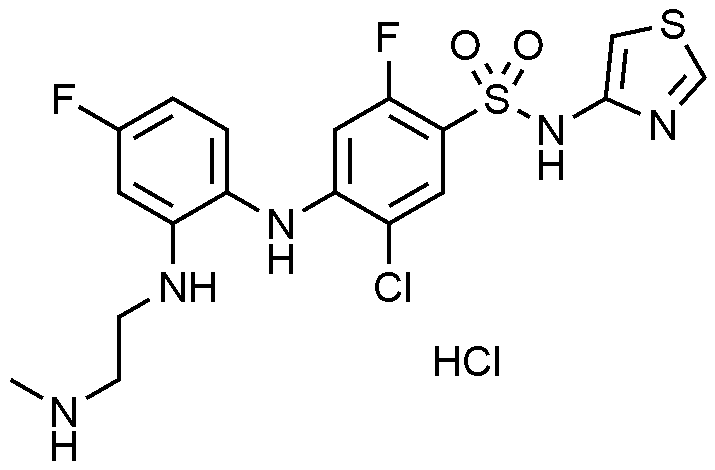
92: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
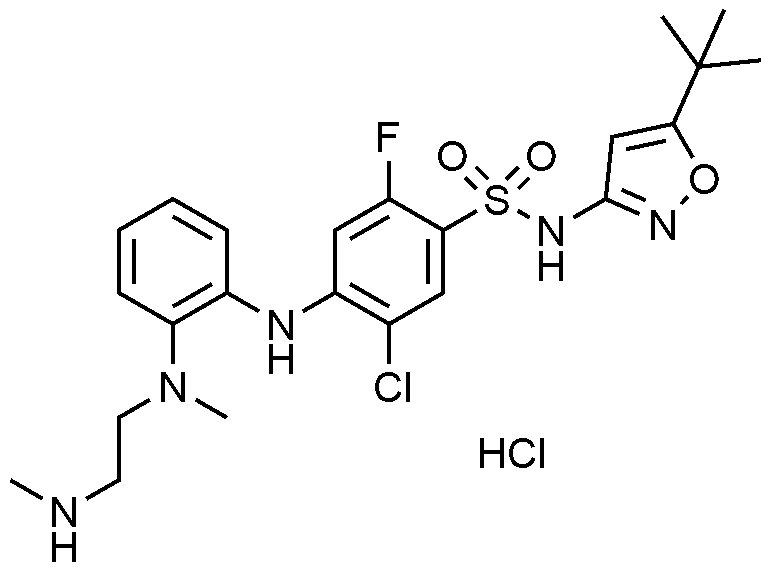
-2-(
메틸(2-(메틸아미노)에
틸)아미노)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
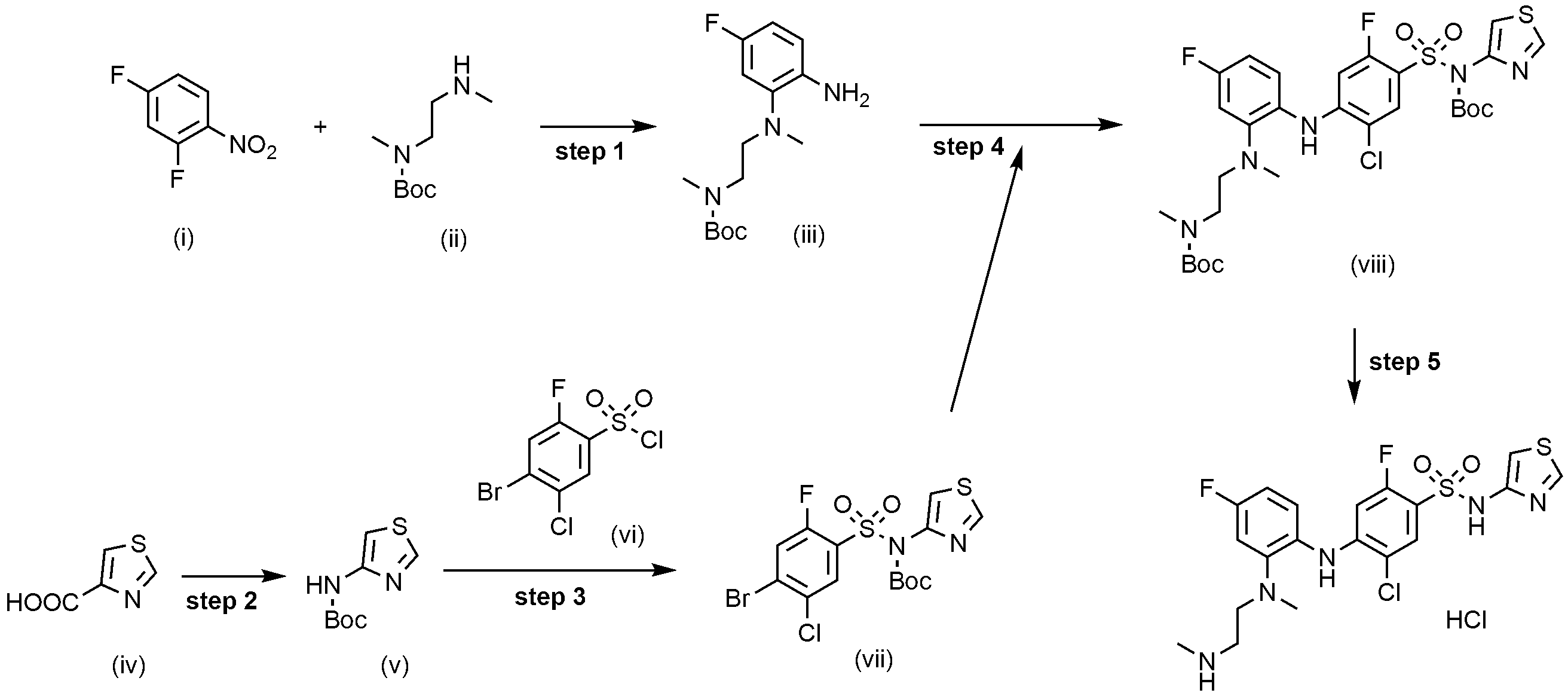
단계 1)
터트
-부틸
(2-((2-아미노-5-플루오로페닐)(메틸)
아미노)에틸)
(메틸)
카바메이트(iii)의 제조
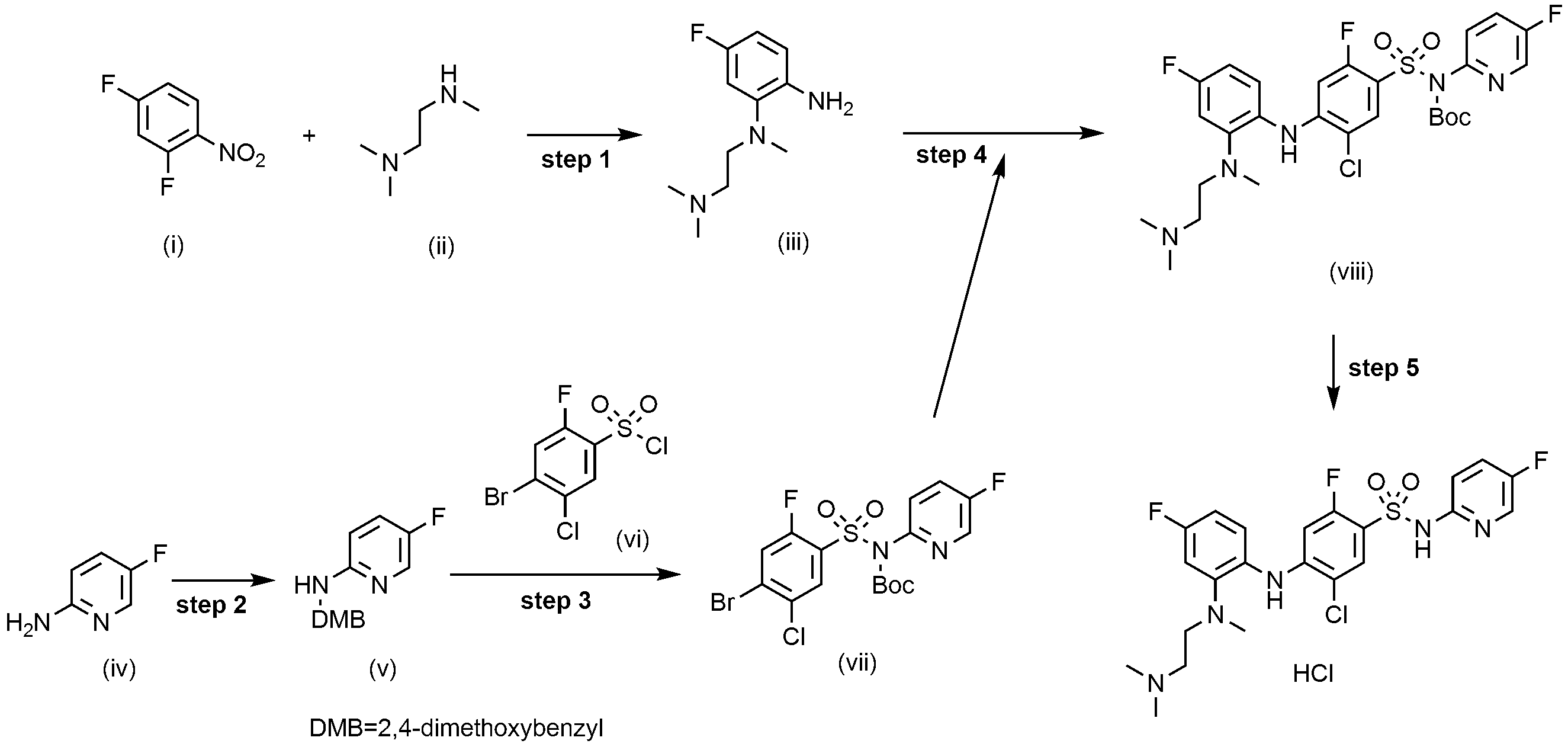
2,4-디플루오로-1-니트로벤젠(i, 2.0 g, 12.6 mmol)과 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii, 2.4 g, 1.0 eq.)을 DMF(20 mL)에 용해한 후 K2CO3(2.6 g, 1.5 eq.)을 넣었다. 내부 온도를 60~70℃로 유지하면서 2시간 교반하고, 반응액이 진한 노란색을 띠게 되면 TLC로 반응 종결을 확인하였다. 실온으로 냉각 후 EA/H2O을 넣고, 교반한 후 층 분리하였다. 분리된 유기층을 MgSO4을 넣고 교반하고, 여과 및 건조하였다. 여과액을 감압 농축한 후 잔사를 MeOH(20 mL)에 용해한 후 Pd/C(0.13 g, 0.1 eq.)를 넣었다. 내부를 수소 가스로 치환하고, 실온에서 6시간 동안 교반한 후 반응액의 노란색이 옅어져 거의 무색이 되면 TLC로 반응 종결을 확인하였다. Celite를 통해 금속 촉매를 여과하였다. 여과액을 감압 농축하여 얻어진 잔사를 column chromatography(Hx/EA = 3/1)로 분리하여 목적 화합물(iii, 2.5 g, 66.9%)을 얻었다.
1H NMR (500 MHz, CDCl3): 6.76(d, 1H), 6.64(m, 2H),3.36(m, 2H), 2.94(m, 2H), 2.86(m, 3H), 2.68(s, 3H), 1.45(s, 9H)
단계 2)
터트
-부틸
싸이아졸
-4-
일카바메이트(v)의
제조
싸이아졸-4-카르복시산(iv, 5.0 g, 38.8 mmol)을 t-BuOH(100 mL)에 용해한 후 TEA(8.1 mL, 1.5 eq.)과 DPPA(7.1 mL, 1.5 eq.)를 넣었다. 내부 온도를 90~100℃로 유지하면서 3일 동안 교반한 후, TLC로 반응 종결을 확인하였다. 반응물을 감압 농축한 후 H2O(50 mL)을 넣고 에틸아세테이트(EA, 100 mL)로 2회 추출하였다. 유기층을 MgSO4을 넣고 교반한 후, 여과 및 건조하였다. 여과액을 감압 농축한 후 잔사를 소량의 EA에 넣고 slurry한 후, 생성된 고체를 여과하여 흰색의 목적 화합물(v, 4.0 g, 51.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.73(s, 1H), 7.24(s, 1H), 1.52(s, 9H)
단계 3)
터트
-부틸
((4-브로모-5-클로로-2-플루오로페닐)
술포닐)
(싸이아졸-
4-일)카바메이트(vii)의 제조
터트-부틸 싸이아졸-4-일카바메이트(v, 4.0 g, 20.0 mmol)를 반응 용기에 담고 질소 가스로 내부를 치환시켰다. 이후 THF(32 mL)에 용해한 후 dry ice-acetone을 이용하여 -78℃로 냉각시켰다. 냉각 후 LiHMDS(22.4 mL, 1.5 eq.)를 천천히 넣어주고 반응물을 30분 동안 교반하였다. 이후 4-브로모-5-클로로-2- 플루오로벤젠술포닐 클로라이드(vi, 6.0 g, 1.0 eq.)를 THF(10 mL)에 용해한 후 반응액에 천천히 넣었다. 반응물을 밤새 교반시키고 TLC로 반응 종결을 확인하였다. H2O(50 mL)을 넣고 Ehtylacetate(EA, 100 mL)로 2회 추출하였다. 유기층에 MgSO4을 넣고 교반하고, 여과 및 건조하였다. 여과액을 감압 농축한 후 잔사를 THF/n-Hexane으로 결정화하여 목적 화합물(vii, 4.4 g, 59.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 9.00(s, 1H), 8.22(d, 1H), 7.90(d, 1H), 7.78(s, 1H), 1.35(s, 9H)
단계 4)
터트
-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(viii)의 제조
터트-부틸 (2-((2-아미노-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(iii, 10.0 g, 33.7 mmol)과 터트-부틸 ((4-브로모-5-클로로-2-플루오로페닐)술포닐)(싸이아졸-4-일)카바메이트(vii, 13.0 g, 1.0 eq.)을 1,4-디옥산(200 mL)에 용해하였다. 상기 반응 용액에 Pd(OAc)2(0.7 g, 0.1 eq), rac-BINAP(4.11 g, 0.2 eq.), Cs2CO3(21.2 g, 2.0 eq.)을 넣었다. 내부 온도를 90~100℃로 유지하면서 5시간 동안 반응시킨 후 TLC로 반응 종결을 확인하였다. H2O(1000 mL)을 넣고 에틸아세테이트(EA, 1000 mL)로 2회 추출하였다. 유기층에 MgSO4을 넣고 교반한 후, 여과 및 건조하였다. 여과액을 감압 농축한 후 잔사를 EA/Hex = 1/4의 이동상으로 Column chromatography 분리하여 목적 화합물(16.0 g, 69.1%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.95(d, 1H), 7.96(d, 1H), 7.68(s, 1H), 7.26(s, 1H), 6.95(t, 1H), 6.8(s, 1H), 6.39(s, 1H), 3.27(s, 2H), 3.14(s, 2H), 2.79(s, 3H), 2.70(d, 3H), 1.40(s, 9H), 1.37(s, 9H)
단계 5) 5-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에틸)
아미노)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(vii, 14.0 g, 20.3 mmol)에 1M HCl in 에틸아세테이트(200 mL)를 넣었다. 50~60℃로 가열하면서 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 얻어진 잔사에 MC(200 mL)를 넣고 1시간 동안 교반시켜 생성된 고체를 여과하여 목적 화합물(9.1 g, 85.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.73(d, 1H), 7.79(d, 1H), 7.26(dd, 1H), 7.03(m, 2H), 6.90(td, 1H), 6.43(d, 1H), 3.26(t, 2H), 3.09(t, 2H), 2.70(s, 3H), 2.65(s, 3H)
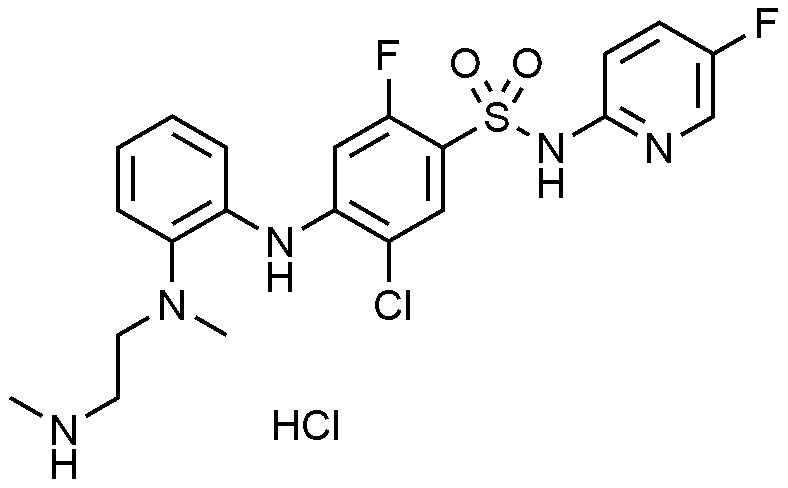
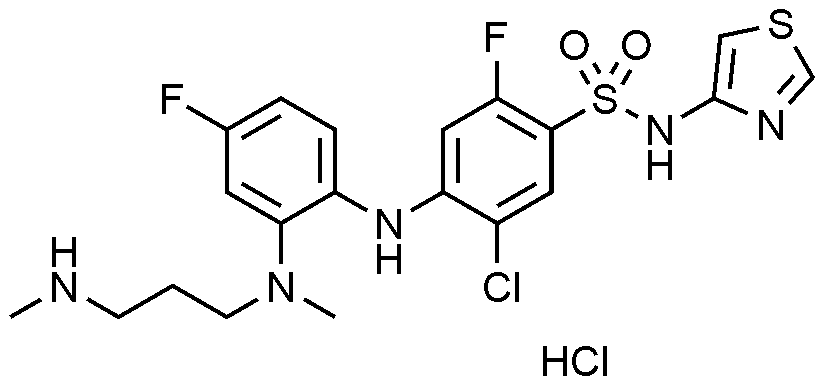
실시예
93: 3
-
클로로
-4-((2-((2-(디메틸아미노)에틸)(
메틸아미노
)-4-
플루오
로페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
상기 실시예 92에서의 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii)를 N,N,N'-트리메틸에탄-1,2-디아민으로, 4-브로모-5-클로로-2-플루오로벤젠술포닐 클로라이드(vi)를 4-브로모-5-클로로벤젠술포닐 클로라이드로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 ((3-클로로-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)페닐)술포닐)(싸이아졸-4-일)카바메이트(0.05 g, 0.09 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 48.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.73(s, 1H), 7.81(s, 1H), 7.54(d, 1H), 7.21(dd, 1H), 7.00(m, 2H), 6.82(dd, 1H), 6.75(d, 1H), 3.20(t, 2H), 2.93(t, 2H), 2.70(s, 3H), 2.55(s, 3H)
실시예
94: 5
-
클로로
-4-((2-((2-(디메틸아미노)에틸)(
메틸
)아미노)-4-
플루오
로페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드의 제조
상기 실시예 92에서의 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii)를 N,N,N'-트리메틸에탄-1,2-디아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 ((5-클로로-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)-2-플루오로페닐)술포닐)(싸이아졸-4-일)카바메이트(0.05 g, 0.08 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 49.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.72(s, 1H), 7.76(d, 1H), 7.2(t, 1H), 6.95(m, 2H), 6.80(t, 1H), 6.38(d, 1H), 3.01(t, 2H), 2.68(s, 3H), 2.40(t, 2H), 2.15(s, 3H)
실시예
95: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)-4-(트리플루오로메틸)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로
라이드의 제조
상기 실시예 92에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-1-니트로-4-(트리플루오로메틸)벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-(트리플루오로메틸)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 55.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.74(s, 1H), 7.88(d, 1H), 7.54(s, 1H), 7.42(m, 2H), 7.06(s, 1H), 7.02(d, 1H), 3.35(t, 2H), 3.16(t, 2H), 2.73(s, 3H), 2.70(s, 3H)
실시예
96: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(5-플루오로피리미딘-2-일)벤젠술폰마이드
하이드로클로
라이드의 제조
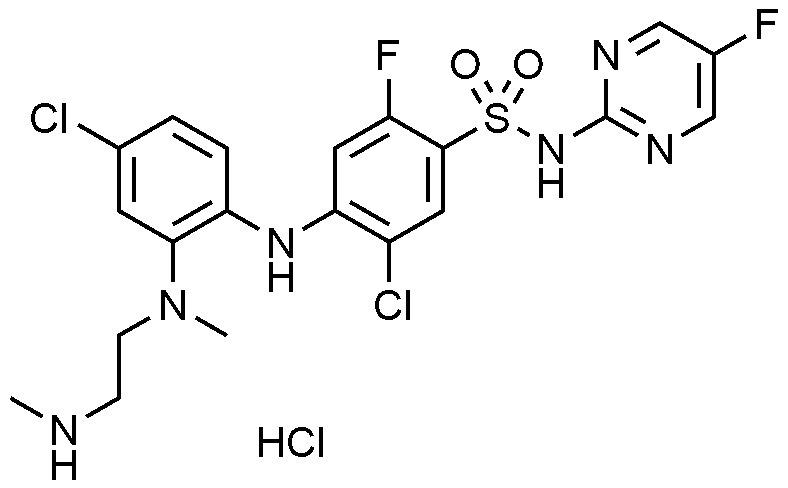
상기 실시예 92의 단계 2 대신 N-(2,4-디메톡시벤질)-5-플루오로피리미딘-2-아민(v)을 제조하였다. 구체적으로, 2-클로로-5-플루오로피리미딘(iv, 0.48 g, 3.62 mmol), (2,4-디메톡시페닐)메탄아민(0.60 g, 1.0 eq.)과 트리메틸아민(0.76 mL, 1.5 eq.)을 EtOH(10 mL)에 용해하였다. 70~80℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 감압 농축하여 얻어진 잔사를 EA/Hex = 1/2의 이동상으로 Column chromatography 분리하여 목적 화합물(v) 0.32 g(수율 34%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.20(s, 2H), 7.13(d, 1H), 6.51(s, 1H), 6.41(d, 1H), 4.44(s, 2H), 3.82(s, 3H), 3.76(s, 3H)
상기 실시예 92에서의 터트-부틸 싸이아졸-4-일카바메이트(v)을 상기 제조한 N-(2,4-디메톡시벤질)-5-플루오로피리미딘-2-아민으로 사용한 것을 제외하고는, 실시예 92의 단계 1, 3, 4 및 5와 동일한 공정을 통해 목적 화합물을 얻었다.
1H NMR (500 MHz, MeOD): 8.43(m, 2H), 7.99(t, 1H), 7.27(dd, 1H), 7.03(d, 1H), 6.88(t, 1H), 6.45(d, 1H), 3.20(t, 2H), 3.10(t, 2H), 2.71(s, 3H), 2.67(s, 3H)
실시예
97: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로피리미딘
-2-일)-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)-4-(트리플루오로메틸)페닐)아미노)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 96에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-1-니트로-4-(트리플루오로메틸)벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리미딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-(트리플루오로메틸)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.47(s, 1H), 8.29(s, 1H), 8.05(m, 1H), 7.53(d, 1H), 7.41(m, 2H), 7.01(t, 1h), 3.45(t, 2H), 3.16(t, 2H), 2.74(s, 3H), 2.69(s, 3H)
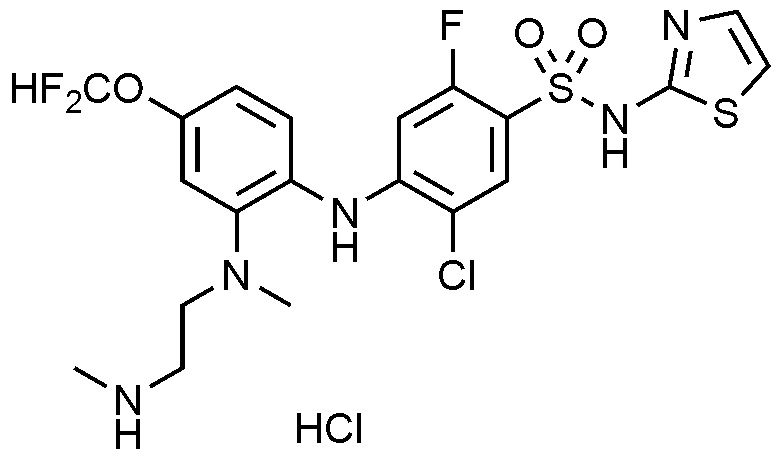
실시예
98: 5
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 92에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-(디플루오로메톡시)-2-플루오로-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-(디플루오로메톡시)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 55.7%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.73(s, 1H), 7.80(d, 1H), 7.29(d, 1H), 7.02(s, 2H), 6.94(d, 1H), 6.85(t, 1H), 6.55(d, 1H), 3.25(t, 2H), 3.10(t, 2H), 2.70(s, 3H), 2.66(s, 3H)
실시예
99: 5
-
클로로
-4-((4-
시아노
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 92에서의 2,4-디플루오로-1-니트로벤젠(i)을 3-플루오로-4-니트로벤조니트릴로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-시아노페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.1%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.75(s, 1H), 7.91(d, 1H), 7.62(d, 1H), 7.47(t, 1H), 7.32(d, 1H), 7.17(d, 1H), 7.07(d, 1H), 3.28(t, 2H), 3.17(t, 2H), 2.71(s, 3H), 2.70(s, 3H)
실시예
100: 5
-
클로로
-4-((4-
시아노
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(5-플루오로피리미딘-2-일)벤젠술폰아미드
하이드로클로
라이드의 제조
상기 실시예 96에서의 2,4-디플루오로-1-니트로벤젠(i)을 3-플루오로-4-니트로벤조니트릴로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리미딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-시아노페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.7%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.43(s, 2H), 8.10(d, 1H), 7.63(s, 1H), 7.48(d, 1H), 7.36(d, 1H), 7.17(d, 1H), 3.34-3.32(m, 2H), 3.19-3.16(m, 2H), 2.72(s, 3H), 2.71(s, 3H)
실시예
101: 5
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(5-플루오로피리미딘-2-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 96에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-(디플루오로메톡시)-2-플루오로-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리미딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-(디플루오로메톡시)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.42(s, 2H), 8.01(d, 1H), 7.33-7.17(m, 3H), 6.71(d, 1H), 3.35-3.32(m, 2H), 3.13-3.10(m, 2H), 2.68(s, 3H), 2.67(s, 3H)
실시예
102: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로피리미딘
-2-일)-4-((2-(
메
틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 96에서의 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리미딘-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 60.7%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.42(s, 2H), 8.00(d, 1H), 7.30(d, 1H), 7.03(d, 1H), 6.94(d, 1H), 6.69(s, 1H), 6.52(d, 1H), 3.34-3.32(m, 2H), 3.12-3.10(m, 2H), 2.70(s, 3H), 2.67(s, 3H)
실시예
103: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(5-플루오로피리딘-2-일)벤젠술폰아미드
하이드로클로라
이드의 제조
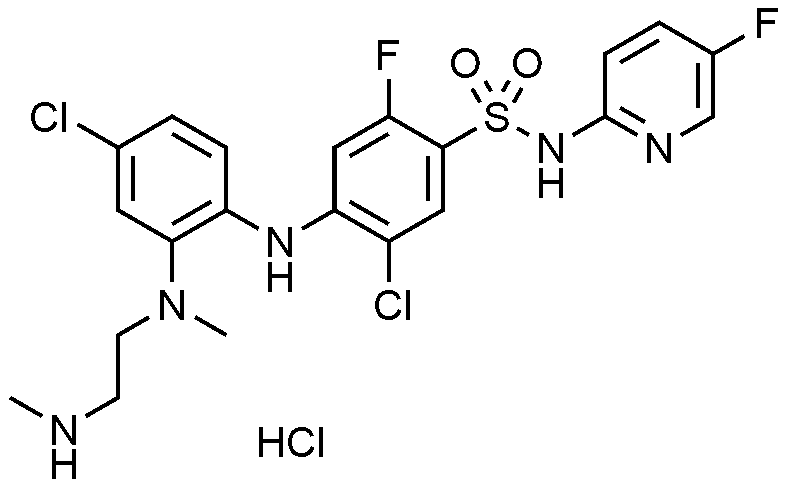
상기 실시예 92의 단계 2 대신 N-(2,4-디메톡시벤질)-5-플루오로피리딘-2-아민(v)을 제조하였다. 구체적으로, 5-플루오로피리딘-2-아민(iv, 0.55 g, 0.01 mmol)과 2,4-디메톡시벤즈알데하이드(0.45 g, 0.9 eq.)를 DCM(10 mL)에 용해시켰다. 1시간 동안 실온 교반시킨 후, 15분 간격으로 소디움 트리아세톡시보로하이드라이드(1.0 g, 1 eq.)를 세 번 첨가하였다. 밤새 교반시킨 후, TLC로 반응 종결을 확인하였다. H2O(10 mL)를 넣고 디클로로메탄(10 mL)으로 2번 추출하였다. 유기층에 MgSO4을 넣고 교반, 여과 건조하였다. 여과액을 감압 농축한 후 얻어진 잔사를 EA/Hex = 1/4의 이동상으로 Column chromatography 분리하여 N-(2,4-디메톡시벤질)-5-플루오로피리딘-2-아민(v) 0.65 g(수율 51%)을 얻었다.
1H NMR (500 MHz, CDCl3): 7.90(d, 1H), 7.16(m, 2H), 6.46(d, 1H), 6.41(d, 1H), 6.34(m, 1H), 4.36(s, 2H), 3.81(s, 3H), 3.77(s, 3H)
상기 실시예 92에서의 터트-부틸 싸이아졸-4-일카바메이트(v)을 상기 제조한 N-(2,4-디메톡시벤질)-5-플루오로피리딘-2-아민으로 사용한 것을 제외하고는, 실시예 92의 단계 1, 3, 4 및 5와 동일한 공정을 통해 목적 화합물을 얻었다.
1H NMR (500 MHz, MeOD): 8.05(d, 1H), 7.89(d, 1H), 7.51(d, 1H), 7.26-6.87(m, 4H), 6.42(d, 1H), 3.38-3.25(m, 2H), 3.10-3.09(m, 2H), 2.69(s, 3H), 2.65(s, 3H)
실시예
104: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에
틸)아미노)페닐)아미노)-N-(피리딘-2-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 피리딘-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((5-클로로-2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(피리딘-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 60.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.01-7.92(m, 2H), 7.29-7.24(m, 3H), 7.03(d, 2H), 6.87(d, 1H), 6.46(d, 1H), 3.42-3.40(m, 2H), 3.11-3.08(m, 2H), 2.70(s, 3H), 2.66(s, 3H)
실시예
105: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에
틸)아미노)페닐)아미노)-N-(싸이아졸-2-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((5-클로로-2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.84(d, 2H), 7.28-7.04(m, 3H), 6.89(d, 1H), 6.74(d, 1H), 6.46(d, 1H), 3.26-3.24(m, 2H), 3.11-3.08(m, 2H), 2.71(s, 3H), 2.66(s, 3H)
실시예
106: 5
-
클로로
-4-((4-
시아노
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(5-플루오로피리딘-2-일)벤젠술폰아미드
하이드로클로라
이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 3-플루오로-4-니트로벤조니트릴로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-시아노페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.05-8.01(m, 2H), 7.62(s, 1H), 7.55-7.46(m, 2H), 7.33(d, 1H), 7.14(d, 1H), 3.34-3.32(m, 2H), 3.18-3.17(m, 2H), 2.72(s, 3H), 2.71(s, 3H)
실시예
107: 5
-
클로로
-4-((4-
시아노
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(피리딘-2-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 3-플루오로-4-니트로벤조니트릴로, 5-플루오로피리딘-2-아민(iv)을 피리딘-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(피리딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-시아노페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 57.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.05(d, 1H), 7.97-7.86(s, 2H), 7.62(s, 1H), 7.46(d, 1H), 7.33-7.19(m, 3H), 7.01-6.97(m, 1H), 3.32-3.31(m, 2H), 3.19-3.16(m, 2H), 2.72(s, 3H), 2.71(s, 3H)
실시예
108: 5
-
클로로
-4-((4-
시아노
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(싸이아졸-2-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 3-플루오로-4-니트로벤조니트릴로, 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)-5-시아노페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 60.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.96(d, 1H), 7.62(s, 1H), 7.46(d, 1H), 7.28-7.14(m, 3H), 6.77(d, 1H), 3.32-3.30(m, 2H), 3.20-3.17(m, 2H), 2.72(s, 3H), 2.71(s, 3H)
실시예
109: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로피리딘
-2-일)-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)-4-(트리플루오로메틸)페닐)아미노)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-1-니트로-4-(트리플루오로메틸)벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-(트리플루오로메틸)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.05(d, 1H), 7.99(d, 1H), 7.53(m, 2H), 7.43(s, 2H), 7.17(m, 1H), 7.02(d, 1H), 3.47(t, 2H), 3.17(t, 2H), 2.74(s, 3H), 2.70(s, 3H)
실시예
110: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)-4-(트리플루오로메틸)페닐)아미노)-N-(피리딘-2-일)벤젠술폰아미드
하이드로클로라
이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-1-니트로-4-(트리플루오로메틸)벤젠으로, 5-플루오로피리딘-2-아민(iv)을 피리딘-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(피리딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-(트리플루오로메틸)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.02(d, 1H), 7.98(t, 1H), 7.86(t 1H), 7.53(s, 1H), 7.40(m, 2H), 7.31(d, 1H), 7.05(d, 1H), 6.99(m, 1H), 3.34(t, 2H), 3.17(t, 2H), 2.74(s, 3H), 2.71(s, 3H)
실시예
111: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)-4-(트리플루오로메틸)페닐)아미노)-N-(싸이아졸-2-일)벤젠술폰아미드
하이드로클로
라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-1-니트로-4-(트리플루오로메틸)벤젠으로, 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)-5-(트리플루오로메틸)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.6%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.93(d, 1H), 7.53(s, 1H), 7.41(m , 2H), 7.13(d, 1H), 7.07(d, 1H), 6.77(d, 1H), 3.34(t, 2H), 3.18(t, 2H), 2.75(s, 3H), 2.71(s, 3H)
실시예
112: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로피리딘
-2-일)-4-((2-(
메
틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리딘-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 61.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.06(d, 1H), 7.91(d, 1H), 7.51(m, 1H), 7.30(m, 2H), 7.22(t, 1H), 7.15(m, 2H), 6.70(d, 1H), 3.26(t, 2H), 3.11(t, 2H), 2.67(s, 6H)
실시예
113: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(피리딘-2-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로, 5-플루오로피리딘-2-아민(iv)을 피리딘-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(피리딘-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 61.6%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.03(d, 1H), 7.96(d, 1H), 7.90(d, 1H), 7.30(t, 3H), 7.23(t, 1H), 7.17(t, 1H), 7.04(m, 1H), 6.73(d, 1H), 3.26(t, 2H), 3.12(t, 2H), 2.68(s, 3H), 2.67(s, 3H)
실시예
114: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(싸이아졸-2-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로, 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 61.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.86(d, 1H), 7.30(m, 2H), 7.20( m, 2H), 7.12(d, 1H), 6.75(m, 2H), 3.26(t, 2H), 3.12(t, 2H), 2.70(s, 3H), 2.68(s, 3H)
실시예
115: 5
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(5-플루오로피리딘-2-일)벤젠술폰아미드
하
이드로클로라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-(디플루오로메톡시)-2-플루오로-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-(디플루오로메톡시)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.06(d, 1H), 7.90(d, 1H), 7.52(m, 1H), 7.29(d, 1H), 7.16(m, 1H), 7.02(d, 1H), 6.94(m, 1H), 6.84(t, 1H), 6.53(d, 1H), 3.26(t, 2H), 3.10(t, 2H), 2.70(s, 3H), 2.66(s, 3H)
실시예
116: 5
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(싸이아졸-2-일)벤젠술폰아미드
하이드로클
로라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-(디플루오로메톡시)-2-플루오로-1-니트로벤젠으로, 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)-5-(디플루오로메톡시)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.7%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.85(d, 1H), 7.29(d, 1H), 7.11(d, 1H), 7.03(d, 1H), 6.94(d, 1H), 6.85(t, 1H), 6.75(d, 1H), 6.58(d, 1H), 3.23(t, 2H), 3.12(t, 2H), 2.72(s, 3H), 2.67(s, 3H)
실시예
117: 5
-
클로로
-4-((4-(
디플루오로메톡시
)-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(피리딘-2-일)벤젠술폰아미드
하이드로클로
라이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-(디플루오로메톡시)-2-플루오로-1-니트로벤젠으로, 5-플루오로피리딘-2-아민(iv)을 피리딘-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(피리딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-(디플루오로메톡시)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.04(d, 1H), 7.95(d, 1H), 7.90(t, 1H), 7.30(m, 2H), 7.06(m, 2H), 6.93(d, 1H), 6.84(t, 1H), 6.56(d, 1H), 3.26(t, 2H), 3.11(t, 2H), 2.70(s, 3H), 2.67(s, 3H)
실시예
118: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로피리딘
-2-일)-4-((4-
메톡시
-2-(메틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이
드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-4-메톡시-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-메톡시페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.05(d, 1H), 7.86(d, 1H), 7.53-7.50(m, 1H), 7.18-7.14(m, 2H), 6.80-6.73(m, 2H), 6.35(d, 1H), 3.82(s, 3H), 3.25-3.23(m, 2H), 3.09-3.07(m, 2H), 2.67(s, 3H), 2.64(s, 3H)
실시예
119: 5
-
클로로
-2-
플루오로
-4-((4-
메톡시
-2-(
메틸(2-(메틸아미노)에
틸)아미노)페닐)아미노)-N-(싸이아졸-2-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-4-메톡시-1-니트로벤젠으로, 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)-5-메톡시페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 60.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.81(d, 1H), 7.20(d, 1H), 7.11(d, 1H), 6.81-6.73(m, 3H), 6.40(d, 1H), 3.82(s, 3H), 3.30-3.28(m, 2H), 3.25-3.24(m, 2H), 2.69(s, 3H), 2.66(s, 3H)
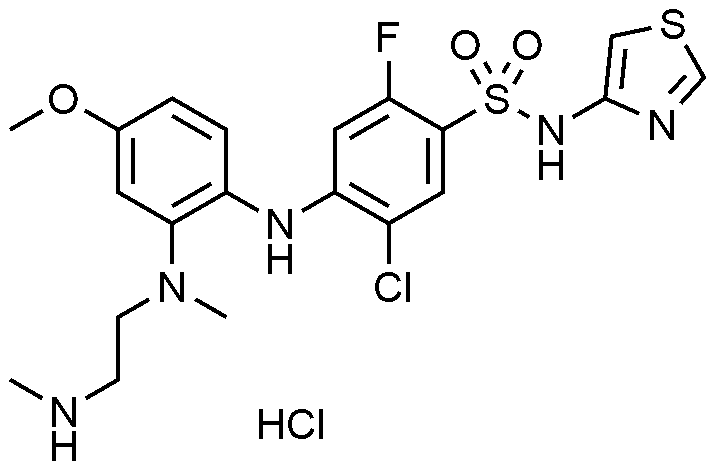
실시예 120: 5 - 클로로 -2- 플루오로 -4-((4- 메톡시 -2-( 메틸(2-(메틸아미노)에틸)아미노 )페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 92에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-4-메톡시-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-메톡시페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 55.5 %)을 얻었다.
1H NMR (500 MHz, MeOD): 8.73(d, 1H), 7.76(d, 1H), 7.18(d, 1H), 7.02(d, 1H), 6.82(d, 1H), 6.75(d, 1H), 6.36(d, 1H), 3.85(s, 3H), 3.26-3.24(m, 2H), 3.09-3.07(m, 2H), 2.69(s, 3H), 2.64(s, 3H)
실시예
121: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 92에서의 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 57.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.74(d, 1H), 7.81(d, 1H), 7.33-7.18 (m, 4H), 7.04(d, 1H), 6.70(d, 1H), 3.26-3.24(m, 2H), 3.12-3.09(m, 2H), 2.69(s, 3H), 2.66(s, 3H)
실시예
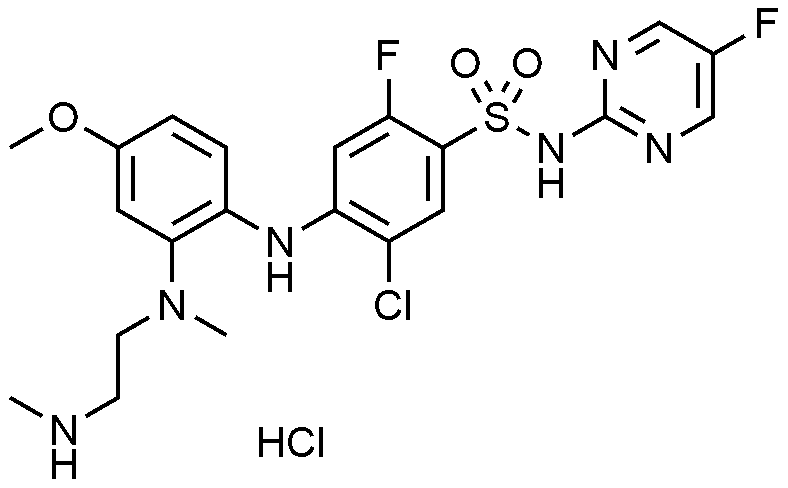
122: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로피리미딘
-2-일)-4-((4-
메톡시
-2-(메틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 96에서의 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-4-메톡시-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리미딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-메톡시페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.42(s, 2H), 7.96(d, 1H), 7.18 (d, 1H), 6.82(d, 1H), 6.76(d, 1H), 6.36(d, 1H), 3.81(s, 3H), 3.27-3.25(m, 2H), 3.17-3.08(m, 2H), 2.70(s, 3H), 2.65(s, 3H)
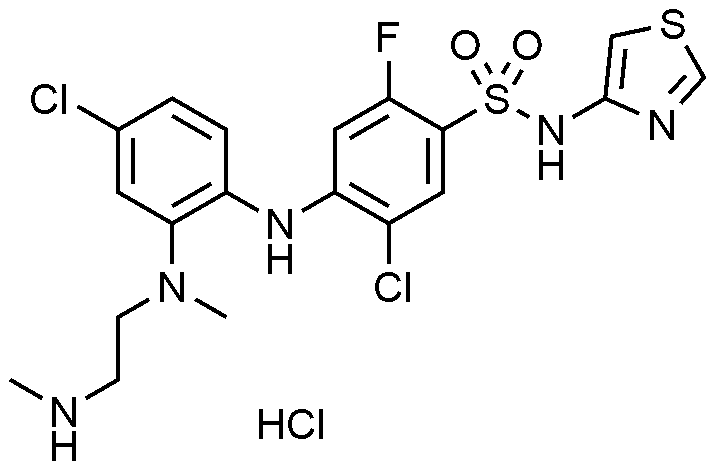
실시예
123: 5
-
클로로
-4-((4-
클로로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 92에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-클로로-2-플루오로-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-클로로페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 55.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.74(s, 1H), 7.81(d, 1H), 7.31-7.14 (m, 3H), 7.04(d, 1H), 6.64(d, 1H), 3.26-3.24(m, 2H), 3.11-3.10(m, 2H), 2.69(s, 3H), 2.66(s, 3H)
실시예
124: 5
-
클로로
-4-((4-
클로로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(5-플루오로피리미딘-2-일)벤젠술폰아미드
하이드로클로
라이드의 제조
상기 실시예 96에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-클로로-2-플루오로-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((5-클로로-2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리미딘-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.42(s, 2H), 8.01(d, 1H), 7.27(d, 2H), 7.15-7.13(m, 1H), 6.64(d, 1H), 3.27-3.25(m, 2H), 3.13-3.11(m, 2H), 2.70(s, 3H), 2.67(s, 3H)
실시예
125: 5
-
클로로
-4-((4-
클로로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(5-플루오로피리딘-2-일)벤젠술폰아미드
하이드로클로라
이드의 제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-클로로-2-플루오로-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((5-클로로-2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리딘-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.06(d, 1H), 7.91(d, 1H), 7.54-7.50(m, 2H), 7.27-7.13(m, 4H), 6.63(d, 1H), 3.27-3.25(m, 2H), 3.11-3.09(m, 2H), 2.69(s, 3H), 2.66(s, 3H)
실시예
126: 5
-
클로로
-4-((4-
클로로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-2-플루오로-N-(싸이아졸-2-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 2,4-디플루오로-1-니트로벤젠(i)을 4-클로로-2-플루오로-1-니트로벤젠으로, 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((5-클로로-2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.87(d, 1H), 7.27(d, 2H), 7.15-7.12(m, 2H), 6.75-6.68(m, 2H), 3.26-3.25(m, 2H), 3.13-3.10(m, 2H), 2.71(s, 3H), 2.68(s, 3H)
실시예
127: 5
-
클로로
-N-(5-
클로로싸이아졸
-2-일)-2-
플루오로
-4-((4-
플루오로
-2-(메틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로
라이드의 제조
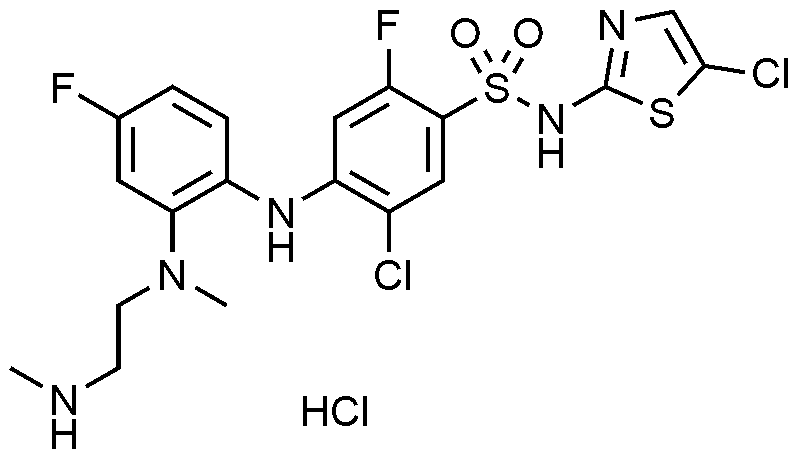
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 5-클로로싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(5-클로로싸이아졸-2-일)-N-(2,4-디메톡시벤질)술파모일)-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.82(d, 1H), 7.29(d, 1H), 7.27(s, 1H), 7.05(d, 1H), 6.90(t, 1H), 6.48(d, 1H), 3.27-3.25(m, 2H), 3.12-3.09(m, 2H), 2.71(s, 3H), 2.67(s, 3H)
실시예
128: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(5-플루오로싸이아졸-2-일)벤젠술폰아미드
하이드로클로
라이드의 제조
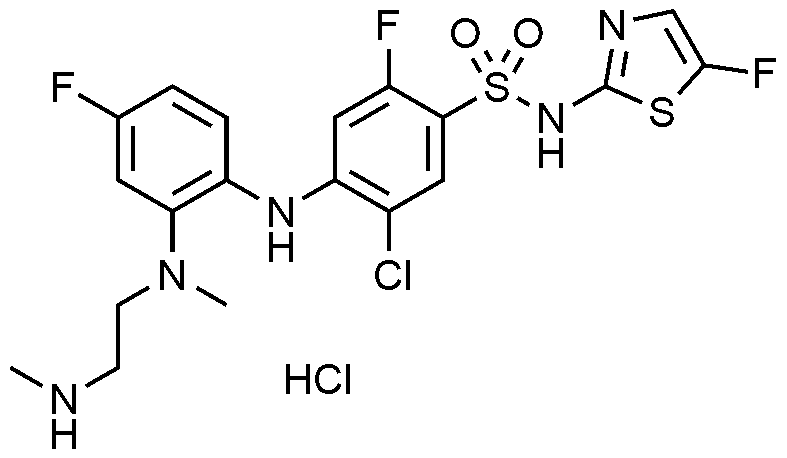
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 5-플루오로싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.82(t, 1H), 7.30(t, 1H), 7.05-6.91(m, 3H), 6.48(d, 1H), 3.27-3.25(m, 2H), 3.12-3.10(m, 2H), 2.72(s, 3H), 2.67(s, 3H)
실시예
129: 5
-
클로로
-N-(5-
클로로싸이아졸
-2-일)-2-
플루오로
-4-((2-(
메
틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 5-클로로싸이아졸-2-아민으로, 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(5-클로로싸이아졸-2-일)-N-(2,4-디메톡시벤질)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.84(d, 1H), 7.33(d, 1H), 7.40(d, 1H), 7.19(m, 3H), 6.75(d, 1H), 3.26(t, 2H), 3.13(t, 2H), 2.70(s, 3H), 2.69(s, 3H)
실시예
130: 5
-
클로로
-N-(5-
클로로싸이아졸
-2-일)-2-
플루오로
-4-((4-
메톡시
-2-(메틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이
드의 제조
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 5-클로로싸이아졸-2-아민으로, 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-4-메톡시-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(5-클로로싸이아졸-2-일)-N-(2,4-디메톡시벤질)술파모일)-5-플루오로페닐)아미노)-5-메톡시페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 58.7%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.79(d, 1H), 7.20(d, 1H), 7.19(s, 1H), 6.80(d, 1H), 6.75(dd, 1H), 6.41(d, 1H), 3.82(s, 3H), 3.26(t, 2H), 3.10(t, 2H), 2.70(s, 3H), 2.68(s, 3H)
실시예
131: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로싸이아졸
-2-일)-4-((2-(
메
틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 5-플루오로싸이아졸-2-아민으로, 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 60.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.84(d, 1H), 7.31(m, 2H), 7.22(m, 2H), 7.00(s, 1H), 6.76(d, 1H), 3.27(t, 2H), 3.13(t, 2H), 2.70(s, 3H), 2.69(s, 3H)
실시예
132: 5
-
클로로
-2-
플루오로
-N-(5-
플루오로싸이아졸
-2-일)-4-((4-
메톡시
-2-(메틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로
라이드의 제조
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 5-플루오로싸이아졸-2-아민으로, 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-4-메톡시-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)-5-메톡시페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.79(t, 1H), 7.22(t, 1H), 6.99(s, 1H), 6.86(d, 1H), 6.78(dd, 1H), 6.40(d, 1H), 3.83(s, 3H), 3.34(t, 2H), 3.11(t, 2H), 2.75(s, 3H), 2.67(s, 3H)
실시예
133: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸
(2-(
메틸아미노
)에틸)아미노)페닐)아미노)-N-(5-메틸아이소옥사졸-3-일)벤젠술폰아미드
하이드로클
로라이드의 제조
상기 실시예 92의 단계 2 및 3 대신 터트-부틸 ((4-브로모-5-클로로-2-플루오로페닐)술포닐)(5-메틸이소옥사졸-3-일)카바메이트(vii)을 제조하였다. 구체적으로, 5-메틸이소옥사졸-3-아민(iv, 1.00 g, 10.19 mmol), (4-브로모-5-클로로-2-플루오로벤젠술포닐 클로라이드(vi, 3.14 g, 1.0 eq.)과 피리딘(2.4 mL, 3.0 eq.)을 DCM(25 mL)에 용해하였다. 실온에서 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응물에 H2O(30 mL)을 넣고 에틸아세테이트로 2회 추출하였다. 유기층에 MgSO4를 넣고 교반, 여과 건조하였다. 감압 농축하여 얻어진 잔사를 EA/Hex = 1/1의 이동상으로 Column chromatography 분리하여 목적 화합물(v) 1.0g (수율 27%)을 얻었다.
1H NMR (500 MHz, CDCl3): 8.66(d, 1H), 7.96(d, 1H), 7.44(d, 1H), 5.88(broad, 1H), 2.33(s, 3H)
상기 제조한 4-브로모-5-클로로-2-플루오로-N-(5-메틸이소옥사졸-3-일)벤젠술폰아미드(v, 1.00 g, 2.71 mmol), N,N-디메틸아미노피리딘(0.06 g, 0.2 eq.)과 디-터트-부틸 디카보네이트(1.1 mL, 2.0 eq.)을 테트라하이드로퓨란(20 mL)에 용해하였다. 실온에서 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응물에 H2O(30 mL)을 넣고 에틸아세테이트로 2회 추출하였다. 유기층에 MgSO4를 넣고 교반한 후, 여과 및 건조하였다. 감압 농축하여 얻어진 잔사를 EA/Hex = 1/2의 이동상으로 Column chromatography 분리하여 목적 화합물(vii) 0.40 g(수율 31%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.19(d, 1H), 7.93(d, 1H), 6.34(s, 1H), 2.49(s, 3H), 1.36(s, 9H)
상기 제조한 터트-부틸 ((4-브로모-5-클로로-2-플루오로페닐)술포닐)(5-메틸이소옥사졸-3-일)카바메이트(vii)를 사용하는 것을 제외하고는, 실시예 1의 단계 1, 4 및 5와 동일한 공정을 통해 목적 화합물을 얻었다.
1H NMR (500 MHz, MeOD): 7.8(d, 1H), 7.34-7.31(m, 2H), 7.25(t, 1H), 7.21-7.19(m, 1H), 6.71(d, 1H), 6.07(s, 1H), 2.70(s, 3H), 2.67(s, 3H), 2.32(s, 3H)
실시예
134: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(5-메틸이소옥사졸-3-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 133에서의 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(5-메틸이소옥사졸-3-일)술파모일)-2-클로로-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 65.6%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.79(d, 1H), 7.21(t, 1H), 7.00(d, 1H), 6.98(t, 1H), 6.41(d, 1H), 5.85(s, 1H), 3.24-3.23(m, 2H), 3.05-3.03(m, 2H), 2.69(s, 3H), 2.58(s, 3H), 2.22(s, 3H)
실시예
135: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(5-메틸-1H-피라졸-3-일)벤젠술폰아미드
하이드로클로라
이드의 제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 터트-부틸 3-아미노-5-메틸-1H-피라졸-1-카복실레이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 3-((N-(터트-부톡시카보닐)-4-((2-((2-((터트-부톡시카보닐)(메틸)아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)-5-클로로-2-플루오로페닐)술폰아미도)-5-메틸-1H-피라졸-1-카복실레이트 (0.05g, 0.07mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 64.7%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.86(1H), 7.27(t, 1H), 7.06(d, 1H), 6.89(t, 1H), 6.47(d, 1H), 6.08(d, 1H), 3.15-3.12(m, 2H), 2.71(s, 3H), 2.67(s, 3H), 2.34(s, 3H)
실시예
136: 5
-
클로로
-2-
플루오로
-4-((2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(5-메틸-1H-피라졸-3-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 터트-부틸 3-아미노-5-메틸-1H-피라졸-1-카복실레이트로, 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 3-((N-(터트-부톡시카보닐)-4-((2-((2-((터트-부톡시카보닐)(메틸)아미노)에틸)(메틸)아미노)페닐)아미노)-5-클로로-2-플루오로페닐)술폰아미도)-5-메틸-1H-피라졸-1-카복실레이트 (0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 65.7%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.88(d, 1H), 7.35-7.21(m, 4H), 6.72(d, 1H), 6.08(s, 1H), 3.35-3.33(m, 2H), 3.14-3.11(m, 2H), 2.72(s, 3H), 2.68(s, 3H), 2.34(s, 3H)
실시예
137: 5
-
클로로
-4-((2-((2-(디메틸아미노)에틸)(
메틸
)아미노)-4-
플루오로페닐
)아미노)-2-플루오로-N-(5-플루오로피리딘-2-일)벤젠술폰아미드
하이드로
클로라이드의 제조
상기 실시예 103에서 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii)를 N,N,N'-트리메틸에탄-1,2-디아민으로 사용하는 것을 제외하고는, 실시예 103와 동일한 방법으로 중간체(viii)를 제조하였다. 얻어진 중간체 5-클로로-N-(2,4-디메톡시벤질)-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)-2-플루오로-N-(5-플루오로피리딘-2-일)벤젠술폰아미드(viii, 0.05 g, 0.08 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 48.3%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.06(d, 1H), 7.88(d, 1H), 7.53(m, 1H), 7.25(dd, 1H), 7.16(dd, 1H), 7.04(m, 1H), 6.88(m, 1H), 6.35(d, 1H), 3.33(t, 2H), 3.20(t, 2H), 2.92(s, 6H), 2.71(s, 3H)
실시예
138: 5
-
클로로
-4-((2-((2-(디메틸아미노)에틸)(
메틸
)아미노)-4-
플루오로페닐
)아미노)-2-플루오로-N-(싸이아졸-2-일)벤젠술폰아미드
하이드로클로라이
드의 제조
상기 실시예 137에서의 5-플루오로피리딘-2-아민(iv)을 싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 5-클로로-N-(2,4-디메톡시벤질)-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)-2-플루오로-N-(싸이아졸-2-일)벤젠술폰아미드(0.05 g, 0.08 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 48.4%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.83(d, 1H), 7.27(m, 1H), 7.12(t, 1H), 7.04(m, 1H), 6.90(t, 1H), 6.75(d, 1H), 6.40(d, 1H), 3.34(t, 2H), 3.22(t, 2H), 2.83(s, 6H), 2.73(s, 3H)
실시예
139: 5
-
클로로
-N-(5-
클로로싸이아졸
-2-일)-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)-2-플루오로벤젠술폰아미드
하이드로클
로라이드의 제조
상기 실시예 137에서의 5-플루오로피리딘-2-아민(iv)을 5-클로로싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 5-클로로-N-(5-클로로싸이아졸-2-일)-N-(2,4-디메톡시벤질)-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)-2-플루오로벤젠술폰아미드(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 47.9%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.82(d, 1H), 7.28(t, 1H), 7.19(d, 1H), 7.05(d, 1H), 6.89(t, 1H), 6.41(d, 1H), 3.30(t, 2H), 3.23(t, 2H), 2.84(s, 6H), 2.74(s, 3H)
실시예
140: 5
-
클로로
-N-(5-
클로로싸이아졸
-2-일)-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)-4-플루오로페닐)아미노)-2-플루오로벤젠술폰아미드
하이드로클
로라이드의 제조
상기 실시예 137에서의 5-플루오로피리딘-2-아민(iv)을 5-클로로싸이아졸-2-아민으로, 2,4-디플루오로-1-니트로벤젠(i)을 2-플루오로-1-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 5-클로로-N-(5-클로로싸이아졸-2-일)-N-(2,4-디메톡시벤질)-4-((2-((2-(디메틸아미노)에틸)(메틸)아미노)페닐)아미노)-2-플루오로벤젠술폰아미드 (0.05g, 0.07mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 48.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.84(d, 1H), 7.31(t, 2H), 7.25(t, 1H), 7.20(t, 2H), 6.40(d, 1H), 3.36(t, 2H), 3.24(t, 2H), 2.86(s, 6H), 2.72(s, 3H)
실시예
141: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(5-메틸싸이아졸-2-일)벤젠술폰아미드
하이드로클로라이
드의 제조
상기 실시예 103에서의 5-플루오로피리딘-2-아민(iv)을 5-메틸싸이아졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-메틸싸이아졸-2-일)술파모일)-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 53.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.83(d, 1H), 7.29(dd, 1H), 7.05(dd, 1H), 6.89(t, 1H), 6.82(s, 1H), 6.47(d, 1H), 3.27(t, 2H), 2.11(t, 2H), 2.72(s, 3H), 2.67(s, 3H), 2.24(s, 3H)
실시예
142: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(2-(메틸아미노)에틸)아미노
)페닐)아미노)-N-(옥사졸-2-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 옥사졸-2-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(옥사졸-2-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.03 g, 0.05 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.01 g, 47.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 1H NMR (500 MHz, MeOD): 7.87(d, 1H), 7.25-7.22(m, 2H), 7.01 (d, 1H), 6.85-6.84(m, 1H), 6.42(d, 1H), 5.48(s, 1H), 3.25-3.24(m, 2H), 3.09-3.07(m, 2H), 2.71(s, 3H), 2.61(s, 3H)
실시예
143: N-(5-(
터트
-부틸)
이소옥사졸
-3-일)-5-
클로로
-2-
플루오로
-4-((4-플루오로-2-(메틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드
로클로라이드의 제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 5-(터트-부틸)이소옥사졸-3-아민으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(5-(터트-부틸)이소옥사졸-3-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.03 g, 0.04 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.01 g, 46.4%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.78(d, 1H), 7.19-7.16(m, 1H), 6.97(d, 1H), 6.82-6.79(m, 1H), 6.42(d, 1H), 5.87(s, 1H), 3.30-3.29(m, 2H), 2.67(s, 3H), 2.64(s, 3H), 1.23(s, 9H)
실시예
144: N-(5-(
터트
-부틸)
이소옥사졸
-3-일)-5-
클로로
-2-
플루오로
-4-((2-(메틸(2-(메틸아미노)에틸)아미노)페닐)아미노)벤젠술폰아미드
하이드로클로라이드
의 제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 5-(터트-부틸)이소옥사졸-3-아민으로, 2,4-디플루오로-1-니트로벤젠(i)을 1-플루오로-2-니트로벤젠으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(5-(터트-부틸)이소옥사졸-3-일)술파모일)-2-클로로-5-플루오로페닐)아미노)페닐)(메틸)아미노)에틸)(메틸)카바메이트(0.03 g, 0.04 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.01 g, 46.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.83(d, 1H), 7.23(d, 2H), 7.14-7.10(m, 2H), 6.70(d, 1H), 5.89(s, 1H), 3.30-3.27(m, 2H), 3.13-3.11(m, 2H), 2.66(s, 6H), 1.23(s, 9H)
실시예
145: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(1,2,4-싸이아디아졸-5-일)벤젠술폰아미드
하이드로클로라
이드의 제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 1,2,4-싸이아다이아졸-5-아민으로, 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트 (ii)을 터트-부틸 메틸(피롤리딘-3-일)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (1-(2-((4-(N-(터트-부톡시카보닐)-N-(1,2,4-싸이아디아졸-5-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.0%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.39(s, 1H), 7.80(d, 1H), 7.14(t, 1H), 6.73(d, 1H), 6.68(t, 1H), 6.08(d, 1H), 3.78(t, 1H), 3.58(dd, 1H), 3.48(m, 1H), 3.40(dd, 1H), 2.67(s, 3H), 2.34(m, 1H), 1.99(m, 1H)
실시예
146: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(1-메틸-1H-피라졸-3-일)벤젠술폰아미드
하이드로클로라이
드의 제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 1-메틸-1H-피라졸-3-아민으로, 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트 (ii)을 터트-부틸 메틸(피롤리딘-3-일)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (1-(2-((4-(N-(터트-부톡시카보닐)-N-(1-메틸-1H-피라졸-3-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.1%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.68(d, 1H), 7.38(s, 1H), 7.13(t, 1H), 6.75(dd, 1H), 6.86(t, 1H), 6.06(d, 1H), 6.00(s, 1H), 3.78(t, 1H), 3.70(s, 3H), 3.56(dd, 1H), 3.48(m, 1H), 3.41(dd, 1H), 3.39(s. 3H), 2.36(m, 1H), 1.98(m, 1H)
실시예
147: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리
딘-1-일)페닐)아미노)-N-(피리미딘-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 피리미딘-4-아민으로, 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트 (ii)을 터트-부틸 메틸(피롤리딘-3-일)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 ((4-((2-(3-((터트-부톡시카보닐)(메틸)아미노)피롤리딘-1-일)-4-플루오로페닐)아미노)-5-클로로-2-플루오로페닐)술포닐)(피리미딘-4-일)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.45(s, 1H), 8.44(s, 1H), 7.95(d, 1H), 7.12(d, 1H), 7.00(t, 1H), 6.72(dd, 1H), 6.66(td, 1H), 6.04(d, 1H), 3.78(t, 1H), 3.56(dd, 1H), 3.47(m, 1H), 3.40(dd, 1H), 2.65(s, 3H), 2.31(m, 1H), 1.98(m, 1H)
실시예
148: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(5-플루오로피리미딘-2-일)벤젠술폰아미드
하이드로클로라
이드의 제조
상기 실시예 96에서의 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트 (ii)을 터트-부틸 메틸(피롤리딘-3-일)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (1-(2-((2-클로로-4-(N-(2,4-디메톡시벤질)-N-(5-플루오로피리미딘-2-일)술파모일)-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 59.8%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.46(s, 2H), 7.94(d, 1H), 7.11(td, 1H), 6.72(d, 1H), 6.66(td, 1H), 6.04(d, 1H), 3.77(t, 1H), 3.57(dd, 1H), 3.48(m, 1H), 3.41(dd, 1H), 2.66(s, 3H), 2.33(m, 1H), 1.99(m, 1H)
실시예
149: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리
딘-1-일)페닐)아미노)-N-(피라진-2-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 96에서의 2-클로로-5-플루오로피리미딘 (iv)을 2-클로로피라진으로, 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트 (ii)을 터트-부틸 메틸(피롤리딘-3-일)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (1-(2-((2-클로로-4-(N-(2,4-디메톡시페닐)-N-(피라진-2-일)술파모일)-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 60.9%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.29(s, 1H), 8.15(s, 1H), 8.09(s, 1H), 7.88(d, 1H), 7.09(dd, 1H), 6.70(dd, 1H), 6.64(t, 1H), 6.05(d, 1H), 5.45(d, 1H), 3.76(m, 1H), 3.54(dd, 1H), 3.44(m, 2H), 2.67(s, 3H), 2.29(m, 1H), 1.90(m, 1H)
실시예
150: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리딘
-1-일)페닐)아미노)-N-(5-메틸이소옥사졸-3-일)벤젠술폰아미드
하이드로클로라이
드의 제조
상기 실시예 133에서의 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii)를 터트-부틸 메틸(피롤리딘-3-일)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 터트-부틸 (1-(2-((4-(N-(터트-부톡시카보닐)-N-(5-메틸이소옥사졸-3-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(0.05 g, 0.06 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.1%)을 얻었다.
1H NMR (500 MHz, MeOD): 7.80(d, 1H), 7.14(dd, 1H), 6.73(d, 1H), 6.69(dd, 1H), 6.09(d, 1H), 6.07(s, 1H), 3.76(t, 1H), 3.58(m, 2H), 3.43(m, 2H), 2.66(s, 3H), 2.32(s, 3H), 2.05(m, 2H)
실시예
151: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(3-(
메틸아미노
)
피롤리
딘-1-일)페닐)아미노)-N-(피리미딘-5-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 133에서의 5-메틸이소옥사졸-3-아민(iv)을 피리미딘-5-아민으로, 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트 (ii)을 터트-부틸 메틸(피롤리딘-3-일)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (1-(2-((4-(N-(터트-부톡시카보닐)-N-(피리미딘-5-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)피롤리딘-3-일)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.2%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.87(s, 1H), 8.59(d, 2H), 7.79(d, 1h), 7.12(td, 1H), 6.73(d, 1H), 6.67(td, 1H), 6.07(d, 1H), 3.76(t, 1H), 3.50(m, 2H), 3.54(m, 2H), 2.67(s, 3H), 2.32(m, 1H), 1.98(m, 1H)
실시예
152: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-((2-(
메틸아미노
)에틸)아미노)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드 하이드로클로라이드의 제조
상기 실시예 92에서의 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii)를 터트-부틸 (2-아미노에틸)(메틸)카바메이트로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)아미노)에틸)(메틸)카바메이트(0.05 g, 0.07 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 56.9%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.72(s, 1H), 7.75(d, 1H), 7.07(t, 1H), 7.00(s, 1H), 6.63(d, 1H), 6.49(t, 1H), 6.05(d, 1H), 3.46(t, 2H), 3.17(t, 2H), 2.70(s, 3H)
실시예
153: 5
-
클로로
-4-((2-((2-(
di메틸아미노
)에틸)아미노)-4-
플루오로페
닐)아미노)-2-플루오로-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 92에서의 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii)를 N,N-디메틸에탄-1,2-디아민(3-(메틸아미노)프로필)카바메이트으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)(2-(di메틸아미노)에틸)카바메이트(0.02 g, 0.0003 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.01 g, 70.5%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.73(s, 1H), 7.75(d, 1H), 7.08(t, 1H), 7.01(s, 1H), 6.66(d, 1H), 6.50(t, 1H), 6.04(d, 1H), 3.53(t, 2H), 3.30(t, 2H), 2.90(s, 6H)
실시예
154: 5
-
클로로
-2-
플루오로
-4-((4-
플루오로
-2-(
메틸(3-(메틸아미노)프
로필)아미노)페닐)아미노)-N-(싸이아졸-4-일)벤젠술폰아미드
하이드로클로라이드의
제조
상기 실시예 92에서의 터트-부틸 메틸(2-(메틸아미노)에틸)카바메이트(ii)를 터트-부틸 메틸(3-(메틸아미노)프로필)카바메이트으로 사용한 것을 제외하고는 동일한 방법으로 중간체를 제조하였다. 얻어진 중간체 터트-부틸 (3-((2-((4-(N-(터트-부톡시카보닐)-N-(싸이아졸-4-일)술파모일)-2-클로로-5-플루오로페닐)아미노)-5-플루오로페닐)(메틸)아미노)프로필)(메틸)카바메이트(0.05 g, 0.7 mmol)에 1M HCl in 에틸아세테이트(5 mL)를 넣었다. 50~60℃로 가열하며 밤새 교반시킨 후 TLC로 반응 종결을 확인하였다. 반응액을 여과하여 목적 화합물(0.02 g, 55.9%)을 얻었다.
1H NMR (500 MHz, MeOD): 8.74(s, 1H), 7.78(d, 1h), 7.25(m, 1H), 7.03(m, 2H), 6.88(m, 1H), 6.29(d, 1H), 3.06(d, 2H), 2.80(d, 2H), 2.70(s, 3H), 2.60(s, 3H), 1.81(d, 2H)
실험예
길항제로서의 활성을 측정하기 위해 소디움이온채널1.7(Nav1.7) 및 소디움이온채널1.5(Nav1.5)에 대한 차단효과 실험을 하기와 같이 수행하였다.
1) 세포배양
hNav1.7 HEK293 세포주는 인간 배아 신장(human embryonic kidney;HEK) 293 세포에 인간 소디움이온채널1.7 유전자(type IX voltage-gated sodium channel alpha subunit)가 안정적으로 발현되어 있는 세포주이며 Millipore에서 구매하여 사용하였다. 배양 배지는 DMEM F-12에 100X NEAA를 1% 비율이 되도록 하고, heat inactivated FBS는 10%가 되도록 섞은 후, 항생제로서 P/S를 1% 비율이 되도록 제조하였다. 계대배양 시 제한효소로서 G-418을 첨가하였으며, T75 플라스크에 약 80% 정도의 밀도가 되도록 37, 5% CO2 incubator에서 2일 또는 3일간 배양한 hNav1.7 HEK293 세포를 0.05% 트립신 용액으로 처리하여 플라스크에서 떨어뜨린 후, 원심 분리하여 세포들을 수집하고 실험에 사용하였다.
hNav1.5 HEK293 세포주는 인간 배아 신장(human embryonic kidney;HEK) 293 세포에 인간 소디움이온채널1.5 유전자(Homo sapiens sodium channel, voltage-gated, type V, alpha subunit (SCN5A))가 안정적으로 발현되어 있는 세포주이며 Creacell에서 구매하여 사용하였다. 배양 배지는 DMEM에 100X L-glutamine을 2% 비율이 되도록 하고, heat inactivated FBS는 10%가 되도록 섞은 후, 항생제로서 P/S를 1% 비율이 되도록 제조하였다. 계대배양시 제한효소로서 G-418을 첨가하였으며, T75 플라스크에 약 80% 정도의 밀도가 되도록 37, 5% CO2 incubator에서 2일 또는 3일간 배양한 hNav1.5 HEK293 세포를 0.05% 트립신 용액으로 처리하여 플라스크에서 떨어뜨린 후, 원심 분리하여 세포들을 수집하고 실험에 사용하였다.
2) 화합물 샘플 제조
본 발명의 실시예에서 제조한 화합물들을 디메틸술폭시드(dimethyl sulfoxide; DMSO)에 용해시켜 실험에 사용하였다. 각 화합물은 90 mM 및 10 mM의 DMSO stock solution으로 제조하여 세포 외부용액(4 mM KCl, 138 mM NaCl, 1 mM MgCl2, 1.8 mM CaCl2, 5.6 mM Glucose, 10 mM HEPES, pH 7.45)에 각 농도별로 희석하여 최종 DMSO의 농도는 0.3% 이하가 되도록 하였다.
3) 소디움이온채널 차단효과 측정
소디움 이온채널의 억제 효과를 측정하기 위하여 Fluxion사의 IonFlux16 Auto patch clamp 기계와 전용 플레이트를 사용하였다. 세포를 세포 외부용액(4 mM KCl, 138 mM NaCl, 1 mM MgCl2, 1.8 mM CaCl2, 5.6 mM Glucose, 10 mM HEPES, pH 7.45)에 분포시킨 뒤 플레이트의 지정된 영역에 분주하고, 제조한 화합물 샘플을 각각의 농도로 희석한 뒤 플레이트의 지정된 영역에 분주하였다. 플레이트에 세포와 화합물 샘플, 그리고 세포 내부용액(100 mM CsF, 45 mM CsCl, 5 mM NaCl, 5 mM EGTA, 10 mM HEPES, pH 7.2)의 분주를 완료하여 기기에 장착하고 설정된 프로그램에 따라 약물의 이온채널에 대한 억제 여부를 측정하였다.
구체적으로, 화합물당 8개의 농도를 설정하였고, 화합물을 처리하기 전 발생한 피크 전류에 대한, 각 농도의 화합물을 50초 동안 세포에 처리한 후 발생한 피크전류의 억제 정도를 백분율로 계산하여 억제 백분율을 구하였으며, 시그마 플롯 프로그램을 사용하여 IC50 값(uM)을 산출하였고, 그 결과는 하기 표 2 내지 표 5에 나타내었다.
| 실시예 |
Nav1.7(IC50) |
실시예 |
Nav1.7(IC50) |
실시예 |
Nav1.7(IC50) |
실시예 |
Nav1.7(IC50) |
| 1 |
0.035 |
21 |
0.066 |
41 |
> 1 |
61 |
> 1 |
| 2 |
0.026 |
22 |
> 1 |
42 |
> 1 |
62 |
> 1 |
| 3 |
0.103 |
23 |
0.357 |
43 |
> 1 |
63 |
> 10 |
| 4 |
0.044 |
24 |
0.049 |
44 |
> 1 |
64 |
1.174 |
| 5 |
0.120 |
25 |
n/a |
45 |
0.236 |
65 |
0.541 |
| 6 |
0.182 |
26 |
0.066 |
46 |
0.686 |
66 |
0.160 |
| 7 |
0.125 |
27 |
> 1 |
47 |
0.375 |
67 |
0.028 |
| 8 |
0.489 |
28 |
> 0.3 |
48 |
0.086 |
68 |
0.103 |
| 9 |
1.505 |
29 |
0.362 |
49 |
0.609 |
69 |
0.241 |
| 10 |
0.396 |
30 |
> 1 |
50 |
0.328 |
70 |
0.050 |
| 11 |
1.007 |
31 |
0.044 |
51 |
n/a |
71 |
0.435 |
| 12 |
0.412 |
32 |
0.017 |
52 |
0.061 |
72 |
0.046 |
| 13 |
0.372 |
33 |
> 1 |
53 |
> 1 |
73 |
0.100 |
| 14 |
0.447 |
34 |
0.241 |
54 |
> 1 |
74 |
0.278 |
| 15 |
0.369 |
35 |
0.205 |
55 |
0.012 |
75 |
0.126 |
| 16 |
0.108 |
36 |
0.051 |
56 |
> 1 |
76 |
0.149 |
| 17 |
0.053 |
37 |
0.058 |
57 |
> 1 |
77 |
0.032 |
| 18 |
> 1 |
38 |
0.027 |
58 |
> 1 |
78 |
0.212 |
| 19 |
> 1 |
39 |
0.053 |
59 |
> 1 |
79 |
0.216 |
| 20 |
0.021 |
40 |
0.013 |
60 |
0.073 |
80 |
0.028 |
| 실시예 |
Nav1.7(IC50) |
실시예 |
Nav1.7(IC50) |
실시예 |
Nav1.7(IC50) |
실시예 |
Nav1.7(IC50) |
| 81 |
0.023 |
101 |
0.10 |
121 |
0.06 |
141 |
0.05 |
| 82 |
|
102 |
0.11 |
122 |
0.47 |
142 |
0.36 |
| 83 |
|
103 |
0.04 |
123 |
0.05 |
143 |
0.19 |
| 84 |
|
104 |
0.11 |
124 |
0.12 |
144 |
>10 |
| 85 |
|
105 |
0.02 |
125 |
0.08 |
145 |
1.40 |
| 86 |
0.277 |
106 |
0.23 |
126 |
0.02 |
146 |
0.39 |
| 87 |
0.140 |
107 |
0.46 |
127 |
0.008 |
147 |
0.25 |
| 88 |
1.929 |
108 |
0.02 |
128 |
0.009 |
148 |
0.11 |
| 89 |
1.216 |
109 |
0.05 |
129 |
0.004 |
149 |
0.30 |
| 90 |
0.352 |
110 |
0.07 |
130 |
0.006 |
150 |
0.36 |
| 91 |
6.581 |
111 |
0.01 |
131 |
0.027 |
151 |
>10 |
| 92 |
0.04 |
112 |
0.22 |
132 |
0.184 |
152 |
|
| 93 |
0.35 |
113 |
0.59 |
133 |
0.67 |
153 |
|
| 94 |
0.10 |
114 |
0.02 |
134 |
0.02 |
154 |
|
| 95 |
0.03 |
115 |
0.07 |
135 |
0.24 |
|
|
| 96 |
0.08 |
116 |
0.05 |
136 |
>10 |
|
|
| 97 |
0.06 |
117 |
0.12 |
137 |
0.30 |
|
|
| 98 |
0.04 |
118 |
0.20 |
138 |
0.24 |
|
|
| 99 |
0.12 |
119 |
0.02 |
139 |
0.06 |
|
|
| 100 |
1.09 |
120 |
0.14 |
140 |
3.67 |
|
|
| 실시예 |
Nav1.5(IC50) |
실시예 |
Nav1.5(IC50) |
실시예 |
Nav1.5(IC50) |
| 1 |
> 10 |
24 |
> 10 |
40 |
> 10 |
| 2 |
> 10 |
26 |
> 10 |
48 |
> 10 |
| 3 |
6.723 |
32 |
> 10 |
52 |
> 10 |
| 9 |
> 10 |
36 |
> 10 |
55 |
> 10 |
| 10 |
> 10 |
37 |
> 10 |
67 |
> 10 |
| 21 |
> 3 |
39 |
> 10 |
|
|
| 실시예 |
Nav1.5(IC50) |
실시예 |
Nav1.5(IC50) |
실시예 |
Nav1.5(IC50) |
| 92 |
25.03 |
101 |
> 10 |
128 |
1.83 |
| 95 |
8.2 |
102 |
> 10 |
148 |
> 10 |
| 96 |
> 10 |
103 |
> 10 |
149 |
> 10 |
| 97 |
> 10 |
104 |
> 10 |
150 |
> 10 |
| 98 |
> 10 |
105 |
> 10 |
151 |
> 10 |
| 99 |
> 10 |
106 |
> 10 |
|
|
| 100 |
> 10 |
127 |
5.54 |
|
|