TW202128162A - 憂鬱症之治療方法 - Google Patents
憂鬱症之治療方法 Download PDFInfo
- Publication number
- TW202128162A TW202128162A TW109138929A TW109138929A TW202128162A TW 202128162 A TW202128162 A TW 202128162A TW 109138929 A TW109138929 A TW 109138929A TW 109138929 A TW109138929 A TW 109138929A TW 202128162 A TW202128162 A TW 202128162A
- Authority
- TW
- Taiwan
- Prior art keywords
- compound
- human
- administered
- dose
- depression
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 96
- 208000020401 Depressive disease Diseases 0.000 title claims abstract description 11
- 229940126062 Compound A Drugs 0.000 claims abstract description 158
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 claims abstract description 158
- FJNPZKZPWVVSON-UHFFFAOYSA-N n-[4-(6-fluoro-3,4-dihydro-1h-isoquinolin-2-yl)-2,6-dimethylphenyl]-3,3-dimethylbutanamide Chemical compound CC1=C(NC(=O)CC(C)(C)C)C(C)=CC(N2CC3=CC=C(F)C=C3CC2)=C1 FJNPZKZPWVVSON-UHFFFAOYSA-N 0.000 claims abstract 5
- 238000011282 treatment Methods 0.000 claims description 34
- 102100034354 Potassium voltage-gated channel subfamily KQT member 2 Human genes 0.000 claims description 26
- 241000282412 Homo Species 0.000 claims description 23
- 102000004257 Potassium Channel Human genes 0.000 claims description 21
- 108020001213 potassium channel Proteins 0.000 claims description 21
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 17
- 230000004044 response Effects 0.000 claims description 16
- 239000003814 drug Substances 0.000 claims description 13
- 229940079593 drug Drugs 0.000 claims description 12
- 230000002708 enhancing effect Effects 0.000 claims description 11
- 208000035475 disorder Diseases 0.000 claims description 10
- 208000019022 Mood disease Diseases 0.000 claims description 9
- 208000020925 Bipolar disease Diseases 0.000 claims description 8
- 208000024714 major depressive disease Diseases 0.000 claims description 8
- 208000012672 seasonal affective disease Diseases 0.000 claims description 8
- 208000019901 Anxiety disease Diseases 0.000 claims description 6
- 230000036506 anxiety Effects 0.000 claims description 6
- 108010006746 KCNQ2 Potassium Channel Proteins 0.000 claims description 5
- 230000002085 persistent effect Effects 0.000 claims description 5
- 201000009916 Postpartum depression Diseases 0.000 claims description 4
- 208000001431 Psychomotor Agitation Diseases 0.000 claims description 4
- 206010038743 Restlessness Diseases 0.000 claims description 4
- 208000028552 Treatment-Resistant Depressive disease Diseases 0.000 claims description 4
- 208000025748 atypical depressive disease Diseases 0.000 claims description 4
- 206010012374 Depressed mood Diseases 0.000 claims description 2
- 230000020796 long term synaptic depression Effects 0.000 claims description 2
- 238000001228 spectrum Methods 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 claims 2
- 230000002035 prolonged effect Effects 0.000 claims 1
- 238000002560 therapeutic procedure Methods 0.000 abstract description 9
- 238000012360 testing method Methods 0.000 description 96
- 241001465754 Metazoa Species 0.000 description 41
- 241000699670 Mus sp. Species 0.000 description 34
- 230000000694 effects Effects 0.000 description 29
- 241000700159 Rattus Species 0.000 description 25
- 238000002474 experimental method Methods 0.000 description 17
- 229960004801 imipramine Drugs 0.000 description 17
- BCGWQEUPMDMJNV-UHFFFAOYSA-N imipramine Chemical compound C1CC2=CC=CC=C2N(CCCN(C)C)C2=CC=CC=C21 BCGWQEUPMDMJNV-UHFFFAOYSA-N 0.000 description 17
- 239000000203 mixture Substances 0.000 description 16
- 230000009182 swimming Effects 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 14
- 229930006000 Sucrose Natural products 0.000 description 14
- 235000013305 food Nutrition 0.000 description 14
- 239000005720 sucrose Substances 0.000 description 14
- 239000003981 vehicle Substances 0.000 description 13
- 210000004556 brain Anatomy 0.000 description 12
- 230000035939 shock Effects 0.000 description 10
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 9
- 239000000935 antidepressant agent Substances 0.000 description 9
- 241000699666 Mus <mouse, genus> Species 0.000 description 8
- 230000002354 daily effect Effects 0.000 description 8
- 229940005513 antidepressants Drugs 0.000 description 7
- 230000006399 behavior Effects 0.000 description 7
- 201000010099 disease Diseases 0.000 description 7
- 210000002683 foot Anatomy 0.000 description 7
- 235000013350 formula milk Nutrition 0.000 description 7
- 239000000725 suspension Substances 0.000 description 7
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 235000013336 milk Nutrition 0.000 description 6
- 239000008267 milk Substances 0.000 description 6
- 210000004080 milk Anatomy 0.000 description 6
- 238000010561 standard procedure Methods 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- 238000007917 intracranial administration Methods 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- 230000000638 stimulation Effects 0.000 description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 230000003542 behavioural effect Effects 0.000 description 4
- 230000001684 chronic effect Effects 0.000 description 4
- 235000012054 meals Nutrition 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 4
- 208000028017 Psychotic disease Diseases 0.000 description 3
- 241000283984 Rodentia Species 0.000 description 3
- 238000000540 analysis of variance Methods 0.000 description 3
- 235000020186 condensed milk Nutrition 0.000 description 3
- 238000000354 decomposition reaction Methods 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 230000003203 everyday effect Effects 0.000 description 3
- 235000020937 fasting conditions Nutrition 0.000 description 3
- 230000008533 pain sensitivity Effects 0.000 description 3
- 238000011458 pharmacological treatment Methods 0.000 description 3
- 239000012896 selective serotonin reuptake inhibitor Substances 0.000 description 3
- 229940124834 selective serotonin reuptake inhibitor Drugs 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 229910001220 stainless steel Inorganic materials 0.000 description 3
- 239000010935 stainless steel Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 238000007492 two-way ANOVA Methods 0.000 description 3
- 238000012795 verification Methods 0.000 description 3
- 230000003442 weekly effect Effects 0.000 description 3
- 208000008811 Agoraphobia Diseases 0.000 description 2
- 208000036864 Attention deficit/hyperactivity disease Diseases 0.000 description 2
- 238000011814 C57BL/6N mouse Methods 0.000 description 2
- 201000001916 Hypochondriasis Diseases 0.000 description 2
- -1 Kv7.2 Natural products 0.000 description 2
- 229940123685 Monoamine oxidase inhibitor Drugs 0.000 description 2
- 208000021384 Obsessive-Compulsive disease Diseases 0.000 description 2
- 229940121991 Serotonin and norepinephrine reuptake inhibitor Drugs 0.000 description 2
- 206010041250 Social phobia Diseases 0.000 description 2
- 229940123445 Tricyclic antidepressant Drugs 0.000 description 2
- 230000001430 anti-depressive effect Effects 0.000 description 2
- 230000004596 appetite loss Effects 0.000 description 2
- 208000015802 attention deficit-hyperactivity disease Diseases 0.000 description 2
- 238000004364 calculation method Methods 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 230000001186 cumulative effect Effects 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 208000024732 dysthymic disease Diseases 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000000977 initiatory effect Effects 0.000 description 2
- 235000021266 loss of appetite Nutrition 0.000 description 2
- 208000019017 loss of appetite Diseases 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 235000010981 methylcellulose Nutrition 0.000 description 2
- 239000002899 monoamine oxidase inhibitor Substances 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 208000019906 panic disease Diseases 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 239000004417 polycarbonate Substances 0.000 description 2
- 238000013105 post hoc analysis Methods 0.000 description 2
- 208000028173 post-traumatic stress disease Diseases 0.000 description 2
- 230000036544 posture Effects 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000000384 rearing effect Effects 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 208000022610 schizoaffective disease Diseases 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 208000011117 substance-related disease Diseases 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 238000012549 training Methods 0.000 description 2
- 239000003029 tricyclic antidepressant agent Substances 0.000 description 2
- 238000005303 weighing Methods 0.000 description 2
- SFLSHLFXELFNJZ-QMMMGPOBSA-N (-)-norepinephrine Chemical compound NC[C@H](O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-QMMMGPOBSA-N 0.000 description 1
- JDEUUKYNTHHAQH-UHFFFAOYSA-N 2,2-dimethylbutanamide Chemical compound CCC(C)(C)C(N)=O JDEUUKYNTHHAQH-UHFFFAOYSA-N 0.000 description 1
- OLQIKGSZDTXODA-UHFFFAOYSA-N 4-[3-(4-hydroxy-2-methylphenyl)-1,1-dioxo-2,1$l^{6}-benzoxathiol-3-yl]-3-methylphenol Chemical compound CC1=CC(O)=CC=C1C1(C=2C(=CC(O)=CC=2)C)C2=CC=CC=C2S(=O)(=O)O1 OLQIKGSZDTXODA-UHFFFAOYSA-N 0.000 description 1
- 206010001497 Agitation Diseases 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 206010063659 Aversion Diseases 0.000 description 1
- 206010011971 Decreased interest Diseases 0.000 description 1
- 206010012289 Dementia Diseases 0.000 description 1
- 238000001061 Dunnett's test Methods 0.000 description 1
- 208000012661 Dyskinesia Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 208000011688 Generalised anxiety disease Diseases 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- 208000030990 Impulse-control disease Diseases 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- 238000001282 Kruskal–Wallis one-way analysis of variance Methods 0.000 description 1
- 206010026749 Mania Diseases 0.000 description 1
- YJPIGAIKUZMOQA-UHFFFAOYSA-N Melatonin Natural products COC1=CC=C2N(C(C)=O)C=C(CCN)C2=C1 YJPIGAIKUZMOQA-UHFFFAOYSA-N 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 229920005372 Plexiglas® Polymers 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 241000700157 Rattus norvegicus Species 0.000 description 1
- 208000000323 Tourette Syndrome Diseases 0.000 description 1
- 208000016620 Tourette disease Diseases 0.000 description 1
- 238000010162 Tukey test Methods 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 230000016571 aggressive behavior Effects 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 230000009118 appropriate response Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 230000001174 ascending effect Effects 0.000 description 1
- 235000008452 baby food Nutrition 0.000 description 1
- 238000009227 behaviour therapy Methods 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 238000011953 bioanalysis Methods 0.000 description 1
- 208000028683 bipolar I disease Diseases 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 235000021152 breakfast Nutrition 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- 238000004422 calculation algorithm Methods 0.000 description 1
- 238000012754 cardiac puncture Methods 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 230000010485 coping Effects 0.000 description 1
- 208000026725 cyclothymic disease Diseases 0.000 description 1
- 238000013480 data collection Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 239000003479 dental cement Substances 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000000221 dopamine uptake inhibitor Substances 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 230000035622 drinking Effects 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 206010015037 epilepsy Diseases 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001917 fluorescence detection Methods 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 235000012631 food intake Nutrition 0.000 description 1
- 238000012048 forced swim test Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 208000029364 generalized anxiety disease Diseases 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000000548 hind-foot Anatomy 0.000 description 1
- 210000004251 human milk Anatomy 0.000 description 1
- 235000020256 human milk Nutrition 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 210000004283 incisor Anatomy 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- 230000009191 jumping Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 235000021056 liquid food Nutrition 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000013178 mathematical model Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 229960003987 melatonin Drugs 0.000 description 1
- DRLFMBDRBRZALE-UHFFFAOYSA-N melatonin Chemical compound COC1=CC=C2NC=C(CCNC(C)=O)C2=C1 DRLFMBDRBRZALE-UHFFFAOYSA-N 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000008587 neuronal excitability Effects 0.000 description 1
- 229960002748 norepinephrine Drugs 0.000 description 1
- SFLSHLFXELFNJZ-UHFFFAOYSA-N norepinephrine Natural products NCC(O)C1=CC=C(O)C(O)=C1 SFLSHLFXELFNJZ-UHFFFAOYSA-N 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 238000010149 post-hoc-test Methods 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 208000020016 psychiatric disease Diseases 0.000 description 1
- 238000013102 re-test Methods 0.000 description 1
- 230000000306 recurrent effect Effects 0.000 description 1
- 238000001223 reverse osmosis Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 201000000980 schizophrenia Diseases 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 230000000405 serological effect Effects 0.000 description 1
- 230000000862 serotonergic effect Effects 0.000 description 1
- 229940076279 serotonin Drugs 0.000 description 1
- 239000003775 serotonin noradrenalin reuptake inhibitor Substances 0.000 description 1
- 210000003625 skull Anatomy 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- 235000021055 solid food Nutrition 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000011550 stock solution Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 201000009032 substance abuse Diseases 0.000 description 1
- 230000003319 supportive effect Effects 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 210000002489 tectorial membrane Anatomy 0.000 description 1
- 238000011426 transformation method Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000011870 unpaired t-test Methods 0.000 description 1
- 210000001835 viscera Anatomy 0.000 description 1
- 235000012431 wafers Nutrition 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/472—Non-condensed isoquinolines, e.g. papaverine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
Landscapes
- Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Pain & Pain Management (AREA)
- Neurology (AREA)
- Organic Chemistry (AREA)
- Psychiatry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Neurosurgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
在某些實施例中,本揭示內容係關於用於治療人類憂鬱症之方法,其中該等方法包含對有此需要的人類經口投與治療有效量之N
-[4-(6-氟-3,4-二氫-1H
-異喹啉-2-基)-2,6-二甲基苯基]-3,3-二甲基丁醯胺(化合物A)。本揭示內容進一步關於療法及化合物A之投與之各種改良方法。
Description
在美國,憂鬱症影響超過2000萬成年人。憂鬱症之特徵係悲傷嚴重到足以或悲傷嚴重持續到足以干擾功能且常常表徵為對活動之興趣或愉悅感降低。TheDiagnostic and Statistical Manual of Mental Disorders
,第五版(DSM-5)依特定症狀對一些憂鬱症進行分類,諸如重度憂鬱症(通常稱為重度憂鬱)或持續性憂鬱症(輕鬱症(dysthymia)),及其他按病因進行分類,諸如經期前情緒障礙、由於另一種醫學病狀引起之憂鬱症、或物質/藥物引起之憂鬱症。另一類憂鬱症包括躁鬱症(躁狂憂鬱症)。憂鬱症之確切病因尚不知曉,但已知遺傳及環境因素在起作用。
憂鬱症之第一線治療通常包括支持藥物、心理治療藥物及抗憂鬱藥中之一者或多者。幾種藥物類別及藥物可用於治療憂鬱症,諸如選擇性血清素再吸收抑制劑(SSRIs)、血清素調節劑(5-HT2
阻斷劑)、血清素-正腎上腺素再吸收抑制劑(SNRIs)、正腎上腺素-多巴胺再吸收抑制劑、非典型抗憂鬱藥、三環抗憂鬱藥、單胺氧化酶抑制劑(MAOIs)、褪黑激素抗憂鬱藥及氯胺酮(ketamine)樣藥物,其中SSRIs常常是首選藥物。然而,就許多人而言,為憂鬱症尋找正確抗憂鬱藥治療可採用試誤法(trial-and-error approach),因為一些抗憂鬱藥僅部分有效且伴有另外局限性,包括治療作用開始緩慢及非所欲的副作用。大多數經批准的抗憂鬱藥具有相同血清素能及去甲基腎上腺素能途徑從而限制機理多樣性且幾乎沒有機會改良患者預後或個人化治療方法。
由於受影響的成年人數量、病症類別之數量及複雜性、及常常第一線抗憂鬱藥之無效性及機理均一性,此項技術仍舊需要新穎且有效之憂鬱症(包括重度憂鬱)治療。本揭示內容藉由提供用於治療憂鬱症之組合物及方法及用途來滿足此需求,且提供其他相關優點。
本揭示內容描述小分子N
-[4-(6-氟-3,4-二氫-1H
-異喹啉-2-基)-2,6-二甲基苯基]-3,3-二甲基丁醯胺(本文中稱為「化合物A」)之某些方法及用途。
在一個實施例中,本揭示內容係關於一種治療有此需要的人類之憂鬱症之方法,該方法包括對人類投與治療有效量之化合物A。在某些情況下,藉由投與化合物A治療的憂鬱症為重度憂鬱症(MDD)、侵擾性情緒失調症、持續性憂鬱症、雙極性病譜型病症(bipolar spectrum disorder)、產後憂鬱、經期前情緒障礙(PMDD)、季節性情感障礙(SAD)、非典型憂鬱、難治型憂鬱(TRD)、與躁動或焦慮相關之憂鬱、失調症伴情緒低落、長時間憂鬱反應或其組合。在某些實施例中,藉由投與化合物A治療的憂鬱症為重度憂鬱症(MDD)。
在另一個實施例中,包含投與治療有效量之化合物A之憂鬱症治療方法進一步包含增強開放人類中之Kv7鉀通道。
在另一個實施例中,本揭示內容係關於一種開放或增強開放人類Kv7鉀通道之方法,該方法包含對人類投與有效量之化合物A,其中該人類患有憂鬱症,諸如彼等本文所述者。
在一些態樣中,Kv7鉀通道為Kv7.2、Kv7.3、Kv7.4或Kv7.5中之一者或多者。在某些情況下,與Kv7.1相比選擇性開放或增強開放Kv7.2、Kv7.3、Kv7.4或Kv7.5鉀通道中之一者或多者。在其他情況下,該方法包含開放或增強開放Kv7.2/Kv7.3 (KCNQ2/3)鉀通道。
在一個實施例中,本揭示內容提供一種治療有此需要的人類之憂鬱症之方法,其中將化合物A經口投與人類。在某些情況下,對人類之經口投與每次投與包含2至200 mg化合物A之劑量。在其他情況下,對人類之經口投與包含每天5至1000 mg之劑量。
化合物A是目前經開發用於治療癲癇病症之小分子,及其作為鉀通道調節劑之用途揭示於美國專利第8,293,911號及第8,993,593號以及美國申請案序號16/409,684及16/410,851,該等案之全部揭示內容係以引用之方式併入本文中。
在參考以下詳細描述後當可明瞭本揭示內容之此等及其他態樣。為此,本文闡述各種參考文獻,其更詳細地描述某些背景資訊及程序且其全文分別以引用之方式併入本文中。
本揭示內容係關於化合物A之新穎且改良之方法及用途,特別是藉由對有此需要的人類患者投與化合物A,包括藉由經口投與來治療憂鬱症。
在以下揭示內容中,闡述某些特定詳細內容以便透徹理解各種實施例。然而,熟習此項技術者應明瞭,可在沒有此等詳細內容下實踐本文所述的方法及用途。在其他情況下,未顯示或詳細描述熟知的結構以避免不必要地混淆實施例之描述。除非上下文另外要求,否則在隨後的整個說明書及申請專利範圍中,詞語「包含(comprise)」及其變化形式(諸如「包含(comprises)」及「包含(comprising)」)應以開放、包容意義來解釋,亦即解釋為「包括(但不限於)」。此外,本文所提供的標題僅係為了方便而並不解釋所主張的發明之範疇或含義。
整個說明書中提及「一個實施例」或「一實施例」時意指結合該實施例描述之特定特徵、結構或特性係包括在至少一個實施例中。因此,在整個說明書中不同位置出現片語「在一個實施例中」或「在一實施例中」不一定均指相同實施例。此外,在一或多個實施例中,特定特徵、結構或特性可以任何適宜方式組合。再者,如本說明書及隨附申請專利範圍中所使用,除非上下文清楚地另作指明,否則單數形式「一」、「一個」及「該」包括複數個指示物。亦應注意,除非上下文清楚地另作指明,否則術語「或」一般以其意義使用,包括「及/或」。
4.1. 定義
如本說明書及隨附申請專利範圍中所用,除非另有相反指明,否則以下術語及縮寫具有所指示的含義:
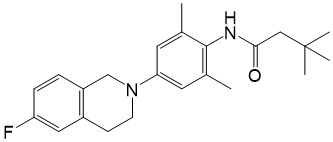
「化合物A」係指具有下式:;
且具有N
-[4-(6-氟-3,4-二氫-1H
-異喹啉-2-基)-2,6-二甲基苯基]-3,3-二甲基丁醯胺之化學名稱之化合物。化合物A之製備及其作為Kv7.2/Kv7.3 (KCNQ2/3)開放劑(opener)之用途揭示於美國專利第8,293,911號及第8,993,593號以及美國申請案序號16/409,684及16/410,851中。化合物A與大多數已知AED’s之不同處在於其強化且增強開放電壓門控鉀通道Kv7.2及Kv7.3 (Kv7.2/Kv7.3),此對於控制神經元興奮性極重要。化合物A係用於本文所述的方法及用途。
如本文所用「治療有效量」係指足以治療所述疾病、病症或病狀或對於人類個體之疾病、病症或病狀或疾病、病症或病狀之一或多種潛在機制具有期望的所述作用之化合物A之量。在某些實施例中,當投與化合物A以治療憂鬱症時,治療有效量係指在投與人類時可治療或減輕人類之憂鬱症,或於患有憂鬱症的人類中展現可檢測之治療作用之化合物A之量。該作用可藉由(例如)憂鬱發作次數減少或藉由憂鬱發作嚴重性降低來檢測。
如本文所用之「治療」係指與投與化合物A相關的改善指定疾病、病症或病狀或該疾病、病症或病狀之一或多種潛在機制,包括減慢或停止人類個體中疾病、病症或病狀或一或多種潛在機制之進展之治療應用。在某些實施例中,當投與化合物A來治療憂鬱症時,治療係指減緩或停止憂鬱症之進展及/或逆轉憂鬱症之治療應用。逆轉憂鬱症與減緩或停止憂鬱症之治療應用之不同處在於利用逆轉方法,不僅憂鬱症之進展停止,而且細胞行為在某種程度上朝著在沒有憂鬱症下所將觀測到的正常狀態發展。在一些實施例中,包含投與化合物A之憂鬱症治療伴隨著一或多個Kv7鉀通道(例如,Kv7.2、Kv7.3、Kv7.4及/或Kv7.5,特別是Kv7.2及/或Kv7.3,視需要與Kv7.1相比)之細胞活性朝著在沒有憂鬱症下所將觀測到的正常程度改變。
「在進食狀況下」係指在介於經口投與有效量(例如在治療有效劑量範圍內)之化合物A前約4小時至投與化合物A後約4小時之間的時間期內已攝入食物之狀況。食物可為固體、液體或具有足夠整體及脂肪含量且不能在胃中快速溶解及吸收之固體及液體食物之混合物。在一些情況下,食物為一餐,諸如早餐、午餐、晚餐或替代地嬰兒食品(例如配方奶或母乳)。可將治療有效量之化合物A經口投與個體,例如,在進餐後約2小時前的約30分鐘之間,最有利地,化合物A之劑量單位係在一餐期間或在進餐後15分鐘內經口投與。
「在禁食狀況下」係指在經口投與治療有效量之化合物A前至少4小時至投與化合物A後約4小時間的時間期內尚未攝入食物之狀況。
4.2. 實施例
在一些實施例中,本揭示內容係關於一種治療有此需要的人類之憂鬱症之方法,該方法包括對人類投與(例如經口)治療有效量之化合物A。在某些情況下,包含投與化合物A來治療之憂鬱症為重度憂鬱症(MDD)、侵擾性情緒失調症、持續性憂鬱症、雙極性病譜型病症、產後憂鬱、經期前情緒障礙(PMDD)、季節性情感障礙(SAD)、非典型憂鬱、難治型憂鬱(TRD)、與躁動或焦慮相關之憂鬱或其組合。在某些實施例中,化合物A之投與量足以降低憂鬱症之嚴重性、憂鬱症之頻率或二者。在某些實施例中,包含投與化合物A來治療之憂鬱症為重度憂鬱症(MDD)。
在一些實施例中,藉由投與治療有效量之化合物A來治療憂鬱症之方法包含增強開放人類中之Kv7鉀通道。
在其他實施例中,本揭示內容係關於一種治療強迫症(OCD)、恐慌症、社交焦慮症、社交恐懼症(social phobia)、廣場恐懼症(agoraphobia)、廣場恐懼症伴恐慌症、疑病症(hypochondriasis)、創傷後壓力症(PTSD)、難治型躁鬱症、廣泛性焦慮症、注意力缺陷/過動障礙(ADHD)、第一型雙相情緒障礙症、第二型雙相情緒障礙症、躁狂症、未另外明示之循環性情感障礙(cyclothymic disorder)及躁鬱症、低落性情感障礙(dysthymic disorder)、未另外明示之憂鬱症、輕度憂鬱、反復性短暫性憂鬱症、憂鬱型精神病、衝動控制障礙、精神分裂症、類精神分裂症、情感性精神分裂症(schizoaffective disorder)、帕金森氏症(Parkinson's disease)、癡呆、阿茲海默氏症(Alzheimer's disease)、亨丁頓氏症(Huntington's disease)、妥瑞症候群(Tourette's syndrome)、攻擊(aggression)、及物質使用及/或濫用或其組合之方法,該方法包含對有此需要的人類投與治療有效量之化合物A。
在某些實施例中,本揭示內容提供一種方法或用途,其包含藉由投與有效量之化合物A來開放或增強開放有此需要的人類中之Kv7鉀通道,諸如Kv7.2、Kv7.3、Kv7.4及/或Kv7.5鉀通道,特別是Kv7.2/Kv7.3 (KCNQ2/3)鉀通道。在一些此類實施例中,該人類患有憂鬱症,諸如本文所述之彼等憂鬱症。
在某些情況下,本文所述之方法或用途包含與Kv7.1相比選擇性地開放或增強開放Kv7鉀通道,諸如Kv7.2、Kv7.3、Kv7.4或Kv7.5中之一者或多者。在一些實施例中,該方法或用途與Kv7.1相比對Kv7.2具有選擇性。在其他實施例中,該方法或用途與Kv7.1相比對Kv7.3具有選擇性。又在其他實施例中,該方法或用途與Kv7.1相比對Kv7.4具有選擇性。在又另外其他實施例中,該方法或用途與Kv7.1相比對Kv7.5具有選擇性。在某些實施例中,該方法或用途與Kv7.1相比對Kv7.2及Kv7.3具有選擇性。在某些實施例中,該方法或用途與其他Kv7鉀通道相比對Kv7.2及Kv7.3具有選擇性。在某些實施例中,該方法或用途與Kv7.4及Kv7.5相比對Kv7.2及Kv7.3具有選擇性。
在一個實施例中,本文所述的方法及用途,諸如治療有此需要的個體之憂鬱症之方法或用途,係藉由投與(例如經口)治療有效量之化合物A(諸如約0.05 mg/kg至約2.0 mg/kg)來達成。更特定代表量包括0.05 mg/kg、0.10 mg/kg、0.20 mg/kg、0.30 mg/kg、0.40 mg/kg、0.5 mg/kg、0.6 mg/kg、0.7 mg/kg、0.80 mg/kg、0.90 mg/kg、1.0 mg/kg、1.1 mg/kg、1.2 mg/kg、1.3 mg/kg、1.4 mg/kg、1.5 mg/kg、1.6 mg/kg、1.7 mg/kg、1.8 mg/kg、1.9 mg/kg及2.0 mg/kg、或藉由使用前述量中之兩者作為端點所建立的任何量範圍。在一些態樣中,該方法或用途包括投與(例如經口)0.1至1.0 mg/kg之化合物A。在一些態樣中,該方法包括投與(例如經口) 0.2至0.5 mg/kg之化合物A。
在一些實施例中,本文所述的方法及用途,諸如治療有此需要的個體之憂鬱症之方法或用途,係藉由以單次或分次劑量投與(例如經口)治療有效量之化合物A(諸如2至200 mg之化合物A)來達成。例如,該方法可包括以單次或分次劑量投與(例如經口)約2 mg、約3 mg、約4 mg、約5 mg、約6 mg、約7 mg、約8 mg、約9 mg、約10 mg、約11 mg、約12 mg、約13 mg、約14 mg、約15 mg、約16 mg、約17 mg、約18 mg、約19 mg、約20 mg、約21 mg、約22 mg、約23 mg、約24 mg、約25 mg、約26 mg、約27 mg、約29 mg、約30 mg、約31 mg、約32 mg、約33 mg、約34 mg、約35 mg、約36 mg、約37 mg、約38 mg、約39 mg、約40 mg、約41 mg、約42 mg、約43 mg、約44 mg、約45 mg、約46 mg、約47 mg、約48 mg、約49 mg、約50 mg、約51 mg、約52 mg、約53 mg、約54 mg、約55 mg、約56 mg、約57 mg、約58 mg、約59 mg、約60 mg、約61 mg、約62 mg、約63 mg、約64 mg、約65 mg、約66 mg、約67 mg、約68 mg、約69 mg、約70 mg、約71 mg、約72 mg、約73 mg、約74 mg、約75 mg、約76 mg、約77 mg、約78 mg、約79 mg、約80 mg、約81 mg、約82 mg、約83 mg、約84 mg、約85 mg、約86 mg、約87 mg、約88 mg、約89 mg、約90 mg、約91 mg、約92 mg、約93 mg、約94 mg、約95 mg、約96 mg、約97 mg、約98 mg、約99 mg、約100 mg、約101 mg、約102 mg、約103 mg、約104 mg、約105 mg、約106 mg、約107 mg、約108 mg、約109 mg、約110 mg、約111 mg、約112 mg、約113 mg、約114 mg、約115 mg、約116 mg、約117 mg、約118 mg、約119 mg、約120 mg、約121 mg、約122 mg、約123 mg、約124 mg、約125 mg、約126 mg、約127 mg、約129 mg、約130 mg、約131 mg、約132 mg、約133 mg、約134 mg、約135 mg、約136 mg、約137 mg、約138 mg、約139 mg、約140 mg、約141 mg、約142 mg、約143 mg、約144 mg、約145 mg、約146 mg、約147 mg、約148 mg、約149 mg、約150 mg、約151 mg、約152 mg、約153 mg、約154 mg、約155 mg、約156 mg、約157 mg、約158 mg、約159 mg、約160 mg、約161 mg、約162 mg、約163 mg、約164 mg、約165 mg、約166 mg、約167 mg、約168 mg、約169 mg、約170 mg、約171 mg、約172 mg、約173 mg、約174 mg、約175 mg、約176 mg、約177 mg、約178 mg、約179 mg、約180 mg、約181 mg、約182 mg、約183 mg、約184 mg、約185 mg、約186 mg、約187 mg、約188 mg、約189 mg、約190 mg、約191 mg、約192 mg、約193 mg、約194 mg、約195 mg、約196 mg、約197 mg、約198 mg、約199 mg或約200 mg或投與(例如經口)藉由使用前述量中之兩者作為端點所建立的任何量範圍。在一些態樣中,該方法或用途包括以單次劑量或分次劑量經口投與5至50 mg之化合物A。在一些態樣中,該方法或用途包括經口投與單次或分次劑量之10、20或25 mg化合物A。在一些態樣中,該方法或用途包括經口投與單次或分次劑量之20 mg化合物A。
在一些態樣中,本文所述的方法及用途,諸如治療有此需要的人類之憂鬱症之方法或用途,係藉由投與(例如經口)至少20 mg化合物A,諸如至少25、30、35、50、75或100 mg之化合物A來達成。在一些實施例中,本文所述的方法及用途,諸如治療有此需要的人類之憂鬱症之方法或用途,係藉由投與(例如經口)每天至少50 mg化合物A,諸如每天至少60、75、85、100、125、150、175或200 mg之化合物A來達成。
在一些實施例中,本文所述的方法及用途,諸如治療有此需要的人類之憂鬱症之方法或用途,係藉由每天投與(例如經口)治療有效量之化合物A,諸如每天5至1000 mg之化合物A,諸如每天5至500 mg或5至250 mg之化合物A來達成。例如,該方法或用途可包括投與(例如經口)每天約5 mg、約10 mg、約15 mg、約20 mg、約25 mg、約30 mg、約35 mg、約40 mg、約45 mg、約50 mg、約55 mg、約60 mg、約65 mg、約70 mg、約75 mg、約80 mg、約85 mg、約90 mg、約95 mg、約100 mg、約105 mg、約110 mg、約115 mg、約120 mg、約125 mg、約130 mg、約135 mg、約140 mg、約145 mg、約150 mg、約155 mg、約160 mg、約165 mg、約170 mg、約175 mg、約180 mg、約185 mg、約190 mg、約195 mg、約200 mg、約205 mg、約210 mg、約215 mg、約220 mg、約225 mg、約230 mg、約235 mg、約240 mg、約245 mg、約250 mg、約255 mg、約260 mg、約265 mg、約270 mg、約275 mg、約280 mg、約285 mg、約290 mg、約295 mg、約300 mg、約305 mg、約310 mg、約315 mg、約320 mg、約325 mg、約330 mg、約335 mg、約340 mg、約345 mg、約350 mg、約355 mg、約360 mg、約365 mg、約370 mg、約375 mg、約380 mg、約385 mg、約390 mg、約395 mg、約400 mg、約405 mg、約410 mg、約415 mg、約420 mg、約425 mg、約430 mg、約435 mg、約440 mg、約445 mg、約450 mg、約455 mg、約460 mg、約465 mg、約470 mg、約475 mg、約480 mg、約485 mg、約490 mg、約495 mg、約500 mg或約1000 mg之化合物A,或每天投與(例如經口)藉由使用前述量中之兩者作為端點所建立的量範圍。在一些態樣中,該方法或用途包括經口投與每天10至200 mg之化合物A,諸如每天10、15、20、25、30、35或40 mg至75、100、125、150、175或200 mg之化合物A,包括每天20至150 mg。在一些態樣中,經口投與包括每天50、75、100或125 mg之化合物A,諸如每天100 mg。
在某些情況下,以上日劑量之化合物A係以每天多次劑量,諸如以每天兩次、三次、四次或五次劑量投與(例如經口)。例如,100 mg之日劑量可以整天五次20 mg、四次25 mg、三次33.3 mg或兩次50 mg劑量投與。
在一些實施例中,以上日劑量之化合物A係以單次劑量投與(例如經口)。例如,每天約5、10、15、20、25、或30 mg至約50、65、75、100、125或150 mg之化合物A可以單次劑量經口投與,包括每天10至25 mg、10至30 mg及10至40 mg以單次劑量,諸如每天10至25 mg以單次劑量。相關地,論述於先前段落中之化合物A之任何劑量可包括在單位劑型中。
在某些實施例中,本文所述的方法及用途,在使用本文所揭示的每日給藥時,在6至9天內,諸如在約1週內達成化合物A之穩態。
在另外實施例中,以上所論述的藉由投與(例如經口)治療有效量之化合物A來治療憂鬱症之方法或用途包含在進食狀況下對人類投與化合物A。在一些實施例中,與對在禁食狀況(亦即沒有食物或在時間上不接近食物之攝入)下的人類經口投與化合物A相比,對在進食狀況(亦即含有食物或在時間上接近食物之攝入)下的人類經口投與化合物A顯著增強化合物A之生物可利用性及暴露。在一些實施例中,與在將相同量之化合物A經口投與在禁食狀況下的人類時相比,對在進食狀況下的人類經口投與化合物A增加化合物A之一或多種藥物動力學參數(例如Cmax
、AUCinf
、Tmax
、t½λz
等)。
在某些實施例中,本文所述的方法及用途以包含化合物A及一或多種醫藥上可接受之載劑或賦形劑之醫藥上可接受之口服組合物之形式投與化合物A。包括在此等組合物中之化合物A之量可對應於本文所述的一或多種量。在一些實施例中,組合物為單位劑量。
包含化合物A之醫藥上可接受之口服組合物之實例包括固體調配物(諸如錠劑、膠囊、含片(lozenges)、糖衣丸(dragées)、顆粒、粉末、薄片(wafers)、多顆粒劑(multi-particulates)及薄膜劑(films))、液體調配物(諸如水溶液、酏劑、酊劑、漿液、懸浮液及分散液)及霧化調配物(諸如霧劑(mists)及噴霧劑)。在一個實施例中,化合物A之醫藥上可接受之口服組合物包括小兒懸浮液或顆粒。所有以上所述量之化合物A可包括在此類調配物中,例如包含5、10、15、10、25、30或35 mg之化合物A之膠囊。
在另一個實施例中,提供用於經口投與化合物A以在經口投與時治療憂鬱症之套組。此類套組包含化合物A之複數種口服單位劑型以及用於經口投與化合物A之說明。
本文描述本揭示內容之另外實施例及實例。此等實施例及實例係例示性且不應解釋為限制所主張發明之範疇。
5. 實例
實施研究以確定化合物A在囓齒動物行為絕望模型(亦即小鼠強迫游泳試驗)中之作用。進一步分析確定強迫游泳試驗中化合物A之總腦與血漿比。實施另外研究以確定公認憂鬱模型中化合物A之作用(若有的話)。
5.1. 實例1. 小鼠強迫游泳試驗
目標:使用小鼠強迫游泳試驗進行研究以評定化合物A之潛在功效。強迫游泳試驗係行為絕望模型,且對各種類型之抗憂鬱藥物之檢測敏感(Can等人,The Mouse Forced Swim Test. J. Vis. Exp. 2012 (59),e3638,DOI:10.3791/3638)。
研究設計:四十(40)隻雄性CD-1小鼠在開始測試之前接受對測試設施之1週適應期(事件概述在表 1
中)。每籠飼養5隻動物,且可不受限制地獲取嚙齒動物飼料(rodent chow)及水(SOP ROD.03.01、SOP ROD.04.01、SOP ROD.18)且保持12h/12h光照/黑暗週期,其中所有實驗活動均在動物的光照週期期間進行。所有動物使用程序均根據加拿大動物照護委員會(Canadian Council on Animal Care) (CCAC)的原則進行。表 1. 研究事件概述
| 研究日 | 關鍵事件 | 程序 |
| -3 | 動物到達 | 適應動物設施 |
| 0 | 強迫游泳試驗 | 一般健康觀測及體重 強迫游泳試驗 血液及腦採集(N = 20隻給予化合物A之動物 |
化合物A之調配物:稱量化合物A(純度99.4%)(不校正純度)且以預期最終濃度的20x溶解於DMSO中。將化合物A之20x DMSO儲備溶液用在水中之0.5%甲基纖維素稀釋20倍以達成最終所需濃度。當化合物A以細懸浮液沉澱時,攪拌或渦旋混合產生均質懸浮液。將上述調配物保持在室溫下且在每次劑量投與前連續攪拌或渦旋混合。測試物品概述於表 2
中。表 2. 測試物品
1
預處理時間。2
Sigma-Aldrich目錄#M0430 (滿足USP測試規格)。3
丙咪嗪為亦可降低躁動及焦慮之症狀之已知三環抗憂鬱劑。
| 測試物品 | BEW | 劑量 | 途徑 | Ppt 1 | 劑量體積 | 媒劑 |
| 化合物A | 1 | 1 mg/kg及3 mg/kg | IP | 30分鐘 | 10 mL/kg | 5% DMSO、0.5%甲基纖維素2 含在逆滲透水中;黏度: 400 cP |
| 丙咪嗪3 | 1.13 | 330 mg/kg | IP | 30分鐘 | 10 mL/kg | 鹽水 |
強迫游泳試驗:四十(40)隻雄性CD-1小鼠接受適宜劑量之媒劑、測試物品或陽性對照(治療概述於表 3
中)。在預定預處理時間(Can等人,2012)後,將動物輕輕放入裝有水(20至25℃)之高玻璃圓筒中。在一段時間的劇烈活動後,小鼠採取特徵性且易於識別之不動姿勢。游泳試驗涉及對不動持續時間進行評分。在6分鐘試驗時程內,記錄第一次不動之潛伏期(單位為秒)。亦測量試驗之最後4分鐘期間的不動持續時間(單位為秒)。未記錄0至2分鐘之活動或不活動。表 3. 治療組之概述
| 組 別 | 治療 | 途徑 | Ptt | 劑量體積 | 組大小 |
| A | 媒劑 | IP | 30分鐘 | 10 mL/kg | N = 10 |
| B | 化合物A (1 mg/kg) | IP | 30分鐘 | 10 mL/kg | N = 10 |
| C | 化合物A (3 mg/kg) | IP | 30分鐘 | 10 mL/kg | N = 10 |
| D | 丙咪嗪(30 mg/kg) | IP | 30分鐘 | 10 mL/kg | N = 10 |
結果:強迫游泳試驗之結果顯示於表 4
及圖1至3中。表 4. 強迫游泳試驗之結果
| 組 別 | 動物ID | 治療組 | 不動潛伏期( 秒) | 不動時間( 秒) | ||
| 0 至2 分鐘 | 2 至6 分鐘 | 0 至6 分鐘 | ||||
| A | A1 | 媒劑 | 80 | 39 | 222 | 261 |
| A2 | 106 | 13 | 226 | 239 | ||
| A3 | 200 | 0 | 188 | 188 | ||
| A4 | 79 | 38 | 209 | 247 | ||
| A5 | 91 | 22 | 119 | 141 | ||
| A6 | 90 | 20 | 148 | 168 | ||
| A7 | 99 | 20 | 190 | 210 | ||
| A8 | 91 | 5 | 199 | 204 | ||
| A9 | 79 | 15 | 121 | 136 | ||
| A10 | 93 | 24 | 192 | 216 | ||
| 平均值 | 100.8 | 19.6 | 181.4 | 201.0 | ||
| 標準偏差 | 11.4 | 3.9 | 12.3 | 13.6 | ||
| B | B1 | 化合物A (1 mg/kg) | 77 | 32 | 142 | 174 |
| B2 | 84 | 28 | 170 | 198 | ||
| B3 | 206 | 0 | 33 | 33 | ||
| B4 | 100 | 16 | 109 | 125 | ||
| B5 | 70 | 20 | 149 | 169 | ||
| B6 | 109 | 4 | 192 | 196 | ||
| B7 | 144 | 0 | 134 | 134 | ||
| B8 | 105 | 7 | 189 | 196 | ||
| B9 | 130 | 0 | 141 | 141 | ||
| B10 | 80 | 20 | 150 | 170 | ||
| 平均值 | 110.5 | 12.7 | 140.9 | 153.6 | ||
| 標準偏差 | 13.0 | 3.8 | 14.4 | 15.8 | ||
| C | C1 | 化合物A (3 mg/kg) | 135 | 0 | 166 | 166 |
| C2 | 165 | 0 | 144 | 144 | ||
| C3 | 155 | 0 | 122 | 122 | ||
| C4 | 86 | 23 | 184 | 207 | ||
| C5 | 150 | 0 | 82 | 82 | ||
| C6 | 127 | 0 | 146 | 146 | ||
| C7 | 192 | 0 | 101 | 101 | ||
| C8 | 162 | 0 | 90 | 90 | ||
| C9 | 83 | 21 | 163 | 184 | ||
| C10 | 105 | 15 | 166 | 181 | ||
| 平均值 | 136.0 | 5.9 | 136.4 | 142.3 | ||
| 標準偏差 | 11.3 | 3.1 | 11.3 | 13.5 | ||
| D | D1 | 丙咪嗪(30 mg/kg) | 224 | 0 | 32 | 32 |
| D2 | 213 | 0 | 45 | 45 | ||
| D3 | 180 | 0 | 63 | 63 | ||
| D4 | 169 | 0 | 133 | 133 | ||
| D5 | 215 | 0 | 84 | 84 | ||
| D6 | 350 | 0 | 10 | 10 | ||
| D7 | 163 | 0 | 126 | 126 | ||
| D8 | 244 | 0 | 42 | 42 | ||
| D9 | 360 | 0 | 0 | 0 | ||
| D10 | 126 | 0 | 102 | 102 | ||
| 平均值 | 224.4 | 0.0 | 63.7 | 63.7 | ||
| 標準偏差 | 24.3 | 0.0 | 14.7 | 14.7 |
統計分析:如表 5 至 14
中所顯示,使用T檢驗、單變數檢驗及鄧恩檢驗(Dunnett’s tests)測試表 4
中之結果之顯著性。表 5. 不動潛伏期結果之 T 檢驗
表 6. 不動潛伏期結果之顯著性的單變數檢驗 (Guadalupe)
表 7. 不動潛伏期結果之鄧恩檢驗 (Guadalupe)
表 8. 2 至 6 分鐘結果之 T 檢驗
表 9. 2 至 6 分鐘結果之顯著性的單變數檢驗 (Guadalupe)
表 10. 2 至 6 分鐘結果之鄧恩檢驗 (Guadalupe)
表 11. 0 至 6 分鐘結果之 T 檢驗
表 12. 0 至 6 分鐘結果之顯著性的單變數檢驗 (Guadalupe)
表 13. 0 至 6 分鐘結果之鄧恩檢驗 (Guadalupe)
| 媒劑 | 1 mg/kg | 3 mg/kg | 丙咪嗪 | |
| 80 | 77 | 135 | 224 | |
| 106 | 84 | 165 | 213 | |
| 200 | 206 | 155 | 180 | |
| 79 | 100 | 86 | 169 | |
| 91 | 70 | 150 | 215 | |
| 90 | 109 | 127 | 350 | |
| 99 | 144 | 192 | 163 | |
| 91 | 105 | 162 | 244 | |
| 79 | 130 | 83 | 360 | |
| 93 | 80 | 105 | 126 | |
| T 檢驗(1 個尾) | 0.290 | 0.021 | 0.000 | |
| T 檢驗(2 個尾) | 0.581 | 0.042 | 0.000 |
| 作用 | Sigma限制參數化 有效假設分解;標準估計誤差50.44372 | ||||
| SS | 自由度 | MS | F | P | |
| 截距 | 817102.2 | 1 | 817102.2 | 321.1161 | 0.000000 |
| 治療組 | 95120.3 | 3 | 31706.8 | 12.4606 | 0.000010 |
| 誤差 | 91604.5 | 36 | 2544.6 |
| 細胞編號 | 事後檢驗(Post Hoc Tests)之概率(2側) 誤差:之間的MSE = 2544.6,df = 36.000 | |
| 治療組 | {1} 100.80 | |
| 1 | 媒劑 | |
| 2 | 1 mg | 0.949581 |
| 3 | 3 mg | 0.290085 |
| 4 | 丙咪嗪30 mg | 0.000018 |
| 媒劑 | 1 mg/kg | 3 mg/kg | 丙咪嗪 | |
| 222 | 142 | 166 | 32 | |
| 226 | 170 | 144 | 45 | |
| 188 | 33 | 122 | 63 | |
| 209 | 109 | 184 | 133 | |
| 119 | 149 | 82 | 84 | |
| 148 | 192 | 146 | 10 | |
| 190 | 134 | 101 | 126 | |
| 199 | 189 | 90 | 42 | |
| 121 | 141 | 163 | 0 | |
| 192 | 150 | 166 | 102 | |
| T 檢驗(1 個尾) | 0.023 | 0.007 | 0.000 | |
| T 檢驗(2 個尾) | 0.046 | 0.015 | 0.000 |
| 作用 | Sigma限制參數化 有效假設分解;標準估計誤差41.83426 | ||||
| SS | 自由度 | MS | F | P | |
| 截距 | 682254.4 | 1 | 682254.5 | 389.8361 | 0.000000 |
| 治療組 | 71959.8 | 3 | 23986.6 | 13.7058 | 0.000004 |
| 誤差 | 63003.8 | 36 | 1750.1 |
| 細胞編號 | 事後檢驗之概率(2側) 誤差:之間的MSE = 1750.1,df = 36.000 | |
| 治療組 | {1} 181.40 | |
| 1 | 媒劑 | |
| 2 | 1 mg | 0.093513 |
| 3 | 3 mg | 0.055570 |
| 4 | 丙咪嗪30 mg | 0.000008 |
| 媒劑 | 1 mg/kg | 3 mg/kg | 丙咪嗪 | |
| 261 | 174 | 166 | 32 | |
| 239 | 198 | 144 | 45 | |
| 188 | 33 | 122 | 63 | |
| 247 | 125 | 207 | 133 | |
| 141 | 169 | 82 | 84 | |
| 168 | 196 | 146 | 10 | |
| 210 | 134 | 101 | 126 | |
| 204 | 196 | 90 | 42 | |
| 136 | 141 | 184 | 0 | |
| 216 | 170 | 181 | 102 | |
| T 檢驗(1 個尾) | 0.018 | 0.003 | 0.000 | |
| T 檢驗(2 個尾) | 0.035 | 0.007 | 0.000 |
| 作用 | Sigma限制參數化 有效假設分解;標準估計誤差45.57429 | ||||
| SS | 自由度 | MS | F | P | |
| 截距 | 785680.9 | 1 | 785680.9 | 378.2738 | 0.000000 |
| 治療組 | 97328.5 | 3 | 32442.8 | 15.6199 | 0.000001 |
| 誤差 | 74772.6 | 36 | 2077.0 |
| 細胞編號 | 事後檢驗之概率(2側) 誤差:之間的MSE = 2077.0,df = 36.000 | |
| 治療組 | {1} 201.00 | |
| 1 | 媒劑 | |
| 2 | 1 mg | 0.066283 |
| 3 | 3 mg | 0.018039 |
| 4 | 丙咪嗪30 mg | 0.000008 |
表 5 至 13
顯示化合物A在小鼠強迫游泳試驗模型中顯示統計學顯著作用。例如,就不動潛伏期、2至6分鐘及0至6分鐘結果而言,3 mg/kg劑量之2尾T檢驗評分分別為0.042、0.015及0.007(例如<0.05)。
血液及腦採集:強迫游泳試驗後,立即用異氟烷吸入劑麻醉所有經給予測試物品之動物,且經由心臟穿刺進行末梢血採集(~1 ml)至EDTA鉀血採集管(SOP ROD.14.02)中。藉由在4℃下以3000 rpm離心5分鐘自全血分離血漿。分離後,立刻將血漿置於冷凍管中且在-80℃下冷凍直至運輸以進行生物分析。血液採集後,按照標準操作程序(SOP ROD.59)將動物斷頭且採集整個腦。稱重腦,快速冷凍,且在-80℃下儲存直至運輸。化合物A之血液及腦濃度顯示於圖4中。1及3 mg/kg兩種劑量之總腦與血漿比(B/P
比)為2.2,表明體內良好的CNS滲透。
5.2. 實例2. 尾懸掛試驗
尾懸掛試驗(TST)已成為用於評定小鼠抗憂鬱樣活動之最廣泛使用的模型之一。該試驗係基於受到短期、不可避免之壓力懸掛其尾之動物將發展不動姿勢之事實。協定描述於Cryan, J.F.等人,Neurosci. Biobehav. Rev. 2005,29:571-625中。
描述:該設備由各三個籠的兩個懸掛單元所組成且能夠使六隻小鼠同時進行測試。使用膠帶將每隻小鼠的尾巴懸掛在連接至應變計之鉤子。應變計拾取小鼠之所有運動且將其傳輸至中央單元,該中央單元將信號數字化。使用LED視覺上展現信號,此允許在線驗證各單元之良好運作。中央單元中包括程度過濾裝置(1至9),其可經設置至所需靈敏度以提供整個身體運動與動物或其內部器官之其他微運動的最大區別。
參數:「不動持續時間」為測量的主要參數。此係自動物運動不會超過藉由程度過濾裝置確定的閾值之期間的累積時間計算得。動物在測試期間消耗的「能量」係藉由以任意單位表示的個別運動之累積幅度來測量。自動物在測試期間消耗的總能量除以動物活動的總時間(任意單位)來計算「運動之力量」。對於所有三個參數,電腦提供資料採集,實驗時間表之生成(隨機化)及結果分組(自動計算每個治療組之平均值、中位數及SEM)。
程序:在測試當天,將小鼠自圈養聚居室移至測試實驗室(在運輸期間,籠子經覆蓋過濾器),在該處立即移去過濾器覆蓋且在該處於進行測試之前使小鼠保持不受打擾至少1小時。然後用藥物處理小鼠,且然後在處理1小時(PO)或30分鐘(IP)後,根據隨機化方案將小鼠藉由尾巴(例如用膠帶)懸掛在TST設備中。測試持續6分鐘以獲得所有三個參數之測量值。實驗在08:00與12:30之間進行。通常,每個治療組使用12隻小鼠。
藥物處理:以描述於以上實例1之表 2
中之濃度調配及投與化合物A及丙咪嗪且在TST之前30分鐘給予。對於各實驗,包括至少一個對照組,在嚴格相同的實驗條件下平行地處理及進行測試。
統計:對於各實驗,使用單向變異數分析(ANOVA)評定參數「不動時間」之統計顯著性,然後在適當時使用鄧恩檢驗進行事後分析。若參數常態性「能量」及「運動之力量」檢驗失敗,則使用Kruskal–Wallis等級間單向變異數分析然後在適當時使用鄧恩檢驗進行事後分析來進行組間比較。對於所有三個參數,p<0.05之值被認為統計學上顯著。
5.3. 實例3. 蔗糖偏愛及顱內自我刺激
蔗糖攝入及顱內自我刺激(ICSS)係囓齒動物中慢性輕度壓力(CMS)引起之行為缺陷之享樂措施。協定描述於Nielsen, C.K.等人,Behav. Brain Res. 2000,107:21-33中。使用CMS模型進行研究以評定化合物A之潛在功效。
個體:使用雄性韋斯(Wistar)大鼠及雄性Pieball Virol Glaxo (PVG)連帽大鼠(hooded rats),在研究開始時,體重分別為250至300 g及220至240 g。將大鼠單獨或成對飼養在聚碳酸酯籠中且維持於12小時光照:黑暗循環(在06:00點燈)。除非檢驗要求,否則動物可自由獲取食物及水。自動控制溫度(22±1℃)、相對濕度(55±5%)及空氣交換(每小時16次)。所有實驗期間每週測量體重。
藥物處理:壓力方案及/或顱內自我刺激期間,每天以描述於以上實例1之表 2
中之濃度調配及投與化合物A及丙咪嗪。對於各實驗,包括至少一個對照組,在嚴格相同的實驗條件下平行地處理及進行測試。
壓力方案:使用兩種不同的壓力方案(CMS-1及CMS-2)。CMS-1之每週均由兩個時段(8及19小時)之食物剝奪;三個時段(6、7及19小時)之水分剝奪;2個時段(7及16小時)之籠傾斜(45°);兩個17小時時段之成對飼養;一個17小時時段在骯髒籠(200 ml水,在100 g鋸末床中)中;一個6小時時段之低強度頻閃照明(150次閃爍:分鐘);及48小時之光照:黑暗反轉組成。CMS-2之每週均由一個17小時時段之生物及水分剝奪,緊接著2小時之限制食物獲取;一個17小時時段之水分剝奪,緊接著1小時暴露於空瓶;一個17小時時段在骯髒籠(200 ml水,在100 g鋸末床中)中成對飼養;八個1小時時段之禁閉於小籠(25x10x10 cm);一個時段之過夜照明;及64小時之週末期間的反轉光照:黑暗週期組成。
5.3.1 享樂措施
蔗糖攝入:每週兩次(週二及週五)獲取大鼠(用於一些實驗之韋斯大鼠及用於其他實驗之PVG連帽大鼠)以消耗1%蔗糖溶液。獲取係由8至10個1小時基線檢驗組成,其中在20小時時段之食物及水分剝奪後,將蔗糖溶液放入其居住籠(home cage)中。藉由在檢驗之前及之後稱量瓶子來測量蔗糖攝入。在穩定基線水平後,在整個實驗中,在CMS協定期間,在相似條件下,以每週時間間隔(週三)測量蔗糖消耗。蔗糖檢驗前的食物及水分剝奪係壓力源,包括在CMS方案中的後續壓力源施加於該壓力源上,先前壓力源歷史並未在任何後續分析中予以考慮。
顱內自我刺激:將大鼠(用於一些實驗之韋斯大鼠及用於其他實驗之PVG連帽大鼠)成對飼養且允許在手術前適應2週。將其麻醉且以門齒桿位於耳間線以下2.7 mm固定在立體定位框架中。將不銹鋼雙極電極以電極尖端相隔0.5 mm單側植入腹側蓋膜區域(VTA)中。所使用的座標為耳間線前3.2 mm、中線側0.6 mm及顱表面腹側8.2 mm。使用五個不銹鋼螺釘及牙科用黏固劑以將電極組件固定於顱骨。術後兩週,訓練各大鼠進行鼻探索(nose-poke)來報償置於聲音衰減盒中之檢驗腔室內的顱內電刺激。將鼻探索入位於側壁中地板上方1 cm的孔(直徑2.5 cm)中會中斷會聚光束,藉此引起透過恆定電流刺激器傳遞的腦刺激。各鼻探索產生0.5秒的單相方波脈衝串,各脈衝持續時間為0.1毫秒。刺激依固定時間間隔1秒強化時間表傳遞以迴避極端刺激密度。電刺激及資料記錄透過電腦及介面進行控制。首先以70 Hz之固定刺激頻率及個別選擇的電流強度(70至300 mA)對大鼠進行訓練以維持最高可能反應率而不引起運動障礙。其每天以40分鐘時程進行訓練,持續約3週。隨後,藉由在維持電流強度恆定的同時逐步改變頻率來建立速率-頻率曲線。以2分鐘時間間隔,降低頻率且然後在範圍1.1至1.9 log Hz (10至85 Hz)內以0.05至0.2 log單位步進增加。各時程包含針對各頻率之15次離散型2分鐘試驗,其中在各試驗開始時進行1次啟動刺激。使用遞減系列之頻率作為熱身階段;亦即;在後續計算中僅使用自遞升階段獲得的資料。分別選擇遞增系列之頻率以產生分別在最大及最小反應率下具有至少兩個相鄰點之遞升曲線。此研究採用曲線變換方法之速率-頻率形式來評定CMS對報償之作用。速率-頻率函數之特性,特別是關於基於操作性馬達:性能能力之分離ICSS報償作用,已得到廣泛驗證及研究。藉由確定將支持最大反應率之50%之頻率(有效頻率(EF50
))來評定ICSS行為。基於「虛線」原理,描述估算EF50之數學模型。此方法給出可靠且穩定之EF50
估算。藉由將觀測到的反應率(鼻探索(NP):2分鐘試驗)模型化為所施加頻率(F)之log10的函數,生成各大鼠之每一檢驗日遞升速率-頻率曲線。該函數由三個線性分段;至最小反應(NPmin
)之水平下漸近線、至最大反應(NPmax
)之水平上漸近線及漸近線之間的線性過渡(a + b*F)組成。僅包括最後一個NPmin
與第一個NPmax
之間的數據(M
)。此可藉由以下公式描述:
1. 考慮M
= {(F
, NP(F
)|max{F|NP(F
) = NPmin
}
≤F
≤ min{F
|NP(F
) NPmax
}}|
2. 藉由最小二乘方程序將f
(F
) min(max(a + b*F, NPmin
), NPmax
)擬合至M中的數據。在不明確之情況下,使用具有最小b之函數。
確定有效頻率(EF50
),定義為將支持最大反應率之50%之頻率。沿著模擬頻率軸之橫向曲線移動,亦即EF50
變化,將反映刺激之報償效用變化。每週兩次(週二及週五)進行速率-頻率測試。當最大反應顯示沒有遞增或遞減傾向且當EF50
改變小於10至12%時,達成穩定反應。隨後將動物分為兩個匹配的組。
5.3.2 實驗之設計
暴露於CMS-1方案之韋斯大鼠中於蔗糖攝入之作用(參見上述):在實驗開始前4週將韋斯大鼠帶入實驗室。除非壓力協定要求,否則將動物單獨飼養。根據基線蔗糖攝入,將動物分為兩個匹配的組。一組大鼠接受CMS-1 6週時間,而另一組維持在標準實驗室條件。
暴露於CMS-1方案之PVG連帽大鼠中於蔗糖攝入之作用(參見上述):在實驗開始前3週將PVG連帽大鼠帶入實驗室。除非壓力協定要求,否則將動物單獨飼養。根據基線蔗糖攝入,將動物分為兩個匹配的組。一組大鼠接受CMS-1 9週時間,而另一組維持在標準實驗室條件。
暴露於CMS-2方案之韋斯大鼠中於ICSS之作用(參見上述):將韋斯大鼠分為一組,單獨飼養且接受10週之CMS-2,及另一組(對照組)在標準實驗室條件下配對飼養。每週兩次確定其EF50
且針對各個別大鼠進行與最後兩次基線測試之平均值之比較。
大鼠應變及壓力方案於ICSS行為之作用(參見上述):將韋斯大鼠分為三個匹配的組;一對照組及兩個分別接受9週之CMS-1及CMS-2之組。將PVG大鼠分為兩個匹配的組;一組接受9週之CMS-2及另一組(對照組)維持在標準實驗室條件。對照組成對飼養。除非壓力協定要求,否則將壓力組中的大鼠單獨飼養。每週兩次確定其EF50
且針對各個別大鼠進行與最後兩次基線測試之平均值之比較。
組織學:完成ICSS測試後,將動物殺死且取出腦並保存在80℃下。在低溫恆溫器上切下12 mm切片,然後用甲苯酚紫染色。電極尖端放置基於Paxinos及Watson立體定位圖譜之額面來確定。
統計分析:除了比較對照組與壓力組測試之間的蔗糖攝入及ICSS資料之常態性或變異數均一性之外,亦可藉由非參數統計來評估資料。基於等級進行雙向變異數分析(ANOVA),將天數及處理(壓力)作為因子及將動物嵌套在處理中,此意指一組參數僅對應於一種觀測。因此,所有觀測均係獨立的。在ICSS實驗中,可能存在壓力組之子分類。若受壓力之動物之總平均反應超過對照組之最大平均反應,則將其歸類為子組。在壓力(子組及主要組)與對照組之間之比較之前,藉由基於等級之雙向ANOVA,將天數及組作為因子及將動物嵌套在組中來比較壓力子組及主要組之反應。每天藉由非成對t檢驗追蹤對治療的顯著主要作用(p<0.05)。為了清晰起見,蔗糖攝入資料及ICSS資料均可表示為平均值±SEM,但仍進行非參數分析。藉由單向或雙向ANOVA來分析通過常態性及變異數均一性測試之體重資料。藉由Tukey檢驗及/或使用基於等級之Kruskal–Wallis ANOVA進行多次比較。
5.4. 實例4. 新穎誘發之食慾不振
新穎產生的進食之抑制(稱為「新環境食慾不振(hyponeophagia)」)提供對慢性(而非急性或亞慢性抗憂鬱治療)作用敏感之焦慮相關措施。協定描述於Dulawa, S.C.及Hen, R.,Neurosci. Biobehav. Rev. 2005,29:771-83中。
個體選擇:使雄性Balb/cJ小鼠維持12 L:12 D時間表(在06:00點燈)且以五隻相同類型小鼠分組飼養。隨意提供食物及水。行為測試在光照階段期間於07:00與17:00之間進行。
設備及程序:以描述於以上實例1之表 2
中之濃度調配及投與化合物A及丙咪嗪,在測試前至少30分鐘施用。藉由利用螢光檢測之液相層析確定化合物A血漿濃度。
慢性測試:給予雄性Balb/cJ小鼠(例如每天1及3 mg/kg化合物A)。將個別小鼠組用於亞慢性與慢性實驗。在治療的第23天,單獨飼養小鼠。訓練小鼠連續三天(第25天至第27天)喝甜煉乳。每天對小鼠提供經稀釋之甜煉乳(1:3;牛奶:水) 30分鐘。牛奶以吸口附著封膜(Parafilm)之10 ml血清吸移管方式提供。吸移管用橡膠塞封閉且透過金屬絲籠蓋定位。居住籠測試在第28天進行,在第28天將小鼠自其籠短暫移出以定位含有牛奶之吸移管,且在將小鼠返送至其籠時開始進行測試。每5分鐘記錄飲用潛伏期及消耗的體積,持續30分鐘。居住籠測試在昏暗照明(約50 lux)下進行。新穎籠式測試在第29天進行,在第29天將小鼠置於設置有含有牛奶之吸移管之尺寸相同但沒有刨花之新乾淨籠中。新穎籠式測試在明亮照明(約1200 lux)下進行,其中在籠下方放置白紙以增強厭惡性。實驗中排除在30分鐘居住籠式測試期間從未飲用的小鼠,因為據推測在訓練期間從未學會喝牛奶。使用另外一組雄性Balb/cJ小鼠(經給予(例如每天1及3 mg/kg化合物A))來實施亞慢性測試。將小鼠單獨飼養,且然後在治療的第1天開始訓練喝牛奶。訓練小鼠在第1天至第3天喝甜煉乳。然後在亞慢性處理4天(居住籠)及5天(新穎籠)後,對其進行新穎誘發之食慾不振測試。
5.5. 實例5. 習得無助模型
習得無助範例係一種憂鬱模型,其中動物暴露於不可預測且不可控制之壓力(例如電擊),且於隨後發展出厭惡但可逃避情況之應對缺陷。協定描述於Chourbaji, S.等人,Brain Res. Protoc. 2005,16:70-8中。
材料:在配備不銹鋼格柵地板(各格柵之直徑:0.5 cm,間距:0.6 cm)之透明有機玻璃電擊腔室(18x18x30 cm3
)中施行電擊程序。在兩隔間穿梭箱中實施雙向迴避測試,該穿梭箱在兩個隔間中之各者的底部均配備紅外光束以分別監測自發穿梭以及對光(條件式)或厭惡性足部電擊(無條件式)刺激之行為反應。穿梭箱由經小門(6 cm寬及7 cm高)隔開之大小相等的隔間(18x18x30 cm3
)組成。穿梭箱之兩個隔間均含有格柵地板(各格柵之直徑:0.5 cm,距離:0.6 cm),通過該格柵地板施加電流,且各隔間之頂部均有信號燈。設計分別用於電擊程序及穿梭箱測試之協定圖表。
熱板:為排除改變的疼痛敏感性作為混淆因素,所有小鼠均在熱板上進行測試。
藥理學處理:該模型利用以描述於以上實例1之表 2
中之濃度調配及投與之化合物A及丙咪嗪進行藥理學驗證,在進行測試前至少30分鐘施用。獲得化合物A之能力來復原於穿梭箱中之無助行為。
動物:購買10週大的雄性C57BL/6N小鼠且在實驗之前於恆定條件下以12小時黑暗-照明週期及22℃之平均室溫適應在聚碳酸酯籠(II型)中之單獨飼養2週,可隨意獲取食物及水。
不可避免之電擊程序:
1. 小鼠在其活動(黑暗)階段期間暴露於不可避免之電擊。將動物在其居住籠中運送至實驗室,且然後放入電擊室。
2. 電擊程序包含連續兩天進行360次打亂足部電擊(0.150 mA)。足部電擊係不可預測的,其具有變化的持續時間(1至3秒)及間隔發作(1至15秒),總時程持續時間總共約52分鐘。在電擊暴露期間,關閉燈。
3. 對照動物經歷相同處理及情境程序,而不接受足部電擊。藉由用70%乙醇徹底清潔,應注意將不接受電擊之對照動物暴露於電擊腔室而不會因經電擊小鼠之氣味而感到不適。每天用肥皂清潔以防止潛在警報物質固定。
習得無助之評定:第二電擊程序後24小時,藉由測試穿梭箱性能來評定動物在黑暗期之習得無助。各試驗均以5秒之光照刺激開始,宣布隨後的最長10秒持續時間之足部電擊(強度:0.150 mA)。試驗間隔(intertrial interval)為30秒。定義以下行為反應:「迴避(avoidance)」為藉由立即更換至另一個隔間而對光刺激之適當反應,「逃逸(escape)」為如對電擊之反應穿梭至另一隔間,而在未嘗試逃逸時為「失敗」。此外,將參數逃逸潛伏期記錄為在足部電擊開始後穿梭至另一隔間中所需的時間。為確定總體活動,記錄第一次足部電擊之前的穿梭(初始活動)以及兩次試驗之間的活動(試驗間隔活動或ITI)。無助測試之總時間持續約20至24分鐘,確切時間取決於動物學習範例及正確做出反應之能力。在各試驗之前,用70%乙醇徹底清洗設備。為強調「真實」習得無助作用之評定(其仰賴於壓力之不可控制性),測試另一動物群組之免疫作用。將此等動物暴露於與在穿梭箱中之習得無助測試相同的預時程,其中該等動物經歷可控之電擊情況。此外,監測預暴露期間之初始活動。
疼痛敏感性:為藉由可影響電擊作用之改變的疼痛敏感性來排除潛在假影,在習得無助程序之前,在52℃之溫度下在熱板上測試一子組之小鼠。監測第一反應(跳躍或舔後爪)之潛伏期。
定義無助:於評定行為參數後,經電擊之動物根據其在穿梭箱測試中之表現歸類為「無助」或「抗性」。將失敗及逃逸潛伏期視為無助之指標,及將k均值(k = 2)叢集演算法應用於接受所述協定之小鼠之資料池。將失敗次數及逃逸潛伏期用作個別動物之表現分數,因為此等失敗次數及逃逸潛伏期係最通常報導的無助指標。此等行為指標經標準化(亦即轉換為Z分數)以防止各變數之範圍差異,其可產生偏差,且然後被無意地用於實施叢集過程。藉助於兩步驟判別式經典分析進一步完善該分類,該分析亦提供遵循此協定識別無助/非無助小鼠之分類公式。
藥理學驗證:協定中對另外的C57BL/6N小鼠進行訓練及測試。在任何藥理學處理之前,使用先前獲得的分類公式(例如定義以上無助),將此等小鼠分類為「無助」或「非無助」,其中考慮失敗次數及逃逸潛伏期。約10天之無助之持續時間要求5至6天之短時間、化合物A處理時間間隔。因此,動物進行5天的化合物A方案。在第6天,協定中對動物進行再測試。再次使用分類公式對各個體進行分類,但現將再測試時程之值用於計算。化合物A處理後此類別取向分類之變化(亦即小鼠自「無助」組變為「非無助」組)被視為所提供的無助操作定義的敏感性指標。藉由在藥理學處理之前/之後評定平方馬氏距離(squared Mahalanobis distance)至非無助組之質心之變化來補償該分析以獲得化合物A作用之連續而非分類之指標。
* * * * *
本說明書中提及的所有美國專利、美國專利申請公開案、美國專利申請案、外國專利、外國專利申請案及非專利公開案之全文均以引用之方式併入本文中。
儘管已略為詳細地描述前述組合物、方法及用途以促進理解,但應明瞭可在隨附申請專利範圍之範疇內實踐某些改變及修改。因此,所描述的實施例應被認為係例示性而不是限制性,及所主張的發明不限於本文所給出的詳細內容,而係可在隨附申請專利範圍之範疇及等效物內進行修改。
圖1顯示小鼠強迫游泳試驗之結果,其包括媒劑、1 mg/kg化合物A、3 mg/kg化合物A及丙咪嗪(imipramine)給藥(x軸)之平均不動潛伏期時間(秒,y軸)之圖形表示。
圖2顯示小鼠強迫游泳試驗之結果,其包括媒劑、1 mg/kg化合物A、3 mg/kg化合物A及丙咪嗪給藥(x軸)之平均不動時間(2至6分鐘)(秒,y軸)之圖形表示。
圖3顯示小鼠強迫游泳試驗之結果,其包括媒劑、1 mg/kg化合物A、3 mg/kg化合物A及丙咪嗪給藥(x軸)之平均不動時間(0至6分鐘)(秒,y軸)之圖形表示。
圖4包括1 mg/kg及3 mg/kg給藥(x軸)之血漿及腦中化合物A濃度(µM,y軸)之圖形表示。
Claims (50)
- 一種治療有此需要的人類之憂鬱症之方法,該方法包含對該人類投與治療有效量之化合物A; 其中化合物A為N -[4-(6-氟-3,4-二氫-1H -異喹啉-2-基)-2,6-二甲基苯基]-3,3-二甲基丁醯胺。
- 如請求項1之方法,其中該方法包含增強開放人類中之Kv7鉀通道。
- 一種增強開放人類中之Kv7鉀通道之方法,該方法包含對該人類投與有效量之化合物A; 其中化合物A為N -[4-(6-氟-3,4-二氫-1H -異喹啉-2-基)-2,6-二甲基苯基]-3,3-二甲基丁醯胺;及 其中該人類患有憂鬱症。
- 如請求項2或3之方法,其中該Kv7鉀通道為Kv7.2、Kv7.3、Kv7.4或Kv7.5中之一者或多者。
- 如請求項4之方法,其中該方法相對於Kv7.1而言選擇性增強開放Kv7.2、Kv7.3、Kv7.4或Kv7.5中之一者或多者。
- 如請求項2之方法,其中該方法包含開放Kv7.2/Kv7.3 (KCNQ2/3)鉀通道。
- 如請求項1至6中任一項之方法,其中該憂鬱症為重度憂鬱症(MDD)、侵擾性情緒失調症、持續性憂鬱症、雙極性病譜型病症(bipolar spectrum disorder)、產後憂鬱、經期前情緒障礙(PMDD)、季節性情感障礙(SAD)、非典型憂鬱、難治型憂鬱(TRD)、與躁動或焦慮相關之憂鬱、失調症伴情緒低落、長時間憂鬱反應或其組合。
- 如請求項1至7中任一項之方法,其中該憂鬱症為重度憂鬱症(MDD)。
- 如請求項1至8中任一項之方法,其中化合物A係經口投與該人類。
- 如請求項1至9中任一項之方法,其中化合物A係以2至200 mg之劑量投與該人類。
- 如請求項10之方法,其中化合物A係以2至100 mg之劑量投與該人類。
- 如請求項10之方法,其中化合物A係以5至50 mg之劑量投與該人類。
- 如請求項10之方法,其中化合物A係以10、20或25 mg之劑量投與該人類。
- 如請求項10之方法,其中化合物A係以20 mg之劑量投與該人類。
- 如請求項1至9中任一項之方法,其中化合物A係以至少20 mg之劑量投與該人類。
- 如請求項15之方法,其中化合物A係以至少50 mg之劑量投與該人類。
- 如請求項15之方法,其中化合物A係以至少100 mg之劑量投與該人類。
- 如請求項1至9中任一項之方法,其中化合物A係以每天5至1000 mg之劑量投與該人類。
- 如請求項18之方法,其中化合物A係以每天5至500 mg之劑量投與該人類。
- 如請求項18之方法,其中化合物A係以每天5至250 mg之劑量投與該人類。
- 如請求項18之方法,其中化合物A係以每天20至150 mg之劑量投與該人類。
- 如請求項18之方法,其中化合物A係以每天100 mg之劑量投與該人類。
- 如請求項1至22中任一項之方法,其中化合物A係以0.05至2.0 mg/kg之劑量投與該人類。
- 如請求項23之方法,其中化合物A係以0.1至1.0 mg/kg之劑量投與該人類。
- 如請求項23之方法,其中化合物A係以0.2至0.5 mg/kg之劑量投與該人類。
- 一種化合物A於製造用於治療有此需要的人類之憂鬱症的藥物之用途; 其中化合物A為N -[4-(6-氟-3,4-二氫-1H -異喹啉-2-基)-2,6-二甲基苯基]-3,3-二甲基丁醯胺。
- 如請求項26之用途,其中治療憂鬱症包含增強開放人類中之Kv7鉀通道。
- 一種化合物A於製造用於增強開放人類中之Kv7鉀通道的藥物之用途; 其中化合物A為N -[4-(6-氟-3,4-二氫-1H -異喹啉-2-基)-2,6-二甲基苯基]-3,3-二甲基丁醯胺;及 其中該人類患有憂鬱症。
- 如請求項27或28之用途,其中該Kv7鉀通道為Kv7.2、Kv7.3、Kv7.4或Kv7.5中之一者或多者。
- 如請求項29之用途,其中增強開放Kv7鉀通道係相對於Kv7.1而言選擇性增強開放Kv7.2、Kv7.3、Kv7.4或Kv7.5中之一者或多者。
- 如請求項27之用途,其中增強開放Kv7鉀通道包含開放Kv7.2/Kv7.3 (KCNQ2/3)鉀通道。
- 如請求項26至31中任一項之用途,其中該憂鬱症為重度憂鬱症(MDD)、侵擾性情緒失調症、持續性憂鬱症、雙極性病譜型病症、產後憂鬱、經期前情緒障礙(PMDD)、季節性情感障礙(SAD)、非典型憂鬱、難治型憂鬱(TRD)、與躁動或焦慮相關之憂鬱、失調症伴情緒低落、長時間憂鬱反應或其組合。
- 如請求項26至32中任一項之用途,其中該憂鬱症為重度憂鬱症(MDD)。
- 如請求項26至33中任一項之用途,其中化合物A係經口投與該人類。
- 如請求項26至34中任一項之用途,其中化合物A係以2至200 mg之劑量投與該人類。
- 如請求項35之用途,其中化合物A係以2至100 mg之劑量投與該人類。
- 如請求項35之用途,其中化合物A係以5至50 mg之劑量投與該人類。
- 如請求項35之用途,其中化合物A係以10、20或25 mg之劑量投與該人類。
- 如請求項35之用途,其中化合物A係以20 mg之劑量投與該人類。
- 如請求項26至34中任一項之用途,其中化合物A係以至少20 mg之劑量投與該人類。
- 如請求項40之用途,其中化合物A係以至少50 mg之劑量投與該人類。
- 如請求項40之用途,其中化合物A係以至少100 mg之劑量投與該人類。
- 如請求項26至34中任一項之用途,其中化合物A係以每天5至1000 mg之劑量投與該人類。
- 如請求項43之用途,其中化合物A係以每天5至500 mg之劑量投與該人類。
- 如請求項43之用途,其中化合物A係以每天5至250 mg之劑量投與該人類。
- 如請求項43之用途,其中化合物A係以每天20至150 mg之劑量投與該人類。
- 如請求項43之用途,其中化合物A係以每天100 mg之劑量投與該人類。
- 如請求項1至47中任一項之用途,其中化合物A係以0.05至2.0 mg/kg之劑量投與該人類。
- 如請求項48之用途,其中化合物A係以0.1至1.0 mg/kg之劑量投與該人類。
- 如請求項48之用途,其中化合物A係以0.2至0.5 mg/kg之劑量投與該人類。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962932724P | 2019-11-08 | 2019-11-08 | |
| US62/932,724 | 2019-11-08 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202128162A true TW202128162A (zh) | 2021-08-01 |
Family
ID=73643360
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW109138929A TW202128162A (zh) | 2019-11-08 | 2020-11-06 | 憂鬱症之治療方法 |
Country Status (19)
| Country | Link |
|---|---|
| US (2) | US12178811B2 (zh) |
| EP (1) | EP4054580A1 (zh) |
| JP (2) | JP2022553569A (zh) |
| KR (1) | KR20220098746A (zh) |
| CN (1) | CN114667146A (zh) |
| AU (1) | AU2020380961A1 (zh) |
| BR (1) | BR112022008580A2 (zh) |
| CA (1) | CA3155812A1 (zh) |
| CL (1) | CL2022001102A1 (zh) |
| CO (1) | CO2022008001A2 (zh) |
| CR (1) | CR20220250A (zh) |
| GE (2) | GEP20257732B (zh) |
| IL (1) | IL292678A (zh) |
| MA (1) | MA56607A1 (zh) |
| MX (1) | MX2022005490A (zh) |
| PE (1) | PE20221766A1 (zh) |
| PH (1) | PH12022551110A1 (zh) |
| TW (1) | TW202128162A (zh) |
| WO (1) | WO2021092439A1 (zh) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GEP20257732B (en) | 2019-11-08 | 2025-02-10 | Xenon Pharmaceuticals Inc | Methods of treating depressive disorders |
| US20230015539A1 (en) | 2019-12-06 | 2023-01-19 | Icahn School Of Medicine At Mount Sinai | Method of treatment with kcnq channel openers |
| EP4291185A1 (en) * | 2021-02-09 | 2023-12-20 | Xenon Pharmaceuticals Inc. | Conjoint therapy for treating seizure disorders |
| KR20240004241A (ko) * | 2021-02-09 | 2024-01-11 | 제논 파마슈티칼스 인크. | 무쾌감증의 치료에 사용하기 위한 전압-게이트 칼륨 채널 오프너 |
Family Cites Families (102)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3639385A (en) | 1968-07-26 | 1972-02-01 | Eastman Kodak Co | Heterocyclic monoazo compounds from n n-diaralkyl anilines and polyester textile materials dyed therewith |
| US3845770A (en) | 1972-06-05 | 1974-11-05 | Alza Corp | Osmatic dispensing device for releasing beneficial agent |
| US4181803A (en) | 1973-12-14 | 1980-01-01 | Eisai Co., Ltd. | Propiophenone derivatives and preparation thereof |
| US4326525A (en) | 1980-10-14 | 1982-04-27 | Alza Corporation | Osmotic device that improves delivery properties of agent in situ |
| DE3337593A1 (de) | 1982-10-27 | 1984-05-03 | Degussa Ag, 6000 Frankfurt | 2-amino-3-acylamino-6-benzylamino-pyridin-derivate mit antiepileptischer wirkung |
| DE3369315D1 (en) | 1982-10-27 | 1987-02-26 | Degussa | Derivatives of 2-amino-3-acylamino-6-benzylamino pyridine with an anti-epileptic activity |
| DE3665538D1 (en) | 1985-01-23 | 1989-10-19 | Asta Pharma Ag | Synergistic combination of flupirtin and non-steroidal anti-phlogistics |
| DE3604575A1 (de) | 1985-02-23 | 1986-08-28 | Degussa Ag, 6000 Frankfurt | Kombination von flupirtin und anticholinergisch wirkenden spasmolytika |
| ATE43789T1 (de) | 1985-02-23 | 1989-06-15 | Asta Pharma Ag | Kombination von flupirtin und anticholinergisch wirkenden spasmolytika. |
| JP2583067B2 (ja) | 1987-08-04 | 1997-02-19 | 住友化学工業株式会社 | モノアゾ化合物およびそれを用いて疎水性繊維材料を染色または捺染する方法 |
| GB8800199D0 (en) | 1988-01-06 | 1988-02-10 | Beecham Group Plc | Pharmaceutical preparation |
| MC2029A1 (fr) | 1988-05-16 | 1990-04-25 | Asta Pharma Ag | (n-heterocyclyl)-3 diamino-2,6 pyridines substituees et leurs n-oxydes,preparation de ces composes et leur application comme medicaments |
| US5629307A (en) | 1989-10-20 | 1997-05-13 | Olney; John W. | Use of ibogaine in reducing excitotoxic brain damage |
| US6004945A (en) | 1990-05-10 | 1999-12-21 | Fukunaga; Atsuo F. | Use of adenosine compounds to relieve pain |
| IN172468B (zh) | 1990-07-14 | 1993-08-14 | Asta Medica Ag | |
| US5643921A (en) | 1990-09-26 | 1997-07-01 | E.R. Squibb & Sons, Inc. | Cardiopulmonary bypass and organ transplant using a potassium channel activator |
| US5234947A (en) | 1991-11-07 | 1993-08-10 | New York University | Potassium channel activating compounds and methods of use thereof |
| DE4200259A1 (de) | 1992-01-08 | 1993-07-15 | Asta Medica Ag | Neue 1,2,4-triaminobenzol-derivate und verfahren zu deren herstellung |
| US5262419A (en) | 1992-06-11 | 1993-11-16 | E. R. Squibb & Sons, Inc. | Method for the prophylaxis and/or treatment of ulcerative gastrointestinal conditions using a potassium channel activator |
| CA2115792C (en) | 1993-03-05 | 2005-11-01 | David J. Mayer | Method for the treatment of pain |
| US5428039A (en) | 1994-02-20 | 1995-06-27 | The Center For Innovative Technology | Method for electively achieving reversible hyperpolarized cardiac arrest |
| WO1996009044A1 (en) | 1994-09-22 | 1996-03-28 | Richard Alan Smith | Compositions useful for the preparation of medicines for treating a variety of intractable disorders |
| US5679706A (en) | 1994-09-30 | 1997-10-21 | Bristol-Myers Squibb Company | Combination of a potassium channel activator and an antiarrhythmic agent |
| MX9703988A (es) | 1994-12-12 | 1998-02-28 | Omeros Med Sys Inc | SOLUCIaN Y MÉTODO DE IRRIGACIaN PARA LA INHIBICIaN DEL DOLOR, LA INFLAMACIaN Y ES ESPASMO. |
| DE19539861A1 (de) | 1995-10-26 | 1997-04-30 | Asta Medica Ag | Verwendung von 4-Amino-4-(4-fluorbenzylamino)-1-ethoxy-carbonylaminobenzen zur Prophylaxe und Behandlung der Folgen der akuten und chronischen zerebralen Minderdurchblutung sowie neurodegenerativer Erkrankungen |
| DE19701694A1 (de) | 1997-01-20 | 1998-07-23 | Asta Medica Ag | Neue Modifikationen des 2-Amino-4-(4-fluorbenzylamino)-l-ethoxycarbonyl-aminobenzen sowie Verfahren zu ihrer Herstellung |
| US5760007A (en) | 1997-07-16 | 1998-06-02 | Ortho Pharmaceutical Corporation | Anticonvulsant derivatives useful in treating neuropathic pain |
| US6218411B1 (en) | 1997-08-08 | 2001-04-17 | Chugai Seiyaku Kabushiki Kaisha | Therapeutics for diabetic complications |
| US6593335B1 (en) | 1997-12-18 | 2003-07-15 | Abbott Laboratories | Potassium channel openers |
| US6265417B1 (en) | 1997-12-18 | 2001-07-24 | Abbott Laboratories | Potassium channel openers |
| US6211171B1 (en) | 1998-05-19 | 2001-04-03 | Dalhousie University | Use of antidepressants for local analgesia |
| JP3441970B2 (ja) | 1998-06-30 | 2003-09-02 | 株式会社サミー | 豆腐の製造方法及び製造装置 |
| CZ20012113A3 (cs) | 1998-12-14 | 2001-11-14 | Cellegy Pharmaceuticals, Inc. | Prostředky a způsoby pro léčbu onemocnění anorektální oblasti |
| US6281211B1 (en) | 1999-02-04 | 2001-08-28 | Euro-Celtique S.A. | Substituted semicarbazides and the use thereof |
| GB9903476D0 (en) | 1999-02-17 | 1999-04-07 | Zeneca Ltd | Therapeutic agents |
| JP2002538221A (ja) | 1999-03-10 | 2002-11-12 | ワーナー−ランバート・カンパニー | 抗てんかん作用を有する化合物を包含する鎮痛組成物およびその使用方法 |
| JP2003521468A (ja) | 1999-03-17 | 2003-07-15 | シグナル ファーマシューティカルズ, インコーポレイテッド | エストロゲンレセプタを変調させるための化合物及び方法 |
| AT409083B (de) | 1999-04-01 | 2002-05-27 | Sanochemia Pharmazeutika Ag | Pharmazeutische, tolperison enthaltende zubereitung zur oralen verabreichung |
| US6610324B2 (en) | 1999-04-07 | 2003-08-26 | The Mclean Hospital Corporation | Flupirtine in the treatment of fibromyalgia and related conditions |
| GB9915414D0 (en) | 1999-07-01 | 1999-09-01 | Glaxo Group Ltd | Medical use |
| PT1200073E (pt) | 1999-07-06 | 2007-03-30 | Lilly Co Eli | Antagonistas selectivos do receptor de iglur5 para o tratamento de enxaqueca |
| US6472165B1 (en) | 1999-08-03 | 2002-10-29 | Arzneimittelwerk Dresden Gmbh | Modulatory binding site in potassium channels for screening and finding new active ingredients |
| ATE380176T1 (de) | 1999-08-04 | 2007-12-15 | Icagen Inc | Benzanilide als öffner des kaliumkanals |
| JP2003506388A (ja) | 1999-08-04 | 2003-02-18 | アイカゲン インコーポレイテッド | 疼痛および不安症を処置または予防するための方法 |
| US6495550B2 (en) | 1999-08-04 | 2002-12-17 | Icagen, Inc. | Pyridine-substituted benzanilides as potassium ion channel openers |
| US6117900A (en) | 1999-09-27 | 2000-09-12 | Asta Medica Aktiengesellschaft | Use of retigabine for the treatment of neuropathic pain |
| US6383511B1 (en) | 1999-10-25 | 2002-05-07 | Epicept Corporation | Local prevention or amelioration of pain from surgically closed wounds |
| US6538004B2 (en) | 2000-03-03 | 2003-03-25 | Abbott Laboratories | Tricyclic dihydropyrazolone and tricyclic dihydroisoxazolone potassium channel openers |
| US20020015730A1 (en) | 2000-03-09 | 2002-02-07 | Torsten Hoffmann | Pharmaceutical formulations and method for making |
| TWI287984B (en) | 2000-10-17 | 2007-10-11 | Wyeth Corp | Pharmaceutical composition for modulating bladder function |
| US6589986B2 (en) | 2000-12-20 | 2003-07-08 | Wyeth | Methods of treating anxiety disorders |
| US6469042B1 (en) | 2001-02-20 | 2002-10-22 | Bristol-Myers Squibb Company | Fluoro oxindole derivatives as modulators if KCNQ potassium channels |
| AU2002338333A1 (en) | 2001-04-04 | 2002-10-21 | Wyeth | Methods for treating hyperactive gastric motility |
| GB0121214D0 (en) | 2001-08-31 | 2001-10-24 | Btg Int Ltd | Synthetic method |
| AU2003202115A1 (en) | 2002-02-12 | 2003-09-04 | Pfizer Inc. | Non-peptide compounds affecting the action of gonadotropin-releasing hormone (gnrh) |
| WO2003097586A1 (en) | 2002-05-17 | 2003-11-27 | Janssen Pharmaceutica N.V. | Aminotetralin-derived urea modulators of vanilloid vr1 receptor |
| WO2003106454A1 (en) | 2002-06-12 | 2003-12-24 | Orchid Chemicals & Pharmaceuticals Ltd | 1h-isoquinoline-oxazolidinone derivaties and their use as antibacterial agents |
| AUPS312602A0 (en) | 2002-06-21 | 2002-07-18 | James Cook University | Organ arrest, protection, preservation and recovery |
| US7419981B2 (en) | 2002-08-15 | 2008-09-02 | Pfizer Inc. | Synergistic combinations of an alpha-2-delta ligand and a cGMP phosphodieterse 5 inhibitor |
| AU2003294441A1 (en) | 2002-11-22 | 2004-06-18 | Bristol-Myers Squibb Company | 1-aryl-2-hydroxyethyl amides as potassium channel openers |
| JP4652816B2 (ja) | 2002-12-23 | 2011-03-16 | アイシーエージェン インコーポレイテッド | カリウムチャネルモジュレータとしてのキナゾリノン |
| NZ540446A (en) | 2002-12-27 | 2008-03-28 | Lundbeck & Co As H | 1,2,4-Triaminobenzene derivatives useful for treating disorders of the central nervous system |
| BRPI0408205A (pt) | 2003-03-14 | 2006-02-14 | Lundbeck & Co As H | derivado de anilina substituìdo, composição farmacêutica, e, uso de uma composição farmacêutica |
| EP1613303A1 (en) | 2003-03-21 | 2006-01-11 | H. Lundbeck A/S | Substituted p-diaminobenzene derivatives |
| AU2004233941A1 (en) | 2003-04-25 | 2004-11-11 | H. Lundbeck A/S | Sustituted indoline and indole derivatives |
| JP2006528231A (ja) | 2003-05-27 | 2006-12-14 | アルタナ ファルマ アクチエンゲゼルシャフト | プロトンポンプ阻害剤と胃腸運動性を変更する化合物との医薬品組合せ物 |
| US20050070570A1 (en) | 2003-06-18 | 2005-03-31 | 4Sc Ag | Novel potassium channels modulators |
| JP2007505142A (ja) | 2003-09-10 | 2007-03-08 | セダーズ−シナイ メディカル センター | 血液脳関門を通過する薬剤のカリウムチャネル媒介性送達 |
| US7799832B2 (en) | 2003-10-23 | 2010-09-21 | Valeant Pharmaceuticals North America | Combinations of retigabine and sodium channel inhibitors or sodium channel-influencing active compounds for treating pains |
| DE10359335A1 (de) | 2003-10-23 | 2005-05-25 | Viatris Gmbh & Co. Kg | Kombinationen aus Kaliumkanalöffnern und Natriumkanalinhibitoren oder Natriumkanal beeinflussenden Wirkstoffen zur Behandlung von Schmerzzuständen |
| ES2235626B1 (es) | 2003-11-10 | 2006-11-01 | Almirall Prodesfarma, S.A. | Formas de administracion masticables, no comprimidas dosificadas individualmente. |
| US8236861B2 (en) | 2004-02-13 | 2012-08-07 | Hormos Medical Corporation | Method for enhancing the bioavailablity of ospemifene |
| TWI357901B (en) | 2004-03-12 | 2012-02-11 | Lundbeck & Co As H | Substituted morpholine and thiomorpholine derivati |
| MXPA06011807A (es) | 2004-04-13 | 2007-02-21 | Icagen Inc | Piridinas policiclicas como moduladores del canal del ion de potasio. |
| WO2005110405A1 (en) | 2004-05-03 | 2005-11-24 | Duke University | Compositions for affecting weight loss |
| UA89503C2 (uk) | 2004-09-13 | 2010-02-10 | Х. Луннбек А/С | Заміщені похідні аніліну |
| EP1813285A4 (en) | 2004-11-19 | 2010-06-09 | Kissei Pharmaceutical | PROPHYLACTIC OR THERAPEUTIC AGENT AGAINST NEUROPATHIC PAIN |
| EP1688141A1 (en) | 2005-01-31 | 2006-08-09 | elbion AG | The use of flupirtine for the treatment of overactive bladder and associated diseases, and for the treatment of irritable bowel syndrome |
| CA2599890C (en) | 2005-03-03 | 2011-05-03 | H. Lundbeck A/S | Substituted pyridine derivatives |
| EP1891089B1 (en) | 2005-06-02 | 2014-11-05 | Merck Sharp & Dohme Corp. | HCV protease inhibitors in combination with food |
| US7683058B2 (en) | 2005-09-09 | 2010-03-23 | H. Lundbeck A/S | Substituted pyrimidine derivatives |
| JP2009535370A (ja) | 2006-05-02 | 2009-10-01 | クリス ルントフェルト | ジストニアおよびジストニア様症状の予防および治療におけるカリウムチャンネル活性剤 |
| WO2008024398A2 (en) * | 2006-08-23 | 2008-02-28 | Valeant Pharmaceuticals International | Derivatives of 4-(n-azacycloalkyl) anilides as potassium channel modulators |
| US8993593B2 (en) * | 2006-08-23 | 2015-03-31 | Valeant Pharmaceuticals International | N-(4-(6-fluoro-3,4-dihydroisoquinolin-2(1H)-yl)-2,6-dimethylphenyl)-3,3-dimethylbutanamide as potassium channel modulators |
| BRPI0719590A2 (pt) | 2006-11-28 | 2014-01-21 | Valeant Pharmaceuticals Int | Análogos de retigabina 1,4 diamino bicíclica como modulares de canal de potássio |
| WO2008144320A2 (en) | 2007-05-17 | 2008-11-27 | Endo Pharmaceuticals, Inc. | Opioid and methods of making and using the same |
| AR070513A1 (es) | 2007-08-01 | 2010-04-14 | Lundbeck & Co As H | Uso de abridores de canales de potasio kcnq para reducir los sintomas o tratar desordenes o afecciones en las cuales se encuentra anulado el sis-tema dopaminergico como por ejemplo esquizofrenia y trastorno depresivo mayor |
| WO2009074594A1 (en) * | 2007-12-11 | 2009-06-18 | Neurosearch A/S | Novel 2-ethyl-methyl-amino-3-amido-6-amino-pyridine derivatives useful as potassium channel activators |
| US20100323016A1 (en) | 2008-07-18 | 2010-12-23 | Biljana Nadjsombati | Modified release formulation and methods of use |
| US20120288544A1 (en) | 2010-01-20 | 2012-11-15 | Glaxo Group Limited | Novel retigabine composition |
| WO2013067591A1 (en) | 2011-11-10 | 2013-05-16 | Relevare Australia Pty Ltd | Topical formulations for pain management |
| US10500216B2 (en) | 2011-11-18 | 2019-12-10 | Corcept Therapeutics, Inc. | Optimizing mifepristone absorption |
| US9248122B2 (en) | 2012-11-28 | 2016-02-02 | Grünenthal GmbH | Heteroquinoline-3-carboxamides as KCNQ2/3 modulators |
| ES3032221T3 (en) * | 2018-02-20 | 2025-07-16 | H Lundbeck As | Alcohol derivatives as kv7 potassium channel openers |
| MA52569B1 (fr) | 2018-05-11 | 2023-11-30 | Xenon Pharmaceuticals Inc | Méthodes pour améliorer la biodisponibilité et l'exposition d'un activateur de canal potassique voltage-dépendant |
| TWI886158B (zh) | 2019-10-10 | 2025-06-11 | 加拿大商再諾製藥公司 | 選擇性鉀通道調節劑之固態晶型 |
| GEP20257732B (en) | 2019-11-08 | 2025-02-10 | Xenon Pharmaceuticals Inc | Methods of treating depressive disorders |
| US20230015539A1 (en) | 2019-12-06 | 2023-01-19 | Icahn School Of Medicine At Mount Sinai | Method of treatment with kcnq channel openers |
| US20210213009A1 (en) | 2019-12-13 | 2021-07-15 | Xenon Pharmaceuticals Inc. | Methods of treating pain |
| KR20240004241A (ko) | 2021-02-09 | 2024-01-11 | 제논 파마슈티칼스 인크. | 무쾌감증의 치료에 사용하기 위한 전압-게이트 칼륨 채널 오프너 |
| EP4291185A1 (en) | 2021-02-09 | 2023-12-20 | Xenon Pharmaceuticals Inc. | Conjoint therapy for treating seizure disorders |
| US12319656B2 (en) | 2021-10-27 | 2025-06-03 | Shanghai Zhimeng Biopharma, Inc. | Compound as potassium channel regulator and preparation and use thereof |
-
2020
- 2020-11-06 GE GEAP202015942A patent/GEP20257732B/en unknown
- 2020-11-06 CN CN202080077815.3A patent/CN114667146A/zh active Pending
- 2020-11-06 BR BR112022008580A patent/BR112022008580A2/pt unknown
- 2020-11-06 JP JP2022524695A patent/JP2022553569A/ja active Pending
- 2020-11-06 MX MX2022005490A patent/MX2022005490A/es unknown
- 2020-11-06 PE PE2022000702A patent/PE20221766A1/es unknown
- 2020-11-06 KR KR1020227017725A patent/KR20220098746A/ko active Pending
- 2020-11-06 PH PH1/2022/551110A patent/PH12022551110A1/en unknown
- 2020-11-06 MA MA56607A patent/MA56607A1/fr unknown
- 2020-11-06 EP EP20816351.9A patent/EP4054580A1/en active Pending
- 2020-11-06 CA CA3155812A patent/CA3155812A1/en active Pending
- 2020-11-06 AU AU2020380961A patent/AU2020380961A1/en active Pending
- 2020-11-06 CR CR20220250A patent/CR20220250A/es unknown
- 2020-11-06 WO PCT/US2020/059481 patent/WO2021092439A1/en not_active Ceased
- 2020-11-06 TW TW109138929A patent/TW202128162A/zh unknown
- 2020-11-06 GE GEAP202415942A patent/GEAP202415942A/en unknown
- 2020-11-09 US US17/093,183 patent/US12178811B2/en active Active
-
2022
- 2022-04-29 CL CL2022001102A patent/CL2022001102A1/es unknown
- 2022-05-02 IL IL292678A patent/IL292678A/en unknown
- 2022-06-06 CO CONC2022/0008001A patent/CO2022008001A2/es unknown
-
2024
- 2024-08-01 US US18/791,918 patent/US20250108044A1/en active Pending
-
2025
- 2025-09-19 JP JP2025155966A patent/JP2026001049A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU2020380961A1 (en) | 2022-05-26 |
| EP4054580A1 (en) | 2022-09-14 |
| CN114667146A (zh) | 2022-06-24 |
| WO2021092439A1 (en) | 2021-05-14 |
| IL292678A (en) | 2022-07-01 |
| JP2026001049A (ja) | 2026-01-06 |
| US20210161886A1 (en) | 2021-06-03 |
| MA56607A1 (fr) | 2022-10-31 |
| CL2022001102A1 (es) | 2023-01-27 |
| US12178811B2 (en) | 2024-12-31 |
| CR20220250A (es) | 2022-08-19 |
| JP2022553569A (ja) | 2022-12-23 |
| PH12022551110A1 (en) | 2024-02-26 |
| GEAP202415942A (en) | 2024-10-28 |
| PE20221766A1 (es) | 2022-11-11 |
| NZ787838A (en) | 2025-08-29 |
| BR112022008580A2 (pt) | 2022-08-09 |
| US20250108044A1 (en) | 2025-04-03 |
| GEP20257732B (en) | 2025-02-10 |
| MX2022005490A (es) | 2022-08-10 |
| KR20220098746A (ko) | 2022-07-12 |
| CO2022008001A2 (es) | 2022-06-10 |
| CA3155812A1 (en) | 2021-05-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TW202128162A (zh) | 憂鬱症之治療方法 | |
| Einat et al. | Inositol reduces depressive-like behaviors in two different animal models of depression | |
| US20240417798A1 (en) | Therapy selection and treatment of neurodegenerative disorders | |
| KR20200015897A (ko) | 수명 및 건강수명을 연장시키기 위한 제제 | |
| EP4104831A1 (en) | A2-73 for treating angelman syndrome, williams syndrome smith-magenis syndrome and multiple sclerosis | |
| Veraksitš | Characterization of behavioural and biochemical phenotype of cholecystokinin-2 receptor deficient mice: changes in the function of the dopamine-and endopioidergic system | |
| EP4681714A2 (en) | Methods of treating the symptoms of autism spectrum disorder | |
| KR20100061548A (ko) | 티몰 및/또는 p-시멘 또는 식물 추출물을 함유하는 인지 개선용 신규 기능식품성 조성물 | |
| JP7449511B2 (ja) | 加齢に伴う認知機能の低下予防又は改善用の組成物 | |
| JP2023550093A (ja) | レット症候群を治療するためのプリドピジンまたはその類似体の使用 | |
| CN104368002B (zh) | 用于治疗痴呆或认知功能障碍的联合用药物 | |
| EA048968B1 (ru) | Способы лечения депрессивных расстройств | |
| RU2844953C1 (ru) | Способы лечения симптомов расстройства аутистического спектра | |
| Gerken | All body systems affect behavior | |
| WO2025231180A9 (en) | Blarcamesine correction of eeg biomarkers in fragile x syndrome | |
| Saraiva | Behaviour Phenotyping of Parkinson’s Disease Animal Models Using Inertial Sensors | |
| WO2023215338A1 (en) | Compositions and methods for treating cluster headache | |
| Day et al. | The Effects of Olive Oil and Oleuropein on Depression and Anxiety | |
| KR20240073798A (ko) | 란소프라졸, 란소프라졸 n-옥사이드, 란소프라졸 n-옥사이드 대사체, 또는 란소프라졸 n-옥사이드 전구물질을 포함하는 신경계 질환 예방 또는 치료용 조성물 | |
| HK40083948A (zh) | 用於治疗天使综合症、威廉综合症、史密斯马吉利综合症和多发性硬化的a2-73 | |
| AU2023314929A1 (en) | Therapy selection and treatment of neurodegenerative disorders | |
| HK40076951A (zh) | 治疗抑郁症的方法 | |
| WO2023215344A2 (en) | Compositions and methods for treating cluster-tic syndrome | |
| CN118613282A (zh) | 神经退行性病症的疗法选择和治疗 | |
| McNeal | Social bonds, cardiovascular function, and serotonin: Insights from an animal model |