AVON-/FLAVANON-DERIVATEN ZUR SYSTEMISCHEN BEHANDLUNG UND PROPHYLAXE VON UV- NDUZIERTEN DERMATOSEN
Beschreibung
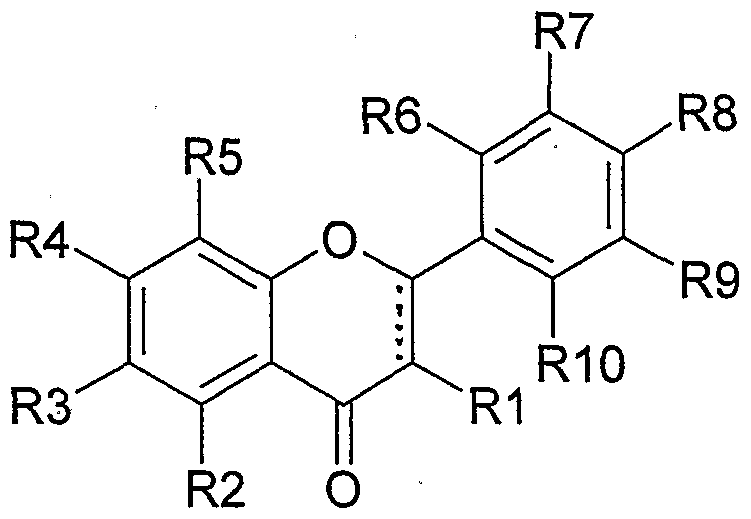
Die Erfindung betrifft die Verwendung von Flavon-/Flavanon-Derivaten der allgemeinen Formel I
in welcher unabhängig voneinander
R1 H, OH oder-O-Gly;
R2, R6, R9 und R10 gleich oder verschieden sein können und H, OH, Alkoxy,
Hydroxyalkoxy oder C3-C -Cycloalkoxy;
R3 H, Cι-C-4-Alkyl oder C3-C7-Cycloalkoxy;
R4 H, OH, -O-Gly, Alkoxy, Hydroxyalkoxy oder C3-C7-Cycloalkoxy;
R5 H, CrC-4-Alkyl, OH, Alkoxy, Hydroxyalkoxy oder C3-C7-Cycloalkoxy;
R7 und R8 gleich oder verschieden sein können und H, OH, Alkoxy, Hydroxyalkoxy,
C3-C7-Cycloalkoxy, Thio(d-C4-)alkyl oder-NR11R12; und
R11 und R12 gleich oder verschieden sein können und H oder Cι-C4-Alkyl bedeuten können; und worin
Alkoxy und Hydroxyalkoxy eine geradkettige oder verzweigte Alkylgruppe mit 1 - 18
C-Atomen enthalten können; und worin
Gly vorhanden oder abwesend sein kann und einen mono- oder oligoglycidischen
Rest bezeichnet; in Verbindung mit den üblichen Hilfs- und Zusatzstoffen zur Herstellung von Arzneimitteln zur systemischen Behandlung und Prophylaxe von
UV-induzierten Dermatosen besonders der polymorphen Lichtdermatose und ihren
Unterformen und/oder unerwünschten Langzeitfolgen von UV-Bestrahlungen, besonders der Lichtalterung, sowie die Verwendung der Verbindungen der allgemeinen Formel I zur Behandlung bzw. Prophylaxe der genannten UV-induzierten Dermatosen durch orale, rectale oder parenterale Verabreichung.
In den Verbindungen der allgemeinen Formel I ist Gly unabhängig von einander vorzugsweise ausgewählt aus der Gruppe von Hexosyl- oder Pentosyl-Resten. Bevorzugt sind Rhamnosyl- oder Glucosyl-Reste. Es können jedoch auch andere Glycosyl-Reste von Vorteil sein, wie beispielsweise Allosyl, Altrosyl, Galactosyl, Gulosyl, Idosyl, Mannosyl, Rutinosyl oder Talosyl.
UV-induzierte Dermatosen auch Photodermatosen genannt, sind nicht infektiöse, entzündliche Hauterkrankungen, deren ursächliche Genese zumeist noch weitgehend unbekannt ist. Vom klinischen Bild her unterscheidet man die Polymorphe Lichtdermatose, die in unterschiedlicher Intensität auftreten kann, die solare Urtikaria, den Lupus erythematodes, die Prurigo aestivalis und andere. Die häufigste UV-induzierte Dermatose ist die Polymorphe Lichtdermatose (im folgenden mit PLD abgekürzt). An ihr leiden ca. 10-20% der kaukasischen Bevölkerung in mitteleuropäischen Ländern. Diese Erkrankung kommt mit einer unterschiedlichen Inzidenz in allen Rassen vor. Obwohl genaue epidemiologische Studien fehlen, scheinen Frauen häufiger als Männer betroffen zu sein. Die PLD wird mit den unterschiedlichsten Synonyma belegt: Sonnenallergie, Mallorca-Akne, etc.
Typischerweise findet man bei dieser UV-induzierten Dermatose ein interindividuell unterschiedliches Erscheinungsbild. Innerhalb eines Patienten manifestiert sich die PLD aber streng monomorph. Es werden folgende Subtypen unterschieden: Plaque- Typ, Erythema-exsudativum-multiforme-artiger Typ der PLD, vesikulo-bullöser Typ der PLD, hämorrhagischer Typ der PLD, fixe PLD. Die PLD Lichtdermatose zeigt histologisch ein entzündliches z.T. perivaskuläres Infiltrat von Lymphozyten. Immunhistochemisch finden sich eine Expression von proinflammatorischen Zytokinen im Bereich der Basalmembran und eine verstärkte Expression von proinflammatorischen Zytokinen um die Gefäße. Die Pathogenese der PLD ist noch nicht vollständig geklärt, es scheint aber deutlich zu sein, daß die pathologisch gesteigerte Reaktion auf UV-Strahlen Folge einer UV-bedingten Freisetzung von
Sauerstoffradikalen ist. Hierdurch werden im Folgenden Signaltransduktionswege in der Zelle verändert. Das pathogenetisch entscheidende Moment ist also die Freisetzung beziehungsweise Generierung von Sauerstoffradikalen.
Die herkömmliche Therapie der UV-induzierten Dermatosen besteht in der topischen oder systemischen Anwendung von Glukokortikosteroiden. Dabei treten Steroidnebenwirkungen, wie z.B. Atrophisierung der Haut, Bildung von Teleangiektasien und die Gefahr einer Hypertrichose auf. Therapieerfolge nach systemischer Gabe von Antihistaminika, Vitaminen oder, Elektrolyten wurden anekdotisch berichtet. Diese positiven therapeutischen Effekte konnten in kontrollierten Studien jedoch nicht bestätigt werden.
Bedeutsamer und von den Patienten in größerem Maße erwünscht sind prophylaktische Maßnahmen, d.h. Methoden, die zur Anwendung kommen, damit UV-induzierte Dermatosen sich gar nicht manifestieren können.
In der Prophylaxe der Photodermatosen werden zum einen phototherapeutische Verfahren eingesetzt, d.h. es wird der Teufel mit Beizebub ausgetrieben. Dieser Ansatz stützt sich auf die Erfahrung, daß sich die Auslösbarkeit einer UV-induzierten Dermatosen nach repetitiven UV-Expositionen abschwächt und die meisten Patienten im Frühsommer oder zu Beginn ihres Urlaubs unter den Hautveränderungen leiden, während das Auftreten der Hautveränderungen seltener im Spätsommer beobachtet wird. Allerdings ist die Hardening-Therapie äußerst zeitaufwendig, sie erfordert regelmässige, zum Teil mehrmonatige Bestrahlungen durch einen photodermatologisch geschulten und erfahrenen Fachmann (Dermatologen) und zeigt nur eine therapeutische Effektivität bei ca. 30% der Patienten.
Eine weitere Möglichkeit ist die topische Applikation von Sonnenschutzcremes. Diese Maßnahme ist bezüglich ihrer Effektivität im Vergleichzur Phototherapie zwar einfacher durchzuführen, aber auch weitaus weniger wirksam. In der Tat ist es so, daß nur ausgewählte Sonnenschutzpräparate überhaut in der Lage sind, einen gewissen Schutz zu bieten. Hierbei handelt es sich um Präparate, die einen extrem hohen Sonnenschutzfaktor aufweisen. Die Applikation eines solch hohen Schutzfaktors erfordert eine sehr große Compliance seitens der Betroffenen, da
diese starke Schutzfunktion nur in Kombination mit physikalischen Filtern zu erreichen ist. Physikalische Filter sind Pigmente, z.B. Titan- oder Zinkoxide, die auch in mikrosomaler Zubereitung einen weißlichen Film auf der Haut hinterlassen. Diese kosmetische Beeinträchtigung sowie die vollständige Verhinderung der Hautpigmentierung durch den hohen Lichtschutzfaktor sind für die meisten Betroffenen nur schwer zu akzeptieren.
Der Einsatz von Antioxidantien in der Prophylaxe der PLD ist bisher nur in topischer Form erfolgt. Eine seit wenigen Jahren auf dem Markt befindliche Sonnenschutzcremekombination beinhaltet Rutosidderivate. Diese Sonnenschutzcreme wird als prophylaktisches Präparat für eine PLD beworben. Allerdings zeigt die Erfahrung, daß die topische Anwendung, die zur Erzielung eines optimalen Ergbenisses eine Vorbehandlunsgzeit von mehreren Wochen vor einer UV-Exposition erfordert, auf eine nur geringe Compliance bei den Betroffenen stößt. Zudem haben die bislang mit diesem Produkt durchgeführten klinischen Studien ergeben, daß diese Präparation nur von beschränkter Wirksamkeit ist. So läßt sich die Entwicklung von Hautveränderungen bei PLD Patienten nicht vollsrtändig verhindern, sondern lediglich abschwächen. Vermutlich ist dies darauf zurückzuführen, daß der topische Applikationsweg nicht optimal ist, um eine ausreichende Quencherkonzentration in den Hautschichten zu erreichen, in denen die Bildung von Sauerstoffradikalen von pathogenetischer Bedeutung ist.
Grundsätzlich ist zur topischen Anwendung von Sonnenschutzcremes im allgemeinen und topischen Antioxidantien im speziellen zu sagen, daß die äusserliche Anwendung folgende grundsätzliche Nachteile hat:
1.) die topische Applikation auf große Körperflächen ist für die Betroffenen extrem lästig und wird deshalb oft nicht konsequent durchgeführt wird (Zeitaufwand, Applikation muss mindestens 20 min. vor der UV-Exposition durchgeführt werden, häufig unangenehmes Empfinden der eingecremten Haut)
2.) die Wirksamkeit topischer Präparate wird durch sekundäre Faktoren wie z.B. fehlende Wasserfestigkeit (Meerwasser, Süßwasser, Schweiß) sowie durch den Abrieb durch Textilien und Bewegung reduziert
3.) hohe Sonnenschutzfaktoren durch physikalische Filter haben eine geringe kosmetische Akzeptanz, da sie einen sichtbaren Film auf der Haut bilden
4.) hohe Sonnenschutzfaktoren verhindern wirkungsvoll die Pigmentierung, dies ist in der Regel unerwünscht
5.) häufige Anwendung von chemischen Sonnenschutzfaktoren erhöht das Risiko einer epikutanen Sensibilisierung, da viele Sonnenschutzfaktoren eine starke Sensibilisierungspotenz besitzen; das Auftreten von photoallergischen Kontaktekzemen auf Lichtschutzfaktoren ist wissenschaftlich gut belegt.
Aufgabe der Erfindung war daher die Bereitstellung einer für den Patienten akzeptablen Möglichkeit der Therapie bzw. der Prophylaxe der genannten Dermatosen, bevorzugt durch orale oder parenterale Verabreichung von geeigneten Wirkstoffen bzw. deren pharmazeutischer Zubereitungsformen.
Überraschenderweise wurde nun gefunden, daß Flavon-/Flavanon-Derivate der allgemeinen Formel I in systemischen Arzneimitteln diese Aufgabe hervorragend erfüllen. Flavone bzw. Flavanone entfalten ihre Wirkung dadurch, daß sie UV- induzierte Sauerstoffradikale quenchen (abpuffern) können. Besonders Rutoside oder Rutosidderivate sind dafür besonders gut geeignet. Zudem wirken Flavone, besonders Rutoside oder Rutosidderivate auch auf Gefäße, indem sie dort eine deutlich endothelabdichtende Wirkung entfalten. Diese Eigenschaft wird schon durch die Gabe von Rutosiden als Ödemprotektiva genutzt. Flavonen, besonders Rutosiden und Rutosidderivaten werden zusätzlich antientzündliche Eigenschaften zugesprochen.
Unerwünschte Nebenwirkungen sind bei diesen Präparaten nur in geringem Ausmaß zu erwarten. Besonders sind aber transiente Transaminasenerhöhungen zu benennen. Bei Rutosid-haltigen Arzneimitteln werden in ca. 1% aller Patienten leichte gastrointestinale Nebenwirkungen beschrieben.
Bevorzugte Flavon-/Flavanonderivate der allgemeinen Formel I sind beispielsweise:
1.) Rutin, (Rutosid; Quercetin-3-rutinosid, 3-[[6-O-(6-Deoxy-α-L-mannopyranosyl)- beta-D-glucopyranosyl]oxy]-2-(3,4-dihydroxyphenyl)-5,7-dihydroxy-4H-1- benzopyran-4-on); sowie dessen Aglycon;
2.) O-ß-Hydroxyethylrutosid, eine Mischung von Mono-, Di-, Tri- und
Tetrahydroxyethyl-Derivaten von Rutin; oder deren Aglycone; sowie der Hauptbestandteil von O-ß-Hydroxyethylrutosid, nämlich
3.) Troxerutin (2-[3,4-Bis(2-hydroxyethoxy)phenyl]-3-[[6-O-(6-deoxy-α-L- mannopyranosyl)-ß-D-glucopyranosyl]oxy]-5-hydroxy-7-(2-hydroxyethoxy)-4H- 1-benzopyran-4-on); sowie dessen Agiycon;
4.) Monoxerutin (2-[3,4-Bishydroxyphenyl]-3-[[6~O-(6-deoxy-α-L-mannopyranosyl)- ß-D-glucopyranosyl]oxy]-5-hydroxy-7-(2-hydroxyethoxy)-4H-1-benzopyran-4- on); sowie dessen Agiycon;
5.) α-Glycosylrutin;
6.) Naringin (7-[[2-O-(6-Deoxy-α-L-mannopyranosyl)-ß-D-glucopyranosyl]oxy]-2,3- dihydro-5-hydroxy-2-(4-hydroxyphenyl)-4H-1-benzopyτan-4-on); sowie dessen Agiycon Naringenin;
7.) Hesperidin (7-[[6-O-(6-Deoxy-α-L-mannopyranosyl)-ß-D-glucopyranosyl]oxy]- 2,3-dihydro-5-hydroxy-2-(3-hydroxy-4-methoxyphenyl)-4H-1-benzopyran-4-on; sowie dessen Agiycon Hesperetin;
8.) Diosmin (3'5,7-Trihydroxy-4'methoxyflavon-7-rhamnoglucosid); sowie dessen Agiycon Diosmetin;
9.) Dihydrorobinctin (3,3',4',5',7-Pentahydroxyflavanon);
10.) Taxifolin (3,3',4',5,7-Pentahydroxyflavanon);
11.) -Eriodictin (3',4',5,7-Tetrahydroxyflavanon-7-rhamnosid); sowie dessen Agiycon Eriodictyol;
12.) Flavanomarein (3',4',7,8-Tetrahydroxyflavanon-7-glucosid); sowie dessen Agiycon;
13.) Isoquercetin (3,3',4',5,7-Pentahydroxyflavanon-3-(ß-D-glucopyranosid); sowie dessen Agiycon;
14.) Leucocyanidin (3,3',4,4',5,7-Hexahydroxyflavan);
15.) Cyrtominetin (6-8-Dimethyl-3',4',5,7-tetrahydroxyflavanon);
16.) 6,8-Dimethyl-5,7-dihydroxy-4'-thiomethylflavanon;
17.) 6,8-Dimethy!-4',5,7-trihydroxy-3'-methoxyflavanon; oder 18.) 6,8-Dimethyl-5,7-dihydroxy-4'-(dimethylamino)-flavanon;
Die Flavon-/Flavanonderivate der allgemeinen Formel I können zu den üblichen Arzneimittelzubereitungen in fester oder flüssiger Form zur Anwendung kommen, wie beispielsweise Pulver, Weich- oder Hart-Kapseln, Tabletten, Dragees, Brausetabletten, Suppositorien, Emulsionen, Öle, Lösungen oder Lyophilisate mit den üblichen Hilfs- und Zusatzstoffen. Lösungen oder Lyophilisate können auch parenteral systemisch verabreicht werden in Form von Injektionen als aufgelöstes Fertigpräparat oder als Lyophilisat, dem eine Verdünnungslösung, z.B. isotonische NaCI-Lösung oder Aqua ad injectabile, zugesetzt wird.
Die Vorteile einer systemischen enteralen oder parenteralen Gabe gegenüber einer topischen Applikation sind:
1.) höhere Wirksamkeit,
2.) deutlich bessere Compliance,
3.) gleichmäßige Gewebespiegel,
4.) höhere Bioverfügbarkeit auch in Gewebekompartimenten, die durch eine topische Applikation nicht erreicht werden können.
In Untersuchungen an Betroffenen hat sich überraschenderweise gezeigt, daß Arzneimittel, die Rutoside oder Rutosidester oder hohe Anteile an anderen Flavonen, mit Ausnahme von Nicotinamid, enthalten, die Auslösbarkeit einer PLD vollständig zu verhindern vermögen und daß diese Eigenschaft auch bei Betroffenen beobachtet werden konnte, bei denen bisher alle anderen bekannten Verfahren versagt haben. Die folgenden Kasuistiken verdeutlichen, daß die Wirksamkeit dieser Arzneimittel der Wirksamkeit topischer oder physikalischer Therapien deutlich überlegen ist.
Fallbeispiele:
FalM :
Weiblicher Patient, 50 Jahre alt, seit 20 Jahren PLD bekannt.
Bisherige Therapien:
1. konventionelle Sonnenschutzmittel: ohne Wirkung;
2. Hardening-Therapie mit PUVA: Verschlechterung der Symptomatik, deshalb Fortführung nicht möglich.
Aufgrund der Schwere des Verlaufs Vorstellung der Patientin in unserer SpezialSprechstunde für Photodermatosen.
Ergebnisse der Phototestungen in unserer Klinik:
Initiale Testung 11/98:
Immediate Pigment Darkening (= UVA-Sofortpigmentierung): 60 J/cm2
Minimale Erythemdosis(=UVB-Empfindlichkeit): 100 mJ/cm2
Photoprovokationstestung oberer Rücken, UVA:
Es konnte nur eine 2-malige Bestrahlung (üblich 3 Mal) durchgeführt werden, da sehr starke Schmerzen im Testareal und am Tag 3 Entwicklung einer PLD mit Papeln, Erythem und Juckreiz. oberer Rücken, UVA + UVB:
Es konnte ebenfalls nur eine 2malige Bestrahlung erfolgen, danach sofort Brennen und Juckreiz.
Diagnose: durch UVA-ausgelöste PLD erneute Testung 5/5/99:
Photoprovokationstestung (Gesäss): massive Erythemreaktion mit Infiltrat, Brennen und Juckreiz nach der 1. Bestrahlung, daraufhin Abbruch der Testung !
6/5/99: Einleitung der Therapie mit einem Rutosidhaltigen Präparat (Tagesdosis: 3000mg O-ß-Hydroxyethylrutosid; 3x2 Tbl./die für insgesamt 2 Wochen) erneute Photoprovokation am 25.5.99:
3-malige Bestrahlung mit UVA wurde diesmal problemlos toleriert, es kam erst nach der 3. Bestrahlung zum Auftreten eines Erythems ohne Papeln oder Infiltration.
Daraufhin Fortsetzung der Therapie bis zum heutigen Tag. Die Patientin gibt an, die Sonne wieder vertragen zu können und außer normalen Sonnenschutzmitteln keine Schutzmassnahmen ergreifen zu müssen.
Kommentar: Dieser Fall belegt die Wirksamkeit eines oral gegebenen Rutosids zur Prophylaxe der PLD. Wichtig ist, daß eine deutlich höhere Wirkung durch dieses Präparat erzielt werden konnte, als durch die Anwendung von topischen Sonnenschutzmitteln oder einer Phototherapie.
Fall 2:
Männlicher Patient, 42 Jahre alt seit 1980 PLD, anamnestisch UVA-getriggert, da Hautveränderungen auch nach Sonnenexposition durch Fensterglas (z.B. beim Autofahren) auftreten.
bisherige Therapie:
Sonnenschutzmittel: zunächst wirksam, jetzt seit 2 Jahren wirkungslos topisches Rutosid-haltiges Präparat: Keine Besserung
Hardening-Therapie (PUVA): wirkungslos
Patient wird seit 1980 in unserer Klinik betreut; stellt sich regelmäßig vor mit der Frage nach neuen therapeutischen Optionen, deshalb erneute Testung:
Photoprovokation vom 2.,3.,4.6.99
Induktion einer PLD am oberen Rücken mit UVA, UVB und UVA + UVB (Ausbildung infiltrierter Erytheme und Papeln (vor allem bei UVA + UVB); Diagnose:PLD
Therapie mit einem Rutosid-haltigen Arzneimittel (Tagesdosis: 3000 mg O-ß- Hydroxyethylrutosid; 3x2 Tbl./die für insgesamt 2 Wochen)