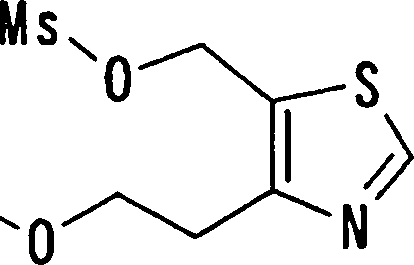
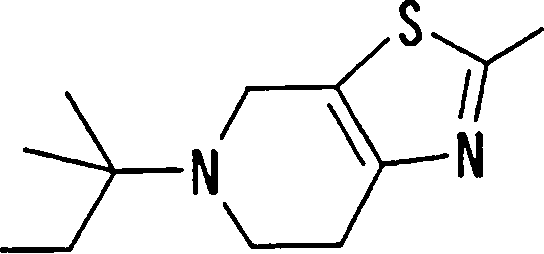
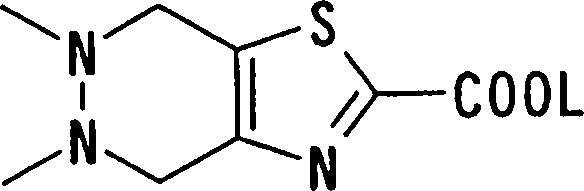
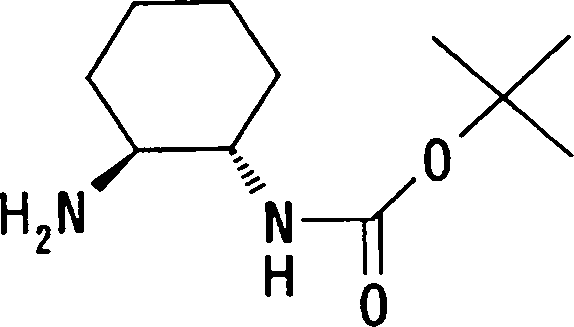
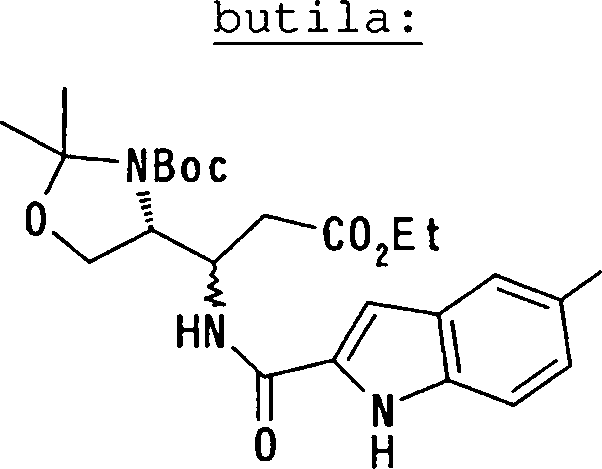
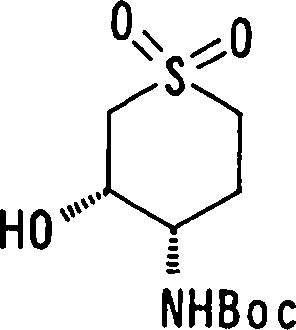
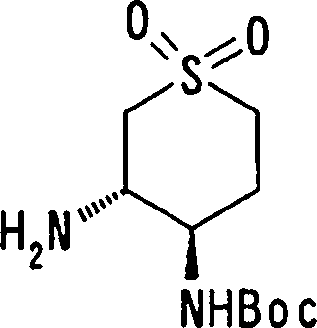
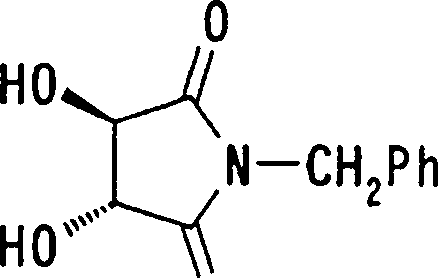
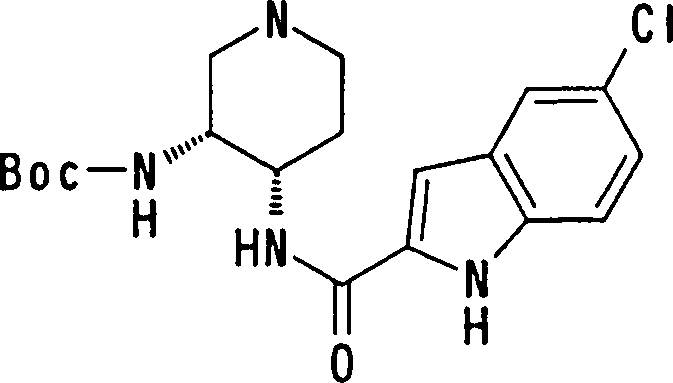
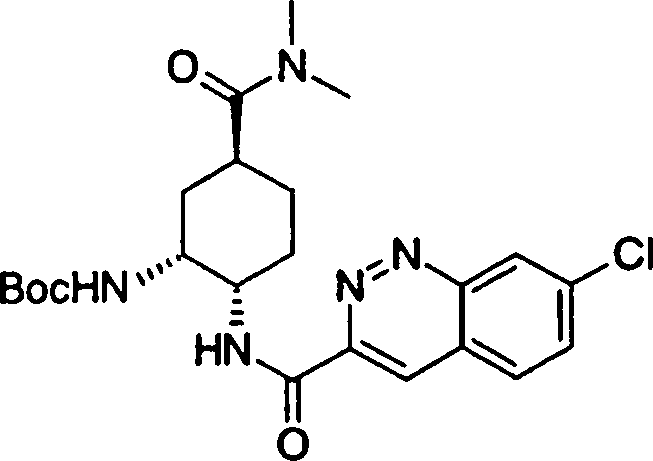
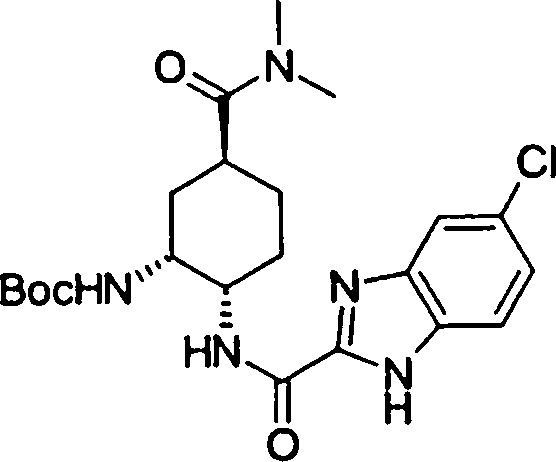
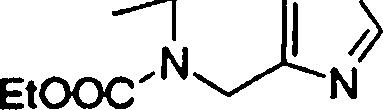
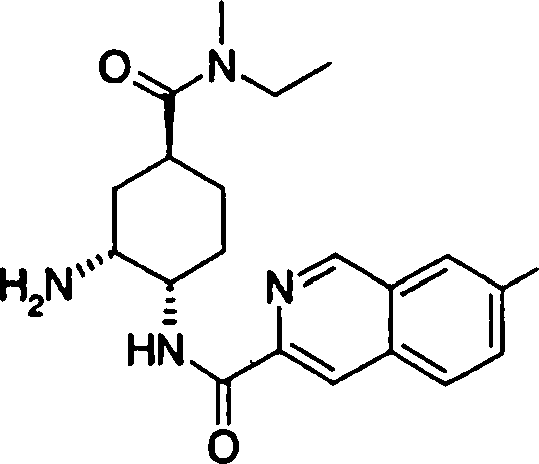
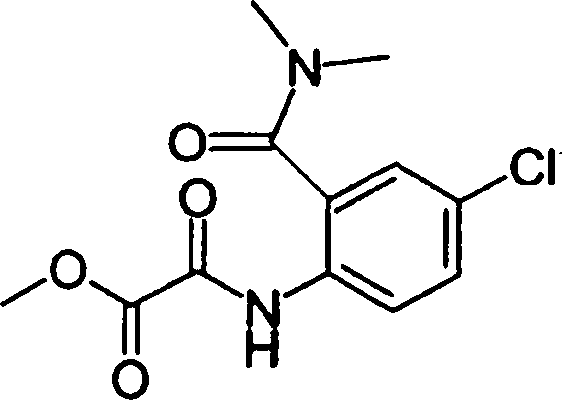
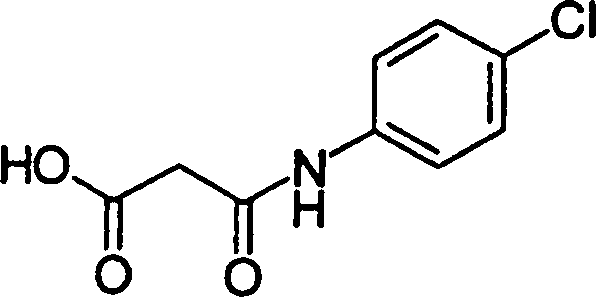
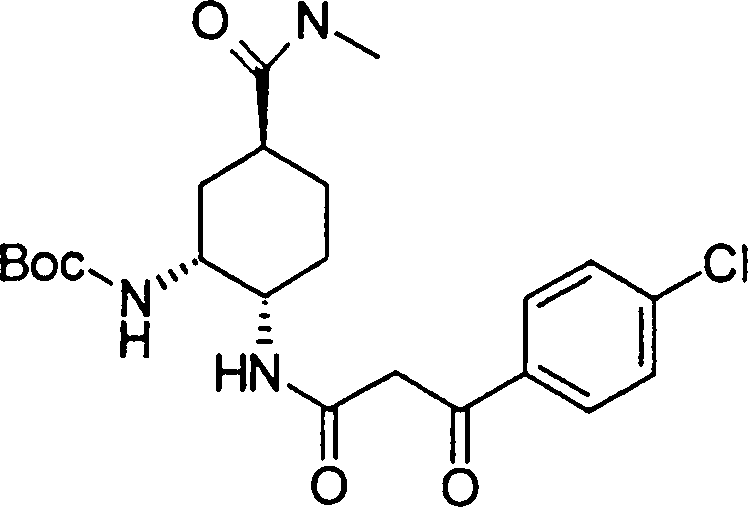
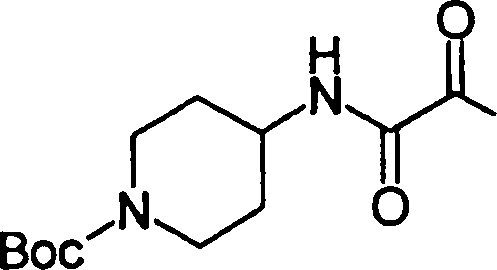
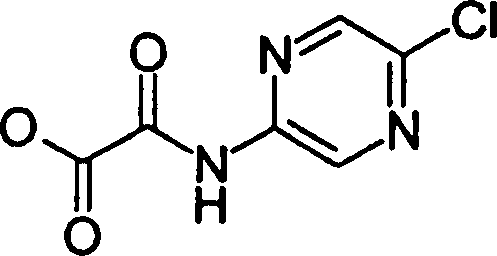
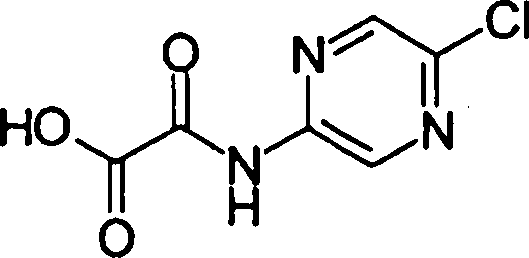
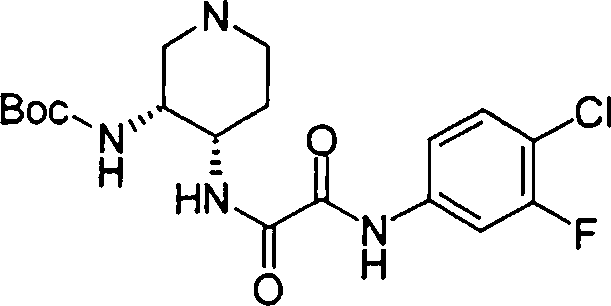
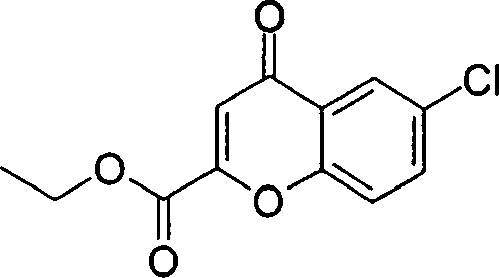
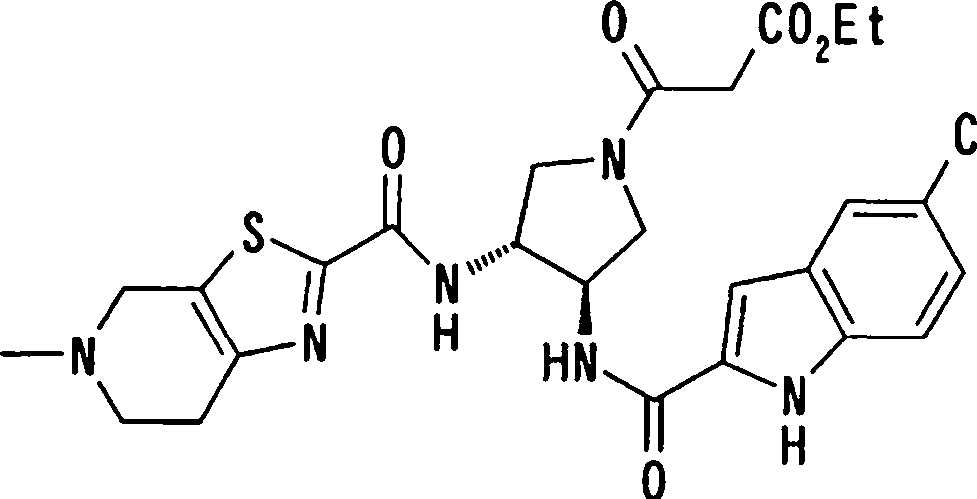
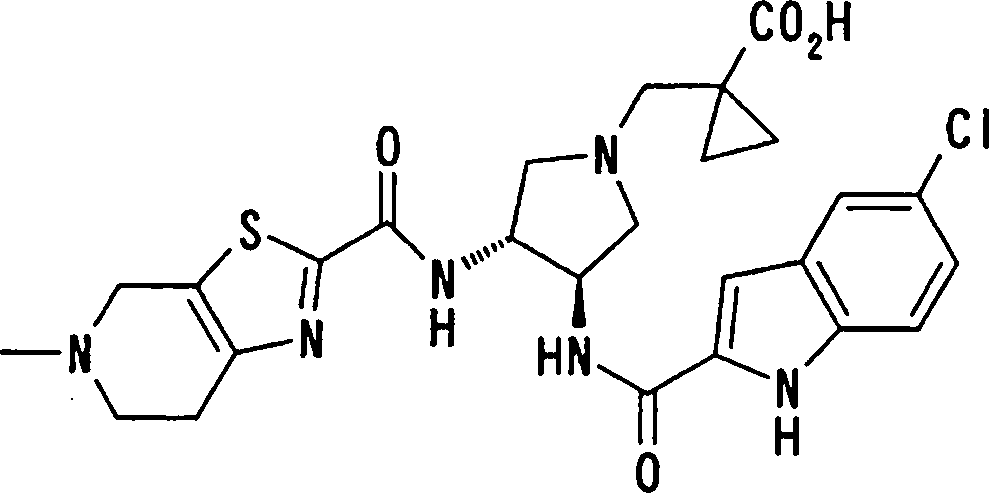
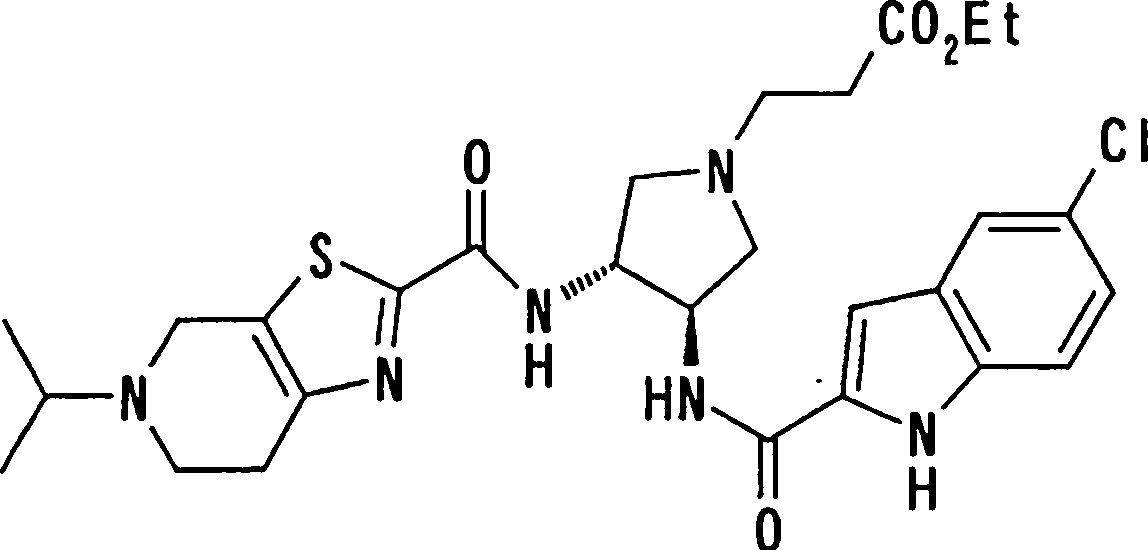
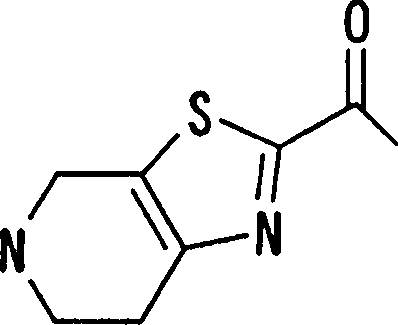
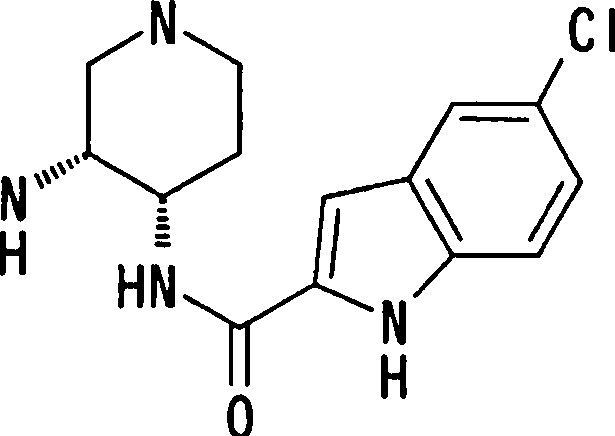
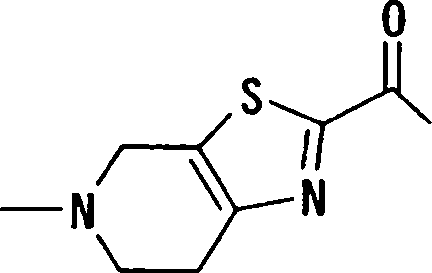
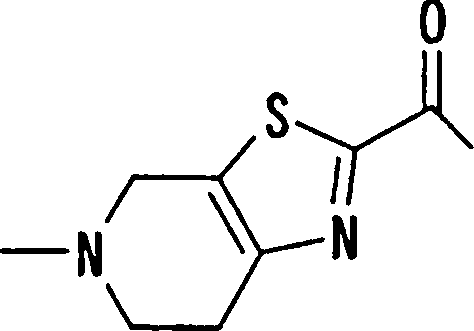
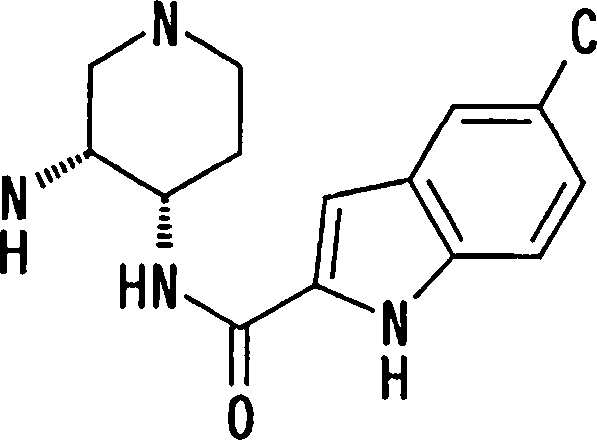
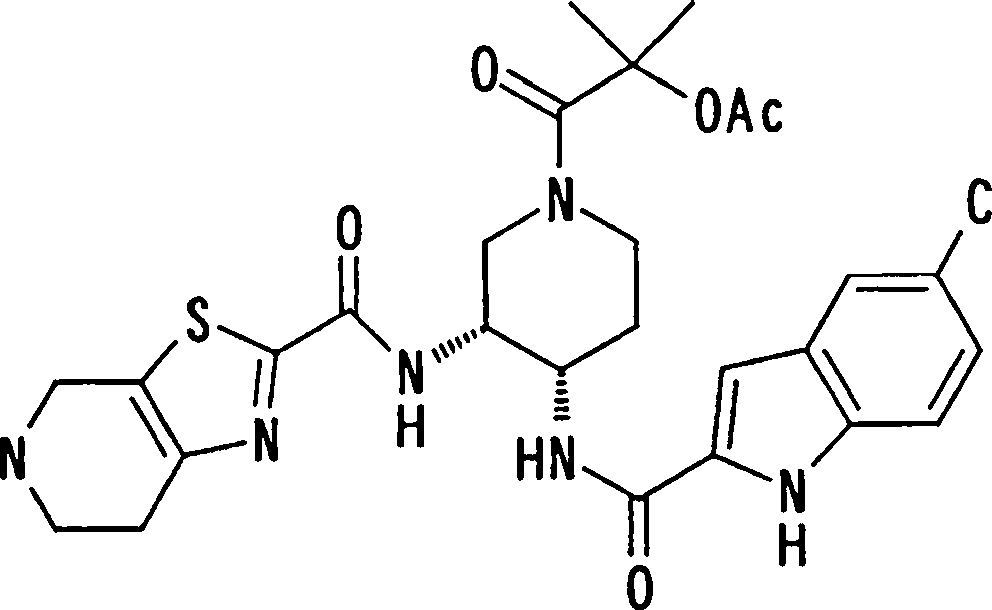
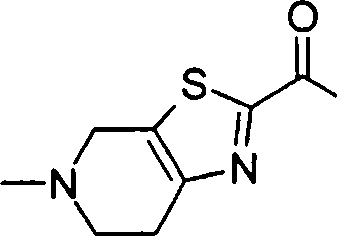
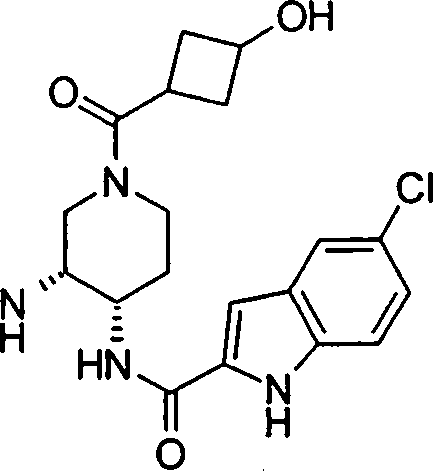
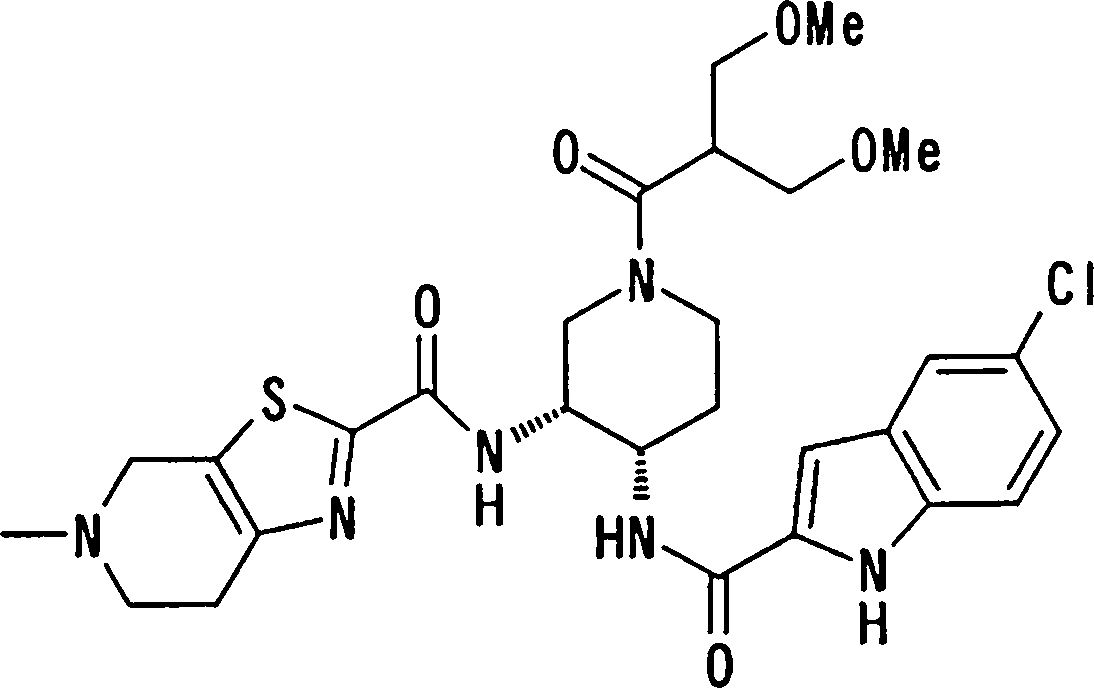
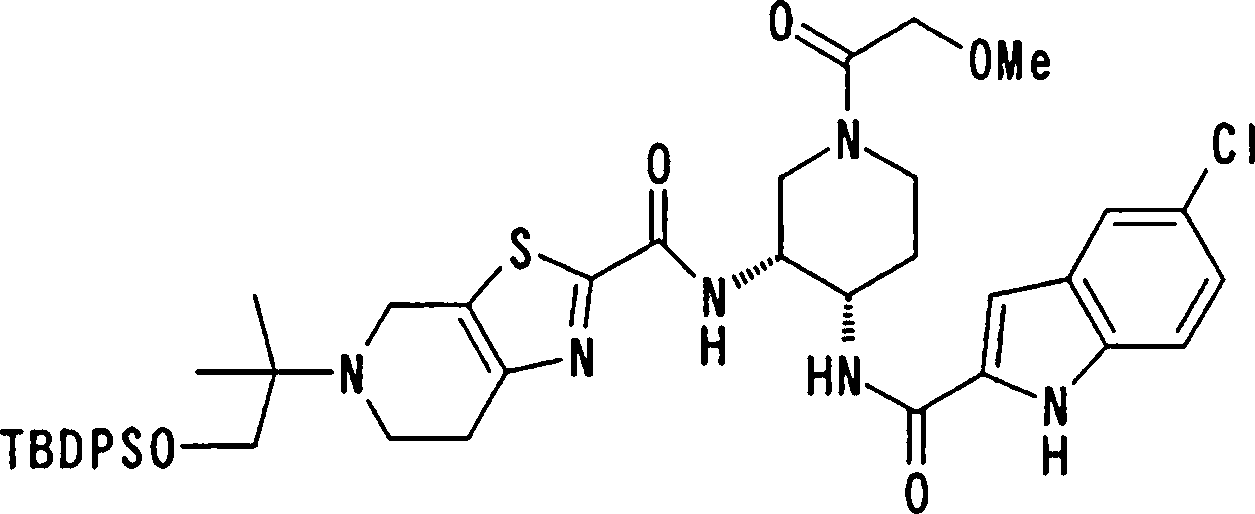
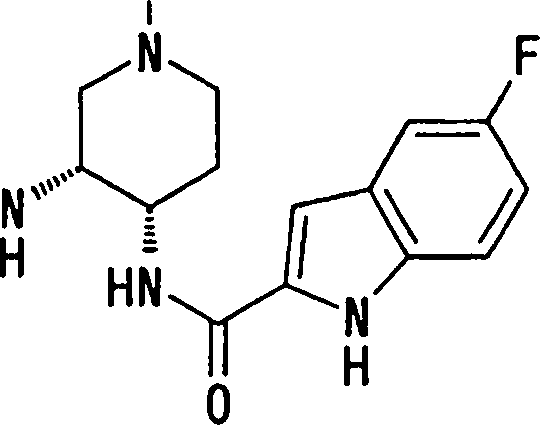
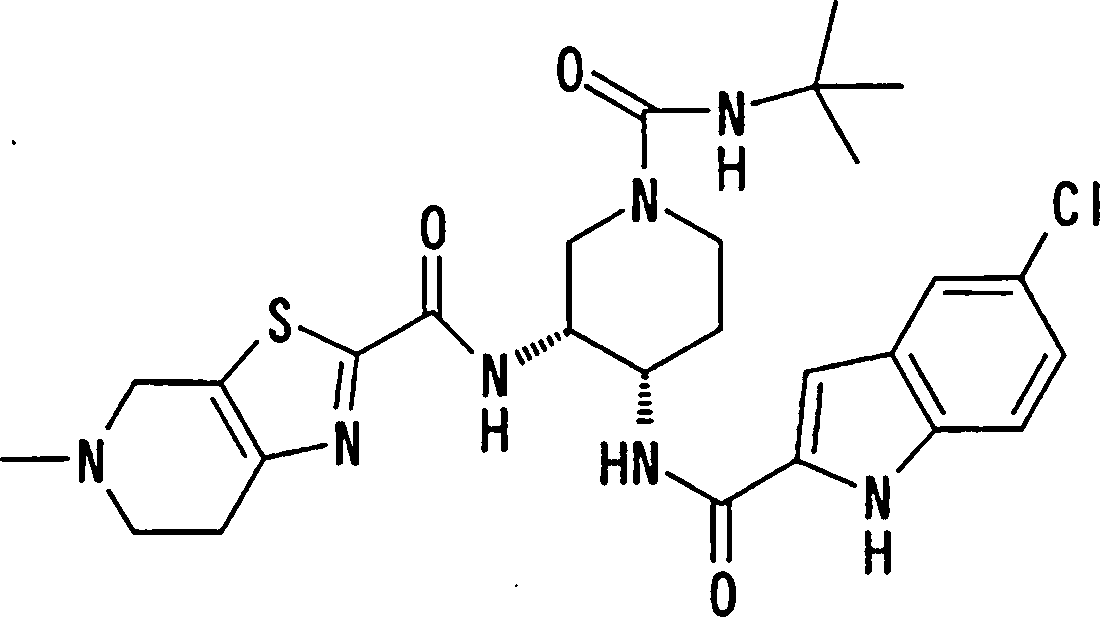
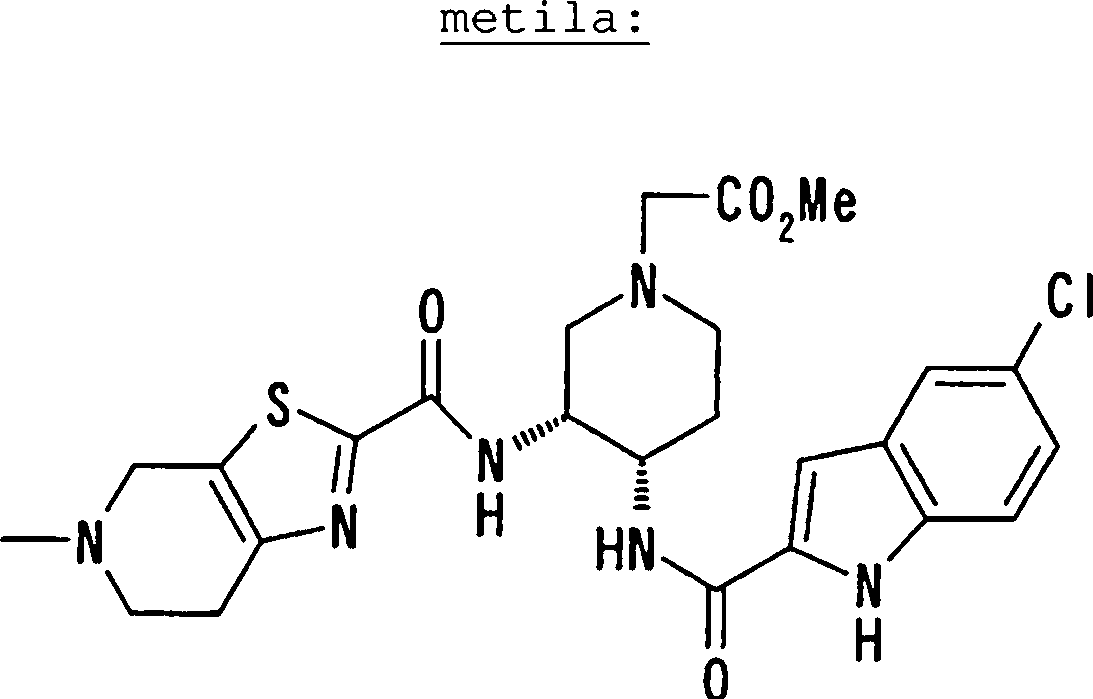
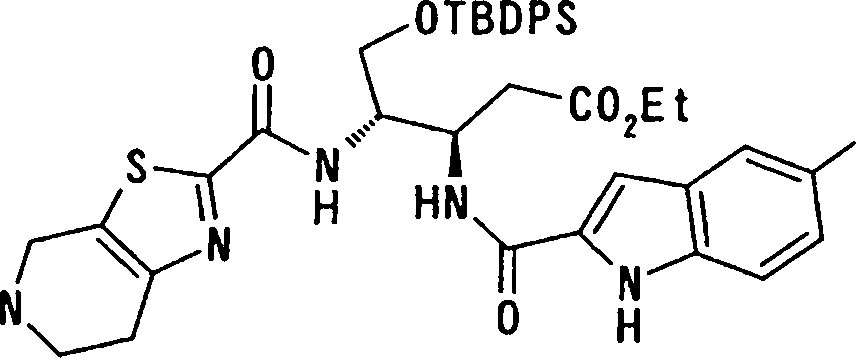
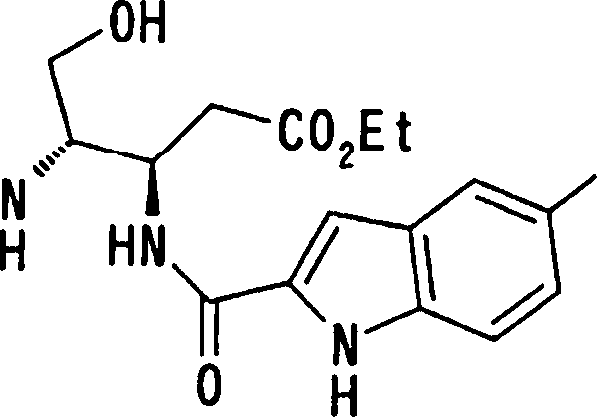
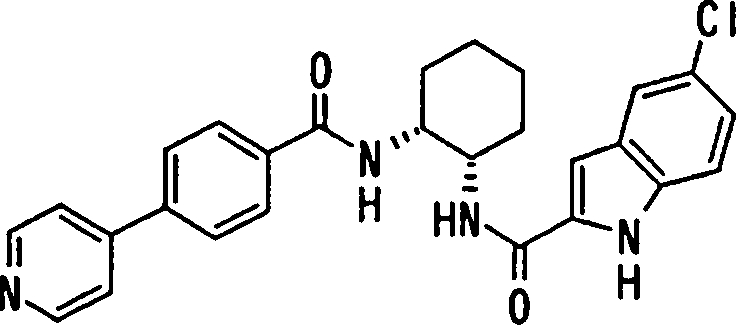
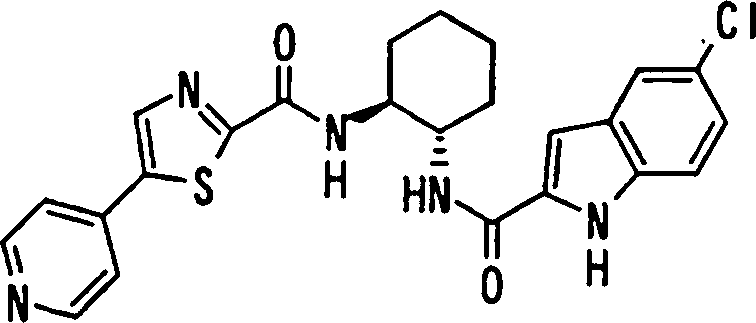
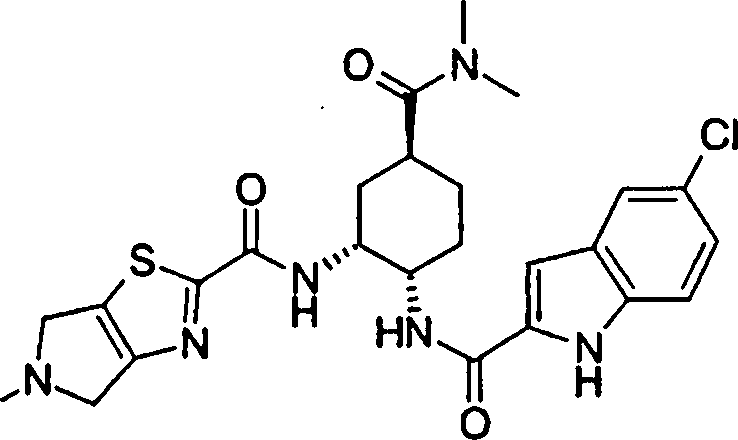
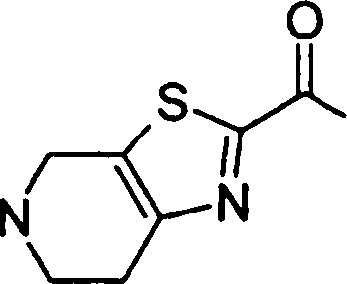
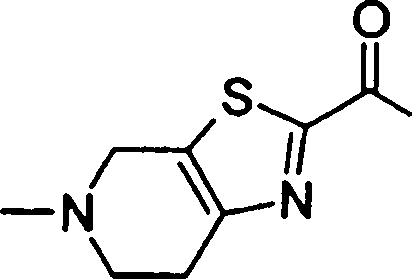
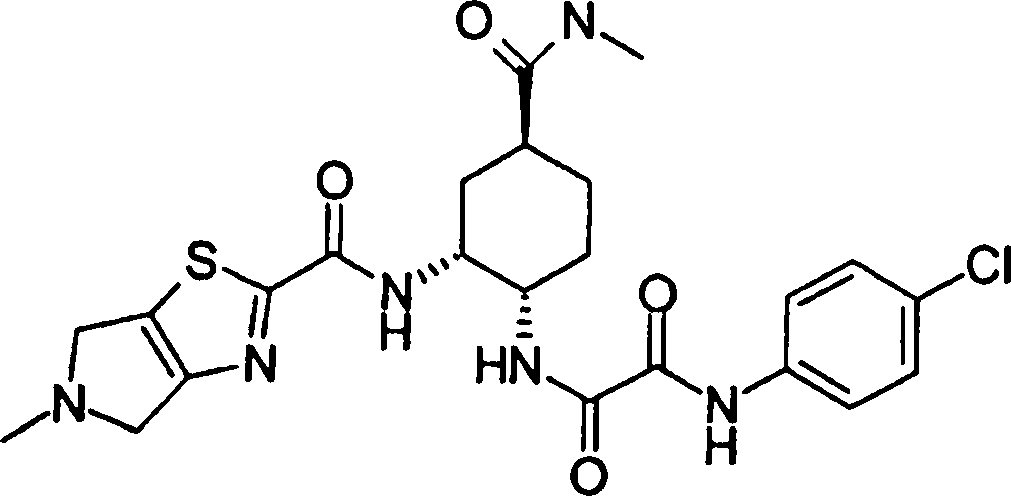
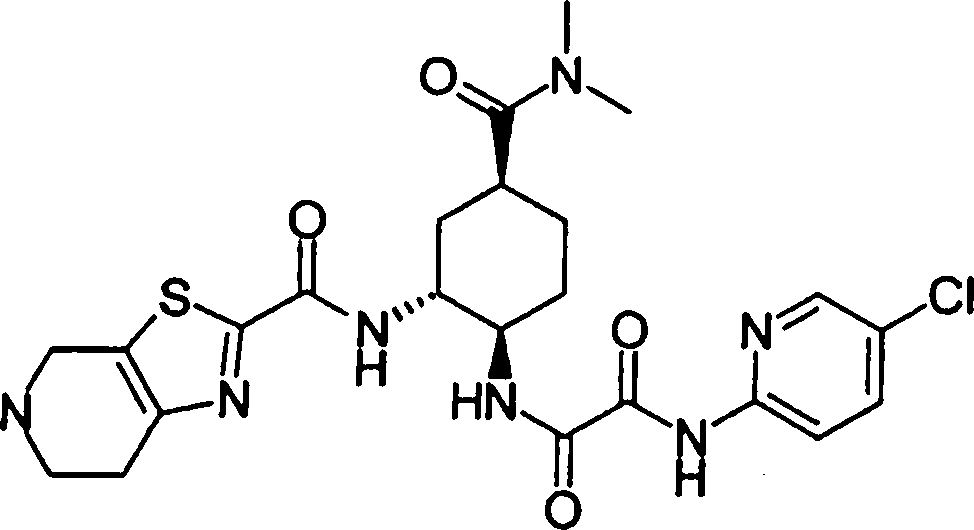
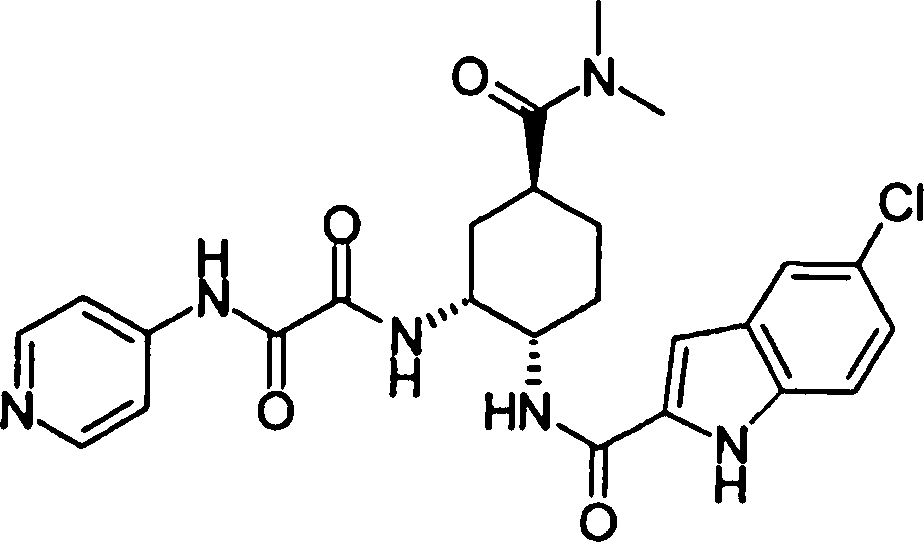
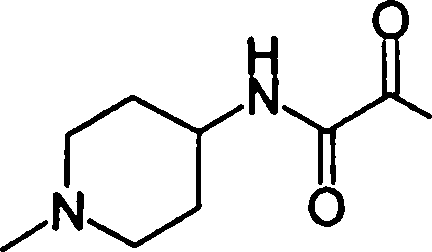
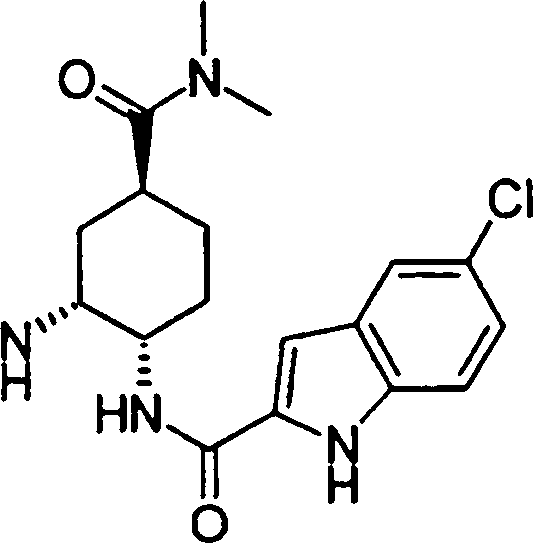
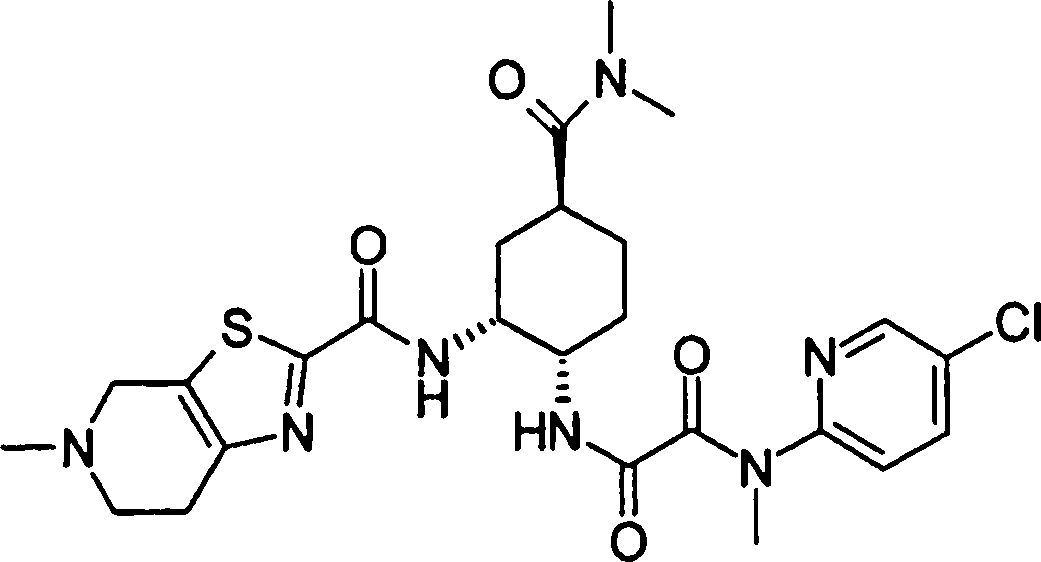
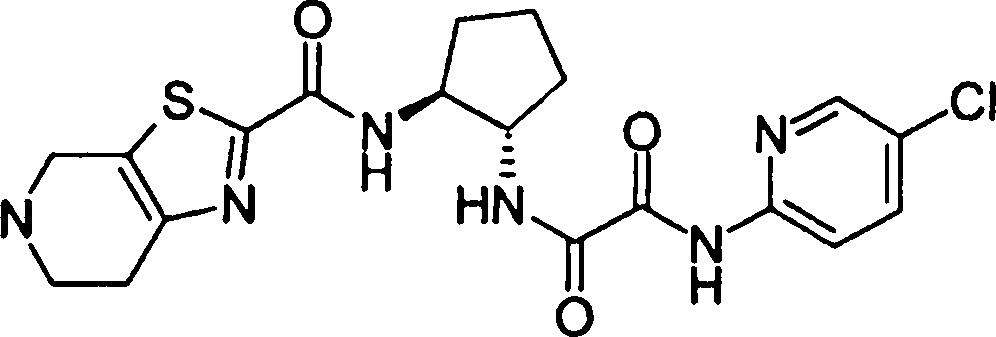
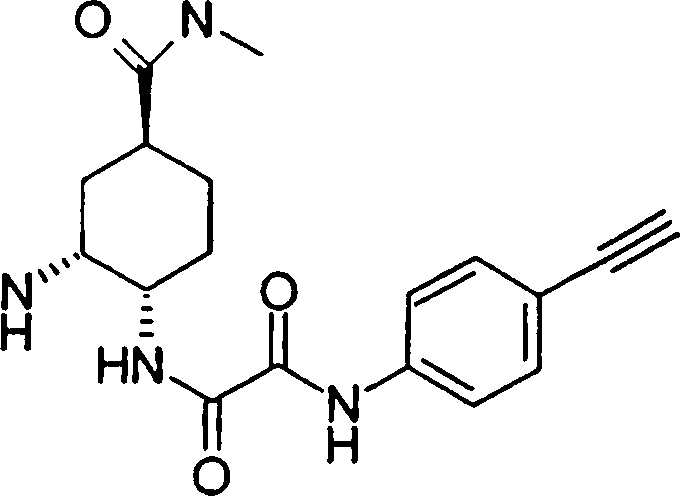
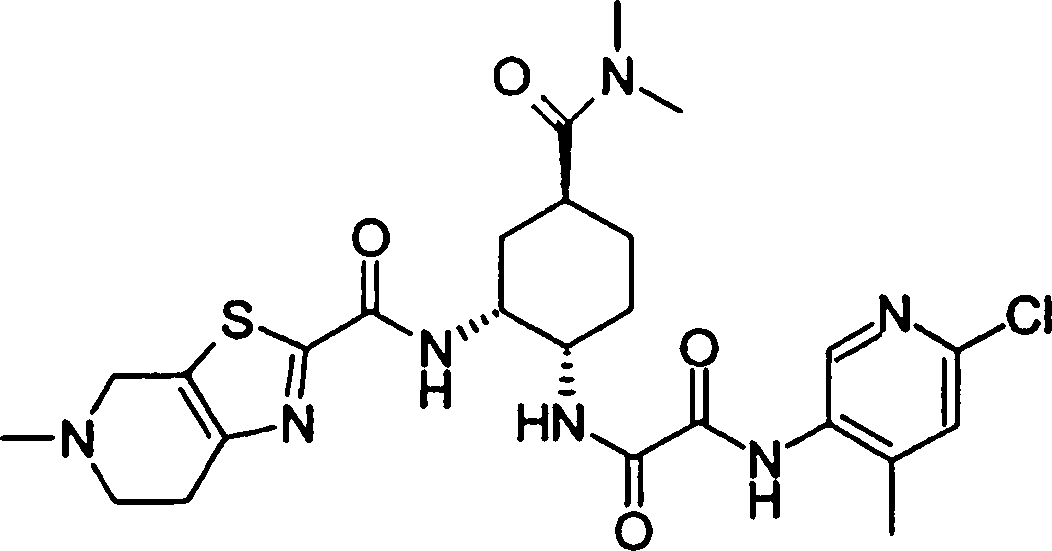
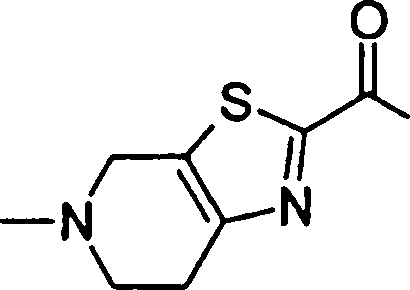
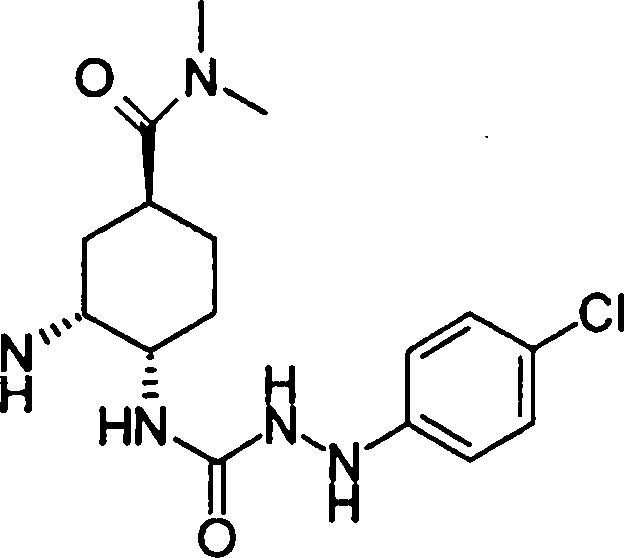
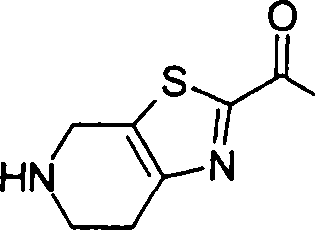
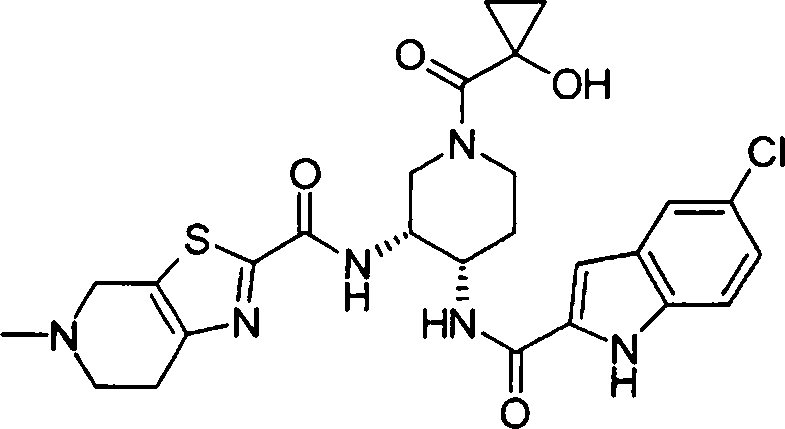
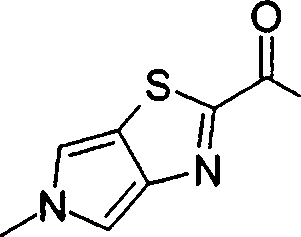
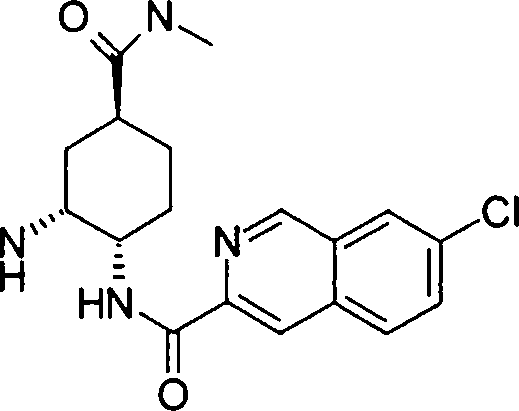
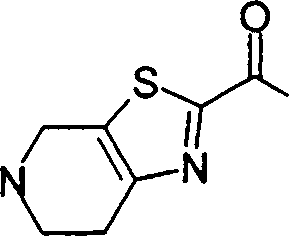
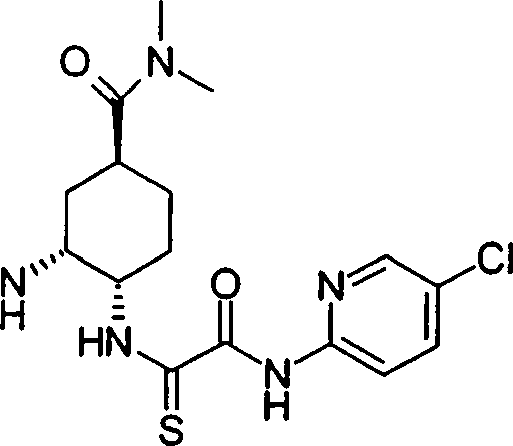
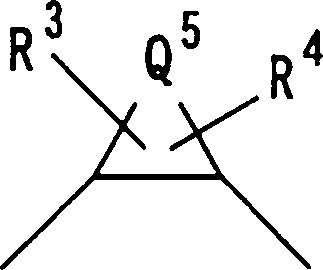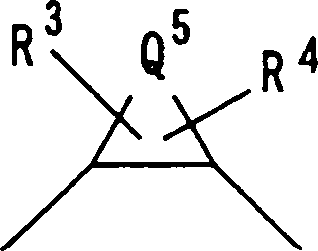(54) Título: COMPOSTOS DERIVADOS DIAMÍNICOS; COMPOSTOS INTERMEDIÁRIOS PARA A PREPARAÇÃO DESTES COMPOSTOS; COMPOSIÇÃO MEDICINAL COMPREENDENDO DITOS COMPOSTOS; E USOS DOS MESMOS PARA PREVENIR E/OU TRATAR TROMBOSE, EMBOLIA E OUTRAS DOENÇAS RELACIONADAS (73) Titular: DAIICHI SANKYO COMPANY, LIMITED, Companhia Japonesa. Endereço: 3-5-1, Nihombashi, Honcho, Chuo-ku, Tokyo 103-8426, JAPÃO(JP) (72) Inventor: TOSHIHARU ΘΗΤΑ; SATOSHI KOMORIYA; TOSHIHARU YOSHINO; KOUICHI UOTO; YUMI NAKAMOTO; HIROYUKI NAITO; AKIYOSHI MOCHIZUKI; TSUTOMU NAGATA; HIDEYUKI KANNO; NORIYASU HAGINOYA; KENJI YOSHIKAWA; MASATOSHI NAGAMOCHI; SYOZO KOBAYASHI; MAKOTO ONO.
Prazo de Validade: 10 (dez) anos contados a partir de 04/12/2018, observadas as condições legais
Expedida em: 04/12/2018
Assinado digitalmente por:
Liane Elizabeth Caldeira Lage
Diretora de Patentes, Programas de Computador e Topografias de Circuitos Integrados
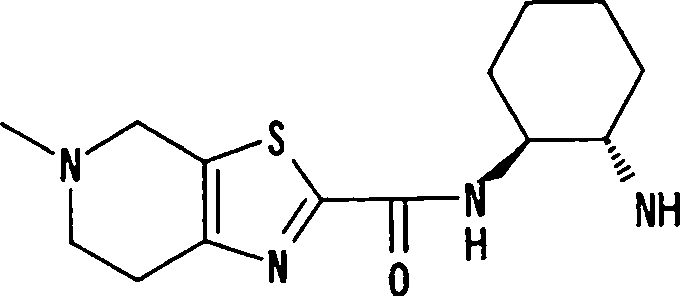
COMPOSTOS DERIVADOS DIAMÍNICOS; COMPOSTOS INTERMEDIÁRIOS PARA A PREPARAÇÃO DESTES COMPOSTOS; COMPOSIÇÃO MEDICINAL COMPREENDENDO DITOS COMPOSTOS; E USOS DOS MESMOS PARA PREVENIR E/OU TRATAR TROMBOSE, EMBOLIA E OUTRAS DOENÇAS RELACIONADAS
CAMPO TÉCNICO DA INVENÇÃO
A presente invenção refere-se a compostos inovadores que inibem o fator de coagulação sangüínea X ativado (aqui doravante abreviado como FXa), para apresentar um forte efeito anticoagulante e podendo ser administrados por via oral, e refere-se também a anticoagulantes ou agentes para prevenir e/ou tratar trombose ou embolia, que compreendem esse composto inovador como um ingrediente ativo.
ANTECEDENTES DA INVENÇÃO
Na angina instável, infarto cerebral, embolia cerebral, infarto do miocárdio, infarto pulmonar, embolia pulmonar, doença de Buerger, trombose venosa profunda, síndrome da coagulação intravascular disseminada, formação de trombos após substituição de válvula, reoclusão após angioplastia e formação de trombo durante a circulação extracorpórea, o estado hipercoagulável é um fator essencial. Portanto, há uma necessidade de se desenvolver anticoagulantes excelentes que tenham boa capacidade de resposta à dose, longa duração, baixo risco de hemorragia e poucos efeitos colaterais, e rápido aparecimento de efeitos suficientes, mesmo por administração oral (Thrombosis Research, Volume 68, páginas 507-512, 1992).
de 08/10/2018, pág. 10/857
Baseado na pesquisa de anticoagulantes que funcionam através de vários mecanismos de ação, sugere-se que os inibidores de FAx são anticoagulantes promissores. Um sistema de coagulação sangüínea compreende uma série de reações nas quais uma grande quantidade de trombina é produzida através de um processo de ampliação por reações enzimáticas em múltiplos estágios, para formar fibrina insolúvel. Em um sistema endógeno, o fator IX ativado ativa-se no fator X em uma membrana fosfolipidica na presença do fator VIII ativado e íons cálcio após reações de múltiplos estágios subseqüentes à ativação de um fator de contato. Em um sistema exógeno, o fator VII ativado ativa o fator X na presença de um fator tecidual. Mais especificamente, a ativação do fator X em FXa no sistema de coagulação é uma reação crucial na formação de trombina. O fator X ativado (FXa) decompõe de forma limitada a protrombina, para produzir trombina em ambos sistemas. Como a trombina produzida ativa fatores de coagulação na corrente superior, a formação de trombina é mais ampliada. Como descrito acima, como o sistema de coagulação na corrente superior de FXa é dividido no sistema endógeno e sistema exógeno, a produção de FXa não pode ser suficientemente inibida por enzimas inibidoras no sistema de coagulação na corrente superior de FXa, levando à produção de trombina. Como o sistema de coagulação compreende reações de autoampliação, a inibição do sistema de coagulação pode ser atingida mais eficientemente inibindo FXa na corrente superior de trombina do que a inibição de trombina de 08/10/2018, pág. 11/857 (Thrombosis Research, Volume 15, páginas 617-629, 1979).
Um outro ponto excelente de inibidores de FXa é uma grande diferença entre uma dose eficaz em um modelo de trombose e um tempo de sangramento em prolongamento em um modelo hemorrágico experimental. A partir deste resultado experimental, os inibidores de FXa são considerados anticoagulantes com baixo risco de hemorragia.
Vários compostos foram relatados como inibidores de FXa. Sabe-se gue a antitrombina III e os pentassacarídeos dependentes de antitrombina III não conseguem genericamente inibir complexos de protrombinase gue desempenham um papel prático na formação de trombos em um corpo vivo (Thrombosis Research, Volume 68, páginas 507-512, 1992; J. Clin. Invest. 71:1383-1389, 1983; Mebio 14:92-97, agosto). Além disso, eles não apresentam eficácia por administração oral. O peptídeo anticoagulante do carrapato (TAP) (Science 248:593-596, 1990) e a antiestasina (J. Biol. Chem. 263:10162-10167, 1988), isolados a partir de ácaros ou sanguessugas, gue são hematófagos, também inibem FXa e apresentam efeitos antitrombóticos contra trombose venosa e trombose arterial. Entretanto, estes compostos são peptídeos de alto peso molecular e estão indisponíveis para administração oral. Como descrito acima, o desenvolvimento de inibidores de FXa de baixo peso molecular independentes de antitrombina III, gue inibem diretamente os fatores de coagulação, foi conduzido.
É, portanto, um objeto da presente invenção fornecer um composto inovador gue tem um forte efeito de 08/10/2018, pág. 12/857 inibidor de FXa e apresenta um efeito antitrombótico de forma rápida, suficiente e persistente por administração oral.
DESCRIÇÃO DA INVENÇÃO
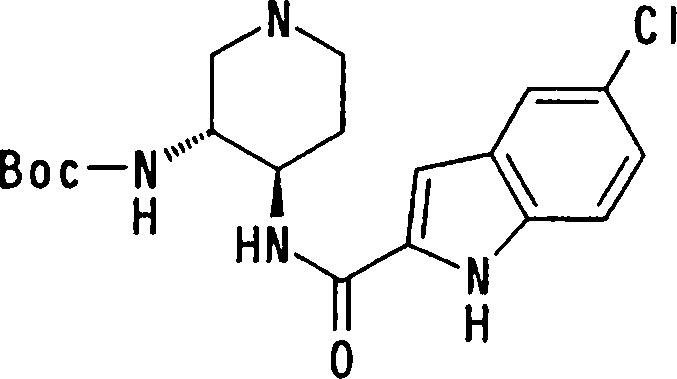
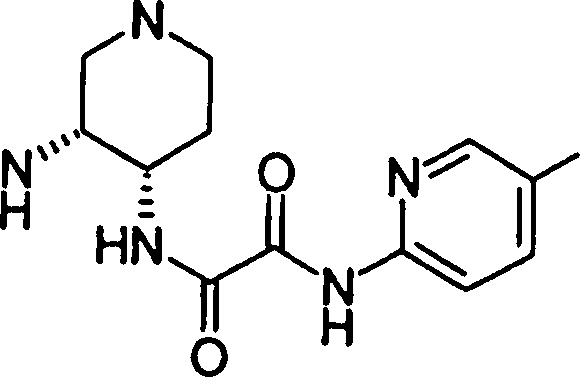
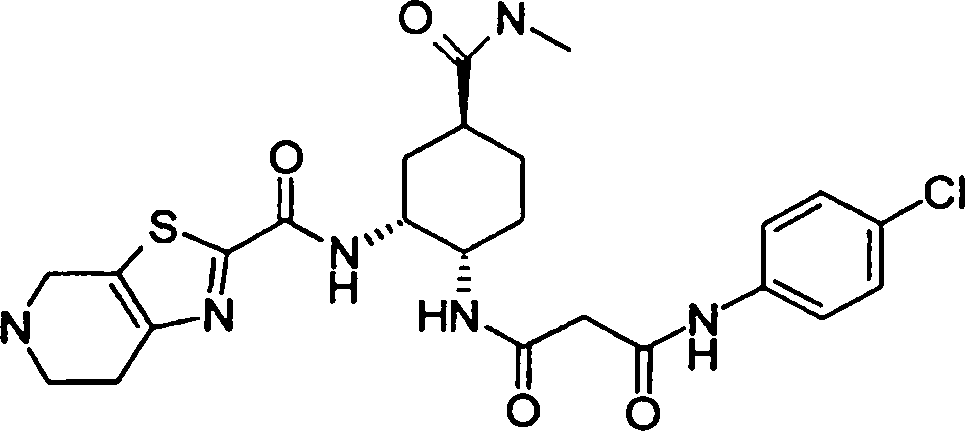
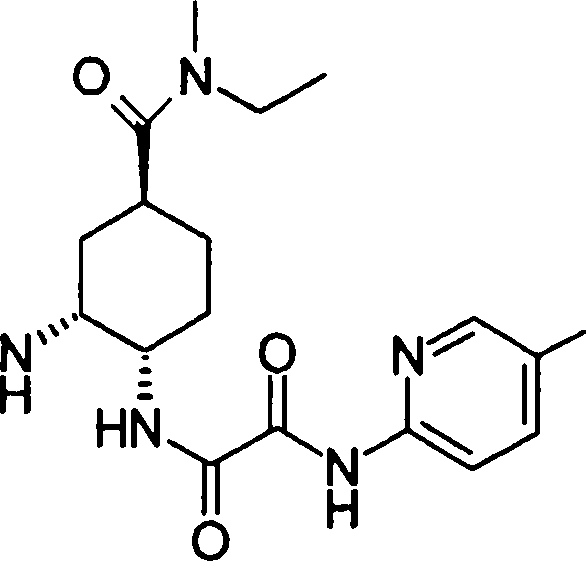
A presente requerente investigou a síntese e os efeitos farmacológicos de inibidores de FXa inovadores. Como resultado, derivados diamínicos, seus sais, e seus solvatos e N-óxidos, que apresentam forte efeito inibidor de FXa e efeito anticoagulante, foram descobertos. Descobriuse também que estes compostos inibem FXa de forma rápida, persistente e intensa e apresentam forte efeito anticoagulante e efeito antitrombótico quando administrados por via oral, e assim sendo, são úteis como profiláticos e remédios para várias doenças baseadas em tromboembolia, levando assim à realização da presente invenção.
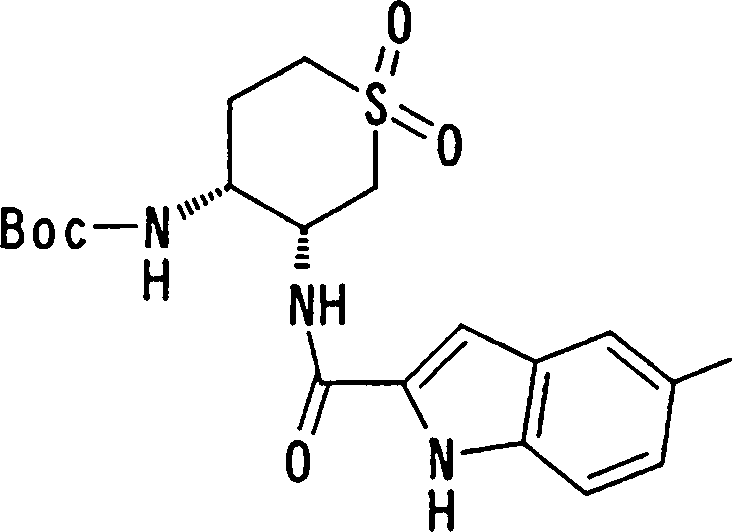
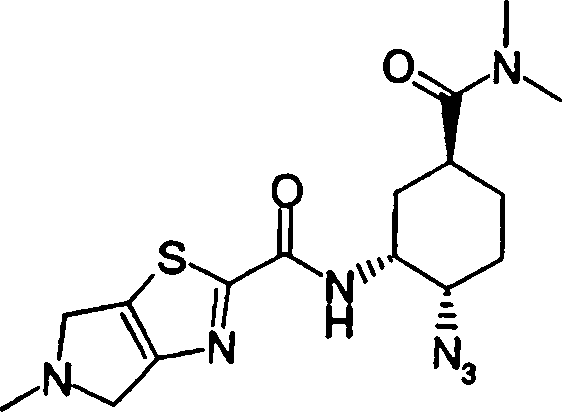
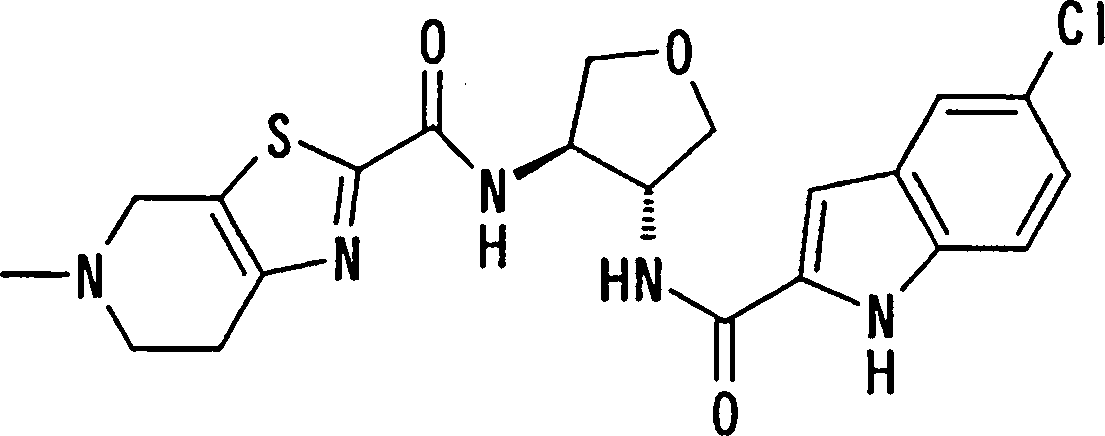
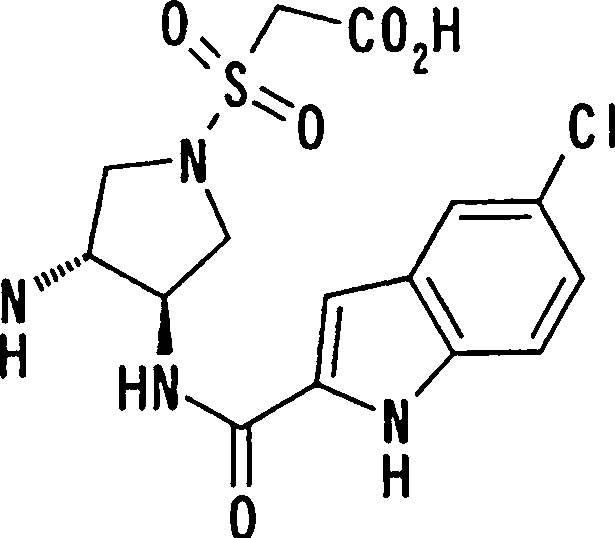
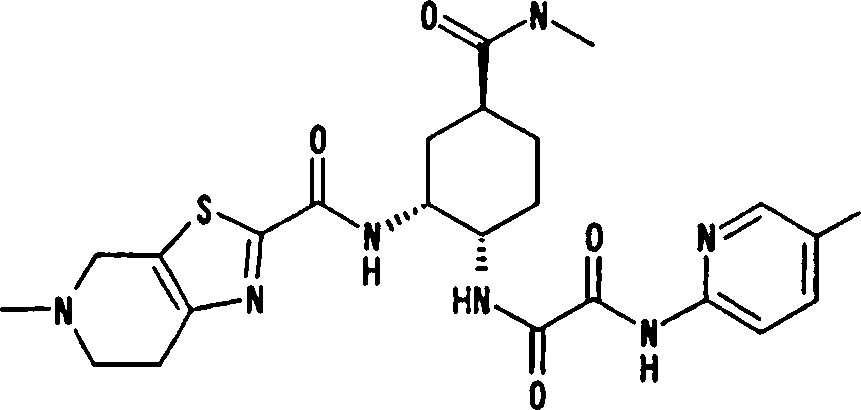
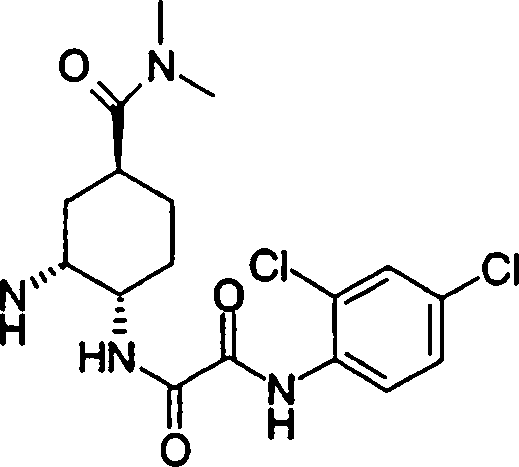
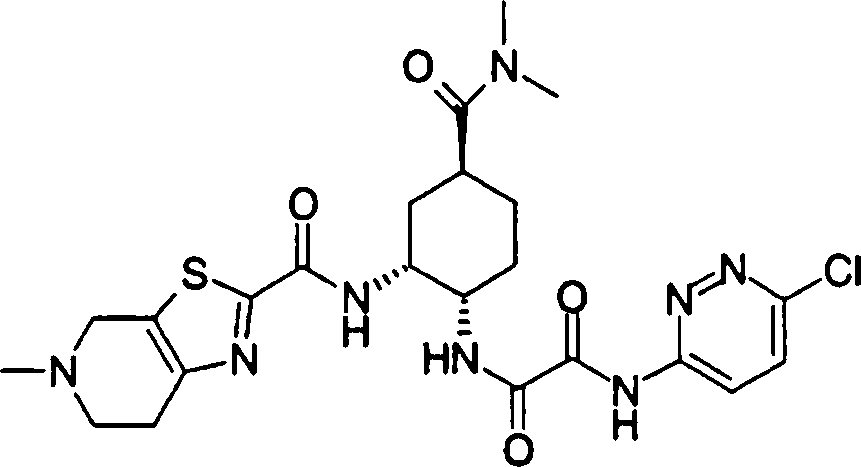
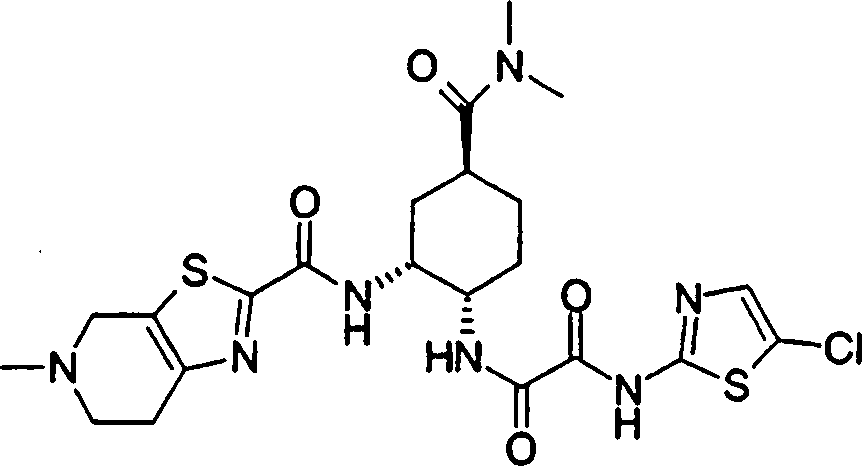
Esta invenção fornece um composto representado pela fórmula genérica (1):
qi_q2_to_n (Ri) -Q3_n(R2) -Tí-Q4 (1) onde
R1 e R2 representam, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila ou um grupo alcóxi;
Q1 representa um grupo hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou de 08/10/2018, pág. 13/857 insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
Q2 representa uma ligação simples, um grupo 5 hidrocarboneto cíclico bivalente, saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico bivalente saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído;
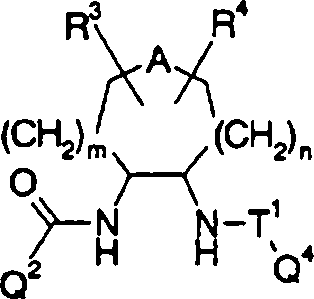
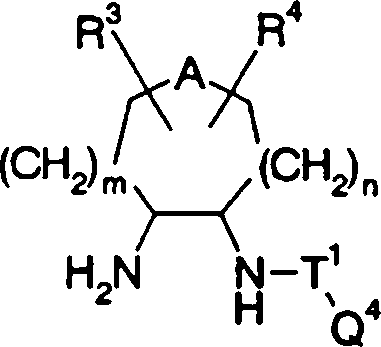
Q3 representa o seguinte grupo:
onde Q5 significa um grupo alquileno com 1 a 8 átomos de carbono, um grupo alquenileno com 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -S0-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH, e R3 e R4 são substituintes no(s) átomo(s) de carbono, átomo(s) de nitrogênio ou um átomo(s) de enxofre de um anel que compreende Q5 e são, um independentemente do outro, um átomo
Petição 870180138821, de 08/10/2018, pág. 14/857 de hidrogênio, um grupo hidroxila, um grupo alquila, um grupo alquenila, um grupo alquinila, um átomo de halogênio, um grupo halo-alquila, um grupo ciano, grupo ciano-alquila, grupo amino, grupo amino-alquila, grupo N-alquil-amino5 alquila, grupo N,N-dialquil-amino-alquila, grupo acila, grupo acil-alquila, grupo acil-amino que pode ser substituído, grupo alcóxi-imino, grupo hidróxi-imino, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo hidróxi-alquila, grupo carboxila, grupo carbóxi10 alquila, grupo alcóxi-carbonila, grupo alcóxi-carbonilalquila, grupo alcóxi-carbonil-alquil-amino, grupo carbóxialquil-amino, grupo alcóxi-carbonil-amino, grupo alcóxicarbonil-amino-alquila, grupo carbamoíla, grupo N-alquilcarbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenil-carbamoíla, grupo N-alquenil-carbamoil-alquila, grupo N-alquenil-N-alquilcarbamoíla, grupo N-alquenil-N-alquil-carbamoil-alquila, grupo N-alcóxi-carbamoíla, grupo N-alquil-N-alcóxi20 carbamoíla, grupo N-alcóxi-carbamoil-alquila, grupo Nalquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquilsulfonila, grupo alquil-sulfonil-alquila, grupo carbonila heterocíclico com 3 a 6 membros que pode ser substituído, grupo carbamoil-alquila, grupo N-alquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo carbamoilóxi-alquila, grupo NPetição 870180138821, de 08/10/2018, pág. 15/857 alquil-carbamoilóxi-alquila, grupo N,N-dialquilcarbamoilóxi-alquila, grupo carbonil-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo arila, grupo aralquila, grupo heteroarila, grupo heteroaril-alquila, grupo alquilsulfonil-amino, grupo aril-sulfonil-amino, grupo alquilsulfonil-amino-alquila, grupo aril-sulfonil-amino-alquila, grupo alquil-sulfonil-amino-carbonila, grupo aril-sulfonilamino-carbonila, grupo alquil-sulfonil-amino-carbonilalquila, grupo aril-sulfonil-amino-carbonil-alquila, grupo oxo, grupo carbamoilóxi, grupo aralquilóxi, grupo carbóxialquilóxi, grupo acilóxi, grupo acilóxi-alquila, grupo arilsulfonila, grupo alcóxi-carbonil-alquil-sulfonila, grupo carbóxi-alquil-sulfonila, grupo alcóxi-carbonil-acila, grupo alcóxi-alquilóxi-carbonila, grupo hidróxi-acila, grupo alcóxi-acila, grupo halo-acila, grupo carbóxi-acila, grupo amino-acila, grupo acilóxi-acila, grupo acilóxi-alquilsulfonila, grupo hidróxi-alquil-sulfonila, grupo alcóxialquil-sulfonila, grupo sulfonila heterocíclico com 3 a 6 membros, que pode ser susbtituído, grupo N-alquil-aminoacila, grupo N,N-dialquil-amino-acila, grupo N,N-dialquilcarbamoil-acila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquil-sulfonila que pode ter um substituinte no(s) grupo(s) alquila, grupo alquil-sulfonil-acila, grupo amino-carbotioíla, grupo Nalquil-amino-carbotioíla, grupo N,N-dialquil-aminocarbotioíla ou um grupo alcóxi-alquil-(tiocarbonila), ou R3 de 08/10/2018, pág. 16/857 e R4 juntos denotam um grupo alquileno com 1 a 5 átomos de carbono, um grupo alquenileno com 2 a 5 átomos de carbono, um grupo alquilenodioxi com 1 a 5 átomos de carbono, ou um grupo carbonildioxi;
|
Q4 |
representa |
um grupo arila |
que |
pode ser |
|
substituído, |
um grupo |
aril-alquenila |
que |
pode ser |
|
susbtituído, |
um grupo |
aril-alquinila |
que |
pode ser |
|
substituído, |
um grupo heteroarila que pode |
ser |
substituído, |
um grupo heteroaril-alquenila que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
T° representa um grupo carbonila ou tiocarbonila;
e
T1 representa um grupo carbonila, um grupo sulfonila, grupo -C(=0)-C(=0)-NR')-, grupo -C(=S)-C(=0)N(R')-, grupo -C(=O)-C(=S)-N(R')-, -C(=S)-C(=S)-N(R')-, onde R' significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcoxi, grupo -C(=0)-A1-N(R)-, onde A1 significa um grupo alquileno com 1 a 5 átomos de carbono, que pode ser substituído, e R significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcoxi, grupo -C(=0)-NH-, grupo -C(=S)-NH-, grupo -C(=0)-NHNH-, grupo -C(=0)-A2-C(=0)-, onde A2 significa uma ligação simples ou um grupo alquileno com 1 a 5 átomos de carbono, um grupo -C(=0)-A3-C(=0)-NH-, onde A3 significa um grupo alquileno com 1 a 5 átomos de carbono, um grupo -C(=0)de 08/10/2018, pág. 17/857
C (=NORa)-N (Rb)-, grupo -C (=S)-C (=NORa)-N (Rb)-, onde Ra significa um átomo de hidrogênio, um grupo alquila ou grupo alcanoíla, e Rb significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C(=0)N=N-, grupo -C(=S)-N=N-, grupo -C (=NORC)-C (=0)-N (Rd)-, onde Rc significa um átomo de hidrogênio, um grupo alquila, grupo alcanoíla, um grupo arila ou aralquila, e Rd significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C (=N-N (Re) (Rf)-C (=0)-N (R9)-, onde Re e R3 significam, um independentemente do outro, um átomo de hidrogênio, um grupo alquila, grupo alcanoíla ou um grupo alquil-(tiocarbonila), e R9 significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, ou um grupo tiocarbonila;
um seu sal, um seu solvato, ou um seu N-óxido.
Esta invenção fornece também um remédio, um inibidor do fator X de coagulação sangüínea ativado, um anticoagulante, um agente para prevenir e/ou tratar trombose ou embolia e um agente para prevenir e/ou tratar infarto cerebral, embolia cerebral, infarto do miocárdio, angina do peito, infarto pulmonar, embolia pulmonar, doença de Buerger, trombose venosa profunda, síndrome da coagulação intravascular disseminada, formação de trombos após substituição de válvula ou articulação, formação de trombos e reoclusão após angioplastia, síndrome da reação inflamatória sistêmica (SIRS), síndrome da disfunção de múltiplos órgãos (MODS), formação de trombos durante a circulação extracorpórea, ou coagulação sangüínea após de 08/10/2018, pág. 18/857 coleta de sangue, onde cada um compreende o composto representado pela fórmula genérica (1) , o seu sal, o seu solvato, ou seu N-óxido.
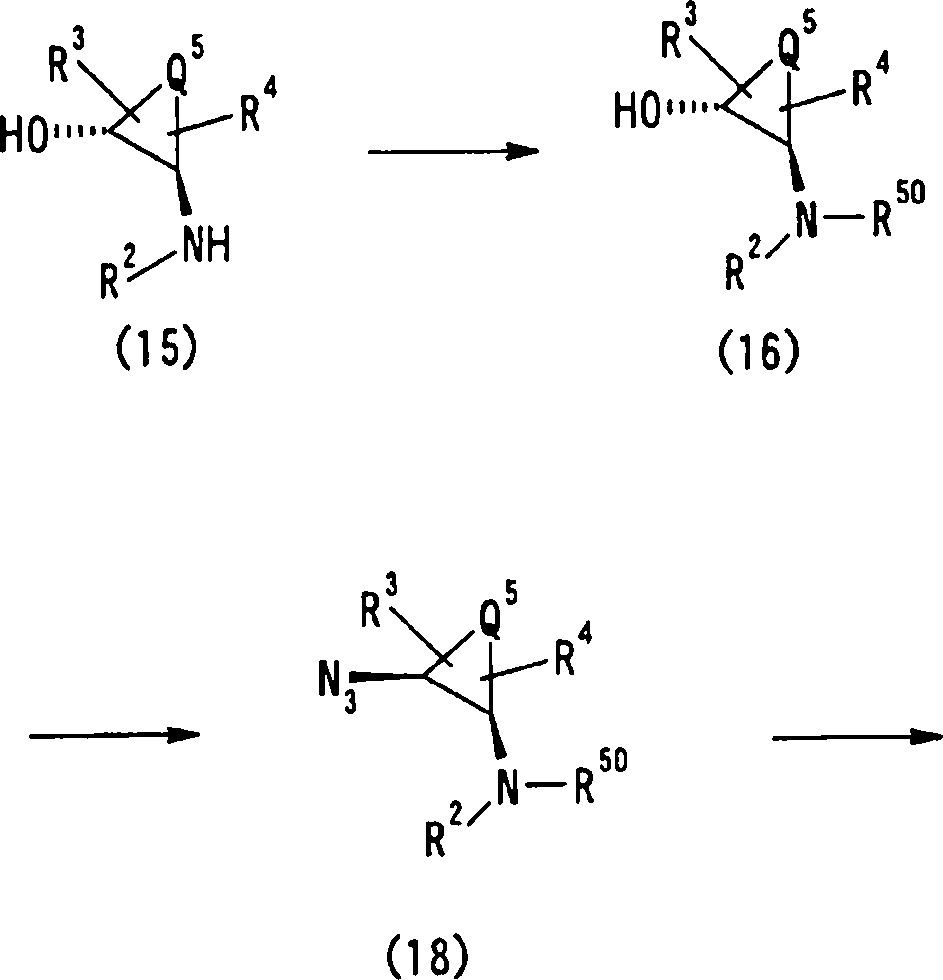
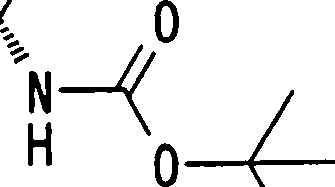
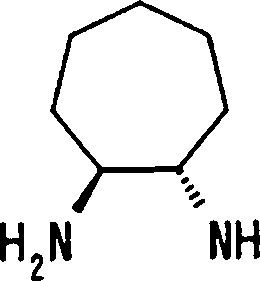
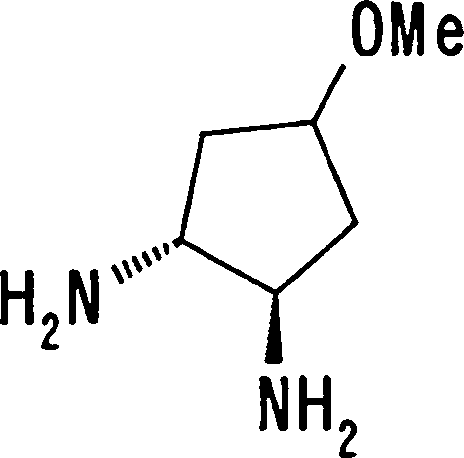
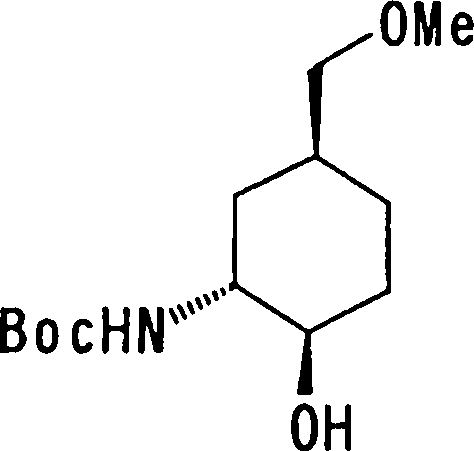
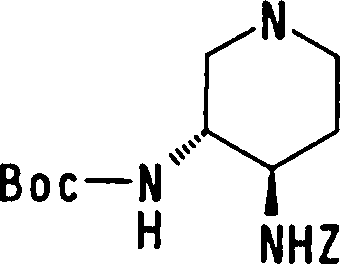
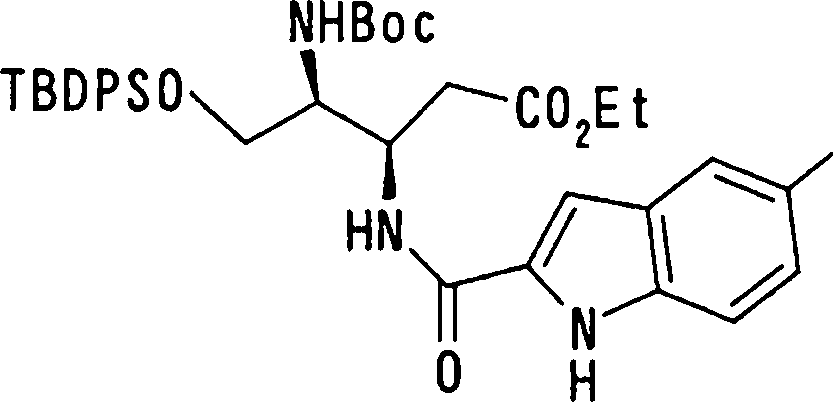
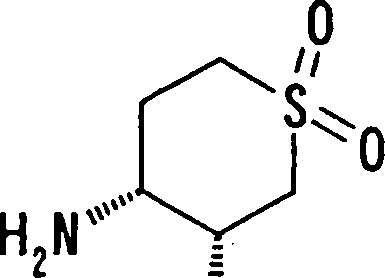
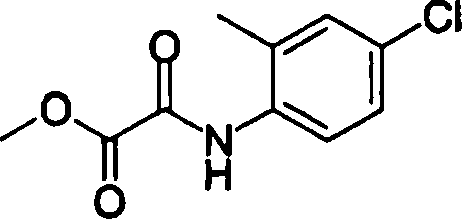
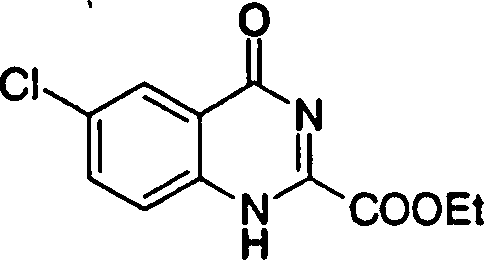
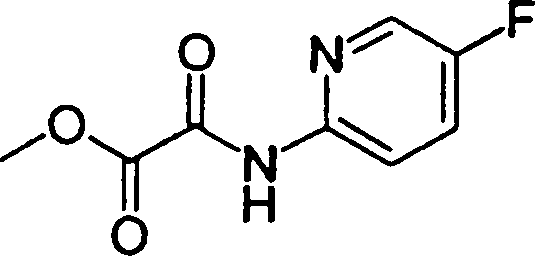
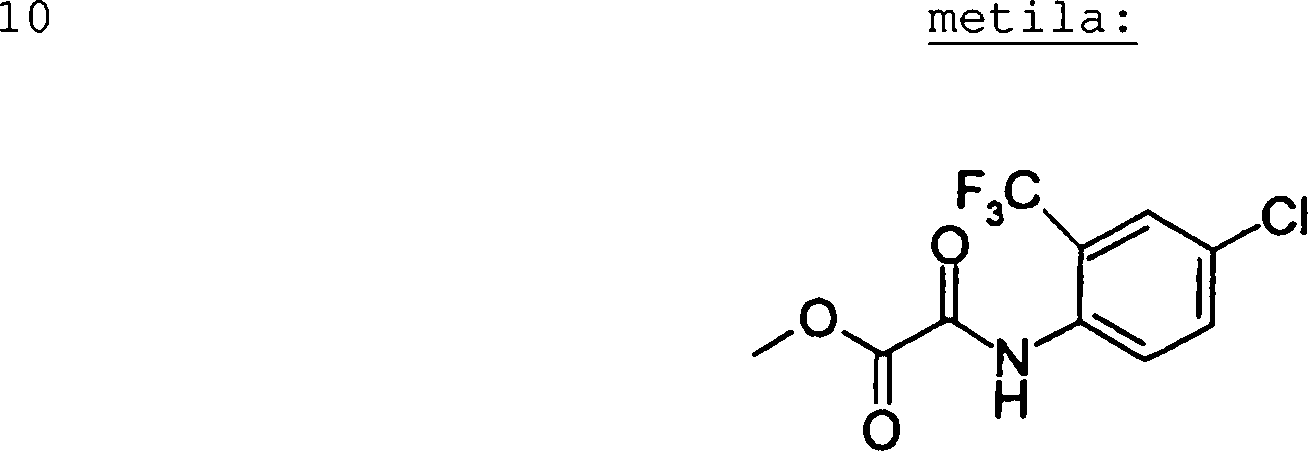
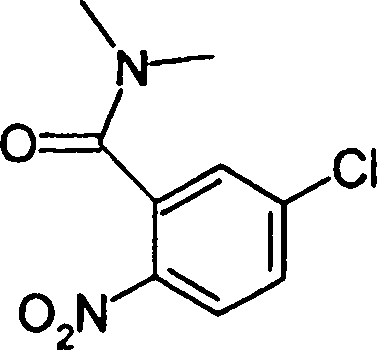
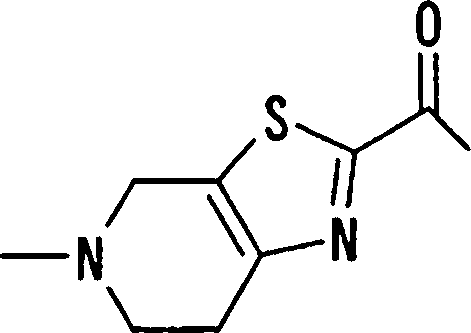
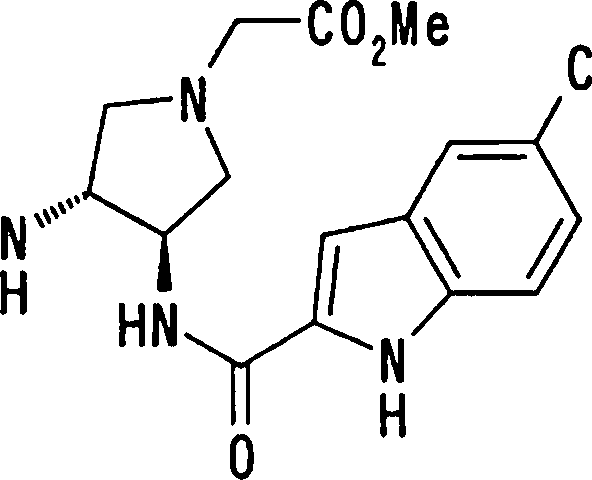
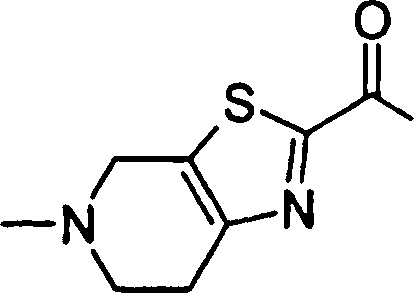
Esta invenção fornece ainda um intermediário útil para preparar o composto representado pela fórmula genérica (D ·
Esta invenção fornece ainda o uso do composto representado pela fórmula genérica (1) , o seu sal, o seu solvato, ou seu N-óxido, para a preparação de um medicamento.
Esta invenção fornece ainda um método para tratar trombose ou embolia, compreendendo administrar uma quantidade eficaz do composto representado pela fórmula genérica (1), o seu sal, o seu solvato, ou seu N-óxido.
MELHOR MODO DE CONDUZIR A INVENÇÃO
Os substituintes nos derivados diamínicos, de acordo com a presente invenção, representados pela fórmula genérica (1), serão aqui doravante descritos.
Grupo Q4
|
0 |
grupo |
Q4 significa um grupo arila |
que pode |
ser |
|
substituído, |
um |
grupo |
aril-alquenila |
que |
pode |
ser |
|
substituído, |
um |
grupo |
aril-alquinila |
que |
pode |
ser |
substituído, um grupo heteroarila que pode ser substituído, um grupo heteroaril-alquenila que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído.
de 08/10/2018, pág. 19/857
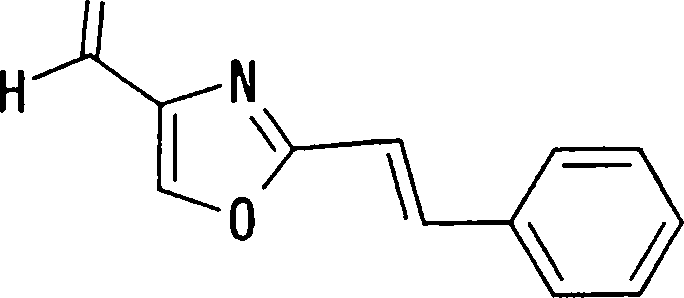
No grupo Q4, o grupo arila pode incluir grupos arila com 6 a 14 átomos de carbono, como por exemplo, os grupos fenila, naftila, antrila e fenantrila. O grupo arilalquenila significa um grupo formado por um grupo arila que tem 6 a 14 átomos de carbono e um grupo alquenileno que tem 2 a 6 átomos de carbono, e seus exemplos podem incluir um grupo estirila. O grupo aril-alquinila significa um grupo formado por um grupo arila que tem 6 a 14 átomos de carbono e um grupo alquinileno que tem 2 a 6 átomos de carbono, e seus exemplos podem incluir um grupo fenil-etinila.
O grupo heteroarila significa um grupo aromático monovalente que tem pelo menos um hetero átomo selecionado entre átomos de oxigênio, enxofre e nitrogênio, e seus exemplos podem incluir grupos heteroarila com 5 ou 6 membros, como por exemplo, os grupos piridila, piridazinila, pirazinila, furila, tienila, pirrolila, tiazolila, oxazolila, pirimidinila e tetrazolila. O grupo heteroarilalquenila significa um grupo formado pelo grupo heteroarila supradescrito e um grupo alquenileno com 2 a 6 átomos de carbono, e seus exemplos podem incluir os grupos tieniletenila e piridil-etenila.
O grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, significa um grupo monovalente derivado de um hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado. O hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado denota um hidrocarboneto bicíclico ou tricíclico fundido, formado fundindo 2 ou 3 hidrocarbonetos cíclicos, de 08/10/2018, pág. 20/857 saturados ou insaturados, com 5 ou 6 membros, que são iguais ou diferentes entre si. Neste caso, os exemplos de hidrocarbonetos cíclicos, saturados ou insaturados, com 5 ou 6 membros, podem incluir ciclo-pentano, ciclo-penteno, ciclo-hexano, ciclo-hexeno, ciclo-hexadieno e benzeno. Os exemplos específicos do grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, podem incluir os grupos indenila, indanila, tetraidronaftila e naftila. Incidentalmente, a posição do grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, ligado a T1 na fórmula genérica (1), não é particularmente limitada.
O grupo heterocíclico bicíclico ou tricíclico fundido, saturado ou insaturado, significa um grupo monovalente derivado de um anel heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado. O anel heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, denota o seguinte anel heterocíclico (1), (2) ou (3) :
(1) : um anel heterocíclico, bicíclico ou tricíclico fundido, formado pela fusão de 2 ou 3 anéis heterocíclicos saturados ou insaturados, tendo 5 a 7 membros, que podem ser iguais ou diferentes entre si;
(2) : um anel heterocíclico, bicíclico ou tricíclico fundido, formado pela fusão de um anel heterocíclico, saturado ou insaturado, tendo 5 a 7 membros, com 1 ou 2 hidrocarbonetos cíclicos, saturados ou insaturados, tendo 5 ou 6 membros; ou (3) : um anel heterocíclico tricíclico fundido, de 08/10/2018, pág. 21/857 formado pela fusão de 2 anéis heterocíclicos, saturados ou insaturados, tendo 5 a 7 membros, com um hidrocarboneto cíclico, saturado ou insaturado, com 5 ou 6 membros.
A posição do grupo heterocíclico bicíclico ou tricíclico fundido, saturado ou insaturado, ligado a T1 na fórmula genérica (1), não é particularmente limitada.
O anel heterocíclico, saturado ou insaturado, com 5 a 7 membros, denota um anel heterocíclico que tem pelo menos um hetero átomo selecionado entre átomos de oxigênio, enxofre e nitrogênio, e seus exemplos específicos podem incluir furano, pirrol, tiofeno, pirazol, imidazol, oxazol, oxazolidina, tiazol, tiadiazol, furazano, pirano, piridina, pirimidina, piridazina, pirrolidina, piperazina, piperidina, oxazina, oxadiazina, morfolina, tiazina, tiadiazina, tiomorfolina, tetrazol, triazol, triazina, tiazepina e oxazepina. O hidrocarboneto cíclico saturado ou insaturado, tendo 5 ou 6 membros, denota o mesmo hidrocarboneto cíclico, saturado ou insaturado, tendo 5 ou 6 membros, que foi indicado na descrição do grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado. Os exemplos específicos do grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, podem incluir os grupos benzofurila, isobenzofurila, benzotienila, indolila, indolinila, isoindolila, isoindolinila, indazolila, quinolila, hidroquinolila, 4-oxodiidroquinolila (diidroquinolin-4-ona), tetraidroquinolila, isoquinolila, tetraidroisoquinolila, cromenila, cromanila, isocromanila, 4H-4-oxobenzopiranila, 3, 4-diidro-4H-4-oxobenzopiranila, 4Hde 08/10/2018, pág. 22/857 quinolizinila, quinazolinila, diidroquinazolinila, tetraidroquinazolinila, quinoxalinila, tetraidroquinoxalinila, cinolinila, tetraidrocinolinila, indolizinila, tetraidroindolizinila, benzotiazolila, tetraidrobenzotiazolila, benzoxazolila, benzoisotiazolila, benzoisoxazolila, benzimidazolila, tetraidronaftiridinila, tetraidrotienopiridila, tetraidrotiazolopiridila, tetraidrotiazolopiridazinila, diidropirrolopiridila, pirrolopirimidinila, piridoquinazolinila, piridopirimidinila, naftiridinila, tienopiridila, tiazolopiridila, tiazolopiridazinila, pirrolopiridila, tetraidropirrolopiridila, diidropirrolopirimidinila, diidropiridoquinazolinila, tetraidropiridopirimidinila, piranotiazolila, diidropiranotiazolila, furopiridila, tetraidrofuropiridila, oxazolopiridila, tetraidrooxazolopiridila, oxazolopiridazinila, tetraidrooxazolopiridazinila, pirrolotiazolila, diidropirrolotiazolila, pirrolooxazolila, diidropirrolooxazolila, tienopirrolila, tiazolopirimidinila,
4-oxotetraidrocinolinila, 1,2,4-benzotiadiazinila, 1,1dioxi-2H-l,2,4-benzotiadiazinila, 1,2,4-benzoxadiazinila, ciclo-pentapiranila, tienofuranila, furopiranila, piridoxazinila, pirazoloxazolila, imidazotiazolila, imidazopiridila, tetraidroimidazopiridila, pirazinopiridazinila, benzoisoquinolila, furocinolila, pirazolotiazolopiridazinila, tetraidropirazolotiazolopiridazinila, hexaidrotiazolopiridazinopiridazinila, de 08/10/2018, pág. 23/857 imidazotriazinila, oxazolopiridila, benzoxepinila, benzoazepinila, tetraidrobenzoazepinila, benzodiazepinila, benzotriazepinila, tienoazepinila, tetraidrotienoazepinila, tienodiazepinila, tienotriazepinila, tiazoloazepinila, tetraidrotiazoloazepinila, 4,5,6,7-tetraidro-5,6tetrametilenotiazolopiridazinila, e 5,6-trimetileno-4,5,6,7tetraidrotiazolopiridazinila.
Nenhuma limitação específica é imposta sobre a forma de fusão do grupo heterocíclico fundido. Por exemplo, o grupo naftiridinila pode ser qualquer um entre os grupos 1,5-, 1,6-, 1,7-, 1,8-, 2,6 e 2,7-naftiridinila, o grupo tienopiridila pode ser qualquer um entre os grupos tieno[2,3-b]piridila, tieno[2,3-c]-piridila, tieno[3,2b] piridila, e tieno[3, 4-c]-piridila, o grupo tienopirrolila pode ser qualquer um entre os grupos tieno[2,3-b]pirrolila e tieno[2,3-b]pirrolila, o grupo tiazolopiridila pode ser qualquer um entre os grupos tiazolo[4,5-b]piridila, tiazolo[4,5-c]piridila, tiazolo[5,4-b]piridila, tiazolo[5,4c] piridila, tiazolo[3,4-a]piridila, e tiazolo[3,2a] piridila, o grupo tiazolopiridazinila pode ser qualquer um entre os grupos tiazolo[4,5-c]piridazinila, tiazolo[4,5d] piridazinila, tiazolo[5,4-c]piridazinila, e tiazolo[3,2b] piridazinila, o grupo pirrolopiridila pode ser qualquer um entre os grupos pirrolo[2,3-b]piridila, pirrolo[2,3c] piridila, pirrolo[3,2-b]piridila, pirrolo[3,2-c]piridila, pirrolo[3,4-b]piridila, e pirrolo[3,4-c]piridila, o grupo piridopirimidinila pode ser qualquer um entre os grupos pirido[2,3-d]pirimidinila, pirido[3,2-d]pirimidinila, de 08/10/2018, pág. 24/857 pirido[3,4-d]pirimidinila, pirido[4,3-d]pirimidinila, pirido[1,2-c]pirimidinila, e pirido[1,2-a]pirimidinila, o grupo piranotiazolila pode ser qualquer um entre os grupos pirano[2,3-d]tiazolila, pirano[4,3-d]tiazolila, pirano[3,4d]tiazolila, e pirano[3,2-d]tiazolila, o grupo furopiridila pode ser qualquer um entre os grupos furo[2,3-b]piridila, furo[2,3-c]piridila, furo[3, 2-b]piridila, furo[3,2-c] piridila, furo[3,4-b]piridila, e furo[3,4-c]piridila, o grupo oxazolopiridila pode ser qualquer um entre os grupos oxazolo[4,5-b]piridila, oxazolo[4,5-c]piridila, oxazolo[5,4b]piridila, oxazolo[5,4-c]piridila, oxazolo[3,4-a]piridila, e oxazolo[3,2-a]piridila, o grupo oxazolopiridazinila pode ser qualquer um entre os grupos oxazolo[4,5-c]piridazinila, oxazolo[4,5-d]piridazinila, oxazolo[5,4-c]piridazinila, e oxazolo[3,4-b]piridazinila, o grupo pirrolotiazolila pode ser qualquer um entre os grupos pirrolo[2,1-b]tiazolila, pirrolo[1,2-c]tiazolila, pirrolo[2,3-d]tiazolila, pirrolo [3,2-d]tiazolila, e pirrolo[3,4-d]tiazolila, o grupo pirrolooxazolila pode ser qualquer um entre os grupos pirrolo[2,1-b]oxazolila, pirrolo[1,2-c]oxazolila, pirrolo [2,3-d]oxazolila, pirrolo[3,2-d]oxazolila, e pirrolo[3,4d]oxazolila, o grupo benzoazepinila pode ser qualquer um entre os grupos ΙΗ-1-benzoazepinila, ΙΗ-2-benzoazepinila, e ΙΗ-3-benzoazepinila, ou pode ser um grupo benzoazepinila do tipo derivado de diidro-oxo, tal como o grupo 4,5-diidro-loxo-lH-2-benzoazepinila, o grupo benzodiazepinila pode ser qualquer um entre os grupos 1H-1,3-benzodiazepinila, 1H-1,4benzodiazepinila, e 1H-1,5-benzodiazepinila, ou pode ser um de 08/10/2018, pág. 25/857 grupo benzodiazepinila do tipo derivado de diidro-oxo, tal como o grupo 4,5-diidro-4-oxo-lH-l,3-benzodiazepinila, o grupo benzotriazepinila pode ser qualquer um entre os grupos 1H-1,3,4-benzotriazepinila e 1H-1,3,5-benzotriazepinila, ou pode ser um grupo benzotriazepinila do tipo derivado de diidro-oxo, tal como benzotriazepinila, e qualquer um entre o grupo 4,5-diidro-5-oxo-lH-l, 3, 4o grupo tienoazepinila pode ser os grupos tieno[2,3-b]azepinila, tieno[2,3-c]azepinila, tieno[2,3-d]azepinila, tieno[3,2-c] 10 azepinila, e tieno [3,2-b] azepinila, ou pode ser um grupo tienoazepinila do tipo derivado de diidro-oxo, tal como o grupo 5, 6, 7,8-tetraidro-4-oxo-4H-tieno[3,2-c]azepinila. Os grupos tienodiazepinila e tienotriazepinila podem ser também quaisquer formas de fusão, ou podem ser aqueles do tipo 15 derivado de diidro-oxo. O grupo benzotaizepinila pode ser qualquer um entre os grupos ΙΗ-1-benzotiazepinila, 1H-2benzotiazepinila, e ΙΗ-3-benzotiazepinila, ou pode ser um grupo benzotiazepinila do tipo derivado de diidro-oxo, tal como o grupo 4,5-diidro-l-oxo-lH-2-benzotiazepinila, e o 20 grupo benzoxazepinila pode ser qualquer um entre os grupos ΙΗ-1-benzoxazepinila, ΙΗ-2-benzoxazepinila e 1H-3benzoxazepinila, ou ele pode ser um grupo benzoxazepinila do tipo derivado de diidro-oxo, tal como o grupo 4,5-diidro-loxo-lH-2-benzoxazepinila. Outras formas de fusão que não 25 estas podem ser admitidas.
Os grupos arila, grupos heteroarila, grupos arilalquenila, grupos heteroaril-alquenila, grupos hidrocarboneto bicíclicos ou tricíclicos fundidos, saturados
Petição 870180138821, de 08/10/2018, pág. 26/857 ou insaturados, e os grupos heterocíclicos, bicíclicos ou tricíclicos fundidos, saturados ou insaturados, supradescritos, podem ter, cada um, 1 a 3 substituintes. Os exemplos de substituintes podem incluir um grupo hidroxila, átomos de halogênio, tais como um átomo de flúor, átomos de cloro, átomo de bromo e átomo de iodo, grupos halo-alquila com 1 a 6 átomos de carbono substituídos por 1 a 3 átomos de halogênio, um grupo amino, um grupo ciano, grupos aminoalquila, um grupo nitro, grupos hidróxi-alquila (como por exemplo, o grupo hidróxi-metila, o grupo 2-hidróxi-etila, etc.), grupos alcóxi-alquila (como por exemplo, o grupo metóxi-metila, o grupo 2-metóxi-etila, etc.), um grupo carboxila, grupos carbóxi-alquila (como por exemplo, o grupo carbóxi-metila, o grupo 2-carbóxi-etila, etc.), grupos alcóxi-carbonil-alquila (como por exemplo, o grupo metóxicarbonil-metila, o grupo etóxi-carbonil-metla, etc.), grupos acila (como por exemplo, grupos alcanoíla, tais como o grupo formila, grupo acetila, e grupo propionila), um grupo amidino, um grupo hidróxi-amidino, grupos alquila lineares, ramificados ou cíclicos, com 1 a 6 átomos de carbono (como por exemplo, o grupo metila, grupo etila, etc.), grupos alcóxi lineares, ramificados ou cíclicos, com 1 a 6 átomos de carbono (como por exemplo, o grupo metóxi, grupo etóxi, etc.), grupos amidino substituídos com um grupo alcóxicarbonila, tendo 2 a 7 átomos de carbono (como por exemplo, o grupo metóxi-carbonil-amidino, o grupo etóxi-carbonilamidino, etc.), grupos alquenila lineares, ramificados ou cíclicos, tendo 2 a 6 átomos de carbono (como por exemplo, o de 08/10/2018, pág. 27/857 grupo vinila, o grupo alila, etc.), grupos alquinila lineares ou ramificados, tendo 2 a 6 átomos de carbono (como por exemplo, o grupo etinila, o grupo propinila, etc.), grupos alcóxi-carbonila lineares, ramificados ou cíclicos, tendo 2 a 6 átomos de carbono (como por exemplo, o grupo metóxi-carbonila, o grupo etóxi-carbonila, etc.), um grupo carbamoíla, grupos mono- ou dialquil-carbamoíia substituídos com grupos alquila lineares, ramificados ou cíclicos, tendo 1 a 6 átomos de carbono no(s) átomo(s) de nitrogênio (como por exemplo, metil-carbamoíia, etil-carbamoíia, dimetilcarbamoíla, etil-metil-carbamoíia, etc.), grupos mono- ou dialquil-amino substituídos com 1 ou 2 grupos alquila lineares, ramificados ou cíclicos, tendo 1 a 6 átomos de carbono (como por exemplo, grupo etil-amino, grupo dimetilamino e grupo metil-etil-amino, etc.), e grupos heterocíclicos de 5 ou 6 membros contendo nitrogênio (como por exemplo, o grupo pirrolidino, grupo piperidino, grupo piperazino, grupo morfolino, etc.).
Como grupo Q4, são preferidos os 12 grupos que se seguem, (a) até (1), dentre os grupos supradescritos. A saber:
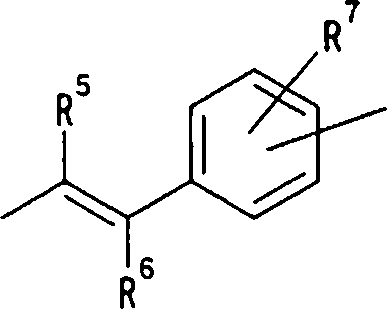
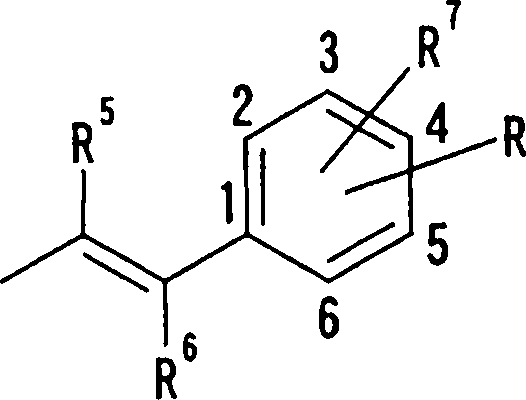
onde R5 e R6 representam, cada um independentemente do de 08/10/2018, pág. 28/857 outro, um átomo de hidrogênio, um grupo ciano, um átomo de halogênio, um grupo alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo, alcóxi-carbonila, grupo alcóxi-carbonil-alquila, ou o grupo fenila que pode ser substituído com um grupo ciano, grupo hidroxila, átomo de halogênio, grupo alquila ou grupo alcóxi, e R7 e R8 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo carbamoíla, grupo N-alquil-carbamoíla, grupo N,N-dialquilcarbamoíla, grupo alcóxi-carbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;

,10 (b) onde R9 e R10 representam, cada um independetemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo carbamoíla, grupo N-alquil-carbamoíla, grupo N,N-dialquilde 08/10/2018, pág. 29/857 carbamoíla, grupo alcóxi-carbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;

R13 (c) onde R11, R12 e R13 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo haloalquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxialquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo carbamoíla, grupo N-alquil-carbamoíla, grupo N,N-dialquil-carbamoíla, grupo alcóxi-carbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;
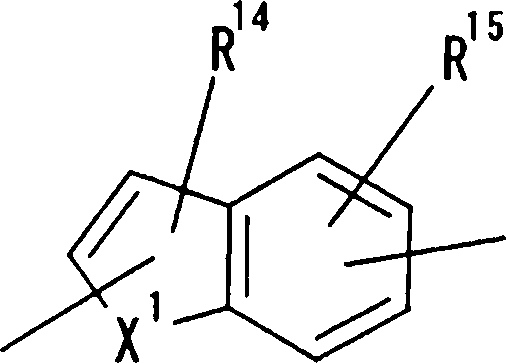
J6 (d) onde X1 representa CH2, CH, NH, NOH, N, O ou S, e R14, R15 e R16 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo
Petição 870180138821, de 08/10/2018, pág. 30/857 hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo carbamoila, grupo N-alquil-carbamoila, grupo N,N-dialquilcarbamoila, grupo alcóxi-carbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;
onde X2 representa NH, N, 0 ou S, X3 representa N, C ou CH, X4 representa N, C ou CH, e R17 e R18 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxialquila, grupo acila, grupo carbamoila, grupo N-alquilcarbamoila, grupo N,N-dialquil-carbamoila, grupo alcóxi15 carbonila, grupo amidino ou grupo alcóxi-carbonil-alquila, excluindo os casos nos quais X3 e X4 são combinações de C e CH, e são ambos C ou CH;
Petição 870180138821, de 08/10/2018, pág. 31 /857
|
onde N indica que |
1 ou |
2 |
|
substituído com |
R19 |
foram |
su |
|
nitrogênio, e |
R19, |
R20 |
e |
|
independentemente |
do |
outro, |
um |
átomos de carbono do anel
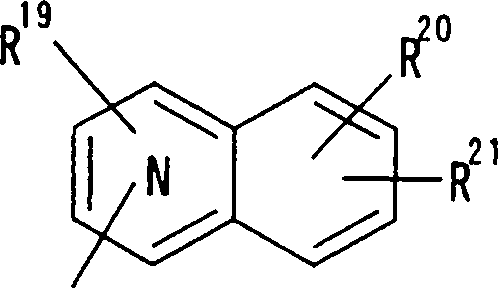
R21 representam, cada um hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxialquila, grupo acila, grupo carbamoíla, grupo N-alquilcarbamoíla, grupo N, N-dialquil-carbamoíia, grupo alcóxicarbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;

onde X5 representa CH2, CH, N ou NH, Z1 representa Ν, NH ou O, Z2 representa CH2, CH, C ou Ν, Z3 representa CH2, CH, S, SO2 ou C=O, X5-Z2 indica que X5 e Z2 estão unidos entre si por uma ligação simples ou ligação dupla, R22 e R23 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo de 08/10/2018, pág. 32/857 carbamoíla, grupo N-alquil-carbamoíla, grupo N,N-dialquilcarbamoíla, grupo alcóxi-carbonila, grupo amidino ou grupo alcóxi-carbonil-alquila, e R24 representa um átomo de hidrogênio ou um grupo alquila;

(h) onde X6 representa 0 ou S, e R25 e R26 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxialquila, grupo acila, grupo carbamoíla, grupo N-alquilcarbamoíla, grupo N, N-dialquil-carbamoíla, grupo alcóxicarbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;

(i) onde R27 e R28 representam, cada um independentemente do 15 outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo haloalquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxiPctição 870180138821, de 08/10/2018, pág. 33/857 alquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo carbamoíla, grupo N-alquil-carbamoíla, grupo N,N-dialquil-carbamoíla, grupo alcóxi-carbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;

onde E1 e E2 representam, cada um independentemente do outro, N ou CH, e R29 e R30 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxialquila, grupo acila, grupo carbamoíla, grupo N-alquilcarbamoí la, grupo N,N-dialquil-carbamoíla, grupo alcóxicarbonila, grupo amidino ou grupo alcóxi-carbonil-alquila;
(k) onde Y1 representa CH ou N, Y2 representa -N (R33)-, onde R33 significa um átomo de hidrogênio ou um grupo alquila que tem 1 a 6 átomos de carbono, O ou S, e R31 e R32 representam, cada um independentemente do outro, um átomo de hidrogênio,
Petição 870180138821, de 08/10/2018, pág. 34/857 um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcoxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo acila, grupo carbamoíla, grupo Nalquil-carbamoíla, grupo N, N-dialquil-carbamoíla, grupo alcóxi-carbonila, grupo amidino ou grupo alcóxi-carbonilalquila; e
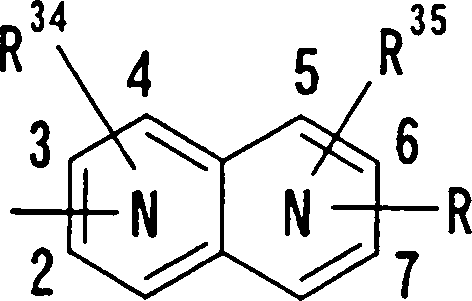
onde os números 1 a 8 indicam posições, cada N indica que um dos átomos de carbono das posições 1 a 4 e qualquer um dos átomos de carbono das posições 5 a 8 foi substituído com um átomo de nitrogênio, e R34, R35 e R36 representam, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo nitro, grupo amino, grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo halo-alquila, grupo hidróxi-alquila, grupo alcoxi, grupo alcóxi-alquila, grupo carboxila, grupo carbóxialquila, grupo acila, grupo carbamoíla, grupo N-alquilcarbamoíla, grupo N,N-dialquil-carbamoíla, grupo alcóxicarbonila, grupo amidino ou grupo alcóxi-carbonil-alquila.
Estes grupos serão aqui doravante descritos.
de 08/10/2018, pág. 35/857
Na descrição de R5 a R36, o átomo de halogênio é um átomo de flúor, cloro, bromo ou iodo, o grupo alquila é um grupo alquila linear, ramificado ou cíclico, tendo 1 a 6 átomos carbono, o grupo alquenila é um grupo alquenila linear, ramificado ou cíclico, tendo 2 a 6 átomos carbono, o grupo alquinila é um grupo alquinila linear ou ramificado, tendo 2 a 6 átomos carbono, o grupo hidróxi-alquila significa o grupo alquila de C1-C6 supradescrito, substituído com um grupo hidroxila, o grupo alcóxi é um grupo alcóxi linear, ramificado ou cíclico, tendo 1 a 6 átomos de carbono, o grupo alcóxi-alquila significa o grupo alquila de C1-C6 supradescrito, substituído com um grupo alcóxi de C1-C6 supradescrito, o grupo carbóxi-alquila significa o grupo alquila de C1-C6 supradescrito, substituído com um grupo carboxila, o grupo acila é um grupo alcanoíla (inclusive formila), tendo 1 a 6 átomos de carbono, um grupo aroíla, tal como um grupo benzoíla ou naftoíla, ou um grupo aril-alcanoíla com o grupo arila de C6-C14 supradescrito, substituído no grupo alcanoíla de C1-C6 supradescrito, o grupo N-alquil-carbamoíla significa um grupo carbamoíla com o grupo alquila de C1-C6 supradescrito substituído no átomo de nitrogênio, o grupo N,N-dialquilcarbamoíla significa um grupo carbamoíla com dois dos grupos alquila de C1-C6 supradescritos substituídos no átomo de nitrogênio, o grupo alcóxi-carbonila é um grupo constituído do grupo alcóxi de C1-C6 supradescrito e um grupo carbonila, o grupo alcóxi-carbonil-alquila significa o grupo alquila de Ci-C6 supradescrito substituído com o grupo alcóxi-carbonila de 08/10/2018, pág. 36/857 de Ci-Cô supradescrito, e o grupo halo-alquila significa o grupo alquila de Ci-Cõ supradescrito substituído com 1 a 3 átomos de halogênio. Incidentalmente, na descrição acima, nenhuma limitação é imposta sobre a posição de substituição.
No seguinte grupo:
|
onde R5, R6, |
R7 e |
R8 |
têm os significados |
definidos |
acima, |
e |
|
os números |
1 a |
6 |
indicam posições, |
R5 e R6, |
cada |
um |
|
independentemente |
do |
outro, é de preferência um |
átomo |
de |
hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo haloalquila. R5 e R6 são, mais preferivelmente, átomos de hidrogênio ou grupos alquila. No caso do grupo alquila, um grupo metila é preferido. Prefere-se que um entre R7 e R8 seja um átomo de hidrogênio e o outro seja um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo haloalquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se de 08/10/2018, pág. 37/857 particularmente um grupo etinila. Como exemplos preferíveis específicos do grupo representado pela fórmula acima, podem ser mencionados os grupos cloro-estirila, flúor-estirila, bromo-estirila e etinil-estirila. A posição substituída pelo átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência particularmente uma posição 4 na fórmula acima, embora ela não deva ser particularmente limitada. Como exemplos preferíveis específicos deles, podem ser mencionados os grupos 4-cloro-estirila, 4-flúor-estirila, 410 bromo-estirila e 4-etinil-estirila.
No seguinte grupo:
onde R9 e R10 têm os mesmos significados definidos acima, e os números 1 a 6 indicam posições, R9 e R10, cada um independentemente do outro, é de preferência um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou grupo alquinila. Prefere-se ainda que R9 seja um átomo de hidrogênio, e que R10 seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, um grupo metila é preferido. Como grupo alquinila, um grupo etinila é particularmente preferido. Como exemplos preferíveis
Petição 870180138821, de 08/10/2018, pág. 38/857 específicos do grupo representado pela fórmula acima, podem ser mencionados os grupos cloro-fenil-etinila, flúor-feniletinila, bromo-fenil-etinila, e etinil-fenil-etinila. A posição substituída pelo átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência particularmente uma posição 4 na fórmula acima, embora ela não deva ser particularmente limitada. Como exemplos preferíveis específicos deles, podem ser mencionados os grupos 4-clorofenil-etinila, 4-flúor-fenil-etinila, 4-bromo-fenil-etinila, e 4-etinil-fenil-etinila.
No seguinte grupo:


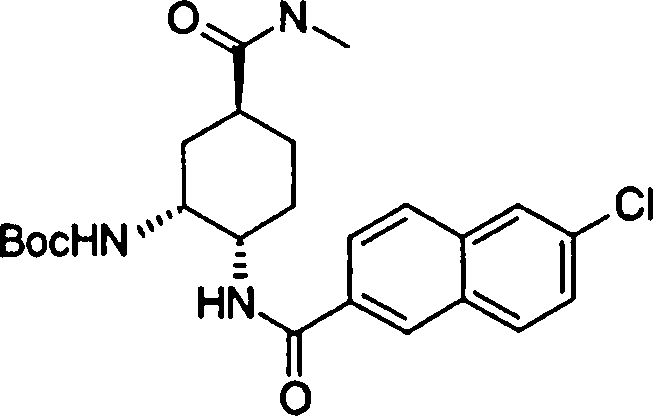
onde R11, R12 e R13 têm os mesmos significados definidos acima, e os números 1 a 8 indicam posições, R11 e R12 são, cada um independentemente do outro, de preferência um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo haloalquila. R11 é de preferência um átomo de hidrogênio, um grupo alquila, um átomo de halogênio, ou um grupo hidroxila, sendo um átomo de hidrogênio particularmente preferido. Prefere-se que um entre R12 e R13 seja um átomo de hidrogênio e o outro seja um átomo de hidrogênio, um grupo ciano, átomo de 08/10/2018, pág. 39/857 de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo halo-alquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. No grupo naftila, um grupo 2-naftila é preferido em detrimento de um grupo 1-naftila. No caso do grupo 2-naftila, uma posição substituída com um átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência uma posição 6 ou 7 na fórmula acima, embora ela não seja particularmente limitada, sendo a posição 6 mais preferida. Estes grupos naftila são, de preferência, substituídos com um átomo de cloro, flúor ou bromo, um grupo alquinila, ou similares, sendo particularmente preferido um grupo que tem um substituinte tal como um átomo de cloro, flúor ou bromo, um grupo alquinila ou similares, na posição supradescrita da fórmula acima. Como exemplos preferíveis específicos deles, podem ser mencionados os grupos 6-cloro-2-naftila, 6-flúor-2naftila, 6-bromo-2-naftila, 6-etinil-2-naftila, 7-cloro-2naftila, 7-flúor-2-naftila, 7-bromo-2-naftila, e 7-etinil-2naftila.
No seguinte grupo:
de 08/10/2018, pág. 40/857
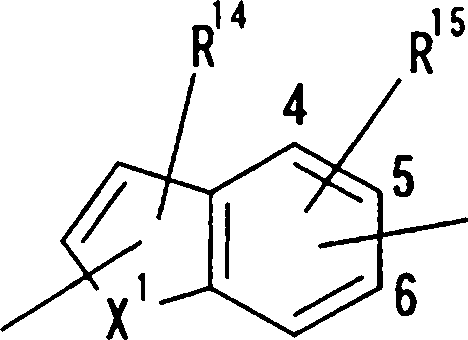
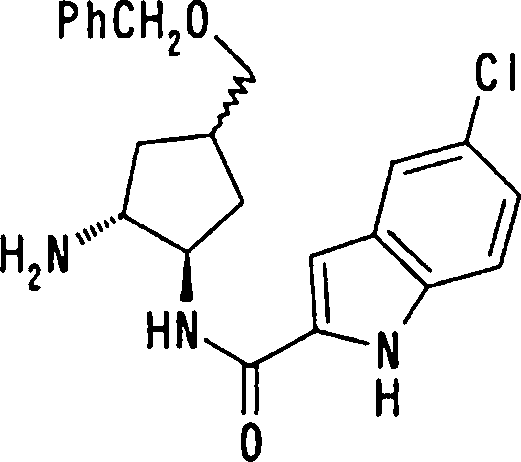
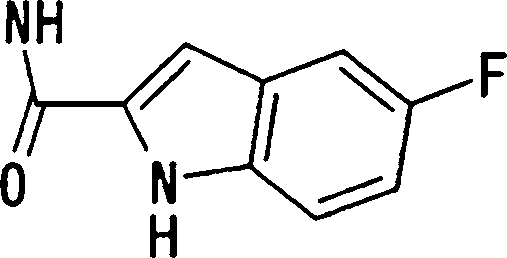
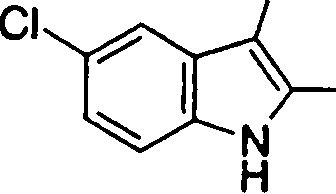
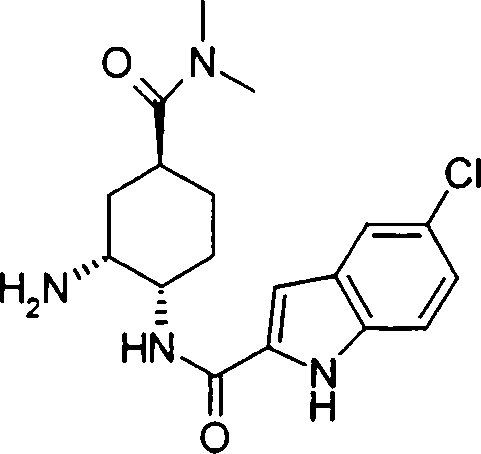
onde X1, R14, R15 e R16 têm os mesmos significados definidos acima, e os números 4 a 7 indicam posições, X1 é de preferência NH, NOH, N, O ou S, sendo NH, O ou S particularmente preferidos. R14 é, de preferência, um átomo de hidrogênio, um átomo de halogênio, um grupo acila, um grupo N-alquil-carbamoíla, um grupo N,N-dialquil-carbamoíla ou um grupo alquila, e R15 e R16 são, cada um independentemente do outro, de preferência, um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo haloalquila. Prefere-se que um entre R15 e R16 seja um átomo de hidrogênio ou halogênio, e o outro seja um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo haloalquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. A posição substituída pelo átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência, uma posição 4, 5 ou 6 na fórmula acima, embora ela não deva ser particularmente limitada. Como de 08/10/2018, pág. 41/857 exemplos preferíveis do grupo representado pela fórmula acima, podem ser mencionados os grupos 5-cloro-indolila, 5flúor-indolila, 5-bromo-indolila, 5-etinil-indolila, 5metil-indolila, 5-cloro-4-flúor-indolila, 5-cloro-3-flúorindolila, 5-flúor-3-cloro-indolila, 5-etinil-3-flúorindolila, 5-cloro-3-(N, N-dimetil-carbamoil)-indolila, 5flúor-3-(N,N-dimetil-carbamoil)-indolila, 5-cloro-3-formilindolila, 5-flúor-3-formil-indolila, 6-cloro-indolila, 6flúor-indolila, 6-bromo-indolila, 6-etinil-indolila, 6metil-indolila, 5-cloro-benzotienila, 5-flúor-benzotienila,
5-bromo-benzotienila, 5-etinil-benzotienila, 5-metilbenzotienila, 5-cloro-4-flúor-benzotienila, 6-clorobenzotienila, 6-flúor-benzotienila, 6-bromo-benzotienila, 6etinil-benzotienila, 6-metil-benzotienila, 5-clorobenzofurila, 5-flúor-benzofurila, 5-bromo-benzofurila, 5etinil-benzofurila, 5-metil-benzofurila, 5-cloro-4-flúorbenzofurila, 6-cloro-benzofurila, 6-flúor-benzofurila, 6bromo-benzofurila, 6-etinil-benzofurila, e 6-metilbenzofurila. A posição do grupo substituinte supradescrito ligado a T1 não é particularmente limitada, porém é, de preferência, uma posição 2 ou 3 na fórmula (d) . Especificamente, os mais preferidos são 5-cloro-indol-2-ila, 5-flúor-indol-2-ila, 5-bromo-indol-2-ila, 5-etinil-indol-2ila, 5-metil-indol-2-ila, 5-cloro-4-flúor-indol-2-ila, 5cloro-3-flúor-indol-2-ila, 3-bromo-5-cloro-indol-2-ila, 3cloro-5-flúor-indol-2-ila, 3-bromo-5-flúor-indol-2-ila, 5bromo-3-cloro-indol-2-ila, 5-bromo-3-flúor-indol-2-ila, 5cloro-3-formil-indol-2-ila, 5-flúor-3-formil-indol-2-ila, 5de 08/10/2018, pág. 42/857 bromo-3-formil-indol-2-ila, 5-flúor-3-formil-indol-2-ila, 5bromo-3-formil-indol-2-ila, 5-etinil-3-formil-indol-2-ila,
5-cloro-3-(N,N-dimetil-carbamoil)-indol-2-ila, 5-flúor-3(N,N-dimetil-carbamoil)-indol-2-ila, 5-bromo-3-(N,N-dimetil5 carbamoil)-indol-2-ila, 5-etinil-3-(N,N-dimetil-carbamoil)indol-2-ila, 6-cloro-indol-2-ila, 6-flúor-indol-2-ila, 6bromo-indol-2-ila, 6-etinil-indol-2-ila, 6-metil-indol-2ila, 5-cloro-indol-3-ila, 5-flúor-indol-3-ila, 5-bromoindol-3-ila, 5-etinil-indol-3-ila, 5-metil-indol-3-ila, 510 cloro-4-flúor-indol-3-ila, 6-cloro-indol-3-ila, 6-flúorindol-3-ila, 6-bromo-indol-3-ila, 6-etinil-indol-3-ila, 6metil-indol-3-ila, 5-cloro-benzotiofen-2-ila, 5-flúorbenzotiofen-2-ila, 5-bromo-benzotiofen-2-ila, 5-etinilbenzotiofen-2-ila, 5-metil-benzotiofen-2-ila, 5-cloro-415 flúor-benzotiofen-2-ila, 6-cloro-benzotiofen-2-ila, 6-flúor20 benzotiofen-2-ila, benzotiofen-2-ila, benzotiofen-3-ila, benzotiofen-3-ila, benzotiofen-3-ila,
5-bromo5-metil6-bromo-benzotiofen-2-ila, 6-etinil 6-metil-benzotiofen-2-ila, 5-cloro
5-flúor-benzotiofen-3-ila,
5-etinil-benzotiofen-3-ila,
5-cloro-4-flúor-benzotiofen-3-ila, 6 cloro-benzotiofen-3-ila, 6-flúor-benzotiofen-3-ila, 6-bromo benzotiofen-3-ila, 6-etinil-benzotiofen-3-ila, 6-metil benzotiofen-3-ila, 5-cloro-benzofuran-2-ila, 5-flúor
5-bromo-benzofuran-2-ila, benzofuran-2-ila,
5-etinil25 benzofuran-2-ila, 5-metil-benzofuran-2-ila, 5-cloro-4-flúorbenzofuran-2-ila, benzofuran-2-ila, benzofuran-2-ila,
6-cloro-benzofuran-2-ila, 6-flúor6-bromo-benzofuran-2-ila, 6-etinil6-metil-benzofuran-2-ila, 5-cloroPetição 870180138821, de 08/10/2018, pág. 43/857 benzofuran-3-ila, benzofuran-3-ila,
5-flúor-benzofuran-3-ila, 5-bromo5-etinil-benzofuran-3-ila, 5-meti1benzofuran-3-ila, 5-cloro-4-flúor-benzofuran-3-ila, 6-clorobenzofuran-3-ila, benzofuran-3-ila, benzofuran-2-ila, benzofuran-2-ila,
6-flúor-benzofuran-3-ila, 6-bromo6-etinil-benzofuran-3-ila, e 6-metilbenzofuran-3-ila, sendo particularmente preferidos os grupos
5- cloro-indol-2-ila, 5-flúor-indol-2-ila, 5-bromo-indol-2ila, 5-etinil-indol-2-ila, 5-metil-indol-2-ila, 5-cloro-4flúor-indol-2-ila, 6-cloro-indol-2-ila, 6-flúor-indol-2-ila,
6- bromo-indol-2-ila, 6-etinil-indol-2-ila, 6-metil-indol-2ila, 5-cloro-3-flúor-indol-2-ila, 3-bromo-5-cloro-indol-2ila, 3-cloro-5-flúor-indol-2-ila, 3-bromo-5-flúor-indol-2ila, 5-bromo-3-cloro-indol-2-ila, 5-bromo-3-flúor-indol-2ila, 5-cloro-3-formil-indol-2-ila, 5-flúor-3-formil-indol-2ila, 5-bromo-3-formil-indol-2-ila, 5-flúor-3-formil-indol-2ila, 5-bromo-3-formil-indol-2-ila, 5-etinil-3-formil-indol2-ila, 5-cloro-3-(N,N-dimetil-carbamoil)indol-2-ila, 5flúor-3-(N,N-dimetil-carbamoil)indol-2-ila, 5-bromo-3-(N,Ndimetil-carbamoil)indol-2-ila, 5-etinil-3-(N,N-dimetilcarbamoil) indol-2-ila, 5-cloro-benzotiofen-2-ila, 5-flúorbenzotiofen-2-ila, 5-bromo-benzotiofen-2-ila, 5-etinilbenzotiofen-2-ila, 5-metil-benzotiofen-2-ila, 5-cloro-4flúor-benzotiofen-2-ila, 6-cloro-benzotiofen-2-ila, 6-flúorbenzotiofen-2-ila, 6-bromo-benzotiofen-2-ila, 6-etinilbenzotiofen-2-ila, 6-metil-benzotiofen-2-ila, 5-cloro5-flúor-benzofuran-2-ila, 5-bromo5-etinil-benzofuran-2-ila, 5-meti1benzofuran-2-ila, 5-cloro-4-flúor-benzofuran-2-ila, 6-clorode 08/10/2018, pág. 44/857 benzofuran-2-ila, 6-flúor-benzofuran-2-ila benzofuran-2-ila, 6-etinil-benzofuran-2-ila, benzofuran-2-ila.
No seguinte grupo:

6-bromo6-metilonde X2, X3, X4, R17 e R18 têm os mesmos significados que definidos acima, e os números 4 a 7 indicam posições, X2 é de preferência NH, O ou S, qualquer um entre X3 e X4 é de preferência CH ou C, e particularmente, de preferência, C. R17 e R18 são, cada um independentemente do outro, um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo haloalquila. Prefere-se que um entre R17 e R18 seja um átomo de hidrogênio e o outro seja um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo halo-alquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. A posição substituída pelo átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência, uma posição 5 ou 6 na fórmula de 08/10/2018, pág. 45/857 acima, embora ela não deva ser particularmente limitada. Como exemplos preferíveis específicos do grupo representado pela fórmula acima, podem ser mencionados os grupos 5-cloroindazolila, 5-flúor-indazolila, 5-bromo-indazolila, 5etinil-indazol-ila, 6-cloro-indazolila, 6-flúor-indazolila,
|
6-bromo-indazolila, |
6-etinil-indazol-ila, |
5-cloro- |
|
benzimidazolila, |
5-flúor-benzimidazolila, |
5-bromo- |
|
benzimidazolila, |
5-etinil-benzimidazolila, |
6-cloro- |
|
benzimidazolila, |
6-flúor-benzimidazolila, |
6-bromo- |
|
benzimidazolila, |
6-etinil-benzimidazolila, |
5-cloro- |
|
benzotiazolila, |
5-flúor-benzotiazolila, |
5-bromo- |
|
benzotiazolila, |
5-etinil-benzotiazolila, |
6-cloro- |
|
benzotiazolila, |
6-flúor-benzotiazolila, |
6-bromo- |
|
benzotiazolila, |
6-etinil-benzotiazolila, |
5-cloro- |
benzoxazolila, 5-flúor-benzoxazolila, 5-bromo-benzoxazolila,
|
5-etinil-benzoxazolila, 6-cloro-benzoxazolila, |
6-flúor- |
|
benzoxazolila, |
6-bromo-benzoxazolila, |
6-etinil- |
|
benzoxazolila, 5 |
-cloro-benzoisotiazolila, |
5-flúor- |
|
benzoisotiazolila, |
5-bromo-benzoisotiazolila, |
5-etinil- |
|
benzoisotiazolila, |
6-cloro-benzoisotiazolila, |
6-flúor- |
|
benzoisotiazolila, |
6-bromo-benzoisotiazolila, |
6-etinil- |
|
benzoisotiazolila, |
5-cloro-benzoisoxazolila, |
5-flúor- |
|
benzoisoxazolila, |
5-bromo-benzoisoxazolila, |
5-etinil- |
|
benzoisoxazolila, |
6-cloro-benzoisoxazolila, |
6-flúor- |
|
benzoisoxazolila, |
6-bromo-benzoisoxazolila, |
6-etinil- |
|
benzoisoxazolila. |
A posição do grupo substituinte |
|
supradescrito ligado |
a T1 não é particularmente |
limitada. |
|
Os grupos mais preferidos são 5-cloro-indazol- |
3-ila, 5- |
de 08/10/2018, pág. 46/857 flúor-indazol-3-ila, 5-bromo-indazol-3-ila, 5-etinilindazol-3-ila, 6-cloro-indazol-3-ila, 6-flúor-indazol-3-ila,
6-bromo-indazol-3-ila, 6-etinil-indazol-3-ila, 5-clorobenzimidazol-2-ila, benzimidazol-2-ila, benzimidazol-2-ila, benzimidazol-2-ila, benzotiazol-2-ila, benzotiazol-2-ila, benzotiazol-2-ila, benzotiazol-2-ila, benzoxazol-2-ila, benzoxazol-2-ila, benzoxazol-2-ila, benzoxazol-2-ila,
5- flúor-benzimidazol-2-ila, 5-bromo5- etinil-benzimidazol-2-ila, 6-cloro6- flúor-benzimidazol-2-ila, 6-bromo6- etinil-benzimidazol-2-ila, 5-cloro5- flúor-benzotiazol-2-ila, 5-bromo5- etinil-benzotiazol-2-ila, 6-cloro6- flúor-benzotiazol-2-ila, 6-bromo6- etinil-benzotiazol-2-ila, 5-cloro5- flúor-benzoxazol-2-ila, 5-bromo5- etinil-benzoxazol-2-ila, 6-cloro6- flúor-benzoxazol-2-ila, 6-bromo6- etinil-benzoxazol-2-ila, 5-clorobenzimidazol-2-ila, benzimidazol-2-ila, benzoisotiazol-3-ila, 5-flúor-benzoisotiazol-3-ila, 5-bromobenzoisotiazol-3-ila, 5-etinil-benzoisotiazol-3-ila, 6cloro-benzoisotiazol-3-ila, 6-flúor-benzoisotiazol-3-ila, 6bromo-benzoisotiazol-3-ila, 6-etinil-benzoisotiazol-3-ila, 5-cloro-benzoisoxazol-3-ila, 5-flúor-benzoisoxazol-3-ila, 5bromo-benzoisoxazol-3-ila, 5-etinil-benzoisoxazol-3-ila, 6cloro-benzoisoxazol-3-ila, 6-flúor-benzoisoxazol-3-ila, 6bromo-benzoisoxazol-3-ila, 6-etinil-benzoisoxazol-3-ila, sendo particularmente preferidos os grupos 5-clorobenzimidazol-2-ila, 5-flúor-benzimidazol-2-ila, 5-bromobenzimidazol-2-ila, 5-etinil-benzimidazol-2-ila, 6-cloro6-flúor-benzimidazol-2-ila, 6-bromo6-etinil-benzimidazol-2-ila, 5-clorode 08/10/2018, pág. 47/857
|
benzotiazol-2-ila, |
5-flúor-benzotiazol-2-ila, |
5-bromo- |
|
benzotiazol-2-ila, |
5-etinil-benzotiazol-2-ila, |
6-cloro- |
|
benzotiazol-2-iia, |
6-flúor-benzotiazol-2-iia, |
6-bromo- |
|
benzotiazol-2-iia, |
6-etinil-benzotiazol-2-iia, |
5-cloro- |
|
benzoxazol-2-ila, |
5-flúor-benzoxazol-2-ila, |
5-bromo- |
|
benzoxazol-2-ila, |
5-etinil-benzoxazol-2-ila, |
6-cloro- |
|
benzoxazol-2-ila, |
6-flúor-benzoxazol-2-ila, |
6-bromo- |
|
benzoxazol-2-ila, |
6-etinil-benzoxazol-2-ila. Dentre estes, |
5-cloro-benzimidazol-2-ila, 5-flúor-benzimidazol-2-ila, 5bromo-benzimidazol-2-ila, 5-etinil-benzimidazol-2-ila, são mais ainda preferidos.
No seguinte grupo:
|
onde N indica |
que |
1 ou |
2 átomos de |
carbono |
do |
anel |
|
substituído com |
R19 |
foram |
substituídos |
com um |
átomo |
de |
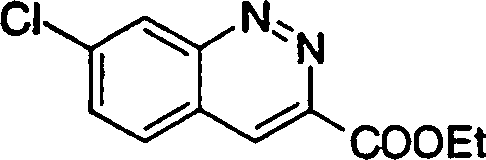
nitrogênio, R19, R20 e R21 têm os mesmos significados definidos acima, e os números 5 a 8 indicam posições, R19, R20 e R21 são, cada um independentemente do outro, de preferência um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo halo-alquila. R19 é particularmente, de preferência, um átomo de hidrogênio. Prefere-se que um entre de 08/10/2018, pág. 48/857 r2o e p2i seja um átomo de hidrogênio e o outro seja um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo haloalquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. A posição substituída com um átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência uma posição 6 ou 7 na fórmula acima, embora ela não seja particularmente limitada. Como seus exemplos preferidos específicos, podem ser mencionados os grupos quinolinila, isoquinolinila e cinolinila. Os mais preferidos são 6-cloro-quinolinila, 6-flúor-quinolinila, 6bromo-quinolinila, 6-etinil-quinolinila, 6-cloroisoquinolinila, 6-flúor-isoquinolinila, 6-bromoisoquinolinila, 6-etinil-isoquinolinila, 7-cloro-cinolinila,
7-flúor-cinolinila, 7-bromo-cinolinila, 7-etinil-cinolinila, sendo particularmente preferidos os grupos 6-cloro-quinolin2-ila, 6-flúor-quinolin-2-ila, 6-bromo-quinolin-2-ila, 6etinil-quinolin-2-ila, 6-cloro-quinolin-3-ila, 6-flúorquinolin-3-ila, 6-bromo-quinolin-3-ila, 6-etinil-quinolin-3ila, 7-cloro-quinolin-2-ila, 7-flúor-quinolin-2-ila, 7bromo-quinolin-2-ila, 7-etinil-quinolin-2-ila, 7-cloroquinolin-3-ila, 7-flúor-quinolin-3-ila, 7-bromo-quinolin-3ila, 7-etinil-quinolin-3-ila, 6-cloro-isoquinolin-3-ila, 6de 08/10/2018, pág. 49/857 flúor-isoquinolin-3-ila, etinil-isoquinolin-3-ila, flúor-isoquinolin-3-ila, etinil-isoquinolin-3-ila, isoquinolin-3-ila, isoquinolin-3-ila,
6- bromo-isoquinolin-3-ila, 67- cloro-isoquinolin-3-ila, 77-bromo-isoquinolin-3-ila, 77-cloro-cinolin-3-ila, 7-flúorcinolin-3-ila, 7-bromo-cinolin-3-ila, 7-etinil-cinolin-3ila. Dentre estes, 6-cloro-quinolin-2-ila, 6-flúorquinolin-2-ila, 6-bromo-quinolin-2-ila, 6-etinil-quinolin-2ila, 7-cloro-quinolin-3-ila, 7-flúor-quinolin-3-ila, 7bromo-quinolin-3-ila, 7-etinil-quinolin-3-ila, 7-cloro7-flúor-isoquinolin-3-ila, 7-bromo7-etinil-isoquinolin-3-ila, 7-clorocinolin-3-ila, 7-flúor-cinolin-3-ila, 7-bromo-cinolin-3-ila e 7-etinil-cinolin-3-ila são ainda mais preferidos.
No seguinte grupo:

.23 (g) onde os números 5 a 8 indicam posições, X5 representa CH2, CH, N ou NH, Z1 representa Ν, NH ou O, Z2 representa CH2, CH, C ou Ν, Z3 representa CH2, CH, S, SO2 ou C=O, X5-Z2 indica que X5 e Z2 estão unidos entre si por uma ligação simples ou ligação dupla, R22, R23 e R24 têm os mesmos significados como definidos acima, R22 e R23 são, cada um independentemente do outro, de preferência, um átomo de hidrogênio, um grupo ciano, um átomo de halogênio, um grupo alquila, grupo de 08/10/2018, pág. 50/857 acima, podem ser diidroquinolinila, diidroquinazolin-2-ila, alquenila, grupo alquinila, ou um grupo halo-alquila. Prefere-se que um entre R22 e R23 seja um átomo de hidrogênio e o outro seja um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo halo-alquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se um grupo etinila. A posição substituída com um átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência uma posição 6 ou 7 na fórmula acima, embora ela não seja particularmente limitada. R24 é, de preferência, um átomo de hidrogênio ou um grupo alquila, e um grupo metila é preferido como grupo alquila. Como R24 prefere-se particularmente um átomo de hidrogênio. Como exemplos preferidos específicos do grupo representado pela fórmula mencionados os grupos 4-oxotetraidroquinolinila, 4-oxo4-oxo-tetraidrocinolinila, 4-oxobenzopiranila, 4-oxo-benzotiadiazinila, 1,l-dioxi-4-oxobenzotiadiazinila e benzoxadiazinila. Como seus grupos preferidos específicos, podem ser mencionados os grupos 6cloro-4-oxo-diidroquinolinila, 6-flúor-4-oxodiidroquinolinila, 6-bromo-4-oxo-diidroquinolinila, 6etinil-4-oxo-diidroquinolinila, 7-cloro-4-oxodiidroquinolinila, 7-flúor-4-oxo-diidroquinolinila, 7-bromode 08/10/2018, pág. 51/857
4-oxo-diidroquinolinila, 7-etinil-4-oxo-diidroquinolinila,
6-cloro-4-oxo-l,4-diidroquinazolinila, 6-flúor-4-oxo-l,4diidroquinazolinila, 6-bromo-4-oxo-l,4-diidroquinazolinila,
6- etinil-4-oxo-l,4-diidroquinazolinila, 7-cloro-4-oxo-l,45 diidroquinazolinila, 7-flúor-4-oxo-l,4-diidroquinazolinila,
7- bromo-4-oxo-l,4-diidroquinazolinila, 7-etinil-4-oxo-l,4diidroquinazolinila, 6-cloro-l,2,3,4-tetraidroquinolinila,
6- flúor-l,2,3,4-tetraidroquinolinila, 6-bromo-l,2,3,4tetraidroquinolinila, 6-etinil-l,2,3,4-tetraidroquinolinila,
7-cloro-l,2,3,4-tetraidroquinolinila, 7-flúor-l,2,3,4tetraidroquinolinila, 7-bromo-l,2,3,4-tetraidroquinolinila,
7- etinil-l,2,3,4-tetraidroquinolinila, 6-cloro-l,2,3,4tetraidro-4-oxocinolinila, 6-flúor-l,2,3,4-tetraidro-4oxocinolinila, 6-bromo-l,2,3,4-tetraidro-4-oxocinolinila, 615 etinil-1,2,3,4-tetraidro-4-oxocinolinila, 7-cloro-l,2,3,4tetraidro-4-oxocinolinila, 7-flúor-l,2,3,4-tetraidro-4oxocinolinila, 7-bromo-l,2,3,4-tetraidro-4-oxocinolinila, 7etinil-1,2,3,4-tetraidro-4-oxocinolinila, 6-cloro-4H-4oxobenzopiranila, 6-flúor-4H-4-oxobenzopiranila, 6-bromo-4H20 4-oxobenzopiranila, 6-etinil-4H-4-oxobenzopiranila, 7-cloro4H-4-oxobenzopiranila, 7-flúor-4H-4-oxobenzopiranila, 7bromo-4H-4-oxobenzopiranila, 7-etinil-4H-4-oxobenzopiranila, 6-cloro-l,l-dioxi-2H-l,2,4-benzotiadiazinila, 6-flúor-l,1dioxi-2H-l,2,4-benzotiadiazinila, 6-bromo-l,l-dioxi-2H25 1,2,4-benzotiadiazinila, 6-etinil-l,l-dioxi-2H-l,2,4benzotiadiazinila, 7-cloro-l,l-dioxi-2H-l,2,4benzotiadiazinila, benzotiadiazinila,
7-flúor-l,l-dioxi-2H-l,2,47-bromo-l,l-dioxi-2H-l, 2,4Petição 870180138821, de 08/10/2018, pág. 52/857 benzotiadiazinila, 7-etinil-l,l-dioxi-2H-l,2,4benzotiadiazinila, 6-cloro-2H-l,2,4-benzoxadiazinila, 6flúor-2H-l,2,4-benzoxadiazinila, 6-bromo-2H-l,2,4benzoxadiazinila, 6-etinil-2H-l,2,4-benzoxadiazinila, 7cloro-2H-l,2,4-benzoxadiazinila, 7-flúor-2H-l,2,4benzoxadiazinila, 7-bromo-2H-l,2,4-benzoxadiazinila, e 7etinil-2H-l,2,4-benzoxadiazinila; sendo preferidos os grupos 6-cloro-4-oxo-l,4-diidroquinolin-2-ila, 6-flúor-4-oxo-l,4diidroquinolin-2-ila, 6-bromo-4-oxo-l,4-diidroquinolin-2ila, 6-etinil-4-oxo-l,4-diidroquinolin-2-ila, 7-cloro-4-oxo1.4- diidroquinolin-2-ila, 7-flúor-4-oxo-l,4-diidroquinolin2-ila, 7-bromo-4-oxo-l,4-diidroquinolin-2-ila, 7-etinil-4oxo-1,4-diidroquinolin-2-ila, 6-cloro-4-oxo-l,4diidroquinazolin-2-ila, 6-flúor-4-oxo-l,4-diidroquinazolin2-ila, 6-bromo-4-oxo-l,4-diidroquinazolin-2-ila, 6-etinil-4oxo-1,4-diidroquinazolin-2-ila, 7-cloro-4-oxo-l,4diidroquinazolin-2-ila, 7-flúor-4-oxo-l,4-diidroquinazolin2-ila, 7-bromo-4-oxo-l,4-diidroquinazolin-2-ila, 7-etinil-4oxo-1,4-diidroquinazolin-2-ila, 6-cloro-l,2,3,4tetraidroquinolin-2-ila, 6-flúor-l,2,3,4-tetraidroquinolin2-ila, 6-bromo-l,2,3,4-tetraidroquinolin-2-ila, 6-etinil1.2.3.4- tetraidroquinolin-2-ila, 6-cloro-l,2,3,4-tetraidro4-oxocinolin-2-ila, 6-flúor-l,2,3,4-tetraidro-4-oxocinolin2-ila, 6-bromo-l,2,3,4-tetraidro-4-oxocinolin-2-ila, 6etinil-1,2,3,4-tetraidro-4-oxocinolin-2-ila, 7-cloro1.2.3.4- tetraidro-4-oxocinolin-2-ila, 7-flúor-l,2,3,4tetraidro-4-oxocinolin-2-ila, 7-bromo-l,2,3,4-tetraidro-4oxocinolin-2-ila, 7-etinil-l,2,3,4-tetraidro-4-oxocinolin-2de 08/10/2018, pág. 53/857 ila, 6-cloro-4H-4-oxobenzopiran-2-ila, 6-flúor-4H-4oxobenzopiran-2-ila, 6-bromo-4H-4-oxobenzopiran-2-ila, 6etinil-4H-4-oxobenzopiran-2-ila, 7-cloro-4H-4-oxobenzopiran2-ila, 7-flúor-4H-4-oxobenzopiran-2-ila, 7-bromo-4H-4oxobenzopiran-2-ila, 7-etinil-4H-4-oxobenzopiran-2-ila, 6cloro-1,l-dioxi-2H-l,2,4-benzotiadiazin-3-ila, 6-flúor-l,1dioxi-2H-l,2,4-benzotiadiazin-3-ila, 6-bromo-l,l-dioxi-2H1,2,4-benzotiadiazin-3-ila, 6-etinil-l,l-dioxi-2H-l, 2,4benzotiadiazin-3-ila, benzotiadiazin-3-ila, benzotiadiazin-3-ila, benzotiadiazin-3-ila,
7-cloro-l,l-dioxi-2H-l,2,47-flúor-l,l-dioxi-2H-l,2,47-bromo-l,l-dioxi-2H-l, 2,47-etinil-l,l-dioxi-2H-l,2,4benzotiadiazin-3-ila, 6-cloro-2H-l,2,4-benzoxadiazin-3-ila,
6- flúor-2H-l,2,4-benzoxadiazin-3-ila, 6-bromo-2H-l,2,4benzoxadiazin-3-ila, 6-etinil-2H-l,2,4-benzoxadiazin-3-ila,
7- cloro-2H-l,2,4-benzoxadiazin-3-ila, 7-flúor-2H-l,2,4benzoxadiazin-3-ila, 7-bromo-2H-l,2,4-benzoxadiazin-3-ila, e
7-etinil-2H-l,2,4-benzoxadiazin-3-ila. Dentre estes, os grupos 6-cloro-4-oxo-l,4-diidroquinolin-2-ila, 6-flúor-4oxo-1,4-diidroquinolin-2-ila, 6-bromo-4-oxo-l,4diidroquinolin-2-ila, 6-etinil-4-oxo-l,4-diidroquinolin-2ila, 6-cloro-4-oxo-l,4-diidroquinazolin-2-ila, 6-flúor-4oxo-1,4-diidroquinazolin-2-ila, 6-bromo-4-oxo-l,4diidroquinazolin-2-ila e 6-etinil-4-oxo-l,4diidroquinazolin-2-ila são particularmente preferidos.
No seguinte grupo:
de 08/10/2018, pág. 54/857

onde X6 representa O ou S, R25 e R26 têm os mesmos significados que aqueles definidos acima, e os números 5 a 8 indicam posições, X6 é de preferência O, e R25 e R26 são, cada um independentemente do outro, de preferência, um átomo de hidrogênio, um grupo ciano, um átomo de halogênio, um grupo alquila, grupo alquenila, grupo alquinila, ou um grupo halo-alquila. Prefere-se que um entre R25 e R26 seja um átomo de hidrogênio e o outro seja um átomo de hidrogênio, um grupo ciano, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila ou grupo halo-alquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se um grupo etinila. A posição substituída com um átomo de halogênio, grupo alquila ou grupo alquinila é, de preferência uma posição 6 ou 7 na fórmula acima, embora ela não seja particularmente limitada. Como seus exemplos específicos, podem ser mencionados os grupos 6-cloro-2H-cromen-3-ila, 6-flúor-2H-cromen-3-ila, 6bromo-2H-cromen-3-ila, 6-etinil-2H-cromen-3-ila, 7-cloro-2Hcromen-3-ila, 7-flúor-2H-cromen-3-ila, 7-bromo-2H-cromen-3de 08/10/2018, pág. 55/857 ila e 7-etinil-2H-cromen-3-ila, sendo particularmente preferidos os grupos 7-cloro-2H-cromen-3-ila, 7-flúor-2Hcromen-3-ila, 7-bromo-2H-cromen-3-ila e 7-etinil-2H-cromen3-ila.
No seguinte grupo:

onde R27 e R28 têm os mesmos significados que definidos acima, e os números 1 a 6 indicam posições, prefere-se que um entre R27 e R28 seja um átomo de hidrogênio ou um átomo de halogênio, e o outro seja um átomo de hidrogênio, um grupo ciano, um grupo nitro, grupo amino, átomo de halogênio, grupo alquila, grupo alquenila, grupo alquinila, grupo haloalquila ou um grupo N,N-dialquil-carbamoila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. Como exemplos específicos do grupo representado pela fórmula acima, podem ser mencionados os grupos fenila, cloro-fenila, flúorfenila, bromo-fenila, etinil-fenila e cloro-flúor-fenila. A posição substituída pelo átomo de halogênio, grupo alquila ou grupo alquinila nesses grupos é, de preferência, de 08/10/2018, pág. 56/857 particularmente uma posição 3 ou 4 na fórmula acima no caso de um substituinte, ou uma combinação de uma posição 4 e uma posição 2 ou 3 na fórmula acima no caso de dois substituintes, embora ela não deva ser particularmente limitada. Como exemplos preferíveis específicos do grupo representado pela fórmula acima, podem ser mencionados os grupos fenila, 4-cloro-fenila, 4-flúor-fenila, 4-bromofenila, 4-etinil-fenila, 3-cloro-fenila, 3-flúor-fenila, 3bromo-fenila, 3-etinil-fenila, 3-cloro-4-flúor-fenila, 4cloro-3-flúor-fenila, 4-cloro-2-flúor-fenila, 2-cloro-4flúor-fenila, 4-bromo-2-flúor-fenila, 2-bromo-4-flúorfenila, 2,4-dicloro-fenila, 2,4-diflúor-fenila, 2,4-dibromofenila, 4-cloro-3-metil-fenila, 4-flúor-3-metil-fenila, 4bromo-3-metil-fenila, 4-cloro-2-metil-fenila, 4-flúor-2metil-fenila, 4-bromo-2-metil-fenila, 3,4-dicloro-fenila,
3,4-diflúor-fenila e 3,4-dibromo-fenila.
No seguinte grupo:

onde Ε1, E2, R29 e R30 têm os mesmos significados que definidos acima, e os números 1 a 6 indicam posições, prefere-se que um entre R29 e R30 seja um átomo de hidrogênio ou um átomo de halogênio, e o outro seja um átomo de hidrogênio, um grupo ciano, um átomo de halogênio, um grupo de 08/10/2018, pág. 57/857 alquila, grupo alquenila, grupo alquinila, ou um grupo haloalquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. Como exemplos específicos do grupo representado pela fórmula acima, podem ser mencionados os grupos piridila, pirimidila e piridazinila. A posição substituída com o átomo de halogênio, grupo alquila ou grupo alquinila nesses grupos é, de preferência, particularmente, uma posição 4 ou 5 na fórmula acima, no caso em que sua ligação ao grupo T1 seja na posição 2 da fórmula acima, embora ela não deva ser particularmente limitada. Como seus exemplos preferidos específicos, podem ser mencionados os grupos 2-piridila, 3-piridila, 4piridila, 4-cloro-2-piridila, 4-flúor-2-piridila, 4-bromo-2piridila, 4-etinil-2-piridila, 4-cloro-3-piridila, 4-flúor3- piridila, 4-bromo-3-piridila, 4-etinil-3-piridila, 5cloro-2-piridila, 5-flúor-2-piridila, 5-bromo-2-piridila, 5etinil-2-piridila, 4-cloro-5-flúor-2-piridila, 5-cloro-4flúor-2-piridila, 5-cloro-3-piridila, 5-flúor-3-piridila, 5bromo-3-piridila, 5-etinil-3-piridila, 5-cloro-2-pirimidila,
5-flúor-2-pirimidila, 5-bromo-2-pirimidila, 5-etinil-2pirimidila, 4-cloro-3-piridazinila, 4-flúor-3-piridazinila,
4- bromo-3-piridazinila, 4-etinil-3-piridazinila, 6-cloro-3piridazinila, 6-flúor-3-piridazinila, 6-bromo-3-piridazinila de 08/10/2018, pág. 58/857 e 6-etinil-3-piridazinila. Os grupos particularmente preferidos são 2-piridila, 3-piridila, 4-piridila, 4-cloro2- piridila, 4-flúor-2-piridila, 4-bromo-2-piridila, 4etinil-2-piridila, 4-cloro-3-piridila, 4-flúor-3-piridila,
4- bromo-3-piridila, 4-etinil-3-piridila, 5-cloro-2-piridila,
5- flúor-2-piridila, 5-bromo-2-piridila, 5-etinil-2-piridila,
4-cloro-5-flúor-2-piridila, 5-cloro-4-flúor-2-piridila, 5cloro-3-piridila, 5-flúor-3-piridila, 5-bromo-3-piridila, 5etinil-3-piridila, 6-cloro-3-piridazinila, 6-flúor-36-bromo-3-piridazinila, 6-etinil-34-cloro-3-piridazinila, 4-flúor-34-bromo-3-piridazinila e 4-etinil-3Dentre estes, 2-piridila, 3-piridila, 4piridila, 5-cloro-2-piridila, 5-flúor-2-piridila, 5-bromo-2piridila, 5-etinil-2-piridila, 5-cloro-4-flúor-2-piridila, 4-cloro-5-flúor-2-piridila, 4-cloro-3-piridazinila, 4-flúor3- piridazinila, 4-bromo-3-piridazinila e 4-etinil-3piridazinila são ainda mais preferidos.
No seguinte grupo:
piridazinila, piridazinila, piridazinila, piridazinila.

onde Y1, Y2, R31 e R32 têm os mesmos significados que definidos acima, e os números 1 a 5 indicam posições, prefere-se que um entre R31 e R32 seja um átomo de hidrogênio de 08/10/2018, pág. 59/857 ou um átomo de halogênio, e o outro seja um átomo de hidrogênio, um grupo ciano, um átomo de halogênio, um grupo alquila, grupo alquenila, grupo alquinila, ou um grupo haloalquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. Como exemplos específicos do grupo representado pela fórmula acima, podem ser mencionados os grupos tienila, pirrolila, furila, oxazolila e tiazolila. A posição substituída com o átomo de halogênio, grupo alquila ou grupo alquinila nesses grupos é, de preferência, particularmente, uma posição 4 ou 5 na fórmula acima, embora ela não seja particularmente limitada. Como seus exemplos preferidos específicos, podem ser mencionados os grupos 4-cloro-2-tienila, 4-flúor-2-tienila,
4-bromo-2-tienila, 4-etinil-2-tienila, 4-cloro-2-pirrolila,
4- flúor-2-pirrolila, 4-bromo-2-pirrolila, 4-etinil-2pirrolila, 4-cloro-2-furila, 4-flúor-2-furila, 4-bromo-2furila, 4-etinil-2-furila, 5-cloro-2-tienila, 5-flúor-2tienila, 5-bromo-2-tienila, 5-etinil-2-tienila, 5-cloro-2tiazolila, 5-flúor-2-tiazolila, 5-bromo-2-tiazolila, 5etinil-2-tiazolila, 5-cloro-2-oxazolila, 5-flúor-2oxazolila, 5-bromo-2-oxazolila e 5-etinil-2-oxazolila. Os grupos particularmente preferidos são 5-cloro-2-tiazolila,
5- flúor-2-tiazolila, 5-bromo-2-tiazolila e 5-etinil-2de 08/10/2018, pág. 60/857 tiazolila.
No seguinte grupo:

onde os números 1 a 8 indicam posições, cada N indica que um dos 4 átomos de carbono nas posições 1 a 4 e qualquer um dos 4 átomos de carbono das posições 5 a 8 foi substituído com um átomo de nitrogênio, e R34 a R36 têm os mesmos significados que definidos acima, a posição de cada átomo de nitrogênio pode estar em qualquer relação posicionai, e R34 é, de preferência, um átomo de hidrogênio ou um átomo de halogênio. Prefere-se que um entre R35 e R36 seja um átomo de hidrogênio ou um átomo de halogênio, e o outro seja um átomo de hidrogênio, um grupo ciano, um átomo de halogênio, um grupo alquila, grupo alquenila, grupo alquinila, ou um grupo halo-alquila. Dentre outros, prefere-se particularmente que o outro grupo seja um átomo de hidrogênio, um átomo de halogênio, um grupo alquila ou um grupo alquinila. Neste caso, o átomo de halogênio é, de preferência, um átomo de flúor, cloro ou bromo. Como grupo alquila, prefere-se um grupo metila. Como grupo alquinila, prefere-se particularmente um grupo etinila. A posição substituída com o átomo de halogênio, grupo alquila ou grupo alquinila não deve ser particularmente limitada. Como exemplos preferidos dos grupos específicos representados de 08/10/2018, pág. 61/857 pela formula acima, podem ser mencionados os grupos 6-cloro 1,5-naftiridin-2-ila, 6-flúor-l,5-naftiridin-2-ila, 6-bromo 1,5-naftiridin-2-ila, 6-etinil-l,5-naftiridin-2-ila, 7 cloro-1,5-naftiridin-2-ila, 7 5 bromo-1,5-naftiridin-2-ila,
6-cloro-l,5-naftiridin-3-ila,
6- bromo-l,5-naftiridin-3-ila,
7- cloro-l,5-naftiridin-3-ila,
7-bromo-l,5-naftiridin-3-ila,
6-cloro-l,7-naftiridin-2-ila, 6-bromo-l,7-naftiridin-2-ila, 6-cloro-l,7-naftiridin-3-ila, 6-bromo-l,7-naftiridin-3-ila,
6- cloro-l,8-naftiridin-2-ila,
6-bromo-l,8-naftiridin-2-ila,
7- cloro-l,8-naftiridin-2-ila, 7-bromo-l,8-naftiridin-2-ila, 7-cloro-l,8-naftiridin-3-ila, 7-bromo-l,8-naftiridin-3-ila,
6-cloro-2,5-naftiridin-3-ila,
6- bromo-2,5-naftiridin-3-ila,
7- cloro-2,5-naftiridin-3-ila, 7-bromo-2,5-naftiridin-3-ila, 7-cloro-2,6-naftiridin-3-ila,
7-bromo-2,6-naftiridin-3-ila,
6-cloro-2,8-naftiridin-3-ila,
6- bromo-2,8-naftiridin-3-ila,
7- cloro-2,8-naftiridin-3-ila, fluor-1,5-naftiridin-2-ila, 77-etinil-l,5-naftiridin-2-ila,
6- flúor-l,5-naftiridin-3-ila,
6- etinil-l,5-naftiridin-3-ila,
7- flúor-l,5-naftiridin-3-ila,
7- etinil-l,5-naftiridin-3-ila, 6-flúor-l,7-naftiridin-2-ila,
6-etinil-l,7-naftiridin-2-ila, 6-flúor-l,7-naftiridin-3-ila,
6-etinil-l,7-naftiridin-3-ila,
6- flúor-l,8-naftiridin-2-ila,
6- etinil-l,8-naftiridin-2-ila,
7- flúor-l,8-naftiridin-2-ila,
7- etinil-l,8-naftiridin-2-ila, 7-flúor-l,8-naftiridin-3-ila,
7-etinil-l,8-naftiridin-3-ila,
6- flúor-2,5-naftiridin-3-ila,
6- etinil-2,5-naftiridin-3-ila,
7- flúor-2,5-naftiridin-3-ila,
7- etinil-2,5-naftiridin-3-ila, 7-flúor-2,6-naftiridin-3-ila,
7-etinil-2,6-naftiridin-3-ila,
6- flúor-2,8-naftiridin-3-ila, 6-etinil-2,8-naftiridin-3-ila,
7- flúor-2,8-naftiridin-3-ila,
Petição 870180138821, de 08/10/2018, pág. 62/857
7-bromo-2,8-naftiridin-3-ila e 7-etinil-2,8-naftiridin-3ila. Os seus exemplos particularmente preferidos incluem 7cloro-2,5-naftiridin-3-ila, 7-flúor-2,5-naftiridin-3-ila, 7bromo-2,5-naftiridin-3-ila, 7-etinil-2,5-naftiridin-3-ila.
Além dos 12 grupos (a) até (1) supramencionados, um grupo tienopirrolila, que pode ser substituído, é preferido. Este grupo pode ter 1 a 3 substituintes, e os exemplos dos substituintes incluem um grupo hidroxila, um grupo nitro, um grupo amino, um grupo ciano, átomos de halogênio, grupos alquila, grupos alquenila, grupos alquinila, grupos halo-alquila, grupos hidróxi-alquila, grupos alcóxi, grupos alcóxi-alquila, um grupo carboxila, grupos carbóxi-alquila, grupos acila, um grupo carbamoíla, grupos N-alquil-carbamoíla, grupos N,N-dialquil-carbamoíla, grupos alcóxi-carbonila, um grupo amidino e grupos alcóxicarbonil-alquila. Dentre estes, os preferidos são um grupo ciano, átomos de halogênio, grupos alquila, grupos alquenila, grupos alquinila e grupos halo-alquila. Como seus exemplos preferidos específicos, podem ser mencionados os grupos 2-cloro-tieno[2,3-b]-pirrol-5-ila, 2-flúortieno[2,3-b]-pirrol-5-ila, 2-bromo-tieno[2,3-b]-pirrol-5ila, e 2-etinil-tieno[2,3-b]-pirrol-5-ila.
Grupo Q1 1 significa um grupo insaturado, com 5 ou 6 um grupo heterocíclico membros, que pode ser bicíclico ou tricíclico
Na presente invenção, Q hidrocarboneto cíclico saturado ou membros, que pode ser substituído, saturado ou insaturado, com 5 a 7 substituído, um grupo hidrocarboneto de 08/10/2018, pág. 63/857 fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído.
Como exemplos do hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, podem ser mencionados os grupos ciclo-pentila, ciclo-pentenila, ciclo-hexila, ciclohexenila, e fenila. Os grupos preferidos são ciclo-pentila, ciclo-hexila e fenila, sendo particularmente preferido um grupo fenila.
O grupo heterocíclico saturado ou insaturado, tendo 5 a 7 membros, significa um grupo heterocíclico monovalente que tem pelo menos um hetero átomo selecionado entre átomos de oxigênio, enxofre e nitrogênio, e seus exemplos podem incluir os grupos furila, pirrolila, tienila, pirazolila, imidazolila, pirazolinila, oxazolila, oxazolinila, tiazolila, tiazolinila, tiadiazolila, furazanila, piranila, piridila, pirimidila, piridazinila, pirrolidinila, piperazinila, piperidinila, oxazinila, oxadiazinila, morfolinila, tiazinila, tiadiazinila, tiomorfolinila, tetrazolila, triazolila, triazinila, azepinila, diazepinila, e triazepinila. Os preferidos são os grupos tienila, pirazolila, imidazolila, oxazolila, tiazolila, tiadiazolila, furazanila, piridila, pirimidila, piridazinila, pirrolidinila, piperazinila, piperidinila, morfolinila, tiadiazinila e triazolila, sendo particularmente preferidos os grupos tienila, tiazolila, pirazolila, imidazolila, piridila, pirimidila, piridazinila, pirrolidinila, piperazinila e piperidinila. Destes grupos de 08/10/2018, pág. 64/857 heterocíclicos, os grupos heterocíclicos que contêm nitrogênio podem estar na forma de N-óxido.
O grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, significa o mesmo grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, descrito na descrição de Q4 na fórmula genérica (1) . Como seus exemplos específicos, podem ser mencionados os grupos indenila, indanila, naftila, tetraidronaftila, antrila e fenantrila, sendo preferidos os grupos indenila, indanila, naftila e tetraidronaftila.
O grupo heterocíclico bicíclico ou tricíclico fundido, saturado ou insaturado, significa o mesmo grupo heterocíclico bicíclico ou tricíclico fundido, saturado ou insaturado, descrito na descrição de Q4 na fórmula genérica (1) . Como seus exemplos específicos, podem ser mencionados os grupos benzofurila, isobenzofurila, indolila, indolinila, isoindolila, benzotienila, isoindolinila, indazolila, quinolila, hidroquinolila, 4-oxo-diidroquinolila (diidroquinon-4-ona), tetraidroquinolila, isoquinolila, tetraidroisoquinolila, cromenila, cromanila, isocromanila, 4H-4-oxobenzopiranila, 3, 4-diidro-4H-4-oxobenzopiranila, 4Hquinolizinila, quinazolinila, diidroquinazolinila, tetraidroquinazolinila, quinoxalila, tetraidroquinoxalila, cinolinila, tetraidrocinolinila, indolizinila, tetraidroindolizinila, benzotiazolila, tetraidrobenzotiazolila, benzoxazolila, benzoisotiazolila, benzoisoxazolila, benzimidazoíla, naftiridinila, tetraidronaftiridinila, tienopiridila, de 08/10/2018, pág. 65/857 tetraidrotienopiridila, tetraidrotiazolopiridila, tetraidrotiazolopiridazinila, diidropirrolopiridila, pirrolopirimidinila, piridoquinazolila, piridopirimidinila, tiazolopiridila, tiazolopiridazinila, pirrolopiridila, tetraidropirrolopiridila, diidropirrolopirimidinila, diidropiridoquinazolila, tetraidropiridopirimidinila, piranotiazolila, diidropiranotiazolila, furopiridila, tetraidrofuropiridila, oxazolopiridila, tetraidrooxazolopiridila, oxazolopiridazinila, tetraidrooxazolopiridazinila, pirrolotiazolila, diidropirrolotiazolila, pirrolooxazolila, diidropirrolooxazolila, tienopirrolila, tiazolopirimidinila, diidrotiazolopirimidinila, 4-oxo-tetraidrocinolinila, 1,2,4benzotiadiazinila, 1,l-dioxi-2H-l,2,4-benzotiadiazinila, 1,2,4-benzoxadiazinila, ciclopentapiranila, tienofuranila, furopiranila, piridoxazinila, pirazoloxazolila, imidazotiazolila, imidazopiridila, tetraidroimidazopiridila, pirazinopiridazinila, benzisoquinolila, furocinolila, pirazolotiazolopiridazinila, tetraidropirazolotiazolopiridazinila, hexaidropirazolotiazolopiridazinila, imidazotriazinila, oxazolopiridila, benzoxepinila, benzoazepinila, tetraidrobenzoazepinila, benzodiazepinila, benzotriazepinila, tienoazepinila, tetraidrotienoazepinila, tienodiazepinila, tienotrizepinila, tiazoloazepinila, tetraidrotiazoloazepinila, 4,5,6,7-tetraidro-5,6tetrametilenotiazolopiridazinila, e 5,6-trimetileno-4,5,6, 7tetraidro-tiazolopiridazinila. Os preferidos são os grupos de 08/10/2018, pág. 66/857 benzotiazolila, tetraidrobenzotiazolila, tienopiridila, tetraidrotienopiridila, tienopirrolila, tiazolopiridila, tetraidrotiazolopiridila, tiazolopiridazinila, tetraidrotiazolopiridazinila, pirrolopirimidinila, diidropirrolopirimidinila, piranotiazolila, diidropiranotiazolila, furopiridila, tetraidrofuropiridila, oxazolopiridila, tetraidrooxazolopiridila, pirrolopiridila, diidropirrolopiridila, tetraidropirrolopiridila, oxazolopiridazinila, tetraidrooxazolopiridazinila, pirrolotiazolila, diidropirrolotiazolila, pirrolooxazolila, diidropirrolooxazolila, tiazolopirimidinila, diidrotiazolopirimidinila, benzoazepinila, tetraidrobenzoazepinila, tiazoloazepinila, tetraidrotiazoloazepinila, 4,5,6,7tetraidro-5,6-tetrametilenotiazolopiridazinila, e 5, 6trimetileno-4,5,6,7-tetraidro-tiazolopiridazinila, sendo particularmente preferidos os grupos tetraidrobenzotiazolila, tetraidrotienopiridila, tetraidrotiazolopiridila, tetraidrotiazolopiridazinila, diidropirrolopirimidinila, diidropiranotiazolila, tetraidrooxazolopiridila, diidropirrolotiazolila, 4,5,6,7-tetraidro-5,6-tetrametilenotiazolopiridazinila, e 5,6-trimetileno-4,5,6, 7-tetraidrotiazolopiridazinila.
Nenhuma limitação específica é imposta sobre a forma de fusão dos grupos heterocíclicos fundidos. Por exemplo, a tienopiridina pode ser qualquer uma entre tieno[2,3-b]piridina, tieno[2,3-c]-piridina, tieno[3,2b]piridina, tieno[3,2-c]piridina, tieno[3,4-b]piridina, e tieno[3,4-c]-piridina, sendo preferidas a tieno[2,3-c]de 08/10/2018, pág. 67/857 piridina e tieno[3,2-c]piridina. A tienopirrolila pode ser qualquer uma entre tieno[2,3-b]pirrolila e tieno[3,2b]pirrolila. A tiazolopiridina pode ser qualquer uma entre tiazolo[4,5-b]piridina, tiazolo[4,5-c]piridina, tiazolo[5,4b] piridina, tiazolo[5,4-c]piridina, tiazolo[3,4-a]piridina e tiazolo[3,2-a]piridina, sendo preferidas a tiazolo[4,5c] piridina e tiazolo[5,4-c]piridina. A tiazolopiridazina pode ser qualquer uma entre tiazolo[4,5-c]piridazina, tiazolo[4,5-d]piridazina, tiazolo[5,4-c]piridazina e tiazolo[3,2-b]piridazina, sendo preferida a tiazolo[4,5d] piridazina. A pirrolopiridina pode ser qualquer uma entre pirrolo[2,3-b]piridina, pirrolo[2,3-c]piridina, pirrolo[3,2b] piridina, pirrolo[3,2-c]piridina, pirrolo[3,4-b]piridina e pirrolo[3,4-c]piridina, sendo preferidas a pirrolo[2,3c] piridina e pirrolo[3,2-c]piridina. A pirrolopirimidina pode ser qualquer uma entre pirrolo[3,4-d]pirimidina, pirrolo[3,2-d]pirimidina e pirrolo[2,3-d]pirimidina, sendo preferida a pirrolo[3,4-d]pirimidina. A piridopirimidina pode ser qualquer uma entre pirido[2,3-d]pirimidina, pirido[3,2-d]pirimidina, pirido[3,4-d]pirimidina, pirido [4,3-d]pirimidina, pirido[1,2-c]pirimidina e pirido[1,2a]pirimidina, sendo preferidas a pirido[3,4-d]pirimidina e pirido[4,3-d]pirimidina. O piranotiazol pode ser qualquer um entre pirano[2,3-d]tiazol, pirano[4,3-d]tiazol, pirano [3,4-d]tiazol e pirano[3,2-d]tiazol, sendo preferidos o pirano[4,3-d]tiazol e pirano[3,4-d]tiazol. A furopiridina pode ser qualquer uma entre furo[2,3-b]piridina, furo[2,3c]piridina, furo[3,2-b]piridina, furo[3,2-c]piridina, furo de 08/10/2018, pág. 68/857 [3,4-b]piridina e furo[3,4-c]piridina, sendo preferidas a furo[2,3-c]piridina e furo[3,2-c]piridina. A oxazolopiridina pode ser qualquer uma entre oxazolo[4,5b]piridina, oxazolo[4,5-c]piridina, oxazolo[5,4-b]piridina, oxazolo[5,4-c]piridina, oxazolo[3,4-a]piridina e oxazolo [3,2-a]piridina, sendo preferidas a oxazolo[4,5-c]piridina e oxazolo[5,4-c]piridina, A oxazolopiridazina pode ser qualquer uma entre oxazolo[4,5-c]piridazina, oxazolo[4,5d]piridazina, oxazolo[5,4-c]piridazina e oxazolo[3,4b]piridazina, sendo preferida a oxazolo[4,5-d]piridazina. O pirrolotiazol pode ser qualquer um entre pirrolo[2,1b] tiazol, pirrolo[1,2-c]tiazol, pirrolo[2,3-d]tiazol, pirrolo[3,2-d]tiazol e pirrolo[3,4-d]tiazol, sendo preferido o pirrolo[3,4-d]tiazol. O pirrolooxazol pode ser qualquer um entre pirrolo[2,1-b]oxazol, pirrolo[1,2-c]oxazol, pirrolo[2,3-d]oxazol, pirrolo[3,2-d]oxazol e pirrolo[3,4d]oxazol, sendo preferido o pirrolo[3,4-d]oxazol. A benzoazepina pode ser qualquer uma entre ΙΗ-1-benzoazepina, ΙΗ-2-benzoazepina e ΙΗ-3-benzoazepina, sendo preferida a 1H3-benzoazepina. A tiazolo[4,5-c]azepina pode ser qualquer uma entre 4H-tiazolo[4,5-c]azepina, 4H-tiazolo[4,5-d]azepina e 4H-tiazolo[5,4-c]azepina, sendo preferida a 4Htiazolo[4,5-d]azepina. A tieno[2,3-c]azepina pode ser qualquer uma entre 4H-tieno[2,3-d]azepina e 4H-tieno[2,3c] azepina, sendo preferida a 4H-tieno[2,3-d]azepina.
Destes grupos heterocíclicos, os grupos heterocíclicos que contêm nitrogênio podem estar na forma de um N-óxido. Incidentalmente, a posição do grupo de 08/10/2018, pág. 69/857 substituinte acima ligado a Q2 não é particularmente limitada.
Os grupos hidrocarboneto cíclicos com 5 ou 6 membros, saturados ou insaturados, os grupos heterocíclicos com 5 a 7 membros, saturados ou insaturados, os grupos hidrocarboneto bicíclicos ou tricíclicos fundidos, saturados ou insaturados, e os grupos heterocíclicos, bicíclicos ou tricíclicos fundidos, saturados ou insaturados, podem ter, cada um, 1 a 3 substituintes. Os exemplos dos substituintes podem incluir um grupo hidroxila; átomos de halogênio, tal como átomo de flúor, átomo de cloro, átomo de bromo e átomo de iodo; grupos halo-metila, tendo 1 a 3 substituintes halógenos; um grupo amino; um grupo ciano; um grupo amidino; um grupo hidróxi-amidino; grupos alguila lineares, ramificados ou cíclicos, tendo 1 a 6 átomos de carbono (agui doravante referidos como grupos alguila de C1-C6, os guais significam grupos alguila lineares, ramificados e cíclicos, como por exemplo, grupos alguila lineares ou ramificados, tais como metila, etila, isopropila e t-butila; grupos ciclo-alguila de C3-C6, tais como o grupo ciclo-propila, grupo ciclo-butila, grupo ciclo-pentila e grupo 1-metilciclo-propila; e grupos ciclo-alguil(C3-C6)-alguila de C1-C6, tal como o grupo ciclo-propil-metila); grupos hidróxialguila de C1-C6, tais como os grupos hidróxi-etila e 1,1dimetil-2-hidróxi-etila; grupos alcóxi de C1-C6, como por exemplo, o grupo metóxi, grupo etóxi e similares; grupos alcóxi (C1-C6) -alguila de C1-C6; um grupo carboxila; grupos carbóxi-alguila de C2-C6, como por exemplo, o grupo carbóxide 08/10/2018, pág. 70/857 metila e similares; grupos alcóxi (C2-C6) -carbonil-alquila de C1-C6, tal como por exemplo, o grupo metóxi-carbonil-metila, grupo t-butóxi-carbonil-metila, e similares; grupos amidino substituídos com um grupo alcóxi-carbonila de C2-C6; grupos alquenila de C2-C6, tal como por exemplo, o grupo vinila, grupo alila, e similares; grupos alquinila de C2-C6, tal como por exemplo, o grupo etinila, grupo propinila, e similares; grupos alcóxi-carbonila de C2-C6, como por exemplo o grupo metóxi-carbonila, grupo etóxi-carbonila, grupo t-butóxi-carbonila, e similares; grupos amino-alquila de C1-C6, como por exemplo, o grupo amino-metila, grupo amino-etila, e similares; grupos alquil (C1-C6) -amino-alquila de C1-C6, como por exemplo, o grupo N-metil-amino-metila, grupo N-etil-amino-metila, e similares; grupos dialquil(CiCô)-amino-alquila de C1-C6, como por exemplo, o grupo N,Ndimetil-amino-metila, grupo N, N-dietil-amino-metila, grupo N-etil-N-metil-amino-etila, e similares; grupos alcóxi(C2Cô)-carbonil-amino-alquila de C1-C6, como por exemplo, o grupo metóxi-carbonil-amino-etila, grupo t-butóxi-carbonilamino-etila, e similares; grupos alcanoíla de C1-C6, como por exemplo, o grupo formila, grupo acetila, grupo metilpropionila, grupo ciclo-pentano-carbonila, e similares; grupos alcanoil (C1-C6) -amino-alquila de C1-C6, como por exemplo, o grupo acetil-amino-metila, e similares; grupos alquil (C1-C6)-sulfonila, como por exemplo, o grupo metanosulfonila e similares; grupos alquil (C1-C6) -sulfonil-aminoalquila de C1-C6, como por exemplo, o grupo metano-sulfonilamino-metila e similares; um grupo carbamoíla; grupos de 08/10/2018, pág. 71/857 alquil (Ci-C6) -carbamoíla, como por exemplo, o grupo metilcarbamaoíla, grupo etil-carbamoíla, grupo isopropilcarbamoíla, grupo t-butil-carbamoíla, e similares; grupos N, N-dialquil (Ci-Ce)-carbamoíla, como por exemplo, o grupo dimetil-carbamoíla, grupo dietil-carbamoíla, grupo metiletil-carbamoíla, e similares; grupos alquil (Ci-Ce)-amino, como por exemplo, o grupo N-metil-amino, N-etil-amino, e similares; grupos dialquil(Ci-Ce)-amino, como por exemplo, o grupo N,N-dimetil-amino, grupo N,N-dietil-amino, N-etil-Nmetil-amino, e similares; grupos heterocíclicos com 5 ou 6 membros, contendo um entre nitrogênio, oxigênio e enxofre, ou dois desses átomos iguais ou diferentes, como por exemplo, o grupo pirrolidinila, grupo piperidinila, grupo piperazinila, grupo morfolinila, grupo piridila, grupo pirimidinila, grupo tetraidropiranila, e similares; grupos heterocíclicos de 5 ou 6 membros acima -alquila de C1-C4 (como por exemplo, o grupo morfolino-metila e similares); e grupo heterocíclico de 5 ou 6 membros acima amino-alquila de C1-C6, como por exemplo, o grupo N-(oxazol-2-il)-aminometila e similares.
Como exemplos específicos de Q1, podem ser mencionados os grupos heterocíclicos bicíclicos tais como 5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-ila, 4,5,6,7 -tetraidrotiazolo[5,4-c]-piridin-2-ila, 5-ciclo-propil-4,5,
6.7- tetraidrotiazolo[5,4-c]-piridin-2-ila, 5-carbóxi-metil4.5.6.7- tetraidrotiazolo[5,4-c]-piridin-2-ila, 5-butil -4,5,
6.7- tetraidrotiazolo[5,4-c]-piridin-2-ila, 5-(4-piridil)4.5.6.7- tetraidrotiazolo[5,4-c]-piridin-2-ila, 5-metilde 08/10/2018, pág. 72/857
4.5.6.7- tetraidrotiazolo[4,5-c]-piridin-2-ila, 6-metil4.5.6.7- tetraidrotieno[2,3-c]-piridin-2-ila, 5-metil4.5.6.7- tetraidrooxazolo[5,4-c]-piridin-2-ila, 5-metil-4,6diidro-5H-pirrolo[3,4-d]-tiazol-2-ila, 5,7-diidro-6-metilpirrolo[3,4-d]-pirimidin-2-ila, 5,6-dimetil-4,5,6,7tetraidrotiazolo[4,5-d]-piridazin-2-ila, 5,6-dimetil4.5.6.7- tetraidrooxazolo[4,5-d]-piridazin-2-ila, 5-dimetilamino-4,5,6,7-tetraidrobenzo[d]-tiazol-2-ila, 5-(4-piridil)4.5.6.7- tetraidrotiazolo[5,4-c]-piridin-2-ila, e 6,7-diidro4H-pirano[4,3-d]-tiazol-2-ila; e grupos heterocíclicos com 5 ou 6 membros, tais como grupos piridila, tais como 4piridila e 2-piridila; grupos diidrooxazolila, tal como 4,5diidrooxazol-2-ila; 4-[N-(4,5-diidrooxazol-2-il)-N-metilamino-metil]-tiofen-2-ila, 4-[N-(4,5-diidrooxazol-2-il)-Nmetil-amino-metil]-3-cloro-tiofen-2-ila, 5-(N-metil-aminometil)-tiazol-2-ila, 5-(N-metil-amino-metil)-tiofen-2-ila, 5-(N-metil-amino-metil)-tiofen-2-ila, 5-(N,N-dimetil-aminometil)-tiazol-2-ila, 5-(N,N-dimetil-amino-metil)-tiofen-2ila, e 5-(N,N-dimetil-amino-metil)-piridin-2-ila.
Incidentalmente, Q1 não está de forma alguma limitado a estes exemplos.
Grupo Q2
O grupo Q2 significa uma ligação simples, um grupo hidrocarboneto cíclico bivalente, saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico bivalente saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, bivalente, saturado ou de 08/10/2018, pág. 73/857 insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído.
No grupo Q2, o grupo hidrocarboneto cíclico bivalente, saturado ou insaturado, com 5 ou 6 membros significa um grupo bivalente derivado do grupo hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, descrito na descrição de Q4 na fórmula genérica (1) . Como seus exemplos específicos, podem ser mencionados os grupos ciclo-hexileno, ciclohexenileno e fenileno, sendo preferidos os grupos ciclo-hexileno e fenileno.
O grupo heterocíclico bivalente saturado ou insaturado, com 5 a 7 membros, significa um grupo bivalente derivado do anel heterocíclico saturado ou insaturado, com 5 a 7 membros, descrito na descrição de Q4 na fórmula genérica (1) . Como seus exemplos específicos, podem ser mencionados os grupos bivalentes derivados de furano, pirrol, tiofeno, pirazol, imidazol, oxazol, oxazolidina, tiazol, tiadiazol, furazano, pirano, piridina, pirimidina, piridazina, pirrolidina, piperazina, piperidina, oxazina, oxadiazina, morfolina, tiazina, tiadiazina, tiomorfolina, tetrazol, triazol, triazina, azepieno, diazepina e triazepina. Dentre estes, os seus exemplos preferidos incluem grupos bivalentes derivados de pirazol, imidazol, oxazol, tiazol, tiadiazol, furazano, piridina, pirimidina, piridazina, pirrolidina, piperazina, piperidina, triazol, triazina, azepieno, diazepina e triazepina.
O hidrocarboneto bicíclico ou tricíclico fundido, de 08/10/2018, pág. 74/857 bivalente, saturado ou insaturado, significa um grupo bivalente derivado do grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, descrito na descrição de Q4 na fórmula genérica (1). Como seus exemplos específicos, podem ser mencionados os grupos bivalentes derivados de indeno, indano, naftaleno, tetraidronaftaleno, antraceno, fenantreno, e similares. Como seus exemplos preferidos, podem ser mencionados os grupos bivalentes derivados de indano e naftaleno.
O grupo heterocíclico, bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, significa um grupo bivalente derivado do anel heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, descrito na descrição de Q4 na fórmula genérica (1). Como seus exemplos específicos, podem ser mencionados os grupos bivalentes derivados de benzofurano, benzotiofeno, indol, isoindol, indazol, guinolina, tetraidroguinolina, isoguinolina, tetraidroisoguinolina, guinazolina, diidroguinazolina, tetraidroguinazolina, guinoxalina, tetraidroguinoxalina, cinolina, tetraidrocinolina, indolizina, tetraidroindolizina, benzotiazol, tetraidrobenzotiazol, naftiridina, tetraidronaftiridina, tienopiridina, tetraidrotienopiridina, tiazolopiridina, tetraidrotiazolopiridina, tiazolopiridina, tetraidrotiazolpiridina, tiazolopiridazina, tetraidrotiazolopiridazina, pirrolopiridina, diidropirrolopiridina, tetraidropirrolopiridina, pirrolopirimidina, diidropirrolopirimidina, diidropiridoguinazolina, piranotiazol, diidropiranotiazol, furopiridina, tetraidrofuropiridina, de 08/10/2018, pág. 75/857 oxazolopiridina, oxazolodiidropiranotiazol, oxazolopiridazina, tiazolo[4,5-d]piridazina, tiazolo[3,2-b]piridazina, tetraidrooxazolopiridinna, piridazina, tetraidrooxazolopiridazina, pirrolotiazol, diidropirrolotiazol, pirrolooxazol, diidropirrolooxazol, e benzoazepina. Como seus exemplos preferidos, podem ser mencionados os grupos bivalentes derivados de benzofurano, benzotiofeno, indol, indazol, quinolina, isoquinolina, tetraidroisoquinolina, benzotiazol, naftiridina, tienopiridina, tiazolopiridina, tetraidrotiazolopiridina, tiazolopiridazina, pirrolopiridina, tetraidropirrolopiridina, piridopirimidina, piranotiazol, furopiridina, oxazolopiridina, pirrolotiazol, diidropirrolotiazol, pirrolooxazol e diidropirrolooxazol. Nenhuma limitação específica é imposta sobre a forma de fusão do grupo heterocíclico fundido. Por exemplo, a naftiridina pode ser qualquer uma entre 1,5-, 1,6-, 1,7-, 1,8-, 2,6- e 2,7naftiridina, a tienopiridina pode ser qualquer uma entre tieno[2,3-b]piridina, tieno[2,3-c]-piridina, tieno[3,2b] piridina, tieno[3,2-c]piridina, tieno[3,4-b]piridina, e tieno[3,4-c]-piridina, a tiazolopiridina pode ser qualquer uma entre tiazolo[4,5-b]piridina, tiazolo[4,5-c]piridina, tiazolo[5,4-b]piridina, tiazolo[5,4-c]piridina, tiazolo[3,4a]piridina e tiazolo[3,2-a]piridina, a tiazolopiridazina pode ser qualquer uma entre tiazolo[4,5-c]piridazina, tiazolo[5,4-c]piridazina e a pirrolopiridina pode ser qualquer uma entre pirrolo[2,3-b]piridina, pirrolo[2,3c] piridina, pirrolo[3,2-b]piridina, pirrolo[3,2-c]piridina, de 08/10/2018, pág. 76/857 pirrolo[3,4-b]piridina e pirrolo[3,4-c]piridina, a pirrolopirimidina pode ser qualquer uma entre pirrolo[3,4d]pirimidina, pirrolo[3,2-d]pirimidina e pirrolo[2,3d]pirimidina, a piridopirimidina pode ser qualquer uma entre pirido[2,3-d]pirimidina, pirido[3,2-d]pirimidina e pirido[3,4-d]pirimidina, o piranotiazol pode ser qualquer um entre pirano[2,3-d]tiazol, pirano[4,3-d]tiazol, pirano[3,4d]tiazol e pirano[3,2-d]tiazol, a furopiridina pode ser qualquer uma entre furo[2,3-b]piridina, furo[2,3-c]piridina, furo[3,2-b]piridina, furo[3,2-c]piridina, furo[3,4b] piridina e furo[3,4-c]piridina, a oxazolopiridina pode ser qualquer uma entre oxazolo[4,5-b]piridina, oxazolo[4,5c] piridina, oxazolo[5,4-b]piridina, oxazolo[5,4-c]piridina, oxazolo[3,4-a]piridina e oxazolo[3,2-a]piridina, a oxazolopiridazina pode ser qualquer uma entre oxazolo[4,5c]piridazina, oxazolo[4,5-d]piridazina, oxazolo[5,4c] piridazina e oxazolo[3,4-b]piridazina, o pirrolotiazol pode ser qualquer um entre pirrolo[2,1-b]tiazol, pirrolo[1,2-c]tiazol, pirrolo[3,2-d]tiazol e pirrolo[3,4d] tiazol, e o pirrolooxazol pode ser qualquer um entre pirrolo[2,1-b]oxazol, pirrolo[1,2-c]oxazol, pirrolo[2,3d]oxazol, pirrolo[3,2-d]oxazol e pirrolo[3,4-d]oxazol, sendo preferido o pirrolo[3,4-d]oxazol. Outras formas de fusão que não estas podem ser consideradas.
Os grupos hidrocarboneto cíclicos bivalentes com 5 ou 6 membros, saturados ou insaturados, os grupos heterocíclicos bivalentes com 5 a 7 membros, saturados ou insaturados, os grupos hidrocarboneto bicíclicos ou de 08/10/2018, pág. 77/857 tricíclicos fundidos, bivalentes, saturados ou insaturados, e os grupos heterocíclicos, bicíclicos ou tricíclicos fundidos, bivalentes, saturados ou insaturados, podem ter, cada um, 1 a 3 substituintes. Os exemplos dos substituintes podem incluir um grupo hidroxila; átomos de halogênio, tal como átomo de flúor, átomo de cloro, átomo de bromo e átomo de iodo; grupos halo-alquila, tendo 1 a 3 átomos de halogênio; um grupo amino; um grupo ciano; grupos aminoalquila; um grupo amidino; um grupo hidróxi-amidino; grupos alquila lineares, ramificados ou cíclicos, tendo 1 a 6 átomos de carbono (como por exemplo, grupo metila, grupo etila, grupo etóxi, etc.), grupos alcóxi lineares, ramificados ou cíclicos, tendo 1 a 6 átomos de carbono (como por exemplo, grupo metoxi, etc.); grupo amidino substituído com grupo alcóxi-carbonila linear, ramificado ou cíclico, tendo 2 a 7 átomos de carbono (como por exemplo, grupo metóxi-carbonil-amidino, grupo etóxi-carbonil-amidino, etc.); grupos alquenila lineares, ramificados ou cíclicos, tendo 2 a 6 átomos de carbono (como por exemplo, grupo vinila, grupo alila, etc.), grupos alquinila lineares ou ramificados, tendo 2 a 6 átomos de carbono (como por exemplo, grupo etinila, grupo propinila, etc.), grupos alcóxi-carbonila lineares, ramificados ou cíclicos, tendo 2 a 6 átomos de carbono (como por exemplo, grupo metóxicarbonila, grupo etóxi-carbonila, etc.), e grupo carbamoíla.
Os grupos preferíveis em Q2 acima são uma ligação simples, grupos hidrocarboneto cíclicos bivalentes com 5 ou 6 membros, saturados ou insaturados, que podem ser de 08/10/2018, pág. 78/857 substituídos, grupos heterocíclicos bivalentes com 5 a 7 membros, saturados ou insaturados, que podem ser substituídos, e grupos heterocíclicos, bicíclicos ou tricíclicos fundidos, bivalentes, saturados ou insaturados, que podem ser substituídos. Particularmente, uma ligação simples, grupos hidrocarboneto cíclicos bivalentes com 5 ou 6 membros, saturados ou insaturados, e grupos heterocíclicos bivalentes, com 5 a 7 membros, saturados ou insaturados, são preferidos.
Quando Q1 é um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, o grupo Q2 é, de preferência, uma ligação simples. Quando Q2 é uma ligação simples na combinação supradescrita, isto significa que a fórmula genérica (1):
qi_q2_to_n (Ri) -q3—n(R2) -Tí-Q4 (1) onde R1, R2, Q1, Q2, Q3, Q4, T° e T1 têm os mesmos significados que definidos acima, passa a ser a seguinte fórmula genérica (1'):
Qi-TO-N (R1)-Q3-N (R2)-T3-Q4 (1') onde Q1 representa o grupo hidrocarboneto bicíclico ou tricíclico fundido acima ou o grupo heterocíclico, bicíclico ou tricíclico fundido acima, e R1, R2, Q3, Q4, T° e T1 têm os mesmos significados que definidos acima.
Especificamente, são preferidos aqueles nos quais o grupo Q1 é um grupo tienopiridila que pode ser substituído; um grupo tetraidrotienopiridila que pode ser de 08/10/2018, pág. 79/857 substituído; um grupo tiazolopiridila que pode ser substituído; um grupo tetraidrotiazolopiridila que pode ser substituído; um grupo tiazolopiridazinila que pode ser substituído; um grupo tetraidrotiazolopiridazinila que pode ser substituído; um grupo piranotiazolila que pode ser substituído; um grupo diidropiranotiazolila que pode ser substituído; um grupo furopiridila que pode ser substituído; um grupo tetraidrofuropiridila que pode ser substituído; um grupo oxazolopiridila que pode ser substituído; um grupo tetraidrooxazolopiridila que pode ser substituído; um grupo pirrolopiridila que pode ser substituído; um grupo diidropirrolopiridila que pode ser substituído; um grupo tetraidropirrolopiridila que pode ser substituído; um grupo pirrolopirimidinila que pode ser substituído; um grupo diidropirrolopirimidinila que pode ser substituído; um grupo oxazolopiridazinila que pode ser substituído; um grupo tetraidrooxazolopiridazinila que pode ser substituído; um grupo pirrolotiazolila que pode ser substituído; um grupo diidropirrolotiazolila que pode ser substituído; um grupo pirrolooxazolila que pode ser substituído; um grupo diidropirrolooxazolila que pode ser substituído; um grupo benzotiazolila que pode ser substituído; um grupo tetraidrobenzotiazolila que pode ser substituído; um grupo tiazolopirimidinila que pode ser substituído; um grupo diidrotiazolopirimidinila que pode ser substituído; um grupo benzoazepinila que pode ser substituído; um grupo tetraidrobenzoazepinila que pode ser substituído; um grupo tiazoloazepinila que pode ser substituído; um grupo de 08/10/2018, pág. 80/857 tetraidrotiazoloazepinila que pode ser substituído; um grupo tienoazepinila que pode ser substituído; um grupo tetraidrotienoazepinila que pode ser substituído; um grupo 4,5,6,7-tetraidro-5,6-tetrametilenotiazolopiridazinila que pode ser substituído; um grupo 5,6-trimetileno-4,5, 6, 7tetraidrotiazolopiridazinila que pode ser substituído, e Q2 é uma ligação simples.
Quando Q1 é um grupo hidrocarboneto cíclico de 5 ou 6 membros, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico de 5 a 7 membros, saturado ou insaturado, que pode ser substituído, o grupo Q2 é, de preferência, um grupo cíclico bivalente de 5 ou 6 membros, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico bivalente de 5 a 7 membros, saturado ou insaturado, que pode ser substituído. Como exemplos preferidos do grupo Q^—Q2, podem ser mencionados os grupos 4-(4-piridil)-fenila, 4-(2-piridil)-fenila, 5—(4 — piridil)-tiazolila, 1-(4-piridil)-piperidila, 4-(4-piridil)piperidila, 4-hidróxi-l-(4-piridil)-piperidin-4-ila, bifenilila, 4-(2-amino-sulfonil-fenil)-fenila, 4-(2-amidinofenil)-fenila, 4-(2-metil-sulfonil-fenil)-fenila, 4—(2— amino-metil-fenil)-fenila, 4-(2-carbamoil-fenil)-fenila, 4(2-imidazolil)-fenila, 4-(l-metil-2-imidazolil)-fenila, 4(2,3,4,5-tetraidropirimidin-2-il)-fenila, 4-(1-metil2,3,4,5-tetraidropirimidin-2-il)-fenila, 4-(5-tetrazolil)fenila, 1-(4-piridil)-piperidin-4-ila, 3-(4-piperidil) isoxazolin-5-ila, 3-(4-amidino-fenil)-isoxazolin-5-ila, 3(4-piperidil)-isoxazolidin-5-ila, 3-(4-amidino-fenil)de 08/10/2018, pág. 81/857 isoxazolidin-5-ila, 2-(4-piperidil)-1,3,4-tiadiazol-5-ila, 2-(4-amino-fenil)-1,3,4-oxadiazol-5-ila, 4-(4-piperidil)piperidin-l-ila, 4-(4-piperidil)-piperazin-l-ila, 4-(4piperazinil)-piperazin-l-ila, 1-(4-pirimidinil)-piperidin-lila, 1-(2-metil-pirimidin-4-il)-piperidin-4-ila, l-(4pirimidinil)-pirrolidin-3-ila, 1-(4-metil-pirimidin-6-il)piperazin-6-ila, 1-(2-metil-pirimidin-4-il)-pirrolidin-4ila, 1-(6-cloro-pirimidin-4-il)-piperidin-4-ila, 5-(4-clorofenil)-tiofen-2-ila, 2-(4-cloro-fenil)-tiazol-4-ila, 3-(4cloro-fenil)-lH-pirrol-2-ila, 4-(4-pirimidinil)-fenila e 4(4-imidazolil)-fenila.
Grupo Q3
O grupo Q3 representa o seguinte grupo:
onde Q5 significa um grupo alquileno que tem 1 a 8 átomos de carbono, um grupo alquenileno que tem 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, cada um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-,
-NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH, os números 1 e 2 significam posições, e R3 e R4 são substituintes no(s) átomo(s) de carbono, átomo(s) de nitrogênio ou átomo(s) de enxofre de um anel que compreende de 08/10/2018, pág. 82/857
Q5 e são, um independentemente do outro, um átomo de hidrogênio, grupo hidroxila, grupo alquila, grupo alquenila, grupo alquinila, átomo de halogênio, grupo halo-alquila, grupo ciano, grupo ciano-alquila, grupo amino, grupo aminoalquila, grupo N-alquil-amino-alquila, grupo N,N-dialquilamino-alquila, grupo acila, grupo acil-alquila, grupo acilamino que pode ser substituído, grupo alcóxi-imino, grupo hidróxi-imino, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo hidróxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo alcóxi-carbonila, grupo alcóxicarbonil-alquila, grupo alcóxi-carbonil-alquil-amino, grupo carbóxi-alquil-amino, grupo alcóxi-carbonil-amino, grupo alcóxi-carbonil-amino-alquila, grupo carbamoíla, grupo Nalquil-carbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenilcarbamoíla, grupo N-alquenil-carbamoil-alquila, grupo Nalquenil-N-alquil-carbamoíla, grupo N-alquenil-N-alquilcarbamoil-alquila, grupo N-alcóxi-carbamoíla, grupo Nalquil-N-alcóxi-carbamoíla, grupo N-alcóxi-carbamoilalquila, grupo N-alquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquil-sulfonila, grupo alquil-sulfonilalquila, grupo carbonila heterocíclico com 3 a 6 membros que pode ser substituído, grupo carbamoil-alquila, grupo Nalquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo de 08/10/2018, pág. 83/857 carbamoilóxi-alquila, grupo N-alquil-carbamoilóxi-alquila, grupo N,N-dialquil-carbamoilóxi-alquila, grupo carbonilalquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo arila, grupo aralquila, grupo heteroarila, grupo heteroaril-alquila, grupo alquil-sulfonil-amino, grupo aril-sulfonil-amino, grupo alquil-sulfonil-amino-alquila, grupo aril-sulfonilamino-alquila, grupo alquil-sulfonil-amino-carbonila, grupo aril-sulfonil-amino-carbonila, grupo alquil-sulfonil-aminocarbonil-alquila, grupo aril-sulfonil-amino-carbonilalquila, grupo oxo, grupo carbamoilóxi, grupo aralquilóxi, grupo carbóxi-alquilóxi, grupo acilóxi, grupo acilóxialquila, grupo aril-sulfonila, grupo alcóxi-carbonil-alquilsulfonila, grupo carbóxi-alquil-sulfonila, grupo alcóxicarbonil-acila, grupo alcóxi-alquilóxi-carbonila, grupo hidróxi-acila, grupo alcóxi-acila, grupo halo-acila, grupo carbóxi-acila, grupo amino-acila, grupo acilóxi-acila, grupo acilóxi-alquil-sulfonila, grupo hidróxi-alquil-sulfonila, grupo alcóxi-alquil-sulfonila, grupo sulfonila heterocíclico com 3 a 6 membros, que pode ser susbtituído, grupo N-alquilamino-acila, grupo N,N-dialquil-amino-acila, grupo N,Ndialquil-carbamoil-acila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquilsulfonila que pode ter um substituinte no(s) grupo(s) alquila, grupo alquil-sulfonil-acila, grupo aminocarbotioíla, grupo N-alquil-amino-carbotioíla, grupo N,Ndialquil-amino-carbotioíla ou um grupo alcóxi-alquilde 08/10/2018, pág. 84/857 (tiocarbonila), ou R3 e R4 juntos denotam um grupo alquileno com 1 a 5 átomos de carbono, um grupo alquenileno com 2 a 5 átomos de carbono, um grupo alquilenodioxi com 1 a 5 átomos de carbono, ou um grupo carbonildioxi.
O grupo que se segue será descrito detalhadamente.
onde Q5, R3 e R4 têm os mesmos significados definidos acima, e os números 1 e 2 indicam posições.
Uma parte da estrutura cíclica que tem o grupo Q5 é um grupo hidrocarboneto cíclico bivalente com 3 a 10 membros, que pode ter uma ligação dupla, ou um grupo heterocíclico bivalente com 5 a 12 membros, contendo 1 ou 2 hetero átomos, de preferência, um grupo hidrocarboneto cíclico bivalente com 3 a 8 membros, ou um grupo heterocíclico bivalente com 5 a 8 membros, e mais preferivelmente, um grupo hidrocarboneto cíclico bivalente com 5 a 7 membros, ou um grupo heterocíclico bivalente com 5 a 7 membros. Dentre outros, prefere-se um grupo no qual Q5 é um grupo alquileno que tem 3 a 6 átomos de carbono ou um grupo - (CH2) m-CH2-A-CH2-(CH2) n-, onde m e n são, cada um independentemente do outro, 0 ou 1, e A tem o mesmo significado definido acima. Particularmente, prefere-se um grupo no qual Q5 é um grupo alquileno que tem 4 átomos de carbono.
de 08/10/2018, pág. 85/857
Este grupo hidrocarboneto cíclico ou grupo heterocíclico pode ter suas estruturas cis e trans na relação entre a posição 1 e a posição 2. Entretanto, a forma trans é preferida no caso do anel de 5 membros, enguanto gue a forma cis e a forma trans são preferidas no anel com 6 ou 7 membros.
Os substituintes R3 e R4 serão agora descritos detalhadamente. O átomo de halogênio significa um átomo de flúor, cloro, bromo ou iodo. Os exemplos do grupo alguila incluem grupos alguila de Οι-Οβ lineares, ramificados ou cíclicos (como por exemplo, grupo metila, grupo ciclopropila, grupo isobutila, e similares) . Os exemplos do grupo halo-alguila incluem os grupos alguila substituídos com 1 a 3 halogênios (como por exemplo, grupo cloro-metila, grupo 1-bromo-etila, grupo triflúor-metila, e similares). Os exemplos do grupo ciano-alguila incluem os grupos alguila de Ci-C6 substituídos com um grupo ciano (como por exemplo, grupo ciano-metila, grupo 1-ciano-etila, e similares). Os exemplos do grupo alguenila incluem grupos alguenila lineares ou ramificados gue têm 2 a 6 átomos de carbono e uma ligação dupla (como por exemplo, grupo vinila, grupo alila, e similares) . Os exemplos do grupo alguinila incluem grupos alguinila lineares ou ramificados gue têm 2 a 6 átomos de carbono e uma ligação tripla (como por exemplo, grupo etinila, grupo propinila, e similares). Os exemplos do grupo acila incluem grupos alcanoíla de Οι-Οβ (como por exemplo, grupo formila, grupo acetila, e similares) , grupos aroíla de C7-C15, tais como um grupo benzoíla e um grupo de 08/10/2018, pág. 86/857 naftoíla, e grupos aril-alcanoíla que são os grupos alcanoíla de C1-C6 substituídos com um grupo arila de C6-C14 (como por exemplo, grupo fenacetila, e similares) . Os exemplos do grupo acil-alquila incluem os grupos alquila de C1-C6 substituídos com o grupo acila (como por exemplo, grupo acetil-metila, e similares). Os exemplos do grupo alcóxi incluem grupos alcóxi de C1-C6 lineares, ramificados ou cíclicos (como por exemplo, grupo metóxi, grupo ciclopropóxi, grupo isopropóxi, e similares). Os exemplos do grupo alcóxi-alquila incluem grupos alquila de C1-C6 substituídos com o grupo alcóxi de C1-C6 (como por exemplo, grupo metóxi-metila, grupo etóxi-metila, e similares). Os exemplos do grupo hidróxi-alquila incluem os grupos alquila de C1-C6 substituídos com um grupo hidroxila (como por exemplo, grupo hidróxi-metila, grupo 1-hidróxi-etila, e similares). Os exemplos do grupo carbóxi-alquila incluem os grupos alquila de C1-C6 substituídos com um grupo carboxila (como por exemplo, grupo carbóxi-metila, grupo 1-carbóxietila, e similares). Os exemplos do grupo alcóxi-carbonila incluem grupos compostos do grupo alcóxi de C1-C6 e um grupo carbonila (como por exemplo, grupo metóxi-carbonila, grupo etóxi-carbonila, e similares). Os exemplos do grupo alcóxicarbonil-alquila incluem os grupos alquila de C1-C6 substituídos com o grupo alcóxi-carbonila de C1-C6 (como por exemplo, grupo metóxi-carbonil-etila, grupo etóxi-carboniletila, e similares). Os exemplos do grupo carbamoil-alquila incluem os grupos alquila de C1-C6 substituídos com um grupo carbamoila (como por exemplo, grupo carbamoil-metila, grupo de 08/10/2018, pág. 87/857 carbamoil-etila, e similares).
Os exemplos do grupo heteroarila incluem os mesmos grupos heteroarila descritos na descrição de Q4 na fórmula genérica (1). Os exemplos do grupo heteroaril-alquila incluem os grupos alquila de Οι-Οβ substituídos com um grupo o grupo heteroarila (como por exemplo, grupo tienil-metila, grupo piridil-etila, e similares). Os exemplos do grupo arila incluem grupos arila que têm 6 a 14 átomos de carbono, tais como um grupo fenila e um grupo naftila. Os grupos arila podem ter 1 a 3 substituintes selecionados entre os grupos alquila de Οι-Οβ, os grupos alcanoíla de Οι-Οβ, um grupo hidroxila, um grupo nitro, um grupo ciano, átomos de halogênio, os grupos alquenila de C2-C6, os grupos alquinila de C2-C6, os grupos halo-alquila de C1-C6, os grupos alcóxi de C1-C6, um grupo carbóxi, um grupo carbamoíla, os grupos alcóxi-carbonila de C1-C6, e similares. Os exemplos do grupo aralquila incluem os alquila de C1-C6 substituídos com os grupos arila de C6-C14 (como por exemplo, grupo benzila, grupo fenetila, e similares). Incidentalmente, na descrição acima, nenhuma limitação é imposta sobre a posição da substituição. Os exemplos do grupo acil-amino, que podem ser substituídos, incluem os grupos amino substituídos com o grupo acila de C1-C6 (como por exemplo, grupo formil-amino, grupo acetil-amino, e similares), e além disso, grupos acila que têm 1 a vários substituintes selecionados entre átomos de halogênio, um grupo hidroxila, grupos alcóxi de C1-C6, um grupoamino, grupos N-alquil(C1-C6)-amino, grupos N,Ndialquil(Ci-Cô)-amino, um grupo carboxila, grupos alcóxi(Cide 08/10/2018, pág. 88/857
Οβ)-carbonila, e similares (como por exemplo, grupo 2metóxi-acetil-amino, grupo 3-amino-propionil-amino, e similares). Os exemplos do grupo acil-amino-alquila incluem os grupos alquila de Οι-Οβ substituídos com o grupo acilamino de Οι-Οβ (como por exemplo, grupo formil-amino-metila, grupo acetil-amino-metila, e similares). Os exemplos do grupo amino-alquila incluem os grupos alquila de Οι-Οβ substituídos com um grupo amino (como por exemplo, grupo amino-metila, grupo 1-amino-etila, e similares). Os exemplos do grupo N-alquil-amino-alquila incluem os grupos amino-alquila de Οι-Οβ substituídos com o grupo alquila de Ci-C6 no átomo de nitrogênio (como por exemplo, grupo Nmetil-amino-metila, grupo N-metil-amino-etila, e similares). Os exemplos do grupo N,N-dialquil-amino-alquila incluem os grupos amino-alquila de Οι-Οβ substituídos respectivamente com dois grupos alquila de Οι-Οβ no átomo de nitrogênio (como por exemplo, grupo N,N-dimetil-amino-metila, grupo Netil-N-metil-amino-etila, e similares). Os exemplos do grupo N-alquenil-carbamoíla incluem grupos carbamoíla substituídos com um grupo alquenila de Οι-Οβ linear ou ramificado (como por exemplo, grupo alil-carbamoíla, e similares). Os exemplos do grupo N-alquenil-carbamoilalquila incluem os grupos alquila de Οι-Οβ substituídos com o grupo N-alquenil(C2-C6)-carbamoíla (como por exemplo, grupo alil-carbamoil-etila, e similares). Os exemplos do grupo N-alquenil-N-alquil-carbamoíla incluem os grupos Nalquenil (C2-C6)-carbamoíla substituídos com um grupo alquila de C1-C6 linear ou ramificado no átomo de nitrogênio (como de 08/10/2018, pág. 89/857 por exemplo, grupo N-alil-N-metil-carbamoíla, e similares). Os exemplos do grupo N-alquenil-N-alquil-carbamoil-alquila incluem os grupos N-alquenil (C2-C6) -carbamoil-alquila substituídos com um grupo alquila de C1-C6 linear ou ramificado no átomo de nitrogênio (como por exemplo, grupo N-alil-N-metil-carbamoil-metila, e similares). Os exemplos do grupo N-alcóxi-carbamoíla incluem grupos carbamoíla substituídos com um grupo alcóxi de C1-C6 linear ou ramificado (como por exemplo, grupo metóxi-carbamoíla, e similares). Os exemplos do grupo N-alcóxi-carbamoil-alquila incluem grupos alquila de C1-C6 lineares ou ramificados substituídos com o grupo N-alcóxi (C2-C6)-carbamoíla (como por exemplo, grupo metóxi-carbamoil-metila, e similares). Os exemplos do grupo N-alquil-N-alcóxi-carbamoíla incluem grupos carbamoíla substituídos com um grupo alcóxi de C1-C6 linear ou ramificado e um grupo alquila de C1-C6 (como por exemplo, grupo N-etil-N-metóxi-carbamoíla, e similares). Os exemplos do grupo N-alquil-N-alcóxi-carbamoil-alquila incluem grupos alquila de C1-C6 lineares ou ramificados substituídos com o grupo N-alquil (Οι-Οβ) -N-alcóxi (Οι-Οβ) carbamoíla (como por exemplo, grupo N-etil-N-metóxicarbamoil-metila, e similares). Os exemplos do grupo carbazoíla, que podem ser substituídos com 1 a 3 grupos alquila, incluem um grupo carbazoíla, e além disso, grupos carbazoíla substituídos com 1 a 3 grupos alquila de C1-C6 lineares ou ramificados (como por exemplo, grupo 1-metilcarbazoíla, grupo 1,2-dimetil-carbazoíla, e similares). Os exemplos do grupo alquil-sulfonila incluem grupos alquil(Cide 08/10/2018, pág. 90/857
C&)-sulfonila lineares, ramificados ou cíclicos (como por exemplo, grupo metano-sulfonila, e similares). Os exemplos do grupo alquil-sulfonil-alquila incluem grupos alquila de Ci-C6 lineares ou ramificados substituídos com o grupo alquil(Ci-C6)-sulfonila (como por exemplo, grupo metanosulfonil-metila, e similares). Os exemplos do grupo alcóxiimino incluem grupos alcóxi(Οι-Οβ)-imino (como por exemplo, grupo metóxi-imino, grupo etóxi-imino, e similares). Os exemplos do grupo alcóxi-carbonil-alquil-amino incluem grupos amino substituídos com o grupo alcóxi (Οι-Οβ) carbonil-alquila (como por exemplo, grupo metóxi-carbonilmetil-amino, grupo etóxi-carbonil-propil-amino, e similares). Os exemplos do grupo carbóxi-alquil-amino incluem grupos amino substituídos com o grupo carbóxialquila de Οι-Οβ (como por exemplo, grupo carbóxi-metilamino, grupo carbóxi-etil-amino, e similares). Os exemplos do grupo alcóxi-carbonil-amino incluem grupos amino substituídos com o grupo alcóxi (Οι-Οβ)-carbonila (como por exemplo, grupo metóxi-carbonil-amino, grupo t-butóxicarbonil-amino, e similares). Os exemplos do grupo alcóxicarbonil-amino-alquila incluem os grupos alquila substituídos com o grupo alcóxi(Ci-Ce)-carbonil-amino (como por exemplo, grupo metóxi-carbonil-amino-metila, grupo tbutóxi-carbonil-amino-etila, e similares). O grupo Nalquil-carbamoíla, que pode ter um substituinte no grupo alquila, significa um grupo carbamoíla substituído com um grupo alquila de Οι-Οβ linear, ramificado ou cíclico, que pode ser substituído com um grupo hidroxila, grupo amino, de 08/10/2018, pág. 91/857 grupo N-alquil (Οι-Οβ)-amino, grupo amidino, átomo de halogênio, grupo carboxila, grupo ciano, grupo carbamoíla, grupo alcóxi de Οι-Οβ, grupo alcanoíla de Οι-Οβ, grupo alcanoil (Ci-Ce)-amino, grupo alquil (Ci-Ce) sulfonil-amino, ou similares, e cujos exemplos incluem o grupo N-metilcarbamoíla, o grupo N-etil-carbamoíla, o grupo N-isopropilcarbamoíla, grupo N-ciclo-propil-carbamoíla, grupo N-(2hidróxi-etil)-carbamoíla, grupo N-(2-flúor-etil)carbamoíla, grupo N-(2-ciano-etil)-carbamoíla, grupo N-(2-metóxi-etil)carbamoíla, grupo N-carbóxi-metil-carbamoíla, grupo N-(2amino-etil)carbamoíla, grupo N-(2-amidinoetil)-carbamoíla, e similares. Os exemplos do grupo N,N-dialquil-carbamoíla, que podem ter um substituinte no(s) grupo(s) alquila, significa um grupo carbamoíla substituído com 2 grupos alquila de Ci-Ce lineares, ramificados ou cíclicos, que podem ser substituídos com um grupo hidroxila, grupo amino, grupo N-alquil (Οι-Οβ) -amino, grupo amidino, átomo de halogênio, grupo carboxila, grupo ciano, grupo carbamoíla, grupo alcóxi de Ci-Ce, grupo alcanoíla de Ci-Ce, grupo alcanoil-amino de Ci-Ce, grupo alquil (Οι-Οβ)-sulfonil-amino, ou similares, e cujos exemplos incluem o grupo N,N-dimetilcarbamoíla, grupo N,N-dietil-carbamoíla, N-etil-N-metilcarbamoíla, grupo N-isopropil-N-metil-carbamoíla, grupo N(2-hidróxi-etil)-N-metil-carbamoíla, grupo N,N-bis-(2hidróxi-etil)-carbamoíla, grupo N,N-bis-(2-flúor-etil)carbamoíla, grupo N-(2-ciano-etil)-N-metil-carbamoíla, grupo N-(2-metóxi-etil)-N-metil-carbamoíla, grupo N-carbóxi-metilN-metil-carbamoíla, grupo N,N-bis-(2-amino-etil)-carbamoíla, de 08/10/2018, pág. 92/857 e similares. Os exemplos do grupo N-alquil-carbamoilalquila, que podem ter um substituinte no(s) grupo(s) alquila, incluem grupos alquila de Οι-Οβ lineares ou ramificados, substituídos com o grupo N-alquil-carbamoíla, que podem ter um substituinte no grupo alquila de Οι-Οβ (como por exemplo, grupo N-metil-carbamoil-metila, grupo N(2-hidróxi-etil)-carbamoil-metila, e similares). Os exemplos do grupo N,N-dialquil-carbamoil-alquila, que podem ter um substituinte no(s) grupo(s) alquila, incluem grupos alquila de Οι-Οβ lineares ou ramificados, substituídos com o grupo N,N-dialquil-carbamoíla, que podem ter um substituinte no(s) grupo (s) alquila de Οι-Οβ (como por exemplo, grupo N, N-dimetil-carbamoil-metila, grupo N-(2-hidróxi-etil)-Ncarbamoil-metila, e similares). O grupo carbonila heterocíclico com 3 a 6 membros, que pode ser substituído, é um grupo constituído de um anel heterocíclico saturado ou insaturado e um grupo carbonila. O anel heterocíclico significa um anel heterocíclico com 3 a 6 membros, contendo 1 a 3 hetero átomos (átomo de nitrogênio, átomo de oxigênio, átomo de enxofre, etc.) . O anel heterocíclico pode ter um substituinte, tal como um grupo hidróxi, um átomo de halogênio, um grupo amino, grupo alquila de C1-C6, ou similares. Como seus exemplos específicos, pode ser mencionado um grupo aziridinilcarbonila, um grupo azetidinilcarbonila, grupo 3-hidróxi-azetidinilcarbonila, grupo 3-metóxi-azetidil-carbonila, grupo pirrolidinilcarbonila, grupo 3-hidróxipirrolidinilcarbonila, grupo 3-flúor-pirrolidinilcarbonila, de 08/10/2018, pág. 93/857 grupo piperidinilcarbonila, grupo piperazinilcarbonila, grupo morfolinilcarbonila, grupo tetraidropiranilcarbonila, grupo piridilcarbonila, grupo furoíla e grupo tiofenocarbonila. Os exemplos do grupo carbonil-alquila heterocíclico com 3 a 6 membros, que podem ser substituídos, incluem os grupos alquila de Οι-Οβ substituídos com o grupo carbonila heterocíclico de 3 a 6 membros que pode ser substituído (como por exemplo, grupo azetidinilcarbonilmetila, grupo pirrolidinilcarboniletila, e similares). Os exemplos do grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que podem ser substituídos, incluem os grupos alquila de Οι-Οβ substituídos com o grupo carbonilóxi heterocíclico de 3 a 6 membros, que é constituído do grupo carbonila heterocíclico de 3 a 6 membros e um átomo de oxigênio (como por exemplo, grupo piperidinil-carbonilóxi-etila, grupo morfolinil-carbonilóximetila, e similares).
Os exemplos do grupo carbamoilóxi-alquila incluem os grupos alquila de Οι-Οβ substituídos com um grupo carbamoilóxi que é constituído de um grupo carbamoíla e um átomo de oxigênio (como por exemplo, grupo carbamoióximetila, grupo carbamoilóxi-etila, e similares). Os exemplos do grupo N-alquil-carbamoilóxi-alquila incluem os grupos alquila de Οι-Οβ substituídos com o grupo N-alquilcarbamoilóxi que é constituído do grupo N-alquil-carbamoíla, que pode ter um substituinte no grupo alquila de Οι-Οβ, e um átomo de oxigênio (como por exemplo, grupo N-metilcarbamoilóxi-metila, grupo N-metil-carbamoilóxi-etila, e de 08/10/2018, pág. 94/857 similares). Os exemplos do grupo N,N-dialguil-carbamoilóxialguila incluem os grupos alguila de Ci-Ce substituídos com o grupo N,N-dialguil-carbamoilóxi gue é constituído do grupo N,N-dialguil-carbamoíla, gue pode ter um substituinte no(s) grupo(s) alguila, e um átomo de oxigênio (como por exemplo, grupo N,N-dimetil-carbamoilóxi-metila, grupo N-etil-N-metilcarbamoilóxi, e similares). Os exemplos do grupo alguilsulfonil-amino incluem grupos amino substituídos com um grupo alguil-sulfonila gue tem o grupo alguila de Ci-Ce (como por exemplo, grupo metil-sulfonil-amino, grupo isopropil-sulfonil-amino, e similares). Os exemplos do grupo aril-sulfonil-amino incluem grupos amino substituídos com um grupo aril-sulfonila gue tem o grupo arila (como por exemplo, grupo fenil-sulfonil-amino, grupo naftil-sulfonilamino, e similares). Os exemplos do grupo alguil-sulfonilamino-alguila incluem os grupos alguila de Ci-Ce substituídos com o grupo alguil(C1-C2)-sulfonil-amino (como por exemplo, grupo metil-sulfonil-amino-etila, grupo metilsulfonil-amino-etila, e similares). Os exemplos do grupo aril-sulfonil-amino-alguila incluem os grupos alguila de ΟιΟβ substituídos com o grupo aril-sulfonil-amino (como por exemplo, grupo fenil-sulfonil-amino-metila, grupo naftilsulfonil-amino-etila, e similares). Os exemplos do grupo alguil-sulfonil-amino-carbonila incluem grupos constituídos do grupo alguil (Ci-Ce) -sulfonil-amino e um grupo carbonila (como por exemplo, grupo metil-sulfonil-amino-carbonila, grupo isopropil-sulfonil-amino-carbonila, e similares). Os exemplos do grupo aril-sulfonil-amino-carbonila incluem de 08/10/2018, pág. 95/857 carbonila, similares).
grupos constituídos do grupo aril-sulfonil-amino e um grupo carbonila (como por exemplo, grupo fenil-sulfonilaminogrupo naftil-sulfonilamino-carbonila, e
Os exemplos do grupo alquil-sulfonil-aminocarbonil-alquila incluem os grupos alquila de Οι-Οβ substituídos com o grupo alquil(Οι-Οβ)-sulfonil-aminocarbonila (como por exemplo, grupo metil-sulfonil-aminocarbonil-metila, grupo isopropil-sulfonil-amino-carbonilmetila, e similares). Os exemplos do grupo aril-sulfonilamino-carbonil-alquila incluem os grupos alquila de Οι-Οβ substituídos com o grupo aril-sulfonil-amino-carbonila (como por exemplo, grupo fenil-sulfonil-amino-carbonil-metila, grupo naftil-sulfonil-amino-carbonil-metila, e similares). O grupo acilóxi significa um grupo constituído do grupo acila e um átomo de oxigênio (como por exemplo, grupo formilóxi, grupo acetilóxi, e similares). Os exemplos do grupo acilóxi-alquila incluem os grupos alquila de Οι-Οβ substituídos com o grupo acilóxi (como por exemplo, grupo formilóxi-metila, grupo acetilóxi-metila, e similares). Os exemplos do grupo aralquilóxi incluem os grupos alcóxi de Ci-C6 substituídos com o grupo arila (como por exemplo, grupo benzilóxi, grupo naftil-metóxi, e similares) . Os exemplos do grupo carbóxi-alquilóxi incluem os grupos alquilóxi substituídos com um grupo carboxila (como por exemplo, grupo carbóxi-metóxi, grupo carbóxi-etóxi, e similares).
Os exemplos do grupo aril-sulfonila incluem grupos aril(C6-C14)-sulfonila (como por exemplo, grupo fenilde 08/10/2018, pág. 96/857 sulfonila, grupo naftil-sulfonila, e similares). Os exemplos do grupo alcóxi-carbonil-alquil-sulfonila incluem grupos constituídos do grupo alcóxi (Οι-Οβ) -carbonil-alquila e um grupo sulfonila (como por exemplo, grupo metóxicarbonil-etil-sulfonila, grupo etóxi-carbonil-etilsulfonila, e similares). Os exemplos do grupo carbóxialquil-sulfonila incluem grupos compostos do grupo carbóxialquila e um grupo sulfonila (como por exemplo, grupo carbóxi-metil-sulfonila, grupo carbóxi-etil-sulfonila, e similares). Os exemplos do grupo alcóxi-carbonil-acila incluem grupos constituídos do grupo alcóxi-carbonil-alquila e um grupo carbonila (como por exemplo, grupo metóxicarbonil-metil-carbonila, grupo etóxi-carbonil-metilcarbonila, e similares). Os exemplos do grupo alcóxialquilóxi-carbonila incluem os grupos alcóxi-carbonila substituídos com o grupo alcóxi de Οι-Οβ (como por exemplo, grupo metóxi-metilóxi-carbonila, grupo metóxi-etilóxicarbonila, e similares). Os exemplos do grupo hidróxi-acila incluem os grupos acila (inclusive alcanoíla de Οι-Οβ e aroíla) substituídos com um grupo hidroxila (como por exemplo, grupo glicoloíla, grupo lactoíla, grupo benziloíla, e similares). Os exemplos do grupo alcóxi-acila incluem os grupos acila substituídos com o grupo alcóxi de Οι-Οβ (como por exemplo, grupo metóxi-acetila, grupo etóxi-acetila, e similares). Os exemplos do grupo halo-acila incluem grupos compostos do grupo halo-alquila e um grupo carbonila (como por exemplo, grupo cloro-metil-carbonila, grupo triflúormetil-carbonila, e similares). Os exemplos do grupo de 08/10/2018, pág. 97/857 carbóxi-acila incluem os grupos acila substituídos com um grupo carboxila (como por exemplo, grupo carbóxi-acetila, grupo 2-carbóxi-propionila, e similares). Os exemplos do grupo amino-acila incluem os grupos acila (inclusive alcanoíla de C1-C6 e aroíla) substituídos com um grupo amino (como por exemplo, grupo amino-metil-carbonila, grupo 1amino-etil-carbonila, e similares). Os exemplos do grupo acilóxi-acila incluem grupos constituídos do grupo acilóxialquila e um grupo carbonila (como por exemplo, grupo formilóxi-metil-carbonila, grupo acetilóxi-metil-carbonila, e similares). Os exemplos do grupo acilóxi-alquil-sulfonila incluem grupos constituídos do grupo acilóxi-alquila e um grupo sulfonila (como por exemplo, grupo formilóxi-metilsulfonila, grupo acetilóxi-metil-sulfonila, e similares). Os exemplos do grupo hidróxi-alquil-sulfonila incluem grupos constituídos do grupo hidróxi-alquila de Οι-Οβ e um grupo sulfonila (como por exemplo, grupo hidróxi-metil-sulfonila, grupo 1-hidróxi-etil-sulfonila, e similares). Os exemplos do grupo alcóxi-alquil-sulfonila incluem os grupos constituídos do grupo alcóxi-alquila de C1-C6 e um grupo sulfonila (como por exemplo, grupo metóxi-metil-sulfonila, grupo etóxi-etil-sulfonila, e similares). Os exemplos do grupo sulfonila heterocíclico com 3 a 6 membros, que pode ser substituído, incluem grupos constituídos do grupo heterocíclico de 3 a 6 membros e um grupo sulfonila (como por exemplo, grupo aziridinil-sulfonila, grupo azetidinilsulfonila, grupo pirrolidinil-sulfonila, grupo piperidinilsulfonila, grupo piperazinil-sulfonila, grupo morfolinilde 08/10/2018, pág. 98/857 sulfonila, grupo tetraidropiranil-sulfonila, e similares). Os exemplos do grupo N-alquil-amino-acila incluem os grupos amino-acila substituídos com o grupo alquila de C1-C6 no átomo de nitrogênio (como por exemplo, grupo N-metil-aminoacetila, grupo N-etila-amino-acetila, e similares). Os exemplos do grupo N,N-dialquil-amino-acila incluem os grupos amino-acila substituídos com os dois grupos alquila de C1-C6 nos átomos de nitrogênio (como por exemplo, grupo N,Ndimetil-amino-acetila, grupo N-etil-N-metil-amino-acetila, e similares). Os exemplos do grupo N,N-dialquil-carbamoilacila, que podem ter um substituinte no(s) grupo(s) alquila, incluem os grupos acila substituídos com o grupo N,Ndialquil-carbamoíla, que podem ter um substituinte no(s) grupo(s) alquila (como por exemplo, grupo N,N-dimetilcarbamoil-acetila, grupo N,N-dietil-carbamoil-acila, grupo N-etil-N-metil-carbamoil-acetila, e similares). Os exemplos do grupo N,N-dialquil-carbamoil-alquil-sulfonila, que podem ter um substituinte no(s) grupo(s) alquila, incluem os grupos constituídos do grupo N,N-dialquil-carbamoíla, que podem ter um substituinte no(s) grupo(s) alquila de C1-C6 e um grupo sulfonila (como por exemplo, grupo N,N-dimetilcarbamoil-metil-sulfonila, grupo N-(2-hidróxi-etil)-N-metilcarbamoil-metil-sulfonila, e similares). Os exemplos do grupo alquil-sulfonil-acila incluem os grupos acila substituídos com o grupo alquil-sulfonila que tem um grupo alquila de C1-C6 (como por exemplo, grupo metil-sulfonilacetila, grupo isopropil-sulfonil-acetila, e similares).
O grupo amino-carbotiol é um grupo representado de 08/10/2018, pág. 99/857 por -C(=S)-NH2, e o grupo N-alquil-amino-carbotiol significa um grupo amino-tiocarbonila substituído com um dos grupos alquila supradescritos, e seus exemplos incluem grupo (metil-amino)-carbotiol, grupo (etil-amino)-carbotiol, e similares. O grupo N,N-dialquil-amino-carbotiol significa um grupo amino-tiocarbonila substituído com dois dos grupos alquila supradescritos, e seus exemplos incluem grupo (dimetil-amino)-carbotiol, grupo (dietil-amino)-carbotiol e grupo (etil-metil-amino)-carbotiol. O grupo alcóxi-alquil(tiocarbonila) significa um grupo constituído do grupo alcóxi-alquila supradescrito e um grupo tiocarbonila, e seus exemplos incluem grupo 2-etóxi-etanotiol e similares.
O grupo alquileno significa um grupo alquileno linear ou ramificado, tendo 1 a 5 átomos de carbono, cujos exemplos incluem grupo metileno, grupo etileno, grupo propileno, e similares. O grupo alquenileno é um grupo alquenileno que tem 2 a 5 átomos de carbono e uma ligação dupla, e seus exemplos incluem grupo vinileno, grupo propenileno, e similares. Os exemplos do grupo alquilenodioxi incluem aqueles que têm 1 a 5 átomos de carbono, tal como grupo metilenodioxo, grupo etilenodioxi, e um grupo propilenodioxi. O grupo carbonildioxi é um grupo representado por -0-0(=0)-0-. Incidentalmente, nenhuma limitação específica é imposta sobre a posição de substituição na descrição acima.
Dentre estes substituintes representados por R3 e R4, o átomo de hidrogênio, o grupo hidroxila, grupo alquila, grupo alquenila, grupo alquinila, átomo de halogênio, grupo de 08/10/2018, pág. 100/857 halo-alquila, grupo amino, grupo hidróxi-imino, grupo alcóxi-imino, grupo amino-alquila, grupo N-alquil-aminoalquila, grupo N,N-dialquil-amino-alquila, grupo acila, grupo acil-alquila, grupo acil-amino que pode ser substituído, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo hidróxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo alcóxi-carbonila, grupo alcóxicarbonil-alquila, grupo alcóxi-carbonil-amino, grupo alcóxicarbonil-amino-alquila, grupo carbamoíla, grupo N-alquil10 carbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla, que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenil-carbamoíla, grupo N-alquenil-carbamoil-alquila, grupo N-alquenil-N-alquilcarbamoíla, grupo N-alcóxi-carbamoíla, grupo N-alquil-N15 alcóxi-carbamoíla, grupo N-alcóxi-carbamoil-alquila, grupo
N-alquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquilsulfonila, grupo alquil-sulfonil-alquila, grupo carbonila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbamoil-alquila, grupo carbamoilóxi-alquila, grupo N-alquil-carbamoilóxi-alquila, grupo N,N-dialquil-carbamoilóxi-alquila, grupo N-alquilcarbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo alquil-sulfonil-amino, grupo alquil-sulfonil-amino-alquila, grupo oxo, grupo acilóxi, grupo acilóxi-alquila, grupo arilPetição 870180138821, de 08/10/2018, pág. 101/857 sulfonila, grupo alcóxi-carbonil-alquil-sulfonila, grupo carbóxi-alquil-sulfonila, grupo alcóxi-carbonil-acila, grupo carbóxi-acila, grupo alcóxi-alquilóxi-carbonila, grupo haloacila, grupo N,N-dialquil-amino-acila, grupo acilóxi-acila, grupo hidróxi-acila, grupo alcóxi-acila, grupo alcóxialquil-sulfonila, grupo N,N-dialquil-carbamoil-acila, grupo N,N-dialquil-carbamoil-alquil-sulfonila, grupo alquilsulfonil-acila, grupo amino-carbonil-tiol, grupo N-alquilamino-carbotiol, grupo N,N-dialquil-amino-carbotiol, grupo alcóxi-alquil-(tiocarbonila), e similares, são preferidos. O grupo alquileno, grupo alquenileno, grupo alquilenodioxi, grupo carbonildioxi, e similares, que são formados por R3 e R4 juntos entre si também são preferidos.
Prefere-se que R3 seja um átomo de hidrogênio, e R4 seja um dos substituintes mencionados acima, como grupos preferidos. Neste caso, os exemplos de um grupo R4 mais preferido incluem o átomo de hidrogênio, o grupo hidroxila, grupo alquila, átomo de halogênio, grupo hidróxi-imino, grupo N-alquil-amino-alquila, grupo N, N-dialquil-aminoalquila, grupo acila, grupo acil-amino que pode ser substituído, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo hidróxi-alquila, grupo carboxila, grupo alcóxi-carbonila, grupo alcóxi-carbonil-alquila, grupo alcóxi-carbonil-amino, grupo carbamoíla, grupo N-alquilcarbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenil-carbamoíla, grupo N-alquenil-carbamoil-alquila, grupo N-alquenil-N-alquilde 08/10/2018, pág. 102/857 carbamoila, grupo N-alquenil-N-alquil-carbamoil-alquila, grupo N-alcóxi-carbamoíla, grupo N-alquil-N-alcóxicarbamoíla, grupo N-alquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquil-sulfonila, grupo alquil-sulfonilalquila, grupo carbonila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbamoil-alquila, grupo N,N-dialquil-carbamoilóxialquila, grupo N-alquil-carbamoil-alquila que pode ter um substituinte no(s) grupo (s) alquila, grupo N,N-dialquilcarbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo alquil-sulfonil-amino, grupo alquilsulfonil-amino-alquila, grupo acilóxi, grupo aril-sulfonila, grupo alcóxi-carbonil-alquil-sulfonila, grupo carbóxialquil-sulfonila, grupo alcóxi-carbonil-acila, grupo carbóxi-acila, grupo alcóxi-alquilóxi-carbonila, grupo haloacila, grupo N,N-dialquil-amino-acila, grupo acilóxi-acila, grupo hidróxi-acila, grupo alcóxi-acila, grupo alcóxialquil-sulfonila, grupo N,N-dialquil-carbamoil-acila, grupo N,N-dialquil-carbamoil-alquil-sulfonila, grupo alquilsulfonil-acila, grupo amino-carbotioíla, grupo N-alquilamino-carbotioíla, grupo N,N-dialquil-amino-carbotioíla, grupo alcóxi-alquil-(tiocarbonila), e similares.
Destes, como exemplos de R4, são particularmente preferidos o átomo de hidrogênio, grupo hidroxila, grupo alquila, grupo N,N-dialquil-amino-alquila, grupo acil-amino que pode ser substituído, grupo acil-amino-alquila, grupo de 08/10/2018, pág. 103/857 alcóxi, grupo alcóxi-alquila, grupo hidróxi-alquila, grupo alcóxi-carbonila, grupo alcóxi-carbonil-amino, grupo carbamoíla, grupo N-alquil-carbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenil-carbamoíla, grupo N-alquenil-carbamoil-alquila, grupo N-alquenil-N-alquil-carbamoíla, grupo N-alquenil-Nalquil-carbamoil-alquila, grupo N-alquil-N-alcóxicarbamoíla, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquil-sulfonila, grupo alquilsulfonil-alquila, grupo carbonila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo N,N-dialquilcarbamoilóxi-alquila, grupo N-alquil-carbamoil-alquila que pode ter um substituinte no grupo alquila, grupo N,Ndialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo alquil-sulfonil-amino, grupo alquil-sulfonil-amino-alquila, grupo acilóxi, grupo acila, grupo alcóxi-alquilóxi-carbonila, grupo halo-acila, grupo N,N-dialquil-amino-acila, grupo hidróxi-acila, grupo alcóxiacila, grupo amino-carbotioíla, grupo N-alquil-aminocarbotioíla, grupo N,N-dialquil-amino-carbotioíla, grupo alcóxi-alquil-(tiocarbonila), e similares.
Como exemplos preferidos de R3 e R4, podem ser mencionados um átomo de hidrogênio, um grupo hidroxila, grupo metila, grupo etila, grupo isopropila, grupo N,Ndimetil-amino-metila, grupo N, N-dimetil-amino-etila, grupo N, N-dietil-amino-metila, grupo acetil-amino, grupo metóxiacetil-amino, grupo acetil-amino-metila, grupo acetil-aminode 08/10/2018, pág. 104/857 etila, grupo metóxi, grupo etóxi, grupo metóxi-metila, grupo metóxi-etila, grupo hidróxi-metila, grupo 2-hidróxi-etila, grupo 1-hidróxi-l-metil-etila, grupo metóxi-carbonila, grupo etóxi-carbonila, grupo metóxi-carbonil-amino, grupo etóxicarbonil-amino, grupo N-alil-carbamoíla, grupo N-alilcarbamoil-metila, grupo N-alil-N-metil-carbamoíla, grupo Nalil-N-metil-carbamoil-metila, grupo N-metóxi-N-metilcarbamoíla, grupo N,N-dimetil-carbazoíla, grupo Ν,Ν,Ν'trimetil-carbazoíla, grupo metano-sulfonila, grupo metanosulfonil-metila, grupo etano-sulfonil-metila, grupo N-metilcarbamoíla, grupo N-etil-carbamoíla, grupo N-propilcarbamoíla, grupo N-isopropil-carbamoíla, grupo N-t-butilcarbamoíla, grupo N-ciclo-propil-carbamoíla, grupo N-ciclopropil-metil-carbamoíla, grupo N-(1-etóxi-carbonil-ciclopropil)-carbamoíla, grupo N-(2-hidróxi-etil)-carbamoíla, grupo N-(2-flúor-etil)-carbamoíla, grupo N-(2-metóxi-etil)carbamoíla, grupo N-(carbóxi-metil)-carbamoíla, grupo N-(2amino-etil)-carbamoíla, grupo N-(2-amidino-etil)-carbamoíla, grupo N,N-dimetil-carbamoíla, grupo N,N-dietil-carbamoíla, grupo N-etil-N-metil-carbamoíla, grupo N-isopropil-N-metilcarbamoíla, grupo N-isopropil-N-metil-carbamoíla, grupo Nmetil-N-propil-carbamoíla, grupo N-(2-hidróxi-etil)-N-metilcarbamoíla, grupo N-(2-flúor-etil)-N-metil-carbamoíla, grupo N,N-bis-(2-hidróxi-etil)-carbamoíla, grupo N,N-bis-(2-flúoretil) -carbamoíla, grupo N-(2-metóxi-etil)-N-metilcarbamoíla, grupo N-carbóxi-metil-N-metil-carbamoíla, grupo N,N-bis-(2-amino-etil)-carbamoíla, grupo azetidinocarbonila, grupo 3-metóxi-azetidino-carbonila, grupo 3de 08/10/2018, pág. 105/857 grupo pirrolidinocarbonila, hidróxi-azetidino-carbonila, grupo 3-hidróxi-pirrolidinocarbonila, grupo 3-flúorpirrolidinocarbonila, grupo 3,4-dimetóxipirrolidinocarbonila, grupo piperidinocarbonila, grupo piperazinocarbonila, grupo morfolinocarbonila, grupo (tetraidropiran-4-il)-carbonila, grupo benzoíla, grupo piridilcarbonila, grupo N-metil-carbamoil-metila, grupo Nmetil-carbamoil-etila, grupo N-etil-carbamoil-metila grupo N-(2-flúor-etil)-carbamoil-metila, grupo N-(2-metóxi-etil)carbamoil-metila, grupo N,N-dimetil-carbamoil-metila, grupo N,N-dimetil-carbamoil-etila, grupo N-(2-flúor-etil)-N-metilcarbamoil-metila, grupo N-(2-metóxi-etil)-N-metil-carbamoilmetila, grupo N,N-dimetil-carbamoilóxi-metila, grupo 2-(Netil-N-metil-carbamoilóxi)-etila, grupo metil-sulfonilamino, grupo etil-sulfonil-amino, grupo metil-sulfonilamino-metila, grupo metil-sulfonil-amino-etila, grupo acetila, grupo propionila, grupo isobutirila, grupo 2metóxi-etóxi-carbonila, grupo triflúor-acetila, grupo N,Ndimetil-amino-acetila, grupo N-etil-N-metil-amino-acetila, grupo hidróxi-acetila, grupo 1,l-dimetil-2-hidróxi-etilcarbonila, grupo metóxi-acetila, grupo 1,1-dimetil-2-metóxietil-carbonila, grupo amino-carbotioíla, grupo (dimetilamino) -carbotiíla, grupo 2-metóxi-eteno-tioíla, e similares.
Como descrito acima, prefere-se que R3 seja um átomo de hidrogênio, e R4 seja um desses substituintes especificados, de preferência, um grupo N,N-dialquilcarbamoí la, que pode ter um substituinte no(s) grupo(s) alquila, e de preferência, particularmente, um grupo N,Nde 08/10/2018, pág. 106/857 dimetil-carbamoíla. Entretanto, R3 e R4 não estão de forma alguma limitados a esses substituintes específicos.
Grupo T°
O grupo T° representa um grupo carbonila ou um grupo tiocarbonila, sendo preferido o grupo carbonila.
Grupo T1 grupo T1 representa um grupo carbonila, grupo sulfonila, grupo -C(=0)-C(=0)-N(R')-, grupo -C(=S)-C(=0)N(R')-, grupo -C(=0)-C(=S)-N(R')-, grupo -C(=S)-C(=S)N(R')-, onde R' significa um átomo de hidrogênio, grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=0)-A1N(R)-, onde A1 significa um grupo alquileno que tem 1 a 5 átomos de carbono, que pode ser substituído, e R significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=0)-NH-, grupo -C(=S)-NH-, grupo C(=0)-NH-NH-, grupo -C(=0)-A2-C(=0)-, onde A2 significa uma ligação simples ou um grupo alquileno que tem 1 a 5 átomos de carbono, grupo C(=0)-A3-C(=0)-NH-, onde A3 significa um grupo alquileno que tem 1 a 5 átomos de carbono, grupo C (=0)-C (=N0Ra)-N (Rb)-, grupo -C (=S)-C (=N0Ra)-N (Rb)-, onde Ra significa um átomo de hidrogênio, um grupo alquila ou grupo alcanoíla, e Rb significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=0)-N=N-, grupo -C(=S)-N=N-, grupo -C (=NORC)-C (=0)-N (Rd)-, onde Rc significa um átomo de hidrogênio, um grupo alquila, grupo alcanoíla, arila ou aralquila, e Rd significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C (=N-N (Re) (Rf)-C (=0)-N (R9)-, onde Re e Rf de 08/10/2018, pág. 107/857 significam, cada um independentemente do outro, um átomo de hidrogênio, um grupo alquila, grupo alcanoíla, ou grupo alquil-(tiocarbonila), e R9 denota um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, ou grupo tiocarbonila.
No grupo acima, o grupo alquileno que tem 1 a 5 átomos de carbono em A1, A2 é A3 significa um grupo alquileno linear, ramificado ou cíclico que tem 1 a 5 átomos de carbono, e seus exemplos incluem os grupos metileno, etileno, propileno, ciclo-propileno, 1,3-ciclo-pentileno, e similares. O grupo alquila em R', R, Ra, Rb, Rc, Rd, Re, Rf e R9 significa um grupo alquila linear, ramificado ou cíclico, tendo 1 a 6 átomos de carbono, e seus exemplos incluem os grupos metila, etila, e similares. O grupo alcóxi significa um grupo alcóxi linear, ramificado ou cíclico, tendo 1 a 6 átomos de carbono, e seus exemplos incluem os grupos metóxi, etóxi, e similares.
Em Ra, Rc, Re e Rf, o grupo alcanoíla significa um grupo constituído de um grupo alquila linear, ramificado ou cíclico, tendo 1 a 6 átomos de carbono e um grupo carbonila, e seus exemplos incluem os grupos acetila, propionila, e similares.
Em Rc, o grupo arila significa um grupo que tem 6 a 14 átomos de carbono, e seus exemplos incluem o grupo fenila, grupo naftila, e similares. O grupo aralquila significa um grupo tal como um grupo alquila linear, ramificado ou cíclico, tendo 1 a 6 átomos de carbono, que está ligado a um grupo arila que tem 6 a 14 átomos de de 08/10/2018, pág. 108/857
100 carbono, e seus exemplos incluem os grupos benzila, fenetila, e similares.
Como T1, prefere-se um grupo carbonila, grupo C(=O)-C(=O)-N(R')-, grupo -C(=S)-C(=0)-N(R')-, grupo -C(=0)5 C (=S)-N (R')-, grupo -C(=S)-C(=S)-N(R')-, e grupo -C(=0)-CH2N(R)-, sendo particularmente preferido um grupo carbonila, grupo -C(=0)-C(=0)-N(R')-, grupo -C(=S)-C(=0)-N(R')-, grupo -C(=O)-C(=S)-N(R')-, e o grupo -C(=S)-C(=S)-N(R')-.
Grupo R1 e Grupo R2
R1 e R2 são, cada um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, de preferência, um átomo de hidrogênio ou um grupo alquila, e mais preferivelmente, um átomo de hidrogênio.
Em R1 e R2, o grupo alquila significa um grupo alquila linear, ramificado ou cíclico, tendo 1 a 6 átomos de carbono, e seus exemplos incluem os grupos metila, etila, e similares. 0 grupo alcóxi significa um grupo alcóxi linear, ramificado ou cíclico, tendo 1 a 6 átomos de carbono, e seus exemplos incluem os grupos metóxi, etóxi, e similares. R1 e R2 são, de preferência, cada um independentemente do outro, um átomo de hidrogênio ou um grupo alquila, e mais preferivelmente, ambos são átomos de hidrogênio.
Quando T1 é um grupo carbonila ou sulfonila, e Q5 no grupo Q3 é um grupo alquileno que tem 1 a 8 átomos de carbono ou um grupo alquenileno que tem 2 a 8 átomos de carbono, Q4 é, de preferência, um grupo (b), (f) , (g) , (h) , (i), (j), (k) e (1) entre os 12 grupos supradescritos, desde
Petição 870180138821, de 08/10/2018, pág. 109/857
101 que N no grupo (f) indique que 2 átomos de carbono do anel substituídos com R19 tenham sido substituídos com um átomo de nitrogênio.
|
|
Quando T1 é um |
grupo carbonila ou |
sulfonila, e |
Q5 |
|
5 no grupo |
Q3 é um grupo |
alquileno que tem 1 |
a 8 átomos |
de |
|
carbono |
ou um grupo alquenileno que tem 2 |
a 8 átomos |
de |
|
carbono, |
o subsituinte |
no grupo Q5 é, de |
preferência, |
um |
grupo N-alquil-carbamoíla ou N,N-dialquil-carbamoíla.
Quando T1 é um grupo -C(=0)-C(=0)-N(R')-, grupo 10 C(=S)-C(=O)-N(R')-, grupo -C(=O)-C(=S)-N(R')-, ou grupo C (=S) -C (=S) —N (R')-, e Q5 no grupo Q3 é um grupo alquileno que tem 1 a 8 átomos de carbono ou um grupo alquenileno que tem 2 a 8 átomos de carbono, Q4 é, de preferência, um grupo (i), (j) ou (k) entre os 12 grupos supradescritos.
Quando T1 é um grupo -C(=0)-C(=0)-N(R')-, grupo C(=S)-C(=O)-N(R')-, grupo -C(=0)-C(=S)-N(R')-, ou grupo C (=S) -C (=S) —N (R')-, e Q5 no grupo Q3 é um grupo alquileno que tem 1 a 8 átomos de carbono ou um grupo alquenileno que tem 2 a 8 átomos de carbono, o substituinte no grupo Q5 é, de preferência, um grupo N-alquil-carbamoíla ou N,Ndialquil-carbamoíla.
Uma característica dos compostos da presente invenção, representados pela fórmula genérica (1), seus sais, seus solvatos, ou seus N-óxidos, reside em uma combinação do grupo T1 e do grupo Q3. A combinação é dividida aproximadamente nos dois seguintes casos (I) e (II) :
(I) um caso no qual T1 é um grupo carbonila,
Petição 870180138821, de 08/10/2018, pág. 110/857
102 sulfonila ou tiocarbonila, e Q3 é o seguinte grupo:
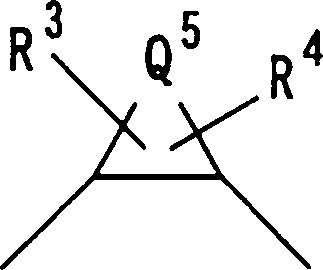
onde Q5 significa um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-, -NH-, -0NH-, -NH-NH-, -S-NH-, -SO-NH- ou -SO2~NH; e (II) um caso no qual T1 é um grupo -C (=0)-C (=0)N(R')-, grupo -C(=S)-C(=0)-N(R')grupo -C(=0)-C(=S)-N(R'), grupo —C(=S)-C(=S)-N(R')-, onde R' significa um átomo de hidrogênio, grupo hidroxila, grupo alquila ou grupo alcóxi, grupo —C(=0)-A1-N(R)-, onde A1 significa um grupo alquileno que tem 1 a 5 átomos de carbono, que pode ser substituído, e R significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=0)-NH-, grupo C(=S)-NH-, grupo -C(=0)-NH-NH-, grupo -C (=0)-A2-C(=0)-, onde A2 significa uma ligação simples ou um grupo alquileno que tem 1 a 5 átomos de carbono, grupo C (=0)-A3-C (=0)-NH-, onde A3 significa um grupo alquileno que tem 1 a 5 átomos de carbono, grupo -C (=0)-C (=N0Ra)-N (Rb)grupo -C (=S)-C (=NORa) N(Rb)-, onde Ra significa um átomo de hidrogênio, um grupo alquila ou grupo alcanoíla, e Rb significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=0)-N=N-, grupo -C(=S)-N=N-, grupo de 08/10/2018, pág. 111/857
103
C (=NORC) —C (=0) -N (Rd)-, onde Rc significa um átomo de hidrogênio, um grupo alquila, grupo alcanoíla, arila ou aralquila, e Rd denota um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=N5 N(Re) (Rf)-C (=0)-N (R9)-, onde Re e Rf significam, cada um independentemente do outro, um átomo de hidrogênio, um grupo alquila, grupo alcanoíla, ou grupo alquil-(tiocarbonila), e R9 denota um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, ou grupo tiocarbonila, e Q3 é o seguinte grupo:
onde Q5 significa um grupo alquileno que tem 1 a 8 átomos de carbono, um grupo alquenileno que tem 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-, -NH-, -0NH-, -NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH.
Nos casos (I) e (II), os seguintes exemplos (i) e (ii) são mencionados como preferidos:
|
20 |
(i) |
um exemplo no qual |
o |
grupo R1 e o grupo |
R2 |
|
são, cada |
um |
independentemente |
do |
outro, um átomo |
de |
|
hidrogênio |
ou |
um grupo alquila, |
o |
grupo Q1 é um grupo |
hidrocarboneto bicíclico ou tricíclico fundido, saturado ou
Petição 870180138821, de 08/10/2018, pág. 112/857
104 insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, o grupo Q2 é uma ligação simples, o grupo Q5 no grupo Q3 é um grupo -(CH2)mCH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou 1, e A tem o mesmo significado que aquele definido acima, o grupo Q4 é selecionado entre os 9 grupos (a) até (h) e (1) dos 12 grupos supradescritos, o grupo T° é um grupo carbonila ou um grupo tiocarbonila, e o grupo T1 é um grupo carbonila ou um grupo sulfonila; e (ii) um exemplo no qual, na fórmula genérica (1) , os grupos R1 e R2 são, cada um independentemente do outro, um átomo de hidrogênio ou um grupo alquila, o grupo Q1 é um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, o grupo Q2 é uma ligação simples, o grupo Q5 no grupo Q3 é um grupo alquileno que tem 3 a 6 átomos de carbono ou um grupo (CH2) m-CH2-A-CH2-(CH2) n-, onde m e n são, um independentemente do outro, 0 ou 1, e A tem o mesmo significado que aquele definido acima, o grupo Q4 é selecionado entre 3 grupos (i), (j) e (k) dos 12 grupos supradescritos, o grupo T° é um grupo carbonila ou um grupo tiocarbonila, e o grupo T1 é um grupo -C(=0)-C(=0)-N(R')-, grupo -C(=S)-C(=0)-N(R')-, grupo -C(=O)-C(=S)-N(R')-, ou um grupo -C(=S)-C(=S)-N(R')-.
Os estereoisômeros ou isômeros ópticos derivados de um átomo de carbono assimétrico podem estar presentes nos de 08/10/2018, pág. 113/857
105 compostos da presente invenção representados pela fórmula genérica (1) . Entretanto, estes estereoisômeros, isômeros ópticos, e suas misturas, estão todos incluídos na presente invenção.
Até agora nenhuma limitação específica foi imposta sobre os sais dos compostos da presente invenção representados pela fórmula genérica (1) , pois eles são sais de uso farmacêutico. Entretanto, seus exemplos específicos incluem sais de ácidos minerais, tais como cloridratos, bromidratos, iodetos ácidos, fosfatos, nitratos e sulfatos; benzoatos; sulfonatos orgânicos tais como metano-sulfonatos, 2-hidróxi-etano-sulfonatos e p-tolueno-sulfonatos; e carboxilatos orgânicos, tais como acetatos, propanoatos, oxalatos, malonatos, succinatos, glutaratos, adipatos, tartaratos, maleatos, malatos e mandelatos. No caso em que os compostos representados pela fórmula genérica (1) têm um grupo ácido, eles podem ser sais de íons de metais alcalinos ou de íons de metais alcalino-terrosos. Nenhuma limitação específica foi imposta sobre seus solvatos até agora, pois eles são solvatos de uso farmacêutico. Como seus exemplos específicos, entretanto, podem ser mencionados hidratos e solvatos com etanol. Quando um átomo de nitrogênio está presente na fórmula genérica (1) , tal composto pode ser convertido em um seu N-óxido.
Na qualidade de compostos de acordo com a presente invenção preferidos, estão os compostos descritos nos exemplos que se seguem e seus sais, bem como os seguintes compostos e seus sais:
de 08/10/2018, pág. 114/857
106
1) 3-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}ciclo-hexil)-[1,6]-naftiridino-7carboxamida;
2) 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}ciclo-hexil)-4-flúor-cinolino-3-carboxamida;
3) 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)10 carbonil]-amino}ciclo-hexil)-4a,8a-diidro-4H-l,2,4benzoxadiazino-3-carboxamida;
4) N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]amino}ciclo-hexil)-6-flúor-4-oxo-l,4-diidroquinolino-215 carboxamida;
5) 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}ciclo-hexil)-5-oxo-4,5-diidro-lH-l, 3, 4benzotriazepino-2-carboxamida;
6) 6-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}ciclo-hexil)-4-oxo-3,4-diidro-2(1H)cinolino-carboxamida;
7) 6-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-225 {[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}ciclo-hexil)-1,2,3, 4-tetraidroquinolino-2carboxamida;
8) N-{ (IR, 2S,5S)-2-{[3-(3-cloro-fenil)-2-propinoil]-amino}Petição 870180138821, de 08/10/2018, pág. 115/857
107
5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
9) N-{(IR,2S,5S)-2-[(4-cloro-benzoil)-amino]-5-[(dimetilamino) -carbonil]-ciclo-hexil}-5-metil-4,5,6,75 tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
10) N-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}5-[(dimetil-amino)-carbonil]-ciclo-hexil}-6-metil-5,6,7,8tetraidro-4H-tiazolo[4,5-d]azepino-2-carboxamida;
11) 5-cloro-N-[(IS,2R,4S)-4-[(dimetil-amino)-carbonil]-210 ({[5-(3-pirrolidinilóxi)-tiazol-2-il]-carbonil}-amino)ciclo-hexil]-indol-2-carboxamida;
12) N1-(4-cloro-fenil)-N2-((IS, 2R) -2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil) -etanodiamida;
13) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R)-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]amino}-ciclo-hexil)-etanodiamida;
14) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R)-2-{[(5-metil-5,6diidro-4H-pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo20 hexil)-etanodiamida;
15) N1-(4-cloro-fenil)-N2-((IS, 2R) -2-{[(5-metil-5, 6-diidro4H-pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil)etanodiamida;
16) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R)-2-{[(5-metil-5,625 diidro-4H-pirrolo[3, 4-d]tiazol-2-il)-carbonil]-amino}-ciclopentil)-etanodiamida;
17) N1-(4-cloro-fenil)-N2-((IS, 2R) -2-{[(5-metil-5, 6-diidro4H-pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-cicloPetição 870180138821, de 08/10/2018, pág. 116/857
108 pentil)-etanodiamida;
18) N1-(4-cloro-fenil)-N2-((IS, 2R)-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-cicloheptil)-etanodiamida;
19) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R)-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]amino}-ciclo-heptil)-etanodiamida;
20) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R)-2-{[(5-metil-5,6diidro-4H-pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo10 heptil)-etanodiamida;
21) N1-(4-cloro-fenil)-N2-((IS, 2R) -2-{[(5-metil-5,6-diidro4H-pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-cicloheptil) -etanodiamida;
22) N1-(5-cloro-6-metil-piridin-2-il)-N2-((IS, 2R, 4S)-415 [(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil)-etanodiamida;
23) N1-(5-cloro-3-metil-piridin-2-il)-N2-((IS, 2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,720 tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil)-etanodiamida;
24) N1-(5-cloro-4-metil-piridin-2-il)-N2-((IS, 2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclo25 hexil)-etanodiamida;
25) N1-(5-cloro-3-hidróxi-fenil)-N2-((IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
Petição 870180138821, de 08/10/2018, pág. 117/857
109
26) N1-(4-cloro-2-hidróxi-fenil)-Ν2-((IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
27) N1-[4-cloro-2-(flúor-metil)-fenil]-N2-((IS, 2R, 4S)-45 [(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil)-etanodiamida;
28) N1-[4-cloro-2-(metóxi-fenil)-fenil]-N2-((IS, 2R, 4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,710 tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil)-etanodiamida;
29) N-{(IR,2S,5S)-2-({[1-(4-cloro-anilino)-ciclo-propil]carbonil}amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida; 15 30) N1-(5-cloro-piridin-2-il)-N2-((IR, 2R, 4R)-4-(hidróximetil)-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin2-il)-carbonil]amino}-ciclo-pentil)-etanodiamida;
31) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-4-(hidróximetil)-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin20 2-il)-carbonil]-amino}-ciclo-pentil)-etanodiamida;
32) N1—((3R,4S)-l-acetil-3-{[(5-metil-4,5, 6, 7tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}piperidin-4-il)-N2-(5-cloro-piridin-2-il)-etanodiamida;
33) N1-(5-cloro-piridin-2-il)-N2-((3R, 4S)-1-(metil25 sulfonil)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-piperidin-4-il)etanodiamida;
34) N1-](IS,2R,4S)-2-{[(3-cloro-benzotiofen-2-il)-carbonil]Petição 870180138821, de 08/10/2018, pág. 118/857
110 amino}-4-[(dimetil-amino)-carbonil]-ciclo-hexil}-N2- (5cloro-piridin-2-il)-etanodiamida;
35) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-4-[(dimetilamino) -carbotioil]-2-{[(5-metil-4,5,6,75 tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil) -etanodiamida;
36) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbotioil]-amino}-ciclo-hexil)10 etanodiamida;
37) N1-(5-cloro-piridin-2-il)-N2-((3R, 4S)-1-(2-metóxietanotioil)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-piperidin-4-il)etanodiamida;
38) N1-(5-cloro-piridin-2-il)-N2-((3R, 4S)-1-(2-metóxiacetil)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin2-il)-carbotioil]-amino}-piperidin-4-il)-etanodiamida;
39) N-[(3R, 4S)-4-({2-[(5-cloro-piridin-2-il)-amino]-2oxoetanotioil}-amino)-1-(2-metóxi-acetil)-piperidin-3-il]-520 metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
40) N-[(3R,4S)-4-({2-[(5-cloro-piridin-2-il)-amino]-2tioxoacetil}-amino)-1-(2-metóxi-acetil)-piperidin-3-il]-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
41) N1-(5-cloro-fenil)-N2-((3R, 4S) -1-(2-metóxi-etanotioil)25 3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}-piperidin-4-il)-etanodiamida;
42) N1-(5-cloro-fenil)-N2-((3R, 4S)-1-(2-metóxi-acetil)-3{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)Petição 870180138821, de 08/10/2018, pág. 119/857
111 carbotioil]-amino}-piperidin-4-il)-etanodiamida;
43) N-[(3R,4S)-4-{[2-[(4-cloro-anilino)-amino]-2oxoetanotioil]-amino}-l-(2-metóxi-acetil)-piperidin-3-il]-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
44) N-[(3R,4S)-4-({2-[(4-cloro-fenil)-amino]-2-tioxoacetil}amino)-1-(2-metóxi-acetil)-piperidin-3-il]-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
45) N1-((IS,2R,4S)-4-(1-azetidinil-carbonil)-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]10 amino}-ciclo-hexil)-N2-(5-cloro-piridin-2-il)-etanodiamida;
46) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]amino}-4-(1-pirrolidinil-carbonil)-ciclo-hexil]etanodiamida;
47) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]amino}-4-(1-piperidinil-carbonil)-ciclo-hexil]-etanodiamida;
48) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]20 amino}-4-(4-morfolinil-carbonil)-ciclo-hexil]-etanodiamida;
49) N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-4-[(metilamino)-carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
50) N1-](IR,2S,5S)-2-({2-[(6-cloro-piridazin-3-il)-amino]-225 oxoetanotioil}-amino)-5-[(dimetil-amino)-carbonil]-ciclohexil }-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida;
51) N1-(5-bromo-fenil)-N2-((3R, 4S)-1-(2-metóxi-acetil)-3Petição 870180138821, de 08/10/2018, pág. 120/857
112 {[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}-piperidin-4-il)-etanodiamida;
52) N1-(5-cloro-piridin-2-il)-N2-((3R, 4S)-1-(2-metóxiacetil)-3-{[4-(piridin-4-il)-benzoil]-amino}-piperidin-45 il)-etanodiamida;
53) N1-(5-cloro-piridin-2-il)-N2-[(3R, 4S)-1-(2-metóxiacetil)-3-({[2-(piridin-4-il)-pirimidin-5-il]-carbonil}amino)-piperidin-4-il]-etanodiamida;
54) N1-(5-cloro-piridin-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetil10 amino)-carbonil]-2-({[2-(piridin-4-il)-pirimidin-5-il]carbonil}-amino)-ciclo-hexil]-etanodiamida;
55) N-{(IR,2S,5S)-2-{[2-(4-cloro-anilino)-2oxoetano(metóxi)-imidoil]-amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,415 c]piridino-2-carboxamida;
56) N-{(IR,2S,5S)-2-{[2-(4-cloro-anilino)-2-(metóxi-imino)acetil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5metil-4,5, 6, 7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
57) N1-(5-cloro-piridin-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetil20 amino)-carbonil]-2-{[(4,4,5-trimetil-5,6-diidro-4Hpirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil]etanodiamida;
58) N1-(5-cloro-piridin-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(4,4-etileno-5-metil-5,6-diidro-4H25 pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil]etanodiamida;
59) N—{(IR,2S,5S)-2-({[(E)-2-(4-cloro-fenil)-etenil]sulfonil}-amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexil}Petição 870180138821, de 08/10/2018, pág. 121/857
113
5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida;
60) N-{(IR,2S,5S)-2-{[(4-cloro-benzil)-sulfonil]-amino}-5[(dimetil-amino)-carbonil]-ciclo-hexil}-5-metil-4,5,6,75 tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
61) N-{(IR,2S,5S)-2-[(2-{[(4-cloro-fenil)-sulfonil]-amino}acetil)-amino]-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
62) N-{(IR,2S,5S)-2-({2-[(5-cloro-pirimidin-2-il)-amino]-210 oxoetanotioil}-amino)-5-[(dimetil-amino)-carbonil]-ciclohexil }-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida;
63) N-{(IR,2S,5S)-2-({2-[(5-cloro-pirazin-2-il)-amino]-2oxoetanotioil}-amino)-5-[(dimetil-amino)-carbonil]-ciclo15 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida;
64) N—[(IR,2S,5S)-5-[(dimetil-amino)-carbonil]-2-({2-[(5flúor-2-tienil)-amino]-2-oxoetanotioil}-amino)-5-ciclohexil]-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-220 carboxamida;
65) N-{(IR,2S,5S)-2-{[2-(3-amino-4-cloro-anilino)-2oxoetanotioil]-amino}-5-[(dimetil-amino)-carbonil]-ciclohexil }-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida;
66) N1-(4-cloro-tiazol-2-il)-N2-((IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
67) N1—((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5Petição 870180138821, de 08/10/2018, pág. 122/857
114 metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}-ciclo-hexil)-N2-(3-flúor-fenil)etanodiamida;
68) N1—((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(55 metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}-ciclo-hexil)-N2-fenil-etanodiamida;
69) N1—((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}-ciclo-hexil)-N2-(piridin-2-il)10 etanodiamida;
70) N1-(5-cloro-piridin-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5,6,6-trimetil-5,6-diidro-4Hpirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil]etanodiamida;
71) N1-(5-cloro-piridin-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(4,4,5,6,6-pentametil-5,6-diidro-4Hpirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil]etanodiamida;
72) N1-(5-cloro-piridin-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetil20 amino)-carbonil]-2-{[(2-metil-2,3-diidro-tiazolo[5,4-d]isoxazol-5-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
73) N1-(5-cloro-piridin-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(2-metil-2,3-diidro-tiazolo[4,5-d]isoxazol-5-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
74) N1-(5-cloro-2-furil)-N2-[(IS, 2R, 4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5, 4c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
75) N1-(5-cloro-oxazol-2-il)-N2-[(IS, 2R, 4S)-4-[(dimetilPetição 870180138821, de 08/10/2018, pág. 123/857
115 amino)-carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida;
76) N1-(5-cloro-lH-imidazol-2-il)-N2-[(IS, 2R, 4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,75 tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil)-etanodiamida;
77) N-{(IR,2S,5S)-2-{[2-(4-cloro-anilino)-l-etóxi-imino-2oxoetil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
78) N-{(IR,2S,5S)-2-{[2-(4-cloro-anilino)-l-fenóxi-imino-2oxoetil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
79) N-{(IR,2S,5S)-2-{[1-(benzilóxi-imino-2-(4-cloroanilino) -oxoetil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo15 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida;
80) N-{(IR,2S,5S)-2-({2-(4-cloro-anilino)-l-hidrazono-2oxoetil}-amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
81) N-{(IR,2S,5S)-2-({2-(4-cloro-anilino)-1-(2-metilhidrazono)-2-oxoetil}-amino)-5-[(dimetil-amino)-carbonil]ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5, 4c]piridino-2-carboxamida;
82) N-{(IR,2S,5S)-2-({2-(5-cloro-piridin-2-il)-amino}-l25 (2,2-dimetil-hidrazono)-2-oxoetil-amino)-5-[(dimetil-amino)carbonil]-ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5, 4c]piridino-2-carboxamida;
83) N-{(IR,2S,5S)-2-{[2-(4-cloro-anilino)-l-metil-imino-2Petição 870180138821, de 08/10/2018, pág. 124/857
116 oxoetil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida;
84) N-{(IR,2S,5S)-2-{[1-(2-acetil-hidrazono)-2-(4-cloroanilino)-2-oxoetil]-amino}-5-[(dimetil-amino)-carbonil]5 ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5, 4c]piridino-2-carboxamida;
85) N-{(IR,2S,5S)-2-({2-(4-cloro-anilino)-1-[(2-etanotioilhidrazono)-2-oxoetil]-amino}-5-[(dimetil-amino)-carbonil]ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5, 4-c] piridino-2-carboxamida; e
86) N-{(IR,2S,5S)-2-{[(E)-3-(5-cloro-piridin-2-il)-2propenoil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida.
O processo de preparação dos derivados diamínicos (1) de acordo com a presente invenção será agora doravante descrito.
Processo de Preparação 1
Um composto representado pela fórmula genérica 20 (1), um seu sal, um seu solvato, ou um seu N-óxido, pode ser preparado, por exemplo, de acordo com o seguinte processo:
Q4-CO2H (3)
HN (R1) -Q3-NHR2 -► HN (R1) -Q3-N (R2) -T4-Q4 (2) (4) q1-q2-co2h (5)
-► Q1-Q2-CO-N (R1)-Q3-N (R2)-T4-Q4
d) onde Q1, Q2, Q3, Q4, R1 e R2 têm os mesmos significados que
Petição 870180138821, de 08/10/2018, pág. 125/857
117 aqueles definidos acima, e T1 representa um grupo carbonila.
Um anidrido de ácido misto, halogeneto de ácido, éster ativado, ou similares, que é derivado a partir do ácido carboxílico (3), pode reagir com a diamina (2), dando o composto (4). O composto (4) resultante pode reagir com o ácido carboxílico (5) sob as mesmas condições, dando o composto (1), de acordo com a presente invenção. Nas etapas de reação acima, os reagentes e condições, que são usados genericamente na síntese de peptídeos, podem ser aplicados. O anidrido de ácido misto pode ser preparado, por exemplo, pela reação de um cloro-formiato, tal como o cloro-formiato de etila ou cloro-formiato de isobutila, com o ácido carboxílico (3), na presença de uma base. O halogeneto de ácido pode ser preparado tratando o ácido carboxílico (3) com um halogeneto de ácido, tal como o cloreto de tionila ou cloreto de oxalila. O éster ativado inclui vários tipos de ésteres. Tal éster pode ser preparado, por exemplo, pela reação de um fenol, tal como p-nitro-fenol, N-hidróxibenzotriazol ou N-hidróxi-succinimida, com o ácido carboxílico (3) , usando um agente condensador, tal como Ν,N'-diciclo-hexil-carbodiimida ou cloridrato de l-etil-3(3-dimetil-amino-propil)-carbodiimida. O éster ativado pode ser preparado também pela reação do ácido carboxílico (3) com triflúor-acetato de pentaflúor-fenila, ou similares, pela reação do ácido carboxílico (3) com hexaflúor-fosfito de 1-benzotriazolilóxi-tripirrolidino-fosfônio, reação do ácido carboxílico (3) com cianofosfato de dietila (método de Shioiri), reação do ácido carboxílico (3) com de 08/10/2018, pág. 126/857
118 trifenilfosfina e dissulfeto de 2,2'-dipiridila (método de Mukaiyama), ou similares. O anidrido de ácido misto, halogeneto de ácido ou éster ativado, do ácido carboxílico (3), assim obtido, pode reagir com a diamina (2) em uma temperatura entre -78 °C e 150 °C, na presença de uma base apropriada, em um solvente inerte, dando o composto (4) . O composto (4) assim obtido pode reagir com um anidrido de ácido misto, halogeneto de ácido ou éster ativado, do ácido carboxílico (5) , sob as mesmas condições, dando o composto (1) de acordo com a presente invenção. Os reagentes e as condições de reação na reação do composto (4) com o ácido carboxílico (5) são iguais àquelas da reação da diamina (2) com o ácido carboxílico (3).
Como exemplos específicos da base usada em cada uma das etapas acima, podem ser mencionados os carbonatos de metais alcalinos ou metais alcalino-terrosos, tais como carbonato de sódio e carbonato de potássio, alcóxidos de metais alcalinos, tais como etóxido de sódio e butóxido de potássio, hidróxidos de metais alcalinos tais como hidróxido de sódio e hidróxido de potássio, e hidretos de metais alcalinos ou metais alcalino-terrosos, tais como hidreto de sódio e hidreto de potássio; bases organometálicas exemplificadas por alquil-lítio, tal como n-butil-lítio, e dialquil-amino-lítio, tal como diisopropilamida-lítio; bases organometálicas exemplificadas por bis-(silil)-amina, tal como bis-(trimetil-silil)-amida-lítio; e bases orgânicas tais como piridina, 2,6-lutidina, colidina, 4-dimetil-aminopiridina, trietil-amina, N-metil-morfolina, diisopropilde 08/10/2018, pág. 127/857
119 etil-amina, e diazabiciclo[5.4.0]-undec-7-eno (DBU).
Os exemplos do solvente inerte usado nesta reação incluem solventes do tipo halogeneto de alquila, tais como dicloro-metano, clorofórmio e tetracloreto de carbono, solventes etéreos tais como tetraidrofurano, 1,2-dimetóxietano e dioxano, solventes aromáticos tais como benzeno e tolueno, e solventes amídicos, tais como N,N-dimetilformamida, N,N-dimetil-acetamida e N-metil-pirrolidin-2-ona. Além destes solventes, um solvente do tipo sulfóxido, tal como sulfóxido de dimetila ou sulfolano, um solvente cetônico, tal como acetona ou metil-etil-cetona, ou similares, pode ser usado em alguns casos.
Processo de Preparação 2
O composto (1), de acordo com a presente invenção, pode ser preparado também com o seguinte processo:
Boc-ON (6)
HN (R1)-Q3-NHR2 -► HN (R1)-Q3-N (R2)-Boc (2) (7) q1-q2-co2h (5) H+
-► Q1-Q2-CO-N (R1) —Q3—N (R2) -Boc -► (8)
Q4-CO2H (3)
Q1-Q2-CO-N (RI) -Q3-HNR2 -► Q1-Q2CO-N (R1) -Q3-N (R2) -U-Q4 (9) (1)
Petição 870180138821, de 08/10/2018, pág. 128/857
120 onde Q1, Q2, Q3, Q4, R1 e R2 têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo carbonila, Boc representa um grupo t-butóxi-carbonila, e Boc-ON representa um grupo 2-(t-butóxi-carbonilóxi-imino)-2-fenilacetonitrila.
Como descrito acima, a diamina (2) é tratada com Boc-ON (6), para preparar o composto (7), onde um dos dois grupos amino foi protegido com o grupo t-butóxi-carbonila. O composto (7) resultante reage com o ácido carboxílico (5) e produz o composto (8). O composto (8) é tratado sucessivamente com um ácido, para dar o composto (9) . O composto (9) reage então com o ácido carboxílico (3), dando o composto (1) de acordo com a presente invenção. O composto (7) pode ser preparado por uma reação em uma temperatura entre -10 °C e 40 °C, na presença de trietilamina, em um solvente tal como dicloro-metano. A reação do composto (7) com o anidrido de ácido misto, halogeneto de ácido ou éster ativado, do ácido carboxílico (5) , é conduzida usando os mesmos reagentes e as mesmas condições de reação descritas no Processo de Preparação 1, com o que o composto (8) pode ser preparado. O composto (8) resultante é tratado com ácido triflúor-acético, ou similares, em uma temperatura entre -2 0 °C e 7 0 °C, como o que a amina (9) pode ser preparada. Na reação da amina (9) resultante com o ácido carboxílico (3), podem ser usados reagentes e condições de reação iguais àqueles descritos no Processo de Preparação 1.
A propósito, o grupo t-butóxi-carbonila do de 08/10/2018, pág. 129/857
121 composto (7) pode ser trocado por outros grupos protetores de amino. Neste caso, o reagente (6) também é trocado por outros reagentes, e as condições da reação, e outros parâmetros similares, devem ser usados de acordo com os reagentes. Como exemplos de outros grupos protetores para os grupos amino, podem ser mencionados um grupo acetila, grupos alcóxi-carbonila, tais como os grupos metóxicarbonila e etóxi-carbonila, grupos aril-metóxi-carbonila, tais como benzilóxi-carbonila, p-metóxi-benzilóxi-carbonila e grupos p- ou o-nitro-benzilóxi-carbonila, grupos arilmetila, tais como os grupos benzila e trifenil-metila, grupos aroíla, tal como o grupo benzoíla, e grupos arilsulfonila, tais como os grupos 2,4-dinitro-benzeno-sulfonila e o-nitro-benzeno-sulfonila. Estes grupos protetores podem ser escolhidos para uso de acordo com a natureza e outros parâmetros do composto cujo grupo amino deve ser protegido. Ao deixar esse grupo protetor, os reagentes e condições podem ser empregados de acordo com o grupo protetor.
Processo de Preparação 3
O composto (1), de acordo com a presente invenção, pode ser preparado reagindo a diamina (2) com halogeneto de sulfonila (10) e depois condensando o produto da reação com o ácido carboxílico (5):
HN (R1) -Q3-NHR2 (2) q4-so2-x (10)
-► HN (R1) -Q3-NR2-T1—Q4 (4)
Petição 870180138821, de 08/10/2018, pág. 130/857
122 q1-q2-co2h (5)
-► Qi-QZ-CO-N (R1) -Q3-N (R2) -T^—Q4 (D onde Q1, Q2, Q3, Q4, R1 e R2 têm os mesmos significados que aqueles definidos acima, T1 representa um grupo sulfonila, e X representa um átomo de halogênio.
A diamina (2) reage com o halogeneto de sulfonila 5 (10) em uma temperatura entre -10 °C e 30 °C, na presença de uma base tal como trietil-amina, em um solvente inerte, dando o composto (4) . O solvente inerte e a base podem ser escolhidos adequadamente para uso entre aqueles descritos no Processo de Preparação 1. O composto (4) resultante é condensado com o ácido carboxílico (5), usando os reagentes e condições descritas no Processo de Preparação 1, com o que o composto (1), de acordo com a presente invenção, pode ser preparado. O halogeneto de sulfonila (10) pode ser sintetizado em uma base apropriada, de acordo com o processo conhecido de domínio público (documentos n°® WO 96/10022 e WO 00/09480) ou um processo de acordo com ele.
Processo de Preparação 4
O composto (1), de acordo com a presente invenção, pode ser preparado também de acordo com o seguinte processo:
Q4-SO2-X (10)
Q1-Q2-CO-N (R1) -Q3-HNR2 -► Q1-Q2-CO-N (R1) -Q3-N (R2) -T4-Q4 (9) (1) onde Q1, Q2, Q3, Q4, R1, R2 e X têm os mesmos significados que
Petição 870180138821, de 08/10/2018, pág. 131/857
123 aqueles definidos acima, e T1 representa um grupo sulfonila.
Mais especificamente, a amina (9) pode reagir com o halogeneto de sulfonila (10) em uma temperatura entre -10 °C e 30 °C, na presença de uma base, em um solvente inerte, dando o composto (1) . 0 solvente inerte e a base podem ser escolhidos adequadamente para uso entre aqueles descritos no Processo de Preparação 1.
Processo de Preparação 5
Nos compostos (1), de acordo com a presente 10 invenção, os isômeros geométricos da forma trans e forma cis na relação entre a posição 1 e posição 2 estão presentes quando Q3 é o seguinte grupo:
onde R3, R4 e Q5 têm os mesmos significados que aqueles definidos acima, e os números 1 e 2 indicam posições.
Os processos de preparação de tais compostos (1), tendo a forma trans e a forma cis, serão aqui doravante descritos.
Processo de Preparação da Forma Trans
Petição 870180138821, de 08/10/2018, pág. 132/857
124
onde R3, R4 e Q5 têm os mesmos significados que aqueles definidos acima.
Como um exemplo da preparação do trans-diol (12a) a partir do alqueno cíclico (11), conhece-se a conversão a partir de, por exemplo, ciclo-hexeno em trans-ciclohexanodiol (Org. Synth. volume III, página 217, 1995). Como um exemplo da preparação da trans-diamina (2a) a partir do trans-diol (12a), relata-se a conversão a partir de Lransciclo-pentanodiol em trans-ciclo-pentano-diamina (documento n° WO 98/30574). A trans-diamina (2a) pode ser preparada a partir do alqueno cíclico (11) de acordo com esses relatórios.
A trans-diamina (2a), preparada de acordo com o processo supradescrito, pode ser convertida no composto trans (1) por qualquer um dos Processos de Preparação 1 a 4 supradescritos.
Processo de Preparação da Forma Cis
Petição 870180138821, de 08/10/2018, pág. 133/857
125
onde R3, R4 e Q5 têm os mesmos significados que aqueles definidos acima.
Como um exemplo da preparação do cis-diol (12b) a partir do alqueno cíclico (11), conhece-se a conversão a partir de, por exemplo, ciclo-hexeno em cis-ciclo-hexanodiol (J. Org. Chem. 63:6094, 1998). Como um exemplo da preparação da cis-diamina (2b) a partir do cis-diol (12b), relata-se a conversão a partir de cis-ciclo-pentanodiol em cis-ciclo-pentano-diamina (documento n2 WO 98/30574). A cis-diamina (2b) pode ser preparada a partir do alqueno cíclico (11) de acordo com esses relatórios.
A cis-diamina (2b), preparada de acordo com o processo supradescrito, pode ser convertida no composto cis (1) por qualquer um dos Processos de Preparação 1 a 4 supradescritos.
Processo de Preparação 6
Como descrito acima, a forma cis ou a forma trans
|
gerada em Q3 pode estar presente nos compostos |
(1) de acordo |
|
com a presente |
invenção, e |
assim sendo, |
os |
isômeros |
|
geométricos |
estão |
presentes. |
Além disso, |
os |
isômeros |
de 08/10/2018, pág. 134/857
126 ópticos podem estar presentes nos respectivos isômeros geométricos. 0 processo de preparação de uma substância opticamente ativa será aqui doravante descrito.
(17)
(7 a) onde Q5, R1, R2, R3 e R4 têm os mesmos significados que aqueles descritos acima, e R50 representa um grupo protetor para o grupo amino.
Com relação ao processo de preparação do derivado amino-álcool (15) opticamente ativo da forma 1,2-trans, por exemplo, o processo de preparação do 1,2-trans-2-amino10 ciclo-pentanol opticamente ativo a partir de óxido de ciclopenteno ou o processo de preparação de 1,2-trans-2-aminociclo-hexanol opticamente ativo a partir de óxido de ciclohexeno, é conhecido (Tetrahedron: Asymmetry 7:843, 1996; J.
Org. Chem. 50:4154, 1985; J. Med. Chem. 41:38, 1998).
Quando o grupo amino do derivado amino-álcool (15) opticamente ativo preparado por um processo já conhecido
Petição 870180138821, de 08/10/2018, pág. 135/857
127 como esse, ou aplicando um processo que reage com um reagente protetor apropriado, o composto (16) pode ser produzido. Como um grupo protetor correspondente a R50 no composto (16) , prefere-se, dentre os grupos protetores normais do tipo acila, um grupo alcóxi-carbonila, tal como metóxi-carbonila, etóxi-carbonila, t-butóxi-carbonila, e similares, um grupo aril-metóxi-carbonila, tal como benzilóxi-carbonila, p-metóxi-benzilóxi-carbonila, p- ou onitro-benzilóxi-carbonila, e similares, ou um grupo arilsulfonila, tal como 2,4-dinitro-benzeno-sulfonila, o-nitrobenzeno-sulfonila e similares. Quando o grupo amino é protegido com, por exemplo, um grupo t-butóxi-carbonila, o derivado amino-álcool (15) pode reagir com dicarbonato de di-t-butila em uma temperatura entre -7 8 °C e 50 °C, em um solvente inerte, dando o composto (16) . O solvente inerte pode ser escolhido adequadamente para uso entre aqueles descritos no Processo de Preparação 1.
O composto (16) pode reagir com cloreto de metanosulfonila em uma temperatura entre -78 °C e 50 °C, na presença de uma base, em um solvente inerte, dando o composto (17) . O solvente inerte pode ser escolhido adequadamente para uso entre aqueles descritos no Processo de Preparação 1. No lugar da base, prefere-se uma base orgânica tal como piridina, 2,6-lutidina, colidina, 4dimetil-amino-piridina, trietil-amina, N-metilmorfolina, diisopropil-etil-amina, e diazabiciclo[5.4.0]-undec-7-eno (DBU), e similares.
O composto (17) pode reagir com azida de sódio em de 08/10/2018, pág. 136/857
128 uma temperatura entre -10 °C e 150 °C, em um solvente apropriado, dando o composto (18). Como solvente, um solvente amida tal como N, N-dimetil-formamida, N,N-dimetilacetamida ou N-metil-pirrolidin-2-ona, um solvente alcoólico tal como metanol ou etanol, um solvente etéreo tal como tetraidrofurano, 1,2-dimetóxi-etano ou dioxano, um solvente benzenóide tal como tolueno, um halogeneto de carbono, tal como dicloro-metano, clorofórmio ou tetracloreto de carbono, acetona, sulfóxido de dimetila, ou um solvente misto de um destes solventes e água, é apropriado.
Como exemplo de um processo para converter o derivado azida (18) no composto (7a), existem muitos processos, tal como um processo de conduzir hidrogenação com catalisador de paládio, catalisador de níquel de Raney ou catalisador de platina, uma reação que usa um agente redutor tal como hidreto de lítio e alumínio, boro-hidreto de sódio ou boro-hidreto de zinco, uma reação que usa zinco na presença de cloreto de níquel ou cloreto de cobalto, uma reação que usa trifenil-fosfina, e similares. As condições apropriadas da reação podem ser selecionadas de acordo com a natureza do composto. Por exemplo, o derivado azida (18) é hidrogenado em uma temperatura entre -10 °C e 70 °C, usando 1 a 20% de paládio sobre carvão como catalisador, em um solvente apropriado, com o que o composto (7a) pode ser preparado. A pressão de hidrogênio pode ser elevada até um nível mais alto do que a pressão atmosférica. Como solvente, é apropriado usar um solvente alcoólico tal como metanol ou etanol, um solvente etéreo tal como de 08/10/2018, pág. 137/857
129 tetraidrofurano, 1,2-dimetóxi-etano ou dioxano, um solvente éster tal como acetato de etila, ácido acético, ácido clorídrico, água, uma mistura destes solventes, ou similares.
A amina opticamente ativa (7a) preparada de acordo com o processo supradescrito pode ser convertida no composto (1) opticamente ativo de acordo com o Processo de Preparação 2 supradescrito. O antípoda (1) da substância opticamente ativa (1), obtido a partir da amina opticamente ativa (7a), também pode ser preparado de acordo com um processo similar.
O composto opticamente ativo (1) pode ser preparado separando o composto (1) racêmico através de uma coluna constituída de um carreador opticamente ativo. É possível também separar o intermediário (2), (4), (7), (8) ou (9), para preparar o composto (1) racêmico através de uma coluna constituída de um carreador opticamente ativo, para isolar o intermediário (2), (4), (7), (8) ou (9) opticamente ativo, e depois preparar o composto (1) opticamente ativo de acordo com qualquer um entre os Processos de Preparação 1 a 4. Como um processo para isolar o composto (1) opticamente ativo, o intermediário (2), (4), (7), (8) ou (9) opticamente ativo, pode-se usar um processo de cristalizar por fracionamento um sal com um ácido carboxílico opticamente ativo, ou pelo contrário, um processo para cristalizar por fracionamento um sal com uma base opticamente ativa.
Processo de Preparação 7
Dentre os compostos (1) de acordo com a presente de 08/10/2018, pág. 138/857
130 invenção, um processo de preparação do composto (lc) contendo heteroátomo(s) no grupo Q3 será aqui doravante descrito detalhadamente.
Um composto representado pela fórmula genérica (lc), um seu sal, um seu solvato ou um seu N-óxido, pode ser preparado de acordo com, por exemplo, o seguinte processo:
n\ r (ch^
H,N NH
R4 (CH2)n q4-co2h (3)
2’ - ” 2 (2c) (CH2),Í (CH2)n ' ( 1 w-T/ (4c)
H2N
Q1-Q2-CO2H (5) ’\ /R< y/ k f /ru (CH2)' (CH2)n O. , 0,_0ΛΚ K-TQ.
(1c) onde Q1, Q2, Q3, Q4, R3, R4, A, m e n têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo carbonila.
Um anidrido de ácido misto, halogeneto de ácido, éster ativado, ou similares, que é derivado a partir do ácido carboxílico (3) , pode reagir com o composto (2c) , dando o composto (4c) . O composto (4c) resultante pode reagir com o ácido carboxílico (5) sob as mesmas condições, dando o composto (lc), de acordo com a presente invenção.
Nas etapas de reação acima, os reagentes e condições, que são usados genericamente na síntese de peptídeos, podem ser aplicados. O anidrido de ácido misto pode ser preparado, por exemplo, pela reação de um cloroformiato, tal como o cloro-f ormiato de etila ou cloroformiato de isobutila, com o ácido carboxílico (3), na presença de uma base. 0 halogeneto de ácido pode ser de 08/10/2018, pág. 139/857
131 preparado tratando o ácido carboxílico (3) com um halogeneto de ácido, tal como o cloreto de tionila ou cloreto de oxalila. O éster ativado inclui vários tipos de ésteres. Tal éster pode ser preparado, por exemplo, pela reação de um fenol, tal como p-nitro-fenol, N-hidróxi-benzotriazol ou Nhidróxi-succinimida, com o ácido carboxílico (3), usando um agente condensador, tal como N,N'-diciclo-hexil-carbodiimida ou cloridrato de l-etil-3-(3-dimetil-amino-propil)carbodiimida. O éster ativado pode ser preparado também pela reação do ácido carboxílico (3) com triflúor-acetato de pentaflúor-fenila, ou similares, pela reação do ácido carboxílico (3) com hexaflúor-fosfito de 1benzotriazolilóxi-tripirrolidino-fosfônio, reação do ácido carboxílico (3) com cianofosfato de dietila (método de Shioiri), reação do ácido carboxílico (3) com trifenilfosfina e dissulfeto de 2,2'-dipiridila (método de Mukaiyama), ou similares. O anidrido de ácido misto, halogeneto de ácido ou éster ativado, do ácido carboxílico (3) , assim obtido, pode reagir com o composto (2c) em uma temperatura sob resfriamento até uma temperatura sob aguecimento, na presença de uma base apropriada, em um solvente inerte, dando o composto (4c) . O composto (4c) assim obtido pode reagir com um anidrido de ácido misto, halogeneto de ácido ou éster ativado, do ácido carboxílico (5), sob as mesmas condições, dando o composto (1) de acordo com a presente invenção. Os reagentes e as condições de reação na reação do composto (4c) com o ácido carboxílico (5) são iguais àguelas da reação da diamina (2c) com o ácido de 08/10/2018, pág. 140/857
132 carboxílico (3).
Como exemplos específicos da base usada em cada uma das etapas acima, podem ser mencionados os carbonatos de metais alcalinos ou metais alcalino-terrosos, tais como carbonato de sódio e carbonato de potássio, alcóxidos de metais alcalinos, tais como etóxido de sódio e butóxido de potássio, hidróxidos de metais alcalinos tais como hidróxido de sódio e hidróxido de potássio, e hidretos de metais alcalinos, tais como hidreto de sódio e hidreto de potássio; bases organometálicas exemplificadas por alquil-lítio, tal como n-butil-lítio, e dialquil-amino-lítio, tal como diisopropilamida-lítio; bases organometálicas exemplificadas por bis-(silil)-amina, tal como bis-(trimetil-silil)-amida lítio; e bases orgânicas tais como piridina, 2,6-lutidina, colidina, 4-dimetil-amino-piridina, trietil-amina, N-metilmorfolina, diisopropil-etil-amina, e diazabiciclo[5.4.0] undec-7-eno (DBU), ou similares.
Os exemplos do solvente inerte usado nesta reação incluem solventes do tipo halogeneto de alquila, tais como cloreto de metileno e clorofórmio, solventes etéreos tais como tetraidrofurano e 1,4-dioxano, solventes aromáticos tais como benzeno e tolueno, e solventes amídicos, tais como N,N-dimetil-formamida. Além destes solventes, um solvente do tipo sulfóxido, tal como sulfóxido de dimetila, um solvente cetônico, tal como acetona, ou similares, pode ser usado em alguns casos.
Nas etapas de preparação supradescritas, processos tais como anexar e retirar um grupo protetor, e a conversão de 08/10/2018, pág. 141/857
133 carbonila, tais benzilóxi-carbonila de um grupo funcional, podem ser aplicados adequadamente, para desta forma preparar o composto (lc).
Como grupo protetor para o grupo amino, é necessário usar somente um grupo protetor, que é usado genericamente como um grupo protetor para o grupo amino nas sínteses de compostos orgânicos, particularmente a síntese de peptídeos. Como seus exemplos, podem ser mencionados os grupos alcóxi-carbonila, tais como t-butóxi-carbonila, metóxi-carbonila e etóxi-carbonila, grupos aril-metóxicomo benzilóxi-carbonila, p-metóxie p- ou o-nitro-benzilóxi-carbonila, grupos aril-metila, tais como benzila, 4-metóxi-benzila e trifenil-metila, grupos alcanoíla, tais como os grupos formila e acetila, grupos aroíla, tais como um grupo benzoíla, e grupos aril-sulfonila, tais como 2,4-dinitrobenzeno-sulfonila e o-nitro-benzeno-sulfonila.
Como grupo protetor para o grupo hidroxila, é necessário usar somente um grupo protetor para o grupo hidroxila, que é usado genericamente nas sínteses de compostos orgânicos. Como seus exemplos, podem ser mencionados grupos alcóxi-metila, tal como um grupo metóximetila, grupos aril-metila, tais como os grupos benzila, 4metóxi-benzila, trifenil-metila, grupos alcanoíla, tal como um grupo acetila, grupos aroíla, tal como um grupo benzoíla, e um grupo t-butil-difenil-silililoxi. Um grupo carbonila pode ser protegido como um éster com um grupo alquila, tal como um grupo metila, grupo etila, grupo t-butila, ou um grupo aril-metila, tal como um grupo benzila. A anexação e de 08/10/2018, pág. 142/857
134 retirada do grupo protetor podem ser conduzidas de acordo com um método conhecido de per si nessas técnicas.
O composto (lc), de acordo com a presente invenção, pode ser convertido em vários derivados, convertendo seu grupo funcional. Por exemplo, um composto no qual A é um átomo de nitrogênio, não tendo qualquer substituinte, pode ser convertido em um composto amida por acilação, usando um anidrido de ácido misto, halogeneto de ácido, éster ativado, ou similares, de acordo com métodos de química orgânica comuns, um composto de sulfonamida pela reação com um halogeneto de sulfonila, e um composto Nalquila pela reação com um halogeneto de alquila, um composto N-arila pela reação com um halogeneto de arila ou um composto carbanato pela reação com um isocianato. Incidentalmente, o composto no qual A é um átomo de nitrogênio, não tendo qualquer substituição, pode ser preparado, por exemplo, tratando o composto (lc), preparado a partir da diamina (2c) , onde A foi protegido com o grupo t-butóxi-carbonila, de acordo com o Processo de Preparação 7, com um ácido.
Os compostos de acordo com a presente invenção assim preparados podem ser isolados e purificados por métodos conhecidos divulgados, como por exemplo, extração, precipitação, cromatografia fracionada, cristalização fracionada, recristalização, etc. Os compostos de acordo com a presente invenção podem ser convertidos nos sais desejados de acordo com reações formadoras de sais normais.
Os isômeros ópticos derivados de um átomo de de 08/10/2018, pág. 143/857
135 carbono assimétrico estão presentes nos compostos da presente invenção. Estes isômeros opticamente ativos podem ser preparados pelo processo de preparação a partir da diamina opticamente ativa (2c), e além disso, um processo para formar uma amina ou ácido opticamente ativo e um sal a partir do composto racêmico (lc) e cristalizando-os de forma fracionada, um processo para separá-los por cromatografia de coluna, usando um carreador opticamente ativo.
composto (lc)n no qual T1 é um grupo sulfonila, 10 pode ser preparado trocando o ácido carboxílico (3) por halogeneto de sulfonila (10) na reação do composto (2c) com o ácido carboxílico (3).
Processo de Preparação 8
O composto (lc), de acordo com a presente invenção, pode ser preparado também de acordo com o seguinte processo:
R4 q4-co2h R
(20)
R — N NH2 H (21) (3) (CH2)n -- Wm r\ y R4
I (ΓΊ5, / \ , (22)
R\ R4 \ I /r*u (CR2)m.x(CH2,n h2n n-t1 2 H '□<
(4C)
QUtf-CO.H (5)
Q1— Q2
R4 <CH2>\ /Wn °v\ \ >N N-t 4 ί “ π Q4 (ic) onde Q1, Q2, Q4, R3, R4, que aqueles definidos n têm e T1
A, m e acima, os mesmos significados representa um grupo
Petição 870180138821, de 08/10/2018, pág. 144/857
136 carbonila, e R51 e R61 representam grupos protetores para o grupo amino.
O composto (21) pode ser preparado removendo o grupo protetor R61 do composto (19) obtido protegendo os grupos amino do composto (2c). Nenhuma limitação específica é imposta sobre os grupos protetores para o aminoácido, ilustrados como R51 e R61, desde que eles sejam grupos usados genericamente na proteção do grupo amino. Entretanto, como seus exemplos típicos, podem ser mencionados os grupos protetores para o grupo amino descritos no Processo de Preparação 7. Neste caso, R51 e R61 devem ser grupos protetores capazes de sair por métodos ou condições diferentes entre si. Como seus exemplos típicos, pode ser mencionada uma combinação na qual R51 é um grupo t-butóxicarbonila, e R61 é um grupo benzilóxi-carbonila. Estes grupos protetores podem ser escolhidos para uso de acordo com a natureza e fatores similares do composto cujo grupo amino deve ser protegido. Ao retirar tal grupo protetor, os reagentes e condições podem ser empregados de acordo com o grupo protetor.
O composto (21) pode ser preparado também convertendo o grupo hidroxila no derivado aminoálcool (20) em um grupo amino. Como um exemplo da preparação do derivado aminoálcool (20) , conhece-se a conversão de metionina em 1,1-dióxido de 3-hidróxi-4-amino-tiopirano (Tetrahedron Lett. 37:7457, 1996), ou similares.
Como um processo para converter o grupo hidroxila no derivado aminoálcool (20) em um grupo amino, pode-se de 08/10/2018, pág. 145/857
137 mencionar um processo no qual o derivado aminoálcool (20) pode reagir com cloreto de metano-sulfonila, cloreto de ptolueno-sulfonila, anidrido triflúro-metano-sulfônico, ou similares, e o produto resultante pode então reagir com amônia, uma aril-alquil-amina primária, tal como benzilamina, p-metóxi-benzil-amina ou 2,4-dimetóxi-benzil-amina, uma aril-alquil-amina secundária, tal como dibenzil-amina, ou uma hidroxilamina, tal como N-benzil-hidroxilamina ou N,O-dibenzil-hidroxilamina, e um grupo benzila ou similares é então removido conforme necessário, preparando desta forma a diamina (21) . O derivado aminoálcool (20) pode ser convertido também na diamina (21) reagindo-o com ftalimida ou succinimida, de acordo com a reação com trifenilfosfina e azodicarboxilato de etila (método de Mukaiyama), ou similares, e depois tratando o produto da reação com hidrazina, N-mtil-hidrazina, ou similares. Quando A na fórmula é SO2, e n é 0, a diamina (21) pode se preparada adicionando amônia, uma aril-alquil-amina primária, tal como amônia, benzil-amina, p-metóxi-benzil-amina ou 2,4-dimetóxibenzil-amina, uma aril-alquil-amina secundária tal como benzil-amina, ou uma hidroxilamina tal como N-benzilhidroxilamina ou N,O-dibenzil-hidroxilamina, a uma solfona cíclica a, β-insaturada formada reagindo o derivado aminoálcool (20) com cloreto de metano-sulfonila, cloreto de p-tolueno-sulfonila, anidrido triflúor-metano-sulfônico, ou similares, e depois tratando o produto da reação com uma base apropriada ou reagindo diretamente o derivado aminoálcool (20) com trifenil-fosfina e azodicarboxilato de de 08/10/2018, pág. 146/857
138 etila, e removendo o grupo benzila ou similar, conforme necessário.
A diamina (21) resultante pode reagir com o ácido carboxilico (3) , dando o composto (22) . 0 grupo protetor
R51 é removido subsequentemente, dando o composto (4c) . 0 composto (4c) pode reagir com o ácido carboxilico (5), dando o composto (lc) de acordo com a presente invenção. Os reagentes e condições de reação na reação do composto (21) com o ácido carboxilico (3) e na reação do composto (4c) com o ácido carboxilico (5) podem ser iguais àqueles descritos no Processo de Preparação 7.
Similarmente, o composto (lc) no qual T1 é um grupo sulfonila pode ser preparado trocando o ácido carboxilico (3) por halogeneto de sulfonila (10) na reação do composto (21) com o ácido carboxilico (3).
Processo de Preparação 9
Um processo de preparação tipico do intermediário (2c) para a preparação descrita no Processo de Preparação 7 será descrito abaixo.
h2n nh2 (2c)
Petição 870180138821, de 08/10/2018, pág. 147/857
139 onde R3, R4, A, m e n têm os mesmos significados que aqueles definidos acima.
Como processos de preparação do derivado diol (23) conhece-se, por exemplo, a conversão de 1,2,3,6tetraidropiridina em l-benzilóxi-carbonil-3,4-cis-diidróxipirrolidina (pedido de patente japonesa publicado, n° 138264/1995), conversão de ácido L-tartárico em (R,R)tetraidrofuranodiol ou (R,R)-N-benzil-pirrolidinodiol (Tetrahedron: Asymmetry 8:1861, 1997), e similares. O derivado diol (23) pode ser preparado usando um processo já conhecido ou aplicando este processo e removendo um grupo protetor ou convertendo um grupo funcional, conforme necessário.
O derivado diol (23) pode reagir com cloreto de metano-sulfonila em uma temperatura sob resfriamento até a temperatura ambiente, na presença de uma base, em um solvente inerte, dando o composto (24) . O solvente inerte pode ser escolhido adequadamente entre aqueles descritos no Processo de Preparação 7. Entretanto, são particularmente preferidos os solventes do tipo halogeneto de alquila, tais como cloreto de metileno e clorofórmio, e solventes etéreos, tais como tetraidrofurano e 1,4-dioxano. Como base, prefere-se uma base orgânica, tal como piridina, 2,6lutidina, 4-dimetil-amino-piridina, trietil-amina, N-metilmorfolina, diisopropil-etil-amina, e diazabiciclo[5.4.0]undec-7-eno (DBU).
O composto (24) pode reagir com azida de sódio em de 08/10/2018, pág. 148/857
140 uma temperatura sob resfriamento até uma temperatura sob aquecimento, em um solvente apropriado, dando o derivado de azida (25). Como solvente, um solvente amida tal como N,Ndimetil-formamida ou N-metil-pirrolidin-2-ona, um solvente alcoólico tal como metanol ou etanol, um solvente etéreo tal como tetraidrofurano ou 1,4-dioxano, um solvente aromático tal como benzeno ou tolueno, um halogeneto de carbono, tal como cloreto de metileno ou clorofórmio, acetona, sulfóxido de dimetila, ou similares, é apropriado. Tal solvente pode ser um solvente misturado com água.
Como exemplo de um processo para converter o derivado azida (25) no composto (2c), existem muitos processos, tal como um processo de conduzir hidrogenação com catalisador de paládio, catalisador de níquel de Raney ou catalisador de platina, uma reação que usa um agente redutor tal como hidreto de lítio e alumínio, boro-hidreto de sódio ou boro-hidreto de zinco, uma reação que usa zinco na presença de cloreto de níquel ou cloreto de cobalto, uma reação que usa trifenil-fosfina, e similares. Os reagentes e condições apropriadas da reação podem ser selecionadas de acordo com a natureza do composto. A pressão de hidrogênio pode ser elevada até um nível mais alto do que a pressão atmosférica. Como solvente, é apropriado usar um solvente alcoólico tal como metanol ou etanol, um solvente amida tal como N,N-dimetil-formamida ou N-metil-pirrolidin-2-ona, um solvente éster tal como acetato de etila, ácido acético, ácido clorídrico, água, uma mistura destes solventes, ou similares. O composto (lc), de acordo com a presente de 08/10/2018, pág. 149/857
141 invenção, pode ser derivado a partir do derivado diamínico (2c) preparado de acordo com o processo supradescrito de acordo com o Processo de Preparação 7.
Quando o derivado diol (23) é trans-3,4-diidróxitetraidrofurano ou 3,4-diidróxi-pirrolidina substituída em trans-1, e similares, substâncias opticamente ativas estão presentes. Estes derivados diol (23) opticamente ativos podem ser convertidos em derivados diamínicos (2c) opticamente ativos, e adicionalmente, em compostos (lc) opticamente ativos, de acordo com a presente invenção, de acordo com o Processo de Preparação 7.
Processo de Preparação 10
Um processo típico de preparação dos compostos (30), (31) e (32) opticamente ativos, incluídos no composto (19) descrito no Processo de Preparação 8, será descrito abaixo. Incidentalmente, a posição de um átomo de carbono assimétrico, indicado no esquema de preparação que se segue, está indicada a título exemplificativo.
Petição 870180138821, de 08/10/2018, pág. 150/857
142
onde m, n, R3, R51 e R61 têm os mesmos significados que aqueles definidos acima, e R71 representa um grupo protetor para o grupo carboxila.
O derivado éster a, β-insaturado opticamente ativo (26) pode ser preparado de acordo com o processo descrito na literatura (J. Org. Chem. 61:581, 1996; J. Org. Chem.
57:6279, 1992; etc.) ou aplicando esse processo. O derivado éster a,β-insaturado opticamente ativo (26) pode reagir com uma amina em uma temperatura sob resfriamento ou sob os aquecimento, em um solvente apropriado, dando diastereoisômeros (27a) e (27b). A amina pode ser escolhida adequadamente para uso entre aquelas descritas no Processo de Preparação 8. O solvente é, de preferência, um solvente orgânico não-reativo com um substrato, produto ou reagente, particularmente um solvente alcoólico tal como metanol ou etanol, ou um solvente etéreo tais como tetraidrofurano,
Petição 870180138821, de 08/10/2018, pág. 151/857
143
1,2-dimetóxi-etano, 1,4-dioxano, e similares. Os diastereoisômeros (27a) e (27b) podem ser preparados também pela reação do derivado éster a,β-insaturado (26) com uma base organometálica, tal como N-benzil-(trimetil-silil)amida-lítio, e similares, aplicando o processo descrito na literatura (J. Org. Chem. 63:7263, 1998). Os diastereoisômeros podem ser separados para uso, por exemplo, o diastereoisômero (27a) na próxima reação.
O composto (27a) é tratado com um ácido em uma temperatura sob resfriamento ou sob aquecimento, em um solvente apropriado, dando o composto (28) . Os exemplos do ácido usado incluem ácido clorídrico, ácido sulfúrico, ácidos de Lewis, tal como trifluoreto de boro, ácido triflúor-acético, ácido p-tolueno-sulfônico, ou similares. Como solvente, usa-se água ou um solvente alcoólico tal como metanol ou etanol. Este solvente pode ser misturado com água. Nesta reação, esse composto deve reagir com um reagente protetor apropriado para o grupo amino, conforme necessário.
O composto (28) pode ser tratado com um ácido em uma temperatura sob resfriamento ou sob aquecimento, em um solvente apropriado, dando o composto (30) opticamente ativo. O ácido usado pode ser escolhido adequadamente para uso entre os ácidos mencionados acima, sendo particularmente preferidos um ácido de Lewis, tal como o trifluoreto de boro, ou o ácido p-tolueno-sulfônico, ou similares. Como solvente usado na reação, usa-se um solvente etéreo tal como 1,4-dioxano ou tetraidrofurano, ou um solvente aromático tal de 08/10/2018, pág. 152/857
144 como benzeno ou tolueno. O composto (30) pode ser preparado também a partir do derivado de azida (29). Como exemplos da preparação do derivado de azida (29) opticamente ativo, conhece-se a conversão do ácido L-aspárgico em (R,R)(3S,4S)-3-amino-4-azido-5-oxotetraidrofurano (Can. J. Chem. 71:1047, 1993), e similares. O derivado de azida opticamente ativo (29) pode ser preparado usando um processo já conhecido ou aplicando este processo e removendo um grupo protetor ou convertendo um grupo funcional, conforme necessário. A azida no derivado de azida (29) pode ser reduzida para um grupo amino, e o produto resultante pode reagir com um reagente protetor apropriado para o grupo amino, dando o composto (30) . Os reagentes e condições da reação usadas na redução da azida (29) podem ser iguais àquelas descritas no processo de converter o derivado de azida (25) no composto (2c).
A parte do grupo hidroxila do composto (28) pode ser convertida em um grupo amino e depois tratada com uma base, dando o composto (31). A conversão do grupo hidroxila do composto (28) no grupo amino pode ser realizada de acordo com, por exemplo, o Processo de Preparação 8. O composto (31) pode ser preparado também tratando o derivado de álcool (28) com um agente oxidante e depois aminando de forma redutora o derivado aldeído resultante. Os exemplos preferidos específicos do agente oxidante usado na reação acima incluem cloro-cromato de piridínio (PCC), dicromato de piridínio (PDC), complexos de trióxido de enxofre e piridina, ou similares. Os exemplos da amina incluem de 08/10/2018, pág. 153/857
145 alquil-aminas primárias, tais como amônia, metil-amina e etil-amina, e aril-alquil-aminas primárias, tais como benzil-amina, p-metóxi-benzil-amina e 2,4-dimetóxi-benzilamina. Como processo redutor, há um processo de conduzir hidrogenação com um catalisador de paládio, catalisador de níquel de Raney ou catalisador de platina, uma reação que usa um agente redutor tal como boro-hidreto de sódio, triacetóxi-bro-hidreto de sódio ou ciano-boro-hidreto de sódio, e os reagentes e condições de reação apropriadas podem ser selecionadas de acordo com a natureza do composto, ou parâmetros similares. A base usada no processo acima pode ser selecionada adequadamente para uso entre aquelas descritas no Processo de Preparação 7. O composto (31) também pode ser preparado usando o composto (30) e uma amina de acordo com o processo descrito na literatura (Tetrahedron Lett. 41:1141, 2000; Heterocycles 53:173, 2000) ou aplicando tal processo. Os exemplos da amina incluem alquil-aminas primárias, tais como amônea, metil-amina e etil-amina, e aril-alquil-aminas primárias, tais como benzil-amina e pmetóxi-benzil-amina.
O composto (31) pode ser tratado com um agente redutor em uma temperatura sob resfriamento ou até uma temperatura sob aquecimento, em um solvente, dando o Os exemplos do agente redutor incluem borano/tetraidrofurano, complexos de borano/sulfeto de metila, e hidreto de lítio e alumínio. Entretanto, os reagentes e condições da reação apropriadas podem ser selecionadas de acordo com a natureza do composto, composto (32). complexos de de 08/10/2018, pág. 154/857
146 ou parâmetros similares. 0 solvente é adequadamente um solvente orgânico não-reativo com um substrato, produto, reagente, ou similares, particularmente um etéreo tais como tetraidrofurano ou 1,4-dioxano.
|
5 |
As |
substâncias |
opticamente |
ativas |
dc) |
dos |
|
compostos |
de |
acordo com |
a presente |
invenção |
podem |
ser |
|
derivadas |
a |
partir dos |
compostos |
(30), (31) |
e |
(32) |
preparados pelo processo descrito acima.
No esquema de preparação supradescrito, uma das 10 substâncias opticamente ativas foi descrita a título exemplificativo. Entretanto, outras substâncias opticamente ativas com conformação diferente entre si também podem ser preparadas de acordo com esquemas de preparação similares, usando respectivamente materiais de partida com conformação diferente entre si.
Processo de Preparação 11
O composto (1) no qual T1 é um grupo -CO-CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima, pode ser preparado de acordo com o seguinte esquema:
Q4-N(R')-CO-CO2H (33)
HN (R1) -Q3-NHR2 -► HN (R1) -Q3-N (R2) -T4-Q4 (2) (4) q1-q2co2h (5)
-► Q1-Q2-CO-N (R1) —Q3—Ν (N (R2) -T4-Q4 (D
Petição 870180138821, de 08/10/2018, pág. 155/857
147 onde Q1, Q2, Q3, Q4, R1, R2, e R' têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -COCO-N(R')-, onde R' tem o mesmo significado que aquele definido acima.
Um halogeneto de ácido, éster ativado, ou similares, que é derivado do ácido carboxílico (33), pode reagir com a diamina (2), dando o composto (4) . O composto (4) resultante pode reagir com o ácido carboxílico (5) sob as mesmas condições, dando o composto (1) de acordo com a presente invenção. Nas etapas de reação acima, os reagentes e condições, que são usados genericamente na síntese de peptídeos, podem ser aplicados. O halogeneto de ácido pode ser preparado tratando o ácido carboxílico (33) com um halogeneto de ácido, tal como o cloreto de tionila ou cloreto de oxalila. O éster ativado inclui vários tipos de ésteres. Este éster pode ser preparado, por exemplo, pela reação de um fenol, tal como p-nitro-fenol, N-hidróxibenzotriazol ou N-hidróxi-succinimida, com o ácido carboxílico (33), usando um agente condensador tal como N,N'-diciclo-hexil-carbodiimida ou cloridrato de l-etil-3(3-dimetil-amino-propil)-carbodiimida. O éster ativado pode ser preparado também pela reação do ácido carboxílico (33) com triflúor-acetato de pentaflúor-fenila, ou similares, pela reação do ácido carboxílico (33) com hexaflúor-fosfito de 1-benzotriazolilóxi-tripirrolidino-fosfônio, reação do ácido carboxílico (33) com cianofosfato de dietila (método de Shioiri), reação do ácido carboxílico (33) com trifenilfosfina e dissulfeto de 2,2'-dipiridila (método de de 08/10/2018, pág. 156/857
148
Mukaiyama), ou similares. O anidrido de ácido misto, halogeneto de ácido ou éster ativado, do ácido carboxílico (33), assim obtido, pode reagir com a diamina (2) em uma temperatura entre -78 °C e 150 °C, na presença de uma base apropriada, em um solvente inerte, dando o composto (4) . O composto (4) assim obtido pode reagir com um anidrido de ácido misto, halogeneto de ácido ou éster ativado, do ácido carboxílico (5) , sob as mesmas condições, dando o composto (1) de acordo com a presente invenção. Os reagentes e as condições de reação na reação do composto (4) com o ácido carboxílico (5) são iguais àquelas da reação da diamina (2) com o ácido carboxílico (33) . As bases e solventes usados nas etapas respectivas podem ser escolhidos adequadamente a partir daqueles descritos no Processo de Preparação 1.
Quando o composto (1) no qual Q3 é o seguinte grupo:
onde R3, R4 e Q5 têm os mesmos significados que aqueles definidos acima, e os números 1 e 2 indicam posições, e a relação entre a posição 1 e a posição 2 é uma forma trans ou forma cis, é preparado, é necessário usar somente a diamina (2a) ou (2b) descrita no Processo de Preparação 5.
Quando o composto (1), no qual um heteroátomo tal como um átomo de nitrogênio, átomo de oxigênio ou átomo de de 08/10/2018, pág. 157/857
149 enxofre, está contido em Q5, é preparado, é necessário somente trocar o ácido carboxílico (3) pelo ácido carboxílico (33) na reação do composto (2c) com o ácido carboxílico (3), como descrito no Processo de Preparação 7.
A saber, o composto (1), no qual um heteroátomo está contido em Q5, no esquema de reações que se segue, o composto (lc) pode ser preparado.
(y-ff-COjH (5)
Q—Q'
R\ I
J V I
R4 (CH2)n 1
Q4 °v\ \ 1 (1C) onde Q1, Q2, Q4, R3, R4, R', A, m e n têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -CO-CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima.
Processo de Preparação 12
O composto (1) no qual T1 é um grupo -CO-CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima, pode ser preparado de acordo com o seguinte esquema:
Q4-N(R')-CO-CO2H (33)
Q1-Q2-CO-N (R1) -Q3-HNR2 > Qi-Q2-CO-N (R1) -Q3-N (R2) -Tx-Q4 (9)
d)
Petição 870180138821, de 08/10/2018, pág. 158/857
150
|
onde Q1, |
Q2, |
Q3, Q4, |
R1, R2, e |
R' têm os mesmos |
significados |
|
que aqueles |
definidos acima, |
e T1 representa um grupo -CO- |
|
CO-N (Re- |
t |
onde R' |
tem o |
mesmo significado |
que aquele |
|
definido |
acima. |
|
|
|
|
5 |
Na |
reação |
da amina |
(9) com o ácido |
carboxílico |
(33) , os mesmos reagentes e condições que aquelas descritas no Processo de Preparação 1 podem ser usadas.
A amina (9) usada neste caso também pode ser preparada de acordo com o esquema que se segue, indicado como um esquema de preparação da amina (41), além do esquema descrito no Processo de Preparação 2.
'W (34)
X.
R\
H.N
Q—0r N
R\ O*
Q5/
(41) (39) (40) onde R3, R4, Q1, Q2 e Q5 têm os mesmos significados que aqueles definidos acima, e R52 representa um grupo protetor para o grupo amino.
O composto (34) no esquema de preparação acima pode ser preparado tratando um ciclo-alqueno com ácido perbenzóico ou um seu derivado, e similares, em um solvente tal como cloreto de metileno, para epoxidá-lo. As condições normais para epoxidação de um alqueno podem ser aplicadas às
Petição 870180138821, de 08/10/2018, pág. 159/857
151 condições desta reação. 0 composto (34) pode ser preparado também de acordo com o processo descrito em J. Org. Chem. 61:8687-8691, 1996, ou um processo correspondente a ele.
composto (34) pode reagir com azida de sódio ou 5 similares de acordo com um método conhecido de per si nessas técnicas, dando a azida (35) . A azida (35) pode ser reduzida cataliticamente, e o grupo amino do composto resultante pode ser protegido, dando o composto (36). Como exemplos do grupo protetor para o grupo amino nesta reação, podem ser mencionados aqueles descritos no Processo de Preparação 2. O composto (36) pode ser convertido na azida (38) de uma maneira similar àquela do processo descrito no Processo de Preparação 5, e o grupo protetor para o seu grupo amino pode ser deixado, dando o composto (39) . O composto (39) pode reagir com o ácido carboxílico (5), dando o composto (40) . O composto (40) pode ser então reduzido cataliticamente, dando o composto (41).
Processo de Preparação 13
O composto
d) no qual um grupo
-CO-CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima, pode ser preparado também trocando a reação do composto (9) com o ácido carboxílico (3) no esquema descrito no Processo de Preparação 2 por uma reação do composto (9) com o composto (33).
Q4-N(R')-CO-CO2H (33)
Q1-Q2-CO-N (R1) -Q3-HNR2 > Q1-Q2-CO-N (R1)-Q3-N (R2)-Ti-Q4 (9)
d)
Petição 870180138821, de 08/10/2018, pág. 160/857
152 onde Q1, Q2, Q3, Q4, R1, R2, e R' têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -C0CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima.
Como condições da reação, podem ser aplicadas aquelas descritas no Processo de Preparação 2.
Quando o composto (1) no qual Q3 é o seguinte grupo:
|
onde R3, |
R4 e Q5 têm |
os mesmos |
significados que aqueles |
|
10 definidos |
acima, e os |
números 1 e |
2 indicam posições, e |
um |
|
heteroátomo tal como |
um átomo |
de nitrogênio, átomo |
de |
|
oxigênio |
ou átomo de enxofre, |
está contido em Q5, |
é |
preparado, é necessário somente trocar o ácido carboxílico (3) pelo ácido carboxílico (33) na reação do composto (21) com o ácido carboxílico (3) , como descrito no Processo de Preparação 8. A saber, o composto (1), no qual um heteroátomo está contido em Q5, no esquema de reações que se segue, o composto (lc) pode ser preparado.
Petição 870180138821, de 08/10/2018, pág. 161/857
153 ο’-σ-οο,,Η (5)
Q—
(1c) onde Q1, Q2, Q4, R3, R4, R', A, m e n têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -CO-CO-N (R')-, onde R' tem o mesmo significado que aquele definido acima, e R51 representa um grupo protetor para o grupo amino.
Processo de Preparação 14 composto (1) no qual T1 é um grupo -CO-A1-N (R)-, onde R representa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, e A1 representa um grupo alquileno que tem 1 a 5 átomos de carbono, que pode ser substituído, pode ser preparado pela reação do composto (9) descrito no Processo de Preparação 2 com Q4-N(R)-A1-CO2H (42) em uma temperatura entre -55 °C e 50 °C, usando um agente condensador, em um solvente inerte. Como exemplos do agente condensador, podem ser mencionados N,N'-diciclohexil-carbodiimida, cloridrato de 1-etil-3-(3-dimetil-aminopropil)-carbodiimida, ou similares. Como exemplos do solvente inerte, podem ser mencionados solventes do tipo halogeneto de alquila, tais como cloreto de metileno, clorofórmio e tetracloreto de carbono, solventes etéreos tais como tetraidrofurano, 1,2-dimetóxi-etano e dioxano, solventes aromáticos tais como benzeno e tolueno, e solventes amídicos tal como N,N-dimetil-formamida.
Petição 870180138821, de 08/10/2018, pág. 162/857
154
Q4-N(R)-A1-CO2H (42)
Q1-Q2-CO-N (R1) -Q3-HNR2 -► Q1-Q2-CO-N (R1) -Q3-NR2-T1-Q4 (9) (1) onde Q1, Q2, Q3, Q4, R1, R2 e R têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -C0A1-N(R)-, onde R representa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, e A1 representa um grupo alquileno que tem 1 a 5 átomos de carbono, que pode ser substituído.
composto (42) descrito no processo de preparação descrito acima pode ser preparado, por exemplo, reagindo uma aril-amina tal como a 4-cloro-anilina com um éster de um ácido bromo-alcanóico em uma temperatura entre 40 e 120 °C, na presença de uma base tal como carbonato de potássio, em um solvente tal como acetonitrila ou N,N-dimetil-formamida, e depois hidrolisando o éster com um álcali tal como hidróxido de lítio, hidróxido de potássio ou hidróxido de sódio. O composto (42) pode ser usado na reação na forma de um sal, tal como um sal de potássio, como ele está.
Processo de Preparação 15
O composto (1), no qual T' é um grupo -C (=0) -NHou um grupo -C(=S)-NH-, pode ser preparado pela reação do composto (9) descrito no Processo de Preparação 2 com um isocianato (Q4-N=C=O) ou isotiocianato (Q4-N=C=S) em uma temperatura entre -20 °C e 50 °C, em um solvente inerte. Os exemplos típicos do solvente inerte estão descritos no
Petição 870180138821, de 08/10/2018, pág. 163/857
155
Processo de Preparação 14. Quando o isocianato ou isotiocianato não é comercializado, o isocianato ou isotiocianato pode ser sintetizado usando métodos comuns.
Q4-N (R' ) -CO-CO2H Sfcli Q4-N=C=S (33)
Q1-Q2-CO-N (R1) -Q3-HNR2 -► QX-Q2-CO-N (Rx)-Q3-NR2-TX-Q4 (9) (1) onde Q1, Q2, Q3, Q4, R1 e R2 têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -C(=0)-NHou um grupo -C(=S)-NH-.
Processo de Preparação 16
O composto (1), no qual T1 é um grupo -CO-NH-NH-, pode ser preparado pela reação do composto (9) descrito no Processo de Preparação 2 com Q4-NH-NH-CC>2Ph, entre a temperatura ambiente e 150 °C, em um solvente inerte, na presença de uma base, caso necessário. Como exemplos típicos do solvente inerte, podem ser mencionados acetonitrila e N,N-dimetil-formamida, e além disso, aqueles descritos no Processo de Preparação 14. Como exemplos da base, podem ser mencionadas piridina, 2,6-lutidina, colidina, 4-dimetil-amino-piridina, trietil-amina, N-metilmorfolina, diisopropil-etil-amina, e diazabiciclo[5.4.0]undec-7-eno (DBU).
Q4-NH-NH-CO2Ph (43)
Q1-Q2-CO-N (R1) -Q3-HNR2 * Q1-Q2-CO-N (R1)-Q3-NR2-Tx-Q4 (9)
d) de 08/10/2018, pág. 164/857
156 onde Q1, Q2, Q3, Q4, R1 e R2 têm os mesmos significados gue agueles definidos acima, T1 representa um grupo -C-NH-NH-, e Ph representa o grupo fenila.
composto (43) descrito no processo de preparação 5 descrito acima pode ser preparado, por exemplo, reagindo uma aril-hidrazina, tal como 4-cloro-fenil-hidrazina, com carbonato de difenila, entre a temperatura ambiente e 120 °C, em um solvente tal como acetonitrila, N,N-dimetilformamida, cloreto de metileno, clorofórmio, tetraidrofurano, 1,2-dimetóxi-etano, dioxano, benzeno ou tolueno.
Processo de Preparação 17
O composto (1) , no gual T1 é um grupo -CO-A2-CO-, onde A2 representa uma ligação simples ou um grupo alguileno gue tem 1 a 5 átomos carbono, pode ser preparado pela reação do composto (9) descrito no Processo de Preparação 2 com Q4CO-A2-CO2H (44) em uma temperatura entre -50 °C e 50 °C, usando um agente condensador, em um solvente inerte. Como exemplos do agente condensador, podem ser mencionados N,N'20 diciclo-hexil-carbodiimida, cloridrato de l-etil-3-(3dimetil-amino-propil)-carbodiimida, ou similares. Como exemplos do solvente, podem ser mencionados agueles descritos no Processo de Preparação 16, ou similares.
Q4-CO-A2-CO2H (44)
Q1-Q2-CO-N (R1) -Q3-HNR2 -► Q1-Q2-CO-N (R1) -Q3-NR2-T1-Q4 (9) (1)
Petição 870180138821, de 08/10/2018, pág. 165/857
157 onde Q1, Q2, Q3, Q4, R1 e R2 têm os mesmos significados gue agueles definidos acima, e T1 representa um grupo -CO-A2-CO-, onde A2 representa uma ligação simples ou um grupo alguileno gue tem 1 a 5 átomos de carbono.
Quando A2 é uma ligação simples, o composto (44) descrito no processo de preparação descrito acima pode ser preparado, por exemplo, hidrolisando um composto (por exemplo, Q4-CO-CO2Et) preparado pela reação de FriedelCrafts de um hidrocarboneto aromático, tal como cloro10 benzeno, ou um composto aromático heterocíclico, tal como tiofeno, com um cloro-oxoacetato (como por exemplo, C1COCChEt), usando um álcali tal como hidróxido de lítio, hidróxido de potássio ou hidróxido de sódio.
Quando A2 é um grupo metileno, o composto (44) pode ser preparado, por exemplo, hidrolisando um derivado cetoéster (como por exemplo, Q4-CO-CH2-CO2Et) obtido pela reação de um cloreto de aril-carbonila, tal como o cloreto de 4-cloro-benzoíla, ou um cloreto de heteroaril-carbonila, tal como o cloreto de tiofenocarbonila, com monocarboxilato monoéster malônico de potássio, na presença de cloreto de magnésio e trietil-amina, com um álcali, tal como hidróxido de lítio, hidróxido de potássio ou hidróxido de sódio. O derivado de cetoéster pode ser usado na reação acima com o composto (9) na forma de um ácido carboxílico obtido por hidrólise após conversão de seu grupo carbonila em etilenocetal. Quando A2 é um grupo alguileno gue tem pelo menos 2 átomos de carbono, o composto (44) pode ser preparado, por exemplo, hidrolisando um derivado cetoéster
Petição 870180138821, de 08/10/2018, pág. 166/857
158 (como por exemplo, Q4-CO-A2-CO2Et) obtido pela reação de Friedel-Crafts de um hidrocarboneto aromático, tal como benzeno, ou um composto aromático heterocíclico, tal como tiofeno, com um monocloreto de monoéster alquileno5 dicarboxílico, usando um álcali tal como hidróxido de lítio, hidróxido de potássio ou hidróxido de sódio.
Processo de Preparação 18 composto (1) , no qual T1 é um grupo -CO-A3-CO-NH, onde A3 representa um grupo alquileno que tem 1 a 5 átomos carbono, pode ser preparado pela reação do composto (9) descrito no Processo de Preparação 2 com Q4-NH-CO-A3-CO2H (45) em uma temperatura entre -50 °C e 50 °C, usando um agente condensador, em um solvente inerte. Como exemplos do agente condensador, podem ser mencionados Ν,N'-diciclo15 hexil-carbodiimida, cloridrato de l-etil-3-(3-dimetil-aminopropil)-carbodiimida, e similares. Os exemplos do solvente inerte incluem solventes do tipo halogeneto de alquila, tais como cloreto de metileno, clorofórmio e tetracloreto de carbono, solventes etéreos tais como tetraidrofurano, 1,220 dimetóxi-etano e dioxano, solventes aromáticos tais como benzeno e tolueno, e solventes amídicos tal como N,Ndimetil-formamida.
Q4-NH-CO-A3-CO2H (45)
Q1-Q2-CO-N (R1) -Q3-HNR2 > Q1-Q2-CO-N (R1) -Q3-NR2-T1-Q4 (9) (D
Petição 870180138821, de 08/10/2018, pág. 167/857
159 onde Q1, Q2, Q3, Q4, R1 e R2 têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -CO-A3-CO-, onde A3 representa grupo alquileno que tem 1 a 5 átomos de carbono.
0 composto (45) pode ser preparado hidrolisando um composto (como por exemplo, Q4-NH-CO-A3-CO2Et) obtido pela reação de uma aril-amina tal como a 4-cloro-anilina ou uma heteroaril-amina, tal como a amino-piridina correspondente a Q4-NH2, com monocarboxilato de monoéster alquileno10 dicarboxílico de potássio, em uma temperatura entre -50 e 50°C, usando um agente condensador, em um solvente inerte, com um álcali, tal como hidróxido de lítio, hidróxido de potássio ou hidróxido de sódio.
Processo de Preparação 19
O composto (1) no qual T1 é um grupo
-CS-CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima, pode ser preparado de acordo com o seguinte esquema:
Q4—N(R')-CO-CH2-S-SO3Na (46)
Q1-Q2-CO-N (R1) -Q3-HNR2 -► Q1-Q2-CO-N (R1) -Q3-N (R2) -l^-Q4 (9) (1) onde Q1, Q2, Q3, Q4, R1, R2, e R' têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -CSCO-N (R')-, onde R' tem o mesmo significado que aquele definido acima.
Petição 870180138821, de 08/10/2018, pág. 168/857
160
Mais especificamente, tiossulfato de sódio (46) e o composto (9) podem ser dissolvidos ou dispersados em um solvente e aquecidos, dando o composto (1) de acordo com a presente invenção. A temperatura da reação é, de preferência, entre 80 e 200°C, particularmente, de preferência, cerca de 150°C. Como solvente usado nesta reação, pode-se mencionar água, álcoois tais como metanol e etanol, solventes básicos tais como piridina e N-metilmorfolina, solventes do tipo halogeneto de alquila, tais como cloreto de metileno e clorofórmio, solventes etéreos tais como tetraidrofurano, 1,2-dimetóxi-etano e dioxano, e solventes amidicos tal como a N,N-dimetil-formamida. Estes solventes podem ser misturados adequadamente para uso. Como exemplos de solventes mistos, pode ser mencionado um solvente misto de metanol e cloreto de metileno, ou similares. Nesta reação, o solvente não é necessariamente refluxado. Por exemplo, quando o solvente misto de metanol e cloreto de metileno é usado, uma solução da reação (ou uma mistura da reação) é aquecida em uma temperatura externa de 150 °C, para remover o solvente por destilação, e o resíduo é então aquecido na mesma temperatura.
Processo de Preparação 20
O composto (1) no qual T1 é um grupo -CO-CS-N(R')-, onde R' tem o mesmo significado que aquele definido acima, pode ser preparado de acordo com o seguinte esquema:
de 08/10/2018, pág. 169/857
161 cich2coci
Q1-Q2-CO-N (R1) -Q3-HNR2 (9)
Na2S2O3
-► Qi-Q2-CO-N (R1) -Q3-N (R2) -COCH2CI (47)
NH(R')-Q4
-► Qi-Q2-CO-N (R1)-Q3-N (R2)-COCH2-SSO3Na -► (48)
Q1-Q2-CO-N (R1) —Q3—N (R2) T4-Q4 (D onde Q1, Q2, Q3, Q4, R1, R2, e R' têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -C0CS-N(R')-, onde R' tem o mesmo significado que aquele definido acima.
Mais especificamente, o composto (9) pode reagir com cloreto de cloro-acetila, na presença de uma base, dando o composto (47). 0 composto (47) pode ser tratado junto com tiossulfato de sódio em um solvente, dando o derivado tiossulfato de sódio (48). 0 derivado tiossulfato de sódio (48) assim obtido pode ser aquecido com uma amina, como por exemplo, HN(R')-Q4, dando o composto (1) de acordo com a presente invenção.
Quanto às condições, solvente e similares, para preparar o composto (47) a partir do composto (9), podem ser aplicadas aquelas usadas comumente na reação de uma amina com cloreto de ácido. Para preparar o composto (48) a partir do composto (47), é necessário somente aquecer o composto (47) junto com tiossulfato de sódio sob refluxo por cerca de 1 hora em um solvente, tal como etanol. Quando o
Petição 870180138821, de 08/10/2018, pág. 170/857
162 composto (47) é um sal com ácido clorídrico, ou similares, a reação pode ser realizada na presença de uma base, tal como bicarbonato de sódio. As condições da preparação do composto (48) não estão limitadas àquelas aqui descritas, e a temperatura e os tipos do solvente e da base podem ser mudados adequadamente. As condições para a reação do composto (48) com HN(R')-Q4 são as mesmas que aquelas descritas no Processo de Preparação 19.
Processo de Preparação 21
O composto (1) no qual T° é um grupo tiocarbonila (-CS-) pode ser preparado de acordo com o seguinte esquema:
H2N—Q3—N (R2) -I^-Q4 (50)
Q1-Q2-CHO -► Q1-Q2-C=N-Q3-N (R2)-T4-Q4 (49) (51)
Ss
-► Q1-Q2-CS-NH-Q3-N (R2) -T4-Q4
d) onde Q1, Q2, Q3, Q4 e R2 têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo -SO2-, CO-, -CO-NH-, -CS-NH-, -CO-NH-NH-, -CO-CO-N(R'), onde R' tem o mesmo significado que aquele definido acima, -CO-CS-N(R'), onde R' tem o mesmo significado que aquele definido acima, CS-CO-N(R'), onde R' tem o mesmo significado que aquele definido acima, -CS-CS-N(R'), onde R' tem o mesmo significado que aquele definido acima, -CO-A1-N (R)-, onde
Petição 870180138821, de 08/10/2018, pág. 171/857
163
A1 e R têm os mesmos significados que aqueles definidos acima, -CO-A2-CO-, onde A2 tem o mesmo significado que aquele definido acima, -CO-A3-CO-NH, onde A3 tem o mesmo significado que aquele definido acima, ou -CO-A3-CO-, onde A3 tem o mesmo significado que aquele definido acima.
Mais especificamente, o composto (49) pode ser submetido à reação de desidratação com a mina (50) , na presença de um catalisador ácido, tal como o ácido ptolueno-sulfônico, dando o composto (51) . O composto (51) pode ser aquecido junto com enxofre em pó em um solvente, tal como um solvente misto de metanol/cloreto de metileno, dando o composto (1) de acordo com a presente invenção. Quanto às condições para preparar o composto (51) a partir do composto (49) e da amina (50), podem ser aplicadas aquelas usadas comumente na preparação de uma base de Schiff. Especificamente, o aquecimento sob refluxo pode ser conduzido na presença de um catalisador ácido em benzeno ou tolueno, sob condições nas quais a água é removida do sistema da reação, usando, por exemplo, um sifão Dean-Stark. Pode-se usar também peneira molecular para remover a água do sistema da reação.
Os intermediários importantes descritos nos Processos de Preparação 1 a 21 dos compostos (1) , de acordo com a presente invenção, serão aqui doravante descritos.
1) Os compostos descritos nos Processos de Preparação 1, 3 e 11, e representados pela seguinte fórmula genérica (4):
HN (R1) —Q3—N (R2) —T1—Q4 (4) de 08/10/2018, pág. 172/857
164 onde R1, R2, Q3 e Q4 têm os mesmos significados que aqueles definidos acima, e T1 representa um grupo carbonila, grupo sulfonila ou grupo -CO-CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima, são importantes como intermediários para preparar os compostos (1) de acordo com a presente invenção.
Dentre os intermediários supradescritos, são preferidos os compostos nos quais T1 é um grupo -CO-CON(R')-, onde R' significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, e os compostos nos quais T1 na fórmula acima é um grupo carbonila, e Q3 é o seguinte grupo:
onde R3 e R4 têm os mesmos significados que aqueles definidos acima, e Q5 significa um grupo - (CH2) m-CH2-A-CH215 (CH2)n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH.
2) Os compostos descritos nos Processos de
Preparação 2, 4 e 12, e representados pela seguinte fórmula genérica (9):
Q1-Q2-C (=0) -N (R1) -Q3-NHR2 (9) onde R1, R2, Q1, Q2 e Q3 têm os mesmos significados que
Petição 870180138821, de 08/10/2018, pág. 173/857
165 aqueles definidos acima, são importantes como intermediários para preparar os compostos (1) de acordo com a presente invenção.
Dentre os intermediários supradescritos, são 5 preferidos os compostos nos quais Q3 é o seguinte grupo:
onde R3 e R4 têm os mesmos significados que aqueles definidos acima, e Q5 significa um grupo - (CH2) m-CH2-A-CH2(CH2)n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH.
3) Os compostos (4c) que se seguem, descritos nos Processos de Preparação 7, 11 e 13, são importantes como intermediários para preparar os compostos (1) de acordo com a presente invenção.
(4C) onde Q4, R3, R4, A, m e n têm os mesmos significados que
Petição 870180138821, de 08/10/2018, pág. 174/857
166 aqueles definidos acima, e T1 representa um grupo carbonila, grupo sulfonila ou grupo -CO-CO-N (R') , onde R' tem o mesmo significado que aquele definido acima.
Dentre os intermediários supradescritos, são 5 preferidos os compostos nos quais T1 na fórmula acima é um grupo -CO-CO-N(R')-, onde R' tem o mesmo significado que aquele definido acima, e os compostos nos quais T1 é um grupo carbonila, e A é um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH.
4) Os compostos (22) que se seguem, descritos nos Processos de Preparação 8 e 13, são importantes como intermediários para preparar os compostos (1) de acordo com a presente invenção.
onde Q4, R3, R4, A, m e n têm os mesmos significados que aqueles definidos acima, T1 representa um grupo carbonila, grupo sulfonila ou grupo -CO-CO-N (R') , onde R' tem o mesmo significado que aquele definido acima, e R51 representa um grupo protetor para o grupo amino.
Dentre os intermediários supradescritos, são preferidos os compostos nos quais T1 na fórmula acima é um
Petição 870180138821, de 08/10/2018, pág. 175/857
167 grupo -CO-CO-N (R')-, onde R' tem o mesmo significado que aquele definido acima, e os compostos nos quais T1 é um grupo carbonila, e A é um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -S0-, -S02-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH.
5) Os compostos (7a) opticamente ativos que se seguem, descritos no Processo de Preparação 6, são importantes como intermediários para preparar os compostos (1) de acordo com a presente invenção.
onde Q5, R1, R2, R3 e R4 têm os mesmos significados que aqueles definidos acima, e R50 representa um grupo protetor para o grupo amino.
Dentre os intermediários supradescritos, são preferidos os compostos nos quais Q5 na fórmula acima é um grupo - (CH2) m-CH2-A-CH2-(CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -S0-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH.
6) Os compostos (21) que se seguem, descritos no
Processo de Preparação 8, são importantes como
Petição 870180138821, de 08/10/2018, pág. 176/857
168 intermediários para preparar os compostos (1) de acordo com a presente invenção.
(21) onde R3, R4, A, m e n têm os mesmos significados que aqueles definidos acima, e R51 representa um grupo protetor para o grupo amino.
Dentre os intermediários supradescritos, são preferidos os compostos nos quais A na fórmula acima é um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -S0-, -S02-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH10 ou -SO2-NH.
7) Os compostos que se seguem, descritos no
Processo de Preparação 10, são importantes como intermediários para preparar os compostos (1) de acordo com a presente invenção. Mais especificamente, os seguintes compostos da forma trans (30), (31) e (32) opticamente ativos:
Petição 870180138821, de 08/10/2018, pág. 177/857
169 onde R3, m e n têm os mesmos significados que aqueles definidos acima, e R51 e R61 representam grupos protetores para o grupo amino, os enanciômeros (30a), (31a) e (32a) dos compostos acima, preparados de uma maneira similar:
N(CH2)m Z (CH2)n (CK2) / (CH2)„ (CH2)m^ (CH2)n
R51-N N-R61 RS-Ü N-R61 r5-K Íj-R61
Η Η , Η Η Η H (30a) (31a) ’ (32a) onde R3, m e n têm definidos acima, e R51 para o grupo amino, os (32b):
os mesmos significados que aqueles e R61 representam grupos protetores compostos da forma cis (30b), (31b) e
N—N-\
W7 TOn (CH2)7 (CK2)n (CH2)/ (CH2)n
RS1-NN-R61 R51-NN-R61 RS1-NÜR61
Η Η , Η Η Η H (30b) (31b) ’ (32b) onde R3, m e n têm os mesmos significados que aqueles 10 definidos acima, e R51 e R61 representam grupos protetores para o grupo amino, e os enanciômeros (30c), (31c) e (32c):
Petição 870180138821, de 08/10/2018, pág. 178/857
170 <CH2)/ z(CH2)n 61
R51—Ν Η
N-RD
Η (30c)
N—
-N
H trs' (31 c)
R\ (CH,)/
RS1—N H (CH2)n 61
N-R H (32c) onde R3, m e n têm os mesmos significados que aqueles definidos acima, e R51 e R61 representam grupos protetores para o grupo amino, são importantes como intermediários para preparar os compostos (1) de acordo com a presente invenção.
Os derivados diamínicos, de acordo com a presente invenção, apresentam intensos efeitos inibitórios sobre o fator X de coagulação sanguínea ativado, e assim sendo, são úteis em medicamentos para mamíferos, inclusive humanos, como anticoagulantes, agentes para prevenir e/ou tratar trombose ou embolia, agentes para prevenir e/ou tratar doenças trombóticas, e agentes para prevenir e/ou tratar infarto cerebral, embolia cerebral, infarto do miocárdio, angina do peito, infarto pulmonar, embolia pulmonar, doença de Buerger, trombose venosa profunda, síndrome da coagulação intravascular disseminada, formação de trombos após substituição de válvula ou articulação, formação de trombos e reoclusão após angioplastia, síndrome da reação inflamatória sistêmica (SIRS), síndrome da doença de múltiplos órgãos (MODS), formação de trombos durante a circulação extracorpórea, ou coagulação sanguínea após coleta de sangue.
Quando um composto de acordo com a presente de 08/10/2018, pág. 179/857
171 invenção é usado como um medicamento para o corpo humano, a dose fica dentro de uma faixa entre 1 mg e 1 g, de preferência 10 a 300 mg, por dia, para um adulto. A dose para animais varia de acordo com o objetivo (tratamento ou prevenção) da administração, tipo e porte do animal a ser tratado, tipo de contágio, e da condição da doença a ser atacada. Entretanto, genericamente, ela fica dentro de uma faixa entre 0,1 e 200 mg, de preferência 0,5 a 100 mg por guilograma de peso ao dia. Entrementes, a administração pode ser uma vez ao dia, ou pode ser dividida em 2 a 4 vezes ao dia. A dose diária pode exceder a faixa acima, caso necessário.
As composições medicinais gue compreendem o composto de acordo com a presente invenção podem ser preparadas selecionando uma forma de preparação apropriada de acordo com um método de preparação para a forma de preparação usada. Como exemplos das formas de preparação das composições medicinais gue compreendem o composto de acordo com a presente invenção como um componente principal, podem ser mencionados comprimidos, pós, grânulos, cápsulas, soluções, xaropes, elixires, suspensões oleosas ou aguosas, ou similares, para preparações orais.
No caso de uma injeção, pode-se usar um estabilizador, um conservante e um auxiliar de dissolução, em uma preparação. Uma solução gue pode conter esses auxiliares em alguns casos pode ser disponibilizada também como uma forma sólida para preparar antes do uso, embalando a solução em um recipiente e depois secando a solução por de 08/10/2018, pág. 180/857
172 liofilização, ou maneira similar. Uma dose ou doses da injeção podem estar contidas também dentro de um recipiente.
Como exemplos das formas de preparação para aplicação externa, podem ser mencionadas soluções, suspensões, emulsões, pomadas, géis, cremes, loções, atomizadores, emplastros ou similares.
Uma preparação sólida pode conter aditivos de uso farmacêutico além do composto da presente invenção. Por exemplo, cargas, extensores, ligantes, desintegradores, aceleradores de dissolução, agentes umectantes, etc., podem ser selecionados adequadamente e misturados, dando uma preparação.
Como exemplos de formas de preparação de uma preparação líquida, podem ser suspensões, emulsões, e similares, agente de suspensão, um emulsificante e/ou similares, em alguns casos.
Os compostos da presente invenção serão descritos detalhadamente abaixo nos itens (A) até (E).
(A): Um composto representado pela fórmula genérica (1):
mencionadas soluções, Elas podem conter um
Q1-C (=0) -N (R1) -Q2-N (R2) -T^—Q3 (1) onde
R1 e R2 representam, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila ou um grupo alcóxi;
Q1 representa um grupo hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico saturado ou insaturado, de 08/10/2018, pág. 181/857
173 com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
Q2 representa o seguinte grupo:
onde Q4 significa um grupo alquileno com 1 a 8 átomos de carbono, um grupo alquenileno com 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -S0-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH, e os números 1 e 2 indicam posições; e
R3 e R4 são substituintes no(s) átomo(s) de carbono, átomo(s) de nitrogênio ou átomo(s) de enxofre de um anel que compreende Q4 e são, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila, um grupo alquenila, um grupo alquinila, um átomo de halogênio, um grupo halo-alquila, um grupo ciano, grupo ciano-alquila, grupo amino, grupo amino-alquila, grupo Nalquil-amino-alquila, grupo N,N-dialquil-amino-alquila, grupo acila, grupo acil-alquila, grupo acil-amino que pode de 08/10/2018, pág. 182/857
174 ser substituído, grupo alcóxi-imino, grupo hidróxi-imino, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxialquila, grupo hidróxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo alcóxi-carbonila, grupo alcóxicarbonil-alquila, grupo alcóxi-carbonil-alquil-amino, grupo carbóxi-alquil-amino, grupo alcóxi-carbonil-amino, grupo alcóxi-carbonil-amino-alquila, grupo carbamoíla, grupo Nalquil-carbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenilcarbamoíla, grupo N-alquenil-carbamoil-alquila, grupo Nalquenil-N-alquil-carbamoíla, grupo N-alquenil-N-alquilcarbamoil-alquila, grupo N-alcóxi-carbamoíla, grupo Nalquil-N-alcóxi-carbamoíla, grupo N-alcóxi-carbamoilalquila, grupo N-alquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquil-sulfonila, grupo alquil-sulfonilalquila, grupo carbonila heterocíclico com 3 a 6 membros que pode ser substituído, grupo carbamoil-alquila, grupo Nalquil-carbamoil-alquila que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo carbamoilóxi-alquila, grupo N-alquil-carbamoilóxi-alquila, grupo N,N-dialquil-carbamoilóxi-alquila, grupo carbonilalquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo arila, grupo aralquila, grupo heteroarila, grupo heteroaril-alquila, de 08/10/2018, pág. 183/857
175 grupo alguil-sulfonil-amino, grupo aril-sulfonil-amino, grupo alguil-sulfonil-amino-alguila, grupo aril-sulfonilamino-alguila, grupo alguil-sulfonil-amino-carbonila, grupo aril-sulfonil-amino-carbonila, grupo alguil-sulfonil-aminocarbonil-alguila, grupo aril-sulfonil-amino-carbonilalguila, grupo oxo, grupo carbamoilóxi, grupo aralguilóxi, grupo carbóxi-alguilóxi, grupo acilóxi, grupo acilóxialguila, grupo aril-sulfonila, grupo alcóxi-carbonil-alguilsulfonila, grupo carbóxi-alguil-sulfonila, grupo alcóxicarbonil-acila, grupo alcóxi-alguilóxi-carbonila, grupo hidróxi-acila, grupo alcóxi-acila, grupo halo-acila, grupo carbóxi-acila, grupo amino-acila, grupo acilóxi-acila, grupo acilóxi-alguil-sulfonila, grupo hidróxi-alguil-sulfonila, grupo alcóxi-alguil-sulfonila, grupo sulfonila heterocíclico com 3 a 6 membros, gue pode ser susbtituído, grupo N-alguilamino-acila, grupo N,N-dialguil-amino-acila, grupo N,Ndialguil-carbamoil-acila gue pode ter um substituinte no(s) grupo(s) alguila, grupo N,N-dialguil-carbamoil-alguilsulfonila gue pode ter um substituinte no(s) grupo(s) alguila, grupo alguil-sulfonil-acila, ou similares, ou R3 e R4 juntos denotam um grupo alguileno com 1 a 5 átomos de carbono, um grupo alguenileno com 2 a 5 átomos de carbono, um grupo alguilenodioxi com 1 a 5 átomos de carbono, ou um grupo carbonildioxi;
|
Q3 |
representa |
um grupo arila |
gue |
pode ser |
|
substituído, |
um grupo |
aril-alguenila |
gue |
pode ser |
|
susbtituído, |
um grupo |
aril-alguinila |
gue |
pode ser |
|
substituído, |
um grupo heteroarila gue pode |
ser |
substituído, |
de 08/10/2018, pág. 184/857
176 um grupo heteroaril-alquenila que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído; e
T1 representa um grupo carbonila ou um grupo sulfonila;
um seu sal, um seu solvato, ou um seu N-óxido.
B) Um composto representado pela fórmula genérica (D :
Q1-Q2-C (=0) -N (R1) -Q3-N (R2) -T^—Q4 (1) onde
R1 e R2 representam, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila ou um grupo alcóxi;
Q1 representa um grupo hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
Q2 representa uma ligação simples, um grupo hidrocarboneto cíclico bivalente, saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico bivalente saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto de 08/10/2018, pág. 185/857
177 bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído;
Q3 representa o seguinte grupo:
onde Q5 significa um grupo alquileno com 1 a 8 átomos de carbono, um grupo alquenileno com 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e
3,
Ά' significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH; e
R3 e R4 são substituintes no(s) átomo(s) de carbono, átomo(s) de nitrogênio ou átomo(s) de enxofre de um anel que compreende Q5 e são, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila, um grupo alquenila, um grupo alquinila, um átomo de halogênio, um grupo halo-alquila, um grupo ciano, grupo ciano-alquila, grupo amino, grupo amino-alquila, grupo Nalquil-amino-alquila, grupo N,N-dialquil-amino-alquila, grupo acila, grupo acil-alquila, grupo acil-amino que pode ser substituído, grupo alcóxi-imino, grupo hidróxi-imino, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxide 08/10/2018, pág. 186/857
178 alquila, grupo hidróxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo alcóxi-carbonila, grupo alcóxicarbonil-alquila, grupo alcóxi-carbonil-alquil-amino, grupo carbóxi-alquil-amino, grupo alcóxi-carbonil-amino, grupo alcóxi-carbonil-amino-alquila, grupo carbamoíla, grupo Nalquil-carbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenilcarbamoíla, grupo N-alquenil-carbamoil-alquila, grupo Nalquenil-N-alquil-carbamoíla, grupo N-alquenil-N-alquilcarbamoil-alquila, grupo N-alcóxi-carbamoíla, grupo Nalquil-N-alcóxi-carbamoíla, grupo N-alcóxi-carbamoilalquila, grupo N-alquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquil-sulfonila, grupo alquil-sulfonilalquila, grupo carbonila heterocíclico com 3 a 6 membros que pode ser substituído, grupo carbamoil-alquila, grupo Nalquil-carbamoil-alquila que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo carbamoilóxi-alquila, grupo N-alquil-carbamoilóxi-alquila, grupo N,N-dialquil-carbamoilóxi-alquila, grupo carbonilalquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo arila, grupo aralquila, grupo heteroarila, grupo heteroaril-alquila, grupo alquil-sulfonil-amino, grupo aril-sulfonil-amino, grupo alquil-sulfonil-amino-alquila, grupo aril-sulfonilde 08/10/2018, pág. 187/857
179 amino-alquila, grupo alquil-sulfonil-amino-carbonila, grupo aril-sulfonil-amino-carbonila, grupo alquil-sulfonil-aminocarbonil-alquila, grupo aril-sulfonil-amino-carbonilalquila, grupo oxo, grupo carbamoilóxi, grupo aralquilóxi, grupo carbóxi-alquilóxi, grupo acilóxi, grupo acilóxialquila, grupo aril-sulfonila, grupo alcóxi-carbonil-alquilsulfonila, grupo carbóxi-alquil-sulfonila, grupo alcóxicarbonil-acila, grupo alcóxi-alquilóxi-carbonila, grupo hidróxi-acila, grupo alcóxi-acila, grupo halo-acila, grupo carbóxi-acila, grupo amino-acila, grupo acilóxi-acila, grupo acilóxi-alquil-sulfonila, grupo hidróxi-alquil-sulfonila, grupo alcóxi-alquil-sulfonila, grupo sulfonila heterocíclico com 3 a 6 membros, que pode ser susbtituído, grupo N-alquilamino-acila, grupo N,N-dialquil-amino-acila, grupo N,Ndialquil-carbamoil-acila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquilsulfonila que pode ter um substituinte no(s) grupo(s) alquila, grupo alquil-sulfonil-acila, ou similares, ou R3 e R4 juntos denotam um grupo alquileno com 1 a 5 átomos de carbono, um grupo alquenileno com 2 a 5 átomos de carbono, um grupo alquilenodioxi com 1 a 5 átomos de carbono, ou um grupo carbonildioxi;
|
Q4 |
representa |
um grupo arila |
que |
pode ser |
|
substituído, |
um grupo |
aril-alquenila |
que |
pode ser |
|
susbtituído, |
um grupo |
aril-alquinila |
que |
pode ser |
|
substituído, |
um grupo heteroarila que pode |
ser |
substituído, |
um grupo heteroaril-alquenila que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, de 08/10/2018, pág. 188/857
180 saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído; e
T1 representa um grupo carbonila, um grupo sulfonila, ou um grupo -C(=0)-C(=0)-NR')-, onde R' significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi;
um seu sal, um seu solvato, ou um seu N-óxido.
C) Um composto representado pela fórmula genérica (D :
Q1-Q2-C (=0) -N (R1) -Q3-N (R2) -T^—Q4 (1) onde
R1 e R2 representam, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila ou um grupo alcóxi;
Q1 representa um grupo hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
Q2 representa uma ligação simples, um grupo hidrocarboneto cíclico bivalente, saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico bivalente saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto de 08/10/2018, pág. 189/857
181 bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído;
Q3 representa o seguinte grupo:
onde Q5 significa um grupo alquileno com 1 a 8 átomos de carbono, um grupo alquenileno com 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e
3,
Ά' significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -SO-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH; e
R3 e R4 são substituintes no(s) átomo(s) de carbono, átomo(s) de nitrogênio ou um átomo de enxofre de um anel que compreende Q5 e são, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila, um grupo alquenila, um grupo alquinila, um átomo de halogênio, um grupo halo-alquila, um grupo ciano, grupo ciano-alquila, grupo amino, grupo amino-alquila, grupo Nalquil-amino-alquila, grupo N,N-dialquil-amino-alquila, grupo acila, grupo acil-alquila, grupo acil-amino que pode ser substituído, grupo alcóxi-imino, grupo hidróxi-imino, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxide 08/10/2018, pág. 190/857
182 alquila, grupo hidróxi-alquila, grupo carboxila, grupo carbóxi-alquila, grupo alcóxi-carbonila, grupo alcóxicarbonil-alquila, grupo alcóxi-carbonil-alquil-amino, grupo carbóxi-alquil-amino, grupo alcóxi-carbonil-amino, grupo alcóxi-carbonil-amino-alquila, grupo carbamoíla, grupo Nalquil-carbamoíla que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenilcarbamoíla, grupo N-alquenil-carbamoil-alquila, grupo Nalquenil-N-alquil-carbamoíla, grupo N-alquenil-N-alquilcarbamoil-alquila, grupo N-alcóxi-carbamoíla, grupo Nalquil-N-alcóxi-carbamoíla, grupo N-alcóxi-carbamoilalquila, grupo N-alquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquil-sulfonila, grupo alquil-sulfonilalquila, grupo carbonila heterocíclico com 3 a 6 membros que pode ser substituído, grupo carbamoil-alquila, grupo Nalquil-carbamoil-alquila que pode ter um substituinte no grupo alquila, grupo N,N-dialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo carbamoilóxi-alquila, grupo N-alquil-carbamoilóxi-alquila, grupo N,N-dialquil-carbamoilóxi-alquila, grupo carbonilalquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo arila, grupo aralquila, grupo heteroarila, grupo heteroaril-alquila, grupo alquil-sulfonil-amino, grupo aril-sulfonil-amino, grupo alquil-sulfonil-amino-alquila, grupo aril-sulfonilde 08/10/2018, pág. 191/857
183 amino-alquila, grupo alquil-sulfonil-amino-carbonila, grupo aril-sulfonil-amino-carbonila, grupo alquil-sulfonil-aminocarbonil-alquila, grupo aril-sulfonil-amino-carbonilalquila, grupo oxo, grupo carbamoilóxi, grupo aralquilóxi, grupo carbóxi-alquilóxi, grupo acilóxi, grupo acilóxialquila, grupo aril-sulfonila, grupo alcóxi-carbonil-alquilsulfonila, grupo carbóxi-alquil-sulfonila, grupo alcóxicarbonil-acila, grupo alcóxi-alquilóxi-carbonila, grupo hidróxi-acila, grupo alcóxi-acila, grupo halo-acila, grupo carbóxi-acila, grupo amino-acila, grupo acilóxi-acila, grupo acilóxi-alquil-sulfonila, grupo hidróxi-alquil-sulfonila, grupo alcóxi-alquil-sulfonila, grupo sulfonila heterocíclico com 3 a 6 membros, que pode ser susbtituído, grupo N-alquilamino-acila, grupo N,N-dialquil-amino-acila, grupo N,Ndialquil-carbamoil-acila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquilsulfonila que pode ter um substituinte no(s) grupo(s) alquila, grupo alquil-sulfonil-acila, ou similares, ou R3 e R4 juntos denotam um grupo alquileno com 1 a 5 átomos de carbono, um grupo alquenileno com 2 a 5 átomos de carbono, um grupo alquilenodioxi com 1 a 5 átomos de carbono, ou um grupo carbonildioxi;
|
Q4 |
representa |
um grupo arila |
que |
pode ser |
|
substituído, |
um grupo |
aril-alquenila |
que |
pode ser |
|
susbtituído, |
um grupo |
aril-alquinila |
que |
pode ser |
|
substituído, |
um grupo heteroarila que pode |
ser |
substituído, |
um grupo heteroaril-alquenila que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, de 08/10/2018, pág. 192/857
184 saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído; e
T1 representa um grupo carbonila, um grupo sulfonila, grupo -C(=0)-C(=0)-NR')-, onde R' significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C(=0)-A1-N(R)-, onde A1 denota um grupo alquileno com 1 a 5 átomos de carbono, que pode ser substituído, e R significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C(=0)NH-, grupo -C(=S)-NH-, grupo -C(=0)-NH-NH-, grupo -C(=0)-A2C (=0) -, onde A2 significa uma ligação simples ou um grupo alquileno com 1 a 5 átomos de carbono, um grupo -C(=0)-A3C (=0) -NH-, onde A3 denota um grupo alquileno com 1 a 5 átomos de carbono;
um seu sal, um seu solvato, ou um seu N-óxido.
D) Um composto representado pela fórmula genérica (D :
qi_q2_to_n (Ri) -Q3-N(R2) -Ti-Q4 (1) onde
R1 e R2 representam, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila ou um grupo alcóxi;
Q1 representa um grupo hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou de 08/10/2018, pág. 193/857
185 insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
Q2 representa uma ligação simples, um grupo hidrocarboneto cíclico bivalente, saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico bivalente saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído;
Q3 representa o seguinte grupo:
onde Q5 significa um grupo alquileno com 1 a 8 átomos de carbono, um grupo alquenileno com 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n~, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -S0-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH, e R3 e R4 são substituintes no(s) átomo(s) de carbono, átomo(s) de nitrogênio ou um átomo de enxofre de um anel que compreende Q5 e são, um independentemente do outro, um átomo de
Petição 870180138821, de 08/10/2018, pág. 194/857
186 hidrogênio, um grupo hidroxila, um grupo alguila, um grupo alguenila, um grupo alguinila, um átomo de halogênio, um grupo halo-alguila, um grupo ciano, grupo ciano-alguila, grupo amino, grupo amino-alguila, grupo N-alguil-aminoalguila, grupo N,N-dialguil-amino-alguila, grupo acila, grupo acil-alguila, grupo acil-amino gue pode ser substituído, grupo alcóxi-imino, grupo hidróxi-imino, grupo acil-amino-alguila, grupo alcóxi, grupo alcóxi-alguila, grupo hidróxi-alguila, grupo carboxila, grupo carbóxialguila, grupo alcóxi-carbonila, grupo alcóxi-carbonilalguila, grupo alcóxi-carbonil-alguil-amino, grupo carbóxialguil-amino, grupo alcóxi-carbonil-amino, grupo alcóxicarbonil-amino-alguila, grupo carbamoíla, grupo N-alguilcarbamoíla gue pode ter um substituinte no grupo alguila, grupo N,N-dialguil-carbamoíla gue pode ter um substituinte no(s) grupo(s) alguila, grupo N-alguenil-carbamoíla, grupo N-alguenil-carbamoil-alguila, grupo N-alguenil-N-alguilcarbamoíla, grupo N-alguenil-N-alguil-carbamoil-alguila, grupo N-alcóxi-carbamoíla, grupo N-alguil-N-alcóxicarbamoíla, grupo N-alcóxi-carbamoil-alguila, grupo Nalguil-N-alcóxi-carbamoil-alguila, grupo carbazoíla gue pode ser substituído com 1 a 3 grupos alguila, grupo alguilsulfonila, grupo alguil-sulfonil-alguila, grupo carbonila heterocíclico com 3 a 6 membros gue pode ser substituído, grupo carbamoil-alguila, grupo N-alguil-carbamoil-alguila gue pode ter um substituinte no grupo alguila, grupo N,Ndialguil-carbamoil-alguila gue pode ter um substituinte no(s) grupo(s) alguila, grupo carbamoilóxi-alguila, grupo Nde 08/10/2018, pág. 195/857
187 alquil-carbamoilóxi-alquila, grupo N,N-dialquil-carbamoilóxi -alquila, grupo carbonil-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo arila, grupo aralquila, grupo heteroarila, grupo heteroaril-alquila, grupo alquil-sulfonil-amino, grupo arilsulfonil-amino, grupo alquil-sulfonil-amino-alquila, grupo aril-sulfonil-amino-alquila, grupo alquil-sulfonil-aminocarbonila, grupo aril-sulfonil-amino-carbonila, grupo alquil-sulfonil-amino-carbonil-alquila, grupo aril-sulfonilamino-carbonil-alquila, grupo oxo, grupo carbamoilóxi, grupo aralquilóxi, grupo carbóxi-alquilóxi, grupo acilóxi, grupo acilóxi-alquila, grupo aril-sulfonila, grupo alcóxicarbonil-alquil-sulfonila, grupo carbóxi-alquil-sulfonila, grupo alcóxi-carbonil-acila, grupo alcóxi-alquilóxicarbonila, grupo hidróxi-acila, grupo alcóxi-acila, grupo halo-acila, grupo carbóxi-acila, grupo amino-acila, grupo acilóxi-acila, grupo acilóxi-alquil-sulfonila, grupo hidróxi-alquil-sulfonila, grupo alcóxi-alquil-sulfonila, grupo sulfonila heterocíclico com 3 a 6 membros, que pode ser susbtituído, grupo N-alquil-amino-acila, grupo N,Ndialquil-amino-acila, grupo N,N-dialquil-carbamoil-acila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,Ndialquil-carbamoil-alquil-sulfonila que pode ter um substituinte no(s) grupo(s) alquila ou grupo alquilsulfonil-acila, ou R3 e R4 juntos denotam um grupo alquileno com 1 a 5 átomos de carbono, um grupo alquenileno com 2 a 5 átomos de carbono, um grupo alquilenodioxi com 1 a 5 átomos de 08/10/2018, pág. 196/857
188 de carbono, ou um grupo carbonildioxi;
|
Q4 |
representa |
um grupo arila |
que |
pode ser |
|
substituído, |
um grupo |
aril-alquenila |
que |
pode ser |
|
susbtituído, |
um grupo |
aril-alquinila |
que |
pode ser |
|
substituído, |
um grupo heteroarila que pode |
ser |
substituído, |
um grupo heteroaril-alquenila que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
T° representa um grupo carbonila ou tiocarbonila;
e
T1 representa um grupo carbonila, um grupo sulfonila, grupo -C(=0)-C(=0)-NR')-, grupo -C(=S)-C(=0)N(R')-, grupo -C(=O)-C(=S)-N(R')-, -C(=S)-C(=S)-N(R')-, onde R' significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C(=0)-A^—N(R)-, onde A1 denota um grupo alquileno com 1 a 5 átomos de carbono, que pode ser substituído, e R significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C(=0)-NH-, grupo -C(=S)-NH-, grupo -C(=0)-NHNH-, grupo -C(=0)-A2-C(=0)-, onde A2 significa uma ligação simples ou um grupo alquileno com 1 a 5 átomos de carbono, um grupo -C (=0) -A3-C (=0) -NH-, onde A3 denota um grupo alquileno com 1 a 5 átomos de carbono, um grupo -C (=0) C (=N0Ra)-N (Rb)-, grupo -C (=S)-C (=N0Ra)-N (Rb)-, onde Ra significa um átomo de hidrogênio, um grupo alquila ou grupo alcanoíla, e Rb denota um átomo de hidrogênio, um grupo de 08/10/2018, pág. 197/857
189 hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=0)-N=N-, grupo -C(=S)-N=N-, ou um grupo tiocarbonila;
um seu sal, um seu solvato, ou um seu N-óxido.
E) Um composto representado pela fórmula genérica (D :
Q1_Q2_T0_N(R1) -Q3-N(R2) -Ti-Q4 (1) onde
R1 e R2 representam, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila ou um grupo alcóxi;
Q1 representa um grupo hidrocarboneto cíclico saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
Q2 representa uma ligação simples, um grupo hidrocarboneto cíclico bivalente, saturado ou insaturado, com 5 ou 6 membros, que pode ser substituído, um grupo heterocíclico bivalente saturado ou insaturado, com 5 a 7 membros, que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, bivalente, saturado ou insaturado, que pode ser substituído;
Q3 representa o seguinte grupo:
de 08/10/2018, pág. 198/857
190
onde Q5 significa um grupo alquileno com 1 a 8 átomos de carbono, um grupo alquenileno com 2 a 8 átomos de carbono, ou um grupo - (CH2) m-CH2-A-CH2- (CH2) n-, onde m e n são, um independentemente do outro, 0 ou um número inteiro entre 1 e 3, e A significa um átomo de oxigênio, um átomo de nitrogênio, um átomo de enxofre, -S0-, -SO2-, -NH-, -O-NH-,
-NH-NH-, -S-NH-, -SO-NH- ou -SO2-NH, e R3 e R4 são substituintes no(s) átomo(s) de carbono, átomo(s) de nitrogênio ou um átomo de enxofre de um anel que compreende Q5 e são, um independentemente do outro, um átomo de hidrogênio, um grupo hidroxila, um grupo alquila, um grupo alquenila, um grupo alquinila, um átomo de halogênio, um grupo halo-alquila, um grupo ciano, grupo ciano-alquila, grupo amino, grupo amino-alquila, grupo N-alquil-aminoalquila, grupo N,N-dialquil-amino-alquila, grupo acila, grupo acil-alquila, grupo acil-amino que pode ser substituído, grupo alcóxi-imino, grupo hidróxi-imino, grupo acil-amino-alquila, grupo alcóxi, grupo alcóxi-alquila, grupo hidróxi-alquila, grupo carboxila, grupo carbóxialquila, grupo alcóxi-carbonila, grupo alcóxi-carbonilalquila, grupo alcóxi-carbonil-alquil-amino, grupo carbóxialquil-amino, grupo alcóxi-carbonil-amino, grupo alcóxicarbonil-amino-alquila, grupo carbamoíla, grupo N-alquilcarbamoíla que pode ter um substituinte no grupo alquila, de 08/10/2018, pág. 199/857
191 grupo N,N-dialquil-carbamoíla que pode ter um substituinte no(s) grupo(s) alquila, grupo N-alquenil-carbamoíla, grupo N-alquenil-carbamoil-alquila, grupo N-alquenil-N-alquilcarbamoíla, grupo N-alquenil-N-alquil-carbamoil-alquila, grupo N-alcóxi-carbamoíla, grupo N-alquil-N-alcóxicarbamoíla, grupo N-alcóxi-carbamoil-alquila, grupo Nalquil-N-alcóxi-carbamoil-alquila, grupo carbazoíla que pode ser substituído com 1 a 3 grupos alquila, grupo alquilsulfonila, grupo alquil-sulfonil-alquila, grupo carbonila heterocíclico com 3 a 6 membros que pode ser substituído, grupo carbamoil-alquila, grupo N-alquil-carbamoil-alquila que pode ter um substituinte no grupo alquila, grupo N,Ndialquil-carbamoil-alquila que pode ter um substituinte no(s) grupo(s) alquila, grupo carbamoilóxi-alquila, grupo Nalquil-carbamoilóxi-alquila, grupo N,N-dialquilcarbamoilóxi-alquila, grupo carbonil-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo carbonilóxi-alquila heterocíclico com 3 a 6 membros, que pode ser substituído, grupo arila, grupo aralquila, grupo heteroarila, grupo heteroaril-alquila, grupo alquilsulfonil-amino, grupo aril-sulfonil-amino, grupo alquilsulfonil-amino-alquila, grupo aril-sulfonil-amino-alquila, grupo alquil-sulfonil-amino-carbonila, grupo aril-sulfonilamino-carbonila, grupo alquil-sulfonil-amino-carbonilalquila, grupo aril-sulfonil-amino-carbonil-alquila, grupo oxo, grupo carbamoilóxi, grupo aralquilóxi, grupo carbóxialquilóxi, grupo acilóxi, grupo acilóxi-alquila, grupo arilsulfonila, grupo alcóxi-carbonil-alquil-sulfonila, grupo de 08/10/2018, pág. 200/857
192 carbóxi-alquil-sulfonila, grupo alcóxi-carbonil-acila, grupo alcóxi-alquilóxi-carbonila, grupo hidróxi-acila, grupo alcóxi-acila, grupo halo-acila, grupo carbóxi-acila, grupo amino-acila, grupo acilóxi-acila, grupo acilóxi-alquilsulfonila, grupo hidróxi-alquil-sulfonila, grupo alcóxialquil-sulfonila, grupo sulfonila heterocíclico com 3 a 6 membros, que pode ser susbtituído, grupo N-alquil-aminoacila, grupo N,N-dialquil-amino-acila, grupo N,N-dialquilcarbamoil-acila que pode ter um substituinte no(s) grupo(s) alquila, grupo N,N-dialquil-carbamoil-alquil-sulfonila que pode ter um substituinte no(s) grupo (s) alquila, grupo alquil-sulfonil-acila, grupo amino-carbotioíla, grupo Nalquil-amino-carbotioíla, grupo N,N-dialquil-aminocarbotioíla ou um grupo alcóxi-alquil-(tiocarbonila), ou R3 e R4 juntos denotam um grupo alquileno com 1 a 5 átomos de carbono, um grupo alquenileno com 2 a 5 átomos de carbono, um grupo alquilenodioxi com 1 a 5 átomos de carbono, ou um grupo carbonildioxi;
|
Q4 |
representa |
um grupo arila |
que |
pode ser |
|
substituído, |
um grupo |
aril-alquenila |
que |
pode ser |
|
susbtituído, |
um grupo |
aril-alquinila |
que |
pode ser |
|
substituído, |
um grupo heteroarila que pode |
ser |
substituído, |
um grupo heteroaril-alquenila que pode ser substituído, um grupo hidrocarboneto bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído, ou um grupo heterocíclico, bicíclico ou tricíclico fundido, saturado ou insaturado, que pode ser substituído;
T° representa um grupo carbonila ou tiocarbonila;
de 08/10/2018, pág. 201/857
193
T1 representa um grupo carbonila, um grupo sulfonila, grupo -C(=0)-C(=0)-NR')-, grupo -C(=S)-C(=0)N(R')-, grupo -C(=0)-C(=S)-N(R')-, -C(=S)-C(=S)-N(R')-, onde R' significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C(=0)-A1-N (R)-, onde A1 denota um grupo alquileno com 1 a 5 átomos de carbono, que pode ser substituído, e R significa um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou um grupo alcóxi, grupo -C(=0)-NH-, grupo -C(=S)-NH-, grupo -C(=0)-NHNH-, grupo -C(=0)-A2-C(=0)-, onde A2 significa uma ligação simples ou um grupo alquileno com 1 a 5 átomos de carbono, um grupo -C (=0)-A3-C (=0)-NH-, onde A3 denota um grupo alquileno com 1 a 5 átomos de carbono, um grupo -C(=0)C (=N0Ra)-N (Rb)-, grupo -C (=S)-C (=N0Ra)-N (Rb)onde Ra significa um átomo de hidrogênio, um grupo alquila ou grupo alcanoíla, e Rb denota um átomo de hidrogênio, um grupo hidroxila, grupo alquila ou grupo alcóxi, grupo -C(=O)-N=N-, grupo -C(=S)-N=N-, ou um grupo tiocarbonila;
um seu sal, um seu solvato, ou um seu N-óxido.
EXEMPLOS
Entretanto, a presente invenção não está limitada a estes exemplos.
Exemplo Referencial 1
Piridin-4-il-carbamato de t-butila:
de 08/10/2018, pág. 202/857
194
Dissolveu-se 4-amino-piridina (10 g) em tetraidrofurano (500 ml) , adicionou-se dicarbonato de di-tbutila (25,5 g) à solução, e a mistura foi agitada à temperatura ambiente por 10 min. A mistura da reação resultante foi concentrada sob pressão reduzida, e os sólidos depositados foram lavados com hexano, para obter o composto do título.
ΗΜΝ-^ (CDC13) δ: l,53(9H,s), 6, 86 (1H, br. s) , 7,30 (2H, DD, J=
1,5, 4,9Hz), 8,44 (2H, DD, J=l, 5, 4,9Hz).
MS (FAB) m/z: 195 (M+H)+.
Exemplo Referencial 2
3-sulfanil-piridin-4-il-carbamato de t-butila
SH
O composto obtido no Exemplo Referencial 1 (61,6
g) foi dissolvido em tetraidrofurano (2.000 ml), e a solução foi agitada a -78 oC por 10 min. Uma solução de n-butillítio em hexano (1,59 mol/1.500 ml) foi adicionada em gotas à solução, e a mistura foi agitada por 10 min e depois por 2 h sob resfriamento com gelo. Depois que a mistura da reação foi resfriada até -78 oC, adicionou-se enxofre em pó (12,2
g) , e a mistura resultante foi aquecida até a temperatura ambiente e agitada por 1 h. Adicionou-se água (1.000 ml) à mistura da reação, para separar uma camada aquosa. Depois de adicionar ácido clorídrico 3 N à camada aquosa, para
Petição 870180138821, de 08/10/2018, pág. 203/857
195 ajustar o pH da camada aquosa para 3 a 4, adicionou-se cloreto de metileno para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 50:1), para obter o composto do título (33,2 g) .
βΜΝ-^ (DMSO-de) δ: l,52(9H,s), 7, 89 (1H, d, J=6,4Hz) , 7,99(1H, d,J-6,4Hz), 8,20(lH,s), 9, 91 (1H, br. s) , .
MS (FAB) m/z: 227 (M+H)+.
Exemplo Referencial 3 tiazolo[5,4-c]-piridina:
O composto obtido no Exemplo Referencial 2 (33,2
g) foi dissolvido em ácido fórmico (250 ml), e a solução foi aquecida sob refluxo por 3 dias. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se ao resíduo uma solução aquosa 5 N de hidróxido de potássio (100 ml) e dietil-éter, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro, e o solvente foi então removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 25:1), para obter o composto do título (9,03 g).
de 08/10/2018, pág. 204/857
196
ΚΜΝ-^ (CDC13) δ: 8, 05 (1Η, d, J=5,4ΗΖ) , 8,70(1H,d,J=5,4Hz),
9,23(1H,s), 9,34(1H,s) .
MS (FAB) m/z: 137 (M+H)+.
Exemplo Referencial 4
5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridina:
O composto obtido no Exemplo Referencial 3 (1, 61
g) foi dissolvido em N,N-dimetil-formamida (50 ml), e adicionou-se à solução iodeto de metila (1,50 ml), a mistura da reação foi agitada a 80 oC por 4 h. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi dissolvido em metanol (100 ml), adicionou-se boro-hidreto de sódio (1,53 g), e a mistura resultante foi agitada à temperatura ambiente por 1 h. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se ao resíduo uma solução aquosa saturada de carbonato de potássio e dietil-éter, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro, e o solvente foi então removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 25:1), para obter o composto do título (1,28 g).
RMN-1!! (CDC13) δ: 2,52(3H,s), 2, 83 (2H, t, J=5, 9Hz) , 2,98(2H, t,J=5,9Hz), 3,70(2H,s), 8,63(lH,s).
MS (FAB) m/z: 155 (M+H)+.
Petição 870180138821, de 08/10/2018, pág. 205/857
197
Exemplo Referencial 5
5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxilato de lítio:
N
COOLi
O composto obtido no Exemplo Referencial 4 (6,43
g) foi dissolvido em tetraidrofurano absoluto (200 ml) , adicionou-se à solução n-butil-lítio (solução 1,47 N em hexano, 34,0 ml) em gotas a -78 oC, e a mistura resultante foi agitada por 4 0 min. Depois de borbulhar dióxido de carbono gasoso para dentro da mistura da reação a -78 oC por
1 h, a mistura da reação foi aquecida até a temperatura ambiente e depois concentrada sob pressão reduzida, para obter o composto do título (9,42 g).
ΗΜΝ-^ (DMSO-de) δ: 2,37(3H,s), 2, 64-2,77 (4H,m) , 3,54(2H,s). MS (FAB) m/z: 199 (M+H)+.
Exemplo Referencial 6
2-amino-6,7-diidrotiazolo[5,4-c]-piridino-5[4H]-carboxilato de t-butila:
Dissolveu-se l-t-butóxi-carbonil-4-piperidona (40,0 g) em ciclo-hexano (80 ml), e adicionou-se à solução o
Petição 870180138821, de 08/10/2018, pág. 206/857
198 ácido p-tolueno-sulfônico monoidratado (191 g) e pirrolidina (17,6 ml) . A mistura foi aquecida sob refluxo por 2 h,
|
enquanto se |
removia |
a |
água usando |
um sifão |
Dean-Stark. |
|
Depois que a |
mistura |
da |
reação foi |
concentrada |
sob pressão |
|
reduzida, o |
resíduo |
foi |
dissolvido |
em metanol |
(60 ml), e |
|
adicionou-se |
enxofre |
em |
pó (6,42 |
g) . Uma |
solução de |
|
cianamida (8 |
,44 g) |
em |
metanol (10 ml) foi |
adicionada |
lentamente em gotas à solução sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente por 5 h. Os materiais sólidos precipitados foram coletados por filtração, para obter o composto do título (31,0 g).
RNIN-iH (DMSO-de) δ: l,41(9H,s), 2, 44 (2H, t, J=5, 6Hz) , 3,57(2H, t,J=5,6HZ), 4,29(2H,s), 6,79(2H,s).
MS (EI) m/z: 255 (M+H)+.
Exemplo Referencial 7
2-bromo-6,7-diidrotiazolo[5,4-c]-piridino-5[4H]-carboxilato de t-butila:
’V
N
Br
Brometo de cobre (II) (1,05 g) foi colocado em suspensão em N,N-dimetil-formamida (20 ml), e adicionou-se nitrito de t-butila (0,696 ml) e o composto obtido no
Exemplo Referencial 6 (1,00 g) sob resfriamento com gelo, a mistura foi aquecida e agitada a 40 oC por 30 min. A mistura da reação foi concentrada sob pressão reduzida, e o de 08/10/2018, pág. 207/857
199 resíduo foi purificado por cromatografia sílica-gel (acetato de etila:hexano 1:5), composto do título (568 mg).
ΗΜΝ-^ (CDC13) δ: l,48(9H,s), 2, 85 (2H, br . s) , de coluna em para obter o
3,72(2H,br.s),
4,56(2H,br.s).
MS (FAB) m/z: 319 (M+H)+.
Exemplo Referencial 8 triflúor-acetato de 2-bromo-4,5,6,7-tetraidrotiazolo[5,4-c]piridina:
O composto obtido no Exemplo Referencial 7 (890 mg) foi dissolvido em cloreto de metileno (2 ml), e adicionou-se à solução o ácido triflúor-acético (15 ml), e a mistura foi agitada à temperatura ambiente por 30 segundos. A mistura da reação foi concentrada sob pressão reduzida, e adicinou-se dietil-éter ao resíduo. Os materiais sólidos precipitados foram coletados por filtração, para obter o composto do título (867 mg).
RMN-1!! (CDC13) δ: 2, 98 (2H, t, J=6, 1Hz) , 3, 45 (2H, t, J=6, 1Hz) ,
4,35(2H,s), 9, 53 (2H, br. s) .
MS (FAB) m/z: 219 (M+H)+.
Exemplo Referencial 9
2-bromo-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridina:
de 08/10/2018, pág. 208/857
200
O composto obtido no Exemplo Referencial 8 (422
mg) foi colocado em suspensão em cloreto de metileno (10 ml), e adicionou-se trietil-amina (0,356 ml) para se obter uma solução. Adicionou-se sucessivamente uma solução aquosa (solução a 35%, 0,202 ml) de formaldeído e triacetóxi-borohidreto de sódio (428 mg) à solução, e a mistura resultante foi agitada à temperatura ambiente por 1 h. Adicionou-se uma solução aquosa saturada (100 ml) de bicarbonato de sódio, cloreto de metileno (100 ml) e uma solução aquosa 3 N (3 ml) de hidróxido de sódio, à mistura da reação, para conduzir uma separação de líquidos. Depois que uma camada orgânica foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter o composto do título (286 mg).
RMN-iH (CDC13) δ: 2,49(3H,s), 2, 79 (2H, t, J=5,7Hz) , 2,85-2,93 (2H,m), 3,58(2H.t,J=l,8Hz).
MS (FAB) m/z: 233 (M+H)+.
Exemplo Referencial 10
5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxilato de lítio:
de 08/10/2018, pág. 209/857
201
O composto obtido no Exemplo Referencial 9 (531 mg) foi diddolvido em dietil-éter absoluto (20 ml) , adicionou-se n-butil-lítio (solução 1,54 N em hexano, 1,63 ml) em gotas a -78 oC, e a mistura foi agitada por 30 min sob resfriamento com gelo. Depois de passar dióxido de carbono por dentro da mistura da reação a -78 oC por 10 min, a mistura foi aquecida até a temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, para obter o composto do título (523 mg).
ΗΜΝ-^ (DMSO-de) δ: 2,37(3H,s), 2, 64-2, 85 (4H,m) , 3,54(2H,s). Exemplo Referencial 11
2-[ (E)-2-fenil-etenil]-oxazolo-4-carboxilato de etila:
A síntese foi conduzida de acordo com o relatório de Panek et al., J. Org. Chem. 61:6496, 1996. Bicarbonato de sódio (22,8 g) e bromo-pirivato de etila (10,5 ml) foram adicionados a uma solução de cinamida (10,0 g) em tetraidrofurano (250 ml) à temperatura ambiente, e a mistura foi aquecida sob refluxo por 48 h. A mistura da reação foi deixada resfriar até a temperatura ambiente, filtrada através de Celite, e depois concentrada sob pressão reduzida, para obter um resíduo. Adicionou-se anidrido triflúor-acético (30 ml) a uma solução deste resíduo em
Petição 870180138821, de 08/10/2018, pág. 210/857
202 tet raidrofurano (30 ml) a 0 °C, e a mistura foi aquecida gradualmente até a temperatura ambiente. Depois de agitar a mistura por 63 h, adicionou-se uma solução aquosa saturada (500 ml) de bicarbonato de sódio e acetato de etila (150 ml) à mistura da reação, e uma camada aquosa foi separada. A camada aquosa foi extraída com acetato de etila (150 ml) . As camadas orgânicas foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio (150 ml), secadas sobre sulfato de sódio anidro, e depois concentradas sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de hexano:acetato de etila 5:1 —> 3:1), para obter o composto do título (10,9 g) .
ΗΜΝ-^ (CDC13) δ: 1,41 (3H, t, J=7, 0Hz) , 4,42 (2H, q, J=7,0Hz) ,
6,96(1H,d,J=l,6,6Hz), 7,30-7,40(3H,m), 7,53(2H,d,J=6,8Hz),
7,63 (1H, d, J=16, 6Hz) , 8,20(lH,s).
Exemplo Referencial 12
2-[(E)-2-fenil-etenil]-oxazolo-4-carbaldeído:
Adicionou-se hidreto de diisobutil-alumínio (solução 1,0 N em hexano, 66 ml) em gotas a uma solução do 20 composto obtido no Exemplo Referencial 11 (8,57 g) em cloreto de metileno (80 ml) a -78 oC. Depois de 15 min, adicionou-se metanol (11 ml) em gotas, e a mistura foi
Petição 870180138821, de 08/10/2018, pág. 211/857
203 aquecida até a temperatura ambiente por 1 h. A mistura da reação foi filtrada através de Celite, e a substância pastosa resultante foi dissolvida em acetato de etila (200 ml) , e adicinou-se uma solução aquosa saturada (200 ml) de cloreto de amônio, e uma camada aquosa foi separada. A camada aquosa foi então extraída com cloreto de metileno (2 x 100 ml) . As camdas orgânicas resultantes foram coletadas e lavadas com uma solução aquosa saturada (100 ml) de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio (100 ml), combinadas com o filtrado obtido pela filtração através de Celite, e depois secadas sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de hexano:acetato de etila 5:1 —» cloreto de metileno:metanol
10:1), para obter o composto do título (5,86 g).
RMN-XH (CDC13) δ: 6,96(1H,d,J=16,6Hz), 7,35-7,45 (3H,m) , 7,56 (2H, d, J=6, 4Hz) , 7, 67 (lH,d, J=16, 6Hz) , 8,26(lH,s), 9,98(lH,s). MS (FAB) m/z: 200 (M+H)+.
Exemplo Referencial 13
2-[ (E)-2-fenil-etenil]-4-vinil-oxazol:
Adicionou-se n-butil-lítio (solução 1,54 N em hexano, 14,2 ml) em gotas a uma solução de brometo de metilPclição 870180138821, de 08/10/2018, pág. 212/857
204 trifenil-fosfônio (8,16 g) em tetraidrofurano (80 ml) a 0 oC, e a mistura foi agitada à temperatura ambiente por 30 min. A mistura da reação foi resfriada novamente até 0 oC, adicionou-se uma solução do composto obtido no Exemplo Refernecial 12 (3,64 g) em tetraidrofurano (20 ml), e a mistura foi aquecida até a temperatura ambiente. Depois de agitar por 2 h, adicionou-se água (200 ml) e acetato de etila (100 ml), e uma camada aquosa foi separada. A camada aquosa foi extraída com acetato de etila (50 ml) . Depois que as camadas orgânicas foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio (100 ml) e secadas sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1 —> 3:1), para obter o composto do título (2,84 g).
RMN-1!! (CDC13) δ: 5, 33 (1H, dd, J=1, 5, 10,7Hz), 5, 98(1H, dd,J=
1,5, 17,6Hz), 6, 56 (1H, dd, J=10,7, 17,6Hz), 6,95(lH,d, J=16, 6
Hz), 7,31-7,42(3H,m), 7,49-7,56(4H,m).
MS (FAB) m/z: 198 (M+H)+.
Exemplo Referencial 14
2-{2-[ (E)-2-fenil-etenil]-oxazol-4-il}-etanol:
Adicionou-se 9-borabiciclo[3.3.1]-nonano (solução de 08/10/2018, pág. 213/857
205
0,5 N em tetraidrofurano, 158 ml) a uma solução do composto obtido no Exemplo Referencial 13 (13,0 g) em tetraidrofurano (500 ml), e a mistura foi agitada à temperatura ambiente por 15 h. Adicionou-se sucessivamente água (10 ml), uma solução aquosa 3 N (80 ml) de hidróxido de sódio e solução aquosa de peróxido de hidrogênio (80 ml) , em gotas, à mistura da reação a 0 oC, e a mistura foi agitada à temperatura ambiente por 6 h. Depois de adicionar água (600 ml) e acetato de etila (200 ml) à mistura da reação resultante, para separar uma camada aquosa, a camada aquosa foi extraída com acetato de etila (200 ml) . Depois que as camadas orgânicas foram coletadas, lavadas com solução aquosa saturada de cloreto de sódio (200 ml) e secadas sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1 —> somente acetato de etila), para obter o composto do título (14,1 g).
RMN-1!! (CDC13) δ: 2,09 (1H, br. s) , 2, 80 (2H, t, J=5, 6Hz) , 3,9020 3, 97(2H,m), 6, 91 (1H, d, J=16, 6Hz) , 7,30-7, 42 (4H, m) , 7,43-7,56 (3H,m) .
MS (FAB) m/z: 216 (M+H)+.
Exemplo Referencial 15
2-(2-{2-[(E)-2-fenil-etenil]-oxazol-4-il}-etii)
-lH-isoindol-1,3(2H)-diona:
Petição 870180138821, de 08/10/2018, pág. 214/857
206
Adicionou-se ftalimida (200 mg), trifenilfosfina (357 mg) e azodicarboxilato de dietila (0,214 ml) a uma solução do composto obtido no Exemplo Referencial 14 (292 mg) em tetraidrofurano (15 ml) à temperatura ambiente, e a mistura foi agitada por 4 h. O solvente da mistura da reação foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (447 mg).
ΗΜΝ-^ (CDC13) δ: 2, 98 (2H, t, J=7,2Hz) , 4,03 (2H, t, J=7,2Hz) ,
6, 88(1H,d,J=16,6Hz), 7, 28-7, 45 (5H,m), 7,48(2H,d,J=7,3Hz),
7,71(2H,dd,J=2,9, 5,4Hz), 7,84(2H,dd,J=2,9, 5,4Hz),
MS (FAB) m/z: 345 (M+H)+.
Exemplo Referencial 16
2-{2-[(E)-2-fenil-etenil]-oxazol-4-il}-etilcarbamato de t-butila:
Depois de adicionar hidrazina monoidratada (1,50 ml) a uma solução do composto obtido no Exemplo Referencial 15 (6,40 g) em etanol (150 ml) à temperatura ambiente e agitar a mistura por 1 h, adicionou-se novamente hidrazina monidratada (0,500 ml) à temperatura ambiente, e a mistura foi agitada por 2 h. Adicionou-se cloreto de metileno (150
Petição 870180138821, de 08/10/2018, pág. 215/857
207 ml), uma solução aquosa saturada (150 ml) de bicarbonato de sódio e dicarbonato de di-t-butila (13,4 g) , à mistura da reação à temperatura ambiente. Depois de agitar por 30 min, uma camada aquosa foi separada e extraída com cloreto de metileno (50 ml). As camadas orgânicas resultantes foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi então removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1 —> 1:1), para obter o composto do título (5,06 g).
ΗΜΝ-^ (CDC13) δ: l,45(9H,s), 2, 75 (2H, t, J=6, 6Hz) , 3,46(2H,dt, J=5,9, 6,6Hz), 4, 92 (lH,br.s) , 6, 91 (1H, d, J=16, 6Hz) , 7,29-7,45 (4H,m), 7,48(1H,d,J=16,6Hz), 7,52(2H,d,J=7,3Hz).
MS (FAB) m/z: 315 (M+H)+, 259 (M-isobuteno+H)+, 315 (M15 Boc+H)+.
Exemplo Referencial 17
2-[(E)-2-fenil-etenil]-6,7-diidrooxazolo[5,4-c]-piridino5(4H)-carboxilato de t-butila:
Adicionou-se p-formaldeído (54,5 mg) e ácido p20 tolueno-sulfônico (7,2 mg) a uma solução do composto obtido no Exemplo Referencial 16 (190 mg) em tolueno (15 ml) à temperatura ambiente. Depois de aquecer sob refluxo por 1 h, a mistura da reação foi deixada resfriar, e adicionou-se
Petição 870180138821, de 08/10/2018, pág. 216/857
208 acetato de etila (15 ml) e uma solução aquosa saturada (15 ml) de bicarbonato de sódio à mistura da reação, para separar uma camada aquosa. Depois de extrair a camada aquosa com acetato de etila (10 ml), as camadas orgânicas resultantes foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano: acetato de etila 3:1 2:1), para obter o composto do título (153 mg).
RMN-iH (CDC13) δ: l,50(9H,s), 2, 67 (2H, br . s) , 3, 73 (2H, br . s) ,
4,55(2H,s), 6, 90 (lH,d, J=16, 1Hz) , 7,29-7,42 (3H, m) , 7,46(lH,d,
J=16,lHz), 7,52(2H,d,J=7,3Hz).
MS (FAB) m/z: 327 (M+H)+, 271 (M-isobuteno+H)+, 227 (M-BocH) + .
Exemplo Referencial 18
2-formil-6,7-diidrooxazolo[5,4-c]-piridino-5(4H)-carboxilato de t-butila:
Adicionou-se acetona (8,0 ml), água (4,0 ml), Nóxido de N-metil-morfolina (577 mg) e uma solução aquosa
0,039 M (3,20 ml) de tetróxido de ósmio a uma solução do composto obtido no Exemplo Referencial 17 (803 mg) em tetraidrofurano (16 ml) à temperatura ambiente, e a mistura
Petição 870180138821, de 08/10/2018, pág. 217/857
209 foi agitada por toda a noite. Adicionou-se acetato de etila (50 ml) e uma solução aquosa a 10% (50 ml) de tiossulfato de sódio à mistura da reação, para separar uma camada aquosa. A camada aquosa foi então extraída com acetato de etila (30 ml). Depois de combinar as camadas orgânicas resultantes e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. Adicionou-se metanol (8,0 ml), água (8,0 ml) e m-periodato de sódio (790 mg) a uma solução do resíduo em tetraidrofurano (16 ml) . Depois de agitar por 3 h, adicionou-se acetato de etila (30 ml) e água (50 ml) à mistura da reação, para separar uma camada aquosa. A camada aquosa foi extraída com acetato de etila (20 ml) . Depois de combinar as camadas orgânicas resultantes, lavar uma uma solução saturada (50 ml) de bicarbonato de sódio e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1 —> 2:1), para obter o composto do título (234 mg) . Como este aldeído era instável, ele foi usado imediatamente na próxima reação. RMN-1H (CDC13) δ: l,49(9H,s), 2, 77 (2H, br . s) , 3, 77 (2H, br . s) ,
4,62(2H,s), 9,70(1H,s) .
Exemplo Referencial 19
6,7-diidrooxazolo[5,4-c]-piridino-2,5(4H)-dicarboxilato de
5-(t-butil)-2-metila:
OMe de 08/10/2018, pág. 218/857
210
Adicionou-se cianeto de sódio (220 mg) e dióxido de manganês (780 mg) a uma solução do composto obtido no Exemplo Referencial 18 (225 mg) em metanol (9,0 ml) à temperatura ambiente. Depois de agitar por 30 min, a mistura da reação foi filtrada através de Celite com acetato de etila. O filtrado foi lavado com água (50 ml) e solução aquosa saturada de cloreto de sódio (50 ml) , e secado sobre sulfato de sódio anidro. 0 solvente foi então removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:2 —> 1:1), para obter o composto do título (120 mg). RMN-1H (CDC13) δ: l,49(9H,s), 2, 73 (2H, br . s) , 3, 74 (2H, br . s) ,
4,01 (3H, s) , 4,59 (2H, s) .
MS (FAB) m/z: 283 (M+H)+.
Exemplo Referencial 20
5-metil-4,5,6,7-tetraidrooxazolo[5,4-c]-piridino-2carboxilato de metila:
Adicionou-se ácido triflúor-acético (15 ml) a uma solução do composto obtido no Exemplo Referencial 19 (500 mg) em cloreto de metileno (15 ml) à temperatura ambiente, e a mistura foi agitada por 10 min. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se à mistura resultante cloreto de metileno (20 ml), trietil-amina (0,495
Petição 870180138821, de 08/10/2018, pág. 219/857
211 ml), ácido acético (205 ml), formalina (0,230 ml) e triacetóxi-boro-hidreto de sódio (570 mg) , à temperatura ambiente. Depois de agitar por 15 min, adicionou-se cloreto de metileno (20 ml) e uma solução aquopsa saturada de bicarbonato de sódio (50 ml), para separar uma camada orgânica. A camada aquosa foi extraída com cloreto de metileno (3 x 20 ml) . Depois de combinar as camadas orgânicas resultantes e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 20:1 —> 10:1), para obter o composto do título (257 mg).
ΗΜΝ-^ (CDC13) δ: 2,52(3H,s), 2, 72-2, 78 (2H, m) , 2,78-2, 83 (2H,
m), 4,00 (3H,s) .
MS (FAB) m/z: 197 (M+H)+, 165 (M-OCH3)+.
Exemplo Referencial 21
5-metil-4,5,6,7-tetraidrooxazolo[5,4-c]-piridino-piridino-2carboxilato de lítio:
Adicionou-se água (6,0 ml) e hidróxido de lítio (99,7 ml) a uma solução do composto obtido no Exemplo Referencial 20 (800 mg) em tetraidrofurano (24 ml) à temperatura ambiente, e a mistura foi agitada por 10 min. A mistura da reação foi concentrada sob pressão reduzida, para de 08/10/2018, pág. 220/857
212 obter o composto do título (825 mg).
RMN-iH (DMSO,d6) δ: 2,37(3H,s), 2, 47 (2H, t, J=5, 6Hz) , 2, 64 (2H, t,J=5,6Hz), 3,43 (2H,s) .
Exemplo Referencial 22
5-cloro-6-flúor-indol-2-carboxilato de metila:
MeOOC
Uma mistura de 3-cloro-4-flúor-oc-azido-cinamato de metila (pedido de patente japonesa publicada, no 149723/1995) (1,85 g) e xileno (140 ml) foi aquecida sob refluxo por 1 h, e o solvente foi então removido por destilação. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno), para obter o composto do título (491 mg).
RMN-1!! (CDC13) δ: 3,95(3H,s), 7, 13-7, 15 (1H, m) , 7,20 (1H, dd, J=
9,3, 0,49Hz), 7,71(1H,d,J=7,3Hz), 8,93(1H,br.s).
MS (FAB) m/z: 227 M+.
Exemplo Referencial 23 ácido 5-cloro-6-flúor-indo1-2-carboxílico:
O composto obtido no Exemplo Referencial 22 (461
Petição 870180138821, de 08/10/2018, pág. 221/857
213 mg) foi dissolvido em solvente misto de tetraidrofurano (15 ml), metanol (10 ml) e água (10 ml), adicionou-se hidróxido de lítio (283 mg) à temperatura ambiente, e a mistura foi agitada por 4 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se ácido clorídrico 1 N ao resíduo para acidificá-lo levemente. O pó resultante foi coletado por filtração e secado, para obter o composto do título (422 mg).
ΡΜΝ-ΧΗ (CDC13) δ: 7,08-7, 10 (1H, m) , 7,34(1H,d,J=9,5Hz), 7,88 (lH,d, J=7, 6Hz) , 12,04(lH,s), 13,16(lH,s).
MS (FAB) m/z: 213 (M+) .
Exemplo Referencial 24
5-(piridin-4-il)-4,5,6,7-tetraidrotiazolo[5,4-c]-piridina:
1) Pentassulfeto de difósforo (500 g) foi colocado em suspensão em formamida (3.000 ml) sob resfriamento com gelo, e a suspensão foi agitada por toda a noite. Adicionou-se água e dietil-éter à mistura da reação, e uma camada orgânica foi separada e secada sobre sulfato de magnésio anidro, e o solvente foi removido por destilação, para obter um óleo. Depois de dissolver o óleo em n-butanol (350 ml) e adicionar à solução 3-cloro-4-oxo-l-piperidinocarboxilato de etila (150 g) , sintetizado de acordo com a literatura (Tetrahedron 39:3767, 1983), a mistura resultante
Petição 870180138821, de 08/10/2018, pág. 222/857
214 foi agitada a 100 oC por 2,5 h. A mistura da reação foi filtrada através de Celite. O filtrado foi lavado com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e depois secado sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno —> acetato de etila:hexano 1:2), para obter 6,7diidrotiazolo[5,4-c]-piridino-5(4H)-carboxilato de etila (79,0 g) .
RMN-!H (CDC13) δ: 1, 30 (3H, t, J=7,3Hz) , 2, 96 (2H, br . s) , 3,82(2H, br.s), 4,19 (2H, q, J=7,3Hz) , 4,73 (2H, br. s) , 8,68(lH,s).
MS (FAB) m/z: 213 (M+H)+.
2) Uma solução aquosa 3,5 N (250 ml) de hidróxido de sódio foi adicionada ao produto da reação (33,5 g) obtido acima, e a mistura foi aquecida sob refluxo por toda a noite. Depois de resfriar a mistura da reação até a temperatura ambiente, adicionou-se dicarbonato de dit-butila (103 g) sob resfriamento com gelo, e a mistura foi agitada por toda a noite à temperatura ambiente. Depois de adicionar ácido clorídrico 3 N à mistura da reação, para ajustar o seu pH até 1 a 2, adicionou-se cloreto de metileno. Depois da separação de uma camada orgânica, a camada orgânica foi lavada sucessivamente com uma solução aquosa de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. Depois que a camada orgânica foi concentrada sob pressão reduzida, o resíduo resultante foi purificado por de 08/10/2018, pág. 223/857
215 cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:2), para obter 6, 7-diidrotiazolo[5,4-c]piridino-5(4H)-carboxilato de t-butila (21,1 g).
RMN-!H (CDC13) δ: l,49(9H,s), 2, 94 (2H, br. s) , 3, 7 6 (2H, br. s) , 4, 68(2H,s), 8, 67(1H,s) .
MS (FAB) m/z: 241 (M+H)+.
3) Adicionou-se ácido triflúor-acético (25 ml) a uma solução do composto (5,00 g) obtido na etapa (2) em cloreto de metileno (25 ml) à temperatura ambiente. Depois de agitar por 10 min, a mistura da reação foi concentrada sob pressão reduzida, e adicionou-se ao resíduo 4-bromopiridina (5,20 g), N, N-dimetil-formamida (30 ml) e trietilamina (15,5 ml) à temperatura ambiente, e a mistura foi agitada a 150 oC por 2 dias e depois deixada resfriar até a temperatura ambiente. Os precipitados incolores foram separados por filtração e o filtrado foi concentrado sob pressão reduzida. Depois disso, adicionou-se cloreto de metileno (50 ml) e uma solução aquosa saturada (100 ml) de bicarbonato de sódio, e a camada aquosa resultante foi saturada com cloreto de sódio. Depois da separação de uma camada orgânica, a camada aquosa resultante foi extraída com cloreto de metileno (5 x 30 ml) . Depois que as camadas orgânicas resultantes foram combinadas e secadas sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1 —> 8:1), para obter o composto do título (2,97 g) .
de 08/10/2018, pág. 224/857
216
RMN-iH (CDC13) δ: 3, 07 (2Η, t, J=5, 9Hz) , 3, 81(2H,t,J=5,9Hz),
4,61(2H,s), 6, 74(2H, t,J=6,5Hz), 8,30 (2H, t, J=6, 5Hz) , 8,7O(1H,
s) .
MS (ESI) m/z: 218 (M+H)+.
Exemplo Referencial 25
2-cloro-6,7-diidro-4H-pirano[4,3-d]-tiazol:
1) Dissolveu-se tetraidro-4H-piran-4-ona (5,0 g) em ciclo-hexano (20 ml), adicionou-se pirrolidina (4,35 ml) e ácido p-tolueno-sulfônico monoidratado (48 mg) , e a mistura foi aquecida sob refluxo por 70 min, enquanto se removia água por sifão Dean-Stark. A mistura da reação foi resfriada até a temperatura ambiente, e o sobrenadante foi retirado e concentrado sob pressão reduzida. O resíduo foi dissolvido em metanol (15 ml), e adicionou-se enxofre em pó (1,60 g) sob resfriamento com gelo. Depois de 15 min, adicionou-se uma solução de cianamida (2,10 g) em metanol (10 ml) em gotas por 20 min, e a mistura foi agitada por 3 dias. O solvente foi removido por destilação sob pressão reduzida, e o foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1 10:1
4:1), para obter 6,7-diidro-4H-pirano[4,3-d]-tiazol-2-ilamina (3,97 g) .
de 08/10/2018, pág. 225/857
217
RMN-iH (CDC13) δ: 2, 66-2,70(2Η,m), 3, 97 (2Η, t, J=5, 6Hz) , 4,63 (2Η,s), 4,94(2H,br.s).
MS (FAB) m/z: 157 (M+H)+.
2) Dissolveu-se cloreto de cobre (II) (4,10 g) em 5 acetonitrila (50 ml), e adicionou-se nitrito de t-butila (3,93 g) em uma parcela sob resfriamento com gelo. Depois de 10 min, o composto obtido na reação supradescrita (3, 97 g) foi adicionado por cerca de 1 h, e a mistura da reação foi agitada à temperatura ambiente por 1 h. A mistura da reação foi aquecida até 65 oC e agitada continuamente por 2 h. Depois de adicionar sílica-gel (20 g) à mistura da reação, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (1,78 g).
RMN-1!! (CDCI3) δ: 2,85-2,89 (2H, m) , 4,02 (2H, t, J=5, 6Hz) , 4,73 (2H,s) .
MS (FAB) m/z: 175 (M+H)+.
Exemplo Referencial 26
6,7-diidro-4H-pirano[4,3-d]-tiazol-2-carboxilato de lítio:
*>— COOL
1) O composto obtido no Exemplo Referencial 25 (1,78 g) foi dissolvido em metanol (30 ml), e adicionou-se 10% de paládio sobre carvão (300 mg) e acetato de sódio (830
Petição 870180138821, de 08/10/2018, pág. 226/857
218 mg) à solução. A mistura foi agitada por 5 dias em uma corrente de hidrogênio de 5 atm. Depois que o catalisador foi separado por filtração, o solvente foi concentrado, e o resíduo foi submetido a cromatografia de coluna em sílicagel (hexano:acetato de etila 2:1), para obter 6,7-diidro-4Hpirano[4,3-d]-tiazol (1,14 g).
ΗΜΝ-^ (CDC13) δ: 2, 97-3, 01 (2H, m) , 4,04 (2H, t, J=5, 6Hz) , 4,87 (2H,s), 8,69(1H,s) .
MS (FAB) m/z: 142 (M+H)+.
2) Depois que o produto obtido acima (1,14 g) foi dissolvido em dietil-éter (30 ml) e resfriado até -78 oC, adicionou-se butil-lítio 1,6 M (6,6 ml), e a mistura foi agitada. Depois de 20 min, conduziu-se borbulhamento com dióxido de carbono por 15 min. A mistura da reação foi aquecida até a temperatura mabiente e concentrada sob pressão reduzida, para obter o composto do título (1,65 g). RMN-1!! (DMSO-ds) δ: 2, 83 (2H, t, J=5, 6Hz) , 3, 92 (2H, t, J=5, 6Hz) ,
4,73 (2H, s) .
Exemplo Referencial 27 tiazolo[4,5-c]-piridina:
Dissolveu-se 3- (t-butóxi-carbonil-amino) -4mercapto-piridina (pedido de patente japonês publicado, no 321691/1992) (9,20 g) em ácido fórmico (60 ml) e aqueceu-se de 08/10/2018, pág. 227/857
219 sob refluxo por 4 h. A mistura da reação foi concentrada sob pressão reduzida, e adicinou-se uma solução aquosa 5 N (100 ml) de hidróxido de potássio e dietil-éter ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se dietil-éter ao resíduo, e os sólidos depositados foram coletados por filtração, para obter o composto do título (3, 97 g) .
ΗΜΝ-^ (CDC13) δ: 7, 93 (1H, d, J=5,4Hz) , 8, 60 (1H, d, J=5, 4Hz) ,
9, 07(1H,s), 9,46(1H,s) .
Exemplo Referencial 28
5-metil-4,5,6,7-tetraidrotiazolo[4,5-c]-piridina:
//
O composto do título foi obtido a partir do 15 composto obtido no Exemplo Referencial 27 de uma maneira similar ao Exemplo Referencial 4.
RMN-1!! (CDC13) δ: 2,52(3H,s), 2, 77 (2H, t, J=5, 4Hz) , 2,92-3,00 (2H,m), 3, 69 (2H, t, J=2,0Hz) , 8,61(lH,s).
MS (FAB) m/z: 155 (M+H)+.
Exemplo Referencial 29
5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxilato de lítio::
Petição 870180138821, de 08/10/2018, pág. 228/857
220
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 28 de uma maneira similar ao Exemplo Referencial 5.
ΚΜΝ-^ (DMSO-de) δ: 2,38(3H,s), 2, 64 (2H, br . s) , 2, 80 (2H, br . s) , 5 3,44(2H,br.s).
Exemplo Referencial 30
2-cloro-N,N-dimetil-4,5,6,7-tetraidrobenzotiazol-6-amina:
Dissolveu-se 2-cloro-4,7-diidro-l,3-benzotiazol-6 (5H)-ona (Helv. Cim. Acta 77:1256, 1994) (2,0 g) em metanol (100 ml), e adicionou-se acetato de amônio (8,2 g) e cianoboro-hidreto de sódio (4,0 g) , para aquecer a mistura sob refluxo por 20 h. Adicionou-se ácido clorídrico à mistura da reação, para decompor o excesso de ciano-boro-hidreto antes de remover o solvente por destilação sib pressão reduzida. O resíduo foi alcalinizado com uma solução 1 N de hidróxido de sódio, e depois extraído com cloreto de metileno. A camada orgânica resultante foi secada sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter um óleo amarelo20 pálido. Este óleo foi dissolvido em metanol (50 ml), e
Petição 870180138821, de 08/10/2018, pág. 229/857
221 adicionou-se uma solução aquosa (4,29 g) de formaldeído e ciano-boro-hidreto de sódio (3,49 g) , agitando a mistura à temperatura ambiente por 12 h. 0 solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno ao resíduo, a camada orgânica foi lavada com uma solução aquosa saturada de bicarbonato de sódio e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 10:1), para obter o composto do título (740 mg).
ΗΜΝ-^ (CDC13) δ: 1,71-1,78 (1H, m) , 2, 10-2,19 (1H, m) , 2,35(6H,
s) , 2, 66-2, 94 (5H, m) .
MS (FAB) m/z: 217 (M+H)+.
Exemplo Referencial 31
6-(dimetil-amino)-4,5,6,7-tetraidrobenzotiazol-2-carboxilato de lítio:
| j>— COOLi
Depois que o composto obtido no Exemplo
Referencial 30 (750 mg) foi dissolvido em dietil-éter (15 ml), e a solução resfriada até -78 oC, adicionou-se t-butillítio 1,5 N (3,5 ml), a mistura foi agitada por 20 min, e depois borbulhou-se dióxido de carbono por cerca de 15 min. A mistura da reação foi aquecida até a temperatura ambiente de 08/10/2018, pág. 230/857
222 e concentrada sob pressão reduzida, para obter o composto do título.
RNIN-iH (DMSO-de) δ: 1,75-1,78 (1H,m) , 1,98-2,07(lH,m), 2,50 (6H,m), 2,64-2,88(5H,m).
Exemplo Referencial 32
2-amino)-4,6-diidro-5H-pirrolo[3,4-d]-tiazolo-5-carboxilato de t-butila:
Dissolveu-se l-t-butóxi-carbonil-3-pirrolidona (1,58 g) em ciclo-hexano (10 ml), adicionou-se ácido ptolueno-sulfônico monoidratado (8,12 mg) e pirrolidina (607 mg), e a mistura foi aquecida sob refluxo por 1,5 h enquanto se removia a água com um sifão Dean-Stark. Depois de retirar o sobrenadante e concentrar sob pressão reduzida, o resíduo foi dissolvido em metanol (5 ml), e adicionou-se enxofre em pó (274 mg) . A mistura foi agitada por 15 min sob resfriamento com gelo. Uma solução de cianamida (377 mg) em metanol (2 ml) foi adicionada lentamente em gotas à mistura da reação, e a mistura foi agitada por toida a noite à temperatura ambiente. A mistura foi aquecida adicionalmente sob refluxo por 2 h, a mistura da reação foi concentrada, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio. A camada orgânica resultante foi secada sobre sulfato de sódio de 08/10/2018, pág. 231/857
223 anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:39), para obter o composto do título (248 mg).
RMN-!H (CDCls) δ: l,50(9H,s), 4,34-4,37 (1H, m) , 4,4 0-4, 45 (1H,
m) , 4,4 9-4,55 (2H, m) , 4,99(2H,m).
Exemplo Referencial 33
2-bromo-4,6-diidro-5H-pirrolo[3,4—d]-tiazolo-5-carboxilato de t-butila:
Colocou-se brometo de cobre (II) em suspensão em N,N-dimetil-formamida, e adicionou-se nitrito de t-butila (256 mg) em gotas à temperatura ambiente. Depois, adicionou-se uma solução do composto obtido no Exemplo Referencial 32 (400 mg) em N, N-dimetil-formamida (1 ml) sob resfiramento com gelo, e a mistura da reação foi aquecida a 60 oC por 1,5 h. Adicionou-se dietil-éter e uma solução aquosa saturada de cloreto de sódio à mistura da reação, e a camada orgânica resultante foi secada sobre sulfato de magnésio anidro e concentrada sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (174 mg).
de 08/10/2018, pág. 232/857
224
RMN-XH (CDCI3) δ: l,51(9H,s), 4,52-4,55(lH,m), 4,57-4, 67 (3H,
m) .
MS (FAB) m/z: 305 (M+H)+.
Exemplo Referencial 34 (5-t-butóxi-carbonil)-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxilato de lítio:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 7 de uma maneira similar àquela do Exemplo Referencial 10.
RMN-XH (DMSO-de) δ: l,42(9H,s), 2, 69-2,77 (2H, m) , 3,603,68(2H,m), 4,51-4,58 (2H, m) .
Exemplo Referencial 35
2-bromo-4-(2-metóxi-2-oxoetil)-tiazolo-5-carboxilato de metila:
MeOOC
MeOOC
Adicionou-se cloreto de cobre (II) (26,8 g) a uma solução de nitrito de t-butila (15,5 g) em acetonitrila (500 ml) de uma só vez sob resfriamento com gelo. Adicionou-se à mistrua de reação uma solução de 2-amino-5-metóxi-carbonilPclição 870180138821, de 08/10/2018, pág. 233/857
225 tiazolo-4-acetato de metila (Yakugaku Zasshi, 86:300, 1966) (23,0 g) em acetonitrila (500 ml) em gotas por 45 min, e a mistura resultante foi agitada por 1 h sob resfriamento com gelo e por 30 min à temperatura ambiente. 0 solvente foi concentrado, e adicionou-se ácido clorídrico a 10% e dietiléter ao resíduo, para separar uma camada orgânica. A camada orgânica foi secada sobres sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (25,9 g).
ΗΜΝ-^ (CDC13) δ: 3,73(3H,s), 3,87(3H,s), 4,21(2H,s).
Exemplo Referencial 36
2-[5-(hidróxi-metii)-tiazol-4-il]-etanol:
Uma solução do composto obtido no Exemplo
Referencial 35 (23, 4 g) em tetraidrofurano (500 ml) foi adicionada em gotas por lha uma suspensão de hidreto de lítio e alumínio (9,03 g) em tetraidrofurano (500 ml) sob resfriamento com gelo. Depois de agitar por mais 1 h sib resfriamento com gelo, adicionou-se sucessivamente água (9 ml), uma solução aquosa a 35% de hidróxido de sódio (9 ml) e água (27 ml), e a mistura foi agitada à temperatura ambiente por 1 h. Depois de adicionar sulfato de magnésio anidro à
Petição 870180138821, de 08/10/2018, pág. 234/857
226 mistura e agitar a mistura resultante, a matéria insolúvel foi removida por filtração com Celite, e o filtrado foi concentrado. 0 resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 7:93), para obter o composto do título (8.64 g).
βΜΝ-^ (CDC13) δ: 3, 01 (2H, t, J=5, 5Hz) , 3, 30 (1H, br . s) , 3,57(1H, br.s), 3, 90 (2H, br. s) , 4,75 (2H, br. s) , 8,66(lH,s).
MS (ESI) m/z: 160 (M+H)+.
Exemplo Referencial 37 metano-sulfonato de 2-(5-{[(metil-sulfonil)oxi]metil}tiazol4-il)-etila:
Ms
Uma solução de cloreto de metanossulfonila em cloreto de metileno (12,6 ml) foi adicionada em gotas a uma solução do composto obtido no Exemplo Referencial 36 (8, 64
g) e trietil-amina (45,4 ml) dissolvidos em cloreto de metileno (500 ml) por 20 min a -78 oC. Depois de agitar a mistura da reação por 15 min a -78 oC e por 1 h a 0 oC, adicionou-se água, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (13,4 g).
RMN-1!! (CDC13) δ: 2,93(3H,s), 3,03(3H,s), 3, 28 (2H, t, 6, 3Hz) ,
4,61 (2H, t, J=6, 3Hz) , 5,44(2H,s), 8,84(lH,s).
Petição 870180138821, de 08/10/2018, pág. 235/857
227
Exemplo Referencial 38
5-(1-metil-ciclo-propil)-4,5,6,7-tetraidrotiazolo-[5,4-c]piridina:
Adicionou-se cloridrato de 1-metil-ciclo-propilamina (J. Org. Chem. 54:1815, 1989) (1,89 g) a cloreto de metileno (20 ml) , contendo o composto obtido no Exemplo Referencial 37 (4,46 g) sob resfriamento com gelo, e a mistura foi agitada por toda a noite à temperatura ambiente. Adicionou-se mais cloridrato de 1-metil-ciclo-propil-amina (1,89 g) , e a mistura foi agitada por 20 h à temperatura ambiente e por 5 h sob refluxo. Adicionou-se cloreto de metileno e água à mistura da reação, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:49), para obter o composto do título (944 mg). ΗΜΝ-^ (CDC13) δ: 0, 40-0, 50 (2H, m) , 0, 68-0, 73 (2H, m) , 1,16(3H,
s), 2,88-2,94(2H,m), 3,03(2H,t,J=5,7Hz), 3,89(2H,br.s), 8,60 (1H,S) .
MS (ESI) m/z: 195 (M+H)+.
de 08/10/2018, pág. 236/857
228
Exemplo Referencial 39
5-(1-metil-ciclo-propil)-4,5,6,7-tetraidrotiazolo-[5,4-c]piridino-2-carboxilato de lítio:
composto do título foi obtido a partir do 5 composto obtido no Exemplo Referencial 38, de uma maneira similar àquela do Exemplo Referencial 5.
ΗΜΝ-^ (DMSO-de) δ: 0, 39 (2H, br . s) , 0, 56 (2H, br . s) , l,10(3H, br.s), 2,66(2H,br.s), 2,89(2H,br.s), 3,75(2H,br.s).
Exemplo Referencial 40
2-[6,7-diidrotiazolo[5,4-c]-piridin-5(4H)-il]-2-metilpropanol:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 37 e 2-amino-2-metil1-propanol, de uma maneira similar àquela do Exemplo
Referencial 38.
RMN-iH (CDC13) δ: l,15(6H,s), 2,91(4H,s), 3,45(2H,s), 3,87 (2H,s), 8,63(1H,s) .
Petição 870180138821, de 08/10/2018, pág. 237/857
229
Exemplo Referencial 41
5-(2-{[t-butil-(difenil)-silil]oxi}-l,1-dimetil-etil)4,5,6,7-tetraidrotiazolo[5,4-c]-piridina:
Adicionou-se t-butil-cloro-difenil-silano (1,93 g) 5 e imidazol (994 mg) a uma solução do composto obtido no Exemplo Referencial 40 (1,24 g) em N,N-dimetil-formamida (5 ml) à temperatura ambiente, e a mistura foi agitada por toda a noite. Adicionou-se água e dietil-éter à mistura da reação, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 1:2), para obter o composto do título (2,46 g) .
RMN-1!! (CDC13) δ: l,07(9H,s), l,15(6H,s), 2, 83-2, 90 (2H, m) ,
2, 93-3, 00 (2H,m) , 3,63(2H,s), 3,97(2H,s), 7,35-7,48 ( 6H, m) ,
7,63-7,70 (4H,m) , 8,58(lH,s).
MS (ESI) m/z: 451 (M+H)+.
Exemplo Referencial 42
5-(2-{[t-butil-(difenil)-silil]oxi}-l,1-dimetil-etil)4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxilato de lítio:
Petição 870180138821, de 08/10/2018, pág. 238/857
230
COOL
TBDPSO
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 41, de uma maneira similar àquela do Exemplo Referencial 5.
RMN-1H (DMSO-de) δ: l,01(9H,s), l,ll(6H,s), 2,55-2, 65 (2H, m) ,
2,80-2,90(2H,m), 3,57(2H,s), 3,80(2H,br.s), 7,40-7,52(6H,m),
7,60-7, 65 (4H,m) .
Exemplo Referencial 43
4,7,8,10-tetraidro-6H-pirazolo[1,2-a]tiazolo[4,5-d]piridazina:
1) Dissolveu-se 4,5-dimetil-tiazol (5,00 g) , Nbromo-succinimida (15,7 g) e a, α-azo-bis-isobutironitrila (362 mg) em dicloro-etileno (500 ml) à temperatura ambiente, e a solução foi aquecida sob refluxo por 1 h. O solvente foi removido por destilação, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:dietil-éter 1:4), para obter 4,5-bis-(bromo-etil)-tiazol (5,24 g).
RMN-1!! (CDC13) Ô: 4,64(2H,s), 4,74(2H,s), 8,75(lH,s).
2) 4,5-bis-(bromo-etil)-tiazol (1,37 g) e cloridrato de 1,2-trimetileno-hidrazina (documento no WO
Petição 870180138821, de 08/10/2018, pág. 239/857
231
95/32965) (732 mg) foram colocados em suspensão em etanol (15 ml) sob resfriamento com gelo, e adicionou-se trietilamina (2,82 ml) em gotas por 5 min. Depois de agitar a mistura à temperatura ambiente por 2 h, o solvente foi removido por destilação, e adicionou-se cloreto de metileno (50 ml) e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 3:47), para obter o composto do título (358 mg).
ΚΜΝ-^ (CDC13) δ: 2, 10-2,25 (2H, m) , 3, 01 (4H, br . s) , 3,95(2H,s), 3,99(2H,br.s), 8,64(1H,s).
MS (FAB) m/z: 182 (M+H)+.
Exemplo Referencial 44
4,5,6,7-tetraidro-6H-pirazolo[1,2-a]tiazolo-[4,5-d]piridazino-2-carboxilato de lítio:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 43, de uma maneira similar àquela do Exemplo Referencial 5.
RMN-1!! (DMSO-de) δ: 1, 90-2, 10 (2H, m) , 2, 60-3, 10 (4H, br . s) ,
3,65-4,00(4H,m).
de 08/10/2018, pág. 240/857
232
4,6,7,8,9,11-hexaidro-piridazino[l,2-a]tiazolo[4,5-d]Exemplo Referencial 45 piridazina:
composto do título foi obtido a partir de 4,55 bis-(bromo-metil)-tiazol (2,20 g) obtido em (1) do Exemplo
Referencial 43 e cloridrato de 1,2-tetrametileno-hidrazina (patente no US 5.726.126), de uma maneira similar àquela do Exemplo Referencial 43.
RMN-!H (CDC13) δ:
1,77(4H,br.s), 2, 20-3, 50(4H,br), 3,92(4H, br . s) , 8,65 (1H, s) .
MS (FAB) m/z: 196 (M+H)+.
Exemplo Referencial 46
4,6,7,8,9,11-hexaidro-piridazino[1,2-a]tiazolo[4,5-d]piridazino-2-carboxilato de lítio:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 45, de uma maneira similar àquela do Exemplo Referencial 5.
Petição 870180138821, de 08/10/2018, pág. 241/857
233
Exemplo Referencial 47
2-(metil-sulfanil)-5,7-diidro-6H-pirrolo[3,4-d]-pirimidino6-carboxilato de t-butila:

Adicionou-se l-t-butóxi-carbonil-3-pirrolidona (4,57 g) a N,N-dimetil-formamida-dimetil-acetal (30 ml) à temperatura ambiente, e a mistura foi aquecida por lha 140 °C. Depois de deixar a mistura da reação resfriar até a temperatura ambiente, ela foi concentrada sob pressão reduzida. Adicinou-se hexano ao resíduo, e o pó amarelo depositado foi coletado por filtração. Este pó foi dissolvido em etanol (100 ml), e adicionou-se sulfato de metil-isotiouréia (9,24 g) e etóxido de sódio (4,52 g) à solução resultante, à temperatura ambiente, e a mistura foi aquecida sob refluxo por 24 h. Adicionou-se uma solução aquosa saturada de cloreto de sódio e éter dietílico à mistura da reação, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro e concentrada sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:99), para obter o composto do título (1,10 g). RMN-1!! (CDC13) δ: l,51(9H,s), 2,57(3H,m), 4, 15-4, 45 (4H, m) ,
8,39(1/2H,s), 8,43(1/2H,s).
MS (FAB) m/z: 268 (M+H)+.
Petição 870180138821, de 08/10/2018, pág. 242/857
234
Exemplo Referencial 48
2-(metil-sulfonil)-5,7-diidro-6H-pirrolo[3,4-d]-pirimidino6-carboxilato de t-butila:
Adicionou-se ácido m-cloro-perbenzóico (1,99 g) a 5 uma solução do composto obtido no Exemplo Referencial 47 (1,08 g) em cloreto de metileno, sob resfriamento com gelo, e a mistura foi agitada por 5 h. Uma solução aquosa saturada de sulfito de sódio, uma solução aquosa saturada de bicarbonato de sódio, e cloreto de metileno, foram adicionados para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, adicionou-se hexano ao resíduo, e o pó depositado foi coletado por filtração, para obter o composto do título (1,09 g) .
ΚΜΝ-^ (CDC13) δ: l,53(9H,s), 3,36(3H,m), 4,77-4, 90 (4H, m) ,
8,77(1/1H,s), 8,81(1/2H,s).
MS (FAB) m/z: 300 (M+H)+.
Exemplo Referencial 49
2-ciano-5,7-diidro-6H-pirrolo[3,4-d]-pirimidino-6carboxilato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 243/857
235
Boc-N
CN
Adicionou-se cianeto de tetrabutil-amônio (1,04 g) a uma solução do composto obtido no Exemplo Referencial 48 (1,05 g) em cloreto de metileno (30 ml) à temperatura ambiente, e a mistura foi agitada à temperatura ambiente por
1 h. Adicionou-se hidróxido de sódio 1 N à mistura da reação, para separar uma camada orgânica, e a camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:acetona 20:1), para obter o composto do título (776 mg).
RMN-!H (CDCI3) δ: l,52(9H,s), 4,70-4,85 (4H, m) , 8,68-8,77 (1H, m).
MS (FAB) m/z: 247 (M+H)+.
Exemplo Referencial 50
2-(metil-sulfonil)-5,7-diidro-6H-pirrolo[3,4-d]-pirimidino2,6-dicarboxilato de 6-t-butila:
Boc—N
COOMe
Adicionou-se ácido clorídrico concentrado (5 ml) a uma solução do composto obtido no Exemplo Referencial 49 (776 mg) em metanol (10 ml) à temperatura ambiente, e a
Petição 870180138821, de 08/10/2018, pág. 244/857
236 mistura foi agitada a 100 oC por 1 h. Depois de deixar resfriar, a mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi dissolvido em metanol (10 ml).
Adicionou-se trietil-amina (2,20 ml) e dicarbonato de di-tbutila (1,37 g) à solução, à temperatura ambiente e agitouse por 1 h. A mistura da reação foi concentrada sob pressão reduzida e adicionou-se cloreto de metileno e uma solução aquosa saturada de cloreto de sódio ao resíduo, para separar uma camada orgânica, e a a camada orgânica foi secada sobres sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 3:97), para obter o composto do título (317 mg). ΚΜΝ-^ (CDC13) δ: l,53(9H,s), 4,09(3H,s), 4,75-4, 85 (4H, m) ,
8,81(1/2H,s), 8,85(1/2H,s).
MS (FAB) m/z: 280 (M+H)+.
Exemplo Referencial 51
5,6-dimetil-4,5,6,7-tetraidrotiazolo[4,5-d]-piridazino-2carboxilato de lítio:
1) Depois de dissolver 4,5-bis-(bromo-metil)tiazol (600 mg) obtido em (1) do Exemplo Referencial 43 em etanol (20 ml) e adicionar cloridrato de 1,2-dimetilhidrazina (294 mg) sob resfriamento com gelo, adicionou-se de 08/10/2018, pág. 245/857
237 trietil-amina (1,23 ml) de uma só vez, e a mistura foi agitada por 30 min à temperatura ambiente e por 30 min a 50 oC. O solvente foi removido por destilação, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:19), para obter 5,6-dimetil4,5,6,7-tetraidrotiazolo[4,5-d]-piridazina (90 mg).
ΗΜΝ-^ (CDC13) δ: 2,43(3H,s), 2,56(3H,s), 3,92(2H,s), 4,06 (2H,br.s), 8,68(1H,s).
MS (FAB) m/z: 170 (M+H)+.
2) O composto do título foi obtido a partir da
5,6-dimetil-4,5,6,7-tetraidrotiazolo[4,5-d]-piridazina, de uma maneira similar àquela do Exemplo Referencial 5.
RMN-!H (DMSO-de) δ: 2,28(3H,s), 2,39(3H,s), 3, 66 (2H, br. s) ,
3,88(2H,br.s).
Exemplo Referencial 52
5-cloro-indol-2-carboxilato de 4-nitro-fenila:
Depois de colocar o ácido 5-cloro-indol-2carboxílico (20 g) em suspensão em cloreto de metileno (1.500 ml), e adicionar N,N-dimetil-formamida (2 ml), adicionou-se cloreto de tionila (11 ml) em gotas à temperatura ambiente. A mistura da reação foi aquecida por toda a noite sob refluxo e depois concentrada sob pressão
Petição 870180138821, de 08/10/2018, pág. 246/857
238 reduzida. O resíduo foi dissolvido em cloreto de metileno (1.000 ml), e adicionou-se trietil-amina (84,7 ml) e pnitro-fenol (14,2 g) à mistura, sob resfriamento com gelo. Depois de agitar por 1 h à temperatura ambiente, a mistura da reação foi concentrada sob pressão reduzida, e adicionouse acetato de etila e ácido clorídrico 0,2 N ao resíduo, para separar uma camada orgânica. A camada orgânica foi lavada sucessivamente com uma solução aquuosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (29,9 g).
ΗΜΝ-^ (CDC13) δ: 7,35 (1H, dd, J=9, 0, 1,7Hz), 7,39-7, 42 (2H, m) ,
7,45(2H,dd,J=7,3, 1,7Hz), 7,73(1H,d,J=1,0Hz), 8,35(2H,dd,
J=7,3, 1,7Hz), 9, 09 (lH,br. s) .
MS (FD) m/z: 316 (M+) .
Exemplo Referencial 53
6-cloro-2-quinolino-carbonitrila:
Dissolveu-se 6-cloro-quinolina (2,50 g) em cloreto de metileno (25 ml) , e adicionou-se ácido m-cloroperbenzóico (3,71 g) sob resfriamento com gelo, e agitou-se a mistura à temperatura ambiente por 1 h. Depois que a mistura da reação foi diluída com cloreto de metileno, a de 08/10/2018, pág. 247/857
239 mistura diluída foi lavada com uma solução aquosa de tiossulfato de sódio e secada sobre sulfato de sódio anidro.
O solvente foi removido por destilação sob pressão reduzida, o resíduo foi dissolvido em cloreto de metileno (40 ml) , e adicionou-se cianeto de trimetil-silila (2,0 ml) e cloreto de N,N-dimetil-carbamoíla (1,50 ml), e aqueceu-se a mistura resultante por 9 h sob refluxo. Depois de adicionar mais cianeto de trimetil-silila (1,0 ml) e cloreto de N,Ndimetil-carbamoíla (0,80 ml), e aquecer a mistura por 16 h sob refluxo, a mistura da reação foi diluída com cloreto de metileno, e adicionou-se uma solução aquosa a 10% (40 ml) de carbonato de potássio, e agitou-se a mistura por 30 min. Depois de separar uma camada orgânica e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. Adicionou-se cloreto de metileno ao resíduo, e os cristais depositados foram coletados por filtração, para obter o composto do título (1,77 g) . Além disso, um licor-mãe foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno), para obter o composto do título (0,80 g).
RMN-1!! (DMSO-de) δ: 7, 94 (1H, dd, J=9, 0, 2,2Hz), 8,09(lH,d,
J=8,5Hz), 8, 15 (1H, d, J=9, 0Hz) , 8, 2 9 (1H, d, J=2,2Hz) , 8,63(1H, d, J=8,5Hz) .
MS (FAB) m/z: 189 (M+H)+.
Exemplo Referencial 54 ácido 6-cloro-2-quinolino-carboxílico:
de 08/10/2018, pág. 248/857
240 ho2c
N
Cl
O composto obtido no Exemplo Referencial 53 (1,73
g) foi dissolvido em ácido clorídriuco concentrado (40 ml), e a solução foi aquecida por 19 h sob refluxo. A mistura da reação foi resfriada até a temperatura ambiente, e os depósitos foram coletados por filtração e depois lavados com água, para obter o composto do título (1,81 g) .
RMN-1!! (DMSO-de) δ: 7, 87 (1H, dd, J=9, 0, 2,4Hz), 8, 10-8,20 (2H,
m) , 8,24(1H,d,J=2,2Hz), 8, 52(1H,d,J=8,5Hz) .
MS (FAB) m/z: 208 (M+H)+.
Exemplo Referencial 55
3-(4-cloro-fenil)-2-(formil-amino)-propionato de metila:
OHC
Colocou-se o cloridrato do éster metílico de (±)(4-cloro-fenil)-alanina (2,00 g) em suspensão em cloreto de metileno (20 ml), e adicionou-se cloridrato de 1-(3-dimetil15 amino-propil)-3-etil-carbodiimida (1,60 g), 1-hidróxi-benzotriazol monoidratado (1,23 g) , N-metilmorfolina (1,90 g) e ácido fórmico (0,30 ml), agitando a mistura por 1 5 min. Depois de repetir 3 vezes um processo no qual mais ácido fórmico (0,30 ml) era adicionado, agitando a mistura por 15
Petição 870180138821, de 08/10/2018, pág. 249/857
241 min, a mistura da reação foi diluída com cloreto de metileno. Depois de lavar uma camada orgânica com água e depois secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. 0 resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 40:1), para obter o composto do título (1,21 g).
ΗΜΝ-^ (CDC13) δ: 3, 10(1H,dd,J=13,9, 5, 6Hz) , 3,18(lH,dd,
J=l,39, 5,9Hz), 3,75(3H,s), 4,95(lH,m), 6,07(lH,br), 7,05 (2H,d,J=8,3Hz), 7,27(2H,d,J=8,3Hz), 8,18(lH,s).
MS (FAB) m/z: 242 (M+H)+.
Exemplo Referencial 56
7-cloro-3-isoquinolino-carboxilato de metila:
MeO2C
O composto obtido no Exemplo Referencial 55 (1,45
g) foi dissolvido em cloreto de metileno (40 ml), e adicionou-se cloreto de oxalila (0,57 ml) em gotas. Depois de agitar a mistura à temperatura ambiente por 30 min, adicionou-se cloreto férrico (1,17 g) em uma temperatura de cerca de -10 oC, e agitou-se a mistura à temperatura ambiente por 4 dias. Adicionou-se ácido clorídrico 1 N, e a mistura resultante foi diluída com cloreto de metileno, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por
Petição 870180138821, de 08/10/2018, pág. 250/857
242 destilação sob pressão reduzida, e o resíduo foi dissolvido em metanol (38 ml), e adicionou-se ácido sulfúrico concentrado (2 ml) , para aquecer a mistura por 20 h sob refluxo. Adicionou-se uma solução aquosa de bicarbonato de sódio à mistura da reação, a mistura resultante foi extraída com cloreto de metileno, e o extrato foi secado sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1 —> acetato de etila), para obter o composto do título (0,25 g).
ΗΜΝ-^ (CDC13) δ: 4,07(3H,s), 7,74 (1H, dd, J=8,8, 2,0Hz), 7,94 (1H, d, J=8, 8Hz) , 8,06 (1H, d, J=2, 0Hz) , 8,59(lH,s), 9,28(lH,s).
Exemplo Referencial 57 cloridrato do ácido 7-cloro-isoquinolino-carboxílico:
O composto obtido no Exemplo Referencial 56 (0,23
g) foi dissolvido em ácido clorídrico concentrado (10 ml) , para aquecer a mistura por 18 h sob refluxo. A temperatura da mistura da reação foi diminuída até a temperatura ambiente, e os depósitos foram coletados por filtração e depois lavados com água, para obter o composto do título (0,21 g) .
de 08/10/2018, pág. 251/857
243
RMN-iH (DMSO-de) δ: 7,96(lH,m), 8,29 (1H, d, J=8,5Hz) , 8,44(1H,
s), 8,72(lH,s), 9, 45(1H,d,J=6,6Hz) .
MS (FAB) m/z: 208 (M+H)+.
Exemplo Referencial 58 (3R)-l-benzil-3-(t-butil-difenil-sililóxi)-pirrolidina:
OTBDPS (3R)-l-benzil-3-hidróxi-pirrolidina (500 μΐ) e imidazol (466 mg) foram dissolvidos em N,N-dimetil-formamida (15 ml), adicionou-se cloreto de t-butil-difenil-silila (1,57 ml) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente por 9 dias. Depois de remover o solvente por destilação sob pressão reduzida e adicionar cloreto de metileno e água ao resíduo, para conduzir separação de líquidos, a camada orgânica resultante foi secada sobres sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi submetido a cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (1,27 g).
ΗΜΝ-^ (CDC13) δ: l,05(9H,s), 1,70-1,85 (1H, m) , 1, 90-2, 00 (1H,
m), 2,45-2,65(3H,m), 2,70-2,80(1H,m), 3,50-3,70(2H,m), 4,354,45(lH,m), 7,20-7,45(11H,m), 7,60-7,70(4H,m).
MS (ESI) m/z: 416 (M+H)+.
Petição 870180138821, de 08/10/2018, pág. 252/857
244
Exemplo Referencial 59
N-[(IR*,2S*)-2-amino-ciclo-propil]-5-cloro-indo1-2carboxamida:
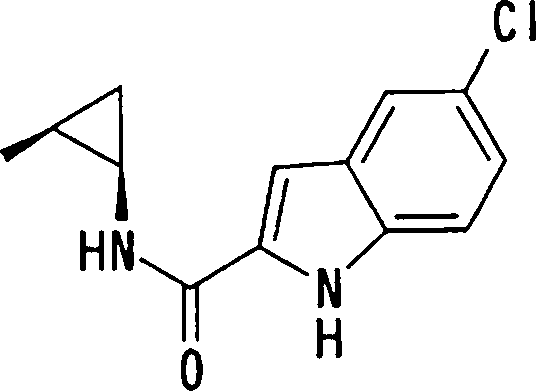
1-Hidróxi-benzotriazol monoidratado (377 mg) , cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (642 mg) e diisopropil-etil-amina (1,95 ml) foram adicionados a uma solução de cloridrato de cis-1,2-ciclopropano-diamina (J. Med. Chem. 41:4723-4732, 1998) (405 mg) e ácido 5-cloro-indol-2-carboxílico (546 mg) em N,N-dimetilformamida (10 ml) à temperatura ambiente, e a mistura foi agitada por 50 h. Depois de concentrar a mistura da reação sob pressão reduzida, adicionou-se cloreto de metileno (50 ml) e uma solução saturada (200 ml) de bicarbonato de sódio, para separar um sólido incolor depositado por filtração. O filtrado foi extraído com cloreto de metileno. Depois de combinar as camadas orgânicas resultante e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, para obter um resíduo. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:7 —> 10:1), para obter o composto do título (110 mg).
de 08/10/2018, pág. 253/857
245
RMN—XH (DMSO-de) δ: 0, 44 (1H, dd, J=10,7, 4,4Hz), l,ll(lH,dd,
J=14,0, 7,4Hz), 2, 63-2,70 (lH,m) , 3, 07-3,16 (1H, m) , 6,77(1H,
s), 6, 97(lH,br.s), 7,23(1H,dd,J=8,9, 1,8Hz), 7,36(1H,d,J=8,9 Hz), 7,60(lH,s), 9,32(lH,s).
MS (FAB) m/z: 250 (M+H)+.
Exemplo Referencial 60
N-[(IR*,2S*)-2-amino-ciclo-butil]-5-cloro-indol-2carboxamida:
O composto do título foi obtido a partir de 10 cloridrato de cis-1,2-ciclo-butano-diamina (J. Am. Chem. Soc. 64:2696-2700, 1942), de uma maneira similar àquela do
Exemplo Referencial 59.
ΗΜΝ^Η (DMSO-dg) δ: 1, 55-2,20 (4H, m) , 3,52-3, 62 (1H, m) , 4,354,50(lH,m), 7, 16 (1H, d, J=8, 7, 2,1Hz), 7,19(lH,s), 7,42(lH,d,
J=8,7Hz), 7,70(1H,d,J=2, 1Hz) , 8.36 (1H,d,J=7, 8Hz) , 11,77(1H, br. s) .
MS (ESI) m/z: 264 (M+H)+.
Exemplo Referencial 61 (IR*,2R*)-2-amino-ciclo-pentil-carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 254/857
246
(±)-trans-1,2-ciclo-pentano-diamina (documento no WO 98/30574) (692 mg) foi dissolvida em cloreto de metileno (10 ml), à qual adicionou-se trietil-amina (1,1 ml) e 2-(tbutóxi-carbonilóxi-imino)-2-fenil-acetonitrila (493 mg), e a mistura foi agitada a 0 oC por 1 h. Depois disso, adicionou mais 2-(t-butóxi-carbonilóxi-imino)-2-fenil-acetonitrila (493 mg), e a mistura foi agitada à temperatura ambiente por 7 h. Adicionou-se água à mistura da reação, para separar uma camada orgânica. A camada orgânica foi lavada com uma solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 9:1), para obter o composto do título (395 mg) .
RMN-!H (CDC13) δ: 1,25-1,40 (2H, m) , l,49(9H,s), 1,59-1,77 (2H,
m) , 1, 92-2, 08 (lH,m), 2,10-2,17(1H,m), 2,98(1H, q, J=7,2Hz) ,
3,48-3,53(lH,m), 4,49(1H,br.s),
MS (ESI) m/z: 201 (M+H)+.
Exemplo Referencial 62 cloridrato de N-[(IR*,2R*)-2-amino-ciclo-pentil]-5-metil4,5,6, 7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 255/857
247


O composto obtido no Exemplo Referencial 61 (175 mg) foi dissolvido em N, N-dimetil-formamida (3 ml), e à solução adicionou-se 5-metil-4,5,6,7-tetraidrotiazolo[5, 4c]-piridino-2-carboxilato de lítio (pureza: 90%, 258 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (252 mg) e 1-hidróxi-benzotriazol monoidratado (60 mg) . A mistura foi agitada à temperatura ambiente por 2 dias. O solvente foi removido por destilação sob pressão reduzida, usando uma bomba, e adicionou-se cloreto de metileno e uma solução saturada de bicarbonato de sódio ao resíduo, para separar uma camada orgânica. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3). 0 óleo amarelo-pálido resultante foi dissolvido em uma solução de ácido clorídrico em etanol (5 ml), e a solução foi agitada à temperatura ambiente por 1 h. Depois, adicionou-se acetato de etila e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se acetato de etila ao resíduo para coletar o precipitado formado por filtração, obtendo desta forma o de 08/10/2018, pág. 256/857
248 composto do título (120 mg).
RMN-iH (DMSO-de) δ: 1,63-1,73(4H,m), 1, 99-2, 06 (2H,m) , 2,91 (3H,s), 3,09-3,14 (lH,m), 3, 25-3, 70(4H,m), 4,27-4,32(1H, m) ,
4,42-4,46(lH,m), 4,68-4,71(1H,m), 8,20-8,23(3H,m), 9,O9(1H, d,J=8,3HZ), 11,82-12,01(lH,m).
MS (ESI) m/z: 281(M+H)+.
Exemplo Referencial 63 cloridrato de N-[(IR*,2R*)-2-amino-ciclo-pentil]-5-cloro-lHindol-2-carboxamida:
O composto obtido no Exemplo Referencial 61 (1,40 g) foi dissolvido em N,N-dimetil-formamida (15 ml), e a esta solução adicionou-se ácido 5-cloro-indol-2-carboxílico (1, 64 g) , cloridrato de 1-(3-dimetil-amino-propil)-3-etilcarbodiimida (2,68 g) e 1-hidróxi-benzotriazol monoidratado (473 mg) . A mistura foi agitada à temperatura ambiente por 23 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução saturada de bicarbonato de sódio ao resíduo, para coletar os precipitados por filtração. Os precipitados foram lavados
Petição 870180138821, de 08/10/2018, pág. 257/857
249 com acetato de etila, cloreto de metileno e metanol. Por outro lado, o filtrado foi separado, para dar uma camada orgânica que foi retirada e secada sobre sulfato de sódio anidro, e o solvente foi então removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 19:1), para obter um óleo amarelo-pálido. Este óleo amarelo-pálido foi combinado com os precipitados obtidos pela filtração e foi dissolvido em cloreto de metileno (10 ml) , e adicionou-se ácido triflúor-acético (10 ml), agitando a mistura à temperatura ambiente por 3 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno e solução aquosa 1 N de hidróxido de sódio ao resíduo, para coletar o precipitado por filtração. A camada orgânica do filtrado foi separada e secada sobre sulfato de sódio anidro. Os precipitados coletados pela filtração foram adicionados a essa solução, e adicionou-se ainda uma solução de ácido clorídrico 4 N em dioxano (20 ml). O solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno (10 ml) e uma solução de ácido clorídrico 4 N em dioxano (10 ml) ao resíduo. O solvente foi removido por destilação sob pressão reduzida. Adicionou-se acetato de etila ao resíduo, para coletar os precipitados por filtração, obtendo desta forma o composto do título (1,83 g).
RMN-1H (DMSO-de) δ: 1, 60-1, 75 (4H, m) , 2,05-2,10 (2H, m) , 3,49 (1H,q,J7,6HZ), 4,27(4H,quinteto,J=7,6HZ) , 7,17 (1H, d,
J=8, 6 Hz), 7,19(lH,s), 7,42 (1H, d, J=8, 6Hz) , 7,70(lH,s), 8,24 de 08/10/2018, pág. 258/857
250 (3Η, br,s), 8,85(1H, d,J7,3HZ), ll,91(lH,s)
MS (ESI) m/z: 278(M+H)+.
Exemplo Referencial 64 (IR*,2R*)-2-amino-ciclo-hexil-carbamato de t-butila:
O composto do título foi trans-1,2-ciclo-hexano-diamina, de àquela do Exemplo Referencial 61.
obtido a partir de (±) uma maneira similar
Ponto de fusão (p.f.) =
79-81 °C.
RMN-iH (CDC13) Ô: 1,05-1,34(4H,m), l,45(9H,s), 1, 68-1,75 (2H,
m), 1, 92-2, 02 (2H,m), 2, 32(1H,dt,J=10,3, 3,9HZ), 3,08-3,20 (lH,m), 4,50 (1H, br, s) .
MS (FAB) m/z: 215(M+H)+.
Exemplo Referencial 65 triflúor-acetato (cloridrato) de N-[(IR*,2R*)-2-amino-ciclo15 hexil]-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 259/857
251 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 64, de uma maneira similar àquela do Exemplo Referencial 62.
ΚΜΝ-^ (DMSO-de) δ: 1, 10-1, 80 (7H,m) , 1,95-2,05(lH,m), 2,97 (3H,s), 3,00-3,20(3H,m), 3, 63(2H,br,s), 3, 72-3, 88 (1H, m) ,
4,61 (2H,br, s) , 7,98(3H,s), 8, 89 (1H, d, J=9, 2HZ) .
MS (FAB) m/z: 295(M+H)+.
O cloridrato foi obtido de uma maneira similar.
Exemplo Referencial 66 (IR*,2S*)-2-amino-ciclo-hexil-carbamato de t-butila
h2n
O composto do título foi obtido a partir de cis1,2-ciclo-hexano-diamina, de uma maneira similar àquela do Exemplo Referencial 61.
RMN-1!! (CDC13) δ: 1,30-1,70 (17H, m) , 2, 98-3, 05 (1H, m) , 3,60 (lH,br,s), 4, 98 (lH,br, s) .
MS (FAB) m/z: 215(M+H)+.
Exemplo Referencial 67 cloridrato (triflúor-acetato) de N-[(IR*,2S*)-2-amino-ciclohexil]-5-metil-4,5,6,7-tetraidrotiazolo[5, 4-c]-piridino-220 carboxamida:
Petição 870180138821, de 08/10/2018, pág. 260/857
252
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 66, de uma maneira similar àquela do Exemplo Referencial 62.
ΗΜΝ-^ (DMSO-de) δ: 1,30-1,90(8H,m), 2,92(3H,s), 3,05-3,79 (5H,m), 4,23 (lH,br,s), 4,34-4,79(2H,m) , 8,01-8,34(3H,m),
8,30-8,49(lH,m), 11,90-12,30(lH,m).
MS (FAB) m/z: 295(M+H} + .
O triflúor-acetato foi obtido de uma maneira similar.
Exemplo Referencial 68 (IR*,2R*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-ciclohexil-carbamato de t-butila:
Ácido 5-cloro-indol-2-carboxílico (2,88 g), 115 hidróxi-benzotriazol monoidratado (2,08 g) e cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (2,95 g) foram adicionados a uma solução do composto obtido no
Petição 870180138821, de 08/10/2018, pág. 261/857
253
Exemplo Referencial 64 (3,00 g) em N,N-dimetil-formamida (10 ml) à temperatura ambiente. Depois de agitar por 3 dias, a mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno (30 ml), uma solução aquosa saturada de bicarbonato de sódio (150 ml) e água (150 ml) ao resíduo. Depois disso, o precipitado incolor formado por filtração e secado, para obter o composto do título (5,21
g) ·
RMN-1H (DMSO—d6) 6: 1, 10-1, 45 (4H,m) , l,21(9H,s), l,68(2H,d,
J=8,lHz), 1, 86(2H,t,J16,2Hz), 3, 22-3, 42(1H,m), 3,69(lH,br,
s),6,66(1H,d,J8,5Hz) , 7,02(lH,s), 7,15 (1H,dd,J=8,5,2,OHz),
7,41(1H,d,J=8,5Hz), 7, 67(1H,d,J2,OHz), 8, 15(1H, d,J=8,1HZ),
11,73(1H,br,s) .
MS (ESI) m/z: 392(M+H)+.
Exemplo Referencial 69 cloridrato de N-[(IR*,2R*)-2-amino-ciclo-hexil]-5-cloroindol-2-carboxamida:
Uma solução de ácido clorídrico em etanol (100 ml) foi adicionada a uma solução do composto obtido no Exemplo
Referencial 68 (5,18 g) em cloreto de metileno (100 ml) à
Petição 870180138821, de 08/10/2018, pág. 262/857
254 temperatura ambiente. Depois de agitar por 2 dias, a mistura da reação foi concentrada sob pressão reduzida, adicionou-se dietil-éter (300 ml) ao resíduo resultante, e o precipitado incolor formado foi coletado por filtração e secado, para obter o composto do título (4,30 g).
RMN-1H (DMSO-de) δ: 1,20-1,36 (2H, m) , 1,36-1,50 (2H, m) , 1,60 (2H,br,s), 1, 90 (lH,d, J=13,OHz) , 2, 07 (1H, d, J=13, 7Hz) , 3,06 (lH,br,s), 3,83-3,96(lH,m), 7,15-7,24(2H,m), 7,45(1H,d,J=8,6
Hz), 7,73(lH,s), 8, 00 (3H,br, s) , 8, 60 (1H, d, J=8,3Hz) , 11,86 (1H,s) .
MS (ESI) m/z: 292(M+H)+.
Exemplo Referencial 70 (IR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-ciclohexil-carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 66, de uma maneira similar àquela do Exemplo Referencial 68.
ΗΜΝ-ΧΗ (DMSO-de) δ: 1,20-1, 45 (11H, m) , 1,45-1, 70 (4H, m) , 1,70l,85(2H,m), 3, 76 (1H, br, s) , 4,08 (1H, br, s) , 6,64 (1H, d,
J=7,6 Hz), 7,12(lH,s), 7,16(1H,dd,J=8,8,2,OHz),
7,43(1H,d,J=8,8 Hz), 7,69(1H,d,J=2,OHz), 7,85(1H,d,J=6,9Hz),
Petição 870180138821, de 08/10/2018, pág. 263/857
255
11,80 (1Η, br, s) .
MS (ESI) m/z: 392(M+H)+.
Exemplo Referencial 71 cloridrato de N-[(IR*,2S*)-2-amino-ciclo-hexil]-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 70, de uma maneira similar àquela do Exemplo Referencial 69.
RMN-1H (DMSO-de) δ: 1,30-1,50(2H,m), 1,55-1,95(6H,m), 3,41 (lH,br,s), 4,32(lH,br,s), 7,19(1H,dd,J=8,7,2,OHz), 7,33 (1H,
s), 7,45(1H,d,J=8,7Hz), 7,60-7,90(4H,m), 8,17(1H,d,J=7,1Hz),
11,91 (1H,s) .
MS (FAB) m/z: 292(M+H)+.
Exemplo Referencial 72 (1R*,2R*)-1,2-ciclo-heptanodiol:
HO 0H
Ciclo-hepteno (3,85 g) foi adicionado parceladamente a uma solução aquosa a 30% de peróxido de
Petição 870180138821, de 08/10/2018, pág. 264/857
256 hidrogênio (45 ml) e ácido fórmico 88% (180 ml), e a mistura foi agitada em uma temperatura entre 40 e 50 oC por lhe depois à temperatura ambiente por toda a noite. 0 solvente foi removido por destilação sob pressão reduzida, e adicionou-se uma solução aquosa a 35% de hidróxido de sódio ao resíduo, para alcalinizá-lo. Depois disso, este resíduo foi agitado em uma temperatura entre 40 e 50 oC por 10 min, e adicionou-se acetato de etila para conduzir separação de líquidos. A camda aquosa resultante foi extraída 4 vezes com acetato de etila. As camadas orgânicas resultantes foram coletadas e secadas sobre sulfato de sódio anidro, e o solvente foi removido sob destilação sob pressão reduzida, para obter o composto do título (4,56 g) .
RMN-1H (CDC13) δ: 1,44-1,56 (6H,m), 1, 63-1,70(2H,m), 1,83l,91(2H,m), 2, 91 (2H,br, s) , 3, 40-3, 44 (2H, m) .
MS (FAB) m/z: 131(M+H)+.
Exemplo Referencial 73 cloridrato de (IR*,2R*)-1,2-ciclo-heptano-diamina:
O composto obtido no Exemplo Referencial 72 (4,56
g) foi dissolvido em cloreto de metileno (35 ml), adicionouse trietil-amina (29 ml) , e a mistura foi resfriada até -78 oC. Adicionou-se lentamente cloreto de metano-sulfonila (8,13 ml), e a mistura foi agitada por 20 min na mesma de 08/10/2018, pág. 265/857
257 temperatura e depois por 1,5 h a 0 oC. Adicionou-se água à mistura da reação para conduzir separação de líquidos, e a camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter um óleo. Este óleo foi dissolvido em N, N-dimetil-formamida (90 ml), adicionou-se azida de sódio (13,65 g) , e a mistura foi agitada a 65 oC por 18 h. Adicionou-se éter e água à mistura da reação, para conduzir separação de líquidos. A camada etérea resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter um óleo.
Este óleo foi dissolvido em etanol (70 ml), adicionou-se paládio sobre carvão a 10% (contendo 50% de água, 4 g) , e a mistura foi agitada por 4 dias em uma atmosfera de hidrogênio (3,5 atm). Depois de separar o paládio sobre carvão por filtração, adicionou-se uma solução de ácido clorídrico 1 N em etanol (70 ml) ao filtrado, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi dissolvido em metanol, adicionou-se acetato de etila, e o solvente foi novamente removido por destilação sob pressão reduzida. O precipitado formado foi coletado por filtração, para obter o composto do título (3,57 g) . RMN-!H (DMSO) 6: 1, 4 4 (4H, br, s) , 1, 73-1, 81 ( 6H, m) , 3,43(2H, br,s), 8, 63 (6H, br, s) .
de 08/10/2018, pág. 266/857
258
MS (ESI) m/z: 129(M+H)+.
Exemplo Referencial 74
N-[(IR*,2S*)-2-amino-ciclo-hexil]-5-cloro-indol-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 73, de uma maneira similar àquela do Exemplo Referencial 59.
ΗΜΝ-^ (DMSO-de) δ: 1, 49-1,52 (4H,m) , 1,72-1,91 (6H,m) , 4,044,10(lH,m), 7, 17-7,23 (2H,m) , 7, 44 (1H, d, J=8, 8Hz) , 7,72 (lH,d,
J=2,0Hz), 7,96(2H,br,s), 8,75(1H,d,J=8,5Hz), 11,89(1H,br,s).
MS (ESI) m/z: 306(M+H)+.
Exemplo Referencial 75 (IR*,2S*)-1,2-ciclo-octanodiol:
HO OH
Ciclo-octeno (4,41 g) foi dissolvido em 15 acetonitrila (45 ml) e água (15 ml), e adicionou-se a esta
Petição 870180138821, de 08/10/2018, pág. 267/857
259 solução N-óxido de N-metil-morfolina (5,15 g) e tetróxido de ósmio microencapsulado (1 g, contendo 10% de tetróxido de ósmio), e a mistura foi agitada em uma temperatura entre 40 e 50 oC por 21 h. O tetróxido de ósmio microencapsulado insolúvel foi removido por filtração, lavado com acetonitrila, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 1:1), para obter o composto do título (4,97 g).
RMN-!H (CDCla) δ: 1,48-1,58 (6H, m) , 1, 64-1,75 (4H, m) , 1,86-1,96 (2H,m), 2,28(2H,d,J=2,9Hz), 3,90(2H,d,J=8,3Hz).
MS (FAB) m/z: 145(M+H)+.
Exemplo Referencial 76 (IR*,2S*)-1,2-diazido-ciclo-octano:
Depois de dissolver cis-1,2-ciclo-octanodiol (4,82
g) em cloreto de metileno (60 ml), adicionar tietil-amina (27,7 ml) à solução e purgar o interior de um vaso com argônio, a mistura foi resfriada até -78 oC e adicionou-se a ela cloreto de metano-sulfonila (7,7 ml, 100 mmol) em gotas. A mistura foi agitada por 1 h na mesma temperatura e depois por 1 h a 0 oC. Depois, adicionou-se água à mistura da reação para conduzir separação de líquidos, e a camada de 08/10/2018, pág. 268/857
260 orgânica resultante foi lavada com água, ácido clorídrico 0,5 N, água e uma solução aquosa saturada de bicarbonato de sódio, e secada obre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi dissolvido em N,N-dimetil-formamida (80 ml), adicionou-se azida de sódio (13,0 g) , e a mistura foi agitada a 65 oC por 19 h. Adicionou-se água e éter à mistura da reação, para conduzir separação de líquidos. A camada etérea resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 6:1), para obter o composto do título (4,85 g).
RMN-1!! (CDCls) δ: 1, 49-1, 64 (6H,m) , 1, 67-1,78 (2H,m) , 1,81-1,97 (4H,m), 3, 74-3, 76 (2H,m) .
Exemplo Referencial 77 cloridrato de (IR*,2S*)-1,2-ciclo-octano-diamina:
O composto obtido no Exemplo Referencial 76 (4,85 g) foi dissolvido em etanol (55 ml), adicionou-se à solução 10% de paládio sobre carvão (contendo 50% de água, 3,0 g), e a mistura foi agitada por 21 h em uma atmosfera de de 08/10/2018, pág. 269/857
261 hidrogênio (4,5 atm) . Depois de separar o catalisador por filtração, adicionou-se uma solução de ácido clorídrico 1 N em etanol (50 ml) ao filtrado, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se acetato de etila ao resíduo, e o precipitado formado foi coletado por filtração, para obter o composto do título (4,14 g) .
ΗΜΝ-ΧΗ (DMSO) δ: 1,51 (6H, br, s) , 1, 69 (2H, br, s) , 1,79-1,99 (4H,m), 3,68-3,70(2H,m), 8,66(6H,br,s).
MS (ESI) m/z: 143(M+H)+.
Exemplo Referencial 78
N-[(IR*,2S*)-2-amino-ciclo-octil]-5-cloro-indol-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 77, de uma maneira similar àquela do Exemplo Referencial 59.
MS (ESI) m/z: 320(M+H)+.
Exemplo Referencial 79 (IR*,2R*)-4-metóxi-l,2-ciclo-pentanodiol (mistura de estereoisômeros da posição 4):
Petição 870180138821, de 08/10/2018, pág. 270/857
262
OMe
Adicionou-se parceladamente hidreto de sódio a 60% (800 mg) a uma solução de 3-ciclo-penten-l-ol (1,68 g) e iodeto de metila (1,25 ml) em tetraidrofurano (20 ml) sob resfriamento com gelo, e a mistura foi agitada por toda a noite à temperatura ambiente. Adicionou-se água e éter à mistura da reação, para separar uma camada orgânica, a camada orgânica foi secada sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida com resfriamento de gelo, para obter 4-metóxi-lciclo-penteno bruto.
Adicionou-se ácido fórmico a 88% (90 ml) e peróxido de hidrogênio a 30% (3,17 ml) ao 4-metóxi-l-ciclopenteno assim obtido, e a mistura foi agitada por toda a noite à temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, e uma solução aquosa a 35% de hidróxido de sódio foi adicionada ao resíduo, para alcalinizar a mistura da reação, e em seguida, agitou-se a 50 oC por 10 min. A mistura da reação foi resfriada até a temperatura ambiente e extraída com acetato de etila, secando a camada orgânica sobre sulfato de magnésio anidro. O solvente foi removido por destilação, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:19), para obter o composto do de 08/10/2018, pág. 271/857
263 título (1,21 g).
ΚΜΝ-Ή (CDC13) δ: 1, 65-1,85 (2H, m) , 2, 15-2, 30 (2Η, m) , 3,28(3Η,
s), 3,90-4,00(2H,m), 4,26(1Η,br,s).
Exemplo Referencial 80 (IR*,2R*)-1,2-diazido-4-metóxi-l,2-ciclo-pentano (mistura de estereoisômeros da posição 4):

O composto obtido no Exemplo Referencial 79 (1,21 g) e trietil-amina (7,66 ml) foram dissolvidos em cloreto de metileno (20 ml), e adicionou-se cloreto de metano-sulfonila (2,13 ml) em gotas por 20 min a -78 oC. Depois de completar a adição das gotas, a mistura foi aquecida até 0 oC e agitada por 80 min, para obter (IR*, 2R*)-1,2-bis-(metanosulfonilóxi)-4-metóxi-ciclo-pentano bruto. Este produto foi dissolvido em N,N-dimetil-formamida (20 ml), e adicionou-se azida de sódio aquecendo e agitando a mistura a 65 °C por 22 horas. Em seuida, adicionou-se azida de sódio (3,57 g) , aquecendo e agitando a mistura a 70 °C por 2 dias. A mistura da reação foi deixada resfriar, e adicionou-se água e dietil-éter, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação, e resíduo foi de 08/10/2018, pág. 272/857
264 purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1), para obter o composto do título (584 mg).
ΗΜΝ-^ (CDC13) δ: 1, 65-1, 80 (2H, m) , 2, 05-2,18 (1H, m) , 2,255 2, 40(lH,m), 3,21(3H,s), 3, 55-3, 65 (1H, m) , 3, 75-3, 90 (2H, m) .
Exemplo Referencial 81 cloridrato de (IR*,2R*)-4-metóxi-l,2-ciclo-pentano-diamina (mistura de estereoisômeros da posição 4):
O composto obtido no Exemplo Referencial 80 (584 mg) foi disolvido em etanol, e adicionou-se paládio sobre carvão a 10% (321 mg) , para conduzir a hidrogenação em temperatura normal e pressão normal por 2 dias. Depois de remover o catalisador por filtração, a mistura da reação foi concentrada, e adicionou-se ao resíduo uma solução de ácido clorídrico 1 N em etanol, e acetato de etila. A mistura foi concentrada, para obter o composto do título (488 mg).
RMN-1!! (CDC13) δ: 1,72-1,83 (1H, m) , 1, 91-2,03 (1H, m) , 2,072,18(1H, m) , 2,37—2, 50 (1H, m) , 3, 19(3H, s), 3, 55—3, 75(2H,br),
3, 85-3, 95(lH,m), 8, 60-8, 90 (6H,br) .
MS (ESI) m/z: 261(2M+H)+.
Petição 870180138821, de 08/10/2018, pág. 273/857
265
Exemplo Referencial 82
N-[(IR*,2R*)-2-amino-4-metóxi-ciclo-pentil]-5-cloro-indo1-2carboxamida (mistura de estereoisômeros da posição 4):
composto obtido no Exemplo Referencial 81 (470 mg) foi colocado em suspensão em N,N-dimetil-formamida (5 ml) , e adicionou-se trietil-amina (0, 966 ml) e 5-cloroindol-2-carboxilato de p-nitro-fenila (805 mg). A mistura foi agitada à temperatura ambiente por 4 dias. Depois disso, o solvente foi removido por destilação sob pressão reduzida, adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio, para conduzir separação de líquidos, e uma camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:9), para obter o composto do título (268 mg).
Exemplo Referencial 83 (lR*,2R*)-4-[(benzilóxi)-metil]-1,2-ciclo-pentanodiol (mistura de estereoisômeros da posição 4):
Petição 870180138821, de 08/10/2018, pág. 274/857
266
composto do título foi obtido benzilando 4hidróxi-metil-l-ciclo-pentano (J. Heterocycl. Chem. 26:451, 1989) com brometo de benzila e depois reagindo o produto com ácido fórmico/peróxido de hidrogênio, de uma maneira similar àquela do Exemplo Referencial 79.
RMN-!H (CDC13) δ: 1,44-1,52 (1H, m) , 1, 77-1,85 (1H, m) , 1,89l,97(lH,m), 2,25-2,35 (lH,m) , 2,46-2, 58 (lH,m) , 3, 40-3, 50 (2H, m) , 3, 89 (lH,br, s) , 4,08(1H,br,s), 4,54(2H,s), 7,27-7,39 (5H,m).
MS (FAB) m/z: 223(M+H)+.
Exemplo Referencial 84 (IR*,2R*)-4-[(benzilóxi)-metil]-1,2-ciclo-pentano-diamina (mistura de estereoisômeros da posição 4):
(IR*,2R*)-4-benzilóxi-metil-1,2-diazido-ciclo-
|
15 pentano foi |
obtido |
a partir do |
composto obtido no |
Exemplo |
|
Referencial |
83, |
de |
uma maneira |
similar |
àquela do |
Exemplo |
|
Referencial |
80. |
0 |
composto do |
título |
foi obtido |
de uma |
Pclição 870180138821, de 08/10/2018, pág. 275/857
267 maneira similar àquela do Exemplo Referencial 81, sem purificar este produto.
Exemplo Referencial 85
N-[(IR*,2R*)-2-amino-4-[(benzilóxi)-metil]-ciclo-pentil]-55 cloro-indol-2-carboxamida (mistura de estereoisômeros da posição 4):
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 84, de uma maneira similar àquela do Exemplo Referencial 59.
RMN-!H (DMSO-de) δ: 1,07-1, 15 (0, 5H,m) , 1, 26-1, 35 (0,5H, m) ,
1,47-1,55(0,5H,m), 1,61-1,79(1H,m), 1,83-1,92(0,5H,m), 1,992,10 (0,5H,m), 2,12-2,20(0,5H,m), 2,27-2,40(1H, m), 3,10-3,20 (lH,m), 3, 33-3, 39(2H,m) , 3,81-3,92(1H,m), 4,48(2H,s), 7,137,20(2H,m), 7,22-7,39(5H,m), 7,43(1H,d,J=8,5Hz), 7,69(1H, d,J=2,2Hz), 8,34(iH,t,J=7,lHz).
MS (FAB) m/z: 398(M+H)+.
Exemplo Referencial 86 (IR*,3R*,6S*)-7-oxabiciclo[4,1.0]-heptano-3-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 276/857
268
COOEt
(IR*,4R*,5R*)-4-iodo-6-oxabiciclo[3.2.1] -octan-7ona (J. Org. Chem. 61:8687, 1996) (14,3 g) foi dissolvida em etanol (130 ml) , adicionou-se uma solução aquosa 2 N de hidróxido de sódio (34,5 ml) sob resfriamento com gelo, e a mistura foi então agitada à temperatura ambiente por 7 h. Depois disso, o solvente foi removido por destilação sob pressão reduzida, adicionou-se água ao resíduo para conduzir extração com cloreto de metileno, e o extrato foi secado sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 83:17), para obter o composto do título (6,54 g).
RMN-XH (CDC13) δ: 1,25 (3H, t, J=7,1Hz) , 1,50-1,70 (2H, m) , 1,71-
Hz) .
Exemplo Referencial 87 (IR*,3R*,6S*)-3-azido-4-hidróxi-ciclo-hexano-carboxilato de etila:
COOEt
OH
Petição 870180138821, de 08/10/2018, pág. 277/857
269
O composto obtido no Exemplo Referencial 86 (13,6
g) foi dissolvido em N,N-dimetil-formamida (100 ml), adicionou-se sucessivamente cloreto de amônio (6,45 g) e azida de sódio (7,8 g) à temperatura ambiente, e a mistura foi então agitada a 75 oC por 12 h. O solvente foi concentrado até cerca de 1/3 do volume, e o resíduo foi diluído com água e acetato de etila, conduzindo agitação por 3 min. A camada orgânica resultante foi separada, lavada com água e uma solução aquosa saturada de cloreto de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (15,8 g).
RMN-1!! (CDCI3) δ: 1, 28 (3H, t, J=7, 1Hz) , 1,37-1, 67 (2H,m) , 1,86l,95(lH,m), 2, 04-2, 18 (2H,m) , 2,32-2,43 (1H, m) , 2,68-2,78 (lH,m), 3,40-3,60(2H,m), 4,17(2H,q,J=7,1Hz).
Exemplo Referencial 88 (IR*,3S*,4S*)-3-[(t-butóxi-carbonil)-amino]-4-hidróxi-ciclohexano-carboxilato de etila:
COOEt
A
ΒοοΝΗγ^
OH de 08/10/2018, pág. 278/857
270
O composto obtido no Exemplo Referencial 87 (100 mg) e dicarbonato de di-t-butila (133 mg) foram dissolvidos em acetato de etila (12 ml) e adicionou-se uma quantidade catalítica de 10% de paládio sobre carvão, agitando a mistura à temperatura ambiente por 12 h em uma atmosfera de hidrogênio. Depois disso, os insolúveis foram removidos por filtração, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (145 mg).
ΗΜΝ-^ (CDC13) δ: 1,28 (3H, t, J=7,1Hz) , l,45(9H,s), 1,38-1,57 (2H,m), 1,86-1,95(lH,m), 2,05-2,17(1H,m), 2,29-2,39 (2H,
m), 2,61-2,68(lH,m), 3,25-3,66(3H,m), 4,17(2H,q,J=7,1Hz),
4,53 (1H, br, s) .
Exemplo Referencial 89 (IR*,3S*,4R*)-4-azido-3-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de etila e (IR*,3S*,4S*)-4-azido-3-[(tbutóxi-carbonil)-amino]-ciclo-hexano-carboxilato de etila:
COOEt
COOEt
BocNH
BocNH
O composto obtido no Exemplo Referencial 88 (16 g) e trietil-amina (38 ml) foram dissolvidos em cloreto de metileno (150 ml), a solução foi resfriada até -78 oC, e de 08/10/2018, pág. 279/857
271 adicionou-se cloreto de metano-sulfonila (13 ml) em gotas na mesma temperatura. Depois de agitar por 15 min na mesma temperatura, a mistura foi aquecida até 0 oC e agitada por 30 min e depois por 2 h à temperatura ambiente. Depois disso, adicionou-se ácido clorídrico 0,1 N, a mistura foi diluída com cloreto de metileno, a camada orgânica resultante foi separada, lavada com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter (IR*,3S*,4S*)-3-[(t-butóxicarbonil)-amino]-[(metano-sulfonil)oxi]-ciclo-hexanocarboxilato de etila bruto.
O produto obtido acima foi dissolvido em N,Ndimetil-formamida (100 ml) , e adicionou-se azida de sódio (18 g) à temperatura ambiente. A mistura foi aquecida até 75 oC e agitada por 12 h. O solvente foi concentrado até cerca de 1/3 do volume, e o resíduo foi diluído com água e acetato de etila, conduzindo agitação por 3 min. A camada orgânica resultante foi separada, lavada com uma solução aquosa saturada de cloreto de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob e o resíduo foi purificado por coluna em sílica-gel (acetato de etila:hexano 1:4), para obter os compostos do título, forma-[(1R*,3S*,4R*)(6,74 g) e forma-(IR*,33*,4S*) (1,32 g)], forma - (IR*,3S*,4R*):
pressão reduzida, cromatografia de de 08/10/2018, pág. 280/857
272
|
RMN-1H |
(CDCla) |
Ô: |
1,26 (3H,t,J=7,1Hz) , 1,45 |
(9H,s), 1,38-2, |
33 |
|
(6H,m), |
2,57-2, |
68 |
(lH,m), 3, 77—4,20 (4H, m) , |
4,63(1H,br,s). |
|
|
forma - |
(IR*,3S |
★
r |
4S*) : |
|
|
|
RMN-1H |
(CDCI3) |
Ô: |
1,27 (3H,t,J=7,1Hz) , 1,46 |
(9H,s), 1,53-2, |
30 |
|
(6H,m), |
2,50-2, |
65 |
(lH,m), 3, 42-3, 72 (2H,m), |
4,15 |
|
|
(2H,q, J: |
=7,1 Hz) |
r |
4, 67(1H,br,s) . |
|
|
Exemplo Referencial 90 (IR*,3S*,4R*)-4-amino-3-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de etila:
COOEt
BocNH'
NH2
O (IR*,3S*,4R*)-4-azido-3-[(t-butóxi-carbonil)amino]-ciclo-hexano-carboxilato de etila obtido no Exemplo Referencial 89 (5,4 g) foi dissolvido em um solvente misto de etanol (10 ml) e acetato de etila (10 ml), e adicionou-se uma quantidade catalítica de 10% de paládio sobre carvão, agitando a mistura à temperatura ambiente por 20 h em uma atmosfera de hidrogênio. Depois de remover os insolúveis por filtração, o solvente foi removido por destilação sob pressão reduzida, para dar o composto do título (4,7 g).
Exemplo Referencial 91 (IR*,3S*,4R*)-3-[(t-butóxi-carbonil)-amino]-4-{[(5-cloroindol-2-il)-carbonil]-amino}-ciclo-hexano-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 281/857
273
composto obtido no Exemplo Referencial 90 (4,62
g) foi dissolvido em cloreto de metileno (50 ml), adicionouse ácido 5-cloro-indol-2-carboxílico (3,63 g) , 1-hidróxibenzotriazol monoidratado (2,43 g) e cloridrato de 1—(3— dimetil-amino-propil)-3-etil-carbodiimida (3,45 g) à temperatura ambiente, e a mistura foi agitada por 12 h. Depois de adicionar ácido clorídrico 0,1 N, e extrair a mistura com cloreto de metileno, a camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 2:3), para obter o composto do título (5,3 g).
ΗΜΝ-^ (CDC13) δ: 1,26 (3H, t, J=7,1Hz) , l,43(9H,s), 1,35- 2,46 (7H,m), 3,91-4,02(lH,m), 4,10-4,22(2H,m), 4,79(1H,br,s),
6,79(lH,s), 7, 18-7,40 (2H,m) , 7,59(lH,s), 8,00 (1H, br, s) , 9,13 (1H, br, s) .
Petição 870180138821, de 08/10/2018, pág. 282/857
274
Exemplo Referencial 92 (IS,3S,6R)-7-oxabiciclo[4.1.0]-heptano-3-carboxilato de etila:
A (IS,4S,5S)-4-iodo-6-oxabiciclo[3.2.1]-octan-7ona (J. Org. Chem. 61:8687, 1996) (89,3 g) foi colocada em suspensão em etanol (810 ml), adicionou-se uma solução aquosa 2 N de hidróxido de sódio (213 ml) , e a mistura foi então agitada à temperatura ambiente por 3 h. Depois de remover o solvente por destilação sob pressão reduzida, e adicionar água ao resíduo para conduzir a extração com cloreto de metileno, o extrato foi secado sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 17:3), para obter o composto do título (41,3 g).
[a]D25 = -58o (C = 1,0, clorofórmio).
Exemplo Referencial 93 (IS,3R,4R)-3-azido-4-hidróxi-ciclo-hexano-carboxilato de etila:
composto obtido no Exemplo Referencial 92 (41 g) foi dissolvido em N,N-dimetil-formamida (300 ml), adicionouse sucessivamente cloreto de amônio (19,3 g) e azida de sódio (23,5 g) à temperatura ambiente, e a mistura foi então agitada a 76 oC por 13 h. A mistura da reação foi filtrada, o filtrado foi concentrado, o produto captado anteriormente pelo filtro foi colocado no resíduo, e adicionou-se água para dissolver o produto coletado. A solução foi extraída com acetato de etila. A camada orgânica resultante foi de 08/10/2018, pág. 283/857
275 lavada com água e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (51,5 g).
[a]D25 = +8o (C = 1,0, clorofórmio).
Exemplo Referencial 94 (IS,3R,4R)-3-[(t-butóxi-carbonil)-amino]-4-hidróxi-ciclohexano-carboxilato de etila:
O composto obtido no Exemplo Referencial 93 (51,2
g) e dicarbonato de di-t-butila (68,1 g) foram dissolvidos em acetato de etila (1.000 ml), adicionou-se 10% de paládio sobre carvão (5,0 g) , e a mistura foi agitada por toda a noite à temperatura ambiente sob uma pressão de hidrogênio de 7 kg/cm2. Depois de remover os insolúveis por filtração, remover o solvente por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1 —> 3:1), e adicionou-se hexano solidificá-lo e obter o composto do título (46,9 g) .
[a]D25 = +25o (C = 1,0, clorofórmio).
Exemplo Referencial 95 (IS,3R,4S)-4-azido-3-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de etila e (IS,3R,4R)-4-azido-3-[(tbutóxi-carbonil)-amino]-ciclo-hexano-carboxilato de etila:
O composto obtido no Exemplo Referencial 94 (53,5
g) e trietil-amina (130 ml) foram dissolvidos em cloreto de metileno (500 ml) , e adicionou-se cloreto de metanosulfonila (42 ml) em gotas por 20 min sob resfriamento em de 08/10/2018, pág. 284/857
276 uma temperatura entre -10 oC e -15 oC. Depois de agitar por 20 min na mesma temperatura, a mistura foi aquecida até a temperatura ambiente em 2 h. A mistura da reação foi resfriada até 0 oC, adicionou-se ácido clorídrico 0,5 N (800 ml) em gotas, e a mistura foi extraída com cloreto de metileno. A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o (IS,3R,4R)-3[(t-butóxi-carbonil)-amino]-4-[(metil-sulfonil)oxi]-ciclohexano-carboxilato de etila bruto.
O produto bruto obtido acima foi dissolvido em N,N-dimetil-formamida (335 ml), e adicionou-se azida de sódio (60,5 g) , agitando a mistura em uma temperatura entre 65 oC e 75 oC por 16 h. A mistura da reação foi filtrada, o filtrado foi concentrado, removendo por destilação 250 ml do solvente, o produto captado pelo filtro foi colocado no resíduo, captado anteriormente pelo filtro foi colocado no resíduo, e o produto coletado foi dissolvido em água e extraído com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter os compostos do título.
forma - [(IS,3R,4S) (18,4 g) e forma - (IS,3R,4R) (3,3 g)] .
de 08/10/2018, pág. 285/857
277 forma - (1S,3R,4S): [CC]d25 = +62° (C=l,0, clorofórmio), forma - (1S,3R,4R): [CC]d25 — -19° (C=l,0, clorofórmio).
Exemplo Referencial 96 (IS,3R,4S)-4-amino-3-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de etila:
O composto obtido no Exemplo Referencial 95 (4,0
g) foi dissolvido em um solvente misto de etanol (150 ml) e acetato de etila (150 ml), e adicionou-se uma quantidade catalítica de 5% de paládio sobre carvão (0,5 g), agitando a mistura à temperatura ambiente por 17 h em uma atmosfera de hidrogênio (5kg/cm2). Depois de remover os insolúveis por filtração, o solvente foi removido por destilação sob pressão reduzida, para dar o composto do título (4,2 g).
Exemplo Referencial 97 (IS,3R,4S)-3-[(t-butóxi-carbonil)-amino]-4-{[(5-cloro-indol2-il)-carbonil]-amino}-ciclo-hexano-carboxilato de etila:
BocHN
O composto obtido no Exemplo Referencial 96 (4,2
g) foi dissolvido em cloreto de metileno (50 ml), adicionouse ácido 5-cloro-indol-2-carboxílico (3,33 g) , 1-hidróxibenzotriazol monoidratado (2,52 g) e cloridrato de l—(3— dimetil-amino-propil)-3-etil-carbodiimida (3,15 g) à de 08/10/2018, pág. 286/857
278 temperatura ambiente, e a mistura foi agitada por 12 h. Depois de adicionar ácido clorídrico 0,1 N, e extrair a mistura com cloreto de metileno, a camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:1), para obter o composto do título (4,36 g).
[a]D25 = -27° (C = 1,0, clorofórmio).
Exemplo Referencial 98 (IR*,3S*,4R*)-4-amino-3-[(t-butóxi-carbonil)-amino]-4-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]
-amino}-ciclo-hexano-carboxilato de etila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 90 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo Referencial 91.
Exemplo Referencial 99
3-ciclo-hexano-l-carboxilato de benzila:
de 08/10/2018, pág. 287/857
279
Ç00CH2Ph ίο
O ácido (±)-ciclo-hexeno-l-carboxílico (50 g) foi dissolvido em N,N-dimetil-formamida (550 ml), e adicionou-se trietil-amina (170 ml) e brometo de benzila (61 ml) sob resfriamento com gelo, agitando a mistura à temperatura ambiente por 12 h. Adicionou-se água, a extração foi conduzida com acetato de etila, e a camada orgânica resultante foi lavada com uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (70,8 g).
EMN-^ (CDC13) δ: 1, 66-1,76 (lH,m) , 2, 00-2, 13 (3H, m) , 2,27-2,29 (2H,m), 2, 58—2, 65 (1H,m) , 5,13(2H,s), 5, 66 (2H, br, s) , 7,297,38 (5H,m) .
Exemplo Referencial 100 (IR*,3S*,6S*)-7-oxabiciclo[4.1.0]-heptano-3-carboxilato de benzila:
ÇOOCH2Ph
COOCH2Ph
Petição 870180138821, de 08/10/2018, pág. 288/857
280 composto
O composto obtido no Exemplo Referencial 99 (40 g) foi dissolvido em cloreto de metileno (500 ml) e adicionouse ácido m-cloro-perbenzóico (86 g) sob resfriamento com gelo, agitando a mistura por 2 h. Depois de adicionar uma solução aquosa de tiossulfato de sódio a 10%, conduzindo agitação por 20 min, uma camada orgânica foi separada, lavada com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:9), para obter o título (23,4 g) e (IR*,3R*,6S*)-7do oxabiciclo[4.1.0]-heptano-3-carboxilato de benzila.
RMN-1H (CDC13) δ: 1,39-1,4 9 (1H, m) , 1,75-1,82 (1H, m) , 1,902,04(3H,m), 2,30(1H,dd,J=14,9, 4,9Hz), 2,54-2,61(1H,m),3,123,14(lH,m), 3, 22-3, 24 (lH,m) , 5,12(2H,s), 7,30-7,39 (5H, m) .
MS (FAB) m/z: 233(M+H)+.
Exemplo Referencial 101 (IR*,3S*,4S*)-4-azido-3-hidróxi-ciclo-hexano-carboxilato de benzila:
de 08/10/2018, pág. 289/857
281
O composto do Exemplo Referencial 100 (52,3 g) foi dissolvido em N,N-dimetil-formamida (1.000 ml), adicionou-se cloreto de amônio (21,9 g) e azida de sódio (18,1 g) , e a mistura foi aquecida até 70 oC e agitada por 24 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se água, para conduzir a extração com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada com sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (61,8 g). RMN-!H (CDC13) δ: 1,51-1, 66 (2H, m) , 1, 91-1, 98 (1H, m) , 2,07-2,10 (lH,m), 2, 27-2, 32 (lH,m), 2,51-2,52(1H,m), 2,81-2,86(1H,m),
3, 30-3, 36 (lH,m) , 3, 70-3, 75 (1H, m) , 5,13(2H,s), 7, 30-7,39 (5H,
m) .
Exemplo Referencial 102 (IR*,3S*,4S*)-4-[(t-butóxi-carbonil)-amino]-3-hidróxi-ciclohexano-carboxilato de benzila:
ÇOOCH2Ph
NHBoc
O composto obtido no Exemplo Referencial 101 (5,27 g) foi dissolvido em tetraidrofurano (25 ml), e adicionou-se trifenil-fosfina (5,53 g) e água (0,55 ml), agitando a mistura à temperatura ambiente por 20 h. Adicionou-se de 08/10/2018, pág. 290/857
282 dicarbonato de di-t-butila (4,82 g) a mistura da reaçao, continuando a agitar por mais 2 h. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia (hexano:acetato de etila 2:1), título (6,22 g).
ΗΜΝ-^ (CDC13) δ: l,44(9H,s), (2H,m), 2,29-2,32 (lH,m) , 2,80
3,42(lH,br,s), 3,59-3,65(1H,m),
12,5Hz), 7,30-7,38(5H,m).
MS (FAB) m/z: 350(M+H)+.
de coluna em silica-gel para obter o composto do
1,59-1, 66 (2H,m) , 1,88-2,00
2,85(lH,m), 3, 02 (1H, br, s) ,
4,56 (lH,br, s) , 5,12(2H,q,J=
Exemplo Referencial 103 (IR*,3S*,4S*)-4-[(t-butóxi-carbonil)-amino]-3-hidróxi-ciclohexano-carboxilato de metila:
COOMe
NHBoc
O composto obtido no Exemplo Referencial 102 (2,54 g) foi dissolvido em acetato de etila (15 ml), e adicionouse uma quantidade catalítica de 10% de paládio sobre carvão à solução. A mistura foi agitada em uma corrente de hidrogênio à temperatura ambiente por 20 h. Depois de remover o catalisador por filtração, o filtrado foi concentrado sob pressão reduzida, para dar o ácido de 08/10/2018, pág. 291/857
283 (IR*,3S*,4S*)-4-[(t-butóxi-carbonil)-amino]-3-hidróxi-ciclohexano-carboxílico, como um óleo incolor. O óleo foi dissolvido em uma mistura de metanol (8 ml) e tolueno (15 ml) , à qual adicionou-se uma solução 2 N de trimetil-silildiazometano em hexano sob resfriamento com gelo, e a mistura resultante foi agitada por 30 min à temperatura ambiente. Depois de remover o solvente por pressão reduzida, o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 1:1), para obter o composto do título (1,82 g).
ΗΜΝ-^ (CDC13) δ: l,44(9H,s), 1,36-2, 32 (7H, m) , 2,74-2, 82 (1H, m) , 3,04(lH,br,s), 3, 33-3, 47(1H,m), 3, 55-3, 65(1H,m), 3,68 (3H,s), 4,56 (1H, br, s) .
MS (FAB) m/z: 274(M+H)+.
Exemplo Referencial 104 (IR*,3R*,4S*)-3-azido-4-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de metila e (IR*,3S*,4S*)-3-azido-4-[(tbutóxi-carbonil)-amino]-ciclo-hexano-carboxilato de metila:
ÇOOMe ÇOOMe
= 3 I
NHBoc NHBoc
O composto obtido no Exemplo Referencial 103 (1,81 g) foi dissolvido em cloreto de metileno (36 ml), e adicionou-se trietil-amina (4, 6 ml) e cloreto de metanode 08/10/2018, pág. 292/857
284 sulfonila (1,63 ml) a -78 oC. Depois de 30 min, a mistura foi aquecida até 0 oC e agitada por 30 min. Adicionou-se ácido clorídrico 1 N, a extração foi conduzida com cloreto de metileno, e a camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada com sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter (IR*,3S*,4S*)-4[(t-butóxi-carbonil)-amino]-3-[(metil-sulfonil)oxi]-ciclohexano-carboxilato de metila.
O produto bruto obtido acima foi dissolvido em
N,N-dimetil-formamida (23 ml), adicionou-se azida de sódio (1,29 g) , e a mistura foi aquecida até 70 oC e agitada por 12 h. Adicionou-se água à mistura da reação, a extração foi conduzida com acetato de etila, e a camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada com sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 3:17), para obter (IR*,3S*,4S*)-3-azido-4-[(t-butóxi-carbonil)-amino]ciclo-hexano-carboxilato (85 mg) e (IR*,3R*,4S*)-3-azido-4[(t-butóxi-carbonil)amino]ciclo-hexano-carboxilato de metila (590 mg).
|
forma - (IR*,3R*,4S*): |
RMN-1H |
(CDC13) δ: |
l,45(9H,s), 1,35- |
|
2,35 (7H,m), 2,45—2,55 |
(lH,m) , |
3,73(3H,s) |
, 3, 67-3, 84(2H,m), |
|
4,70( 1H, br, s) . |
|
|
|
|
MS (FAB) m/z: 299(M±H)+. |
|
|
|
|
forma - (IR*,3S*,4S*): |
RMN-1H |
(CDCI3) δ: |
l,45(9H,s), 1,56- |
Petição 870180138821, de 08/10/2018, pág. 293/857
285
2,25(7H,m), 2, 68-2, 80 (1H,m) , 3,70(3H,s), 3, 48-3, 68(2H,m),
4,56(1H,br,s).
MS (FAB) m/z: 299(M+H)+.
Exemplo Referencial 105 (IR*,3R*,4S*)-3-amino-4-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de metila:
COOMe
H2N
NHBoc
O composto (IR*,3R*,4S*) (230 mg) obtido no
Exemplo Referencial 104 foi dissolvido em acetato de etila (8 ml), e adicionou-se uma quantidade catalítica de 10% de paládio sobre carvão, agitando a mistura à temperatura ambiente por 20 h em uma atmosfera de hidrogênio. Os insolúveis foram removidos por filtração, e o filtrado foi concentrado sob pressão reduzida, para obter o composto do título (220 mg).
Exemplo Referencial 106 (IR*,3R*,4S*)-4-[(t-butóxi-carbonil)-amino]-3-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il-carbonil]amino}-ciclo-hexano-carboxilato de metila:
Petição 870180138821, de 08/10/2018, pág. 294/857
286
COOMe
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 105 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo Referencial 91.
RMN-XH (CDC13) δ: l,46(9H,s), 1,53-1, 95 (5H, m) , 2,17-2,24 (lH,m), 2,50(3H,s), 2,50-2,53 (1H, m) , 2, 80-2, 96 (4H, m) , 3,67 (3H,s), 3,69-3,74(lH,m), 4,10(2H,br,s), 4,88(1H,br,s).
MS (FAB) m/z: 453(M+H)+.
Exemplo Referencial 107 (IR*,3R*,4S*)-4-[(t-butóxi-carbonil)-amino]-3-{[(5-metilcloro-indol-2-il)carbonil]-amino}-ciclo-hexano-carboxilato de metila:
COOMe
NHBoc
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 105, de uma maneira similar àquela do Exemplo Referencial 91.
Petição 870180138821, de 08/10/2018, pág. 295/857
287
RMN-* 1 2 H (CDC13) δ: l,33(9H,s), 1, 42-2,47 ( 6H, m) , 2,78-2,88 (lH,m), 3,70(3H,s), 3, 86—4,15 (2H,m) , 4, 65—4,75 (lH,m) , 6,86 (lH,br,s), 7,18—7,38 (2H,m) , 7,57—7, 61 (1H, m) , 8, 32 (1H, br, s) . MS (ESI) m/z: 450(M+H)+.
Exemplo Referencial 108 (IS,3R,6R)-7-oxabiciclo[4.1.0]-heptano-3-carboxilato de benzila:
1) O (IR)-3-ciclo-hexeno-l-carboxilato de benzila
|
foi obtido |
a |
partir |
do |
ácido (IR)-3-ciclo-hexeno-l- |
|
carboxílico |
(J. |
Am. Chem. |
Soc. 100:5199, 1978), de uma |
|
maneira similar |
àquela do |
Exemplo Referencial 99. |
|
2) |
0 |
composto |
do |
título foi obtido a partir do |
|
produto descrito acima, |
de |
uma maneira similar àquela do |
Exemplo Referencial 100.
MS (FAB) m/z: 233(M+H)+.
Exemplo Referencial 109 (IS,3S,4S)-4-[(t-butóxi-carbonil)-amino]-3-hidróxi-ciclohexano-carboxilato de benzila:
1) O (IR, 3S,4S)-4-azido-3-hidróxi-ciclo-hexano20 carboxilato de benzila foi obtido a partir do composto obtido no Exemplo Referencial 108, de uma maneira similar àquela do Exemplo Referencial 101.
2) O composto do titulo foi obtido a partir do produto descrito acima, de uma maneira similar àquela do
Exemplo Referencial 102.
MS (FAB) m/z: 350(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 296/857
288
Exemplo Referencial 110 (IR,3R,4S)-3~azido-4-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de benzila:
NHBoc
O composto do título foi obtido a partir do 5 composto obtido no Exemplo Referencial 109, de uma maneira similar àquela do Exemplo Referencial 104.
RNIN-iH (CDC13) δ: l,45(9H,s), 1,52-1, 66 (2H, m) , 1,83-2,01 (3H,m), 2,20-2,28 (lH,m), 2,51-2,54 (lH,m), 3,77 (2H,br,s),
4,70(lH,br,s), 5,15(2H,ABq,J=12,2Hz), 7,33-7,38(5H,m).
MS (FAB) m/z: 375(M+H)+.
Exemplo Referencial 111 (IR,3R,4S)-3-azido-4-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de metila:
COOMe
NHBoc
O composto obtido no Exemplo Referencial 110 (3,5
g) foi dissolvido em tetraidrofurano (130 ml) e adicionou-se
Petição 870180138821, de 08/10/2018, pág. 297/857
289 água (16 ml) e hidróxido de lítio (291 mg) sob resfriamento com gelo. Depois de 10 min, a mistura foi aquecida até a temperatura ambiente, continuando a agitar. Depois de 20 h, a reação foi interrompida, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi submetido a uma cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:20), para obter o ácido (IR,3R,4S)-3-azido-4-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxílico (3,34 g) , como um óleo amarelo-pálido.
Este produto foi dissolvido em metanol (18 ml) e tolueno (64 ml) , adicionou-se uma solução de trimetil-silil-diazometano 2 N em hexano, sob resfriamento com gelo. Depois de 10 min, a mistura foi aquecida até a temperatura ambiente e aquecida por 2 h. Depois de remover o solvente por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (3,35 g).
RMN-!H (CDCls) δ: l,45(9H,s), 1, 57-1, 63 (2H, m) , 1,82-1,85 (lH,m), 1,95-1,99(2H,m), 2,20-2,28(lH,m), 2,48-2,51(1H,m),
3, 73(3H,s), 3, 78 (2H, br, s) , 4, 70-4,72 (lH,m) .
MS (FAB) m/z: 299(M+H)+.
Exemplo Referencial 112 (IR,3R,4S)-4-[(t-butóxi-carbonil)-amino]-3-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il-carbonil]25 amino}-ciclo-hexano-carboxilato de metila:
Petição 870180138821, de 08/10/2018, pág. 298/857
290
COOMe
1) 0 (IR,3R,4S)-3-amino-4-[(t-butóxi-carbonil)amino]ciclo-hexano-carboxilato de metila foi obtido a partir do composto obtido no Exemplo Referencial lll, de uma maneira similar àquela do Exemplo Referencial 105.
2) O composto do título foi obtido a partir do produto descrito acima e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo
Referencial 106.
MS (FAB) m/z: 453 (M+H)+.
Exemplo Referencial 113 (1R*,2S*,5S*)-5-amino-carbonil-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexano-carboxilato de t-butila:
O composto obtido no Exemplo Referencial 91 (590
Petição 870180138821, de 08/10/2018, pág. 299/857
291 mg) foi dissolvido em um solvente misto de etanol (3 ml) e tetraidrofurano (6 ml), adicionou-se uma solução 1 N de hidróxido de sódio (2,5 ml) à temperatura ambiente, e a mistura foi agitada por 12 h. 0 solvente foi removido por destilação, para obter sódio (IR*,3S*,4R*)-3-[(t-butóxicarbonil )-amino]-4-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexano-carboxilato. Este produto foi colocado em suspensão em N,N-dimetil-formamida (4 ml), adicionou-se dicarbonato de di-t-butila (654 mg) e bicarbonato de amônio (1 g) à temperatura ambiente, e a mistura foi agitada por 18 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se água, para conduzir a extração com clorofórmio. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada com sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3), para obter o composto do título (82 mg).
MS (ESI) m/z: 435 (M+H)+.
Exemplo Referencial 114 (IR,6S)-{[(benzilóxi)-carbonil]-amino}-3-ciclo-hexen-l-ilcarbamato de benzila:
HN
COOCH2Ph de 08/10/2018, pág. 300/857
292 cloridrato de 4-ciclo-hexeno-l,2-diamina (4,0 g) foi dissolvido em um solvente misto de água (20 ml) e acetonitrila (20 ml), adicionou-se cloro-formiato de benzila (7,66 ml) e carbonato de potássio (14,9 g) , e a mistura foi agitada à temperatura ambiente por 3 dias. A mistura da reação foi vertida sobre água, para conduzir extração com cloreto de metileno. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno), para obter o composto do título (8,22 g) .
ΗΜΝ-^ (CDC13) δ: 2,03(2H,m), 2,53 (2H, d, J=17, 1Hz) , 3,77 (2H,m) , 5, 03 (2H, q, J=12,3Hz) , 5, 09 (2H, q, J=12,3Hz) , 5,59(2H,s),
7,32 (10H,m) .
MS (ESI) m/z: 381(M+H)+.
Exemplo Referencial 115 (IR*,2S*)-2-{[(benzilóxi)-carbonil]-amino}-5-hidróxi-ciclohexil-carbamato de benzila:
PhCH2OOC
O composto obtido no Exemplo Referencial 114 (10
Petição 870180138821, de 08/10/2018, pág. 301/857
293
g) foi dissolvido em tetraidrofurano absoluto (70 ml), adicionou-se complexo de sulfeto de dimetila e borano (7,4 ml) a 0 oC, e a mistura foi aquecida gradualmente até a temperatura ambiente e agitada por 14 h. Adicionou-se gelo à mistura da reação, para decompor o excesso de borano, e adicionou-se uma solução aquosa 1 N de hidróxido de sódio a 30% (80 ml), agitando a mistura por 1 h como ela está. A mistura da reação foi extraída com acetato de etila, a camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 2:1), para obter o composto do título (9,2 g).
RMN-1!! (CDC13) δ: l,98(lH,m), 2,08(lH,m), 2,30(lH,m), 3,43 (2H,m), 3,73(lH,m), 5,06(6H,m), 7,32(10H,s).
MS (ESI) m/z: 399(M+H)+.
Exemplo Referencial 116 (lR*,2S*)-2-{[(benzilóxi)-carbonil]-amino}-5-oxo-ciclohexil-carbamato de benzila
PhCH2OOC
Adicionou-se sulfóxido de dimetila (8,2 ml) a uma de 08/10/2018, pág. 302/857
294 solução de cloreto de oxalila (9,9 ml) em cloreto de metileno (90 ml) a -60 oC, e adicionou-se uma solução do composto obtido no Exemplo Referencial 115 (9,2 g) em tetraidrofurano (90 ml) foi adicionada à mistura de uma só vez. Depois de 1 h, a temperatura da mistura foi elevada para -40 oC, e adicionou-se trietil-amina (26 ml) de uma só vez. A mistura foi aquecida até a temperatura ambiente como ela estava, e foi agitada por 3 h. A mistura da reação foi vertida sobre água e extraída com cloreto de metileno. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:1), para obter o composto do título (8,0 g).
RMN-1!! (CDCls) δ: 2,27-2,43 (4H, m) , 2,78 (1H, dd, J=14,4,3, 9Hz) ,
3,86(2H,m), 5,08(4H,m), 5,22(2H,m), 7,32(10H,m).
MS (ESI) m/z: 397(M+H)+.
Exemplo Referencial 117 (lR*,2S*)-2-{[(benzilóxi)-carbonil]-amino}-5,5-dimetóxiciclo-hexil-carbamato de benzila
PhCH2OOC
de 08/10/2018, pág. 303/857
295 composto obtido no Exemplo Referencial 116 (3,89 g) foi dissolvido em um solvente misto de metanol (15 ml) e tetraidrofurano (15 ml), adicionou-se 2,2-dimetóxi-propano (10,7 ml) e ácido p-tolueno-sulfônico (187 mg), e a mistura foi agitada à temperatura ambiente por 3 h. O solvente foi concentrado, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio, para conduzir extração com acetato de etila. Depois de lavar a camada orgânica resultante com solução aquosa saturada de cloreto de sódio e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:2), para obter o composto do título (3,54 g) . ΗΜΝ-Ή (CDC13) δ: 1,30-1,41 (4H, m) , l,93(lH,m), 2,38(lH,m),
3,19(6H,s), 3,46(lH,m), 3,59(lH,m), 5, 03 (2H, q, J=12, 5Hz) ,
5,09(2H,q,J=12,5Hz), 7,32 (10H,s) .
Exemplo Referencial 118
N-[(IR*,2S*)-2-amino-4,4-dimetóxi-ciclo-hexil]-5-cloroindol-2-carboxamida e N-[(IR*,2S*)-2-amino-5,5-dimetóxi20 ciclo-hexil]-5-cloro-indol-2-carboxamida
O composto obtido no Exemplo Referencial 117 (1,45
Petição 870180138821, de 08/10/2018, pág. 304/857
296
g) foi dissolvido em metanol (12 ml) , e adicionou-se 10% de paládio sobre carvão (290 mg), agitando a mistura à temperatura ambiente por 20 h em uma atmosfera de hidrogênio. Adicionou-se mais paládio a 10% sobre carvão (290 mg) e metanol (10 ml), agitando a mistura por 8 h. A mistura da reação foi filtrada através de Celite, licor-mãe foi concentrado, e o resíduo foi dissolvido em N,N-dimetilformamida (10 ml) . Adicionou-se ácido 5-cloro-indol-2carboxílico (320 mg), cloridrato de 1-(3-dimetil-aminopropil)-3-etil-carbodiimida (377 mg), 1-hidróxi-benzotriazol monoidratado (301 mg) e N-metil-morfolina (360 ml) , e a mistura foi agitada à temperatura ambiente por 14 h. A mistura da reação foi vertida sobre uma solução aquosa de bicarbonato de sódio e extraída com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi isolado e purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:metanol 93:7), para obter N-[(IR*,2S*)2-amino-4,4-dimetóxi-ciclo-hexil]-5-cloro-indol -2- carboxamida (ou N-[(IR*,2S*)-2-amino-5,5-dimetóxi-ciclo-hexil]-5cloro-indol-2-carboxamida) (98 mg) e N-[(IR*,2S*)-2-amino5,5-dimetóxi-ciclo-hexil]-5-cloro-indol-2- carboxamida (ou N-[(IR*,2S*)-2-amino-4,4-dimetóxi-ciclo-hexil]-5-cloro-indol -2-carboxamida) (105 mg).
N-[(IR*,2S*)-2-amino-4,4-dimetóxi-ciclo-hexil]-5-cloroindol-2-carboxamida:
de 08/10/2018, pág. 305/857
297
RMN—XH (CDCI3) δ: 145-1,50(2H,m), 2, 06-2, 10 (2H, m) , 2,34(1H, d,J=13,lHz), 2,78 (1H, dt, J=2, 9, 13,1Hz), 3,18(3H,s), 3,23 (3H,s), 3, 75-3, 77 (lH,m), 6,24(1H,d,J=8,3Hz) , 6,79(lH,s),
7,23 (1H, dd, J=8,8, 2,0Hz), 7,35 (1H, d, J=8, 8Hz) , 7,60(lH,d,J=
8,8Hz), 9,53(lH,br, s) .
MS (ESI) m/z: 352(M±H)+.
N-[(IR*,2S*)-2-amino-5,5-dimetóxi-ciclo-hexil]-5-cloroindol-2-carboxamida:
RMN-1H (CDCI3) δ: 1,83-1,87 (1H, m) , 1, 97-2,01 (1H, m) , 2,39(1H, br,J=13,2 Hz), 2, 86-2, 90(1H,m) , 3, 22-3, 28(1OH,m) , 4,00-4,02 (lH,m), 6,77(lH,s), 7,23 (1H, d, J=8, 5Hz) , 7,37 (1H, d, J=8, 5Hz) . MS (ESI) m/z: 352(M+H)+.
Exemplo Referencial 119 (7R*,8S*)-7-{[(benzilóxi)-carbonil]-amino}-1,4-dioxaespiro [4.5]-dec-8-il-carbamato de benzila:
PhCH200C
O composto obtido no Exemplo Referencial 116 (4,0
g) foi dissolvido em tetraidrofurano absoluto (30 ml) e adicionou-se etilenoglicol (5,6 ml) e ácido p-toluenosulfônico (192 mg) , agitando a mistura à temperatura ambiente por 17 h. A mistura da reação foi vertida sobre uma solução aquosa saturada de bicarbonato de sódio e
Petição 870180138821, de 08/10/2018, pág. 306/857
298 extraída com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:1), para obter o composto do título (4,23 g).
ΚΜΝ-^ (CDC13) δ: 1, 65-1,71 (4H, m) , 2,00(lH,m), 2,ll(lH,m),
3,49(lH,m), 3,73(lH,m), 3,93(4H,s), 5, 03 (2H, q, J=12,2Hz) ,
5, 08 (2H, q, J=12,2Hz) , 7,32(10H,s).
MS (ESI) m/z: 441(M+H)+.
Exemplo Referencial 120
N-[(7R*,8S*)-7-amino-l,4-dioxaespiro[4.5]-dec-8-il]-5-cloroindol-2-carboxamida e N-[(7R*,8S*)-8-amino-l,4-dioxaespiro [4.5]-dec-7-il]-5-cloro-indo1-2-carboxamida:
N-[(7R*,8S*) -7- amino-1,4-dioxaespiro[4.5]-dec-8il]-5-cloro-indol-2-carboxamida (ou N-[(7R*,8S*)-8-amino1,4-dioxaespiro[4.5]-dec-7-il]-5-cloro-indol-2-carboxamida) e N-[(7R*,8S*)-8-amino-l,4-dioxaespiro[4.5]-dec-7-il]-5Pclição 870180138821, de 08/10/2018, pág. 307/857
299 cloro-indol-2-carboxamida (ou Ν-[(7R*,8S*)-7-amino-l,4dioxaespiro[4.5]-dec-8-il]-5-cloro-indol-2-carboxamida) foram obtidos a partir do composto obtido no Exemplo Referencial 119, de uma maneira similar àquela do Exemplo
Referencial 118.
N-[(7R*,8S*)-7-amino-l,4-dioxaespiro[4.5]-dec-8-il]-5-cloroindol-2-carboxamida (ou N-[(7R*,8S*)-8-amino-l,4-dioxaespiro [4.5]-dec-7-il]-5-cloro-indol-2-carboxamida):
RMN-1H (CDC13) δ: 1, 68-1,81 (4H, m) , 2,ll(2H,m), 2, 87 (1H, td, J=
6,80(lH,s), 7,24(1H,d,J=9,OHz), 7,35(1H,d,J=9,OHz), 7,61 (1H
s) , 9, 47(br,s,1H) .
MS (ESI) m/z: 350(M+H)+.
N-[(7R*, 8S*) -8-amino-l,4-dioxaespiro[4.5]-dec-7-il]-5-cloro15 indol-2-carboxamida (ou N-[(7R*,8S*)-7-amino-l,4-dioxaespiro [4.5]-dec-8-il]-5-cloro-indol-2-carboxamida):
RMN-iH (CDC13) δ: l,65(2H,m), l,88(lH,m), l,96(lH,m), 2,31 (1H, dd, J=12, 9, 3,2Hz), 2,96(lH,m), 3,98(lH,m), 4,02(4H,s),
4,12(lH,m), 6,77(lH,s), 7,06 (1H, br, s) , 7,23 (1H, dd, J=8, 8, 2,0 20 Hz), 7,37(1H,d,J=8,8Hz), 7, 62(1H,d,J=2,OHz), 9,49(1H,br,s) .
MS (ESI) m/z: 350(M+H)+.
Exemplo Referencial 121 (IR,6S)-6-[(t-butóxi-carbonil)-amino]-3-ciclo-hexen-l-ilcarbamato de t-butila:
BocHN
NHBoc
Petição 870180138821, de 08/10/2018, pág. 308/857
300
O cloridrato de cis-4-ciclo-hexeno-l,2-diamina (4,0 g) foi dissolvido em um solvente misto de água (40 ml) e acetonitrila (40 ml), e adicionou-se carbonato de di-tbutila (11,8 g) e trietil-amina (12 ml), e a mistura foi agitada à temperatura ambiente por 4,5 h. A mistura da reação foi vertida sobre água para conduzir extração com cloreto de metileno, e a camada de cloreto de metileno resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (6,12 g).
ΚΜΝ-^ (CDC13) δ: l,44(18H,s), 1, 98 (2H, dd, J=9, 3, 15, 9Hz) ,
2,48 (2H,br,d, J=15, 9Hz) , 3,66 (2H,br,s), 4,88 (2H, br, s) ,
5,58(2H,d,J=2,7Hz).
Exemplo Referencial 122 (IR*,2S*)-2-[(t-butóxi-carbonil)-amino]-5-hidróxi-ciclohexil-carbamato de t-butila (mistura de estereoisômeros):
OH
BocHN'
NHBoc
O composto obtido no Exemplo Referencial 121 (6,1
g) foi dissolvido em tetraidrofurano absoluto (40 ml), e de 08/10/2018, pág. 309/857
301 adicionou-se complexo de sulfeto de dimetila e borano (2,22 ml) sob resfriamento com gelo. A mistura foi agitada por 16 h enquanto ela era aquecida gradualmente até a temperatura ambiente como ela estava. Adicionou-se gelo à mistura da reação, e adicionou-se uma solução aquosa de hidróxido de sódio a 30% (50 ml) , agitando a mistura à temperatura ambiente por 2 h como ela está. A mistura da reação foi extraída com acetato de etila, a camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:2 2:1), para obter o composto do título (6,1 g).
RMN-1!! (CDC13) δ: l,42(9H,s), l,43(9H,s), 1, 83-1, 67 (5H, m) ,
2,15(lH,m), 2,22(lH,s), 3,34(lH,m), 3,78(lH,m), 4,15 (lH,s), 4,98(1H,q,J=9,OHz), 5,02(1H,q,J=9,OHz).
MS (ESI) m/z: 331(M+H)+.
Exemplo Referencial 123 (IR*,2S*)-2-[(t-butóxi-carbonil)-amino]-5-oxo-ciclo-hexilcarbamato de t-butila:
BocHN
NHBoc
Petição 870180138821, de 08/10/2018, pág. 310/857
302
Dissolveu-se cloreto de oxalila (8,2 ml) e sulfóxido de dimetila (6,8 ml) em cloreto de metileno (100 ml) a -60 oC, e adicionou-se uma solução do composto (mistura de estereoisômeros) do composto obtido no Exemplo Referencial 122 (6,32 g) em tetraidrofurano (80 ml), de uma só vez, e a mistura foi agitada por 1 h. A temperatura da mistura foi elevada até -40 oC, e adicionou-se trietil-amina (21 ml). A mistura foi aquecida até a temperatura ambiente. Depois de 3 horas, a mistura da reação foi vertida sobre água e extraída com cloreto de metileno. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:1), para obter o composto do título (3,8 g).
RMN-XH (CDC13) δ: l,43(9H,s), 1,44 (9H,s), 2,24-2,36 (3H,m),
2,39-2,44 (2H,m), 2, 75(1H, dd,J=14,6,2,9Hz), 3,66-3,81(2H,m),
4,95-4,90(lH,m), 4,97-5,03(lH,m).
Exemplo Referencial 124 (IR*,2S*)-2-[(t-butóxi-carbonil)-amino]-5-(metóxi-imino)ciclo-hexil-carbamato de t-butila:
NOMe
NHBoc de 08/10/2018, pág. 311/857
303
O composto obtido no Exemplo Referencial 123 (1,5
g) foi dissolvido em metanol (30 ml), e adicionou-se cloridrato de O-metil-hidroxamina (572 mg) e piridina (737 ml), agitando a mistura à temperatura ambiente por 17 h. Depois de concentrar a mistura da reação, adicionou-se água para conduzir extração com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (1,52 g).
ΗΜΝ-!Η (CDC13) δ: l,44(18H,s), l,64(lH,m), 2,16(2H,m), 2,44 (lH,m), 3, 45-3, 63 (3H,m) , 3,82(3H,s), 4,93(lH,m).
Exemplo Referencial 125 (IR*,2S*)-2-[(t-butóxi-carbonil)-amino]-5-{[t-butil(difenil)-silil]oxi}-ciclo-hexil-carbamato de t-butila (Estereoisômero A):
NHBoc
O composto do título foi obtido a partir do composto (mistura de estereoisômeros) obtido no Exemplo Referencial 122, de uma maneira similar àquela do Exemplo de 08/10/2018, pág. 312/857
304
Referencial 58, e o (IR*,2S*)-2-[(t-butóxi-carbonil)-amino]5-hidróxi-ciclo-hexil-carbamato de t-butila (Estereoisômero
B) foi recuperado.
ΗΜΝ-^ (CDC13) δ: l,03(9H,s), l,39(9H,s), l,40(9H,s), 1,72 (lH,m), l,86(lH,m), 2,13(lH,m), 3,24(2H,m), 3,65(lH,m), 4,83 (lH,m) , 7,37 (10H,m) .
Exemplo Referencial 126 (IR*,2S*)-2-{[(benzilóxi)-carbonil]-amino}-5-hidróxi-5metil-ciclo-hexil-carbamato de benzila:
PhCH2OOC
Colocou-se cloreto de cério anidro (6,4 g) em suspensão em tetraidrofurano (50 ml), e a suspensão foi resfriada até -78 oC em uma atmosfera de argônio. Uma solução de metil-lítio (solução 1,14 N em dietil-éter, 22,5 ml) foi adicionada à suspensão, e a mistura foi agitada a 15 78 oC por 30 min. Uma solução do composto obtido no Exemplo
Referencial 116 (3,0 g) em tetraidrofurano (50 ml) foi adicionada em gotas a -78 oC, e a mistura foi agitada por 30 min. A mistura da reaçãofoi vertida sobre uma solução aquosa a 3% de ácido acético (100 ml), e adicionou-se dietil-éter (50 ml), agitando a mistura à temperatura ambiente por 10 min. A mistura da reação foi extraída com
Petição 870180138821, de 08/10/2018, pág. 313/857
305 acetato de etila, e a camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado duas vezes por cromatografia de coluna em sílica-gel (metanol:clorofórmio 0:100 —> 1:19), para obter o composto do título (Estereoisômero A) (780 mg) e o composto do título (Estereoisômero B) (1,1 g).
Estereoisômero A:
RMN-1H (CDC13) δ: l,26(3H,s), 1, 27-2, 08 (6H, m) , 3, 48 (1H, br, s) , 3, 59(lH,br,s), 5, 02-5, 09 (5H, m) , 5, 33(1H,br,s), 7,30-7,32(10
H,s) .
MS (FAB) m/z: 413(M+H)+.
Estereoisômero B:
RMN-iH (CDCls) δ: l,25(3H,s), 1, 29-2, 07 (6H, m) , 3, 39 (1H, br, s) , 3, 82 (lH,br, s) , 5, 02-5, 23 (6H, m) , 7,30(lOH,s).
MS(FAB) m/z: 413(M+H)+.
Exemplo Referencial 127 (3R*,4S*)-3,4-diamino-l-metil-ciclo-hexanol (Estereoisômero A):
Petição 870180138821, de 08/10/2018, pág. 314/857
306
Colocou-se 10% de paládio sobre carvão (350 mg) em suspensão em uma solução do composto (Estereoisômero A) (780 mg) obtido no Exemplo Referencial 126 em metanol (100 ml), e a suspensão foi agitada por 5 h em uma atmosfera de hidrogênio. 0 catalisador foi removido por filtração, o filtrado foi concentrado sob pressão reduzida. Depois de dissolver o resíduo em cloreto de metileno (100 ml), e secar a solução sobre sulfato de sódio anidro, o solvente foi removido por destilação, para obter o composto do título (Estereoisômero A) (190 mg).
EMN-iH (CDC13) δ: l,22(3H,s), 1, 25-2, 48 (11H, m) , 2,62(lH,br,
s) , 2,78 (1H, br, s) .
Exemplo Referencial 128
Mistura de N-[(IR*,2S*)-2-amino-4-hidróxi-4-metil-ciclohexil]-5-cloro-indol-2-carboxamida (Estereosiômero A) e N[(IR*,2S*)-2-amino-5-hidróxi-5-metil-ciclo-hexil]-5-cloroindol-2-carboxamida (Estereosiômero A)
O composto do título foi obtido a partir do composto (Estereoisômero A) obtido no Exemplo Referencial
127 e do ácido 5-cloro-indol-2-carboxílico, de uma maneira de 08/10/2018, pág. 315/857
307 similar àquela do Exemplo Referencial 59.
RNIN-iH (CDCI3) δ: l,32(3H,s), 1,34-2, 29 (6H, m) , 4,42-4,70 (4H,br), 7,13(2H,s), 7,50(2H,s), 8,00(lH,s), ll,0(lH,br).
Exemplo Referencial 129 (lR*,2R*,5S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5(hidróxi-metil)-ciclo-hexil-carbamato de t-butila:
1) (IR*,3S*,4S*)-3-[(t-butóxi-carbonil)-amino]-4{[ (5-cloro- indol -2- il) -carbonil] -amino} -ciclo- hexanocarboxilato de etila foi obtido a partir da forma 10 (IR*,3S*,4S*) obtida no Exemplo Referencial 89, de uma maneira similar àquela descrita nos Exemplos Referenciais 90 e 91.
ΗΜΝ-^ (CDC13) δ: 1,22-1,72 (6H, m) , 2, 15-2, 28 (2H, m) , 2,41-2,49 (lH,m), 2,85 (lH,brs), 3, 62-3, 75 (lH,m), 5 3, 78-3, 92 (lH,m), 4,12-4,28(2H,m), 4,56-4,63(1H,m), 6,88(1H,brs),
7,20(lH,dd, J=8, 8 e 2,0Hz), 7,33 (1H, d, J=8, 8Hz) , 7,527,57(lH,m), 7,59 (1H, d, J=2, OHz) , 9,24 (lH,s).
M3 (ESI) m/z: 464 (M+H)+.
2) O produto descrito acima (735 mg) foi
Petição 870180138821, de 08/10/2018, pág. 316/857
308 dissolvido em cloreto de metileno (10 ml), adicionou-se uma solução 1 N de hidreto de diisobutil-alumínio em hexano (5 ml) a -78 oC, e a mistura foi agitada por 3 h e depois por 30 min a 0 oC. Adicionou-se uma solução aquosa de cloreto de amônio a -78 oC, a mistura foi extraída com cloreto de metileno, e a camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 19:1), para obter o composto do título (480 mg) .
ΗΜΝ-^ (CDC13) δ: 1,20-2,30 (7H, m) , 3, 60-3,86 (4H, m) , 4,64(1H, br,s), 6,87(lH,s), 7,20—7,48 (3H, m) , 9, 15 (1H, br, s) .
MS (ESI) m/z: 422(M+H)+.
Exemplo Referencial 130 (lR*,3R*,6S*)-3-(metóxi-metil)-oxabiciclo[4.1.0]-heptano:
y0Me
1) (IR*,4R*,5R*)-4-iodo-6-oxabiciclo[3.2.1]-octan7-ona (2,8 g) foi dissolvida em um solvente misto de tetraidrofurano (27 ml) e água (3 ml), adicionou-se ácido de 08/10/2018, pág. 317/857
309 clorídrico concentrado (0,1 ml), e a mistura foi aquecida sob refluxo por 1 h. O solvente foi removido por destilação sob pressão reduzida, para obter o ácido (IR*,4R*,5R*)-3hidróxi-4-iodo-ciclo-hexano-carboxílico (3,23 g) , como um sólido incolor.
2) O produto (3,22 g) obtido pela reação descrita acima foi dissolvido em tetraidrofurano (50 ml), adicionou-se complexo de sulfeto de dimetila e borano (solução 2 M em tetraidrofurano, 47 ml) sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente por 12 h. O solvente foi removido por destilação sob pressão reduzida, o resíduo foi dissolvido em isopropanol (10 ml) , adicionou-se uma solução aquosa 1 N (12 ml) de hidróxido de sódio, e a mistura foi agitada por 12 h. Depois de concentrar o solvente até 1/5 do volume, a mistura da reação foi diluída com água e cloreto de metileno, agitando-a por 10 min. Uma camada orgânica foi separada e lavada sucessivamente com uma solução aquosa saturada de cloreto de amônio e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:2), para obter o (lR*,3R*,6S*)-7oxabiciclo[4.1.0]-hept-3-il-metanol (1,25 g) , como um óleo incolor.
3) O produto (4,63 g) obtido pela reação em (2) foi dissolvido em tetraidrofurano (50 ml) , e depois de 08/10/2018, pág. 318/857
310 adicionou-se bis-(timetil-silil)-amida potássica (solução 0,5 N em tolueno, 80 ml), à solução a 78 °C após agitação a mesma temperatura por 10 minutos, e iodeto de metila (2, 93 ml). Depois de aquecer a mistura até 0 oC, ela foi agitada por 1 h, interrompida rapidamente com uma solução aquosa saturada de cloreto de amônio, e depois diluída com dietiléter. Uma camada orgânica foi separada, lavada com solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (3,7 g). ΗΜΝ-^ (CDC13) δ: 0, 89-1, 63 (5H, m) , 1, 80-2,05 (2H, m) , 1,89-3,06 (4H,m) , 3,16 (3H, s) .
Exemplo Referencial 131 (lR*,2R*,4S*)-2-azido-4-(metóxi-metii)-ciclo-hexanol:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 130, de uma maneira similar àquela do Exemplo Referencial 87.
RMN-!H (CDC13) δ: 1,45-1,70 (5H, m) , 1,77-1, 95 (2H, m) , 1,98-2,08 (lH,m), 3, 30 (2H, d, J=6, 8Hz) , 3,35(3H,s), 3, 45-3, 65 (2H, m) .
Petição 870180138821, de 08/10/2018, pág. 319/857
311
Exemplo Referencial 132 (IR*,2R*,5S*)-2-hidróxi-5-(metóxi-metii)-ciclo-hexilcarbamato de t-butila:
composto do título foi obtido a partir do 5 composto obtido no Exemplo Referencial 131, de uma maneira similar àquela do Exemplo Referencial 88.
ΚΜΝ^Η (CDC13) δ: 1, 35-2,01 (16H, m) , 3, 05 (1H, br, s) , 3,32(2H,d, J=7,lHz), 3,34(3H,s), 3,44-3,62(2H,m), 4,59 (1H, br, s) .
Exemplo Referencial 133 (IR*,2S*,5S*)-2-azido-5-(metóxi-metii)-ciclo-hexil-carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 132 através do metsulfonato do mesmo, de uma maneira similar àquela do Exemplo
Petição 870180138821, de 08/10/2018, pág. 320/857
312
Referencial 89.
RMN-iH (CDCI3) δ: 1,31-1, 93 (16H, m) , 3,27(2Η,d,J=6,4Hz), 3,32 (3H,s), 3,57-3,70(lH,m), 3,67(1H,br,s), 3,95(1H,br,s).
Exemplo Referencial 134 (IR*,2S*,5S*)-2-amino-5-(metóxi-metil)-ciclo-hexil-carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 133, de uma maneira similar àquela do Exemplo Referencial 90.
Exemplo Referencial 135 (lR*,2S*,5S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5(metóxi-metil)-ciclo-hexil-carbamato de t-butila:
BocHN
Petição 870180138821, de 08/10/2018, pág. 321/857
313 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 134 e ácido 5-cloroindol-2-carboxílico, de uma maneira similar àquela do Exemplo Referencial 91.
ΕΜΝ-^ (CDC13) δ: 1, 12-2,31 (16H, m) , 3, 14-3,30 (2H, m) , 3,34 (3H,s), 3, 92 (1H, br, s) , 4, 13 (1H, br, s) , 4,88 (1H, br, s) , 6,82 (lH,s), 7,21 (lH,br.d,J=8, 8Hz) , 7,33 (1H,d,J=8,8Hz) , 7,6O(1H,
s) , 8,09(IH,br,s), 9, 42(2H,br,s) .
MS (ESI) m/z: 436(M+H)+.
Exemplo Referencial 136 (lR*,2S*,5S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5(hidróxi-metil)-ciclo-hexil-carbamato de t-butila:
BocHN
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 91, de uma maneira similar àquela do Exemplo Referencial 129.
ΗΜΝ-^ (CDC13) δ: 0, 78-2,30 (16H, m) , 3, 41-3,59 (3H, m) , 3,863,95 (lH,m), 4,12-4,20(1H,m), 4,82-4,91(1H,m), 6,81(lH,s),
7,17-7,40 (2H,m) , 7,60(lH,s), 8, 03 (1H, br, s) , 9,18 (lH,br,s). MS (ESI) m/z: 422(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 322/857
314
Exemplo Referencial 137 (IR*,2S*,5S*)-5-(azido-metil)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-(hidróxi-metil)-ciclo-hexil-carbamato de t-butila:
0 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 136, de uma maneira similar àquela do Exemplo Referencial 80.
Exemplo Referencial 138
3-ciclo-hexen-l-il-carbamato de t-butila:
NHBoc
A?
O ácido 3-ciclo-hexeno-l-carboxílico (25,3 g) foi dissolvido em t-butanol (250 ml), adicionou-se trietil-amina (28 ml) e difenil-fosforil-azida (43,0 ml), e a mistura foi agitada por 1 h à temperatura ambiente, e por 2 dias a 90 oC. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de
Petição 870180138821, de 08/10/2018, pág. 323/857
315 coluna em sílica-gel (cloreto de metileno), e depois purificado novamente por cromatografia de coluna em sílicagel (hexano:acetato de etila 20:1), para obter o composto do título (24,9 g) .
EMN-^ (CDC13) δ: l,45(9H,s), 1, 45-1, 60 (1H, m) , 1, 80-1, 90 (2H, m), 2,05-2,20(2H,m), 2,35-2,45(1H,m), 5,65-5,75(1H,m).
Exemplo Referencial 139 (3R*,4S*)-3,4-diidróxi-ciclo-hexil-carbamato de t-butila:
NHBoc
O composto obtido no Exemplo Referencial 138 (1,24
g) foi dissolvido em um solvente misto de acetonitrila (15 ml) e água (5 ml), adicionou-se N-óxido de N-metil-morfolina (0,90 g) e tetróxido de ósmio a 10% microencapsulado (1 g),
|
e a |
mistura |
foi agitada a cerca de 80 oC por 1 |
dia. Depois |
|
de |
remover |
os insolúveis por filtração, o |
filtrado foi |
|
15 concentrado |
sob pressão reduzida. 0 resíduo |
assim obtido |
|
foi |
purificado por cromatografia de coluna em sílica-gel |
(cloreto de metileno:metanol 20:1), para obter o composto do título (1,28 g).
RMN-1!! (CDC13) δ: 1, 15-1,30 (1/2H, m) , 1,35-2,00 (15H, m) , 2,1520 2,30(3/2H,m), 2, 40-2, 60(1H,m), 3,64(lH,br), 3, 75-3, 90(3/2H,
m) , 4,00 (l/2H,br) .
Petição 870180138821, de 08/10/2018, pág. 324/857
316
MS (FAB) m/z: 232(M+H)+.
Exemplo Referencial 140 (3R*,4S*)-3,4-diazido-ciclo-hexil-carbamato de t-butila (Estereoisômero A e Estereoisômero B):
NHBoc
Os compostos do título (Estereoisômero A e Estereoisômero B) foram obtidos a partir do composto obtido no Exemplo Referencial 139, de uma maneira similar àquela do
Exemplo Referencial 80.
Estereoisômero A:
RMN-XH (CDC13) δ: l,45(9H,s), 1,40-1,55 (1H, m) , (3H,m), 1, 95-2, 15 (2H,m) , 3,53(lH,m), 3,59(lH,br)
m), 4,70(1H,br).
Estereoisômero B:
1,55-1,80
3,80(1H,
RMN-XH (CDCI3)
1,80-2,00 (2H,m)
3,77 (lH,br), 3, δ: l,27(lH,m), l,44(9H,s), 1,4 , 2,00-2,15(lH,m), 2,21(lH,m), (lH,br) , 4,34 (lH,br) .
0-1
55(1H,m), (lH,m) ,
Exemplo Referencial 141 (IS,3R,4S)-4-{[(benzilóxi)-carbonil]-amino)-3-[(t-butóxicarbonil) -amino] -ciclo-hexano-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 325/857
317
COOEt
BocHN
O composto obtido no Exemplo Referencial 96 (3,10
g) foi dissolvido em tetraidrofurano (50 ml), e adicionou-se uma solução aquosa saturada (50 ml) de bicarbonato de sódio. Depois de adicionar cloreto de benzilóxi-carbonila (1,71 ml) em gotas Pa mistura da reação sob resfriamento com gelo, a mistura foi agitada à temperatura ambiente por 4 dias. Adicionou-se acetato de etila (200 ml) e água (200 ml) à mistura da reação, para conduzir separação de líquidos. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. Os sólidos depositados foram coletados por filtração, para obter o composto do título (3,24 g) . ΡΜΝ-!Η (CDC13) δ: 1,24(3H,t,J=7,1Hz), 1,29-1,44(1H,m), 1,44 (9H,s), l,44(9H,s), 1,51-1,64(1H,m), 1,72-2,10(4H,m), 2,2715 2, 43(lH,m), 3, 60-3, 73 (1H, m) , 4,00-4, 18 (3H, m) , 4,62(1H, br,s), 5,01—5,13(2H,m), 5,26(1H,br,s), 7,27—7,38(5H,m).
Exemplo Referencial 142 ácido (IS,3R,4S)-4-{[(benzilóxi)-carbonil]-amino}-3-[ (t— butóxi-carbonil)-amino]-ciclo-hexano-carboxílico:
Petição 870180138821, de 08/10/2018, pág. 326/857
318
COOH
BocHN
O composto obtido no Exemplo Referencial 141 (620 mg) foi dissolvido em tetraidrofurano (20 ml), e adicionouse uma solução aquosa (10 ml) de hidróxido de lítio monoidratado (93 mg), agitando a mistura à temperatura ambiente por 16 h. Depois de adicionar mais hidróxido de lítio monoidratado (217 mg) à mistura da reação, e agitar a mistura à temperatura ambiente por 2 h, a mistura da reação foi neutralizada com ácido clorídrico 1 N e extraída com cloreto de metileno. Uma camada orgânica foi lavada com 10 solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (600 mg).
RMN-1!! (CDC13) δ: 1, 22-2,20 (6H, m) , l,44(9H,s), 2, 45 (1H, br, s) , 15 3, 60-3, 80(1H,br), 4,09 (1H,br,s), 4,66 (1H,br,s), 5,00-5,20 (2H,m), 5, 26 (1H, br, s) , 7,20—7,40 (5H, m) .
MS (ESI) m/z: 393(M+H)+.
Exemplo Referencial 143 (IS,2R,4S)-2-[(t-butóxi-carbonil)-amino]-4-[(dimetil-amino)20 carbonil]-ciclo-hexil-carbamato de benzila:
Petição 870180138821, de 08/10/2018, pág. 327/857
319
BocHN
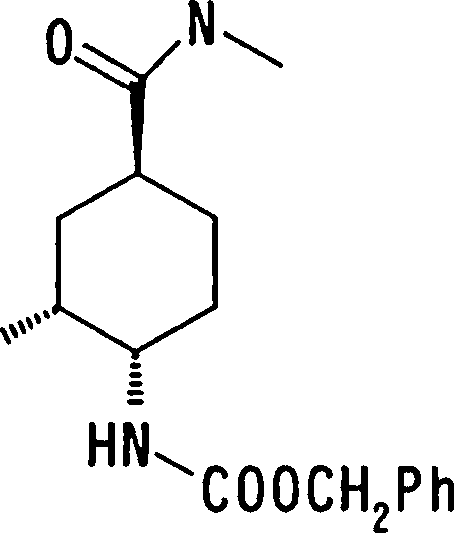
Depois de colocar em suspensão o composto obtido no Exemplo Referencial 142 (600 mg) e cloridrato de dimetilamina (240 mg) em cloreto de metileno (50 ml) , uma quantidade apropriada de tetraidrofurano foi adicionada à suspensão, para preparar uma solução. A esta solução adicionou-se trietil-amina (0,41 ml), cloridrato de l—(3— dimetil-amino-propil)-3-etil-carbodiimida (422 mg) e 1hidróxi-benzotriazol monoidratado (338 mg) , agitando a mistura à temperatura ambiente por 1 h. Adicionou-se mais cloridrato de dimetil-amina (480 mg) e trietil-amina (0,82 ml) à mistura da reação, agitando a mistura à temperatura ambiente por mais 18 h. A mistura da reação foi vertida sobre água para separar uma camada orgânica. Depois disso, a camada orgânica foi lavada com ácido clorídrico 1 N e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 3:47 —> 2:23), para obter o composto do título (620 mg).
de 08/10/2018, pág. 328/857
320
EMN-iH (CDCI3) δ: 1,20-1,50(2H,m), l,44(9H,s), 1,50-2, 10 (4Η,
m) , 2, 60 (lH,br,t, J=ll, 6Ηζ) , 2,93(3H,s), 3,02(3H,s), 3,70(1Η, br,s), 4, 14(1H, br, s) , 4,65(1H,br,s), 5, 00—5,30(3H,m), 7,26—
7,40(5H,m).
MS (ESI) m/z = 420 (M+H)+.
Exemplo Referencial 144 (IR,2S,5S)-2-amino-5-[(dimetil-amino)-carbonil]-ciclo-hexilcarbamato de t-butila:
0.
BocHN
Adicionou-se 10% de paládio sobre carvão (57 g) a uma solução do composto obtido no Exemplo Referencial 143 (190 g) em metanol (8.000 ml), e a mistura foi agitada por 3 h sob uma pressão de hidrogênio (7 atm) . Depois de remover o catalisador por filtração, o filtrado foi concentrado sob pressão reduzida. Depois de adicionar tolueno ao resíduo e concentrar a mistura sob pressão reduzida, adicionou-se hexano (2.500 ml), para solidificar um produto. O produto foi coletado por filtração e secado, para obter o composto do título (121 g) .
EMN-iH (CDC13) δ: 1,20-1,77 (6H, m) , l,45(9H,s), 2,20- 2,35 (1H,
Petição 870180138821, de 08/10/2018, pág. 329/857
321 br), 2, 63-2, 74 (lH,m) , 2,92(3H,s), 3,02(3H,s), 3, 02-3, 11 (2H,
m), 3,74-3,82(lH,m), 4,88-5,00(1H,br).
MS (ESI) m/z: 286(M+H)+.
Exemplo Referencial 145 (lR,2S,5S)-2-{[(6-cloro-quinolin-2-il)-carbonil]-amino}ciclo-hexil-carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e do composto obtido no Exemplo Referencial 54, de uma maneira similar àquela do Exemplo Referencial 91.
RMN-!H (CDC13) δ: l,41(9H,br), 1, 50-1,70 (1H, m) , 1,75-1,95 (2H,m), 1,95-2,25(3H,m), 2, 65-2,80 (1H, m) , 2,96(3H,s), 3,07 (3H,s), 4, 15-4, 30 (lH,m) , 4,30-4,4 0 (1H, m) , 4,95(lH,br), 7,66 (1H, d, J=8,8Hz) , 7,84(lH,s), 8, 00 (1H, d, J=8, 8Hz) , 8,19(lH,d,J=
8,6Hz), 8,30(1H,d,J=8,6Hz).
MS (FAB) m/z: 475(M+H)+.
Exemplo Referencial 146 (lR,2S,5S)-2-{[(7-cloro-quinolin-3-il)-carbonil]-amino}-5[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 330/857
322
Cl composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e do composto obtido no Exemplo Referencial 57, de uma maneira similar àquela do Exemplo Referencial 91.
RMN-1!! (CDC13) δ: 1, 30-1, 65 (10H, br) , 1,75-1,90 (2H, m) , 1,902,25(3H,m), 2, 65-2, 90 (1H, br) , 2,96 (3H,s), 3,08(3H,s), 4,204,30(lH,m), 4,30-4,40 (lH,m) , 4,93(lH,br), 7,68(lH,m), 7,90 (lH,br), 7,99(lH,s), 8, 35-8, 70 (2H, m) , 9,01(lH,br).
MS (FAB) m/z: 475(M+H)+.
Exemplo Referencial 147
2-bromo-5-isopropil-4,5,6,7-tetraidrotiazolo[5,4-c]piridina:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 8, de uma maneira similar àquela do Exemplo Referencial 9.
Petição 870180138821, de 08/10/2018, pág. 331/857
323
RMN-iH (CDC13) δ: 1,13(6Η,d,J=6,5Ηζ), 2,86(4H,s), 2,89-3,00 (lH,m), 3,70(2Η,s).
Exemplo Referencial 148
5-isopropil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-25 carboxilato de lítio:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 147, de uma maneira similar àquela do Exemplo Referencial 10.
RMN-1!! (DMSO-de) δ: 1, 05 (6H, d, J=6, 4Hz) , 2,68-2,70(2H,m),
2,75—2,77 (2H, m) , 2,87-2, 93 (1H, m) , 3,66(2H,s).
Exemplo Referencial 149
5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxilato de 4-nitro-fenila:
O composto do título foi obtido a partir do 15 composto obtido no Exemplo Referencial 10 e p-nitro-fenol, de uma maneira similar àquela do Exemplo Referencial 52.
Petição 870180138821, de 08/10/2018, pág. 332/857
324
RMN-iH (CDC13) δ: 2,55(3H,s), 2, 88 (2H, t, J=5,7Hz) , 3,06- 3,12 (2H,m), 3,80(2H,s), 7,46 (2H, d, J=9, 3Hz) , 8,32 (2H, d, J=9, 3Hz) . MS (ESI) m/z: 320 (M+H+) .
Exemplo Referencial 150
3-oxo-ciclo-butano-carboxilato de benzila:
0=y>— C02CH2Ph
Adicionou-se trietil-amina (2,0 ml) e brometo de benzila (1,2 ml) a uma solução do ácido 3-oxo-ciclo-butanocarboxílico (J. Org. Chem. 53:3841-3843, 1981) (995 mg) em tetraidrofurano (5,0 ml), e a mistura foi agitada à temperatura ambiente por 2 h. A mistura da reação foi diluída com acetato de etila, e o lavada sucessivamente com ácido clorídrico 1 N, uma solução aquosa saturada de bicarbonato de sódio e solução salina saturada, e secada sobre sulfato de sódio anidro. O solvente foi então removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:6), para obter o composto do título (886 mg).
ΗΜΝ-^ (CDC13) δ: 3, 22-3, 33 (3H, m) , 3, 37-3, 48 (2H, m) , 5,19(2H,
s), 7,31-7,42(5H,m).
MS (FAB) m/z: 205 (M+H+) .
Exemplo Referencial 151
3-hidróxi-ciclo-butano-carboxilato de benzila:
de 08/10/2018, pág. 333/857
325
HO—<Q>—CO2CH2Ph
Adicionou-se boro-hidreto de sódio (76 mg) a uma solução do composto obtido no Exemplo Referencial 150 (781 mg) em um solvente misto de tetraidrofurano (10 ml) e metanol (0,5 ml) a 0 oC, e a mistura foi agitada à mesma temperatura ambiente por 30 min. A mistura da reação foi diluída com acetato de etila, e o extrato foi lavado com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, nesta ordem, e secada sobre sulfato de sódio anidro. O solvente foi então removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:2), para obter o composto do título (770 mg).
ΗΜΝ-Ή (CDC13) δ: 2,13-2,27 (3H, m) , 2, 55-2,71 (3H, m) , 4,1415 4,23 (11-1,m) , 5,12(2H,s), 7,28-7,39 (5H, m) .
MS (FAB) m/z: 207 (Μ+Ή) .
Exemplo Referencial 152 ácido 3-hidróxi-ciclo-butano-carboxílico:
HO-<^>- CO2H
Adicionou-se 10% de paládio sobre carvão (108 mg) a uma solução do composto obtido no Exemplo Referencial 151 (706 mg) em etanol (10 ml), e a mistura foi agitada à
Petição 870180138821, de 08/10/2018, pág. 334/857
326 temperatura ambiente por 2 h em uma atmosfera de hidrogênio.
Depois de remover o catalisador por filtração através de
Celite, o filtrado foi concentrado sob pressão reduzida, para obter o composto do título (399 mg).
RMN-1!! (CD3OD) δ: 2,00-2,21 (2H, m) , 2, 41-2, 61 (3H, m) , 4,014,13(lH,m).
Exemplo Referencial 153
3-metóxi-ciclo-butano-carboxilato de benzila:
MeO—<^>- C02CH2Ph
Adicionou-se iodeto de metila (194 μΐ) e óxido de prata (237 mg) a uma solução do composto obtido no Exemplo Referencial 151 (317 mg) em N, N-dimet il-f ormamida (3,0 ml), e a mistura foi agitada a 45 oC por 1 h. Adicionou-se mais iodeto de metila (194 μη e óxido de prata (226 mg) à mistura da reação, e a mistura foi agitada a 45 oC por 16 h.
Depois de remover o catalisador por filtração, o filtrado foi concentrado sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:10), para obter o composto do título (152 mg).
ΗΜΝ-^ (CDC13) δ: 2,14-2,24 (2H, m) , 2, 44-2,54 (2Η, m) , 2,592,72(lH,m), 3,21(3H,s), 3, 73-3, 81 (1H, m) , 5,ll(2H,s), 7,227,39 (5H,m) .
MS (ESI) m/z: 221 (M+H+) .
Petição 870180138821, de 08/10/2018, pág. 335/857
327
Exemplo Referencial 154 ácido 3-metóxi-ciclo-butano-carboxílico:
MeO^C^CO2H composto do título foi obtido a partir do composto obtido no Exemplo Referencial 153, de uma maneira similar àquela do Exemplo Referencial 152.
RMN-1H (CDC13) δ: 2,17-2,27 (2H,m) , 2,48-2,58 (2H, m) , 2,622,73(lH,m), 3,25(3H,s), 3, 76-3, 86 (1H, m) , 8, 60-9, 30 (1H, br) .
Exemplo Referencial 155
3-metóxi-2-(metóxi-metil)-propionato de metila:
MeO2C
OMe
OMe
Adicionou-se metóxido de sódio (1,21 g) a uma solução de 2-(bromo-metil)-acrilato de metila (1,0 ml) em metanol (10 ml), e a mistura foi aquecida sob refluxo por 26 h. Depois de resfriar, a mistura da reação foi diluída com dietil-éter, e o precipitado foi coletado por filtração e o filtrado concentrado sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (726 mg).
RMN-1!! (CDCI3) δ: 2, 90-2, 9 6 (1H, m) , 3,34(6H,s), 3,57(2H,dd,
Petição 870180138821, de 08/10/2018, pág. 336/857
328
J=9,3, 5,9Hz), 3, 64(2H,dd,J=9,3, 6, 6Hz) , 3,73(3H,s).
RMN-13C (CDC13) δ: 172,71, 70,31, 59, 91, 46, 49.
MS (ESI) m/z: 163(M+H+).
Exemplo Referencial 156 ácido tetraidro-2H-pirano-4-carboxílico:
Adicionou-se tetraidro-4H-pirano-4,4-dicarboxilato de dimetila (4,04 g) a ácido clorídrico a 20% (20 ml), e a mistura foi aquecida sob refluxo por 19 h. Adicionou-se água à mistura da reação para conduzir extração com dietil10 éter. Depois de lavar a camada orgânica resultante com solução aquosa saturada de cloreto de sódio e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. Depois disso, o resíduo resultante foi solidificado com hexano, os sólidos resultantes foram coletados por filtração e lavados, para obter o composto do título (2,63 g).
RMN-1H (CDCI3) δ: 1,75-1, 95 (4H,m) , 2, 55-2, 65 (1H, m) , 3,403,52(2H,m), 3, 93-4,05 (2H, m) .
Exemplo Referencial 157
3-{[t-butil-(difenil)-silil]oxi}-2,2-dimetil-propionato de
Petição 870180138821, de 08/10/2018, pág. 337/857
329
O composto do título foi obtido a partir de 2,2dimetil-3-hidróxi-propionato de metila, de uma maneira similar àquela do Exemplo Referencial 41.
ΗΜΝ-^ (CDC13) δ: l,03(9H,s), l,20(6H,s), 3, 64-3, 68 (5H, m) ,
7,38-7,44(6H,m), 7,63-7,65(4H,m).
Exemplo Referencial 158 ácido 3-{[t-butii-(difenil)-silil]oxi}-2,2-dimetilpropiônico:
ho2c
OTBDPS
Adicionou-se água (0,24 ml) a uma suspensão composta de t-butóxido de potássio (5,32 g) em dietil-éter (100 ml) sob resfriamento com gelo, e a mistura foi agitada por 5 min. O composto obtido no Exemplo Referencial 157 (2,22 g) foi adicionado a essa suspensão, e a mistura resultante foi agitada por toda a noite à temperatura ambiente. Adicionou-se água à mistura da reação, e a mistura foi acidificada com ácido clorídrico 1 N e extraída vezes com dietil-éter. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:6), para obter o composto do título (735 mg).
RMN-!H (CDC13) δ: 1,04 (9H, d, J=0, 7Hz) , l,22(6H,s), 3,65(2H,s),
7,36-7,45(6H,m), 7,64-7,66(4H,m).
de 08/10/2018, pág. 338/857
330
Exemplo Referencial 159 3-metóxi-2,2-dimetil-propionato de metila:
MeO2C
OMe
Uma solução de 3-hidróxi-2,2-dimetil-propionato de metila (25,0 g) em tetraidrofurano (300 ml) foi adicionada em gotas a uma suspensão composto de uma suspensão de hidreto de sódio (8,32 g) em óleo a 60% e tetraidrofurano (100 ml) sob resfriamento com gelo, e a mistura foi agitada a 60 °C por 1 h. Adicionou-se iodeto de metila (53,7 g) à mistura da reação, e a mistura resultante foi agitada a temperatura ambiente por 2 h. Adicionou-se água cuidadosamente para conduzir extração duas vezes com cloreto de metileno. Depois de lavar a camada orgânica resultante com solução aquosa saturada de cloreto de sódio e depois secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o óleo resultante foi destilado, para obter o composto do título (12,8 g). Ponto de ebulição: 140-142 °C (pressão normal).
RMN-1H (CDC13) δ: 1, 19(6H,d,J=l,OHz), 3, 33(3]-1,d,J=l,OHz),
3,38(2H,d,J=l,OHz), 3,69(3H,d,J=l,OHz).
Exemplo Referencial 160 ácido 3-metóxi-2,2-dimetil-propiônico:
de 08/10/2018, pág. 339/857
331
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 159, de uma maneira similar àquela do Exemplo Referencial 158.
ΗΜΝ-^ (CDC13) δ: 1,22 (6H, d, J=0,7Hz) , 3, 38 (3H, d, J=0,7Hz) ,
3,40(2H,d,J=0,7Hz).
Exemplo Referencial 161 ácido 1-(metóxi-carbonil)-ciclo-propano-carboxílico:
MeO2C CO2H
Dissolveu-se 1, 1-ciclo-propano-carboxilato de dimetila (25 g) em metanol (250 ml), e a solução foi resfriada com gelo. Depois, adicionou-se uma solução aquosa 1 N de hidróxido de sódio (158 ml) em gotas, e a mistura resultante foi aquecida até a temperatura ambiente e agitada por toda a noite. Depois de remover o metanol por destilação, o resíduo foi lavado com clorofórmio, e uma camada aquosa foi resfriada com gelo, teve seu pH ajustado para pH 2 com ácido clorídrico concentrado e foi extraída com acetato de etila. O extrato foi secado sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (16,8 g). ΗΜΝ-!Η (CDC13) δ: 1,76-1,80 (2H, m) , 1, 82-1, 88 (2H, m) , 3,79(3H,
s) , 12,73 (lH,br) .
Exemplo Referencial 162
1-(hidróxi-metil)-ciclo-propano-carboxilato de metila:
de 08/10/2018, pág. 340/857
332
MeOzC
OH composto obtido no Exemplo Referencial 161 (9,0
g) e trietil-amina (9,7 ml) foram dissolvidos em tetraidrofurano (180 ml) , e a solução foi resfriada até -10 oC, à qual adicionou-se cloro-formiato de isobutila (9,1 ml) em gotas, e a mistura resultante foi agitada por 1 h. Por outro lado, dissolveu-se boro-hidreto de sódio (7,1 g) em tetraidrofurano (100 ml)/água (25 ml) e resfriou-se com gelo. Enquanto se removia os insolúveis por filtração, a solução preparada anteriormente foi adicionada em gotas, e a mistura resultante foi agitada na mesma temperatura por 1 h. A mistura da reação foi vertida sobre uma solução aquosa a 10% de ácido cítrico, para conduzir extração com acetato de etila. Depois de lavar o extrato com solução aquosa saturada de cloreto de sódio e depois secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:9 —» 2:1), para obter o composto do título (4,25 g) .
EMN-iH (CDC13) δ: 0, 87-0, 93(2H,m), 1, 28-1,30(2H,m), 3,63(2H,
s) , 3, 70(3H,s) .
Exemplo Referencial 163
1-(bromo-metii)-ciclo-propano-carboxilato de metila:
de 08/10/2018, pág. 341/857
333
MeO2C
Br
Adicionou-se trifenilfosfina (10 g) e tetrabrometo de carbono (16 g) a uma solução do composto obtido no Exemplo Referencial 162 (4,20 g) em cloreto de metileno (168 ml) à temperatura ambiente sob uma atmosfera de nitrogênio.
Depois de 2 min, uma solução aquosa saturada de bicarbonato de sódio foi adicionada à mistura anterior. Depois de lavar a camada orgânica resultante com solução aquosa saturada de cloreto de sódio e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida.
O residuo resultante foi purificado por cromatografia de coluna em silica-gel (acetato de etila:hexano 1:19), para obter o composto do título (2,15 g).
ΗΜΝ-^ (CDC13) δ: 1,00-1,05 (2H, m) , 1, 52-1,59 (2Η, m) , 3, 61 (2Η,
s) , 3, 73(3Η,s) .
Exemplo Referencial 164 (4S)-4-[ (E)-3-etóxi-3-oxo-l-propenil]-2,2-dimetil-l,3oxazolidino-3-carboxilato de t-butila:
Uma solução oxazolidino-3-carboxilato de (4)-4-formil-2,2-dimetil-l,3de t-butila (11,7 g), (carboetóxiPclição 870180138821, de 08/10/2018, pág. 342/857
334 metileno)-trifenilfosforano (20,7 g) e tolueno (100 ml), foi aquecida e agitada a 100 °C por 18 h. A mistura da reação foi concentrada e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 8:1), para obter o composto do título (17 g).
βΜΝ-^ (CDC13) δ: 1,29(3H,t,J=6,6Hz), 1, 43-1,56 (15H, m) , 3,80 (1H, dd,J=9,0,2,4Hz), 4, 09(1H,dd,J=9,0,6,6Hz), 4,11-4,23(2H,
m) , 4,30-4, 61 (lH,m) , 5, 83-6, 02 (1H, m) , 6, 74-6, 89 (lH,m). Exemplo Referencial 165 (4 S)-4-[1-(benzil-amino)-3-etóxi-3-oxopropil]-2,2-dimetil1,3-oxazolidino-3-carboxilato de t-butila:
Uma solução do composto obtido no Exemplo Referencial 164 (22, 2 g) , benzil-amina (16 g) e etanol (100 ml), foi aquecida sob refluxo por 2 dias. A mistura da reação foi concentrada, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 8:1), para obter o composto do título (26 g).
ΚΜΝ-^ (CDC13) δ: 1,25 (3H, t, J=6, 6Hz) , 1,42-1, 63 (15H, m) , 2,2420 2,33 (0,5H,m), 2, 4 0-2,50(1H,m), 2, 63-2, 74(0,5H, m) , 3,41-3,52 (lH,m), 3, 67-3, 80 (lH,m) , 3,83(2H,s), 3, 89-4,00 (1H, m) , 4,034,22(4H,m), 7,23-7,45 (5H, m) .
Petição 870180138821, de 08/10/2018, pág. 343/857
335
Exemplo Referencial 166 (4S)-4-(l-amino-3-etóxi-3-oxopropil)-2,2-dimetil-l,3oxazolidino-3-carboxilato de t-butila:
CO2Et
Adicionou-se 10% de paládio sobre carvão (10 g) a 5 uma solução do composto obtido no Exemplo Referencial 165 (13,6 g) em etanol (200 ml), e a mistura foi agitada por 2 dias sob uma atmosfera de hidrogênio. Os insolúveis foram removidos através de um leito de Celite, e o filtrado foi concentrado sob pressão reduzida, para obter o composto do título (10,5 g) .
EMN-iH (DMSO-de) δ: 1, 19(1,5H,t,J=6,6Hz), l,20(l,5H,t,
J=6,6Hz), 1, 32-1, 50 (15H,m), 2, 63-2,81(2H,m), 3, 22-3, 34(2H,
m) , 3,93(1H,dd,J=10,0,6,8Hz), 4,08(2H,q,J=6,6Hz), 4,20-4,30 (lH,m) .
Exemplo Referencial 167 (4S)—4—(1—{[(benzilóxi)-carbonil]-amino}-3-etóxi-3oxopropil)-2,2-dimetil-l,3-oxazolidino-3-carboxilato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 344/857
336 ^—NBoc
CO2E t
NHZ composto obtido no Exemplo Referencial 166 (3,0
g) foi colocado em suspensão aquosa a 9% (56 ml) de bicarbonato de sódio, e adicionou-se uma solução de N(benzilóxi-carbonilóxi)-succinimida (2,3 g) em dioxano (12 ml) em gotas à suspensão sob resfriamento com gelo. A mistura resultante foi agitada por 3 h enquanto a temperatura do sistema era elevada gradualmente até a temperatura ambiente. A mistura da reação foi diluída com acetato de etila e lavada com água, uma solução aquosa a 10% de ácido cítrico e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. O solvente foi então removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio), para obter o composto do título (3,8 g).
ΗΜΝ-^ (CDC13) δ: 1,23 (3H, t, J=6, 6Hz) , l,48(9H,s), 1,56(6H
s), 2,40-2,51(2H,m), 2,63-2,70(2H,m), 3,92-4,04(1H,m), 4,06-
Exemplo Referencial 168 (3S,4S)-3-{[(benzilóxi)-carbonil]-amino}-4-[(t-butóxicarbonil) -amino] -5-hidróxi-valerato de etila (composto com baixa polaridade) e (3R,4S)-3-{[(benzilóxi)-carbonil]amino}-4-[(t-butóxi-carbonil)-amino]-5-hidróxi-valerato de 08/10/2018, pág. 345/857
337 de etila (composto com alta polaridade):
Composto de baixa polaridade
Composto de alta polaridade
|
Adicionou-se |
ácido triflúor |
-acético |
(100 |
ml) em |
|
gotas a uma solução |
do composto |
obtido |
no |
Exemplo |
|
Referencial 167 (30 g) |
em cloreto de |
metileno |
(100 |
ml) sob |
resfriamento com gelo, e a mistura foi agitada por 3 h, enquanto a temperatura do sistema era elevada gradualmente até a temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo resultante foi dissolvido em cloreto de metileno (100 ml). Adicionou-se sucessivamente trietil-amina (20 ml) e uma solução de dicarbonato de di-t-butila (19 g) em cloreto de metileno (100 ml) em gotas a essa solução sob resfriamento com gelo, e a mistura foi agitada por 4 h, enquanto a temperatura do sistema era elevada até a temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1), para obter o composto do título com baixa polaridade (7,6 g) e o composto do título com alta polaridade (10 g).
Composto de baixa polaridade:
ΚΜΝ-^ (CDC13) δ: 1,24 (3H, t, J=6, 6Hz) , l,42(9H,s), 2,63(2H, de 08/10/2018, pág. 346/857
338 d,J=4,4Hz), 3,30-3,41(lH,m), 3,50 (1H,t,J=9, 7Hz) , 3,65(lH,t,
J=9,7Hz), 3, 75(1H, d,J=ll,7Hz), 3, 90-4, 00(1H,m) , 4,03-4,23 (2H,m), 5,12(2H,s), 5, 13-5, 25 (1H, m) , 5, 79-6, 02 (1H, m) , 7,327,41 (5H,m) .
Composto de alta polaridade:
ΗΜΝ-^ (CDC13) δ: 1,22 (3H, t, J=6, 6Hz) , l,41(9H,s), 2,50-2,70 (2H,m), 3, 20-3,31(lH,m), 3,43-3,51(1H,m), 3, 56-3, 70(1H,m),
3,74-3,78(lH,m), 4,00-4,19(2H,m), 4,23-4,30(1H,m), 4,784,89(lH,m), 5,10(2H,s), 5, 56-5, 67 (1H, m) , 7,31-7,40 (5H, m) .
Exemplo Referencial 169 metano-sulfonato de (3R,4S)-4-[(metil-sulfonil)oxi]tetraidro-3-furanila
Adicionou-se sucessivamente trietil-amina (12,0 ml) e cloreto de metano-sulfonila (3,6 ml) em gotas a uma solução de 1,4-anidroeritritol (5,0 g) em cloreto de metileno (50 ml) sob resfriamento com gelo, e a mistura foi agitada por 10 min sob resfriamento com gelo. A mistura da reação foi diluída com cloreto de metileno e lavada com ácido clorídrico a 10%, uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. Depois de lavar a camada orgânica resultante e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, para obter o composto do
Petição 870180138821, de 08/10/2018, pág. 347/857
339 título (9,2 g) RMN-XH (CDC13) (2H,dd,J=ll,2, δ: 3,15(6H,s), 3,99(2H,dd,J=ll,2,2,5Hz), 4,6Hz), 5,10-5,20(2H,m).
Exemplo Referencial 170
4, 16 (3R,4S)-3,4-diazidotetraidrofurano:
Composto obtido no Exemplo Referencial 169 (9,2 g) foi dissolvido em N,N-dimetil-formamida (50 ml), adicionouse azida de sódio (18 g) , e a mistura resultante foi aquecida e agitada a 100 oC por 18 h. A mistura da reação foi diluída com acetato de etila e lavada com água e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (3,8 g).
RMN-XH (CDC13) δ: 3,83(2H,dd,J=8,6,2,OHz), 3,96-4,12(4H,m).
Exemplo Referencial 171 dicloridrato de (3R,4S)-tetraidro-3,4-furanodiamina:
h2n h2n
Petição 870180138821, de 08/10/2018, pág. 348/857
340
O composto obtido no Exemplo Referencial 170 (3,8
g) foi dissolvido em etanol (50 ml) , adicionou-se 10% de paládio sobre carvão (1,0 g) à solução, e a mistura foi agitada por 18 h sob uma atmosfera de hidrogênio. Os insolúveis foram removidos através de um leito de Celite, e o filtrado foi concentrado sob pressão reduzida. Adicionouse uma solução de ácido clorídrico 1 N em etanol ao resíduo resultante, dando o sal cloridrato. O cloridrato foi recristalizado em um solvente misto de etanol e dietil-éter, para obter o composto do título (2,0 g).
RNIN-iH (CDC13) δ: 3, 90 (2H, dd, J=9, 0, 3, 7Hz) , 4, 01-4, 13 (4H, m) ,
8,84(6H,s).
Exemplo Referencial 172
N-[(3R*,4S*)-4-amino-tetraidro-3-furanil]-5-cloro-indol-2carboxamida:
O ácido 5-cloro-indol-2-carboxílico (0,29 g) , 1hidróxi-benzotriazol monoidratado (0,2 g) e cloridrato de 1(3-dimetil-amino-propil)-3-etil-carbodiimida (0,6 g) foram adicionados sucessivamente a uma solução do composto obtido no Exemplo Referencial 171 (0,5 g) em N,N-dimetil-formamida (10 ml), e a mistura foi aquecida e agitada a 50 oC por um de 08/10/2018, pág. 349/857
341 dia. A mistura da reação foi concentrada, e o resíduo resultante foi diluído com um solvente misto de clorofórmio e Metanol (9:1) e lavado com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 95:5), para obter o composto do título (0,2 g).
RMN-1H (CDC13) δ: 1,80-1,92(1H,m), 3,62(1H,dd,J=9,3, 4,2Hz),
3, 68-3, 80(2H,m), 4, 06(1H, dd,J=9,3,5,6Hz), 4,21(1H,dd,J=9,3,
6,8Hz), 4,36-4,52 (2H,m) , 6,87(lH,s), 7,24 (1H, dd, J=8,8,
2,OHz), 7,36(1H,d,J=8,8Hz), 7,44-7,56(1H,m), 7,62(1H,d,J=2,O
Hz), 9,41 (1H,s) .
Exemplo Referencial 173 (4R)-4-[(E)-3-etóxi-3-oxo-l-propenil]-2,2-dimetil-l,3oxazolidino-3-carboxilato de t-butila:
C02Et
O composto do título foi obtido a partir de (4S)20 4-formil-2,2-dimetil-l,3-oxazolidino-3-carboxilato de tbutila, de uma maneira similar àquela do Exemplo Referencial
164 .
Petição 870180138821, de 08/10/2018, pág. 350/857
342
RMN-XH (CDC13) δ: 1,29(3Η,t,J=6,6Ηζ), 1,40-1,60(15Η,m), 3,80 (1Η,dd,J=9,0,2,4Ηζ), 4,09(1Η,dd,J=9,0,6,6Ηζ), 4,11-4,21 (2Η,
m), 4,32-4,64(lH,m), 5,78-6,01(1Η,m), 6,67-6,89(1Η,m).
Exemplo Referencial 174 (4R)-4-[1-(benzil-amino)-3-etóxi-3-oxo-l-propil]-2,2dimetil-1,3-oxazolidino-3-carboxilato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 173, de uma maneira similar àquela do Exemplo Referencial 165.
ΗΜΝ-Ή (CDC13) δ: 1,25 (3H, t, J=6, 6Hz) , 1, 40-1, 61 (15H, m) , 2,212,32 (0,5H,m), 2,40-2,51(1H,m) , 2,61-2,72(0,5H,m) , 3,43-3,50 (lH,m), 3, 67-3, 80 (lH,m) , 3,83(2H,s), 3, 90-4,03 (1H, m) , 4,044,22(4H,m), 7,20-7,40 (5H, m) .
Exemplo Referencial 175 (4R)-4-(l-{[(5-cloro-indol-2-il)-carbonil]-amino}-3-etóxi-3oxopropil)-2,2-dimetil-1,3-oxazolidino-3-carboxilato de t-
Pctição 870180138821, de 08/10/2018, pág. 351/857
343 composto do título foi obtido reduzindo o composto obtido no Exemplo Referencial 174, de uma maneira similar àquela do Exemplo Referencial 166, para remover o grupo benzila e depois condensando-o com ácido 5-cloro5 indol-2-carboxílico, de uma maneira similar àquela do Exemplo Referencial 172.
ΗΜΝ-^ (CDC13) δ: 1, 23 (1, 5H, t, J6, 6Hz) , 1,25 (1,5H, t, J=6, GHz) ,
1,50(4,5H, s), 1,54(4,5H,s), l,62(6H,s), 2,50-2,70(1,5H,m),
2,86(0,5H,dd,J=16,4,5,5Hz), 3,80-3,90(0,5H,m), 4,00-4,31 (5H,m), 4,41-4,67(0,5H,m), 6,85(0,5H,s), 6,87(0,5H,s), 7,107,20(lH,m), 7,34(0,5H,d,J=8,8Hz), 7,38(0,5H,d,J=8,8Hz), 7,57 (0,5H,s), 7,63(0,5H,s), 7, 88(0,5H,d,J=7,6Hz), 8,54(0,5H,d,J= 7,6Hz), 9, 40(0,5H,s), 9,54(0,5H,s) .
Exemplo Referencial 176 (3R,4R)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-6oxotetraidro-2H-piran-3-il-carbamato de t-butila (composto com baixa polaridade) e (3R,4S)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-6-oxotetraidro-2H-piran-3-il-carbamato de t-butila (composto com alta polaridade):
Petição 870180138821, de 08/10/2018, pág. 352/857
344
Adicionou-se uma solução aquosa 1 N (4,0 ml) de hidróxido de sódio a uma solução do composto obtido no Exemplo Referencial 175 (1,0 g) em etanol (20 ml), e a mistura foi agitada por 4 h. Adicionou-se ácido cítrico à mistura da reação, para ajustar o pH da mistura da reação para 4,0. A mistura da reação foi extraída com acetato de etila, e a camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi dissolvido em metanol (50 ml), e adicionou-se ácido toluenosulfônico monoidratado (0,1 g) à solução, agitando a mistura resultante por 18 h. A mistura da reação foi diluída com acetato de etila e lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 99:1), para obter o composto do título com baixa polaridade (0,3 g) e o composto do título com alta polaridade (0,3 g).
Composto de baixa polaridade:
RMN-!H (CDC13) δ: l,45(9H,s), 2,70 (1H, dd, J=16, 5, 4, 9Hz) , 2,85 (1H, dd,J=16,5,4,6Hz), 3, 50-3,61(1H,m), 3, 71-3,81(2H,m),
4,30-4,40 (lH,m) , 5, 30 (1H, d, J=9, 5Hz) , 6,89(lH,s), 7,23(lH,dd,
J=8,8,2,OHz), 7,38(1H,d,J=8,8Hz), 7, 62(1H,d,J=2,OHz), 7,93 (1H, d, J=9, 5Hz) , 9,30(lH,s).
de 08/10/2018, pág. 353/857
345
Composto de alta polaridade:
ΗΜΝ-^ (CDC13) δ: l,39(9H,s), 2,75(1H,dd,J=16,5,4,9Hz), 2,82 (1H, dd,J=16,5,4,6Hz), 3, 41-3,52(2H,m), 3,71-3,82 (1H,m),
3, 85-3, 94 (lH,m), 5,03(1H,d,J=9,3Hz), 6,99(lH,s), 7,22-7,31 (lH,m), 7,34(1H,d,J=8,8Hz), 7, 61(1H, d,J=2,OHz), 7,83(lH,d,
J=9,3Hz), 9,28 (1H,s) .
Exemplo Referencial 177
1,1,3-trioxo-hexaidro-l-tiopiran-4-il-carbamato de t-butila:
Uma solução do éster metílico de N-t-butóxi10 carbonil-L-metionina (60,2 g) em tetraidrofurano (900 ml) foi resfriada até -78 oC, à qual adicionou-se bis-(trimetilsilil)-amida potássica 0,5 M (solução em tolueno, 900 ml) em gotas, e a mistura foi agitada por 2 h a -78 oC e por 4,5 h à temperatura ambiente. Adicionou-se uma solução aquosa 1 M de cloreto de amônio, e a mistura foi agitada. A mistura da reação foi submetida à separação de líquidos, e a camada orgânica resultante foi então lavada com água e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e os sólidos formados foram coletados por filtração, para obter o composto do título (12,4 g) . A camada aquosa separada anteriormente foi extraída duas vezes
Petição 870180138821, de 08/10/2018, pág. 354/857
346 com acetato de etila, e as camadas orgânicas resultantes foram combinadas, lavadas com água e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. As camadas aquosas usadas na lavagem foram combinadas adicionalmente, e extraídas novamente com acetato de etila, e o extrato foi lavado com solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. Os extratos de acetato de etila foram combinados, secados e depois concentrados sob pressão reduzida, para obter o composto do título (27,7 g) (quantidade total do composto do título: 40,1 g).
ΚΜΝ-^ (CDC13) δ: l,45(9H,s), 1, 85-1, 96 (1H, m) , 2,76-2,78 (lH,m), 3, 34-3, 46 (2H,m), 4,05(1H,dd,J=13,5, 3, 7Hz) , 4,14(1H, d,J=13,5Hz), 4,38-4,44 (lH,m) , 5,46(lH,br).
MS (ESI) m/z: 262(M—H)-.
Exemplo Referencial 178 (3R*,4R*)-3-hidróxi-l,1-dioxo-hexaidro-l-tiopiran-4-ilcarbamato de t-butila:
Adicionou-se boro-hidreto de sódio (2,17 g) a uma suspensão do composto obtido no Exemplo Referencial 177 (10,1 g) em metanol (200 ml), e a mistura foi agitada à temperatura ambiente por 2 h. A mistura da reação foi
Petição 870180138821, de 08/10/2018, pág. 355/857
347 concentrada sob pressão reduzida. Depois, adicionou-se acetato de etila e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir separação de líquidos, e a camada aquosa resultante foi extraída duas vezes com acetato de etila. As camadas orgânicas resultantes foram combinadas, secadas sobre sulfato de magnésio anidro e depois concentradas sob pressão reduzida, para obter o composto do título (9,96 g).
βΜΝ-^ (CDC13) δ: l,44(9H,s), 2, 21-2, 36 (2H, m) , 3, 03-3, 17 (2H,
m), 3,26-3,28(2H,m), 3,77-3,80(2H,m), 4,26-4,28(1H,m), 5,055,07(lH,m).
MS (ESI) m/z: 264(M-H)-.
Exemplo Referencial 179 (3R*,4R*)-3-amino-l,1-dioxo-hexaidro-l-tiopiran-4-il-
|
carbamato de t-butila (composto de baixa polaridade) e |
|
(3R*,4S*) - |
-3-amino-l,1-dioxo-hexaidro-l-tiopiran-4-il- |
|
carbamato |
de t-butila (composto de alta polaridade): |
Composto de baixa polaridade (modificação racêmica)
Composto de alta polaridade (modificação racêmica)
Adicionou-se azodicarboxilato de dietila (6,96 g) a uma solução do composto obtido no Exemplo Referencial 178 (9,66 g) e trifenilfosfina (10,5 g) em tetraidrofurano (150 de 08/10/2018, pág. 356/857
348 ml), e a mistura foi agitada à temperatura ambiente por 4,5 h. Depois de concentrar a mistura da reação sob pressão reduzida, adicionou-se dietil-éter ao resíduo, e os sólidos formados foram coletados por filtração. Os sólidos assim coletados foram purificados por cromatografia de coluna em sílica-gel (hexano:acetato de etila 7:3), para obter uma mistura (7,25 g) contendo 1,1-dioxo-l,2,3,4-tetraidro-piran4-il-carbamato de t-butila, como um sólido incolor. O licor-mãe foi concentrado sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 7:3), para obter uma mistura (9,18 g) contendo 1,1-dioxo-l,2,3,4-tetraidro-piran4-il-carbamato de t-butila, como um sólido incolor (quantidade total: 16,4 g). As misturas assim obtidas foram dissolvidas em dioxano (60 ml), e adicionou-se solução aquosa de amônea a 28% (60 ml) . A mistura resultante foi agitada a 60 oC por 4,5 h em um tubo vedado. Depois de deixar resfriar, a mistura da reação foi concentrada sob pressão reduzida. Depois de remover o dioxano por destilação, o resíduo foi extraído 5 vezes com cloreto de metileno. As camadas orgânicas resultantes foram combinadas e concentradas sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 96:4), para obter o composto do título com baixa polaridade (2,31 g) e o composto do título com alta polaridade (4,31 g).
Composto de baixa polaridade:
RMN-!H (CDC13) δ: l,44(9H,s), 2,14-2,2 8 (2H, m) , 3,01-3,08 (3H, de 08/10/2018, pág. 357/857
349
m) , 3, 23(1H,dd,J=13,8, 3,9Hz), 3, 47-3, 49(1H,m), 3,71-3,76 (lH,m), 5,32(1H,d,J=7,3Hz).
MS (531) m/z: 265(M+H+).
Composto de alta polaridade:
RMN-!H (CDCls) δ: l,45(9H,s), 1, 94-2, 01 (1H, m) , 2,37-2,44 (lH,m) , 2,91 (lH,dd,J=ll,2, 14,1Hz), 3, 04-3, 07(2H, m) , 3,123,19(lH,m), 3, 26-3, 30 (lH,m) , 3, 39-3, 42 (1H, m) , 4,62(lH,br).
MS (ESI) m/z: 265(M+H+).
Exemplo Referencial 180 (2S,3S)-2,3-bis-(metóxi-metóxi)-1,4-butanodiol:
ch3och2o ch3och2o
0H
OH
Adicionou-se cloro-metil-metil-éter (4,8 ml) em gotas a uma solução de L-tartarato de dietila (8,6 g) , diisopropil-etil-amina (40 ml) e cloreto de metileno (40 ml) sob resfriamento com gelo, e a mistura foi agitada por 18 h, enquanto a temperatura do sistema era aumentada gradualmente até a temperatura ambiente. A mistura da reação foi concentrada, e o resíduo resultante foi diluído com acetato de etila e lavado com ácido clorídrico a 10%, uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi dissolvido em tetraidrofurano. A
Petição 870180138821, de 08/10/2018, pág. 358/857
350 solução foi adicionada em gotas a uma suspensão de hidreto de lítio e alumínio (2,2 g) em tetraidrofurano sob resfriamento com gelo, e a mistura foi agitada por 2 h sob resfriamento com gelo. Depois, adicionou-se cuidadosamente uma solução aquosa a 10% de sulfato ácido de sódio sob resfriamento com gelo, a mistura foi agitada por 1 h, e a mistura da reação foi diluída com solução aquosa saturada de cloreto de sódio e extraída com acetato de etila. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (3,0 g).
ΚΜΝ-^ (CDC13) δ: 1,55-1, 64 (2H, m) , 3,44(6H,s), 3, 70-3, 81 (6H,
m) , 4,70(2H,d,J=6,9Hz), 4,76(2H,d,J=6,9Hz) .
Exemplo Referencial 181 (3S,4S)-3,4-bis-(metóxi-metóxi)-tetraidrofurano:
CH3OCH2(\ ch3och2o'
Adicionou-se azodicarboxilato de dietila (2,46 g) em gotas a uma solução do composto obtido no Exemplo Referencial 180 (3,0 g), trifenilfosfina (4,5 g), tetraidrofurano (10 ml)e tolueno (40 ml), e a mistura foi agitada à temperatura ambiente por 4 dias. A mistura da reação foi concentrada sob pressão reduzida, adicionou-se um solvente misto (160 ml) de hexano e dietil-éter (1:1) ao resíduo resultante, e a mistura foi agitada por 3 h. Os de 08/10/2018, pág. 359/857
351 insolúveis depositados foram então coletados por filtração. 0 filtrado foi concentrado, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1), para obter o composto do título (1,95 g).
ΗΜΝ-^ (CDC13) δ: 3,38(6H,s), 3, 80 (2H, dd, J=9, 2, 1,7Hz) , 4,00 (2H, dd, J=9, 2, 4,4Hz), 4,23 (2H, dd, J=4,4, 1,7Hz), 4,67(2H,d,J= 6,9Hz), 4,71(2H,d,J=6,9Hz).
Exemplo Referencial 182 (3S,4S)-tetraidro-3,4-furanodiol:
Adicionou-se ácido clorídrico concentrado (2,1 ml) a uma solução do composto obtido no Exemplo Referencial 181 (1,95 g) em metanol (6,0 ml), e a mistura foi agitada por 18 h. Depois de concentrar a mistura da reação e diluir o resíduo resultante com clorofórmio, e secar sobre carbonato de potássio, o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (0,52 g) . RMN—XH (CDC13) δ: 1,77 (2H, d, J=4,7Hz) , 3, 73 (2H, d, J=1O, 2Hz) ,
4,08(2H,dd,J=10,2,3,7Hz), 4,18-4,34(2H,m).
Exemplo Referencial 183 (3S,4S)-tetraidro-3,4-furanodiamina:
Petição 870180138821, de 08/10/2018, pág. 360/857
352
Ο composto do título foi obtido a partir do composto obtido no Exemplo Referencial 182, de uma maneira similar aos processos descritos nos Exemplos Referenciais
169 a 171.
RMN-1!! (CDC13) δ: 1, 35-1, 46 (4H,m) , 3, 19 (2H, dd, J=5, 6, 4,1Hz),
3,50(2H,dd,J=9,0, 4,1Hz), 4,09(2H,dd,J=9,0, 5,6Hz).
Exemplo Referencial 184 (2R,3R)-2,3-bis-(metóxi-metóxi)-1,4-butanodiol:
CH3OCH2O,„ OH
CH3OCH2(T^—OH
O composto do título foi obtido a partir de D10 tartarato de dietila, de uma maneira similar àquela do
Exemplo Referencial 180.
ΗΜΝ-1!!: igual àquela do enanciômero no Exemplo Referencial
180.
Exemplo Referencial 185 (3R,4R)-3,4-bis-(metóxi-metóxi)-tetraidrofurano:
ch3och2o„„.
CH30CH20‘
Petição 870180138821, de 08/10/2018, pág. 361/857
353 composto do título foi obtido a composto obtido no Exemplo Referencial 184, de similar àquela do Exemplo Referencial 181.
EMN-1!!: igual àquela do enanciômero no Exemplo
181.
Exemplo Referencial 186 (3R,4R)-tetraidro-3,4-furanodiol:
partir do uma maneira
Referencial composto do título foi obtido a composto obtido no Exemplo Referencial 185, de similar àquela do Exemplo Referencial 182.
RNIM-1!!: igual àquela do enanciômero no Exemplo
182.
Exemplo Referencial 187 (3R,4R)-tetraidro-3,4-furanodiamina:
partir do uma maneira
Referencial
O composto do título foi obtido a composto obtido no Exemplo Referencial 186, de similar àquela do Exemplo Referencial 183.
1H-NMR (CDC13) δ: igual àquela do enanciômero partir do uma maneira no Exemplo
Petição 870180138821, de 08/10/2018, pág. 362/857
354
Referencial 183.
Exemplo Referencial 188 (3R,4R)-l-benzil-3,4-diidróxi-2,5-pirrolidinodiona:
Ácido L-tartárico (30 g) e benzilamina (22 ml) 5 foram adicionados a xileno (150 ml), e a mistura foi aquecida sob refluxo a 150 oC por 3 h, usando um sifão DeanStark. Depois de deixar a mistura da reação resfriar por toda a noite, os cristais foram coletados por filtração e lavados com acetona. 0 produto bruto resultante foi recristalizado em etanol, para obter o composto do título (23,2 g) .
RMN-iH (DMSO-de) δ: 4,36-4 , 40 (2H, m) , 4,55 (cada ΙΗ,ΑΒ tipo d,J=15Hz), 6,26—6,30(2H,m), 7,25—7,35(5H,m).
Exemplo Referencial 189 (3S,4S)-l-benzil-3,4-pirrolidinodiol:
H0
H0
X>-CH,Ph
O composto obtido no Exemplo Referencial 188 (11
g) foi dissolvido em tetraidrofurano (110 ml), e adicionouse hidreto de lítio e alumínio (5,69 g) parceladamente à
Petição 870180138821, de 08/10/2018, pág. 363/857
355 solução sob resfriamento com gelo. A mistura foi aquecida até a temperatura ambiente por 1 hora e depois sob refluxo por lhe por mais uma noite. Depois de deixar a mistura da reação resfriar, adicionou-se água (5,7 ml), uma solução aquosa a 15% (5,7 ml) de hidróxido de sódio, e água (17,1 ml), nesta ordem, sob resfriamento com gelo, e a mistura foi aquecida até a temperatura ambiente e agitada por 1 h. Depois de filtrar os depósitos através de Celite e concentrar o licor-mãe sob pressão reduzida, o resíduo resultante foi recristalizado em acetato de etila, para obter o composto do título (6,35 g).
RMN-XH (CDC13) δ: 2,40-2,44(2H,m), 2, 88-2, 92(2H,m), 3,58(cada ΙΗ,ΑΒ tipo d,J=7,8Hz), 4,04(2H,t,J=4,2Hz), 7,25-7,34(5H,m).
Exemplo Referencial 190 metano-sulfonato de (3S,4S)-l-benzil-4-[(metilsulfonil)oxi]-pirrolidinila:
MsO
MsO
,.UN CH’Ph
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 189, de uma maneira similar àquela do Exemplo Referencial 169.
RMN-XH (CDCI3) δ: 2,7 6 (2H, dd, J=ll, 4, 6Hz) , 3,08(6H,s), 3,64 (2H,d,J=2,5Hz), 3, 68—3, 75(2H,m), 5,12—5,15(2H,m), 7,27—7,35 (5H,m).
de 08/10/2018, pág. 364/857
356
Exemplo Referencial 191 (3S,4S)-3,4-bis-[(metil-sulfonil)oxi]-1-pirrolidinocarboxilato de t-butila:
MsO
MsO
N-Boc
O composto obtido no Exemplo Referencial 190 (1,57 g) foi dissolvido em 1,2-dicloro-etano (16 ml), adicionou-se cloro-formiato de 1-cloro-etila (0,73 ml) à temperatura ambiente, e a mistura resultante foi aquecida sob refluxo por 4 h. Depois de remover o solvente por destilação sob pressão reduzida, adicionou-se metanol (16 ml) ao resíduo resultante, e a mistura resultante foi aquecida sob refluxo por 1 h, deixada resfriar, e concentrada. Os cristais obtidos por recristalização em acetato de etila foram coletados por filtração, para obter o cloridrato de (3S,4S)3, 4-bis-[(metil-sulfonil)oxi]-1-pirrolidina (1,30 g) , como cristais incolores. Adicionou-se dicarbonato de di-t-butila (1,15 ml) a uma solução do cloridrato assim obtido e trietil-amina (1,40 ml) em cloreto de metileno (26 ml), e a mistura foi agitada por toda a noite à temperatura ambiente. Depois de concentrar a mistura da reação, o resíduo foi diluído com acetato de etila, lavado com água e solução aquosa saturada de cloreto de sódio, e secado sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por de 08/10/2018, pág. 365/857
357 cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:9 —» 1:1), para obter o composto do título (1,40 g).
ΗΜΝ-^ (CDC13) δ: l,47(9H,s), 3,12(6H,s), 3, 70-3, 73 (2H, m) ,
3,79(1H,d,J=4,5Hz), 3,82(1H,d,J=4,5Hz), 5,19(2H,br).
Exemplo Referencial 192 (3R,4R)-3,4-diazido-l-pirrolidino-carboxilato de t-butila:
C
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 191, de uma maneira similar àquela do Exemplo Referencial 170.
ΚΜΝ-^ (CDC13) δ: l,47(9H,s), 3,37-3,46(2H,m), 3,64- 3,71(2H, m), 3,96(2H,t,J=3,2Hz).
Exemplo Referencial 193 (3R,4R)-3-amino-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-115 carboxilato de t-butila:
Boc
Petição 870180138821, de 08/10/2018, pág. 366/857
358 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 192, de uma maneira similar àquela dos Exemplos Referenciais 171 e 172.
RMN-1H (DMSO-de) δ: l,39(9H,s), 2, 95-3, 00 (1H, m) , 3,09-3,13 (lH,m), 3, 52(1H,dd,J=10, 6,5Hz), 3, 68(1H,dd,J=10, 7,8Hz),
4,04-4,09 (2H,m), 7,16(lH,s), 7,18(lH,s), 7,42 (1H, d, J=8, 5
Hz), 7,69(1H,d,J=l,5Hz), 8,50(1H,d,J=6,5Hz), 11,77 (1H,br) .
Exemplo Referencial 194 (3S)-5-oxotetraidro-3-furanil-carbamato de t-butila:
BocHÍC^7
Adicionou-se dicarbonato de di-t-butila (4,1 g) e
10% de paládio sobre carvão (0,4 g) a uma solução de (3S)—(— )-tetraidro-5-oxo-3-furanil-carbamato de benzila (3,3 g) em tetraidrofurano (20 ml) , e a mistura foi agitada por 1 dia em uma atmosfera de hidrogênio. Depois de filtrar os insolúveis através de um leito de Celite, o filtrado foi concentrado sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1), para obter o composto do título (1,5 g).
ΗΜΝ^Η (CDC13) δ: l,45(9H,s), 2, 45 (1H, dd, J=17,8, 2,7Hz),
2,86(lH,dd,J=17,8, 7,3Hz), 4,12-4,23(1H,m), 4,54-4,62(2H,m),
4,85-4,95(lH,m).
Petição 870180138821, de 08/10/2018, pág. 367/857
359
Exemplo Referencial 195 (3S,4S)-4-azido-5-oxotetraidro-3-furanil-carbamato de tbutila:
BocHN
Adicionou-se bis-(trimetil-silil)-amida de lítio 1
M (solução em tetraidrofurano, 8,65 ml) em gotas a uma solução do composto obtido no Exemplo Referencial 194 (0,87
g) em tetraidrofurano (20 ml) a -78 oC, e a mistura foi agitada por 30 min. Depois de adicionar uma solução de ptolueno-sulfonil-azida (1,02 g) em tetraidrofurano (10 ml), e agitar a mistura por 5 min, adicionou-se trimetil-clorosilano (1,7 ml), e a mistura foi agitada por 2 h, enquanto a temperatura do sistema era aumentada gradualmente até a temperatura ambiente. A mistura da reação foi diluída com dietil-éter, lavada com ácido clorídrico a 10%, adicionou-se 5% de uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e depois foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1), para obter o composto do título (0,62 g).
ΚΜΝ-^ (CDC13) δ: l,46(9H,s)
4,09(lH,dt,J=15,3, 7,6Hz)
4,12-4,23(lH,m), 4,37-4,50(1H,m) , 4,54 (1H,dd,J=9,0,7,6Hz) de 08/10/2018, pág. 368/857
360
4,81-4,90(lH,m).
Exemplo Referencial 196 (3S,4S)-4-{[(5-cloro-indo1-2-i1)-carbonil]-amino}-5oxotetraidro-3-furanil-carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 195, de uma maneira similar àquela dos Exemplos Referenciais 90 e 91.
RMN-!H (CDC13) δ: l,44(9H,s), 4,01-4, 13 (1H, m) , 4,20- 4,36 (1H, m) , 4,78-4,93 (2H,m) , 6,15(lH,s), 6,93(lH,s), 7,03-7, 11 (1H,
m) , 7,20-7,28 (lH,m) , 7,30 (1H, d, J8, 8Hz) , 7,61(lH,s), 9,27 (1H,S) .
Exemplo Referencial 197 (3S,4S)-4-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-5-oxotetraidro-3-furanil15 carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 369/857
361 composto do título foi obtido produzindo (3S,4S)-4-amino-5-oxotetraidro-3-furanil-carboxilato de tbutila a partir do composto obtido no Exemplo Referencial 195, de uma maneira similar àquela do Exemplo Referencial
90, e depois reagindo com o composto obtido no Exemplo
Referencial 10, de acordo com as condições de reação do Exemplo Referencial 91.
RMN-1H (CDC13) δ: l,44(9H,s), 2,52(3H,s), 2, 83 (2H, t, J=5, 9
Hz), 2,79-3, 02 (2H,m), 3,74 (2H,s), 4,03-4,12(1H,m), 4,21-4,36 (lH,m), 4,80-4,95(2H,m), 6,14-6,24(1H,m), 7,76-7,85(1H,m).
Exemplo Referencial 198
2-[(3S)—3—[(t-butóxi-carbonil)-amino]-2-{[(5-cloro-indol-2il)-carbonil]-amino}-4-hidróxi-butanoil)-amino]
-acetato de etila:
O composto obtido no Exemplo Referencial 196 (0,4
g), cloridrato do éster etílico de glicina (1,0 g) e trietil-amina (1,0 ml) foram adicionados a etanol (20 ml), e a mistura foi aquecida e agitada a 60 oC por 18 h. A mistura da reação foi diluída com clorofórmio e lavada com
Petição 870180138821, de 08/10/2018, pág. 370/857
362 uma solução aquosa a 10% de ácido cítrico e solução aquosa saturada de cloreto de sódio. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 98:2), para obter o composto do título (0,31 g).
RMN-1H (DMSO-de) δ: 1, 17(3H,t,J=7,OHz), l,34(6H,s), 1,36 (3H,s), 3, 51—3, 63 (0, 6H,m) , 3,72-3,80(2H,m), 4,06(2H,q,J=7,O
Hz), 4,11-4,23(1,4H,m), 4,67-4,82(1H,m), 4,85-4,91(1H,m),
6,48(0,4H,d,J=9,5Hz), 6, 80(0,6H,d,J=9,5Hz), 7,10-7,22(2H,m),
7,42(1H,d,J=8,8Hz), 7,72(0, 4H,d,J=2,OHz), 7,73(0,6H,d,J=2,O
Hz), 8,23-8,31(0,6H,m) , 8,34-8,41(0,4H,m), 8,43-8, 50 (lH,m),
11,83 (1H,s) .
Exemplo Referencial 199 cloridrato de 2-((4R)-4-amino-3-{[(5-cloro-indol-2-il)carbonil]-amino}-2-oxopirrolidin-l-il)acetato de etila:
|
0 composto |
do título foi |
obtido |
convertendo |
o |
|
composto obtido no Exemplo Referencial |
198 em |
um derivado |
de |
|
20 pirrolidona, usando |
as condições de |
reação |
descritas |
no |
|
Exemplo Referencial |
181, e depois removendo |
um grupo |
t- |
Petição 870180138821, de 08/10/2018, pág. 371/857
363 butóxi-carbonila, de uma maneira similar àquela do Exemplo
Referencial 69.
RMN-1H (DMSO-de) δ: 1,17(2H,t,J=7,OHz), 1,23(1H,t,J=7,OHz),
3,31—3,40(0,6H,m), 3, 57(0, 4H,d,J=ll,2Hz), 3,90-4,23(4H,m),
4,42(0,6H,dd,J=12,0,6,1Hz), 4,50-4,60(0,4H,m), 4,62(0,6H,dd,
J=12,0, 3,9Hz), 5, 12-5, 23 (0, 4H,m) , 7, 17 (0, 4H, s) , 7,20(0,4H, dd,J=8,8,2,OHz) , 7,28(0,6H,dd,J=8,8, 2,OHz), 7,30(0,6H,s),
7,44(0,4H, d, J8,8HZ), 7,50(0,6H,d,J=8,8Hz), 7,75(1H,d,J=2,O
Hz), 8,20-8,33(lH,m), 8,71-8,94(3,6H,m), 9,22-9,35(0,4H,m),
11,97 (0,4H,s), 12,44(0,6H,s) .
Exemplo Referencial 200 (3R,4S)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-l-metil-5oxopirrolidin-3-il)-acetato de t-butila:
BocHN
O composto do título foi obtido tratando um 15 composto obtido pela reação do composto obtido no Exemplo Referencial 196 com metil-amina (solução a 40% em metanol) , em um derivado de pirrolidona, de uma maneira similar àquela do Exemplo Referencial 198, sob as mesmas condições de reação descritas no Exemplo Referencial 181.
RMN-iH (CDC13) δ: l,43(9H,s), 2,90(3H,s), 4,26 (1H, br, s) , 4,36 (2H,m), 4,51—4,52(1H,m), 5,35(1H,br,s), 6,95—6,99(2H,m),
Petição 870180138821, de 08/10/2018, pág. 372/857
364
7,22-7,32 (3H,m), 7,63(lH,s), 8, 95 (1H, br, s) .
Exemplo Referencial 201
N-[(3S,4R)-4-amino-l-metil-2-oxopirrolidin-3-il]-5-cloroindol-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 200 de uma maneira similar àquela do Exemplo Referencial 69.
RMN-1H (CDC13) δ: 2, 95 (3H, d, J5, 1Hz) , 3, 91-3, 93 (1H, m) , 4,19 (1H,d,J3,7HZ), 4,36(1H,dd,J=ll, 1,7HZ), 4,48(1H,dd,J=ll,
2,OHZ), 6,90-6,97(2H,m), 7,21-7,33(2H,m), 7,62(1H,d,J=2,O
Hz), 8,90 (1H,s) .
Exemplo Referencial 202
3,6-diidro-l(2H)-piridino-carboxilato de t-butila:
Boc i
Adicionou-se dicarbonato de di-t-butila (6,55 g) a 15 uma mistura de 1,2,3,6-tetrahidropiridina (2,50 g) e uma
Petição 870180138821, de 08/10/2018, pág. 373/857
365 solução aquosa a 10% (3,0 ml) de carbonato de sódio, e a mistura foi agitada à temperatura ambiente por 20 h. Adicionou-se água à mistura da reação, para conduzir extração com acetato de etila. A camada orgânica resultante foi lavada com ácido clorídrico 0,5 N, água, uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, nesta ordem, e secada sobre sulfato de sódio anidro. 0 solvente foi então removido por destilação sob pressão reduzida, para obter o composto do título (5,08 g).
ΗΜΝ-^ (CDC13) δ: l,47(9H,s), 2, 12 (2H, br, s) , 3,48(2H,t,J=
5, 6Hz), 3,88(2H,br,s), 5,60(1H,br,s), 5, 78—5, 90(1H,m) .
Exemplo Referencial 203 (3R*,4S*)-3,4-diidróxi-l-piperidino-carboxilato de t-butila:
O composto obtido no Exemplo Referencial 202 (18,45 g) foi dissolvido em acetonitrila (200 ml), e adicionou-se água (38 ml), uma solução aquosa 0, 039 M (82 ml) de tetróxido de ósmio e N-óxido de N-metil-morfolina (23,13 g). A mistura foi agitada à temperatura ambiente por
17 horas. Um excesso de agente oxidante foi tratado com uma solução aquosa saturada de sulfito de sódio, para conduzir extração com acetato de etila. A camada orgânica resultante
Petição 870180138821, de 08/10/2018, pág. 374/857
366 foi lavada com água, ácido clorídrico 0,5 N, uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, secada sobre sulfato de sódio
|
anidro e depois |
concentrada |
sob |
pressão reduzida. |
0 resíduo |
|
5 resultante foi |
purificado |
por |
cromatografia de |
coluna em |
|
sílica-gel (hexano:acetato |
de |
etila 1:3), para |
obter o |
composto do título (15,0 g).
RNIN-^ (CDCls) δ: l,46(9H,s), 1, 60-1,73 (1H, m) , 1,77-1, 90 (1H,
m) , 2,68(lH,br,s), 2,80-3, 20(1H,br), 3, 22-3, 32 (1H,m) , 3,42 (1H, dd,J=14,3,3,4Hz), 3, 50-3, 62 (2H,m), 3, 77(1H, brs), 3,813,92(lH,m).
Exemplo Referencial 204 (3R*,4S*)-3,4-bis-[(metil-sulfonil)oxi]-1-piperidinocarboxilato de t-butila:
Boc
I
OMs
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 203, de uma maneira similar àquela do Exemplo Referencial 169.
RMN-!H (CDCI3) δ: l,47(9H,s), 1, 85-1, 97 (1H, m) , 2, 08-2,20 (1H,
m) , 3, 00-4,20 (4H,m) , 3,12(6H,s), 4,85 (1H, br, s) , 4,94(1H, br, s) .
Petição 870180138821, de 08/10/2018, pág. 375/857
367
Exemplo Referencial 205 (3R*,4S*)-3,4-diazido-l-piperidino-carboxilato de t-butila:
Boc i
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 204, de uma maneira similar àquela do Exemplo Referencial 170.
RMN-!H (CDC13) δ: l,47(9H,s), 1,70-1,80 (1H, m) , 1, 90-2, 00 (1H,
m), 3, 05—4,00 (6H,m) .
Exemplo Referencial 206 (3R*,4S*)-3,4-diamino-l-piperidino-carboxilato de t-butila:
Boc
nh2
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 205, de uma maneira similar àquela do Exemplo Referencial 171.
RMN-1!! (CDCI3) δ: l,46(9H,s), 1,48-1, 60 (2H, m) , 1, 80-2, 10 (4H, br), 2, 85-2, 91(2H,m), 2,97(1H,br,s), 3, 09(1H,dd,J=13,6,
2,7Hz), 3, 74 (1H, dd, J=13, 6, 4,2Hz) , 3,81(lH,s).
Petição 870180138821, de 08/10/2018, pág. 376/857
368
Exemplo Referencial 207 (3R*,4S*)-3~amino-4-{[(5-cloro-indol-2-il)-carbonil]-amino}1-piperidino-carboxilato de t-butila:
Boc
O composto obtido no Exemplo Referencial 206 (3,23 5 g) foi dissolvido em N,N-dimetil-formamida (100 ml), e adicionou-se trietil-amina (2,08 ml) e o composto obtido no Exemplo Referencial 52 (3,80 g) à solução. A mistura foi agitada à temperatura ambiente por 3 dias. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se água ao resíduo para conduzir extração com cloreto de metileno. A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, secada sobre sulfato de sódio anidro, e depois concentrada sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1 —>
10:1), para obter o composto do título (2,70 g).
RIM-1!! (DMSO-de) δ: 1,40-1,58 (3H,m) , l,41(9H,s), 1,75-1,90 (lH,m), 2,95 (lH,br,s), 2, 98-3, 05(1H,m), 3,19-3,28(1H,m),
3,74(lH,dd,J=19,5, 15,4Hz), 3,79(1H,br,s), 4,04-4,12(1H,m),
Petição 870180138821, de 08/10/2018, pág. 377/857
369
7, 17 (1Η, dd, J=8,7, 1,9Hz), 7,21(lH,s), 7,42(1H,d,J=8,7Hz),
7,68(1H,d,J=l,9Hz), 8, 00(1H, br,d,J=7,6Hz), ll,80(lH,s). Exemplo Referencial 208 (3R*,4S*)-3-amino-4-{[(5-meti1-4,5,6,7-tetraidrotiazolo[5,4—
c]-piridin-2-il)-carbonil]-amino}-1-piperidino-carboxilato de t-butila:
O composto obtido no Exemplo Referencial 206 (3,23 g) foi dissolvido em N,N-dimetil-formamida (100 ml), e adicionou-se trietil-amina (2,08 ml). O composto obtido no Exemplo Referencial 149 (3,83 g) foi então adicionado, e a mistura foi agitada à temperatura ambiente por 3 dias. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se água ao resíduo para conduzir extração com cloreto de metileno. A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 10:1 —> 5:1), para obter o composto do título (2,27 g).
RMN-1!! (CDC13) δ: 1, 30-1, 62 (3H, m) , l,47(9H,s), 1,78-1,88 de 08/10/2018, pág. 378/857
370 (lH,m), 2,51(3H,s), 2,81(2H,t,J=5,9Hz), 2,85-2, 98(3H,m) ,
3,00-3,15(2H,m), 3,71(2H,s), 3, 80-4, 15 (3H, m) , 7,7 9 (1H, br, s) . Exemplo Referencial 209 (3R*,4S*)-3~amino-4-{[(flúor-indol-2-il)-carbonil]-amino}-15 piperidino-carboxilato de t-butila:
Boc
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 206 e ácido 5-flúorindol-2-carboxílico, de uma maneira similar àquela do Exemplo Referencial 172.
RMN-!H (CDC13) δ: 1, 40-1, 70 (3H, m) , l,48(9H,s), 2,79-2,92 (lH,m), 2, 99-3,14 (lH,m) , 4,00-4,23 (3H, m) , 6,85(lH,s), 7,04 (1H,td,J=9,0,2,4Hz), 7,07-7,20(1H,br), 7,27(1H,dd,J=9,0, 2,4
Hz), 7,35(1H,d,J=9,0, 4,4Hz), 9,25-9,50(1H,br).
MS (ESI)m/z: 377(M+H)+.
Exemplo Referencial 210 (3S,4R)-5-azido-3-{[(benzilóxi)-carbonil]-amino}-4-[(tbutóxi-carbonil)-amino]-valerato de etila:
CO2Et
Petição 870180138821, de 08/10/2018, pág. 379/857
371
Adicionou-se sucessivamente trietil-amina (4,80 ml) e cloreto de metano-sulfonila (1,55 ml) em gotas a uma solução do composto (3S,4S) obtido no Exemplo Referencial 168 (composto com baixa polaridade) (7,1 g) em cloreto de metileno (100 ml) sob resfriamento com gelo, e a mistura foi agitada por 30 min sob resfriamento com gelo. A mistura da reação foi diluída com clorofórmio e lavada com uma solução aquosa a 10% de ácido cítrico, uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, para obter um derivado de metano-sulfonila (9,20 g). Uma solução do derivado de metano-sulfonila assim obtido, azida de sódio (5,64 g) e N, N-dimetilformamida (100 ml) foi agitada a 80 oC por 20 h. A mistura da reação foi diluída com acetato de etila e lavada com água e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio), para obter o composto do título (5,42 g) . RMN-!H (CDC13) δ: 1, 24 (3H, t, J=7, 1Hz) , l,43(9H,s), 2,56-2,68 (2H,m), 3, 48-3, 60 (2H,m), 3, 88-3, 97 (lH,m), 4,04-4,20 (3H,m),
4,88-4,97(1H,br), 5,10(2H,s), 5,60-5,75(1H,br), 7,30-7,40 (5 H,m) .
MS (ESI) m/z: 436(M+H)+.
de 08/10/2018, pág. 380/857
372
Exemplo Referencial 211 (4S,5R)-5-[(t-butóxi-carbonil)-amino]-2-oxo-piperidin-4-ilcarbamato de benzila
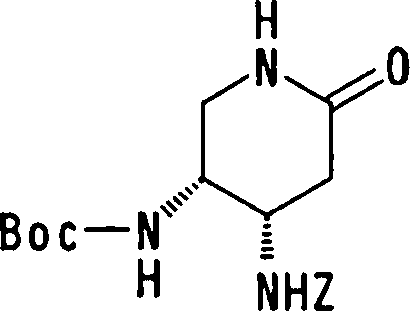
Um catalisador Lindlar (2,71 g) foi adicionado a uma solução do composto obtido no Exemplo Referencial 210 (5,42 g) em um solvente misto de etanol (150 ml) e tetraidrofurano (10,0 ml), e a mistura foi agitada por 3 h sob uma atmosfera de hidrogênio, e depois por 14 h sob nitrogênio. Depois de remover os insolúveis através de um leito de Celite, e concentrar o filtrado sob pressão reduzida, o resíduo resultante foi dissolvido em tetraidrofurano (30 ml), e adicionou-se trietil-amina (3,0 ml) a ele. A mistura foi agitada à temperatura ambiente por 1,5 h. A mistura da reação foi diluída com acetato de etila e lavada com uma solução aquosa a 10% de ácido cítrico, uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 25:1), para obter o composto do título (2,50 g).
de 08/10/2018, pág. 381/857
373
EMN-iH (CDC13) δ: l,44(9H,s), 2, 30-2, 50 (1H, br) , 2,65-2,90
br), 5,ll(2H,s), 5, 55—5, 60 (1H, br) , 5, 65—5, 90 (1H, br) , 6,25—
6,55(lH,br), 7,28-7,40 (5H, m) .
MS (ESI) m/z: 364(M+H)+.
Exemplo Referencial 212 (3R,4S)-5-[(t-butóxi-carbonil)-amino]-piperidin-4-ilcarbamato de benzila
Boc—N =
Η NHZ
Adicionou-se complexo de borano:tetraidrofurano 1
M (solução em tetraidrofurano, 34,0 ml) em gotas a uma solução de tetraidrofurano (70 ml) do composto obtido no Exemplo Referencial 211 (2,49 g) sob resfriamento com gelo, e a mistura foi agitada por 20 h, enquanto a temperatura do sistema era elevada gradualmente até a temperatura ambiente. Adicionou-se metanol (100 ml) à mistura da reação, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se etanol (45 ml), água (5 ml) e trietil-amina (10 ml) ao resíduo, e a mistura foi aquecida sob refluxo por 24 h. A mistura da reação foi concentrada, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol:água 7:3:1, camada inferior), para obter o composto do título (1.61 g).
de 08/10/2018, pág. 382/857
374
RMN-iH (CDCI3) δ: l,44(9H,s), 1,65-1,72(2H,m), 2,67(lH,t,J=
12,OHz), 2, 82(12H,d,J=12,OHz), 2,90-3,10(1H,br), 3,60-3,80 (2H,m), 3, 90-4, 00 (lH,m), 5, 00-5, 20(2H,m), 5, 40-5, 60(2H,br),
7,25-7,74(5H,m).
MS (FAB) m/z: 350(M+H)+.
Exemplo Referencial 213 (3R,4S)-1-acetil-4-{[(benzilóxi)-carbonil]-amino}-piperidin4-il-carbamato de t-butila:
O composto do título foi obtido pela reação do 10 composto obtido no Exemplo Referencial 212 com cloreto de acetila e trietil-amina, em cloreto de metileno.
RMIS!-^ (CDC13) δ: l,44(9H,s), 1,85-2, 15 (2H, m) , 2, 07 (1,5H, s) ,
2, 14(1,5H,s), 2, 75-2, 90 (lH,m) , 3, 10-3,20 (0,5H, m) , 3,25-3,35 (0,5H,br,d,J=14,2Hz), 3, 65-4, 05 (3H,m) , 4,38-4,47(0,5H,br,d,
J=13,OHz), 4,5,4-4,63(0,5H,m), 4,69-4, 83(1H,br), 4,98-5,20 (2,5H,m), 5,90-6,05(0,5H,br), 7,30-7,40(5H,m).
MS (ESI) m/z: 392(M+H)+.
Exemplo Referencial 214 (3R, 4S)-1-acetil-4-{[(5-cloro-indol-2-il)-carbonil]-amino}20 1-piperidino-carboxilato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 383/857
375
Adicionou-se 10% de paládio sobre carvão (532 mg) a uma solução do composto obtido no Exemplo Referencial 213 (745 mg) em etanol (50 ml) , e a mistura foi agitada à temperatura ambiente por 16 h sob uma atmosfera de hidrogênio. Os insolúveis foram removidos por filtração através de Celite, e o filtrado foi então concentrado sob pressão reduzida. O resíduo resultante foi tratado com ácido 5-cloro-indol-2-carboxílico (467 mg) , de uma maneira similar àquela do Exemplo Referencial 68, para obter o composto do título (650 mg).
ΚΜΝ-^ (CDC13) δ: l,52(9H,s), 1, 60-1,80 (2H, m) , 2,12(lH,s),
2,16(2H,s), 2, 30-2, 45 (0, 5H,m) , 2, 67-2, 82 (0,3H, m) , 2,89(0,7H, d,J=13,7Hz) , 3, 23(0,7H,t,J=12,9Hz), 3, 37(0,3H,d,J=13,7Hz),
3, 81-3, 95 (lH,m) , 4,05-4,33 (2H, m) , 4, 62-4,72 (0, 3H,br), 4,77 (0,7H,d,J=13,7Hz), 5,10-5,27(1H,m), 6,81(0,3H,br,s), 6,85 (0,7H,s), 7, 21 (lH,br,d, J=8, 8Hz) , 7,34 (1H, d, J=8, 8Hz) , 7,57 (0,3H,br,s), 7, 61 (0, 7H, s) , 8,55-8, 65 (0,5H, br) , 9,43-9,53 (0,7H,br), 9, 60-9, 70 (0, 3H,br) .
MS (ESI) m/z: 435(M+H)+.
Exemplo Referencial 215 (3R,4R)-5-azido-3-{[(benzilóxi)-carbonil]-amino}-4-[(tbutóxi-carbonil)-amino]-valerato de etila:
Petição 870180138821, de 08/10/2018, pág. 384/857
376
CO2Et
|
|
0 composto do |
título foi |
obtido a |
partir |
do |
|
composto |
(3R,4S) (composto de alta |
polaridade) |
obtido |
no |
|
Exemplo |
Referencial 168, |
de uma maneira similar |
àquela |
do |
|
Exemplo |
Referencial 210. |
|
|
|
|
ΗΜΝ-Ή (CDC13) δ: 1,23 (3H, t, J=6, 6Hz) , l,42(9H,s), 2,51- 2,63 (2H,m), 3, 43-3, 50 (2H,m), 3, 84-3, 92(1H,m), 4,03-4,23(3H,m), 5,10(2H,s), 5,11—5,24(lH,m), 5,54-5,60(1H,m), 7,32-7,44 (5H,m).
Exemplo Referencial 216 (4R,5R)-5-[(t-butóxi-carbonil)-amino]-2-oxo-piperidin-4-ilcarbamato de benzila:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 215, de uma maneira similar àquela do Exemplo Referencial 211.
RMN-1H (DMSO-dg) δ: l,35(9H,s), 2, 19 (1H, dd, J=17, 4 , 9,1Hz),
2,41-2,51 (lH,m), 2, 97(1H,t,J=9,1Hz), 3,00-3,11(1H,m), 3,513,64(lH,m), 3, 67-3, 73 (1H, m) , 5,00(2H,s), 6, 71-6, 80 (1H, m) ,
7,20-7,30(5H,m), 7,44-7,52(1H,m), 8,30(lH,s).
Petição 870180138821, de 08/10/2018, pág. 385/857
377
Exemplo Referencial 217 (3R,4R)-3-[(t-butóxi-carbonil)-amino]-piperidin-4-ilcarbamato de benzila:
composto do título foi obtido tratando o 5 composto obtido no Exemplo Referencial 216, de uma maneira similar àquela do Exemplo Referencial 212.
RMN-1H (CDC13) δ: l,39(9H,s), 2, 05 (2H, d, J=12, 9Hz) , 2,4O(1H, t,J=ll,OHz), 2,63(1H,t,J=12, OHz) , 3,09 (1H,d,J=12,OHz) , 3,31 (lH,d,J=ll,OHz) , 3, 42-3, 53(2H,m) , 4,80-4,91(1H,m) , 5,09(2H,
s), 5,23-5,32(lH,m), 7,34-7,41(5H,m).
Exemplo Referencial 218 (3R,4R)-1-acetil-4-{[(benzilóxi)-carbonil]-amino}-piperidin3-il-carbamato de t-butila:
O composto do título foi obtido tratando o 15 composto obtido no Exemplo Referencial 217, de uma maneira similar àquela do Exemplo Referencial 213.
Petição 870180138821, de 08/10/2018, pág. 386/857
378
ΚΜΝ-Ή (CDC13) δ: l,42(9H,s), 1,53-1,67(lH,m), 1,89-2,00 (lH,m), 2, 09(1,5H, s) , 2,15(1,5Η,s), 2,57(1Η,t,J=12,ΟΗζ),
2,78(1H,t,J=12,OHz), 3,20-3,30(1H,m), 3,40-3,56(2H,m), 4,234,31(lH,m), 4,45-4,56 (lH,m) , 5,01-5,08 (lH,m), 5,10(2H,s),
7,32-7,44(5H,m).
Exemplo Referencial 219 (3R,4R)-1-acetil-4-{[(5-cloro-indol-2-il)-carbonil]-amino}piperidin-3-il-carbamato de t-butila:
O composto do título foi obtido tratando o 10 composto obtido no Exemplo Referencial 218, de uma maneira similar àquela do Exemplo Referencial 214.
RMN-!H (CDC13) δ: l,35(9H,s), 1,42-1,56 (2H, m) , 2, 00-2, 10 (1H,
m), 2, 12(1,5H,s), 2, 17(1,5H,s), 2,31-2,43 (1H,m) , 2,67-3,00 (lH,m), 3, 55-3, 63 (lH,m), 3, 78-4,00 (1H, m) , 4,03-4,21(1H,m),
4,78-5,24(2H,m), 6,91(0,5H,s), 6,92(0,5H,s), 7,22-7,32 (1H,
m) , 7,33 (1H, d, J=8, 8Hz) , 7,58(lH,s), 9, 45 (0, 51-1, s) , 9,51 (0,5H, s) .
Exemplo Referencial 220 (3R,4S)-3-[(t-butóxi-carbonil)-amino]-1-(2-metóxi-acetil)20 piperidin-4-il-carbamato de benzila:
Petição 870180138821, de 08/10/2018, pág. 387/857
379
OMe
composto do título foi obtido tratando o composto obtido no Exemplo Referencial 212 e cloreto de metóxi-acetila, de uma maneira similar àquela do Exemplo
Referencial 213.
RMN-XH (CDC13) δ: l,44(9H,s), 1,70-2, 15 (2H, m) , 2,70- 2,85 (lH,m), 2, 90-3, 30 (lH,m) , 3, 35-3, 70(1H, m) , 3,43(3H,s), 3,753,90(2H,m), 3,90-4,25(3H,m), 4,40-4,80(1H,m), 5,05-5,09(1H,
m) , 5, 10(2H, br,s), 7,30—7,40(5H,m) .
MS (ESI) m/z: 322 (M+H+) .
Exemplo Referencial 221 (3R,4S)-4-{[(5-cloro-indol-2-il)-carbonil]-amino)-1-(2metóxi-acetil)-piperidin-3-il-carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 220, de uma maneira
Petição 870180138821, de 08/10/2018, pág. 388/857
380 similar àquela do Exemplo Referencial 214.
RMN-iH (CDC13) δ: l,52(9H,s), 1,60-1,80(lH,m), 2,20-2, 40 (1H, m), 2,70-2,80(0,6H,m), 2,90-3,00(0,4H,m), 3,15-3,30(0,4H,m), 3,32—3,40(0,6H,m), 3,46,3,49(total 3H, cada s), 3,85—4,30 (5H,m), 4,55—4,80(1H,m), 5,11(0,4H,br,s), 6,05(0,6H,br,s),
6,86(lH,s), 7,20(1H,dd,J=8,7, 2,0Hz), 7,33(1H,dd,J=8,7Hz),
7,61(lH,s), 8,40-8, 60 (lH,m) , 9, 41 (1H, br, s) .
MS (FAB) m/z: 465(M+H)+.
Exemplo Referencial 222 (3R,4R)-3-[(t-butóxi-carbonil)-amino]-1-(2-metóxi-acetil)piperidin-4-il-carbamato de benzila:
OMe
O composto do titulo foi obtido a partir do composto obtido no Exemplo Referencial 217 e cloreto de metóxi-acetila, de uma maneira similar àquela do Exemplo
Referencial 213.
RMIS!-^ (CDC13) δ: 1,41(9H,: m), 2,63(1H,t,J=12,OHz), (lH,m), 3,32-3,41(5H,m),
4,50-4,63(lH,m), 5,03-5, (5H,m) .
5), 1, 45-1, 67 (lH,m) , 2,01-2,14 (1H,
2,75(1H,t,J=12,OHz), 3,20- 3,30
3, 4 4-3, 56(2H,m) , 4,21-4,32(1H,m) ,
08(lH,m), 5,09(2H,s), 7,32-7,40
Petição 870180138821, de 08/10/2018, pág. 389/857
381
Exemplo Referencial 223 (3R,4R)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-1-(2metóxi-acetii)-piperidin-3-il-carbamato de t-butila:
composto do título foi obtido a partir do 5 composto obtido no Exemplo Referencial 222 e ácido 5-cloroindol-2-carboxílico, de uma maneira similar àquela do
Exemplo Referencial 214.
RMN-1!! (CDC13) δ: l,35(9H,s), 1,41-1,56 (2H,m) , 2,11- 2,23 (0,5H,m), 2,34—2,50(0,5H,m), 2,78—2,89(0,5H,m), 3,01—3,12 (0,5H,m), 3,42(5H,s), 3, 45-3, 56 (1H, m) , 3, 78-3, 8 9 (1H, m) ,
4,00-4,21 (2H,m) , 4,78-5, 21 (2H,m) , 6, 91 (0,5H, s) , 6,93(0,5H,
s), 7,23(1H,dd,J=8,8,2,OHz), 7,33(1H,d,J=8,8Hz), 7,59(lH,s),
9, 37(0,5H,s), 9, 54(0,5H,s) .
Exemplo Referencial 224 (3R,4S)-3-{[(benzilóxi)-carbonil]-amino}-4-[(t-butóxicarbonil ) -amino]-5-{[t-butii-(difenil)-silil]oxi}
-valerato de etila
Petição 870180138821, de 08/10/2018, pág. 390/857
382
TBDPSO
co2e t
Trietil-amina (0,47 ml), imidazol (0,19 g) e tbutil-cloro-fenil-silano (0,7 ml) foram adicionados sucessivamente a uma solução do composto (3R,4S) (composto de alta polaridade) (0,74 g) obtido no Exemplo Referencial 5 168 em N,N-dimetil-formamida (30 ml) sob resfriamento com gelo, e a mistura foi agitada por 4 dias enquanto a temperatura do sistema era elevada gradualmente até a temperatura ambiente. A mistura da reação foi diluída com acetato de etila e lavada com uma solução aquosa a 10% de 10 ácido cítrico e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 8:1), para 15 obter o composto do título (0,85 g).
RMN-1H (CDC13) δ: l,07(9H,s), 1, 19 (3H, t, J=7,4Hz) , l,40(9H,s),
2,40-2,50(lH,m), 2, 60(1H,dd,J=15,9,4,5Hz), 3, 56-3, 67 (1H,m),
3,74(lH,dd,J=11,2,4,5Hz), 3,78-3,89(1H,m)
Hz), 4,21-4,30(lH,m), 4,99-5,13(3H,m),
7,40-7,53(6H,m), 7,60-7,72(4H,m).
Exemplo Referencial 225 (3R,4S)-3-[(t-butóxi-carbonil)-amino]-5-{[t-butil-(difenil)
4, 08(2H,q,J=7,4
5,41-5,52(lH,m), silil]oxi}-3-{[(5-cloro-indol-2-il)-carbonil]-amino}·
Petição 870180138821, de 08/10/2018, pág. 391/857
383 valerato de etila
O composto do título foi obtido removendo o grupo benzilóxi-carbonila do composto obtido no Exemplo
Referencial 224 e condensando com ácido 5-cloro-indol-2carboxílico, de uma maneira similar àquela do Exemplo
Referencial 214.
RMN-1!! (CDC13) δ: l,10(9H,s), 1, 20(3H,t,J=7,4Hz), l,32(9H,s), 2,40-2,52 (lH,m), 2, 71(1H, dd,J=15,9,4,5Hz), 3,67-3,81 (2H,m),
4,00-4,20 (2H,m), 4, 56-4, 74 (1H,m), 5,00-5,11(1H,m), 6,81(1H,
s), 7,21(1H,dd,J=8,8,2,OHz), 7,32(1H,d,J=8,8Hz), 7,40-7,50 (6H,m), 7,58(1H,d,J=8,5Hz), 7,63-7,74(5H,m), 9,01-9,14(1H,m) Exemplo Referencial 226 (3R*,4R*)-3-{[(5-meti1-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-1, 1-dioxo-hexaidro-ltiopiran-4-il-carbamato de t-butila
Petição 870180138821, de 08/10/2018, pág. 392/857
384 composto do título foi obtido a partir do composto (3R*,4R*) (composto de baixa polaridade) obtido no Exemplo Referencial 179 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo
Referencial 68.
RMN-1H (CDC13) δ: l,43(9H,s), 2, 30-2, 37 (2H, m) , 2,51(3H,s),
2,82-2,85(2H,m), 2,92-2,95(2H,m), 3,17-3,20(4H,m), 3,40-3,43 (lH,m), 3, 69-3, 77 (2H,m) , 3, 97-3, 98 (1H, m) , 4,98(lH,br), 5,25 (lH,br) .
Exemplo Referencial 227 cloridrato de N-(3R*,4R*)-4-amino-l,1-dioxo-hexaidro-ltiopiran-3-il]-5-metil-4,5,6,7-tetraidrotiazolo [5,4-c]piridino-2-carboxamida:
O composto do título foi obtido tratando o 15 composto obtido no Exemplo Referencial 226, de uma maneira similar àquela do Exemplo Referencial 69.
RMN-1!! (DMSO-dg) δ: 2,2 9-2,33 (2H, m) , 2,93(3H,s), 3,16(2H,br), 3,40(2H,br), 3,52(2H,br), 3, 69-3, 76 (3H, m) , 4,48(lH,br),
4,71-4,82 (2H,m) , 8,34(2H,br), 8,82(lH,br).
MS (ESI) m/z: 345(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 393/857
385
Exemplo Referencial 228 (3R*,4R*)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-1,1dioxo-hexaidro-l-tiopiran-4-il-carbamato de t-butila:
composto do título foi obtido a partir do 5 composto (3R*,4R*) (composto de baixa polaridade) obtido no Exemplo Referencial 179 e do ácido 5-cloro-indol-2carboxílico, de uma maneira similar àquela do Exemplo
Referencial 68.
RMN-1H (DMSO-de) δ: l,34(9H,s), 2,09(2H,br), 3,07(lH,d,J=
12,6Hz), 3, 24-3, 28 (lH,m) , 3,48(2H,br), 4,12(lH,br), 4,53(1H, br), 7,04(lH,s), 7,16-7, 18 (2H, m) , 7,44 (1H, d, J=8, 7Hz) , 7,67 (1H,S), 8,37(lH,br), ll,81(lH,s).
MS (ESI) m/z: 442(M+H)+.
Exemplo Referencial 229 cloridrato de N-(3R*,4R*)-4-amino-l,1-dioxo-hexaidro-ltiopiran-3-il]-5-cloro-indol-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 394/857
386
composto do título foi obtido tratando o composto obtido no Exemplo Referencial 228, de uma maneira similar àquela do Exemplo Referencial 69.
RMN-1!! (DMSO-de) δ: 2,24-2,33 (2H, m) , 3,43-3, 55 (3H, m) , 3,603,66(lH,m), 3,77(lH,br), 4,75-4,79 (1H, m) , 7, 18-7,21 (2H, m) ,
7,46(1H,d,J=8,8Hz), 7,72(1H,d,J=l,7Hz), 8,39(2H,br), 8,58 (1H, d, J=6, 8Hz) , ll,93(lH,s).
MS (ESI) m/z: 342(M+H)+.
Exemplo Referencial 230 (3R*,4S*)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-1,1-dioxo-hexaidro-ltiopiran-4-il-carbamato de t-butila
O composto do título foi obtido a partir do composto (3R*,4S*) (composto de alta polaridade) obtido no
Exemplo Referencial 179 e do composto obtido no Exemplo
Petição 870180138821, de 08/10/2018, pág. 395/857
387
Referencial 10, de uma maneira similar àquela do Exemplo
Referencial 98.
RNIN-iH (CDC13) δ: l,32(9H,s), 2, 14-2,24 (1H, m) , 2,33-2,38 (1H, m) , 2,50(3H,s), 2, 78-2, 83 (2H,m) , 2,86-2, 95(2H,m) , 3,08-3,14 (3H,m), 3, 55(1H,d,J=13,4Hz), 3, 68 (1H, d, J=15, 5Hz) , 3,72(lH,d, J=15,5Hz), 3,86-3,88(lH,m), 4,45-4,53(1H,m), 4,75(1H,d,J=8,5
Hz), 7,76(1H,d,J=8,3Hz).
MS (ESI) m/z: 445(M+H)+.
Exemplo Referencial 231 cloridrato de N-(3R*,4S*)-4-amino-l,1-dioxo-hexaidro-ltiopiran-3-il]-5-metil-4,5,6,7-tetraidrotiazolo [5,4-c]piridino-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 230, de uma maneira similar àquela do Exemplo Referencial 69.
RMIS!-^ (DMSO-de) δ: 2,03-2, 12 (1H, m) , 2,51(lH,br), 2,93(3H,s), 3, 14 (2H, d, J=12,2Hz) , 3,28(2H,br), 3,33(2H,br), 3,48(3H,br),
3,72(2H,br), 4,49(2H,br), 4,71-4,74 (1H, m) , 8,38(2H,br),
9,21-9,24(lH,m).
Exemplo Referencial 232 (3R*,4R*)-3-{[(5-flúor-indol-2-il)-carbonil]-amino}-1,1dioxo-hexaidro-l-tiopiran-4-il-carbamato de t-butila
Petição 870180138821, de 08/10/2018, pág. 396/857
388
composto do título foi obtido a partir do composto (3R*,4R*) (composto de baixa polaridade) obtido no Exemplo Referencial 179 e do ácido 5-flúor-indol-2carboxílico, de uma maneira similar àquela do Exemplo
Referencial 68.
RMN-!H (DMSO-de) δ: l,37(9H,s), 2, 10-2, 13 (2H, m) , 3,06(lH,br), 3, 37-3, 49 (3H,m) , 4,13(lH,br), 4,57(lH,br), 6, 95-7,01 (2H, m) ,
7,14(lH,br), 7, 30(1H,d,J=8,5Hz), 7,41(1H, dd,J=8,8,4,5Hz),
8,28(lH,br), 11,68(1H,s).
MS (ESI) m/z: 426(M+H)+.
Exemplo Referencial 233 cloridrato de N-(3R*,4R*)-4-amino-l,1-dioxo-hexaidro-ltiopiran-3-il]-5-flúor-indol-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 397/857
389
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 232, de uma maneira similar àquela do Exemplo Referencial 69.
ΗΜΝ-^ (DMSO-de) δ: 2,25-2,31 (1H,m) , 2,47(lH,br), 3,3O(1H, br), 3, 49-3, 53 (2H,m) , 3, 60-3, 66 (1H, m) , 3,78(lH,br), 4,79(1H br), 7, 01-7,05(lH,m) , 7,21(lH,s), 7,38(1H, d,J=9,OHz), 7,44
MS (ESI) m/z: 326(M+H)+.
Exemplo Referencial 234 (3R)-3-{[(benzilóxi)-carbonil]-amino}-4-[(t-butóxicarbonil) -amino] -5-oxovalerato de etila:
HN /Boc
OHC
NHZ
Adicionou-se complexo de trióxido de enxofre/ piridina (1,5 g) gradualmente a um solvente misto constituído do composto (3R,4S) (composto de alta polaridade) (0,5 g) obtido no Exemplo Referencial 168, sulfóxido de dimetila (6,8 ml) e trietil-amina (2,6 ml), e a mistura foi agitada por 20 min. A mistura da reação foi vertida sobre água e extraída com acetato de etila. A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. A camada orgânica foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi de 08/10/2018, pág. 398/857
390
purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (0,51 g).
ΚΜΝ-^ (CDC13) δ: 1,25 (3H, t, J=7,4Hz) , l,44(9H,s), 2,51-2,70 (2H,m), 4, 01-4,23(2H,m), 4,45-4,67(1H,m), 5, 00-5, 23 (2H,s),
5, 24-5, 42 (lH,m) , 7,23-7,43 (5H, m) , 9, 63 (0, 5H, s) , 9,67(0,5H,s) Exemplo Referencial 235 (4R)-5-[(t-butóxi-carbonil)-amino]-1-metil-2-oxopiperidin-4il-carbamato de benzila:
I
Boc^ h NHZ
Adicionou-se sucessivamente ácido acético (0,27 ml) e metilamina 2 M (solução em tetraidrofurano, 1,0 ml) a uma solução do composto obtido no Exemplo Referencial 234 (0,51 g) em etanol (10 ml) sob resfriamento com gelo, e a mistura foi agitada por 1 h, enquanto a temperatura do sistema era elevada gradualmente até a temperatura ambiente.
Adicionou-se ciano-boro-hidreto de sódio (0,15 g), agitando a mistura por 18 h. A mistura da reação foi diluída com clorofórmio e lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. A camada orgânica foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi dissolvido em tolueno
Petição 870180138821, de 08/10/2018, pág. 399/857
391 (20 ml) . Adicionou-se trietil-amina (2 ml) a esta solução, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 98:2), para obter o composto do título (0,28 g).
RMU-iH (DMSO-de) δ: 1,36 (3, 6H, s) , 1,38 (5, 4H, s) , 2,22-2,43 (lH,m), 2,44-2,61(lH,m), 2,72(1,2H,s), 2,80(1,8H,s), 3,10 (0,5H, dd,J=12,5,8,3Hz), 3, 21-3,30(0,5H,m) , 3, 33-3, 45(1H,m),
3, 56-3, 82 (lH,m), 3, 89-4, 00 (lH,m), 4,94(1H,d,J=8,1Hz), 5,00 (l,2H,s), 5,01(0,8H,s), 6,89-7,02(0,5H,m), 7,23-7,44(5,5
H,m) .
Exemplo Referencial 236 (4R)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-l-metil-6oxo-piperidin-3-il-carbamato de t-butila:
Boc
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 235 e do ácido 5cloro-indol-2-carboxílico, de uma maneira similar àquela do Exemplo Referencial 214.
ΗΜΝ(2H,m)
3,91 (0 (DMSO-de) δ: 1,24 (5, 4H, s) , 2,80(3H,s), 3, 10-3, 20 (lH,m)
4H,m), 4,02-4,10(0,6H,m),
1,35 (3, 6H, s) , 2, , 3,30-3,52(lH,m)
4,20-4,31(0,6H,m),
43-2,56 , 3,83—
4,43—
Petição 870180138821, de 08/10/2018, pág. 400/857
392
4,54 (0,4H,m) , 6, 94(Ο, 6Η,d,J=8,1Hz), 7,08(lH,s), 7,16(1H, dd, J=8,8, 2,OHz), 7, 42(1H,d,J=8,8Hz), 7,69(1H,d,J=2,OHz), 8,30 (0,4H,s), 8, 36(0,4H,d,J=7,3Hz), 8,43(0,6H,d,J=8,3Hz), 11,75 (0,6H,s), 11,78(0,4H,s).
Exemplo Referencial 237 cloridrato do ácido 4-(piridin-4-il)-benzóico:
Dissolveu-se cloridrato de 4-bromo-piridina (11,7 g) e ácido 4-carbóxi-fenil-bórico (10,0 g) em um solvente misto de tolueno (250 ml) e água (250 ml) , adicionou-se sucessivamente tetrakis-(trifenil-fosfina)-paládio(0) (5,0
g) e carbonato de sódio anidro (25,4 g) , e a mistura foi aquecida sob refluxo a 120 oC por 19 h. Depois disso, a mistura da reação foi resfriada até a temperatura ambiente, e adicionou-se acetato de etila à mistura da reação, para extraí-la com água. Adicionou-se ácido clorídrico concentrado à camada aquosa, para acidificá-la. A camada aquosa foi lavada com acetato de etila e depois concentrada, e os sólidos depositados foram coletados, para obter o composto do título (8,37 g).
RMN-iH (DMSO-ds) δ: 8, 11 (2H, d, J=8, 8Hz) , 8, 14 (2H, d, J=8, 8Hz) ,
8,35(2H,d,J=6,6Hz), 8,97(2H,d,J=6,6Hz).
MS (FAB) m/z: 200(M+H)+.
Exemplo Referencial 238 4-(piridin-4-il)-benzoato de metila:
Petição 870180138821, de 08/10/2018, pág. 401/857
393
COOMe
composto obtido no Exemplo Referencial 237 (12,4 g) foi dissolvido em metanol (200 ml) , adicionou-se ácido sulfúrico concentrado (5 ml) à temperatura ambiente, e a mistura foi aquecida sob refluxo por 3 h. Depois de completada a reação, o solvente foi removido por destilação, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para extraí-lo com acetato de etila. O extrato foi secado sobre sulfato de sódio anidro, o solvente foi removido por destilação, e adicionou-se hexano ao resíduo, para solidificá-lo, obtendo desta forma o composto do título (9,86 g).
ΗΜΝ-^ (CDC13) δ: 3,96(3H,s), 7,54 (2H, d, J=5, 9Hz) , 7,71(2H,d,
J=8,3Hz), 8,16(2H,d,J=8,3Hz), 8,71(2H,d,J=5,9Hz).
Exemplo Referencial 239
N-óxido de 4-[4-(metóxi-carbonil)-fenil]-piridina:
O composto obtido no Exemplo Referencial 238 (1,49 g) foi dissolvido em cloreto de metileno (30 ml), adicionouse ácido m-cloro-perbenzóico a 70% (3,46 g), e a mistura foi agitada à temperatura ambiente por 1 h. Adicionou-se uma solução aquosa de sulfito de sódio, para conduzir separação de 08/10/2018, pág. 402/857
394 de líquidos. A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e depois secada sobre sulfato de sódio anidro. 0 solvente foi removido por destilação, para obter o composto do título 5 (1,33 g) .
RMN-XH (DMSO) δ: 3,88(3H,s), 7, 86 (2H, d, J=7,2Hz) , 7,94(2H,d,
J=8,3Hz), 8,05(2H,d,J=8,3Hz), 8,30(2H,d,J=7,2Hz).
MS (FAB) m/z: 230(MH+H)+.
Exemplo Referencial 240
N-óxido de 4-(4-carbóxi-fenil)-piridina:
o—N*
//
COOH
O composto obtido no Exemplo Referencial 239 (802 mg) foi dissolvido em dioxano (20 ml) , adicionou-se uma solução aquosa 1 N de hidróxido de sódio, e a mistura foi refluxada por lhe depois agitada à temperatura ambiente por 2 h. Adicionou-se ácido clorídrico 1 N (5 ml) para neutralizá-la. Depois disso, adicionou-se água (5 ml), e o precipitado formado foi coletado por filtração, para obter o composto do título (627 mg).
RMN-XH (DMSO) δ: 7,85(2H,d,J=7,2Hz), 7,91(2H,d,J8,3Hz), 8,03 (2H,d,J=8,3Hz), 8,30(2H,d,J=7,2Hz).
Exemplo Referencial 241
N-óxido de 2-(4-carbóxi-fenil)-1-piridina:
Petição 870180138821, de 08/10/2018, pág. 403/857
395
COOH
O composto do título foi obtido a partir de 2bromo-piridina, de uma maneira similar àquelas dos Exemplos Referenciais 237, 238, 239 e 240.
RMN-1!! (DMSO-dg) δ: 7, 41-7, 45 (2H, m) , 7, 65-7, 69(1H,m) , 7,94 (2H,d,J=8,3Hz), 8,02(2H,d,J=8,3Hz), 8,34-8,38(1H,m), 13,09 (1H,s)
MS (FAB) m/z: 216(M+H)+.
Exemplo Referencial 242
2-(4-cloro-anilino)-2-oxoacetato de etila:
Adicionou-se sucessivamente trietil-amina (1,52 ml) e cloro-oxoacetato de etila (1,11 ml) a uma solução de 4-cloro-anilina (1,16 q) em cloreto de metileno (26 ml), e a mistura foi aqitada à temperatura ambiente por 14 h. Depois disso, adicionou-se uma solução aquosa saturada de bicarbonato de sódio à mistura da reação, para conduzir separação de líquidos, a camada orqânica resultante foi lavada sucessivamente com uma solução aquosa de ácido
Petição 870180138821, de 08/10/2018, pág. 404/857
396 cítrico a 10% e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. Depois, o solvente foi concentrado sob pressão reduzida, adicionou-se hexano ao resíduo para depositar cristais, e os cristais foram coletados por filtração e secados, para obter o composto do título (1,89 g) .
ΚΜΝ-^ (CDC13) δ: 1,43 (3H, t, J=7,1Hz) , 4,42 (2H, q, J=7,1Hz) ,
7,34(2H,d,J=8,8Hz), 7, 60(2H, d, J=8, 8Hz), 8,86(1H,br,s) .
MS (ESI)m/z: 228(M+H)+.
Exemplo Referencial 243
2-[(4-cloro-piridin-2-il)-amino]-2-oxoacetato de metila:
Dissolveu-se 2-amino-5-cloro-piridina (1,16 g) e trietil-amina (1,51 ml) em cloreto de metileno (26 ml), adicionou-se cloro-acetato de etila (1,10 ml) à solução sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente por 14 h. Depois disso, adicionou-se uma solução aquosa saturada de bicarbonato de sódio à mistura da reação, para conduzir separação de líquidos, a camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1). Os de 08/10/2018, pág. 405/857
397 sólidos amarelo-pálidos assim obtidos foram dissolvidos em metanol (20 ml), e a solução foi agitada a 50 oC por 11 h. A mistura da reação foi concentrada sob pressão reduzida, e os cristais depositados foram coletados por filtração e secados, para obter o composto do título (0,43 g).
RMN-1!! (CDO13) δ: 3,99(3H,s), 7,73 (1H, dd, J=8,8,2,2Hz) , 8,24 (1H,d,J=8,8Hz), 8,31(1H, d, J=2,2Hz), 9,39(1H,br,s) .
MS (ESI) m/z: 215(M+H)+.
Exemplo Referencial 244 ácido (IS)-3-ciclo-hexeno-l-carboxílico:
COOH
O sal (R)-(+)-α-metil-benzil-amínico (J. Am. Chem.
Soc. 100:5199-5203, 1978) (95,0 g) do ácido (IS)-3-ciclohexeno-l-carboxílico foi dissolvido em uma mistura de acetato de etila (1,6 1) e ácido clorídrico 2 N (1,6 1) .
Depois de separar uma camada orgânica, uma camada aquosa foi extraída com acetato de etila (2 x 500 ml) . As camadas orgânicas foram combinadas e lavadas com solução aquosa saturada de cloreto de sódio (2 x 300 ml) , para retirar uma camada orgânica. Depois de extrair uma camada aquosa com acetato de etila (2 x 200 ml), a camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio (100 ml). Todas as camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro, e depois concentradas
Petição 870180138821, de 08/10/2018, pág. 406/857
398 sob pressão reduzida, para obter o composto do título (48,3
g) · [CC]25d = -104° (c = 1, clorofórmio) .
ΗΜΝ-^ (CDC13) δ: 1, 66-1,77 (1H, m) , 2, 00-2,20 (3H, m) , 2,202,38(2H,m), 2,57-2,65(1H,m), 5,65-5,75(2H,m).
Exemplo Referencial 245 (IS,4S,5S)-4-iodo-6-oxabiciclo[3.2.1]-octan-7-ona:
Adicionou-se iodo (125,4 g) a uma mistura do composto obtido no Exemplo Referencial 244 (48,0 g), cloreto de metileno (580 ml), iodeto de potássio (82,1 g) , bicarbonato de sódio (42,0 g) e água (530 ml), a uma temperatura interna de 5 °C, e a mistura resultante foi agitada à temperatura ambiente por 3 h. Depois de adicionar uma solução aquosa 1 N (800 ml) de tiossulfato de sódio à mistura da reação, a mistura resultante foi extraída com cloreto de metileno (1 1, 500 ml) . A camada orgânica resultante foi lavada com uma solução aquosa (300 ml) de bicarbonato de sódio, água (500 ml) e solução aquosa saturada de cloreto de sódio (300 ml), secada sobre sulfato de magnésio anidro, e depois concentrada. Os cristais depositados foram coletados por filtração, lavados com de 08/10/2018, pág. 407/857
399 hexano e depois secados, para obter o composto do título (89,5 g) .
Ponto de fusão (p.f.) 130-131 °C [CC]25d = -41° (c = 1, clorofórmio) .
RMN-1H (CDC13) δ: 1, 78-1, 96 (2H,m) , 2,12 (1H, dd, J=16, 5Hz, 5,2
Hz), 2,35-2,50(2H,m), 2,65-2,70 (lH,m), 2,80(1H,d,J=12,2
Hz), 4,45-4,55 (lH,m), 4,77- 4,87(1H,m).
Exemplo Referencial 246 (IS,3S,6R)-7-oxabiciclo[4.1.0]-heptano-3-carboxilato de etila:
Uma solução aquosa 2 N de hidróxido de sódio (213 ml) foi adicionada a uma suspensão do composto obtido no Exemplo Referencial 245 (89, 3 g) em etanol (810 ml), e a mistura foi agitada à temperatura ambiente por 3 h. A mistura da reação foi concentrada sob pressão reduzida em um banho de aquecimento a 35 °C, e adicionou-se água (500 ml) ao óleo resultante, para conduzir extração com cloreto de metileno (500 ml e 300 ml) . O extrato foi lavado com água (300 ml) e secado sobre sulfato de magnésio anidro e depois concentrado sob pressão reduzida. 0 óleo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 85:15), para obter o composto do
Petição 870180138821, de 08/10/2018, pág. 408/857
400 título (41,3 g).
[CC]25d = -58° (c = 1, clorofórmio) .
RMN-iH (CDC13) δ: 1,25 (3H, t, J=7,2Hz) , 1,50-1,70 (2H, m) , 1,71l,82(lH,m), 2,08-2,28 (4H,m) , 3,16(2H,s), 4, 12 (2H, q, J=7,2Hz) . Exemplo Referencial 247 (IS,3R,4R)-3-azido-4-hidróxi-ciclo-hexano-carboxilato de etila:
Uma mistura do composto obtido no Exemplo Referencial 246 (41, 0 g) , N,N-dimetil-formamida (300 ml), cloreto de amônio (19,3 g) e azida de sódio (23,5 g) foi agitada a 76 °C por 13 h. Depois disso, os insolúveis foram removidos por filtração, o filtrado foi concentrado sob pressão reduzida sem solidificar, e o produto retirado anteriormente por filtração foi adicionado ao resíduo, e a mistura foi dissolvida em água (500 ml) . A solução foi extraída com acetato de etila (500 ml e 400 ml) , e o extrato foi lavado com água e solução aquosa saturada de cloreto de sódio, secado sobre sulfato de sódio anidro, e depois concentrado, para obter o composto do título (51,5 g).
[0C]25d = +8° (c = 1, clorofórmio).
ΗΜΝ-Ή (CDC13) δ: 1,28 (3H, t, J=7, 1Hz) , 1,37-1,64 (3H, m) , 1,86de 08/10/2018, pág. 409/857
401 l,95(lH,m), 2, 04—2, 16 (1H,m) , 2,32-2,41 (1Η, rrl) , 2,44(lH,br
s), 2,68-2,78(lH,m), 3,45-3,60(2H,m), 4,17(2H,q,J=7,1Hz).
Exemplo Referencial 248 (IS,3R,4R)-3-[(t-butóxi-carbonil)-amino]-4-hidróxi-ciclohexano-carboxilato de etila:
N H
OH
Uma mistura do composto obtido no Exemplo
Referencial 247 (51,2 g) , dicarbonato de di-t-butila (68,1
g) , 5% de paládio sobre carvão (5,0 g) e acetato de etila (1.000 ml) foi agitada por toda a noite à temperatura ambiente sob uma pressão de hidrogênio (7 kg/cm2) . Um óleo obtido filtrando a mistura da reação e concentrando o filtrado foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1 —> 3:1). O produto purificado foi cristalizado em hexano, para obter o composto do título (46,9 g) . O licor-mãe foi purificado adicionalmente por cromatografia de coluna em sílica-gel (clorofórmio:metanol 100:1), para obter o composto do título (6,74 g).
[0C]25d = +25° (c = 1, clorofórmio).
ΗΜΝ-^ (CDC13) δ: 1,28 (3H, t, J=7, 1Hz) , 1, 38-1,57 (3H, m) , 1,45 (9H,s), 1, 86-1, 95 (lH,m), 2,05-2,17(1H,m), 2,29-2,39(1H,m) de 08/10/2018, pág. 410/857
402
2, 61—2, 68(1Η,m), 3,34(1H,br,s), 3, 39-3, 48 (lH,m) , 3,53-3,64 (lH,m), 4,10-4,24(2H,m), 4,54(1H,br,s).
Exemplo Referencial 249 (IS,3R,4S)-4-azido-3-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de etila:

Adicionou-se cloreto de metanossulfonila (42 ml) em gotas a uma solução contendo o composto obtido no Exemplo Referencial 248 (53, 5 g) , cloreto de metileno (500 ml) e trietil-amina (130 ml) por 20 min em uma temperatura entre 10°C e -15°C. A mistura foi aquecida até a temperatura ambiente por 2 h e agitada por 2 h. Adicionou-se ácido clorídrico 0,5 N em gotas à mistura da reação a 0 °C, para acidificá-la, e a extração foi conduzida com cloreto de metileno (500 ml e 300 ml) . A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, secada sobre sulfato de magnésio anidro e depois concentrada sob pressão reduzida. Os cristais assim obtidos foram dissolvidos em N,N-dimetil-formamida (335 ml), adicionou-se azida de sódio (60,5 g) , e a mistura foi agitada em uma temperatura entre 67 °C e 75 °C por 16 h. Depois disso, a de 08/10/2018, pág. 411/857
403 mistura da reação foi filtrada, o filtrado foi concentrado sob pressão reduzida até remover por destilação 250 ml do solvente. O resíduo foi combinado com o produto retirado anteriormente por filtração, e a mistura foi dissolvida em água (500 ml) . A solução foi extraída com acetato de etila (1 1 e 300 ml), e o extrato foi lavado com solução aquosa saturada de cloreto de sódio (400 ml e 200 ml), secado sobre sulfato de sódio anidro e depois concentrado. Os cristais assim obtidos foram purificados por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1), para obter o composto do título (18,4 g).
[CC]25d = +62° (c = 1, clorofórmio) .
ΚΜΝ-^ (CDC13) δ: 1,26 (3H, t, J=7, 1Hz) , 1,35-2,00 (15H, s) , 2,602,68 (lH,m), 3,80-3,96(2H,m), 4,15(2H,q,J=7,1Hz), 4,61(1H, br,s).
Exemplo Referencial 250 ácido (IS,3R,4S)-4-azido-3-[(t-butóxi-carbonil)-amino]ciclo-hexano-carboxílico:
Adicionou-se hidróxido de lítio (102 mg) e água (5 ml) a uma solução do composto obtido no Exemplo Referencial 249 (1, 0 g) em tetraidrofurano (25 ml). Depois de agitar de 08/10/2018, pág. 412/857
404 por 17 h, adicionou-se mais hidróxido de lítio (50 mg) , agitando a mistura por 4 h. Adicionou-se ácido clorídrico 1 N (6,3 ml) à mistura da reação, para conduzir extração com acetato de etila. Depois de secar a camada orgânica resultante, o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (980 mg). ΗΜΝ-^ (CDC13) δ: 1,30-2,20 (6H, m) , l,45(9H,s), 2,70-2, 80 (1H,
m) , 3, 94(2H,br,s), 4,73(1H,br,s) .
Exemplo Referencial 251 (IR,2S,5S)-2-azido~5-[(dimetil-amino)-carbonil]-ciclo-hexilcarbamato de t-butila:
O composto obtido no Exemplo Referencial 250 (4,77 g) foi dissolvido em cloreto de metileno (150 ml) , ao qual adicionou-se cloridrato de dimetil-amina (3,26 g), cloridrato de l-etil-3-(3-dimetil-amino-propil)-carbodiimida (4,60 g), 1-hidróxi-benzotriazol monoidratado (3,24 g) e Nmetilmorfolina (8,09 g) , e a mistura foi agitada à temperatura ambiente por 18 h. Adicionou-se uma solução aquosa saturada de bicarbonato de sódio à mistura da reação, para conduzir separação de líquidos. A camada orgânica resultante foi então secada, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi
Petição 870180138821, de 08/10/2018, pág. 413/857
405 purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:50), para obter o composto do título (4,90 g).
ΚΜΝ-Ή (CDC13) δ: 1,30-1, 90 (4H, m) , l,45(9H,s), 1,97-2,18 (2H,m), 2,75-2, 85 (lH,m) , 2,92(3H,s), 3,02(3H,s), 3,68-3,80 (lH,m), 4,05-4,20(lH,m), 4,55-4,75(1H,m).
Exemplo Referencial 252
N-{(1R,2S,5S)-2-azido-5-[(dimetil-amino)-carbonil]-ciclohexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-5carboxamida:
O composto obtido no Exemplo Referencial 251 (9,13 g) foi dissolvido em cloreto de metileno (100 ml), e adicionou-se uma solução de ácido clorídrico em etanol (100 ml), agitando a mistura à temperatura ambiente por 1 min. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo resultante foi dissolvido em N,N-dimetil-formamida (200 ml). À solução adicionou-se o composto obtido no Exemplo Referencial 10 (7,75 g) , 1-hidróxi-benzotriazol monoidratado (4,47 g) , cloridrato de 1-etil-3-(3-dimetilPclição 870180138821, de 08/10/2018, pág. 414/857
406 amino-propil)-carbodiimida (11,2 g) e trietil-amina (2,02 ml) , e a mistura foi agitada por toda a noite à temperatura ambiente. Adicionou-se mais composto obtido no Exemplo Referencial 10 (2,38 g) e cloridrato de l-etil-3-(3-dimetilamino-propil)-carbodiimida (5,60 g) , agitando a mistura por 3 dias. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3), para obter o composto do título (7,38 g).
RMN-1!!, (CDC13) δ: 1,72-1, 97 (4H, m) , 2, 10-2,27 (2H, m) , 2,51(3H,
s), 2, 77-305 (HH,m) , 3, 68 (1H, d, J=15, 4Hz) , 3,74(lH,d,J= 15,4
Hz), 3,86-3,93(lH,m), 4,54-4,60(1H,m), 7,25(1H,d,J=7,6Hz).
Exemplo Referencial 253
N-{(IR,2S,5S)-2-amino-5-[(dimetil-amino)-carbonil]-ciclohexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-5carboxamida:
de 08/10/2018, pág. 415/857
407
Adicionou-se 10% de paládio sobre carvão (6,0 g) a uma solução do composto obtido no Exemplo Referencial 252 (9,0 g) em metanol (300 ml), e a mistura foi agitada intensamente à temperatura ambiente por 11 h, sob uma pressão de hidrogênio de 4 atm. 0 catalisador foi removido por filtração, e o filtrado foi concentrado sob pressão reduzida, para obter o composto do título (7,67 g).
RMN-1H (CDC13) δ: 1,42-1,54 (1H, m) , 1, 66-1,89 (5H, m) , 2,302,40(lH,m), 2,51(3H,s), 2, 68-3, 05 (6H, m) , 2,92(3H,s), 3,00 (3H,s), 3,10-3,18(lH,m), 3,65-3,77(2H,m), 4,21-4,28(1H,m),
7,52(1H,d,J=6,1Hz).
Exemplo Referencial 254
2-(4-flúor-anilino)-2-oxoacetato de metila:
O.
O composto do título foi obtido a partir de 415 flúor-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-1!! (CDC13) δ: 3,98(3H,s), 7, 00-7, 14 (2H, m) , 7,55-7,68 (2H,m), 8,85 (1H, br, s) .
MS (ESI) m/z: 198(M+H)+.
Exemplo Referencial 255
2-(4-bromo-anilino)-2-oxoacetato de metila:
Petição 870180138821, de 08/10/2018, pág. 416/857
408
Br
Ο.
Ο composto do título foi obtido a partir de 4bromo-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-1!! (CDC13) δ: 3,98(3H,s), 7, 49 (2H, d, J=9, OHz) , 7,55(2H,d,
J=9,OHz), 8,85(1H,br,s).
MS (FAB) m/z: 258 M+.
Exemplo Referencial 256
2-(4-cloro-2-metil-anilino)-2-oxoacetato de metila:
O composto do título foi obtido a partir de 410 cloro-2-metil-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-iH (CDC13) δ: 2,31(3H,s), 3,99(3H,s), 7, 15-7,30 (2H, m) ,
7,98 (1H, d, J=8, 8Hz) , 8,77(lH,br).
MS (FAB) m/z: 228(M+H)+.
Exemplo Referencial 257
2-(4-cloro-3-metil-anilino)-2-oxoacetato de metila:
Petição 870180138821, de 08/10/2018, pág. 417/857
409
O composto do título foi obtido a partir de 4cloro-3-metil-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-1H (CDC13) δ: 2,39(3H,s), 3,98(3H,s), 7,33 (1H, d, J=12,5
Hz), 7,44(1H,dd,J=12,5, 2,5Hz), 7,53(1H,d,J=2,5Hz), 8,81(1H, br, s) .
MS(ESI) m/z: 228(M+H)+.
Exemplo Referencial 258
2-(4-cloro-2-flúor-anilino)-2-oxoacetato de metila:
O composto do título foi obtido a partir de 4cloro-2-flúor-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-iH (CDC13) δ: 3,99(3H,s), 7, 15-7,24 (2H, m) , 8,33(lH,t,
J=8,4Hz), 9, 05 (lH,br, s) .
MS (ESI) m/z: 232(M+H)+.
Exemplo Referencial 259
2-(2,4-diflúor-anilino)-2-oxoacetato de metila:
O composto do título foi obtido a partir de 2,4diflúor-anilina e cloro-oxoacetato de metila, de uma maneira
Petição 870180138821, de 08/10/2018, pág. 418/857
410 similar àquela do Exemplo Referencial 242.
RMN-XH (CDCI3) δ: 3,99(3H,s), 6, 87-7, 00 (2H, m) , 8,29-8,38 (1H,
m) , 8,99 (1H, br, s) .
MS (ESI) m/z: 215 M+.
Exemplo Referencial 260
2-(3,4-diflúor-anilino)-2-oxoacetato de metila:
O composto do título foi obtido a partir de 3,4diflúor-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-XH (CDCI3) δ: 3,98(3H,s), 7, 10-7, 28 (2H, m) , 7, 67-7,78 (1H,
m) , 8,83 (lH,br, s) .
MS (ESI) m/z: 215 M+.
Exemplo Referencial 261
2-ΟΧΟ-2-(piridin-4-il-amino)-acetato de metila:
O composto do título foi obtido a partir de 4amino-piridina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-XH (CDCI3) δ: 3,99(3H,s), 7, 58 (2H, dd, J=4,8, 1, 6Hz) , 8,60 (2H,dd,J=4,8, 1,6Hz), 9,04(1H,br,s).
Petição 870180138821, de 08/10/2018, pág. 419/857
411
Exemplo Referencial 262
2-[(5-bromo-piridin-2-il)-amino]-2-oxoacetato de metila:
composto do título foi obtido a partir de 2amino-5-bromo-piridina e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
RMN-1!! (CDC3) δ: 3,99(3H,s), 7, 87 (1H, dd, J=8, 8,2,4Hz) , 8,19 (1H,d,J=8,8Hz), 8,41(1H,d,J=2,4Hz), 9,38(1H,br,s).
MS (FAB) m/z: 259 M+.
Exemplo Referencial 263
2-[(6-cloro-piridin-3-il)-amino]-2-oxoacetato de etila:
Dissolveu-se 5-amino-2-cloro-piridina (386 mg) em N,N-dimetil-formamida (8 ml), e adicionou-se 2-etóxi-3oxoacetato de potássio (469 mg), cloridrato de l-etil-3-(3dimetil-amino-propil)-carbodiimida (863 mg) e 1-hidróxi15 benzotriazol monoidratado (203 mg), agitando a mistura à temperatura ambiente por 2 dias. Depois disso, o solvente foi removido por destilação sob pressão reduzida, adicionouse cloreto de metileno e solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir separação de
Petição 870180138821, de 08/10/2018, pág. 420/857
412 líquidos, e a camada orqanica resultante foi secada sobre sulfato de sódio anidro.
sob pressão reduzida, cromatoqrafia de coluna etila 2:1), para obter composto do título.
ΗΜΝ-^ (CDC13) δ: 1,43' 7,36(1H,d,J=8,7Hz), 8,24
2,7Hz) , 9, 03 (lH,br, s) .
Exempl
2-[ (6-cloro-piridazin-3Depois, o solvente foi concentrado o resíduo foi purificado por em sílica-qel (hexano:acetato de um resíduo (200 mq) que contém o
3H,t,J=7,2Hz), 4,44(2H,q,J=7,2Hz), (1H, dd, J=8, 7, 2,7Hz), 8,55(lH,d,J= ) Referencial 264 il)-amino]-2-oxoacetato de metila:
Dissolveu-se 3-amino-6-cloro-piridazina (516 mq) em piridina (26 ml), e adicionou-se sucessivamente trietilamina (665 μΐ) e cloro-oxoacetato de metila (441 μΐ) sob resfriamento com qelo, aqitando a mistura à temperatura ambiente por 14 h. Depois de adicionar áqua à mistura da reação, para conduzir separação de líquidos, a camada orqânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (784 mq).
RIM-1!! (CDC13) δ: 4,03(3H,s), 7, 59 (1H, d, J=9, 3Hz) , 8,52(lH,d,
J=9,3Hz), 9,88(lH,br,s).
MS (FAB) m/z: 215M+.
Petição 870180138821, de 08/10/2018, pág. 421/857
413
Exemplo Referencial 265
2-[(5-cloro-tiazol-2-il)-amino]-2-oxoacetato de metila:
composto do título foi obtido a partir de 2amino-5-cloro-tiazol e cloro-oxoacetato de metila, de uma maneira similar àquela do Exemplo Referencial 242.
ΗΜΝ-^ (CDC13) δ: 4,02(3H,s), 7,48(lH,s), 11, 03 (1H, br, s) .
MS (331) m/z: 221(M+H)+.
Exemplo Referencial 266
2-[(5-cloro-piridin-2-il)-amino]-2-oxoacetato de lítio:
-Cl
Adicionou-se áqua (5,0 ml) e hidróxido de lítio (128 mq) a uma solução do composto obtido no Exemplo Referencial 243 (1,12 q) em tetraidrofurano (20 ml) à temperatura ambiente, e a mistura foi aqitada por 5 h. O solvente foi removido por destilação sob pressão reduzida, adicionou-se hexano (30 ml) aos sólidos brancos resultantes, e a mistura foi aqitada por 30 min. Os sólidos foram coletados por filtração e depois secados, para obter o composto do título (1,02 q) .
RMN-1!! (DMSO-de) δ: 7, 90 (1H, dd, J=8, 9, 2, 6Hz) , 8,12(lH,d,
Petição 870180138821, de 08/10/2018, pág. 422/857
414
J=8,9Hz), 8,34(1H, d,J=2,6Hz), 10,18(lH,s).
Exemplo Referencial 267
2-(4-cloro-anilino)-acetato de etila:
Dissolveu-se 4-cloro-anilina (2,0 g) em 5 acetonitrila (20 ml) , e adicionou-se bromo-acetato de etila (2,1 g) e carbonato de potássio (2,2 g), agitando a mistura a 60 °C por 2 dias. A mistura da reação foi filtrada através de um leito de Celite e o filtrado foi concentrado sob pressão reduzida. O resíduo resultante foi purificado 10 por cromatografia de coluna em sílica-gel (hexano:clorofórmio 2:1), para obter o composto do título (2,3 g) .
RMN-1!! (CDC13) δ: 1,30 (3H, t, J=7,3Hz) , 3,86(2H,s), 4,24 (2H,q, J=7,3Hz), 4,26-4,35 (lH,m), 6, 53(2H,dd,J=6,6, 2,2Hz), 7,14 (2H,dd,J=6,6, 2,2Hz).
Exemplo Referencial 268
2-(4-cloro-2-flúor-anilino)-acetato de etila:
O composto do título foi obtido a partir de 4Pclição 870180138821, de 08/10/2018, pág. 423/857
415 cloro-2-flúor-anilina e bromo-acetato de etila, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 267.
ΗΜΝ-^ (CDC13) δ: 1,29 (3H, t, J=7, 3Hz) , 3,91(2H,s), 4,22 (2H,q, J=7,3Hz), 4,42-4,51 (lH,m), 6, 49 (1H, t, J=8, 8Hz) , 6,98(lH,dt,
J=8,8, 2,5Hz), 7,01(1H,dd,J=ll,3, 2,5Hz).
Exemplo Referencial 269
2-[((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]10 amino}-ciclo-hexil)-amino]-2-oxoacetato de etila:
O composto obtido no Exemplo Referencial 253 (1,5
g) foi dissolvido em N,N-dimetil-formamida (15 ml), e adicionou-se 3-etóxi-3-oxoacetato de potássio (962 mg), cloridrato de l-etil-3-(3-dimetil-amino-propil)-carbodiimida (1,18 g) e 1-hidróxi-benzotriazol monoidratado (227 mg), agitando a mistura à temperatura ambiente por 14 h. Depois disso, o solvente foi removido por destilação sob pressão reduzida, adicionou-se cloreto de metileno e solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi
Petição 870180138821, de 08/10/2018, pág. 424/857
416 removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3), para obter o composto do título (1,13 g).
ΗΜΝ-^ (CDC13) δ: 1,37 (3H, t, J=7,1Hz) , 1,55-2, IS (6H, m) , 2,52 (3H,s), 2,77-2,89 (3H,m) , 2, 94 (5H, br, s) , 3,06(3H,s), 3,71 (1H,d,J=15,5Hz), 3,73(1H,d,J=15,5Hz), 4,06-4,13(1H,m), 4,32 (2H,q,J=7,ll-{z), 4,60-4,63(1H,m), 7,39(1H,d,J=8,3Hz), 7,83 (1H,d,J=7,6Hz).
MS (ESI) m/z: 466(M+H)+.
Exemplo Referencial 270
2-[((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-amino]-2-oxoacetato de lítio:
O composto obtido no Exemplo Referencial 269 (1,13
g) foi dissolvido em tetraidrofurano (20 ml), metanol (10 ml) e água (10 ml), e adicionou-se hidróxido de lítio (58 mg), agitando a mistura à temperatura ambiente por 30 min. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (1,10 g).
RMN-1!! (DMSO-de) δ: 1,41-1,73 (4H, m) , 2, 00-2, 07 (2H, m) , 2,39
Petição 870180138821, de 08/10/2018, pág. 425/857
417 (3H,s), 2, 74-2, 99 (HH,m) , 3,67(2H,s), 3, 82-3, 88 (1H, m) , 4,284,30(lH,m), 8, 66-8,70 (2H,m) .
Exemplo Referencial 271
N-{(1R,2S,5S)-2-azido~5-[(dimetil-amino)-carbonil]-ciclo5 hexil}-5-metil-5,6-diidro-4H-pirrolo[3,4-d]-tiazolo-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 293 e do composto obtido no Exemplo Referencial 251, de uma maneira similar àquela do processo descrito no Exemplo Referencial 252.
ΚΜΝ-^ (CDC13) δ: 1, 73-1,87 (4H, m) , 2, 11-2,20 (2H, m) , 2,67 (3H,s), 2,85-2, 90 (lH,m) , 2,93(3H,s), 3,00(3H,s), 3,90-4,10 (5H,m), 4,57-4,62(lH,m), 7,20-7,22(1H,m).
MS (FAB) m/z: 378(M+H)+.
Exemplo Referencial 272
N-{(IR,2S,5S)-2-amino-5-[(dimetil-amino)-carbonil]-ciclohexil} -5-metil-5,6-diidro-4H-pirrolo[3,4-d]-tiazolo-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 426/857
418
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 271, de uma maneira similar àquela do processo descrito no Exemplo Referencial
253.
RMN-1!! (CDC13) δ: 1, 67-1, 97 (6H, m) , 2,36-2, 40 (1H, m) , 2,67 (3H,s), 2,92(3H,s), 3,00(3H,s), 3, 07-3, 18 (1H, m) , 3,92-3,95 (2H,m), 4,02-4,06(2H,m), 4,23-4,26(1H,m), 7,50-7,52(1H,m).
Exemplo Referencial 273
5-cloro-4-flúor-indol-2-carboxilato de metila:
Adicionou-se etanol (100 ml) a hidreto de sódio (teor: 60%, 4,7 g) a 0 °C sob uma atmosfera de argônio, e a mistura foi agitada por 10 min. Depois disso, adicionou-se 2-nitro-propano (11 ml) à mistura da reação, agitando a mistura por 10 min, adicionou-se 1-(bromo-metil)-3-cloro-215 flúor-benzeno (10 g), agitando a mistura resultante à temperatura ambiente por 3,5 h. O precipitado foi removido por filtração, e o filtrado foi concentrado sob pressão
Petição 870180138821, de 08/10/2018, pág. 427/857
419 pressão reduzida, cromatografia de reduzida. O resíduo foi fracionado entre dietil-éter e água, e uma camada orgânica foi lavada sucessivamente com uma solução aquosa 1 N de hidróxido de sódio, água e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob e o resíduo foi purificado por coluna em sílica-gel (acetato de etila:hexano 3:7), para obter 3-cloro-2-flúor-benzaldeído (5,5 g) , como um óleo amarelo-pálido. Adicionou-se metanol (20 ml) a hidreto de sódio (teor: 60%, 1,6 g) a 0 °C sob uma atmosfera de argônio, e a mistura foi agitada por 10 min. A mistura da reação foi resfriada até -20 °C, e o 3-cloro-2flúor-benzaldeído (5,5 g) bruto e uma solução de 2-azidoacetato de metila (5,0 g) em metanol (10 ml) foram adicionados dentro de 20 min. A temperatura da mistura da reação foi elevada para 0 °C, e depois disso, a mistura foi agitada por 2,5 h, e adicionou-se água a ela. A mistura da reação foi concentrada sob pressão reduzida, o resíduo foi extraído com um solvente misto de cloreto de metileno e acetato de etila. O extrato foi lavado com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (tolueno:hexano 3:17), para obter 2azido-3-[(cloro-2-flúor)-fenil]-acrilato de metila (2,6 g) . Este produto foi dissolvido em xileno (50 ml) , e a solução foi agitada em uma temperatura entre 130 °C e 140 °C por 3 h. A mistura da reação foi concentrada e o resíduo de 08/10/2018, pág. 428/857
420 resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno) e depois cristalizado em dietil-éter/hexano, para obter o composto do título (440 mg) .
ΗΜΝ-^ (DMSO-d6) δ: 4,08(3H,s), 7,20(lH,s), 7,31-7,38 (2H, m) . MS (FAB) m/z: 228(M+H)+.
Exemplo Referencial 274 ácido 5-cloro-4-flúor-indol-2-carboxílico:
O composto obtido no Exemplo Referencial 273 (440 mg) foi dissolvido em tetraidrofurano (10 ml), adicionou-se uma solução aquosa (5 ml) dc hidróxido dc lítio (160 mg), c a mistura foi agitada à temperatura ambiente por 4 h. Depois disso, adicionou-se mais uma solução aquosa (5 ml) de hidróxido de lítio (240 mg) à mistura da reação, a mistura foi agitada por mais 1 h, e a mistura da reação foi concentrada sob pressão reduzida. O resíduo foi neutralizado com ácido clorídrico 1 N e extraído 3 vezes com acetato de etila. As camadas orgânicas resultantes foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio e secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (390 mg).
RMN-1!! (DMSO-de) δ: 6,79(lH,s), 7, 16-7,26 (2H,m) .
de 08/10/2018, pág. 429/857
421
MS (FAB) m/z: 214(M+H)+.
Exemplo Referencial 275 l-benzil-5-cloro-indol-2-carboxilato de etila:
Dissolveu-se 5-cloro-indol-2-carboxilato de etila (1,4 g) em N,N-dimetil-formamida (30 ml), e adicionou-se carbonato de potássio (2,9 g) e cloreto de benzila (2,4 ml). A mistura foi aquecida até e agitada por 1,5 h sobre um banho de aquecimento controlado a 100 °C. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi vertido sobre gelo/água e extraído com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:19) e cristalizado em dietil-éter/hexano, para obter o composto do título (1,6 g) .
EMN-^ (CDC3) δ: 1,36 (3H, t, J=7,1Hz) , 4,33 (2H, q, J=7, 1Hz) ,
5,83(2H,s), 7, 00-7, 02 (2H,d) , 7,20-7,38 ( 6H, m) , 7,67(lH,d,
J=l,7Hz) .
Exemplo Referencial 276 l-benzil-5-cloro-3-flúor-indol-2-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 430/857
422
Cl
F
COOEt
Adicionou-se triflato de 1-flúor-2,6-dicloropiridínio (4,4 g) a uma solução do composto obtido no Exemplo Referencial 275 (2,2 g) em cloreto de metileno (30 ml), e a mistura foi aquecida sob refluxo por 3 dias. A mistura da reação foi fracionada entre dietil-éter e água, e uma camada aquosa foi extraída com acetato de etila. As camadas orgânicas resultantes foram combinadas, lavadas sucessivamente com ácido clorídrico 1 N, água e solução aquosa saturada de cloreto de sódio, e depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:24), para obter o composto do título bruto (2,8 g). Uma parte deste produto foi purificada por cromatografia preparatória de fina camada em sílica-gel, para obter o composto do título.
RMN-1H (DMSO-ds) δ: 1,25 (3H, t, J=7 , 1Hz) , 4,29 (2H, q, J=7,1Hz)
9,0, 2,1Hz), 7,69(1H,dd,J=9,0, 2,1Hz), 7,78(1H,d,J=2,1Hz).
Exemplo Referencial 277
5-cloro-3-flúor-indol-2-carboxilato de etila:
Cl
V—COOEt
Petição 870180138821, de 08/10/2018, pág. 431/857
423
O composto bruto (1,4 g) obtido no Exemplo Referencial 276 foi dissolvido em anisol (30 ml), e adicionou-se parceladamente cloreto de alumínio (2, 9 g) à solução sob resfriamento com gelo. A mistura da reação foi agitada à temperatura ambiente por 30 min, e adicionou-se mais cloreto de alumínio (2,9 g), agitando a mistura por 18 h. Adicionou-se cloreto de alumínio (8,0 g) à mistura da reação, e a mistura foi agitada por 5 h, à qual adicionou-se água. A mistura da reação foi extraída com acetato de etila, as camadas orgânicas resultantes foram lavadas sucessivamente com solução aquosa saturada de bicarbonato de sódio de solução aquosa saturada de cloreto de sódio, e depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno), para obter o composto do título (470 mg).
RMN-1!! (CDC3) δ: 1,43 (3H, t, J=7,2Hz ) , 4 , 45 (2H, q, J=7,2Hz) ,
7,25—7,31(2H,m), 7,66(1H,d,J=0,73Hz), 8,53(1H,br,s).
MS (FAB) m/z: 242(M+H)+.
Exemplo Referencial 278 ácido 5-cloro-3-flúor-indol-2-carboxílico:
COOH
O composto do título foi obtido a partir do de 08/10/2018, pág. 432/857
424 composto obtido no Exemplo Referencial 277, de uma maneira similar àquela do Exemplo Referencial 274.
RMN-iH (DMSO-de) δ: 7,31 (1H, dd, J=8, 8, 1,9Hz), 7,42(lH,dd,
J=8,8, 1,9Hz), 7,70 (1H, d, J=l, 9Hz) , ll,78(lH,s).
MS (FAB) m/z: 214(M+H)+.
Exemplo Referencial 279 (1R,2S,5S)~{[(5-cloro-3-flúor-indol-2-il)-carbonil]-amino}5-[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de tbutila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e do composto obtido no Exemplo Referencial 278, de uma maneira similar àquela do Exemplo Referencial 97.
ΗΜΝ-^ (CDC3) δ: l,45(9H,s), 1,73-2,11 (6H,m) , 2, 65 (1H, br, s) ,
2, 96(3H,s), 3,07(3H,s), 4,20 (1H, br, s) , 4,28 (1H, br, s) , 4,78 (lH,br) , 7,23-7,30 (3H,m) , 7,58(lH,s), 9,03(lH,s).
MS (FAB) m/z: 481(M+H)+.
Exemplo Referencial 280
3-bromo-5-cloro-indol-2-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 433/857
425
Br
Cl
O^coce.
Η
Adicionou-se N-bromo-succinimida (440 mg) a uma solução de 5-cloro-indol-2-carboxilato de etila (500 ml) em N,N-dimetil-formamida (10 ml). A mistura da reação foi agitada à temperatura ambiente por 18 h, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi fracionado entre acetato de etila e água, e uma camada aquosa foi extraída com acetato de etila. As camadas orgânicas resultantes foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio e depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:9), e o pó branco assim obtido foi lavada com hexano, para obte ro composto do título (680 mg).
RMN-!H (CDC3) δ: 1,42-1,48 (3H, m) , 4,43-4,49 (2H, m) , 7,30-7,32 (2H,m), 7, 65 (1H, d, J=0, 74Hz) , 9,ll(lH,s).
MS (FAB) m/z: 303(M+H)+.
Exemplo Referencial 281 ácido 3-bromo-5-cloro-indol-2-carboxílico:
COOH
Petição 870180138821, de 08/10/2018, pág. 434/857
426 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 280, de uma maneira similar àquela do Exemplo Referencial 274.
RMN-1H (DMSO-de) δ: 7,35 (1H, dd, J=8, 8, 2,OHz), 7,4 8-7,53 (2H,
m), 12,33 (1H,s) .
MS (FAB) m/z: 275(M+H)+.
Exemplo Referencial 282 (lR,2S,5S)-2-{[(3-bromo-5-cloro-indol-2-il)-carbonil]amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e do composto obtido no Exemplo Referencial 281, de uma maneira similar àquela do Exemplo Referencial 97.
ΕΜΝ^Η (CDC3) δ: l,42(9H,s), 1,58-2, 17 (6H, m) , 2,70 (1H, br, s) ,
2,96(3H,s), 3,07(3H,s), 4,23-4,28 (2H, m) , 4,83(lH,br), 7,347,41(3H,m), 7,52(lH,s), 9,76(lH,s).
MS (FAB) m/z: 542(M+H)+.
Exemplo Referencial 283
3-cloro-5-flúor-indol-2-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 435/857
427
Cl
Dissolveu-se 5-flúor-indol-2-carboxilato de etila (2,0 g) em N,N-dimetil-formamida (20 ml), e adicionou-se uma solução de N-cloro-succinimida (1,4 g) em N,N-dimetilformamida (10 ml) em gotas à solução. A mistura foi agitada à temperatura ambiente por 18 h, e a mistura da reação foi diluída com acetato de etila e lavada sucessivamente com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa satura de cloreto de sódio. A camada orgânica resultante foi então secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 5:1), para obter o composto do título (1,9 g).
RMN-!H (CDC3) δ: 1, 45 (, 3H, t, J=7, 4Hz) , 4,46 (2H, q, J=7, 4Hz) ,
7,14 (lH,dt,J=8,0,2,7Hz) , 7,32-7,36 (2H, m) , 8,91(lH,br).
Exemplo Referencial 284 ácido 3-cloro-5-cloro-indol-2-carboxílico:
Cl
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 283, de uma maneira
Petição 870180138821, de 08/10/2018, pág. 436/857
428 similar àquela do Exemplo Referencial 274.
RMN-iH (DMSO-de) δ: 7,20 (1H, dt, J=8,8, 2,4Hz), 7,31(lH,dd,
J=8,8,2,4HZ) , 7,46(1H,dd,J=8,8, 4,4Hz), 12, 12(lH,br).
Exemplo Referencial 285
5-cloro-3-formil-indol-2-carboxilato de etila:
Depois de adicionar oxicloreto de fósforo (2,0 ml) a N-metil-formanilida (2,9 g) , e a mistura ser agitada por 15 min, adicionou-se 1,2-dicloro-etano (50 ml) e 5-cloroindol-2-carboxilato de etila (4,0 g) , a mistura resultante foi aquecida sob refluxo por 1 h. A mistura da reação foi vertida sobre uma solução aquosa (28 ml) de acetato de sódio (14 g) sob resfriamento com gelo. Depois de agitar por 18 h, os insolúveis foram coletados por filtração. Este produto foi lavado sucessivamente com água e dietil-éter, para obter o composto do título (3,56 g).
RMN-1!! (DMSO-de) δ: 1, 38 (3H, t, J=7, 1Hz) , 4,44 (2H, q, J=7, 1Hz) ,
7,38 (1H,dd,J=8,0, 1,4Hz), 7,56(1H,d,J=8,OHz), 8,19(lH,d,
J=l,4HZ), 10,53 (1H,s) .
Exemplo Referencial 286 ácido 5-cloro-3-formil-indol-2-carboxílico:
Petição 870180138821, de 08/10/2018, pág. 437/857
429
O composto obtido no Exemplo Referencial 285 (1,0
g) foi dissolvido em etanol (10 ml), adicionou-se uma solução aquosa 1 N de hidróxido de sódio (10 ml) em gotas, agitando a mistura a 50 °C por 2 h. Adicionou-se ácido clorídrico 1 N (11 ml) à mistura da reação, a mistura da reação foi agitada, e os insolúveis foram coletados por filtração, para obter o composto do título (0,86 g).
RMN-1H (DMSO-de) δ: 7,39 (1H, d, J=8, OHz) , 7,55 (1H, d, J=8, OHz) ,
8,20(lH,s), 10,58(lH,s), 12, 90 (1H, br) .
Exemplo Referencial 287 ácido 5-cloro-3-etóxi-carbonil-indol-3-carboxílico:
O composto obtido no Exemplo Referencial 286 (1,5
g) e ácido sulfâmico (1,7 g) foram dissolvidos em uma
|
mistura |
de |
t-butanol |
(30 ml) e água |
(30 ml) , e adicionou-se |
|
clorito |
de |
sódio (1 |
,6 g) , agitando |
a mistura por 8 h. |
A |
|
mistura |
da |
reação |
foi diluída com |
água e extraída |
com |
|
acetato |
de |
etila, e |
o extrato foi lavado sucessivamente |
com |
ácido clorídrico 1 N e solução aquosa saturada de cloreto de sódio, e secado sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi recristalizado em um solvente misto de éter isopropílico e hexano, para obter o composto do título (0,7 de 08/10/2018, pág. 438/857
430
RMN-XH (DMSO—dô) δ: 1,34(3H,t,J=7,1Hz), 4,38(2H,q,J=7,1Hz),
7,33(1H,dd,J=8,0, 1,4Hz), 7, 52 (1H, d, J=8, OHz) , 7,97(lH,d,J=
1,4Hz) , 12,75 (lH,br) .
Exemplo Referencial 288
5-cloro-3-[(dimetil-amino)-carbonil]-indol-2-carboxilato de etila:
CONMe.
COOEt
O composto obtido no Exemplo Referencial 287 (0,7
g) foi dissolvido em N,N-dimetil-formamida (10 ml), e adicionou-se cloridrato de dimetil-amina (0,26 g) , ΙΙΟ hidróxi-benzotriazol monoidratado (0,43 g) e cloridrato de l-etil-3-(3-dimetil-amino-propil)-carbodiimida (1,0 g), agitando a mistura à temperatura ambiente por 2 dias. Depois de diluir a mistura da reação com acetato de etila e lavar com ácido clorídrico 1 N, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e solução aquosa satura de cloreto de sódio, nesta ordem, e a camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi recristalizado em um solvente misto de éter isopropílico e hexano, para obter o composto do título (0,6
g) ·
RMN-XH (DMSO-de) δ: 1,29 (3H, t, J=7, 1Hz) , 2,78(3H,s), 3,04 (3H,s), 4,30(2H,q,J=7,1Hz), 7,31(1H,dd,J=8,0, 1,4Hz), 7,45
Petição 870180138821, de 08/10/2018, pág. 439/857
431 (1Η,d,J=1,4Ηζ), 7,48(1H,d,J=8,OHz), 12,29(lH,s).
Exemplo Referencial 289 ácido 5-cloro-3-[(dimetil-amino)-carbonil]-indol-2carboxílico:
CONMe.
COOH
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 288, de uma maneira similar àquela do Exemplo Referencial 286.
RMN-íH (DMSO-dg) δ: 2,91(6H,s), 7, 29 (1H, d, J=8, OHz) , 7,44(1H, d,J=8,OHz), 7,47(lH,s), 12,16(lH,s).
Exemplo Referencial 290
5-(fenil-sulfonil)-5,6-diidro-4H-pirrolo[3,4-d]-tiazol:
Dissolveu-se benzenossulfonamida (683 mg) e 4,5bis-(bromo-metil)-tiazol (M. Al. Hariri, O. Galley, F. Pautet, H. Fillion, Eur. J. Org. Chem. 593-594, 1998) (1,10
g) em N,N-dimetil-formamida (10 ml), adicionou-se hidreto de sódio (60% em óleo, 357 mg) de uma só vez, e a mistura foi agitada à temperatura ambiente por 3 h. Adicionou-se água e cloreto de metileno, para conduzir separação de líquidos.
Petição 870180138821, de 08/10/2018, pág. 440/857
432
Depois disso, a camada orgânica resultante foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:acetato de etila
9:1), para obter o composto do título (137 mg).
βΜΝ-^ (CDC3) δ: 4, 60-4, 63 (2H, m) , 4,70-4,73 (2H, m) , 7,527,64(3H,m), 7,88-7, 92 (2H, m) , 8,71(lH,s).
MS (FAB) m/z: 267(M+H)+.
Exemplo Referencial 291 dibromidrato de 5,6-diidro-4H-pirrolo[3,4-d]-tiazol:
Uma mistura do composto obtido no Exemplo Referencial 290 (800 mg) , fenol (800 μΐ) e ácido bromídrico a 47% (5,00 ml) foi aquecida sob refluxo por 2 h. Depois disso, a mistura da reação foi resfriada até a temperatura ambiente, adicionou-se acetato de etila e água, para conduzir separação de líquidos. A camada aquosa resultante foi concentrada sob pressão reduzida. Adicionou-se acetato de etila ao resíduo, o procipitado foi coletado por filtração, para obter o composto do título (521 mg).
RMN-1!! (DMSO—dô) δ: 4,42 (2H, br, s) , 4,56 (2H, br, s) , 9,14(lH,s).
MS (FAB) m/z: 127(M+H)+.
Exemplo Referencial 292 5-metil-5,6-diidro-4H-pirrolo[3,4-d]-tiazol:
Petição 870180138821, de 08/10/2018, pág. 441/857
433
Ο composto do título foi obtido a partir do composto obtido no Exemplo Referencial 291, de uma maneira similar àquela do Exemplo Referencial 9.
RMN-1!! (CDC13) δ: 2,67(3H,s), 3, 95-3, 99 (2H, m) , 4,01-4, 05 (2H,
m) , 8,69 (1H, s) .
MS (ESI) m/z: 141 (M+H)+.
Exemplo Referencial 293
5-metil-5,6-diidro-4H-pirrolo[3,4-d]-tiazol-2-carboxilato de lítio:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 292, de uma maneira similar àquela do Exemplo Referencial 5.
ΗΜΝ-^ (DMSO-de) δ: 2,52(3H,s), 3, 73 (2H, t, J=3,2Hz) , 3, 87 (2H, t,J=3,2Hz).
Exemplo Referencial 294 (IR,2S,5S)-2-[(6-cloro-2-naftoil)-amino]-5-[(dimetil-amino)carbonil]-ciclo-hexil-carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 442/857
434
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e ácido 6-cloronaftaleno-2-carboxílico (Eur. J. Chem-Chi. Ther. 19:205-214, 1984), de uma maneira similar àquela do Exemplo Referencial
97.
RMN-1!! (CDC13) δ: 1,30-2,00 (15H, m) , 2, 60-2,80 (1H, m) , 2,96(3H, s), 3,09(3H,s), 4, 00-4,20(lH,m) , 4,20-4,30(1H,m), 4,75-4,95 (lH,m), 7,44 (lH,d, J=9,OHz) , 7,70-7, 95 (5H, m) , 8,31(lH,s).
MS (FAB) m/z: 474(M+H)+.
Exemplo Referencial 295 (E)-3-(morfolin-4-il)-2-acrilato de etila:
N^^^OEt
Dissolveu-se propionato de etila (2,0 ml) em cloreto de metileno (20 ml), e adicionou-se morfolina em gotas sob resfriamento com gelo. Depois de agitar à temperatura ambiente por 1 h, a mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1), para obter o composto do título
Petição 870180138821, de 08/10/2018, pág. 443/857
435 (3,72 g) .
RMN-iH (CDCI3) δ: 1, 26 (3H, t, J=7, 1Hz) , 3, 21(4H,t,J=5,1Hz),
3,71(4H,t,J=5,1Hz), 4,14(2H,q,J=7,1Hz), 4,70(1H, d, J=13, 4Hz) , 7,36(1H,d,J=13,4Hz).
MS (FAB) m/z: 186(M+H)+.
Exemplo Referencial 296 tetraflúor-borato de 3-cloro-benzeno-diazônio
Dissolveu-se 3-cloro-anilina (2,0 g) em um solvente misto de água (30 ml) e ácido clorídrico concentrado (3,5 ml), e adicionou-se nitrito de sódio (1,30 g) sob resfriamento com gelo, agitando a mistura por 10 min. Depois disso, adicionou-se ácido clorídrico concentrado (5,3 ml) e tetraflúor-borato de sódio (6,90 g) à mistura da reação, agitando a mistura por 30 min sob resfriamento com gelo, o precipitado foi coletado por filtração e lavado com água, adicionou-se metanol e dietil-éter, para obter o composto do título (2,63 g) . Este composto foi usado na próxima reação como ele estava.
Exemplo Referencial 297
7-cloro-cinolino-3-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 444/857
436
O composto obtido no Exemplo Referencial 295 (1,45 g) foi dissolvido em acetonitrila (100 ml), e o composto obtido no Exemplo Referencial 296 foi adicionado. Depois de agitar à temperatura ambiente por 1 h, a mistura foi aquecida sob refluxo por 7 dias. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno —> cloreto de metileno:acetato de etila
10:1, e depois hexano:acetato de etila 4:1 —> 1:1), para obter o composto do título (0,25 g).
RMN-1H (CDC13) δ: 1,53 (3H, t, J=7,1Hz) , 4,62 (2H, q, J=7, 1Hz) ,
7,80(1H,dd,J=8,8, 2,OHz), 7,95(1H,d,J=8,8Hz), 8,64(lH,s),
8,68(1H,d,J=2,0Hz)
Exemplo Referencial 298 ácido 7-cloro-cinolino-3-carboxílico:
Cl
COOH
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 297, de uma maneira similar àquela do Exemplo Referencial 286.
RMIS!-^ (DMSO-de) δ: 8, 02 (1H, dd, J=8,8, 2,OHz), 8,34(lH,d,J=
8, 8Hz), 8,70(lH,s), 8,90(lH,s).
MS (FAB) m/z: 209(M+H)+.
Exemplo Referencial 299 (lR,2S,5S)-2-{[(7-cloro-cinolin-3-il)-carbonil]-amino}-5[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de tPclição 870180138821, de 08/10/2018, pág. 445/857
437 butila:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e do composto obtido no Exemplo Referencial 298, de uma maneira similar àquela do Exemplo Referencial 97.
RMN-1H (CDC3) δ: l,36(9H,s), 1,80-2, 20 (5H, m) , 2,72(lH,m),
2,96(3H,s), 3,07(3H,s), 3, 49(1H,d,J=3,7Hz), 4,30-4,45 (2H, m) , 4,87 (lH,br), 7,77(1H,dd,J=8,8, 2,OHz), 7, 96(1H,d,J=8,8Hz),
8, 59 (2H,br) , 8,72 (1H, s) .
MS (FAB) m/z: 476(M+H)+.
Exemplo Referencial 300 (lR,2S,5S)-2-{[(5-ΙΗ-benzimidazol-2-i1)-carbonil]-amino} - 5[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de tbutila:
Petição 870180138821, de 08/10/2018, pág. 446/857
438
Adicionou-se 10% de paládio sobre carvão (50 mg) a uma solução do composto obtido no Exemplo Referencial 143 (235 mg) em tetraidrofurano (5,0 ml), e a mistura foi agitada por toda a noite à temperatura ambiente sob uma atmosfera de hidrogênio. Adicionou-se a uma solução do produto obtido filtrando a mistura da reação, e concentrando o filtrado, ácido 5-cloro-benzimidazol-2-carboxílico (Bull. Chem. Soc. Jpn. 62:2668, 1989) (165 mg) em N,N-dimetilformamida (5,0 ml) e 1-hidróxi-benzotriazol monoidratado (100 mg) e cloridrato de l-etil-3-(3-dimetil-amino-propil)carbodiimida (171 mg) à temperatura ambiente, e a mistura foi agitada por 4 dias. Depois de concentrar a mistura da reação, adicionou-se cloreto de metileno, uma solução aquosa saturada de bicarbonato de sódio e água, para conduzir separação de líquidos, e a camada aquosa resultante foi extraída com cloreto de metileno. Depois de combinar as camadas orgânicas e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 10:1), para obter o composto do título (250 mg).
RMN-!H (DMSO-de) δ: 1,01-2,00 ( 6H, m) , l,34(9H,s),
2,79 (3H, s) , 2,80-2, 95 (lH,m), 2,98(3H,s), 3, 89-4,06 (2H,m) ,
7,08 (lH,d,J= 6, 6Hz), 7,31 (1H, d, J=8, 5Hz) , 7, 62 (2H, br, s) ,
8,47 (lH,d, J=8,5 Hz) , 13, 46 (1H, br, s) .
MS(ESI) m/z: 466(M+H)+.
de 08/10/2018, pág. 447/857
439
Exemplo Referencial 301
3-(4-flúor-fenil)-2-{[(4-metil-fenil)-sulfonil]-amino}propionato de metila:
Dissolveu-se 2-amino-3-(4-flúor-fenil)-propionato 5 de metila (2,01 g) , cloreto de p-tolueno-sulfonila (2,25 g) e 4-dimetil-amino-piridina (309 mg) em clorofórmio (30 ml) , e adicionou-se piridina (3,0 ml), aquecendo a mistura sob refluxo por 4,5 h. Adicionou-se mais cloreto de p-toluenosulfonila (2,20 g), e a mistura foi aquecida sob refluxo por
3,5 h. A mistura da reação foi vertida sobre gelo e ácido clorídrico 1 N (17 ml), para conduzir separação de líquidos. A camada orgânica resultante foi lavada sucessivamente com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 9:1 —> 2:1), para obter o composto do título (2,89 g) . RMN-1H (CDC3) δ: 2,41(3H,s), 2, 90-3, 10 (2H, m) , 3,51(3H,s),
4,10-4,20(lH,m), 5,04(1H,d,J=9,OHz), 6,85-6,95(2H,m), 7,007,10(2H,m), 720-7,30 (2H,m) , 7, 60-7,70 (2H, m) .
MS (331) m/z: 352(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 448/857
440
Exemplo Referencial 302 7-flúor-2-[(4-metil-fenil)-sulfonil]-l,2,3,4tetraidroisoquinolino-3-carboxilato de metila:
.Ts
COOMe
O composto obtido no Exemplo Referencial 301 (1,50 g) e paraformaldeído (207 mg) foram dissolvidos em clorofórmio (40 ml), e o sistema foi purgado com argônio. Depois, adicionou-se complexo de triflúor-borano/dietil-éter (1,20 ml), e a mistura foi agitada à temperatura ambiente por 7,5 h. A mistura da reação foi vertida sobre gelo e uma solução aquosa saturada de bicarbonato de sódio, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (1,45 g).
RMN-1!! (CDC13) δ: 2,42(3H,s), 3, 15 (2H, d, J=3, 9Hz) , 3,46(3H,
s), 4,45 (1H,d,J=15,9Hz) , 4,69 (1H,d,J=15,9Hz) , 5,01(lH,t,
J=4,4Hz), 6, 70-6, 80 (lH,m) , 6, 80-6, 90 (1H, m) , 7,00- 7,1O(1H,
m) , 7,29(2H,d,J=8,1Hz), 7,72(2H,d,J=8,3Hz) .
MS (331) m/z: 364(M+H)+.
Exemplo Referencial 303
7-flúor-isoquinolino-3-carboxilato de metila:
de 08/10/2018, pág. 449/857
441
O composto obtido no Exemplo Referencial 302 (1,45
COOMe
g) foi dissolvido em N,N-dimetil-formamida (40 ml). Introduziu-se oxigênio nesta solução, e a solução foi agitada a 100 °C por 3,5 h. Depois disso, a mistura da reação foi concentrada sob pressão reduzida, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos, a camada orgânica resultante foi lavada sucessivamente com uma solução aquosa de ácido cítrico a 10% e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. 0 solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 1:1), para obter o composto do título (0,59 g).
ΗΜΝ-^ (CDC3) δ: 4,07(3H,s), 7, 55-7, 65 (1H, m) , 7, 65-7,75 (1H,
m) , 8,00-8,05 (lH,m) , 8,61(lH,s), 9,30(lH,s).
MS (ESI) m/z: 206(M+H)+.
Exemplo Referencial 304 cloridrato do ácido 7-flúor-isoquinolino-3-carboxílico:
COOH
O composto obtido no Exemplo Referencial 303 (1,45
g) foi dissolvido em ácido clorídrico concentrado (18 ml), e de 08/10/2018, pág. 450/857
442 a solução foi aquecida sob refluxo por 2,5 h. A mistura da reação foi resfriada, e os cristais foram coletados por filtração, lavados com água e depois secados, para obter o composto do título (0,46 g).
ΗΜΝ-Ή (DMSO-de) δ: 7, 90-8, 00 (lH,m) , 8, 15-8,25 (1H, m) , 8,408,50(lH,m), 8,82(lH,s), 9,55(lH,s).
MS (FAB) m/z: 192(M+H)+.
Exemplo Referencial 305
7-cloro-2H-cromeno-3-carboxilato de etila:
Dissolveu-se 4-cloro-2-hidróxi-benzaldeído (Acta Chem. Scand. 53:258, 1999) (510 mg) em tetraidrofurano (40 ml), adicionou-se hidreto de sódio (60% em óleo, 157 mg), e a mistura foi agitada à temperatura ambiente por 2 h. Uma solução de 2-dietil-fosfono-acrilato de etila (<7. Org. Chem. 43:1256, 1978) (769 mg) em tetraidrofurano (10 ml) foi adicionada à mistura da reação, e a mistura resultante foi agitada à temperatura ambiente por 2 h, e depois aquecida por toda a noite sob refluxo. Depois de resfriar a mistura da reação até a temperatura ambiente, adicionou-se água e dietil-éter, para conduzir separação de líquidos. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 10:1), para de 08/10/2018, pág. 451/857
443 obter o composto do título (247 mg).
RMN-1H (DMSO-de) δ: 1,33(3H,t,J=7,1Hz), 4,27 (2H, q, J=7, 1Hz) ,
4,99(2H,d,J=1,2Hz), 6, 85(1H, d,J=l,2Hz), 6, 89(1H, dd,J=8,1, 2,OHz), 7,04(1H,d,J=8,1Hz), 7,38 (1H,d,J=l,OHz).
MS (EI) m/z: 238 (M+) .
Exemplo Referencial 306 ácido 7-cloro-2H-cromeno-3-carboxílico:
Cl
COOH
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 305, de uma maneira similar àquela do Exemplo Referencial 274.
RMN-íH (DMSO-ds) δ: 4,92 (1H, d, J=2 , OHz) , 6, 95 (1H, d, J=2, OHz) ,
7,01 (III, dd, J=8, 1, 2,2llz), 7,35 (III, d, J=8, lllz) , 7,44(111,s).
MS (EI) m/z: 210 M+.
Exemplo Referencial 307 (lR,2S,5S)-2-{[((E)-3-(4-cloro-fenil)-2-propenoil]-amino} - 5[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de tbutila:
Petição 870180138821, de 08/10/2018, pág. 452/857
444 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e ácido 4-clorocinâmico, de uma maneira similar àquela do Exemplo
Referencial 97.
RMN-1H (CDC3) δ: 1,30-1,55 (3H, m) , l,48(9H,s), 1,60-2,30 (4H,m), 2,57-2, 70 (lH,m) , 2,95(3H,s), 3,06(3H,s), 4,01(lH,br
s), 4, 10-4,20 (lH,m) , 4,78(1H,br,s), 6, 30(1H, d,J=15,6Hz),
7,02(lH,s), 7,31(2H,d,J=8,5 Hz), 7, 40(2H, d,J=8,5Hz), 7,52 (1H,d,J=15,6Hz).
MS (ESI)m/z: 450(M+H)+.
Exemplo Referencial 308
6-cloro-4-oxo-l,4-diidroquinolino-2-carboxilato de metila:
Adicionou-se acetileno-dicarboxilato de dimetila (13,5 ml) a uma solução de 4-cloro-anilina (12,76 g) em metanol (150 ml), e a mistura foi aquecida sob refluxo por 8 h. A mistura da reação foi concentrada sob pressão reduzida, o resíduo foi dissolvido em difenil-éter (70 ml), e a solução foi aquecida sob refluxo a 240 °C por 4 h. Depois de resfriar a mistura da reação, um solvente misto de hexano e dietil-éter foi adicionado, e os cristais depositados foram coletados por filtração e lavados, para obter o composto do título (11,09 g).
RMN-!H (DMSO-de) δ: 3,97(3H,s), 7,76 (1H, dd, J=9, 0, 2,5Hz),
Petição 870180138821, de 08/10/2018, pág. 453/857
445
7,90-8,05(2H,m), 12,28(1H,br,s).
MS (331) m/z: 238(M+H)+.
Exemplo Referencial 309 ácido 6-cloro-4-oxo-l,4-diidroquinolino-2-carboxílico:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 308, de uma maneira similar àquela do Exemplo Referencial 286.
RMN-1!! (DMSO-dg) δ: 6, 90-7,05 (1H, m) , 7, 90-8, 05 (2H, m) , 10,1010,30(lH,m), 12, 13 (lH,br, s) .
MS (331) m/z: 224 (M+H)+.
Exemplo Referencial 310 (lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de tbutila:
(263
Adicionou-se água (10 ml) e mg) a uma solução do composto hidróxido de lítio obtido no Exemplo
Petição 870180138821, de 08/10/2018, pág. 454/857
446
Referencial 97 (5, 00 g) em tetraidrofurano (40 ml), e a mistura foi agitada à temperatura ambiente por toda a noite. A mistura da reação foi filtrada, o filtrado foi concentrado, e adicionou-se 1-hidróxi-benzotriazol monoidratado (1,75 g) , cloridrato de l-etil-3-(3-dimetilamino-propil)-carbodiimida (3,32 g) e diisopropil-etil-amina (11,3 ml), a uma solução do resíduo resultante e cloridrato de dimetil-amina (1,85 g) ) em N,N-dimetil-formamida (100 ml) à temperatura ambiente. A mistura resultante foi agitada por 2 dias. Depois de concentrar a mistura da reação, adicionou-se cloreto de metileno, uma solução aquosa saturada de bicarbonato de sódio e água, para conduzir separação de líquidos. A camada orgânica resultante foi extraída com cloreto de metileno. As camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi então removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:acetona 2:1 —>
1:1), para obter o composto do título (4,59 g).
RMN-1!! (CDC3) δ: 1, 60-1, 7 6 (2H, m) , l,73(9H,s), 1, 76- 1, 87(1H,
m) , 1, 93 (1H, br, s) , 2,14 (1H, br, s) , 2,28 (1H, br, s) , 2,65(lH,br,
s) , 2,95(3H,s), 3,05(3H,s), 4,01 (1H, br, s) , 4,21 (1H, br, s) ,
4,84 (lH,br, s) , 6, 81 (1H, br, s) , 7,20 (1H, dd, J=8, 8, 1,9Hz), 7,36 (1H,d,J=8,8Hz), 7,59(lH,br, s), 8,02(1H,br,s), 1O,O6(1H, br, s) .
MS (FAB) m/z: 465(M+H)+.
de 08/10/2018, pág. 455/857
447
Exemplo Referencial 311 (lR,2S,5S)-2-{[(5-flúor-indol-2-il)-carbonil]-amino} - 5[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de tbutila:
1) 0 (IS,3R,4S)-3-[(t-butóxi-carbonil)-amino]-4{[ (5-flúor-indol-2-il)-carbonil]-amino}-ciclo-hexanocarboxilato de etila foi obtido a partir do composto obtido no Exemplo Referencial 96 e ácido 5-flúor-indol-2carboxílico, de uma maneira similar àquela do Exemplo
Referencial 91.
RMN-!H (CDC13) δ: 1,26 (3H,t,J=7, 1Hz) , l,52(9H,s), 1,67-2,41 (7H,m), 3,97(lH,br, s) , 4,15(2H,q,J=7,1Hz), 4,08-4,22(1H,m),
6,83(lH,s), 7, 00—7, 05 (lH,m) , 7,32-7,36 (1H, m) , 8,02(lH,s),
9, 51(1H,s) .
MS (FAB) m/z: 448(M+H)+.
2) O composto do título foi obtido a partir do composto obtido acima, de uma maneira similar àquela do Exemplo Referencial 310.
RMN-!H (CDCI3) δ: l,52(9H,s), 1,57-1, 79 (2H, m) , 1,79-2,00 (2H,m), 2, 14 (lH,br, s) , 2,31 (1H, br, s) , 2,65 (1H, br, s) , 2,95 (3H,s), 3,07(3H,s), 4,02 (1H, br, s) , 4, 17-4,25 (1H, m) , 4,8O(1H,
Petição 870180138821, de 08/10/2018, pág. 456/857
448
s) , 7,35(1H,dd,J=9,0,4,3Hz), 7,91(1H,br,s), 9,49(1H,br,s) .
MS (FAB) m/z: 447(M+H)+.
Exemplo Referencial 312
2-amino-6,6-dimetil-6,7-diidrotiazolo[4,5-c]-piridino-5(4H)carboxilato de etila:

Depois de colocar cianeto de cobre (I) (918 mg) em suspensão em tetraidrofurano (50 ml) sob uma atmosfera de argônio, a suspensão foi resfriada até -20 °C, adicionou-se n-butil-lítio (solução 1,56 N em hexano, 6,41 ml) em gotas por 5 min, a mistura foi agitada a -20 °C por 30 min. Depois disso, a mistura da reação foi resfriada até -50 °C, adicionou-se hidreto de diisobutil-alumínio (solução 1,00 M em hexano) em gotas por 20 min, e a mistura foi agitada a 50 °C por 1 h. Uma solução de 2,2-dimetil-5-oxo-5,6-diidro2H-piridino-l-carboxilato de etila (Helv. Chim. Acta 81:303, 1998) (986 mg) em tetraidrofurano (5 ml) foi gotejada sobre a mistura da reação em 2 h. Depois de elevar a temperatura da mistura da reação até -20 °C, adicionou-se bromo (4,90 ml) de uma só vez, e a mistura foi agitada a -20 °C por 30 min. Adicionou-se água e acetato de etila à mistura da reação, para conduzir separação de líquidos. A camada orgânica resultante foi lavada com uma solução aquosa saturada de sulfito de sódio e secada sobre sulfato de sódio de 08/10/2018, pág. 457/857
449 anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi dissolvido em N,N-dimetilformamida (10 ml), adicionou-se tiouréia (760 mg), e a mistura foi agitada por toda a noite a 50 °C Depois de remover o solvente por destilação, adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio, para conduzir separação de líquidos. A camada orgânica foi secada sobre sulfato de sódio anidro, e o solvente foi então removido por destilação. O resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 4:1), para obter o composto do título (412 mg).
EMN-^ (CDC3) δ: 1,25 (3H, t, J=7, 1Hz) , l,54(6H,s), 2,65-2,67 (2H,m), 4,09(2H,q,J=7,1Hz), 4,44-4,46(2H,m), 4,78(2H,br,s).
Exemplo Referencial 313
2-bromo-6,6-dimetil-6,7-diidrotiazolo[4,5-c]-piridino-5(4H)carboxilato de etila:
EtOOC
Colocou-se brometo de cobre (II) (431 mg) em suspensão em acetonitrila (8 ml) , e adicionou-se nitrito de t-butila (249 mg) em gotas à temperatura ambiente. Depois disso, uma solução do composto obtido no Exemplo Referencial 312 (412 mg) em acetonitrila (8 ml) foi adicionada à mistura da reação sob resfriamento com gelo, a mistura foi aquecida até 50 °C e agitada por 15 min. 0 solvente foi removido por de 08/10/2018, pág. 458/857
450 destilação sob pressão reduzida, e adicionou-se dietil-éter e ácido clorídrico a 10% ao resíduo, para conduzir separação de líquidos. A camada orgânica foi secada sobre sulfato de magnésio anidro e concentrada sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 6:1), para obter o composto do título (151 mg).
ΗΜΝ-ΧΗ (CDC3) δ: 1,26 (3H, t, J=7, 1Hz) , l,55(6H,s), 2,79-2,81 (2H,m), 4,10(2H,q,J=7,1Hz), 4,65-4,67(2H,m).
MS (ESI) m/z: 319(M+H)+.
Exemplo Referencial 314
6,6-dimetil-6,7-diidrotiazolo[4,5-c]-piridino-5(4H)carboxilato de etila:
Adicionou-se n-butil-lítio (solução 1,56 N em hexano, 1,04 ml) a uma solução do composto obtido no Exemplo Referencial 313 (432 mg) em dietil-éter (5 ml) a -78 °C, e a mistura foi agitada a -78 °C por 30 min. Adicionou-se água e dietil-éter à mistura da reação, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de magnésio anidro, e o solvente foi então removido por destilação, para obter o composto do título (307 mg).
RMN-1!! (CDC3) δ: 1,28 (3H, t, J=7, 1Hz) , l,55(6H,s), 2,90(2H,s)
4,12 (2H, q, J=7,1Hz) , 4,75(2H,m), 8,63(lH,s).
de 08/10/2018, pág. 459/857
451
Exemplo Referencial 315
6, 6-dimetil-4,5,6,7-tetraidrotiazolo[ 4,5-c]-piridina:
HN composto obtido no Exemplo Referencial 314 (307 mg) foi dissolvido em um solvente misto de água (15 ml) , etanol (5 ml) e dioxano (5 ml) , e adicionou-se hidróxido de lítio (598 mg) a esta mistura de reação, aquecendo a mistura sob refluxo por 7 dias. Depois de deixar a mistura da reação resfriar até a temperatura ambiente, adicionou-se água e cloreto de metileno, para conduzir separação de líquidos. A camada orgânica resultante foi extraída 6 vezes com cloreto de metileno. As camadas orgânicas resultantes foram secadas sobre sulfato de sódio anidro, e o solvente foi então removido por destilação, para obter o composto do título (207 mg).
ΗΜΝ-^ (CDC3) δ: l,23(6H,s), 2,71-2,73 (2H, m) , 4,09-4,11 (2H,m), 8, 61(1H, s) .
MS (ESI) m/z: 168 (M+)
Exemplo Referencial 316
6,6-dimetil-6,7-diidrotiazolo[4,5-c]-piridino-5(4H) 20 carboxilato de t-butila:
Boc'
Petição 870180138821, de 08/10/2018, pág. 460/857
452
O composto obtido no Exemplo Referencial 315 (207 mg) foi dissolvido em cloreto de metileno (5 ml), e adicionou-se dicarbonato de di-t-butila (404 mg) e 4-(N,Ndimetil-amino)-piridina (151 mg), agitando a mistura à temperatura ambiente por 2 h. Adicionou-se mais dicarbonato de di-t-butila (404 mg) , e a mistura foi agitada por toda a noite à temperatura ambiente. Depois disso, adicionou-se mais dicarbonato de di-t-butila (1,00 g) , e a mistura foi agitada por 1 h. Adicionou-se cloreto de metileno e ácido clorídrico a 10%, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1), para obter o composto do título (95,4 mg).
RMN-1!! (CDC3) δ: l,47(9H,s), l,52(6H,s), 2,87(2H,s), 4,69 (2H,s), 8, 62(1H,s) .
MS (331) m/z: 269(MH+H)+.
Exemplo Referencial 317
4-cloro-5-(1,3-dioxolan-2-il)-tiazol-2-carboxilato de lítio:
Cl
Dissolveu-se
2,4-dicloro-tiazol-5-carbaldeído etileno acetal (J. Chem. Soc. Perkin Trans. 1:97, 1992) (2,26 g) em tetraidrofurano (15 ml), e adicionou-se n-butilde 08/10/2018, pág. 461/857
453 lítio (solução 1,5 N em hexano, 6,8 ml) sob resfriamento com gelo seco/acetona, agitando a mistura por 20 min. Depois, introduziu-se dióxido de carbono na mesma temperatura. A mistura da reação foi aquecida gradualmente até a temperatura ambiente em 1,5 h, e depois, concentrada. Adicionou-se hexano à mistura da reação, para transformar o produto em pó. O produto foi coletado por filtração e colocado em suspensão em acetato de etila, e o pó formado foi coletado novamente por filtração, para obter o composto do título (1,65 g) .
Exemplo Referencial 318
4-cloro-5-(1,3-dioxolan-2-il)-tiazol-2-carboxilato de etila:
O composto obtido no Exemplo Referencial 317 (242 mg) e etanol (0,2 ml) foram dissolvidos em N,N-dimetil15 formamida (2 ml), e adicionou-se 1-hidróxi-benzotriazol monoidratado (136 mg) e cloridrato de 1-(3-dimetil-aminopropil ) -3-etil-carbodiimida (250 mg), agitando a mistura à temperatura ambiente por uma noite. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se dietil20 éter e ácido clorídrico diluído, para separar uma camada orgânica. A camada orgânica foi lavada com água e uma solução aquosa saturada de bicarbonato de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido
Petição 870180138821, de 08/10/2018, pág. 462/857
454 por destilação sob pressão reduzida, para obter o composto do título (170 mg).
RMN-iH (CDC3) δ: 1,43 (3H, t, J=7,3Hz) , 4,00-4,10 (2H, m) , 4,104,20(2H,m), 4,48 (2H, q, J=7, 3Hz) , 6,15(lH,s)
MS (ESI) m/z: 264(M+H)+.
Exemplo Referencial 319
4-cloro-5-formil-tiazol-2-carboxilato de etila:
O composto obtido no Exemplo Referencial 318 (132 mg) foi dissolvido em dietil-éter (5 ml), e adicionou-se ácido clorídrico a 20%, agitando a mistura à temperatura ambiente por 7 h. Uma solução aquosa saturada de bicarbonato de sódio foi adicionada à mistura da reação, para conduzir extração com dietil-éter. O extrato foi secado sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (110 mg).
RMN-1!! (CDC3) δ: 1, 4 6 (3H, t, J=7,1Hz ) , 4,52 (2H, q, J=7,1Hz) ,
10,12(1H,s).
Exemplo Referencial 320
4-azido-5-formil-tiazol-2-carboxilato de etila:
OHC s
COOEt
N
Petição 870180138821, de 08/10/2018, pág. 463/857
455
O composto obtido no Exemplo Referencial 319 (5,15 g) foi dissolvido em sulfóxido de dimetila (30 ml), e adicionou-se azida de sódio (1,52 g) , agitando a mistura à temperatura ambiente por 2,5 h. Adicionou-se gelo/água à mistura da reação, para conduzir extração com dietil-éter. O extrato foi lavado duas vezes com água e depois secado sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 24:1), para obter o composto do título (1,78 g).
ΗΜΝ-^ (CDC3) δ: 1,45 (3H, t, J=7, 1Hz) , 4,50 (2H, q, J=7, 1Hz) ,
9, 95(1H,s) .
Exemplo Referencial 321
6-metil-6,7-diidrotiazolo[4,5-d]-pirimidino-2-carboxilato de etila:
O composto obtido no Exemplo Referencial 320 (1,56 g) foi dissolvido em cloreto de metileno (20 ml), e adicionou-se ácido acético (2 ml) , metil-amina (solução 2 N em tetraidrofurano, 21 ml) e triacetóxi-boro-hidreto de sódio (2,98 g), agitando a mistura. Depois de 1 h, adicionou-se mais triacetóxi-boro-hidreto de sódio (2,98 g), e continuou-se a agitação por mais 5 h. Adicionou-se uma solução aquosa 0,5 N de hidróxido de sódio à mistura da de 08/10/2018, pág. 464/857
456 reação, para alcalinizá-la. Depois de extrair a mistura da reação com cloreto de metileno, o extrato foi secado sobre sulfato de magnésio anidro. 0 solvente foi removido por destilação sob pressão reduzida, para obter um óleo marrom (1,43 g) . Este óleo foi dissolvido em etanol (50 ml), adicionou-se 10% de paládio sobre carvão (2,0 g), para conduzir hidrogenação em condições normais de temperatura e pressão. Depois de 2,5 h, o catalisador foi removido por filtração, e o filtrado foi concentrado. O resíduo foi dissolvido em cloreto de metileno (30 ml), e adicionou-se ortoformiato de trimetila (0,7 ml) e complexo de trifluoreto de boro/dietil-éter (0,3 ml), agitando a mistura à temperatura ambiente por 15 h. Uma solução aquosa saturada de bicarbonato de sódio foi adicionada à reação, para conduzir extração com cloreto de metileno. O extrato foi secado sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 97:3), para obter o composto do título (100 mg).
RMN-1!! (CDC3) δ: 1,41 (3H, t, J=7,1Hz) , 2,95(3H,s), 4,44(2H,q,
J=7,lHz), 4,87(2H,s), 7,06(lH,s).
MS (ESI) m/z: 226(M+H)+.
Exemplo Referencial 322
6-metil-6,7-diidrotiazolo[4,5-d]-pirimidino-2-carboxilato de lítio:
/>—COOU
Petição 870180138821, de 08/10/2018, pág. 465/857
457 composto (463 mg) foi dissolvido em tetraidrofurano (20 ml), e adicionou-se hidróxido de lítio (54,1 mg) e água (4 ml), agitando a mistura à temperatura ambiente por 4,5 h. 0 solvente foi removido por destilação sob pressão reduzida e o resíduo foi secado por meio de uma bomba a vácuo, para obter o composto do título (460 mg). ΗΜΝ-^ (DMSO-de) δ: 2,86(3H,s), 4,71(2H,s), 7,03(lH,s).
Exemplo Referencial 323 (IR,2S,5S)-2-azido-5-{[etil-(metil)-amino]-carbonil}-ciclo10 hexil-carbamato de t-butila:
N.
composto do título foi obtido condensando o composto obtido no Exemplo Referencial 250 com etil-metilamina.
RMN-1!! (CDC3) δ: 1, 08, 1,18 (total 3H, cada t,J=7,lHz), 1,46 (9H,s), 1, 52-1, 80(4H,m), 2, 04-2, 08(2H,m), 2,71-2,77(1H,m),
2,89, 2, 98(total 3H,cada s) , 3, 32, 3, 39(total 2H,cada q,J=7,lHz), 3,74-3,76(lH,m), 4,09-4,11(1H,m), 4,60(1H,br,s). MS (EI) m/z: 326(M+H)+.
Exemplo Referencial 324 (lR,2S,5S)-2-{[(7-cloro-isoquinolin-3-il)-carbonil]-amino}5-{[etil-(metil)-amino]-carbonil}-ciclo-hexil-carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 466/857
458
BocHN
Cl
O composto obtido no Exemplo Referencial 323 (1,44 g) foi dissolvido em metanol (20 ml) , adicionou-se 10% de paládio sobre carvão (150 mg) , e a mistura foi agitada sob uma atmosfera de hidrogênio. Depois de 24 h, o catalisador foi removido por filtração, e o solvente foi então concentrado sob pressão reduzida, para obter um óleo incolor. Este óleo foi usado na próxima reação como ele estava.
O óleo obtido acima foi dissolvido em cloreto de metileno (30 ml), e o composto obtido no Exemplo Referencial 57 (850 mg), cloridrato de 1-etil-3-(3-dimetil-aminopropil)-carbodiimida (1,27 g) , 1-hidróxi-benzotriazol monoidratado (900 mg) e N-metil-morfolina (1,34 g) , foram adicionados, agitando a mistura à temperatura ambiente. Depois de 17 h, adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio e água, para conduzir separação de líquidos, e a camada orgânica resultante foi secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi submetido a uma cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:50), para obter o composto do título (1,61 g).
de 08/10/2018, pág. 467/857
459
RMN-iH (CDC13) δ: 1, 10,1,22 (total 3Η, cada t,J=7,lHz), 1,43 (9H,s), 1,84—2, 17 (6H,m) , 2, 66 (1H, br, s) , 2, 92, 3, 03(total
3H,cada s) , 3, 35—3, 44(2H,m), 4,20—4,30(2H,m), 5,30(1H,br,s),
7,70(1H,d,J=8,6Hz), 7,92(1H,d,J=8,6Hz), 8,00(lH,s), 8,4O(1H, 5 br,s), 8,56(lH,s), 9,03(lH,s).
MS (FAB) m/z: 489(M+H)+.
Exemplo Referencial 325
N-((IS,2R,4S)-2-amino-4-[(7-cloro-isoquinolin-3-il)carbonil]-4-{[etil-(metil)-amino]-carbonil}-ciclo-hexil)-710 cloro-isoguinolino-3-carboxamida:
O composto obtido no Exemplo Referencial 324 (1,60 g) foi dissolvido em solução de ácido clorídrico em etanol (25 ml), e a solução foi agitada à temperatura ambiente por 30 min. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa 1 N de hidróxido de sódio, para conduzir separação de líquidos. A camada aquosa resultante foi extraída com cloreto de metileno, e as camadas orgânicas foram combinadas e secadas sobre carbonato de potássio. O solvente foi removido por destilação sob pressão reduzida, adicionou-se hexano ao resíduo, e o precipitado foi coletado por
Petição 870180138821, de 08/10/2018, pág. 468/857
460 filtração, para obter o composto do título (1,22 RMN-1H (DMSO-de) δ: 1,10, 1,23 (total 3H, cada
1,26(2H,br,s), 1,69-2,11(6H,m), 2,89(1H,br,s), (total 3H,cada s) , 3,38—3,45(2H,m), 3,52(lH,s), s), 7,70(1H,dd,J=8,8, 2,OHz), 7,94(1H,d,J=8,8Hz) J=2,OHz), 8,50 (lH,br, s) , 8,59(lH,s), 9,ll(lH,s). MS (FAB) m/z: 389(M+H)+.
g) · t,J=7,lHz),
2,93, 3,05
4,18 (lH,br,
8, 02(1H,d,
Exemplo Referencial 326 (IR*,3S*,4S*)-3-[(t-butóxi-carbonil)-amino]-4-{[t-butil10 (difenil)-silil]oxi}-ciclo-hexano-carboxilato de etila:
COOEt
BocHN'
OTBDPS
O composto obtido no Exemplo Referencial 88 (28,0
g) foi dissolvido em N, N-dimetil-formamida (500 ml), e adicionou-se cloreto de t-butil-difenil-silila (63,5 ml) e imidazol (19,9 g) . Depois disso, a mistura foi agitada à temperatura ambiente por 10 h, adicionou-se acetato de etila e água à mistura da reação, para conduzir separação de líquidos. A camada aquosa resultante foi extraída com acetato de etila, e as camadas orgânicas foram combinadas, lavadas duas vezes com água e secadas sobre sulfato de sódio anidro. Depois disso, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de
Petição 870180138821, de 08/10/2018, pág. 469/857
461 metileno:metanol 47:3), para obter o composto do título (52,5 g), contendo 0,4 molécula de N,N-dimetil-formamida. RMN-XH (CDC3) δ: l,07(9H,s), 1,27 (3H, t, J=7, 1Hz) , l,38(9H,s),
1,43-1,59(3H,m), 1,63-1,67(1H,m), 1,92-1,98(1H,m), 2,255 2,32(lH,m), 2,37-2,42(1H,m), 3,66 (1H,br,s), 3,80(1H,br,s),
4,16(2H,q,J=7,1Hz), 4,32(1H,d,J=8,1Hz), 7,34-7,46(6H,m),
7,65 -7,73 (4H,m) .
Exemplo Referencial 327 (lR*,2R*,5S*)-2-{[t-butil-(difenil)-silil]oxi}-5-(hidróxi10 metil)-ciclo-hexano-carboxilato de t-butila:
Colocou-se hidreto de lítio (7,11 g) em suspensão em dietil-éter absoluto (100 ml) a 0 °C, enquanto se purgava com argônio, e adicionou-se uma solução do composto obtido no Exemplo Referencial 326 (52,5 g) em dietil-éter (500 ml), em gotas, por 30 min. Depois de agitar a 0 °C por 30 min, adicionou-se metanol (100 ml) à mistura da reação. A lama resultante foi removida por filtração através de Celite, e o filtrado foi concentrado. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (29,6 g).
RMN-XH (CDC3) δ: l,07(9H,s), 1,32-1,74 (16H, m) , l,87(lH,t,
J=10,4Hz), 3, 35-3, 55(2H,m), 3,71(1H,br,s), 3,79 (1H,br,s),
4,36 (lH,br, s) , 7,34-7,44 (6H, m) , 7, 65-7,72 (4H,m).
Petição 870180138821, de 08/10/2018, pág. 470/857
462
Exemplo Referencial 328 metanossulfonato de (IR*,3S*,4S*)-3-[(t-butóxi-carbonil)amino]4-{[t-butil-(difenil)-silil]oxi}-ciclo-hexil)-metila:
composto obtido no Exemplo Referencial 327 (29,5 5 g) foi dissolvido em cloreto de metileno (200 ml), e adicionou-se piridina (20 ml) e cloreto de metanossulfonila (9,5 ml), agitando a mistura à temperatura ambiente por 6 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se acetato de etila e água ao resíduo, para conduzir separação de líquidos. A camada aquosa resultante foi extraída com acetato de etila, e as camadas orgânicas foram combinadas, lavadas duas vezes com água e depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1), para obter o composto do título (29,8 g) .
RMN-1!! (CDC3) δ: l,08(9H,s), l,38(9H,s), 1, 43-1, 61 (5H, m) ,
1,86-1,89 (2H,m) , 3,02(3H,s), 3, 77 (1H, br, s) , 3, 81 (1H, br, s) ,
4, 10(2H,d,J=5,4Hz), 4,32 (1H,br,s), 7,35-7, 45(6H,m), 7,647,68 (4H,m) .
MS (ESI) m/z: 562(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 471/857
463
Exemplo Referencial 329 (lR*,2R*,5S*)-2-{[t-butil-(difenil)-silil]oxi}-5-(cianometil)-ciclo-hexano-cabamato de t-butila:
composto obtido no Exemplo Referencial 328 (29,8 5 g) foi dissolvido em N,N-dimetil-formamida (400 ml), e adicionou-se cianeto de sódio (3,64 g), agitando a mistura a 80 °C por 11 h. Adicionou-se acetato de etila e uma solução aquosa saturada de bicarbonato de sódio à mistura da reação, para conduzir separação de líquidos. A camada aquosa resultante foi extraída duas vezes com acetato de etila, e as camadas orgânicas foram combinadas, lavadas com uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 5:1), para obter o composto do título (20,6 g) .
RMN-1!! (CDC3) δ: l,08(9H,s), l,38(9H,s), 1, 43-1, 68 (5H, m) ,
1,79-1,85(lH,m), 1,88-1,95(1H,m), 2,32(2H,d,J=7,1Hz), 3,77 (lH,br,s), 3,82(1H,br,s), 4,32(1H,br,d,J=6,8Hz), 7,35—7,45 (6H,m), 7,65—7,71(4H,m).
Petição 870180138821, de 08/10/2018, pág. 472/857
464
Exemplo Referencial 330 (lR*,2R*,5S*)-2-{[t-butil-(difenil)-silil]oxi}-5-(oxo-etil)ciclo-hexano-cabamato de t-butila:
BocHN
O composto obtido no Exemplo Referencial 329 (2,0
g) foi dissolvido em cloreto de metileno absoluto (20 ml), e o sistema foi purgado com argônio e depois resfriado até -78 °C. Adicionou-se hidreto de diisobutil-alumínio (solução 0,95 M em hexano, 8,55 ml) em gotas à solução. A temperatura da reação foi então deixada subir até a temperatura ambiente e agitada por 3 h. A mistura da reação foi resfriada até 0 °C, e adicionou-se metanol (10 ml) em gotas. A lama resultante foi removida por filtração através de Celite, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 1:0 49:1), para obter o composto do título (1,45 g).
RMN-1!! (CDO13) δ: l,07(9H,s), l,38(9H,s), 1, 43-1,54 (5H, m) ,
1,82-1,88(lH,m), 2,06 (1H,br,s), 2,42-2, 43(2H,m), 3,72(1H, br,s), 3,77(1H,br,s), 4,38(1H,br,s), 7, 34—7, 44(6H,m) , 7,65—
7,68(4H,m), 9, 77 (1H, t, J=l, 7Hz) .
MS (FAB) m/z: 496(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 473/857
465
Exemplo Referencial 331 ácido 2-((IR*,3S*,4S*)-3-[(t-butóxi-carbonil)-amino]-4-{[tbutil-(difenil)-silil]oxi}-ciclo-hexil-acético:
BocHN
OTBDPS
O composto obtido no Exemplo Referencial 330 (8,40 g) foi dissolvido em um solvente misto de água (33 ml) e tbutanol (120 ml), e adicionou-se 2-metil-2-buteno (8,08 ml), fosfato diácido de potássio diidratado (2,64 g) e clorito de sódio (3,45 g) , agitando a mistura à temperatura ambiente por 1,5 h. Adicionou-se cloreto de metileno e água à mistura da reação, para diluí-la. Ajustou-se o pH da camada aquosa resultante para um pH de cerca de 4 com ácido clorídrico 1 Ν. A separação de líquidos foi conduzida, e a camada aquosa resultante foi extraída duas vezes com cloreto de metileno. As camadas orgânicas foram combinadas e secadas sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1 —» 1:1), para obter o composto do título (7,62 g).
RMN-1!! (CDC3) δ: l,07(9H,s), 1,22-1, 63 (15H, m) , l,82(lH,br,
s), 2,17 (lH,br,s), 2,27-2,33(1H,m) , 3,69(1H,br,s), 3,84(1H, br,s), 7,00(1H,br,s), 7,33—7,42(6H,m), 7,63—7,65(4H,m).
de 08/10/2018, pág. 474/857
466
MS (ESI) m/z: 512(M+H)+.
Exemplo Referencial 332 (lR*,2R*,5S*)-2-{[t-butil-(difenil)-silil]oxi}-5-(2(dimetil-amino)-2-oxoetil]-ciclo-hexano-cabamato de tbutila:

O composto obtido no Exemplo Referencial 331 (7,62 g) foi dissolvido em N,N-dimetil-formamida (150 ml), e adicionou-se cloridrato de dimetil-amina (6,07 g), cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (8,56 g) , 1-hidróxi-benzotriazol monoidratado (1,01 mg) e trietil-amina (10,3 ml), agitando a mistura à temperatura ambiente por 4 dias. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi extraída com cloreto de metileno, e as camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 1:1) . O solvente foi removido por destilação sob pressão reduzida, adicionou-se hexano ao resíduo, e o de 08/10/2018, pág. 475/857
467 precipitado branco formado foi coletado por filtração, para obter o composto do título (6,42 g).
RMN-iH (CDC3) δ: l,08(9H,s), 1, 38 (9H, br, s) , 1,43-1,55 (5H, m) ,
1,79-1,86 (lH,m), 2,03 (1H,br,s), 2,21-2,32(2H,s), 2,94 (3H,
s) , 3,03(3H,s), 3,74 (lH,br,s), 3,80 (1H, br, s) , 4,49(lH,br,
s), 7,33-7,44(6H,m), 7,64-7,69(4H,m).
MS (ESI) m/z: 539(M+H)+.
Exemplo Referencial 333 (lR*,2R*,5S*)-5-(2-(dimetil-amino)-2-oxoetil]-2-hidróxi10 ciclo-hexano-cabamato de t-butila:
O
BocHN'^G
OH
O composto obtido no Exemplo Referencial 332 (6,36 g) foi dissolvido em tetraidrofurano (50 ml), e adicionou-se fluoreto de tetrabutil-amônio (solução 1 N em tetraidrofurano, 17,85 ml), agitando a mistura à temperatura ambiente por 13 h. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 24:1), para obter o composto do título (3,49 g) .
RMN-1!! (CDC3) δ: l,44(9H,s), 1, 4 6-1, 60 (4H, m) , 1,79-1,84 (2H,
m) , 2,28-2,35 (3H, s) , 2, 82 (1H, br, s) , 2,95(3H,s), 3,01(3H,s),
3,56(2H,br,s), 4, 67(1H,br,s),
Petição 870180138821, de 08/10/2018, pág. 476/857
468
MS (ESI) m/z: 301(M+H)+.
Exemplo Referencial 334 metanossulfonato de ((IR*,2R*,4S*)-2-[(t-butóxi-carbonil)amino]4-[2-(dimetil-amino)-2-oxoetil]-ciclo-hexila:
BocHN
0 composto obtido no Exemplo Referencial 333 (8,05
g) foi dissolvido em cloreto de metileno (50 ml) , e a solução foi resfriada até -78 °C sob uma atmosfera de argônio, adicionando cloreto de metanossulfonila (2,70 ml) em gotas. Depois de deixar a temperatura da mistura subir para 0 °C e agitar por 30 min, agitou-se à temperatura ambiente por 2 h. Adicionou-se água à mistura da reação, para conduzir separação de líquidos, e a camada aquosa resultante foi extraída com cloreto de metileno. As camadas orgânicas foram combinadas, lavadas com água, e secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 1:1 —> 0:1), para obter o composto do título (3,63 g) . RMN-1!! (CDC3) δ: l,43(9H,s), 1,59-1,74 (4H, m) , 1,85- 2,30(5H,
m) , 2,95(3H,s), 3,00(3H,s), 3,10(3H,s), 3, 7 9-3, 83 (1H, m) ,
4,72(1H,br,s), 4,91(1H,br,s),
Petição 870180138821, de 08/10/2018, pág. 477/857
469
MS (ESI) m/z: 379(M+H)+.
Exemplo Referencial 335 (IR*,2R*,5S*)-2-azido-5-(2-(dimetil-amino)-2-oxoetil]-ciclohexano-cabamato de t-butila:
BocHN
O
O composto obtido no Exemplo Referencial 334 (3,62
g) foi dissolvido em N,N-dimetil-formamida (20 ml), e adicionou-se azida de sódio (3,11 g) , agitando a mistura a 75 °C por 17 h. A mistura da reação foi vertida sobre um solvente misto de água e acetato de etila, para conduzir separação de líquidos. A camada aquosa resultante foi extraída duas vezes com acetato de etila, e as camadas orgânicas foram combinadas, lavadas com água, uma solução aquosa saturada de bicarbonato de sódio e uma solução aquosa saturada de cloreto de sódio, e secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila), para obter o composto do título (20,6 g).
RMN-1!! (CDC3) δ: 1, 14-1,21 (1H, m) , 1,33-1, 40 (1H, m) , 1,45 (9H
s), 1,61-1,71(lH,m), 1,78-1,91(3H,m), 2,22-2,27(3H,m), 2,94
br,s).
de 08/10/2018, pág. 478/857
470
MS (ESI) m/z: 326(M+H)+.
Exemplo Referencial 336 cloridrato de N-{(IR*,2S*,4R*)-2-amino-4-[2-(dimetil-amino)2-oxoetil]-ciclo-hexil}-5-cloro-indol-2-carboxamida:
O composto do título foi obtido tratando, de uma maneira similar àquela do Exemplo Referencial 69, um produto obtido reduzindo cataliticamente o composto obtido no Exemplo Referencial 335, de uma maneira similar àquela do Exemplo Referencial 324, e depois condensando-o com o ácido
5-cloro-indol-2-carboxílico.
RMN-1!! (DMSO—dô) δ: 1, 16-1, 19 (1H, m) , 1,51-1,56 (1H, m) , 1,70l,73(lH,m), 1,81-1,91(2H,m), 1,99-2,03(1H,m), 2,19-2,30(3H,
m) , 2,83(3H,s), 2,99(3H,s), 3, 63 (1H, br, s) , 4,08 (1H, br, s) ,
7,19(1H,dd,J=8,7,1,7Hz), 7,35(lH,s), 7,44 (1H,d,J=8,7Hz),
7,69(1H,d,J=l,7Hz), 8,22(3H,br,s), 8,62(1H,d,J=7,1Hz), 11,91 (1H,s) .
MS (ESI) m/z: 377(M+H)+.
Exemplo Referencial 337 (lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-520 (hidróxi-metil)-ciclo-hexano-carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 479/857
471
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 97, de uma maneira similar àquela da etapa (2) do Exemplo Referencial 129.
Exemplo Referencial 338 metanossulfonato de ((IS,3R,4S)-3-[(t-butóxi-carbonil)amino]-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-ciclohexil ) -metila:
composto obtido no Exemplo Referencial 337 (500 mg) e trietil-amina (329 ml) foram colocados em suspensão em tetraidrofurano (8 ml)/cloreto de metileno (8 ml), e a suspensão foi resfriada até -78 °C. Depois de adicionar cloreto de metano-sulfonila (138 ml) em gotas à suspensão, a temperatura da suspensão foi elevada gradualmente até -5 °C, e a suspensão foi agitada por 15 h na mesma temperatura.
Depois de concentrar a mistura da reação, adicionou-se água ao resíduo, para conduzir extração 3 vezes com cloreto de
Petição 870180138821, de 08/10/2018, pág. 480/857
472 metileno. As camadas orgânicas foram lavadas com solução aquosa saturada de cloreto de sódio, e secadas sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (654 mg) .
RMN-1!! (CDC3) δ: l,57(9H,s), 1, 84-2, 01 (4H, m) , 2,28-2,31 (1H,
m) , 3,04(3H,s), 3,68(lH,s), 3, 74-3, 75 (1H, m) , 3,91- 3,93(1H,
m) , 4,02-4,12 (2H,m), 4, 18-4,20 (lH,m) , 4,85 (1H, br, s) , 6,81 (lH,s), 7,21(1H, dd, J=2,0,8,8Hz), 7,34(1H,d,J=8,8Hz), 7,60 (lH,s), 8,02 (lH,br, s) , 9, 27 (1H, br, s) .
MS (ESI) m/z: 500(M+H)+.
Exemplo Referencial 339 (lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5[(metil-sulfanil)-metil]-ciclo-hexano-carbamato de t-butila:
O composto obtido no Exemplo Referencial 338 (654 mg) foi dissolvido em N,N-dimetil-formamida (8 ml), e adicionou-se uma solução aquosa a 15% de tiometóxido de sódio (1,8 ml), agitando a mistura à temperatura ambiente por 4 h. A mistura da reação foi vertida sobre água e extraída 3 vezes com acetato de etila. As camadas orgânicas resultantes foram lavadas com solução aquosa saturada de cloreto de sódio, secadas sobre sulfato de sódio anidro, e
Petição 870180138821, de 08/10/2018, pág. 481/857
473 depois concentradas. 0 resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 24:1), para obter o composto do título (492 mg) .
ΗΜΝ-^ (CDC3) δ: l,52(9H,s), 1, 87-3, 04 (13H, m) , 3, 91-3, 94 (1H,
m) , 4, 12-4, 15 (lH,m) , 4,95 (1H, br, s) , 6,81(lH,s), 7,19(lH,dd,
J=8,8, 1,2Hz), 7,35 (1H, d, J=8, 8Hz) , 7,57(lH,s), 9,82(lH,br,
s) .
MS (ESI) m/z: 452(M+H)+.
Exemplo Referencial 340 (lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5[(metil-sulfonil)-metil]-ciclo-hexano-carbamato de t-butila:
O composto obtido no Exemplo Referencial 339 (300 mg) foi dissolvido em cloreto de metileno (10 ml), e adicionou-se ácido m-cloro-perbenzóico (70%, 400 mg) a 0 °C sob agitação. Depois de continuar a agitação por 1 h como ela está, a mistura da reação foi vertida sobre água e extraída 3 vezes com acetato de etila. As camadas orgânicas resultantes foram lavadas com solução aquosa saturada de cloreto de sódio, secadas sobre sulfato de sódio anidro, e depois concentradas. Depois disso, o resíduo foi purificado
Petição 870180138821, de 08/10/2018, pág. 482/857
474 por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 24:1), a separação de líquidos foi conduzida com uma solução aquosa saturada de bicarbonato de sódio e acetato de etila, e a camada orgânica resultante foi concentrada, para obter o composto do título (254 mg).
RMN-1H (CDC3) δ: 1,44-2, 19 (13H, m) , 2, 22-2,30 (2H, m) , 2,893,25(7H,m), 3, 93-4, 15 (2H, m) , 4,98 (1H, br, s) , 6,82(lH,s),
7,21 (1H,dd,J=8,8,2,OHZ), 7,34(1H,d,J=8,8Hz), 7,60 (1H,br,s),
9, 54 (lH,br, s) .
Exemplo Referencial 341 (5-cloro-tien-3-il)-metanol:
HO
Cl
O ácido 5-cloro-tiofeno-3-carboxílico (Monatsch.
Chem. 120:53, 1989) (6,93 g) foi dissolvido em tetraidrofurano (750 ml), e adicionou-se trietil-amina (27,3 ml) e cloro-formiato de etila (18,7 ml), agitando a mistura à temperatura ambiente por 2,5 h. Uma solução aquosa (41 ml) de boro-hidreto de sódio (19,3 g) foi adicionada em gotas por 10 min, e a mistura foi agitada à temperatura ambiente por 18,5 h. Depois disso, adicionou-se ácido acético à mistura da reação, para acidificá-la, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se água e cloreto de metileno ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi lavada com água e uma solução aquosa saturada
Petição 870180138821, de 08/10/2018, pág. 483/857
475 de bicarbonato de sódio. Depois de secar a camada orgânica, o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:4), para obter o composto do título (5,17 g).
RNIN-1!! (CDC3) δ: 1,63(1H,t,J=5,8Hz), 4,59 (2H, d, J=5, 3Hz) ,
6,91(lH,d,J=l,7Hz), 6,98-6,99(lH,m).
Exemplo Referencial 342
5-cloro-tiofeno-3-carbaldeído:
O composto obtido no Exemplo Referencial 341 (5,17 g) foi dissolvido em cloreto de metileno (400 ml), e adicionou-se dióxido de manganês (51,3 g), agitando a mistura à temperatura ambiente por 15 h. Depois disso, a mistura da reação foi filtrada, o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (2,84 g).
ΗΜΝ-^ (CDC3) δ: 7,35 (1H, d, J=l, 7Hz) , 7, 88 (1H, d, J=1,7Hz) , 9,75 (1H,S) .
Exemplo Referencial 343
2-azido-3-(5-cloro-tien-3-il)-acrilato de etila:
EtO2C
Cl de 08/10/2018, pág. 484/857
476
Depois de adicionar etanol (15 ml) a uma solução de etóxido de sódio a 20% em etanol (10,7 ml), e resfriar a mistura até 0 °C, uma mistura do composto obtido no Exemplo
Referencial 342 (1,01 g) e azido-acetato de etila (3,55 g) foi adicionada em gotas por 30 min, e a mistura resultante foi agitada a 0 °C por 3 h. Uma solução resfriada de cloreto de amônio foi adicionada à mistura da reação, para conduzir extração 3 vezes com dietil-éter. As camadas orgânicas foram combinadas, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (acetato de etila:hexano 1:49), para obter o composto do título (1,04
g) ·
ΗΜΝ-^ (CDC3) δ: 1,38 (3H, t, J=7,1Hz) , 4,34 (2H, q, J=7, 1Hz) ,
6,75(lH,s), 7,39(1H,d,J=l,7Hz), 7,54(1H,d,J=1,7Hz).
Exemplo Referencial 344
2-cloro-6H-tieno-[2,3-b]-pirrol-5-carboxilato de etila:
Cl \X>-COOEt s H
O composto obtido no Exemplo Referencial 343 (0,97 g) foi dissolvido em xileno (20 ml) , e a solução foi aquecida sob refluxo por 30 min. Depois de deixar a mistura da reação resfriar, o solvente foi removido por destilação sob pressão reduzida. Adicionou-se hexano ao resíduo, e os sólidos formados foram coletados por filtração, para obter o composto do título (0,608 g).
de 08/10/2018, pág. 485/857
477
RMN—XH (CDCI3) δ: 1, 38(3H, t,J=7,OHz), 4,35(2H,q,J=7,OHz),
6,90(lH,s), 7,00(1H,d,J=l,9Hz), 9,32(lH,br).
Exemplo Referencial 345 ácido 2-cloro-6H-tieno-[2,3-b]-pirrol-5-carboxílico:
Cl fs(
COOH
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 344, de uma maneira similar àquela do Exemplo Referencial 274.
RMN-íH (CD3OD) Ô: 3,35(lH,s), 6,94(lH,s), 6,96(lH,s).
MS (ESI) m/z: 200(M—H)-.
Exemplo Referencial 346
1-cloro-4-(2,2-dibromo-vinil)-benzeno:
Biv ^Br
Dissolveu-se 4-cloro-benzaldeído (2,81 g) em cloreto de metileno (300 ml), e adicionou-se tetrabrometo de carbono (13,3 g) e trifenilfosfina (21,0 g) , agitando a mistura à temperatura ambiente por 90 min. Depois disso, os insolúveis depositados foram removidos por filtração, e o filtrado foi concentrado sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 20:1), para obter o composto do
Petição 870180138821, de 08/10/2018, pág. 486/857
478 título (5,54 g).
RMN-iH (CDC3) δ: 7,33 (2H, d, J=8,5Hz) , 7,43(lH,s), 7,47(2H,d,
J=8,5Hz) .
MS (EI) m/z: 296 (M+)
Exemplo Referencial 347 ácido 3-(4-cloro-fenil)-2-propiólico:
c|-^>—=“CO2H composto obtido no Exemplo Referencial 346 (1,0
g) foi dissolvido em tetraidrofurano (30 ml), e adicionou-se n-butil-lítio (solução 1,59 N em hexano, 4,46 ml) em gotas a
-78 °C sob uma atmosfera de argônio. A temperatura da mistura da reação foi deixada subir até a temperatura ambiente e agitou-se por 1 h. A mistura da reação foi resfriada novamente até -78 °C, agitada por 2 min sob uma atmosfera de dióxido de carbono e depois aquecida até a temperatura ambiente. Depois de concentrar a mistura da reação sob pressão reduzida, adicionou-se solução aquosa satura de cloreto de sódio e acetato de etila ao resíduo, para conduzir separação de líquidos. Adicionou-se ácido clorídrico 3 N à camada aquosa resultante, para acidificá20 la, e a extração foi conduzida com acetato de etila. A camada orgânica resultante foi secada sobre sulfato de sódio anidro e concentrada sob pressão reduzida, para obter o composto do título (453 mg).
ΗΜΝ-^ (DMSO-de) δ: 7, 55 (2H, d, J=8, 5Hz) , 7, 66 (2H, d, J=8, 5Hz) ,
Petição 870180138821, de 08/10/2018, pág. 487/857
479
13,90(1Η,br,s).
MS (EI) m/z: 180 (M+) .
Exemplo Referencial 348
6-cloro-4-oxo-l,4-diidroguinazolino-2-carboxilato de etila:
Adicionou-se cloro-oxoacetato de etila (2,0 ml) a uma solução de 2-amino-5-cloro-benzamida (2,50 g) em piridina (15 ml), e a mistura foi agitada à temperatura ambiente por 18 h. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo resultante foi dissolvido em ácido acético (50 ml). Adicionou-se anidrido acético (5,0 ml) à solução, e a mistura foi aquecida sob refluxo por 16 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se etanol ao resíduo. Os cristais depositados foram coletados por filtração e lavados, para obter o composto do título (2,71 g).
ΚΜΝ-^ (DMSO-de) δ: 1,35 (3H, t, J=7,1Hz) , 4,38 (2H, q, J=7, 1Hz) ,
7,85 (1H, d, J=8, 6Hz) , 7, 91 (1H, dd, J=8, 6, 2, 3Hz) , 8,10(lH,d,J=
2,3Hz) , 12,85 (lH,br, s) .
MS (ESI) m/z: 253(M+H)+.
Exemplo Referencial 349 ácido 6-cloro-4-oxo-l,4-diidroquinazolino-2-carboxílico:
de 08/10/2018, pág. 488/857
480
Adicionou-se hidróxido de lítio (263 mg) a uma solução do composto obtido no Exemplo Referencial 348 (1,26
g) em um solvente misto de água (5 ml) e tetraidrofurano (15 ml) , e a mistura foi agitada à temperatura ambiente por 18
h. A mistura da reação foi neutralizada com ácido clorídrico 1 N (11 ml) sob resfriamento com gelo e agitada por 1 h. Os cristais depositados foram coletados por filtração e lavados, para obter o composto do título (0,96
9) ·
ΚΜΝ-^ (DMSO-de) δ: 7,50-8, 20 (3H, m) , 12, 44 (1H, br, s) .
MS (ESI) m/z: 265(M+H+CH3CN)+.
Exemplo Referencial 350
2-cloro-N-(4-cloro-fenil)-acetamida:
H
Dissolveu-se p-cloro-anilina (3,82 g) em acetato 15 de etila (30 ml), e adicionou-se cloreto de cloro-acetila (2,39 ml) à temperatura ambiente, agitando a mistura por 1 h. Depois de aquecer e agitar a mistura da reação a 60 °C por 3,5 h, os cristais depositados foram coletados por filtração, para obter o composto do título (4,78 g) . O
Petição 870180138821, de 08/10/2018, pág. 489/857
481 filtrado foi concentrado até cerca de ¼ do volume, e os cristais depositados foram coletados por filtração, para obter o composto do título (1,01 g).
ΗΜΝ-^ (CDC3) δ: 4,19(2H,s), 7, 33 (2H, d, J=9, OHz) , 7,51(2H, d,J=9,OHz), 8,22 (lH,br, s) .
Exemplo Referencial 351
S-[2-(4-cloro-anilino)-2-oxoetil]-tiossulfato de sódio:
O composto obtido no Exemplo Referencial 350 (5,79 g) foi dissolvido em etanol (140 ml), e adicionou-se uma solução aquosa (140 ml) de tiossulfato de sódio pentaidratado (7,04 g) de uma só vez a 70 °C, aquecendo a mistura sob refluxo por 1,5 h. A mistura da reação foi concentrada até cerca de 1/10 do volume, e os cristais
|
depositados foram |
coletados |
por filtração, |
para obter o |
|
15 composto do título |
(8,20 g) . |
|
|
|
RMN-1!! (DMSO-dg) δ: |
3, 73 (2H, s) |
, 7,35(2H,d,J=8, |
5Hz), 7,57(2H, |
d,J=8,8Hz), 10,30(lH,s).
Exemplo Referencial 352
Petição 870180138821, de 08/10/2018, pág. 490/857
482
Dissolveu-se 2-amino-5-cloro-piridina (3,85 g) em acetato de etila (60 ml), e adicionou-se cloreto de cloroacetila (2,39 ml) à temperatura ambiente, agitando a mistura por 1 h. Depois de aquecer e agitar a mistura da reação a
60 °C por 30 min, adicionou-se mais cloreto de cloro-acetila (0,5 ml), e a mistura foi agitada a 60 °C por mais 1 h. O pó depositado foi coletado por filtração, para obter o composto do título (6,18 g) .
βΜΝ-Ή (DMSO-de) δ: 4,36(2H,s), 7, 94 (1H, dd, J=8,8, 2,7Hz),
8,09(1H,d,J=8,8Hz), 8,40(1H,d,J=2,7Hz), ll,03(lH,s).
Exemplo Referencial 353
S-{2-[(5-cloro-piridin-2-il)-amino]-2-oxoetil}-tiossulfato de sódio:
Uma solução aquosa (130 ml) de tiossulfato de 15 sódio pentaidratado (6,35 g) e bicarbonato de sódio (2,15 g) foi adicionada a uma solução do composto obtido no Exemplo Referencial 352 (6,18 g) em etanol (130 ml) de uma só vez a °C sob agitação, e a mistura foi aquecida sob refluxo a 110 °C por 2 h. A mistura da reação foi concentrada até obter sólidos, sob pressão reduzida, e adicionou-se etanol (500 ml) ao resíduo. A mistura resultante foi aquecida e extraída duas vezes. O extrato foi concentrado até cerca de
Petição 870180138821, de 08/10/2018, pág. 491/857
483
1/20 do volume, e adicionou-se dietil-éter. Os insolúveis depositados foram coletados por filtração, para obter o composto do título (6,65 g).
ΚΜΝ-^ (DMSO-de) δ : 3,77 (2H,s), 7,89 (1H, dd, J=9,0, 2,7Hz), 5 8,09 (lH,d, J=9,OHz) , 8, 34 (1H, d, J=2, 7Hz) , 10,57(lH,s).
Exemplo Referencial 354 cloridrato de N-{(IR,2S,5S)-2-[(2-cloro-acetil)-amino]-5[(dimetil-amino)-carbonil]-ciclo-hexil}-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto obtido no Exemplo Referencial 253 (100 mg) foi dissolvido em acetato de etila (10 ml), e adicionouse cloreto de cloro-acetila (21,6 μΐ), aquecendo e agitando a mistura a 60 °C por 30 min. Depois de deixar a mistura da reação resfriar, os insolúveis foram coletados por filtração e dissolvidos em cloreto de metileno/metanol, e o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título bruto (112 mg).
RIM-1!! (DMSO-de) δ: 1,35-1,50 (1H,m) , 1,55-2, 00 (5H,m) , 2,78(3
H,s), 2,98(3H,s), 3, 00-3, 25 (5H, m) , 3,17(3H,s), 3,80-3,90 (lH,m), 3, 96 (1H, d, J=12, 9Hz) , 4, 00-4, 15 (1H, m) , 4,02(lH,d,J=
Petição 870180138821, de 08/10/2018, pág. 492/857
484
12,9Hz), 4,45—4,70(2Η,m), 7, 85-8, 00(1Η, br) , 8,12(lH,d,J=
7,3Hz), 8,35(1H,d,J=8,3Hz).
MS (ESI) m/z: 442(M+H)+.
Exemplo Referencial 355
S-{2-[((1S,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-amino]-2-oxoetil}-tiossulfato de sódio:
O composto obtido no
Exemplo
Referencial 354 (106 mg) foi dissolvido em etanol (1,5 ml), e adicionou-se uma solução aquosa de tiossulfato de sódio pentaidratado (55 mg) e bicarbonato de sódio (18,6 mg) de uma só vez a 90 °C sob agitação. A mistura resultante foi aquecida sob refluxo por 1 h. A mistura da reação foi concentrada até obter sólidos, sob pressão reduzida, e adicionou-se etanol (10 ml) ao
|
resíduo. A |
mistura resultante |
foi aquecida |
e extraída. |
0 |
|
extrato foi |
concentrado até |
cerca de k |
do volume, |
e |
|
adicionou-se |
éter isopropílico |
(10 ml). |
Os insolúveis |
|
depositados |
foram coletados por filtração, |
para obter |
o |
|
composto do |
título (72 mg). |
|
|
|
RMN-1!! (DMSO-de) δ: 1, 35-1,50 (1H, m) , 1,55-1,90 (5H, m) , 2,40 de 08/10/2018, pág. 493/857
485 (3H,s), 2,78(3H,s), 2, 80-3, 10(5H,m), 2,96(3H,s), 3,44(1H, d, J=14,2Hz), 3, 50(1H, d,J=14,2Hz), 3,68(2H,s), 3,75-3,90(1H,m), 4,45-4,50(lH,m), 8,01(1H,d,J=7,4Hz), 8,15(1H,d,J=8,3Hz).
Exemplo Referencial 356
2-[(5-cloro-tien-2-il)-amino]-2-oxoacetato de metila:
n 'S
Adicionou-se trietil-amina (1,25 ml) e difenilfosforil-azida (1,55 ml) a uma suspensão de ácido 5-clorotiofeno-2-carboxílico (0,99 g) em tolueno (20 ml) , e a mistura foi agitada a 80 °C por 1 h. Depois de resfriar a mistura da reação até a temperatura ambiente, adicionou-se t-butanol (2 ml) , e a mistura foi aquecida sob refluxo por 19 h. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno (200 ml) ao resíduo resultante. A mistura resultante foi lavada sucessivamente com água destilada, uma solução aquosa a 10% de ácido cítrico, água destilada, uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi submetido a uma cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1), para obter 5-cloro-2-tienil-carbamato de t-butila (1,05 g).
RMN-1!! (CDC3) δ: l,51(9H,s), 6, 21 (1H, d, J=3,1Hz) , 6,60(lH,d, de 08/10/2018, pág. 494/857
486
J=3,1Hz), 6,91(lH,br,s).
MS (ESI) m/z: 234(M+H)+.
Depois disso, o produto obtido acima (1,87 g) foi adicionado a uma solução 4 N (40 ml) de ácido clorídrico em dioxano, a mistura foi agitada à temperatura ambiente por 4 h, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi colocado em suspensão em tetraidrofurano (50 ml), e adicionou-se bicarbonato de sódio (2,02 g) e cloro-oxoacetato de metila (0,883 ml) sob resfriamento com gelo, agitando a mistura à temperatura ambiente por 18 h. Depois de remover o solvente por destilação sob pressão reduzida, e adicionar água e cloreto de metileno ao resíduo, para conduzir separação de líquidos, a camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro, e depois concentrada sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (1,44 g).
RMN-1!! (CDC3) δ: 3,98(3H,s), 6, 61 (1H, d, J=4,2Hz) , 6,75(lH,d,
J=4,2Hz), 9, 42 (lH,br, s) .
MS (FAB) m/z: 220(M+H)+.
Exemplo Referencial 357
2-[(5-flúor-piridin-2-il)-amino]-2-oxoacetato de metila:
de 08/10/2018, pág. 495/857
487 composto do título foi obtido a partir de 2amino-5-flúor-piridina e cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 242.
ΗΜΝ-^ (CDC3) δ: 3,99(3H,s), 7, 48-7, 53 (1H, m) , 8,21(lH,d,
J=2,9Hz), 8,27-8,31(lH,m), 9,41(1H,br,s).
MS (FAB) m/z: 198(M+H)+.
Exemplo Referencial 358
2-[4-cloro-2-(trifllúor-metii)-anilino]-2-oxoacetato de
O composto do título foi obtido a partir de 4cloro-2-triflúor-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 242.
RMN-!H (CDC3) δ: 4,01(3H,s), 7,58(lH,dd, J=8, 8,2,2Hz) , 7,65 (1H,d,J=2,2Hz), 8,34(1H,d,J=8,8Hz), 9,30(1H,br,s) .
MS (EI) m/z: 281(M+H)+.
Exemplo Referencial 359 ácido 2-[4-clor0-2-(trifllúor-metii)-anilino]-2-oxoacético:
Petição 870180138821, de 08/10/2018, pág. 496/857
488
Adicionou-se hidróxido de lítio (28 mg) a uma solução do composto obtido no Exemplo Referencial 358 (297 mg) em um solvente misto de tetraidrofurano (7 ml) e água (3 ml), e a mistura foi agitada à temperatura ambiente por 2 h. Adicionou-se ácido clorídrico 1 N (8 ml) e cloreto de metileno (20 ml) à mistura da reação, para conduzir separação de líquidos. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi secado, para obter o composto do título (291 mg).
ΗΜΝ-^ (CDC3) δ: 7, 61 (1H, dd, J=8,8, 2,5Hz), 7,68(lH,d,J=
2,5Hz), 8,26(1H,d,J=8,8Hz), 9,36(1H,br,s).
Exemplo Referencial 360 5-cloro-N,N-dimetil-2-nitro-benzamida:
O composto do título foi obtido condensando o ácido 5-cloro-2-nitro-benzóico com dimetil-amina, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 143.
RMN-1!! (CDC3) Ô: 2,86(3H,s), 3,16(3H,s), 7,38 (1H, d, J=2,2Hz) , 7,51(1H,dd,J=8,8,2,2Hz), 8,15 (lH,d, J=8, 8Hz).
Exemplo Referencial 361
2-amino-5-cloro-N,N-dimetil-benzamida:
de 08/10/2018, pág. 497/857
489
Adicionou-se cloreto de ferro (III) hexaidratado (9,93 g) e zinco em pó (8,01 g) a uma solução do composto obtido no Exemplo Referencial 360 (2,8 g) em um solvente misto de N,N-dimetilformamida (80 ml) e água (40 ml), e a mistura foi aquecida sob refluxo por 20 min. A mistura da reação foi filtrada através de Celite 545, e adicionou-se acetato de etila (200 ml) ao filtrado, para conduzir separação de líquidos. A camada aquosa resultante foi lavada com acetato de etila (2 x 100 ml) , e as camadas orgânicas foram combinadas, lavadas com água destilada e secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi submetido a uma cromatografia de coluna em sílica-gel (cloreto de metileno:hexano 1:1 1:0, e depois metanol:cloreto de metileno 1:100), para obter o composto do título (2,41 g).
RMN-1H (CDC3) δ: 3,13(6H,s), 4,33(2H,br), 6, 65 (1H, d, J=8,5
Hz), 7,07(1H,d,J=2,2Hz), 7,11(1H,dd,J=8,5,2,2Hz).
MS (ESI) m/z: 240(M+MeCH)+.
Exemplo Referencial 362
2-{4-cloro-2-[(dimetil-amino)-carbonil]-anilino}-2oxoacetato de metila:
de 08/10/2018, pág. 498/857
490
O composto do título foi obtido a composto obtido no Exemplo Referencial 361 oxoacetato de metila, de uma maneira similar processo descrito no Exemplo Referencial 242.
partir do e cloroàquela do
RMN-XH
2,4Hz), (CDC3) δ: 3,09(6H,br),
7,41(1H,d,J=8,8, 2,4Hz),
3,9613H,s), 7,30(lH,d,J=
8,34(1H, d,J=8,8Hz), 10,46 (lH,br) .
MS (ESI) m/z: 285(M+H)+.
Exemplo Referencial 363
4-cloro-2-metóxi-anilina:
O composto do título foi obtido a partir de 5cloro-2-nitro-anisol, de uma maneira similar àquela do processo descrito no Exemplo Referencial 361.
RMN-XH (CDC3) δ: 3, 65-3, 95 (2H, br) , 3,87(3H,s), 6,61(lH,d,
J=8,8Hz), 6, 74-6, 78 (2H,m) .
MS (ESI) m/z: 199(M+MeCN+H)+.
Exemplo Referencial 364
2-(4-cloro-2-metóxi-anilino)-2-oxoacetato de metila:
Petição 870180138821, de 08/10/2018, pág. 499/857
491
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 363 e clorooxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo Referencial 242.
RMN-1!! (CDCL3) δ: 3,92(3H,s), 3,97(3H,s), 6, 90 (1H, d, J=2,2Hz) , 6,98(1H,dd,J=8,8, 2,2Hz), 8,35(1H,d,J=8,8HZ), 9,33-9,44(1H, br) .
MS (ESI) m/z: 244 (M+H)+.
Exemplo Referencial 365
2-(4-cloro-anilino)-2-(hidróxi-imino)-acetato de etila:
O composto do título foi obtido a partir de 4cloro-anilina (3,03 g) e 2-cloro-2-hidróxi-imino-acetato de etila, de uma maneira similar àquela do processo descrito na literatura (Gilchrist, T. L.; Peek, Μ. E.; Rees, C. W.; J.
Chem. Soc. Chem. Commun., 1975, 913).
RMN-1!! (CDC3) δ: 1, 26 (3H, t, J=7,1Hz) , 1, 60-1,80 (1H, br) , 4,28 (2H,q,J=7,lHz), 6, 85(2H,d,J=8,6Hz), 7,24(2H,d,J=8,6Hz),
8,15-8,45(lH,br).
Petição 870180138821, de 08/10/2018, pág. 500/857
492
MS (ESI) m/z: 243(M+H)+.
Exemplo Referencial 366 (IR,2S,5S)-2-{[2-(4-cloro-anilino)-2-(hidróxi-imino)acetil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil5 carbamato de t-butila:
composto obtido no Exemplo Referencial 144 (597 mg) foi adicionado a uma solução do composto obtido no Exemplo Referencial 365 (350 mg) em etanol (5,0 ml), e a mistura foi agitada a 70 °C por 3 dias. Depois disso, a mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 30:1), para obter o composto do título (180 mg).
ΗΜΝ-^ (CD3OD) δ: l,46(9H,s), 1,47-1,84 (6H, m) , 1,88- 1,95 (lH,m), 2,90(3H,s), 3,08(3H,s), 3, 90-3, 97 (1H, m) , 4,11- 4,17 (lH,m), 6,84(2H,d,J=8,8Hz), 7,18(2H,d,J=8,8Hz).
MS (ESI) m/z: 504(M+Na)+.
Exemplo Referencial 367 (3R,4S)-4-{[2-(4-cloro-anilino)-2-oxoacetii]-amino}-!-(220 metóxi-acetii)-piperidin-3-il-carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 501/857
493 γν
Ο composto do título foi obtido a partir do composto obtido no Exemplo Referencial 374 e do composto obtido no Exemplo Referencial 220, de uma maneira similar àquela do processo descrito no Exemplo Referencial 214.
RMN-!H (CDC3) δ: l,45(9H,s), 1, 55-1,75 (1H, br) , 1,94-2,07 (lH,br), 2,70-3, 00 (lH,m) , 3, 10-3, 37 (1H, m) , 3,44(3H,s), 3,884,22(4H,m), 4,55-4,69(1H,br), 4,80-4,90(0,51-1,br), 5,365,48(0,5H,br), 7, 20-7, 30(1H,br) , 7,32(2H,d,J=8,8Hz), 7,62 (2H,d,J=8,8Hz), 8,20-8,40(1H,br), 9,15-9,25(1H,br).
MS (ESI) m/z: 469(M+H)+.
Exemplo Referencial 368 (3R,4S)-4-({2-[(5-cloro-piridin-2-il)-amino]-2-oxoacetil}amino)-1-(2-metóxi-acetil)-piperidin-3-il-carbamato de tbutila:
O composto do título foi obtido a partir do
Petição 870180138821, de 08/10/2018, pág. 502/857
494 composto obtido no Exemplo Referencial 266 e do composto obtido no Exemplo Referencial 220, de uma maneira similar àquela do processo descrito no Exemplo Referencial 214.
ΗΜΝ-^ (CDC3) δ: l,45(9H,s), 1, 65-2, 30 (2H, br) , 2,68- 3,02 (lH,m), 3,10-3,35(lH,m) , 3,44(3H,s), 3, 80-4,25(4H, m) , 4,454,70(lH,m), 5,05-5,20(0,5H,m), 5,80-5,93(0,5H,m), 7,307,40 (lH,br), 7,71(lH,br d,J=8,7Hz), 7,95-8,05 (0,3H, br) ,
8,19 (lH,brd,J=8,8Hz), 8,31(1H,br,s), 8,38-8,53(0,7H,br), 9, 74-9, 84 (lH,br) .
MS (ESI) m/z: 470(M+H)+.
Exemplo Referencial 369 (3R,4S)-4-({2-[(5-bromo-piridin-2-il)-amino]-2-oxoacetil}amino)-1-(2-metóxi-acetil)-piperidin-3-il-carbamato de tbutila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 375 e do composto obtido no Exemplo Referencial 220, de uma maneira similar àquela do processo descrito no Exemplo Referencial 214.
RMN-!H (CDC3) δ: l,47(9H,s), 1, 50-1,75 (1H, m) , 1,95- 2,13(1H, br), 2,70-2, 98 (lH,m), 3, 05-3, 36 (1H, m) , 3,45(3H,s), 3,804,24(4H,m), 4,57-4,73(1H,br) , 4, 85-4,95(0,25H,br) , 5,10-5,15
Petição 870180138821, de 08/10/2018, pág. 503/857
495 (0,25H,br), 5, 45—5, 58(Ο,5H,br), 7,30-7,38(11-1, m) , 7,84 (1Η,dd,J=8,8,2,2Hz), 8, 16(1Η, d,J=8,8Ηζ), 8,30-8,55(1Η,br),
8,4 0(1Η,d,J=2,2Ηζ), 9, 68(1Η,br,s) .
Exemplo Referencial 370
3-(4-cloro-anilino)-3-oxopropionato de etila:
Adicionou-se sucessivamente etil-malonato de potássio (3,2 g) , 1-hidróxi-benzotriazol (2,1 g) e cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (4,5 g) a uma solução de 4-cloro-anilina (2,0 g) em N,N10 dimetil-formamida (20 ml) à temperatura ambiente, e a mistura foi agitada à temperatura ambiente por 2 h. A mistura da reação foi diluída com acetato de etila e lavada com uma solução aquosa saturada de bicarbonato de sódio, uma solução aquosa a 10% de ácido cítrico e solução aquosa saturada de cloreto de sódio. Depois disso, a camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (4,0 g).
RPIN-iH (CDC3) δ: 1,33 (3H, t, J=7,3Hz) , 3,47(2H,s), 4,26(2H, q,J=7,3Hz), 7, 29(2H,d,J=8,8Hz), 7,51(2H,d,J=8,8Hz) , 9,32 (1H, br, s) .
Exemplo Referencial 371 ácido 3- (4-cloro-anilino)-3-oxopropiônico:
Petição 870180138821, de 08/10/2018, pág. 504/857
496
Uma solução 1 N de hidróxido de sódio (10 ml) foi adicionada em gotas a uma solução do composto obtido no Exemplo Referencial 370 (1,0 g) em etanol (10 ml) à temperatura ambiente, e a mistura foi agitada por 2 h.
Adicionou-se ácido clorídrico 1 N (10 ml) à mistura da reação, a mistura foi agitada, a os insolúveis foram depositados e depois coletados por filtração, para obter o composto do título (0,5 g).
RMN-1!! (DMSO-de) δ: 3, 34 (2H, s) , 7, 35 (2H, d, J=8, 8Hz) , 7,59 (2H, d, J=8,8Hz) , 10,26(lH,s), 12, 66 (1H, br, s) .
Exemplo Referencial 372 3-(3-cloro-anilino)-3-oxopropionato de etila:
O composto do título foi obtido condensando 3cloro-anilina com etil-malonato de potássio, de uma maneira similar àquela do processo descrito no Exemplo Referencial
370.
RMN-1!! (CDC3) δ: 1, 33 (3H, t, J=7, 3Hz) , 3,47(2H,s), 4,26 (2H,q,J=7,3Hz), 7,09(1H,d,J=8,8Hz), 7,22-7,26(1H,m), 7,39 (1H, d, J=8, 8Hz) , 7,69(lH,s), 9, 35 (1H, br, s) .
Petição 870180138821, de 08/10/2018, pág. 505/857
497
Exemplo Referencial 373 ácido 3- (3-cloro-anilino)-3-oxopropiônico:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 372, de uma maneira similar àquela do processo descrito no Exemplo Referencial
371.
ΚΜΝ-^ (DMSO-de) δ: 3,35(2H,s), 7,11 (1H, d, J=8,8Hz) , 7,33 (1H,t,J=8,8Hz), 7,39(1H,d,J=8,8Hz), 7,78(lH,s), 10,31(lH,s),
12,67(1H,br,s).
Exemplo Referencial 374 ácido 2-(4-cloro-anilino)-2-oxoacético:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 242, de uma maneira similar àquela do processo descrito no Exemplo Referencial
359.
RMN-1!!, (DMSO-de) δ: 7,37 (2H, d, J=8, 8Hz) , 7,79 (2H, d, J=8, 8Hz) , 10,66(1H,s).
Petição 870180138821, de 08/10/2018, pág. 506/857
498
Exemplo Referencial 375 ácido 2-[(5-bromo-piridin-2-il)-amino]-2-oxoacético:
composto do título foi obtido a partir do
|
composto obtido |
no |
Exemplo Referencial |
262, de |
uma maneira |
|
5 similar àquela |
do |
processo descrito no |
Exemplo |
Referencial |
|
359. |
|
|
|
|
|
RMN-íH (DMSO-de) |
Ô: |
7, 95-8, 00 (lH,m) , 8, 08 (1H, dd, J= |
=8,8,2,OHz), |
8,50(1H,d,J=2,OHz), 10,74(lH,s).
Exemplo Referencial 376 ácido 4-cloro-3-flúor-benzóico:
Adicionou-se clorito de sódio (17 g) parceladamente a uma solução de 4-cloro-3-flúor-benzaldeído (10 g), ácido amido-sulfúrico (18 g) , álcool t-butílico (50 ml) e água (50 ml) , sob resfriamento com gelo, e a mistura foi agitada por 4 dias, enquanto a temperatura do sistema era aumentada gradualmente até a temperatura ambiente. A mistura da reação foi diluída com acetato de etila e lavada
Petição 870180138821, de 08/10/2018, pág. 507/857
499 com água, ácido clorídrico 1 N e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, e remover o solvente por destilação sob pressão reduzida, o resíduo resultante foi recristalizado em um solvente misto de éter diisopropílico e hexano, para obter o composto do título (11,2 g).
βΜΝ-^ (DMSO-de) δ: 7,72(1H,dt,J=8,3,1,5Hz), 7,77(lH,dt,
J=8,3,1,6Hz), 7,82(1H,dt,J=9,7,1,5Hz), 13,45(lH,s).
Exemplo Referencial 377
2-(4-cloro-3-flúor-anilino)-2-oxoacetato de metila:
O composto do título foi obtido submetendo o composto obtido no Exemplo Referencial 376 a uma reação de rearranjo de Curtius e depois condensando este produto com cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo Referencial 356.
RMN-1!! (CDC3) δ: 3,99(3H,s), 7, 25-7, 27 (1H, m) , 7,39(lH,t,J=
8,5Hz), 7,72(1H,dd,J=1O,4,2,4Hz), 8,90 (1H,br,s) .
Exemplo Referencial 378 ácido 2-(4-cloro-3-flúor-anilino)-2-oxoacético:
Petição 870180138821, de 08/10/2018, pág. 508/857
500
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 377, de uma maneira similar àquela do processo descrito no Exemplo Referencial
359.
RMN-1!! (DMSO-dg) δ: 7,52 (1H, t, J=8, 8Hz) , 7, 63 (1H, dd, J=8, 8,
2,2Hz), 7,88(1H,dd,J=12,0, 2,2Hz), 10,83(1H,br,s).
Exemplo Referencial 379 3-(4-cloro-fenil)-3-oxopropionato de etila:
|
|
Adicionou- |
se trietil-amina |
(17 ml) |
e cloreto |
de |
|
10 magnésio |
(5,5 |
g) |
a uma suspensão |
de etil-malonato |
de |
|
potássio |
(8,2 |
g) |
em acetato de |
etila |
(100 ml) |
sob |
resfriamento com gelo, e a mistura foi agitada por 18 h, enquanto a temperatura do sistema era aumentada gradualmente até a temperatura ambiente. Por outro lado, uma suspensão composta de ácido 4-cloro-benzóico (5,0 g), cloreto de tionila (12 ml), N,N-dimetil-formamida (1 gota) e tolueno (100 ml) foi aquecida sob refluxo por 1 h, e a mistura da reação foi então concentrada. O resíduo resultante foi dissolvido em acetato de etila, e a solução foi adicionada
Petição 870180138821, de 08/10/2018, pág. 509/857
501 em gotas à mistura da reação preparada anteriormente, sob resfriamento com gelo. A mistura resultante foi agitada por 18 h, enquanto a temperatura do sistema era elevada gradualmente até a temperatura ambiente. Adicionou-se uma solução aquosa a 10% de ácido cítrico à mistura da reação, e a mistura foi agitada por 30 min, para separar a camada orgânica resultante. A camada orgânica foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi isolado e purificado por cromatografia de coluna em sílicagel (clorofórmio), para obter o composto do título (6,4 g). ΗΜΝ-Ή (CDC3) δ: 1,26 (3H, t, J=7,3Hz) , 3,96(2H,s), 4,21(2H,q,
J=7,3Hz), 7,46(2H,d,J=8,8Hz), 7,89(2H,d,J=8,8Hz).
Exemplo Referencial 380
3-(4-cloro-fenil)-3-hidróxi-propionato de etila:
Adicionou-se boro-hidreto de sódio (0,2 g) parceladamente a uma solução do composto obtido no Exemplo Referencial 379 (1, 0 g) em tetraidrofurano (10 ml), e a mistura foi agitada por 2 h, enquanto a temperatura do sistema era elevada gradualmente até a temperatura ambiente. Adicionou-se uma solução aquosa a 10% de ácido cítrico à mistura da reação, e a mistura resultante foi extraída com de 08/10/2018, pág. 510/857
502 acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi isolado e purificado por cromatografia de coluna em sílica-gel (clorofórmio), para obter o composto do título (0,56 g).
RMN-1H (CDC3) δ: 1,27 (3H, t, J=7, 3Hz) , 2, 70 (1H, d, J=7,8Hz) , 2,71 (1H,d,J=3,4Hz), 3,37 (1H,d,J=3,4Hz), 4,18(2H,q,J=7,3 Hz) ,
5,09—5,13(1H,m), 7,30-7,35(5H,m).
Exemplo Referencial 381 ácido 3-(4-cloro-fenil)-3-hidróxi-propiônico:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 380, de uma maneira similar àquela do processo descrito no Exemplo Referencial
359.
RMN-iH (DMSO-de) δ: 3, 25-3, 32 (1H, m) , 4, 89-4, 95 (1H, m) , 5,455,53(lH,m), 7,35-7,36(5H,m), 12,11-12,18(1H,m).
MS (ESI,anion) m/z: 198(M-H).
Exemplo Referencial 382 (lR,2S,5S)-2-{[3-(4-cloro-fenil)-3-hidróxi-propanoil]amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 511/857
503
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 144 com o composto obtido no Exemplo Referencial 381, de uma maneira similar àquela do processo descrito no Exemplo Referencial 91.
RMN-1!! (CDC3) δ: 1,21-1,44 (2H, m) , l,46(9H,s), 1,76-1,92 (2H,m), 1, 95—2,10(2H,m), 2,40—2,55(2H,m), 2,55—2, 68(1H,m),
2,94(3H,s), 3,05(3H,s), 3, 82-3, 96 (1H, m) , 4,02-4, 17 (1H, m) ,
4,65-4,80(2H,m), 5,03-5,13(1H,m), 7,28-7,33(5H,m).
MS (ESI) m/z: 468(M+H)+.
Exemplo Referencial 383 (lR,2S,5S)-2-{[3-(4-cloro-fenil)-3-oxopropanoil]-amino} - 5[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de tbutila:
Petição 870180138821, de 08/10/2018, pág. 512/857
504
Adicionou-se dióxido de manganês (0,47 g) a uma solução do composto obtido no Exemplo Referencial 382 (0,5
g) em 1.4-dioxano (20 ml) à temperatura ambiente, e a mistura foi agitada por 4 dias. Os insolúveis foram removidos por filtração através de um leito de Celite, e o filtrado resultante foi concentrado sob pressão reduzida, para obte ro composto do título (0,46 g).
ΚΜΝ-^ (DMSO-de) δ: 1,28-1, 39 (lH,m) , l,40(9H,s), 1,41-1,63 (3H,m), 2,25-2,42(2H,m), 2,76(3H,s), 2,90-2,97(1H,m), 2,98 (3H,s), 3,56(2H,s), 3, 89-3, 97 (1H, m) , 4,88-4,98 (1H, m) , 6,656,70(lH,m), 7,30-7,35(4H,m), 7,33(1H,dd,J=2,9,1,7Hz).
MS (ESI,anion) m/z: 464(M-H).
Exemplo Referencial 384 (IS,3R,4R)-4-azido-3-[(t-butóxi-carbonil)-amino]-ciclo15 hexano-carboxilato de etila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 248, de uma maneira similar àquela do processo descrito no Exemplo Referencial
249.
[0C]25d = +62° (c = 1, clorofórmio) .
RMN-1!! (CDC3) δ: 1, 27 (3H, t, J=7,1Hz) , l,46(9H,s), l,61(lH,s),
1,61-1,71(2H,m) , 1,81-1,90(1H,m) , 1, 97-2, 03(1H,m) , 2,22Pclição 870180138821, de 08/10/2018, pág. 513/857
505
2,28(lH,m), 2,56-2,60(1H,m), 3,54(1H,br,s), 3,63-3,68(1H,m), 4,16(2H,q,J=7,1Hz), 4,58(1H,br,s).
Exemplo Referencial 385 (IR,2R,5S)-2-azido~5-[(dimetil-amino-carbonil)-ciclo-hexil5 carbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 384, de uma maneira similar àquelas dos Exemplos Referenciais 250 e 251.
RMN-1!! (CDC3) δ: l,46(9H,s), 1, 40-2, 20 (6H, m) , 2,70-2, 80 (1H,
m) , 2,93(3H,s), 3,03(3H,s), 3, 60-3, 78 (1H, m) , 3, 83-3, 95 (1H,
m), 4,65(1H,d,J=7,2Hz).
Exemplo Referencial 386 (IR,2R,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-2oxoacetil}-amino)-5-[(dimeti1-amino-carboni1)-ciclo-hexil-
Pclição 870180138821, de 08/10/2018, pág. 514/857
506
O composto do título foi obtido convertendo o grupo azida do composto obtido no Exemplo Referencial 385 em um grupo amino, de uma maneira similar àquela do processo descrito no Exemplo Referencial 90, e depois condensando este produto com o composto obtido no Exemplo Referencial 266, de uma maneira similar àquela do processo descrito no Exemplo Referencial 91.
ΗΜΝ-^ (CDC3) δ: 1, 13-2,25 (16H, m) , 2,94(3H,s), 3,03(3H,s),
3,60-3,78(lH,m), 4,13-4,31(1H,m), 4,45-4,65(1H,m), 7,8O(1H, dd,J=8,8,2,4Hz), 8,03(1H,br,s), 8,21(1H,d,J=8,8Hz), 8,29(1H, d,J=2,4Hz), 9, 71(1H,s) .
MS (ESI) m/z: 468(M+H)+.
Exemplo Referencial 387
N-{(IR,2R,5S)-2-azido-5-[(dimetil-amino-carbonil)-ciclohexil }-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 385 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do processo descrito no Exemplo Referencial 252.
ΗΜΝ-^ (CDC3) δ: 1,75-2,08 (6H, m) , 2, 20-2, 32 (1H, m) , 2,51(3H,
Petição 870180138821, de 08/10/2018, pág. 515/857
507
s) , 2,75—2, 97 (4H, m) , 2,95(3H,s), 3,04(3H,s), 3, 65-3, 80 (3H,
m), 4,27-4,39(lH,m), 7,17-7,28(1H,m).
MS (ESI) m/z: 392(M+H)+.
Exemplo Referencial 388
4-[(2-metóxi-2-oxoacetil)-amino]-piperidino-l-carboxilato de t-butila:
O composto do título foi obtido a partir de (4amino-N-t-butóxi-carbonil)-piperidina e cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo Referencial 242.
RMN-iH (DMSO-de) δ: l,46(9H,s), 1, 34-1,51 (2H, m) , 1, 89-1, 98 (2 H,m), 2, 82-2, 96 (2H,m) , 3,91(3H,s), 3, 88-4, 14 (3H, m) , 6,967,07 (lH,m) .
MS (FAB) m/z: 287(M+H)+.
Exemplo Referencial 389
4-{[2—({(lR,2S,5S)-2-{[2-[(5-cloro-indol-2-il)-carbonil]amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-amino)-2oxoacetil]-amino}-piperidino-l-carboxilato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 516/857
508
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 310 e do composto obtido no Exemplo Referencial 388, de uma maneira similar àquela do processo descrito no Exemplo Referencial 191.
ΡΜΝ-^ (DMSO-de) δ: l,46(9H,s), 1,35-2, 28 (11H, m) , 2,70-3,18 (9H,m), 3, 80-4,57 (4H,m) , 6,78(lH,s), 7, 15-8, 12 (6H, m) , 9,45 (lH,s) .
MS (FAB) m/z: 617(M+H)+.
Exemplo Referencial 390
2-[(5-cloro-piridin-2-il)-(metil)-amino]-2-oxoacetato de metila:
O composto do título foi obtido a partir de 5cloro-N-metil-2-piridinoamina e cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no
Exemplo Referencial 242.
RMN-1!! (CDC3) δ: 3,43(3H,s), 3,81(3H,s), 7, 08 (1H, br, s) , 7,687,78(lH,m), 8,27 (ΙΗ+br, s) .
MS (ESI) m/z: 229(M+H)+.
Exemplo Referencial 391
2-[(5-cloro-pirimidin-2-il)-(metil)-amino]-2-oxoacetato de
Petição 870180138821, de 08/10/2018, pág. 517/857
509
O composto do título foi obtido a partir de 2amino-5-cloro-pirimidina e cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 242.
RMN-XH (CDC3) δ: 4,00(3H,s), 8,63(2H,s), 9, 58 (1H, br, s) .
MS (ESI) m/z: 215(M+H)+.
Exemplo Referencial 392
N-((1R,2S,5S)-2-azido-5-{[etil-(metil)-amino]-carbonil}ciclo-hexil)-5-metil-5,6-diidrotiazolo-4H-pirrolo[3,4-d]10 tiazolo-2-carboxamida:
N,
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 323 e do composto obtido no Exemplo Referencial 293, de uma maneira similar àquela do processo descrito no Exemplo Referencial 252.
RMN-XH (CDC3) δ: 1,08, l,15(3H,cada t,J=7,lHz), 1,74-1,88 (4H,m), 2, 12-2,22 (2H,m) , 2,67(3H,s), 2, 81-2, 86 (lH,m) , 2,89,
2,96(3H,cada s), 3,28-3,43(2H,m), 3,91-4,10(5H,m), 4,60-4,62 (lH,m), 7,21(1H,d,J=7,6Hz).
MS (ESI) m/z: 392(M+H)+.
Exemplo Referencial 393
2-(4-cloro-3-metóxi-anilino)-2-oxoacetato de metila:
Petição 870180138821, de 08/10/2018, pág. 518/857
510
O composto do título foi obtido reduzindo 2-cloro5-nitro-anisol, de uma maneira similar àquela do processo descrito no Exemplo Referencial 361, para um derivado amino, e depois condensando o derivado amino com cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo Referencial 242.
ΗΜΝ-^ (CDC3) δ: 3,93(3H,s), 3,98(3H,s), 7, 00 (1H, dd, J=8, 5,
2,4HZ), 7,33(1H,d,J=8, 5Hz) , 7,57 (1H,d,J=2,4Hz) , 8,89(1H, br, s) .
Exemplo Referencial 394 ácido 2-(4-cloro-3-metóxi-anilino)-2-oxoacético:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 393, de uma maneira similar àquela do processo descrito no Exemplo Referencial
359.
ΗΜΝ-^ (DMSO-de) δ: 3,81(3H,s), 7, 36 (1H, d, J=8,7Hz) , 7,43 (1H,d,J=8,7Hz), 7,65(1H,d,J=2,2Hz), 10,79(lH,s).
MS (ESI, anion) m/z: 228(M-H)-.
Petição 870180138821, de 08/10/2018, pág. 519/857
511
Exemplo Referencial 395
N1- {(1S,2R,4S)-2-amino-4-[(dimetil-amino)-carbonil]-ciclohexil } -N2-(4-cloro-3-metóxi-fenil)-etanodiamida:
composto do título foi obtido condensando o 5 composto obtido no Exemplo Referencial 144 com o composto obtido no Exemplo Referencial 394, de uma maneira similar àquela do processo descrito no Exemplo Referencial 97, tratando este produto com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo Referencial
69, e depois neutralizando-o com uma solução aquosa 1 N de hidróxido de sódio.
RMN-XH (CDC3) δ: 1,4 8-2, 0 0 (8H, m) , 2, 84-2, 93 (1H, m) , 2,95(3H,
s), 3,08(3H,s), 3, 33-3, 35 (lH,m) , 3, 89-3, 94 (4H, m) , 7,O6(1H, dd,J=8,5,2,2Hz), 7,32(1H,d,J=8,5Hz), 7,56(1H, d, J=2,2Hz) ,
8,05(1H,d,J=8,5Hz), 9,43(1H,br,s).
MS (ESI) m/z: 397 (M+) .
Exemplo Referencial 396 2-(4-etinil-anilino)-2-oxoacetato de metila:
Petição 870180138821, de 08/10/2018, pág. 520/857
512
composto do título foi obtido a partir de 4etinil-anilina e cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo Referencial
242.
ΗΜΝ-^ (CDC3) δ: 3,09(lH,s), 3,98(3H,s), 7,50 (2H, d, J=8, 4Hz) ,
7,62(2H,d,J=8,4Hz), 8, 89(1H,br,s) .
Exemplo Referencial 397
2-(4-etinil-anilino)-2-oxoacetato de sódio:
NaO
O composto do título foi obtido hidrolisando o 10 composto obtido no Exemplo Referencial 396 com hidróxido de sódio, de uma maneira similar àquela do processo descrito no
Exemplo Referencial 266.
ΗΜΝ-^ (DMSO-de) δ: 4,06(lH,s), 7, 39 (2H, d, J=8,4Hz) , 7,80(2H, d,J=8,4Hz), 10, 33 (lH,br, s) .
Exemplo Referencial 398
2-[(5-cloro-pirazin-2-il)-amino]-2-oxoacetato de metila:
Petição 870180138821, de 08/10/2018, pág. 521/857
513 composto do título foi obtido a partir de 4amino-5-cloro-pirazina, sintetizada de acordo com a literatura (Sato, Nobuhiro et al., J. Heterocycl. Chem. 19(3):673-4, 1982) e cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 242.
ΗΜΝ-^ (CDC3) δ: 4,02(3H,s), 8, 35 (1H, d, J=l, 5Hz) , 9,37(lH,d,
J=l,5Hz), 9,41(lH,br,s).
MS (FAB) m/z: 216(M+H)+.
Exemplo Referencial 399 ácido 2-[(5-cloro-pirazin-2-il)-amino]-2-oxoacético:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 398, de uma maneira similar àquela do processo descrito no Exemplo Referencial
359.
RMN-1!! (DMSO-de) δ: 8,62(lH,s), 9, 02 (1H, br, s) , ll,30(lH,s),
MS (EI) m/z: 201 M+.
Exemplo Referencial 400 ácido 2-(4-cloro-3-nitro-anilino)-2-oxoacético:
Petição 870180138821, de 08/10/2018, pág. 522/857
514
O composto do título foi obtido condensando 4cloro-3-nitro-anilina com cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 242, e depois hidrolisando este produto, de uma maneira similar àquela do processo descrito no Exemplo
Referencial 359.
RMN-iH (DMSO-de) δ: 7, 76 (1H, dd, J=8, 8Hz) , 8, 04 (1H, dd, J=8,8, 2,4Hz), 8,55(1H,d,J=2,4Hz), 11,24 (lH,s).
Nenhum próton atribuível ao ácido carboxílico foi observado. MS (EI) m/z: 244 M+.
Exemplo Referencial 401
2-(4-cloro-2-nitro-anilino)-2-oxoacetato de sódio:
NaO
O composto do título foi obtido condensando 4cloro-2-nitro-anilina com cloro-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo Referencial 242, hidrolisando este produto, de uma maneira similar àquela do processo descrito no Exemplo Referencial 266, dissolvendo o resíduo resultante em metanol, adicionando uma solução aquosa 1 N de hidróxido de sódio, e coletando o precipitado formado por filtração.
RMN-iH (DMSO-de) δ: 7,84 (1H, dd, J=9, 0, 2, 5Hz) , 8,20(lH,d,J=
2,5Hz), 8, 67 (lH,d, J=9,OHz) , ll,89(lH,s).
Petição 870180138821, de 08/10/2018, pág. 523/857
515
Exemplo Referencial 402
6-cloro-4-metil-3-piridino-amina:
Dissolveu-se 2-cloro-4-metil-5-nitro-pindina (173 mg) em etanol (5 ml) , e adicionou-se uma quantidade catalítica de catalisador de níquel de Raney, agitando a mistura à temperatura ambiente por 9 h sob uma atmosfera de hidrogênio. O catalisador foi solvente foi removido por dest O resíduo foi purificado por sílica-gel (hexano:acetato de composto do título (113 mg). RMN-1!! (CDC13) δ: 2,13(3H,s),
7,74 (1H,5).
MS (EI) m/z: 142 M+.
removido por filtração, e o lação sob pressão reduzida, cromatografia de coluna em etila 3:2), para obter o
3, 85 (2H, br, 5) , 6,96(lH,s),
Exemplo Referencial 403
N1-(2-amino-fenil)-N2-(4-cloro-fenil)-etanoamida:
O composto do título foi obtido condensando 1,2Pclição 870180138821, de 08/10/2018, pág. 524/857
516 benzeno-diamina com o composto obtido no Exemplo Referencial
374, de uma maneira similar àquela do processo descrito no
Exemplo Referencial 59.
ΗΜΝ-^ (DMSO—dô) δ: 5, 00 (2H, s) , 6, 59-6, 63 (1H, m) , 6,78(lH,dd,
J=8,l, 1,2Hz), 6, 96—7, 01(1H,m), 7,25(1H,dd,J=7,8, 1,2Hz),
7,44(2H,d,J=8,8Hz), 7,91(2H,d,J=8,8HZ), 10,04(lH,s), 10,91 (1H,5) .
MS (FAB): 290(M+H)+.
Exemplo Referencial 404
N-((1R,2S,5S)-2-azido-5-{[etil-(metil)-amino]-carbonil}ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 323 com ácido clorídrico, realizando a desproteção, e depois condensando este produto com o composto obtido no Exemplo Referencial
10.
RMN-!H (CDC13) δ: 1,08(1/2 de 3H, t, J=7,2Hz) , 1,14(1/2 de 3H, t,J=7,2Hz), 1,70-1,90(4H,m), 2,10-2,25(2H,m), 2,52(3H,s),
2,78-3,00(8H,m), 3,25-3,45(2H,m), 3,69(1H,d,J=13,4Hz), 3,73 (1H,d,J=13,4Hz), 3,87—3,95(lH,m), 4,55-4,62(1H,m), 7,26(1H,
Petição 870180138821, de 08/10/2018, pág. 525/857
517 d,J=7,6Hz).
Exemplo Referencial 405
2-(4-cloro-fenil)-1-hidrazino-carboxilato de fenila:
Dissolveu-se cloridrato de (4-cloro-fenil)hidrazina (3,00 g) em tetraidrofurano (50 ml), adicionou-se dietil-éter (50 ml) e uma solução aquosa saturada de bicarbonato de sódio. Uma camada orgânica foi separada, secada sobre sulfato de sódio anidro, e depois concentrada, dando (4-cloro-fenil)-hidrazina como um sólido marrom. Este produto foi dissolvido em benzeno (15 ml), e a solução foi aquecida sob refluxo, à qual adicionou-sc uma solução dc carbonato de difenila (5,22 g) em benzeno (8,0 ml) foi adicionada em gotas por pelo menos 30 min. Depois de refluxar por 19 h, a mistura da reação foi deixada resfriar, e foi concentrada. Depois, adicionou-se benzeno (15 ml) ao resíduo. A mistura foi submetida a tratamento com ultrasom, dando uma suspensão. Depois de adicionar hexano (50 ml) à suspensão, e agitar a mistura por 30 min, os insolúveis foram coletados por filtração e secados, para dar o composto do título (1,05 g).
RMN-iH (CDC13) δ: 5, 8 6 (H, br, s) , 6, 83-6, 92 (3H, m) , 7,17(1H, br,s), 7,20-7,32(4H,m), 7,37(2H,t,J=7,7Hz).
MS (ESI) m/z: 263(M+H)+.
de 08/10/2018, pág. 526/857
518
Exemplo Referencial 406
5-t-butóxi-carbonil-5,6-diidro-4H-pirrolo[3,4-d]-tiazolo-2carboxilato de lítio:
O composto do título foi obtido a partir do 5 composto obtido no Exemplo Referencial 33, de uma maneira similar àquela do processo descrito no Exemplo Referencial
10.
ΗΜΝ-^ (DMSO-de) δ: l,46(9H,s), 4,30-4,70 (4H,m) .
Exemplo Referencial 407
1-hidróxi-ciclo-propano-carboxilato de benzila:
O.
OH
OBn
Adicionou-se trietil-amina (1,0 ml) e brometo de benzila (650 μΐ) a uma solução do ácido 1-hidróxi-ciclopropano-carboxílico (409 mg) em tetraidrofurano (3,0 ml), e a mistura foi agitada à temperatura ambiente por 23 h.
Adicionou-se cloreto de metileno e ácido clorídrico 1 N à mistura da reação, para separar a mistura em duas camadas. Uma camada orgânica foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio
Petição 870180138821, de 08/10/2018, pág. 527/857
519 anidro. Um produto bruto foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 4:1), para obter o composto do título (607 mg).
ΗΜΝ-^ (CDC13) δ: 1, 16 (2H, dd, J=7, 9, 4,9Hz), 1,32 (2H, dd, J=7, 9, 5 4,9Hz), 3, 09 (0, 5H, s) , 3, 11 (0,5H, s) , 5,17(2H,s), 7,30-7,39 (5H,m) .
MS (FAB) m/z: 192(M+H)+.
Exemplo Referencial 408
1-metóxi-ciclo-propano-carboxilato de benzila:
OBn
Adicionou-se hidreto de sódio a 60% em óleo (345 mg) e iodeto de metila 900 μΐ) a uma solução do composto obtido no Exemplo Referencial 407 (600 mg) em tetraidrofurano (5,0 ml), e a mistura foi aquecida sob refluxo por 28 h. Adicionou-se acetato de etila e uma solução aquosa saturada de carbonato de amônio à mistura da reação, para separar a mistura em duas camadas. Uma camada orgânica foi lavada com uma solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. Um produto bruto foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 10:1), para obter o composto do título (340 mg).
EMN-iH (CDC13) δ: 1, 16(2H, dd,J=7,9,4,8Hz), 1,31(2H,dd,J=7,9,
4,8Hz), 3,42(3H,s), 5,18(2H,s), 7,30-7,39 (5H, m) .
MS (FAB) m/z: 207(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 528/857
520
Exemplo Referencial 409 ácido 1-metóxi-ciclo-propano-carboxílico:
OH
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 408, de uma maneira similar àquela do processo descrito no Exemplo Referencial
152.
ΗΜΝ-^ (CDC13) δ: 1,23 (2H, dd, J=8, 0, 4,9Hz), 1,38 (2H, dd, J=8, 0, 4,9Hz), 3,45(3H,s), 8, 80-9, 00 (1H, br) .
Exemplo Referencial 410 (3R,4S)-4-({7-cloro-isoquinolin-3-il}-carbonil)-amino}-1-(2metóxi-acetil)-piperidin-3-il-carbamato de t-butila:
θγ'Ό''
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 220, de uma maneira similar àquela do processo descrito no Exemplo Referencial
214 .
RMN-1!! (CDC13) δ: l,46(9H,br s) , 1, 62-1, 80 (1H, m) , 2,04-2,22 (lH,m), 2, 95-3, 32 (lH,m) , 3, 38-3, 53(1H, m) , 3,46(3H,s), 3,84Pctição 870180138821, de 08/10/2018, pág. 529/857
521
3,95(lH,m), 4, 02-4,27 (3H, m) , 4,30-4, 65 (2Η, m) , 4,87-4, 98 (0,5
Η,br), 5,32-5,43(0,5H,br), 7,71(1Η,dd,J=8,8,2,ΟΗζ), 7,94 (1Η, d, J=8, 8Ηζ) , 8,02(lH,s), 8,55-8, 66 (0,7Η, br) , 8,58(lH,s),
8,73-8,85 (0,3H,br) , 9,14(lH,br s) .
MS (ESI) m/z: 477(M+H)+.
Exemplo Referencial 411 (3R,4S)-4-{[2-(4-cloro-3-flúor-anilino)-2-oxoacetil]-amino}1-(2-metóxi-acetil)-piperidin-3-il-carbamato de t-butila:
θγ'Ό''
O composto do título foi obtido condensando o 10 composto obtido no Exemplo Referencial 220 com o composto obtido no Exemplo Referencial 337, de uma maneira similar àquela do processo descrito no Exemplo Referencial 214. RMN-1!! (CDC13) δ: l,46(9H,s), 1, 60-1,75 (1H, m) , 1, 92-2, 08 (1H,
m) , 2, 68—2, 80(0, 5H,m), 2, 88—3, 03(0,5H,m), 3, 06—3, 24(0,5H,m),
3, 27-3, 36 (0,5H,m) , 3,45(3H,s), 3, 90-4,22 (5H, m) , 4,56-4,71 (lH,m), 4, 80-4, 92 (0, 3H,br) , 5, 44-5, 54 (0,7H, br) , 7,24(lH,d,
J=12,9Hz), 7,35(1H,t,J=8,3Hz), 7,72(1H,dd,J=8,3,2,3Hz),
8,20-8,42(1H,br), 9,18-9,28(lH,br).
MS (ESI) m/z: 487(M+H)+.
Exemplo Referencial 412 (3R,4S)-4-({2-[(5-cloro-2-tienil)-amino]-2-oxoacetil]amino}-!-(2-metóxi-acetil)-piperidin-3-il-carbamato de tPctição 870180138821, de 08/10/2018, pág. 530/857
522 butila:
°^0
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 220 e o sal de lítio de um ácido carboxílico obtido hidrolisando o composto obtido no Exemplo Referencial 356, de uma maneira similar àquela do processo descrito no Exemplo Referencial 214. RMN-1H (CDCls) δ: l,45(9H,s), 1,55-1,75 (1H, br) , 1,90-2,10 (lH,br), 2, 68-2, 80(0, 7H,m), 2, 90-3, 03(0,3H,br) , 3,07-3,22 (0,3H,br), 3,25-3,35(0,7H,br), 3,45(3H,s), 3,83-4,22(5H,m),
4,55-4,70 (lH,br), 4,80-4,90 (0,2H,br), 5,07-5,14(0,2H,br),
5,44-5,55(0,6H,br), 6,58-6,64(1H,br), 6,73(1H,d,J=3,9Hz),
8,05-8,27(1H,br), 9,65-9,88(lH,br).
MS (FAB) m/z: 475(M+H)+.
Exemplo Referencial 413
5-metil-5H-pirrolo[3,4-d]-tiazolo-2-carboxilato de etila:
N
1) Adicionou-se 2-tiooxoacetato de etila (26,75 g) a uma solução de 3-bromo-2-butanona (26,36 g) em etanol (250
Petição 870180138821, de 08/10/2018, pág. 531/857
523 ml), e a mistura foi aquecida sob refluxo por 14 h. Depois de resfriar a mistura da reação, ela foi concentrada, e adicionou-se acetato de etila e solução aquosa saturada de cloreto de sódio, para separar a mistura em duas camadas. Uma camada orgânica foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa satura de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 6:1), para obter 4,5-dimetil-tioazol-2-carboxilato de etila (19,53 g). RMN-!H (CDC13) δ: 1, 42 (3H, t, J=7,1Hz) , 2,42(3H,s), 2,44(3H,s), 4,45(2H, q,J=7,1Hz) .
2) Adicionou-se N-bromo-succinimida (62,42 g) e 2,2'-azo-bis-isobutironitrila (227 mg) a uma solução do produto supradescrito (19,53 g) em 1,2-dicloro-etano (500 ml), e a mistura foi refluxada por 42 h. Depois de resfriar a mistura da reação adicionou-se água e cloreto de metileno, para separar a mistura em duas camadas. Uma camada orgânica foi lavada com uma solução aquosa saturada de cloreto de sódio, e depois concentrada sob pressão reduzida, para obter um produto bruto (40, 54 g) , como um óleo marrom-escuro. Adicionou-se trietil-amina (8,0 ml) e uma solução 2 M de tetraidrofurano (11,0 ml) em metil-amina foram adicionadas ao produto bruto (8,41 g) , e a mistura foi agitada à temperatura ambiente por 3 dias. Depois de concentrar a mistura da reação sob pressão reduzida, adicionou-se cloreto de metileno e solução aquosa saturada de cloreto de sódio ao de 08/10/2018, pág. 532/857
524 resíduo, para separar a mistura em duas camadas. Uma camada orgânica foi lavada com uma solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. 0 solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 3:1), para obter o composto do título (270 mg).
βΜΝ-^ (CDC13) δ: 1,45 (3H, t, J=7, 1Hz) , 3,91(3H,s), 4,48(2H,q,
J=7,1Hz), 6,73(1H,d,J=l,7Hz),7,30(1H,d,J=l,7Hz).
Exemplo Referencial 414
6-cloro-4-oxo-4H-cromeno-2-carboxilato de etila:
Adicionou-se hidreto de sódio a cerca de 60% em óleo (1,68 g) a etanol (10 ml) sob purga com argônio, e a mistura foi agitada à temperatura ambiente por 10 min.
Depois de adicionar oxalato de dietila (3,36 ml), adicionouse uma solução de 5'-cloro-2'-hidróxi-acetofenona (2,82 g) em etanol (20 ml) em gotas. Adicionou-se mais etanol (40 ml), e a mistura foi refluxada por 1,5 h e agitada a 50 °C por 14 h. Adicionou-se ácido sulfúrico concentrado (1,5 ml) e etanol (10 ml) à mistura da reação, e a mistura resultante foi refluxada por 5 h. Depois de resfriar, o solvente foi diminuído até a metade do volume por concentração sob pressão reduzida. Adicionou-se tolueno e uma solução aquosa
Petição 870180138821, de 08/10/2018, pág. 533/857
525
N de hidróxido de sódio (15 ml) à mistura da reação concentrada. A extração foi conduzida com acetato de etila, e a camada orgânica resultante foi lavada com uma solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro. Depois de remover o solvente por destilação sob pressão reduzida, e purificar o resíduo por cromatografia de coluna em sílica-gel (hexano:acetato de etila 7:1), os sólidos resultantes foram lavados com hexano, para obter o composto do título (1,20 g).
RMN-XH (CDC13) δ: 1,44(3H,t,J=7,1Hz), 4,47(2H,q,J=7,1Hz),
7,12(lH,s), 7, 58 (1H, d, J=9, OHz) , 7,69(1H,dd,J=9,0, 2,7Hz),
8,16(1H,d,J=2,7Hz).
MS (ESI) m/z: 293(M+MeCN+H)+.
Exemplo Referencial 415 ácido 6-cloro-4-oxo-4H-cromeno-2-carboxílico:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 414, de uma maneira similar àquela do processo descrito no Exemplo Referencial
359.
ΗΜΝ-ΧΗ (CDC13) δ: 7,12(lH,s), 7, 60 (1H, d, J=8, 8Hz) , 7,69(lH,dd, J=8,8, 2,7Hz), 8,15(1H,d,J=2,7Hz).
MS (FAB) m/z: 225(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 534/857
526
Exemplo Referencial 416 (IS,3R,4S)-4-amino-3-[(t-butóxi-carbonil)-amino]-ciclohexano-carboxilato de etila:
composto do título foi obtido a partir do 5 composto obtido no Exemplo Referencial 249, de uma maneira similar àquela do processo descrito no Exemplo Referencial
90.
RMN-1!! (CDC13) δ: 1,20-1,80 (4H, m) , 1,25 (3H, t, J=7, 3Hz) , 1,46 (9H,s), 1,85-2,00(lH,m), 2,10-2,20(1H,m), 2,30-2,45(1H,m),
2, 90-3, 00 (lH,m) , 3,84(lH,br s) , 4,12 (2H, q, J=7,3Hz) ,
4,75 (1H, br s) .
Exemplo Referencial 417 (lR,2S,5S)-2-{[(6-cloro-4-oxo-4H-cromen-2-il)-carbonil]amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil-carbamato de t-butila:
Adicionou-se N,N-dimetil-formamida (0,02 ml) a uma
Petição 870180138821, de 08/10/2018, pág. 535/857
527 solução do composto obtido no Exemplo Referencial 415 (213 mg) em cloreto de tionila (2,0 ml), a mistura foi refluxada por 15 min. A mistura da reação foi concentrada sob pressão reduzida, e tetraidrofurano (4,0 ml).
o resíduo foi dissolvido em
A esta solução adicionou-se trietil-amina (500 μΐ) e o composto obtido no Exemplo Referencial 144 (294 mg), e a mistura foi agitada à temperatura ambiente por 15 min. Adicionou-se acetato de etila e uma solução aquosa a 10% de ácido cítrico, para separar a mistura da reação em duas camadas. Uma camada orgânica foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa satura de cloreto de sódio, secada sobre sulfato de sódio anidro, e depois concentrada sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 30:1), para obter o composto do título (230 mg) .
RMN-1!! (CDCls) δ: 1, 33-1, 7 7 (3H, m) , l,50(9H,s), 1, 81-2,34 (3H,
m) , 2, 63-2, 80 (lH,m) , 2,95(3H,s), 3,10(3H,s), 3, 90-4,04 (1H, br), 4,18-4,31(1H,br), 4,93-5,12(1H,br), 7,13(lH,s), 7,55 (1H, d,J=8,8Hz), 7, 66(1H, dd,J=8,8,2,4Hz), 8, 14(1H, d,J=2,4Hz),
8,77-8,92(lH,br).
MS (ESI) m/z: 492(M+H)+.
Exemplo Referencial 418 (3R, 4S)-4-{[(7-cloro-cinolin-3-il)-carbonil]-amino}-!-(2metóxi-acetil)-piperidin-3-il-carbamato de t-butila:
de 08/10/2018, pág. 536/857
528
Ο composto do título foi obtido a partir do composto obtido no Exemplo Referencial 220 e o sal de lítio de um ácido carboxílico obtido hidrolisando o éster descrito no Exemplo Referencial 297, de uma maneira similar àquela do 5 processo descrito no Exemplo Referencial 214.
RMN-1!! (CDC13) δ: l,38(9H,s), 1, 65-1, 90 (1H, m) , 1, 90-2, 15 (1H,
m) , 2, 80-3, 00(0, 6H,m), 3,00-3,15(0,4H,m), 3, 20-3, 50(1H,m),
3,46(3H,s), 3, 80—4,70 (6H,m) , 4,87(0,4H,br s) , 5,30(0,6H,br
s), 7,78(1H,d,J=8,8Hz), 7, 97(1H,d,J=8,8Hz), 8,61(lH,s),
8, 62-8, 90 (1H,br) , 8,73(lH,s),
MS (ESI) m/z: 478(M+H)+.
Exemplo Referencial 419 (lR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-2oxoacetil}-amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexil15 carbamato de t-butila:
O composto do título foi obtido condensando o
Petição 870180138821, de 08/10/2018, pág. 537/857
529 composto obtido no Exemplo Referencial 144 com o composto obtido no Exemplo Referencial 266, de uma maneira similar àquela do processo descrito no Exemplo Referencial 68.
ΗΜΝ-^ (CDC13) δ: 1,35-1, 65 (1H, m) , l,45(9H,s), 1,65-1,89 (2H,m), 1,90-2,10(3H,m) , 2,56-2,74(1H,br) , 2,95(3H,s), 3,06 (3H,s), 3,94-4,01(lH,m), 4,18-4,27(1H,m), 4,70-4,90(0,7H, br), 5, 80-6, 20 (0, 3H,br) , 7, 68 (1H, dd, J' +8, 9, 2, 6HZ) , 7,83(1H, brs), 8, 14 (lH,brd, J=7,8Hz) , 8,30(lH,s), 9,72(lH,s).
MS (ESI) m/z: 468(M+H)+.
Exemplo Referencial 420 cloridrato de N1-{(IS, 2R, 4S)-2-amino-4-[(dimetil-amino)carbonil]-ciclo-hexil}-N2-(5-cloro-piridin-2-il)etanodiamida:
O composto do título foi obtido a partir do 15 composto obtido no Exemplo Referencial 419, de uma maneira similar àquela do processo descrito no Exemplo Referencial
69.
RMN-1!! (DMSO-de) δ: 1, 38-1,51 (1H, m) , 1,65-1,85 (3H, m) , 1,962,10(2H, m) , 2,81(3H,s), 3,07(3H,s), 3, 23-3, 33 (1H, m) , 3,74 (lH,br s), 3, 84-3, 92(lH,m) , 8,02(1H,dd,J=9,0, 2,5Hz), 8,07 (1H,d,J=9,OHZ), 8,34 (3H,br s) , 8, 46 (1H, d, J=2, 5Hz) , 8,96(1H,
Petição 870180138821, de 08/10/2018, pág. 538/857
530 d,J=6,6Hz), 10,34(1H,s).
MS (ESI) m/z: 368(M+H)+.
Exemplo Referencial 421
2-[({(lR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-25 oxoacetil}-amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexil}amino)-carbonil]-6,7-diidrotieno[3,2-c]-piridino-5(4H)carboxilato de t-butila:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 420 com o ácido 5-(t10 butóxi-carbonil)-4,5,6,7-tetraidrotieno[3,2-c]-piridino-2carboxílico (documento n° WO 94/21599).
RMN-1!! (CDC13) δ: l,50(9H,s), 1,73-1,95 (3H,m) , 1,95-2,06 (lH,m), 2, 08-2,20 (2H,m) , 2,82(3H,br s) , 2,94(3H,s), 3,03(3H,
s), 3, 60-3, 80 (2H,m) , 3, 96-4, 08 (1H, m) , 4,44(2H,br s) , 4,66 (lH,br s), 6,74(lH,br s) , 7,20-7,32 (1H, m) , 7,66(lH,dd,
J=9,0, 2,4Hz), 8,13(1H,d,J=9,OHz), 8,13-8,25(1H,m), 8,28 (1H, d, J=2, 4Hz) , 9,75(lH,s).
MS (ESI) m/z: 633(M+H)+.
Exemplo Referencial 422
2-cloro-N-(4-flúor-fenil)-acetamida:
Petição 870180138821, de 08/10/2018, pág. 539/857
531
Ο composto do título foi obtido a partir de pflúor-anilina, de uma maneira similar àquela do processo descrito no Exemplo Referencial 350.
RMN-1H (CDC13) δ: 4,19(2H,s), 7, 05 (2H, t, J=8, 6Hz) , 7,51(2H, dd,J=9,l, 4,7Hz), 8,19(lH,br s) .
Exemplo Referencial 423
S-[2-(4-flúor-anilino)-2-oxoetil]-tiossulfato de sódio:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 422, de uma maneira similar àquela do processo descrito no Exemplo Referencial
351.
RMN-1H (DMSO-de) δ: 3, 72 (2H, s) , 7, 14 (2H, t, J=9, OHz) , 7,56(2H, dd,J=9,0, 5,1Hz), 10,21(lH,s).
Exemplo Referencial 424 (lR,2S,5S)-5-[(dimetil-amino)-carbonil]-2-{[2-(4-flúoranilino)-2-oxoetanotioil]-amino}-ciclo-hexil-carbamato de tbutila:
Petição 870180138821, de 08/10/2018, pág. 540/857
532
O composto obtido no Exemplo Referencial 144 (1,1
g) e o composto obtido no Exemplo Referencial 423 (1,2 g) foram dissolvidos em N-metil-morfolina (20 ml) , e a temperatura do banho foi aumentada da temperatura ambiente até 140 °C por 15 min, aquecendo e agitando a mistura por 15 min na mesma temperatura. Depois de deixar resfriar, adicionou-se gelo/água à mistura da reação, para coletar os insolúveis por filtração. Este produto foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 200:1 —> 197:3), para obter o composto do título (1,43 g).
RMN-1!!
(lH,m) (CDC13) δ: l,45(9H,s), 1,70-2, 10 (5H, m) , 2,10-2,30
4, 65-4, 85 (lH,m) , 7, 06 (2H, t, J=8, 5Hz) , 7,50- 7,70(2H (2H,m)
m) , 9, 75-9, 95 (lH,m) , 10,13(lH,s).
MS (ESI) m/z: 467(M+H)+.
Exemplo Referencial 425 cloridrato de 2-cloro-N-(5-flúor-piridin-2-il)-acetamida:
Cl
O composto do título foi obtido a partir de 2amino-5-flúor-piridina, de uma maneira similar àquela do processo descrito no Exemplo Referencial 352.
RMN-1!! (DMSO-de) δ: 4,35(2H,s), 7, 74-7,82 (í H, m) , 8,10(lH,dd
J=9,0, 4,2Hz), 8,36(1H,d,J=2,9Hz), 10,94 (lH,br s).
MS (ESI) m/z: 188(M+H)+.
de 08/10/2018, pág. 541/857
533
Exemplo Referencial 426
S-{2-[(5-flúor-piridin-2-il)-amino]-2-oxoetil}-tiossulfato de sódio:
NaO3S composto do título foi obtido a partir do 5 composto obtido no Exemplo Referencial 425, de uma maneira similar àquela do processo descrito no Exemplo Referencial
353.
RMN-!H (DMSO-de) δ: 3,75(2H,s), 7, 67-7, 77 (1H, m) , 8,07(lH,dd,
J=9,2,4,2Hz), 8,28(1H,d,J=2,9Hz), 10,48(lH,s).
Exemplo Referencial 427 (lR,2S,5S)-5-[(dimetil-amino)-carbonil]-2-({2-[(5-flúorpiridin-2-il)-amino]-2-oxoetanotioil}-amino)-ciclo-hexilcarbamato de t-butila:
Uma solução do composto obtido no Exemplo 15 Referencial 144 (1,20 g) em piridina (70 ml) foi aqucida até 120 °C, e adicionou-se o composto obtido no Exemplo
Referencial 426 (2, 42 g) . Depois de agitar a mistura por 30
Petição 870180138821, de 08/10/2018, pág. 542/857
534 min, a mistura da reação foi deixada resfriar até a temperatura ambiente, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se cloreto de metileno (100 ml), uma solução aquosa saturada de bicarbonato de sódio (100 ml) e água (50 ml) ao resíduo resultante, para conduzir separação de líquidos. Uma camada aquosa foi então extraída com cloreto de metileno. As camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi então removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:tetraidrofurano 1:1). Depois disso, os sólidos foram transformados em lama em éter isopropílico (40 ml) por 1 h, coletados por filtração e secados, para obter o composto do título (920 mg).
RMN-1!! (CDCI3) δ: l,47(9H,s), 1,70-2, 10 (5H, m) , 2,27(lH,br s)
10,57(1H,s).
MS (ESI) m/z: 468(M+H)+.
Exemplo Referencial 428 (IR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-2oxoetanotioil}-amino)-5-[(dimetil-amino)-carbonil]-ciclohexil } -carbamato de t-butila:
Boc•Cl
Petição 870180138821, de 08/10/2018, pág. 543/857
535
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e do composto obtido no Exemplo Referencial 353, de uma maneira similar àquela do processo descrito no Exemplo Referencial 247.
ΚΜΝ-^ (CDC13) δ: l,43(9H,s), 1,65-2,35(6H,m), 2,70(lH,br s) , 2,95(3H,s), 3,09(3H,s), 4,30-4,60 (2H, m) , 4,87(l/2H,br s) ,
6,92(l/2H,br s) , 7, 69 (1H, dd, J=8, 9, 2,6Hz), 7, 95-8,20 (1H, br) , 8,29(lH,s), 9, 67 (l/2H,br s) , 9,93(l/2H,br s) , 1O,54(1H, br
s) .
Exemplo Referencial 429
2-cloro-4,5,6,7-tetraidrobenzotiazol-6-il-formamida:
S^/CI
Adicionou-se acetato de amônio (18,58 g) e cianoboro-hidreto de sódio (10,68 g) a uma solução de 2-cloro-5oxo-4,5,6,7-tetraidrobenzo[d]tiazol (Helv. Cím. Acta
77:1256, 1994) (4,53 g) em metanol (200 ml), e a mistura foi aquecida sob refluxo. Depois de 19 h, adicionou-se ácido clorídrico para decompor o excesso de reagentes, antes de concentrar a mistura da reação sob pressão reduzida. Depois disso, o resíduo foi alcalinizado com uma solução aquosa 1 N de hidróxido de sódio, e adicionou-se cloreto de metileno, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida.
Petição 870180138821, de 08/10/2018, pág. 544/857
536
O resíduo resultante foi submetido a uma cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1), e o solvente foi removido por destilação sob pressão reduzida, para obter um óleo amarelo-pálido (2,42 g) . Este óleo foi dissolvido em cloreto de metileno (100 ml), e adicionou-se ácido fórmico (530 μΐ), cloridrato de 1-(3-dimetil-aminopropil ) -3-et il-carbodiimida (3,68 g), 1-hidróxi-benzotriazol (2,60 g) e N-metil-morfolina (3,88 g) , agitando a mistura à temperatura ambiente. Depois de 20 h, adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio à mistura da reação, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1), para obter o composto do título (2,21 g).
RMN-1!! (CDC13) δ: 1, 93-2,11 (2H, m) , 2, 63-2, 69 (1H, m) , 2,83-2,89
(lH,br s), 8,17 (1H,s) .
Exemplo Referencial 430
N-(2-cloro-4,5,6,7-tetraidrobenzotiazol-6-il)-N-metilcarbamato de t-butila:
O de 08/10/2018, pág. 545/857
537
Uma solução 1 M do complexo borano/tetraidrofurano (14,6 ml) foi adicionada a uma solução do composto obtido no Exemplo Referencial 429 (2,11 g) em tetraidrofurano (50 ml), e a mistura foi aquecida sob refluxo. Depois de 15 h, adicionou-se mais uma quantidade da solução 1 M (6,0 ml) do complexo borano/tetraidrofurano em tetraidrofurano, aquecendo a mistura sob refluxo. Depois de 4 h, adicionouse etanol (10 ml) e ácido clorídrico 1 N (15 ml), aquecendo a mistura sob refluxo. Depois de 3 h, a mistura da reação foi concentrada sob pressão reduzida. Adicionou-se uma solução aquosa 1 N de hidróxido de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi dissolvido em cloreto de metileno (50 ml), e adicionou-se trietil-amina (1,28 g) e dicarbonato de di-t-butila (2,21 g), agitando a mistura à temperatura ambiente. Depois de 30 min, adicionou-se cloreto de metileno e ácido clorídrico 1 N, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (hexano:acetato de etila 2:1), para obter o composto do título (2,26 g).
RMN-XH (CDCls) δ: l,47(9H,s), 1, 96-1, 98 (2H, m) , 2,80-2, 96 (7H,
m), 4,40—4,50(lH,m).
MS (FAB) m/z: 303(M+H)+.
de 08/10/2018, pág. 546/857
538
Exemplo Referencial 431
N- (2-[({ (lR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-2oxoacetil}-amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexil}amino)-carbonil]-4,5,6,7-tetraidrobenzotiazol-6-il)-N5 carbamato de t-butila:
Depois de resfriar uma solução do composto obtido no Exemplo Referencial 430 (1,0 g) em dietil-éter (10 ml) e tetraidrofurano (5 ml) até -78 °C, adicionou-se uma solução 1,6 N de t-butil-lítio em pentano (3,1 ml), e a mistura foi agitada por 20 min. Introduziu-se então dióxido de carbono por 20 min. A mistura da reação foi aquecida até a tmeperatura ambiente e concentrada sob pressão reduzida, dando 6-[(t-butóxi-carbonil)-(metil)-amino]-4,5, 6, 7tertraidrobenzotiazol-2-carboxilato de lítio.
O sal de lítio (350,2 mg) do ácido carboxílico obtido pela reação supradescrita, cloridrato de l—(3— dimetil-amino-propil)-3-etil-carbodiimida (287,6 mg), 1hidróxi-benzotriazol (202,7 mg) e N-metil-morfolina (0,319 ml) foram adicionados a uma solução do composto obtido no
Exemplo Referencial 420 (490,5 mg) em N,N-dimetil-formamida (20 ml) , e a mistura foi agitada à temperatura ambiente por
Petição 870180138821, de 08/10/2018, pág. 547/857
539 dias. 0 solvente foi removido por destilação sob pressão reduzida, e adicionou-se água e cloreto de metileno ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi então lavada sucessivamente com uma solução aquosa saturada de bicarbonato de sódio de solução aquosa saturada de cloreto de sódio. A camada orgânica foi secada sobre sulfato de sódio anidro, concentrada sob pressão reduzida, e purificada por cromatografia de coluna em sílica-gel (cloreto de metilenozmetanol 40:1 —> 20:1), para obter o composto do título (323,9 mg).
RNIN-iH (CDC13) δ: 1,48, 1, 49 (total 9H, cada s) , 1,60-1,92 (4H,m), 1, 95-2,20 (6H,m) , 2,78-3, 10 (3H, m) , 2,83(3H,s), 2,95 (3H,s), 3, 06, 3, 07(total 3H,cada s), 4,05—4,15(1H,m), 4,20— 4,60(11-1,m), 4,63-4,73(lH,m), 7,39(1H,d,J=8,6Hz), 7,68(1H, dt,J=8,8,2,6Hz), 7,95-8,10(1H,m), 8,13-8,22(1H,m), 8,30-8,35 (lH,m) , 9, 72 (lH,brs) .
MS (ESI) m/z: 662(M+H)+.
Exemplo Referencial 432 cloridrato de N-{(IS,2R,4S)-2-amino-4-[(dimetil-amino)20 carbonil]-ciclo-hexil}-5-cloro-indol-2-carboxamida:
O composto do título foi obtido desprotegendo o
Petição 870180138821, de 08/10/2018, pág. 548/857
540 composto obtido no Exemplo Referencial 310, de uma maneira similar àquela do processo descrito no Exemplo Referencial
69.
RMN-XH (DMSO-de) δ: 1,43-1,56 (0, 5H,m) , 1,72-1, 97 (4,5H, m) ,
2,82(3H,s), 3,06(3H,s), 3, 11-3, 26 (1H, m) , 3, 75-3, 84 (1H, m) ,
4,07-4,14(lH,m), 4,22-4,41(1H,m), 7,19 (1H,dd,J=2,0, 8,8Hz),
7,29 (lH,d, J=2,OHz) , 7, 45 (1H, d, J=8, 8Hz) , 7,72(lH,s), 8,07(3H, br), 8,47(lH,m), 11,85 (1H, br) .
Exemplo Referencial 433
2-[(5-cloro-piridin-2-il)-amino]-2-oxoacetato de lítio:
Adicionou-se cloro-oxoacetato de metila (78,7 ml) em gotas a uma suspensão de 20amino-5-cloro-piridina (100 g) e bicarbonato de sódio (78,4 g) em tetraidrofurano (2.000 ml), e a mistura foi agitada à temperatura ambiente por 2 h.
Depois de adicionar a mistura da reação a uma mistura de dietil-éter (2.000 ml), cloreto de amônio (62,4 g) e água (1.000 ml), a separação de líquidos foi realizada. A camada aquosa resultante foi extraída com cloreto de metileno. As camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter 2-[(5-cloro-piridin-2-il)amino]-2-oxoacetato de metila (162 g). Adicionou-se água (450 ml) e hidróxido de lítio (18,2 g) a uma solução deste
Petição 870180138821, de 08/10/2018, pág. 549/857
541 éster (160 g) em tetraidrofurano (1.800 ml). Depois de agitar a mistura à temperatura ambiente por 2 h, o solvente foi removido por destilação sob pressão reduzida, e adicionou-se hexano (3.000 ml) ao resíduo resultante, agitando a mistura por 3 h. Os sólidos foram coletados por filtração e secados. Adicionou-se acetonitrila (1.000 ml) aos sólidos, e a mistura foi agitada por 1 h. Os sólidos formados foram coletados por filtração, lavados com dietiléter (500 ml) e depois secados, para obter o composto do título (158 g).
ΚΜΝ-^ (DMSO-d6) δ: 7, 92 (1H, dd, J=9, 1,2, 7Hz) , 8, 13 (1H, dd, J=
9,1, 0,5Hz), 8,36 (1H, dd, J=2, 7, 0,5Hz), 10,19(lH,s).
Exemplo Referencial 434 (lR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-2oxoacetil}-amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexilcarbamato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 144 e do composto obtido no Exemplo Referencial 433, de uma maneira similar àquela do processo descrito no Exemplo Referencial 91.
RMN-!H (CDC13) δ: 1,25-1,55 (lH,m) , l,45(9H,s), 1,60-2,15 de 08/10/2018, pág. 550/857
542 (5H,m), 2, 56-2, 74 (1H,br) , 2,95(3H,s), 3,06(3H,s), 3,90-4,01 (lH,m), 4,18-4,27(1H, rfl) , 4,70-4, 85(0,7H,br) , 5,70-6,00 (0,3H,br), 7,70(1H,dd,J=8,8,2,4HZ), 7,75-8, 00(1H,br), 8,16 (lH,brd,J=8,8HZ), 8,30(1H,d,J=2,4HZ), 9,73(lH,s).
MS (ESI) m/z: 468(M+H)+.
Exemplo Referencial 435 cloridrato de N1-{(IS, 2R, 4S)-2-amino-4-[(dimetil-amino)carbonil]-ciclo-hexil}-N2-(5-cloro-piridin-2-il)etanodiamida:
H,N
O composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 434, de uma maneira similar àquela do Exemplo Referencial 69.
RMN-1!! (DMSO-de) δ: 1,38-1,51 (1H, m) , 1, 65-1,85 (3H, m) , 1,922,09(2H,m), 2,80(3H,s), 3,06(3H,s), 3, 20-3, 32 (1H, m) , 3,5515 4,40 (2H,br), 8, 02(1H,dd,J=9,1, 2,5Hz), 8, 07(1H,d,J=9,1Hz),
8,15-8,40(3H,br), 8,45(1H,d,J=2,5Hz), 8,96(1H,d,J6,6Hz),
10,33 (1H,s) .
Exemplo 1 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)20 carbonil]-amino}-ciclo-propil)-5-meti1-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 551/857
543

Adicionou-se 1-hidróxi-benzotriazol monoidratado (71 mg) e cloridrato de 1-(3-dimetil-amino-propil)-3-etilcarbodiimida (100 mg) a uma solução do composto obtido no Exemplo Referencial 59 (108 mg) e do composto obtido no Exemplo Referencial 10 (124 mg) em N,N-dimetil-formamida (3 ml) à temperatura ambiente, e a mistura foi agitada por 8 dias. Depois de concentrar a mistura da reação sob pressão reduzida, usando uma bomba a vácuo, adicionou-se água (50 ml) e uma solução aquosa saturada de bicarbonato de sódio (50 ml) ao resíduo, para conduzir a extração com cloreto de metileno. As camadas orgânicas resultantes foram combinadas e secadas sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:metanol 10:1). Depois de adicionar ácido clorídrico 1 N, cloreto de metileno e metanol à substância amorfa assim obtida, a mistura foi concentrada para obter o composto do título (72 mg).
RMN-1!! (DMSO-de) δ: 1, 15-1,35 (2H, m) , 2,88(3H,s), 2,95-3,25 (4H,m), 3, 35-3, 75(2H,m), 4,32-4,45(1H,m), 4,68(1H,br,J=
15,4Hz), 7,08 (1H,S), 7, 17 (1H, dd, J=8, 6, 2,1Hz), 7,41(lH,d,J=
8,6Hz), 7,70(lH,s), 8,50(1H,br,J=11, OHz) , 8,56(1H,br,s) ,
11,56(lH,br,J=19,3Hz), 11,86(1H,s).
MS (FAB) m/z: 430(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 552/857
544
Exemplo 2 cloridrato de N-((IR*,2S*)-2-{ [ (5-cloro-indol-2-il)carbonil]-amino}-ciclo-butil)-5-metil-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:

O composto obtido no Exemplo Referencial 10 (136 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etilcarbodiimida (255 mg) e 1-hidróxi-benzotriazol monoidratado (90 mg) foram adicionados a uma solução do composto obtido no Exemplo Referencial 60 (117 mg) em N,N-dimetil-formamida (5 ml), e a mistura foi agitada por toda a noite à temperatura ambiente. 0 solvente foi removido por destilação sob pressão reduzida, usando uma bomba a vácuo, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi lavada com uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 7:93). Depois disso, adicionou-se acetato de etila e uma solução 1 N de ácido clorídrico em etanol ao composto assim obtido, para de 08/10/2018, pág. 553/857
545 acidificá-lo, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se novamente acetato de etila, e o precipitado formado foi coletado por filtração e secado, para obter o composto do título (56 mg).
ΗΜΝ-^ (DMSO-de) δ: 2,00-2,35 (4H, m) , 2,88(3H,m), 3, 10 (2H, br,s), 3, 20-3, 75 (3H,m) , 4,20-4, 85 (3H, m) , 7,09(lH,s), 7,16 (1H, d, J=8, 8Hz) , 7,38 (1H, d, J=8, 8Hz) , 7,71(lH,s), 8,63(lH,d,
J=8,3Hz), 8,85(1H,d,J=8,6Hz), 10,85-11,20(1H,br), 11,81 (lH,s) .
MS (FAB) m/z: 444(M+H)+.
Exemplo 3 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-pentil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Adicionou-se ácido 5-cloro-indol-2-carboxílico (80 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etilcarbodiimida (98 mg), 1-hidróxi-benzotriazol monoidratado (23 mg) e trietil-amina (141 μΐ) a uma solução do composto obtido no Exemplo Referencial 62 (120 mg) em N,N-dimetil20 formamida (5 ml), e a mistura foi agitada à temperatura ambiente por 3 dias. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao
Petição 870180138821, de 08/10/2018, pág. 554/857
546 resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi lavada com uma solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 93:7). Depois disso, adicionou-se acetato cloreto de metileno (5 ml) e uma solução 1 N de ácido clorídrico em etanol (282 μΐ) ao sólido amarelo-pálido assim obtido, adicionou-se acetato de etila, e o precipitado formado foi coletado por filtração, para obter o composto do título (109 mg).
RMN-1H (DMSO-de) δ: 1, 64-1, 74 (4H, m) , 1, 98-2,02 (2H, m) , 2,89 (3H,s), 3, 14(2H,br,s), 3, 47-3, 65 (2H, m) , 4,29-4,63 (4H, m) ,
7, 10 (1H, d, J=l, 5Hz) , 7,14 (1H, dd,J=8,5, 2,OHz), 7,38(lH,d,J=
8,5Hz), 7, 68 (1H, d, J=2, OHz) , 8,55 (1H, d, J=8,5Hz) , 8,91(lH,d,
J=8,5Hz), 11,49 (lH,br, s) , ll,76(lH,s).
MS (ESI) m/z: 458(M+H)+.
Exemplo 4 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
de 08/10/2018, pág. 555/857
547
O composto obtido no Exemplo Referencial 67 (400 mg) foi colocado em suspensão em cloreto de metileno (10 ml), adicionou-se tiretil-amina (0,514 ml) e cloreto de (5cloro-l-fenil-sulfonil-indol)-2-sulfonila (pedido de patente japonesa publicado n° 2000-119253) (319 mg) , e a mistura foi agitada à temperatura ambiente por 15 min. Depois de adicionar água à mistura da reação, para conduzir separação de líquidos, a camada orgânica resultante foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter uma substância espumosa amarelo-pálida. Esta substância foi dissolvida em tetraidrofurano (3 ml) , e adicionou-se metanol (2 ml) e uma solução aquosa 1 N (1,5 ml) de hidróxido de sódio, aquecendo a mistura sob refluxo por 2 h. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno e ácido clorídrico 1 N ao resíduo, para conduzir separação de líquidos. Depois disso, a camada orgânica resultante foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3). Adicionouse ácido clorídrico 1 N (1 ml) ao produto resultante, e a mistura foi concentrada sob pressão reduzida, para obte ro composto do título (108 mg).
RMN-1!! (DMSO-de) δ: 1, 20-1, 78 (8H, m) , 2,94(3H,s), 3,13(2H, br,s), 3,22-3,40(lH,m), 3,44-3,70(3H,m), 3,83-3,95(lH,m), de 08/10/2018, pág. 556/857
548
4,20-4,70 (lH,m) , 6,78 (lH,s), 7, 18-7, 30 (2H, m) , 7,44(lH,s),
7,69 (lH,br, s) , 8,09 (1H, br, s) , ll,92(lH,s).
MS (FAB) m/z: 508(M+H)+.
Exemplo 5 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Adicionou-se ácido 5-cloro-indol-2-carboxílico (109 mg), 1-hidróxi-benzotriazol monoidratado (9 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (321 mg), e trietil-amina (0, 232 ml) a uma solução do composto obtido no Exemplo Referencial 65 (300 mg) em N,Ndimet il-f ormamida (20 ml) , e a mistura foi agitada por toda a noite à temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, usando uma bomba a vácuo, e adicionou-se cloreto de metileno e água, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 25:1), para obter uma substância espumosa incolor. Esta substância foi colocada
Petição 870180138821, de 08/10/2018, pág. 557/857
549 em suspensão em ácido clorídrico 1 Ν (1 ml), e a suspensão foi concentrada sob pressão reduzida, para obter o composto do título (203 mg).
RMN-1H (DMSO-de) δ: 1,25-1,40 (2H,m) , 1, 46-1,81 (4H,m) , 1,885 l,98(2H,m), 2,89(3H,s), 3, 00-3, 76 (5H, m) , 3, 86-3, 97 (1H, m) ,
4,00-4, 10 (lH,m) , 4,25-4,72 (1H, m) , 7,03(lH,s), 7,12(lH,dd,
J=8, 5, 1,2Hz) , 7,38(1H,d,J=8,5Hz), 7,64(lH,s), 8,28(lH,d,J=
8,5Hz), 8,54 (1H, d, J=8, 5Hz) , ll,70(lH,s)
MS (FAB) m/z: 472(M+H)+.
Exemplo 6 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do 15 composto obtido no Exemplo Referencial 67 e ácido 5-cloroindol-2-carboxílico, de uma maneira similar àquela do
Exemplo 5.
RMN-1H (DMSO-de) δ: 1,35-1,70 (6H, m) , 1,80-2,06 (2H, m) , 2,89 (3H, s), 3,00-3,27 (2H,m), 3,35-3,51 (lH,m), 3,57-3,82(1H,
m) , 4,15-4,30(2H,m), 4,32-4,48(1H,m), 4, 60-4,74(1H,m), 7,15 (1H,S), 7,17(1H,dd,J=8,8,2,OHz) , 7,41(1H,d,J=8,6Hz), 7,70 (lH,d, J=2,OHz) , 8, 14 (lH,br, s) , 8,36-8,48 (1H, m) , ll,51(lH,br,
Petição 870180138821, de 08/10/2018, pág. 558/857
550
s) , 11,86 (1H, s) .
MS (FAB) m/z: 472(N+H)+.
Exemplo 7 cloridrato de N-{(IR*,2S*)-2-[(6-cloro-2-naftoil)-amino]5 ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título (186 mg) foi obtido dissolvendo o composto obtido no Exemplo Referencial 67, ácido 6-cloro-naftaleno-2-carboxílico (Eur. J. Chem. Chim. 10 Ther. 19:205-214, 1984) (148 mg), trietil-amina (0,298 ml) e
1-hidróxi-benzotriazol monoidratado (11 mg) em N,N-dimetilformamida (20 ml), e fazendo com que o cloridrato de l—(3 — dimetil-amino-propil)-3-etil-carbodiimida (412 mg) reaja de uma maneira similar àquela do Exemplo 5.
RMN-1!! (DMSO-de) δ: 1, 40-1,56 (2H, m) , 1,57-1,77 (4H, m) , 1,902,10(2H,m), 2,90(3H,s), 3, 13 (2H, br, s) , 3, 28-3, 74 (2H, m) , 4,26 (2H,br,s), 4,30-4, 74 (2H,m), 7, 59 (1H, d, J=8, 6Hz) , 7,90(lH,d,
J=8,6Hz), 7,98(1H,d,J=8,3Hz), 8,03-8,11(2H,m), 8,25-8,58(3H,
m), 11,52(lH,br,s).
MS (FAB) m/z: 483(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 559/857
551
Exemplo 8 cloridrato de N-((IR*,2R*)-2-{[(6-cloro-l-benzotiofen-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
0 composto do título (239 mg) foi obtido dissolvendo o composto obtido no Exemplo Referencial 65 (255 mg), o ácido 6-cloro-benzo[b]tiofeno-2-carboxílico (pedido de patente japonesa publicado n° 2000-119253) (141 mg), trietil-amina (0,276 ml) e 1-hidróxi-benzotriazol monoidratado (10 mg) em N,N-dimetil-formamida (20 ml), e fazendo com que o cloridrato de 1-(3-dimetil-amino-propil)3-etil-carbodiimida (382 mg) reaja de uma maneira similar àquela do Exemplo 5.
RMN-XH (DMSO-de) δ: 1,2 0-1, 98 (8H, m) , 2,88(3H,s), 3,00- 3,72 (4H,m), 3, 84-4, 09 (2H,m) , 4,20-4,75(2H,m), 7,41(1H,dd,J=8,6,
1,7Hz), 7, 91 (1H, d, J=8, 6Hz) , 7,99(lH,s), 8,12(lH,s), 8,548,67(2H,m), 11,53 (1H, br, s) .
MS (FAB) m/z: 489(M+H)+.
Exemplo 9 cloridrato de N-((IR*,2R*)-2-{[(5-flúor-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 560/857
552
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 65 e do ácido 5flúor-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 5.
ΗΜΝ-^ (DMSO-de) δ: 1,20-1,38 (2H, m) , 1,40-1,57 (1H, m) , 1,54I, 68(lH,m), 1,71 (2H, d, J=7, 3Hz) , 1, 88 (2H, d, J=12, OHz) , 2,86 (3H,s), 2, 95-3, 24 (2H,m) , 3, 40 (1H, br, s) , 3, 63 (1H, br, s) , 3,90 (lH,br,s), 3,97-4,10(lH,m), 4,20-4,44(1H,m), 4,53-4,70(1H,
m) , 6,98(1H,dd,J=9,2,2,3Hz), 7,01(lH,s), 7,31-7,39(2H,m),
8,26(1H,d,J=8,6Hz), 8, 59(1H,d,J=8,4Hz), 11,21(1/2H,br,s),
II, 42 (l/2H,br, s) , ll,60(lH,s).
MS (ESI) m/z: 456(M+H)+.
Exemplo 10 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-6-flúor-indol-2-il)15 carbonil]-amino}-ciclo-hexil)-5-metil-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do
Petição 870180138821, de 08/10/2018, pág. 561/857
553 composto obtido no Exemplo Referencial 65 e do composto obtido no Exemplo Referencial 23, de uma maneira similar àquela do Exemplo 5.
RMN-1H (DMSO-de) δ: 1,20-1,40(2H,m), 1,40-1,80 (4H, m) , 1,805 2, 00(2H,m), 2,87(3H,s), 3, 01 (2H, br, s) , 3, 30-3, 80 (2H, m) , 3,81 —3,97(2H,m), 4,20-4, 80 (2H,m), 7,06(lH,s), 7,28(1H,d,J=10,O
Hz), 7,86(1H,d,J=7,3Hz), 8,32(1H,d,J=8,5Hz), 8,59(lH,d,J=
8,5Hz), 11,77 (1H,s) .
MS (FAB) m/z: 490(M+H)+.
Exemplo 11 cloridrato de N-((IR*,2S*)-2-{[(5-bromo-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 67 e do ácido 5bromo-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 5.
RMN-iH (DMSO-dg) δ: 1, 43 (2H, br, s) , 1, 61 (4H, br, s) , 1,80-2,10 (2H,m), 2,88(3H,s), 3, 00-3, 26 (2H, m) , 3, 40 (1H, br, s) , 3,65 (lH,br,s), 4,22 (lH,br, s) , 4,26 (1H, br, s) , 4, 41 (1H, br, s) , 4,67 (1H, d, J=15, 6Hz) , 7,14(lH,s), 7, 2 8 (1H, d, J=8,7Hz) , 7,37(lH,d,
J=8,7Hz), 7,84(lH,s), 8,13(1H,br,s), 8, 33-8,52(1H,m) , 11,51 (lH,br, s) , 11,86 (1H, s) .
Petição 870180138821, de 08/10/2018, pág. 562/857
554
MS (ESI) m/z: 515 (M+) .
Exemplo 12 cloridrato de N-((IR*,2S*)-2-{[(5-etinil-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:

Adicionou-se trietil-amina (6 ml), N,N-dimetilformamida (5 ml), trimetil-silil-acetileno (0,250 ml) e acetato de paládio (20 mg) a uma solução (2 ml) do composto obtido no Exemplo 11 (300 mg) em tetraidrofurano e trifenilfosfina (70 mg) à temperatura ambiente. Depois de agitar a 90 °C por 2 h, a mistura da reação foi deixada resfriar até a temperatura ambiente, e adicionou-se cloreto de metileno (20 ml) e uma solução aquosa saturada de bicarbonato de sódio (30 ml) , para conduzir a separação de líquidos. A camada orgânica foi extraída com cloreto de metileno (3 x 10 ml) , as camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter um resíduo. O resíduo resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:acetona:metanol 10:10:1), para obter sólidos incolores. Este produto foi dissolvido em metanol de 08/10/2018, pág. 563/857
555 (6 ml), adicionou-se carbonato de potássio (120 mg), e a mistura foi agitada por 1 h. Adicionou-se cloreto de metileno (20 ml) e água (20 ml) à mistura da reação, para conduzir separação de líquidos. A camada aquosa resultante foi extraída com cloreto de metileno (2 x 15 ml), a camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:acetona:metanol 10:10:1), e dissolvido em água/metanol/cloreto de metileno. A solução resultante foi então concentrada, para obter o composto do título (72 mg).
ΗΜΝ-^ (CDC13) δ: 1,50-2,25 (8H, m) , 2,53(3H,s), 2, 85 (2H, br, s)
7,42(2H,m), 7, 61 (1H, br, s) , 7,80-7, 97 (2H, m) , 9,72(lH,s).
MS (FAB) m/z: 462(M+H)+.
Exemplo 13 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)20 carbonil]-amino}-ciclo-hexil)-5,6-dimetil-4,5,6,7tetraidrotiazolo[4,5-d]-piridazino-2-carboxamida:
/
Cl
O composto do título foi obtido a partir do
Petição 870180138821, de 08/10/2018, pág. 564/857
556 composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 51, de uma maneira similar àquela do Exemplo 2.
RMN-1H (DMSO-de) δ: 1,35-1,50 (2H, m) , 1,50-1,75 (4H, m) , 1,805 2,10 (2H,m), 2,70 (3H, br, s) , 2,79 (3H,br,s), 4, 10-4,70 ( 6H, m) ,
7,10-7,27 (2H,m), 7,41 (1H, d, J=8, 8Hz) , 7,70(lH,s), 8,12(1H, d,J=6,8Hz), 8,47 (1H, d, J=7, 6Hz) , ll,85(lH,s).
MS (FAB) m/z: 487(M+H)+.
Exemplo 14
N-((lR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil)-6,7-diidrotiazolo-4H-pirano[4,3-d]-tiazol-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 26, de uma maneira similar àquela do Exemplo 2.
RMN-1!! (DMSO-de) δ: 1, 36-1, 72 (6H, m) , 1,90-2, 10 (2H, m) , 2,802,87(2H,m), 3, 93 (2H, t, J=5, CHz) , 4,20-4,32 (2H, m) , 4,81(2H,s),
7,12(lH,s), 7,15(1H,dd,J=8,8, 2,OHz), 7,41(1H,d,J=8,8Hz),
7,67(1H, d,J=l,7Hz), 8, 11(1H, d, J=6,6Hz), 8,36(1H,d,J=8,3Hz),
11,78(1H,s).
MS (FAB) m/z: 459(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 565/857
557
Exemplo 15 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[4,5-c]-piridino-2-carboxamida:
0 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 29, de uma maneira similar àquela do Exemplo 2.
ΕΜΝ-^ (DMSO-de) δ: 1,32-1, 74 (6H,m) , 1, 82-2, 10 (2H,m) , 2,92 (3H,s), 3,12-3,50(3H,m), 3,69(1H,br,s), 4,13-4,39(3H,m),
4,51(lH,br,s), 7,10-7,19(2H,m) , 7,41(1H,d,J=8,6Hz), 7,68(1H, s), 8, 10 (lH,br, s) , 8, 40 (1H, br, s) , 11,41 (1H, br, s) , 11,87(1H,
s) .
MS (FAB) m/z: 472(M+H)+.
Exemplo 16 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5, 6, 7tetraidrotiazolo[4,5-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 566/857
558 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 69 e do composto obtido no Exemplo Referencial 21, de uma maneira similar àquela do Exemplo 2.
RMN-1H (DMSO-de) δ: 1,23-1,39 (2H, m) , 1, 40-1,81 (4H, m) , 1,82l,98(2H,m), 2,60-3,00(5H,m), 3,20-3,70(2H,m), 3,87-3,96(1H,
m), 3,98-4,10(lH,m), 4,12-4,70 (2H,m), 7,04 (1H,d,J=1,5Hz),
7, 12 (1H, dd, J=8,8,2,OHz) , 7, 38 (1H, d, J=8, 8Hz) , 7,65(lH,d,J=
2,OHz), 8,33(1H,d,J=8,6Hz), 8,72(1H,d,J=8,CHz), 11,61(1H, br,s), 11,72 (1H,s) .
MS (FAB) m/z: 456(M+H)+.
Exemplo 17 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-4,5,6,7-tetraidrotieno[3,2-c]15 piridino-2-carboxamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 71 com ácido 5-tbutóxi-carbonil-4,5,6,7-tetraidrotieno[3, 2-c]-piridino-2carboxílico (documento n° WO 94/21599), e tratando o produto formado com ácido clorídrico, para desproteger, de uma maneira similar àquela do Exemplo 2.
RMN-iH (DMSO-de) δ: 1, 42 (2H, br, s) , 1,56-1,76 (4H, m) , 1,98Pctição 870180138821, de 08/10/2018, pág. 567/857
559
2,ll(2H,m), 3,04 (2H,br,s), 3, 32-3, 45 (2H, m) , 4, 15 (3H, br, s) ,
4,26 (lH,br, s) , 7,14 (1H,dd,J=8,8,2,OHz), 7,23(lH,s), 7,41 (1H, d, J=8, 8Hz) , 7,62(lH,s), 7,77(lH,s), 8, 18-8,30 (2H, m) ,
9, 42 (2H,br, s) , ll,92(lH,s).
MS (FAB) m/z: 457(M+H)+.
Exemplo 18 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6, 7tetraidrotieno[3,2-c]-piridino-2-carboxamida:
O composto obtido no Exemplo 17 (171 mg) foi colocado em suspensão em cloreto de metileno (10 ml), e adicionou-se trietil-amina (0,104 ml), agitando a mistura à temperatura ambiente por 10 min. Depois, adicionou-se ácido acético (0,059 ml) à mistura da reação, adicionou-se uma solução aquosa de formaldeído a 35% (0,070 ml) e triacetóxiboro-hidreto de sódio (118 mg), e a mistura foi agitada à temperatura ambiente por 30 min. Depois disso, adicionou-se uma solução aquosa 1 N de hidróxido de sódio (3 ml) à mistura da reação, e adicionou-se água para conduzir separação de líquidos. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, o solvente foi então removido por destilação sob pressão reduzida, e o
Petição 870180138821, de 08/10/2018, pág. 568/857
560 resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 50:3), para obter uma substância espumosa incolor. Esta substância foi colocada em suspensão em ácido clorídrico 1 N, e a suspensão foi concentrada sob pressão reduzida, para obter o composto do título (85 mg).
RMN-1H (DMSO-de) δ: 1, 40 (2H, br, s) , 1,50-1, 71 (4H, m) , 1,97-2,05 (2H,m), 2,87(3H,s), 2, 98-3, 20(1H, m) , 3, 30-3,38(2H, m) , 3,543,70(lH,m), 4, 05-4,42(4H,m), 7,14 (1H,d,J=8,6Hz), 7,23(lH,s),
7,40 (1H, d, J=8, 6Hz) , 7,63(lH,s), 7,77(lH,s), 8, 17-8,27 (2H, m) ,
10,83 (lH,br, s) , 11, 92(lH,s).
MS (FAB) m/z: 471(M+H)+.
Exemplo 19 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)15 carbonil]-amino}-ciclo-hexil)-6-(dimetil-amino)-4,5,6,7tetraibenzotiazol-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 31, de uma maneira similar àquela do Exemplo 2.
RMN-XH (DMSO-de) δ: 1, 44 (2H, br, s) , 1, 52-1, 68 (4H, m) , 1,87-2,08 (3H,m), 2,30-2, 40 (lH,m) , 2, 65-2,75(1H, m) , 2,77(6H,s), 2,95Pctição 870180138821, de 08/10/2018, pág. 569/857
561
3,17(2H,m), 3, 30-3, 70(2H, m) , 4,15-4,30(2H,m) , 7,10-7,20(2Η,
m), 7,41(1Η,d,J=8,6Ηζ), 7,69(lH,s), 8,11(1Η,d,J=5,1Hz), 8,34 (1H, d, J=8,1Hz) , 10, 95 (lH,br, s) , ll,83(lH,s).
MS (FAB) m/z: 500(M+H)+.
Exemplo 20 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-(piridin-4-il)-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Depois de adicionar n-butil-lítio (solução 1,60 N em hexano, 0,704 ml) em gotas a uma solução do composto obtido no Exemplo Referencial 24 (204 mg) em tetraidrofurano (3 ml) a -78 °C, a mistura foi agitada a 0 °C por 30 min. Depois de resfriar a mistura da reação até -78 °C novamente, ela foi aquecida até a temperatura ambiente em 20 min, enquanto se borbulhava dióxido de carbono, e a mistura da reação foi concentrada sob pressão reduzida. O composto obtido no Exemplo Referencial 71 (400 mg), 1-hidróxibenzotriazol monoidratado (254 mg), cloridrato de l—(3— dimetil-amino-propil)-3-etil-carbodiimida (360 mg) e isopropil-amina (0,491 ml) foram adicionados a uma solução do resíduo resultante em N,N-dimetil-formamida (6 ml) à temperatura ambiente. Depois de agitar por 3 dias, a
Petição 870180138821, de 08/10/2018, pág. 570/857
562 mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno (30 ml), uma solução aquosa saturada de bicarbonato de sódio (100 ml) e água (100 ml) ao resíduo, para conduzir separação de líquidos. A camada aquosa resultante foi extraída com cloreto de metileno (4 x 15 ml) , as camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:metanol 20:1 —> 10:1), e dissolvido em ácido clorídrico 1 N/metanol/cloreto de metileno. A solução resultante foi então concentrada, para obter o composto do título (245 mg).
RMN-1H (DMSO-de) δ: 1, 42 (2H, br, s) , 1, 60 (4H, br, s) , 1,84-1,94 (lH,m), 1, 94-2, 08 (lH,m) , 2, 97(2H,br,s), 3, 97-4,13 (2H, m) ,
4, 19 (lH,br, s) , 4,27 (lH,br,s), 5,03(2H,s), 7, 13 (1H, br, s) ,
7,16(1H,dd,J=8,8, 2,OHz), 7,32(2H,br,s), 7,40(1H,d,J=8,8Hz),
7,68 (1H,d,J=2,OHz), 8,15(1H,br,J=7,3Hz), 8,31(2H,d,J=5,9
Hz), 8,39 (1H, d, J=8,1Hz) , ll,90(lH,s), 14,03 (1H, br, s) .
MS (ESI) m/z: 535(M+H)+.
Exemplo 21 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-heptil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 571/857
563 composto do título foi obtido a partir do
|
composto obtido no |
Exemplo Referencial 74 |
e do composto |
|
obtido |
no Exemplo |
Referencial 10, de uma |
maneira similar |
|
àquela |
do Exemplo 2. |
|
|
|
ΗΜΝ-Ή |
(DMSO-de) δ: |
1,51-155,(4H,m), 1,75-1 |
,80(6H,m), 2,88 |
|
(3H,s), |
3, 12 (lH,br |
, s) , 3, 35—3, 63(4H,m), |
4,10-4,13(lH,m), |
4,29-4,61(2H,m), 7,O6(1H, s), 7,14 (1H,dd,J=8,8, 2,OHz),
7,39 (1H,d,J=8,8Hz), 7, 67(1H,d,J=2,OHz), 8,46(1H,d,J=8,3Hz), 8,77 (lH,d, J=8,3Hz) , 11,21-11,35 (1H, m) , ll,71(lH,s).
MS (ESI) m/z: 486(M+H)+.
Exemplo 22 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-octil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 78 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2.
RMN-iH (DMSO-de) δ: 1, 61-2,06 (12H, m) , 2,90(3H,s), 3,08-3,17 (2H,m), 3, 43-3, 45 (lH,br,s), 3,67(1H,br,s), 4,43 (3H,br,s),
4,67(lH,br,s), 7,16-7,18(2H,m), 7,42(1H,d,J=8,8HZ), 7,7O(1H,
s), 8,24 (lH,br,s), 8,58(1H,d,J=8,3Hz), 11,43, 11, 63(1H,cada
Petição 870180138821, de 08/10/2018, pág. 572/857
564 br, s) , 11,80 (1H, s) .
MS (ESI) m/z: 500(M+H)+.
Exemplo 23 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)5 carbonil]-amino}-ciclo-pentil)-4,5,6,7-tetraidrotiazolo[5,4c]-piridino-2-carboxamida:
O composto do título foi obtido tratando um produto obtido pela reação do composto obtido no Exemplo Referencial 63 com o composto obtido no Exemplo Referencial
34, com ácido clorídrico, de uma maneira similar àquela do
Exemplo 2.
RMN-1!! (DMSO-de) δ: 1, 60-1,82 (4H, m) , 1,91-2, 15 (2H, m) , 3,08 (2H,s), 3, 37-3, 49 (2H,m) , 4,28-4,56 (4H, m) , 7,13(lH,s), 7,15 (1H, d, J=8, 8Hz) , 7, 40 (1H, d, J=8, 8Hz) , 7,69(lH,s), 8,61(lH,d,
J=8,3HZ), 8,88 (1H, d, J=8, 3HZ) , 10, 05 (2H, br, s) , ll,82(lH,s).
MS (FAB) m/z: 444 (M+H)+.
Exemplo 24 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-pentil)-5-isopropil-4,5,6,720 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 573/857
565

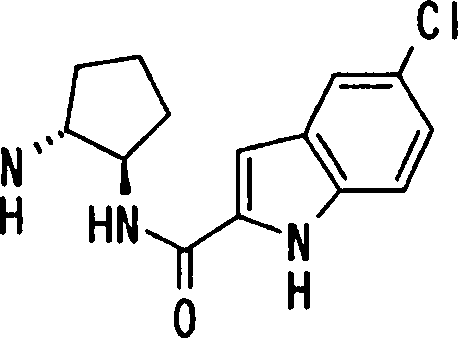
O composto obtido no Exemplo 23 (30 mg) foi colocado em suspensão em cloreto de metileno (20 ml) , e adicionou-se trietil-amina (260 μΐ), agitando a mistura à temperatura ambiente por 15 min. Adicionou-se ácido acético (179 μΐ) e acetona (920 μΐ) à mistura da reação, e a mistura resultante foi agitada à temperatura ambiente por 2 min. Adicionou-se triacetóxi-boro-hidreto de sódio (796 mg) à mistura da reação, agitando à temperatura ambiente por 5 h. Adicionou-se uma solução aquosa 1 N de hidróxido de sódio (10 ml) à mistura da reação, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. 0 resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter uma substância espumosa incolor. Esta substância foi dissolvida em cloreto de metileno, e adicionou-se uma solução 1 N de ácido clorídrico em etanol (1 ml) . A solução foi concentrada sob pressão reduzida, para obter o composto do título (205 mg).
RMN-1!! (DMSO-de) δ: 1,27-1, 39 (6H,m), 1,58-1, 80 (4H,m), 1,952,10(2H,m), 3, 00-3, 12 (lH,m) , 3, 25-3, 45 (2H, m) , 3,59-3,77 (2H,m), 4,25—4, 39 (lH,m), 4,40—4,55 (2H,m), 4,57—4,65 (1H, m) ,
7,1O(1H, s), 7,14(1H,d,J=8,8Hz), 7,38 (1H,d,J=8,8Hz), 7,68 de 08/10/2018, pág. 574/857
566 (1Η, s), 8,56(1H,d,J=8,8Hz), 8,90 (1H,d,J=8,8Hz), 11,39(1H, br,s), 11,76(0,5H,s), 11,80(0,5H,s).
MS (FAB) m/z: 486 (M+H)+.
Exemplo 25 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-pentil)-5-etil-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto obtido no Exemplo 23 (500 mg) foi dissolvido em N,N-dimetil-formamida (10 ml), e adicionou-se trietil-amina (576 μΐ) e iodeto de etila (329 μΐ), agitando a mistura por toda a noite à temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se água para coletar os insolúveis por filtração. Este produto foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter uma substância espumosa marrom-pálida. Esta substância foi colocada em suspensão em solução 1 N de ácido clorídrico, e suspensão foi concentrada sob pressão reduzida, para obter o composto do título (180 mg).
RMN-1!! (DMSO—dô) δ: 1, 32 (3H, t, J=7,1Hz ) , 1, 60-1, 80 (4H, m) , 1,96-2,10(2H,m), 3, 20-3, 39(5H,m) , 3, 70-3, 80(1H,m), 4,26-4,58 (3H,m), 4,68-4,79 (lH,m) , 7,ll(lH,s), 7, 15 (1H, dd, J=8, 8, 2,0 de 08/10/2018, pág. 575/857
567
Hz), 7,39 (1H, d, J=8, 8Hz) , 7, 69(1H,d,J=1,5Hz), 8,55(lH,d,
J=8,5Hz), 8,92(1H,d,J=8,5Hz), 11,38(1H, br, s) , 11,70-11,80 (lH,m) .
MS (FAB) m/z: 472(M+H)+.
Exemplo 26 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-pentil)-5-(1-metil-ciclo-propil)4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do 10 composto obtido no Exemplo Referencial 63 e do composto obtido no Exemplo Referencial 39, de uma maneira similar àquela do Exemplo 2.
RMN-1H (DMSO-de) δ: 0, 81 (2H, br, s) , 1,20-1,55 (5H, br) , 1,55l,80(4H,m), 1, 95-2, 12 (2H,m) , 3, 05-3, 40 (2H, br) , 3,60-3,80 (2H,br), 4,25-4,80(4H,m), 7,10(lH,s), 7,16(1H,d,J=8,8Hz),
7,39(1H,d,J=8,8Hz), 7,69(lH,s), 8,53(1H,d,J=8,6Hz), 8,858,95(lH,m), 10,60-10,90(1H,br), 11,73(1H,br,s).
MS (FAB) m/z: 498(M+H)+.
Exemplo 27 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-4-metóxi-ciclo-pentil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida
Petição 870180138821, de 08/10/2018, pág. 576/857
568 (Estereoisômero A e Estereoisômero B):
Uma mistura dos compostos do título, isto é, o
Estereoisômero A e o Estereoisômero B, foi sintetizada condensando o composto (mistura de estereoisômeros da posição 4) obtido no Exemplo Referencial 82 (268 mg) com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2. Os isômeros foram isolados por cromatografia de coluna em sílica-gel, e depois convertidos nos cloridratos, para obter os compostos do título [Estereoisômero A (75 mg) e Estereoisômero B (70 mg)].
Estereoisômero A:
ΗΜΝ-^ (DMSO-de) δ: 1, 70-2, 15 (4H,m) , 2,90(3H,s), 3,00-3,90 (5H,m), 4, 10-4,80(4H,m), 7,08 (lH,s), 7, 16(1H,d,J=8,8Hz),
7,38(1H,d,J=8,8Hz), 7,69(lH,s), 8,56(1H,d,J=8,8Hz), 8,88 (1H,d,J=8,3Hz), 10,96(1H,br,s), 11,75(1H,br,s).
MS (FAB) m/z: 488(M+H)+.
Estereoisômero B:
ΗΜΝ-^ (DMSO-de) δ: 1, 60-2, 10 (4H,m) , 2,89(3H,s), 3, 00-3, 70 (7 H,m), 3,70-3,90(lH,m), 4,20-4,80(4H,m), 7,05-7,20(2H,m),7,38 (1H, d, J=8, 8Hz) , 7,68(lH,s), 8,59 (1H, d, J=8,3Hz) , 8,90(lH,d,
J=8,5Hz), 11,26(lH,br,s), 11,74 (1H,br,s) .
MS (FAB) m/z: 488(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 577/857
569
Exemplo 28 cloridrato de N-((IR*,2R*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-4-(hidróxi-metil)-ciclo-pentil]-5-(1,1dimetil-2-hidróxi-etil)-4,5,6,7-tetraidrotiazolo[5,4-c]5 piridino-2-carboxamida (Estereoisômero A):
1) Os Estereoisômeros A e B de N-((IR*,2R*)-4[(benzilóxi) -metil] -2- { (5-cloro-indol-2-il) -carbonil}amino)-ciclo-pentil)-5-(2-{[t-butil- (difenil) -silil] oxi}1,1-dimetil-etil)-4,5,6,7-tetraidrotiazolo [5,4-c]-piridino10 2-carboxamida foram obtidos a partir do composto obtido no
Exemplo Referencial 85 e do composto obtido no Exemplo Referencial 42, de uma maneira similar àquela do Exemplo 2.
Estereoisômero A:
RMN-1!! (CDC13) δ: l,05(9H,s), 1,168, 1, 171 (6H, cada s) , 1,5315 l,61(lH,m), 1,7 6-1,88 (1H, m) , 2,30-2,37 (2H, m) , 2,78-2,79 (2H,
m) , 2, 87-2, 90(lH,m), 2, 96-3, 00(1H,m), 3, 37-3, 47 (2H,m), 3,58 (2H,s), 3,96(lH,q,J=13,1Hz), 4,41-4,45(1H,m), 4,51-4,57 (2H,m), 6,88(1H,d,J=l,5Hz) , 7,17(1H,dd,J=8,8,2, OHz) , 7,237,43(12H,m), 7,52(1H,d,J=7,6Hz), 9,37(1H,br,s).
Estereoisômero B:
RMN-iH (CDCI3) δ: l,05(9H,s), l,17(6H,s), 1, 43-1, 47 (1H, m) ,
1,85-1,88(lH,m), 2,09-2,14 (lH,m), 2,58-2,63 (lH,m), 2,78Pctição 870180138821, de 08/10/2018, pág. 578/857
570
2,79(2H,m), 2,86-2,90(1H,m), 2, 96-3, 00(lH,m), 3,38-3,46 (2H,m), 3,59(2H,s), 3,95(1H,q,J=13,3Hz), 4,15-4,20(lH,m),
4,45-4,56(3H,m), 6, 74(1H,d,J=2,OHz), 7,16(1H,dd,J=8,8, 2,0
HZ), 7,27-7,43(12H,m), 7,57(1H,,d,J=2,OHz), 9,48(1H,br,s).
2) O Estereoisômero A acima (288 mg) foi colocado em suspensão em cloreto de metileno (20 ml), e adicionou-se sulfeto de dimetila (1,15 ml) e cloreto de alumínio anidro (350 mg), agitando a mistura à temperatura ambiente por 1 h. Adicionou-se uma solução aquosa 1 N de hidróxido de sódio (10 ml) à mistura da reação, e a mistura foi extraída com cloreto de metileno. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 9:1), para obter 5—(2—{[t— butil-(difenil)-silil]oxi}-l,1-dimetil-etil)-N-[(IR*, 2R)-2{[(5-cloro-indol-2-il)-carbonil]-amino}-4- (hidróxi-metil)ciclo-pentil)-4,5,6,7-tetraidrotiazolo[5,4-c] -piridino -2carboxamida (Estereoisômero A) (184 mg).
RMN-1H (CDC13) δ: l,04(9H,s), l,15(6H,s), 1, 54-1, 62 (1H, m) ,
1,73-1,81(lH,m), 1,99-2,25(2H,m), 2,34-2,38(2H,m), 2,67-2,85 (3H,m), 2, 92-2, 97 (lH,m) , 3, 48-3, 62 (4H,m) , 3,93(lH,q, J=15, 6
Hz), 4,20-4,28 (lH,m), 4,47-4,56(lH,m) , 6,89(lH,s), 7,11-7,18 (lH,m), 7,24-7,27 (lH,m) , 7,32-7,43 (6H, m) , 7,54(1H, d,J=l,7
Hz), 7,63(4H,dd,J=7,8,1,5Hz) , 7, 90-7, 92 (2H,m), 1O,13(1H, br, s) .
MS (FAB) m/z: 784(M-s-H)+.
3) O Estereoisômero A (180 mg) obtido na etapa (2)
Petição 870180138821, de 08/10/2018, pág. 579/857
571 descrita acima foi dissolvido em uma solução 1 N de fluoreto de tetrabutil-amônio em tetraidrofurano (2 ml), e a solução foi agitada por toda a noite à temperatura ambiente. Adicionou-se cloreto de metileno, uma solução aquosa 1 N de hidróxido de sódio e cloreto de sódio à mistura da reação, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 19:1). O pó assim obtido foi dissolvido em metanol, e adicionou-se uma solução 1 N de ácido clorídrico em etanol (229 μΐ), à qual adicionou-se acetato de etila. O solvente foi removido sob pressão reduzida, para obter o composto do título (63 mg). RMN-1H (DMSO-de) δ: 1, 33-1, 50 (8H, m) , 1, 70-1, 91 (2H, m) , 2,072,14(lH,m), 2,23-2,24(lH,m), 3,04-3,10(lH,m), 3,27-3,44 (4H, m) , 3, 57-3, 70 (2H,m), 3, 92-3, 95 (lH,m), 4,29-4,72 (4H,m),
5,81 (lH,br,s), 7,ll(lH,s), 7,15 (1H, dd,J=8,6, 2,OHz),
7,39(1H, d,J=8,6Hz), 7, 68 (1H, d, J=2, OHz) , 8, 53-8, 5 6 (1H, m) ,
8,83(lH,d, J=8,3Hz), 10, 36 (1H, br, s) , 11, 75, 11, 77 (1H, cada s) . MS (ESI) m/z: 546(M+H)+.
Exemplo 29 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-4,7,8,10-tetraidro-6Hpirazolo[1,2-a]-tiazolo[4,5-d]-piridazino-2-carboxamida:
de 08/10/2018, pág. 580/857
572
Cl
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 44, de uma maneira similar àquela do Exemplo 2.
RMN-XH (DMSO-de) δ: 1,35-1,50 (2H, m) , 1, 61 (4H, br, s) , 1,802,00(2H,m), 2,27 (2H,br,s), 2,80-4,80(10H,m), 7,14 (1H,d,J=1,5
Hz), 7, 17(1H, dd, J=8,5,2,OHz), 7,41(1H,d,J=8,5Hz), 7,7O(1H, d,J=2,OHz), 8, 09 (1H, d, J=7, 3Hz) , 8,44 (1H, br, s) , 11,81(1H, br,s).
MS (FAB) m/z: 499(M+H)+.
Exemplo 30 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-4,6,7,8,9,10hexaidropiridazino[l,2-a]-tiazolo[4,5-d]-piridazino-2-
composto do título foi obtido a partir do
Petição 870180138821, de 08/10/2018, pág. 581/857
573 composto obtido no Exemplo Referencial 46 e do composto obtido no Exemplo Referencial 71, de uma maneira similar àquela do Exemplo 2.
RMN-1!! (DMSO-de) δ: 1, 35-1, 55 (2H, m) , 1,55-2, 10 (10H, m) , 2,805 4,80(lOH,m), 7,10-7,25(2H,m), 7,42(1H,d,J=8,8Hz), 7,72(1H, d,J=l,7Hz), 8,12(1H,br,s), 8,41(1H,br,s), 11,83(1H,br,s).
MS (FAB) m/z: 513(M+H)+.
Exemplo 31 cloridrato de 5-cloro-N-{(IR*,2S*)-2-[(5,6-diidro-4H10 pirrolo[3,4-d]-tiazol-2-il-carbonil)-amino]-ciclo-hexil}indol-2-carboxamida:
O composto obtido no Exemplo Referencial 33 (171 mg) foi dissolvido em dietil-éter (5 ml) em uma atmosfera de argônio, e a solução foi resfriada até -78 °C, e a esta solução adicionou-se n-butil-lítio (solução 1,60 N em hexano, 385 μΐ) em gotas. Depois de agitar a mistura da reação por 10 min a -78 °C, e borbulhar dióxido de carbono dentro da mistura da reação por 20 min, ela foi aquecida até a temperatura ambiente. Depois de concentrar a mistura da reação sob pressão reduzida, o resíduo foi dissolvido em N,N-dimetil-formamida (10 ml). A esta solução adicionou-se o composto obtido no Exemplo Referencial 71 (184 mg) , 1Pclição 870180138821, de 08/10/2018, pág. 582/857
574 hidróxi-benzotriazol monoidratado (76 mg) e cloridrato de 1(3-dimetil-amino-propil)-3-etil-carbodiimida (215 mg). A mistura resultante foi agitada por 3 dias. A mistura da reação foi concentrada, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 3:97). Depois de adicionar uma solução de ácido clorídrico em etanol (5 ml) ao produto assim obtido, a mistura foi agitada à temperatura ambiente por 1 h, e a mistura da reação foi concentrada. Adicionou-se acetato de etila ao resíduo, para solidificá-lo. O pó resultante foi coletado por filtração, para obter o composto do título (31 mg).
RMN-1H (DMSO-de) δ: 1, 35-1, 52 (2H, m) , 1, 55-1, 80 (4H, m) , 1,822,05(2H,m), 4,22 (1H, br, s) , 4,28 (1H, br, s) , 4,38(2H,s), 4,56(2
H,s), 7,14-7,20 (2H,m), 7,42 (1H,d,J=8,6Hz), 7,71(1H,d,J=l,7
Hz), 8,10(1H,d,J=7,1Hz) , 8,45(1H,d,J=7,8Hz) 10,10-10,50 (2H,br), 11, 83 (1H, br, s) .
MS (FAB) m/z: 444(M+H)+.
Exemplo 32
2-{[((IR*,2S*)-2-[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil)-amino]-carbonil}-5,7-diidro-6H-pirrolo[3,4-d]pirimidino-6-carboxilato de t-butila:
de 08/10/2018, pág. 583/857
575
Depois de hidrolisar o composto obtido no Exemplo Referencial 50 com hidróxido de lítio, ele foi reagido com o composto obtido no Exemplo Referencial 71, de uma maneira similar àquela do Exemplo 2, para obter o composto do título.
RMN-1!! (CDC13) δ: l,54(9H,s), 1,55-2,30 (8H, m) , 4,23(1H, br,s), 4,53(1H,br,s), 4,74—4, 83(4H,m), 6, 99(1H,d,J=1,5Hz),
7,19(1H, dd,J=8,8, 2,1Hz), 7, 34 (1H, d, J=8, 8Hz) , 7,62(lH,d,J=
2,1Hz), 8,11(lH,br,s), 8,48-8,53(1H,br), 8, 70-8,76(1H,br),
9, 60-9, 70 (lH,br) .
MS (ESI) m/z: 539(M+H)+.
Exemplo 33 cloridrato de N-((IR*,2S*)-2-[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-6-metil-6,7-diidro-5Hpirrolo[3,4-d]-pirimidino-2-carboxamida:
Adicionou-se ácido triflúor-acético (1 ml) a uma solução do composto obtido no Exemplo 32 (34,0 mg) dissolvido em cloreto de metileno (1 ml) à temperatura
Petição 870180138821, de 08/10/2018, pág. 584/857
576 orgamca.
sódio anidro.
ambiente, e a mistura foi agitada por 1 h. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi dissolvido em cloreto de metileno (1 ml) , e adicionou-se a esta solução trietil-amina (17,6 μΐ) , ácido acético (7,21 μΐ) , formalina a 35% (8,13 μΐ) e triacetóxi-boro-hidreto de sódio (20,1 mg), à temperatura ambiente. A mistura resultante foi agitada por 1 h. Adicionou-se cloreto de metileno (10 ml) e solução aquosa saturada de bicarbonato de sódio (10 ml) à mistura da reação, para separar uma camada A camada orgânica foi secada sobre sulfato de O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 7:93) . Adicionou-se uma solução 1 N de ácido clorídrico em etanol, e acetato de etila, ao produto assim obtido, para solidificá-lo, e os sólidos resultantes foram coletados por filtração, para obte ro composto do título (8,0 mg) .
RMN-1H (DMSO-de) δ: 1, 40-1, 55 (2H, m) , 1, 55-1, 75 (4H, m) , 1,802,05(2H,m), 2, 98 (3H, br, s) , 4,28 (2H, br, s) , 4, 65 (4H, br, s) ,
7,14-7,20(2H,m), 7,41(1H,d,J=8,8Hz), 7,69(1H,d,J=2,OHz),
8,17 (1H, d, J=6, 9Hz) , 8, 65 (1H, d, J=8, 3Hz) , 8,93(lH,s), 11,73 (lH,br,s), 11, 82 (1H, br, s) .
MS (FAB) m/z: 453(M+H)+.
Exemplo 34 cloridrato de N-((IR*,2S*)-2-[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-4,5, 6, 7-tetraidrotiazolo[5, 4c]-piridino-2-carboxamida:
de 08/10/2018, pág. 585/857
577
composto do título foi obtido tratando o produto obtido no Exemplo Referencial 71 e o composto obtido no Exemplo Referencial 34 com ácido clorídrico, de uma maneira similar àquela do Exemplo 2.
RMN-1H (DMSO—dô) δ: 1, 39-1, 52 (2H, m) , 1, 62 (4H, br, s) , 1,862,09(2H,m), 3,03 (2H,br,s), 3, 40-3, 47(2H,m), 4,17-4,32(2H,m), 4,44 (2H,s), 7,15(lH,s), 7, 17 (1H, dd, J=8, 6, 2, OHz) , 7,41(1H, d,J=8,6Hz), 7,71(lH,s), 8,10-8,15(1H,m), 8,40-8,47(1H,m),
9, 69 (2H,br, s) , ll,85(lH,s).
MS (FAB) m/z: 458(M+H)+.
Exemplo 35 cloridrato de N-((IR*,2S*)-2-[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-(2-metóxi-etil)-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 34 e de brometo de 2metóxi-etila, de uma maneira similar àquela do Exemplo 25.
Petição 870180138821, de 08/10/2018, pág. 586/857
578
RMN-1H (DMSO-de) δ: 1, 44 (2Η, br, s) , 1, 62 (4H, br, s) , 1,85-2,10 (2H,m), 2, 76-3, 21 (6H,m) , 3,28(3H,s), 3, 64 (2H, br, s) , 4,004,52(4H,m), 7,14(lH,s), 7, 17 (1H, dd, J=8, 8, 2,OHz), 7,41(lH,d,
J=8,8HZ), 7,70(1H,d,J=2,OHz), 8, 08-8,20(1H,m) , 8,36-8,48(1H,
m), 11,84 (1H,s).
MS (FAB) m/z: 516(M+H)+.
Exemplo 36 cloridrato de 2-[2-{[((IR*,2S*)-2-[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-amino]-carbonil-6,7-diidro10 tiazolo[5,4-c]-piridin-5(4H)-il]-acetato de metila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 34 e de bromo-acetato de metila, de uma maneira similar àquela do Exemplo 25. RMIs!-^ (CDC13) δ: 1,52-1, 98 (7H, m) , 2, 17 (1H, br, s) , 2,87-3,10 (4H,m), 3,49(2H,s), 3,76(3H,s), 3, 93 (1H, d, J=15,4Hz) , 3,99 (1H, d, J=15, 4Hz) , 4,22 (lH,br, s) , 4,45 (1H, br, s) , 6,86(lH,d,
J=l,2Hz), 7, 18(1H,dd,J=8,8, 2,OHz), 7,33(1H,d,J=8,8Hz),
7,58-7, 63 (2H,m), 7,87(1H,br,s), 9, 88(1H, br, s) .
MS (FAB) m/z: 530(M+H)+.
Exemplo 37 cloridrato de N-((IR*,2S*)-2-[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-isopropil-4,5,6,7Pctição 870180138821, de 08/10/2018, pág. 587/857
579 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 34 e acetona, de uma maneira similar àquela do Exemplo 24.
RMN-1!! (DMSO-de) δ: 1, 18-1,73 (8H, m) , 1,81-2, 10 (2H, m) , 2,973,16(lH,m), 3, 20-3, 41 (2H,m) , 3, 52-3, 80 (2H, m) , 4,19-4,31 (2H,
m), 4,34-4,77(2H,m) , 7,17(lH,s), 7,18(1H,dd,J=8,8, 2,0 Hz),
7,42(1H,d,J=8,8Hz), 7,71(1H,d,J=2,OHz), 8,15(1H,br,s), 8,288,51(lH,m), 11,31 (lH,br, s) , ll,86(lH,s).
MS (FAB) m/z: 500(M+H)+.
Exemplo 38 cloridrato de N-((IR*,2S*)-2-[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-(tetraidro-2H-piran-4-il)4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Cl
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 34 e de tetraidro-4Hpiran-4-ona, de uma maneira similar àquela do Exemplo 24.
Petição 870180138821, de 08/10/2018, pág. 588/857
580
RMN-XH (DMSO-de) δ: 1,30-3,56(19H,m), 3,70-4,01(3H,m), 4,174,30(2H,m), 4,32-4,80(1H,m), 7,15(lH,s), 7,17(1H,dd,J=8,6,
2,OHz), 7,41(1H,d,J=8,6Hz), 7,71(1H,d,J=2,OHz), 8,14 (lH,br,
s), 8,39 (lH,br, s) , ll,84(lH,s).
MS (FAB) m/z: 542(M+H)+.
Exemplo 39
2-[2-{[((lR*,2S*)-2-[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil)-amino]-carbonil}-6,7-diidrotiazolo[5,4-c]piridin-5(4H0-Í1]-etil-carbamato de t-butila:
Cl
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 34 e N-(t-butóxicarbonil) -amino-acetaldeído (<7. Org. Chem. 53:3457, 1988), de uma maneira similar àquela do Exemplo 24.
RMN-XH (CDC13) Ô: l,44(9H,s), 1,54-1, 98 (7H, m) , 2,10-2,20 (lH,m), 2,74(2H,br,s), 2,92(4H,br,s), 3,34(2H,br,s), 3,84 (2H,br, s) , 4,21 (lH,br, s) , 4,45 (1H, br, 5) , 6,86(lH,s), 7,19(1H, dd,J=8,8, 2,OHz), 7,33 (1H,d,J=8,8Hz) , 7,57-7, 63 (2H,m), 7,81 (lH,br,s), 9, 66 (1H, br, s) .
MS (FAB) m/z: 601(N+H)+.
Exemplo 40 cloridrato de 5-(2-amino-acetil)-N-((IR*,2S*)-2-[(5-cloroindol-2-il)-carbonil]-amino}-ciclo-hexil)-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 589/857
581
composto obtido no Exemplo 39 (450 mg) foi dissolvido em cloreto de metileno (5 ml), e adicionou-se uma solução saturada de ácido clorídrico em etanol (30 ml), agitando a mistura à temperatura ambiente por 1 min. A mistura da reação foi concentrada sob pressão reduzida, adicionou-se acetato de etila ao resíduo, e os sólidos depositados foram coletados por filtração, para obter o composto do título (367 mg) .
RMN-íH (DMSO-ds) δ: 1,38-1, 50 (2H, m) , 1,61 (4H, br, s) , 1,8510 2, 08(2H,m), 3, 00-4, 62(12H, m) , 7,14(lH,s), 7,16 (1H,dd,J=8,8,
2,OHz), 7,41(1H,d,J=8,8Hz) , 7,69 (1H,d,J=2,OHZ), 8,12 (lH,d,
J=6, 6Hz) , 8, 15-8, 68 (4H,m) , ll,85(lH,s).
MS (FAB) m/z: 501(M+H)+.
Exemplo 41 cloridrato de N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-{2-[(metil-sulfonil)-amino]etil}-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 590/857
582 composto obtido no Exemplo 40 (110 mg) foi dissolvido em piridina (3 ml), adicionou-se cloreto de metano-sulfonila (30 μΐ) , e a mistura foi agitada por toda a noite à temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se um solvente misto 85:15 de cloreto de metileno e metanol, e adicionou-se água, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter uma substância espumosa amarelo-pálida. Esta substância foi colocada em suspensão em ácido clorídrico 1 N (0,3 ml), e a suspensão foi concentrada sob pressão reduzida, para obter o composto do título (63 mg).
RMN-1H (DMSO-de) δ: 1, 38-1, 50 (28,m) , 1, 55-1, 70 (4H,m) , 1,862,05(2H,m), 2,97(3H,s), 3, 02-3, 25 (2H, m) , 3, 30-3, 60 (5H, m) ,
3, 78 (lH,br, s) , 4,18-4,30 (2H,m) , 4,45-4,86 (2H,m) , 7,14(lH,s),
7,16(1H,dd,J=8,8, 2,OHz), 7,40(1H,d,J=8,8Hz), 7,41(1H,br,s),
7,69(1H,d,J=2,OHz), 8,09(1H,br,s), 8,43(1H,br,s), 11,18(1H, br, s) , 11,82 (1H, s) .
MS (FAB) m/z: 579(M+H)+.
Exemplo 42
2-[2-{[((IR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}25 ciclo-hexil)-amino]-carbonil}-6,7-diidrotiazolo[5,4-c]piridin-5(4H)-il]-etil-carbamato de metila:
Petição 870180138821, de 08/10/2018, pág. 591/857
583
Cl

O composto obtido no Exemplo 40 (144 mg) foi dissolvido em piridina (3 ml), adicionou-se trietil-amina (138 μΐ) , e a mistura foi agitada à temperatura ambiente por 5 min. Uma solução, preparada adicionando trifosgênio (49 mg) a tetraidrofurano (1 ml) contendo metanol (20 μΐ) , foi adicionada em gotas àquela solução. Depois de agitar por 1 h, a mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi dissolvido em um solvente misto 9:1 de cloreto de metileno e metanol. Adicionou-se água à solução para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter uma substância espumosa incolor. Esta substância foi colocada em suspensão em ácido clorídrico 1 N (0,2 ml), e a suspensão foi concentrada sob pressão reduzida, para obter o composto do título (60 mg).
RMN-1H (DMSO-de) δ: 1, 38-1,50 (2H, m) , 1,61 (4H, br, s) , 1,852,04 (2H,m), 2, 80-3, 4 9 (8H, m) , 3,52(3H,s), 3, 62-4, 91 (4H, m) ,
7,14 (lH,s), 7,16(1H,dd,J=8,8,2,OHz), 7,37(1H,br,s), 7,40 (1H, d, J=8, 8Hz) , 7,70(lH,s), 8, 11 (1H, d, J=6, 8Hz) , 8,40(lH,br,
s) , 11,05(1H, br, s), 11,82(1H,br,s) .
de 08/10/2018, pág. 592/857
584
MS (FAB) m/z: 559(M+H)+.
Exemplo 43 cloridrato de 5-[2-(acetil-amino)-etil]-N-((IR*,2S*)-2-{[(5cloro-indol-2-il)-carbonil]-amino}-ciclo-hexil)-5-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
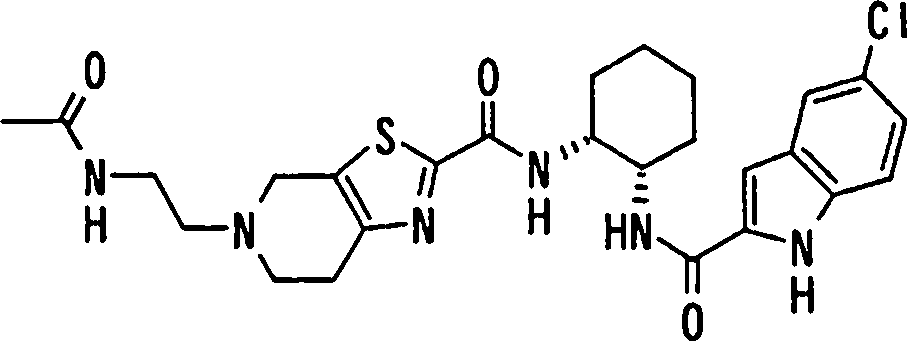
O composto obtido no Exemplo 40 (90 mg) foi dissolvido em N, N-dimetil-formamida (3 ml), adicionou-se trietil-amina (65 μΐ) e anidrido acético (22 μΐ), e a mistura foi agitada por toda a noite à temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa 0,3 N de hidróxido de sódio ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter uma substância espumosa incolor. Esta substância foi colocada em suspensão em ácido clorídrico 1 N (0,3 ml), e a suspensão foi concentrada sob pressão reduzida, para obter o composto do título (73 mg). RMN-1!! (DMSO-ds) δ: 1,39-1,52 (2H, m) , 1,54-1, 70 (4H, m) , 1,83(3
H,s), 1,84-2,06(2H,m), 3,02-3,87(8H,m), 4,16-4,32(2H,m), de 08/10/2018, pág. 593/857
585
4,40-4,52 (lH,m) , 4,78-4, 88 (1H, m) , 7,14(lH,s), 7,16 (lH,d,
J=8,6Hz), 7,40 (1H,d,J=8,6Hz) , 7,70(lH,s), 8,07-8,17(1H, m) ,
8,22-8,30 (lH,m), 8, 38-8, 52(1H,m), 11,14(1H,br,s), 11,83 (lH,s) .
MS (FAB) m/z: 543(M+H)+.
Exemplo 44
N-((lR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil)-5-(2-hidróxi-etil)-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Cl
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 34 e 2-bromo-etanol, de uma maneira similar àquela do Exemplo 25.
RMN-1!! (DMSO-dg) δ: 1,37-1, 69 (6H, m) , 1,86-2,03 (2H, m) , 2,542,61(2H,m), 2, 75—2, 86 (4H, m) , 3, 52—3, 59 (2H, m) , 3,75(2H,s),
4,47 (1H, t, J=5, 4Hz) , 7,12(lH,s), 7, 16 (1H, dd, J=8, 8,2, OHz) ,
7,40(1H,d,J=8,8Hz), 7,70(lH,s), 8, 05-8,13(1H,m), 8,28-8,35 (lH,m) , 11,78 (1H, s) .
MS (FAB) m/z: 502(M+H)+.
Exemplo 45 cloridrato de 5-butil-N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 594/857
586
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 34 e n-bromo-butano, de uma maneira similar àquela do Exemplo 25.
RMN-iH (DMSO-de) δ: 0, 88 (3H, t, J=7,2Hz) , 1,20-1,70 (1OH, m) ,
1,87-2,05(2H,m), 2,55-3,40(8H,m), 4,16-4,30(2H,m), 7,13(1H,
s), 7,16(1H,d,J=8,8Hz), 7,40(1H,d,J=8,8Hz), 7,69(lH,s), 8,05 —8,14(lH,m), 8,35 (lH,br, s) , ll,81(lH,s).
MS (FAB) m/z: 514(M+H)+.
Exemplo 46
5-acetil-N-((lR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]amino}-ciclo-hexil)-5-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto obtido no Exemplo 34 (100 mg) foi dissolvido em N, N-dimetil-formamida (3 ml), adicionou-se trietil-amina (84 μΐ) e anidrido acético (29 μΐ), e a mistura foi agitada à temperatura ambiente por 3 h. A mistura da reação foi concentrada sob pressão reduzida, e
Petição 870180138821, de 08/10/2018, pág. 595/857
587 adicionou-se cloreto de metileno e ácido clorídrico 1 N ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter o composto do título (86 mg).
βΜΝ-^ (CDC13) δ: 1,52-1,85 (5H, m) , 1, 91 (2H, br, s) , 2,10-2,28 (4H,m), 2, 77-3, 00 (2H,m) , 3, 70-4,00(2H, m) , 4,19-4,38 (lH,m), 4,45 (lH,br, s) , 4,68-4,99 (2H, m) , 6,85(lH,s), 7,177,22(lH,m), 7,30-7, 39(1H, m) , 7,50-7, 84(3H, m) , 9,72-10,05 (lH,m) .
MS (FAB) m/z: 500(M+H)+.
Exemplo 47
N-((lR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil)-5-{2-[(metil-sulfonil)-amino]-etil}-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Cl
O composto obtido no Exemplo 34 (100 mg) foi dissolvido em piridina (3 ml) , adicionou-se trietil-amina (168 μΐ) e cloreto de metano-sulfonila (48 μΐ) , e a mistura foi agitada por toda a noite à temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, e de 08/10/2018, pág. 596/857
588 adicionou-se um cloreto de metileno e ácido clorídrico 1 N ao resíduo, para separar uma camada orgânica. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:1), para obter o composto do título (79 mg).
RMN-1!! (CDC13) δ: 1,50-1, 82 (5H, m) , 1, 90 (2H, br, s) , 2,13(1H, br,s), 2,89(3H,s), 2,91-2,98(2H,m), 3,60-3,70(2H,m), 4,30 (lH,br,s), 4,44 (lH,br, s) , 4,58(2H,s), 6,87(lH,s), 7,19(1H, d,J=8,8Hz), 7,34 (1H, d, J=8, 8Hz) , 7, 61 (3H, br, s) , 9,91(1H, br, s) .
MS (FAB) m/z: 536(M+H)+.
EXEMPLO 48 cloridrato de 5-metil-N-((IR*,2S*)-2-{[(5-metil-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-4,5,6,7-tetraidrotiazolo [5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do
|
composto obtido no |
Exemplo |
Referencial |
67 e ácido 5-metil- |
|
indo1-2-carboxílico, |
de |
uma maneira |
similar àquela do |
|
Exemplo 5. |
|
|
|
|
RMN-1!! (DMSO-ds) δ: |
1,35-1, |
50(2H,m), 1, |
50-1,80(4H,m), 1,85- |
de 08/10/2018, pág. 597/857
589
2,07(2H,m), 2,36(3H,s), 2,88(3H,s), 3, 12 (2H, br, s) , 3,53 (2H,br,s), 4, 15—4, 30(2H,m), 4,30-4, 80(2H,br) , 7,00 (1H,dd,J= 8,4,1,5Hz), 7, 05(1H,d,J=l,5Hz), 7,30 (1H,d,J=8,4Hz) , 7,38 (lH,s), 8,00(1H,d,J=7,3Hz), 8,43(1H,br,s), 11,45(1H,br,s),
11,49(1H,br,s).
MS (FAB) m/z: 452(M+H)+.
Exemplo 49 (lR*,3S*,4R*)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-3{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)10 carbonil]-amino}-ciclo-hexano-carboxilato de etila:
O composto obtido no Exemplo Referencial 91 (1,40
g) foi colocado em suspensão em etanol (8 ml), e adicionouse uma solução saturada de ácido clorídrico em etanol (10 ml) à temperatura ambiente, agitando a mistura por 12 h. O solvente foi removido por destilação sob pressão reduzida, para obter cloridrato de (IR*,3S*,4R*)-3-amino-4-{[(5-cloroindol-2-il)-carbonil]-amino}-ciclo-hexano-carboxilato de etila (1,25 g).
O composto do título foi obtido a partir do produto supradescrito e do composto obtido no Exemplo
Referencial 10, de uma maneira similar àquela do Exemplo 2.
RMN-iH (CDC13) δ: 1,29 (3H, t, J=7, 1Hz) , 1,52-1,80 (2H, m) , 2,03Pclição 870180138821, de 08/10/2018, pág. 598/857
590
2,37(4H,m), 2,53(3H,s), 2,57-2,71 (1H, m) , 3,73 e 3,78(total lH,cada d,J=14,4Hz), 4,08-4,17 (lH,m), 4,18 (2H,q,J=7,2Hz) ,
4,55-4, 65 (lH,m), 6,85(1H,br,s), 7,21(1H,dd,J=8,8, 2,OHz),
7,33(1H,d,J=8,8Hz), 7,48(1H,d,J=7,6Hz), 7,63(1H,d,J=2,OHz),
7,98(1H,d,J=7,6Hz), 9,30 (lH,s).
MS (ESI) m/z: 544(M+H)+.
Exemplo 50 (lS,3R,4S)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-3-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)10 carbonil]-amino}-ciclo-hexano-carboxilato de etila:
O composto obtido no Exemplo Referencial 97 (4,2
g) foi colocado em suspensão em etanol (25 ml) , e adicionouse uma solução saturada de ácido clorídrico em etanol (55 ml) à temperatura ambiente, agitando a mistura por 11 h. O solvente foi removido por destilação sob pressão reduzida, para obter sólidos incolores (4,15 g).
Este produto (4,15 g) foi dissolvido em N,Ndimetil-formamida (40 ml), e adicionou-se o composto obtido no Exemplo Referencial 10 (1,72 g) , 1-hidróxi-benzotriazol monoidratado (2,15 g) , e cloridrato de 1-(3-dimetil-aminopropil)-3-etil-carbodiimida (2,15 g), a esta solução, à temperatura ambiente, agitando a mistura por 39 h. A
Petição 870180138821, de 08/10/2018, pág. 599/857
591 mistura da reação foi concentrada sob pressão reduzida, e adicionou-se água ao resíduo, para conduzir extração com clorofórmio. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de magnésio anidro. 0 solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 100:1), para obter o composto do título (1,71 g).
[0C]D = -94° (C = 1, clorofórmio)
Exemplo 51 (IR*,3R*,4S*)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-ciclo-hexano-carboxilato de metila:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 107 com uma solução de ácido clorídrico em etanol, e depois condensando este composto com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 49.
RMN-XH (DMSO-de) δ: 1, 55-1,80 (3H,m) , 1,80-2,20 (3H,m) , 2,602,75(lH,m), 2,92(3H,s), 3, 15-3, 30 (1H, m) , 3, 30-3, 50 (4H, m) ,
3,57(3H,s), 3, 55-3, 70 (lH,m) , 4,20-4,30(1H,m), 4,30-4,40
Petição 870180138821, de 08/10/2018, pág. 600/857
592 (lH,m), 7,02(lH,s), 7,17(1H,dd,J=8,5, 2,OHz), 7,41(lH,d,
J=8,5Hz), 7,71(lH,s), 8, 20-8, 35 (1H, m) , 8, 35- 8, 45 (lH,m),
11,82 (lH,br)
MS (FAB) m/z: 530(M+H)+.
Exemplo 52 (lR*,3S*,4R*)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-ciclo-hexano-carboxilato de etila:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 98 com uma solução saturada de ácido clorídrico em etanol, e depois condensando-o com ácido 5-cloro-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 49.
RMN-iH (CDC13) δ: 1,29 (3H, t, J=7,1Hz) , 1,82-2,30 (6H,m) , 2,49 (3H, s), 2,62-2,73 (lH,m), 3,74-3,85 (2H,m), 3,85- 10
3,93(2H,m), 3,71(2H,s), 4, 12-4,2 9 (3H, m) , 4,4 9-4,59 (1H, m) ,
6,89(lH,br,s), 7,21(1H,dd,J=8,8, 2,OHz), 7,32(1H,d,J=8,8Hz), 7,33 (lH,br,s), 7,41 (lH,br,s), 7, 62 (1H, br, s) , 9,37(lH,s).
MS (ESI) m/z: 544(M+H)+.
Exemplo 53 (IR*,3R*,4S*)-4-{[ (5-cloro-indol-2-il)-carbonil]-amino}-3{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)Petição 870180138821, de 08/10/2018, pág. 601/857
593 carbonil]-amino}-ciclo-hexano-carboxilato de metila:
composto do título foi obtido tratando o composto obtido no Exemplo Referencial 106 com uma solução 4 N de ácido clorídrico em dioxano, e depois condensando-o com ácido 5-cloro-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 49.
EMN-iH (DMSO-de) δ: 1,65-1,80(3H,m), 1,80-2,10(2H,m), 2,152,25(lH,m), 2,55-2,70(1H,m), 2,89(3H,s), 3,05-3,20(1H,m),
3, 30—3, 50 (4H, m) , 3, 55—3, 65 (1H, m) , 3,62(3H,s), 4,20— 4,30 (lH,m), 4,35-4, 45 (lH,m), 7,19 (1H, dd, J=8, 8, 1,2Hz) , 7,23(1H,
s), 7,43(1H,d,J=8,8Hz), 7,73(lH,s), 8, 03(1H,d,J=6,8Hz),
8,73(1H,d,J=8,5Hz), 11,15-1,38(1H,m), ll,85(lH,s).
MS (FAB) m/z: 530(M+H)+.
Exemplo 54 (IR,3R,4S)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-3-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-ciclo-hexano-carboxilato de metila:
Petição 870180138821, de 08/10/2018, pág. 602/857
594 composto do título foi obtido tratando o composto obtido no Exemplo Referencial 112 com uma solução 4 N de ácido clorídrico em dioxano, e depois condensando-o com ácido 5-cloro-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 49.
ΚΜΝ-^ (DMSO-de) δ: 1, 67-1, 76 (3H, m) , 1,88-1,91 (1H, m) , 2,01 (lH,br,s), 2,13-2,22(lH,m), 2,52-2,67(4H,m), 2,86(2H,br,s),
3,04 (2H,br,s), 3,33-3,41(1H,m), 3,61(3H,s), 4,22-4,36(3H,
m), 7,17-7,22 (2H,m), 7,42 (1H,d,J=8,8Hz), 7,72 (lH,s), 8,00 (1H,d,J=6,9Hz), 8,68(1H,d,J=8,6Hz), 11,80 (lH,s).
MS (FAB) m/z: 530(M+H)+.
Exemplo 55
N-((IR*,2S*,5S*)-5-(amino-carbonil)-2-{[(5-cloro-indol-2il)-carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,715 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 113 com uma solução 4 N de ácido clorídrico em dioxano, e depois condensando-o com o composto obtido no Exemplo Referencial 10.
ΗΜΝ-^ (CDC13) δ: 0,78-2,40 (7H, m) , 2,53(3H,s), 2,80-2,8 9 (1H, m), 2,91-3,00(lH,m), 3,68-3,76(2H,m), 4,08-4,19(lH,m), 4,544,65(lH,m), 6, 80 (1H, br, s) , 7,21 (1H, dd, J=8, 4, 1,6Hz), 7,33
Petição 870180138821, de 08/10/2018, pág. 603/857
595 (1Η,d,J=8,4Hz), 7, 38-7, 43 (lH,m) , 7,49-7,55(1H,m), 7,63(1Η, br,s), 9, 14(1Η,br,s) .
MS (ESI) m/z: 515(M+H)+.
Exemplo 56 ácido (IR*,3S*,4R*)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin2-il)-carbonil]-amino}-ciclo-hexano-carboxílico:
composto obtido no Exemplo 49 (916 mg) foi colocado em suspensão em um solvente misto de etanol (10 ml) e tetraidrofurano (8 ml), e adicionou-se uma solução aquosa 1 N (3,3 ml) de hidróxido de sódio à temperatura ambiente, agitando a mistura por 12 h na mesma temperatura. Depois de adicionar ácido clorídrico 1 N (3,3 ml), o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi lavado com dietil-éter, para obter o composto do título (712 mg).
Exemplo 57 cloridrato de N-{(IR*,2S*,5S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}20 5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 604/857
596


Adicionou-se trietil-amina (0,25 ml), cloridrato de dimetil-amina (133 mg), 1-hidróxi-benzotriazol monoidratado (53 mg), e cloridrato de 1-(3-dimetil-aminopropil ) -3-etil-carbodiimida (75 mg), a uma suspensão (10 ml) do composto obtido no Exemplo 56 (168 mg) em clorofórmio, e a mistura foi agitada por 72 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se água ao resíduo, para conduzir extração com clorofórmio. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 93:7). Os sólidos incolores assim obtidos (135 mg) foram colocados em suspensão em etanol (5 ml), e a esta suspensão adicionou-se solução 1 N (0,5 ml) de ácido clorídrico em etanol. A mistura foi agitada por 2 h, e o solvente foi removido por destilação, para obter o composto do título (112 mg).
RMN-1!! (DMSO-ds) δ: 1, 42-2, 07 (6H, m) , 2, 73-3, 70 (1OH, m) , 2,88 (3H,s), 2,97(3H,s), 4, 03-4,20 (lH,m), 4,51-4,67 (lH,m), 7,04 (lH,br,s), 7, 16 (lH,br, J=8, 8Hz) , 7,41 (1H, d, J=8, 8Hz) , 7,68(1H, de 08/10/2018, pág. 605/857
597 br,s), 8,32—8,47(2H,m), 10,76(1H,br,s).
MS (ESI) m/z: 543(M+H)+.
Exemplo 58 ácido (lS,3R,4S)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}5 3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-ciclo-hexano-carboxílico:
O composto obtido no Exemplo 50 (1,6 g) foi colocado em suspensão em um solvente misto de etanol (20 ml) e tetraidrofurano (15 ml), e adicionou-se uma solução aquosa 1 N (5,9 ml) de hidróxido de sódio à temperatura ambiente, agitando a mistura por 12 h na mesma temperatura. Depois de adicionar ácido clorídrico 1 N (5, 9 ml) , o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi lavado com água e dietil-éter, para obter o composto do título (1,19 g) .
Ponto de fusão: 234-236 °C [OC]d = -57° (C = 1,0, metanol)
Exemplo 59 cloridrato de N-{(IR*,2S*,5S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(ciclo-propil-amino)-carbonil]-cicloPclição 870180138821, de 08/10/2018, pág. 606/857
598 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo 58 e ciclo-propil-amina, de uma maneira similar àquela do Exemplo 57.
RMN-1H (DMSO-d6) δ: 0, 32-0, 40 (2H, m) , 0, 53-0, 63 (2H, m) , 1,502,10(6H,m), 2, 25-2, 40 (lH,m) , 2,45-2,70 (2H, m) , 2,91(3H,s),
3, 05-3, 80 (3H,m), 4,05-4,17(1H,m) , 4,30-4,55(2H,m) , 4,554,80(lH,m), 7,03(1H,d,J=l,5Hz), 7,16(1]-1,dd,J=8,8,2,OHz) ,
7,41(1H,d,J=8,8Hz), 7,68(1H,d,J=2,OHz), 7,86(1H,br,J=3,4Hz),
8,06 (lH,br,s), 8,40 (1H, br, J=7, 6Hz) , 11,20-11, 60 (lH,br),
11,79(1H,S) .
MS (FAB) m/z: 555(M+H)+.
Exemplo 60 cloridrato de N-[(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-(pirrolidin-l-il-carbonil)-ciclo-hexil]5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 607/857
599
composto do título foi obtido a partir do composto obtido no Exemplo 58 e pirrolidina, de uma maneira similar àquela do Exemplo 57.
ΚΜΝ-^ (DMSO-de) δ: 1,45-2, 10 (10H, m) , 2, 75-2, 90 (2H, m) , 2,90 (3H,s), 3,10-3,70(H,m), 4,05-4,20(1H,m), 4,25-4,80(3H,m),
7,05(lH,s), 7, 17(1H, d, J=8,7Hz), 7,41 (1H, d, J=8,7Hz) , 7,69(1H, s), 8,32(1H,br,J=7,6Hz), 8,38(1H,br,J=7,1Hz), ll,22(lH,br,
s), 11,78(1H,s).
MS (FAB) m/z: 569(M+H)+.
Exemplo 61 cloridrato de N-[(IR*,2S*,5S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-(4-morfolinil-carbonil)-ciclo-hexil]-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 608/857
600
O composto do título foi obtido a partir do composto obtido no Exemplo 56 e morfolina, de uma maneira similar àquela do Exemplo 57.
RMN-1H (DMSO-de) δ: 1,40-2,05(6H,m), 2,75-3,70(18H,m), 4,025 4,17(lH,m), 4,55-4,69(1H,m), 7,05(1H,br,s), 7,17(1H,br,J=8,8
Hz), 7,41(1H,d,J=8,8Hz), 7,67(1H,br,s), 8,35(1H,d,J=7,6Hz),
8,40(1H,d,J=7,6Hz), 10,79(1H,br,s).
MS (ESI) m/z: 585(N+H)+.
Exemplo 62
N-{(lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5[(etil-amino)-carbonil]-ciclo-hexil}-5-meti1-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto obtido no Exemplo 58 (150 mg) foi dissolvido em N,N-dimetil-formamida (3 ml), e a esta solução adicionou-se cloridrato de N-etil-amina (119 mg), 1-hidróxibenzotriazol monoidratado (79 mg), cloridrato de l—(3— dimetil-amino-propil)-3-etil-carbodiimida (112 mg) e trietil-amina (326 μΐ) , e a mistura foi agitada à temperatura ambiente por 4 dias. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio ao resíduo,
Petição 870180138821, de 08/10/2018, pág. 609/857
601 para conduzir extração com cloreto de metileno. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3) . 0 sólido assim obtido foi dissolvido em cloreto de metileno, e a esta solução adicionou-se uma solução 1 N (171 μΐ) de ácido clorídrico em etanol. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se metanol e dietil-éter ao resíduo, para coletar o precipitado formado por filtração, obtendo desta forma o composto do título (74 mg).
RNIN-iH (DMSO-de) δ: 0, 99 (3H, t, J=7, 2Hz) , 1,57-2, 02 (6H, m) , 2,33-2,38 (lH,m), 2,92(3H,s), 3, 01-3, 08 (2H, m) , 3, 17-3, 20 (2H, s), 3, 45-3, 70(2H,m) , 4,10-4,17(1H,m) , 4,40-4,69(3H,m), 7,04 (1H,d,J=2,OHz), 7,17(1H,dd,J=8,8, 2,OHZ), 7,41(1H,d,J=8,8
Hz), 7, 69(1H,d,J=2,OHz), 7,78-7,81(1H,m), 8,08-8,12(1H,m),
8,40(1H,d,J=8,1Hz), 11,23(1H,br,s), 11,79 (1H,br,s) .
MS (FAB) m/z: 543(M+H)+.
Exemplo 63 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
de 08/10/2018, pág. 610/857
602
O composto obtido no Exemplo 58 (900 mg) foi dissolvido em N,N-dimetil-formamida (50 ml), e a esta solução adicionou-se cloridrato de dimetil-amina (304 mg) , 1-hidróxi-benzotriazol monoidratado (262 mg) , cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (369 mg) e diisopropil-etil-amina (1,83 ml), e a mistura foi agitada à temperatura ambiente por 12 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir extração com cloreto de metileno. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3). Os sólidos assim obtidos foram dissolvidos em cloreto de metileno, e a esta solução adicionou-se uma solução 1 N (1,49 ml) de ácido clorídrico em etanol. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se metanol e dietil-éter ao resíduo, para coletar o precipitado formado por filtração, obtendo desta forma o composto do título (777 mg).
[OC]d = -53,9° (18 °C, c = 0, 505, metanol)
RMN-!H (DMSO-de) δ: 1, 45-1, 60 (1H, m) , 1, 70-1, 85 (3H, m) , 1,902,05(2H,m), 2,80(3H,s), 2,91(3H,s), 2, 95-3, 10 (1H, m) , 2,97 (3H,s), 3, 10—3,75(4H,m), 4,05—4,15(1H,m), 4,35—4,75(3H,m) ,
7,05(lH,s), 7,16(1H, dd,J=8,7,2,1Hz), 7,41(1H, d,J=8,6Hz),
7,67(lH,s), 8, 30-8, 45 (2H,m) , 11, 63 (1H, br) , ll,78(lH,s).
MS (FAB) m/z: 543(M+H)+.
de 08/10/2018, pág. 611/857
603
Exemplo 64 cloridrato de N-((IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-{[(2-metóxi-etil)-(metil)-amino]carbonil}-ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,45 c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 58, de uma maneira similar àquela do Exemplo 57.
RMN-1H (DMSO-de) δ: 1,50-1,99(6H,m), 2,80, 3,01(3H,cada s) ,
2,91(3H,s), 3, 03 (lH,br, s) , 3,16(2H,s), 3,23(3H,s), 3,35-3,67 (6H,m), 4, 09-4,16(lH,m), 4,43-4,67(3H,m), 7,04-7,06(1H,m),
7,16(1H,dd,J=8,8, 2,OHz), 7,42(1H,d,J=8,8Hz), 7,69(1H,br,s),
8,29-8,41(2H,m), 11,59(1H,br,s), 11,80(1H,br,s).
MS (FAB) m/z: 587(M+H)+.
Exemplo 65 cloridrato de N-((IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-{[(2-hidróxi-etil)-(metil)-amino]carbonil}-ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,ίο] -piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 612/857
604
O composto do título foi obtido a partir do composto obtido no Exemplo 58, de uma maneira similar àquela do Exemplo 57.
RMN-1H (DMSO-de) δ: 1,50-1,55 (1H, m) , 1,74-1,84 (3H, m) , 1,945 l,97(2H,m), 2, 67, 3,02(3H,cada s) , 2,91(3H,s), 3,10-3,68 (9H,m), 4,11-4,13(lH,m) , 4,43-4,66(4H,m) , 7,05(lH,s), 7,16 (1H,dd,J=8,7, 2,OHz), 7,41(1H,d,J=8, 7Hz) , 7,68(lH,s), 8,348,40(2H,m), 11,47 (1H, br, s) , ll,79(lH,s).
MS (FAB) m/z: 573(M+H)+.
Exemplo 66 cloridrato de N-((IR,2S,5S)-5-(1-azetidinil-carbonil)-2{[(5-cloro-indol-2-il)-carbonil]-amino}-ciclo-hexil)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 613/857
605
O composto do título foi obtido a partir do composto obtido no Exemplo 58, de uma maneira similar àquela do Exemplo 57.
RMN-1H (DMSO-de) δ: 1, 47-1,55 (1H, m) , 1, 65-1,82 (3H, m) , 1,885 2,01(2H,m), 2, 16(2H,quint.,J=7,6Hz), 3,17-3,67(5H,m), 3,82 (2H,t,J=7,6Hz), 4,02-4,14(3H,m), 4,43-4,67(3H,m), 7,O6(1H,
s), 7, 17(1H,dd,J=8,7, 1,7Hz), 7, 41(1H,d,J=8,7Hz), 7,69(1H, br,s), 8, 31(1H,d,J=7,6Hz), 8,38 (1H, d, J=7, 6Hz) , ll,41(lH,br,
s), 11,80 (1H,s) .
MS (FAB) m/z: 555(M+H)+.
Exemplo 67 cloridrato de N-((IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-{[(3S)-3-flúor-pirrolidinil]-carbonil}ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]15 piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 58 e (S)-flúor-pirrolidina (Synlett. 1995, página 55), de uma maneira similar àquela do Exemplo 57.
RMN-1H (DMSO-de) δ: 1, 23-3, 77 (22H,m) , 4,11-4,16 (1H, m) , 4,584,51(lH,m), 5, 23-5, 42 (lH,m) , 7,05(lH,s), 7, 16 (1H, d, J=8, 3Hz) ,
Petição 870180138821, de 08/10/2018, pág. 614/857
606
7,42(1Η,d,J=8,3Hz), 7,68(lH,s), 8, 34-8, 37(2Η, m) , 11,78 (1H,
s) .
MS (FAB) m/z: 587(M+H)+.
Exemplo 68 (IR*,3R*,4S*)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-ciclo-hexano-carboxilato de lítio:
O composto obtido no Exemplo 51 (1,20 g) foi dissolvido em tetraidrofurano (32 ml) , e adicionou-se sucessivamente hidróxido de lítio (60,8 mg) e água (4 ml), sob resfriamento com gelo, agitando a mistura à temperatura ambiente por 14 h. O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (1,12
9) ·
RMN-iH (DMSO-de) δ: 1, 55-1, 70 (2H, m) , 1,70-2,05 (4H, m) , 2,102,20(lH,m), 2,25-2,40 (4H,m) , 2,50-2,80 (4H, m) , 3, 45-3, 65 (3H,
m), 4,10—4,30(2H,m), 7,00—7,20(2H,m), 7,50—7,65(2H,m).
Exemplo 69 cloridrato de N-((IR*,2S*,4S*)-2-{[(5-cloro-indol-2-il)20 carbonil]-amino}-4-[(dimetil-amino)-carbonil]-ciclo-hexil}5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 615/857
607
O composto do título foi obtido a partir do composto obtido no Exemplo 68 e dimetil-amina, de uma maneira similar àquela do Exemplo 57.
RMN-1!! (DMSO-dg) δ: 1,40-1,60(2H,m), 1,65-1,80(2H,m), 1,955 2,10(2H,m), 2,84(3H,s), 2, 90-3, 05 (1H, m) , 2,92(3H,s), 3,06 (3H,s), 3,15—3,75(4H,m), 4,25—4,75(4H,m), 7,02(1H,d,J=1,5
Hz), 7,15(1H,dd,J=8,8, 2,1Hz), 7,41(1H,d,J=8,8Hz), 7,69(1H, d,J=2,lHz), 8,05(1H,d,J=7,7Hz), 8,63(1H,d,J=7,7Hz), 11,20 (lH,br) , 11,79 (1H, s) .
MS (FAB) m/z: 543(M+H)+.
Exemplo 70 cloridrato de N-((IR, 2S, 5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-{[(3R)-3-hidróxi-pirrolidinil]-carbonil}ciclo-hexil-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]15 piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 616/857
608
1) O composto obtido no Exemplo Referencial 58 (1,18 g) foi dissolvido em metanol (12 ml), adicionou-se ácido clorídrico 1 N (240 μΐ) e hidróxido de paládio (221 mg) , e introduziu-se hidrogênio para conduzir a redução catalítica sobre condições normais de temperatura e pressão por 4,5 h. O catalisador foi removido por filtração, e o filtrado foi concentrado até tornar-se sólido, sob pressão reduzida, para obter o cloridrato de (3R)-3-{[t-butil(difenil)-silil]oxi}-pirrolidina (984 mg).
O produto assim obtido (249 mg) , o produto obtido no Exemplo 58 (295 mg), cloridrato de 1-(3-dimetil-aminopropil)-3-etil-carbodiimida (126 mg) e 1-hidróxibenzotriazol monoidratado (87 mg), foram dissolvidos em N,Ndimetil-formamida (10 ml) . Adicionou-se diisopropil-etilamina (450 μΐ) em gotas à solução sob resfriamento com gelo, e a mistura foi agitada à temperatura ambiente por 12 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi submetido a uma cromatografia de coluna em sílica-gel (metanol:cloreto de metileno: 3:97), para obter N((IR,2S,5S)-5-[((3R)-3-{[t-butil-(difenil)-silil]oxi}pirrolidinil)-carbonil]-2-{[(5-cloro-indol-2-il)-carbonil]amino}-ciclo-hexil-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida (248 mg).
de 08/10/2018, pág. 617/857
609
RMN-1 H (CDC13) 8: l,06(9H,s), 1, 50-1, 60(1H,m), 1,75-2,10 (5H,m), 2,20-2,50(2H,m), 2,54(3H, d,J=2,8Hz), 2, 60-3, 00(5H,
m) , 3, 30-3, 80(6H,m), 4,10-4,20(lH,m), 4,40-4,70 (2H,m), 6,85 (lH,s), 7,15—7,25(1H,m), 7,30—7,50(8H,m), 7,60—7,70(5H,m),
7, 90-8, 00 (lH,m) , 9,38(lH,s).
MS (FAB) m/z: 823(M+H)+.
2) O produto acima (240 mg) foi dissolvido em piridina (10 ml) , e adicionou-se complexo de ácido
|
fluorídrico/piridina |
(3,0 |
ml) |
em |
gotas sob |
resfriamento com |
|
gelo, agitando a mistura |
a 0 |
°C |
por 4,5 |
h. Adicionou-se |
|
acetato de etila |
(80 |
ml) |
à |
mistura |
da reação sob |
resfriamento com gelo, para diluí-la. Depois de adicionar bicarbonato de sódio a esta solução para alcalinizá-la, conduziu-se a separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno: 1:19 —> 1:9). O produto purificado bruto resultante foi dissolvido em cloreto de metileno e metanol, e a esta solução adicionou-se solução (225 μΐ) de ácido clorídrico 1 N em etanol, para secá-la uma vez. Adicionou-se metanol e dietil-éter ao resíduo para solidificá-lo, obtendo desta forma o composto do título (114 mg).
RMN-!H (DMSO-de) δ: 1, 50-1, 60 (1H, m) , 1, 70-2,10 ( 6H, m) , 2,752,85(lH,m), 2,92(3H,s), 3, 10-3, 80 (8H, m) , 4,10-5,10 (6H,m) , 7,05 (1H, d, J=l, 7Hz) , 7,16 (1H, dd, J=8, 8, 1,7Hz), 7,42(lH,d,J=
8,8Hz), 7,68(lH,s), 8, 30-8, 45 (2H, m) , 11, 10-11, 40 (lH,m) , de 08/10/2018, pág. 618/857
610
11,78(1Η,s).
MS (FAB) m/z: 585(M+H)+.
Exemplo 71
N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5,55 dimetóxi-ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridino-2-carboxamida ou N-((IR*,2S*)-2-{[(5-cloroindol-2-il)-carbonil]-amino}-4,4-dimetóxi-ciclo-hexil)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 118 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2.
RMN-1H (CDC13) 6: 2,11-215(1H,m), 2,21-2,25(1H,m), 2,4115 2,43(lH,m), 2,46 (3H,s), 2,7 0-2,75 (1H, m) , 2,81(lH,m), 3,21 (3H,s), 3,24(3H,s), 3,49 (lH,s), 3,58 (1H, d, J=15, 6Hz) , 3,71 (1H,d,J=15,6Hz), 3,87-3,93(1H, m), 4,26-4,29(1H,m), 6,85(1H, d,J=2,OHz), 7,19(1H,dd,J=8,5, 2,0 Hz), 7,30(1H,d,J=8,5Hz),
7,62(1H,s), 9,21(1H,s) .
Exemplo 72
N-((IR*, 2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5oxo-ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida ou N-((IR*,2S*)-2-{[(5-cloro-indol-2il)-carbonil]-amino}-4-oxo-ciclo-hexil)-5-metil-4,5,6,725 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto obtido no Exemplo Referencial 71 (100 mg) foi dissolvido em clorofórmio (2 ml), e adicionou-se ácido triflúor-acético (0,5 ml) e água (0,5 ml), agitando a
Petição 870180138821, de 08/10/2018, pág. 619/857
611 mistura à temperatura ambiente por 3,5 h. Uma solução aquosa saturada de bicarbonato de sódio foi adicionada à mistura da reação, para conduzir a extração com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:metanol 19:1). Os sólidos brancos assim obtidos foram dissolvidos em metanol (4 ml), e a esta solução adicionou-se solução de ácido clorídrico 1 N em etanol (0,38 ml) . O solvente foi removido por destilação sob pressão reduzida, para obter o composto do título (35 mg) .
RMN-1H (DMSO-de) δ: 1, 83-1, 90 (1H, m) , 2,08-2,10 (1H, m) , 2,282,32(lH,m), 2,50-2,5 9 (1H, m) , 2,87(3H,s), 2, 96 (1H, t, J=13, O
Hz), 3,06-3,10(2H,m), 3,33-3,36(3H,m), 4,02-4,04(2H,m), 4,55
-4,57(2H,m), 7,03(lH,s), 7,15(lH,d,J= 8,8Hz), 7,38(lH,d,J=
8,8Hz), 7,69(lH,s), 8,43(1H,d,J=8,8Hz), 8,91(1H,d,J=8,8Hz) ,
11,75(1H,s).
Exemplo 73
N-((IR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5(hidróxi-imino)-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida ou N((IR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-4(hidróxi-imino)-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida de 08/10/2018, pág. 620/857
612 composto obtido no Exemplo 72 (133 mg) foi dissolvido em um solvente misto de piridina (8 ml) e metanol (8 ml) , e adicionou-se cloridrato de hidroxilamina (30 mg), agitando a mistura à temperatura ambiente por 3 dias. A mistura da reação foi concentrada, e adicionou-se água para conduzir a extração com acetato de etila. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 97:3 —»
17:3), para obter o composto do título (131 mg).
RMN-!H (CDCls) δ: 1, 43-1, 86 (3H) , 1, 98-2,03 (1H, m) , 2,26-2,30 (lH,m), 2,45(3H,s), 2, 47-2,51 (lH,m) , 2, 67-2,71 (lH,m) , 2,7815 2,86(3H,m), 3, 86-3, 43 (2H, m) , 4,16-4,24 (2H,m) , 6,85(lH,s),
7,16-7,13 (lH,m) , 7,20-7,24 (lH,m) , 7,46, 7,50(total lH,s),
7,56—7, 64 (2H,m) , 9, 59, 9, 62 (total 1H, s) .
Exemplo 74
N-((7R*,8S*)-8-{[(5-cloro-indol-2-il)-carbonil]-amino}-!,420 dioxaespiro[4.5]dec-7-il-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida ou N((7R*,8S*)-7-{[(5-cloro-indol-2-il)-carbonil]-amino}-!,4dioxaespiro[4.5]dec-8-il-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 120 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2.
Petição 870180138821, de 08/10/2018, pág. 621/857
613
RMN-1 H (CDCls) δ: 1, 69-1, 87(6H,m), 2,14-2,17((1H,m), 2,302,32(lH,m), 2,47(3H,s), 2,7 0-2,75 (1H, m)
2,81-2,89(2H,m)
3,89-3,91(lH,m)
2,OHz), 7,19(1H
3, 58 (1H, d, J=15, 4Hz) , 3,72(lH,d,J= 15,4Hz)
dd,J=8,8, 2,OHz), 7,30(1H,d,J=8,8Hz), 7,38 (1H,d,J=7,3Hz)
7, 62 (lH,d, J=2,OHz) , 9,15(lH,s).
Exemplo 75
N-((IR*, 2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5(metóxi-imino)-ciclo-hexil)-5-metil-4,5, 6, 710 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida ou N((IR*, 2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-4(metóxi-imino)-ciclo-hexil)-5-metil-4,5,6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
1) O composto obtido no Exemplo Referencial 124 (2,21 g) foi dissolvido em cloreto de metileno (30 ml), a adicionou-se ácido triflúor-acético (6 ml), agitando a mistura à temperatura ambiente por 1,5 h. A mistura da reação foi concentrada, secada com uma bomba a vácuo e depois dissolvida em N,N-dimetil-formamida (20 ml), e a esta solução adicionou-se ácido 5-cloro-indol-2-carboxílico (500 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etilcarbodiimida (593 mg), 1-hidróxi-benzotriazol monoidratado (473 mg) e N-metil-morfolina (2,8 ml) . A mistura foi agitada à temperatura ambiente por 10 h. Adicionou-se mais ácido 5-cloro-indol-2-carboxílico (242 mg), cloridrato de 1(3-dimetil-amino-propil)-3-etil-carbodiimida (237 mg) e 1hidróxi-benzotriazol monoidratado (189 mg) , agitando a mistura por 4 h. Adicionou-se uma solução aquosa saturada
Petição 870180138821, de 08/10/2018, pág. 622/857
614 de bicarbonato de sódio à mistura da reação, para conduzir a extração com acetato de etila e com um solvente misto de acetato de etila e tetraidrofurano. As camadas orgânicas resultantes foram lavadas com solução aquosa saturada de cloreto de sódio e secadas sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 97:3 —»
4:3), para obter N-[(IR*,2S*)-2-amino-5-(metóxi-imino)ciclo-hexil]-5-cloro-indol-2-carboxamida (368 mg) e N[(1R*,2S*) -2- amino-4-(metóxi-imino)-ciclo-hexil]-5-cloroindol-2-carboxamida (300 mg).
2) O composto do título (mistura de isômeros sin e anti no grupo metóxi-imino) foi obtido a partir de um dos compostos descritos acima, N-[(IR*,2S*)-2-amino-5-(metóxiimino) -ciclo-hexil] -5-cloro-indol-2-carboxamida e N[(1R*,2S*) -2- amino-4-(metóxi-imino)-ciclo-hexil]-5-cloroindol-2-carboxamida, e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2. RMN-1H (CDC13) δ: 1, 84-2,00 (3H, m) , 2,2 6-2,5 6 (3H, m) , 2,46(3H,
s), 2,80-2,83 (4H,m) , 3, 57 (1H, q, J=15, 4Hz) , 3,70(lH,q,J= 15,4
Hz), 3,84, 3,85(total 3H,s), 4,08-4,14(lH,m), 4,26-4,30 (lH,m), 6,84 (lH,s), 7,17(1H,d,J=8,8Hz), 7,27(1H,d,J=8,8Hz),
7,46-7,48 (2H,m) , 7,56(1H, m) , 9, 42, 9, 55(total lH,s).
Exemplo 76
N-((IR*, 2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5(hidróxi-ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridino-2-carboxamida (Estereoisômero A) ou Nde 08/10/2018, pág. 623/857
615 ((IR*, 2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-4(hidróxi-ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridino-2-carboxamida (Estereoisômero A):
1) N-((IR*,2S*)-2-amino-4-{[t-butil-(difenil) 5 silil] oxi} -ciclo -hexil) -5-cloro-indol-2-carboxamida (Estereoisômero A) e N-((1R*,2S*) -2- amino-5-{[t-butil(difenil)-silil]oxi}-ciclo-hexil) -5- cloro- indol -2carboxamida (Estereoisômero B) foram obtidos submetendo a forma (1R*,2S*) obtida no Exemplo Referencial 125 à des-(t10 butil)-carbonilação, da mesma maneira que na etapa (1) do Exemplo 75, e reagindo o produto formado com ácido 5-cloroindol-2-carboxílico.
2) N-((IR*,2S*)-5-{[t-butil-(difenil)-silil]oxi}2-{[(5-cloro-indol-2-il)-carbonil] -amino} -ciclo-hexil)-515 metil-4,5, 6, 7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida (Estereoisômero A) ou N-((IR*,2S*)-4-{[t-butil-(difenil)silil]oxi}-2-{[(5-cloro-indol-2-il)-carbonil] -amino}-ciclohexil) -5-metil-4,5,6,7-tetraidrotiazolo[5, 4-c] -piridino -2carboxamida (Estereoisômero A) foi obtido a partir do composto obtido pela reação acima e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2.
RMN-!H (CDCls) δ: l,06(9H,s), 1, 55-1, 61 (1H, m) , 1,85-1,90 (lH,m), 2,18-2,25(lH,m), 2,46(3H,s), 2,51(2H,d,J=7,6Hz),
2,72(lH,m), 3,56(lH,s), 3, 57 (1H, d, J=15, 3Hz) , 3,72(lH,d,J=
15,3Hz), 3,76(lH,m), 3, 88-3, 95 (lH,m) , 6,78(lH,s), 7,17(1H, dd,J=2,O, 8,8Hz), 7,37-7,44 (7H,m) , 7,59(lH,s), 7,65-7,68 (6H,m), 9, 30(1H, s) .
Petição 870180138821, de 08/10/2018, pág. 624/857
616
3) 0 composto do título foi obtido a partir do composto obtido pela reação acima, da mesma maneira que aquela descrita na etapa (3) do Exemplo 28.
RMN-iH (DMSO-de) δ: 1, 25-1, 30 (2H, m) , 1, 45-1, 64 (2H, m) ,
1,86(1H,d,J=9,OHz) ,
2,75-2,79(2H,m), 3,
3,96-4,02(2H,m), 4, dd,J=2,O, 8,8Hz), 7,
J=7,8Hz), 8,54(lH,d,
1, 982,03 (lH,m) , 2,33(3H,s), 2,69(2H,m),
54(1H, d, J=15,6Hz), 3,62(1H,d,J=15,6Hz), (lH,d, J=4,2Hz) , 7,00(lH,s), 7,14(1H, (1H, d, J=8, 8Hz) , 7,66(lH,s), 8,20(lH,d, J=7,8Hz), 11,69(1H,s).
Exemplo 77
N-((IR*, 2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5(hidróxi-5-metil-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida (Estereoisômero Al) ou N-((IR*,2S*)-2-{[(5-cloro-indol-215 il)-carbonil]-amino}-4-(hidróxi-4-metil-ciclo-hexil)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida (Estereoisômero A2):
Os compostos do título foram obtidos reagindo o composto obtido no Exemplo Referencial 128 com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2.
Estereoisômero Al:
RMN-!H (DMSO-de) δ: l,24(3H,s), 1, 33-1, 82 (4H, m) , 2,34(3H,s),
2, 67-3, 64 (8H,m), 4,02-4,10 (2H,m) , 4, 67 (1H, br, s) , 7,O2(1H,
s), 7,13(1H, d,J=8,6Hz), 7,38(1H,d,J=8,6Hz), 7, 66(1H,d,J=2,O
Hz), 8,21-8,26(1H,br), 8,59(1H,d,J=8,1Hz), 11,73(1H,br,s).
MS (FAB) m/z: 5O2(M+H)+.
Estereoisômero A2:
Petição 870180138821, de 08/10/2018, pág. 625/857
617
RMN-1H (DMSO-de) δ: l,25(3H,s), 1,33-1,79 (4H, m) , 2,33(3H,s),
2, 65-3, 63 (8H,m) , 3, 88-3, 94 (1H, m) , 4,20,4,25 (1H, m) , 4,59(1H, br), 7,01(lH,s), 7, 13(1H, d,J=7,8Hz), 7,38(1H,d,J=8,6Hz), 7,67(1H, s), 8,29(lH,br), 8, 43 (1H, d, J=9, 3Hz) , 11, 67 (1H, br) .
MS (FAB) m/z: 502(M+H)+.
Exemplo 78
N-[(lR*,2R*,5S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}5-(hidróxi-metil)-ciclo-hexil]-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 129 com uma solução de ácido clorídrico em etanol, e depois condensando-o com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 49.
RMN-1H (DMSO-de) δ: 1,42-1, 90 (51-1,m) , 2, 07-2,26 (3H,m) , 2,46 (3H,s), 2, 67-2, 95 (4H,m), 3, 55-3, 80(4H,m), 3, 80-3, 95(1H,m),
4,13-4,25(lH,m), 6,84(1H,br,s), 7,17 (1H,dd,J=8,8, 2,OHz),
7,23-7,35(2H,m), 7,43(1H,d,J=7,2Hz), 7,58(1H,br,s), 9,29(1H,
s) .
MS (ESI) m/z: 502(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 626/857
618
Exemplo 79
N-[(lR*,2R*,5S*)-2~{[(5-cloro-indol-2-il)-carbonil]-amino}5-(metóxi-metil)-ciclo-hexil]-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
0 composto do título foi obtido tratando o composto obtido no Exemplo Referencial 135 com uma solução de ácido clorídrico em etanol, e depois condensando-o com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 49.
RMN-1H (CDC13) δ: 1,20-1,38 (1H, m) , 1,50-1,67 (2H, m) , 1,882,03(2H,m), 2, 03-2, 14 (1H, m) , 2,21-2,32 (1H, m) , 2,53(3H,s),
2,75-2, 95 (2H,m) , 3, 20-3, 35 (2H, m) , 3,37(3H,s), 3,71(lH,d,J=
16,0Hz), 3,76(lH,d,J=16,0Hz), 4,04-4,13(1H,m), 4,53-4,62(1H,
m) , 6,85(lH,d, J=2,OHz) , 7, 19 (1H, dd, J=8, 8, 2,OHz), 7,33(1H, d,J=8,8Hz), 7,54(1H,d,J=7,2Hz), 7,63(1H,d,J=2,OHz), 8,O7(1H, d,J=5,6Hz), 9, 49 (lH,br, s) .
Exemplo 80
N-((IR*, 2R*, 5S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}5-{[(metil-sulfonil)-amino]-metil}-ciclo-hexil)-5-metil20 4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 627/857
619

1) O composto obtido no Exemplo Referencial 137 (437 mg) foi dissolvido em etanol (5 ml), e adicionou-se uma solução 4 N (5 ml) de ácido clorídrico em dioxano à temperatura ambiente, agitando a mistura por 13 h. O solvente foi removido por destilação, o resíduo foi dissolvido em N,N-dimetil-formamida (10 ml), e a esta solução adicionou-se trietil-amina (0,7 ml), o composto obtido no Exemplo Referencial 10 (300 mg) , 1-hidróxibenzotriazol monoidratado (162 mg) e cloridrato de l—(3 — dimetil-amino-propil)-3-etil-carbodiimida (230 mg). A mistura foi agitada por 13 h, e adicionou-se água à mistura da reação, para conduzir a extração com clorofórmio. A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 97:3), para obter N-((IR*,2R*,5S*)-5(azido-metil)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida (330 mg).
de 08/10/2018, pág. 628/857
620
RMN-1 H (DMSO-de) δ: 1, 15-2,08 (7H, m) , 2,33(3H,s), 2,34-2,95 (6H,m), 3,64(2H,s), 4,05-4,17 (1H, m) , 4,3 6-4,4 7 (1H, m) , 7,02 (lH,s), 7,15(1Η,dd,J=8,8, 2,OHz), 7,40(1H,d,J=8,8Hz), 7,67 (lH,d,J=2,OHz), 8,02(1H,d,J=7,6Hz), 8,44(1H,d,J=7,6Hz), 11,8 (1H,S) .
2) O composto obtido pela reação acima (300 mg) foi dissolvido em etanol (8 ml) , e adicionou-se uma quantidade catalítica de 10% de paládio sobre carvão, agitando a mistura à temperatura ambiente por 168 h em uma atmosfera de hidrogênio. Os insolúveis foram filtrados, e o solvente foi removido por destilação. A N-((IR*,2R*,5S*)-5(amino-metil) -2- {[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil) -5- metil -4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida bruta (150 mg) assim obtida foi dissolvida em clorofórmio (6 ml), e adicionou-se trietilamina (0,2 ml) e cloreto de metano-sulfonila (0,035 ml), agitando a mistura por 13 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se água ao resíduo, para conduzir a extração com clorofórmio. A camada orgânica resultante foi lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de magnésio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 24:1), para obter o composto do título (56 mg) .
RMN-1H (CDCls) δ: 1, 18-1, 34 (2H, m) , 1, 50-1, 75 (4H, m) , 1,90de 08/10/2018, pág. 629/857
621
2,30(4H,m), 2,53(3H,s), 2,78-2, 90 (2H, m) , 2,90-3, 05 ( 6H, m) ,
3, 20 —3,30(lH,m), 3,68- 3, 81 (2H, m) , 3, 98- 4,08(lH,m), 4,544,62 (lH,m), 6, 10-6, 19 (1H, m) , 6,86(lH,s), 7,19 (1H, dd, J=8,8, 2,OHz), 7,35 (1H,d,J=8,8Hz) , 7,52 (1H,d,J=7,6Hz) , 7,62 (lH,d, J=2,OHz) , 8,21 (1H, d, J=5, 6Hz) , 9,89(lH,s).
MS (ESI) m/z: 579(M+H)+.
Exemplo 81 triflúor-acetato de N-{(IR*,2R*,5S*)-2-{[(5-cloro-indol-2il)-carbonil]-amino}-5-[(dimetil-amino)-metil]-ciclo-hexil}10 5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
O composto do título foi obtido a partir da amina obtida na etapa (2) do Exemplo 80, de uma maneira similar àquela do Exemplo 24.
RMN-iH (DMSO-dg) δ: 1, 15-2,22 (7H, m) , 2,40-2, 65 (2H, m) , 2,682,85(6H,m), 2,92-3,08(5H,m), 3,10-3,18(2H,m), 4,08-4,20(1H,
m) , 4,35-4,51 (2H,m) , 7,04(lH,s), 7, 14-7,20 (1H, m) , 7,41(lH,d,
J=8,8Hz), 7,67(lH,s), 8, 25-8, 42 (2H, m) , 9, 11 (1H, br, s) , 9,89 (1H,s) .
MS (ESI) m/z: 529(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 630/857
622
Exemplo 82 (3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-3-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil ] -amino } -ciclo-hexil-carbamato de t-butila (Isômero B) e (3R*,4S*)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil ] -amino } -ciclo-hexil-carbamato de t-butila (Isômero B):

composto obtido no Exemplo Referencial (Estereoisômero B) (1,79 g) foi dissolvido em tetraidrofurano (36 ml), e adicionou-se 10% de paládio sobre carvão (0,40 g) , agitando a mistura à temperatura ambiente por 20 h em uma atmosfera de hidrogênio. Depois de remover o catalisador por filtração, o filtrado foi concentrado sob pressão reduzida, e o resíduo foi dissolvido em N,N-dimetilformamida (36 ml), e a esta solução adicionou-se 5-cloro10 indol-2-carboxilato de p-nitro-fenila (2,02 g) , agitando a mistura por 16 h. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se acetato de etila e água ao resíduo, para coletar os insolúveis por filtração. O produto foi lavado com acetato de etila, para obter (3R*,4S*)-3-amino-4-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil-carbamato (ou (3R*,4S*)-4-amino-3-{[(5-cloroPclição 870180138821, de 08/10/2018, pág. 631/857
623 indol-2-il)-carbonil]-amino}-ciclo-hexil-carbamato) de tbutila (Isômero Bl) (1,49 g). A camada orgânica do filtrado foi lavada com água e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 30:1 —»
10:1), para obter (3R*,4S*)-4-amino-3-{[(5-cloro-indol-2il)-carbonil]-amino}-ciclo-hexil-carbamato de t-butila (ou (3R*,4S*)-3-amino-4-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil-carbamato de t-butila) (Isômero B2) (0,37 g) .
Um dos compostos do título foi obtido a partir do Isômero Bl e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 2.
RMN-!H (DMSO-de) δ: 1, 25-1, 50 (1H, m) , l,37(9H,s), 1,50-1,65 (lH,m), 1, 75-2,20 (4H,m) , 2,37(3H,s), 2,7 0-3, 00 (4H, m) , 3,603,80 (3H,m), 4,13 (1H, br, s) , 4,43 (1H, br, s) , 6, 92 (1H, d, J=7,1
Hz), 7,05(lH,s), 7,17(1H, dd,J=8,8, 2,2Hz), 7,41(1H,d,J=8,8
Hz), 7,69(lH,s), 8, 15(1H,d,J=7,8Hz), 8, 37(1H,d,J=7,1Hz),
11, 78(1H, s) .
MS (FAB) m/z: 587(M+H)+.
O outro composto do título foi obtido a partir do Isômero B2, da mesma maneira.
RMN-1H (DMSO-de) δ: 1, 15-1, 30 (1H, m) , l,35(9H,s), 1,45-1,60 (lH,m), 1, 65-1, 75(lH,m), 1, 85-1, 95(lH,m), 2,05-2,20(2H,m) ,
2,34(3H,s), 2, 65-2,85 (4H,m), 3, 55-3, 70 (3H,m), 4,05-4,14(1
H,m), 4,40(lH,br,s), 6,80(1H,d,J=7,3Hz), 7,15-7,25(2H,m),
7,43(lH,d, J=8,8Hz), 7,73 (1H, d, J=2, OHz) , 8, 05 (1H, d, J=6, 6Hz) ,
8,51(lH,d, J=8,8Hz), ll,82(lH,s).
de 08/10/2018, pág. 632/857
624
MS (FAB) m/z: 587(M+H)+.
Exemplo 83 cloridrato de N-(IR*,2S*)-5-amino-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5, 6, 75 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida (ou N(IR*,2S*)-4-amino-2-{[(5-cloro-indol-2-il)-carbonil]-amino}ciclo-hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida) (Estereoisômero B):
composto (Estereoisômero B) (1,11 g) sintetizado a partir do Isômero Bl no Exemplo 82 foi colocado em suspensão em cloreto de metileno (20 ml), e adicionou-se uma solução de ácido clorídrico em etanol (20 ml) , agitando a mistura à temperatura ambiente por 2 h. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por filtração em gel (Sephadex LH-20, metanol), para obter o composto do título (1,05 g).
RMN-1H (DMSO-de) δ: 1,55-1, 65 (1H, m) , 1,75-1,90(2H,m), 1,952,20(2H,m), 2, 20-2, 40 (1H, m) , 2,90(3H,s), 3, 10-3, 20 (1H, m) ,
3,20-3,50(3H,m), 3,65-3,75(1H,m), 4,10-4,20(1H,m), 4,3520 4,50(lH,m), 4,55-4,65(1H,m), 4,65-4,75(1H,m), 7,07(lH,s),
7,17 (1H,dd,J=8,8, 2,OHz), 7,42(1H,d,J=8,8Hz), 7,69(lH,s),
8,05-8,30(3H,br), 8,40-8,50(2H,m), 11,70-11,90(2H,m).
MS (FAB) m/z: 487(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 633/857
625
Exemplo 84
N-{(IR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5[(metil-sulfonil)-amino]-ciclo-hexil}-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida ou N5 {(IR*,2S*)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-4[(metil-sulfonil)-amino]-ciclo-hexil}-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida (Estereoisômero B):
O composto obtido no Exemplo 83 (0,20 g) foi colocado em suspensão em cloreto de metileno (7 ml), e adicionou-se trietil-amina (0,16 ml) e cloreto de metanosulfonila (28 μΐ), agitando a mistura à temperatura ambiente por 20 h. Depois de diluir a mistura da reação com cloreto de metileno, ela foi lavada com uma solução aquosa de hidróxido de sódio e secada sobre sulfato de sódio anidro.
O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 30:1 —>
15:1), para obter o composto do título (67,9 g).
ΚΜΝ-^ (DMSO-de) δ: 1, 40-1,55 (1H, m) , 1, 65-1,85 (2H, m) , 1,902,05(2H,m), 2,15-2,25(1H,m), 2,41(3H,s), 2,75-2,95(4H,m),
Petição 870180138821, de 08/10/2018, pág. 634/857
626
2,92 (3H,s), 3,55-3,80(3H,m), 4,10-4,20(1H,m), 4,45-4,55(1H, m) , 7,08(lH,s), 7,15-7,20(2Η,m), 7,41(1H,d,J=8,8Hz), 7,69 (lH,s), 8,27(1H,d,J=7,3Hz), 8,33(1H,d,J=8,1Hz), ll,77(lH,s). MS (FAB) m/z: 565 (M+H)+.
Exemplo 85
N-((IR*,2S*)-5-acetil-amino-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida ou N((IR*,2S*)-4-acetil-amino-2-{[(5-cloro-indol-2-il)10 carbonil]-amino}-ciclo-hexil)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida (Estereoisômero B):
O composto (Estereoisômero B) (0,20 g) obtido no Exemplo 83 foi colocado em suspensão em cloreto de metileno (7 ml), e adicionou-se trietil-amina (0,16 ml) e anidrido acético (34 μΐ) , agitando a mistura à temperatura ambiente por 20 h. Adicionou-se cloreto de metileno e uma solução aquosa de hidróxido de sódio à mistura da reação, para separar os insolúveis por filtração. A camada orgânica do filtrado foi lavada com água e secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão
Petição 870180138821, de 08/10/2018, pág. 635/857
627
|
reduzida. 0 |
resíduo |
resultante |
foi purificado |
por |
|
cromatografia |
de coluna em sílica-gel (cloreto |
de |
|
metileno:metanol |
15:1 |
10:1) , para |
obter o composto |
do |
|
título (0,12 g) . |
|
|
|
|
|
ΗΜΝ^Η (DMSO-de) |
δ: 1,35- |
-1,50(1H, m) , |
1,55-1,70(lH,m), 1 |
, 80 |
(3H,s), 1, 80-2, 05(3H,m) , 2, 05-2,20(1Η,m) , 2,47(3H,s), 2,803,00(4H,m), 3,75-4,00(3H,m), 4,15-4,30(1H, m) , 4,45-4,55(1H,
m), 7,07(lH,s), 7,17(1H,dd,J=8,8,1,OHz), 7,41(1H,d,J=8,8Hz), 7,69(lH,s), 7, 89 (1H, d, J=7, 3Hz) , 8,24 (1H, d, J=8, 1Hz) , 8,31(1H, d,J=7,3Hz), ll,77(lH,s).
MS (FAB) m/z: 528(M+H)+.
Exemplo 86 cloridrato de N-((IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-{[metóxi-(metil)-amino]-carbonil}-ciclo15 hexil)-5-metil-4,5,6,7-tetraidrotiazolo[5, 4-c]-piridino-2carboxamida:
O composto obtido no Exemplo 58 (250 mg) foi dissolvido em N,N-dimetil-formamida (5 ml), e adicionou-se cloridrato de N,O-dimetil-hidroxilamina (142 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (111 mg), 1-hidróxi-benzotriazol monoidratado (89 mg) e N-metilPclição 870180138821, de 08/10/2018, pág. 636/857
628 morfolina (213 ml), agitando a mistura à temperatura ambiente por 19 h. Depois de concentrar a mistura da reação, adicionou-se uma solução aquosa de bicarbonato de sódio ao resíduo, para conduzir a extração com acetato de etila. Depois de lavar a camada orgânica resultante com solução aquosa saturada de cloreto de sódio e secar sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida. 0 resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3 —» 23:2), para obter um sólido amorfo incolor (179 mg) . Este produto foi dissolvido em metanol/tetraidrofurano, e adicionou-se uma solução (960 ml) de ácido clorídrico 1 N em etanol, para obter o composto do título.
RMN-!H (DMSO-de) δ: 1, 57-1, 91 (4H, m) , 1, 96-2,00 (1H, m) , 2,102,21(lH,m), 2,92(3H,s), 2, 93-3, 03 (2H, m) , 3,08(3H,s), 3,103,28(2H,m), 4,16-4,19(1H,m), 4,50-4,52(1H,m), 4,69(1H,br,s),
7,06 (lH,s), 7,17 (1H,dd,J=8,8, 1,5Hz), 7,42 (1H,d,J=8,8Hz),
7,70(lH,s), 8, 33 (lH,br, s) , 8, 41 (1H, d, J=7, 8Hz) , 11,81(1H, br, s) .
MS (ESI) m/z: 559(M+H)+.
Exemplo 87 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(2,2-dimetil-hidrazino)-carbonil]-ciclo25 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5, 4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 637/857
629
Η
Ο composto do título foi obtido a partir do composto obtido no Exemplo 58 e N,N-dimetil-hidrazina, de uma maneira similar àquela do Exemplo 57.
RMN-1H (DMSO-de) δ: 1,49-1,54 (lH,m) , 1,76-1,81 (2H, m) , 1,891,93 (2H,m), 2,07-2,17(1H,m), 2,33-3, 60(14H, m) , 4,15-4,19 (lH,m), 4,40-4,47 (2H,m) , 4,70-4,72 (1H, m) , 7,04(lH,s), 7,17 (1H,dd,J=8,5, 2,OHz), 7,42(1H,d,J=8,5Hz) , 7,70(lH,s), 8,178,22(lH,m), 8,41-8,43(1H,m), 11,80(1H,br,s).
MS (ESI) m/z: 558(M+H)+.
Exemplo 88 cloridrato de 6-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-2-quinolinocarboxamida:
Petição 870180138821, de 08/10/2018, pág. 638/857
630
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 145 com uma solução de ácido clorídrico em etanol, de uma maneira similar àquela do Exemplo 49, e depois condensando este composto com o composto obtido no Exemplo Referencial 10.
ΗΜΝ-Ή (DMSO-de) δ: 1, 45-1, 60 (1H, m) , 1,75-1,90 (3H, m) , 1,902,00(lH,m), 2, 00-2, 20 (lH,m) , 2,80(3H,s), 2,90(3H,s), 2,99 (3H,s), 3,10-3,30(5H,m), 3,56(lH,br), 4,10-4,20(1H,m), 4,404,70 (2H,m), 7,88(2H,s), 8, 15 (1H, d, J=8, 6Hz) , 8,22 (lH,s),
8,52 (1H,d,J=8,6Hz), 8,72(1H,d,J=8,3Hz), 8,89(1H,d,J=8,3Hz).
MS (FAB) m/z: 555(M+H)+.
Exemplo 89 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-4-flúor-indol-2il)-carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo15 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 144 com o composto obtido no Exemplo Referencial 274, de uma maneira similar àquela do processo descrito no Exemplo Referencial 91, e
Petição 870180138821, de 08/10/2018, pág. 639/857
631 tratando o composto resultante com uma solução 4 N de ácido clorídrico em dioxano, e depois com o composto obtido no Exemplo Referencial 10.
RMN-1H (DMSO—d6) δ:1,24-1,98(6H, m) , 2,33-3, 33(6H,m), 2,81 (3H,s), 2,90(3H,s), 2,99(3H,s), 4, 12 (1H, br, s) , 4,30-4,70 (lH,m), 4, 60 (1H, br, s) , 7,21(lH,s), 7,27 (2H, br, s) , 8,37(lH,d, J=8,lHz), 8,43(1H,d,J=7,6Hz), 12,ll(lH,s).
MS (FAE) m/z: 561(M+H)+.
Exemplo 90 cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-isoquinolino-3carboxamida:
O composto do título foi obtido tratando o 15 composto obtido no Exemplo Referencial 146 com uma solução de ácido clorídrico em etanol, de uma maneira similar àquela do Exemplo 49, e depois condensando este composto com o composto obtido no Exemplo Referencial 10.
RMN-iH (DMSO-de) δ: 1, 45-1, 65 (1H, m) , 1,70-1,85 (3H, m) , 1,9520 2,10(lH,m), 2, 10-2, 20 (1H, m) , 2,80(3H,s), 2,92(3H,s), 2,96 (3H,s), 2, 95-3,10(lH,m), 3,10-3,40(3H,m), 3, 70-3, 80(1H,m),
Petição 870180138821, de 08/10/2018, pág. 640/857
632
4,20-4,30(lH,m), 4,40-4,60(2H,m), 4,65-4,80(1H,m), 7,83-7,93 (lH,m), 8, 26 (1Η, d, J=8, 8Ηζ) , 8,38(lH,s), 8,60(lH,s), 8,859,00(2H,m), 9, 30-9, 40 (lH,m) .
MS (FAB) m/z: 555(M+H)+.
Exemplo 91 cloridrato de N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-tetraidrofuran-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto obtido no Exemplo Referencial 10 (0, 1
g), adicionou-se sucessivamente 1-hidróxi-benzotriazol monoidratado (78 mg) e cloridrato de 1-(3-dimetil-aminopropil ) -3-etil-carbodiimida (0,2 g) a uma solução do composto obtido no Exemplo Referencial 172 (0,12 g) em N,Ndimetil-formamida (20 ml), e a mistura foi agitada à temperatura ambiente por 1 dia. Depois de concentrar a mistura da reação, diluir o resíduo resultante com clorofórmio:metanol 9:1, e lavar com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio, a camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado
Petição 870180138821, de 08/10/2018, pág. 641/857
633
|
por cromatografia |
de |
coluna em |
silica- |
gel |
|
(clorofórmio:metanol |
95:5), |
para obter uma |
base livre |
do |
|
composto do título. |
Este |
produto foi tratado com |
uma |
solução de ácido clorídrico em etanol, para obter o composto 5 do título (0,1 g).
RMN-1H (CDC13) δ: 2,50(3H,s), 2, 70-2, 90 (4H, m) , 3,67(lH,s),
3,70 (lH,s), 3,86 (1H, dd, J=9, 2, 6, 3Hz) , 3,97 (1H, dd, J=9, 7,
4,1Hz), 4,15(1H,dd,J=9,7, 5,8Hz), 4,24 (1H,dd,J=9,2,7,OHz),
4,75-4,89(lH,m), 4, 92-5, 03(1H,m) , 6,88(lH,s), 7,20(1H,dd,J=
8,8, 2,OHz), 7,33(1H,d,J=8,8Hz), 7,35-7,43(1H,m), 7,58(lH,d,
J=2,OHz), 7, 64 (1H, d, J=7,1Hz) , 9,38(lH,s).
N5 (FAB) m/z: 460(M+H+).
Exemplo 92
N-((3S,4S)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}15 tetraidrofuran-3-il)-5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 183, de acordo com os processos do Exemplo Referencial 172 e do Exemplo 91.
RMN-iH (CDC13) δ: 2,51(3H,s), 2, 83 (2H, t, J=5, 3Hz) , 2,93 (2H,t, J=5,3Hz), 3,72(2H,s), 3, 78-3, 89(2H,m), 4,31(1H,dd,J=9,2,7,
Petição 870180138821, de 08/10/2018, pág. 642/857
634
3Ηζ) , 4,41-4,56(2H,m), 4,63-4,75(1Η,m), 6,88(lH,s), 7,22 (1Η,dd,J=8,8, 2,OHz), 7,32 (1H,d,J=8,8Hz), 7,35-7,46 (lH,m), 7,55(1H,d,J=7,1Hz), 7,60(1H,d,J=2,OHz), 9,38(lH,s).
MS (FAB) m/z: 460(M+H+).
Exemplo 93 cloridrato de N-((3R,4R)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-tetraidrofuran-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do 10 composto obtido no Exemplo Referencial 187, de acordo com os processos do Exemplo Referencial 172 e do Exemplo 91.
1H-NMR e MS (FAB): Iguais àquelas do enanciômero no Exemplo
92.
Exemplo 94 (3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidino-l-carboxilato de t-butila:
Petição 870180138821, de 08/10/2018, pág. 643/857
635 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 193 e do composto obtido no Exemplo Referencial 10, de acordo com o processo do Exemplo 91.
Ponto de fusão: 190-192 °C
ΡΜΝ-!Η (CDC13) δ: l,45(9H,s), 2,46(3H,s), 2,74-2, 81 (4H, m) ,
3,24-3,37(2H,m), 3,54-3,70(2H,m), 3,96-4,00(1H,m), 4,154,23(lH,m), 4,50-4, 65 (1H, m) , 4,77-4,82 (1H, m) , 6,79, 6,87 (total 1H,cada s) , 712—7,95(5H,m), 9,91,9,97(total lH,cada
s) .
MS (FAB) m/z: 559 (M+H+) .
Exemplo 95 cloridrato de N-((3R,4R)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-pirrolidin-3-il)-5-metil-4,5,6,715 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto obtido no Exemplo 94 (170 mg) foi dissolvido em cloreto de metileno (3 ml) , e adicionou-se ácido triflúor-acético (2 ml) à temperatura ambiente, agitando a mistura por 1 h. Depois de concentrar a mistura da reação, adicionou-se clorofórmio e uma solução aquosa saturada de bicarbonato de sódio. A camada orgânica
Petição 870180138821, de 08/10/2018, pág. 644/857
636 resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. 0 resíduo resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (clorofórmio:metanol:água 7:3:1 - camada inferior).
Adicionou-se uma solução de ácido clorídrico em metanol ao produto resultante pretendido, para obter o composto do título (90 mg), como um cloridrato (a RMN foi medida na forma de uma base livre).
Ponto de fusão: 248-250 °C (decomposto).
RMN-1!! (CDC13) δ: 2,44(3H,s), 2, 70-2, 80 (4H, m) , 2, 97-3, 05 (2H,
m) , 3, 46-3, 68 (4H,m), 4,49-4,52 (lH,m), 4, 60-4,65 (lH,m),
6,86(lH,s), 7, 05-7, 08 (lH,m) , 7,20 (1H, d, J=8, 5Hz) , 7,44(lH,s),
7,89(2H,br), 10, 51 (1H, br) .
MS (FAB) m/z: 459 (M+H+) .
Exemplo 96 cloridrato de N-((3S,4S)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-5-oxotetraidrofuran-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido removendo o grupo t-butóxi-carbonila do composto obtido no Exemplo Referencial
Petição 870180138821, de 08/10/2018, pág. 645/857
637
196, de uma maneira similar àquela do Exemplo Referencial 69, e reagindo o produto resultante com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 91.
RMN-1H (DMSO-de) δ: 2,90(3H,s), 3, 02-3, 17 (2H, m) , 3,23-3,34 (4H,m), 4,20(1H,t,J=8,6Hz), 4,61(1H,t,J=8,6Hz), 4,92-5,01 (lH,m), 5, 14-5, 26 (lH,m) , 7,09(lH,s), 7, 19 (1H, dd, J=8, 8, 2,0
Hz), 7,41(1H,d,J=8,8Hz), 7,73(1H,d,J=2,OHz), 9,27(lH,d,
J=6,8Hz), 9, 35(1H,d,J=6,8Hz), 11,22-11,33 (1H,m), 11,89(1H,
s) .
MS (FAB) m/z: 474 (M+H+) .
Exemplo 97 cloridrato de N-((3S,4S)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-2-oxotetraidrofuran-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido removendo o grupo t-butóxi-carbonila do composto obtido no Exemplo Referencial 197, de uma maneira similar àquela do Exemplo Referencial 69, e reagindo o produto resultante com o ácido 5-cloro20 indol-2-carboxílico, de uma maneira similar àquela do Exemplo 91.
Petição 870180138821, de 08/10/2018, pág. 646/857
638
RMN-iH (DMSO-de) δ: 2,52(3H,s), 2, 83 (2H, t, J=5, 9Hz) , 2,913,00(2H,m), 3,73(2H,s), 4,23(1H,t,J=8,6HZ), 4,40- 4,53(1H,
m), 4,96(1H,dd,J=10,8, 5,2Hz), 5,16(1H,dd,J=9,2, 7,3Hz),
7,01(lH,s), 7,25(1H,dd,J=8,8, 2,OHz), 7,34(1H,d,J=8,8Hz),
7,52(lH,d,J=2,OHz), 8,01(1H,d,J=5,4Hz), 8,51-8,63(1H,m),
9, 22(1H,s) .
MS (FAE) m/z: 474 (M+H+) .
Exemplo 98 cloridrato de (3S,4R)-2-(3-{[(5-cloro-indol-2-il)10 carbonil]amino}-4-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridin-2-il)-carbonil]-amino}-2-oxopirrolidin-l-il) acetato de etila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 199 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 91. A RMN foi medida na forma de uma base livre.
RMN-XH (DMSO-de) δ: 1, 19 (3H, t, J=7, 1Hz) , 2,35(3H,s), 2,712,84(2H,m), 2,80-2, 90 (2H, m) , 3, 40 (1H, d, J=10, 3Hz) , 3,61(2H,d,
J=lO,8Hz), 3,84(1H,dd,J=10,3, 5,6Hz), 4,01-4,23(4H,m), 4,804,94(lH,m), 5, 04 (1H, t, J=8, 6Hz) , 7,01(lH,s), 7, 16 (1H, dd, J=
Petição 870180138821, de 08/10/2018, pág. 647/857
639
8,8, 2,OHz), 7,40(1H,d,J=8,8Hz), 7,69(1H,d,J=2,OHz), 8,73 (1H,d,J=8,6Hz), 8,90(1H,d,J=8,8Hz), 11, 86(lH,s).
MS (FAB) m/z: 559 (M+H+) .
Exemplo 99
N-((3S,4S)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-1metil-5-oxopirrolidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 201 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 91.
RMIS!-^ (CDC13) δ: 2,49(3H,s), 2, 77-2, 82 (2H, m) , 2, 86-2, 91 (5H, m) , 3,69(2H,d,J=l,2Hz), 4,39-4,54(3H,m), 4,93-4, 98(1H,m),
6,98(1H,d,J=l,2Hz), 7,05-7,34(3H,m), 7,63(1H,d,J=2,OHz),
8, 11 (1H, d, J=7,8Hz) , 9,00(lH,s).
MS (FAB) m/z: 487 (M+H+) .
Exemplo 100
2-[((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)20 carbonil]-amino}-pirrolidin-l-il)-sulfonil]-acetato de metila:
Petição 870180138821, de 08/10/2018, pág. 648/857
640
0. /~~C0,Me 2 —N
Cl
O composto obtido no Exemplo 95 (230 mg) e trietil-amina (0,10 ml) foram dissolvidos em cloreto de metileno (6,9 ml), e a mistura foi resfriada com gelo.
Adicionou-se cloreto de metóxi-carbonil-metano-sulfonila (Synthesis, página 321, 1975) (105 mg), e a mistura resultante foi aquecida até a temperatura ambiente e agitada por toda a noite. A mistura da reação foi diluída com clorofórmio, lavada com água e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (clorofórmio:metanol 20:1), e pulverizado com metanol/água, para obter o composto do título (150 mg).
ΚΜΝ-ΧΗ (CDC13) δ: 2,48(3H,s), 2, 76-2, 86 (4H, m) , 3, 49-3, 73 (4H
m) , 3,87(3H,s), 3, 94-3, 98 (1H, m) , 4, 08-4, 11 (1H, m) , 4,13(2H
s), 4, 69-4, 72(lH,m) , 4,88-4,91(1H,m), 6,89(lH,s), 7,12-
9, 92(1H,s) .
MS (FAB) m/z: 595 (M+H+) .
Petição 870180138821, de 08/10/2018, pág. 649/857
641
Exemplo 101 ácido 2-[((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}4~{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-sulfonil]-acético:
O composto obtido no Exemplo 100 (100 mg) foi dissolvido em tetraidrofurano (4 ml)/água (1 ml), e a mistura foi resfriada com gelo. Adicionou-se hidróxido de lítio monoidratado (7,8 mg), e a mistura resultante foi aquecida até a temperatura ambiente e agitada por 4 h.
Depois de neutralizar a mistura da reação com ácido clorídrico 1 N, ela foi concentrada. Os depósitos foram coletados por filtração, lavados com água e etanol a 50%, e secados por toda a noite a 50 °C sob pressão reduzida, para obter o composto do título (87 mg).
ΚΜΝ-^ (DMSO-de) δ: 2,50(3H,s), 2,92(4H,s), 3, 34-3, 43 (4H, m) , 3, 76-3, 85 (2H,m) , 4,27(cada ΙΗ,ΑΒ tipo d,J=14,5Hz), 4,654,71(lH,m), 4,78-4,84(lH,m), 7,14(lH,s), 7,18(1H,d,J=8,8Hz), 7,40(1H,d,J=8,8HZ), 7,72(lH,s), 8,87(1H,d,J=7,8Hz), 9,12(1H, d,J=8,2Hz), 11,83(1H,s).
Petição 870180138821, de 08/10/2018, pág. 650/857
642
Exemplo 102
2-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-acetato de metila:
O composto obtido no Exemplo 95 (230 mg) e carbonato de potássio (90 mg) foram dissolvidos em N,Ndimetil-formamida (4,6 ml), e a mistura foi resfriada com gelo. Adicionou-se bromo-acetato de metila (0,062 ml), e a mistura resultante foi agitada por 45 min. A mistura da reação foi diluída com acetato de etila, lavada com água e solução aquosa saturada de cloreto de sódio, e depois secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (clorofórmio:metanol 10:1), e pulverizado com metanol/água, para obter o composto do título (190 mg).
RMN-1!! (CDC13) δ: 2,35(2H,s), 2,48(3H,s), 2,73-2, 95 (4H, m) ,
3, 34-3, 42 (2H,m), 3, 4 6 (2H, q, J=6, 5Hz) , 3, 67 (2H, q, J=6, 5Hz) ,
3,75(3H,s), 4, 57-4, 71 (2H,m) , 6,91(lH,s), 7, 10-7, 13 (1H, m) ,
7,31 (lH,d, J=9,OHz) , 7,53(lH,s), 7,77 (1H, d, J=8, OHz) , 7,87 (1H, d, J=6, 8Hz) , 10,22(lH,s).
Petição 870180138821, de 08/10/2018, pág. 651/857
643
MS (FAB) m/z: 531 (M+H+) .
Exemplo 103 ácido 2-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}4-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)5 carbonil]-amino}-pirrolidin-l-il)-acético:
O composto do título foi obtido a partir do composto obtido no Exemplo 102, de uma maneira similar àquela do Exemplo 101.
RMN-LH (DMSO-de) δ: 2,42(3H,s), 2, 69-2,87 (6H, m) , 3,13(lH,t,
J=9,0Hz), 3,22 (lH,t,J=9,OHz) , 3,33(cada ΙΗ,ΑΒ tipo d,J=6,8
Hz), 3,72(2H,s), 4, 53-4, 60 (lH,m) , 4, 65-4, 72 (1H, m) , 7,16-7,20 (2H,m), 7,42(1H,d,J=8,8Hz), 7,70(lH,s), 8,85 (1H,d,J=7,5Hz), 9, 00 (1H, d, J=8, 3Hz) , ll,79(lH,s).
Exemplo 104
3-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-propionato de metila:
Petição 870180138821, de 08/10/2018, pág. 652/857
644
composto do título foi obtido a partir do composto obtido no Exemplo 95 e de 3-bromo-propionato de metila, de uma maneira similar àquela do Exemplo 102.
ΗΜΝ-^ (CDC13) δ: 1, 96-2,20 (2H, m) , 2,49(3H,s), 2,61-2,96 (8H,m), 3,17-3,21 (2H,m) , 3, 62-3, 72 (2H, m) , 3,69(3H,s), 4,464,49(lH,m), 4,56-4,61(1H,m), 6,87(lH,s), 7,05-7,14(1H,m),
7,32 (lH,d, J=9,2Hz) , 7,53(lH,s), 7, 65-7,71 (2H, m) , 10,02(1H,
s) .
MS (FAB) m/z: 545 (M+H+) .
Exemplo 105 ácido 3-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}4-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il) carbonil]-amino}-pirrolidin-l-il)-propiônico:
Petição 870180138821, de 08/10/2018, pág. 653/857
645 composto do título foi obtido a partir do composto obtido no Exemplo 104, de uma maneira similar àquela do Exemplo 101.
RMN-1H (DMSO-de) δ: 2,38(3H,s), 2, 39-2, 84 (10H, m) , 2,93(lH,t, 5 J=8,8Hz), 3, 05(1H,t,J=8,8Hz), 3,65(2H,s), 4,51-4,56(1H,m),
4,63-4, 68 (lH,m), 7, 16-7,19(2H,m), 7,41(1H,d,J=8,8Hz), 7,69 (lH,s), 8,81(1H,d,J=7,8Hz) 8,97(1H,d,J=8,3Hz), ll,75(lH,s).
Exemplo 106
3-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(510 meti1-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-3-oxopropionato de etila:
O composto do título foi obtido a partir do composto obtido no Exemplo 95 e de cloreto de etil-manolila, de uma maneira similar àquela do Exemplo 100.
RMN-1H (DMSO—d6) Ô: 1,20 (3H, t, J=7, OHz) , 2,37(3H,s), 2,732,75(2H,m), 2, 82-2, 84 (2H, m) , 3, 35-3, 38 (2H, m) , 3,64(2H,s),
3, 68-3, 83 (2H,m) , 3, 91-4,00 (2H, m) , 4, 10(2H,q,J=7,0Hz) , 4,614,84 (2H,m), 7,13(lH,s), 7, 18 (1H, dd, J=8, 5, 2,OHz), 7,41(1H, d,J=8,5Hz), 7,72(lH,s), 8,73 (1H, t, J=9, OHz) , 9, 10 (1H, d, J=9, O
Hz), 11,79 (1H,s) .
Petição 870180138821, de 08/10/2018, pág. 654/857
646
Exemplo 107 ácido 3-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}4-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-3-oxopropiônico:
O composto do título foi obtido a partir do composto obtido no Exemplo 106, de uma maneira similar àquela do Exemplo 101.
RMN-1H (DMSO-dg) δ: 2,39(3H,s), 2,77(2H,s), 2,85(2H,s), 3,293,55 (4H,m), 3,68 (2H, s) , 3,82-4,01 (2H,m), 4, 62-4,68 (1H, m) ,
4,77-4,86 (lJ-l,m), 7,14(lH,s), 7, 18 (1H, d, J=8, 8Hz) , 7,41(1H, d,J=8,8Hz), 7,72(lH,s), 8,75 (1H,t,J=8, 8Hz) , 9,12 (1H,d,J=7, 8
Hz), 11,81(1H,s).
Exemplo 108
1-[((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-415 {[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-metil]-ciclo-propanocarboxilato de metila:
Petição 870180138821, de 08/10/2018, pág. 655/857
647
composto do título foi obtido a partir do composto obtido no Exemplo 95 e de 1-(bromo-etil)-ciclopropano-carboxilato de metila, de uma maneira similar àquela do Exemplo 102.
RMN-1H (CDC13) δ: 0, 78-0, 79 (2H, m) , 1,24-1,26 (2H, m) , 2,49(3H,
s), 2, 62-2, 88 (6H,m) , 3, 20-3, 28 (2H, m) , 3,66(3H,s), 3,61-3,75 (4H,m), 4, 45-4, 62 (2H,m) , 6,86(lH,s), 7, 12-7, 15 (1H, m) , 7,247,28(lH,m), 7, 52 (1H, d, J=8, 5Hz) , 7,54(lH,s), 7, 69 (1H, d, J=8, O
Hz), 10,00 (1H,s) .
MS (ESI) m/z: 571 (M+H+) .
Exemplo 109 ácido 1-[((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}4~{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-metil]-ciclo-propano15 carboxílico:
Petição 870180138821, de 08/10/2018, pág. 656/857
648 composto do título foi obtido a partir do composto obtido no Exemplo 108, de uma maneira similar àquela do Exemplo 101.
RMN-1H (DMSO-de) δ: 0,73-0,78(2H,m), 1,04-1,07 (2H, m) , 2,37 (3H,s), 2, 65-2, 84 (6H,m), 3, 11-3,20 (4H, m) , 3,64(2H,s), 4,594,74 (2H,m), 7,16(lH,s), 7,17(1H,d,J=8,5Hz), 7,40(1H,d,J=8,5 Hz), 7,70(lH,s), 8,84(1H,d,J=7,5Hz) , 9,12(1H,d,J=7,5Hz) ,
11,77 (lH,s) .
Exemplo 110 (3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(5isopropil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidino-l-carboxilato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 193 e no Exemplo
Referencial 148, de uma maneira similar àquela do Exemplo
91.
RMN-1H (CDC13) δ: 1, 12 (6H, d, J=6, 6Hz) , l,47(9H,s), 2,83-2,88 (4H,m), 2, 94-2, 99 (lH,m), 3, 20-3, 29(1H,m), 3,31-3,42 (1H, m) ,
3,75-3,81(2H,m), 3,98(1H,t,J=8,5Hz), 4,15-4,35(2H,m), 4,50Pctição 870180138821, de 08/10/2018, pág. 657/857
649
4,65(lH,m), 6,85,6,91(total 1H,cada s), 7,15—7,90(5H,m),
9,41, 9,50(total lH,cada s) .
Exemplo lll
N-((3R,4R)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}5 pirrolidin-3-il)-5-isopropil-4,5,6,7-tetraidrotiazolo[5, 4c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 110, de uma maneira similar àquela do Exemplo 95.
RMN-XH (CDC13) δ: 1, 13 (6H, d, J=6, 3Hz) , 2,85 (4H, br, s) , 2,963,05(3H,m), 4,51-4,52(1H,m), 4,76-4, 80(2H,m), 5,36-5,39 (2H,m), 5,53-5,58(lH,m), 7,17-7,19(lH,m), 7,27-7,31(2H,m),
7,57(lH,s), 7,64(2H,br), 9,82(lH,br).
Exemplo 112
3-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(5isopropil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-pirrolidin-l-il)-propionato de etila:
Petição 870180138821, de 08/10/2018, pág. 658/857
650
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 111 e 3-bromopropionato de etila, de uma maneira similar àquela do Exemplo 102.
EMN-iH (CDC13) δ: 1, 14(6H,d,J=6,5Hz), 1,26(3H,t,J=7,ΟΗζ),
2,51(3H,t,J=7,OHz), 2,63(1H,dd,J=9,5, 6,5Hz), 2,73-2,91(6H,
m), 2,95-3,02(lH,m), 3,22(2H,q,J=7,ΟΗζ), 3,81(cada ΙΗ,ΑΒ tipo d,J=14,5Hz), 4, 16(2H, q,J=7,ΟΗζ), 4 , 4 0—4 , 4 5 (1H, m) , 4,52— 4,59(lH,m), 6, 88(1H,d,J=2,ΟΗζ), 7, 17-7, 19(1H,m), 7,30-7,32 (2H,m), 7,59(lH,s), 7,62(lH,s), 9, 56(lH,s).
MS (FAB) m/z: 587 (M+H+) .
Exemplo 113 ácido 3-((3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}4-{[(5-isopropil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-215 il)-carbonil]-amino}-pirrolidin-l-il)-propiônico:
Petição 870180138821, de 08/10/2018, pág. 659/857
651 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 112, de uma maneira similar àquela do Exemplo 101.
RMN-1H (DMSO-de) δ: 1,04(6H,d,J=6,6Hz), 2,40 (2H, q, J=7, OHz) ,
2,50(4H,s), 2, 60-2, 74 (4H,m) , 2, 90-2, 94 (2H, m) , 3, 02-3, 06 (1H,
m), 3,20-3,35(2H,m), 4,50-4,53(1H,m), 4,61-4,65(1H,m), 7,157,18(2H,m), 7,41 (1H, d, J=8, 8Hz) , 7,68(lH,s), 8,78 (1H, d, J=7,5
Hz), 8, 90 (lH,d, J=8,OHz) , ll,73(lH,s).
Exemplo 114 cloridrato de N-((3R, 4R)-l-acetil-4-{[(5-cloro-indol-2-il)carbonil]-amino}-pirrolidin-3-il)-5-isopropil-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 111 e anidrido acético, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 254-258 °C (decomposto).
RMN-1H (DMSO-de) δ: 1,34-1,37 (6H, m) , l,96(3H,s), 3,30-3,55 (5H,m), 3, 66-3, 82(3H,m), 3, 95(1H,q,J=8,3Hz), 4,45-4,82(4H,
m) , 7,15(lH,s), 7,18 (1H, d, J=9, OHz) , 7,41 (1H, d, J=9, 0Hz) ,
7,71(lH,s), 8, 75-8, 81 (lH,m) , 9, 21 (1H, d, J=8, 0Hz) , 11,32(1H,
Petição 870180138821, de 08/10/2018, pág. 660/857
652 br), 11,83(1H,d,J=7,3Hz).
MS (FAB) m/z: 529(M+H+).
Exemplo 115 cloridrato de N-((3R, 4R)-4-{[(5-cloro-indol-2-il)-carbonil]5 amino}-!-(metil-sulfonil)-pirrolidin-3-il)-5-isopropil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 111 e cloreto de metano-sulfonila, de uma maneira similar àquela do Exemplo
100.
Ponto de fusão: 200-235 °C (decomposto).
RMN-1!! (DMSO-de) δ: 1, 32-1,36 (6H, m) , 3,32(3H,s), 3,43-3,46 (5H,m), 3, 68-3, 75 (4H,m) , 4,48(lH,m), 4,62-4,72 (2H, m) , 4,83 (1H, t, J=5, 5Hz) , 7,14(lH,s), 7, 18 (1H, d, J=8, 6Hz) , 7,40(lH,d,
J=8,6Hz), 7,72(lH,s), 8,82(lH,br), 9, 20 (1H, d, J=8, 3Hz) , 11,30 (lH,br), 11,86(1H,d,J=7,5Hz).
MS (FAB) m/z: 565 (M+H+) .
Exemplo 116 cloridrato de (3R,4R)-3-{[(5-cloro-indol-2-il)-carbonil]amino}-4-{[(5-isopropil-4,5,6,7-tetraidrotiazolo[5, 4-c]Petição 870180138821, de 08/10/2018, pág. 661/857
653 piridin-2-il)-carbonil]-amino}-pirrolidino-1-carboxilato de
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 111 e cloro-formiato de etila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 225-228 °C (decomposto).
RMN-1H (DMSO-d6) δ: 1,20 (3H, t, J=7, OHz) , 1,31-1,37 (6H, m) ,
3,33-3,45(5H,m), 3,66-3,75(4H,m), 4,05(2H,q,J=7,OHz), 4,454,77 (4H,m), 7,15(lH,s), 7, 17 (1H, dd, J=8, 8, 2,OHz), 7,41(1H, d,J=8,8Hz), 7,71 (1H,d,J=2,OHz), 8,77(1H,d,J=7,OHz), 9,20 (1 H, d,J=8,0Hz), 11,30(lH,br), 11,83(1H,d,J=7,5Hz).
MS (FAB) m/z: 559 (M+H+) .
Exemplo 117 (3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-3-{[(515 metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-piperidino-l-carboxilato de t-butila:
Boc
Petição 870180138821, de 08/10/2018, pág. 662/857
654 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 207 e no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 91. Ponto de fusão: 152-154 °C (decomposto).
RMN-1H (CDC13) δ: l,53(9H,s), 1, 62-1,80 (1H, m) , 2,23-2,30 (1H,
m) , 2,52(3H,s), 2, 75-3, 05 (5H, m) , 3, 10-3, 25 (1H, m) , 3,68-3,82 (2H,m), 4, 15-4,45 (4H,m) , 6,89(lH,s), 7, 19 (1H, dd, J=8, 8, 1,8
Hz), 7,32(1H,d,J=8,8Hz), 7, 92(1H,d,J=1,8Hz), 7,75(1H,br,s),
8,21 (lH,br, s) , 9, 39 (1H, s) .
MS (ESI) m/z: 573(M+H)+.
Exemplo 118 dicloridrato de N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 117, de uma maneira similar àquela do Exemplo 95.
Ponto de fusão: 240-258 °C (decomposto).
ΡΜΝ-ΧΗ (DMSO-de) δ: 1,85-2,00 (1H, m) , 2, 05-2,20 (2H, m) , 2,93 (3H,s), 3, 05-3, 60(7H,m), 3, 65-3, 75(1H,m), 4,10-4,52(2H,m),
4,60-4,75(2H,m), 7,10-7,21(2H,m), 7,43(1H,d,J=8,6Hz), 7,70
Petição 870180138821, de 08/10/2018, pág. 663/857
655 (lH,s), 8, 50(1H,br,d,J=7,8Hz), 8, 90-9, 05 (2H, m) , 9,27(lH,br,
s), 11,9(lH,br,d,J=13,4Hz).
MS (ESI) m/z: 473(M+H)+.
Exemplo 119 (3R*,4S*)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-4-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-piperidino-l-carboxilato de t-butila:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 208 e ácido 5-cloro10 indol-2-carboxílico, de uma maneira similar àquela do Exemplo 91.
Ponto de fusão: 187-189 °C (decomposto).
RMN-XH (CDC13) δ: l,48(9H,s), 1,72-1, 90 (1H, m) , 2, 00 (1H, br, s) , 2,00-2,10(lH,m), 2,45(3H,s), 2,60-2,70(2H,m), 2,70-2,80 (2H,
m), 3, 23(1H,t,J=10,8Hz), 3, 35-3, 50(1H,m), 3, 50-3, 72(2H,m),
3,90-4,20(2H,m), 4,30-4,40(1H,m), 4,45-4,55(1H,m), 6,85(1H, d,J=l,5Hz), 7, 17(1H, dd,J=8,8,1,9Hz), 7,20-7,30(1H,m), 7,33 (1H,d,J=8,8Hz), 7,58(1H,d,J=l,9Hz), 10,17(lH,s).
MS (ESI) m/z: 573 (M+H+) .
Exemplo 120 dicloridrato de N-((3R*,4S*)-3-{[(5-cloro-indol-2-il)Petição 870180138821, de 08/10/2018, pág. 664/857
656 carbonil]-amino}-piperidin-4-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
composto do título foi obtido a partir do 5 composto obtido no Exemplo 119, de uma maneira similar àquela do Exemplo 95.
Ponto de fusão: 276-278 °C (decomposto).
πΜΝ-^ (DMSO-de) δ: 1, 77-1,88 (1H, m) , 2, 40-2, 50 (2H, m) , 2,89 (3H,s), 2, 90-3, 20 (4H,m) , 3, 30-3, 50 (2H, m) , 3, 63(1H,br,s),
4,33-4,47 (2H,m) , 4, 62-4,75(2H, m) , 7, 18(1H, dd,J=8,8, 1,9Hz),
7,42(1H, d,J=8,8Hz), 7,48(1H,br,s), 7, 71(1H,d,J=l,9Hz), 8,66 (lH,br,s), 8, 95 (1H, d, J=8, 1Hz) , 9, 20-9, 30 (1H, m) , 9,45-9,70 (lH,m), ll,61(lH,s), ll,90(lH,s).
MS (ESI) m/z: 473(M+H)+.
Exemplo 121 (3R*,4S*)-4-{[(5-flúor-indol-2-il)-carbonil]-amino}-3-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-piperidino-carboxilato de t-butila:
Boc
Petição 870180138821, de 08/10/2018, pág. 665/857
657 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 209 e no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 91. ΡΜΝ-^ (CDC13) δ: l,53(9H,s), 1, 65-1,78 (1H, m) , 2,23-2,32 (lH,br), 2,52(3H,s), 2,78-3,03(5H,m), 3,15-3,24(1H,br),
3, 68-3, 82 (2H,br) , 4, 16-4, 45 (4H, br) , 6,91(lH,s), 7,02 (lH,td, J=9,0,2,7Hz), 7,30(1H,dd,J=9,0,2,7Hz), 7,34 (1H, dd, J=9, 0, 4, 4Hz), 7,65-7,90(1H,br), 8,10-8,40(1H,br), 9,31-9,41(1H,br). MS (ESI) m/z: 557 (M+H+) .
Exemplo 122 dicloridrato de N-((3R*,4S*)-4-{[(5-flúor-indol-2-il)carbonil]-amino}-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do 15 composto obtido no Exemplo 121, de uma maneira similar àquela do Exemplo 95.
Ponto de fusão: 236-245 °C (decomposto).
RMN-1!! (DMSO-dg) δ: 1, 85-1, 98 (1H, br) , 2, 06-2, 18 (1H, br) , 2,89 (3H,s), 3, 05-3, 75 (8H, s) , 4,34-4,54 (2H,br), 4,60-4,75 (2H,br), 7,04 (lH,td,J=9, 3, 2,4Hz), 7,15(1H,br,s) , 7,37-7,44 (2H,m), 8,46(1H,d,J=7,8Hz), 8, 88-9, 00 (1H,br), 9, 09-9, 27 (2H,
Petição 870180138821, de 08/10/2018, pág. 666/857
658 br), 11,55-11,75(1H,br), 11,76-11,84(1H,br).
MS (FAB) m/z: 457 (M+H+) .
Exemplo 123 cloridrato de N-((3R*,4S*)-1-acetil-4-{[(5-cloro-indol-25 ii)-carbonil]-amino}-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo 118 e anidrido acético, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 215-225 °C (decomposto).
RMN-1H (DMSO-de) δ: 1,65-1,85(1H,m), 1,88,2,06 (total 3H, cada s), 1,90-2,10(lH,m), 2,91(3H,s), 3,00-3,30(2H,m), 3,303,55(2H,m), 3,60-3,90(3H,m), 3,98-4,50(4H,m), 4,65-4,75(1H,
m), 7,09(1H,d,J=15,6Hz), 7,17(1H,d,J=8,8Hz), 7,41(1H,d,J=8,8
Hz), 7,71(lH,s), 8,23-8,53(2H,m), 11,20-11,55(1H,m), 11,85 (1H,br,d,J=5,4Hz).
MS (ESI) m/z: 515 (M+H+) .
Exemplo 124 cloridrato de N-((3R*,4S*)-1-acetil-3-{[(5-cloro-indol-220 ii)-carbonil]-amino}-piperidin-4-il)-5-metil-4,5,6,7Pctição 870180138821, de 08/10/2018, pág. 667/857
659 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo 120 e anidrido acético, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 225-250 °C (decomposto).
ΚΜΝ-^ (DMSO-de) δ: 1, 65-1,80 (1H, m) , 1,81, 2, 05 (total 3H, cada s), 2,00-2,20(1H,m), 2,70-2,85(1H,m), 2,89(3H,s), 3,003,20(2H,m), 3, 20-3, 50(2H,m) , 3,64(1H,br,s), 3, 78-4,30(2H,m),
4,30-4,50 (3H,m), 4,55-4,75(1H,m) , 7, 05-7,23(2H,m) , 7,38-7,48 (lH,m), 7,70—7, 80 (1H, m) , 7, 79, 8, 12 (total lH,cada d,J=6,8Hz),
8,73, 8, 83 (total lH,cada d,J=8,3Hz), 11,20—11,50 (lH,m) ,
11,89, 11,92(total 1H,cada s).
MS (FAB) m/z: 515 (M+H+) .
Exemplo 125 cloridrato de N-((3R*,4S*)-l-acetil-4-{[(5-flúor-indol-2il)-carbonil]-amino}-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 668/857
660
O composto do título foi obtido a partir do composto obtido no Exemplo 122 e anidrido acético, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 202 °C (decomposto).
ΚΜΝ-^ (DMSO-de) δ: 1, 67-1,85 (1H, m) , 1,87 (1,5H, s) , 1,872,10(lH,m), 2,06 (1,5H,s), 2,88-2, 96(3H,br,s) , 3, 05- 3, 30(2H,
m) , 3, 32-3, 83(5H,br) , 3, 97-4,33(2H,m), 4,35-4,50(2H,br),
4,67-4,78(1H,br), 7,01-7,14(2H,m), 7,38-7,44(2H,m), 8,258,50(2H,m), 10,85-11, 15 (1H, br) , 11,72-11, 80 (lH,br).
MS (FAB) m/z: 499 (M+H+).
Exemplo 126 cloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1-(metil-sulfonil)-piperidin-3-il]-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
II o=s—
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de metanosulfonila, de uma maneira similar àquela do Exemplo 100. Ponto de fusão: 225-230 °C (decomposto).
RMN-1!! (DMSO-dg) δ: 1, 80-1, 90 (1H, m) , 2, 05-2, 15 (1H, m) , 2,30Pctição 870180138821, de 08/10/2018, pág. 669/857
661
2,80(5H,m), 2, 85-3, 80 (9H, m) , 4,20-4,90 (4H, m) , 7,08 (lH,d,J=
I, 7Hz), 7, 18(1Η, dd,J=8,7, 1,7Hz), 7,42(1Η, d,J=8,7Hz), 7,77 (lH,s), 8, 02-8, 20 (lH,m) , 8,40-8,50 (1Η, m) , 11,00-11,60 (1Η, m) ,
II, 87(1Η, s) .
MS (ESI) m/z: 551 (Μ+Η+) .
Exemplo 127 cloridrato de N-[(3R*,4S*)-3-{[(5-cloro-indol-2-il) carbonil]-amino}-1-(metil-sulfonil)-piperidin-4-il]-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 120 e cloreto de metanosulfonila, de uma maneira similar àquela do Exemplo 100. Ponto de fusão: 228-245 °C (decomposto).
RMN-1H (DMSO-de) δ: 1, 75-1,85 (1H, m) , 2,25-2,40 (1H, m) , 2,4015 2, 60(2H,m), 2, 76 (3H, br, s) , 2,90(3H,s), 2,93-3, 05 (3H, m) ,
3,12(1H,d,J=10,6Hz), 3,55-3,80(2H,m), 4,25-4,40(4H,m), 7,17 (1H,d,J=l,7Hz), 7, 19(1H,dd,J=8,7,2,OHz), 7,43(1H,d,J=8,7Hz),
7,74(1H,d,J=2,OHz), 8, 03(1H,d,J=6,6Hz), 8,78(1H,d,J=7,4Hz),
10,90-11,20(lH,br,s), 11,89(1H,s).
MS (ESI) m/z: 551 (Μ+Ή) .
Petição 870180138821, de 08/10/2018, pág. 670/857
662
Exemplo 128 cloridrato de N-[(3R*,4S*)-4-{[(5-flúor-indol-2-il)carbonil]-amino}-1-(metil-sulfonil)-piperazin-3-il]-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
II o=s—
0 composto do título foi obtido a partir do composto obtido no Exemplo 122 e cloreto de metanosulfonila, de uma maneira similar àquela do Exemplo 100. Ponto de fusão: 216-250 °C (decomposto).
ΡΜΝ-^ (DMSO-de) δ: 1,80-1, 90 (1H,m) , 2,01-2,12(lH,m), 2,92 (3H,s), 2,94(3H,s), 3, 00-3, 80 (8H, m) , 4,28-4,53 (3H, m) , 4,604,80 (lH,br), 7,01-7,12(2H,m), 7,37-7,44(2H,m), 8,00-8,18 (lH,br), 8, 39-8, 50(1H,br) , 11, 00-11, 60(1H,br) , 11,72-11,80 (1H,br).
MS (FAB) m/z: 535 (m+H+) .
Exemplo 129 cloridrato de (3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin2-il)-carbonil]-amino}-piperidino-l-carboxilato de metila:
Petição 870180138821, de 08/10/2018, pág. 671/857
663
composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloro-formiato de metila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 248-253 °C (decomposto).
RMN-1!! (DMSO-de) δ: 1, 65-1, 78 (1H, m) , 1,88-2,03 (1H, m) , 2,90 (3H,s), 3, 00-3, 80 (9H,m), 3, 80-3, 90(1H,m), 3, 95-4,08(1H, m) ,
4,20-4,70(4H,m), 7,10(lH,s), 7, 17(1H,dd,J=8,8,1,8Hz), 7,42 (1H,d,J=8,8Hz), 7,71(1H,d,J=l,8Hz), 8,29(1H,br,s), 8,41(1H, d,J=8,lHz), 11,29 (1H, br, s) , ll,85(lH,s).
MS (ESI) m/z: 531 (M+H+) .
Exemplo 130 cloridrato de (3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin2-il)-carbonil]-amino}-piperidino-l-carboxilato de etila:
Petição 870180138821, de 08/10/2018, pág. 672/857
664 composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloro-formiato de etila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 215-225 °C (decomposto).
RMN-1H (DMSO-de) δ: 0, 85-1,30 (3H, m) , 1, 65-1,78 (1H, m) , 1,902,03(lH,m), 2,90(3H,s), 3, 10-3, 40 (4H, m) , 3, 48 (1H, br, s) , 3,65 (lH,br,s), 3, 75—4, 15 (4H, m) , 4,25 (1H, br, s) , 4,32— 4,50(2H,m), 4,66(lH,br,s), 7,09(lH,s), 7, 18(1H,dd,J=8,8, 2,OHz), 7,41 (1H,d,J=8,8Hz), 7,71(1H,d,J=2,OHz), 8,23(1H,br,s), 8,45(1H, br, d, J=8,1Hz) , 11,50 (1H, br, s) , ll,86(lH,s).
MS (ESI) m/z: 545 (M+H+) .
Exemplo 131 cloridrato de (3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin15 2-il)-carbonil]-amino}-piperidino-l-carboxilato de 2-metóxi-
composto do título foi obtido a partir do 20 composto obtido no Exemplo 118 e cloro-formiato de 2-metóxiPctição 870180138821, de 08/10/2018, pág. 673/857
665 etila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 224-226 °C (decomposto).
RMN-1H (DMSO-de) δ: 1, 68-1,78 (1H, m) , 1, 90-2,03 (1H, m) , 2,89 (3H,s), 3, 00-3, 75 (HH,m) , 3, 80-3, 90 (1H, m) , 3,95-4,18 (3H,m),
4,20-4,70(4H,m), 7,10(lH,s), 7, 17(1H,dd,J=8,8,2,OHz), 7,41 (1H,d,J=8,8Hz), 7,71(1H,d,J=2,OHz), 8,26(1H,br,s), 8,42(1H, d,J=7,8Hz), 11,30 (lH,br, s) , ll,86(lH,s).
MS (ESI) m/z: 575 (M+H+) .
Exemplo 132 cloridrato de (3R*,4S*)-3-{[(5-cloro-indol-2-il)-carbonil]amino}-4-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin2-il)-carbonil]-amino}-piperidino-l-carboxilato de etila:
OEt
O composto do título foi obtido a partir do composto obtido no Exemplo 120 e cloro-formiato de etila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 213-225 °C (decomposto).
RMN-iH (DMSO-dg) δ: 0, 75-1,30 (3H, m) , 1, 60-1,72 (1H, m) , 2,122,25(lH,m), 2,89(3H,s), 2, 95-3, 20 (4H, m) , 3, 40-3, 88 (4H, m) ,
3,90-4,10(2H,m) , 4,10-4,30(2H,m) , 4,30-4, 40 (1H,m) , 4,4020 4,80(lH,m), 7,10(lH,s), 7, 18 (1H, dd, J=8, 8, 2,OHz), 7,43(lH,d,
Petição 870180138821, de 08/10/2018, pág. 674/857
666
J=8,8Hz), 7,74(lH,s), 8, 03 (1H, d, J=5, 6Hz) , 8,79(lH,s), 11,37 (1H,s), 11,88 (1H,s) .
MS (ESI) m/z: 545 (M+H+) .
Exemplo 133 cloridrato de N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-l-propionil-piperidin-3-il) -5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de propionila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 214-228 °C (decomposto).
RMN-1!! (DMSO-dg) δ: 0, 88-1, 10 (3H, m) , 1,70-2,05 (2H, m) , 2,062,60(2H,m), 2,91(3H,s), 3, 14 (2H, br, s) , 3, 20-3, 90 (5H, m) ,
3,95-4,80(5H,m), 7,09(1H,d,J=ll,0Hz), 7,17 (1H,dd,J=8,8,
1,2 Hz), 7,41(1H,d,J=8,8Hz), 7,71(lH,s), 8,20-8,50(2H,m),
11,00-11,40 (lH,m) , ll,86(lH,s).
MS (ESI) m/z: 529(M+H+).
Exemplo 134 cloridrato de N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)20 carbonil]-amino}-1-isobutiril-piperidin-3-il)-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 675/857
667
composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de isobutirila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 266-272 °C (decomposto).
RMN-1H (DMSO-de) δ: 0,80-1,15(6H,m), 1,70-2,05 (2H, m) , 2,652,80(lH,m), 2,90(3H,s), 2, 90-4,80 (12H,m) , 7,09 (1H, d, J=ll, O
HZ), 7,17(1H,dd,J=8,8, 2,OHz), 7,41 (1H,d,J=8,8Hz) , 7,71(1H,
s), 8,00-8,30(lH,m), 8,30-8,50(11H,m), 10,95-11,50(1H,m),
11,86(1H,s).
MS (ESI) m/z: 543 (M+H+) .
Exemplo 135 cloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-!-(2,2-dimetil-propanoil)-piperidin-3-il]5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-
Pclição 870180138821, de 08/10/2018, pág. 676/857
668 composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de pivaloíla, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 250-255 °C (decomposto).
RMN-1H (DMSO—dê) δ: l,20(9H,s), 1,70-1,81 (1H, m) , 1,90- 2,00 (lH,m), 2,88(3H,s), 3, 10 (2H, br, s) , 3,20-3, 70 (4H, m) , 3,954,08(lH,m), 4, 10-4,20(lH,m) , 4,25-4,35(1H, m) , 4,35-4,80(3H,
m) , 7,10(lH,s), 7, 16 (1H, dd, J=8, 8, 1,9Hz), 7,41(lH,d,J=
8,8Hz), 7, 69(1H,d,J=l,9Hz), 8,06(1H,br,s), 8,38(1H,d,J=7,8
Hz), 11,31 (lH,br, s) , ll,84(lH,s).
MS (ESI) m/z: 557 (M+H+) .
Exemplo 136 cloridrato de N-[ (3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-!-(3,3-dimetil-butanoil)-piperidin-3-il]-515 metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de t-butil-acetila, de uma maneira similar àquela do Exemplo 100.
Petição 870180138821, de 08/10/2018, pág. 677/857
669
Ponto de fusão: 260-265 °C (decomposto).
RMN-XH, (DMSO-de) δ: 0,91,1,04 (total 9H,cada s) , 1,68-1,82 (lH,m), 1, 93-2, 40 (3H,m) , 2,91(3H,s), 3, 00-3,20(2H, m) , 3,204,80(lOH,m), 7,08(lH,s), 7, 17 (1H, dd, J=8,7, 1,2Hz), 7,41(1H, d,J=8,7Hz), 7, 69(1H,d,J=7,6Hz), 7,93-8,18(1H,m), 8,38-8,45 (lH,m), 10,95-11,30(lH,m), 11,80-11,90(1H,m).
MS (ESI) m/z: 571 (M+H+) .
Exemplo 137 cloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)10 carbonil]-amino}-!-(2,2,2-triflúor-acetil)-piperidin-3-il]5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
°ycF3
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e anidrido triflúor-acético, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 262-267 °C (decomposto).
RMN-XH (DMSO-de) δ: 1,82-1, 98 (1H, m) , 2, 05-2,21 (1H, m) , 2,89 (3H,s), 3,05-3,20(2H,m), 3,40-3,75(4H,m), 3,85-3,95(1H,m),
4,00-4,07 (lH,m) , 4,20-4,70 (4H, m) , 7,10(lH,s), 7,18(lH,dd,
J=8, 6, 1, 9Hz) , 7, 41(1H,d,J=8,6Hz), 7,72(lH,s), 8,47(lH,dd,
Petição 870180138821, de 08/10/2018, pág. 678/857
670
J=22,4, 7,9Hz), 8,60(lH,br), 11,08 (1H, br, s) , 11, 87(lH,s).
MS (ESI) m/z: 569 (M+H+) .
Exemplo 138 cloridrato de N-[(3R*,4S*)-4-{ [ (5-cloro-indol-2-il) 5 carbonil]-amino}-!-(ciclo-propil-carbonil)-piperidin-3-il]5-metil-4,5,6,7-tetraidrotiazolo[5, 4-c]-piridino-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de ciclo-propano10 carbonila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 280-286 °C (decomposto).
ΡΜΝ-^ (DMSO-de) δ: 0,25-0, 80 (4H, m) , 1, 65-2, 15 (4H, m) , 2,91 (3H,s), 2, 90-3, 20 (3H,m), 3, 35-3, 70(2H,m), 4,00-4,80 ( 6H,m),
7,06(lH,s), 7,18(1H,d,J=8,8Hz), 7,42(1H,d,J=8,7Hz), 7,71(1H, 15 s), 8,18(1H,br,s), 8,40, 8,48 (total 1H,cada br,s), 11,11 (lH,br, s) , 11,85 (1H, s) .
MS (ESI) m/z: 542 (M+H+) .
Exemplo 139 cloridrato de N-[ (3R*,4S*)-4-{[(5-cloro-indol-2-il) Petição 870180138821, de 08/10/2018, pág. 679/857
671 carbonil]-amino}-1-(ciclo-butil-carbonil)-piperidin-3-il]-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
composto do título foi obtido a partir do 5 composto obtido no Exemplo 118 e cloreto de ciclo-butanocarbonila, de uma maneira similar àquela do Exemplo 100. Ponto de fusão: 271-275 °C (decomposto).
RMN-1H (DMSO-de) δ: 1,60-2,30(8H,m), 2,89(3H,s), 3,12(2H,br,
s), 3, 20-3, 75(6H,m) , 3, 75-3, 90(1H,m) , 4,05-4,80(4H,m), 7,08 (lH,s), 7, 15(1H,dd,J=9,0, 2,OHz), 7,39(1H, d, J=9,OHz), 7,68 (lH,d, J=2,OHz) , 8, 15 (lH,br, s) , 8,39(lH,br), 11, 19 (1H, br, s) ,
11,84 (1H,s) .
MS (ESI) m/z: 555 (M+H+) .
Exemplo 140 cloridrato de N-[ (3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-!-(ciclo-pentil-carbonil)-piperidin-3-il]5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 680/857
672
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de ciclo-pentanocarbonila, de uma maneira similar àquela do Exemplo 100. Ponto de fusão: 254-260 °C (decomposto).
RMN-1!! (DMSO-de) δ: 1,30-2,10(1OH,m), 2,90(3H,s), 3,00-3,20 (2H,m), 3, 20-3, 75 (5H,m) , 3, 80-4,80 (6H, m) , 7,09(lH,s), 7,17 (lH,dd, J=8,7,2,OHz) , 7, 42 (1H, d, J=8, 7Hz) , 7,71(lH,s), 7,958,30(lH,m), 8, 35-8, 50 (lH,m) , 11,23 (1H, br, s) , ll,85(lH,s).
MS (ESI) m/z: 569 (M+H+) .
Exemplo 141 acetato de 2-((3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin2-il)-carbonil]-amino}-piperidin-l-il)-2-oxoetila:
Petição 870180138821, de 08/10/2018, pág. 681/857
673 composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de acetóxi-acetila, de uma maneira similar àquela do Exemplo 100.
RMN-1H (CDC13) δ: 1,70-2,00 (1H, m) , 2, 05-2, 48 (3H, m) , 2,51(3H,
s), 2,70-3,05(4H,m), 3,05-4,10(5H,m), 4,20-4,48(1H,m), 4,505,10(4H,m), 6, 87 (lH,br, s) , 7, 10-7, 82 (4H, m) , 7,32 (1H, d, J=8,8
Hz) , 8,35 (lH,br,s), 9, 34, 9, 45(total 1H, cada br,s).
MS (ESI) m/z: 573 (M+H+) .
Exemplo 142 cloridrato de N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-l-glicoloil-piperidin-3-il) -5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
0<^0H
O composto obtido no Exemplo 141 (301,8 mg) foi dissolvido em tetraidrofurano (10 ml) e adicionou-se uma 15 solução aquosa 1 N de hidróxido de sódio (0,53 ml), agitando a mistura à temperatura ambiente por 18 h. Adicionou-se água à mistura da reação, para conduzir a extração com cloreto de metileno. A camada orgânica resultante foi lavada sucessivamente com água e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, o
Petição 870180138821, de 08/10/2018, pág. 682/857
674 resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1 —> 10:1), e o solvente foi removido por destilação sob pressão reduzida. O produto purificado assim obtido foi dissolvido em etanol (3 ml) e cloreto de metileno (2 ml) , e adicionou-se uma solução 1 N de ácido clorídrico em etanol, agitando a mistura por 30 min. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi solidificado com dietil-éter, para obter o composto do título (195 mg).
Ponto de fusão: 216-230 °C (decomposto).
RMN-1H (DMSO-de) δ: 1,70-1,80 (1H, m) , 1,88-2, 10 (2H, m) , 2,68 (3H,s), 3,18(2H,s), 3, 08-3, 70(5H, m) , 3, 80-3, 95(1H,m) , 4,004,25 (3H,m), 4,25-4,50 (2H, m) , 4,50-4, 65 (1H, m) , 7,09(lH,d,J=
11,0Hz), 7, 17(1H, dd,J=8,8, 2,OHz), 7,42 (1H,d,J=8,8Hz) , 7,71 (lH,s), 8,33(lH,br,s), 8,35-8,50(1H,m) , 10,80-11,30(1H, br,s), 11,84 (lH,br, s) .
Exemplo 143 cloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-!-(2-metóxi-acetil)-piperidin-3-il]-520 metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 683/857
675 composto do título foi obtido a partir do composto obtido no Exemplo 118, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 214-228 °C (decomposto).
RMN-1H (DMSO-de) δ: 1, 70-1,80 (1H, m) , 1,85-2,05 (1H, m) , 2,90 (3H,s), 3, 00-3, 20 (2H,m) , 3,16(3H,s), 3, 22-3,82 (7H, m) , 3,884,80(5H,m), 7,09(1H,d,J=9,OHz), 7,17(1H,dd,J=8,8,1,9Hz),
7,42(1H,d,J=8,8Hz), 7,70(1H,d,J=1,9Hz), 8,29(1H,br,s),8,408,50(lH,m), 11,34 (lH,br, s) , ll,86(lH,s).
MS (ESI) m/z: 545(M+H)+.
Exemplo 144 cloridrato de N-[(3R*,4S*)-4-{[(5-flúor-indol-2-il)carbonil]-amino}-!-(2-metóxi-acetil)-piperidin-3-il)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-
composto do título foi obtido a partir do composto obtido no Exemplo 122 e cloreto de metóxi-acetila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 190-208 °C (decomposto).
RMN-1H (DMSO-de) δ: 1, 70-1,83 (1H, br) , 1,85-2, 10 (1H, m) , 2,91
Petição 870180138821, de 08/10/2018, pág. 684/857
676 (3H,s), 3, 00—3, 55(10H, m) , 3,62-3,85(1H,m), 3,90-4,50(6H,m),
4,63-4,78(1H,br), 7,04(1H,td,J=9,4,2,4Hz), 7,07-7,13(1H,br) , 7,37-7,44(lH,m), 8,16-8,49(2H,m), 11,30-11,70(1H,br), 11,7211,80 (lH,br) .
MS (FAB) m/z: 529(M+H+).
Exemplo 145
N-[(3R*,4S*)-1-(3-(t-butil-(difenil)-silil}-oxi)-2,2dimetil-propanoil)-4-{[(5-flúor-indol-2-il)-carbonil]amino}-piperidin-3-il)-5-metil-4,5, 6, 7-tetraidrotiazolo[5, 410 c]-piridino-2-carboxamida:
Adicionou-se cloreto de tionila (3,0 ml) e uma quantidade catalítica de dimetil-formamida a uma solução do composto obtido no Exemplo Referencial 158 (261 mg) em clorofórmio (10 ml), e a mistura foi agitada por toda a noite a 60 °C. A mistura da reação foi concentrada por toda a noite a 60 °C. A mistura da reação foi concentrada sob pressão reduzida, dando um óleo amarelo-pálido. O composto do título foi obtido a partir deste produto e do composto obtido no Exemplo 118 (200 mg) , de uma maneira similar àquela do Exemplo 100.
Petição 870180138821, de 08/10/2018, pág. 685/857
677
Ponto de fusão: 153 °C (decomposto).
RMN-iH (CDC13) δ: l,07(9H,s), 1, 39 (6H, d, J=3, 9Hz) , l,57(lH,br, s), 2,26(1H,d,J=10,7Hz), 2,57(3H,s), 2,86(4H,s), 2,97-3,01 (2H,m), 3,78(4H,s), 4,20 (1H, br, s) , 4,33 (1H, d, J=13Hz) , 4,42 (lH,br,s), 4, 67(1H,d,J=13Hz), 6,88(lH,s), 7,20-7,23(1H,m),
7,32-7,46(7H,m), 7,647,65(6H,m), 7,86(1H,d,J=6,8Hz), 8,23 (1H,s), 9, 10(1H,s) .
Exemplo 146
N-[(3R*,4S*)-4-{[(5-flúor-indol-2-il)-carbonil]-amino}-1-(310 hidróxi-2,2-dimetil-propanoil)-piperidin-3-il)-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Adicionou-se fluoreto de tetrabutil-amônio (solução 1 M em tetraidrofurano, 0,594 ml) a uma solução do composto obtido no Exemplo 145 (241 mg) em tetraidrofurano (30 ml) sob resfriamento com gelo, e a mistura foi agitada por toda a noite à temperatura ambiente. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo resultante foi dissolvido em cloreto de metileno. A solução foi lavada com água e solução aquosa saturada de cloreto de sódio, e secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo
Petição 870180138821, de 08/10/2018, pág. 686/857
678 resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:metanol 9:1), para obter o composto do título (116 mg).
Ponto de fusão: 220 °C (decomposto).
ΡΜΝ-^ (DMSO-de) δ: 1, 17 (6H, d, J=8, 3Hz) , 1,79 (1H, br, s) , 1,91l,97(lH,m), 2,49(3H,s), 2,87(4H,s), 3, 35-3, 50 (4H, m) , 3,81 (lH,br,s), 3,97(lH,m), 4,10-4, 15 (1H, m) , 4,32 (1H, br, s) , 4,42 (lH,br,s), 4,52 (1H,t,J=5, 7Hz) , 7,10(lH,s), 7,16-7,19(1H,m) ,
7,42 (1H,d,J=8,8Hz), 7,69(lH,s), 8,11(1H,d,J=8,8Hz), 8,37(1H, d,J=7,3HZ), ll,8(lH,s).
MS (FAB) m/z: 573 (M+H+) .
Exemplo 147
N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-1-(3metóxi-2,2-dimetil-propanoil)-piperidin-3-il)-5-metil15 4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
|
|
0 composto do título |
foi obtido a |
partir |
do |
|
composto |
obtido no Exemplo 118 |
e do composto |
obtido |
no |
|
Exemplo |
Referencial 160, de uma |
maneira similar |
àquela |
do |
|
Exemplo |
145. |
|
|
|
Ponto de fusão: 240 °C (decomposto).
Petição 870180138821, de 08/10/2018, pág. 687/857
679
RMN-iH (CDC13) δ: l,34(3H,s), l,37(3H,s), 1, 65-1,77 (1H, m) ,
2,33—2,37 (1H, m) , 2,53(3H,s), 2, 82-3, 29 ( 6Η, m) , 3,34(3H,s),
3,41 (1H,d,J=9,3Hz), 3, 56(1H,d,J=9,3Hz), 3, 76(2H,d,J=5,9Hz),
4,26(lH,m), 4,44-4,53(2H,m), 4,82(1H,d,J=13,7Hz), 6,88(lH,d,
J=l,5Hz), 7,20-7,23(lH,m), 7,33(1H,d,J=8,8Hz), 7,64 (lH,d,J=
1,5Hz), 7,90(1H,d,J=7,1Hz), 8,22(1H,d,J=5,1Hz), 9,18(lH,s). MS (FAB) m/z: 587 (M+H+) .
Exemplo 148 acetato de 2-((3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]10 amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin2-il)-carbonil]-amino}-piperidin-l-il)-1,1-dimeti1-2oxoetila:
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de 2-acetóxi15 isobutirila, de uma maneira similar àquela do Exemplo 100. Ponto de fusão: 190 °C (decomposto).
ΚΜΝ-^ (CDC13) δ: 1,56-1, 67 (8H, m) , 2,08(3H,s), 2,35(lH,d,
J=10,5Hz), 2,52(3H,s), 2,82-2,84(2H,m), 2,90-2,96(2H,m),
3, 14 (lH,br, s) , 3,75(2H,s), 4,25 (1H, br, s) , 4,40-4,47 (1H, m) ,
4,54(lH,br,s), 4, 80(1H, br,s), 6,86(lH,s), 7,20-7,33(3H,m),
Petição 870180138821, de 08/10/2018, pág. 688/857
680
7,64 (lH,d, J=l,7Hz) , 7, 76 (1H, d, J=7,3Hz) , 9,ll(lH,s).
MS (FAB) m/z: 601 (M+H+) .
Exemplo 149
N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-1-(25 hidróxi-2-metil-propanoil)-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Adicionou-se metóxido de sódio (76,8 mg) a uma solução do composto obtido no Exemplo 148 (190 mg) em metanol (50 ml) , e a mistura foi agitada por toda a noite à temperatura ambiente. Depois de concentrar a mistura da reação sob pressão reduzida, o resíduo resultante foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:metanol 9:1), para obter o composto do título (130 mg).
Ponto de fusão: 190 °C (decomposto).
RMN-XH (CDC13) δ: l,53(3H,s), 1,56-1,78 (5H, m) , 2,34(lH,d,J=
10,5Hz), 2,53(3H,s), 2, 83-2, 86(2H,m) , 2,91-2,93(2H,m) , 3,30 (1H, d, J=12, 5Hz) , 3,75(2H,s), 4,2 8 (1H, d, J=5, 6Hz) , 4,43(lH,s),
4,65(1H,d,J=13,5Hz), 4,95(1H, d, J=13,5Hz),6,92(1H,d,J=l,5Hz),
Petição 870180138821, de 08/10/2018, pág. 689/857
681
7,20—7,23(1Η,m), 7,33(1H,d,J=8,6Hz), 7,65(1H,d,J=2,OHz),
8,43 (1H, d, J5, 6Hz) , 9,14(lH,s).
MS (FAB) m/z: 559 (M+H+) .
Exemplo 150 cloridrato de N-{(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1-[(3-hidróxi-ciclo-butil)-carbonil ] piperidin-3-il)-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto obtido no Exemplo 118 (306 mg) , n10 metil-morfolina (200 μη, 1 -hidróxi-benzotriazol monoidratado (87 mg), e cloridrato de 1-(3-dimetil-aminopropil)-3-etil-carbodiimida (197 mg), foram adicionados a uma solução do composto obtido no Exemplo Referencial 152 (117 mg) em um solvente misto de tetraidrofurano (20 ml), cloreto de metileno (3,0 ml) e N,N-dimetil-formamida (2,0 ml), e a mistura foi agitada à temperatura ambiente por 3 dias. A mistura da reação foi diluída com cloreto de metileno, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio, para separar a mistura em duas camadas. A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio, secada sobre
Petição 870180138821, de 08/10/2018, pág. 690/857
682 sulfato de sódio anidro e depois concentrada sob pressão reduzida. 0 resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 10:1), para obter uma base livre (207 mg) do composto do título. A base livre foi tratada com uma solução 1 N de ácido clorídrico em etanol, para obter o composto do título.
Ponto de fusão: 200 °C (decomposto).
RMN-1H (DMSO-de) δ: 1,78-2,10(4H,m), 2, 24-2, 68 (3H, m) , 2,7510 5,20(14H,m), 2,91(3H,s), 7, 08 (0,5H, s) , 7,09 (0,5H, s) , 7,18 (1H,dd,J=8,8, 2,OHz), 7,42(1H,d,J=8,8Hz), 7,70(1H,d,J=2,O
Hz), 8,05-8,28(1H,br), 8,38(0,5H,br,d,J=7,3Hz), 8,43(0,5H, br,d,J=8,3Hz), 10,80-11,25(1H,br), 11,84(1H,br,s).
MS (ESI) m/z: 571 (M+H+) .
Exemplo 151 cloridrato de N-{(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1-[(metóxi-ciclo-butil)-carbonil]piperidin-3-il)-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
foi obtido a partir do e do composto obtido no
O composto do título composto obtido no Exemplo 118
Petição 870180138821, de 08/10/2018, pág. 691/857
683
Exemplo Referencial 154, de uma maneira similar àquela do Exemplo 150.
Ponto de fusão: 191 °C (decomposto).
RMN-1H (DMSO-de) δ: 1, 69-2,23 (4H, m) , 2, 25-2,40 (1H, m) , 2,715 2,84 (0,5H,m) , 2, 89-3, 93 (9, 5H, m) , 2,91(3H,5), 3,01(lH,s),
3,14(2H,s), 4, 05-4, 80 (5H,m) , 7,09(lH,s), 7,18(1H,d,J=8, 4
Hz), 7,42 (1H,d,J=8, 4Hz) , 7,70(lH,s), 8,00-8,30(1H, br) , 8,368,53(lH,m), 11,25-11,75(11-1, br) , 11,85(1H,br,s) .
MS (ESI) m/z: 585 (M+H+) .
Exemplo 152 cloridrato de N-{(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1-[3-metóxi-2-(metóxi-metil)-propanoil]piperidin-3-il]-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido condensando um ácido carboxílico obtido pela hidrólise do composto obtido no Exemplo Referencial 155 com o composto obtido no Exemplo 118, de uma maneira similar àquela do Exemplo 150.
Ponto de fusão: 178-184 °C (decomposto).
Petição 870180138821, de 08/10/2018, pág. 692/857
684
RMN-1H (DMSO-de) δ: 1,69-1,82 (lH,m), 1, 84-2, 04 (1H,m) , 2,91(3 H,s), 3,00-3,75(17H,m), 3,95-4,55(5H,m), 4,60-4,80(1H,m),
7,10(lH,br,s), 7,18(1H,dd,J=8,8, 2,OHz), 7,42(1H,d,J=8,8
Hz), 7,69(0,5H,br,s), 7,71(1H,br,s), 8,18—8,28(1H,br), 8,35—
8,50(lH,br), 11,83 (1H, br, s) .
MS (ESI) m/z: 603 (M+H+) .
Exemplo 153 cloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-(tetraidro-2H-piran-4-il-carbonil)10 piperidin-3-il]-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
|
O composto |
do título |
foi obtido a |
partir |
do |
|
composto obtido no |
Exemplo 118 |
e do composto |
obtido |
no |
|
Exemplo Referencial |
15 6, de uma |
maneira similar |
àquela |
do |
Exemplo 150.
Ponto de fusão: 225-248 °C (decomposto).
RMN-íH (DMSO-dg) δ: 1, 55-1, 68 (4H, m) , 1,70-1,85 (1H, m) , 1,852,05(lH,m), 2, 60-2, 95 (lH,m) , 2,89(3H,s), 2,95-3, 20 (3H, m) ,
3, 20-4,00 (9H,m) , 4, 00-4, 80 (4H,m) , 7,08(lH,s), 7,17(lH,dd,
Petição 870180138821, de 08/10/2018, pág. 693/857
685
J=8,8, 2,OHz), 7,42 (1H, d, J=8, 8Hz) , 7,71(lH,s), 8,00-8,30 (lH,m), 8,35—8,50 (1H, m) , 11, 16 (1H, br, s) , ll,85(lH,s).
MS (ESI) m/z: 585 (M+H+) .
Exemplo 154 cloridrato de N-((3R*,4S*)-l-benzoil-4-{[(5-cloro-indol-2il)-carbonil]-amino}-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de benzoíla, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 215-225 °C (decomposto).
RMN-iH (DMSO-de) δ: 1, 75-1, 90 (1H, m) , 1,90-2,20 (1H, m) , 2,93 (3H,s), 3, 10-4,00(8H,m), 4, 05-4, 80(4H,m), 7,00-7, 60(5H,m),
7,08 (lH,s), 7,16 (1H,dd,J=8,8, 1,6Hz), 7,40 (1H,d,J=8,8Hz),
7,71 (lH,d, J=l, 6Hz) , 8, 31 (1H, br, s) , 8,4 6 (1H, br, s) , 11,39(1H, br,s),11,86(1H,s).
MS (FAB) m/z: 577 (Μ+Ή) .
Petição 870180138821, de 08/10/2018, pág. 694/857
686
Exemplo 155 (3R*,4S*)-3-({[5—(2—{[t-butil-(difenil)-silil]oxi}-l, 1dimetil-etil)-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il]carbonil}-amino)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}5 piperidino-l-carboxilato de t-butila:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 207 e do composto obtido no Exemplo Referencial 42, de uma maneira similar àquela do Exemplo 91.
EMN-iH (DMSO-de) δ: l,00(9H,s), l,12(6H,s), 1, 15-1,50 (9H, m) , 1,63-1,75(lH,m), 1,82-2,00(lH,m), 2,60-2,80(3H,m), 2,832,95(2H,m), 3,12-3,30(1H,m) , 3,30(2H,s), 3,58(2H,s), 3,854,10 (2H,m), 4, 19(1H,br,s), 4,37 (1H, br, s) , 7,04(lH,s), 7,16 (1H,d,J=9,OHz), 7, 30-7, 50 (7H,m) , 7,50-7, 65 (4H, m) , 7,7O(1H,
s), 7,99 (1H, d, J=6, 8Hz) , 8, 45 (1H, br, s) , ll,82(lH,s).
MS (ESI)m/z: 869 (M+H)+.
Exemplo 156 dicloridrato de 5-(2-{[t-butil-(difenil)-silil]oxi}-l, 1dimetil-etil)-N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)20 carbonil]-amino}-piperidin-3-il)-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 695/857
687
TBDPSO
composto do título composto obtido no Exemplo 155, àquela do Exemplo 95.
foi obtido tratando o de uma maneira similar
RMN-1!! (DMSO-de) δ: l,04(9H,s), 1,43, 1,48 (total 6H, cada s) ,
1,85-2,00(lH,m), 2,05-2,20(1H,m), 2,95-3,20(2H,m), 3,25-3,60 (6H,m), 3, 80—3, 90 (lH,m), 3, 95—4,05 (lH,m), 4,45—4,55 (1H, m) ,
4,60-4,85(3H,m), 7,10-7,20(2H,m), 7,35-7,55(7H,m), 7,55-7,75 (5H,m), 8, 52 (lH,dd, J=14,4,7, 8Hz) , 8,93(lH,br), 9,20-9,40 (2H,m), 11,30-11,50(lH,m), 11,87,11,92(total 1H,cada s).
MS (ESI) m/z: 769 (M+H+).
Exemplo 157
5- (2-{[t-butil-(difenil)-silil]oxi}-l,1-dimetil-etii)-N[(3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-1-(2metóxi-acetil)-piperidin-3-il]-4,5,6,7-tetraidrotiazolo[5, 415
c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 696/857
688 composto do título foi obtido a partir do composto obtido no Exemplo 156 e cloreto de metóxi-acetila, de uma maneira similar àquela do Exemplo 100.
ΗΜΝ-^ (CDC13) δ: l,07(9H,s), l,20(6H,s), 1, 60-1, 85 (1H, m) ,
2,25-2,40(lH,m), 2,36(2H,s), 2,70-3, 20 (4H, m) , 3, 20- 3, 55 (4H,
m) , 3, 55-3, 70(2H,m) , 3,95-4,10(3H,m) , 4,10-4,90(4H,m), 6,90 (1H,d,J=l,5Hz) , 7,15-7,30(2H,m) , 7,30-7,50(6H,m) , 7,60-7,70 (5H,m), 8, 15-8,22 (lH,m) , 8, 46 (1H, d, J=5,1Hz) , 9,28(lH,s).
MS (ESI) m/z: 842 (M+H+) .
Exemplo 158 cloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-!-(2-metóxi-acetil)-piperidin-3-il]-5-(2hidróxi-1,1-dimetil-etil)-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 157, de uma maneira similar àquela do Exemplo 146.
Ponto de fusão: 221-232 °C (decomposto).
EMN-iH (DMSO-de) δ: l,32(3H,s), l,40(3H,s), 1,70-1, 85 (1H, m) ,
1,85-2,10(lH,m), 2,60-3,35(8H,m), 3,40-3,82(3H,m), 3,85-4,05 (3H,m), 4, 05-4,35(2H,m) , 4,50-4,60(1H,m), 4,55-4,80(2H,m) ,
Petição 870180138821, de 08/10/2018, pág. 697/857
689
5,75—5,85(1Η,m), 7, 08(1H,br,s), 7, 17(1H, d,J=8,8Hz), 7,41 (1H, d,J=8,8Hz), 7,71(lH,s), 8,20-8, 35(lH,m) , 8,40-8,55 (1H,
m) , 10,00-10,35 (lH,m) , ll,87(lH,s).
MS (ESI) m/z: 603 (M+H+) .
Exemplo 159 (3R*,4S*)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-3-{[(5isopropil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-piperidino-l-carboxilato de t-butila:
Boc
O composto do título foi obtido a partir do 10 composto obtido no Exemplo Referencial 209 e do composto obtido no Exemplo Referencial 148, de uma maneira similar àquela do Exemplo 91.
RMN-1!! (CDC13) δ: 1, 16 (6H, d, J=6, 6Hz) , l,53(9H,s), 1,65-1,80 (lH,m), 2, 23-2, 32(lH,m), 2, 80-3,10(6H,m), 3,10-3,25(1H,m),
3, 80-3, 90 (2H,m) , 4, 00-4,50 (4H,m) , 6,91(lH,s), 6,95-7,05 (lH,m), 7,25—7, 40(2H,m), 7,74(1H,br, s) , 8,21(1H,br,s), 9,30 (1H,s) .
MS (ESI) m/z: 585 (M+H+) .
Exemplo 160 dicloridrato de N-( (3R*,4S*)-4-{[(5-flúor-indol-2-il)carbonil]-amino}-piperidin-3-il)-5-isopropil-4,5,6,7Pctição 870180138821, de 08/10/2018, pág. 698/857
690 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo 159, de uma maneira similar àquela do Exemplo 95.
RMN-1!! (DMSO-de) δ: 1,28-1,40 (6H,m) , 1,85-2,00 (1H, m) , 2,052,20(lH,m), 2, 40-2, 60 (lH,m) , 2, 95-3, 90 (8H,m) , 4,40-4,55(2H,
m), 4,60—4,75(2H,m), 7,00—7,20(2H,m), 7,30—7,50(2H,m), 8,45—
8,60(lH,m), 8, 85-9, 05 (lH,m) , 9, 05-9, 50 (2H, m) , 11,60-11,90 (2H,m) .
MS (ESI) m/z: 4 85 (M+H+) .
Exemplo 161 cloridrato de N-( (3R*,4S*)-4-{[(5-flúor-indol-2-il)carbonil]-amino}-!-(2-metóxi-acetil)-piperidin-3-il)-5isopropil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-215 carboxamida:
Petição 870180138821, de 08/10/2018, pág. 699/857
691 composto do título foi obtido a partir do composto obtido no Exemplo 160 e cloreto de metóxi-acetila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 214-228 °C (decomposto).
ΡΜΝ-^ (DMSO-de) δ: 1,25-1,40(6H,m), 1, 68-1,82 (1H, m) , 1,852,10(lH,m), 2, 90-3, 60 (8H,m), 3, 60-3, 85 (2H, m) , 3,85-4,40 (5H,
m) , 4,40-4,55 (2H,m), 4,60-4,75 (lH,m), 7, 00- 10 7, 15(2H,m),
7,35-7,50(2H,m), 8, 15-8,50(2H,m), 10, 80-11, 30(1H,m), 11,73 (1H,d,J6,6Hz).
MS (ESI) m/z: 557 (M+H+) .
Exemplo 162 cloridrato de N-{(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1-[(dimetil-amino)-carbonil]-piperidin-3il}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-215 carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e cloreto de N,N-dimetilcarbamoíla, de uma maneira similar àquela do Exemplo 100. Ponto de fusão: 267-270 °C (decomposto).
RMN-1!! (DMSO-dg) δ: 1, 65-1, 78 (1H, m) , 1, 97-2, 10 (1H, m) , 2,70
Petição 870180138821, de 08/10/2018, pág. 700/857
692 (6H,s), 2,90(3H,s), 2,95-3,80(8H,m), 4,25-4,80(4H,m), 7,08 (lH,s), 7, 16(1H, dd,J=8,8,1,8Hz), 7,41(1H,d,J=8,8Hz), 7,70 (lH,s), 8,31(lH,br,s), 8,40(1H, d, J=+7,3Hz), 11,15-11,60 (1H,
m), 11,82 (1H,s) .
MS (ESI) m/z: 544 (M+H+) .
Exemplo 163 cloridrato de N-{(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1-[(etil-amino)-carbonil]-piperidin-3-il}10
5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 118 e isocianato de etila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 221-235 °C (decomposto).
EMN-iH (DMSO-de) δ: O, 98(3H, t,J=7,1Hz), 1, 60-1,70(1H,m),
1,80-1,95(lH,m), 2,90(3H,s), 2,95-3,40(6H,m), 3,40-4,00(4H,
m) , 4,25-4,80 (4H,m) , 6, 60-6, 80 (1H, m) , 7,09(lH,s), 7,16(1H, dd,J=8,8,1,9Hz), 7,41(1H,d,J=8,8Hz), 7, 68(1H, d, J=1, 9Hz) ,
8,02(lH,br,s), 8,35(1H,d,J=7,1Hz), 11,20-11,70(1H,m), 11,82 (1H,s) .
Petição 870180138821, de 08/10/2018, pág. 701/857
693
MS (FAB) m/z : 544 (M+H+) .
Exemplo 164 cloridrato de N-((3R*,4S*)-1-[(t-butil-amino)-carbonil]-4{[(5-cloro-indol-2-il)-carbonil]-amino}-piperidin-3-il)-55 metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo 118 e isocianato de t-butila, de uma maneira similar àquela do Exemplo 100.
Ponto de fusão: 236-238 °C (decomposto).
RMN-1!! (DMSO-de) δ: l,21(9H,s), 1, 60-1,70 (1H, m) , 1,80-1,90 (lH,m), 2,87(3H,s), 3, 00-3, 4 0 (6H, m) , 3, 4 9 (1H, br, s) , 3,803,90 (lH,m), 3, 90-4, 00 (lH,m), 4,20-4,35 (2H,m), 4,47 (lH,br, s), 5,90(lH,s), 7,06(lH,s), 7,16 (1H, dd, J=8, 8, 1, 9Hz) ,
7,41 (1H,d,J=8,8Hz), 7,67(1H,d,J=1,9Hz), 8, 04(1H,d,J=6,8Hz),
8,34 (lH,d, J=7,3Hz) , 11,22 (1H, br, s) , ll,79(lH,s).
MS (FAB) m/z: 572 (M+H+) .
Exemplo 165 dicloridrato de 2-((3R*,4S*)-4-{[(5-cloro-indol-2-il)Petição 870180138821, de 08/10/2018, pág. 702/857
694 carbonil]-amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridin-2-il)-carbonil]-amino}-piperidin-3-il)-acetato de
composto do título foi obtido a partir do 5 composto obtido no Exemplo 118 e bromo-acetato de metila, de uma maneira similar àquela do Exemplo 102.
Ponto de fusão: 253-255 °C (decomposto).
RMN-1!! (DMSO-de, 80°C) δ: 1, 95-2,10 (1H, m) , 2,10-2,25 (1H, m) ,
2,88 (3H,s), 3, 00-3, 73 (8H,m) , 3,75(3H,s), 3, 97-4, 15 (2H, m) ,
4,30-4,80 (4H,m), 7, 08-7, 20(2H,m) , 7,44(1H,d,J=8,6Hz), 7,63 (lH,d, J=2,OHz) , 8, 42 (1H, d, J=7, 3Hz) , 8, 62 (1H, br, s) , 11,82(1H, br,s).
MS (ESI) m/z: 545 (M+H+) .
Exemplo 166 cloridrato do ácido 2-( (3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridin-2-il)-carbonil]-amino}-piperidin-3-il)-acético:
Petição 870180138821, de 08/10/2018, pág. 703/857
695
O composto do título foi obtido tratando o composto obtido no Exemplo 165, de uma maneira similar àquela do Exemplo 101.
Ponto de fusão: 234-240 °C (decomposto).
RMN-1!! (DMSO-dg) δ: 1, 75-1, 95 (1H, m) , 2,05-2,20 (1H, m) , 2,88 (3H,s), 2, 95-3, 90 (10H,m) , 4,20-4,70(4H,m), 7,ll(lH,s), 7,16 (1H,dd,J=8,8, 2,OHz), 7,41(1H,d,J=8,8Hz), 7,66(1H,d,J=2,O
Hz), 8,46 (lH,br,d, J=7,8Hz) , 8,65 (lH,br,s), 11,6012,70(2H, br,s), 11, 91 (1H, br, s) .
Exemplo 167 dicloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-!-(2-metóxi-etil)-piperidin-3-il]-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 704/857
696 composto do título foi obtido tratando o composto obtido no Exemplo 118 e 2-bromo-etil-metil-eter, de uma maneira similar àquela do Exemplo 102 (A RMN foi medida na forma de uma base livre).
Ponto de fusão: 238-242 °C (decomposto).
RMN-XH (CDC13) δ: 1,75-1,83 (2H, m) , 2, 27-2, 39 (2H, m) , 2,52(3H,
s), 2,60-2,66(lH,m), 2,69-2,75(1H,m), 2,81-2,90(2H,m), 2,963,07(2H,m), 3,41(3H,s), 3, 53-3, 60 (2H, m) , 3,75(cada ΙΗ,ΑΒ tipo d,J=15,5Hz), 4,02-4,05 (lH,m) , 4,40(lH,br), 6,88(lH,d,
J=l,5Hz), 7,18-7,21(lH,m) , 7,31-7,33(1H,m) , 7,63(1H,d,J=1,5
Hz), 8,17(lH,d,J=5,OHz), 8,26(1H,d,J=7,OHz), 9,30(1H,br,s). MS (FAB) m/z: 531 (M+H+) .
Exemplo 168 dicloridrato de N-[(3R*,4S*)-4-{[(5-cloro-indol-2-il)15 carbonil]-amino}-!-(2-flúor-etil)-piperidin-3-il]-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo 118 e brometo de 2-flúor-etila, de uma maneira similar àquela do Exemplo 102 (A RMN foi medida na forma de uma base livre).
Petição 870180138821, de 08/10/2018, pág. 705/857
697
Ponto de fusão: 228-233 °C (decomposto).
RMN-1H (CDCI3) δ: 1,77(2H,dq,J=12,5, 4,OHz), 2,28-2,32(1H,m), 2,41(1H,t,J=12,5Hz), 2,52(3H,s), 2,65(1H,d,J=10,5Hz), 2,762,81(lH,m), 2,83-2,86(3H,m), 2,98-3,05(3H,m), 3,75(cada 1H,
AB tipo d,J=15,5Hz), 4,02-4,08(1H,m), 4,45(lH,br), 4,544,59(lH,m), 4, 64-4,70(1H,m), 6, 87(1H,d,J=1,5Hz), 7,19-7,22 (lH,m), 7, 32(1H,d,J=8,5Hz), 7, 64(1H,d,J=2,OHz), 8,ll(lH,d,
J=5,5Hz), 8,20 (1H, d, J=7, 3Hz) , 9,30(lH,br).
MS (FAB) m/z: 519(M+H+).
Exemplo 169 cloridrato de N-((3R, 4S)-l-acetil-4-{[(5-cloro-indol-2-il)carbonil]-amino}-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Uma solução 4 N de ácido clorídrico em dioxano 15 (7,0 ml) foi adicionada a uma solução (5 ml) do composto obtido no Exemplo Referencial 214 (630 mg) em dioxano, e a mistura foi agitada à temperatura ambiente por 1 h. A mistura da reação foi concentrada sob pressão reduzida. Os sólidos amarelos assim obtidos (590 mg) e o composto obtido no Exemplo Referencial 10 (379 mg) foram usados para obter uma base livre (330 mg) do composto do título, de uma
Petição 870180138821, de 08/10/2018, pág. 706/857
698 maneira similar àquela do Exemplo 91. Esta base livre foi tratada com solução de ácido clorídrico em etanol, para obter o composto do título (A RMN foi realizada na forma de uma base livre).
Ponto de fusão: 202-222 °C (decomposto).
ΗΜΝ-^ (DMSO-de) δ: 1, 65-1,85 (1H, m) , 1, 87,2, 0 6 (total 3H,cada
s), 1,88-2,10(lH,m) , 2,37(3H,s), 2, 65-2, 77(2H, m) , 2,79-2,89 (2H,m), 2, 99-3, 09 (0, 5H,m) , 3, 30-3, 52 (2H, m) , 3,64(2H,s), 3,70-3,80(0,5H,m), 3,96-4,21(2H,m), 4,27(1H,br,s), 4,35-4,48 (lH,m), 7,07,7,11(total 1H,cada s), 7,18(1H,d,J=8,8Hz), 7,42 (1H, d, J=8, 8Hz) , 7,71(lH,s), 8, 16-8, 22 (1H, m) , 8,37, 8,46 (total lH,cada d,J=7,8Hz), 11,81, 11,83(total 1H,cada s).
MS (ESI) m/z: 515 (M+H+) .
[CC]25d = -56° (C = 0,50, metanol)
Exemplo 170 cloridrato de N-((3R,4R)-l-acetil-4-{[(5-cloro-indol-2-il)carbonil]-amino}-piperidin-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do 20 composto obtido no Exemplo Referencial 219 e do Exemplo
Petição 870180138821, de 08/10/2018, pág. 707/857
699
Referencial 10, de uma maneira similar àquela do Exemplo
169.
Ponto de fusão: 221-238 °C.
RMN-1H (DMSO-de) δ: 1,45-1,56 (0, 5H,m) , 1, 60-1,70 (0,5H, m) ,
1,89-2,01 (lH,m) , 2,05(3H,s), 2,51-2, 67 (1H, m) , 2,88(3H,s),
3, 00-3, 22 (3H,m), 3, 31-3,40(3H,m), 3, 56-3, 67(0,5H,m), 3,784,02(1,5H,m), 4,22-4,44(2H,m), 4,56-4,72(1H,m), 7,02(lH,s),
7,15(lH,dd, J=8,8,2,OHz) , 7, 37 (1H, d, J=8, 8Hz) , 7,67(lH,d,J=
2,OHz), 8,42(1H,d,J=9,8Hz), 8,67-8,78(1H,m), 11,02-11,14 (lH,m), 11,72(0,5H,s), 11,74(0,5H,s) .
MS (FAB) m/z: 515 (M+H+) .
[CC]25d = -105,4° (c = 0,58, metanol).
Exemplo 171 cloridrato de N-[(3R,4S)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-!-(2-metóxi-acetil)-piperidin-3-il]-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 221, de uma maneira similar àquela do Exemplo 169.
Ponto de fusão: 207-220 °C.
Petição 870180138821, de 08/10/2018, pág. 708/857
700
RMN-XH (DMSO-de) δ: 1, 70-1,80 (1Η, m) , 1,85-2,05(1H, m) , 2,90 (3H,s), 3, 00-3, 20 (2H,m) , 3,16(3H,s), 3, 22-3,82 (7H, m) , 3,884,80(5H,m), 7, 09(1H, d,J=9,OHz), 7, 17 (1H, dd, J=8, 8, 1,9Hz),
7,42(1H,d,J=8,8Hz), 7,70(1H,d,J=1,9Hz), 8,29(1H,br,s), 8,405 8,50(lH,m), 11,20-11,50 (1H, m) , ll,85(lH,s).
MS (ESI) m/z: 545 (M+H+) .
[CC]25d = -53,4° (c = 0,52, metanol).
Exemplo 172 cloridrato de N-[(3R, 4R)-4-{[(5-cloro-indol-2-il)-carbonil]10 amino}-!-(2-metóxi-acetil)-piperidin-3-il]-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 223, de uma maneira similar àquela do Exemplo 169.
Ponto de fusão: 213-230 °C.
RMN-XH (DMSO-dg) δ: 1,45-1,56(0, 5H, m) , 1, 61-1,70(0,5H,m),
1,89-2,00 (lH,m) , 2,05(3H,s), 2,45-2, 67 (1H, m) , 2,88(3H,s),
3,00-3,21(4H,m), 3,32-3,56(7H,m), 3,78-3,89(2H,m), 4,004,24(2H,m), 4,26-4,43(2H,m), 7,02(lH,s), 7, 13(1H,dd,J=8,8,
2,0 Hz), 7,37(1H, d, J=8, 8Hz), 7,67(1H,d,J=2,OHz), 8,41 (lH,d,
Petição 870180138821, de 08/10/2018, pág. 709/857
701
J=9,8Hz), 8, 74(1H,d,J=9,8Hz), 10, 80-10, 90 (lH,m) , 11,72 (1H,
s) .
MS (FAB) m/z: 545 (M+H+) .
[CC]25d = -100,3° (c = 0,51, metanol).
Exemplo 173 cloridrato de N-((3R,4R)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-6-oxotetraidro-2H-piran-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do 10 composto com baixa polaridade obtido no Exemplo Referencial 176 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 169.
RMN-1!! (DMSO-de) δ: 2, 41-2,56 (2H, m) , 2,91(3H,s), 3,01-3,23 (lH,m), 3, 24-3, 56 (5H,m), 3, 62-3, 67(1H,m), 4,21-4,44(1H,m),
4,56-4,78(2H,m), 7,ll(lH,s), 7,16(1H,dd,J=8,8, 2,OHz), 7,22 (1H,d,J=8,5Hz), 7,41(1H,d,J=8,8Hz), 7,69(1H,d,J=2,OHz), 8,40 —8,50(lH,m), 11,34-11,56 (lH,m) , ll,82(lH,s).
MS (FAB) m/z: 488 (M+H+) .
Exemplo 174 cloridrato de N-((3R,4S)-4-{[(5-cloro-indol-2-il)-carbonil]amino}-6-oxotetraidro-2H-piran-3-il)-5-metil-4,5,6,7Pclição 870180138821, de 08/10/2018, pág. 710/857
702 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido a partir do composto com alta polaridade obtido no Exemplo Referencial 176 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 169.
RMN-1H (DMSO-de) δ: 2,41-2,56(2H,m), 2,91(3H,s), 3,23-3,41 (2H,m), 3,43-3,50(2H,m), 3,56-3,67(2H,m), 4,37(1H,dd,J=13,9, 7,1Hz), 4,40-4,50 (lH,m) , 4,56-4,78 (2H, m) , 7,12(lH,s), 7,17 (lH,dd,J=8,8,2,OHz) , 7,41(1H,d,J=8,8Hz), 7,71(1H,d,J=2,OHz), 10 8,44 (1H,d,J=8,5Hz) , 8,15(1H,d,J=8,5Hz) , 11,42-11,53(1H,m),
11,79(1H,S) .
MS (FAB) m/z: 488 (M+H+) .
Exemplo 175 (3R,4S)-5-{[t-butil-(difenil)-silil]oxi}-3-{[(5-cloro-indol15 2-il)-carbonil]-amino}-4-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}valerato de etila:
Petição 870180138821, de 08/10/2018, pág. 711/857
703
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 225, de uma maneira similar àquela do Exemplo 169.
RMN-1H (CDC13) δ: l,09(9H,s), 1,21 (3H, t, J=7, 4Hz) , 2,49(3H,s), 5 2, 65 (1H, dd, J=15, 9, 5,4Hz), 2, 67-2, 90 (5H, m) , 3,60(lH,d,J=
14,9Hz), 3,72(1H,d,J=14,9Hz), 3,78-3,91(2H,m), 4,00-4,21(2H, m) , 4,43-4,50(lH,m) , 4,78-4,89 (1H, m) , 6,81(lH,s), 7,2O(1H, dd,J=8,8, 2,OHz), 7,32-7,52(m,7H), 7,63-7,74(6H,m), 7,898,01 (lH,m) , 9, 18 (1H, s) .
Exemplo 176 (3R,4S)-3-{[(5-cloro-indol-2-il)-carbonil]-amino}-5-hidróxi4-{[(5-meti1-4,5,6,7-tetraidrotiazolo[5, 4-c]-piridin-2-il)carbonil]-amino}-valerato de etila:
Depois de adicionar ácido fluorídrico/piridina 15 (0,4 ml) em gotas a uma solução do composto obtido no
Exemplo 75 (0,54 g), piridina (4,0 ml) e tetraidrofurano (10 ml) sob resfriamento com gelo, a mistura da reação foi agitada por 18 h, enquanto a temperatura dela era aumentada gradualmente até a temperatura ambiente. A mistura da reação foi concentrada, e o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel
Petição 870180138821, de 08/10/2018, pág. 712/857
704 (clorofórmio:metanol 9:1), para obter o composto do título (0,31 g) .
RMN-1H (CDC13) δ: 1,20 (3H, t, J=7, 4Hz) , 2,49(3H,s), 2,67-2,90 (6H,m), 3,62-3,74(3H,m), 3,78-3,94(1H,m), 4,00-4,20(2H,m),
4,30-4,40 (lH,m), 4, 80-4, 89(1H,m), 6,93(lH,s), 7,23(1H,dd,J=
8,8, 2,OHz), 7,33(1H,d,J=8,8Hz), 7,56(1H,d,J=8,5Hz), 7,61 (lH,d, J=2,OHz) , 7,88 (1H, d, J=8, 5Hz) , 9,29(lH,s).
Exemplo 177 cloridrato de N-((3S,4R)-4-{[(5-cloro-indol-2-il)-carbonil]10 amino}-6-oxotetraidro-2H-piran-3-il)-5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Uma solução 4 N de ácido clorídrico em dioxano (20 ml) foi adicionada ao composto obtido no Exemplo 176 (0,31
g), e a mistura foi agitada sob refluxo por 4 h. A mistura da reação foi concentrada, e o resíduo resultante foi recristalizado em dietil-éter, para obter o composto do título (0,23 g).
Ponto de fusão: 221-238 °C (decomposto).
RMN-1H e MS (FAB): iguais àquelas do enanciômero no Exemplo
174.
Petição 870180138821, de 08/10/2018, pág. 713/857
705
Exemplo 178 cloridrato de N-((3R*,4R*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1,1-dioxo-hexaidro-l-tiopiran-3-il) -5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-
Uma base livre do composto do título foi obtida a partir do composto obtido no Exemplo Referencial 227 e ácido 5—cloro-indol—2-carboxílico, de uma maneira similar àquela do Exemplo 91. Esta base livre foi tratada com uma solução de ácido clorídrico em etanol, para obter o composto do título.
Ponto de fusão: 241-244 °C.
ΗΜΝ-^ (DMSO-de) δ: 2,14(lH,br), 2, 30-2, 34 (1H, m) , 2,92(3H,s), 3, 10-3, 18 (2H,m) , 3,41(4H,br), 3,68(2H,br), 4,44(lH,br),
4,63-4,78(3H,m), 7,16-7,18(lH,m), 7,21(lH,s), 7,43 (lH,d,J=
8,5Hz), 7, 67 (lH,d, J4,6Hz) , 8,39(lH,br), 8,94(lH,br), 11,82 (1H,br).
MS (ESI) m/z: 522 (M+H+) .
Exemplo 179 cloridrato de N-( (3R*,4R*)-4-{[(5-flúor-indol-2-il) Petição 870180138821, de 08/10/2018, pág. 714/857
706 carbonil]-amino}-1,1-dioxo-hexaidro-l-tiopiran-3-il)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Uma base livre do composto do título foi obtida a 5 partir do composto obtido no Exemplo Referencial 227 e ácido 5-flúor-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 91. Esta base livre foi tratada com uma solução de ácido clorídrico em etanol, para obter o composto do título.
Ponto de fusão: 243-245 °C.
RMN-!H (DMSO-de) δ: 2,14(lH,br), 2, 30-2, 33 (1H, m) , 2,92(3H,s), 3,13(2H,br), 3,51(4H,br), 3,63(2H,br), 4,63(3H,br), 4,78(1H, br), 7,01-7,05(lH,m) , 7,21(lH,s), 7, 37-7,44(2H, m) , 8,36(1H, br), 8,93(1H,d,J=6,8Hz), 11,72(1H,br).
MS (ESI) m/z: 506 (M+H+) .
Exemplo 180 cloridrato de N-( (3R*,4R*)-3-{[(5-cloro-indol-2-il)carbonil]-amino}-1,1-dioxo-hexaidro-l-tiopiran-4-il)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-220 carboxamida:
Petição 870180138821, de 08/10/2018, pág. 715/857
707
Uma base livre do composto do título foi obtida a partir do composto obtido no Exemplo Referencial 229 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 91. Esta base livre foi tratada com uma solução de ácido clorídrico em etanol, para obter o composto do título.
Ponto de fusão: 242-247 °C.
ΡΜΝ-!Η (DMSO-de) δ: 2,16 (lH,br), 2,45 (lH,br), 2,93 (3H,s),
3,13(2H,br), 3,26(4H,br), 3,69(2H,br), 4,45(lH,br), 4,654,77(3H,m), 7,01(lH,s), 7, 17 (1H, dd, J=8,7, 1,4Hz), 7,43(1H, d,J=8,5Hz), 7,69(lH,s), 8,35-8,4 0 (1H, m) , 9,04(lH,br), 11,86 (1H,S) .
MS (ESI) m/z: 522 (M+H+) .
Exemplo 181 cloridrato de N-( (3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1,1-dioxo-hexaidro-l-tiopiran-3-il)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 716/857
708
Uma base livre do composto do título foi obtida a partir do composto obtido no Exemplo Referencial 231 e do ácido 5-cloro-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 91. Esta base livre foi tratada com uma solução de ácido clorídrico em etanol, para obter o composto do título.
Ponto de fusão: 244-249 °C.
RMN-1H (DMSO-de) δ: 2, 17-2,2 7 (2H, m) , 2,90(3H,s), 3,09(lH,br), 3, 18-3, 21 (2ll,m) , 3, 31-3, 34 (211, m) , 3, 60-3, 67 (311, m) , 4,41-4,49 (2H,m), 4,54-4,59 (2H,m) , 7,04(lH,s), 7, 09-7, 13 (1H, m) , 7,39 (1H,d,J=8,5Hz), 7,61(1H,d,J=9,9Hz), 8,52-8,56(1H,m), 8,838,85(lH,m), 11,65(1H,d,J=ll,9Hz).
MS (ESI) m/z: 522 (M+H+) .
Exemplo 182 cloridrato de N- ( (3R*,4S*)-4-{[(5-flúor-indol-2-il) carbonil]-amino}-1,1-dioxo-hexaidro-l-tiopiran-3-il)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 717/857
709
Uma base livre do composto do título foi obtida a partir do composto obtido no Exemplo Referencial 231 e do ácido 5-flúor-indol-2-carboxílico, de uma maneira similar àquela do Exemplo 91. Esta base livre foi tratada com uma solução de ácido clorídrico em etanol, para obter o composto do título.
Ponto de fusão: 236-241 °C.
RMN-1!! (DMSO-de) δ: 2,2 0-2,2 4 (2H, m) , 2,89(3H,s), 3,07(lH,br), 3,19-3,22(2H,m), 3,60-3,66(4H,m), 4,43-4,58(5H,m), 6,95-7,00 (lH,m), 7,04(lH,s), 7,32-7,38(2H,m) , 8,50 (1H,d,J=8,5Hz),
8,83 (1H, d, J=8, 5Hz) , ll,59(lH,s).
MS (ESI) m/z: 506 (M+H+) .
Exemplo 183 cloridrato de N-((3R*,4R*)-3-{[(5-flúor-indol-2-il)15 carbonil]-amino}-1,1-dioxo-hexaidro-l-tiopiran-4-il)-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-
Pclição 870180138821, de 08/10/2018, pág. 718/857
710
Uma base livre do composto do título foi obtida a partir do composto obtido no Exemplo Referencial 233 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 91. Esta base livre foi tratada com uma solução de ácido clorídrico em etanol, para obter o composto do título.
Ponto de fusão: 244-249 °C.
RMN-1H (DMSO-de) δ: 2, 12-2, 18 (1H, m) , 2,50(lH,br), 2,92(3H,s), 3,17(3H,br), 3,50-3,61(5H, m) , 4,45(lH,br), 4,62-4,78(3H, m) ,
6, 98-7,03 (2H,m) , 7, 36-7, 42 (2H, m) , 8,30(lH,br), 9,00(lH,d,J=
8,OHz), 11,74 (1H,s) .
MS (ESI) m/z: 506 (M+H+) .
Exemplo 184
N-((3S,4R)-4-{[(5-cloro-indol-2-il)-carbonil]-amino}-!15 metil-6-oxopiperidin-3-il)-5-metil-4,5, 6, 7tetraidrotiazolo[5,4-c]-piridino-2-carboxamida (composto de baixa polaridade) e N-((3R,4R)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-l-metil-6-oxopiperidin-3-il)-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida 20 (composto de alta polaridade):
Composto de baixa polaridade Composto de alta polaridade
Petição 870180138821, de 08/10/2018, pág. 719/857
711 composto do título foi obtido a partir do composto com alta polaridade obtido no Exemplo Referencial 236 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do Exemplo 169.
Composto de baixa polaridade:
Ponto de fusão: 189-203 °C (decomposto).
RMN-iH (CDCla) δ: 2,52(3H,s), 2,59(1H,q,J=8,8Hz), 2,712,78(2H,m), 2,8 9-3, 00 (2H, m) , 3,03(3H,s), 3, 12 (1H, dd, J=17, 6,
5,4Hz), 3, 43(1H, dd,J=12,7,5,1Hz), 3,70(1H,d,J=15,2Hz), 3,77 (1H, d,J=15,2Hz), 3, 83(1H, dd,J=12,7,3,9Hz), 4,55-4,67(2H,m),
6,99(lH,s), 7,23(1H,dd,J=8,8,2,OHz), 7,33(1H,d,J=8,8Hz),
7, 65(lH,d,J=2,OHz), 8, 07(1H,d,J=5,1Hz), 8, 16(1H,d,J=5,4Hz),
9, 43(1H,s) .
MS (FAB) m/z: 501 (M+H+) .
Composto de alta polaridade:
Ponto de fusão: 183-195 °C (decomposto).
RMN-1H (DMSO-de) δ: 2,33(3H,s), 2,41-2,50 (1H, m) , 2,62-2,73 (3H, m), 2,75-2,81(lH,m), 2,82(3H,s), 3,21-3,32(2H,m), 3,343,50(2H,m), 3,55(1H,d,J=15,4Hz), 3,63(1H,d,J15,4Hz), 4,3020 4,40 (0, 5H,m) , 4,50—4, 60 (0, 5H, m) , 7,04(lH,s), 7,15 (1H, dd, J=
8,8, 2,OHz), 7,38(1H,d,J=8,8Hz), 7, 67(1H,d,J=2,OHz), 8,49 (1H, d, J=8, 5Hz) , 8, 71 (1H, d, J=8, 5Hz) , ll,74(lH,s).
MS (FAB) m/z: 501 (M+H+) .
Exemplo 185 cloridrato de 5-cloro-N-((IR*,2S*)-2-{[4-(piridin-4-il)benzoil]-amino}-ciclo-hexil)-indol-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 720/857
712
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 237, de uma maneira similar àquela do processo descrito no Exemplo 2.
RMN-XH (DMSO-de) δ: 1,40-1,52(2H,m), 1,60-1,80 (4H, m) , 1,962,10(2H,m), 4,24-4, 39 (2H,m) , 7, 15 (1H, dd, J=8, 8, 2,OHz), 7,21 (1H, s), 7,40(1H,d,J=8,8Hz), 7, 64(1H,d,J=2,OHz), 8,06(4H,s), 8,18(1H,J=7,3Hz), 8,34-8,42(3H,m), 8,94(2H,d,J=6,9Hz), 11,91 (1H,s) .
MS (FAB)m/z: 473(M+H)+.
Exemplo 186
N-óxido de 4-(4-{[ ( (IR*,2S*)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-ciclo-hexil)-amino]-carbonil}-fenil)piridina:
Cl
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 240, de uma maneira similar àquela do processo descrito no Exemplo 2.
Petição 870180138821, de 08/10/2018, pág. 721/857
713
RMN-1H (DMSO-de) δ: 1,40-1,52(2H,m), 1, 60-1,80 (4Η, m) , 1,882,00(2H,m), 4,21-4, 36 (2H,m) , 7, 12-7, 18 (2Η, m) , 7,41(lH,d,J=
8,6Hz), 7,66(lH,s), 7, 80-7, 87(4Η,m) , 7,91 (2Η, d, J=8,3Ηζ) ,
8,01(1Η,d,J=7,6Ηζ), 8, 09(1H,d,J=7,3Hz), 8,27(2H,d,J=6,6Hz), ll,79(lH,s).
MS (FAB) m/z: 489(M+H)+.
Exemplo 187 cloridrato de 5-cloro-N-((IR*,2S*)-2-{[4-(piridin-2-il)benzoil]-amino}-ciclo-hexil)-indol-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do ácido 4-(2piridil)-benzóico (pedido de patente japonesa publicado n° 2000-119253), de uma maneira similar àquela do processo descrito no Exemplo 2.
RMN-1H (DMSO-de) δ: 1,39-1, 51 (2H, m) , 1, 60-1,80 (4H, m) , 1,892,00(2H,m), 4,24-4,38 (2H,m) , 7,12-7,16(2H, m) , 7,36-7,39(1H,
m) , 7,42(1H,d,J=8,8Hz), 7,66(1H,d,J=2,0Hz), 7,87-7, 90(1H,m),
7,92(2H,d,J=8,3Hz), 7,98-8,11(3H,m), 8,15(2H,d,J=8,3Hz),
8,69(1H,d,J=4,6Hz), ll,80(lH,s).
MS (FAB) m/z: 473(M+H)+.
Exemplo 188
N-óxido de 2-(4-{[((IR*,2S*)-2-{[(5-cloro-indol-2-il)Petição 870180138821, de 08/10/2018, pág. 722/857
714 carbonil]-amino}-ciclo-hexil)-amino]-carbonil}-fenil)piridina:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 71 e do composto obtido no Exemplo Referencial 241, de uma maneira similar àquela do processo descrito no Exemplo 2.
RMN-iH (DMSO-de) δ: 1,39-1,51 (2H, m) , 1, 60-1,79 (4H, m) , 1,892,00(2H,m), 4,23-4,37(2H,m) , 7,12-7,17(2H,m) , 7,39-7,43(3H,
m) , 7, 61-7,64(lH,m), 7, 67(1H,d,J=2,OHz), 7,89(4H,s), 8,0010 8,06(lH,m), 8,08-8, 02 (1H, m) , 8, 32-8, 35 (1H, m) , ll,79(lH,s).
MS (FAB) m/z: 489(M+H)+.
Exemplo 189 cloridrato de 5-cloro-N-[(IR*,2R*)-2-({[5-(4-(piridin-2-il)tiazol-2-il]-carbonil}-amino)-indo1-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 69 e do 5—(4—
Petição 870180138821, de 08/10/2018, pág. 723/857
715 piridil)-tiazol-2-carboxilato de lítio (pedido de patente japonesa publicado n° 2000-143623), de uma maneira similar àquela do processo descrito no Exemplo 2.
ΗΜΝ-^ (DMSO-de) δ: 1,44 (2H, br, s) , 1, 65 (4H, br, s) , 1,85-2,06 (2H,m), 4,23 (lH,br, s) , 4,30 (1H, br, s) , 7, 14-7,23 (2H, m) , 7,41 (1H, d, J=8, 8Hz) , 7,69(lH,s), 8, 04-8, 13 (2H, m) , 8,13(lH,d,J=
8,8Hz), 8,59(lH,d, J=8,OHz) , 8, 75-8, 87 (3H, m) , 11, 83(lH,s).
MS (ESI)m/z: 480(M+H)+.
Exemplo 190 cloridrato de 5-cloro-N-[(IR*,2S*)-2-({[1-(piridin-4-il)piperidin-4-il]-carbonil}-amino)-ciclo-hexil]-indo1-2carboxamida:
Colocou-se o ácido 1-(4-piridil)-piperidino-4carboxílico (Tetrahedron 44:7095, 1998) (206 mg) em suspensão em cloreto de metileno (50 ml), e adicionou-se cloreto de tionila (144 μΐ) sob resfriamento com gelo, agitando a mistura por 30 min. Depois de adicionar trietilamina (969 μΐ) à mistura da reação, o composto obtido no Exemplo Referencial 71 (328 mg) foi adicionado, agitando a mistura à temperatura ambiente por 30 min. A mistura da reação foi concentrada sob pressão reduzida, adicionou-se água ao resíduo, a mistura foi concentrada sob pressão
Petição 870180138821, de 08/10/2018, pág. 724/857
716 reduzida, e o precipitado depositado foi coletado por filtração, para obter o composto do título (310 mg).
ΗΜΝ-^ (DMSO-de) δ: 1,30-2,00 (10H, m) , 2, 74 (1H, br, s) , 3, 18 (2H, q,J=12,3Hz), 4,03(lH,br,s), 4, 10-4,25(3H,m), 7,15-7,55(4H,
m), 7,42(1H,d,J=8,8Hz), 7,65(lH,s), 7,91(1H,d,J=8,8Hz),
8,20-8,35 (3H,m) , ll,91(lH,s), 13, 47 (1H, br, s) .
MS (FAB) m/z: 480(M+H)+.
Exemplo 191 cloridrato de N1-(4-cloro-fenil)-N2-((IS, 2R,4S)-4-[(dimetil10 amino)-carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo [5,4c]-piridin-2-il)-carbonil]-amino}-ciclo-hexil}-etanodiamida:
O composto obtido no Exemplo Referencial 242 (288 mg) foi dissolvido em tetraidrofurano (8,0 ml), adicionou-se sucessivamente hidróxido de lítio (46 mg) e água (1,0 ml), e a mistura foi agitada à temperatura ambiente por 2 h. A mistura da reação foi concentrada sob pressão reduzida, para obter um produto bruto (292 mg) de 2-(4-cloro-anilino)-2oxoacetato de lítio, como um sólido incolor. Este produto bruto e o composto obtido no Exemplo Referencial 253 foram dissolvidos em N,N-dimetil-formamida (15 ml), a adicionou-se
1-hidróxi-benzotriazol monoidratado (164 mg) e cloridrato de
Petição 870180138821, de 08/10/2018, pág. 725/857
717
1-(3-dimetil-amino-propil)-3-etil-carbodiimida (251 mg), agitando a mistura à temperatura ambiente por 64,5 h. O solvente foi removido por destilação sob pressão reduzida, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos, e a camada orgânica resultante foi secada sobre sulfato de sódio anidro. Depois de remover o solvente foi removido por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3). Os sólidos amarelo-pálidos assim obtidos foram dissolvidos em cloreto de metileno, adicionou-se uma solução 1 N (0,52 ml) de ácido clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se metanol e dietil-éter ao resíduo, e o precipitado formado foi coletado por filtração, para obter o composto do título (245 mg). RMN-!H (DMSO-de) δ: 1, 45-1, 55 (1H, m) , 1, 60-1, 80 (3H, m) , 1,952,10(2H,m), 2,79(3H,s), 2,80-3, 00 (1H, m) , 2,92(3H,s), 2,94 (3H,s), 3, 10-3,40(2H,m), 3, 40-3, 80(2H,m), 3, 95-4,05 (lH,m),
4,40-4,80(3H,m), 7,40(2H,d,J=8,8Hz), 7,83(2H,d,J=8,8Hz),
8,75(lH,d, J=7,lHz), 9, 00-9, 10 (1H, br) , 10,81(lH,s), 11,4511, 75 (lH,m) .
MS (FAB) m/z: 547(M+H)+.
Exemplo 192 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS, 2R,4S)-4[(dimetil-amino)-carbonil]-2-{ [ (5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil}-etanodiamida:
de 08/10/2018, pág. 726/857
718
O composto obtido no Exemplo Referencial 243 (240 mg) foi dissolvido em tetraidrofurano (8,0 ml), adicionou-se sucessivamente hidróxido de lítio (41 mg) e água (1,0 ml) à solução, e a mistura foi agitada à temperatura ambiente por 2,5 h. A mistura da reação foi concentrada sob pressão reduzida, para obter 2-[ (5-cloro-piridin-2-il)-amino]-2oxoacetato de lítio, como um sólido incolor (249 mg).
Por outro lado, adicionou-se 10% de paládio sobre carvão (200 mg) a uma solução do composto obtido no Exemplo Referencial 252 (293 mg) em metanol (10 ml) , e a mistura foi agitada à temperatura ambiente por 18 h sob uma atmosfera de hidrogênio. Depois de remover o paládio sobre carvão por filtração, o filtrado foi concentrado sob pressão reduzida, para obter um composto bruto (259 mg) de N-{ (IR,2S,5S)-2amino-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5-meti14,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida.
Este produto bruto (259 mg) e o sal de lítio (249 mg) preparado acima foram adicionados a N,N-dimetilformamida (15 ml), e adicionou-se 1-hidróxi-benzotriazol monoidratado (166 mg) e cloridrato de 1-(3-dimetil-aminopropil ) -3-et il-carbodiimida (235 mg), agitando a mistura à temperatura ambiente por 63,5 h. O solvente foi removido de 08/10/2018, pág. 727/857
719 sob pressão reduzida, o cromatografia de coluna por destilação sob pressão reduzida, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos, e a camada orgânica resultante foi secada sobre sulfato de sódio anidro. Depois de remover o solvente por destilação resíduo foi purificado por em sílica-gel (cloreto de metileno:metanol 93:7). Os sólidos amarelo-pálidos assim obtidos foram dissolvidos em cloreto de metileno, adicionouse uma solução 1 N (0, 885 ml) de ácido clorídrico em etanol à solução, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se metanol e dietil-éter ao resíduo, e o precipitado formado foi coletado por filtração, para obter o composto do título (209 mg).
RMN-1!! (DMSO-de) δ: 1, 40-1, 57 (1H, m) , 1, 60-1, 80 (3H, m) , 1,952,13(2H,m), 2,79(3H,s), 2,80-3, 00 (1H, m) , 2,92(3H,s), 2,94 (3H,s), 3,10-3,40(2H,m), 3,40-3,80(2H,m), 3,95-4,05(lH,m),
4,37-4,80(3H,m), 7,90-8,10(2H,m), 8, 45(1H,d,J=2,2Hz), 8,71 (lH,d, J=7, 6Hz) , 9, 10-9, 30 (1H,br) , 10,26(lH,s), 11,30-11,60 (lH,br) .
MS (FAB) m/z: 548(M+H)+.
Exemplo 193 cloridrato de N1-(3-cloro-fenil)-N2-((IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
de 08/10/2018, pág. 728/857
720

O composto obtido no Exemplo Referencial 270 (222 mg) e 3-cloro-anilina (63 μΐ) foram dissolvidos em N,Ndimetil-formamida (10 ml), e adicionou-se 1-hidróxibenzotriazol monoidratado (68 mg) e cloridrato de l—(3 — dimetil-amino-propil)-3-etil-carbodiimida (144 mg), agitando a mistura à temperatura ambiente por 40 h. O solvente foi removido por destilação sob pressão reduzida, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos, e a camada orgânica resultante foi secada sobre sulfato de sódio anidro. Depois de remover o solvente por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 30:1). Os sólidos amarelo-pálidos assim obtidos foram dissolvidos em cloreto de metileno, adicionouse uma solução 1 N (0,50 ml) de ácido clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se dietil-éter ao resíduo, e o precipitado formado foi coletado por filtração, para obter o composto do título (174 mg).
RMN-1!! (DMSO-de) δ: 1, 45-1, 62 (1H, m) , 1,65-1,90(3H,m), 1,982,20(2H,m), 2,79(3H,s), 2, 88-3, 10 (1H, m) , 2,93(3H,s), 2,94 de 08/10/2018, pág. 729/857
721 (3H,s), 3,15-3, 40(2H,m), 3,40-3,90(2H,m),
4,40-4,80(3H,m), 7,19(1H,dd,J=9,3, 2,OHz),
Hz), 7,77(1H,d,J=8,3Hz), 7,92-8,05(1H,m),
Hz), 8,95-9,20(1H,br), 10,87(lH,s), 11,25-11 Exemplo 194
3,95-4,10(lH,m) 7,37(1H,d,J=8, 8,75(1H,d,J=7, , 45 (lH,br) .
cloridrato de N1-((IS, 2R, 4S)-4-[(dimetil-amino)-carbonil]-2{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-ciclo-hexil)-N2-(4-flúor-fenil)etanodiamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 254, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-íH (DMSO-dg) δ: 1, 40-2, 13 (6H,m) , 2,77(3H,s), 2,93(3H,s), 2,97(3H,s), 3,12-3,82(7H,m) , 3, 93-4, 04(1H, m) , 4,38-4,46(1H,
m) , 4,35-4,75(lH,m) , 7,11-7,21(2H,m), 7, 72-7,84 (2H,m), 8,73 (lH,d, J=7, 6Hz) , 8, 93-9, 02 (lH,m) , 10,70(lH,s).
MS (FAB) m/z: 531(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 730/857
722
Exemplo 195 cloridrato de N1-(4-bromo-fenil)-N2-((IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4c]-piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:

O composto obtido no Exemplo Referencial 255 (152 mg) foi dissolvido em tetraidrofurano (5,0 ml), adicionou-se sucessivamente uma solução aquosa (1,20 ml) 1 N de hidróxido de sódio e metanol (5,0 ml), e a mistura foi agitada à temperatura ambiente por 2,5 h. A mistura da reação foi concentrada sob pressão reduzida, adicionou-se cloreto de metileno (10 ml) e ácido clorídrico 1 N (2,0 ml) ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, e o solvente foi removido por destilação sob pressão reduzida, para obter um produto bruto (280 mg) de ácido 2-(4-bromoanilino)-2-oxoacético, como um sólido incolor. Este produto bruto e o composto obtido no Exemplo Referencial 253 (280 mg) foram dissolvidos em N,N-dimetil-formamida (30 ml), e adicionou-se 1-hidróxi-benzotriazol monoidratado (90 mg) e cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (226 mg), agitando a mistura à temperatura ambiente por uma de 08/10/2018, pág. 731/857
723 noite. O solvente foi removido por destilação sob pressão reduzida, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos, e a camada orgânica resultante foi secada sobre sulfato de sódio anidro. Depois de remover o solvente por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 97:3). Os sólidos amarelo-pálidos assim obtidos foram dissolvidos em cloreto de metileno, adicionou-se uma solução 1 N (191 μΐ) de ácido clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se metanol e dietil-éter ao resíduo, e o precipitado formado foi coletado por filtração, para obter o composto do título (103 mg). RMN-1H (DMSO-de) δ: 1, 43-1, 57 (1H, m) , 1, 59-1, 80 (3H, m) , 1,972,10(2H,m), 2,79(3H,s), 2,84-2, 98 (7H, m) , 3, 18 (2H, br, s) , 3,39 —3,72(2H,m), 3, 95-4,05 (1H, m) , 4,20-4,80 (3H,m) , 7,53(2H,d,J=
8,8Hz), 7,77(2H,d,J=8,8Hz), 8,75(1H,d,J=7,3Hz) , 8,97-9,09 (lH,m), 10,82(lH,s), 11, 11 (1H, br, s) .
MS (FAB) m/z: 591(M+H)+.
Exemplo 196 cloridrato de N1-(4-cloro-2-metil-fenil)-N2-((IS, 2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5, 4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
de 08/10/2018, pág. 732/857
724
composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 256, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
ΗΜΝ-^ (DMSO-de) δ: 1, 45-1,55 (1H, m) , 1, 60-1,80 (3H, m) , 2,002,10(2H,m), 2,19(3H,s), 2,79(3H,s), 2,80-3, 00 (7H, m) , 3,31 (2H,br,s), 3, 40-3, 70(2H,br) , 3, 95-4, 05(1H, m) , 4,35-4,70(3H,
m) , 7, 20-7, 30 (ΙΗ,πι) , 7,35 (1H, d, J=2,5Hz ) , 7 , 43 (1H, d, J=8, 6Hz) ,
8,76 (lH,d, J=6, 6Hz) , 9, 00-9, 15 (1H, br) , 10,19(lH,s).
MS (FAB) m/z: 561(M+H)+.
Exemplo 197 cloridrato de N1-(4-cloro-3-metil-fenil)-N2-((IS,2R,4S)-415 [(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 733/857
725 composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 257, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-1H (DMSO-de) δ: 1, 47-1,53 (1H,m) , 1, 68-1, 80 (3H,m) , 1,982,09(2H,m), 2,29(3H,s), 2,79(3H,s), 2,80-3, 00 (1H, m) , 2,95 (6H,s), 3,17-3,19 (3H,m), 3, 40-3, 80(1H,m), 3, 93-4,02(1H,m),
4,44-4,56(3H,m), 7,38(1H,d,J=8,8Hz), 7,65(1H,d,J=8,8Hz),
7,74(lH,s), 8,75(1H,d,J=7,8Hz), 8,96(1H,d,J=8,OHz), 10,69 (1H,S) .
MS (FAB) m/z: 561(M+H)+.
Exemplo 198 cloridrato de N1-(4-cloro-2-flúor-fenil)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5, 4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto do título foi obtido hidrolisando o 20 composto obtido no Exemplo Referencial 258, condensando o hidrolisado com o composto obtido no Exemplo Referencial
Petição 870180138821, de 08/10/2018, pág. 734/857
726
253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-1H (DMSO-de) δ: 1, 40-1,55 (1H, m) , 1,58-1,80 (3H, m) , 1,955 2,12(2H,m), 2,77(3H,s), 2, 80-3, 00 (1H, m) , 2,91(3H,s), 2,92 (3H,s), 3,10-3,40(2H,m), 3,40-3,80(2H,m), 3,95-4,05(1H,m),
4,30-4,80(3H,m), 7,29(1H,d,J=8,5Hz), 7,52(1H,dd,J=10,3, 2,0
Hz), 7,61(1H,t,J=8,4Hz), 8,72(1H,d,J=6,8Hz), 9,00-9,20 (1H, br), 10,38(lH,s), 11,20-11,45 (1H, br) .
MS (FAB) m/z: 565(M+H)+.
Exemplo 199 cloridrato de N1-(2,4-dicloro-fenil)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}15 ciclo-hexil)-etanodiamida:
O composto obtido no Exemplo Referencial 270 (300 mg) foi dissolvido em N,N-dimetil-formamida (5 ml), e adicionou-se 2,4-dicloro-anilina (165 mg), cloridrato de 1(3-dimetil-amino-propil)-3-etil-carbodiimida (260 mg) e 120 hidróxi-benzotriazol monoidratado (91 mg), agitando a mistura à temperatura ambiente por 2 dias. O solvente foi
Petição 870180138821, de 08/10/2018, pág. 735/857
727 removido por destilação sob pressão reduzida, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos, e a camada orgânica resultante foi secada sobre sulfato de sódio anidro. Depois de remover o solvente por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3), para obter uma base livre cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (140 mg) e 1-hidróxi-benzotriazol monoidratado (110 mg) foram adicionados, agitando a mistura à temperatura ambiente por 18 h. O solvente foi removido por destilação, o resíduo foi fracionado entre água e acetato de etila, e uma camada aquosa foi extraída com acetato de etila. As camadas orgânicas resultantes foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio e depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:19), e o solvente foi removido por destilação sob pressão reduzida. Uma pequena quantidade de metanol foi adicionada ao resíduo, e adicionou-se dietil-éter em gotas, enquanto se irradiava com ondas de ultra-som, para coletar o precipitado formado por filtração. Este produto foi lavado com dietil-éter, para obter o composto do título (60 mg). RMN-XH (DMSO-de) δ: 1, 45-1, 77 (4H, m) , 2,03-2,12 (2H, m) , 2,79 (3H,s), 2, 92-2, 96 (7H,m) , 3, 25 (2H, br, s) , 3, 49 (1H, br, s) , 3,69 (lH,br,s), 3, 98-4,04 (lH,m) , 4,40-4,43 (lH,m) , 4,45(lH,br, s), de 08/10/2018, pág. 736/857
728
4,69(1Η,br,s), 7,48(1H,dd,J=8,5, 2,4Hz), 7,75(1H,d,J=2,4Hz),
7,89(1H,d,J=8,5Hz), 8,75(1H,d,J=6,8Hz), 9,21(1H,br,s), 10,25 (lH,s), 11,55(1H,br,s).
MS (FAB) m/z: 581(M+H)+.
Exemplo 200
N1-(3,4-dicloro-fenil)-N2-((IS, 2R, 4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
|
agitada à |
temperatura , |
amk |
|
e cloreto |
de |
metileno |
à |
|
separação |
de |
líquidos |
• |
|
extraída |
com |
cloreto |
de |
Dissolveu-se 3,4-dicloro-anilina (1,62 g) em cloreto de metileno (20 ml) , e adicionou-se sucessivamente trietil-amina (1,67 ml) e cloro-oxoacetato de metila (1,01 ml) sob resfriamento com gelo, e a mistura resultante foi ente por 21 h. Adicionou-se água mistura da reação, para conduzir A camada aquosa resultante foi metileno. As camadas orgânicas foram combinadas e secadas sobre sulfato de magnésio anidro, e o solvente foi removido por destilação sob pressão reduzida. O resíduo resultante foi dissolvido em etanol (50 ml) , e adicionou-se sucessivamente água (25 ml) e hidróxido de lítio monoidratado (629 mg), agitando a mistura à de 08/10/2018, pág. 737/857
729 temperatura ambiente por 12,5 h. Adicionou-se mais hidróxido de lítio monoidratado (629 mg), agitando a mistura à temperatura ambiente por 5,5 h. A mistura foi concentrada sob pressão reduzida, para solidificar. Adicionou-se água e dietil-éter ao resíduo, para conduzir separação de líquidos. Adicionou-se ácido clorídrico à camada aquosa resultante, para acidificá-la. Os sólidos formados foram coletados por filtração, para obter um produto bruto (1,62 g) de ácido 2(3,4-dicloro-anilino)-2-oxoacético, como um sólido incolor. Este produto bruto (191 mg) e o composto obtido no Exemplo Referencial 253 foram dissolvidos em N,N-dimetil-formamida (10 ml) , e adicionou-se 1-hidróxi-benzotriazol monoidratado (110 mg) e cloridrato de 1-(3-dimetil-amino-propil)-3-etilcarbodiimida (157 mg) , agitando a mistura à temperatura ambiente por 67 h. O solvente foi removido por destilação sob pressão reduzida, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e acetato de etila ao resíduo, para conduzir separação de líquidos, e a camada aquosa resultante foi extraída 3 vezes com cloreto de metileno. As camadas orgânicas foram combinadas e secadas sobre sulfato de sódio anidro. Depois de remover o solvente por destilação sob pressão reduzida, o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 95:5), para obter o composto do título (154 mg).
RMN-!H (CDCls) δ: 1, 77-1, 88 (1H, m) , 1, 91-1, 95 (1H, m) , 2,05-2,10 (3H,m), 2,51(3H,s), 2,77-2, 99 (6H,m) , 2,95(3H,s), 3,05(3H,s),
3,68(1H,d,J=15,5Hz), 3,74(1H,d,J=15,5Hz), 4,08-4,13(1H,m), de 08/10/2018, pág. 738/857
730
4,69—4,72 (1Η, m) , 7,40(2H,s), 7, 41(1Η,d,J=7,7Ηζ), 7,90(lH,s),
8,01(1H,d,J=7,7Hz), 9,27(lH,s).
MS (ESI) m/z: 581(M+H)+.
Exemplo 201
N1-(2,4-diflúor-fenil)-N2-((IS, 2R, 4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 259 e condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-1!! (CDC13) δ: 1,55-1, 62 (1H, m) , 1, 67-1,98 (2H, m) , 2,01-2,18 (4H,m), 2,52(3H,s), 2,77-3,00(4H,m), 2,95(3H,s),2,99(3H,s),
3,65-3,78(2H,m), 4,06-4,15(lH,m), 4,66-4,73(1H,m), 6,85-6,94 (2H,m), 7,38(1H,d,J=8,5Hz), 7,96(1H,d,J=7,3Hz), 8,22-8,29 (lH,m) , 9, 36 (lH,br) .
Exemplo 202
N1-(3,4-diflúor-fenil)-N2-((IS, 2R, 4S)-4-[(dimetil-amino)20 carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 739/857
731
composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 260 e condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, de uma maneira similar àquela do processo descrito no
Exemplo 191.
RMN-!H (CDC13) δ: 1,56-1,73 (1H, m) , 1,77-1,99 (2H, m) , 2,00-2,18 (4H,m), 2,52(3H,s), 2,75-3, 00 (4H, m) , 2,95(3H,s), 3,06(3H,s),
3, 64-3, 79(2H,m) , 4,05-4,14(1H,m) , 4, 68-4,75(1H,m) , 7,097,21(2H,m), 7,38 (1H, d, J=8, 8Hz) , 7,72 (1H, ddd, J=12, 0, 7,1, 2,6
Hz), 7, 95 (1H, d, J=7,8Hz) , 9,22(lH,br).
Exemplo 203
N1-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-N2-(piridin-4-il)-etanodiamida:
O composto do título foi obtido hidrolisando o
Petição 870180138821, de 08/10/2018, pág. 740/857
732 composto obtido no Exemplo Referencial 261, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-1H (DMSO-de) δ: 1,40-2,10(6H,m), 2,77(3H,s), 2, 927(3H,s), 2, 933 (3H,s), 3, 05-4,20 (8H,m), 4,40-4,55 (1H, m) , 8,27 (2H,d, J=6,8Hz), 8,67(1H,d,J=8,0Hz), 8,71(2H,d,J=6,8Hz), 9,10-9,30 (lH,br) , 11,81 (1H, s) .
MS (FAB) m/z: 514(M+H)+.
Exemplo 204 cloridrato de N1-(5-bromo-piridin-2-il)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5, 4-c]-piridin-2-il)-carbonil]-amino}15 ciclo-hexil)-etanodiamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 262, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 195.
Petição 870180138821, de 08/10/2018, pág. 741/857
733
EMN-iH (DMSO-de) δ: 1, 43-1,57 (1Η, m) , 1, 61-1,81 (3H, m) , 1,982,15(2H,m), 2,79(3H,s), 2,86(3H,s), 2,89-3, 01 (4H, m) , 3, 18 (2H, br,s), 3,50 (2H,br,s), 3,95—4,05 (lH,m), 4,35—4, 62 (3H,m),
7,97(lH,d,J=9,OHz), 8, 12(1H,dd,J=9,0,2,4Hz), 8,52(1H,d,J=2,
4Hz), 8,70(1H,d,J=7,5Hz), 9,18(1H,d,J=7,5Hz), 10,25 (lH,br,
s) .
MS (FAB) m/z: 592(M+H)+.
Exemplo 205 cloridrato de N1-(6-cloro-piridin-3-il)-N2-((IS,2R,4S)-410 [(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto obtido no Exemplo Referencial 263 (200 mg), que era um produto bruto, foi dissolvido em metanol (10 ml) , aquecendo a solução até 50 °C, e adicionou-se uma solução aquosa 1 N (3 ml) de hidróxido de sódio, agitando a mistura por 5 min. A esta mistura adicionou-se ácido clorídrico 1 N, para ajustar o pH até uma acidez fraca. O solvente foi removido por destilação sob pressão reduzida, para obter um resíduo que continha ácido 2-[(2-cloropiridin-5-il)-amino]-oxoacético. Este resíduo e o composto
Petição 870180138821, de 08/10/2018, pág. 742/857
734 obtido no Exemplo Referencial 253 (250 mg) foram dissolvidos em N,N-dimetil-formamida (5 ml), e adicionou-se cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (328 mg) e 1-hidróxi-benzotriazol monoidratado (46 mg) , agitando a mistura à temperatura ambiente por 3 dias. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 47:3), para obter uma base livre do composto do título, como um sólido amarelo-pálido. Este produto foi dissolvido em cloreto de metileno, adicionou-se uma solução 1 N (862 μΐ) de ácido clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Uma pequena quantidade de metanol foi adicionada ao resíduo, e adicionou-se acetato de etila e dietil-éter em gotas, enquanto se irradiava com ondas de ultra-som, para coletar o precipitado formado por filtração. Este produto foi lavado com dietil-éter, para obter o composto do título (229 mg). RMN-!H (DMSO-de) δ: 1, 46-1, 75 (4H, m) , 1, 99-2,09 (2H, m) , 2,79 (3H,s), 2,92-2,95(7H,m), 3,12-3,53(3H,m),3,70(1H,br,s), 3,99 —4,06(lH,m), 4,44 (2H, br, s) , 4, 69, 4,73 (1H, cada s) , 7,53(1H, d,J=8,5Hz), 8, 23-8, 25 (lH,m) , 8, 72-8, 77 (lH,m) , 8,85(lH,s),
9,07, 9,16(lH,cada d,J=8,lHz), 11, 09 (1H, d, J=8,1Hz) , 11,78 (1H, br, s) .
de 08/10/2018, pág. 743/857
735
MS (FAB) m/z: 548(M+H)+.
Exemplo 206 cloridrato de N1-(6-cloro-piridazin-3-il)-N2-((IS, 2R, 4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,75 tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 264, condensando o hidrolisado com o composto obtido no Exemplo Referencial
253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
EMN-^ (DMSO-de) δ: 1, 44-1, 57 (1H, m) , 1, 62-1,80 (3H, m) , 2,002,10(2H,m), 2,79(3H,s), 2,86 (3H, br, s) , 2,94(3H,s), 2,95-10
3,01(lH,m), 3, 14-3, 23 (2H, m) , 3, 45-3, 63 (2H, m) , 3, 96-4,08 (1H,
m) , 4,40-4, 60 (3H,m), 7,97(1H,d,J=9,3Hz), 8,26(1H, d, J=9, 3Hz) , 8,69(1H,d,J=7,6Hz), 9,20(1H,d,J=7,6Hz), ll,06(lH,s).
MS (FAB) m/z: 549(M+H)+.
Exemplo 207 cloridrato de N1-(5-cloro-tiazol-2-il)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7Pclição 870180138821, de 08/10/2018, pág. 744/857
736 tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil ) -etanodiamida:
composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 265, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-!H (DMSO-dg) δ: 1, 35-2, 10 (6H, m) , 2,77(3H,s), 2,92(3H,s),
2, 93(3H,s), 3, 05-4,23 (8H,m), 4,32-4,80 (2H,m), 7,59 (lH,s),
8, 63(1H, d,J=7,6Hz), 9, 14(1H,d,J=7,6Hz) .
MS (FAB) m/z: 554(M+H)+.
Exemplo 208 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-415 [(dimetil-amino)-carbonil]-2-{[(5-metil-5,6-diidro-4Hpirrolo[3, 4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil)etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 745/857
737
O composto obtido no Exemplo Referencial 266 (210 mg) e o composto obtido no Exemplo Referencial 272 (350 mg) foram dissolvidos em N,N-dimetil-formamida (15 ml), e adicionou-se 1-hidróxi-benzotriazol monoidratado (205 mg) e cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (290 mg) , agitando a mistura à temperatura ambiente por 20 h. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio e acetato de etila ao resíduo, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro, o solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1). Os sólidos amarelo-pálidos assim obtidos foram dissolvidos em cloreto de metileno, adicionou-se uma solução 1 N (0,46 ml) de ácido clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se metanol e dietil-éter ao resíduo, e o precipitado formado foi coletado por filtração, para obter o composto do título (248 mg). RMN-1!! (DMSO-de) δ: 1, 47-1, 50 (1H, m) , 1, 69-1, 7 6 (3H, m) , 1,982,06(2H,m), 2,79(3H,s), 2,95(3H,s), 2, 98-3, 05 (lH,m) , 3,10 (3H,s), 3, 49-4, 62 (6H,m) , 7, 98-8, 03 (2H,m) , 8,45(lH,s), 8,73 (1H, d, J=7, 6Hz) , 9, 10 (1H, d, J=8,OHz) , 10,30(lH,s).
MS (FAB) m/z: 534(M+H)+.
Exemplo 209 cloridrato de N-{(IR,2S,5S)-2-{[2-(4-cloro-anilino)-acetil]amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil}-5-metilde 08/10/2018, pág. 746/857
738
4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto obtido no Exemplo Referencial 267 (2,3
g) foi dissolvido em etanol (10 ml), e adicionou-se uma solução aquosa 1 N (20 ml) de hidróxido de sódio, agitando a mistura à temperatura ambiente por 2 h. Depois de adicionar ácido clorídrico 1 N (20 ml) à mistura da reação, a mistura foi diluída com água e agitada por 30 min. Os insolúveis depositados foram coletados por filtração, para obter o ácido 2-(4-cloro-anilino)-acético (1,05 g) , como um sólido incolor. Este sólido e o composto obtido no Exemplo Referencial 253 (0,25 g) foram dissolvidos em N,N-dimetilformamida (10 ml), e adicionou-se 1-hidróxi-benzotriazol monoidratado (0,11 g) e cloridrato de 1-(3-dimetil-aminopropil ) -3-etil-carbodiimida (0,23 g) , agitando a mistura à temperatura ambiente por 4 dias. Depois que a mistura da reação foi diluída com clorofórmio e lavada com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada cloreto de sódio, a camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel de 08/10/2018, pág. 747/857
739 (clorofórmio:metanol 97:3). 0 sólido amarelo-pálido assim obtido foi dissolvido em etanol, adicionou-se uma solução 1 N de ácido clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se metanol e dietil-éter ao resíduo, e o precipitado formado foi coletado por filtração, para obter o composto do título (0,15 g). ΗΜΝ-^ (DMSO-de) δ: 1,35-1,41 (lH,m) , 1,59-1,80 (3H, m) , 1,82I, 95(2H,nB, 2,76(3H,s), 2,93(3H,s), 2,94(3H,s), 2,99-3,10 (lH,m), 3, 10-3, 22 (2H,m) , 3, 42-3, 60 (2H, m) , 3, 60-15 3, 77(2H,
m) , 3, 80-3, 90(lH,m) , 4,35-4,48(2H,m), 4, 68-4,80(1H,m), 6,40 (1H,d,J=6,7Hz), 6,44(1H,d,J=6,7Hz),6,90 (1H,d,J=6,7Hz), 7,00 (lH,d,J=6,7Hz), 7, 70-7, 89 (lH,m), 8,35-8,42(11-{,m), 11,05II, 38 (lH,m) .
Exemplo 210 cloridrato de N-{ (IR, 2S,5S)-2-{[2-(4-cloro-2-flúor-anilino) acetil]-amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil} - 5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 268, condensando o hidrolisado com o composto obtido no Exemplo Referencial
253, e depois tratando o produto da condensação com ácido
Petição 870180138821, de 08/10/2018, pág. 748/857
740 clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 209.
RMN-1H (DMSO-de) δ: 1,35-1, 42 (1H, m) , 1, 55-1,78 (3H, m) , 1,802,00(2H,m), 2,76(3H,s), 2,92(3H,s), 2,94(3H,s), 2,99-3,10 (lH,m), 3,10-3,22(2H,m), 3,42-3,60(2H,m), 3,60-3,77(2H,m),
3,85-4,00(lH,m), 4,33-4,48(2H,m), 4,65-4,80(1H,m), 6,41(1H, t,J=8,8Hz), 6,73(1H,dt,J=8,8, 1,2Hz), 7,08(1H,dd,J=ll,7, 1,2
Hz), 7,78-7,92(lH,m), 8,35-8,42(1H,m), 11,18-11,50(1H, m). Exemplo 211 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil}4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 432 com o composto obtido no Exemplo Referencial 34, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 2.
RMN-iH (DMSO-dg) δ : 1,45-1, 60 (1H, m) , 1, 7 0-2, 15 (6H, m) , 2,80 (3H,s), 2,97(3H,s), 2, 95—3, 15 (2H, m) , 3, 35—3, 55 (2H, m) , 4,05—
4,20(lH,m), 4,46(2H,s), 4,50-4,65 (1H, m) , 7,05(lH,s), 7,16 (1H,dd,J=8,8, 2,2Hz), 7,41(1H,d,J=8, 8Hz) , 7,68(lH,s), 8,30Pclição 870180138821, de 08/10/2018, pág. 749/857
741
8,45(lH,br), 9, 30-9, 50 (1H, br) , ll,78(lH,s).
MS (ESI) m/z: 529(M+H)+.
Exemplo 212
N-{(lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-55 [(dimetil-amino)carbonil]-ciclo-hexil}-5-(4,5-diidro-oxazol2-il)-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto obtido no Exemplo 211 (250 mg) foi colocado em suspensão em cloreto de metileno, e adicionou-se uma solução aquosa de bicarbonato de sódio, agitando a mistura intensamente. A camada orgânica resultante foi separada e secada sobre sulfato de sódio anidro. Adicionouse então trietil-amina (0,5 ml) e isocianato de bromo-etila (43 μΐ), agitando a mistura à temperatura ambiente por 20 h. Adicionou-se uma solução aquosa saturada de bicarbonato de sódio, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 22:3), para obter o composto do título (227 mg).
RMN-iH (CDC13) δ: 1,50-2, 15 (4H, m) , 2, 15-2, 40 (2H, m) , 2,80-3,00
Petição 870180138821, de 08/10/2018, pág. 750/857
742 (lH,m), 2,97(3H,s), 3,ll(3H,s), 3, 70-3, 95 (4H, m) , 4,10-4,30 (lH,m), 4,30-4,50 (2H,m) , 4, 60-4,70 (lH,m) , 4,74(2H,s), 6,85 (lH,s), 7,21 (lH,dd, J=8, 8, 2,2Hz), 7,34(1H,d,J=8,8Hz), 7,50 (lH,br,s), 7,62(lH,s), 7,87 (1H, br, s) , 9, 48 (1H, br, s) .
MS (531) m/z: 598(M+H)+.
Exemplo 213 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-4-flúor-indol-2il)-carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclohexil } -5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-210 carboxamida:
O composto obtido no Exemplo 144 (140 mg) foi dissolvido em N,N-dimetil-formamida (10 ml), e o composto obtido no Exemplo Referencial 274 (100 mg), cloridrato de 1(3-dimetil-amino-propil)-3-etil-carbodiimida (140 mg) e 115 hidróxi-benzotriazol monoidratado (110 mg) foram adicionados, agitando a mistura à temperatura ambiente por 18 h. O solvente foi removido por destilação sob pressão reduzida, o resíduo foi fracionado entre água e acetato de etila, e uma camada aquosa foi extraída com acetato de etila. As camadas orgânicas resultantes foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio e
Petição 870180138821, de 08/10/2018, pág. 751/857
743 depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:19), dando (IR,2S,5S)-2-{[(5-cloro-4-flúor-indol-2-il)-carbonil]amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil-carbamato de t-butila (260 mg).
O pó assim obtido foi dissolvido em cloreto de metileno (5 ml), adicionou-se uma solução 4 N (1,2 ml) de ácido clorídrico em dioxano. Depois de agitar a mistura da reação à temperatura ambiente por 3,5 h, o solvente foi removido por destilação sob pressão reduzida. Adicionou-se cloreto de metileno (10 ml) ao resíduo, e a mistura foi concentrada. Depois de repetir este processo 3 vezes, o resíduo foi secado sob pressão reduzida, para obter N{(IS,2R,5S)-2-amino-4-[(dimetil-amino)-carbonil]-ciclohexil }-5-cloro-4-flúor-indol-2-carboxamida bruta. Este produto foi dissolvido em N,N-dimetil-formamida (50 ml), e adicionou-se o composto obtido no Exemplo Referencial 10 (150 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etilcarbodiimida (140 mg) e 1-hidróxi-benzotriazol monoidratado (110 mg) , agitando a mistura à temperatura ambiente por 18 h. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi fracionado em um solvente misto de água/acetato de etila/tetraidrofurano, e uma camada aquosa foi extraída com acetato de etila. As camadas orgânicas resultantes foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio e depois secadas sobre sulfato de 08/10/2018, pág. 752/857
744 de sódio anidro. 0 solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:19), para obter uma base livre (270 mg) do composto do título. Este produto foi dissolvido em cloreto de metileno (10 ml), e adicionou-se uma solução 1 N (0,72 ml) de ácido clorídrico em etanol, agitando a mistura à temperatura ambiente por 30 min. Os cristais depositados foram coletados por filtração, para obter o composto do título (200 mg).
RMN-XH (DMSO-de) δ: 1,24-1,98(6H,m), 2, 33-3,33 (6H, m) , 2,81 (3H,s), 2,90(3H,s), 2,99(3H,s), 4, 12 (1H, br, s) , 4,30-4,70 (lH,m), 4,60 (lH,br, s) , 7,21(lH,s), 7,27 (2H, br, s) , 8,37(1H, d,J=8,lHz), 8,43 (1H, d, J=7, 6HZ) , 12,ll(lH,s).
MS (FAB) m/z: 561(M+H)+.
Exemplo 214 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-3-flúor-indol-2il)-carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclohexil }-5-meti1-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-220 carboxamida:
O composto obtido no Exemplo 279 (250 mg) foi
Petição 870180138821, de 08/10/2018, pág. 753/857
745 dissolvido em cloreto de metileno (60 ml), e adicionou-se uma solução 4 N (1,3 ml) de ácido clorídrico em dioxano. Depois de agitar a mistura da reação à temperatura ambiente por 5,5 h, adicionou-se mais solução 4 N (0,65 ml) de ácido clorídrico em dioxano, e a mistura foi agitada à temperatura ambiente por 1 h. O solvente foi removido por destilação sob pressão reduzida, adicionou-se cloreto de metileno (10 ml) ao resíduo, e a mistura foi concentrada. Este processo foi repetido 3 vezes. O resíduo foi secado sob pressão reduzida, o produto bruto assim obtido foi dissolvido em N,N-dimetil-formamida (50 ml), e adicionou-se o composto obtido no Exemplo Referencial 10 (160 mg), cloridrato de 1(3-dimetil-amino-propil)-3-etil-carbodiimida (150 mg) e 1hidróxi-benzotriazol monoidratado (120 mg) , agitando a mistura à temperatura ambiente por 18 h. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi fracionado em um solvente misto de água/acetato de etila, e uma camada aquosa foi extraída com acetato de etila. As camadas orgânicas resultantes foram combinadas, lavadas com solução aquosa saturada de cloreto de sódio e depois secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado duas vezes por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 2:23 —» 1:9), para obter uma base livre (260 mg) do composto do título. Este produto foi dissolvido em cloreto de metileno, e adicionou-se uma solução 1 N (0,69 ml) de ácido clorídrico em etanol, agitando a mistura à temperatura ambiente por 30 de 08/10/2018, pág. 754/857
746 min. 0 solvente foi removido por destilação. 0 resíduo foi dissolvido em metanol, e adicionou-se dietil-éter e hexano.
Os cristais assim obtidos depositados foram coletados por filtração, para obter o composto do título (230 mg).
RMN-XH (DMSO-de) δ: 1,50-1,56 (1H, m) , 1, 73-1,78 (3H, m) , 1,942,02(2H,m), 2, 33-3, 55 (6H, m) , 2,80(3H,s), 2,92(3H,s), 2,98 (3H,s), 4,17(lH,br,s), 4,30-4,80(1H,br), 4,62(1H,br,s), 7,25 (lH,d,J=8,8, 1,7Hz), 7,40 (1H, d, J=8,8, 1,7Hz), 7,65(lH,d,
J=l,7Hz), 7,72(1H,d,J=5, 9Hz) , 8,74(1H,d,J=8, OHz) , 10,8510 11,35(1H, br), ll,71(lH,s).
MS (FAB) m/z: 561(M+H)+.
Exemplo 215 cloridrato de N-{(IR,2S,5S)-2-{[(3-bromo-5-cloro-indol-2il)-carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclo15 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 282 com uma solução 4 N de ácido clorídrico em dioxano, e condensando o composto assim tratado com o composto obtido no Exemplo Referencial
Petição 870180138821, de 08/10/2018, pág. 755/857
747
10, de uma maneira similar àquela do processo descrito no Exemplo 214.
EMN-iH (DMSO-de) δ: 1,51-2,01 (6H, m) , 2, 33-3,29 (7H, m) , 2,81 (3H,s), 2,88(3H,s), 3,01(3H,s), 4,20 (1H, br, s) , 4,48(lH,br),
4,70-4,73 (lH,m), 7, 29(1H, dd, J=8, 9, 1,8Hz), 7,45-7,49(2H,m),
7,80(1H,d,J=7,6Hz), 8,76(1H,d,J=8,8Hz), 12,31(lH,s).
MS (FAB) m/z: 622(M+H)+.
Exemplo 216 cloridrato de N-{(IR,2S,5S)-2-{[(3-cloro-5-flúor-indol-2il)-carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclohexil }-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 253 e do composto obtido no Exemplo Referencial 284, de uma maneira similar àquela do processo descrito no Exemplo 5.
RMN-1!! (DMSO-dg) δ: 1, 40-1,51 (1H, m) , 1,75-2,00 (5H, m) , 2,79 (3H,s), 2,92(3H,s), 2,99(3H,s), 3, 10-3,21 (3H, m) , 3,29-3,41 (4H,m), 4,11-4,21(lH,m), 4,62-4,75(1H,m), 7, 14(1H,dt,J=8,8,
2,4Hz), 7,24(1H,dd,J=8,8, 2,4Hz), 7,45(1H,dd,J=8,8, 4,4Hz),
7,69(1H,d,J=2,5Hz), 8,79(1H,d,J=2,5Hz), 12,10(lH,s).
Petição 870180138821, de 08/10/2018, pág. 756/857
748
MS (FAB) m/z: 561(M+H)+.
Exemplo 217 cloridrato de N-{(IR,2S,5S)-2-{[(3-cloro-3-formil-indol-2il)-carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclo5 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 253 e do composto obtido no Exemplo Referencial 286, de uma maneira similar àquela do processo descrito no Exemplo 5.
RMN-1H (DMSO-de) δ: 1, 40-1, 51 (1H, m) , 1,75-1,89(4H,m), 1,902,01(lH,m), 2,80(3H,s), 2,91(3H,s), 3,03(3H,s), 3,05-3,33 (3H,m), 3, 60-3,71(lH,m), 4,11-4,21(1H,m), 4,32-4,44 (1H, m) ,
4,62-4,75 (2H,m) , 7, 35 (1H, dd, J=8, 0, 1,4Hz) , 7,56 (lH,d,J=8,0
Hz), 8,21 (1H, d, J=l, 4Hz) , 8, 65 (1H, t, J=7,4Hz) , 9,92 (lH,d,J=
6,5Hz), 10,15(1H,t,J=9,1Hz), 13,00(1H,dt,J=6,4Hz).
MS (FAB) m/z: 571(M+H)+.
Exemplo 218 cloridrato de 5-cloro-N2-{ (IS,2R,4S)-4-[(dimetil-amino) carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c] piridin-2-il) -carbonil ] -amino} -ciclo-hexil-N3, N3-dimet ilPclição 870180138821, de 08/10/2018, pág. 757/857
749 indol-2,3-dicarboxamida:
composto do título foi obtido a partir do composto obtido no Exemplo Referencial 253 e do composto obtido no Exemplo Referencial 289, de uma maneira similar àquela do processo descrito no Exemplo 5.
RMN-1H (DMSO-de) δ: 1, 40-1,51 (1H,m) , 1,75-2, 01 (5H,m) , 2,78 (9H,s), 2,93(3H,s), 3,01(3H,s), 3, 10-3, 33 (3H, m) , 3,40-3,50 (lH,m), 3, 65-3,75 (lH,m), 4,01-4,09(1H,m), 4,32-4,44(1H,m),
4,62-4,75 (2H,m), 7, 25(1H, d, J=8,OHz), 7,40-107,50 (2H,m), 8,62 (lH,br), 9,08(lH,br), 12,28 (1H, br) .
MS (FAB) m/z: 614(N+H)+.
Exemplo 219 cloridrato de N-{ (IR, 2S,5S)-2-[(6-cloro-2-naftoil)-amino]-5[(dimetil-amino)carbonil]-ciclo-hexil}-5-metil-4,5,6,715 tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 758/857
750
O composto obtido no Exemplo Referencial 294 (270 mg) foi dissolvido em cloreto de metileno (10 ml), e adicionou-se uma solução 1 N (10 ml) de ácido clorídrico em etanol, agitando a mistura por 90 min. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi dissolvido em N,N-dimetil-formamida (7 ml) . O composto obtido no Exemplo Referencial 10 (110 mg) , cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (100 mg) e 1-hidróxi-benzotriazol monoidratado (70 mg) , agitando a mistura à temperatura ambiente por 23 h. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se água para conduzir extração com acetato de etila. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado duas vezes por cromatografia de coluna em sílica-gel (cloreto de metileno :metanol 20:1 —» 10:1) . A base livre assim obtida foi dissolvida em metanol, e adicionou-se uma solução 1 N (0,30 ml) de ácido clorídrico em etanol. O resíduo foi lavado com acetato de etila, para obter o composto do título (130 mg).
RMN-1!! (DMSO-de) δ: 1, 45-1, 60 (1H, m) , 1, 70-1, 90 (3H, m) , 1,902,10(2H,m), 2,81(3H,s), 2,91(3H,s), 3,00(3H,s), 3,00-3,22 (3H,m), 3,53(2H,br), 4,10-4,20 (lH,m) , 4,30-4,70 (3H,m) , 7,59 (1H,dd,J=8,8, 2,2Hz), 7,87(1H, d,J=8,5Hz), 7, 96(1H, d,J=8,5
Hz), 8, 02(1H,d,J=8,8Hz), 8, 10(1H,d,J=2,2Hz), 8,33(lH,s),
8,43(1H, d, J=8,lHz), 8, 52 (1H, d, J=7,3Hz) .
MS(FAB) m/z: 554 (M+H)+.
de 08/10/2018, pág. 759/857
751
Exemplo 220 cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino) carbonil]-2-{[(5-meti1-4,5,6,7-tetraidrotiazolo[5,4-c] piridin-2-il)-carbonil]-amino}-ciclo-hexil)-cinolino-3carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 299 com uma solução de ácido clorídrico em etanol, e depois condensando-o com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do processo descrito no Exemplo 219.
RMN-iH (CDC13) δ: 1,50-1, 65 (1H, m) , 1,70-1, 90 (3H, m) , 2,05-2,15 (lH,m), 2, 15-2,30 (lH,m) , 2,81(3H,s), 2,85-3, 05 (8H, m) , 3,15 3,25(2H,m), 3, 40-3, 80(1H, m) , 4,25-4, 80(4H,m) , 8,02 (1H,dd,J=
8,8, 2,OHz), 8, 38 (1H, d, J=8, 8Hz) , 8,66(lH,s), 8,91(lH,s),
8, 96 (1H, d, J=7,3Hz) , 9,53(lH,br).
MS (FAB) m/z: 556(M+H)+.
Exemplo 221 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-benzimidazol-2-il)carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
de 08/10/2018, pág. 760/857
752
composto do título foi obtido tratando o composto obtido no Exemplo Referencial 300 com uma solução de ácido clorídrico em etanol, e depois condensando-o com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do processo descrito no Exemplo 219.
RMN-1!! (DMSO-dg) δ: 1, 45-1, 60 (1H, m) , 1,60-1,83 (3H, m) , 2,002,20 (2H,m), 2,78 (3H,s), 2,92 (6H,s), 3,00-3,30(3H,m), 3,47 (2H,br,s), 4,10-4,75 (4H,m) , 7,30 (1H, d, J=8, 8Hz) , 7,62(lH,d,J=
12,5Hz), 7,63(lH,s), 8,75-8, 87(1H, m) , 9,09 (1H,dd,J=12, 5,
8,8Hz), 11,20-11,4O(1H,m) .
MS (FAB) m/z: 546(M+H)+.
Exemplo 222 cloridrato de N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-ΣΙ [(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)15 carbonil]-amino}-ciclo-hexil)-7-flúor-isoquinolino-3carboxamida:
Petição 870180138821, de 08/10/2018, pág. 761/857
753 composto do título foi obtido a partir do composto obtido no Exemplo Referencial 253 e do composto obtido no Exemplo Referencial 304, de uma maneira similar àquela do processo descrito no Exemplo 5.
RMN-iH (DMSO-de) δ: 1,50-1, 60 (lH,m) , 1, 70-1,85 (3H, m) , 1,952,05(lH,m), 2,10-2,20(lH,m), 2,80(3H,s), 2,90-3,90(5H,m),
2,93(3H,s), 2,96(3H,s), 4, 10-4,75 (4H, m) , 7,75-7,85 (1H, m) ,
8,00-8,05 (lH,m), 8,30-8,35 (1H, m) , 8,61(lH,s), 8,93 (2H,d,J= 7,3Hz), 9,31(lH,s).
MS (FAB) m/z: 539(M+H)+.
Exemplo 223 cloridrato de N-{(IR,2S,5S)-2-{[(7-cloro-2H-cromen-3-il)carbonil]-amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto obtido no Exemplo Referencial 252 (220 mg) foi dissolvido em metanol (10 ml), e adicionou-se 10% de paládio sobre carvão (180 mg), agitando a mistura à temperatura ambiente por 4 h em uma atmosfera de hidrogênio. Depois de filtrar a mistura da reação, o filtrado foi concentrado sob pressão reduzida, e o resíduo foi dissolvido em N,N-dimetil-formamida (30 ml) . 0 composto obtido no
Petição 870180138821, de 08/10/2018, pág. 762/857
754
Exemplo Referencial 306 (108 mg), cloridrato de l—(3— dimetil-amino-propil)-3-etil-carbodiimida (196 mg) e 1hidróxi-benzotriazol monoidratado (78 mg), foram adicionados, agitando a mistura à temperatura ambiente por uma noite. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir extração de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado duas vezes por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 100:3), para obter uma substância espumosa amarela. Esta substância espumosa foi dissolvida em cloreto de metileno (2 ml) , adicionou-se uma solução 1 N (363 μΐ) de ácido clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se dietil-éter ao resíduo. O precipitado formado foi coletado por filtração, para obter o composto do título (175 mg).
RMN-!H (DMSO-de) δ: 1, 40-1, 52 (1H, m) , 1, 55-1, 96 (5H, m) , 2,78 (3H,s), 2,90(3H,s), 2,98(3H,s), 3,01-3,12 (lH,m) , 3,13-3,28 (2H,m), 3, 40-3, 85(2H,m), 3, 92-4,00 (lH,m) , 4,35-4,80(3H,m),
4,84 (1H, d, J=14,5Hz) , 4,8 9 (1H, d, J=14,5Hz) , 6,92(lH,s), 6,98 (1H,dd,J=8,1,1, 7Hz) , 7,08(lH,s), 7,17(1H,d,J=8,3Hz), 8,12 (1H,d,J=8,1Hz), 8, 34(1H, d, J=8,1Hz) .
MS (FAB) m/z: 558(M+H)+.
Exemplo 224 cloridrato de N-{(IR,2S,5S)-2-{[(E)-3-(cloro-fenil)-2de 08/10/2018, pág. 763/857
755 propenoil]-amino}-5-[(dimetil-amino)carbonil]-ciclo-hexil}5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
composto do título foi obtido tratando o 5 composto obtido no Exemplo Referencial 307 com uma solução de ácido clorídrico em etanol, e depois condensando-o com o composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do processo descrito no Exemplo 219.
ΗΜΝ-^ (DMSO-de) δ: 1,35-1, 55 (1H,m) , 1,55-1,90 (4H, m) , 2,79 (3H,s), 2,92(3H,s), 2,99(3H,s), 3, 05-3, 30 (3H, m) , 3, 40-0 3, 55 (lH,m), 3, 60-3, 75 (lH,m) , 3, 93-4,03 (2H,m), 4,35-4,50 (lH,m),
4,50-4, 60 (lH,m), 4,60-4,75 (lH,m), 6,65 (11-1,d,J=15, 7Hz) ,
7,35(1H,d,J=15,7Hz), 7,44(1H,d,J=8,6Hz), 7,55(1H,d,J=8,6Hz), 8,03(1H,d,J=8,1Hz), 8,34 (1H,br,s), 11,25-11, 70(1H,br) .
MS (ESI) m/z: 530(N+H)+.
Exemplo 225 cloridrato de 6-cloro-N-((IS,2R,4S)-4-[(dimetil-amino) carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c] piridin-2-il)-carbonil]-amino}-ciclo-hexil)-4-oxo-l, 420 diidroquinolino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 764/857
756
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 253 e do composto obtido no Exemplo Referencial 309, de uma maneira similar àquela do processo descrito no Exemplo 5.
RMN-1!! (DMSO-de) δ: 1,43-1, 60 (1H, m) , 1, 65-2,10 (3H, m) , 2,79 (3H,s), 2,92(3H,s), 2,99(3H,s), 3, 05-3, 20 (2H, m) , 3,20-3,80 (5H,m), 4, 08—4,20 (lH,m), 4,35—4,50 (lH,m), 4,60—4,70 (1H, m) , 4,70(1H,d,J=15,6Hz), 6,77 (1H,br,s), 7,73(1H,d,J=8,9Hz), 7,94 (1H,d,J=8,9Hz), 7,97(1H,d,J=2,2Hz), 8,54(1H,br,s), 8,80-9,00 (lH,m), 11,18-11,42(1H,br), 11,70-12,50(1H,br).
MS (ESI) m/z: 571(M+H)+.
Exemplo 226
2-[({(lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5[(dimetil-amino)-carbonil]-ciclo-hexil}-amino)-carbonil]4,6-diidro-5H-pirrolo[3,4-d]tiazol-5-carboxilato de tbutila:
Boc
Petição 870180138821, de 08/10/2018, pág. 765/857
757
1) O composto obtido no Exemplo Referencial 310 (1,46 g) foi dissolvido em cloreto de metileno (10 ml), e adicionou-se uma solução (10 ml) de ácido clorídrico em etanol à temperatura ambiente, agitando a mistura por 1 h. Depois de completada a reação, o solvente foi removido por destilação, adicinou-se etanol, a mistura foi concentrada, e adicionou-se éter diisopropílico ao resíduo, para solidificá-lo. Os sólidos resultantes foram coletados por filtração para obter cloridrato de N-{(IS,2R,4S)-2-amino-4[(dimetil-amino)-carbonil]-ciclo-hexil}-5-cloro-indol-2carboxamida .
2) Este produto foi dissolvido em N,N-dimetilformamida (5 ml), e adicionou-se o composto obtido no Exemplo Referencial 406 (1, 31 g) , cloridrato de l—(3— dimetil-amino-propil)-3-etil-carbodiimida (1,36 g) e 1hidróxi-benzotriazol monoidratado (640 mg) foram adicionados, agitando a mistura à temperatura ambiente por 3 dias. A mistura da reação foi concentrada sob pressão reduzida, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir extração de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:19), para obter o composto do título (1,22 g).
RMN-!H (CDC13) δ: l,53(9H,s), 1, 7 0-2,4 0 ( 6H, m) , 2,80-3,20 (7H,m), 4,15—4,25(1H,m), 4,55—4,80(5H,m), 6,83(1H,d,J=l,5 de 08/10/2018, pág. 766/857
758
Hz), 7,20(1H,dd,J=8,8, 2,OHz), 7,33(1H,d,J=8,8Hz), 7,407,50(lH,m), 7,61(1H,br,s), 7,72—7,80(11-i,m), 9,41(1H,br,s). MS (ESI) m/z: 615(M+H)+.
Exemplo 227 cloridrato de 5-cloro-N-{(IS,2R,4S)-2-[[(5,6-diidro-4Hpirrolo[3, 4-d]-tiazol-2-il)-carbonil]-amino]-4-[(dimetilamino) carbonil]-ciclo-hexil}-indo1-2-carboxamida:
O composto obtido no Exemplo Referencial 226 (1,22 g) foi dissolvido em cloreto de metileno (5 ml), e adicionou-se uma solução (10 ml) de ácido clorídrico em etanol, agitando a mistura por 1 h. Depois de concentrar a mistura da reação, adicionou-se uma solução aquosa saturada de bicarbonato de sódio e cloreto de metileno, para conduzir separação de líquidos, e a camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:9), para obter uma base livre (636 mg) do composto do título, como um sólido vítreo incolor. A base livre (200 mg) foi dissolvida em uma solução 1 Ν (1 ml) de ácido clorídrico em etanol. Depois de concentrar a solução, de 08/10/2018, pág. 767/857
759 adicionou-se acetato de etila, para solidificar o resíduo.
pó incolor assim obtido foi coletado por filtração e secado, para obter o composto do título (195 mg).
RMN-1H (DMSO-de) δ: 1, 45-1, 60 (lH,m) , 1,70-1, 90 (3H, m) , 1,905 2,05(2H,m), 2,80(3H,s), 2,98(3H,s), 2, 98-3, 15 (1H, m) , 4,054,20(lH,m), 4,44 (2H,br,s), 4,58(3H,br,s), 7,05(1H,d,J=1,5
Hz), 7,16(1H,dd,J=8, 7, 1,8Hz) , 7,42 (1H,d,J=8,7Hz) , 7,68 (1H, d,J=l,8Hz), 8,38(1H,d,J=7,8Hz), 8,42(1H,d,J=7,8Hz), 10,4510,65(2H,br), 11,78(1H,br,s).
MS (FAB) m/z: 515(M+H)+.
Exemplo 228 cloridrato de 5-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(5-meti1-5,6-diidro-4H-pirrolo[3,4-d]-tiazol2-il)-carbonil]-amino}-ciclo-hexil}-indol-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 227 e formalina, de uma maneira similar àquela do processo descrito no Exemplo 18.
RMN-íH (DMSO-de) δ: 1, 45-1, 60 (1H, m) , 1, 65-1,90 (3H, m) , 1,902,05(2H,m), 2,80(3H,s), 2,98(3H,s), 2, 98-3, 06 (1H, m) , 3,06 (3H,s), 4,05-4,20(lH,m), 4,30-5,00(5H,br,s), 7,04(1H,d,J=1,7
Hz), 7, 17 (1H, dd, J=8, 8, 2, 1Hz) , 7,41 (1H, d, J=8, 8Hz) 7,68(lH,d,
Petição 870180138821, de 08/10/2018, pág. 768/857
760
J=2,lHz), 8, 36 (1H, d, J=7, 8Hz) , 8, 42(1H, d,J=8,1Hz), 11,78(1H, br,s), 12, 14 (1H, br, s) .
MS (FAB) m/z: 529(M+H)+.
Exemplo 229
2-[ ({ (IR,2S,5S)-5-[(dimetil-amino)-carbonil]-2-{[(5-flúorindol-2-il)-carbonil]-amino}-ciclo-hexil}-amino)-carbonil]4,6-diidro-5H-pirrolo[3,4-d]tiazol-5-carboxilato de tbutila:
O composto do título foi obtido a partir do 10 composto obtido no Exemplo Referencial 311 e do composto obtido no Exemplo Referencial 406, de uma maneira similar àquela do processo descrito no Exemplo 5.
RMN-XH (CDC13) δ: l,53(9H,s), 1, 60-2, 40 (6H, m) , 2,80-3,20 (7H,m), 4,15-4,25(lH,m), 4,55-4,80(5H,m), 6,84-6,87(1H,m),
7,01(1H,dt,J=2,4,9,1HZ), 7,25-7,30(1H,m), 7,34 (1H,dd,J=9,1,
4,3Hz), 7,42-7,49(lH,m), 7,70-7,50(1H,m), 9,37-9,45(1H,m).
MS (ESI) m/z: 599(M+H)+.
Exemplo 230 cloridrato de N-{(IS,2R,4S)-2-[[(5,6-diidro-4H-pirrolo[3,420 d]-tiazol-2-il)-carbonil]-amino]-4-[(dimetil-amino)carbonil]-5-flúor-indo1-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 769/857
761
composto do título foi obtido a partir do composto obtido no Exemplo 229, de uma maneira similar àquela do processo descrito no Exemplo 227.
RMN-1H (DMSO-dg) δ: 1, 45-1, 60 (1H, m) , 1,65-1, 90 (3H,m), 1,905 2,10(2H,m), 2,80(3H,s), 2,97(3H,s), 2, 98-3, 15 (1H, m) , 4,054,20(lH,m), 4,35—4,50 (2H, m) , 4,58 (3H, br, s) , 6, 97—7, 10 (2H, m) ,
7,35-7,47 (2H,m), 8, 34(1H,d,J=7,8Hz), 8, 41(1H, d,J=8,1Hz),
10,53(2H,br,s), 11,68(1H,br,s).
MS (FAB) m/z: 499(M+H)+.
Exemplo 231 cloridrato de N-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2{[(5-meti1-5,6-diidro-4H-pirrolo[3,4-d]tiazol-2-il)~ carbonil]-amino}-ciclo-hexil}-5-flúor-indol-2-carboxamida:
O composto do título foi obtido a partir do 15 composto obtido no Exemplo Referencial 230 e formalina, de
Petição 870180138821, de 08/10/2018, pág. 770/857
762 uma maneira similar àquela do processo descrito no Exemplo
18.
RMN-1H (DMSO-de) δ: 1,45-1,60(1H,m), 1, 65-1, 90 (3H, m) , 1,902,10(2H,m), 2,80(3H,s), 2, 90-3, 20 (7H, m) , 4,05-4,20 (lH,m),
4,30-5, 00 (5H,br,s), 6,95-7,10(2H,m), 7,35-7,50 (2H,m), 8,33 (1H,d,J=7,6Hz),8,41(1H,d,J=8,1Hz),11,67(lH,br,5), 12,37 (1H, br, s) .
MS (FAB) m/z: 513(M+H)+.
Exemplo 232 cloridrato de N-{(IR,2S,5S)-2-[(6-cloro-2-naftoli)-amino]-5[(dimetil-amino)-carbonil]-ciclo-hexil}-5-meti1-5,6-diidro4H-pirrolo[3,4-d]tiazol-2-carboxamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 294 e do composto obtido no Exemplo Referencial 293, de uma maneira similar àquela do processo descrito no Exemplo 226.
RMN-1!! (DMSO-de) δ: 1, 48-1, 56 (1H, m) , 1,71-1,84 (3H, m) , 1,952,04(2H,m), 2,81(3H,s), 3,00(3H,s), 3,02(3H,s), 3,06-3,15 (2H,m), 4,13-4,14(lH,m), 4,52-4,63(4H,m), 7,60(1H, d, J=8,5
Hz), 7,87(1H,d,J=8,8Hz), 7,96(1H,d,J=8,5Hz), 8,01(1H,d,J=8,8
Petição 870180138821, de 08/10/2018, pág. 771/857
763
Hz), 8,10(lH,s), 8,32(lH,s), 8, 45 (1H, d, J=8, 1Hz) , 8,51(lH,d,
J=7,3Hz) .
MS (FAB) m/z: 540(M+H)+.
Exemplo 233 cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-5,6-diidro-4H-pirrolo[3,4-d]tiazol-2il)-carbonil]-amino}-ciclo-hexil}cinolino-3-carboxamida e cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-5H-pirrolo[3,4-d]tiazol-2-il)10 carbonil]-amino}-ciclo-hexil}-cinolino-3-carboxamida:
Uma solução 4 N (3,0 ml) de ácido clorídrico em dioxano foi adicionada a uma suspensão do composto obtido no Exemplo Referencial 299 (330 mg) em um solvente misto de dioxano (3,0 ml) e cloreto de metileno (3,0 ml), e a mistura foi agitada à temperatura ambiente por 30 min. O solvente
Petição 870180138821, de 08/10/2018, pág. 772/857
764 foi removido por destilação sob pressão reduzida, e o pó branco assim obtido foi dissolvido em N,N-dimetil-formamida (5,0 ml), e o composto obtido no Exemplo Referencial 293 (172 mg), cloridrato de 1-(3-dimetil-amino-propil)-3-etil5 carbodiimida (192 mg) e 1-hidróxi-benzotriazol monoidratado (130 mg) foram adicionados, agitando a mistura à temperatura ambiente por 15 h. O solvente foi removido por destilação sob pressão reduzida, adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo.
A camada orgânica resultante foi lavada com solução aquosa saturada de cloreto de sódio e depois secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1). Adicionou-se uma solução (0,35 ml) de ácido clorídrico em etanol a uma solução do composto altamente polar assim obtido, formado principalmente em etanol (4,0 ml), e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se etanol e dietil-éter ao resíduo, e o precipitado formado foi coletado por filtração, para obter cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetilamino) -carbonil]-2- {[(5-metil-5,6-diidro-4H-pirrolo[3, 4-d] tiazol-2-il)-carbonil]-amino}-ciclo-hexil}cinolino-3- carboxamida (184 mg), um produto principal.
RMN-!H (DMSO-de) δ: 1, 50-1, 65 (1H,m) , 1, 70-1, 90 (3H,m) , 2,032,12 (lH,m), 2,15-2,30 (lH,m), 2,81 (3H,s), 2, 90-3, 05 (lH,m) , 2,96 (3H,s), 3,07 (3H,s), 4,28-4,37(lH,m), 4,40-4,95(5H,br),
8, 02 (1H, d, J=8, 8Hz) , 8, 38 (1H, d, J=8, 8Hz) , 8,66(lH,s), 8,91(1H,
Petição 870180138821, de 08/10/2018, pág. 773/857
765
s) , 8, 97 (1H, d, J=7,1Hz) , 9,43-9,57(1H,br) , 11,75-11, 95(Ο,5H, br), 12,35—11,55(0,5H,br).
MS (FAB) m/z: 542(M+H)+.
Na purificação pela cromatografia de coluna em 5 sílica-gel, obteve-se também 7-cloro-N-((IS,2R,4S)-4[(dimetil-amino) - carbonil]-2-{[(5-metil-5H-pirrolo[3,4-d] tiazol-2-il)-carbonil]-amino}-ciclo-hexil}-cinolino-3-carboxamida como um subproduto.
RMN-^ (CDC13) δ: 1, 90-2,25 (6H, m) , 2, 85-3, 00 (lH,m) , 2,95(3H,
s), 3,05(3H,s), 3,91(3H,s), 4,43-4,54 (1H, m) , 4,86-4, 95 (1H,
m) , 6,70 (1H, d, J=l, 5Hz) , 7,19 (1H, d, J=l, 5Hz) , 7,59 (lH,d,J=
8,8Hz), 7,76(1H,d,J=8, 8Hz) , 7,95(1H,d,J=8, 8Hz) , 8,53(lH,s),
8, 64 (lH,d, J=8,OHz) , 8,73(lH,s).
MS (FAB) m/z: 540(M+H)+.
Exemplo 234 cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(5-meti1-5,6-diidro-4H-pirrolo[3, 4-d]tiazol-2il)-carbonil]-amino}-ciclo-hexil}isoquinolino-3-carboxamida:
O composto obtido no Exemplo Referencial 146 (500 mg) foi dissolvido em uma solução (5 ml) de ácido clorídrico
Petição 870180138821, de 08/10/2018, pág. 774/857
766 em etanol, e a mistura foi agitada à temperatura ambiente por 30 min. 0 solvente foi removido por destilação sob pressão reduzida, e o resíduo foi dissolvido em N,N-dimetilformamida (7 ml), e adicionou-se o composto obtido no Exemplo Referencial 293 (299 mg) , 1-hidróxi-benzotriazol monoidratado (71 mg), e cloridrato de 1-(3-dimetil-aminopropil) -3-etil-carbodiimida (403 mg), a esta solução, agitando a mistura à temperatura ambiente por uma noite. O solvente foi removido por destilação sob pressão reduzida, e adicionou-se uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para conduzir extração com cloreto de metileno. As camadas orgânicas resultantes foram secadas sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi
|
purificado |
por |
cromatografia |
de coluna |
em |
sílica-gel |
|
(cloreto de |
metileno:metanol |
93:7), para |
obter |
uma base |
|
livre (260 |
mg) |
do composto |
do título, |
como |
um sólido |
|
amarelo-pálido. |
Este produto |
foi dissolvido em |
cloreto de |
|
metileno, adicionou-se uma |
solução (961 |
μΐ) |
de ácido |
clorídrico em etanol, e o solvente foi removido por destilação sob pressão reduzida. Adicionou-se uma pequena quantidade de metanol ao resíduo, e adicionou-se dietil-éter em gotas para coletar o precipitado formado por filtração. Este produto foi lavado com dietil-éter, para obter o composto do título (260 mg).
RMN-!H (DMSO-de) δ: 1, 47-1, 56 (1H, m) , 1, 71-1, 75 (3H, m) , 1,95l,99(lH,m), 2,12-2,15 (lH,m) , 2,78(3H,s), 2,95(3H,s), 2,98 (lH,br,s), 3,05(3H,s), 4,19-4,22 (1H, m) , 4,44-4,52 (3H,m) , de 08/10/2018, pág. 775/857
767
4,74-4,88(2H,m), 7, 87(1H,dd,J=8,8, 1,7Hz), 8,24(1H,d,J=8,8
Hz), 8, 36(1H,d,J=l,7Hz), 8,58(lH,s), 8, 90-8, 92 (2H, m) , 9,30 (lH,s), 12,65-12,75(lH,m).
MS (FAB) m/z: 541(M+H)+.
Exemplo 235
2-[({(lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-5[(dimetil-amino)-carbonil]-ciclo-hexil}-amino)-carbonil]6,6-dimetil-6,7-tetraidrotiazolo[4,5-c]piridino-5(H)carboxilato de t-butila:
O composto obtido no Exemplo Referencial 316 (95,4 mg) foi dissolvido em dietil-éter (1 ml) em uma atmosfera de argônio, e adicionou-se t-butil-lítio (solução 1,60 N em pentano, 244 μΐ) em gotas a -78 °C. Depois de agitar a mistura por lha -78 °C, borbulhou-se dióxido de carbono na mistura da reação por 10 min. A mistura da reação foi aquecida até a temperatura ambiente. Depois de concentrar a mistura da reação sob pressão reduzida, o resíduo foi dissolvido em N,N-dimetil-formamida (5 ml). Adicionou-se sucessivamente à solução o composto obtido no Exemplo
Referencial 432 (178 mg), 1-hidróxi-benzotriazol monoidratado (48,0 mg), e cloridrato de 1-(3-dimetil-aminopropil ) -3-etil-carbodiimida (136 mg). A mistura foi agitada
Petição 870180138821, de 08/10/2018, pág. 776/857
768 por toda a noite à temperatura ambiente. A mistura da reação foi concentrada, e adicionou-se cloreto de metileno e uma solução aquosa saturada de bicarbonato de sódio ao resíduo, para separar uma camada orgânica. A camada orgânica foi secada sobre sulfato de sódio anidro, e o solvente foi então removido por destilação sob pressão reduzida. O resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (metanol:cloreto de metileno 1:19), para obter o composto do título (140 mg). ΗΜΝ-^ (CDC13) δ: l,50(9H,s), l,52(3H,s), l,54(3H,s), 1,702,10 (4H,m), 2,15-2,45(2H,m) , 2,80-3, 20(9H, m) , 4,10-4,25 (lH,br), 4, 60-4,75(3H,m), 6, 85(1H, br,s), 7,21(1H, dd,J=8,8,
1,8Hz), 7,34(1H, d,J=8,8Hz), 7,48(1H, d,J=7,3Hz), 7,61-7,63 (lH,m), 7,89(1H, br, s), 9,27(1H,br,s) .
MS (ESI) m/z: 657(M+H)+.
Exemplo 236 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}6,6-dimetil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
composto
O composto do título foi obtido a partir do obtido no Exemplo 235, de uma maneira similar de 08/10/2018, pág. 777/857
769 àquela do processo descrito no Exemplo 227.
RMN-1H (DMSO-de) δ: l,40(6H,s), 1,45-1, 60 (1H, m) , 1,70-2,05 (5H,m), 2,81(3H,s), 2,95-3,15(6H,m), 4,05-4,20(1H,br), 4,254,45(2H,m), 4,55-4, 65 (1H, m) , 7, 06 (1H, d, J=l, 7Hz) , 7,17(lH,dd,
J=8,8,2,OHz), 7,42(1H,d,J=8,8Hz), 7, 68(1H,d,J=2,OHz), 8,348,39(2H,m), 9, 77 (1H, br, s) , 9, 84 (1H, br, s) , 11,79 (1H, br, s) .
MS (ESI) m/z: 557(M+H)+.
Exemplo 237
2-[ ({ (lR,2S,5S)-2-{[(5-cloro-indol-2-il)-carbonil]-amino}-510 [(dimetil-amino)-carbonil]-ciclo-hexil}-amino)-carbonil]5,7-diidro-6H-pirrolo[3,4-d]pirimidino-6-carboxilato de t-
composto obtido no Exemplo Referencial 50 (1,27
g) foi dissolvido em tetraidrofurano (48 ml), e adicionou-se hidróxido de lítio (117 mg) e água (6,0 ml), agitando a mistura à temperatura ambiente à temperatura ambiente por 4,5 h. A mistura da reação foi secada até tornar-se um sólido sob pressão reduzida, para obter um sal de lítio de ácido carboxílico bruto (1,24 g). Este produto foi condensado com o composto obtido no Exemplo Referencial 432,
Petição 870180138821, de 08/10/2018, pág. 778/857
770 de uma maneira similar à do processo descrito na etapa (2) do Exemplo 226, para obter o composto do título.
RMN-iH (CDC13) δ: 1,50-1,70 (1H, m) , l,54(9H,s), 1, 80-2, 10 (3H,
m) , 2,25-2,50 (2H,m) , 2,85-2, 95 (1H, m) , 2,99(3H,s), 3,14(3H,
s), 4,15-4,25(lH,m), 4,65-4,75 (1H, m) , 4,80-4,90 (4H, m) , 6,97 (lH,s), 7,15-7,25(lH,m), 7,30-7,40(1H,m), 7,60-7,65(1H,m),
8,15-8,25 (lH,m), 8, 40-8, 45 (lH,m), 8,75-8, 85 (lH,m), 9,409, 45 (lH,m) .
MS (ESI) m/z: 611(M+H)+.
Exemplo 238 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}6-metil-6,7-diidro-5H-pirrolo[3,4-d]pirimidino-2carboxamida:
O composto obtido no Exemplo 237 (367 mg) foi dissolvido em cloreto de metileno (10 ml), e adicionou-se ácido triflúor-acético (10 ml), agitando a mistura à temperatura ambiente por 2 h. A mistura da reação foi secada até tornar-se um sólido, sob pressão reduzida. O composto do título foi obtido a partir do produto bruto assim obtido e formalina, de uma maneira similar àquela do
Petição 870180138821, de 08/10/2018, pág. 779/857
771 processo descrito no Exemplo 18.
RMN-1H (DMSO-de) δ: 1,50-1, 60 (1H, m) , 1, 65-2,10 (5H, m) , 2,81 (3H,s), 2, 90-3,00 (lH,m) , 2,96(3H,s), 3,05(3H,s), 4,10-4,20 (lH,m), 4,55-4, 65 (lH,m) , 4,65-4,90(4H, br) , 7,O6(1H,5), 7,15 (1H,dd,J=8,7, 2,1Hz), 7,41(1H,d,J=8,8Hz), 7,66(1H,d,J=1,7
Hz), 8,35-8, 45(lH,m), 8,57(1H,d,J=8,1Hz) , 9,00(lH,s), 11,80 (lH,s), 11,90-12,20(lH,m).
MS (FAB) m/z: 524(M+H)+.
Exemplo 239 cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(6-metil-6,7-diidrotiazolo[4,5-d]pirimidin-2il)-carbonil]-amino}-ciclo-hexil)-isoquinolino-3carboxamida:
O composto do título foi obtido tratando o 15 composto obtido no Exemplo Referencial 146 com uma solução de ácido clorídrico em etanol, e depois condensando-o com o composto obtido no Exemplo Referencial 332, de uma maneira àquela do processo descrito no Exemplo 49.
RMN-1H (DMSO-de) δ: 1, 50-1, 60 (1H, m) , 1,70-1,90 (3H, m) , 1,9020 2, 15(2H,m), 2,81(3H,s), 2,95(3H,s), 2, 90-3, 05 (1H, m) , 3,26 (3H,s), 4,20-4,55(2H,m) , 5,00(2H,s), 7,91(1H,d,J=8,8Hz) ,
Petição 870180138821, de 08/10/2018, pág. 780/857
772
8,27(1Η,d,J=8,8Hz), 8,37(lH,s), 8,54(lH,s), 8,62(lH,s), 8,79 (1H, d, J=8,3Hz) , 8, 94 (1H, d, J=8, 1Hz) , 9,32(lH,s).
MS (ESI) m/z: 554 (M+H)+.
Exemplo 240 cloridrato de 7-cloro-N-((IS,2R,4S)-4-{[etil-(metil)-amino]carbonil}-2-{[(5-meti1-4,5,6,7-tetraidrotiazolo[5,4c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-isoquinolino3-carboxamida:
O composto do título foi obtido a partir do 10 composto obtido no Exemplo Referencial 325 e do composto obtido no Exemplo Referencial 10, de uma maneira àquela do processo descrito no Exemplo 2.
RMN-1H (DMSO-de) δ: 0,98, l,04(3H,cada t,J=7,lHz), 1,52-1,60 (lH,m), 1,74-1,77(3H,m), 1,96-2,05(1H,m), 2,15-2,18(1H,m),
2,77-2, 93(8H,m), 3, 17-3,32(3H,m), 3, 49(1H,br,s), 4,22(1H, br,s), 4, 41-4, 45(lH,m), 4,51(1H,br,s), 4,69-4,72(1H,m), 7,89 (1H, d, J=8, 7Hz) , 8, 26 (1H, d, J=8, 7Hz) , 8,37(lH,s), 8,60(lH,s),
8,91-8,98(2H,m), 9,32(1H,d,J=6,6Hz), 11,39,11,53(1H,cada m). MS (FAB) m/z: 569(M+H)+.
Exemplo 241 cloridrato de N-{(IR*,2S*,5S*)-2-{[(5-cloro-indol-2-il)Petição 870180138821, de 08/10/2018, pág. 781/857
773 carbonil]-amino}-5-[2-(dimetil-amino)-2-oxoetil]-ciclohexil } -5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
composto do título foi obtido a partir do 5 composto obtido no Exemplo Referenciai 336 e do composto obtido no Exemplo Referencial 10, de uma maneira àquela do processo descrito no Exemplo 2.
ΗΜΝ-^ (DMSO-de) δ: 1, 13-1,22 (1H, m) , 1,40-1,46 (1H, m) , 1,68I, 99 (5H,m), 2, 18-2,29 (2H, m) , 2,80(3H,s), 2,92(3H,s), 2,96 (3H,s), 3, 22 (2H,br, s) , 3, 49 (1H, br, s) , 3, 70 (1H, br, s) , 4,094.16 (lH,m), 4,42-4, 46(2H,m) , 4,67 (1H,br,s), 7,03(lH,s),
7.16 (1H,dd,J=8,5, 1,5Hz), 7,42(1H,d,J=8,5Hz) , 7,67(lH,s),
8,01 (1H, d,J=8,5Hz), 8,40(1H,d,J=7,8Hz) , 11,35-11,58 (1H, m) ,
II, 76 (1H,br,s).
MS (FAB) m/z: 557(M+H)+.
Exemplo 242 cloridrato de N-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(metil-sulfonil)-metil]-ciclo-hexil}-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 782/857
774
composto do título foi obtido tratando o composto obtido no Exemplo Referencial 340 com uma solução de ácido clorídrico em etanol, e depois condensando-o com o composto obtido no Exemplo Referencial 10, de uma maneira àquela do processo descrito no Exemplo 219.
ΗΜΝ-^ (DMSO-de) δ: 1,35-1, 40 (1H, m) , 1,55-1, 62 (1H, m) , 1,701,76 (lH,m), 1, 88-1, 94 (lH,m) , 2,03-2, 07(1H,m), 3, 60-3, 73(2H,
m) , 4,11-4,16(lH,m), 4,40-4,42(2H,m), 4,68-4,73(1H,m), 7,05 (1H,S), 7,16 (1H,dd,J=2,0,8,8Hz), 7,41 (1H,d,J=8,8Hz), 7,68 (1H,S), 8, 26 (1H, d, J=7, 8Hz) , 8,39 (1H, d, J=7, 8Hz) , 11,78(1H, br,s).
MS (ESI) m/z: 564(M+H)+.
Exemplo 243
N-{(IR,2S,5S)-2-{[(2-cloro-6H-tieno[2,3-b]pirrol-5-il)15 carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
Petição 870180138821, de 08/10/2018, pág. 783/857
775 composto do título foi obtido pela hidrogenação do composto obtido no Exemplo Referencial 252, e depois condensando-o com o composto obtido no Exemplo Referencial 345, de uma maneira àquela do processo descrito no Exemplo
223.
ΚΜΝ-^ (CDC13) δ: 1,56-1, 66 (1H, m) , 1,76-1,93 (2H, m) , 2,022,06(lH,m), 2, 19-2, 26 (lH,m) , 2,30-2,34 (1H, m) , 2,52(3H,s),
2,79-2,88 (3H,m), 2,91-2,94 (2H,m), 2,96 (3H,s), 3,09(3H,s), 3,69-3,77(2H,m), 4,13-4,19(lH,m), 4,58-4,61(1H,m), 6,72 (1H,
s), 6,84(lH,s), 7,50(1H,d,J=7,3Hz), 7,60(1H,d,J=5,8Hz),
10,54 (lH,br) .
MS (ESI) m/z: 549(M+H)+.
Exemplo 244 cloridrato de N-{(IR,2S,5S)-2-{[3-(cloro-fenil)-215 propinoil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
O composto do título foi obtido pela hidrogenação do composto obtido no Exemplo Referencial 252, e depois condensando-o com o composto obtido no Exemplo Referencial 347, de uma maneira àquela do processo descrito no Exemplo
Petição 870180138821, de 08/10/2018, pág. 784/857
776
223.
RMN-1H (DMSO-de) δ: 1,38-1,50 (1H, m) , 1,58-1, 92 (4H, m) , 2,78(3Η, s) , 2,90 (3H,s), 2,97 (3H,s), 3, 01-3, 24 (3Η, m) , 3, 26-3, 80 (2Η, m) , 3, 90-3, 98 (lH,m), 4,30-4,78(3Η,m), 7,51(1Η,d,J=8,8Ηζ),
7,57(1Η,d,J=8,8Ηζ), 8,34(1Η,d,J=8,8Ηζ), 8,83(1Η,d,J=7,8Hz).
MS (FAB) m/z: 528(M+H)+.
Exemplo 245 cloridrato de 6-cloro-N-((IR, 2S,5S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,410 c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-4-oxo-l,4diidroquinazolino-2-carboxamida:
O composto do título foi obtido pela hidrogenação do composto obtido no Exemplo Referencial 252, e depois condensando-o com o composto obtido no Exemplo Referencial
349, de uma maneira àquela do processo descrito no Exemplo
223.
RMN-1H (DMSO-de) δ: 1, 45-1, 60 (1H, m) , 1,70-1, 90 (3H, m) , 1,902,20(3H,m), 2,80(3H,s), 2,93(3H,s), 2,97(3H,s), 2,98-3,80 (4H,m), 4,05-4,20(2H,m), 4,35-4,80(3H,m), 7,63(1H,d,J=8,3
Hz), 7,90 (lH,d, J=7,3Hz) , 8,75-9,00 (2H,m), 11,00-11,50 (1H, br), 12,53(1H,br,s).
MS (ESI) m/z: 573(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 785/857
777
Exemplo 246
N-{ (IR,2S,5S)-2-{ [2-(4-cloro-anilino)-2-oxoetano-tioil] amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
0 composto obtido no Exemplo Referencial 253 (184 mg) e o composto obtido no Exemplo Referencial 351 (150 mg) foram dissolvidos em um solvente misto de metanol (1 ml) e cloreto de metileno (4 ml), a solução foi aquecida e agitada a 150 °C, e o aquecimento foi continuado por 5 min, após remover o solvente por destilação. Depois de deixar a mistura da reação resfriar, o produto formado foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno;metanol 24:1), para obter o composto do título (59 mg) .
ΗΜΝ-^ (CDC13) δ: 1, 65-1, 90 (2H, m) , 1, 90-2, 00 (1H, m) , 2,00-2,15 (2H,m), 2,20-2,30 (lH,m) , 2,52(3H,s), 2,75-2, 95 (5H, m) , 2,96 (3H,s), 3,07 (3H,s), 3,68 (1H, d, J=15,2Hz) , 3,75 (lH,d,J=
15,7Hz), 4,45-4, 60(lH,m), 4, 80-4, 85(1H,m), 7,31(2H,d,J=8,8
Petição 870180138821, de 08/10/2018, pág. 786/857
778
Hz), 7,44(1H,d,J=8,6Hz), 7,60(2H,d,J=8,8Hz), 9,99(lH,d,J=
7,6Hz), 10,15 (1H,s) .
MS (ESI) m/z: 563(M+H)+.
Exemplo 247
N-{(lR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-2oxoetano-tioil}-amino)-5-[(dimetil-amino)-carbonil]-ciclohexil } -5-meti1-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2carboxamida:
O composto obtido no Exemplo Referencial 253 (184 mg) e o composto obtido no Exemplo Referencial 353 (150 mg) foram dissolvidos em um solvente misto de metanol (0,3 ml) e cloreto de metileno (0,3 ml), a solução foi aquecida e agitada a 150 °C, e o aquecimento foi continuado por 5 min, após remover o solvente por destilação. Depois de deixar a mistura da reação resfriar, o produto formado foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno;metanol 24:1), para obter o composto do título (52 mg) .
RMN-1H (CDC13) δ: 1,60-2,00(3H,m),2,00-2,20(2H,m), 2,25-2,40 (lH,m), 2,53(3H,s), 2, 80-2, 95 (5H, m) , 2,96(3H,5), 3,08(3H,
Petição 870180138821, de 08/10/2018, pág. 787/857
779
s) , 3, 70(1H,d,J=15,4Hz), 3,75(1H,d,J=15,4Hz), 4,45-4, 60(1H,
m) , 4,75-4,85(lH,m), 7,45(1H,d,J=8,3Hz), 7, 67(1H,dd,J=8,8,
2,5Hz), 8, 18(1H,d,J=8,8Hz), 8,31(1H, d,J=2,OHz), 10,06(lH,d,
J=6,3Hz), 10,56(1H,s).
MS (ESI) m/z: 564(M+H)+.
Exemplo 248
N-{(lR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)-amino]-2tiooxoacetil}-amino)-5-[(dimetil-amino)-carbonil]-ciclohexil } -5-meti1-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-
composto obtido no Exemplo Referencial 355 (72 mg) e 2-amino-5-cloro-piridina (100 mg) foram dissolvidos em um solvente misto de metanol (0,2 ml) e cloreto de metileno (0,2 ml), a solução foi aquecida e agitada a 150 °C, e o aquecimento foi continuado por 8 min, após remover o solvente por destilação. Depois de deixar a mistura da reação resfriar, o produto formado foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno;metanol 23:2), para obter o composto do título (4 mg) .
Petição 870180138821, de 08/10/2018, pág. 788/857
780
RMN-XH (CDCI3) δ: 1, 60-2, 00 (3H,m), 2, 00-2, 20 (3H, m) , 2,53(3H,
s), 2,75-3, 00 (5H,m) , 2,95(3H,s), 3,05(3H,s), 3, 65-3, 80 (2H,
m) , 4, 05-4, 15 (lH,m) , 4, 70-4,80 (1H, m) , 7,28(lH,d), 7,43(lH,d, J=9,3Hz), 7,75(1H,dd,J=8,8, 2,7Hz), 8,41(1H,d,J=2,7Hz), 9,05 (1H,d,J=8,8HZ), 11,56(1H,5).
MS (ESI) m/z: 564(M+H)+.
Exemplo 249 cloridrato de N1-(5-cloro-2-tienil)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,710 tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclohexil ) -etanodiamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 356, condensando o hidrolisado com o composto obtido no Exemplo Referencial
253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-XH (DMSO-de) δ: 1, 40-1,55 (1H,m) , 1, 60-1,85 (3H,m) , 2,94 (3H,s), 3, 15-3, 30(2H,m), 3, 50-3, 80(2H,m), 3, 95-4,05(1H,m),
4,35-4, 90(3H,m), 6, 90(1H,d,J=4,2Hz), 6,94(1H,d,J=4,2Hz),
Petição 870180138821, de 08/10/2018, pág. 789/857
781
8,72(1Η,d,J=7,3Ηζ), 9,13 (1H,br,s), 11,21(1H,br,s), 12,32(1H, br, s) .
MS (ESI) m/z: 553 (M+H)+.
Exemplo 250 cloridrato de N-{(IR,2S,5S)-2-{[(4-cloro-anilino)-carbonil]amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
Adicionou-se isocianato de 4-cloro-fenila (76,8 mg) a uma solução do composto obtido no Exemplo Referencial 253 em cloreto de metileno (20 ml) , e a mistura foi agitada à temperatura ambiente por 24 h. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 20:1 —» 10:1), para remover o solvente por destilação. O resíduo foi dissolvido em etanol (2 ml) e cloreto de metileno (2 ml) , adicionou-se uma solução 1 N (0,4 ml) de ácido clorídrico em etanol, agitando a mistura à temperatura ambiente por 30 min. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi solidificado com dietil-éter, para obter o composto do de 08/10/2018, pág. 790/857
782 título (160 mg) .
RMN-1H (DMSO-de) δ: 1,35-1,50(1H, m) , 1, 60-1,90 (5H, m) , 2,79 (3H,s), 2,92(3H,s), 3,00(3H,s), 3, 10-3, 60 (4H, m) , 3,60-3,90 (2H,m), 4,35-4,80(3H,m), 6,26(1H,br,s), 7,23(2H,d,J=9,OHz),
7,37 (2H,d, J=9,OHz) , 8, 53 (1H, br, s) , 8,72 (1H, br, s) , 11,35,
11,67 (total lH,cada s) .
MS (ESI) m/z: 519(M+H)+.
Exemplo 251 cloridrato de N1-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-210 {[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)carbonil]-amino}-ciclo-hexil)-N2-(5-flúor-piridin-2-il)etanodiamida:etanodiamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 357, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RM!!-^ (DMSO-de) δ: 1, 47-1,53 (1H, m) , 1, 68-1,75 (3H, m) , 1,9920 2, 10(2H,m), 2,80(3H,s), 2,80-3, 00 (1H, m) , 2,95(6H,s), 3,18Pclição 870180138821, de 08/10/2018, pág. 791/857
783
3,21 (2H,m), 3,40-3,80(2H,m), 3,87-4,82(4H,m), 7,82-7,85(1H, m), 8,01-8,05(lH,m), 8,40(1H,d,J=2,9Hz), 8,71(1H,d,J=7,7Hz),
9, 13 (1H, d, J=7,3Hz) , 10,27(lH,s).
MS (FAB) m/z: 532(N+H)+.
Exemplo 252 cloridrato de N1-(4-cloro-fenil)-N2-((IS, 2R,4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-5,6-diidro-4H-pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
O composto do título foi obtido tratando o 10 composto obtido no Exemplo Referencial 242 e do composto obtido no Exemplo Referencial 272, de uma maneira àquela do processo descrito no Exemplo 191.
RMN-1!! (DMSO-dg) δ: 1, 47-1, 51 (1H, m) , 1,69-1,75(3H,m), 1,982,05(2H,m), 2,80(3H,s), 2,95(3H,s), 2, 98-3,04 (1H, m) , 3,10 (3
H,s), 3,40-4,61(6H,m), 7,41(2H,d,J=8,8Hz), 7,81(2H,d,J=8,8
Hz), 8,76(1H,d,J=7,6Hz), 8,95(1H,d,J=8,3Hz), 10,79(lH,s).
MS (FAB) m/z: 533(M+H)+.
Exemplo 253 cloridrato de N1-[4-cloro-2-(triflúor-metil)-fenil]-N220 ((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metilPctição 870180138821, de 08/10/2018, pág. 792/857
784
4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-etanodiamida:
Cl
Adicionou-se cloreto de tionila (1 ml) a uma solução (10 ml) do composto obtido no Exemplo Referencial 359 (269 mg), e a mistura foi agitada a 75 °C por 30 min. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi secado. Ao resíduo adicionou-se uma solução (7 ml) do composto obtido no Exemplo Referencial 253 (286 mg) e piridina (3 ml) em cloreto de metileno, sob resfriamento com gelo. A mistura foi agitada por 2 h, enquanto a temperatura do sistema era elevada até a temperatura ambiente. Adicionou-se uma solução aquosa saturada de bicarbonato de sódio (10 ml) à mistura da reação, para conduzir separação de líquidos. A camada orgânica resultante foi secada sobre sulfato de sódio anidro. O solvente foi removido por destilação sob pressão reduzida, e o resíduo resultante foi submetido a uma cromatografia de coluna em sílica-gel (cloreto de metileno;metanol 20:1) e cromatografia de coluna em LH-20 (peneira molecular, metanol), para obter uma base livre (90 de 08/10/2018, pág. 793/857
785 mg) do composto do título, como um sólido amorfo amarelopálido. Adicionou-se cloreto de metileno (5 ml), etanol (5 ml) e uma solução 1 N de ácido clorídrico em etanol (1 ml) ao produto, conduziu-se a remoção e secagem sob pressão reduzida, para obter o composto do título.
ΗΜΝ-^ (DMSO-de) δ: 1, 41-1,55 (1H, m) , 1,59-1,80 (3H, m) , 3,303,58(2H,m), 3, 60-3,78 (1H, m) , 3, 94-4, 04(1H,m), 4,35-4,63 (2H,m), 4, 64-4, 80 (lH,m) , 7,73-7, 82 (2H, m) , 7,85(lH,s), 8,688,73(lH,m), 9, 18 (1H, br, s) , 10,31(lH,s).
MS (ESI)m/z: 615(M+H).
Exemplo 254 cloridrato de N1-{4-cloro-2-[(dimetil-amino)-carbonol]fenil }-N2-((IS, 2R, 4S)-4-[(dimetil-amino)-carbonil]-2-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)15 carbonil]-amino}-ciclo-hexil)-etanodiamida:
O composto do título foi obtido hidrolisando o 20 composto obtido no Exemplo Referencial 362, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo
Petição 870180138821, de 08/10/2018, pág. 794/857
786 descrito no Exemplo 191.
EMN-iH (DMSO-de) δ: 1,42-1,56 (1H,m) , 1,59-1,82 (3H, m) , 1,982,14(2H,m), 2,79(3H,s), 2,91(3H,s), 2,93(3H,s), 2,95(3H,s),
2,98(3H,s), 3,10-3,30(4H,m) , 3, 62-3, 79(1H, m) , 3,92-4,01(1H,
m) , 4,34-4,50 (2H,m), 4, 66-4,79 (lH,m), 7, 52 (1H,d,J=2,4Hz) ,
7,55(1H,dd,J=2,4, 8,5Hz), 8, 05(1H, d,J=8,5Hz), 8,75(lH,br),
9,10-9,24(lH,m), 10, 52(1H, s) .
MS (ESI) m/z: 618(M+H)+.
Exemplo 255 cloridrato de N1-[4-cloro-2-(hidróxi-metil)-fenil]-N2((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-etanodiamida:
O composto do título foi obtido condensando o 15 composto obtido no Exemplo Referencial 270 com 4-cloro-2hidróxi-metil-anilina, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 199.
RMN-1!! (DMSO-de) δ: 1, 42-1,57 (1H, m) , 1,58-1,81 (3H, m) , 1,9820 2, 14(2H,m), 2,79(3H,s), 2,93(6H,s), 3, 12-3,58 (4H, m) , 3,67Pctição 870180138821, de 08/10/2018, pág. 795/857
787
3,80(lH,m), 3, 94-4,04 (lH,m), 4,37-4,50 (1, 5H, m) , 4,55 (2H,s), 4,67—4,80 (1Η,m), 5, 77-5,92(0,5H,m), 7,37(1H, dd, J=2, 4, 8, 6Hz) , 7,42(1Η,d,J=2,4Ηζ), 7,91 (1Η,d,J=8,6Hz), 8,74-8,81(1H,m),
9, 03-9, 19 (lH,m) , 10,79(lH,s).
MS (ESI) m/z: 577(M+H)+.
Exemplo 256 cloridrato de N1-(4-cloro-2-metóxi-fenil)-N2-((IS, 2R, 4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}10 ciclo-hexil)-etanodiamida:
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 364, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
RMN-1H (DMSO-de) δ: 1, 40-1, 55 (1H, m) , 1, 58-1,79 (3H, m) , 1,942,ll(2H,m), 2,77(3H,s), 2,92(6H,s), 3, 05-3, 55 (4H, m) , 3,653,75(lH,br), 3,90(3H,s), 3, 91-4, 00 (1H, m) , 4,36-4,47 (2H, br) ,
4,65-4,77(1H,br), 7,04(1H,dd,J=8,5, 2,OHz), 7,20(1H,d,J=2,O
Petição 870180138821, de 08/10/2018, pág. 796/857
788
Hz), 8, 06(1H, d,J=8,5Hz), 8,65-8,80(1H,br), 9,10-9,25(1H,br),
9,74(lH,s), 11,10-11,35(1H,br).
MS (ESI) m/z: 577(M+H)+.
Exemplo 257 cloridrato de N-{(IR,2S,5S)-2-{[2-(4-cloro-anilino)-2(hidróxi-imino)-acetil]-amino}-5-[(dimetil-amino)-carbonil]5-ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido desprotegendo o 10 composto obtido no Exemplo Referencial 366 pelo tratamento com ácido clorídrico, condensando o produto desprotegido com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
214.
ΗΜΝ^Η (DMSO-de) δ: 1, 41-1,53 (1H, m) , 1,57-1,77 (3H, m) , 1,882,04(2H,m), 2,77(3H,s), 2,91(6H,s), 3, 00-3, 60 (4H, m) , 3,653,74(lH,br), 3,87-3,96(1H,m), 4,37-4,48(2H,m), 4, 66-4,76(1H,
m) , 6, 70 (2H, d, J=8, 8Hz) , 7,04 (1H, d, J=8, 8Hz) , 7,10(lH,d,J=
Petição 870180138821, de 08/10/2018, pág. 797/857
789
8,8Hz), 8,40—8,53(2Η,m), 8,57-8, 66 (1Η, m) , 10,30-10,47 (lH,br), 10,66-10,76(1Η,br).
MS (ESI) m/z: 562(M+H)+.
Exemplo 258 cloridrato de N1-(4-cloro-fenil)-N2-((3R, 4S)-1-(2-metóxiacetil)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-piperidin-4-il)-etanodiamida:
O composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 367 pelo tratamento com ácido clorídrico, condensando o produto desprotegido com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
214 .
RMN-1!! (DMSO-de) δ: 1, 60-1, 72 (1H, m) , 1, 99-2,22 (1H, m) , 2,90 (3H,s), 3, 03-4, 80 (17H,m), 7,40 (2H, d, J=8,8Hz) , 7,83(2H,d,J=
8,8Hz), 8, 56-8, 73 (1H,br) , 9, 14-9, 33 (1H, br) , 10,83(lH,s),
11,20-11,55(lH,br).
MS (ESI) m/z: 549(M+H)+.
Exemplo 259 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((3R,4S)-1-(2Pctição 870180138821, de 08/10/2018, pág. 798/857
790 metóxi-acetil)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-piperidin-4-il)-etanodiamida:
O composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 368 pelo tratamento com ácido clorídrico, condensando o produto desprotegido com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
214 .
EMN-^ (DMSO-de) δ: 1, 60-1, 72 (1H, m) , 1, 98-2,20 (1H, m) , 2,90 (3H,s), 3,00-4,77(17H,m), 7,20-7,35(0,8H,br), 7,48-7,56 (0,2 H,br), 7,94-8,07(1H,br), 8,40-8,70(1H,br), 8,48-8,70(1H,br),
9,23-9,45(1H,br), 10,21-10,35(1H,br), 11,30-11,70(1H,br).
MS (ESI) m/z: 550(M+H)+.
Exemplo 260 cloridrato de N1-(5-bromo-piridin-2-il)-N2-((3R, 4S)-1-(2metóxi-acetil)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-piperidin-4-il)-etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 799/857
791
Ο composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 369 pelo tratamento com ácido clorídrico, condensando o produto desprotegido com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
214 .
RMN-1!! (DMSO-ds) δ: 1, 60-1,73 (lH,m), 1,97-2,20 (lH,m), 2,90 (3H,s), 3,03—3,52(7H,m), 3,64—4,07(5H,m), 4,10—4,50(4H,m),
4,65-4,78(lH,m), 7,28-7,35(0,2H,m), 7,97(1H,d,J=8,8Hz), 8,11 (1H,dd,J=8,8,2,2Hz),8,51(1H,d,J=2,2Hz),8,55-8,67(lH,m), 9,22
-9,41(lH,m), 10,20-10,31(0,8H,m), 11,25-11,70(1H,br).
MS (ESI) m/z: 594(M+H)+.
Exemplo 261 cloridrato de N1-(4-cloro-fenil)-N3-((IS, 2R, 4S)-4-[(dimetilamino) -carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo [5,4c]-piridin-2-il)-carbonil]-amino}-ciclo-hexil)-malonamida:
Petição 870180138821, de 08/10/2018, pág. 800/857
792 composto do título foi obtido condensando o composto obtido no Exemplo Referencial 371 com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 5.
RMN-1H (DMSO-de) δ: 1,32-1,50 (1H,m) , 1,55-1,87 (5H,m) , 2,78 (3H,m), 2,92(3H,s), 2,98 (3H,s), 2, 99-3, 00 (lH,m), 3,05-3,50 (5H,m), 3, 65-3, 75 (lH,m) , 3, 80-3, 92(1H,m), 4,35-4,45 (1H, m) ,
4,45-4,55 (lH,m), 4, 65-4,80(1H,m), 7,34(2H,d,J=8,8 Hz) , 7,58 (2H,d,J=8,8Hz), 8,00-8,10(1H,m), 8,30-8,40(1H,m), 1O,29(1H, d,J=12,5Hz), 12, 40(1H, br,s) .
MS (FAB) m/z: 561(M+H)+.
Exemplo 262 cloridrato de N1-(3-cloro-fenil)-N3-((IS, 2R, 4S)-4-[(dimetil15 amino)-carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4—
c]-piridin-2-il)-carbonil]-amino}-ciclo-hexil)-malonamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 373 com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira
Petição 870180138821, de 08/10/2018, pág. 801/857
793 similar àquela do processo descrito no Exemplo 5.
RMN-iH (DMSO-de) δ: 1,32-1,50(1H,m), 1,55-1,90 (5H, m) , 2,77 (3H,s), 2,91 (3H,s), 2,98 (3H,s), 2,99-3,00(1H,m), 3,05-3,50 (5H, m), 3,65-3,80(lH,m), 3,80-3,90(1H,m), 4,35-4,50 (lH,m),
4,50-4,60(lH,m), 4,65-4,80(1H,m), 7,09(1H,d,J=8,8Hz), 7,31 (lH,d, J=8,8Hz) ,7,38 (lH,t, J=8,8Hz) , 7,79(lH,s), 8,00-8,10 (lH,m), 8, 30-8, 40(lH,m), 10,28(1H,d,J=12,5Hz), 11,67 (1H, br, s) .
MS (FAB) m/z: 561(M+H)+.
Exemplo 263 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS,2R,4S)-4{[etil-(metil)-amino]-carbonil}-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
Adicionou-se 10% de paládio sobre carvão (0,3 g) a uma solução do composto obtido no Exemplo Referencial 404 (0,33 g) em etanol (20 ml), e a mistura foi agitada à temperatura ambiente por 24 h, sob uma atmosfera de hidrogênio. Depois de remover os insolúveis foram removidos por filtração através de um leito de Celite, e o filtrado
Petição 870180138821, de 08/10/2018, pág. 802/857
794 foi concentrado sob pressão reduzida. O resíduo resultante (0,37 g) foi dissolvido em N, N-dimetilformamida (20 ml), e adicionou-se sucessivamente o composto obtido no Exemplo 266, 1-hidróxi-benzotriazol monoidratado (0,2 g) e cloridrato de 1-(3-dimetil-amino-propil)-3-etil-carbodiimida (0,37 g) , agitando a mistura à temperatura ambiente por 18 h. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo resultante foi diluído com um solvente misto de clorofórmio e metanol (9:1) e lavado com uma solução aquosa saturada de bicarbonato de sódio e solução aquosa saturada de cloreto de sódio. Depois de secar a camada orgânica resultante sobre sulfato de sódio anidro, e remover o solvente por destilação sob pressão reduzida, o resíduo resultante foi purificado por cromatografia de coluna em sílica-gel (clorofórmio:metanol 95:5), concentrando a fração pretendida. Adicionou-se uma solução 1 N de ácido clorídrico em etanol, para formar um cloridrato. Este sal foi recristalizado em um solvente misto de metanol e dietil-éter, para obter o composto do título (0,28 g).
RMN-!H (DMSO-de) δ: 0, 95(1, 5H, t,J=6,9Hz), 1, 42(1, 5H,t,J=6,9
Hz), 1, 40-1, 52(lH,m), 1, 60-1, 78(3H,m), 1, 92-2,11(2H,m), 2,74 (3H,s), 2,90(3H,s), 3, 10-3,38(5H,m), 3, 40-3, 52(lH,m), 3,683,70(lH,m), 3, 96-4,05 (lH,m) , 4,41(2H,s), 4,7 0 (1H, d, J=15, 9
Hz), 8, 00-8, 01 (2H,m) , 8,44(lH,s), 8, 71 (1H, dd, J=10,1, 2,2
HZ), 9, 14(0, 5H,d,J=7,8Hz), 9, 22(0, 5H,d,J=8,3Hz), 10,24(0,5H,
s), 10,28(Ο,5H,S), 11,48(lH,br,s), 11,61(1H,br,s).
MS (FAB) m/z: 562(M+H)+.
de 08/10/2018, pág. 803/857
795
Exemplo 264 cloridrato de N1-(4-cloro-fenil)-N2-((IS, 2R, 4S)-4-{ [etil(metil)-amino]-carbonil}-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}5 ciclo-hexil)-etanodiamida:
composto do título foi obtido convertendo o composto obtido no Exemplo Referencial 404 em uma amina, condensando a amina com o composto obtido no Exemplo Referencial 374, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 263.
ΗΜΝ-Ή (DMSO-de) δ: 0, 97 (1,5H, t, J=6, 9Hz) , 1, 04 (1,5H, t, J=6, 9
Hz), 1,40-1,60(lH,m), 1,60-1,80(3H,m), 3,40-3,52 (lH,m),
3, 65-3, 80 (lH,m) , 3, 90-4,05 (1H, m) , 4,40 (2H,s), 4,70(lH,d,J=
15,9Hz), 7,39 (2H,d,J=8,8Hz), 7,82 (2H,d,J=8,8Hz), 8,75(1H, dd,J=10,l, 2,2Hz), 9,00(0,5H,d,J=7,8Hz), 9,08(0,5H,d,J=8,3
Hz), 10, 81(1H,d,J=4,9Hz), 11,45(1H,br,s).
MS (FAB) m/z: 561(M+H)+.
Exemplo 265 cloridrato de N1-(5-bromo-piridin-2-il)-N2-((IS, 2R, 4S)-4Pctição 870180138821, de 08/10/2018, pág. 804/857
796 {[etil-(metil)-amino]-carbonil}-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
composto do título foi obtido convertendo o 5 composto obtido no Exemplo Referencial 404 em uma amina, condensando a amina com o composto obtido no Exemplo Referencial 375, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 263.
EMN-iH (DMSO-de) δ: 1, 02(1,5H,t,J=6,9Hz), 1, 08(1,5H,t,J=6,9
Hz), 1,49-1,60(lH,m), 1,60-1,86(3H,m), 2,00-2,20(2H,m), 2,81 (3H,s), 2,97(3H,s), 3,15-3,42(6H,m), 3,50-3,60(1H,m), 3,703,82(lH,m), 4,48(2H,s), 4,77 (1H, d, J=15, 9Hz) , 8,04(lH,d,J=
8,8Hz), 8, 17(1H,d,J=8,8Hz), 8,58(lH,s), 8,78(1H,dd,J=10,1,
2,2Hz),9,21(0,5H,d,J=7,8Hz), 9, 29(0,5H,d,J=8,3Hz), 10,29 (0,5H,s), 10,33(0,5H,s), 11,53(0,5H,br,s), 11,65(0,5H,br,s).
MS (FAB) m/z: 607(M+H)+.
Exemplo 266 cloridrato de N1-(4-cloro-3-flúor-fenil)-N2-((IS,2R,4S)-420 [(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7Pctição 870180138821, de 08/10/2018, pág. 805/857
797 tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
composto do título foi obtido convertendo o composto obtido no Exemplo Referencial 252 em uma amina, condensando a amina com o composto obtido no Exemplo Referencial 378, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 263.
RMN-XH (DMSO-dg) δ: 1, 44-1, 52 (1H, m) , 1,65-1,76 (3H, m) , 2,0110 2, 07(2H,m), 2,77(3H,s), 2,93(6H,s), 2, 94-3, 00 (1H, m) , 3,103,38(3H,m), 3, 68-3, 70 (1H, m) , 3, 96-4, 05 (1H, m) , 4,42(2H,s),
4,70(1H,d,J=15,9Hz), 7,56(1H,t,J=8,8Hz), 7,68(1H,d,J=8,8Hz), 7,90(1H,dd,J=ll,7, 1,5Hz), 8,73(1H,dd,J=12,5, 7,3Hz), 9,06 (lH,dd,J=12,5, 8,1Hz), 11,01(1H,d,J=5,8Hz), 11,30-11,42 (1H,m).
MS (FAB) m/z: 565(M+H)+.
Exemplo 267
N-{(IR,2S,5S)-2-{[3-(4-cloro-fenil)-3-oxopropanoil]-amino}5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5-metil-4,5,6,720 tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 806/857
798
composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 383 pelo tratamento com ácido clorídrico, condensando o produto desprotegido com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
214 .
RMN-1!! (CDC13) (base livre) δ: 1,22-1,32 (1H, m) , 1,49-1, 92 (3H,
m) , 1,95-2,10(2H,m) , 2,53(3H,s), 2, 70-2, 79(1H, m) , 2,80-2,90 (2H,m), 2,93(6H,s), 2, 95-3, 09 (2H, m) , 3,72(2H,s), 3,87(2H,s),
4,05-4,19 (lH,m) , 4, 60-4,70 (1H, m) , 7,20-7, 40 (2H, m) , 7,42(2H, d,J=8,3Hz), 7,87(2H,d,J=8,3Hz) .
MS (FAB) m/z: 546(M+H)+.
Exemplo 268 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IR,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-5H-pirrolo[3,4-d]tiazol-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 807/857
799
O composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 386 pelo tratamento com ácido clorídrico, e condensando o produto desprotegido com o composto obtido no Exemplo Referencial 293, de uma maneira similar àquela do processo descrito no Exemplo 214. RMN-1H (DMSO-de) δ: 1, 00-2,35 (7H, m) , 2,96(3H,s), 3,04(3H,s), 3, 85-3, 95 (lH,m) , 3,88(3H,s), 4, 60-475 (1H, m) , 6,68(lH,d,J=
2,OHz), 7,17 (1H, d, J=2, OHz) , 7,20-7,32 (lH,m) 7,67 (lH,dd,J=
8,8, 2,8Hz), 7,99(1H,d,J=8,4Hz), 8,21(1H,d,J=8,8Hz), 8,25 (1H, d, J=2,8Hz),9,64 (1H,s) .
HRMS (FAB) m/z: 532, 1520(M+H)+.
(Calculado: C23H27CIN7O4S: 532, 1534).
Exemplo 269 cloridrato de N1-[(5-cloro-piridin-2-il)-amino]-N2((IR,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-etanodiamida:
O composto do título foi obtido reduzindo o composto obtido no Exemplo Referencial 387, de uma maneira similar àquela do processo descrito no Exemplo Referencial de 08/10/2018, pág. 808/857
800
253, e condensando o produto da redução com o composto obtido no Exemplo Referencial 266, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 208.
RMN-XH (DMSO-de) δ: 1,50-1,98(6H,m), 2,82(3H,s), 2,91 (3H,s), 2,95(3H,s), 2, 86-3, 92(7H,m) , 4,30-4,81(2H,m), 7,92-8,09(2H,
m) , 8,39-8,47 (lH,m) , 8, 56-8, 72 (2H, m) , 10,17(lH,s).
MS (ESI) m/z: 548(M+H)+.
Exemplo 270
N1-(4-cloro-fenil)-N2-((IS, 2R, 4S) -4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
O composto do título foi obtido reduzindo o composto obtido no Exemplo Referencial 387, de uma maneira similar àquela do processo descrito no Exemplo Referencial 253, e condensando o produto da redução com o sal de lítio obtido hidrolisando o composto obtido no Exemplo Referencial 242, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
de 08/10/2018, pág. 809/857
801
RMISI-1!! (DMSO-de) δ: 1,50-1, 97 (6H,m), 2,82(3H,s), 2,91(3H,s), 2,98(3H,s), 2,83-3, 88 (7H,m) , 4,30-4,7 9 (2H, m) , 7,37(2H,d,
J=8,8Hz), 7,89(2H,d,J=8,8Hz), 8,34(1H,d,J=8,4Hz), 8,63(lH,d, J=8,8Hz), 10,72 (1H,s) .
MS (ESI) m/z: 547(M+H)+.
Exemplo 271 cloridrato de N1-{ (IR,2S,5S)-2-{ [ (5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}N2- (piridin-4-il)-etanodiamida:
O composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 310 pelo tratamento com ácido clorídrico, condensando o composto 2-[(piridin-4il)-amino]-2-oxoacetato de lítio obtido hidrolisando o composto obtido no Exemplo Referencial 261, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
191.
EMN-iH (DMSO-de) δ: 1,40-2, 01 (6H,m) , 2,79(3H,s), 3,01 (3H,s), 3,00-3,18(lH,m) , 4,02-4,19(1H,m) , 4,45-4,55(1H,m) , 7,O9(1H,
s), 7,13-7,22(lH,m), 7,41(1H,d,J=8,4Hz), 7,64(1H,br,s), 8,28
Petição 870180138821, de 08/10/2018, pág. 810/857
802 (2Η,d,J=6,8Ηζ), 8, 36(1H,d,J=8,OHz), 8, 62 (1H, d, J=8, 8Hz) , 8,72 (2H, d, J=6, 8Hz) , ll,74(lH,s), ll,83(lH,s).
MS (FAB) m/z: 511(M+H)+.
Exemplo 272 cloridrato de N1-{ (IR,2S,5S)-2-{ [ (5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}N2- (piridin-3-il)-etanodiamida:
O composto do título foi obtido usando 2[(piridin-3-il)-amino]-2-oxoacetato de metila obtido condensando 3-amino-piridina com 2-cloro-2-oxoacetato de metila, de uma maneira similar àquela do processo descrito no Exemplo Referencial 242, e o composto obtido no Exemplo Referencial 310, como matérias-primas, de uma maneira similar àquela do processo descrito no Exemplo 271.
RMN-1H (DMSO-de) δ: 1, 40-2,05 (6H, m) , 2,80(3H,s), 3,02(3H,s),
2,92-3,15 (lH,m), 4,02-4,17(1H,m), 4,42-4,58(1H,m), 7,1O(1H,
s), 7,12-7,19(lH,m), 7,40(1H,d,J=8,4Hz), 7,62-7,87(2H,m),
8,36-8, 64 (4H,m) , 9,18(lH,s), ll,39(lH,s), ll,79(lH,s).
MS (FAB) m/z: 511(N+H)+.
Petição 870180138821, de 08/10/2018, pág. 811/857
803
Exemplo 273 cloridrato de N1-{(IR,2S,5S)-2-{[(5-cloro-indol-2-il)carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}N2- (piperidin-4-il)-etanodiamida:
Adicionou-se uma solução 4 N (8,0 ml) de ácido clorídrico em dioxano a uma solução do composto obtido no
Exemplo Referencial 389 (400 mg) em etanol (5,0 ml) à temperatura ambiente, e a mistura foi agitada na mesma temperatura por 5 h. O solvente foi removido por destilação sob pressão reduzida, o resíduo foi lavado com cloreto de metileno, e os insolúveis foram removidos por filtração e lavados, para obter o composto do título (320 mg).
RMIS!-1!! (DMSO-de) δ: 1,38-1, 92 (1OH,m) , 2,77(3H,s), 2,96(3H,s), 2,82-3, 35(6H,m), 3,88-4,10(2H,m) , 4,34-4,43(1H,m) , 7,O5(1H,
s), 7,11-7,17(lH,m) , 7,38(1H,d,J=8,8Hz) , 7,65(lH,s), 8,25 (lH,d,J=8,OHz), 8, 34(1H,d,J=7,6Hz), 8, 89(1H,d,J=8,4Hz), ll,75(lH,s) .
MS (ESI) m/z: 517(M+H)+.
Exemplo 274 cloridrato de N1-{ (IR,2S,5S)-2-{ [(5-cloro-indol-2-il)Petição 870180138821, de 08/10/2018, pág. 812/857
804 carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclo-hexil}N2- (1-metil-piperidin-4-il)-etanodiamida:
O composto do título foi obtido metilando o composto obtido no Exemplo Referencial 273, de uma maneira similar àquela do processo descrito no Exemplo Referencial 9, e tratando-o com ácido clorídrico.
RMN-1H (DMSO-de) δ: 1,40-2, 01 (11H,m) , 2,67 (3H,s), 2,98 (3H,
s), 2,85-4,48(7H,m), 7,07(lH,s), 7,16(1H,dd,J-8,8,2,OHz),
7,40(1H,d,J=8,8Hz), 7,68(1H,d,J=2,OHz), 8,25-8,35(1H,m),
8,37(lH,d,J=7,6Hz), 8,90-9,02(1H,m), 9,82(1H,br,s), 11,78 (1H,S) .
MS (ESI) m/z: 531(M+H)+.
Exemplo 275 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-415 [(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil))-N1-metil-etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 813/857
805
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 390, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
EMN-iH (DMSO-de) δ: 1, 32-1, 97 (6H, m) , 2,42-2,51 (1H, m) , 2,76 (3H,s), 2,91(3H,s), 2,93(3H,s), 3,27(3H,s), 3, 00-, 80 (8H, m) ,
7,45(lH,br,s), 7, 88-7, 97 (1H, m) , 8,25-8,41(2H,m), 8,78-8,91 (lH,m) .
MS (FAB) m/z: 562(M+H)+.
Exemplo 276 cloridrato de N1-(5-cloro-pirimidin-2-il)-N2-((IS, 2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,715 tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 814/857
806
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 391, condensando o hidrolisado com o composto obtido no Exemplo Referencial 253, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 191.
ΗΜΝ-^ (DMSO-de) δ: 1,38-2, 10 (7H, m) , 2,77(3H,s), 2,90(3H,s), 2,93(3H,s), 3, 04-4, 80 (8H,m) , 8, 60-8,70 (2H, m) , 8,82(2H,s),
9,08(lH,br,s), 10, 64(1H, s) , 11,57(1H,br,s) .
MS (FAB) m/z: 549(M+H)+.
Exemplo 277 cloridrato de N1-(4-cloro-fenil)-N2-((IS, 2R, 4S)-4-{ [etil(metil)-amino]-carbonil}-2-{[(5-metil-5,6-diidro-4Hpirrolo[3,4-d]-tiazol-2-il)-carbonil]-amino}-ciclo-hexil)-
O composto do título foi obtido reduzindo o 20 composto obtido no Exemplo Referencial 392, de uma maneira similar àquela do processo descrito no Exemplo Referencial 253, e condensando o produto da redução com o ácido carboxílico obtido hidrolisando o composto obtido no Exemplo
Petição 870180138821, de 08/10/2018, pág. 815/857
807
Referencial 242, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 195.
ΗΜΝ-^ (DMSO—dô) δ: 0,96, l,02(3H,cada t,J=7,OHz), 1,47-1,58 5 (lH,m), 1, 65-1,77 (3H,m), 1, 98-2, 08(2H,m), 2,76-2,91(4H,m),
3,07(3H,s), 3,19—3,41(2H,m), 3, 98-4,04(1H,m), 4,42 (1H,br,s), 4,46-4,94(4H,m), 7,41(2H,d,J=8,8Hz), 7,83(2H,d,J=8,8Hz),
8,74-8,80 (lH,m) , 9, 02 (1H, d, J=7, 3Hz) , 10,82(lH,s), 12,41(1H, br, s) .
MS (FAB) m/z: 547(M+H)+.
Exemplo 278 cloridrato de N1-(5-bromo-piridin-2-il)-N2-((IS,2R,4S)-4{[etil-(metil)-amino]-carbonil}-2-{[(5-metil-5,6-diidro-4Hpirrolo[3,4-d]-tiazol-2-il)-carbonil]-amino}-ciclo-hexil)15 etanodiamida:
O composto do título foi obtido a partir do 20 composto obtido no Exemplo Referencial 392 e do composto obtido no Exemplo Referencial 262, de uma maneira àquela do processo descrito no Exemplo 277.
Petição 870180138821, de 08/10/2018, pág. 816/857
808
RMN-1H (DMSO-de) δ: 0,90-1,08(3Η,m), 1,40-2,13(6Η,m), 2,703,53(13H,m), 3, 92-4, 08 (1Η, m) , 4,35-4,47 (1Η, m) , 7,95(lH,d,J=
8,8Ηζ), 8,10(1Η,dd,J=8,8, 2,4Hz), 8,50-8,55(1Η,m), 8,68-8,78 (lH,m), 9, 12-9, 18 (lH,m) , 10,26(lH,s).
MS (FAB) m/z: 592(M+H)+.
Exemplo 279 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS,2R,4S)-4{[etil-(metil)-amino]-carbonil}-2-{[(5-metil-5,6-diidro-4Hpirrolo[3,4-d]-tiazol-2-il)-carbonil]-amino}-ciclo-hexil)10 etanodiamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 392 e do composto obtido no Exemplo Referencial 243, de uma maneira àquela do processo descrito no Exemplo 277.
RMN-1H (DMSO-de) δ: [0, 95 (t, J=7, OHz) , 1, 01 (t, J=6, 8Hz) , 3H] ,
1,45-1,72 (4H,m) , 1, 96-2, 07 (2H, m) , 2,74-2, 90 (4H, m) , 3,06(3H,
s), 3,18-3,40 (2H,m) , 3, 95-4,02 (1H, m) , 4,41(1H,br,5), 4,544,90 (4H,m), 8, 00 (2H, br, s) , 8,45(lH,s), 8,70-8,75 (1H, m) ,
9,15 (lH,br,s), 10, 27 (1H, br, s) , 12,2 9 (1H, br, s) .
MS (ESI) m/z: 548(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 817/857
809
Exemplo 280 cloridrato de N1-(4-cloro-3-metóxi-fenil)-N2-((IS, 2R, 4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}5 ciclo-hexil)-etanodiamida:
O composto do título foi obtido condensando o 10 composto obtido no Exemplo Referencial 395 com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 2.
RMN-1!! (DMSO-dg) δ: 1, 46-1,54 (1H, m) , 1,67-1,77 (3H, m) , 2,0115 2,10(2H,m), 2,79(3H,s), 2, 92-2, 98 (7H, m) , 3, 21 (2H, br, s) , 3,49 (lH,br,s), 3, 69 (lH,br, s) , 3,80(3H,S), 3, 98-4,03 (1H, m) , 4,424,50(2H,m), 4, 69 (1H, br, s) , 7,37 (1H, d, J=8,7Hz) , 7,48(lH,dd,
J=8,7, 2,2Hz), 7,72(1H,d,J=2,2Hz), 8,75(1H,d,J=7,3Hz), 9,06 (lH,br,s), 10,77(lH,s), 11,44 (1H, br, s) .
MS (FAB) m/z: 577(M+H)+.
Exemplo 281 cloridrato de N1-(4-cloro-fenil)-N2-((IR*,2R*)-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]Petição 870180138821, de 08/10/2018, pág. 818/857
810
O composto do título foi obtido hidrolisando o composto obtido no Exemplo Referencial 242, condensando o hidrolisado com o composto obtido no Exemplo Referencial 62, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 195.
RMN-1!! (DMSO-dg) δ: 1, 65-1, 73 (4H, m) , 1,91-1,96 (2H, m) , 2,91 (3H,s), 3,15(2H,br,s), 3, 49 (1H, br, s) , 3, 66 (1H, br, s) , 4,324,42(3H,m), 4, 66 (1H, br, s) , 7,40(2H,d,J=8,9Hz), 7,84(2H,d,J=
8,9 Hz), 8,92(1H,d,J=8,5Hz), 9,03(1H,d,J=8,3Hz), 10,76 (1H,
s) , 11,32 (lH,br, s) .
MS (FAB) m/z: 462(M+H)+.
Exemplo 282 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IR*,2R*)-ΣΙ [(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)20 carbonil]-amino}-ciclo-pentil)-etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 819/857
811 composto do título foi obtido condensando o composto obtido no Exemplo Referencial 62 com o composto obtido no Exemplo Referencial 266, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 208.
RMN-1H (DMSO-de) δ: 1,71 (4H, br, s) , 1, 96 (2H, br, s) , 2,90(3H,s), 3, 14(1H,br,s), 3, 21(1H,br,s), 3, 47(1H,br,s), 3, 68(1H,br,s),
4,34-4,45 (3H,m), 4,66(1H,br,s), 7, 99-8, 06 (2H, m) , 8,43-8,44 (lH,m), 8, 94(1H,d,J=8,3Hz), 9, 20(1H,d,J=8,5Hz), 10,20(lH,br,
s) , 11,78 (1, lH,br, s) .
MS (FAB) m/z: 463 (M+H)+.
Exemplo 283
N1-((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]15 amino}-ciclo-hexil)-N2-(4-etil-fenil)-etanodiamida:
O composto do título foi obtido condensando o 20 composto obtido no Exemplo Referencial 252 com o composto obtido no Exemplo Referencial 397, de uma maneira similar àquela do processo descrito no Exemplo 263.
Petição 870180138821, de 08/10/2018, pág. 820/857
812
RMN-1H (CDC13) δ: 1, 67-2, 16 (6H,m) , 2,51(3H,s), 2,76-2, 91 (5Η,
m) , 2,94(3H,s), 3,04(3H,s), 3,07(lH,s), [ 3, 65 (1H, d, J=15, 5
Hz), 3,73(lH,d,J=15,5Hz)AB pattern], 4,09-4,16(1H,m), 4,724,75(lH,m), 7,42-7,46(3H,m), 7,58 (2H, d, J=8, 5Hz) , 8,02(lH,d,
J=8,1Hz), 9,36 (1H,s) .
MS (FAB) m/z: 537(M+H)+.
Exemplo 284 cloridrato de N1-(5-cloro-pirazin-2-il)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,710 tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 253 com o composto obtido no Exemplo Referencial 399, de uma maneira similar àquela do processo descrito no Exemplo 97, e depois tratando o produto da condensação com ácido clorídrico.
RM!!-^ (DMSO-de) δ: 1, 44-1,52 (1H, m) , 1, 65-1,77 (3H, m) , 2,002,10 (2H,m), 2,77(3H,s), 2, 91-2, 97 (7H, m) , 3, 20 (2H, br, s) ,
3,48 (lH,br,s), 3,68(1H,br,s), 3, 97-4,02(1H,m), 4,40-4,46 (2H,m), 4,68(lH,br,s), 8, 64(1H,d,J=1,2Hz), 8,70(1H,d,J=7,3
Petição 870180138821, de 08/10/2018, pág. 821/857
813
Hz), 9,02(lH,s), 9, 21 (1H, br, s) , 10, 91 (1H, br, s) , 11,5O(1H, br, s) .
MS (FAB) m/z: 549(M+H)+.
Exemplo 285 cloridrato de N1-(4-cloro-3-nitro-fenil)-N2-((IS, 2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,Ίtetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto do título foi obtido condensando o 10 composto obtido no Exemplo Referencial 253 com o composto obtido no Exemplo Referencial 400, de uma maneira similar àquela do processo descrito no Exemplo 97, e depois tratando o produto da condensação com ácido clorídrico.
RMN-iH (DMSO-de) δ: 1, 44-1,53 (1H, m) , 1,66-1,73(3H,m), 1,9715 2, 07(2H,m), 2,77(3H,s), 2,89—3, 05 (7H, m) , 3, 20 (2H, br, 5) , 3,55 (2H,br,s), 4, 00 (lH,br, s) , 4, 44 (1H, br, s) , 4,52 (2H, br, s) , 7,75 (1H, d, J=8, 8Hz) , 8, 08 (1H, d, J=8, 8Hz) , 8,59(lH,s), 8,71 (lH,d,
J=7,3Hz), 9,07 (lH,d, J=8,OHz) , ll,24(lH,s), 11,58 (1H, br, s) .
MS (FAB) m/z: 592(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 822/857
814
Exemplo 286 cloridrato de N1-(4-cloro-2-nitro-fenil)-N2-((IS, 2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
composto do título foi obtido condensando o 10 composto obtido no Exemplo Referencial 253 com o composto obtido no Exemplo Referencial 401, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 208.
ΗΜΝ-Ή (DMSO-de) δ: 1, 46-1,54 (1H, m) , 1, 66-1,77 (3H, m) , 2,0315 2,10(2H,m), 2,79(3H,s), 2,90-2,93(7H,m), 3,17-3,28(2H,m),
3, 49 (lH,br, s) , 3, 68 (1H, br, s) , 3, 99-4, 04 (1H, m) , 4,41(lH,br,
s), 4,46(lH,br,s), 4,68(1H,br,s), 7, 89(1H,d,J=9,OHz), 8,208,21 (2H,m), 8, 73 (1H, d, J=6, 4Hz) , 9, 28 (1H, br, s) , ll,49(lH,br,
s) , 11,56 (1H, s) .
MS (FAB) m/z: 592(M+H)+.
Exemplo 287 cloridrato de N1-(3-amino-4-cloro-fenil)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7Pctição 870180138821, de 08/10/2018, pág. 823/857
815 tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:

O composto obtido no Exemplo 285 (236 mg) foi dissolvido em etanol (25 ml) e adicionou-se uma quantidade catalítica de níquel de Raney, agitando a mistura à temperatura ambiente por 17 h sob uma atmosfera de hidrogênio. Depois disso, adicionou-se mais uma quantidade catalítica de níquel de Raney, agitando a mistura por mais 7 h. O catalisador foi removido por filtração, e o solvente foi removido por destilação sob pressão reduzida. O resíduo foi purificado por cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 23:2), para obter um sólido amarelo-pálido (101 mg) . Este produto foi dissolvido em cloreto de metileno, e adicionou-se uma solução 1 N (360 μΐ) de ácido clorídrico em etanol. O solvente foi removido por destilação sob pressão reduzida, adicionou-se uma pequena quantidade de metanol ao resíduo, e adicionou-se dietil-éter em gotas, enquanto se irradiava com ondas ultra-som, coletando o precipitado formado. Este produto foi lavado com dietil-éter, para obter o composto do título (95 mg).
de 08/10/2018, pág. 824/857
816
RMN-iH (DMSO-de) δ: 1, 45-1,53 (1Η, m) , 1,66-1,73(3Η,m), 1,972,10(2H,m), 2,78(3H,s), 2, 91-2, 94 (7Η, br, s) , 3,11-3,19 (1H,
m) , 3,29 (lH,br,s), 3,48 (lH,br,s), 3, 69 (1H, br, s) , 3,95—4,02 (lH,m), 4,44 (2H, br, s) , 4, 68, 4,72(1H, cada br,s), 4,86 (2,5H,br,s), 6, 98(1H,dd,J=8,5, 1,9Hz), 7,14(1H,d,J=8,5Hz),
7,35, 7, 38 (1H, cada br,s), 8, 72—8, 77(1H,m) [8,91(d,J=7,8Hz),
8,99(d,J=8,5Hz),1H], 10,45, 10,47(1H,cada br,s), 11,74(1H, br, s) ,
MS (FAB) m/z: 562(M+H)+.
Exemplo 288 cloridrato de N1-(2-amino-4-cloro-fenil)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto do título foi obtido a partir do composto obtido no Exemplo 286, de uma maneira similar àquela do processo descrito no Exemplo 287.
ΚΜΝ-^ (DMSO-de) δ: 1, 45-1, 77 (4H, m) , 2, 06-2,09 (2H, m) , 2,78 (3H,s), 2,92 (7H,br,s), 3,12-3,19(1H,m), 3, 26-3, 28(1H,m),
3, 48 (lH,br,s), 3,70(1H,br,s), 4, 00-4,44(5, 7H,m), 4,70, 4,74
Petição 870180138821, de 08/10/2018, pág. 825/857
817 (lH,cada br,s), 6, 63—6, 66 (1H, m) , 6,85(1H,br,s), 7,18—7,21 (1
H,m), 8,77-8,81(lH,m), [8,97(d,J=7,8Hz), 9,06(d,J=8,1Hz),
1H], 9,98(lH,s), 11, 60 (lH,br, s) .
MS (FAB) m/z: 562(M+H)+.
Exemplo 289 cloridrato de N1-(6-cloro-4-metil-piridin-3-il)-N2((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-etanodiamida:
O composto do titulo foi obtido condensando o composto obtido no Exemplo Referencial 270 com o composto obtido no Exemplo Referencial 402, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 199.
EMN-^ (DMSO-de) δ: 1, 45-1,54 (1H, m) , 1, 65-1,77 (3H, m) , 2,022,08 (2H,m), 2,22(3H,s), 2,79(3H,s), 2,89-2, 93 (7H, m) , 3,19 (2H,br,s), 3,54(2H,br,s), 13,99-4,04(1H,m), 4,40-4,42(1H,m), 4,50 (2H,br, s) , 7,49(lH,s), 8,32(lH,s), 8,75 (1H, d, J=7, 1Hz) ,
9, 09 (1H, d, J=7,3Hz) , 10,48(lH,s), 11,40 (0, 9H, br, s) .
MS (FAB) m/z: 562(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 826/857
818
Exemplo 290 cloridrato de N-{ (IR, 2S,5S)-2-({[(E)-2-(4-cloro-fenil)diazenil]-carbonil}-amino)-5-[(dimetil-amino)-carbonil]ciclo-hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5, 4-c]piridino-2-carboxamida:
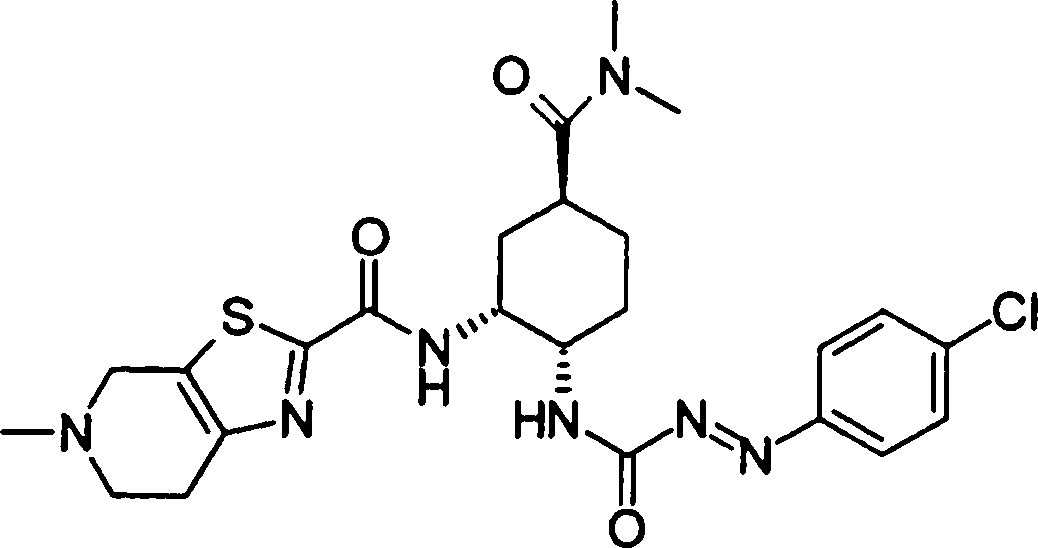
Depois de adicionar 10% de paládio sobre carvão (200 mg) a uma solução do composto obtido no Exemplo Referencial 252 (700 mg) em tetraidrofurano (10 ml) e agitar a mistura à temperatura ambiente por 2 dias sob uma atmosfera de hidrogênio, a mistura da reação foi filtrada e o composto obtido no Exemplo Referencial 405 (470 mg) foi adicionado a uma solução de uma amina obtida concentrando o filtrado em formamida (5,0 ml), agitando a mistura a 95 °C por 18 h. Depois de concentrar a mistura da reação e adicionar uma solução aquosa saturada de bicarbonato de sódio (50 ml) , água (50 ml) e cloreto de metileno (30 ml) , para conduzir separação de líquidos, a camada aquosa resultante foi extraída com cloreto de metileno (2 x 20 ml). As camadas orgânicas foram combinadas, secadas sobre sulfato de sódio anidro, concentradas e purificadas por de 08/10/2018, pág. 827/857
819 cromatografia de coluna em sílica-gel (cloreto de metileno:metanol 12:1). Este produto purificado foi tratado com uma solução 1 N de ácido clorídrico em etanol, para obter o composto do título (100 mg).
ΚΜΝ-^ (DMSO-de) δ: 1, 40-1, 60 (lH,m) , 1, 65-2,05 (5H, m) , 2,80 (3H,s), 2,91(3H,s), 2,99(3H,s), 3, 00-3, 20 (2H, m) , 3,20-3,32 (lH,m), 3,43(1H,br,s), 3,69(1H,br,s), 3,95(1H,br,s), 4,45 (lH,br,s), 4, 60-4, 80 (2H,m) , 7, 68 (2H, d, J=8,7Hz) , 7,83(2H,d,
J=8,7Hz), 8,41 (lH,br,s), 8,68(1H,d,J=7,6Hz), 11,40-11,80(1H, br) .
MS (ESI) m/z: 532(N+H)+.
Exemplo 291 cloridrato de N-{(IR,2S,5S)-2-({2-(4-cloro-fenil)hidrozina]carbonil}amino)-5-[(dimetil-amino)carbonil]ciclo-hexil}-515 metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido mudando as 20 condições da reação na reação descrita no Exemplo 290 para condições nas quais a agitação foi conduzida a 40 °C por 3 dias.
Petição 870180138821, de 08/10/2018, pág. 828/857
820
RMN-XH (DMSO-de) δ: 1, 30-1, 50 (1Η, m) , 1,50-1,80 (3H, m) , 1,80l,97(2H,m), 2,76(3H,s), 2,80-3, 05 (2Η, m) , 2,91(6H,s), 3,053,30(2H,m), 3, 47(2H,br,s), 4,30-4,50(2H,m), 4,72(1H,t,J=12,8 Hz), 6,40-6,60(2H,m), 6,55-6,70(2H,m), 6, 95-7,20(2H,m),
7,88 (lH,d,J=ll,3Hz), 8,48-8,65(1H,m), 11,48-11,80(1H,br).
MS (ESI) m/z: 534(M+H)+.
Exemplo 292 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(4,5,6,710 tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 34 com o composto obtido no Exemplo Referencial 420, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 17.
RMN-XH (DMSO-de) δ: 1, 45-1,55 (1H, m) , 1, 60-1,80 (3H, m) , 1,952,10 (2H,m), 2,78(3H,s), 2, 85-3, 00 (4H, m) , 3,ll(2H,br s) ,
3,40-3,55 (2H,m), 3,95-4,07(1H,m), 4,37-4,45(1H,m), 4,48(2H, brs), 8,00-8,01(2H,m), 8,10(1H,d,J=7,1Hz), 8,43-8,47(1H,m),
9, 16 (1H, d, J=7,8Hz) , 9, 43 (2H, br s) , 10,27(lH,s).
Petição 870180138821, de 08/10/2018, pág. 829/857
821
MS (FAB) m/z: 534(M+H)+.
Exemplo 293 cloridrato de N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-1-[(1-hidróxi-ciclo-propil)-carbonil]5 piperidin-3-il)- 5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 118 com o ácido 1hidróxi-ciclo-propano-carboxílico, e depois, tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 150.
RMN-iH (DMSO-de) δ: 0,60-0,90(3H,br), 0, 92-1, 03 (1H, m) , 1,711,84 (lH,m), 1, 85-2, 03 (lH,m) , 2,91(3H,s), 3,00-3, 80 (7H,m),
4,05-4,80 (5H,m) , 6, 28-6, 42 (1H, br) , 7,09(lH,s), 7,18 (lH,dd,
J=8,8, 1,5Hz), 7,42(1H,d,J=8,8Hz), 7,70(1H,d,J=l,5Hz), 8,148,29(lH,br), 8,41 (1H, br d, J=7, 6Hz) , ll,83(lH,s).
MS (ESI) m/z: 557(M+H)+.
Exemplo 294 cloridrato de N-((3R*,4S*)-4-{[(5-cloro-indol-2-il)carbonil]-amino}-!-[(1-metóxi-ciclo-propil)-carbonil]piperidin-3-il)- 5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]Petição 870180138821, de 08/10/2018, pág. 830/857
822 piridino-2-carboxamida:
0 composto do título foi obtido condensando o composto obtido no Exemplo Referencial 118 com o composto obtido no Exemplo Referencial 409, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 150.
RMN-1H (DMSO-de) δ: 0, 65-1,05 (4H,m) , 1,74-1,88 (lH,m) , 1,922,10(lH,m), 2,91(3H,s), 3, 00-3, 80 (1OH, m) , 4,05-4,83 ( 6H, m) ,
7,08(lH,s), 7,18(1H,dd,J=8,6, 2,OHz), 7,42(1H,d,J=8,6Hz),
7,71(1H,d,J=2,0Hz), 8,08-8,30(1H,br), 8,41(1H,br d,J=7,8Hz), 10, 60-10,80 (0,5H,br) , 10, 85-11,05 (0, 5H, br) , 11,84(1H,5).
Exemplo 295 cloridrato de 7-cloro-N-((3R,4S)-1-(2-metóxi-acetil)-3-{[(5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)carbonil]-amino}-piperidin-4-il)-3-isoquinolino-carboxamida:
Petição 870180138821, de 08/10/2018, pág. 831/857
823 composto do título foi obtido tratando o composto obtido no Exemplo Referencial 410 com uma solução 4 N de ácido clorídrico em dioxano para desprotegê-lo, condensando o produto desprotegido com o composto obtido no
Exemplo Referencial 10, e depois submetendo o produto da condensação a um novo tratamento com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
219.
ΗΜΝ-^ (DMSO-de) δ: 1, 60-1,80 (1H, m) , 2, 13-2,38 (1H, m) , 2,90(3
H,s), 3, 00-3, 87 (10H,m), 3,89-4,10 (2H,m), 4, 15-4,58 (4H, m) ,
4,60-4,78(lH,m), 7,89(1H,d,J=8,8Hz), 8,25(1H,d,J=8,8Hz),
8,37(lH,s), 8,61(lH,s), 8,70-8,95(1H,m), 11,45-11,65(0,5H, br) .
MS (ESI) m/z: 557(M+H)+.
Exemplo 296 cloridrato de N1-(4-cloro-3-flúor-fenil)-N2-((3R, 4S)-1-(2metóxi-acetil)-3-{[(5-meti1-4,5,6,7-tetraidrotiazolo[5,4-c]piridin-2-il)-carbonil]-amino}-piperidin-4-il)-etanodiamida:
O composto do título foi obtido tratando o 20 composto obtido no Exemplo Referencial 411 com uma solução 4 N de ácido clorídrico em dioxano para desprotegê-lo,
Petição 870180138821, de 08/10/2018, pág. 832/857
824 condensando o produto desprotegido com o composto obtido no Exemplo Referencial 10, e depois submetendo o produto da condensação a um novo tratamento com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo
219.
RMN-1H (DMSO-de) δ: 1, 60-1,72 (1H, m) , 1, 98-2,21 (1H, m) , 2,91 (3H,s), 3, 00-3, 52(9H,m), 3, 56-4, 05(3H,m), 4,08-4,50(4H,m), 4,60-4,78(1H,br), 7, 56(1H,t,J=8,8Hz), 7,70(1H, d,J=9,OHz),
7,91(1H,dd,J=8,8, 2,3Hz), 8,50-8,72(1H,m), 9,15-9,35(1H,m), ll,02(lH,s), 11,15-11,33(0,5H,br), 11,35-11,50(0,5H,br).
MS (FAB) m/z: 567(M+H)+.
Exemplo 297 cloridrato de N1-(5-cloro-2-tienil)-N2-((3R,4S)-1-(2-metóxiacetil)-3-{[(5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]15 piridin-2-il)-carbonil]-amino}-piperidin-4-il)-etanodiamida:
°γν
O composto do título foi obtido tratando o 20 composto obtido no Exemplo Referencial 412 com uma solução 4 N de ácido clorídrico em dioxano para desprotegê-lo, condensando o produto desprotegido com o composto obtido no Exemplo Referencial 10, e depois submetendo o produto da condensação a um novo tratamento com ácido clorídrico, de
Petição 870180138821, de 08/10/2018, pág. 833/857
825 uma maneira similar àquela do processo descrito no Exemplo
219.
RMN-iH (DMSO-d6) δ: 1, 60-1,73 (1H,m) , 1, 96-2, 19 (1H, m) , 2,91 (3H,s), 3, 04-3, 54(9H,m), 3, 60-4, 05(3H,m), 4,07-4,34(3H,m),
4,35-4,54(1H,br), 4, 60-4, 80(1H,br), 6, 89(1H, d, J=4,2Hz) , 6,93 (1H,d,J=4,2Hz), 8, 48-8, 70(lH,m), 9,18-9,40(1H,m), 12,31 (lH,s) .
MS (ESI) m/z: 555(M+H)+.
Exemplo 298 cloridrato de N-{(IR,2S,5S)-2-{[2-(4-cloro-fenóxi)-acetil]amino)-5-[(dimetil-amino)-carbonil]-ciclo-hexil}-5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2-carboxamida:
O composto do título foi obtido reduzindo o composto obtido no Exemplo Referencial 252, condensando o produto da redução com o ácido p-cloro-fenóxi-acético, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 223.
RMN-1!! (DMSO-de) δ: 1, 35-1,47 (lH,m), 1,55-1, 90 (5H, m) , 2,77(3
H,s), 2,92(3H,s), 2,96(3H,s), 2, 98-3, 10 (1H, m) , 3,10-3,80 (3H,m), 3,85—3,95(1H,m), 4,35—4,50(4H,m), 4,50-4,80(1H,br),
Petição 870180138821, de 08/10/2018, pág. 834/857
826
6,85(2Η,d,J=8,5Ηζ), 7,15-7,35(1H,br), 7,88-8,03(1H,br), 8,46 (1H,d,J=8,8Hz), 11,30-11, 65 (lH,br) .
MS (FAB) m/z: 534(M+H)+.
Exemplo 299 cloridrato de 7-cloro-N-((IS,2R,4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-5H-pirrolo[3,4-d]tiazol-2-il)carbonil]-amino}-ciclo-hexil)-3-isoguinolino-carboxamida:
O composto do título foi obtido condensando o sal de lítio do ácido carboxílico obtido no Exemplo Referencial
413 com um composto obtido desprotegendo o composto obtido no Exemplo Referencial 146 pelo tratamento com um ácido, e depois tratando o produto da condensação com ácido clorídrico.
RMN-1H (DMSO-de) δ: 1,00-1, 11 (2H, m) , 1,45-1,60 (1H, m) , 1,6515 l,85(lH,m), 1,95-2,06(1H,m), 2,10-2,24(1H,m), 2,78(3H,s),
2,87-3, 02 (lH,m) , 2,94(3H,s), 3,88(3H,s), 4, 16-4,27 (1H, m) ,
4,45-4,56 (lH,m) , 7,03(lH,s), 7,55(lH,s), 7,87 (lH,br d, J=8,3 Hz), 8,24(lH,br d,J=8,8Hz), 8,33(lH,s), 8,59(lH,s),
8,85 (lH,br d, J=7, 6Hz) , 9, 01 (1H, br d, J=7,8Hz) , 9,28(lH,s).
MS (ESI) m/z: 539(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 835/857
827
Exemplo 300 cloridrato de N-{(IR,2S,5S)-2-{[(6-cloro-4-oxo-4H-cromen-2il)-carbonil]-amino}-5-[(dimetil-amino)-carbonil]-ciclohexil }-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-25 carboxamida:
O composto do título foi obtido condensando um 10 composto obtido tratando o composto no Exemplo Referencial 417 com uma solução 4 N de ácido clorídrico em dioxano com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 219. 15 RMN-1!! (DMSO-de) δ: 1, 40-1,53 (1H, m) , 1,67-2,04 (5H, m) , 2,402,53(lH,m), 2,80(3H,s), 2,92(3H,s), 3,01(3H,s), 3,09-3,22 (3H,m), 3, 66-3, 77 (lH,m), 4,01-4,10 (1H,m), 4,34-4,49(1H,m),
4,58-4,76(2H,m), 6,80(1H,d,J=4,9Hz), 7,59-7,70(1H,m), 7,908,00(lH,m), 7,96(lH,s), 8,52-8, 60 (1H, m) , 8,80-8, 90 (1H, m) ,
11, 10-11,25(0,5H,br), 11,40-11,55 (0, 5H,br) .
MS (ESI) m/z: 572(M+H)+.
Exemplo 301 cloridrato de 7-cloro-N-((3R,4S)-1-(2-metóxi-acetil-3-{[(-5metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)Petição 870180138821, de 08/10/2018, pág. 836/857
828 carbonil]-amino}-piperidin-4-il)-3-cinolino-carboxamida:
composto do titulo foi obtido condensando um composto obtido tratando o composto no Exemplo Referencial 418 com uma solução 4 N de ácido clorídrico em dioxano com o composto obtido no Exemplo Referencial 10, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 219. RMN-1!! (DMSO-de) δ: 1, 70-1,80 (1H, m) , 1,85-2,05 (1H, m) , 2,90 (3H,s), 3, 00-3, 20 (2H,m) , 3,16(3H,s), 3,22-3, 82 (7H, m) , 3,8810 4,80(5H,m), 7, 09 (1H, d, J=9, 0Hz) , 7, 17 (1H, dd, J=8, 8, 1,9Hz),
7,42(1H,d,J=8,8Hz), 7,70(1H,d,J=1,9Hz), 8,29(lH,br s), 8,408,50(lH,m), 11,20-11,50 (lH,br m) , ll,85(lH,s).
MS (ESI) m/z: 558(M+H)+.
Exemplo 302 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS,2R,4S)-4[(dimetil-amino)-carbonil]-2-{[(5-metil-4,5,6,7tetraidrotieno[3,2-c]-piridin-2-il)-carbonil]-amino}-ciclohexil ) -etanodiamida:
Petição 870180138821, de 08/10/2018, pág. 837/857
829 composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 421 com ácido clorídrico, metilando o composto desprotegido de uma maneira similar àquela do processo descrito no Exemplo 18, e depois tratando-o com ácido clorídrico.
RMN-1H (DMSO-de) δ: 1, 42-1, 58 (1H, m) , 1,59-1,80 (3H, m) , 1,83I, 95(lH,m), 1, 97-2, 10 (lH,m) , 2,78(3H,s), 2,89(3H,s), 2,96 (3H,s), 3, 00-3,10(lH,m), 3,10-3,20(2H,m), 3, 45-3, 80(1H,m),
3,90-4,00(2H,m), 4,00-4,50(3H,m), 7,77(lH,s), 7,95-8,05(3H,
m) , 8,44(1H, t, J=l, 6Hz) , 8,90(1H,d,J=8,6Hz), 10,25(lH,s),
II, 12 (lH,br s) .
MS (ESI) m/z: 547(M+H)+.
Exemplo 303 cloridrato de N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-415 [(dimetil-amino)-carbonil]-2-{[(5-isopropil-4,5,6,7tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]-amino}ciclo-hexil)-etanodiamida:
O composto do título foi obtido condensando o composto obtido no Exemplo Referencial 418 com o composto obtido no Exemplo Referencial 420, e depois tratando o produto da condensação com ácido clorídrico, de uma maneira
Petição 870180138821, de 08/10/2018, pág. 838/857
830 similar àquela do processo descrito no Exemplo 2.
RMN-iH (DMSO-de) δ: 1,30-1,40(6H,m), 1,38-1,58 (1H, m) , 1,59I, 82(3H,m), 1,95-2,13(2H,m), 2, 40-2, 65 (lH,m) , 2,49(3H,s),
2,87-3,55(4H,m), 2,49(3H,s), 3,60-3,82(2H,m), 3,93-4,04(1H,
m) , 4,37-4,55(2H,m), 4,55-4,72(1H,m), 7,94-8,10(2H,m), 8,43 (lH,s), 8,64-8,77(lH,m), 9,12(1/2H,d,J=7,8Hz), 9,24(l/2H,d,
J=7,8Hz), 10,22 (l/2H,s), 10,26 (l/2H,s), 11,25 (l/2H,br s),
II, 44(l/2H,br s).
MS (FAB) m/z: 578(M+H)+.
Exemplo 304 cloridrato de N-((IR,2S,5S)-5-[(dimetil-amino)-carbonil]-2{[2-(4-flúor-anilino)-2-oxoetanotioil]-amino}-ciclo-hexil)5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 424 com ácido clorídrico para desprotegê-lo, condensando o composto desprotegido com o composto obtido no Exemplo Referencial 10, e depois submetendo o produto da condensação a um novo tratamento com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 219.
Petição 870180138821, de 08/10/2018, pág. 839/857
831
RMN-iH (DMSO-de) δ: 1, 45-1, 60 (1Η, m) , 1,60-1,80(3Η,m), 2,002,10(lH,m), 2,20-2,35(lH,m), 2,79(3H,s), 2,93(3H,s), 2,95 (3H,s), 2, 95—3,10(1H,m), 3,10-3,30(2H,m), 3,403,60(1H,m), 3,60-3,80(lH,m), 4,35-4,50(1H,m), 4,504,60(1H,m), 4,60-4,80 (2H,m), 7,20(2H,t,J=8,8Hz), 7,77(2H,dd,J=9,0, 5,1Hz), 8,80 (lH,br), 10,42(lH,s), 10, 93 (1H, br) , 11,28 (1H, br) .
MS (ESI) m/z: 547(M+H)+.
Exemplo 305 cloridrato de N-[(IR,2S,5S)-5-[(dimetil-amino)-carbonil]-210 {[2-(5-flúor-piridin-2-il)amino]-2-oxoetanotioil]-amino}ciclo-hexil]-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]piridino-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 427 com ácido clorídrico para desprotegê-lo, condensando o composto desprotegido com o composto obtido no Exemplo Referencial 10, e depois submetendo o produto da condensação a um novo tratamento com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 219.
RMN-1H (DMSO-de) δ: 1, 43-1,57 (1H, m) , 1, 64-1,87 (3H, m) , 2,00 (lH,br s), 2, 17-2,34 (lH,m) , 2,78(3H,s), 2,90(3H,s), 2,95(3H,
Petição 870180138821, de 08/10/2018, pág. 840/857
832
s) , 2, 95—3,10 (lH,m) , 3,10-3,30(2H,m), 3, 4 0-3, 60(1H,m), 3,68 (lH,br s), 4,44(lH,br s), 4,45-4,56(1H,m) , 4,60-4,73(2H,m) ,
7,80-7, 90 (lH,m), 8,08(1H,dd,J=9,1, 3,9Hz), 8,41(1H,d,J=2,9
Hz), 8,79 (1H, d, J=6, 6Hz) , 10,49(lH,s), ll,07(lH,br s) , 11,69 (lH,br) .
MS (ESI) m/z: 548(M+H)+.
Exemplo 306 cloridrato de N-{(IR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)amino]-2-oxoetanotioil}-amino)-5-[(dimetil-amino)-carbonil]10 ciclo-hexil}-5-metil-5H-pirrolo[3,4-c]-tiazol-2-carboxamida:
O composto do título foi obtido tratando o composto obtido no Exemplo Referencial 428 com ácido clorídrico para desprotegê-lo, e depois condensando o composto desprotegido com o composto obtido no Exemplo
Referencial 293, de uma maneira similar àquela do processo descrito no Exemplo 219.
RMN-iH (DMSO-de) δ: 1, 45-1,58 (1H, m) , 1,63-1,73 (2H, m) , 1,73l,87(2H,m), 2, 00-2, 10 (1H, m) , 2,20-2,35 (1H, m) , 2,79(3H,s),
2,95 (3H,s), 2, 96-3,10 (lH,m) , 3,89(3H,s), 4,48-4,58 (1H, m) ,
4,60-4,70(lH,m), 7,05(1H,d,J=1,7Hz), 7,55(1H,d,J=1,7Hz),
8,00 (1H, dd, J=8, 9, 2,4Hz), 8, 05 (1H, d, J=8, 9Hz) , 8,44(lH,d,J=
Petição 870180138821, de 08/10/2018, pág. 841/857
833
2,4Hz), 8, 71(1Η,d,J=7,3Ηζ), 10,57(lH,s), 11,13(1Η,d,J=7,8
Hz) .
MS (FAB) m/z: 548(M+H)+.
Exemplo 307 cloridrato de N-{(IR,2S,5S)-2-({2-[(5-cloro-piridin-2-il)amino]-2-oxoetanotioil}-amino)-5-[(dimetil-amino)-carbonil]ciclo-hexil}-5-meti1-5,6-diidro-4H-pirrolo[3,4-d]-tiazol-2carboxamida:
O composto do título foi obtido tratando o 10 composto obtido no Exemplo Referencial 428 com ácido clorídrico para desprotegê-lo, condensando o composto desprotegido com o composto obtido no Exemplo Referencial
293 sob uma atmosfera de argônio, e depois submetendo o produto da condensação a um novo tratamento com ácido clorídrico, de uma maneira similar àquela do processo descrito no Exemplo 219.
RMN-iH (DMSO-ds) δ: 1,42-1, 58 (1H,m) , 1,65-1,87(3H,m), 1,97 2,10(lH,m), 2, 17-2,30 (lH,m) , 2,80(3H,s), 2,96(3H,s), 2,983,10(lH,m), 3,07(3H,s), 4,30-5, 00 (6H, m) , 8,00-8, 10 (1H, m) ,
8,46(1H,d,J=2,4Hz), 8, 79(1H,t,J=7,3Hz), 10,54(lH,s), 11,04 (lH,d, J=7,8Hz) , 12,24(lH,br s) .
Petição 870180138821, de 08/10/2018, pág. 842/857
834
MS (ESI) m/z: 550(M+H)+.
Exemplo 308
N1-(5-cloro-piridin-2-il)-N2-[(1S, 2R, 4S)-4-[(dimetil-amino)carbonil]-2-({[6-(dimetil-amino)-4,5,6,75 tetraidrobenzotiazol-2-il]-carbonil}-amino)-ciclo-hexil] etanodiamida:
O composto do título foi obtido desprotegendo o composto obtido no Exemplo Referencial 431 com ácido clorídrico, metilando o composto desprotegido de uma maneira similar àquela do processo descrito no Exemplo 18, e depois tratando-o com ácido clorídrico.
ΗΜΝ-^ (DMSO-de) δ: 1, 42-1,58 (1H, m) , 1,59-1,80 (3H, m) , 1902,12(3H,m), 2, 30-2, 45 (1H, m) , 2,70-3, 00 (11H, m) , 2,92(3H,s),
3,00-3,20(2H,m) , 3, 25-3, 45(1H,m) , 3, 63-380(1H,m) , 3,88-4,02 (lH,m), 4,35-4,47 (lH,m) , 8,02(lH,s), 8, 42-8, 55(1H,m) , 8,608,68(lH,m), 8,93(1H,dd,J=14,5, 8,2Hz), 9,19(1H,dd,J=17,7,
8,2Hz), 10,28(lH,s), 10,91(lH,br s) .
MS (ESI) m/z: 576(M+H)+.
Exemplo 309 cloridrato de N-{(IR,2S,5S)-2-[({[(4-cloro-fenil)-sulfonil]amino}-carbonil)-amino]-5-[(dimetil-amino)-carbonil]-cicloPctição 870180138821, de 08/10/2018, pág. 843/857
835 hexil}-5-metil-4,5,6,7-tetraidrotiazolo[5,4-c]-piridino-2carboxamida:
Adicionou-se isocianato de 4-cloro-fenil-sulfonila (148 μΐ) a uma solução do composto obtido no Exemplo Referencial 253 (328,0 mg) em cloreto de metileno (10 ml), e a mistura foi agitada à temperatura ambiente por 24 h. O solvente foi removido por destilação sob pressão reduzida, e o resíduo foi purificado por cromatografia preparatória de fina camada em sílica-gel (cloreto de metileno:metanol 9:1). O produto assim obtido foi dissolvido em etanol (2 ml) e adicionou-se cloreto de metileno (2 ml) e uma solução 1 N (0,25 ml) de ácido clorídrico em etanol, agitando a mistura à temperatura ambiente por 30 min. A mistura da reação foi concentrada sob pressão reduzida, e o resíduo foi solidificado com dietil-éter, para obter o composto do título (104,3 mg).
RMN-1!! (DMSO-de) δ: 1,25-1, 45 (1H, m) , 1,45-1,80 (5H, m) , 2,76 (3H,s), 2,94(3H,s), 2,97(3H,s), 3, 00-3, 80 (6H, m) , 4,35-4,85 (3H,m), 6,53(lH,brs), 7,66(2H,d,J=8,5Hz), 7,86(2H,d,J=8,5
Hz), 8,50-8,82(lH,m) , 10,64 (1H,br s) , 11,10-11,80(1H,br) .
MS (ESI) m/z: 583(M+H)+.
Petição 870180138821, de 08/10/2018, pág. 844/857
836
Exemplo 310
N1-(5-cloro-piridin-2-il)-N2-((IS, 2R, 4S)-4-[(dimetil-amino)carbonil]-2-{[(5-metil-4,5,6,7-tetraidrotiazolo[ 5,4-c]piridin-2-il)-carbonil]-amino}-ciclo-hexil)-etanodiamida:
O composto do título foi obtido a partir do composto obtido no Exemplo Referencial 435 e do composto obtido no Exemplo Referencial 10, de uma maneira similar àquela do processo descrito no Exemplo 2.
RMN-1!! (CDC13) δ: 1, 60-1, 98 (3H, m) , 2, 00-2, 16 (3H, m) , 2,52(3H,
s), 2,78-2, 90 (3H,m) , 2, 92-2, 98 (2H, m) , 2,95(3H,s), 3,06(3H,
s), 3,69(1H,d,J=15,4Hz), 3,75(1H,d,J=15,4Hz), 4,07-4,15(1H,
m) , 4, 66-4,72 (lH,m), 7,40(1H,d,J=8,8, 0,6Hz), 7,68(1H,dd,J=
8,8, 2,4Hz), 8,03(1H,d,J=7,8Hz), 8,16(1H,dd,J=8,8, 0,6Hz),
8,30 (1H, dd, J=2, 4, 0, 6Hz) , 9,72(lH,s).
MS (ESI) m/z: 548(M+H)+.
Exemplo 311 p-toluenossulfonato de N1-(5-cloro-piridin-2-il)-N2((IS,2R,4S)-4-[(dimetil-amino)-carbonil]-2-{[(5-metil4,5,6,7-tetraidrotiazolo[5,4-c]-piridin-2-il)-carbonil]amino}-ciclo-hexil)-etanodiamida monoidratado:
Petição 870180138821, de 08/10/2018, pág. 845/857
837
composto obtido no Exemplo 310 (6,2 g) foi dissolvido em cloreto de metileno (120 ml), adicionou-se a esta solução uma solução (11,28 ml) do ácido ptoluenossulfônico em etanol a 1 mol/litro, e o solvente foi removido por destilação. Adicionou-se etanol (95 ml) contendo 15% de água ao resíduo, e a mistura foi agitada a 60 °C para dissolvê-lo. A solução foi então resfriada até a temperatura ambiente e agitada por 1 dia. Os cristais depositados foram coletados por filtração, lavados com etanol e secados à temperatura ambiente por 2 h sob pressão reduzida, para obter o composto do título (7,4 g).
RMN-1!! (DMSO-de) δ: 1, 45-1,54 (1H, m) , 1,66-1,78 (3H, m) , 2,032,10(2H,m), 2,28(3H,s), 2,79(3H,s), 2, 91-3, 02 (1H, m) , 2,93 (3H,s), 2,99(3H,s), 3, 13-3, 24 (2H, m) , 3,46-3, 82 (2H, m) , 3,9815 4,04 (lH,m), 4,43-4,80 (3H, m) , 7, 11 (2H, d, J=7,8Hz) , 7,46(2H,d,
J=8,2Hz), 8,01(2H,d,J=l,8Hz), 8,46(1H,t,J=1,8Hz), 8,75(lH,d, J=6, 9Hz) , 9, 10-9, 28 (1H,br) , 10, 18 (1H, br) , 10,29(lH,s).
MS (ESI) m/z: 548(M+H)+.
Análise Elementar: C24H30CIN7O4S · C7H8O3S · H2O
Calculado: C: 50,43; H: 5,46; N: 13,28; Cl: 4,80; S: 8,69
Encontrado: C: 50,25; H: 5,36; N: 13,32; Cl: 4,93; S: 8,79
Petição 870180138821, de 08/10/2018, pág. 846/857
838
Ponto de fusão: 245~248 °C (decomposto).
Exemplo de Teste 1
Determinação do Efeito Inibitório de FXa (valor de
ICso) :
Soluções de cada composto do teste em DMSO a 5% (10 μΐ) , cujas concentrações foram ajustadas adequadamente de forma escalonada, tampão Tris (Tris 100 mM, cloreto de potássio 200 mM, 0,2% de BSA, pH 7,4) (40 μΐ) e 0,0625 U/ml de FXa humano (Enzyme Research Laboratories, Inc., dissolvido e diluído com tampão Tris) (10 μΐ) foram colocados respectivamente em furos de uma microplaca de 96 furos, e adicionou-se uma solução aquosa 750 μΜ (40 μΐ) de S-2222 (Chromogenix Co.). A absorbância a 405 nm foi medida para 10 min à temperatura ambiente, a fim de determinar um aumento na absorbância (ÁOD/min). Como controle usou-se tampão Tris no lugar do composto do teste.
A inibição percentual (%) calculada usando a equação que se segue na concentração final do composto do teste e a concentração final do composto do teste foram plotadas no eixo da ordenada e no eixo da abscissa do papel logarítmico de probabilidade normal, respectivamente, para determinar a dose inibitória média (valor de IC50) ·
Inibição percentual (%) = [1 - (ÁOD/min do composto do teste) 4- (ÁOD/min do controle) ] x 100
Resultado
Na Tabela 1, demonstra-se que os compostos de acordo com a presente invenção têm um efeito inibidor de FXa potente.
TABELA 1
Petição 870180138821, de 08/10/2018, pág. 847/857
839
|
Composto |
Efeito Inibidor de
FXa Humano (IC50) :
nM |
Composto |
Efeito Inibidor de
FXa Humano (IC50) :
nM |
|
Ex. 3 |
86 |
Ex. 143 |
5, 8 |
|
Ex. 7 |
83 |
Ex. 164 |
4,8 |
|
Ex. 11 |
92 |
Ex. 191 |
1,2 |
|
Ex. 54 |
4,2 |
Ex. 192 |
2,0 |
|
Ex. 62 |
3, 5 |
Ex. 194 |
5, 0 |
|
Ex. 63 |
2,5 |
Ex. 204 |
1,5 |
|
Ex. 74 |
1,4 |
Ex. 246 |
3,1 |
|
Ex. 101 |
26 |
Ex. 247 |
1,9 |
|
Ex. 130 |
4,5 |
Ex. 248 |
5,4 |
|
Ex. 138 |
4,4 |
|
Exemplo de Teste 2
Determinação da Atividade anti-FXa no Plasma de Ratos Após Administração Oral:
(A) Administração e Coleta de Sangue:
Uma solução do fármaco (1 mg/ml) obtida dissolvendo ou colocando em suspensão um composto do teste (10 mg) em metil-celulose a 0,5% foi administrada por via oral a ratos (10 ml/kg) . Depois de 0,5, 1, 2 e 4 horas a partir da administração do fármaco, o sangue (0,5 ml) foi coletado através da veia jugular, usando uma seringa que continha uma solução aquosa a 3,13% (p/v) (50 μΐ) de citrato trissódico diidratado (quantidade de sangue coletada: 0,45 ml). Para os ratos de um grupo de controle, a mesma coleta
Petição 870180138821, de 08/10/2018, pág. 848/857
840 de sangue foi conduzida após a administração de uma solução de metil-celulose a 0,5%. Cada amostra de sangue foi centrifugada a 1.500 x g por 10 min a 4 °C, para separar o plasma, e o plasma foi conservado a -40 °C até ser usado na determinação da atividade anti-FXa que se segue.
(B) Determinação da Atividade Inibitória de FXa no
Plasma:
Na determinação da atividade anti-FXa no plasma, usou-se S-2222 como substrato. Misturou-se tampão Tris (Tris 100 mM, cloreto de potássio 200 mM, 0,2% de BSA, pH 7,4) (5.456 μΐ), FXa humano (2,5 U/ml, 4 4 μΐ) e água (550 μΐ) . A solução de FXa humano resultante foi usada no teste que se segue.
O plasma (5 μΐ) de ratos obtido de acordo com o procedimento (A) descrito acima foi colocado em furos de uma microplaca de 96 furos e adicionou-se seqüencialmente a solução de FXa supradescrita (55 μΐ) e uma solução aquosa 750 μΜ (40 μΐ) de S-2222. Imediatamente após isto, a absorbância a 405 nm foi medida à temperatura ambiente por meio de um espectrofotômero SPECTRAmax 340 ou 190 (Molecular Devices Co., E.U.A.), determinando desta forma uma velocidade de reação (ÁOD/min).
|
A atividade |
anti-FXa, |
isto |
é, a |
inibição |
|
percentual (%) foi calculada de |
acordo |
com a |
seguinte |
|
equação: |
|
|
|
|
|
Inibição percentual (%) |
= [1 - (ÁOD/min da |
amostra) |
4- (valor |
médio de ÁOD/min do grupo de controle)] x 100 de 08/10/2018, pág. 849/857
841
Resultado
Os compostos descritos nos Exemplos 63, 191, 192,
194 e 204 apresentaram uma atividade inibitória de FXa potente de 62 a 96% em uma dose oral de 10 mg/kg.
APLICABILIDADE INDUSTRIAL
Os derivados ciclo-diamínicos de acordo com a presente invenção apresentam um efeito inibitório de FXa potente sobre o fator X de coagulação sangüinea ativado, e são úteis como medicamentos, inibidores do fator X de coagulação sangüinea ativado, anticoagulantes, agentes para prevenir e/ou tratar trombose ou embolia, agentes para prevenir e/ou tratar doença trombótica e agentes para prevenir e/ou tratar infarto cerebral, embolia cerebral, infarto do miocárdio, angina do peito, infarto pulmonar, embolia pulmonar, doença de Buerger, trombose venosa profunda, síndrome da coagulação intravascular disseminada, formação de trombo após substituição de válvula ou articulação, formação de trombo e reoclusão após angioplastia, síndrome da resposta inflamatória sistêmica (SIRS), síndrome da disfunção de múltiplos órgãos (MODS), formação de trombo durante circulação extracorpórea, ou coagulação do sangue após retirada do sangue.
Petição 870180138821, de 08/10/2018, pág. 850/857