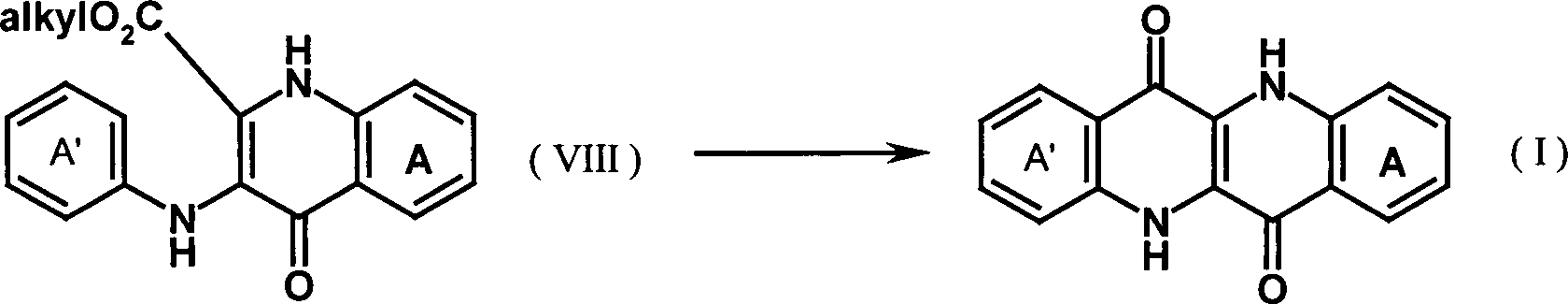DE60201345T2 - Epindolidionpigmente - Google Patents
Epindolidionpigmente Download PDFInfo
- Publication number
- DE60201345T2 DE60201345T2 DE60201345T DE60201345T DE60201345T2 DE 60201345 T2 DE60201345 T2 DE 60201345T2 DE 60201345 T DE60201345 T DE 60201345T DE 60201345 T DE60201345 T DE 60201345T DE 60201345 T2 DE60201345 T2 DE 60201345T2
- Authority
- DE
- Germany
- Prior art keywords
- alkyl
- formula
- compounds
- parts
- phenyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000000049 pigment Substances 0.000 claims abstract description 18
- 239000003086 colorant Substances 0.000 claims abstract description 15
- 239000000976 ink Substances 0.000 claims abstract description 7
- 239000004753 textile Substances 0.000 claims abstract description 4
- 239000002537 cosmetic Substances 0.000 claims abstract description 3
- 238000004040 coloring Methods 0.000 claims abstract 3
- 150000001875 compounds Chemical class 0.000 claims description 47
- 125000000217 alkyl group Chemical group 0.000 claims description 20
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 20
- 238000006243 chemical reaction Methods 0.000 claims description 17
- 238000000034 method Methods 0.000 claims description 16
- 229910052739 hydrogen Inorganic materials 0.000 claims description 13
- 239000001257 hydrogen Substances 0.000 claims description 13
- 150000002431 hydrogen Chemical class 0.000 claims description 11
- 238000002360 preparation method Methods 0.000 claims description 11
- 229910052736 halogen Inorganic materials 0.000 claims description 9
- 150000002367 halogens Chemical class 0.000 claims description 9
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 claims description 7
- 125000006704 (C5-C6) cycloalkyl group Chemical group 0.000 claims description 6
- 125000003545 alkoxy group Chemical group 0.000 claims description 6
- ZVSKZLHKADLHSD-UHFFFAOYSA-N benzanilide Chemical compound C=1C=CC=CC=1C(=O)NC1=CC=CC=C1 ZVSKZLHKADLHSD-UHFFFAOYSA-N 0.000 claims description 6
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 6
- 125000001624 naphthyl group Chemical group 0.000 claims description 6
- 229920000137 polyphosphoric acid Polymers 0.000 claims description 6
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 5
- 239000000460 chlorine Substances 0.000 claims description 5
- 229910052801 chlorine Inorganic materials 0.000 claims description 5
- 229920003023 plastic Polymers 0.000 claims description 5
- 239000004033 plastic Substances 0.000 claims description 5
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 5
- 239000003973 paint Substances 0.000 claims description 4
- 125000003118 aryl group Chemical group 0.000 claims description 3
- 239000000463 material Substances 0.000 claims description 3
- 230000037361 pathway Effects 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 22
- 239000002904 solvent Substances 0.000 abstract description 12
- 238000000576 coating method Methods 0.000 abstract description 6
- 230000005012 migration Effects 0.000 abstract description 4
- 238000013508 migration Methods 0.000 abstract description 4
- NUJGNDIAVBGFHG-UHFFFAOYSA-N 5,11-dihydroquinolino[3,2-b]quinoline-6,12-dione Chemical class N1C2=CC=CC=C2C(=O)C2=C1C(=O)C1=CC=CC=C1N2 NUJGNDIAVBGFHG-UHFFFAOYSA-N 0.000 abstract description 3
- 238000004519 manufacturing process Methods 0.000 abstract description 3
- 229920001131 Pulp (paper) Polymers 0.000 abstract description 2
- 229920000642 polymer Polymers 0.000 abstract 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 32
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 24
- 239000000047 product Substances 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 17
- -1 benzanilide radical Chemical class 0.000 description 16
- 239000000843 powder Substances 0.000 description 11
- MSXVEPNJUHWQHW-UHFFFAOYSA-N 2-methylbutan-2-ol Chemical compound CCC(C)(C)O MSXVEPNJUHWQHW-UHFFFAOYSA-N 0.000 description 9
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 9
- 239000011541 reaction mixture Substances 0.000 description 8
- MHCVCKDNQYMGEX-UHFFFAOYSA-N 1,1'-biphenyl;phenoxybenzene Chemical compound C1=CC=CC=C1C1=CC=CC=C1.C=1C=CC=CC=1OC1=CC=CC=C1 MHCVCKDNQYMGEX-UHFFFAOYSA-N 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Chemical compound C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 5
- 150000003254 radicals Chemical group 0.000 description 5
- 239000000725 suspension Substances 0.000 description 5
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 4
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 4
- 238000001035 drying Methods 0.000 description 4
- 239000004800 polyvinyl chloride Substances 0.000 description 4
- 229920000915 polyvinyl chloride Polymers 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- 0 *N(c(ccc(N)c1)c1N(*)C1=O)C1=O Chemical compound *N(c(ccc(N)c1)c1N(*)C1=O)C1=O 0.000 description 3
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 3
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N N-phenyl amine Natural products NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 3
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 239000004305 biphenyl Substances 0.000 description 3
- 235000010290 biphenyl Nutrition 0.000 description 3
- 238000009835 boiling Methods 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 238000004043 dyeing Methods 0.000 description 3
- 239000003822 epoxy resin Substances 0.000 description 3
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 229920000647 polyepoxide Polymers 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 3
- 239000008096 xylene Substances 0.000 description 3
- ULOIAOPTGWSNHU-UHFFFAOYSA-N 2-butyl radical Chemical compound C[CH]CC ULOIAOPTGWSNHU-UHFFFAOYSA-N 0.000 description 2
- IIVWHGMLFGNMOW-UHFFFAOYSA-N 2-methylpropane Chemical compound C[C](C)C IIVWHGMLFGNMOW-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- 229920000877 Melamine resin Polymers 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- CIUQDSCDWFSTQR-UHFFFAOYSA-N [C]1=CC=CC=C1 Chemical class [C]1=CC=CC=C1 CIUQDSCDWFSTQR-UHFFFAOYSA-N 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 150000001448 anilines Chemical class 0.000 description 2
- 150000004982 aromatic amines Chemical class 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- ZCILODAAHLISPY-UHFFFAOYSA-N biphenyl ether Natural products C1=C(CC=C)C(O)=CC(OC=2C(=CC(CC=C)=CC=2)O)=C1 ZCILODAAHLISPY-UHFFFAOYSA-N 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- DOIRQSBPFJWKBE-UHFFFAOYSA-N dibutyl phthalate Chemical compound CCCCOC(=O)C1=CC=CC=C1C(=O)OCCCC DOIRQSBPFJWKBE-UHFFFAOYSA-N 0.000 description 2
- WYACBZDAHNBPPB-UHFFFAOYSA-N diethyl oxalate Chemical compound CCOC(=O)C(=O)OCC WYACBZDAHNBPPB-UHFFFAOYSA-N 0.000 description 2
- 229920001971 elastomer Polymers 0.000 description 2
- QUPDWYMUPZLYJZ-UHFFFAOYSA-N ethyl Chemical compound C[CH2] QUPDWYMUPZLYJZ-UHFFFAOYSA-N 0.000 description 2
- VEUUMBGHMNQHGO-UHFFFAOYSA-N ethyl chloroacetate Chemical compound CCOC(=O)CCl VEUUMBGHMNQHGO-UHFFFAOYSA-N 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 239000005457 ice water Substances 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- WCYWZMWISLQXQU-UHFFFAOYSA-N methyl Chemical compound [CH3] WCYWZMWISLQXQU-UHFFFAOYSA-N 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- LQNUZADURLCDLV-UHFFFAOYSA-N nitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC=C1 LQNUZADURLCDLV-UHFFFAOYSA-N 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- 229920001225 polyester resin Polymers 0.000 description 2
- 239000004645 polyester resin Substances 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 239000004848 polyfunctional curative Substances 0.000 description 2
- 238000006116 polymerization reaction Methods 0.000 description 2
- 239000004814 polyurethane Substances 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 239000011591 potassium Substances 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 230000000630 rising effect Effects 0.000 description 2
- 239000005060 rubber Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- HEMHJVSKTPXQMS-UHFFFAOYSA-M sodium hydroxide Inorganic materials [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 2
- MFRIHAYPQRLWNB-UHFFFAOYSA-N sodium tert-butoxide Chemical compound [Na+].CC(C)(C)[O-] MFRIHAYPQRLWNB-UHFFFAOYSA-N 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 125000001424 substituent group Chemical group 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- NJVOHKFLBKQLIZ-UHFFFAOYSA-N (2-ethenylphenyl) prop-2-enoate Chemical compound C=CC(=O)OC1=CC=CC=C1C=C NJVOHKFLBKQLIZ-UHFFFAOYSA-N 0.000 description 1
- AZUYLZMQTIKGSC-UHFFFAOYSA-N 1-[6-[4-(5-chloro-6-methyl-1H-indazol-4-yl)-5-methyl-3-(1-methylindazol-5-yl)pyrazol-1-yl]-2-azaspiro[3.3]heptan-2-yl]prop-2-en-1-one Chemical compound ClC=1C(=C2C=NNC2=CC=1C)C=1C(=NN(C=1C)C1CC2(CN(C2)C(C=C)=O)C1)C=1C=C2C=NN(C2=CC=1)C AZUYLZMQTIKGSC-UHFFFAOYSA-N 0.000 description 1
- ZNQVEEAIQZEUHB-UHFFFAOYSA-N 2-ethoxyethanol Chemical compound CCOCCO ZNQVEEAIQZEUHB-UHFFFAOYSA-N 0.000 description 1
- QSNSCYSYFYORTR-UHFFFAOYSA-N 4-chloroaniline Chemical compound NC1=CC=C(Cl)C=C1 QSNSCYSYFYORTR-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- 229920000178 Acrylic resin Polymers 0.000 description 1
- 239000004925 Acrylic resin Substances 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- OLSHHFCQRNBAAK-UHFFFAOYSA-N CCN(c(ccc(N)c1)c1N1)C1=O Chemical compound CCN(c(ccc(N)c1)c1N1)C1=O OLSHHFCQRNBAAK-UHFFFAOYSA-N 0.000 description 1
- ZNVVKZDSSWMTGQ-UHFFFAOYSA-N CCOC(CNc(cc1)ccc1Cl)=O Chemical compound CCOC(CNc(cc1)ccc1Cl)=O ZNVVKZDSSWMTGQ-UHFFFAOYSA-N 0.000 description 1
- CTCHXZUMFHNSHM-UHFFFAOYSA-N Cc(cc1)cc(N2)c1NC2=O Chemical compound Cc(cc1)cc(N2)c1NC2=O CTCHXZUMFHNSHM-UHFFFAOYSA-N 0.000 description 1
- MQIUGAXCHLFZKX-UHFFFAOYSA-N Di-n-octyl phthalate Natural products CCCCCCCCOC(=O)C1=CC=CC=C1C(=O)OCCCCCCCC MQIUGAXCHLFZKX-UHFFFAOYSA-N 0.000 description 1
- 239000004640 Melamine resin Substances 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 1
- MKYBYDHXWVHEJW-UHFFFAOYSA-N N-[1-oxo-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propan-2-yl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical group O=C(C(C)NC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 MKYBYDHXWVHEJW-UHFFFAOYSA-N 0.000 description 1
- 235000019502 Orange oil Nutrition 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 229920000297 Rayon Polymers 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 239000002174 Styrene-butadiene Substances 0.000 description 1
- YUDRVAHLXDBKSR-UHFFFAOYSA-N [CH]1CCCCC1 Chemical compound [CH]1CCCCC1 YUDRVAHLXDBKSR-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 125000005907 alkyl ester group Chemical group 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- BJQHLKABXJIVAM-UHFFFAOYSA-N bis(2-ethylhexyl) phthalate Chemical compound CCCCC(CC)COC(=O)C1=CC=CC=C1C(=O)OCC(CC)CCCC BJQHLKABXJIVAM-UHFFFAOYSA-N 0.000 description 1
- MTAZNLWOLGHBHU-UHFFFAOYSA-N butadiene-styrene rubber Chemical compound C=CC=C.C=CC1=CC=CC=C1 MTAZNLWOLGHBHU-UHFFFAOYSA-N 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- FOCAUTSVDIKZOP-UHFFFAOYSA-M chloroacetate Chemical compound [O-]C(=O)CCl FOCAUTSVDIKZOP-UHFFFAOYSA-M 0.000 description 1
- 229940089960 chloroacetate Drugs 0.000 description 1
- 239000004567 concrete Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 150000001991 dicarboxylic acids Chemical class 0.000 description 1
- QGBSISYHAICWAH-UHFFFAOYSA-N dicyandiamide Chemical compound NC(N)=NC#N QGBSISYHAICWAH-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000006253 efflorescence Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 239000012943 hotmelt Substances 0.000 description 1
- 229910000042 hydrogen bromide Inorganic materials 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N hydrogen bromide Substances Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 1
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- 238000004898 kneading Methods 0.000 description 1
- 239000002649 leather substitute Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 150000005002 naphthylamines Chemical class 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 239000010502 orange oil Substances 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 150000002918 oxazolines Chemical class 0.000 description 1
- 125000000636 p-nitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)[N+]([O-])=O 0.000 description 1
- 239000000123 paper Substances 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 229920001568 phenolic resin Polymers 0.000 description 1
- 230000000485 pigmenting effect Effects 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 238000006068 polycondensation reaction Methods 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 229920005749 polyurethane resin Polymers 0.000 description 1
- NTTOTNSKUYCDAV-UHFFFAOYSA-N potassium hydride Chemical compound [KH] NTTOTNSKUYCDAV-UHFFFAOYSA-N 0.000 description 1
- 229910000105 potassium hydride Inorganic materials 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 206010037844 rash Diseases 0.000 description 1
- 239000001054 red pigment Substances 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- CGRKYEALWSRNJS-UHFFFAOYSA-N sodium;2-methylbutan-2-olate Chemical compound [Na+].CCC(C)(C)[O-] CGRKYEALWSRNJS-UHFFFAOYSA-N 0.000 description 1
- 239000011115 styrene butadiene Substances 0.000 description 1
- 229920003048 styrene butadiene rubber Polymers 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229920003002 synthetic resin Polymers 0.000 description 1
- 239000000057 synthetic resin Substances 0.000 description 1
- 125000003698 tetramethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 239000012463 white pigment Substances 0.000 description 1
- 239000002023 wood Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/24—Benzimidazoles; Hydrogenated benzimidazoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached in position 2
- C07D235/26—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B15/00—Acridine dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Inks, Pencil-Leads, Or Crayons (AREA)
- Paints Or Removers (AREA)
- Ink Jet (AREA)
- Ink Jet Recording Methods And Recording Media Thereof (AREA)
- Developing Agents For Electrophotography (AREA)
- Plural Heterocyclic Compounds (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Indole Compounds (AREA)
Description
- Die Erfindung betrifft neue Dibenzo[b,g][1,5]naphthyridin-6,12(5H,11H)dionverbindungen, auch Epindolidionverbindungen genannt, sowie deren Verwendung als Pigmente. Die Erfindung betrifft ferner ein besonders vorteilhaftes Verfahren zur Herstellung dieser Epindolidionverbindungen.
- In
US 3,334,102 wird die Herstellung von Epindolidionverbindungen der folgenden allgemeinen Formel: beschrieben, wobei die mit A bezeichneten Ringe Halogenatome oder Methoxygruppen tragen. - Dabei geht das in
US 3,334,102 bzw. J. Org. Chem., 33(11), 4004 (1968), genannte Herstellungsverfahren von Dihydroxyfumarsäuredimethylester und einfachen Anilinen aus. Die inUS 3,334,102 genannten Pigmente zeigen in Polyolefinen und Lacken einen grün- bis rotgelben Farbton. - Aufgabe der Erfindung ist die Bereitstellung von neuen orange bis roten Pigmenten mit hoher Echtheit gegenüber Lösungsmitteln, Migrierung und Licht, die gute Wärmestabilitäten und eine hohe Tönungskraft aufweisen und leicht dispergierfähig sind.
- Aufgabe der Erfindung ist weiterhin die Bereitstellung eines Verfahrens, mit dem die neuen Pigmente erhältlich sind, das von einfach zugänglichen Zwischenprodukten ausgeht.
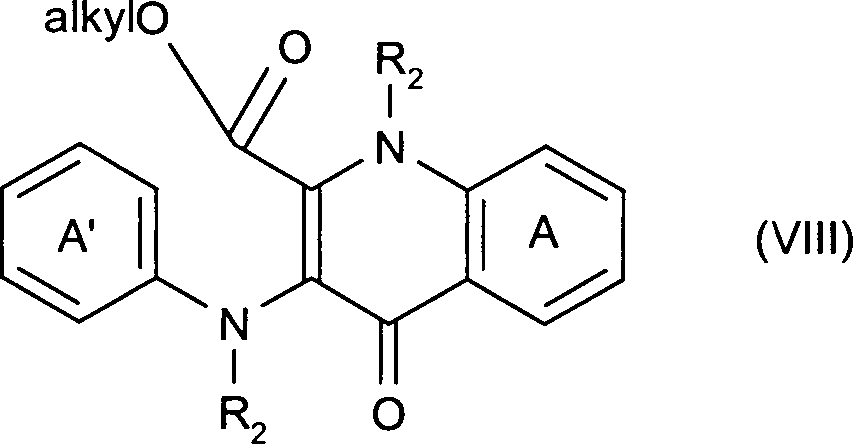
- Gegenstand der vorliegenden Erfindung sind zum einen Verbindungen der allgemeinen Formel (I) wobei A' einen gegebenenfalls substituierten aromatischen Ring oder ein anelliertes heteroaromatisches Ringsystem und A ein anelliertes heteroaromatisches Ringsystem darstellt und beide R2 für Wasserstoff, C1–2-Alkyl, Phenyl oder -COOR mit R gleich C1-8-Alkyl stehen.
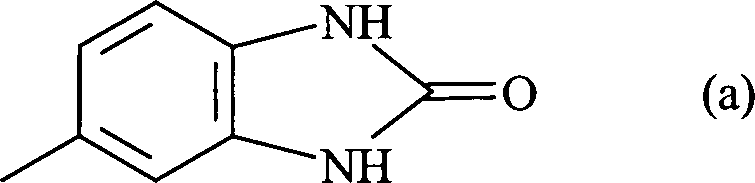
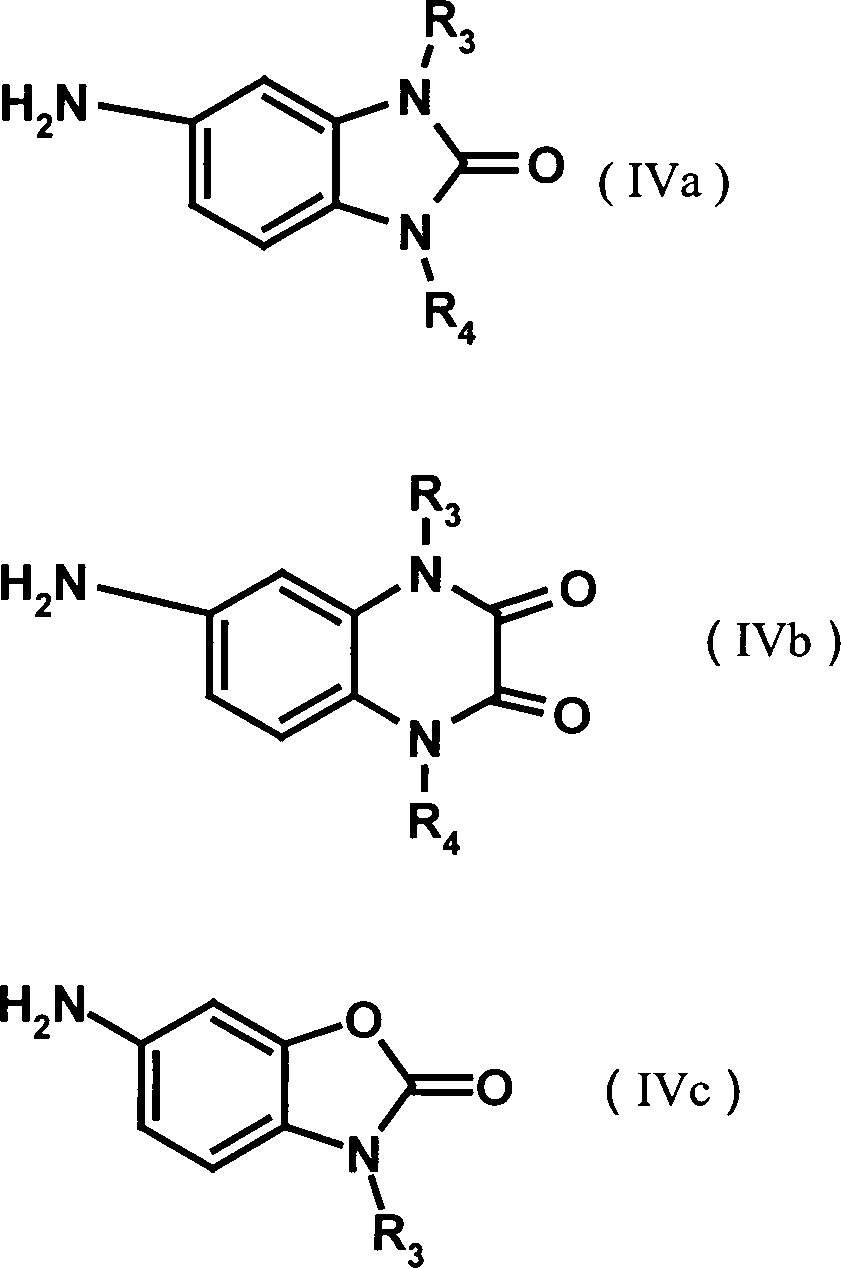
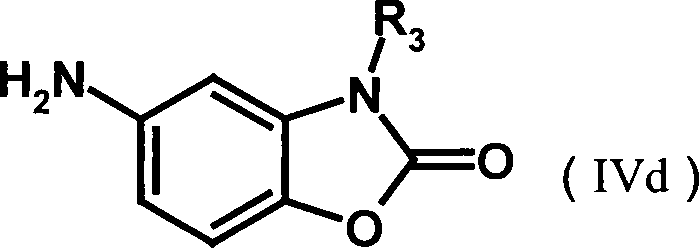
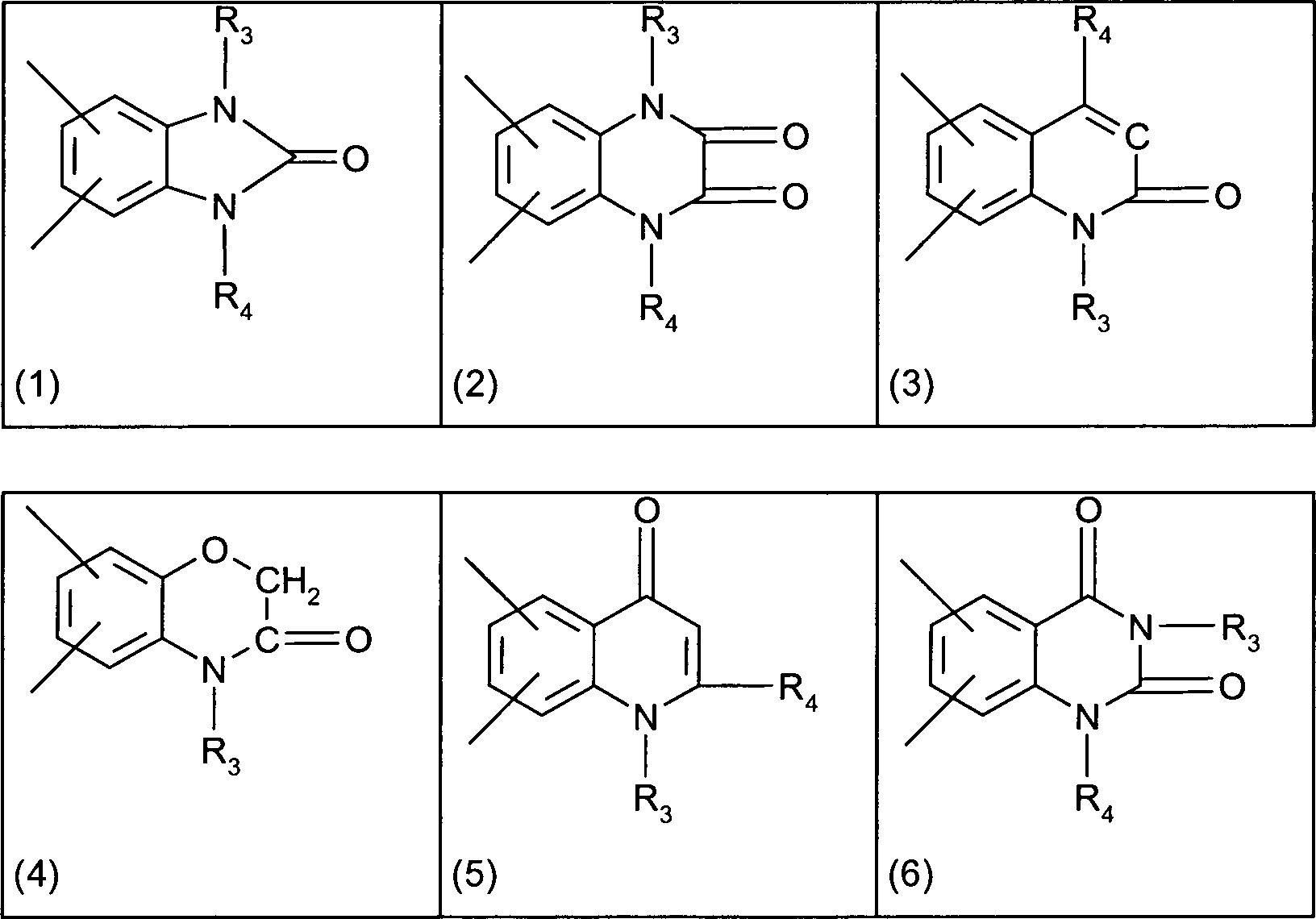
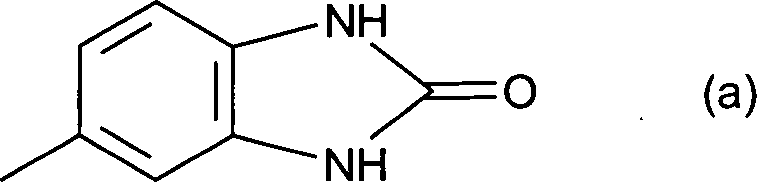
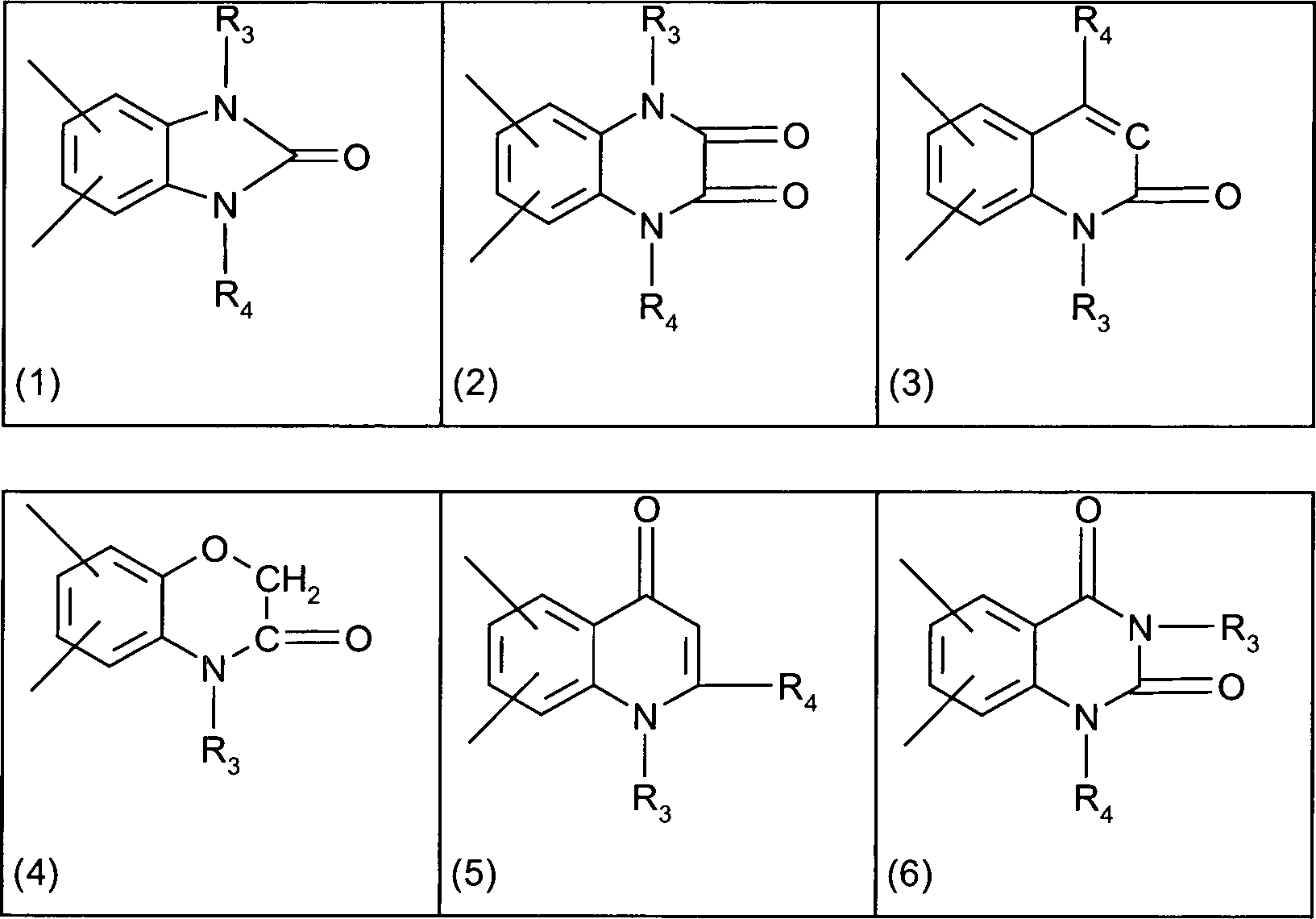
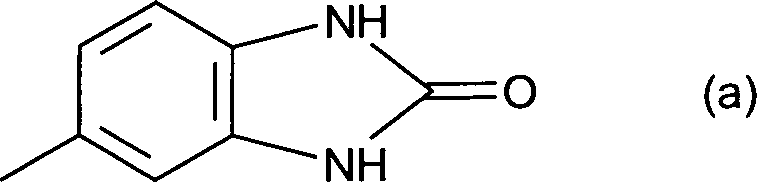
- Der mit A bezeichnete Kern enthält linear, in 2,3-Stellung, oder angular, in 1,2- oder in 3,4-Stellung, anelliert einen Ring mit den Restgliedern der Formelteile (1) bis (11) wobei R3 und R4 unabhängig voneinander Wasserstoff, C1–8-Alkyl, C5–6-Cycloalkyl, Benzyl, Benzanilid oder Naphthyl bedeuten, wobei Phenylgruppen ein- oder mehrfach durch Reste aus der Gruppe Halogen, Nitrogruppen, C1–8-Alkyl, Phenyl, -COOR und C1–2-Alkoxy, bevorzugt Chlor, C1–4-Alkyl, Phenyl oder -COOR mit R gleich C1–8-Alkyl substituiert sein können, oder R3 und/oder R4 einen Rest der Formel (a) bedeuten.
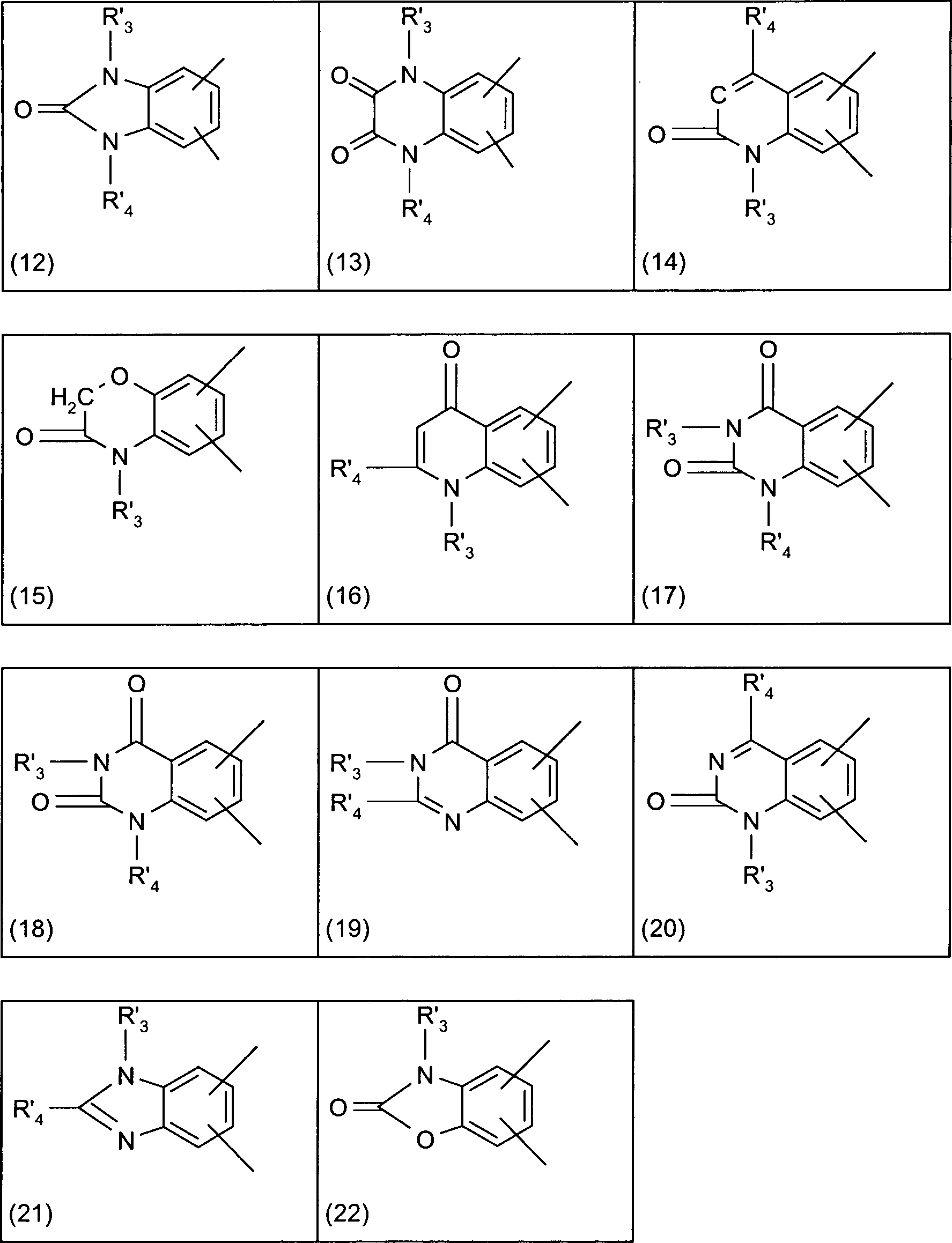
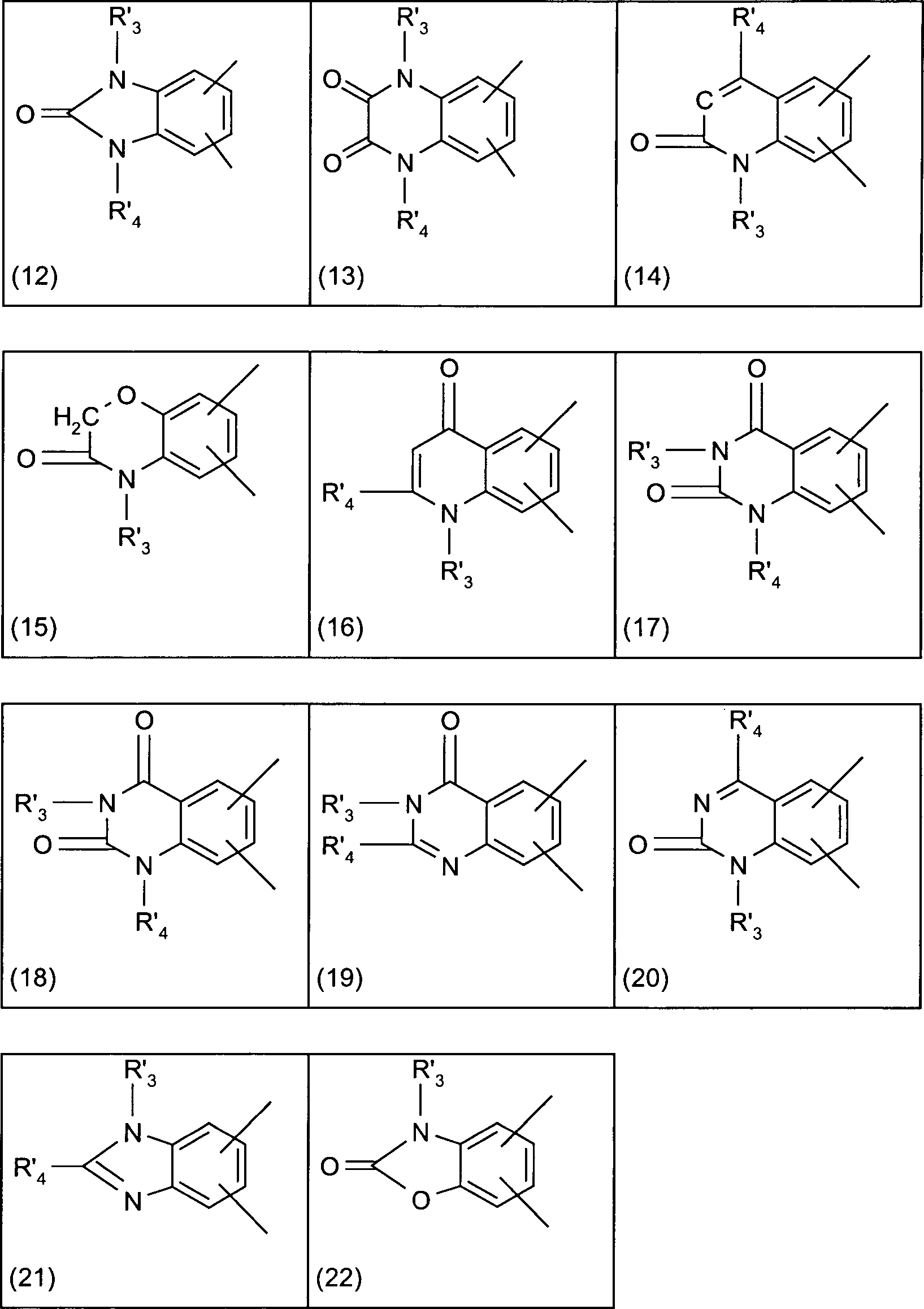
- Der mit A' bezeichnete Kern enthält bei A' als anelliertes heteroaromatisches Ringsystem linear, in 2,3-Stellung, oder angular, in 1,2- oder in 3,4-Stellung, anelliert einen Ring mit den unter den Formelteilen (12) bis (22) ausgewählten Restgliedern: wobei R'3 und R'4 unabhängig voneinander Wasserstoff, C1–8-Alkyl, C5–6-Cycloalkyl, Benzyl, Benzanilid oder Naphthyl bedeuten, wobei Phenylgruppen ein- oder mehrfach durch Reste aus der Gruppe Halogen, Nitrogruppen, C1–8-Alkyl, Phenyl, -COOR mit R gleich C1–8-Alkyl und C1–2-Alkoxy, bevorzugt Chlor, C1–4-Alkyl, Phenyl oder COOR mit R gleich C1–8-Alkyl substituiert sein können.
-
-
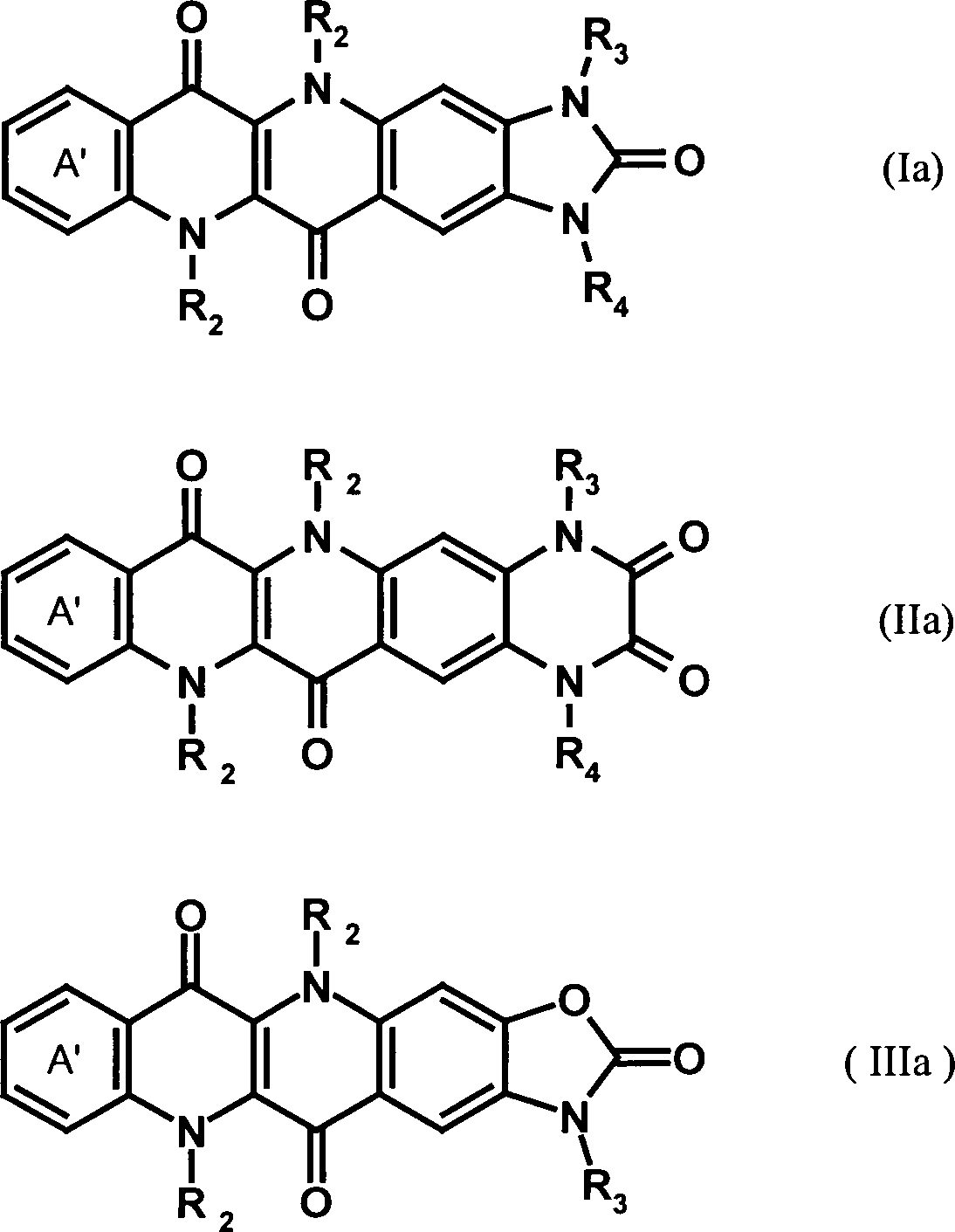
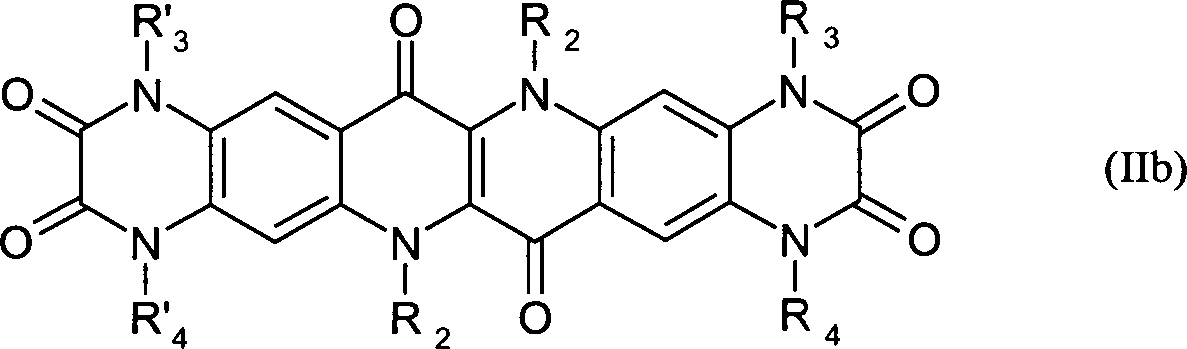
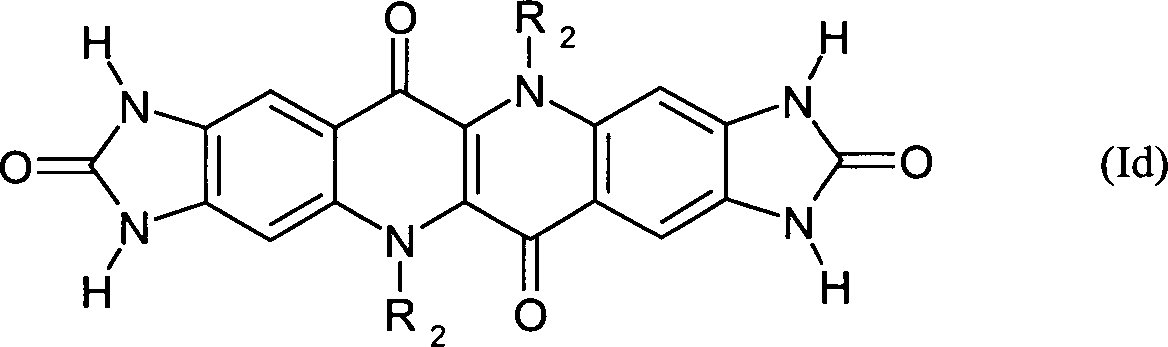
- Besonders bevorzugte Verbindungen sind solche der Formel (Ib) und (IIb) wobei R2, R3, R4, R'3 und R'4 die obengenannte Bedeutung haben. Besonders bevorzugte Verbindungen sind weiterhin solche der Formel (Ic) wobei R2, R3 und R4 die obengenannte Bedeutung haben und R1 für Wasserstoff, Halogen oder C1–8-Alkyl steht.
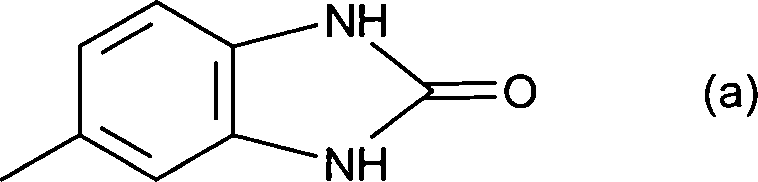
- Die Substituenten R3 und R4 bedeuteten unabhängig voneinander bevorzugt Wasserstoff, einen Methylrest, einen Ethylrest, einen n- oder i-Propylrest, einen n-, i-, sec.- oder tert.-Butylrest, einen Cyclohexylrest, einen gegebenenfalls substituierten Benzanilidrest, einen Naphthylrest, einen Rest der Formel (a) einen gegebenenfalls durch Halogen, bevorzugt Chlor, oder Nitrogruppen, Phenyl, C1-8-Alkyl, bevorzugt C1–4-Alkyl und C1–2-Alkoxy, ein- oder mehrfach substituierten Phenylrest.
- Der oben bei der Bedeutungsbestimmung von R3 oder R4 erwähnte substituierte Phenylrest ist bevorzugt unter o-, m-, p-Methyl-, Ethyl-, Chlor-, Methoxyphenyl, 2,4- und 3,5-Dimethylphenyl, 2,5-Dichlor-, Dimethoxy-, Diethoxyphenyl, m-, p-Nitrophenyl, 2,5-Dichlor-, 2,5-Diethoxy-4-nitrophenyl, 2-Methoxy-4-nitrophenyl, 3-Chlor-4-methyl, 3-Chlor-4-methoxyphenyl und p-Ethoxyphenyl ausgewählt.
-
- Die Substituenten R'3 und R'4 sind unabhängig voneinander bevorzugt ein Methylrest, ein Ethylrest, ein n- oder i-Propylrest, ein n-, i-, sec.- oder tert.-Butylrest.
- Bevorzugte Epindolidionverbindungen sind solche, bei denen R2 und R4 Wasserstoff und R3 ein Methyl-, Ethyl-, Propyl- oder Butylsubstituent sind.
- Bevorzugte symmetrisch tetrasubstituierte Verbindungen sind Tetramethyl-, Tetraethyl-Tetrapropyl- (n- oder i-) sowie Tetrabutyl- (n-, i-, sec.- oder tert.-) substituierten Verbindungen.
-
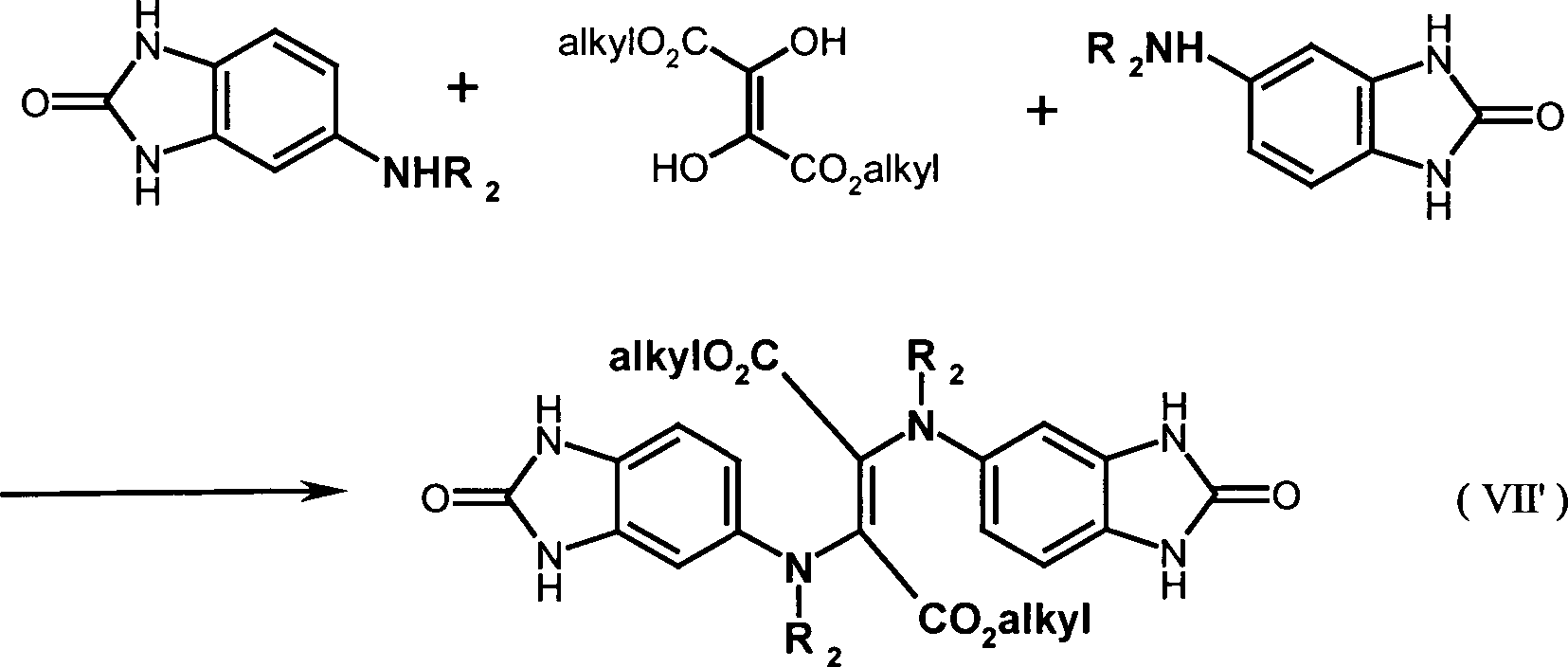
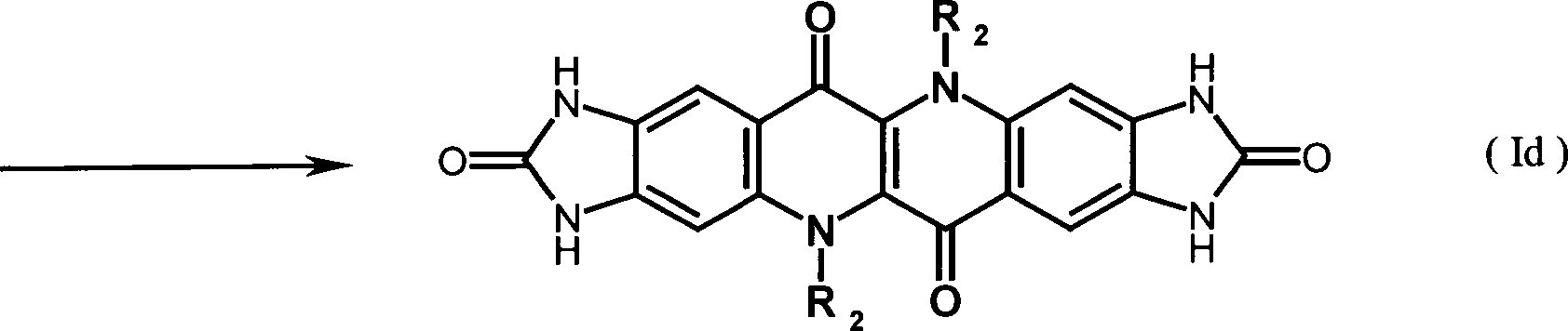
- Nach einem Aspekt betrifft die Erfindung ein Verfahren zur Herstellung von Epindolidionverbindungen der oben definierten Formel (Id), gekennzeichnet durch folgenden Reaktionspfad:
-
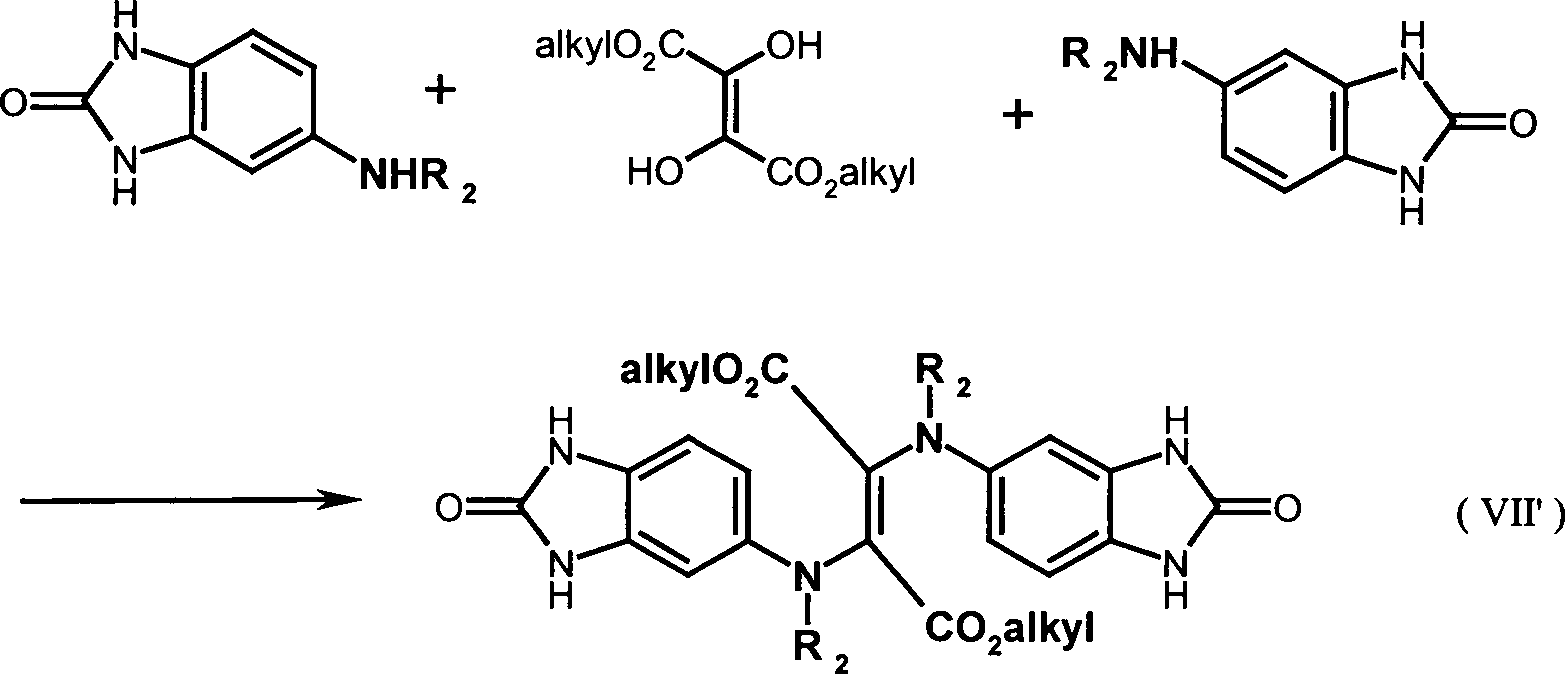
- Nach einem weiteren Aspekt betrifft die Erfindung ein Verfahren zur Herstellung der Epindolidionverbindungen der Formel (I'), bei dem man zunächst ein Arylamin mit einem Chloressigsäurealkylester oder einem Bromessigsäurealkylester in einem Lösungsmittel gegebenenfalls in Gegenwart einer als das Wasserstoffchlorid oder -bromid bindendes Mittel wirkenden Base kondensiert. Als Lösungsmittel wird das Verfahren beispielsweise in Alkoholen, Toluol, Xylol oder einem Xylolgemisch, Nitrobenzol, Chlorbenzol, Dimethylformamid oder Dimethylacetamid oder N-Methylpyrrolidon durchgeführt. Die Umsetzung erfolgt bevorzugt in Ethanol, tert.-Amylalkohol oder Toluol. Die Umsetzungstemperatur liegt bevorzugt bei 10 bis 150°C. Als Base dient eine anorganische oder organische Base aus der Reihe der in der organischen Synthese gängigen Basen wie Natriumacetat, Natriumcarbonat, Natrium- oder Kaliumhydroxid oder Triethylamin.
-
-
- Die Herstellung von Verbindungen der Formel (IV'), insbesondere der Formeln (IV'a) bis (IV'd), ist in
EP 0911337 A beschrieben. - In einer zweiten Verfahrensstufe kondensiert man den N-Arylglycinalkylester mit einem Dialkyloxalat in einem Lösungsmittel in Gegenwart einer starken Base. Dabei erfolgt das Verfahren in dem zur ersten Stufe gleichartigen Lösungsmittel. Die Umsetzung erfolgt bevorzugt in Ethanol, tert.-Amylalkohol oder Toluol. Die Umsetzungstemperatur liegt bevorzugt bei 10 bis 150°C. Als starke Base kommen Natrium- oder Kaliumalkoholat, Natrium- oder Kaliumhydrid, Natrium- oder Kaliumdialkylamid oder eine sonstige gemeinhin zur Herstellung von Carbanionen eingesetzte starke Base in Frage. Als starke Base wird bevorzugt Natriumethanolat, Natrium-tert.-butanolat oder Natrium tert.-amylat eingesetzt. Dabei beträgt die Menge der Base 1 bis 200 Mol-%, bezogen auf den N-Arylglycinalkylester.
- Bevorzugt beträgt das Molverhältnis von N-Arylglycinalkylester und Dialkyloxalat 1:1.
-
-
- Die Herstellung der Verbindungen der Formel (IV), insbesondere der Formeln (IV'a) bis (IV'd), ist in
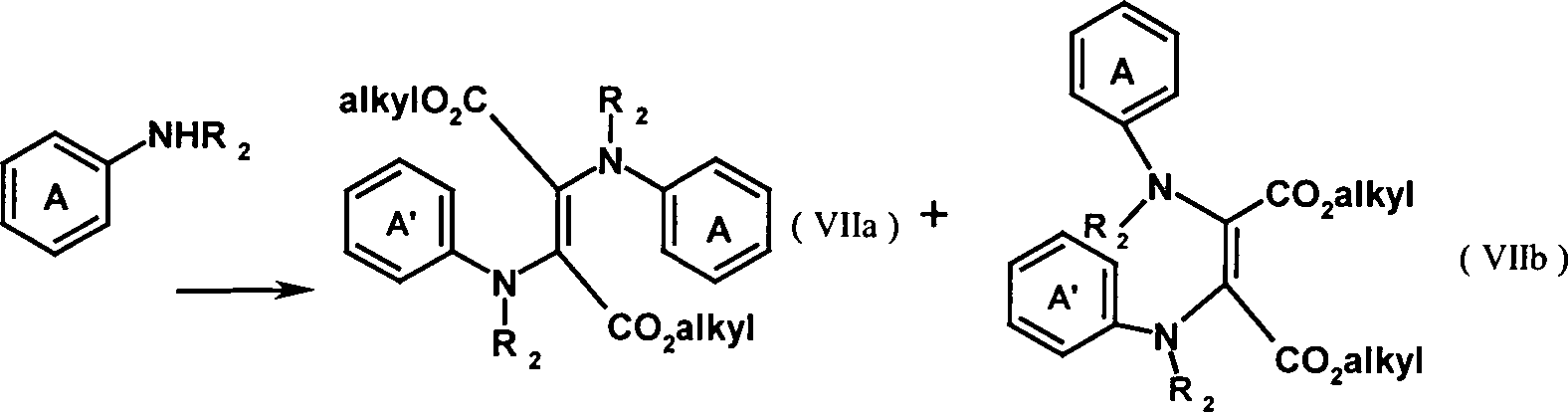
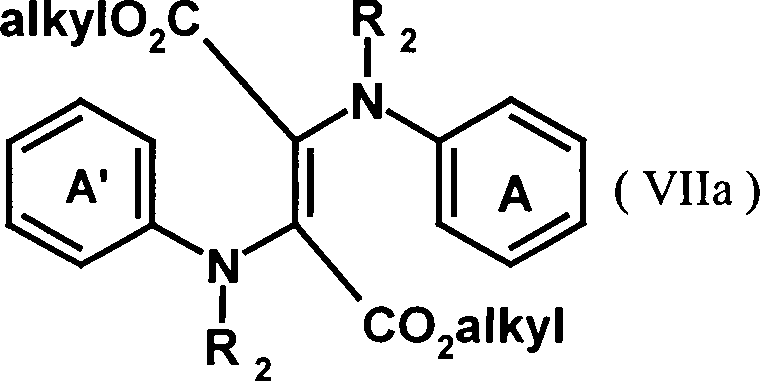
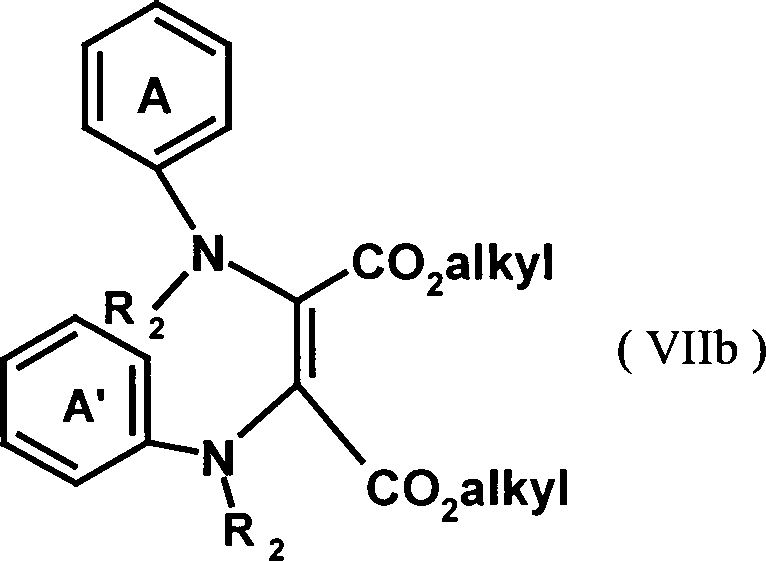
EP 0911337 A beschrieben. - Die Umsetzung erfolgt bevorzugt in Ethanol, tert.-Amylalkohol oder Toluol. Die Umsetzungstemperatur liegt bevorzugt bei 10 bis 200°C. Als Säure dient eine der in der organischen Synthese üblichen anorganischen oder organischen Säuren, wie Schwefelsäure, Salzsäure, Essigsäure oder para-Toluolsulfonsäure.
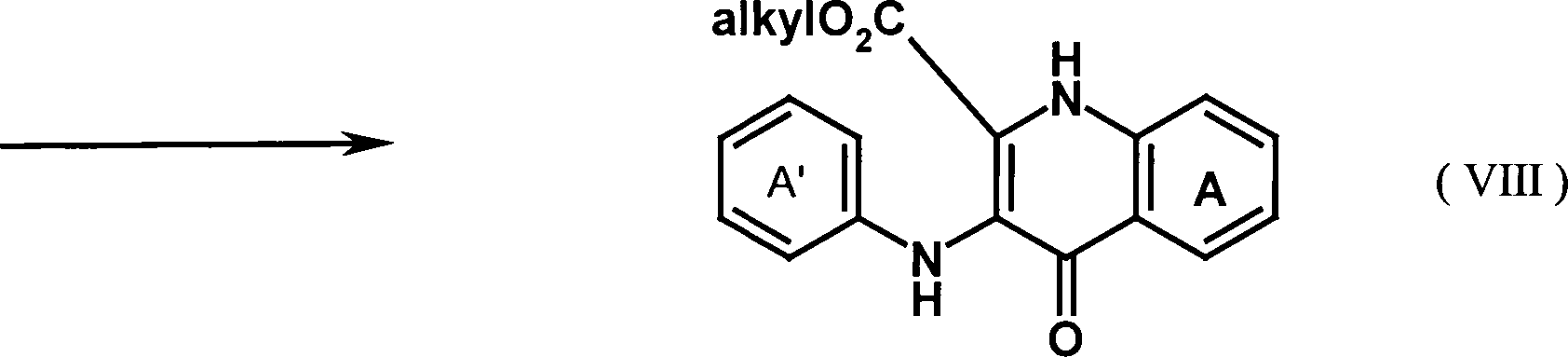
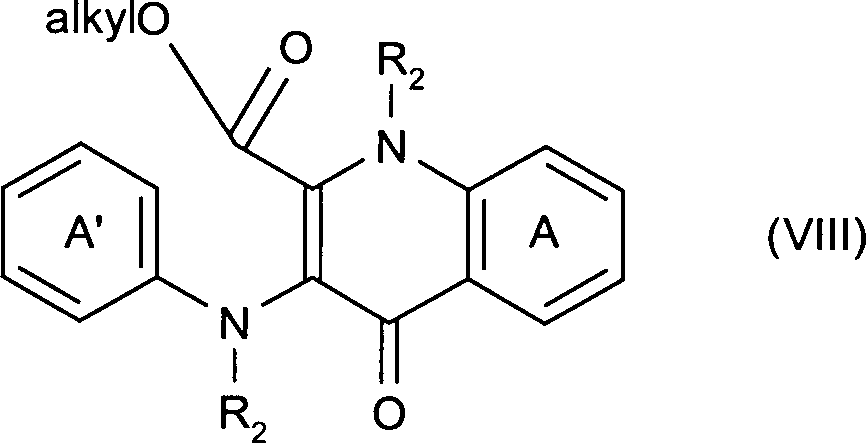
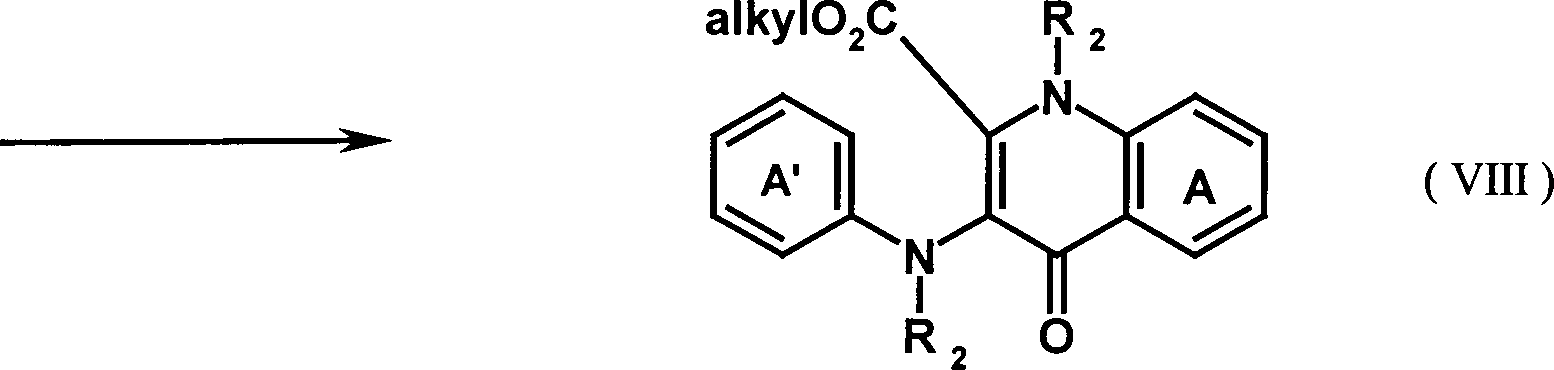
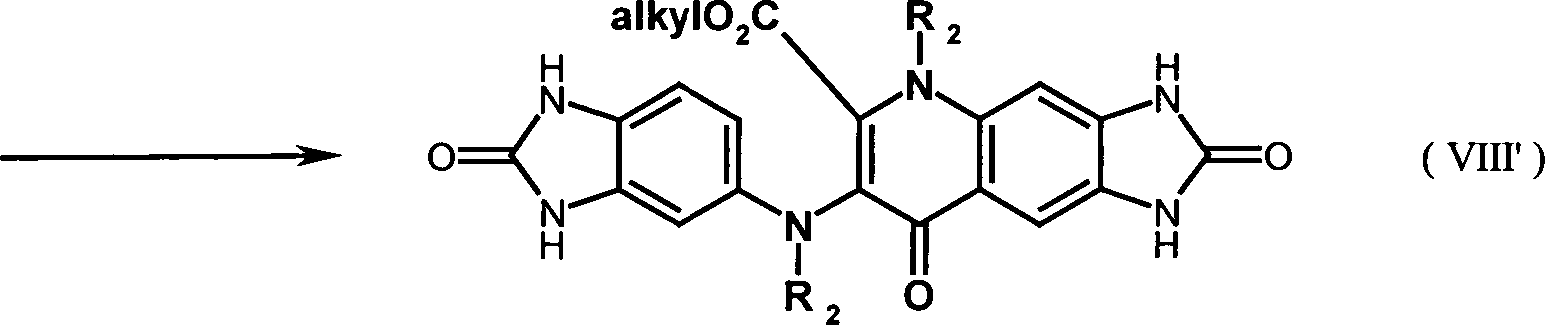
- In einer vierten Verfahrensstufe werden die in Stufe 3 erhaltenen Produkte (VIIa) und (VIIb) durch Erhitzen in einem ierten hochsiedenden Lösungsmittel zu dem im nachstehenden Fliessdiagramm gezeigten Zwischenprodukt (VIII) cyclisiert. Als hochsiedendes Lösungsmittel kommen zur Durchführung des Verfahrens beispielsweise Diphenyloxid, eine auch als Dowtherm-A bekannte Mischung aus Biphenyl und Diphenyloxiden sowie alle beliebigen Lösungsmittel mit einem Siedepunkt von über 240°C in Betracht. Die Umsetzungstemperatur liegt dabei bevorzugt bei 200 bis 280°C.
- Schliesslich wird das in Stufe 4 erhaltene monocyclisierte Produkt in einer fünften Stufe durch Erhitzen in Polyphosphorsäure oder konzentrierter Schwefelsäure weiter zur Epindolidionverbindung cyclisiert. Dabei liegt die Umsetzungstemperatur bevorzugt bei 100 bis 180°C.
- Als Hauptvorteil dieses Verfahrens sei zu nennen, dass man damit ohne weiteres auch asymmetrische Epindolidionverbindungen herstellen kann.
- Im folgenden Reaktionsschema werden die Stufen des oben beschriebenen Verfahrens veranschaulicht.
- REAKTIONSSCHEMA
- Zur weiteren Verbesserung der Pigmenteigenschaften kann man die Rohpigmente bei erhöhten Temperaturen, so beispielsweise bei 60 bis 200°C, insbesondere bei 70 bis 150°C und bevorzugt bei 75 bis 100°C, in organischen Lösungsmitteln behandeln. Diese auch als Finish bekannte Behandlung erfolgt bevorzugt in Kombination mit einer Mahlung oder Knetung.
- Nach einem weiteren Aspekt betrifft die Erfindung auch die Zwischenverbindungen der Formeln (VIIa), (VIIb) und der Formel (VIII) gemäss dem obigen Reaktionsschema.
- Erfindungsgemässe Epindolidionverbindungen der Formel (I) eignen sich insbesondere als Pigmente.
- Die erfindungsgemässen Pigmente eignen sich zum Färben von Kunststoffmassen, worunter lösungsmittelfreie und lösungsmittelhaltige Massen aus Kunststoffen oder Kunstharzen verstanden werden (in Anstrichfarben auf öliger oder wässriger Grundlage, in Lacken verschiedener Art, zum Spinnfärben von Viskose oder Celluloseacetat, zum Pigmentieren von Kunststoffen, beispielsweise Polyamid, Polyethylen, Polystyrol, Polyvinylchlorid, Kautschuk und Kunstleder). Sie können auch in Druckfarben für das graphische Gewerbe, für die Papiermassenfärbung, für die Beschichtung von Textilien oder für den Pigmentdruck Verwendung finden.
- Die erhaltenen Färbungen zeichnen sich durch ihre hervorragende Hitze-, Licht- und Wetterechtheit, Chemikalienbeständigkeit, ihre Farbstärke und die sehr guten applikatorischen Eigenschaften, z.B. Kristallisierechtheit und Dispergierechtheit und insbesondere durch ihre Migrier-, Ausblüh-, Überlackier- und Lösungsmittelechtheit aus.
- Des weiteren sind die erfindungsgemässen Pigmente auch geeignet als Farbmittel in elektrophotographischen Tonern und Entwicklern, wie z.B. ein- oder zweikomponentigen Pulvertonern (auch Ein- oder Zweikomponenten-Entwickler genannt), Magnettonern, Flüssigtonern, Polymerisationstonern sowie weiteren Spezialtonern.
- Typische Tonerbindemittel sind Polymerisations-, Polyadditions- und Polykondensationsharze wie Styrol-, Styrolacrylat-, Styrolbutadien-, Acrylat-, Polyester- und Phenol-Epoxidharze, Polysulfone, Polyurethane, einzeln oder in Kombination, sowie Polyethylen und Polypropylen, die noch weitere Inhaltsstoffe, wie Ladungssteuermittel, Wachse oder Fliessmittel, enthalten können oder im Nachhinein zugesetzt bekommen können.
- Ein weiteres Anwendungsgebiet der erfindungsgemässen Pigmente ist ihre Verwendung als Farbmittel in Pulvern und Pulverlacken, insbesondere triboelektrisch oder elektrokinetisch versprühten Pulverlacken, die zur Oberflächenbeschichtung von Gegenständen aus beispielsweise Metall, Holz, Kunststoff, Glas, Keramik, Beton, Textilmaterial, Papier oder Kautschuk zur Anwendung kommen.
- Als Pulverlackharze werden typischerweise Epoxidharze, carboxyl- und hydroxylgruppenhaltige Polyesterharze, Polyurethan- und Acrylharze zusammen mit üblichen Härtern eingesetzt. Auch Kombinationen von Harzen finden Verwendung. So werden beispielsweise häufig Epoxidharze in Kombination mit carboxyl- und hydroxylgruppenhaltigen Polyesterharzen eingesetzt. Typische Härterkomponenten (in Abhängigkeit vom Harzsystem) sind beispielsweise Säureanhydride, Imidazole sowie Dicyandiamid und deren Abkömmlinge, verkappte Isocyanate, Bisacylurethane, Phenol- und Melaminharze, Triglycidylisocyanurate, Oxazoline und Dicarbonsäuren.
- Ausserdem eignen sich die erfindungsgemässen Pigmente als Farbmittel in Tintenstrahldrucktinten auf wässriger und nichtwässriger Basis sowie in solchen Tinten, die nach dem Hot-Melt-Verfahren arbeiten.
- Die erfindungsgemässen Pigmente eignen sich ferner für Kosmetika, wie Nagellacke oder Makeup.
- In den folgenden Beispielen bedeuten die Teile Gewichtsteile und die Prozente Gewichtsprozente. Die Temperaturen sind in Celsiusgraden angegeben. Ein Volumenteil entspricht dem Volumen eines Gewichtsteils Wasser.
- BEISPIEL 1a
- In 349 Teile Chloressigsäureethylester werden 525 Teile Anilin eingetragen. Das Gemisch wird auf 80°C erhitzt. Nach 20 Minuten springt die Reaktion an, wobei die Temperatur innert einer Stunde auf 120°C steigt. Die Temperatur nimmt langsam wieder ab und stellt sich nach 30 Minuten auf 90°C ein. Das Reaktionsgemisch wird 3 Stunden lang bei 90°C weitergerührt und anschliessend auf 50°C abgekühlt und auf 875 Teile Wasser gegeben. Die Suspension wird abfiltriert und mit 1000 Teilen aus einer Mischung von Alkohol und Wasser in einem Verhältnis von 1:9 nachgewaschen. Das Produkt wird mit Wasser chloridfrei gewaschen, aus Cyclohexan umkristallisiert und bei 20°C im Vakuum getrocknet. Man erhält 310 Teile weisser Kristalle einer Verbindung der nachstehenden Formel Ausbeute: 62% Schmelzpunkt: 54,5–55,5°C
- BEISPIEL 1b
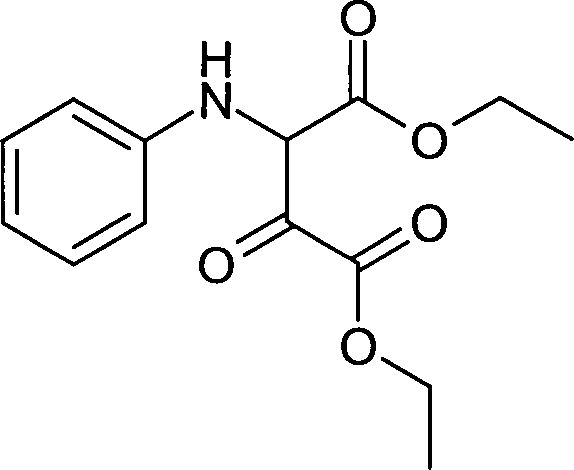
- Man löst 35,3 Teile Natriumethanolat in 235 Teilen Ethanol. Man gibt zuerst 69,3 Teile Oxalsäurediethylester und anschliessend 84 Teile des in Beispiel 1a hergestellten Produkts in den Reaktor. Das Gemisch wird anschliessend 24 Stunden lang bei 25°C gerührt. Dann wird Ethanol im Vakuum abdestilliert. Der Rückstand wird unter kräftigem Rühren mit 352 Teilen Wasser und 33 Teilen Essigsäure versetzt. Zur Extrahierung des Produkts werden 282 Teile Toluol zugesetzt. Die organische Phase wird von der wässrigen Phase abgetrennt und nochmal mit 282 Teilen Wasser gewaschen. Nach dem Abziehen der Toluolphase verbleiben 118,7 Teile eines roten Öls, das ohne weitere Reinigung in der nächsten Stufe eingesetzt wird.
- BEISPIEL 1e
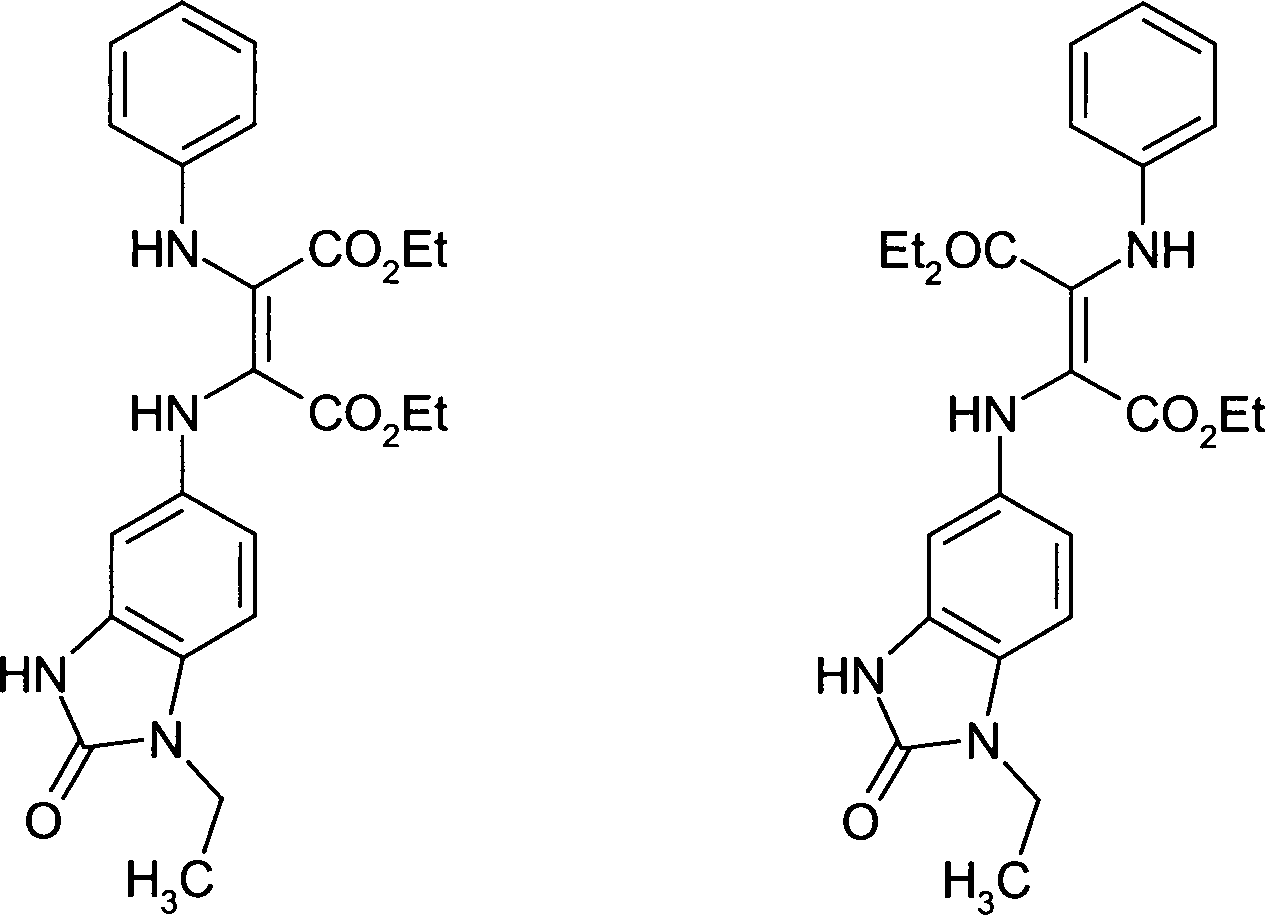
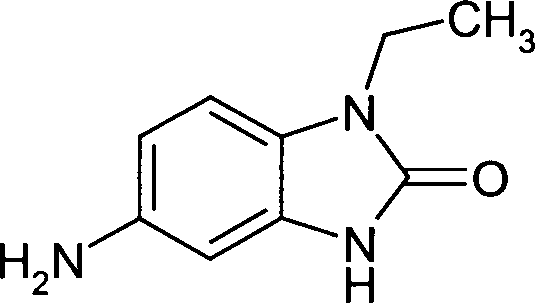
- Man löst 110 Teile des in Beispiel 1 b hergestellten Produkts in 335 Teilen Ethanol. Die Lösung wird mit 71,4 Teilen des nachstehenden Amins versetzt und anschliessend 6 Stunden lang am Rückfluss erhitzt. Das Reaktionsgemisch wird anschliessend mit einem Eiswasserbad auf 0°C abgekühlt, abfiltriert und mit 50 Teilen Ethanol kalt nachgewaschen. Nach dem Trocknen bei 40°C im Vakuum erhält man 44,2 Teile eines grauen Pulvers als Gemisch von Verbindungen der nachstehenden Formel
- BEISPIEL 1d
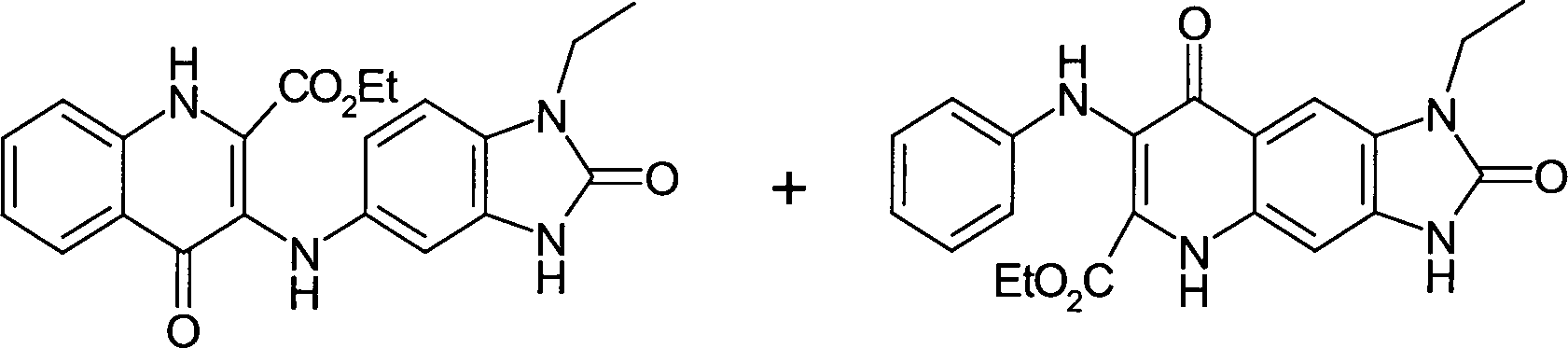
- Man suspendiert 22,6 Teile des in Beispiel 1c erhaltenen Produkts in 30 Teilen Dowtherm A und erhitzt auf 85°C, wobei man eine Lösung erhält. Diese Lösung fügt man innert 15 Minuten einem weiteren, schon mit 70 Teilen Dowtherm A beschickten und auf 258°C vorerhitzten Reaktor zu. Das bei der Reaktion entstandene Ethanol wird abdestilliert. Das Reaktionsgemisch wird nach Ende der Zugabe 15 Minuten lang auf 250°C erhitzt und anschliessend auf 25°C abgekühlt. Das ausgefallene Produkt wird abfiltriert, zunächst mit 50 Teilen Dowtherm A und anschliessend mit 700 Teilen Hexan gewaschen und bei 80°C im Vakuum getrocknet. Man erhält 16,6 Teile eines braunen Pulvers einer Mischung von Verbindungen der nachstehenden Formel
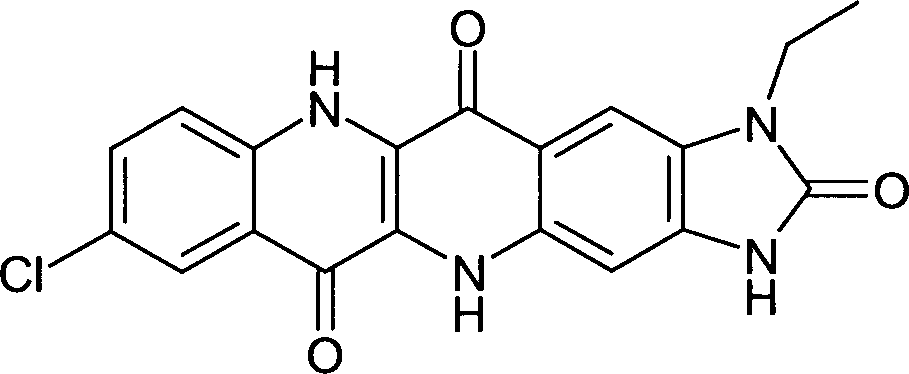
- BEISPIEL 1e
- In einem Reaktor werden 16 Teile Polyphosphorsäure (H3PO4-Gehalt 85%) und 1,6 Teile des in Beispiel 1d isolierten Produkts gemischt und allmählich auf 150°C erhitzt und 4 Stunden lang bei dieser Temperatur gerührt. Anschliessend wird das Reaktionsgemisch auf 60°C abgekühlt und mit 235 Teilen Wasser versetzt. Die Suspension wird abfiltriert und mit Wasser nachgewaschen. Nach dem Trocknen bei 80°C im Vakuum erhält man 1,2 Teile eines orange Pulvers einer Verbindung der nachstehenden Formel
- BEISPIEL 2a
- In 304 Teile Chloressigsäureethylester werden 639,4 Teile p-Chloranilin eingetragen. Das Gemisch wird auf 80°C erhitzt. Nach 20 Minuten springt die Reaktion an, wobei die Temperatur innert einer Stunde auf 115°C steigt. Die Temperatur nimmt langsam wieder ab und stellt sich nach 30 Minuten auf 90°C ein. Das Reaktionsgemisch wird 3 Stunden lang bei 90°C weitergerührt und anschliessend auf 50°C abgekühlt und auf 300 Teile Wasser und 400 Teile Eis gegeben. Die Suspension wird abfiltriert und mit 5000 Teilen Wasser nachgewaschen. Das Produkt wird mit Wasser chloridfrei gewaschen, aus Cyclohexan umkristallisiert und bei 20°C im Vakuum getrocknet. Man erhält 346,4 Teile weisser Kristalle einer Verbindung der nachstehenden Formel Ausbeute: 67% Schmelzpunkt: 94–95°C
- BEISPIEL 2b
- Man löst 119,3 Teile Natriumethanolat in 800 Teilen Ethanol. Man gibt zuerst 236 Teile Oxalsäurediethylester und anschliessend 341,6 Teile des in Beispiel 2a hergestellten Produkts in den Reaktor. Das Gemisch wird anschliessend 24 Stunden lang bei 25°C gerührt. Dann wird Ethanol im Vakuum abdestilliert. Der Rückstand wird unter kräftigem Rühren mit 1200 Teilen Wasser und 112 Teilen Essigsäure versetzt. Zur Extrahierung des Produkts werden 960 Teile Toluol zugesetzt. Die organische Phase wird von der wässrigen Phase abgetrennt und nochmal mit 320 Teilen Wasser gewaschen. Nach dem Abziehen der Toluolphase verbleiben 500 Teile eines orange Öls, das ohne weitere Reinigung in der nächsten Stufe eingesetzt wird.
- BEISPIEL 2e
- Man löst 487,1 Teile des in Beispiel 2b hergestellten Produkts in 1325 Teilen Ethanol. Die Lösung wird mit 281,4 Teilen des nachstehenden Amins versetzt und anschliessend 6 Stunden lang am Rückfluss erhitzt. Das Reaktionsgemisch wird anschliessend mit einem Eiswasserbad auf 0°C abgekühlt, abfiltriert und mit 1000 Teilen Ethanol kalt nachgewaschen. Nach dem Trocknen bei 40°C im Vakuum erhält man 284,6 Teile eines grauen Pulvers als Gemisch von Verbindungen der nachstehenden Formel
- BEISPIEL 2d
- Man suspendiert 100 Teile des in Beispiel 2c erhaltenen Produkts in 1050 Teilen Dowtherm A und erhitzt auf 150°C, wobei man eine Lösung erhält. Diese Lösung fügt man innert 15 Minuten einem weiteren, schon mit 787 Teilen Dowtherm A beschickten und auf 258°C vorerhitzten Reaktor zu. Das bei der Reaktion entstandene Ethanol wird abdestilliert. Das Reaktionsgemisch wird nach Ende der Zugabe 15 Minuten lang auf 250°C erhitzt und anschliessend auf 25°C abgekühlt. Das ausgefallene Produkt wird abfiltriert, zunächst mit 150 Teilen Dowtherm A und anschliessend mit 800 Teilen Ethanol gewaschen und bei 80°C im Vakuum getrocknet. Man erhält 64 Teile eines braunen Pulvers einer Mischung von Verbindungen der nachstehenden Formel
- BEISPIEL 2e
- In einem Reaktor werden 470 Teile Polyphosphorsäure (H3PO4-Gehalt 85%) und 47 Teile des in Beispiel 1d isolierten Produkts gemischt und allmählich auf 150°C erhitzt und 4 Stunden lang bei dieser Temperatur gerührt. Anschliessend wird das Reaktionsgemisch auf 60°C abgekühlt und mit 235 Teilen Wasser versetzt. Die Suspension wird abfiltriert und mit Wasser nachgewaschen. Nach dem Trocknen bei 80°C im Vakuum erhält man 41,6 Teile eines orange Pulvers einer Verbindung der nachstehenden Formel
- BEISPIEL 3a
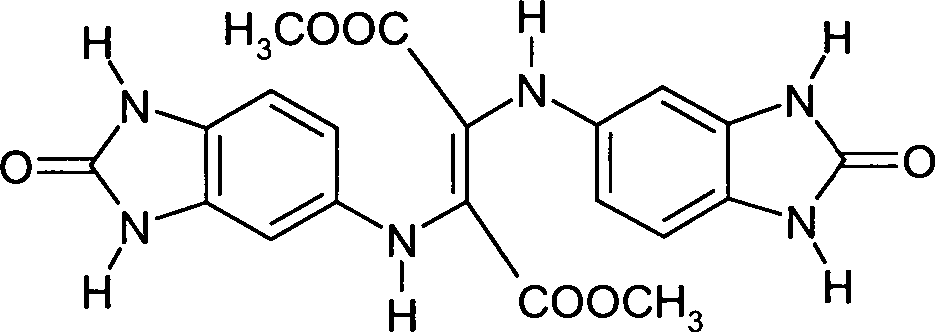
- Man suspendiert 103,1 Teile 2,3-Dihydroxyfurmarsäuredimethylester in 371 Teilen Methanol. Man versetzt mit 192,1 Teilen 5-Aminobenzimidazolo-2-on und 5 Teilen konzentrierter Salzsäure. Das Gemisch wird 6 Stunden lang am Rückfluss erhitzt. Die Suspension wird auf 5°C abgekühlt und der Niederschlag abfiltriert, mit Methanol gewaschen und bei 60°C im Vakuum getrocknet. Man erhält 93,1 Teile einer Verbindung der nachstehenden Formel
- BEISPIEL 3b
- Man erhitzt 278 Teile einer Mischung von Biphenyl- und Diphenylether zum Sieden und versetzt mit einer Lösung von 93,1 Teilen des Produkts aus Beispiel 3a in 693 Teilen einer Mischung von Biphenyl- und Diphenylether bei 130°C innert 30 Minuten. Das Gemisch wird innert 30 Minuten auf 255°C erhitzt und auf 50°C abgekühlt. Der Niederschlag wird abfiltriert, mit Petrolether gewaschen und bei 60°C im Vakuum getrocknet. Man erhält 73,7 Teile einer Verbindung der nachstehenden Formel
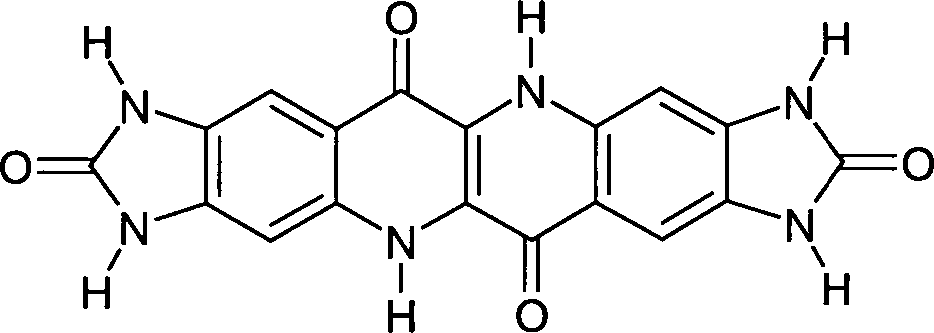
- BEISPIEL 3e
- Zu 535 Teilen Polyphosphorsäure gibt man bei 145 bis 150°C 73,7 Teile des Produkts aus Beispiel 3b und hält 2 Stunden lang bei 145 bis 150°C. Das Gemisch wurde bei 0°C auf 2500 Teile Wasser gegeben. Der Niederschlag wird abfiltriert, mit Wasser gewaschen und bei 60°C im Vakuum getrocknet. Man erhält 54,6 Teile einer Verbindung der nachstehenden Formel ANWENDUNGSBEISPIEL 1
4 Teile des Pigments gemäss der nachstehenden Tabelle werden mit 96 Teilen einer Mischung aus 50 Teilen einer 60prozentigen Lösung von Co-Aldehyd-Melaminharzlösung in Butanol, 10 Teilen Xylol und 10 Teilen Ethylenglykolmonoethylether 24 Stunden lang in einer Kugelmühle gemahlen. - Die dabei erhaltene Dispersion wird auf Aluminiumblech gespritzt, 30 Minuten lang abgelüftet und dann 30 Minuten lang bei 120°C eingebrannt. Man erhält so einen der nachstehenden Tabelle entsprechend gefärbten Film mit sehr guter Migrierechtheit sowie guter Licht- und Wetterbeständigkeit.
- ANWENDUNGSBEISPIEL 2
- Beispiel für die Herstellung einer 0,1%ig gefärbten PVC-Folie (Verschnitt Buntpigment zu Weisspigment 1:5):
-
- 16,5 Teile einer Weichmachermischung, bestehend aus gleichen Teilen Dioctylphthalat und Dibutylphthalat, werden mit
- 0,05 Teilen des Pigments gemäss der nachstehenden Tabelle und
- 0,25 Teilen Titandioxid gemischt. Dann werden
- 33,5 Teile Polyvinylchlorid zugegeben.
- Das Gemisch wird 10 Minuten lang auf einem Zweiwalzenstuhl mit Friktion gewalzt, wobei sich das bildende Fell mit einem Spatel fortlaufend zerschnitten und zusammengerollt wird. Dabei wird die eine Walze auf einer Temperatur von 40°C und die andere auf einer Temperatur von 140° gehalten. Anschliessend wird das Gemisch als Fell abgezogen und 5 Minuten lang bei 160° zwischen zwei polierten Metallplatten gepresst. So erhält man eine gefärbte PVC-Folie hoher Brillianz mit sehr guter Migrations- und Lichtechtheit.
Claims (13)
- Epindolidionverbindungen der allgemeinen Formel (I) wobei der mit A bezeichnete Kern ein anelliertes heteroaromatisches Ringsystem darstellt, das linear, in 2,3-Stellung, oder angular, in 1,2- oder in 3,4-Stellung, anelliert einen Ring mit den unter den Formelteilen (1) bis (11) ausgewählten Restgliedern enthält: wobei R3 und R4 unabhängig voneinander Wasserstoff, C1–8-Alkyl, C5–6-Cycloalkyl, Benzyl, Benzanilid oder Naphthyl bedeuten, wobei Phenylgruppen ein- oder mehrfach durch Reste aus der Gruppe Halogen, Nitrogruppen, C1–8-Alkyl, Phenyl, -COOR mit R gleich C1–8-Alkyl und C1–2-Alkoxy, bevorzugt Chlor, C1–4-Alkyl, Phenyl oder -COOR mit R gleich C1–8-Alkyl substituiert sein können, oder R3 und/oder R4 einen Rest der Formel (a) bedeuten, wobei der mit A' bezeichnete Kern einen gegebenenfalls substituierten aromatischen Ring oder ein anelliertes heteroaromatisches Ringsystem darstellt, das linear, in 2,3-Stellung, oder angular, in 1,2- oder in 3,4-Stellung, anelliert einen Ring mit den unter den Formelteilen (12) bis (22) ausgewählten Restgliedern enthält: wobei R'3 und R'4 unabhängig voneinander Wasserstoff, C1–8-Alkyl, C5–6-Cyclo-alkyl, Benzyl, Benzanilid oder Naphthyl bedeuten, wobei Phenylgruppen ein- oder mehrfach durch Reste aus der Gruppe Halogen, Nitrogruppen, C1–8-Alkyl, Phenyl, -COOR mit R gleich C1–8-Alkyl und C1–2-Alkoxy substituiert sein können, und R2 Wasserstoff, C1–12-Alkyl oder Phenyl oder -COOR mit R gleich C1–8-Alkyl bedeutet.
- Epindolidionverbindungen der allgemeinen Formel (I') wobei der mit A bezeichnete Kern ein anelliertes heteroaromatisches Ringsystem darstellt, das linear, in 2,3-Stellung, oder angular, in 1,2- oder in 3,4-Stellung, anelliert einen Ring mit den unter den Formelteilen (1) bis (11) ausgewählten Restgliedern enthält: wobei R3 und R4 unabhängig voneinander Wasserstoff, C1–8-Alkyl, C5–6-Cycloalkyl, Benzyl, Benzanilid oder Naphthyl bedeuten, wobei Phenylgruppen ein- oder mehrfach durch Reste aus der Gruppe Halogen, Nitrogruppen, C1–8-Alkyl, Phenyl, -COOR mit R gleich C1–8-Alkyl und C1–2-Alkoxy, bevorzugt Chlor, C1–4-Alkyl, Phenyl oder -COOR mit R gleich C1–8-Alkyl substituiert sein können, oder R3 und/oder R4 einen Rest der Formel (a) bedeuten, wobei der mit A' bezeichnete Kern einen gegebenenfalls substituierten aromatischen Ring oder ein anelliertes heteroaromatisches Ringsystem darstellt, das linear, in 2,3-Stellung, oder angular, in 1,2- oder in 3,4-Stellung, anelliert einen Ring mit den unter den Formelteilen (12) bis (22) ausgewählten Restgliedern enthält: wobei R'3 und R'4 unabhängig voneinander C1–8-Alkyl, C5–6-Cycloalkyl, Benzyl, Benzanilid oder Naphthyl bedeuten, wobei Phenylgruppen ein- oder mehrfach durch Reste aus der Gruppe Halogen, Nitrogruppen, C1–8-Alkyl, Phenyl, -COOR mit R gleich C1–8-Alkyl und C1–2-Alkoxy substituiert sein können, und R2 Wasserstoff, C1–12-Alkyl oder Phenyl oder -COOR mit R gleich C1–8-Alkyl bedeutet.
- Verwendung der Verbindungen der Formel (I) gemäss Anspruch 1 als Pigmente.
- Verwendung der Verbindungen der Formel (I) gemäss Anspruch 1 als Farbmittel zur Einfärbung von Kunststoffmassen oder Papiermassen, als Farbmittel in elektrophotographischen Tonern und Entwicklern, als Farbmittel in Tintenstrahldrucktinten, als Farbmittel in der Lackindustrie, als Farbmittel für den Textildruck oder als Druckfarbe im graphischen Gewerbe, als Farbmittel in Kosmetika.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0103011.3A GB0103011D0 (en) | 2001-02-07 | 2001-02-07 | Improvements in or relating to chemical compounds |
| GB0103011 | 2001-02-07 | ||
| PCT/IB2002/000369 WO2002062796A1 (en) | 2001-02-07 | 2002-02-06 | Epindolidione pigments |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60201345D1 DE60201345D1 (de) | 2004-10-28 |
| DE60201345T2 true DE60201345T2 (de) | 2005-02-24 |
Family
ID=9908274
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60201345T Expired - Fee Related DE60201345T2 (de) | 2001-02-07 | 2002-02-06 | Epindolidionpigmente |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US7307170B2 (de) |
| EP (1) | EP1379527B1 (de) |
| JP (1) | JP4173004B2 (de) |
| KR (1) | KR20030072401A (de) |
| CN (1) | CN1491226A (de) |
| AT (1) | ATE277047T1 (de) |
| DE (1) | DE60201345T2 (de) |
| GB (1) | GB0103011D0 (de) |
| WO (1) | WO2002062796A1 (de) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN100384626C (zh) * | 2005-01-28 | 2008-04-30 | 浙江凯喜雅国际股份有限公司 | 一种横机针织毛衫数码喷印工艺 |
| EP2796512A1 (de) * | 2005-03-24 | 2014-10-29 | Cabot Corporation | Fluorchinolonchinolone und diese enthaltende Tintenstrahltintenzusammensetzungen |
| US7691197B2 (en) * | 2005-10-21 | 2010-04-06 | Cabot Corporation | Method of preparing yellow pigments |
| CN103145708B (zh) * | 2013-03-25 | 2015-04-15 | 百合花集团股份有限公司 | 制备表吲哚二酮及其衍生物的方法 |
| CN103159762B (zh) * | 2013-03-25 | 2015-04-15 | 华东理工大学 | 表吲哚二酮衍生物及其用途 |
| AT513830B1 (de) | 2013-08-14 | 2014-08-15 | Universität Linz | Verfahren zum Aufbringen einer organischen Halbleiterschicht auf der Basis von Epindolidion auf einen Träger |
| KR101766379B1 (ko) * | 2016-05-04 | 2017-08-08 | 정문교 | 에핀돌리디온 유도체 및 도판트를 포함하는 oled |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4142890A (en) * | 1977-05-20 | 1979-03-06 | Eastman Kodak Company | Photosensitive trans-epindolidione pigment for migration imaging processes |
| DE3144180A1 (de) * | 1980-11-10 | 1982-06-24 | Eastman Kodak Co., 14650 Rochester, N.Y. | Elektrisch photosensitives pigment und verwendung desselben |
| FR2706475B1 (fr) | 1993-06-16 | 1997-08-29 | Sandoz Sa | Teinture dans la masse de polymères synthétiques. |
| EP0766498B1 (de) * | 1995-09-29 | 2001-01-24 | Eastman Kodak Company | Organische elektrolumineszente Vorrichtungen mit hoher thermischer Stabilität |
| JP3206457B2 (ja) * | 1996-10-28 | 2001-09-10 | 東洋インキ製造株式会社 | インクジェットインキおよびインクジェットインキセット |
| JPH10189246A (ja) * | 1996-10-31 | 1998-07-21 | Mitsui Chem Inc | 有機電界発光素子 |
| JPH11130972A (ja) * | 1997-09-01 | 1999-05-18 | Toyo Ink Mfg Co Ltd | 有機顔料 |
| JP3775904B2 (ja) * | 1997-09-24 | 2006-05-17 | 三井化学株式会社 | 有機電界発光素子 |
| GB9824314D0 (en) | 1998-11-06 | 1998-12-30 | Clariant Int Ltd | New hetercyclic compounds |
| GB0002966D0 (en) | 2000-02-10 | 2000-03-29 | Clariant Int Ltd | New triphendioxazine pigments |
-
2001
- 2001-02-07 GB GBGB0103011.3A patent/GB0103011D0/en not_active Ceased
-
2002
- 2002-02-06 CN CNA02804651XA patent/CN1491226A/zh active Pending
- 2002-02-06 WO PCT/IB2002/000369 patent/WO2002062796A1/en not_active Ceased
- 2002-02-06 DE DE60201345T patent/DE60201345T2/de not_active Expired - Fee Related
- 2002-02-06 US US10/467,041 patent/US7307170B2/en not_active Expired - Fee Related
- 2002-02-06 AT AT02710233T patent/ATE277047T1/de not_active IP Right Cessation
- 2002-02-06 KR KR10-2003-7010363A patent/KR20030072401A/ko not_active Withdrawn
- 2002-02-06 EP EP02710233A patent/EP1379527B1/de not_active Expired - Lifetime
- 2002-02-06 JP JP2002563149A patent/JP4173004B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| KR20030072401A (ko) | 2003-09-13 |
| GB0103011D0 (en) | 2001-03-21 |
| JP4173004B2 (ja) | 2008-10-29 |
| DE60201345D1 (de) | 2004-10-28 |
| ATE277047T1 (de) | 2004-10-15 |
| CN1491226A (zh) | 2004-04-21 |
| US7307170B2 (en) | 2007-12-11 |
| WO2002062796A8 (en) | 2002-09-26 |
| US20040138451A1 (en) | 2004-07-15 |
| EP1379527A1 (de) | 2004-01-14 |
| JP2004525215A (ja) | 2004-08-19 |
| WO2002062796A1 (en) | 2002-08-15 |
| EP1379527B1 (de) | 2004-09-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0889046B1 (de) | Triphendioxazine und ihre Verwendung als Pigmente | |
| DE60201345T2 (de) | Epindolidionpigmente | |
| DE69833135T2 (de) | Triphendioxazinverbindungen | |
| EP1611206B1 (de) | Heterocyclische farbmittel auf basis von benzodipyrrolen | |
| DE2542408A1 (de) | Neue disazopigmente und verfahren zu deren herstellung | |
| DE60104719T2 (de) | Verfahren zur herstellung von triphendioxazinpigmenten | |
| CH469789A (de) | Verfahren zur Herstellung von Naphth-(2,3-b-)indolizin-6,11-dion-12-carbonsäure-phenylamid-Pigmenten | |
| EP0088920A2 (de) | Isoindolinfarbstoffe und deren Verwendung | |
| EP1132432B1 (de) | Verfahren zur Herstellung von Pigmenten | |
| DE2924142A1 (de) | Bis-isoindolinpigmente, verfahren zu deren herstellung und verwendung | |
| EP0761764A1 (de) | Wasserunlösliche Azofarbmittel auf Basis von Aminochinazolindionen | |
| EP1706459B1 (de) | Triphendioxazinpigmente | |
| EP0022076B1 (de) | Iminoisoindolinonfarbstoffe, Verfahren zu deren Herstellung und deren Verwendung | |
| DE3007329A1 (de) | Isoindolinfarbstoffe | |
| EP0581245A1 (de) | Wasserunlösliche Azofarbmittel | |
| EP1713802B1 (de) | Mesoionische pigmente auf basis von 2,4-dioxopyrimidinen | |
| EP1639047B1 (de) | Heterocyclische farbmittel auf basis von diazabenzoisoindolen | |
| DE2342815A1 (de) | Neue dioxazinfarbstoffe | |
| DE1569773C (de) | Pigment der Bis (tetrachlor isoindo Im 1 on 3 yhdenimino) aryl reihe und Verfahren zu dessen Herstellung | |
| EP0602009A2 (de) | Heterocyclische Verbindungen | |
| DE2400561A1 (de) | Iminoisoindolinonfarbstoffe und verfahren zu deren herstellung | |
| DE1569608C (de) | Triphendioxazinfarbstoffe, deren Herstellung und Verwendung | |
| EP0055380A1 (de) | Disazoverbindungen, Verfahren zu ihrer Herstellung und ihre Verwendung | |
| EP0170987A1 (de) | Benzimidazol-2-carbonsäure-Derivate | |
| DE1951249A1 (de) | Anthrachinonpigmente |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8339 | Ceased/non-payment of the annual fee |