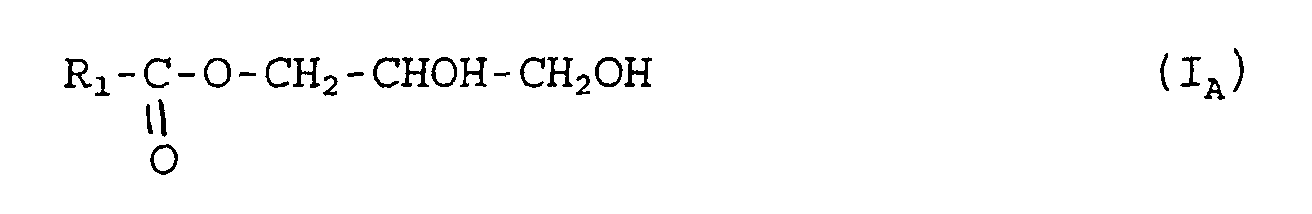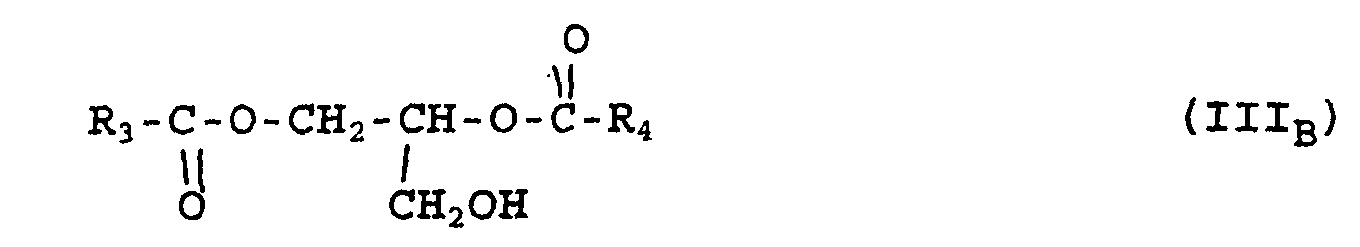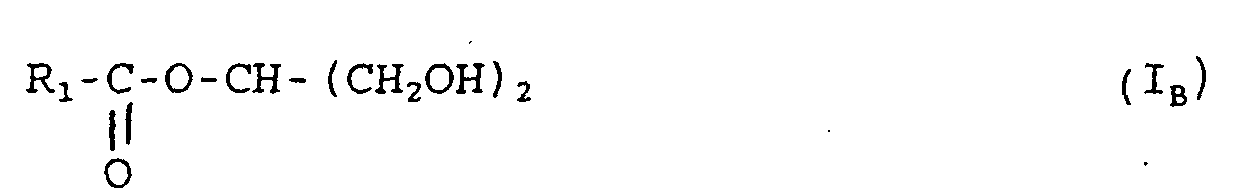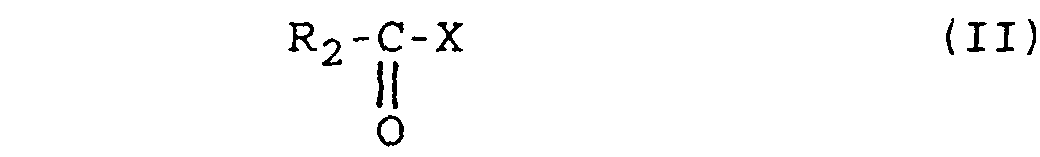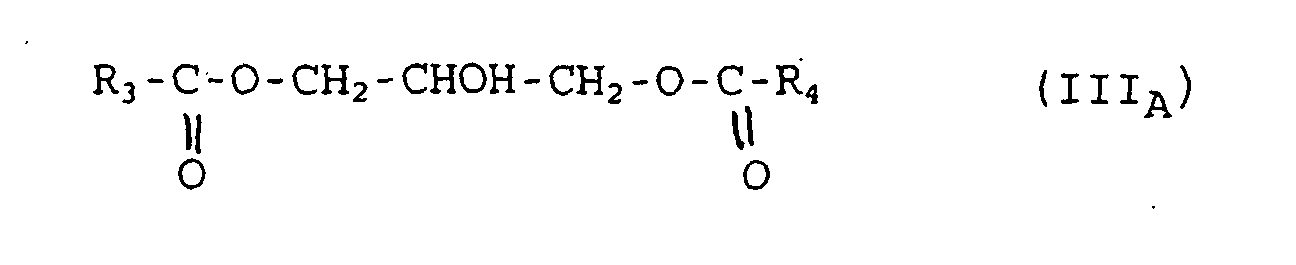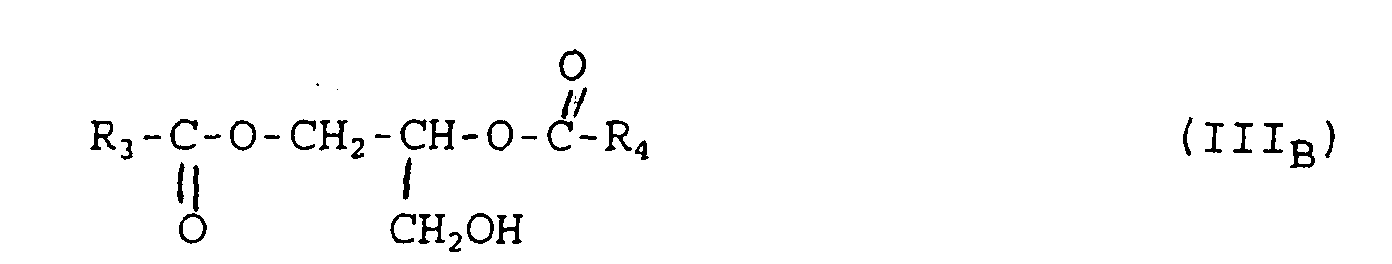EP1522570A2 - Additif d'onctuosite pour carburant - Google Patents
Additif d'onctuosite pour carburant Download PDFInfo
- Publication number
- EP1522570A2 EP1522570A2 EP05000389A EP05000389A EP1522570A2 EP 1522570 A2 EP1522570 A2 EP 1522570A2 EP 05000389 A EP05000389 A EP 05000389A EP 05000389 A EP05000389 A EP 05000389A EP 1522570 A2 EP1522570 A2 EP 1522570A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- carbon atoms
- acid
- chosen
- formula
- additive according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L10/00—Use of additives to fuels or fires for particular purposes
- C10L10/08—Use of additives to fuels or fires for particular purposes for improving lubricity; for reducing wear
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/143—Organic compounds mixtures of organic macromolecular compounds with organic non-macromolecular compounds
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/19—Esters ester radical containing compounds; ester ethers; carbonic acid esters
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/19—Esters ester radical containing compounds; ester ethers; carbonic acid esters
- C10L1/191—Esters ester radical containing compounds; ester ethers; carbonic acid esters of di- or polyhydroxyalcohols
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/222—Organic compounds containing nitrogen containing at least one carbon-to-nitrogen single bond
- C10L1/224—Amides; Imides carboxylic acid amides, imides
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/1802—Organic compounds containing oxygen natural products, e.g. waxes, extracts, fatty oils
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/192—Macromolecular compounds
- C10L1/198—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds homo- or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon to carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/18—Organic compounds containing oxygen
- C10L1/192—Macromolecular compounds
- C10L1/198—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds homo- or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon to carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid
- C10L1/1985—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds homo- or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon to carbon double bond, and at least one being terminated by an acyloxy radical of a saturated carboxylic acid, of carbonic acid polyethers, e.g. di- polygylcols and derivatives; ethers - esters
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/222—Organic compounds containing nitrogen containing at least one carbon-to-nitrogen single bond
- C10L1/2222—(cyclo)aliphatic amines; polyamines (no macromolecular substituent 30C); quaternair ammonium compounds; carbamates
- C10L1/2225—(cyclo)aliphatic amines; polyamines (no macromolecular substituent 30C); quaternair ammonium compounds; carbamates hydroxy containing
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/232—Organic compounds containing nitrogen containing nitrogen in a heterocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/232—Organic compounds containing nitrogen containing nitrogen in a heterocyclic ring
- C10L1/233—Organic compounds containing nitrogen containing nitrogen in a heterocyclic ring containing nitrogen and oxygen in the ring, e.g. oxazoles
- C10L1/2335—Organic compounds containing nitrogen containing nitrogen in a heterocyclic ring containing nitrogen and oxygen in the ring, e.g. oxazoles morpholino, and derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C10—PETROLEUM, GAS OR COKE INDUSTRIES; TECHNICAL GASES CONTAINING CARBON MONOXIDE; FUELS; LUBRICANTS; PEAT
- C10L—FUELS NOT OTHERWISE PROVIDED FOR; NATURAL GAS; SYNTHETIC NATURAL GAS OBTAINED BY PROCESSES NOT COVERED BY SUBCLASSES C10G OR C10K; LIQUIFIED PETROLEUM GAS; USE OF ADDITIVES TO FUELS OR FIRES; FIRE-LIGHTERS
- C10L1/00—Liquid carbonaceous fuels
- C10L1/10—Liquid carbonaceous fuels containing additives
- C10L1/14—Organic compounds
- C10L1/22—Organic compounds containing nitrogen
- C10L1/234—Macromolecular compounds
- C10L1/238—Macromolecular compounds obtained otherwise than by reactions involving only carbon-to-carbon unsaturated bonds
Definitions
- the present invention relates to a fuel containing a lubricity additive to improve the properties lubricating fuels, whether it is engine fuel (diesel) or aviation fuel (jet fuel), and more particularly low-grade diesel fuels sulfur.
- the gas oils have been added to anti-wear additives, known to some in the field of lubricants, of the type of fatty acid esters and dimers unsaturated fatty acids, aliphatic amines, esters of fatty acids and diethanolamine, and acids aliphatic monocarboxylic long chain as described in US Patents 2,527,889, US 4,185,594, US 4,204,481 and US 4208190.
- anti-wear additives known to some in the field of lubricants, of the type of fatty acid esters and dimers unsaturated fatty acids, aliphatic amines, esters of fatty acids and diethanolamine, and acids aliphatic monocarboxylic long chain as described in US Patents 2,527,889, US 4,185,594, US 4,204,481 and US 4208190.
- Most of these additives have power sufficient lubricant but at concentrations far too much high which is very economically unfavorable to purchase.
- additives containing dimer acids can not be used in fuels fueling vehicles in which the fuel may be in contact with the lubricating oil, because these acids form by chemical reaction with detergents usually used in lubricants, deposits that can accelerate the wear process.
- US Patent 4,609,376 advocates the use of anti-wear additives obtained from mono- and polycarboxylic and polyhydric alcohols in fuels containing alcohols in their composition.
- Another chosen route is to introduce oils plants or their esters in fuels to improve their lubricity or lubricity.
- oils plants or their esters can be found in rapeseed, flax, soybean, sunflower or their esters (see EP 635.558 and EP 605.857).
- one of the major disadvantages of these esters is their low lubricity at a concentration of less than 0.5 % by weight in fuels.
- the present invention aims to solve the problems encountered with the additives proposed by the prior art, that is to say to improve the lubricating power of the fuels desulphurized and partially deflavored, while remaining compatible with other additives, including detergents, lubricating oils, in particular by not forming deposits and by reducing the cost price, in particular by less additive content, well below 0.5%.
- the monoesters and di esters obtained from the oils are preferred. of the group consisting of lauric oils, from coconut or palm, rich in saturated alkyl chains of 12 to 14 carbon atoms, palmitic oils from palm, lard or tallow, containing a major amount of saturated alkyl chains.
- linoleic oils derived from sunflower, corn, or rapeseed containing a high content of linoleic acid
- linolenic linseed oils comprising significant contents of tri-unsaturated alkyl chains containing from 1 to 18 carbon atoms
- ricinoleic oils derived from castor oil derived from castor oil.
- the preferred monoesters and diesters of glycerol obtained from polycyclic acids comprise an R 1 or R 3 and / or R 4 consisting of at least two rings each of 5 to 6 atoms of which at most one is optionally a heteroatom such as nitrogen or oxygen and the others are carbon atoms, these two rings having in addition two carbon atoms in common, preferably vicinal, said cycles being saturated or unsaturated .
- They are preferably monoesters of glycerol of natural resin acids obtained from the distillation residues of natural oils extracted from coniferous trees, in particular coniferous conifers.
- abietic acid acid esters are preferred. dihydroabietic, tetrahydroabietic acid, acid dehydroabietic, neoabietic acid, pimaric acid, of levopimaric acid and parastrinic acid.
- Esters and amides of formula (II) can be easily obtained by reaction of an alcohol compound, amine and / or alkanolamine with an organic acid such as oleic acid or a simple ester such as methyl oleate operating in the conditions known per se by the man of the esterification and amidation processes.
- the alcohols used to obtain the compound (II) are chosen from the group consisting of methanol, ethanol, propanol, isopropanol, butanol, isobutanol, pentanol or else ethyl 2 hexanol, and / or oxyalkylated alcohols of formula R (O-CH 2 -CHR ') n -OH wherein R is an alkyl group of 1 to 6 carbon atoms, R' is hydrogen or an alkyl group of 1 to 4 carbon atoms and n an integer ranging from 1 to 5 such as methylcellosolve, butylcellosolve, butyldiglycol and 1-butoxy-propanol.
- the primary amines or secondary compounds used to obtain the compound (II) are selected from the group consisting of methylamine, ethylamine, propylamine, butylamine, isobutylamine, ethyl-2-hexylamine, decylamine, dodecylamine, stearylamine and oleylamine, N, N-diethylamine, N, N-dipropylamine, N, N-dibutylamine, N, N-di (ethyl-2-hexyl) amine, methyldecylamine, N-methyldodecylamine, N-methyloleylamine.
- alkanolamines selected from amines of 1 to 18 carbon atoms substituted by at least one hydroxyl, -hydroxymethyl, hydroxyethyl or hydroxypropyl such as ethanolamine, diethanolamine, triethanolamine, isopropanolamine, diisopropanolamine, triisopropanolamine, N-methylethanolamine, tris (hydroxymethyl) aminomethane, (N-hydroxyethyl) methylimidazoline, (N-hydroxyethyl) heptadecenylimidazoline.
- hydroxyl, -hydroxymethyl, hydroxyethyl or hydroxypropyl such as ethanolamine, diethanolamine, triethanolamine, isopropanolamine, diisopropanolamine, triisopropanolamine, N-methylethanolamine, tris (hydroxymethyl) aminomethane, (N-hydroxyethyl) methylimidazoline, (N-hydroxyethyl) heptadecen
- Additives obtained by physical mixing according to the invention are used to improve the lubricity Diesel fuels for land-based engines, possibly in mixture with at least one oxygenated compound selected from the group formed alcohols, ethers and esters, as well as with any additive used to improve fuel quality, such as as detergent, dispersant, antioxidant and antifoam or even biofuel.
- a second object of the invention corresponds to fuels containing between 25 and 2500 ppm, and preferably 100 to 1000 ppm by weight of at least one additive used according to the invention dispersed in a diesel fuel defined by the ASTM D-975.
- the purpose of this example is to compare the power lubricant additives lubricity according to the invention to that known lubricity additives with regard to wear in the conditions of the HFRR (High Frequency Reciprocating Rig) test as described by the standard procedure CEC-F06-A96 in SAE article 932692 by J. W. HADLEY of the University of Liverpool.
- HFRR High Frequency Reciprocating Rig
- the additives according to the invention will be referenced X i while the comparative additives will be referenced T i .
- a first additive T 1 is the product of the reaction of oleic acid with diethanolamine. This reaction is carried out in a 500 ml tetracol flask into which 84.6 g of oleic acid and 105.3 g of xylene and then 31.5 g of diethanolamine are first introduced over a period of 10 minutes. The whole is then maintained under reflux of xylene for 6 hours to remove 6.4 ml of water. The final product obtained contains 50% of active ingredient, of yellow-orange color.
- the infrared spectroscopic analysis shows absorption bands at 3500 cm -1 at 1730 cm -1 and 1650 cm -1, corresponding to the hydroxyl, ester and amide functions, respectively.
- the second additive T 2 is the product of the reaction of a tall oil acid and diethanol amine.
- the tall oil acid used is a combination of 70% of a mixture of fatty acids (55% oleic acid, 38% linoleic acid, 5% palmitic acid and 2% linolenic acid) and 30% % of resin acids, having an acid value of 185 mg KOH per gram.
- the procedure is as for T 1 by introducing 80 g of tall oil acid, 28.2 g of diethanolamine and 98.6 g of xylene successively into the flask and maintaining a reflux of xylene for 6 hours.
- the final reaction product is a yellow-orange, clear and viscous liquid having a residual acid number of 0.21 mg KOH per gram.
- the third additive T 3 is a mixture of alkyl esters, mono, di and trialkyl esters, glycerol mainly comprising glycerol monooleate.
- the first additive according to the invention X 1 is a physical mixture of 2 g of the additive T 2 and 1 g of the additive T 3 .
- the second additive according to the invention X 2 is a physical mixture of 2 g of the additive T 1 and 1 g of the additive T 3 .
- the additive T 4 is the glycerol trioleate sold by the company FLUKA.
- the third additive according to the invention X 3 is the product of the reaction of glycerol trioleate T 4 with diethanolamine. Operation in a tetracol flask as for T 1 by mixing 80 g of glycerol trioleate and 18.5 g of diethanolamine, and then heating the whole at 150 ° C for 4 hours.
- the additive T 5 is a soybean triglyceride oil with an average molecular weight of about 870, composed of 28% oleic acid, 50% linoleic acid, 8% linolenic acid, 3% stearic acid, 10% palmitic acid and 1% arachidic acid.
- the fourth additive according to the invention X 4 is the product of the reaction of 87 g of T 4 with 21 g of diethanolamine, the mixture being stirred at 150 ° C. for 6 hours.
- the additive X 4 is a fluid, yellow-orange liquid, having infrared spectroscopy absorption bands characteristic of alcohol, ester and amide functions.
- the fifth additive according to the invention, X 5 is obtained under the same conditions as the additive X 4 , but using 87 g of T 4 and 15.75 g of diethanolamine.
- the sixth additive according to the invention X 6 is obtained under the same conditions as the additive X 4 but using 27 g of the additive T 5 and 26 g of diethanolamine.
- the seventh additive according to the invention, X 7 is obtained under the same conditions as the additive X 4 but replacing the diethanolamine with 24 g of tris (hydroxymethyl) aminomethane.
- the eighth additive according to the invention X 8 is obtained under the same conditions as the additive X 4 , but using as triglyceride castor oil, with an average molecular weight of about 927, composed of 87% of ricinoleic acid, 7% oleic acid and 3% stearic acid.
- the gas oils A, B and C thus additivated were subjected to the HFRR test, which consists of imposing, together with a steel ball in contact with a stationary metal plate, a pressure corresponding to a weight of 200 g and an alternating displacement of 1 mm. at a frequency of 50Hz.
- the ball in motion is lubricated by the test composition.
- the temperature is maintained at 60 ° C throughout the duration of the test, ie 75mn.
- the lubricating power is expressed by the average value of the diameters of the wear impression of the ball on the plate.
- a small wear diameter indicates good lubricity; conversely, a large wear diameter reflects a power all the more insufficient that the wear diameter is high.
- X 1 and X 2 have lower wear characteristics, which are therefore much better than those of T 1 , T 2 and T 3 , which reflects the synergistic effect of lubricity according to the invention.
- X 3 corresponds to the reaction product obtained according to the process of the invention, diethanolamine on glycerol trioleate. It is noted as before the interest of the additive thus obtained with regard to the wear characteristics obtained by T 4 .
Landscapes
- Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Emergency Medicine (AREA)
- Combustion & Propulsion (AREA)
- Liquid Carbonaceous Fuels (AREA)
- Lubricants (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Solid Fuels And Fuel-Associated Substances (AREA)
Abstract
Description
| Gazole A | Gazole B | Gazole C | |
| Distillation (NFM 07-022) | |||
| Point initial | 183 | 165 | 168,5 |
| Point à 10% volume | 227 | 208,5 | 208 |
| 20% volume | 247 | 227,5 | 226 |
| 50% volume | 290 | 276 | 274,5 |
| 80% volume | 334 | 317,5 | 317 |
| 90% volume | 354 | 334 | 336 |
| Point final | 373 | 357,5 | 364 |
| Masse volumique à 15 °C (NFT 60-172) | 0,8508 | 0,8360 | 0,8364 |
| Indice de cétane calculé (ASTM D4737) | 51.3 | 50 | 53 |
| % soufre (ppm) | 480 | 270 | 455 |
| Pouvoir lubrifiant HFRR (CEC F06A96) (µm) | 425 | 772 | 550 |
Claims (10)
- Additif d'onctuosite composé de :dans lesquelles R3 et R4 , identiques ou différents, sont choisis parmi les chaínes alkyles linéaires ou faiblement ramifiées, saturées ou insaturées, comprenant de 8 à 24 atomes de carbone, et les groupements cycliques et polycycliques comprenant de 8 à 60 atomes de carbone.de 5 à 25% en poids d'au moins un monoester de glycérol de formules (IA) et/ou (IB) ci-après : avec R1 choisi parmi les chaínes alkyles linéaires ou faiblement ramifiées, saturées ou insaturées, comprenant de 8 à 24 atomes de carbone, et les groupements cycliques et polycycliques comprenant de 8 à 60 atomes de carbone,de 35 à 75 % en poids d'au moins un composé de formule (II) ci-après ; dans laquelle R2 est une chaíne alkyle linéaire ou faiblement ramifiée, saturée ou insaturée, comprenant de 8 à 24 atomes de carbone, et X est choisi parmi (i) les groupements OR0, R0 étant un reste hydrocarboné comprenant de 1 à 8 atomes de carbone, éventuellement substitué par un ou plusieurs groupements esters, et (ii) les groupements dérivant d'amines primaires et/ou secondaires, d'alcanolamines de chaíne hydrocarbonée aliphatique, linéaire ou ramifiée, comprenant de 1 à 18 atomes de carbone.
- Additif selon la revendication 1 caractérisée en ce que les monoesters de glycérolde formule (I) et les diesters de formule (III) avec, respectivement, R1 ou, R3 et R4 constitués d'une chaine alkyle sont choisis parmi les monoesters et les diesters obtenus à partir des huiles du groupe constitué par les huiles lauriques, issues du coprah ou de palme, riches en chaínes alkyles saturés de 12 à 14 atomes de carbone, les huiles palmitiques issues de palme, de saindoux ou de suif, renfermant une quantité majeure de chaínes alkyles saturées à 16 atomes de carbone, les huiles linoléïques issues du tournesol, du maïs, ou du colza, contenant une forte teneur en acide linoléïque, les huiles linoléniques du lin comprenant des teneurs notables en chaínes alkyles tri-insaturées de 1 à 18 atomes de carbone, et les huiles ricinoléÏques issues du ricin.
- Additif selon l'une des revendications 1 et 2 caractérisée en ce que les monoesters de glycérol de formule (I) et les diesters de glycérol de formule (III) comprennent un R1 ou, R3 et/ou R4 constitués d'au moins deux cycles formés chacun de 5 à 6 atomes dont l'un au plus est éventuellement un hétéroatome tel que l'azote ou l'oxygène et les autres sont des atomes de carbone, ces deux cycles ayant en outre deux atomes de carbone en commun, de préférence vicinaux, ces dits cycles étant saturés ou insaturés.
- Additif selon la revendication 3 caractérisée en ce que les monoesters et les diesters de glycérol de formules (I) et (III) sont obtenus à partir d'acides résiniques naturels contenus dans les résidus de distillation des huiles naturelles extraites des arbres résineux, notamment de conifères résineux.
- Additif selon la revendication 4 caractérisée en ce que les esters d'acides résiniques sont choisis dans le groupe constitué par les esters d'acide abiétique, d'acide dihydroabiétique, d'acide tétrahydroabiétique, d'acide déhydroabiétique, d'acide néoabiétique, d'acide pimarique, d'acide lévopimarique et d'acide parastrinique.
- Additif selon l'une des revendications 1 à 5 caractérisée en ce que les esters et les amides de formule (II) sont obtenus par réaction d'un composé alcool, amine, et /ou alcanolamine sur un acide carboxylique tel que l'acide oléïque ou encore l'oléate de méthyle.
- Additif selon la revendications 6 caractérisée en ce que les alcools sont choisis parmi les alcanols du groupe constitué par le méthanol, l'éthanol, le propanol, l'isopropanol, le butanol, l'isobutanol, le pentanol ou encore l'éthyl 2 hexanol, et/ou les alcools oxyalkylés de formule R(O-CH2-CHR')n-OH dans laquelle R est un groupement alkyle de 1 à 6 atomes de carbone, R' est l'hydrogène ou un groupement alkyle de 1 à 4 atomes de carbone et n un nombre entier variant de 1 à 5 tels que le méthylcellosolve, le butylcellosolve, le butyldiglycol et le 1-butoxy-propanol.
- Additif selon la revendication 6 caractérisée en ce les amines sont des amines primaires et secondaires choisies dans le groupe constitué par la méthylamine, l'éthylamine, la propylamine, la butylamine, l'isobutylamine, l'éthyl-2-hexylamine, la décylamine, la dodécylamine, la stéarylamine et l'oléylamine, la N,N-diéthylamine, la N,N-dipropylamine, la N,N-dibutylamine, la N,N-di(éthyl-2)hexylamine, la N-méthyldécylamine, la N-méthyldodécylamine, la N-méthyloléylamine.
- Additif selon la revendication 6 caractérisée en ce que les alcanolamines sont choisies parmi les amines comprenant de 1 à 18 atomes de carbones substituées par au moins un groupement hydroxylé, -hydroxyméthylé, hydroxyéthylé ou hydroxypropylé telles que l'éthanolamine, la diéthanolamine, la triéthanolamine, l'isopropanolamine, la diiosopropanolamine, la triisopropanolamine, la N-méthyléthanolamine, le tris-(hydroxyméthyl)-aminométhane, la (N-hydroxyéthyl)-méthylimidazoline, la (N-hydroxyéthyl)-heptadécénylimidazoline.
- Additif selon l'une quelconque des revendications 1 à 9, en mélange avec un additif pour améliorer la qualité du carburant, choisi parmi les additifs détergents, dispersants, anti-oxydant et antimousse.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR9716538A FR2772783A1 (fr) | 1997-12-24 | 1997-12-24 | Additif d'onctuosite pour carburant |
| FR9716538 | 1997-12-24 | ||
| FR9803225A FR2772784B1 (fr) | 1997-12-24 | 1998-03-17 | Additif d'onctuosite pour carburant |
| FR9803225 | 1998-03-17 | ||
| EP98963589A EP0961820B1 (fr) | 1997-12-24 | 1998-12-22 | Additif d'onctuosite pour carburant |
Related Parent Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP98963589.1 Division | 1998-12-22 | ||
| EP98963589A Division EP0961820B1 (fr) | 1997-12-24 | 1998-12-22 | Additif d'onctuosite pour carburant |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP1522570A2 true EP1522570A2 (fr) | 2005-04-13 |
| EP1522570A3 EP1522570A3 (fr) | 2005-11-30 |
Family
ID=26234024
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP98963589A Revoked EP0961820B1 (fr) | 1997-12-24 | 1998-12-22 | Additif d'onctuosite pour carburant |
| EP05000389A Withdrawn EP1522570A3 (fr) | 1997-12-24 | 1998-12-22 | Additif d'onctuosite pour carburant |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP98963589A Revoked EP0961820B1 (fr) | 1997-12-24 | 1998-12-22 | Additif d'onctuosite pour carburant |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US6511520B1 (fr) |
| EP (2) | EP0961820B1 (fr) |
| JP (1) | JP3226497B2 (fr) |
| KR (1) | KR100598227B1 (fr) |
| AR (1) | AR014163A1 (fr) |
| AT (1) | ATE290057T1 (fr) |
| BR (1) | BR9807728B1 (fr) |
| CA (1) | CA2281635C (fr) |
| DE (1) | DE69829167T2 (fr) |
| ES (1) | ES2242310T3 (fr) |
| FR (1) | FR2772784B1 (fr) |
| HU (1) | HU222537B1 (fr) |
| ID (1) | ID23178A (fr) |
| MY (1) | MY121333A (fr) |
| NO (1) | NO994055L (fr) |
| PL (1) | PL189103B1 (fr) |
| PT (1) | PT961820E (fr) |
| RU (1) | RU2167919C1 (fr) |
| WO (1) | WO1999033938A1 (fr) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2910477A1 (fr) * | 2006-12-22 | 2008-06-27 | Total France Sa | Fluxant et ses applications. |
Families Citing this family (79)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6224642B1 (en) * | 1999-11-23 | 2001-05-01 | The Lubrizol Corporation | Additive composition |
| EP1272594B2 (fr) * | 2000-03-31 | 2009-11-25 | Texaco Development Corporation | Composition de carburant destinee a ameliorer la distribution de charge modifiant le coefficient de frottement |
| US6524353B2 (en) * | 2000-09-07 | 2003-02-25 | Texaco Development Corporation | Method of enhancing the low temperature solution properties of a gasoline friction modifier |
| DE10058356B4 (de) | 2000-11-24 | 2005-12-15 | Clariant Gmbh | Brennstofföle mit verbesserter Schmierwirkung, enthaltend Umsetzungsprodukte aus Fettsäuren mit kurzkettigen öllöslichen Aminen |
| JP2002309275A (ja) * | 2001-04-13 | 2002-10-23 | Nippon Oil Corp | ガソリンエンジンシステム |
| US7357819B2 (en) * | 2001-05-07 | 2008-04-15 | Victorian Chemicals International Pty Ltd | Fuel blends |
| DE10143021A1 (de) * | 2001-09-01 | 2003-03-20 | Cognis Deutschland Gmbh | Schmierfähigkeitsverbesserer für Dieselöl |
| DE10156024A1 (de) * | 2001-11-15 | 2003-05-28 | Cognis Deutschland Gmbh | Additive für schwefelarme Treibstoffe |
| US6759438B2 (en) | 2002-01-15 | 2004-07-06 | Chevron U.S.A. Inc. | Use of oxygen analysis by GC-AED for control of fischer-tropsch process and product blending |
| US6824574B2 (en) * | 2002-10-09 | 2004-11-30 | Chevron U.S.A. Inc. | Process for improving production of Fischer-Tropsch distillate fuels |
| RU2247090C1 (ru) * | 2003-12-03 | 2005-02-27 | Цельнер Михаил Ефимович | Бетонная смесь, добавка для бетонной смеси "биотех-нм", модифицированный добавкой "биотех-нм" цемент (варианты) |
| AU2005227863A1 (en) * | 2004-02-06 | 2005-10-13 | Jeffrey P. Reistroffer | Linear incendiary strand and method for prescribed fire ignition |
| RU2254358C1 (ru) * | 2004-02-19 | 2005-06-20 | Общество с ограниченной ответственностью "АЛЬКОР 91" | Присадка к углеводородному топливу |
| MY182828A (en) | 2004-09-28 | 2021-02-05 | Malaysian Palm Oil Board Mpob | Fuel lubricity additive |
| DE102006016588A1 (de) * | 2006-04-06 | 2007-10-18 | Rohmax Additives Gmbh | Kraftstoffzusammensetzungen umfassend nachwachsende Rohstoffe |
| US8444720B2 (en) | 2006-09-21 | 2013-05-21 | Afton Chemical Corporation | Alkanolamides and their use as fuel additives |
| US20080141582A1 (en) * | 2006-12-13 | 2008-06-19 | Angela Priscilla Breakspear | Additive Composition |
| US7626063B2 (en) * | 2007-05-11 | 2009-12-01 | Conocophillips Company | Propane utilization in direct hydrotreating of oils and/or fats |
| FR2925909B1 (fr) * | 2007-12-26 | 2010-09-17 | Total France | Additifs bifonctionnels pour hydrocarbures liquides obtenus par greffage a partir de copolymeres d'ethylene et/ou de propylene et d'esters vinyliques |
| FR2925916B1 (fr) * | 2007-12-28 | 2010-11-12 | Total France | Terpolymere ethylene/acetate de vinyle/esters insatures comme additif ameliorant la tenue a froid des hydrocarbures liquides comme les distillats moyens et les carburants ou combustibles |
| CA2770134C (fr) * | 2008-08-05 | 2018-01-16 | Spirit Of The 21St Century Group, Llc | Combustibles modifies renfermant de la triglycerine comportant au moins un groupe hydroxyle et methode de fabrication et utilisation associee |
| FR2940314B1 (fr) | 2008-12-23 | 2011-11-18 | Total Raffinage Marketing | Carburant de type gazole pour moteur diesel a fortes teneurs en carbone d'origine renouvelable et en oxygene |
| FR2943678B1 (fr) | 2009-03-25 | 2011-06-03 | Total Raffinage Marketing | Polymeres (meth)acryliques de bas poids moleculaire, exempts de composes soufres,metalliques et halogenes et de taux de monomeres residuels faible,leur procede de preparation et leurs utilisations |
| FR2947558B1 (fr) | 2009-07-03 | 2011-08-19 | Total Raffinage Marketing | Terpolymere et ethylene/acetate de vinyle/esters insatures comme additif ameliorant la tenue a froid des hydrocarbures liquides comme les distillats moyens et les carburants ou combustibles |
| FR2969620B1 (fr) | 2010-12-23 | 2013-01-11 | Total Raffinage Marketing | Resines alkylphenol-aldehyde modifiees, leur utilisation comme additifs ameliorant les proprietes a froid de carburants et combustibles hydrocarbones liquides |
| KR101084833B1 (ko) | 2011-02-01 | 2011-11-21 | 곽동린 | 내연기관 오일용 수분 제거제 |
| FR2971254B1 (fr) | 2011-02-08 | 2014-05-30 | Total Raffinage Marketing | Compositions liquides pour marquer les carburants et combustibles hydrocarbones liquides, carburants et combustibles les contenant et procede de detection des marqueurs |
| KR101265478B1 (ko) | 2011-08-22 | 2013-05-21 | 한국석유관리원 | 윤활성 향상제 |
| FR2987052B1 (fr) | 2012-02-17 | 2014-09-12 | Total Raffinage Marketing | Additifs ameliorant la resistance a l'usure et au lacquering de carburants de type gazole ou biogazole |
| FR2991992B1 (fr) | 2012-06-19 | 2015-07-03 | Total Raffinage Marketing | Compositions d'additifs et leur utilisation pour ameliorer les proprietes a froid de carburants et combustibles |
| FR2994695B1 (fr) | 2012-08-22 | 2015-10-16 | Total Raffinage Marketing | Additifs ameliorant la resistance a l'usure et au lacquering de carburants de type gazole ou biogazole |
| FR3000101B1 (fr) | 2012-12-21 | 2016-04-01 | Total Raffinage Marketing | Composition gelifiee de carburant ou combustible hydrocarbone et procede de preparation d'une telle composition |
| FR3000102B1 (fr) | 2012-12-21 | 2015-04-10 | Total Raffinage Marketing | Utilisation d'un compose viscosifiant pour ameliorer la stabilite au stockage d'un carburant ou combustible hydrocarbone liquide |
| FR3005061B1 (fr) | 2013-04-25 | 2016-05-06 | Total Raffinage Marketing | Additif pour ameliorer la stabilite a l'oxydation et/ou au stockage de carburants ou combustibles hydrocarbones liquides |
| FR3021663B1 (fr) | 2014-05-28 | 2016-07-01 | Total Marketing Services | Composition gelifiee de carburant ou combustible hydrocarbone liquide et procede de preparation d'une telle composition |
| EP3056527A1 (fr) | 2015-02-11 | 2016-08-17 | Total Marketing Services | Copolymeres a blocs et leur utilisation pour ameliorer les proprietes a froid de carburants ou combustibles |
| EP3056526A1 (fr) | 2015-02-11 | 2016-08-17 | Total Marketing Services | Copolymeres a blocs et leur utilisation pour ameliorer les proprietes a froid de carburants ou combustibles |
| WO2017006141A1 (fr) | 2015-07-06 | 2017-01-12 | Rhodia Poliamida E Especialidades Ltda | Compositions de diesel présentant un indice de cétane et des performances de pouvoir lubrifiant améliorés |
| EP3144059A1 (fr) | 2015-09-16 | 2017-03-22 | Total Marketing Services | Procédé servant à préparer des microcapsules par émulsion double |
| CN105419890B (zh) * | 2015-12-31 | 2017-03-08 | 临沂冠亚商贸有限公司 | 一种燃油添加剂及其制备方法 |
| FR3054240B1 (fr) | 2016-07-21 | 2018-08-17 | Total Marketing Services | Utilisation de copolymeres pour ameliorer les proprietes a froid de carburants ou combustibles |
| FR3054225B1 (fr) | 2016-07-21 | 2019-12-27 | Total Marketing Services | Copolymere utilisable comme additif detergent pour carburant |
| FR3054224B1 (fr) | 2016-07-21 | 2020-01-31 | Total Marketing Services | Copolymere et son utilisation comme additif detergent pour carburant |
| FR3054223A1 (fr) | 2016-07-21 | 2018-01-26 | Total Marketing Services | Copolymere et son utilisation comme additif detergent pour carburant |
| EP3635079B1 (fr) * | 2017-06-02 | 2024-04-17 | Hindustan Petroleum Corporation Limited | Formulation destinée à augmenter le pouvoir lubrifiant de carburants |
| FR3071850B1 (fr) | 2017-10-02 | 2020-06-12 | Total Marketing Services | Composition d’additifs pour carburant |
| FR3072095B1 (fr) | 2017-10-06 | 2020-10-09 | Total Marketing Services | Composition d'additifs pour carburant |
| FR3073522B1 (fr) | 2017-11-10 | 2019-12-13 | Total Marketing Services | Nouveau copolymere et son utilisation comme additif pour carburant |
| FR3074499B1 (fr) | 2017-12-06 | 2020-08-28 | Total Marketing Services | Utilisation d'un copolymere particulier pour prevenir les depots sur les soupapes des moteurs a injection indirecte essence |
| FR3074497B1 (fr) | 2017-12-06 | 2020-09-11 | Total Marketing Services | Composition d’additifs pour carburant |
| FR3074498B1 (fr) | 2017-12-06 | 2020-09-11 | Total Marketing Services | Composition d’additifs pour carburant |
| FR3075813B1 (fr) | 2017-12-21 | 2021-06-18 | Total Marketing Services | Utilisation de polymeres reticules pour ameliorer les proprietes a froid de carburants ou combustibles |
| FR3080382B1 (fr) | 2018-04-23 | 2020-03-27 | Total Marketing Services | Composition de carburant a forte puissance et effet fuel eco |
| FR3081879B1 (fr) | 2018-05-29 | 2020-11-13 | Total Marketing Services | Composition de carburant et procede de fonctionnement d’un moteur a combustion interne |
| FR3083799B1 (fr) | 2018-07-16 | 2021-03-05 | Total Marketing Services | Additifs pour carburant, de type sucre-amide |
| FR3085383B1 (fr) | 2018-08-28 | 2020-07-31 | Total Marketing Services | Composition d'additifs comprenant au moins un copolymere, un additif fluidifiant a froid et un additif anti-sedimentation |
| FR3085384B1 (fr) | 2018-08-28 | 2021-05-28 | Total Marketing Services | Utilisation de copolymeres specifiques pour ameliorer les proprietes a froid de carburants ou combustibles |
| FR3087788B1 (fr) | 2018-10-24 | 2021-06-25 | Total Marketing Services | Association d'additifs pour carburant |
| WO2020109568A1 (fr) | 2018-11-30 | 2020-06-04 | Total Marketing Services | Composé d'amidoamine grasse quaternaire destiné à être utilisé comme additif pour carburant |
| FR3091539B1 (fr) | 2019-01-04 | 2021-10-01 | Total Marketing Services | Utilisation de copolymères spécifiques pour abaisser la température limite de filtrabilité de carburants ou combustibles |
| FR3092334B1 (fr) | 2019-01-31 | 2022-06-17 | Total Marketing Services | Utilisation d’une composition de carburant à base d’hydrocarbures paraffiniques pour nettoyer les parties internes des moteurs diesels |
| FR3092333B1 (fr) | 2019-01-31 | 2021-01-08 | Total Marketing Services | Composition de carburant à base d’hydrocarbures paraffiniques |
| FR3101882B1 (fr) | 2019-10-14 | 2022-03-18 | Total Marketing Services | Utilisation de polymères cationiques particuliers comme additifs pour carburants et combustibles |
| FR3103493B1 (fr) | 2019-11-25 | 2021-12-10 | Total Marketing Services | Additif de lubrifiance pour carburant |
| FR3103815B1 (fr) | 2019-11-29 | 2021-12-17 | Total Marketing Services | Utilisation de diols comme additifs de détergence |
| FR3103812B1 (fr) | 2019-11-29 | 2023-04-07 | Total Marketing Services | Utilisation de composés alkyl phénol comme additifs de détergence |
| FR3110913B1 (fr) | 2020-05-29 | 2023-12-22 | Total Marketing Services | Composition d’additifs pour carburant moteur |
| FR3110914B1 (fr) | 2020-05-29 | 2023-12-29 | Total Marketing Services | Utilisation d’une composition de carburant pour nettoyer les parties internes des moteurs essence |
| FR3113063B1 (fr) | 2020-07-31 | 2022-08-12 | Total Marketing Services | Utilisation de copolymères à distribution de masse molaire spécifique pour abaisser la température limite de filtrabilité de carburants ou de combustibles |
| FR3122435B1 (fr) | 2021-04-30 | 2023-05-12 | Total Marketing Services | Composition de carburant riche en composés aromatiques et en composés oxygénés |
| FR3122434B1 (fr) | 2021-04-30 | 2024-06-14 | Total Marketing Services | Composition de carburant riche en composés aromatiques, en paraffines et en éthanol, et son utilisation notamment dans des véhicules de compétition |
| FR3119625B1 (fr) | 2021-07-02 | 2023-02-17 | Totalenergies Marketing Services | Composition de carburant riche en composés aromatiques, en paraffines et en éther, et son utilisation dans des véhicules automobiles |
| FR3125298B1 (fr) | 2021-07-19 | 2025-10-17 | Totalenergies Marketing Services | Utilisation d’une composition d’additifs pour réduire les émissions des véhicules Diesel |
| FR3135463B1 (fr) | 2022-05-12 | 2024-05-17 | Totalenergies Onetech | Composition de carburant à faible impact en émissions de CO2, et son utilisation notamment dans des véhicules neufs |
| FR3137103B1 (fr) | 2022-06-23 | 2026-02-20 | Totalenergies Onetech | Composition de carburant à faible impact en émissions de CO2, et son utilisation notamment dans des véhicules neufs |
| FR3143624A1 (fr) | 2022-12-19 | 2024-06-21 | Totalenergies Onetech | Composition de carburant comprenant une base renouvelable, un ester d’acide gras et un additif alkyle-phénol |
| FR3144623A1 (fr) | 2022-12-30 | 2024-07-05 | Totalenergies Onetech | Composition d’additifs pour carburant comprenant au moins une arylamine secondaire et au moins un nitroxyde |
| FR3146480A1 (fr) | 2023-03-08 | 2024-09-13 | Totalenergies Onetech | Additifs pour carburants et carburants comprenant ledit additif |
| FR3151857A1 (fr) | 2023-08-01 | 2025-02-07 | Totalenergies Onetech | Composition d’additifs a base d’huiles lubrifiantes au moins en partie re-raffinees |
Family Cites Families (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2206168A (en) * | 1932-08-22 | 1940-07-02 | Procter & Gamble | Process for manufacturing fatty esters |
| US2345632A (en) * | 1939-05-20 | 1944-04-04 | Nat Oil Prod Co | Polyamides |
| US2363778A (en) * | 1942-12-01 | 1944-11-28 | Du Pont | Stabilization of organic substances |
| US2527889A (en) * | 1946-08-19 | 1950-10-31 | Union Oil Co | Diesel engine fuel |
| US3133104A (en) * | 1962-06-08 | 1964-05-12 | Ethyl Corp | Stable lead alkyl compositions and a method for preparing the same |
| US3969233A (en) * | 1971-10-12 | 1976-07-13 | Lucas William J | Biodegradable internal combustion engine lubricants and motor fuel compositions |
| US4344771A (en) * | 1978-08-23 | 1982-08-17 | Phillips Petroleum Company | Fuel and lubricant additives from acid treated mixtures of vegetable oil derived amides and esters |
| US4204481A (en) * | 1979-02-02 | 1980-05-27 | Ethyl Corporation | Anti-wear additives in diesel fuels |
| US4208190A (en) * | 1979-02-09 | 1980-06-17 | Ethyl Corporation | Diesel fuels having anti-wear properties |
| US4308200A (en) * | 1980-07-10 | 1981-12-29 | Champion International Corporation | Extraction of coniferous woods with fluid carbon dioxide and other supercritical fluids |
| US4515740A (en) * | 1980-10-16 | 1985-05-07 | Phillips Petroleum Company | Method of forming solid form fuel additives |
| US4617026A (en) * | 1983-03-28 | 1986-10-14 | Exxon Research And Engineering Company | Method for improving the fuel economy of an internal combustion engine using fuel having hydroxyl-containing ester additive |
| US4504280A (en) * | 1983-08-17 | 1985-03-12 | Phillips Petroleum Company | Fuel additives from SO2 treated mixtures of amides and esters derived from vegetable oil, tall oil acid, or aralkyl acid |
| US4609376A (en) * | 1985-03-29 | 1986-09-02 | Exxon Research And Engineering Co. | Anti-wear additives in alkanol fuels |
| CA1237282A (fr) * | 1985-04-12 | 1988-05-31 | Canadian Patents And Development Limited/Societe Canadienne Des Brevets Et D'exploitation Limitee | Preparation de melange combustible a base de tall oil |
| GB8510719D0 (en) * | 1985-04-26 | 1985-06-05 | Exxon Chemical Patents Inc | Fuel compositions |
| US4729769A (en) * | 1986-05-08 | 1988-03-08 | Texaco Inc. | Gasoline compositions containing reaction products of fatty acid esters and amines as carburetor detergents |
| US4919683A (en) * | 1988-12-22 | 1990-04-24 | Texaco Inc. | Stable middle distillate fuel-oil compositions |
| JPH0665528A (ja) * | 1992-08-19 | 1994-03-08 | Ohtsu Tire & Rubber Co Ltd :The | 木材用精油入り塗料 |
| US5522906A (en) * | 1993-04-22 | 1996-06-04 | Kao Corporation | Gasoline composition |
| GB9315205D0 (en) * | 1993-07-22 | 1993-09-08 | Exxon Chemical Patents Inc | Additives and fuel compositions |
| CA2149685C (fr) * | 1994-06-30 | 1999-09-14 | Jacques Monnier | Conversion en additif pour carburant diesel de tallol dont on a extrait le brai |
| US5454842A (en) * | 1994-12-02 | 1995-10-03 | Exxon Research & Engineering Co. | Cetane improver compositions comprising nitrated fatty acid derivatives |
| GB9514480D0 (en) * | 1995-07-14 | 1995-09-13 | Exxon Chemical Patents Inc | Additives and fuel oil compositions |
| KR100403664B1 (ko) * | 1994-12-13 | 2004-02-11 | 엑손 케미칼 패턴츠 인코포레이티드 | 연료유조성물 |
| GB9502041D0 (en) * | 1995-02-02 | 1995-03-22 | Exxon Chemical Patents Inc | Additives and fuel oil compositions |
| JP3379866B2 (ja) * | 1995-04-24 | 2003-02-24 | 花王株式会社 | 軽油添加剤および軽油組成物 |
| US5578090A (en) * | 1995-06-07 | 1996-11-26 | Bri | Biodiesel fuel |
| GB2307246B (en) * | 1995-11-13 | 2000-04-12 | Ethyl Petroleum Additives Ltd | Fuel additive |
| GB2307247B (en) * | 1995-11-13 | 1999-12-29 | Ethyl Petroleum Additives Ltd | Fuel additive |
| DE19614722A1 (de) * | 1996-04-15 | 1997-10-16 | Henkel Kgaa | Kältestabiles Schmier- und Kraftstoffadditiv |
| FR2752850A1 (fr) * | 1996-08-27 | 1998-03-06 | Inst Francais Du Petrole | Compositions d'additifs ameliorant le pouvoir lubrifiant des carburants et carburants les contenant |
-
1998
- 1998-03-17 FR FR9803225A patent/FR2772784B1/fr not_active Expired - Fee Related
- 1998-07-16 JP JP20235798A patent/JP3226497B2/ja not_active Expired - Fee Related
- 1998-12-22 AT AT98963589T patent/ATE290057T1/de active
- 1998-12-22 PT PT98963589T patent/PT961820E/pt unknown
- 1998-12-22 KR KR1019997007492A patent/KR100598227B1/ko not_active Expired - Fee Related
- 1998-12-22 CA CA002281635A patent/CA2281635C/fr not_active Expired - Fee Related
- 1998-12-22 ES ES98963589T patent/ES2242310T3/es not_active Expired - Lifetime
- 1998-12-22 BR BRPI9807728-7A patent/BR9807728B1/pt not_active IP Right Cessation
- 1998-12-22 EP EP98963589A patent/EP0961820B1/fr not_active Revoked
- 1998-12-22 PL PL98335330A patent/PL189103B1/pl not_active IP Right Cessation
- 1998-12-22 HU HU0001251A patent/HU222537B1/hu not_active IP Right Cessation
- 1998-12-22 RU RU99120297/04A patent/RU2167919C1/ru not_active IP Right Cessation
- 1998-12-22 WO PCT/FR1998/002823 patent/WO1999033938A1/fr not_active Ceased
- 1998-12-22 DE DE69829167T patent/DE69829167T2/de not_active Expired - Lifetime
- 1998-12-22 ID IDW990919A patent/ID23178A/id unknown
- 1998-12-22 EP EP05000389A patent/EP1522570A3/fr not_active Withdrawn
- 1998-12-22 US US09/355,992 patent/US6511520B1/en not_active Expired - Fee Related
- 1998-12-23 MY MYPI98005849A patent/MY121333A/en unknown
- 1998-12-23 AR ARP980106647A patent/AR014163A1/es active IP Right Grant
-
1999
- 1999-08-23 NO NO19994055A patent/NO994055L/no not_active Application Discontinuation
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2910477A1 (fr) * | 2006-12-22 | 2008-06-27 | Total France Sa | Fluxant et ses applications. |
| WO2008077888A1 (fr) * | 2006-12-22 | 2008-07-03 | Total Raffinage Marketing | Fluxant et ses applications |
Also Published As
| Publication number | Publication date |
|---|---|
| EP0961820A1 (fr) | 1999-12-08 |
| EP1522570A3 (fr) | 2005-11-30 |
| ATE290057T1 (de) | 2005-03-15 |
| HUP0001251A2 (hu) | 2000-08-28 |
| NO994055D0 (no) | 1999-08-23 |
| DE69829167T2 (de) | 2006-04-13 |
| CA2281635A1 (fr) | 1999-07-08 |
| HUP0001251A3 (en) | 2001-02-28 |
| PL189103B1 (pl) | 2005-06-30 |
| JP3226497B2 (ja) | 2001-11-05 |
| BR9807728B1 (pt) | 2010-05-18 |
| JPH11209766A (ja) | 1999-08-03 |
| DE69829167D1 (de) | 2005-04-07 |
| US6511520B1 (en) | 2003-01-28 |
| NO994055L (no) | 1999-10-20 |
| FR2772784B1 (fr) | 2004-09-10 |
| MY121333A (en) | 2006-01-28 |
| HU222537B1 (hu) | 2003-08-28 |
| RU2167919C1 (ru) | 2001-05-27 |
| CA2281635C (fr) | 2009-02-17 |
| AR014163A1 (es) | 2001-02-07 |
| PL335330A1 (en) | 2000-04-25 |
| PT961820E (pt) | 2005-07-29 |
| WO1999033938A1 (fr) | 1999-07-08 |
| KR100598227B1 (ko) | 2006-07-07 |
| ES2242310T3 (es) | 2005-11-01 |
| BR9807728A (pt) | 2000-02-15 |
| ID23178A (id) | 2000-03-23 |
| EP0961820B1 (fr) | 2005-03-02 |
| FR2772784A1 (fr) | 1999-06-25 |
| KR20000071202A (ko) | 2000-11-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0961820B1 (fr) | Additif d'onctuosite pour carburant | |
| EP1310547B1 (fr) | Carburant pour moteurs diesel a faible teneur en soufre | |
| FR2772783A1 (fr) | Additif d'onctuosite pour carburant | |
| EP2231728B1 (fr) | Utilisation de copolymères d'éthylène et/ou de propylène et d'esters vinyliques modifiés par greffage comme additifs bifonctionnels de lubrifiance et de tenue à froid pour hydrocarbures liquides | |
| AU673607B2 (en) | Gas oil composition | |
| JP5727554B2 (ja) | 炭化水素混合物用潤滑剤組成物及びその製品 | |
| FR2994695A1 (fr) | Additifs ameliorant la resistance a l'usure et au lacquering de carburants de type gazole ou biogazole | |
| EP2697344A1 (fr) | Lubrifiant cylindre pour moteur marin deux temps | |
| EP2814917A1 (fr) | Additifs ameliorant la resistance a l'usure et au lacquering de carburants de type gazole ou biogazole | |
| WO2001038463A1 (fr) | Utilisation de sels d'acide gras d'oligoamines alcoxylees comme agents ameliorants du pouvoir lubrifiant de produits petroliers | |
| CA2527324A1 (fr) | Combustible emulsionne eau / hydrocarbures, sa preparation et ses utilisations | |
| FR2752850A1 (fr) | Compositions d'additifs ameliorant le pouvoir lubrifiant des carburants et carburants les contenant | |
| US20080098642A1 (en) | Lubricity Improving Additive Composition for Low Sulfur Diesel Fuel | |
| KR100501609B1 (ko) | 연료유 조성물용 윤활 첨가제 | |
| EP4065670A1 (fr) | Additif de lubrifiance pour carburant | |
| EP3918040A1 (fr) | Utilisation d'une composition de carburant à base d'hydrocarbures paraffiniques pour nettoyer les parties internes des moteurs diesels | |
| EP4065671B1 (fr) | Utilisation de composés alkyl phénol comme additifs de détergence pour essences | |
| EP4065672B1 (fr) | Utilisation de diols comme additifs de détergence | |
| FR3055135A1 (fr) | Procede de fabrication d'un additif de lubrifiance pour carburant a faible teneur en soufre. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AC | Divisional application: reference to earlier application |
Ref document number: 0961820 Country of ref document: EP Kind code of ref document: P |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI NL PT SE |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI NL PT SE |
|
| RIC1 | Information provided on ipc code assigned before grant |
Ipc: 7C 07C 231/02 A Ipc: 7C 10L 1/14 B Ipc: 7C 10L 1/22 B Ipc: 7C 10L 10/04 B Ipc: 7C 10M 105/56 B Ipc: 7C 10M 111/02 B Ipc: 7C 07C 213/06 B Ipc: 7C 10L 1/18 B Ipc: 7C 07C 67/03 B Ipc: 7C 10M 105/32 B Ipc: 7C 08K 5/00 B |
|
| 17P | Request for examination filed |
Effective date: 20060415 |
|
| AKX | Designation fees paid |
Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI NL PT SE |
|
| 17Q | First examination report despatched |
Effective date: 20071120 |
|
| RAP1 | Party data changed (applicant data changed or rights of an application transferred) |
Owner name: TOTAL RAFFINAGE MARKETING |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION IS DEEMED TO BE WITHDRAWN |
|
| 18D | Application deemed to be withdrawn |
Effective date: 20120703 |