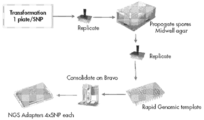
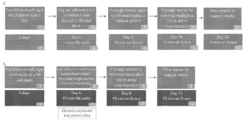
본 발명은 자동화된 고 처리량 플랫폼에서 사상균류를 유전적으로 조작하는 데 고유의 많은 과제를 극복한다. 본 발명에 제공된 방법은 형질전환체의 자동화 된 스크리닝과 함께 자동화된 공동-형질전환을 사용하여 유전자 변화를 혼입함으로써 균류 생산 균주를 생성하도록 디자인되어, 성적 교차를 거치지 않고 두 균주 사이에 유전자 특성을 교환할 수 있다. 본 발명은 또한 다수의 원형질체를 생성하기 위한 절차 및 추후 사용을 위해 이들을 저장하는 수단을 포함한다. 쉽게 구입 가능한 적격 세포의 대량 배치는 자동화를 크게 촉진할 수 있다.
다음의 용어는 당해 기술 분야에서 통상의 지식을 가진 자에 의해 잘 이해되는 것으로 생각되지만, 다음 정의는 본 발명에 개시된 주제의 설명을 용이하게 하기 위해 제시된다.
용어 하나("a" 또는 "an")는 그 실체 중 하나 이상을 의미하며, 즉 복수의 지시대상을 의미할 수 있다. 이와 같이, 용어 "하나", "하나 이상" 및 "적어도 하나"라는 본 발명에서 상호 교환적으로 사용된다. 또한, 부정관사에 의한 "한 요소"에 대한 언급은, 내용이 분명하게는 요소의 하나 및 단지 하나가 존재하는 것을 요구하지 않는 한, 하나 이상의 요소가 존재하는 가능성을 배제하지 않는다.
본 발명에 사용된 용어 "세포 생물", "미세유기체" 또는 "미생물"은 광범위하게 이해되어야 한다. 이 용어들은 상호 교환적으로 사용되며, 두 원핵생물 영역인 박테리아와 고세균뿐만 아니라 특정 진핵생물 균류(예를 들어, 본 발명에 기술된 사상균류) 및 원생 생물을 포함하나 이에 제한되지 않는다. 일부 실시태양에서, 본 발명은 본 발명에 제공된 목록/표 및 도면의 "미세유기체" 또는 "세포유기체" 또는 "미생물"을 의미한다. 이런 특성화는 표와 도면의 확인된 분류학적 속과 확인된 분류학적 종뿐만 아니라 상기 표 또는 도면의 임의의 유기체의 다양한 신규하고 새로운 확인된 또는 디자인된 균주를 의미할 수 있다. 동일한 특성화는 실시예에서와 같이, 명세서의 다른 부분에서 이런 용어의 인용에 대해서도 마찬가지이다.
본 발명에 사용된 용어 "다핵체" 또는 "다핵체 유기체"는 다핵 세포 또는 다핵 세포를 포함하는 유기체를 의미할 수 있다. 다핵 세포는 세포 응집에 이어 덩어리 내부의 세포막의 용해로부터 생성되는 대핵세포질체와 반대로, 세포질 분열을 수반하지 않는 다수의 핵분열에서 초래될 수 있다. 본 발명에 제공된 방법, 조성물 및 시스템과 관련된 다핵체 유기체의 예는 원생 생물(예를 들어, 조류, 원생 동물, 변형균강(끈적균류), 폐포, 식물, 균류 (예를 들어, 사상균류) 및/또는 후생 동물(예를 들어, 초파리류(Drosphila spp)를 포함할 수 있다.
용어 "원핵 생물"은 당업계에 공지되어 있으며 핵 또는 다른 세포 기관을 함유하지 않는 세포를 의미한다. 원핵생물은 일반적으로 두 영역, 박테리아와 고세균의 하나로 분류된다. 고세균과 박테리아 영역의 유기체 사이의 명확한 차이는 16S 리보솜 RNA에서 뉴클레오타이드 염기 서열의 근본적인 차이에 기초한다.
용어 "고세균는 전형적으로 특이한 환경에서 발견되고 세포벽에서 리보솜 단백질의 수 및 뮤라민산의 부족을 포함하는 몇몇 기준에 의해 나머지 원핵 생물과 구별되는 멘도시쿠테스(Mendosicutes) 문의 유기체의 범주를 의미한다. ssrRNA 분석에 기초하여, 고세균은 두 계통발생학적으로 다른 그룹으로 구성된다: 크렌고세균(Crenarchaeota) 및 유리고세균(Euryarchaeota). 생리학을 기초로, 고세균은 세 가지 유형으로 구성될 수 있다: 메테인 생성균(methanogens)(메테인을 생성하는 원핵 생물); 고염성 세균(extreme halophiles)(매우 높은 농도의 염(NaCl)에서 사는 원핵 생물; 및 고온성(초고온성) 세균(extreme(hyper) thermophilus)(초고온에서 사는 원핵 생물). 박테리아와 구별되는 통일된 고세균의 특징(즉, 세포벽, 에스터-연결 막 지질 등에 뮤레인 없음)이외에, 이런 원핵 생물은 이들의 특정한 서식 환경에 적응시키는 특이한 구조 또는 생화학적 특성을 나타낸다. 크렌고세균은 주로 초고온성 황 의존성 원핵 생물로 이루어지며 유리고세균은 메테인 생성균과 고염성 세균을 함유한다.
"박테리아" 또는 "진정세균(eubacteria)"는 원핵 생물의 영역을 의미한다. 박테리아는 다음과 같이 적어도 11개의 구별된 그룹을 포함한다: (1) 그람 양성 (그람+) 박테리아, 2개위 주요 세부구분이 존재한다: (1) 높은 G+C 그룹(액티노마이세테스, 마이코박테리아, 마이르코콕커스, 기타) (2) 낮은 G+C 그룹(바실러스, 클로스트리디아, 락토바실러스, 스타필로콕키, 스트렙토콕키, 마이코플라스마스); (2) 프로테오박테리아, 예를 들어, 보라색 광합성 + 비 광합성 그람 음성 박테리아 (대부분의 "일반적인" 그람 음성 박테리아 포함); (3) 사이아노박테리아, 예를 들면, 산소성 광영양생물; (4) 스피로체테스 및 관련 종; (5) 플랭크토마이세스; (6) 박테로이데스, 플라보박테리아; (7) 클라마이디아; (8) 녹색 황 박테리아; (9) 녹색 비 황 박테리아(또한 혐기성 광영양식물); (10) 방사성 저항성 마이크로콕키 및 동족; (11) 써모토가(Thermotoga) 및 써모시포 써모필레스(Thermosipho thermophiles).
"진핵 생물"은 세포가 막 내에 둘러싸인 핵 및 다른 소기관을 함유하는 임의의 유기체이다. 진핵 생물은 분류군(Eukarya 또는 Eukaryota)에 속한다. 진핵 생물 세포를 원핵 생물(박테리아와 고세균)와 구분시키는 정의하는 특징은 막으로 둘러싸인 유전자 물질, 특히 유전자 물질을 함유하고 핵막에 의해 둘러싸인 핵을 가진다는 것이다.
용어 "유전자 변형된 숙주 세포", "재조합 숙주 세포" 및 및 "재조합 균주"는 본 발명에서 상호 교환적으로 사용되고 본 발명의 클로닝 및 형질전환 방법에 의해 유전자 변형된 숙주 세포를 의미한다. 따라서, 이 용어는 유전자 변경, 변형 또는 조작되어, 숙주 세포가 유도된 자연 발생 유기체와 비교하여 변경, 변형 또는 상이한 유전자형 및/또는 표현형을 나타내는(예를 들어, 유전자 변형이 미생물의 핵산 서열 암호화에 영향을 미칠 때) 숙주 세포(예를 들어, 박테리아, 효모 세포, 곰팡이 세포, CHO, 인간 세포 등)를 포함한다. 일부 실시태양에서, 이 용어는 문제의 특정 재조합 숙주 세포뿐만 아니라 이런 숙주 세포의 자손 또는 잠재적 자손을 의미하는 것으로 이해된다.
용어 "야생형 미생물" 또는 "야생형 숙주 세포"는 자연에서 발생하는 세포, 즉 유전자 변형되지 않은 세포를 기술한다.
"부모 균주(parent strain)" 또는 "부모 균주(parental strain)" 또는 "부모"라는 용어는 돌연변이 균주가 유래된 숙주 세포를 의미할 수 있다. 따라서, "부모 균주" 또는 "부모 균주"는 게놈이 당업계에 공지된 임의의 방식에 의해 교란되고/되거나 본 발명에 제공되어 하나 이상의 돌연변이 균주를 생성하는 숙주 세포 또는 세포이다. "부모 균주" 또는 "부모 균주"는 야생형 균주의 게놈과 동일한 게놈을 갖거나 갖지 않을 수 있다.
용어 "유전자 조작된"은 (예를 들어, 삽입, 결실, 돌연변이 또는 핵산의 대체에 의한) 숙주 세포의 게놈의 임의적 조작을 의미할 수 있다.
용어 "대조군" 또는 "대조군 숙주 세포"는 유전자 변형 또는 실험적 치료의 효과를 측정하기 위한 적절한 비교기 숙주 세포를 의미한다. 일부 실시태양에서, 대조군 숙주 세포는 야생형 세포이다. 다른 실시태양에서, 대조군 숙주 세포는 치료 숙주 세포를 분화시키는 유전자 변형(들)을 제외하고, 유전자 변형된 숙주 세포와 유전적으로 동일하다. 일부 실시태양에서, 본 발명은 대조군 숙주 세포(예를 들어, 균주 개량 프로그램의 기초로 사용된 S1 균주)로서의 부모 균주의 사용을 교시한다. 다른 실시태양에서, 숙주 세포는 치료 숙주 세포에서 테스트되는 특정 프로모터 또는 SNP가 결여된 유전적으로 동일한 세포일 수 있다.
본 발명에 사용된 용어 "대립 유전자(들)"은 유전자의 하나 이상의 대안 형태의 임의의 것을 의미하며, 이의 모두 대립 유전자는 적어도 하나의 형질 또는 특성과 관련된다. 이배체 세포에서, 소정의 유전자의 두 대립 유전자는 한 쌍의 상동 염색체 상에 상응하는 유전자좌를 차지한다. 본 발명의 실시태양에서, 본 발명은 QTL, 즉 하나 이상의 유전자 또는 조절 서열을 포함할 수 있는 게놈 영역에 관한 것이기 때문에, 일부 경우에 대신 "합체형"(즉, 염색체 분절의 대립 유전자)을 의미하는 것이 더 정확하다. 그러나, 이러한 경우에 "대립 유전자"라는 용어는 "합체형"이라는 용어를 포함하는 것으로 이해되어야 한다.
본 발명에 사용된 용어 "유전자좌"(복수 유전자좌)는 예를 들어 유전자 또는 유전자 마커가 발견되는 염색체 상의 특정 장소 또는 장소들 또는 위치를 의미한다.
본 발명에 사용된 용어 "유전적으로 연결된"은 교차를 통해 분리하기가 어려워 번식 동안 높은 비율로 공동유전되는 2개 이상의 형질을 의미한다.
본 발명에 사용된 바와 같이 "재조합" 또는 "재조합 사건"은 염색체 교차 또는 독립된 분류를 의미한다. 용어 "재조합"은 재조합 사건의 결과로 발생하는 새로운 유전자 구성을 갖는 유기체를 의미한다.
본 발명에 사용된 바와 같이 용어 "표현형"은 개체의 유전적 구성(즉, 유전자형)과 환경 사이의 상호작용으로부터 기인하는 개별 세포, 세포 배양, 유기체 또는 유기체의 그룹의 관찰 가능한 특성을 의미한다.
본 발명에 사용된 바와 같이, 핵산 서열 또는 단백질 서열을 기술할 때 용어 "키메라" 또는 "재조합체"는 적어도 2개의 이종 폴리 뉴클레오타이드 또는 2개의 이종 폴리펩타이드를 단일 거대분자 속에 연결하거나 적어도 하나의 천연 핵산 또는 단백질 서열의 하나 이상의 요소를 재배열하는 핵산 또는 단백질 서열을 의미한다. 예를 들어, 용어 "재조합체"는 예를 들어, 화학적 합성 또는 유전 공학 기술에 의한 핵산의 분리된 단편의 조작에 의해 서열의 두 개의 분리된 단편의 인공적 조합을 의미할 수 있다.
본 발명에 사용된 바와 같이 "합성 뉴클레오타이드 서열" 또는 "합성 폴리뉴클레오타이드 서열"은 자연에서 발생하는 것으로 알려지지 않았거나 자연 발생적이지 않은 뉴클레오타이드 서열이다. 일반적으로, 이런 합성 뉴클레오타이드 서열은 임의의 다른 자연 발생 뉴클레오타이드 서열과 비교할 때 적어도 하나의 뉴클레오타이드 차이를 포함할 것이다.
본 발명에 사용된 용어 "핵산"은 임의의 길이의 중합체 형태의 리보뉴클레오타이드 또는 데옥시리보뉴클레오타이드 또는 이의 유사체를 의미한다. 이 용어는 분자의 1 차 구조를 의미하며, 따라서 이중 나선 및 단일 가닥의 DNA뿐 아니라 이중 및 단일 가닥의 RNA를 포함한다. 또한, 메틸화 및/또는 캡핑된 핵산과 같은 변형된 핵산, 변형된 염기를 함유하는 핵산, 골격 변형 등과 같은 변형 핵산을 포함한다. 용어 "핵산" 및 "뉴클레오타이드 서열"은 상화 교환적으로 사용된다.
본 발명에 사용된 용어 "DNA 스캐폴드" 또는 "핵산 스캐폴드"는 인공적으로 생성된 핵산 스캐폴드 또는 스캐폴드로서 용도가 변경되는 자연 발생 서열을 의미한다. 본 발명의 한 실시태양에서, 핵산 스캐폴드는 합성 데옥시리보핵산 스캐폴드이다. 합성 스캐폴드의 데옥시리보뉴클레오타이드는 퓨린 및 피리미딘 염기 또는 다른 천연, 화학적 또는 생화학적으로 변형된, 비 천연 또는 유도체화된 데옥시리보뉴클레오타이드 염기를 포함할 수 있다. 본 발명에 보다 상세하게 기술된 바와 같이, 본 발명의 핵산 스캐폴드는 생물학적 경로, 즉 생합성 효소에 관여하는 2개 이상의 단백질을 공간적 및 시간적으로 조립하고 고정화시켜 기능성 복합체를 생성하는 데 이용된다. 스캐폴드 상의 각각의 생물학적 경로 단백질의 조립 및 고정은 스캐폴드의 단백질 결합 서열 중 하나, 즉 단백질 도킹 부위와 키메라 생합성 효소의 상응하는 DNA 결합 부분 사이의 결합 상호 작용을 통해 일어난다. 따라서, 핵산 스캐폴드는 하나 이상의 서브 유닛을 포함하고, 각각의 서브 유닛은 둘 이상의 상이한 키메라 생물학적 경로 단백질의 결합을 수용하기 위해 둘 이상의 단백질-결합 서열을 포함한다.
본 발명에 사용된 "DNA 결합 서열" 또는 "DNA 결합 부위"는 본 발명의 키메라 생합성 유전자의 DNA-결합 도메인 부분에 의해 인식되고 결합되는 특이적 핵산 서열을 의미한다. 많은 DNA-결합 단백질 도메인 및 이들의 동족 결합 파트너 인식 부위(즉, 단백질 결합 부위)는 당업계에 잘 알려져 있다. 예를 들어, 다수의 징크 핑거 결합 도메인 및 그의 상응하는 DNA 단백질 결합 표적 부위는 당업계에 공지되어 있으며 본 발명에 사용하기에 적합하다. 다른 DNA 결합 도메인은 류신 지퍼 결합 도메인 및 이의 상응하는 DNA 단백질 결합 부위, 날개 나선 결합 도메인 및 상응하는 DNA 단백질 결합 부위, 날개 나선 턴-나선(hleix-turn-helix) 결합 도메인 및 상응하는 DNA 단백질 결합 부위, HMG-박스 결합 도메인 및 이의 상응하는 DNA 단백질 결합 서열, 나선-루프-나선 결합 도메인 및 이의 상응하는 DNA 단백질 결합 서열, 및 나선-턴-나선 결합 도메인 및 이의 상응하는 DNA 단백질 결합 서열을 를 포함하나 제한되지 않는다. 공지된 DNA 단백질 결합 서열을 갖는 다른 공지된 DNA 결합 도메인은 면역 글로불린 DNA 도메인, B3 DNA 결합 도메인 및 TAL 효과기 DNA 결합 도메인을 포함한다. 본 발명의 핵산 스캐폴드 서브유닛은 상기 언급된 단백질 결합 부위 중 임의의 둘 이상을 포함할 수 있다.
본 발명에 사용된 용어 "유전자"는 생물학적 기능과 관련된 DNA의 임의의 단편을 의미한다. 따라서, 유전자는 암호화 서열 및/또는 그의 발현에 요구되는 조절 서열을 포함하나 이에 제한되지 않는다. 유전자는 또한, 예를 들어, 다른 단백질에 대한 인식 서열을 형성하는 비 발현 DNA 단편을 포함할 수 있다. 유전자는 관심 공급원으로부터의 클로닝 또는 공지되거나 예측된 서열 정보로부터의 합성을 포함하는 다양한 공급원으로부터 얻을 수 있고, 원하는 파라미터를 갖도록 디자인된 서열을 포함할 수 있다.
본 발명에 사용된 용어 "상동 기관(homologous)" 또는 "동족체 (homologue)"또는 "오르쏘로그(ortholog)"는 당업계에 공지되어 있고 공통 조상 또는 가족 구성원을 공유하고 서열 동일성의 정도에 기초하여 결정되는 관련 서열을 의미한다. 용어 "상동성", "상동 기관", "실질적으로 유사" 및 "상응하게 실질적으로"는 본 발명에서 상호 교환적으로 사용된다. 이들은 하나 이상의 뉴클레오타이드 염기의 변화가 유전자 발현을 중재하거나 특정 표현형을 생성시키는 핵산 단편의 능력에 영향을 미치지 않는 핵산 단편을 의미한다. 이런 용어는 또한 초기의 변형되지 않은 단편에 비해 생성된 핵산 단편의 기능적 특성을 실질적으로 변화시키지 않는 하나 이상의 뉴클레오타이드의 결실 또는 삽입과 같은 본 발명의 핵산 단편의 변형을 의미한다. 따라서, 당업자가 알 수 있는 바와 같이, 본 발명은 특정 예시적인 서열 이상을 포함하는 것으로 이해된다. 이런 용어는 한 종, 아종, 품종, 품종 또는 균주에서 발견된 유전자 및 다른 종, 아종, 품종, 품종 또는 균주에서 상응하는 또는 동등한 유전자 사이의 관계를 기술한다. 본 발명을 위해서, 상동성 서열이 비교된다. "상동 서열" 또는 "상동체"또는 "오르쏘로그"는 기능적으로 관련이 있다고 생각되고, 믿거나 알려진다. 기능적 관계는 (a) 서열 동일성 및/또는 (b) 동일하거나 유사한 생물학적 기능을 포함하나 이에 제한되지 않는 다수의 방식 중 임의의 하나로 표시될 수 있다. 바람직하게는, (a) 및 (b) 모두가 표시된다. 상동성은 Current Protocols in Molecular Biology(F.M. Ausubel et al., eds., 1987) Supplement 30, 섹션 7.718, 표 7.71에서 논의된 바와 같은 당해분야에서 용이하게 이용 가능한 소프트웨어 프로그램을 사용하여 결정될 수있다. 일부 정렬 프로그램은 맥벡터(MacVector)(Oxford Molecular Ltd, Oxford, U.K.), ALIGN 플러스(Plus)(Scientific and Educational Software, Pennsylvania) 및 AlignX(Vector NTI, Invitrogen, Carlsbad, CA)이다. 다른 정렬 프로그램은 기본 매개변수를 사용하여 시퀀처(Sequencher)(Gene Codes, Ann Arbor, Michigan)이다.
본 발명에 사용된 용어 "내인성" 또는 "내인성 유전자"는 숙주 세포 게놈 내에서 자연적으로 발견되는 위치에서 자연 발생 유전자를 의미한다. 본 발명과 관련하여, 이종 프로모터를 내인성 유전자에 작동 가능하게 연결시키는 것은 이 유전자가 자연적으로 존재하는 위치에서 기존 유전자 앞에 이종성 프로모터 서열을 유전적으로 삽입하는 것을 의미한다. 본 발명에 기재된 내인성 유전자는 본 발명의 방법 중 어느 하나에 따라 돌연변이된 자연 발생 유전자의 대립 유전자를 포함할 수있다.
본 발명에 사용된 용어 "외인성"는 용어 "이종성(heterologous)"과 상호 교환적으로 사용되고, 자연 공급원 이외의 일부 공급원으로부터 유도하는 물질을 의미한다. 예를 들어, 용어 "외인성 단백질" 또는 "외인성 유전자"는 비 자연 공급원 또는 위치의 단백질 또는 유전자 및 생물학적 시스템에 공급된 단백질 또는 유전자를 의미한다.
본 발명에 사용된 용어 "이종 변형"은 특정 생물학적 시스템에 고유한 공급원 이외의 공급원(예를 들어, 본 발명에 제공된 바와 같은 숙주 세포)으로부터 유래된 변형, 또는 특정 생물학적 시스템에 고유하지만 비 천연 컨텍스트/위치/장소에서 발견된다. 따라서, 변형은 상기 변형이 이미 있거나 도입될 생물학적 시스템(예를 들어, 본 발명에 제공된 바와 같은 숙주 세포, 또는 숙주 세포 내의 비 천연 상황/위치/장소)과 관련하여 비 천연이거나 자연적으로 발생하지 않는다. 따라서 이종 변형은 생물학적 시스템(예를 들어, 본 발명에 제공된 숙주 세포, 또는 숙주 내의 이종 상황/위치/장소)에 인위적으로 도입된 것으로 간주될 수 있다. 변형은 유전자 또는 후성 유전적 변이, 파괴 또는 교란일 수 있다. 유전자 변이, 파괴 또는 교란은, 예를 들어 유전자의 천연 프로모터 및/또는 터미네이터의 상기 숙주에 고유하지 않은 프로모터 및/또는 터미네이터에 의한 대체 또는 비 천연 이종 상황/위치/장소로 이동한 숙주 유기체 내로부터의 프로모터 및/또는 터미네이터일 수 있다. 유전자 변이, 파괴 또는 교란은 천연 또는 자연 발생 유전자를 비 천연 또는 자연 발생 유전자, 예를 들어 선택 가능한 마커 유전자로 대체할 수 있다. 또는, 유전적 변이, 파괴 또는 교란은 천연 또는 자연 발생 유전자를 비 천연 상황/위치/장소에 위치되는 숙주 게놈 내에서 다른 천연 유전자(예를 들어, 프로모터)로 대체 또는 교환할 수 있다. 유전자 변이, 파괴 또는 교란은 천연 또는 자연 발생 유전자를 비 천연 또는 자연 발생 유전자 형태로 대체할 수 있다. 유전자의 비 천연 또는 자연 발생 형태는 특정 숙주 세포에서 자연적으로 발견되지 않는 유전자의 돌연변이 형태 및/또는 이종 프로모터 및/또는 터미네이터에 작동 가능하게 연결된 특정 숙주 세포에서 자연적으로 발견되지 않은 유전자의 돌연변이 형태일 수 있다.
본 발명에 사용된 용어 "뉴클레오타이드 변화"는 당업계에서 잘 알려진 바와 같이, 예를 들어 뉴클레오타이드 치환, 결실 및/또는 삽입을 의미한다. 예를 들어 돌연변이는 침묵 치환, 추가 또는 결실을 생성하나 암호화된 단백질의 특성 또는 활성 또는 단백질이 어떻게 만들어지는지를 변형하지 않는 변경을 함유한다.
본 발명에서 사용된 용어 "단백질 변형"은 당업계에 잘 알려진 바와 같이, 예를 들어 아미노산 치환, 아미노산 변형, 결실 및 또는 삽입을 의미한다.
본 발명에 사용된 용어 핵산 또는 폴리펩타이드의 "적어도 일부" 또는 "단편"은 전장 분자를 포함하는 전장 분자의 이런 서열 또는 임의의 더 큰 단편의 최소 크기 특성을 갖는 부분을 의미한다. 본 발명의 폴리뉴클레오타이드 단편은 유전자 조절 요소의 생물학적 활성 부분을 암호화할 수있다. 유전자 조절 요소의 생물학적 활성 부분은 유전자 조절 요소를 포함하는 본 발명의 폴리뉴클레오타이드 중 하나의 일부를 분리하고 본 발명에 기재된 바와 같은 활성을 평가함으로써 제조될 수 있다. 유사하게, 폴리펩타이드의 일부는 전장 폴리펩타이드까지 이르는 4개 아미노산, 5개 아미노산, 6개 아미노산, 7개 아미노산 등일 수 있다. 사용될 부분의 길이는 특정 용도에 따라 다를 것이다. 하이브리드화 프로브로서 유용한 핵산의 일부는 12개 뉴클레오타이드 정도로 짧을 수 있으며; 일부 실시태양에서, 이것은 20개 뉴클레오타이드이다. 에피토프로서 유용한 폴리펩타이드의 일부는 4개의 아미노산 정도로 짧을 수 있다. 전장 폴리펩타이드의 기능을 수행하는 폴리펩타이드의 일부는 일반적으로 4개 이상의 아미노산보다 길 수 있다.
변이체 폴리뉴클레오타이드는 또한 DNA 셔플링과 같은 돌연변이 및 재조합 절차로부터 유도된 서열을 포함한다. 그러한 DNA 셔플링을위한 전략은 당업계에 공지되어있다. 예를 들어, Stemmer(1994) PNAS 91:10747-10751; Stemmer(1994) Nature 370:389-391; Crameri et al.(1997) Nature Biotech. 15:436-438; Moore et al.(1997) J. Mol. Biol. 272:336-347; Zhang et al.(1997) PNAS 94:4504-4509; Crameri et al.(1998) Nature 391:288-291; 및 미국 특허 제5,605,793호 및 제5,837,458호 참조.
본 발명에 개시된 폴리뉴클레오타이드의 PCR 증폭을 위해, 임의의 관심 유기체로부터 추출된 cDNA 또는 게놈 DNA로부터의 상응하는 DNA 서열을 증폭시키기 위한 PCR 반응에 사용하기 위해 올리고뉴클레오타이드 프라이머가 디자인될 수 있다. PCR 프라이머 및 PCR 클로닝을 디자인하기 위한 방법은 당업계에 일반적으로 공지되어 있으며, Sambrook et al.(2001) Molecular Cloning: A Laboratory Manual (3rd ed., Cold Spring Harbor Laboratory Press, Plainview, New York). See also Innis et al., eds. (1990) PCR Protocols: A Guide to Methods and Applications (Academic Press, New York); Innis and Gelfand, eds. (1995) PCR Strategies (Academic Press, New York); and Innis and Gelfand, eds. (1999) PCR Methods Manual (Academic Press, New York)에 개시된다. PCR의 공지된 방법은 쌍을 이룬 프라이머, 네스티드 프라이머, 단일 특이적 프라이머, 축퇴성 프라이머, 유전자 특이적 프라이머, 벡터 특이적 프라이머, 부분적 불일치 프라이머 등을 사용하는 방법을 포함하나 이에 제한되지 않는다.
본 발명에 사용된 용어 "프라이머"는 DNA 중합효소를 부착시키는 증폭 표적에 대한 어닐링을 행할 수 있어, 프라이머 연장 생성물의 합성이 유도되는 조건하에 놓일 때, 즉, 뉴클레오타이드 및 DNA 중합효소와 같은 중합화제의 존재하에서 및 적절한 온도 및 pH에서 DNA 합성의 개시점으로서 작용하는 올리고뉴클레오타이드를 의미한다. (증폭) 프라이머는 증폭 효율을 최대화하기 위해 바람직하게는 단일 가닥이다. 바람직하게는, 프라이머는 올리고데옥시리보뉴클레오타이드이다. 프라이머는 중합화제의 존재 하에서 증량 생성물의 합성을 시작하기에 충분히 길어야한다. 프라이머의 정확한 길이는 프라이머의 온도 및 조성(A/T 대 G/C 함량)을 포함하는 많은 요소에 따라 달라질 것이다. 한 쌍의 양방향성 프라이머는 PCR 증폭과 같은 DNA 증폭 기술 분야에서 일반적으로 사용되는 것과 같은 하나의 순방향 및 역방향 프라이머로 구성된다.
용어 "엄격성" 또는 "엄격한 혼성화 조건"은 혼성화의 안정성에 영향을 주는 혼성화 조건, 예를 들어 온도, 염 농도, pH, 포름아마이드 농도 등을 의미할 수 있다. 이러한 조건은 특이적 결합을 최대화하고 표적 핵산 서열에 대한 프라이머 또는 프로브의 비특이적 결합을 최소화하기 위해 경험적으로 최적화된다. 사용된 용어는 프로브 또는 프라이머가 다른 서열보다 검출 가능하게 더 큰 정도로 (예를 들어, 배경보다 적어도 2배) 이의 표적 서열에 혼성화될 조건에 대한 언급을 포함한다. 엄격한 조건은 서열 의존성이며 다른 상황에서 상이할 것이다. 긴 서열은 고온에서 특이적으로 혼성화된다. 일반적으로, 엄격한 조건은 정의된 이온 강도 및 pH에서 특정 서열에 대한 열 융점(Tm)보다 약 5℃ 낮은 것으로 선택된다. Tm은 상보적 표적 서열의 50%가 완벽하게 매치된 프로브 또는 프라이머에 혼성화되는 온도(정의된 이온 강도 및 pH 하에서)이다. 전형적으로, 엄격한 조건은 염 농도가 pH 7.0 내지 8.3에서 약 1.0 M Na+ 이온 미만, 전형적으로는 약 0.01 내지 1.0 M Na+ 이온 농도(또는 다른 염)이고 온도는 짧은 프로브 또는 프라이머(예를 들어, 10 내지 50개 뉴클레오타이드)의 경우 적어도 약 30℃이고 긴 프로브 또는 프라이머(예를 들어, 50개 초과 뉴클레오타이드)의 경우 적어도 약 60℃이다. 엄격한 조건은 또한 포름아마이드와 같은 불안정화제의 첨가로 성취될 수 있다. 예시적인 낮은 엄격한 조건 또는 "감소된 엄격한 조건"은 37℃에서 30% 포름아마이드, 1M NaCl, 1% SDS의 완충액에 의한 혼성화 및 40℃에서 2 x SSC의 세척을 포함한다. 예시적인 높은 엄격 조건은 37℃에서 50% 포름아마이드, 1M NaCl, 1% SDS에서 하이브리드화 및 60℃에서 0.1 x SSC 세척을 포함한다. 하이브리드화 절차는 당업계에 주지되어 있으며 예를 들어, Ausubel et al., 1998 and Sambrook et al., 2001에 의해 기술된다. 일부 실시태양에서, 엄격한 조건은 1 mM Na2EDTA, 0.5%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%, 15%, 16%, 17%, 18%, 19% 또는 20%와 같은 45℃의 0.5-20% 황산 도데실 나트륨을 함유하는 0.25 M Na2HPO4 완충액(pH 7.2)에서의 혼성화, 및 뒤이은 55℃ 내지 65℃에서 0.1%(w/v) 황산 도데실 나트륨을 함유하는 5 x SSC 세척이다.
본 발명에 사용된 용어 "프로모터"는 암호화 서열 또는 기능성 RNA의 발현을 제어할 수있는 DNA 서열을 의미한다. 일부 실시태양에서, 프로모터 서열은 근위 및 더 원위 상류 요소로 구성되고, 후자의 요소는 종종 인핸서로 의미된다. 따라서, "인핸서"는 프로모터 활성을 자극할 수 있는 DNA 서열이며, 프로모터의 선천적인 요소 또는 프로모터의 수준 또는 조직 특이성을 향상시키기 위해 삽입된 이종성 요소일 수 있다. 프로모터는 천연 유전자로부터 완전히 유도되거나 자연계에서 발견되는 다른 프로모터로부터 유도된 상이한 요소로 구성되거나 심지어 합성 DNA 단편을 포함할 수 있다. 상이한 프로모터가 상이한 조직 또는 세포 유형, 또는 상이한 발달 단계 또는 상이한 환경 조건에 대한 반응으로 유전자의 발현을 지시할 수 있음은 당업자에게 이해된다. 본 발명에 기술된 방법 및 시스템에 사용하기 위한 프로모터는 상기 프로모터의 제어하에 유전자 또는 유전자의 발현이 특정 작용제의 존재 및/또는 부재에 의해 조절되도록 유도될 수 있다. 유도성 프로모터는 전사 활성이 화학적 또는 물리적 조건, 예를 들어 알코올, 테트라사이클린, 스테로이드, 금속 또는 당업계에 공지된 다른 화합물의 존재 또는 부재 또는 빛 또는 저온 또는 고온의 존재 또는 부재에 의해 조절되는 임의의 프로모터일 수 있다. 또한, 대부분의 경우에, 조절 서열의 정확한 경계가 완전히 정의되지 않았기 때문에, 일부 변이체의 DNA 단편은 동일한 프로모터 활성을 가질 수 있다는 것이 추가로 인식된다.
본 발명에 사용된 "터미네이터"는 일반적으로 게놈 DNA에서 유전자의 말단을 표시하고 전사를 정지시킬 수 있는 DNA 서열의 섹션을 의미한다. 터미네이터는 천연 유전자로부터 전체적으로 유래되거나, 자연에서 발견된 상이한 터미네이터로부터 유래된 상이한 요소로 구성되거나, 심지어 합성 DNA 단편을 포함할 수 있다. 당업자는 상이한 터미네이터가 상이한 조직 또는 세포 유형, 또는 상이한 발달 단계에서, 또는 상이한 환경 조건에 반응하여 유전자의 발현을 지시할 수 있음을 이해한다.
본 발명에서 사용된 용어 "재조합 구조체", "발현 구조체", "키메라 구조체", "구조체" 및 "재조합 DNA 구조체"는 본 발명에서 상호 교환적으로 사용된다. 재조합 구조체는 천연에서 함께 발견되지 않는 조절 및 암호화 서열과 같은 핵산 단편의 인위적인 조합을 포함한다. 예를 들어, 키메라 구조체는 상이한 공급원으로부터 유도된 조절 서열 및 암호화 서열, 또는 동일한 공급원으로부터 유도되지만 자연계에서 발견되는 것과 상이한 방식으로 배열된 조절 서열 및 암호화 서열을 포함할 수 있다. 이러한 구조체는 그 자체로 사용되거나 벡터와 함께 사용될 수 있다. 벡터가 사용되는 경우 벡터의 선택은 당업자에게 주지된 바와 같이 숙주 세포를 형질 전환하는데 사용될 방법에 의존한다. 예를 들어, 플라스미드 벡터가 사용될 수 있다. 당업자는 본 발명의 분리된 핵산 단편을 포함하는 숙주 세포를 성공적으로 형질전환, 선별 및 증식시키기 위해 벡터 상에 존재해야 하는 유전자 요소를 잘 알고 있다. 당업자는 또한 상이한 독립적인 형질전환 사건이 발현의 상이한 수준 및 패턴을 유도한다는 것을 인식할 것이며(Jones et al., (1985) EMBO J. 4 : 2411-2418; De Almeida et al., (1989) Mol. Gen Genetics 218 : 78-86), 따라서 다수의 사건은 원하는 발현 수준 및 패턴을 나타내는 라인을 수득하기 위해 선별돼야한다. 이러한 선별은 다른 것들 중에서, DNA의 서던 분석, mRNA 발현의 노던 분석, 단백질 발현의 면역 블로 팅 분석 또는 표현형 분석에 의해 실행될 수 있다. 벡터는 자율적으로 복제하거나 숙주 세포의 염색체에 통합될 수있는 플라스미드, 바이러스, 박테리오파지, 프로-바이러스, 파지미드, 트랜스포존, 인공 염색체 등일 수있다. 벡터는 또한 자율적으로 복제하지 않는 네이키드 RNA 폴리뉴클레오타이드, 네이키드 DNA 폴리뉴클레오타이드, 동일한 가닥 내의 DNA 및 RNA 모두로 구성된 폴리뉴클레오타이드, 폴리-라이신-컨쥬게이드된 DNA 또는 RNA, 펩타이드-컨쥬게이드된 DNA 또는 RNA, 리포좀-컨쥬게이드된 DNA 등일 수 있다. 본 발명에 사용된 용어 "발현"은 기능적 최종 산물, 예를 들어 mRNA 또는 단백질(전구체 또는 성숙)의 생산을 의미한다.
"작동 가능하게 연결된"은 추가 폴리뉴클레오타이드의 전사를 초래하는 추가의 올리고뉴클레오타이드 또는 폴리뉴클레오타이드에 의한 본 발명에 따른 프로모터 폴리뉴클레오타이드의 순차적 배열을 의미한다.
본 발명에서 사용된 용어 "관심 생성물" 또는 "생체분자"는 원료로부터 미생물에 의해 생성된 임의의 생성물을 의미한다. 일부 경우에, 관심 생성물은 소분자, 효소, 펩타이드, 아미노산, 유기산, 합성 화합물, 연료, 알코올 등일 수 있다. 예를 들어, 관심 생성물 또는 생체분자는 임의의 1차 또는 2차 세포외 대사산물일 수 있다. 1차 대사산물은 특히 에탄올, 시트르산, 락트산, 글루탐산, 글루탐산염, 라이신, 트레오닌, 트립토판 및 다른 아미노산, 비타민, 폴리사카라이드 등일 수 있다. 2차 대사산물은 특히 페니실린과 같은 항생물질 또는 사이클로스포린 A와 같은 면역 억제제, 지베렐린과 같은 식물 호르몬, 로바스타틴과 같은 스타틴 약물, 그리세오풀빈과 같은 살균제 등일 수 있다. 관심 생성물 또는 생체분자는 또한 카탈라아제, 아밀라아제, 펙티나아제, 글루코오스 아이소머라제, 셀룰라아제, 헤미셀룰라아제, 리파아제, 락타아제, 스트렙토 키나아제 및 여러 다른 것을 포함하는 미생물 효소와 같은 미생물에 의해 생성된 임의의 세포내 성분일 수 있다. 세포내 성분은 또한 인슐린, B형 간염 백신, 인터페론, 과립구 콜로니-자극 인자, 스트렙토키나아제 및 기타와 같은 재조합 단백질을 포함할 수 있다. 관심 생성물은 또한 "관심 단백질"을 의미할 수 있다.
용어 "관심 단백질"은 일반적으로 사상균류에서 발현되기를 원하는 임의의 폴리펩타이드를 의미한다. 이러한 단백질은 효소, 기질-결합 단백질, 표면-활성 단백질, 구조 단백질 등일 수 있으며, 높은 수준으로 발현될 수 있으며, 상업화를 위한 것일 수 있다. 관심의 단백질은 변이 균주 및/또는 부모 균주에 비해 내인성 유전자 또는 이종성 유전자에 의해 암호화될 수 있다. 관심 단백질은 세포 내에서 또는 분비된 단백질로서 발현될 수 있다. 관심 단백질이 자연적으로 분비되지 않으면, 단백질을 암호화하는 폴리뉴클레오타이드는 당업계에 공지된 기술에 따라 신호 서열을 갖도록 변형될 수 있다. 분비되는 단백질은 자연적으로 발현되는 내인성 단백질일 수 있으나 이종성일 수 있다. 이종성은 단백질에 의해 암호화된 유전자가 사상균류 숙주 세포에서 천연 조건하에 생성되지 않음을 의미한다. 본 발명의 사상균류에 의해 생성될 수 있는 효소의 예는 탄수화물 분해 효소, 예를 들어, 엔도글루카나아제, 베타-글루카나아제, 셀로바이오하이드롤라제 또는 베타-글루코시다아제, 헤미셀룰라제와 같은 셀룰라제, 또는 자일라나제, 자일로시다제, 만나나제, 갈락타나제, 갈락토시다제, 람노갈락투로나제, 아라비나제, 갈락토로나제, 리가아제와 같은 펙틴 분해 효소 또는 녹말분해 효소; 피타아제와 같은 포스파타제, 리파아제와 같은 에스테라제, 단백질 분해 효소, 산화 효소와 같은 산화환원 효소, 트랜스퍼라제 또는 이성질화 효소이다.
용어 "탄소원"은 일반적으로 세포 성장을 위한 탄소원으로 사용되기에 적합한 물질을 의미한다. 탄소원은 바이오매스 가수분해물, 전분, 수크로오스, 셀룰로오스, 헤미셀룰로오스, 자일로오스 및 리그닌뿐만 아니라 이들 기질의 단량체 성분을 포함하나 이에 제한되지 않는다. 탄소원은 폴리머, 탄수화물, 산, 알코올, 알데하이드, 케톤, 아미노산, 펩타이드 등을 포함하나 이에 제한되지 않는 다양한 형태의 다양한 유기 화합물을 포함할 수 있다. 이들은, 예를 들어, 글루코오스, 덱스트로스(D-글루코오스), 말토오스, 올리고사카라이드, 폴리사카라이드, 포화 또는 불포화 지방산, 숙시네이트, 락테이트, 아세테이트, 에탄올 등, 또는 이의 혼합물과 같은 다양한 모노사카라이드를 포함한다. 광합성 유기체는 광합성의 산물로서 탄소원을 추가로 생산할 수 있다. 일부 실시태양에서, 탄소원은 바이오매스 가수분해물 및 글루코오스로부터 선택될 수 있다.
용어 "공급원료"는 미생물 또는 발효 공정에 공급되는 원료 또는 원료의 혼합물로서 다른 생성물이 제조될 수 있는 것으로 정의된다. 예를 들어, 바이오매스 또는 바이오매스에서 유도된 탄소 화합물과 같은 탄소 공급원은 발효 공정에서 관심 생성물(예를 들어, 소분자, 펩타이드, 합성 화합물, 연료, 알코올 등)을 생산하는 미생물의 공급원료이다. 그러나, 공급원료는 탄소 공급원 이외의 영양분을 함 유할 수 있다.
용어 "체적 생산성" 또는 "생산 속도"는 단위 시간당 매질의 부피당 형성된 생성물의 양으로 정의된다. 체적 생산성은 시간당 리터 당 그램(g/L/h)으로 보고될 수 있다.
용어 "비 생산성"은 생성물의 형성 속도로 정의된다. 비 생산성은 본 발명에서 시간당 세포 건조 중량의 그래당 그램 생성물(g/g CDW/h)의 비 생산성으로서 더 정의된다. 소정의 미생물에 대한 OD600에 대한 CDW의 관계를 사용하여, 비 생산성은 시간당 600nm(OD)(g/L/h/OD)에서 배양액의 광학 밀도당 배양 배지당 그램 생성물로 표현될 수 있다.
용어 "수율"은 원료의 단위 중량당 수득된 생성물의 양으로 정의되며 g 기질 당 g 생성물(g/g)로 표현될 수 있다. 수율은 이론적 수율의 백분율로 표현될 수있다. "이론적 수율"은 생성물을 제조하는데 사용된 신진대사 경로의 화학양론에 따라 결정된 소정량의 기질당 생성될 수 있는 최대 생성물로 정의된다.
용어 "역가(titre 또는 titer)"는 용액의 강도 또는 용액 속의 물질의 농도로 정의된다. 예를 들어, 발효액에서 관심 생성물(예를 들어, 소분자, 펩타이드, 합성 화합물, 연료, 알코올 등)의 역가는 발효액 1 리터당 용액 속 관심 제품의 g(g/L)로 기술된다.
용어 "총 적가"는 용액 속의 관심 생성물, 적용 가능한 경우 기체상의 관심 생성물, 공정으로부터 제거되고 공정에서 최초 부피 또는 공정에서 작동 부피에 따라 회수된 임의의 관심 생성물을 포함하나 이에 제한되지 않는 공정에서 생산된 모든 관심 생성물의 합으로 정의된다.
본 발명에 사용된 용어 "HTP 유전 디자인 라이브러리" 또는 "라이브러리"는 본 발명에 따른 유전자 교란의 집합을 의미한다. 일부 실시태양에서, 본 발명의 라이브러리는 i) 데이터베이스 또는 다른 컴퓨터 파일에서 서열 정보의 집합, ii) 상기한 일련의 유전자 요소를 암호화하는 유전자 구조체의 집합, 또는 iii) 상기 유전자 요소를 포함하는 숙주 세포 균주로서 입증될 수 있다. 일부 실시태양에서, 본 발명의 라이브러리는 개별 요소의 집합(예를 등러, PRO 스왑 라이브러리를 위한 프로모터 집합 또는 STOP 스왑 라이브러리를 위한 터미네이터 집합)을 의미할 수 있다. 다른 실시태양에서, 본 발명의 라이브러리는 프로모터::유전자, 유전자:터미네이터, 또는 심지어 프로모터:유전자:터미네이터의 조합과 같은 유전자 요소의 조합을 의미할 수 있다. 일부 실시태양에서, 본 발명의 라이브러리는 숙주 유기체에서 라이브러리의 각 구성원을 적용하는 효과와 관련된 메타 데이터를 추가로 포함한다. 예를 들어, 본 발명에서 사용된 라이브러리는 특정 종에서 하나 이상의 표현형에 대한 이들 조합의 얻어진 효과와 함께 프로모터::유전자 서열 조합의 집합을 포함할 수 있으며, 따라서 미래 프로모터 스왑에 상기 조합을 사용하는 미래 예측 가치를 개량시킨다.
본 발명에서 사용된 용어 "SNP"는 작은 핵 다형성(들)을 의미할 수 있다. 일부 실시태양에서, 본 발명의 SNP는 광범위하게 해석되어야하며, 단일 뉴클레오타이드 다형성, 서열 삽입, 결실, 역전 및 다른 서열 치환을 포함한다. 본 발명에서 사용된 용어 "비 동의" 또는 비 동의 SNP"는 숙주 세포 단백질에서 암호화 변화를 유도하는 돌연변이를 의미할 수 있다.
게놈 공학의 "고 처리량(HTP)" 방법은 상기 방법의 적어도 하나의 단계를 수행하기 위한 자동화 장비(예를 들어, 액체 핸들러 또는 플레이트 핸들러 머신)의 적어도 하나의 부품의 이용을 필요로 할 수 있다.
CRISPR/Cas 시스템은 플라스미드 및 파지 내에 존재하는 것과 같은 외래 유전자 요소에 대한 내성을 부여하고 획득된 면역의 형태를 제공하는 원핵 생물 면역 시스템이다. CRISPR은 Clustered Regularly Interspaced Short Palindromic Repeat를 나타내고 cas는 CRISPR 관련 시스템을 나타내며 CRISPR 복합체와 관련된 작은 cas 유전자를 의미한다.
CRISPR-Cas 시스템은 클래스 1 또는 클래스 2 시스템으로 가장 광범위하게 특징 지워진다. 이 두 시스템의 주요 특징은 Cas-이펙터 모듈의 특성이다. 클래스 1 시스템은 간섭을 중재하기 위해 복합체("캐스케이드 복합체"로 지칭됨)에 다수의 Cas 단백질의 조립을 필요로 하는 반면, 클래스 2 시스템은 간섭을 중재하기 위해 큰 단일 Cas 효소를 사용한다. 클래스 1 및 클래스 2 시스템 각각은 특정 Cas 단백질의 존재에 기초하여 다수의 CRISPR-Cas 유형으로 추가로 분할된다. 예를 들어, 클래스 1 시스템은 다음 세 가지 유형으로 나뉜다: Cas3 단백질을 포함하는 유형 I 시스템; Cas10 단백질을 함유하는 유형 III 시스템; 및 Cas8 유사 단백질인 Csf1 단백질을 함유하는 추정 유형 IV 시스템. 클래스 2 시스템은 일반적으로 클래스 1 시스템보다 덜 일반적이며 다음 세 가지 유형으로 더 나뉜다: Cas9 단백질을 포함하는 유형 II 시스템; Cas12a 단백질(Cpf1으로 이미 알려지고 본 발명에서 Cpf1으로 지칭됨), Cas12b(C2c1으로 이미 알려짐), Cas12c(C2c3으로 이미 알려짐), Cas12d(CasY로 이미 알려짐) 및 Cas12e(CasX로 이미 알려짐)를 포함하는 유형 V 시스템; 및 Cas13a(C2c2로 이미 공지됨), Cas13b 및 Cas13c를 포함하는 유형 VI 시스템. Pyzocha et al., ACS Chemical Biology, Vol. 13 (2), pgs. 347-356. 한 실시 태양에서, 본 발명에 제공된 방법에 사용하기 위한 CRISPR-Cas 시스템은 클래스 2 시스템이다. 한 실시태양에서, 본 발명에 제공된 방법에 사용하기 위한 CRISPR-Cas 시스템은 유형 II, 유형 V 또는 유형 VI 클래스 2 시스템이다. 한 실시태양에서, 본 발명에 제공된 방법에 사용하기 위한 CRISPR-Cas 시스템은 Cas9, Cas12a, Cas12b, Cas12c, Cas12d, Cas12e, Cas13a, Cas13b, Cas13c 또는 이의 상동체, 오쏘로그 또는 파라로그로부터 선택된다.
본 발명에 개시된 방법에 사용된 CRISPR 시스템은 본 발명에서 Cas 이펙터 단백질로 지칭되는 하나 이상의 핵산 유도된 CRISPR-관련(Cas) 뉴클레아제를 포함하는 Cas 이펙터 모듈을 포함한다. 일부 실시태양에서, Cas 단백질은 하나 또는 다수의 뉴클레아제 도메인을 포함할 수 있다. Cas 이펙터 단백질은 단일 가닥 또는 이중 가닥 핵산 분자(예를 들어, DNA 또는 RNA 핵산)를 표적으로 할 수 있고 이중 가닥 또는 단일 가닥 브레이크를 생성할 수 있다. 일부 실시태양에서, Cas 이펙터 단백질은 야생형 또는 자연 발생 Cas 단백질이다. 일부 실시태양에서, Cas 이펙터 단백질은 돌연변이체 Cas 단백질이며, 여기서 하나 이상의 돌연변이, 삽입 또는 결실은 WT 또는 자연 발생 Cas 단백질(예를 들어, 부모 Cas 단백질)에서 만들어져 부모 Cas 단백질과 비교하여 하나 이상의 변경된 특성을 갖는 Cas 단백질을 생성한다.
일부 경우에, Cas 단백질은 야생형(WT) 뉴클레아제이다. 본 발명에 사용하기에 적합한 Cas 단백질의 비 제한적 예는 C2cl, C2c2, C2c3, Cas1, Cas1B, Cas2, Cas3, Cas4, Cas5, Cas6, Cas7, Cas8, Cas9 (Csn1 및 Csx12로도 알려져 있음), Cas10을 포함한다. , Cpfl, Csy1, Csy2, Csy3, Cse1, Cse2, Csc1, Csc2, Csa5, Csn2, Csm1, Csm2, Csm3, Csm4, Csm5, Csm6, Cmr1, Cmr3, Cmr4, Cmr5, Cmr6, Csb1, Csb2, Csb2, Csb2 Csx14, Csx100, Csx16, CsaX, Csx3, Csxl, Csx15, Csf1, Csf2, Csf3, Csf4, MAD1-20, SmCsm1, 이의 상동체, 오쏘로그, 변이체, 돌연변이체 또는 변형 버전이다. 적합한 핵산 가이드된 뉴클레아제(예를 들어, Cas 9)는 다음을 포함하나 이에 제한되지 않는 속으로부터의 유기체로부터 형성될 수 있다: 티오마이크로스피라(Thiomicrospira), 숙시니비브리오(Succinivibrio), 칸디다투스(Candidatus), 포르피로모나스(Porphyromonas), 애시도모노코쿠스(Acidomonococcus), 프레보텔라(Prevotella), 스미셀라(Smithella), 모락셀라(Moraxella), 시너지스테스(Synergistes), 프란세셀라(Francisella), 렙토스피라(Leptospira), 카테니박테리움(Catenibacterium), 칸들레리아(Kandleria), 클로스티리듐(Clostridium), 도레아(Dorea), 코프로코커스(Coprococcus), 엔테로코커스(Enterococcus), 프룩토바실루스(Fructobacillus), 웨이셀라(Weissella), 페디오코커스(Pediococcus), 코리네박터(Corynebacter), 셔터렐라(Sutterella), 레지오넬라(Legionella), 트레포네마(Treponema), 로즈부리아(Roseburia), 필리팩터(Filifactor), 유박테리움(Eubacterium), 스트렙토코커스(Streptococcus), 락토 바실러스(Lactobacillus), 마이코플라스마(Mycoplasma), 박터로이데스(Bacteroides), 플라비볼라(Flaviivola), 플라보박테리움(Flavobacterium), 스파에로차에타(Sphaerochaeta), 아조스피릴룸(Azospirillum), 글루코나세토박터(Gluconacetobacter), 네이세리아(Neisseria), 로즈부리아(Roseburia), 파비바쿨룸(Parvibaculum), 스파릴로코커스(Staphylococcus), 니트라티프락토(Nitratifractor), 마이코플라즈마(Mycoplasma), 알리사이클로바실러스(Alicyclobacillus), 브레비바실러스(Brevibacilus), 바실러스(Bacillus), 카노박테리움(Carnobacterium), 클로스트리디아리듐(Clostridiaridium), 클로스트리듐(Clostridium), 데설포나트로눔(Desulfonatronum), 데설포비브리오(Desulfovibrio), 헬코코커스(Helcococcus), 렙토트리키아(Leptotrichia), 리스테리아(Listeria), 메타노메티오필러스(Methanomethyophilus), 메틸로박테리움(Methylobacterium), 오피투타세애(Opitutaceae), 팔루디박터(Paludibacter), 로도박터(Rhodobacter), 스파애로차에타(Sphaerochaeta), 튜베리바실러스(Tuberibacillus) 및 캄필로박터(Campylobacter). 이러한 속의 유기체 종은 다른 상황에서는 본 발명에서 논의된 바와 같을 수 있다.
적합한 핵산 가이드된 뉴클레아제(예를 들어, Cas9)는 다음을 포함하나 이에 제한되지 않는 문으로부터의 유기체로부터 유래될 수 있다: 피르미쿠테(Firmicute), 악티노박테리아(Actinobacteria), 박테로이데테스(Bacteroidetes), 프로테오박테리아(Proteobacteria), 스피로카테스(Spirochates) 및 테네리쿠테스(Tenericutes). 적합한 핵산 가이드된 뉴클레아제는 다음을 포함하나 이에 제한되지 않는 강으로부터의 유기체로부터 유래될 수 있다: 에리스필로트리치아(Erysipelotrichia), 클로스트리디아(Clostridia), 바실리(Bacilli), 악티노박테리아(Actinobacteria), 박테로이데테스(Bacteroidetes), 플라보박테리아(Flavobacteria), 알파프로테오박테리아(Alphaproteobacteria), 베타프로테오박테리아(Betaproteobacteria), 감마프로테오박테리아(Gammaproteobacteria), 델타 프로테오박테리아(), 엡실론프로테오박테리아(Epsilonproteobacteria), 스피로케아테스(Spirochaetes) 및 몰리쿠테스(Mollicutes). 적합한 핵산 가이드된 뉴클레아제는 다음을 포함하나 이에 제한되지 않는 목으로부터의 유기체로부터 유래될 수 있다: 클로스트리디알레스(Clostridiales), 락토바실알레스(Lactobacillales), 액티노마세탈레스(Actinomycetales), 박테로이달레스(Bacteroidales), 플라보박테리알레스(Flavobacteriales), 리조비알레스(Rhizobiales), 로도스피릴알레스(Rhodospirillales), 버크홀데리알레스(Burkholderiales), 네이세리알레스(Neisseriales), 레지오넬라레스(Legionellales), 나우틸리알레스(Nautiliales), 캄필로박터알레스(Campylobacterales), 스피로차에탈레스(Spirochaetales), 마이코플라스마탈레스(Mycoplasmatales), 및 티오트리칼레스(Thiotrichales). 적합한 핵산 가이드된 뉴클레아제는 다음을 포함하나 이에 제한되지 않는 과로부터의 유기체로부터 유래될 수 있다: 라치노스피라세애(Lachnospiraceae), 엔테로콕커세애(Enterococcaceae), 레우코노스토카세애(Leuconostocaceae), 락토바실라세애(Lactobacillaceae), 스트렙토코카세애(Streptococcaceae), 펩토스트렙토코카세애(Peptostreptococcaceae), 스타필로코카세애(Staphylococcaceae), 유박테리아세애(Eubacteriaceae), 코리네박터리네애(Corynebacterineae), 박터로이다세애(Bacteroidaceae), 플라보박테리움(Flavobacterium), 크리요모오르파세애(Cryomoorphaceae), 로도비애세(Rhodobiaceae), 로도스피릴라세애(Rhodospirillaceae), 아세토박테라세애(Acetobacteraceae), 슈테렐라세애(Sutterellaceae), 네이세리아세애(Neisseriaceae), 레지오넬라세애(Legionellaceae), 나우틸라세애(Nautiliaceae), 캄필로박터라세애(Campylobacteraceae), 스피로차에타세애(Spirochaetaceae), 마이코플라스마타세애(Mycoplasmataceae), 및 플란시셀라세애(Francisellaceae).
본 발명의 방법, 시스템 및 조성물에 사용하기에 적합한 다른 핵산 가이드된 뉴클레아제(예를 들어, Cas9)는 다음을 포함하나 이에 제한되지 않는 유기체로부터 유래된 것들을 포함한다: 티오마이크로스피라 에스피. XS5(Thiomicrospira sp . XS5), 유박테리아 렉탈(Eubacterium rectale), 숙시니비브리오(Succinivibrio), 덱스트라이노솔벤스(dextrinosolvens), 칸디다투스 메타노플라스마 터미툼(Candidatus Methanoplasma termitum), 칸디다투스 메타노메틸로필루스 알부스(Candidatus Methanomethylophilus alvus), 포르필로모나스 크레비오리카니스(Porphyromonas crevioricanis), 플라보박터리움 브란치오필룸(Flavobacterium branchiophilum), 애시도모노코커스 에스피(Acidomonococcus sp .), 라치노스피라세애 박테리움 스미스 COE1(Lachnospiraceae bacterium COE1), 프레보텔라 브레비스(Prevotella brevis) ATCC 19188, 스미텔라 에스피 SCADC(Smithella sp. SCADC), 모렉셀라 보노쿨리(Moraxella bovoculi), 시너지스테스 조네시(Synergistes jonesii), 박테로이데테스(Bacteroidetes) 경구 분류군 274, 프란시셀라 툴라렌시스(Francisella tularensis), 렙토스피라 이나다이 세로바 라임 str(Leptospira inadai serovar Lyme str. 10), 아시도모노코커스 sp.(Acidomonococcus sp.) 결정 구조(5B43) S. 뮤탄스(S. mutans), S. 아갈락티애(S. agalactiae), S. 에퀴시밀리스(S. equisimilis), S. 산구이니스(S. sanguinis), S. 뉴모니아(S. pneumonia); C. 제주니(C. jejuni), C, 콜리(C. coli); N. 살수기니스(N. salsuginis), N. 터가쿠스(N. tergarcus); S.아우리쿨라리스(S. auricularis), S. 카노수스(S. carnosus); N. 메닌기티데스(N. meningitides), N. 고노르호애(N. gonorrhoeae); L. 모노사이토게네스(L. monocytogenes), L. 이바노비(L. ivanovii); C. 보툴리넘(C. botulinum), C.디피시엘(C. difficile), C. 테타니(C. tetani), C. 소르델리(C. sordellii); 프란시셀라 툴라렌시스 l(Francisella tularensis l), 프레보텔라 알벤시스(Prevotella albensis), 라치노스피라세애 박테리움(Lachnospiraceae bacterium) MC2017 1, 부티리비브리오 프로테오클라스티쿠스(Butyrivibrio proteoclasticus), 퍼레그리니박테리아 박테리움(Peregrinibacteria bacterium) GW2011_GWA2_33_10, 파쿠박테리아 박테리움(Parcubacteria bacterium) GW2011_GWC2_ 44_17, 스미텔라 sp.(Smithella sp.) SCADC, 마이크로케노마테스(Microgenomates), 애시다미노코커스 sp.(Acidaminococcus sp.) BV3L6, 라치노스피라세애 박테리움(Lachnospiraceae bacterium) MA2020, 칸디다투스 메타노플라스스마 터미텀(Candidatus Methanoplasma termitum), 유박테리움 엘리겐스(Eubacterium eligens), 모락셀라 보보쿨리(Moraxella bovoculi) 237, 렙토스피라 이나다이(Leptospira inadai), 라치노스피라세애 박테리움(Lachnospiraceae bacterium) ND2006, 포피로모나스 그레비오리카니스 3(Porphyromonas crevioricanis 3), 프로보텔라 디시엔스(Prevotella disiens), 포피로모나스 마카카애(Porphyromonas macacae), 카케니박테리움 sp.(Catenibacterium sp.) CAG:290, 칸델리아 비툴리나(Kandleria vitulina), 클로스티리알레스 박테리움(Clostridiales bacterium) KA00274, 라치노스피라세애 박테리움(Lachnospiraceae bacterium) 3-2, 도레아 론지카테나(Dorea longicatena), 코프로코커스 카투스(Coprococcus catus) GD/7, 엔테로코커스 쿨룸배(Enterococcus columbae) DSM 7374, 프룩토바실루스 sp.(Fructobacillus sp .) EFB-N1, 웨이셀라 할로톨레란스(Weissella halotolerans), 페디오코커스 아시딜락티시(Pediococcus acidilactici), 락토바실루스 커바투스(Lactobacillus curvatus), 스트렙토코커스 피오게네스(Streptococcus pyogenes), 락토바실루스 버스몰덴시스(Lactobacillus versmoldensis) 및 필리팩터 알로시스(Filifactor alocis) ATCC 35896. U.S. Pat. Nos. 8,697,359; 8,771,945; 8,795,965; 8,865,406; 8,871,445; 8,889,356; 8,895,308; 8,906,616; 8,932,814; 8,945,839; 8,993,233; 8,999,641; 9,822,372; 9,840,713; U.S. Pat. App. No. 13/842,859 (US 2014/0068797 A1); 9,260,723; 9,023,649; 9,834,791; 9,637,739; U.S. Pat. App. No. 14/683,443 (US 2015/0240261 A1); U.S. Pat. App. No. 14/743,764 (US 2015/0291961 A1); 9,790,490; 9,688,972; 9,580,701; 9,745,562; 9,816,081; 9,677,090; 9,738,687; U.S. App. No. 15/632,222 (US 2017/0369879 A1); U.S. App. No. 15/631,989; U.S. App. No. 15/632,001; 및 U.S. Pat. No. 9,896,696 참조, 이의 각각은 본 발명에 참조로 포함된다.
일부 실시태양에서, Cas 이펙터 단백질은 다음 활성 중 하나 이상을 포함한다:
닉카제 활성, 즉 핵산 분자의 단일 가닥을 절단하는 능력;
이중 가닥 뉴클레아제 활성, 즉 이중 가닥 핵산의 양쪽 가닥을 절단하고 이중 가닥 파괴를 생성하는 능력;
엔도뉴클레아제 활성;
엑소뉴클레아제 활성; 및/또는
헬리카제 활성, 즉 이중 가닥 핵산의 나선 구조를 풀 수 있는 능력.
본 발명의 양태에서, 용어 "가이드 핵산"은 1) 표적 서열에 혼성화할 수 있는 가이드 서열(본 발명에서 "표적 단편"으로 지칭됨) 및 2) 본 발명에 기재된 바와 같은 핵산 가이드된 뉴클레아제(본 발명에서 "스캐폴드 단편"으로 지칭됨)와 (단독으로 또는 tracrRNA 분자와의 조합으로) 상호 작용할 수 있는 스캐폴드 서열을 포함하는 폴리뉴클레오타이드를 의미한다. 가이드 핵산은 DNA일 수 있다. 가이드 핵산은 RNA일 수 있다. 가이드 핵산은 DNA 및 RNA를 모두 포함할 수 있다. 가이드 핵산은 변형된 비 천연 발생 뉴클레오타이드를 포함할 수 있다. 가이드 핵산이 RNA를 포함하는 경우, RNA 가이드 핵산은 본 발명에 개시된 바와 같은 플라스미드, 선형 구조체 또는 편집 카세트와 같은 폴리뉴클레오타이드 분자 상의 DNA 서열에 의해 암호화될 수 있다.
일부 실시태양에서, 본 발명에 기재된 가이드 핵산은 RNA 가이드 핵산("가이드 RNA" 또는 "gRNA")이고 표적화 단편 및 스캐폴드 단편을 포함한다. 일부 실시태양에서, gRNA의 스캐폴드 다편은 하나의 RNA 분자에 포함되고 표적화 단편은 다른 별도의 RNA 분자에 포함된다. 이러한 실시태양은 본 발명에서 "이중 분자 gRNA" 또는 "두 분자 gRNA" 또는 "이중 gRNA"로 지칭된다. 일부 실시태양에서, gRNA는 단일 RNA 분자이고 본 발명에서 "단일 가이드 RNA" 또는 "sgRNA"로 지칭된다. 용어 "가이드 RNA" 또는 "gRNA"는 두 분자 가이드 RNA 및 sgRNA를 모두 지칭한다.
gRNA의 DNA-표적화 단편은 표적 핵산 서열의 서열에 상보적인 뉴클레오타이드 서열을 포함한다. 이와 같이, gRNA의 표적화 단편은 혼성화(즉, 염기쌍)를 통해 서열-특이적 방식으로 표적 핵산과 상호 작용하고, 표적화 단편의 뉴클레오타이드 서열은 gRNA가 결합할 표적 DNA 내의 위치를 결정한다. 적절한 정렬 알고리즘을 사용하여 최적으로 정렬될 때, 가이드 서열과 이에 상응하는 표적 서열 사이의 상보성 정도는 약 50%, 60%, 75%, 80%, 85%, 90%, 95%, 97.5%, 99%이거나 50%, 60%, 75%, 80%, 85%, 90%, 95%, 97.5%, 99% 초과이다. 최적 정렬은 서열 정렬을 위한 임의의 적합한 알고리즘을 사용하여 결정될 수 있다. 일부 실시태양에서, 가이드 서열은 약 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 45, 50, 75개의 뉴클레오타이드 길이이거나 약 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 45, 50, 75개 초과의 뉴클레오타이드 길이이다. 일부 실시태양에서, 가이드 서열은 길이가 약 75, 50, 45, 40, 35, 30, 25, 20개 미만의 뉴클레오타이드이다. 양태에서, 가이드 서열은 10-30개의 뉴클레오타이드 길이이다. 가이드 서열은 15-20개의 뉴클레오타이드 길이일 수 있다. 가이드 서열은 15개의 뉴클레오타이드 길이일 수 있다. 가이드 서열은 16개의 뉴클레오타이드 길이일 수 있다. 가이드 서열은 17개의 뉴클레오타이드 길이일 수 있다. 가이드 서열은 18개의 뉴클레오타이드 길이일 수 있다. 가이드 서열은 19개의 뉴클레오타이드 길이일 수 있다. 가이드 서열은 20개의 뉴클레오타이드 길이일 수 있다.
가이드 RNA의 스캐폴드 단편은 하나 이상의 Cas 이펙터 단백질과 상호 작용하여 리보핵단백질 복합체(본 발명에서 CRISPR-RNP 또는 RNP-복합체로 지칭됨)를 형성한다. 가이드 RNA는 상기 기재된 표적화 단편을 통해 결합된 폴리펩타이드를 표적 핵산 서열 내의 특정 뉴클레오타이드 서열로 보낸다. 가이드 RNA의 스캐폴드 단편은 서로 상보적이고 이중 가닥 RNA 이중체를 형성하는 두 줄기의 뉴클레오타이드를 포함한다. 표적화 뉴클레아제 복합체의 형성을 촉진하기 위해 스캐폴드 서열 내에서 충분한 서열은 스캐폴드 서열 내에서 2개의 서열 영역의 길이를 따라 상보성 정도, 예를 들어 2차 구조를 형성하는 데 관여하는 하나 또는 두 개의 서열 영역을 포함할 수 있다. 일부 경우에, 하나 또는 두 개의 서열 영역은 동일한 폴리 뉴클레오타이드 상에 포함되거나 암호화된다. 일부 경우에, 하나 또는 두 개의 서열 영역은 별도의 폴리뉴클레오타이드 상에 포함되거나 암호화된다. 최적의 정렬은 임의의 적합한 정렬 알고리즘에 의해 결정될 수 있고, 하나 또는 두 개의 서열 영역 내에서의 자기 상보성과 같은 2차 구조를 추가로 설명할 수 있다. 일부 실시태양에서, 최적으로 정렬될 때 2개의 짧은 길이를 따라 하나 또는 2개의 서열 영역 사이의 상보성의 정도는 약 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 97.5%, 99%이거나 약 25%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 97.5%, 99% 초과이다. 일부 실시태양에서, 2개의 서열 영역 중 하나 이상은 약 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 40, 50개의 뉴클레오타이드 길이이거나 약 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 40, 50개 초과의 뉴클렐오타이드 길이이다.
본 발명의 gRNA의 스캐폴드 서열은 2차 구조를 포함할 수 있다. 2차 구조는 유사 노트 영역 또는 스템 루프 구조를 포함할 수 있다. 일부 예에서, 가이드 핵산 및 핵산 가이드된 뉴클레아제의 상용성은 가이드 RNA의 2차 구조 영역 내에서 또는 가이드 RNA의 인접 서열에 의해 적어도 부분적으로 결정된다. 일부 경우에, 가이드 핵산의 핵산 가이드된 뉴클레아제에 대한 결합 동역학은 스캐폴드 서열 내의 2차 구조에 의해 부분적으로 결정된다. 일부 경우에, 가이드 핵산의 핵산 가이드된 뉴클레아제에 대한 결합 동역학은 스캐폴드 서열과 핵산 서열에 의해 부분적으로 결정된다.
gRNA-Cas 이펙터 단백질 조합에 대한 양립 가능한 스캐폴드 서열은 천연 Cas 뉴 클레아제 유전자좌에 인접한 서열을 스캐닝함으로써 발견될 수 있다. 다시 말해, 천연 Cas 뉴클레아제는 상응하는 양립 가능한 가이드 핵산 또는 스캐폴드 서열에 근접한 게놈에서 암호화될 수 있다.
핵산 가이드된 뉴클레아제는 뉴 클레아제 내인성 숙주 내에서 발견되지 않은 가이드 핵산과 양립 가능할 수 있다. 이러한 직교 가이드 핵산은 경험적 테스트에 의해 결정될 수 있다. 직교 가이드 핵산은 상이한 박테리아 종으로부터 유래되거나 비 천연적으로 발생하도록 합성되거나 다른 상황에서 조작될 수 있다. 공통 핵산 가이드된 뉴클레아제와 양립할 수 있는 직교 가이드 핵산은 하나 이상의 공통적인 특징을 포함할 수 있다. 공통적인 특징은 유사 노트 영역 외부의 시퀀스를 포함할 수 있다. 공통적인 특징은 유사 노트 영역을 포함할 수 있다. 공통적인 특징은 1차 시퀀스 또는 2차 구조를 포함할 수 있다.
가이드 핵산은 가이드 서열을 변형함으로써 원하는 표적 서열을 표적화하도록 조작될 수 있어서, 가이드 서열이 표적 서열에 상보적이며, 따라서 가이드 서열과 표적 서열 사이의 혼성화를 가능하게 한다. 조작된 가이드 서열을 갖는 가이드 핵산은 조작된 가이드 핵산으로 지칭될 수 있다. 조작된 가이드 핵산은 종종 자연적으로 발생하지 않으며 자연에서 발견되지 않는다.
일부 실시태양에서, 본 발명은 gRNA를 암호화하는 폴리뉴클레오타이드를 제공한다. 일부 실시태양에서, gRNA-암호화 핵산은 발현 벡터, 예를 들어 재조합 발현 벡터에 포함된다. 일부 실시태양에서, 본 발명은 부위 지향적 변형 폴리펩타이드를 암호화하는 폴리뉴클레오타이드를 제공한다. 일부 실시태양에서, 부위 지향적 변형 폴리펩타이드를 암호화하는 폴리뉴클레오타이드는 발현 벡터, 예를 들어 재조합 발현 벡터에 포함된다.
일부 실시태양에서, 본 발명은 표적 핵산 서열을 포함하는 숙주 세포 내로 도입될 수 있는 RNP-복합체를 형성하도록 부위 지향적 변형 폴리펩타이드와 복합체화되는 gRNA를 제공하며 이를 위해 gRNA의 표적 단편은 상보적인 서열을 포함한다. 핵산 가이드된 뉴클레아제는 당 업계에 공지되고/되거나 본 발명에 제공된 임의의 핵산 가이드된 뉴클레아제일 수 있다(예를 들어, Cas9). 핵산 가이드된 뉴클레아제는 RNA(예를 들어, gRNA)에 의해 가이드될 수 있고 따라서 RNA 가이드된 뉴클레아 제 또는 RNA 가이드된 엔도뉴 클레아제로 지칭된다.
균주 개량의 전통적인 방법
균주 개량에 대한 전통적인 접근법은 크게 두 가지 유형의 접근법으로 분류 될 수 있다: 지시된(directed) 균주 조작 및 무작위 돌연변이유발.
균주 개량의 지시된 조작 방법은 특정 유기체의 소수의 유전자 요소의 계획된 교란을 필요로 한다. 이러한 접근법은 전형적으로 특정 생합성 또는 발달 프로그램을 조절하는데 중점을 두고 있으며, 상기 경로에 영향을 미치는 유전적 및 대사적 요인에 대한 사전 지식에 의존한다. 이의 가장 간단한 실시태양에서, 지시된 조작은 하나의 유기체로부터 동일하거나 상이한 종의 다른 유기체로 특성화된 형질(예를 들어, 유전자, 프로모터, 또는 측정 가능한 표현형을 생산할 수 있는 다른 유전 요소)의 전달을 필요로 한다.
균주 조작에 대한 무작위 접근법은 성능 개량을 확인하기 위한 광범위한 선별과 함께 부모 균주의 무작위 돌연변이유발을 필요로 한다. 이러한 무작위 돌연변이를 일으키기 위한 접근법은 자외선 복사에너지 또는 에틸 메테인설포네이트와 같은 돌연변이유발 화학물질에 대한 노출을 포함한다. 무작위적이며 매우 예측할 수 없음을 통해, 균주 개량에 대한 이런 전통적인 접근법은 보다 지시된 유전자 조작에 비해 몇 가지 장점을 가졌다. 첫째, 많은 산업 유기체는 유전자 및 대사성 레파토리의 관점에서 특성이 좋지 않아서(좋지 않게 유지되어), 불가능한 것은 아니지만 대안적인 직접적인 개량 접근법을 어렵게 만들었다.
둘째, 비교적 특성이 규명된 시스템에서도, 산업 성능 개량을 초래하는 유전자형 변화는 예측하기 어렵고, 때때로 알려지고 알려지지 않은 기능의 많은 유전자에서 누적 돌연변이를 필요로 하는 상위성 표현형으로만 나타난다.
또한, 수년 동안, 소정의 산업용 유기체에서 직접적인 게놈 돌연변이를 만드는데 필요한 유전자 도구는 이용할 수 없거나 사용이 매우 느리고 및/또는 어려웠다.
그러나, 종래의 균주 개량 프로그램의 확장된 적용은 소정의 균주 계보에서 점진적으로 감소된 이득을 가져오고, 궁극적으로는 추가 균주 효율에 대한 소진된 가능성을 야기한다. 유익한 무작위 돌연변이는 상대적으로 드문 경우이며 큰 선별 풀과 높은 돌연변이율을 필요로 한다. 이것은 필연적으로 "개량된" 균주에서 많은 중립적인 및/또는 해로운(또는 부분적으로 해로운) 돌연변이의 부주의한 누적을 초래하여, 궁극적으로 미래 효율성 향상에 대한 장애물을 형성한다.
전통적인 누적 개량 접근법의 다른 한계는 임의의 균주 메트릭에 대한 임의의 특정 돌연변이의 효과에 대한 정보가 거의 또는 전혀 없다는 것이다. 이것은 근본적으로 유익한 돌연변이를 결합 및 통합하거나 중립적이거나 해로운 돌연변이유발성 "수하물(baggage)"을 제거하는 연구자의 능력을 제한한다.
돌연변이성 계통 내에서 균주 간의 돌연변이를 무작위로 재조합시키는 다른 접근법 및 기술이 존재한다. 예를 들어, DNA 셔플링, 진화 또는 분자 육종으로 때때로 불리는 반복적 서열 재조합에 대한 몇몇 포맷 및 예가 미국 특허출원, Ser. No. 08/198,431, filed Feb. 17, 1994, Serial No. PCT/US95/02126, filed, Feb. 17, 1995, Ser. No. 08/425,684, filed Apr. 18, 1995, Ser. No. 08/537,874, filed Oct. 30, 1995, Ser. No. 08/564,955, filed Nov. 30, 1995, Ser. No. 08/621,859, filed. Mar. 25, 1996, Ser. No. 08/621,430, filed Mar. 25, 1996, Serial No. PCT/US96/05480, filed Apr. 18, 1996, Ser. No. 08/650,400, filed May 20, 1996, Ser. No. 08/675,502, filed Jul. 3, 1996, Ser. No. 08/721, 824, filed Sep. 27, 1996, and Ser. No. 08/722,660 filed Sep. 27, 1996; Stemmer, Science 270:1510 (1995); Stemmer et al., Gene164:49-53 (1995); Stemmer, Bio/Technology 13:549-553 (1995); Stemmer, Proc. Natl. Acad. Sci. U.S.A. 91:10747-10751 (1994); Stemmer, Nature370:389-391 (1994); Crameri et al., Nature Medicine 2(1):1-3 (1996); Crameri et al., Nature Biotechnology 14:315-319 (1996)에 기술되며, 이의 각각은 모든 목적을 위해 그 전문이 본 발명에 참조로 포함된다.
이들은 돌연변이 균주를 통한 게놈 재조합을 용이하게 하는 원형질 융합 및 전체 게놈 셔플링과 같은 기술을 포함한다. 효모 및 사상균류와 같은 일부 산업용 미생물의 경우, 자연 교배 주기가 쌍을 이루는 방식의 게놈 재조합에도 이용될 수 있다. 이런 방식으로, 해로운 돌연변이는 부모 균주에 의한 돌연변이체를 "백-크로싱"하여 제거될 수 있고 유익한 돌연변이가 강화될 수 있다. 또한, 두 가지 다른 균주 계통의 유익한 돌연변이가 잠재적으로 결합될 수 있어서, 단일 균주 계통을 자체로 돌연변이시킴으로써 얻을 수 있는 것보다 추가적인 개량 가능성을 형성할 수 있다. 그러나, 이런 접근법은 본 발명의 방법을 사용하여 피하게 되는 많은 제한을 받는다.
예를 들어, 상기한 바와 같은 전통적인 재조합 접근법은 느리고 돌연변이를 교환하기 위한 비교적 적은 수의 랜덤 재조합 크로스오버 사건에 의존하며, 따라서 임의의 소정의 주기 또는 시간 기간에서 시도될 수 있는 조합의 수에 제한이 있다. 또한, 선행 기술의 자연 재조합 사건은 본질적으로 무작위이지만, 이들은 또한 게놈 위치 편향에 영향을 받는다.
가장 중요한 것은, 전통적인 접근법은 개개의 돌연변이의 영향에 대한 정보를 거의 제공하지 않으며, 재조합 돌연변이의 무작위적인 분포로 인해 많은 특정 조합이 생성 및 평가될 수 없다.
종래의 균주 개량 프로그램과 관련된 여러 상기한 문제를 극복하기 위해, 본 발명은 연산적으로 구동되고 분자 생물학, 자동화, 데이터 분석 및 기계 학습 프로토콜을 통합하는 독특한 HTP 게놈 공학 플랫폼을 개시한다. 이 통합 플랫폼은 HTP 유전자 디자인 라이브러리를 구축하는데 사용되는 한 벌의 HTP 분자 도구 세트를 사용한다. 이러한 유전자 디자인 라이브러리는 아래에 자세히 설명될 것이다.
본 개시된 HTP 플랫폼 및 이의 독특한 미생물 유전자 디자인 라이브러리는 미생물 균주 개발 및 진화의 패러다임을 근본적으로 변화시킨다. 예를 들어, 산업용 미생물 균주를 개발하는 전통적인 돌연변이유발 기반의 방법은 수년간의 무작위 돌연변이유발 동안 축적된 중대한 돌연변이유발성 부하에 의해 부담을 진 미생물을 결국 유발할 것이다.
이러한 문제점을 해결하는(즉, 이들 미생물에 의해 축적된 유전자 수하물을 제거하는) 능력은 수십 년 동안 미생물 연구자들을 회피하였다. 그러나, 본 발명에 개시된 HTP 플랫폼을 이용하여, 이들 산업용 균주는 "재활"될 수 있고 해로운 유전 자 돌연변이가 확인되고 제거될 수 있다. 부합하게, 유익한 것으로 확인된 유전자 돌연변이는 유지될 수 있고 일부 경우에 개량될 수 있다. 생성된 미생물 균주는 이들의 부모의 균주와 비교하여 우수한 표현형 형질(예를 들어, 관심 화합물의 개량된 생산)을 나타낸다.
또한, 본 발명에서 교시된 HTP 플랫폼은 개별 돌연변이가 미생물 균주 성능에 미치는 효과를 확인, 특징화 및 정량화할 수 있다. 이 정보, 즉 소정의 유전자 변화 x가 숙주 세포 표현형 y에 대해 갖는 효과(예를 들어, 화합물 또는 관심 생성물의 생산)는 생성될 수 있고, 이후에 논의되는 미생물 HTP 유전자 디자인 라이브러리에 저장될 수 있다. 즉, 각 유전자 순열에 대한 서열 정보 및 숙주 세포 표현형에 대한 이의 효과는 하나 이상의 데이터베이스에 저장되며, 후속 분(예를 들어, 아래에서 논의되는 바와 같이 상위성 매핑)에 이용가능하다. 본 발명은 또한 유전자 삽입 구조체의 형태로, 또는 상기 유전자 순열을 함유하는 하나 이상의 숙주 세포 생물체의 형태로 귀중한 유전자 순열을 물리적으로 보호/저장하는 방법을 교시한다(예를 들어, 이하에서 논의되는 라이브러리 참조).
이들 HTP 유전 디자인 라이브러리를 정교한 데이터 분석 및 기계 학습 과정과 통합된 반복적 과정에 결합시키면 숙주 세포를 개량하기 위한 극적으로 상이한 방법론이 나타난다. 따라서, 교시된 플랫폼은 숙주 세포 균주를 개발하는 이전에 논의된 전통적인 방법과 근본적으로 상이하다. 교시된 HTP 플랫폼은 이전 방법과 관련된 많은 단점을 겪지 않는다. HTP 분자 도구 세트와 아래 논의된 유도된 유전자 디자인 라이브러리를 참조하면 이러한 장점과 다른 장점이 분명해질 것이다.
개관
본 발명의 목적은 사상균류 세포 또는 이로부터 유래된 원형질체를 형질전환하고 정제된 형질전환체를 선별하기 위한 고 처리량 방법을 제공함으로써 상기 한계를 극복하는 것이다. 일반적으로, 본 발명에 기술된 방법 및 시스템은 사상균류 세포로부터의 원형질체의 제조, 제조된 원형질체의 형질전환, 원형질체 제조를 위해 균사를 제조하는 데 사용된 성장 조건을 변경함으로써 단일 핵을 함유하는 원형질체의 정제를 수반한다. 균주 정제는 선택 및 카운터 선택, 및 선택적으로 정확한 표현형을 보유하는 정제된 형질전환체의 선별 및/또는 관심 생성물의 생산을 통해 성취된다. 관심 생산물은 원하는 수율, 생산성 또는 역가로 생산될 수 있다. 바람직하게는, 원형질체가 사용되지만, 이 방법은 다른 균류 세포 유형에도 적용 가능하다. 일부 경우에, 본 발명에 제공된 방법 및 시스템은 처리량이 높다. 일부 경우에, 본 발명에 제공된 방법 및 시스템은 반 자동화(예를 들어, 형질전환 또는 선택, 카운터 선택) 단계를 포함한다. 일부 경우에, 본 발명에 제공된 방법 및 시스템은 완전 자동화 단계를 포함한다. 일부 경우에, 본 발명에 제공된 방법 및 시스템은 처리량이 높고, 그 단계가 반 자동화(예를 들어, 형질전환 또는 선택, 카운터 선택) 또는 완전 자동화이다. 본 발명에 사용된 바와 같이, 고 처리량은 하루에 약 1,000개 이상의 형질전환체를 평가할 수 있는 본 발명에 제공된 임의의 부분 또는 완전 자동화 방법을 의미할 수 있고, 특히 하루에 5,000개 이상의 형질전환체를 평가할 수 있는 방법 및 가장 특히 하루에 10,000개 이상의 형질전환체를 평가할 수 있는 방법을 의미할 수 있다. 또한, 방법이 수행되는 적합한 부피는 상업적으로 이용 가능한(깊은 웰) 미세적정 플레이트의 부피, 즉 1ml보다 작고, 바람직하게는 500ul보다 작고, 보다 바람직하게는 250ul보다 작고, 가장 바람직하게는 1.5ul 내지 250ul이고, 여전히 가장 바람직하게는 10ul 내지 100ul이다.
원형질체를 제조하는데 사용되는 사상균류 세포는 이의 홀로모프, 텔레모프 또는 아나모프를 포함하는 당업계에 공지되거나 본 발명에 기술된 임의의 사상균류 균주일 수 있다. 원형질체의 제조는 본 발명에 기술되거나 원형질체 제조를 위한 당업계의 임의의 공지된 방법을 사용하여 수행될 수 있다.
원형질체의 형질전환은 본 발명에서 제공되는 바와 같이 사상균류 게놈에서 소정의 유전자좌로 통합되도록 디자인된 적어도 하나의 폴리뉴클레오타이드에 의해 일어날 수 있다. 한 바람직한 실시태양에서, 원형질체는 본 발명에 제공된 바와 같이 적어도 2개의 폴리뉴클레오타이드로 공동 형질전환되어 각각의 폴리뉴클레오타이드 구조체는 사상균류 게놈 내의 상이한 소정의 유전자좌로 통합되도록 디자인된다. 소정의 유전자좌는 표적 사상균류 유전자(예를 들어, 단백질 생성물의 유전자가 시트르산 생산에 관여한다) 또는 사상균류 게놈에 존재하는 선별 가능한 마커 유전자에 대한 것일 수 있다. 본 발명에 제공된 방법 또는 시스템을 사용하여 원형질체를 형질전환하거나 공동 형질전환시키는 데 사용하기 위한 폴리뉴클레오타이드는 돌연변이 및/또는 유전자 제어 요소(들)를 포함하거나 함유하는 표적 사상균류 유전자(예를 들어, 단백질 생성물의 유전자가 시트르산 생산에 관여한다)의 서열을 포함할 수 있다. 돌연변이는 단일 뉴클레오타이드 다형성, 서열 삽입, 결실, 역위 및 다른 서열 교체와 같은 작은 핵 다형성일 수 있다. 유전자 제어 요소는 프로모터 서열(내인성 또는 이종성) 및/또는 터미네이터 서열(내인성 또는 이종성)일 수 있다. 프로모터는 유도성일 수 있다. 본 발명에 제공된 방법 또는 시스템을 사용하여 원형질체를 형질전환 또는 공동-형질전환에 사용하기 위한 폴리뉴클레오타이드는 선별 가능한 마커 유전자의 서열을 포함할 수 있다. 본 발명에 제공된 방법 또는 시스템을 사용하여 원형질체를 형질전환 또는 공동-형질전환에 사용하기 위한 폴리뉴클레오타이드는 폴리뉴클레오타이드의 각각의 개별 부분이 형질전환된 원형질체의 게놈에서 동일한 표적 부위에서 통합되는 경우에만 형질전환된 원형질체에 전체 폴리뉴클레오타이드의 통합이 발생하도록 둘 이상의 부분으로 분리될 수 있다 폴리뉴클레오타이드의 각 부분은 본 발명에 제공된 바와 같은 돌연변이 및/또는 유전자 제어 요소를 포함할 수 있다. 한 실시태양에서, 본 발명에 제공된 방법 및 시스템은 2개의 폴리뉴클레오타이드에 의한 본 발명에 제공된 원형질체의 공동-형질전환을 필요로 하며 제 1 폴리뉴클레오타이드는 돌연변이 및/또는 유전자 제어 요소(들)를 포함하거나 함유하는 표적 사상균류 유전자(예를 들어, 단백질 생성물의 유전자가 시트르산 생산에 관여한다)의 서열을 포함하는 반면, 제 2 폴리뉴클레오타이드는 선택 가능한 마커 유전자의 서열을 포함한다. 이 실시태양에 덧붙여, 제 2 폴리뉴클레오타이드는 원형질체 게놈에서 추가 선택 가능한 마커 유전자로 통합되도록 디자인될 수 있는 반면, 제 1 폴리뉴클레오타이드는 표적 사상균류 유전자에 대한 유전자좌 또는 선택적으로 추가 선택 가능한 마커 유전자의 유전자좌로 통합되도록 디자인될 수 있다. 본 발명에 제공되는 임의의 실시태양에서 선택 가능한 마커 유전자는 본 발명에 기재된 임의의 선택 가능한 마커 유전자일 수 있다.
또한, 본 발명의 목적은 사상균류 세포로부터 복수의 원형질체를 제조하고 저장하는 방법을 제공하는 것이다. 이 방법은 균류 배양액의 사상균류 세포로부터 세포벽을 제거하는 단계, 원형질체를 분리하는 단계, 분리된 원형질체를 적어도 다이메틸 설폭사이드(DMSO)를 포함하는 혼합물에 재현탁하는 단계 및 분리된 원형질체를 저장하는 단계를 필요로 할 수 있다. 저장은 적어도 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 또는 24시간 동안 일 수 있다. 저장은 적어도 1, 7, 14, 30일 이상 동안 일 수 있다. 저장은 적어도 3, 6, 12개월 이상 동안 일 수 있다. 저장은 4, -20 또는 -80℃에서 일 수 있다. 균류 배양액은 적어도 500ml, 1리터, 2리터, 3리터, 4리터 또는 5리터 부피의 배양액일 수 있다. 사상균류 세포는 본 발명에 제공되거나 당업계에 공지된 임의의 사상균류일 수 있다. 원형질체의 제조 전에, 균류 배양액은 적어도 6, 8, 10, 12, 14, 16, 18, 20, 22 또는 24시간 동안 배양될 수 있다. 한 실시태양에서, 균류 배양액은 원형질체의 제조 후 적어도 70%의 원형질체가 균질 성인 조건하에서 성장된다. 다른 실시태양에서, 세포벽을 제거하는 단계는 효소 소화에 의해 수행된다. 효소 소화는 베타-글루카나제 및 폴리갈락투로나제를 포함하는 효소의 혼합물로 수행될 수 있다. 효소 소화는 비노테이스트(VinoTaste) 농축액으로 수행될 수 있다. 또 다른 실시태양에서, 상기 방법은 원형질체를 저장하기 전에 DMSO를 포함하는 혼합물에 폴리에틸렌 글리콜(PEG)을 첨가하는 단계를 더 포함한다. PEG는 50%, 40%, 30%, 20%, 15%, 10%, 5% 이하의 최종 농도로 첨가될 수 있다. 또 다른 실시태양에서, 상기 방법은 원형질체를 저장하기 전에 상기 원형질체를 미세적정 플레이트에 분배하는 단계를 더 포함한다. 미세적정 플레이트는 6웰, 12웰, 24웰, 96웰, 384웰 또는 1536웰 플레이트일 수 있다.
유전자 디자인 및 미생물 조작: 한 벌의 HTP 분자 도구 및 HTP 유전자 디자인 라이브러리를 이용하는 균주 개량에 대한 체계적인 조합 접근법
상기한 바와 같이, 본 발명은 균주를 통한 유전자 변화의 반복적인 체계적 도입 및 제거를 통해 미생물을 조작하기 위한 신규한 HTP 플랫폼 및 유전자 디자인 전략을 제공한다. 이 플랫폼은 HTP 유전자 디자인 라이브러리의 생성을 가능하게 하고 소정의 숙주 균주 속에 유전자 변이의 효율적 수행을 허용하는 한 벌의 분자 도구에 의해 지원된다.
본 발명의 HTP 유전자 디자인 라이브러리는 특정 미생물(예를 들어, 사상균류) 균주 배경 속에 도입될 수 있는 가능한 유전자 변형의 공급원으로 작용한다. 이러한 방식으로, HTP 유전자 디자인 라이브러리는 소정의 미생물 균주의 초기 또는 추가 조작에 적용될 수 있는 유전자 다양성의 저장소 또는 유전자 교란의 집합이다. 숙주 균주에 대한 실행을 위한 유전자 디자인을 프로그래밍하는 기술은 각각이 본 발명에 참조로 인용된 "Microbial Strain Design System and Methods for Improved Large Scale Production of Engineered Nucleotide Sequences,"이라는 명칭의 계류중인 미국 특허 출원, Serial No. 15/140,296 및 계류중인 국제 출원 Serial No PCT/US17/29725에 기술된다.
이 플랫폼에서 이용되는 HTP 분자 도구 세트는 특히 (1) 프로모터 스왑 (PRO 스왑), (2) SNP 스왑, (3) 개시/중지 코돈 교환, (4) STOP 스왑 및 (5) 서열 최적화를 포함할 수 있다. 본 발명의 HTP 방법은 또한 (6) 상위성 매핑 프로토콜을 포함하는 HTP 도구 세트의 통합/조합 사용을 지시하는 방법을 교시한다. 상기한 바와 같이, 이 한 벌의 분자 도구는 단독 또는 조합으로 HTP 유전자 디자인 숙주 세포 라이브러리의 형성을 가능하게 한다.
입증된 바와 같이, 상기한 HTP 미생물 조작 플랫폼의 내용에서 상기한 HTP 유전자 디자인 라이브러리의 이용은 유익한 "원인성" 돌연변이 또는 유전자 절편의 확인 및 통합 및 수동적 또는 해로운 돌연변이 또는 유전자 절편의 확인 및 제거를 가능하게 한다. 이 새로운 접근법은 전통적인 무작위 돌연변이유발 또는 지시된 유전자 조작으로는 달성할 수 없었던 균주 성능의 신속한 개량을 가능하게 한다. 유전자 부담의 제거 또는 유전자 부담이 없는 균주로의 유익한 변화의 통합은 추가적인 개량을 가능하게 할 수 있는 추가 무작위 돌연변이유발을 위한 새롭고 강력한 출발점을 제공한다.
일부 실시태양에서, 본 발명은 직교 유익한 변화가 돌연변이유발성 균주 계통의 다양한 이산 분지를 통해 확인됨에 따라, 이들은 또한 더 나은 실행 균주로 신속하게 통합될 수 있음을 교시한다. 이러한 돌연변이는 지시된 유전 공학 기술로 얻은 개량을 가진 균주와 같이 돌연변이유발 계통의 일부가 아닌 균주로 통합될 수 있다.
일부 실시태양에서, 본 발명은 발현 및 비 발현 유전 요소를 포함하는 다수의 이종 게놈 영역에 걸친 돌연변이의 게놈 전체 조합 효과를 분석하고 수집된 정보(예를 들어, 실험 결과)를 사용하여 균주 향상을 일으키는 것으로 예상된 돌연변이 조합을 예측한다는 점에서 공지된 균주 개량 접근법과 상이하다.
일부 실시태양에서, 본 발명은 i) 산업용 미생물 및 개시된 발명을 통한 개량에 순종하는 다른 숙주 세포, ii) 하류 분석을 위한 다양성 풀 생성, iii) 고 처리량 선별 및 대형 변이체 풀의 서열화를 위한 방법 및 하드웨어 iv) 게놈 전체 돌연변이의 시너지 효과의 기계 학습 계산 분석 및 예측을 위한 방법 및 하드웨어, 및 v) 고 처리량 균주 조작을 위한 방법.
다음 분자 도구 및 라이브러리는 예시적인 미생물의 예에 의해 논의된다. 당업자는 본 발명의 HTP 분자 툴이 진핵생물 세포 및 고차원 생명 형태를 포함하는 임의의 숙주 세포와 양립할 수 있다는 것을 인식할 것이며, 예를 들어, 동일한 원리와 과정이 사상균류 세포(예를 들어, 아스퍼길루스 니거)에 사용될 수 있다.
미생물 조작 플랫폼에서 이용되는 다양한 HTP 유전자 디자인 라이브러리의 생성을 가능하게 하는 확인된 HTP 분자 도구 세트의 각각은 이제 논의될 것이다.
1. 프로모터 스왑: 프로모터 스왑 미생물 균주 라이브러리의 유도를 위한 분자 도구
일부 실시태양에서, 본 발명은 전체 숙주 균주 표현형에 유익한 효과를 나타내기 위해 최적 발현 특성(예를 들어, 수율 또는 생산성)을 갖는 프로모터를 선별하는 방법을 교시한다.
예를 들어, 일부 실시태양에서, 본 발명은 다양한 발현 강도(예를 들어, 아래에서 논의된 프로모터 래더) 또는 뛰어난 조절 특성(예를 들어, 선택된 유전자에 대한 엄격한 조절 제어)을 나타내는 하나 이상의 프로모터를 확인 및/또는 숙주 세포 내에서 하나 이상의 프로모터의 변이체를 생성시키는 방법을 교시한다. 이들 확인된 및/또는 생성된 프로모터의 특정 조합은 프로모터 래더로서 함께 그룹화될 수 있으며, 이는 보다 상세히 이하에서 설명된다.
당해 프로모터 래더는 소정의 관심 유전자와 결합된다. 따라서, 프로모터 P1-P8(다양한 발현 강도를 나타내는 것으로 확인된 및/또는 생성된 8개의 프로모터를 나타냄)이 있고 프로모터 래더를 미생물에서 관심 단일 유전자와 결합시킨다면(즉, 소정의 표적 유전자에 작동 가능하게 연결된 소정의 프로모터에 의해 미생물을 유전적으로 조작한다), 8개 프로모터의 각 조합의 효과는 조작된 미생물이 표적 유전자와 결합된 특정 프로모터(들)를 제외하고 그렇지 않다면 동일한 유전자 배경을 갖는 것을 고려하여, 각 조합적 노력으로부터 생성되는 각각의 조작된 균주를 특성화함으로써 확인될 수 있다.
이 과정을 통해 조작되어 생성된 미생물은 HTP 유전자 디자인 라이브러리를 형성한다.
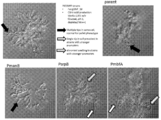
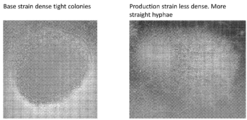
특정 실시태양에서, 본 발명에 제공된 프로모터 스와핑(PRO 스왑) 방법은 표 1에 도시된 프로모터 래더로부터의 각 프로모터를 특정 조건하에서 성장될 때 사상균류 세포의 형태에 역할을 하거나 영향을 미치는 것으로 보이거나 의심되는 유전자(표적 형태학적 유전자로 지칭됨)와 체계적으로 연관시키는 것을 수반한다. 유전자의 교란는 원하는 형태학적 표현형을 야기할 수 있다. 바람직한 표현형은 생산 배지(예를 들어, CAP 배지)의 침지 배양에서 성장할 때 비-균사, 펠렛 형태일 수 있다. 따라서, 하나가 프로모터 P1-P4(다양한 발현 강도를 나타내는 것으로 확인 및/또는 생성된 표 1로부터 4개의 프로모터를 나타냄)를 갖고 프로모터 래더를 미생물에서 관심 단일 표적 형태학적 유전자와 연관시키는 경우(즉, 주어진 표적 형태학적 유전자에 작동 가능하게 연결된 주어진 프로모터로 미생물을 유전자 조작하는 경우), 4개의 프로모터의 각 조합의 효과는 조작된 미생물이 특정 표적 형태학적 유전자와 연관된 특정 프로모터(들)를 제외하고 동일한 유전자 배경을 갖는 것을 고려하면, 각각의 조합 노력으로 인한 각각의 조작된 균주를 특성화함으로써 확인할 수 있다. 이 과정을 통해 조작된 최종 미생물은 HTP 형태학적 유전자 디자인 라이브러리를 형성할 수 있다. 사상균류 세포의 형태에 역할을 하거나 영향을 미치는 것으로 보이거나 의심되는 유전자는 당업계에 공지되고/되거나 본 발명에 제공된 임의의 유전자일 수 있다.
HTP 유전자 디자인 라이브러리는 이 과정을 통해 형성되는 실제의 물리적 미생물 균주 집합을 의미할 수 있으며, 각각의 구성원 균주는 그렇지 않다면 동일한 유전자 배경으로 특정 표적 유전자에 작동 가능하게 연결된 소정의 프로모터를 나타내며, 상기 라이브러리는 "프로모터 스왑 미생물 균주 라이브러리"로 불린다. 사상균류(예를 들어, A. 니거)의 특정 맥락에서, 라이브러리는 "프로모터 스왑 사상균류 균주 라이브러리" 또는 "프로모터 스왑 A. 니거 균주 라이브러리"로 지칭될 수 있지만, 사상균류 또는 A. 니거가 미생물 또는 다핵체 유기체의 구체적인 예이기 때문에 용어는 다음과 같이 동의어로 사용될 수 있다.
또한, HTP 유전자 디자인 라이브러리는 유전자 교란의 집합-이 경우 소정의 유전자에 작동 가능하게 연결된 소정의 프로모터 x)을 의미할 수 있으며-상기 집합은 "프로모터 스왑 라이브러리"로 불린다.
또한, 미생물을 조작하기 위해 프로모터 P1-P8을 포함하는 동일한 프로모터 래더를 이용할 수 있으며, 여기서 8개의 프로모터의 각각은 10개의 상이한 유전자 표적에 작동 가능하게 연결된다. 이 절차의 결과는 관심 표적 유전자에 작동 가능하게 연결된 특정 프로모터를 제외하고, 그렇지 않다면 유전적으로 동일하게 간주되는 80개의 미생물이 될 것이다. 이런 80개 미생물은 적절하게 선별되고 특징화되고 다른 HTP 유전자 디자인 라이브러리를 생성한다. HTP 유전자 디자인 라이브러리에서 미생물 균주의 특성화는 관계형 데이터베이스, 객체 지향 데이터베이스 또는 고도로 분산된 NoSQL 데이터베이스를 포함하여 임의의 데이터 저장 구조물에 저장될 수 있는 정보와 데이터를 생성한다. 이 데이터/정보는, 예를 들어, 소정의 유전자 표적에 작동 가능하게 연결된 경우 소정의 프로모터(예를 들어, P1-P8) 효과일 수 있다. 이 데이터/정보는 또한 둘 이상의 프로모터 P1-P8을 소정의 유전자 표적에 작동 가능하게 연결시킴으로써 초래하는 광범위한 세트의 조합적 효과일 수 있다.
8개 프로모터 및 10개 표적 유전자의 상기 예는 개념이 다양한 발현 강도 및 임의의 소정 수의 표적 유전자의 제시에 기초하여 함께 그룹화된 임의의 소정의 수의 프로모터와 함께 적용될 수 있기 때문에, 단지 예시적이다. 당업자는 또한 임의의 유전자 표적 앞에서 둘 이상의 프로모터를 작동 가능하게 연결시키는 능력을 인식할 것이다. 따라서, 일부 실시태양에서, 본 발명은 프로모터 래더로부터의 1, 2, 3개 이상의 프로모터가 하나 이상의 유전자에 작동 가능하게 연결된 프로모터 스왑 라이브러리를 교시한다.
요약하면, 유기체에서 다양한 유전자의 발현을 유도하는 다양한 프로모터를 이용하면 관심 형질을 최적화하는 강력한 수단이다. 본 발명자들이 개발한 프로모터 스와핑의 분자 도구는 적어도 하나의 조건하에서 적어도 하나의 유전자좌의 발현을 변화시키는 것으로 입증된 프로모터 서열의 래더(예를 들어, 표 1)를 사용한다. 그런 다음 이 래더는 고 처리량 게놈 공학을 사용하여 유기체에서 유전자 그룹(예를 들어, 본 발명에 제공된 FungiSNP_18과 동일한 경로 내에서)에 체계적으로 적용된다. 이 유전자 그룹은 여러 가지 방법의 임의의 하나를 기초로 한 관심 형질에 영향을 줄 가능성을 갖는 것으로 결정된다. 이것은 공지된 기능에 기초한 선택 또는 관심 형질에 대한 영향 또는 이전에 결정된 유익한 유전자 다양성에 기초한 알고리즘 선택을 포함할 수 있다. 일부 실시태양에서, 유전자의 선택은 소정의 숙주 내 모든 유전자를 포함할 수 있다. 다른 실시태양에서, 유전자의 선택은 무작위로 선택된 소정의 숙주 내 모든 유전자의 서브세트일 수 있다.
유전자에 연결된 프로모터 서열을 함유하는 생물의 생성된 HTP 유전자 디자인 미생물 균주 라이브러리는 고 처리량 선별 모델에서 성능에 대해 평가되고, 증가 된 성능을 유도하는 프로모터-유전자 연관이 결정되고, 정보가 데이터베이스에 저장된다. 유전자 교란의 집합(즉, 소정의 유전자 y에 작동 가능하게 연결된 소정의 프로모터 x)은 "프로모터 스왑 라이브러리"를 형성하며, 이는 미생물 공학 처리에 이용될 잠재적인 유전자 교란의 공급원으로서 이용될 수 있다. 시간이 지남에 따라, 유전자 교란의 더 큰 세트가 더 큰 다양성의 숙주 세포 배경에 대해 실행되기 때문에, 각 라이브러리는 임의의 관심 배경에 대한 표적화된 변화를 더욱 정확하고 예측되게 디자인하는데 사용될 수 있는 실험적으로 확인된 데이터의 모음으로서 더욱 강력해진다.
유기체에서 유전자의 전사 수준은 유기체 행동에 영향을 미치는 제어의 핵심 포인트이다. 전사는 번역(단백질 발현)과 밀접하게 연관되며, 어떤 단백질은 유기체의 행동을 결정하는 양에서 발현된다. 세포는 수천 가지의 서로 다른 유형의 단백질을 발현하며, 이러한 단백질은 복잡한 복합적인 방식으로 상호작용하여 기능을 생성한다. 단백질 세트의 발현 수준을 체계적으로 변화시킴으로써, 기능이 복잡성으로 인해 예측하기 어렵도록 변형될 수 있다. 일부 변경은 성능을 증가시킬 수 있고 성능을 평가하기 위한 메커니즘과 연관되어, 이 기술은 개량된 기능을 가진 유기체의 생성을 가능하게 한다.
소분자 합성 경로의 상황에서, 효소는 기질로 시작하여 관심 소형 분자로 끝나는 직선 또는 가지 사슬에 있는 소형 분자 기질 및 생성물을 통해 상호작용한다. 이러한 상호작용이 순차적으로 연결되기 때문에, 이 시스템은 분산된 제어를 나타내며, 하나의 효소의 발현을 증가시키면 다른 효소가 속도 제한될 때까지만 경로 유속을 증가시킬 수 있다.
대사 조절 분석(MCA)은, 실험 데이터 및 제 1 원리로부터, 어느 효소 또는 효소들이 속도를 제한하는지를 결정하는 방법이다. 그러나, MCA는 새로운 속도 제한 효소를 결정하기 위한 각 발현 수준 변경 후에 광범위한 실험이 필요하기 때문에 제한적이다. 프로모터 스와핑은 이러한 상황에서 유리한데, 이는 이 경로에서 각 효소에 대한 프로모터 래더의 적용을 통해, 제한 효소가 발견되고, 속도 제한이 되는 새로운 효소를 찾기 위해 동일한 과정을 수행될 수 있기 때문이다. 또한, 기능에 대한 판독은 관심 소형 분자의 더 나은 생산이기 때문에, 어떤 효소가 제한되는지 결정하는 실험은 생산을 늘리는 공학과 동일하여, 개발 시간을 단축시킨다. 일부 실시태양에서, 본 발명은 다중 단위 효소의 개별 서브유닛을 암호화하는 유전자에 대한 PRO 스왑의 적용을 교시한다. 또 다른 실시태양에서, 본 발명은 개개의 효소 또는 전체 생합성 경로를 조절할 책임이 있는 유전자에 PRO 스왑 기술을 적용하는 방법을 교시한다.
일부 실시태양에서, 본 발명의 프로모터 스왑 도구는 선택된 유전자 표적의 최적 발현을 확인하는데 사용된다. 일부 실시태양에서, 프로모터 스왑의 목표는 대사 경로 또는 유전자 경로에서 병목을 감소시키기 위해 표적 유전자의 발현을 증가시키는 것일 수 있다. 다른 실시태양에서, 프로모터 스왑의 목표는 상기 표적 유전자의 발현이 요구되지 않을 때 숙주 세포에서 불필요한 에너지 소비를 피하기 위해 표적 유전자의 발현을 감소시키는 것일 수 있다.
전사, 수송 또는 신호 전달과 같은 다른 세포 시스템의 상황에서, 다양한 합리적인 방법이 사용되어 어떤 단백질이 발현 변화의 표적이고 그 변화가 무엇이어야하는지를 선험적으로 시험하고 밝혀낼 수 있다. 이러한 합리적인 방법은 성능 개량을 위해 테스트해야하는 교란의 수를 줄이지만, 상당한 비용이 든다. 유전자 결실 연구는 이의 존재가 특정 기능에 필수적인 단백질을 확인하고 중요한 유전자는 과다 발현될 수 있다. 단백질 상호작용의 복잡성으로 인해, 성능을 향상시키는데 종종 효과가 없다. 세포에서 단백질 수준의 함수로서, 첫 번째 원칙으로부터, 전사 또는 신호전달 행동을 기술하려고 시도하는 다양한 유형의 모델이 개발되었다. 이러한 모델은 종종 발현 변화가 상이한 기능이나 개량된 기능으로 이어질 수 있는 표적을 제안한다. 이 모델의 기초가 되는 가설은 단순하고 매개변수는 측정하기가 어려워서, 특히 비-모델 유기체에 대해 이런 모델이 한 예측은 종종 부정확하다. 유전자 삭제와 모델링 모두에 의해, 어떻게 특정 유전자에 영향을 미치는 지를 결정하는데 필요한 실험은 성능을 개량시키는 변화를 만드는 후속 작업과는 상이하다. 프로모터 스와핑은 이러한 어려움을 회피하는데, 이는 특정 교란의 중요성을 강조하는 구성된 균주가 이미 개량된 균주이기 때문이다.
따라서, 특정 실시태양에서, 프로모터 스와핑은 다음을 포함하는 다단계 공정이다:
1. "래더"로서 작용하는 "x" 프로모터의 세트를 선택하는 단계. 이상적으로 이런 프로모터는 다수의 게놈 유전자좌 전체에서 매우 가변적인 발현을 유도하는 것으로 나타났지만, 유일한 요구조건은 일부 유전자 발현을 교란시키는 것이다.
2. 표적화하기 위한 "n" 유전자의 세트를 선택하는 단계. 이 세트는 게놈의 모든 오픈 리딩 프레임(ORF) 또는 ORF의 서브세트일 수 있다. 서브세트는 기능과 관련된 ORF에 대한 주석을 사용하고, 이전에 입증된 유익한 교란(이전 프로모터 스왑 또는 이전 SNP 스왑)에 대한 관계에 의해, 이전에 생성된 교란 사이의 상위성 상호작용에 기초한 알고리즘 선택에 의해, 표적에 대한 유익한 ORF에 관한 가설에 기초한 다른 선택 기준 또는 무작위 선택을 통해 선택될 수 있다. 다른 실시태양에서, "n" 표적 유전자는 비-암호화 RNA를 포함하는 비-단백질 암호화 유전자를 포함할 수 있다. 한 실시태양에서, "n" 유전자의 세트는 S. 세레비시애 SLN1 유전자의 오쏘로그 및 동일한 경로의 일부인 하나 이상의 유전자의 오쏘로그일 수 있다. S. 세레비시애 SLN1 유전자 및 동일한 경로의 일부인 하나 이상의 유전자의 오쏘로그는 상기 유전자의 야생형 또는 의 돌연변이 형태일 수 있다. 한 실시태양에서, 사상균류 균주 또는 숙주 세포는 A. 니거이고, 선택된 "n" 유전자 세트는 표 4의 SNP이다. 다른 실시태양에서, A. 니거는 숙주 세포, "n" 세트 선택된 유전자는 표 4의 SNP 함유 유전자의 비-SNP 또는 야생형 버전이다. A. 니거가 숙주 세포인 경우, "n" 유전자 세트는 동일한 경로의 일부인 하나 이상의 유전자 이외에 표 4에서 발견된 FungiSNP_9에 대한 유전자일 수 있다. A. 니거가 숙주 세포인 경우, "n" 유전자 세트는 동일한 경로의 일부인 하나 이상의 유전자 외에 표 4에서 발견된 FungiSNP_12에 대한 유전자일 수 있다. A. 니거가 숙주 세포인 경우, "n" 유전자 세트는 동일한 경로의 일부인 하나 이상의 유전자 이외에 표 4에서 발견된 FungiSNP_40에 대한 유전자일 수 있다. 바람직한 실시태양에서, A. 니거가 숙주 세포인 경우, "n" 유전자 세트는 동일한 경로의 일부인 하나 이상의 유전자 이외에 표 4의 FungiSNP_18에 대한 유전자(즉, S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그의 돌연변이 형태)일 수 있다. S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그 및/또는 동일한 경로의 하나 이상의 유전자는 유전자의 야생형 또는 돌연변이 형태일 수 있다. S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그의 돌연변이 형태는 SEQ ID NO: 13을 갖는 형태일 수 있다. 경로에서 하나 이상의 유전자는 S. 세레비지애 Ypd1, Skn7, Ssk1 및 Ssk2 유전자 또는 이들의 임의의 조합의 A. 니거 오르쏘로그일 수 있다. 동일한 경로의 일부인 하나 이상의 유전자는 SEQ ID NO: 15, 16, 17, 18, 19 또는 이들의 임의의 조합으로 표시되는 핵산 서열로부터 선택될 수 있다.
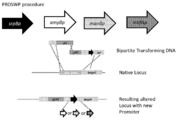
3. 다음과 같은 유전자 변형을 신속하게- 및 일부 실시태양에서, 병렬-수행하는 고 처리량 균주 조작 단계: 천연 프로모터가 표적 유전자 n의 앞에 존재하고 이의 서열이 알려질 때, 천연 프로모터를 래더에 있는 x 프로모터의 각각으로 대체한다. 천연 프로모터가 존재하지 않거나 이의 서열이 알려지지 않을 때, 유전자 n의 앞에 있는 래더에 x 프로모터의 각각을 삽입한다(예를 들어, 도 10 참조). 이러한 방식으로, 균주의 "라이브러리"(HTP 유전자 디자인 라이브러리라고도 불림)가 구성되며, 라이브러리의 각 구성원은 그렇지 않으면 동일한 유전자 상황에서, n 표적에 작동 가능하게 연결된 x 프로모터의 한 예이다. 상기한 바와 같이, 프로모터의 조합이 삽입되어 라이브러리가 구성되는 조합 가능성의 범위를 확장시킬 수 있다.
4. 하나 이상의 메트릭에 대한 성능이 최적화되는 성능을 나타내는 상황에서 균주의 라이브러리의 고 처리량 선별 단계.
이 기본 과정은 특히 다음과 같은 방법으로 균주 성능에 추가 개량을 제공하는데 확장될 수 있다: (1) 반복 과정에서 한 번에 하나씩 또는 단일 단계에서 다중 변화로서 단일 균주 배경 속에 다수의 유익한 교란을 통합하는 단계. 다중 교란은 정의된 변경의 특정 세트 또는 부분적으로 무작위화된 조합 라이브러리의 변화일 수 있다. 예를 들어, 표적 세트가 한 경로의 모든 유전자인 경우, 이전 라이브러리 균주의 개량된 구성원 또는 구성원들 속으로 교란의 라이브러리의 순차적 재생은 어느 유전자가 임의의 소정의 반복에서 속도를 제한하는지와 관계없이 한 경로에서 각 유전자의 발현 수준을 최적화할 수 있다; (2) 각 교란의 상호작용에 기초하여 최적의 교란 세트를 예측하기 위해 그 데이터를 사용하는 알고리즘 속에 라이브러리의 개별 및 조합 생성으로부터 성능 데이터를 제공하는 단계; 및 (3) 위의 두 접근법의 조합을 실행하는 단계.
상기 논의된 분자 도구 또는 기술은 프로모터 스와핑으로서 특징화되지만, 프로모터에 제한되지 않으며 표적 세트의 발현 수준을 체계적으로 변화시키는 다른 서열 변화를 포함할 수 있다. 한 세트의 유전자의 발현 수준을 변화시키는 다른 방법은 다음을 포함할 수 있다: a) 리보좀 결합 부위의 래더(또는 진핵생물에서 코작 서열); b) 각각의 표적의 개시 코돈을 각각의 다른 개시 코돈으로 대체하는 단계(즉, 아래 논의된 개시/정지 코돈 교환); c) 다양한 mRNA 안정화 또는 불안정화 서열을 전사체의 5' 또는 3' 말단 또는 임의의 다른 위치에 부착하는 단계; d) 단백질 내의 임의의 위치에 다양한 단백질 안정화 또는 불안정화 서열을 부착하는 단계.
이 접근법은 산업용 미생물에 의해 본 발명에서 예시되었지만, 원하는 형질이 유전자 돌연변이 집단에서 동정될 수 있는 임의의 유기체에 적용 가능하다. 예를 들어, 이것은 CHO 세포, 효모, 곤충 세포, 조류뿐만 아니라 식물과 같은 다세포 유기체의 성능을 개량시키는데 사용될 수 있다.
2. SNP 스왑 : SNP 스왑 미생물 균주 라이브러리 유도를 위한 분자 도구
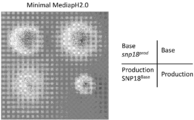
특정 실시태양에서, SNP 스와핑은 미생물 균주를 개량하기 위한 무작위 돌연변이유발 접근법이 아니라 오히려 균주 전체에서 개별 소핵 다형질 뉴클레오타이드 돌연변이(즉, SNP)의 체계적 도입 또는 제거(즉, "SNP 스와핑")를 필요로 한다. 도 9는 본 발명의 사상균류 세포에서 SNP 스와핑 라운드를 개념적으로 도시한다. 사상균류 세포에서 SNP 스와핑의 유용성의 입증이 도 42에 도시되어있다.
한 실시태양에서, 본 발명에 제공된 방법 및 시스템은 개별 SNP 또는 SNP의 조합과 함께 사상균류 포함하는 사상균류 라이브러리를 생성하기 위해 SNP 스와핑에 이용된다. 조합 SNP 스와핑은 도 37에 도시된 바와 같이 이분자 변환을 사용하여 달성될 수 있다.
이 과정을 통해 조작된 미생물은 HTP 유전자 디자인 라이브러리를 형성한다.
HTP 유전자 디자인 라이브러리는 이 과정을 통해 형성된 실제의 물리적 미생물 균주 집합을 의미할 수 있으며, 각각의 구성원 균주는 그렇지 않으면 동일한 유전자 배경에서 소정의 SNP의 존재 또는 부재를 나타내며, 상기 라이브러리는 "SNP 스왑 미생물 균주 라이브러리"로 불린다. 사상균류(예를 들어, A. 니거)의 특정 맥락에서, 라이브러리는 "SNP 스왑 사상균류 균주 라이브러리" 또는 "SNP 스왑 A. 니거 균주 라이브러리"로 지칭될 수 있지만, 사상균류는 미생물 또는 다핵체 유기체의 구체적인 예이기 때문에 용어는 다음과 같이 동의어로 사용될 수 있다.
또한, HTP 유전자 디자인 라이브러리는 유전자 교란의 집합을 의미할 수 있으며-이 경우 소정의 SNP가 존재하거나 존재하지 않는다-상기 집합은 "SNP 스왑 라이브러리"로 불린다.
일부 실시태양에서, SNP 스와핑은 확인된 유익한 성능 효과를 가진 표적 SNP "빌딩 블록"의 최적 조합에 의한 숙주 유기체의 재구성을 필요로 한다. 따라서, 일부 실시태양에서, SNP 스와핑은 다수의 유익한 돌연변이를 반복 과정에서 한 번에 하나씩 또는 단일 단계에서 다중 변화로서 단일 균주 배경 속에 다수의 유익한 교란을 통합하는 단계를 필요로 한다. 다중 변화는 정의된 변화의 특정한 세트 또는 돌연변이의 부분적으로 무작위화된 라이브러리일 수 있다.
다른 실시태양에서, SNP 스와핑은 또한 반복 과정에서 한 번에 하나씩 또는 단일 단계에서 다중 변화로서 균주로부터 유해한 것으로 확인된 다중 돌연변이를 제거하는 단계를 필요로 한다. 다중 변화는 정의된 변화의 특정한 세트 또는 돌연변이의 부분적으로 무작위화된 라이브러리일 수 있다. 일부 실시태양에서, 본 발명의 SNP 스와핑 방법은 유익한 SNP의 첨가 및 유해 및/또는 중성 돌연변이의 제거를 모두 포함한다.
SNP 스와핑은 개량된 관심 형질에 대한 돌연변이유발 및 선택에 영향을 받은 균주의 계통에서 유익한 및 유해한 돌연변이 둘 다를 확인하고 이용하기 위한 강력한 도구이다. SNP 스와핑은 돌연변이유발성 계통에서 개별 돌연변이의 영향을 체계적으로 결정하기 위해 고 처리량 게놈 공학 기술을 사용한다. 게놈 서열은 알려진 성능 개량을 갖는 돌연변이유발성 계통의 하나 이상의 세대에 걸쳐 균주에 대해 결정된다. 고 처리량 게놈 공학은 초기 계통 균주에서 개량된 균주로부터 돌연변이를 반복하고, 및/또는 나중 균주의 돌연변이를 초기 균주 서열로 되돌리는데 체계적으로 사용된다. 이들 균주의 성능을 평가하고 개량된 관심 표현형에 대한 각각의 개별 돌연변이의 기여가 결정될 수 있다. 상기한 바와 같이, 이 과정으로부터 초래된 미생물 균주는 분석되고/특성화되어, 숙주 균주 전체에서 미생물 균주 개량을 알릴 수 있는 SNP 스왑 유전자 디자인 라이브러리의 기초를 형성한다.
유해한 돌연변이의 제거는 즉각적인 성능 개량을 제공할 수 있고, 돌연변이유발 부담이 없는 균주 배경에 유익한 돌연변이의 통합은 균주 성능을 신속하고 크게 개량시킬 수 있다. SNP 스와핑 과정을 통해 생산된 다양한 미생물 균주는 HTP 유전자 디자인 SNP 스와핑 라이브러리를 형성하는데, 이는 다양한 추가/삭제/또는 통합된 SNP를 포함하지만 그렇지 않으면 동일한 유전자 배경을 가진 미생물 균주이다.
이전에 논의된 바와 같이, 성능 개량을 위한 무작위 돌연변이유발 및 후속 선별은 산업용 균주 개량을 위해 일반적으로 사용되는 기술이며, 대규모 제조에 현재 사용되는 많은 균주가 수년의 기간, 때때로 10년에 걸쳐 반복적으로 이 공정을 사용하여 개발되었다. UV 복사에너지 또는 에틸 메테인설포네이트와 같은 돌연변이유발 화학물질에 대한 노출과 같은 게놈 돌연변이를 생성하는 무작위 접근법은 다음과 같은 이유로 산업용 균주 개량에 바람직한 방법이었다: 1) 산업용 유기체는 유전적으로 또는 대사적으로 특성이 좋지 않을 수 있으므로 지시된 개량 접근법에 대한 표적 선택을 어렵거나 불가능하게 한다; 2) 비교적 잘 특성화된 시스템에서도, 산업용 성능 개선을 초래하는 변화는 예측하기 어렵고 알려진 기능이 없는 유전자의 교란을 필요로 할 수 있다. 3) 소정의 산업용 유기체에서 지시된 게놈 돌연변이를 만들기 위한 유전자 도구는 사용할 수 없거나 매우 느리거나 및/또는 사용하기 어렵다.
그러나, 상기 방법의 상기 이점에도 불구하고, 다수의 공지된 단점이 있다. 유익한 돌연변이는 비교적 드문 사건이며, 고정된 선별 용량으로 이러한 돌연변이를 찾기 위해서는, 돌연변이 속도가 충분히 높아야 한다. 이것이 원치 않는 중성 및 부분적으로 해로운 돌연변이가 유익한 변화와 함께 균주에 통합되는 것을 초래한다. 시간이 지남에 따라 이런 '돌연변이유발 부담'은 증가되어, 전반적인 견고함과 성장 속도와 같은 주요 형질이 결핍된 균주를 초래한다. 궁극적으로 '돌연변이유발 부담'은 무작위 돌연변이유발을 통한 성능의 개량을 얻기가 점차 더 어렵거나 불가능하게 한다. 적절한 도구가 없다면, 균주 계통의 다른 및 유사한 부문에서 발견된 유익한 돌연변이를 통합하는 것은 불가능하다.
SNP 스와핑은 돌연변이유발 계통 내의 균주를 비교할 때 관찰된 일부 또는 모든 돌연변이를 체계적으로 반복하거나 회귀시킴으로써 이러한 제한을 극복하는 접근법이다. 이 방법으로 유익한('원인성') 돌연변이가 확인되고 통합될 수 있으며 및/또는 해로운 돌연변이가 확인되고 제거될 수 있다. 이것은 추가 무작위 돌연변이유발 또는 표적화된 유전자 공학에 의해 달성될 수 없는 균주 성능의 신속한 개량을 허용한다.
유전자 부담의 제거 또는 유전자 부담이 없는 균주로의 유익한 변화의 통합은 추가 개량을 가능하게 할 수 있는 추가의 무작위 돌연변이유발을 위한 새롭고 견고한 출발점을 제공한다.
또한, 수직 유익한 변화가 돌연변이유발성 균주 계통의 다양하고, 구별된 분지를 통해 확인되므로, 이들 균주는 보다 우수한 실행 균주로 신속하게 통합될 수있다. 이런 돌연변이는 지시된 유전 공학에 의해 얻은 개량을 가진 균주와 같이 돌연변이유발 계통의 일부가 아닌 균주로 통합될 수 있다.
돌연변이유발 계통 내에서 균주 간의 돌연변이를 무작위로 재조합시키는 다른 접근법 및 기술이 존재한다. 이들은 원형질체 융합 및 돌연변이 균주 전체에서 게놈 재조합을 촉진하는 전체 게놈 셔플링과 같은 기술을 포함한다. 효모 및 사상 균류와 같은 일부 산업용 미생물의 경우, 자연 교배 주기가 쌍을 이루는 게놈 재조합에 이용될 수 있다. 이런 식으로, 해로운 돌연변이는 부모 균주에 의한 "백-크로싱(back-crossing)"에 의해 제거될 수 있고 유익한 돌연변이는 통합될 수 있다. 그러나, 이런 접근법은 본 발명의 SNP 스와핑 방법을 사용하여 우회되는 많은 제한을 받는다.
예를 들어, 이런 접근법은 돌연변이를 교환하기 위해 상대적으로 적은 수의 무작위 재조합 크로스오버 사건에 의존하기 때문에, 균주 성능을 최적화하기 위해 재조합 및 선별의 많은 사이클을 필요로 할 수 있다. 또한, 자연 재조합 사건은 본질적으로 무작위이지만, 이것은 게놈 위치 편향에 영향을 받고 일부 돌연변이는 해결하기 어려울 수 있다. 이런 접근법은 추가 게놈 서열 분석 및 분석 없이 개별 돌연변이의 영향에 대한 정보도 거의 제공하지 않는다. SNP 스와핑은 무작위적인 접근 방식이 아니기 때문에 이러한 근본적인 한계를 극복하기보다는 오히려 균주 전체에서 개별 돌연변이의 체계적인 도입 또는 제거이기 때문에 이런 근보적인 제한을 극복한다.
일부 실시태양에서, 본 발명은 다양성 풀의 유기체들 사이에 존재하는 SNP 서열 다양성을 확인하는 방법을 교시한다. 다양성 풀은 분석을 위해 사용된 소정의 수 n의 미생물일 수 있으며, 상기 미생물의 게놈은 "다양성 풀"을 나타낸다.
특정 양태에서, 다양성 풀은 특정 시점(S1Gen1)에서 "기준선" 또는 "표준" 유전자 서열을 갖는 본래의 부모 균주(S1) 및 상기 S1 균주로부터 유도/성장되고 S1의 기준선 게놈과 관련하여 다른 게놈(S2- n Gen2- n )을 갖는 임의의 수의 후속 자손 균주(S2- n )일 수 있다.
예를 들어, 일부 실시태양에서, 본 발명은 다양성 풀에서 미생물 게놈을 서열화하여 각 균주에 존재하는 SNP를 확인하는 것을 교시한다. 한 실시태양에서, 다양성 풀의 균주는 역사적인 미생물 생산 균주이다. 따라서, 본 발명의 다양성 풀은 예를 들어 산업용 표준 균주 및 전통적인 균주 개량 프로그램을 통해 생산된 하나 이상의 돌연변이 산업용 균주를 포함할 수 있다.
일부 실시태양에서, 다양성 풀 내의 SNP는 "표준 균주"를 참조하여 결정된다. 일부 실시태양에서, 표준 균주는 야생형 균주이다. 다른 실시태양에서, 표준 균주는 임의의 돌연변이유발을 받기 전에 원래의 산업용 균주이다. 표준 균주는 실무자에 의해 정의될 수 있으며 원래의 야생형 균주 또는 원래의 산업용 균주일 필요는 없다. 기본 균주는 단순히 "기본", "표준" 또는 원래의 유전자 배경으로 간주 될 수 있는 것의 대표이며, 이로 인해 상기 표준 균주로부터 유도되거나 개발된 후속 균주는 비교될 것이다.
다양성 풀 내의 모든 SNPS가 확인되면, 본 발명은 개별적으로 및/또는 그룹으로 SNP의 효과(예를 들어, 관심 표현형의 생성)를 묘사(즉, 정량화 및 특성화)하기 위한 SNP 스와핑 및 선별 방법을 교시한다.
일부 실시태양에서, 본 발명의 SNP 스와핑 방법은 돌연변이된 균주(예를 들어, S 2-n Gen 2-n 으로부터 균주)에서 확인된 하나 이상의 SNP를 표준 균주(S1Gen1) 또는 야생형 균주에 도입하는 단계("웨이브 업")를 포함한다.
다른 실시태양에서, 본 발명의 SNP 스와핑 방법은 돌연변이된 균주(예를 들어, S 2-n Gen 2-n 으로부터 균주)에서 확인된 하나 이상의 SNP를 제거하는 단계("웨이브 다운")를 포함한다.
일부 실시태양에서, 하나 이상의 SNP 변화(도입 또는 제거)를 포함하는 각각의 생성된 균주는 본 발명의 하나 이상의 기준(예를 들어, 관심 화학물질 또는 생성물의 생산)하에서 배양되고 분석된다. 분석된 각 숙주 균주로부터의 데이터는 특정 SNP 또는 숙주 균주에 존재하는 SNP 그룹과 관련되거나 연관되며 미래 사용을 위해 기록된다. 따라서, 본 발명은 임의의 수의 관심 미생물 유전자 또는 표현형 형질에 대한 소정의 SNP의 효과를 확인할 수 있는 크고 고도로 주석화된 HTP 유전자 디자인 미생물 균주 라이브러리의 생성을 가능하게 한다. 이런 HTP 유전자 디자인 라이브러리에 저장된 정보는 HTP 게놈 공학 플랫폼의 기계 학습 알고리즘에 정보를 제공하고 과정의 미래 반복을 지시하여, 궁극적으로 매우 바람직한 특성/형질을 갖는 진화된 유기체를 유도한다.
3. 개시/정지 코돈 교환: 개시/정지 코돈 미생물 균주 라이브러리 유도를 위한 분자 도구
일부 실시태양에서, 본 발명은 개시 및 정지 코돈 변이체를 스와핑하는 방법을 교시한다. 예를 들어, 에스. 크레비시애(S. cerevisiae) 및 포유동물에 대한 전형적인 정지 코돈은 각각 TAA(UAA) 및 TGA(UGA)이다. 단핵구 식물의 전형적인 정지 코돈은 TGA(UGA)인 반면, 곤충과 대장균은 보통 TAA(UAA)를 정지 코돈으로 사용한다(Dalphin et al.(1996) Nucl. Acids Res. 24: 216-218). 다른 실시태양에서, 본 발명은 TAG(UAG) 정지 코돈의 사용을 교시한다.
본 발명은 스와핑 개시 코돈을 유사하게 교시한다. 일부 실시태양에서, 본 발명은 대부분의 유기체(특히, 진핵생물)에 의해 이용되는 ATG(AUG) 개시 코돈의 사용을 교시한다. 일부 실시태양에서, 본 발명은 원핵 생물이 ATG(AUG)를 가장 많이 사용하고 이어서 GTG(GUG) 및 TTG(UUG)를 사용하는 것을 교시한다.
다른 실시태양에서, 본 발명은 ATG 개시 코돈을 TTG로 대체시키는 것을 교시한다. 일부 실시태양에서, 본 발명은 ATG 개시 코돈을 GTG로 대체시키는 것을 교시한다. 일부 실시태양에서, 본 발명은 GTG 개시 코돈을 ATG로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 GTG 개시 코돈을 TTG로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 TTG 개시 코돈을 ATG로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 TTG 개시 코돈을 GTG로 대체하는 것을 교시한다.
다른 실시태양에서, 본 발명은 TAA 정지 코돈을 TAG로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 TAA 정지 코돈을 TGA로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 TGA 정지 코돈을 TAA로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 TGA 정지 코돈을 TAG로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 TAG 정지 코돈을 TAA로 대체하는 것을 교시한다. 일부 실시태양에서, 본 발명은 TAG 정지 코돈을 TGA로 대체시키는 것을 교시한다.
4. STOP
스왑
: STOP
스왑
미생물 균주 라이브러리 유도를 위한 분자 도구
일부 실시태양에서, 본 발명은 세포 유전자 전사의 최적화를 통해 숙주 세포 생산성을 개량시키는 방법을 교시한다. 유전자 전사는 전사 개시(RNAp 모집 및 전사 복합체 형성), 신장(가닥 합성/확장) 및 전사 종결(RNAp 분리 및 종결)을 포함하는 여러 별개의 생물학적 현상의 결과이다. (예를 들어, 프로모터를 변화시키거나 조절 전사 인자를 유도함으로써) 유전자의 전사 조절을 통한 유전자 발현의 제어에 많은 관심이 집중되었지만, 유전자 터미네이터 서열의 조절을 통한 전사의 조절에 대해서는 비교적 적은 노력이 있었다 .
전사가 유전자 발현 수준에 영향을 미치는 가장 명백한 방법은 프로모터 또는 인핸서 강도 및 트랜스 활성화 인자의 조합에 의해 조절될 수있는 Pol II 개시 속도를 이용하는 것이다(Kadonaga, JT. 2004 "Regulation of RNA polymerase II transcription by sequence-specific DNA binding factors" Cell. 2004 Jan 23; 116(2):247-57). 진핵생물에서, 연신율은 교차 스플라이싱에 영향을 줌으로써 유전자 발현 양상을 결정할 수있다(Cramer P. et al., 1997 "Functional association between promoter structure and transcript alternative splicing." Proc Natl Acad Sci U S A. 1997 Oct 14; 94(21):11456-60). 유전자에 대한 실패한 종결은 Pol II에 대한 프로모터의 접근성을 감소시킴으로써 하류 유전자의 발현을 손상시킬 수 있다(Greger IH. et al., 2000 "Balancing transcriptional interference and initiation on the GAL7 promoter of Saccharomyces cerevisiae." Proc Natl Acad Sci U S A. 2000 Jul 18; 97(15):8415-20). 전사 간섭으로 알려진 이 과정은 특히 진핵 생물과 관련이 있는데 이는 이들이 종종 밀접하게 이격된 유전자를 갖기 때문이다.
종결 서열은 또한 서열이 속하는 유전자의 발현에 영향을 미칠 수 있다. 예를 들어, 연구들은 진핵생물에서 비효율적인 전사 종결은 비접합 pre-mRNA의 축적을 초래한다는 것을 보여준다(West, S., and Proudfoot, N.J., 2009 "Transcriptional Termination Enhances Protein Expression in Human Cells" Mol Cell. 2009 Feb 13; 33(3-9); 354-364 참조). 다른 연구들은 또한 3'말단 처리가 비효율적인 종결에 의해 지연될 수 있다는 것을 보여주었다(West, S et al., 2008 "Molecular dissection of mammalian RNA polymerase II transcriptional termination." Mol Cell. 2008 Mar 14; 29(5):600-10.). 전사 종결은 또한 합성 부위로부터 전사체를 방출함으로써 mRNA 안정성에 영향을 미칠 수 있다.
진핵생물에서 전사 메커니즘의 종결
진핵생물에서 전사 종결은 RNA 폴리머라제 II와 관련된 단백질 인자에 의해 인식되는 터미네이터 신호를 통해 작동한다. 일부 실시태양에서, 절단 및 폴리아데닐화 특이성 인자(CPSF) 및 절단 자극 인자(CstF)는 RNA 폴리머라제 II의 카복실 말단 도메인으로부터 폴리-A 신호로 전달된다. 일부 실시태양에서, CPSF 및 CstF 인자는 또한 종결 부위에 다른 단백질을 모집하고, 그런 후에 전사 복합체로부터 전사체를 절단하고 mRNA를 유리시킨다. 종결은 또한 mRNA 전사체의 폴리아데닐화를 유발한다. 입증된 진핵생물 종결 인자 및 보존된 구조의 예시적 예는 본 문서의 뒷부분에서 논의된다.
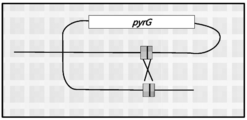
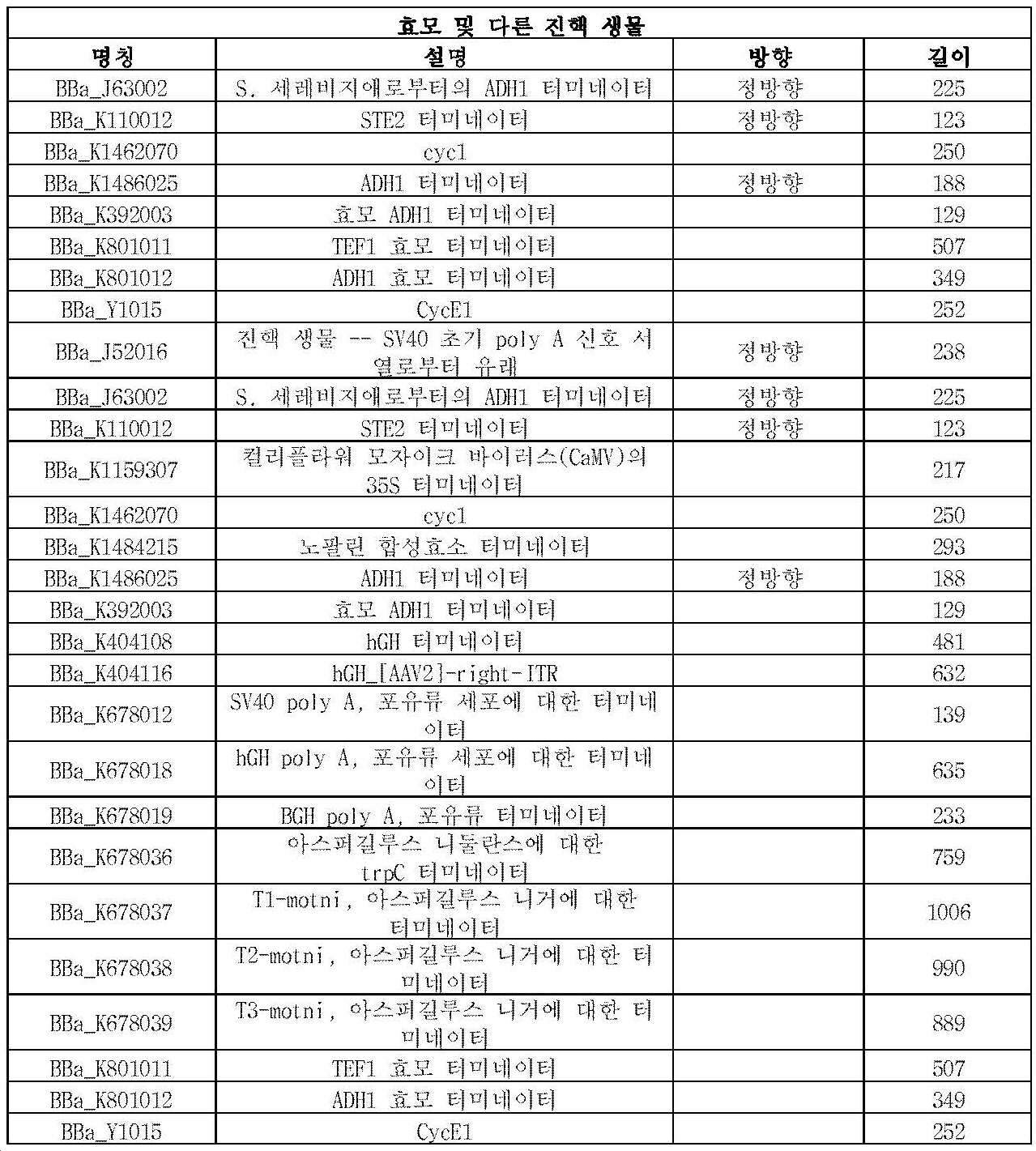
터미네이터 서열 또는 신호는 발현될 서열의 3' 말단에 작동 가능하게 연결될 수 있다. 다양한 공지된 균류 터미네이터가 본 발명의 숙주 균주에서 기능할 가능성이 있다. 예는 A. 니둘란스 trpC 터미네이터, A. 니거 알파-글루코시다제 터미네이터, A. 니거 글루코아밀라제 터미네이터, 뮤코 미헤이 카복실 프로테아제 터미네이터(미국 특허 번호 5,578,463 참조), 크리소스포리움 터미네이터 서열, 예를 들어 EG6 터미네이터 및 트라이코더마 리이세이 셀로바이오하이드롤라제 터미네이터이다. 한 실시태양에서, 터미네이터 서열은 직접 반복체(DR)이다. 한 실시태양에서, 터미네이터 서열은 천연 A. 니거 pyrG 터미네이터이다. 천연 A. 니거 pyrG 서열은 SEQ ID NO. 5의 서열을 가질 수 있다.
터미네이터 스와핑(STOP 스왑)
일부 실시태양에서, 본 발명은 전체 숙주 균주 생산성에 유익한 효과를 생성하기위한 최적 발현 성질을 갖는 종결 서열("터미네이터")을 선택하는 방법을 교시한다.
예를 들어, 일부 실시태양에서, 본 발명은 다양한 발현 강도(예를 들어, 하기 논의되는 터미네이터 래더)를 나타내는 하나 이상의 터미네이터를 확인하고 및/또는 숙주 세포 내에서 하나 이상의 터미네이터의 변이체를 생성하는 방법을 교시한다. 이들 확인된 및/또는 생성된 터미네이터의 특정 조합은 터미네이터 래더로서 함께 그룹화될 수 있으며, 이는 보다 상세히 이하에서 설명된다.
당해 터미네이터 래더는 소정의 관심 유전자와 결합된다. 따라서, 터미네이터 T1-T8(다양한 발현 강도를 나타내는 것으로 확인된 및/또는 생성된 8개의 터미네이터를 나타냄)이 있고 터미네이터 래더를 숙주 세포에서 관심 단일 유전자와 결합시킨다면(즉, 소정의 표적 유전자에 작동 가능하게 연결된 소정의 터미네이터에 의해 숙주 세포 유전적으로 조작한다), 8개 터미네이터의 각 조합의 효과는 조작된 숙주 세포가 표적 유전자와 결합된 특정 터미네이터(들)를 제외하고 그렇지 않다면 동일한 유전자 배경을 갖는 것을 고려하여, 각 조합적 노력으로부터 생성되는 각각의 조작된 균주를 특성화함으로써 확인될 수 있다. 이 과정을 통해 조작되어 생성된 숙주 세포는 HTP 유전자 디자인 라이브러리를 형성한다.
HTP 유전자 디자인 라이브러리는 이 과정을 통해 형성되는 실제의 물리적 미생물 균주 집합을 의미할 수 있으며, 각각의 구성원 균주는 그렇지 않다면 동일한 유전자 배경으로 특정 표적 유전자에 작동 가능하게 연결된 소정의 터미네이터를 나타내며, 상기 라이브러리는 "터미네이터 스왑 미생물 균주 라이브러리" 또는 "STOP 스왑 미생물 균주 라이브러리"로 불린다. 사상균류(예를 들어, A. 니거)의 특정 맥락에서, 라이브러리는 "터미네이터 스왑 사상균류 균주 라이브러리", "터미네이터 스왑 A. 니거 라이브러리", "STOP 스왑 사상균류 균주 라이브러리" 또는 "STOP 스왑 A. 니거 균주 라이브러리"로 지칭될 수 있지만, 사상균류 또는 A. 니거는 미생물의 구체적인 예이기 때문에 용어는 다음과 같이 동의어로 사용될 수 있다.
또한, HTP 유전자 디자인 라이브러리는 유전자 교란의 집합을 의미할 수 있으며-이 경우 소정의 유전자 y에 작동 가능하게 연결된 소정의 터미네이터 x-상기 집합은 "STOP 스왑 라이브러리"로 불린다.
또한, 미생물을 조작하기 위해 터미네이터 T1-T8을 포함하는 동일한 터미네이터 래더를 이용할 수 있으며, 8개의 터미네이터 각각은 10개의 상이한 유전자 표적에 작동 가능하게 연결된다. 이 절차의 결과는 관심 표적 유전자에 작동 가능하게 연결된 특정 터미네이터를 제외하고, 그렇지 않으면 유전적으로 동일하게 간주되는 80개의 숙주 세포 균주일 것이다. 이런 80개의 숙주 균주는 적절하게 선별되고 특성화될 수 있으며 다른 HTP 유전자 디자인 라이브러리를 생성할 수 있다. HTP 유전자 디자인 라이브러리에 미생물 균주의 특성화는 관계형 데이터베이스, 객체 지향 데이터베이스 또는 고도로 분산된 NoSQL 데이터베이스를 포함하나 이에 제한되지 않는 임의의 데이터베이스에 저장될 수 있는 정보와 데이터를 생성한다. 이런 데이터/정보는, 예를 들어, 소정의 유전자 표적에 작동 가능하게 연결될 때 소정의 터미네이터(예를 들어, T1-T8) 효과를 포함할 수 있다. 이 데이터/정보는 또한 둘 이상의 프로모터 T1-T8을 소정의 유전자 표적에 작동 가능하게 연결시킴으로써 초래되는 보다 광범위한 세트의 조합 효과일 수 있다.
상기 8개의 터미네이터 및 10개의 표적 유전자의 예는 단지 예시적인데, 이는 개념이 다양한 발현 강도 및 소정 수의 표적 유전자의 표시에 기초하여 함께 그룹화된 임의의 소정의 수의 프로모터와 함께 적용될 수 있기 때문이다.
요약하면, 다양한 터미네이터를 이용하여 유기체에서 다양한 유전자의 발현을 조절하는 것은 관심 형질을 최적화하는 강력한 도구이다. 본 발명자에 의해 개발된 터미네이터 스와핑의 분자 도구는 하나 이상의 조건하에서 적어도 하나의 유전자좌의 발현을 변화시키는 것으로 입증된 터미네이터 서열의 래더를 사용한다. 그런 후에 이 래더는 고 처리량 게놈 기술을 사용하여 유기체에서 한 유전자 그룹에 체계적으로 적용된다. 이 유전자 그룹은 여러 가지 방법 중 하나를 기반으로 관심 형질에 영향을 주는 높은 가능성을 갖는 것으로 결정된다. 이들은 알려진 기능에 기초한 선택 또는 관심 형질에 대한 영향 또는 이전에 결정된 유익한 유전자 다양성에 기초한 알고리즘 선택을 포함할 수 있다.
유전자에 연결된 터미네이터 서열을 함유하는 유기체의 생성된 HTP 유전자 디자인 미생물 라이브러리는 고 처리량 선별 모델에서의 성능에 대해 평가되고, 증가된 성능을 유도하는 프로모터-유전자 연관이 결정되고 정보는 데이터베이스에 저장된다. 유전자 교란의 집합(즉 소정의 유전자 y에 연결된 소정이 터미네이터 x)은 "터미네이터 스왑 라이브러리"를 형성하며, 이것은 미생물 조작 처리에 이용될 잠재적인 유전자 변형의 공급원으로 이용될 수 있다. 시간이 지남에 따라, 더 큰 세트의 유전자 교란이 더 큰 다양성의 미생물 배경에 대해 실행되기 때문에, 각 라이브러리는 임의의 관심 배경에 대한 표적화된 변화를 더욱 정확하고 예측되게 디자인하는데 사용될 수 있는 실험적으로 확인된 데이터의 모음으로서 더욱 강력해진다. 즉 일부 실시태양에서, 본 발명은 본 발명의 유전자 디자인 라이브러리의 임의의 것과 관련된 메타 데이터 내에 삽입된 이전의 실험 결과에 기초한 숙주 세포 속으로의 하나 이상의 유전자 변화를 도입하는 것을 교시한다.
따라서, 특정 실시태양에서, 터미네이터 스와핑은 다음을 포함하는 다단계 공정이다:
1. "래더"로서 작용하는 "x" 터미네이터의 세트를 선택하는 단계. 이상적으로 이런 터미네이터는 다수의 게놈 유전자좌 전체에서 매우 가변적인 발현을 유도하는 것으로 나타났지만, 유일한 요구조건은 일부 유전자 발현을 교란시키는 것이다.
2. 표적화하기 위한 "n" 유전자의 세트를 선택하는 단계. 이 세트는 게놈의 모든 오픈 리딩 프레임(ORF) 또는 ORF의 서브세트일 수 있다. 서브세트는 기능과 관련된 ORF에 대한 주석을 사용하고, 이전에 입증된 유익한 교란(이전 프로모터 스왑 STOP 스왑 또는 SNP 스왑)에 대한 관계에 의해, 이전에 생성된 교란 사이의 상위성 상호작용에 기초한 알고리즘 선택에 의해, 표적에 대한 유익한 ORF에 관한 가설에 기초한 다른 선택 기준 또는 무작위 선택을 통해 선택될 수 있다. 다른 실시태양에서, "n" 표적 유전자는 비-암호화 RNA를 포함하는 비-단백질 암호화 유전자를 포함할 수 있다.
3. 다음과 같은 유전자 변형을 신속하게- 및 일부 실시태양에서, 병렬-수행하는 고 처리량 균주 조작 단계: 천연 터미네이터가 표적 유전자 n의 3' 말단에 존재하고 이의 서열이 알려질 때, 천연 터미네이터를 래더에 있는 x 터미네이터의 각각으로 대체한다. 천연 터미네이터가 존재하지 않거나 이의 서열이 알려지지 않을 때, 유전자 정지 코돈 이후 래더에 x 터미네이터의 각각을 삽입한다.
이러한 방식으로, 균주의 "라이브러리"(HTP 유전자 디자인 라이브러리라고도 불림)가 구성되며, 라이브러리의 각 구성원은 그렇지 않으면 동일한 유전자 상황에서, n 표적에 작동 가능하게 연결된 x 터미네이터의 한 예이다. 상기한 바와 같이, 터미네이터의 조합이 삽입되어 라이브러리가 구성되는 조합 가능성의 범위를 확장시킬 수 있다.
4. 하나 이상의 메트릭에 대한 성능이 최적화되는 성능을 나타내는 상황에서 균주의 라이브러리의 고 처리량 선별 단계.
이 기본 과정은 특히 다음과 같은 방법으로 균주 성능에 추가 개량을 제공하는데 확장될 수 있다: (1) 반복 과정에서 한 번에 하나씩 또는 단일 단계에서 다중 변화로서 단일 균주 배경 속에 다수의 유익한 교란을 통합하는 단계. 다중 교란은 정의된 변경의 특정 세트 또는 부분적으로 무작위화된 조합 라이브러리의 변화일 수 있다. 예를 들어, 표적 세트가 한 경로의 모든 유전자인 경우, 이전 라이브러리 균주의 개량된 구성원 또는 구성원들 속으로 교란의 라이브러리의 순차적 재생은 어느 유전자가 임의의 소정의 반복에서 속도를 제한하는지와 관계없이 한 경로에서 각 유전자의 발현 수준을 최적화할 수 있다; (2) 각 교란의 상호작용에 기초하여 최적의 교란 세트를 예측하기 위해 그 데이터를 사용하는 알고리즘 속에 라이브러리의 개별 및 조합 생성으로부터 성능 데이터를 제공하는 단계; 및 (3) 위의 두 접근법의 조합을 실행하는 단계.
이 접근법은 산업용 미생물에 의해 본 발명에서 예시되었지만, 원하는 형질이 유전자 돌연변이 집단에서 동정될 수 있는 임의의 유기체에 적용 가능하다. 예를 들어, 이것은 CHO 세포, 효모, 곤충 세포, 조류뿐만 아니라 식물과 같은 다세포 유기체의 성능을 개량시키는데 사용될 수 있다.
5. 서열 최적화: 최적화된 서열 미생물 균주 라이브러리 유도를 위한 분자 도구
한 실시태양에서, 본 발명의 방법은 숙주 유기체에 의해 발현된 하나 이상의 유전자를 최적화하는 코돈을 포함한다. 다양한 숙주에서 발현을 향상시키기 위해 코돈을 최적화하는 방법은 당해 분야에 공지되어 있고, 문헌에 기술된다(그 전체가 본 발명에 참조로 포함된 미국 특허출원 공개공보 제2007/0292918호 참조). 특정 원핵 또는 진핵 숙주(Murray et al. (1989) Nucl. Acids Res.17 : 477-508 참조)에 의해 선호되는 코돈을 함유하는 최적화된 암호화 서열은, 예를 들어, 번역 속도를 증가시키거나 또는 최적화되지 않은 서열로부터 생산된 전사체와 비교할 때, 더 긴 반감기와 같은 바람직한 특성을 갖는 재조합 RNA 전사체를 생성하도록 제조된다.
단백질 발현은 전사, mRNA 프로세싱 및 안정성 및 번역 개시에 영향을 미치는 인자를 포함하는 다수의 인자에 의해 지배된다. 따라서 최적화는 임의의 특정 유전자의 많은 서열 특징의 임의의 것을 처리할 수 있다. 특정 예로서, 드문 코돈 유도 번역 일시 중지는 감소된 단백질 발현을 초래할 수 있다. 드문 코돈 유도 번역 일시 중지는 숙주 유기체에서 거의 사용되지 않는 관심 폴리뉴클레오타이드에서 코돈의 존재를 포함하며 이용가능한 tRNA 풀에서의 희소성 때문에 단백질 번역에 부정적인 영향을 미칠 수 있다.
대안적인 번역 개시는 또한 감소된 이종 단백질 발현을 초래할 수 있다. 대안적인 번역 개시는 의도하지 않게 리보솜 결합 부위(RBS)로서 기능할 수 있는 모티프를 함유하는 합성 폴리뉴클레오타이드 서열을 포함할 수 있다. 이런 위치는 유전자 내부 위치로부터 잘린 단백질의 번역을 시작할 수 있다. 정제 과정에서 제거하기 어려울 수 있는 절단된 단백질을 생산할 가능성을 줄이는 한 가지 방법은 최적화된 폴리뉴클레오타이드 서열로부터 추정된 내부 RBS 서열을 제거하는 것을 포함한다.
반복체-유도된 폴리머라제의 슬리파지(slippage)는 감소된 이종 단백질 발현을 초래할 수 있다. 반복체-유도된 폴리머라제의 슬리파지는 프레임변이 돌연변이를 초래할 수 있는 DNA 폴리머라제의 슬리파지 또는 스터터링(stuttering)을 유발하는 것으로 밝혀진 뉴클레오타이드 서열 반복을 필요로 한다. 이러한 반복체는 또한 RNA 폴리머라제의 슬리파지를 유발할 수 있다. 높은 G+C 함량 편향을 갖는 유기체에서, G 또는 C 뉴클레오타이드 반복체로 구성된 더 높은 등급의 반복체가 존재할 수 있다. 따라서, RNA 폴리머라제의 슬리파지를 유도하는 가능성을 줄이는 한 가지 방법은 G 또는 C 뉴클레오타이드의 연장된 반복체를 변경하는 것을 포함한다.
2차 구조를 간섭하면 또한 감소된 이종 단백질 발현을 초래할 수 있다. 2차 구조는 RBS 서열 또는 개시 코돈을 격리할 수 있고 단백질 발현의 감소와 상관관계가있다. 스템루프 구조는 또한 전사 일시 중지 및 약화에 관여할 수 있다. 최적화 된 폴리뉴클레오타이드 서열은 RBS 내에 최소 2차 구조 및 뉴클레오타이드 서열의 유전자 암호화 영역을 함유하여 개량된 전사 및 번역을 가능하게 한다.
예를 들어, 최적화 공정은 숙주에 의해 발현되는 원하는 아미노산 서열을 확인함으로써 시작될 수있다. 아미노산 서열로부터 후보 폴리뉴클레오타이드 또는 DNA 서열이 디자인될 수 있다. 합성 DNA 서열의 디자인 동안, 코돈 사용의 빈도는 숙주 발현 유기체의 코돈 사용과 비교될 수 있고 드문 숙주 코돈은 합성 서열로부터 제거될 수있다. 또한, 합성 후보 DNA 서열은 바람직하지 않은 효소 제한 부위를 제거하고 원하는 신호 서열, 링커 또는 비번역 영역을 추가 또는 제거하기 위해 변형될 수 있다. 합성 DNA 서열은 G/C 반복체 및 스템-루프 구조와 같이 번역 과정을 방해할 수 있는 2차 구조의 존재에 대해 분석될 수 있다.
6. 상위성 매핑 - 유익한 유전자 통합을 가능하게 하는 예측 분석 도구
일부 실시태양에서, 본 발명은 유익한 유전자 변형을 예측하고 숙주 세포 내로 결합시키는 상위성 매핑 방법을 교시한다. 유전자 변형은 상기한 HTP 분자 도구 세트(예를 들어, 프로모터 스왑, SNP 스왑, 개시/정지 코돈 교환, 서열 최적화 및 STOP 스왑)의 임의의 것에 의해 일어날 수 있고 이러한 유전자 변형의 효과는 유도된 HTP 유전자 디자인 미생물 균주 라이브러리의 특성화로부터 알 수 있다. 따라서, 본 발명에서 사용된 용어 상위성 매핑은 숙주 성능의 증가를 초래할 수 있는유전자 변형의 조합(예를 들어 유익한 SNP 또는 유익한 프로모터/표적 유전자 결합)의 조합을 확인하는 방법을 포함한다.
실시태양에서, 본 발명의 상위성 맵핑 방법은 2개의 상이한 작용기로부터의 유익한 돌연변이의 조합이 동일한 작용기로부터의 돌연변이의 조합과 비교하여, 숙주 성능을 개량시키가 더 쉽다는 아이디어에 기초한다. 예를 들어, Costanzo, The Genetic Landscape of a Cell, Science, Vol. 327, Issue 5964, Jan. 22, 2010, pp. 425-431 참조(전문이 본 발명에 참조로 포함).
동일한 작용기로부터의 돌연변이는 동일한 메카니즘에 의해 작용할 가능성이 더 높으며, 따라서 전체 숙주 성능에 대해 음성 또는 중성 상위성을 나타내기가 더 쉽다. 대조적으로, 상이한 작용기로부터의 돌연변이는 독립적인 메카니즘에 의해 작동하기 쉽고, 이로 인해 개량된 숙주 성능 및 일부 경우에 상승 효과를 유도할 수 있다.
따라서, 일부 실시태양에서, 본 발명은 상이한 작용기에 속하는 것으로 예측되는 SNP를 확인하기 위해 SNP 돌연변이를 분석하는 방법을 교시한다. 일부 실시태양에서, SNP 작용기 유사성은 돌연변이 상호작용 프로파일의 코사인 유사성을 계산함으로써 결정된다. 본 발명은 또한 돌연변이 유사성 행렬 또는 덴드로그램을 통한 SNP의 비교를 예시한다.
따라서, 상위성 매핑 절차는 하나 이상의 유전자 배경에 상기 돌연변이의 효율적이고 효과적인 통합을 위해 하나 이상의 유전자 배경에 적용된 다양성의 유전 돌연변이를 그룹화 및/또는 순위화하는 방법을 제공한다.
양태에서, 통합은 표적 생체분자의 생산을 위해 최적화된 신규 균주를 생성하는 목적으로 수행된다. 교시된 상위성 매핑 절차를 통해, 돌연변이의 기능적 그룹화를 확인하는 것이 가능하며 이런 기능적 그룹화는 바람직하지 않은 상위성 효과를 최소화하는 통합 전략을 가능하게 한다.
상기한 바와 같이, 산업용 발효에 사용하기 위한 미생물의 최적화는 중요하고 경제, 사회 및 자연계에 대한 광범위하게 관련된 어려운 문제이다. 전통적으로, 미생물 조작은 무작위 돌연변이유발의 느리고 불확실한 과정을 통해 수행되었다. 이런 접근법은 인위적으로 부과된 선택 압력에 적응할 수 있는 세포의 자연적 진화 능력을 활용한다. 이런 접근법은 유익한 돌연변이의 희귀성, 근본적인 적합함 환경의 견고함에 의해 제한되며 보다 일반적으로 세포 및 분자 생물학의 최신기술을 충분히 활용하지 못한다.
현대의 접근법은 기계적 수준에서 세포 기능의 새로운 이해 및 특정 표현형 말단에 대해 표적화된 유전자 조작을 수행하는 새로운 분자 생물학 도구를 활용한다. 실제로, 이런 합리적인 접근법은 생물학의 근본적인 복잡성에 의해 혼란스럽게 된다. 인과관계 매커니즘은, 특히 관찰된 유익한 효과가 있는 두 개 이상의 변화를 결합하려고 시도할 때 잘 이해되지 않는다. 때로는 순 긍정적인 결과가 예상보다 낮을 수도 있고 경우에 따라 예상보다 높을 수도 있지만, 유전자 변화의 이런 통합은 긍정적인 결과(원하는 표현형 활동의 증가로 측정됨)를 가져온다. 다른 경우, 이런 조합은 순 중성 효과 또는 순 부정적인 효과를 일으킨다. 이 현상은 상위성으로 불리고 미생물 공학(및 일반적으로 유전자 공학)에 대한 근본적인 도전 중 하나이다.
상기한 바와 같이, 본 HTP 게놈 공학 플랫폼은 전통적인 미생물 공학 접근법과 관련된 많은 문제점을 해결한다. 현재의 HTP 플랫폼은 자동화 기술을 사용하여 한 번에 수백 또는 수천 개의 유전자 변이를 실행한다. 특정 양태에서, 상기한 합리적인 접근법과는 달리, 개시된 HTP 플랫폼은 전문이 본 발명에 참조로 포함된 Microbial Strain Design System And Methods For Improved Large-Scale Production Of Engineered Nucleotide Sequences 이란 제목의 미국 특허 출원 제15/140,296호에 개시된 바와 같이 수천 개의 돌연변이체의 병렬 건설을 가능하게 하여 관련 게놈 공간의 큰 서브세트를 보다 효과적으로 탐사할 수 있게 한다. 공학적 염기 서열의 개선 된 대규모 생산을위한 시스템 및 방법으로서, 본 명세서에서 그 전체가 참고로 인용된다. "모든 것"을 시도함으로써, 현재의 HTP 플랫폼은 제한된 생물학적 이해에 의해 유도된 어려움을 회피한다.
그러나, 동시에, 본 HTP 플랫폼은 게놈 공간의 조합 폭발성 크기 및 유전자 상호작용의 복잡성을 고려하여 생성된 데이터 세트를 해석하는 계산 기술의 효과에 의해 근본적으로 제한되는 문제에 직면한다. 원하는 결과를 산출하는 조합의 비 무작위 선택을 최대화하는 방식으로 광대한 조합 공간의 서브세트를 탐구하는 기술이 필요하다.
다소 유사한 HTP 접근법이 효소 최적화의 경우에 효과적이라는 것이 증명되었다. 이 틈새 문제에서, 관심 게놈 서열(약 1000 염기)은 일부 복잡한 물리적 구성을 가진 단백질 사슬을 암호화한다. 정확한 구성은 구성 원자 구성요소 사이의 집단적 전자기 상호작용에 의해 결정된다. 짧은 게놈 서열과 물리적으로 구속된 접힘 문제의 조합은 탐욕 최적화 전략(greedy optimization strategies)에 특히 적합하다. 즉, 모든 잔기에서 서열을 개별적으로 돌연변이시키고, 생성된 돌연변이를 뒤섞어 서열 활성 반응 모델링과 양립가능한 해상도로 로컬 서열 공간을 효과적으로 샘플링하는 것이 가능하다.
그러나, 생체 분자에 대한 완전한 게놈 최적화를 위해, 이런 잔기-중심 접근법은 몇 가지 중요한 이유 때문에 불충분하다. 첫째, 생체 분자에 대한 게놈 최적화와 관련된 관련 서열 공간의 기하 급수적인 증가 때문이다. 둘째, 생체분자 합성에서 조절, 발현 및 대사 상호작용의 추가된 복잡성 때문이다. 본 발명자들은 교시 된 상위성 매핑 절차를 통해 이러한 문제점을 해결하였다.
상기 돌연변이를 하나 이상의 유전자 배경 속에 더 효율적이고 효과적으로 통합하기 위해서 돌연변이의 집합 사이의 상위성 상호작용을 모델링하는 교시된 방법은 획기적이며 당업계에서 매우 필요하다.
상위성 매핑 절차를 기술할 때, 용어 "더 효율적" 및 "더 효과적인"은 특정 표현형 목표와 관련하여 통합 균주 사이의 바람직하지 않은 상위성 상호작용의 회피를 의미한다.
상기 과정이 일반적으로 상기에 상세하게 설명되었으므로, 더 구체적인 워크 플로우 예가 이제 설명될 것이다.
첫째, M 돌연변이 및 하나 이상의 유전자 배경(예를 들어, 부모 사상균류 균주)의 라이브러리로 시작한다. 라이브러리의 선택이나 유전자 배경의 선택은 여기에 설명된 방법에 특이적이지 않다. 그러나 특정 구현예에서, 돌연변이의 라이브러리는 SNP 스왑 라이브러리, 프로모터 스왑 라이브러리 또는 본 발명에 설명된 임의의 다른 돌연변이 라이브러리를 독점적으로 또는 조합하여 포함할 수 있다.
한 구현예에서, 단일 유전자 배경만이 제공된다. 이 경우, 구별된 유전자 배경(미생물 돌연변이)의 집합이 이 단일 배경에서 먼저 생성될 것이다. 이것은 소정의 배경에 돌연변이의 기본 라이브러리(또는 이의 일부 서브세트)를 적용, 예를 들어, 특정 SNP의 HTP 유전 디자인 라이브러리 또는 특정 프로모터의 HTP 유전 디자인 라이브러리의 특정 유전자 배경에 대해 적용함으로써 달성되어 본 발명에 포함된 소정의 HTP 유전자 디자인 라이브러리로부터의 특정 유전자 변형을 제외하고는 동일한 유전자 배경을 가진 미생물 돌연변이 개체군(아마도 100 또는 1,000)을 생성할 수 있다. 아래에서 상세히 설명하는 바와 같이, 이 실시태양은 조합 라이브러리 또는 쌍을 이루는 라이브러리를 유도할 수 있다.
또 다른 구현예에서, 구별된 알려진 유전자 배경의 집합이 간단히 주어질 수있다. 아래에서 상세히 설명되는 바와 같이, 이 실시태양은 조합 라이브러리의 서브세트를 유도할 수 있다.
한 특정 구현예에서, 이런 배경 사이의 유전자 배경 및 유전자 다양성의 수 (돌연변이 또는 서열 편집 거리 등의 수로 측정)는 이 방법의 효과를 최대화하도록 결정된다.
유전자 배경은 천연, 고유한 또는 야생형 균주 또는 돌연변이된 조작 균주일 수 있다. N개의 구별된 배경 균주는 벡터 b로 나타낼 수 있다. 한 실시예에서, 배경 b는 N개의 돌연변이된 배경 균주 b = m0b0 = (m1b0, m2b0, ... mNb0)를 형성하기 위해 N개의 일차 돌연변이 m0 = (m1, m2, ... mN)을 야생형 배경 균주 b0에 적용하여 형성된 조작된 배경을 나타낼 수 있으며, 여기서, mib0는 배경 균주 b0에 대한 돌연변이 mi의 적용을 나타낸다.
각각의 경우에(즉, 하나의 제공된 유전자 배경 또는 유전자 배경의 집합), 결과는 N개의 유전적으로 구별된 배경의 집합이다. 관련 표현형은 각 배경에 대해 측정된다.
둘째, M 돌연변이 m1의 집합에서 각 돌연변이는 N개의 배경 균주 b의 집합 내의 각 배경에 적용되어 M × N 돌연변이체의 집합을 형성한다. N개의 배경이 그 자체로 돌연변이 m0의 기본 세트(위에 설명된 대로)를 적용하여 얻은 구현예에서, 돌연변이체의 생성된 집합은 때로는 조합 라이브러리 또는 쌍을 이루는 라이브러리로 불릴 수 있다. 공지된 배경의 집합이 명시적으로 제공되는 다른 구현예에서, 돌연변이체의 생성된 세트는 조합 라이브러리의 서브세트로 불릴 수 있다. 조작된 배경 벡터의 생성과 유사하게, 실시태양에서, 입력 인터페이스(202)(도 14 참조)는 돌연변이 벡터 m1과 배경 벡터 b 및 교차 곱과 같은 특정 연산을 수신한다.
상기 조작된 배경 예를 계속하면, MxN 조합 라이브러리를 형성하는 것은 m1 x m0b0에 의해 형성되는 행렬로 표현될 수 있으며, b의 N 배경에 적용된 m1의 교차 곱 b = m0b0, m1에서 각 돌연변이는 b 내의 각 배경 균주에 적용된다. 생성된 MxN 행렬의 각 i번째 행은 m1 내 i번째 돌연변이의 배경 집합 b 내의 모든 균주에 대한 적용을 나타낸다. 하나의 실시태양에서, m1 = m0이고 행렬은 출발 균주 b0에 동일한 돌연변이의 쌍을 이루는 적용을 나타낸다. 이 경우 행렬은 대각선(M = N) 근처에서 대칭이며 대각선은 동일한 돌연변이의 2회 적용을 나타내기 때문에 모든 분석에서 무시될 수 있다.
실시태양에서, MxN 행렬을 형성하는 것은 입력 인터페이스(202)(도 14 참조)에 복합 표현 m1 x m0b0을 입력함으로써 달성될 수 있다. 표현의 구성요소 벡터는 하나 이상의 DNA 명세를 통해 명시적으로 지정된 요소로 직접 입력되거나 인터프리터(204)에 의한 해석 동안 벡터의 검색을 가능하게 하기 위해 라이브러리(206)에 대한 호출로서 입력될 수있다. 인터프리터(204), 실행 엔진(207), 주문 배치 엔진(208) 및 공장(210)을 통해 "Microbial Strain Design System and Methods for Improved Large Scale Production of Engineered Nucleotide Sequences,"이라는 제목의 미국 특허출원 제15/140,296호에 개시된 바와 같이, LIMS 시스템(200)은 입력 표현에 의해 지정된 미생물 균주를 생성한다.
셋째, 도 19를 참조하면, 분석 장비(214)(도 14 참조)는 MxN 조합 라이브러리 행렬(4202) 내의 각각의 돌연변이체에 대한 표현형 반응을 측정한다. 이와 같이, 응답의 집합은 MxN 응답 행렬 R로 해석될 수 있다. R의 각 요소는 rij = y(mi, mj)로 나타낼 수 있으며, 여기서 y는 돌연변이 mi에 의해 돌연변이된 조작된 집합 b 내의 배경 균주 bj의 응답(성능)을 나타낸다. 단순성과 실용성을 위해, m1 = m0인 쌍을 이루는 돌연변이를 가정한다. 돌연변이의 세트가 상을 이루는 돌연변이 라이브러리를 나타내는 경우, 생성된 행렬은 유전자 상호작용 행렬 또는 보다 구체적으로 돌연변이 상호작용 행렬로 불릴 수 있다.
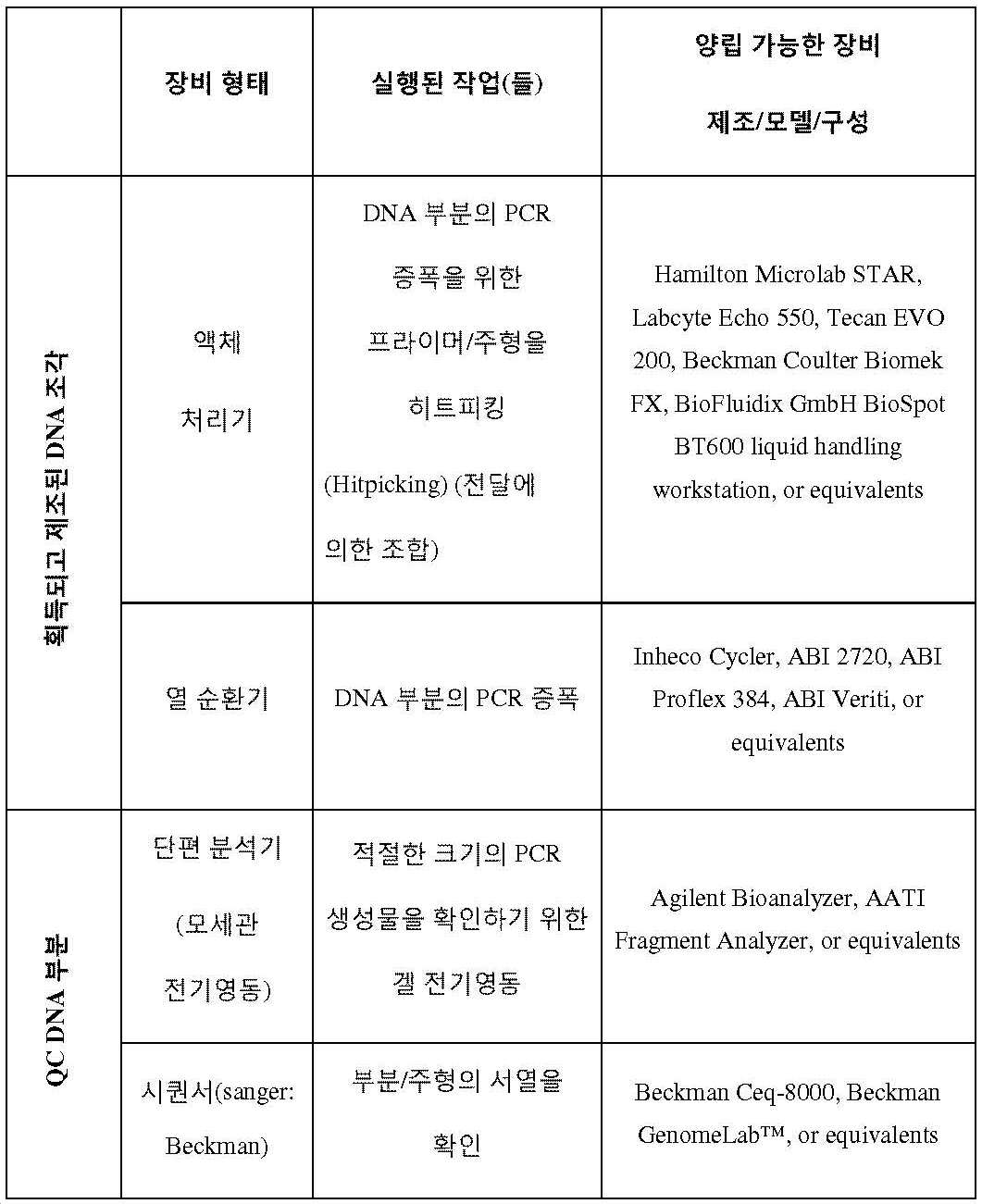
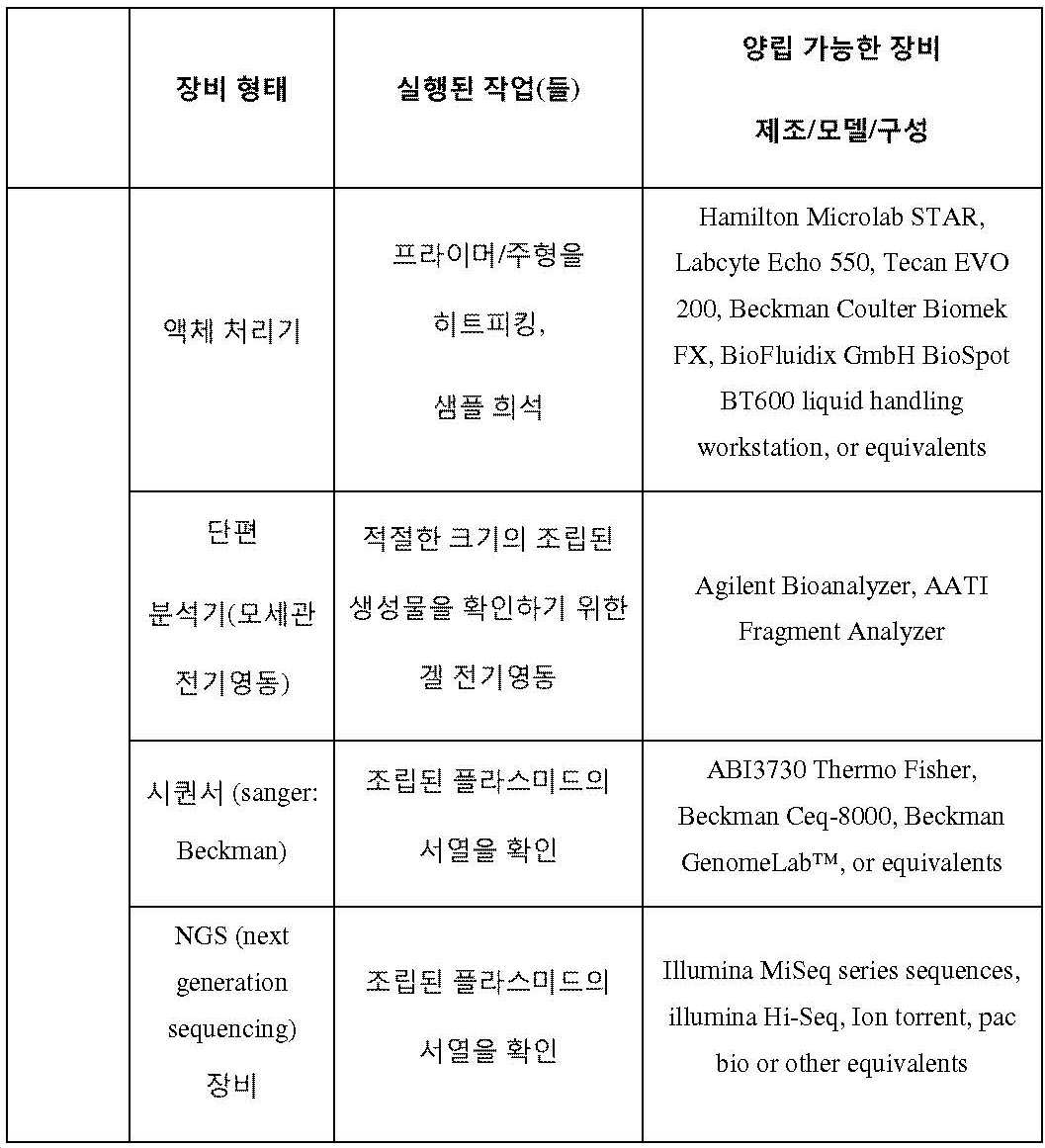
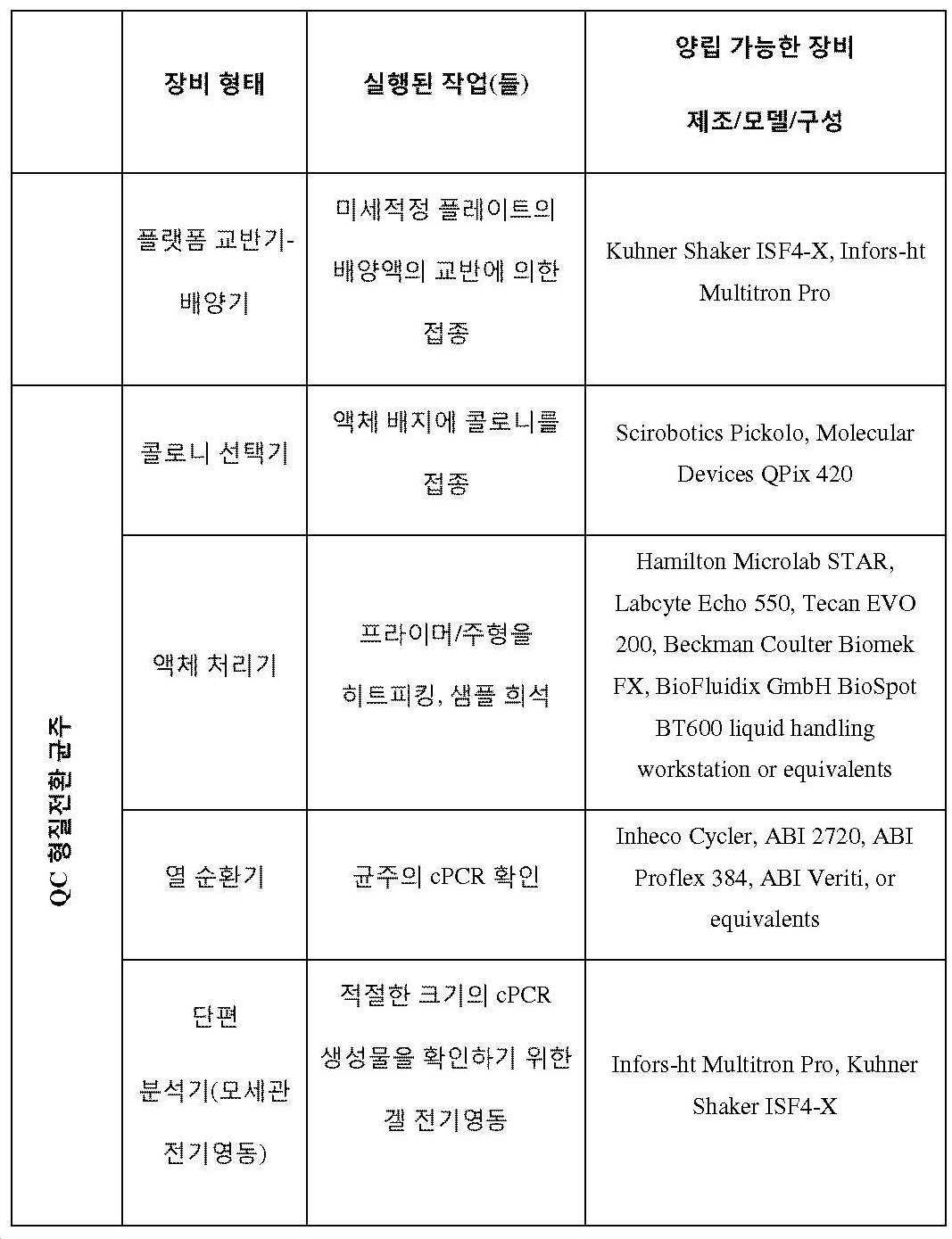
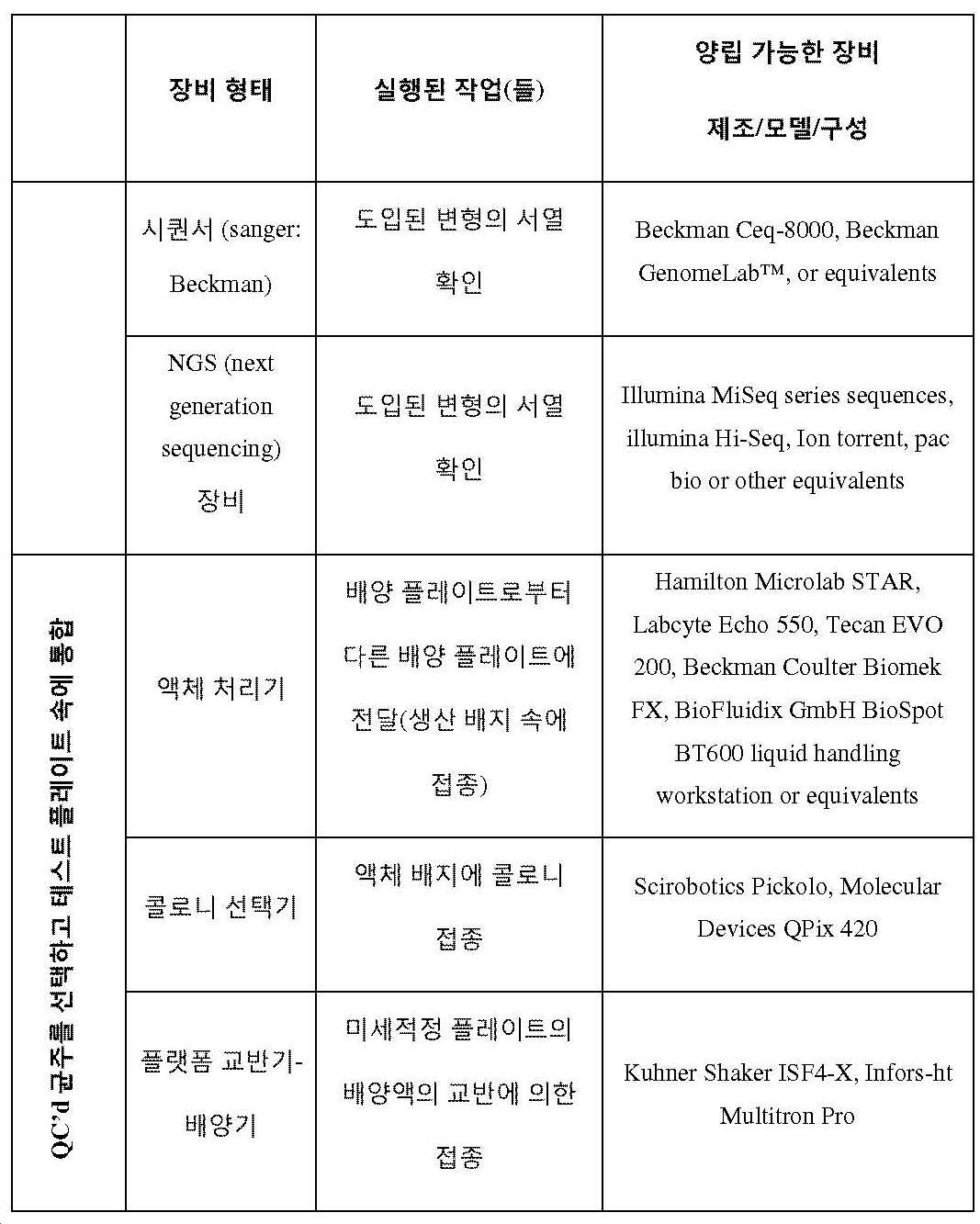
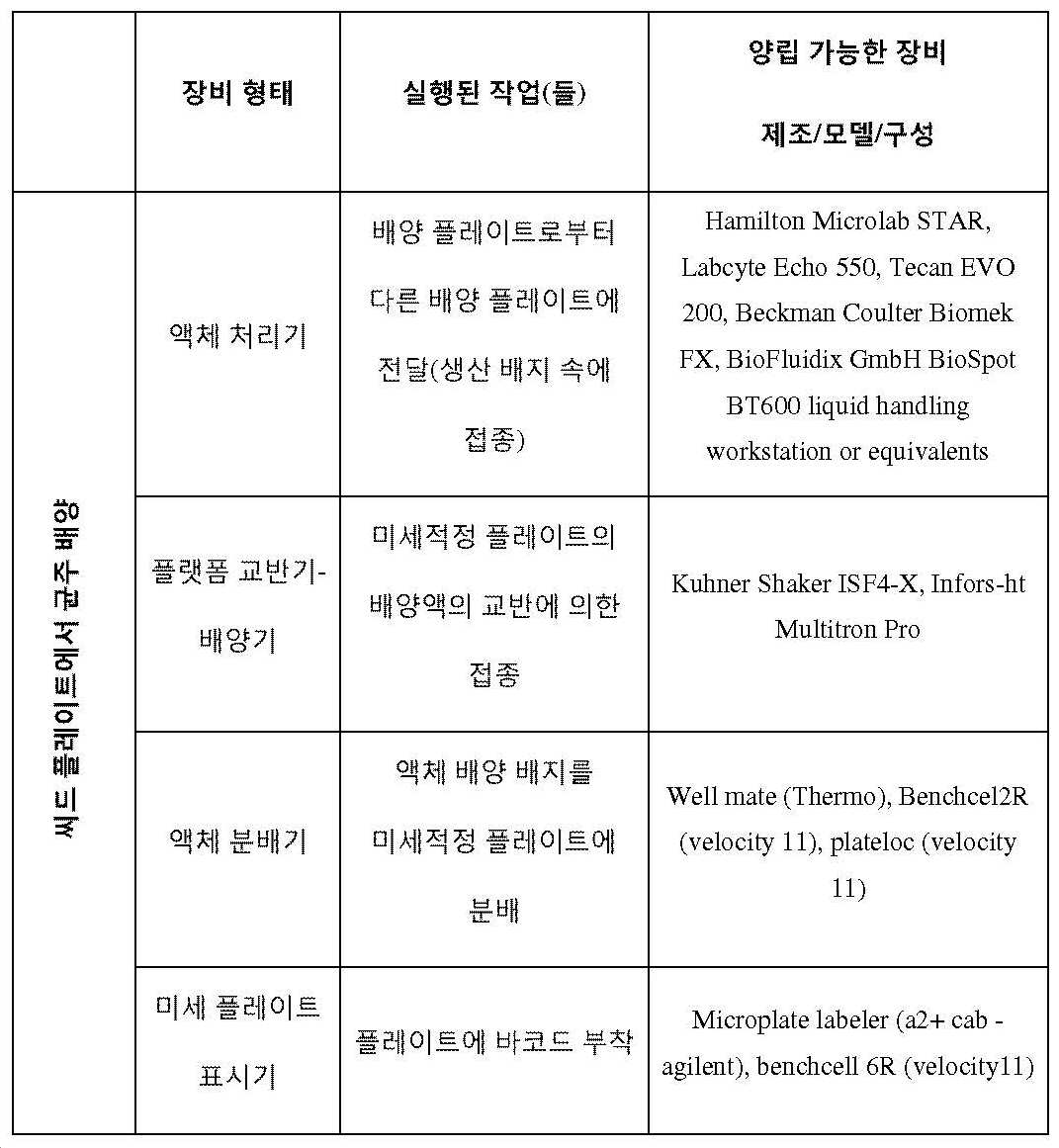
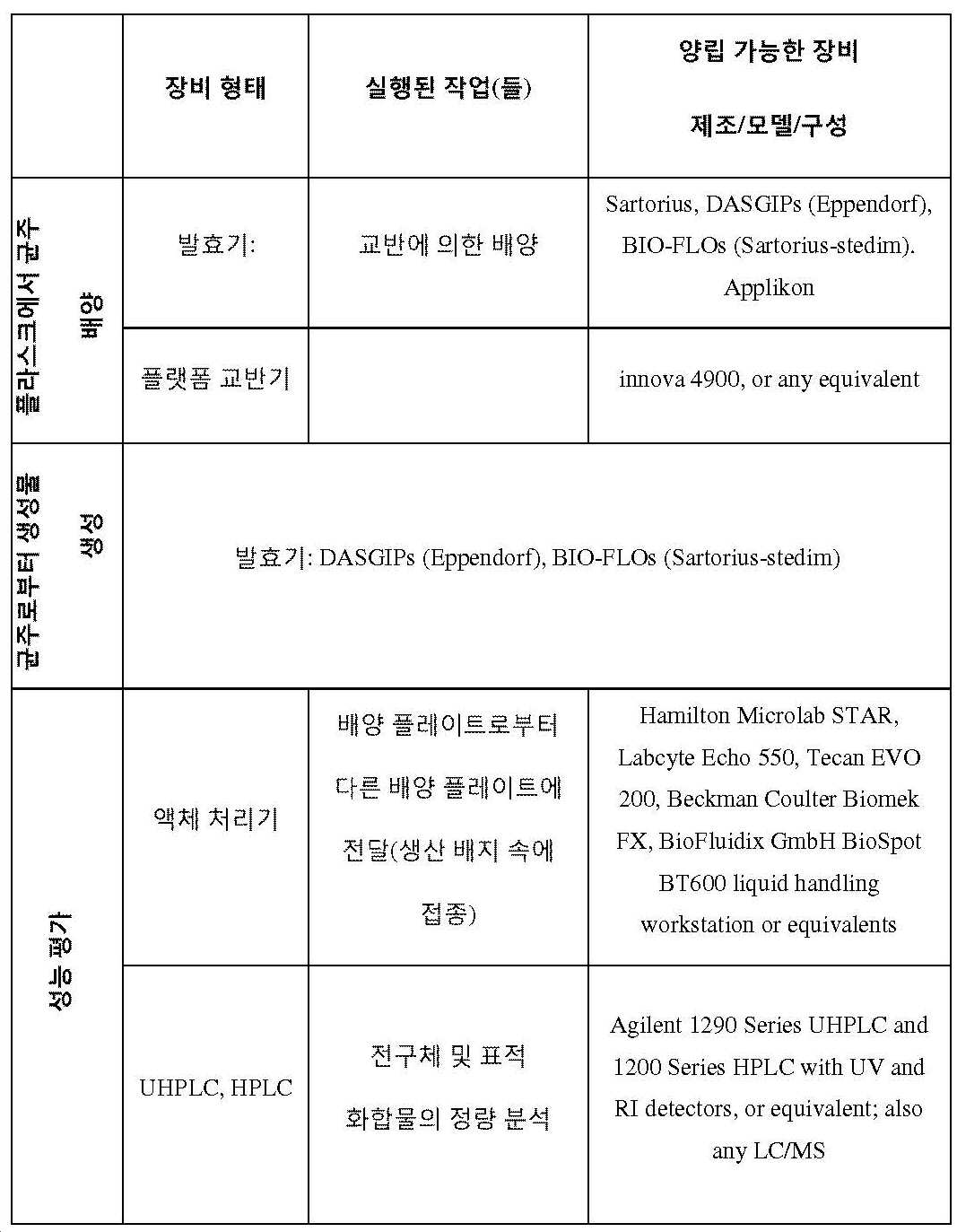
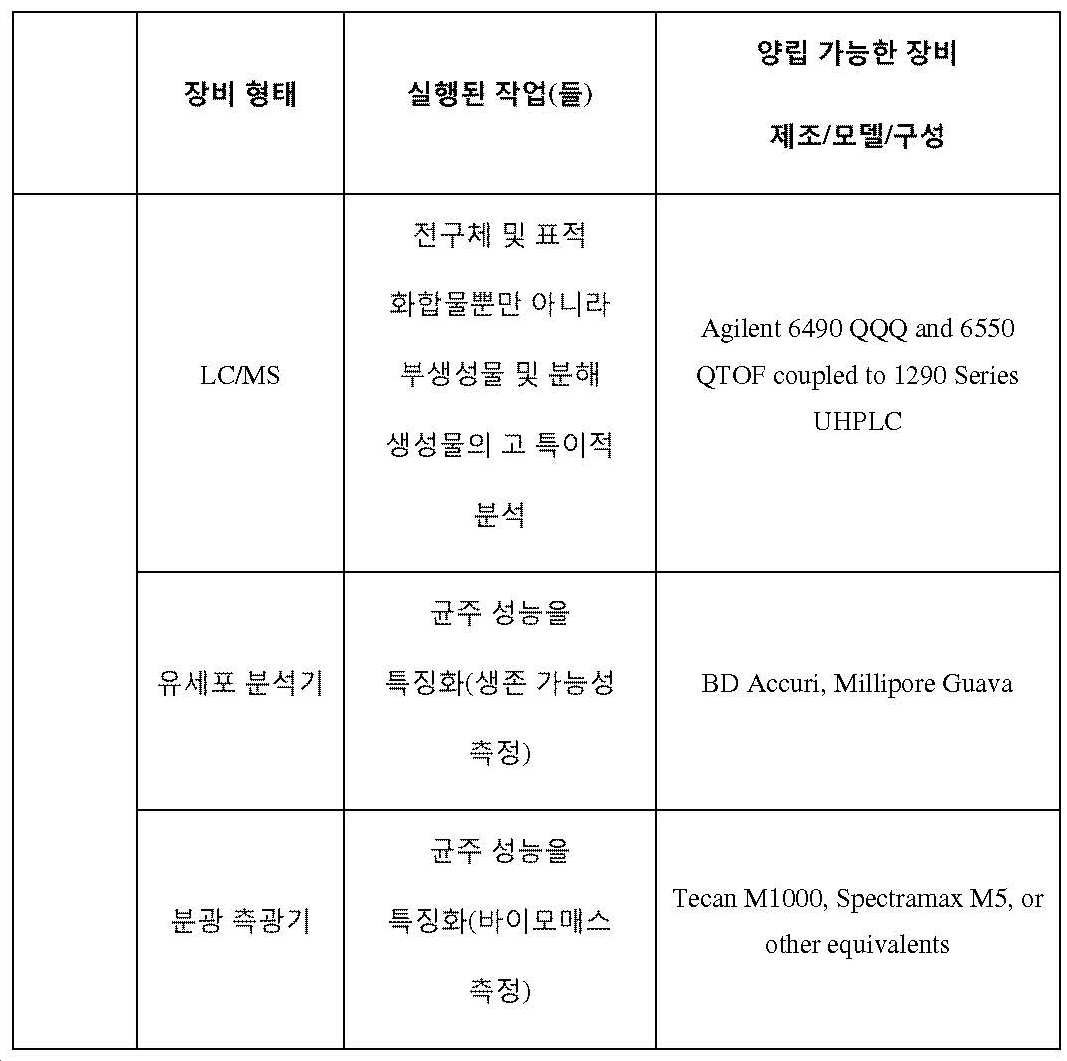
당업자는, 일부 실시태양에서, 상위성 효과 및 예측 균주 디자인과 관련된 작업이, 예를 들어 분석 장비(214)(도 14 참조) 또는 인간의 구현에 의한 LIMS 시스템(200)의 자동화 수단을 통해 또는 자동화 및 수동 수단의 조합을 통해 완전히 수행될 수 있다는 것을 인식할 것이다. 작업이 완전히 자동화되지 않으면, 예를 들어, 분석 장비 (214)와 같은 LIMS 시스템(200)의 요소는, 예를 들어, 자신의 작업 능력을 통해 결과를 생성하기 보다는 작업의 인간 수행 결과를 수신할 수 있다. 본 발명의 다른 곳에서 기술된 바와 같이, 분석 장비(214)와 같은 LIMS 시스템(200)의 구성요소는 전체적으로 또는 부분적으로 하나 이상의 컴퓨터 시스템에 의해 구현될 수 있다. 일부 실시태양에서, 특히 예측 균주 디자인과 관련된 작업이 자동 및 수동 수단의 조합에 의해 수행되는 경우, 분석 장비(214)는 컴퓨터 하드웨어, 소프트웨어 또는 펌웨어(또는 이들의 조합)뿐만 아니라 아래 표 3에 열거된 것과 같은 인간 작업자에 의해 작동된 장비, 예를 들어 "성능 평가" 범주에 나열된 장비를 포함할 수 있다.
넷째, 분석 장비(212)(도 14 참조)는 응답 행렬을 정규화한다. 정규화는 편향을 제거하고 및/또는 이 방법에 특이적인 효과의 관련 부분을 분리할 목적으로 측정된 응답 값을 조정하는 수동 및/또는 자동화 프로세스로 구성된다. 도 19와 관련하여, 제 1 단계(4202)는 정규화된 측정 데이터를 얻는 단계를 포함 할 수 있다. 일반적으로, 예측 균주 디자인 및 상위성 매핑에 관한 청구항에서, "성능 측정" 또는 "측정된 성능" 등의 용어는 일부 방식으로 처리되지 않거나 처리딘 측정 데이터, 예를 들어, 정규화된 데이터를 반영하는 메트릭을 기술하는데 사용될 수 있다. 특정 구현예에서, 정규화는 측정된 응답 값으로부터 이전에 측정된 배경 응답을 뺌으로써 수행될 수 있다. 그 구현예에서, 생성된 응답 요소는 rij = y(mi, mj) - y(mj)로서 형성될 수 있으며, 여기서 y(mj)는 1차 돌연변이 mj의 부모 균주 b0에 대한 적용에 의해 유발된 조직돤 집합 b 내의 조작된 배경 균주 bj의 반응이다. 정규화된 응답 행렬의 각 행은 상응하는 돌연변이에 대한 응답 프로파일로 취급된다는 것에 유의한다. 즉, i번째 행은 j = 1 내지 N에 대한 모든 배경 균주 bj에 적용된 상응하는 돌연변이 mi의 상대적 효과를 기술한다.
쌍을 이루는 돌연변이의 예와 관련하여, 2개의 돌연변이로부터 생성된 균주의 성능/반응은 개별적으로 돌연변이의 각각에 대한 균주의 성능/반응보다 크거나, 작거나 같을 수 있다. 이 효과는 "상위성"으로 알려져 있으며, 일부 실시태양에서, eij = y(mi, mj) - (y(mi) + y(mj)로 나타낼 수있다. 이런 수학 표현의 변형이 가능하며, 예를 들어 개별 변화가 생물학적으로 어떻게 상화작용하는지에 따라 달라질 수 있다. 상기한 바와 같이, 동일한 작용기로부터의 돌연변이는 동일한 메카니즘에 의해 작동하기 쉽고, 따라서 전체 숙주 성능에 대해 음성 또는 중성 상위성을 나타내기 쉽다. 반대로, 상이한 작용기로부터의 돌연변이는 독립적인 메카니즘에 의해 작동하기 쉽고, 이는 예를 들어 여분의 돌연변이 효과를 감소시킴으로써 개량된 숙주 수행을 유도할 수 있다. 따라서, 유사하지 않은 반응을 일으키는 돌연변이는 유사한 반응을 일으키는 돌연변이보다 부가적인 방식으로 결합하기 쉽다. 이것은 다음 단계에서 유사성 계산을 유도한다.
다섯째로, 분석 장비(214)는 응답들 사이의 유사성-쌍을 이루는 돌연변이 실시예에서, 응답 행렬(4204) 내에서 i번째 돌연변이와 j번째(예를 들어, 1차) 돌연변이의 영향 사이의 유사성을 측정한다. R의 i번째 행은 N개의 배경 균주에 대한 i번째 돌연변이 mi의 성능 영향을 나타내며, 이의 각각은 자체로 상기한 대로 조작된 돌연변이의 결과일 수 있다는 것을 상기한다. 따라서 i번째와 j번째 돌연변이의 영향 사이의 유사성은 유사성 행렬 S를 형성하기 위해 각각 i번째와 j번째 행, ρi및 ρj 사이의 유사성 sij로 각각 나타낼 수 있다. 유사성은 교차-상관관계 또는 절대 코사인 유사성, 예를 들어 sij = abs(cos(ρi, ρj)과 같은 많은 공지된 기술을 사용하여 측정될 수 있다.
코사인 유사성과 같은 메트릭에 대한 대안 또는 보완으로서, 응답 프로파일은 클러스터링되어 유사성의 등급을 결정할 수 있다. 클러스터링은 적절한 거리 측정(예를 들어, 유클리드(Euclidean), 해밍(Hamming) 등)과 함께 거리 기반 클러스터링 알고리즘(예를 들어, k-평균, 계층적 응집 등)의 사용에 의해 수행될 수 있다. 대안적으로, 클러스터링은 적절한 유사성 척도(예를 들어, 코사인, 상관관계 등)를 갖는 유사성 기반 클러스터링 알고리즘(예를 들어, 스펙트럼, 최소-커트 등)을 사용하여 수행될 수 있다. 물론, 거리 측정은 임의의 수의 표준 기능 작업(예를 들어, 지수 함수)을 통해 유사성 측정치로 매핑될 수 있고 그 반대의 경우도 가능하다. 일 구현예에서, 계층적 응집 클러스터링은 절대 코사인 유사성과 함께 사용될 수 있다.
클러스터링의 한 예로서, C를 k개의 구별된 클러스터로의 돌연변이 mi의 클러스터링이라하자. C를 클러스터 멤버십 행렬이라 하며, 여기서 cij는 돌연변이 i가 클러스터 j에 속하는 정도, 0과 1 사이의 값이다. 돌연변이 i와 j의 사이의 클러스터 기반 유사성은 CixCj(C의 i번째 및 j번째 행의 도트 곱)으로 제공된다. 일반적으로, 클러스터 기반의 유사성 행렬은 CCT(즉, C 곱 C-트랜스포즈)로 제공된다. 하드 클러스터링의 경우(돌연변이가 정확하게 하나의 클러스터에 속한다), 두 돌연변이 사이의 유사성은 동일한 클러스터에 속하면 1이고 그렇지 않은 경우 0이다.
Costanzo, The Genetic Landscape of a Cell, Science, Vol. 327, Issue 5964, Jan. 22, 2010, pp. 425-431(그 전문이 본 명세서에서 참조로 포함됨)에 기술된 바와 같이, 돌연변이 반응 프로파일의 이런 클러스터링은 세포의 근본적인 기능적 조직의 대강의 매핑에 관한 것이다. 즉, 함께 집단화되는 돌연변이는 근본적인 생물학적 과정이나 대사 경로와 관련되는 경향이 있다. 이런 돌연변이는 본 명발명에서는 "작용기"라고 부른다. 이 방법의 주요 관측은 두 돌연변이가 동일한 생물학적 과정 또는 경로에 의해 작동한다면, 관측된 효과(및 주목할만하게 관찰된 이점)가 중복될 수 있다는 것이다. 반대로, 두 개의 돌연변이가 구별된 메커니즘에 의해 작동한다면, 유익한 효과가 중복될 가능성이 적을 것이다.
여섯째, 상위성 효과에 기초하여, 분석 장비(214)는 비유사 응답을 유도하는 돌연변이의 쌍을 선택하는데, 예를 들어, 도 19(4206)에 도시된 바와 같이 이들의 코사인 유사성 메트릭이 유사성 임계치 아래로 떨어지거나 이들의 반응이 충분히 분리된 클러스터들 내에 있다. 이들의 비유사성에 근거하여, 선택된 쌍의 돌연변이는 유사한 쌍보다 배경 균주로 통합되어야 한다.
충분히 비유사한 응답을 유도하는 선택된 쌍의 돌연변이에 기초하여, LIMS 시스템(예를 들어, 인터프리터(204), 실행 엔진(207), 주문 배치기(208) 및 공장(210)의 모든 또는 일부 조합)이 그 선택된 돌연변이(4208)를 가진 미생물 균주를 디자인하는데 사용될 수 있다. 실시태양에서, 이하 및 본 발명의 다른 곳에서 기술된 바와 같이, 상위성 효과는 균주 선택을 가중하거나 여과하기 위해 예측 모델 속에서 형성될 수 있거나 예측 모델과 함께 사용될 수있다.
일부 바람직한 예측 모델을 통해 특정 배경 속에 라이브러리로부터의 돌연변이의 집합을 통합함으로써 얻어진 가상의 균주의 성능(즉, 점수)을 추정할 수 있다고 가정한다. 교시된 방법에서 이용된 대표적인 예측 모델은 "Computational Analysis and Prediction of Effects of Genome-Wide Genetic Design Criteria."의 더 큰 섹션에서 발견된 "Predictive Strain Design"란 제목의 이하 섹션에 제공된다.
선형 회귀와 같은 예측 균주 디자인 기술을 사용하는 경우, 분석 장비(214)는 단지 충분하게 비유사한 돌연변이를 유지하기 위해 회귀 결과를 필터링하여 낮은 유사성 척도를 가진 돌연변이에 모델을 제한할 수 있다. 대안적으로, 예측 모델은 유사성 행렬로 가중될 수 있다. 예를 들어, 일부 실시태양은 제안된 돌연변이의 상호의존성을 특성화하기 위해 유사성 행렬을 사용하여 가중된 최소 제곱 회귀(weighted least squares regression)를 이용할 수 있다. 한 예로서, 가중치 부여는 회귀 모델에 "커널" 트릭을 적용함으로써 수행될 수 있다. ("커널 트릭"이 많은 기계 학습 모델링 접근법에 일반적이기 때문에, 이런 재-가중 전략은 선형 회귀에 제한되지 않는다.)
이런 방법은 당업자에게 공지되어 있다. 실시태양에서, 커널은 요소 1 - w * sij를 갖는 행렬이고, 여기서 1은 단위 행렬의 요소이고, w는 0과 1 사이의 실수 값이다. w = 0일 때, 이것은 표준 회귀 모델로 감소한다. 실제로, w의 값은 쌍을 이루는 조합 구조체 및 이의 관련 효과 y (mi, mj)에 대해 평가될 때 예측 모델의 정확성(r2 값 또는 루트 평균 제곱 에러(RMSE))에 연결될 것이다. 하나의 간단한 구현예에서, w는 w = 1-r2로 정의된다. 이 경우, 모델이 완전히 예측 가능한 경우, w = 1-r2 = 0이고 통합은 예측 모델만을 기반으로 하며 통합은 상위성 매핑 절차만 기반으로 한다. 각각의 반복 동안, 정확도를 평가하여 모델 성능이 개량되는지 여부를 결정할 수 있다.
본 발명에 기재된 상위성 매핑 절차는 어느 모델이 분석 장비(214)에 의해 사용되는지에 의존하지 않는 것이 명백해야 한다. 이런 예측 모델을 고려하면, 조합 통합을 통해 돌연변이 라이브러리에 접근할 수 있는 모든 가상의 균주를 점수매기고 순위를 매기는 것이 가능하다.
일부 실시태양에서, 상위성 효과를 설명하기 위해, 비유사한 돌연변이 반응 프로파일은 예측 모델로부터 각 가상 균주와 연관된 점수 및 순위를 증대하기 위해 분석 모델(214)에 의해 사용될 수 있다. 이 절차는 대체로 점수의 재-가중화로서 생각될 수 있어서 비유사한 응답 프로파일을 가진 후보 균주(예를 들어, 클러스터의 다양성으로부터 얻은 균주)를 지지할 수 있다. 하나의 간단한 구현예에서, 균주는 비유사성 임계값을 만족하지 않거나 동일한 클러스터(적당한 가중치를 가짐)로부터 얻은 구성 돌연변이의 수만큼 감소된 점수를 가질 수 있다. 한 특정 구현예에서, 가상 균주의 성능 평가는 (다시 적당한 가중치에 의해) 가상의 균주와 관련된 구성 돌연변이의 모든 쌍과 관련된 유사성 행렬의 항의 합계만큼 감소될 수 있다.가상 균주는 이러한 증가된 점수를 사용하여 순위가 다시 매겨질 수 있다. 실제로, 이런 재-가중 계산은 초기 점수 추정과 함께 수행될 수 있다.
결과는 혼동하는 상위성 상호작용을 보다 효과적으로 피하기 위해 증가된 점수 및 순위를 가진 가상 균주의 집합이다. 가상 균주는 이 시점에서 만들어질 수 있거나 후속 분석이나 사용을 위해 다른 계산 방법으로 넘겨질 수 있다.
당업자는 본 발명에 기술된 바와 같이 상위성 매핑 및 반복적인 예측 균주 디자인이 단지 쌍을 이루는 돌연변이를 사용하는 것에 제한되지 않고 배경 균주에 더 많은 돌연변이를 동시에 적용하는 것으로 확장될 수 있음을 인식할 것이다. 다른 실시태양에서, 추가적인 돌연변이가 본 발명에 기재된 예측 방법에 따라 선택된 돌연변이를 사용하여 이미 돌연변이된 균주에 순차적으로 적용될 수 있다. 다른 실시태양에서, 상위성 효과는 서로 약간 다른 다수의 균주 배경에 동일한 유전자 변이를 적용하고 돌연변이된 균주 배경 사이에 양성 반응 프로파일에 임의의 유의한 차이가 있음을 나타냄으로써 귀속된다.
유전자 설계 및 미생물 공학:
표적화
뉴클레아제를 이용한 지시된 게놈 편집
대사 공학은 분자의 대사, 조절 및 이화 작용에 직간접적으로 관련된 주요 유전자의 변경에 크게 의존한다. 대사 경로를 변경하기 위해 게놈에 단일 뉴클레오타이드 다형성, 삽입 또는 결실과 같은 작고 큰 변화를 정확하게 도입하는 것이 종종 유용하다. 이러한 변화는 또한 프로모터, 터미네이터, 유전자, 또는 심지어 유전자 클러스터와 같은 더 큰 영역의 유전 물질을 도입, 결실 또는 대체하는 데 사용될 수 있다.
서열 상동성을 통해, 이들 crRNA는 Cas 뉴클레아제를 특정 외인성 유전 물질로 안내하며, 이는 또한 프로토스페이서 인접 모티프(PAM)로 알려진 뉴클레아제-특이적 서열을 함유해야 한다. CRISPR 복합체는 외래 DNA에 결합하여 이를 절단한다.
본 발명에 제공된 한 양태에서, 관심 분자 또는 생물학적 제제를 생성하는 관심 대사 경로를 함유하는 균류의 숙주 또는 부모 균주(예를 들어, 본 발명에 제공된 사상균류)는 CRISPR에 의해 변형될 수 있다. 한 실시태양에서, 형질전환될 수 있는 원형질체는 본 발명에 제공된 원형질체화 방법을 사용하여 숙주 또는 부모 균주로부터 생성되고 리보핵단백질 복합체(RNP-복합체 또는 CRISPR RNP)로 형질전환된다. RNP-복합체는 본 발명에 제공된 바와 같은 가이드 핵산(예를 들어, 가이드 RNA(gRNA))과 복합체화된 본 발명에 제공된 바와 같은 핵산 가이드된 뉴클레아제(예를 들어, Cas9)를 포함한다. RNA에 의해 가이드될 때, 핵산 가이드된 뉴클레아 제는 본 발명에서 RNA 가이드된 뉴클레아제 또는 RNA 가이드된 엔도뉴클레아제로 지칭될 수 있다. 가이드 핵산(예를 들어, gRNA)은 균류의 숙주 또는 부모 균주(예를 들어, 본 발명에 제공된 사상균류)에 존재하는 표적 유전자 또는 핵산 서열의 일부에 상보적인 가이드 서열인 표적화 단편을 포함할 수 있다. 한 실시태양에서, 원형질체는 2개 이상의 RNP-복합체로 형질전환되어 각각의 RNP-복합체가 가이드 핵산(예를 들어, gRNA)과 복합체화된 핵산 가이드된 엔도뉴클레아제(예를 들어, Cas9)를 포함할 수 있다. 일부 경우에, 2개 이상의 RNP-복합체에서 각각의 가이드 핵산(예를 들어, gRNA)은 상이한 표적 유전자 또는 핵산 서열에 상보적인 가이드 서열을 포함할 수 있다. 일부 경우에, 2개 이상의 RNP-복합체에서 각각의 가이드 핵산(예를 들어, gRNA)은 동일한 표적 유전자 또는 핵산 서열에 대한 가이드 서열을 포함할 수 있다. 3개 이상의 RNP-복합체가 있는 경우, 동일한 표적 유전자 또는 핵산 서열에 상보적인 가이드 서열을 포함할 수 있는 RNP-복합체의 서브 세트 및 상이한 표적 유전자 또는 핵산에 상보적인 가이드 서열을 포함할 수 있는 RNP-복합체의 서브 세트 또는 서브 세트들이 존재할 수 있다. 2개 이상의 RNP-복합체가 그들 각각의 표적화 단편을 통해 동일한 표적 핵산 서열로 향하는 경우, 각각의 RNP-복합체는 상기 표적 유전자 또는 핵산의 상이한 또는 분리된 부분에 상보적인 가이드 서열 또는 표적화 단편을 포함할 수 있다. 이들 실시태양에 더하여, 다중 유전자좌를 표적으로 하는 다중 gRNA는 동일한 세포 또는 유기체에서 발현될 수 있다 (gRNA의 다중 발현). 풀된 gRNA 라이브러리는 주어진 표현형에 중요한 유전자를 식별하는 데 사용될 수 있다. 전사 활성화 또는 억제뿐만 아니라 유전자 녹아웃에 대한 현재 라이브러리를 이용할 수 있다. 차세대 서열 분석의 힘과 결합된 CRISPR은 게놈 전체 스크리닝을 위한 강력한 시스템이 될 수 있다. 각각의 gRNA는 트랜스 활성화 crRNA(tracrRNA)에 어닐링된 CRISPR RNA(crRNA)를 포함하거나 crRNA 및 tracrRNA를 포함하는 단일 전사체를 포함하는 단일 gRNA(sgRNA)를 포함할 수 있다.
한 실시태양에서, 숙주 또는 부모 균류은 기능하는 NHEJ 경로를 갖는다. 이 실시태양에 추가로, 단일 RNP-복합체 또는 다수의 RNP-복합체를 갖는 숙주 또는 부모 균류으로부터 유래된 원형질체의 형질전환은 NHEJ 경로를 통해 복구되는 게놈에서 표적 유전자(들) 내에서 가닥 파괴(들)를 생성한다. NHEJ 경로를 사용한 복구는 표적 유전자(들) 내에서 삽입 결실을 유발할 수 있다. 표적 유전자(들)에서의 인델은 아미노산 결실, 삽입 또는 프레임 시프트 돌연변이를 일으켜서 표적 유전자(OR)의 오픈 리딩 프레임(ORF) 내에서 조기 정지 코돈을 초래할 수 있다. 추가의 실시태양에서, 표적 유전자(들) 내의 가닥 파괴는 상동성 지정 복구(HDR)를 사용하여 복구될 수 있다. 숙주 또는 부모 균류으로부터 유래된 원형질체를 공여체 DNA 서열과 함께 형질 전환함으로써 HDR 매개 복구가 촉진될 수 있다. 공여자 DNA 서열은 원하는 유전자 교란(예를 들어, 결실, 삽입 및/또는 단일 뉴클레오타이드 다형성)을 포함할 수 있다. 이 실시태양에서, RNP는 하나 이상의 gRNA에 의해 지정된 표적 유전자를 절단한다. 공여자 DNA는 이후 대사 경로 또는 관심 분자/생물학적 변형을 위해 원하는 유전자 교란을 포함시키기 위해 상동 재조합 기구의 주형으로 사용될 수 있다. 공여자 DNA는 단일 가닥, 이중 가닥 또는 이중 가닥 플라스미드일 수 있다. 공여자 DNA는 PAM 서열이 없거나 재분열을 방지하기 위해 스크램블, 변경 또는 비 기능적 PAM을 포함할 수 있다. 일부 경우에, 공여자 DNA는 기능성 또는 비 변경된 PAM 부위를 포함할 수 있다(도 56a-b 참조). 공여자 DNA에서 돌연변이 또는 편집된 서열(상동성 영역에 의해 플랭킹됨)은 돌연변이(들)이 게놈에 혼입된 후 RNP에 의한 재분열을 방지한다. 일부 실시태양에서, 기능성 NHEJ 경로를 갖지 않는 숙주 또는 부모 균류으로부터 유래된 원형질체에서 형질 전환을 수행함으로써 HDR 경로가 유리할 수 있다. NHEJ 경로의 비활성화는 본 발명에 제공된 임의의 방법을 사용하여 달성될 수 있다.
일부 실시태양에서, 원형질체는 RNP 복합체, 공여체 DNA 및 선택 가능한 마커를 포함하는 벡터와 공동 형질전환될 수 있다. 벡터는 단지 형질전환 가능한 원형질체의 확인 및/또는 생존을 가능하게 함으로써 다른 성분과 상호작용할 수 있다. 이것은 변형되고 정확하게 편집된 균주를 쉽게 식별할 수 있다. 플라스미드가 경화될 수 있기 때문에 반복적인 편집이 가능하다. 도 53 참조.
상기 실시태양에 추가로, 본 발명에 제공된 방법에 사용하기 위한 핵산 가이드된 뉴클레아제는 당업계에 공지되고/되거나 본 발명에 제공된 임의의 핵산 가이드된 뉴클레아제일 수 있다. 한 실시태양에서, 핵산 가이드된 뉴클레아제는 클래스 2 CRISPR-Cas 시스템 핵산 가이드된 뉴클레아제이다. 클래스 2 CRISPR-Cas 시스템 핵산 가이드된 뉴클레아제는 다음 중 하나 이상으로부터 선택될 수 있다: 본 발명에 기술된 유형 II,유형 IIA, 유형 IIB, 유형 IIC, 유형 V 및 유형 VI 핵산 가이드된 뉴클레아제. 클래스 2 CRISPR-Cas 시스템 핵산 가이드된 뉴클레아제는 다음 중 하나 이상일 수 있다: Cas9, Cas12a, Cas12b, Cas12c, Cas12d, Cas12e, Cas13a, Cas13b, Cas13c 또는 이의 동족체, 오르쏘로그, 돌연변이체, 변이체 또는 변형된 버전.
유전자 디자인에 순응하는 유기체
개시된 HTP 게놈 공학 플랫폼은 산업용 미생물 세포 배양물(예를 들어, A. 니거)로 예시되지만, 원하는 형질이 유전자 돌연변이 집단에서 확인될 수 있는 임의의 숙주 세포 유기체에 적용 가능하다.
또한, 도입부에서 설명된 바와 같이, 본 발명은 사상균류 시스템에서 숙주 세포 특성을 개선하고 그러한 시스템 사상균류의 발달을 이전에 막았던 많은 문제를 해결하기 위한 HTP 게놈 공학 플랫폼을 제공한다.
따라서, 본 발명에 사용된 용어 "미생물"은 광범위하게 해석되어야 한다. 미생물은 두 가지 원핵생물 영역인 박테리아와 고세균뿐만 아니라 특정 진핵생물 균류와 원생 생물을 포함한다. 그러나, 특정 양태에서, 곤충, 식물 및 동물과 같은 "보다 높은" 진핵생물이 본 발명에 교시된 방법에서 이용될 수 있다.
적합한 숙주 세포는 박테리아 세포, 조류 세포, 식물 세포, 균류 세포, 곤충 세포 및 포유류 세포를 포함하나 이에 제한되지 않는다. 한 예시적인 실시태양에서, 적합한 숙주 세포는 A. 니거를 포함한다.
한 실시태양에서, 본 발명에 제공된 방법 및 시스템은 배양 배지에서 다른 이런 요소로부터 용이하게 분리될 수 있고 자체를 복제할 수 있는 사상균류로부터 유래된 균류 요소를 사용한다. 예를 들어, 균류 요소는 포자, 번식물, 균사 단편, 원형질체 또는 미세펠렛일 수 있다. 한 바람직한 실시태양에서, 본 발명에 제공된 시스템 및 방법은 사상균류로부터 유래된 원형질체를 이용한다. 적합한 사상균류 숙주 세포는, 예를 들어, 자낭균문(Ascomycota), 불완전균문(Deuteromycota), 접합균문(Zygomycota) 또는 불완전균문(Fungi imperfecti)의 임의의 사상 형태를 포함한다. 적합한 사상균류 숙주 세포는, 예를 들어, 균류 아문의 임의의 사상 형태를 포함한다(예를 들어, 참조로 본 발명에 포함된 Hawksworth et al., In Ainsworth and Bisby's Dictionary of The Fungi, 8th edition, 1995, CAB International, University Press, Cambridge, UK 참조). 특정의 예시적이나 비 제한적인 실시태양에서, 사상균류 숙주 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스퍼길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 필리바시듐(Filibasidium), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 또는 텔레모프 또는 아나모프 및 이의 동의어 또는 분류학 동의어의 종의 세포일 수 있다. 한 실시태양에서, 사상균류는 A. 니거(A. niger) 그룹의 A. 니둘란스(A. nidulans), A. 오리재(A. oryzae), A. 소재(A. sojae) 및 아스퍼길루스로 이루어진 그룹으로부터 선택된다. 한 바람직한 실시태양에서, 사상균류는 아스퍼길루스 니거(Aspergillus niger)이다.
한 실시태양에서, 사상균류는 아스퍼길루스 포에티두스(Aspergillus foetidus) ACM 3996(= FRR 3558), 마그나포르테 그리씨아(Magnaporthe grisea) Guy-11 또는 파네로차에트 크리소스포리움(Phanerochaete chrysosporium) RP78로부터 선택된 생산 균주이다. 별도의 실시태양에서, 사상균류는 당업계에 공지된 A. 니거 생산 균주이다. 본 발명에 제공된 방법에 사용하기 위한 A. 니거 생산 균주의 예는 A. 니거 ATCC 11414, ATCC 1015, ACM 4992(=ATCC 9142), ACM 4993(=ATCC 10577), ACM 4994(=ATCC 12846), ATCC26550, ATCC 11414, N402, CBS 513.88 또는 NRRL3(ATCC 9029, CBS 120.49)을 포함할 수 있다.
본 발명의 다른 실시태양에서, 균류 종의 특정 돌연변이체는 본 발명에 제공된 방법 및 시스템에 사용된다. 한 실시태양에서, 본 발명에 제공된 고 처리량 및/또는 자동화 된 방법 및 시스템에 적합한 균류 종의 특정 돌연변이체가 사용된다. 이런 돌연변이체의 예는 매우 잘 원형질인 균주; 주로 또는 더욱 바람직하게는, 단일 핵을 갖는 원형질체만을 생산하는 균주; 미세적정 플레이트에서 효율적으로 재생하는 균주, 빠르게 재생하는 균주 및/또는 폴리뉴클레오타이드(예를 들어, DNA) 분자를 효율적으로 흡수하는 균주, 단일 클론의 분리를 방지하고 및/또는 배양액의 점도를 증가시키도록 복잡하게 되지 않는 배양액에서 균사를 생산하는 세포와 같은 저점도의 배양액을 생산하는 균주, 무작위 통합(예를 들어, 무능력하게된 비 상동성 말단 결합 경로) 또는 이들의 조합을 감소시킨 균주일 수 있다.
또 다른 실시태양에서, 본 발명에 제공된 방법 및 시스템에서 사용하기 위한 특정 돌연변이체 균주는 예를 들어, 우리딘-요구 돌연변이체 균주와 같은 선별가능한 마커 유전자가 없는 균주일 수 있다. 이들 돌연변이체 균주는 각각 pyrG 또는 pyrE 유전자에 의해 코딩되는 오로티딘 5 포스페이트 디카르복실라제(OMPD) 또는 오로테이트 p-리보실 트랜스퍼라제(OPRT)에서 결핍될 수 있다(T. Goosen et al., Curr Genet. 1987, 11 : 499 503 J. Begueret et al, Gene., 1984, 32: 487 92).
한 실시태양에서, 본 발명에 제공된 방법 및 시스템에서 사용하기 위한 특정 돌연변이체 균주는 보다 짧은 균사 및 보다 효모 유사 외관을 특징으로 하는 소형 세포 형태를 갖는 균주이다. 이러한 돌연변이체의 예는 US20140220689에 기재된 바와 같이 변경된 gas 1 발현을 갖는 사상균류 세포일 수 있다.
또 다른 실시태양에서, 본 발명에 제공된 방법 및 시스템에서 사용하기 위한 돌연변이 균주는 상동성 재조합에서 매우 효율적이고 및/또는 무작위 통합에서 극도로 비효율적인 방식으로 DNA 복구 시스템에서 변형된다. 동종 재조합에 의해 숙주 세포의 게놈으로 핵산 구조체의 표적화된 통합, 즉 소정의 표적 유전자좌에서의 통합의 효율은 숙주 세포의 증가된 상동성 재조합 능력 및/또는 감소된 비 상동성 재조합 능력에 의해 증가될 수 있다. 동종 재조합의 증대는 상동성 재조합에 관련된 하나 이상의 유전자(예를 들어, Rad51 및/또는 Rad52 단백질)를 과발현시킴으로써 달성될 수 있다. 본 발명의 숙주 세포에서 비 상동성 재조합 또는 비 상동성 말단 결합(NHEJ) 경로의 제거, 파괴 또는 감소는, 예를 들어, 항체, 화학적 억제제, 단백질 억제제, 물리적 억제제, 펩타이드 억제제 또는 비 상동성 재조합(NHR) 또는 NHEJ 경로(예를 들어, 효모 KU70 또는 효모 KU80 또는 이의 상동체)의 구성요소에 대항하는 안티-센스 또는 RNAi 분자의 사용과 같은 당업계에 공지된 임의의 방법에 의해 성취될 수 있다. 한 실시태양에서, 단일 비 상동성 말단 결합 경로의 활성은 억제되거나 감소된다. 다른 실시태양에서, 비 상동성 말단 결합 경로의 조합의 활성은 억제되거나 감소되어 비 상동성 말단 결합 경로의 하나의 활성이 손상되지 않은 상태로 유지된다. 또 다른 실시태양에서, 모든 비 상동성 말단 결합 경로의 활성은 감소되거나 억제된다. NHEJ 경로의 억제는 Arras SMD, Fraser JA (2016), "Chemical Inhibitors of Non-Homologous End Joining Increase Targeted Construct Integration in Cryptococcus neoformans" PloS ONE 11 (9): e0163049에 기술된 바와 같이 화학적 억제제를 사용하여 달성될 수 있으며, 이의 내용은 본 발명에 참조로 포함된다. NHEJ 경로의 비활성화 또는 감소를 촉진하기 위한 화학적 억제제(들) 로의 처리는 원형질체의 생성 전 및/또는 도중에 이루어질 수 있다. 선택적으로, 본 발명에 제공된 방법에서 사용하기 위한 숙주 세포는 NHR 경로의 하나 이상의 유전자(예를 들어, 효모 ku70, ku80 또는 상동체)에서 결핍될 수 있다. 이런 돌연변이의 예는 WO 05/95624에 기술된 바와 같은 결핍 hdfA 또는 hdfB 유전자를 가진 세포이다. 본 발명에 제공된 방법에서 사용하기 위한 숙주 세포에서 NHR을 억제하는데 사용하기 위한 화학적 억제제의 예는 Arras SDM et al (2016) Chemical Inhibitors of Non-Homologous End Joining Increase Targeted Construct Integration in Cryptococcus neoformans. PloS One 11(9)에 기술된 바와 같이 W7, 클로르프로마진, 바닐린, Nu7026, Nu7441, 미린, SCR7, AG14361 또는 이의 조합이다.
한 실시태양에서, 본 발명에 제공된 방법 및 시스템에 사용하기 위한 사상균류 세포의 돌연변이 균주는 비활성화된 또는 감소된 비 상동성 말단 결합 경로(NHEJ) 경로를 가지며 배양액(예를 들어, 심층 배양액)에서 배양될 때 효모 유사 비 균사체 형성 표현형을 보유한다.
다른 실시태양에서, 본 발명에 제공된 방법 및 시스템에 사용하기 위한 사상균류 세포는 화학적 억제제(예를 들어, W7, 클로르프로마진, 바닐린, Nu7026, Nu7441, 미린, SCR7, AG14361 또는 이들의 임의의 조합)에 의한 치료로 인해 비활성화되거나 감소된 NHEJ 경로를 가지며 배양액(예를 들어, 심층 배양액)에서 성장할 때 효모-유사 비-균사체 형성 표현형을 갖는다. 한 실시태양에서, 화학적 억제제는 W7이다. 도 29에 반영된 바와 같이, 사상균류 숙주 세포(예를 들어, A. 니거)는 숙주 균주에 의존할 수 있는 W7의 최소 억제 농도(MIC)로 처리될 수 있다.
일부 실시태양에서, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 클론 집단으로 분리된다. 일부 실시태양에서, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 분리 전에 형질 전환된다. 일부 실시태양에서, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 미세적정 플레이트 또는 미세적정 웰에서 클론 집단으로 분리된다. 상기 실시태양에 추가로, 클론 집단은 단일 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠릿으로부터 유래된다. 일부 실시태양에서, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 희석된 용액에 있으며, 단일 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠릿만이 미세적정 플레이트 또는 웰로 전달된다. 일부 실시태양에서, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 단일 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛으로 광학적으로 구별될 수 있는 농도로 희석된 후, 단독으로 마이크로 플레이트 또는 웰에 전달된다. 일부 실시태양에서, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 하나의 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠릿을 미세적정 플레이트 또는 웰로 전달할 수 있는 통계적 확률이 존재하는 푸아송 분포를 사용하여 희석된다. 일부 실시태양에서, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 미세적정 플레이트 또는 웰을 포함하는 임의의 용기로 전달된다. 일부 실시태양에서, 광학적 구별은 CellenONE, Berkeley Lights Beacon 기기, FACS 기기, Cytena 또는 다른 유사한 기기에 의해 수행된다. 본 발명에 제공된 방법에 사용하기 위해 단일 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠릿을 분리하기 위한 워크 플로우의 예는 도 54b에서 볼 수 있다. 상기 실시태양 중 임의의 것에 추가로, 포자, 번식체, 균사 단편, 원형질체 또는 마이크로 펠렛은 본 발명에 제공된 임의의 균류 세포로부터 유래될 수 있다. 한 실시태양에서, 균류 세포는 사상균류 세포이다. 사상균류 세포는 본 발명에 제공된 사상균류 세포, 예를 들어 A. 니거일 수 있다.
유전자 디자인 및
HTP
미생물 공학 플랫폼에서 활용을 위한 유전자 다양성 풀 생성
일부 실시태양에 있어서, 본 발명의 방법은 유전자 디자인으로서 특징화된다. 본 발명에 사용된 용어 유전자 디자인은 새로운 우수한 숙주 세포를 디자인하고 생성하기 위해 특정 유전자, 유전자의 일부, 프로모터, 종결 코돈, 5'UTR, 3'UTR 또는 다른 DNA 서열의 가장 최적의 변이체의 확인 및 선택을 통한 숙주 유기체 게놈의 재구성 또는 변형을 의미한다.
일부 실시태양에서, 본 발명의 유전자 디자인 방법의 제 1 단계는 새로운 숙주 게놈이 재구성될 수 있는 복수의 서열 변형을 갖는 초기 유전자 다양성 풀 집단을 얻는 것이다.
일부 실시태양에서, 본 발명에 교시된 유전자 디자인 방법의 후속 단계는 상기한 HTP 분자 도구 세트(예를 들어, SNP 스와핑 또는 프로모터 스와핑)의 하나 이상을 사용하여 HTP 유전자 디자인 라이브러리를 구축한 다음, 숙주 세포에서의 시험을위한 특정 게놈 변형의 라이브러리를 제공함으로써 게놈 공학 과정의 동인으로서 작용하는 것이다.
현존하는 야생형 균주로부터의 다양성 풀 사용하기
일부 실시태양에서, 본 발명은 소정의 야생형 집단의 미생물 중에서 존재하는 서열 다양성을 확인하는 방법을 교시한다. 따라서, 다양성 풀은 분석을 위해 사용된 소정의 수 n개의 야생형 미생물일 수 있으며, 상기 미생물의 게놈은 "다양성 풀"을 나타낸다.
일부 실시태양에서, 다양성 풀은 상기 야생형 미생물 중 자연적 유전자 변이에 존재하는 현존하는 다양성의 결과일 수 있다. 이 변이는 소정의 숙주 세포의 균주 변이체로부터 얻을 수 있고 미생물이 완전히 다른 종인 결과일 수도 있다. 유전자 변이는 자연 발생 여부와 상관없이 균주의 유전자 서열에서 어떠한 차이도 포함할 수 있다. 일부 실시태양에서, 유전자 변이는 다른 것들 중에서 SNP 스왑, PRO 스왑, 개시/정지 코돈 스왑 또는 STOP 스왑을 포함할 수 있다.
현존하는 산업용 균주 변이체로부터의 다양성 풀 사용하기
본 발명의 다른 실시태양에서, 다양성 풀은 전통적인 균주 개량 과정 동안 생성된 균주 변이체(예를 들어, 무작위 돌연변이를 통해 생성되고 수년 동안 개량된 수율을 위해 선택된 하나 이상의 숙주 유기체 균주)이다. 따라서, 일부 실시태양에서, 다양성 풀 또는 숙주 유기체는 역사적 생산 균주의 집합을 포함할 수 있다.
다양성 풀은 특정 시점(S1Gen1)에서 "기준선" 유전자 서열을 갖는 본래의 부모 균주(S1) 및 상기 S1 균주로부터 유도/성장되고 S1의 기준선 게놈과 관련하여 다른 게놈(S2- n Gen2- n )을 갖는 임의의 수의 후속 자손 균주(S2- n 로 일반화될 수 있는 S2, S3, S4, S5, 등)일 수 있다.
예를 들어, 일부 실시태양에서, 본 발명은 다양성 풀에서 미생물 게놈을 서열화하여 각 균주에 존재하는 SNP를 확인하는 것을 교시한다. 한 실시태양에서, 다양성 풀의 균주는 역사적인 미생물 생산 균주이다. 따라서, 본 발명의 다양성 풀은 예를 들어 산업용 표준 균주 및 전통적인 균주 개량 프로그램을 통해 생산된 하나 이상의 돌연변이 산업용 균주를 포함할 수 있다.
다양성 풀 내의 모든 SNPS가 확인되면, 본 발명은 개별적으로 및/또는 그룹으로 SNP의 효과(예를 들어, 관심 표현형의 생성)를 묘사(즉, 정량화 및 특성화)하기 위한 SNP 스와핑 및 선별 방법을 교시한다. 따라서, 상기한 바와 같이, 교시된 플랫폼에서의 초기 단계는 복수의 서열 변이체, 예를 들어 SNP를 가진 초기 유전자 다양성 풀 집단을 얻는 것을 수 있다. 그런 후에, 교시된 플랫폼의 후속 단계는 상기한 HTP 분자 도구 세트(예를 들어, SNP 스와핑 또는 프로모터 스와핑)의 하나 이상을 사용하여 HTP 유전자 디자인 라이브러리를 구축한 다음, 숙주 세포에서의 시험을위한 특정 게놈 변형의 라이브러리를 제공함으로써 게놈 공학 과정의 동인으로서 작용하는 것이다.
일부 실시태양에서, 본 발명의 SNP 스와핑 방법은 돌연변이된 균주(예를 들어, S 2-n Gen 2-n 으로부터 균주)에서 확인된 하나 이상의 SNP를 표준 균주(S1Gen1) 또는 야생형 균주에 도입하는 단계를 포함한다.
다른 실시태양에서, 본 발명의 SNP 스와핑 방법은 돌연변이된 균주(예를 들어, S 2-n Gen 2-n 으로부터 균주)에서 확인된 하나 이상의 SNP를 제거하는 단계를 포함한다.
돌연변이유발을 통해 다양성 풀 만들기
일부 실시태양에서, 세포의 소정의 다양성 집단에서 관심 돌연변이는 돌연변이유발 화학물질 또는 방사선을 포함하는 돌연변이 균주를 위한 임의의 수단에 의해 인위적으로 생성될 수 있다. 용어 "돌연변이유발"은 본 발명에서 세포질 핵산 물질에서 하나 이상의 유전자 변형을 유도하는 방법을 의미하기 위해 사용된다.
용어 "유전자 변형"은 DNA의 임의의 변경을 말한다. 대표적인 유전자 변형은 뉴클레오타이드 삽입, 결실, 치환 및 이들의 조합을 포함하며, 단일 염기만큼 작거나 수만 염기만큼 클 수 있다. 따라서, 용어 "유전자 변형"은 뉴클레오타이드 서열의 역전 및 염색체의 영역을 포함하는 DNA의 위치 또는 배향이 변경되는 다른 염색체 재배열을 포함한다. 염색체 재배열은 염색체 내 재배치 또는 염색체 간 재배치를 포함할 수 있다.
한 실시태양에서, 현재 청구된 주제에 사용된 돌연변이유발 방법은 실질적으로 무작위라서 유전자 돌연변이가 돌연변이유발될 핵산 물질 내의 임의의 이용 가능한 뉴클레오타이드 위치에서 발생할 수 있다. 달리 말하면, 한 실시태양에서, 돌연변이유발은 특정 뉴클레오타이드 서열에서 발생의 우선성성 또는 증가 빈도를 나타내지 않는다.
본 발명의 방법은 자외선, X-레이 방사선, 감마선 방사선, N-에틸-N-나이트로소우레아(ENU), 메틸나이트로우레아(MNU), 프로카바진(PRC), 트라이에틸렌 멜라민(TMS), 아크릴아마이드 모노머(AA), 클로람부실(CHL), 멜팔란(MLP), 사이클로포스파미드(CPP), 다이에틸 설페이트(DES), 에틸 메테인 설포네이트(EMS), 메틸 메테인 설포네이트(MMS), 6-머캡토퓨린(6-MP), 마이토마이신-C(MMC), N-메틸-N'-나이트로-N-나이트로소구아니딘(MNNG), 3H2O 및 우레탄(UR)(예를 들어, Rinchik, 1991; Marker et al., 1997; and Russell, 1990 참조). 추가적인 돌연변이유발 인자는 http://www.iephb.nw.ru/~spirov/hazard/mutagen_lst.html에 기재된 것을 포함하여 당업자에게 주지되어 있다.
용어 "돌연변이유발"은 또한 세포 기능을 변경(예를 들어, 표적화된 돌연변이에 의해) 또는 세포 기능을 조절하여 돌연변이유발의 속도, 품질 또는 범위를 향상시키는 방법을 포함한다. 예를 들어, 세포는 DNA 수리, 돌연변이원 대사, 돌연변이원 감수성, 게놈 안정성 또는 이들의 조합에서 기능장애 또는 결핍이 되도록 변형되거나 조절될 수 있다. 따라서 정상적으로 게놈 안정성을 유지하는 유전자 기능의 파괴는 돌연변이유발을 향상시키는데 사용될 수 있다. 파괴의 대표 표적은 DNA 리가아제 I(Bentley et al, 2002) 및 카제인 키나아제 I(미국 특허 제6,060,296 호)를 포함하나 이에 제한되지 않는다.
일부 실시태양에서, 부위-특이적 돌연변이유발(예를 들어, 변형기 부위 유도 돌연변이유발 키트(Clontech)와 같은 상업적으로 구입할 수 있는 키트를 사용한 프라이머-유도 돌연변이유발)를 사용하여 핵산 서열 전체에 걸쳐 순서대로 다수의 변화를 일으킨다 본 발명의 절단 효소를 코딩하는 핵산을 생성한다.
하나 이상의 돌연변이유발 인자에 노출시 유전자 돌연변이의 빈도는 치료의 투여량 및/또는 반복을 변화시킴으로써 조절될 수 있으며, 특정 용도에 맞게 조절될 수 있다.
따라서, 일부 실시태양에서, 본 발명에 사용된 "돌연변이유발"은 본 발명에 기술된 기술의 임의의 것에 의한 오류 경향성 PCR 돌연변이유발, 올리고뉴클레오타이드 유도 돌연변이유발, 부위 유발성 돌연변이유발 및 반복적인 서열 재조합을 포함하는 돌연변이를 유도하기 기술 분야에 공지된 모든 기술을 포함한다.
다양성을 생성하기 위한 단일 유전자좌 돌연변이
일부 실시태양에서, 본 발명은 게놈 DNA의 선택된 부분을 도입, 결실 또는 치환함으로써 세포 집단을 돌연변이하는 것을 교시한다. 따라서, 일부 실시태양에서, 본 발명은 돌연변이를 특정 유전자좌에 대한 돌연변이를 표적화하는 방법을 교시한다. 다른 실시태양에서, 본 발명은 표적 DNA 영역을 선택적으로 편집하기 위해 ZFNs, TALENS 또는 CRISPR과 같은 유전자 편집 기술의 사용을 교시한다.
다른 실시태양에서, 본 발명은 숙주 유기체의 외부에서 선택된 DNA 영역을 돌연변이시킨 다음 돌연변이된 서열을 숙주로 유기체 속에 역삽입하는 것을 교시한다. 예를 들어, 일부 실시태양에서, 본 발명은 다양한 발현 성질을 갖는 다양한 프로모터 변이체를 생성하기 위해 천연 또는 합성 프로모터를 돌연변이하는 것을 교시한다(이하 프로모터 래더 참조). 다른 실시태양에서, 본 발명은 ProSAR(Fox et al, 2007. 본 발명에 참조로 포함된 "Improving catalytic function by ProSAR-driven enzyme evolution." Nature Biotechnology Vol 25 (3) 338-343)와 같은 단일 유전자 최적화 기술과 양립된다.
일부 실시태양에서, DNA의 선택된 영역은 천연 변이체의 유전자 셔플링 또는 합성 올리고체, 플라스미드-플라스미드 재조합, 바이러스 플라스미드 재조합, 바이러스-바이러스 재조합에 의한 셔플링을 통해 시험관 내에서 생성된다. 다른 실시태양에서, 게놈 영역은 에러-유발PCR(error-prone PCR)을 통해 생성된다.
일부 실시태양에서, 선택된 유전자 영역에서의 돌연변이 생성은 "재조립 PCR"에 의해 달성된다. 간략하게, 올리고뉴클레오타이드 프라이머 (올리고)는 관심 핵산 서열의 단편의 PCR 증폭을 위해 합성되어, 올리고뉴클레오타이드의 서열은 두 단편의 교차점과 겹쳐진다. 겹쳐진 영역은 전형적으로 약 10 내지 100개 뉴클레오타이드 길이이다. 단편의 각각은 이런 프라이머 세트로 증폭된다. 그런 다음 PCR 제품은 재조립 프로토콜에 따라 "재조립"된다. 요약하면, 어셈블리 프로토콜에서, PCR 생성물은 먼저, 예를 들어, 겔 전기영동 또는 크기 배제 크로마토그래피에 의해 프라이머로부터 정제된다. 정제된 생성물은 함께 혼합되고 추가 프라이머가 없이 중합 효소 및 데옥시뉴클레오시드 트라이포스페이트(dNTP's) 및 적절한 버퍼 염의 존재하에서 약 1-10 사이클의 변성, 재어닐링 및 확장이 실시된다("셀프-프라이밍"). 유전자에 인접한 프라이머로 후속 PCR이 사용되어 완전히 재조합되고 뒤섞인 유전자의 수율을 증폭시킨다.
본 발명의 일부 실시태양에서, 위에서 논의한 것과 같은 돌연변이된 DNA 영역이 돌연변이체 서열에 대해 농축되어 다중 돌연변이체 스펙트럼, 즉 돌연변이의 가능한 조합이 보다 효율적으로 표본추출된다. 일부 실시태양에서, 돌연변이된 서열은 재조립 반응 이전에 시험관 내에서 친화성-정제 물질을 증폭시키는 바람직한 단계 의해 mutS 단백질 친화성 매트릭스를 통해 확인된다(Wagner et al., Nucleic Acids Res. 23(19):3944-3948 (1995); Su et al., Proc. Natl. Acad. Sci. (U.S.A.), 83:5057-5061(1986)). 이 증폭된 물질은 이후 본 발명의 후반부에서 설명하는 바와 같이 조립 또는 재조립 PCR 반응에 투입된다.
프로모터 래더
프로모터는 유전자가 전사되는 속도를 조절하고 다양한 방식으로 전사에 영향을 미칠 수 있다. 예를 들어, 구조성 프로모터는 내부 또는 외부 세포 조건에 관계없이 일정한 비율로 관련 유전자의 전사를 지시하지만, 조절 가능한, 조율 가능한 또는 유도 가능한 프로모터는 내부 및/또는 외부 세포, 예를 들어, 성장 속도, 온도, 특정 환경 화학물질에 대한 반응 등에 따라 유전자가 전사되는 속도를 증가 또는 감소시킨다. 프로모터는 정상적인 세포 컨텍스트로부터 격리될 수 있으며 사실상 모든 유전자의 발현을 조절하도록 조작되어 세포 성장, 생산 수율 및/또는 기타 관심 표현형의 효과적인 변형을 가능하게 한다.
프로모터 서열은 본 발명에 제공된 사상균류 숙주 세포에서 발현되도록 본 발명에 제공된 임의의 서열의 5' 말단에 작동 가능하게 연결될 수 있다. 다양한 공지의 균류 프로모터는, 예를 들어 C1 엔도글루카나제의 프로모터 서열, 55 kDa 셀룰로오스바이오하이드롤라제(CBH1), 글리세르알데하이드-3-포스페이트 탈수소 효소 A, C. 크라이소스포리움으로부터의 GARG 27K 및 30 kDa 자일라나제(Xy1F) 프로모터뿐만 아니라 미국 특허 미국 특허 4,935,349; 5,198,345; 5,252,726; 5,705,358; 및 5,965,384; 및 PCT 출원 WO 93/07277에 기술된 아스퍼킬루스 프로모터와 같은 본 발명으 숙주 균주에서 기능성일 수 있다. 한 실시태양에서, 본 발명에 제공된 방법 및 시스템에 사용하기 위한 프로모터는 유도성 프로모터이다. 유도성 프로모터는 전사 활성이 화학 물질, 예를 들어 알코올, 테트라사이클린, 스테로이드, 금속 또는 당업계에 공지된 다른 화합물의 존재 또는 부재에 의해 조절되는 임의의 프로모터일 수 있다. 유도성 프로모터는 전사 활성이 빛 또는 저온 또는 고온의 존재 또는 부재에 의해 조절되는 임의의 프로모터일 수 있다. 한 실시태양에서, 유도 성 프로모터는 srpB 유전자, amyB 유전자, manB 유전자 또는 mbfA 유전자와 같은 사상균류 유전자로부터 선택된다. 한 실시태양에서, 유도성 프로모터는 표 1에 열거된 프로모터로부터 선택된다. 한 실시태양에서, 유도성 프로모터는 포도당에 의해 억제된 이화 대사물이다.
일부 실시태양에서, 본 발명은 하류 유전자 디자인 방법에서 사용하기 위한 프로모터 래더 라이브러리를 생산하는 방법을 교시한다. 예를 들어, 일부 실시태양에서, 본 발명은 하나 이상의 프로모터를 확인하고 및/또는 다양한 발현 강도 또는 우수한 조절 특성을 나타내는 숙주 세포 내 하나 이상의 프로모터의 변이체를 생성하는 방법을 교시한다. 이들 확인된 및/또는 생성된 프로모터의 특정 조합은 프로모터 래더로서 함께 그룹화될 수 있으며, 이는 보다 상세히 후술된다.
일부 실시태양에서, 본 발명은 프로모터 래더의 사용을 교시한다. 일부 실시태양에서, 본 발명의 프로모터 래더는 연속 범위의 발현 프로파일을 나타내는 프로모터를 포함한다. 예를 들어, 일부 실시태양에서, 프로모터 래더는 자극, 또는 구성성 발현을 통해 다양한 발현 강도를 나타내는 자연, 고유 또는 야생형 프로모터를 확인함으로써 생성된다(예를 들어, 도 13). 이러한 확인된 프로모터는 프로모터 래더로서 함께 그룹화될 수 있다.
다른 실시태양에서, 본 발명은 상이한 조건에 걸쳐 다양한 발현 프로파일을 나타내는 프로모터 래더의 생성을 교시한다. 예를 들어, 일부 실시태양에서, 본 발명은 발효의 상이한 단계에 전체에서 퍼진 발현 피크를 갖는 프로모터의 래더를 생성하는 것을 교시한다. 다른 실시태양에서, 본 발명은 특정 자극에 반응하여 상이한 발현 피크 동역학을 갖는 프로모터의 래더를 생성하는 것을 교시한다(도 13 참조). 당업자는 본 개시의 조절 프로모터 래더가 임의의 하나 이상의 조절 프로파일을 나타낼 수 있다는 것을 인식할 것이다.
일부 실시태양에서, 본 발명의 프로모터 래더는 연속적인 범위의 반응에 걸쳐 예측 가능한 방식으로 유전자 발현을 교란시키도록 디자인되었다. 일부 실시태양에서, 프로모터 래더의 연속 특성은 균주 개량 프로그램에 추가의 예측력을 제공한다. 예를 들어, 일부 실시태양에서, 선택된 대사 또는 신호 전달 경로의 스와핑 프로모터 또는 종결 서열은 가장 최적의 발현 비율 또는 프로파일을 확인하는 숙주 세포 성능 곡선을 생성할 수 있다; 부적절한 환경에서 불필요한 과발현이나 잘못된 발현을 피하면서 표적 유전자가 더 이상 특정 반응이나 유전자 캐스케이드에 대한 제한 요소가 되지 않는 균주를 생산한다. 선택될 수 있는 예시적인 신호 전달 경로는 숙주 세포 형태를 제어하거나 영향을 주는 역할을 하는 것으로 확인되었거나 그 역할을하는 것으로 의심되는 신호 전달 경로일 수 있다. 따라서, 일부 실시태양에서, 형태를 제어하거나 영향을 미치는 것으로 입증되거나 또는 의심되는 유전자에 대한 스와핑 프로모터는 형태와 관련하여 숙주 세포 성능 곡선을 생성할 수 있다; 부적절한 환경에서 불필요한 과발현이나 잘못된 발현을 피하면서 표적 유전자가 더 이상 특정 반응이나 유전자 캐스케이드에 대한 제한 요소가 되지 않는 균주를 생산한다. 형태를 제어하거나 영향을 미치는 것으로 입증되거나 또는 의심되는 유전자의 예는 당업계에 공지되거나 본 발명에 제공된 임의의 그러한 유전자일 수 있다. 일부 실시태양에서, 프로모터 래더는 원하는 프로파일을 나타내는 자연, 고유 또는 야생형 프로모터를 확인함으로써 생성된다. 다른 실시태양에서, 프로모터 래더는 자연 발생 프로모터를 돌연변이시켜 다수의 돌연변이 프로모터 서열을 유도함으로써 생성된다. 이들 돌연변이된 프로모터의 각각은 표적 유전자 발현에 대한 효과에 대해 시험된다. 일부 실시태양에서, 편집된 프로모터는 다양한 조건에 걸쳐 발현 활성에 대해 시험되어 각 프로모터 변이체의 활성이 문서화/특징화/주석처리되고 데이터베이스에 저장된다. 생성된 편집된 프로모터 변이체는 뒤이어 그 발현의 강도에 기초하여 배열된 프로모터 래더로 조직화된다(예를 들어, 상부 근처의 고도로 발현된 변이체 및 하부 근처의 약화된 발현에 의해, 따라서 "래더"라는 용어를 유도한다).
일부 실시태양에서, 본 발명은 확인된 자연 발생 프로모터 및 돌연변이된 변이체 프로모터의 조합인 프로모터 래더를 교시한다.
일부 실시태양에서, 본 발명은 하기 기준을 모두 만족하는: 1) 구조성 프로모터의 래더를 나타내며; 2) 이상적으로 100개 염기쌍 미만의 짧은 DNA 서열에 의해 암호화될 수 있는 자연, 고유 또는 야생형 프로모터를 확인하는 방법을 교시한다. 일부 실시태양에서, 본 발명의 구조성 프로모터는 두 개의 선택된 성장 조건 (전형적으로, 산업용 재배 동안 경험된 조건들 간에 비교됨)에 걸쳐 일정한 유전자 발현을 나타낸다. 일부 실시태양에서, 본 발명의 프로모터는 ~60 염기쌍 코어 프로모터 및 26-40 염기쌍 길이의 5' UTR로 구성될 것이다.
일부 실시태양에서, 상기 확인된 자연 발생 프로모터 서열 중 하나 이상이 유전자 편집을 위해 선택된다. 일부 실시태양에서, 자연 프로모터는 상기 임의의 돌연변이 방법을 통해 편집된다. 다른 실시태양에서, 본 발명의 프로모터는 원하는 서열을 갖는 새로운 프로모터 변이체를 합성함으로써 편집된다.
2015년 12월 07일에 출원된 미국 특허 출원 제 62/264,232호 및 2016년 12월 7일에 츨원된 국제 출원 No. PCT/US2016/06564의 전체 개시 내용은 모든 목적을 위해 그 전문이 본 발명에 참고로 포함된다.
본 발명의 프로모터의 비 제한적인 리스트가 하기 표 1에 제공된다. 프로모터 서열의 각각은 이종 프로모터 또는 이종 프로 프로모터 뉴클레오타이드로 불릴 수 있다.
본 발명의 선택된 프로모터 서열
|
SEQ
ID NO:
|
프로모터 짧은 명칭
|
프로모터 명칭
|
| 1 |
manBp |
아스퍼길루스 니거로부터의
manB 프로모터 |
| 2 |
amyBp |
아스퍼길루스 오리재로부터의
amyB 유전자 |
| 3 |
srpBp |
아스퍼길루스 니거로부터의
srpB 프로모터 |
| 4 |
mbfAp |
아스퍼길루스 니거로부터의 mbfA 프로모터 |
일부 실시태양에서, 본 발명의 프로모터는 상기 표 1로부터의 프로모터와 적어도 100%, 99%, 98%, 97%, 96%, 95%, 94%, 93%, 92%, 91%, 90%, 89%, 88%, 87%, 86%, 85%, 84%, 83%, 82%, 81%, 80%, 79%, 78%, 77%, 76%, 또는 75% 서열 동일성을 나타낸다.
터미네이터 래더
일부 실시태양에서, 본 발명은 3' 위치에서 하나 이상의 전사 종결 서열을 RNA 암호화 요소의 말단에 제공함으로써 유전적으로 조작된 숙주 균주를 개량시키는 방법을 교시한다. 일부 실시태양에서, 본 발명은 종결 서열의 첨가가 유전적으로 조작된 숙주에서 선택된 유전자의 RNA 전사 효율을 개선시킨다는 것을 교시한다. 다른 실시태양에서, 본 발명은 종결 서열의 첨가가 유전적으로 조작된 숙주에서 선택된 유전자의 RNA 전사 효율을 감소시킨다는 것을 교시한다. 따라서, 일부 실시태양에서, 본 발명의 터미네이터 래더는 다양한 전사 효율을 나타내는 터미네이터 서열(예를 들어, 하나의 약한 터미네이터, 하나의 평균 터미네이터 및 하나의 강한 프로모터)을 나타내는 일련의 터미네이터 서열을 포함한다.
전사 종결 서열은 임의의 뉴클레오타이드 서열일 수 있으며, 이는 임의의 뉴클레오타이드 서열일 수 있으며, 이는 오픈 리딩 프레임을 암호화하는 뉴클레오타이드 서열의 전사 하류에 위치될 때, 오픈 리딩 프레임의 전사 종료를 일으킨다. 이런 서열은 당업계에 공지되어 있으며 원핵생물, 진핵생물 또는 파지 기원일 수 있다. 터미네이터 서열의 예로는 PTH-터미네이터, pET-T7 터미네이터, T3-Tφ 터미네이터, pBR322-P4 터미네이터, 수포성 스트라마티스 바이러스 터미네이터, rrnB-T1 터미네이터, rrnC 터미네이터, TTadc 전사 터미네이터 및 Matα(α 인자) 전사 터미네이터, 고유 α-인자 전사 종결 서열, ADR1 전사 종결 서열, ADH2 전사 종결 서열 및 GAPD 전사 종결 서열과 같은 효모-인식 종결 서열을 포함하나 이에 제한되지 않는다. 전사 종결 서열의 포괄적인 목록은 http://partsregistry.org/Terminators/Catalog에서 구입할 수 있는 iGEM 레지스트리에서 발견될 수 있다.
일부 실시태양에서, 전사 종결 서열은 폴리머라제-특이적이거나 비특이적일 수 있지만, 본 실시태양에서 사용하기 위해 선택된 전사 터미네이터는 선택된 프로모터와 '기능적 조합'을 형성해야 하는데, 이는 터미네이터 서열이 프로모터에서 개시되는 RNA 폴리머라제의 유형에 의한 전사를 종결시킬 수 있어야 한다는 것을 의미한다. 예를 들어, 일부 실시태양에서, 본 발명은 진핵생물 RNA pol II 프로모터 및 진핵생물 RNA pol II 터미네이터, T7 프로모터 및 T7 터미네이터, T3 프로모터 및 T3 터미네이터, 효모- 인식 프로모터 및 효모-인식 종결 서열 등은 일반적으로 기능적 조합을 형성할 것임을 교시한다. 사용된 전사 종결 서열의 상동성은 또한 전사가 소정의 프로모터로부터 종결되는 효율에 기초하여 선택될 수 있다. 예를 들어, 이종성 전사 터미네이터 서열은 RNA 암호화 요소의 전사 하류에 제공되어 소정의 프로모터로부터 적어도 60%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 91%, 적어도 92%, 적어도 93%, 적어도 94%, 적어도 95%, 적어도 96%, 적어도 97%, 적어도 98% 또는 적어도 99%의 종결 효율을 달성할 수 있다.
일부 실시태양에서, 조작된 발현 구조체로부터의 RNA 전사 효율은 3' 위치에 2개 이상의 헤어핀을 포함하는 2차 구조를 형성하는 핵산 서열을 RNA 암호화 요소의 말단에 제공함으로써 개선될 수 있다. 특정 이론에 얽매이기를 원하지 않으며, 2차 구조는 전사 신장 복합체를 불안정화시키고 폴리머라제가 DNA 주형으로부터 분리되게 하여, 비 기능성 서열의 비생산적인 전사를 최소화하고 목적하는 RNA의 전사를 증가시킨다. 따라서, 2개 이상의 인접한 헤어핀을 포함하는 2차 구조를 형성하는 종료 서열이 제공될 수 있다. 일반적으로, 헤어핀은 자체가 접혀서 암이 단일 가닥 루프에 의해 연결되는 쌍을 이루는 스템 영역을 형성할 수 있는 회문식 뉴클레오타이드 서열에 의해 형성될 수 있다. 일부 실시태양에서, 종결 서열은 2, 3, 4, 5, 6, 7, 8, 9, 10개 이상의 인접한 헤어핀을 포함한다. 일부 실시태양에서, 인접한 헤어핀은 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 또는 15개의 쌍을 이루지 않는 뉴클레오타이드에 의해 분리된다. 일부 실시태양에서, 헤어핀 스템은 길이가 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30개 이상의 염기쌍 길이를 포함한다. 특정 실시태양에서, 헤어핀 스템은 12 내지 30개 염기쌍 길이이다. 특정 실시태양에서, 종결 서열은 약 9 내지 25개 염기쌍을 포함하는 스템 영역을 갖는 둘 이상의 중간 크기의 헤어핀을 포함한다. 일부 실시태양에서, 헤어핀은 1, 2, 3, 4, 5, 6, 7, 8, 9 또는 10개 뉴클레오타이드의 루프 형성 영역을 포함한다. 일부 실시태양에서, 루프 형성 영역은 4-8개 뉴클레오타이드를 포함한다. 특정 이론에 얽매이기를 원하지 않으며, 2차 구조의 안정성은 종단 효율과 관련될 수 있다. 헤어핀의 안정성은 길이, 불일치(mismatches) 또는 이를 함유하는 돌출(bulges)의 수 및 쌍을 이루는 영역의 염기 구성에 의해 결정된다. 구아닌과 시토신 사이의 결합은 3개의 수소 결합을 가지며 2개만 있는 아데닌-티민 결합에 비해 더 안정하다. 헤어핀 형성 회문식 뉴클레오타이드 서열의 G/C 함량은 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90% 이상일 수 있다. 일부 실시태양에서, 헤어핀 형성 회문식 뉴클레오타이드 서열의 G/C 함량은 적어도 80%이다. 일부 실시태양에서, 종결 서열은 원핵생물, 진핵생물 또는 파지 기원의 하나 이상의 전사 종결 서열로부터 유도된다. 일부 실시태양에서, 일련의 4, 5, 6, 7, 8, 9, 10개 이상의 아데닌(A)을 암호화하는 뉴클레오타이드 서열은 종결 서열에 대해 3'에 제공된다.
일부 실시태양에서, 본 발명은 일련의 탠덤 종결 서열의 사용을 교시한다. 일부 실시태양에서, 일련의 2, 3, 4, 5, 6, 7개 이상의 첫 번째 전사 터미네이터 서열은 dsRNA 암호화 요소의 최종 뉴클레오타이드에 대해 직접 3' 또는 dsRNA 암호화 요소의 최종 뉴클레오타이드에 대해 적어도 1-5, 5-10, 10-15, 15-20, 20-25, 25-30, 30-35, 35-40, 40-45, 45-50, 50-100, 100-150, 150-200 , 200-300, 300-400, 400-500, 500-1,000개 이상의 뉴클레오타이드 3'의 거리에 놓일 수 있다. 탠덤 전사 터미네이터 서열 사이의 뉴클레오타이드의 수는 변할 수 있으며, 예를 들어, 전사 터미네이터 서열은 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 10-15, 15-20, 20-25, 25-30, 30-35, 35-40, 40-45, 45-50개 이상의 뉴클레오타이드에 의해 분리될 수 있다. 일부 실시태양에서, 전사 터미네이터 서열은 구조 예측 알고리즘에 의해 결정된 바와 같이 이들의 예측된 2차 구조에 기초하여 선택될 수 있다. 구조 예측 프로그램은 당업계에 주지되어 있으며, 예를 들어, CLC 메인 워크벤치(Main Workbench)를 포함한다.
당업자는 본 발명의 방법이 임의의 종결 서열과 양립할 수 있음을 인식할 것이다. 본 발명의 전사 종결 서열의 전체 목록은 하기 표 1.1에 제공된다. 한 실시태양에서, 본 발명의 전사 터미네이터는 표 1.1에 제공된 터미네이터 서열의 오르쏘로그일 수 있다. 예를 들어, 숙주 세포가 아스퍼길루스인 경우, 종결 서열은 표 1.1로부터 선택된 비-아스퍼길루스 종결 서열의 오르쏘로그일 수 있다.
[표 1.1]
본 발명의 종결 서열의 포괄적인 목록.
가설-주도 다양성 풀과 언덕 오르기(Hill Climbing)
본 발명은 본 개시의 HTP 게놈 조작 방법은 숙주 세포 성능에서 상당한 이득을 달성하기 위해 사전 유전자 지식을 필요로 하지 않는다는 것을 교시한다. 실제로, 본 발명은 무작위 돌연변이유발 및 이미 존재하는 숙주 세포 변이체들 사이의 유전자 다양성의 확인(예를 들어, 야생형 숙주 세포와 산업 변이체 사이의 비교)을 포함하는 여러 기능적으로 불가지론적인 접근법을 통해 다양성 풀을 생성하는 방법을 교시한다.
그러나, 일부 실시태양에서, 본 발명은 또한 하류 HTP 조작에 사용될 유전자 다양성 돌연변이를 디자인하는 가설-주도적 방법을 교시한다. 즉, 일부 실시태양에서, 본 발명은 선택된 돌연변이의 지시된 디자인을 교시한다. 일부 실시태양에서, 지시된 돌연변이는 본 발명의 조작 라이브러리(예컨대, SNP 스왑, PRO 스왑 또는 STOP 스왑)에 포함된다.
일부 실시태양에서, 본 발명은 유전자 주석, 가설된(또는 확인된) 유전자 기능, 또는 게놈 내의 위치에 기초한 지시된 돌연변이의 생성을 교시한다. 본 발명의 다양성 풀은 숙주 세포의 성능이 증가된 문헌에 관련된 특정 대사 경로 또는 유전자 경로에 관여한다고 가설된 유전자의 돌연변이를 포함할 수 있다. 다른 실시태양에서, 본 발명의 다양성 풀은 또한 개량된 숙주 성능과 관련된 유전자에 대한 돌연변이를 포함할 수 있다. 또 다른 실시태양에서, 본 발명의 다양성 풀은 알고리즘 예측 기능 또는 다른 유전자 주석에 기초한 유전자에 대한 돌연변이를 포함할 수 있다.
일부 실시태양에서, 본 발명은 가설 주도 돌연변이의 표적을 우선순위화하기위한 "껍질"에 기초한 접근법을 교시한다. 표적 우선순위화를 위한 껍질 비유는 단지 소수의 1차 유전자가 숙주 세포의 성능(예를 들어, 단일 생체분자의 생산)의 특정 측면의 대부분을 담당한다는 가설에 기초한다. 이들 1차 유전자는 껍질의 코어에 위치되고, 제 2 층에서 2차 효과 유전자, 3차 껍질에서 3차 효과 및 ... 등이 이어진다. 예를 들어, 한 실시태양에서, 껍질의 코어는 선택된 대사 경로 내의 중요한 생합성 효소를 암호화하는 유전자를 포함할 수 있다. 제 2 껍질 상에 위치하는 유전자는 생성물 전환 또는 피드백 신호 전달을 담당하는 생합성 경로 내의 다른 효소를 암호화하는 유전자를 포함할 수 있다. 이러한 예시적인 은유하에서의 제 3층 유전자는 생합성 경로의 발현을 조절하거나 숙주 세포 내에서 일반적인 탄소 플럭스를 조절하는 조절 유전자를 포함할 것이다.
본 발명은 또한 모든 확인된 돌연변이로부터 성능 이득을 최적화하기 위한 "언덕 오르기(hill climb)" 방법을 교시한다. 일부 실시태양에서, 본 발명은 HTP 다양성 라이브러리에서 무작위, 자연 또는 가설-주도 돌연변이는 숙주 세포 성능과 관련된 유전자의 확인을 초래할 수 있음을 교시한다. 예를 들어, 본 방법은 유전자 암호화 서열 상에 또는 그 부근에 위치한 하나 이상의 유익한 SNP를 확인할 수 있다. 이 유전자는 숙주 세포 성능과 관련이 있을 수 있으며, 이의 확인은 유기체의 조합 유전자 돌연변이 공간에서 성능 "언덕"의 발견과 유사할 수 있다.
일부 실시태양에서, 본 발명은 SNP 돌연변이로 구현된 확인된 언덕 주변의 조합 공간을 탐색하는 방법을 교시한다. 즉, 일부 실시태양에서, 본 발명은 그 유전자 노드로부터 얻어진 성능 이득(즉, 언덕 오르기)을 최적화하기 위해 확인된 유전자 및 관련 조절 서열의 교란을 교시한다. 따라서, 본 발명의 방법에 따르면, 유전자는 무작위 돌연변이유발에서 유도된 다양성 라이브러리에서 먼저 확인될 수 있지만, 나중에 동일한 유전자 내 다른 서열의 지시된 돌연변이를 통해 균주 개량 프로그램에서 사용하기 위해 개량될 수 있다.
언덕 오르기의 개념은 또한 단일 유전자 서열을 둘러싸는 조합 공간의 탐색을 넘어 확장될 수 있다. 일부 실시태양에서, 특정 유전자의 돌연변이는 숙주 세포 성능에 대한 특정 대사 경로 또는 유전자 경로의 중요성을 나타낼 수 있다. 예를 들어, 일부 실시태양에서, 단일 RNA 분해 유전자에서 돌연변이가 현저한 숙주 성능 증가를 초래한다는 발견은 숙주 유기체로부터 추가적인 성능 이득을 추출하기 위한 수단으로서 관련 RNA 분해 유전자를 돌연변이시키는 기초로서 사용될 수 있다. 당업자는 지시된 유전자 디자인에 대한 상기 껍질 및 언덕 오르기 접근법의 변형을 인식할 것이다.
형태학-관련 유전자
본 발명에 제공된 방법, 균주 및 시스템에 사용하기 위한 형태 관련 유전자는 사상균류 진핵 미생물(예를 들어, 사상균류 숙주 세포 또는 균주)의 형태를 제어하거나 이에 영향을 미치는 것으로 입증되거나 의심되는 것으로 당업계에 공지된 임의의 유전자일 수 있다. 숙주 세포의 형태를 조절하는 유전자는 본 발명에 제공된 임의의 유전자일 수 있다. 한 실시태양에서, 유전자는 S. 세레비지애 SLN1의 오르쏘로그이다. 다른 실시태양에서, 형태 관련 유전자는 S. 세레비지애 SLN1 유전자의 오르쏘로그와 동일한 경로로부터의 임의의 유전자일 수 있다. 동일한 경로의 일부인 유전자는 S. 세레비지애 Ypd1, Skn7, Ssk1 및 Ssk2 유전자의 오르쏘로그 또는 이들의 임의의 조합으로부터 선택될 수 있다. 다른 실시태양에서, 유전자는 핵산 SEQ ID NO: 11을 갖는 A. 니거 유전자의 오르쏘로그 및/또는 핵산 SEQ ID NO: 11을 가진 A. 니거 유전자의 상기 오르쏘로그의 동일한 생화학적 경로에 있는 임의의 유전자이다. 다른 실시태양에서, 유전자는 핵산 SEQ ID NO: 12를 갖는 A. 니거 유전자의 오르쏘로그 및/또는 핵산 SEQ ID NO: 12를 가진 A. 니거 유전자의 상기 오르 쏘로그의 동일한 생화학적 경로에 있는 임의의 유전자이다. 다른 실시태양에서, 유전자는 핵산 SEQ ID NO: 14를 갖는 A. 니거 유전자의 오르쏘로그 및/또는 핵산 SEQ ID NO:14를 가진 A. 니거 유전자의 상기 오르쏘로그의 동일한 생화학적 경로에 있는 임의의 유전자이다.
본 발명에 제공된 방법, 균주 및 시스템에 사용하기 위한 형태 관련 유전자는 A. 니거의 형태를 제어하거나 영향을 주는 역할을 하는 것으로 입증되거나 또는 의심되는 것으로 당업계에 공지된 임의의 유전자일 수 있다. 한 실시태양에서, 유전자는 SEQ ID NO: 11, 12, 13 또는 14로부터 선택된 핵산 서열을 갖는 SNP 함유 유전자이다(표 4 참조). 한 실시태양에서, 유전자는 복수의 유전자이다. 복수의 유전자는 SEQ ID NO: 11, 12, 13 또는 14로부터 선택된 핵산 서열과 SNP 함유 유전자의 임의의 조합일 수 있다. 복수의 유전자는 SEQ ID NO: 11로부터 선택된 핵산 서열을 갖는 SNP 함유 유전자 및 동일한 생화학적 경로 내에 존재하는 임의의 유전자의 임의의 조합일 수 있다. 복수의 유전자는 SEQ ID NO: 12로부터 선택된 핵산 서열을 갖는 SNP 함유 유전자 및 동일한 생화학적 경로 내에 존재하는 임의의 유전자의 임의의 조합일 수 있다. 복수의 유전자는 SEQ ID NO: 13으로부터 선택된 핵산 서열을 갖는 SNP 함유 유전자 및 동일한 생화학적 경로 내에 존재하는 임의의 유전자의 임의의 조합일 수 있다. 복수의 유전자는 SEQ ID NO: 14로부터 선택된 핵산 서열을 갖는 SNP 함유 유전자 및 동일한 생화학적 경로 내에 존재하는 임의의 유전자의 임의의 조합일 수 있다. 한 실시태양에서, 유전자는 SEQ ID NO: 11, 12, 13 또는 14로부터 선택된 핵산 서열을 갖는 유전자의 야생형 또는 비 SNP 함유 버전이다(표 4 참조).
한 실시태양에서, A. 니거 숙주 세포의 형태를 조절하는 유전자는 S. 세레비 지애 SLN1 유전자의 A. 니거 오르쏘로그이다. S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그는 야생형 형태 또는 돌연변이 형태일 수 있다. S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그의 돌연변이 형태는 표 4로부터의 FungiSNP_18일 수 있거나 또는 SEQ ID NO: 13의 핵산 서열을 가진 FungiSNP_18일 수 있다. 다른 실시태양에서, 형태 관련 유전자는 S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그와 동일한 경로로부터의 임의의 유전자일 수 있다. 동일한 경로의 일부인 유전자는 S. 세레비지애 Ypd1, Skn7, Ssk1 및 Ssk2 유전자의 오르쏘로그 또는 이들의 임의의 조합으로부터 선택될 수 있다. 동일한 경로의 일부인 유전자는 SEQ ID NO: 15, 16, 17, 18, 19 또는 이들의 임의의 조합으로 표시되는 핵산 서열로부터 선택될 수 있다.
형태 관련 유전자는 다이 등("Identification of Genes Associated with Morphology in Aspergillus niger by Using Suppression Subtractive Hybridization" Applied and Environmental Microbiology, Apr. 2004, p. 2474-2485)에 개시된 유전자 또는 오르쏘로그의 임의의 것일 수 있고, 이의 내용은 전문이 참조로 본 발명에 포함된다. 형태-관련 유전자는 gas1 유전자, sfb3 유전자, seb1 유전자, mpg1 유전자, crz1 유전자 및 tps2 유전자로부터 선택될 수 있다. 임의의 형태 관련 유전자의 발현이 유전자가 사상균류 또는 균사 형태 또는 펠렛 형태를 촉진하는지에 따라 증가 또는 감소될 수 있다.
본 발명에 기술된 바와 같이, 본 발명에 제공된 임의의 형태 관련 유전자 또는 이의 돌연변이체(예를 들어, 표 4의 FungiSNP 9, 12, 18 또는 40)의 발현은 유전자의 천연 프로모터를 천연 프로모터와 상이한 수준(예를 들어, 더 높거나 더 낮은)에서 발현을 부여하는 이종 프로모터로로 대체함으로써 제어될 수 있다. 이종 프로모터는 표 1로부터 선택될 수 있다. 천연 프로모터의 대체는 본 발명에 제공된 바와 같은 PRO 스왑 방법을 사용하여 수행될 수 있다.
본 발명의 또 다른 목적은 S. 세레비지애 SLN1 유전자의 숙주 세포의 오르쏘로그의 이종 변형을 포함하는 사상균류 숙주 세포를 제공하는 것이며, 이에 의해 S. 세레비지애 SLN1 유전자의 변형 오르쏘로그가 이종 변형이 없는 부모 사상균류 숙주 세포에 비해 감소된 활성 및/또는 감소된 발현을 가진다. 사상균류 숙주는 비-균사, 펠릿 형성 표현형을 보유할 수 있다. 이 펠렛 표현형은 사상균류 숙주 세포의 세포가 상기 이종 변형을 보유하지 않은 세포에 비해 실질적으로 감소된 양 및/또는 실질적으로 덜 활성 형태의 S. 세레비지애 SLN1 유전자의 기능성 오르쏘로그를 생산하게 하는 S. 세레비지애 SLN1 유전자의 오르쏘로그에서 이종 변형을 보유하는 사상균류 숙주 세포에 기인할 수 있다. 사상균류 숙주 세포 및 이로부터 유래된 사상균류 숙주 세포의 임의의 부모 균주는 당업계에 공지된 및/또는 본 발명에 제공된 임의의 사상균류, 예를 들어 A. 니거일 수 있다. 한 실시태양에서, 사상균류 숙주 세포는, 예를 들어, 고체 배지 상에서와 같은 비 심층 성장 조건하에서 성장될 때 부모 균주와 비교하여 정상적으로 포자화된다. 다른 실시태양에서, 사상균류 숙주 세포는, 표 4로부터의 SNP 함유 유전자의 오르쏘로그의 하나, 전부 또는 조합이 사상균류 숙주 세포에서 발현될 때에만, 예를 들어, 고체 배지 상에서와 같은 비 심층 성장 조건하에서 성장될 때 부모 균주와 비교하여 정상적으로 포자화된다. 한 실시태양에서, 사상균류 숙주 세포는 A. 니거이고, 상기 A. 니거 숙주 세포는 표 4로부터의 SNP 함유 유전자의 오르쏘로그의 하나, 전부 또는 조합이 상기 A. 니거 숙주 세포에서 발현될 때에만, 예를 들어, 고체 배지 상에서와 같은 비 심층 성장 조건하에서 성장될 때 부모 균주와 비교하여 정상적으로 포자화된다. 또 다른 실시태양에서, 사상균류 숙주 세포는, 표 4로부터의 SNP 함유 유전자의 오르쏘로그의 하나, 전부 또는 조합이 사상균류 숙주 세포에서 발현될 때에만, 예를 들어, 고체 배지 상에서와 같은 비 심층 성장 조건하에서 성장될 때 부모 균주와 비교하여 정상적으로 포자화된다. 심층 배양 조건은 CAP 배지에서 변이 균주를 성장시키는 것을 포함할 수 있다. CAP 매질은 망간을 포함할 수 있고 킬레이트제가 실질적으로 없을 수 있다. 망간은 적어도 13ppb 이상인 양으로 존재할 수 있다.
S. 세레비지애 SLN1 유전자의 오르쏘로그에 대한 유전자 변경은 야생형 형태의 유전자의 S. 세레비지애 SLN1 유전자의 돌연변이된 오르쏘로그에 의한 대체, 유전자의 천연 프로모터와 비교하여 S. 세레비지애 SLN1 단백질의 오르쏘로그에 대한 유전자를 보다 약하게 발현하는 이종성 프로모터에 의한 대체 또는 이의 조합일 수 있다. 대안적으로, S. 세레비지애 SLN1 유전자의 오르쏘로그에 대한 유전자 변경은 S. 세레비지애 SLN1 유전자의 오르쏘로그의 제거 및 선택 가능한 마커 유전자에 의한 대체일 수 있다. S. 세레비지애 SLN1 유전자의 오르쏘로그의 돌연변이된 형태는 SNP, 비-센스 돌연변이, 미스센스 돌연변이, 결실, 삽입 또는 이들의 임의의 조합을 포함할 수 있다. 한 실시태양에서, 사상균류 숙주 세포는 A. 니거이고 S. 세레비지애 SLN1 단백질의 A. 니거 오르쏘로그는 SEQ ID NO: 13에 의해 암호화될 수 있다. 이종성 프로모터는 표 1에 열거된 프로모터로부터 선택될 수 있다. 한 실시태양에서, 이종 프로모터는 manB 또는 amyB 프로모터이다. 이 실시태양에 더하여, 이종 프로모터는 SEQ ID NO: 1 또는 SEQ ID NO: 2일 수 있다. 선택 가능한 마커는 본 발명에 제공된 영양 요구성 마커 유전자, 비색 마커 유전자, 항생제 내성 유전자 또는 방향성 마커 유전자로부터 선택될 수 있다.
S. 세레비지애 SLN1 단백질의 실질적으로 감소된 양 및/또는 실질적으로 덜 활성인 형태의 기능성 오르쏘 로그를 보유하는 사상균류 숙주 세포는 S. 세레비지애 SLN1 유전자의 오르쏘로그와 동일한 경로의 일부인 하나 이상의 유전자에서의 유전자 파괴 또는 변형을 추가로 포함할 수 있다. 동일한 경로의 일부인 하나 이상의 유전자는 S. 세레비지애 Ypd1, Skn7, Ssk1 및 Ssk2 유전자의 오르쏘로그 또는 이들의 임의의 조합으로부터 선택될 수 있다. 한 실시태양에서, 사상균류 숙주 세포는 A. 니거이고, S. 세레비지애 SLN1, Ypd1, Skn7, Ssk1 및 Ssk2 유전자의 오르 쏘로그는 A. 니거 오르쏘로그 또는 이의 돌연변이체이다. 이 실시태양에 더하여, 동일한 경로의 일부인 하나 이상의 유전자는 SEQ ID NO: 15, 16, 17, 18, 19 또는 이들의 임의의 조합으로 표시되는 핵산 서열로부터 선택될 수 있다. 사상균류 숙주 세포는 사상균류 형태를 제어하는 데 역할을 하는 것으로 알려진 상이한 경로의 일부인 하나 이상의 유전자에서의 유전자 파괴 또는 변형을 추가로 포함할 수 있다. 상이한 경로의 일부인 하나 이상의 유전자는 본 발명에 제공된 임의의 유전자일 수 있다. 상이한 경로의 일부인 하나 이상의 유전자는 SEQ ID NO: 11, 12, 14 또는 이들의 임의의 조합으로 표시되는 핵산 서열을 갖는 유전자의 A. 니거 오르쏘로그로부터 선택될 수 있다. 한 실시태양에서, 사상균류 숙주 세포는 A. 니거이고 상이한 경로의 일부인 하나 이상의 유전자는 SEQ ID NO: 11, 12, 14 또는 임의의 조합으로 표시되는 핵산 서열을 갖는 A. 니거 유전자이다. 다른 실시태양에서, 사상균류 숙주 세포는 A. 니거이고, 상이한 경로의 일부인 하나 이상의 유전자는 SEQ ID NO: 11, 12, 14 또는 이들의 임의의 조합으로 나타내어진 핵산 서열을 갖는 A. 니거 유전자의 비-SNP 함유 버전이다.
S. 세레비지애 SLN1 유전자의 오르쏘로그와 동일한 경로의 일부이거나 사상균류 형태를 제어하는 데 역할을 하는 것으로 알려진 상이한 경로의 일부인 하나 이상의 유전자에 대한 유전자 파괴 또는 변형은 야생형 형태의 유전자의 돌연변이 형태의 유전자에 의한 대체, 유전자의 천연 프로모터의 천연 프로모터에 비해 유전자의 발현을 변형(예를 들어, 더 높거나 더 낮은)시키는 이종 프로모터에 의한 대체 또는 이의 조합일 수 있다. 프로모터는 표 1에 열거된 프로모터일 수 있다. 대안적으로, S. 세레비지애 SLN1 유전자의 오르쏘로그와 동일한 경로의 일부 또는 사상균류 형태를 제어하는 역할을 하는 것으로 알려진 상이한 경로의 일부인 하나 이상의 유전자에 대한 유전자 파괴 또는 변형은 유전자의 제거 및 선택 가능한 마커 유전자에 의한 대체일 수 있다. 선택 가능한 마커는 본 발명에 제공된 영양 요구성 마커 유전자, 비색 마커 유전자, 항생제 내성 유전자 또는 방향성 마커 유전자로부터 선택될 수 있다.
실질적으로 감소된 양 및/또는 실질적으로 덜 활성인 형태의 S. 세레비지애 SLN1 단백질을 보유하는 사상균류의 변이 균주를 생성하는 방법이 본 발명에 제공된다. 상기 방법은 본 발명에 제공된 바와 같이 PRO 스왑 방법, SNP 스왑 방법 또는 PRO 스왑 및 SNP 스왑 방법의 조합을 수행하는 단계를 포함할 수 있다.
본 발명의 또 다른 목적은 SEQ ID NO. 11, 12, 14 또는 이의 임의의 조합으로부터 선택된 핵산 서열을 갖는 A. 니거 유전자의 숙주 세포의 오르쏘로그의 이종 변형을 포함하는 사상균류 숙주 세포를 제공하는 것이며, 이에 의해 SEQ ID NO. 11, 12, 14 또는 이의 임의의 조합으로부터 선택된 핵산 서열을 갖는 A. 니거 유전자의 변형 오르쏘로그가 이종 변형(들)이 없는 부모 사상균류 숙주 세포에 비해 감소된 활성 및/또는 감소된 발현을 가진다. 사상균류 숙주는 SEQ ID NO. 11, 12, 14 또는 이의 임의의 조합의 선택된 핵산 서열을 갖는 A. 니거 유전자의 오르쏘로그에 대한 이종 변형을 보유하는 사상균류 숙주 세포에 의해 심층 배양에서 성장될 때 부모 균주의 세포와 비교하여 비-균사, 펠릿 형성 표현형을 보유할 수 있다. SEQ ID NO. 11, 12, 14 또는 이의 임의의 조합의 핵산 서열을 갖는 A. 니거 유전자의 오르쏘로그의 보유는 숙주 세포의 세포들이 심층 배양 조건하에서 성장될 때 부모 숙주 세포의 세포와 비교하여 상기 SEQ ID NOs를 갖는 A. 니거의 오르쏘로그에 의해 암호화된 실질적으로 감소된 양 및/또는 실질적으로 덜 활성 형태의 기능성 단백질을 생산하게 할 수 있다. 사상균류 숙주 세포 및 상기 사상균류 숙주 세포의 부모 균주는 당업계에 공지된 및/또는 본 발명에 제공된 임의의 사상균류, 예를 들어 A. 니거일 수 있다. 한 실시태양에서, 사상균류 숙주 세포는, 예를 들어, 고체 배지 상에서와 같은 비 심층 성장 조건하에서 성장될 때 부모 균주와 비교하여 정상적으로 포자화된다. 일부 경우에, SEQ ID NOs; 11, 12 또는 14를 갖는 A. 니거 유전자의 오르쏘로그는 유전적으로 추가로 변형된다. 추가 유전자 변형은 천연 프로모터와 비교하여 더욱 약하게 유전자를 발현하는 이종 프로모터에 의한 유전자의 천연 프로모터의 대체일 수 있다. 선택적으로, 추가 유전자 변형은 SEQ ID NOs; 11, 12 또는 14를 갖는 A. 니거 유전자의 오르쏘로그의 제거 및 선택 가능한 마커 유전자에 의한 대체일 수 있다. 선택 가능한 마커는 본 발명에 제공된 영양 요구성 마커 유전자, 비색 마커 유전자, 항생제 내성 유전자 또는 방향성 마커 유전자로부터 선택될 수 있다. 이종 프로모터는 표 1에 열거된 프로모터로부터 선택될 수 있다. 한 실시태양에서, 이종 프로모터는 manB 또는 amyB 프로모터이다. 이 실시태양에 더하여, 이종 프로모터는 SEQ ID NO: 1 또는 SEQ ID NO: 2의 핵산 서열을 가질 수 있다. 심층 배양 조건은 CAP 배지에서 변이주를 성장시키는 것을 포함할 수 있다. CAP 매질은 망간을 포함할 수 있고 킬레이트제가 실질적으로 없을 수 있다. 망간은 13ppb 이상인 양으로 존재할 수 있다. 사상균류 숙주 세포가 A. 니거인 실시태양에서, SEQ ID NO. 11, 12, 14 또는 이의 야생형 버전으로부터 선택된 핵산 서열을 갖는 A. 니거 유전자는 본 발명에 상세히 기술된 이종 변형을 포함할 수 있다는 것을 이해해야 한다.
SEQ ID NOs: 11, 12 또는 14로부터 선택된 서열을 갖는 A. 니거 유전자의 오르쏘로그에 의해 암호화된 실질적으로 감소된 양 및/또는 실질적으로 덜 활성인 형태의 기능성 단백질을 보유하는 사상균류 숙주 세포는 동일한 경로의 일부인 하나 이상의 유전자에 유전자 파괴 또는 변형을 추가로 포함할 수 있다. 사상균류 숙주 세포는 사상균류 형태를 제어하는 데 역할을 하는 것으로 알려진 상이한 경로의 일부인 하나 이상의 유전자에 유전자 파괴 또는 변형을 추가로 포함할 수 있다. 상이한 경로의 일부인 하나 이상의 유전자는 본 발명에 제공된 임의의 유전자일 수 있다. 사상균류 형태를 제어하는 역할을 하는 것으로 알려진 동일한 경로의 일부 또는 상이한 경로의 일부인 하나 이상의 유전자에 대한 유전자 파괴 또는 변형은 야생형 형태의 유전자의 돌연변이 형태의 유전자에 의한 대체, 천연 프로모터의 유전자의 천연 프로모터에 비해 유전자의 발현을 변형(예를 들어, 더 높거나 더 낮은)시키는 이종 프로모터에 의한 대체 또는 이의 조합일 수 있다. 프로모터는 표 1에 열거된 프로모터일 수 있다. 대안적으로, 사상균류 형태를 제어하는 역할을 하는 것으로 알려진 동일한 경로의 일부 또는 상이한 경로의 일부인 하나 이상의 유전자에 대한 유전자 파괴 또는 변형은 유전자의 제거 및 선택 가능한 마커 유전자에 의한 대체일 수 있다. 선택 가능한 마커는 본 발명에 제공된 영양 요구성 마커 유전자, 비색 마커 유전자, 항생제 내성 유전자 또는 방향성 마커 유전자로부터 선택될 수 있다.
SEQ ID NO: 11, 12 또는 14를 갖는 A. 니거 유전자의 오르쏘로그에 의해 암호화된 실질적으로 감소된 양 및/또는 실질적으로 덜 활성인 형태의 기능성 단백질을 보유하는 사상균류의 변이 균주를 생성하는 방법이 본 발명에 제공된다. 상기 방법은 본 발명에 제공된 바와 같이 PRO 스왑 방법, SNP 스왑 방법 또는 PRO 스왑 및 SNP 스왑 방법의 조합을 수행하는 단계를 포함할 수 있다.
본 발명의 또 다른 목적은 숙주 세포의 형태를 조절하는 유전자에 작동 가능하게 연결된 프로모터를 포함하는 사상균류 숙주 세포를 제공하는 것으로, 상기 프로모터는 유전자와 이종이며, 상기 프로모터는 SEQ ID NOs. 1-4로 이루어진 그룹으로부터 선택된 서열을 갖는다. 사상균류 숙주 세포는 당업계에 공지되고/되거나 본 발명에 제공되는 임의의 사상균류, 예를 들어 A. 니거일 수 있다. 일부 경우에, 균류 숙주 세포는, 예를 들어, 고체 배지 상에서와 같은 비 심층 성장 조건하에서 성장될 때 숙주 세포의 부모 균주와 비교하여 정상적으로 포자화되나, 심층 배양 조건하에서 성장될 때 비 균사, 펠렛 형태를 형성한다. 일부 경우에, 숙주 세포는 형태를 조절하는 하나 이상의 유전자를 포함하여 상기 하나 이상의 유전자 각각이 이종 프로모터에 연결되도록 할 수 있다. 숙주 세포의 형태를 조절하는 하나 이상의 유전자는, 단독으로 또는 조합하여, 예를 들어 SEQ ID NO: 11, 12, 13 또는 14로 표시되는 SNP 함유 유전자 서열 또는 표 4의 오르쏘로그와 같은 본 발명에 제공된 바와 같은 임의의 유전자일 수 있다. 일부 경우에, SEQ ID NO: 11, 12, 13 또는 14로 표시되는 SNP 함유 유전자 서열 또는 표 4의 오르쏘로그는 각각의 SNP 함유 유전자 서열과 동일한 경로로부터의 하나 이상의 유전자와 조합될 수 있다. 한 실시태양에서, 하나 이상의 유전자는, 단독 또는 조합하여, SEQ ID NO: 11, 12, 13 또는 14로부터 선택된 핵산 서열을 갖는 유전자의 야생형 또는 비-SNP 함유 버전 또는 이의 오르쏘로그이다. 다른 실시태양에서, SEQ ID NO: 11, 12, 13 또는 14로부터 선택된 핵산 서열을 갖는 유전자의 야생형 또는 비-SNP 함유 버전 또는 이의 오르쏘로그는 개개의 야생형 또는 비-SNP 함유 유전자 서열과 동일한 경로로부터의 하나 이상의 유전자와 조합될 수 있다. 한 실시태양에서, 숙주 세포의 형태를 조절하는 유전자는 S. 세레비지애 SLN1 유전자의 오르쏘로그 또는 동일한 신호 전달 경로의 유전자일 수 있다. 동일한 신호 전달 경로의 일부인 하나 이상의 유전자는 S. 세레비지애 Ypd1, Skn7, Ssk1 및 Ssk2 유전자의 오르쏘로그 또는 이들의 임의의 조합으로부터 선택될 수 있다. 한 실시태양에서, 사상균류 숙주 세포는 A. 니거이고, 동일한 신호 전달 경로의 일부인 하나 이상의 유전자는 SEQ ID NO: 15, 16, 17, 18, 19 또는 이들의 임의의 조합으로 표시되는 핵산 서열로부터 선택될 수 있다. S. 세레비지애 SLN1 유전자의 오르쏘로그는 유전자의 야생형 또는 돌연변이 형태일 수 있다. 한 실시태양에서, 사상균류 숙주 세포는 A. 니거이고 S. 세레비지애 SLN1 유전자의 돌연변이된 A. 니거 오르쏘로그는 SEQ ID NO: 13의 핵산 서열을 갖는다. 심층 배양 조건은 CAP 배지에서 변이 균주를 성장시키는 것을 포함할 수 있다. CAP 매질은 망간을 포함할 수 있고 킬레이트제가 실질적으로 없을 수 있다. 망간은 적어도 13ppb 이상인 양으로 존재할 수 있다.
세포 배양 및 발효
본 발명의 세포는 임의의 바람직한 생합성 반응 또는 선택을 위해 적절하게 변형된 통상적인 영양 배지에서 배양될 수 있다. 일부 실시태양에서, 본 발명은 프로모터를 활성화시키기 위해 배지를 유도하는 배양을 교시한다. 일부 실시태양에서, 본 발명은 형질전환체(예를 들어, 항생제)의 선택 제제 또는 억제 조건(예를 들어, 높은 에탄올 조건)하에 성장하기에 적합한 유기체의 선택 제제를 포함하는 선택 제제를 갖는 배지를 교시한다. 일부 실시태양에서, 본 발명은 세포 성장을 위해 최적화된 배지에서 세포 배양물을 성장시키는 것을 교시한다. 다른 실시태양에서, 본 발명은 생산 수율에 최적화된 배지에서 세포 배양물을 성장시키는 것을 교시한다. 일부 실시태양에서, 본 발명은 세포 성장을 유도할 수 있는 배지에서 배양 물을 배양하는 것을 교시하며 최종 생성물 생산을 위한 필수 전구체(예를 들어, 에탄올 생산을 위한 높은 수준의 당)를 포함한다.
온도, pH 등과 같은 배양 조건은 발현을 위해 선택된 숙주 세포와 함께 사용하기에 적합한 것들이며, 당업자에게 명백할 것이다. 언급한 바와 같이, 박테리아, 식물, 동물(포유류 포함) 및 고세균 기원 세포를 포함하는 많은 세포의 배양 및 생산에 대한 많은 참고 자료가 이용될 수 있다. 예를 들어, Sambrook, Ausubel (all supra), as well as Berger, Guide to Molecular Cloning Techniques, Methods in Enzymology volume 152 Academic Press, Inc., San Diego, CA; and Freshney (1994) Culture of Animal Cells, a Manual of Basic Technique, third edition, Wiley-Liss, New York and the references cited therein; Doyle and Griffiths (1997) Mammalian Cell Culture: Essential Techniques John Wiley and Sons, NY; Humason (1979) Animal Tissue Techniques, fourth edition W.H. Freeman and Company; and Ricciardelle et al., (1989) In Vitro Cell Dev. Biol. 25:1016-1024, all of which are incorporated herein by reference. For plant cell culture and regeneration, Payne et al. (1992) Plant Cell and Tissue Culture in Liquid Systems John Wiley & Sons, Inc. New York, N.Y.; Gamborg and Phillips (eds) (1995) Plant Cell, Tissue and Organ Culture; Fundamental Methods Springer Lab Manual, Springer-Verlag (Berlin Heidelberg N.Y.); Jones, ed. (1984) Plant Gene Transfer and Expression Protocols, Humana Press, Totowa, N.J. and Plant Molecular Biology (1993) R. R. D. Croy, Ed. Bios Scientific Publishers, Oxford, U.K. ISBN 0 12 198370 6 참조하고, 이의 전문은 참조로 본 발명에 포함된다. 일반적으로 세포 배양 배지는 Atlas and Parks (eds.) The Handbook of Microbiological Media (1993) CRC Press, Boca Raton, Fla에서 설명되며, 이는 참조로 본 발명에 포함된다. 세포 배양에 대한 추가 정보는 Life Science Research Cell Culture Catalogue from Sigma-Aldrich, Inc (St Louis, Mo.) ("Sigma-LSRCCC") 및, 예를 들어, The Plant Culture Catalogue and supplement also from Sigma-Aldrich, Inc (St Louis, Mo.) ("Sigma-PCCS")와 같은 구입가능한 상업용 논문에서 발견되며, 이의 전부는 참조로 본 발명에 포함된다.
사용될 배양 배지는 적절한 방식으로 각각의 균주의 요구를 충족시켜야한다. 다양한 유기체에 대한 배양 배지에 대한 설명은 American Bacteriology Society (Washington D.C., USA, 1981)의 "General Bacteriology Methods for Manual"에 제공된다.
또한, 본 발명은 a) 적절한 배지에서 본 발명에 따른 미생물을 배양하여 발효액을 생성하는 단계; b) a)의 발효액 및/또는 미생물의 세포에 관심 생성물을 농축시키는 단계를 포함하여 관심 생성물의 발효성 제조를 위한 방법을 추가로 제공한다.
일부 실시태양에서, 본 발명은 생산된 미생물이 원하는 유기-화학적 화합물을 생산하기 위한, 예를 들어 WO 05/021772에 기술된 바와 같이 연속적으로 또는 배치 공정(배치 배양) 또는 페드 배치(fed-batch) 또는 반복된 페드 배치에서 불연속적으로 배양될 수 있음을 교시한다. 알려진 배양 방법에 관한 일반적인 내용은 Chmiel(Bioprozeβtechnik. 1: Einfuhrung in die Bioverfahrenstechnik (Gustav Fischer Verlag, Stuttgart, 1991))에 의한 교과서 또는 Storhas(Bioreaktoren and periphere Einrichtungen (Vieweg Verlag, Braunschweig/Wiesbaden, 1994))에 의한 교과서에서 이용할 수 있다.
일부 실시태양에서, 본 발명의 세포는 배치 또는 연속 발효 조건하에 성장된다.
고전적인 배치 발효는 폐쇄된 시스템이며, 배지의 조성물은 발효의 시작시에 설정되고 발효 동안 인공적인 변형을 겪지 않는다. 배치 시스템의 변형은 본 발명에서 사용되는 페드 배치 발효이다. 이 변형에서, 기질은 발효가 진행됨에 따라 증분으로 첨가된다. 페드 배치 시스템은 이화생성물 억제가 세포의 신진대사를 억제 할 가능성이 있고 배지에 제한된 양의 기질을 갖는 것이 바람직한 경우에 유용하다. 배치 및 페드 배치 발효는 일반적이고 당업계에 일반적으로 주지되어 있다.
연속 발효는 정의된 발효 배지가 생물 반응기에 연속적으로 첨가되고 동일한 양의 조건 배지가 관심의 목적하는 생체분자 생성물의 가공 및 수확을 위해 동시에 제거되는 시스템이다. 일부 실시태양에서, 연속 발효는 일반적으로 세포가 주로 대수기 성장하는 일정한 고밀도로 배양물을 유지시킨다. 일부 실시태양에서, 연속 발효는 일반적으로 정지기 또는 늦은 대수기/정지기 성장시에 배양물을 유지시킨다. 연속 발효 시스템은 정지기 성장 조건을 유지하기 위해 노력한다.
연속 발효 공정을 위한 영양소 및 성장 인자를 조절하는 방법뿐만 아니라 생성물 형성의 속도를 최대화하기 위한 기술은 산업용 미생물학 분야에 잘 알려져 있다.
예를 들어, 본 발명의 배양물에 대한 탄소원의 비 제한적인 목록은 당 및 수화물, 예를 들어 글루코오스, 수크로오스, 락토오스, 프룩토오스, 말토오스, 당밀, 사탕무 또는 사탕수수 가공에 의한 수크로오스-함유 용액, 전분, 전분 가수분해물 및 셀룰로오스; 오일 및 지방, 예를 들어, 대두유, 해바라기유, 땅콩유 및 코코넛 지방; 지방산, 예를 들어 팔미트산, 스테아르산 및 리놀레산; 알코올, 예를 들어 글리세롤, 메탄올 및 에탄올; 및 유기산, 예를 들어 아세트산 또는 젖산을 포함한다.
본 발명의 배양물을 위한 질소 공급원의 비 제한적인 목록은 펩톤, 효모 추출물, 고기 추출물, 맥아 추출물, 옥수수 침지액, 콩가루 및 우레아와 같은 유기 질소 함유 화합물; 또는 황산 암모늄, 염화 암모늄, 인산 암모늄, 탄산 암모늄 및 질산 암모늄과 같은 무기 화합물을 포함한다. 질소원은 개별적으로 또는 혼합물로서 사용될 수 있다.
본 발명의 배양물을 위한 가능한 인 공급원의 비 제한적인 목록은 인산, 인산 이수소 칼륨 또는 인산 수소 이칼륨 또는 상응하는 나트륨 함유 염을 포함한다.
배양 배지는 추가로 성장에 필수적인, 나트륨, 칼륨, 마그네슘, 칼슘 및 철과 같은 금속의 염화물 또는 황산염 형태의 염을 포함한다.
마지막으로, 아미노산, 예를 들어 호모 세린 및 비타민, 예를 들어 티아민, 바이오틴 또는 판토텐산과 같은 필수 성장 인자가 상기 언급된 물질에 추가로 사용될 수 있다.
일부 실시태양에서, 배양물의 pH는 수산화 나트륨, 수산화 칼륨, 암모니아 또는 수성 암모니아; 또는 인산 또는 황산과 같은 산성 화합물을 포함하나 이에 제한되지 않는 임의의 산 또는 염기, 또는 완충 염에 의해 적절한 방식으로 조절될 수 있다. 일부 실시태양에서, pH는 일반적으로 6.0 내지 8.5, 바람직하게는 6.5 내지 8의 값으로 조절된다.
일부 실시태양에서, 본 발명의 배양물은 소포제, 예를 들어 지방산 폴리글리콜 에스터를 포함할 수 있다. 일부 실시태양에서, 본 발명의 배양물은 예를 들어 항생제와 같은 적합한 선택 물질을 첨가함으로써 배양물의 플라스미드를 안정화시키도록 변형된다.
일부 실시태양에서, 배양은 호기성 조건하에 수행된다. 이러한 조건을 유지하기 위해, 예를 들어 공기와 같은 산소 또는 산소 함유 기체 혼합물이 배양물 내로 도입된다. 과산화수소가 풍부한 액체를 사용하는 것도 가능하다. 발효는, 적절한 경우에, 상승된 압력, 예를 들어 0.03 내지 0.2 MPa의 상승된 압력에서 수행된다. 배양의 온도는 통상 20℃ 내지 45℃, 바람직하게는 25℃ 내지 40℃, 특히 바람직하게는 30℃ 내지 37℃이다. 배치 또는 페드 배치 공정에서, 배양은 바람직하게는 회수하고자 하는 관심의 목적하는 생성물(예를 들어, 유기-화학적 화합물)의 양이 형성될 때까지 계속된다. 이 목표는 일반적으로 10시간 내지 160시간 이내에 달성될 수 있다. 연속 공정에서, 더 긴 배양 시간이 가능하다. 미생물의 활성은 발효 배지 및/또는 상기 미생물의 세포에서 관심 생성물의 농축(축적)을 초래한다.
일부 실시태양에서, 배양은 혐기성 조건하에 수행된다.
선별
일부 실시태양에서, 본 발명은 고 처리량 초기 선별을 교시한다. 다른 실시태양에서, 본 발명은 또한 성능 데이터의 견고한 탱크-기반 검증을 교시한다(도 6b 참조).
일부 실시태양에서, 고 처리량 선별 공정은 생물 반응기에서의 균주의 성능을 예측하도록 디자인된다. 상기한 바와 같이, 배양 조건은 생물체에 적합하고 생물 반응기 조건을 반영하도록 선택된다. 개별 콜로니를 집어 96웰 플레이트로 옮기고 적당한 시간 동안 배양한다. 이어서 세포를 종자 배양 또는 생산 배양을 위해 새로운 96웰 플레이트로 옮긴다. 배양액은 다양한 시간 동안 배양되어, 다중 측정이 실행될 수 있다. 다중 측정은 생성물, 바이 매스 또는 생물 반응기에서 균주의 성능을 예측하는 다른 특성의 측정을 포함할 수 있다. 고 처리량의 배양 결과는 생물 반응기 성능을 예측하는데 사용된다.
일부 실시태양에서, 탱크-기반 성능 검증은 고 처리량 선별에 의해 분리된 균주의 성능을 확인하기 위해 사용된다. 생산성 또는 수율과 같은 관련 균주 성능 특성에 대한 벤치 스케일 발효 반응기(예를 들어, 본 발명의 표 3에 개시된 반응기)를 사용하여 후보 균주를 선별한다.
생성물 회수 및 정량화
관심 생성물의 생산을 위한 선별 방법은 당업자에게 공지되어 있으며 본 명세서 전반에 걸쳐 논의된다. 이러한 방법은 본 발명의 균주를 선별할 때 사용될 수있다.
일부 실시태양에서, 본 발명은 비 분비된 세포내 생성물을 생산하도록 디자인된 균주를 개량시키는 방법을 교시한다. 예를 들어, 본 발명은 세포내 효소, 오일, 약제 또는 다른 가치있는 작은 분자 또는 펩타이드를 생성하는 세포 배양물의 견고성, 수율, 효율 또는 전반적인 바람직함을 개선시키는 방법을 교시한다. 비 분비된 세포내 생성물의 회수 또는 분리는 용해 및 본 발명에 기술된 것을 포함하여 당해 분야에 주지된 회수 기술에 의해 달성될 수 있다.
예를 들어, 일부 실시태양에서, 본 발명의 세포는 원심 분리, 여과, 침전 또는 다른 방법에 의해 수확될 수 있다. 이어서, 수확된 세포는 동결-해동 사이클링, 초음파 처리, 기계적 파쇄 또는 세포 용해제의 사용, 또는 당업자에게 공지된 다른 방법을 포함하는 임의의 편리한 방법으로 파괴된다.
관심의 생성된 생성물, 예를 들면, 폴리펩타이드는 당업계에 공지된 다수의 방법 중 임의의 방법에 의해 회수/분리될 수 있으며 임의로 정제될 수 있다. 예를 들어, 생성물 폴리 펩타이드는 원심 분리, 여과, 추출, 분무 건조, 증발, 크로마토 그래피(예를 들어, 이온 교환, 친화성, 소수성 상호작용, 크로마토포커싱 및 크기 배제) 또는 침전을 포함하나 이에 제한되지 않는 통상적인 절차에 의해 영양 배지로부터 분리될 수 있다. 최종적으로, 고성능 액체 크로마토 그래피(HPLC)가 최종 정제 단계에서 사용될 수 있다. (예를 들어, Purification of intracellular protein as described in Parry et al., 2001, Biochem. J.353:117, and Hong et al., 2007, Appl. Microbiol. Biotechnol. 73:1331, 참조, 모두는 참조로 본 발명에 포함된다).
상기한 참조문헌 이외에, 다양한 정제 방법은, 예를 들어, Sandana (1997) Bioseparation of Proteins, Academic Press, Inc.; Bollag et al. (1996) Protein Methods, 2nd Edition, Wiley-Liss, NY; Walker (1996) The Protein Protocols HandbookHumana Press, NJ; Harris and Angal (1990) Protein Purification Applications: A Practical Approach, IRL Press at Oxford, Oxford, England; Harris and Angal Protein Purification Methods: A Practical Approach, IRL Press at Oxford, Oxford, England; Scopes (1993) Protein Purification: Principles and Practice 3rd Edition, Springer Verlag, NY; Janson and Ryden (1998) Protein Purification: Principles, High Resolution Methods and Applications, Second Edition, Wiley-VCH, NY; and Walker (1998) Protein Protocols on CD-ROM, Humana Press, NJ에 개시된 것들을 포함하여 당업계에 주지되어 있으며, 이의 전부는 본 발명에 참조로 포함된다.
일부 실시태양에서, 본 발명은 분비된 생성물을 생산하도록 디자인된 균주를 개량시키는 방법을 교시한다. 예를 들어, 본 발명은 귀중한 작은 분자 또는 펩타이드를 생산하는 세포 배양물의 견고성, 수율, 효율 또는 전반적인 바람직함을 개선시키는 방법을 교시한다.
일부 실시태양에서, 면역학적 방법을 사용하여 본 발명의 세포에 의해 생산된 분비된 또는 분비되지 않은 생성물을 검출 및/또는 정제하는데 사용될 수 있다. 한 예시적 접근법에서, 통상적인 방법을 사용하여 생성물 분자(예를 들어, 인슐린 폴리펩타이드 또는 이의 면역원성 단편에 대해)에 대해 생성된 항체는 비드 상에 고정화되고, 엔도글루카나아제가 결합되고 침전되는 조건하에 세포 배양 배지와 혼합된다. 일부 실시태양에서, 본 발명은 효소-결합 면역흡착 분석법(ELISA)의 사용을 교시한다.
다른 관련 실시태양에서, 면역크로마토그래피가 미국 특허 제5,002,303호, 미국 특허 제5,591,645호, 미국 특허 제4,855,240호, 미국 특허 제4,435,504호, 미국 특허 제4,980,298호 및 Se-Hwan Paek, et al., "Development of rapid One-Step Immunochromatographic assay, Methods", 22, 53-60, 2000에 개시된 바와 같이 사용되며, 이의 각각은 참조로 본 발명에 포함된다. 일반적인 면역크로마토그래피는 2개의 항체를 사용하여 표본을 검출한다. 제 1 항체는 시험 용액 중에 또는 시험 용액을 떨어뜨린 다공성 막으로 제조된 대략 직사각형 형태의 시험편의 말단 부분에 존재한다. 이 항체는 라텍스 입자 또는 금 콜로이드 입자(이 항체는 이하에서 표지 항체로 불릴 것이다)로 표지한다. 떨어뜨린 시험 용액이 검출될 표본을 포함하는 경우, 표지된 항체는 표본을 인식하여 표본과 결합한다. 표본과 표지된 항체의 복합체는 모세관 현상에 의해 여과지로 만들어지고 표지된 항체를 포함하는 말단의 반대편 말단에 부착된 흡수체를 향하여 흐른다. 이 흐름 동안, 표본과 표지 항체의 복합체가 다공질 막의 중간에 존재하는 제 2 항체(이하에서 태핑 항체로 불릴 것이다)에 의해 인식되어 포획되고, 그 결과, 복합체는 가시광 신호로서 다공성 막 상의 검출부 상에 나타내고 검출된다.
일부 실시태양에서, 본 발명의 선별 방법은 측광 검출 기술(흡수, 형광)에 기초한다. 예를 들어, 일부 실시태양에서, 검출은 항체에 결합된 GFP와 같은 형광 단 검출기의 존재에 기초할 수 있다. 다른 실시태양에서, 측광 검출은 세포 배양 물로부터의 원하는 생성물 상의 축적에 기초할 수 있다. 일부 실시태양에서, 생성물은 배양물의 UV 또는 상기 배양물로부터의 추출물을 통해 검출될 수 있다.
당업자는 본 발명의 방법이 관심의 임의의 바람직한 생체분자 생성물을 생산하는 숙주 세포와 양립할 수 있음을 인식할 것이다. 하기 표 2는 본 발명의 범위 내에 포함되는 생성물 카테고리, 생체분자 및 숙주 세포의 비 제한적 목록을 제공한다. 이들 실시예는 설명의 목적으로 제공되며, 어떠한 방식으로도 본 개시된 기술의 응용가능성을 제한하려는 것이 아니다.
본 발명의 숙주 세포 및 관심 생성물의 비 제한적 목록.
|
제품 카테고리
|
생성물
|
숙주 카테고리
|
숙주
|
| 향신료 & 향료 |
아가우드 |
효모 |
Saccharomyces
cerevisiae
|
| 향신료 & 향료 |
암브록스 |
효모 |
Saccharomyces
cerevisiae
|
| 향신료 & 향료 |
누트카톤 |
효모 |
Saccharomyces
cerevisiae
|
| 향신료 & 향료 |
파출리 오일 |
효모 |
Saccharomyces
cerevisiae
|
| 향신료 & 향료 |
사프론 |
효모 |
Saccharomyces
cerevisiae
|
| 향신료 & 향료 |
산델우드 오일 |
효모 |
Saccharomyces
cerevisiae
|
| 향신료 & 향료 |
발렌센 |
효모 |
Saccharomyces
cerevisiae
|
| 향신료 & 향료 |
바닐린 |
효모 |
Saccharomyces
cerevisiae
|
| 식품 |
CoQ10/유비퀴놀 |
효모 |
Schizosaccharomyces
pombe
|
| 식품 |
오메가 3 지방산 |
미세조류 |
Schizochytrium
|
| 식품 |
오메가 6 지방산 |
미세조류 |
Schizochytrium
|
| 식품 |
비타민 B2 |
사상균류 |
Ashbya
gossypii
|
| 식품 |
에리쓰리톨 |
효모-유사 균류 |
Torula
coralline
|
| 식품 |
에리쓰리톨 |
효모-유사 균류 |
Pseudozyma
tsukubaensis
|
| 식품 |
에리쓰리톨 |
효모-유사 균류 |
Moniliella
pollinis
|
| 식품 |
스테비올 글리코사이드 |
효모 |
Saccharomyces
cerevisiae
|
| 유기산 |
시트르산 |
사상균류 |
Aspergillus
niger
|
| 유기산 |
시트르산 |
사상균류 |
Aspergillus
carbonarius
|
| 유기산 |
시트르산 |
사상균류 |
Aspergillus
aculeatus
|
| 유기산 |
시트르산 |
효모 |
Pichia
guilliermondii
|
| 유기산 |
글루콘산 |
사상균류 |
Aspergillus
niger
|
| 유기산 |
이타콘산 |
사상균류 |
Aspergillus
terreus
|
| 유기산 |
이타콘산 |
사상균류 |
Aspergillus
niger
|
| 유기산 |
LCDAs - DDDA |
효모 |
Candida
|
| 유기산 |
코지산 |
사상균류 |
Aspergillus
oryzae
|
| 유기산 |
코지산 |
사상균류 |
Aspergillus
flavus
|
| 유기산 |
코지산 |
사상균류 |
Aspergillus
tamarii
|
| 유기산 |
코지산 |
사상균류 |
Aspergillus
oryzae
|
| 유기산 |
옥살산 |
사상균류 |
Aspergillus
niger
|
| 유기산 |
숙신산 |
사상균류 |
Aspergillus
saccarolyticus
|
| 유기산 |
락트산 |
사상균류 |
Aspergillus
niger
|
| 유기산 |
락트산 |
사상균류 |
Aspergillus
brasiliensis
|
| 지질 강하제 |
로바스타틴 |
사상균류 |
Aspergillus
terreus
|
| 멜라닌생성 억제제 |
터레인 |
사상균류 |
Aspergillus
terreus
|
| 면역억제제 |
사이클로스포린 A |
사상균류 |
Aspergillus
terreus
|
| 항증식 억제제 |
아스퍼푸라논 |
사상균류 |
Aspergillus
terreus
|
| 항증식 억제제 |
아스퍼푸라논 |
사상균류 |
Aspergillus
nidulans
|
| 콜레스테롤 저하제 |
파이리파이로펜 |
사상균류 |
Aspergillus
fumigatus
|
| 항생제 |
페니실린 |
사상균류 |
Aspergillus
oryzae
|
| 항생제 |
페니실린 |
사상균류 |
Aspergillus
nidulans
|
| 항균제 |
푸마길린 |
사상균류 |
Aspergillus
fumigatus
|
| 항암제 |
푸미트레모긴 C |
사상균류 |
Aspergillus
fumigatus
|
| 항암제 |
스피로트리프로스타틴 |
사상균류 |
Aspergillus
fumigatus
|
| 항암제; 항균제 |
필나불린 |
사상균류 |
Aspergillus
ustus
|
| 항암제 |
페닐아시틴 |
사상균류 |
Aspergillus
ustus
|
| 항암제 |
스테파시딘 A & B |
사상균류 |
Aspergillus
ochraceus
|
| 항암제 |
아스퍼페나메이트 |
사상균류 |
Aspergillus
flavus
|
| 콜로사이토키닌 길항제 |
아스퍼리신 |
사상균류 |
Aspergillus
alliaceus
|
| 산업용 효소 |
알파-아밀라제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
알파-아밀라 |
사상균류 |
Aspergillus
oryzae
|
| 산업용 효소 |
아미노펩티다제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
아미노펩티다제 |
사상균류 |
Aspergillus
oryzae
|
| 산업용 효소 |
아미노펩티다제 |
사상균류 |
Aspergillus
sojae
|
| 산업용 효소 |
AMP 디아미나제 |
사상균류 |
Aspergillus
melleus
|
| 산업용 효소 |
카탈라제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
셀룰라제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
키모신 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
에스테라제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
알파-글루코시다제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
베타-글루카나제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
베타-글루카나제 |
사상균류 |
Aspergillus
aculeatus
|
| 산업용 효소 |
글루코스 옥시다제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
글루타미나제 |
사상균류 |
Aspergillus
oryzae
|
| 산업용 효소 |
글루타미나제 |
사상균류 |
Aspergillus
sojae
|
| 산업용 효소 |
베타-D-글루코시다제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
이눌리나제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
락타아제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
리파아제 |
사상균류 |
Aspergillus
niger
|
| 산업용 효소 |
리파아제 |
사상균류 |
Aspergillus
oryzae
|
| 산업용 효소 |
자일라나제 |
사상균류 |
Aspergillus
niger
|
선택 기준 및 목표
본 발명의 방법에 적용되는 선택 기준은 균주 개량 프로그램의 특정 목표에 따라 달라질 것이다. 본 발명은 임의의 프로그램 목표를 충족시키도록 조정될 수 있다. 예를 들어, 일부 실시태양에서, 프로그램 목표는 즉각적인 시간 제한없이 반응의 단일 배치 수율을 최대화하는 것일 수 있다. 다른 실시태양에서, 프로그램 목표는 특정 생성물을 생산하거나 특정 비율의 생성물을 생산하기 위해 생합성 수율을 재조정하는 것일 수 있다. 다른 실시태양에서, 프로그램 목표는 폴리머의 탄소 사슬을 길게하는 것과 같이 생성물의 화학적 구조를 변형시키는 것일 수 있다. 일부 실시태양에서, 프로그램 목표는 수율, 역가, 생산성, 부산물 제거, 공정 이상현상에 대한 내성, 최적 성장 온도 및 성장율과 같은 성능 특성을 개선하는 것일 수 있다. 일부 실시태양에서, 프로그램 목표는 미생물에 의해 생성된 관심 생성물의 부피 생산성, 비 생산성, 수율 또는 역가에 의해 측정된 바와 같이 개량된 숙주 성능이다.
다른 실시태양에서, 프로그램 목표는 투입량 당 최종 생성물 수율(예를 들어, 수크로오스의 파운드당 생산된 총 에탄올의 양)의 관점에서 상업적 균주의 합성 효율을 최적화하는 것일 수 있다. 다른 실시태양에서, 프로그램 목표는 예를 들어 배치 완료율 또는 연속 배양 시스템에서의 수율로 측정된 합성 속도를 최적화하는 것일 수 있다. 다른 실시태양에서, 프로그램 목표는 특정 파지에 대한 균주 저항성을 증가시키거나, 그렇지 않으면 배양 조건 하에서 균주 생력/강건성을 증가시키는 것일 수 있다.
일부 실시태양에서, 균주 개량 프로젝트는 하나 이상의 목표에 종속될 수 있다. 일부 실시태양에서, 변형 프로젝트의 목표는 품질, 신뢰성 또는 전반적인 수익성에 달려있다. 일부 실시태양에서, 본 발명은 상기한 균주 특성의 하나 이상을 가진 관련된 선택된 돌연변이 또는 돌연변이 그룹을 교시한다.
당업자는 특정 프로젝트 목표를 달성하기 위해 어떻게 균주 선택 기준을 맞춤하는지를 인식할 것이다. 예를 들어, 반응 포화시 균주의 단일 배치 최대 수율의 선택은 높은 단일 배치 수율을 가진 균주를 확인하는데 적절할 수 있다. 다양한 온도 및 조건에서 수율의 일관성에 기반한 선택은 견고성 및 신뢰성이 증가된 균주를 확인하는데 적절할 수 있다.
일부 실시태양에서, 초기 고 처리량 단계 및 탱크-기반 검증에 대한 선택 기준은 동일할 것이다. 다른 실시태양에서, 탱크-기반 선택은 추가 및/또는 상이한 선택 기준하에서 작동할 수 있다. 예를 들어, 일부 실시태양에서, 고 처리량 균주 선택은 단일 배치 반응 완료 수율에 기초할 수 있지만, 탱크-기반 선택은 반응 속도에 대한 수율에 기초한 선택을 포함하도록 확대될 수 있다.
서열화
일부 실시태양에서, 본 발명은 본 발명에 기재된 유기체의 전체-게놈 서열화를 교시한다. 다른 실시태양에서, 본 발명은 또한 본 발명의 방법에 대한 품질 조절제로서의 플라스미드, PCR 생성물 및 다른 올리고의 서열화를 교시한다. 크고 작은 프로젝트를 위한 서열화 방법은 당업자에게 주지되어 있다.
일부 실시태양에서, 핵산을 서열화하는 임의의 고 처리량 기술이 본 발명의 방법에 사용될 수 있다. 일부 실시태양에서, 본 발명은 전체 게놈 서열화를 교시한다. 다른 실시태양에서, 본 발명은 유전자 변이를 확인하기위한 앰플리콘 서열화 울트라 딥 서열화를 교시한다. 일부 실시태양에서, 본 발명은 또한 태그맨테이션 (tagmentation)을 포함하는 신규한 라이브러리 제조 방법을 교시한다(WO/2016/073690 참조). DNA 서열화 기술은 표지된 터미네이터 또는 프라이머를 사용하는 고전적인 다이데옥시 서열화 반응(생거 방법) 및 슬라브 또는 모세관에서의 겔 분리; 가역적으로 종결된 표지된 뉴클레오타이드를 사용하는 합성에 의한 서열화, 열서열화; 454 서열화; 표지된 올리고 뉴클레오타이드 프로브의 라이브러리에 대한 대립유전자 특이적 혼성화; 결찰이 뒤따르는 표지된 클론의 라이브러리에 대한 대립유전자 특이적 혼성화를 사용하는 합성에 의한 서열화; 중합 단계 동안 표지된 뉴클레오타이드의 혼입의 실시간 모니터링; 폴로니 서열화; 및 SOLiD 서열화를 포함한다.
본 발명의 한 양태에서, 연속적으로 서열화되는 고체 표면상의 개별 분자를 공간적으로 분리하는 단계를 포함하는 서열화의 고 처리량 방법이 사용된다. 이런 고체 표면은 비다공성 표면(솔렉사 서열화, 예를 들어, Bentley et al, Nature, 456: 53-59 (2008) or Complete Genomics sequencing, e.g. Drmanac et al, Science, 327: 78-81 (2010)), 비드-또는 입자 결합 주형을 포함할 수 있는 웰의 어레이(454 서열화, 예를 들어, Margulies et al, Nature, 437: 376-380 (2005) or Ion Torrent sequencing, U.S. patent publication 2010/0137143 or 2010/0304982), 미세가공된 막(SMRT 서열화, 예를 들어, Eid et al, Science, 323: 133-138 (2009)) 또는 비드 어레이(폴로니 서열화 또는 SOLiD 서열화, 예를 들어, Kim et al, Science, 316: 1481-1414 (2007))를 포함할 수 있다.
다른 실시태양에서, 본 발명의 방법은 분리된 분자가 고체 표면상에서 공간적으로 분리되기 전 또는 후에 분리된 분자를 증폭시키는 단계를 포함한다. 사전 증폭은 에멀젼 PCR, 또는 롤링 써클 증폭과 같은 에멀젼-기초 증폭을 포함할 수 있다. 또한 벤틀레이 등(상기) 및 제조사 지시(예를 들어, TruSeq™ Sample Preparation Kit and Data Sheet, Illumina, Inc., San Diego, Calif., 2010); 및 추가로 참조로 포함된 다음 참조문헌: 미국 특허 제6,090,592호; 제6,300,070호; 제7,115,400호; 및 EP0972081B1에 기술된 바와 같이 개별 주형 분자가 고체 표면상에서 공간적으로 분리된 후, 브리지 PCR에 의해 평행하게 증촉되어 분리된 클론 집단 또는 클러스터를 형성한 후, 서열화되는 솔렉사-기초 서열화가 교시된다.
한 실시태양에서, 고체 표면상에 배치되고 증폭된 개개의 분자는 cm2당 적어도 105 클러스터의 밀도; 또는 cm2당 적어도 5x105의 밀도; 또는 cm2당 적어도 106 클러스터의 밀도로 클러스터를 형성한다. 한 실시태양에서, 상대적으로 높은 에러율을 갖는 서열화 화학 반응이 사용된다. 이런 실시태양에서, 이런 화학 반응에 의해 생산된 평균 품질 점수는 서열 판독 길이의 단조 감소 함수이다. 한 실시태양에서, 이런 감소는 서열 판독의 0.5%가 1-75 위치에서 적어도 하나의 오차를 가지며; 서열 판독의 1%가 76-100 위치에서 적어도 하나의 오차를 가지며; 서열 판독의 2%가 101-125 위치에서 적어도 하나의 오차를 갖는 것에 상응한다.
게놈-전체 유전자 디자인 기준의 효과의 전산 분석 및 예측
일부 실시태양에서, 본 발명은 소정의 숙주 균주에 포함되는 특정 유전자 변형의 효과를 예측하는 방법을 교시한다. 추가의 양태에서, 본 발명은 숙주가 특정 표현형 형질 또는 균주 매개변수를 갖기 위해 소정의 숙주 균주에 포함되어야 하는 제안된 유전자 변형을 생성하는 방법을 제공한다. 소정의 양태에서, 본 발명은 신규 숙주 균주를 디자인하는데 이용될 수 있는 예측 모델을 제공한다. 신규한 숙주 균주는, 예를 들어, A. 니거와 같은 사상균류 숙주 균주일 수 있다.
일부 실시태양에서, 본 발명은 선별의 각 라운드의 수행 결과를 분석하는 방법 및 다음 선별 라운드에서 균주 성능을 향상시키도록 예측된 새로운 제안된 게놈-전체 서열 변형을 생성하는 방법을 교시한다.
일부 실시태양에서, 본 발명은 시스템이 이전의 선별 결과에 기초하여 숙주 균주에 대해 제안된 서열 변형을 생성하는 것을 교시한다. 일부 실시태양에서, 본 시스템의 권고는 직전 선별 검사의 결과에 기초한다. 다른 실시태양에서, 본 시스템의 권고는 하나 이상의 선별 검사의 누적 결과에 기초한다.
일부 실시태양에서, 본 시스템의 권고는 이전에 개발된 HTP 유전자 디자인 라이브러리에 기초한다. 예를 들어, 일부 실시태양에서, 본 시스템은 이전의 선별로부터의 결과를 저장하고, 그 결과를 동일 또는 상이한 숙주 유기체에서 상이한 프로젝트에 적용하도록 디자인된다.
다른 실시태양에서, 본 시스템의 권고는 과학적인 통찰력에 기초한다. 예를 들어, 일부 실시태양에서, 권고는 (주석된 유전자 데이터베이스 및 관련 문헌과 같은 출처로부터의) 유전자의 공지된 특성, 코돈 최적화, 전사 미끄러짐, uORF 또는 다른 가설 주도 서열 및 숙주 최적화에 기초한다.
일부 실시태양에서, 시스템 또는 예측 모델에 의해 권장되는 숙주 균주에 대해 제안된 서열 변형은 다음을 포함하는 개시된 분자 도구 세트의 하나 이상을 이용함으로써 수행된다: (1) 프로모터 스왑, (2) SNP 스왑, (3) 코돈 교환 개시/중지, (4) 서열 최적화, (5) 스왑 중지, (5) 상위성 매핑.
본 발명에 기술된 HTP 유전자 공학 플랫폼은 임의의 특정 미생물 또는 표현형 형질에 대해 불가지론적이다(예를 들어, 특정 화합물의 생산). 즉, 본 발명에서 교시된 플랫폼 및 방법은 숙주 세포가 임의의 바람직한 표현형 형질을 갖도록 조작하기 위해 임의의 숙주 세포와 함께 사용될 수 있다. 또한, 하나의 새로운 숙주 세포를 생성하기 위해 사용된 소정의 HTP 유전자 공학 공정으로부터 얻은 교훈은, 교시된 방법 동안 발생하는 무수한 공정 매개변수의 저장, 특징화 및 분석의 결과로서, 임의의 수의 다른 숙주 세포에 적용할 수 있다. 특정 양태에서, 숙주 세포는 당업계에 공지된 임의의 다핵체 유기체일 수 있다. 예를 들어, 숙주 세포는 사상균류 숙주 세포일 수 있다. 본 발명에 사용하기 위한 사상균류 숙주 세포의 한 예는 A. 니거일 수 있다.
상위성 맵핑 섹션에서 언급된 바와 같이, HTP 유전자 디자인 라이브러리로부터의 돌연변이의 집합을 일부 바람직한 예측 모델을 통해 특정 배경으로 통합시킴으로써 얻어진 가상 균주의 성능(별칭, 점수)을 추정하는 것이 가능하다. 이런 예측 모델을 감안할 때, 조합 통합을 통해 돌연변이 라이브러리에 접근할 수 있는 모든 가상 균주를 채점하고 순위를 매기는 것이 가능하다. 아래 섹션은 본 HTP 플랫폼에서 사용되는 특정 모델에 대해 간략히 설명한다.
예측 균주 디자인
본 발명에 기술된 것은 유전자 변화 및 균주 성능을 기술하는 방법, 균주에서 변화의 구성에 기초하여 균주 성능을 예측하는 방법, 높은 예측된 성능을 갖는 후보 디자인을 추천하는 방법, 및 2차 고려사항, 예를 들어, 현존하는 균주에 대한 유사성, 상위성 또는 예측의 신뢰를 최적화를 위해 예측을 필터링하는 방법을 포함하는 예측 균주 디자인에 접근법이 본 발명에 기술된다.
균주 디자인 모델에 대한 입력
한 실시태양에서, 설명의 용이함을 위해, 입력 데이터는 두 구성요소: (1) 유전자 변화의 세트 및 (2) 상대적 균주 성능을 포함할 수 있다. 당업자는 이 모델이 다양한 입력을 고려하면서 과적합에 대한 상반되는 고려사항을 염두하면서 용이하게 확장될 수 있음을 인식할 것이다. 유전자 변화 이외에, 조절될 수 있는 입력 매개변수(독립변수)의 일부는 세포 유형(속, 종, 균주, 계통 발생 특성 등) 및 발효가 세포에 의해 수행되는 동안 공정 매개변수(예를 들어, 환경 조건, 취급 장비, 개조 기술, 등)이다.
유전자 변화의 세트는 HTP 유전자 디자인 라이브러리라 불리는 유전자 교란의 이전에 논의된 집합으로부터 유래될 수 있다. 상대적 균주 성능은 임의의 소정의 파라미터 또는 관심 표현형 특성(예를 들어, 화합물, 소분자 또는 관심 생성물의 생산)에 기초하여 평가될 수 있다.
세포 유형은 원핵생물 및 진핵생물 시스템, 속, 종, 균주, 조직 배양(vs. 분산 세포) 등과 같은 일반적인 카테고리에서 특정될 수 있다. 조절될 수 있는 공정 파라미터는 온도, 압력, 반응기 구성 및 배지 조성물을 포함할 수 있다. 반응기 구성의 예는 반응기의 부피, 공정이 배치인지 또는 연속적인지 여부, 및 연속적이면 체적 유량 등을 포함한다. 또한, 세포가 존재하는 구조를 특정할 수 있다. 배지 조성물의 예는 전해질, 영양소, 폐기물, 산, pH 등의 농도를 포함한다.
예측 균주 모델을 만드는데 사용되는 초기 선형 회귀 모델에서 사용될 선택된 HTP 유전자 디자인 라이브러리로부터의 유전자 변화 세트
예측 균주 디자인 모델을 생성하기 위해, 동일한 미생물 종의 균주의 유전적 변화가 먼저 선택된다. 각 유전자 변화의 이력도 제공된다(예를 들어, 이 균주 계보에서 가장 최근의 변형 -"마지막 변화"를 도시한다). 따라서, 이 균주의 성능을 부모의 성능과 비교하는 것은 "최종 변화" 돌연변이의 성능에 관한 데이터 포인트를 나타낸다.
제조된 균주 성능 평가
교시된 모델의 목적은 균주에 도입된 유전자 변화의 구성에 기초하여 균주 성능을 예측하는 것이다. 비교를 위한 표준을 구축하기 위해, 균주 성능은 분석 플레이트당 균주당 평균 성능을 먼저 계산함으로써 공통 기준 균주에 대해 상대적으로 계산된다. 그런 후에 상대적인 성능은 동일한 플레이트 내에서 조작된 균주 및 공통 기준 균주 사이의 평균 성능에 차이로 계산된다. 계산을 플레이트 내 비교로 제한하면 고려중인 샘플 모두가 동일한 실험 조건을 얻을 수 있음을 보장한다.
도 41은 입력 데이터에 대한 상대적 균주 성능의 분포가 고려중인 가정적인 실시예를 도시한다. 0의 상대적 성능은 조작된 균주가 인-플레이트 기본 또는 "참조" 균주에 동일하게 잘 수행되었음을 나타낸다. 0보다 크게 수행할 수 있는 균주를 확인하는 예측 모델의 능력이 중요하다. 더구나, 그리고 더 일반적으로, 임의의 소정의 균주는 일부 기준에 의해 이의 부모보다 우월한지 여부가 중요하다. 실제로, 기준은 부모 수준 이상의 일부 임계값을 충족하거나 초과하는 생성물 역가일 수 있으며, 원하는 방향으로 부모와 통계적으로 유의미한 차이를 갖는 것은 대신에 또는 추가로 사용될 수도 있다. 기본 또는 "참조" 균주의 역할은 단순히 플레이트 내 또는 플레이트 간의 비교를 위한 추가된 표준화 요소로서 작용하는 것이다.
염두에 두어야 할 개념은 부모 균주 및 기준 균주의 차이점이다. 부모 균주는 돌연변이유발의 현재 라운드에 사용된 배경이다. 기준 균주는 특히 플레이트 간의 비교를 용이하게 하기 위해 모든 플레이트에서 사용되는 대조군 균주이며 일반적으로 위에 언급된 "기본 균주"입니다. 그러나 기본 균주(예를 들어, 야생형 또는 산업용 균주는 전체 성능을 벤치마크하는데 사용된다)는 소정의 라운드의 균주 개량에서 돌연변이유발 표적이라는 의미에서 반드시 "기본"이 아니기 때문에, 보다 설명적인 용어는 "기준 균주"이다.
요약하면, 기본/기준 균주는 제조된 균주의 성능을 벤치마크하는데 사용되는 반면, 부모 균주는 관련 유전자 배경에서 특이적 유전자 변화의 성능을 벤치마크하는데 사용된다.
선형 회귀 분석에 의한 제조된 균주의 성능 순위 매김
개시된 모델의 목적은 제조된 균주에 도입된 유전자 변화의 구성의 함수로서, 상대적 균주 성능을 기술함으로써, 제조된 균주의 성능을 순위매기기 위한 것이다. 본 발명 전반에 걸쳐 논의된 바와 같이, 다양한 HTP 유전자 디자인 라이브러리는 조작된 균주에 도입되는 가능한 유전자 변화(예를 들어, 유전자 교란/변경)의 레퍼토리를 제공한다. 선형 회귀는 현재 설명된 전형적인 예측 모델의 기초이다.
유전자 변화 및 상대적 성능에 대한 이의 효과는 회귀-기반 모델링에 대한 예시적인 입력을 포함한다. 균주 성능은 균주에 포함된 유전자 변화의 구성의 함수로서 공통 기본 균주에 상대적으로 평가된다.
제조된 균주를
특징화하는
선형 회귀
선형 회귀는 구현 및 해석의 용이함 때문에 기술된 HTP 게놈 공학 플랫폼에 대한 매력적인 방법이다. 얻어진 회귀 계수는 각 유전자 변화의 존재에 기인한 상대적 균주 성능의 평균 증가 또는 감소로 해석될 수 있다.
예를 들어, 일부 실시태양에서, 이 기술은 최초 프로모터를 다른 프로모터로 변경하면 평균 약 1, 2, 3, 4, 5, 6, 7, 8, 9, 10개 이상 단위만큼 상대적 균주 성능을 개량시키고, 따라서 어떠한 음성 상위성 상호작용의 부재시에 잠재적으로 매우 바람직한 변화라고 결론 내리게 한다(참고: 입력은 단위가 없는 정규화 값).
따라서, 교시된 방법은 선형 회귀 모델을 사용하여 다양한 교시된 라이브러리로부터의 그들의 게놈에 도입된 다양한 유전자 교란을 갖는 제조된 균주를 기술하고/특성화하고 순위를 매긴다.
예측 디자인
모델링
구축된 균주로부터의 데이터를 사용하는 상기한 선형 회귀 모델은 아직 제조되지 않은 균주에 대한 성능 예측을 수행하는데 사용될 수 있다.
절차는 다음과 같이 요약될 수 있다: 가능한 모든 형태의 유전자 변화를 인 실리코로 생성한다 → 회귀 모델을 사용하여 상대적인 균주 성능을 예측한다 → 성능에 의해 후보 균주 디자인을 순서화한다. 따라서 회귀 모델을 이용하여 아직 제조되지 않은 균주의 성능을 예측함으로써, 이 방법은 더 적은 실험을 수행하는 동시에 고성능 균주의 생산을 가능하게 한다.
구성 생성
아직 제조되지 않은 균주의 성능을 예측하기 위한 모델을 구축하는 경우, 첫 번째 단계는 일련의 디자인 후보를 생산하는 것이다. 이것은 균주의 유전자 변화의 총 수를 고정한 다음, 가능한 모든 유전자 변화의 조합을 정의함으로써 이루어진다. 예를 들어, 잠재적 유전자 변화/교란의 총 수를 29(예를 들어, 유전자 교란의 영역이 29인 한 29개 가능한 SNP 또는 29개 상이한 프로모터 또는 이의 임의의 조합)으로 설정한 후 29개 잠재적 유전자 변화의 모든 가능한 3-구성원 조합을 디자인하도록 결정할 수 있으며, 이것이 3,654개 후보 균주 디자인을 생성할 것이다.
상기한 3,654개 후보 균주에 대한 문맥을 제공하기 위해, n!/((n-r)! * r!)을 사용하여 n개의 가능한 구성원으로부터 크기 r의 비 중복 그룹의 수를 계산할 수 있다고 생각한다. r = 3이면 n = 29는 3,654를 제공한다. 따라서, 29개 잠재적 변화의 모든 가능한 3개 구성원 조합을 디자인하면, 결과는 3,654개 후보 균주이다.
새로운 균주 디자인의 성능 예측
입력으로서 조합 구성으로 위에서 구축된 선형 회귀 분석을 사용하여, 각각의 후보 디자인의 예상된 상대 성능을 예측할 수 있다. 예를 들어, 상위 100개 예상 균주 디자인에 대한 변화의 조성물은 2-차원 지도에 요약될 수 있고, 여기서 x축은 잠재적 유전자 변화의 풀(29개 가능한 유전자 변화)을 열거하고, y축은 순위 순서를 도시한다.
예측 정확도는 새로운 관찰이 모델을 반복적으로 재훈련하고 재구성하는데 사용됨에 따라 시간이 지남에 따라 증가해야 한다. 본 발명자에 의한 연구 결과는 예측 모델이 반복적으로 재훈련되고 개량될 수 있는 방법을 설명한다. 모델 예측의 품질은 예측된 값과 관찰된 값 사이의 연관성의 강도를 나타내는 상관 계수 또는 평균 모델 오차의 척도인 평균 제곱근 오차를 포함하는 여러 방법을 통해 평가될 수 있다. 모델 평가에 선택된 메트릭을 사용하여, 시스템은 모델이 재훈련되어야 할 때에 대한 규칙을 정의할 수 있다.
상기 모델에 대한 몇 가지 설명되지 않은 가정은 다음을 포함한다: (1) 상위성 상호작용이 없다; (2) 예측 모델을 구축하기 위해 사용된 유전자 변화/교란은 유전자 변형의 제안된 조합으로서 모두 동일한 배경에서 만들어진다.
2차 기능에 대한
필터링
상기 설명된 예는 예측된 숙주 세포 성능에 기초한 선형 회귀 예측에 초점을 두었다. 일부 실시태양에서, 본 선형 회귀 방법은 포화 바이오매스, 저항성 또는 다른 측정가능한 숙주 세포 특징과 같은 비-생체분자 인자에도 적용될 수 있다. 따라서, 본 발명의 방법은 또한 제조할 후보자의 우선순위를 정할 때 예측된 성능 이외의 다른 특징을 고려하는 것을 교시한다. 추가적인 관련 데이터가 있다고 가정하면, 비선형 항도 회귀 모델에 포함된다.
기존의 균주와의 밀접성
이미 제조된 것과 유사한 예측된 균주는 상위 예측 후보가 아니더라도 시간 및 비용을 절감할 수 있다
변화의 다양성
상기한 모델을 구축할 때, 유전자 변화가 상위성 상화작용의 존재에 의해 진정으로 부가적일 것을 확신할 수 없다(선형 회귀에 의해 가정되고 상기 가정으로 언급됨). 그러므로, 유전자 변화 비유사성의 지식은 긍정적인 가산성의 가능성을 증가시키는데 사용될 수 있다. 예를 들어, 상위 균주로부터의 변화가 동일한 대사 경로에 있고 유사한 성능 특성을 갖는 것을 아는 경우, 그 정보는 변화의 비유사한 구성을 가진 다른 상위 균주를 선택하는데 사용될 수 있다. 상위성 매핑에 관한 위의 섹션에서 설명한 바와 같이, 예측된 최고의 유전자 변화는 상당히 비유사한 응답 프로파일을 가진 돌연변이에 대한 선택을 제한하기 위해 필터링될 수 있다. 대안적으로, 선형 회귀는 예측을 가중하기 위해 유사성 매트릭스를 사용하는 가중된 최소 자승 회귀(weighted least squares regression)일 수 있다.
예측된 성능의 다양성
마지막으로, 예측 모델을 검증하고 후속적으로 개량하기 위해, 중간 또는 나쁜 예측된 성능을 가진 균주를 디자인하도록 선택할 수 있다.
반복 균주 디자인 최적화
실시태양에서, 주문 배치 엔진(208)은 공장(210)에 공장 주문을 하여 상위 후보 돌연변이를 포함하는 미생물 균주를 제조한다. 피드백-루프 방식에서, 결과는 분석 장비(214)에 의해 분석되어 어느 미생물이 원하는 표현형 특성을 나타내는지를 결정할 수있다(314). 분석 단계 동안, 변형된 균주 배양물은 평가되어 성능, 즉 산업적 규모로 생산되는 능력을 포함하는 원하는 표현형 특성의 발현을 측정한다. 예를 들어, 분석 단계는, 다른 것들 중에서, 콜로니 건강의 지표로서 미생물 콜로니 성장을 측정하기 위해 플레이트의 이미지 데이터를 사용한다. 분석 장비(214)는 유전자 변화를 표현형 성능과 상관시키고 결과적인 유전자형-표현형 상관 데이터를 라이브러리(206)에 저장될 라이브러리에 저장하여 장래의 미생물 생산을 알려주는데 사용된다.
특히, 충분히 높게 측정된 성능을 실제로 초래하는 후보 변화는 표에 데이터베이스의 행으로서 추가될 수 있다. 이러한 방식으로, 최고의 성능 돌연변이가 감독된 기계 학습 방식으로 예측 균주 디자인 모델에 추가된다.
LIMS는 이전의 공장 가동으로부터 개발된 상관관계에 기초하여 디자인/제조/테스트/분석 사이클을 반복한다. 후속 사이클 동안, 단독으로 또는 인간 조작자와 함께 분석 장비(214)는 상관관계 데이터를 사용하여 유전자 변형을 미세하게 조정하여 더 미세한 정교성(granularity)으로 더 나은 표현형 성능을 달성하도록 입력 인터페이스(202)로 다시 입력하기 위한 기본 균주로서 최고의 후보를 선택할 수 있다. 이러한 방식으로, 본 발명의 실시태양의 실험실 정보 관리 시스템은 품질 개선 피드백 루프를 구현한다.
요약하면, 도 16의 흐름도를 참조하면, 반복 예측 균주 디자인 작업 흐름은 다음과 같이 기술될 수 있다:
입력과 출력 변수의 훈련 세트, 예를 들어, 입력으로 유전자 변화 및 출력으로 성능 특성을 생성한다(3302). 생성은 이전의 유전자 변화 및 이러한 유전자 변화를 포함하는 미생물 균주의 상응하는 측정된 성능에 기초하여 분석 장비(214)에 의해 수행될 수 있다.
훈련 세트를 기반으로 초기 모델(예를 들어, 선형 회귀 모델)을 개발한다(3304). 이는 분석 장비(214)에 의해 수행될 수 있다.
디자인 후보 균주를 생성한다(3306).
한 실시태양에서, 분석 장비(214)는 변화의 조합의 형태로, 배경 균주에 대해 행해지는 유전자 변화의 수를 고정시킬 수 있다. 이런 변화를 나타내기 위해, 분석 장비(214)는 변화의 조합을 나타내는 하나 이상의 DNA 세부사항 표현을 해석자(204)에 제공할 수 있다. (이런 유전자 변화 또는 이런 변화를 포함하는 미생물 균주는 "테스트 입력"으로 불릴 수 있다) 해석자(204)는 하나 이상의 DNA 세부사항을 해석하고, 실행 엔진(207)은 DNA 세부사항을 실행하여 이런 변화에 대한 개별 후보 후보자 디자인 균주를 나타내는 분석된 출력으로 DNA 세부사항을 채운다.
모델에 기초하여, 분석 장비(214)는 각각의 후보 디자인 균주의 예상 성능을 예측한다(3308).
분석 장비(214)는 최고의 예측된 성능을 가진 제한된 수, 예를 들어, 100개의 후보 디자인을 선택한다(3310).
상위성 매핑과 관련하여 본 발명의 다른 곳에서 설명된 바와 같이, 분석 장비(214)는 예를 들어, 상위성 효과에 대한 상위 디자인을 필터링하거나, 예측 모델 속에 상위성을 고려하여 상위성과 같은 2차 효과를 설명할 수 있다.
주문 배치 엔진(208)에 의해 생성된 공장 주문에 기초하여 필터링된 후보 균주를(공장(210)에서)제조한다(3312).
분석 장비(214)는 선택된 균주의 실제 성능을 측정하고 우수한 실제 성능을 기초로 제한된 수의 선택된 균주를 선택하고(3314), 디자인 변화와 이의 얻어진 성능을 예측 모델에 추가한다 (3316). 선형 회귀 예에서, 디자인 변화 및 이의 관련 성능의 세트를 표에 새로운 행으로 추가한다.
분석 장비(214)는 새로운 디자인 후보 균주의 생성으로 다시 반복하고(3306), 정지 조건이 만족될 때까지 반복을 지속한다. 정지 조건은, 예를 들어, 수율, 성장률 또는 역가와 같은 성능 메트릭을 만족시키는 적어도 하나의 미생물 균주의 측정된 성능을 포함할 수 있다.
상기 예에서, 변형 디자인의 반복 최적화는 기계 학습을 구현하기 위해 피드백 및 선형 회귀를 사용한다. 일반적으로, 기계 학습은 제한된 수의 표지된 데이터의 예를 사용하고 알려지지 않은 데이터에 동일한 작업을 실행하여 정보 작업의 수행(예를 들어, 분류 또는 회귀)시에, 매개 변수, 기술 또는 기타 기능과 같은 성능 기준의 최적화로 기술될 수 있다. 상기 선형 회귀 예와 같은 감독된 기계 학습에서, 기계(예를 들어, 컴퓨팅 디바이스)는 예를 들어 훈련 데이터에 의해 나타난 패턴, 카테고리, 통계적 관계 또는 다른 속성을 확인함으로써 학습한다. 그런 다음 학습 결과는 새로운 데이터가 동일한 패턴, 카테고리, 통계적 관계 또는 기타 속성을 나타낼 것인지를 예측하는데 사용된다.
본 발명의 실시태양은 훈련 데이터가 이용가능할 때 다른 감독된 기계 학습 기술을 사용할 수 있다. 훈련 데이터가 없는 경우, 실시태양은 감독되지 않은 기계 학습을 채택할 수 있다. 대안적으로, 실시태양은 소량의 표지된 데이터 및 다량의 비표지된 데이터를 사용하는 반-감독된 기계 학습을 채택할 수 있다. 실시태양은 또한 기계 학습 모델의 성능을 최적화하기 위해 가장 관련이 있는 특징의 서브세트를 선택하기 위해 특징 선택을 채택할 수 있다. 선형 회귀에 대한 대안으로서 또는 선형 회귀에 추가로 선택된 기계 학습 접근법의 유형에 따라, 실시태양은, 예를 들어, 로지스틱 회귀, 신경망, 지지 벡터 기계(SVM), 결정 트리, 숨겨진 마르코프 모델, 베이지안 네트워크, 그램 슈미트, 보강-기반 학습, 계층적 클러스터링을 포함하는 클러스터 기반 학습, 유전자 알고리즘 및 당업계에 공지된 임의의 다른 적절한 학습 기계를 채택할 수 있다. 특히, 실시태양은 로지스틱 회귀를 이용하여 분류 자체와 함께 분류(예를 들어, 상이한 기능 그룹으로 유전자의 분류)의 확률을 제공할 수 있다. 예를 들어, Shevade, A simple and efficient algorithm for gene selection using sparse logistic regression, Bioinformatics, Vol. 19, No. 17 2003, pp. 2246-2253, Leng, et al., Classification using functional data analysis for temporal gene expression data, Bioinformatics, Vol. 22, No. 1, Oxford University Press (2006), pp. 68-76를 참조하고, 이의 전부는 전문이 참조로 본 발명에 포함된다.
실시태양은, 특히 심층 신경망(DNN)으로 알려진 형태로 기계 학습 작업을 수행함에 있어 인기가 증가하고 있는 것으로 밝혀진 그래픽 처리 장치(GPU) 가속 아키텍처를 채택할 수 있다. 본 발명의 실시태양은 GPU 기반 딥 러닝 인터페이스: A Performance and Power Analysis, NVidia Whitepaper, November 2015, Dahl, et al., Multi-task Neural Networks for QSAR Predictions, Dept. of Computer Science, Univ. of Toronto, June 2014 (arXiv:1406.1231 [stat.ML])에 기술된 것과 같은 GPU-기반 기계 학습을 채택할 수 있고, 이의 전부는 전문이 참조로 본 발명에 포함된다. 본 발명의 실시태양에 적용할 수 있는 기계 학습 기술은 다른 참조문헌 중에서, Libbrecht, et al., Machine learning applications in genetics and genomics, Nature Reviews: Genetics, Vol. 16, June 2015, Kashyap, et al., Big Data Analytics in Bioinformatics: A Machine Learning Perspective, Journal of Latex Class Files, Vol. 13, No. 9, Sept. 2014, Prompramote, et al., Machine Learning in Bioinformatics, Chapter 5 of Bioinformatics Technologies, pp. 117-153, Springer Berlin Heidelberg 2005에서 발견될 수 있고, 이의 전부는 전문이 참조로 본 발명에 포함된다.
반복적인 예측 균주 디자인: 실시예
다음은 위에서 설명한 반복적인 예측 균주 디자인 작업 흐름의 예시적인 응용을 제공한다.
훈련 입력 및 출력 변수의 초기 세트가 준비되었다. 이 세트는 정의된 유전자 구성을 가진 1864개의 고유한 조작 균주로 구성되었다. 각 균주는 5 내지 15개의 조작된 변화를 포함하였다. 총 336개의 고유한 유전자 변화가 훈련에 존재하였다.
초기 예측 컴퓨터 모델이 개발되었다. 구현은 일반 선형 모델(4차 다항 커널에 의한 커널 릿지 회귀)을 사용하였다. 구현은 두 가지 뚜렷한 표현형(수율 및 생산성)을 만든다. 아래 도시된 바와 같이, 이들 표현형은 가중치 합계로 결합되어 순위에 대한 단일 점수를 얻는다. 다양한 모델 매개 변수, 예를 들어, 정규화 인자는 지정된 훈련 데이터에 대해 k 배 교차 검증을 통해 조정되었다.
상기 구현은 상기 상위성 매핑 섹션에 기술된 바와 같이 상호작용 효과의 어떠한 명백한 분석도 포함하지 않는다. 그러나, 당업자가 이해할 수 있는 바와 같이, 구현된 일반 선형 모델은 암시적으로 커널의 2차, 3차 및 4차 항을 통해 상호작용 효과를 포착할 수 있다.
모델은 훈련 이후 훈련 세트에 대해 훈련되었고, 훈련 데이터에 대한한 수율 모델의 현저한 품질 적합성을 나타낸다.
그런 후에 후보 균주가 생성되었다. 이 실시태양은 부모 균주에 대한 새로운 유전자 변화의 도입과 관련된 일련의 제조 제약을 포함한다. 여기서, 후보자는 단순히 변화의 원하는 수의 함수로 간주되지 않는다. 대신에, 분석 장비(214)는, 출발점으로서, 고성능 메트릭("종자 균주")을 갖는 것으로 알려진 이전에 디자인된 균주의 집합을 선택한다. 분석 장비(214)는 각각의 종자 균주에 유전자 변화를 개별적으로 적용한다. 도입된 유전자 변화는 종자 균주에 이미 존재하는 것들을 포함하지 않는다. 다양한 기술적, 생물학적 또는 다른 이유로, 특정 돌연변이가 명시적으로 요구되거나 명시적으로 배재된다.
모델에 기초하여, 분석 장비(214)는 후보 균주 디자인의 성능을 예측하였다. 분석 장비(214)는 관심있는 두 표현형에 대한 예측된 성능(수율 및 생산성)에 기초하여 후보를 "최상"에서 "최악"으로 순위를 매긴다. 특히, 분석 장비(214)는 가중 합을 사용하여 후보 균주에 점수를 매긴다:
점수 = 0.8 * 수율/ 최대(수율) + 0.2 * 생산성/최대(생산성),
여기서 수율은 후보 균주에 대한 예측된 수율을 나타내고,
최대(수율)는 모든 후보 균주에 대한 최대 수율을 나타내며,
생산성은 후보 균주의 생산성을 나타내며,
최대(생산성)은 모든 후보 균주에 대한 최대 생산성을 나타낸다.
분석 장비(214)는 용량 제약 및 작업 제약 모두를 부과함으로써 후보의 랭킹 된 목록으로부터 최종 세트의 권고를 생성한다. 일부 실시태양에서, 용량 제한은48개 컴퓨터 생성 후보 디자인 균주와 같은 소정의 수로 설정될 수 있다.
훈련된 모델(위에 설명됨)은 각각의 후보 균주의 예상된 성능(수율 및 생산성에 대해)을 예측하는 데 사용될 수 있다. 분석 장비(214)는 위에 제공된 스코어링 함수를 사용하여 후보 균주를 평가할 수 있다. 용량 및 작업 제약이 적용되어 48개 후보 균주의 필터된 세트를 생산할 수 있다.
필터된 후보 균주는 주문 배치 엔진(208)에 의해 생성된 공장 주문에 기초하여(공장(210)에서) 제조된다(3312). 순서는 후보 균주에 해당하는 DNA 세부사항에 기초할 수 있다.
실제로, 제조 공정은 예측된 실패율을 가지므로 균주의 무작위로 세트가 제조되지 않는다.
분석 장비(214)는 실제 수율 및 생산성 성능을 측정하는데 사용될 수 있다. 분석 장비(214)는 3개의 기준; 모델 정확성; 균주 성능 개량; 인간 전문가가 생성 한 디자인에 대한 동등성(또는 개량)에 기초하여 모델 및 권장 균주를 평가할 수 있다.
수율 및 생산성 표현형은 권장 균주에 대해 측정되고 모델에 의해 예측된 값과 비교될 수 있다.
다음으로, 분석 장비(214)는 각각의 권장 균주에 대한 부모 균주로부터의 성능 변화율을 계산한다. 예측 정확도는 예측된 값과 관측된 값 간의 연관성을 나타내는 상관 계수 또는 평균 모델 오차의 척도인 평균 제곱근 오차를 포함하는 여러 방법을 통해 평가될 수 있다.
여러 라운드의 실험에 걸쳐, 모델 예측은 표류할 수 있고, 새로운 유전자 변화가 예측 정확도를 향상시키기 위해 훈련 입력에 추가될 수 있다. 이 실시예의 경우, 디자인 변경과 이의 결과로 얻은 성능이 예측 모델에 추가되었다(3316).
서비스로서의 게놈 디자인 및 공학
본 발명의 실시태양에서, 도 15의 LIMS 시스템 소프트웨어(3210)는 도 32의 클라우드 컴퓨팅 시스템(3202)에서 구현되어, 다수의 사용자가 본 발명의 실시태양에 따라 미생물 균주를 디자인 및 제조할 수 있게 한다. 도 15는 본 발명의 실시태양에 따른 클라우드 컴퓨팅 환경(3204)을 도시한다. 도 15에 도시된 것과 같은 클라이언트 컴퓨터(3206)는 인터넷과 같은 네트워크(3208)를 통해 LIMS 시스템에 접근한다. 실시태양에서, LIMS 시스템 애플리케이션 소프트웨어(3210)는 클라우드 컴퓨팅 시스템(3202)에 상주한다. LIMS 시스템은 도 15에 도시된 유형의 하나 이상의 프로세서를 사용하는 하나 이상의 컴퓨팅 시스템을 사용할 수 있다. 클라우드 컴퓨팅 시스템 자체는 네트워크를 통해 LIMS 시스템 어플리케이션(3210)을 클라이언트 컴퓨터(3206)에 인터페이스하는 네트워크 인터페이스(3212)를 포함한다. 네트워크 인터페이스(3212)는 클라이언트 컴퓨터(3206)에서 클라이언트 애플리케이션이 LIMS 시스템 소프트웨어(3210)에 접근할 수 있게 하는 어플리케이션 프로그래핑 인터페이스(API)를 포함할 수 있다. 특히, API를 통해, 네트워크 컴퓨터(3026)는 입력 인터페이스(202), 해석자(204), 실행 엔진(207), 주문 배치 엔진(208), 공장(210)을 구동하는 소프트웨어뿐만 아니라 테스트 장비(212) 및 분석 장비(214)를 제한 없이 포함하는 LIMS 시스템(200)의 구성요소에 접근할 수 있다. 서비스로서 소프트웨어(SaaS) 소프트웨어 모듈(3214)은 클라이언트 컴퓨터(3206)에 서비스로서 LIMS 시스템 소프트웨어(3210)을 제공한다. 클라우드 관리 모듈(3216)은 클라이언트 컴퓨터들(3206)에 의해 LIMS 시스템(3210)에 대한 접근을 관리한다. 클라우드 관리 모듈(3216)은 당업계에 공지된 멀티테넌트 애플리케이션, 가상화 또는 다른 아키텍처를 사용하는 클라우드 아키텍처가 여러 사용자에게 서비스를 제공하는 것을 가능하게 한다. 도 44는 사상균류 숙주 세포 시스템에 적용된 LIMS 시스템의 유용성의 원리의 증거를 나타낸다.
게놈 자동화
본 발명의 방법의 자동화는 다중 테스트 균주 변이체로부터의 표적 생성물의 높은 처리량의 표현형 선별 및 확인을 동시에 가능하게 한다.
상기한 게놈 공학 예측 모델링 플랫폼은 수백 및 수천 개의 돌연변이체 균주가 고 처리량 방식으로 구축된다는 사실에 전제된다. 아래에 설명된 로봇 및 컴퓨터 시스템은 이런 고 처리량 공정이 수행될 수있는 구조적 메커니즘입니다.
일부 실시태양에서, 본 발명은 숙주 세포 생산성을 개선하거나 산업 균주를 재활시키는 방법을 교시한다. 이 공정의 일부로서, 본 개시는 DNA를 조립하고, 새로운 균주를 제조하고, 플레이트에서 배양물을 선별하고, 탱크 발효 모델에서 배양 물을 선별하는 방법을 교시한다. 일부 실시태양에서, 본 발명은 새로운 숙주 균주를 생성하고 테스트하는 상기한 방법의 하나 이상이 자동화 로봇에 의해 보조되는 것을 교시한다.
일부 실시태양에서, 본 발명은도 6a-b에 도시된 바와 같이 고 처리량 균주 공학 플랫폼을 교시한다.
HTP 로봇 시스템
일부 실시태양에서, 본 발명에 제공된 방법 및 시스템은 자동화된 단계를 포함한다. 예를 들어, 본 발명에 기술된 바와 같이 원형질체의 생성, 원형질체의 형질전환, 정제 전에 NGS에 의한 형질전환된 원형질체의 선별, 선택/카운터 선택을 통한 동핵성 원형질체의 정제, 정제 후 NGS에 의한 형질전환된 원형질체의 선별은 자동화될 수 있다. 본 발명에 기술된 바와 같이, 방법 및 시스템은 관심 단백질 또는 대사 산물의 생성을 위해 정제된 동핵성 형질전환체를 선별하는 추가 단계를 포함할 수 있다. 본 발명의 자동화된 방법은 로봇 시스템을 포함할 수 있다. 본 발명에 약술된 시스템은 일반적으로 96- 또는 384-웰 미세적정 플레이트의 사용에 관한 것일 수 있지만, 당업자에 의해 이해될 수 있는 바와 같이, 임의의 수의 상이한 플레이트 또는 구성이 사용될 수 있다. 또한, 본 발명에 약술된 단계 중 임의의 단계 또는 모든 단계가 자동화될 수 있으며; 따라서, 예를 들어, 시스템은 완전히 또는 부분적으로 자동화될 수 있다. 자동화된 방법과 시스템은 고 처리량일 수 있다. 본 발명의 목적상, 고 처리량 스크리닝은 하루에 약 1,000개 이상의 형질전환체를 평가할 수 있는 부분적으로 또는 완전히 자동화된 방법, 특히 하루에 5,000개 이상의 형질전환체를 평가할 수 있는 방법을 의미할 수 있고, 가장 구체적으로는 하루에 10,000개 이상의 형질전환체를 평가할 수 있는 방법에 관한 것이다. 부분적으로 또는 완전히 자동화된 방법은 하나 이상의 액체 취급 단계의 사용을 수반할 수있다.
본 발명에 기술된 바와 같이, 본 발명에 제공된 방법 및 시스템은 본 발명에 기술된 바와 같이 생성되고 정제된 형질전환체가 관심 생성물의 생산을 위해 선별 또는 테스트되도록 선별 단계를 포함할 수 있다. 관심 생성물은 예를 들어 알코올, 제약, 대사 산물, 단백질, 효소, 아미노산 또는 산(예를 들어, 시트르산)과 같은 본 발명에 제공된 임의의 관심 생성물일 수 있다. 따라서, 본 발명에 제공된 방법 및 시스템은 본 발명의 방법에 따라 정제된 클론 콜로니 또는 배양액을 관심 생성물의 발현 및 분비를 허용하고 후속적으로 생성된 관심 생성물을 회수하는 조건하에서 배양하는 단계를 추가로 포함할 수 있다. 본 발명에 기재된 바와 같이, 관심 생성물은 외인성 및/또는 이종성 단백질 또는 외인성 및/또는 이종성 단백질의 발현의 결과로서 생성된 대사 산물일 수 있다.
일부 실시태양에서, 본 발명의 자동화 방법은 로봇 시스템을 포함한다. 본 발명에 개략된 시스템은 일반적으로 96- 또는 384-웰 미세 역가 플레이트의 사용에 관한 것이지만, 당업자라면 알 수 있듯이, 임의의 수의 상이한 플레이트 또는 구성이 사용될 수 있다. 또한, 본 발명에 개략된 단계의 일부 또는 전부는 자동화될 수 있고, 따라서, 예를 들어, 시스템은 완전히 또는 부분적으로 자동화될 수 있다.
일부 실시태양에서, 본 발명의 자동화 시스템은 하나 이상의 작업 모듈을 포함한다. 예를 들어, 일부 실시태양에서, 본 발명의 자동화 시스템은 DNA 합성 모듈, 벡터 클로닝 모듈, 균주 변형 모듈, 선별 모듈 및 서열화 모듈을 포함한다 (도 7 참조).
당업자가 알 수 있는 바와 같이, 자동화 시스템은 액체 핸드러; 하나 이상의 로봇 암; 마이크로플레이트의 위치 결정을 위한 플레이트 핸들러; 플레이트 씰러 (plate sealers), 플레이트 피어서(plate piercers), 비 교차 오염 플레이트상의 웰을 위한 뚜껑을 제거하고 대체하는 자동화 뚜껑 처리기; 일회용 팁에 의해 샘플 배급을 위한 일회용 팁 어셈블리; 샘플 분배를 위한 세척 가능한 팁 어셈블리; 96 웰 로딩 블록; 통합 열 순환기; 냉각된 시약 랙; 미세적정 플레이트 피펫 위치(선택적으로 냉각됨); 플레이트와 팁을 위한 스태킹 타워; 마그네틱 비드 가공 스테이션; 여과 시스템; 플레이트 교반기; 바코드 판독기 및 애플리케이터; 및 컴퓨터 시스템을 포함하나 이에 제한되지 않는 매우 다양한 구성요소를 포함할 수 있다. 도 8은 본 발명의 통합된 사상균류 균주 개량 프로그램의 개관을 나타낸다.
일부 실시태양에서, 본 발명의 로봇 시스템은 유전자 표적화 및 재조합 분야의 공정에서의 모든 단계를 수행하기 위한 고 처리량 피펫팅을 가능하게 하는 자동화된 액체 및 입자 취급을 포함한다. 이것은 흡인, 분배, 혼합, 희석, 세척, 정확한 체적 이동과 같은 액체 및 입자 조작; 피펫 팁의 회수 및 폐기; 단일 샘플 흡인으로 다중 전달을 위한 동일한 부피의 반복적 피펫팅을 포함한다. 이런 조작은 교차 오염이 없는 액체, 입자, 세포 및 유기체 전달이다. 이 장비는 필터, 막 및/또는 도터 플레이트에 대한 마이크로 플레이트 샘플의 자동화 반복, 고밀도 전달, 전체 플레이트 연속 희석 및 고용량 작업을 수행한다.
자동 시스템은 당업계에 공지된 임의의 공지된 자동 고 처리량 시스템일 수 있다. 예를 들어, 자동화 시스템은 자동화된 미생물 취급 도구일 수 있으며 일본 특허 출원 공개 번호 11-304666에 기재되어있다. 이 장치는 개별 세포를 함유하는 미세 방울의 전달이 가능하며, 본 발명의 균류 균주는 그 형태로 인해 이 장치를 이용한 개별 클론의 미세 조작이 가능할 것으로 예상된다. 본 발명의 방법 및 시스템에 사용하기 위한 자동화 시스템의 추가의 예는 Beydon et al., J. Biomol. Screening 5:13 21 (2000)에 기술된 자동화 미생물 고 처리량 스크리닝 시스템이다. 본 발명에서 사용하기 위한 자동화 시스템은 맞춤형 자동화 액체 취급 시스템일 수 있다. 일부 실시태양에서, 본 발명의 맞춤형 자동화 액체 처리 시스템은 TECAN 머신(예를 들어, 맞춤형 TECAN Freedom Evo)이다.
일부 실시태양에서, 본 발명의 자동화 시스템은 다중 웰 플레이트, 딥 웰 플레이트, 정사각형 플레이트, 시약 트로프, 테스트 튜브, 미니 튜브, 마이크로퓨즈 튜브, 냉동 튜브, 필터, 마이크로 어레이 칩, 광섬유, 비드, 아가로스 및 아크릴 아마이드 겔을 위한 플랫폼과 양립가능하며 다른 고상 매트릭스 또는 플랫폼은 업그레이드 가능한 모듈식 데크에 수용된다. 일부 실시태양에서, 본 발명의 자동화 시스템은 공급원 및 출력 샘플, 시약, 샘플 및 시약 희석액, 분석 플레이트, 샘플 및 시약 저장조, 피펫 팁 및 활성 팁 세척 스테이션을 배치하기 위한 다중 위치 작업 표면을 위한 적어도 하나의 모듈 데크를 포함한다.
일부 실시태양에서, 본 발명의 자동화 시스템은 고 처리량 전기 천공 시스템을 포함한다. 일부 실시태양에서, 고효율 전기 천공 시스템은 96 또는 384-웰 플레이트에서 세포를 형질전환시킬 수 있다. 일부 실시태양에서, 고효율 전기 천공 시스템은 VWR® 고 처리량 전기 천공 시스템, BTX™, Bio-Rad® Gene Pulser MXcell™ 또는 다른 다중-웰 전기 천공 시스템을 포함한다.
일부 실시태양에서, 통합된 열 순환기 및/또는 열 조절기는 0℃ 내지 100℃에서 샘플을 배양하는 정확한 온도 제어를 제공하도록 제어된 블록 또는 플랫폼과 같은 열 교환기의 온도를 안정화하는데 사용된다.
일부 실시태양에서, 본 발명의 자동화 시스템은 액체, 입자, 세포 또는 다중 세포 유기체를 로봇 공학적으로 조작할 수 있는 단일 또는 다중 자기 프로브, 친 화성 프로브, 리플리케이터 또는 피펫터를 갖는 교환 가능한 머신-헤드(단일 또는 다중 채널)과 양립가능하다. 다중 웰 또는 다중 튜브 자기 분리기 및 여과 스테이션은 단일 또는 다중 샘플 형식으로 액체, 입자, 세포 및 유기체를 조작한다.
일부 실시태양에서, 본 발명의 자동화 시스템은 카메라 비전 및/또는 분광계 시스템과 양립가능하다. 따라서, 일부 실시태양에서, 본 발명의 자동화 시스템은 진행중인 세포 배양물에서 색 및 흡수 변화를 검출 및 기록할 수 있다.
일부 실시태양에서, 본 발명의 자동화 시스템은 시스템이 다수의 애플리케이션을 수행할 수 있게 하는 다중 하드웨어 애드온(add-on)으로 융통성 있고 적응할 수 있도록 디자인된다. 소프트웨어 프로그램 모듈은 방법의 생성, 수정 및 실행을 허용한다. 시스템의 진단 모듈은 설정, 장비 정렬 및 모터 작동을 허용한다. 맞춤형 도구, 랩웨어 및 액체 및 입자 전달 패턴은 다양한 응용 프로그램이 프로그램되고 실행되게 한다. 데이터베이스는 방법 및 매개변수 저장을 허용한다. 로봇 및 컴퓨터 인터페이스는 장비 간의 통신을 허용한다.
따라서, 일부 실시태양에서, 본 발명은 도 11 및 12에 도시된 바와 같이 고 처리량 균주 공학 플랫폼을 교시한다.
당업자는 본 발명의 HTP 공학 방법을 수행할 수 있는 다양한 로봇 플랫폼을 인식할 것이다. 아래의 표 3은 도 11 및 12에서 기술된 바와 같이 본 발명의 HTP 공학 단계의 각 단계를 수행할 수 있는 과학적 장비의 포괄적 목록을 제공한다.
[표 3]
본 발명의 HTP 공학 방법과 양립가능한 과학 장비의 포괄적 목록.
컴퓨터 시스템 하드웨어
도 17은 본 발명의 실시태양에 따라 비 일시적 컴퓨터 판독 가능 매체(예를 들어, 메모리)에 저장된 프로그램 코드를 실행하는데 사용될 수 있는 컴퓨터 시스템(800)의 한 예를 도시한다. 컴퓨터 시스템은 애플리케이션에 따라 인간 사용자 및/또는 다른 컴퓨터 시스템과 인터페이스하기 위해 사용될 수 있는 입력/출력 서브 시스템(802)을 포함한다. I/O 서브 시스템(802)은 예를 들어, 입력을 위한 키보드, 마우스, 그래픽 사용자 인터페이스, 터치 스크린, 또는 다른 인터페이스, 및 예를 들어 애플리케이션 프로그램 인터페이스(APIs)를 포함하는 출력을 위한 LED 또는 다른 평면 디스플레이를 포함할 수 있다. LIMS 시스템의 구성요소와 같은 본 발명의 실시태양의 다른 요소는 컴퓨터 시스템(800)과 같은 컴퓨터 시스템으로 구현될 수 있다.
프로그램 코드는 2차 메모리(810) 또는 메인 메모리(808) 또는 둘 다에서 의 영구 저장장치와 같은 비 일시적인 매체에 저장될 수 있다. 메인 메모리 808)는 랜덤 액세스 메모리(RAM)와 같은 휘발성 메모리 또는 리드 온리 메모리(ROM)와 같은 비 휘발성 메모리뿐만 아니라 명령들 및 데이터에 대한보다 빠른 접근를 위한 상이한 수준의 캐시 메모리를 포함할 수 있다. 2차 메모리는 솔리드 스테이트 드라이브, 하드 디스크 드라이브 또는 광 디스크와 같은 영구 저장장치를 포함할 수 있다. 하나 이상의 프로세서(804)는 하나 이상의 비 일시적인 매체로부터 프로그램 코드를 판독하고 컴퓨터 시스템이 본 실시태양에 의해 수행된 방법을 완성할 수 있도록 코드를 실행한다. 당업자는 프로세서(들)가 소스 코드를 섭취하고 소스 코드를 프로세서(들)(804)의 하드웨어 게이트 레벨에서 이해할 수 있는 머신 코드로 해석 또는 컴파일할 수 있다는 것을 이해할 것이다. 프로세서(들)(804)은 컴퓨팅 집약적인 작업을 처리하기 위한 그래픽 처리 장치(GPU)를 포함할 수 있다. 특히, 기계 학습에서, 하나 이상의 CPU(804)는 하나 이상의 GPU(804)로 대량의 데이터 처리를 오프로드할 수 있다.
프로세서(들)(804)는 네트워크 인터페이스 카드, WiFi 트랜시버 등과 같은 하나 이상의 통신 인터페이스(807)를 통해 외부 네트워크와 통신할 수 있다. 버스 (805)는 I/O 서브시스템(802), 프로세서(들)(804), 주변 장치(806), 통신 인터페이스(807), 메모리(808) 및 영구 저장장치(810)와 통신가능하게 연결된다. 본 발명의 실시태양은 이런 대표적 아키텍처에 제한되지 않는다. 대안적 실시태양은 상이한 배열 및 유형의 구성요소, 예를 들어 입출력 구성요소 및 메모리 서브시스템을 위한 개별 버스를 사용할 수 있다.
당업자는 본 발명의 실시태양의 요소의 일부 또는 전부 및 이들의 수반되는 작업이 컴퓨터 시스템(800)의 하나 이상의 프로세서 및 하나 이상의 메모리를 포함하는 하나 이상의 컴퓨터 시스템에 의해 전체적으로 또는 부분적으로 구현될 수 있다는 것을 이해할 것이다. 특히, LIMS 시스템(200)의 요소 및 본 발명에 기술된 임의의 로봇 및 다른 자동화 시스템 또는 장치는 컴퓨터로 구현될 수 있다. 일부 요소 및 기능은 국소적으로 구현될 수 있고, 다른 것들은 예를 들어, 클라이언트- 서버 방식과 같은, 상이한 서버를 통해 네트워크 도처에 분산된 방식으로 구현될 수 있다. 특히 도 15와 같이, 서버 측 작업은 서비스로서 소프트웨어(SaaS) 방식으로 여러 클라이언트에 이용될 수 있다.
본 내용에서 구성요소라는 용어는 소프트웨어, 하드웨어 또는 펌웨어(또는 이들의 임의의 조합) 구성요소를 포괄적으로 의미한다. 구성요소는 일반적으로 지정된 입력(들)을 사용하여 유용한 데이터 또는 다른 출력을 생성할 수 있는 기능적 구성요소이다. 구성요소는 자급식일 수 있거나 아닐 수 있다. 애플리케이션 프로그램("애플리케이션"이라고도 함)은 하나 이상의 구성요소를 포함할 수 있으며 구성요소는 하나 이상의 애플리케이션 프로그램을 포함할 수 있다.
일부 실시태양은 다른 모듈 또는 애플리케이션 구성요소와 함께 구성요소의 일부, 전부를 포함하거나 하나도 포함하지 않는다. 여전히, 다양한 실시태양은 이들 구성요소의 둘 이상을 단일 모듈에 통합하고 및/또는 이들 구성요소의 하나 이상의 기능의 일부를 다른 구성요소와 연관시킬 수 있다.
용어 "메모리"는 정보를 저장하기 위해 사용되는 임의의 장치 또는 메커니즘일 수 있다. 본 발명의 일부 실시태양에 따르면, 메모리는 휘발성 메모리, 비 휘발성 메모리 및 동적 메모리의 임의의 유형을 포함하나 이에 제한되는 것은 아니다. 예를 들어, 메모리는 랜덤 액세스 메모리, 메모리 저장 장치, 광학 메모리 장치, 자기 매체, 플로피 디스크, 자기 테이프, 하드 드라이브, SIMMs, SDRAM, DIMMs, RDRAM, DDR RAM, SODIMMS, 지울 수 있는 프로그램가능한 리드 온리 메모리(EPROMs), 전기적으로 지울 수 있는 프로그램가능한 리드 온리 메모리(EEPROMs), 컴팩트 디스크, DVDs 및/또는 이와 동일한 종류일 수 있다. 일부 실시태양에 따르면, 메모리는 하나 이상의 디스크 드라이브, 플래시 드라이브, 데이터베이스, 로컬 캐시 메모리, 프로세서 캐시 메모리, 관계형 데이터베이스, 플랫 데이터베이스, 서버, 클라우드 기반 플랫폼 및/또는 이와 동일한 종류를 포함할 수 있다. 또한, 당업자는 정보를 저장하기 위한 많은 부가적인 장치 및 기술이 메모리로서 사용될 수 있다는 것을 이해할 것이다.
메모리는 프로세서 상의 하나 이상의 애플리케이션 또는 모듈을 실행하기 위한 명령을 저장하는데 사용될 수 있다. 예를 들어, 일부 실시태양에서 메모리는 본 발명에 개시된 하나 이상의 모듈 및/또는 애플리케이션의 기능을 실행하는데 필요한 명령의 전부 또는 일부를 수용하기 위해 사용될 수 있다.
유전자 디자인 예측을 기반으로 하는 HTP 미생물 균주 공학: 예시적 작업 흐름
일부 실시태양에서, 본 발명은 본 발명의 전산 분석 시스템의 권고에 기초한 새로운 숙주 유기체의 지시된 공학을 교시한다.
일부 실시태양에서, 본 발명은 모든 유전자 디자인 및 클로닝 방법과 양립할 수 있다. 즉, 일부 실시태양에서, 본 발명은 폴리머라제 연쇄 반응, 제한 효소 절단, 결찰, 상동성 재조합, RT PCR 및 당업계에 일반적으로 공지된 다른 기술과 같은 전통적인 클로닝 기술의 사용을 교시하고 예를 들어 참조로 본 발명에 포함된 Sambrook et al. (2001) Molecular Cloning: A Laboratory Manual(3rd ed., Cold Spring Harbor Laboratory Press, Plainview, New York에 기술된다.
일부 실시태양에서, 복제된 서열은 본 발명에서 교시된 임의의 HTP 유전자 디자인 라이브러리, 예를 들면: 프로모터 스왑 라이브러리로부터의 프로모터, SNP 스왑 라이브러리로부터의 SNP, 개시/중지 코돈 변화 라이브러리로부터의 개시 또는 중지 코돈, STOP 스왑 라이브러리의 터미네이터 또는 서열 최적화 라이브러리로부터의 서열 최적화의 임의의 것으로부터 가능성을 포함할 수 있다.
또한, 특정 구조체에 포함되어야 하는 정확한 서열 조합은 상위성 맵핑 기능에 의해 통지될 수 있다.
다른 실시태양에서, 복제된 서열은 합리적인 디자인(가설-주도적) 및/또는 과학 출판물과 같은 다른 소스에 기초한 서열에 기초한 서열을 또한 포함할 수 있다.
일부 실시태양에서, 본 발명은 i) 맞춤형 SNP 특이적 DNA를 생성하는 단계, ii) SNP 특이적 구조체를 조립하는 단계, (iii) SNP 특이적 DNA로 표적 숙주 세포를 형질전환시키는 단계, 및 iv) 모든 선택 마커를 루프아웃하는 단계를 포함하는 지시된 공학의 방법을 교시한다(도 2 참조).
도 6a는 DNA의 획득 및 조립, 임의의 필수적 벡터의 조립, 숙주 세포의 형질전환 및 선택 마커의 제거를 포함하는 본 발명의 균주 공학 방법의 일반적인 작업 흐름을 도시한다.
특정 DNA 올리고 뉴클레오타이드 제조
일부 실시태양에서, 본 발명은 숙주 세포 유기체의 DNA 절편을 삽입 및/또는 교체 및/또는 변경 및/또는 삭제하는 것을 교시한다. 일부 양태에서, 본 발명에 교시된 방법은 숙주 유기체의 게놈 속에 포함될 관심 올리고뉴클레오타이드(즉, 표적 DNA 절편)를 제조하는 것을 포함한다. 일부 실시태양에서, 본 발명의 표적 DNA 절편은 공지된 주형으로부터의 복제 또는 절단, 돌연변이 또는 DNA 합성을 포함하여 당업계에 공지된 임의의 방법을 통해 얻을 수있다. 일부 실시태양에서, 본 발명은 표적 DNA 서열(예를 들어, GeneArt™, GeneMaker™, GenScript™, Anagen™, Blue Heron™, Entelechon™, GeNOsys, Inc., 또는 Qiagen™)을 생산하기 위한 상업적으로 구입가능한 유전자 합성 생성물과 양립가능하다.
일부 실시태양에서, 표적 DNA 절편은 숙주 유기체의 선택된 DNA 영역에 SNP를 포함시키도록(예를 들어, 유익한 SNP를 첨가하여) 디자인된다. 다른 실시태양에서, DNA 절편은 숙주 유기체의 DNA로부터 SNP를 제거하도록(예를 들어, 해로운 또는 중성 SNP를 제거하도록) 디자인된다.
일부 실시태양에서, 본 발명의 방법에서 사용된 올리고뉴클레오타이드는 당 업계에 공지된 효소적 또는 화학적 합성 방법 중 임의의 방법을 사용하여 합성될 수 있다. 올리고뉴클레오타이드는 제어된 공극 유리(CPG), 폴리스티렌 비드 또는 CPG를 함유할 수 있는 열가소성 폴리머로 구성된 막과 같은 고체 지지체 상에서 합성될 수 있다. 올리고 뉴클레오타이드는 미세유체역학(Tian et al., Mol. BioSyst., 5, 714-722 (2009)) 또는 둘 다의 조합을 제공하는 공지된 기술(Jacobsen et al., 미국 특허 출원 제 2011/0172127호 참조)을 사용하여 병렬 마이크로스케일로 어레이 상에서 합성될 수 있다.
어레이 상에 또는 미세유체역학을 통한 합성은 보다 낮은 시약 사용을 통해 비용을 감소시킴으로써 통상적인 고체 지지체 합성에 비해 이점을 제공한다. 유전자 합성에 필요한 규모는 작아서, 어레이 또는 미세유체역학을 통해 합성된 올리고 뉴클레오타이드 생성물의 규모가 허용가능하다. 그러나, 합성된 올리고뉴클레오타이드는 고체 지지체 합성을 사용할 때보다 품질이 떨어진다(이하의 Tian 참조; 또한 Staehler et al., U.S. Pat. App. No. 2010/0216648 참조).
퍼옥시 음이온 탈보호를 사용하여 1980년대에 처음으로 기술되었기 때문에 종래의 4단계 포스포아미다이트 화학에서 많은 발전이 이루어져왔다(예를 들어, Sierzchala, et al. J. Am. Chem. Soc., 125, 13427-13441 (2003) using peroxy anion deprotection; Hayakawa et al., U.S. Pat. No. 6,040,439 for alternative protecting groups; Azhayev et al, Tetrahedron 57, 4977-4986 (2001) for universal supports; Kozlov et al., Nucleosides, Nucleotides, and Nucleic Acids, 24 (5-7), 1037-1041 (2005) for improved synthesis of longer oligonucleotides through the use of large-pore CPG; and Damha et al., NAR, 18, 3813-3821 (1990) for improved derivatization 참조)
합성 유형에 관계없이, 생성된 올리고뉴클레오타이드는 보다 긴 올리고뉴클레오타이드를 위한 더 작은 빌딩 블록을 형성할 수 있다. 일부 실시태양에서, 더 작은 올리고뉴클레오타이드는 폴리머라제 연쇄 조립(PCA), 리가아제 연쇄 반응 (LCR) 및 열역학적으로 균형 잡힌 인사이드-아웃 합성(TBIO)과 같은 당업계에 공지 된 프로토콜을 사용하여 함께 결합될 수 있다(Czar et al. Trends in Biotechnology, 27, 63-71 (2009) 참조). PCA에서, 원하는 긴 제품의 전체 길이에 걸쳐있는 올리고뉴클레오타이드는 어닐링되고 여러 사이클(일반적으로 약 55 사이클)에서 연장되어 전장 생성물을 최종적으로 얻는다. LCR은 리가아제 효소를 사용하여 제 3 올리고뉴클레오타이드에 모두 어닐링되는 두 올리고뉴클레오타이드에 연결시킨다. TBIO 합성은 목적 생성물의 중심에서 시작하여 유전자의 5' 말단에서 포워드 가닥과 상동성이고 유전자의 3' 말단에서 리버스 가닥과 상동성인 중첩 올리고뉴클레오타이드를 사용함으로써 점진적으로 양방향으로 연장된다.
더 큰 이중 가닥 DNA 단편을 합성하는 다른 방법은 상위-가닥 PCR(TSP)을 통해 더 작은 올리고뉴클레오타이드를 조합하는 것이다. 이 방법에서, 복수의 올리고뉴클레오타이드는 원하는 생성물의 전체 길이에 걸쳐 있고 인접한 올리고뉴클레오타이드(들)에 중첩 영역을 포함한다. 증폭은 범용 포워드 및 리버스 프라이머로 수행될 수 있으며, 증폭의 다중 사이클을 통해 전장 이중 가닥 DNA 생성물이 형성된다. 이런 생성물은 선택적인 오류 보정 및 원하는 이중 가닥 DNA 단편 최종 생성물을 생성하는 추가 증폭을 진행될 수 있다.
TSP의 한 방법에서, 전장의 원하는 생성물을 형성하도록 결합되어질 더 작은 올리고뉴클레오타이드의 세트는 40-200 염기 길이이고 적어도 약 15-20 염기만큼 서로 중첩된다. 실제적인 목적을 위해, 중첩 영역은 올리고뉴클레오타이드의 특정 어닐링을 보장할만큼 충분히 길어야 하고 사용된 반응 온도에서 어닐링하기에 충분한 높은 용융 온도(Tm)를 가져야 한다. 중첩은 소정의 올리고뉴클레오타이드가 인접한 올리고뉴클레오타이드에 의해 완전히 중첩되는 지점까지 연장될 수 있다. 중첩의 양은 최종 생성물의 품질에 영향을 미치지 않는 것으로 보입니다. 어셈블리의 첫 번째 및 마지막 올리고뉴클레오타이드 빌딩 블록은 포워드 및 리버스 증폭 프라이머에 대한 결합 위치를 포함해야 한다. 하나의 실시태양에서, 첫 번째 및 마지막 올리고뉴클레오타이드의 최종 말단 서열은 보편적 프라이머의 사용을 허용하도록 상보성의 동일한 서열을 포함한다.
DNA 단편 조립/맞춤형 플라스미드 복제
일부 실시태양에서, 본 발명은 숙주 유기체의 게놈에 원하는 표적 DNA 부분(예를 들어, 특정 SNP를 포함)을 삽입할 수 있는 DNA 단편을 제조하는 방법을 교시한다. 도 1은 다양성 풀의 변화를 증가시키기 위한 본 발명의 DNA 재조합 방법을 도시한다. 관련 종으로부터의 게놈 영역과 같은 DNA 단편은 물리적 또는 효소적/화학적 수단을 통해 절단될 수 있다. 절단된 DNA 영역은 용융되어 다시 어닐링되어 중첩되는 유전자 영역이 중합 효소 연장 반응을 일으킨다. 후속 용융/연장 반응은 생성물이 하나 이상의 출발 서열의 요소 및 프로모터를 포함하는 키메라 DNA로 재 조립될 때까지 수행된다. SNP 스왑에 대한 전체 디자인, 생성, 조립, QC, 형질전환, 루프 아웃 및 QC 프로세스에 대한 일반적인 방식이 도 2에 도시되어있다. 이 방식은 본 발명에 제공된 다른 HTP 툴(예를 들어, PROswp, STOPswp)에 적용될 수 있음에 유의해야 한다. 일부 실시태양에서, 본 발명은 표적 DNA, 상동성 암 및 적어도 하나의 선택 마커를 포함하는 선형 DNA 단편을 생성하는 방법을 교시한다(도 45 및 46 참조).
일부 실시태양에서, 본 발명은 숙주 유기체(A. 니거와 같은 사상균류)로의 DNA 단편의 형질전환에 적합한 임의의 방법과 양립 가능하다. 일부 실시태양에서, 본 발명은 원하는 표적 DNA 섹션이 클로닝되고 이로부터 증폭될 수있는 플라스미드 또는 어셈블리 벡터의 사용을 교시한다. 사용될 때, 어셈블리 벡터는 숙주 세포 (예를 들어, 효모 및/또는 대장균)에서의 증식에 필요할 수 있는 임의의 복제 기점을 추가로 포함할 수 있다. 특정 예에서, 표적 DNA는 상업용 벡터(예를 들어, DNA2.0 맞춤형 또는 GATEWAY® 벡터)와 같은 임의의 저장소 또는 카탈로그 생성물로부터 얻을 수 있는 벡터, 구조체 또는 플라스미드에 삽입될 수 있다. 사상균류 숙주 세포와 같은 숙주 세포를 궁극적으로 형질전환시키기 위한 선형 DNA 단편을 생성하기 위한 플라스미드의 사용은 숙주 게놈에 통합될 원하는 유전자를 포함하는 표적 DNA 구조체의 일부를 합성하고, 어셈블리 벡터와 함께 표적 DNA 구조체의 일부로 효모 세포를 형질전환시키고, 상기 형질전환된 효모 세포로부터 표적 DNA 구조체를 함유하는 조립된 플라스미드를 분리하고, 대장균에서 분리된 플라스미드를 전파시키고, 사상균류 숙주 세포의 형질전환 전에 숙주 게놈으로 통합될 원하는 유전자를 포함하는 DNA 단편을 생성하도록 대장균으로부터 표적 DNA 구조체를 PCR 증폭시키는 것을 수반할 수 있다.
대안의 실시태양에서, 숙주 게놈(예를 들어, 사상균류 세포)에 통합될 원하는 유전자를 포함하는 선형 DNA 단편(들)의 조립 또는 생성은 융합 PCR을 사용하는 것을 수반할 수 있다. 융합 PCR은, 예를 들어, 전문이 참조로 본 발명에 포함되는 Yu et al, Fungal Genetics and Biology, vol 41, pages 973-981 (2004)에 기술된 방법을 포함하는 당업계에 공지된 임의의 융합 PCR 방법을 사용하여 수행될 수 있다. 도 45는 이들 사이에서 분할된 마커 유전자(즉, pyrG)를 포함하는 2개의 선형 DNA 단편을 생성하기 위해 융합 PCR을 사용하는 방법을 도시한다. 개념적으로, 융합 PCR은 본 발명에 제공된 표적 유전자 돌연변이 및/또는 선택 가능한 마커 유전자를 포함하는 임의의 구조체를 생성하는 데 사용될 수 있다.
본 발명에 제공된 방법에 사용하기 위한 선형 DNA 단편은 본 발명에 기재된 바와 같은 선택 및/또는 카운터 선택을 위한 마커를 포함할 수 있다. 마커는 당업계에 공지되고/되거나 본 발명에 제공된 임의의 마커일 수 있다. 선형 DNA 단편은 본 발명에 제공된 임의의 조절 서열(들)을 추가로 포함할 수 있다. 조절 서열은, 예를 들어, 숙주 세포(예를 들어, 사상균류 세포)의 유전자 기계에 의해 사용되는 프로모터, 개시, 정지, 신호, 분비 및/또는 종결 서열과 같은 당업계에 공지되고/되거나 본 발명에 제공된 임의의 조절 서열일 수 있다.
일부 실시태양에서, 본 발명의 조립/복제 방법은 다음 조립 전략: i) II형 통상적인 복제, ii) II형 S-매개 또는 "골든 게이트" 복제(예를 들어, Engler, C., R. Kandzia, and S. Marillonnet. 2008 "A one pot, one step, precision cloning method with high-throughput capability". PLos One 3:e3647; Kotera, I., and T. Nagai. 2008 "A high-throughput and single-tube recombination of crude PCR products using a DNA polymerase inhibitor and type IIS restriction enzyme." J Biotechnol 137:1-7.; Weber, E., R. Gruetzner, S. Werner, C. Engler, and S. Marillonnet. 2011 Assembly of Designer TAL Effectors by Golden Gate Cloning. PloS One 6:e19722 참조), iii) GATEWAY® 재조합, iv) TOPO® 복제, 엑소뉴클레아제 매개 어셈블리(Aslanidis and de Jong 1990. "Ligation-independent cloning of PCR products (LIC-PCR)." Nucleic Acids Research, Vol. 18, No. 20 6069), v) 상동성 재조합, vi) 비 상동성 말단 결합, vii) 깁슨 어셈블리(Gibson et al., 2009 "Enzymatic assembly of DNA molecules up to several hundred kilobases" Nature Methods 6, 343-345) 또는 이의 조합의 적어도 하나를 사용할 수 있다. 모듈형 IIS 기반 조립 전략은 PCT 공개공보 WO 2011/154147에 개시되며, 그 내용은 본 발명에 참고로 포함된다.
일부 실시태양에서, 본 발명은 하나 이상의 선별 마커를 갖는 벡터의 클로닝을 교시한다. 다양한 선택 마커 유전자는 선택적 압력하에서 원핵생물 세포(예를 들어, 암피실린, 카나마이신, 테트라사이클린, 클로람페니콜, 제오신, 스펙티노마이신/스트렙토마이신) 또는 진핵생물 세포(예컨대, 제네티신, 네오마이신, 하이그로마이신, 푸로마이신, 블라스티시딘, 제오신)에서 선택을 위한 항생제 저항을 암호화하는 것이 당업계에 주지되어 있다. 다른 마커 시스템은 성공적으로 형질유도된 숙주 세포에서 발현된 녹색 또는 적색 형광 단백질과 같은 X-gal 또는 형광 리포터(fluorescent reporter)의 존재하에서 양성 클론을 선택하기 위해 박테리아에서 사용된 주지된 청색/백색 선별 시스템과 같은 원하거나 원하지 않는 세포의 선별 및 확인을 허용한다. 대다수가 원핵생물 시스템에서만 기능하는 선택 마커의 또 다른 부류는 생산자 세포를 죽이는 독성 유전자 생성물을 발현하는 "사멸 유전자"라고도하는 역 선택가능한 마커 유전자에 관한 것이다. 이러한 유전자의 예는 sacB, rpsL (strA), tetAR, pheS, thyA, gata-1 또는 ccdB를 포함하며, 그 기능은 (Reyrat et al. 1998 "Counterselectable Markers: Untapped Tools for Bacterial Genetics and Pathogenesis." Infect Immun. 66(9): 4011-4017)에 설명된다.
도 18은 본 발명의 한 실시태양에 따른 DNA 어셈블리와 관련된 작업 흐름을 도시한다. 이 과정은 4 단계로 나뉘어진다: 부분 생성, 플라스미드/구조체 어셈블리, 플라스미드/구조체 QC 및 형질전환을 위한 플라스미드/구조체 준비. 부품 생성 동안, 실험실 정보 관리 시스템(LIMS)에 의해 고안된 올리고는 올리고 서열 판매자로부터 주문받고 PCR을 통해 숙주 유기체로부터 표적 서열을 증폭하는데 사용된다. 이러한 PCR 부분은 세척하여 오염물을 제거하고 단편 분석, 관찰된 단편 크기 대 이론적 단편 크기의 인 실리코(in silico) 품질 관리 비교 및 DNA 정량화에 의해 성공에 대해 평가된다. 도 18에 도시된 바와 같이, 한 실시태양에서, 부분은 어셈블리 벡터와 함께 효모로 형질전환되고 동종 재조합을 통해 플라스미드로 조립된다. 조립된 플라스미드는 효모로부터 분리되고, 후속 조립 품질 제어 및 증폭을 위해 대장균으로 형질전환된다. 플라스미드 조립 품질 관리 동안, 각 플라스미드의 여러 복제물을 분리하고, 롤링 서클 증폭(Rolling Circle Amplification(RCA))을 사용하여 증폭되고, 효소 분해 및 단편 분석에 의해 올바른 조립에 대해 평가된다. QC 과정 동안 확인된 올바르게 조립된 플라스미드는 영구적인 원료를 생성하기 위해 히트 픽(hit picked)되고 게놈 통합을 촉진하는 데 필요한 임의의 플랭킹 서열을 포함하는 특정 유전자 구조체는 플라스미드로부터 PCR 증폭되어 표적 숙주 유기체(예를 들어, 사상균류 숙주 세포)로의 형질전환 전에 정량화되고 단편 분석을 통해 QC된 선형 DNA 단편을 생성한다. 또한, 도 18에 도시된 바와 같이, 별도의 실시태양에서, 부분은 융합 DNA(예를 들어, 도 45 및 46 참조)를 수행하여 선형 DNA 단편을 생성하는데, 이는 표적 숙주 유기체(예를 들어, 사상균 숙주 세포)로의 형질 전환 전에 단편 및 서열 분석을 통해 QC된다.
원형질체화
방법
한 실시태양에서, 본 발명에 제공된 방법 및 시스템은 본 발명에 제공된 바와 같이 다핵체 유기체(예를 들어, 사상균류 세포)로부터의 원형질체의 생성을 이용한다. 원형질체의 제조에 적합한 절차는 예를 들어 EP 238,023 및 Yelton et al.(1984, Proc. Natl. Acad. Sci. USA 81:1470-1474)에 기술된 것을 포함하는 당업계에 공지된 임의의 방법일 수 있다. 한 실시태양에서, 원형질체는 예비 배양된 사상균류 세포의 배양물을 하나 이상의 용균 효소 또는 이의 혼합물로 처리함으로써 생성된다. 용균 효소는 베타-글루카나아제 및/또는 폴리갈락투로나제일 수 있다. 한 실시태양에서, 원형질체 생성용 효소 혼합물은 비노테이스트(VinoTaste) 농축물이다. 다핵체 유기체(예를 들어, 사상균류 세포)의 배양을 예비 배양하고, 이어서 본 발명에서 제공된 방법 및 조성물에 사용하기 위해 그로부터 원형질체를 생성 및 이용하는 데 사용되는 많은 파라미터가 변할 수 있다. 예를 들어, 접종물 크기, 접종물 방법, 전 배양 배지, 전 배양 시간, 배양 전 온도, 혼합 조건, 세척 완충액 조성물, 희석 비, 용균 효소 처리 동안 완충제 조성물 사용된 용균 효소의 형태 및/또는 농도, 용균 효소에 의한 배양 시간, 원형질체 세척 절차 및/또는 완충액, 실제 형질전환 동안 원형질체 및/또는 폴리뉴클레오타이드 및/또는 형질전환 시약의 농도, 형질전환 동안 물리적 매개변수, 얻어진 형질전환체까지의 형질전환 이후 절차의 변형이 존재할 수 있다. 일부 경우에, 이러한 변이는 원형질체의 수 및 형질전환 효율을 최적화하기 위해 이용될 수 있다. 하나의 실시태양에서, 다핵체 유기체는 본 발명에 제공된 사상균류 세포(예를 들어, A. 니거)이다. 이 실시태양에 더하여, 예비 배양 배지는 YPD 또는 완전 배지일 수 있다. 예비 배양 배지의 부피는 적어도, 최대 또는 약 50ml, 100ml, 150ml, 200ml, 250ml, 300ml, 350ml, 400ml, 450ml, 500ml, 550ml, 600ml, 650ml, 700ml, 750ml, 800ml, 850ml, 900ml, 950ml 또는 1000ml일 수있다. 예비 배양 배지의 부피는 약 50ml 내지 약 100ml, 약 100ml 내지 약 150ml, 약 150ml 내지 약 200ml, 약 200ml 내지 약 250ml, 약 250ml 내지 약 300ml, 약 300ml 내지 약 350ml, 약 350ml 내지 약 400ml, 약 400ml 내지 약 450ml, 약 450ml 내지 약 500ml, 약 500ml 내지 약 550ml, 약 550ml 내지 약 600ml, 약 600 약 650ml 내지 약 650ml, 약 650ml 내지 약 700ml, 약 700ml 내지 약 750ml, 약 750ml 내지 약 800ml, 약 800ml 내지 약 850ml, 약 850ml 내지 약 900ml, 약 900ml 약 950ml 또는 약 950ml 내지 약 1000ml일 수 있다. 일부 경우에, 복수의 배양물이 배양되고 이어서 원형질체화된다. 복수의 배양물은 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, 20, 25, 50, 75, 100, 150, 200, 300, 400, 500 이상일 수 있다. 하나의 실시태양에서, 예비 배양 제제는 100ml의 풍부 배지(예를 들어, YPD 또는 완전 배지)에 106 포자/ml를 접종하고 예비 배양 제제를 30℃에서 14-18시간 사이에서 배양함으로써 제조된다. 다른 실시태양에서, 예비 배양 제제는 500ml의 풍부 배지(예를 들어, 효모 곰팡이 브로쓰, YPD 또는 완전 배지)에 적어도 106 포자/ml를 접종하고 예비 배양 제제를 30℃에서 14-18시간에서 배양함으로써 제조된다. 원형질체화 전에, 다핵체 유기체는 당업계에 공지된 임의의 방법, 예를 들어 원심 분리에 의해 분리될 수 있다. 한 실시태양에서, 다핵체 유기체는 사상균류(예를 들어, A. 니거)이다. 이 실시태양에 추가로, 효모 곰팡이 브로쓰(YMB)에 106 포자/ml의 사상균류 세포를 접종하고 30℃에서 16시간 동안 성장시켰다. 이 실시태양에 추가로, 예비 배양 제제에서 성장된 사상균류 세포는 원심 분리에 의해 분리될 수 있다. 본 발명에 제공된 방법 및 조성물에 사용하기 위해 본 발명에 제공된 예비 배양 제제는 약, 적어도 또는 최대 0.5g, 1g, 1.5g, 2g, 2.5g, 3g, 3.5g, 4g 또는 5g의 습윤 중량의 후속 원형질체화를 위한 일정량의 균사를 생성할 수 있다. 다핵체 유기체(예를 들어, 사상균류)의 예비 배양/재배는 도 28에 도시된 바와 같이 고 처리량 시스템(HTP)에서의 워크 플로우의 일부일 수 있다. HTP 시스템은 자동화 또는 반자동화될 수 있다. 도 28에 도시된 바와 같이, 유기체의 사전-배양은 106 포자/ml의 유기체(예를 들어, A. 니거)와 함께 소규모의 부피(예를 들어, 100ml)의 포자 배지(도 28의 PDA 배지)를 접종하고 30℃에서 14-16시간 동안 성장시키는 것을 수반할 수 있다. 도 28에 도시된 바와 같이, 예비 배양 동안, 워크 플로우는 예비 배양 유기체(예를 들어, A. 니거)로부터 원형질체를 생성하기 위한 효소 용액이 생성되는 단계를 포함할 수 있다. 효소 용액은 1.2M MgSO4를 포함하는 포스페이트 완충액 중의 Vinotaste pro(Novozymes) 효소 믹스로 구성될 수 있다. 사전 배양 후, 미라클로스를 통한 여과 후 균사를 수집할 수 있고 수집된 균사 10ul 내지 20ml와 함께 2.8L 플라스크에 약 500ml의 완전한 배지를 접종함으로써 대규모 배양액을 배양할 수 있다. 접종물 크기는 예비 배양 단계로부터 수득된 배양물의 OD에 기초하여 가변적일 수 있다. 대규모 배양은 200rpm에서 진탕하면서 80% 습도에서 30℃ 또는 18℃에서 6-18 시간 동안 성장될 수 있다. 배양 후, 배양 액(들)은 하나 이상의 세척에 의한 원심 분리에 의해 분리되고 재현탁될 수 있다. 한 실시태양에서, 배양액은 본 발명에 기재된 바와 같은 원형질체 완충액에 재현 탁되고 본 발명에 기재된 바와 같은 원형질체화된다. 원심 분리는 5500-6100 x g에서 10-15분 동안 4℃에서 500ml 원심 분리 튜브에서 수행될 수 있다. 하나 이상의 세척 각각은 10-50ml의 세척 완충액(예를 들어, 10% 글리세롤을 함유한 물)에서 수행될 수 있고, 5500-6100 x g에서 10-15분 동안 4℃에서 원심 분리될 수 있다.
상기 기재된 바와 같은 분리 후, 다핵체 유기체(예를 들어, A. 니거와 같은 사상균류 세포)는 원형질체 완충액에 재현탁되어, 원형질체 완충액이 원형질체 생성을 위해 본 발명에 제공된 바와 같은 하나 이상의 효소(예를 들어, VinoTaste pro 농축액(노보자임))를 포함할 수 있다. 한 실시태양에서, 원형질체 완충제는 고농도의 삼투압(예를 들어, MgSO4와 같은 삼투압의 1M 이상)을 갖는다. 높은 삼투압 농도(예를 들어, 1.2 M MgSO4)를 갖는 원형질체 완충액을 사용하는 실시태양에서, 효소 처리(예를 들어, VinoTaste pro 농축액(노보자임))를 위한 배양 시간은 약 30℃에서 약 14-16시간일 수 있다. 재현탁에 사용되는 원형질체 완충제의 부피는 50ml, 100ml, 150ml, 200ml, 250ml, 300ml, 350ml, 400ml, 450ml, 500ml, 550ml, 600ml, 650ml, 700ml, 750ml, 800ml, 850ml, 900ml, 950ml 또는 1000ml일 수 있다. 재현탁에 사용되는 원형질체 완충제의 부피는 약 50ml 내지 약 100ml, 약 100ml 내지 약 150ml, 약 150ml 내지 약 200ml, 약 200ml 내지 약 250ml, 약 250ml 내지 약일 수있다 300ml, 약 300ml 내지 약 350ml, 약 350ml 내지 약 400ml, 약 400ml 내지 약 450ml, 약 450ml 내지 약 500ml, 약 500ml 내지 약 550ml, 약 550ml 내지 약 600ml 약 600ml 내지 약 650ml, 약 650ml 내지 약 700ml, 약 700ml 내지 약 750ml, 약 750ml 내지 약 800ml, 약 800ml 내지 약 850ml, 약 850ml 내지 약 900ml, 약 900ml 내지 약 950ml 또는 약 950ml 내지 약 1000ml일 수 있다. 한 실시태양에서, 사상균류 세포는 예를 들어 도 28에 도시된 바와 같이 500ml의 풍부 배지(예를 들어, YPD 또는 완전 배지)에서 성장되고 균사(도 28에 도시된 바와 같이 약 1g의 습윤 질량일 수 있음)를 100ml의 세척 완충제(예를 들어, 1.2M MgSO4를 갖는 100mM 인산 나트륨 완충제, pH 5.5)로 헹구는 미라클로스를 통한 여과에 의해 분리하고; 1L 병에 원형질체 효소 혼합물(예를 들어, VinoTaste pro 농축액(노보자임))을 포함하는 약 500ml의 원형질체 완충제(예를 들어, 도 28에서 1.2M MgSO4 pH 5.5를 갖는 100mM 인산 나트륨 완충제)에 재현탁시켰다. 효소 검사에서 균사는 현미경 검사를 통해 원형질체 형성을 계속 모니터링하면서 140rpm에서 진탕하면서 30℃에서 14-16시간 동안 배양될 수 있다.
한 실시태양에서, NHEJ 경로의 하나 이상의 화학적 억제제는 제공된 바와 같이 원형질체 완충제에 첨가된다. 하나 이상의 화학적 억제제는 W7, 클로르프로마진, 바닐린, Nu7026, Nu7441, 미린, SCR7, AG14361 또는 이들의 임의의 조합으로부터 선택될 수 있다. 원형질체 완충액에 대한 하나 이상의 화학적 억제제의 첨가는 원형질체화 과정 동안 어느 시점에서나 일어날 수 있다. 한 실시태양에서, 하나 이상의 화학적 억제제에 의한 처리는 전체 원형질체화 절차를 위한 것이다. 별도의 실시태양에서, 하나 이상의 화학적 억제제에 의한 처리는 전체 원형질체화 절차보다 적다. 하나 이상의 화학적 억제제에 의한 처리는 약 1, 5, 10, 15, 20, 30, 45, 60, 90, 120, 150, 180, 210, 240, 270 또는 300분 동안 수행될 수 있다. 한 실시태양에서, 공동-다핵체 세포(예를 들어, 사상균류 세포)는 W-7로 처리된다. 다른 실시태양에서, 공동-다핵체 세포(예를 들어, 사상균류 세포)는 SCR-7로 처리된다.
효소 처리 이후, 원형질체는 삼투압 안정화 완충액에 재현탁될 수 있다. 이런 완충액의 조성물은 종, 응용분야 및 필요에 따라 달라질 수 있다. 그러나, 전형적으로, 이런 완충액은 0.5 내지 2M 사이의 수크로오스, 시트레이트, 만니톨 또는 소르비톨과 같은 유기 성분을 함유한다. 더욱 바람직하게는 0.75 내지 1.5 M; 가장 바람직하게는 1M이다. 그렇지 않으면 이들 완충액은 KCl, MgSO4, NaCl 또는 MgCl2와 같은 무기 삼투압 안정화 성분을 0.1 내지 1.5M의 농도로 함유한다. 바람직하게는 0.2 내지 0.8M; 보다 바람직하게는 0.3 내지 0.6M, 가장 바람직하게는 0.4M이다. 가장 바람직한 안정화 완충액은 STC(소르비톨, 0.8M, CaCl2, 25mM, 트리스, 25mM, pH 8.0) 또는 KCl- 시트레이트(KCl, 0.3-0.6M; 시트레이트, 0.2%(w/v))이다. 원형질체는 1 x 105 내지 1 x 1010 cells/ml 또는 ml당 1-3 x 107 원형질체 사이의 농도로 사용될 수 있다. 바람직하게는, 농도는 1 x 106 내지 1 x 109이고; 보다 바람직하게는 농도는 1 x 107 내지 5 x 108이고; 가장 바람직하게는 농도는 1 x 108 cells/ml이다. 형질감염의 효율을 높이기 위해 운반체 DNA(연어 정자 DNA 또는 비 암호화 벡터 DNA)가 형질전환 혼합물에 첨가될 수 있다. DNA는 0.01 내지 10㎍; 바람직하게는 0.1 내지 5㎍; 보다 더 바람직하게는 0.25 내지 2㎍; 가장 바람직하게는 0.5 내지 1㎍의 농도로 사용된다.
한 실시태양에서, 생성 및 후속 분리 및 세척 후에, 원형질체는 하나 이상의 동결방지제와 혼합된다. 동결방지제는 글리콜, 다이메틸 설폭사이드(DMSO), 폴리올, 당, 2-메틸-2,4-펜테인다이올(MPD), 폴리바이닐피롤리돈(PVP), 메틸셀룰로오스, C-결합 부동액 당단백질(C-AFGP) 또는 이의 조합일 수 있다. 본 발명에 제공된 방법 및 시스템에서 동결방지제로서 사용하기 위한 글리콜은 에틸렌 글리콜, 프로필렌 글리콜, 폴리프로필렌 글리콜(PEG), 글리세롤 또는 이들의 조합으로부터 선택될 수 있다. 본 발명에 제공된 방법 및 시스템에서 동결방지제로서 사용하기 위한 폴리올은 프로페인-1,2-다이올, 프로페인-1,3-다이올, 1,1,1-트리스-(하이드록시메틸)에테인(THME) 및 2-에틸-2-(하이드록시메틸)-프로페인-1,3-다이올(EHMP) 또는 이의 조합으로부터 선택될 수 있다. 본 발명에 제공된 방법 및 시스템에서 동결방지제로서 사용하기위한 당은 트레할로오스, 수크로오스, 글루코오스, 라피노오스, 덱스트로오스 또는 이의 조합으로부터 선택될 수 있다. 한 실시태양에서, 원형질체는 DMSO와 혼합된다. DMSO는 적어도, 최대, 미만, 초과, 동일 또는 약 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 12.5%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 또는 75% w/v 또는 v/v의 최종 농도로 원형질체와 혼합될 수 있다. 원형질체/동결방지제(예를 들어, DMSO) 혼합물은 저장 전에 미세역가 플레이트에 분배될 수 있다. 원형질체/동결방지제(예를 들어, DMSO) 혼합물은 예를 들어 -20℃ 또는 -80℃와 같이 본 발명에 제공된 바와 같이 장기간 보존(예를 들어, 몇 시간, 일(들), 주(들), 달(들), 년(들))을 위해 본 발명에 제공된 임의의 온도로 저장될 수 있다. 한 실시태양에서, 추가의 동결방지제(예를 들어, PEG)가 원형질체/DMSO 혼합물에 첨가된다. 또 다른 실시태양에서, 추가의 동결 방지제(예를 들어, PEG)는 저장 전에 원형질체/DMSO 혼합물에 첨가된다. PEG는 본 발명에 제공된 임의의 PEG일 수 있으며 본 발명에 제공된 바와 같이 임의의 농도(예를 들어, w/v 또는 v/v)로 첨가될 수 있다. 한 실시태양에서, PEG 용액은 STC 완충액 속 40% w/v로 제조된다. 그런 후에 이 40% PEG-STC의 20% v/v가 원형질체에 첨가될 수 있다. 예를 들어, 800 마이크로리터의 1.25 x 107 원형질체는 200 마이크로리터의 40% PEG-STC를 가지며 1ml의 최종 부피를 생성한다. 그런 후에 70 마이크로리터의 DMSO가 이 1ml에 첨가되어 이 제제를 7% v/v DMSO로 만들 수 있다.
본 발명에 제공된 임의의 예비 배양, 배양 및/또는 원형질체화 프로토콜은 고 처리량 방식으로 수행될 수 있다. 예를 들어, 예비 배양, 배양 및 원형질체화는 워크 플로우의 일부로서 수행될 수 있어서, 상기 워크 플로우는 도 28에 도시된 바와 같이 고 처리량(HTP) 프로토콜의 일부를 나타낸다. 고 처리량 프로토콜은 임의의 단계 및/또는 모든 단계에 대해 자동 액체 취급을 이용할 수 있다.
숙주 세포의 형질전환
일부 실시태양에서, 본 발명의 벡터 또는 구조체는 형질전환, 형질감염, 형질도입, 바이러스 감염, 유전자 총 또는 Ti- 매개 유전자 전달을 포함하는 다양한 기술 중 임의의 것을 사용하여 숙주 세포(예를 들어, 사상균류 세포 또는 이로부터 유래된 원형질체)로 도입될 수 있다(Christie, P.J., and Gordon, J.E., 2014 "The Agrobacterium Ti Plasmids" Microbiol SPectr. 2014; 2(6); 10.1128 참조). 특정 방법은 인산 칼슘 형질감염, DEAE-덱스트란 매개 형질감염, 지방감염 또는 전기천공법을 포함한다(Davis, L., Dibner, M., Battey, I., 1986 "Basic Methods in Molecular Biology"). 다른 형질전환 방법은, 예를 들어, 리튬 아세테이트 형질전환 및 전기천공법을 포함하며, 예를 들어, Gietz et al., Nucleic Acids Res. 27:69-74 (1992); Ito et al., J. Bacterol. 153:163-168 (1983); 및 Becker and Guarente, Methods in Enzymology 194:182-187 (1991) 참조. 일부 실시태양에서, 형질전환된 숙주 세포는 재조합 숙주 균주로 지칭된다.
일부 실시태양에서, 본 발명은 96-웰 플레이트 로봇 플랫폼 및 본 발명의 액체 취급 기계를 사용하는 세포의 고 처리량 형질전환을 교시한다.
하나의 실시태양에서, 본 발명에 제공된 방법 및 시스템은 본 발명에 기술된 바와 같이 사상균류 세포로부터 유도된 원형질체에 대한 핵산의 전달을 필요로 한다. 또 다른 실시태양에서, 본 발명에 제공된 방법 및 시스템에 의해 이용되는 형질전환은 본질적으로 고 처리량이고 및/또는 본 발명에 기술된 바와 같이 부분적으로 또는 완전히 자동화된다. 부분적으로 또는 완전히 자동화된 방법은 본 발명에 제공된 바와 같이 자동화된 액체 취급의 하나 이상의 액체 취급 단계를 수반할 수 있다.
이 실시태양에 추가하여, 형질전환은 본 발명에 기술된 바와 같이 구조체 또는 발현 구조체를 미세적정 플레이트에 첨가하고 본 발명에 제공된 방법에 의해 생성된 원형질체를 미세적정 플레이트의 각 웰에 분취함으로써 수행된다. 원형질체의 형질전환/형질감염을 위한 적절한 절차는, 예를 들어, 국제 특허 출원 PCT/NL99/00618, PCT/EP99/202516, Finkelstein and Ball (eds.), Biotechnology of filamentous fungi, technology and products, Butterworth-Heinemann (1992), Bennett and Lasure (eds.) More Gene Manipulations in fungi, Academic Press (1991), Turner, in: Puhler (ed), Biotechnology, second completely revised edition, VHC (1992) protoplast fusion, 및 EP635574B에 기술된 the Ca-PEG mediated protoplast transformation에 기술된 것을 포함하는 당업계에 공지된 임의의 것일 수 있다. 대안적으로, 사상균류 숙주 세포 또는 이로부터 유도된 원형질체의 형질전환은 또한, 예를 들어 Chakraborty 및 Kapoor, Nucleic Acids Res. 18:6737(1990)에 의해 기술된 전기천공과 같은 전기천공, 예를 들어 Christiansen et al., Curr. Genet. 29:100 102 (1995); Durand et al., Curr. Genet. 31:158 161 (1997); and Barcellos et al., Can. J. Microbiol. 44:1137 1141 (1998)에 기술된 DNA의 아그로박테리움 투메파시엔스 매개 형질전환, 탄도 도입 또는 예를 들어 미국특허 제5,516,670호 및 제5,753,477호에 기술된 세포의 "자기-탄도" 형질감염에 의해 실행될 수 있다. 한 실시태양에서, 본 발명에 제공된 방법 및 시스템에서 사용되는 형질전환 절차는, 예를 들어 PEG 매개 형질전환과 같이 본 발명에 제공되는 바와 같이 고 처리량 및/또는 자동화될 수 있는 것이다.
본 발명에 기술된 방법을 사용하여 생성된 원형질체의 형질전환은 당업계에 공지된 임의의 형질전환 시약의 사용을 통해 촉진될 수 있다. 적절한 형질전환 시약은 폴리에틸렌 글리콜(PEG), FUGENE® HD(Roche), Lipofectamine® 또는 OLIGOFECTAMINE®(Invitrogen), TRANSPASS®D1(New England Biolabs), LYPOVEC® 또는 LIPOGEN®(Invivogen)으로부터 선택될 수 있다. 한 실시태양에서, PEG가 가장 바람직한 형질전환/형질감염 시약이다. PEG는 다른 분자량으로 이용할 수 있으며 다른 농도로 사용될 수 있다. 바람직하게는 PEG 4000은 10% 내지 60%, 보다 바람직하게는 20% 내지 50%, 가장 바람직하게는 40%로 사용된다. 한 실시태양에서, PEG는 본 발명에 기술된 바와 같이 저장 전에 원형질체에 첨가된다.
선택된 서열의
루핑
아웃
일부 실시태양에서, 본 발명은 숙주 유기체로부터 DNA의 선택된 영역을 루핑 아웃하는 방법을 교시한다. 루핑 아웃 방법은 Nakashima et al. 2014 "Bacterial Cellular Engineering by Genome Editing and Gene Silencing." Int. J. Mol. Sci. 15(2), 2773-2793에 기술될 수 있다. 일부 실시태양에서, 본 발명은 양성 형질전환 체로부터 선택 마커를 루핑 아웃하는 것을 교시한다. 루핑 아웃 결실 기술은 당해 분야에 공지되어 있으며 (Tear et al. 2014 "Excision of Unstable Artificial Gene-Specific inverted Repeats Mediates Scar-Free Gene Deletions in Escherichia coli." Appl. Biochem. Biotech. 175:1858-1867)에 기술된다. 본 발명에서 제공된 방법에 사용된 루핑 아웃 방법은 단일-교차 상동성 재조합 또는 이중-교차 상동성 재조합을 사용하여 수행될 수 있다. 한 실시태양에서, 본 발명에 기술된 바와 같이 선택된 영역을 루핑하는 것은 본 발명에 기술된 바와 같이 단일-교차 상동성 재조합을 사용하는 것을 수반할 수 있다.
먼저, 루프 아웃 구조체가 (예를 들어 상동성 재조합, CRISPR 또는 다른 유전자 편집 기술을 통해) 숙주 유기체의 게놈 내의 선택된 표적 영역 내로 삽입된다. 한 실시태양에서, 이중-교차 상동성 재조합이 도 3에 도시된 바와 같은 구조체 또는 구조체들을 루프-인시키기 위해 구조체 또는 구조체들과 숙주 세포 게놈 사이에 사용된다. 삽입된 구조체 또는 구조체들은 현존하는 또는 숙주 서열 근처에 도입된 직접 반복체인 서열을 갖도록 디자인되어, 직접 반복체가 루핑 아웃 및 결실이 예정된 DNA의 영역에 인접하게 된다. 일단 삽입되면, 루프 아웃 구조체 또는 구조체들은 선택 영역의 결실을 위해 역 선택될 수 있다(예를 들어, 도 4 참조; 선택 유전자에 대한 내성의 결핍). 루프-인 및 루프-아웃 과저의 추가 예시는 도 36-37에 도시된다.
당업자는 루프 아웃 절차의 설명이 게놈으로부터 원하지 않는 영역을 삭제하는 하나의 예시적인 방법을 나타내는 것을 인식할 것이다. 실제로, 본 발명의 방법은 CRISPR, TALENS, FOK 또는 다른 엔도뉴클레아제를 통한 유전자 편집을 포함하나 이에 제한되지 않는 게놈 결실에 대한 임의의 방법과 양립될 수 있다. 당업자는 상 동성 재조합 기술을 통해 게놈의 원하지 않는 영역을 대체할 수 있는 능력을 인식할 것이다.
형질전환을 위한 구조체
한 실시태양에서, 본 발명에 제공된 방법 및 시스템은 적어도 하나의 핵산으로 사상균류 세포 또는 이로부터 유래된 원형질체의 형질전환 또는 형질감염을 수반한다. 형질전환 또는 형질감염은 본 발명에 기술된 방법 및 시약을 사용할 수 있다. 원형질체의 생성은 본 발명에 제공된 임의의 방법을 사용하여 수행될 수 있다. 원형질체 생성 및/또는 형질전환은 본 발명에 제공된 바와 같이 고 처리량 및/또는 자동화될 수 있다. 핵산은 DNA, RNA 또는 cDNA일 수 있다. 핵산은 폴리뉴클레오타이드일 수 있다. 본 발명에 제공된 방법 및 시스템을 사용하여 사상균류 세포 또는 이로부터 유래된 원형질체를 형질전환시키는데 사용하기 위한 핵산 또는 폴리뉴클레오타이드는 변형 균주 및/또는 부모 균주에 대한 내인성 유전자 또는 이종성 유전자일 수 있다. 내인성 유전자 또는 이종성 유전자는 본 발명에 기술된 바와 같이 관심 생성물 또는 단백질을 암호화할 수 있다. 본 발명에 기술된 바와 같이, 관심 단백질은 사상균류에서 발현되기를 원하는 폴리펩타이드를 지칭할 수 있다. 이런 단백질은 효소, 기질-결합 단백질, 표면-활성 단백질, 구조 단백질 등일 수 있으며, 높은 수준으로 발현될 수 있고, 상업화를 위한 것일 수 있다. 관심 단백질은 세포 내에서 또는 분비된 단백질로서 발현될 수 있다. 내인성 유전자 또는 이종성 유전자는 돌연변이를 포함할 수 있고 및/또는 하나 이상의 유전자 제어 또는 조절 요소의 제어하에 있거나 작동 가능하게 연결될 수 있다. 돌연변이는, 예를 들어, 삽입, 결실, 치환 및/또는 단일 뉴클레오타이드 다형성과 같은 본 발명에 제공된 임의의 돌연변이일 수 있다. 하나 이상의 유전자 제어 또는 조절 요소는 프로모터 서열 및/또는 터미네이터 서열일 수 있다. 내인성 유전자 또는 이종성 유전자는 하나의 발현 구조체 상에 존재할 수 있거나 또는 도 36-38에 도시된 바와 같은 다중 발현 구조체에 걸쳐 분할될 수 있다. 다수의 발현 구조체에 걸쳐 분할될 때, 내인성 유전자 또는 이종성 유전자의 각각의 부분은 돌연변이를 포함할 수 있고/있거나 하나 이상의 유전자 제어 또는 조절 요소의 제어하에 있을 수 있거나 이에 작동 가능하게 연결될 수 있다. 한 실시태양에서, 내인성 유전자 또는 이종성 유전자는 이분자이고, 상기 내인성 유전자 또는 이종성 유전자는 상기 두 부분 각각이 별개의 구조체 상에 존재하도록 두 부분으로 분할된다. 한 실시태양에서, 유전자는 FungiSNP_9 (SEQ ID NO: 11), FungiSNP_12 (SEQ ID NO: 12), FungiSNP_18 (SEQ ID NO: 13) 또는 FungiSNP_40 (SEQ ID NO: 14)이다. 다른 실시태양에서, 유전자는 표 1의 임의의 프로모터에 융합되거나 작동 가능하게 연결된 FungiSNP_9 (SEQ ID NO: 11), FungiSNP_12 (SEQ ID NO: 12), FungiSNP_18 (SEQ ID NO: 13) or FungiSNP_40 (SEQ ID NO: 14)이다. 다른 실시태양에서, 유전자는 FungiSNP_18 (SEQ ID NO: 13)이다. 다른 실시태양에서, 유전자는 표 1의 man8p 또는 amy8p 프로모터에 융합되거나 작동 가능하게 연결된 FungiSNP_18 (SEQ ID NO: 13)이다.
프로모터 서열 및/또는 터미네이터 서열은 변형 균주 및/또는 부모 균주에 대해 내인성 또는 이종성일 수 있다. 프로모터 서열은 발현될 서열의 5' 말단에 작동 가능하게 연결될 수 있다. 다양한 공지된 균류 프로모터는, 예를 들어 C1 엔도글루카나아제, 55kDa 셀로바이오하이드롤라제(CBH1), 글리세르알데하이드-3-포스페이트 디하이드로게나제 A, C. 러크노웬스 GARG 27K의 프로모터 서열 및 크리소스포리움(Chrysosporium)으로부터의 30kDa 자일라나제(xy1F) 프로모터뿐만 아니라 예를 들어 미국 특허. 미국 특허 제4,935,349호; 제5,198,345호; 제5,252,726호; 제5,705,358호; 및 제5,965,384호; 및 PCT 출원 WO 93/07277에 기술된 아스퍼길루스 프로모터와 같은 개시된 숙주 균주에서 기능적일 수 있다. 한 실시태양에서, 본 발명에 제공된 방법 및 시스템에 사용하기 위한 프로모터는 유도성 프로모터이다. 유도성 프로모터는 전사 활성이 화학 물질, 예를 들어 알코올, 테트라사이클린, 스테로이드, 금속 또는 당업계에 공지된 다른 화합물의 존재 또는 부재에 의해 조절되는 임의의 프로모터일 수 있다. 유도성 프로모터는 전사 활성이 빛 또는 저온 또는 고온의 존재 또는 부재에 의해 조절되는 임의의 프로모터일 수 있다. 한 실시태양에서, 유도성 프로모터는 예를 들어 A. 니거 아밀라제 B 유전자에 대한 프로모터와 같은 글루코오스(예를 들어, 도 37 참조)에 의해 억제된 이화산물이다. 한 실시태양에서, 유도성 프로모터는 srpB 유전자, amyB 유전자, manB 유전자 또는 mbfA 유전자와 같은 사상균류 유전자로부터 선택된다. 한 실시태양에서, 유도성 프로모터는 표 1에 열거된 프로모터로부터 선택된다.
터미네이터 서열은 발현될 서열의 3' 말단에 작동 가능하게 연결될 수 있다. 다양한 공지된 균주 터미네이터는 본 발명의 숙주 균주에서 기능적일 수 있다. 예는 에이. 니둘란스(A. nidulans) trpC 터미네이터, 에이 니거(A.niger) 알파-글루코시다제 터미네이터, 에이. 니거(A.niger) 글루코아밀라아제 터미네이터, 무코르 미에헤이(Mucor miehei) 카복실 프로테아제 터미네이터(미국 특허 제5,578,463호 참조), 크리소스포륨 터미네이터 서열, 예를 들어, EG6 터미네이터, 및 트라이코더마 리세이(Trichoderma reesei) 셀로바이오하이드롤라제 터미네이터이다. 한 실시 태양에서, 터미네이터 서열은 직접 반복체(DR)이다. 한 실시태양에서, 본 발명의 전사 터미네이터 서열은 표 1.1에 열거된 터미네이터 서열 또는 표 1.1에 제공된 종결 서열의 오르쏘로그로부터 선택될 수 있다. 예를 들어, 숙주 세포가 아스퍼길루스인 경우, 터미네이터 서열은 표 1.1로부터 선택된 비-아스퍼길루스 종결 서열의 오르쏘로그일 수 있다.
한 실시태양에서, 사상균류 세포로부터 생성된 원형질체는 둘 이상의 핵산 또는 폴리뉴클레오타이드로 공동 형질전환된다. 이 실시태양에 더하여, 둘 이상의 폴리뉴클레오타이드의 적어도 하나는 원형질체가 생성되는 사상균류 균주에 대해 내인성 유전자 또는 이종성 유전자이고 둘 이상의 폴리뉴클레오타이드의 적어도 하나는 선택 가능한 마커에 대한 유전자이다. 선택 가능한 마커 유전자는 본 발명에 제공된 임의의 선택 가능한 마커일 수 있다. 상기한 바와 같이, 둘 이상의 핵산 또는 폴리뉴클레오타이드의 각각은 개별 부분으로 분할되어 각각의 개별 부분은 개별 구조체 상에 존재할 수 있다(도 36-38 참조).
한 실시태양에서, 사상균류 세포 또는 이로부터 유래된 원형질체를 형질전환 또는 형질감염시키는데 사용하기 위한 각각의 핵산 또는 폴리뉴클레오타이드는 핵산 또는 폴리뉴클레오타이드의 5', 3' 또는 5' 및 3' 말단 모두 상에서 형질전환될 사상균류 세포 또는 이로부터 유래된 원형질체의 게놈의 소정의 표적 유전자좌에 존재하는 DNA 서열과 상동인 서열을 포함한다. 핵산 또는 폴리뉴클레오타이드는 형질전환을 위해 사용되는 사상균류 세포에 대한 내인성 유전자 또는 이종성 유전자 또는 선택 가능한 마커 유전자일 수 있어서 사상균류 숙주 세포 게놈 내의 소정의 유전자좌와 상동성이 있는 서열이 내인성, 이종성, 또는 선택 가능한 마커 유전자에 인접한다. 한 실시태양에서, 각각의 핵산 또는 폴리뉴클레오타이드는, 예를 들어 pBLUESCRIPT®(Stratagene)와 같은 당업계에 공지된 임의의 방법을 사용하여 클로닝 벡터 속에 복제된다. 적절한 클로닝 벡터는 사용된 사상균류 숙주 세포의 염색체에서 소정의 표적 유전자좌에서 통합할 수 있는 것일 수 있다. 바람직한 통합형 클로닝 벡터는 클로닝 벡터의 이런 소정의 유전자좌로의 통합을 표적으로 하기 위해 결실되거나 대체될 DNA 서열과 상동인 DNA 단편을 포함할 수 있다. 표적화된 통합을 촉진시키기 위해, 클로닝 벡터는 숙주 세포 또는 이로부터 유도된 원형질체의 형질전환 전에 선형화될 수 있다. 바람직하게는, 클로닝 벡터의 적어도 하나, 그러나 바람직하게는 양 말단이 결실 또는 치환될 DNA 서열과 상동성인 서열에 인접하도록 선형화가 수행된다. 일부의 경우, 짧은 상동성 연쇄 DNA는, 예를 들어, 통합될 핵산 또는 폴리뉴클레오타이드의 양쪽 면 상에 PCR을 통해 첨가될 수 있다. 통합될 핵산 또는 폴리뉴클레오타이드 서열에 인접한 상동성 서열의 길이는 바람직하게는 2kb 미만, 심지어 바람직하게는 1kb 미만, 더욱 바람직하게는 0.5kb 미만, 더욱 바람직하게는 0.2kb 미만, 더욱 바람직하게는 0.1kb 미만, 더욱 바람직하게는 50bp 미만 및 가장 바람직하게는 30bp 미만이다. 통합될 핵산 또는 폴리뉴클레오타이드 서열에 인접하는 상동성 서열의 길이는 약 30bp 내지 약 1000bp, 약 30bp 내지 약 700bp, 약 30bp 내지 약 500bp, 약 30bp 내지 약 300bp, 약 30bp 내지 약 200bp, 및 약 30bp 내지 약 100bp로 변할 수 있다. 사상균류 세포 또는 이로부터 유래된 원형질체를 형질전환시키는데 사용하기 위한 핵산 또는 폴리뉴클레오타이드는 발현 카세트로서 존재될 수 있다. 한 실시태양에서, 클로닝 벡터는 pUC19이다. 이 실시태양에 추가하여, 본 발명에 제공되는 마커 서열을 함유하는 클로닝 벡터는 당업계에 공지된 깁슨 어셈블리를 사용하여 구조체를 제작함으로써 표적 서열과 연관될 수 있다. 선택적으로, 표적화 서열은 융합 PCR에 의해 첨가될 수 있다. 마커에 연결되지 않은 동시 형질전환을 위한 표적화 서열은 게놈 DNA로부터 증폭될 수 있다.
이론적으로, 사상균류 게놈 내의 모든 유전자좌는 본 발명에 제공된 핵산 또는 폴리뉴클레오타이드를 포함하는 발현 카세트의 표적 통합을 위해 선택될 수 있다. 바람직하게는, 표적화가 일어나게 될 유전자좌는 이런 유전자좌에 존재하는 야생형 유전자가 발현 카세트에 포함된 유전자로 대체될 때, 수득된 돌연변이체가, 예를 들어, 본 발명에 기술된 바와 같은 선택/카운터 선택 계획과 같은 소정의 분석법에 의해 탐지 가능한 변화를 나타내는 것이다. 한 실시태양에서, 본 발명에 기술된 바와 같은 사상균류 세포로부터 생성된 원형질체는 제 1 구조체 또는 발현 카세트 및 제 2 구조체 또는 발현 카세트로 공동 형질전환되어 제 1 구조체 또는 발현 카세트가 원형질체 게놈의 제 1 유전자좌로 통합되도록 디자인되는 반면 제 2 구조체 또는 발현 카세트가 원형질체 게놈의 제 2 유전자좌로 통합되도록 디자인된다. 제 1 유전자좌 및 제 2 유전자좌로의 통합을 용이하게 하기 위해, 제 1 구조체 또는 발현 카세트는 제 1 유전자좌와 상동성인 서열에 인접한 반면, 제 2 구조체 또는 발현 카세트는 제 2 유전자좌와 상동성인 서열에 인접한다. 한 실시태양에서, 제 1 구조체 또는 발현 카세트는 내인성 유전자에 대한 서열을 포함하는 반면 제 2 구조체는 선택 가능한 마커 유전자에 대한 서열을 포함한다. 이 실시태양에 추가하여, 제 2 유전자좌는 본 발명에 제공된 방법 및 시스템에 사용된 원형질체 게놈에 존재하는 추가의 선택 가능한 마커 유전자에 대한 서열을 함유하는 반면, 제 1 유전자좌는 본 방법에 제공된 방법 및 시스템에 사용된 원형질체 게놈에 존재하는 원형질체 게놈에 존재하는 내인성 표적 유전자에 대한 서열을 함유한다. 별도의 실시태양에서, 제 1 구조체 또는 발현 카세트는 내인성 유전자 또는 이종성 유전자에 대한 서열을 포함하는 반면, 제 2 구조체는 제 1 선택 가능한 마커 유전자에 대한 서열을 포함한다. 이 별도의 실시태양에 추가하여, 제 2 유전자좌는 본 발명에 제공된 방법 및 시스템에서 사용된 원형질체 게놈에 존재하는 제 2 선택 가능한 마커 유전자에 대한 서열을 함유하는 반면, 제 1 유전자좌는 본 발명에 제공된 방법 및 시스템에서 사용된 원형질 게놈에 존재하는 제 3 선택 가능한 마커 유전자에 대한 서열을 함유한다. 상기 각 실시태양에서, 내인성 유전자 및/또는 이종성 유전자는 본 발명에 제공된 바와 같은 돌연변이(예를 들어, SNP) 및/또는 유전자 제어 또는 조절 요소를 포함할 수 있다.
동핵성
원형질체의 정제
당업자가 이해할 수 있는 바와 같이, 사상균류로부터 유래된 원형질체는 종종 하나 이상의 핵을 함유할 수 있어서 본 발명에 제공된 구조체(예를 들어, 삽입 DNA 단편)에 의한 후속 형질전환이 이핵성인 원형질체를 생산할 수 있어서 구조체(예를 들어, 삽입 DNA 단편)는 원형질체에 존재하는 여러 핵의 부분의 서브세트 속에 포함된다. 형질전환 이후 이핵성 원형질체의 숫자 또는 백분율을 감소시키기 위해서, 전략은, 예를 들어, 내용이 전체로 참조로 본 발명에 포함된 Roncero et al., 1984, Mutat. Res. 125:195에 기술된 방법을 사용하여 형질전환 이전에 사상균류 숙주 세포로부터 유래된 원형질체 집단에서 단핵 원형질체의 백분율을 증가시키는데 사용될 수 있다.
다른 실시태양에서, 개별 포자로부터 유래된 클론 집단을 분리하는 방법이 본 발명에 제공된다. 일부 경우에, 개별 균류 포자는 상기 원형질체의 유전적 교란 후에 균류 균주로부터 유래된 원형질체로부터 포자화된다. 개별 포자로부터 유래 된 클론 집단을 분리하는 방법은 본 발명에 제공된 임의의 방법을 사용하여 유전자 교란 후 동핵성 균류 균주의 분리를 촉진하거나 도울 수 있다. 이 실시태양에 더하여, 다수의 포자(예를 들어, 최종적으로 사상균류 세포 또는 균주로부터 유래된 포자)가 재현탁되어 액체 현탁액을 생성할 수 있고, 개별 부피의 액체 현탁액에서 개별 포자가 예를 들어 미세적정 플레이트와 같은 기판의 웰 또는 반응 영역에 배치 또는 분배될 수 있다. 미세적정 플레이트는 96웰, 384웰 또는 1536웰 플레이트일 수 있다.
미세적정 플레이트 내의 각각의 반응 영역 또는 웰이 단일 개별 균류 포자를 함유하거나 균류 포자를 함유하지 않을 가능성이 높은 통계적 확률을 달성하기 위해, 재현탁된 복수의 포자는 희석될 수 있다. 한 실시태양에서, 희석은 포자의 현탁액이 농축된 것이기 때문에 현탁액의 분배되거나 불연속적인 부피가 하나의 포자를 함유하거나 함유하지 않을 확률이 푸아송 분포에 따른다. 이 실시태양에 추가로, 웰의 90% 초과는 포자를 함유하지 않으므로 비어있다. 나머지 웰 중 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 99.5% 초과는 단일 세포를 가질 것이고, 2%, 1%, 0.5% 또는 0% 미만은 2개 이상의 세포를 가질 것이다. 포자의 현탁액의 분배는 본 발명에 제공되고/되거나 당업계에 공지된 임의의 액체 취급 장치를 사용하여 달성될 수 있다.
다른 실시태양에서, 복수의 포자의 재현탁 및 희석 후, 현탁액의 이산 체적은 이산 체적에서 단일 개별 균류 포자의 존재 또는 부재에 대해 선별된다. 이 실시태양에 더하여, 현탁액의 이산 체적이 단일의 개별 균류 포자만을 함유하는 경우, 상기 이산 체적은 웰 또는 반응 영역으로 분포, 배치 또는 분배된다. 선별은 본 발명에 제공되고(표 3 참조)/되거나 당업계에 공지된 임의의 단일 세포/포자 분배 장치를 사용하여 수행될 수 있다. 한 실시태양에서, 장치는 단일 세포 또는 포자를 광학적으로 식별한다. 이 장치는 FACS 장치, CellenONE 장치, Cytena 단일 셀 프린터 또는 버클리 라이트 비콘(Berkeley Lights Beacon) 장치일 수 있다. 재현탁 및 희석 전에, 복수의 개별 균류 포자는 본 발명에 제공되고(표 3 참조) 및/또는 당업계에 공지된 임의의 장치를 사용하여 선택되거나 분리될 수 있다. 포자의 재현탁 및 희석은 본 발명에 제공되고(표 3 참조)/되거나 당업계에 공지된 임의의 장치를 사용하여 달성될 수 있다.
이산 체적에서 단일 개별 균류 포자의 존재 또는 부재에 대한 선별 후에, 개별 포자를 웰 또는 반응 영역을 포함하는 기질의 웰 또는 반응 영역에 분포 또는 분배하기 위한 본 발명에 기술된 방법은 복수의 포자로부터의 단일의 개별적인 생존 가능한 포자를 함유하는 기질의 웰 또는 반응 영역의 적어도 70%, 75%, 80%, 85%, 90%, 95%, 99% 또는 99.5%를 생성할 수 있다. 웰 또는 반응 영역을 포함하는 기질의 웰 또는 반응 영역에 개별 포자를 분배하기 위해 본 발명에 기술된 방법을 사용하면 복수의 포자로부터의 단일의 개별적인 생존 가능한 포자를 함유하는 기질의 웰 또는 반응 영역의 70%, 75%, 80%, 85%, 90%, 95%, 99% 또는 99.5% 초과를 생성할 수 있다. 웰 또는 반응 영역을 포함하는 기질의 웰 또는 반응 영역에 개별 포자를 분배하기 위해 본 발명에 기술된 방법을 사용하면 복수의 포자로부터의 단일의 개별적인 생존 가능한 포자를 함유하는 기질의 웰 또는 반응 영역의 실질적으로 전부를 생성할 수 있다. 웰 또는 반응 영역을 포함하는 기질의 웰 또는 반응 영역에 개별 포자를 분배하기 위해 본 발명에 기술된 방법을 사용하면 복수의 포자로부터의 단일의 개별적인 생존 가능한 포자를 함유하는 기질의 웰 또는 반응 영역의 전부 또는 100%를 생성할 수 있다. 웰 또는 반응 영역을 포함하는 기질의 웰 또는 반응 영역에 개별 포자를 분배하기 위해 본 발명에 기술된 방법을 사용하면 미세적정 플레이트 내의 웰의 적어도 70%, 75%, 80%, 85%, 90%, 95%, 99% 또는 99.5% 또는 70%, 75%, 80%, 85%, 90%, 95%, 99% 또는 99.5% 초과가 단일 개별 생존 가능한 포자를 함유하는 통계적 확률을 생성할 수 있다. 웰 또는 반응 영역을 포함하는 기질의 웰 또는 반응 영역에 개별 포자를 분배하기 위해 본 발명에 기술된 방법을 사용하면 미세적정 플레이트 내의 웰의 전부 또는 실질적으로 전부가 단일 개별 생존 가능한 포자를 함유하는 통계적 확률을 생성할 수 있다. 기판은 미세적정 플레이트일 수 있다. 미세적정 플레이트는 96웰, 384웰 또는 1536웰 플레이트일 수 있다.
복수의 개별 균류 포자는 사상균류 균주로부터 유래될 수 있다. 사상균류 균주는 아클리아(Achlya), 아크레모니움(Acremonium), 아스퍼길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프 또는 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택될 수 있다. 한 실시태양에서, 사상균류 균주는 아스퍼길루스 니거(Aspergillus niger)이다. 다른 실시태양에서, 사상균류 균주는 비 균사체 형성 표현형을 갖는다. 또 다른 실시태양에서, 사상균류 균주는 비 기능성 비 상동성 말단 결합(NHEJ) 경로를 갖는다. NHEJ 경로는 세포를 NHEJ 경로의 구성요소에 대항하는 항체, 화학적 억제제, 단백질 억제제, 물리적 억제제, 펩타이드 억제제 또는 안티-센스 또는 RNAi 분자에 노출시킴으로써 비 기능적으로 만들어진다.
복수의 개별 포자를 재현탁시키기 위해 사용되는 액체는 배양 배지 또는 완충액일 수 있다. 또한, 웰 또는 반응 영역은 특정 유전적 교란을 함유하는 포자를 선택하는 역할을 하는 선택적 배지를 포함할 수 있어서, 유전적 변이에 대해 선택적인 배지를 포함하는 반응 영역 또는 웰에서 분포된 개별 균류 포자를 배양하는 것은 원하는 유전자 교란을 포함하는 개별 포자에서 유도된 콜로니의 확인 및 선택을 용이하게 한다.
형질전환 전에 단핵성 원형질체의 수 또는 백분율을 증가시키기 위한 전략을 사용하거나 그에 더하여, 단핵 또는 다핵인지의 여부와 상관없이, 원형질체(및 상기 원형질체의 재생에 의해 유래된 콜로니)를 동종 이식 후-형질전환으로 유도하기 위한 전략이 이용될 수 있다. 본 발명에서 제공되는 바와 같이, 원하는 또는 관심 표적 유전자에 대해 동핵성인 원형질체 (및 이로부터 유래된 콜로니)의 수 또는 백분율을 증가시키는 것은 형질전환된 원형질체 또는 형질전환된 원형질체 집단으로부터 유래된 콜로니를 하나 이상의 선택 가능한 마커의 존재 및/또는 부재에 기초하여 선택 및/또는 카운터 선택하는 것을 수반할 수 있다. 하나 이상의 선택 가능한 마커는 본 발명에 제공된 바와 같은 임의의 선택 가능한 마커 또는 선택 가능한 마커의 조합일 수 있고, 선택 및/또는 카운터-선택 방식은 본 발명에 제공된 임의의 이러한 방식일 수 있다.
동핵성
형질전환체의 확인
본 발명에 제공된 방법에 의해 생성된 동핵성 형질전환체는 표현형 선별, 서열-기반 선별 또는 이들의 조합을 사용하여 확인될 수 있다. 다시 말해서, 표현형 선별, 서열-기반 선별 또는 이들의 조합은 구조체(예를 들어, 삽입 DNA 단편)로 상기 원형질체의 형질전환 후 원형질체로부터 유래된 콜로니에서 부모 유전자형의 존재 또는 부재를 검출하는 데 사용될 수 있다. 동핵성 형질전환체의 확인 또는 검출은 하나 이상의 선택 가능한 마커 유전자의 도입 및/또는 상실을 유지하면서 본 발명에 제공된 바와 같이, 상기 형질전환체를 선택 및/또는 카운터 선택 체계에 적용하기 전 및/또는 후에 일어날 수 있다. 표현형 선별은 식별 가능한 표현형(성장 및/또는 비색 변화의 변화)을 갖는 형질전환체를 식별하는 데 사용될 수 있는 반면, 서열-기반 선별은 본 발명에 제공된 구조체 또는 구조체들의 형질전환 및 통합 후 식별 가능한 표현형이 있거나 없는 형질전환체를 확인하는 데 사용될 수 있다.
서열-기반 선별
본 발명에 기재된 바와 같이, 서열-기반 선별은 형질전환체에서 원하는 또는 표적 구조체의 존재 또는 부재를 결정하는 데 사용될 수 있다. 이러한 방식으로, 서열-기반 서열 분석은 원하는 유전자 또는 구조체의 통합이 특정 형질전환체에서 발생했는지 여부를 평가하는 데 사용될 수 있다. 서열-기반 선별은 원하는 유전자, 돌연변이 또는 구조체를 함유하는 다핵 세포 또는 다핵 세포 집단에서 핵의 백분율을 결정하는 데 사용될 수 있다. 또한, 서열-기반 선별은 원하는 표적 통합을 경험 한 형질전환체 집단의 백분율을 결정하는 데 사용될 수 있다. 구조체는 본 발명에 기술된 임의의 구조체 또는 복수의 구조체일 수 있다. 일부 경우에, 원하는 유전자, 돌연변이 또는 구조체를 포함하는 핵의 백분율 또는 비율이 원하는 유전자, 돌연변이 또는 구조체를 포함하는 핵 대 상기 원하는 유전자, 돌연변이 또는 구조체가 결여된 핵의 백분율 또는 비율이 특정 임계값 미만인 경우 서열-기반 선별의 결과는 정제 계획(예를 들어, 동핵성 정제)을 선택하는 데 사용될 수 있다.
일반적으로, 서열-기반 선별은 원하는 돌연변이 또는 구조체를 함유할 수 있는 형질전환체를 분리하는 것을 수반할 수 있다. 각각의 형질전환체는 하나 또는 복수의 핵을 함유할 수 있어서, 복수의 핵 중 하나 또는 각각의 핵은 형질전환 동안 도입된 핵산 단편(예를 들어, 돌연변이를 포함하는 하나 이상의 구조체 또는 유전자)을 함유할 수 있다. 형질전환은 본 발명에 제공된 바와 같이 DNA의 특정 단편 (예를 들어, 돌연변이를 포함하는 하나 이상의 구조체 또는 유전자)을 갖는 원형질체의 형질전환을 표적화으로 할 수 있다.
일부 경우에, 분리 후, 서열-기반 선별은 표적 유전자(도입된 구조체) 및 표적의 순도에 영향을 미치는 배지(즉, 선택적 배지) 상의 야생형 또는 부모 유전자 둘 모두와 핵의 혼합물을 함유하거나 임의의 특정 표현형 또는 형질에 대해 완전히 비 선택적일 수 있는 형질전환체를 전파시키는 것을 수반하여, 형질전환체로부터 유래된 콜로니를 생성한다. 한 실시태양에서, 각각의 분리된 형질전환체 또는 이로부터 유래된 콜로니의 일부는 예를 들어 한천을 포함하는 옴니트레이(Omnitray)(도 30 및 도 31의 시드 플레이트 참조)와 같은 미세적정 플레이트의 웰로 옮겨지거나 그 안에 배치되며 여기서 형질전환체 또는 이로부터 유래된 콜로니의 일부는 포자 형이다. 미세적정 플레이트는 96웰, 384웰 또는 1536웰 미세적정 플레이트일 수 있다.
단독으로 또는 전파와 조합하여 분리 후, 핵산(예를 들어, DNA)은 형질전환 체 또는 그로부터 유래된 콜로니 또는 포자로부터 추출될 수 있다. 도 30에 도시 된 바와 같이, 핵산 분리는 형질전환체로부터 유래된 포자로부터 유래될 수 있고 미세적정 플레이트 형식으로 수행될 수 있으며, 자동화된 액체 취급을 이용할 수 있다. 핵산 추출은 당업계에 공지된 임의의 공지된 핵산 추출 방법 및/또는 예를 들어 PrepmanTM(ThermoFischer Scientific)과 같은 시판 키트를 사용하여 수행될 수있다. 한 실시태양에서, 형질전환체로부터 유래된 포자로부터 추출된 핵산은 DNA의 증폭을 가능하게 하는 비등 준비 방법을 사용하여 수행된다(도 32 참조). 비등 준비 방법은 포자를 소량의 성장 배지에 접종하는 것을 포함할 수 있다. 한 실시태양에서, 포자는 PCR에 적합한 플레이트에서 96개의 웰로 분리되며, 각 웰은 소량의 성장 배지를 포함한다. 포자는 10 내지 16시간 동안 성장할 수 있으며, 이는 포자가 PCR을 억제할 수 있는 안료를 폐기하는 것을 도울 수 있다. 또한, 성장은 또한 각각의 웰의 게놈 DNA 함량을 증가시키는 역할을 할 수 있는 여러 라운드의 핵 분열을 촉진할 수 있다. 이어서, 밤새 "미니 배양액"은 세포 용해를 보조할 뿐만 아니라 용해 동안 방출될 DNA를 안정화시키는 완충제가 보충될 수 있다. 적합한 완충액의 한 예는 PrepMan Ultra(Thermo Fisher)일 수 있다. 적절한 완충제의 다른 예는 소량의 이온성 세제를 함유하는 트리스 완충 용액을 포함할 수 있다. 이어서, 미니 배양액 완충액 혼합물은 15분 내지 1시간의 임의의 배양 시간 동안 열 순환기에서 99℃로 가열될 수 있다.
핵산 추출 후, 서열-기반 선별은 도입된 표적 유전자 또는 구조체에 대한 모핵(즉, 형질전환되지 않은 핵)을 포함하는 표적 또는 돌연변이 핵의 백분율 또는 비율을 평가하는 데 실행될 수 있다. 서열-기반 선별은 핵산의 서열을 결정 또는 검출하는 데 사용될 수 있는 당업계에 공지된 임의의 방법일 수 있다. 서열-기반 선별을 수행하기 위해 사용된 방법은 핵산 서열 분석 방법 또는 혼성화-기반 분석법으로부터 선택될 수 있다. 본 발명에 제공된 방법에 의해 이용되는 핵산 서열 분석 또는 기술은 차세대 서열 분석(NGS) 시스템 또는 분석법일 수 있다. 특정 핵산 서열을 검출하기 위한 혼성화 기반 분석법은 마이크로어레이 또는 nCounter 시스템(Nanostring)의 사용을 수반할 수 있다. 서열-기반 선별을 수행하기 전에, 추출된 핵산은 표적 유전자에 대한 프라이머 쌍(들)을 갖는 PCR을 사용하여 증폭될 수 있다.
핵산 서열 분석 방법을 이용하는 실시태양에서, PCR에 사용된 프라이머 쌍은 암호화된 인덱싱 프라이머를 사용하여 2차 증폭에 사용될 수 있는 어댑터 서열을 포함할 수 있다. 2차 증폭 반응에 의해 생성된 앰플리콘은 암호화된 인덱스 프라이머에 대한 서열 분석 프라이머를 이용한 다중 서열 분석을 사용하여 서열 분석될 수 있다. 서열 분석은 당업계에 공지된 임의의 유형의 서열 분석을 사용하여 수행될 수 있다. 한 실시태양에서, 서열 분석은 차세대 서열 분석(NGS)이다. NGS는 예를 들어 Illumina NGS와 같은 당업계에 공지된 임의의 공지된 NGS 방법일 수 있다. 도 30은 형질전환, 포자 형성, 핵산 추출 및 NGS 기반 서열 기반 선별이 자동 또는 반자동 방식으로 수행되는 워크 플로우의 실시태양을 도시한다. 도 25, 26, 34 및 35에 도시된 바와 같이, 다중 서열 분석 반응으로부터의 데이터는 표적 핵의 존재 또는 부재를 결정하기 위해 사용될 수 있다. 일부 경우에, 다중 서열 분석 반응으로부터의 데이터는 또한 표적 웰 내의 형질전환체에 대한 모핵 대 돌연변이 핵의 비율을 결정하는 데 사용될 수 있다(도 34 및 35 참조). 이 실시태양에 더하여, 모체 대 돌연변이 핵의 백분율 또는 비율을 정량화하기 위해 표준 곡선이 생성될 수 있다. 표준 곡선은 도 33에 도시된 바와 같이 공지된 비율의 모체 대 돌연변이 핵을 함유하는 균주로부터 분리된 핵산을 증폭 및 선별하고 이어서 복수의 테스트 샘플의 근사치를 결정하기 위해 공지된 비율로 나타내는 모체 대 돌연변이 앰플리콘을 사용하여 함으로써 생성될 수 있다.표준 곡선을 생성하는 데 사용된 균주는 테스트 샘플과 동일한 플레이트 세트에서 처리(예를 들어, 분리, 전파 및 추출)될 수 있다.
한 실시태양에서, 서열-기반 서열 분석은 각각의 형질전환체의 동핵성 상태를 평가 또는 결정하기 위해 선택 및/또는 카운터-선택 후에 사용된다. 서열-기반 서열 분석 후 선택 및/또는 카운터-선택은 본 발명에 기술된 바와 같이 다중 서열 분석을 사용할 수 있고 자동화되거나 반자동화될 수 있다. 서열-기반 서열 분석 후 선택 및/또는 카운터-선택은 또한 이핵성 형질전환체의 존재 및/또는 양(예를 들어, 비율)을 결정하는 수단으로서 본 발명에 기술된 바와 같이 표준 곡선의 생성을 이용할 수 있다.
형질전환체의 순도를 결정하기 위한 서열-기반 선별의 사용
본 발명에 논의된 바와 같이, 본 발명에 제공된 방법, 시스템 및 워크 플로우에서 다핵성 숙주 세포(예를 들어, 사상균류 숙주 세포)로부터 생성된 원형질체는 다핵성일 수 있다. 이어서, 본 발명에 제공된 것과 같은 하나 이상의 구조체로 형질전환된 원형질체는 게놈에 통합된 특정 구조체 또는 구조체들을 갖는 다수의 핵의 일부 또는 백분율만을 함유할 수 있다. 형질전환된 구조체의 성질에 따라, 형질전환된 원형질체로부터 유래된 콜로니는 콜로니에 존재하는 혼합된 핵 집단으로 인해 식별 가능한 표현형을 생성하지 않을 수 있다. 따라서, 서열-기반 선별의 사용은 원하는 구조체 또는 구조체들을 포함하는 핵 대 원하는 구조체 또는 구조체들을 포함하는 핵의 혼합 집단에서 핵의 백분율을 결정하는 데 필수적일 수 있다. 도 33-35는 혼합된 집단의 핵을 갖는 세포를 함유하는 콜로니에서 모체 대 돌연변이 체 핵을 검출하기 위한 NGS 기반 선별의 유용성을 보여준다. 한 실시태양에서, NGS 기반 선별은 도입된 구조체 또는 구조체들을 갖는 원하는 백분율의 핵을 함유하는 이로부터 유래된 형질전환체 또는 균주를 확인하기 위해 사용된다. 원하는 백분율은 임계값 백분율일 수 있으며, 이에 따라 상기 임계값 이상에서 형질전환체 또는 이로부터 유래된 균주는 원하는 관심 생성물 또는 이의 수준을 생성한다. 관심 생성물은 표 2에 나열된 생성물에서 선택될 수 있다. 원하는 백분율은 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% 또는 100%일 수 있다. 백분율은 본 발명에 기술된 표준 곡선을 이용하여 결정될 수 있다.
표현형 선별
본 발명에 기술된 바와 같이, 표현형 선별은 서열-기반 선별 또는 형질전환체와 조합하여 사용될 수 있다. 일부 경우에, 서열-기반 선별의 결과는 동핵성 형질전환체의 분리를 보장하기 위해 정제 계획을 결정하는 데 사용될 수 있다. 또한, 표현형 선별/정제에 의해 수득된 분리물이 동핵성인지를 평가하기 위해 표현형 선별/정제 후에 서열-기반 선별을 이용할 수 있다.
본 발명에 제공된 방법, 조성물 또는 시스템을 사용하여 생성된 형질전환체의 표현형 선별은 하나 이상의 선택 가능한 마커의 사용을 이용할 수 있다. 선택 가능한 마커는 종종 형질전환되지 않은 균주에 대해 이질적인 특정 유형의 내성을 제공하는 유전자 생성물을 암호화할 수 있다. 이것은 일반적으로 중금속, 항생제 또는 살생물제에 대한 내성일 수 있다. 원영양성은 또한 비 항생성 변종의 유용한 선택 가능한 마커일 수 있다. 영양요구성 마커는 숙주 세포에서 영양 부족을 일으킬 수 있으며, 이런 결함을 수정하는 유전자는 선택에 사용될 수 있다.
당업계에서 사용되는 광범위한 선택 가능한 마커가 있으며 이들 중 일부 또는 전부가 본 발명에 제공된 방법 및 시스템에 적용될 수 있다. 본 발명에 사용하기 위한 선택 가능한 마커 유전자는 영양요구성 마커, 원영양성 마커, 우성 마커, 열성 마커, 항생제 내성 마커, 이화 마커, 효소 마커, 형광 마커, 발광 마커 또는 이들의 조합일 수 있다. 이들의 예는 amdS(아세트아마이드/플루오로아세트아마이드), ble(블레오마이신-플레오마이신 내성), hyg(hygromycinR), nat(nourseotricin R), pyrG(우라실/5FOA), nlaD(질산염/염소산염), sutB(설페이트/셀레네이트), eGFP(녹색 형광 단백질) 및 모든 상이한 색상 변이체, aygA(표색 마커), met3(메티오닌/셀레네이트), pyrE(오로테이트 P-리보실 트랜스페라제), trpC(안트라닐레이트 신타아제), argB(오르니틴 카바모일트랜스페라제), bar(포스핀오트리신 아세틸트랜스페라제), 돌연변이 아세토락테이트 신타아제(설폰일우레아 내성) 및 네오마이신 포스포트랜스페라제(아미노글리코시드 내성)을 포함하나 이에 제한되지 않는다.
한 실시태양에서, 단일 선택 마커는 다핵체 유기체의 게놈에서 표적 유전자의 특이적 돌연변이의 표현형 효과를 조사하기 위해 사용된다. 다핵 유기체는 A. 니거와 같은 사상균류일 수 있다. 표적 유전자는 생합성 경로에 관여하는 유전자, 예를 들어 시트르산 생산에 관여하는 유전자일 수 있다. 이러한 유형의 실시태양의 예는 도 39에서 볼 수 있다. 도 39의 상단에, A. 니거에서 시트르산 생산에 관여하는 유전자와 상동성인 서열에 의해 플랭킹된 pyrG 유전자를 포함하는 결실 구조체는 돌연변이(예를 들어, SNP)를 포함하고 천연 pyrG 유전자가 결여된 시트르산 생산 유전자의 버전을 포함하는 숙주 원형질체 내로 도입된다. pyrG 구조체의 상동 재조합은 본 발명에 기술된 pyrG 유전자의 존재에 기초하여 선택될 수 있는 형질 전환체를 생성한다. 또한, 형질전환체는 상기 돌연변이가 경로에서 수행하는 역할을 알리기 위해 사용될 수 있는 결실 표현형을 가질 수 있다. 대안적으로, 도 39의 하부는 숙주 원형질체에서 천연 pyrG 유전자좌에 상동성인 서열에 의해 플랭킹된 특정 돌연변이(예를 들어, SNP)를 갖는 시트르산 생산에 관여하는 유전자를 포함하는 구조체가 숙주 원형질체에 도입되는 실시태양을 도시한다. 구조체와 천연 pyrG 유전자좌 사이의 상동성 재조합은 FOA를 포함하는 배지 상에 상기 형질전환체를 성장시킴으로써 선택될 수 있는 형질전환체를 생성할 수 있다. 도입된 SNP의 표현형 효과는 본 발명에 기재된 바와 같이 평가될 수 있다.
본 발명의 다른 실시태양은 사상균류에서 활성인 두 개 이상의 선택 마커의 사용을 수반한다. 사용될 수 있는 선택 마커의 광범위한 조합이 있으며, 이들 모두는 본 발명에 제공된 선택/카운터 선택 계획에 적용될 수 있다. 예를 들어, 선택/카운터 선택 계획은 영양요구성 마커, 원영양성 마커, 우성 마커, 열성 마커, 항생제 내성 마커, 이화 마커, 효소 마커, 형광 마커 및 발광 마커의 조합을 이용할 수 있다. 제 1 마커는 순방향 모드(즉, 능동 통합이 발생하는 경우)에서 선택하기 위해 사용될 수 있는 반면 추가 마커는 역방향 모드(즉, 오른쪽 유전자좌에서 능동 통합이 발생하는 경우)에서 선택하기 위해 사용될 수 있다. 선택/카운터 선택은 동시 형질전환에 의해 수행될 수 있어서 선택 가능한 마커가 별도의 벡터 상에 존재할 수 있거나 또는 본 발명에 기술된 바와 같은 내인성 유전자 또는 이종성 유전자와 동일한 핵산 단편 또는 벡터 내에 존재할 수 있다.
한 실시태양에서, 본 발명의 동핵성 원형질체 정제 계획은 사상균류 숙주 세포로부터 생성된 원형질체를 내인성 유전자 또는 이종성 유전자에 대한 서열을 포함하는 제 1 구조체 및 제 1 선택 가능한 마커 유전자에 대한 서열을 포함하는 제 2 구조체로 공동 형질전환시키는 것을 수반하여 제 1 구조체는 제거되거나 불활성화되는 표적 유전자에 대한 서열을 포함하는 원형질체 게놈의 제 1 유전자좌에 배향되는 반면, 제 2 구조체는 제 2 선택 가능한 마커 유전자에 대한 서열을 포함하는 원형질체 게놈의 제 2 유전자좌에 배향된다. 한 실시태양에서, 제 1 구조체는 내인성 유전자 또는 이종성 유전자에 대한 서열을 포함하고, 제거되거나 불활성화되는 표적 유전자는 제 3 선택 가능한 마커 유전자에 대한 것이다. 별도의 실시태양에서, 제 1 구조체는 내인성 유전자에 대한 서열을 포함하고 제거되거나 불활성화되는 표적 유전자는 형질전환 이전에 원형질체의 게놈에 존재하는 내인성 유전자의 모방체이다. 본 발명에 기술된 바와 같이, 제 1 구조체의 내인성 유전자 또는 이종성 유전자는 돌연변이(예를 들어, SNP) 및/또는 유전자 조절 또는 제어 요소(예를 들어, 프로모터 및/또는 터미네이터)를 포함할 수 있다. 제 1, 제 2 및/또는 제 3 선택 가능한 마커는 당업계에 공지된 및/또는 본 발명에 기술된 임의의 영양요구성 마커, 원영양성 마커, 우성 마커, 열성 마커, 항생제 내성 마커, 이화 마커, 효소 마커, 형광 마커 및 발광 마커일 수 있다. 특정 유전자좌로 배향되도록 하기 위하여, 각각의 구조체는 본 발명에 기술된 바와 같이 원형질체 게놈의 원하는 유전자좌와 상동성인 뉴클레오타이드에 인접된다.
제 1 구조체가 내인성 유전자 또는 이종성 유전자에 대한 서열을 포함하고, 제거되거나 불활성화되는 표적 유전자가 제 3 선택 가능한 마커 유전자에 대한 것 인 실시태양의 예는 도 23a에 도시된다. 이 예에서, 제 1 구조체는 비색 선택 가능한 마커 유전자 aygA에 대한 유전자좌로 통합되는 SNP를 포함하는 사상균류에서 시트르산 생산에 관여하는 내인성 유전자에 대한 서열을 포함하는 반면, 제 2 구조체는 영양요구성 마커 유전자 met3에 대한 유전자좌로 통합되는 영양요구성 마커 유전자 pyrG에 대한 서열을 포함한다. 이 예에서, 사상균류 숙주 세포는 pyrG 음성 또는 우라실 영양요구성이다. 따라서, 동핵성 원형질체 형질전환체의 정제는 상기 형질전환체를 우라실이 없는 최소 배지에서 성장시키는 것을 수반한다. 도 23a에 도시된 바와 같이, 동핵성 형질전환체는 우라실 원영양체일뿐만 아니라 순수한 황색을 띠게 되어 pyrG 유전자의 편입 및 aygA 유전자의 제거를 나타낸다. 임의의 잔여 이핵성 콜로니의 카운터 선택 및 제거는 셀렌산염을 함유하는 최소 배지(우라실을 갖거나 갖지 않음)에 형질전환체를 순차적으로 플레이팅하여 수행될 수 있고, 이에 의해 met3 + 핵을 갖는 형질전환체는 셀렌산염의 존재에서 사망할 것이다. met3 유전자와 유사하게 작용하는 다른 마커는, 예를 들어, 본 실시태양에서 기술된 선택/카운터 선택 계획에서 사용될 수 있는 질산염 환원효소를 암호화하는 niaA 유전자일 수 있다. niaA 유전자의 경우, 사상균류 숙주 세포는 niaA+ 일 수 있으며, 이에 의해 제 2 구조체의 정확한 통합은 카운터 선택 동안 사용된 염소산염에 내성인 niaA- 자손을 생성한다. 한 실시태양에서, 제 1 및/또는 제 2 구조체의 원형질체 게놈으로의 정확한 통합의 확인은, 예를 들어 차세대 서열화(NGS)를 사용하여 원형질체의 게놈을 서열화함으로써 확인된다.
제 1 구조체가 내인성 유전자에 대한 서열을 포함하고 제거되거나 불활성화되는 표적 유전자가 형질전환 이전에 원형질체의 게놈에 존재하는 내인성 유전자의 모방체인 실시태양의 한 예는 도 24에 도시된다. 이 예에서, 제 1 구조체는 상기 SNP가 없는 상기 내인성 유전자에 대한 유전자좌로 통합되는 SNP를 포함하는 사상균류에서 시트르산 생산에 관여하는 내인성 유전자에 대한 서열을 포함하는 반면, 제 2 구조체는 비색 선택 가능한 마커 유전자 aygA에 대한 유전자좌로 통합되는 영양요구성 마커 유전자 pyrG에 대한 서열을 포함한다. 이 예에서, 사상균류 숙주 세포는 pyrG 음성 또는 우라실 영양요구성이다. 따라서, 동핵성 원형질체 형질전환체의 정제는 상기 형질전환체를 우라실이 없는 최소 배지에서 성장시키는 것을 수반한다. 도 24에 도시된 바와 같이, 동핵성 형질전환체는 우라실 원영양체일뿐만 아니라 순수한 황색을 띠게 되어 pyrG 유전자의 편입 및 aygA 유전자의 제거를 나타낸다. 한 실시태양에서, 제 1 및/또는 제 2 구조체의 원형질체 게놈으로의 정확한 통합의 확인은, 예를 들어 차세대 서열화(NGS)를 사용하여 원형질체의 게놈을 서열화함으로써 확인된다. 사용되는 NGS 시스템 또는 방법은 예를 들어 Illumina NGS와 같은 당업계에 공지된 임의의 NGS 시스템 또는 방법일 수 있다.
한 실시태양에서, 제 2 구조체는 재활용 가능한 또는 가역 가능한 마커를 암호화하는 발현 카세트를 포함한다. 재활용 가능한 또는 가역 가능한 마커는 파괴 neo-pyrG-neo 발현 카세트일 수 있다. neo- pyrG -neo 구조체는 사상균류 숙주 세포 (예를 들어, A.niger)의 ura-균주에서 상기 실시태양에 기술된 바와 같은 제 1 구조체에 의해 공동 형질전환될 수 있고 동핵성 형질전환체는 상기한 바와 같이 우라실 결핍 배지 상에 플레이팅하고 순수한 황색 우라실 원영양체를 선택함으로써 선택될 수 있다. 이어서, pyrG 선택의 사용은 상기 동핵성 형질전환체를 배지를 함유하는 5-FOA에 플레이팅하고 상기 5-FOA 배지 상에 성장하는 형질전환체를 선택함으로써 재생될 수 있어서, 상기 형질전환체는 pyrG 유전자의 제거를 초래하는 neo 반복체 사이의 염색체 내 재조합을 겪었다는 것을 나타낸다.
추가의 실시태양에서, 본 발명에 제공된 바와 같은 공동 형질전환을 사용하는 대신에, 본 발명의 상동성 원형질체 정제 방식은, 특정 유전자에 대한 서열을 포함하는 결실 구조체를 가진 사상균류 숙주 세포로부터 생성된 원형질체를 형질전환시키는 것을 수반하여 구조체는 표적 유전자가 제거되거나 불활성화되는 서열을 포함하는 원형질체 게놈의 원하는 유전자좌를 향하게 된다. 특정 유전자 좌위로 향하기 위해, 구조체는 본 발명에 기재된 바와 같은 원형질체 게놈에서 원하는 유전자좌와 상동성인 뉴클레오타이드에 의해 플랭킹된다. 이러한 유형의 구조체/형질전환의 사용은 특정 생화학적 경로에서 특정 유전자의 역할에 대한 정보를 제공하는데 사용될 수 있다. 한 실시태양에서, 결실 구조체의 원형질체 게놈으로의 정확한 통합의 확인은 예를 들어 차세대 서열 분석(NGS)과 같은 것을 이용하여 원형질체의 게놈을 서열 분석함으로써 확인된다. 사용되는 NGS 시스템 또는 방법은 예를 들어 Illumina NGS와 같은 당업계에 공지된 임의의 NGS 시스템 또는 방법일 수 있다. 이 실시예의 예는 도 39에 도시되어 있다. 하나의 경우에, 사상균류 숙주 세포는 pyrG 음성이고 결실 구조체는 선택 가능한 마커 유전자(예를 들어, 도 39의 pyrG 유전자)를 포함하지만, 표적 유전자는 SNP이다. 따라서, 동핵체 원형질체 형질전환체의 정제는 우라실이 없는 최소 배지에서 상기 형질전환체를 성장시키는 것을 수반한다. 다른 경우에, 사상균류 숙주 세포는 pyrG 양성이고 결실 구조체는 SNP를 포함하는 반면, 표적 유전자는 선택 가능한 마커 유전자(예를 들어, 도 39의 pyrG 유전자)이다. 따라서, 동핵성 원형질체 형질전환체의 정제는 FOA를 포함하는 최소 배지에서 상기 형질전환체를 성장시키는 것을 수반한다.
또 다른 실시태양에서, 돌연변이된 유전자(예를 들어, SNP)는 돌연변이된 유전자의 여러 부분의 형질전환 및 통합을 통해 다핵체 유기체(예를 들어, A. 니거와 같은 사상균류)의 게놈에서 표적 유전자좌에 통합되어 돌연변이 유전자의 여러 부분 각각이 별도의 구조체 상에 존재한다. 다수의 구조체의 각각은 돌연변이된 유전자의 고유 부분 및 다른 다수의 구조체 중 하나에도 존재하는 돌연변이된 유전자의 중첩 부분을 포함하여 유기체 게놈에서 돌연변이 유전자의 기능적 복제물을 생성하는 다수의 구조체의 재조합을 용이하게 할 수 있다. 돌연변이된 유전자의 각 부분을 유기체의 원하는 유전자좌로 통합하는 것을 용이하게 하기 위해, 다수의 구조체 각각은 구조체에서 구조체에서 돌연변이 유전자의 일부를 플랭킹하는 유기체의 게놈에서 원하는 유전자좌와 상동성인 뉴클레오타이드를 추가로 포함할 수 있다. 일부 경우에, 돌연변이된 유전자는 2개의 구조체에 걸쳐 분할되고 2개의 구조체의 이분자 형질전환을 통해 유기체 내로 도입된다. 이 개념의 한 예가 도 36에 도시되어있다. 도 36의 좌측 열에 도시된 바와 같이, pyrG 마커 유전자는 2개의 구조체로 분할되어 각각의 구조체가 pyrG의 고유한 부분 및 다른 구조체와 겹치는 부분을 포함한다. 또한, 각각의 구조체는 숙주 유기체 게놈에서 aygA 마커 유전자와 상동성인 서열을 추가로 포함하여 2개의 구조체에서의 상동성 서열의 각각의 부분이 또한 SNP를 함유한다. 본 발명에 제공된 임의의 방법을 사용한 형질전환 후 2개의 구조체의 재조합은 2개의 SNP를 포함하는 전체 pyrG 마커 유전자의 삽입을 초래한다. 전적으로 통합된 pyrG 마커 유전자를 함유하는 형질전환체 및 루프-아웃을 통해 pyrG 마커 유전자를 상실한 형질전환체를 함유하는 형질전환체는 본 발명에 기술된 바와 같이 선택/카운터 선택을 통해 검출될 수 있다. 특히, 루프 아웃은 FOA를 이용하여 배지 상에서 형질전환체를 성장시킴으로써 선택될 수 있다.
이분자 변환의 다른 예가 도 37에 도시되어있다. 도 37은 균류(예를 들어, A. 니거)에서의 조합 SNPSWP의 예를 도시하며, 여기서 표적 유전자(즉, aygA 유전자)의 다수의 돌연변이가 단일 형질 전환에서 돌연변이 및 분할 마커 유전자(발산 pyrG 유전자)의 일부를 각각 포함하는 2개의 별개의 구조체의 모체 aygA 유전자로의 통합에 의해 원형질체 게놈 내로 도입된다. 도 37에 도시된 바와 같이, 각각의 pyrG 유전자 함유 구조체의 중첩 부분과 구조체 및 숙주 게놈에서 aygA 유전자의 상동성 부분 사이의 성공적인 재조합에 의해, 전체 pyrG 유전자 각각의 발현은 글루코오스에 의한 이화 작용 억제를 통해 제어될 수 있다. 따라서, 원하는 재조합 및 통합 이벤트가 발생한 형질전환체의 성장이 유리하도록 형질전환체를 글루코오스 상에서 성장시킴으로써 형질전환체를 선택할 수 있다. 또한, FOA를 이용하여 배지 상에서 형질전환체를 성장시킴으로써 루프-아웃이 촉진될 수 있다. 당업자에 의해 이해될 수 있는 바와 같이, 도 37에 도시된 개념은 돌연변이(예를 들어, SNP)의 조합을 표적 유전자에 도입하고 이어서 상기 조합의 표현형 효과를 테스트하는 데 사용될 수 있다. 표현형 효과는 외인성 단백질의 원하는 특성 또는 활성의 생성일 수 있다. 관심의 특성 또는 활성은 외인성 단백질과 관련된 임의의 물리적, 물리 화학적, 화학적, 생물학적 또는 촉매적 특성, 또는 이런 특성의 개선, 증가 또는 감소를 의미할 수 있다. 표현형 효과는 또한 하나 이상의 대사 산물의 생산 또는 생산 부족일 수 있다. 표현형 효과는 또한 단백질 또는 대사 산물의 양을 증가시키거나 감소시킬 수 있다. 또한, 돌연변이의 특정 조합을 함유하는 균주를 제작하기 위해 유사한 기술을 사용하여 추가의 돌연변이가 도입될 수 있다는 것이 고려된다.
도 36의 중간 및 오른쪽 열은 표적 유전자에서 돌연변이의 표적화된 통합을 갖는 형질전환체를 생성하기 위해 본 발명에 제공된 방법 및 시스템에 사용될 수 있는 추가 접근법을 예시한다. 한 실시태양에서, 다핵체 유기체(예를 들어, 사상균류)의 공동 형질전환은 숙주 유기체 게놈에서 원하는 유전자좌에 상동성인 서열, 돌연변이(예를 들어, SNP) 및 터미네이터 반복체(예를 들어, 직접 반복체(DR)에 의해 플랭킹된 마커 유전자(예를 들어, pyrG)의 일부를 갖는 표적 유전자 및 제 1 구조체 상의 마커 유전자의 중첩 부분 및 제 2 테미네이터 반복체(DR) 및 숙주 유기체 게놈에서 원하는 유전자좌에 상동성인 서열에 의해 플랭킹된 마커 유전자의 나머지를 포함하는 제 2 구조체를 사용하여 실행된다. 구조체의 성공적인 재조합 및 원하는 유전자좌로의 통합을 포함하는 형질전환체는 본 발명에 제공된 임의의 선택/카운터 선택 방식(예를 들어, aygA 기반 선택 및 pyrG 카운터 선택의 손실)을 사용하여 분리될 수 있다. 도 36의 우측 열은 돌연변이 및 하나 이상의 선택 가능한 마커(예를 들어, 항생제 내성 유전자(ampR) 및 영양 요구성 마커 유전자 (pyrG))를 갖는 표적 유전자의 복제물을 포함하는 구조체와 루프-인 단일 크로스 오버 이벤트를 사용하여 표적 유전자(예를 들어, aygA)에서 돌연변이(예를 들어, SNP)의 통합의 예를 도시한다.
라이브러리 생성
본 발명의 다른 양태는 균류 돌연변이 라이브러리 및 본 발명에 개시된 방법에 의해 제조된 곰팡이 돌연변이 라이브러리의 제작 및 선별을 포함할 수 있다. 도 5에 도시된 바와 같이, 균류 라이브러리는 균류 균주를 제작하기 위한 플랫폼에 혼입될 수 있다. 라이브러리는 당업자에게 공지된 방법을 사용하여, 임의의 통합 형질전환 수단으로 본 발명에 따른 균류 숙주의 형질전환에 의해 수득될 수 있다. 본 발명에 제공된 방법 및 시스템을 사용하여 생성된 바람직한 숙주 균주에 기초한 균류의 라이브러리는 소형화 및/또는 고효율 포맷 선별 방법에서 외인성 단백질의 원하는 특성 또는 활성에 대해 처리 및 선별될 수 있다. 관심 특성 또는 활성은 라이브러리 멤버의 외인성 단백질과 관련된 임의의 물리적, 물리화학적, 화학적, 생물학적 또는 촉매적 특성, 또는 이런 특성의 향상, 증가 또는 감소를 의미할 수 있다. 라이브러리는 또한 외인성 및/또는 내인성 단백질의 존재로 인해 생산되는 대사산물 또는 대사산물과 관련된 특성 또는 활성에 대해 선별될 수 있다. 라이브러리는 또한 이런 단백질 또는 대사산물의 증가된 또는 감소된 양을 생산하는 균류에 대해 선별될 수 있다.
한 실시태양에서, 본 발명에 제공된 방법 및 시스템은 복수의 원형질체를 생성하여 복수의 원형질체로부터 각각의 원형질체가 복수의 제 1 구조체로부터의 단일의 제 1 구조체로 변형되고 복수의 제 2 구조체로부터의 단일의 제 2 구조체로 형질전환된다. 이 실시태양에 더하여, 복수의 제 1 구조체로부터의 각각의 제 1 구조체 내의 제 1 폴리뉴클레오타이드는 상이한 돌연변이 및/또는 유전자 제어 또는 조절 요소를 포함하는 반면, 복수의 제 2 구조체로부터 각각의 제 2 구조체의 제 2 폴리뉴클레오타이드는 동일하다. 상기 방법은 사상균류 세포의 라이브러리를 생성하기 위해 2회 이상 본 발명에 기술된 바와 같은 선택/카운터 선택을 사용하여 동핵성 형질전환체를 형질전환 및 정제하는 단계를 더 포함하여 라이브러리 내의 각각의 사상균류 세포가 상이한 돌연변이 및/또는 유전자 제어 또는 조절 요소를 갖는 제 1 폴리뉴클레오타이드를 포함한다. 한 실시태양에서, 제 1 폴리뉴클레오타이드는 표적 사상균류 유전자 또는 돌연변이를 포함하는 이종성 유전자에 대한 서열을 포함하여 반복 과정이 원형질체의 재생시에 사상균류 세포의 라이브러리를 생성하여 라이브러리의 각 멤버가 표적 사상균류 유전자 또는 별개의 돌연변이가 있는 이종성 유전자를 포함한다. 본 발명에 기술된 바와 같이, 제 1 폴리뉴클레오타이드는 하나 이상의 구조체 사이에서 분할되어 각각의 구조체는 숙주 유기체 내로 도입될 때 구조체 사이의 상동 재조합을 용이하게 하기 위해 제 1 폴리뉴클레오타이드의 중첩 부분을 포함할 수 있다. 또한, 제 1 폴리뉴클레오타이드의 중첩 부분을 포함하는 각각의 구조체는 재조합 제 1 폴리뉴클레오타이드의 원하는 유전자좌 내로의 통합을 용이하게 하기 위해 숙주 게놈에서 원하는 유전자좌와 상동성인 서열을 추가로 포함할 수 있다. 한 실시태양에서, 돌연변이는 SNP이고, 따라서 상기 방법은 SNPSwap 라이브러리를 생산한다. 한 실시태양에서, 표적 사상균류 유전자는 시트르산 생산에 관여하는 유전자이고 복수의 제 1 구조체는 표 4에 제공된 SNP의 라이브러리이다. 다른 실시태양에서, 제 1 폴리뉴클레오타이드는 유전자 제어 또는 조절 요소에 작동 가능하게 연결된 표적 사상균류 유전자 또는 이종성 유전자에 대한 서열을 포함하여 본 발명에 기술된 반복 과정이 원형질체의 재생시에 사상균류 세포의 라이브러리를 생성하여 라이브러리의 각 멤버가 별개의 유전자 제어 또는 조절 요소에 작동 가능하게 연결된 표적 사상균류 유전자 또는 이종성 유전자를 포함한다. 한 실시태양에서, 유전자 제어 또는 조절 요소는 프로모터이고 따라서 상기 방법은 프로모터 또는 PRO 라이브러리를 생산한다. 한 실시태양에서, 유전자 제어 또는 조절 요소는 터미네이터이며 따라서 상기 방법은 터미네이터 또는 STOP 라이브러리를 생산한다. 프로모터 및/또는 터미네이터 서열은 본 발명에 제공된 방법 및 시스템에서 사용되는 사상균류 숙주 세포에서의 발현을 위해 본 발명에 제공되거나 및/또는 당업계에 공지된 프로모터 또는 터미네이터 서열일 수 있다. 한 실시태양에서, 프로모터는 유도성 프로모터이다.
A. 니거에서 시트르산 생산에 잠재적으로 관여하는 SNP
|
돌연변이 명칭
|
위치
|
서열 변화
|
배향
|
Contig
|
설명
|
암호화 도메인에서
SNP
|
형태학적 표현형
|
| FungiSNP_01 |
50669-680224 |
~>~ |
680224 |
chr_1_1 |
|
|
|
| FungiSNP_02 |
1172974 |
G>A |
+ |
chr_1_1 |
방향족 아미노산 아미노트랜스페라제 및 관련 단백질 |
X |
|
| FungiSNP_03 |
367948 |
C>T |
+ |
chr_1_2 |
|
|
|
| FungiSNP_04 |
549014 |
C>G |
- |
chr_1_2 |
|
|
|
| FungiSNP_05 |
1330718 |
G>A |
+ |
chr_1_2 |
|
|
|
| FungiSNP_06 |
662258 |
G> |
+ |
chr_2_1 |
타우린 이화작용 다이옥시다아제 TauD/TfdA |
X |
|
| FungiSNP_07 |
673547 |
G>A |
- |
chr_2_1 |
알파/베타 하이드롤라제 |
X |
|
| FungiSNP_08 |
946654 |
T> |
+ |
chr_2_1 |
|
|
|
| FungiSNP_09 |
641661 |
T>A |
- |
chr_2_2 |
수도우리
딜레이트 합성효소 활성 |
X |
X |
| FungiSNP_10 |
2316591 |
G>A |
+ |
chr_2_2 |
|
|
|
| FungiSNP_11 |
935908 |
A>G |
- |
chr_3_1 |
세린/트레오닌 단백질 키나아제 |
X |
|
| FungiSNP_12 |
205638 |
T>A |
+ |
chr_3_2 |
전사 인자 |
X |
X |
| FungiSNP_13 |
268107 |
T>C |
+ |
chr_3_3 |
|
|
|
| FungiSNP_14 |
186943 |
A>T |
+ |
chr_3_4 |
|
|
|
| FungiSNP_15 |
276232 |
C>T |
+ |
chr_3_4 |
|
|
|
| FungiSNP_16 |
1287891 |
T>C |
- |
chr_4_1 |
세린/트레오닌 단백질 키나아제 |
X |
|
| FungiSNP_17 |
1639965 |
A>T |
+ |
chr_4_1 |
|
|
|
| FungiSNP_18 |
1826343 |
G>A |
- |
chr_4_1 |
감각 변환 히스티딘 키나아제 |
X |
X |
| FungiSNP_19 |
1358794 |
C>A |
+ |
chr_4_2 |
|
|
|
| FungiSNP_20 |
1466380 |
CTA> |
+ |
chr_4_2 |
만니톨-1-포스페이트-5-디하이드로지나아제 |
X |
|
| FungiSNP_21 |
1700330 |
C>A |
- |
chr_4_2 |
토모신 및 관련 SNARE-상호작용 단백질 |
X |
|
| FungiSNP_22 |
2873296 |
A>G |
+ |
chr_4_2 |
|
|
|
| FungiSNP_23 |
815022 |
G>A |
+ |
chr_5_2 |
알려지지 않은 기능 |
X |
|
| FungiSNP_24 |
831672 |
G>A |
- |
chr_5_2 |
사이토크롬 c 헴(heme)
결합 위치 |
X |
|
| FungiSNP_25 |
1507652 |
>A |
+ |
chr_5_2 |
|
|
|
| FungiSNP_26 |
442488 |
T>C |
+ |
chr_6_1 |
|
|
|
| FungiSNP_27 |
93202-103239 |
~>~ |
+ |
chr_6_2 |
|
|
|
| FungiSNP_28 |
972833 |
A>T |
+ |
chr_6_2 |
|
|
|
| FungiSNP_29 |
972932 |
A> |
+ |
chr_6_2 |
|
|
|
| FungiSNP_30 |
1183094 |
G> |
+ |
chr_6_2 |
조효소 Q (유비퀴논)
생합성에 관여하는 모노옥시다아제 |
X |
|
| FungiSNP_31 |
1701762 |
T>G |
+ |
chr_6_2 |
|
|
|
| FungiSNP_32 |
236406 |
G>A |
- |
chr_7_1 |
세포외 알려지지 않은 기능 |
X |
|
| FungiSNP_33 |
2350056 |
A> |
+ |
chr_7_1 |
|
|
|
| FungiSNP_34 |
375013 |
C>T |
+ |
chr_8_1 |
|
|
|
| FungiSNP_35 |
1272037 |
C>T |
+ |
chr_8_1 |
|
|
|
| FungiSNP_36 |
281612 |
T>C |
+ |
chr_8_2 |
알려지지 않은 기능 |
X |
|
| FungiSNP_37 |
565087 |
A>G |
+ |
chr_8_2 |
|
|
|
| FungiSNP_38 |
865958 |
A> |
+ |
chr_8_2 |
|
|
|
| FungiSNP_39 |
947633 |
A> |
+ |
chr_8_2 |
|
|
|
| FungiSNP_40 |
2482267 |
G>A |
+ |
chr_8_2 |
특징화되지 않은 보존성 코일드-코일 단백질(coiled-coil protein) |
X |
X |
| FungiSNP_41 |
2486601 |
G> |
+ |
chr_8_2 |
마그네슘 의존성 포스파타제 |
X |
|
| FungiSNP_42 |
2709491 |
T>C |
+ |
chr_8_2 |
|
|
|
| FungiSNP_43 |
2708043 |
>A |
~ |
chr_8_2 |
GTPase-활성 단백질 |
X |
|
실시예
하기 실시예는 본 발명의 다양한 실시태양을 설명하기 위해 제공되며 어떠한 방식으로든 본 발명을 제한하려는 것은 아니다. 청구항의 범위에 의해 정의된 바와 같이, 본 발명의 취지 내에 포함되는 변경 및 다른 용도는 당업자에 의해 인식될 것이다.
아래에서 단지 독자를 돕기 위해 내용의 간략한 표(즉, 표 5)가 제공된다. 이런 표의 내용의 어떤 것도 본 출원의 실시예 또는 설명의 범위를 제한하지 않는다.
실시예 부분에 대한 내용의 표
|
실시예
#
|
제목
|
간략한 설명
|
|
1
|
사상균류의 HTP 게놈 공학: 사상균류 원형질체의 생성 및 저장 |
HTP 게놈 공학 방법에 사용하기 위한 원형질체 생성 및 저장 방법을 기술한다 |
|
2
|
사상균류의 HTP 게놈 공학: 형질전환체를 생성하는 대안적인 방법 |
HTP 게놈 공학 방법에 사용하기 위한 원형질체 생성을 위한 대체 방법 기술한다 |
|
3
|
사상균류의 HTP 게놈 공학: 사상균류 원형질체의 동시 형질전환의 입증 - 개념 증명 |
사상균류의 HTP 공동형질전환에 대한 원리 증명을 기술한다 |
|
4
|
사상균류의 HTP 게놈 공학: 사상균류 원형질체의 공동 형질전환의 증명-비색 선택/카운터 선택을 이용하는 개념 증명 |
사상균류 원형질체에서 선택/카운터 선택을 사용하기 위한 원리 증명을 위한 HTP 방법을 기술한다 |
|
5
|
사상균류의 HTP 게놈 공학 - 진핵생물 아스퍼길루스 니거 ATCC11414에서 시트르산 생산을 개량시키는 HTP SNP 라이브러리 균주 개량 프로그램의 실행 |
A. 니거의 SNP 라이브러리 균주 개선 프로그램에 대한 HTP 방법을 기술한다 |
|
6
|
사상균류의 HTP 게놈 공학: 상이한 유전적 배경을 갖는 사상균류에서 SNP를 검출하는 차세대 서열 분석(NGS)의 능력의 입증 |
사상균류에서 SNP를 검출하기 위해 NGS를 사용하는 방법을 기술한다 |
|
7
|
사상균류의 HTP 게놈 공학: 사상균류에서 SNPSWP를 검출하는 차세대 서열 분석(NGS)의 능력의 입증 |
사상균류에서 SNPSWP를 검출하기 위해 NGS를 사용하는 방법을 기술한다 |
|
8
|
사상균류의 HTP 게놈 공학: 사상균류 원형질체의 공동 형질전환의 입증-원리의 추가 증거 |
여러 구조체에 걸쳐 마커 및 원하는 유전자 돌연변이 분할과 함께 사상균류의 HTP 공동형질전환을 기술한다 |
|
9
|
Cas9 리보핵산 단백질(RNP) 형질전환을 사용하는 사상균류의 비-상동성 말단 결합(NHEJ) 및 HR-매개 게놈 편집은 원하는 편집을 위한 직접적인 선택 없이 SNP, 삽입 및 인델(indel)을 가능하게 한다 |
사상균류, 예를 들어, A. 니거를 편집하기 위한 RNA 가이드된 엔도뉴클레아제의 이용을 기술한다 |
|
10
|
PAM 부위를 스크램블링하지 않고 단일 SNP를 도입하기 위해 Cas9 리보핵산단백질(RNP) 형질전환을 사용하는 사상균류의 HR-매개 게놈 편집 |
사상균류, 예를 들어, A. 니거를 편집하기 위한 DNA 가이드된 뉴클레아제의 이용을 기술한다 |
|
11
|
접시에서 형질전환된 균류 균주의 클론 집단으로의 정제 |
형질전환 후 포자의 자동 분리를 통해 균일한 유전자형으로 균류을 정제하는 HTP 방법을 기술한다 |
|
12
|
사상균류의 HTP 게놈 공학: 사상균류 형태에 영향을 미치는 유전자의 확인 |
심층 CAP 배양에서 비-균사, 펠렛 표현형으로 사상균류 균주를 생성하는 SNP 교환 방법을 기술한다 |
|
13
|
사상균류의 HTP 게놈 공학: 사상균류 형태학에서 역할 하는 확인된 유전자의 역할 확인 - 확인된 형태 대조군 유전자의 결실 |
추정 형태학적으로 관련된 유전자를 녹아웃하여 심층 CAP 배양에서 사상균류 균주의 형태에 역할을 하는 확인 유전자를 기술한다 |
|
14
|
사상균류의 HTP 게놈 공학: 유전자 발현을 변경하여 사상균류 세포 형태를 변경함으로써 사상균에서 PROSWP의 시연 |
추정 형태학적으로 관련된 유전자의 발현을 제어하기 위해 사상균류에서 이용되는 PROSWP 라이브러리를 기술한다 |
실시예
1: 사상균류의
HTP
게놈 공학: 사상균류 원형질체의 생성 및 저장
원형질체의 생성
도 20a에 도시된 바와 같이, 100밀리리터의 완전 배지를 106 conidia/ml의 아스퍼길루스 니거로 접종하고 30℃에서 150rpm으로 밤새 성장시켰다. 밤새 성장 이후, 균사체를 미라클로스를 통해 배양액을 여과함으로써 회수하였다. 이어서, 균사체를 멸균수로 완전히 헹구었다. 다음의 실시예에서 기술된 실험을 위해, 두 개의 A. 니거 균주, A. 니거 균주 1015 및 A. 니거 균주 11414를 사용하였다. 그 후 회수하고 세척된 균사체를 VinoTaste Pro(VTP) 효소 칵테일로 효소 분해하였다. 각 균주의 특징은 도 43에 도시된다.
A. 니거 균주 1015에 대하여, 효소 분해는 원형질체 완충액(1.2M 황산 마그네슘, 50mM 인산염 완충액, pH 5) 속 60mg/ml의 VTP 50ml를 먼저 제조함으로써 수행하였다. VTP를 용해시킨 후, 완충액을 깨끗한 오크리지(Oakridge) 튜브에 넣고 15,000 x g에서 15분 동안 회전시켰다. 그런 후에 용액을 원심 분리 후 필터 멸균하였다. 완료된 후, 회수된 균사체의 일부를 VTP 용액에 첨가하고 균사체를 2~4시간 동안 30℃에서 80rpm에서 분해시켰다. VTP 분해 동안 다양한 간격으로, 작은 샘플을 원형질체(즉, 분생자보다 크고 삼투압 용해에 민감한 대형 원형 세포)의 존재에 대해 400배 배율로 검사하였다. 균사체의 대부분 또는 전부가 분해될 때, 배양액을 멸균된 미라클로스를 통해 여과하여 원형질체를 함유하는 25ml의 플로우-스루(flow-through)를 2개의 50ml 팔콘 튜브의 하나에 분리시켰다. 각 25ml 샘플에, 5ml의 0.4M ST 완충액(0.4M 소르비톨, 100mM 트리스, pH 8)을 부드럽게 덮었다. 그런 후에, 덮여진 샘플을 ST와 소화 완충액 사이에 가시 층을 형성하기 위해 4℃에서 15분 동안 800 x g에서 회전시켰다. 그런 후에 원형질체를 피펫으로 제거하고 25ml의 ST 용액(1.0M 소르비톨, 50mM 트리스, pH 8.0)과 부드럽게 혼합하고 10분 동안 800 x g에서 재회전시켰다. 원형질체를 튜브의 바닥에 펠렛화해야 한다. 그런 후에 원형질체를 25ml의 ST 용액에 재현탁시킨 다음, 10분 동안 800 x g에서 원심분리하여 수집하였다.
A. 니거 균주 11414에 대해, 효소 분해는 원형질체 완충액(0.6M 황산 암모늄, 50mM 말레산, pH 5.5) 속 30mg/ml의 VTP 40ml를 먼저 제조함으로써 수행하였다. 회수된 균사체의 전부를 VTP 용액에 첨가하고 균사체를 3~4시간 동안 70rpm에서 30℃로 분해시켰다. VTP 분해 동안 다양한 간격으로, 작은 샘플을 원형질체의 존재에 대해 400배 배율로 검사하였다. 균사체의 대부분 또는 전부가 분해될 때, 배양액을 멸균된 미라클로스를 통해 여과하였다. 그런 후에 여과액을 4℃에서 10분 동안 800 x g으로 회전시켜 세포를 펠렛화하였다. 25ml의 ST 용액(1.0M 소르비톨, 50mM 트리스, pH 8.0)을 첨가하고 세포를 재현탁시키고 재회전시켰다. 그런 후에 세포를 10ml의 STC 완충액(1.0M 소르비톨, 50mM 트리스, pH 8.0, 50mM CaCl2)에서 세척하고 10분 동안 800 x g에서 원심분리하여 수집하였다. 원형질체(~108/ml)를 계수하고 1.2 x 107/ml로 조정하였다.
효소 분해 이후, A. 니거 균주(즉, 1015 또는 11414)로부터 생성된 원형질체에 대해, 20% v/v의 40% PEG 용액(STC 완충액 속 40% PEG-4000)을 원형질체에 첨가하고 부드럽게 혼합하고 7% v/v의 다이메틸 설폭사이드(DMSO)를 첨가하여 8% PEG/7% DMSO 용액을 제조하였다. 재현탁 이후, 원형질체를 도 20a에 나타낸 바와 같이 자동화 액체 핸들러를 사용하여 96웰(25-50 마이크로리터) 미세적정 플레이트에 분배하고 형질전환 이전에 적어도 -80℃에서 저장하였다.
실시예
2: 사상균류의
HTP
게놈 공학: 형질전환체를 생성하는 대안적인 방법
도 27에 도시된 바와 같이, 500 밀리리터의 완전한 배지에 106 conidia/ml의 아스퍼길루스 니거를 접종하고 300℃에서 150 rpm으로 밤새 성장시켰다. 밤새 성장한 후, 미라클로스를 통해 배양액을 여과하여 균사체를 수확하였다. 이어서, 균사체를 멸균수로 철저히 헹구었다. 이어서, 수거 및 세척된 균사체를 VinoTaste Pro (VTP) 효소 칵테일로 효소 분해시켰다.
효소 분해는 원형질체화 완충제(1.2M 황산 마그네슘, 50mM 포스페이트 완충제, pH 5)에서 60ml/ml의 VTP 50ml를 먼저 제조함으로써 수행되었다. VTP를 용해시킨 후, 완충액을 깨끗한 오크리지 튜브에 넣고 15분 동안 15,000 x g에서 회전시켰다. 이어서, 용액을 원심 분리 후 여과 멸균하였다. 일단 만들어지면, 수확된 균사체의 일부를 VTP 용액에 첨가하고 균사체를 300℃에서 80rpm에서 2~4시간 동안 분해시켰다. VTP 분해 동안 다양한 간격으로, 작은 샘플을 원형질체(즉, 원뿔보다 크고 삼투 용해에 민감한 큰 원형 세포)의 존재에 대해 400배 확대하에 검사하였다. 균사체의 대부분 또는 전부가 분해되었을 때, 배양액을 멸균 미라클로스를 통해 여과하고 여과액을 눈금 실린더로 수집하였다. 여과된 원형질체를 눈금 실린더로 옮기고, 낮은 삼투압 농도의 완충액(0.4M ST 완충액 (0.4M 소르비톨, 100mM 트리스, pH 8) 5ml)을 부드럽게 중첩시켰다. 그런 후에, 중첩된 샘플을 4℃에서 15분 동안 800 x g에서 회전시킨 후 원형질체를 피펫으로 제거하고 25ml의 ST 용액(1.0M 소르비톨, 50mM 트리스, Ph 8.0)과 부드럽게 혼합하고 10분 동안 800 x g에서 다시 회전시켰다. 그런 후에 원형질체를 ST 용액 25ml에 재현탁시키고 800 x g에서 10분 동안 원심 분리하여 수집하였다.
실시예
3: 사상균류의
HTP
게놈 공학: 사상균류 원형질체의 동시 형질전환의 입증 - 개념 증명.
표적 DNA의 준비
도 20a-c에 도시된 자동화 사상균류 형질전환 및 선별 방법에 대한 개념 증명(POC)을 제공하려는 노력에서, 아스퍼길루스 니거 argB 유전자의 DNA 서열을 얻었고 적절한 판독 프레임을 결정하였다. 한 세트의 SNP는 A. 니거 게놈의 argB 유전자좌 내로 상기 SNP의 임의의 것의 유전자의 통합이 argB 유전자의 무효 돌연변이를 일으킬 수 있도록 디자인되었다. 이 디자인은 깁슨 어셈블리를 사용하여 구조체를 제조하는데 사용된 올리고머 세트를 예측한 인 실리코 구조체로서 생성되었다.
원형질체의 자동화 형질전환
실시예 1에서 기술된 바와 같이 생성되고 96웰 플레이트(100 마이크로리터 원형질체/웰)에 저장된 A. 니거 균주 1015로부터 유래된 원형질체에 자동화 액체 핸들러를 사용하여 전통적인 PEG 칼슘 매개 형질전환을 적용하여 SNP DNA 구조체를 96웰 플레이트에 원형질체-PEG/DMSO 혼합물과 결합시켰다. 보다 구체적으로, 100 마이크로리터의 원형질체에, 1 내지 10 마이크로그램의 SNP DNA 구조체(10 마이크로리터 이하의 부피로)를 첨가하고 혼합물을 15분 동안 얼음 상에서 배양하였다. 이 혼합물에, 1ml의 40% PEG를 첨가하고 실온에서 15분 동안 배양하였다. 이어서, 10ml 최소 배지 + 1M 소르비톨을 첨가하고 30℃에서 1시간 동안 80rpm에서 진탕시켰다. 이런 배양 후, 원형질체를 5분 동안 800 x g에서 회전시킨 다음 1M 소르비톨 및 0.8% 한천을 함유하는 12ml의 최소 배지에 재현탁시켰다. 다음날, 추가의 자동화 액체 처리 단계를 사용하여, 원형질체를 선택적 배지(즉, 최소 배지 + 아르기닌) 및 비 선택적 배지(즉, 최소 배지)에 플레이트하였다. 자동화 형질전환 프로토콜로 생성된 원형질체의 성공적인 형질전환은 아르기닌에 대한 영양요구성일 것이고 따라서 SNP 구조체에 의한 argB 유전자의 표적화로 인해 아르기닌이 결핍된 최소 배지에서 성장하지 않을 것으로 예상된다.
도 21에 도시된 바와 같이, 약 3%의 형질전환체를 아르기닌이 결핍된 최소 배지에서 성장의 결핍에 의해 입증되는 정확한(즉, argB) 유전자좌에서 표적 DNA 구조체의 통합을 나타내었다. 정확한 유전자좌에 구조체를 함유하는 SNP의 통합의 확인은 차세대 서열화를 통해 확인될 것이다.
실시예
4: 사상균류의
HTP
게놈 공학: 사상균류 원형질체의 공동 형질전환의 증명-비색 선택/카운터 선택을 이용하는 개념 증명.
이 실시예는 사상균류 세포의 자동화 HTP 공동 형질전환에 대한 추가적인 개념 증명을 입증하며 원하는 형질전환체의 분리를 위한 선택/카운터 선택의 사용을 추가로 입증한다.
아스퍼길루스
니거
원형질체 형성 및 형질전환
아스퍼길루스 니거의 진핵생물 균류 균주, ATCC 1015의 대량(500ml)의 원형질체를 실시예 1에 기술된 바와 같이 베타-글루카나아제 활성을 함유하는 상업적으로 구입가능한 효소 혼합물을 사용하여 생성시켰다. 원형질체를 원심분리에 의해 효소 혼합물로부터 분리하였고 궁극적으로 실시예 1에 기술된 방법에 의해 염화칼슘을 함유하는 완충액에 재현탁시켰다.
실시예 1에 기술된 바와 같이 원형질체를 분취하고 다이메틸 설폭사이드 및 폴리에틸렌 글리콜(PEG)의 현탁액을 함유하는 용기에서 영하 80℃로 동결시켰다. 일부 실시태양에서, 본 발명은 각 웰에서 25-50 마이크로리터의 원형질체를 함유하는 96-웰 미세적정 플레이트의 원료가 이 기술을 사용하여 대규모 게놈 편집 캠페인을 위한 큰 배치로 제조되고 동결시킬 수 있음을 교시한다.
전통적인 PEG 칼슘 매개 형질 전환은 96 웰 내의 원형질체-PEG 혼합물과 DNA를 조합한 자동화 액체 핸들러에 의해 수행되었다. 추가적인 자동화 액체 처리 단계를 사용하여 변형 후 선택적 배지로 형질전환시켰다.
형질전환체의 자동화된 선별
하기에 보다 상세히 설명하는 바와 같이, 기능성 pyrG 유전자가 결여된 이 실시예(즉, pyrG-)에서 사용된 A. 니거 세포는 우라실의 부재하에서 형질전환된 세포가 성장할 수 있게 하는 기능적 pyrG 유전자로 형질전환되었다. 도 23a-b에 도시된 바와 같이, 이 실시예의 pyrG 유전자는 A. 니거의 야생형 met3 유전자의 위치에 포함되도록 추가로 디자인되어, 자연 발생 met3 유전자에 대한 파괴를 포함시켰다. met3 유전자를 파괴하면 메티오닌 영양요구주가 되는 돌연변이체를 추가로 생성하여, 형질전환체를 확인하기 위한 2차 선별 방법을 제공한다.
우라실 없는 선택 배지 상에서 성장한 형질전환체를 분리하고 제 2 미세적정 플레이트의 개별 웰에 넣었다. 제 2 미세적정 플레이트의 형질전환체를 2 내지 3일 동안 성장시키고 포자성화시킨 다음, 물 및 소량의 세제로 이루어진 액체에 재현 탁시켜 저장 및 하류 자동화 선별에 적합한 포자 원료를 생성시켰다.
상기한 포자 원료의 각각의 작은 분취액을 사용하여 액체 배지를 제 3 96개 웰 PCR 플레이트에 접종하였다. 이 작은 배양물은 밤새 고정 배양기에서 성장되어 노란색-색소 함유 포자가 발아하여 선택 및 하류 단계에 보다 잘 적응하는 균사를 형성한다.
배양 단계 후, 제 3 PCR 플레이트의 균사를 상업적으로 구입 가능한 완충액을 첨가하고 99℃까지 20분 동안 배양물을 가열하여 용해시켰다. 그런 후에 플레이트를 원심분리하여 세포/세포기관 펠렛으로부터 DNA 현탁액 상등액을 분리하였다. 그런 후에 DNA 추출물을 PCR 분석에 사용하여 원하는 DNA 돌연변이를 포함하는 세포주를 확인하였다.
SNP의 통합을 위한 공동 형질전환-SNP의 디자인
아스퍼길루스 니거 유전자 aygA의 DNA 서열을 수득하고 적절한 판독 프레임을 결정하였다. 4개의 구별된 유형의 돌연변이가 디자인되었고, 통합되면 널 돌연변이(null mutation)가 일어날 수 있다.
돌연변이는 프레임 내 정지 코돈, 작은 2개의 염기쌍 결실, 3개의 염기쌍 통합 및 더 큰 100개 염기쌍 결실을 포함하는 단일 염기쌍 변화를 포함하고 이들 모두는 적절하게 통합되면 aygA 활성을 제거할 것이다. aygA 활성이 결핍된 균주는 황색 포자의 표현형을 갖는다. 이 디자인은 깁슨 어셈블리를 사용하여 구조체를 만드는데 사용된 한 세트의 올리고머를 예측하는 인 실리코 구조체로서 생성되었다.
공동-형질질환에 의한 SNP의 통합
상기한 형질전환 접근법을 사용하여, 작은 변화를 함유하는 앰플리콘을 아스 페르길루스 니거 균주 1015의 게놈에 포함시켰다. 이전에 논의된 바와 같이, 아스 페르길루스 니거의 균주는 비 기능성 pyrG 유전자를 포함하고, 따라서 외인성 우라실의 부재시에 성장할 수 없었다. pyrG 유전자를 성공적으로 통합한 세포는 이제 우라실의 부재시에 성장할 수 있었다. 이 pyrG+ 형질전환체 중, aygA 유전자에 작은 돌연변이가 통합된 분리물은 황색 포자의 표현형을 나타내었다.(도 22 및 23a 참조). 돌연변이의 존재는 SNP 교환을 표적으로 하는 영역을 함유하는 작은 앰플리콘의 서열화를 통해 또한 탐지된다(도 23b).
실시예
5: 사상균류의
HTP
게놈 공학 - 진핵생물
아스퍼길루스
니거
ATCC11414에서 시트르산 생산을 개량시키는
HTP
SNP 라이브러리 균주 개량
프로그
램의 실행
상기 실시예 3은 고 처리량 방식으로 본 발명의 유전자 공학 기술을 자동화하는 기술을 기술한다. 이 실시예는 아스퍼길루스 니거 ATCC11414의 특정 HTP 균주 개량에 상기 기술을 적용한다.
아스퍼길루스 니거는 발효를 통한 시트르산의 대규모 생산에 사용되는 사상 균류의 종이다. 이 종의 여러 균주는 분리되어 시트르산 및 기타 유기산의 생산을 위한 다양한 능력을 갖는 것을 입증되었다. 본 발명의 HTP 균주 공학 방법은 원인성 대립 유전자를 조합하고 유해한 대립 유전자를 제거하여 시트르산 생산을 개량시키는데 사용될 수 있다.
천연 A.
니거
균주
변이체로부터의
SNP를 위한 유전자 디자인 라이브러리의 확인.
A. 니거 균주 ATCC 1015는 20세기 초반에 시트르산 생산자로 확인되었다. ATCC 11414로 명명된 이 균주의 분리물은 부모에 비해 증가된 시트르산 수율을 나타내는 것으로 이후에 밝혀졌다(도 43 참조). 예를 들어, A. 니거 균주 ATCC 1015는 질산 암모늄을 함유하지만 철 및 망간 양이온이 결핍된 배지에서 140g의 글루코오스로부터 7g의 시트르산을 평균적으로 생산한다. 한편, 분리물 균주 ATCC 11414는 동일한 조건 하에서 10배의 수율 증가(70g의 시트르산)를 나타내었다. 더욱이, 균주 ATCC 11414 포자는 발아되어 1015 균주의 포자보다 시트르산 생산 배지에서 더 잘 자란다.
이들 표현형 차이에 대한 잠재적인 유전자 원인을 확인하기 위해, ATCC 1015 및 ATCC 11414 균주 모두의 게놈을 서열화하고 분석하였다. 최종 분석은 1015 및 11414 균주를 구별하는 43개의 SNP를 확인하였다(즉 표 4).
원인성 대립 유전자 교환
원형질체는 실시예 1에 기술된 바와 같이 형질전환을 위해 ATCC 1015 균주("기본 균주")로부터 제조하였다. 그런 후에 상기한 43개 SNP의 각각을 본 발명의 유전자 편집 기술을 통해 기본 균주 속에 개별적으로 도입하였다(도 24 참조). 각 SNP는 상기한 바와 같이 기능적 pyrG 및 aygA 유전자 돌연변이와 함께 형질전환되었다. aygA 유전자좌를 표적으로 하는 성공적인 유전자를 갖는 형질전환체는 황색 포자를 생산하였다(도 24).
성공적인 통합을 위한 선별
추정 SNP를 함유하는 형질전환체를 분리하고 포자 원료를 상기한 바와 같이 증식시켰다. 추정 SNP를 함유하는 DNA 영역을 포함하는 앰플리콘을 차세대 서열화로 분석하였다. 이 접근법을 사용하여 부모 DNA의 존재하에서도 각 형질전환체 내에서 성공적인 통합 사건을 결정할 수 있다. 이 능력은 동일한 세포에서 상이한 유전자형을 갖는 핵을 포함하는 이핵체(heterokaryon)로서 성장할 수 있는 곰팡이에서의 표적을 결정하는데 필수적이다.
형질전환체를 원하는 SNP 변화의 존재에 대해 추가로 확증하였다. 황색 포자의 표현형을 가진 공동 형질전환체는 또한 대략 30%의 분리물에 시트르산 SNP의 적절한 통합을 함유하였다(도 25 및 26).
다음으로, 생성된 SNP 스왑 미생물 균주 라이브러리를 표현형적으로 선별하여 시트르산 생산에 유익한 SNP를 확인할 것이다. 이 정보는 증가된 구연산 생성을 갖는 A. 니거 균주를 유도하기 위해 본 발명에 기술된 게놈 공학의 HTP 방법과 관련하여 이용될 것이다.
실시예
6:
사상균류의
HTP
게놈 공학: 상이한 유전적 배경을 갖는 사상균류에서 SNP를 검출하는 차세대 서열 분석(
NGS
)의 능력의 입증.
이 실시예는 NGS가 어떻게 표적 유전자 부모 균주의 특정 배경에서 표적 유전자 돌연변이를 검출하는 데 사용될 수 있는지의 예를 입증한다.
서열 기반 선별 대 표현형 선별의 감수성을 테스트하기 위해, 표적 유전자 (또는 테스트 도메인)에서 단일 SNP에 의해 상이한 한 쌍의 균주를 공지된 비율로 혼합하고 96-웰 미세적정 플레이트에서 성장시켰다. 사용된 균주는 부모 균주(pyrG-, met +, (P)) 및 돌연변이 균주(pyrG +, met-, (M))이었다. 부모 균주 포자는 최소 배지(MM)에서 자랄 때 검은색 또는 어두운 색으로 나타나고, 돌연변이 균주 포자는 MM에서 자랐을 때 노란색 또는 밝은 색으로 나타낸다. 테스트된 P:M의 비는 1:0, 10:1, 5:1, 1:1, 1:5, 1:10, 및 0:1이었다. 도 33에 도시된 바와 같이, 우라실이 보충되고(+UU) 메티오닌이 없는(-met) MM에 플레이트되었을 때, 부모 포자(P)만 자라는 반면, 돌연변이 포자(M)만이 met을 가지며(+met) 우라실이 없는(-UU) MM에서 자란다. 도 33 및 도 34의 상단의 플레이트에 도시된 바와 같이, +UU 및 +met인 MM 상에 플레이트될 때, P 및 M 포자 모두 성장되어 가장 낮은 비(1:10)의 P/M 포자 조차도 가장 높은 비(10:1) P/M 포자와 시작적으로 동일한 검은 색 콜로니를 생산하였다. 다시 말해서, aygA 유전자(M 포자)에서의 단일 염기쌍 돌연변이는 황색 포자의 존재를 초래하고; 그러나, 부모 aygA 유전자(P 포자)를 함유하는 단지 몇 개의 핵의 존재는 검은 포자를 함유하는 콜로니를 초래하였다. 따라서, 표현형 선별을 통해 돌연변이 유전자를 보유함에 따라 비 선택적 배지에서 소량의 부모 포자를 갖는 콜로니에 점수를 매기는 것은 어려웠다. 다시 말해, 돌연변이의 존재는 심지어 적은 수의 부모 유전자의 복제물에 의해 가려져서 사상균류 숙주에서 표현형 선별의 한계를 강조한다.
표현형 선별의 한계를 해결하기 위해, 표적 유전자 돌연변이의 존재를 도 33의 96 웰 플레이트의 각 웰에서 NGS 서열 분석을 사용하여 평가하였다. 여기서, 도 33에 사용된 테스트 도메인에서 단일 SNP에 의해 상이한 균주 쌍으로부터의 핵산은 본 발명에 기술된 비등 제조 방법을 사용하고 있었다. DNA 추출을 96-웰 미세적정 플레이트 포맷으로 수행하여 복제 플레이트를 도 33의 플레이트로부터 생성하여 DNA 추출은 복제 플레이트의 각 웰에서 수행하고 분리된 DNA를 자동 액체 처리 시스템(예를 들어, 애질런트 브라보 시스템)을 사용하여 추가 미세적정 플레이트로 옮기고, 여기서 Illumina 기반 서열 분석(NGS 서열 분석)을 각 웰에서 수행하였다. 도 34에 도시된 바와 같이, NGS 서열 분석은 부모 및 돌연변이 DNA뿐만 아니라 이들의 혼합물의 존재를 검출할 수 있었으며, 이로써 NGS 데이터는 동일한 샘플에서 단일 염기쌍 변화의 혼합물을 명확하게 보여 주었다. 도 33 및 34 모두에서 실행된 실험은 동핵성 상태를 강제하지 않은 성장 조건을 사용하여 수행되었다는 것을 고려하면, 데이터는 NGS 서열 분석이 균주 제작 과정 동안 품질 제어 단계로서 이용되어 특정 성장 조건하에서 특정 균주에서의 특정 구조체(들)에 대한 형질전환/공동-형질전환의 효율 또는 빈도를 평가할 수 있음을 보여 주었다. 다시 말해, NGS는 특정 형질전환체의 순도를 평가하거나 결정하는 데 사용될 수 있다. 일부 경우에, 선택/카운터 선택이 필요한지 결정하기 위해 NGS가 사용될 수 있다.
선택 계획에 따라 NGS가 돌연변이 대 vs. 부모 표적 유전자의 존재, 부재 또는 백분율을 검출하는 능력을 평가하기 위해, 도 33에 도시된 실험으로부터의 모체, 돌연변이체 및 혼합된 돌연변이체/부모 포자를 돌연변이체 또는 부모 유전자형에 대해 동핵성인 콜로니의 존재를 강제하는 조건하에서 성장시켰다. 보다 구체적으로, 혼합 집단 중 일부는 부모 유전자형 또는 핵을 선호하는 배지(즉, 우라실이 보충되고 메티오닌이 없는 최소 배지)에서 성장시킨 반면, 혼합 집단 중 일부는 돌연변이 유전자형 또는 핵을 선호하는 배지(즉, 우라실이 보충되고 메티오닌이 없는 최소 배지)에서 성장시켰다. 도 35에 도시된 바와 같이, 선택적 배지는 우라실이 보충되고 메티오닌이 없는 최소 배지에서 성장할 때 부모 핵 또는 우라실이 보충되고 메티오닌이 없는 최소 배지에서 성장할 때 돌연변이 핵에 대한 동핵성 상태로 핵의 혼합 집단을 강제하였다. 또한, 선택에 의한 이런 동핵성 상태의 강제는 NGS에 의해 쉽게 검출되었다. NGS는 특정 유형의 핵뿐만 아니라 이들의 혼합물에 대해 완전히 동핵성인 집단을 쉽게 검출하였다. 따라서, NGS는 특정 선택/카운터 선택 방식의 효능을 평가하기 위해 본 발명에 제공된 바와 같은 균주 제작 과정 동안 사용될 수 있다. 이는 특이적 돌연변이의 도입이 식별 가능한 표현형 또는 부모 유전자형을 함유하는 심지어 낮은 백분율의 핵에 의해 가려질 수 있는 표현형을 생성하지 않을 때 특히 유용할 수 있다. 이 예는 또한 도입된 DNA 삽입물에 대해 동핵성인 돌연변이체 또는 도입된 DNA 삽입물을 보유하는 임계값 백분율의 핵산을 갖는 형질전환체를 분리하기 위해 형질전환체를 단독으로 또는 표현형 선별과 함께 선별하는 방법으로서 NGS의 유용성을 예시한다. 임계값 백분율은 상기 형질전환체가 원하는 수준의 생성물을 생성하는 백분율일 수 있다. 생성물은 당업계에 알려진 임의의 생성물일 수 있다. 생성물은 표 2의 생성물에서 선택할 수 있다. 임계값 백분율은50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99% 또는 100%일 수 있다.
실시예 7: 사상균류의 HTP 게놈 공학: 사상균류에서 SNPSWP를 검출하는 차세대 서열 분석( NGS )의 능력의 입증.
이 실시예는 NGS가 어떻게 표적 유전자 부모 균주의 특정 배경에서 표적 유전자 돌연변이를 검출하기 위해 사용될 수 있는지의 예를 입증한다. SNP 스와핑 및 스크리닝 방법에 대한 전체 프로세스의 일반적인 방식은 도 20b-c에서 확인할 수 있다.
도 38에 도시된 바와 같이, 동일한 핵에서 다중 통합, 이소성 통합 및/또는 SNP 및 비-SNP의 존재를 검출하는 NGS를 사용하여 서열 분석 기반 스크리닝의 능력을 테스트하기 위해, 특정 구조체가 상동 재조합을 통해 숙주 A. 니거 게놈의 aygA 유전자좌에 도입되는 3가지 상이한 시나리오를 조사할 것이다. 첫 번째 시나리오에서, pyrG 마커 유전자는 두 구조체 사이에 분할되어 pyrG 유전자의 중첩 부분이 두 구조체에 존재한다. 제 1 구조체는 숙주 게놈에 존재하는 aygA 유전자와 상동성인 서열을 추가로 포함하고, 제 2 구조체는 pyrG 유전자의 일부에 3', 숙주 ayaA 유전자의 제 2 부분에 상동성인 서열을 추가로 포함한다. 두 구조체에서, aygA 유전자와 상동성인 서열은 돌연변이(즉, SNP)를 추가로 포함한다. 두 번째 시나리오는 첫 번째 시나리오와 유사한 두 가지 구조체를 사용하지만 제 2 구조체만 aygA 유전자와 상동성인 돌연변이(즉, SNP)를 포함한다. 마지막으로, 제 3 시나리오는 제 2 시나리오에서 사용된 것과 유사한 2개의 구조체를 이용하지만, 제 1 또는 제 2 구조체는 aygA 유전자와 상동성인 서열에서 돌연변이(즉, SNP)를 포함하지 않는다.
A. 니거 숙주가 배양되고, A. 니거의 원형질체가 생성될 것이고 각각의 구조체는 실시예 4에 기재된 방법을 사용하여 원형질체로 형질전환될 것이다. 형질전환 후, 형질전환체는 온전한 aygA 유전자의 존재(검은 포자) 또는 온전한 aygA 유전자의 손실(노란 포자)에 대해 표현형적으로 선별될 것이다. 추가로, 각각의 형질 전환체는 복제 플레이팅될 것이고, 복제 플레이트로부터의 DNA는 실시예 6에 기술 된 바와 같이 NGS를 사용하여 추출 및 선별될 것이다. 표현형 및 서열-기반 선별 둘 다에 대한 예상 결과는 도 8에 요약되어 있다.
실시예
8: 사상균류의
HTP
게놈 공학: 분할
마커
루프-아웃(Split-Marker Loop-Out)을 이용한 사상균류에서 SNPSWP의 입증.
이 실시예는 도 3-4에 도시된 분할 마커 루프-아웃 절차를 사용하여 사상균류 세포에서 SNP SWP 방법에 대한 원리 증명을 입증한다. SNP 스와핑 및 스크리닝 방법에 대한 전체 프로세스의 일반적인 방식은 도 20b-c에서 확인할 수 있다.
실시예 4 및 5에서, 사상균류에서 표적화된 SNPSWP는 2개의 선형 DNA 단편을 사용하여 숙주의 형질전환에 의해 수행되었다. 단편 중 하나는 DNA를 흡수한 세포의 분리를 허용하는 선택 가능한 마커를 함유하였다. 두 번째 독립 단편은 원하는 표현형에 대한 영향에 대해 테스트될 단일 염기쌍 변화를 함유하였다. 이 예에서, 2개의 단편이 사용된다. 그러나, 이들 단편 둘 모두는 마커 유전자를 플랭킹하는 DNA의 직접 반복체 내에 SNP를 함유한다. 각 단편은 선택 가능한 마커의 절반만 함유한다. 단편이 독립적으로 통합되면 이들은 마커 유전자를 재구성하지 않으며 형질전환체가 발생하지 않을 것이다. 마커가 기능성 유전자를 형성하기 위해 재조합 할 때, 비 동종 말단 결합을 통해 그렇게 할 것이다. 이것이 일어날 때, 플랭킹 서열이 또한 표적화된 유전자좌에서 적절히 통합될 가능성이 훨씬 더 클 것이다. 마커가 유전자좌에 통합되면, 직접 반복체는 마커 서열의 손실을 초래할 수 있는 불안정한 통합을 제공할 것이다. 마커를 잃어버린 균주는 유전자와 관련하여 적절한 위치와 맥락에서 원하는 SNP를 남길 것이다. 궁극적으로, SNP가 필수 유전자 내에 있고 유전자의 파괴가 치명적일 수 있는 경우 실시예 4 및 5에 기술된 접근법이 사용될 수 있다. 실시예 4 및 5의 접근법에서, 공동 형질전환의 표적화 효율은 5-15% 사이에서 변할 수 있다. 대조적으로, 본 실시예의 방법은 마커가 SNP에 연결되고 표적화 효율이 거의 100%이기 때문에 바람직할 수 있다.
본 실시예의 방법을 수행하기 위해, 1015 부모 균주 및 11414 부모 균주로부터의 A. 니거 숙주 세포를 배양하고, 원형질체로 전환시키고, 상기 실시예 4에 기재된 바와 같이 형질전환시키고 도 20b-c에 도시된 접근법에 도시하였다. 이 실시 예에서, 도 46에 도시된 바와 같이, 각각의 부모 균주로부터의 원형질체는 2개의 구조체("분할 마커 구조체")와 공동-형질 전환되었으며, 여기서 2개의 구조체의 각각은 선택 가능한 마커의 중첩 부분(즉, 도 45 및 46의 pyrG)을 함유하고 표적 SNP를 포함하는 직접 반복 서열에 의해 플랭킹되었다. 분할 마커 구조체는 도 45 및 46에 도시된 바와 같이 융합 PCR을 사용하여 생성하였고 45에 도시된 바와 같이 단편 분석기를 사용하여 품질 관리(QC) 하였다. 또한, 이들 구조체의 각각은 숙주 세포 게놈에서 표적 SNP로의 통합을 지시하기 위해 각각의 구조체의 직접 반복 부분을 플랭킹하는 서열을 함유하였다. 본 발명에 기재된 서열-기반 선별을 사용하여 형질전환체를 선별함으로써 정확한 통합을 평가 하였다.
분할-
마커
접근법을 이용한 유전 공학
분할 마커 매개 SNP 교환의 초기 단계는 단계 1 및 2로서 도 20b에 도시되었다. 단계 2에서, 형질전환 DNA는 SNP를 적절한 유전자좌에 표적화하기 위해 상동성 DNA에 융합된 마커의 비-상보적인 절반을 함유하는 2개의 개별 선형 단편으로 구성된다. 형질전환체를 선택 배지에 놓고 성장시켰다. DNA의 안정적인 통합을 갖는 적절히 보완된 균주가 콜로니를 형성하였다. 이들 콜로니는 100-200 마이크로리터의 선택적인 한천 배지를 함유하는 미세적정 플레이트의 개별 웰에 대해 손으로 또는 자동 플랫폼에 의해 선택되었다. 선택된 형질전환체는 단계 4에 지시된 바와 같이 포자를 성장시키고 전파시켰다. A. 니거의 포자는 무핵이며 본질적으로 클론이다. 형질전환된 균주를 적은 수의 포자를 취해 다시 선택 배지에 플레이팅하여 동핵체(세포 내의 모든 핵이 동일한 유전자형임)로 정제하였다. 이 과정은 도 20b에서 화살표로 표시된다. 소수의 클론 포자에 대한 개체수의 반복 감소는 각 웰에서 동핵체를 생성하였다. 이어서, 웰 내의 이들 정제된 균주를 선택 가능한 마커를 함유하는 균주에 독성이 있는 카운더 선택제를 함유하는 배지에 플레이팅하였다. SNP를 함유하는 직접 반복체에 의해 플랭킹되는 마커를 차지하는 균주는 직접 반복체의 크기와 직접적으로 상관되는 빈도로 마커를 상실하였다. 예를 들어, 1,00개의 염기 쌍 직접 반복체는 100개의 염기 쌍 직접 반복체보다 안정적이지 않다. 이 루프 아웃 단계는 도 60의 단계 6이다. 도 60은 분할 마커 통합 및 루프 아웃을 사용하여 수행된 SNPSWP 캠페인의 데이터를 포함한다.
결과
이 실시예에서, 1200개가 넘는 개별 루프 아웃 샘플을 NGS를 사용하여 선별하였다. 이 세트로부터, 119개의 성공적인 균주를 생성하였고 도 60의 좌측 상단 모서리에 점으로 나타냈는데 이는 그 웰로부터의 100%의 앰플리콘이 생산 균주로부터의 SNP를 함유하기 때문이다. 원형 영역으로 지정된 샘플은 이 유전자좌에서 원하는 SNP를 갖는 앰플리콘과 천연 염기쌍을 모두 함유하였다. 이들 균주는 포자 번식 및 도 20b의 단계 4 및 5에 나타낸 통과(passing)를 사용하여 동핵성이 될 수 있다. QC를 통과한 119개의 샘플은 원하는 변형 균주 특성에 미치는 영향을 분석할 수 있다. 다양한 SNP 위치에 걸친 SNP 도입의 성공률이 도 61에 도시되어있다.
실시예
9:
Cas9
리보핵산 단백질(
RNP
) 형질전환을 사용하는 사상균류의 비-상동성 말단 결합(
NHEJ
) 및 HR-매개 게놈 편집은 원하는 편집을 위한 직접적인 선택 없이 SNP, 삽입 및 인델(indel)을 가능하게 한다.
이 실시예는 원하는 편집을 직접 선택하지 않고 NHEJ 능숙한 배경에서 용이한 게놈 편집의 추가 수단을 설명한다. 이러한 방법은 편집을 선택하지 않거나 선택 가능한 마커를 루핑하지 않고 게놈 편집의 신속한 생성을 가능하게 하여 고 처리량 게놈 편집에 유용할 수 있다.
AygA 유전자를 표적으로 하는 2개의 crRNA 서열을 디자인하였다. 이 유전자의 파괴는 null 돌연변이를 일으켜, 검은 야생형 포자보다는 포자 함유 황색 안료를 생성하는 균주를 생성한다. NHEJ-매개 오류가 발생하기 쉬운 수리에 의해 또는 유전자 번역을 방해하는 상동성 재조합 공여자를 제공함으로써 파과가 가능할 수 있다.
Cas9 RNP의 조립(도 47). 화학적으로 변형된 crRNA(표 6 참조) 및 tracrRNA (Synthego로부터 입수)를 뉴클레아제가 없는 TE 완충액에서 250pmol/μL로 만들었다. 5μL의 crRNA(250 μM) 및 10μL tracrRNA(250 μM)를 10μL의 5X 어닐링 버퍼 (Synthego)와 혼합하여 50μL의 H20으로 만들었다. 혼합물을 10분 동안 78℃로, 이어서 30분 동안 37℃로 만듦으로써 샘플을 어닐링하였다. 이어서 샘플을 15분에 걸쳐 실온으로 만들었다. 0.7 uL STC 완충액(1.0M 소르비톨, 50 mM 트리스, pH 8.0, 50mM CaCl2)에서 1.5μL의 crRNA/tracrRNA 복합체(25 μM)와 1μL의 3.22μg/μL EnGen Cas9(뉴잉글랜드 바이오랩스로부터 입수)를 혼합함으로써 Cas9 RNP를 제조하였다. 이는 1.875 mol의 RNA 복합체/ 1 mol Cas9의 비율 및 1μg/μL의 Cas9의 총 농도이었다. 복합체를 실온에서 10분 동안 배양함으로써 형성하였다.
STC에서 RNP 복합체의 2배 희석을 먼저 수행하여 형질전환을 수행하였다. 이어서, 1μL의 이 복합체(0.5 ug Cas9 함유)를 STC에서 A. 푸미가투스(A. fumigatus)로부터의 AMA1 기원 및 pyrG를 함유하는 500ng의 벡터와 STC에서 총 10μL까지 혼합하였다. 이 RNP 혼합물을 실시예 1에 기술된 바와 같이 제조하고 동결시킨 1015(PyrG-)의 10μL의 해동된 원형질체(즉, 1015 아스퍼길루스 균주)에 첨가하고 혼합하였다. 얼음에서 배양한 후, STC에서 실온 40% PEG 4000의 1mL를 원형질체 RNP 혼합물에 첨가하고, 이를 와류하고 실온에서 15분 동안 배양하였다. 이어서 원형질체를 12mL의 용융된 최소 배지 + 1M 소르비톨 및 0.8% 한천과 혼합하고 10cm 페트리디쉬 상에 플레이팅하였다. 응고 후, 추가 8mL의 용융된 최소 배지 + 1M 소르비톨 및 0.8% 한천으로 형질전환체를 오버레이하였다. 형질전환체의 10배 희석액도 상기와 같이 플레이팅 하였다(도 48).
crRNA 프로토 스페이서 서열
| SEQ ID NO: |
crRNA 명칭 |
crRNA 프로토스페이서 서열 |
| 6 |
aygA.1 |
UCAGUCUAUCCGUUUCACGA |
| 7 |
aygA.3 |
UUCCCACGAAGCGAUCACGG |
| 8 |
control |
aUgUgUcagagacaacUcAa |
2개의 crRNA/tracrRNA/Cas9 복합체와의 공동형질전환을 위해, crRNA 및 tracrRNA 쌍을 개별적으로 어닐링하고 Cas9에 개별적으로 복합체화시켰다. 복합체화 후, 형질전환 전에 crRNA/tracrRNA에 복합체화된 동량의 Cas9를 함께 혼합하였다.
상동 재조합 실험의 경우, PCR 및 정제를 통해 gBlocks를 증폭시켜 공여자를 생성하였다. 정제된 생성물(800 ng)을 RNP 및 플라스미드에 첨가하고 상기와 같이 형질전환시켰다. RNP 절단은 외인적으로 제공되는 공여자로 HR을 자극하여 DNA 복구 메커니즘을 상향조절하였다. 상동 재조합 공여자 서열은 ayg.1 crRNA 프로토스페이서 절단 부위 주위의 AygA 유전자에 대해 400-500bp의 상동체가 플랭킹된 돌연변이된 영역을 함유하도록 디자인되었다. 서열은 이 실험에 사용된 2개의 상동성 공여자를 보여준다. DJV_03_pyrG_insertion_in_AygA는 AygA 유전자에 대한 상동성의 5' 및 3' 영역(대문자)에 의해 플랭킹된 프로모터 및 터미네이터(소문자)를 갖는 pyrG를 도시한다(도 51, SEQ ID NO: 9). 상동성 영역은 crRNA 프로토 스페이서 AygA.1의 예측된 절단 부위를 플랭킹한다. DJV_07_4bp_insertion_in_AygA는 AygA 유전자에 대해 상동성의 5' 및 3' 영역(대문자)에 의해 플랭킹된 4 bp 삽입(소문자)을 포함한다(도 52, SEQ ID NO: 10).
표현형은 : (1) 콜로니를 세고 나중에 무성 성장 콜로니의 색을 채점하고 (2) 무성 성장 전에 식민지를 채집한 후 무성 성장 후 개별 분리된 콜로니를 채점하거나, (3) 형질전환 후 5-7일의 개별 포자를 분리하고 이들 포자들을 발아시키고 자극함으로써 결정하였다. 도 49는 방법 1을 사용하여 분생자에서의 표현형 색 변화의 콜로니 카운팅 및 스코어링 결과를 도시하며, 형질전환된 콜로니의 35-40%가 황색 분생자를 생성하는 것으로 추정되었다. 습식 챔버에서 37 ℃에서 하룻밤 동안 정적 인큐베이터에서 이들 3가지 방법 중 하나로부터의 포자를 20μL 효모 몰드 배지에 접종함으로써 유전자형을 결정하였다. 50μL의 프리프만 울트라 샘플 제조 시약을 혼합하고 혼합물을 98℃에서 30분 동안 배양한 다음 원심 분리하여 펠릿 용 해물을 배양함으로써 배양물을 용해시켰다.
절단 부위 또는 절단 부위들을 플랭킹하는 영역은 생거 화학에 의해 증폭되고 서열 분석되었다(도 49d 및 도 49e). 생성된 서열화된 앰플리콘을 사용하여 황색 분생자에서 NHEJ-매개된 인델의 존재를 확인하였다. 상동성 재조합을 테스트하기 위해, PCR 프라이머는 정방향 프라이머가 복구 단편과 상동성인 게놈 영역의 상류에서 어닐링되고, 리버스 프라이머는 복구 단편과 상동성인 영역 내에서 어닐링되도록 디자인되었다. 이 PCR 방식은 통합되지 않은 공여자가 아닌 게놈 DNA만이 AygA 유전자좌에서 PCR 앰플리콘을 생성할 수 있음을 보장한다. 상동성 재조합 분석을 위해, CellenONE을 통해 분류된 포자는 표현형화되고 이어서 유전자형화되고; pyrG 페이로드는 26-36%의 효율로 삽입되었고, 4 bp 페이로드는 86%의 효율로 삽입되었다(도 50a-c).
실시예
10: PAM 부위를
스크램블링하지
않고 단일 SNP를 도입하기 위해
Cas9
리보핵산단백질(RNP) 형질전환을 사용하는 사상균류의 HR-매개 게놈 편집.
이 실시예는 PAM 부위를 스크램블링 또는 변경하지 않고 원하는 편집을 직접 선택하지 않고 단일 SNP를 도입하기 위해 Cas9 RNP-복합체 형질전환을 사용하여 NHEJ 숙련 백그라운드에서 용이한 게놈 편집의 추가 수단을 설명한다. 이러한 방법은 편집을 위해 선택하거나 선택 가능한 마커를 루핑하지 않고 게놈 편집의 신속한 생성을 가능하게 하여 고 처리량 게놈 편집에 유용할 수 있다.
0.2㎍ EnGen Cas9(어닐링된 Ayg.1 cr/tracRNA에 복합체화 됨)을 350ng의 이중 가닥 DNA 공여체 및 STC 완충액에서 4μL로 만든 A. 푸미가투스로부터의 AMA1 기원 및 pyrG를 함유하는 200ng의 벡터와 혼합함으로써 형질전환을 수행하였다. 이를 40μL의 원형질체에 첨가하고 실시예 9에서와 같이 형질전환시켰다. 이중 가닥 공여자 DNA는 5' 및 3' 측에 AygA 유전자에 대한 50 bp의 상동성이 플랭킹된 단일 넌센스 돌연변이에 대해 암호화된다; 공여자는 2개의 상보적 올리고를 어닐링함으로써 만들어졌다. 개별 콜로니를 선택하고, 콜로니로부터의 포자를 사용하여 게놈 DNA를 성장, 분리 및 PCR 증폭시켰다. 분리된 24개 콜로니 중 2개는 검은 포자와 황색 포자의 혼합물을 포함하고 2개는 단지 노란 포자를 포함하고 20개만 검은 포자를 포함하였다. 24개의 서열 중 8개가 성공적으로 PCR 증폭되고 서열 분석되었다. 이들 중에서, 검사된 8개의 서열 중 3개는 추가 돌연변이 없이 원하는 돌연변이를 함유하였다(예를 들어, 도 56b의 야생형 및 돌연변이 흔적을 참조). 나머지 서열은 야생형 AygA 유전자이었다. 결과적으로, 이 실시예는 2개의 어닐링된 올리고가 프로토스페이서 부위의 PAM 또는 시드 영역을 변경하지 않고 SNP를 생성할 수 있음을 입증한다.
실시예
11: 접시에서 형질전환된 균류 균주의 클론 집단으로의 정제
많은 사상균류는 그들의 생애주기에서 식물 성장이 개별 세포에 다수의 핵이 존재하는 상태를 포함하는 단계를 갖는다. 이것은 이러한 유기체를 유전적으로 조작하는 능력에 영향을 미cls다. 원하는 돌연변이를 포함하지 않는 핵으로부터 정제하여 하나의 핵에서 임의의 유전자 변화를 복제해야 한다. 이 핵을 분리하는 한 가지 방법은 유기체가 무성 재생식의 단계를 거치게 하는 것이며, 생성되는 포자가 거의 동일한 유전자형을 갖지 소수의 핵을 함유한다. 개별 포자를 분리함으로써, 이들 포자로부터 번식된 균주는 원하는 생산 특성을 함유할 것이다. 이 실시예는 단일 포자, 따라서 고 충실도 및 높은 처리량을 갖는 표적화된 돌연변이를 함유하는 클론 균류 균주를 분리하는 방법을 설명한다. 이 방법은 개량된 균류 생산 균주의 빠른 생성 및 정제를 가능하게 한다.
전통적으로, 포자 정제는 선택 배지를 함유하는 개별 페트리 플레이트 상에 포자를 스트리킹함으로써 수행될 수 있다. 이 방법에서, 동일한 균사 내에 핵의 혼합물을 함유하는 각각의 형질전환된 콜로니로부터 포자 현탁액을 제조할 수 있다. 포자 현탁액을 멸균 루프를 사용하여 수집한 다음 한천 플레이트에 사분면으로 뿌려 포자가 각 줄에 따라 희석되도록 할 수 있다. 최종 플레이트는 모든 다른 것으로부터 분리되어 클론 개체로 분리될 수 있는 몇개의 포자를 함유해야 한다.
본 발명에 제시된 방법은 각각의 형질전환에 대해 개별 페트리 플레이트/디시를 사용할 필요성을 제거하고 균주를 제작하기 위한 미세적정 플레이트의 사용을 용이하게 한다. 페트리 플레이트는 크고 자동화와 양립되지 않으므로 고 처리량으로 확장할 수 있는 기능을 제한한다. 가장 중요하게는, 본 방법은 웰의 >97%에서 클론 집단을 생성할 수 있는 반면, 당업계의 방법에 공지된 전통적인 방법은 연속적인 계대(선택 과정의 반복 적용은 매우 비효율적일 수 있음) 후에도 클론 집단을 생성하지 않을 수 있다. 본 발명에 상세히 기술된 접근법에서, 개별 클론 균주는 고 처리량 자동화에 간단한 통합을 용이하게 할 수 있는 추가 스크리닝을 위해 미세적정 플레이트의 웰에 배치된다. 이 방법은 또한 페트리 플레이트 상에서 콜로니 성장이 필요 없는 형질전환체의 분리를 용이하게 하여 균주 제작 전체가 미세적정 형식으로 발생할 수 있다. 당 업계에 공지된 전통적인 방법과 본 실시예에 기술된 방법 사이의 워크 플로우 비교에 대해 도 54a 및 54b 참조
아스퍼길루스 니거 또는 관련 균류 미생물은 하나 이상의 관심 대사 산물, 화학 물질 또는 생물학적 제제를 생산할 수 있다. 형질전환 프로토콜은 공여자 DNA를 갖는 A. 니거 포자의 형질전환을 요구한다. 포자는 푸아송 분포를 통해 또는 단일 세포 분배에 광학적으로 미세적정 플레이트에 클론적으로 분리/증착된다.
형질전환시, 아스퍼길루스 니거는 플레이트되고 포자화되도록 성장된다. 생성된 포자는 액체에 현탁되고 희석된다. 희석은 두 가지 방법 중 하나로 수행된다.
제 1 유형의 희석에서, 포자는 분배된 부피에 존재하는 단지 하나의 포자 또는 포자의 푸아송 분포에 따른 통계적 확률이 있는 농도로 희석된다. 포자는 ECHO, BIOSPOT 또는 기타 액체 처리 장치를 사용하여 발아할 수 있는 미세적정 플레이트에 분배된다. 일반적으로 이 방법은 단일 포자를 포함하는 각 웰에 대해 많은 빈 웰을 생성할 수 있으며, 2개의 포자를 포함하는 웰은 매우 적다.
제 2 유형의 희석에서, 포자는 단일 세포로서 광학적으로 구별될 수 있는 농도로 희석된다. 분배에 사용되는 기기에 따라 농도가 다를 수 있다. 단일 세포가 액적 내에 존재한다는 광학적 검증 후, 그 액적은 미세적정 플레이트에 분배된다. 다량의 포자가 분배된 부피에 있거나 없으면, 이들은 폐기물 수집 또는 재흡입에 투입될 수 있다. 푸아송 분포 방식(위의 첫 번째 희석 유형)과 비교할 때 각 출력 데이터 웰은 단일 셀이 있고 비어 있거나 이중 포자 웰이 훨씬 적을 것으로 예상할 수 있다.
제 2 유형의 희석을 위한 기기는 (1) 광학 기기와 조합된 미세 유체를 사용하여 단일 포자만이 미세적정 플레이트 내로 분배되어 발아될 수 있는지 시각적으로 확인하는 CellenONE 기구; (2) 세포 또는 포자를 마이크로 채널로 플러싱한 다음 개별 세포 또는 포자를 성장 및 복제할 수 있는 미세 유지 펜 속에 밀도록 레이저를 사용하는 버클리 라이트 비콘 기기; (3) 미세유체 유동 채널을 사용하여 형광을 검출할 수 있는 광학 센서를 지나 개별 세포를 이동시키고, 형광 신호에 기초하여 웰을 출력하도록 세포를 분류할 수 있는 FACS 기구를 포함한다. 불행히도, 현재 시장에 나와있는 유일한 FACS 시스템은 단일 소스에서 여러 대상으로 셀을 정렬하거나 여러 소스에서 선택하여 단일 대상으로 정렬하도록 설계되었다. 많은 출처에서 여러 목적지로 세포를 쉽게 분류할 수 있는 기계를 개발해야 하는 경우, 분류 된 세포가 (자연적으로 또는 유전자 공학을 통해) 형광 활성을 가져야 한다는 최종 요구 사항과 함께 이 실시예에서 설명한 고 처리량 사용 사례에 적합하다; (4) Cytena 기기, CellenONE 기기와 유사한 광학 및 미세 유체 기술을 사용하여 작동하지만 고 처리량/플레이트 기반 입력과 양랍되지 않는다. 이 카트리지는 일회용 카트리지를 사용하여 소스 액체를 유지하며 수동으로 기계에 볼트로 고정해야 FACS 기계와 유사한 처리량 제한을 제공한다. CellenONE은 충실도가 높은 단일 포자를 인쇄할 수 있다. 55a-55c 참조.
실시예
12: 사상균류의
HTP
게놈 공학: 사상균류 형태에 영향을 미치는 유전자의 확인
이 실시예는 균류 세포 형태를 제어하는 데 역할을 하는 유전자를 확인하기 위해 사상균류, 아스퍼길루스 니거의 SNPSWAP 방법에서 SNP 스왑 라이브러리의 사용을 입증한다. 특히, 이 실시예는 A. 니거 돌연변이 균주에서 비-균사체 형성, 펠릿 유사 형태 표현형을 부여하는 유전자 그룹의 확인을 기술하고, 여기서 세포는 심층 배양에서 성장될 때 다수의 팁을 갖는 각각의 세포에 대해 더 단단하고 더 긴 표현형을 유지한다. 이러한 유형의 성장은 교반 탱크 발효에 유리할 수 있다.
아스퍼길루스 니거는 발효를 통한 시트르산의 대규모 생산에 사용되는 사상균류의 한 종류이다. 이 종의 다수 균주는 분리되어 시트르산 및 다른 유기산의 생산에 대한 다양한 능력을 갖는 것으로 나타났다. A. 니거 균주 ATCC 1015는 20세기 초에 시트르산 생산자로 확인되었다. ATCC 11414로 명명된 이 균주의 분리체는 나중에 모체에 비해 증가된 시트르산 수율을 나타내는 것으로 밝혀졌다. 예를 들어, A. 니거 균주 ATCC 1015는 평균적으로 질산 암모늄을 함유하지만 철 및 망간 양이온이 모두 없는 배지에서 140g의 포도당으로부터 7g의 시트르산을 생성한다. 한편, 분리 균주 ATCC 11414는 동일한 조건하에서 10배 수율 증가(70g의 시트르산)를 나타낸다. 더욱이, 균주 ATCC 11414 포자는 균주 1015의 포자보다 시트르산 생산 배지에서 발아하고 더 잘 자란다.
이들 표현형 차이에 대한 잠재적 유전자원을 확인하기 위해, ATCC 1015 및 ATCC 11414 균주의 게놈을 서열 분석하고 분석하였다. 결과 분석 결과 1015 및 11414 균주를 구별하는 43개의 SNP가 확인되었다(표 4 참조). 이들 43개의 SNP 중 18개가 각각의 유전자의 암호화 도메인에 있는 것으로 밝혀졌다(표 4 참조).
상이한 배양 조건하에서 사상균류의 형태/성장을 제어하는 데 잠재적인 역할을 하는 유전자를 확인하기 위해, 표 4로부터의 43개의 SNP는 표 4로부터의 각각의 개별 SNP를 염기 1015 균주에 체계적으로 도입하고 생성된 부모 및 돌연변이 균주 사이의 형태학적 관점으로부터 표현형 차이를 조사하기 위해 본 발명에 기술된 SNP 스왑 공정에 사용하였다. 반대로, 11414 생산 균주에서 동일한 유형의 공정이 수행되었으므로, 11414의 게놈에 이미 존재하는 표 4의 각 SNP는 체계적으로 각 유전자의 야생형 버전으로 대체되었고 부모와 돌연변이 균주 사이의 형태의 최종 차이가 주목되었다.
원형질체 형질전환을 위한 구조체
이 실시예에서, 각각의 균주(즉, 1015 및 11414)는 2개의 구조체("분할 마커 구조체")와 함께 공동 형질전환되었고, 여기서 2개의 구조체 각각은 선택 가능한 마커의 중첩 부분(즉, (도 45 및 46에서 pyrG)을 함유하였고에 45 및 도 46에 도시된 바와 같이 직접 반복 서열에 의해 플랭킹되었다. 분할-마커 구조체는 융합 PCR을 사용하여 생성되었고 도 46에 도시된 바와 같이 단편 분석기를 사용하여 품질 관리(QC'd) 되었다. 또한, 이들 구조체 각각은 표 4로부터의 각각의 SNP에 대한 각각의 표적 유전자에서 숙주 세포 게놈으로의 통합을 지시하기 위해 각 구조체의 직접 반복 부분을 플랭킹하는 서열을 추가로 포함하였다. 1015 염기 균주 원형질체의 경우, 분할 구조체에서의 직접 반복체는 표 4로부터의 SNP 중 하나를 포함한다(도 3 참조). 대조적으로, 11414 생산 균주 원형질체의 경우, 직접 반복체는 표 4의 SNP를 포함하지 않았다.
A. 니거 기본 균주 1015 및 생산 균주 11414를 배양하고, 원형질체로 전환시키고, 본 발명에 기술된 바와 같이 형질전환시키고 선별하였다. 요약하면, 이러한 각 단계는 다음과 같다.
원형질체의 생성
500ml의 완전한 배지에 106 conidia/ml를 접종하고 A. 니거 1015 기본 균주 및 A. 니거 11414 생산 균주 모두에 대해 300℃에서 150 rpm으로 밤새 성장시켰다. 밤새 성장시킨 후, 미라클로스를 통해 각 배양액을 여과하여 균사체를 수확하였다. 이어서, 균사체를 멸균수로 철저히 헹구었다. 이어서, 두 균주로부터 수거 및 세척 된 균사체를 각각 VinoTaste Pro(VTP) 효소 칵테일로 효소 분해시켰다.
원형질체 완충제(1.2M 황산 마그네슘, 50 mM 포스페이트 완충제, pH 5)에서 60ml/ml의 VTP 50ml를 먼저 제조함으로써 두 균주에 대한 균사의 효소 분해를 수행 하였다. VTP를 용해시킨 후, 완충액을 깨끗한 오크리지 튜브에 넣고 15분 동안 15,000 x g에서 회전시켰다. 이어서, 용액을 원심 분리 후 여과 멸균하였다. 일단 만들어지면, 수확된 균사체의 일부를 VTP 용액에 첨가하고 균사체를 30℃에서 80rpm으로 ~2-4시간 동안 분해시켰다. VTP 분해 동안 다양한 간격으로, 작은 샘플을 원형질체(즉, 분생자보다 크고 삼투 용해에 민감한 큰 원형 세포)의 존재에 대해 400배 확대하에 검사하였다. 각각의 균주에 대한 균사체의 대부분 또는 전부가 분해될 때, 각각의 균주로부터의 배양액을 멸균 미라클로스를 통해 여과하고 여액을 눈금 실린더로 수집하였다. 여과된 원형질체를 눈금 실린더로 옮기고, 낮은 삼투압 농도의 완충액(5ml의 0.4M ST 완충액 (0.4M 소르비톨, 100mM 트리스, pH 8))을 부드럽게 오버레이한 다음, 중첩된 샘플을 800 x g에서 회전시켰다. 40℃에서 15분 후 원형질체를 피펫으로 제거하고 25ml의 ST 용액(1.0M 소르비톨, 50mM 트리스, Ph 8.0)과 부드럽게 혼합하고 10분 동안 800 xg에서 재회전시켰다. 이어서, 각각의 균주로부터의 원형질체를 각각 25ml의 ST 용액에 개별적으로 재현탁시키고 10분 동안 800 x g에서 원심 분리에 의해 수집하였다.
원형질체의 형질전환
원심 분리 후, 두 균주로부터의 원형질체는 궁극적으로 염화칼슘을 함유하는 완충액에 재현 탁되었다. 후속 적으로, 두 균주로부터의 원형질체는 자동화 된 액체 핸들러를 사용하여 전통적인 PEG 칼슘 매개 형질 전환을 받았고, 이는 상기 기재된 분할 구조물로부터의 DNA를 96 웰에서 원형 질질 -PEG 혼합물과 조합 하였다.
형질전환체의 선별
상기한 바와 같이, 본 실시예에서 사용된 분할 마커 구조체는 pyrG 마커 유전자를 플랭킹하는 직접 반복체를 포함하였고, 이후 마커 유전자를 루핑 아웃하는 데 사용되었다. 결과적으로, 루프 아웃 구조체를 함유하는 균주는 선택 영역의 결실을 위해 카운터 선택되었다(예를 들어, 도 45 및 도 4 참조; pyrG 유전자의 부재). 본 발명에 기술된 바와 같은 서열-기반 선별에 의해 정확한 통합을 추가로 평가하였다. 또한, 본 발명에 제공된 바와 같은 형질전환체의 동핵성 성질을 평가하기 위해 NGS를 사용하여 돌연변이 균주를 선별하였다. 낮은 pH(도 62) 또는 삼투 스트레스(도 63) 하에서 성장하거나 포자화하는(도 64) 상기 균주 능력을 평가하기 위해, 동핵성 또는 실질적으로 동핵성 돌연변이 균주를 다양한 보충물이 있거나(도 62 및 63 참조) 또는 다양한 보충물이 없는(도 64 참조) 최소 배지 상에 플레이팅하였다. 또한, 돌연변이 균주는 심층 생산 배지에서 그들의 표현형을 평가하기 위해 CAP 배지에서 심층 배양액로서 성장되었다.
결과
기본 A. 니거 균주 1015 내로 표 4 사이에 공유된 4개의 SNP의 개별적 통합은 형태학적 표현형을 생성하였다. 특히, FungiSNP_9 (SEQ ID NO: 11), FungiSNP_12 (SEQ ID NO: 12), FungiSNP_18 (SEQ ID NO: 13) 또는 FungiSNP_40 (SEQ ID NO: 14)을 1015 게놈 생성 돌연변이 균주에 통합하면 CAP 배지에서 심층 배양에서 성장될 때 비-균사체, 펠릿 형태를 생산CAP 배지에 침지 된 배양 물로서 성장될 때 펠릿 형태를 생성하였다.
균류 형태에 영향을 미치는 4개의 SNP를 함유하는 유전자의 역할은 웨이브 다운 실험에서 추가로 입증되었고, 이 4개의 SNP 각각의 제거는 관찰된 형태학적 표현형을 구제하였다. 4개의 SNP의 서열은 첨부된 서열 목록에서 찾을 수 있으며, 추정 또는 알려진 단백질 기능은 표 4에서 찾을 수 있다.
도 62에 도시된 바와 같이, 기본 SNP18을 함유하는 균주는 저 pH 배지에서 더 빠르게 성장한다. 기본 균주(즉, 도 62의 기본 snp18prod)에서 생산 균주(11414)로부터의 FungiSNP_18의 존재는 염기(즉, 도 62의 기본)와 비교하여 pH2 배지에서 생성된 콜로니의 방사상 성장을 감소시켰다. 대조적으로, 생산 균주(즉, 도 62의 생산 SNP18Base)에서 기본 균주로부터 야생형 버전의 FungiSNP_18의 존재는 도 62의 기본 및 생산 균주와 비교하여 상기 균주에서 방사상 성장을 허용하였다. 또한, 생산 균주에 존재하는 다른 SNP가 또한 방사상 성장을 낮추는 데 기여하는 것으로 보인다(도 62의 snp18prod보다 작은 생산 참조).
도 63에 도시된 바와 같이, 기본 SNP18을 함유하는 균주(즉, 야생형 버전의 FungiSNP_18)는 삼투 스트레스를 제공하는 배지에서 더 빠르게 성장한다. 기본 균주에서 생산 균주(11414)로부터 FungiSNP_18의 존재(즉, 도 63의 기본 snp18prod)는 기본(즉, 도 63의 기본)과 비교하여 삼투 스트레스 하에서 생성된 콜로니의 방사상 성장을 감소시켰다. 대조적으로, 생산 균주(즉, 도 63의 생산 SNP18Base)에서 염기 균주로부터 야생형 버전의 FungiSNP_18의 존재는 도 63의 기본 및 생산 균주와 비교하여 상기 균주에서 방사상 성장을 허용하였다. 또한, 생산 균주에 존재하는 다른 SNP는 또한 방사상 성장을 낮추는 데 기여하는 것으로 보인다(도 63의 기본 snp18prod보다 작은 생산 참조).
흥미롭게도, 각각의 FungiSNP_9, FungiSNP_12 또는 FungiSNP_40을 함유하는 염기 균주는 심층 배양액에서 성장하지 않을 때(예를 들어, 플레이트 상에서) 정상적으로 성장하고 포자화된다. 기본 균주(즉, 1015)에서 FungiSNP_18을 발현하는 것은 도 64에 도시된 바와 같이 방사상 성장률(감소) 및 포자에 영향을 나타내었다.
실시예
13: 사상균류의
HTP
게놈 공학: 사상균류 형태학에서 역할하는 확인된 유전자의 역할의 확인 - 확인된 형태 대조군 유전자의 결실
이 실시예는 실시예 12에서 균류 형태에서 역할을 하는 것으로 확인된 4개의 유전자의 역할의 확인을 입증한다. 특히, 이 실시예는 A. 니거 균주 1015 및 11414에서 본 발명에 기술된 HTP 방법을 사용하여 4개의 유전자 각각을 낙킹 아웃하거나 결실시키는 것을 기술한다.
A. 니거 기본 균주 1015 및 생산 균주 11414를 배양하고, 원형질체로 전환시키고, 실시예 12에 기재된 바와 같이 형질 전환시키고 선별하였다.
원형질체 형질전환을 위한 구조체
이 실시예에서, 각각의 균주(즉, 1015 및 11414)로부터의 원형질체는 일련의 단일 구조체로 형질전환되었으며, 이로 인해 일련의 각 구조체는 마커 유전자의 숙주 세포 게놈으로의 통합을 유도하기 위해 실시예 12에서 확인된 관심 4개 유전자 중 하나를 플랭킹하는 게놈 서열에 상보적인 서열에 의해 플랭킹된 선택 가능한 마커 유전자(즉, pyrG)를 함유하였다. 도 39에 도시된 바와 같이, 마커 유전자를 4개의 유전자 중 하나(1015 균주에서 4개의 야생형 유전자 중 하나 및 11414 균주에서 4 개의 SNP 중 하나)의 유전자좌에 통합시키면 상기 야생형 유전자 또는 개개의 균주의 유전자좌로부터의 유전자를 함유하는 SNP를 필수적으로 제거하는 역할을 하였다.
성장 후, 본 발명에 제공된 바와 같은 형질전환의 동핵성 성질을 평가하기 위해 NGS를 사용하여 돌연변이 균주를 선별하였다. 심층 생산 배지에서 이들의 표현형을 평가하기 위해 CAP 배지에 심층 배양액으로서 포자화 또는 성장하는 상기 균주 능력을 평가하기 위해, 동핵성 또는 실질적으로 동핵성 돌연변이 균주를 배지 상에 플레이팅하였다.
결과
기본 1015 균주 및 11414 생산 균주로부터 4개의 유전자 각각을 제거하면 상기 4개의 유전자 각각이 균류 형태에 영향을 미치는 역할을 분명히 한다는 점에서 실시예 12의 결과를 확인하였다. 특히, 실시예 12에서와 같이, 1015 균주에서 FungiSNP_18을 함유하는 유전자 또는 11414 균주에서 FungiSNP_18을 함유하는 유전자의 비-SNP 함유 버전의 제거는 심층 배양 조건하에서 가장 현저한 표현형을 생성하였으며, 상기 균주는 펠릿과 유사한 형태를 가졌다. 또한, 도 65에 도시된 바와 같이. 도 65에 나타낸 바와 같이, FungiSNP18 및 FungiSNP40 유전자의 결실은 모든 조건하에서 단단한 형태를 초래하였다. 이 데이터는 결실 표현형이 SNP 자체보다 더 현저하다(형태에 대한 더 강한 영향)는 것을 고려하면 SNP가 기능 돌연변이의 손실이 아님을 나타낼 수 있다. 따라서, 이들 유전자의 발현을 변경시키는 것은 발효기에서의 성장에 바람직한 방식으로 형태에 영향을 미칠 수 있는 것으로 보인다.
흥미롭게도, 1015 균주에서 FungiSNP_18을 함유하는 유전자의 비-SNP 함유 버전의 결실은 상기 변이체 1015 균주에서 음성 포자 표현형을 생성하여 상기 변이체 1015 균주가 포자화 능력을 상실시켰다(도 66 참조). 이러한 포자 손실은 FungiSNP_18 유전자가 제거된 11414 균주에서 관찰되지 않았다. 11414 및 1015 균주의 유전적 배경이 표 4에 존재하는 SNP와 별도로 동일하다는 것을 감안할 때, 이는 11414 유전적 배경에서 표 4의 SNP의 하나 또는 전부 또는 일부 조합의 존재는 FungiSNP_18이 제거될 때 생성되는 음성 포자 표현형을 제거하는 데 충분하다는 것을 암시하였다. 다시 말하면, SNP18 활성이 없을 때 생산 균주에서 포자를 유지하기 위해 상위성으로 작용하는 다른 돌연변이(SNP)가 있다.
FungiSNP_9, FungiSNP_12 또는 FungiSNP_40 또는 이들의 비-SNP 함유 버전을 각각 제거함으로써 생성된 변이체 11414 또는 1015 균주에서 포자 손실이 관찰되지 않았다는 것을 주목해야 한다.
또한, 본 실시예에서 심층 배양 조건하에서 관찰된 형태학적 표현형은 4개의 유전자 각각에 대해 실시예 12에서보다 현저한데, 이는 성공적인 형질전환체가 본질적으로 결실 표현형을 나타내는 실험 디자인에 기인할 수 있음에 주목해야 한다. 더욱이, 11414 균주의 표현형은 또한 1015 기본 균주와 비교하여 이 균주에 존재하는 다른 SNP 중 하나 이상에 의한 표현형에 대한 기여로 인해 더욱 두드러졌다.
실시예
14: 사상균류의
HTP
게놈 공학: 유전자 발현을 변경하여 사상균류 세포 형태 변경
이 실시예는 사상균류 형태를 제어하는 데 역할을 하는 것으로 생각되는 실시예 1 및 2로부터 확인된 FungiSNP_9, FungiSNP_12, FungiSNP_18 및 FungiSNP_40 유전자의 발현 조절의 효과를 테스트하기 위해 사상균류 세포에서 자동화된 HTP PROSWP 방법의 사용을 보여줌으로써 사상균류 세포에서 자동화된 HTP PROSWP 방법의 원리 증명으로서 작용한다.
본 실시예에서, 실시예 12 및 13에서 확인된 FungiSNP_18 유전자(즉, SEQ ID NO: 13)의 발현은 본 발명에 기재된 PROSWP 방법을 사용하여 표 1로부터의 4개의 프로모터 중 하나를 갖는 주석이 달린 천연 프로모터로 대체하여 A. 니거 1015 기본 균주 및 A. 니거 11414 생산 균주 모두에서 조절하였다. 보다 구체적으로, 각 FungiSNP에 대한 각각의 균주(즉, 1015 부모 균주 또는 11414 부모 균주)에 대해, (4) 변이체 또는 돌연변이 균주 세트가 생성되었으며, 여기서 제 1 변이주는 표 1에 기술된 srp8p 프로모터의 제어하에서 상기 후보 FungiSNP (FungiSNP_9 (SEQ ID NO: 11); _12 (SEQ ID NO: 12); _18 (SEQ ID NO: 13); _40 (SEQ ID NO: 14)) 유전자를 포함하는 제 1 구조체를 발현하며, 제 2 변이주는 표 1에 기술된 amy8p 프로모터의 제어하에 상기 후보 FungiSNP 유전자를 갖고, 제 3 변이주는 표 1에 기술 된 man8p 프로모터의 제어하에 상기 후보 FungiSNP 유전자를 갖고, 제 4 변이주는 표 1에 기술된 mbfAp 프로모터의 제어하에 상기 후보 FungiSNP 유전자를 갖는다. 변이체를 생성하는 데 사용된 각각의 구조체는 후보 FungiSNP 유전자를 플랭킹하는 서열 및 개개의 후보 FungiSNP 유전자의 유전자좌로 구조체의 통합을 진행하는 역할을 하는 프로모터를 추가로 포함하였다. 이 실시예에서 사용된 이분자 구조체 디자인 및 통합 계획의 일반적인 설명이 도 67에 도시되어있다.
이들의 생성 후, (4) 변이주를 생성하기 위해 사용된 각각의 후보 FungiSNP에 대한 각각의 구조체는 A. 니거 1015 기본 균주 및 A. 니거 11414 생산 균주 둘 다에 대해 생성된 원형질체로 개별적으로 형질전환되었다. 두 균주에 대한 원형질체를 배양하고, 원형질체로 전환시키고, 형질전환 및 선별하여 상기 실시예에 기재된 표현형 및/또는 서열-기반 선별을 사용하여 실질적으로 동핵성 원형질체를 선택 하였다. 따라서, 각각의 개별 구조체의 형질전환은 도 40에 일반적으로 도시된 바와 같이 각각의 후보 FungiSNP에 대한 각 부모 균주에 대해 4개의 변이체 또는 돌연변이 균주를 생성시켰다. 이어서, 이들 균주의 각각의 형태학적 표현형을 관찰하고 상기 유전자에 대한 천연 프로모터의 제어하에 확인된 유전자를 포함하는 돌연변이 균주의 형태학적 표현형과 비교하였다. 그런 다음 확인된 각 유전자에 대해 이상적인 발현 수준을 결정하였다.
결과
전체적으로, 표 1의 상이한 프로모터로 각각의 형태 제어 유전자 표적(즉, FungiSNP_9, _12, _18 및 _40)에 대한 프로모터 스와핑은 이들 유전자의 발현을 제어하는 것이 형태에 영향을 미치는 것으로 밝혀졌다(도 68 참조). 약한 manB 프로모터 하에서 SNP18을 함유하는 균주는 다른 프로모터 조합을 함유하는 균주보다 더 단단한 콜로니 형태를 가졌다. SNP18 대조군의 영향은 낮은 pH에서보다 삼투압 스트레스에서 더 두드러졌다. 또한, 약한 manB 프로모터 하에서 SNP40을 함유하는 균주는 테스트된 모든 성장 조건하에서 다른 프로모터 조합을 함유하는 균주보다 콜로니 형태에 현저한 영향을 미쳤다.
도 69에 도시된 바와 같이, 표 1의 상이한 프로모터와 형태 제어 유전자 표적 12(FungiSNP_12; SEQ ID NO: 12)의 프로모터 스와핑은 강도가 낮은 프로모터가 균사에서 황색 안료를 나타내고 콜로니의 가장자리에서 일부 변형된 형태가 관찰됨을 나타냈다. 황색 안료의 존재는 변이체 또는 돌연변이 균주가 대사 스트레스를 겪고 있음을 나타냈다.
또한, 표 1과 상이한 프로모터로 형태 제어 유전자 표적 18(FungiSNP_18; SEQ ID NO: 13)의 프로모터 스와핑은 2개의 약한 프로모터로 이 유전자의 발현을 제어하는 것이 형태에 영향을 미치는 것으로 밝혀졌다(도 57, 58 및 70 참조). 예를 들어, manB 융합 및 amyB 융합을 함유하는 균주는 다중 팁 표현형을 유지한 반면, 보다 높은 발현 srpB 및 mbfA를 갖는 균주는 다중 팁 표현형이 결여되어 대신 비정상적인 팽윤을 나타냈다(도 57 참조). 도 58의 이미지는 시트르산 생산 배지에서 30℃에서 24시간 동안 성장한 균주이다. 도 57의 이미지는 30℃에서 48시간 동안 시트르산 생산 배지에서 성장된 다양한 비 천연 프로모터-FungiSNP_18 융합체를 발현하는 부모 11414 균주뿐만 아니라 11414 균주이다. 168시간 동안 배양될 때, 더 높은 발현 프로모터를 갖는 균주 및 부모 균주 대조군은 모두 긴 사상균류를 함유하였다. 프로모터 융합, amyB 및 manB로부터의 발현 수준이 더 낮은 균주는 펠릿으로 유지되었다. 도 70에 도시된 바와 같이, 약한 프로모터에 의해 구동될 때, SNP_18은 생산 균주보다 기본 균주에서 더 심각한 형태학적 표현형을 갖는다.
실시예 13으로부터의 결실 실험의 결과와 유사하게, 1015 균주에서 FungiSNP_18 유전자의 발현 감소는 도 59에 도시된 바와 같이 포자 손실을 경험한 세포를 생성하였다. 이러한 포자 손실은 11414 돌연변이 균주에서 관찰되지 않았다. 다시, 11414 및 1015 균주의 유전적 배경이 표 4에 존재하는 SNP와 별도로 동일하다는 것을 감안할 때, 이는 11414의 유전적 배경에서 표 4로부터의 SNP의 하나, 전부 또는 일부 조합의 존재가 FungiSNP_18의 발현이 감소될 때 생성된 음성 포자형 표현형을 구제하는 데 충분하다는 것을 암시한다.
SEQ ID NO 식별자를 가진 본 발명의 서열
본 발명의 추가
실시태양
본 발명에 의해 고려된 다른 주제는 이하의 번호를 매긴 실시태양에서 기술된다:
1. a) 복수의 원형질체를 제공하는 단계, 여기서 원형질체는 사상균류 세포의 배양액으로부터 제조된다;
b) 복수의 원형질체를 제 1 구조체 및 제 2 구조체로 형질전환시키는 단계, 여기서 제 1 구조체는 원형질체의 게놈에서 제 1 유전자좌와 상동인 뉴클레오타이드가 양쪽면의 측면에 위치하는 제 1 폴리뉴클레오타이드를 포함하고 제 2 구조체는 원형질체의 게놈에서 제 2 유전자좌와 상동인 뉴클레오타이드가 양쪽면의 측면에 위치하는 제 2 폴리뉴클레오타이드를 포함하며, 형질전환은 상동성 재조합에 의해 제 1 구조체의 제 1 유전자좌로의 통합 및 제 2 구조체의 제 2 유전자좌로의 통합을 초래하며, 적어도 제 2 유전자좌는 원형질체 게놈에서 제 1 선택 가능한 마커 유전자이고 제 1 폴리뉴클레오타이드는 돌연변이 및/또는 유전자 제어 요소를 포함한다;
c) 선택 및 역선택을 수행함으로써 동핵성 형질전환체를 정제하는 단계; 및
d) 사상균류 세포의 재생에 도움이 되는 배지에서 정제된 형질전환체를 성장시키는 단계를 포함하여 사상균류 균주를 생산하는 방법.
2. 제 1 실시태양에 있어서,
제 1 구조체가 구조체 A 및 구조체 B로 분할되고, 구조체 A는 제 1 폴리뉴클레오타이드의 제 1 부분 및 제 1 폴리뉴클레오타이드의 제 1 부분에 대한 제 1 유전자좌 5'와 상동성인 뉴클레오타이드를 포함하고, 구조체 B는 제 1 폴리뉴클레오타이드의 제 2 부분 및 제 1 폴리뉴클레오타이드의 제 2 부분에 대한 제 1 유전자좌 3'와 상동성인 뉴클레오타이드를 포함하며, 제 1 폴리뉴클레오타이드의 제 1 부분 및 제 2 부분은 중첩 상보적 서열을 포함하는 방법.
3. 제 1 또는 제 2 실시태양에 있어서,
제 1 구조체가 구조체 A 및 구조체 B로 분할되고, 구조체 A는 제 2 폴리뉴클레오타이드의 제 1 부분 및 제 2 폴리뉴클레오타이드의 제 1 부분에 대한 제 1 유전자좌 5'와 상동성인 뉴클레오타이드를 포함하고, 구조체 B는 제 2 폴리뉴클레오타이드의 제 2 부분 및 제 2 폴리뉴클레오타이드의 제 2 부분에 대한 제 1 유전자좌 3'와 상동성인 뉴클레오타이드를 포함하며, 제 2 폴리뉴클레오타이드의 제 1 부분 및 제 2 부분은 중첩 상보적 서열을 포함하는 방법.
4. 제 1 내지 제 3 실시태양 중 어느 하나에 있어서,
복수의 원형질체로부터 각각의 원형질체는 복수의 제 1 구조체로부터 단일의 제 1 구조체 및 복수의 제 2 구조체로부터 단일의 제 2 구조체로 형질전환되고, 복수의 제 1 구조체로부터의 각 제 1 구조체에서 제 1 폴리뉴클레오타이드는 상이한 돌연변이 및/또는 유전자 제어 요소를 포함하고; 복수의 제 2 구조체로부터의 각 제 2 구조체에서 제 2 폴리뉴클레오타이드는 동일한 방법.
5. 제 4 실시태양에 있어서,
사상균류 세포의 라이브러리를 생성하기 위해 단계 a-d를 반복하는 단계를 더 포함하며, 라이브러리에서 각각의 사상균류 세포는 상이한 돌연변이 및/또는 유전자 제어 요소를 갖는 제 1 폴리뉴클레오타이드를 포함하는 방법.
6. 제 1 내지 제 5 실시태양 중 어느 하나에 있어서,
제 1 폴리뉴클레오타이드는 표적 사상균류 유전자 또는 이종성 유전자를 암호화하는 방법.
7. 제 1 내지 제 6 실시태양 중 어느 하나에 있어서,
돌연변이는 단일 뉴클레오타이드 다형성인 방법.
8. 제 1 내지 제 7 실시태양 중 어느 하나에 있어서,
유전자 제어는 프로모터 서열 및/또는 터미네이터 서열인 방법.
9. 제 1 내지 제 8 실시태양 중 어느 하나에 있어서,
유전자 제어 요소는 프로모터 서열이고, 프로모터 서열은 표 1에 열거된 프로모터 서열로부터 선택되는 방법.
10. 제 1 내지 제 9 실시태양 중 어느 하나에 있어서,
복수의 원형질체는 미세적정 플레이트의 웰에 분포되는 방법.
11. 제 1 내지 제 10 실시태양 중 어느 하나에 있어서,
단계 a-d는 미세적정 플레이트의 웰에서 실행되는 방법.
12. 제 10 또는 제 11 실시태양에 있어서,
미세적정 플레이트는 96웰, 384웰 또는 1536웰 미세적정 플레이트인 방법.
13. 제 1 내지 제 12 실시태양 중 어느 하나에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
14. 제 1 내지 제 13 실시태양 중 어느 하나에 있어서,
사상균류 세포는 아스퍼길루스 니거(Aspergillus niger)로부터 유래되는 방법.
15. 제 1 내지 제 14 실시태양 중 어느 하나에 있어서,
사상균류 세포는 비 균사체 형성 표현형을 갖는 방법.
16. 제 1 내지 제 15 실시태양 중 어느 하나에 있어서,
균류 세포는 비 기능성 비 상동성 말단 결합(NHEJ) 경로를 갖는 방법.
17. 제 16 실시태양에 있어서,
비 기능성 NHEJ 경로는 세포를 NHEJ 경로의 구성요소에 대항하는 항체, 화학적 억제제, 단백질 억제제, 물리적 억제제, 펩타이드 억제제 또는 안티-센스 또는 RNAi 분자에 대한 노출 때문인 방법.
18. 제 17 실시태양에 있어서,
화학적 억제제는 W-7인 방법.
19. 제 6 내지 제 18 실시태양 중 어느 하나에 있어서,
제 1 유전자좌는 표적 사상균류 유전자를 위한 것인 방법.
20. 제 1 내지 제 18 실시태양 중 어느 하나에 있어서,
제 1 유전자좌는 원형질체 게놈에서 제 2 선택 가능한 마커 유전자를 위한 것인 방법.
21. 제 20 실시태양에 있어서,
제 2 선택 가능한 마커 유전자는 영양요구성 마커 유전자, 비색성 마커 유전자 또는 방향성 마커 유전자인 방법.
22. 제 1 내지 제 21 실시태양 중 어느 하나에 있어서,
제 1 선택 가능한 마커 유전자는 영양요구성 마커 유전자, 비색성 마커 유전자 또는 방향성 마커 유전자인 방법.
23. 제 1 내지 제 22 실시태양 중 어느 하나에 있어서,
제 2 폴리뉴클레오타이드는 영양요구성 마커 유전자, 방향성 마커 유전자 또는 항생제 내성 유전자인 방법.
24. 제 21 또는 제 22 실시태양에 있어서,
비색성 마커 유전자는 aygA 유전자인 방법.
25. 제 21 내지 제 23 실시태양 중 어느 하나에 있어서,
영양요구성 마커 유전자는 argB 유전자, trpC 유전자, pyrG 유전자 또는 met3 유전자인 방법.
26. 제 21 내지 제 23 실시태양 중 어느 하나에 있어서,
방향성 마커 유전자는 아세트아미다아제(amdS) 유전자, 질산염 환원효소 유전자(nlaD) 또는 황산염 투과효소(Sut B) 유전자인 방법.
27. 제 23 실시태양에 있어서,
항생제 내성 유전자는 ble 유전자이며, ble 유전자는 페오마이신에 내성을 부여하는 방법.
28. 제 19 실시태양에 있어서,
제 1 선택 가능한 마커 유전자는 aygA 유전자이고 제 2 폴리뉴클레오타이드는 pyrG 유전자인 방법.
29. 제 20 내지 제 27 실시태양 중 어느 하나에 있어서,
제 1 선택 가능한 마커 유전자는 met3 유전자이고, 제 2 선택 가능한 마커 유전자는 aygA 유전자이고 제 2 폴리뉴클레오타이드는 pyrG 유전자인 방법.
30. 제 1 내지 제 29 실시태양 중 어느 하나에 있어서,
복수의 원형질체는 사상균류 세포의 배양액에서 사상균류 세포로부터 세포벽을 제거하는 단계; 복수의 원형질체를 분리하는 단계; 및 다이메틸 설폭사이드(DMSO)을 포함하는 혼합물에 분리된 복수의 원형질체를 재현탁하는 단계에 의해 제조되며, DMSO의 최종 농도가 7% v/v 이하인 방법
31. 제 30 실시태양에 있어서,
혼합물은 단계 a-d를 실행하기 전에 적어도 -20℃ 또는 -80℃에 저장되는 방법.
32. 제 30 또는 31 실시태양에 있어서,
배양액은 적어도 1리터의 부피인 방법.
33. 제 30 또는 31 실시태양에 있어서,
배양액은 원형질체의 제조에 이전에 적어도 12시간 동안 성장되는 방법
34. 제 30 내지 제 33 실시태양 중 어느 하나에 있어서,
균류 배양액은 적어도 70%의 원형질체가 더 작고 더 적은 핵을 함유하는 조건하에서 성장되는 방법.
35. 제 30 내지 제 34 실시태양 중 어느 하나에 있어서,
세포벽을 제거하는 단계는 효소 분해에 의해 실행되는 방법.
36. 제 35 실시태양에 있어서,
효소 분해는 베타-글루카나아제 및 폴리갈락투로나제를 포함하는 효소의 혼합물로 실행되는 방법.
37. 제 30 내지 제 36 실시태양 중 어느 하나에 있어서,
원형질체를 저장하기 전에 DMSO를 포함하는 혼합물에 40% v/v 폴리에틸렌 글리콜(PEG)을 첨가하는 단계를 더 포함하는 방법.
38. 제 37 실시태양에 있어서,
PEG는 8% v/v 이하의 최종 농도로 첨가되는 방법.
39. 제 1 내지 제 38 실시태양 중 어느 하나에 있어서,
단계 a-d는 자동화되는 방법.
40. 사상균류 세포를 포함하는 균류 배양액으로부터 원형질체를 제조하는 단계, 여기서 원형질체를 제조하는 단계는 균류 배양액의 사상균류 세포로부터 세포벽을 제거하는 것을 포함한다;
원형질체를 분리하는 단계; 및
분리된 원형질체를 7% v/v 이하의 최종 농도의 다이메틸 설폭사이드(DMSO)를 포함하는 혼합물에 재현탁시키는 단계를 포함하여 저장을 위한 사상균류 세포를 제조하는 방법.
41. 제 40 실시태양에 있어서,
혼합물은 적어도 -20℃ 또는 -80℃에서 저장되는 방법.
42. 제 40 내지 제 42 실시태양 중 어느 하나에 있어서,
균류 배양액은 적어도 1리터 부피인 방법.
43. 제 40 내지 제 42 실시태양 중 어느 하나에 있어서,
균류 배양액은 원형질체의 제조 전에 적어도 12시간 동안 성장되는 방법.
44. 제 40 내지 제 43 실시태양 중 어느 하나에 있어서,
균류 배양액은 적어도 70%의 원형질체가 더 작고 더 적은 핵을 함유하는 조건하에서 성장되는 방법.
45. 제 40 내지 제 44 실시태양 중 어느 하나에 있어서,
세포벽을 제거하는 단계는 효소 분해에 의해 실행되는 방법.
46. 제 45 실시태양에 있어서,
효소 분해는 베타-글루카나아제 및 폴리갈락투로나제를 포함하는 효소의 혼합물로 실행되는 방법.
47. 제 40 내지 제 46 실시태양 중 어느 하나에 있어서,
원형질체를 저장하기 전에 DMSO를 포함하는 혼합물에 40% v/v 폴리에틸렌 글리콜(PEG)을 첨가하는 단계를 더 포함하는 방법.
48. 제 47 실시태양에 있어서,
PEG는 8% v/v 이하의 최종 농도로 첨가되는 방법.
49. 제 40 내지 제 48 실시태양 중 어느 하나에 있어서,
원형질체를 저장하기 전에 원형질체를 미세적정 플레이트에 분배하는 단계를 더 포함하는 방법.
50. 제 40 내지 제 49 실시태양 중 어느 하나에 있어서,
균류 배양액의 사상균류 세포는 비 균사체 형성 표현형을 갖는 방법.
51. 제 40 내지 제 50 실시태양 중 어느 하나에 있어서,
균류 배양액의 사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프 또는 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
52. 제 50 실시태양에 있어서,
균류 배양액의 사상균류 세포는 아스퍼길루스 니거(Aspergillus niger) 또는 텔레모프 또는 아나모프인 방법.
53. 균류 생산 균주를 생성하기 위한 시스템으로서,
하나 이상의 프로세서; 및
하나 이상의 프로세서의 적어도 하나에 작동 가능하게 결합되고 하나 이상의 프로세서의 적어도 하나에 의해 실행될 때, 시스템이 다음 작업을 행하도록 저장된 명령을 갖는 하나 이상의 메모리를 포함하는 시스템:
a) 사상균류 세포의 배양액으로부터 유래된 복수의 원형질체를 제 1 구조체 및 제 2 구조체로 형질전환시킨다, 여기서 제 1 구조체는 원형질체의 게놈에서 제 1 유전자좌와 상동인 뉴클레오타이드가 양쪽면의 측면에 위치하는 제 1 폴리뉴클레오타이드를 포함하고 제 2 구조체는 원형질체의 게놈에서 제 2 유전자좌와 상동인 뉴클레오타이드가 양쪽면의 측면에 위치하는 제 2 폴리뉴클레오타이드를 포함하며, 형질전환은 상동성 재조합에 의해 제 1 구조체의 제 1 유전자좌로의 통합 및 제 2 구조체의 제 2 유전자좌로의 통합을 초래하며, 적어도 제 2 유전자좌는 원형질체 게놈에서 제 1 선택 가능한 마커 유전자이고 제 1 폴리뉴클레오타이드는 돌연변이 및/또는 유전자 제어 요소를 포함한다;
b) 선택 및 역선택을 수행함으로써 동핵성 형질전환체를 정제한다; 및
c) 사상균류 세포의 재생에 도움이 되는 배지에서 정제된 형질전환체를 성장시킨다.
54. 제 53 실시태양에 있어서,
제 1 구조체가 구조체 A 및 구조체 B로 분할되고, 구조체 A는 제 1 폴리뉴클레오타이드의 제 1 부분 및 제 1 폴리뉴클레오타이드의 제 1 부분에 대한 제 1 유전자좌 5'와 상동성인 뉴클레오타이드를 포함하고, 구조체 B는 제 1 폴리뉴클레오타이드의 제 2 부분 및 제 1 폴리뉴클레오타이드의 제 2 부분에 대한 제 1 유전자좌 3'와 상동성인 뉴클레오타이드를 포함하며, 제 1 폴리뉴클레오타이드의 제 1 부분 및 제 2 부분은 중첩 상보적 서열을 포함하는 방법.
55.제 53 또는 제 54 실시태양에 있어서,
제 1 구조체가 구조체 A 및 구조체 B로 분할되고, 구조체 A는 제 2 폴리뉴클레오타이드의 제 1 부분 및 제 2 폴리뉴클레오타이드의 제 1 부분에 대한 제 1 유전자좌 5'와 상동성인 뉴클레오타이드를 포함하고, 구조체 B는 제 2 폴리뉴클레오타이드의 제 2 부분 및 제 2 폴리뉴클레오타이드의 제 2 부분에 대한 제 1 유전자좌 3'와 상동성인 뉴클레오타이드를 포함하며, 제 2 폴리뉴클레오타이드의 제 1 부분 및 제 2 부분은 중첩 상보적 서열을 포함하는 방법.
56. 제 53 내지 제 55 실시태양 중 어느 하나에 있어서,
복수의 원형질체로부터 각각의 원형질체는 복수의 제 1 구조체로부터 단일의 제 1 구조체 및 복수의 제 2 구조체로부터 단일의 제 2 구조체로 형질전환되고, 복수의 제 1 구조체로부터의 각 제 1 구조체에서 제 1 폴리뉴클레오타이드는 상이한 돌연변이 및/또는 유전자 제어 요소를 포함하고; 복수의 제 2 구조체로부터의 각 제 2 구조체에서 제 2 폴리뉴클레오타이드는 동일한 시스템.
57. 제 53 내지 제 56 실시태양 중 어느 하나에 있어서,
사상균류 세포의 라이브러리를 생성하기 위해 단계 a-c를 반복하는 단계를 더 포함하며, 라이브러리에서 각각의 사상균류 세포는 상이한 돌연변이 및/또는 유전자 제어 요소를 갖는 제 1 폴리뉴클레오타이드를 포함하는 시스템.
58. 제 53 내지 제 57 실시태양 중 어느 하나에 있어서,
돌연변이는 단일 뉴클레오타이드 다형성인 시스템.
59. 제 53 내지 제 58 실시태양 중 어느 하나에 있어서,
유전자 제어 요소는 프로모터 서열 및/또는 터미네이터 서열인 시스템.
60. 제 53 내지 제 58 실시태양 중 어느 하나에 있어서,
유전자 제어 요소는 프로모터 서열이고, 프로모터 서열은 표 1에 열거된 프로모터 서열로부터 선택되는 방법.
61. 제 53 내지 제 60 실시태양 중 어느 하나에 있어서,
단계 a-c는 미세적정 플레이트의 웰에서 실행되는 시스템.
62. 제 61 실시태양에 있어서,
미세적정 플레이트는 96웰, 384웰 또는 1536웰 미세적정 플레이트인 시스템.
63. 제 53 내지 제 62 실시태양 중 어느 하나에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프 또는 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 시스템.
64. 제 53 내지 제 62 실시태양 중 어느 하나에 있어서,
사상균류 세포는 아스퍼길루스 니거(Aspergillus niger)인 시스템.
65. 제 53 내지 제 64 실시태양 중 어느 하나에 있어서,
사상균류 세포는 비 균사체 형성 표현형을 갖는 시스템.
66. 제 53 내지 제 65 실시태양 중 어느 하나에 있어서,
균류 세포는 비 기능성 비 상동성 말단 결합 경로를 갖는 시스템.
67. 제 66 실시태양에 있어서,
NHEJ 경로는 세포를 NHEJ 경로의 구성요소에 대항하는 항체, 화학적 억제제, 단백질 억제제, 물리적 억제제, 펩타이드 억제제 또는 안티-센스 또는 RNAi 분자에 노출시킴으로써 비 기능적으로 만들어지는 시스템.
68. 제 67 실시태양에 있어서,
화학적 억제제는 W-7인 시스템.
69. 제 53 내지 제 68 실시태양 중 어느 하나에 있어서,
제 1 유전자좌는 표적 사상균류 유전자를 위한 것인 시스템.
70. 제 53 내지 제 68 실시태양 중 어느 하나에 있어서,
제 1 유전자좌는 원형질체 게놈에서 제 2 선택 가능한 마커 유전자를 위한 것인 시스템.
71. 제 70 실시태야에 있어서,
제 2 선택 가능한 마커 유전자는 영양요구성 마커 유전자, 비색성 마커 유전자 또는 방향성 마커 유전자로부터 선택되는 시스템.
72. 제 53 내지 제 71 실시태양 중 어느 하나에 있어서,
제 1 선택 가능한 마커 유전자는 영양요구성 마커 유전자, 비색성 마커 유전자 또는 방향성 마커 유전자로부터 선택되는 시스템.
73. 제 53 내지 제 72 실시태양 중 어느 하나에 있어서,
제 2 폴리뉴클레오타이드는 영양요구성 마커 유전자, 방향성 마커 유전자 또는 항생제 내성 유전자로부터 선택되는 시스템.
74. 제 71 또는 제 72 실시태양에 있어서,
비색성 마커 유전자는 aygA 유전자인 시스템.
75. 제 71 내지 제 73 실시태양 중 어느 하나에 있어서,
제 71 항 또는 제 72 항에 있어서,
영양요구성 마커 유전자는 argB 유전자, trpC 유전자, pyrG 유전자 또는 met3 유전자로부터 선택되는 시스템.
76. 제 71 내지 제 73 실시태양 중 어느 하나에 있어서,
방향성 마커 유전자는 아세트아미다아제(amdS) 유전자, 질산염 환원효소 유전자(nlaD) 또는 황산염 투과효소(Sut B) 유전자로부터 선택되는 시스템.
77. 제 73 실시태양에 있어서,
항생제 내성 유전자는 ble 유전자이며, ble 유전자는 페오마이신에 내성을 부여하는 시스템.
78. 제 69 실시태양에 있어서,
제 1 선택 가능한 마커 유전자는 aygA 유전자이고 제 2 폴리뉴클레오타이드는 pyrG 유전자인 시스템.
79. 제 71 내지 제 73 실시태양 중 어느 하나에 있어서,
청구항 79
제 70 항에 있어서,
제 1 선택 가능한 마커 유전자는 met3 유전자이고, 제 2 선택 가능한 마커 유전자는 aygA 유전자이고 제 2 폴리뉴클레오타이드는 pyrG 유전자인 시스템.
80. 제 53 내지 제 79 실시태양 중 어느 하나에 있어서,
복수의 원형질체는 사상균류 세포의 배양액에서 사상균류 세포로부터 세포벽을 제거하는 단계; 복수의 원형질체를 분리하는 단계;
및 7% v/v 이하의 최종 농도로 다이메틸 설폭사이드(DMSO)을 포함하는 혼합물에 분리된 복수의 원형질체를 재현탁하는 단계에 의해 제조되는 시스템.
81. 제 80 실시태양에 있어서,
혼합물은 단계 a-c를 실행하기 전에 적어도 -20℃ 또는 -80℃로 저장되는 시스템.
82. 제 80 또는 제 81 실시태양에 있어서,
배양액은 적어도 1리터의 부피인 시스템.
83. 제 80 내지 제 82 실시태양 중 어느 하나에 있어서,
배양액은 원형질체의 제조에 이전에 적어도 12시간 동안 성장되는 시스템.
84. 제 80 내지 제 83 실시태양 중 어느 하나에 있어서,
균류 배양액은 적어도 70%의 원형질체가 더 작고 더 적은 핵을 함유하는 조건하에서 성장되는 시스템.
85. 제 80 내지 제 83 실시태양 중 어느 하나에 있어서,
세포벽을 제거하는 단계는 효소 분해에 의해 실행되는 시스템.
86. 제 85 실시태양에 있어서,
효소 분해는 베타-글루카나아제 및 폴리갈락투로나제를 포함하는 효소의 혼합물로 실행되는 시스템.
87. 제 53 내지 제 86 실시태양 중 어느 하나에 있어서,
원형질체를 저장하기 전에 DMSO를 포함하는 혼합물에 40% v/v 폴리에틸렌 글리콜(PEG)을 첨가하는 단계를 더 포함하는 시스템.
88. 제 87 실시태양에 있어서,
PEG는 8% v/v 이하의 최종 농도로 첨가되는 시스템.
89. 다음 단계를 포함하여 원하는 표현형을 획득하기 위해 사상균류를 진화시키는 게놈 공학의 고 처리량(HTP) 방법:
a. 동일한 게놈 균주 배경을 갖는 초기의 복수의 사상균류의 게놈을 교란시켜 독특한 유전자 변이를 갖는 개별 사상균류 균주를 포함하는 초기 HTP 유전자 디자인 사상균류 균주 라이브러리를 생성하는 단계;
b. 원하는 표현형을 위한 초기 HTP 유전자 디자인 사상균류 균주 라이브러리의 개별 균주를 선별 및 선택하는 단계;
c. 선행 단계에서 선별된 적어도 두 개의 개별 사상균류 균주에 존재하는 유전자 변이로부터 선택된 유전자 변이의 독특한 조합을 각각 포함하는 후속 복수의 사상균류 미생물을 제공하여 후속 HTP 유전자 디자인 사상균류 균주 라이브러리를 생성하는 단계;
d. 원하는 표현형을 위한 후속 HTP 유전자 디자인 사상균류 균주 라이브러리의 개별 사상균류 균주를 선별 및 선택하는 단계;
e. 사상균류 미생물이 원하는 표현형을 획득할 때까지 선형 또는 비선형 방식으로 단계 c)-d)를 1회 이상 반복하는 단계, 여기서 각각의 후속 반복은 선행 HTP 유전자 디자인 사상균류 균주 라이브러리의 적어도 두 개의 개별 사상균류 균주 중에서 선택된 유전자 변이의 조합인 독특한 유전자 변이를 제공하는 개별 사상균류 균주를 포함하는 새로운 HTP 유전자 디자인 사상균류 균주 라이브러리를 생성한다.
90. 제 89 실시태양에 있어서,
초기 HTP 유전자 디자인 사상균류 균주 라이브러리는 프로모터 스왑 미생물 균주 라이브러리, SNP 스왑 미생물 균주 라이브러리, 개시/정지 코돈 미생물 균주 라이브러리, 최적화된 서열 미생물 균주 라이브러리, 터미네이터 스왑 미생물 균주 라이브러리, 및 이들의 임의의 조합으로 이루어진 그룹으로부터 선택된 적어도 하나를 포함하는 게놈 공학의 HTP 방법.
91. 제 89 실시태양에 있어서,
초기 HTP 유전자 디자인 사상균류 균주 라이브러리는 프로모터 스왑 미생물 균주 라이브러리를 포함하는 게놈 공학의 HTP 방법.
92. 제 89 실시태양에 있어서,
초기 HTP 유전자 디자인 사상균류 균주 라이브러리는 하나 이상의 BCD (bicistronic design) 조절 서열을 함유하는 프로모터 스왑 미생물 균주 라이브러리를 포함하는 게놈 공학의 HTP 방법.
93. 제 89 실시태양에 있어서,
초기 HTP 유전자 디자인 사상균류 균주 라이브러리는 SNP 스왑 미생물 균주 라이브러리를 포함하는 게놈 공학의 HTP 방법.
94. 제 89 실시태양에 있어서,
초기 HTP 유전자 디자인 사상균류 균주 라이브러리가 다음을 포함하는 미생물 균주 라이브러리를 포함하는 게놈 공학의 HTP 방법:
a. 키메라 생합성 효소를 암호화하는 하나 이상의 폴리뉴클레오타이드로서, 상기 키메라 생합성 효소는 :
i. 사상균류에서 조절 경로에 관여하는 효소;
ii. DNA 결합 부위에 결합할 수 있는 DNA 결합 도메인에 번역적으로 융합되고; 및
b. 키메라 생합성 효소의 DNA 결합 도메인에 상응하는 DNA 결합 부위를 포함하는 적어도 하나의 DNA 스캐폴드 서열.
95. 제 89 실시태양에 있어서,
후속 HTP 유전자 디자인 사상균류 균주 라이브러리는 초기 HTP 유전자 디자인 사상균류 균주 라이브러리에서 유전자 변이로부터 유래된 완전한 조합 균주 라이브러리인 게놈 공학의 HTP 방법.
96. 제 89 실시태양에 있어서,
후속 HTP 유전자 디자인 사상균류 균주 라이브러리는 초기 HTP 유전자 디자인 사상균류 균주 라이브러리에서 유전자 변이로부터 유래된 완전한 조합 균주 라이브러리의 서브세트인 게놈 공학의 HTP 방법.
97. 제 89 실시태양에 있어서,
후속 HTP 유전자 디자인 사상균류 균주 라이브러리는 선행 HTP 유전자 디자인 사상균류 균주 라이브러리에서 유전자 변이로부터 유래된 완전한 조합 균주 라이브러리인 게놈 공학의 HTP 방법.
98. 제 89 실시태양에 있어서,
후속 HTP 유전자 디자인 사상균류 균주 라이브러리는 선행 HTP 유전자 디자인 사상균류 균주 라이브러리에서 유전자 변이로부터 유래된 완전한 조합 균주 라이브러리의 서브세트인 게놈 공학의 HTP 방법.
99. 제 89 실시태양에 있어서,
게놈을 교란시키는 단계는 랜덤 돌연변이유발, 표적 서열 삽입, 표적 서열 결실, 표적 서열 교체, 및 이의 임의의 조합으로 이루어진 그룹으로부터 선택된 적어도 하나의 방법을 사용하는 단계를 포함하는 게놈 공학의 HTP 방법.
100. 제 89 실시태양에 있어서,
초기 복수의 사상균류 미생물은 산업용 생산 사상균류 균주로부터 유도된 독특한 유전자 변이를 포함하는 게놈 공학의 HTP 방법.
101. 제 89 실시태양에 있어서,
초기 복수의 사상균류 미생물은 S1Gen1으로 표시된 산업용 생산 균주 미생물 및 SnGenn으로 표시된 이로부터 유도된 임의의 수의 후속 미생물 세대를 포함하는 게놈 공학의 HTP 방법.
102. 제 89 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 게놈 공학의 HTP 방법.
103. 제 89 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 게놈 공학의 HTP 방법.
104. 다음 단계를 포함하는 SNP 스왑 사상균류 균주 라이브러리를 생성하는 방법:
a. 기준 사상균류 균주 및 제 2 사상균류 균주를 제공하는 단계, 여기서 제 2 사상균류 균주는 기준 사상균류 균주에 존재하지 않는 단일 뉴클레오타이드 다형성, DNA 삽입 및 DNA 결실로부터 선택된 복수의 확인된 유전자 변이를 포함한다; 및
b. 기준 사상균류 균주 또는 제 2 사상균류 균주의 게놈을 교란시켜 상기 복수의 개별 균주의 각각의 균주 내에서 발견된 독특한 유전자 변이를 갖는 복수의 개별 사상균류 균주를 포함하는 초기 SNP 스왑 사상균류 균주 라이브러리를 생성하는 단계, 상기 각각의 독특한 유전자 변이는 기준 사상균류 균주와 제 2 사상균류 균주 사이의 복수의 확인된 유전자 변이로부터 선택된 단일 유전자 변이에 상응한다.
105. 제 104 실시태양에 있어서,
기준 사상균류 균주의 게놈이 제 2 사상균류 균주에서 발견되는 확인된 단일 뉴클레오타이드 다형성, DNA 삽입, 또는 DNA 결실 중 하나 이상을 첨가하도록 교란되는 방법.
106. 제 104 실시태양에 있어서,
제 2 사상균류 균주의 게놈이 기준 사상균류 균주에서 발견되는 않는 확인된 단일 뉴클레오타이드 다형성, DNA 삽입 또는 DNA 결실 중 하나 이상을 제거하도록 교란되는 방법.
107. 제 104 실시태양에 있어서,
독특한 유전자 변이를 갖는 생성된 복수의 개별 사상균류 균주가 함께 참조 사상균류 균주 및 제 2 사상균류 균주 사이의 모든 확인된 유전자 변이의 완전한 조합 라이브러리를 포함하는 방법.
108. 제 104 실시태양에있어서,
독특한 유전자 변이를 갖는 생성된 복수의 개별 사상균류 균주가 함께 사상균류 균주 및 제 2 사상균류 균주 사이의 모든 확인된 유전자 변이의 완전한 조합 라이브러리의 서브세트를 포함하는 방법.
109.제 104 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
110. 제 104 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 방법.
111. 다음 단계를 포함하는 생산 사상균류 균주의 표현형 성능을 재건 및 개량시키는 방법:
a. 부모 계통의 사상균류 균주 및 이로부터 유도된 생산 사상균류 균주를 제공하는 단계, 여기서 생산 사상균류 균주는 부모 계통 미생물 균주에 존재하지 않는 단일 뉴클레오타이드 다형성, DNA 삽입 및 DNA 결실로부터 선택된 복수의 확인된 유전자 변이를 포함한다;
b. 부모 계통 사상균류 균주 또는 생산 사상균류 균주의 게놈을 교란시켜, 사상균류 균주의 초기 라이브러리를 생성하는 단계, 여기서 초기 라이브러리에서 각 균주는 부모 계통 사상균류 균주 및 생산 사상균류 균주 사이의 복수의 확인된 유전자 변이로부터의 독특한 유전자 변이를 포함한다;
c. 기준 사상균류 균주에 대한 표현형 성능 개량을 위한 초기 라이브러리의 개별 균주를 선별 및 선택하여 표현형 성능 개량을 부여하는 독특한 유전자 변이를 확인하는 단계;
d. 선행 단계에서 선별된 적어도 2개의 개별 사상균류 균주에 존재하는 유전자 변이로부터 선택된 유전자 변이의 독특한 조합을 각각 포함하는 후속 복수의 사상균류 미생물을 제공하여 후속 사상균류 균주 라이브러리를 생성하는 단계;
e. 기준 사상균류 균주에 대한 표현형 성능 개량을 위한 후속 라이브러리의 개별 균주 선별 및 선택하여 추가 표현형 성능 개량을 부여하는 유전자 변이의 독특한 조합을 확인하는 단계; 및
f. 사상균류 균주가 생산 사상균류 균주의 표현형 성능에 비해 원하는 수준의 개량된 표현형 성능을 나타낼 때까지 선형 또는 비선형 방식으로 단계 d)-e)를 1회 이상 반복하는 단계, 여기서 각각의 후속 반복은 미생물 균주의 새로운 라이브러리를 생성하며, 새로운 라이브러리에서 각 균주는 선행 라이브러리의 적어도 두 개의 개별 사상균류 균주 중에서 선택된 유전자 변이의 조합인 유전자 변이를 포함한다.
112. 제 111 실시태양에 있어서,
사상균류 균주의 초기 라이브러리는 부모 계통 사상균류 균주와 생산 사상균류 균주 사이의 확인된 유전자 변이를 모두 포함하는 완전 조합 라이브러리인 방법.
113. 제 111 실시태양에 있어서,
사상균류 균주의 초기 라이브러리는 부모 계통 사상균류 균주와 생산 사상균류 균주 사이의 확인된 유전자 변이를 모두 포함하는 완전 조합 라이브러리의 서브세트인 방법.
114. 제 111 실시태양에 있어서,
사상균류 균주의 후속 라이브러리는 초기 라이브러리의 완전한 조합 라이브러리인 방법.
115. 제 111 실시태양에 있어서,
사상균류 균주의 후속 라이브러리는 초기 라이브러리의 완전한 조합 라이브러리의 서브세트인 방법.
116. 제 111 실시태양에 있어서,
사상균류 균주의 후속 라이브러리가 선행 라이브러리의 완전한 조합 라이브러리인 방법.
117. 제 111 실시태양에 있어서,
사상균류 균주의 후속 라이브러리가 선행 라이브러리의 완전한 조합 라이브러리의 서브세트인 방법.
118. 제 111 실시태양에 있어서,
부모 계통 사상균류 균주의 게놈은 생산 사상균류 균주에서 발견되는 확인된 단일 뉴클레오타이드 다형성, DNA 삽입 또는 DNA 결실의 하나 이상을 첨가하도록 교란되는 방법.
119. 제 111 실시태양에 있어서,
생산 사상균류 균주의 게놈은 부모 계통 사상균류 균주에서 발견되지 않은 확인된 단일 뉴클레오타이드 다형성, DNA 삽입 또는 DNA 결실의 하나 이상을 제거하도록 교란되는 방법.
120. 제 111 실시태양에 있어서,
게놈을 교란시키는 단계는 랜덤 돌연변이 유발, 표적화된 서열 삽입, 표적화 된 서열 결실, 표적화된 서열 대체, 및 이들의 조합으로 이루어진 그룹으로부터 선택된 적어도 하나의 방법을 이용하는 것을 포함하는 방법.
121. 제 111 실시태양에 있어서,
단계 d)-e)는 후속 라이브러리의 생산 사상균류 균주의 표현형 성능이 생산 사상균류 균주의 표현형 성능과 비교하여 측정된 표현형 변수에서 적어도 10% 증가를 나타낼 때까지 반복되는 방법.
122. 제 111 실시태양에 있어서,
단계 d)-e)는 후속 라이브러리의 생산 사상균류 균주의 표현형 성능이 생산 사상균류 균주의 표현형 성능과 비교하여 측정된 표현형 변수에서 적어도 1배 증가를 나타낼 때까지 반복되는 방법.
123. 제 111 실시태양에 있어서,
단계 f)의 개선된 표현형 성능은 관심 생성물의 부피 생산성, 관심 생성물의 비생산성, 관심 생성물의 수율, 관심 생성물의 역가 및 이들의 조합으로 이루어진 그룹으로부터 선택되는 방법.
124. 제 111 실시태양에 있어서,
단계 f)의 개선된 표현형 성능은 소분자, 효소, 펩타이드, 아미노산, 유기산, 합성 화합물, 연료, 알코올, 1차 세포외 대사 산물, 2차 세포외 대사 산물, 세포내 성분 분자 및 이들의 조합으로 이루어진 그룹으로부터 선택된 관심 생성물의 증가되거나 더욱 효율적인 생산인 방법.
125. 제 111 실시태양에 있어서,
확인된 유전자 변이는 프로모터 스왑 라이브러리로부터 인공 프로모터 스왑 유전자 변이를 추가로 포함하는 방법.
126. 제 111 실시태양에 있어서,
사상균류 균주의 초기 라이브러리, 또는
사상균류 균주의 후속 라이브러리의 적어도 하나 이상의 미생물 균주의 게놈을 조작하여 내인성 사상균류 표적 유전자에 작동 가능하게 연결된 프로모터 래더로부터의 하나 이상의 프로모터를 포함하게 하는 단계를 추가로 포함하는 방법.
127. 제 111 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
128. 제 111 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 방법.
129. 다음 단계를 포함하여 프로모터 스왑 사상균류 라이브러리를 생성하는 방법:
a. 기본 사상균류 균주에 내인성인 복수의 표적 유전자 및 프로모터 래더를 제공하는 단계, 여기서 상기 프로모터 래더는 기본 사상균류 균주에서 상이한 발현 프로파일을 나타내는 복수의 프로모터를 포함한다; 및
b. 기본 사상균류 균주의 게놈을 조작하여, 상기 복수의 개별 사상균류 균주의 각 균주 내에서 발견된 독특한 유전적 변이를 갖는 복수의 개별 사상균류 균주를 포함하는 초기 프로모터 스왑 사상균류 균주 라이브러리를 생성하는 단계, 여기서 상기 독특한 유전자 변이의 각각은 기본 사상균류 균주에 내인성인 표적 유전자 중 하나에 작동 가능하게 연결된 프로모터 래더로부터의 하나 이상의 프로모터를 포함한다.
130. 제 129 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
131. 제 129 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 방법.
132. 다음 단계를 포함하는 생산 사상균류 균주의 표현형 성능을 개량시키기 위한 프로모터 스왑 방법:
a. 기본 사상균류 균주 및 프로모터 래더에 내인성인 복수의 표적 유전자를 제공하는 단계, 여기서 상기 프로모터 래더는 기본 사상균류 균주에서 상이한 발현 프로파일을 나타내는 복수의 프로모터를 포함한다; 및
b. 기본 사상균류 균주의 게놈을 조작하여, 상기 복수의 개별 사상균류 균주의 각 균주 내에서 발견된 독특한 유전적 변이를 갖는 복수의 개별 사상균류 균주를 포함하는 초기 프로모터 스왑 사상균류 균주 라이브러리를 생성하는 단계, 여기서 상기 독특한 유전자 변이의 각각은 기본 사상균류 균주에 내인성인 표적 유전자 중 하나에 작동 가능하게 연결된 프로모터 래더로부터의 하나 이상의 프로모터를 포함한다.
c. 기준 사상균류 균주에 대한 표현형 성능 개량을 위한 초기 프로모터 스왑 사상균류 균주 라이브러리의 개별 사상균류 균주를 선별 및 선택하여 표현형 성능 개량을 부여하는 독특한 유전자 변이를 확인하는 단계;
d. 선행 단계에서 선별된 적어도 2개의 개별 사상균류 균주에 존재하는 유전자 변이로부터 선택된 유전자 변이의 독특한 조합을 각각 포함하는 후속 복수의 사상균류 미생물을 제공하여 후속 프로모터 스왑 사상균류 균주 라이브러리를 생성하는 단계;
e. 기준 사상균류 균주에 대한 표현형 성능 개량을 위한 후속 프로모터 스왑 사상균류 균주 라이브러리의 개별 사상균류 균주 선별 및 선택하여 추가 표현형 성능 개량을 부여하는 유전자 변이의 독특한 조합을 확인하는 단계; 및
f. 사상균류 균주가 생산 사상균류 균주의 표현형 성능에 비해 원하는 수준의 개량된 표현형 성능을 나타낼 때까지 선형 또는 비선형 방식으로 단계 d)-e)를 1회 이상 반복하는 단계, 여기서 각각의 후속 반복은 미생물 균주의 새로운 프로모터 스왑 사상균류 균주 라이브러리를 생성하며, 새로운 라이브러리에서 각 균주는 선행 라이브러리의 적어도 두 개의 개별 사상균류 균주 중에서 선택된 유전자 변이의 조합인 유전자 변이를 포함한다.
133. 제 132 실시태양에 있어서,
후속 프로모터 스왑 사상균류 균주 라이브러리는 초기 프로모터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리인 프로모터 스왑 방법.
134. 제 132 실시태양에 있어서,
후속 프로모터 스왑 사상균류 균주 라이브러리는 초기 프로모터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리의 서브세트인 프로모터 스왑 방법.
135. 제 132 실시태양에 있어서,
후속 프로모터 스왑 사상균류 균주 라이브러리는 선행 프로모터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리인 프로모터 스왑 방법.
136. 제 132 실시태양에 있어서,
후속 프로모터 스왑 사상균류 균주 라이브러리는 선행 프로모터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리의 서브세트인 프로모터 스왑 방법.
137. 제 132 실시태양에 있어서,
단계 d)-e)는 후속 프로모터 스왑 사상균류 균주 라이브러리의 사상균류 균주의 표현형 성능이 생산 사상균류 균주의 표현형 성능과 비교하여 측정된 표현형 변수에서 적어도 10% 증가를 나타낼 때까지 반복되는 프로모터 스왑 방법.
138. 제 132 실시태양에 있어서,
단계 d)-e)는 후속 프로모터 스왑 사상균류 균주 라이브러리의 사상균류 균주의 표현형 성능이 생산 사상균류 균주의 표현형 성능과 비교하여 측정된 표현형 변수에서 적어도 1배 증가를 나타낼 때까지 반복되는 프로모터 스왑 방법.
139. 제 132 실시태양에 있어서,
단계 f)의 개선된 표현형 성능은 관심 생성물의 부피 생산성, 관심 생성물의 비생산성, 관심 생성물의 수율, 관심 생성물의 역가 및 이들의 조합으로 이루어진 그룹으로부터 선택되는 프로모터 스왑 방법.
140. 제 132 실시태양에 있어서,
단계 f)의 개선된 표현형 성능은 소분자, 효소, 펩타이드, 아미노산, 유기산, 합성 화합물, 연료, 알코올, 1차 세포외 대사 산물, 2차 세포외 대사 산물, 세포내 성분 분자 및 이들의 조합으로 이루어진 그룹으로부터 선택된 관심 생성물의 증가되거나 더욱 효율적인 생산인 프로모터 스왑 방법.
141. 제 132 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 프로모터 스왑 방법.
142. 제 132 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 프로모터 스왑 방법.
143. 다음 단계를 포함하는 터미네이터 스왑 사상균류 균주 라이브러리를 생성하는 방법:
a. 기본 사상균류 균주 및 터미네이터 래더에 내인성인 복수의 표적 유전자를 제공하는 단계, 여기서 상기 터미네이터 래더는 기본 사상균류 균주에서 상이한 발현 프로파일을 나타내는 복수의 프로모터를 포함한다; 및
b. 기본 사상균류 균주의 게놈을 조작하여, 상기 복수의 개별 사상균류 균주의 각 균주 내에서 발견된 독특한 유전적 변이를 갖는 복수의 개별 사상균류 균주를 포함하는 초기 터미네이터 스왑 사상균류 균주 라이브러리를 생성하는 단계, 여기서 상기 독특한 유전자 변이의 각각은 기본 사상균류 균주에 내인성인 표적 유전자 중 하나에 작동 가능하게 연결된 터미네이터 래더로부터의 하나 이상의 터미네이터를 포함한다.
144. 제 143 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
145. 제 143 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 방법.
146. 다음 단계를 포함하는 생산 사상균류 균주의 표현형 성능을 개량시키기 위한 터미네이터 스왑 방법:
a. 기본 사상균류 균주 및 터미네이터 래더에 내인성인 복수의 표적 유전자를 제공하는 단계, 여기서 상기 터미네이터 래더는 기본 사상균류 균주에서 상이한 발현 프로파일을 나타내는 복수의 터미네이터를 포함한다; 및
b. 기본 사상균류 균주의 게놈을 조작하여, 상기 복수의 개별 사상균류 균주의 각 균주 내에서 발견된 독특한 유전적 변이를 갖는 복수의 개별 사상균류 균주를 포함하는 초기 터미네이터 스왑 사상균류 균주 라이브러리를 생성하는 단계, 여기서 상기 독특한 유전자 변이의 각각은 기본 사상균류 균주에 내인성인 표적 유전자 중 하나에 작동 가능하게 연결된 터미네이터 래더로부터의 하나 이상의 터미네이터를 포함한다.
c. 기준 사상균류 균주에 대한 표현형 성능 개량을 위한 초기 터미네이터 스왑 사상균류 균주 라이브러리의 개별 사상균류 균주를 선별 및 선택하여 표현형 성능 개량을 부여하는 독특한 유전자 변이를 확인하는 단계;
d. 선행 단계에서 선별된 적어도 2개의 개별 사상균류 균주에 존재하는 유전자 변이로부터 선택된 유전자 변이의 독특한 조합을 각각 포함하는 후속 복수의 사상균류 미생물을 제공하여 후속 터미네이터 스왑 사상균류 균주 라이브러리를 생성하는 단계;
e. 기준 사상균류 균주에 대한 표현형 성능 개량을 위한 후속 터미네이터 스왑 사상균류 균주 라이브러리의 개별 사상균류 균주 선별 및 선택하여 추가 표현형 성능 개량을 부여하는 유전자 변이의 독특한 조합을 확인하는 단계; 및
f. 사상균류 균주가 생산 사상균류 균주의 표현형 성능에 비해 원하는 수준의 개량된 표현형 성능을 나타낼 때까지 선형 또는 비선형 방식으로 단계 d)-e)를 1회 이상 반복하는 단계, 여기서 각각의 후속 반복은 미생물 균주의 새로운 터미네이터 스왑 사상균류 균주 라이브러리를 생성하며, 새로운 라이브러리에서 각 균주는 선행 라이브러리의 적어도 두 개의 개별 사상균류 균주 중에서 선택된 유전자 변이의 조합인 유전자 변이를 포함한다.
147. 제 146 실시태양에 있어서,
후속 터미네이터 스왑 사상균류 균주 라이브러리는 초기 터미네이터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리인 터미네이터 스왑 방법.
148. 제 146 실시태양에 있어서,
후속 터미네이터 스왑 사상균류 균주 라이브러리는 초기 터미네이터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리의 서브세트인 터미네이터 스왑 방법.
149. 제 146 실시태양에 있어서,
후속 터미네이터 스왑 사상균류 균주 라이브러리는 선행 터미네이터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리인 터미네이터 스왑 방법.
150. 제 146 실시태양에 있어서,
후속 터미네이터 스왑 사상균류 균주 라이브러리는 선행 터미네이터 스왑 사상균류 균주 라이브러리의 완전한 조합 라이브러리의 서브세트인 터미네이터 스왑 방법.
151. 제 146 실시태양에 있어서,
단계 d)-e)는 후속 터미네이터 스왑 사상균류 균주 라이브러리의 사상균류 균주의 표현형 성능이 생산 사상균류 균주의 표현형 성능과 비교하여 측정된 표현형 변수에서 적어도 10% 증가를 나타낼 때까지 반복되는 터미네이터 스왑 방법.
152. 제 146 실시태양에 있어서,
단계 d)-e)는 후속 터미네이터 스왑 사상균류 균주 라이브러리의 사상균류 균주의 표현형 성능이 생산 사상균류 균주의 표현형 성능과 비교하여 측정된 표현형 변수에서 적어도 1배 증가를 나타낼 때까지 반복되는 터미네이터 스왑 방법.
153. 제 146 실시태양에 있어서,
단계 f)의 개선된 표현형 성능은 관심 생성물의 부피 생산성, 관심 생성물의 비생산성, 관심 생성물의 수율, 관심 생성물의 역가 및 이들의 조합으로 이루어진 그룹으로부터 선택되는 터미네이터 스왑 방법.
154. 제 146 실시태양에 있어서,
단계 f)의 개선된 표현형 성능은 소분자, 효소, 펩타이드, 아미노산, 유기산, 합성 화합물, 연료, 알코올, 1차 세포외 대사 산물, 2차 세포외 대사 산물, 세포내 성분 분자 및 이들의 조합으로 이루어진 그룹으로부터 선택된 관심 생성물의 증가되거나 더욱 효율적인 생산인 터미네이터 스왑 방법.
155. 제 146 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 터미네이터 스왑 방법.
156. 제 146 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 터미네이터 스왑 방법.
157. 숙주 세포의 내인성 유전자에 작동 가능하게 연결된 프로모터를 포함하는 사상균류 숙주 세포로서, 여기서 프로모터는 내인성 유전자와 이종성이며, 프로모터는 SEQ ID Nos. 1-4로 이루어진 그룹으로부터 선택된 서열을 갖는 사상균류 숙주 세포.
158. 제 157 실시태양에 있어서,
사상균류 숙주 세포는 내인성 유전자에 작동 가능하게 연결된 프로모터 없이 기준 사상균류 균주의 표현형 성능과 비교하여 개량된 표현형 성능의 원하는 수준을 갖는 사상균류 숙주 세포.
159. 제 157 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 터미네이터 사상균류 숙주 세포.
160. 제 157 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 사상균류 숙주 세포.
161. 사상균류 균주 라이브러리로서, 여기서 라이브러리 내 각각의 사상균류 균주는 숙주 세포의 내인성 유전자에 작동 가능하게 연결된 프로모터를 포함하며, 프로모터는 내인성 유전자와 이종성이며, 프로모터는 SEQ ID Nos. 1-4로 이루어진 그룹으로부터 선택된 서열을 갖는 사상균류 균주 라이브러리.
162. 제 161 실시태양에 있어서,
사상균류 세포는 아클리아(Achlya), 아크레모니움(Acremonium), 아스페르길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프, 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 터미네이터 사상균류 균주 라이브러리.
163. 제 161 실시태양에 있어서,
사상균류는 아스퍼길루스 니거인 사상균류 균주 라이브러리.
164. 다음을 포함하여 단일 균류 포자로부터 유래된 클론 집단을 분리하는 방법:
(a) 액체 현탁액에 복수의 균류 포자를 제공하는 단계, 여기서 복수의 균류 포자는 균류 균주로부터 유래되었다;
(b) 이산 체적의 액체 현탁액을 복수의 반응 영역을 포함하는 기질의 개별 반응 영역에 분배하는 단계, 여기서 복수의 반응 영역의 각 반응 영역은 성장 매질을 포함하며, 여기서 분배는 적어도 개별 반응 영역의 적어도 75%는 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함한다;
(c) 성장 배지를 포함하는 반응 영역에서 분배된 하나의 생존 가능한 균류 포자를 배양하는 단계; 및
(d) 반응 영역에서 성장하는 클론 집단을 선택하여 하나의 균류 포자로부터 유래된 클론 집단을 분리하는 단계.
165. 제 164 실시태양에 있어서,
이산 체적의 하나의 균류 포자의 존재 또는 부재에 대해 이산 체적을 스크리닝하는 단계를 추가로 포함하며, 하나의 균류 포자를 함유하는 이산 체적만이 단계(b)에 대해 선택되는 방법.
166. 제 165 실시태양에 있어서,
분배는 개별 반응 영역의 적어도 80%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
167. 제 165 실시태양에 있어서,
분배는 개별 반응 영역의 적어도 90%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
168. 제 165 실시태양에 있어서,
분배는 개별 반응 영역의 적어도 95%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
169. 제 165 실시태양에 있어서,
분배는 개별 반응 영역의 적어도 99%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
170. 제 165 실시태양에 있어서,
분배는 개별 반응 영역의 실질적으로 전부가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
171. 제 165 내지 제 171 실시태양 중 어느 하나에 있어서,
이산 체적의 스크리닝은 이산 체적에서 단일 균류 포자의 존재 또는 부재를 광학적으로 구별하는 것을 수반하는 방법.
172. 제 171 실시태양에 있어서,
스크리닝은 이산 체적의 하나의 균류 포자의 존재 또는 부재를 광학적으로 구별할 수 있는 미세 유체 장치를 사용하여 수행되는 방법.
173. 다음을 포함하여 단일 균류 포자로부터 유래된 클론 집단을 분리하는 방법:
(a) 액체 현탁액에 복수의 균류 포자를 제공하는 단계, 여기서 복수의 균류 포자는 균류 균주로부터 유래되었다;
(b) 액체 현탁액을 희석하는 단계, 여기서 희석은 제한 희석이다;
(c) 이산 체적의 액체 현탁액을 복수의 반응 영역을 포함하는 기질의 개별 반응 영역에 분배하는 단계, 여기서 복수의 반응 영역의 각 반응 영역은 성장 매질을 포함하며, 여기서 제한 희석은 각각의 반응 영역에 분배된 희석의 이산 체적이 푸아송 분포를 따르는 생존 가능한 포자를 하나 또는 전혀 포함하지 않을 확률을 초래하며, 이에 의해 복수의 반응 영역에서 반응 영역의 90% 초과가 생존 가능한 포자를 함유하지 않으며 하나 이상의 생존 가능한 포자를 함유하는 반응 영역의 90% 초과는 단지 하나의 생존 가능한 포자를 함유한다;
(d) 성장 배지를 포함하는 반응 영역에서 분배된 하나의 생존 가능한 균류 포자를 배양하는 단계; 및
(e) 반응 영역에서 성장하는 클론 집단을 선택하여 하나의 균류 포자로부터 유래된 클론 집단을 분리하는 단계.
174. 제 164 내지 제 173 실시태양 중 어느 하나에 있어서,
반응 영역은 미세적정 플레이트에 존재하는 방법.
175. 제 174 실시태양에 있어서,
미세적정 플레이트는 96웰, 384웰 또는 1536웰을 함유하는 방법.
176. 제 164 내지 제 173 실시태양 중 어느 하나에 있어서,
균류 균주는 사상균류 균주인 방법.
177. 제 176 실시태양에 있어서,
사상균류 균주는 아클리아(Achlya), 아크레모니움(Acremonium), 아스퍼길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프 또는 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
178. 제 177 실시태양에 있어서,
사상균류 균주는 아스퍼길루스 니거 또는 이의 텔레모프 또는 아니모프인 방법.
179. 제 178 실시태양에 있어서,
사상균류 세포는 비 균사체 펠렛 형태를 갖는 방법.
180. 제 179 실시태양에 있어서,
사상균류 균주는 S. 세레비지애(S. cerevisiae) SLN1 유전자의 오르쏘로그의 돌연변이 형태를 발현하는 방법.
181. 제 180 실시태양에 있어서,
S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그의 돌연변이 형태의 핵산 서열은 SEQ ID NO: 13인 방법.
182. 제 179 또는 제 180 실시태양에 있어서,
S. 세레비지애 SLN1 유전자의 오르쏘로그의 돌연변이 형태는 SEQ ID NO: 1 또는 2로부터 선택된 프로모터 서열에 작동 가능하게 연결되는 방법.
183. 제 164 내지 제 182 실시태양 중 어느 한 하나에 있어서,
균류 균주는 유전자 교란을 갖는 방법.
184. 제 183 실시태양에 있어서,
유전자 교란은 단일 뉴클레오타이드 다형성, DNA 삽입, DNA 결실 또는 이들의 임의의 조합으로부터 선택되는 방법.
185. 제 183 또는 제 184 실시태양에 있어서,
유전자 교란은 원형질체를 리보핵단백질 복합체(RNP-복합체)로 형질전환시킴으로써 균류 균주로부터 유래된 원형질체로 도입되는 방법.
186. 제 185 실시태양에 있어서,
RNP-복합체는 가이드 RNA(gRNA)와 복합체화된 RNA 가이드된(guided) 엔도뉴클레아제를 포함하는 방법.
187. 제 186 실시태양에 있어서,
RNA 가이드된 엔도뉴클레아제는 클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제인 방법.
188. 제 187 실시태양에 있어서,
클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제는 타입 II, 타입 V 또는 타입 VI RNA 가이드된 엔도뉴클레아제인 방법.
189. 제 187 실시태양에 있어서,
클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제는 Cas9, Cas12a, Cas12b, Cas12c, Cas12d, Cas12e, Cas13a, Cas13b, Cas13c 또는 이의 동족체, 오쏘로그, 돌연변이체, 변이체 또는 변형된 버전으로부터 선택되는 방법.
190. 제 189 실시태양에 있어서,
클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제는 Cas9 또는 이의 동족체, 오쏘로그 또는 파라로그인 방법.
191. 제 186 실시태양에 있어서,
gRNA는 CRISPR RNA (crRNA) 단독이거나 트랜스 활성화 CRISPR RNA(tracrRNA)에 어닐링된 CRISPR RNA (crRNA)인 방법.
192. 제 186 실시태양에 있어서,
gRNA는 tracrRNA 및 crRNA를 포함하는 단일 가이드 RNA(sgRNA)인 방법.
193. 제 191 또는 제 192 실시태양에 있어서,
crRNA는 균류 균주의 게놈 내의 표적 유전자에 상보적인 가이드 서열을 포함하고, 여기서 원형질체 내로의 RNP-복합체의 도입은 표적 유전자 내로의 유전적 교란의 도입을 용이하게 하는 방법.
194. 제 193 실시태양에 있어서,
표적 유전자의 유전자 교란은 표적 유전자에서 DNA 말단을 생성하기 위한 RNP-복합체에 의해 표적 유전자의 절단과 이후 비-상동성 말단 결합(NHEJ) 경로에 의한 표적 유전자에서 DNA 말단의 비 동종 말단 결합에 의해 촉진되는 방법.
195. 제 193 실시태양에 있어서,
돌연변이된 버전의 표적 유전자를 포함하는 공여체 DNA를 공동-형질전환시키는 단계를 추가로 포함하며, 여기서 돌연변이된 버전의 표적 유전자는 표적 유전자 유전자좌에 상동성인 뉴클레오타이드에 의해 양쪽면 상에 플랭킹되는 방법.
196. 제 195 실시태양에 있어서,
표적 유전자의 유전자 교란은 표적 유전자에서 DNA 말단을 생성하기 위한 RNP-복합체에 의해 표적 유전자의 절단과 이후 상동성 재조합을 통한 표적 유전자의 공여자 DNA에 의한 대체에 의해 촉진되는 방법.
197. 제 185 항 내지 제 196 실시태양 중 어느 하나에 있어서,
단계(b)는 선택 가능한 마커를 포함하는 벡터를 공동-형질전환시키는 단계를 추가로 포함하는 방법.
198. 제 197 실시태양에 있어서,
선택 가능한 마커는 형질전환 적격 균류 균주로부터 유래된 클론 집단을 선택하기 위해 단계 (d) 동안 사용되는 방법.
199. 제 183 또는 제 184 실시태양에 있어서,
유전자 교란은 복수의 원형질체를 제 1 구조체 및 제 2 구조체로 형질전환시킴으로써 균류 균주로부터 유래된 원형질체 내로 도입되고, 여기서 제 1 구조체는 제 1 유전자좌에 상동성인 뉴클레오타이드에 의해 양쪽면 상에 플랭킹된 제 1 폴리뉴클레오타이드를 포함하며 제 2 구조체는 원형질체의 게놈에서,제 2 유전자좌에 상동성인 뉴클레오타이드에 의해 양쪽면 상에 플랭킹된 제 2 폴리뉴클레오타이드를 포함하고, 여기서 형질전환은 상동성 재조합에 의한 제 1 구조체의 제 1 유전자좌로의 통합 및 제 2 구조체의 제 2 유전자좌로의 통합을 초래하며, 여기서 적어도 제 2 유전자좌는 원형질체 게놈에서 제 1 선택 가능한 마커 유전자이고, 제 1 폴리뉴클레오타이드는 유전자 교란을 포함하는 방법.
200. 제 199 실시태양에 있어서,
선택 가능한 마커 유전자는 유전자 교란을 포함하는 균류 균주로부터 유래된 클론 집단의 선택을 용이하게 하기 위해 단계 (d) 동안 사용되는 방법.
201. 제 195 내지 제 200 실시태양 중 어느 하나에 있어서,
균류 균주는 비 기능적 비 동종 말단 결합 (NHEJ) 경로를 보유하는 방법.
202. 제 201 실시태양에 있어서,
NHEJ 경로는 균류 균주를 NHEJ 경로의 구성요소에 대항하는 항체, 화학적 억제제, 단백질 억제제, 물리적 억제제, 펩타이드 억제제 또는 안티-센스 또는 RNAi 분자의 성분에 노출시킴으로써 비 기능적으로 만들어지는 방법.
203. 제 202 실시태양에 있어서,
화학적 억제제는 W-7인 방법.
204. 다음을 포함하는 사상균류 균주를 생산하는 방법:
a) 복수의 원형질체를 제공하는 단계, 여기서 원형질체는 사상균류 세포의 배양액으로부터 제조된다;
b) 복수의 원형질체로부터의 각각의 원형질체를 리보핵단백질 복합체(RNP-복합체)로 형질전환시키는 단계; 및
c) 부모 사상균류 균주에 대한 표현형 성능 개량을 위해 형질전환된 원형질체로부터 유래된 개별 사상균류 균주를 선택하고 선별함으로써 표현형 성능 개량을 제공하는 선택된 개별 사상균주 균주의 게놈에서 유전자 교란을 확인하는 단계.
205. 제 204 실시태양에 있어서,
유전자 교란은 단일 뉴클레오타이드 다형성, DNA 삽입, DNA 결실 또는 이들의 임의의 조합으로부터 선택되는 방법.
206. 제 204 또는 제 205 실시태양에 있어서,
RNP-복합체는 가이드 RNA(gRNA)와 복합체화된 RNA 가이드된(guided) 엔도뉴클레아제를 포함하는 방법.
207. 제 206 실시태양에 있어서,
RNA 가이드된 엔도뉴클레아제는 클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제인 방법.
208. 제 207 실시태양에 있어서,
클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제는 타입 II, 타입 V 또는 타입 VI RNA 가이드된 엔도뉴클레아제인 방법.
209. 제 207 실시태양에 있어서,
클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제는 Cas9, Cas12a, Cas12b, Cas12c, Cas12d, Cas12e, Cas13a, Cas13b, Cas13c 또는 이의 동족체, 오쏘로그, 돌연변이체, 변이체 또는 변형된 버전으로부터 선택되는 방법.
210. 제 209 실시태양에 있어서,
클래스 2 CRISPR-Cas 시스템 RNA 가이드된 엔도뉴클레아제는 Cas9 또는 이의 동족체, 오쏘로그 또는 파라로그인 방법.
211. 제 206 실시태양에 있어서,
gRNA는 CRISPR RNA (crRNA) 단독이거나 트랜스 활성화 CRISPR RNA(tracrRNA)에 어닐링된 CRISPR RNA (crRNA)인 방법.
212. 제 206 실시태양에 있어서,
gRNA는 tracrRNA 및 crRNA를 포함하는 단일 가이드 RNA(sgRNA)인 방법.
213. 제 211 또는 제 212 실시태양에 있어서,
crRNA는 균류 균주의 게놈 내의 표적 유전자에 상보적인 가이드 서열을 포함하고, 여기서 원형질체 내로의 RNP-복합체의 도입은 표적 유전자 내로의 유전적 교란의 도입을 용이하게 하는 방법.
214. 제 213 실시태양에 있어서,
표적 유전자의 유전자 교란은 표적 유전자에서 DNA 말단을 생성하기 위한 RNP-복합체에 의해 표적 유전자의 절단과 이후 비-상동성 말단 결합(NHEJ) 경로에 의한 표적 유전자에서 DNA 말단의 비 동종 말단 결합에 의해 촉진되는 방법.
215. 제 213 실시태양에 있어서,
단계(b)는 돌연변이된 버전의 표적 유전자를 포함하는 공여체 DNA를 공동-형질전환시키는 단계를 추가로 포함하며, 여기서 돌연변이된 버전의 표적 유전자는 표적 유전자 유전자좌에 상동성인 뉴클레오타이드에 의해 양쪽면 상에 플랭킹되는 방법.
216. 제 215 실시태양에 있어서,
표적 유전자의 유전자 교란은 표적 유전자에서 DNA 말단을 생성하기 위한 RNP-복합체에 의해 표적 유전자의 절단과 이후 상동성 재조합을 통한 표적 유전자의 공여자 DNA에 의한 대체에 의해 촉진되는 방법.
217. 제 204 내지 제 216 실시태양 중 어느 하나에 있어서,
단계(b)는 선택 가능한 마커를 포함하는 벡터를 공동-형질전환시키는 단계를 추가로 포함하는 방법.
218. 제 217 실시태양에 있어서,
선택 가능한 마커는 부모 사상균류 균주에 대한 표현형 성능 개량을 위한 후속 선별을 위한 형질전환 적격 개별 사상균류 균주를 선택하기 위해 단계 (c) 동안 사용되는 방법.
219. 제 215 내지 제 218 실시태양 중 어느 하나에 있어서,
부모 사상균류 균주는 비 기능적 비 동종 말단 결합 (NHEJ) 경로를 보유하는 방법.
220. 제 219 실시태양에 있어서,
NHEJ 경로는 균류 균주를 NHEJ 경로의 구성요소에 대항하는 항체, 화학적 억제제, 단백질 억제제, 물리적 억제제, 펩타이드 억제제 또는 안티-센스 또는 RNAi 분자의 성분에 노출시킴으로써 비 기능적으로 만들어지는 방법.
221. 제 220 실시태양에 있어서,
화학적 억제제는 W-7인 방법.
222. 제 204 내지 제 221 실시태양 중 어느 하나에 있어서,
사상균류 균주의 표현형 성능 개량은 부모 사상균류 균주의 표현형 성능과 비교하여 관심 생성물에 대해 측정된 표현형 변수의 적어도 10% 증가를 포함하는 방법.
223. 제 204 내지 제 221 실시태양 중 어느 하나에 있어서,
사상균류 균주의 표현형 성능 개량은 부모 사상균류 균주의 표현형 성능과 비교하여 관심 생성물에 대해 측정된 표현형 변수의 적어도 1배 증가를 포함하는 방법.
224. 제 222 또는 제 223 실시태양에 있어서,
측정된 표현형 변수는 관심 생성물의 부피 생산성, 관심 생성물의 특정 생산성, 관심 생성물의 수율, 관심 생성물의 역가 및 이들의 조합으로 이루어진 그룹으로부터 선택되는 방법.
225. 제 222 또는 제 223 실시태양에 있어서,
측정된 표현형 변수는 관심 생성물의 증가되거나 보다 효율적인 생산인 방법.
226. 제 222 또는 제 223 실시태양에 있어서,
관심 생성물은 소분자, 효소, 펩타이드, 아미노산, 유기산, 합성 화합물, 연료, 알코올, 1차 세포 외 대사 산물, 2차 세포 외 대사 산물, 세포 내 성분 분자 및 이들의 조합으로 이루어진 그룹으로부터 선택되는 방법.
227. 제 204 내지 제 226 실시태양 중 어느 하나에 있어서,
부모 사상균류 균주는 아클리아(Achlya), 아크레모니움(Acremonium), 아스퍼길루스(Aspergillus), 아우레오바시디움(Aureobasidium), 비제르칸데라(Bjerkandera), 세리포리오프시스(Ceriporiopsis), 세팔로스포리움(Cephalosporium), 크리소스포리움(Chrysosporium), 코칠리오불루스(Cochliobolus), 코리나스쿠스(Corynascus), 크리포넥트리아(Cryphonectria), 크립토콕쿠스(Cryptococcus), 코프리누스(Coprinus), 코리오루스(Coriolus), 디플로디아(Diplodia), 엔도디스(Endothis), 푸사리움(Fusarium), 지베렐라(Gibberella), 글리오클라디움(Gliocladium), 휴미콜라(Humicola), 하이포크레아(Hypocrea), 미셀리오프토라(Myceliophthora)(e.g., Myceliophthora thermophila), 뮤코르(Mucor), 뉴로스포라(Neurospora), 페니실린(Penicillium), 포도스포라(Podospora), 플레비아(Phlebia), 피로미세스(Piromyces), 피리쿨라리아(Pyricularia), 리조뮤코르(Rhizomucor), 리조푸스(Rhizopus), 스키조필룸(Schizophyllum), 시스탈리듐(Scytalidium), 스포로트리쿰(Sporotrichum), 탈라로마이세스(Talaromyces), 써모아스쿠스(Thermoascus), 티에라비아(Thielavia), 트라마테스(Tramates), 톨리포클라디움(Tolypocladium), 트리코더마(Trichoderma), 버티실리움(Verticillium), 볼바리엘라(Volvariella) 종 또는 텔레모프 또는 아나모프 및 이의 동의어 또는 분류학 동의어로부터 선택되는 방법.
228. 제 227 실시태양에 있어서,
사상균류 균주는 아스퍼길루스 니거 또는 이의 텔레모프 또는 아니모프인 방법.
229. 제 228 실시태양에 있어서,
사상균류 세포는 비 균사체 펠렛 형태를 갖는 방법.
230. 제 229 실시태양에 있어서,
사상균류 균주는 S. 세레비지애(S. cerevisiae) SLN1 유전자의 오르쏘로그의 돌연변이 형태를 발현하는 방법.
231. 제 230 실시태양에 있어서,
S. 세레비지애 SLN1 유전자의 A. 니거 오르쏘로그의 돌연변이 형태의 핵산 서열은 SEQ ID NO: 13인 방법.
232. 제 230 또는 제 231 실시태양에 있어서,
S. 세레비지애 SLN1 유전자의 오르쏘로그의 돌연변이 형태는 SEQ ID NO: 1 또는 2로부터 선택된 프로모터 서열에 작동 가능하게 연결되는 방법.
233. 제 204 내지 제 232 실시태양 중 어느 하나에 있어서,
단계(c) 이전에 개별 사상균류 균주로부터 유래된 분리된 클론 집단을 생성하는 단계를 추가로 포함하는 방법.
234. 제 233 실시태양에 있어서,
분리는 다음을 포함하는 방법: (i) 형질전환된 원형질체를 복수의 균류 포자를 생성하도록 유도하는 단계, 여기서 복수의 균류 포자로부터의 각각의 균류 포자는 하나의 형질전환된 원형질체로부터 유래된다;
(ii) 하나의 형질전환된 원형질체로부터 유래된 복수의 균류 포자를 액체에 재현탁시켜 액체 현탁액을 생성하는 단계;
(iii) 이산 체적의 액체 현탁액을 복수의 반응 영역을 포함하는 기질의 개별 반응 영역에 분배하는 단계, 여기서 복수의 반응 영역의 각 반응 영역은 성장 매질을 포함하며, 여기서 분배는 적어도 개별 반응 영역의 적어도 75%는 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함한다; 및
(iv) 성장 배지를 포함하는 반응 영역에서 분배된 하나의 생존 가능한 균류 포자를 배양하여 개별 사상균류 균주로부터 유래된 분리된 클론 집단을 생성하는 단계.
235. 제 234 실시태양에 있어서,
이산 체적에서 하나의 균류 포자의 존재 또는 부재를 광학적으로 선별하는 방법을 추가로 포함하며, 여기서 하나의 균류 포자를 함유하는 이산 체적만이 단계(iii)에 대해 선택되는 방법.
236. 제 235 실시태양에 있어서,
분배는 개별 반응 영역의 적어도 80%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
237. 제 235 실시태양에 있어서,
분배는 개별 반응 영역의 적어도 90%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
238. 제 234 실시태양에 있어서,
분배는 개별 반응 영역의 적어도 95%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
239. 제 234 항에 있어서,
분배는 개별 반응 영역의 적어도 99%가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
240. 제 234 실시태양에 있어서,
분배는 개별 반응 영역의 실질적으로 전부가 복수의 균류 포자로부터의 하나 이하의 생존 가능한 균류 포자를 포함하지 않을 가능성을 초래하는 방법.
241. 제 235 실시태양에 있어서,
이산 체적의 스크리닝은 이산 체적에서 단일 균류 포자의 존재 또는 부재를 광학적으로 구별하는 것을 수반하는 방법.
242. 제 231 실시태양에 있어서,
스크리닝은 이산 체적의 하나의 균류 포자의 존재 또는 부재를 광학적으로 구별할 수 있는 미세 유체 장치를 사용하여 수행되는 방법.
243. 제 233 실시태양에 있어서,
분리는 다음을 포함하는 방법: (i) 형질전환된 원형질체를 복수의 균류 포자를 생성하도록 유도하는 단계, 여기서 복수의 균류 포자로부터의 각각의 균류 포자는 하나의 형질전환된 원형질체로부터 유래된다; (ii) 하나의 형질전환된 원형질체로부터 유래된 복수의 균류 포자를 액체에 재현탁시켜 액체 현탁액을 생성하는 단계; (iii) 액체 현탁액을 희석하는 단계, 여기서 희석은 제한 희석이다; (c) 이산 체적의 액체 현탁액을 복수의 반응 영역을 포함하는 기질의 개별 반응 영역에 분배하는 단계, 여기서 복수의 반응 영역의 각 반응 영역은 성장 매질을 포함하며, 여기서 제한 희석은 각각의 반응 영역에 분배된 희석의 이산 체적이 푸아송 분포를 따르는 생존 가능한 포자를 하나 또는 전혀 포함하지 않을 확률을 초래하며, 이에 의해 복수의 반응 영역에서 반응 영역의 90% 초과가 생존 가능한 포자를 함유하지 않으며 하나 이상의 생존 가능한 포자를 함유하는 반응 영역의 90% 초과는 단지 하나의 생존 가능한 포자를 함유한다; (v) 성장 배지를 포함하는 반응 영역에서 분배된 하나의 생존 가능한 균류 포자를 배양하는 단계; 및 (vi) 반응 영역에서 성장하는 클론 집단을 선택하여 하나의 균류 포자로부터 유래된 클론 집단을 분리하는 단계.
244. 제 234 내지 제 243 실시태양 중 어느 하나에 있어서,
반응 영역은 미세적정 플레이트에 존재하는 방법.
245. 제 244 실시태양에 있어서,
미세적정 플레이트는 96웰, 384웰 또는 1536웰을 함유하는 방법.
본 발명에 인용된 모든 참고문헌, 기사, 간행물, 특허, 특허 간행물 및 특허 출원은 모든 목적을 위해 그 전문이 참조로 포함된다. 그러나 본 발명에 언급된 모든 참고문헌, 기사, 출판물, 특허, 특허 간행물 및 특허 출원은 세계 어느 나라에서든 유효한 선행 기술을 구성하거나 보통의 일반 지식의 일부를 구성한다는 인정 또는 어떠한 형태의 제안으로 간주되어서는 안 된다.
또한, 다음의 특정 출원이 본 qkfaud에 참고로 포함된다: 20016년 12월30일에 출원된 미국 출원 No. 15/396,230 (U.S. Pub. No. US 2017/0159045 A1); 2016년 12월 7일에 출원된 PCT/US2016/065465(WO 2017/100377 A1); 2016년 4월27일에 출원된 미국 출원 No. 15/140,296 (US 2017/0316353 A1); 2017년 4월26일에 출원된 PCT/US2017/029725 (WO 2017/189784 A1); 2016년 12월7일에 출원된 PCT/US2016/ 065464(WO 2017/100376 A2); 2016년 12월7일에 출원된 미국 출원 No. 62/431,409, 2015년 12월7일에 출원된 미국 특허 No. 62/264,232; 및 2016년 7월 29일에 출원된 No. 62/368,786. 또한, 다음 특정 출원이 본 발명에 참조로 포함된다: 2017년 12월 29일에 출원된 PCT / US2017 / 069086; 및 2016년 12월 30일에 출원된 제 No. 62/441,040.