RU2201932C2 - Модифицированные в боковой цепи эпотилоны - Google Patents
Модифицированные в боковой цепи эпотилоны Download PDFInfo
- Publication number
- RU2201932C2 RU2201932C2 RU99120378/04A RU99120378A RU2201932C2 RU 2201932 C2 RU2201932 C2 RU 2201932C2 RU 99120378/04 A RU99120378/04 A RU 99120378/04A RU 99120378 A RU99120378 A RU 99120378A RU 2201932 C2 RU2201932 C2 RU 2201932C2
- Authority
- RU
- Russia
- Prior art keywords
- epothilone
- modified
- oxide
- epothilones
- protected
- Prior art date
Links
- 238000000034 method Methods 0.000 claims abstract description 32
- 150000001204 N-oxides Chemical class 0.000 claims abstract description 12
- 238000006243 chemical reaction Methods 0.000 claims abstract description 11
- 125000003158 alcohol group Chemical group 0.000 claims abstract description 3
- 238000006735 epoxidation reaction Methods 0.000 claims abstract description 3
- 150000002118 epoxides Chemical class 0.000 claims abstract description 3
- 238000001465 metallisation Methods 0.000 claims abstract description 3
- 229930013356 epothilone Natural products 0.000 claims description 31
- HESCAJZNRMSMJG-KKQRBIROSA-N epothilone A Chemical class C/C([C@@H]1C[C@@H]2O[C@@H]2CCC[C@@H]([C@@H]([C@@H](C)C(=O)C(C)(C)[C@@H](O)CC(=O)O1)O)C)=C\C1=CSC(C)=N1 HESCAJZNRMSMJG-KKQRBIROSA-N 0.000 claims description 30
- HESCAJZNRMSMJG-HGYUPSKWSA-N epothilone A Natural products O=C1[C@H](C)[C@H](O)[C@H](C)CCC[C@H]2O[C@H]2C[C@@H](/C(=C\c2nc(C)sc2)/C)OC(=O)C[C@H](O)C1(C)C HESCAJZNRMSMJG-HGYUPSKWSA-N 0.000 claims description 10
- 150000003883 epothilone derivatives Chemical class 0.000 claims description 10
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 claims description 8
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 claims description 8
- 238000010934 O-alkylation reaction Methods 0.000 claims description 8
- 238000004519 manufacturing process Methods 0.000 claims description 7
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 6
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 claims description 6
- 229910052739 hydrogen Inorganic materials 0.000 claims description 6
- 239000001257 hydrogen Substances 0.000 claims description 6
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 6
- 125000000217 alkyl group Chemical group 0.000 claims description 5
- 150000001875 compounds Chemical class 0.000 claims description 5
- 239000003153 chemical reaction reagent Substances 0.000 claims description 4
- ASQQEOXYFGEFKQ-UHFFFAOYSA-N dioxirane Chemical compound C1OO1 ASQQEOXYFGEFKQ-UHFFFAOYSA-N 0.000 claims description 4
- 150000004965 peroxy acids Chemical class 0.000 claims description 4
- 125000005843 halogen group Chemical group 0.000 claims description 3
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 claims description 2
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 claims description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 claims description 2
- QXRSDHAAWVKZLJ-OXZHEXMSSA-N Epothilone B Natural products O=C1[C@H](C)[C@H](O)[C@@H](C)CCC[C@@]2(C)O[C@H]2C[C@@H](/C(=C\c2nc(C)sc2)/C)OC(=O)C[C@H](O)C1(C)C QXRSDHAAWVKZLJ-OXZHEXMSSA-N 0.000 claims description 2
- 150000008064 anhydrides Chemical class 0.000 claims description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 claims description 2
- 239000003054 catalyst Substances 0.000 claims description 2
- 238000003776 cleavage reaction Methods 0.000 claims description 2
- 229910000071 diazene Inorganic materials 0.000 claims description 2
- RAABOESOVLLHRU-UHFFFAOYSA-N diazene Chemical compound N=N RAABOESOVLLHRU-UHFFFAOYSA-N 0.000 claims description 2
- 230000002255 enzymatic effect Effects 0.000 claims description 2
- QXRSDHAAWVKZLJ-PVYNADRNSA-N epothilone B Chemical compound C/C([C@@H]1C[C@@H]2O[C@]2(C)CCC[C@@H]([C@@H]([C@@H](C)C(=O)C(C)(C)[C@@H](O)CC(=O)O1)O)C)=C\C1=CSC(C)=N1 QXRSDHAAWVKZLJ-PVYNADRNSA-N 0.000 claims description 2
- 229910052736 halogen Inorganic materials 0.000 claims description 2
- 150000002367 halogens Chemical class 0.000 claims description 2
- 125000005842 heteroatom Chemical group 0.000 claims description 2
- 230000003301 hydrolyzing effect Effects 0.000 claims description 2
- 229910052751 metal Inorganic materials 0.000 claims description 2
- 239000002184 metal Substances 0.000 claims description 2
- 238000007254 oxidation reaction Methods 0.000 claims description 2
- 230000007017 scission Effects 0.000 claims description 2
- 125000000218 acetic acid group Chemical group C(C)(=O)* 0.000 claims 3
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 claims 2
- 150000002440 hydroxy compounds Chemical class 0.000 claims 1
- 239000000126 substance Substances 0.000 abstract 2
- 230000015572 biosynthetic process Effects 0.000 abstract 1
- 230000000694 effects Effects 0.000 abstract 1
- 238000005984 hydrogenation reaction Methods 0.000 abstract 1
- 238000003786 synthesis reaction Methods 0.000 abstract 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 96
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 24
- 239000000243 solution Substances 0.000 description 14
- 239000000047 product Substances 0.000 description 13
- 239000002904 solvent Substances 0.000 description 11
- 238000005160 1H NMR spectroscopy Methods 0.000 description 10
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 7
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 6
- 239000000203 mixture Substances 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- 238000012746 preparative thin layer chromatography Methods 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical compound [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 3
- 235000019341 magnesium sulphate Nutrition 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 238000004809 thin layer chromatography Methods 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 2
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000012230 colorless oil Substances 0.000 description 2
- FFHWGQQFANVOHV-UHFFFAOYSA-N dimethyldioxirane Chemical compound CC1(C)OO1 FFHWGQQFANVOHV-UHFFFAOYSA-N 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 239000011888 foil Substances 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- 238000002953 preparative HPLC Methods 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 235000010265 sodium sulphite Nutrition 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- -1 trimethyloxonium tetrafluoroborate Chemical compound 0.000 description 2
- FCCNKYGSMOSYPV-DEDISHTHSA-N (-)-Epothilone E Natural products O=C1[C@H](C)[C@H](O)[C@@H](C)CCC[C@H]2O[C@H]2C[C@@H](/C(=C\c2nc(CO)sc2)/C)OC(=O)C[C@H](O)C1(C)C FCCNKYGSMOSYPV-DEDISHTHSA-N 0.000 description 1
- UWKQJZCTQGMHKD-UHFFFAOYSA-N 2,6-di-tert-butylpyridine Chemical compound CC(C)(C)C1=CC=CC(C(C)(C)C)=N1 UWKQJZCTQGMHKD-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- YNJSNEKCXVFDKW-UHFFFAOYSA-N 3-(5-amino-1h-indol-3-yl)-2-azaniumylpropanoate Chemical compound C1=C(N)C=C2C(CC(N)C(O)=O)=CNC2=C1 YNJSNEKCXVFDKW-UHFFFAOYSA-N 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical class OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- 239000012043 crude product Substances 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 238000002451 electron ionisation mass spectrometry Methods 0.000 description 1
- FCCNKYGSMOSYPV-UHFFFAOYSA-N epothilone E Natural products O1C(=O)CC(O)C(C)(C)C(=O)C(C)C(O)C(C)CCCC2OC2CC1C(C)=CC1=CSC(CO)=N1 FCCNKYGSMOSYPV-UHFFFAOYSA-N 0.000 description 1
- FCCNKYGSMOSYPV-OKOHHBBGSA-N epothilone e Chemical compound C/C([C@@H]1C[C@@H]2O[C@@H]2CCC[C@@H]([C@@H]([C@@H](C)C(=O)C(C)(C)[C@@H](O)CC(=O)O1)O)C)=C\C1=CSC(CO)=N1 FCCNKYGSMOSYPV-OKOHHBBGSA-N 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- MWOOGOJBHIARFG-UHFFFAOYSA-N vanillin Chemical compound COC1=CC(C=O)=CC=C1O MWOOGOJBHIARFG-UHFFFAOYSA-N 0.000 description 1
- FGQOOHJZONJGDT-UHFFFAOYSA-N vanillin Natural products COC1=CC(O)=CC(C=O)=C1 FGQOOHJZONJGDT-UHFFFAOYSA-N 0.000 description 1
- 235000012141 vanillin Nutrition 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/04—Ortho-condensed systems
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Epoxy Compounds (AREA)
- Polyesters Or Polycarbonates (AREA)
- Other Resins Obtained By Reactions Not Involving Carbon-To-Carbon Unsaturated Bonds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Silicon Polymers (AREA)
Abstract
Изобретение относится к способу получения модифицированных в 16,17-положении эпотилонов, согласно которому защищенные в положении 3,7 или незащищенные эпотилоны А или В а) гидрируют по двойной связи в положении 16,17 либо в) по двойной связи в положении 16,17 проводят эпоксидирование и в случае необходимости полученный эпоксид восстанавливают до спирта в положении 16, к способу получения эпотилон-N-оксидов, при котором защищенные в положении 3,7 или незащищенные эпотилоны А или В переводят в N-оксид, полученный N-оксид при необходимости подвергают реакции Катара; способу получения модифицированных в С-19 положении эпотилонов путем металлизирования в положении С-19 защищенных или незащищенных эпотилонов А или В, а также к модифицированным эпотилонам общей формулы I. 5 с. и 12 з.п.ф-лы, 1 табл.
Description
Известны эпотилоны А и В (см., например, заявки DE 4138042, WO 9310121, WO 9719086).
Известный уровень техники предлагает эпотилоны А и В в качестве терапевтических средств. В журнале PNAS USA, 95 (1998) 1369-1374, эпоталоны упоминаются в качестве ценных терапевтических средств. Благодаря их терапевтическим действиям в журнале Angew. Chem. Int. Ed., 36 (1997) 2097-2103, предусмотрено даже создание обширной библиотеки подобного рода соединений (extensive library of compounds).
Итак, настоящее изобретение относится к способу получения модифицированных в положении 16, 17 эпотилонов, согласно которому защищенные в положении 3, 7 или незащищенные эпотилоны А и В
а) либо гидрируют по двойной связи в положении 16, 17, либо
б) к двойной связи в положении 16, 17 присоединяют атом галогена, либо
в) по двойной связи в положении 16, 17 проводят эпоксидирование и в случае необходимости полученный эпоксид восстанавливают до спирта в положении 16.
а) либо гидрируют по двойной связи в положении 16, 17, либо
б) к двойной связи в положении 16, 17 присоединяют атом галогена, либо
в) по двойной связи в положении 16, 17 проводят эпоксидирование и в случае необходимости полученный эпоксид восстанавливают до спирта в положении 16.
Предлагаемый согласно изобретению способ отличается тем, что в случае
- способа (а) гидрируют диимином или водородом в присутствии гетерогенного или гомогенного металлического катализатора или в случае
- способа (в) эпоксидируют надкислотой или диоксираном.
- способа (а) гидрируют диимином или водородом в присутствии гетерогенного или гомогенного металлического катализатора или в случае
- способа (в) эпоксидируют надкислотой или диоксираном.
Далее, изобретение относится к способу получения 2,3-ненасыщенных эпотилон -N-оксидов, при котором либо
(i) защищенные в положении 3, 7 эпотилоны А или В известным образом переводят в N-оксид и с помощью основания удаляют заместитель в положении 3 с получением двойной связи в положении 2, 3, либо
(ii) защищенные или незащищенные в положении 7 эпотилоны А или В, имеющие в положении 2, 3 двойную связь, известным образом переводят в N-оксид и
в случае необходимости полученный N-оксид подвергают O-алкилированию, в результате чего получают соответствующий продукт О-алкилирования.
(i) защищенные в положении 3, 7 эпотилоны А или В известным образом переводят в N-оксид и с помощью основания удаляют заместитель в положении 3 с получением двойной связи в положении 2, 3, либо
(ii) защищенные или незащищенные в положении 7 эпотилоны А или В, имеющие в положении 2, 3 двойную связь, известным образом переводят в N-оксид и
в случае необходимости полученный N-оксид подвергают O-алкилированию, в результате чего получают соответствующий продукт О-алкилирования.
Далее, настоящее изобретение относится к способу получения эпотилон-N-оксидов, при котором защищенные в положении 3, 7 или незащищенные эпотилоны А или В известным образом переводят в N-оксид, и полученный N-оксид в случае необходимости подвергают O-алкилированию, в результате чего получают соответствующий продукт O-алкилирования.
Предлагаемый согласно изобретению способ может отличаться тем, что N-оксидирование осуществляют с помощью надкислоты или диоксирана, а для необязательного 0-алкилирования используют электрофильные алкильные, арильные или гетероарильные реагенты, в частности, метилйодид или триметилоксоний-тетрафторборат.
Далее, предлагаемый способ может отличаться тем, что полученный N-оксид подвергают реакции Катада, в частности, в соответствии со справочником Houben-Weyl, т. Е7b, стр. 646.
Далее, предлагаемый способ может отличаться тем, что реакцию Катада осуществляют с помощью активированного производного карбоновой кислоты, в частности ее ангидрида или хлорангидрида.
Далее, предлагаемый способ может отличаться тем, что реакцию каталитического гидрирования Катада осуществляют с помощью ацетангидрида и полученные 21-ацетоксиэпотилоны в случае необходимости известным образом расщепляют до 21-оксиэпотилонов А или В (эпотилоны Е и F соответственно).
Далее, предлагаемый способ может отличаться тем, что необязательное расщепление проводят гидролитическим или ферментативным путем.
Далее, изобретение относится к способу получения модифицированных в С-19 положении эпотилонов, согласно которому защищенные в положении 3, 7 или незащищенные эпотилоны А или В металлизируют в положении С-19 и известным образом с помощью электрофильных реагентов улавливают в виде модифицированных в положении С-19 алкил-, арил-, гетероарил-, галоген-, кислород- или серозамещенных эпотилонов.
Предлагаемый способ может отличаться тем, что металлизацию проводят с помощью бутиллития.
Далее, изобретение относится к способу получения модифицированных в С-27 положении эпотилонов, при котором аллильную группу в положениях С-17, С-16 и С-27 известным образом по С-27-метильной группе замещают гетероатомом.
Предлагаемый способ может отличаться тем, что С-27-метильную группу замещают атомом брома, в частности, с помощью N-бромсукцинимида, и полученный бромид в случае необходимости переводят в С-27-окси-соединение.
Наконец, настоящее изобретение относится к соединениям, полученным по предлагаемому способу.
ПРИМЕР 1: ДИЭПОКСИЭПОТИЛОН А. (1а)
К раствору эпотилона А (5 мг, 10 мкмоль) в ацетоне (1 мл) при 0oС добавляют диметилдиоксиран (0,4 мл, 28 мкмоль, 0,07 М в ацетоне). Температуру полученного раствора в течение нескольких часов доводят до комнатной температуры, при которой продолжают перемешивать в течение 20 ч. Поскольку по данным ТСХ устанавливают наличие остатка исходного продукта, добавляют потом еще диметилдиоксиран (0,25 мл, 17 мкмоль) и перемешивают реакционную смесь еще в течение 20 часов при комнатной температуре. Наконец, удаляют растворитель и остаток очищают с помощью метода препаративной тонкослойной хроматографии (ПСХ) (0,25 х 200 х 200 мм, 10% МеОН:CH2Cl2). В результате выделяют следующие продукты:
1. 1,4 мг (27%) диэпоксиэпотилона А (смесь 3:2 эпимеров в положениях 16 и 17). Rf 0,63 (10% МеОН:CH2Cl2); Rt: 6,79 (изомер 1) и 7,39 (изомер 2) мин (RP 18, 250 х 4 мм, МеОН:H2O 65:35, 1 мл/мин); МС: (m/z)=510 (M+); 1H-ЯМР (400 МГц, CDCl3, выбранные сигналы, изомер 1): δ=6,96 (с, 1Н, Н-19), 5,48 (дд, J=12,2 и 2,5 Гц, 1Н, Н-15), 4,37 (дш, J=10,7 Гц, 1Н, Н-3), 4,10 (с, 1Н, Н-17), 3,67 (дд, J=5,6 и 2,5 Гц, 1Н, Н-7), 3,14 (квд, J=6,6 и 2,5 Гц, 1Н, Н-6), 3,00 (ддд, J=9,7, 3,6 и 2,5 Гц, 1Н, Н-13), 2,88 (дт, J=8,6 и 3,6 Гц, 1Н, Н-12), 2,71 (с, 3Н, Н-21), 2,53 (дд, J=13,7 и 11,7 Гц, 1Н, Н-2а), 1,41 (с, 3Н, Н-22), 1,27 (с, 3Н, Н-26), 1,17 (д, J=6,6 Гц, 3Н, Н-24), 1,08 (с, 3Н, Н-23), 0,97 (д, J=7,1 Гц, 3Н, Н-25); (изомер 2) δ=6,98 (с, 1Н, Н-19), 5,11 (дд, J=11,7 и 2,5 Гц, 1Н, Н-15) 4,27 (дш, J=10,7 Гц, 1Н, Н-3), 4,14 (с, 1Н, Н-17), 3,06 (квд, J=6,6 и 2,9 Гц, 1Н, Н-6), 2,96 (ддд, J=9,7, 3,6 и 2,5 Гц, 1H, Н-13), 2,31 (дт, J=14,7 и 2,0 Гц, 1Н, H-14a), 1,36 (с, 3Н, Н-22), 1,15 (д, J=6,6 Гц, 3Н, Н-24), 1,14 (с, 3Н, Н-26), 1,07 (с, 3Н, Н-23).
К раствору эпотилона А (5 мг, 10 мкмоль) в ацетоне (1 мл) при 0oС добавляют диметилдиоксиран (0,4 мл, 28 мкмоль, 0,07 М в ацетоне). Температуру полученного раствора в течение нескольких часов доводят до комнатной температуры, при которой продолжают перемешивать в течение 20 ч. Поскольку по данным ТСХ устанавливают наличие остатка исходного продукта, добавляют потом еще диметилдиоксиран (0,25 мл, 17 мкмоль) и перемешивают реакционную смесь еще в течение 20 часов при комнатной температуре. Наконец, удаляют растворитель и остаток очищают с помощью метода препаративной тонкослойной хроматографии (ПСХ) (0,25 х 200 х 200 мм, 10% МеОН:CH2Cl2). В результате выделяют следующие продукты:
1. 1,4 мг (27%) диэпоксиэпотилона А (смесь 3:2 эпимеров в положениях 16 и 17). Rf 0,63 (10% МеОН:CH2Cl2); Rt: 6,79 (изомер 1) и 7,39 (изомер 2) мин (RP 18, 250 х 4 мм, МеОН:H2O 65:35, 1 мл/мин); МС: (m/z)=510 (M+); 1H-ЯМР (400 МГц, CDCl3, выбранные сигналы, изомер 1): δ=6,96 (с, 1Н, Н-19), 5,48 (дд, J=12,2 и 2,5 Гц, 1Н, Н-15), 4,37 (дш, J=10,7 Гц, 1Н, Н-3), 4,10 (с, 1Н, Н-17), 3,67 (дд, J=5,6 и 2,5 Гц, 1Н, Н-7), 3,14 (квд, J=6,6 и 2,5 Гц, 1Н, Н-6), 3,00 (ддд, J=9,7, 3,6 и 2,5 Гц, 1Н, Н-13), 2,88 (дт, J=8,6 и 3,6 Гц, 1Н, Н-12), 2,71 (с, 3Н, Н-21), 2,53 (дд, J=13,7 и 11,7 Гц, 1Н, Н-2а), 1,41 (с, 3Н, Н-22), 1,27 (с, 3Н, Н-26), 1,17 (д, J=6,6 Гц, 3Н, Н-24), 1,08 (с, 3Н, Н-23), 0,97 (д, J=7,1 Гц, 3Н, Н-25); (изомер 2) δ=6,98 (с, 1Н, Н-19), 5,11 (дд, J=11,7 и 2,5 Гц, 1Н, Н-15) 4,27 (дш, J=10,7 Гц, 1Н, Н-3), 4,14 (с, 1Н, Н-17), 3,06 (квд, J=6,6 и 2,9 Гц, 1Н, Н-6), 2,96 (ддд, J=9,7, 3,6 и 2,5 Гц, 1H, Н-13), 2,31 (дт, J=14,7 и 2,0 Гц, 1Н, H-14a), 1,36 (с, 3Н, Н-22), 1,15 (д, J=6,6 Гц, 3Н, Н-24), 1,14 (с, 3Н, Н-26), 1,07 (с, 3Н, Н-23).
2. 0,8 мг (16%) N-оксида эпотилона A. Rf: 0,44 (10% МеОН:СН2Сl2); Rt: 4,25 мин (RP 18, 250 х 4 мм, МеОН:Н2O 65:35, 1 мл/мин); МС: (m/z)=510 (M+); 1H-ЯМР: см. Способ 1.
ПРИМЕР 2: ДИГИДРОЭПОТИЛОН А. (1в)
К раствору эпотилона А (11 мг, 22 мкмоля) в этаноле (2 мл) добавляют палладий на активированном угле (5 мг, 10%), после чего полученную черную суспензию в течение 24 ч при комнатной температуре подвергают воздействию атмосферы водорода. Поскольку реакция по данным ТСХ проходит неполностью, добавляют еще одну порцию палладия на угле, после чего реакционную смесь в течение еще 20 ч перемешивают в атмосфере водорода. Разделение продуктов осуществляют с помощью ПСХ (1 х 200 х 200 мм, 10% МеОН:CH2Cl2). В результате выделяют следующие продукты:
1. 0,5 мг (5%; дигидроэпотилона A. Rf: 0,60 (10% МеОН:СН2Сl2); Rt: 10,80 мин (RP 18, 250 х 4 мм, МеОН:Н2O 65:35, 1 мл/мин); MC (m/z)=496 (M+), 478, 408, 308; 1H-ЯМР (400 МГц), CDCl3, выбранные сигналы): δ=7,05 (д, J=6,6 Гц, 1H, ОН), 6,77 (с, 1H, H-19), 5,23 (дд, J=12,4 и 2,3 Гц, 1Н, H-15) 4,42 (ддд, J= 11,7, 6,6 и 3,0 Гц, 1H, Н-3), 3,70 (ддд, J=5,3 и 2 Гц, 1H, Н-7), 3,12 (квд, J= 6,6 и 3,0 Гц, 1H, Н-6), 3,07 (д, J=12,7 Гц, 1H, Н-17а), 2,96 (ддд, J= 9,7, 3,6 и 2,0 Гц, 1H, Н-13), 2,91 (ддд, J=9,7, 3,6 и 2,6 Гц, 1H, Н-12), 2,68 (с, 3Н, Н-21), 2,51 (дд, J=13,7 и 11,7 Гц, 1H, Н-2а), 2,24 (д; J=12,7 Гц, 1H, H-17b), 2,19 (м, 1H, Н-16), 2,13 (дд, J=13,7 и 3,0 Гц, 1H, Н-2b), 1,35 (с, 3Н, Н-22), 1,15 (д, J=6,6 Гц, 3Н, Н-24), 1,09 (с, 3Н, Н-23), 0,99 (д, J=7,1 Гц, 3Н, Н-25), 0,93 (д, J=6,6 Гц, 3Н, Н-26).
К раствору эпотилона А (11 мг, 22 мкмоля) в этаноле (2 мл) добавляют палладий на активированном угле (5 мг, 10%), после чего полученную черную суспензию в течение 24 ч при комнатной температуре подвергают воздействию атмосферы водорода. Поскольку реакция по данным ТСХ проходит неполностью, добавляют еще одну порцию палладия на угле, после чего реакционную смесь в течение еще 20 ч перемешивают в атмосфере водорода. Разделение продуктов осуществляют с помощью ПСХ (1 х 200 х 200 мм, 10% МеОН:CH2Cl2). В результате выделяют следующие продукты:
1. 0,5 мг (5%; дигидроэпотилона A. Rf: 0,60 (10% МеОН:СН2Сl2); Rt: 10,80 мин (RP 18, 250 х 4 мм, МеОН:Н2O 65:35, 1 мл/мин); MC (m/z)=496 (M+), 478, 408, 308; 1H-ЯМР (400 МГц), CDCl3, выбранные сигналы): δ=7,05 (д, J=6,6 Гц, 1H, ОН), 6,77 (с, 1H, H-19), 5,23 (дд, J=12,4 и 2,3 Гц, 1Н, H-15) 4,42 (ддд, J= 11,7, 6,6 и 3,0 Гц, 1H, Н-3), 3,70 (ддд, J=5,3 и 2 Гц, 1H, Н-7), 3,12 (квд, J= 6,6 и 3,0 Гц, 1H, Н-6), 3,07 (д, J=12,7 Гц, 1H, Н-17а), 2,96 (ддд, J= 9,7, 3,6 и 2,0 Гц, 1H, Н-13), 2,91 (ддд, J=9,7, 3,6 и 2,6 Гц, 1H, Н-12), 2,68 (с, 3Н, Н-21), 2,51 (дд, J=13,7 и 11,7 Гц, 1H, Н-2а), 2,24 (д; J=12,7 Гц, 1H, H-17b), 2,19 (м, 1H, Н-16), 2,13 (дд, J=13,7 и 3,0 Гц, 1H, Н-2b), 1,35 (с, 3Н, Н-22), 1,15 (д, J=6,6 Гц, 3Н, Н-24), 1,09 (с, 3Н, Н-23), 0,99 (д, J=7,1 Гц, 3Н, Н-25), 0,93 (д, J=6,6 Гц, 3Н, Н-26).
2. 8 мг (72%) 15-деокси-дигидроэпотилоновой кислоты. Rf: 0,10 (10% МеОН: СН2Сl2).
ПРИМЕР 3: 16-ОКСИЭПОТИЛОН А. (1б)
К раствору диэпоксиэпотилона А (7 мг, 14 мкмолей) (смесь (1:1) эпимеров в положении С-16) в этаноле (2 мл) добавляют палладий на активированном угле (10 мг, 10%), после чего полученную черную суспензию в течение 24 ч при комнатной температуре подвергают воздействию атмосферы водорода. Поскольку реакция по данным ТСХ проходит неполностью, добавляют еще одну порцию палладия на угле, после чего реакционную смесь в течение еще 80 ч перемешивают в атмосфере водорода. Разделение продуктов осуществляют с помощью ПСХ (1 х 200 х 200 мм, 10% МеОН:СН2Сl2). В результате выделяют следующие продукты:
1. 3 мг (43%) 16-оксиэпотилона А (изомера 1). Rf: 0,38 (10% МеОН: СН2Сl2); Rt: 6,65 мин (RP 18, 250 х 4 мм, MeOH:H2O 65:35, 1 мл/мин); 1Н-ЯМР (400 МГц, СDСl3, выбранные сигналы): δ=6,85 (с, 1Н, Н-19), 5,02 (дд, J=11,7 и 2,0 Гц, 1Н, Н-15), 4,38 (дш, J=11,2 Гц, 1Н, Н-3), 3,67 (дд, J=4 и 3 Гц, 1Н, Н-7), 3,14 (квд, J=6,8 и 3,0 Гц, 1Н, Н-6), 2,95 (д, J=15,3 Гц, 1Н, Н-17а), 2,89 (д, J=15,3 Гц, 1Н, Н-17b), 2,89 (ддд, J=10,2, 3,6 и 2,0 Гц, 1Н, Н-13), 2,81 (ддд, J=9,7, 3,6 и 2,5 Гц, 1Н, Н-12), 2,70 (с, 3Н, Н-21), 2,53 (дд, J=15,8 и 11,7 Гц, 1Н, Н-2а), 2,14 (дд, J=15,8 и 2,0 Гц, 1Н, Н-2b), 2,08 (дт, J= 14,3 и 2,0 Гц, 1Н, Н-14а), 1,39 (с, 3Н, Н-22), 1,25 (с, 3Н, Н-26), 1,19 (д, J= 6,6 Гц, 3Н, Н-24), 1,05 (с, 3Н, Н-23), 0,99 (д, J=7,1 Гц, 3Н, Н-25).
К раствору диэпоксиэпотилона А (7 мг, 14 мкмолей) (смесь (1:1) эпимеров в положении С-16) в этаноле (2 мл) добавляют палладий на активированном угле (10 мг, 10%), после чего полученную черную суспензию в течение 24 ч при комнатной температуре подвергают воздействию атмосферы водорода. Поскольку реакция по данным ТСХ проходит неполностью, добавляют еще одну порцию палладия на угле, после чего реакционную смесь в течение еще 80 ч перемешивают в атмосфере водорода. Разделение продуктов осуществляют с помощью ПСХ (1 х 200 х 200 мм, 10% МеОН:СН2Сl2). В результате выделяют следующие продукты:
1. 3 мг (43%) 16-оксиэпотилона А (изомера 1). Rf: 0,38 (10% МеОН: СН2Сl2); Rt: 6,65 мин (RP 18, 250 х 4 мм, MeOH:H2O 65:35, 1 мл/мин); 1Н-ЯМР (400 МГц, СDСl3, выбранные сигналы): δ=6,85 (с, 1Н, Н-19), 5,02 (дд, J=11,7 и 2,0 Гц, 1Н, Н-15), 4,38 (дш, J=11,2 Гц, 1Н, Н-3), 3,67 (дд, J=4 и 3 Гц, 1Н, Н-7), 3,14 (квд, J=6,8 и 3,0 Гц, 1Н, Н-6), 2,95 (д, J=15,3 Гц, 1Н, Н-17а), 2,89 (д, J=15,3 Гц, 1Н, Н-17b), 2,89 (ддд, J=10,2, 3,6 и 2,0 Гц, 1Н, Н-13), 2,81 (ддд, J=9,7, 3,6 и 2,5 Гц, 1Н, Н-12), 2,70 (с, 3Н, Н-21), 2,53 (дд, J=15,8 и 11,7 Гц, 1Н, Н-2а), 2,14 (дд, J=15,8 и 2,0 Гц, 1Н, Н-2b), 2,08 (дт, J= 14,3 и 2,0 Гц, 1Н, Н-14а), 1,39 (с, 3Н, Н-22), 1,25 (с, 3Н, Н-26), 1,19 (д, J= 6,6 Гц, 3Н, Н-24), 1,05 (с, 3Н, Н-23), 0,99 (д, J=7,1 Гц, 3Н, Н-25).
2. 3 мг (43%) 16-Оксиэпотилона А (изомера 2). Rf: 0,31 (10% MeOH: CH2Cl2); Rt: 6,10 мин (RP 18, 250 х 4 мм, МеОН:Н2О 65:35, 1 мл/мин); 1Н-ЯМР (300 МГц, СDСl3, выбранные сигналы): δ=6,85 (с, 1Н, Н-19), 5,21 (дд, J=11,3 и 1,9 Гц, 1Н, Н-15), 4,42 (дш, J=10,5 Гц, 1Н, Н-3), 3,71 (сш, 1Н, Н-7), 3,21 (д, J=14,3 Гц, 1Н, Н-17а), 3,13 (квд, J=6,8 и 3,0 Гц, 1Н, Н-6), 3,09 (дт, J= 9,8 и 3,4 Гц, 1Н, Н-13), 2,87 (дт, J=9,4 и 3,0 Гц, 1Н, Н-12), 2,73 (д, J= 14,3 Гц, 1Н, Н-17b), 2,68 (с, 3Н, Н-21), 2,63 (дд, J=16,6 и 11,7 Гц, 1Н, Н-2а), 2,27 (дт, J=14,7 и 2,3 Гц, 1Н, Н-14а), 2,24 (дд, J=16,6 и 2,6 Гц, 1Н, Н-2b), 1,39 (с, 3Н, Н-22), 1,22 (с, 3Н, Н-26), 1,19 (д, J=6,8 Гц, 3Н, Н-24), 1,05 (с, 3Н, Н-23), 0,99 (д, J=7,2 Гц, 3Н, Н-25).
ЭПОТИЛОН A-N-оксид (2а):
К 100 мг эпотилона А в 1 мл дихлорметана добавляют 100 мг 70%-ной м-хлорнадбензойной кислоты в 0,5 мл дихлорметана. После перемешивания в течение 6 ч при комнатной температуре продукт разбавляют дихлорметаном и последовательно экстрагируют путем встряхивания раствором сульфита натрия для разложения избыточной надкислоты и раствором бикарбоната натрия. Потом растворитель упаривают в вакууме, а остаток разделяют с помощью препаративной ВЭЖХ на RP-18-колонке с нуклеосилом (250 х 20 мм, растворитель - смесь метанола и воды 60:40). Выход - 60 мг бесцветного масла.
К 100 мг эпотилона А в 1 мл дихлорметана добавляют 100 мг 70%-ной м-хлорнадбензойной кислоты в 0,5 мл дихлорметана. После перемешивания в течение 6 ч при комнатной температуре продукт разбавляют дихлорметаном и последовательно экстрагируют путем встряхивания раствором сульфита натрия для разложения избыточной надкислоты и раствором бикарбоната натрия. Потом растворитель упаривают в вакууме, а остаток разделяют с помощью препаративной ВЭЖХ на RP-18-колонке с нуклеосилом (250 х 20 мм, растворитель - смесь метанола и воды 60:40). Выход - 60 мг бесцветного масла.
Rf - 0,60 (силикагель, ТХ, алюминиевая фольга, растворитель - смесь дихлорметана и метанола 9:1),
ESI-MC (отрицательные ионы) m/z 510;
УФ (метанол); λмакс 240 нм;
13С-ЯМР (CDCl3): С-1 70,5, С-2 39,9, С-3 70,8, С-4 55,1, С-5 221,4, С-6 40,9, С-7 72,9, С-8 37,6, С-9 31,8, С-10 22,8, С-11, 28,0, С-12 58,0, С-13 55,8, С-14 32,2, С-15 75,5, С-16 144,5, С-17 111,4, С-18 143,4, С-19 110,3, С-20 145,6, С-21 13,5, С-22 15,4, С-23 23,3, С-24 12,0, С-25 16,5, С-27 18,2 ppm;
1Н-ЯМР (СDCl3); 2а-Н 2,12 дд, 2b-Н 2,47 дд, 3-Н 4,55 дд, 3-ОН 6,48 ш, 6-Н 3,25 дкв, 7-Н 3,72 дд, 8-Н 1,81 м, 9а-Н 1,34 м, 9b-Н 1,56 м, 10-Н2 1,48 м, 11а-Н 1,27 м, 11b-H 1,87 м, 12-Н 2,92 ддд, 13-Н 2,98 м, 14а-Н 1,67 ддд, 14b-Н 2,23 д, 15-Н 5,33 д, 17-Н 6,82 с, 19-Н 7,09 с, 21-Н3 2,61с, 22-Н3 1,02 с, 23-Н3 1,42 с, 24-Н3, 1,18 д, 25-Н3, 0,99 д, 27-Н3 2,04 с ppm.
ESI-MC (отрицательные ионы) m/z 510;
УФ (метанол); λмакс 240 нм;
13С-ЯМР (CDCl3): С-1 70,5, С-2 39,9, С-3 70,8, С-4 55,1, С-5 221,4, С-6 40,9, С-7 72,9, С-8 37,6, С-9 31,8, С-10 22,8, С-11, 28,0, С-12 58,0, С-13 55,8, С-14 32,2, С-15 75,5, С-16 144,5, С-17 111,4, С-18 143,4, С-19 110,3, С-20 145,6, С-21 13,5, С-22 15,4, С-23 23,3, С-24 12,0, С-25 16,5, С-27 18,2 ppm;
1Н-ЯМР (СDCl3); 2а-Н 2,12 дд, 2b-Н 2,47 дд, 3-Н 4,55 дд, 3-ОН 6,48 ш, 6-Н 3,25 дкв, 7-Н 3,72 дд, 8-Н 1,81 м, 9а-Н 1,34 м, 9b-Н 1,56 м, 10-Н2 1,48 м, 11а-Н 1,27 м, 11b-H 1,87 м, 12-Н 2,92 ддд, 13-Н 2,98 м, 14а-Н 1,67 ддд, 14b-Н 2,23 д, 15-Н 5,33 д, 17-Н 6,82 с, 19-Н 7,09 с, 21-Н3 2,61с, 22-Н3 1,02 с, 23-Н3 1,42 с, 24-Н3, 1,18 д, 25-Н3, 0,99 д, 27-Н3 2,04 с ppm.
21-АЦЕТОКСИЭПОТИЛОН А (=21-АЦЕТИЛЭПОТИЛОН Е) (3а):
К 50 мг эпотилона А-Н-оксида (2а) в 0,5 мл дихлорметана добавляют 0,05 мл 2,6-ди-трет-бутилпиридина и 0,1 мл ацетангидрида. После нагревания массы в течение 15 мин до 75oС упаривают в вакууме растворитель и реагенты, а остаток разделяют методом препаративной ВЭЖХ на RP-18-колонке с нуклеосилом (250 х 20 мм, растворитель - смесь метанола и воды 60:40). Выход - 30 мг бесцветного масла.
К 50 мг эпотилона А-Н-оксида (2а) в 0,5 мл дихлорметана добавляют 0,05 мл 2,6-ди-трет-бутилпиридина и 0,1 мл ацетангидрида. После нагревания массы в течение 15 мин до 75oС упаривают в вакууме растворитель и реагенты, а остаток разделяют методом препаративной ВЭЖХ на RP-18-колонке с нуклеосилом (250 х 20 мм, растворитель - смесь метанола и воды 60:40). Выход - 30 мг бесцветного масла.
Rf - 0,50 (силикагель, ТХ, алюминиевая фольга, растворитель - смесь дихлорметана и метанола 95:5),
ESI-MC (отрицательные ионы) m/z 552;
УФ (метанол); λмакс 210, 250 нм;
1H-ЯMP (СDСl3, сигналы, отличающиеся от 2а): 15-Н 5,45 дд, 17-Н 6,60 с, 19-Н 7,15 с, 21-Н2 5,25 с, СН3СО 2,15 с ррm.
ESI-MC (отрицательные ионы) m/z 552;
УФ (метанол); λмакс 210, 250 нм;
1H-ЯMP (СDСl3, сигналы, отличающиеся от 2а): 15-Н 5,45 дд, 17-Н 6,60 с, 19-Н 7,15 с, 21-Н2 5,25 с, СН3СО 2,15 с ррm.
ЭПОТИЛОН Е (3б):
К 10 мг 21-ацетоксиэпотилона А (3а) в 0,5 мл метанола добавляют одну каплю концентрированного раствора аммиака, нагревают 1 ч до 40oС и выпаривают в вакууме досуха. Затем полученный остаток разделяют препаративной тонкослойной хроматографией. Выход - 6 мг. Продукт идентичен с оригинальной пробой эпотилона Е.
К 10 мг 21-ацетоксиэпотилона А (3а) в 0,5 мл метанола добавляют одну каплю концентрированного раствора аммиака, нагревают 1 ч до 40oС и выпаривают в вакууме досуха. Затем полученный остаток разделяют препаративной тонкослойной хроматографией. Выход - 6 мг. Продукт идентичен с оригинальной пробой эпотилона Е.
ПРИМЕР 4: 19-МЕТИЛЭПОТИЛОН А (4б)
К раствору эпотилона А (15 мг, 30 мкмолей) в ТГФ (1 мл) при -90oС добавляют н-бутиллития (10 мкл, 160 мкмолей, 1,6 М в гексане). В результате раствор моментально окрашивается в золотисто-оранжевый цвет. После перемешивания в течение 15 мин при -90oС к реакционному раствору добавляют метилйодид (100 мкл, 1,6 ммоля). Полученный в результате зеленовато-желтый раствор нагревают до -30oС и завершают реакцию 2 мл буфера (рН - 7,0). Затем эмульсию с помощью 0,1 н. соляной кислоты доводят до значения рН 6. После насыщения эмульсии твердым хлористым натрием водную фазу экстрагируют CH2Cl2 (2 х 5 мл) и этилацетатом (5 мл), после чего собранные органические фазы высушивают сульфатом магния, фильтруют и, наконец, растворитель удаляют на ротационном испарителе. Очистка осуществляется методом ПСХ (1 х 200 х 200 мм, 10% MeOH:CH2Cl2) и ВЭЖХ (RР 18, 250 х 16 мм МеОН: Н2О 65:35). Выделяют следующие продукты:
1. 2,5 мг (17%) 19-метилэпотилона A. Rf: 0,50 (10% МеОН:СН2Сl2); Rt: 11,70 мин (RP 18, 250 х 4 мм, МеОН:Н2О 65:35, 1 мл/мин); МС: (m/z)=508 (М+), 420, 320; 1H-ЯМР (300 МГц, СDСl3, выбранные сигналы): δ=6,41 (с, 1Н, Н-17), 5,46 (дд, J= 9,0 и 2,3 Гц, 1Н, Н-15), 4,15 (дд, J=10,5 и 3,0 Гц, 1Н, Н-3), 3,77 (дд, J= 8 и 4 Гц, 1Н, Н-7), 3,20 (квд, J=6,8 и 4,5 Гц, 1Н, Н-6), 3,04 (дт, J= 7,5 и 3,8 Гц, 1Н, Н-13), 2,91 (дт, J=7,5 и 3,8 Гц, 1Н, Н-12), 2,61 (с, 3Н, Н-21), 2,51 (дд, J=14,4 и 10,5 Гц, 1Н, Н-2а), 2,38 (дд, J=14,4 и 3,0 Гц, 1Н, Н-2b), 2,32 с, 3Н, Н-27), 2,15 (ддд, J=15,1, 3,8 и 3,0 Гц, 1Н, Н-14а), 2,01 (д, J=1,5 Гц, 3Н, Н-26), 1,91 (дт, J=15,1 и 8,8 Гц, 1Н, Н-14b), 1,34 (с, 3Н, Н-22), 1,16 (д, J=6,8 Гц, 3Н, Н-24), 1,10 (с, 3Н, Н-23), 1,00 (д, J=6,8 Гц, 3Н, Н-25).
К раствору эпотилона А (15 мг, 30 мкмолей) в ТГФ (1 мл) при -90oС добавляют н-бутиллития (10 мкл, 160 мкмолей, 1,6 М в гексане). В результате раствор моментально окрашивается в золотисто-оранжевый цвет. После перемешивания в течение 15 мин при -90oС к реакционному раствору добавляют метилйодид (100 мкл, 1,6 ммоля). Полученный в результате зеленовато-желтый раствор нагревают до -30oС и завершают реакцию 2 мл буфера (рН - 7,0). Затем эмульсию с помощью 0,1 н. соляной кислоты доводят до значения рН 6. После насыщения эмульсии твердым хлористым натрием водную фазу экстрагируют CH2Cl2 (2 х 5 мл) и этилацетатом (5 мл), после чего собранные органические фазы высушивают сульфатом магния, фильтруют и, наконец, растворитель удаляют на ротационном испарителе. Очистка осуществляется методом ПСХ (1 х 200 х 200 мм, 10% MeOH:CH2Cl2) и ВЭЖХ (RР 18, 250 х 16 мм МеОН: Н2О 65:35). Выделяют следующие продукты:
1. 2,5 мг (17%) 19-метилэпотилона A. Rf: 0,50 (10% МеОН:СН2Сl2); Rt: 11,70 мин (RP 18, 250 х 4 мм, МеОН:Н2О 65:35, 1 мл/мин); МС: (m/z)=508 (М+), 420, 320; 1H-ЯМР (300 МГц, СDСl3, выбранные сигналы): δ=6,41 (с, 1Н, Н-17), 5,46 (дд, J= 9,0 и 2,3 Гц, 1Н, Н-15), 4,15 (дд, J=10,5 и 3,0 Гц, 1Н, Н-3), 3,77 (дд, J= 8 и 4 Гц, 1Н, Н-7), 3,20 (квд, J=6,8 и 4,5 Гц, 1Н, Н-6), 3,04 (дт, J= 7,5 и 3,8 Гц, 1Н, Н-13), 2,91 (дт, J=7,5 и 3,8 Гц, 1Н, Н-12), 2,61 (с, 3Н, Н-21), 2,51 (дд, J=14,4 и 10,5 Гц, 1Н, Н-2а), 2,38 (дд, J=14,4 и 3,0 Гц, 1Н, Н-2b), 2,32 с, 3Н, Н-27), 2,15 (ддд, J=15,1, 3,8 и 3,0 Гц, 1Н, Н-14а), 2,01 (д, J=1,5 Гц, 3Н, Н-26), 1,91 (дт, J=15,1 и 8,8 Гц, 1Н, Н-14b), 1,34 (с, 3Н, Н-22), 1,16 (д, J=6,8 Гц, 3Н, Н-24), 1,10 (с, 3Н, Н-23), 1,00 (д, J=6,8 Гц, 3Н, Н-25).
2. Около 50% эпотилона А.
ПРИМЕР 5: 19-БРОМЭПОТИЛОН А (4 а)
К раствору эпотилона А (25 мг, 50 мкмолей) в ТГФ (2,5 мл) при -90oС добавляют н-бутиллития (160 мкл, 225 мкмолей, 1,6 М в гексане). Раствор сразу же окрашивается в золотисто-оранжевый цвет. После перемешивания в течение 15 мин при -90oС добавляют N-бромсукцинимида (27 мг, 150 мкмолей) в ТГФ (0,5 мл). Полученный раствор постепенно обесцвечивается. Полученную в результате коричневатую реакционную смесь нагревают до -30oС и с помощью 0,1 н. соляной кислоты (1 мл) доводят до значения рН 6,5. После насыщения твердым хлоридом натрия водную фазу экстрагируют CH2Cl2 (2 х 5 мл) и этилацетатом (5 мл), собранные органические фазы высушивают сульфатом магния, фильтруют, а растворитель удаляют на ротационном испарителе. Очистка осуществляется методом ПСХ (1 х 200 х 200 мм, 10% MeOH:CH2Cl2) и ВЭЖХ (RP 18, 250 х 16 мм, MeOH:H2O 65:35). Выделяют следующие продукты:
1. 2,6 мг (9%) 19-бромэпотилона A. Rf: 0,53 (10% MeOH:CH2Cl2); Rt: 20,78 мин (RP 18, 250•4 мм, МеОН:Н2О 65:35, 1 мл/мин); MC: (m/z)=574 и 572 (М+), 556, 554, 468, 466, 386, 384, 341; 1H-ЯМР (300 МГц, СDСl3, выбранные сигналы): δ=6,43 (с, 1Н, Н-17), 5,46 (дд, J=8,7 и 2,3 Гц, 1Н, Н-15), 4,13 (ддд, J= 9,4, 6,0 и 3,8 Гц, 1Н, H-3), 3,80 (дд, J=8 и 4 Гц, 1H, H-7), 3,38 (д, J= 6,0 Гц, 1Н, ОН), 3,22 (квд, J=6,8 и 5,3 Гц, 1H, Н-6), 3,05 (дт, J=8,3 и 4,1 Гц, 1H, Н-13), 2,91 (дт, J=7,5 и 3,7 Гц, 1H, Н-12), 2,66 (с, 3Н, Н-21), 2,55 (дд, J=14,7 и 9,4 Гц, 1H, Н-2а), 2,47 (дд, J=14,7 и 3,8 Гц, 1H, Н-2b), 2,16 (д, J=1,1 Гц, 3Н, Н-26), 2,14 (дт, J=14,7 и 3,8 Гц, 1H, H-14a), 1,90 (дт, J= 15 и 8,3 Гц, 1Н, H-14b), 1,34 (с, 3Н, Н-22), 1,17 (д, J=6,8 Гц, 3Н, Н-24), 1,11 (с, 3Н, Н-23), 1,01 (д, J=6,8 Гц, 3Н, Н-25).
К раствору эпотилона А (25 мг, 50 мкмолей) в ТГФ (2,5 мл) при -90oС добавляют н-бутиллития (160 мкл, 225 мкмолей, 1,6 М в гексане). Раствор сразу же окрашивается в золотисто-оранжевый цвет. После перемешивания в течение 15 мин при -90oС добавляют N-бромсукцинимида (27 мг, 150 мкмолей) в ТГФ (0,5 мл). Полученный раствор постепенно обесцвечивается. Полученную в результате коричневатую реакционную смесь нагревают до -30oС и с помощью 0,1 н. соляной кислоты (1 мл) доводят до значения рН 6,5. После насыщения твердым хлоридом натрия водную фазу экстрагируют CH2Cl2 (2 х 5 мл) и этилацетатом (5 мл), собранные органические фазы высушивают сульфатом магния, фильтруют, а растворитель удаляют на ротационном испарителе. Очистка осуществляется методом ПСХ (1 х 200 х 200 мм, 10% MeOH:CH2Cl2) и ВЭЖХ (RP 18, 250 х 16 мм, MeOH:H2O 65:35). Выделяют следующие продукты:
1. 2,6 мг (9%) 19-бромэпотилона A. Rf: 0,53 (10% MeOH:CH2Cl2); Rt: 20,78 мин (RP 18, 250•4 мм, МеОН:Н2О 65:35, 1 мл/мин); MC: (m/z)=574 и 572 (М+), 556, 554, 468, 466, 386, 384, 341; 1H-ЯМР (300 МГц, СDСl3, выбранные сигналы): δ=6,43 (с, 1Н, Н-17), 5,46 (дд, J=8,7 и 2,3 Гц, 1Н, Н-15), 4,13 (ддд, J= 9,4, 6,0 и 3,8 Гц, 1Н, H-3), 3,80 (дд, J=8 и 4 Гц, 1H, H-7), 3,38 (д, J= 6,0 Гц, 1Н, ОН), 3,22 (квд, J=6,8 и 5,3 Гц, 1H, Н-6), 3,05 (дт, J=8,3 и 4,1 Гц, 1H, Н-13), 2,91 (дт, J=7,5 и 3,7 Гц, 1H, Н-12), 2,66 (с, 3Н, Н-21), 2,55 (дд, J=14,7 и 9,4 Гц, 1H, Н-2а), 2,47 (дд, J=14,7 и 3,8 Гц, 1H, Н-2b), 2,16 (д, J=1,1 Гц, 3Н, Н-26), 2,14 (дт, J=14,7 и 3,8 Гц, 1H, H-14a), 1,90 (дт, J= 15 и 8,3 Гц, 1Н, H-14b), 1,34 (с, 3Н, Н-22), 1,17 (д, J=6,8 Гц, 3Н, Н-24), 1,11 (с, 3Н, Н-23), 1,01 (д, J=6,8 Гц, 3Н, Н-25).
2. Около 60% эпотилона А (см. примеры 1а-5а в конце описания).
Пример на получение эпотилон B-N-оксида
К раствору 2 ммоль м-хлорпербензойной кислоты в 11 мл дихлорметана добавили 507 мг (1 ммоль) эпотилона В и перемешивали 3 часа при комнатной температуре. Добавляли этилацетат и избыток пербензойной кислоты восстанавливали раствором сульфита натрия. Органический слой сушили посредством сульфата магния и выпаривали до получения 0,6 г сырого продукта, содержащего 390 мг (75%) желаемого продукта, определенного путем ВЭЖХ-хроматографии. Разделение проводили хроматографически на HD-SIL С-18, 35-70 мкм, колонка (диаметр 9 см, длина 83 см) посредством системы растворителей 45% ацетонитрил / 55% аммонийно-ацетатный буфер 50 мМ при рН 7,5, определение при 254 нм, выход 207 мг. DC: Rf=0,19 (силикагель Si60, дихлорметан/метанол 95:5, определение посредством системы ванилин/серная кислота, серо-голубое окрашивание при нагревании до 120oС);
ВЭЖХ: Rf= 4,1 мин (нуклеосил, С-18, 7 мкм, колонка 250 х 4 мм, система растворителей метанол/вода 70:30, 1 мл/мин, определение при 254 нм);
УФ (МеОН): λмакс(ε) = 283 sh (log ε 3,22), 264 sh (3,63) 236 nm (4,19);
ИК (KBr): =3439, 2963, 2936, 2877, 1740, 1689 см-1;
1Н-ЯМР (CDCl3): δ= 2,13 (dd, J=12,9, 12,0, 2-На); 2,47 (t=12,0, 2-Hb); 4,58 (m, 3-H); 3,29 (dq, J=2,0, 5,8, 6-Н); 3,70 (d, J=5,8, 7-Н); 1,20-1,90 (m, 8-H, 9-H2, 10-H2, 11-H2); 2,75 (m, 13-H); 1,66 (m, 14-Ha); 2,23 (dbr, J= 15,6); 5,32 (d, J=11,6, 15-Н); 6,79 (sbr, 17-H); 7,08 (s, 19-H); 2,60 (s, 21-Н3); 1,02 (s, 22-Н3); 1,27 (s, 23-H3); 1,16 (d, J=6,8, 24-Н3); 0,99 (d, J=7,1, 25-Н3); 1,41 (s, 26-Н3); 2,07 (s, 27-Н3);
13С-ЯМР (150 МГц, CDCl3): δ=170,5 (С-1), 40,0 (С-2), 70,9 (С-3), 55,1 (С-4), 221,4 (С-5), 40,7 (С-6), 72,5 (С-7), 37,3 (С-8), 31,5 (С-9), 22,0 (С-10), 33,3 (С-11), 62,3 (С-12), 63,0 (С-13), 33,4 (С-14), 75,6 (С-15), 144,3 (С-16), 111,1 (С-17), 143,3 (С-18), 110,3 (С-19), 144,7 (С-20), 13,4 (С-21), 15,3 (С-22), 23,2 (С-23), 12,5 (С-24), 16,5 (С-25), 22,2 (С-26), 18,2 (С-27); [a] EI-MS (70 eV): m/z (%) 523,2604 (40 M+), ber. (C27H41NO7S) 523,2629, 424 (38), 336 (42), 194 (18), 182 (75), 154 (100), 126 (42).
К раствору 2 ммоль м-хлорпербензойной кислоты в 11 мл дихлорметана добавили 507 мг (1 ммоль) эпотилона В и перемешивали 3 часа при комнатной температуре. Добавляли этилацетат и избыток пербензойной кислоты восстанавливали раствором сульфита натрия. Органический слой сушили посредством сульфата магния и выпаривали до получения 0,6 г сырого продукта, содержащего 390 мг (75%) желаемого продукта, определенного путем ВЭЖХ-хроматографии. Разделение проводили хроматографически на HD-SIL С-18, 35-70 мкм, колонка (диаметр 9 см, длина 83 см) посредством системы растворителей 45% ацетонитрил / 55% аммонийно-ацетатный буфер 50 мМ при рН 7,5, определение при 254 нм, выход 207 мг. DC: Rf=0,19 (силикагель Si60, дихлорметан/метанол 95:5, определение посредством системы ванилин/серная кислота, серо-голубое окрашивание при нагревании до 120oС);
ВЭЖХ: Rf= 4,1 мин (нуклеосил, С-18, 7 мкм, колонка 250 х 4 мм, система растворителей метанол/вода 70:30, 1 мл/мин, определение при 254 нм);
УФ (МеОН): λмакс(ε) = 283 sh (log ε 3,22), 264 sh (3,63) 236 nm (4,19);
ИК (KBr): =3439, 2963, 2936, 2877, 1740, 1689 см-1;
1Н-ЯМР (CDCl3): δ= 2,13 (dd, J=12,9, 12,0, 2-На); 2,47 (t=12,0, 2-Hb); 4,58 (m, 3-H); 3,29 (dq, J=2,0, 5,8, 6-Н); 3,70 (d, J=5,8, 7-Н); 1,20-1,90 (m, 8-H, 9-H2, 10-H2, 11-H2); 2,75 (m, 13-H); 1,66 (m, 14-Ha); 2,23 (dbr, J= 15,6); 5,32 (d, J=11,6, 15-Н); 6,79 (sbr, 17-H); 7,08 (s, 19-H); 2,60 (s, 21-Н3); 1,02 (s, 22-Н3); 1,27 (s, 23-H3); 1,16 (d, J=6,8, 24-Н3); 0,99 (d, J=7,1, 25-Н3); 1,41 (s, 26-Н3); 2,07 (s, 27-Н3);
13С-ЯМР (150 МГц, CDCl3): δ=170,5 (С-1), 40,0 (С-2), 70,9 (С-3), 55,1 (С-4), 221,4 (С-5), 40,7 (С-6), 72,5 (С-7), 37,3 (С-8), 31,5 (С-9), 22,0 (С-10), 33,3 (С-11), 62,3 (С-12), 63,0 (С-13), 33,4 (С-14), 75,6 (С-15), 144,3 (С-16), 111,1 (С-17), 143,3 (С-18), 110,3 (С-19), 144,7 (С-20), 13,4 (С-21), 15,3 (С-22), 23,2 (С-23), 12,5 (С-24), 16,5 (С-25), 22,2 (С-26), 18,2 (С-27); [a] EI-MS (70 eV): m/z (%) 523,2604 (40 M+), ber. (C27H41NO7S) 523,2629, 424 (38), 336 (42), 194 (18), 182 (75), 154 (100), 126 (42).
Определена также цитотоксическая активность эпотилон B-N-оксида, полученные данные приведены в таблице.
Claims (15)
1. Способ получения модифицированных в 16,17-положении эпотилонов, согласно которому защищенные в положении 3,7 или незащищенные эпотилоны А или В а) гидрируют по двойной связи в положении 16,17 либо в) по двойной связи в положении 16,17 проводят эпоксидирование и, в случае необходимости, полученный эпоксид восстанавливают до спирта в положении 16.
2. Способ по п.1, отличающийся тем, что в случае способа (а) гидрируют диимином или водородом в присутствии гетерогенного или гомогенного металлического катализатора или в случае способа (в) эпоксидируют надкислотой или диоксираном.
3. Способ получения эпотилон-N-оксидов, при котором защищенные в положении 3,7 или незащищенные эпотилоны А или В известным образом переводят в N-оксид, и полученный N-оксид при необходимости подвергают реакции Катада.
4. Способ по п.3, отличающийся тем, что N-оксидирование осуществляют надкислотой или диоксираном.
5. Способ по п.3, отличающийся тем, что реакцию Катада осуществляют с помощью активированного производного карбоновой кислоты, в частности, ее ангидрида или хлорангидрида.
6. Способ по п.5, отличающийся тем, что реакцию Катада осуществляют с помощью ацетангидрида и полученные 21-ацетоксиэпотилоны, в случае необходимости, известным образом расщепляют на 21-оксипотилоны А или В (эпотилоны Е и F соответственно).
7. Способ по п.6, отличающийся тем, что необязательное расщепление проводят гидролитическим или ферментативным путем.
8. Способ получения модифицированных в С-19 положении эпотилонов, согласно которому защищенные в положении 3,7 или незащищенные эпотилоны А или В металлизируют в положении С-19 и известным образом с помощью электрофильных реагентов улавливают в виде модифицированных в положении С-19 алкил-, галоген-, серозамещенных эпотилонов.
9. Способ по п.8, отличающийся тем, что металлизацию проводят с помощью бутиллития.
10. Способ получения модифицированных в С-27 положении эпотилонов, при котором алкильную группу в положениях 17,16 и 27 известным образом по С-27-метильной группе замещают гетероатомом.
11. Способ по п.10, отличающийся тем, что С-27-метильную группу замещают атомом брома, в частности, с помощью N-бромсукцинимида, и полученный бромид, в случае необходимости, переводят в С-27-оксисоединение.
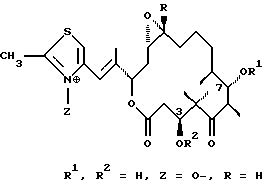
12. Модифицированные эпотилоны общей формулы I
где А обозначает R3OCH2 или метил;
V обозначает Н, алкил, атом галогена, S-алкил, S-арил или Si(алкил)3;
W обозначает Н, ОН, атом галогена;
R обозначает Н или метил;
R1 обозначает Н, ацетил, или силил;
R2 обозначает Н, ацетил, или силил;
R3 обозначает Н или ацетил;
Х обозначает ОН или Н;
Y обозначает Н или ОН, или
Х и Y вместе обозначают двойную связь или -О-, в случае необходимости Z обозначает О-.
где А обозначает R3OCH2 или метил;
V обозначает Н, алкил, атом галогена, S-алкил, S-арил или Si(алкил)3;
W обозначает Н, ОН, атом галогена;
R обозначает Н или метил;
R1 обозначает Н, ацетил, или силил;
R2 обозначает Н, ацетил, или силил;
R3 обозначает Н или ацетил;
Х обозначает ОН или Н;
Y обозначает Н или ОН, или
Х и Y вместе обозначают двойную связь или -О-, в случае необходимости Z обозначает О-.
13. Модифицированные эпотилоны общей формулы I по п.12, полученные способом по любому из пп.1-11.
14. Модифицированный эпотилон общей формулы I по п.12, представляющий собой эпотилон-N-оксид (эпотилон А-N-оксид), полученный тем, что незамещенный в положении 3,7 эпотилон А известным образом переводят в N-оксид, полученный N-оксид при необходимости подвергают О-алкилированию с получением продукта О-алкилирования.
15. Модифицированный эпотилон по п.12, представляющей собой соединение формулы
16. Модифицированный эпотилон по п.12, представляющий собой соединение формулы
17. Модифицированный эпотилон общей формулы I по п.12, представляющий собой эпотилон-N-оксид (эпотилон В-N-оксид), полученный тем, что незащищенный в положении 3,7 эпотилон B известным образом переводят в N-оксид, полученный N-оксид при необходимости подвергают О-алкилированию с получением продукта О-алкилирования.
16. Модифицированный эпотилон по п.12, представляющий собой соединение формулы
17. Модифицированный эпотилон общей формулы I по п.12, представляющий собой эпотилон-N-оксид (эпотилон В-N-оксид), полученный тем, что незащищенный в положении 3,7 эпотилон B известным образом переводят в N-оксид, полученный N-оксид при необходимости подвергают О-алкилированию с получением продукта О-алкилирования.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19707505 | 1997-02-25 | ||
| DE19707505.3 | 1997-02-25 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU99120378A RU99120378A (ru) | 2001-07-20 |
| RU2201932C2 true RU2201932C2 (ru) | 2003-04-10 |
Family
ID=7821415
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU99120378/04A RU2201932C2 (ru) | 1997-02-25 | 1998-02-25 | Модифицированные в боковой цепи эпотилоны |
Country Status (24)
| Country | Link |
|---|---|
| US (1) | US6359140B1 (ru) |
| EP (2) | EP1201666A3 (ru) |
| JP (1) | JP2001513098A (ru) |
| KR (1) | KR100494179B1 (ru) |
| CN (2) | CN1544436A (ru) |
| AR (1) | AR011878A1 (ru) |
| AT (1) | ATE221888T1 (ru) |
| AU (1) | AU736062B2 (ru) |
| BR (1) | BR9807742B1 (ru) |
| CA (1) | CA2281105A1 (ru) |
| CZ (1) | CZ298027B6 (ru) |
| DE (2) | DE19880193D2 (ru) |
| DK (1) | DK0975638T3 (ru) |
| ES (1) | ES2183338T3 (ru) |
| HU (1) | HU228851B1 (ru) |
| IL (1) | IL131343A (ru) |
| NO (1) | NO327211B1 (ru) |
| NZ (1) | NZ337195A (ru) |
| PL (1) | PL190422B1 (ru) |
| PT (1) | PT975638E (ru) |
| RU (1) | RU2201932C2 (ru) |
| TW (1) | TW480263B (ru) |
| WO (1) | WO1998038192A1 (ru) |
| ZA (1) | ZA981575B (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2343155C2 (ru) * | 2002-09-13 | 2009-01-10 | Новартис Аг | Способ получения производных эпотилона |
Families Citing this family (99)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK1186606T4 (da) | 1995-11-17 | 2011-12-05 | Biotechnolog Forschung Gmbh | Epothilonderivater, deres fremstilling og anvendelse |
| DK1367057T3 (da) | 1996-11-18 | 2009-01-19 | Biotechnolog Forschung Gmbh | Epothiloner E og F |
| WO1999001124A1 (en) | 1996-12-03 | 1999-01-14 | Sloan-Kettering Institute For Cancer Research | Synthesis of epothilones, intermediates thereto, analogues and uses thereof |
| US6204388B1 (en) | 1996-12-03 | 2001-03-20 | Sloan-Kettering Institute For Cancer Research | Synthesis of epothilones, intermediates thereto and analogues thereof |
| US20050043376A1 (en) * | 1996-12-03 | 2005-02-24 | Danishefsky Samuel J. | Synthesis of epothilones, intermediates thereto, analogues and uses thereof |
| US6867305B2 (en) | 1996-12-03 | 2005-03-15 | Sloan-Kettering Institute For Cancer Research | Synthesis of epothilones, intermediates thereto and analogues thereof |
| US6660758B1 (en) | 1996-12-13 | 2003-12-09 | The Scripps Research Institute | Epothilone analogs |
| US6441186B1 (en) * | 1996-12-13 | 2002-08-27 | The Scripps Research Institute | Epothilone analogs |
| US6380394B1 (en) * | 1996-12-13 | 2002-04-30 | The Scripps Research Institute | Epothilone analogs |
| PT975638E (pt) * | 1997-02-25 | 2002-12-31 | Biotechnolog Forschung Mbh Gbf | Epothilons modificados nas cadeias laterais |
| US6605599B1 (en) | 1997-07-08 | 2003-08-12 | Bristol-Myers Squibb Company | Epothilone derivatives |
| US6365749B1 (en) | 1997-12-04 | 2002-04-02 | Bristol-Myers Squibb Company | Process for the preparation of ring-opened epothilone intermediates which are useful for the preparation of epothilone analogs |
| US6320045B1 (en) | 1997-12-04 | 2001-11-20 | Bristol-Myers Squibb Company | Process for the reduction of oxiranyl epothilones to olefinic epothilones |
| US6683100B2 (en) | 1999-01-19 | 2004-01-27 | Novartis Ag | Organic compounds |
| US6399638B1 (en) | 1998-04-21 | 2002-06-04 | Bristol-Myers Squibb Company | 12,13-modified epothilone derivatives |
| US6498257B1 (en) * | 1998-04-21 | 2002-12-24 | Bristol-Myers Squibb Company | 2,3-olefinic epothilone derivatives |
| DE19826988A1 (de) * | 1998-06-18 | 1999-12-23 | Biotechnolog Forschung Gmbh | Epothilon-Nebenkomponenten |
| PT987268E (pt) * | 1998-08-05 | 2002-09-30 | Biotechnolog Forschung Mbh Gbf | Agentes farmaceuticos contendo n-oxido de epotilona a e/ou n-oxido de epotilona b |
| US6780620B1 (en) | 1998-12-23 | 2004-08-24 | Bristol-Myers Squibb Company | Microbial transformation method for the preparation of an epothilone |
| US6596875B2 (en) | 2000-02-07 | 2003-07-22 | James David White | Method for synthesizing epothilones and epothilone analogs |
| DE19907588A1 (de) * | 1999-02-22 | 2000-08-24 | Biotechnolog Forschung Gmbh | C-21 Modifizierte Epothilone |
| BR0008379A (pt) | 1999-02-22 | 2002-09-24 | Biotechnolog Forschung Gmbh | Epotilonas modificadas em c-21 |
| US20020058286A1 (en) * | 1999-02-24 | 2002-05-16 | Danishefsky Samuel J. | Synthesis of epothilones, intermediates thereto and analogues thereof |
| US6291684B1 (en) | 1999-03-29 | 2001-09-18 | Bristol-Myers Squibb Company | Process for the preparation of aziridinyl epothilones from oxiranyl epothilones |
| US7125875B2 (en) | 1999-04-15 | 2006-10-24 | Bristol-Myers Squibb Company | Cyclic protein tyrosine kinase inhibitors |
| PL215901B1 (pl) | 1999-04-15 | 2014-02-28 | Bristol Myers Squibb Co | Cykliczny inhibitor bialkowych kinaz tyrozynowych, jego zastosowanie oraz kompozycja farmaceutyczna zawierajaca taki zwiazek |
| AU772750C (en) * | 1999-04-30 | 2005-02-24 | Schering Aktiengesellschaft | 6-alkenyl-, 6-alkinyl- and 6-epoxy-epothilone derivatives, process for their production, and their use in pharmaceutical preparations |
| AR023792A1 (es) * | 1999-04-30 | 2002-09-04 | Bayer Schering Pharma Ag | Derivados 6-alquenilo- y 6-alquinilo-epotilona, los procedimientos para prepararlos y su empleo en productos farmaceuticos |
| AU775373B2 (en) | 1999-10-01 | 2004-07-29 | Immunogen, Inc. | Compositions and methods for treating cancer using immunoconjugates and chemotherapeutic agents |
| US6518421B1 (en) | 2000-03-20 | 2003-02-11 | Bristol-Myers Squibb Company | Process for the preparation of epothilone analogs |
| US6593115B2 (en) | 2000-03-24 | 2003-07-15 | Bristol-Myers Squibb Co. | Preparation of epothilone intermediates |
| US6589968B2 (en) * | 2001-02-13 | 2003-07-08 | Kosan Biosciences, Inc. | Epothilone compounds and methods for making and using the same |
| UA75365C2 (en) * | 2000-08-16 | 2006-04-17 | Bristol Myers Squibb Co | Epothilone analog polymorph modifications, a method for obtaining thereof (variants), a pharmaceutical composition based thereon |
| HU229349B1 (en) | 2001-01-25 | 2013-11-28 | Bristol Myers Squibb Co | Methods for preparation of pharmaceutical composition containing epothilone analogs useful for treatment of cancer |
| NZ526871A (en) | 2001-01-25 | 2006-01-27 | Bristol Myers Squibb Co | Pharmaceutical dosage forms of epothilones for oral administration |
| IL156580A0 (en) | 2001-01-25 | 2004-01-04 | Bristol Myers Squibb Co | A method for formulating an epothilone analog for parenteral use and pharmaceutical preparations including an epothilone analog |
| US6893859B2 (en) * | 2001-02-13 | 2005-05-17 | Kosan Biosciences, Inc. | Epothilone derivatives and methods for making and using the same |
| PL363363A1 (en) | 2001-02-20 | 2004-11-15 | Bristol-Myers Squibb Company | Epothilone derivatives for the treatment of refractory tumors |
| BR0207487A (pt) | 2001-02-20 | 2004-08-10 | Brystol Myers Squibb Company | Método de tratamento de tumores em mamìferos e uso de compostos de epotilona |
| KR20030084952A (ko) * | 2001-02-27 | 2003-11-01 | 게젤샤프트 퓌어 비오테크놀로기쉐 포르슝 엠베하(게베에프) | 에포틸론의 분해 및 에티닐 치환된 에포틸론 |
| WO2002072085A1 (en) | 2001-03-14 | 2002-09-19 | Bristol-Myers Squibb Company | Combination of epothilone analogs and chemotherapeutic agents for the treatment of proliferative diseases |
| MXPA03010909A (es) | 2001-06-01 | 2004-02-17 | Bristol Myers Squibb Co | Derivados de epotilona. |
| TW200303202A (en) | 2002-02-15 | 2003-09-01 | Bristol Myers Squibb Co | Method of preparation of 21-amino epothilone derivatives |
| EP1485090B1 (en) * | 2002-03-08 | 2007-10-10 | Novartis AG | Combinations comprising an epothilone derivative and an imidazotetrazinone |
| AU2003218107A1 (en) | 2002-03-12 | 2003-09-29 | Bristol-Myers Squibb Company | C12-cyano epothilone derivatives |
| SI1483251T1 (sl) | 2002-03-12 | 2010-03-31 | Bristol Myers Squibb Co | C cian epotilonski derivati |
| TW200403994A (en) | 2002-04-04 | 2004-03-16 | Bristol Myers Squibb Co | Oral administration of EPOTHILONES |
| TW200400191A (en) | 2002-05-15 | 2004-01-01 | Bristol Myers Squibb Co | Pharmaceutical compositions and methods of using C-21 modified epothilone derivatives |
| US7405234B2 (en) | 2002-05-17 | 2008-07-29 | Bristol-Myers Squibb Company | Bicyclic modulators of androgen receptor function |
| WO2003105828A1 (en) | 2002-06-14 | 2003-12-24 | Bristol-Myers Squibb Company | Combination of epothilone analogs and chemotherapeutic agents for the treatment of proliferative diseases |
| DE60330407D1 (de) | 2002-08-23 | 2010-01-14 | Sloan Kettering Inst Cancer | Synthese von Epothilonen, Zwischenprodukte davon, Analoga und ihre Verwendung |
| US7649006B2 (en) | 2002-08-23 | 2010-01-19 | Sloan-Kettering Institute For Cancer Research | Synthesis of epothilones, intermediates thereto and analogues thereof |
| US6921769B2 (en) | 2002-08-23 | 2005-07-26 | Sloan-Kettering Institute For Cancer Research | Synthesis of epothilones, intermediates thereto and analogues thereof |
| BRPI0314133A8 (pt) | 2002-09-23 | 2017-09-19 | Bristol Myers Squibb Co | Processo para isolamento de epotilona b, métodos para cultivo de microorganismo que produza epotilona a ou b e para purifiação de apotilona |
| US7632858B2 (en) | 2002-11-15 | 2009-12-15 | Bristol-Myers Squibb Company | Open chain prolyl urea-related modulators of androgen receptor function |
| US7820702B2 (en) | 2004-02-04 | 2010-10-26 | Bristol-Myers Squibb Company | Sulfonylpyrrolidine modulators of androgen receptor function and method |
| US7378426B2 (en) | 2004-03-01 | 2008-05-27 | Bristol-Myers Squibb Company | Fused heterotricyclic compounds as inhibitors of 17β-hydroxysteroid dehydrogenase 3 |
| US7696241B2 (en) | 2004-03-04 | 2010-04-13 | Bristol-Myers Squibb Company | Bicyclic compounds as modulators of androgen receptor function and method |
| US7625923B2 (en) | 2004-03-04 | 2009-12-01 | Bristol-Myers Squibb Company | Bicyclic modulators of androgen receptor function |
| EP1824458A1 (en) * | 2004-11-18 | 2007-08-29 | Bristol-Myers Squibb Company | Enteric coated bead comprising epothilone or an epothilone analog, and preparation and administration thereof |
| AR052142A1 (es) * | 2004-11-18 | 2007-03-07 | Bristol Myers Squibb Co | Perla recubierta enterica que comprende ixabepilona, y preparacion y administracion de la misma |
| US7772177B2 (en) | 2005-05-18 | 2010-08-10 | Aegera Therapeutics, Inc. | BIR domain binding compounds |
| AU2007250443B2 (en) | 2006-05-16 | 2013-06-13 | Pharmascience Inc. | IAP BIR domain binding compounds |
| MX2009005849A (es) | 2006-12-04 | 2009-08-12 | Univ Illinois | Composiciones y metodos para tratar cancer con adn rico en cpg y cupredoxinas. |
| WO2011098904A1 (en) | 2010-02-12 | 2011-08-18 | Aegera Therapeutics, Inc. | Iap bir domain binding compounds |
| AU2011255647A1 (en) | 2010-05-18 | 2012-11-15 | Cerulean Pharma Inc. | Compositions and methods for treatment of autoimmune and other diseases |
| CN103442737B (zh) | 2011-01-20 | 2017-03-29 | 得克萨斯系统大学董事会 | Mri标记、递送和提取系统及其制造方法和用途 |
| WO2012171020A1 (en) | 2011-06-10 | 2012-12-13 | Mersana Therapeutics, Inc. | Protein-polymer-drug conjugates |
| CN102863474A (zh) | 2011-07-09 | 2013-01-09 | 陈小平 | 一类治疗细胞增殖性疾病的铂化合物、其制备方法和应用 |
| CN102993239A (zh) | 2011-09-19 | 2013-03-27 | 陈小平 | 离去基团含氨基或烷胺基的丁二酸衍生物的铂类化合物 |
| CN104768962B (zh) | 2012-11-17 | 2017-04-05 | 北京市丰硕维康技术开发有限责任公司 | 离去基团是含氨基或烷氨基的丙二酸衍生物的铂类化合物 |
| CA2892863C (en) | 2012-12-10 | 2022-03-15 | Mersana Therapeutics, Inc. | Polymeric scaffold based on phf for targeted drug delivery |
| WO2014093640A1 (en) | 2012-12-12 | 2014-06-19 | Mersana Therapeutics,Inc. | Hydroxy-polmer-drug-protein conjugates |
| HK1219879A1 (zh) | 2013-06-11 | 2017-04-21 | Bayer Pharma Aktiengesellschaft | 用於治疗癌症的包含mps-1激酶抑制剂和有丝分裂抑制剂的组合 |
| CA2927022C (en) | 2013-10-11 | 2018-08-21 | Asana Biosciences, Llc | Protein-polymer-drug conjugates |
| EA032231B1 (ru) | 2013-10-11 | 2019-04-30 | Мерсана Терапьютикс, Инк. | Конъюгаты белок-полимер-лекарственное средство |
| US11617799B2 (en) | 2016-06-27 | 2023-04-04 | Tagworks Pharmaceuticals B.V. | Cleavable tetrazine used in bio-orthogonal drug activation |
| US11135307B2 (en) | 2016-11-23 | 2021-10-05 | Mersana Therapeutics, Inc. | Peptide-containing linkers for antibody-drug conjugates |
| JP7320458B2 (ja) | 2017-06-22 | 2023-08-03 | メルサナ セラピューティクス インコーポレイテッド | 薬物担持ポリマースキャフォールドおよびタンパク質-ポリマー-薬物コンジュゲートを製造する方法 |
| EP3787691A1 (en) | 2018-05-04 | 2021-03-10 | Tagworks Pharmaceuticals B.V. | Tetrazines for high click conjugation yield in vivo and high click release yield |
| ES2975330T3 (es) | 2018-05-04 | 2024-07-04 | Tagworks Pharmaceuticals B V | Compuestos que comprenden un enlazador para aumentar la estabilidad del trans-cicloocteno |
| AU2019369340A1 (en) | 2018-10-29 | 2021-05-20 | Mersana Therapeutics, Inc. | Cysteine engineered antibody-drug conjugates with peptide-containing linkers |
| EP4382129A3 (en) | 2019-06-17 | 2024-07-03 | Tagworks Pharmaceuticals B.V. | Compounds for fast and efficient click release |
| IL289094A (en) | 2019-06-17 | 2022-02-01 | Tagworks Pharmaceuticals B V | Tetrazines for increasing the speed and yield of the "click release" reaction |
| JP2024532537A (ja) | 2021-09-06 | 2024-09-05 | ヴェラクサ バイオテック ゲーエムベーハー | 真核生物における遺伝暗号の拡張のための新規アミノアシルtRNA合成酵素変異体 |
| ES3039688T3 (en) | 2021-11-25 | 2025-10-23 | Veraxa Biotech Gmbh | Improved antibody-payload conjugates (apcs) prepared by site-specific conjugation utilizing genetic code expansion |
| CA3238627A1 (en) | 2021-11-25 | 2023-06-01 | Christine Kohler | Improved antibody-payload conjugates (apcs) prepared by site-specific conjugation utilizing genetic code expansion |
| KR20240119102A (ko) | 2021-12-08 | 2024-08-06 | 유럽피안 몰레큘러 바이올로지 래보러토리 | 표적화 접합체의 제조를 위한 친수성 테트라진-관능화 페이로드 |
| EP4372000A3 (en) | 2022-02-15 | 2024-07-17 | Tagworks Pharmaceuticals B.V. | Masked il12 protein |
| JP2025524728A (ja) | 2022-07-15 | 2025-07-30 | フィアン セラピューティクス エルティーディー | 抗体-薬物複合体 |
| IL320221A (en) | 2022-10-12 | 2025-06-01 | Tagworks Pharmaceuticals B V | Strained bicyclo-nonanes |
| CN120569216A (zh) | 2023-01-20 | 2025-08-29 | 巴斯夫欧洲公司 | 稳定型生物聚合物组合物、其制造和用途 |
| KR20250169530A (ko) | 2023-03-10 | 2025-12-03 | 태그웍스 파마슈티컬스 비.브이. | 개선된 t-링커를 갖는 트랜스-사이클로옥텐 |
| AU2024300552A1 (en) | 2023-07-27 | 2026-01-29 | Veraxa Biotech Gmbh | Hydrophilic trans-cyclooctene (hytco) compounds, constructs and conjugates containing the same |
| WO2025056807A1 (en) | 2023-09-15 | 2025-03-20 | Basf Se | Stabilized biopolymer composition, their manufacture and use |
| WO2025149667A1 (en) | 2024-01-12 | 2025-07-17 | Pheon Therapeutics Ltd | Antibody drug conjugates and uses thereof |
| WO2025174248A1 (en) | 2024-02-16 | 2025-08-21 | Tagworks Pharmaceuticals B.V. | Trans-cyclooctenes with "or gate" release |
| WO2026043376A1 (en) | 2024-08-22 | 2026-02-26 | Tagworks Pharmaceuticals B.V. | Trans-cyclooctene formulations |
| WO2026078060A1 (en) | 2024-10-08 | 2026-04-16 | Basf Se | Tocopherol alkoxylates for biopolymer stabilization |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4138042C2 (de) * | 1991-11-19 | 1993-10-14 | Biotechnolog Forschung Gmbh | Epothilone, deren Herstellungsverfahren sowie diese Verbindungen enthaltende Mittel |
| DK1186606T4 (da) * | 1995-11-17 | 2011-12-05 | Biotechnolog Forschung Gmbh | Epothilonderivater, deres fremstilling og anvendelse |
| US6441186B1 (en) * | 1996-12-13 | 2002-08-27 | The Scripps Research Institute | Epothilone analogs |
| PT975638E (pt) * | 1997-02-25 | 2002-12-31 | Biotechnolog Forschung Mbh Gbf | Epothilons modificados nas cadeias laterais |
-
1998
- 1998-02-25 PT PT98912388T patent/PT975638E/pt unknown
- 1998-02-25 AU AU67249/98A patent/AU736062B2/en not_active Ceased
- 1998-02-25 ES ES98912388T patent/ES2183338T3/es not_active Expired - Lifetime
- 1998-02-25 JP JP53730098A patent/JP2001513098A/ja not_active Withdrawn
- 1998-02-25 BR BRPI9807742-2A patent/BR9807742B1/pt not_active IP Right Cessation
- 1998-02-25 RU RU99120378/04A patent/RU2201932C2/ru not_active IP Right Cessation
- 1998-02-25 DE DE19880193T patent/DE19880193D2/de not_active Expired - Lifetime
- 1998-02-25 EP EP02001063A patent/EP1201666A3/de not_active Ceased
- 1998-02-25 KR KR10-1999-7007773A patent/KR100494179B1/ko not_active Expired - Fee Related
- 1998-02-25 EP EP98912388A patent/EP0975638B1/de not_active Expired - Lifetime
- 1998-02-25 CA CA002281105A patent/CA2281105A1/en not_active Abandoned
- 1998-02-25 CN CNA031597866A patent/CN1544436A/zh active Pending
- 1998-02-25 PL PL98335329A patent/PL190422B1/pl unknown
- 1998-02-25 WO PCT/EP1998/001060 patent/WO1998038192A1/de not_active Ceased
- 1998-02-25 IL IL13134398A patent/IL131343A/en not_active IP Right Cessation
- 1998-02-25 AT AT98912388T patent/ATE221888T1/de active
- 1998-02-25 DE DE59805110T patent/DE59805110D1/de not_active Expired - Lifetime
- 1998-02-25 HU HU0002189A patent/HU228851B1/hu unknown
- 1998-02-25 ZA ZA981575A patent/ZA981575B/xx unknown
- 1998-02-25 CZ CZ0286599A patent/CZ298027B6/cs not_active IP Right Cessation
- 1998-02-25 CN CN98802842A patent/CN1128803C/zh not_active Expired - Fee Related
- 1998-02-25 NZ NZ337195A patent/NZ337195A/en unknown
- 1998-02-25 DK DK98912388T patent/DK0975638T3/da active
- 1998-02-26 AR ARP980100851A patent/AR011878A1/es unknown
- 1998-05-28 TW TW087102758A patent/TW480263B/zh not_active IP Right Cessation
-
1999
- 1999-08-17 US US09/376,754 patent/US6359140B1/en not_active Expired - Lifetime
- 1999-08-24 NO NO19994071A patent/NO327211B1/no not_active IP Right Cessation
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2343155C2 (ru) * | 2002-09-13 | 2009-01-10 | Новартис Аг | Способ получения производных эпотилона |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2201932C2 (ru) | Модифицированные в боковой цепи эпотилоны | |
| US6610736B1 (en) | 16-Halogen-epothilone derivatives, method for producing them and their pharmaceutical use | |
| KR20020005737A (ko) | 6-알케닐-,6-알키닐- 및 6-에폭시-에포틸론 유도체, 그의제조 방법 및 제약 제제로서 그의 용도 | |
| Riefert et al. | Approach to the Core Structure of 15-epi-Exiguolide | |
| HUP0303895A2 (hu) | Epotilonok lebontása | |
| MXPA99007546A (en) | Epothilones with a modified side chain | |
| Tóth et al. | Synthesis of vinca alkaloids and related compounds. Part 108: Efficient convergent synthetic pathway to the ibophyllidine skeleton IV. First synthesis of (±)-18-hydroxy-20-epiibophyllidine | |
| EP0987268B1 (en) | Pharmaceutical agents containing epothilone A-N-oxide and/or epothilone B-N-oxide | |
| DE19930111A1 (de) | C-21 Modifizierte Epothilone | |
| Yamashita et al. | Stereoselective synthesis of the left wing of Caribbean ciguatoxin | |
| Toth et al. | Synthesis of Vinca Alkaloids and Related Compounds. Part 107. An Efficient Convergent Synthetic Pathway to Build up the Ibophyllidine Skeleton III. Total Synthesis of ((plus/minus))-Ibophyllidine and | |
| HK1023774B (en) | Epothilone b-n-oxide and preparation method thereof | |
| RU2397177C2 (ru) | СПОСОБ ПОЛУЧЕНИЯ 2-ДЕГИДРО-3-ЭПИ-20-ГИДРОКСИЭКДИЗОНА, МИНОРНОГО ЭКДИСТЕРОИДА СЕМЯН РАСТЕНИЙ Froelichia floridana | |
| HK1070897A (en) | 3,7-protected epothilones n-oxides and preparation method thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20070226 |