Verfahren zur Herstellung von
Progesteron-Derivaten
Die Erfindung betrifft ein Verfahren zur Herstellung von ProgesteronDerivaten der allgemeinen Formel I
worin
┉ eine Einfachbindung oder eine Doppelbindung symbolisiert,
X ein Wasserstoffatom, ein Fluoratom oder eine Methylgruppe darstellt und
V eine Methylengruppe, eine Ethylengruppe, eine Ethylidengruppe oder eine Vinylidengruppe bedeutet,
welches dadurch gekennzeichnet ist, daß man ein Nitril der allgemeinen
worin
┉ X und V die oben genannte Bedeutung besitzen und worin
bedeuten und W ein Wasserstoffatom darstellt oder worin
Y eine Alkyloxygruppe mit bis zu 4 Kohlenstoffatomen,
eine Bezylgruppe oder eine Acyloxygruppe mit 2 bis 8 Kohlenstoffatomen sybolisiert und Z und W zwei Wasserstoffatome darstellen oder gemeinsam eine Kohlenstoff-Kohlenstoff-Bindung bedeuten,
mit einem Grignard-Reagenz der allgemeinen Formel III
CH3-Mg-Z (III). worin Z ein Chloratom oder ein Bromatom symbolisiert, umsetzt und die gebildeten Zwischenprodukte mittels Säuren hydrolysiert.
Llnter einer Alkylendioxygruppe Y und Z der Nitrile der allgemeinen
Formel II soll beispielsweise eine 1,2-Ethylendιoxygruppe, eine
1,3-Propylendioxygruppe, eine 2,2-Dimethyl-1,3-propylendιoxygruppe oder eine 2,3-Butylendioxygruppe verstanden werden.
Geeignete Alkoxygruppen Z sind beispielsweise die Methoxygruppe, die Ethoxygruppe, die Isopropyloxygruppe oder die tert.-Butyloxygruppe.
Geeignete Acyloxygruppen sind unter anderem die Acetoxygruppe, die
Propionyloxygruppe, die Dimethylacetoxygruppe, die Trimethylacetoxygruppe und die Benzoyloxygruppe.
Das für die Durchführung des erfindungsgemaßen Verfahrens benotigte
Grignard-Reagenz kann in üblicher Weise hergestellt werden, beispielsweise indem man Methylchlorid oder Methylbromid in einem Ether wie Diethylether, Dusopropylether, Dibutylether, 1,2-Dimethoxyethan oder Tetrahydrofuran mit Magnesiumspänen umsetzt. Wegen seines relativ niedrigen Siedepunktes und nicht zu niedrigen Flammenpunktes ist Tetrahydrofuran besonders geeignet. Diese Grignard-Reagenzien können direkt zur Umsetzung mit den Nitrilen der allgemeinen Formel II verwendet werden. Zweckmäßigerweise wird aber vor der Umsetzung der Ether durch Destillation weitgehend entfernt und durch Toluol ersetzt. (Fs sei angemerkt, daß Toluol gegenüber Benzol den Vorteil der wesentlich geringeren Toxizitat und gegenüber den Xylolen den Vorteil des niedrigen Siedepunktes hat). Dies hat nicht nur den Vorteil daß ein Großteil des Ethers problemlos wiedergewonnen werden kann, sondern darüberhinaus, daß die Reaktion unter milden Bedingungen durchgeführt werden kann und die Aufarbeitung der Reaktionsmischung sehr erleichtert wird.
Zur Durchfuhrung der Reaktion werden zur Erzielung hoher Ausbeuten an Verfahrensprodukt mindestens 4 Mol Grignard-Reagenz benötigt. Die Reaktion wird bei einer Temperatur von -20° C bis +10° C - vorzugsweise bei -5° C bis +5° C - durchgeführt. Unter diesen Bedingungen betragt die Reaktionszeit etwa 30 bis 180 Minuten.
Nach erfolgter Umsetzung wird die Reaktionsmischung wie bei Grignard-Reaktionen üblich zersetzt. Diese Zersetzung kann beispielsweise mit einer wässrigen Lösung des Tetranatriumsalzes der Ethylendiamintetraessigsäure erfolgen, jedoch ist dieses Reagenz etwas aufwendig. Als recht zweckmäßig und problemlos hat sich die Zersetzung der Reaktionsmischung mit wassriger Ammoniumchlorid-Lösung erwiesen.
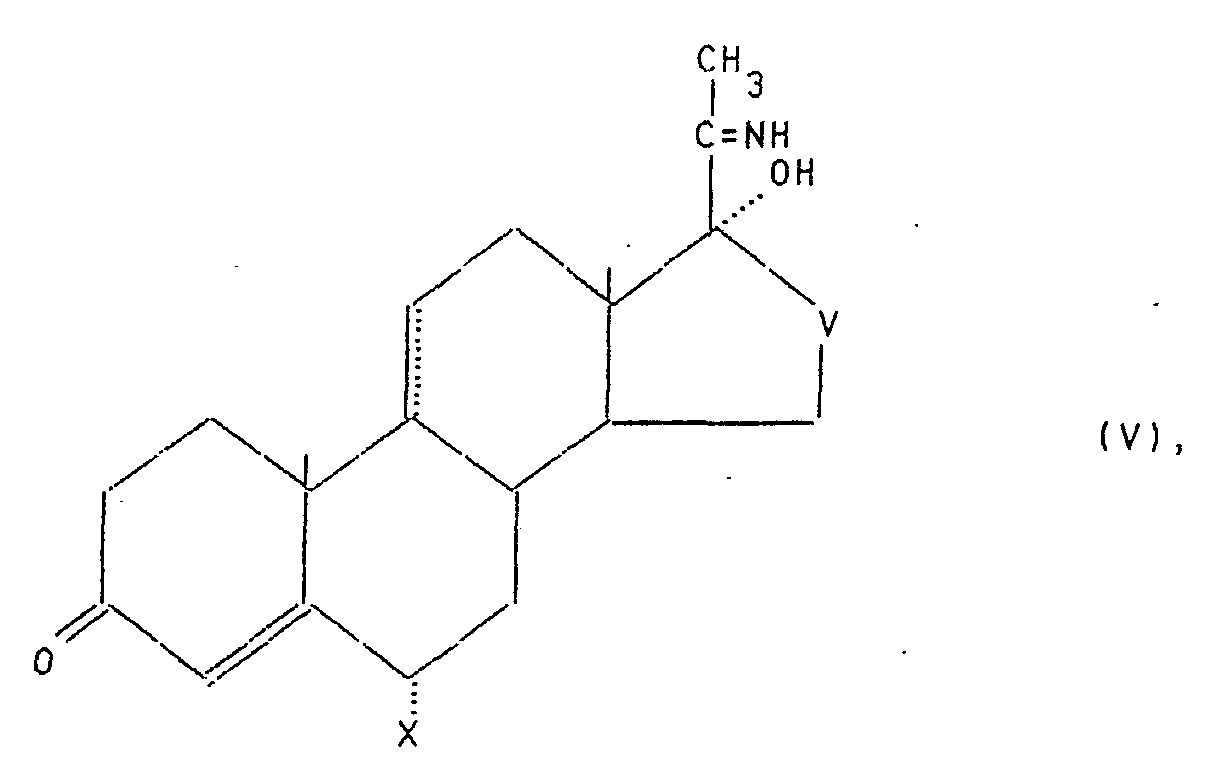
Nach erfolgter Zersetzung kann das Toluol mittels Wasserdampfdestillation entfernt werden und man erhält ein Zwischenprodukt, welches aus einem Gemisch des Progesteron-Derivates der allgemeinen Formel I und den Iminoverbindungen der Formeln IV und V
(in diesen Formeln haben ....., X, Y,Z,W und V die oben genannte Bedeutung) besteht.
Dieses Produkt kann problemlos mittels Säuren zu den Progesteron-Derivaten der allgemeinen Formel I hydrolysiert werden.
Diese Hydrolyse läßt sich beispielsweise so durchführen, daß man das Zwischenprodukt in einem niederen Alkohol - wie Methanol, Ethanol oder Isopropanol löst, mit einer Säure, wie Salzsäure, Schwefelsäure oder p-Toluolsulfonsäure versetzt und erhitzt. Nach erfolgter Umsetzung kann das Reaktionsprodukt beispielsweise mit Wasser ausgefällt werden, wobei man zweckmäßigerweise dafür Sorge trägt, daß die Säure neutralisiert wird.
Nach den bislang vorliegenden Versuchen betagt die Ausbeute an
Verfahrensprodukt ca. 90 % der Theorie. Sie kann möglicherweise durch Optimierung der Verfahrensparameter weiter gesteigert werden.
Es ist für den Fachmann sehr überraschend, daß die Progesteron-Derivate der allgemeinen Formel I durch direkte Grignardierung von Nitrilen der allgemeinen Formel II hergestellt werden können.
Bereits 1959 hatten P. de Ruggieri et. al. aus Cyanhydrinen von
17-Oxosteroiden 17α-Hydroxy-pregnan-20-on-Derivate hergestellt. Sie hatten zu diesem Zweck die 17-Hydroxygruppe der Cyanhydrine durch Umsetzen mit 2,3-Dιhydropyran verethert und dann den 17-Tetrahydropyranylether mit einem Grignard-Reagenz der Formel III umgesetzt. Die direkte
Grignardierung von ungeschützten Cyanhydrinen ist nach Meinung der Autoren nicht möglich, da das Grignard-Reagenz zur Dissoziation des Cyanhydrins führt, wobei das Ausgangsketon entsteht, welches mit dem Grignard-Reagenz das entsprechende Methylcarbinol bildet. (J. Amer. Chem. Soc, 81, 1959, p 5725).
Auch L.F. Fieser et. al. (L.F. Fieser und M. Fieser "Steroide" Verlag Chemie, Weinheim DE. 1961, p 742) und E. Oliveto 13 . Fried and J.E.
Edwards ( Ed ) "Organic Reactions in Steroid Chemistry" Vol. II; van
Nostrand Reinhold Comp. New York et. al. 1972, p 132) vertraten die Ansicht, die direkte Grignardierung von ungeschützten Cyanhydrinen sein nicht möglich.
Wenn Synthesen dieser Art durchgeführt wurden, wurden selbst in neuerer
Zeit als Ausgangssubstanzen stets Cyanhydrine verwendet, deren 17-Hydroxygruppe geschützt war. Siehe beispielsweise
K. Annen et. al. DE-A 34 27 486
I. Nitta et al. Bull Chem. Soc, Jpn. 58, 1985, 978
V. H. van Rhennen US-A 4,500,461
J.V.M. Batist et. al. EP-A 0263569 und
A.E.V. Popova et. al. ref. CA. 102, 1985, 167.005e
Die Vorteile des erfindungsgemäßen Verfahrens liegen nicht nur darin, daß ein Reaktionsschritt eingespart wird, sie liegen auch in der sehr einfachen Durchführbarkeit des erfindungsgemäßen Verfahrens und der hohen Ausbeute an Verfahrensprodukt.
Das nachfolgende Ausführungsbeispiel dient zur näheren Erläuterung des erfindungsgemäßen Verfahrens:
Ausfuhrungsbeispiel
Aus 219 1 einer 3 molren Lösung von Methylmagnesiumchlorid in Tetrahydrofuran werden unter Stickstoff 100 1 Tetrahydrofuran bei Normaldruck abdestilliert. Dann setzt man der Mischung 725 1 Toluol so zu, daß die Temperatur 80° C nicht untersteigt und destilliert 300 1 TetrahydrofuranToluol Mischung ab.
Man läßt die Lösung auf 0° C erkalten, versetzt sie unter Rühren innerhalb von 30 Minuten mit einer Suspension von 50 kg 3,3-Ethylendioxy-17ß-5-androsten-17α-ol in 150 1 Toluol, wobei die Temperatur 5° C nicht übersteigen soll und rührt noch eine Stunde lang bei 5° C.
Dann setzt man der Reaktionsmischung eine Lösung von 25 kg Ammoniumchlorid in 200 1 Wasser so zu, daß die Reaktionstemperatur 80° C nicht übersteigt, säuert sie mit Salzsäure an bis zum pH-6,5 erwärmt sie 20 Minuten lang unter Rühren auf 80° C, trennt die organische Phase ab, wäscht die wässrige Phase mit 200 1 Toluol, vereinigt die organischen Phasen, versetzt sie mit 200 1 Wasser und destilliert das Toluol mittels Wasserdampfdestillation ab.
Nach Erkalten des Reaktionsgemisches wird das abgeschiedene Zwischenprodukt abfiltriert, mit Wasser gewaschen, in 500 1 Methanol eingetragen, mit 6,5 1 konzentrierter Salzsäure versetzt und 15 Minuten unter Rückfluß erhitzt. Dann läßt man die Mischung erkalten, trägt sie in eine Lösung von 12,5 kg Natriumacetat in 25 1 Wasser ein, destilliert 400 1 Methanol ab und versetzt den Rückstand langsam mit 500 1 Wasser.
Das abgeschiedene Produkt wird abfiltriert, mit Wasser gewaschen und bei 50° C im Umlufttrockenschrank getrocknet.
Man erhält so 48 kg 17α-Hydroxy-4-pregnen-3,20-dion vom Schmelzpunkt 210-213° C. (Reinheit laut HPCL 93 %).