Verfahren zur Kernchlorierung von meta-Xylol
Die vorliegende Erfindung betrifft ein Nerfahren zur Kernchlorierung von m-Xylol zu einem Gemisch von 4-Chlor-l,3-dimethylbenzol und 2-Chlor-l,3-dimethylbenzol mit elementarem Chlor in Gegenwart eines Katalysators und eines Co-Katalysators.
Monokernchlorierte m-Xylole sind wertvolle Zwischenprodukte zur Herstellung von Agro- und Pharmawirkstoffen, sowie zur Herstellung von Vorprodukten von Poly- meren.
Die Kernchlorierung von m-Xylol mit elementarem Chlor ist bekannt. Beispielsweise wird in J. Org. Chem 41, 1976, 3580 - 3582 beschrieben, dass bei der Mono- chlorierung von m-Xylol in Gegenwart üblicher Lewis-Säure-Katalysatoren wie bei- spielsweise Jod, FeCl3 oder SbCl3 ein Isomerenverhältnis von 4-Chlor-l,3-dimethyl- benzol zu 2-Chlor-l,3-dimethylbenzol von ca. 3,0 : 1 erhalten wird. 4-Chlor-l,3-di- methylbenzol ist das wertvollere Isomer, so dass eine Reihe von Verfahren zur Erhöhung des Anteils an 4-Chlor-l,3-dimethylbenzol beschrieben wurden.
Aus US-A-4, 190,609 ist ein Verfahren zur Kernchlorierung von m-Xylol mit elementarem Chlor bekannt, wobei in Gegenwart von Lewis-Säuren als Katalysatoren und bestimmten substituierten Thianthrenen als Co-Katalysatoren gearbeitet wird. Dadurch kann zwar ein Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2-Chlor- 1,3-dimethylbenzol von 3,62 : 1 erreicht werden, aber nachteilig an der Verwendung der Thianthrene ist, dass Verbindungen dieser Klasse ähnlich wie die entsprechenden
Dioxine wirken, d.h. toxisch sind.
In EP 126 669 AI werden katalytische Systeme zur Kernchlorierung von Aromaten beschrieben, die aus Lewis-Säuren und Ν-substituierten Phenothiazinen bestehen. Ein Beispiel für die Kemchlorierung von m-Xylol findet sich nicht.
Ein grundsätzlich anderes Verfahren besteht in der Kemchlorierung von m-Xylol mit Chlor in Gegenwart von Zeolithen als Katalysatoren. In J. Catal. 150, 1994, 430-433 wird beschrieben, dass bei Verwendung eines KL-Zeolithen in 1,2-Dichlorethan als Lösungsmittel ein Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2-Chlor-l,3-di- methylbenzol von bis zu 6,5 : 1 erreicht werden kann, wobei in diesem Fall aber über
61 % des eingesetzten m-Xylols nicht umgesetzt werden. Nachteilig an einer Verfahrensführung in Gegenwart von Zeolithen ist weiterhin die Verwendung eines Lösungsmittels und des heterogenen Katalysators, wodurch bei der Aufarbeitung des Reaktionsgemisches zusätzliche Destillations- und Filtrationsscl ritte notwendig werden.
Die Aufgabe der vorliegenden Erfindung bestand darin, ein Verfahren zur Kernchlorierung von m-Xylol unter Verwendung eines einfach zu handhabenden Katalysatorsystems zur Verfügung zu stellen, wobei ein möglichst hohes Verhältnis von 4- Chlor-l,3-dimethylbenzol zu 2-Chlor-l,3-dimethylbenzol erreicht werden soll.
Die gestellte Aufgabe wird auf überraschend einfache Weise dadurch gelöst, dass als Co-Katalysatoren benzokondensierte Thiazepine oder Thiazocine eingesetzt werden.
Die Erfindung betrifft demnach ein Verfahren zur Kemchlorierung von m-Xylol mit elementarem Chlor in Gegenwart von Friedel-Crafts-Katalysatoren, wobei als Co- Katalysatoren benzokondensierte Thiazepine oder Thiazocine einsetzt werden.
Geeignete Friedel-Crafts-Katalysatoren für das erfindungsgemäße Verfahren sind als solche bekannt. Als Beispiele seien genannt: Antimonchloride, Antimonoxide,
Aluminiumchlorid, Eisen(π)-chlorid, Eisen(III)-chlorid, Tellurchloride, Bleichloride, Molybdänchloride, Zinnchloride, Wolframchloride, Titanchloride, Zinkchloride, Bortrichlorid und Bortrifluorid.
Es können auch Elemente und Elementverbindungen, die während der Chlorierung einen Friedel-Crafts-Katalysator, d.h. eine Lewis-Säure bilden, eingesetzt werden
(Vorläufer für Friedel-Crafts-Katalysatoren), beispielsweise die Metalle oder Halbmetalle Antimon, Eisen, Blei, Zinn, Zink, Molybdän, Tellur oder Aluminium oder deren Oxide, Sulfide, Carbonyle oder Salze, z. B. Carbonate. Beispiele für in Frage kommende Elementarverbindungen sind: Antimonoxide, Eisenoxide, Eisensulfide, Bleisulfide, Zinnsulfide, Zinksulfide, Eisencarbonyle, Molybdäncarbonyle und Bor- phoshphat. Anstelle der erwähnten Chloride können auch die entsprechenden Fluoride, Bromide und gegebenenfalls Iodide der genannten Elemente eingesetzt werden.
Bevorzugt werden im erfindungsgemäßen Verfahren Antimonchloride, Eisen, Eisenoxide, Eisensulfide, Eisencarbonyle und Eisen(ιTI)-Chlorid als Friedel-Crafts- Katalysator eingesetzt. Besonders bevorzugt ist Eisen(III)-chlorid.
Friedel-Crafts-Katalysatoren und/oder deren Vorläufer können einzeln oder als be- liebige Gemische untereinander eingesetzt werden.
Die Menge des Friedel-Crafts-Katalysators bzw. seines Vorläufers kann in weiten Grenzen variiert werden. So ist häufig bereits bei einem Zusatz von 0,0005 Gew.% eine Katalysatorwirkung erkennbar. Andererseits können auch 5 Gew.% oder mehr des Friedel-Crafts-Katalysators zugesetzt werden, jedoch bieten solche hohen
Mengen im allgemeinen keinen Vorteil, bringen aber gegebenenfalls bei der Aufarbeitung Nachteile mit sich. Üblicherweise wird der Friedel-Crafts-Katalysator in einer Menge von 0,001 bis 1,0 Gew.%, bevorzugt 0,005 bis 0,5 Gew.% eingesetzt. Alle diese Mengenangaben sind auf die Menge des eingesetzten m-Xylols bezogen.
Im erfindungsgemäßen Verfahren werden als Co-Katalysatoren Thiazepine oder Thiazocine eingesetzt. Verfahren zur Herstellung solcher Verbindungen sind bekannt und beispielsweise in US-A-4,948,886 beschrieben.
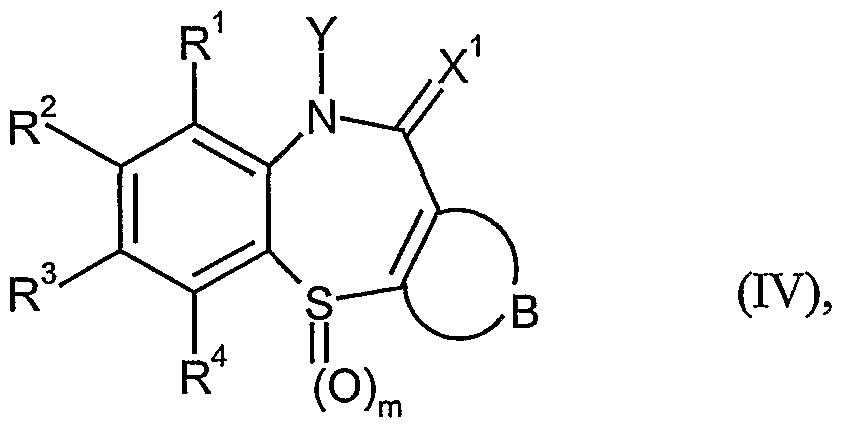
Beispielsweise können als Co-Katalysatoren Benzothiazepine der Formeln
woπn
R1, R2, R3, R4 gleich oder verschieden sind und für Wasserstoff, Hydroxy, Amino, Cyano, Halogen, Νitro, Νitroso, Sulfonyl, Sulfoxyl, Tosyl, Mercapto, Carboxyl, Carboxyamid, Carbalkoxy, Dithiocarboxyl, Thiocarboxyamid, Dithiocarbalkoxy, gegebenenfalls substituiertes Alkyl, Aryl, Heteroaryl,
Alkoxy, Aryloxy, Heteroaryloxy, Acyloxy, Alkylthio, Arylthio, Hetero- arylthio, Acylthio, Acyl, Thioacyl oder Acylamino stehen und weiterhin untereinander einen oder mehrere gesättigte oder ungesättigte, gegebenenfalls substituierte isocyclische oder heterocyclische Kohlenstoffringe mit bis zu 8 C-Atomen bilden können,
R5, R6, R7 und R8 gleich oder verschieden sind und die Bedeutung von R1 bis R4 besitzen, mit der Ausnahme, dass sie untereinander keine Ringe bilden können,
Y Wasserstoff, gegebenenfalls substituiertes Alkyl, Aryl, Heteroaryl, Acyl,
Thioacyl, Acyloxy, Arylamino oder Acylamino bedeutet,
X1, X2, oder X3 unabhängig voneinander jeweils eine der folgende Gruppierungen bedeutet:
wobei
R9 und R10 gleich oder verschieden sind und die Bedeutung von R5 bis R8 haben,
Z die Bedeutung von Y hat mit der Ausnahme, dass Z nicht gleich H sein kann,
A die Anellierung eines gegebenenfalls substituierten gesättigten isocyclischen oder heterocyclischen Rings mit bis zu 8 C-Atomen bedeutet,
B die Anellierung eines gegebenenfalls substituierten ungesättigten isocyclischen oder heterocyclischen Rings mit bis zu 8 C-Atomen bedeutet und
m 0 oder 1 bedeutet,
eingesetzt werden.
Weiterhin können als Co-Katalysatoren beispielsweise Verbindungen der Formel
R21 und R22 unabhängig voneinander Wasserstoff, Hydroxy, Amino, Cyano, Halogen, Nitro, Carboxyl, Halogencarbonyl, Carboxyamid, Alkoxycarbonyl, Alkyl, Aryl, Alkoxy, Aryloxy, Acyloxy, Alkylthio, Arylthio, Acylthio, Acyl,
Thioacyl oder Acylamino bedeuten,
R23 für Wasserstoff oder Chlor steht und weiterhin mit einem der Reste R21 oder R22 bei benachbarter Substitution und gemeinsam mit den substituierten C- Atomen einen anellierten gesättigten, ungesättigten oder aromatischen iso- cyclischen oder heterocyclischen Ring mit 5 bis 8 Ringatomen bilden kann,
R24 Wasserstoff, Alkyl, Aryl, Halogen, Alkylthio, Arylthio, Alkoxy, Aryloxy,
Amino, Hydrazino, Alkylhydrazino oder Phenylhydrazino bedeutet,
m, n und o unabhängig voneinander den Wert 0 oder 1 annehmen können, wobei jedoch n und o nicht gleichzeitig den Wert 0 annehmen dürfen,
R , R und R unabhängig voneinander Wasserstoff, Alkyl, Alkoxy, Phenyl, Acyloxy, Cyano, Halogen, Carboxyl, Alkoxycarbonyl, Phenoxy oder Acyl bedeuten, wobei R und R oder R und R gemeinsam mit den substituierten C-Atomen einen gesättigten , ungesättigten oder aromatischen iso- cyclischen oder heterocyclischen Ring mit 5 bis 8 Ringatomen bilden können,
unabhängig voneinander Wasserstoff, Alkyl oder Halogen bedeuten, wobei R
26 und R
28 oder R
28 und R
210 gemeinsam eine Doppelbildung bilden können, wobei weiterhin R
25 und R
26 gemeinsam doppelt gebundenen Sauerstoff, Schwefel oder R
21 ^substituierten Stickstoff darstellen können,
91 1 wobei R Alkyl, Aryl, Acyl, Alkylamino oder Arylamino bedeutet,
eingesetzt werden.
Weiterhin können als Co-Katalysatoren beispielsweise Verbindungen der Formel
in der
R und R unabhängig voneinander Wasserstoff, Hydroxy, Amino, Cyano,
Halogen, Nitro, -Cs-Alkyl, nicht substituiertes oder durch R31 und R32 sub- stituiertes Phenyl (mit Ausnahme der erneuten Substitution durch R31- und
^9
R -substituiertes Phenyl), Q-Cs-Alkoxy, Phenoxy, -Cs-Acyloxy, C Cs- Acyl oder -Cs-Alkoxycarbonyl bedeuten,
R für Wasserstoff oder Chlor steht und weiterhin mit einem der Reste R oder R32 und gemeinsam mit den substituierten C-Atomen einen anellierten gesättigten, ungesättigten oder aromatischen isocyclischen oder heterocyclischen Ring mit 5 - 8 Ringatomen bilden kann,
R34, R36 und R40 unabhängig voneinander Wasserstoff, -Cs-Alkyl, nicht sub- stituiertes oder durch R31 und R32 substituiertes Phenyl (mit Ausnahme der erneuten Substitution durch R31- und R32-substituiertes Phenyl), -Cs-Acyl,
Cr -Alkoxycarbonyl, Cyano, Halogen, Carboxyl, CrCs-Alkoxy, CrC8-
Alkylthio, Phenylthio, Benzylthio, Phenoxy oder CrC8- Acyloxy bedeuten,
R35, R37 und R39 unabhängig voneinander Wasserstoff, CrCs-Alkyl, Halogen, C Cs-
Alkoxy oder Ci-Cs-Alkylthio bedeuten,
R38 Wasserstoff, -Cs-Alkyl, nicht substituiertes oder durch R31- und R32-sub- stituiertes Phenyl (mit Ausnahme der erneuten Substitution durch R - und R32-substituiertes Phenyl), Cι-C8-Acyl, Ci- -Thioacyl, Halogencarbonyl oder -Cδ- Alkoxycarbonyl bedeuten und
p für eine der Zahlen 0 oder 1 steht,
wobei weiterhin
die Substituentenpaare R34 und R35, R36 und R37, sowie R39 und R40 unabhängig voneinander doppelt gebundenen Sauerstoff, Schwefel oder R38-substituierten Stickstoff bedeuten können und wobei weiterhin
die Substituentenpaare R35 und R36 sowie R38 und R39 unabhängig voneinander eine Doppelbindung bilden können und wobei weiterhin
die Substituentenpaare R34 und R37 sowie R38 und R39 unabhängig voneinander 3- bis 5-gliedriges Alkylen bilden können, bei dem 1 oder 2 C-Atome durch Sauerstoff, Schwefel oder R38-substituierten Stickstoff ersetzt sein können, und wobei weiterhin
R40 auch die Bedeutung Hydrazino, d-Cs-Alkylhydrazino oder Phenylhydrazino annehmen kann,
eingesetzt werden.
Weiterhin können als Co-Katalysatoren beispielsweise Verbindungen der Formel
in der
R41 und R42 unabhängig voneinander Wasserstoff, Cyano, Halogen, Carboxyl, Alkoxycarboxyl, Alkyl, Aryl, Alkoxy, Aryloxy oder Acyl, bevorzugt Wasserstoff, Methyl, Ethyl, Propyl, Isopropyl bedeuten,
R 43 für Wasserstoff, Alkyl oder Chlor, bevorzugt für Wasserstoff steht und weiterhin mit einem der Reste R41 und R42 bei benachbarter Substitution und gemeinsam mit den substituierten C-Atomen einen anellierten gesättigten, ungesättigten oder aromatischen, isocyclischen oder heterocyclischen Ring mit 5 bis 8 Ringatomen bilden kann,
R44 und R45 unabhängig voneinander Wasserstoff, Alkyl, Aryl, Halogen, Alkoxy, Aryloxy, Acyl oder Acyloxy , bevorzugt Wasserstoff, Methyl, Ethyl, Propyl, Isopropyl bedeuten oder gemeinsam mit den substituierten C-Atomen einen gesättigten oder ungesättigten, isocyclischen oder heterocyclischen Ring mit 5 bis 8 Ringatomen bilden können,
R46 Wasserstoff, Alkyl, Aryl oder durch Alkyl oder Aryl substituiertes Silyl, bevorzugt Wasserstoff bedeutet und
den Wert 0 oder 1 annehmen kann,
eingesetzt werden.
Weiterhin können als Co-Katalysatoren beispielsweise Verbindungen der Formel
in der
R51 und R52 unabhängig voneinander Wasserstoff, Hydroxy, Amino, Cyano, Halogen, Nitro, Alkylsulfonyl, Phenylsulfonyl, Alkylsulfoxyl, Phenyl- sulfoxyl, Tosyl, Mercapto, Carboxyl, Halogencarbonyl, Carboxyamid, Alkoxycarbonyl, Thiocarboxyamid, Alkyl, Aryl, Heteroaryl, Alkoxy, Aryloxy, Heteroaryloxy, Acyloxy, Alkylthio, Arylthio, Heteroarylthio, Acyl- thio, Acyl, Thioacyl oder Acylamino bedeuten,
R53 für Wasserstoff oder Chlor steht und weiterhin mit einem der Reste R5 oder R52 und gemeinsam mit den substituierten C-Atomen einen anellierten gesättigten, ungesättigten oder aromatischen isocyclischen oder heterocyclischen Ring mit 5 bis 8 Ringatomen bilden kann,
R54 Wasserstoff, Alkyl, Aryl, Heteroaryl, Acyl, Thioacyl, Halogencarbonyl oder Alkoxycarbonyl bedeutet,
X51 und X52 unabhängig voneinander für doppelt gebundenen Sauerstoff, Schwefel oder R57-substituierten Stickstoff stehen wobei R57 den Bedeutungsumfang von R54 mit Ausnahme von Wasserstoff hat,
r, s und t unabhängig voneinander den Wert 0 oder 1 annehmen können und
R und R unabhängig voneinander an einem oder an zwei der zwischen dem S- und dem N-Atom in 8-Ring befindlichen C-Atomen stehen können, sofern diese C-Atome nicht durch X bzw. X besetzt sind, und den Bedeutungsumfang von R51 bzw. R52 haben, wobei bei benachbarter Substitution auch mit den substituierten C-Atomen ein gesättigter, ungesättigter oder aromatischer isocyclischer oder heterocyclischer Ring mit 5 bis 8 Ringatomen gebildet werden kann und wobei weiterhin R55 und R56 gemeinsam auch doppelt gebundenen Sauerstoff oder Schwefel bedeuten können,
eingesetzt werden.
Bevorzugt werden als Co-Katalysatoren Verbindungen eingesetzt, die einen sieben- gliedrigen N- und S-haltigen Heterocyclus enthalten.
Insbesondere bevorzugt werden als Co-Katalysatoren Verbindungen der Formel (I) eingesetzt, wobei
R1, R2, R3, R4 und Y für Wasserstoff stehen,
X1 für =O steht,
X2 und X3 unabhängig voneinander jeweils
Ra
<
H
bedeuten,
wobei
R9 für Wasserstoff, Methyl, Ethyl, Propyl oder Isopropyl steht, und
m 0 bedeutet.
Ebenfalls bevorzugt werden als Co-Katalysatoren Verbindungen der Formel (VI) ein- gesetzt, wobei
R1, R2, R3, R4 gleich oder verschieden sind und für Wasserstoff, Methyl, Ethyl, Propyl oder Isopropyl stehen,
R7 und R8 Wasserstoff bedeuten,
Y für Wasserstoff steht,
X1 für =0 steht,
m die Zahl 0 bedeutet und
A die Annelierung eines gesättigten isocyclischen Rings mit 6 C-Atomen bedeutet.
Weiterhin bevorzugt werden als Co-Katalysatoren Verbindungen der Formel (ViTI) eingesetzt, wobei
R21, R22, R26, R28 gleich oder verschieden sind und für Wasserstoff, Methyl, Ethyl, Propyl oder Isopropyl stehen,
R23 für Wasserstoff steht,
R Methylthio, Ethylthio, Propylthio oder Isopropylthio bedeutet,
m und o den Wert 0 annehmen,
n den Wert 1 annimmt und
R und R gemeinsam mit den substituierten C-Atomen einen gesättigten iso- cyclischen Ring mit 6 Ringatomen bilden.
Es ist weiterhin möglich, die Co-Katalysatoren in Kombination mit anderen, nicht als Co-Katalysatoren beschriebenen Elementen oder Verbindungen im erfindungsgemäßen Verfahren einzusetzen.
Die Co-Katalysatoren können sowohl einzeln als auch im Gemisch mehrerer von ihnen eingesetzt werden.
Die Mengen an eingesetztem Co-Katalysator können in weiten Grenzen variieren. Mengen unter 0,0001 Gew.% sind weniger vorteilhaft, da dann die co-katalytische
Wirkung nachläßt. Es können sogar Mengen von 5 Gew.% oder mehr an Co-Katalysator eingesetzt werden, jedoch bieten diese hohen Mengen im allgemeinen keinen Vorteil, verursachen aber gegebenenfalls Nachteile bei der Aufarbeitung. Die erfindungsgemäß zu verwendenden Co-Katalysatoren können daher beispielsweise in einer Menge von 0,0001 - 1,0 Gew.-%, bevorzugt 0,0005 - 0,5 Gew.%, besonders bevorzugt 0,001 - 0,1 Gew.%, jeweils bezogen auf die Menge des eingesetzten m- Xylols eingesetzt werden.
Das Molverhältnis von Friedel-Crafts-Katalysator(en) bzw. Vorläufern davon und Co-Katalysator(en) kann im erfindungsgemäßen Verfahren in weiten Grenzen variiert werden. Geeignet ist z. B. ein molares Verhältnis von Friedel-Crafts- Katalysatoren bzw. Vorläufern davon zu Co-Katalysator von 100:1 bis 1:50 bevorzugt 75:1 bis 1:10, besonders bevorzugt 50:1 bis 1:2.
Das erfindungsgemäße Verfahren wird zweckmäßigerweise in flüssiger Phase durchgeführt. Gegebenenfalls kann in Verdünnung mit einem inerten Lösungsmittel gearbeitet werden.
Geeignete Lösungsmittel sind solche, die durch Chlor unter den Bedingungen einer
Kernchlorierung nicht angegriffen werden und dem Fachmann hierfür bekannt sind, wie beispielsweise Methylenchlorid, Chloroform, Tetrachlorkohlenstoff, Essigsäure. Bevorzugt wird ohne Lösungsmittel gearbeitet.
Die Menge des Chlors wird bevorzugt so gewählt, dass ein Chloriergrad von nicht wesentlich höher als 1 resultiert. Man verwendet beispielsweise eine Menge von 0,7 bis 1,1 mol Chlor, bevorzugt 0,8 bis 1 mol Chlor, bezogen auf die Menge an eingesetztem m-Xylol.
Die erfindungsgemäß durchzuführende Kemchlorierung kann grundsätzlich bei einer
Temperatur vom Erstarrungspunkt bis zum Siedepunkt des Reaktionsgemisches durchgeführt werden. Im allgemeinen liegt die Reaktionstemperatur bei -30 bis 120°C, bevorzugt bei -10 bis 100°C, besonders bevorzugt bei 0 bis 70°C.
Der Reaktionsdrack kann normal, vermindert oder erhöht sein und ist grundsätzlich unkritisch. Wegen der kostengünstigen Durchführung ist Normaldruck bevorzugt. Erhöhter Druck kann beispielsweise dann angezeigt sein, wenn oberhalb des Siedepunktes eines tiefsiedenden Lösungs-mittels gearbeitet werden soll. In diesem Fall kann beispielsweise unter dem sich von selbst einstellenden Eigendruck des Reaktionsgemisches gearbeitet werden.
Der Wassergehalt der Reaktionsmischung ist im allgemeinen unkritisch. Es ist bevorzugt, alle Einsatzstoffe nicht speziell zu trocknen, sondern sie mit dem geringen Wassergehalt einzusetzen, mit dem sie üblicherweise in der chemischen Technik vor- liegen. Es ist jedoch möglich, einzelne oder alle Stoffe des Reaktionsgemisches speziell zu trocknen. Üblicherweise sollte der Wassergehalt der Einsatzstoffe nicht
über den Sättigungsgrenzen der jeweiligen Einsatzstoffe liegen. Erfindungsgemäß bevorzugt sind Wassergehalte im Chloriergemisch bis zu 250 ppm, besonders bevorzugt bis zu 150 ppm, ganz besonders bevorzugt bis zu 100 ppm.
Für die praktische Durchfuhrung des erfindungsgemäßen Verfahrens ist die Reihenfolge der Zugabe der einzelnen Komponenten zum Reaktionsgemisch beliebig. Hierbei läßt sich das Verfahren sowohl kontinuierlich als auch diskontinuierlich durchführen. Beispielsweise legt man m-Xylol bei der gewünschten Reaktionstemperatur vor, gibt Friedel-Crafts- und Co-Katalysator zu und dosiert das Chlor bis zum ge- wünschten Chloriergrad ein. Anschließend kann das Chloriergemisch direkt durch
Destillation aufgearbeitet werden. Die Katalysatorkomponenten bleiben im Sumpf zurück.
Das erfmdungsgemäße Verfahren erlaubt die Kemchlorierung von m-Xylol mit erhöhtem Anteil an 4-Chlor-l,3-dimethylbenzol mit niedrigsten Aufwandmengen an
Friedel-Crafts- und Co-Katalysatoren. Da das Verfahren vorzugsweise ohne Lösungsmittel durchgeführt wird, ist eine einfache Aufarbeitung durch direkte Destillation des Produktgemisches möglich.
Mit dem erfindungsgemäßen Verfahren lassen sich beispielsweise Verhältnisse von
4-Chlor-l,3-dimethylbenzol zu 2-Chlor-l,3-dimethylbenzol von 8,05:1 erreichen und liegen damit sogar höher als die mit Zeolith-Katalysatoren bisher erzielten Isomerenverhältnisse.
Die folgenden Beispiele sollen das erfindungsgemäße Verfahren verdeutlichen, ohne es jedoch einzuschränken.
Beispiele
Beispiel 1
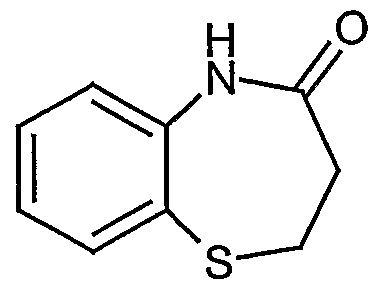
In einem geschwärzten Chlorierbecher wurden 100 Gew.-Teile m-Xylol vorgelegt. Danach wurden 152 ppm FeCl3 und 45 ppm des Co-Katalysators der Formel
zugegeben. Bei 50°C wurden in 5 h 95 mol% Chlor (bezogen auf m-Xylol) gleich- mäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 6,13 % m-Xylol, 80,11 % 4-Chlor-l,3-dimethylbenzol, 12,39 % 2- Chlor-l,3-dimethylbenzol, 1,31 % an dichlorierten m-Xylolen und 0,06 % unbekannte Produkte.
Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2-Chlor-l,3-dimethylbenzol betrug somit 6,47:1.
Beispiel 2
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co-
Katalysators 35 ppm des Co-Katalysators der Formel
zugegeben wurden. Danach wurden bei 50°C in 5 h mit 95 mol% Chlor (bezogen auf m-Xylol) gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 6,21 % m-Xylol, 78,43 % 4-Chlor-l,3-dimethylbenzol, 12,92 % 2-Chlor-l,3-dimethylbenzol, 2,37 % dichlorierte m-Xylole und 0,07 % un- bekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2-Chlor-l,3- dimethylbenzol betrug somit 6,07:1.
Beispiel 3
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co-
Katalysators 40 ppm des Co-Katalysators der Formel
und anstelle von FeCl3 250 ppm SbCl3 eingesetzt wurden. Bei 40°C wurden in 6 h
95 mol% Chlor (bezogen auf m-Xylol) gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 6,87 % m-Xylol, 78,50 % 4-Chlor-l,3-dimethylbenzol, 13,34 % 2-Chlor-l,3-dimethylbenzol, 1,20 % dichlorierte m-Xylole und 0,09 % unbekannte Produkte, entsprechend einem Ver- hältnis von 4-Chlor-l,3-dimethylbenzol zu 2-Chlor-l,3-dimethylbenzol von 5,88:1.
Beispiel 4
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co- Katalysators 56 ppm des Co-Katalysators der Formel
eingesetzt wurden. Anschließend wurden bei 50°C 95 mol% Chlor (bezogen auf m- Xylol) in 5 h gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 7,75 % m-Xylol, 80,31 % 4-Chlor-l,3-dimethyl- benzol, 9,98 % 2-Chlor-l,3-dimethylbenzol, 1,86 % dichlorierte m-Xylole und 0,10 % unbekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2- Chlor-l,3-dimethylbenzol betrug somit 8,05:1.
Beispiel 5
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co- Katalysators 41 ppm des Co-Katalysators der Formel
eingesetzt wurden. Anschließend wurden bei 50°C 95 mol% Chlor (bezogen auf m- Xylol) in 5 h gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 5,82 % m-Xylol, 81,31 % 4-Chlor-l,3-dimethyl- benzol, 10,71 % 2-Chlor-l,3-dimethylbenzol, 2,04 % dichlorierte m-Xylole und 0,12 % unbekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2- Chlor-l,3-dimethylbenzol betrug somit 7,59:1.
Beispiel 6
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co- Katalysators 47 ppm des Co-Katalysators der Formel
eingesetzt wurden. Anschließend wurden bei 50°C 95 mol% Chlor (bezogen auf m- Xylol) in 5 h gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 7,37 % m-Xylol, 73,15 % 4-Chlor-l,3-dimethyl- benzol, 17,67 % 2-Chlor-l,3-dimethylbenzol, 1,40 % dichlorierte m-Xylole und 0,41 % unbekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2- Chlor-l,3-dimethylbenzol betrug somit 4,14:1.
Beispiel 7
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co- Katalysators 40 ppm des Co-Katalysators der Formel
eingesetzt wurden. Anschließend wurden bei 50°C 95 mol% Chlor (bezogen auf m-
Xylol) in 5 h gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 5,39 % m-Xylol, 80,57 % 4-Chlor-l,3-dimethyl- benzol, 12,49 % 2-Chlor-l,3-dimethylbenzol, 1,48 % dichlorierte m-Xylole und
0,07 % unbekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2- Chlor-l,3-dimethylbenzol betrug somit 6,45:1.
Beispiel 8
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co- Katalysators 42 ppm des Co-Katalysators der Formel
eingesetzt wurden. Anschließend wurden bei 50°C 95 mol% Chlor (bezogen auf m- Xylol) in 5 h gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 7,32 % m-Xylol, 77,54 % 4-Chlor-l,3-dimethyl- benzol, 12,22 % 2-Chlor-l,3-dimethylbenzol, 2,75 % dichlorierte m-Xylole und 0,17 % unbekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2-
Chlor-l,3-dimethylbenzol betrug somit 6,35:1.
Beispiel 9
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co-
Katalysators 42 ppm des Co-Katalysators der Formel
eingesetzt wurden. Anschließend wurden bei 50°C 95 mol% Chlor (bezogen auf m- Xylol) in 5 h gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 8,65 % m-Xylol, 70,70 % 4-Chlor-l,3-dimethyl- benzol, 15,91 % 2-Chlor-l,3-dimethylbenzol, 4,36 % dichlorierte m-Xylole und 0,38 % unbekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2-
Chlor-l,3-dimethylbenzol betrug somit 4,44:1.
Beispiel 10
Das Verfahren des Beispiels 1 wurde wiederholt, wobei anstelle des dortigen Co-
Katalysators 60 ppm des Co-Katalysators der Formel
eingesetzt wurden. Anschließend wurden bei 50°C 95 mol% Chlor (bezogen auf m-
Xylol) in 5 h gleichmäßig schnell eingeleitet. Die gaschromatographische Analyse des Reaktionsgemisches ergab 6,06 % m-Xylol, 77,59 % 4-Chlor-l,3-dimethyl- benzol, 14,97 % 2-Chlor-l,3-dimethylbenzol, 1,13 % dichlorierte m-Xylole und 0,25 % unbekannte Produkte. Das Verhältnis von 4-Chlor-l,3-dimethylbenzol zu 2- Chlor-l,3-dimethylbenzol betrug somit 5,18:1.