WO2023007712A1 - (r,s)-ニコチンの製造方法 - Google Patents
(r,s)-ニコチンの製造方法 Download PDFInfo
- Publication number
- WO2023007712A1 WO2023007712A1 PCT/JP2021/028399 JP2021028399W WO2023007712A1 WO 2023007712 A1 WO2023007712 A1 WO 2023007712A1 JP 2021028399 W JP2021028399 W JP 2021028399W WO 2023007712 A1 WO2023007712 A1 WO 2023007712A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- compound
- nicotine
- production method
- equilibrium mixture
- pseudooxynicotine
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
Definitions
- the present invention relates to a method for producing (R,S)-nicotine.
- Nicotine is a kind of alkaloid contained in plants and is a natural product. Nicotine has two optical isomers, (R)-nicotine and (S)-nicotine, and most nicotine extracted from plants is the S-isomer. By the way, various investigations have been made to chemically synthesize nicotine.
- Patent Document 1 describes a racemic mixture of (R)-nicotine and (S)-nicotine from 1-methyl-3-nicotinoyl-2-pyrrolidone or a salt thereof using a one-pot process. )-nicotine”) or a salt thereof.
- Patent Document 2 describes the reaction of N-methyl-2-pyrrolidone or a salt thereof with a nicotinic acid salt compound in the presence of a solvent and a base to form 1-methyl-3-nicotinoyl-2-pyrrolidone or a salt thereof. , discloses the reduction of said 1-methyl-3-nicotinoyl-2-pyrrolidone or a salt thereof with a solution of Na 2 S 2 O 4 to produce racemic nicotine or a salt thereof.
- Patent Document 3 discloses a method for producing racemic nicotine starting from N-vinyl-2-pyrrolidinone and a nicotinic acid ester.
- an object of the present invention is to provide a method for producing (R,S)-nicotine by a simpler method.
- Aspect 1 isolating a specific compound from an equilibrium mixture of pseudooxynicotine; and reducing said compound.
- Aspect 2 The production method according to aspect 1, wherein the isolation step comprises isolating a compound represented by formula (b) described below from the equilibrium mixture.
- Aspect 3 3.
- Aspect 4 The production method according to any one of aspects 1 to 3, wherein the isolation step and the reduction step are performed under an inert atmosphere.
- Aspect 5 The production method according to any one of aspects 1 to 4, wherein the isolation step and the reduction step are performed consecutively.
- Aspect 6 The production method according to any one of aspects 1 to 5, wherein hydrogen is used as a reducing agent in the reduction step.
- Aspect 7 The production method according to any one of aspects 1 to 6, wherein substantially no amino alcohol is produced in the reduction step.
- Aspect 8 (R,S)-nicotine obtained by the production method according to any one of aspects 1 to 7.
- Aspect 9 A process for producing a compound represented by formula (b), comprising distilling an equilibrium mixture of pseudooxynicotine to isolate the compound represented by formula (b) as described below.
- X to Y includes X and Y which are the end values.
- the method of manufacture comprises isolating a specific compound from an equilibrium mixture of pseudooxynicotine and reducing the compound.
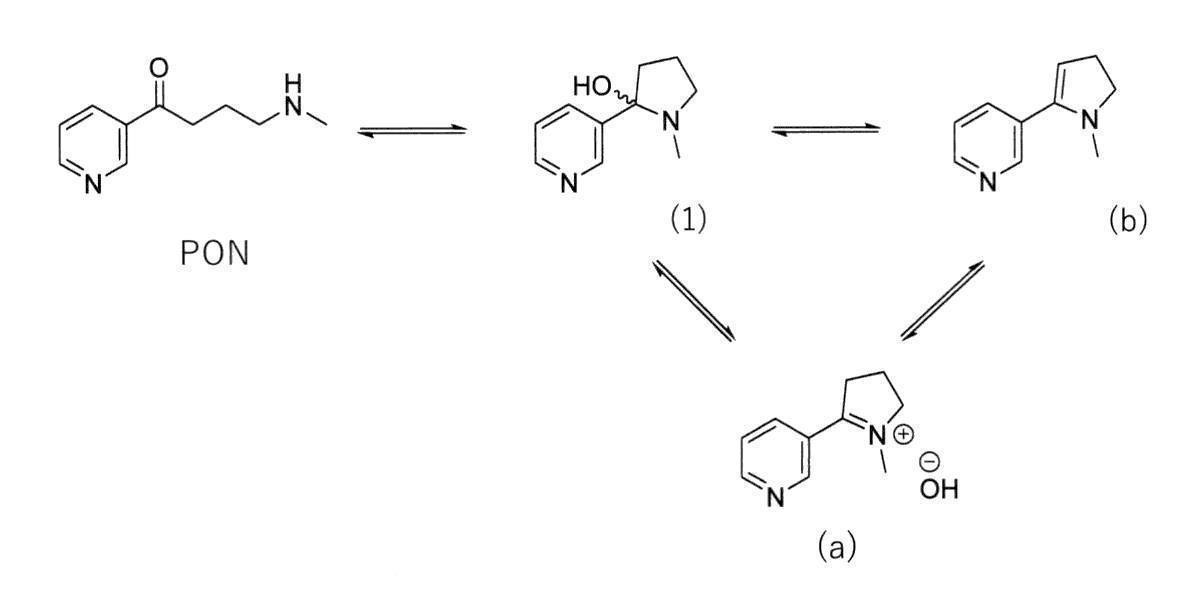
- Isolation step Pseudooxynicotine is a compound represented by PON in the following formula. Pseudooxynicotine exists as an equilibrium mixture under the conditions used in this production method (Patent Document 4: International Publication No. 2014/174505). The conditions used in this production method are not limited as long as the isolation and reduction can be carried out, but in one embodiment, the conditions are room temperature or higher. In the present invention, the mixture of the four compounds in the scheme below is referred to as the pseudooxynicotine equilibrium mixture or simply the equilibrium mixture.
- Pseudooxynicotine can be produced by a known method, for example, a method of reacting N-methyl-2-pyrrolidone or a salt thereof with a nicotinic acid salt compound in the presence of a solvent and a base, followed by acid hydrolysis and alkalinization. is mentioned.
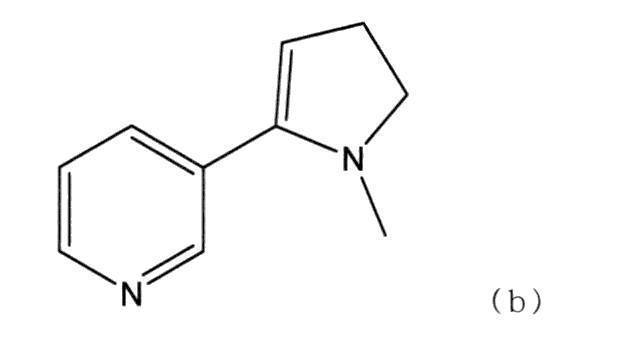
- the compound represented by the chemical formula (b) in the above scheme (3-(1-methyl-4,5-dihydro-1H-pyrrol-2-yl)pyridine, hereinafter simply referred to as "compound b", other (similar to the compound of ) is preferably isolated.
- compound b other (similar to the compound of ) is preferably isolated.
- the inventors have surprisingly found that only compound b can be easily removed from the equilibrium mixture by distillation. Furthermore, since this compound b does not contain an oxygen atom as will be described later, by-products are less likely to be produced in the reduction step.
- Distillation is preferably carried out under reduced pressure.
- the pressure in distillation is more preferably 80 Pa or less, still more preferably 70 Pa or less, and particularly preferably 60 Pa or less.
- the lower limit of the pressure is not limited as long as the distillation is possible, but is preferably 20 Pa or higher, more preferably 30 Pa or higher, and particularly preferably 40 Pa or higher.
- the distillation temperature is preferably 60° C. or higher, more preferably 80° C. or higher, and its upper limit is preferably 140° C. or lower, more preferably 130° C. or lower.
- Compound b is isolated in this step, and isolation in the present invention means that the substance obtained in the isolation step is pure compound b, and that the substance substantially consists of compound b. include. In one embodiment, the substance consists essentially of compound b, which means that the substance does not contain 100 ppm or more of other components. Isolation is therefore also screening for the compound of interest.
- the reduction step is preferably carried out in the presence of a solvent. Moreover, it is preferable to use a catalyst for the reduction step.
- the reduction step preferably uses a metal catalyst and a hydrogen donor.
- the metal catalyst known metal catalysts such as transition metals can be used, but palladium on carbon (Pd/C) is preferable from the viewpoint of availability.
- the hydrogen donor is not limited, but is preferably hydrogen (gas) or ammonium formate, more preferably hydrogen (gas).
- the solvent is not limited, an alcohol such as methanol or an ester such as ethyl acetate is preferred.
- the reduction step includes adding about 1 to 20% by weight of Pd/C (the amount of Pd to compound b is preferably 0.1 to 2% by weight) with respect to compound b, and removing an excess amount of hydrogen. It can be carried out by mixing in methanol solvent.
- This step can be performed at room temperature (about 10 to 30°C) or higher. Although the upper limit of the temperature is not limited, it can be, for example, reflux conditions. Moreover, this step can be carried out at normal pressure.
- the reduction step can also be performed in a hydrogen atmosphere by substituting hydrogen in the system.
- This reduction reaction reduces the double bond on the pyrrolidine ring of compound b to produce (R,S)-nicotine. If the equilibrium mixture is directly subjected to the reduction reaction, an aminoalcohol is produced as a by-product in addition to (R,S)-nicotine, resulting in a decrease in yield and complication of subsequent purification steps.
- the present inventors have found that if only a single substance can be extracted from an equilibrium mixture and the substance can be reduced with substantially no oxygen atoms present in the substrate or reactant, the by-product aminoalcohol is generated in principle. I came up with the idea that the yield would not decrease without In fact, it was found that (R,S)-nicotine can be efficiently produced by isolating the compound b containing no oxygen atoms from the equilibrium mixture and reducing it.
- this step has the advantage that aminoalcohols, which are by-products, are not substantially produced.
- Substantially no by-products means that the target product does not contain 100 ppm or more of by-products in one aspect.
- no compound presumed to be an amino alcohol by-product was detected on TLC.
- the content of by-products can be said to be less than 100 ppm. Therefore, (R,S)-nicotine can be obtained in high yield by this production method.
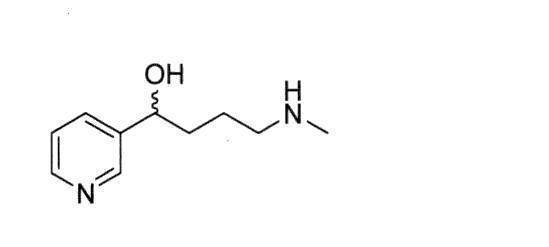
- An aminoalcohol is a compound having an alkane skeleton containing a hydroxy group and an amino group, and in one aspect is a compound having the following structure.
- the reduction step be carried out continuously with the distillation step. This is because decomposition of the compound b can be suppressed.
- both steps are performed sequentially under an inert atmosphere.
- To perform both steps continuously means to perform both steps without providing another step between them.
- the other step is a storage step or the like.
- the production method may further include a known purification step.
- this production method may further comprise a step of separating the R-isomer or S-isomer from the obtained (R,S)-nicotine.
- (R,S)-Nicotine The (R,S)-nicotine obtained by this production method has the advantage of containing extremely few impurities as described above. Therefore, (R,S)-nicotine is useful in fields such as pharmaceuticals and smoking articles.
- Example 1 Selective acquisition of compound b 3-(1-methyl-4,5-dihydro-1H-pyrrol-2-yl)pyridine
- the equilibrium mixture of pseudooxynicotine obtained in Example 1 was subjected to Kugelrohr distillation. to obtain compound b as a distillate. Distillation conditions were as follows. Pressure: 40-60Pa Temperature: Gradually heated from 80°C to 125°C. The obtained liquid after distillation was analyzed by 1 H-NMR and 13 C-NMR and identified as compound b. The analytical results are shown in FIGS. 1 and 2.
- FIG. 1 The analytical results are shown in FIGS. 1 and 2.
- Example 2 Reduction Into a flask under a nitrogen atmosphere was weighed 2 wt% Pd/C (7.54 mg) with respect to compound b. The Pd concentration in Pd/C was 10 wt%, so the amount of Pd relative to compound b was 0.2 wt%. After evacuating the inside of the flask, the inside of the system was replaced with nitrogen gas again. 3 mL of methanol solvent was added to the flask, and the inside of the system was replaced with hydrogen. A solution prepared by dissolving 377 mg of compound b (2.35 mmol) in 5 mL of methanol solvent was added dropwise, and the contents were stirred at room temperature to conduct a reaction.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
シュードオキシニコチンの平衡混合物から特定の化合物を単離する工程、および当該化合物を還元する工程を備える、(R,S)-ニコチンの製造方法。好ましくは、前記単離工程は、前記平衡混合物から式(b)で表される化合物を単離することを含む。
Description
本発明は、(R,S)-ニコチンの製造方法に関する。
ニコチンは植物に含まれるアルカロイドの一種であり天然物である。ニコチンには(R)-ニコチンと(S)-ニコチンの2つの光学異性体があり、植物から抽出されるニコチンのほとんどはS体である。ところで、ニコチンを化学的に合成することが種々検討されている。例えば特許文献1は、1-メチル-3-ニコチノイル-2-ピロリドンまたはその塩からワンポットプロセスを用いてラセミニコチン((R)-ニコチンと(S)-ニコチンのラセミ混合物。以下「(R,S)-ニコチン」ともいう。)またはその塩を製造する方法を開示する。特許文献2は、溶媒および塩基の存在下において、N-メチル-2-ピロリドンまたはその塩を、ニコチン酸塩化合物と反応させて1-メチル-3-ニコチノイル-2-ピロリドンまたはその塩を形成し、当該1-メチル-3-ニコチノイル-2-ピロリドンまたはその塩を、Na2S2O4の溶液を用いて還元して、ラセミニコチンまたはその塩を製造することを開示する。特許文献3は、N-ビニル-2-ピロリジノンとニコチン酸エステルを出発物とし、ラセミニコチンを製造する方法を開示する。
(R,S)-ニコチン(ラセミニコチン)をより簡便な方法で製造することへの要求が存在する。かかる事情に鑑み、本発明は、より簡便な方法で(R,S)-ニコチンを製造する方法を提供することを課題とする。
発明者らは、特定の化合物を単離して、これを還元することで、前記課題を解決できることを見出した。すなわち、前記課題は以下の本発明によって解決される。
態様1
シュードオキシニコチンの平衡混合物から特定の化合物を単離する工程、および
当該化合物を還元する工程、を備える、
(R,S)-ニコチンの製造方法。
態様2
前記単離工程が、前記平衡混合物から後述する式(b)で表される化合物を単離することを含む、態様1に記載の製造方法。
態様3
前記単離工程が、シュードオキシニコチンの平衡混合物を蒸留して前記式(b)で表される化合物を単離することを含む、態様2に記載の製造方法。
態様4
前記単離工程および還元工程を不活性雰囲気下において行う、態様1~3のいずれかに記載の製造方法。
態様5
前記単離工程および還元工程を連続して行う、態様1~4のいずれかに記載の製造方法。
態様6
前記還元工程において還元剤として水素を用いる、態様1~5のいずれかに記載の製造方法。
態様7
前記還元工程において、アミノアルコールが実質的に生成しない、態様1~6のいずれかに記載の製造方法。
態様8
態様1~7のいずれかに記載の製造方法で得られた(R,S)-ニコチン。
態様9
シュードオキシニコチンの平衡混合物を蒸留して後述する式(b)で表される化合物を単離する工程を備える、式(b)で表される化合物の製造方法。
態様1
シュードオキシニコチンの平衡混合物から特定の化合物を単離する工程、および
当該化合物を還元する工程、を備える、
(R,S)-ニコチンの製造方法。
態様2
前記単離工程が、前記平衡混合物から後述する式(b)で表される化合物を単離することを含む、態様1に記載の製造方法。
態様3
前記単離工程が、シュードオキシニコチンの平衡混合物を蒸留して前記式(b)で表される化合物を単離することを含む、態様2に記載の製造方法。
態様4
前記単離工程および還元工程を不活性雰囲気下において行う、態様1~3のいずれかに記載の製造方法。
態様5
前記単離工程および還元工程を連続して行う、態様1~4のいずれかに記載の製造方法。
態様6
前記還元工程において還元剤として水素を用いる、態様1~5のいずれかに記載の製造方法。
態様7
前記還元工程において、アミノアルコールが実質的に生成しない、態様1~6のいずれかに記載の製造方法。
態様8
態様1~7のいずれかに記載の製造方法で得られた(R,S)-ニコチン。
態様9
シュードオキシニコチンの平衡混合物を蒸留して後述する式(b)で表される化合物を単離する工程を備える、式(b)で表される化合物の製造方法。
本発明によれば、より簡便な方法で(R,S)-ニコチンを製造する方法を提供できる。
以下、本発明を詳細に説明する。本発明において「X~Y」はその端値であるXおよびYを含む。
1.製造方法
本製造方法は、シュードオキシニコチンの平衡混合物から特定の化合物を単離する工程、および当該化合物を還元する工程を備える。
(1)単離工程
シュードオキシニコチンは、下記式中PONで表される化合物である。シュードオキシニコチンは、本製造方法で用いる条件では平衡混合物として存在する(特許文献4:国際公開第2014/174505号)。本製造方法で用いる条件とは、前記単離および還元が実施できる条件であれば限定されないが、一態様において室温以上である。本発明においては、下記スキームの4つの化合物の混合物を、シュードオキシニコチンの平衡混合物または単に平衡混合物と称する。シュードオキシニコチンは公知の方法で製造でき、例えば、溶媒および塩基の存在下において、Nメチル-2-ピロリドンまたはその塩を、ニコチン酸塩化合物と反応させ、次いで酸加水分解、アルカリ化を行う方法が挙げられる。
本製造方法は、シュードオキシニコチンの平衡混合物から特定の化合物を単離する工程、および当該化合物を還元する工程を備える。
(1)単離工程
シュードオキシニコチンは、下記式中PONで表される化合物である。シュードオキシニコチンは、本製造方法で用いる条件では平衡混合物として存在する(特許文献4:国際公開第2014/174505号)。本製造方法で用いる条件とは、前記単離および還元が実施できる条件であれば限定されないが、一態様において室温以上である。本発明においては、下記スキームの4つの化合物の混合物を、シュードオキシニコチンの平衡混合物または単に平衡混合物と称する。シュードオキシニコチンは公知の方法で製造でき、例えば、溶媒および塩基の存在下において、Nメチル-2-ピロリドンまたはその塩を、ニコチン酸塩化合物と反応させ、次いで酸加水分解、アルカリ化を行う方法が挙げられる。
本工程では、上記スキームにおける化学式(b)で表される化合物(3-(1-methyl-4,5-dihydro-1H-pyrrol-2-yl)pyridine、以下単に「化合物b」ともいう、他の化合物についても同様)を単離することが好ましい。本発明者は、驚くべきことに、蒸留によって平衡混合物から化合物bのみを容易に取り出せることを見出した。さらに、この化合物bは、後述するとおり酸素原子を含まないので、還元工程において副生成物を生成しにくい。
蒸留は減圧下で実施されることが好ましい。蒸留における圧力は、より好ましくは80Pa以下、さらに好ましくは70Pa以下、特に好ましくは60Pa以下である。当該圧力の下限は、蒸留が可能な範囲であれば限定されないが、好ましくは20Pa以上、より好ましくは30Pa以上、特に好ましくは40Pa以上である。蒸留温度は、好ましくは60℃以上、より好ましくは80℃以上であり、その上限は好ましくは140℃以下、より好ましくは130℃以下である。本工程において化合物bが単離されるが、本発明において単離とは、単離工程で得た物質が、純品の化合物bであること、および当該物質が実質的に化合物bからなる場合を含む。当該物質が実質的に化合物bからなるとは、一態様において当該物質が100ppm以上の他の成分を含有しないことをいう。したがって、単離とは対象の化合物を選別することでもある。
(2)還元工程
平衡混合物から単離された化合物は、好ましくは化合物bであるので、以下、化合物bを還元することを例として、本工程を説明する。
平衡混合物から単離された化合物は、好ましくは化合物bであるので、以下、化合物bを還元することを例として、本工程を説明する。
1)条件
還元工程は、溶媒存在下で実施されることが好ましい。また、還元工程には触媒を用いることが好ましい。限定されないが、還元工程は金属触媒と水素供与体を用いることが好ましい。金属触媒として遷移金属などの公知の金属触媒を用いることができるが、入手容易性等の観点からパラジウム炭素(Pd/C)が好ましい。水素供与体は限定されないが、好ましくは水素(ガス)またはギ酸アンモニウムであり、より好ましくは水素(ガス)である。溶媒は限定されないが、メタノール等のアルコール、または酢酸エチルなどのエステルが好ましい。一態様として、還元工程は、化合物bに対して1~20重量%程度のPd/C(化合物bに対するPdの量は、好ましくは0.1~2重量%)を加え、過剰量の水素をメタノール溶媒中で混合することで実施できる。
還元工程は、溶媒存在下で実施されることが好ましい。また、還元工程には触媒を用いることが好ましい。限定されないが、還元工程は金属触媒と水素供与体を用いることが好ましい。金属触媒として遷移金属などの公知の金属触媒を用いることができるが、入手容易性等の観点からパラジウム炭素(Pd/C)が好ましい。水素供与体は限定されないが、好ましくは水素(ガス)またはギ酸アンモニウムであり、より好ましくは水素(ガス)である。溶媒は限定されないが、メタノール等のアルコール、または酢酸エチルなどのエステルが好ましい。一態様として、還元工程は、化合物bに対して1~20重量%程度のPd/C(化合物bに対するPdの量は、好ましくは0.1~2重量%)を加え、過剰量の水素をメタノール溶媒中で混合することで実施できる。
本工程は、室温(10~30℃程度)またはそれよりも高い温度で実施できる。温度の上限は限定されないが、例えば還流条件下とすることができる。また、本工程は常圧で実施できる。還元工程は、系内を水素で置換し、水素雰囲気下で行うこともできる。
この還元反応によって、化合物bのピロリジン環上の二重結合が還元され、(R,S)-ニコチンが生成する。平衡混合物をそのまま還元反応に供してしまうと、(R,S)-ニコチンの他に副生成物としてアミノアルコールが生成し、収率低下ならびにその後の精製工程の煩雑化を招く。本発明者らは、平衡混合物から単一の物質だけを取り出し、実質的に基質、反応剤に酸素原子が存在しない状態で当該物質を還元できれば、副生成物であるアミノアルコールは原理的に発生せず、収率が低下しないことを着想した。実際に、平衡混合物から酸素原子を含まない化合物bを単離し、これを還元することで、効率よく(R,S)-ニコチンを製造できることを達成した。
2)副生成物
前述のとおり、本工程では、副生成物であるアミノアルコールが実質的に生成しないという利点がある。副生成物が実質的に生成しないとは、一態様において目的生成物が100ppm以上の副生成物を含有しないことをいう。例えば実施例2において、副生成物であるアミノアルコールと推測される化合物はTLC上では検出されなかった。この場合、TLCの検出限界を考慮すると、副生成物の含有量は100ppm未満といえる。したがって本製造方法により、高い収率で(R,S)-ニコチンを得ることができる。アミノアルコールとは、ヒドロキシ基およびアミノ基を含有するアルカン骨格を有する化合物であり、一態様において以下の構造を有する化合物である。
前述のとおり、本工程では、副生成物であるアミノアルコールが実質的に生成しないという利点がある。副生成物が実質的に生成しないとは、一態様において目的生成物が100ppm以上の副生成物を含有しないことをいう。例えば実施例2において、副生成物であるアミノアルコールと推測される化合物はTLC上では検出されなかった。この場合、TLCの検出限界を考慮すると、副生成物の含有量は100ppm未満といえる。したがって本製造方法により、高い収率で(R,S)-ニコチンを得ることができる。アミノアルコールとは、ヒドロキシ基およびアミノ基を含有するアルカン骨格を有する化合物であり、一態様において以下の構造を有する化合物である。
3)蒸留工程との連続実施
還元工程は、前記蒸留工程と連続して実施されることが好ましい。化合物bが分解することを抑制できるからである。好ましくは、両工程は不活性雰囲気下で連続して実施される。両工程を連続して実施するとは、両工程の間に他の工程を設けることなく両工程を実施することをいう。一態様において他の工程とは保存工程等である。
還元工程は、前記蒸留工程と連続して実施されることが好ましい。化合物bが分解することを抑制できるからである。好ましくは、両工程は不活性雰囲気下で連続して実施される。両工程を連続して実施するとは、両工程の間に他の工程を設けることなく両工程を実施することをいう。一態様において他の工程とは保存工程等である。
(3)他の工程
本製造方法は、公知の精製工程をさらに備えていてもよい。また、本製造方法は得られた(R,S)-ニコチンから、R体またはS体を分離する工程をさらに備えていてもよい。
本製造方法は、公知の精製工程をさらに備えていてもよい。また、本製造方法は得られた(R,S)-ニコチンから、R体またはS体を分離する工程をさらに備えていてもよい。
2.(R,S)-ニコチン
本製造方法で得られる(R,S)-ニコチンは、前述のとおり不純物が極めて少ないという利点を有する。よって、(R,S)-ニコチンは、医薬および喫煙物品等の分野において有用である。
本製造方法で得られる(R,S)-ニコチンは、前述のとおり不純物が極めて少ないという利点を有する。よって、(R,S)-ニコチンは、医薬および喫煙物品等の分野において有用である。
[製造例1]シュードオキシニコチンの合成
二口ナスフラスコに2.4gのNaH(100mmol、2.0eq)を加え、30mLのトルエンで2回洗浄し、活性化させた。当該フラスコ内に10mLのシクロペンチルメチルエーテル(CPME)を加えた後、5.0g(50mmol、1.0等量)のN-メチルピロリドンを20mLのCPMEに溶解した溶液を加えて60℃で30分間撹拌した。次いで、フラスコ内に9.1gのニコチン酸エチル(60mmol、1.2等量)を20mLのCPMEに溶解した溶液を加え、85℃で加熱撹拌し反応を行った。反応終了後、6MのHClを加えて中和し、中性になったことを確認してから酢酸エチルで中間体1(8.8g、収率86%)を抽出した。
二口ナスフラスコに2.4gのNaH(100mmol、2.0eq)を加え、30mLのトルエンで2回洗浄し、活性化させた。当該フラスコ内に10mLのシクロペンチルメチルエーテル(CPME)を加えた後、5.0g(50mmol、1.0等量)のN-メチルピロリドンを20mLのCPMEに溶解した溶液を加えて60℃で30分間撹拌した。次いで、フラスコ内に9.1gのニコチン酸エチル(60mmol、1.2等量)を20mLのCPMEに溶解した溶液を加え、85℃で加熱撹拌し反応を行った。反応終了後、6MのHClを加えて中和し、中性になったことを確認してから酢酸エチルで中間体1(8.8g、収率86%)を抽出した。
4gの当該中間体1(20mmol)に対して6MのH2SO4を50mL添加し、72時間リフラックス加熱した。反応終了後、pHが13になるまで水酸化ナトリウムを加えた。当該反応液を、エーテルを用いて分液し、ブラインを用いて油相を洗浄後、硫酸マグネシウムを用いて油相を乾燥した。当該油相から、ロータリーエバポレーターを用いて溶媒を留去し、目的のシュードオキシニコチンを56%の収率で得た。
[実施例1] 化合物b 3-(1-methyl-4,5-dihydro-1H-pyrrol-2-yl)pyridineの選択的取得
実施例1で得られたシュードオキシニコチンの平衡混合物をクーゲルロール蒸留に供し、蒸留物として化合物bを得た。蒸留条件は以下のとおりとした。
圧力:40~60Pa
温度:80℃から125℃まで徐々に加熱した。
得られた蒸留後の液体を1H-NMRと13C-NMRで分析し、化合物bであることを同定した。分析結果を図1および図2に示す。
実施例1で得られたシュードオキシニコチンの平衡混合物をクーゲルロール蒸留に供し、蒸留物として化合物bを得た。蒸留条件は以下のとおりとした。
圧力:40~60Pa
温度:80℃から125℃まで徐々に加熱した。
得られた蒸留後の液体を1H-NMRと13C-NMRで分析し、化合物bであることを同定した。分析結果を図1および図2に示す。
[実施例2] 還元
フラスコに、窒素雰囲気下で、化合物bに対して2重量%のPd/C(7.54mg)を量り取った。Pd/C中のPd濃度は10重量%であったので、化合物bに対するPdの量は0.2重量%であった。フラスコ内を真空引きした後に、再度系内を窒素ガスで置換した。フラスコ内に、3mLのメタノール溶媒を加え、系内を水素置換した。5mLのメタノール溶媒に377mgの化合物b(2.35mmol)を溶解させた溶液を滴下し、室温で内容物を撹拌して反応を行った。反応終了後、パラジウム炭素をろ過し、メタノール溶媒を留去した。シリカゲルクロマトグラフィーで精製後、目的の(R,S)-ニコチンを70%の収率で得た。副生成物であるアミノアルコールと推測される化合物は、TLC上では検出されなかった。
フラスコに、窒素雰囲気下で、化合物bに対して2重量%のPd/C(7.54mg)を量り取った。Pd/C中のPd濃度は10重量%であったので、化合物bに対するPdの量は0.2重量%であった。フラスコ内を真空引きした後に、再度系内を窒素ガスで置換した。フラスコ内に、3mLのメタノール溶媒を加え、系内を水素置換した。5mLのメタノール溶媒に377mgの化合物b(2.35mmol)を溶解させた溶液を滴下し、室温で内容物を撹拌して反応を行った。反応終了後、パラジウム炭素をろ過し、メタノール溶媒を留去した。シリカゲルクロマトグラフィーで精製後、目的の(R,S)-ニコチンを70%の収率で得た。副生成物であるアミノアルコールと推測される化合物は、TLC上では検出されなかった。
Claims (9)
- シュードオキシニコチンの平衡混合物から特定の化合物を単離する工程、および
当該化合物を還元する工程、を備える、
(R,S)-ニコチンの製造方法。 - 前記単離工程が、シュードオキシニコチンの平衡混合物を蒸留して前記式(b)で表される化合物を単離することを含む、請求項2に記載の製造方法。
- 前記単離工程および還元工程を不活性雰囲気下において行う、請求項1~3のいずれかに記載の製造方法。
- 前記単離工程および還元工程を連続して行う、請求項1~4のいずれかに記載の製造方法。
- 前記還元工程において還元剤として水素を用いる、請求項1~5のいずれかに記載の製造方法。
- 前記還元工程において、アミノアルコールが実質的に生成しない、請求項1~6のいずれかに記載の製造方法。
- 請求項1~7のいずれかに記載の製造方法で得られた(R,S)-ニコチン。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2021/028399 WO2023007712A1 (ja) | 2021-07-30 | 2021-07-30 | (r,s)-ニコチンの製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2021/028399 WO2023007712A1 (ja) | 2021-07-30 | 2021-07-30 | (r,s)-ニコチンの製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2023007712A1 true WO2023007712A1 (ja) | 2023-02-02 |
Family
ID=85086588
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2021/028399 Ceased WO2023007712A1 (ja) | 2021-07-30 | 2021-07-30 | (r,s)-ニコチンの製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| WO (1) | WO2023007712A1 (ja) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014174505A2 (en) * | 2013-04-22 | 2014-10-30 | Perrigo Api Ltd. | A process for the preparation of nicotine comprising the enzymatic reduction of 4- (methylamino) -1- (pyridin-3- yl) butan-1-one |
| CN107011321A (zh) * | 2017-03-27 | 2017-08-04 | 华健 | 一种人工合成消旋体尼古丁的制备方法 |
| CN112876454A (zh) * | 2020-03-25 | 2021-06-01 | 深圳梵活生命科学股份有限公司 | 一种人工合成(r,s)-尼古丁盐的制备方法 |
-
2021
- 2021-07-30 WO PCT/JP2021/028399 patent/WO2023007712A1/ja not_active Ceased
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014174505A2 (en) * | 2013-04-22 | 2014-10-30 | Perrigo Api Ltd. | A process for the preparation of nicotine comprising the enzymatic reduction of 4- (methylamino) -1- (pyridin-3- yl) butan-1-one |
| CN107011321A (zh) * | 2017-03-27 | 2017-08-04 | 华健 | 一种人工合成消旋体尼古丁的制备方法 |
| CN112876454A (zh) * | 2020-03-25 | 2021-06-01 | 深圳梵活生命科学股份有限公司 | 一种人工合成(r,s)-尼古丁盐的制备方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3044212B1 (en) | Process for the large scale production of 1h- [1,2,3]triazole and its intermediate 1-benzyl-1h-[1,2,3]triazole | |
| JP2009057376A5 (ja) | ||
| KR20100029332A (ko) | 하이드록시클로로퀸의 신규 제조방법 | |
| CN118772081B (zh) | 一种制备n-甲基-2,3-二氢苯并噻嗪-4-酮的方法 | |
| JP2009062360A (ja) | シナカルセットの製造方法 | |
| JPH01193246A (ja) | 2,3―ジクロロピリジンの製造法 | |
| WO2023007712A1 (ja) | (r,s)-ニコチンの製造方法 | |
| TWI855165B (zh) | 製備(r)-4-胺基茚烷及其對應醯胺的方法 | |
| US5099067A (en) | Use of ammonium formate as a hydrogen transfer reagent for reduction of chiral nitro compounds with retention of configuration | |
| JP4397990B2 (ja) | 3−アルキルフラバノノール誘導体の精製法 | |
| KR100743617B1 (ko) | 고광학순도를 갖는 키랄 3-히드록시 피롤리딘 및 그유도체를 제조하는 방법 | |
| JPH053858B2 (ja) | ||
| JP2004131399A (ja) | シス−ヘキサヒドロイソインドリンの製造法 | |
| WO2023007710A1 (ja) | (r,s)-ニコチンの製造方法 | |
| CN119285542B (zh) | 一种利用自然光诱导羰基化反应构建6-氯-4-苯基喹啉-2(1h)-酮化合物的方法 | |
| CN117820139B (zh) | 一种2-叔丁基胺基苯甲醛类衍生物的制备方法 | |
| JP4099630B2 (ja) | パーフルオロアルキル化合物の製造方法 | |
| JP4314602B2 (ja) | 光学活性3−ヒドロキシピロリジン誘導体の製造方法 | |
| JP3382681B2 (ja) | 含フッ素化合物およびその製法 | |
| CN113968883A (zh) | 光学色酮衍生物及其制备方法 | |
| JP4896476B2 (ja) | メチルオキシメチルアミノピリジン誘導体及びその製造方法 | |
| JP4825969B2 (ja) | 第3級アルコールの製造方法 | |
| JP4480802B2 (ja) | 臭素化剤 | |
| JPH01121268A (ja) | 3,5−ジクロロピリジンの製造法 | |
| WO2004050604A2 (en) | Process for preparing terbinafine by using platinum as catalyst |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 21951911 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 21951911 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: JP |