WO2024253016A1 - 塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイス - Google Patents
塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイス Download PDFInfo
- Publication number
- WO2024253016A1 WO2024253016A1 PCT/JP2024/019859 JP2024019859W WO2024253016A1 WO 2024253016 A1 WO2024253016 A1 WO 2024253016A1 JP 2024019859 W JP2024019859 W JP 2024019859W WO 2024253016 A1 WO2024253016 A1 WO 2024253016A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- chloride ion
- external force
- electrode
- sensor
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M1/00—Apparatus for enzymology or microbiology
- C12M1/34—Measuring or testing with condition measuring or sensing means, e.g. colony counters
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/04—Determining presence or kind of microorganism; Use of selective media for testing antibiotics or bacteriocides; Compositions containing a chemical indicator therefor
- C12Q1/06—Quantitative determination
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/28—Electrolytic cell components
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/28—Electrolytic cell components
- G01N27/30—Electrodes, e.g. test electrodes; Half-cells
- G01N27/333—Ion-selective electrodes or membranes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
Definitions
- the present invention relates to a chloride ion sensor and a device using the same for detecting cancer cells and/or evaluating the malignancy of cancer cells.
- Non-Patent Document 1 Various molecules that recognize chloride ions have been known.
- the ionophore Bisthiourea-1 can be used as an ion-responsive membrane in an ion-selective electrode (Non-Patent Document 1).
- this molecule needs to be supported on a resin, which poses problems in terms of diffusibility and compatibility.
- the detection limit for chloride ions when this molecule is used is at the micromolar level, which poses problems in terms of detection sensitivity.
- N-Ethoxycarbonylmethyl-6-methoxyquinolinium bromide MQAE
- 6-methoxy-N-(3-sulfopropyl)quinolinium SPQ
- MQAE N-Ethoxycarbonylmethyl-6-methoxyquinolinium bromide
- SPQ 6-methoxy-N-(3-sulfopropyl)quinolinium
- this method examines whether fixed cells are cancer cells or not, so it is not possible to diagnose how cancer cells behave in the body in a short period of time.
- the method described in the above Patent Document 1 can be used to measure the invasiveness of live, unfixed cancer cells, which could not be evaluated by conventional diagnostic methods.
- Chloride ions have also been detected using oligoindole-based foldamers, and it has been shown that due to the accumulation effect of oligoindoles, the binding affinity for chloride ions is greatest in the order octamers > hexamers > tetramers (Non-Patent Document 2).
- the present invention aims to provide a chloride ion sensor and a device using the same for detecting cancer cells and/or evaluating the malignancy of cancer cells.
- chloride ions can be detected with high sensitivity by modifying the surface of an electrode with a compound having a specific structure, and also discovered that such a highly sensitive chloride ion sensor can be used to detect cancer cells and/or evaluate the malignancy of cancer cells, leading to the invention.
- a chloride ion sensor which is an electrode modified by [2]
- a device for detecting cancer cells and/or evaluating the malignancy of cancer cells comprising one or more chloride ion sensors according to any one of [1] to [6] and a pressure-insertion force sensor, characterized in that the pressure-insertion force sensor includes an external force applying means and an external force measuring means, and measures the external force while applying an external force to a test cell in vitro, and the chloride ion sensor measures chloride ions discharged from the cell.
- the pressure-insulation force sensor is a cantilever.
- the cantilever has a cell pressure probe at its tip.
- a method for screening a chloride ion channel inhibitor using a device including one or more chloride ion sensors according to any one of [1] to [6] and a pressure force sensor comprising:
- the device is characterized in that the pressure-insertion force sensor includes an external force applying means and an external force measuring means, and measures the external force while applying an external force to a test cell in vitro, and the chloride ion sensor measures chloride ions discharged from the cell, administering a test substance to the cells;
- the method includes a step of measuring the external force applied to the cell while measuring the external force and measuring the chloride ions excreted from the cell; and a step of screening the test substance as a candidate substance for a chloride ion channel inhibitor using the level of the chloride ions as an index.
- the present invention provides a chloride ion sensor and a device using the same for detecting cancer cells and/or assessing the malignancy of cancer cells.
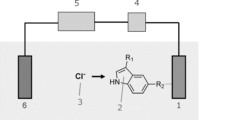
- FIG. 2 is a schematic diagram illustrating the chloride ion detection mechanism of the present invention.
- FIG. 13 shows the device output when an external force is applied to a cell-pressure cantilever using an atomic force microscope (AFM).
- AFM atomic force microscope
- FIG. 13 is a schematic diagram of an experimental system using a press-in force sensor.
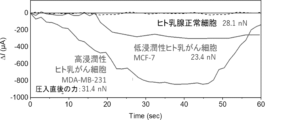
- FIG. 13 shows the measurement results of the press-in force sensor when human breast cancer cells are pressed in.
- This figure shows the measurement results of chloride ions expelled from three types of cells when an external force was applied to them.
- the time immediately after applying an external force to a single cell was set as 0 sec. 1 shows the results of measuring the amount of chloride ions expelled from cells when an external force was applied for 30 seconds to cells to which a chloride ion channel inhibitor had been added. * indicates p ⁇ 0.001.
- One embodiment of the present invention comprises: A chloride ion sensor having a chloride ion detection electrode, The chloride ion detection electrode has at least a part of the electrode surface containing the following compound: The electrode is a chloride ion sensor.
- the pyrrole ring site is a site that recognizes chloride ions
- R2 is a site that transmits the electron density change and dipole moment change accompanying ion capture to an electrode as an electron-conjugated anchor.
- the compound can selectively capture chloride ions due to the proton-donating ability of the pyrrole ring site. With the capture of chloride ions, an electron density change occurs in the pyrrole ring, and is transmitted to the electrode via the conjugated benzene ring and R2 . From the viewpoint of efficiently recognizing chloride ions and transmitting the electron density change and dipole moment change accompanying ion capture to the electrode, the compound can be suitably used in chloride ion detection.
- R1 is H, COOH, C ⁇ N, CHO, NO2 or halogens, preferably H. More preferably, it is an electron-withdrawing substituent that enhances the hydrogen bond donor property of the pyrrole ring moiety.
- R1 is a halogen, it may be any halogen element, for example, fluorine, chlorine, bromine, or iodine.
- R2 is an electron-conjugated anchor that transmits changes in electron density and dipole moment accompanying ion capture to the electrode, and therefore may have a structure having a molecular skeleton with ⁇ -electron conjugation.
- R2 is C ⁇ CH, SH, PO3H2 or COOH , preferably C ⁇ CH, before immobilization on the electrode.
- These functional groups have binding affinity with various electrodes, such as precious metal electrodes and oxide electrodes, as described below, and therefore the compound can be suitably immobilized on the electrode.
- R 2 is preferably C ⁇ C- for immobilizing a compound on a precious metal electrode.
- the R 2 portion of the compound does not need to be directly bonded to the electrode, and the R 2 portion may be bonded to the electrode via a group that serves as a linker, as long as it can transmit the electron density change and dipole moment change associated with chloride ion capture to the electrode.
- R2 when an amino group is added to R2 (e.g., when an amino group is added to C ⁇ C- to form C ⁇ C- NH2 ), a group that reacts with the amino group, such as a succinimide group, can be bonded to the electrode surface.
- the R2 portion is bonded to the electrode using the reactive residues of the amino group and succinimide group as a linker.
- R 2 is C ⁇ C-
- an embodiment can be mentioned in which a group that forms a 1,2,3-triazole ring by [3+2] dipolar cycloaddition reaction with C ⁇ C-, such as an azide group, is bonded to the electrode surface.
- the compound used in the present invention is not particularly limited as long as it can recognize chloride ions, but it is preferable that the compound has a high binding affinity to chloride ions.
- the binding constant Ka( Cl- ) with chloride ions may be 105M -1 or more, 106M -1 or more, or 107M -1 or more.
- the compound used in the present invention is preferably a compound represented by the following chemical formula, namely, 5-Ethynyl-1H-indole (hereinafter, also referred to as 5-EnIND).
- the compounds used in the present invention may be commercially available products or may be synthesized.
- commercially available products for example, 5-ethynyl-1H-indole (5-EnIND, Asta Tech, Inc., Product Code: 94615, CAS: 889108-48-9) can be used.
- the synthesis method is not particularly limited, and the compound can be synthesized by any method known to those skilled in the art (Non-Patent Documents 3-4).
- the material of the chloride ion detection electrode may be, for example, a precious metal such as gold, platinum, silver, or copper, or an oxide such as aluminum oxide (III) (Al 2 O 3 ), titanium oxide (IV) (TiO 2 ), or silicon dioxide (SiO 2 ).
- a precious metal such as gold, platinum, silver, or copper
- an oxide such as aluminum oxide (III) (Al 2 O 3 ), titanium oxide (IV) (TiO 2 ), or silicon dioxide (SiO 2 ).
- the electrode is preferably a precious metal electrode such as gold, platinum, silver, or copper
- the electrode is preferably an oxide electrode such as aluminum oxide (III) (Al 2 O 3 ), titanium oxide (IV) (TiO 2 ), or silicon dioxide (SiO 2 )
- the electrode is preferably an oxide electrode such as aluminum oxide (III) (Al 2 O 3 ), titanium oxide (IV) (TiO 2 ), or silicon dioxide (SiO 2 ).
- the manner in which the compound is immobilized on the electrode is not particularly limited, but it is preferable that the compound is arranged in the form of a monolayer on the electrode, and it is more preferable that the compound is arranged as densely as possible.
- intermolecular interactions between 5-EnIND molecules include ⁇ - ⁇ interactions between phenyl rings, hydrophobic interactions, and hydrogen bonds between NH sites of indole rings.
- solvents that do not easily cause solvation include dimethyl sulfoxide, which is an aprotic solvent.
- the electrode surface is modified with the above compound, but for example, 5% or more, 10% or more, 20% or more, 30% or more, 40% or more, 50% or more, 60% or more, 70% or more, 80% or more, 90% or more, or 100% of the electrode surface area may be modified with the above compound.
- the method for modifying the electrode surface with a compound can be appropriately selected depending on the type of electrode, the type of R2, etc., and can be carried out by methods known to those skilled in the art.
- Methods for modifying a noble metal electrode or an oxide electrode with a compound include, for example, a solution impregnation method, a vacuum deposition method, and a Langmuir-Blodgett method.
- a solution impregnation method e.g., a solution impregnation method, a vacuum deposition method, and a Langmuir-Blodgett method.
- 5-EnIND is modified on the surface of a gold electrode by the solution impregnation method, it can be carried out by the method shown below.
- the surface of other noble metal electrodes or oxide electrodes can also be modified with compounds by the same modification method.
- the surface of a noble metal electrode or oxide electrode can also be modified by the same modification method. After the gold electrode is exposed to oxygen plasma, the surface is washed with 2-propanol and then with distilled water.
- ⁇ 5-EnIND is immobilized as a covalently bonded monolayer via a gold-alkyne complexation reaction.
- 5-EnIND can be immobilized by immersing a gold thin film substrate in a 5-EnIND solution or dropping the solution onto the substrate and holding the substrate at a desired temperature for a desired time. It is preferable to immobilize the substrate in a light-shielded state.
- the temperature and time are not particularly limited as long as 5-EnIND can be immobilized, but the temperature can be, for example, 40°C to 80°C, 50°C to 70°C, or 55°C to 65°C, and the time can be, for example, 1 hour to 24 hours, 3 hours to 8 hours, or 5 hours to 7 hours.
- the electrode is allowed to stand for a desired period of time until it reaches room temperature. Wash with 2-propanol and then with distilled water to thoroughly wash away the 5-EnIND solution adhering to the surface, and dry with nitrogen gas.
- the chloride ion sensor of this embodiment may further include a reference electrode, which may be, for example, an unmodified gold electrode or a silver/silver chloride electrode, for example, an electrode having an internal solution of 3 M NaCl aqueous solution.
- a reference electrode which may be, for example, an unmodified gold electrode or a silver/silver chloride electrode, for example, an electrode having an internal solution of 3 M NaCl aqueous solution.
- the chloride ion sensor of this embodiment has a field effect transistor (FET)
- the FET may have a control gate terminal
- the reference electrode may be incorporated into the control gate terminal of the FET.
- the chloride ion sensor of this embodiment may further include a field effect transistor (FET).
- FET field effect transistor
- the chloride ion detection mechanism shown in FIG. 1 can be exemplified, and a potentiometric measurement system via a FET can be constructed by incorporating an electrode modified with the compound used in the present invention into the floating gate terminal of the FET.
- the pyrrole ring site in the compound used in the present invention acts as a receptor to capture the target chloride ion, causing a change in potential at the chloride ion detection electrode.
- the chloride ion in the solution can be detected by measuring the change in gate potential when the potential at the reference electrode is set as the reference potential.
- the FET to be used is not particularly limited as long as it can be used to measure chloride ions, and any FET can be used, for example, an n-type FET.
- the method of incorporating the chloride ion detection electrode into the gate terminal of the FET is not particularly limited, and can be performed by a method known to those skilled in the art.
- the potential difference generated between the chloride ion detection electrode and the reference electrode can be obtained as the output voltage or drain current of the FET source follower circuit, and the output voltage or drain current can be used as an index of the chloride ion level.
- an FET that exhibits an operation mode called a depression type i.e., an operation mode in which the drain current exhibits a linear variation range when the gate voltage is 0 V
- a depression type i.e., an operation mode in which the drain current exhibits a linear variation range when the gate voltage is 0 V
- the chloride ion sensor of this embodiment may include other components in addition to the above-mentioned FET, chloride ion detection electrode, and reference electrode, and may include other components such as a voltage measuring device, a power supply, an A/D conversion circuit, and a memory. These other components may be configured, for example, together with the FET as one device that constitutes a FET source follower circuit.
- Another embodiment of the present invention is a method for measuring chloride ions in a solution to be measured, comprising the step of contacting the above-mentioned chloride ion sensor with the solution to be measured.
- the solution to be measured may be any solution containing chloride ions.
- the solvent of the solution to be measured may be an aqueous electrolyte solution such as 4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid (HEPES) containing any concentration of NaBr, or may be an isotonic solution. It is preferable that the solvent itself does not contain or substantially does not contain chloride ions, and for example, the chloride ion concentration may be 100 pM or less, 10 pM or less, 1 pM or less, 0.1 pM or less, or 0.01 pM or less.
- an isotonic solution is not particularly limited as long as it has an osmotic pressure approximately the same as that of body fluids, and the osmotic pressure may be, for example, 250 to 320 mOsm/L, 260 to 310 mOsm/L, 270 to 300 mOsm/L, or 280 to 290 mOsm/L.
- the solvent of the solution to be measured is a liquid that does not contain or substantially does not contain electrolytes, and an isotonic solution that does not contain or substantially does not contain chloride ions can be suitably used. Examples of such isotonic solutions include glucose solutions and sucrose solutions.
- the glucose concentration is not particularly limited as long as it allows chloride ions to be detected with high sensitivity, but it can be, for example, a 5.0 to 6.0% (w/v) glucose solution, preferably a 5.2 to 5.8% (w/v) glucose solution, and more preferably a 5.4 to 5.6% (w/v) glucose solution.
- the pH of the solution is not particularly limited and can be adjusted as desired. For example, it may be 7.0 to 8.0.
- Contact with the solution to be measured can be achieved, for example, by immersing the chloride ion detection electrode of the chloride ion sensor in the solution to be measured.
- the measurement method of this embodiment can measure chloride ions, for example, by measuring the potential difference generated between the chloride ion detection electrode and the reference electrode using the chloride ion sensor.
- the potential difference can be obtained as the output voltage or drain current of the FET source follower circuit, and the output voltage or drain current can be used as an index of the chloride ion level.
- the chloride ion level may, for example, represent the concentration or amount of chloride ions, and may indicate a higher chloride ion level by a greater decrease in the output voltage in the solution being measured compared to an output voltage in a control solution that is free or substantially free of chloride ions, or may indicate a higher chloride ion level by a greater decrease in the drain current in the solution being measured compared to the drain current in a control solution that is free or substantially free of chloride ions.
- a calibration curve between the output voltage or drain current and the chloride ion level may be prepared in advance, and the concentration or amount of chloride ions may be calculated using this calibration curve.
- Another embodiment of the present invention is a device for detecting cancer cells and/or evaluating the malignancy of cancer cells, comprising one or more of the above-mentioned chloride ion sensors and an insertion force sensor, characterized in that the insertion force sensor includes an external force applying means and an external force measuring means, and measures the external force while applying an external force to a test cell in vitro, and the chloride ion sensor measures chloride ions excreted from the cell.
- the external force application means may be any means that applies pressure to the cell membrane from outside the cell, but a mode in which the cell membrane is pressed by mechanical means is preferable. Also, it is preferable that the force applied to the cell membrane from outside the cell is a force that stretches the cell membrane in the lateral direction (parallel to the cell membrane). It may be a mode in which the cell membrane is pressed from the outside, or a mode in which the cell membrane is pulled.
- the external force is preferably applied using a member having a contact surface equivalent to about 1/10 of the surface area of the cell (e.g., a contact area of 30-300 ⁇ m 2 ).
- a member may be, for example, a member having a cell presser that contacts the cell at its tip to apply pressure, or a member having a flat tip.
- the shape of the cell presser is not limited as long as it has the above-mentioned contact surface, and may be pyramidal (conical or pyramidal with an apex angle that does not destroy the cell membrane even when a desired pressure is applied to the cell membrane), cylindrical, prismatic, truncated conical, truncated pyramidal, spherical (including approximately spherical), or hemispherical (including approximately hemispherical).
- the material of the cell presser is not particularly limited as long as it has the above-mentioned contact surface, and examples thereof include organic polymers and metals.
- the size of the cell presser is not limited as long as it has the above-mentioned contact surface.
- the diameter at the base may be 5 to 20 ⁇ m, and if it is spherical or hemispherical, the particle size may be 5 to 20 ⁇ m.
- Examples include cantilevers used in scanning probe microscopes (SPMs) and atomic force microscopes (AFMs), and tipless cantilevers with the above-mentioned cell indenter attached to their tips.
- the material of the cell presser is not particularly limited, but examples include silicon (such as single crystal silicon), silicon nitride, gold, chromium, indium arsenide, silica, polyethylene terephthalate, polyethylene, polypropylene, polystyrene, polycarbonate, and acrylic resin.
- the strength of the applied external force may be such that the excretion of chloride ions through the cell membrane is observed, and it is preferable that the strength is such that the cell membrane can be stretched laterally, for example, 1 to 100 nN, and preferably 5 to 50 nN.
- the duration of application of the external force may be any duration sufficient for observing the discharge of chloride ions due to the application of the external force, and may be, for example, 1 second to 15 minutes, or 10 seconds to 2 minutes.
- the external force measuring means may be any means capable of measuring the external force applied to the cell.
- SPM scanning probe microscope
- AFM atomic force microscope
- an external force can be applied to a cell using a cantilever used in the SPM or AFM, and the external force can be measured by the SPM or AFM.
- the cantilever may have a piezoelectric element for measuring the pressure force.
- SPM and AFM are not used as the means for measuring external force
- a cantilever-type device having a piezoelectric element for measuring the pressure force can be used.
- a device for moving the cantilever up and down e.g.
- Stampo Unit SU100, Olympus can also be used to press the cantilever into the cell and apply an external force.
- the advantage is that it is not necessary to use expensive equipment such as SPM and AFM, since the external force applied to the cell can be measured simply by using a device for moving the cantilever up and down.
- a piezoelectric element for measuring the pressure force may be provided at the base of the cantilever, and the external force applied to the cell can be measured by measuring the resistance change of the piezoelectric element when the cell is pressed in.
- the resistance change of the piezoelectric element may be measured by converting it into a voltage using, for example, a Wheatstone bridge circuit known to those skilled in the art.
- the measurement principle of the press-in force sensor is shown below.
- the cell is pressed into the cell with a cell presser attached to the tip of a cell press-in cantilever located in the center of the press-in force, and the strain generated at the base of the cantilever during this process is measured as a resistance change by a piezoelectric element for measuring the press-in force.
- the piezo-resistance element is also affected by temperature changes in the solution. Therefore, by placing a temperature compensating piezoelectric element near the piezo-element for measuring the press-in force and performing a differential measurement of these two elements, the effects of temperature changes can be eliminated.
- the electrode having the above-mentioned compound modified on its surface which is used to detect chloride ions as a chloride ion sensor, is placed near an external force application means such as a cantilever in the device, but may be on a structure different from the external force application means, or the external force application means such as a cantilever may also function as a chloride ion detection electrode, i.e., the tip of the cantilever may be an electrode having the above-mentioned compound modified on its surface.
- the external force application means functions as a chloride ion detection electrode, it is preferable that the part of the external force application means that comes into contact with the cells and the part modified with the above-mentioned compound are separated. This allows the chloride ion sensor to measure chloride ions without being affected by the negative charge on the cell surface.
- the distance between the chloride ion detection electrode and the external force application portion of the external force application means is not particularly limited as long as it is possible to detect chloride ions discharged by the cell, but is, for example, 100 ⁇ m or less, 90 ⁇ m or less, 80 ⁇ m or less, 70 ⁇ m or less, 60 ⁇ m or less, or 50 ⁇ m or less.
- the lower limit is not particularly limited, but is, for example, 20 ⁇ m or more, 30 ⁇ m or more, or 40 ⁇ m or more. The closer this distance is, the higher the detection sensitivity of chloride ions discharged by the test cell can be.
- Each of the above devices may be provided with one or more chloride ion sensors, and when more than one is provided, the number of chloride ion sensors may be, for example, two, three, four or more.
- chloride ions released by cells to which an external force is applied can be efficiently detected.
- the chloride ion detection electrodes in the chloride ion sensors are arranged so as to surround the area where an external force is applied to the cells.
- the chloride ion sensor detects chloride ions released from cells when cells are pressed using a chloride ion detection electrode placed near the cell presser.
- a chloride ion detection electrode placed near the cell presser.
- Another embodiment of the present invention is a method for detecting cancer cells and/or evaluating the malignancy of cancer cells, comprising the steps of applying an external force to test cells and measuring chloride ions by the above-mentioned chloride ion measurement method.
- the method of this embodiment makes it possible to detect cancer cells and evaluate their malignancy. Based on the evaluation results, doctors can determine the course of cancer treatment. For example, if a patient is diagnosed with cancer cells or the cancer cells are determined to be highly malignant, appropriate treatment such as cancer resection surgery can be performed. In this way, the method does not include medical procedures performed by doctors, etc., but can provide data to assist doctors in diagnosing cancer.
- the potential difference between the chloride ion detection electrode and the reference electrode caused by applying an external force to the test cell can be obtained as the output voltage or drain current of the FET source follower circuit, and the output voltage or drain current can be used as an index of the chloride ion level discharged by the test cell into the measurement target solution.
- the chloride ion level for example, represents the concentration or amount of chloride ions.
- a larger decrease in the output voltage in the measurement target solution compared to the output voltage in a control solution that does not contain or substantially does not contain chloride ions may indicate a higher chloride ion level
- a larger decrease in the drain current in the measurement target solution compared to the drain current in a control solution that does not contain or substantially does not contain chloride ions may indicate a higher chloride ion level.
- a calibration curve between the output voltage or drain current and the chloride ion level may be prepared in advance, and the concentration or amount of chloride ions may be calculated using this calibration curve.
- the cancer cells to be analyzed may be mammalian cancer cells, such as human, mouse, or rat cancer cells, but are preferably human cancer cells.
- the cancer cells may be established cultured cells or may be cancer cells isolated from a living body. Cancer tissue may also be used directly for analysis.
- There are no particular limitations on the type of cancer and examples include breast cancer, stomach cancer, lung cancer, pancreatic cancer, liver cancer, colon cancer, prostate cancer, and cervical cancer.
- the test cell when the level of chloride ions discharged by applying an external force to a test cell is higher than the level of chloride ions discharged by applying an external force to a control normal cell, the test cell can be evaluated as being a cancer cell.
- the change in drain current when a drain voltage of 5 V and a gate voltage of 0 V are input as the control voltage for the FET is used as an indicator of chloride ion levels
- the drain current in a control solution that does not contain or substantially does not contain chloride ions e.g., a solution containing normal cells to which an external force has been applied
- the decrease in drain current in a measurement solution containing test cells to which an external force has been applied is, for example, 50 ⁇ A or more, 100 ⁇ A or more, 150 ⁇ A or more, or 200 ⁇ A or more
- the test cells can be evaluated as being cancer cells.
- the test cells can be evaluated as being cancer cells by combining not only the chloride ion level but also other indicators.
- the test cell when the chloride ion level discharged by applying an external force to a test cell in the above-mentioned device is higher than the chloride ion level discharged by applying an external force to a cancer cell with low invasiveness, the test cell can be evaluated as having a high malignancy.
- the malignancy of a cancer is an index that comprehensively indicates invasiveness, metastatic ability, etc., and when invasiveness or metastatic ability is high, the malignancy of the cancer can be evaluated as high.
- the test cells can be evaluated as having high malignancy.
- the test cells can be evaluated as being highly malignant by combining not only the chloride i
- each step of this embodiment may be taken from the above sections ⁇ Chloride ion sensor>, ⁇ Device for detecting cancer cells and/or assessing the malignancy of cancer cells>, or ⁇ Method for measuring chloride ions>.
- Another embodiment of the present invention is a method for screening chloride ion channel inhibitors using a device comprising one or more of the above chloride ion sensors and a pressure force sensor, comprising:
- the device is characterized in that the pressure-insertion force sensor includes an external force applying means and an external force measuring means, applies an external force to a test cell in vitro while measuring the external force, and the chloride ion sensor measures chloride ions discharged from the cell, administering a test substance to the cells;
- the method includes the steps of: applying an external force to the cell while measuring the external force and measuring chloride ions excreted from the cell; and screening the test substance as a candidate for a chloride ion channel inhibitor using the level of the chloride ions as an index.
- the screening step may be a step of screening the test substance as a candidate substance for a chloride ion channel inhibitor in any one of the following cases (1) to (3): (1) the level of chloride ions excreted by cells administered with the test substance due to the load of an external force is lower than the level of chloride ions measured in the same manner using cells not administered with the test substance; (2) The level of chloride ions excreted by the cells administered with the test substance due to the load of an external force is equivalent to or lower than the level of chloride ions measured in the same manner using low-invasive cancer cells or normal cells; (3) The level of chloride ions excreted by the cells administered with the test substance due to the application of an external force is lower than a predetermined cutoff value.
- the screening method is not particularly limited, but may optionally include additional steps. For example, it may include a step of conditioning the cells in advance, or a step of identifying the screened candidate substance as a chloride ion channel inhibitor.
- test substance is not particularly limited, but examples include compounds, antibodies, antigen-binding fragments, peptides, nucleic acids, etc.
- the amount of test substance administered to the cells and the reaction time of the test substance with the cells are not particularly limited and can be adjusted as appropriate depending on the type of test substance.
- the cells are not particularly limited, but are preferably cancer cells, and more preferably highly invasive cancer cells.
- highly invasive human breast cancer cells may be used as the cells, and in this case, the less invasive cancer cells and normal cells in (2) above may be less invasive human breast cancer cells and human mammary epithelial cells, respectively.
- the chloride ion channel expressed in the cells used in this embodiment is not particularly limited as long as the cells can be used in the screening method of this embodiment, and examples thereof include ClC chloride ion channels (ClC-2, ClC-3, ClC-4, ClC-6, ClC-7, etc.), calcium-dependent chloride ion channels (TMEM16A, TMEM16B, Best1, Best2, etc.), and volume-sensitive outwardly rectifying anion channels (CLIC1, LRRC8A, etc.).
- the screening method of this embodiment measures chloride ions discharged by applying an external force to the cells
- the chloride ion channel expressed in the cells is a channel that discharges chloride ions by applying an external force to the cells
- volume-sensitive outwardly rectifying anion channels such as CLIC1 and LRRC8A, which are channels that detect cell swelling, and CLIC1 is particularly preferable.
- Example 1 Preparation of an ion sensor
- the surface of the detection electrode was modified with 5-ethynyl-1H-indole (5-EnIND, Asta Tech, Inc., Product Code: 94615, CAS: 889108-48-9).
- 5-EnIND was dissolved in dimethyl sulfoxide (DMSO) to prepare a 10 mM 5-EnIND solution.
- DMSO dimethyl sulfoxide
- the gold thin film surface to be the detection electrode was irradiated with oxygen plasma, washed with 2-propanol, washed with distilled water, and dried with nitrogen gas.
- the gold thin film substrate was immersed in the 5-EnIND solution or the solution was dropped onto the substrate, and the substrate was kept on a hot plate at 60°C in a light-shielded state for 6 hours. This resulted in the immobilization of 5-EnIND as a monolayer by covalent bonding via the gold-alkyne complexation reaction. After leaving the substrate at 25°C for 12 hours, the substrate was washed with 2-propanol and then with distilled water to thoroughly wash the 5-EnIND solution attached to the surface, and then dried with nitrogen gas.
- Example 2 Incorporation of detection electrodes into FET and titration experiment A gold electrode modified with 5-EnIND (hereafter, 5-EnIND-modified electrode) was incorporated into the floating gate terminal of an FET to construct a potentiometric measurement system via an FET ( Figure 1). To examine the chloride ion recognition ability of the 5-EnIND-modified electrode by titration experiments, the electrode was incorporated into the floating gate terminal of an FET source follower circuit (BCT-2, BioCMOS).
- BCT-2 FET source follower circuit
- 4-ethynyl-1H-indole (4-EnIND) is a structural isomer of 5-EnIND.
- R2 at the 4th or 5th position of EnIND is preferred for bonding to an electrode.
- an electrode was prepared using 4-EnIND in the same manner as for 5-EnIND.
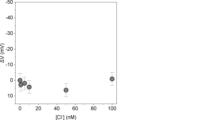
- the potential response of the FET source follower circuit to changes in chloride ion concentration was confirmed using the prepared electrode, and when 4-EnIND was used, almost no potential change was observed (Figure 3). Although both have the same pyrrole ring moiety (NH moiety) as 5-EnIND as a hydrogen bond donor responsible for ion capture, the reason for this difference in potential response is thought to be due to the difference in the formation state of each monolayer.
- 5-EnIND which has an alkyne moiety that bonds to a gold electrode added to the 5th position, is thought to have a steric hindrance advantage in forming a monolayer compared to 4-EnIND added to the 4th position. For this reason, it is assumed that the density of EnIND in the monolayer is higher when 5-EnIND is applied compared to when 4-EnIND is applied.
- the factors that contribute to the recognition of chloride ions in aqueous solution include the accumulation effect of EnIND and the formation of a hydrophobic field, so it is presumed that the binding affinity for chloride ions is reduced on the 4-EnIND-modified electrode.
- the reasons for the enhanced response at lower concentrations are thought to be, for example, the absence of contaminating anions that inhibit chloride ion recognition, and the small effect of the Debye shielding effect, which resulted in a stronger change in electron density accompanying ion capture by the 5-EnIND monolayer, which induced a change in the electrode potential.
- Example 3 Structure of a MEMS cantilever type device
- MEMS Micro Electro Mechanical Systems
- This device is a device that combines a pressure-insertion force sensor and a chloride ion (Cl - ) sensor.
- the cantilever-type device used in Example 3 is a device that has two chloride ion sensors in the vicinity of the pressure-insertion force sensor, and specifically, the distance between the chloride ion detection electrode and the center of the cell indenter is set to 60 ⁇ m.
- the chloride ion detection electrode was formed by selectively dropping 5-EnIND solution onto the electrode material using an inkjet device and holding it in a hot chamber at 60°C for 6 hours.
- the cantilever was then washed with 2-propanol and then with distilled water to thoroughly remove unbound 5-EnIND, and used for chloride ion detection.
- An untreated gold electrode was placed near the base of the MEMS, and used as a control gate terminal to set the reference potential for chloride ion measurement.
- the chloride ion detection electrode of the MEMS was connected to the gate terminal of a commercially available n-type FET (Toshiba Semiconductor 2SK241Y) via a flexible wiring board.
- the source and drain terminals of the FET and the control gate terminal of the MEMS were connected to a source meter (Keithley Instruments 2636B), respectively, to control input and output.
- Example 4 Calibration of a MEMS cantilever-type device using an atomic force microscope
- the MEMS cantilever device was fixed on a dish and immersed in a 5.5% glucose solution, and an external force was applied using an AFM.
- the cantilever was lowered using a pyramidal tip until the force applied to the cantilever reached 5, 10, 30, or 50 nN.
- the response of the press-in force sensor of the cantilever device when this external force was applied was measured, and a calibration curve was created (Figure 6). Based on this calibration curve, the press-in force was actually measured when cells were pressed into the device.
- Example 5 Measurement of ions excreted from cells when hypotonic stimulation is applied
- Highly invasive human breast cancer cells MDA-MB-231 ATCC, Product Code: HTB-26
- the cell medium was replaced with a 5.5% glucose solution, and the FET sensor was brought close to the cells on the dish.
- the solution was then replaced with a 160 mOsm hypotonic phosphate buffer solution to induce chloride ion excretion.
- the FET sensor was used for measurement, the sensor response was confirmed approximately 15 seconds after the phosphate buffer solution was replaced (Figure 7).
- Figure 8A shows a schematic diagram of an experimental system using a pressure force sensor
- Figure 8B shows the results of measuring the pressure force when human breast cancer cells were pressed into the cell.
- the pressure force on the vertical axis is a value calculated based on the calibration curve in Figure 6.
- the pressure force was detected by contacting the cell with the cell presser.
- the cantilever was held in a state where the cell presser was in contact with the cell, and the cell was pressed into the cell for a certain period of time. It was confirmed that the pressure force returned to its initial value by removing the load thereafter. The maximum value immediately after pressing was taken as the pressure force.
- Example 7 Measurement of ions excreted from cells when external force is applied
- Highly invasive human breast cancer cells MDA-MB-231, low-invasive human breast cancer cells MCF-7 (JCRB Cell Bank, Product Code: JCRB0134), and human mammary epithelial cells MCF10A (ATCC, Product Code: CRL-10317) were seeded at 5 ⁇ 104 cells each and cultured overnight in a CO2 incubator.
- the cell medium was replaced with 5.5% glucose solution, and the FET sensor fused cantilever type device was brought close to a single cell on the dish and the cantilever was lowered to press the cell.
- Example 8 Evaluation of ion efflux ability of cells to which a chloride ion channel inhibitor has been added
- Highly invasive human breast cancer cells MDA-MB-231, low-invasive human breast cancer cells MCF-7, and human mammary epithelial cells MCF10A were seeded at 5 ⁇ 104 cells each and cultured overnight in a CO2 incubator.
- chloride ion channel inhibitor IAA-94 final concentration 100 ⁇ M; Sigma Aldrich, Product Code: I117, CAS: 54197-31-8) was added to the medium and reacted for 1 hour in a CO2 incubator.
- the cell medium was replaced with 5.5% glucose solution, and the FET sensor fused cantilever type device was brought close to a single cell on the dish and the cantilever was lowered to press the cell.
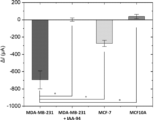
- the drain current was measured 30 seconds after pressing, and the FET sensor responded to untreated MDA-MB-231 cells, and chloride ions were excreted, whereas no sensor response was observed in IAA-94-added cells ( Figure 10).
- this device can be used to evaluate the effects of chloride ion channel inhibitors that receive mechanical stimuli. This device may be useful for screening chloride ion channel inhibitors that contribute to the invasion of cancer cells.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Organic Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Microbiology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Food Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Toxicology (AREA)
- Sustainable Development (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
電極表面の少なくとも一部を下記化合物:(式中、 R1は、H、COOH、C≡N、CHO、NO2又はハロゲン類であり; R2は、C≡C-、S-、P(=O)(O-)2又はCOO-である) で修飾することにより、高感度に塩化物イオンの検出を行えることを見出したことにより、その電極を含む塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスを提供することができた。
Description
本発明は、塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスに関する。
これまでに塩化物イオンを認識する様々な分子が知られている。例えば、イオノフォアであるBisthiourea-1は、イオン選択性電極におけるイオン応答膜として使用できることが示されている(非特許文献1)。
しかしながら、当該分子は、イオン応答膜として使用する際には樹脂への担持を要するため、拡散性や相溶性の観点において課題を有するものであり、また当該分子を用いたときの塩化物イオンの検出限界はマイクロモーラーレベルであるため、検出感度の観点においても課題を有するものであった。
しかしながら、当該分子は、イオン応答膜として使用する際には樹脂への担持を要するため、拡散性や相溶性の観点において課題を有するものであり、また当該分子を用いたときの塩化物イオンの検出限界はマイクロモーラーレベルであるため、検出感度の観点においても課題を有するものであった。
また、塩化物イオンと結合することで蛍光強度が減少する細胞膜透過性の蛍光色素として、例えば、N-Ethoxycarbonylmethyl-6-methoxyquinolinium bromide(MQAE)や6-methoxy-N-(3-sulfopropyl)quinolinium(SPQ)が知られており、本発明者らは、これまでにこれらの蛍光色素を用いたがん細胞の評価方法を開発した(特許文献1)。当該方法は、がん細胞に対して機械的に外力を印加することにより塩化物イオン排出を誘導するものであって、本発明者らが、高浸潤性のがん細胞は塩化物イオン排出能が高いことを見出したことによるものである。従来から行われている細胞診や組織診といった診断方法は、診断までに1日~数日時間を要するものである。またこの手法では固定後の細胞ががん細胞か否かを調べるものであったため、がん細胞が体内でどのように振る舞うかを短時間で診断することができなかった。上述の特許文献1に記載の方法によれば、従来の診断方法では評価できなかった固定されていない生きたがん細胞の浸潤能測定に活用することができる。しかしながら、蛍光色素の消光反応に依存する方法では原理的にS/N比の増大が難しく、当該方法による塩化物イオンの検出限界はマイクロモーラーレベルからミリモーラーレベルであるため、より高感度で塩化物イオンを測定できる方法が望まれていた。
また、オリゴインドールベースのフォルダマーを用いた塩化物イオンの検出も行われており、オリゴインドールの集積効果により、オクタマー>ヘキサマー>テトラマーの順番で塩化物イオンに対する結合親和性が大きいことが示されている(非特許文献2)。
Anal. Chem. 1997, 69, 1038
J. Am. Chem. Soc. 2005, 127, 12214
Eur. J. Med. Chem. 2012, 56, 263-270
Bioorg. Med. Chem. 2006, 14, 3825-3834
本発明は、塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスを提供することを目的とするものである。
本発明者らは、上記課題を解決するために鋭意検討した結果、特定の構造を有する化合物を電極表面に修飾することにより、高感度に塩化物イオンの検出を行えることを見出し、また、そのような高感度な塩化物イオンセンサをがん細胞の検出及び/又はがん細胞の悪性度評価のために用いることができることを見出し、本発明に想到した。
すなわち、本発明は以下の通りである。
[1]塩化物イオン検出電極を有する、塩化物イオンセンサであって、
前記塩化物イオン検出電極は、電極表面の少なくとも一部が下記化合物:
(式中、
R1は、H、COOH、C≡N、CHO、NO2又はハロゲン類であり;
R2は、C≡C-、S-、P(=O)(O-)2又はCOO-である)
によって修飾された電極である、塩化物イオンセンサ。
[2]R1がHであり、及び/又はR2がC≡C-である、[1]に記載の塩化物イオンセンサ。
[3]前記化合物が、5-Ethynyl-1H-indoleである、[1]又は[2]に記載の塩化物イオンセンサ。
[4]前記電極が金電極である、[1]~[3]の何れかに記載の塩化物イオンセンサ。
[5]さらに参照電極を有する、[1]~[4]の何れかに記載の塩化物イオンセンサ。
[6]さらに電界効果トランジスタ(FET)を有する、[1]~[5]の何れかに記載の塩化物イオンセンサ。
[7]1又は複数個の[1]~[6]の何れかに記載の塩化物イオンセンサと、圧入力センサを備える、がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスであって、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とする、デバイス。
[8]前記圧入力センサがカンチレバーである、[7]に記載のデバイス。
[9]前記カンチレバーが、先端部に細胞圧子を有する、[8]に記載のデバイス。
[10]前記カンチレバーが、根元部に圧入力計測用ピエゾ素子を有する、[8]又は[9]に記載のデバイス。
[11]前記圧入力センサが、温度補償用ピエゾ素子を有する、[7]~[10]の何れかに記載のデバイス。
[12]前記塩化物イオン検出電極と、前記外力負荷手段における外力負荷部の中心との距離が、100μm以下である、[7]~[11]の何れかに記載のデバイス。
[13][1]~[6]の何れかに記載の塩化物イオンセンサを、測定対象溶液に接触させる工程を含む、測定対象溶液における塩化物イオンの測定方法。
[14]前記測定対象溶液の溶媒が、塩化物イオンの濃度が100pM以下の等張液である、[13]に記載の方法。
[15]被検細胞に外力を負荷する工程、及び被検細胞が排出する塩化物イオンを[13]または[14]に記載される方法により測定する工程を含む、がん細胞を検出するための及び/又はがん細胞の悪性度を評価するための方法。
[16]1又は複数個の[1]~[6]の何れかに記載の塩化物イオンセンサと、圧入力センサを備えるデバイスを用いた、塩化物イオンチャネル阻害剤のスクリーニング方法であって、
前記デバイスは、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とするデバイスであり、
被験物質を細胞に投与する工程;
前記細胞に外力を負荷しつつ外力を測定し、且つ前記細胞から排出される塩化物イオンを測定する工程;及び
前記塩化物イオンのレベルを指標として、前記被験物質が塩化物イオンチャネル阻害剤の候補物質としてスクリーニングする工程を含む、方法。
[1]塩化物イオン検出電極を有する、塩化物イオンセンサであって、
前記塩化物イオン検出電極は、電極表面の少なくとも一部が下記化合物:
(式中、
R1は、H、COOH、C≡N、CHO、NO2又はハロゲン類であり;
R2は、C≡C-、S-、P(=O)(O-)2又はCOO-である)
によって修飾された電極である、塩化物イオンセンサ。
[2]R1がHであり、及び/又はR2がC≡C-である、[1]に記載の塩化物イオンセンサ。
[3]前記化合物が、5-Ethynyl-1H-indoleである、[1]又は[2]に記載の塩化物イオンセンサ。
[4]前記電極が金電極である、[1]~[3]の何れかに記載の塩化物イオンセンサ。
[5]さらに参照電極を有する、[1]~[4]の何れかに記載の塩化物イオンセンサ。
[6]さらに電界効果トランジスタ(FET)を有する、[1]~[5]の何れかに記載の塩化物イオンセンサ。
[7]1又は複数個の[1]~[6]の何れかに記載の塩化物イオンセンサと、圧入力センサを備える、がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスであって、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とする、デバイス。
[8]前記圧入力センサがカンチレバーである、[7]に記載のデバイス。
[9]前記カンチレバーが、先端部に細胞圧子を有する、[8]に記載のデバイス。
[10]前記カンチレバーが、根元部に圧入力計測用ピエゾ素子を有する、[8]又は[9]に記載のデバイス。
[11]前記圧入力センサが、温度補償用ピエゾ素子を有する、[7]~[10]の何れかに記載のデバイス。
[12]前記塩化物イオン検出電極と、前記外力負荷手段における外力負荷部の中心との距離が、100μm以下である、[7]~[11]の何れかに記載のデバイス。
[13][1]~[6]の何れかに記載の塩化物イオンセンサを、測定対象溶液に接触させる工程を含む、測定対象溶液における塩化物イオンの測定方法。
[14]前記測定対象溶液の溶媒が、塩化物イオンの濃度が100pM以下の等張液である、[13]に記載の方法。
[15]被検細胞に外力を負荷する工程、及び被検細胞が排出する塩化物イオンを[13]または[14]に記載される方法により測定する工程を含む、がん細胞を検出するための及び/又はがん細胞の悪性度を評価するための方法。
[16]1又は複数個の[1]~[6]の何れかに記載の塩化物イオンセンサと、圧入力センサを備えるデバイスを用いた、塩化物イオンチャネル阻害剤のスクリーニング方法であって、
前記デバイスは、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とするデバイスであり、
被験物質を細胞に投与する工程;
前記細胞に外力を負荷しつつ外力を測定し、且つ前記細胞から排出される塩化物イオンを測定する工程;及び
前記塩化物イオンのレベルを指標として、前記被験物質が塩化物イオンチャネル阻害剤の候補物質としてスクリーニングする工程を含む、方法。
本発明により、塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスを提供することができた。
<塩化物イオンセンサ>
本発明の一実施態様は、
塩化物イオン検出電極を有する、塩化物イオンセンサであって、
前記塩化物イオン検出電極は、電極表面の少なくとも一部が下記化合物:
によって修飾された電極である、塩化物イオンセンサである。
本発明の一実施態様は、
塩化物イオン検出電極を有する、塩化物イオンセンサであって、
前記塩化物イオン検出電極は、電極表面の少なくとも一部が下記化合物:
によって修飾された電極である、塩化物イオンセンサである。
本発明に用いられる化合物は、ピロール環部位が塩化物イオンを認識する部位であり、R2が電子共役アンカーとしてイオン捕捉に伴う電子密度変化や双極子モーメント変化を電極に伝える部位である。当該化合物は、ピロール環部位が有するプロトン供与性により、塩化物イオンを選択的に捕捉することができる。塩化物イオンの捕捉に伴い、ピロール環の電子密度変化が生じ、共役されたベンゼン環及びR2を介して電極に伝達される。塩化物イオンを効率的に認識し、イオン捕捉に伴う電子密度変化や双極子モーメント変化を電極に伝えることができるという観点から、塩化物イオン検出において当該化合物を好適に利用できる。
R1は、H、COOH、C≡N、CHO、NO2又はハロゲン類であり、好ましくはHである。ピロール環部位の水素結合ドナー性を増強する電子吸引性置換基がより好ましい。R1がハロゲン類である場合、任意のハロゲン元素でよいが、例えば、フッ素、塩素、臭素、ヨウ素が挙げられる。
R2は、電子共役アンカーとしてイオン捕捉に伴う電子密度変化や双極子モーメント変化を電極に伝える部位であるために、π電子共役性を有する分子骨格を有する構造であればよく、例えばR2は、電極への固定化後はC≡C-、S-、P(=O)(O-)2又はCOO-であり、好ましくはC≡C-である。R2は、電極への固定化前はC≡CH、SH、PO3H2又はCOOHであり、好ましくはC≡CHである。これらの官能基は、後述の貴金属電極、酸化物電極の各種電極との結合親和性を有するため、当該化合物を電極に好適に固定することができる。
細胞、組織が存在する生理条件下では、還元性物質が多量に共存する可能性がある。貴金属電極への化合物の固定化にはチオール基を介した結合が汎用されているところ、当該チオール基を介した結合が還元性物質により還元されることによって、当該貴金属電極から当該化合物が脱離する可能性がある。そのため、生理条件下での使用を指向した場合、において貴金属電極上への化合物の固定化には、R2はC≡C-であることが好ましい。ただし、上記化合物はR2部分が直接電極に結合している必要はなく、塩化物イオン捕捉に伴う電子密度変化や双極子モーメント変化を電極に伝えることができる限りにおいて、R2部分がリンカーとなる基を介して電極に結合されてもよい。
例えば、R2にアミノ基を付加するとき(例えばC≡C-にアミノ基を付加してC≡C-NH2とするとき)、電極表面にそのアミノ基に反応する基、例えばスクシンイミド基が結合している態様を挙げることができる。このとき、これらのアミノ基とスクシンイミド基の反応残基部分をリンカーとしてR2部分が電極に結合される。
また、R2がC≡C-であるとき、電極表面にC≡C-と[3+2]双極子付加環化反応によって1,2,3-トリアソゾール環を形成する基、例えばアジド基が結合している態様を挙げることができる。このとき、銅(I)およびトリス[(1-べンジル-1H-1,2,3-トリアゾール-4-イル)メチル]アミンを触媒として用いることにより、これらのC≡C-とアジド基が反応して1,2,3-トリアゾール環を形成することができる。すなわち、C≡C-であるR2とアジド基とが一体としてリンカーとなることにより、化合物が電極に結合される。
細胞、組織が存在する生理条件下では、還元性物質が多量に共存する可能性がある。貴金属電極への化合物の固定化にはチオール基を介した結合が汎用されているところ、当該チオール基を介した結合が還元性物質により還元されることによって、当該貴金属電極から当該化合物が脱離する可能性がある。そのため、生理条件下での使用を指向した場合、において貴金属電極上への化合物の固定化には、R2はC≡C-であることが好ましい。ただし、上記化合物はR2部分が直接電極に結合している必要はなく、塩化物イオン捕捉に伴う電子密度変化や双極子モーメント変化を電極に伝えることができる限りにおいて、R2部分がリンカーとなる基を介して電極に結合されてもよい。
例えば、R2にアミノ基を付加するとき(例えばC≡C-にアミノ基を付加してC≡C-NH2とするとき)、電極表面にそのアミノ基に反応する基、例えばスクシンイミド基が結合している態様を挙げることができる。このとき、これらのアミノ基とスクシンイミド基の反応残基部分をリンカーとしてR2部分が電極に結合される。
また、R2がC≡C-であるとき、電極表面にC≡C-と[3+2]双極子付加環化反応によって1,2,3-トリアソゾール環を形成する基、例えばアジド基が結合している態様を挙げることができる。このとき、銅(I)およびトリス[(1-べンジル-1H-1,2,3-トリアゾール-4-イル)メチル]アミンを触媒として用いることにより、これらのC≡C-とアジド基が反応して1,2,3-トリアゾール環を形成することができる。すなわち、C≡C-であるR2とアジド基とが一体としてリンカーとなることにより、化合物が電極に結合される。
本発明に用いられる化合物は、塩化物イオンを認識できる限り特に限定されないが、塩化物イオンに対する結合親和性が大きいことが好ましい。例えば、塩化物イオンとの結合定数であるKa(Cl-)が、105 M-1以上であってよく、106 M-1以上であってよく、107 M-1以上であってよい。
特に限定されないが、本発明に用いられる化合物は市販品を用いてもよく、合成したものを用いてもよい。市販品を用いる場合は、例えば5-ethynyl-1H-indole(5-EnIND, Asta Tech, Inc., Product Code: 94615, CAS: 889108-48-9)を用いることができる。合成する場合は、その合成方法は特に限定されず、当業者に既知の任意の方法により合成することができる(非特許文献3~4)。
塩化物イオン検出電極の素材は、例えば、金、白金、銀、銅等の貴金属、酸化アルミニウム(III) (Al2O3)、酸化チタン(IV) (TiO2)、二酸化ケイ素 (SiO2)等の酸化物であってよい。電極の素材によって、当業者は表面修飾する化合物のR2や溶液の種類等を適切に選択できる。R2がC≡C-またはS-であるとき、電極は金、白金、銀、銅等の貴金属電極であることが好ましく、R2がP(=O)(O-)2であるとき、電極は酸化アルミニウム(III) (Al2O3)、酸化チタン(IV) (TiO2)等の酸化物電極であることが好ましく、R2がCOO-であるとき、電極は酸化アルミニウム(III) (Al2O3)、酸化チタン(IV) (TiO2)、二酸化ケイ素 (SiO2)等の酸化物電極であることが好ましい。
上記化合物の電極上への固定化様式は特に制限されないが、電極上において単分子膜状に配置されることが好ましく、また、できるだけ化合物が高密度に配置されることがより好ましい。
単分子膜状又は高密度に配置するために、5-EnIND同士の分子間相互作用を極力阻害しないよう、溶媒和を起こしにくい溶媒中で固定化反応を行うことが望ましい。5-EnIND同士の分子間相互作用とは、例えばフェニル環同士にはたらくπ-π相互作用、疎水性相互作用が挙げられ、またはインドール環のNH部位間にはたらく水素結合が挙げられる。溶媒和を起こしにくい溶媒とは、例えば非プロトン性溶媒であるジメチルスルホキシドが挙げられる。また、単分子膜状を保持するために、電極に固定化されていないフリーの5-EnINDを十分に取り除くことが望ましく、プロトン性溶媒であるアルコールで洗浄し、さらに水で洗浄することにより、十分に残留分子を取り除くことが望ましい。
単分子膜状に配置されることにより、非特許文献2におけるフォルダマーを用いた実験により示された集積効果と同様に、結合親和性の増強効果を生じることができる。これにより、測定対象溶液に含まれる塩化物イオン濃度が低い場合であっても、塩化物イオンを検出することができる。
単分子膜状又は高密度に配置するために、5-EnIND同士の分子間相互作用を極力阻害しないよう、溶媒和を起こしにくい溶媒中で固定化反応を行うことが望ましい。5-EnIND同士の分子間相互作用とは、例えばフェニル環同士にはたらくπ-π相互作用、疎水性相互作用が挙げられ、またはインドール環のNH部位間にはたらく水素結合が挙げられる。溶媒和を起こしにくい溶媒とは、例えば非プロトン性溶媒であるジメチルスルホキシドが挙げられる。また、単分子膜状を保持するために、電極に固定化されていないフリーの5-EnINDを十分に取り除くことが望ましく、プロトン性溶媒であるアルコールで洗浄し、さらに水で洗浄することにより、十分に残留分子を取り除くことが望ましい。
単分子膜状に配置されることにより、非特許文献2におけるフォルダマーを用いた実験により示された集積効果と同様に、結合親和性の増強効果を生じることができる。これにより、測定対象溶液に含まれる塩化物イオン濃度が低い場合であっても、塩化物イオンを検出することができる。
電極表面の少なくとも一部が上記化合物によって修飾されているとは特に限定されないが、例えば、電極表面積の5%以上、10%以上、20%以上、30%以上、40%以上、50%以上、60%以上、70%以上、80%以上、90%以上、100%が上記化合物によって修飾されているものであってよい。
電極の表面に化合物を修飾する方法は電極の種類やR2の種類等に応じて適宜選択でき、当業者に既知の方法により行うことができる。
貴金属電極又は酸化物電極に化合物を修飾する方法として、例えば、溶液含漬法、真空蒸着法、Langmuir-Blodgett法を挙げることができる。
例えば、溶液含漬法によって、金電極表面に5-EnINDを修飾するとき、以下に示すような方法で行うことができる。他の貴金属電極又は酸化物電極の表面に対しても、同様の修飾方法にて化合物を修飾することができる。また、他の化合物を用いたときも同様の修飾方法にて貴金属電極又は酸化物電極の表面に修飾することができる。
・金電極に対して酸素プラズマ照射処理を行った後に、表面を2-プロパノールで洗浄し、さらに蒸留水で洗浄する。
・金-アルキン錯形成反応を介して、5-EnINDを共有結合された単分子膜として固定化する。具体的には、金薄膜基板を5-EnIND溶液に浸漬ないし同基板上に当該溶液を滴下して、任意の温度で任意の時間保持することにより固定化することができる。遮光状態にて固定化することが好ましい。このときの温度及び時間は、5-EnINDを固定化できる限り特に限定されないが、温度は、例えば40℃~80℃、50℃~70℃、55℃~65℃とすることができ、時間は、例えば、1時間~24時間、3時間~8時間、5時間~7時間とすることができる。
・固定化後の電極が室温になるまで任意の時間静置する。
・2-プロパノールで洗浄し、さらに蒸留水で洗浄することによって表面に付着した5-EnIND溶液を十分に洗浄し、窒素ガスによって乾燥する。
貴金属電極又は酸化物電極に化合物を修飾する方法として、例えば、溶液含漬法、真空蒸着法、Langmuir-Blodgett法を挙げることができる。
例えば、溶液含漬法によって、金電極表面に5-EnINDを修飾するとき、以下に示すような方法で行うことができる。他の貴金属電極又は酸化物電極の表面に対しても、同様の修飾方法にて化合物を修飾することができる。また、他の化合物を用いたときも同様の修飾方法にて貴金属電極又は酸化物電極の表面に修飾することができる。
・金電極に対して酸素プラズマ照射処理を行った後に、表面を2-プロパノールで洗浄し、さらに蒸留水で洗浄する。
・金-アルキン錯形成反応を介して、5-EnINDを共有結合された単分子膜として固定化する。具体的には、金薄膜基板を5-EnIND溶液に浸漬ないし同基板上に当該溶液を滴下して、任意の温度で任意の時間保持することにより固定化することができる。遮光状態にて固定化することが好ましい。このときの温度及び時間は、5-EnINDを固定化できる限り特に限定されないが、温度は、例えば40℃~80℃、50℃~70℃、55℃~65℃とすることができ、時間は、例えば、1時間~24時間、3時間~8時間、5時間~7時間とすることができる。
・固定化後の電極が室温になるまで任意の時間静置する。
・2-プロパノールで洗浄し、さらに蒸留水で洗浄することによって表面に付着した5-EnIND溶液を十分に洗浄し、窒素ガスによって乾燥する。
本実施形態の塩化物イオンセンサは、さらに参照電極を有してもよく、前記参照電極は、例えば、未修飾の金電極であってもよく、銀/塩化銀電極であってもよい。銀/塩化銀電極としては、例えば内部溶液を3 M NaCl水溶液としたものを使用できる。
例えば、後述のように、本実施形態の塩化物イオンセンサが電界効果トランジスタ(FET)を有するものであるときには、FETは制御ゲート端子を有してもよい。参照電極はFETの制御ゲート端子に組み込まれていてもよい。
例えば、後述のように、本実施形態の塩化物イオンセンサが電界効果トランジスタ(FET)を有するものであるときには、FETは制御ゲート端子を有してもよい。参照電極はFETの制御ゲート端子に組み込まれていてもよい。
本実施形態の塩化物イオンセンサは、さらに電界効果トランジスタ(FET)を有してもよい。例えば、図1に示す塩化物イオン検出機構を例示することができ、本発明に用いられる化合物によって修飾された電極をFETの浮遊ゲート端子に組み込むことでFETを介したポテンショメトリック測定系を構築することができる。具体的には、本発明に用いられる化合物におけるピロール環部位がレセプタとして、標的である塩化物イオンを捕捉することにより、塩化物イオン検出電極に電位変化が生じる。そして、参照電極における電位を基準電位としたときのゲート電位の変化を測定することにより、溶液中の塩化物イオンを検出できる。
使用するFETは、塩化物イオンの測定に使用できる限り特に限定されず、任意のものを使用することができ、例えば、n型FETを使用することができる。塩化物イオン検出電極をFETのゲート端子に組み込む方法は特に限定されず、当業者に既知の方法によって行うことができる。例えば、塩化物イオン検出電極と参照電極との間に生じる電位差を、FETソースフォロワ回路の出力電圧又はドレイン電流として取得することができ、その出力電圧又はドレイン電流を塩化物イオンレベルの指標とすることができる。
また、FETをソースフォロワ回路に組み込まず単体の素子として本実施形態の塩化物イオンセンサに利用する場合には、デプレッション型と呼ばれる動作モード(すなわち、ゲート電圧0 V時にドレイン電流が線形変動領域範囲を示す動作モード)を示すFETが好ましい。これにより、印加電圧0 V前後にて電流ないし電圧の変動性を有することになるため、溶液中にてゲート電位を規定する参照電極は、電極自身や溶液中の電解質物質の酸化還元反応による電気分解を抑制することができる。
使用するFETは、塩化物イオンの測定に使用できる限り特に限定されず、任意のものを使用することができ、例えば、n型FETを使用することができる。塩化物イオン検出電極をFETのゲート端子に組み込む方法は特に限定されず、当業者に既知の方法によって行うことができる。例えば、塩化物イオン検出電極と参照電極との間に生じる電位差を、FETソースフォロワ回路の出力電圧又はドレイン電流として取得することができ、その出力電圧又はドレイン電流を塩化物イオンレベルの指標とすることができる。
また、FETをソースフォロワ回路に組み込まず単体の素子として本実施形態の塩化物イオンセンサに利用する場合には、デプレッション型と呼ばれる動作モード(すなわち、ゲート電圧0 V時にドレイン電流が線形変動領域範囲を示す動作モード)を示すFETが好ましい。これにより、印加電圧0 V前後にて電流ないし電圧の変動性を有することになるため、溶液中にてゲート電位を規定する参照電極は、電極自身や溶液中の電解質物質の酸化還元反応による電気分解を抑制することができる。
本実施形態の塩化物イオンセンサは、上述のFET、塩化物イオン検出電極、参照電極以外の他の構成要素を含んでよく、他の構成要素として、例えば、電圧測定器、電源、A/D変換回路、メモリを含んでもよい。これらの他の構成要素は、例えば、FETと共に、FETソースフォロワ回路を構成する1つのデバイスとして構成されていてもよい。
<塩化物イオンの測定方法>
本発明の他の実施態様は、上記塩化物イオンセンサを、測定対象溶液に接触させる工程を含む、測定対象溶液における塩化物イオンの測定方法である。
本発明の他の実施態様は、上記塩化物イオンセンサを、測定対象溶液に接触させる工程を含む、測定対象溶液における塩化物イオンの測定方法である。
測定対象溶液は、塩化物イオンを含む任意の溶液であってよい。測定対象溶液の溶媒は、任意濃度のNaBrを含む4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid(HEPES)等の電解質水溶液でもよく、または等張液でもよい。当該溶媒自体は塩化物イオンを含まないまたは実質的に含まないものであることが好ましく、例えば、塩化物イオンの濃度が100pM以下、10pM以下、1pM以下、0.1pM以下、0.01pM以下であってよい。本発明において等張液とは、体液の浸透圧とほぼ同じ浸透圧を有する液体であれば特に限定されず、例えばその浸透圧は250~320mOsm/L、260~310mOsm/L、270~300mOsm/L、280~290mOsm/Lであってよい。高感度化の観点からは、測定対象溶液の溶媒は電解質類を含まないまたは実質的に含まない液体であることが好ましく、塩化物イオンを含まないまたは実質的に含まない等張液を好適に利用できる。そのような等張液としては、例えばグルコース溶液、スクロース溶液を挙げることができる。グルコース溶液を用いる場合、グルコース濃度は塩化物イオンを高感度に検出できる限り特に限定されないが、例えば5.0~6.0%(w/v)グルコース溶液とすることができ、好ましくは5.2~5.8%(w/v)グルコース溶液、より好ましくは5.4~5.6%(w/v)グルコース溶液とすることができる。溶液のpHは特に限定されず、所望に応じて任意で調整することができる。例えば、7.0~8.0としてもよい。
測定対象溶液への接触は、例えば、塩化物イオンセンサにおける塩化物イオン検出電極を測定対象溶液に浸漬することにより行うことができる。
本実施形態の測定方法は、例えば、上記塩化物イオンセンサによって塩化物イオン検出電極と参照電極との間に生じる電位差を測定することにより、塩化物イオンを測定することができる。当該電位差は、FETソースフォロワ回路の出力電圧又はドレイン電流として取得することができ、その出力電圧又はドレイン電流を塩化物イオンレベルの指標とすることができる。
塩化物イオンレベルとは、例えば、塩化物イオンの濃度や量を表すものである。塩化物イオンを含まないまたは実質的に含まない対照溶液における出力電圧と比較したときの、測定対象溶液における出力電圧の低下が大きいほど塩化物イオンレベルが高いことを示してもよく、また、塩化物イオンを含まないまたは実質的に含まない対照溶液におけるドレイン電流と比較したときの、測定対象溶液におけるドレイン電流の低下が大きいほど塩化物イオンレベルが高いことを示してもよい。
また、例えば予め出力電圧又はドレイン電流と、塩化物イオンレベルとの間の検量線を準備してもよく、この検量線を用いることにより塩化物イオン濃度や量を算出してもよい。
また、例えば予め出力電圧又はドレイン電流と、塩化物イオンレベルとの間の検量線を準備してもよく、この検量線を用いることにより塩化物イオン濃度や量を算出してもよい。
本実施形態における塩化物イオンセンサに関する記載は、上記<塩化物イオンセンサ>の項における記載を援用できる。
<がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイス>
本発明の他の実施態様は、1又は複数個の上記塩化物イオンセンサと、圧入力センサを備える、がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスであって、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とする、デバイスである。
被検細胞に外力を負荷し、塩化物イオン検出電極に生じた電位変化を検出することによって、外力負荷により被検細胞が溶液中に排出した塩化物イオンを検出できる。
本発明の他の実施態様は、1又は複数個の上記塩化物イオンセンサと、圧入力センサを備える、がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスであって、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とする、デバイスである。
被検細胞に外力を負荷し、塩化物イオン検出電極に生じた電位変化を検出することによって、外力負荷により被検細胞が溶液中に排出した塩化物イオンを検出できる。
外力負荷手段は、細胞外から細胞膜に対して圧力を負荷する手段であればいかなる手段で行ってもよいが、機械的手段によって細胞膜を押し付ける態様が好ましい。また、細胞外から細胞膜に対して圧力を負荷することで、細胞膜を横(細胞膜と平行)方向に伸張させる力であることが好ましい。外部から細胞膜を押し付ける態様でもよいし、細胞膜を引っ張る態様でもよい。
外力の負荷は、細胞の表面積と同等~1/10程度の接触面(例えば、接触面積30~300 μm2)を持った部材を用いて行うことが好ましい。このような部材は、例えば、先端部において細胞に接触して圧力を加える細胞圧子を有する部材であってよく、先端部が平板状の部材であってもよい。細胞圧子は上記のような接触面を有するものであればその形状は制限されず、ピラミッド状(細胞膜に所望の圧力を負荷しても細胞膜を破壊しない程度の頂角を有する円錐状又は角錐状)、円柱状、角柱状、円錐台状、角錐台状、球状(略球状含む)、半球状(略半球状含む)でもよい。細胞圧子は上記のような接触面を有するものであればその素材は特に制限されず、有機ポリマー、金属が例示される。細胞圧子は上記のような接触面を有するものであればその大きさは制限されず、例えば、ピラミッド状、円柱状、角柱状、円錐台状、角錐台状の場合は、その底面における直径が5~20 μmであってよく、球状、半球状の場合は、粒径が5~20 μmであってよい。
一例として、走査型プローブ顕微鏡(SPM)、原子間力顕微鏡(AFM)で使用されるカンチレバーや、チップレスカンチレバーの先端部に上記のような細胞圧子を接着させたものが挙げられる。
一例として、走査型プローブ顕微鏡(SPM)、原子間力顕微鏡(AFM)で使用されるカンチレバーや、チップレスカンチレバーの先端部に上記のような細胞圧子を接着させたものが挙げられる。
細胞圧子の材質は特に限定されないが、例えば、シリコン(単結晶シリコン等)、窒化シリコン、金、クロム、ヒ化インジウム、シリカ、ポリエチレンテレフタレート、ポリエチレン、ポリプロピレン、ポリスチレン、ポリカーボネート、アクリル樹脂が挙げられる。
負荷される外力の強度は外力負荷により細胞膜を介して塩化物イオンの排出が観察される程度であればよく、細胞膜を横方向に伸張させることができる強度であることが好ましいが、例えば1~100 nNであり、好ましくは5~50 nNである。
外力の負荷時間は外力負荷に基づく塩化物イオンの排出が観察されるのに十分な時間であればよく、例えば1秒間~15分間、10秒間~2分間が挙げられる。
外力の負荷時間は外力負荷に基づく塩化物イオンの排出が観察されるのに十分な時間であればよく、例えば1秒間~15分間、10秒間~2分間が挙げられる。
外力測定手段は、細胞に負荷される外力を測定できる手段であればいかなる手段で行ってもよい。
例えば、外力測定手段として走査型プローブ顕微鏡(SPM)、原子間力顕微鏡(AFM)を用いる場合、SPM、AFMで用いるカンチレバーにより細胞へ外力を負荷し、SPM、AFMによりその外力を測定することができる。任意でカンチレバーに圧入力計測用ピエゾ素子を有してもよい。
また、外力測定手段としてSPM、AFMを用いない場合、例えば、圧入力計測用ピエゾ素子を有するカンチレバー型デバイスを用いることができる。カンチレバー型デバイスを用いる場合、細胞に圧入し外力を印加するためにカンチレバーを上下操作する装置(例えばスタンポユニットSU100、オリンパス)をさらに用いることができる。カンチレバーを上下操作する装置を使用するだけで、細胞に負荷する外力を測定できるため、SPM、AFM等の高価な設備を使用する必要がない点がメリットである。
例えば、外力測定手段として走査型プローブ顕微鏡(SPM)、原子間力顕微鏡(AFM)を用いる場合、SPM、AFMで用いるカンチレバーにより細胞へ外力を負荷し、SPM、AFMによりその外力を測定することができる。任意でカンチレバーに圧入力計測用ピエゾ素子を有してもよい。
また、外力測定手段としてSPM、AFMを用いない場合、例えば、圧入力計測用ピエゾ素子を有するカンチレバー型デバイスを用いることができる。カンチレバー型デバイスを用いる場合、細胞に圧入し外力を印加するためにカンチレバーを上下操作する装置(例えばスタンポユニットSU100、オリンパス)をさらに用いることができる。カンチレバーを上下操作する装置を使用するだけで、細胞に負荷する外力を測定できるため、SPM、AFM等の高価な設備を使用する必要がない点がメリットである。
上記いずれの外力測定手段を用いた場合であっても、カンチレバーの根元部に圧入力計測用ピエゾ素子を有してよく、細胞圧入時の当該ピエゾ素子の抵抗変化を測定することにより、細胞に負荷された外力を測定することができる。ピエゾ素子の抵抗変化は、例えば、当業者に既知のホイートストンブリッジ回路を用いて電圧に変換することにより測定してもよい。
上記圧入力センサは、温度補償用ピエゾ素子を有してもよい。圧入力計測用ピエゾ素子の近傍に温度補償用ピエゾ素子を配置し、これらの2つの素子の差動計測を行うことで温度変化の影響を除去することができる。
特に限定されないが圧入力センサの計測原理の一例を示す。圧入力中央にある細胞圧入カンチレバーの先端に装着した細胞圧子で細胞を圧入し、その際にカンチレバー根元部に生じる歪を圧入力計測用ピエゾ素子で抵抗変化として計測する原理である。またピエゾ抵抗素子は溶液の温度変化の影響を受ける。そのため、圧入力計測用ピエゾ素子の近傍に温度補償用ピエゾ素子を配置し、これらの2つの素子の差動計測を行うことで温度変化の影響を除去可能である。
塩化物イオンセンサとしての塩化物イオンの検出に用いられる上記化合物を表面に修飾された電極は、当該デバイスにおけるカンチレバー等の外力負荷手段の近傍に配置されるが、外力負荷手段とは異なる構造上に存在してもよいし、または、カンチレバー等の外力負荷手段がさらに塩化物イオン検出電極としての機能を有するものであってもよく、すなわちカンチレバーの先端部が上記化合物を表面に修飾された電極であってもよい。外力負荷手段が塩化物イオン検出電極としての機能を有するものである場合、外力負荷手段における細胞と接触する部分と上記化合物が表面に修飾された部分とは分離されていることが好ましい。これにより、塩化物イオンセンサが細胞表面の負電荷による影響を受けることなく、塩化物イオンの測定を行うことができる。
塩化物イオン検出電極と、外力負荷手段の外力負荷部、例えば細胞圧子の中心との距離は、細胞が排出した塩化物イオンを検出できる限り特に限定されないが、例えば100μm以下、90μm以下、80μm以下、70μm以下、60μm以下、50μm以下である。下限は特に限定されないが、例えば20μm以上、30μm以上、40μm以上である。この距離が近いほど被検細胞が排出する塩化物イオンの検出感度を高めることができる。
上記デバイス1個あたりに、塩化物イオンセンサは1個備えてもよく、複数個備えてもよく、複数個備える場合は、例えば2個、3個、4個又はそれ以上の個数備えることができる。塩化物イオンセンサを複数個備えることにより、外力が負荷された細胞が排出する塩化物イオンを効率的に検出することができる。塩化物イオンセンサを複数個備えるものであるとき、塩化物イオンセンサにおける塩化物イオン検出電極は、細胞に外力を加える部位を取り囲むように配置されるものであることが好ましい。
塩化物イオンセンサは細胞圧入時に細胞から放出される塩化物イオンを細胞圧子近傍に配置された塩化物イオン検出電極で検出する。特に限定されないが、MEMS加工技術により細胞圧子の中心から検出電極までの距離を100μm以下にすることによりイオンが溶液中に拡散する前に高感度に検出することが可能になる。
本実施形態に係るデバイスにおける塩化物イオンセンサに関する記載は、上記<塩化物イオンセンサ>の項における記載を援用できる。
<がん細胞を検出するための及び/又はがん細胞の悪性度を評価するための方法>
本発明の他の実施態様は、被検細胞に外力を負荷する工程、及び上記塩化物イオンの測定方法により塩化物イオンを測定する工程を含む、がん細胞を検出するための及び/又はがん細胞の悪性度を評価するための方法である。
本発明の他の実施態様は、被検細胞に外力を負荷する工程、及び上記塩化物イオンの測定方法により塩化物イオンを測定する工程を含む、がん細胞を検出するための及び/又はがん細胞の悪性度を評価するための方法である。
本実施形態の方法によれば、がん細胞の検出やがん細胞の悪性度を評価することができる。その評価結果に基づき、医師はがん治療の方針を決定することができる。例えば、がん細胞を有すると診断されたり、がん細胞の悪性度が高いと判定されたりする場合には、がん切除手術等の適切な処理を行うことができる。このように当該方法は、医師等による医療行為を含むものではなく、医師によるがんの診断を補助するためのデータを提供することができる。
被検細胞に外力を負荷し、塩化物イオン検出電極に生じた電位変化を検出することによって、外力負荷により被検細胞が測定対象溶液中に排出した塩化物イオンを検出できる。そしてその塩化物イオンのレベルによって、がん細胞の検出及び/又はがん細胞の悪性度評価を行うことができる。
例えば、被検細胞に外力を負荷したことにより、塩化物イオン検出電極と参照電極との間に生じる電位差を、FETソースフォロワ回路の出力電圧又はドレイン電流として取得することができ、その出力電圧又はドレイン電流を、被検細胞が測定対象溶液中に排出した塩化物イオンレベルの指標とすることができる。塩化物イオンレベルとは、例えば、塩化物イオンの濃度や量を表すものである。塩化物イオンを含まないまたは実質的に含まない対照溶液における出力電圧と比較したときの、測定対象溶液における出力電圧の低下が大きいほど塩化物イオンレベルが高いことを示してもよく、また、塩化物イオンを含まないまたは実質的に含まない対照溶液におけるドレイン電流と比較したときの、測定対象溶液におけるドレイン電流の低下が大きいほど塩化物イオンレベルが高いことを示してもよい。
また、例えば予め出力電圧又はドレイン電流と、塩化物イオンレベルとの間の検量線を準備してもよく、この検量線を用いることにより塩化物イオン濃度や量を算出してもよい。
例えば、被検細胞に外力を負荷したことにより、塩化物イオン検出電極と参照電極との間に生じる電位差を、FETソースフォロワ回路の出力電圧又はドレイン電流として取得することができ、その出力電圧又はドレイン電流を、被検細胞が測定対象溶液中に排出した塩化物イオンレベルの指標とすることができる。塩化物イオンレベルとは、例えば、塩化物イオンの濃度や量を表すものである。塩化物イオンを含まないまたは実質的に含まない対照溶液における出力電圧と比較したときの、測定対象溶液における出力電圧の低下が大きいほど塩化物イオンレベルが高いことを示してもよく、また、塩化物イオンを含まないまたは実質的に含まない対照溶液におけるドレイン電流と比較したときの、測定対象溶液におけるドレイン電流の低下が大きいほど塩化物イオンレベルが高いことを示してもよい。
また、例えば予め出力電圧又はドレイン電流と、塩化物イオンレベルとの間の検量線を準備してもよく、この検量線を用いることにより塩化物イオン濃度や量を算出してもよい。
解析対象のがん細胞については、哺乳動物由来のがん細胞であればよく、例えば、ヒト、マウス、ラットのがん細胞が挙げられるが、ヒトのがん細胞であることが好ましい。がん細胞は株化された培養細胞でもよいし、生体から単離されたがん細胞でもよい。また、がん組織をそのまま解析に使用してもよい。がんの種類は特に制限されず、例えば、乳がん、胃がん、肺がん、すい臓がん、肝がん、大腸がん、前立腺がん、子宮頸がんが挙げられる。
例えば、上記デバイスにおいて、被検細胞に外力を負荷したことにより排出される塩化物イオンレベルが、対照である正常細胞に外力を負荷したことにより排出される塩化物イオンレベルと比較して高いとき、当該被検細胞ががん細胞であると評価することができる。
例えば、FETの制御電圧としてドレイン電圧5 V、ゲート電圧0 Vを入力したときのドレイン電流の変化を塩化物イオンレベルの指標とする場合、塩化物イオンを含まないまたは実質的に含まない対照溶液(例えば、外力を負荷した正常細胞を含む溶液)におけるドレイン電流が0 μAであるとき、外力を負荷した被検細胞を含む測定対象溶液におけるドレイン電流の低下が、例えば50 μA以上、100 μA以上、150 μA以上、200 μA以上であるとき、当該被検細胞ががん細胞であると評価することができる。
また、塩化物イオンレベルだけでなく、他の指標と組み合わせて当該被検細胞ががん細胞であると評価することもできる。
例えば、FETの制御電圧としてドレイン電圧5 V、ゲート電圧0 Vを入力したときのドレイン電流の変化を塩化物イオンレベルの指標とする場合、塩化物イオンを含まないまたは実質的に含まない対照溶液(例えば、外力を負荷した正常細胞を含む溶液)におけるドレイン電流が0 μAであるとき、外力を負荷した被検細胞を含む測定対象溶液におけるドレイン電流の低下が、例えば50 μA以上、100 μA以上、150 μA以上、200 μA以上であるとき、当該被検細胞ががん細胞であると評価することができる。
また、塩化物イオンレベルだけでなく、他の指標と組み合わせて当該被検細胞ががん細胞であると評価することもできる。
また、例えば、上記デバイスにおいて、被検細胞に外力を負荷したことにより排出される塩化物イオンレベルが、浸潤能が低いがん細胞に外力を負荷したことにより排出される塩化物イオンレベルと比較して高いとき、当該被検細胞の悪性度が高いと評価することができる。ここで、がんの悪性度とは浸潤性及び転移能等を総合的に示す指標であり、浸潤性又は転移能が高いとき、がんの悪性度が高いと評価することができる。
例えば、FETの制御電圧としてドレイン電圧5 V、ゲート電圧0 Vを入力したときのドレイン電流の変化を塩化物イオンレベルの指標とする場合、塩化物イオンを含まないまたは実質的に含まない対照溶液(例えば、外力を負荷した正常細胞を含む溶液)におけるドレイン電流が0 μAであるとき、外力を負荷した被検細胞を含む測定対象溶液におけるドレイン電流の低下が、例えば、100 μA以上、200 μA以上、300 μA以上、400 μA以上、500 μA以上、600 μA以上、700 μA以上、800 μA以上であり、且つ、外力を負荷した浸潤能が低いがん細胞を含む溶液におけるドレイン電流の低下よりも大きいとき、当該被検細胞は悪性度が高いと評価することができる。
また、塩化物イオンレベルだけでなく、他の指標と組み合わせて当該被検細胞の悪性度が高いと評価することもできる。
例えば、FETの制御電圧としてドレイン電圧5 V、ゲート電圧0 Vを入力したときのドレイン電流の変化を塩化物イオンレベルの指標とする場合、塩化物イオンを含まないまたは実質的に含まない対照溶液(例えば、外力を負荷した正常細胞を含む溶液)におけるドレイン電流が0 μAであるとき、外力を負荷した被検細胞を含む測定対象溶液におけるドレイン電流の低下が、例えば、100 μA以上、200 μA以上、300 μA以上、400 μA以上、500 μA以上、600 μA以上、700 μA以上、800 μA以上であり、且つ、外力を負荷した浸潤能が低いがん細胞を含む溶液におけるドレイン電流の低下よりも大きいとき、当該被検細胞は悪性度が高いと評価することができる。
また、塩化物イオンレベルだけでなく、他の指標と組み合わせて当該被検細胞の悪性度が高いと評価することもできる。
本実施形態の各工程における記載は、上記<塩化物イオンセンサ>、<がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイス>、又は<塩化物イオンの測定方法>の項における記載を援用できる。
<塩化物イオンチャネル阻害剤のスクリーニング方法>
本発明の他の実施形態は、1又は複数個の上記塩化物イオンセンサと、圧入力センサを備えるデバイスを用いた、塩化物イオンチャネル阻害剤のスクリーニング方法であって、
前記デバイスは、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とするデバイスであり、
被験物質を細胞に投与する工程;
前記細胞に外力を負荷しつつ外力を測定し、且つ前記細胞から排出される塩化物イオンを測定する工程;及び
前記塩化物イオンのレベルを指標として、前記被験物質が塩化物イオンチャネル阻害剤の候補物質としてスクリーニングする工程を含む、方法である。
本発明の他の実施形態は、1又は複数個の上記塩化物イオンセンサと、圧入力センサを備えるデバイスを用いた、塩化物イオンチャネル阻害剤のスクリーニング方法であって、
前記デバイスは、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とするデバイスであり、
被験物質を細胞に投与する工程;
前記細胞に外力を負荷しつつ外力を測定し、且つ前記細胞から排出される塩化物イオンを測定する工程;及び
前記塩化物イオンのレベルを指標として、前記被験物質が塩化物イオンチャネル阻害剤の候補物質としてスクリーニングする工程を含む、方法である。
前記スクリーニングする工程は、以下(1)~(3)の何れかの場合に、前記被験物質が塩化物イオンチャネル阻害剤の候補物質としてスクリーニングする工程であってよい。
(1)外力負荷により前記被験物質を投与した細胞が排出した塩化物イオンのレベルが、前記被験物質を投与していない細胞を用いて同様に測定した塩化物イオンのレベルと比較して低い;
(2)外力負荷により前記被験物質を投与した細胞が排出した塩化物イオンのレベルが、低浸潤性がん細胞または正常細胞を用いて同様に測定した塩化物イオンのレベルと比較して同等又は低い;
(3)外力負荷により前記被験物質を投与した細胞が排出した塩化物イオンのレベルが、あらかじめ定められたカットオフ値よりも低い。
(1)外力負荷により前記被験物質を投与した細胞が排出した塩化物イオンのレベルが、前記被験物質を投与していない細胞を用いて同様に測定した塩化物イオンのレベルと比較して低い;
(2)外力負荷により前記被験物質を投与した細胞が排出した塩化物イオンのレベルが、低浸潤性がん細胞または正常細胞を用いて同様に測定した塩化物イオンのレベルと比較して同等又は低い;
(3)外力負荷により前記被験物質を投与した細胞が排出した塩化物イオンのレベルが、あらかじめ定められたカットオフ値よりも低い。
スクリーニング方法は、特に限定されないが、追加の工程を任意で含んでもよい。例えば、事前に細胞を調整する工程や、スクリーニングした候補物質を塩化物イオンチャネル阻害剤として同定する工程等を含んでもよい。
被験物質は、特に限定されないが、例えば、化合物、抗体、抗原結合フラグメント、ペプチド、核酸等が挙げられる。
被験物質の細胞への投与量や被験物質の細胞との反応時間は、特に限定されず、被験物質の種類に応じて適宜調整することができる。
細胞は、特に限定されないが、がん細胞であることが好ましく、高浸潤性がん細胞であることがより好ましい。例えば、細胞として高浸潤性ヒト乳がん細胞を用いてもよく、このとき、上記(2)における低浸潤性がん細胞または正常細胞としては、それぞれ低浸潤性ヒト乳がん細胞、ヒト乳腺上皮細胞を用いてもよい。
本実施形態に用いる細胞に発現する塩化物イオンチャネルは、当該細胞を本実施形態のスクリーニング方法に用いることができる限り特に限定されないが、例えば、ClC塩化物イオンチャネル(ClC-2、ClC-3、ClC-4、ClC-6、ClC-7等)、カルシウム依存性塩化物イオンチャネル(TMEM16A、TMEM16B、Best1、Best2等)、容積感受性外向整流性アニオンチャネル(CLIC1、LRRC8A等)が挙げられる。本実施形態のスクリーニング方法は、細胞に外力を負荷することにより排出される塩化物イオンを測定することから、細胞に発現する塩化物イオンチャネルは、細胞に外力を負荷することにより塩化物イオンを排出するチャネルであることが好ましく、細胞の膨張を感知するチャネルであるCLIC1、LRRC8A等の容積感受性外向整流性アニオンチャネルがより好ましく、CLIC1が特に好ましい。
本実施形態の塩化物イオンセンサ、圧入力センサ、デバイス等に関する記載は、上記<塩化物イオンセンサ>、<がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイス>、又は<塩化物イオンの測定方法>の項における記載を援用できる。
以下に実施例を用いて本発明を説明するが、本発明はこれら実施例に限定されるものではない。
<実施例1 イオンセンサ作製>
5-ethynyl-1H-indole(5-EnIND, Asta Tech, Inc., Product Code: 94615, CAS: 889108-48-9)により検出電極の表面修飾を行った。はじめに、5-EnINDをジメチルスルホキシド(DMSO)に溶解させ、10 mMの5-EnIND溶液を調製した。続いて、検出電極となる金薄膜表面に対し、酸素プラズマ照射処理を行ったのちに、2-プロパノールで洗浄し、さらに蒸留水で洗浄し、窒素ガスによって乾燥させた。金薄膜基板を5-EnIND溶液に浸漬ないし同基板上に当該溶液を滴下し、60℃のホットプレート上にて遮光状態にて6時間保持した。これにより、金-アルキン錯形成反応を介した共有結合による5-EnINDの単分子膜としての固定化を図った。その後、25℃にて12時間静置したのちに、2-プロパノールで洗浄し、さらに蒸留水で洗浄することによって表面に付着した5-EnIND溶液を十分に洗浄し、窒素ガスによって乾燥させた。
5-ethynyl-1H-indole(5-EnIND, Asta Tech, Inc., Product Code: 94615, CAS: 889108-48-9)により検出電極の表面修飾を行った。はじめに、5-EnINDをジメチルスルホキシド(DMSO)に溶解させ、10 mMの5-EnIND溶液を調製した。続いて、検出電極となる金薄膜表面に対し、酸素プラズマ照射処理を行ったのちに、2-プロパノールで洗浄し、さらに蒸留水で洗浄し、窒素ガスによって乾燥させた。金薄膜基板を5-EnIND溶液に浸漬ないし同基板上に当該溶液を滴下し、60℃のホットプレート上にて遮光状態にて6時間保持した。これにより、金-アルキン錯形成反応を介した共有結合による5-EnINDの単分子膜としての固定化を図った。その後、25℃にて12時間静置したのちに、2-プロパノールで洗浄し、さらに蒸留水で洗浄することによって表面に付着した5-EnIND溶液を十分に洗浄し、窒素ガスによって乾燥させた。
<実施例2 FETへの検出電極の組み込みと滴定実験>
5-EnINDによって修飾された金電極(以下、5-EnIND修飾電極)は、FETの浮遊ゲート端子に組み込むことでFETを介したポテンショメトリック測定系を構築した(図1)。滴定実験による5-EnIND修飾電極の塩化物イオン認識能の検討にあたっては、FETソースフォロワ回路(BioCMOS社製,BCT-2)の浮遊ゲート端子に当該電極を組み込むことで測定を行った。なお、5-EnIND修飾電極と対となる制御ゲート端子には、3 M NaCl水溶液を内部溶液とした銀/塩化銀参照電極(BAS社製)を用いることで、電解質水溶液中におけるゲートの基準電位とした。続いて、緩衝剤として10 mMの4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid(HEPES)および電解質として100 mMのNaBrを含むpH 7.4の水溶液を調製し、当該水溶液に任意濃度のNaClを適宜添加することで標準溶液とした。
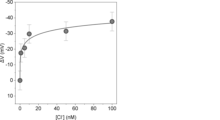
各濃度の塩化物イオン水溶液を電極上に導入し、参照電極と5-EnIND修飾電極間の電位差をFETソースフォロワ回路の出力電圧として取得した。この際、NaCl濃度(すなわち、塩化物イオン濃度)が0 nMにおける出力電位値を基準とし、各濃度において得られた出力電圧値の差分(ΔV)をとることで濃度依存性を確認した。その結果、塩化物イオン濃度の増加に伴って出力電圧の低下が認められ、10 nM以下の濃度範囲において直線的な電位応答が得られた(図2)。5-EnIND中のピロール環部位(NH部位)が水素結合を介して塩化物イオンを捕捉し、その際に起こる5-EnIND中の電子密度の変化が電極電位を変化させたことで、当該変化が生じたと考えられる。
一般に、水素結合性の分子認識は水分子の夾雑による阻害される。これを避けるために、非プロトン性有機溶剤(例えば、DMSO)を添加することが多い。しかしながら、上記のように非プロトン性有機溶媒を含まない溶液中でイオン選択的な電位応答が得られた。その要因として、例えば、(1)固液界面において単分子膜状に5-EnINDが密集されたことで水素結合ドナーの集積効果が発現したこと、(2)インドールの有する疎水性により固液界面近傍への水分子の近接が阻害されたことが考えられる。また、当該変化は夾雑イオンである臭化物イオンの過剰量存在下において得られたことから、5-EnIND修飾電極は塩化物イオン選択性を有することが示唆された。
5-EnINDによって修飾された金電極(以下、5-EnIND修飾電極)は、FETの浮遊ゲート端子に組み込むことでFETを介したポテンショメトリック測定系を構築した(図1)。滴定実験による5-EnIND修飾電極の塩化物イオン認識能の検討にあたっては、FETソースフォロワ回路(BioCMOS社製,BCT-2)の浮遊ゲート端子に当該電極を組み込むことで測定を行った。なお、5-EnIND修飾電極と対となる制御ゲート端子には、3 M NaCl水溶液を内部溶液とした銀/塩化銀参照電極(BAS社製)を用いることで、電解質水溶液中におけるゲートの基準電位とした。続いて、緩衝剤として10 mMの4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid(HEPES)および電解質として100 mMのNaBrを含むpH 7.4の水溶液を調製し、当該水溶液に任意濃度のNaClを適宜添加することで標準溶液とした。
各濃度の塩化物イオン水溶液を電極上に導入し、参照電極と5-EnIND修飾電極間の電位差をFETソースフォロワ回路の出力電圧として取得した。この際、NaCl濃度(すなわち、塩化物イオン濃度)が0 nMにおける出力電位値を基準とし、各濃度において得られた出力電圧値の差分(ΔV)をとることで濃度依存性を確認した。その結果、塩化物イオン濃度の増加に伴って出力電圧の低下が認められ、10 nM以下の濃度範囲において直線的な電位応答が得られた(図2)。5-EnIND中のピロール環部位(NH部位)が水素結合を介して塩化物イオンを捕捉し、その際に起こる5-EnIND中の電子密度の変化が電極電位を変化させたことで、当該変化が生じたと考えられる。
一般に、水素結合性の分子認識は水分子の夾雑による阻害される。これを避けるために、非プロトン性有機溶剤(例えば、DMSO)を添加することが多い。しかしながら、上記のように非プロトン性有機溶媒を含まない溶液中でイオン選択的な電位応答が得られた。その要因として、例えば、(1)固液界面において単分子膜状に5-EnINDが密集されたことで水素結合ドナーの集積効果が発現したこと、(2)インドールの有する疎水性により固液界面近傍への水分子の近接が阻害されたことが考えられる。また、当該変化は夾雑イオンである臭化物イオンの過剰量存在下において得られたことから、5-EnIND修飾電極は塩化物イオン選択性を有することが示唆された。
5-EnINDの構造異性体として4-ethynyl-1H-indole (4-EnIND)があるが、EnINDにおける4位と5位のいずれの位置に存在するR2を介して電極と結合することが好ましいかを調べた。まず、4-EnINDを用いて、5-EnINDの場合と同様に電極を調製した。調製した電極を用いて、塩化物イオン濃度変化に対するFETソースフォロワ回路の電位応答性を確認したところ、4-EnINDを用いた場合は、電位変化はほとんど確認できなかった(図3)。イオン捕捉を担う水素結合ドナーとして5-EnINDと同じピロール環部位(NH部位)を擁するにも関わらず、このような電位応答性の違いが生じた理由として、それぞれの単分子膜としての形成状態の違いに起因すると考えられる。金電極と結合するアルキン部位が5位に付加された5-EnINDは、4位に付加された4-EnINDと比べて単分子膜形成に際して立体障害的に有利であると考えられる。このため、4-EnINDを適用した場合と比較して、5-EnINDを適用した際は単分子膜中のEnINDがより高密度であると想定される。前述の通り、水溶液中での塩化物イオンの認識が達成される要因として、EnINDの集積効果や疎水場の形成が挙げられることから、4-EnIND修飾電極上では塩化物イオンに対する結合親和性が低下したものと推察される。
細胞排出イオンの検知には更なる高感度化が必要となる。そこで、細胞評価時に用いる電解質類を含まない5.5%グルコース水溶液中における塩化物イオン濃度の変化を同様に測定した。この際、銀/塩化銀参照電極の電位安定効果は得られないことから、未修飾の金電極を5-EnIND修飾電極と対となる制御ゲート端子として用いた。その結果、HEPES-NaBr緩衝水溶液中よりも更なる低濃度領域での電位応答が確認できた(図4)。より低濃度での応答が増強した理由として、例えば、塩化物イオン認識を阻害する夾雑アニオンが存在しないこと、デバイ遮蔽効果の影響が小さいため5-EnIND単分子膜のイオン捕捉に伴う電子密度の変化がより強く電極電位の変化を誘発したことが考えられる。
<実施例3 MEMSカンチレバー型デバイスの構造>
図5に作製したMEMS(Micro Electro Mechanical Systems)カンチレバー型デバイスの模式図を示す。当該デバイスは、圧入力センサと塩化物イオン(Cl-)センサを兼備するデバイスである。実施例3において用いられるカンチレバー型デバイスは、圧入力センサの近傍に2つの塩化物イオンセンサを有するデバイスであり、具体的には、塩化物イオン検出電極と細胞圧子の中心との距離を60 μmとした。
塩化物イオン検出電極は、インクジェット装置によって、その素材となる電極に5-EnIND溶液を選択的に滴下し、60℃のホットチャンバー内にて6時間保持することで検出電極を形成した。その後、当該カンチレバーを2-プロパノールで洗浄し、さらに蒸留水で洗浄することによって未結合の5-EnINDを十分に洗浄し、塩化物イオン検出に用いた。また、MEMSの根元付近に未処理の金電極を配置し、当該金電極を制御ゲート端子として用いることで塩化物イオン測定における基準電位とした。測定に際し、MEMSの塩化物イオン検出電極はフレキシブル配線基板を介して、市販のn型FET(東芝セミコンダクタ製 2SK241Y)のゲート端子に接続した。また、FETのソース・ドレイン端子およびMEMSの制御ゲート端子は、ソースメータ(Keithley Instruments製2636B)にそれぞれ接続することで、入出力制御を行った。
図5に作製したMEMS(Micro Electro Mechanical Systems)カンチレバー型デバイスの模式図を示す。当該デバイスは、圧入力センサと塩化物イオン(Cl-)センサを兼備するデバイスである。実施例3において用いられるカンチレバー型デバイスは、圧入力センサの近傍に2つの塩化物イオンセンサを有するデバイスであり、具体的には、塩化物イオン検出電極と細胞圧子の中心との距離を60 μmとした。
塩化物イオン検出電極は、インクジェット装置によって、その素材となる電極に5-EnIND溶液を選択的に滴下し、60℃のホットチャンバー内にて6時間保持することで検出電極を形成した。その後、当該カンチレバーを2-プロパノールで洗浄し、さらに蒸留水で洗浄することによって未結合の5-EnINDを十分に洗浄し、塩化物イオン検出に用いた。また、MEMSの根元付近に未処理の金電極を配置し、当該金電極を制御ゲート端子として用いることで塩化物イオン測定における基準電位とした。測定に際し、MEMSの塩化物イオン検出電極はフレキシブル配線基板を介して、市販のn型FET(東芝セミコンダクタ製 2SK241Y)のゲート端子に接続した。また、FETのソース・ドレイン端子およびMEMSの制御ゲート端子は、ソースメータ(Keithley Instruments製2636B)にそれぞれ接続することで、入出力制御を行った。
<実施例4 原子間力顕微鏡を用いたMEMSカンチレバー型デバイスのキャリブレーション>
MEMSカンチレバー型デバイスをディッシュ上に固定し、5.5%グルコース溶液に浸漬した状態でAFMを用いた外力印加を行った。先端形状がピラミッド型の探針を用いてカンチレバーにかかる力が5, 10, 30, 50 nNに達するまでカンチレバーを下降させることで、外力印加を行った。この外力が印加されたときのカンチレバー型デバイスの圧入力センサの応答を測定し、検量線を作成した(図6)。この検量線に基づいて、実際に細胞を圧入時の圧入力計測を行った。
MEMSカンチレバー型デバイスをディッシュ上に固定し、5.5%グルコース溶液に浸漬した状態でAFMを用いた外力印加を行った。先端形状がピラミッド型の探針を用いてカンチレバーにかかる力が5, 10, 30, 50 nNに達するまでカンチレバーを下降させることで、外力印加を行った。この外力が印加されたときのカンチレバー型デバイスの圧入力センサの応答を測定し、検量線を作成した(図6)。この検量線に基づいて、実際に細胞を圧入時の圧入力計測を行った。
<実施例5 低浸透圧刺激印加時における細胞排出イオンの測定>
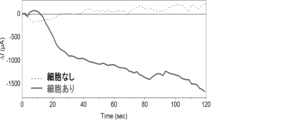
高浸潤性ヒト乳がん細胞MDA-MB-231(ATCC, Product Code: HTB-26)を5×104細胞播種し、CO2インキュベーターで一晩培養した。測定の直前に細胞の培地を5.5%グルコース溶液に置換し、FETセンサをディッシュ上の細胞近傍に接近させた後、溶液を160 mOsmの低張リン酸緩衝液に置換することで塩化物イオンの排出を誘導した。この時FETセンサによる測定を行ったところ、リン酸緩衝液置換直後の約15秒後からセンサの応答が確認された(図7)。なお、本測定では、継時変化における測定信号の安定化を図るため、FETの制御電圧としてドレイン電圧5 V、ゲート電圧0 Vを入力し、ドレイン電流の変化をイオン捕捉に伴う信号として測定した。
一方で、細胞が播種されていないディッシュを用いて同様にグルコース溶液からリン酸緩衝液に置換した場合の測定を行った結果、FETセンサの応答は確認されなかったことから、このセンサを用いて細胞群から排出された塩化物イオンを測定可能であることが示唆された。
高浸潤性ヒト乳がん細胞MDA-MB-231(ATCC, Product Code: HTB-26)を5×104細胞播種し、CO2インキュベーターで一晩培養した。測定の直前に細胞の培地を5.5%グルコース溶液に置換し、FETセンサをディッシュ上の細胞近傍に接近させた後、溶液を160 mOsmの低張リン酸緩衝液に置換することで塩化物イオンの排出を誘導した。この時FETセンサによる測定を行ったところ、リン酸緩衝液置換直後の約15秒後からセンサの応答が確認された(図7)。なお、本測定では、継時変化における測定信号の安定化を図るため、FETの制御電圧としてドレイン電圧5 V、ゲート電圧0 Vを入力し、ドレイン電流の変化をイオン捕捉に伴う信号として測定した。
一方で、細胞が播種されていないディッシュを用いて同様にグルコース溶液からリン酸緩衝液に置換した場合の測定を行った結果、FETセンサの応答は確認されなかったことから、このセンサを用いて細胞群から排出された塩化物イオンを測定可能であることが示唆された。
<実施例6 圧入力計測結果>
図8Aに圧入力センサを用いた実験系の模式図を示し、図8Bにヒト乳がん細胞圧入時の圧入力計測結果を示す。縦軸の圧入力は図6の検量線に基づいて算出された値である。細胞に細胞圧子が接触させることにより圧入力を検出した。細胞に細胞圧子を接触させた状態でカンチレバーを保持することで、一定時間細胞を圧入した。その後除荷することにより圧入力が初期値に戻っていることが確認できた。圧入直後の最大値を圧入力として取得した。
図8Aに圧入力センサを用いた実験系の模式図を示し、図8Bにヒト乳がん細胞圧入時の圧入力計測結果を示す。縦軸の圧入力は図6の検量線に基づいて算出された値である。細胞に細胞圧子が接触させることにより圧入力を検出した。細胞に細胞圧子を接触させた状態でカンチレバーを保持することで、一定時間細胞を圧入した。その後除荷することにより圧入力が初期値に戻っていることが確認できた。圧入直後の最大値を圧入力として取得した。
<実施例7 外力印加時における細胞排出イオンの測定>
高浸潤性ヒト乳がん細胞MDA-MB-231、低浸潤性ヒト乳がん細胞MCF-7(JCRB細胞バンク, Product Code: JCRB0134)、ヒト乳腺上皮細胞MCF10A(ATCC, Product Code: CRL-10317)をそれぞれ5×104細胞播種し、CO2インキュベーターで一晩培養した。測定の直前に細胞の培地を5.5%グルコース溶液に置換し、FETセンサ融合カンチレバー型デバイスをディッシュ上の単一細胞上に接近させ、カンチレバーを下降させることで、細胞を圧入した。その結果、正常細胞であるヒト乳腺上皮細胞ではFETセンサの応答が観察されなかったのに対し、二種類のがん細胞ではどちらも圧入後にセンサ応答が確認されたことから、本デバイスで単一細胞が排出する塩化物イオンを検出可能であることが示された(図9)。さらに、がん細胞の浸潤性の高低に応じた信号変化が得られたことから、塩化物イオン排出能に基づいたがん細胞の浸潤性評価が可能であると考えられた。
高浸潤性ヒト乳がん細胞MDA-MB-231、低浸潤性ヒト乳がん細胞MCF-7(JCRB細胞バンク, Product Code: JCRB0134)、ヒト乳腺上皮細胞MCF10A(ATCC, Product Code: CRL-10317)をそれぞれ5×104細胞播種し、CO2インキュベーターで一晩培養した。測定の直前に細胞の培地を5.5%グルコース溶液に置換し、FETセンサ融合カンチレバー型デバイスをディッシュ上の単一細胞上に接近させ、カンチレバーを下降させることで、細胞を圧入した。その結果、正常細胞であるヒト乳腺上皮細胞ではFETセンサの応答が観察されなかったのに対し、二種類のがん細胞ではどちらも圧入後にセンサ応答が確認されたことから、本デバイスで単一細胞が排出する塩化物イオンを検出可能であることが示された(図9)。さらに、がん細胞の浸潤性の高低に応じた信号変化が得られたことから、塩化物イオン排出能に基づいたがん細胞の浸潤性評価が可能であると考えられた。
<実施例8 塩化物イオンチャネル阻害剤添加細胞のイオン排出能評価>
高浸潤性ヒト乳がん細胞MDA-MB-231、低浸潤性ヒト乳がん細胞MCF-7、ヒト乳腺上皮細胞MCF10Aをそれぞれ5×104細胞播種し、CO2インキュベーターで一晩培養した。MDA-MB-231細胞に対して、塩化物イオンチャネル阻害剤のIAA-94(終濃度100 μM; Sigma Aldrich, Product Code: I117, CAS: 54197-31-8)を培地に添加し、CO2インキュベーターで1時間反応させた。測定の直前に細胞の培地を5.5%グルコース溶液に置換し、FETセンサ融合カンチレバー型デバイスをディッシュ上の単一細胞上に接近させ、カンチレバーを下降させることで、細胞を圧入した。圧入から30秒後のドレイン電流値を計測した結果、無処理のMDA-MB-231細胞ではFETセンサの応答が確認され塩化物イオンが排出されている一方、IAA-94添加細胞ではセンサ応答が観察されなかった(図10)。以上のように、本デバイスを用いることで機械刺激を受容する塩化物イオンチャネルの阻害剤の効果を評価可能であることが示された。本デバイスはがん細胞の浸潤に寄与する塩化物イオンチャネルの阻害剤スクリーニングに利用できると考えられる。
高浸潤性ヒト乳がん細胞MDA-MB-231、低浸潤性ヒト乳がん細胞MCF-7、ヒト乳腺上皮細胞MCF10Aをそれぞれ5×104細胞播種し、CO2インキュベーターで一晩培養した。MDA-MB-231細胞に対して、塩化物イオンチャネル阻害剤のIAA-94(終濃度100 μM; Sigma Aldrich, Product Code: I117, CAS: 54197-31-8)を培地に添加し、CO2インキュベーターで1時間反応させた。測定の直前に細胞の培地を5.5%グルコース溶液に置換し、FETセンサ融合カンチレバー型デバイスをディッシュ上の単一細胞上に接近させ、カンチレバーを下降させることで、細胞を圧入した。圧入から30秒後のドレイン電流値を計測した結果、無処理のMDA-MB-231細胞ではFETセンサの応答が確認され塩化物イオンが排出されている一方、IAA-94添加細胞ではセンサ応答が観察されなかった(図10)。以上のように、本デバイスを用いることで機械刺激を受容する塩化物イオンチャネルの阻害剤の効果を評価可能であることが示された。本デバイスはがん細胞の浸潤に寄与する塩化物イオンチャネルの阻害剤スクリーニングに利用できると考えられる。
1 電極
2 レセプタ
3 標的
4 FET
5 電源・測定器
6 参照電極
7 Cl-検出電極
8 細胞圧子
9 細胞圧入カンチレバー
10 圧入力計測用ピエゾ素子
11 温度補償用ピエゾ素子
12 細胞圧入用カンチレバー型デバイス
13 細胞
14 治具
15 計測器
2 レセプタ
3 標的
4 FET
5 電源・測定器
6 参照電極
7 Cl-検出電極
8 細胞圧子
9 細胞圧入カンチレバー
10 圧入力計測用ピエゾ素子
11 温度補償用ピエゾ素子
12 細胞圧入用カンチレバー型デバイス
13 細胞
14 治具
15 計測器
Claims (16)
- R1がHであり、及び/又はR2がC≡C-である、請求項1に記載の塩化物イオンセンサ。
- 前記化合物が、5-Ethynyl-1H-indoleである、請求項1に記載の塩化物イオンセンサ。
- 前記電極が金電極である、請求項1に記載の塩化物イオンセンサ。
- さらに参照電極を有する、請求項1に記載の塩化物イオンセンサ。
- さらに電界効果トランジスタ(FET)を有する、請求項1に記載の塩化物イオンセンサ。
- 1又は複数個の請求項1~6の何れか一項に記載の塩化物イオンセンサと、圧入力センサを備える、がん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイスであって、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンレベルを測定することを特徴とする、デバイス。
- 前記圧入力センサがカンチレバーである、請求項7に記載のデバイス。
- 前記カンチレバーが、先端部に細胞圧子を有する、請求項8に記載のデバイス。
- 前記カンチレバーが、根元部に圧入力計測用ピエゾ素子を有する、請求項8に記載のデバイス。
- 前記圧入力センサが、温度補償用ピエゾ素子を有する、請求項7に記載のデバイス。
- 前記塩化物イオン検出電極と、前記外力負荷手段における外力負荷部の中心との距離が、100 μm以下である、請求項7に記載のデバイス。
- 請求項1~6の何れか一項に記載の塩化物イオンセンサを、測定対象溶液に接触させる工程を含む、測定対象溶液における塩化物イオンの測定方法。
- 前記測定対象溶液の溶媒が、塩化物イオンの濃度が100 pM以下の等張液である、請求項13に記載の方法。
- 被検細胞に外力を負荷する工程、及び被検細胞が排出する塩化物イオンを請求項13に記載される方法により測定する工程を含む、がん細胞を検出するための及び/又はがん細胞の悪性度を評価するための方法。
- 1又は複数個の請求項1~6の何れか一項に記載の塩化物イオンセンサと、圧入力センサを備えるデバイスを用いた、塩化物イオンチャネル阻害剤のスクリーニング方法であって、
前記デバイスは、前記圧入力センサが外力負荷手段と外力測定手段を含み、インビトロで、被検細胞に外力を負荷しつつ外力を測定し、前記塩化物イオンセンサが、当該細胞から排出される塩化物イオンを測定することを特徴とするデバイスであり、
被験物質を細胞に投与する工程;
前記細胞に外力を負荷しつつ外力を測定し、且つ前記細胞から排出される塩化物イオンを測定する工程;及び
前記塩化物イオンのレベルを指標として、前記被験物質が塩化物イオンチャネル阻害剤の候補物質としてスクリーニングする工程を含む、方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2025526079A JPWO2024253016A1 (ja) | 2023-06-06 | 2024-05-30 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023-093435 | 2023-06-06 | ||
| JP2023093435 | 2023-06-06 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2024253016A1 true WO2024253016A1 (ja) | 2024-12-12 |
Family
ID=93795991
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2024/019859 Ceased WO2024253016A1 (ja) | 2023-06-06 | 2024-05-30 | 塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイス |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JPWO2024253016A1 (ja) |
| WO (1) | WO2024253016A1 (ja) |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH041239A (ja) * | 1990-04-18 | 1992-01-06 | Tokuyama Soda Co Ltd | イオン感応膜の製造方法 |
| JPH04124162A (ja) * | 1990-09-14 | 1992-04-24 | Joko:Kk | 塩化物イオン選択性電極および電極用感応物質 |
| JPH05142191A (ja) * | 1991-11-18 | 1993-06-08 | Hitachi Ltd | イオン選択性電極 |
| JPH1010078A (ja) * | 1996-06-24 | 1998-01-16 | Hitachi Ltd | 塩素イオンセンサ |
| JPH10318973A (ja) * | 1997-05-15 | 1998-12-04 | Hitachi Ltd | 塩素イオン感応膜及びその製造方法 |
| JPH11337515A (ja) * | 1998-05-29 | 1999-12-10 | Hitachi Ltd | 陰イオン選択性電極 |
| JP2017106823A (ja) * | 2015-12-10 | 2017-06-15 | 東亜ディーケーケー株式会社 | 塩素イオン選択性電極 |
| JP2021191238A (ja) * | 2020-06-05 | 2021-12-16 | 国立研究開発法人産業技術総合研究所 | がん細胞の評価方法および評価デバイス |
-
2024
- 2024-05-30 WO PCT/JP2024/019859 patent/WO2024253016A1/ja not_active Ceased
- 2024-05-30 JP JP2025526079A patent/JPWO2024253016A1/ja active Pending
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH041239A (ja) * | 1990-04-18 | 1992-01-06 | Tokuyama Soda Co Ltd | イオン感応膜の製造方法 |
| JPH04124162A (ja) * | 1990-09-14 | 1992-04-24 | Joko:Kk | 塩化物イオン選択性電極および電極用感応物質 |
| JPH05142191A (ja) * | 1991-11-18 | 1993-06-08 | Hitachi Ltd | イオン選択性電極 |
| JPH1010078A (ja) * | 1996-06-24 | 1998-01-16 | Hitachi Ltd | 塩素イオンセンサ |
| JPH10318973A (ja) * | 1997-05-15 | 1998-12-04 | Hitachi Ltd | 塩素イオン感応膜及びその製造方法 |
| JPH11337515A (ja) * | 1998-05-29 | 1999-12-10 | Hitachi Ltd | 陰イオン選択性電極 |
| JP2017106823A (ja) * | 2015-12-10 | 2017-06-15 | 東亜ディーケーケー株式会社 | 塩素イオン選択性電極 |
| JP2021191238A (ja) * | 2020-06-05 | 2021-12-16 | 国立研究開発法人産業技術総合研究所 | がん細胞の評価方法および評価デバイス |
Non-Patent Citations (1)
| Title |
|---|
| YAMAGISHI AYANA, ITO FUMIE, NAKAMURA CHIKASHI: "Study on Cancer Cell Invasiveness via Application of Mechanical Force to Induce Chloride Ion Efflux", ANALYTICAL CHEMISTRY, AMERICAN CHEMICAL SOCIETY, vol. 93, no. 26, 6 July 2021 (2021-07-06), pages 9032 - 9035, XP093247276, ISSN: 0003-2700, DOI: 10.1021/acs.analchem.1c01589 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2024253016A1 (ja) | 2024-12-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9018019B2 (en) | Engineered conductive polymer films to mediate biochemical interactions | |
| Ahmad et al. | An electrochemical sandwich immunosensor for the detection of HER2 using antibody-conjugated PbS quantum dot as a label | |
| Zagitova et al. | Voltammetric chiral recognition of naproxen enantiomers by N-tosylproline functionalized chitosan and reduced graphene oxide based sensor | |
| KR102657461B1 (ko) | 단일-세포 세포내 나노-ph 프로브 | |
| Lee et al. | Peptide-imprinted poly (hydroxymethyl 3, 4-ethylenedioxythiophene) nanotubes for detection of α synuclein in human brain organoids | |
| Hu et al. | The inhibition of fluorescence resonance energy transfer between quantum dots for glucose assay | |
| JPS59225343A (ja) | 生化学リガンドを有する診断装置 | |
| US20140231274A1 (en) | Single molecule detection method and single molecule detection apparatus for biological molecule, and disease marker testing apparatus | |
| KR20050100367A (ko) | 소용적 샘플 내의 분자 분석용 방법 및 장치 | |
| Chocholova et al. | Advanced antifouling zwitterionic layer based impedimetric HER2 biosensing in human serum: Glycoprofiling as a novel approach for breast cancer diagnostics | |
| Yadav et al. | Fabrication of alkoxysilane substituted polymer-modified disposable biosensing platform: Towards sperm protein 17 sensing as a new cancer biomarker | |
| BR112020014894A2 (pt) | Eletrodo para uso na detecção eletroquímica de uma espécie alvo, espectrômetro eletroquímico, uso de um eletrodo e método eletroquímico de detecção de uma espécie alvo | |
| Nishitani et al. | Polymeric nanofilter biointerface for potentiometric small-biomolecule recognition | |
| Saha et al. | Selective pathological and intracellular detection of human serum albumin by photophysical and electrochemical techniques using a FRET-based molecular probe | |
| Lu et al. | Ultrasensitive electrochemical detection of CYFRA 21-1 via in-situ initiated ROP signal amplification strategy | |
| ES2769288T3 (es) | Un electrodo y uso del mismo | |
| Ahmadi et al. | Affinity-based electrochemical biosensor with antifouling properties for detection of lysophosphatidic acid, a promising early-stage ovarian cancer biomarker | |
| Altunkök et al. | Development of potentıometrıc bıosensor for dıagnosıs of prostate cancer | |
| Adu et al. | Rapid and label-free A2 peptide epitope decorated CoFe2O4-C60 nanocomposite-based electrochemical immunosensor for detecting visceral leishmaniasis | |
| Prats‐Alfonso et al. | Cancer Prognostics by Direct Detection of p53‐Antibodies on Gold Surfaces by Impedance Measurements | |
| Wang et al. | A pendulum-type electrochemical aptamer-based sensor for continuous, real-time and stable detection of proteins | |
| Nhu et al. | An evaluation of a gold surface functionalization procedure for antibody binding and protein detection using 11-mercaptoundecanoic acid (11-MUA) | |
| WO2024253016A1 (ja) | 塩化物イオンセンサ並びにそれを用いたがん細胞の検出及び/又はがん細胞の悪性度評価のためのデバイス | |
| US20150219579A1 (en) | Method for detecting autoantibodies | |
| Yaman et al. | Fabrication of trastuzumab conjugated curcumin nanoparticles based impedimetric cytosensor for the cancer cell detection |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 24819247 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2025526079 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2025526079 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |