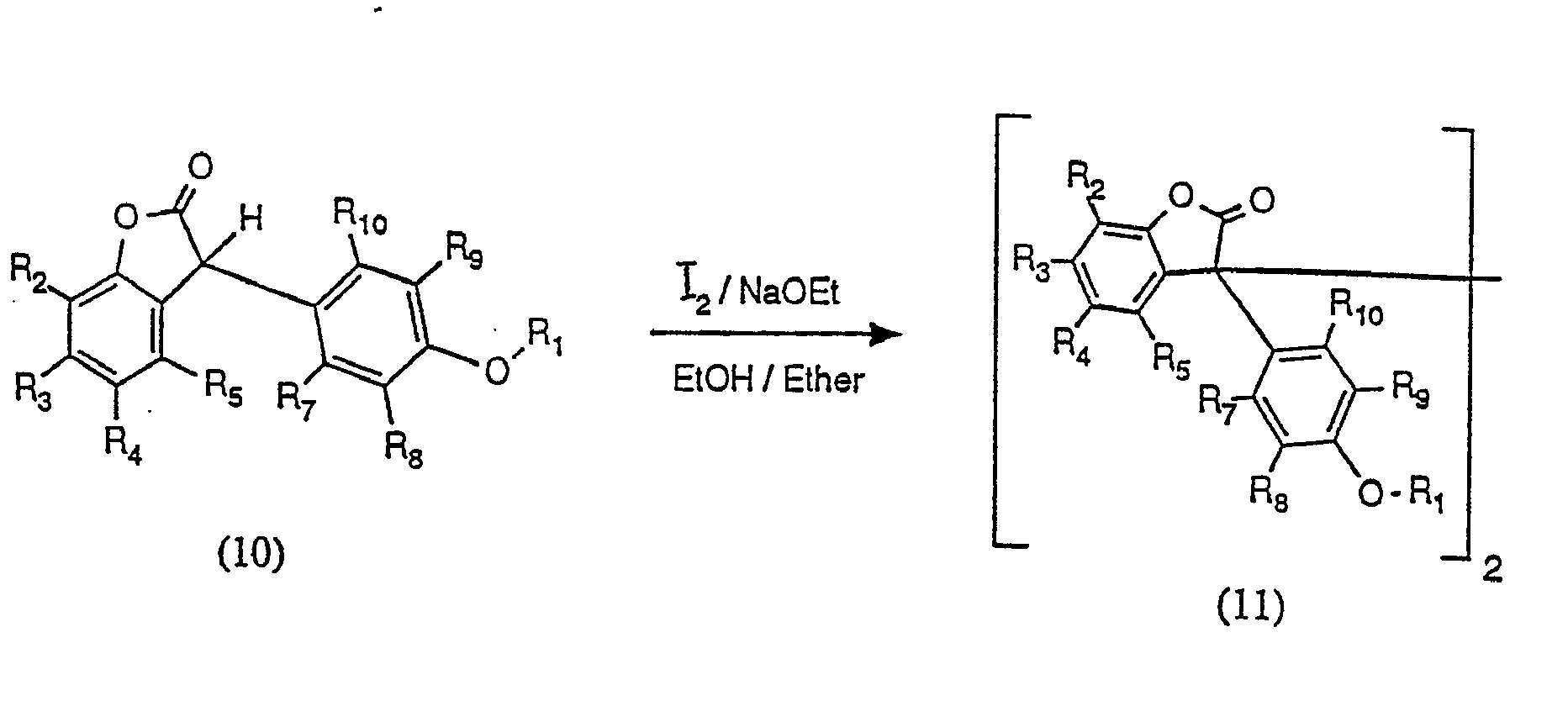
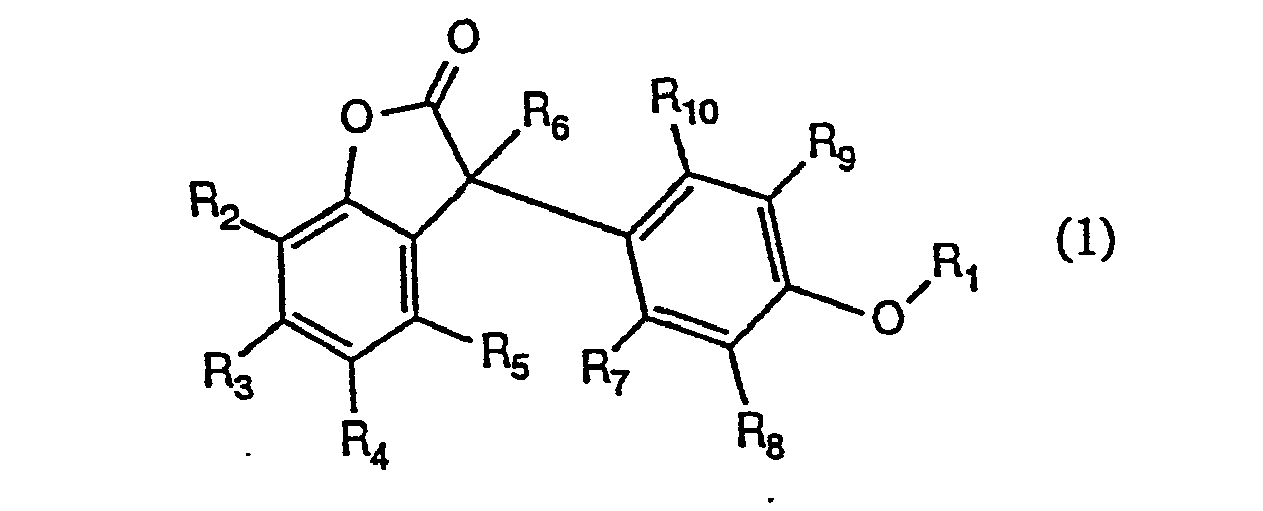
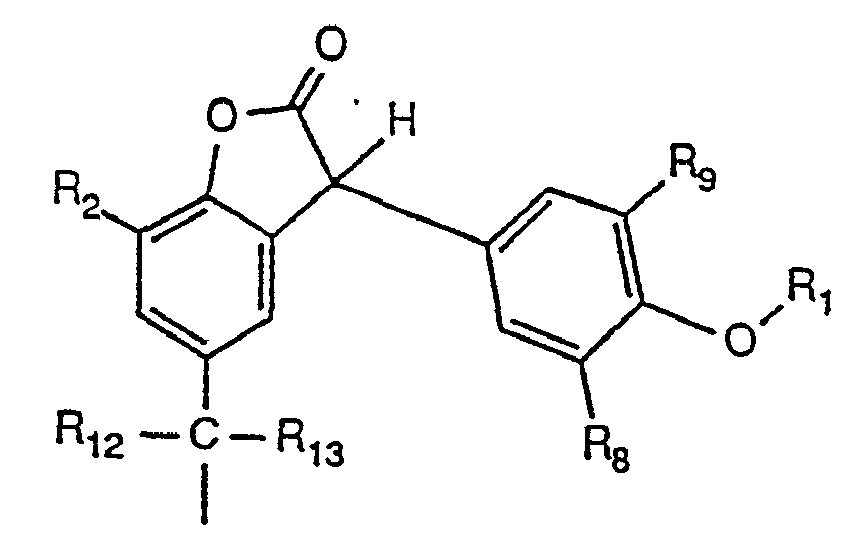
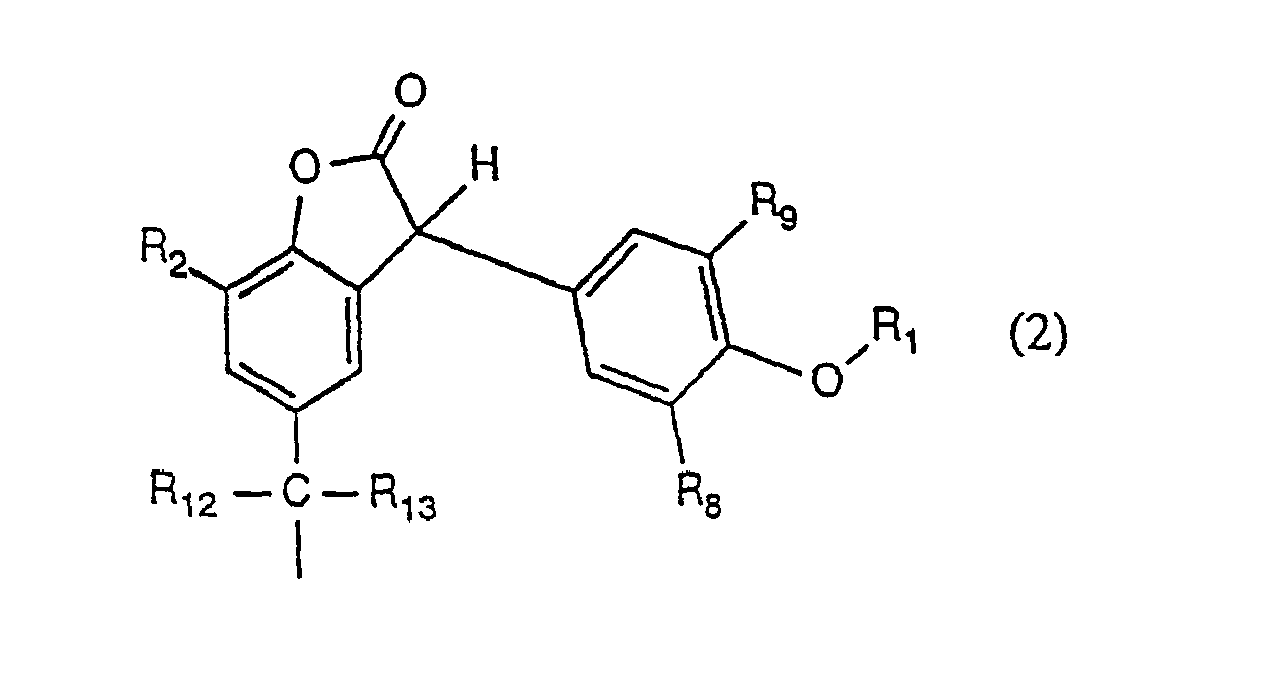
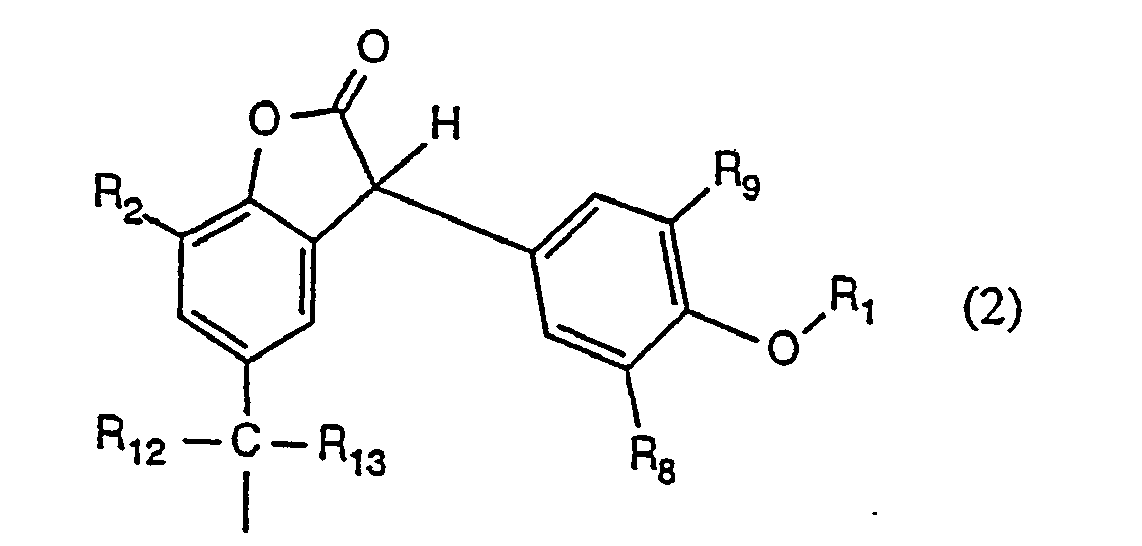
BE1006549A3 - Application de 3-(alcoxyphenyl)benzofuranne-2-onescomme stabilisants et nouveaux composes de ce typ e - Google Patents
Application de 3-(alcoxyphenyl)benzofuranne-2-onescomme stabilisants et nouveaux composes de ce typ e Download PDFInfo
- Publication number
- BE1006549A3 BE1006549A3 BE9300513D BE9300513D BE1006549A3 BE 1006549 A3 BE1006549 A3 BE 1006549A3 BE 9300513 D BE9300513 D BE 9300513D BE 9300513 D BE9300513 D BE 9300513D BE 1006549 A3 BE1006549 A3 BE 1006549A3
- Authority
- BE
- Belgium
- Prior art keywords
- alkyl
- hydrogen
- phenyl
- substituted
- radical
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims description 71
- 239000003381 stabilizer Substances 0.000 title claims description 17
- ACZGCWSMSTYWDQ-UHFFFAOYSA-N 3h-1-benzofuran-2-one Chemical compound C1=CC=C2OC(=O)CC2=C1 ACZGCWSMSTYWDQ-UHFFFAOYSA-N 0.000 title description 5
- 125000005036 alkoxyphenyl group Chemical group 0.000 title description 4
- -1 benzoyloxyl Chemical group 0.000 claims description 180
- 239000001257 hydrogen Substances 0.000 claims description 90
- 229910052739 hydrogen Inorganic materials 0.000 claims description 90
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 70
- 239000000203 mixture Substances 0.000 claims description 68
- 125000000217 alkyl group Chemical group 0.000 claims description 59
- 150000002431 hydrogen Chemical class 0.000 claims description 58
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 57
- 125000003545 alkoxy group Chemical group 0.000 claims description 31
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 29
- 239000001301 oxygen Substances 0.000 claims description 29
- 229910052760 oxygen Inorganic materials 0.000 claims description 29
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 28
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 25
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 23
- 125000004432 carbon atom Chemical group C* 0.000 claims description 23
- 229910052717 sulfur Inorganic materials 0.000 claims description 23
- 239000011593 sulfur Substances 0.000 claims description 23
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 22
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 21
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 20
- 238000000034 method Methods 0.000 claims description 17
- 125000004400 (C1-C12) alkyl group Chemical group 0.000 claims description 15
- 125000003342 alkenyl group Chemical group 0.000 claims description 15
- 125000003884 phenylalkyl group Chemical group 0.000 claims description 14
- 125000000304 alkynyl group Chemical group 0.000 claims description 13
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 13
- 125000005605 benzo group Chemical group 0.000 claims description 12
- 229910052751 metal Inorganic materials 0.000 claims description 12
- 239000002184 metal Substances 0.000 claims description 12
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 12
- 239000011368 organic material Substances 0.000 claims description 12
- 230000006641 stabilisation Effects 0.000 claims description 12
- 238000011105 stabilization Methods 0.000 claims description 12
- 230000015556 catabolic process Effects 0.000 claims description 10
- 238000006731 degradation reaction Methods 0.000 claims description 10
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 claims description 8
- 230000001590 oxidative effect Effects 0.000 claims description 8
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 8
- XRBCRPZXSCBRTK-UHFFFAOYSA-N phosphonous acid Chemical compound OPO XRBCRPZXSCBRTK-UHFFFAOYSA-N 0.000 claims description 6
- 150000001768 cations Chemical class 0.000 claims description 5
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 4
- 229910052799 carbon Inorganic materials 0.000 claims description 4
- 229910052702 rhenium Inorganic materials 0.000 claims description 4
- OJMIONKXNSYLSR-UHFFFAOYSA-N phosphorous acid Chemical compound OP(O)O OJMIONKXNSYLSR-UHFFFAOYSA-N 0.000 claims description 3
- 229920001059 synthetic polymer Polymers 0.000 claims description 2
- 125000004642 (C1-C12) alkoxy group Chemical group 0.000 claims 1
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 claims 1
- 125000004209 (C1-C8) alkyl group Chemical group 0.000 claims 1
- 229920001577 copolymer Polymers 0.000 description 38
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 37
- 150000003254 radicals Chemical class 0.000 description 35
- 229920000642 polymer Polymers 0.000 description 25
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 22
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 21
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 20
- 229920001228 polyisocyanate Polymers 0.000 description 19
- 239000005056 polyisocyanate Substances 0.000 description 19
- 238000002844 melting Methods 0.000 description 18
- 230000008018 melting Effects 0.000 description 18
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 16
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 15
- 150000002148 esters Chemical class 0.000 description 15
- 238000002360 preparation method Methods 0.000 description 15
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 14
- 239000006260 foam Substances 0.000 description 13
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 12
- 239000004952 Polyamide Substances 0.000 description 12
- 239000004743 Polypropylene Substances 0.000 description 12
- 229920002647 polyamide Polymers 0.000 description 12
- 229920002857 polybutadiene Polymers 0.000 description 12
- 239000004814 polyurethane Substances 0.000 description 12
- 239000003054 catalyst Substances 0.000 description 11
- 229920000570 polyether Polymers 0.000 description 11
- 239000000047 product Substances 0.000 description 11
- 239000002253 acid Substances 0.000 description 10
- 229920002635 polyurethane Polymers 0.000 description 10
- 239000011541 reaction mixture Substances 0.000 description 10
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 238000006243 chemical reaction Methods 0.000 description 9
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 9
- 239000005062 Polybutadiene Substances 0.000 description 8
- 239000004698 Polyethylene Substances 0.000 description 8
- 229920001684 low density polyethylene Polymers 0.000 description 8
- 239000004702 low-density polyethylene Substances 0.000 description 8
- 239000000463 material Substances 0.000 description 8
- 229910052757 nitrogen Inorganic materials 0.000 description 8
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 8
- 229920000573 polyethylene Polymers 0.000 description 8
- 229920000098 polyolefin Polymers 0.000 description 8
- 229920001155 polypropylene Polymers 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 7
- 239000002671 adjuvant Substances 0.000 description 7
- 150000001298 alcohols Chemical class 0.000 description 7
- 150000001412 amines Chemical class 0.000 description 7
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 7
- 229920006324 polyoxymethylene Polymers 0.000 description 7
- 239000000126 substance Substances 0.000 description 7
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 6
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 6
- 239000004721 Polyphenylene oxide Substances 0.000 description 6
- 239000004417 polycarbonate Substances 0.000 description 6
- 229920000915 polyvinyl chloride Polymers 0.000 description 6
- 239000004800 polyvinyl chloride Substances 0.000 description 6
- 229920000877 Melamine resin Polymers 0.000 description 5
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 5
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 5
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 5
- 229920000122 acrylonitrile butadiene styrene Polymers 0.000 description 5
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 5
- 239000012964 benzotriazole Substances 0.000 description 5
- 150000001993 dienes Chemical class 0.000 description 5
- 150000004665 fatty acids Chemical group 0.000 description 5
- 229920001903 high density polyethylene Polymers 0.000 description 5
- 239000004700 high-density polyethylene Substances 0.000 description 5
- 239000012948 isocyanate Substances 0.000 description 5
- 150000002513 isocyanates Chemical class 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 5
- 239000003921 oil Substances 0.000 description 5
- 239000012074 organic phase Substances 0.000 description 5
- 150000002989 phenols Chemical class 0.000 description 5
- 229920000728 polyester Polymers 0.000 description 5
- 238000006116 polymerization reaction Methods 0.000 description 5
- 229920005862 polyol Polymers 0.000 description 5
- 230000000087 stabilizing effect Effects 0.000 description 5
- 229940113165 trimethylolpropane Drugs 0.000 description 5
- 125000006702 (C1-C18) alkyl group Chemical group 0.000 description 4
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 4
- ALVZNPYWJMLXKV-UHFFFAOYSA-N 1,9-Nonanediol Chemical compound OCCCCCCCCCO ALVZNPYWJMLXKV-UHFFFAOYSA-N 0.000 description 4
- ICKWICRCANNIBI-UHFFFAOYSA-N 2,4-di-tert-butylphenol Chemical compound CC(C)(C)C1=CC=C(O)C(C(C)(C)C)=C1 ICKWICRCANNIBI-UHFFFAOYSA-N 0.000 description 4
- KXPXKNBDCUOENF-UHFFFAOYSA-N 2-(Octylthio)ethanol Chemical compound CCCCCCCCSCCO KXPXKNBDCUOENF-UHFFFAOYSA-N 0.000 description 4
- CXUYVOHLQSZWCW-UHFFFAOYSA-N 5,7-ditert-butyl-3-(4-ethoxyphenyl)-3h-1-benzofuran-2-one Chemical compound C1=CC(OCC)=CC=C1C1C(C=C(C=C2C(C)(C)C)C(C)(C)C)=C2OC1=O CXUYVOHLQSZWCW-UHFFFAOYSA-N 0.000 description 4
- CKPKHTKLLYPGFM-UHFFFAOYSA-N 6,6-dimethylheptane-1,1-diol Chemical compound CC(CCCCC(O)O)(C)C CKPKHTKLLYPGFM-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 229920002943 EPDM rubber Polymers 0.000 description 4
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical class C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- 229920005830 Polyurethane Foam Polymers 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-N Propionic acid Chemical class CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 4
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 4
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 4
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 4
- 125000003118 aryl group Chemical group 0.000 description 4
- TZCXTZWJZNENPQ-UHFFFAOYSA-L barium sulfate Chemical compound [Ba+2].[O-]S([O-])(=O)=O TZCXTZWJZNENPQ-UHFFFAOYSA-L 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 238000009833 condensation Methods 0.000 description 4
- 230000005494 condensation Effects 0.000 description 4
- 235000014113 dietary fatty acids Nutrition 0.000 description 4
- 239000000194 fatty acid Substances 0.000 description 4
- 229930195729 fatty acid Natural products 0.000 description 4
- HHLFWLYXYJOTON-UHFFFAOYSA-N glyoxylic acid Chemical compound OC(=O)C=O HHLFWLYXYJOTON-UHFFFAOYSA-N 0.000 description 4
- 230000006698 induction Effects 0.000 description 4
- ZFSLODLOARCGLH-UHFFFAOYSA-N isocyanuric acid Chemical group OC1=NC(O)=NC(O)=N1 ZFSLODLOARCGLH-UHFFFAOYSA-N 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- DNIAPMSPPWPWGF-UHFFFAOYSA-N monopropylene glycol Natural products CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 4
- FPQJEXTVQZHURJ-UHFFFAOYSA-N n,n'-bis(2-hydroxyethyl)oxamide Chemical compound OCCNC(=O)C(=O)NCCO FPQJEXTVQZHURJ-UHFFFAOYSA-N 0.000 description 4
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 4
- 229940117969 neopentyl glycol Drugs 0.000 description 4
- 150000002815 nickel Chemical class 0.000 description 4
- 239000012299 nitrogen atmosphere Substances 0.000 description 4
- 235000019198 oils Nutrition 0.000 description 4
- 229920001200 poly(ethylene-vinyl acetate) Polymers 0.000 description 4
- 229920000647 polyepoxide Polymers 0.000 description 4
- 229920006380 polyphenylene oxide Polymers 0.000 description 4
- 239000011496 polyurethane foam Substances 0.000 description 4
- 235000013772 propylene glycol Nutrition 0.000 description 4
- 229920005989 resin Polymers 0.000 description 4
- 239000011347 resin Substances 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 229910052938 sodium sulfate Inorganic materials 0.000 description 4
- 235000011152 sodium sulphate Nutrition 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 238000005507 spraying Methods 0.000 description 4
- 238000003756 stirring Methods 0.000 description 4
- YODZTKMDCQEPHD-UHFFFAOYSA-N thiodiglycol Chemical compound OCCSCCO YODZTKMDCQEPHD-UHFFFAOYSA-N 0.000 description 4
- 229920002554 vinyl polymer Polymers 0.000 description 4
- BPXVHIRIPLPOPT-UHFFFAOYSA-N 1,3,5-tris(2-hydroxyethyl)-1,3,5-triazinane-2,4,6-trione Chemical compound OCCN1C(=O)N(CCO)C(=O)N(CCO)C1=O BPXVHIRIPLPOPT-UHFFFAOYSA-N 0.000 description 3
- YEWBOZCFGXOUQW-UHFFFAOYSA-N 2,6,7-trioxa-1-phosphabicyclo[2.2.2]octan-4-ylmethanol Chemical compound C1OP2OCC1(CO)CO2 YEWBOZCFGXOUQW-UHFFFAOYSA-N 0.000 description 3
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 3
- YHXHKYRQLYQUIH-UHFFFAOYSA-N 4-hydroxymandelic acid Chemical compound OC(=O)C(O)C1=CC=C(O)C=C1 YHXHKYRQLYQUIH-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 3
- 239000005977 Ethylene Substances 0.000 description 3
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 3
- SJRJJKPEHAURKC-UHFFFAOYSA-N N-Methylmorpholine Chemical compound CN1CCOCC1 SJRJJKPEHAURKC-UHFFFAOYSA-N 0.000 description 3
- 229920002396 Polyurea Polymers 0.000 description 3
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 3
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 125000001931 aliphatic group Chemical group 0.000 description 3
- 239000003513 alkali Substances 0.000 description 3
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 3
- FQUNFJULCYSSOP-UHFFFAOYSA-N bisoctrizole Chemical compound N1=C2C=CC=CC2=NN1C1=CC(C(C)(C)CC(C)(C)C)=CC(CC=2C(=C(C=C(C=2)C(C)(C)CC(C)(C)C)N2N=C3C=CC=CC3=N2)O)=C1O FQUNFJULCYSSOP-UHFFFAOYSA-N 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 239000007859 condensation product Substances 0.000 description 3
- 238000002425 crystallisation Methods 0.000 description 3
- 230000008025 crystallization Effects 0.000 description 3
- 150000001991 dicarboxylic acids Chemical class 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 229920001971 elastomer Polymers 0.000 description 3
- 239000003995 emulsifying agent Substances 0.000 description 3
- 239000003822 epoxy resin Substances 0.000 description 3
- 238000001125 extrusion Methods 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 239000003063 flame retardant Substances 0.000 description 3
- 239000004872 foam stabilizing agent Substances 0.000 description 3
- 238000005187 foaming Methods 0.000 description 3
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 150000002739 metals Chemical class 0.000 description 3
- 150000004702 methyl esters Chemical class 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 150000005673 monoalkenes Chemical class 0.000 description 3
- 239000000178 monomer Substances 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- AQSJGOWTSHOLKH-UHFFFAOYSA-N phosphite(3-) Chemical class [O-]P([O-])[O-] AQSJGOWTSHOLKH-UHFFFAOYSA-N 0.000 description 3
- 239000004014 plasticizer Substances 0.000 description 3
- 229920000058 polyacrylate Polymers 0.000 description 3
- 150000003077 polyols Chemical class 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 239000011734 sodium Substances 0.000 description 3
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 3
- 229920000468 styrene butadiene styrene block copolymer Polymers 0.000 description 3
- 229920001897 terpolymer Polymers 0.000 description 3
- 229920001169 thermoplastic Polymers 0.000 description 3
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 3
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 3
- YHMYGUUIMTVXNW-UHFFFAOYSA-N 1,3-dihydrobenzimidazole-2-thione Chemical compound C1=CC=C2NC(S)=NC2=C1 YHMYGUUIMTVXNW-UHFFFAOYSA-N 0.000 description 2
- KGRVJHAUYBGFFP-UHFFFAOYSA-N 2,2'-Methylenebis(4-methyl-6-tert-butylphenol) Chemical compound CC(C)(C)C1=CC(C)=CC(CC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=C1O KGRVJHAUYBGFFP-UHFFFAOYSA-N 0.000 description 2
- SLUKQUGVTITNSY-UHFFFAOYSA-N 2,6-di-tert-butyl-4-methoxyphenol Chemical compound COC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 SLUKQUGVTITNSY-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- RZEFQGHPKYOLKG-UHFFFAOYSA-N 2-hydroxy-2-(4-hydroxy-3,5-dimethylphenyl)acetic acid Chemical compound CC1=CC(C(O)C(O)=O)=CC(C)=C1O RZEFQGHPKYOLKG-UHFFFAOYSA-N 0.000 description 2
- ONUIVMPUJMCSLI-UHFFFAOYSA-N 2-hydroxy-2-(4-phenylmethoxyphenyl)acetic acid Chemical compound C1=CC(C(C(O)=O)O)=CC=C1OCC1=CC=CC=C1 ONUIVMPUJMCSLI-UHFFFAOYSA-N 0.000 description 2
- KWAGEZBPBJTIMD-UHFFFAOYSA-N 2-hydroxy-2-(4-tetradecoxyphenyl)acetic acid Chemical compound CCCCCCCCCCCCCCOC1=CC=C(C(O)C(O)=O)C=C1 KWAGEZBPBJTIMD-UHFFFAOYSA-N 0.000 description 2
- HXIQYSLFEXIOAV-UHFFFAOYSA-N 2-tert-butyl-4-(5-tert-butyl-4-hydroxy-2-methylphenyl)sulfanyl-5-methylphenol Chemical compound CC1=CC(O)=C(C(C)(C)C)C=C1SC1=CC(C(C)(C)C)=C(O)C=C1C HXIQYSLFEXIOAV-UHFFFAOYSA-N 0.000 description 2
- XOUQAVYLRNOXDO-UHFFFAOYSA-N 2-tert-butyl-5-methylphenol Chemical compound CC1=CC=C(C(C)(C)C)C(O)=C1 XOUQAVYLRNOXDO-UHFFFAOYSA-N 0.000 description 2
- RXFCIXRFAJRBSG-UHFFFAOYSA-N 3,2,3-tetramine Chemical compound NCCCNCCNCCCN RXFCIXRFAJRBSG-UHFFFAOYSA-N 0.000 description 2
- YEXOWHQZWLCHHD-UHFFFAOYSA-N 3,5-ditert-butyl-4-hydroxybenzoic acid Chemical compound CC(C)(C)C1=CC(C(O)=O)=CC(C(C)(C)C)=C1O YEXOWHQZWLCHHD-UHFFFAOYSA-N 0.000 description 2
- HCILJBJJZALOAL-UHFFFAOYSA-N 3-(3,5-ditert-butyl-4-hydroxyphenyl)-n'-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyl]propanehydrazide Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)NNC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 HCILJBJJZALOAL-UHFFFAOYSA-N 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- 239000004604 Blowing Agent Substances 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 2
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 2
- 229920010126 Linear Low Density Polyethylene (LLDPE) Polymers 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- JKIJEFPNVSHHEI-UHFFFAOYSA-N Phenol, 2,4-bis(1,1-dimethylethyl)-, phosphite (3:1) Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC=C1OP(OC=1C(=CC(=CC=1)C(C)(C)C)C(C)(C)C)OC1=CC=C(C(C)(C)C)C=C1C(C)(C)C JKIJEFPNVSHHEI-UHFFFAOYSA-N 0.000 description 2
- 229920002367 Polyisobutene Polymers 0.000 description 2
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 description 2
- 235000021355 Stearic acid Nutrition 0.000 description 2
- 239000002174 Styrene-butadiene Substances 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 2
- 239000003490 Thiodipropionic acid Substances 0.000 description 2
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 2
- 229920001807 Urea-formaldehyde Polymers 0.000 description 2
- JXSPFIRUFALMSP-UHFFFAOYSA-N [3-(4-ethoxyphenyl)-2-oxo-3h-1-benzofuran-5-yl] 2,2-dimethylpropanoate Chemical compound C1=CC(OCC)=CC=C1C1C2=CC(OC(=O)C(C)(C)C)=CC=C2OC1=O JXSPFIRUFALMSP-UHFFFAOYSA-N 0.000 description 2
- 239000006096 absorbing agent Substances 0.000 description 2
- 150000001241 acetals Chemical class 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 229920000800 acrylic rubber Polymers 0.000 description 2
- 239000012190 activator Substances 0.000 description 2
- 239000001361 adipic acid Substances 0.000 description 2
- 235000011037 adipic acid Nutrition 0.000 description 2
- 230000032683 aging Effects 0.000 description 2
- 150000001299 aldehydes Chemical class 0.000 description 2
- 150000001336 alkenes Chemical class 0.000 description 2
- 229920000180 alkyd Polymers 0.000 description 2
- 230000000844 anti-bacterial effect Effects 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 229920001400 block copolymer Polymers 0.000 description 2
- FACXGONDLDSNOE-UHFFFAOYSA-N buta-1,3-diene;styrene Chemical compound C=CC=C.C=CC1=CC=CC=C1.C=CC1=CC=CC=C1 FACXGONDLDSNOE-UHFFFAOYSA-N 0.000 description 2
- MTAZNLWOLGHBHU-UHFFFAOYSA-N butadiene-styrene rubber Chemical compound C=CC=C.C=CC1=CC=CC=C1 MTAZNLWOLGHBHU-UHFFFAOYSA-N 0.000 description 2
- VPKDCDLSJZCGKE-UHFFFAOYSA-N carbodiimide group Chemical group N=C=N VPKDCDLSJZCGKE-UHFFFAOYSA-N 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 229910002091 carbon monoxide Inorganic materials 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- WZHCOOQXZCIUNC-UHFFFAOYSA-N cyclandelate Chemical group C1C(C)(C)CC(C)CC1OC(=O)C(O)C1=CC=CC=C1 WZHCOOQXZCIUNC-UHFFFAOYSA-N 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- LPIQUOYDBNQMRZ-UHFFFAOYSA-N cyclopentene Chemical compound C1CC=CC1 LPIQUOYDBNQMRZ-UHFFFAOYSA-N 0.000 description 2
- 230000009849 deactivation Effects 0.000 description 2
- GYZLOYUZLJXAJU-UHFFFAOYSA-N diglycidyl ether Chemical class C1OC1COCC1CO1 GYZLOYUZLJXAJU-UHFFFAOYSA-N 0.000 description 2
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 2
- POULHZVOKOAJMA-UHFFFAOYSA-N dodecanoic acid Chemical compound CCCCCCCCCCCC(O)=O POULHZVOKOAJMA-UHFFFAOYSA-N 0.000 description 2
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 239000000806 elastomer Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 150000002118 epoxides Chemical class 0.000 description 2
- 125000004494 ethyl ester group Chemical group 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 229920006242 ethylene acrylic acid copolymer Polymers 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 2
- 229920000554 ionomer Polymers 0.000 description 2
- IQPQWNKOIGAROB-UHFFFAOYSA-N isocyanate group Chemical group [N-]=C=O IQPQWNKOIGAROB-UHFFFAOYSA-N 0.000 description 2
- 229920000092 linear low density polyethylene Polymers 0.000 description 2
- 239000004707 linear low-density polyethylene Substances 0.000 description 2
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical compound O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 2
- 229960002510 mandelic acid Drugs 0.000 description 2
- JDSHMPZPIAZGSV-UHFFFAOYSA-N melamine Chemical compound NC1=NC(N)=NC(N)=N1 JDSHMPZPIAZGSV-UHFFFAOYSA-N 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 229940098779 methanesulfonic acid Drugs 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- WSFSSNUMVMOOMR-NJFSPNSNSA-N methanone Chemical compound O=[14CH2] WSFSSNUMVMOOMR-NJFSPNSNSA-N 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- FTWUXYZHDFCGSV-UHFFFAOYSA-N n,n'-diphenyloxamide Chemical compound C=1C=CC=CC=1NC(=O)C(=O)NC1=CC=CC=C1 FTWUXYZHDFCGSV-UHFFFAOYSA-N 0.000 description 2
- 229920003052 natural elastomer Polymers 0.000 description 2
- 229920001194 natural rubber Polymers 0.000 description 2
- 229920006173 natural rubber latex Polymers 0.000 description 2
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 2
- 235000006408 oxalic acid Nutrition 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- QQVIHTHCMHWDBS-UHFFFAOYSA-N perisophthalic acid Natural products OC(=O)C1=CC=CC(C(O)=O)=C1 QQVIHTHCMHWDBS-UHFFFAOYSA-N 0.000 description 2
- ZQBAKBUEJOMQEX-UHFFFAOYSA-N phenyl salicylate Chemical compound OC1=CC=CC=C1C(=O)OC1=CC=CC=C1 ZQBAKBUEJOMQEX-UHFFFAOYSA-N 0.000 description 2
- 235000021317 phosphate Nutrition 0.000 description 2
- 239000000049 pigment Substances 0.000 description 2
- 229920001281 polyalkylene Polymers 0.000 description 2
- 229920001707 polybutylene terephthalate Polymers 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 229920000193 polymethacrylate Polymers 0.000 description 2
- 229920006389 polyphenyl polymer Polymers 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 2
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 2
- CXMXRPHRNRROMY-UHFFFAOYSA-N sebacic acid Chemical compound OC(=O)CCCCCCCCC(O)=O CXMXRPHRNRROMY-UHFFFAOYSA-N 0.000 description 2
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 2
- NASFKTWZWDYFER-UHFFFAOYSA-N sodium;hydrate Chemical compound O.[Na] NASFKTWZWDYFER-UHFFFAOYSA-N 0.000 description 2
- 239000008117 stearic acid Substances 0.000 description 2
- 229920000638 styrene acrylonitrile Polymers 0.000 description 2
- 239000011115 styrene butadiene Substances 0.000 description 2
- 229920003048 styrene butadiene rubber Polymers 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 150000003512 tertiary amines Chemical class 0.000 description 2
- 239000004416 thermosoftening plastic Substances 0.000 description 2
- 150000003606 tin compounds Chemical class 0.000 description 2
- RUELTTOHQODFPA-UHFFFAOYSA-N toluene 2,6-diisocyanate Chemical class CC1=C(N=C=O)C=CC=C1N=C=O RUELTTOHQODFPA-UHFFFAOYSA-N 0.000 description 2
- HVLLSGMXQDNUAL-UHFFFAOYSA-N triphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OC=1C=CC=CC=1)OC1=CC=CC=C1 HVLLSGMXQDNUAL-UHFFFAOYSA-N 0.000 description 2
- AVWRKZWQTYIKIY-UHFFFAOYSA-N urea-1-carboxylic acid Chemical group NC(=O)NC(O)=O AVWRKZWQTYIKIY-UHFFFAOYSA-N 0.000 description 2
- JOYRKODLDBILNP-UHFFFAOYSA-N urethane group Chemical group NC(=O)OCC JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- 238000004383 yellowing Methods 0.000 description 2
- BOXSVZNGTQTENJ-UHFFFAOYSA-L zinc dibutyldithiocarbamate Chemical compound [Zn+2].CCCCN(C([S-])=S)CCCC.CCCCN(C([S-])=S)CCCC BOXSVZNGTQTENJ-UHFFFAOYSA-L 0.000 description 2
- HQEPZWYPQQKFLU-UHFFFAOYSA-N (2,6-dihydroxyphenyl)-phenylmethanone Chemical compound OC1=CC=CC(O)=C1C(=O)C1=CC=CC=C1 HQEPZWYPQQKFLU-UHFFFAOYSA-N 0.000 description 1
- HJIAMFHSAAEUKR-UHFFFAOYSA-N (2-hydroxyphenyl)-phenylmethanone Chemical class OC1=CC=CC=C1C(=O)C1=CC=CC=C1 HJIAMFHSAAEUKR-UHFFFAOYSA-N 0.000 description 1
- ATLWFAZCZPSXII-UHFFFAOYSA-N (2-octylphenyl) 2-hydroxybenzoate Chemical compound CCCCCCCCC1=CC=CC=C1OC(=O)C1=CC=CC=C1O ATLWFAZCZPSXII-UHFFFAOYSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical group O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- NAWXUBYGYWOOIX-SFHVURJKSA-N (2s)-2-[[4-[2-(2,4-diaminoquinazolin-6-yl)ethyl]benzoyl]amino]-4-methylidenepentanedioic acid Chemical compound C1=CC2=NC(N)=NC(N)=C2C=C1CCC1=CC=C(C(=O)N[C@@H](CC(=C)C(O)=O)C(O)=O)C=C1 NAWXUBYGYWOOIX-SFHVURJKSA-N 0.000 description 1
- FKFOHTUAFNQANW-UHFFFAOYSA-N (3,5-ditert-butyl-4-hydroxyphenyl) octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 FKFOHTUAFNQANW-UHFFFAOYSA-N 0.000 description 1
- KWXSCYIIFPGCNI-UHFFFAOYSA-N (4-tert-butylphenyl)-(2,6-dihydroxyphenyl)methanone Chemical compound C1=CC(C(C)(C)C)=CC=C1C(=O)C1=C(O)C=CC=C1O KWXSCYIIFPGCNI-UHFFFAOYSA-N 0.000 description 1
- GOZHNJTXLALKRL-UHFFFAOYSA-N (5-benzoyl-2,4-dihydroxyphenyl)-phenylmethanone Chemical compound OC1=CC(O)=C(C(=O)C=2C=CC=CC=2)C=C1C(=O)C1=CC=CC=C1 GOZHNJTXLALKRL-UHFFFAOYSA-N 0.000 description 1
- OJOWICOBYCXEKR-KRXBUXKQSA-N (5e)-5-ethylidenebicyclo[2.2.1]hept-2-ene Chemical compound C1C2C(=C/C)/CC1C=C2 OJOWICOBYCXEKR-KRXBUXKQSA-N 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- ZBBLRPRYYSJUCZ-GRHBHMESSA-L (z)-but-2-enedioate;dibutyltin(2+) Chemical compound [O-]C(=O)\C=C/C([O-])=O.CCCC[Sn+2]CCCC ZBBLRPRYYSJUCZ-GRHBHMESSA-L 0.000 description 1
- 0 *C(c(c(*)c(*)c(*)c1*)c1O1)(C1=O)c(cc1*)cc(*)c1O* Chemical compound *C(c(c(*)c(*)c(*)c1*)c1O1)(C1=O)c(cc1*)cc(*)c1O* 0.000 description 1
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 1
- VCMZIKKVYXGKCI-UHFFFAOYSA-N 1,1-bis(2,4-ditert-butyl-6-methylphenyl)-2,2-bis(hydroxymethyl)propane-1,3-diol dihydroxyphosphanyl dihydrogen phosphite Chemical compound OP(O)OP(O)O.C(C)(C)(C)C1=C(C(=CC(=C1)C(C)(C)C)C)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1C)C(C)(C)C)C(C)(C)C VCMZIKKVYXGKCI-UHFFFAOYSA-N 0.000 description 1
- GFNDFCFPJQPVQL-UHFFFAOYSA-N 1,12-diisocyanatododecane Chemical compound O=C=NCCCCCCCCCCCCN=C=O GFNDFCFPJQPVQL-UHFFFAOYSA-N 0.000 description 1
- OYWRDHBGMCXGFY-UHFFFAOYSA-N 1,2,3-triazinane Chemical class C1CNNNC1 OYWRDHBGMCXGFY-UHFFFAOYSA-N 0.000 description 1
- GIWQSPITLQVMSG-UHFFFAOYSA-N 1,2-dimethylimidazole Chemical compound CC1=NC=CN1C GIWQSPITLQVMSG-UHFFFAOYSA-N 0.000 description 1
- BLWNLYFYKIIZKR-UHFFFAOYSA-N 1,3,7,9-tetratert-butyl-11-(6-methylheptoxy)-5h-benzo[d][1,3,2]benzodioxaphosphocine Chemical compound C1C2=CC(C(C)(C)C)=CC(C(C)(C)C)=C2OP(OCCCCCC(C)C)OC2=C1C=C(C(C)(C)C)C=C2C(C)(C)C BLWNLYFYKIIZKR-UHFFFAOYSA-N 0.000 description 1
- OHTRJOZKRSVAOX-UHFFFAOYSA-N 1,3-diisocyanato-2-methylcyclohexane Chemical class CC1C(N=C=O)CCCC1N=C=O OHTRJOZKRSVAOX-UHFFFAOYSA-N 0.000 description 1
- MYXZTICARLPUED-UHFFFAOYSA-N 1,3-diisocyanatocyclobutane Chemical compound O=C=NC1CC(N=C=O)C1 MYXZTICARLPUED-UHFFFAOYSA-N 0.000 description 1
- ALQLPWJFHRMHIU-UHFFFAOYSA-N 1,4-diisocyanatobenzene Chemical compound O=C=NC1=CC=C(N=C=O)C=C1 ALQLPWJFHRMHIU-UHFFFAOYSA-N 0.000 description 1
- CDMDQYCEEKCBGR-UHFFFAOYSA-N 1,4-diisocyanatocyclohexane Chemical class O=C=NC1CCC(N=C=O)CC1 CDMDQYCEEKCBGR-UHFFFAOYSA-N 0.000 description 1
- JDLQSLMTBGPZLW-UHFFFAOYSA-N 1-(1-hydroxyethyl)-2,2,6,6-tetramethylpiperidin-4-ol Chemical compound CC(O)N1C(C)(C)CC(O)CC1(C)C JDLQSLMTBGPZLW-UHFFFAOYSA-N 0.000 description 1
- MQQKTNDBASEZSD-UHFFFAOYSA-N 1-(octadecyldisulfanyl)octadecane Chemical compound CCCCCCCCCCCCCCCCCCSSCCCCCCCCCCCCCCCCCC MQQKTNDBASEZSD-UHFFFAOYSA-N 0.000 description 1
- VMDYMJSKWCVEEB-UHFFFAOYSA-N 1-[3,5-bis[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyl]-1,3,5-triazinan-1-yl]-3-(3,5-ditert-butyl-4-hydroxyphenyl)propan-1-one Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)N2CN(CN(C2)C(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)C(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 VMDYMJSKWCVEEB-UHFFFAOYSA-N 0.000 description 1
- NFDXQGNDWIPXQL-UHFFFAOYSA-N 1-cyclooctyldiazocane Chemical compound C1CCCCCCC1N1NCCCCCC1 NFDXQGNDWIPXQL-UHFFFAOYSA-N 0.000 description 1
- AXFVIWBTKYFOCY-UHFFFAOYSA-N 1-n,1-n,3-n,3-n-tetramethylbutane-1,3-diamine Chemical compound CN(C)C(C)CCN(C)C AXFVIWBTKYFOCY-UHFFFAOYSA-N 0.000 description 1
- CERBPMIFGVSKSJ-UHFFFAOYSA-N 1-n,6-n-diacetylhexanedihydrazide Chemical compound CC(=O)N(N)C(=O)CCCCC(=O)N(N)C(C)=O CERBPMIFGVSKSJ-UHFFFAOYSA-N 0.000 description 1
- KEXRSLVRFLEMHJ-UHFFFAOYSA-N 1-o,4-o-bis[(4-tert-butyl-3-hydroxy-2,6-dimethylphenyl)methyl] benzene-1,4-dicarbothioate Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C)=C1COC(=S)C1=CC=C(C(=S)OCC=2C(=C(O)C(=CC=2C)C(C)(C)C)C)C=C1 KEXRSLVRFLEMHJ-UHFFFAOYSA-N 0.000 description 1
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 description 1
- IOHCSOXUCWUZQJ-UHFFFAOYSA-J 2,2'-spirobi[1,3,2-benzodioxastannole] Chemical compound O1c2ccccc2O[Sn]11Oc2ccccc2O1 IOHCSOXUCWUZQJ-UHFFFAOYSA-J 0.000 description 1
- GGPLWEZGITVTJX-UHFFFAOYSA-N 2,2,4-trimethyl-1,4,2-oxazasilinane Chemical compound CN1CCO[Si](C)(C)C1 GGPLWEZGITVTJX-UHFFFAOYSA-N 0.000 description 1
- BWJKLDGAAPQXGO-UHFFFAOYSA-N 2,2,6,6-tetramethyl-4-octadecoxypiperidine Chemical compound CCCCCCCCCCCCCCCCCCOC1CC(C)(C)NC(C)(C)C1 BWJKLDGAAPQXGO-UHFFFAOYSA-N 0.000 description 1
- JVSFQJZRHXAUGT-UHFFFAOYSA-N 2,2-dimethylpropanoyl chloride Chemical compound CC(C)(C)C(Cl)=O JVSFQJZRHXAUGT-UHFFFAOYSA-N 0.000 description 1
- BJELTSYBAHKXRW-UHFFFAOYSA-N 2,4,6-triallyloxy-1,3,5-triazine Chemical compound C=CCOC1=NC(OCC=C)=NC(OCC=C)=N1 BJELTSYBAHKXRW-UHFFFAOYSA-N 0.000 description 1
- UUAIOYWXCDLHKT-UHFFFAOYSA-N 2,4,6-tricyclohexylphenol Chemical compound OC1=C(C2CCCCC2)C=C(C2CCCCC2)C=C1C1CCCCC1 UUAIOYWXCDLHKT-UHFFFAOYSA-N 0.000 description 1
- OSPBEQGPLJSTKW-UHFFFAOYSA-N 2,4,6-tris[(3,5-ditert-butyl-4-hydroxyphenyl)methyl]phenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CC=2C=C(CC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)C(O)=C(CC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)C=2)=C1 OSPBEQGPLJSTKW-UHFFFAOYSA-N 0.000 description 1
- LXWZXEJDKYWBOW-UHFFFAOYSA-N 2,4-ditert-butyl-6-[(3,5-ditert-butyl-2-hydroxyphenyl)methyl]phenol Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC(CC=2C(=C(C=C(C=2)C(C)(C)C)C(C)(C)C)O)=C1O LXWZXEJDKYWBOW-UHFFFAOYSA-N 0.000 description 1
- DXCHWXWXYPEZKM-UHFFFAOYSA-N 2,4-ditert-butyl-6-[1-(3,5-ditert-butyl-2-hydroxyphenyl)ethyl]phenol Chemical compound C=1C(C(C)(C)C)=CC(C(C)(C)C)=C(O)C=1C(C)C1=CC(C(C)(C)C)=CC(C(C)(C)C)=C1O DXCHWXWXYPEZKM-UHFFFAOYSA-N 0.000 description 1
- CZNRFEXEPBITDS-UHFFFAOYSA-N 2,5-bis(2-methylbutan-2-yl)benzene-1,4-diol Chemical compound CCC(C)(C)C1=CC(O)=C(C(C)(C)CC)C=C1O CZNRFEXEPBITDS-UHFFFAOYSA-N 0.000 description 1
- DVQDEYTXFHYBNP-UHFFFAOYSA-N 2,5-di(pentan-2-yl)phenol Chemical compound CCCC(C)C1=CC=C(C(C)CCC)C(O)=C1 DVQDEYTXFHYBNP-UHFFFAOYSA-N 0.000 description 1
- HZSSKAQAXMTSHT-UHFFFAOYSA-N 2,5-ditert-butyl-4-(dimethoxyphosphorylmethyl)phenol Chemical compound COP(=O)(OC)CC1=CC(C(C)(C)C)=C(O)C=C1C(C)(C)C HZSSKAQAXMTSHT-UHFFFAOYSA-N 0.000 description 1
- FLLRQABPKFCXSO-UHFFFAOYSA-N 2,5-ditert-butyl-4-methoxyphenol Chemical compound COC1=CC(C(C)(C)C)=C(O)C=C1C(C)(C)C FLLRQABPKFCXSO-UHFFFAOYSA-N 0.000 description 1
- JFGVTUJBHHZRAB-UHFFFAOYSA-N 2,6-Di-tert-butyl-1,4-benzenediol Chemical compound CC(C)(C)C1=CC(O)=CC(C(C)(C)C)=C1O JFGVTUJBHHZRAB-UHFFFAOYSA-N 0.000 description 1
- RPLXHDXNCZNHRA-UHFFFAOYSA-N 2,6-bis(dodecylsulfanylmethyl)-4-nonylphenol Chemical compound CCCCCCCCCCCCSCC1=CC(CCCCCCCCC)=CC(CSCCCCCCCCCCCC)=C1O RPLXHDXNCZNHRA-UHFFFAOYSA-N 0.000 description 1
- LKALLEFLBKHPTQ-UHFFFAOYSA-N 2,6-bis[(3-tert-butyl-2-hydroxy-5-methylphenyl)methyl]-4-methylphenol Chemical compound OC=1C(CC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=CC(C)=CC=1CC1=CC(C)=CC(C(C)(C)C)=C1O LKALLEFLBKHPTQ-UHFFFAOYSA-N 0.000 description 1
- FRAQIHUDFAFXHT-UHFFFAOYSA-N 2,6-dicyclopentyl-4-methylphenol Chemical compound OC=1C(C2CCCC2)=CC(C)=CC=1C1CCCC1 FRAQIHUDFAFXHT-UHFFFAOYSA-N 0.000 description 1
- JBYWTKPHBLYYFJ-UHFFFAOYSA-N 2,6-ditert-butyl-4-(2-methylpropyl)phenol Chemical compound CC(C)CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 JBYWTKPHBLYYFJ-UHFFFAOYSA-N 0.000 description 1
- GJDRKHHGPHLVNI-UHFFFAOYSA-N 2,6-ditert-butyl-4-(diethoxyphosphorylmethyl)phenol Chemical compound CCOP(=O)(OCC)CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 GJDRKHHGPHLVNI-UHFFFAOYSA-N 0.000 description 1
- SCXYLTWTWUGEAA-UHFFFAOYSA-N 2,6-ditert-butyl-4-(methoxymethyl)phenol Chemical compound COCC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 SCXYLTWTWUGEAA-UHFFFAOYSA-N 0.000 description 1
- HWCZIOQRLAPHDF-UHFFFAOYSA-N 2,6-ditert-butyl-4-[(3,5-ditert-butyl-4-hydroxyphenyl)methoxymethyl]phenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(COCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 HWCZIOQRLAPHDF-UHFFFAOYSA-N 0.000 description 1
- QHPKIUDQDCWRKO-UHFFFAOYSA-N 2,6-ditert-butyl-4-[2-(3,5-ditert-butyl-4-hydroxyphenyl)propan-2-yl]phenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(C(C)(C)C=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 QHPKIUDQDCWRKO-UHFFFAOYSA-N 0.000 description 1
- FURXDDVXYNEWJD-UHFFFAOYSA-N 2,6-ditert-butyl-4-[[4-(3,5-ditert-butyl-4-hydroxyanilino)-6-octylsulfanyl-1,3,5-triazin-2-yl]amino]phenol Chemical compound N=1C(NC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=NC(SCCCCCCCC)=NC=1NC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 FURXDDVXYNEWJD-UHFFFAOYSA-N 0.000 description 1
- JMCKNCBUBGMWAY-UHFFFAOYSA-N 2,6-ditert-butyl-4-[[4-(3,5-ditert-butyl-4-hydroxyphenoxy)-6-octylsulfanyl-1,3,5-triazin-2-yl]oxy]phenol Chemical compound N=1C(OC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=NC(SCCCCCCCC)=NC=1OC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 JMCKNCBUBGMWAY-UHFFFAOYSA-N 0.000 description 1
- RTOZVEXLKURGKW-UHFFFAOYSA-N 2,6-ditert-butyl-4-[[4-[(3,5-ditert-butyl-4-hydroxyphenyl)methyl]-2,3,5,6-tetramethylphenyl]methyl]phenol Chemical compound CC=1C(C)=C(CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)C(C)=C(C)C=1CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 RTOZVEXLKURGKW-UHFFFAOYSA-N 0.000 description 1
- LBOGPIWNHXHYHN-UHFFFAOYSA-N 2-(2-hydroxy-5-octylphenyl)sulfanyl-4-octylphenol Chemical compound CCCCCCCCC1=CC=C(O)C(SC=2C(=CC=C(CCCCCCCC)C=2)O)=C1 LBOGPIWNHXHYHN-UHFFFAOYSA-N 0.000 description 1
- DFYQRCOZAAHDOU-UHFFFAOYSA-N 2-(2-hydroxyethoxy)ethanol;2-[2-(2-hydroxyethoxy)ethoxy]ethanol Chemical compound OCCOCCO.OCCOCCOCCO DFYQRCOZAAHDOU-UHFFFAOYSA-N 0.000 description 1
- JECYNCQXXKQDJN-UHFFFAOYSA-N 2-(2-methylhexan-2-yloxymethyl)oxirane Chemical compound CCCCC(C)(C)OCC1CO1 JECYNCQXXKQDJN-UHFFFAOYSA-N 0.000 description 1
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 1
- PLQQATDGWPYICR-UHFFFAOYSA-N 2-(3-tert-butyl-4-hydroxyphenyl)-2-hydroxyacetic acid Chemical compound CC(C)(C)C1=CC(C(O)C(O)=O)=CC=C1O PLQQATDGWPYICR-UHFFFAOYSA-N 0.000 description 1
- AIDZEBURWFUXBF-UHFFFAOYSA-N 2-(4-butoxyphenyl)-2-hydroxyacetic acid Chemical compound CCCCOC1=CC=C(C(O)C(O)=O)C=C1 AIDZEBURWFUXBF-UHFFFAOYSA-N 0.000 description 1
- HLVSZJXMJIOGRO-UHFFFAOYSA-N 2-(4-cyclohexyloxyphenyl)-2-hydroxyacetic acid Chemical compound C1=CC(C(C(O)=O)O)=CC=C1OC1CCCCC1 HLVSZJXMJIOGRO-UHFFFAOYSA-N 0.000 description 1
- QWCRGALPJIRGTD-UHFFFAOYSA-N 2-(4-ethoxyphenyl)-2-hydroxyacetic acid Chemical compound CCOC1=CC=C(C(O)C(O)=O)C=C1 QWCRGALPJIRGTD-UHFFFAOYSA-N 0.000 description 1
- XHSYHDYCRPFUPK-UHFFFAOYSA-N 2-(4-hexoxyphenyl)-2-hydroxyacetic acid Chemical compound CCCCCCOC1=CC=C(C(O)C(O)=O)C=C1 XHSYHDYCRPFUPK-UHFFFAOYSA-N 0.000 description 1
- ZMWRRFHBXARRRT-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-4,6-bis(2-methylbutan-2-yl)phenol Chemical compound CCC(C)(C)C1=CC(C(C)(C)CC)=CC(N2N=C3C=CC=CC3=N2)=C1O ZMWRRFHBXARRRT-UHFFFAOYSA-N 0.000 description 1
- LHPPDQUVECZQSW-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-4,6-ditert-butylphenol Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC(N2N=C3C=CC=CC3=N2)=C1O LHPPDQUVECZQSW-UHFFFAOYSA-N 0.000 description 1
- IYAZLDLPUNDVAG-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-4-(2,4,4-trimethylpentan-2-yl)phenol Chemical compound CC(C)(C)CC(C)(C)C1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 IYAZLDLPUNDVAG-UHFFFAOYSA-N 0.000 description 1
- ITLDHFORLZTRJI-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-5-octoxyphenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1N1N=C2C=CC=CC2=N1 ITLDHFORLZTRJI-UHFFFAOYSA-N 0.000 description 1
- RTNVDKBRTXEWQE-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-6-butan-2-yl-4-tert-butylphenol Chemical compound CCC(C)C1=CC(C(C)(C)C)=CC(N2N=C3C=CC=CC3=N2)=C1O RTNVDKBRTXEWQE-UHFFFAOYSA-N 0.000 description 1
- XQESJWNDTICJHW-UHFFFAOYSA-N 2-[(2-hydroxy-5-methyl-3-nonylphenyl)methyl]-4-methyl-6-nonylphenol Chemical compound CCCCCCCCCC1=CC(C)=CC(CC=2C(=C(CCCCCCCCC)C=C(C)C=2)O)=C1O XQESJWNDTICJHW-UHFFFAOYSA-N 0.000 description 1
- YQQAAUCBTNZUQQ-UHFFFAOYSA-N 2-[1-(2-hydroxy-3,5-dimethylphenyl)butyl]-4,6-dimethylphenol Chemical compound C=1C(C)=CC(C)=C(O)C=1C(CCC)C1=CC(C)=CC(C)=C1O YQQAAUCBTNZUQQ-UHFFFAOYSA-N 0.000 description 1
- FESJNIGBEZWAIB-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-(2-hydroxy-3-octoxypropoxy)phenol Chemical compound OC1=CC(OCC(O)COCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 FESJNIGBEZWAIB-UHFFFAOYSA-N 0.000 description 1
- BZQCIHBFVOTXRU-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-(3-butoxy-2-hydroxypropoxy)phenol Chemical compound OC1=CC(OCC(O)COCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 BZQCIHBFVOTXRU-UHFFFAOYSA-N 0.000 description 1
- ZSSVCEUEVMALRD-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-(octyloxy)phenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 ZSSVCEUEVMALRD-UHFFFAOYSA-N 0.000 description 1
- DBYBHKQEHCYBQV-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-dodecoxyphenol Chemical compound OC1=CC(OCCCCCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 DBYBHKQEHCYBQV-UHFFFAOYSA-N 0.000 description 1
- WPMUMRCRKFBYIH-UHFFFAOYSA-N 2-[4,6-bis(2-hydroxy-4-octoxyphenyl)-1,3,5-triazin-2-yl]-5-octoxyphenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(OCCCCCCCC)=CC=2)O)=NC(C=2C(=CC(OCCCCCCCC)=CC=2)O)=N1 WPMUMRCRKFBYIH-UHFFFAOYSA-N 0.000 description 1
- NPUPWUDXQCOMBF-UHFFFAOYSA-N 2-[4,6-bis(4-methylphenyl)-1,3,5-triazin-2-yl]-5-octoxyphenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1C1=NC(C=2C=CC(C)=CC=2)=NC(C=2C=CC(C)=CC=2)=N1 NPUPWUDXQCOMBF-UHFFFAOYSA-N 0.000 description 1
- HHIVRACNDKRDTF-UHFFFAOYSA-N 2-[4-(2,4-dimethylphenyl)-6-(2-hydroxy-4-propoxyphenyl)-1,3,5-triazin-2-yl]-5-propoxyphenol Chemical compound OC1=CC(OCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(OCCC)=CC=2)O)=N1 HHIVRACNDKRDTF-UHFFFAOYSA-N 0.000 description 1
- HHPDFYDITNAMAM-UHFFFAOYSA-N 2-[cyclohexyl(2-hydroxyethyl)amino]ethanol Chemical compound OCCN(CCO)C1CCCCC1 HHPDFYDITNAMAM-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- BJOUYEJIPJSCNW-UHFFFAOYSA-N 2-butyl-2-[(3,5-ditert-butyl-2-hydroxyphenyl)methyl]propanedioic acid Chemical compound CCCCC(C(O)=O)(C(O)=O)CC1=CC(C(C)(C)C)=CC(C(C)(C)C)=C1O BJOUYEJIPJSCNW-UHFFFAOYSA-N 0.000 description 1
- UIXRDRQSWYSVNK-UHFFFAOYSA-N 2-butyl-4,6-dimethylphenol Chemical compound CCCCC1=CC(C)=CC(C)=C1O UIXRDRQSWYSVNK-UHFFFAOYSA-N 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- AKNMPWVTPUHKCG-UHFFFAOYSA-N 2-cyclohexyl-6-[(3-cyclohexyl-2-hydroxy-5-methylphenyl)methyl]-4-methylphenol Chemical compound OC=1C(C2CCCCC2)=CC(C)=CC=1CC(C=1O)=CC(C)=CC=1C1CCCCC1 AKNMPWVTPUHKCG-UHFFFAOYSA-N 0.000 description 1
- WBIQQQGBSDOWNP-UHFFFAOYSA-N 2-dodecylbenzenesulfonic acid Chemical compound CCCCCCCCCCCCC1=CC=CC=C1S(O)(=O)=O WBIQQQGBSDOWNP-UHFFFAOYSA-N 0.000 description 1
- ZPIRWAHWDCHWLM-UHFFFAOYSA-N 2-dodecylsulfanylethanol Chemical compound CCCCCCCCCCCCSCCO ZPIRWAHWDCHWLM-UHFFFAOYSA-N 0.000 description 1
- NCWTZPKMFNRUAK-UHFFFAOYSA-N 2-ethyl-4,6-bis(octylsulfanylmethyl)phenol Chemical compound CCCCCCCCSCC1=CC(CC)=C(O)C(CSCCCCCCCC)=C1 NCWTZPKMFNRUAK-UHFFFAOYSA-N 0.000 description 1
- 125000006176 2-ethylbutyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- TWRACJAECSIJHY-UHFFFAOYSA-N 2-hydroxy-2-(4-hydroxy-2-methyl-3-propan-2-ylphenyl)acetic acid Chemical compound CC(C)C1=C(O)C=CC(C(O)C(O)=O)=C1C TWRACJAECSIJHY-UHFFFAOYSA-N 0.000 description 1
- RBQYTVXHDIGUCS-UHFFFAOYSA-N 2-hydroxy-2-(4-hydroxy-3-methylphenyl)acetic acid Chemical compound CC1=CC(C(O)C(O)=O)=CC=C1O RBQYTVXHDIGUCS-UHFFFAOYSA-N 0.000 description 1
- CPJIBSRAXFIORV-UHFFFAOYSA-N 2-hydroxy-2-(4-methoxy-3,5-dimethylphenyl)acetic acid Chemical compound COC1=C(C)C=C(C(O)C(O)=O)C=C1C CPJIBSRAXFIORV-UHFFFAOYSA-N 0.000 description 1
- YCUMCHOROBWGAS-UHFFFAOYSA-N 2-hydroxy-2-(4-octadecoxyphenyl)acetic acid Chemical compound CCCCCCCCCCCCCCCCCCOC1=CC=C(C(O)C(O)=O)C=C1 YCUMCHOROBWGAS-UHFFFAOYSA-N 0.000 description 1
- NEVRBTWYCJLPLD-UHFFFAOYSA-N 2-hydroxy-2-(4-octoxyphenyl)acetic acid Chemical compound CCCCCCCCOC1=CC=C(C(O)C(O)=O)C=C1 NEVRBTWYCJLPLD-UHFFFAOYSA-N 0.000 description 1
- BQKGHWPYMKEBPM-UHFFFAOYSA-N 2-hydroxy-2-(4-prop-2-ynoxyphenyl)acetic acid Chemical compound OC(=O)C(O)C1=CC=C(OCC#C)C=C1 BQKGHWPYMKEBPM-UHFFFAOYSA-N 0.000 description 1
- MZZYGYNZAOVRTG-UHFFFAOYSA-N 2-hydroxy-n-(1h-1,2,4-triazol-5-yl)benzamide Chemical compound OC1=CC=CC=C1C(=O)NC1=NC=NN1 MZZYGYNZAOVRTG-UHFFFAOYSA-N 0.000 description 1
- WBJWXIQDBDZMAW-UHFFFAOYSA-N 2-hydroxynaphthalene-1-carbonyl chloride Chemical compound C1=CC=CC2=C(C(Cl)=O)C(O)=CC=C21 WBJWXIQDBDZMAW-UHFFFAOYSA-N 0.000 description 1
- QOBAIZKSUYMWJZ-UHFFFAOYSA-N 2-methoxycarbonyl-3-(4-methoxyphenyl)prop-2-enoic acid Chemical compound COC(=O)C(C(O)=O)=CC1=CC=C(OC)C=C1 QOBAIZKSUYMWJZ-UHFFFAOYSA-N 0.000 description 1
- LXBGSDVWAMZHDD-UHFFFAOYSA-N 2-methyl-1h-imidazole Chemical compound CC1=NC=CN1 LXBGSDVWAMZHDD-UHFFFAOYSA-N 0.000 description 1
- GAODDBNJCKQQDY-UHFFFAOYSA-N 2-methyl-4,6-bis(octylsulfanylmethyl)phenol Chemical compound CCCCCCCCSCC1=CC(C)=C(O)C(CSCCCCCCCC)=C1 GAODDBNJCKQQDY-UHFFFAOYSA-N 0.000 description 1
- VSKJLJHPAFKHBX-UHFFFAOYSA-N 2-methylbuta-1,3-diene;styrene Chemical compound CC(=C)C=C.C=CC1=CC=CC=C1.C=CC1=CC=CC=C1 VSKJLJHPAFKHBX-UHFFFAOYSA-N 0.000 description 1
- 125000003229 2-methylhexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- ZYJXQDCMXTWHIV-UHFFFAOYSA-N 2-tert-butyl-4,6-bis(octylsulfanylmethyl)phenol Chemical compound CCCCCCCCSCC1=CC(CSCCCCCCCC)=C(O)C(C(C)(C)C)=C1 ZYJXQDCMXTWHIV-UHFFFAOYSA-N 0.000 description 1
- YFHKLSPMRRWLKI-UHFFFAOYSA-N 2-tert-butyl-4-(3-tert-butyl-4-hydroxy-5-methylphenyl)sulfanyl-6-methylphenol Chemical compound CC(C)(C)C1=C(O)C(C)=CC(SC=2C=C(C(O)=C(C)C=2)C(C)(C)C)=C1 YFHKLSPMRRWLKI-UHFFFAOYSA-N 0.000 description 1
- WYFBLIAPFJXCBF-UHFFFAOYSA-N 2-tert-butyl-4-(dioctadecoxyphosphorylmethyl)-6-methylphenol Chemical compound CCCCCCCCCCCCCCCCCCOP(=O)(OCCCCCCCCCCCCCCCCCC)CC1=CC(C)=C(O)C(C(C)(C)C)=C1 WYFBLIAPFJXCBF-UHFFFAOYSA-N 0.000 description 1
- RKLRVTKRKFEVQG-UHFFFAOYSA-N 2-tert-butyl-4-[(3-tert-butyl-4-hydroxy-5-methylphenyl)methyl]-6-methylphenol Chemical compound CC(C)(C)C1=C(O)C(C)=CC(CC=2C=C(C(O)=C(C)C=2)C(C)(C)C)=C1 RKLRVTKRKFEVQG-UHFFFAOYSA-N 0.000 description 1
- BCHSGIGAOYQMPC-UHFFFAOYSA-N 2-tert-butyl-4-[1-(5-tert-butyl-4-hydroxy-2-methylphenyl)-3-dodecylsulfanylbutyl]-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(CC(C)SCCCCCCCCCCCC)C1=CC(C(C)(C)C)=C(O)C=C1C BCHSGIGAOYQMPC-UHFFFAOYSA-N 0.000 description 1
- PFANXOISJYKQRP-UHFFFAOYSA-N 2-tert-butyl-4-[1-(5-tert-butyl-4-hydroxy-2-methylphenyl)butyl]-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(CCC)C1=CC(C(C)(C)C)=C(O)C=C1C PFANXOISJYKQRP-UHFFFAOYSA-N 0.000 description 1
- JJBOJSJSDIRUGY-UHFFFAOYSA-N 2-tert-butyl-4-[2-(5-tert-butyl-4-hydroxy-2-methylphenyl)-4-dodecylsulfanylbutan-2-yl]-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(C)(CCSCCCCCCCCCCCC)C1=CC(C(C)(C)C)=C(O)C=C1C JJBOJSJSDIRUGY-UHFFFAOYSA-N 0.000 description 1
- XMUNJUUYEJAAHG-UHFFFAOYSA-N 2-tert-butyl-5-methyl-4-[1,5,5-tris(5-tert-butyl-4-hydroxy-2-methylphenyl)pentyl]phenol Chemical compound CC1=CC(O)=C(C(C)(C)C)C=C1C(C=1C(=CC(O)=C(C=1)C(C)(C)C)C)CCCC(C=1C(=CC(O)=C(C=1)C(C)(C)C)C)C1=CC(C(C)(C)C)=C(O)C=C1C XMUNJUUYEJAAHG-UHFFFAOYSA-N 0.000 description 1
- MQWCQFCZUNBTCM-UHFFFAOYSA-N 2-tert-butyl-6-(3-tert-butyl-2-hydroxy-5-methylphenyl)sulfanyl-4-methylphenol Chemical compound CC(C)(C)C1=CC(C)=CC(SC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=C1O MQWCQFCZUNBTCM-UHFFFAOYSA-N 0.000 description 1
- GPNYZBKIGXGYNU-UHFFFAOYSA-N 2-tert-butyl-6-[(3-tert-butyl-5-ethyl-2-hydroxyphenyl)methyl]-4-ethylphenol Chemical compound CC(C)(C)C1=CC(CC)=CC(CC=2C(=C(C=C(CC)C=2)C(C)(C)C)O)=C1O GPNYZBKIGXGYNU-UHFFFAOYSA-N 0.000 description 1
- UHLYPUYAVHSKBN-UHFFFAOYSA-N 2-tert-butyl-6-[1-[3-tert-butyl-2-hydroxy-5-(2-methylpropyl)phenyl]ethyl]-4-(2-methylpropyl)phenol Chemical compound CC(C)(C)C1=CC(CC(C)C)=CC(C(C)C=2C(=C(C=C(CC(C)C)C=2)C(C)(C)C)O)=C1O UHLYPUYAVHSKBN-UHFFFAOYSA-N 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- ODJQKYXPKWQWNK-UHFFFAOYSA-N 3,3'-Thiobispropanoic acid Chemical compound OC(=O)CCSCCC(O)=O ODJQKYXPKWQWNK-UHFFFAOYSA-N 0.000 description 1
- GUCMKIKYKIHUTM-UHFFFAOYSA-N 3,3,5,5-tetramethyl-1-[2-(3,3,5,5-tetramethyl-2-oxopiperazin-1-yl)ethyl]piperazin-2-one Chemical compound O=C1C(C)(C)NC(C)(C)CN1CCN1C(=O)C(C)(C)NC(C)(C)C1 GUCMKIKYKIHUTM-UHFFFAOYSA-N 0.000 description 1
- AIBRSVLEQRWAEG-UHFFFAOYSA-N 3,9-bis(2,4-ditert-butylphenoxy)-2,4,8,10-tetraoxa-3,9-diphosphaspiro[5.5]undecane Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC=C1OP1OCC2(COP(OC=3C(=CC(=CC=3)C(C)(C)C)C(C)(C)C)OC2)CO1 AIBRSVLEQRWAEG-UHFFFAOYSA-N 0.000 description 1
- YLUZWKKWWSCRSR-UHFFFAOYSA-N 3,9-bis(8-methylnonoxy)-2,4,8,10-tetraoxa-3,9-diphosphaspiro[5.5]undecane Chemical compound C1OP(OCCCCCCCC(C)C)OCC21COP(OCCCCCCCC(C)C)OC2 YLUZWKKWWSCRSR-UHFFFAOYSA-N 0.000 description 1
- PZRWFKGUFWPFID-UHFFFAOYSA-N 3,9-dioctadecoxy-2,4,8,10-tetraoxa-3,9-diphosphaspiro[5.5]undecane Chemical compound C1OP(OCCCCCCCCCCCCCCCCCC)OCC21COP(OCCCCCCCCCCCCCCCCCC)OC2 PZRWFKGUFWPFID-UHFFFAOYSA-N 0.000 description 1
- PYSRRFNXTXNWCD-UHFFFAOYSA-N 3-(2-phenylethenyl)furan-2,5-dione Chemical compound O=C1OC(=O)C(C=CC=2C=CC=CC=2)=C1 PYSRRFNXTXNWCD-UHFFFAOYSA-N 0.000 description 1
- KJEKRODBOPOEGG-UHFFFAOYSA-N 3-(3,5-ditert-butyl-4-hydroxyphenyl)-n-[3-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoylamino]propyl]propanamide Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)NCCCNC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 KJEKRODBOPOEGG-UHFFFAOYSA-N 0.000 description 1
- WPMYUUITDBHVQZ-UHFFFAOYSA-M 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CC(C)(C)C1=CC(CCC([O-])=O)=CC(C(C)(C)C)=C1O WPMYUUITDBHVQZ-UHFFFAOYSA-M 0.000 description 1
- WPMYUUITDBHVQZ-UHFFFAOYSA-N 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoic acid Chemical compound CC(C)(C)C1=CC(CCC(O)=O)=CC(C(C)(C)C)=C1O WPMYUUITDBHVQZ-UHFFFAOYSA-N 0.000 description 1
- CXHHIIBSROSZSQ-UHFFFAOYSA-N 3-(4-ethoxyphenyl)-5-hydroxy-3h-1-benzofuran-2-one Chemical compound C1=CC(OCC)=CC=C1C1C2=CC(O)=CC=C2OC1=O CXHHIIBSROSZSQ-UHFFFAOYSA-N 0.000 description 1
- YCGKJPVUGMBDDS-UHFFFAOYSA-N 3-(6-azabicyclo[3.1.1]hepta-1(7),2,4-triene-6-carbonyl)benzamide Chemical compound NC(=O)C1=CC=CC(C(=O)N2C=3C=C2C=CC=3)=C1 YCGKJPVUGMBDDS-UHFFFAOYSA-N 0.000 description 1
- OHXAOPZTJOUYKM-UHFFFAOYSA-N 3-Chloro-2-methylpropene Chemical compound CC(=C)CCl OHXAOPZTJOUYKM-UHFFFAOYSA-N 0.000 description 1
- PZMWHOITXWIHBP-UHFFFAOYSA-N 3-[hydroxy(phenyl)methoxy]-3-oxopropanoic acid Chemical class OC(=O)CC(=O)OC(O)C1=CC=CC=C1 PZMWHOITXWIHBP-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000000474 3-butynyl group Chemical group [H]C#CC([H])([H])C([H])([H])* 0.000 description 1
- SAEZGDDJKSBNPT-UHFFFAOYSA-N 3-dodecyl-1-(1,2,2,6,6-pentamethylpiperidin-4-yl)pyrrolidine-2,5-dione Chemical compound O=C1C(CCCCCCCCCCCC)CC(=O)N1C1CC(C)(C)N(C)C(C)(C)C1 SAEZGDDJKSBNPT-UHFFFAOYSA-N 0.000 description 1
- FBIXXCXCZOZFCO-UHFFFAOYSA-N 3-dodecyl-1-(2,2,6,6-tetramethylpiperidin-4-yl)pyrrolidine-2,5-dione Chemical compound O=C1C(CCCCCCCCCCCC)CC(=O)N1C1CC(C)(C)NC(C)(C)C1 FBIXXCXCZOZFCO-UHFFFAOYSA-N 0.000 description 1
- UPMLOUAZCHDJJD-UHFFFAOYSA-N 4,4'-Diphenylmethane Diisocyanate Chemical compound C1=CC(N=C=O)=CC=C1CC1=CC=C(N=C=O)C=C1 UPMLOUAZCHDJJD-UHFFFAOYSA-N 0.000 description 1
- MDWVSAYEQPLWMX-UHFFFAOYSA-N 4,4'-Methylenebis(2,6-di-tert-butylphenol) Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 MDWVSAYEQPLWMX-UHFFFAOYSA-N 0.000 description 1
- QRLSTWVLSWCGBT-UHFFFAOYSA-N 4-((4,6-bis(octylthio)-1,3,5-triazin-2-yl)amino)-2,6-di-tert-butylphenol Chemical compound CCCCCCCCSC1=NC(SCCCCCCCC)=NC(NC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=N1 QRLSTWVLSWCGBT-UHFFFAOYSA-N 0.000 description 1
- GQBHYWDCHSZDQU-UHFFFAOYSA-N 4-(2,4,4-trimethylpentan-2-yl)-n-[4-(2,4,4-trimethylpentan-2-yl)phenyl]aniline Chemical compound C1=CC(C(C)(C)CC(C)(C)C)=CC=C1NC1=CC=C(C(C)(C)CC(C)(C)C)C=C1 GQBHYWDCHSZDQU-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- UQAMDAUJTXFNAD-UHFFFAOYSA-N 4-(4,6-dichloro-1,3,5-triazin-2-yl)morpholine Chemical compound ClC1=NC(Cl)=NC(N2CCOCC2)=N1 UQAMDAUJTXFNAD-UHFFFAOYSA-N 0.000 description 1
- VGEJJASMUCILJT-UHFFFAOYSA-N 4-[2-[4,6-bis[2-(3,5-ditert-butyl-4-hydroxyphenyl)ethyl]-1,3,5-triazin-2-yl]ethyl]-2,6-ditert-butylphenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC=2N=C(CCC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)N=C(CCC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)N=2)=C1 VGEJJASMUCILJT-UHFFFAOYSA-N 0.000 description 1
- NLMUXXXNYDOUDZ-UHFFFAOYSA-N 4-[4,4-bis(5-tert-butyl-4-hydroxy-2-sulfanylphenyl)butan-2-yl]-2-tert-butyl-5-sulfanylphenol Chemical compound C(C)(C)(C)C=1C(=CC(=C(C=1)C(CC(C)C1=C(C=C(C(=C1)C(C)(C)C)O)S)C1=C(C=C(C(=C1)C(C)(C)C)O)S)S)O NLMUXXXNYDOUDZ-UHFFFAOYSA-N 0.000 description 1
- FROCQMFXPIROOK-UHFFFAOYSA-N 4-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]benzene-1,3-diol Chemical compound CC1=CC(C)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(O)=CC=2)O)=N1 FROCQMFXPIROOK-UHFFFAOYSA-N 0.000 description 1
- IYUSCCOBICHICG-UHFFFAOYSA-N 4-[[2,4-bis(3,5-ditert-butyl-4-hydroxyphenoxy)-1h-triazin-6-yl]oxy]-2,6-ditert-butylphenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(ON2N=C(OC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)C=C(OC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)N2)=C1 IYUSCCOBICHICG-UHFFFAOYSA-N 0.000 description 1
- BOQNWBDBDUWBMT-UHFFFAOYSA-N 4-[[bis[(3,5-ditert-butyl-4-hydroxyphenyl)methyl]amino]methyl]-2,6-ditert-butylphenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CN(CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 BOQNWBDBDUWBMT-UHFFFAOYSA-N 0.000 description 1
- WTWGHNZAQVTLSQ-UHFFFAOYSA-N 4-butyl-2,6-ditert-butylphenol Chemical compound CCCCC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 WTWGHNZAQVTLSQ-UHFFFAOYSA-N 0.000 description 1
- HVCNXQOWACZAFN-UHFFFAOYSA-N 4-ethylmorpholine Chemical compound CCN1CCOCC1 HVCNXQOWACZAFN-UHFFFAOYSA-N 0.000 description 1
- WSSSPWUEQFSQQG-UHFFFAOYSA-N 4-methyl-1-pentene Chemical compound CC(C)CC=C WSSSPWUEQFSQQG-UHFFFAOYSA-N 0.000 description 1
- UXMKUNDWNZNECH-UHFFFAOYSA-N 4-methyl-2,6-di(nonyl)phenol Chemical compound CCCCCCCCCC1=CC(C)=CC(CCCCCCCCC)=C1O UXMKUNDWNZNECH-UHFFFAOYSA-N 0.000 description 1
- LZAIWKMQABZIDI-UHFFFAOYSA-N 4-methyl-2,6-dioctadecylphenol Chemical compound CCCCCCCCCCCCCCCCCCC1=CC(C)=CC(CCCCCCCCCCCCCCCCCC)=C1O LZAIWKMQABZIDI-UHFFFAOYSA-N 0.000 description 1
- 125000000590 4-methylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- JJHKARPEMHIIQC-UHFFFAOYSA-N 4-octadecoxy-2,6-diphenylphenol Chemical compound C=1C(OCCCCCCCCCCCCCCCCCC)=CC(C=2C=CC=CC=2)=C(O)C=1C1=CC=CC=C1 JJHKARPEMHIIQC-UHFFFAOYSA-N 0.000 description 1
- BBJXKDUAIUJELD-UHFFFAOYSA-N 4-oxo-4-(2,2,6,6-tetramethylpiperidin-1-yl)oxybutanoic acid Chemical compound CC1(C)CCCC(C)(C)N1OC(=O)CCC(O)=O BBJXKDUAIUJELD-UHFFFAOYSA-N 0.000 description 1
- KDVYCTOWXSLNNI-UHFFFAOYSA-N 4-t-Butylbenzoic acid Chemical compound CC(C)(C)C1=CC=C(C(O)=O)C=C1 KDVYCTOWXSLNNI-UHFFFAOYSA-N 0.000 description 1
- ISAVYTVYFVQUDY-UHFFFAOYSA-N 4-tert-Octylphenol Chemical compound CC(C)(C)CC(C)(C)C1=CC=C(O)C=C1 ISAVYTVYFVQUDY-UHFFFAOYSA-N 0.000 description 1
- UWSMKYBKUPAEJQ-UHFFFAOYSA-N 5-Chloro-2-(3,5-di-tert-butyl-2-hydroxyphenyl)-2H-benzotriazole Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC(N2N=C3C=C(Cl)C=CC3=N2)=C1O UWSMKYBKUPAEJQ-UHFFFAOYSA-N 0.000 description 1
- WZZMHDCUKZFCQT-UHFFFAOYSA-N 5h-benzo[d][1,3,2]benzodioxaphosphocine Chemical compound O1POC2=CC=CC=C2CC2=CC=CC=C21 WZZMHDCUKZFCQT-UHFFFAOYSA-N 0.000 description 1
- VPOKLVDHXARWQB-UHFFFAOYSA-N 7,7,9,9-tetramethyl-3-octyl-1,3,8-triazaspiro[4.5]decane-2,4-dione Chemical compound O=C1N(CCCCCCCC)C(=O)NC11CC(C)(C)NC(C)(C)C1 VPOKLVDHXARWQB-UHFFFAOYSA-N 0.000 description 1
- RREANTFLPGEWEN-MBLPBCRHSA-N 7-[4-[[(3z)-3-[4-amino-5-[(3,4,5-trimethoxyphenyl)methyl]pyrimidin-2-yl]imino-5-fluoro-2-oxoindol-1-yl]methyl]piperazin-1-yl]-1-cyclopropyl-6-fluoro-4-oxoquinoline-3-carboxylic acid Chemical compound COC1=C(OC)C(OC)=CC(CC=2C(=NC(\N=C/3C4=CC(F)=CC=C4N(CN4CCN(CC4)C=4C(=CC=5C(=O)C(C(O)=O)=CN(C=5C=4)C4CC4)F)C\3=O)=NC=2)N)=C1 RREANTFLPGEWEN-MBLPBCRHSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- RSWGJHLUYNHPMX-UHFFFAOYSA-N Abietic-Saeure Natural products C12CCC(C(C)C)=CC2=CCC2C1(C)CCCC2(C)C(O)=O RSWGJHLUYNHPMX-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 239000004925 Acrylic resin Substances 0.000 description 1
- 229920000178 Acrylic resin Polymers 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 239000004254 Ammonium phosphate Substances 0.000 description 1
- 239000004114 Ammonium polyphosphate Substances 0.000 description 1
- OGBVRMYSNSKIEF-UHFFFAOYSA-N Benzylphosphonic acid Chemical class OP(O)(=O)CC1=CC=CC=C1 OGBVRMYSNSKIEF-UHFFFAOYSA-N 0.000 description 1
- 229930185605 Bisphenol Natural products 0.000 description 1
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 1
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 1
- LERMQUULPSCGHK-UHFFFAOYSA-N C(C)(=O)OCCCC.C(C)(=O)OCCCC.[Sn] Chemical compound C(C)(=O)OCCCC.C(C)(=O)OCCCC.[Sn] LERMQUULPSCGHK-UHFFFAOYSA-N 0.000 description 1
- LSNKBUYFYZQKQL-UHFFFAOYSA-N C(CCCCC(C)C)OC(CCC1=CC(=C(C(=C1)C(C)(C)C)O)C(C)(C)C)=S Chemical compound C(CCCCC(C)C)OC(CCC1=CC(=C(C(=C1)C(C)(C)C)O)C(C)(C)C)=S LSNKBUYFYZQKQL-UHFFFAOYSA-N 0.000 description 1
- DJXCZMFQIWCJQM-UHFFFAOYSA-N CC1=CC(=CC(=C1O)C)CSCCCCCCCCCCCCCCCCCCOC(=O)C Chemical compound CC1=CC(=CC(=C1O)C)CSCCCCCCCCCCCCCCCCCCOC(=O)C DJXCZMFQIWCJQM-UHFFFAOYSA-N 0.000 description 1
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical class NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 1
- VOPWNXZWBYDODV-UHFFFAOYSA-N Chlorodifluoromethane Chemical compound FC(F)Cl VOPWNXZWBYDODV-UHFFFAOYSA-N 0.000 description 1
- 229920001634 Copolyester Polymers 0.000 description 1
- 239000004338 Dichlorodifluoromethane Substances 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- 239000004593 Epoxy Substances 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 244000043261 Hevea brasiliensis Species 0.000 description 1
- 239000013032 Hydrocarbon resin Substances 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- OKOBUGCCXMIKDM-UHFFFAOYSA-N Irganox 1098 Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)NCCCCCCNC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 OKOBUGCCXMIKDM-UHFFFAOYSA-N 0.000 description 1
- 239000005639 Lauric acid Substances 0.000 description 1
- 229920005863 Lupranol® Polymers 0.000 description 1
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical class [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 1
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 1
- 239000004594 Masterbatch (MB) Substances 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- GYCMBHHDWRMZGG-UHFFFAOYSA-N Methylacrylonitrile Chemical compound CC(=C)C#N GYCMBHHDWRMZGG-UHFFFAOYSA-N 0.000 description 1
- SVYKKECYCPFKGB-UHFFFAOYSA-N N,N-dimethylcyclohexylamine Chemical compound CN(C)C1CCCCC1 SVYKKECYCPFKGB-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- AKNUHUCEWALCOI-UHFFFAOYSA-N N-ethyldiethanolamine Chemical compound OCCN(CC)CCO AKNUHUCEWALCOI-UHFFFAOYSA-N 0.000 description 1
- IGFHQQFPSIBGKE-UHFFFAOYSA-N Nonylphenol Natural products CCCCCCCCCC1=CC=C(O)C=C1 IGFHQQFPSIBGKE-UHFFFAOYSA-N 0.000 description 1
- 229920000571 Nylon 11 Polymers 0.000 description 1
- 229920000299 Nylon 12 Polymers 0.000 description 1
- 229920001007 Nylon 4 Polymers 0.000 description 1
- 229920002292 Nylon 6 Polymers 0.000 description 1
- IWGBGUINMSOOKP-UHFFFAOYSA-N OC1=C(C(=O)CCCCCCCCCCC)C=NN1C1=CC=CC=C1 Chemical compound OC1=C(C(=O)CCCCCCCCCCC)C=NN1C1=CC=CC=C1 IWGBGUINMSOOKP-UHFFFAOYSA-N 0.000 description 1
- RCZRMCMDNRCJSE-UHFFFAOYSA-N OP(O)OP(O)O.C(C)(C)(C)C1=C(C(=CC(=C1)C(C)(C)C)C(C)(C)C)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1C(C)(C)C)C(C)(C)C)C(C)(C)C Chemical compound OP(O)OP(O)O.C(C)(C)(C)C1=C(C(=CC(=C1)C(C)(C)C)C(C)(C)C)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1C(C)(C)C)C(C)(C)C)C(C)(C)C RCZRMCMDNRCJSE-UHFFFAOYSA-N 0.000 description 1
- HFXDDXVWOZZBCG-UHFFFAOYSA-N OP(O)OP(O)O.C(CCCCCCC(C)C)OC(O)(C(CO)(CO)CO)OCCCCCCCC(C)C Chemical compound OP(O)OP(O)O.C(CCCCCCC(C)C)OC(O)(C(CO)(CO)CO)OCCCCCCCC(C)C HFXDDXVWOZZBCG-UHFFFAOYSA-N 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 240000005428 Pistacia lentiscus Species 0.000 description 1
- 239000004962 Polyamide-imide Substances 0.000 description 1
- 229920003006 Polybutadiene acrylonitrile Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 229920000388 Polyphosphate Polymers 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 229920001328 Polyvinylidene chloride Polymers 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- KHPCPRHQVVSZAH-HUOMCSJISA-N Rosin Natural products O(C/C=C/c1ccccc1)[C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 KHPCPRHQVVSZAH-HUOMCSJISA-N 0.000 description 1
- 102100037205 Sal-like protein 2 Human genes 0.000 description 1
- 101710192308 Sal-like protein 2 Proteins 0.000 description 1
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 229920000147 Styrene maleic anhydride Polymers 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 239000004433 Thermoplastic polyurethane Substances 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 239000012963 UV stabilizer Substances 0.000 description 1
- 239000004708 Very-low-density polyethylene Substances 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- FDLQZKYLHJJBHD-UHFFFAOYSA-N [3-(aminomethyl)phenyl]methanamine Chemical compound NCC1=CC=CC(CN)=C1 FDLQZKYLHJJBHD-UHFFFAOYSA-N 0.000 description 1
- YIMQCDZDWXUDCA-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCC(CO)CC1 YIMQCDZDWXUDCA-UHFFFAOYSA-N 0.000 description 1
- BEIOEBMXPVYLRY-UHFFFAOYSA-N [4-[4-bis(2,4-ditert-butylphenoxy)phosphanylphenyl]phenyl]-bis(2,4-ditert-butylphenoxy)phosphane Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC=C1OP(C=1C=CC(=CC=1)C=1C=CC(=CC=1)P(OC=1C(=CC(=CC=1)C(C)(C)C)C(C)(C)C)OC=1C(=CC(=CC=1)C(C)(C)C)C(C)(C)C)OC1=CC=C(C(C)(C)C)C=C1C(C)(C)C BEIOEBMXPVYLRY-UHFFFAOYSA-N 0.000 description 1
- YUDRVAHLXDBKSR-UHFFFAOYSA-N [CH]1CCCCC1 Chemical compound [CH]1CCCCC1 YUDRVAHLXDBKSR-UHFFFAOYSA-N 0.000 description 1
- JJLKTTCRRLHVGL-UHFFFAOYSA-L [acetyloxy(dibutyl)stannyl] acetate Chemical compound CC([O-])=O.CC([O-])=O.CCCC[Sn+2]CCCC JJLKTTCRRLHVGL-UHFFFAOYSA-L 0.000 description 1
- UKLDJPRMSDWDSL-UHFFFAOYSA-L [dibutyl(dodecanoyloxy)stannyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)O[Sn](CCCC)(CCCC)OC(=O)CCCCCCCCCCC UKLDJPRMSDWDSL-UHFFFAOYSA-L 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 150000001253 acrylic acids Chemical class 0.000 description 1
- 229920006243 acrylic copolymer Polymers 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 239000004840 adhesive resin Substances 0.000 description 1
- 229920006223 adhesive resin Polymers 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 229910001854 alkali hydroxide Inorganic materials 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 150000001447 alkali salts Chemical class 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000005250 alkyl acrylate group Chemical group 0.000 description 1
- 150000001347 alkyl bromides Chemical class 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- PYHXGXCGESYPCW-UHFFFAOYSA-N alpha-phenylbenzeneacetic acid Natural products C=1C=CC=CC=1C(C(=O)O)C1=CC=CC=C1 PYHXGXCGESYPCW-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- KVLCHQHEQROXGN-UHFFFAOYSA-N aluminium(1+) Chemical compound [Al+] KVLCHQHEQROXGN-UHFFFAOYSA-N 0.000 description 1
- 229940007076 aluminum cation Drugs 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 229910000148 ammonium phosphate Inorganic materials 0.000 description 1
- 235000019289 ammonium phosphates Nutrition 0.000 description 1
- 235000019826 ammonium polyphosphate Nutrition 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 229910052787 antimony Inorganic materials 0.000 description 1
- WATWJIUSRGPENY-UHFFFAOYSA-N antimony atom Chemical compound [Sb] WATWJIUSRGPENY-UHFFFAOYSA-N 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000004760 aramid Substances 0.000 description 1
- 229920003235 aromatic polyamide Polymers 0.000 description 1
- 239000010425 asbestos Substances 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 239000003899 bactericide agent Substances 0.000 description 1
- UKMSUNONTOPOIO-UHFFFAOYSA-M behenate Chemical compound CCCCCCCCCCCCCCCCCCCCCC([O-])=O UKMSUNONTOPOIO-UHFFFAOYSA-M 0.000 description 1
- 229940116224 behenate Drugs 0.000 description 1
- UTTHLMXOSUFZCQ-UHFFFAOYSA-N benzene-1,3-dicarbohydrazide Chemical compound NNC(=O)C1=CC=CC(C(=O)NN)=C1 UTTHLMXOSUFZCQ-UHFFFAOYSA-N 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 150000001559 benzoic acids Chemical class 0.000 description 1
- KCXMKQUNVWSEMD-UHFFFAOYSA-N benzyl chloride Chemical compound ClCC1=CC=CC=C1 KCXMKQUNVWSEMD-UHFFFAOYSA-N 0.000 description 1
- 229940073608 benzyl chloride Drugs 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 125000006267 biphenyl group Chemical group 0.000 description 1
- VKVSLLBZHYUYHH-UHFFFAOYSA-N bis(2,2,6,6-tetramethyl-1-octoxypiperidin-3-yl) butanedioate Chemical compound CC1(C)N(OCCCCCCCC)C(C)(C)CCC1OC(=O)CCC(=O)OC1C(C)(C)N(OCCCCCCCC)C(C)(C)CC1 VKVSLLBZHYUYHH-UHFFFAOYSA-N 0.000 description 1
- NLMFVJSIGDIJBB-UHFFFAOYSA-N bis(2,2,6,6-tetramethyl-1-octoxypiperidin-3-yl) decanedioate Chemical compound CC1(C)N(OCCCCCCCC)C(C)(C)CCC1OC(=O)CCCCCCCCC(=O)OC1C(C)(C)N(OCCCCCCCC)C(C)(C)CC1 NLMFVJSIGDIJBB-UHFFFAOYSA-N 0.000 description 1
- YWDBZVIHZORXHG-UHFFFAOYSA-N bis(2,2,6,6-tetramethylpiperidin-1-yl) decanedioate Chemical compound CC1(C)CCCC(C)(C)N1OC(=O)CCCCCCCCC(=O)ON1C(C)(C)CCCC1(C)C YWDBZVIHZORXHG-UHFFFAOYSA-N 0.000 description 1
- OJZRGIRJHDINMJ-UHFFFAOYSA-N bis(3,5-ditert-butyl-4-hydroxyphenyl) hexanedioate Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(OC(=O)CCCCC(=O)OC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 OJZRGIRJHDINMJ-UHFFFAOYSA-N 0.000 description 1
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 1
- OHJMTUPIZMNBFR-UHFFFAOYSA-N biuret Chemical group NC(=O)NC(N)=O OHJMTUPIZMNBFR-UHFFFAOYSA-N 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- OCWYEMOEOGEQAN-UHFFFAOYSA-N bumetrizole Chemical compound CC(C)(C)C1=CC(C)=CC(N2N=C3C=C(Cl)C=CC3=N2)=C1O OCWYEMOEOGEQAN-UHFFFAOYSA-N 0.000 description 1
- PLOYJEGLPVCRAJ-UHFFFAOYSA-N buta-1,3-diene;prop-2-enoic acid;styrene Chemical compound C=CC=C.OC(=O)C=C.C=CC1=CC=CC=C1 PLOYJEGLPVCRAJ-UHFFFAOYSA-N 0.000 description 1
- HQABUPZFAYXKJW-UHFFFAOYSA-N butan-1-amine Chemical compound CCCCN HQABUPZFAYXKJW-UHFFFAOYSA-N 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- GGAUUQHSCNMCAU-UHFFFAOYSA-N butane-1,2,3,4-tetracarboxylic acid Chemical compound OC(=O)CC(C(O)=O)C(C(O)=O)CC(O)=O GGAUUQHSCNMCAU-UHFFFAOYSA-N 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 150000004648 butanoic acid derivatives Chemical class 0.000 description 1
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical class OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 239000004359 castor oil Substances 0.000 description 1
- 235000019438 castor oil Nutrition 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical compound OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 229920001727 cellulose butyrate Polymers 0.000 description 1
- 229920003086 cellulose ether Polymers 0.000 description 1
- 229920006218 cellulose propionate Polymers 0.000 description 1
- DHZSIQDUYCWNSB-UHFFFAOYSA-N chloroethene;1,1-dichloroethene Chemical compound ClC=C.ClC(Cl)=C DHZSIQDUYCWNSB-UHFFFAOYSA-N 0.000 description 1
- HGAZMNJKRQFZKS-UHFFFAOYSA-N chloroethene;ethenyl acetate Chemical compound ClC=C.CC(=O)OC=C HGAZMNJKRQFZKS-UHFFFAOYSA-N 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 150000001879 copper Chemical class 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 229920006037 cross link polymer Polymers 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 150000001925 cycloalkenes Chemical class 0.000 description 1
- FNIATMYXUPOJRW-UHFFFAOYSA-N cyclohexylidene Chemical group [C]1CCCCC1 FNIATMYXUPOJRW-UHFFFAOYSA-N 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- WTVNFKVGGUWHQC-UHFFFAOYSA-N decane-2,4-dione Chemical compound CCCCCCC(=O)CC(C)=O WTVNFKVGGUWHQC-UHFFFAOYSA-N 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 150000008050 dialkyl sulfates Chemical class 0.000 description 1
- 150000001470 diamides Chemical class 0.000 description 1
- 150000004985 diamines Chemical class 0.000 description 1
- MNNHAPBLZZVQHP-UHFFFAOYSA-N diammonium hydrogen phosphate Chemical compound [NH4+].[NH4+].OP([O-])([O-])=O MNNHAPBLZZVQHP-UHFFFAOYSA-N 0.000 description 1
- 239000012973 diazabicyclooctane Substances 0.000 description 1
- RJGHQTVXGKYATR-UHFFFAOYSA-L dibutyl(dichloro)stannane Chemical compound CCCC[Sn](Cl)(Cl)CCCC RJGHQTVXGKYATR-UHFFFAOYSA-L 0.000 description 1
- JGFBRKRYDCGYKD-UHFFFAOYSA-N dibutyl(oxo)tin Chemical compound CCCC[Sn](=O)CCCC JGFBRKRYDCGYKD-UHFFFAOYSA-N 0.000 description 1
- 239000012975 dibutyltin dilaurate Substances 0.000 description 1
- 235000019404 dichlorodifluoromethane Nutrition 0.000 description 1
- QGBSISYHAICWAH-UHFFFAOYSA-N dicyandiamide Chemical compound NC(N)=NC#N QGBSISYHAICWAH-UHFFFAOYSA-N 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- ZJIPHXXDPROMEF-UHFFFAOYSA-N dihydroxyphosphanyl dihydrogen phosphite Chemical compound OP(O)OP(O)O ZJIPHXXDPROMEF-UHFFFAOYSA-N 0.000 description 1
- 125000005442 diisocyanate group Chemical group 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 239000004205 dimethyl polysiloxane Substances 0.000 description 1
- XXBDWLFCJWSEKW-UHFFFAOYSA-N dimethylbenzylamine Chemical compound CN(C)CC1=CC=CC=C1 XXBDWLFCJWSEKW-UHFFFAOYSA-N 0.000 description 1
- VNSRQBDLLINZJV-UHFFFAOYSA-N dioctadecyl 2,2-bis[(3,5-ditert-butyl-2-hydroxyphenyl)methyl]propanedioate Chemical compound C=1C(C(C)(C)C)=CC(C(C)(C)C)=C(O)C=1CC(C(=O)OCCCCCCCCCCCCCCCCCC)(C(=O)OCCCCCCCCCCCCCCCCCC)CC1=CC(C(C)(C)C)=CC(C(C)(C)C)=C1O VNSRQBDLLINZJV-UHFFFAOYSA-N 0.000 description 1
- LTYMSROWYAPPGB-UHFFFAOYSA-N diphenyl sulfide Chemical class C=1C=CC=CC=1SC1=CC=CC=C1 LTYMSROWYAPPGB-UHFFFAOYSA-N 0.000 description 1
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Polymers C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical group [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- BRWZYZWZBMGMMG-UHFFFAOYSA-J dodecanoate tin(4+) Chemical compound [Sn+4].CCCCCCCCCCCC([O-])=O.CCCCCCCCCCCC([O-])=O.CCCCCCCCCCCC([O-])=O.CCCCCCCCCCCC([O-])=O BRWZYZWZBMGMMG-UHFFFAOYSA-J 0.000 description 1
- 229940060296 dodecylbenzenesulfonic acid Drugs 0.000 description 1
- MCPKSFINULVDNX-UHFFFAOYSA-N drometrizole Chemical compound CC1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 MCPKSFINULVDNX-UHFFFAOYSA-N 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- QHZOMAXECYYXGP-UHFFFAOYSA-N ethene;prop-2-enoic acid Chemical compound C=C.OC(=O)C=C QHZOMAXECYYXGP-UHFFFAOYSA-N 0.000 description 1
- BXOUVIIITJXIKB-UHFFFAOYSA-N ethene;styrene Chemical group C=C.C=CC1=CC=CC=C1 BXOUVIIITJXIKB-UHFFFAOYSA-N 0.000 description 1
- 238000006266 etherification reaction Methods 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- ZUNGGJHBMLMRFJ-UHFFFAOYSA-O ethoxy-hydroxy-oxophosphanium Chemical compound CCO[P+](O)=O ZUNGGJHBMLMRFJ-UHFFFAOYSA-O 0.000 description 1
- UHESRSKEBRADOO-UHFFFAOYSA-N ethyl carbamate;prop-2-enoic acid Chemical class OC(=O)C=C.CCOC(N)=O UHESRSKEBRADOO-UHFFFAOYSA-N 0.000 description 1
- SHZIWNPUGXLXDT-UHFFFAOYSA-N ethyl hexanoate Chemical compound CCCCCC(=O)OCC SHZIWNPUGXLXDT-UHFFFAOYSA-N 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 239000005038 ethylene vinyl acetate Substances 0.000 description 1
- 229920006226 ethylene-acrylic acid Polymers 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 150000002191 fatty alcohols Chemical class 0.000 description 1
- SLGWESQGEUXWJQ-UHFFFAOYSA-N formaldehyde;phenol Chemical compound O=C.OC1=CC=CC=C1 SLGWESQGEUXWJQ-UHFFFAOYSA-N 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000000855 fungicidal effect Effects 0.000 description 1
- 239000000417 fungicide Substances 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 230000026030 halogenation Effects 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- AHAREKHAZNPPMI-UHFFFAOYSA-N hexa-1,3-diene Chemical compound CCC=CC=C AHAREKHAZNPPMI-UHFFFAOYSA-N 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-M hexadecanoate Chemical compound CCCCCCCCCCCCCCCC([O-])=O IPCSVZSSVZVIGE-UHFFFAOYSA-M 0.000 description 1
- RRAMGCGOFNQTLD-UHFFFAOYSA-N hexamethylene diisocyanate Chemical compound O=C=NCCCCCCN=C=O RRAMGCGOFNQTLD-UHFFFAOYSA-N 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 229920005669 high impact polystyrene Polymers 0.000 description 1
- 239000004797 high-impact polystyrene Substances 0.000 description 1
- 150000002429 hydrazines Chemical class 0.000 description 1
- 229920006270 hydrocarbon resin Polymers 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 229920002681 hypalon Polymers 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 239000012774 insulation material Substances 0.000 description 1
- 239000012212 insulator Substances 0.000 description 1
- 150000004694 iodide salts Chemical class 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001261 isocyanato group Chemical group *N=C=O 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 238000004898 kneading Methods 0.000 description 1
- 150000003951 lactams Chemical class 0.000 description 1
- 150000002596 lactones Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 229910052748 manganese Inorganic materials 0.000 description 1
- 239000011572 manganese Substances 0.000 description 1
- 125000002960 margaryl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 1
- 239000006078 metal deactivator Substances 0.000 description 1
- 229910001507 metal halide Inorganic materials 0.000 description 1
- 229910052987 metal hydride Inorganic materials 0.000 description 1
- 150000004681 metal hydrides Chemical class 0.000 description 1
- 229910000000 metal hydroxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 125000005394 methallyl group Chemical group 0.000 description 1
- UJRDRFZCRQNLJM-UHFFFAOYSA-N methyl 3-[3-(benzotriazol-2-yl)-5-tert-butyl-4-hydroxyphenyl]propanoate Chemical compound CC(C)(C)C1=CC(CCC(=O)OC)=CC(N2N=C3C=CC=CC3=N2)=C1O UJRDRFZCRQNLJM-UHFFFAOYSA-N 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- CRVGTESFCCXCTH-UHFFFAOYSA-N methyl diethanolamine Chemical compound OCCN(C)CCO CRVGTESFCCXCTH-UHFFFAOYSA-N 0.000 description 1
- NYBDEQVBEYXMHK-UHFFFAOYSA-N methyl prop-2-enoate;5-phenylpenta-2,4-dienenitrile Chemical compound COC(=O)C=C.N#CC=CC=CC1=CC=CC=C1 NYBDEQVBEYXMHK-UHFFFAOYSA-N 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- GRVDJDISBSALJP-UHFFFAOYSA-N methyloxidanyl Chemical group [O]C GRVDJDISBSALJP-UHFFFAOYSA-N 0.000 description 1
- 239000010445 mica Substances 0.000 description 1
- 229910052618 mica group Inorganic materials 0.000 description 1
- 239000012778 molding material Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- UKJARPDLRWBRAX-UHFFFAOYSA-N n,n'-bis(2,2,6,6-tetramethylpiperidin-4-yl)hexane-1,6-diamine Chemical compound C1C(C)(C)NC(C)(C)CC1NCCCCCCNC1CC(C)(C)NC(C)(C)C1 UKJARPDLRWBRAX-UHFFFAOYSA-N 0.000 description 1
- MJNLXAZOTQSLTM-UHFFFAOYSA-N n-[[[ethylaminomethyl(dimethyl)silyl]oxy-dimethylsilyl]methyl]ethanamine Chemical compound CCNC[Si](C)(C)O[Si](C)(C)CNCC MJNLXAZOTQSLTM-UHFFFAOYSA-N 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- DARUEKWVLGHJJT-UHFFFAOYSA-N n-butyl-1-[4-[4-(butylamino)-2,2,6,6-tetramethylpiperidin-1-yl]-6-chloro-1,3,5-triazin-2-yl]-2,2,6,6-tetramethylpiperidin-4-amine Chemical compound CC1(C)CC(NCCCC)CC(C)(C)N1C1=NC(Cl)=NC(N2C(CC(CC2(C)C)NCCCC)(C)C)=N1 DARUEKWVLGHJJT-UHFFFAOYSA-N 0.000 description 1
- BLBLVDQTHWVGRA-UHFFFAOYSA-N n-butyl-3-[4-[4-(butylamino)-1,2,2,6,6-pentamethylpiperidin-3-yl]-6-chloro-1,3,5-triazin-2-yl]-1,2,2,6,6-pentamethylpiperidin-4-amine Chemical compound CCCCNC1CC(C)(C)N(C)C(C)(C)C1C1=NC(Cl)=NC(C2C(N(C)C(C)(C)CC2NCCCC)(C)C)=N1 BLBLVDQTHWVGRA-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229920005615 natural polymer Polymers 0.000 description 1
- 150000002816 nickel compounds Chemical class 0.000 description 1
- MGFYIUFZLHCRTH-UHFFFAOYSA-N nitrilotriacetic acid Chemical compound OC(=O)CN(CC(O)=O)CC(O)=O MGFYIUFZLHCRTH-UHFFFAOYSA-N 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- SNQQPOLDUKLAAF-UHFFFAOYSA-N nonylphenol Chemical compound CCCCCCCCCC1=CC=CC=C1O SNQQPOLDUKLAAF-UHFFFAOYSA-N 0.000 description 1
- JFNLZVQOOSMTJK-KNVOCYPGSA-N norbornene Chemical compound C1[C@@H]2CC[C@H]1C=C2 JFNLZVQOOSMTJK-KNVOCYPGSA-N 0.000 description 1
- 239000002667 nucleating agent Substances 0.000 description 1
- DMFXLIFZVRXRRR-UHFFFAOYSA-N octyl 3-[3-tert-butyl-5-(5-chlorobenzotriazol-2-yl)-4-hydroxyphenyl]propanoate Chemical compound CC(C)(C)C1=CC(CCC(=O)OCCCCCCCC)=CC(N2N=C3C=C(Cl)C=CC3=N2)=C1O DMFXLIFZVRXRRR-UHFFFAOYSA-N 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 125000001117 oleyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])/C([H])=C([H])\C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000005416 organic matter Substances 0.000 description 1
- 229920000620 organic polymer Polymers 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 238000010525 oxidative degradation reaction Methods 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- 125000000913 palmityl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002958 pentadecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- UKODFQOELJFMII-UHFFFAOYSA-N pentamethyldiethylenetriamine Chemical compound CN(C)CCN(C)CCN(C)C UKODFQOELJFMII-UHFFFAOYSA-N 0.000 description 1
- RGSFGYAAUTVSQA-UHFFFAOYSA-N pentamethylene Natural products C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 1
- 150000002978 peroxides Chemical class 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 150000004707 phenolate Chemical class 0.000 description 1
- 229920001568 phenolic resin Polymers 0.000 description 1
- 229960000969 phenyl salicylate Drugs 0.000 description 1
- ZPNJBTBYIHBSIG-UHFFFAOYSA-N phenyl-(2,2,6,6-tetramethylpiperidin-4-yl)methanone Chemical compound C1C(C)(C)NC(C)(C)CC1C(=O)C1=CC=CC=C1 ZPNJBTBYIHBSIG-UHFFFAOYSA-N 0.000 description 1
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N phenylbenzene Natural products C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 150000003018 phosphorus compounds Chemical class 0.000 description 1
- 239000012994 photoredox catalyst Substances 0.000 description 1
- 125000005498 phthalate group Chemical class 0.000 description 1
- XNGIFLGASWRNHJ-UHFFFAOYSA-L phthalate(2-) Chemical compound [O-]C(=O)C1=CC=CC=C1C([O-])=O XNGIFLGASWRNHJ-UHFFFAOYSA-L 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920001627 poly(4-methyl styrene) Polymers 0.000 description 1
- 229920001084 poly(chloroprene) Polymers 0.000 description 1
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 1
- 229920001643 poly(ether ketone) Polymers 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 229920002312 polyamide-imide Polymers 0.000 description 1
- 229920002480 polybenzimidazole Polymers 0.000 description 1
- 229920001083 polybutene Polymers 0.000 description 1
- 229920001225 polyester resin Polymers 0.000 description 1
- 239000004645 polyester resin Substances 0.000 description 1
- 229920006393 polyether sulfone Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229940068886 polyethylene glycol 300 Drugs 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 229920001195 polyisoprene Polymers 0.000 description 1
- 239000002685 polymerization catalyst Substances 0.000 description 1
- ODGAOXROABLFNM-UHFFFAOYSA-N polynoxylin Chemical compound O=C.NC(N)=O ODGAOXROABLFNM-UHFFFAOYSA-N 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920005996 polystyrene-poly(ethylene-butylene)-polystyrene Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920002620 polyvinyl fluoride Polymers 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 239000003361 porogen Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 125000001844 prenyl group Chemical group [H]C([*])([H])C([H])=C(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000037452 priming Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- SCUZVMOVTVSBLE-UHFFFAOYSA-N prop-2-enenitrile;styrene Chemical compound C=CC#N.C=CC1=CC=CC=C1 SCUZVMOVTVSBLE-UHFFFAOYSA-N 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 230000002787 reinforcement Effects 0.000 description 1
- WBHHMMIMDMUBKC-XLNAKTSKSA-N ricinelaidic acid Chemical compound CCCCCC[C@@H](O)C\C=C\CCCCCCCC(O)=O WBHHMMIMDMUBKC-XLNAKTSKSA-N 0.000 description 1
- WBHHMMIMDMUBKC-QJWNTBNXSA-M ricinoleate Chemical compound CCCCCC[C@@H](O)C\C=C/CCCCCCCC([O-])=O WBHHMMIMDMUBKC-QJWNTBNXSA-M 0.000 description 1
- 229940066675 ricinoleate Drugs 0.000 description 1
- 229960003656 ricinoleic acid Drugs 0.000 description 1
- FEUQNCSVHBHROZ-UHFFFAOYSA-N ricinoleic acid Natural products CCCCCCC(O[Si](C)(C)C)CC=CCCCCCCCC(=O)OC FEUQNCSVHBHROZ-UHFFFAOYSA-N 0.000 description 1
- 229910052895 riebeckite Inorganic materials 0.000 description 1
- 239000005060 rubber Substances 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229940116351 sebacate Drugs 0.000 description 1
- CXMXRPHRNRROMY-UHFFFAOYSA-L sebacate(2-) Chemical compound [O-]C(=O)CCCCCCCCC([O-])=O CXMXRPHRNRROMY-UHFFFAOYSA-L 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 230000035939 shock Effects 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 229910052814 silicon oxide Inorganic materials 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 235000009518 sodium iodide Nutrition 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- NESLWCLHZZISNB-UHFFFAOYSA-M sodium phenolate Chemical compound [Na+].[O-]C1=CC=CC=C1 NESLWCLHZZISNB-UHFFFAOYSA-M 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 238000009987 spinning Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 150000003440 styrenes Chemical class 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000003871 sulfonates Chemical class 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 229910021653 sulphate ion Inorganic materials 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 229920003051 synthetic elastomer Polymers 0.000 description 1
- 239000005061 synthetic rubber Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- KKEYFWRCBNTPAC-UHFFFAOYSA-L terephthalate(2-) Chemical compound [O-]C(=O)C1=CC=C(C([O-])=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-L 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 150000005622 tetraalkylammonium hydroxides Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- 239000004753 textile Substances 0.000 description 1
- 239000003017 thermal stabilizer Substances 0.000 description 1
- 230000008646 thermal stress Effects 0.000 description 1
- 229920002725 thermoplastic elastomer Polymers 0.000 description 1
- 239000012815 thermoplastic material Substances 0.000 description 1
- 229920002803 thermoplastic polyurethane Polymers 0.000 description 1
- 235000019303 thiodipropionic acid Nutrition 0.000 description 1
- IUTCEZPPWBHGIX-UHFFFAOYSA-N tin(2+) Chemical class [Sn+2] IUTCEZPPWBHGIX-UHFFFAOYSA-N 0.000 description 1
- KSBAEPSJVUENNK-UHFFFAOYSA-L tin(ii) 2-ethylhexanoate Chemical class [Sn+2].CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O KSBAEPSJVUENNK-UHFFFAOYSA-L 0.000 description 1
- YONPGGFAJWQGJC-UHFFFAOYSA-K titanium(iii) chloride Chemical compound Cl[Ti](Cl)Cl YONPGGFAJWQGJC-UHFFFAOYSA-K 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- KHPCPRHQVVSZAH-UHFFFAOYSA-N trans-cinnamyl beta-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OCC=CC1=CC=CC=C1 KHPCPRHQVVSZAH-UHFFFAOYSA-N 0.000 description 1
- 238000005809 transesterification reaction Methods 0.000 description 1
- YJGJRYWNNHUESM-UHFFFAOYSA-J triacetyloxystannyl acetate Chemical compound [Sn+4].CC([O-])=O.CC([O-])=O.CC([O-])=O.CC([O-])=O YJGJRYWNNHUESM-UHFFFAOYSA-J 0.000 description 1
- 150000003918 triazines Chemical class 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- CYRMSUTZVYGINF-UHFFFAOYSA-N trichlorofluoromethane Chemical compound FC(Cl)(Cl)Cl CYRMSUTZVYGINF-UHFFFAOYSA-N 0.000 description 1
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- IVIIAEVMQHEPAY-UHFFFAOYSA-N tridodecyl phosphite Chemical compound CCCCCCCCCCCCOP(OCCCCCCCCCCCC)OCCCCCCCCCCCC IVIIAEVMQHEPAY-UHFFFAOYSA-N 0.000 description 1
- IMNIMPAHZVJRPE-UHFFFAOYSA-N triethylenediamine Chemical compound C1CN2CCN1CC2 IMNIMPAHZVJRPE-UHFFFAOYSA-N 0.000 description 1
- 125000005591 trimellitate group Chemical group 0.000 description 1
- CYTQBVOFDCPGCX-UHFFFAOYSA-N trimethyl phosphite Chemical compound COP(OC)OC CYTQBVOFDCPGCX-UHFFFAOYSA-N 0.000 description 1
- CNUJLMSKURPSHE-UHFFFAOYSA-N trioctadecyl phosphite Chemical compound CCCCCCCCCCCCCCCCCCOP(OCCCCCCCCCCCCCCCCCC)OCCCCCCCCCCCCCCCCCC CNUJLMSKURPSHE-UHFFFAOYSA-N 0.000 description 1
- HQUQLFOMPYWACS-UHFFFAOYSA-N tris(2-chloroethyl) phosphate Chemical compound ClCCOP(=O)(OCCCl)OCCCl HQUQLFOMPYWACS-UHFFFAOYSA-N 0.000 description 1
- WGKLOLBTFWFKOD-UHFFFAOYSA-N tris(2-nonylphenyl) phosphite Chemical compound CCCCCCCCCC1=CC=CC=C1OP(OC=1C(=CC=CC=1)CCCCCCCCC)OC1=CC=CC=C1CCCCCCCCC WGKLOLBTFWFKOD-UHFFFAOYSA-N 0.000 description 1
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229920006337 unsaturated polyester resin Polymers 0.000 description 1
- 150000003672 ureas Chemical class 0.000 description 1
- 239000002966 varnish Substances 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 235000019871 vegetable fat Nutrition 0.000 description 1
- 229920001866 very low density polyethylene Polymers 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- XOOUIPVCVHRTMJ-UHFFFAOYSA-L zinc stearate Chemical compound [Zn+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O XOOUIPVCVHRTMJ-UHFFFAOYSA-L 0.000 description 1
- CHJMFFKHPHCQIJ-UHFFFAOYSA-L zinc;octanoate Chemical compound [Zn+2].CCCCCCCC([O-])=O.CCCCCCCC([O-])=O CHJMFFKHPHCQIJ-UHFFFAOYSA-L 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/77—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D307/78—Benzo [b] furans; Hydrogenated benzo [b] furans
- C07D307/82—Benzo [b] furans; Hydrogenated benzo [b] furans with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to carbon atoms of the hetero ring
- C07D307/83—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/04—Oxygen-containing compounds
- C08K5/15—Heterocyclic compounds having oxygen in the ring
- C08K5/151—Heterocyclic compounds having oxygen in the ring having one oxygen atom in the ring
- C08K5/1535—Five-membered rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Furan Compounds (AREA)
Description
APPLICATION DE 3-(ALCOXYPHENYL)BENZOFURANNE-2-ONES COMME STABILISANTS ET NOUVEAUX COMPOSES DE CE TYPE.
La présente invention concerne des compositions contenant une matière organique, de préférence un polymère, et des 3-(alcoxyphényl)benzofuranne-2-ones comme stabilisants, l’utilisation de ceux-ci pour la stabilisation de matières organiques contre la dégradation oxydative, thermique ou induite par la lumière, ainsi que de nouvelles 3-(alcoxyphényl)-benzofuranne-2-ones.
Différents 3-(alcoxyphényl)benzofuranne-2-ones ont été décrites, par exemple par M. Auger et al., Bull. Soc. Chim. Fr. 1970, 4024; L. Jurd, Aust. J. Chem. 21, 347 (1978) et C.S. Foote et al., J. Amer. Chem. Soc. 92, 586 (1973) et dans le DE-A- 3 006 268.
L'utilisation de quelques benzofuranne-2-ones comme stabilisants pour polymères organiques est connue, par exemple dans ÜS-A-4 325 863; US-A-4 338 244 et EP-A-415 887.
Cela étant, les présents inventeurs ont trouvé qu'un groupe particulier de ces benzofuranne-2-ones est particulièrement approprié comme stabilisant pour des matières organiques contre la dégradation oxydative, thermique ou induite par la lumière.
La présente invention concerne donc des compositions contenant a) une matière organique soumise à la dégradation oxydative, thermique ou induite par la lumière et b) au moins un composé répondant à la formule (1):
dans laquelle Ri représente un alkyle Ci-C2s, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle C5-C8 non substitué ou substitué par un alkyle C1-C4; un alcényle C3-C25, un alcynyle C3-C25 ou un alkyle C3-C25 interrompu par l'oxygène, le soufre ou un radical ^N-Ri6, où R16 représente un hydrogène ou un alkyle Ci-Cg, R2, R3, R4 et Rs représentent chacun, indépendamment l'un de l'autre, l'hydrogène, un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle C5-C8 non substitué ou substitué par un alkyle C1-C4; un alcoxyle Ci-Ci8, un hydroxyle, un alcanoyloxyle C1-C25, un alcénoyloxyle C3-C25, un alcanoyloxyle C3-C25 interrompu par l'oxygène, le soufre ou un radical^N-Ri6; un cycloalkylcarbonyloxyle Cg-Cg, un benzoyloxyle ou un benzoyloxyle substitué par un alkyle C1-C12, Ri6 signifiant comme ci-dessus, ou encore les radicaux R2 et R3 ou les radicaux R4 et R5 forment ensemble, et avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4, en outre, représente un groupement - (CH2) n“CORn, où n est égal à 0, à 1 ou à 2, Θ et Ru est un hydroxyle, [-0 1/r M1*], un alcoxyle Ci-Cis
Ri4 et Ris représentant chacun, indépendamment l'un de l'autre, un hydrogène ou un alkyle Ci-Cis, M étant un cation métallique r-valent et r étant égal à 1, 2 ou 3, R7, Rs, R9 et Ri0 représentent chacun, indépendamment l'un de l'autre, un hydrogène, un alkyle C1-C4 ou un alcoxyle C4-C4 à la condition qu'au moins un des radicaux R7, R s, R9 et Ri0 soit l'hydrogène et lorsque R3, R5, R g, R7 et Rio sont de l'hydrogène, R4 signifie, en outre, un radical de la formule (2) :
où Ri, R2, Rs et Rg ont la signification ci-dessus et R12 et R13 représentent, indépendamment l'un de l'autre, l'hydrogène, le CF3, un alkyle C1-C12 ou un phényle, ou R12 et R13 forment ensemble et avec l'atome de C auquel ils sont liés un cycle cycloalkylidène C5-C8 non substitué ou porteur d'un à trois alkyles C1-C4; Rg signifie l'hydrogène ou un radical de la formule (3) :
où Ri, R2, R3/· Ε·4λ rsa R7 r R8r R9 et Rio ont la signification ci-dessus, et le composé de formule (4) étant exclu.
L·'alkyle avec un nombre d'atomes de carbone allant jusqu'à 25 représente un radical ramifié ou non ramifié tel que, par exemple, le méthyle, l'éthyle, le propyle, 1'isopropyle, le n-butyle, le sec-butyle, l'isobutyle, le tert-butyle, le 2-éthylbutyle, le n-pentyle, 11isopentyle, le 1-méthylpentyle, le 1,3-diméthylbutyle, le n-hexyle, le 1-méthylhexyle, le n-heptyle, 1 ' isoheptyle, le 1,1,3,3-tétraméthylbutyle, le 1-méthylheptyle, le 3-méthylheptyle, le n-octyle, le 2-éthylhexyle, le 1,1,3-triméthylhexyle, le 1,1,3,3-tetraméthylpentyle, le nonyle, le décyle, l'undécyle, le 1- méthylundécyle, le dodécyle, le 1,1,3,3,5,5-hexaméthylhexyle,le tridécyle, le tetradécyle, le pentadécyle, 1'hexadécyle, 1'heptadécyle, 11octadécyle, l'eicosyle ou le docosyle. Une des significations préférées de R2 et de R4 est par exemple un alkyle C].-Ci8. Une des significations préférées de R4 est un alkyle Ci~C4.
Un phénylalkyle C7-C9 représente, par exemple, le benzyle, 1’α-méthylbenzyle, 1'α,α-diméthylbenzyle ou le 2- phényléthyle. Le benzyle est préféré.
Le phényle substitué par un alkyle Ci~C4, contenant un nombre de groupes alkyles compris de préférence entre 1 et 3, plus particulièrement égal à 1 ou à 2, représente, par exemple, l'o-, le m- ou le p-méthylphényle, le 2,3-diméthylphényle, le 2,4-diméthylphényle, le 2,5-diméthylphényle, le 2,6-diméthylphényle, le 3,4-diméthylphényle, le 3,5-diméthylphényle, le 2-méthyl-6-éthylphényle, le 4-tert-butylphényle, le 2-éthylphényle ou le 2,6-diéthylphényle.
Un cycloalkyle C5-C8 non substitué ou substitué par un alkyle Ci~C4 représente, par exemple, le cyclopentyle, le méthylcyclopentyle, le diméthylcyclopentyle, le cyclohexyle, le méthylcyclohexyle, le diméthylcyclohexyle, le triméthylcyclohexyle, le tert-butylcyclohexyle, le cycloheptyle ou le cyclooctyle. On préfère le cyclohexyle et le tert-butylcyclohexyle.
Un alcényle avec un nombre d'atomes de carbone compris entre 3 et 25 représente un radical ramifié ou non ramifié tel que, par exemple, le propényle, le 2-butényle, le 3-butényle, 1'isobutényle, le n-2,4-pentadiényle, le 3-méthyl-2-butényle, le n-2-octényle, le n-2-dodecényle, 1'iso-dodecényle, l'oléyle, le n-2-octadecényle ou le n-4-octadecényle.
Un alcynyle comportant un nombre d'atomes de carbone compris entre 3 et 25 représente un radical ramifié ou non ramifié tel que, par exemple, le propynyle (-CH2-C=CH) , le 2-butynyle, le 3-butynyle le n-2-octynyle ou le n-2-dodécynyle.
Un alkyle C3-C25 interrompu par l’oxygène, le soufre ou ^N-Rie représente, par exemple, CH3-O-CH2CH2- , CH3-S-CH2CH2-/ CH3-NH-CH2CH2-, CH3-N (CH3) -CH2CH2-, CH3-O-CH2CH2-O-CH2CH2-, CH3- (0-CH2CH2-) 2O-CH2CH2- , CH3-(0-CH2CH2-)30-CH2CH2- ou CH3-(0-CH2CH2-) 4O-CH2CH2-. On préfère le méthoxy-hexyle.
Un alcoxyle comportant un nombre d’atomes de carbone allant jusqu'à 18 représente un radical ramifié ou non ramifié tel que, par exemple, le méthoxyle, l’éthoxyle, le propoxyle, 1 ’ isopropoxyle, le n-butoxyle, 1’isobutoxyle, le pentoxyle, l’isopentoxyle, l’hexoxyle, l’heptoxyle, l’octoxyle, le décyloxyle, le tetradécyloxyle, l’hexadécyloxyle ou 1’octadécyloxyle.
Un alcanoyloxyle comportant un nombre d’atomes de carbone allant jusqu'à 25 représente un radical ramifié ou non ramifié tel que, par exemple, le formyloxyle, 1’acétyloxyle, le propionyloxyle, le butanoyloxyle, le pentanoyloxyle, 1’hexanoyloxyle, 1’heptanoyloxyle, 1’octanoyloxyle, le nonanoyloxyle, le décanoyloxyle, 1'undécanoyloxyle, le dodécanoyloxyle, le tridécanoyloxyle, le tetradécanoyloxyle, le pentadécanoyloxyle, 1 ’hexadécanoyloxyle, l'heptadécanoyloxyle, l'octadécanoyloxyle, 1’eicosanoyloxyle ou le docosanoyloxyle.
Un alcénoyloxyle comportant un nombre d’atomes de carbone compris entre 3 et 25 représente un radical ramifié ou non ramifié tel que, par exemple, le propénoyloxyle, le 2-buténoyloxyle, le 3-buténoyloxyle, 1'isobuténoyloxyle, le n-2,4-pentadiénoyloxyle, le 3-méthyl-2-buténoyloxyle, le n-2-octénoyloxyle, le n-2- dodécénoyloxyle, 1'iso-dodécénoyloxyle, 1'oléoyloxyle, le n-2-octadécénoyloxyle ou le n-4-octadécénoyloxyle. ün alcanoyloxyle C3-C25 interrompu par l'oxygène, le soufre ou ^N-Ri6 représente, par exemple, ch3-o-ch2-coo-, ch3-s-ch2coo-, ch3-nh-ch2coo-, ch3-n (ch3) -ch2coo-, ch3-o-ch2ch2-o-ch2coo- , ch3- (0-CH2CH2-) 2o-ch2coo-, ch3-(o-ch2ch2-)3o-ch2coo- ou ch3- (0-CH2CH2-) 4o-ch2coo- .
Un cycloalkylcarbonyloxyle C6-C9 représente, par exemple, le cyclopentylcarbonyloxyle, le cyclohexylcarbonyloxyle, le cycloheptylcarbonyloxyle ou le cyclooctylcarbonyloxyle. Le cyclohexylcarbonyloxyle est préféré.
Un benzoyloxyle substitué par un alkyle Ci-Ci2 représente, par exemple, l'o-, le m- ou le p-méthylbenzoyloxyle, le 2,3-diméthylbenzoyloxy, le 2,4-diméthylbenzoyloxy, le 2,5-diméthylbenzoyloxyle, le 2,6-diméthylbenzoyloxyle, le 3,4-diméthylbenzoyloxyle, le 3.5- diméthyIbenzoy1oxy1e , le 2-méthyl-6-éthylbenzoyloxyle, le 4-tert-butylbenzoyloxyle, le 2-éthylbenzoyloxyle, le 2,4,β-triméthylbenzoyloxyle, le 2.6- diméthyl-4-tert-butylbenzoyloxyle ou le 3,5-di-tert-butylbenzoyloxyle.
Le cation métallique mono-, di- ou trivalent est de préférence un cation de métal alcalin ou alcalino-terreux ou d'aluminium, par exemple Na+, K+, Mg++, Ca++ ou Al+++.
Un cycle cycloalkylidène C5-C8 non substitué ou substitué par un alkyle C1-C4, contenant de préférence 1 à 3, plus particulièrement 1 ou 2 radicaux alkyles ramifiés ou non ramifiés, représente, par exemple, le cyclopentylidène, le méthylcyclopentylidène, le diméthylcyclopentylidène, le cyclohexylidène, le méthylcyclohexylidène, le diméthylcyclohexylidène, le triméthylcyclohexylidène, le tert-butylcyclohexylidène, le cycloheptylidène ou le cyclooctylidène. Le cyclohexylidène ou le tert-butylcyclohexylidène sont préférés.
L'intérêt se porte sur les formulations contenant des composés de formule (1) où Rj représente un alkyle Ci-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle Cs-Cg non substitué ou substitué par un alkyle C1-C4; un alcényle C3-C25 ou un alkyle C3-C25 interrompu par l'oxygène, le soufre ou ^N-Ri6 et R12 et Ri 3 représentent, indépendamment l'un de l'autre, un hydrogène, un alkyle Ci-C12 ou un phényle.
D'un intérêt particulier sont des compositions contenant des composés de formule (1) où Ri représente un alkyle C1-C18, un benzyle, un phényle, un phényle substitué par un alkyle C1-C4, un cycloalkyle C5-C8, un alcényle C3-Ci8, un alcynyle C3-Ci8 ou un alkyle C3-Ci8 interrompu par l'oxygène, le soufre ou le > -Ri 6, R2, R31 R4 et R5 représentent, indépendamment l'un de l'autre, un hydrogène, un alkyle Ci-Cis, un benzyle, un phényle, un cycloalkyle Cs-C8, un alcoxyle Ci-C8, un hydroxyle, un alcanoyloxyle Ci-Ci8, un alcénoyloxyle C3~Ci8 ou un benzoyloxyle, R4 représente, en outre, un radical - (CH2) 2~C0Ru, ou les radicaux R2 et R3 ou les radicaux R4 et Rs forment ensemble et avec les atomes de carbone auxquels ils sont liés, un cycle benzénique.
Les compositions où au moins deux des symboles R2, R3, R4 et R5 dans la formule (1) sont l'hydrogène sont des compositions préférées.
Egalement préférées sont les compositions où R3 et R5 dans la formule (1) sont l'hydrogène.
On apprécie beaucoup également les compositions dans lesquelles Ri dans la formule (1) représente un alkyle Ci~Ci8, un benzyle, un phényle, un cyclohexyle, un alcényle C3-C12, un alcynyle C3-C12 ou un alkyle C3~Ci8 interrompu par l'oxygène, R3, R5, R7 et Rio représentent, indépendamment l'un de l'autre, l'hydrogène ou un alkyle C1-C4, R2 représente l'hydrogène, un alkyle Ci~Ci8, un phényle ou un cyclohexyle, ou les radicaux R2 et R3 forment ensemble et avec les atomes de carbone auxquels ils sont liés un cycle benzénique, R4 représente l'hydrogène, un alkyle C1-C12, un phényle, un cyclohexyle, un hydroxyle, un alcanoyloxyle C1-C12, un alcoxyle Ci-Cs ou un radical - (CH2) n-CORn où n est égal à 0, 1 ou 2 et Ru représente un hydroxyle ou un alcoxyle C1-C12, R4 représente, en outre, un radical de la formule (2) :
(2) où Ri, R2, Re et Rg ont les significations indiquées ci-dessus, et Ri2 et Ri3 représentent, indépendamment l'un de l'autre, l'hydrogène, CF3, un alkyle C1-C12 ou un phényle, ou R12 et Ri3 forment ensemble, et avec l'atome de carbone auquel ils sont liés, un cycle cycloalkylidène C5-C8.
Un intérêt particulier se porte sur les compositions où Ri dans la formule (1) représente un alkyle C2-Ci8, un benzyle, un phényle, un phényle substitué par un alkyle C1-C4, un cycloalkyle Cs-Cq, un alcényle C3-Ci8, un alcynyle C3-Ci8 ou un alkyle C3-Ci8 interrompu par l'oxygène, le soufre ou ^2N-Ri6.
ün intérêt particulier se porte également sur les compositions où Ri dans la formule (1) est un méthyle et un des résidus R7, R8, R9 et Rio au moins est autre que 1'hydrogène.
Des compositions où, dans la formule (1) , Ri est un méthyle et R8 un alkyle Ci**C4 ou un alcoxyle C1-C4 sont également préférées .
On apprécie beaucoup aussi les compositions pour lesquelles, dans la formule (1), Ri représent un méthyle.
On apprécie tout particulièrement les compositions où Ri dans la formule (1) représente un alkyle Ci-Ci8, un benzyle, un phényle, un cyclohexyle, un alcényle C3-C4, un alcynyle C3-C4 ou un alkyle C3-C6 interrompu par l'oxygène, R2 représente l'hydrogène, un alkyle Ci-Ci8, un phényle ou un cyclohexyle, R3, R4, R5 et R10 sont l'hydrogène, ou bien les radicaux R2 et R3 forment ensemble, avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4 représente l'hydrogène, un alkyle C1-C6, un phényle, un cyclohexyle, un hydroxyle, un pivaloyloxyle, un alcoxyle C1-C4 ou un radical - (CH2) 2~C0Rii, où Ru représente un alkyle C1-C4, R8 et R9 représentent, indépendamment l'un de l'autre, l'hydrogène, un alkyle C1-C4 ou un alcoxyle 0ι-04ί et, lorsque Rg est un hydrogène, R4 représente, en outre, un radical de la formule (2)
(2) où Rlr R2, R8 et Rg ont une signification identique à celle ci-dessus et R3.2 et R13 représentent, indépendamment l'un de l'autre, CF3 ou un alkyle C1-C4, Rg représente l'hydrogène ou un radical de formule (3)
(3) ou Ri , R2 , R3 , R4 , R5 , R7, Re , R9 et Rio ont la signification ci-dessus.
Les composés de formule (1) conformes à la présente invention sont appropriés à la stabilisation de matières organiques contre la dégradation thermique, oxydative ou induite par la lumière.
On donne ci-dessous des exemples de telles matières : 1. Polymères de mono- ou de dioléfines, tels que le polypropylène, le polyisobutylène, le polybutène, le poly-4-méthylpentène-1, le polyisoprène ou le polybutadiène ainsi que les polymères de cyclooléfines, par exemple du cyclopentène ou du norbornène; ensuite le polyéthylène (qui peut être réticulé), par exemple le polyéthylène de haute densité (HDPE), le polyéthylène de basse densité (LDPE), le polyéthylène linéaire de basse densité (LLDPE), le polyéthylène ramifié de basse densité (VLDPE).
Les polyoléfines, c'est-à-dire les polymères de monooléfines, telles que mentionnées au paragraphe précédent, notamment le polyéthylène et le polypropylène, peuvent être préparés selon différents procédés, en particulier selon les méthodes suivantes : a) par voie radicalaire (habituellement sous haute pression et à haute température).
b) à l'aide d'un catalyseur, celui-ci contenant en général un ou plusieurs métaux du groupe IVb, Vb, VIb ou VIII. Ces métaux possèdent, en général, un ou plusieurs ligands (coordinats), tels que des oxydes, des halogénures, des alcoolates, des esters, des éthers, des amines, des alkyles, des alcényles et/ou des aryles, qui peuvent être liés par coordination π, ou σ. Ces complexes métalliques peuvent être libres ou fixés sur un support tel que, par exemple, le chlorure de magnésium activé, le chlorure de titane(III), l'oxyde d'aluminium ou l'oxyde de silicium. Ces catalyseurs peuvent être solubles ou insolubles dans le milieu de polymérisation. Les catalyseurs peuvent aussi être actifs tels que dans la polymérisation ou on peut utiliser d’autres activateurs, tels que, par exemple, des alkyl-métaux, des hydrures métalliques, des halogénures d'alkyl-métaux, des oxydes d'alkyl-métaux ou des alkyloxanes métalliques, où les métaux sont des éléments des groupes la, lia et/ou Ilia. Les activateurs peuvent être modifiés, par exemple par d'autres groupes esters, éthers, amines ou silyléthers. Ces systèmes catalytiques sont habituellement nommés, catalyseurs Phillips, Standard Oil Indiana, Ziegler(-Natta), TNZ (DuPont), métallocènes ou Single Site Catalysers (SSC).
2. Mélanges de polymères mentionnés au point 1), par exemple mélanges de polypropylène avec du polyisobutylène, de polypropylène avec du polyéthylène (par exemple PP/HDPE, PP/LDPE) et mélanges de différents types de polyéthylène (par exemple LDPE/HDPE).
3. Copolymères de mono- et de dioléfines entre elles ou avec d'autres monomères vinyliques comme, par exemple, les copolymères éthylène-propylène, le polyéthylène linéaire à basse densité (LLDPE) et des mélanges de celui-ci avec le polyéthylène à basse densité (LDPE), les copolymères propylène-butène-1, les copolymères propylène-isobutylène, les copolymères éthylène-butène-1, les copolymères éthylène-hexène, les copolymères éthylène-méthylpentène, les copolymères éthylène-heptène, les copolymères éthylène-octène, les copolymères propylène-butadiène, les copolymères isobutylène-isoprène, les copolymères éthylène-acrylate d'alkyle, les copolymères éthylène-méthacrylate d'alkyle, les copolymères éthylène-acétate de vinyle et leurs copolymères avec le monoxyde de carbone, ou les copolymères éthylène-acide acrylique et leurs sels (ionomères), ainsi que des terpolymères de l’éthylène avec le propylène et avec un diène, tel que l'hexadiène, le dicyclopentadiène ou 1’éthylidène-norbornène; ensuite des mélanges de tels copolymères entre eux et avec les polymères mentionnés en 1), par exemple les mélanges de polypropylène et de copolymères éthylène-propylène de LDPE et de copolymères éthylène-acétate de vinyle, de LDPE et de copolymères éthylène-acide acrylique, de LLDPE et de copolymères éthylène-acétate de vinyle, de LLDPE et de copolymères éthylène-acide acrylique, et des copolymères polyalkylène/monoxyde de carbone construits en alternance ou statistiquement, ainsi que leurs mélanges avec d'autres polymères, tels que des polyamides.
4. Résines hydrocarbures (par exemple C5-C9), y compris leurs modifications hydrogénées (par exemple résines adhésives), et mélanges de polyalkylènes et d'amidon.
5. Polystyrène, poly-(p-méthylstyrène), poly-(a- méthylstyrène).
6. Copolymères de styrène ou d'a-méthylstyrène avec des diènes ou des dérivés acryliques, tels que des copolymères styrène-butadiène, styrène-acrylonitrile, styrène-méthacrylate d'alkyle, styrène-butadiène-acrylate et -méthacrylate d'alkyle, styrène-anhydride maléique, styrène-acrylonitrile-acrylate de méthyle; mélanges hautement résistants au choc de copolymères du styrène et d'un autre polymère tel que, par exemple, un polyacrylate, un polymère de diène ou un terpolymère éthylène-propylène-diène; également des copolymères séquencés du styrène, tels que styrène-butadiène-styrène, styrène-isoprène-styrène, styrène-éthylène /butylène-styrène ou le styrène-éthylène /propylène-styrène .
7. Copolymères greffés de styrène ou d'a-méthylstyrène, tels que styrène sur poly-butadiène, styrène sur copolymères polybutadiène-styrène- ou polybutadiène-acrylonitrile, styrène et acrylonitrile (ou encore méthacrylonitrile) sur polybutadiène; styrène, acrylonitrile et méthacrylate de méthyle sur polybutadiène; styrène et anhydride maléique sur polybutadiène; styrène, acrylonitrile et anhydride maléique ou maléimide sur polybutadiène; styrène et maléimide sur polybutadiène, styrène et acrylates ou méthacrylates d'alkyles sur polybutadiène, styrène et acrylnitrile sur terpolymères éthylène-propylène-diène, styrène et acrylonitrile sur polyacrylates d’alkyles ou polyméthacrylates d'alkyles, styrène et acrylonitrile sur copolymères acrylate-butadiène, ainsi que leurs mélanges avec d'autres copolymères mentionnés en 6) , connus par exemple sous la dénomination de polymères ABS, MBS, ASA ou AES.
8. Polymères halogénés, par exemple le polychloroprène, le caoutchouc chloré, le polyéthylène chloré ou chlorosulfoné, des copolymères d'éthylène et d'éthylène chloré, les homo- et les copolymères d'épichlorhydrine, plus particulièrement des polymères de composés vinyliques halogénés, tels que le poly-(chlorure de vinyle), le poly-(chlorure de vinylidène), le poly-(fluorure de vinyle), le poly-(fluorure de vinylidène); ainsi que leurs copolymères, tels que les copolymères chlorure de vinyle-chlorure de vinylidène, chlorure de vinyle-acétate de vinyle ou chlorure de vinylidène-acétate de vinyle.
9. Polymères provenant d'acides α, β non-saturés et de leurs dérivés, tels que polyacrylates et polyméthacrylates, polyméthacrylates de méthyle, polyacrylamides et polyacrylonitriles rendus résilients par modification avec de l'acrylate de butyle.
10. Copolymères des monomères mentionnés en 9) entre eux ou avec d'autres monomères non saturés, par exemple copolymères acrylonitrile-butadiène, copolymères acrylonitrile-acrylate d'alkyle, copolymères acrylonitrile-acrylate d'alcoxyalkyle, copolymères acrylonitrile-halogénure de vinyle ou terpolymères acrylonitrile-méthacrylate d'alkyle-butadiène.
11. Polymères provenant d'alcools ou d'amines insaturés, ou de leurs dérivés acylés ou de leurs acétals, tels que l'alcool polyvinylique, l'acétate, le stéarate, le benzoate, le maléate de polyvinyle, le polyvinyl- butyral, le phtalate de polyallyle, la poly-(allyl-mélamine); ainsi que leurs copolymères avec les oléfines mentionnées au point 1).
12. Homo- et copolymères d'éthers cycliques, tels que des poly-(alkylène-glycols), le poly-oxiranne, le poly-(oxyde de propylène) ou leurs copolymères avec des éthers bis-glycidyliques.
13. Polyacétals, tels que le polyoxyméthylène ainsi que des polyoxyméthylènes renfermant des comonomères, comme par exemple l'oxyde d'éthylène; des polyacétals modifiés par des polyuréthannes thermoplastiques, des acrylates ou le MBS.
14. Polyphénylèneoxydes et -sulfures et leurs mélanges avec des polymères des styrènes ou des polyamides.
15. Polyuréthannes dérivés, d'une part, de polyéthers, de polyesters ou de polybutadiènes à radicaux hydroxy terminaux et, d'autre part, de polyisocyanates aliphatiques ou aromatiques, ainsi leurs précurseurs.
16. Polyamides et copolyamides dérivant de diamines et d'acides dicarboxyliques et/ou d'acides aminocarboxyliques ou des lactames correspondants, tels que le polyamide 4, le polyamide 6, les polyamides 6/6, 6/10, 6/9, 6/12, 4/6 et 12/12, le polyamide 11, le polyamide 12, les polyamides aromatiques dérivant de la m-xylène-diamine et de l'acide adipique; polyamides préparés à partir d'hexaméthylènediamine et de l'acide iso- et/ou téréphtalique et, le cas échéant, d'un élastomère comme agent modifiant, par exemple, le poly-2,4,4,-triméthylhexaméthylèneteréphtalamide ou le poly-m-phénylène-isophthalamide. Des copolymères séquencés des polyamides précédemment mentionnés, avec des polyoléfines, des copolymères d'oléfines, des ionomères ou des élastomères liés chimiquement ou greffés; ou avec les polyéthers, tels que le polyéthylèneglycol, le polypropylèneglycol ou le polytetraméthylèneglycol. Ensuite des polyamides ou des copolyamides modifiés par l'EPDM ou 11ABS; ainsi que les polyamides condensés lors de la mise en oeuvre ("systèmes polyamides RIM").
17. Polyurées, polyimides, polyamide-imides et polybenzimidazoles.
18. Polyesters dérivant d'acides dicarboxyliques et de dialcools, et/ou d'acides hydroxycarboxyliques ou des lactones correspondantes, tels que le polytéréphtalate d'éthylène, le polytéréphtalate de butylène, le polytéréphtalate de 1,4-diméthylol-cyclohexane, le polyhydroxybenzoate ainsi que des polyéther-esters séquencés, dérivant de polyéthers à radicaux hydroxy terminaux; ensuite, des polyesters modifiés par des polycarbonates ou le MBS.
19. Polycarbonates et polyestercarbonates.
20. Polysulfones, polyéthersulfones et polyéthercétones.
21. Polymères réticulés dérivant, d'une part, d'aldéhydes et, d'autre part, de phénols, d'urée ou de mélamine, tels que les résines phénol-formaldéhyde, urée-formaldéhyde et mélamine-formaldéhyde.
22. Résines alkyde siccatives et non siccatives.
23. Résines polyesters non saturées dérivant de copolyesters d'acides dicarboxyliques saturés et non saturés et d'alcools polyfonctionnels, ainsi que de composés vinyliques comme agents réticulants, et leurs dérivés peu combustibles, modifiés par halogénation.
24. Résines acryliques réticulables dérivant d'esters d'acides acryliques substitués, par exemple d'époxy-acrylates, d'acrylates uréthannes ou d'acrylates polyesters.
25. Résines alkydes, résines polyesters et résines acrylates, réticulées avec des résines de mélamine, des résines d'urée, des polyisocyantes ou des résines époxy.
26. Résines époxy réticulées dérivant de polyépoxydes, par exemple d'éthers bis-glycidyliques ou de diépoxydes cycloaliphatiques.
27. Polymères naturels, tels que la cellulose, le caoutchouc naturel, la gélatine ainsi que leurs dérivés polymères homologues chimiquement modifiés, tels que les acétates, les propionates et les butyrates de cellulose, ou des éthers de cellulose, tels que la méthylcellulose; ainsi que les résine de colophane et dérivés.
28. Mélanges (polyblends) des polymères précités, par exemple PP/EPDM, polyamide/EPDM ou ABS, PVC/EVA, PVC/ABS, PVC/MBS, PC/ABS, PBTP/ABS, PC/ASA, PC/PBT, PVC/CPE, PVC/acrylates, POM/PUR thermoplastique, PC/PUR thermoplastique, POM/acrylate, POM/MBS, PPO/HIPS, PPO/PA 6.6 et copolymères, PA/HDPE, PA/PP, PA/PPO.
29. Substances organiques naturelles et synthétiques, qui sont des composés monomères purs ou leurs mélanges, par exemple des huiles minérales, des graisses huiles et cires animales ou végétales, des huiles, cires et graisses à base d’esters synthétiques (par exemple phtalates, adipates, phosphates ou trimellitates), ainsi que des mélanges d'esters synthétiques avec des huiles minérales dans un rapport quelconque, tels qu'ils sont utilisés, par exemple, sous forme de préparations pour filatures ainsi que leurs émulsions aqueuses.
30. Emulsions aqueuses de caoutchoucs naturels et synthétiques, tels que le latex de caoutchouc naturel ou des latex de copolymères styrène-butadiène carboxylés.
Les matières organiques préférées soint des polymères, par exemple des polymères synthétiques, notamment des polymères thermoplastiques. On préfère tout particulièrement les polyoléfines, les copolymères de styrène, le caoutchouc polybutadiène et les polyuréthannes. On préfère par exemple le polypropylène et le polyéthylène en tant que polyoléfines.
Les compositions conformes à l'invention sont utilisées également pour la fabrication de polyuréthannes, notamment pour la préparation de mousses souples de polyuréthannes. Les compositions conformes à l'invention et les produits à base de celles-ci sont alors protégés de façon efficace contre la dégradation. Plus particulièrement, on évite le grillage des noyaux (scorching) au cours de la fabrication de mousses.
Les polyuréthannes sont obtenus, par exemple, par réaction de polyéthers, de polyesters ou de polybutadiènes à radicaux hydroxyles terminaux, avec des polyisocyanates aliphatiques ou aromatiques.
Les polyéthers comportant des groupes hydroxyles terminaux sont connus et sont préparés, par exemple, par polymérisation d'époxydes, tels que l'oxyde d'éthylène, l'oxyde de propylène, l'oxyde de butylène, la tétrahydrofuranne, l'oxyde de styrène ou l'épichlorhydrine, seuls, par exemple en présence de BF3, ou par fixation de ces époxydes, le cas échéant, en mélange ou successivement, sur des composants d'amorçage porteurs d'atomes d'hydrogène réactifs, tels que l'eau, des alcools, l'ammoniac ou des amines, par exemple 1'éthylène-glycol, le propylène glycol-(l,3) et -(1,2), le triméthylol-propane, le 4,4 *-dihydroxy-diphénylpropane, l'aniline, 1'éthanolamine ou l'éthylène diamine. Des polyéthers de saccharose peuvent aussi être utilisés conformément à l'invention. Souvent, on préfère des polyéthers comportant principalement (jusqu'à 90% en poids par rapport à tous les groupes OH présents dans le polyéther) des groupes OH primaires. Les polyéthers modifiés par des polymères vinyliques, tels qu'ils se forment, par exemple, au cours de la polymérisation du styrène et de 1 *acrylonitrile en présence de polyéthers, sont également appropriés, ainsi que les polybutadiènes comportant des groupes OH.
Ces composés ont en règle générale un poids moléculaire de 400 à 10 000. Ce sont des composés polyhydroxylés, plus particulièrement des composés comportant un nombre de groupes hydroxyles compris entre 2 et 8, notamment des polyéters dont le poids moléculaire est compris entre 800 et 10 000, de préférence entre 1000 et 6000, et contenant par exemple au moins deux, en règle générale entre 2 et 8, mais de préférence entre 2 et 4 groupes hydroxyles, tels qu’ils sont connus en soi pour la préparation de polyuréthannes homogènes et de polyuréthannes alvéolaires.
Bien entendu, on peut utiliser des mélanges des composés ci-dessus comportant au moins deux atomes d'hydrogène capables de réagir avec des isocyanates, notamment ceux dont le poids moléculaire est compris entre 400 et 10 000.
Comme polyisocyanates on peut considérer des polyisocyanates aliphatiques, cycloaliphatiques, araliphatiques, aromatiques et hétérocycliques, par exemple le diisocyanute d'éthylène, le 1,4-diisocyanate de tetraméthylène, le 1,6-diisocyanate d'hexaméthylène, le 1,12-diisocyanato-dodécane, le 1,3-diisocyanato-cyclobutane, les 1,3- et 1,4-diisocyanato-cyclohexanes ainsi que n'importe quel mélange de ces isomères, le 1-isocyanato-3,3,5-triméthyl-5-isocyanotométhyl-cyclo-hexane, les 2,4- et 2,6-di-isocyanato-hexahydrotoluènes ainsi que des mélanges quelconques de ces isomères, 1'hexahydro-1,3- et/ou -1,4-phénylènediisocyanate, le perhydro-2,4'- et/ou -4,4'-diphénylméthane diisocyanate, le 1,3- et 1,4-phénylènediisocyanate, les 2,4- et 2,6-di-isocyanato-toluènes ainsi que n'importe quel mélange de ces isomères, le diphénylméthane-2,4'- et/ou -4,4'-diisocyanate, le naphthylène-1,5-diisocyanate, le triphénylméthane-4,4',4"-triisocyanate, des polyphényl-polyméthylène-polyisocyanates tels qu'obtenus par condensation de l'aniline et du formaldéhyde, suivie d'une phosgénation, les isocyanates de m- et de p-isocyanato-phénylsulfonyle, des arylpolyisocyanates perchlorés, des polyisocyanates comportant des groupes carbodiimides, des polyisocyanates comportant des groupes allophanates, des polyisocyanates comportant des groupes isocyanurates, des polyiisocyanates comportant des groupes uréthannes, des polyisocyanates comportant des groupes d'urée acylés, des polyisocyanates comportant des groupes biurets, des polyisocyanates comportant des groupes esters, des produits de réaction des isocyanates ci-dessus avec des acétals, et des polyisocyanates comportant des résidus d'acides gras polymères.
Il est également possible d'utiliser les résidus de distillation comportant des groupes isocyanates, obtenus au cours de la fabrication industrielle d'isocyanates, le cas échéant dissous dans un ou plusieurs des polyisocyanates pré-cités. Il est en outre possible d'utiliser n'importe quel mélange des polyisocyanates précités.
En règle générale, on préfère les polyisocyanates facilement accessibles techniquement, par exemple les 2,4- et 2,6-diisocyanato-toluènes ainsi que n'importe quels mélanges de ces isomères ("TDI"), les polyphényl-polyméthylène-polyisocyanates préparés par condensation d'aniline et de formaldéhyde suivie de phosgénation ("MDI brut") et les polyisocyanates comportant des groupes carbodiimides, des groupes uréthannes, des groupes allophanates, des groupes isocyanates, des groupes urées ou biurets ("polyisocyanates modifiés").
Il convient plus particulièrement de faire remarquer l'effet des composés conformes à l'invention contre la dégradation thermique et oxydative, surtout au cours de contraintes thermiques, telles que celles qui apparaissent au cours de la mise en oeuvre des matières thermoplastiques. Les composés conformes à l'invention sonr donc particulièrement appropriés comme stabilisants au cours de la mise en oeuvre.
Les composés de formule (1) sont ajoutés à la matière à stabiliser en des quantités comprises de préférence entre 0,0005 et 5%, plus particulièrement entre 0,001 et 2%, par exemple entre 0,01 et 2%, par rapport au poids de la matière organique à stabiliser.
Outre les composés de formule (1) , les compositions conformes à l'invention peuvent contenir d'autres co-stabilisants, tels que les suivants : 1. Antioxydants 1.1. Monophénols alkylés, par exemple le 2,6-di-tert-butyl-4-méthylphénol, le 2-butyl-4,6-diméthylphénol, le 2.6- di-tert-butyl-4-éthylphénol, le 2,6-di-tert-butyl-4-n-butylphénol, le 2,6-di-tert-butyl-4-isobutylphénol, le 2.6- di-cyclopentyl-4-méthylphénol, le 2-(a-méthyl- cyclohexyl)-4,6-diméthylphénol, le 2,6-di-octadécyl-4-méthylphénol, le 2,4,6-tricyclohexylphénol, le 2,6-di-tert-butyl-4-méthoxyméthylphénol, le 2, 6-di-nonyl-4-méthylphénol, le 2,4-diméthyl-6-(1'-méthyl-undec-1'-yl)-phénol, le 2,4-diméthyl-6-(11-méthyl-heptadec-1*-yl)-phénol, le 2,4-diméthyl-6-(1*-méthyl-tridec-1*-yl)-phénol et leurs mélanges.
1.2. Alkylthlométhylphénols. par exemple le 2,4-bis- (octylthiométhyl)-6-tert-butylphénol, le 2,4-bis-(octylthiométhyl)-6-méthylphénol, le 2,4-bis- (octylthiométhyl)-6-éthylphénol, et le 2,6-bis-(dodécylthiométhyl)-4-nonylphénol.
1.3. Hydroqyinones_e£_hy.dÎ.o..g,h.3lnotgs_alkylées, par exemple le 2,6-di-tert-butyl-4-méthoxyphénol, la 2,5-di-tert-buty1-hydroquinone, la 2,5-di-tert-amyl-hydroquinone, le 2,6-diphényl-4-octadécyloxyphénol, la 2.6- di-tert-butyl-hydroquinone, le 2,5-di-tert-butyl-4-hydroxyanisole, le 3,5-di-tert-butyl-4-hydroxyanisole, le stéarate de 3,5-di-tert-butyl-4-hydroxyphényle, et l'adipate de bis-(3,5-di-tert-butyl-4-hydroxyphényle) .
1.4. Sulfures de diphényles hydroxylés, par exemple le 2,2'-thio-bis-(6-tert-butyl—4-méthylphénol), le 2,2'-thio-bis-(4-octylphénol) , le 4,4,-thio-bis-(6-tert-butyl-3-méthylphénol), le 4,4’-thio-bis-(6-tert-butyl-2-méthylphénol), le 4,41-thio-bis-(3,6-di-sec-pentyl-phénol), et le disulfure de 4,41-bis-(2,6-diméthyl-4-hydroxyphényle).
1.5. Alkylidène-bisphénols. par exemple le 2,2'-méthylène-bis-(6-tert-butyl-4-méthylphénol), le 2,2'-méthylène-bis-(6-tert-butyl-4-éthylphénol) , le 2,2'- méthylène-bis-[4-méthyl-6-(α-méthyl-cyclohexyl)-phénol], le 2,2'-méthylène-bis-(4-méthyl-6-cyclohexylphénol), le 2,2'-méthylène-bis-(6-nonyl-4-méthylphénol), le 2,2'-méthylène-bis-(4,6-di-tert-butylphénol) , le 2,2'-éthylidène-bis-(4,6-di-tert-butylphénol), 2,2'-éthylidène-bis-(6-tert-butyl-4- isobutylphénol) , le 2,2 '-méthylène-bis [ 6-(0C- méthylbenzyl)-4-nonylphénol], le 2,2'-méthylène-bis-[βία, OC-di-méthylbenzyl) -4-nonylphénol], le 4,4' -méthylène- bis-(2, 6-di-tert-butylphénol), le 4,4’-méthylène-bis-(6-tert-butyl-2-méthylphénol), le 1,1-bis-(5-tert-butyl-4-hydroxy-2-méthylphényl)-butane, le 2,6-bis-(3-tert-butyl-5-méthyl-2-hydroxybenzyl)-4-méthylphénol, le 1,1,3-tris- (5-tert-butyl-4-hydroxy-2-mercaptophényl) -butane, le 1,1-bis-(5-tert-butyl-4-hydroxy-2-méthyl-phényl)-3-n-dodécylthio-butane, le bis-[3,3-bis-(3'-tert-butyl-4’-hydroxy-phényl)-butyrate] de 1'éthylèneglycol, le bis-(3-tert-butyl-4-hydroxy-5-méthyl-phényl)-dicyclopentadiène, le téréphtalate de bis- [2- (3 ' -tert-butyl-2 ' -hydroxy-5 '-méthyl-benzyl) -6-tert-butyl-4-méthyl-phényle], le 1,1-bis-(3,5-diméthyl-2-hydroxyphényl)-butane, le 2,2-bis-(3,5-di-tert-butyl-4-hydroxy-phényl)-propane, le 2,2-bis-(5-tert-butyl-4-hydroxy-2-méthylphényl)-4-n-dodécylthio-butane et le 1,1,5,5-tétrakis-(5-tert-butyl-4-hydroxy-2-méthyl-phényl)-pentane.
1.6. Composés 0-, N- et S-benzylioues. par exemple l'oxyde de bis-(3,5-di-tert-butyl-4-hydroxy-benzyle), le 4-hydroxy-3,5-diméthyl-benzylthio-acétate d'octadécyle, la tris-(3,5-di-tert-butyl-4-hydroxybenzyl)-amine, le dithiotéréphtalate de bis- (4-tert-butyl-3-hydroxy-2, 6-diméthylbenzyle), le sulfure de bis-(3,5-di-tert-butyl-4-hydroxybenzyle) et le 3,5-di-tert-butyl-4-hydroxybenzylthio-acétate d'iso-octyle.
1.7. Malonates hydroxybenzylés, par exemple le 2,2-bis- (3,5-di-tert-butyl-2-hydroxybenzyl)-malonate de dioctadécyle, le 2-(3-tert-butyl-4-hydroxy-5- méthylbenzyl)-malonate de di-octadécyle, le 2,2-bis-(3,5-di-tert-butyl-4-hydroxybenzyl)-malonate de bis-(dodécylthio-éthyle et le 2,2-bis-(3,5-di-tert-butyl-4-hydroxybenzy1)-malonate de bis-[4-(l,l,3,3- tétraméthylbutyl)-phényle].
1.8. Composés aromatiques hydroxybenzyliquesf par exemple le 1,3,5-tris-(3,5-di-tert-buty1-4 - hydroxybenzyl)-2,4,6-triméthylbenzène, le 1,4-bis-(3,5-di-tert-butyl-4-hydroxybenzyl) -2,3,5, 6-tetraméthyl-benzène, et le 2,4,6-tris-(3,5-di-tert-butyl-4-hydroxybenzyl)-phénol.
1.9. Composés triaziniques, par exemple, la 2,4-bis-octylthio-6- (3,5-di-tert-butyl-4-hydroxyanilino)-1,3,5-triazine, la 2-octylthio-4,6-bis-(3, 5-di-tert-butyl-4-hydroxyanilino)-1,3,5-triazine, la 2-octylthio-4,6-bis-(3,5-di-tert-butyl-4-hydroxyphénoxy) -1,3,5-triazine, la 2,4,6-tris- (3,5-di-tert-butyl-4-hydroxyphénoxy)-1,2,3-triazine, 1 ' isocyanurate de tris-(3,5-di-tert-butyl-4-hydroxybenzyle), 1'isocyanurate de tris-(4-tert-butyl-3-hydroxy-2,6-diméthylbenzyle) , la 2,4, 6-tris-(3,5-di-tert-butyl-4-hydroxyphényl-éthyl)-1,3,5-triazine, la 1,3,5-tris-(3,5-di-tert-butyl-4-hydroxyphényl-propionyl)-hexahydro-1,3,5-triazine et 1'isocyanurate de tris-(3,5-dicyclohexyl-4-hydroxybenzyle).
1.10. Benzyl-phosphonates. par exemple le (2,5-ditert-butyl-4-hydroxybenzyl)-phosphonate de diméthyle, le (3,5-di-tert-butyl-4-hydroxybenzyl)-phosphonate de diéthyle, le (3,5-di-tert-butyl-4-hydroxybenzyl)-phosphonate de dioctadécyle, le (5-tert-butyl-4-hydroxy-3-méthyl-benzyl)-phosphonate de dioctadécyle, le (5-tert-butyl-4-hydroxy-3-méthylbenzyl) -phosphonate de dioctadécyle, le sel calcique du (3, S-di-tert-butylM-hydroxybenzyl)-phosphonate de monoéthyle.
1.11. Acylaminophénols, par exemple le 4-hydroxy-anilide de l'acide laurique, le 4-hydroxy-anilide de l'acide stéarique, le N-(3,5-di-tert-butyl-4-hydrophényl)-carbamate d'octyle.
1.12. Ester de l'acide β-(3,5-di-tert-butyl-4-hvdroxyphényl) -propionique avec des alcools mono- ou polyhydroxylés, tels que le inéthanol, l'éthanol, l'octadécanol, le 1,6-hexane-diol, le 1,9-nonanediol, 1'éthylène-glycol, le 1,2-propanediol, le néopentylglycol, le thiodiéthylène-glycol, le diéthylène-glycol, le triéthylène-glycol, le pentaérythritol, 1'isocyanurate de tris-(hydroxyéthyle), le N,N'-bis-(hydroxyéthyl)-oxalamide, le 3-thia-undécanol, le 3-thiapentadécano1, le triméthylhexanediol, le triméthylolpropane, le 4-hydroxyméthyl-l-phospha-2,6,7-trioxabicyclo[2.2.2]-octane.
1.13. Ester de l'acide ft-(5-tert-butyl-4-hvdroxyr3-méthylphényl) -propionique, avec des alcools mono- ou polyhydroxylés,. comme par exemple le méthanol, l'éthanol, l'octadécanol, le 1,6-hexanediol, le 1,9-nonanediol, l'éthylène-glycol, le 1,2-propanediol, le néopentylglycol, le thiodiéthylène-glycol, le diéthylène-glycol, le triéthylène-glycol, le pentaérythritol, 1'isocyanurate de tris-(hydroxyéthyle), le N,N'-bis-(hydroxyéthyl)-oxalamide, le 3-thia-undécanol, le 3-1hiapentadécano1, le triméthylhexanediol, le triméthylol-propane, le 4-hydroxyméthyl-l-phopha-2,6,7-trioxabicyclo[2.2.2]octane.
1.14. Ester de l'acide β-(3,5-dicvcloh_exyl-4-hydroxyohényl)-propionique avec des alcools mono- ou polyhydroxylés, tels que le méthanol, l'éthanol, l'octadécanol, le 1,6-hexanediol, le 1,9-nonanediol, l'éthylène-glycol, le 1,2-propanediol, le néopentylglycol, le thiodiéthylène-glycol, le diéthylène-glycol le triéthylène-glycol, le pentaérythritol, 1'isocyanurate de tris-(hydroxyéthyle), le N,N'-bis-(hydroxyéthyl)-oxalamide, le 3-thia-undécanol, le 3-thiapentadécano1, le triméthylhexanediol, le triméthylol-propane, le 4- hydroxyméthyl-l-phospha-2,6,7-trioxabicyclo[2.2.2]-octane.
1.15. Esters_ds_11 acide_(3.5-di-tert-butyl-4- hydroxyphényl)-acétique avec des alcools mono- ou polyhydroxylés, tels que le inéthanol, l'éthanol, 1’octadécanol, le 1,β-hexanediol, le 1,9-nonanediol, 1'éthylène-glycol, le 1,2-propanediol, le néopentylglycol, le thiodiéthylène-glycol, le diéthylène-glycol, le triéthylène-glycol, le pentaérythritol, 1'isocyanurate de tris-(hydroxy-éthyle), le N,N'-bis-(hydroxyéthyl)-oxalamide, le 3-thia-undécanol, le 3-thiapentadécanol, le triméthylhexanediol, le triméthylolpropane, le 4-hydroxyméthyl-l-phospha-2,6,7-trioxabicyclo[2.2.2]-octane.
1.16. Ami de s_de_I_'.a.c.i.de_fi- (3, s-di-tert-butyl-4- hvdroxvphényl)-propioniaue, tels que la N,N'-bis-(3,5-di-tert-butyl-4-hydroxyphénylpropionyl)-hexaméthylène diamine, la N,N'-bis-(3,5-di-tert-butyl-4-hydroxy-phénylpropionyl)-triméthylènediamine, la N,N'-bis-(3,5-di-tert-butyl-4-hydroxyphénylpropionyl)-hydrazine.
2. Abs-Q.rbeurs d'UV et photostabilisants 2.1. 2-(2 * -(hydroxyphényl)-benzotriazoles. tels que le 2-(2'-hydroxy-5'méthylphényl)-benzotriazole, le 2-(3',5'-di-tert-butyl-2'-hydroxyphényl)-benzotriazole, le 2-(5'-tert-buty1-2'-hydroxyphényl)-benzotriazole, le 2-(2'-hydroxy-5'-(1,1,3,3-tetraméthylbutyl)phényl)-benzotriazole, le 2-(3',5'-di-tert-butyl-2'-hydroxyphényl)-5-chloro-benzotriazole, le 2-(3'-tert-butyl-2'-hydroxy-5'-méthylphényl)-5-chloro-benzotriazole, le 2-(3'-sec-butyl-5'-tert-butyl-2'-hydroxyphényl)-benzotriazole, le 2-(2'-hydroxy-4'-octoxyphényl)-benzotriazole, le 2-(3',5'-di-tert-amyl-2'-hydroxyphényl)-benzotriazole, le 2- (3 1,5 ' -bis- (α,α-diméthylbenzyl) -2 ' -hydroxyphényl) - benzotriazole, un mélange de 2-(3'-tert-butyl-2'-hydroxy-5'-(2-octyloxycarbonyléthyl)-phényl)-5-chloro- benzotriazole, 2-(31-tert-butyl-51-[2-(2-éthylhexyloxy)-carbonyléthyl]-2’-hydroxyphényl)-5-chloro-benzotriazole, 2-(31-tert-butyl-2'-hydroxy-51-(2-méthoxycarbonyl-éthyl)phényl)-5-chloro-benzotriazole, 2-(3'-tert-butyl-2'-hydroxy-51-(2-méthoxycarbonyléthyl)phényl)-benzotriazole, 2-(31-tert-butyl-2'-hydroxy-5'-(2-octyloxy-carbonyléthyl)-phényl-benzotriazole, 2-(31-tert-butyl-51-[2-(2-éthylhexyloxy)carbonyléthyl]-2’-hydroxyphényl)-benzotriazole, 2-(3’-dodécyl-21-hydroxy-5'-méthyl-phényl)-benzotriazole, et 2-(3 '-tert-butyl-2'-hydroxy-5'-(2-isooctyloxycarbonyléthyl)phényl-benzotriazole, le 2,2’-méthylène-bis[4-(1,1,3,3-tetraméthylbutyl)-6-benzo-triazol-2-yl-phénol]; le produit de transestérification de 2-[3’-tert-butyl-5'-(2-méthoxycarbonyléthyl)-2'-hydroxyphényl]-benzotriazole avec le polyéthylène-glycol 300; [R-CH2CH2-COO(CH2)3]2 avec R = 3'-tert-butyl-4'- hydroxy-51-2H-benzotriazol-2-yl-phényle.
2.2. 2-Hydroxybenzophénones, par exemple les dérivés 4-hydroxy, 4-méthoxy-, 4-octoxy-, 4-décyloxy-, 4-dodécyloxy-, 4-benzyloxy-, 4,2’,4'-trihydroxy-, 2’-hydroxy-4,4'-diméthoxy.
2.3. Esters d'acides benzoïques éventuellement substitués exemple le salicylate de 4-tert-butyle, le salicylate de phényle, le salicylate d'octylphényle, le dibenzoyl-résorcinol, le bis-(4-tert-butyl-benzoyl-résorcinol) , le benzoyl-résorcinol, l'ester 2,4-di-tert-butylphénylique d’acide 3,5-di-tert-butyl-4-hydroxybenzoïque, l’ester hexadécylique d’acide 3,5-di-tert-butyl-4-hydroxybenzoïque, l’ester octadécylique d'acide 3,5-di-tert-butyl-4-hydroxybenzoïque, l'ester 2-méthyl-4,6-di-tert-butylphénylique d'acide 3,5-di-tert-butyl-4 -hydroxybenzo ique .
2.4. Acrylates, par exemple l’ester éthylique ou l’ester isooctylique d'acide a-cyano-β,β-diphénylacrylique, l’ester méthylique d'acide α-mét hoxycarbony 1-cinnamique, l'ester méthylique ou butylique d'acide a-cyano-fi-méthyl-p-méthoxy-cinnamique, l'ester méthylique d'acide α-méthoxycarbonyl-p-méthoxy-cinnamique, la Ν-(β-méthoxycarbonyl-B-cyanovinyl)-2-méthyl-indoline.
2.5. Composés du nickel, par exemple des complexes du nickel du 2,21-thio-bis-[4-(1,1,3,3-tetraméthylbutyl)-phénol], tels que le complexe 1:1 ou le complexe 1:2, le cas échéant avec coordinats complémentaires, tels que la n-butylamine, la triéthanolamine ou la N-cyclohexyl-diéthanolamine, le dibutyldithiocarbamate de nickel, des sels de nickel d'esters monoalkyliques d'acide (4-hydroxy-3,5-di-tert-butylbenzyl)phosphonique, tels que l'ester méthylique et l'ester éthylique, des complexes du nickel de cétoximes, telle que l'oxime de l'undécyl-(2-hydroxy-4-méthyl)-cétone, des complexes du nickel du l-phényl-4-lauroyl-5-hydroxy-pyrazole, le cas échéant avec des coordinats complémentaires.
2.6. Amines à empêchement stérique par exemple le sébaçate de bis-(2,2,6,6-tetraméthyl-pipéridyle), le succinate de bis-(2,2,6,6-tetraméthyl-pipéridyle) , le sébaçate de bis-(1,2,2,6,6-pentaméthylpipéridyle), l'ester bis-(1,2,2,6,β-pentaméthyl-pipéridylique) de l'acide (n-butyl)-(3,5-di-tert-butyl-4-hydroxybenzyl)-malonique, le produit de condensation de la 1-hydroxyéthyl-2,2,6,6-tétraméthyl-4-hydroxypipéridine avec l'acide succinique, le produit de condensation de la N,N'-bis-(2,2,6,6-tetraméthyl-4-pipéridyl)-hexa-méthylènediamine et de la 4-tert-octylamino-2,6-dichloro-1,3,5-s-triazine, le nitriloacétate de tris-(2,2,6,6-tetraméthyl-4-pipéridyle), le butane-1,2,3,4-tétracarboxylate de tétrakis-(2,2,6,6-tétraméthyl-4-pipéridyle), la 1,1'-(1,2-éthanediyl)-bis(3,3,5,5-tétraméthyl-pipérazinone), la 4-benzoyl-2,2,6,6-tétraméthylpipéridine, le 4-stéaryloxy-2,2,6,6-tétraméthylpipéridine, le 2-n-butyl-2-(2-hydroxy-3,5-di-tert-butylbenzyl) -malonate de bis-(1,2,2,6,6-pentaméthylpipéridyle), la 3-n-octyl-7,7,9,9-tétraméthyl-1,3,8-triazaspiro[4.5]décane-2,4-dione, le sébaçate de bis-(l-octyloxy-2,2,6,6-tétraméthy1- pipéridyle) , le succinate de bis-(l-octyloxy-2,2,6,6-tétraméthylpipéridyle), le produit de condensation de la N, N * -bis-(2,2,6,6-tétraméthyl-4-pipéridyl)-hexa-méthylènediamine et de la 4-morpholino-2,6-dichloro-1,3,5-triazine, le produit de condensation de la 2-chloro-4, 6-bis- (4-n-butylamino-2,2, 6, 6-tétraméthyl-pipéridyl)-1,3,5-triazine et du l,2-bis-(3-aminopropylamino)éthane, le produit de la condensation de la 2-chloro-4,6-bis-(4-n-butylamino-l,2,2,6,6-penta-méthylpipéridyl)-1,3,5-triazine et du l,2-bis-(3-aminopropylamino)-éthane, la 8-acétyl-3-dodécyl-7,7,9,9-tétraméthyl-1,3/8-triazospiro[4.5]décane-2,4-dione, la 3- dodécyl-l- (2,2,6,6-tétraméthyl-4-pipéridyl)-pyrro-lidine-2,5-dione, la 3-dodécyl-l-(1,2,2,6,6-pentaméthyl- 4- pipéridyl)-pyrrolidine-2,5-dione.
2.7. Diamides de l'acide oxalique, par exemple le 4,4'- di-octyloxy-oxanilide, le 2,2'-di-octyloxy-5,5’-di-tert-butyl-oxanilide, le 2,21-di-dodécyloxy-5,5'-di-tert-butyl-oxanilide, le 2-éthoxy-21-éthyl-oxanilide, le Ν,Ν'-bis-(3-diméthylpropyl)-oxalamide, le 2-éthoxy-5-tert-butyl-2'-éthyl-oxanilide et son mélange avec le 2-éthoxy-21-éthyl-5,4'-di-tert-butyl-oxanilide, des mélanges d'oxanilides o- et p-méthoxy- ainsi que o- et p-éthoxy di-substitués.
2.8. 2-(2-Hydroxvphényl)-1,3,5-triazines, par exemple la 2,4, 6-tris(2-hydroxy-4-octyloxy-phényl)-1,3,5-triazine, la 2-(2-hydroxy-4-octyloxyphényl)-4, 6-bis-(2,4-diméthyl-phényl)-1,3,5-triazine, la 2-(2,4-dihydroxyphényl)-4,6-bis(2,4-diméthylphényl)-1,3,5-triazine, la 2,4-bis-(2-hydroxy-4-propyloxyphényl)-6-(2,4-diméthylphényl)-1,3,5-triazine, la 2-(2-hydroxy-4-octyloxyphényl)-4,6-bis(4-méthylphényl)-1,3,5-triazine, la 2-(2-hydroxy-4-dodécyloxyphényl)-4,6-bis(2,4-diméthylphényl)-1,3,5-triazine, la 2-[2-hydroxy-4-(2-hydroxy-3-butyloxy-propyloxy)phényl]-4,6-bis(2,4-diméthylphényl)-1,3,5-triazine, la 2-[2-hydroxy-4-(2-hydroxy-3-octyloxy- propyloxy)phényl]-4,6-bis(2,4-diméthylphényl)-1,3,5-triazine.
3. Désactivants de métaux, par exemple, le N,N'-diphényl-oxalamide, la N-salicylal-N*-salicyloyl-hydrazine, la Ν,Ν'-bis-(salicyloyl)-hydrazine, le N, N ' -bis-(3,5-di-tert-butyl-4-hydroxy-phénylpropionyl)-hydrazine, le 3-salicyloylamino-l,2,4-triazole, le bis-(benzylidène-hydrazide) de l’acide oxalique, l’oxanilide, le dihydrazide d’acide isophthalique, le bis-(phénylhydrazide) d'acide sébacique, le bis-(N-acétyl-hydrazide) de l'acide adipique, le N,N'-bis-salicyloyl-oxaldihydrazide, le bis-(N-salicyloyl-hydrazide) de l’acide thio-dipropionique.
4. Phosohites et phosphonites. par exemple le phosphite de triphényle, un phosphite de diphényle et d'alkyle, un phosphite de phényle et de dialkyle, le phosphite de tris-(nonylphényle), le phosphite de trilauryle, le phosphite de trioctadécyle, le diphosphite de distéaryl-pentaérythritol, le phosphite de tris-(2,4-di-tert-butylphényle), le diphosphite de diisodécyl-pentaérythritol, le diphosphite de bis-(2,4-di-tert-butylphényl)-pentaérythritol, le diphosphite de bis-(2,6-di-tert-butyl-4-méthylphényl)-pentaérythritol, le diphosphite de bis-isodécyloxy-pentaérythritol, le diphosphite de bis-(2,4-di-tert-butyl-6-méthylphényl)-pentaérythritol, le diphosphite de bis-(2,4,6-tri-tert-butylphényl)-pentaérythritol, le triphosphite de tristéaryl-sorbitol, le 4,4 ’-biphénylène-diphosphonite de tétrakis-(2,4-di-tert-butylphényle), la 6-isooctyloxy-2,4,8,10-tétra-tert-butyl-12H-dibenzo[d,g]-1,3,2-dioxaphosphocine, la 6-fluoro-2,4,8,10-tetra-tert-butyl-12-méthyl~di-benzo[d,g]-1,3,2-dioxaphosphocine, le phosphite de bis-(2,4-di-tert-butyl-6-méthylphényle) et de méthyle, le phosphite de bis-(2,4-di-tert-butyl-6-méthylphényle) et d’éthyle.
5. Décomposeurs de peroxydes, par exemple des esters de l'acide β-thio-dipropionique, tels que, l’ester laurylique, stéarylique, myristylique ou tridécylique, le mercaptobenzimidazole, le sel de zinc du 2-mercaptobenzimidazole, le dibutyl-dithiocarbamate de zinc, le disulfure de dioctadécyle, le tétrakis-[(β-dodécyltbio)-propionate] de pentaérythritol.
6. Stabilisants de polyamides, tels que des sels de cuivre en combinaison avec des iodures et/ou des composés de phosphore et des sels du manganèse bivalent .
7. Co-stabilisants basiques, tels la mélamine, la poly-(vinyl-pyrrolidone), la cyanoguanidine, le cyanurate de triallyle, des dérivés d’urée, des dérivés de l’hydrazine, des amines, des polyamides, des polyuréthannes, des sels de métaux alcalins ou alcalino-terreux d'acides gras supérieurs, par exemple le stéarate de Ca, le stéarate de Zn, le béhénate de Mg, le stéarate de Mg, le ricinoléate de Na, le palmitate de K, le pyrocatécholate d’antimoine ou le pyrocatécholate d’étain.
8. Agents de nucléation, tels que l’acide 4-tert-butylbenzoïque, l’acide adipique, l’acide diphénylacétique.
9. Charges et renforts, tels que le carbonate de calcium, des silicates, des fibres de verre, l'amiante, le talc, le kaolin, le mica, le sulfate de baryum, des oxydes et hydroxydes métalliques, le noir de carbone, le graphite.
10. Autres additifs, par exemple des plastifiants, des lubrifiants, des émulsifiants, des pigments, des azureurs optiques, des ignifugeants, des antistatiques ou des porogènes.
Les co-stabilisants sont ajoutés par exemple à des concentrations comprises entre 0,01 et 10%, par rapport au poids total de la matière à stabiliser. L’incorporation des composés de formule (1) ainsi que, le cas échéant, d’autres additifs dans la matière organique polymère est effectuée à l’aide de méthodes connues, par exemple avant ou au cours du moulage, ou encore par dépôt des composés dissous ou dispersés sur la matière organique polymère, éventuellement avec évaporation ultérieure du solvant. Au moment d’être ajoutés à la matière à stabiliser les composés de formule (1) peuvent également être sous forme d’un mélange-maître où ils se trouvent en une concentration comprise entre 2,5 et 25% en poids.
On peut également ajouter les composés de formule (1) avant ou au cours de la polymérisation ou avant la réticulation.
Pour être incorporés dans la matière à stabiliser les composés de formule (1) peuvent être purs ou encapsulés dans des cires, des huiles ou des polymères.
On peut aussi déposer les composés de formule (1) par projection sur le polymère à stabiliser. Ils sont capables de diluer d'autres adjuvants (par exemple, les additifs courants ci-dessus), ou leurs produits de fusion, de sorte qu'on peut également les projeter sur le polymère à stabiliser simultanément avec ces adjuvants. L'addition par projection au cours de la désactivation des catalyseurs de polymérisation est particulièrement avantageuse, auquel cas on peut utiliser pour la projection par exemple la vapeur utilisée pour la désactivation.
Dans le cas de polyoléfines qui ont été polymérisées sous forme de sphères, il peut par exemple être avantageux d'appliquer les composés de formule (1), éventuellement avec d'autres adjuvants, par projection. On peut utiliser les matières ainsi stabilisées sous les formes les plus variées, par exemple en feuilles, en fibres, en rubans, en matières à mouler, en profilés ou comme liants pour vernis, adhésifs ou mastics.
Lors de la préparation de polyuréthannes on peut en outre ajouter, en tant qu'agents porogènes, de l'eau et/ou des substances organiques volatiles. Comme agents porogènes organiques, entrent en ligne de compte par exemple l'acétone, l'acétate d'éthyle, des alcanes halogénosubstitués, tels que le chlorure de méthylène, le chloroforme, le chlorure d'éthylidène, le chlorure de vinylidène, le monofluorotrichlorométhane, le chlorodifluorométhane, le dichlorodifluorométhane, ou encore le butane, l'hexane, l'heptane ou l'éther diéthylique. On peut obtenir un effet porogène également par addition de composés qui se décomposent à des températures supérieures à la température ambiante avec dégagement de gaz, par exemple d'azote; il pourra s'agir par exemple de composés azoïques, tels que, l'azo-isobutyronitrile.
La préparation de polyuréthannes est avantageusement exécutée en présence de catalyseurs appropriés. On utilise des catalyseurs connus, comme par exemple des amines tertiaires, telles que la triéthylamine, la tributylamine, la N-méthyl-morpholine, la N-éthyl-morpholine, la N-coco-morpholine, la Ν,Ν,Ν',Ν'-tetraméthylène-éthylènediamine , le 1,4-diazabicyclo[2.2.2]octane, la N-méthy1-N'-diméthylaminoéthyl-pipérazine, la N,N-diméthy1-benzylamine, l'adipate de bis-(Ν,Ν-diéthylamino-éthyle), la pentaméthyl-diéthylène-triamine, la bis-(N,N-diméthylcyclohexylamine, la N,N,N',N'-tétraméthyl-l,3-butane-diamine, la N,N-diméthyl-ft-phényléthylamine, le 1,2-diméthyl-imidazole et le 2-méthylimidazole, ainsi que des bases de Mannich, connues en soi, dérivant d'amines secondaires, telles que la diméthylamine, et d'aldéhydes, de préférence du formaldéhyde, ou de cétones, telles que l'acétone, la méthyl-éthyl-cétone ou la cyclohexanone, et de phénols, tels que le phénol, le nonylphénol ou un bisphénol.
Comme amines tertiaires comportant des atomes d'hydrogène capables de réagir avec des groupes isocyanato, en tant que catalyseurs, on citera par exemple la triéthanolamine, la triisoproanolamine, la N- méthyldiéthanolamine, la N-éthyl-diéthanolamine, la N,N-diméthyl-éthanolamine ainsi leurs produits de réaction avec des oxydes d'alkylènes, tels que l'oxyde de propylène et/ou l'oxyde d'éthylène.
En outre, comme autres catalyseurs, on peut prendre en compte des silaamines renfermant des liaisons carbone-silicium, telles que la 2,2,4-triméthyl-2-silamorpholine et le 1,3-diéthylaminométhyl-tetraméthyl-disiloxane, ou encore des bases azotées, telles que l'hydroxyde de tetraalkylammonium, des hydroxydes alcalins, comme l'hydroxyde de sodium, des phénolates alcalins, tels que le phénolate de sodium, ou des alcoolates alcalins, tels que le méthylate de sodium, ou des hexahydrotriazines, ou encore des composés organométalliques, plus particulièrement des composés organiques de l'étain, par exemple des sels d'étain(II) d'acides carboxyliques, tels que l'acétate d'étain(II), l'octoate d'étain(II), I 'éthylhexoate d'étain(II), et le laurate d'étain(II), et des composés d'étain(IV), tels que l'oxyde de dibutyl-étain, le dichlorure de dibutylétain, le diacétate de dibutylétain, le dilaurate de dibutylétain, le maléate de dibutylétain ou le diacétate de dibutylétain. Bien entendu, on peut utiliser tous les catalyseurs indiqués ci-dessus sous forme de mélanges.
II existe, le cas échéant, d'autres adjuvants connus en soi, par exemple des agents tensio-actifs, tels que les émulsifiants ou des stabilisants de mousses.
En tant qu'émulsifiants, on peut prendre en compte, par exemple, des sels de sodium de sulfonates d'huile de ricin ou des sels d'acides gras avec des amines, tels les sels formés par la diéthylamine et l'acide oléique ou le diéthanolamine et l'acide stéarique! Comme adjuvants tensio-actifs, on peut également utiliser des sels alcalins ou des sels d'ammonium d'acides sulfoniques, tels que l'acide dodécylbenzène-sulfonique ou l'acide dinaphthylméthanedisulfonique, ou d'acides gras, tels que l'acide ricinoléique, ou d'acides gras polymères.
Comme stabilisants de mousses, on considère en premier lieu des polyéthersiloxanes, notamment ceux qui sont solubles dans l'eau. En général, ces composés ont une structure telle qu'un copolymère d'oxyde d'éthylène et d'oxyde de propylène est lié avec un radical de polydiméthylsiloxane.
Comme autres adjuvants, il peut en outre y avoir, dans les compositions, des retardateurs de réaction, par exemple des substances à réaction acide, telles que l'acide chlorhydrique ou des halogénures d'acides organiques, des régulateurs cellulaires connus dans l'état de la technique, tels que des paraffines ou des alcools gras, ou des poly-diméthylsiloxanes, ainsi que des pigments ou des colorants et des ignifugeants connus dans l'état de la technique, par exemple le phosphate de tris-chloroéthyle, le phosphate de tricrésyle ou le phosphate et le polyphosphate d'ammonium, puis des stabilisants contre le vieillissement et les conditions météorologiques, des plastifiants et des substances bactéricides et fongicides ainsi que des charges, telles que le sulfate de baryum, la silice (kieselguhr), le noir de carbone ou le blanc d'Espagne.
D'autres exemples d'adjuvants tensio-actifs éventuels et de stabilisants de mousses ainsi que de régulateurs cellulaires, de retardateurs de réaction, de stabilisants, d'ignifigeants, de plastifiants, de colorants et de charges ainsi que de fongicides et de bactéricides et ainsi des détails sur les méthodes d'utilisation et les effets de ces susbtances sont connus de l'homme de métier.
On peut préparer les polyuréthannes sous une forme quelconque, par exemple sous forme de fibres. De préférence, on prépare des mousses, et on peut alors, en choisissant convenablement les composants, obtenir des mousses élastiques ou des mousses rigides ou tout autre produit situé entre ces deux extrêmes.
On préfère la préparation des mousses polyuréthanne à partir de composants de base liquides : dans ce cas ou bien on mélange les substances de base à faire réagir entre elles, par un procédé à une seule étape, ou bien on prépare tout d'abord, à partir d'un polyol et d'un excès de polyisocyanate, un pré-adduit comportant des groupes NCO-, que l'on fait mousser, par exemple par réaction avec de l'eau.
On fait réagir les composants de réaction par le procédé à une seule étape, le procédé de prépolymère ou le procédé de semi-prépolymère connus, et pour cela on se sert souvent d'équipements mécaniques, connus de l'homme de métier.
Au cours de la préparation de mousses, on réalise souvent le moussage dans des moules. Pour cela, on amène le mélange réactionnel dans un moule. Pour les moules, on utilise un métal, par exemple l'aluminium, ou une matière plastique, par exemple une résine époxy. Le mélange réactionnel expansible mousse dans le moule et donne des pièces moulées. On peut alors réaliser le moussage dans le moule de telle façon que la pièce moulée présente à sa surface une structure alvéolaire, mais on peut le réaliser également de telle façon que la pièce moulée présente une croûte compacte et un noyau alvéolaire. Pour ce faire on amène dans le moule assez de mélange réactionnel expansible pour que la mousse formée remplisse tout juste le moule. Mais on peut également travailler de façon ce que la quantité de mélange réactionnel expansible amenée dans le moule soit supérieure à celle nécessaire pour remplir l'intérieur du moule par la mousse. Dans ce dernier cas, on travaille en surcharge ("overcharging").
Souvent on peut simultanément utiliser, au cours du moussage dans le moule, des "agents séparateurs externes", tels que des huiles de silicones. Mais on peut utiliser aussi des "agents séparateurs internes", éventuellement en mélange avec des agents séparateurs externes.
On peut préparer également des mousses durcissables à froid. Bien entendu, on peut préparer des mousses également par expansion de blocs ou par le procédé connu sur double tapis transporteur.
On peut préparer également des mousses de polyuréthannes souples, semi-rigides ou rigides. Elles trouvent des applications connues pour des produits de ce genre, par exemple comme matelas ou comme matières de rembourrage de sièges dans l'ameublement et l'industrie automobile, ainsi que pour la fabrication d'armatures, telles que celles qui sont utilisées dans l'industrie automobile, et enfin en tant qu'amortisseurs et matériaux de calorifugeage ou bien comme isolants contre le froid, par exemple dans l'industrie du bâtiment ou pour la fabrication d'appareils réfrigérants, ou dans l'industrie du textile, par exemple pour la fabrication d'épaulettes.
La présente invention concerne également un procédé de stabilisation d'une matière organique contre la dégradation oxydative, thermique ou induite par la lumière, caractérisé en ce qu'on incorpore dans cette matière, ou on applique sur cette matière au moins un composé de formule (1).
Comme on l'a déjà mis en évidence, on utilise les composés conformes à l'invention très avantageusement en tant que stabilisants dans des polyoléfines, principalement en tant que stabilisants thermiques. La stabilisation est excellente lorsqu'on les utilise, par exemple, en combinaison avec des phosphites ou des phosphonites organiques. Les composés conformes à l'invention présentent alors l'avantage d'être efficaces déjà en quantités infimes. On les utilise en des quantités comprises, par exemple, entre 0,0001 et 0,015, plus particulièrement entre 0,0001 et 0,008 % en poids par rapport à la polyoléfine. Le phosphite ou le phosphonite organiques sont utilisés avantageusement en quantités comprises de 0,01 et 2, notamment entre 0,01 et 1 % en poids, également par rapport à la polyoléfine. Comme phosphites ou phosphonites organiques on utilise de préférence ceux qui sont décrits dans la demande de brevet allemand P 4202276.2 [Cf. notamment les revendication de ce brevet, les exemples ainsi que les pages 5, dernier paragraphe jusqu'à la page 11] . Des phosphites et phosphonites particulièrement avantageux sont mentionnés également au point 4 de la liste des co-stabilisants ci-dessus.
L'invention a pour objet également de nouveaux composés répondant à la formule (5)
où Ri représente un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle Ci-C4, un cycloalkyle Cs-C8 non substitué ou substitué par un alkyle C1-C4; un alcényle C3-C25, un alcynyle C3-C25 ou un alkyle C3-C25 interrompu par l'oxygène, le soufre ou un radical ^.N-Ri6j R16 représentant l'hydrogène ou un alkyle Ci-Cg, R2 représente l'hydrogène, un alkyle Ci~ C2s, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle C5-Cg non substitué ou substitué par un alkyle C1-C4; un alcanoyloxyle C1-C25, un alcénoyloxyle C3-C25, un alcanoyloxyle C3-C25 interrompu par l'oxygène, le soufre ou N-Ri6; un cycloalkylcarbonyloxyle C6-C9, un benzoyloxyle ou un benzoyloxyle substitué par un alkyle C1-C12, Ri6 ayant la même signification que ci-dessus, R3 est un hydrogène, R4 et R5 représentent, indépendamment l'un de l'autre, l'hydrogène, un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle Cs-Cg non substitué ou substitué par un alkyle C1-C4; un alcoxyle Ci-Cia, un alcanoyloxyle C3.-C25, un alcénoyloxyle ¢3-025, un alcanoyloxyle C3-C25 interrompu par l'oxygène, le soufre ou^,N-Ri6; un cycloalkyl-carbonyloxyle C6-C9, un benzoyloxyle ou un benzoyloxyle substitué par un alkyle C3.-C12, Rie ayant la même signification que ci-dessus, ou, en outre, les symboles R2 et R3 ou les symboles R4 et R5 forment ensemble, et avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4, en outre, représente un radical - (CH2) n-CORn, où n est égal à 0, 1
Qr ou 2 et Ru représente un hydroxyle, [-0 1/r Mr+], un alcoxyle Ci-Cxs ou ^.R14
- N
Ris, Ri4 et R15 représentant, indépendamment l’un de l'autre, l'hydrogène ou un alkyle Οχ-Οχβ, M étant un cation métallique r-valent et r étant égal à 1, 2 ou 3, R8 et Rg représentent, indépendamment l'un de l'autre, l'hydrogène, un alkyle C1-C4 ou un alcoxyle C1-C4, et, lorsque R5 et Rg sont des hydrogènes, R4 représente en outre un radical de la formule (2) :
où Ri, R2/ Re et R9 ont la même signification que ci-dessus et R12 et R13 représentent, indépendamment l’un de l’autre, l'hydrogène, CF3, un alkyle C1-C12 ou un phényle, ou Ri2 et Ri3 forment ensemble, et avec l’atome de carbone auquel ils sont liés, un cycle cycloalkylidène C5-C8 non substitué ou substitué par 1 à 3 alkyles C1-C4; Rq représente un hydrogène ou un radical de la formule (6)
où Ri, R2, R3, R4, Rs, R8 et Rg ont la même signification que ci-dessus, sous réserve qu’au moins un des symboles R2, R4 et R5 soit autre que l'hydrogène, et le composé de formule (4) est exclu.
Les groupes préférés des nouveaux composés de formule (1) satisfont aux conditions préférées exprimées ci-dessus pour des composés conformes à l’invention.
En outre, on préfère des composés de formule (5) où Ri représente un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle Cs-C8 non substitué ou substitué par un alkyle C1-C4/ un alcényle C3-C25 ou un alkyle C3-C25 interrompu par l’oxygène, le soufre ou ^-Rig, et R12 et R13 signifient, indépendamment l’un de l’autre, l'hydrogène, un alkyle Ci-Ci2 ou un phényle.
De même, on préfère des composés de formule (5) où Ri représente un alkyle Ci-Ci8, un benzyle, un phényle, un phényle porteur d'un alkyle en C1-C4, un cycloalkyle C5-C8, un alcényle C3-Ci8, un alcynyle C3-C18 ou un alkyle C3-Ci8 interrompu par l'oxygène, le soufre ou ^N-R16, R2 représente un hydrogène, un alkyle Ci-Ci8, un benzyle, un phényle, un cycloalkyle Cs-Ca, un alcanoyloxyle Cj.-Cis, un alcénoyloxyle C3-Ci8 ou un benzoyloxyle, R4 et R5 sont, indépendamment l’un de l'autre, l'hydrogène, un alkyle Ci-C13, un benzyle, un phényle, un phényle substitué par un alkyle C1-C4, un cycloalkyle C5-C8, un alcoxyle Ci-C8, un alcanoyloxyle Cj-Cis, un alcénoyloxyle C3-C1B ou un benzoyloxyle, en outre R4 signifie un radical - (CH2) n-CORn, ou les symboles R2 et R3 ou les symboles R4 et R5, forment ensemble, et avec les atomes de carbone, auxquels ils sont liés, un cycle benzo.
On préfère également des composés de formule (5) où au moins deux des résidus R2, R3, R4 et R5 sont des hydrogènes.
De même, on préfère des composés de formule (5) où R3 et R5 sont des hydrogènes.
Un intérêt particulier est suscité par les composés de formule (5) où Ri est un méthyle, au moins deux des symboles R8 et Rg sont autres que l'hydrogène.
De même, on préfère des composés de formule (5) où Ri est un méthyle et R8 un alkyle C1-C4 ou un alcoxyle Ci~ C4.
On préfère particulièrement des composés de formule (5) où Ri est un méthyle.
De même, on préfère des composés de formule (5) où Ri signifie un alkyle C1-C13, un benzyle, un phényle, un cyclohexyle, un alcényle C3-C4, un alcynyle C3-C4 ou un alkyle C3-C6 interrompu par l'oxygène, R2 signifie l'hydrogène, un alkyle Ci-Ci8, un phényle ou un cyclohexyle, R3 est un hydrogène ou les radicaux R2 et R3 forment, avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4 représente un hydrogène, un alkyle C1-C6, un phényle, un cyclohexyle, un pivaloyloxyle, un alcoxyle C1-C4 ou un radical - (CH2) 2-C0Rh, où Ru signifie un alkyle Cx~C4, R5 est l’hydrogène, R8 et Rg signifient, indépendamment l'un de l’autre, un hydrogène, un alkyle Cx~C4 ou un alcoxyle Cx-C4, et, lorsque R6 est un hydrogène, R4 signifie, en outre, un radical de la formule (2) :
où Rx, R2, Re et R9 signifient comme ci-dessus et Rx2 et Rx3 représentent, indépendamment l’un de l'autre, CF3 ou un alkyle Cx-C4, Rê signifie l’hydrogène ou un radical de la formule (6) :
où Rx, R2, R3, R4, R5/ Re et Rg ont la même signifification que ci-dessus.
Les composés de formule (1) conformes à l’invention peuvent être préparés par des procédé connus en soi.
Par exemple, de façon préférentielle, un phénol de la formule (7)
où R2, R3, R4 et R5 ont les significations indiquées, est mis à régir à une température élevée, plus particulièrement à des températures comprises entre 130 et 200°, à l’état fondu ou dans un solvant, le cas échéant sous un vide modéré, avec un acide mandélique substitué sur le cycle phényle de la formule (8) où Ri, R7, R8, R9 et Rio ont les significations indiquées et Ri peut, en outre, être l'hydrogène. On préfère réaliser la réaction dans un solvant, tel que l'acide acétique ou l'acide formique, et dans un domaine de températures compris entre 50 et 130 °C. La réaction peut être catalysée par addition d'un acide, tel que l'acide chlorhydrique, l'acide sulfurique ou l'acide méthanesulfonique. La réaction peut être réalisée, par exemple, de la façon décrite dans les références bibliographiques citées dans l'introduction de la description.
Les acides mandéliques substitués sur le cycle phényle de la formule (8) sont connus dans la littérature ou peuvent être préparés, par exemple, de façon analogue selon W. Bradley et al. J. Chem. Soc. 1956 1622; EP-A-146 269 ou DE 2 944 295.
Les phénols de la formule (7) sont connus également ou on peut les obtenir par des procédés connus .
On peut préparer les composés bisphénoliques de la formule (9) selon Houben-Weyl, Methoden der organischen Chemie, tome 6/lc, 1030.
Les phénols obtenus par cette réaction qui répondent à la formule (1) où Ri signifie l'hydrogène, peuvent être éthérifiés par des méthodes d'éthérification généralement connues, par exemple selon Organikum 1986, pages 194-200, par exemple par alkylation dans des conditions basiques avec un halogénure d'alkyle de formule Ri1Br, un sulfate de dialkyle de formule (Ri1)2S04 ou un tosylate d'alkyle de formule
où Rj! représente Ri à l'exception de l'hydrogène.
La dimérisation des composés de formule (10) pour la préparation de composés de formule (1) où R6 est un groupe de la formule (3) [composés de formule (11)], est effectuée par oxydation avec, par exemple, l'iode, dans des conditions basiques, dans un solvant organique, à température ambiante. La base sera en particulier l'éthylate de sodium, et le solvant 1'éthanol ou l'éther diéthylique.
Les exemples suivants expliquent plus en détail l'invention. Les indications en parties ou en pourcentages sont relatives au poids.
Exemple 1 : Préparation de la 5,7-di-tert-butyl-3-(4-éthoxyphényl)-benzofuranne-2-one (composés (101), tableau 1)
On agite pendant 2 h à 140-150 °C sous l'azote un mélange de 309 g (1,50 Mol) de 2,4-di-tert-butyl-phénol et 196,2 g (1,0 Mol) d'acide 4-éthoxymandélique. Ensuite, on continue à agiter pendant 1,5 h à 150 °C sous un vide modéré (50 mbar) . On distille l'excès de 2,4-di-tert-butylphénol sous vide poussé. On obtient 337,7 g (92%) de 5,7-di-tert-butyl-3-(4-éthoxyphényl)-benzofuranne-2-one, point de fusion 132-134 °C, (composé (101), tableau 1), par cristallisation du résidu dans 150 ml de xylène et de 250 ml d'éthanol.
A partir des phénols correspondants et des acides mandéliques substitués, on prépare de façon analogue, comme dans l'exemple 1, les composés de (102) à (128), ainsi que (130) et de (136) à (141).
Mode opératoire pour la préparation d'acides 4-alcoxy-mandéliques : 20,8 g (0,10 Mol) de monohydrate de sel sodique d'acide 4-hydroxymandélique et 6,6 g (0,10 Mol) d'hydroxyde de potassium avec 1,0 g (6,7 mMol) d'iodure de sodium sont dissous dans 75 ml de méthanol. Puis, on ajoute 0,12 Mol d’un bromure d'alkyle (on utilise le chlorure de méthallyle dans le cas du méthallyle) et on fait bouillir pendant 16 h sous reflux en atmosphère d'azote. On concentre le mélange réactionnel dans un évaporateur rotatif sous vide et le résidu est acidifié par l'acide chlorhydrique concentré. On extrait le produit trois fois par l'acétate de butyle. Les phases organiques sont lavées à l'eau, réunies, séchées sur sulfate de sodium et concentrées dans un évaporateur rotatif sous vide. On obtient par cristallisation du résidu dans du toluène/benzène les acides 4-alcoxy-mandéliques, par exemple l'acide 4-méthallyloxy-mandélique, point de fusion 121-126° (65%); l'acide 4-n-tetradécyloxy-mandélique, point de fusion 104-107°C (68%); l'acide 4-n-tetradécyloxy-mandélique, point de fusion 104-107°C (68%); l'acide 4-n-octoxy-mandélique, point de fusion 96-99°C (58%); l'acide 4-n-hexoxy-mandélique, point de fusion 103-106°C (69%); l'acide 4-n-octadécyloxy-mandélique, point de fusion 103-109°C (29%); l'acide 4-n-butoxy-mandélique, point de fusion 132-134°C (67%); l'acide 4-cyclohexyloxy-mandélique, point de fusion 147-151 °C (10%) et l'acide 4-propargyloxy-mandélique, résine (66%) .
Préparation de l'acide 4-benzyloxy-mandélique :
On agite pendant 17 heures à 70°C une solution de 41,6 g (0,20 Mol) de monohydrate de sel sodique d'acide 4-hydroxymandélique, de 9,6 g (0,24 Mol) d'hydroxyde de sodium et de 27,9 g (0,22 Mol) de chlorure de benzyle dans 50 ml d'eau. Par la suite, on dilue avec 50 ml d'eau et on ajoute encore une fois 4,0 g (0,10 Mol) d'hydroxyde de sodium. Le mélange réactionnel est porté à l'ébullition pendant une heure sous reflux, puis refroidi, acidifié par l'acide chlorhydrique concentré et on filtre le produit qui a précipité. On lave alors le résidu avec de l'eau froide, puis on le sèche sous vide poussé. On obtient 35,6 g (69%) d'acide 4-benzyloxy-mandélique, point de fusion 148-155°C.
Mode opératoire pour la préparation d'acides 4-alcoxy-3,5-diméthylmandéliquee :
On ajoute goutte à goutte, en 15 min environ, 0,0375 Mol de sulfate de dlalkyle à une solution, agitée à 10Û°C, de 4,9 g (0,025 Mol) d'acide 3,5-diméthyl-4-hydroxymandélique et de 3,0 g (0,075 Mol) d’hydroxyde de sodium dans 10 ml d'eau. Ensuite, on continue à agiter le mélange réactionnel à 100 °C pendant 1 heure encore. Après refroidissement, on acidifie avec l'acide chlorhydrique concentré et on extrait le produit précipité à deux reprises avec chaque fois 30 ml d'acétate d'éthyle. On lave les phases organiques avec de l'eau, on les réunit, sèche sur sulfate de sodium et concentre dans un évaporateur rotatif sous vide. On obtient des acides 4-alcoxy-3, 5-diméthyl-mandéliques, par exemple l’acide 3,5-diméthyl-4-méthoxy-mandélique, point de fusion 134-136°C (83%) ou l’acide 4-éthoxy-3,5-diméthylmandêlique, résine (81%).
Mode opératoire pour la préparation d’acides 4-hydroxy-mandéliques î
On dissout 0,30 Mol de phénol de départ dans 150 ml de solution 2N d'hydroxyde de sodium en atmosphère d'azote. Après refroidissement à +5°C, on ajoute 4,8 g (0,12 Mol) d'hydroxyde de sodium et 13,3 ml (0,12 Mol) d’acide glyoxalique aqueux et on agite le mélange réactionnel pendant 4 heures à température ambiante. Après chaque fois 4 heures, on ajoute deux fois encore 0,12 Mol d'hydroxyde de sodium et d’acide glyoxylique (total de 0,36 Mol), Par la suite, on agite pendant 12 heures encore, puis on neutralise avec de l'acide chlorhydrique concentré et on lave deux fois avec chaque fois 75 ml d'éther de pétrole. On acidifie alors la phase aqueuse avec de l’acide chlorhydrique concentré et on extrait à plusieurs reprises avec de l'éther. Les phases organiques sont réunies, séchées sur sulfate de magnésium et concentrées dans un évaporateur rotatif sous vide. Ainsi, on obtient les produits suivants : l'acide 3,5-diméthyl-4-hydroxymandélique, point de fusion 132-135°C (85%), l'acide 4-hydroxy-3-méthyl- mandélique, point de fusion 115-120°C, rendement 55%; l'acide 4-hydroxy-3-tert-butyl-mandélique, point de fusion 156-158°C, rendement 26%; et l'acide 3-isopropyl-4-hydroxy-2-méthyl-mandélique, point de fusion 114-119°C, rendement 20%.
Exemple 2 : Préparation de la bis-3,3'-[5,7-di-tert- butyl-3-(4-éthoxyphényl)benzofuranne-2-one] (composé (129), tableau 1).
On ajoute en atmosphère d'azote 16,5 g (45 mMol) de 5,7-di-tert-butyl-3-(4-éthoxyphényl)benzofuranne-2-one (composé (101), exemple 1) à une solution d'éthylate de sodium préparée par addition de 1,04 g (45 mMol) de sodium à 60 ml d'éthanol absolu. Ensuite, pendant environ 10 minutes, on ajoute goutte à goutte à température ambiante une solution de 5,7 g (45 mMol) d'iode dans 45 ml d'éther diéthylique. On agite le mélange réactionnel pendant 5 minutes encore, on fait réagir ensuite avec 2,0 g (10,6 mMol) de pyrosulfite de sodium et on dilue avec 250 ml d'eau. On extrait le précipité obtenu avec du chlorure de méthylène. Puis, les phases organiques sont séparées, lavées avec de l'eau, séchées sur sulfate de sodium et concentrées dans un évaporateur rotatif sous vide. On obtient 15,4 g (94%) de bis-3,3'-[5,7-di-tert-butyl-3-(4 -éthoxyphényl)benzofuranne-2-one], point de fusion 219-222°C (composé (129), tableau 1) par cristallisation du résidu dans éthanol/chlorure de méthylène.
Exemple 3 : Préparation de la 3-(4-éthoxyphényl)-5- pivaloyloxy-benzofuranne-2-one (composé (135), tableau 1)
On ajoute en atmosphère d'azote, à 95 °C, 2,41 g (20,0 mMol) de chlorure de pivaloyle goutte à goutte pendant 10 min. à une suspension agitée de 2,70 g (10,0 mMol) de 3-(4-éthoxyphényl)-5-hydroxy-benzofuranne-2-one (composé (136), tableau 1, exemple 1) dans 10 ml de xylène et 0,1 ml d’acide méthane sulfonique. Ensuite, on fait boullir sous reflux le mélange réactionnel homogène, clair, pendant 2,5 heures encore, puis on le concentre sous un vide modéré. Le résidu est repris dans du dichlorométhane et lavé avec une solution saturée de bicarbonate de sodium et avec de l'eau. On réunit les phases organiques, on les sèche sur sulfate de sodium et on les concentre dans un évaporateur rotatif sous vide. Le résidu donne 1,95 g (55%) de 3-(4-éthoxyphényl)-5-pivaloyloxy-benzofuranne-2-one, huile (composé (135) , tableau 1) .
Le radical
dans le tableau 1 représente un radical cyclohexyle.
Tableau. 1
Tableau 1. (suite).
Tableau 1 (suite) ~
Tableau 1 (suite) -
Tableau 1 (suite)·
Tableau 1 (suite)
Tableau 1 (suite)
Tableau 1 (suite)
Tableau 1 (suite)
Tableau 1 (suite)
Tableau 1 (suite
Exemple 4 : Stabilisation du polypropylène au cours de l'extrusion multiple.
On mélange 1,3 kg de polypropylène en poudre (Profax 6501) préstabilisé avec 0,025 % d1Irganox®1076 (ester n-octadécylique de l'acide 3-[3,5-di-tert-butyl-4-hydroxyphényl]propionique (ayant un indice de fusion de 3,2 mesuré à 230°C et avec 2,16 kg), avec 0,05% d'Irganox®1010 (tétrakis-[3-(3, 5-di-tert-butyl-4-hydroxyphényle)-propionate] de pentaérythritol, 0,05% de stéarate de calcium, 0,03% de dihydrotalcite(DHT 4A®, Kyowa Chemical Industry Co. Ltd., [Mg4.sAl2 (OH) 13C03.3,5 H20] ) et 0,015% d'un composé figurant au tableau 1. Ce mélange est extrudé dans une extrudeuse équipée d'un cylindre d'un diamètre de 20 mm et d’une longueur de 400 mm à une vitesse de 100 tours par minute, où les températures des 3 trois zones de chauffage sont ajustées à : 260 °C, 270°C et 280°C. On passe le profilé dans un bain d'eau afin de le refroidir et ensuite on procède à sa granulation. On répète l'extrusion des granulés. On mesure l'indice de fusion après 3 extrusions (à 230°C avec 2,16 kg). La forte augmentation de l'indice de fusion signifie une importante dégradation de la chaîne, donc une mauvaise stabilisation. Les résultats ont rassemblés dans le tableau 2.
Tableau 2 :______
_
Exemple 5 : Stabilisation du polyéthylène au cours du traitement.
On mélange 100 parties de polyéthylène en poudre (Lupolen®52 60 Z) avec 0,05 partie de tétrakis[3-(3,5-di-tert-buty1-4-hydroxyphényl)-propionate] de pentaérythritol, 0,05 partie de phosphite de tris-(2,4-di-tert-butyl-phényle) et 0,05 partie d’un composé du tableau 1 et on malaxe le mélange dans un plastographe Brabender à 220°C et 50 tours par minute. On enregistre en continu la résistance au malaxage exprimée sous la forme d'un couple de torsion pendant la durée de cette opération. Au cours du malaxage, le polymère, après une constance relativement longue, commence à se réticuler, ce qui se manifeste sous forme d'une augmentation rapide du couple de torsion. Dans le tableau 3, la durée est exprimée comme mesure de l'effet stabilisant jusqu'à une augmentation sensible du couple de torsion. Plus ce temps est long, plus l'effet stabilisant est bon.
Tableau 3 :
_____
Exemple 6 : Stabilisation d'élastomères thermoplastique à base de styrène.
Dans un plastographe Brabender, on malaxe pendant 30 minutes à 200 °C et 60 tours par minute, 7 0 g de styrène-butadiène-styrène (SBS, ©Finaprène 416) avec 0,25% du stabilisant du tableau 1 à étudier. La pente de la courbe du couple de torsion exprime le temps d'induction, c'est-à-dire la durée de malaxage en minutes jusqu'à l'augmentation de la valeur du couple de torsion de 1 Nm après la valeur minimum du couple de torsion. L'importante augmentation du temps d'induction signifie une bonne stabilisation. Les résultats sont indiqués dans le tableau 4.
Tableau 4_
Exemple 7 : Stabilisation du caoutchouc de polybutadiène.
On malaxe pendant 30 minutes à 160 °C 70 g de polymère (Buna CB 529 C) avec 0,25% du stabilisant à essayer, indiqué dans le tableau 1, dans un plastographe Brabender et à 60 tours par minute. Le temps d'induction est lu sur la courbe du couple de torsion, c'est-à-dire la durée de malaxage en minutes jusqu'à l'augmentation du couple de torsion de 1 Nm après le minimum du couple de torsion. L'augmentation importante du temps d'induction signifie une bonne stabilisation. Les résultats sont rassemblés dans le tableau 5.
Tableau 5______________ ____________________
Exemple 8 : Stabilisation d'une mousse souple polyéther-polyuréthanne.
On dissout 470 mg (0,3% par rapport au polyol) d'un mélange stabilisant conforme à l'invention (tableau 6) dans 157 g d'un polyéther-polyol exempt d'antioxydants, ®Lupranol 2045 (polyéther-polyol trifonctionnel avec groupes hydroxyles primaires; indice d'hydroxyle 35 mg KOH/g, teneur en eau inférieure à 0,1%, indice d'acidité inférieur à 0,1 mg KOH/g). On ajoute 10,24 g d'une solution contenant 1,74 ®TECOSTAB [polysilicone de la société Goldschmidt, DE], 0,48 g de diazabicyclooctane [catalyseur aminé] et 0,8 g d'eau et on agite vigoureusement pendant 60 secondes à 100 tours/min. Ensuite, on ajoute 3,2 g d'une solution contenant 0,32 g d'octoate de zinc (catalyseur) dans 2,9 g du polyol ci-dessus et on répète l'agitation vigoureuse pendant 60 secondes à 100 tours/minute. Immédiatement après, tout en agitant intensément, on ajoute 98 g d'un isocyanate (©Lupranat T80 de la société BASF; mélange de diisocyanates de toluylène-2,4- et toluylène-2,6) et 6 secondes après, on verse le mélange dans un moule revêtu. On mesure la température exothermique au cours de l’expansion en un bloc de mousse. Les blocs de mousse sont refroidis dans une étuve à 5°C pendant 24 h et stockés. On découpe des tranches d’une épaisseur de 2 cm dans le milieu des blocs et à partir de celles-ci, on découpe des éprouvettes rondes (de forme cylindrique) à l'aide d’une perceuse. Les échantillons sont mis dans un bêcher et soumis au viellissement à l’air à 190°C dans un thermostat à bloc Alu préchauffé. On détermine le jaunissement selon la norme ASTM D-1925, exprimé en Yellowness Index (YI). Plus tardivement apparaît le jaunissement, plus le Yellowness Index est bas, et plus la stabilisation est bonne. Les résultats sont rassemblés dans le tableau 6.
Tableau 6 :
A01 est un mélange de diphénylamines polyalkylées (®Irganox 5057) AO2 est le 4,4 ’-thio-bis (6-tert-butyl-3-méthylphénol) (®Santonox R) A03 est le 2,2'-méthylène-bis(6-tert-butyl-4- mé thylphénol)
Claims (24)
1. Composition contenant a) une matière organique soumises à la dégradation oxydative, thermique ou induite par la lumière et b) au moins un composé selon la formule (1)
où Ri représente un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle Ci~ C4, un cycloalkyle Cs-Cg non substitué ou substitué par un alkyle C1-C4, un alcényle C3-C25, un alcynyle C3-C25 ou un alkyle C3-C25 interrompu par l'oxygène, le soufre ou un radical^N-Risr Ri6 représentant l'hydrogène ou un alkyle Ci-Cg, R2, R3/· R4 et R5 représentent chacun, indépendamment l'un de l'autre, l'hydrogène, un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle Cs-Cg non substitué ou substitué par un alkyle C1-C4; un alcoxyle Ci-Cig, un hydroxyle, un alcanoyloxyle C1-C25, un alcénoyloxyle C3-C25/ un alcanoyloxyle C3-C25 interrompu par l'oxygène, le soufre ou un radical^N-Ri6, un cycloalkylcarbonyloxyle C6-C9, un benzoyloxyle ou un benzoyloxyle substitué par un alkyle Ci-C12 et Ri6 a la même signification que ci-dessus, ou encore, les radicaux R2 et R3 ou les radicaux R4 et R5 forment ensemble, avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4 représente en outre un radical -(CH2)ft-CORu où n est égal à 0, 1 ou 2 et Ru représente un hydroxyle, un [-0® 1/r Mr+], un alcoxyle Ci“C18 ou
Ri4 et Ri5 représentent, indépendamment l'un de l'autre, l'hydrogène ou un alkyle Ci-Cig, M est un cation métallique r-valent et r est égal à 1, 2 ou 3, R7, R8, Rg et Rio représentent, indépendamment l'un de l'autre, l'hydrogène, un alkyle C1-C4 ou un alcoxyle C1-C4, à condition qu'au moins un des symboles R7, Re/ R9 et Rio soit un hydrogène, et, lorsque R3, R5, R6, R7 et Ri0 sont des hydrogènes, R4, signifie en outre un radical de la formule (2) : (2) où Ri, R2, Rg et Rg ont la signification ci-dessus et R12 et R13 représentent, indépendamment l'un de l'autre, l'hydrogène, CF3, un alkyle C1-C12 ou un phényle, ou R12 et R13 forment ensemble, avec l'atome de carbone auquel ils sont liés, un cycle cycloalkylidène Cs-Cg non substitué ou substitué par 1 à 3 alkyles C1-C4; Rô représente un hydrogène ou un radical de la formule (3):
OÙ Ri, R2 , R-4/· R5 r R 71 R9 et Rio Ont la signification ci-dessus, et le composé de formule (4) est exclu.
2. Composition selon la revendication 1 où Ri signifie un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle Cs-Cg non substitué ou substitué par un alkyle C1-C4 ; un alcényle C3-C25 ou un alkyle C3-C25 interrompu par l'oxygène, le soufre ou^.N-R16, et Ri2 et Ris, représentent chacun, indépendamment l'un de l'autre, un hydrogène, un alkyle C1-C12 ou un phényle.
3. Composition selon la revendication 1, où Ri représente un alkyle Ci-Cis, un benzyle, un phényle, un phényle substitué par un alkyle C1-C4, un cycloalkyle C5-C8, un alcényle C3-Cie, un alcynyle C3-C18 ou un alkyle C3-C18 interrompu par l'oxygène, le soufre ou^N-Ri6, R2, R3, R4 et R5 représentent, indépendamment l'un de l'autre, un alkyle Ci-Ci3, un benzyle, un phényle, un cycloalkyle C5-C8, un alcoxyle Ci-Cs, un hydroxyle, un alcanoyloxyle Ci-Cis, un alcénoyloxyle C3-C18 ou un benzoyloxyle, R4, représente en outre un radical - (CH2) n-CORn, ou les radicaux R2 et R3 ou les radicaux R4 et R5 forment ensemble, avec les atomes de carbone auxquels ils sont liés, un cycle benzo.
4. Composition selon la revendication 1 où au moins deux des symboles R2, R3, R4 et R5 représentent un hydrogène.
5. Composition selon la revendication 1 où R3 et R5 sont 11hydrogène.
6. Composition selon la revendication 1 où Ri représente un alkyle Ci-Ci8, un benzyle, un phényle, un cyclohexyle, un alcényle C3-C12, un alcynyle C3-C12 ou un alkyle C3-Ci8 interrompu par l’oxygène, R3, R5, R7 et Rio sont, indépendamment l'un de l'autre, un hydrogène ou un alkyle C1-C4, R2 représente un hydrogène, un alkyle Cx~ Ci8, un phényle ou un cyclohexyle, ou les radicaux R2 et R3 forment, avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4 représente un hydrogène, un alkyle Ci-C12, un phényle, un cyclohexyle, un hydroxyle, un alcanoyloxyle C1-C12, un alcoxyle Ci-C8 ou un radical - (CH2) n"CORu où n est égal à 0, 1 ou 2 et Ru représente un hydroxyle ou un alcoxyle C1-C12, R4 représente en outre un radical de formule (2) :
où Ri, R2, Rs et Rg ont la signification ci-dessus et Ri2 et R13 représentent chacun, indépendamment l'un de l'autre, un hydrogène, CF3, un alkyle Cx~Ci2 ou un phényle ou R32 et Ri3 forment ensemble, avec l'atome de C auquel ils sont liés, un cycle cycloalkylidène Cs-Cg.
7. Composition selon la revendication 1 où Rx représente un alkyle C2-C18, un benzyle, un phényle, un phényle substitué par un alkyle Ci~C4, un cycloalkyle C5-C8, un alcényle C3-Cx8, un alcynyle C3-C18 ou un alkyle C3-Cx8 interrompu par l'oxygène, le soufre ou^N-Rx6·
8. Composition selon la revendication 1 où, lorsque Ri est un méthyle, au moins un des symboles R7, Rs, R9 et Rio n'est pas l'hydrogène.
9. Composition selon la revendication 1 où, lorsque Rj. est un méthyle, Rs représente un alkyle C1-C4 ou un alcoxyle C1-C4.
10. Composition selon la revendication 1 où Ri représente un alkyle Ci-Cisr un benzyle, un phényle, un cyclohexyle, un alcényle C3-C4, un alcynyle C3-C4 ou un alkyle C3-C6 interrompu par l'oxygène, R2 représente un hydrogène, un alkyle Ci-Cis, un phényle ou un cyclohexyle, R3, R5, R7 et Rio sont des hydrogènes, ou les radicaux R2 et R3 forment ensemble, avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4 représente un hydrogène, un alkyle C1-C6, un phényle, un cyclohexyle, un hydroxyle, un pivaloyloxyle, un alcoxyle C1-C4 ou un radical - (CH2) 2-CORn où Ru représente un alkyle C1-C4, R8 et R9 représentent, indépendamment l'un de l'autre, un hydrogène, un alkyle C1-C4 ou un alcoxyle C1-C4, et lorsque Rç est un hydrogène, R4 représente en outre un radical de la formule (2) :
où Ri, R2, R8 et R9 ont la signification ci-dessus et R12 et R13 représentent chacun, indépendamment l'un de l'autre, CF3 ou un alkyle C1-C4, Rê représente un hydrogène ou un radical de la formule (3)
où Rlf R2, R3, r4/ r5 , R7, Rs , r9 et Ri0 ont la signification ci-dessus.
11. Composition selon la revendication 1 où le composant a) est un polymère synthétique.
12. Composition selon la revendication 1 où le composant b) est présent en une quantité comprise entre 0,0005 et 5% par rapport au poids du composant a).
13. Composition selon la revendication 1, contenant en outre un phosphite ou un phosphonite organique.
14. Composé de formule (5)
où Rx représente un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle C5-C8 non substitué ou substitué par un alkyle Ci-Ci ; un alcényle C3-C25, un alcynyle C3-C25 ou un alkyle C3-C25 interrompu par l'oxygène, le soufre ou ^N-R1S, R16 représentant un hydrogène ou un alkyle Ci-C8, R2 représente un hydrogène, un alkyle C1-C25, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle C5-C8 non substitué ou substitué par un alkyle C1-C4 ; un alcanoyloxyle C1-C25, un alcénoyloxyle C3-C25, un alcanoyloxyle C3-C25 interrompu par l'oxygène, le soufre ou > -r16; un cycloalkylcarbonyloxyle C6-Cg, un benzoyloxyle ou un benzoyloxyle substitué par un alkyle C1-C12, et Ris a la signification ci-dessus, R3 est un hydrogène, R4 et R5, représentent chacun indépendamment l’un de l'autre, un hydrogène, un alkyle Ci-C2s, un phénylalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle C5-C8 non substitué ou substitué par un alkyle C1-C4 ; un alcoxyle Ci-Cis, un alcanoyloxyle C1-C25, un alcénoyloxyle C3-C25, un alcanoyloxyle C3-C25 interrompu par l'oxygène, le soufre ou ^N-Ri6 ; un cycloalkylcarbonyloxyle C6-C9, un benzoyloxyle ou un benzoyloxyle substitué par un alkyle C1-C12, et Ri6 a la signification ci-dessus, ou encore les radicaux R2 et R3 ou les radicaux R4 et R5 forment, avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4 représente en outre un radical -(CH2)n-CORn où n est égal à 0, 1 ou 2 et Ru représente un hydroxyle, [-0® 1/r Mr+], un alcoxyle C3.-C18 ou ^*Ri5, Ri4 et R15 représentent, indépendamment l'un de l'autre, un hydrogène ou un alkyle Ci-Cie, M est un cation métallique de valence égale à r et r est égal à 1, 2 ou 3, Ra et Rg représentent, indépendamment l'un de l'autre, un hydrogène, un alkyle C1-C4 ou un alcoxyle C1-C4, et, lorsque R5 et R6 sont des hydrogènes, R4, représente en outre un radical de formule (2) :
où Ri, R2, Re et Rg ont la signification ci-dessus et R12 et R13 représentent chacun, indépendamment l'un de l'autre, un hydrogène, CF3, un alkyle Ci~Ci2 ou un phényle ou forment ensemble, avec l'atome de C auquel ils sont liés, un cycle cycloalkylidène C5-C9 porteur de 1 à 3 alkyles Ci-C4; Rô représente l'hydrogène ou un radical de formule (6) :
où Rlf R2, R3, R4, R5, Rs et R9 ont la signification ci-dessus , à la condition qu’au moins un des symboles R2, R4 et R5 soient autres que l'hydrogène, et le composé de formule (4) est exclu.
15. Composés selon la revendication 14 où Ri représente un alkyle C1-C25/ un phényalkyle C7-C9, un phényle non substitué ou substitué par un alkyle C1-C4, un cycloalkyle Cs-C8 non substitué ou substitué par un alkyle C1-C4; un alcényle C3-C25 ou un alkyle C3-C25 interrompu par l'oxygène, le soufre ou ^N-Ri6, et R12 et R13 représentent, indépendamment l'un de l'autre, un alkyle C1-C12 ou un phényle.
16. Composés selon la revendication 14 où Ri représente un alkyle Ci-Cie, un benzyle, un phényle, un phényle substitué par un alkyle C1-C4 ; un cycloalkyle Cs-C8, un alcényle C3-Ci8, un alcynyle C3-Ci8 ou un alkyle C3-Ci8 interrompu par l'oxygène, le soufre ou ^N-Rie/ R2 représente un hydrogène, un alkyle Ci-Ci8, un benzyle, un phényle, un cycloalkyle Cs-C8, un alcénoyloxyle Ci~ Ci8, un alcénoyloxyle C3~Ci8 ou un benzoyloxyle, R4 et R5 sont, indépendamment l'un de l'autre, un hydrogène, un alkyle Cx-Cis, un benzyle, un phényle, un phényle substitué par un alkyle C1-C4 ; un cycloalkyle C5-C8, un alcoxyle Cx-Cs, un alcanoyloxyle Cx-Rxs, un alcénoyloxyle C3-C18 ou un benzoyloxyle, R4, représente en outre un radical (CH2) n“CORxx, ou les radicaux R2 et R3 ou les radicaux R4 et R5 forment, avec les atomes de carbone auxquels ils sont liés, un cycle benzo.
17. Composés selon la revendication 14, où au moins deux des symboles R2, R3, R4 et R5 sont l'hydrogène.
18. Composés selon la revendication 14 où R3 et R5 sont 1'hydrogène.
19. Composés selon la revendication 14 où Rx représente un alkyle C2-C18, un benzyle, un phényle, un phényle substitué par un alkyle Cx~C4 ; un cycloalkyle C5-C8, un alcényle C3-CX8, un alcynyle C3-CX8 ou un alkyle interrompu par l'oxygène, le soufre ou^N-Rx6.
20. Composés selon la revendication 14 où, lorsque Rx est un méthyle, au moins un des symboles R8 et Rg représente 1'hydrogène.
21. Composés selon la revendication 14 dans lesquels, lorsque Ri est un méthyle, Rs représente un alkyle en C1-C4 ou un alcoxy en C1-C4.
22. Composés selon la revendication 14 où Rx représente un alkyle Cx-Cxa, un benzyle, un phényle, un cyclohexyle, un alcényle C3~C4, un alcynyle C3~C4 ou un alkyle C3-C6 interrompu par l'oxygène, R2 représente l'hydrogène, un alkyle Cx-C18, un phényle ou un cyclohexyle, R3 est un hydrogène, ou les radicaux R2 et R3 forment, avec les atomes de carbone auxquels ils sont liés, un cycle benzo, R4 représente un hydrogène, un alkyle Cx~C6, un phényle, un cyclohexyle, un pivaloyloxyle, un alcoxyle Cx~C4 ou un radical -(CH2)2-CORxx où Rxx représente un alkyle Cx-C4, R5 est un hydrogène, Rs et R9 représentent, indépendamment l'un de l'autre, l'hydrogène, un alkyle C1-C4 ou un alcoxyle Ci-C4, et, lorsque Rs est un hydrogène, R4 représente en outre un radical de formule (2) :
où Ri, R2, Re et Rg ont la signification ci-dessus et R12 et R13 représentent, indépendamment l'un de l'autre, CF3 ou un alkyle C1-C4, R6 représente un hydrogène ou un radical de formule (6)
où Ri, R2, R3, R4, R5, Rs et Rg ont la signification ci-dessus .
23. Utilisation des composés répondant à la formule (1) définie dans la revendication 1 comme stabilisants de matières organiques contre la dégradation oxydative, thermique ou induite par la lumière.
24. Procédé pour la stabilisation d'une matière organique contre la dégradation oxydative, thermique ou induite par la lumière, caractérisé en ce qu’on incorpore à cette matière, ou on applique sur cette matière, au moins un composé répondant à la formule (1) définie dans la revendication 1.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CH165492 | 1992-05-22 | ||
| CH165492 | 1992-05-22 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| BE1006549A3 true BE1006549A3 (fr) | 1994-10-11 |
Family
ID=4215518
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BE9300513A BE1006730A4 (fr) | 1992-05-22 | 1993-05-18 | Application de 3-(alcoxyphenyl)benzofuranne-2-ones comme stabilisants et nouveaux composes de ce type. |
| BE9300513D BE1006549A3 (fr) | 1992-05-22 | 1993-05-18 | Application de 3-(alcoxyphenyl)benzofuranne-2-onescomme stabilisants et nouveaux composes de ce typ e |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BE9300513A BE1006730A4 (fr) | 1992-05-22 | 1993-05-18 | Application de 3-(alcoxyphenyl)benzofuranne-2-ones comme stabilisants et nouveaux composes de ce type. |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US5367008A (fr) |
| JP (1) | JPH06287185A (fr) |
| KR (1) | KR100286117B1 (fr) |
| BE (2) | BE1006730A4 (fr) |
| CA (1) | CA2096486A1 (fr) |
| CZ (1) | CZ290111B6 (fr) |
| DE (1) | DE4316876A1 (fr) |
| FR (1) | FR2691470B1 (fr) |
| GB (1) | GB2267088B (fr) |
| IT (1) | IT1264453B1 (fr) |
| NL (1) | NL9300784A (fr) |
| SK (1) | SK49593A3 (fr) |
| TW (1) | TW260686B (fr) |
Families Citing this family (190)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH686306A5 (de) * | 1993-09-17 | 1996-02-29 | Ciba Geigy Ag | 3-Aryl-benzofuranone als Stabilisatoren. |
| IT1269197B (it) | 1994-01-24 | 1997-03-21 | Ciba Geigy Spa | Composti 1-idrocarbilossi piperidinici contenenti gruppi silanici atti all'impiego come stabilizzanti per materiali organici |
| TW350859B (en) * | 1994-04-13 | 1999-01-21 | Ciba Sc Holding Ag | HALS phosphonites as stabilizers |
| TW297822B (fr) * | 1994-04-13 | 1997-02-11 | Ciba Geigy Ag | |
| TW317568B (fr) * | 1994-04-13 | 1997-10-11 | Ciba Sc Holding Ag | |
| US5556973A (en) | 1994-07-27 | 1996-09-17 | Ciba-Geigy Corporation | Red-shifted tris-aryl-s-triazines and compositions stabilized therewith |
| EP0711804A3 (fr) | 1994-11-14 | 1999-09-22 | Ciba SC Holding AG | Stabilisateurs à la lumière latents |
| TW303381B (fr) | 1994-12-05 | 1997-04-21 | Ciba Sc Holding Ag | |
| TW399079B (en) * | 1995-05-12 | 2000-07-21 | Ciba Sc Holding Ag | Polyether polyol and polyurethane compositions protected against oxidation and core scorching |
| TW325490B (en) | 1995-06-23 | 1998-01-21 | Ciba Sc Holding Ag | Polysiloxane light stabilizers |
| US6493838B1 (en) * | 1995-09-29 | 2002-12-10 | Kabushiki Kaisha Toshiba | Coding apparatus and decoding apparatus for transmission/storage of information |
| EP0771814A1 (fr) | 1995-11-02 | 1997-05-07 | Ciba SC Holding AG | Modifications amorphes et cristallines 1,1',1''-nitrilotriéthyl-tris (2,2'-méthylène-bis-(4,6-di-tert-butyl-phényl)) phosphite |
| US6521681B1 (en) | 1996-07-05 | 2003-02-18 | Ciba Specialty Chemicals Corporation | Phenol-free stabilization of polyolefin fibres |
| DE59702969D1 (de) * | 1996-10-30 | 2001-03-08 | Ciba Sc Holding Ag | Stabilisatorkombination für das Rotomolding-Verfahren |
| EP0850946A1 (fr) * | 1996-12-24 | 1998-07-01 | Ciba SC Holding AG | Dérivés cycliques d'acides phosphiniques comme stabilisants |
| DE59810298D1 (de) * | 1997-02-05 | 2004-01-15 | Ciba Sc Holding Ag | Stabilisatoren für Pulverlacke |
| ES2149678B1 (es) | 1997-03-06 | 2001-05-16 | Ciba Sc Holding Ag | Estabilizacion de policarbonatos, poliesteres y policetonas. |
| DE19714614A1 (de) * | 1997-04-09 | 1998-10-15 | Agfa Gevaert Ag | Farbfotografisches Silberhalogenidmaterial |
| DE19820157B4 (de) | 1997-05-13 | 2010-04-08 | Clariant Produkte (Deutschland) Gmbh | Neue Verbindungen auf Basis von Polyalkyl-1-oxa-diazaspirodecan-Verbindungen |
| JPH1160556A (ja) * | 1997-08-11 | 1999-03-02 | Sumitomo Chem Co Ltd | ピペリジン系化合物、その製法及びその用途 |
| CA2312999A1 (fr) * | 1997-12-08 | 1999-06-17 | Cytec Technology Corp. | Aminotriazines a substitution amine encombree et a coiffe terminale morpholino, ainsi que leur utilisation en tant que photostabilisants |
| GB2333296B (en) * | 1998-01-15 | 2000-09-27 | Ciba Sc Holding Ag | Stabilisers and anti-ozonants for elastomers |
| US6239276B1 (en) | 1998-06-22 | 2001-05-29 | Cytec Technology Corporation | Non-yellowing para-tertiary-alkyl phenyl substituted triazine and pyrimidine ultraviolet light absorbers |
| US6297377B1 (en) | 1998-06-22 | 2001-10-02 | Cytec Technology Corporation | Benzocycle-substituted triazine and pyrimidine ultraviolet light absorbers |
| AU4695699A (en) | 1998-06-22 | 2000-01-10 | Ciba Specialty Chemicals Holding Inc. | Poly-trisaryl-1,3,5-triazine carbamate ultraviolet light absorbers |
| JP2002518486A (ja) | 1998-06-22 | 2002-06-25 | サイテク・テクノロジー・コーポレーシヨン | 赤側にシフトしたトリスアリール−1,3,5−トリアジン紫外線光吸収剤 |
| GB2343007B (en) | 1998-10-19 | 2001-11-07 | Ciba Sc Holding Ag | Colour photographic material |
| US6441071B1 (en) | 1999-09-01 | 2002-08-27 | Dow Global Technologies Inc. | Polycarbonate resin compositions comprising cyanacrylic acid ester stabilizer compounds |
| GB0004437D0 (en) | 2000-02-25 | 2000-04-12 | Clariant Int Ltd | Synergistic combinations of phenolic antioxidants |
| GB0004436D0 (en) * | 2000-02-25 | 2000-04-12 | Clariant Int Ltd | Synergistic stabilizer compositions for thermoplastic polymers in prolonged contact with water |
| PT1282630E (pt) | 2000-05-19 | 2006-09-29 | Ciba Sc Holding Ag | Processo para reducao do peso molecular de polipropileno usando esteres de hidroxilamina. |
| GB0019465D0 (en) * | 2000-08-09 | 2000-09-27 | Clariant Int Ltd | Synergistic stabilizer for color stable pigmented thermoplastic polyners in prolonged contact with water |
| ITMI20012085A1 (it) | 2000-10-17 | 2003-04-09 | Ciba Sc Holding Ag | Polpropilene metallocene stabilizzato |
| US6867250B1 (en) | 2000-10-30 | 2005-03-15 | Cytec Technology Corp. | Non-yellowing ortho-dialkyl aryl substituted triazine ultraviolet light absorbers |
| US6727300B2 (en) | 2000-11-03 | 2004-04-27 | Cytec Technology Corp. | Polymeric articles containing hindered amine light stabilizers based on multi-functional carbonyl compounds |
| US6545156B1 (en) | 2000-11-03 | 2003-04-08 | Cytec Technology Corp. | Oligomeric hindered amine light stabilizers based on multi-functional carbonyl compounds and methods of making same |
| US6414155B1 (en) | 2000-11-03 | 2002-07-02 | Cytec Technology Corp. | Oligomeric hindered amine light stabilizers based on multi-functional carbonyl compounds and methods of making same |
| US6492521B2 (en) | 2000-11-03 | 2002-12-10 | Cytec Technology Corp. | Hindered amine light stabilizers based on multi-functional carbonyl compounds and methods of making same |
| US7122135B2 (en) * | 2000-11-13 | 2006-10-17 | Supresta U.S. Llc | Blend of organophosphorus flame retardant, lactone stabilizer, and phosphate compatibilizer |
| MXPA03005754A (es) | 2001-01-15 | 2003-09-10 | Ciba Sc Holding Ag | Recipiente para material a granel, intermedio, flexible y atiestatico. |
| GB0104371D0 (en) * | 2001-02-22 | 2001-04-11 | Clariant Int Ltd | Color improving stabilizing compositions comprising leucine |
| DE60205734T2 (de) * | 2001-03-20 | 2006-03-09 | Ciba Speciality Chemicals Holding Inc. | Flammhemmende zusammensetzungen |
| GB0119137D0 (en) * | 2001-08-06 | 2001-09-26 | Clariant Int Ltd | Property enhancement of polyamides by co-condensation with lightstabilizers |
| DE10204690A1 (de) * | 2002-02-06 | 2003-08-07 | Clariant Gmbh | Verfahren zur Herstellung synergistischer Stabilisatormischungen |
| US20030225191A1 (en) | 2002-04-12 | 2003-12-04 | Francois Gugumus | Stabilizer mixtures |
| DE10254548A1 (de) | 2002-11-21 | 2004-06-17 | Basf Ag | Verwendung UV-Absorber enthaltender Polymerpulver zur Stabilisierung von Polymeren gegen die Einwirkung von UV-Strahlung |
| KR101114272B1 (ko) | 2003-02-26 | 2012-03-28 | 시바 홀딩 인크 | 수 혼화성의 입체적으로 속박된 하이드록시 치환된 알콕시아민 |
| MY145571A (en) | 2003-12-19 | 2012-02-29 | Ciba Holding Inc | Fluorocarbon terminated oligo-and poly-carbonates as surface modifiers |
| WO2005070913A1 (fr) * | 2004-01-22 | 2005-08-04 | University Of Ottawa | Antioxydants thermiquement modules |
| JP5524449B2 (ja) | 2004-10-25 | 2014-06-18 | チバ ホールディング インコーポレーテッド | 機能性ナノ粒子 |
| CN101048378B (zh) | 2004-11-02 | 2013-12-25 | 西巴特殊化学品控股有限公司 | N-烷氧基胺的合成方法 |
| US7390912B2 (en) * | 2004-12-17 | 2008-06-24 | Milliken & Company | Lactone stabilizing compositions |
| EP1676887B1 (fr) | 2004-12-29 | 2007-05-23 | Ciba Specialty Chemicals Holding Inc. | Composition et procédé pour améliorer la stabilité thermique et la résistance aux intempéries de polymères polyuréthanes segmentés |
| JP2008545556A (ja) * | 2005-05-26 | 2008-12-18 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニー | ねじれネマチック液晶を含む高強度多層ラミネート |
| WO2006128091A2 (fr) * | 2005-05-26 | 2006-11-30 | E. I. Du Pont De Nemours And Company | Lamines multicouches a haute resistance comprenant des cristaux liquides nematiques en helice |
| CN100345836C (zh) * | 2005-10-17 | 2007-10-31 | 湘潭大学 | 一种苯并呋喃酮类稳定剂及其应用 |
| CN101351525A (zh) * | 2005-12-29 | 2009-01-21 | 纳幕尔杜邦公司 | 用于降低红外线辐射的透射的组合物 |
| WO2009003930A1 (fr) | 2007-06-29 | 2009-01-08 | Basell Poliolefine Italia S.R.L. | Composition polyoléfinique irradiée comprenant un stabilisateur non phénolique |
| CN101801676B (zh) | 2007-07-18 | 2012-10-03 | 巴斯夫欧洲公司 | 激光敏感涂料制剂 |
| WO2009027180A1 (fr) | 2007-08-28 | 2009-03-05 | Basf Se | Mélange stabilisant |
| DE102007040925A1 (de) | 2007-08-30 | 2009-03-05 | Bayer Materialscience Ag | Thermoplastische Zusammensetzungen mit geringer Trübung |
| CA2698837C (fr) | 2007-09-04 | 2015-11-24 | Basf Se | Phosphines cycliques utilisees comme retardateurs de flamme |
| WO2009034016A1 (fr) | 2007-09-13 | 2009-03-19 | Basf Se | Agents de couplage silanes pour caoutchoucs chargés |
| EP2215156B1 (fr) | 2007-11-28 | 2013-01-09 | Basf Se | Mélange de stabilisants liquide |
| AU2009238220A1 (en) * | 2008-04-18 | 2009-10-22 | Commonwealth Scientific And Industrial Research Organisation | Condensation polymers with modified properties |
| ITMI20080739A1 (it) | 2008-04-23 | 2009-10-24 | 3V Sigma Spa | Ammine stericamente impedite oligomeriche e loro uso come stabilizzanti per polimeri |
| ITMI20080747A1 (it) | 2008-04-24 | 2009-10-25 | 3V Sigma Spa | Miscele di ammine stericamente impedite per la stabilizzazione di polimeri |
| KR101693875B1 (ko) | 2008-05-15 | 2017-01-17 | 바스프 에스이 | 에멀전 중합화 고무용 기본 안정화 시스템 |
| JP5260418B2 (ja) | 2008-06-26 | 2013-08-14 | 住友化学株式会社 | ポリエステル組成物 |
| WO2010023155A2 (fr) | 2008-08-27 | 2010-03-04 | Basf Se | Compositions retardatrices de flamme contenant des agents dispersants polymères |
| JP5377647B2 (ja) | 2008-08-28 | 2013-12-25 | ビーエーエスエフ ソシエタス・ヨーロピア | 無生物有機材料のための安定剤 |
| EP2331625B1 (fr) | 2008-09-05 | 2012-01-18 | THOR GmbH | Composition retardatrice de flamme renfermant un dérivé de l'acide phosphonique |
| EP2160945A1 (fr) | 2008-09-09 | 2010-03-10 | Polymers CRC Limited | Article antimicrobien |
| US7988881B2 (en) * | 2008-09-30 | 2011-08-02 | E. I. Du Pont De Nemours And Company | Multilayer laminates comprising chiral nematic liquid crystals |
| EP2340276B1 (fr) | 2008-10-23 | 2020-11-25 | DataLase Ltd | Additifs absorbant la chaleur |
| EP2342295A1 (fr) | 2008-10-27 | 2011-07-13 | DataLase Ltd | Composition de revêtement pour le marquage de substrats |
| US8399096B2 (en) | 2008-10-31 | 2013-03-19 | E I Du Pont De Nemours And Company | High-clarity ionomer compositions and articles comprising the same |
| EP2186845A1 (fr) | 2008-11-18 | 2010-05-19 | Basf Se | Polymères fonctionnalisés d'ammonium en tant qu'additifs antistatiques |
| WO2010072768A1 (fr) | 2008-12-23 | 2010-07-01 | Basf Se | Agglomérat absorbant les uv |
| JP5712141B2 (ja) | 2008-12-30 | 2015-05-07 | イー・アイ・デュポン・ドウ・ヌムール・アンド・カンパニーE.I.Du Pont De Nemours And Company | 高透明度のブレンドイオノマー組成物およびそれを含む物品 |
| CN102325812A (zh) | 2008-12-31 | 2012-01-18 | 纳幕尔杜邦公司 | 具有低雾度和高耐湿性的离聚物组合物以及包含该组合物的制品 |
| WO2010076278A1 (fr) | 2009-01-05 | 2010-07-08 | Basf Se | Dispersants phosphorés pour particules inorganiques dans des matrices polymères |
| IT1393333B1 (it) | 2009-02-09 | 2012-04-20 | 3V Sigma Spa | Nuove ammine stericamente impedite e loro uso come stabilizzanti per polimeri |
| US8802151B2 (en) | 2009-03-24 | 2014-08-12 | Basf Se | Preparation of shaped metal particles and their uses |
| WO2010112395A1 (fr) | 2009-04-02 | 2010-10-07 | Basf Se | Hydroxybenzylthioethers substitues par s-perfluoroalkyle et leurs derives utilises en tant que modificateurs de surface |
| EP2451746B1 (fr) | 2009-07-07 | 2019-02-27 | Basf Se | Composition comprenant des particules de bronze de potassium-césium-tungstène et l'utilisation de ces particules |
| CN102471535B (zh) | 2009-07-24 | 2013-12-11 | 巴斯夫欧洲公司 | 在芳族和/或杂芳族环氧树脂中作为阻燃剂的二膦衍生物 |
| US8286405B1 (en) * | 2009-08-11 | 2012-10-16 | Agp Plastics, Inc. | Fire and impact resistant window and building structures |
| EP2467424A1 (fr) | 2009-08-18 | 2012-06-27 | Basf Se | Module photovoltaïque à encapsulant de polymère stabilisé |
| EP2467878A1 (fr) | 2009-08-18 | 2012-06-27 | Basf Se | Module photovoltaïque uv-stabilisé |
| EP2470023A2 (fr) | 2009-08-27 | 2012-07-04 | Polymers CRC Ltd. | Composition de nanoparticules d'oxyde de zinc et d'argent |
| BR112012005454A2 (pt) | 2009-09-10 | 2015-09-08 | Basf Se | composto, composição, e, métodos para estabilizar um material orgânico suscetível à degradação oxidativa, térmica ou induzida por luz e para aprimorar retardância de chama de um material orgânico. |
| EP2319832A1 (fr) | 2009-10-20 | 2011-05-11 | Basf Se | Amines entravées stériquement |
| CN102666698B (zh) | 2009-11-27 | 2014-07-02 | 巴斯夫欧洲公司 | 具有uv稳定化包封材料的光伏组件 |
| CN103201264B (zh) | 2010-03-05 | 2016-03-23 | 巴斯夫欧洲公司 | 位阻胺 |
| WO2011107513A1 (fr) | 2010-03-05 | 2011-09-09 | Basf Se | Amines stériquement masquées |
| AR080385A1 (es) | 2010-03-09 | 2012-04-04 | Polymers Crc Ltd | Procedimiento para la preparacion de un articulo antimicrobiano |
| IT1399477B1 (it) | 2010-03-15 | 2013-04-19 | 3V Sigma Spa | Miscele di ammine stericamente impedite per la stabilizzazione di polimeri |
| CN102958361A (zh) | 2010-06-24 | 2013-03-06 | 巴斯夫欧洲公司 | 除草组合物 |
| RU2013103600A (ru) | 2010-06-29 | 2014-08-10 | Басф Се | Способ улучшения свойств текучести расплавов полимеров |
| EP2402390A1 (fr) | 2010-06-30 | 2012-01-04 | Basf Se | Particules avec stabilisateur léger d'amine entravé stériquement et polymère organique microporeux |
| US9550941B2 (en) | 2010-10-20 | 2017-01-24 | Basf Se | Sterically hindered amine light stabilizers with a mixed functionalization |
| EP2630166B1 (fr) | 2010-10-20 | 2019-06-12 | Basf Se | Stabilisants lumière oligomères à fonctionnalisation spécifique |
| IT1403086B1 (it) | 2010-10-28 | 2013-10-04 | 3V Sigma Spa | Nuove ammine stericamente impedite polimeriche e loro uso come stabilizzanti per polimeri |
| KR101854892B1 (ko) | 2010-11-16 | 2018-05-04 | 바스프 에스이 | 중합체를 위한 안정화제 조성물 |
| US11267951B2 (en) | 2010-12-13 | 2022-03-08 | Cytec Technology Corp. | Stabilizer compositions containing substituted chroman compounds and methods of use |
| UA123990C2 (uk) | 2010-12-13 | 2021-07-07 | Сайтек Текнолоджи Корп. | Технологічні добавки і їх застосування в ротаційному формуванні |
| ITMI20110802A1 (it) | 2011-05-10 | 2012-11-11 | 3V Sigma Spa | Miscele di ammine stericamente impedite per la stabilizzazione di polimeri |
| WO2013041592A1 (fr) | 2011-09-23 | 2013-03-28 | Borealis Ag | Stabilisation de matière organique avec des composés de mannich à base d'aminotriazine |
| BR112014021586B1 (pt) | 2012-03-20 | 2021-08-03 | Basf Se | Composição, processo para uma proteção de um material orgânico, e, uso de um composto |
| US9328219B2 (en) | 2012-03-20 | 2016-05-03 | Basf Se | Polyamide compositions with improved optical properties |
| JP2015516996A (ja) | 2012-03-20 | 2015-06-18 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | ポリアミド樹脂の固体特性を改善するための尿素化合物 |
| BR112014022977B1 (pt) | 2012-03-20 | 2020-12-29 | Basf Se | composição polimérica, uso de um composto da fórmula i, artigo moldado e composto |
| JP6155683B2 (ja) * | 2012-05-23 | 2017-07-05 | 横浜ゴム株式会社 | ゴム組成物および空気入りタイヤ |
| NZ726849A (en) | 2012-06-13 | 2018-06-29 | Cytec Tech Corp | Stabilizer compositions containing substituted chroman compounds and methods of use |
| EP2872496B1 (fr) | 2012-07-13 | 2018-02-28 | Basf Se | Polyglycol bis-[3-(7-tert-butyl-2-oxo-3-phenyl-3h-benzofuran-5-yl-) propanoyl] utilisés comme stabilisateurs de matières organiques |
| JP6241702B2 (ja) * | 2012-09-14 | 2017-12-06 | 国立大学法人九州大学 | メカノクロミック材料 |
| KR102335051B1 (ko) | 2013-07-08 | 2021-12-07 | 바스프 에스이 | 신규 광 안정화제 |
| KR102294024B1 (ko) | 2013-09-27 | 2021-08-27 | 바스프 에스이 | 건축 재료를 위한 폴리올레핀 조성물 |
| WO2015055563A1 (fr) | 2013-10-17 | 2015-04-23 | Basf Se | Stabilisants optiques à amine encombrée à base de triazine, pipéridine et pyrrolidine |
| WO2015077635A2 (fr) | 2013-11-22 | 2015-05-28 | Polnox Corporation | Antioxydants macromoléculaires basés sur deux types de fractions par molécule : structures, leurs procédés de fabrication et d'utilisation |
| EP2876126A1 (fr) | 2013-11-25 | 2015-05-27 | Basf Se | Mélange stabilisateur |
| TWI685524B (zh) | 2013-12-17 | 2020-02-21 | 美商畢克美國股份有限公司 | 預先脫層之層狀材料 |
| MX378343B (es) | 2014-02-17 | 2025-03-10 | Basf Se | Derivados de 3-fenil-benzofuran-2-ona que contienen fosforo como estabilizantes. |
| KR102366443B1 (ko) | 2014-04-29 | 2022-02-23 | 바스프 에스이 | 다층 필름 및 그의 용도 |
| EP3143082B1 (fr) | 2014-05-15 | 2020-11-18 | Basf Se | Stabilisateur hautement efficace |
| WO2016020322A1 (fr) | 2014-08-05 | 2016-02-11 | Basf Se | Dérivés de 3-phényl-benzofuran-2-one diphosphite utilisés en tant que stabilisants |
| EP3050919A1 (fr) | 2015-01-29 | 2016-08-03 | Basf Se | Matériaux contenant de la lignocellulose comprenant des mélanges de sels d'acides carbamiques n-substitués |
| SA116370295B1 (ar) | 2015-02-20 | 2016-12-06 | باسف اس اى | رقائق، وأشرطة وفتائل أحادية من البولي أوليفين مثبتة للضوء |
| AU2016294860B2 (en) | 2015-07-20 | 2021-01-28 | Basf Se | Flame retardant polyolefin articles |
| EP3328928B1 (fr) | 2015-07-27 | 2020-12-16 | Basf Se | Mélange d'additif |
| US10590263B2 (en) | 2015-08-10 | 2020-03-17 | Basf Se | 3-phenyl-benzofuran-2-one derivatives containing phosphorus as stabilizers |
| ES2765411T3 (es) | 2016-01-21 | 2020-06-09 | Basf Se | Mezcla de aditivos para la estabilización de poliol y poliuretano |
| MY199339A (en) | 2016-09-12 | 2023-10-24 | Basf Se | Additive mixture |
| US10421851B2 (en) | 2016-09-30 | 2019-09-24 | Vanderbilt Chemicals, Llc | Low emissions scorch inhibitor for polyurethane foam |
| JP7741626B2 (ja) | 2017-02-09 | 2025-09-18 | ダウ グローバル テクノロジーズ エルエルシー | 低レベルのアルデヒド放出を有するポリウレタンフォーム |
| BR112019017144A2 (pt) | 2017-02-20 | 2020-04-14 | Dow Global Technologies Llc | poliuretano que tem emissões de aldeído reduzidas |
| IL268963B2 (en) | 2017-03-28 | 2024-12-01 | Basf Se | Light stabilizer mixture |
| EP3619261B1 (fr) | 2017-05-03 | 2022-08-10 | Basf Se | Agents de nucléation, leur méthode de production et les compositions polymériques associées |
| IT201700073726A1 (it) | 2017-06-30 | 2018-12-30 | 3V Sigma Spa | Ammine impedite polimeriche |
| WO2019008002A1 (fr) | 2017-07-03 | 2019-01-10 | Basf Se | Sels métalliques phénoliques et leurs acides phénoliques utilisés comme stabilisants de polymères |
| US10941285B2 (en) | 2017-07-06 | 2021-03-09 | Basf Se | Stabilized polyolefin compositions comprising benzofuranones and acid scavengers |
| IT201700078234A1 (it) | 2017-07-11 | 2019-01-11 | 3V Sigma Spa | Ammine impedite |
| EP3684858A1 (fr) | 2017-09-18 | 2020-07-29 | Basf Se | Mélange d'additifs |
| WO2019192943A1 (fr) | 2018-04-04 | 2019-10-10 | Basf Se | Utilisation d'une composition absorbant les rayonnements ultraviolets comme stabilisant lumière pour un article polymère artificiel façonné |
| US11773277B2 (en) | 2018-04-04 | 2023-10-03 | Basf Se | Use of an ultraviolet radiation absorbing polymer composition (UVRAP) as an UV absorbing agent in a coating for non-living and non-keratinous materials |
| CA3103741A1 (fr) | 2018-06-21 | 2019-12-26 | Basf Se | Derives de 3-phenyl-benzofuran-2-one diphosphate utilises comme stabilisants |
| JP7397851B2 (ja) | 2018-08-02 | 2023-12-13 | ダウ グローバル テクノロジーズ エルエルシー | ポリウレタン発泡体のアルデヒド排出量を減少させるための方法 |
| US11453742B2 (en) | 2018-08-02 | 2022-09-27 | Dow Global Technologies Llc | Methods for reducing aldehyde emissions in polyurethane foams |
| KR102648668B1 (ko) | 2018-08-02 | 2024-03-19 | 다우 글로벌 테크놀로지스 엘엘씨 | 폴리우레탄 폼에서 알데히드 방출을 감소시키는 방법 |
| JP7253037B2 (ja) | 2018-08-02 | 2023-04-05 | ダウ グローバル テクノロジーズ エルエルシー | ポリウレタン発泡体のアルデヒド排出量を減少させるための方法 |
| CN112771108B (zh) | 2018-08-22 | 2023-05-05 | 巴斯夫欧洲公司 | 稳定的滚塑聚烯烃 |
| SG11202105659PA (en) | 2018-12-04 | 2021-06-29 | Basf Se | Polyethylene or polypropylene articles |
| WO2020126752A1 (fr) | 2018-12-21 | 2020-06-25 | Basf Se | Composition de polypropylène |
| CN113544126B (zh) | 2019-03-08 | 2024-11-08 | 巴斯夫欧洲公司 | 位阻胺稳定剂混合物 |
| MX2021010990A (es) | 2019-03-12 | 2021-10-01 | Basf Se | Articulos de polimero artificial conformados. |
| US20220282064A1 (en) | 2019-07-30 | 2022-09-08 | Basf Se | Stabilizer composition |
| JP7421638B2 (ja) | 2019-08-30 | 2024-01-24 | ダウ グローバル テクノロジーズ エルエルシー | ポリエーテルポリオールおよびポリウレタン発泡体のアルデヒド排出量を減少させるための方法 |
| US20230102449A1 (en) | 2020-02-10 | 2023-03-30 | Basf Se | Light stabilizer mixture |
| AU2021225338A1 (en) | 2020-02-26 | 2022-09-08 | Basf Se | Additive mixtures for rheology modification of polymers |
| CN115175958B (zh) | 2020-02-27 | 2024-09-17 | 巴斯夫欧洲公司 | 聚烯烃组合物 |
| MX2023005137A (es) | 2020-11-03 | 2023-05-26 | Basf Se | Metodo para estabilizar un material organico mediante el uso de una mezcla estabilizante. |
| JP2023553075A (ja) | 2020-12-09 | 2023-12-20 | ビーエーエスエフ ソシエタス・ヨーロピア | 有機材料をベースとする成形物品 |
| CA3201706A1 (fr) | 2020-12-09 | 2022-06-16 | Gregor Huber | Melanges d'additifs |
| JP2022155208A (ja) | 2021-03-30 | 2022-10-13 | 住友化学株式会社 | 亜リン酸エステル化合物、その製造方法及びその用途 |
| BR112023019545A2 (pt) | 2021-04-01 | 2023-10-31 | Basf Se | Mistura estabilizadora, composição, artigo, e, usos do pelo menos um composto e da mistura estabilizadora |
| WO2022243306A1 (fr) | 2021-05-21 | 2022-11-24 | Rhodia Operations | Systèmes de résine polymère stabilisée comportant des hétéropolyoxométalates destinés à des propriétés antimicrobiennes et leurs utilisations |
| JP2022183907A (ja) | 2021-05-31 | 2022-12-13 | 住友化学株式会社 | 亜リン酸エステル組成物 |
| JP7670567B2 (ja) | 2021-07-15 | 2025-04-30 | 住友化学株式会社 | フェノール化合物、有機材料用安定剤、樹脂組成物、及び有機材料の安定化方法 |
| MX2024000839A (es) | 2021-07-17 | 2024-02-08 | Basf Se | Una mezcla de aditivos para la estabilizacion de material organico. |
| EP4396256A1 (fr) | 2021-09-02 | 2024-07-10 | Basf Se | Combinaison de stabilisants pour la prévention de la dégradation de polymères synthétiques |
| EP4402205A1 (fr) | 2021-09-16 | 2024-07-24 | Basf Se | Formulation de stabilisant |
| WO2023117951A1 (fr) | 2021-12-21 | 2023-06-29 | Basf Se | Appareil de génération d'un élément d'accès numérique |
| CA3244478A1 (fr) | 2022-01-01 | 2023-07-06 | Cytec Industries Inc. | Compositions polymères comprenant des accélérateurs de densification et procédés de moulage par rotation pour fabriquer des articles creux à partir de celles-ci |
| TW202340391A (zh) | 2022-01-18 | 2023-10-16 | 德商巴地斯顏料化工廠 | 具有混合金屬氧化物粒子之成型人造聚合物製品 |
| CN118556103A (zh) | 2022-01-18 | 2024-08-27 | 巴斯夫欧洲公司 | 具有闭孔金属氧化物颗粒的成型人造聚合物制品 |
| JP7798608B2 (ja) | 2022-03-03 | 2026-01-14 | 住友化学株式会社 | 加工安定剤、有機材料組成物、及び有機材料の安定化方法。 |
| CA3257269A1 (fr) | 2022-05-24 | 2023-11-30 | Basf Se | Composition de polycarbonate contenant une combinaison d'hydroxyphényl triazines et d'absorbeurs d'uv |
| CN119731255A (zh) | 2022-08-19 | 2025-03-28 | 巴斯夫欧洲公司 | 添加剂用于改善聚乙烯的加工的用途 |
| CN119855855A (zh) | 2022-09-07 | 2025-04-18 | 巴斯夫欧洲公司 | 用自由基引发剂和硫代尿烷对聚合物进行流变学改性 |
| KR20250078966A (ko) | 2022-09-29 | 2025-06-04 | 바스프 에스이 | 히드록시페닐 트리아진으로 안정화된 중합체를 위한 공-안정화제 |
| JP2024053404A (ja) | 2022-10-03 | 2024-04-15 | 住友化学株式会社 | 安定剤、有機材料組成物、及び有機材料の安定化方法 |
| CN120418346A (zh) | 2022-12-21 | 2025-08-01 | 巴斯夫欧洲公司 | 用于改善聚乙烯的加工的方法 |
| JP2024100231A (ja) | 2023-01-13 | 2024-07-26 | 住友化学株式会社 | 加工安定剤、樹脂組成物、および有機材料の安定化方法。 |
| WO2024153547A1 (fr) | 2023-01-16 | 2024-07-25 | Basf Se | Co-stabilisants d'hydroxyphényltriazine pour polyesters stabilisés |
| CN120615102A (zh) | 2023-01-16 | 2025-09-09 | 巴斯夫欧洲公司 | 用于稳定的聚氨酯的苯基三嗪共稳定剂 |
| WO2024208842A1 (fr) | 2023-04-04 | 2024-10-10 | Basf Se | Compositions polymères thermoplastiques contenant des mélanges stabilisants |
| WO2025087886A1 (fr) | 2023-10-26 | 2025-05-01 | Basf Se | Tuyau en polyoléfine comprenant un minéral d'hydrotalcite et un hydrazide |
| WO2025223984A1 (fr) | 2024-04-22 | 2025-10-30 | Basf Se | Articles ignifuges comprenant de l'acide polylactique |
| WO2026046898A1 (fr) | 2024-08-30 | 2026-03-05 | Basf Se | Film intercouche pour verre feuilleté comprenant un absorbeur uv de résorcinol triazine |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3452094A (en) * | 1967-07-19 | 1969-06-24 | Geigy Chem Corp | N - 2 - phenyl - 2 - (2 - hydroxy - 1 - naphthyl) ethyl-n-substituted amines and salts thereof |
| NL6809840A (fr) * | 1968-07-11 | 1970-01-13 | ||
| FR2440350A1 (fr) * | 1978-11-03 | 1980-05-30 | Hoechst France | Procede de fabrication de l'acide parahydroxymandelique racemique |
| BE881495A (fr) * | 1979-02-05 | 1980-08-01 | Sandoz Sa | Procede de stabilisation de matieres organiques polymeres |
| GB2042562B (en) * | 1979-02-05 | 1983-05-11 | Sandoz Ltd | Stabilising polymers |
| DE3006268A1 (de) * | 1980-02-20 | 1981-08-27 | Agfa-Gevaert Ag, 5090 Leverkusen | Farbphotografisches aufzeichnungsmaterial mit nicht diffundierenden elektronendonor-vorlaeuferverbindungen |
| GB2151611B (en) * | 1983-12-16 | 1987-08-26 | Ici Plc | Manufacturing process for benzodifuranones |
| US5175312A (en) * | 1989-08-31 | 1992-12-29 | Ciba-Geigy Corporation | 3-phenylbenzofuran-2-ones |
| EP0415887B1 (fr) * | 1989-08-31 | 1994-10-05 | Ciba-Geigy Ag | 3-Phényl-benzofuran-3-ones |
| GB2252325A (en) * | 1991-01-31 | 1992-08-05 | Ciba Geigy Ag | Stabilised polyolefin |
| TW206220B (fr) * | 1991-07-01 | 1993-05-21 | Ciba Geigy Ag | |
| US5252643A (en) * | 1991-07-01 | 1993-10-12 | Ciba-Geigy Corporation | Thiomethylated benzofuran-2-ones |
| EP0543778A1 (fr) * | 1991-11-19 | 1993-05-26 | Ciba-Geigy Ag | Compositions de polyéther-polyol et de polyuréthanne protégées contre l'oxidation et la décoloration de noyau |
-
1993
- 1993-05-05 TW TW082103519A patent/TW260686B/zh active
- 1993-05-07 NL NL9300784A patent/NL9300784A/nl active Search and Examination
- 1993-05-11 GB GB9309665A patent/GB2267088B/en not_active Expired - Fee Related
- 1993-05-14 IT IT93MI000991A patent/IT1264453B1/it active IP Right Grant
- 1993-05-17 CZ CZ1993919A patent/CZ290111B6/cs not_active IP Right Cessation
- 1993-05-17 US US08/064,186 patent/US5367008A/en not_active Expired - Lifetime
- 1993-05-17 SK SK495-93A patent/SK49593A3/sk unknown
- 1993-05-18 CA CA002096486A patent/CA2096486A1/fr not_active Abandoned
- 1993-05-18 FR FR9305960A patent/FR2691470B1/fr not_active Expired - Fee Related
- 1993-05-18 BE BE9300513A patent/BE1006730A4/fr not_active IP Right Cessation
- 1993-05-18 BE BE9300513D patent/BE1006549A3/fr active
- 1993-05-19 JP JP5140217A patent/JPH06287185A/ja active Pending
- 1993-05-19 KR KR1019930008764A patent/KR100286117B1/ko not_active Expired - Fee Related
- 1993-05-19 DE DE4316876A patent/DE4316876A1/de not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| CZ290111B6 (cs) | 2002-06-12 |
| JPH06287185A (ja) | 1994-10-11 |
| GB9309665D0 (en) | 1993-06-23 |
| FR2691470B1 (fr) | 1995-02-10 |
| GB2267088A (en) | 1993-11-24 |
| NL9300784A (nl) | 1993-12-16 |
| FR2691470A1 (fr) | 1993-11-26 |
| ITMI930991A1 (it) | 1994-11-14 |
| GB2267088B (en) | 1996-01-24 |
| BE1006730A4 (fr) | 1994-11-29 |
| ITMI930991A0 (it) | 1993-05-14 |
| KR940005736A (ko) | 1994-03-22 |
| KR100286117B1 (ko) | 2001-04-16 |
| US5367008A (en) | 1994-11-22 |
| IT1264453B1 (it) | 1996-09-23 |
| TW260686B (fr) | 1995-10-21 |
| SK49593A3 (en) | 1994-05-11 |
| CZ91993A3 (en) | 1993-12-15 |
| CA2096486A1 (fr) | 1993-11-23 |
| DE4316876A1 (de) | 1993-11-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BE1006549A3 (fr) | Application de 3-(alcoxyphenyl)benzofuranne-2-onescomme stabilisants et nouveaux composes de ce typ e | |
| BE1007037A3 (fr) | 3-(acyloxyphenyl) benzofuran-2-ones comme stabilisants. | |
| BE1005299A3 (fr) | Bis-(benzofuranne-2-ones) et leur application a la stabilisation de matieres organiques. | |
| FR2678615A1 (fr) | Benzofuranne-2-ones thiomethylees, leur preparation et leur application comme stabilisants de matieres organiques. | |
| SK279840B6 (sk) | 3-(dihydrobenzofuran-5-yl)benzofuran-2-óny, kompoz | |
| EP0670842B1 (fr) | Modification beta-cristalline de 2,2',2''-nitrilo triethyl-tris-(3,3',5,5'-tetra-tert-butyl-1,1'-biphenyl-2,2'-diyl)phosphite] | |
| BE1008476A5 (fr) | Composes piperidiques, composition stabilisee par ces composes, procede les utilisant et leur utilisation pour stabiliser une matiere organique. | |
| EP0670843B1 (fr) | Modification alpha-cristalline de 2,2',2"-nitrilo triethyl-tris-(3,3',5,5'-tetra-tert-butyl-1,1'-biphenyl-2,2'-diyl)phosphite] | |
| FR2763338A1 (fr) | Nouveaux composes a base de derives de polyalkyl-1-oxa- diazaspirodecane | |
| CZ284155B6 (cs) | Stabilizátory na bázi oligomerních HALS-fosfitů a HALS-fosfonitů | |
| EP0594539B1 (fr) | Phosphites de phényle comme stabilisants pour matériaux organiques | |
| FR2680367A1 (fr) | Phosphite de 4-piperidyle methyle a l'azote et son application comme stabilisant pour matieres organiques. | |
| BE1006547A5 (fr) | Esters d'acides carboxyliques d'hydroxyphenylalcanols comme stabilisants. | |
| FR2718742A1 (fr) | Phosphites et phosphoramides de composés stabilisants à la lumière de type amine encombrée utilisables comme stabilisants. | |
| BE1009841A3 (fr) | Hals-phosphoramides comme stabilisants. | |
| US5260430A (en) | Diphenyl acetic acid derivatives | |
| FR2707292A1 (fr) | s-Triazines phénoliques et leur utilisation comme stabilisants pour des matières organiques. | |
| FR2718741A1 (fr) | Phosphonites de composés stabilisants à la lumière de type amine encombrée utilisables comme stabilisants. | |
| CZ197293A3 (en) | Tetra-(n-alkyl-2,2,6,6-tetramethylpiperidin-4-yl) -4,4'-diphenylbisphosphinites | |
| FR2718743A1 (fr) | Bisphénylphosphites de composés stabilisants à la lumière de type amine encombrée monomères et oligomères utilisables comme stabilisants. | |
| FR2744443A1 (fr) | Bisphenols substitues par un groupe norbornene en tant qu'antioxydants |