[0001] A invenção se refere à novos compostos orgânicos, processos para a preparação destes, a aplicação destes em um processo para o tratamento do corpo humano ou animal, o uso destes - sozinhos ou em combinação com um ou mais outros compostos farmaceuticamente ativos - para o tratamento de uma doença inflamatória ou obstrutiva das vias aéreas, tal como asma, distúrbios de ocorrência comum em conexão com transplantes, ou uma doença proliferativa, tal como uma doença de tumor que pode ser sólido ou líquido; um método para o tratamento de uma tal doença em animais, especialmente em seres humanos, e o uso de um tal composto - sozinho ou em combinação com um ou mais outros compostos farmaceuticamente ativos - para a produção de uma preparação farmacêutica para o tratamento das referidas doenças.
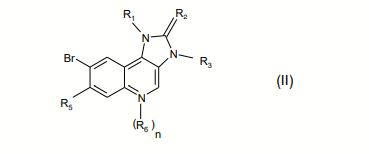
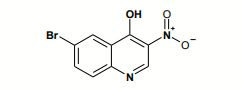
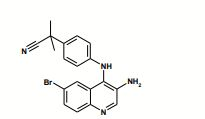
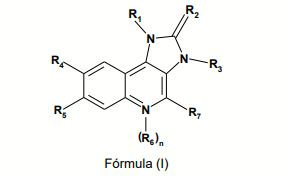
[0002] A presente invenção se refere a compostos de Fórmula (I)
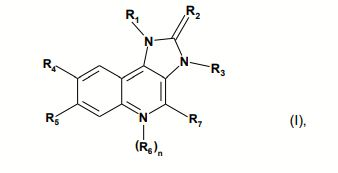
na qual Ri é naftila ou fenila em que a referida fenila é substituída por um ou dois substituintes independentemente selecionados do grupo que consiste em halogênio; alquila inferior não-substituída ou substituída por halogênio, ciano, imidazolila ou triazolila; cicloalquila; amino substituído por um ou dois substituintes independentemente selecionados do grupo que consiste em alquila inferior, alquil sulfonil inferior, alcóxi inferior e alquilamino inferior de alcóxi inferior; piperazinila não-substituída ou substituída por um ou dois substituintes independentemente selecionados do grupo que consiste em alquila inferior e alquil sulfonil inferior; 2-oxo-pirrolidinila; alquila inferior de alcóxi inferior; imidazolila; pirazolila; e triazolila; R2 é O ou S; R3 é alquila inferior; R4 é piridila não-substituída ou substituída por halogênio, ciano, alquila inferior, alcóxi inferior ou piperazinila não-substituída ou substituída por alquila inferior; pirimidinila não-substituída ou substituída por alcóxi inferior; quinolinila não-substituída ou substituída por halogênio; quinoxalinila; ou fenila substituída com alcóxi; Rs é hidrogênio ou halogênio; n é 0 ou 1; R6 é óxido; com a condição de que se n = 1, 0 átomo de N portando 0 radical Re apresenta uma carga positiva; R7 é hidrogênio ou amino; ou um tautômero destes, ou um sal farmaceuticamente aceitável, ou um hidrato ou solvato destes.
[0003] Os termos gerais empregados aqui anteriormente e daqui em diante de preferência têm dentro do contexto desta descrição os significados seguintes, a menos que de outra forma indicado:
[0004] O prefixo "inferior" denota um radical tendo até e inclusive um máximo de 7, especialmente até e inclusive um máximo de 4 átomos de carbono, os radicais em questão sendo ou lineares ou ramificados com única ou múltipla ramificação.
[0005] Onde a forma plural é empregada para compostos, sais, e outros mais, esta é adotada para referir-se também a um único composto, sal, ou similar.
[0006] Em uma modalidade preferida, alquila tem até um máximo de 12 átomos de carbono e é especialmente alquila inferior.
[0007] Alquila inferior é de preferência alquila com a partir de e inclusive 1 até e inclusive 7, de preferência a partir de e inclusive 1 a e inclusive 4, e é linear ou ramificada; de preferência, alquila inferior é butila, tal como n-butila, sec-butila, isobutila, terc-butila, propila, tal como n-propila ou isopropila, etila ou de preferência metila.
[0008] Cicloalquila é de preferência cicloalquila com a partir de e inclusive 3 até e inclusive 6 átomos de carbono no anel; cicloalquila é de preferência ciclopropila, ciclobutila, ciclopentila ou ciclo-hexila.
[0009] Alquila que é substituída por halogênio é de preferência perfluoroalquila tal como trifluorometila.
[00010] Halogênio é especialmente flúor, cloro, bromo, ou iodo, especialmente flúor, cloro, ou bromo.
[00011] Devido à relação íntima entre os novos compostos na forma livre e aqueles na forma de seus sais, inclusive aqueles sais que podem ser empregados como intermediários, por exemplo, na purificação ou identificação dos novos compostos, qualquer referência aos compostos livres aqui anteriormente e daqui em diante deve ser entendida como referência também aos sais correspondentes, quando apropriado e conveniente.
[00012] Sais são formados, por exemplo, como sais de adição de ácido, de preferência com ácidos orgânicos ou inorgânicos, de compostos de Fórmula I com um átomo de nitrogênio básico, especialmente os sais farmaceuticamente aceitáveis. Ácidos inorgânicos adequados são, por exemplo, ácidos halogenos, tais como ácido clorídrico, ácido sulfúrico, ou ácido fosfórico. Ácidos orgânicos adequados são, por exemplo, ácidos carboxílicos, fosfônicos, sulfônicos ou sulfâmicos, por exemplo, ácido acético, ácido propiônico, ácido octanoico, ácido decanoico, ácido de dodecanoico, ácido glicólico, ácido lático, ácido fumárico, ácido sucínico, ácido malônico, ácido adípico, ácido pimélico, ácido subérico, ácido azeláico, ácido málico, ácido tartárico, ácido cítrico, aminoácidos, tais como ácido glutâmico ou ácido aspártico, ácido maleico, ácido hidroximaleico, ácido metilmaleico, ácido ciclo-hexanocarboxílico, ácido adamantanocarboxílico, ácido benzoico, ácido salicílico, ácido 4- aminossalicílico, ácido ftálico, ácido fenilacético, ácido mandélico, ácido cinâmico, ácido metano- ou etano-sulfônico, ácido 2- hidroxietanossulfônico, ácido etano-1,2-dissulfônico, ácido benzenossulfônico, ácido 4-toluenossulfônico, ácido 2- naftalenossulfônico, ácido 1,5-naftaleno-dissulfônico, ácido 2- ou 3- metilbenzenossulfônico, ácido metilsulfúrico, ácido etilsulfúrico, ácido dodecilsulfúrico, ácido N-ciclo-hexilsulfâmico, ácido N-metil-, N-etil- ou N-propil-sulfâmico, ou outros ácidos protônicos orgânicos, tais como ácido ascórbico.
[00013] Para propósitos de isolamento ou purificação também é possível empregar sais farmaceuticamente inaceitáveis, por exemplo, picratos ou percloratos. Para uso terapêutico, somente sais farmaceuticamente aceitáveis ou compostos livres são empregados (onde aplicáveis na forma de preparações farmacêuticas), e estes são por esse motivo preferidos. Ri é de preferência fenila em que a referida fenila é substituída por um ou dois substituintes independentemente selecionados do grupo que consiste em halogênio; alquila inferior substituída por halogênio, ciano, imidazolila ou triazolila; amino substituído por um ou dois substituintes independentemente selecionados do grupo que consiste em alquila inferior e alquil sulfonil inferior; piperazinila em que a referida piperazinila é não-substituída ou substituída por um ou dois substituintes de alquila inferior; imidazolila; pirazolila; e triazolila. R2 é de preferência O. R3 é de preferência Me. R4 é de preferência pirimidinila ou piridila não-substituída ou substituída por halogênio, ciano, alquila inferior, alcóxi inferior ou piperazinila não-substituída ou substituída por alquila inferior; quinolinila não-substituída ou substituída por halogênio; quinoxalinila; ou fenila substituída com alcóxi. Rs é de preferência hidrogênio. n é de preferência 0. R7 é de preferência hidrogênio.
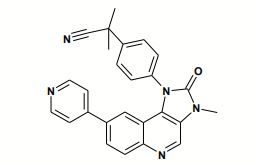
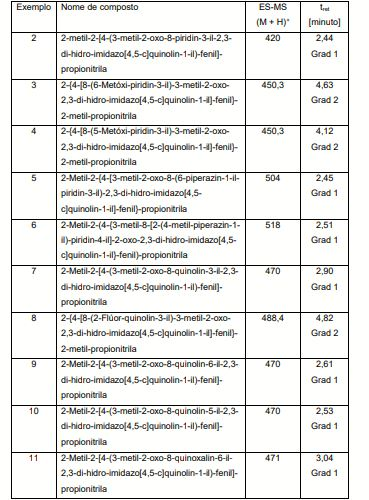
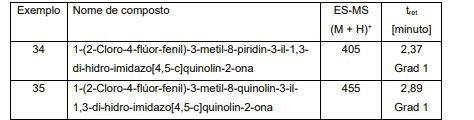
[00014] Um composto preferido é um composto escolhido do grupo que consiste em: 2-Metil-2-[4-(3-metil-2-oxo-8-piridin-4-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila; 2-Metil-2-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila; 2-{4-[8-(6-Metóxi-piridin-3-il)-3-metil-2-oxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il]-fenil}-2-metil-propionitrila; 2-{4-[8-(5-Metóxi-piridin-3-il)-3-metil-2-oxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il]-fenil}-2-metil-propionitrila; 2-Metil-2-{4-[3-metil-2-oxo-8-(6-piperazin-1-il-piridin-3-il)-2,3- di-hidro-imidazo[4,5-c]quinolin-1-il]-fenil}-propionitrila; 2-Metil-2-(4-{3-metil-8-[2-(4-metil-piperazin-1 -il)-piridin-4-il]-2- oxo-2,3-d i-hidro-imidazo[4,5-c]quinolin-1-il}-fenil)-propionitrila; 2-Metil-2-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila; 2-{4-[8-(2-Flúor-quinolin-3-il)-3-metil-2-oxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il]-fenil}-2-metil-propionitrila; 2-Metil-2-[4-(3-metil-2-oxo-8-quinolin-6-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila; 2-Metil-2-[4-(3-metil-2-oxo-8-quinolin-5-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila; 2-Metil-2-[4-(3-metil-2-oxo-8-quinoxalin-6-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila; 2-Etil-2-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-butironitrila; 2-Etil-2-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-butironitrila; 1-[3-Flúor-4-(2-oxo-pirrolidin-1-il)-fenil]-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Flúor-4-(2-oxo-pirrolidin-1-il)-fenil]-3-metil-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti I-1 -[4-(2-oxo-pirrol id in-1 -i l)-fen i l]-8-pirid in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti I-1 -[4-(2-oxo-pirrolidin-1 -i l)-fen i l]-8-q u inol in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1-{4-[Bis-(2-metóxi-etil)-amino]-3-flúor-fenil}-3-metil-8-piridin- 3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-{4-[Bis-(2-metóxi-etil)-amino]-3-flúor-fenil}-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -{4-[Bis-(2-metóxi-etil)-amino]-fenil}-3-metil-8-piridin-3-il-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-{4-[Bis-(2-metóxi-etil)-amino]-fenil}-3-metil-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-1 -naftalen-2-il-8-piridin-3-il-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 3-Metil-1 -naftalen-2-il-8-quinolin-3-il-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 1 -(2-Cloro-fenil)-3-metil-8-piridin-3-il-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 1 -(2-C loro-fen i l)-3-meti l-8-q u inol in-3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-pirid in-3-i I-1 -o-tolil-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 3-Meti l-8-q u inol in-3-i I-1 -o-tolil-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 1-(2-Etil-fenil)-3-metil-8-piridin-3-il-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 1-(2-Etil-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 3-Metil-8-piridin-3-il-1 -(2-trifluorometil-fenil)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Metil-8-quinolin-3-il-1 -(2-trifluorometil-fenil)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -(4-Flúor-2-metil-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -(4-Flúor-2-metil-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -(2-Cloro-4-flúor-fenil)-3-metil-8-piridin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -(2-Cloro-4-flúor-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-fenil)-3-metil-8-piridin-3-il-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona; 1 -(3-C loro-fen i l)-3-meti l-8-q u inol in-3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Metil-8-piridin-3-il-1-(3-trifluorometil-fenil)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Metil-8-quinolin-3-il-1 -(3-trifluorometil-fenil)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -(4-Metoximeti l-fen i l)-3-meti l-8-pirid in-3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -(4-Metoximetil-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -[2-Cloro-4-(2-metóxi-etil)-fenil]-3-metil-8-piridin-3-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[2-Cloro-4-(2-metóxi-etil)-fenil]-3-metil-8-quinolin-3-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[4-(2-Metóxi-etil)-fenil]-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 1 -[4-(2-Metóxi-etil)-fenil]-3-metil-8-piridin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 2-Metil-2-[4-(3-metil-2-oxo-5-óxi-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila; 2-Metil-2-[4-(3-metil-2-oxo-5-óxi-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila; 2-[4-(7-Flúor-3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila; 2-[4-(7-Flúor-3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila; N-Metil-N-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-metanossulfonamida; Éster de terc-butila de ácido metil-[4-(3-metil-2-oxo-8-piridin- 3-il-2,3-di-hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-carbâmico; Metil-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1 -il)-fenil]-amida de ácido etanossulfônico; Metil-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1 -il)-fenil]-amida de ácido etanossulfônico; N-Etil-N-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-metanossulfonamida; N-Etil-N-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-metanossulfonamida; 2-[4-(3-Etil-2-oxo-8-piridin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1 -il)-fenil]-2-metil-propionitrila; 1-[3-Flúor-4-(4-metanossulfonil-piperazin-1-il)-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Flúor-4-(4-metanossulfonil-piperazin-1-il)-fenil]-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Flúor-4-piperazin-1 -i l-fen i l)-3-meti l-8-q u inol in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Flúor-4-piperazin-1 -i l-fen i l)-3-meti l-8-pirid in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti I-1 -[4-(4-metil-piperazin-1 -i l)-fen i l]-8-q u inol in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti I-1 -[4-(4-metil-piperazin-1 -i l)-fen i l]-8-pirid in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1-[2-Cloro-4-(4-metil-piperazin-1-il)-fenil]-3-metil-8-quinolin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[2-Cloro-4-(4-metil-piperazin-1 -il)-fenil]-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-3-metil-8-quinolin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(4-lmidazol-1 -i l-2-meti l-fen i l)-3-meti l-8-q u inol in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(4-lmidazol-1 -i l-2-meti l-fen i l)-3-meti l-8-pirid in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti I-1 -(4-pirazol-1 -i l-fen i l)-8-q u inol in-3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Meti I-1 -(4-pirazol-1 -i l-fen i l)-8-pirid in-3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-q u inol in-3-i I-1 -(4-[1,2,4]triazol-1 -i l-fen i I)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-pirid in-3-i I-1 -(4-[1,2,4]triazol-1 -i l-fen i I)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; 3-Metil-1 -[4-(4-metil-piperazin-1 -il)-3-trifluorometil-fenil]-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-1 -[4-(4-metil-piperazin-1 -il)-3-trifluorometil-fenil]-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-piperazin-1 -i l-fen i l)-3-meti l-8-q u inol in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-piperazin-1 -i l-fen i l)-3-meti l-8-pirid in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-piperazin-1 -il-fenil)-8-(6-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-(3-Cloro-4-piperazin-1-il-fenil)-8-(5-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(6-Metóxi-piridin-3-il)-3-metil-1 -[4-(4-metil-piperazin-1 -il)-3- trifluorometil-fenil]-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(5-Metóxi-piridin-3-il)-3-metil-1 -[4-(4-metil-piperazin-1 -il)-3- trifluorometil-fenil]-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[2-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(6-metóxi-piridin- 3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[2-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(5-metóxi-piridin- 3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-C loro-4-pi perazin-1 -i l-fen i l)-3-meti l-8-q u inoxal in-6-i I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-1-(4-piperazin-1-il-3-trifluorometil-fenil)-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-1-(4-piperazin-1-il-3-trifluorometil-fenil)-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(6-Metóxi-pirid in-3-i l)-3-meti I-1 -(4-piperazin-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(5-Metóxi-pirid in-3-i l)-3-meti I-1 -(4-piperazin-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-1-(4-piperazin-1-il-3-trifluorometil-fenil)-8-quinoxalin-6- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1-il)-fenil]-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1 -il)-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(4-etil-piperazin-1-il)-fenil]-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(4-etil-piperazin-1-il)-fenil]-3-metil-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[3-Cloro-4-(4-isopropil-piperazin-1 -il)-fenil]-3-metil-8-piridin- 3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[3-C loro-4-(4-isopropi l-pi perazin-1 -i l)-fen i l]-3-meti I-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[3-Cloro-4-(4-isopropil-piperazin-1 -i l)-fen i l]-3-meti I-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[3-C loro-4-(4-isopropi l-pi perazin-1 -i l)-fen i l]-3-meti I-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[4-(4-Etil-piperazin-1 -il)-3-trifluorometil-fenil]-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[4-(4-Etil-piperazin-1 -il)-3-trifluorometil-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[4-(4-Etil-piperazin-1 -il)-3-trifluorometil-fenil]-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[4-(4-Etil-piperazin-1 -il)-3-trifluorometil-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-8-(6-piperazin-1 -il-piridin-3-il)-1 -(3-trifluorometil-fenil)- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(6-Metóxi-piridin-3-il)-3-metil-1-(3-trifluorometil-fenil)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 8-(6-Metóxi-piridin-3-il)-3-metil-1-(3-trifluorometil-fenil)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-imidazol-1 -i l-fen i l)-3-meti l-8-pirid in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-imidazol-1 -i l-fen i l)-3-meti l-8-q u inol in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 2-Metil-2-[4-(3-metil-8-quinolin-3-il-2-tioxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila; 2-Metil-2-{4-[3-metil-8-(2-metil-piridin-4-il)-2-oxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il]-fenil}-propionitrila; 5-{1-[4-(Ciano-dimetil-metil)-fenil]-3-metil-2-oxo-2,3-di-hidro- 1 H-imidazo[4,5-c]quinolin-8-il}-piridina-2-carbonitrila; 2-[4-(4-Amino-3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila; 1-[4-(3-Metil-2-oxo-8-piridin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1 -il)-fenil]-ciclopropanocarbonitrila; 1-[4-(3-Metil-2-oxo-8-quinolin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1 -il)-fenil]-ciclopropanocarbonitrila; 1 -{4-[8-(6-Metóxi-piridin-3-il)-3-metil-2-oxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il]-fenil}-ciclopropanocarbonitrila; 1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(6-metóxi-piridin- 3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(5-metóxi-piridin- 3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-3-metil-8-quinoxalin- 6-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-(3-Cloro-4-piperazin-1-il-fenil)-8-(2-metóxi-pirimidin-5-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-C loro-4-pi perazin-1 -i l-fen i l)-3-meti l-8-pirim id in-5-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-piperazin-1 -il-fenil)-8-(2-metóxi-pirimidin-5-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-piperazin-1 -i l-fen i l)-3-meti l-8-pirim id in-5-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-piperazin-1 -il-fenil)-3-metil-8-(2-metil-piridin-4-il)- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1-[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1-il)-fenil]-8-(6-metóxi- piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1 -il)-fenil]-8-(5-metóxi- piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[4-(c/s-3,5-Dimetil-piperazin-1 -il)-3-trifluorometil-fenil]-8-(6- metóxi-piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -[4-(c/s-3,5-Dimetil-piperazin-1 -il)-3-trifluorometil-fenil]-8-(5- metóxi-piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(2-Metóxi-pirim id in-5-i l)-3-meti I-1 -(4-pi perazin-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-1 -(4-piperazin-1 -il-3-trifluorometil-fenil)-8-pirimidin-5-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 5-[3-Metil-2-oxo-1-(4-piperazin-1-il-3-trifluorometil-fenil)-2,3- di-hidro-1 H-imidazo[4,5-c]quinolin-8-il]-piridina-2-carbonitrila; 3-Meti l-8-(2-meti l-pirid in-4-i I)-1 -(4-pi perazin-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(3,4-Dimetóxi-fenil)-3-metil-1 -(4-piperazin-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-pirid in-3-i I-1 -(4-[1,2,4]triazol-1 -i l-3-trif luorometi I- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-q u inol in-3-i I-1 -(4-[1,2,4]triazol-1 -i l-3-trif luorometi I- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(6-Metóxi-pirid in-3-i l)-3-meti I-1 -(4-[1,2,4]triazol-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(5-Metóxi-pirid in-3-i l)-3-meti I-1 -(4-[1,2,4]triazol-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 5-[3-Metil-2-oxo-1 -(4-[1,2,4]triazol-1 -i l-3-trif luorometi l-fen i I)- 2,3-di-hidro-1 H-imidazo[4,5-c]quinolin-8-il]-piridina-2-carbonitrila; 8-(6-F lúor-pirid in-3-i l)-3-meti I-1 -(4-[1,2,4]triazol-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(2,6-D imetóxi-pirid in-3-i l)-3-meti I-1 -(4-[1,2,4]triazol-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-pirim id in-5-i I-1 -(4-[ 1,2,4]triazol-1 -i l-3-trif luorometi I- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(2-Metóxi-pirim id in-5-i l)-3-meti I-1 -(4-[1,2,4]triazol-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(2,4-D imetóxi-pirim id in-5-i l)-3-meti I-1 -(4-[1,2,4]triazol-1 -i I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti I-1 -(4-pirazol-1 -i l-3-trif luorometi l-fen i l)-8-pirid in-3-i I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Metil-1 -(4-pirazol-1 -il-3-trifluorometil-fenil)-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(6-Metóxi-pirid in-3-i l)-3-meti I-1 -(4-pirazol-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 8-(5-Metóxi-pirid in-3-i l)-3-meti I-1 -(4-pirazol-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-[1,2,4]triazol-1 -i l-fen i l)-3-meti l-8-pirid in-3-i I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(3-Cloro-4-[1,2,4]triazol-1 -i l-fen i l)-3-meti l-8-q u inol in-3-i I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(4-lmidazol-1 -il-3-trifluorometil-fenil)-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(4-lmidazol-1 -il-3-trifluorometil-fenil)-3-metil-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(4-lmidazol-1 -il-3-trifluorometil-fenil)-8-(6-metóxi-piridin-3- il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(4-lmidazol-1 -il-3-trifluorometil-fenil)-8-(5-metóxi-piridin-3- il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-pirid in-3-i I-1 -(4-[1,2,4]triazol-1 -i Imeti l-fen i I)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 3-Meti l-8-q u inol in-3-i I-1 -(4-[1,2,4]triazol-1 -i Imeti l-fen i I)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; 1 -(4-1 m idazol-1 -i Imeti l-fen i l)-3-meti l-8-pirid in-3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona; e 1 -(4-lmidazol-1 -i Imeti l-fen i l)-3-meti l-8-q u inol in-3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona; ou um tautômero deste, ou um sal farmaceuticamente aceitável, ou um hidrato ou solvato deste.
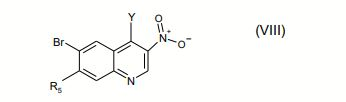
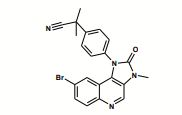
[00015] Preferidos são também compostos de Fórmula la,
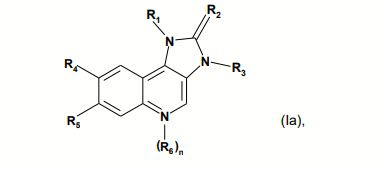
em que Ri é naftila ou fenila em que a referida fenila é substituída por um ou dois substituintes independentemente selecionados do grupo que consiste em halogênio; alquila inferior não-substituída ou substituída por halo ou ciano; amino substituído por um ou dois substituintes independentemente selecionados do grupo que consiste em alquila inferior, alquil sulfonil inferior, alcóxi inferior e alquilamino inferior de alcóxi inferior; piperazinila em que a referida piperazinila é não-substituída ou substituída por um ou dois substituintes independentemente selecionados do grupo que consiste em alquila inferior e alquil sulfonil inferior; 2-oxo-pirrolidinila; alquila inferior de alcóxi inferior; imidazolila; pirazolila e triazolila; R2é O ou S; R3é alquila inferior; R4é piridila não-substituída ou substituída por alcóxi inferior ou piperazinila não-substituída ou substituída por alquila inferior, ou quinolinila não-substituída ou substituída por halogênio, ou quinoxalinila; Rs é hidrogênio ou halogênio; n é 0 ou 1; RΘé óxido; com a condição de que se n = 1, o átomo de N portando o radical Re apresenta uma carga positiva; ou um tautômero destes, ou um sal farmaceuticamente aceitável, ou um hidrato ou solvato destes.
[00016] Surpreendentemente, foi constatado recentemente que os compostos de Fórmula I, têm propriedades farmacológicas vantajosas e inibem a atividade das lipídeo cinases, tais como a PI3 cinase e/ou membros da família de proteína cinase relacionada com PI3 cinase (também chamada PIKK e inclui DNA-PK, ATM, ATR, hSMG-1 e mTOR), tais como a DNA proteína cinase, e podem ser empregados para tratar doenças ou distúrbios que dependem da atividade das referidas cinases.
[00017] Levando em consideração sua inibição de enzimas de fosfatidilinositol 3-cinase, compostos de Fórmula (I) em forma livre ou de sal farmaceuticamente aceitável, são úteis no tratamento de condições que são mediadas pela ativação das enzimas de PI3 cinase, tais como condições proliferativas, inflamatórias ou alérgicas, ou distúrbios de ocorrência comum em conexão com transplantes.
[00018] O tratamento de acordo com a invenção pode ser sintomático ou profilático.
[00019] Preferido é um composto de Fórmula (I) para uso no tratamento de uma doença proliferativa selecionada de um tumor benigno ou maligno, carcinoma do cérebro, rim, fígado, glândula suprarrenal, bexiga, mama, estômago, tumores gástricos, ovários, cólon, reto, próstata, pâncreas, pulmão, vagina ou tiróide, sarcoma, glioblastomas, mieloma múltiplo ou câncer gastrointestinal, especialmente carcinoma de cólon ou adenoma colorretal ou um tumor do pescoço e cabeça, uma hiperproliferação epidérmica, psoríase, hiperplasia da próstata, uma neoplasia, uma neoplasia de caráter epitelial, linfomas, um carcinoma mamário ou uma leucemia. Outras doenças incluem síndrome de Cowden, doença de Lhermitte-Dudos e síndrome de Bannayan-Zonana, ou doenças nas quais a trilha de PI3K/PKB é anormalmente ativada.
[00020] Compostos de acordo com a invenção são úteis no tratamento de doenças inflamatórias ou obstrutivas das vias aéreas, resultando, por exemplo, na redução de lesão de tecido, inflamação de vias aéreas, hiper-reatividade brônquica, remodelação ou progressão da doença. Doenças inflamatórias ou obstrutivas das vias aéreas às quais a presente invenção é aplicável incluem asma de qualquer que seja o tipo ou gênese que inclui tanto a asma intrínseca (não alérgica) quanto a asma extrínseca (alérgica), asma branda, asma moderada, asma severa, asma bronquítica, asma induzida por exercícios, asma ocupacional e asma induzida em seguida à infecção bacteriana. O tratamento de asma também deve ser entendido como tratamento abrangente de pacientes, por exemplo, de menos de 4 ou 5 anos de idade, apresentando sintomas de respiração difícil e diagnosticados ou diagnosticáveis como "crianças ofegantes", uma categoria de paciente estabelecida de grande preocupação médica e agora frequentemente identificada como asmáticos incipientes ou de fase precoce. (Para conveniência esta condição asmática particular é referida como "síndrome da criança ofegante").
[00021] A eficácia profilática no tratamento de asma é comprovada pela frequência reduzida ou severidade do ataque sintomático, por exemplo, do ataque asmático agudo ou broncoconstritor, melhora na função pulmonar ou hiper-reatividade das vias aéreas melhorada. Ela também pode ser comprovada por exigência reduzida quanto a outra terapia sintomática, isto é, terapia para ou pretendida para restringir ou abortar ataque sintomático quando ele ocorrer, por exemplo, antiinflamatória (por exemplo, corticosteróide) ou broncodilatória. O benefício profilático em asma pode ser em particular evidente em pacientes propensos à "crise matinal". "Crise matinal" é uma síndrome asmática reconhecida, comum a uma porcentagem substancial de asmáticos e caracterizada por ataque de asma, por exemplo, entre as horas de aproximadamente 4 a 6 horas da manhã, isto é, em um momento normalmente distante substancialmente de qualquer terapia de asma sintomática anteriormente administrada.
[00022] Os compostos de acordo com a Fórmula I podem ser empregados para outras doenças e condições inflamatórias ou obstrutivas das vias aéreas às quais a presente invenção é aplicável e incluem lesão pulmonar aguda (ALI), síndrome da angústia respiratória aguda de adulto (ARDS), doença pulmonar, das vias aéreas ou do pulmão obstrutiva crônica (COPD, COAD ou COLD), incluindo bronquite crônica ou dispnéia associada com esta, enfisema, assim como exacerbação de hiper-reatividade das vias aéreas consequente a outra terapia de fámaco, em particular outra terapia de fármaco inalado. A invenção também é aplicável ao tratamento de bronquite de qualquer que seja o tipo ou gênese incluindo, por exemplo, bronquite aguda, araquídica, catarral, crupal, crônica ou ftinóide. Outras doenças inflamatórias ou obstrutivas das vias aéreas às quais a presente invenção é aplicável incluem pneumoconiose (uma doença inflamatória, geralmente ocupacional, dos pulmões, frequentemente acompanhada por obstrução de vias aéreas, ou crônica ou aguda, e ocasionada por inalação repetida de poeiras) de qualquer que seja o tipo ou gênese, incluindo, por exemplo, aluminose, antracose, asbestose, calicose, ptilose, siderose, silicose, tabacose e bissinose.
[00023] Levando em consideração sua atividade anti-inflamatória, em particular em relação à inibição de ativação de eosinófilos, os compostos também são úteis no tratamento de distúrbios relacionados com eosinófilos, por exemplo, eosinofilia, em particular distúrbios das vias aéreas relacionados com eosinófilos (por exemplo, envolvendo infiltração eosinofílica mórbida de tecidos pulmonares) incluindo hipereosinofilia quando ela atinge as vias aéreas e/ou pulmões assim como, por exemplo, distúrbios das vias aéreas relacionados com eosinófilos consequentes ou concomitantes à síndrome de Lõffler, pneumonia eosinofílica, infestação parasitária (em particular metazoária) (incluindo eosinofilia tropical), aspergilose broncopulmonar, poliarterite nodosa (incluindo síndrome de Churg- Strauss), granuloma eosinofílico e distúrbios relacionados com eosinófilos afetando as vias aéreas ocasionados por reação ao fármaco.
[00024] Os compostos da invenção também são úteis no tratamento de condições inflamatórias ou alérgicas da pele, por exemplo, psoríase, dermatite de contato, dermatite atópica, alopecia em áreas, eritema multiforme, dermatite herpetiforme, escleroderma, vitiligo, angiite por hipersensibilidade, urticária, penfigóide bolhoso, lúpus eritematoso, pênfigo, epidermólise bolhosa adquirida, e outras condições inflamatórias ou alérgicas da pele.
[00025] Os compostos da invenção também podem ser empregados para o tratamento de outras doenças ou condições, tais como doenças ou condições que têm um componente inflamatório, por exemplo, tratamento de doenças e condições do olho tais como conjuntivite, ceratoconjuntivite seca, e conjuntivite vernal, doenças que afetam o nariz incluindo rinite alérgica, e doença inflamatória na qual reações autoimunes estão implicadas ou tendo um componente ou etiologia autoimune, incluindo distúrbios hematológicos autoimunes (por exemplo, anemia hemolítica, anemia aplásica, anemia eritrocitária pura e trombocitopenia idiopática), lúpus eritematoso sistêmico, policondrite, esclerodoma, granulomatose de Wegener, dermatomiosite, hepatite ativa crônica, miastenia grave, síndrome de Steven-Johnson, espru idiopática, doença inflamatória do intestino autoimune (por exemplo, colite ulcerativa e doença de Crohn), oftalmopatia endócrina, doença de Graves, sarcoidose, alveolite, pneumonite por hipersensibilidade crônica, esclerose múltipla, cirrose biliar primária, uveíte (anterior e posterior), ceratoconjuntivite seca e ceratoconjuntivite primaveral, fibrose pulmonar intersticial, artrite psoriática e glomerulonefrite (com e sem síndrome nefrótica, por exemplo, incluindo síndrome nefrótica diopática ou nefropatia de alteração minai).
[00026] Além disso, a invenção provê o uso de um composto de acordo com as definições anexas, ou um sal farmaceuticamente aceitável, ou um hidrato ou solvato deste para a preparação de um medicamento para o tratamento de uma doença proliferativa, uma doença inflamatória ou uma doença respiratória obstrutiva, ou um distúrbio de ocorrência comum em conexão com transplante.
[00027] A eficácia dos compostos de Fórmula I e sais destes como inibidores de PI3 cinase pode ser demonstrada tal como segue:
[00028] A reação de cinase foi executada em um volume final de 50 pL por cavidade de uma placa 96 cavidades COSTAR de meia área. As concentrações finais de ATP e fosfatidil inositol no ensaio foram de 5 pM e 6 pg/mL respectivamente. A reação foi iniciada pela adição de PI3 cinase p110β. Os componentes do ensaio foram adicionados por cavidade como segue: • 10 pL de composto de teste em DMSO a 5% por cavidade em colunas 2-1. • A atividade total foi determinada por adição de 10 pL de DMSO a 5% vol/vol nas primeiras 4 cavidades da coluna 1 e as últimas 4 cavidades da coluna 12. • A base foi determinada por adição de 10 pM de composto de controle às últimas 4 cavidades da coluna 1 e às primeiras 4 cavidades da coluna 12. • 2 mL de ‘Mistura de ensaio' foram preparados por placa: 1,912 mL de tampão de ensaio de HEPES 8,33 pL de matéria-prima de ATP a 3 mM fornecendo uma concentração final de 5 pM por cavidade 1 pL de [33P]ATP na data da atividade fornecendo 0,05 pCi por cavidade 30 pL de matéria-prima de PI a 1 mg/mL a 3 fornecendo uma concentração final de 6 pg/mL por cavidade 5 pL de matéria-prima de MgCh a 1M fornecendo uma concentração final de 1 mM por cavidade • 20 pL da mistura de ensaio foram adicionados /cavidade. • 2 mL de ‘Mistura de enzima' foram preparados por placa (x pL de PI3 cinase p110β em 2 mL de tampão de cinase). A ‘Mistura de enzima' foi mantida em gelo durante a adição às placas de ensaio. • 20 pl de ‘Mistura de enzima' foram adicionados /cavidade para iniciar a reação. • A placa foi em seguida incubada à temperatura ambiente durante 90 minutos. • A reação foi terminada pela adição de 50 pL de suspensão de contas WGA-SPA por cavidade. • A placa de ensaio foi lacrada empregando-se TopSeal-S e incubada à temperatura ambiente durante pelo menos 60 minutos. • A placa de ensaio foi em seguida centrifugada a 1500 rpm durante 2 minutos empregando-se a centrífuga de bancada Jouan. • A placa de ensaio foi contada empregando-se um Packard TopCount, cada cavidade sendo contada durante 20 segundos.
[00029] * O volume de enzima será dependente da atividade enzimática da batelada em uso.
[00030] Alguns dos compostos apresentam um certo nível de seletividade contra os diferentes parálogos PI3K alfa, gama e delta. Descrição de ensaio bioquímico para DNA-PK:
[00031] O ensaio foi feito empregando-se o kitV7870 de Promega, que quantificou a atividade de proteína cinase dependente de DNA, tanto em preparações de enzima purificadas quanto em extratos nucleares celulares. DNA-PK é uma serina/ treonina proteína cinase nuclear que requer DNA de fita dupla (dsDNA) para a atividade. A ligação de dsDNA à enzima resulta na formação da enzima ativa e também coloca o substrato mais íntimo à enzima, permitindo que a reação de fosforilação prossiga.
[00032] Tampão de reação X5 de DNA-PK (HEPES a 250 mM, KCI a 500 mM, MgCI2 a 50 mM, EGTA a 1 mM, EDTA a 0,5 mM, DTT a 5 mM, pH a 7,5 com KOH) foi diluído de 1/5 em água desionizada e BSA (matéria-prima = 10 mg/mL) foi adicionado para uma concentração final de 0,1 mg/mL.
[00033] O tampão de ativação foi feito de 100 pg/mL de DNA de timo de bezerro em tampão de controle (Tris-HCI a 5 mM (pH 7,4), EDTA a 5 mM (pH 8,0)).
[00034] Por tubo, a mistura de reação foi composta de: 2,5 pl de tampões de ativação ou controle, 5 pl de tampão de reação X5, 2,5 pl de substrato de peptídeo biotinilado derivado de p53 (matéria-prima = 4 mM), 0,2 pl de BSA (matéria-prima a 10 mg/mL) e 5 pl de [y-32P] ATP (5 pl de ATP frio a 0,5 mM + 0,05 pl de Redivue [y-32P] ATP = Amersham AA0068-250 pCi, 3000 Ci/mmols, 10 pCi/pl).
[00035] A enzima de DNA-PK (Promega V5811, concentração = 100 U/pL) foi diluída de 1/10 em tampão de reação de X1 e mantida em gelo até o uso iminente. 10,8 pl da enzima diluída foram incubados com 1,2 pl de compostos a 100 pM (diluídos de 1/100 em água de matéria-prima a 10 mM em DMSO puro) durante 10 minutos, à temperatura ambiente. Durante este tempo, 15,2 pl da mistura de reação foram adicionados a tubos de tampa de rosca, ocultos atrás de vidro Perspex. 9,8 pl da enzima foram em seguida transferidos para os tubos contendo a mistura de reação e depois de 5 minutos de incubação, a 30°C, a reação foi interrompida por adição de 12,5 pl de tampão de terminação (cloridrato de guanidina a 7,5 M).
[00036] Depois de misturar bem, uma alíquota de 10pl de cada tubo foi colocada em uma membrana de captura de biotina SAM2R que foi deixada secar durante alguns minutos. A membrana foi em seguida lavada extensivamente para remover o [y-32P] ATP livre excessivo e proteínas não biotiniladas: uma vez durante 30 segundos em 200 ml de NaCI a 2M, 3 vezes durante 2 minutos cada em 200 ml de NaCI a 2M, 4 vezes durante 2 minutos cada em NaCI a 2M em H3PO4 a 1% e duas vezes durante 30 segundos cada em 100 ml de água desionizada. A membrana foi em seguida deixada secar ao ar à temperatura ambiente durante 30 a 60 minutos.
[00037] Cada quadrado de membrana foi separado empregando-se fórceps e tesoura e colocado em um frasco de cintilação, após 0 que 8 ml de líquido de cintilação (Flo-Scint 6013547 de Perkin-Elmer) foram adicionados. A quantidade de 32P incorporado no substrato de peptídeo biotinilado de DNA-PK foi em seguida determinada por contagem de cintilação líquida.
[00038] A eficácia dos compostos da presente invenção bloqueando a ativação da trilha de PI3K/PKB pode ser demonstrada em vias celulares como segue:
Protocolo para a detecção de fosfo-PKB e fosfo-GSK3β.
[00039] No dia 1, células U87MG (ATCC N° HTB-14) são tripsinadas, contadas em uma câmara de Neubauer, e diluídas em meio RPMI 1640 completo fresco para uma concentração final de 6 x 105células/mL Placas de cultura de tecido de dez (10) cm são em seguida carregadas com 10 mL da suspensão de células, e incubadas durante 18 horas.
[00040] No dia 2, o meio nas placas é descartado e substituído por meio RPMI 1640 completo contendo ou DMSO ou inibidores [compostos de Fórmula (I)]. Depois de 30 minutos de contato, o meio é rapidamente removido por aspiração e as células enxaguadas duas vezes com PBS pré-resfriado. As células são em seguida colocadas em gelo e imediatamente lisadas. Amostras de proteína são em seguida resolvidas por SDS-PAGE e transferidas para membrana Immbilon-P para detecção dos níveis de GSK3β endógeno, PKB, FosfoT308-PKB e FosfoS9-GSK3β por Western-blotting. As membranas são em seguida secas e revestidas com película de polietileno, e a quimioluminescência medida em um gabinete de luz Multilmage™ (Alpha Innotech Corp) acionado com o software FluorChem® (Alpha Innotech Corp).
[00041] Os dados são analisados com o software AlphaEasy, plotados como % de controle (células tratadas com DMSO em condições experimentais idênticas empregadas para inibidores de cinase) com SigmaPlot® ((SSPI Inc, versão 7) como uma curva de regressão (Cúbica Logística de Quatro Parâmetros) e valores de IC50 são adequadamente determinados.
[00042] Há também experimentos para demonstrar a atividade antitumor de compostos da Fórmula (I) in vivo.
[00043] Camundongos nus/nus atímicos Harlan fêmeas com tumores U87MG de glioblastomas humanos transplantados s.c. podem ser empregados para determinar a atividade antitumor de inibidores de PI3 cinase. No dia 0, com os animais sob narcose de foreno peroral, um fragmento de tumor de aproximadamente 25 mg é colocado sob a pele no flanco esquerdo dos animais e o pequeno ferimento feito através de incisão é fechado por meio de clipes de sutura. Quando os tumores atingem um volume de 100 mm3, os camundongos são divididos aleatoriamente em grupos de 6 a 8 animais e o tratamento começa. O tratamento é realizado durante um período de 2 a 3 semanas com administração perorai, intravenosa ou intraperitoneal uma vez diariamente (ou menos frequentemente) de um composto de Fórmula (I) em um veículo adequado em doses definidas. Os tumores são medidos duas vezes por semana com um calibrador corrediço e o volume dos tumores é calculado.
[00044] Como uma alternativa à linhagem de células U87MG, outras linhagens de células também podem ser empregadas da mesma maneira, por exemplo, • a linhagem de células de adenocarcinoma de mama MDA-MB 468 (ATCC N° HTB 132; veja também In Vitro14, 911-15 [1978]); • a linhagem de células de carcinoma de mama MDA-MB 231 (ATCC N° HTB-26; veja também In Vitro12, 331 [1976]); • a linhagem de células de carcinoma de mama MDA-MB 453 (ATCC N° HTB-131); • a linhagem de células de carcinoma de cólon Colo 205 (ATCC N° CCL 222; veja também Cancer Res. 38. 1345-55 [1978]); • a linhagem de células DU 145 de carcinoma de prostate DU 145 (ATCC N° HTB 81; veja também Cancer Res. 37, 4049-58 [1978]), • a linhagem de células PC-3 de carcinoma de próstata PC-3 (especialmente preferida; ATCC N° CRL 1435; veja também Cancer Res. 40, 524-34 [1980]) e a linhagem de células de carcinoma de próstata PC-3M; • o adenocarcinoma pulmonar humano A549 (ATCC N° CCL 185; veja também Int. J. Cancer 17, 62-70 [1976]), • a linhagem de células NCI-H596 (ATCC N° HTB 178; veja também Science 246, 491-4 [1989]); • a linhagem de células de câncer pancreático SUIT-2 (veja Tomioka e outros, Cancer Res. 61, 7518-24 [2001]).
[00045] Os compostos da invenção apresentam atividade inibidora de células T. Mais particular, os compostos da invenção impedem a ativação e/ou proliferação de células T em, por exemplo, solução aquosa, por exemplo, como demonstrado de acordo com o método de teste seguinte. O MLR bidirecional é executado de acordo com procedimentos-padrão (J. Immunol. Methods, 1973, 2, 279 e Meo T. e outros, Immunological Methods, Nova Iorque, Imprensa Acadêmica, 1979, 227-39). Resumidamente, células de baço de camundongos CBA e BALB/c (1,6 x 105 células de cada cepa por cavidade em placas de microtítulo de cultura de tecido de fundo plano, 3,2 x 105 no total) são incubadas em meio de RPMI contendo FCS a 10%, 100 U/mL de penicilina, 100 pg/mL de estreptomicina (Gibco BRL, Basel, Suíça), 2- mercaptoetanol a 50 pM (Fluka, Buchs, Suíça) e compostos diluídos em série. Sete etapas de diluição de três vezes em duplicatas por composto de teste são executadas. Depois de quatro dias de incubação, 1 pCi de 3H-timidina é adicionado. As células são colhidas depois de um período de incubação de cinco horas adicionais, e a 3H- timidina incorporada é determinada de acordo com procedimentos- padrão. Os valores de base (controle reduzido) do MLR são a proliferação de células BALB/c somente. Os controles reduzidos são subtraídos de todos os valores. Os controles elevados sem qualquer amostra são considerados como 100% de proliferação. O percentual de inibição pelas amostras é calculado, e as concentrações requeridas para 50% de inibição (valores de IC50) são determinadas. Neste ensaio, os compostos da invenção têm valores de IC50 na faixa de 1 nM a 10 pM, de preferência de 10 nM a 100 nM.
[00046] Um composto da Fórmula (I) também pode ser empregado para a vantagem em combinação com outros compostos antiproliferativos. Tais compostos antiproliferativos incluem, mas não estão limitados a inibidores de aromatase; antiestrogênios; inibidores de topoisomerase I; inibidores de topoisomerase II; compostos ativos de microtúbulo; composto de alquilação; inibidores de histona desacetilase; compostos que induzem processos de diferenciação celular, inibidores de ciclo-oxigenase; inibidores de MMP; inibidores de mTOR; anti-metabólitos antineoplásicos; compostos de platina; compostos direcionando/ diminuindo uma atividade de proteína ou lipídeo cinase e também compostos antiangiogênicos; compostos que direcionam, diminuem ou inibem a atividade de uma proteína ou lipídeo fosfatase; agonistas de gonadorrelina; antiandrogênios; inibidores de metionina aminopeptidase; bisfosfonatos; modificadores de resposta biológicos; anticorpos antiproliferativos; inibidores de heparanase; inibidores de isoformas oncogênicas de Ras; inibidores de telomerase; inibidores de proteassoma; compostos empregados no tratamento de malignidades hematológicas; compostos que direcionam, diminuem ou inibem a atividade de Flt-3; inibidores de Hsp90 tais como 17-AAG (17- alquilaminogeldanamicina, NSC330507), 17-DMAG (17- dimetilaminoetilamino-17-desmetóxi-geldanamicina, NSC707545), IPI- 504, CNF1010, CNF2024, CNF1010 de Conforma Therapeutics; temozolomida (TE MO DAL®); inibidores de proteína de fuso de cinesina, tais como SB715992 ou SB743921 de GlaxoSmithKline, ou pentamidina/ clorpromazina de CombinatoRx; inibidores de MEK tais como ARRY142886 de Array PioPharma, AZD6244 de AstraZeneca, PD181461 de Pfizer e leucovorina.
[00047] A expressão "inibidor de aromatase"tal como empregada aqui se refere a um composto que inibe a produção de estrogênio, isto é a conversão dos substratos androstenodiona e testosterona para estrona e estradiol, respectivamente. A expressão inclui, mas não está limitada a esteroides, especialmente atamestano, exemestano e formestano e, em particular, não esteroides, especialmente aminoglutetimida, rogletimida, piridoglutetimida, trilostano, testolactona, cetoconazol, vorozol, fadrozol, anastrozol e letrozol. Exemestano pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada AROMASIN. Formestano pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada LENTARON. Fadrozol pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada AFEMA. Anastrozol pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada ARIMIDEX. Letrozol pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada FEMARA ou FEMAR. Aminoglutetimida pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada ORIMETEN. Uma combinação da invenção compreendendo um agente quimioterapêutico que é um inibidor de aromatase é particularmente útil para o tratamento de tumores positivos quanto a receptores de hormônio, por exemplo, tumores de mama.
[00048] O termo "antiestrogênio" tal como empregado aqui se refere à um composto que antagoniza o efeito de estrogênios ao nível de receptor de estrogênio. O termo inclui, mas não está limitado a tamoxifeno, fulvestranto, raloxifeno e cloridrato de raloxifeno. Tamoxifeno pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada NOLVADEX. Cloridrato de raloxifeno pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada EVISTA. Fulvestranto pode ser formulado como descrito em US 4.659.516 ou pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada FASLODEX. Uma combinação da invenção compreendendo um agente quimioterapêutico que é um antiestrogênio é particularmente útil para o tratamento de tumores positivos quanto a receptores de estrogênio, por exemplo, tumores de mama.
[00049] O termo "antiandrogênio" tal como empregado aqui se refere à qualquer substância que seja capaz de inibir os efeitos biológicos de hormônios androgênicos e inclui, mas não está limitado a, bicalutamida (CASODEX), que pode ser formulada, por exemplo, como descrito em US 4.636.505.
[00050] A expressão "agonista de gonadorrelina" tal como empregada aqui inclui, mas não é limitada a abarelix, gosserrelina e acetato de gosserrelina. Gosserrelina é descrita em US 4.100.274 e pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada ZOLADEX. Abarelix pode ser formulado, por exemplo, tal como descrito em US 5.843.901.
[00051] A expresão "inibidor de topoisomerase I" tal como empregada aqui inclui, mas não é limitado a topotecana, gimatecana, irinotecana, camptotecina e seus análogos, 9-nitrocamptotecina e o conjugado PNU-166148 de camptotecina macromolecular (composto A1 em WO99Z 17804). Irinotecana pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada CAMPTOSAR. Topotecana pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada HYCAMTIN.
[00052] A expressão "inibidor de topoisomerase II" tal como empregada aqui inclui, mas não é limitada às antraciclinas tais como doxorrubicina (incluindo formulação lipossômica, por exemplo, CAELYX), daunorrubicina, epirrubicina, idarrubicina e nemorrubicina, as antraquinonas mitoxantrona e losoxantrona, e as podofilotoxinas etoposídeo e teniposídeo. Etoposídeo pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada ETOPOPHOS. Teniposídeo pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada VM 26-BRISTOL Doxorrubicina pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada ADRIBLASTIN ou ADRIAMYCIN. Epirrubicina pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada FARMORUBICIN. Idarrubicina pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada ZAVEDOS. Mitoxantrona pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada NOVANTRON.
[00053] A expressão "agente ativo de microtúbulo" se refere a compostos de estabilização de microtúbulos e desestabilização de microtúbulos e inibidores de polimerização de microtubulina incluindo, mas não limitados a taxanos, por exemplo, paclitaxel e docetaxel, alcalóides de vinca, por exemplo, vimblastina, especialmente sulfato de vimblastina, vincristina especialmente sulfato de vincristina, e vinorelbina, discodermolidas, cochicina e epotilonas e derivados destas, por exemplo, epotilona B ou D ou derivados destas. Paclitaxel pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, TAXOL. Docetaxel pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada TAXOTERE. Sulfato de vinblastina pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada VINBLASTIN R.P.. Sulfato de vincristina pode ser adminitrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada FARMISTIN. Discodermolida pode ser obtida, por exemplo, tal como descrito em US 5.010.099. Estão também incluídos os derivados de Epotilona que estão descritos em WO98/10121, US 6.194.181, WO 98/25929, WO 98/08849, WO 99/43653, WO 98/22461 e WO 00/31247. Especialmente preferidos são Epotilona A e/ou B.
[00054] A expressão "agente de alquilacão" tal como empregada aqui inclui, mas não está limitada a, ciclofosfamida, ifosfamida, melfalana ou nitrosouréia (BCNU ou Gliadel). Ciclofosfamida pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada CICLOSTYN. Ifosfamida pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada HOLOXAN.
[00055] A expressão "inibidores de histona desacetilase" ou "inibidores de HDAC" se refere a compostos que inibem a histona desacetilase e que possuem atividade antiproliferativa. Esta inclui compostos descritos em WO 02/22577, especialmente N-hidróxi-3-[4- [[(2-hidroxietil)[2-(1 H-indol-3-il)etil]-amino]metil]fenil]-2E-2- propenamida, N-hidróxi-3-[4-[[[2-(2-metil-1/-/-indol-3-il)-etil]- amino]metil]fenil]-2E-2-propenamida e sais farmaceuticamente aceitáveis destes. Ela também inclui especialmente ácido hidroxâmico de suberoilanilida (SAHA).
[00056] A expressão "antimetabólito antineoplástico" inclui, mas não está limitada a, 5-Fluorouracila ou 5-FU, capecitabina, gencitabina, compostos de desmetilação de DNA, tais como 5-azacitina e decitabina, metotrexato e edatrexato, e antagonistas de ácido fólico como pemetrexed. Capecitabina pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada XELODA. Gencitabina pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada GEMZAR.
[00057] A expressão "composto de platina" tal como empregada aqui inclui, mas não está limitada a, carboplatina, c/s-platina, cisplatina e oxaliplatina. Carboplatina pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada CARBOPLAT. Oxaliplatina pode ser administrada, por exemplo, na forma tal como ela é comercializada, por exemplo, sob a marca registrada ELOXATIN.
[00058] A expressão "compostos direcionando/ diminuindo uma atividade de proteína ou lipídeo cinase; ou uma atividade de proteína ou lipídeo fosfatase; ou também compostos antiangiogênicos" tal como empregada aqui inclui, mas não está limitada a, inibidores de proteína tirosina cinase e/ou serina e/ou treonina cinase ou inibidores de lipídeo cinase, por exemplo, a) compostos direcionando, diminuindo ou inibindo a atividade dos receptores de fator de crescimento derivados de plaqueta (PDGFR), tais como compostos que direcionam, diminuem ou inibem, a atividade de PDGFR, especialmente compostos que inibem o receptor de PDGF, por exemplo, um derivado de N-fenil-2-pirimidina- amina, por exemplo, imatinib, SU101, SU6668 e GFB-111; b) compostos direcionando, diminuindo ou inibindo a atividade dos receptores do fator de crescimento de fibroblastos (FGFR); c) compostos direcionando, diminuindo ou inibindo a atividade do receptor de fator de crescimento semelhante à insulina I (IGF-IR), tais como compostos que direcionam, diminuem ou inibem a atividade de IGF-IR, especialmente compostos que inibem a atividade de cinase de receptor de IGF-I, tais como aqueles compostos descritos em WO 02/092599, ou anticorpos que direcionam o domínio extracelular do receptor de IGF-I ou seus fatores de crescimento; d) compostos direcionando, diminuindo ou inibindo a atividade da família de tirosina cinase receptora de Trk, ou inibidores de efrina B4; e) composto direcionando, diminuindo ou inibindo a atividade da família de tirosina cinase receptora de Axl; f) compostos direcionando, diminuindo ou inibindo a atividade da tirosina cinase receptora de Ret; g) composto direcionando, diminuindo ou inibindo a atividade da tirosina cinase receptora de K/f/SCFR, por exemplo, imatinib; h) compostos direcionando, diminuindo ou inibindo a atividade das tirosina cinases receptoras de C-kit - (parte da família de PDGFR), tais como compostos que direcionam, diminuem ou inibem a atividade da família de tirosina cinase receptora de c-Kit, especialmente compostos que inibem o receptor de c-Kit, por exemplo, imatinib; i) composto direcionando, diminuindo ou inibindo a atividade de membros da família de c-Abl, seus produtos de fusão de gene (por exemplo, BCR-Abl cinase) e mutantes, tais como compostos que direcionam diminuem ou inibem a atividade de membros da família c- Abl e seus produtos de fusão de gene, por exemplo, um derivado de N- fenil-2-pirimidina-amina, por exemplo, imatinib ou nilotinibe (AMN107); PD180970; AG957; NSC 680410; PD173955 de ParkeDavis; ou dasatinibe (BMS-354825); j) compostos direcionando, diminuindo ou inibindo a atividade dos membros da família de proteína cinase C (PKC) e Raf de serina/treonina cinases, membros dentre os membros da família de MEK, SRC, JAK, FAK, PDK1, PKB/Akt, e Ras/MAPK, e/ou membros da família de cinase dependente de ciclina (CDK) e são especialmente aqueles derivados de estaurosporina descritos em US 5.093.330, por exemplo, midostaurina; exemplos de outros compostos incluem, por exemplo, UCN-01, safingol, BAY 43-9006, Briostatina 1, Perifosina; llmofosina; RO 318220 e RO320432; GO 6976; Isis 3521; LY333531/LY379196; compostos de isoquinolina tais como aqueles descritos em WO00/09495; FTIs; PD184352 ou QAN697 (um inibidor de P13K) ou AT7519 (inibidor de CDK); k) compostos direcionando, diminuindo ou inibindo a atividade de inibidores de proteína-tirosina cinase, tais como compostos que direcionam, diminuem ou inibem a atividade de inibidores proteína-tirosina cinase incluem, mesilato de imatinib (GLEEVEC) ou tirfostina. Uma tirfostina é de preferência um composto de baixo peso molecular (Mr < 1500), ou um sal farmaceuticamente aceitável deste, especialmente um composto selecionado da classe de benzilidenomalonitrila ou da classe de S-arilbenzenomalonirilo ou bi- substrato quinolina de compostos, mais especialmente qualquer composto selecionado do grupo que consiste em Tirfostina A23/RG- 50810; AG 99; Tirfostina AG 213; Tirfostina AG 1748; Tirfostina AG 490; Tirfostina B44; (+) enantiômero de Tirfostina B44; Tirfostina AG 555; AG 494; Tirfostina AG 556, AG957 e adafostina (éster de adamantila de ácido 4-{[(2,5-di-hidroxifenil)metil]amino}-benzoico; NSC 680410, adafostina); l) compostos direcionando, diminuindo ou inibindo a atividade da família de fator de crescimento epidérmico de tirosina cinases receptoras (EGFR, ErbB2, ErbB3, ErbB4 como homo- ou heterodímeros) e seus mutantes, tais como compostos que direcionam, diminuem ou inibem a atividade da família de receptores do fator de crescimento epidérmico são especialmente compostos, proteínas ou anticorpos que inibem membros da família de tirosina cinase receptora de EGF, por exemplo, receptor de EGF, ErbB2, ErbB3 e ErbB4 ou ligam-se a EGF ou ligantes relacionados a EGF, e são em particular aqueles compostos, proteínas ou anticorpos monoclonais genericamente e especificamente descritos em WO 97/02266, por exemplo, o composto do ex. 39, ou em EP 0 564 409, WO 99/03854, EP 0520722, EP 0 566 226, EP 0 787 722, EP 0 837 063, US 5.747.498, WO 98/10767, WO 97/30034, WO 97/49688, WO 97/38983 e, especialmente, WO 96/30347 (por exemplo, composto conhecido como CP 358774), WO 96/33980 (por exemplo, composto ZD 1839) e WO 95/03283 (por exemplo, composto ZM105180);, por exemplo, trastuzumabe (Herceptin®), cetuximabe (Erbitux®), Iressa, Tarceva, OSI-774, CI-1033, EKB-569, GW-2016, E1.1, E2.4, E2.5, E6.2, E6.4, E2.11, E6.3 ou E7.6,3, e derivados de 7H-pirrolo-[2,3- d]pirimidina que estão descritos em WO 03/013541; e m) compostos direcionando, diminuindo ou inibindo a atividade do receptor c-Met, tais como compostos que direcionam, diminuem ou inibem a atividade de c-Met, especialmente compostos que inibem a atividade de cinase do receptor de c-Met, ou anticorpos que direcionam o domínio extracelular de c-Met ou ligam-se a HGF.
[00059] Outros compostos anti-angiogênicos incluem compostos que têm outro mecanismo para sua atividade, por exemplo, não relacionado a inibição de proteína ou lipídeo cinase, por exemplo, talidomida (THALOMID) e TNP-470.
[00060] Compostos que direcionam, diminuem ou inibem a atividade de uma proteína ou lipídeo fosfatase são, por exemplo, inibidores de fosfatase 1, fosfatase 2A, ou CDC25, por exemplo, ácido ocadáico ou um derivado deste.
[00061] Compostos que induzem processos de diferenciação celular são, por exemplo, ácido retinoico, a-, y- ou õ-tocoferol ou a-, y- ou δ- tocotrienol.
[00062] A expressão inibidor de ciclo-oxigenase tal como empregada aqui inclui, mas não está limitada a, por exemplo, inibidores de Cox-2, ácido 2-arilaminofenilacético substituído por 5- alquila e derivados, tais como celecoxibe (CELEBREX), rofecoxibe (VIOXX), etoricoxibe, valdecoxibe ou um ácido 5-alquil-2- arilaminofenilacético, por exemplo, ácido acético de 5-metil-2-(2'-cloro- 6'-fluoroanilino)fenila, lumiracoxibe.
[00063] O termo "bisfosfonatos" tal como empregado aqui inclui, mas não está limitado a, ácido etridônico, clodrônico, tiludrônico, pamidrônico, alendrõnico, ibandrônico, risedrônico e zoledrônico. "Ácido Etridrônico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada DIDRONEL. "Ácido clodrônico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada BONEFOS. "Ácido tiludrônico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada SKELID. "Ácido pamidrônico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada AREDIA®. "Ácido alendrõnico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada FOSAMAX. "Ácido ibandrônico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada BONDRANAT. "Ácido risedrônico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada ACTONEL. "Ácido zoledrônico" pode ser administrado, por exemplo, na forma tal como ele é comercializado, por exemplo, sob a marca registrada ZOMETA.
[00064] A expressão "inibidores de mTOR" se refere à compostos que inibem o alvo mamífero de rapamicina (mTOR) e que possuem atividade antiproliferativa tais como sirolimo (Rapamune®), everolimo (Certican®), CCI-779 e ABT578.
[00065] A expressão "inibidor de heparanase" tal como empregada aqui se refere a compostos que direcionam, diminuem ou inibem degradação de sulfato de heparina. A expressão inclui, mas não está limitada a, PI-88.
[00066] A expressão "modificador de resposta biológica" tal como empregada aqui se refere a uma linfocina ou interferons, por exemplo, interferon y.
[00067] A expressão "inibidor de isoformas oncogênicas de Ras", por exemplo, H-Ras, K-Ras, ou N-Ras, tal como empregada aqui se refere a compostos que direcionam, diminuem ou inibem a atividade oncogênica de Ras, por exemplo, um "inibidor de farnesil transferase", por exemplo, L-744832, DK8G557 ou R115777 (Zarnestra).
[00068] A expressão "inibidor de telomerase"tal como empregada aqui se refere a compostos que direcionam, diminuem ou inibem a atividade de telomerase. Compostos que direcionam, diminuem ou inibem a atividade de telomerase são especialmente compostos que inibem o receptor de telomerase, por exemplo, telomestatina.
[00069] A expressão "inibidor de metionina aminopeptidase"tal como empregada aqui se refere a compostos que direcionam, diminuem ou inibem a atividade de metionina aminopeptidase. Compostos que direcionam, diminuem ou inibem a atividade de metionina aminopeptidase são, por exemplo, bengamida ou um derivado desta.
[00070] A expressão "inibidor de proteassoma" tal como empregada aqui se refere a compostos que direcionam, diminuem ou inibem a atividade do proteassoma. Compostos que direcionam, diminuem ou inibem a atividade do proteassoma incluem, por exemplo, Bortezomida (Velcade®) e MLN 341.
[00071] A expressão "inibidor de metaloproteinase matriz" ou ("inibidor de MMP") tal como empregada aqui inclui, mas não está limitada a, peptidomimético de colágeno e inibidores peptidomimético e não peptidomimético, derivados de tetraciclina, por exemplo, inibidor batimastate peptidomiméticos de hidroxamato e seu análogo oralmente biodisponível marismastate (BB-2516), prinomastate (AG3340), metastate (NSC 683551), BMS-279251, BAY 12-9566, TAA211, MMI270B ou AAJ996.
[00072] A expressão "compostos empregados no tratamento de malignidades hematológicas"tal como empregada aqui inclui, mas não está limitada a, inibidores de tirosina cinase do tipo FMS, por exemplo, compostos direcionando, diminuindo ou inibindo a atividade receptores de tirosina cinase do tipo FMS (Flt-3R); interferon, 1-b-D- arabinofuransilcitosina (ara-c) e bissulfano; e inibidores de ALK, por exemplo, compostos que direcionam, diminuem ou inibem linfoma anaplásico cinase.
[00073] Compostos que direcionam, diminuem ou inibem a atividade de receptores de tirosina cinase do tipo FMS (Flt-3R) são especialmente compostos, proteínas ou anticorpos que inibem membros da família de cinase receptora de Flt-3R, por exemplo, PKC412, midostaurina, um derivado de estaurosporina, SU11248 e MLN518.
[00074] A expressão "inibidores de HSP90" tal como empregada aqui inclui, mas não está limitada a, composto direcionando, diminuindo ou inibindo a atividade de ATPase intrínseca de HSP90; degradando, direcionando, diminuindo ou inibindo as proteínas clientes de HSP90 por meio da trilha de proteossoma de ubiquitina. Compostos direcionando, diminuindo ou inibindo a atividade de ATPase intrínseca de HSP90 são especialmente compostos, proteínas ou anticorpos que inibem a atividade de ATPase de HSP90, por exemplo, 17-alilamino, 17-demetoxigeldanamicina (17AAG), um derivado de geldanamicina; outros compostos relacionados com geldanamicina; radicicol e inibidores de HDAC.
[00075] A expressão "anticorpos antiproliferativos" tal como empregada aqui inclui, mas não está limitada a, trastuzumabe (Herceptin®), Trastuzumab-DM1, erbitux, bevacizumabe (Avastin®), rituximabe (Rituxan®, PRO64553 (anti-CD40) e Anticorpo 2C4. Por anticorpos é pretendido, por exemplo, anticorpos monoclonais intactos, anticorpos policlonais, anticorpos multiespecíficos formados de pelo menos 2 anticorpos intactos, e fragmentos de anticorpos contanto que eles apresentem a atividade biológica desejada.
[00076] Para o tratamento de leucemia mielóide aguda (AML), compostos de Fórmula (I) podem ser empregados em combinação com terapias-padrões de leucemia, especialmente em combinações com terapias empregadas para o tratamento de AML. Em particular, os compostos de Fórmula (I) podem ser administrados em combinação com, por exemplo, inibidores de farnesil transferase e/ou outros fármacos úteis para o tratamento de AML, tais como Daunorrubicina, Adriamicina, Ara-C, VP-16, Teniposídeo, Mitoxantrona, Idarrubicina, Carboplatina e PKC412.
[00077] A expressão "compostos antileucêmicos" inclui, por exemplo, Ara-C, um análogo de pirimidina, que é o derivado de 2'-alfa- hidróxi ribose (arabinosídeo) de desoxicitidina. Também incluído está o analógico de purina hipoxantina, 6-mercaptopurina (6-MP) e fosfato de fludarabina.
[00078] Compostos que direcionam, diminuem ou inibem atividade de inibidores de histona desacetilase (HDAC) tais como butirato de sódio e ácido suberoilanilida hidroxâmico (SAHA) inibem a atividade das enzimas conhecidas como histona desacetilases. Inibidores de HDAC específicos incluem MS275, SAHA, FK228 (antigamente FR901228), Tricostatina A e compostos descritos em US 6.552.065, em particular, N-hidróxi-3-[4-[[[2-(2-metil-1 H-indol-3-il)-etil]- amino]metil]fenil]-2E-2-propenamida, ou um sal farmaceuticamente aceitável deste e N-hidróxi-3-[4-[(2-hidroxietil){2-(1 H-indol-3-il)etil]- amino]metil]fenil]-2E-2-propenamida, ou um sal farmaceuticamente aceitável deste, especialmente o sal de lactato.
[00079] Antagonistas de receptor de somatostatina tais como empregados aqui se referem a compostos que direcionam, tratam ou inibem o receptor de somatostatina tal como octreotida, e SOM230.
[00080] Métodos de danificar células de tumor se referem a métodos tais como radiação ionizantes. A expressão "radiação ionizante" referida acima e daqui em diante se refere à radiação ionizante que ocorre como ou raios eletromagnéticos (tais raios X e raios gama) ou partículas (tais como partículas alfa e beta). A radiação Ionizante é fornecida em, mas não limitada a, terapia de radiação e é conhecida na técnica. Veja Hellman, Principles of Radiation Therapy, Cancer, em Principles and Practice of Oncology, Devita e outros, Eds., 4a Edição, Vol. 1, páginas 248-275 (1993).
[00081] A expressão aglutinantes de EDG tal como empregado aqui se refere a uma classe de imunossupressores que modula recirculação de linfócito, tal como FTY720.
[00082] A expressão inibidores de ribonucleotídeo redutase se refere à análogos de nucleosídeo de pirimidina ou purina incluindo, mas não limitados a, fludarabina e/ou citosina arabinosídeo (ara-C), 6- tioguanina, 5-fluorouracila, cladribina, 6-mercaptopurina (especialmente em combinação com ara-C contra ALL) e/ou pentostatina. Inibidores de ribonucleotídeo redutase especialmente são hidroxiuréia ou derivados de 2-hidróxi-1 H-isoindol-1,3-diona, tais como PL-1, PL-2, PL-3, PL 4, PL-5, PL-6, PL-7 ou PL-8 mencionados em Nandy e outros, Acta Oncológica,Vol. 33, n° 8, páginas 953-961 (1994).
[00083] A expressão "inibidores de S-adenosilmetionina descarboxilase" tal como empregada aqui inclui, mas não está limitada aos compostos descritos em US 5.461.076.
[00084] Também incluídos estão em particular aqueles compostos, proteínas ou anticorpos monoclonais de VEGF descritos em WO 98/35958, por exemplo, 1-(4-cloroanilino)-4-(4-piridilmetil)ftalazina ou um sal farmaceuticamente aceitável destes, por exemplo, o sucinato, ou em WO 00/09495, WO 00/27820, WO 00/59509, WO 98/11223, WO 00/27819 e EP 0 769 947; aqueles tais como descritos por Prewett e outros, Cancer Res, Vol. 59, pp. 5209-5218 (1999); Yuan e outros, Proc Natl Acad Sci USA, Vol. 93, pp. 14765-14770 (1996); Zhu e outros, Cancer Res, Vol. 58, pp. 3209-3214 (1998); e Mordenti e outros, Toxicol Pathol, Vol. 27, n° 1, pp. 14-21 (1999); em WO 00/37502 e WO 94/10202; ANGIOSTATIN, descrito por O'Reilly e outros, Cell, Vol. 79, pp. 315-328 (1994); ENDOSTATIN, descrito por O'Reilly e outros, Cell, Vol. 88, pp. 277-285 (1997); amidas de ácido antranilico; ZD4190; ZD6474; SU5416; SU6668; bevacizumabe; ou anticorpos de anti-VEGF ou anticorpos de receptor de anti-VEGF, por exemplo, rhuMAb e RHUFab, aptâmero de VEGF, por exemplo, Macugon; inibidores de FLT-4, inibidores de FLT-3, anticorpo de lgG1 de VEGFR-2, Angiozima (RPI 4610) e Bevacizumabe (Avastin®).
[00085] Terapia fotodinâmica tal como empregado aqui se refere a terapia que usa certas substâncias químicas conhecidas como compostos de fotossensibilização para tratar ou prevenir cânceres. Exemplos de terapia fotodinâmica incluem tratamento com compostos, tais como, por exemplo, VISUDYNE e sódio de porfimer sódio.
[00086] Esteroides angiostáticos tais como empregados aqui referem-se aos compostos que bloqueiam ou inibem angiogênese, tais como, por exemplo, anecortave, triancinolona, hidrocortisona, 11-a-epi- hidrocotisol, cortexolona, 17-cc-hidroxiprogesterona, corticosterona, desoxicorticosterona, testosterona, estrona e dexametasona.
[00087] Implantes compreendendo corticosteróides referem-se aos compostos, tais como, por exemplo, fluocinolona, dexametasona.
[00088] Outras compostos quimioterapêuticos incluem, mas não estão limitados a, alcalóides de planta, compostos hormonais e antagonistas; modificadores de resposta biológicos, de preferência linfocinas ou interferons; oligonucleotídeos de anti-sentido ou derivados de oligonucleotídeo; shRNA ou siRNA; ou compostos heterogêneos ou compostos com outro ou desconhecido mecanismo de ação.
[00089] Os compostos da invenção também são úteis como compostos co-terapêuticos para uso em combinações com outras substâncias de fármacos tais como substâncias de fármaco anti- inflamatório, broncodilatório ou anti-histamínico, particularmente no tratamento de doenças de vias aéreas obstrutivas ou inflamatórias tais como aquelas mencionadas aqui anteriormente, por exemplo, como potencializadores de atividade terapêutica de tais fármacos ou como um meio de reduzir os efeitos colaterais de dosagem ou potenciais exigidos de tais fármacos. Um composto da invenção pode ser misturado com a outra substância farmacológica em uma composição farmacêutica fixa ou pode ser administrado separadamente, antes, simultaneamente com ou depois da outra substância farmacológica. Consequentemente, a invenção inclui uma combinação de um composto da invenção como descrito aqui anteriormente com uma substância farmacológica anti-inflamatório, broncodilatório, anti- histamínico ou antitussígeno, o referido composto da invenção e a referida substância farmacológica estando na mesma ou diferente composição farmacêutica.
[00090] Drogas anti-inflamatórias adequadas incluem esteroides, em particular glicocorticosteróides tais como budesonida, dipropionato de beclametasona, propionato de fluticasona, ciclesonida ou furoato de mometasona, ou esteroides descritos em WO 02/88167, WO 02/12266, WO 02/100879, WO 02/00679 (especialmente aqueles dos Exemplos 3, 11, 14, 17, 19, 26, 34, 37, 39, 51, 60, 67, 72, 73, 90, 99 e 101), WO 03/035668, WO 03/048181, WO 03/062259, WO 03/064445, WO 03/072592, agonistas de receptor de glicocorticóide não esteroidal tais como aqueles descritos em WO 00/00531, WO 02/10143, WO 03/082280, WO 03/082787, WO 03/104195, WO 04/005229; antagonistas de LTB4 tais como LY293111, CGS025019C, CP- 195543, SC-53228, BIIL 284, ONO 4057, SB 209247 e aqueles descritos em US 5451700; antagonistas de LTD4 tais como montelukast e zafirlukast; inibidores de PDE4 tais como cilomilaste (Ariflo® GlaxoSmithKline), Roflumilaste (Byk Gulden), V-11294A (Napp), BAY19-8004 (Bayer), SCH-351591 (Schering-Plough), Arofilline (Almirall Prodesfarma), PD189659/PD168787 (Parke-Davis), AWD-12-281 (Asta Medica), CDC-801 (Celgene), SelCID(TM) CC- 10004 (Celgene), VM554/UM565 (Vernalis), T-440 (Tanabe), KW-4490 (Kyowa Hakko Kogyo), e aqueles descritos em WO 92/19594, WO 93/19749, WO 93/19750, WO 93/19751, WO 98/18796, WO 99/16766, WO 01/13953, WO 03/104204, WO 03/104205, WO 03/39544, WO 04/000814, WO 04/000839, WO 04/005258, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/018431, WO 04/018449, WO 04/018450, WO 04/018451, WO 04/018457, WO 04/018465, WO 04/019944, WO 04/019945, WO 04/045607 e WO 04/037805; agonistas de A2a tais como aqueles descritos em EP 409595A2, EP 1052264, EP 1241176, WO 94/17090, WO 96/02543, WO 96/02553, WO 98/28319, WO 99/24449, WO 99/24450, WO 99/24451, WO 99/38877, WO 99/41267, WO 99/67263, WO 99/67264, WO 99/67265, WO 99/67266, WO 00/23457, WO 00/77018, WO 00/78774, WO 01/23399, WO 01/27130, WO 01/27131, WO 01/60835, WO 01/94368, WO 02/00676, WO 02/22630, WO 02/96462, WO 03/086408, WO 04/039762, WO 04/039766, WO 04/045618 e WO 04/046083; antagonistas de A2b tais como aqueles descritos em WO 02/42298; e agonistas de beta-2 adrenoceptor tais como albuterol (salbutamol), metaproterenol, terbutalina, salmeterol fenotero, procaterol, e especialmente, formoterol e sais farmaceuticamente aceitáveis destes, e compostos (em forma livre ou de sal ou de solvato) de Fórmula I de WO 0075114, cujo documento é incorporado aqui por referência, de preferência compostos dos Exemplos destes, especialmente um composto de Fórmula
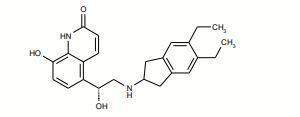
e sais farmaceuticamente aceitáveis destes, assim como compostos (em forma livre ou de sal ou de solvato) de Fórmula I de WO 04/16601, e também compostos de WO 04/033412.
[00091] Fármacos broncodilatórios adequados incluem compostos anticolinérgicos ou antimuscarínicos, em particular brometo de ipratrópio, brometo de oxitrópio, sais de tiotrópio e CHF 4226 (Chiesi), e glicopirrolato, mas também aqueles descritos em WO 01/04118, WO 02/51841, WO 02/53564, WO 03/00840, WO 03/87094, WO 04/05285, WO 02/00652, WO 03/53966, EP 424021, US 5171744, US 3714357, WO 03/33495 e WO 04/018422.
[00092] Substâncias de fármaco de anti-histamínico adequadas incluem cloridrato de cetirizina, acetaminofeno, fumarato de clemastina, prometazina, loratidina, desloratidina, difenidramina e cloridrato de fexofenadina, activastina, astemizol, azelastina, ebastina, epinastina, mizolastina e tefenadina assim como aqueles descritos em WO 03/099807, WO 04/026841 e JP 2004107299.
[00093] Outras combinações úteis de compostos da invenção com fármacos anti-inflamatórios são aqueles com antagonistas de receptores de quimiocina, por exemplo, CCR-1, CCR-2, CCR-3, CCR- 4, CCR-5, CCR-6, CCR-7, CCR-8, CCR-9 e CCR10, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, particularmente antagonistas de CCR-5 tais como antagonistas Schering-Plough SC-351125, SCH-55700 e SCH- D, antagonistas de Takeda tais como cloreto de N-[[4-[[[6,7-di-hidro-2- (4-metilfenil)-5H-benzo-ciclo-hepten-8-il]carbonil]amino]fenil]- metil]tetra-hidro-N,N-dimetil-2H-piran-4-amínio (TAK-770), e antagonistas de CCR-5 descritos em US 6166037 (particularmente reivindicações 18 e 19), WO 00/66558 (particularmente reivindicação 8), WO 00/66559 (particularmente reivindicação 9), WO 04/018425 e WO 04/026873.
[00094] A estrutura dos compostos ativos identificados por números de código, nomes genéricos ou de comerciais podem ser retirados da edição atual do compêndio padrão "The Merck Index" ou de bases de dados, por exemplo, Patentes Internacionais (por exemplo, Publicações Mundiais de IMS).
[00095] Os compostos acima citados, que podem ser empregados em combinação com um composto da Fórmula (I), podem ser preparados e administrados como descrito na técnica, tal como nos documentos citados acima.
[00096] Um composto da Fórmula (I) também pode ser empregado para vantagem em combinação com processos terapêuticos conhecidos, por exemplo, a administração de hormônios ou especialmente radiação.
[00097] Um composto de Fórmula (I) pode ser empregado em particular empregado como um radiossensibilizante, especialmente para o tratamento de tumores que apresentam fraca sensibilidade à radioterapia.
[00098] Por "combinação", neste contexto é pretendido ou uma combinação fixa em uma forma unitária de dosagem, ou um kit de partes para a administração combinada onde um composto da Fórmula (I) e um parceiro de combinação podem ser administrados independentemente ao mesmo tempo ou separadamente em intervalos de tempo que especialmente permitem que os parceiros da combinação apresentem um efeito cooperativo, por exemplo, sinérgico.
[00099] A invenção também fornece uma preparação farmacêutica, compreendendo um composto de Fórmula I tal como definido aqui, ou um N-óxido ou um tautômero deste, ou um sal farmaceuticamente aceitável de um tal composto, ou um hidrato ou solvato deste, e pelo menos um veículo farmaceuticamente aceitável.
[000100] Um composto de Fórmula I pode ser administrado sozinho ou em combinação com um ou mais outros compostos terapêuticos, possível terapia de combinação tomando a forma de combinações fixas ou a administração de um composto da invenção e um ou mais outros compostos terapêuticas sendo alternados ou administrados independentemente um do outro, ou a administração combinada de combinações fixas e um ou mais outros compostos terapêuticos. Um composto da Fórmula I pode ademais ou além disso ser administrado especialmente para terapia de tumor em combinação com quimioterapia, radioterapia, imunoterapia, fototerapia, intervenção cirúrgica, ou uma combinação destas. A terapia de longa duração é igualmente possível como uma terapia adjuvante no contexto de outras estratégias de tratamento, como descrito acima. Outros possíveis tratamentos são terapia para manter o estado do paciente após a regressão do tumor, ou mesmo terapia quimiopreventiva, por exemplo, em pacientes em risco.
[000101] A dosagem do ingrediente ativo depende de uma variedade de fatores incluindo tipo, espécies, idade, peso, sexo e condição médica do paciente; a severidade da condição a ser tratada; a via de administração; a função renal e hepática do paciente; e a composto particular empregado. Um médico, clínico ou veterinário versado na técnica pode facilmente determinar e prescrever a quantidade eficaz da fármaco requerido para prevenir, agir contra ou interromper o progresso da condição. A precisão ótima na obtenção da concentração de fármaco na faixa que produz eficácia requer um regime baseado na cinética da disponibilidade do fármaco para direcionar sítios. Isto envolve uma consideração da distribuição, equilíbrio, e eliminação de um fármaco.
[000102] A dose de um composto da Fórmula I ou um sal farmaceuticamente aceitável deste para ser administrado aos animais de sangue quente, por exemplo, seres humanos de aproximadamente 70 kg de peso corporal, é preferível de aproximadamente 3 mg a aproximadamente 5 g, mais preferível de aproximadamente 10 mg a aproximadamente 1,5 g, mais preferível de cerca de 100 mg a cerca de 1000 mg por pessoa por dia, dividido de preferência em 1 a 3 doses únicas que podem, por exemplo, seja do mesmo tamanho. Normalmente, crianças recebem a metade da dose de adulto.
[000103] Os compostos da invenção podem ser administrados por qualquer via convencional, em particular parenteralmente, por exemplo, na forma de soluções ou suspensões injetáveis, entericamente, por exemplo, oralmente, por exemplo, na forma de comprimidos ou cápsulas, topicamente, por exemplo, na forma de loções, géis, unguentos ou cremes, ou em um forma nasal ou uma de supositório. Administração tópica é, por exemplo, para a pele. Uma forma adicional de administração tópica é para o olho. Composições farmacêuticas compreendendo um composto da invenção em associação com pelo menos um veículo ou diluente farmacêutico aceitável podem ser fabricadas de maneira convencional misturando com um veículo ou diluente farmaceuticamente aceitável.
[000104] A invenção se refere também a composições farmacêuticas compreendendo uma quantidade eficaz, especialmente uma quantidade eficaz no tratamento de um dos distúrbios acima citados, de um composto de Fórmula I ou um N-óxido ou um tautômero destes junto com veículos farmaceuticamente aceitáveis que são adequados para administração tópica, enteral, por exemplo, oral ou retal, ou parenteral e que pode ser inorgânica ou orgânica, sólida ou líquida. Estas são empregadas para administração oral especialmente comprimidos ou cápsulas de gelatina que compreendem o ingrediente ativo junto com diluentes, por exemplo, lactose, dextrose, manitol, e/ou glicerol, e/ou lubrificantes e/ou polietileno glicol. Comprimidos também podem incluir aglutinantes, por exemplo, silicato de alumínio e magnésio, amidos, tais como amido de milho, trigo ou arroz, gelatina, metilcelulose, carboximetilcelulose de sódio e/ou polivinilpirrolidona, e, se desejado, desintegradores, por exemplo, amidos, ágar, ácido algínico ou um sal destes, tais como alginato de sódio, e/ou misturas efervescentes, ou adsorventes, tinturas, aromatizantes e adoçantes. Também é possível empregar os compostos farmacologicamente ativos da presente invenção na forma de composições administráveis parenteralmente ou na forma de soluções de infusão. As composições farmacêuticas podem ser esterilizadas e/ou podem compreender excipientes, por exemplo, conservantes, estabilizadores, compostos de umectação e/ou emulsificantes, solubilizantes, sais para regulação da pressão osmótica e/ou tampões. As composições farmacêuticas presentes, que podem, se desejado, compreender outra substâncias farmacologicamente ativas são preparadas de uma maneira conhecida per se, por exemplo, por meio de processos de agitação convencional, granulação, confecção, dissolução ou liofilização, e compreendem aproximadamente de 1% a 99%, especialmente de aproximadamente 1% a aproximadamente 20%, de ingrediente(s) ativo(s).
[000105] Adicionalmente, a presente invenção fornece um composto de Fórmula I ou um N-óxido ou um tautômero deste, ou um sal farmaceuticamente aceitável de um tal composto, para uso em um método para o tratamento do corpo humano ou animal.
[000106] A presente invenção se refere também ao uso de um composto de Fórmula I ou um tautômero desta, ou um sal farmaceuticamente aceitável de um tal composto, para a preparação de um medicamento para o tratamento de uma doença proliferativa, uma doença inflamatória, ou uma doença de via aérea obstrutiva, ou distúrbios de ocorrência comum em conexão com transplantes.
[000107] Além disso, a invenção se refere a um método para o tratamento de uma doença proliferativa que responde a uma inibição de lipídeo cinases e/ou cinases de proteína relacionada com PI3- cinase, em particular a cinase PI3, e/ou atividade de proteína cinase de DNA, que compreende administrar a um composto de Fórmula I ou um N-óxido ou um tautômero deste, ou um sal farmaceuticamente aceitável, ou um hidrato ou solvato deste, em que os radicais e símbolos têm os significados como definido acima, em uma quantidade eficaz contra a referida doença, a um animal de sangue quente, em particular para seres humanos, requerendo tais tratamentos.
[000108] Além disso, a invenção se refere a uma composição farmacêutica para o tratamento de tumores sólidos ou líquidos em animais de sangue quente, incluinso seres humanos, compreendendo uma dose antitumoralmente eficaz de um composto da Fórmula I como descrito acima ou um sal farmaceuticamente aceitável de um tal composto junto com um veículo farmacêutico.
[000109] A invenção também fornece um processo para a preparação de um composto de Fórmula I de acordo com a reivindicação 1, ou um sal farmaceuticamente aceitável deste, caracterizado pelo fato de que é um derivado de imidazoquinolina da Fórmula II.
[000110] Um composto da invenção pode ser preparado por processos que, embora não aplicados até agora para os novos compostos da presente invenção, são conhecidos per se, especialmente por um processo caracterizado pelo fato de que para a síntese de um composto da Fórmula I em que os símbolos Ri, R2, Rs, R4 R5 R6 e n são tais como definidos para um composto da Fórmula I, um composto da Fórmula II
em que R1, R2, R3, R5, R6 e n são tais como definidos para um composto da Fórmula I é reagido com um ácido borônico da Fórmula III R4-B(OH)2 ou de Fórmula llla
em que R4 é tal como definido para um composto da Fórmula I na presença de uma base e um catalisador em um solvente adequado; onde os compostos de partida II e III acima também podem estar presentes com grupos funcionais na forma protegida se necessário e/ou na forma de sais, com a condição de que um grupo de formação de sal esteja presente e a reação em forma de sal seja possível; quaisquer grupos de proteção em um derivado protegido de um composto da Fórmula I são removidos; e, se assim desejado, um composto obtenível de Fórmula I é convertido em outro composto de Fórmula I ou um N-óxido deste, um composto livre de Fórmula I é convertido em um sal, um sal obtenível de um composto de Fórmula I é convertido no composto livre ou outro sal, e/ou uma mistura de compostos isoméricos de Fórmula I é separada nos isômeros individuais.
[000111] Na descrição mais detalhada do processo abaixo, R1, R2, R3, R4, Rs, Re e n são tais como definidos para compostos de Fórmula I, a menos que de outra forma indicado.
[000112] A reação de composto de Fórmula II e III é realizada de preferência sob as condições de uma reação de Suzuki, de preferência em uma mistura de um solvente aprótico polar tal como DMF e água na presença de um catalisador, especialmente um catalisador de metal nobre, tal como paládio (II), de preferência dicloreto de bis(trifenilfosfina)paládio (II); na presença de uma base como carbonato de potássio.
Grupos de proteção
[000113] Se um ou mais outros grupos funcionais, por exemplo, carbóxi, hidróxi, amino, ou mercapto, são ou necessitam ser protegidos em um composto de Fórmulas II ou III, porque eles não devem tomar parte na reação, estes são grupos semelhantes que são normalmente empregados na síntese de compostos de peptídeo, e também de cefalosporinas e penicilinas, assim como derivados de ácido nucleico e açúcares.
[000114] Os grupos de proteção já podem estar presentes em precursores e devem proteger os grupos funcionais envolvidos contra reações secundárias não desejadas, tais como acilações, eterificações, esterificações, oxidações, solvólise, e reações similares. É uma característica de grupos de proteção que eles induzem a si mesmos facilmente, isto é sem reações secundárias não desejadas, à remoção, tipicamente por acetólise, protonólise, solvólise, redução, fotólise ou também por atividade de enzima, por exemplo, sob condições análogas às condições fisiológicas, e que eles não estão presentes nos produtos finais. O versado sabe, ou pode facilmente estabelecer, quais grupos de proteção são adequados com as reações mencionadas aqui acima e daqui em diante.
[000115] A proteção de tais grupos funcionais por tais grupos de proteção, os próprios grupos de proteção, e suas reações de remoção são descritos, por exemplo, em trabalhos de referência padrão, tais como J. F. W. McOmie, "Protective Groups in Organic Chemistry", Plenum Press, Londres e Nova Iorque 1973, em T. W. Greene, "Protective Groups in Organic Synthesis", Wiley, Nova Iorque 1981, em "The Peptides"; Volume 3 (editores: E. Gross e J. Meienhofer), Academic Press, Londres e Nova Iorque 1981, em "Methoden der organischen Chemie"(Methods of organic chemistry), Houben Weyl, 4° edição, Volume 15/1, Georg Thieme Verlag, Stuttgart 1974, em H.-D. Jakubke e H. Jescheit, "Aminosãuren, Peptide, Proteine"(Amino acids, peptides, proteins), Verlag Chemie, Weinheim, Deerfield Beach, e Basel 1982, e em Jochen Lehmann, "Chemie der Kohlenhydrate: Monosaccharide und Derivate"(Chemistry of carbohydrates: monosaccharides and derivatives), Georg Thieme Verlag, Stuttgart 1974.
Etapas de processo adicionais
[000116] Nas etapas de processo adicionais, veículos como desejado, grupos funcionais dos compostos de partida que não devem tomar parte na reação podem estar presentes em forma desprotegida ou podem ser protegidos, por exemplo, por um ou mais dos grupos de proteção mencionados aqui acima em "grupos de proteção". Os grupos de proteção são em seguida completa ou parcialmente removidos de acordo com um dos métodos descrito lá.
[000117] Sais de um composto de Fórmula I com um grupo formador de sal pode ser preparado de uma maneira conhecida per se. Sais de adição de ácido de compostos de Fórmula I podem ser, desse modo, obtidos por tratamento com um ácido ou com um reagente de permuta de ânion adequado. Um sal com duas moléculas de ácido (por exemplo, um di-halogeneto de um composto de Fórmula I) também pode ser convertido em um sal com uma molécula de ácido por composto (por exemplo, um monohalogeneto); isto pode ser feito por aquecimento até uma fusão, ou, por exemplo, aquecendo como um sólido sob um vácuo elevado à temperatura elevada, por exemplo, de 130 a 170°C, uma molécula ácido sendo expelida por molécula de um composto de Fórmula I.
[000118] Sais normalmente podem ser convertidos em compostos livres, por exemplo, por tratamento com compostos básicos adequados, por exemplo, com carbonatos de metal de álcali, hidrogenocarbonatos de metal de álcali, ou hidróxidos de metal de álcali, tipicamente carbonato de potássio ou hidróxido de sódio.
[000119] Misturas estereoisoméricas, por exemplo, misturas de diastereômeros, podem ser separadas nos seus isômeros correspondentes de uma maneira conhecida per si por meios de métodos de separação adequados. Misturas diastereoméricas, por exemplo, podem ser separadas em seus diastereômeros individuais por meios de cristalização fracionadas, cromatografia, distribuição de solvente, e procedimentos similares. Esta separação pode ocorrer ou no nível de um composto de partida ou em um próprio composto de Fórmula I. Enantiômeros podem ser separados pela formação de sais diastereoméricos, por exemplo, por formação de sal com um ácido quiral enantiomericamente puro, ou por meios de cromatografia, por exemplo, por HPLC, empregando-se substratos cromatográficos com ligantes quirais.
[000120] Um composto da Fórmula I, em que R2 é O, pode ser convertido no composto respectivo em que R2 é S, por exemplo, empregando-se um composto de enxofre adequado, por exemplo, empregando reação com reagente de Lawesson (2,4-bis-(4- metoxifenil)2,4-ditioxo-1,2,3,4-ditiafosfetan) em um solvente adequado tal como dioxano.
[000121] Deve ser enfatizado que reações análogas às conversões mencionadas neste capítulo podem também ocorrer ao nível de intermediários adequados.
Condições de processo gerais
[000122] Todos as etapas de processo descritas aqui podem ser realizadas sob condições de reação conhecidas, de preferência sob aquelas especificamente mencionadas, na ausência de ou normalmente na presença de solventes ou diluentes, de preferência tais como são inertes aos reagentes empregados e capazes de dissolver estes, na ausência ou presença de catalisadores, agentes de condensação ou agentes de neutralisação, por exemplo, permutadores de íons, tipicamente permutadores de cátion, por exemplo, na forma de H+, dependendo do tipo de reação e/ou reagentes em temperatura reduzido, normal, ou elevada, por exemplo, na faixa de -100°C a cerca de 190°C, de preferência de cerca de -80°C a cerca de 150°C, por exemplo, a -80 a -60°C, à temperatura ambiente , a - 20 a 40°C ou no ponto de ebulição do solvente empregado, sob pressão atmosférica ou em um vaso fechado, onde apropriado sob pressão, e/ou em uma atmosfera inerte, por exemplo, sob argônio ou nitrogênio.
[000123] Sais podem estar presentes em todos os compostos de partida e transitórios, se estes contêm grupos de formação de sal. Sais também podem estar presentes durante a reação de tais compostos, contanto que a reação não seja atrapalhada por meio destes.
[000124] Em todas as fases de reação, misturas isoméricas que ocorrem podem ser separadas em seus isômeros individuais, por exemplo, diastereômeros ou enantiômeros, ou em qualquer mistura de isômeros, por exemplo, racematos ou misturas diastereoméricas, tipicamente como descrito sob "Etapas de processo adicionais."
[000125] Os solventes dos quais aqueles podem ser selecionados que são adequados para a reação em questão incluem água, ésteres, por exemplo, tipicamente alquil inferior-alcanoatos inferiores, por exemplo, acetato de etila, éteres, tipicamente éteres alifáticos, por exemplo, dietiléter, ou éteres cíclicos, por exemplo, tetra-hidrofurano, hidrocarbonetos aromáticos líquidos, tipicamente benzeno ou tolueno, álcoois, tipicamente metanol, etanol ou 1- ou 2-propanol, 1-butanol, nitrilas, tipicamente acetonitrila, hidrocarbonetos halogenados, tipicamente diclorometano, amidas de ácido, tipicamente dimetilformamida, bases, tipicamente bases de nitrogênio heterocíclico, por exemplo, piridina, ácidos carboxílicos, tipicamente ácidos alcanocarboxílicos inferiores, por exemplo, ácido acético, anidridos de ácido carboxílico, tipicamente anidridos de ácido de alcano inferior, por exemplo, anidrido acético, hidrocarbonetos cíclicos, lineares, ou ramificados, tipicamente ciclo-hexano, hexano, ou isopentano, ou misturas destes solventes, por exemplo, soluções aquosas, a menos que de outra forma estabelecido na descrição do processo. Tais misturas de solventes também podem ser empregadas em processamento, por exemplo, através de cromatografia ou distribuição.
[000126] Os compostos de Fórmula I, incluindo seus sais, também são obteníveis na forma de hidratos, ou seus cristais podem incluir, por exemplo, o solvente empregado por cristalização (presente como solvatos).
[000127] Na modalidade preferida, um composto de Fórmula I é preparado de acordo com ou em analogia aos processos e etapas de processo definidos nos Exemplos.
Materiais de partida
[000128] Novos materiais de partida e/ou intermediários, assim como processos para a preparação destes, são também o objeto desta invenção. Na modalidade preferida, tais materiais de partida são empregados e condições de reação também selecionadas de modo a permitir os compostos preferidos serem obtidos.
[000129] Materiais de partida da Fórmula II e III são conhecidos, comercialmente disponíveis, ou podem ser sintetizados em analogia a ou de acordo com métodos que são conhecidos na técnica.
[000130] por exemplo, um composto da Fórmula II, em que n é 0, pode ser preparado pela alquilação de um composto amino da Fórmula IV,
em que Ri, R2 e Rs têm os significados como fornecidos na Fórmula I com um composto da Fórmula V R3-X (V) em que R3 tem 0 significado como fornecido na Fórmula I e X é halogênio ou outro grupo de partida adequado, na presença de uma base, por exemplo, hidróxido de sódio, em um solvente adequado, por exemplo, uma mistura de diclorometano e água, de preferência na presença de um catalisador de transferência de fase, por exemplo, brometo de tetrabutilamônio, a uma temperatura entre 0 °C e 50 °C, de preferência à temperatura ambiente.
[000131] Um composto da Fórmula II, em que n é 0, pode ser convertido no composto respectivo em que n é 1, por exemplo, empregando-se um oxidante apropriado, por exemplo, empregando reação com ácido meta-cloroperbenzoico em um solvente apropriado tal como diclorometano à temperatura ambiente .
[000132] Um composto da Fórmula IV, em que R2 é O, pode ser preparado pela ciclização de um composto de diamino da Fórmula VI,
em que Ri e Rs têm os significados como fornecidos na Fórmula I com cloroformiato de triclorometila na presença de uma base, tal como trietilamina em um solvente apropriado, tal como diclorometano.
[000133] Um composto da Fórmula VI pode ser preparado pela redução de um composto de nitro da Fórmula VII,
em que Ri e Rs têm os significados como fornecidos na Fórmula I.
[000134] A redução de preferência ocorre na presença de um agente de redução adequado, tal como hidrogênio na presença de um catalisador apropriado, tal como níquel de Raney sob pressão, por exemplo, entre 1,1x105 e 2x105 pa (1,1 e 2 bar), em um solvente apropriado, por exemplo, um álcool ou éter, tal como metanol ou tetra- hidrofurano ou uma mistura destes. A temperatura de reação é de preferência entre 0 e 80 °C, especialmente 15 a 30 °C.
[000135] Um composto da Fórmula VII pode ser preparado pela reação de um composto VIII
em que Rs é tal como definido para um composto da Fórmula I e Y é halogênio ou outro grupo de partida adequado, é reagido com um composto da Fórmula IX, R1-NH2 (IX) em que Ri é tal como definido para um composto da Fórmula I, em uma temperatura entre 0 °C e 50 °C, de preferência à temperatura ambiente em um solvente adequado, isto é ácido acético.
[000136] Todos os materiais de partida restantes tais como materiais de partida da Fórmula III, IV e V são conhecidos, capazes de serem preparados de acordo com processos conhecidos, ou comercialmente obteníveis; em particular, eles podem ser preparados empregando processos como descrito nos Exemplos. Abreviações: EtOAc acetato de etila Me metila m.p. ponto de fusão Boc terc-butoxicarbonila conc. concentrado DMF N,N-dimetilformamida ES-MS espectrometria de massa por eletrovaporização Grad gradiente h hora(s) HPLC cromatografia líquida de alta pressão litro(s) l litro(s) min minuto(s) MS espectro de massa Prep. HPLC C18 de fase reversa de HPLC preparativa sat. saturado rt temperatura ambiente tret tempo de retenção de HPLC em minuto TFA ácido trifluoroacético THF tetra-hidrofurano
[000137] Os Exemplos seguintes servem para ilustrar a invenção sem limitação da invenção em seu escopo.
[000138] As temperaturas são medidas em graus Celsius (°C). A menos que de outra forma indicado, as reações ocorrem à temperatura ambiente (RT).
[000139] Relações de solventes (por exemplo, em eluentes ou misturas de solventes) são determinadas em volume por volume (v/v).
[000140] Gradiente linear de HPLC entre A = H2O/TFA 1000:1 e B = acetonitrila/TFA 1000:1 Grad 1:2- 100% de B em 4,5 minutos e 1 minuto a 100% de B; coluna: Chromolith Performance 100 mm x 4,5 mm (Merck, Darmstadt, Alemanha); taxa de fluxo 2 ml/minuto. Detecção a 215 nM Grad 2: 2 - 100% de B em 5 minutos e 2 minutos a 100% de B; coluna: fase inversa de Cie Nucleosil; 150 mm x 4,6 mm (SMT, Burkard Instruments, Dietikon, Suíça); taxa de fluxo: 2,0 ml/minuto. Detecção a 215 nm. Exemplo 1 2-Metil-2-[4-(3-metil-2-oxo-8-piridin-4-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1-il)-fenil]-propionitrila
[000141] 37 mg (0,3 mmol) de ácido 4-piridinaborônico (Aldrich, Buchs, Suíça), 8 mg de dicloreto de bis(trifenilfosfina)paládio (II) (Fluka, Buchs, Suíça) e 0,5 ml de uma solução a 1 M de Na2COa são adicionados a uma solução de 84 mg (0,2 mmol) de 2-[4-(8-bromo-3- metil-2-oxo-2,3-di-hidro-imidazo[4,5-c]quinolin-1-il)-fenil]-2-metil- propionitrila (Exemplo 1i) em 2 ml de DMF. A mistura é agitada durante 1 hora a 100°C. Depois deste tempo, a mistura é extinguida com NaHCOs aquoso saturado e extraída com EtOAc (2x). A camada orgânica é lavada com salmoura, seca sobre Na2SO4, filtrada e evaporada a vácuo. O resíduo é carregado em sílica-gel e purificado através de cromatografia instantânea (CFhCh-MeOH 97:3 a 18:1) para produzir 0 composto do título como um sólido esbranquiçado. ES-MS: 420 (M + H)+; HPLC analítica: tret = 2,40 minutos (Grad 1). Exemplo 1a Ácido 5-bromo-2-(2-nitro-vinilamino)-benzoico
[000142] Uma suspensão de 25 g (16 mmols) de ácido 2-amino-5- bromo-benzoico (Fluka, Buchs, Suíça) em H2O-HCI (37%) (10:1) é agitada durante 8 horas e em seguida filtrada (solução A). 8,17 g (255 mmols) de nitrometano (Fluka, Buchs, Suíça) são adicionados durante 10 min a uma mistura resfriada com banho de gelo de 35 g de gelo e 15,3 g (382 mmols) de NaOH. Depois de agitar durante 1 hora a 0 °C e 1 hora à temperatura ambiente , a solução é adicionada a 0 °C para 28 g de gelo e 42 ml de HCI (37%) (solução B). as soluções A e B são combinadas e a mistura de reação é agitada durante 18 horas à temperatura ambiente. O precipitado amarelo é filtrado, lavado com H2O e seco a vácuo a 40°C para produzir 0 composto do título. ES-MS: 287, 289 (M + H)+, padrão Br; 1H RMN (DMSO-de): õ 13,7 - 14,6/br s (1H), 12,94/d (1H), 8,07/d (1H), 8,03/dd (1H), 7,83/dd (1H), 7,71/d (1H), 6,76/d (1H). Exemplo 1b 6-Bromo-3-nitro-quinolin-4-ol
[000143] 29 g (101 mmols) de ácido 5-bromo-2-(2-nitro-vinilamino)- benzoico (Exemplo 1a) e 11,9 g (121 mmols) de acetato de potássio em 129 ml (152 mmols) de anidrido acético são agitados durante 1,5 horas a 120 °C. O precipitado é filtrado e lavado com ácido acético até que 0 filtrado fique incolor, em seguida é lavado com H2O e seco a vácuo para produzir 0 composto do título. ES-MS: 269, 271 (M + H)+, padrão Br; HPLC analítica: tret= 2,70 minutos (Grad 1). Exemplo 1c 6-Bromo-4-cloro-3-nitro-quinolina
[000144] 20 g (74,3 mmols) de 6-bromo-3-nitro-quinolin-4-ol (Exemplo 1b) em 150 ml (1,63 mol) de POCI3 são agitados durante 45 minutos a 120 °C. A mistura é resfriada à temperatura ambiente e despejada lentamente em água gelada. O precipitado é filtrado, lavado com água gelada, e dissolvido em CH2CI2. A fase orgânica é lavada com salmoura fria, e a fase aquosa é descartada. Depois de secar sobre MgSCU, 0 solvente orgânico é evaporado até a secura para fornecer 0 composto do título. 1H RMN (CDCh): δ 9,20/s (1H), 8,54/d (1H), 8,04/d (1H), 7,96/dd (1H); HPLC analítica: Let = 4,32 minutos (Grad 1). Exemplo 1d 2-metil-2-(4-nitro-fenil)-propionitrila
[000145] A 15 g (92,5 mmols) de (4-nitro-fenil)-acetonitrila (Fluka, Buchs, Suíça), 1,64 mg (5,09 mmols) de brometo de tetrabutilamônio (Fluka, Buchs, Suíça) e 43,3 g (305 mmols) de iodometano em 125 mL de CH2CI2 são adicionados 10 g (250 mmols) de NaOH em 125 ml de água. A mistura de reação é agitada durante 20 horas à temperatura ambiente. Depois deste tempo, a camada orgânica é separada, seca sobre MgSO4, e evaporada até a secura. O resíduo é dissolvido em dietiléter e tratado com carvão preto durante 30 minutos, filtrado sobre Celita e evaporado a vácuo para produzir 0 composto do título como um sólido amarelo-pálido. HPLC analítica: tret= 3,60 minutos (Grad 1). Exemplo 1e (2-(4-amino-fenil)-2-metil-propionitrila
[000146] 16 g (84,1 mmols) de 2-metil-2-(4-nitro-fenil)-propionitrila (Exemplo 1d) e 4,16 g de Raney-Ni são agitados em 160 ml de THF- MeOH (1:1) sob 1,1x105 Pa (1,1 bar) de H2 durante 12 horas à temperatura ambiente. Após a conclusão da reação, 0 catalisador é filtrado e 0 filtrado é evaporado até a secura. O resíduo é purificado através de cromatografia instantânea em sílica-gel (hexano-EtOAc 3:1 a 1:2) para produzir 0 composto do título como um óleo. ES-MS: 161 (M + H)+; HPLC analítica: tret= 2,13 minutos (Grad 1). Exemplo 1f 2-[4-(6-Bromo-3-nitro-quinolin-4-ilamino)-fenil]-2-metil- propionitrila
[000147] 18 g (62,6 mmols) (Exemplo 1c) e 11 g (68,9 mmols) de (2-(4-amino-fenil)-2-metil- propionitrila (Exemplo 1e) são dissolvidos em 350 ml de ácido acético e agitados durante 2 horas. Depois deste tempo, água é adicionada e o precipitado amarelo é filtrado e lavado com H2O. O sólido é dissolvido em EtOAc-THF (1:1), lavado com NaHCOs aquoso saturado e seco sobre MgSCU. A fase orgânica é evaporada até a secura para produzir 0 composto do título como um sólido amarelo. ES-MS: 411, 413 (M + H)+, padrão Br; HPLC analítica: tret= 3,69 minutos (Grad 1). Exemplo 1g 2-[4-(3-amino-6-bromo-quinolin-4-ilamino)-fenil]-2-metil- propionitrila
[000148] 24 g (58,4 mmols) de 2-[4-(6-bromo-3-nitro-quinolin-4- ilamino)-fenil]-2-metil-propionitrila (Exemplo 1e) são agitados em 300 ml de MeOH-THF (1:1) 1,1 x105 Pa (sob 1,1 bar) de H2 na presença de 8,35 g de Raney-Ni durante 1 hora. Depois da conclusão da reação, o catalisador é filtrado e o filtrado é evaporado até a secura para produzir 0 composto do título como uma espuma amarela. ES-MS: 381, 383 (M + H)+, padrão Br; HPLC analítica: tret= 3,21 minutos (Grad 1). Exemplo 1h 2-[4-(8-Bromo-2-oxo-2,3-di-hidro-imidazo[4,5-c]quinolin-1-il)-fenil]- 2-metil-propionitrila
[000149] Uma solução de 5 g (13,1 mmols) de 2-[4-(3-amino-6- bromo-quinolin-4-ilamino)-fenil]-2-metil-propionitrila (Exemplo 1g) e 1,59 g (15,7 mmols) de trietilamina em 120 ml de CH2CI2 é adicionada durante 40 minutos a uma solução de 2,85 g (14,4 mmols) de cloroformiato de triclorometila (Fluka, Buchs, Suíça) em 80 ml de CH2CI2 a 0°C com um banho de gelo. A mistura de reação é agitada durante 20 minutos a esta temperatura e em seguida é extinguida com NaHCOs aquoso saturado, agitada durante 5 minutos e extraída com CH2CI2. A camada orgânica é seca sobre Na2SO4, filtrada e evaporada a vácuo para produzir 0 composto do título bruto como um sólido amarronado. ES-MS: 407, 409 (M + H)+, padrão Br; HPLC analítica: tret = 3,05 minutos (Grad 1). Exemplo 1i 2-[4-(8-Bromo-3-metil-2-oxo-2,3-di-hidro-imidazo[4,5-c]quinolin-1- i l)-fen i l]-2-meti l-propion itri la
[000150] A uma solução de 3,45 g (8,47 mmols) de 2-[4-(8-bromo-2- oxo-2,3-di-hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila (Exemplo 1 h), 1,8 g (12,7 mmols) de iodometano (Fluka, Buchs, Suíça) e 273 mg (0,847 mmol) de brometo de tetrabutilamônio (Fluka, Buchs, Suíça) em 170 ml de CH2CI2 é adicionada uma solução de 508 mg (12,7 mmols) de NaOH (Fluka, Buchs, Suíça) em 85 ml de H2O. A mistura de reação é agitada durante 2 dias e 900 mg (6,35 mmols) de iodometano e 254 mg (6,35 mmols) de NaOH em 5 ml de H2O são adicionados. A mistura de reação é agitada durante 1 dia à temperatura ambiente . Depois deste tempo, a reação é extinguida com H2O e extraída com CH2CI2 (2x). A camada orgânica é lavada com salmoura, seca sobre Na2SÜ4, filtrada e evaporada a vácuo para produzir o composto do título como um sólido bege. ES-MS: 421, 423 (M + H)+, padrão Br; HPLC analítica: tret = 3,15 minutos (Grad 1).
[000151] Os compostos seguintes (Tabela 1) são preparados de uma maneira similar tal como descrito no exemplo 1 por reação de 2-[4-(8-bromo-3-metil-2-oxo-2,3-di-hidro-imidazo[4,5-c]quinolin-1-il)- fenil]-2-metil-propionitrila (Exemplo 1i), com o ácido borônico apropriado:
[000152] Exemplo 2: ácido 3-piridinaborônico (Aldrich, Buchs, Suíça),
[000153] Exemplo 3: ácido 4-metóxi-3-piridilborônico (Frontier Scientific, Logan, E.U.A.),
[000154] Exemplo 4: éster de pinecol de ácido 3-metoxipiridina-5- borônico (Frontier Scientific, Logan, E.U.A.)
[000155] Exemplo 5: Éster de terc-butila de ácido 4-[5-(4,4,5,5- tetrametil-[1,3,2]dioxaborolan-2-il)-piridin-2-il]-piperazina-1 - carboxílico (CB Research & Development, New castle, E.U.A.)
[000156] Exemplo 6: 1-Metil-4-[4-(4,4,5,5-tetrametil- [1,3,2]dioxaborolan-2-il)-piridin-2-il]-piperazina (Oakwood Products, West Columbia, E.U.A.),
[000157] Exemplo 7: ácido 3-quinolinaborônico (Aldrich, Buchs, Suíça),
[000158] Exemplo 8: ácido 2-fluoroquinolina-3-borônico (Lancaster, Morecambe, REINO UNIDO),
[000159] Exemplo 9: ácido 6-quinolinaborônico (Asychem, Durham, E.U.A.),
[000160] Exemplo 10: ácido 5-quinolinaborônico (Asychem, Durham, E.U.A.), e
[000161] Exemplo 11: cloridrato de ácido 6-benzopirazinaborônico (Asychem, Durham, E.U.A.) Tabela 1
[000162] Os compostos seguintes (Tabela 2) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-(4-amino-fenil)-2- etil-butironitrila (Exemplo 12a), e com o ácido borônico apropriado: Tabela 2
[000163] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 1e empregando iodoetano (Fluka, Buchs, Suíça) no Exemplo 1d. Composto do título: ES-MS: 189 (M + H)+, padrão Br; HPLC analítica: tret= 2,50 minutos (Grad 1).
[000164] Os compostos seguintes (Tabela 3) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 1-(4-amino-2-flúor- fenil)-pirrolidin-2-ona (Exemplo 14a), e com o ácido borônico apropriado: Tabela 3
[000165] 650 mg (2,9 mmols) de 1-(2-flúor-4-nitro-fenil)-pirrolidin-2- ona (Exemplo 14b) e 65 mg de Pd/C a 10% são agitados em 15 ml de MeOH/THF (1:1) sob 1,1 bar de H2 durante 2 horas à temperatura ambiente. Após a conclusão da reação, o catalisador é filtrado e o filtrado é evaporado a vácuo para produzir o composto do título como um sólido esbranquiçado. ES-MS: 195 (M+H)+; HPLC analítica: tret = 1,91 minuto (Grad 1).
Exemplo 14b
1-(2-Flúor-4-nitro-fenil)-pirrolidin-2-ona
[000166] A 468 mg (5,5 mmols) de 2-pirrolidona (Fluka, Buchs, Suíça) em 10 ml de DMF a 0°C são adicionados 240 mg (5,5 mmols) de 55% de NaH em óleo. A mistura de reação é agitada durante 30 minutos a 0°C e durante 30 minutos à temperatura ambiente . Depois deste tempo, 795 mg (5 mmols) de 3,4-difluoronitrobenzeno (Aldrich, Buchs, Suíça) são adicionados e a mistura de reação é agitada durante 1 hora à temperatura ambiente . A mistura de reação é extinguida com HCI aquoso a 1 M e extraída com EtOAc (2x). As camadas orgânicas são lavadas com NaHCOs aquoso saturado e com salmoura (3x), secas sobre MgSO4, filtradas e evaporadas. O resíduo é purificado através de cromatografia instantânea em sílica-gel (hexano-EtOAc 5:1 a 1:3) para produzir o composto do título como um sólido. ES-MS: 225 (M+H)+; HPLC analítica: tret= 2,99 minutos (Grad 1).
[000167] Os compostos seguintes (Tabela 4) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 1-(4-amino-fenil)- pirrolidin-2-ona (Exemplo 16a), e com o ácido borônico apropriado: Tabela 4
[000168] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 14a iniciando com 1-(4-nitro-fenil)-pirrolidin- 2-ona (Acros, Basel, Suíça). Composto do título: ES-MS: 177 (M+H)+; HPLC analítica: tret= 2,71 minutos (Grad 1).
[000169] Os compostos seguintes (Tabela 5) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-flúor-N1,N1-bis-(2- metóxi-etil)-benzeno-1,4-diamina (Exemplo 18a), e com o ácido borônico apropriado: Tabela 5
[000170] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 14a iniciando com (2-flúor-4-nitro-fenil)-bis- (2-metóxi-etil)-amina (Exemplo 18b). Composto do título: ES-MS: 243 (M+H)+; HPLC analítica: tret= 1,98 minuto (Grad 1).
Exemplo 18b
(2-Flúor-4-nitro-fenil)-bis-(2-metóxi-etil)-amina
[000171] 1,13 g (7,1 mmols) de 3,4-difluoronitrobenzeno (Aldrich, Buchs, Suíça), 1,04 g (7,81 mmols) de bis(2-metoxietil)amina (Fluka, Buchs, Suíça) e 1,96 g (14,2 mmols) de K2CO3 em 7 ml de DMSO são agitados durante 1,5 hora à temperatura ambiente e em seguida aquecidos a 80°C durante 4 horas. A mistura de reação é extinguida com H2O e extraída com EtOAc (2x). As camadas orgânicas são lavadas com salmoura (3x), seca sobre MgSÜ4, filtrada e evaporada. O resíduo é purificado através de cromatografia instantânea em sílica-gel (hexano-EtOAc 6:1 a 5:1) para produzir 0 composto do título como um óleo amarelo. ES-MS: 273 (M+H)+.
[000172] Os compostos seguintes (Tabela 6) são preparados de uma maneira similar tal como descrito no Exemplo 1 bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com etil)-benzeno-1,4-diamina (Exemplo 20a), e com apropriado: Tabela 6
[000173] O composto do título é obtido de uma maneira similar como no Exemplo 18b iniciando com 4-fluoronitrobenzeno (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 225 (M+H)+; HPLC analítica: tret = 1,94 minuto (Grad 1).
[000174] Os compostos seguintes (Tabela 7) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-naftilamina (Aldrich, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 7
[000175] Os compostos seguintes (Tabela 8) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-cloroanilina (Fluka, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 8
[000176] Os compostos seguintes (Tabela 9) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-toluldina (Fluka, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 9
[000177] Os compostos seguintes (Tabela 10) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-etilanilina (Aldrich, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 10
[000178] Os compostos seguintes (Tabela 11) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-trifluorometilanilina (Fluka, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 11
[000179] Os compostos seguintes (Tabela 12) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 4-flúor-2-metilanilina (Aldrich, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 12
[000180] Os compostos seguintes (Tabela 13) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6-bromo- 4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-cloro-4-fluoroanilina (Aldrich, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 13
[000181] Os compostos seguintes (Tabela 14) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 3-cloroanilina (Fluka, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 14
[000182] Os compostos seguintes (Tabela 15) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 3-trifluorometilanilina (Fluka, Buchs, Suíça), e com o ácido borônico apropriado: Tabela 15
[000183] Os compostos seguintes (Tabela 16) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6- bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 4-metoximetilanilina (Exemplo 38a), e com o ácido borônico apropriado: Tabela 16
[000184] O composto do título é conhecido na literatura (descrita em Journal of Chemical Society. Perkin Trans I, 2001, p. 955). Composto do título: ES-MS: 138 (M + H)+; HPLC analítica: tret= 1,76 minutos (Grad 1).
[000185] Os compostos seguintes (Tabela 17) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6-bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 2-cloro-4-(2- metóxi-etil)-fenilamina (Exemplo 42a), e com o ácido borônico apropriado: Tabela 17
[000186] 2 g de (13,2 mmols) de 4-(2-metóxi-etil)-fenilamina (Exemplo 42b) e 1,85 g (13,9 mmols) de N-clorossuccinimida (Aldrich, Buchs, Suíça) em 26 ml de isopropanol são agitados à temperatura ambiente durante 30 minutos. A mistura de reação é evaporada até a secura e o resíduo é levado em EtOAc. As camadas orgânicas são lavadas com NaHCOs aquoso saturado (2x), secas sobre MgSO4, filtradas e evaporadas. O resíduo é purificado através de cromatografia instantânea em sílica-gel (hexano-EtOAc 5:1 a 2:1) para produzir o composto do título como um óleo. ES-MS: 186 (M + H)+; HPLC analítica: tret = 2,42 minutos (Grad 1).
Exemplo 42b
4-(2-Metóxi-etil)-fenilamina
[000187] O composto do título é conhecido na literatura (descrita em Synthetic communications, 1985, 15, p. 1131). Composto do título: ES-MS: 152 (M + H)+; HPLC analítica: tret = 1,84 minutos (Grad 1).
[000188] Os compostos seguintes (Tabela 18) são preparados de uma maneira similar tal como descrito no Exemplo 1 por reação de 6-bromo-4-cloro-3-nitro-quinolina (Exemplo 1c) com 4-(2-metóxi- etil)-fenilamina (Exemplo 42b), e com o ácido borônico apropriado: Tabela 18
[000189] Os compostos seguintes (Tabela 19) são preparados de uma maneira similar tal como descrito no Exemplo 1 empregando 2- [4-(8-bromo-3-metil-2-oxo-5-óxi-2,3-di-hidro-imidazo[4,5-c]quinolin- 1 -il)-fenil]-2-metil-propionitrila (Exemplo 46a) com o ácido borônico apropriado: Tabela 19
[000190] 880 mg (2,09 mmols) de 2-[4-(8-bromo-3-metil-2-oxo- 2,3-di-hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila (Exemplo 1i) e 696 mg (2,3 mmols) de ácido m-cloroperbenzoico (Aldrich, Buchs, Suíça) em 40 ml de CH2CI2 são agitados à temperatura ambiente durante 2 horas. A mistura de reação é extinguida com Na2COs aquoso a 10% e extraída com CH2CI2 (2x). As camadas orgânicas são lavadas com Na2COs aquoso a 10% e com salmoura, secas sobre Na2SO4, filtradas e evaporadas. O resíduo é triturado em EtOAc quente, em seguida resfriado a -18°C e filtrado para produzir 0 composto do título como um sólido amarelo. ES-MS: 437, 439 (M + H)+, padrão Br; HPLC analítica: tret = 3,45 minutos (Grad 1).
[000191] Os compostos seguintes (Tabela 20) são preparados de uma maneira similar tal como descrito no Exemplo 1 empregando 6-bromo-4-cloro-7-flúor-3-nitro-quinolina (Exemplo 48a), e 0 ácido borônico requerido: Tabela 20
[000192] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 1c iniciando de ácido 2-amino-5-bromo- 4-flúor-benzoico (ES-MS: 232, 234 M-H, padrão Br; síntese descrita em Macromolecules, 1997, 30, p. 1964). Composto do título: HPLC analítica: tret= 4,07 minutos (Grad 1).
Exemplo 50
N-Metil-N-r4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro-imidazor4,5- c]quinolin-1-il)-feniH-metanossulfonamida
[000193] 62 mg (0,128 mmol) de éster de terc-butila de ácido metil- [4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro-imidazo[4,5-c]quinolin-1-il)- fenil]-carbâmico (Exemplo 50a) são tratados com 2,5 ml de HCI a 1 M em dioxano à temperatura ambiente durante 1 hora, e em seguida a solução é evaporada até a secura. O resíduo é produzido em 2 ml de CH2CI2 junto com 414 pl (5,13 mmols) de piridina e 66 mg (0,579 mmol) de mesilcloreto (Fluka, Buchs, Suíça). A solução é agitada à temperatura ambiente durante 17,5 horas, e em seguida 15 mg (0,129 mmol) de mesilcloreto são adicionados e a mistura de reação é agitada à temperatura ambiente durante 5,5 horas. A reação é extinguida com NaHCOs aquoso saturado e extraída com CH2CI2 (2x). As camadas orgânicas são lavadas com salmoura, secas sobre Na2SO4, filtradas e evaporadas. O resido é purificado através de HPLC preparativa para produzir o composto do título como um sólido amarelado. ES-MS: 460 (M + H)+; HPLC analítica: tret= 2,25 minutos (Grad 1).
Exemplo 50a
Éster de terc-butila de ácido metil-[4-(3-metil-2-oxo-8-piridin-3-il- 2,3-di-hidro-imidazo[4,5-c]quinolin-1-il)-fenil]-carbâmico
[000194] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 1 por reação de 6-bromo-4-cloro-3-nitro- quinolina (Exemplo 1c) com éster de terc-butila de ácido (4-amino- fenil)-carbâmico (Fluka, Buchs, Suíça) e empregando ácido 3- pirinaborônico (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 482 (M + H)+; HPLC analítica: tret= 2,77 minutos (Grad 1).
Exemplo 51
Éster de terc-butila de ácido metil-[4-(3-metil-2-oxo-8-piridin-3-il-2,3- di-hidro-imidazo[4,5-c]quinolin-1-il)-fenil]-carbâmico
[000195] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 50 empregando ácido 3-quinolinaborônico (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 510 (M + H)+; HPLC analítica: tret= 2,65 minutos (Grad 1).
[000196] Os compostos seguintes (Tabela 21) são preparados de uma maneira similar tal como descrito no Exemplo 50 empregando cloreto de etanossulfonila (Fluka, Buchs, Suíça) e com o ácido borônico apropriado. Tabela 21
[000197] Os compostos seguintes (Tabela 22) são preparados de uma maneira similar tal como descrito no Exemplo 50 empregando éster de terc-butila de ácido etil-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di- hidro-imidazo[4,5-c]quinolin-1-il)-fenil]-carbâmico (ES-MS: 496 (M + H)+; HPLC analítica: tret= 2,88 minutos (Grad 1)) ou éster de terc-butila de ácido etil-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1-il)-fenil]-carbâmico (ES-MS: 546 (M + H)+; HPLC analítica: tret= 3,29 minutos (Grad 1)), respectivamente. Tabela 22
[000198] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 1 por reação de 2-[4-(8-bromo-2-oxo-2,3- di-hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila (Exemplo 1h) com iodoetano (Fluka, Buchs, Suíça) e empregando ácido 3- piridinaborônico. ES-MS: 434 (M + H)+; HPLC analítica: tret = 2,55 minutos (Grad 1).
Exemplo 57
1-[3-Flúor-4-(4-metanossulfonil-piperazin-1-il)-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000199] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 1 empregando 3-flúor-4-(4- metanossulfonil-piperazin-1 -il)-fenilamina (Exemplo 57a) e ácido 3- quinolinaborônico. Composto do título: ES-MS: 583,5 (M+H)+; HPLC analítica: tret= 4,12 minutos (Grad 2).
Exemplo 57a
3-Flúor-4-(4-metanossulfonil-piperazin-1-il)-fenilamina
[000200] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 14a empregando 1-(2-flúor-4- nitro-fenil)-4-metanossulfonil-piperazina (Exemplo 57b). Composto do título: ES-MS: 274,3 (M+H)+; HPLC analítica: tret = 3,50 minutos (Grad 2).
Exemplo 57b
1-(2-Flúor-4-nitro-fenil)-4-metanossulfonil-piperazina
[000201] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 18b empregando 1- metanossulfonil-piperazina (ChemBridge Corporation, San Diego, E.U.A.). Composto do título: ES-MS: 304,3 (M+H)+; HPLC analítica: tret = 4,94 minutos (Grad 2).
Exemplo 58
1-[3-Flúor-4-(4-metanossulfonil-piperazin-1-il)-fenil]-3-metil-8- pi rid i n-3-i 1-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000202] O composto do título é preparado de uma maneira similar tal como descrito no Exemplo 57 empregando 3- piridinaborônico. Composto do título: ES-MS: 533,4 (M+H)+; HPLC analítica: tret= 3,75 minutos (Grad 2).
Exemplo 59
1 -(3-Flúor-4-piperazin-1 -i l-fen 11 )-3-meti I -8-q u i nol i n -3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000203] O composto do título é preparado de uma maneira similar descrita no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-flúor-fenil)-piperazina-1 -carboxílico (Exemplo 59a) e ácido 3-quinolinaborônico. A remoção do grupo de proteção de terc- butoxicarbonila é realizada empregando-se HCI a 4 N em dioxano seguindo protocolos conhecidos na técnica (The peptides, Vol. 3; ed. Edhard Gross e Johannes Meienhofer, Academic Press, Nova Iorque). Composto do título: ES-MS: 505,4 (M+H)+; HPLC analítica: tret = 3,63 minutos (Grad 2).
Exemplo 59a
éster de terc-butila de ácido 4-(4-amino-2-flúor-fenil)-piperazina-1- carboxílico
[000204] O composto do título é obtido tal como descrito no Exemplo 14a empregando éster de terc-butila de ácido 4-(2-flúor-4- nitro-fenil)-piperazina-1-carboxílico (Exemplo 59b). Composto do título: ES-MS: 296,3 (M+H)+; HPLC analítica: tret= 4,18 minutos (Grad 2).
Exemplo 59b
éster de terc-butila de ácido 4-(2-flúor-4-nitro-fenil)-piperazina-1- carboxílico
[000205] O composto do título é obtido tal como descrito no Exemplo 18b empregando éster de terc-butila de ácido piperazina-1- carboxílico (Aldrich, Buchs, Suíça) e conduzindo a reação à temperatura ambiente . Composto do título: ES-MS: 326,3 (M+H)+; HPLC analítica: tret= 5,84 minutos (Grad 2).
Exemplo 60
1 -(3-Flúor-4-piperazin-1 -i l-fen i l)-3-meti I -8-pi rid I n-3-i 1-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000206] O composto do título é preparado tal como descrito no Exemplo 59 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 455,4 (M+H)+; HPLC analítica: tret= 3,39 minutos (Grad 2).
Exemplo 61
3-metil-1 -[4-(4-metil-piperazin-1 -I l)-fen 11] -8-q u I nol I n -3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000207] O composto do título é preparado tal como descrito no Exemplo 1 empregando 4-(4-metil-piperazin-1-il)-fenilamina (Acros, Morris Plains, Nova Jersey, E.U.A.) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 501,5 (M+H)+; HPLC analítica: tret = 3,78 minutos (Grad 2).
Exemplo 62
3-metil-1 -[4-(4-metil-piperazin-1 -i l)-fen i l]-8-pi rid i n -3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000208] O composto do título é obtido tal como descrito no Exemplo 61 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 451,3 (M+H)+; HPLC analítica: tret= 3,49 minutos (Grad 2).
Exemplo 63
1 -[2-Cloro-4-(4-metil-piperazin-1 -I l)-fen i l]-3-m eti l-8-q u i nol i n-3-i 1-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000209] O composto do título é obtido tal como descrito no Exemplo 1 empregando (6-bromo-3-nitro-quinolin-4-il)-[2-cloro-4-(4- metil-piperazin-1-il)-fenil]-amina (Exemplo 63a) e ácido 3- quinolinaborônico. Composto do título: ES-MS: 535,4 (M+H)+; HPLC analítica: tret= 3,93 minutos (Grad 2).
Exemplo 63a
(6-Bromo-3-nitro-quinolin-4-il)-[2-cloro-4-(4-metil-piperazin-1-il)- fenil]-amina
[000210] 5 ml de N-metilpiperazina são adicionados a uma solução de 600 mg (1,5 mmol) de (6-bromo-3-nitro-quinolin-4-il)-(2- cloro-4-flúor-fenil)-amina (Exemplo 63b) em 2 ml de DMSO. A reação é aquecida a 180 °C durante 1 hora em um forno de micro-onda (Emrys Optimizer, Personal Chemistry). Depois deste tempo, a solução é concentrada até a secura e o composto bruto é purificado através de MPLC preparativa. Composto do título: ES-MS: 476,3, 478,3, 480,3 (M+H)+; HPLC analítica: tret= 4,28 minutos (Grad 2).
Exemplo 63b
(6-Bromo-3-nitro-quinolin-4-il)-(2-cloro-4-flúor-fenil)-amina
[000211] O composto do título é obtido tal como descrito no Exemplo 1f empregando 2-cloro-4-flúor-fenilamina (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 396,1, 398,1, 400,1 (M+H)+; HPLC analítica: tret= 5,69 minutos (Grad 2).
Exemplo 64
1 -[2-Cloro-4-(4-metil-piperazin-1 -I l)-fen 11] -3-meti I -8-pi rid i n-3-i 1-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000212] O composto do título é obtido tal como descrito no Exemplo 63 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 485,3 (M+H)+; HPLC analítica: tret= 3,58 minutos (Grad 2).
Exemplo 65
1 -[3-Cloro-4-(4-metil-piperazin-1 -i l)-fen 11] -3-meti I -8-q u I nol I n -3-i I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000213] O composto do título é obtido tal como descrito no Exemplo 1 empregando 3-cloro-4-(4-metil-piperazin-1-il)-fenilamina (Exemplo 65a) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 536,4 (M+H)+; HPLC analítica: tret= 3,78 minutos (Grad 2).
Exemplo 65a
3-Cloro-4-(4-metil-piperazin-1-il)-fenilamina
[000214] 298 mg (0,92 mmol) de éster de terc-butila de ácido [3- cloro-4-(4-metil-piperazin-1-il)-fenil]-carbámico (Exemplo 65b) são dissolvidos em 5 ml de HCI a 4 N em dioxano. A solução é agitada durante 4 horas a 50 °C, e depois deste tempo água é adicionada e o pH é ajustado para 8 com NaHCOs. A suspensão é extraída com n- butanol. A fase orgânica é lavada com água, seca sobre MgSÜ4 e evaporada até a secura para fornecer o composto do título. Composto do título: ES-MS: 226,2 (M+H)+; HPLC analítica: tret = 3,09 minutos (Grad 2).
Exemplo 65b
éster de terc-butila de ácido [3-cloro-4-(4-metil-piperazin-1-il)- fenil]-carbâmico
[000215] 583 mg (2 mmols) de éster de terc-butila de ácido [4-(4- metil-piperazin-1-il)-fenil]-carbâmico (Exemplo 65c) são dissolvidos em 10 ml de isopropanol e 286 mg (2,1 mmols) de N-clorossuccinimida são adicionados. A solução é agitada durante 1 hora à temperatura ambiente e 100 ml de água são adicionados. A suspensão é extraída com EtOAc e a fase orgânica é lavada com água, seca sobre MgSCU e evaporada até a secura. O resíduo é purificado por MPLC para fornecer o composto do título. Composto do título: ES-MS: 326,3 (M+H)+; HPLC analítica: tret= 4,43 minutos (Grad 2).
Exemplo 65c
Éster de terc-butila de ácido [4-(4-metil-piperazin-1-il)-fenil]- carbâmico
[000216] 478 mg (2,5 mmols) de 4-(4-metilpiperazino)anilina (Acros, Nova Jersey, E.U.A.) são dissolvidos em 10 ml de THF e 0,67 ml (3 mmols) de BOC2O e 0,49 ml (3,5 ml) de trietilamina são adicionados. Depois de agitar durante 16 horas à temperatura ambiente, a solução é evaporada até a secura e 0 resíduo é dissolvido em 100 ml de EtOAc. A suspensão é lavada com água, seca sobre MgSO4 e evaporada até a secura para fornecer 0 composto do título. Composto do título: ES- MS: 292,2 (M+H)+; HPLC analítica: tret = 4,15 minutos (Grad 2).
Exemplo 66
1 -[3-Cloro-4-(4-metil-piperazin-1 -i l)-fen i I] -3-meti I -8-pi rid i n-3-i 1-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000217] O composto do título é obtido tal como descrito no Exemplo 65 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 485,4 (M+H)+; HPLC analítica: tret= 3,53 minutos (Grad 2).
Exemplo 67
1 -(4-lmidazol-1 -i l-2-m eti l-fen i l)-3-meti I -8-q u i nol i n -3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000218] O composto do título é obtido tal como descrito no Exemplo 1 empregando 4-imidazol-1-il-2-metil-fenilamina (Exemplo 68a) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 483,4 (M+H)+; HPLC analítica: tret= 3,78 minutos (Grad 2).
Exemplo 67a
4-lmidazol-1-il-2-metil-fenilamina
[000219] O composto do título é obtido tal como descrito no Exemplo 18a/b empregando 5-flúor-2-nitrotolueno (Aldrich, Buchs, Suíça) e 1H- pirazol (Fluka, Buchs, Suíça). Composto do título: ES-MS: 174,2 (M+H)+; HPLC analítica: tret= 3,20 minutos (Grad 2).
Exemplo 68
1 -(4-lmidazol-1 -i l-2-m eti l-fen i l)-3-meti I -8-pi rid i n-3-i 1-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000220] O composto do título é obtido tal como descrito no Exemplo 67 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 433,3 (M+H)+; HPLC analítica: tret= 3,46 minutos (Grad 2).
Exemplo 69
3-metil-1 -(4-pirazol-1 -I l-fen I l)-8-q u I nol I n -3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000221] O composto do título é obtido tal como descrito no Exemplo 1 empregando 4-pirazol-1-il-fenilamina (Exemplo 69a) e ácido 3- quinolinaborônico. Composto do título: ES-MS: 469,4 (M+H)+; HPLC analítica: tret = 4,18 minutos (Grad 2).
Exemplo 69a
4-Pirazol-1-il-fenilamina
[000222] O composto do título é obtido tal como descrito no Exemplo 18a/b empregando 1-flúor-4-nitro-benzeno (Fluka, Buchs, Suíça) e 1H- pirazol (Fluka, Buchs, Suíça). Composto do título: ES-MS: 160,2 (M+H)+; HPLC analítica: tret = 3,61 minutos (Grad 2).
Exemplo 70
3-Metil-1-(4-pirazol-1-il-fenil)-8-piridin-3-il-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona
[000223] O composto do título é obtido tal como descrito no Exemplo 69 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 419,3 (M+H)+; HPLC analítica: tret = 3,80 minutos (Grad 2).
Exemplo 71
3-Meti l-8-q u i nol i n -3-i I-1 -(4-[1,2,4]triazol-1 -I l-fen i l)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000224] O composto do título é obtido tal como descrito no Exemplo 1 empregando 4-[1,2,4]triazol-1 -il-fenilamina (Exemplo 71a) e ácido 3- quinolinaborônico. Composto do título: ES-MS: 470,3 (M+H)+; HPLC analítica: tret= 3,99 minutos (Grad 2).
Exemplo 71a
4-[1,2,4]Ttriazol-1 -il-fenilamina
[000225] O composto do título é obtido tal como descrito no Exemplo 18a/b empregando 1-flúor-4-nitro-benzeno (Fluka, Buchs, Suíça) e 1,2,4-triazol (Fluka, Buchs, Suíça). Composto do título: ES-MS: 161,2 (M+H)+; HPLC analítica: tret= 3,29 minutos (Grad 2).
Exemplo 72
3-Meti l-8-pi rid i n -3-i I-1 -(4-[1,2,4]triazol-1 -i l-fen i I )-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000226] O composto do título é obtido tal como descrito no Exemplo 71 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 420,3 (M+H)+; HPLC analítica: tret= 3,68 minutos (Grad 2).
Exemplo 73
3-Metil-1-[4-(4-metil-piperazin-1-il)-3-trifluorometil-fenil]-8-quinolin- 3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000227] O composto do título é obtido tal como descrito no Exemplo 1 empregando 4-(4-metil-piperazin-1 -il)-3-trifluorometil-fenilamina (Exemplo 73a) e ácido 3-quinolinaborônico. Composto do título: ES- MS: 569,5 (M+H)+; HPLC analítica: tret = 4,08 minutos (Grad 2).
Exemplo 73a
4-(4-metil-piperazin-1-il)-3-trifluorometil-fenilamina
[000228] O composto do título é obtido tal como descrito no Exemplo 18a/b empregando 2-flúor-5-nitrobenzotrifluoreto (Aldrich, Buchs, Suíça) e N-metilpirezarina. Composto do título: ES-MS: 260,2 (M+H)+; HPLC analítica: tret= 3,59 minutos (Grad 2).
Exemplo 74
3-Metil-1-[4-(4-metil-piperazin-1-il)-3-trifluorometil-fenil]-8-piridin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000229] O composto do título é obtido tal como descrito no Exemplo 73 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 519,4 (M+H)+; HPLC analítica: tret= 3,78 minutos (Grad 2).
Exemplo 75
1 -(3-Cloro-4-piperazin-1 -i l-fen I l)-3-meti I -8-q u i nol i n -3-i I-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000230] O composto do título é obtido tal como descrito no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-cloro-fenil)- piperazina-1-carboxílico (Exemplo 75a) e ácido 3-quinolinaborônico e a remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 521,4 (M+H)+; HPLC analítica: tret= 3,68 minutos (Grad 2).
Exemplo 75a
Éster de terc-butila de ácido 4-(4-amino-2-cloro-fenil)-piperazina-1- carboxílico
[000231] O composto do título é obtido tal como descrito no Exemplo 1e empregando éster de terc-butila de ácido 2-cloro-4-(4-nitro-fenil)- piperazina-1-carboxílico (Exemplo 75b) como material de partida. Composto do título: ES-MS: 312,2, 314,3 (M+H)+; HPLC analítica: tret = 4,58 minutos (Grad 2).
Exemplo 75b
Éster de terc-butila de ácido 2-cloro-4-(4-nitro-fenil)-piperazina-1- carboxílico
[000232] A uma solução de 1,25 g (4 mmols) de éster de terc-butila de ácido 4-(4-nitro-fenil)-piperazina-1-carboxílico (Exemplo 75c) em 10 ml de isopropanol são adicionados 0,72 g (4,2 mmols) de N- clorossuccinimida. A solução é agitada durante 6 horas a 50° C. Depois deste tempo, a solução é evaporada até a secura e o resíduo é dissolvido em 100 ml de EtOAc. A solução é extraída com água, seca sobre MgSÜ4 e evaporada até a secura para fornecer o composto do título: ES-MS: 342,2, 344,2 (M+H)+; HPLC analítica: tret = 5,70 minutos (Grad 2).
Exemplo 75c
Éster de terc-butila de ácido 4-(4-nitro-fenil)-piperazina-1- carboxílico
[000233] A uma solução de 0,45 ml (4 mmols) de 4-fluoronitrobenzo (Aldrich, Buchs, Suíça) em 10 ml de DMSO são adicionados 1,12 g (6 mmols) de éster de terc-butila de ácido piperazina-1-carboxílico (Aldrich, Buchs, Suíça) e 1,1 g (8 mmols) de K2CO3. A suspensão é agitada durante 1 hora a 100 °C. Depois deste tempo, 100 ml de AcOEt são adicionados e a suspensão é extraída com água. A solução orgânica é seca sobre MgSO4 e evaporada até a secura para fornecer 0 composto do título: ES-MS: 307,3 (M+H)+; HPLC analítica: tret = 5,72 minutos (Grad 2).
Exemplo 76
1 -(3-Cloro-4-piperazin-1 -i l-fen i l)-3-meti I -8-pi rid i n-3-i 1-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000234] O composto do título é obtido tal como descrito no Exemplo 75 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 471,3 (M+H)+; HPLC analítica: tret= 3,42 minutos (Grad 2).
Exemplo 77
1 -(3-Cloro-4-piperazin-1 -i l-fen i l)-8-(6-m etóxi-pi rid i n -3-i l)-3-meti I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000235] O composto do título é obtido tal como descrito no Exemplo 75 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 501,4 (M+H)+; HPLC analítica: tret= 3,76 minutos (Grad 2).
Exemplo 78
1 -(3-Cloro-4-piperazin-1 -I l-fen i l)-8-(5-metóxi-pi rid i n-3-i l)-3-m eti 1-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000236] O composto do título é obtido tal como descrito no Exemplo 75 empregando 3-Metóxi-5-(4,4,5,5-tetrametil-[1,3,2]dioxaborolan-2-il)- piridina (Frontier Scientific, Logan, E.U.A.). Composto do título: ES-MS: 501,4 (M+H)+; HPLC analítica: tret= 3,55 minutos (Grad 2).
Exemplo 79
8-(6-Metóxi-piridin-3-il)-3-metil-1-[4-(4-metil-piperazin-1-il)-3- trifluorometil-fenil]-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000237] O composto do título é obtido tal como descrito no Exemplo 73 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 549,2 (M+H)+; HPLC analítica: tret= 3,89 minutos (Grad 2).
Exemplo 80
8-(5-Metóxi-piridin-3-il)-3-metil-1-[4-(4-metil-piperazin-1-il)-3- trifluorometil-fenil]-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000238] O composto do título é obtido tal como descrito no Exemplo 73 empregando ácido 3-metóxi-5-piridinaborônico. Composto do título: ES-MS: 549,2 (M+H)+; HPLC analítica: tret= 3,67 minutos (Grad 2).
Exemplo 81
1-[2-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(6-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000239] O composto do título é obtido tal como descrito no Exemplo 63 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 515,4 (M+H)+; HPLC analítica: tret= 3,73 minutos (Grad 2).
Exemplo 82
1-[2-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(5-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000240] O composto do título é obtido tal como descrito no Exemplo 63 empregando 3-Metóxi-5-(4,4,5,5-tetrametil-[1,3,2]dioxaborolan-2-il)- piridina. Composto do título: ES-MS: 515,4 (M+H)+; HPLC analítica: tret = 3,58 minutos (Grad 2).
Exemplo 83
1 -(3-Cloro-4-piperazin-1 -il-fenil)-3-metil-8-quinoxalin-6-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000241] O composto do título é obtido tal como descrito no Exemplo 75 empregando HCI de ácido benzopirazina-5-borônico (Asymchem, Durham, NC, E.U.A.). Composto do título: ES-MS: 522,4 (M+H)+; HPLC analítica: tret= 3,70 minutos (Grad 2).
Exemplo 84
3-Meti 1-1 -(4-piperazin-1 -I l-3-trif I uorometi I -fen I l)-8-q u i nol i n-3-i 1-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000242] O composto do título é obtido tal como descrito no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-trifluorometil- fenil)-piperazina-1-carboxílico (Exemplo 84a). Composto do título: ES- MS: 555,0 (M+H)+; HPLC analítica: tret= 3,86 minutos (Grad 2).
Exemplo 84a
éster de terc-butila de ácido 4-(4-amino-2-trifluorometil-fenil)- piperazina-1 -carboxílico
[000243] O composto do título é obtido tal como descrito no Exemplo 1e empregando éster de terc-butila de ácido 4-(4-nitro-2-trifluorometil- fenil)-piperazina-1-carboxílico (Exemplo 84b) como material de partida. Composto do título: ES-MS: 346,2 (M+H)+; HPLC analítica: tret = 4,95 minutos (Grad 2).
Exemplo 84b
Éster de terc-butila de ácido 4-(4-nitro-2-trifluorometil-fenil)- piperazina-1 -carboxílico
[000244] O composto do título é obtido tal como descrito no Exemplo 75c empregando 1-flúor-4-nitro-2-trifluorometil-benzeno como material de partida. Composto do título: ES-MS: 375,3 (M-H) -.
Exemplo 85
3-Meti 1-1 -(4-piperazin-1 -i l-3-trif I uorometi I -fen i l)-8-pi rid i n -3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000245] O composto do título é obtido tal como descrito no Exemplo 84 empregando ácido 3-piridinaborônico. Composto do título: ES-MS: 505,4 (M+H)+; HPLC analítica: tret= 3,61 minutos (Grad 2).
Exemplo 86
8-(6-Metóxi-piridin-3-il)-3-metil-1-(4-piperazin-1-il-3-trifluorometil- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000246] O composto do título é obtido tal como descrito no Exemplo 84 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 535,4 (M+H)+; HPLC analítica: tret= 3,93 minutos (Grad 2).
Exemplo 87
8-(5-Metóxi-piridin-3-il)-3-metil-1-(4-piperazin-1-il-3-trifluorometil- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000247] O composto do título é obtido tal como descrito no Exemplo 84 empregando 3-metóxi-5-(4,4,5,5-tetrametil-[1,3,2]dioxaborolan-2-il)- piridina. Composto do título: ES-MS: 535,4 (M+H)+; HPLC analítica: Let = 3,71 minutos (Grad 2).
Exemplo 88
3-Metil-1-(4-piperazin-1-il-3-trifluorometil-fenil)-8-quinoxalin-6-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000248] O composto do título é obtido tal como descrito no Exemplo 84 empregando HCI de ácido benzopirazina-5-borônico. Composto do título: ES-MS: 556,0 (M+H)+; HPLC analítica: tret = 3,92 minutos (Grad 2).
Exemplo 89
1-[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1-il)-fenil]-3-metil-8-piridin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000249] O composto do título é obtido tal como descrito no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-cloro-fenil)- 2,6-cis-dimetil-piperazina-1-carboxílico (Exemplo 89a) e ácido 3- piridinaborônico e a remoção do grupo de proteção de terc- butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 499 (M+H)+; HPLC analítica: tret= 2,24 minutos (Grad 1).
Exemplo 89a
Éster de terc-butila de ácido 4-(4-amino-2-cloro-fenil)-2,6-cis- dimetil-piperazina-1 -carboxílico
[000250] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1e iniciando com éster de terc-butila de ácido 4-(2-cloro-4-nitro-fenil)-2,6-cis-dimetil-piperazina-1-carboxílico (Exemplo 89b). Composto do título: ES-MS: 340 (M+H)+; HPLC analítica: tret= 3,35 minutos (Grad 1).
Exemplo 89b
Éster de terc-butila de ácido 4-(2-cloro-4-nitro-fenil)-2,6-cis- dimetil-piperazina-1 -carboxílico
[000251] 983 mg (3,64 mmols) de 1-(2-cloro-4-nitro-fenil)-3,5-c/s- dimetil-piperazina (Exemplo 89c), 1,59 g (7,29 mmols) Boc-anidrido (Fluka, Buchs, Suíça) em 5 ml de THF e 5,47 ml (5,47 mmols) K2CO3 aquoso a 1 M são agitados à temperatura ambiente durante 72 horas. A mistura de reação é extinguida com salmoura e extraída com CH2CI2 (2x). As camadas orgânicas combinadas são lavadas com HCI aquoso a 1 M, com salmoura, secas sobre MgSCX filtradas e evaporadas. O resíduo é purificado através de cromatografia instantânea (CH2CI2- MeOH 1:0 a 39:1) para produzir 0 composto do título como um sólido rosado. ES-MS: 370 (M+H)+; HPLC analítica: tret = 4,73 minutos (Grad 1).
Exemplo 89c
1-(2-Cloro-4-nitro-fenil)-3,5-c/s-dimetil-piperazina
[000252] 1,0 g (5,21 mmols) de 3,4-dicloronitrobenzeno (Fluka, Buchs, Suíça), 624 mg (5,47 mmols) de c/s-2,6-dimetilpiperazina (Aldrich, Buchs, Suíça) e 580 mg (5,73 mmols) de trietilamina em 20 ml de EtOH são aquecidos em um forno de micro-onda a 170°C durante 6 horas e 180°C durante 2 horas. A mistura de reação é evaporada até a secura e em seguida levada em EtOAc. As camadas orgânicas são com HCI(5x) aquoso a 1 M e as camadas aquosas combinadas são basificadas com NaHCOs e extraídas com CH2CI2 (3*), lavadas com salmoura, secas sobre MgSO4, filtradas e evaporadas até a secura para produzir 0 composto do título como um sólido amarelo. ES-MS: 270 (M+H)+; HPLC analítica: tret = 2,72 minutos (Grad 1).
Exemplo 90
1-[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1-il)-fenil]-3-metil-8-quinolin- 3-11-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000253] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 89 empregando ácido 3-quinolinaborônico e remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 549 (M+H)+; HPLC analítica: tret= 2,60 minutos (Grad 1).
Exemplo 91
1 -[3-Cloro-4-(4-etil-piperazin-1 -I l)-fen 11] -3-meti l-8-pi rid I n -3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000254] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 3-cloro-4-(4-etil-piperazin-1- il)-fenilamina (Zerenex, Greater Manchester, REINO UNIDO) e ácido 3- piridinaborônico. Composto do título: ES-MS: 499 (M+H)+; HPLC analítica: tret= 2,24 minutos (Grad 1).
Exemplo 92
1 -[3-Cloro-4-(4-etil-piperazin-1 -i l)-fen i I] -3-meti I -8-q u i nol i n -3-i I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000255] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 3-cloro-4-(4-etil-piperazin-1- il)-fenilamina (Zerenex, Greater Manchester, REINO UNIDO) e ácido 3- quinolinaborônico. Composto do título: ES-MS: 549 (M+H)+; HPLC analítica: tret= 2,58 minutos (Grad 1).
Exemplo 93
1-[3-Cloro-4-(4-isopropil-piperazin-1-il)-fenil]-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000256] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 3-cloro-4-(4-isopropil- piperazin-1-il)-fenilamina (Exemplo 93a) e ácido 3-piridinaborônico. Composto do título: ES-MS: 513 (M+H)+; HPLC analítica: tret = 2,32 minutos (Grad 1).
Exemplo 93a
3-Cloro-4-(4-isopropil-piperazin-1-il)-fenilamina
[000257] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1e empregando 1-(2-Cloro-4-nitro-fenil)-4- isopropil-piperazina (Exemplo 93b). Composto do título: ES-MS: 254 (M+H)+; HPLC analítica: tret= 1,80 minutos (Grad 1).
Exemplo 93b
1-(2-Cloro-4-nitro-fenil)-4-isopropil-piperazina
[000258] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 89c empregando N-isopropilpiperazina (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 284 (M+H)+; HPLC analítica: tret= 2,76 minutos (Grad 1).
Exemplo 94
1-[3-Cloro-4-(4-isopropil-piperazin-1-il)-fenil]-3-metil-8-quinolin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000259] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 3-cloro-4-(4-isopropil- piperazin-1-il)-fenilamina (Exemplo 93a) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 563 (M+H)+; HPLC analítica: tret = 2,68 minutos (Grad 1).
Exemplo 95
1-[4-(c/s-3,5-Dimetil-piperazin-1-il)-3-trifluorometil-fenil]-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000260] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-trifluorometil-fenil)-2,6-cis-dimetil-piperazina-1-carboxílico (Exemplo 95a) e ácido 3-piridinaborônico e a remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 533 (M+H)+; HPLC analítica: tret= 2,37 minutos (Grad 1).
Exemplo 95a
Éster de terc-butila de ácido 4-(4-amino-2-trifluorometil-fenil)-2,6- cis-dimetil-piperazina-1 -carboxílico
[000261] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1e iniciando com éster de terc-butila de ácido 4-(4-nitro-2-trifluorometil-fenil)-2,6-cis-dimetil-piperazina-1- carboxílico (Exemplo 95b). Composto do título: ES-MS: 374 (M+H)+; HPLC analítica: tret= 3,79 minutos (Grad 1).
Exemplo 95b
Éster de terc-butila de ácido cis-2,6-dimetil-4-(4-nitro-2- trifluorometil-fenil)-piperazina-1 -carboxílico
[000262] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 89b iniciando com c/s-3,5-Dimetil-1-(4-nitro- 2-trifluorometil-fenil)-piperazina (Exemplo 89c). Composto do título: ES- MS: 404 (M+H)+; HPLC analítica: tret = 4,76 minutos (Grad 1).
Exemplo 95c
c/s-3,5-Dimetil-1-(4-nitro-2-trifluorometil-fenil)-piperazina
[000263] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 18b iniciando com c/s-2,6-dimetilpiperazina (Aldrich, Buchs, Suíça) e 2-flúor-5-nitrobenzotrifluoreto (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 304 (M+H)+; HPLC analítica: tret = 2,89 minutos (Grad 1).
Exemplo 96
1-[4-(c/s-3,5-Dimetil-piperazin-1-il)-3-trifluorometil-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000264] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-trifluorometil-fenil)-2,6-cis-dimetil-piperazina-1 -carboxílico (Exemplo 95a) e ácido 3-quinolinaborônico e a remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 583 (M+H)+; HPLC analítica: tret= 2,71 minutos (Grad 1).
Exemplo 97
1-[4-(4-Etil-piperazin-1-il)-3-trifluorometil-fenil]-3-metil-8-piridin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000265] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 4-(4-etil-piperazin-1-il)-3- trifluorometil-fenilamina (Exemplo 97a) e ácido 3-piridinaborônico. Composto do título: ES-MS: 533 (M+H)+; HPLC analítica: tret = 2,38 minutos (Grad 1).
Exemplo 97a
4-(4-etil-piperazin-1-il)-3-trifluorometil-fenilamina
[000266] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 95a/c empregando N-etilpiperazina (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 274 (M+H)+; HPLC analítica: tret= 2,01 minutos (Grad 1).
Exemplo 98
1-[4-(4-Etil-piperazin-1-il)-3-trifluorometil-fenil]-3-metil-8-quinolin- 3-ÍI-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000267] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 4-(4-etil-piperazin-1-il)-3- trifluorometil-fenilamina (Exemplo 97a) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 583 (M+H)+; HPLC analítica: tret = 2,73 minutos (Grad 1).
Exemplo 99
1 -[4-(4-Etil-piperazin-1 -i l)-3-trifl uorometi l-fen i l]-3-meti l-8-pi rid i n-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000268] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 4-(4-isopropil-piperazin-1-il)- 3-trifluorometil-fenilamina (Exemplo 99a) e ácido 3-piridinaborônico. Composto do título: ES-MS: 547 (M+H)+; HPLC analítica: tret = 2,45 minutos (Grad 1).
Exemplo 99a
4-(4-lsopropil-piperazin-1-il)-3-trifluorometil-fenilamina
[000269] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 95a/c empregando N-isopropilpiperazina (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 288 (M+H)+; HPLC analítica: tret= 2,17 minutos (Grad 1).
Exemplo 100
1 -[4-(4-Etil-piperazin-1 -il)-3-trifluorometil-fenil]-3-metil-8-quinolin- 3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000270] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 4-(4-isopropil-piperazin-1-il)- 3-trifluorometil-fenilamina (Exemplo 99a) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 597 (M+H)+; HPLC analítica: tret = 2,82 minutos (Grad 1).
Exemplo 101
3-Metil-8-(6-piperazin-1 -i l-pi rid i n -3-i l)-1 -(3-trifluorometil-fenil)-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000271] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 2-trifluorometilanilina (Fluka, Buchs, Suíça) e éster de terc-butila de ácido 4-[5-(4,4,5,5-tetrametil- [1,3,2]d ioxaborolan-2-i l)-pirid in-2-i l]-pi perazina-1 -carboxílico (CB Research &Development, New castle, E.U.A.) e a remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 505 (M+H)+; HPLC analítica: tret = 2,47 minutos (Grad 1).
Exemplo 102
8-(6-Metóxi-piridin-3-il)-3-metil-1-(3-trifluorometil-fenil)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000272] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 2-trifluorometilanilina (Fluka, Buchs, Suíça) e ácido 2-metóxi-5-piridinaborônico (Lancaster, Morecambe, REINO UNIDO). Composto do título: ES-MS: 451 (M+H)+; HPLC analítica: tret= 3,28 minutos (Grad 1).
Exemplo 103
8-(6-Metóxi-piridin-3-il)-3-metil-1-(3-trifluorometil-fenil)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000273] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 2-trifluorometilanilina (Fluka, Buchs, Suíça) e cloridrato de ácido 6-benzopirazinaborônico (Asychem, Durham, E.U.A.). Composto do título: ES-MS: 472 (M+H)+; HPLC analítica: tret= 3,15 minutos (Grad 1).
Exemplo 104
1 -(3-Cloro-4-imidazol-1 -i l-fen i l)-3-meti I -8-pi rid i n-3-i 1-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000274] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 3-cloro-4-imidazol-1 -il- fenilamina (Exemplo 104a) e ácido 3-piridinaborônico. Composto do título: ES-MS: 453 (M+H)+; HPLC analítica: tret= 2,09 minutos (Grad 1).
Exemplo 104a
3-Cloro-4-imidazol-1-il-fenilamina
[000275] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1e iniciando com 1-(2-cloro-4-nitro-fenil)-1H- imidazol (Exemplo 104b). Composto do título: ES-MS: 194 (M+H)+; HPLC analítica: tret= 1,84 minuto (Grad 1).
Exemplo 104b
1-(2-Cloro-4-nitro-fenil)-1H-imidazol
[000276] 1,0 g (5,21 mmols) de 3,4-dicloronitrobenzeno (Fluka, Buchs, Suíça), 532 mg (7,81 mmols) de imidazol (Aldrich, Buchs, Suíça) e 1,35 g (10,4 mmols) de base de Hünig em 4 ml de DMA são aquecidos em um forno de micro-onda a 180°C durante 1 hora e 40 minutos. A mistura de reação é extinguida com NaHCOs aquoso saturado e extraída com EtOAc (2x). As camadas orgânicas são lavadas com NaHCOs aquoso saturado (3x), com salmoura, seca sobre MgSO4, filtrada e evaporada. O resíduo é purificado através de cromatografia instantânea em sílica-gel (CH2Cl2-MeOH 1:0 a 93:7) para produzir o composto do título como um óleo. ES-MS: 224 (M + H)+; HPLC analítica: tret= 2,11 minutos (Grad 1).
Exemplo 105
1 -(3-Cloro-4-imidazol-1 -i l-fen i l)-3-m eti l-8-q u i nol i n-3-i 1-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000277] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 3-cloro-4-imidazol-1-il- fenilamina (Exemplo 104a) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 503 (M+H)+; HPLC analítica: tret= 2,44 minutos (Grad 1).
Exemplo 106
2-Metil-2-[4-(3-metil-8-quinolin-3-il-2-tioxo-2,3-di-hidro-imidazo[4,5- c]quinolin-1 -il)-fenil]-propionitrila
[000278] 100 mg (0,213 mmol) de 2-Metil-2-[4-(3-metil-2-oxo-8- quinolin-3-il-2,3-di-hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila (Exemplo 7) e 95 mg (0,234 mmol) de reagente de Lawesson (Fluka, Buchs, Suíça) em 1 ml de dioxano são aquecidos a 100°C durante 96 horas. A mistura de reação é extinguida com NaHCOs aquoso saturado e extraída com CH2CI2 (2x). As camadas orgânicas são lavadas com NaHCOs aquoso saturado, secas sobre Na2SO4, filtradas e evaporadas. O resíduo é purificado através de HPLC preparativa para fornecer 0 composto do título como um sólido esbranquiçado. ES-MS: 486 (M + H)+; HPLC analítica: tret= 3,29 minutos (Grad 1).
Exemplo 107
2-Metil-2-{4-[3-metil-8-(2-metil-piridin-4-il)-2-oxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il]-fenil}-propionitrila
[000279] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando ácido 2-metil-4- piridilborônico (Asymchem, Durham, E.U.A.). Composto do título: ES- MS: 434 (M+H)+; HPLC analítica: tret= 2,44 minutos (Grad 1).
Exemplo 108
5-{1-[4-(Ciano-dimetil-metil)-fenil]-3-metil-2-oxo-2,3-di-hidro-1H- imidazo[4,5-c]quinolin-8-il}-piridina-2-carbonitrila
[000280] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 2-ciano-5-(4,4,5,5-tetrametil- 1,3,2-dioxaborolan-2-il)piridina (Frontier Scientific, Logan, E.U.A.). Composto do título: ES-MS: 445,5 (M+H)+; HPLC analítica: tret = 4,42 minutos (Grad 2).
Exemplo 109
2-[4-(4-Amino-3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-2-metil-propionitrila
[000281] 110 mg (0,182 mmol) de 2-{4-[4-(4-metóxi-benzilamino)-3- metil-2-oxo-8-quinolin-3-il-2,3-di-hidro-imidazo[4,5-c]quinolin-1-il]-fenil}- 2-metil-propionitrila (Exemplo 109a) em 1,1 ml de TFA são agitados à temperatura ambiente durante 24 horas e em seguida a 35°C durante 5 horas. A mistura de reação é purificada através de HPLC preparativa para fornecer o composto do título como um sólido esbranquiçado. ES- MS: 485 (M + H)+; HPLC analítica: tret= 2,86 minutos (Grad 1).
Exemplo 109a
2-{4-[4-(4-Metóxi-benzilamino)-3-metil-2-oxo-8-quinolin-3-il-2,3-di- hidro-imidazo[4,5-c]quinolin-1-il]-fenil}-2-metil-propionitrila
[000282] 100 mg (0,198 mmol) de 2-[4-(4-cloro-3-metil-2-oxo-8- quinolin-3-il-2,3-di-hidro-imidazo[4,5-c]quinolin-1-il)-fenil]-2-metil- propionitrila (Exemplo 109b), 27 mg (0,278 mmol) de terc-butanolato de sódio, 11 mg (0,02 mmol) de catalisador de SK-CC01-A e 33 mg (0,238 mmol) de 4-metoxibenzilamina em 0,4 ml de tolueno de degaseificado sob argônio são aquecidos a 100°C durante 22 horas. A mistura de reação é extinguida com NaHCOa aquoso saturado e extraída com CH2CI2 (2x). As camadas orgânicas são lavadas com NaHCOs aquoso saturado, secas sobre Na2SO4, filtradas e evaporadas para fornecer 0 composto do título como um sólido marrom bruto. ES- MS: 605 (M + H)+; HPLC analítica: tret= 3,29 minutos (Grad 1).
Exemplo 109b
2-[4-(4-Cloro-3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1-il)-fenil]-2-metil-propionitrila
[000283] 1 g (2,06 mmol) de 2-Metil-2-[4-(3-metil-2-oxo-5-óxi-8- quinolin-3-il-2,3-di-hidro-imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila (Exemplo 109c) e 948 mg (6,18 mmols) de POCh em 25 ml de tolueno são aquecidos a 100°C durante 5 horas. São adicionados 948 mg (6,18 mmols) de POCh e a mistura de reação é aquecida a 100°C durante 15,5 horas. A mistura de reação é extinguida com NaHCOs aquoso saturado e extraída com CH2CI2 (2x). As camadas orgânicas são lavadas com NaHCOs aquoso saturado, salmoura, secas sobre Na2SO4, filtradas e evaporadas para fornecer 0 composto do título bruto. ES-MS: 504 (M + H)+; HPLC analítica: tret = 3,56 minutos (Grad 1).
Exemplo 109c
2-Metil-2-[4-(3-metil-2-oxo-5-óxi-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila
[000284] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 2-[4-(8-bromo-3-metil-2-oxo- 5-óxi-2,3-di-hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila (Exemplo 109d) e ácido 3-quinolinaborônico. Composto do título: ES- MS: 486 (M + H)+; HPLC analítica: tret= 3,14 minutos (Grad 1).
Exemplo 109d
2-[4-(8-Bromo-3-metil-2-oxo-5-óxi-2,3-di-hidro-imidazo[4,5- c]quinolin-1 -il)-fenil]-2-metil-propionitrila
[000285] 2 g (4,75 mmols) de 2-[4-(8-bromo-3-metil-2-oxo-2,3-di- hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila (Exemplo 1 i) e 1,58 g (5,22 mmols) ácido 3-cloroperbenzoico em 90 ml de CH2CI2 são agitados à temperatura ambiente durante 2 horas. A mistura de reação é lavada com Na2COa aquoso a 10% e salmoura, secas sobre Na2SO4, filtradas e evaporadas. O sólido é triturado em acetato de etila para fornecer o composto do título bruto. ES-MS: 337, 339 (M + H)+, padrão Br; HPLC analítica: tret = 3,47 minutos (Grad 1).
Exemplo 110
1-[4-(3-Metil-2-oxo-8-piridin-3-il-2,3-di-hidro-imidazo[4,5-c]quinolin- 1-il)-fenil]-ciclopropanocarbonitrila
[000286] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 1-(4-amino-fenil)- ciclopropanocarbonitrila (Exemplo 110a) e ácido 3-piridinaborônico. Composto do título: ES-MS: 418 (M+H)+; HPLC analítica: tret = 3,82 minutos (Grad 2).
Exemplo 110a
1-(4-amino-fenil)-ciclopropanocarbonitrila
[000287] 750 mg (4 mmols) de ácido 4-(1-ciano-ciclopropil)-benzoico (Exemplo 110b) em 20 ml de terc-butanol são agitados na presença de 0,86 ml (4 mmols) de azida de difenilfosforila (DPPA, Fluka, Buchs, Suíça) e 0,59 ml (4 mmols) de trietilamina a 95°C durante 3 horas. São adicionados 0,43 ml (2 mmols) de DPPA e 0,29 ml (2 mmols) de trietilamina e a mistura de reação é agitada a 95°C durante 30 minutos. A mistura de reação é evaporada até a secura e em seguida é extraída em EtOAc e lavada com H2O, seca sobre Na2SO4, filtrada e evaporada. O sólido é separado através de cromatografia instantânea (CH2Cl2-MeOH 99:1). O composto purificado é tratado em 5 ml de HCI a 4 M em dioxano à temperatura ambiente durante 2 horas. O produto desprotegido bruto é purificado através de cromatografia instantânea (CH2Cl2-MeOH 98:2). O produto é triturado em MeOH para produzir 0 composto do título. HPLC analítica: tret = 3,68 minutos (Grad 2).
Exemplo 110b
Ácido 4-(1 -ciano-ciclopropil)-benzoico
[000288] A 2 g (12,4 mmols) de ácido 4-(cianometil)benzoico (Ubichem, Eastleigh, REINO UNIDO) e 10,9 ml (124 mmols) de 1,2- dibromoetano (Fluka, Buchs, Suíça) resfriados a 0°C com um banho de gelo é adicionado uma solução de 14,4 g (62 mmols) de cloreto de benziltrietilamônio em 50 ml de NaOH aquoso a 8 M. A mistura de reação é agitada durante noite à temperatura ambiente e em seguida é acidificada para pH 1 - 2 com HCI aquoso a 6 M e é extraída com EtOAc. A camada orgânica é lavada com H2O (2x) e evaporada até a secura. O sólido é triturado em MeOH para fornecer 0 composto do título bruto. ES-MS: 186 (M - H)_; HPLC analítica: tret = 4,43 minutos (Grad 2).
Exemplo 111
1-[4-(3-Metil-2-oxo-8-quinolin-3-il-2,3-di-hidro-imidazo[4,5- c]quinolin-1-il)-fenil]-ciclopropanocarbonitrila
[000289] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 1-(4-amino-fenil)- ciclopropanocarbonitrila (Exemplo 110a) e ácido 3-quinolinaborônico. Composto do título: ES-MS: 468 (M+H)+; HPLC analítica: tret =4,14 minutos (Grad 2).
Exemplo 112
1-{4-[8-(6-Metóxi-piridin-3-il)-3-metil-2-oxo-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il]-fenil}-ciclopropanocarbonitrila
[000290] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando 1-(4-amino-fenil)- ciclopropanocarbonitrila (Exemplo 110a) e ácido 2-metóxi-5- piridinaborônico. Composto do título: ES-MS: 448,5 (M+H)+; HPLC analítica: tret = 4,42 minutos (Grad 2).
Exemplo 113
1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(6-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000291] O composto do título é obtido tal como descrito no Exemplo 65 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 515 (M+H)+; HPLC analítica: tret= 3,83 minutos (Grad 2).
Exemplo 114
1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-8-(5-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000292] O composto do título é obtido tal como descrito no Exemplo 65 empregando 3-metóxi-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)piridina. Composto do título: ES-MS: 515,5 (M+H)+; HPLC analítica: Vet = 3,60 minutos (Grad 2).
Exemplo 115
1-[3-Cloro-4-(4-metil-piperazin-1-il)-fenil]-3-metil-8-quinoxalin-6-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000293] O composto do título é obtido tal como descrito no Exemplo 65 empregando cloridrato de ácido 6-benzopirazinaborônico. Composto do título: ES-MS: 536,6 (M+H)+; HPLC analítica: tret = 3,80 minutos (Grad 2).
Exemplo 116
1-(3-Cloro-4-piperazin-1-il-fenil)-8-(2-metóxi-pirimidin-5-il)-3-metil- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000294] O composto do título é obtido tal como descrito no Exemplo 75 empregando ácido 2-metóxi-5-pirimidinaborônico (Frontier Scientific, Logan, E.U.A.). Composto do título: ES-MS: 502 (M+H)+; HPLC analítica: tret= 2,40 minutos (Grad 1).
Exemplo 117
1-(3-Cloro-4-piperazin-1-il-fenil)-3-metil-8-pirimidin-5-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000295] O composto do título é obtido tal como descrito no Exemplo 75 empregando ácido 5-pirimidinaborônico (Frontier Scientific, Logan, E.U.A.). Composto do título: ES-MS: 472 (M+H)+; HPLC analítica: tret = 2,26 minutos (Grad 1).
Exemplo 118
1 -(3-Cloro-4-piperazin-1 -i l-fen i l)-3-meti I -8-(2-meti I-pi rid i n-4-i l)-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000296] O composto do título é obtido tal como descrito no Exemplo 75 empregando ácido 2-picolina-4-borônico. Composto do título: ES- MS: 485 (M+H)+; HPLC analítica: tret= 2,14 minutos (Grad 1).
Exemplo 119
1-[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1-il)-fenil]-8-(6-metóxi- piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000297] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 89 empregando ácido 2-metóxi-5- piridinaborônico e a remoção do grupo de proteção de terc- butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 529 (M+H)+; HPLC analítica: tret= 2,66 minutos (Grad 1).
Exemplo 120
1-[3-Cloro-4-(c/s-3,5-dimetil-piperazin-1-il)-fenil]-8-(5-metóxi- piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000298] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 89 empregando 3-metóxi-5-(4,4,5,5- tetrametil-1,3,2-dioxaborolan-2-il)piridina e a remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 529 (M+H)+; HPLC analítica: tret= 2,40 minutos (Grad 1).
Exemplo 121
1-[4-(c7s-3,5-Dimetil-piperazin-1-il)-3-trifluorometil-fenil]-8-(6- metóxi-piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2- ona
[000299] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-trifluorometil-fenil)-2,6-cis-dimetil-piperazina-1 -carboxílico (Exemplo 95a) e ácido 2-metóxi-5-piridinaborônico e a remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 563 (M+H)+; HPLC analítica: tret= 2,76 minutos (Grad 1).
Exemplo 122
1-[4-(c/s-3,5-Dimetil-piperazin-1-il)-3-trifluorometil-fenil]-8-(5- metóxi-piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2- ona
[000300] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 empregando éster de terc-butila de ácido 4-(4-amino-2-trifluorometil-fenil)-2,6-cis-dimetil-piperazina-1-carboxílico (Exemplo 95a) e 3-metóxi-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)piridina e remoção do grupo de proteção de terc-butoxicarbonila de uma maneira similar tal como descrito no Exemplo 59. Composto do título: ES-MS: 563 (M+H)+; HPLC analítica: tret= 2,50 minutos (Grad 1).
Exemplo 123
8-(2-Metóxi-pirimidin-5-il)-3-metil-1 -(4-piperazin-1 -I I-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000301] O composto do título é obtido tal como descrito no Exemplo 84 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 536,5 (M+H)+; HPLC analítica: tret= 3,78 minutos (Grad 2).
Exemplo 124
3-Meti 1-1 -(4-piperazin-1 -i l-3-trif I uorom eti l-fen i l)-8-pi ri m id i n -5-i I-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000302] O composto do título é obtido tal como descrito no Exemplo 84 empregando ácido 5-pirimidinaborônico. Composto do título: ES- MS: 506 (M+H)+; HPLC analítica: tret= 3,66 minutos (Grad 2).
Exemplo 125
5-[3-Metil-2-oxo-1-(4-piperazin-1-il-3-trifluorometil-fenil)-2,3-di- hidro-1H-imidazo[4,5-c]quinolin-8-il]-piridina-2-carbonitrila
[000303] O composto do título é obtido tal como descrito no Exemplo 84 empregando 2-ciano-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)piridina. Composto do título: ES-MS: 530,6 (M+H)+; HPLC analítica: tret = 3,89 minutos (Grad 2).
Exemplo 126
3-Metil-8-(2-metil-piridin-4-il)-1-(4-piperazin-1-il-3-trifluorometil- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000304] O composto do título é obtido tal como descrito no Exemplo 84 empregando ácido 2-metil-4-piridilborônico. Composto do título: ES- MS: 519 (M+H)+; HPLC analítica: tret= 3,63 minutos (Grad 2).
Exemplo 127
8-(3,4-Dimetóxi-fenil)-3-metil-1-(4-piperazin-1-il-3-trifluorometil- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000305] O composto do título é obtido tal como descrito no Exemplo 84 empregando ácido 3,4-dimetoxifenilborônico (Aldrich, Buchs, Suíça). Composto do título: ES-MS: 564 (M+H)+; HPLC analítica: tret = 2,68 minutos (Grad 1).
Exemplo 128
3-Meti l-8-pi rid I n -3-i I-1 -(4-[1,2,4]triazol-1 -I l-3-trif I uorometi I -fen i l)-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000306] O composto do título é obtido tal como descrito no Exemplo 1 empregando 4-[1,2,4]triazol-1 -il-3-trifluorometilfenilamina (Exemplo 128a). Composto do título: ES-MS: 488 (M+H)+; HPLC analítica: tret = 3,72 minutos (Grad 2).
Exemplo 128a
4-[1,2,4]Triazol-1-il-3-trifluorometil-fenilamina
[000307] O composto do título é obtido de uma maneira similar como descrito no Exemplo 71a empregando 1 -flúor-4-nitro-2-trifluorometil- benzeno (Aldrich, Buchs, Suíça) e 1,2,4-triazol (Fluka, Buchs, Suíça). Composto do título: ES-MS: 229 (M+H)+; HPLC analítica: tret = 4,14 minutos (Grad 2).
Exemplo 129
3-Meti l-8-q u i nol i n-3-i 1-1 -(4-[1,2,4]triazol-1 -i l-3-trif I uorometi I -fen i I)- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000308] O composto do título é obtido tal como descrito no Exemplo 128 empregando ácido 3-quinolinaborônico. Composto do título: ES- MS: 538 (M+H)+; HPLC analítica: tret = 4,03 minutos (Grad 2).
Exemplo 130
8-(6-Metóxi-piridin-3-il)-3-metil-1 -(4-[1,2,4]triazol-1 -il-3-trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000309] O composto do título é obtido tal como descrito no Exemplo 128 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 518 (M+H)+; HPLC analítica: tret= 4,25 minutos (Grad 2).
Exemplo 131
8-(5-Metóxi-pirídin-3-il)-3-metil-1 -(4-[1,2,4]trlazol-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000310] O composto do título é obtido tal como descrito no Exemplo 128 empregando 3-metóxi-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)piridina. Composto do título: ES-MS: 518 (M+H)+; HPLC analítica: tret = 3,85 minutos (Grad 2).
Exemplo 132
5-[3-Metil-2-oxo-1 -(4-[1,2,4]triazol-1 -il-3-trifluorometil-fenil)-2,3-di- hidro-1 H-imidazo[4,5-c]quinolin-8-il]-piridina-2-carbonitrila
[000311] O composto do título é obtido tal como descrito no Exemplo 128 empregando 2-ciano-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)piridina. Composto do título: ES-MS: 513,6 (M+H)+; HPLC analítica: tret= 4,21 minutos (Grad 2).
Exemplo 133
8-(6-F I úor-pi rid I n -3-i l)-3-meti I-1 -(4-[1,2,4]triazol-1 -I l-3-trifl uorometi I - fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000312] O composto do título é obtido tal como descrito no Exemplo 128 empregando ácido 2-flúor-5-piridinaborônico (Frontier Scientific, Logan, E.U.A.). Composto do título: ES-MS: 506 (M+H)+; HPLC analítica: tret= 4,19 minutos (Grad 2).
Exemplo 134
8-(2,6-Dimetóxi-piridin-3-il)-3-metil-1 -(4-[1,2,4]triazol-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000313] O composto do título é obtido tal como descrito no Exemplo 128 empregando ácido 2,6-dimetóxi-3-piridinaborônico (Lancaster, Morecambe, REINO UNIDO). Composto do título: ES-MS: 548,6 (M+H)+; HPLC analítica: tret= 4,54 minutos (Grad 2).
Exemplo 135
3-Metil-8-pirimidin-5-il-1 -(4-[1,2,4]triazol-1 -il-3-trifluorometil-fenil)- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000314] O composto do título é obtido tal como descrito no Exemplo 128 empregando ácido 5-pirimidinaborônico. Composto do título: ES- MS: 489,6 (M+H)+; HPLC analítica: tret= 3,93 minutos (Grad 2).
Exemplo 136
8-(2-Metóxi-pirimidin-5-il)-3-metil-1 -(4-[1,2,4]triazol-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000315] O composto do título é obtido tal como descrito no Exemplo 128 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 519 (M+H)+; HPLC analítica: tret= 4,12 minutos (Grad 2).
Exemplo 137
8-(2,4-Dimetóxi-pirimidin-5-il)-3-metil-1 -(4-[1,2,4]triazol-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000316] O composto do título é obtido tal como descrito no Exemplo 128 empregando ácido 2,4-dimetóxi-5-piridinaborônico (Frontier Scientific, Logan, E.U.A.). Composto do título: ES-MS: 549 (M+H)+; HPLC analítica: tret= 4,19 minutos (Grad 2).
Exemplo 138
3-Meti 1-1 -(4-pirazol-1 -i l-3-trif I uorometi I -fen i l)-8-pi rid i n -3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000317] O composto do título é obtido tal como descrito no Exemplo 1 empregando 4-pirazol-1-il-3-trifluorometil-fenilamina (Exemplo 137a). Composto do título: ES-MS: 487 (M+H)+; HPLC analítica: tret = 3,92 minutos (Grad 2).
Exemplo 138a
4-Pirazol-1-il-3-trifluorometil-fenilamina
[000318] O composto do título é obtido de uma maneira similar como o Exemplo 71a empregando 1-flúor-4-nitro-2-trifluorometil-benzeno (Aldrich, Buchs, Suíça) e pirazol (Fluka, Buchs, Suíça). Composto do título: ES-MS: 228 (M+H)+; HPLC analítica: Let = 4,58 minutos (Grad 2).
Exemplo 139
3-Meti 1-1 -(4-pirazol-1 -I l-3-trifl uorometi I -fen I l)-8-q u I nol I n-3-i 1-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000319] O composto do título é obtido tal como descrito no Exemplo 138 empregando ácido 3-quinolinaborônico. Composto do título: ES- MS: 537 (M+H)+; HPLC analítica: tret = 4,29 minutos (Grad 2).
Exemplo 140
8-(6-Metóxi-piridin-3-il)-3-metil-1-(4-pirazol-1-il-3-trifluorometil- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000320] O composto do título é obtido tal como descrito no Exemplo 138 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 517 (M+H)+; HPLC analítica: tret= 4,57 minutos (Grad 2).
Exemplo 141
8-(5-Metóxi-piridin-3-il)-3-metil-1-(4-pirazol-1-il-3-trifluorometil- fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000321] O composto do título é obtido tal como descrito no Exemplo 138 empregando 3-metóxi-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)piridina. Composto do título: ES-MS: 517 (M+H)+; HPLC analítica: Let = 4,07 minutos (Grad 2).
Exemplo 142
1 -(3-Cloro-4-[1,2,4]triazol-1 -i l-fen i l)-3-meti I -8-pi rid i n-3-i 1-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000322] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 iniciando com 3-cloro-4-[1,2,4]triazol-1 -il- fenilamina (Exemplo 142a). Composto do título: ES-MS: 454 (M+H)+; HPLC analítica: tret= 2,28 minutos (Grad 1).
Exemplo 142a
3-Cloro-4-[1,2,4]triazol-1 -il-fenilamina
[000323] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 104a/b iniciando com 1,2,4-triazol. Composto do título: ES-MS: 195 (M+H)+; HPLC analítica: tret = 2,09 minutos (Grad 1).
Exemplo 143
1 -(3-Cloro-4-[1,2,4]triazol-1 -I l-fen I l)-3-meti I -8-q u I nol I n -3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000324] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 142 iniciando com ácido 3- quinolinaborônico. Composto do título: ES-MS: 504 (M+H)+; HPLC analítica: tret= 2,67 minutos (Grad 1).
Exemplo 144
1 -(4-lmidazol-1 -I l-3-trifl uorometi I -fen I l)-3-m eti l-8-pi rid I n -3-i I-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona
[000325] O composto do título é obtido tal como descrito no Exemplo 1 empregando 4-pirazol-1-il-3-trifluorometil-fenilamina (Exemplo 144a). Composto do título: ES-MS: 487 (M+H)+; HPLC analítica: tret = 3,54 minutos (Grad 2).
Exemplo 144a
4-lmidazol-1 -il-3-trifluorometil-fenilamina
[000326] O composto do título é obtido de uma maneira similar como o Exemplo 138a empregando imidazol. Composto do título: ES-MS: 228 (M+H)+; HPLC analítica: tret = 3,73 minutos (Grad 2).
Exemplo 145
1 -(4-lmidazol-1 -i l-3-trif I uorometi I -fen i l)-3-m eti l-8-q u i nol i n-3-i 1-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona
[000327] O composto do título é obtido tal como descrito no Exemplo 144 empregando ácido 3-quinolinaborônico. Composto do título: ES- MS: 537 (M+H)+; HPLC analítica: tret= 3,83 minutos (Grad 2).
Exemplo 146
1-(4-lmidazol-1-il-3-trifluorometil-fenil)-8-(6-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000328] O composto do título é obtido tal como descrito no Exemplo 144 empregando ácido 2-metóxi-5-piridinaborônico. Composto do título: ES-MS: 517 (M+H)+; HPLC analítica: tret= 3,90 minutos (Grad 2).
Exemplo 147
1-(4-lmidazol-1-il-3-trifluorometil-fenil)-8-(5-metóxi-piridin-3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000329] O composto do título é obtido tal como descrito no Exemplo 144 empregando 3-metóxi-5-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)piridina. Composto do título: ES-MS: 517 (M+H)+; HPLC analítica: tret = 3,64 minutos (Grad 2).
Exemplo 148
3-Meti l-8-piridIn-3-iI-1 -(4-[1,2,4]triazol-1 -i I m eti l-fen i l)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000330] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 iniciando com 4-[1,2,4]Triazol-1 -ilmetil- fenilamina (Exemplo 148a). Composto do título: ES-MS: 434 (M+H)+; HPLC analítica: tret= 2,13 minutos (Grad 1).
Exemplo 148a
4-[1,2,4]Triazol-1 -ilmetil-fenilamina
[000331] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1e iniciando com 1-(4-nitro-benzil)-1H- [1,2,4]triazol (Exemplo 148b). Composto do título: ES-MS: 175 (M+H)+; HPLC analítica: tret= minutos (Grad 2).
Exemplo 148b
1 -(4-Nitro-benzil)-1 H-[1,2,4]triazol
[000332] 1,0 g (4,63 mmols) de brometo de 4-nitrobenzila (Fluka, Buchs, Suíça), 799 mg (11,6 mmols) de 1,2,4-triazol e 0,692 mL (4,63 mmols) de 1,5-diazabiciclo[5,4,0]-5-undeceno (Fluka, Buchs, Suíça) em 10 ml de CH2CI2 são agitados à temperatura ambiente durante 1,5 hora. A mistura de reação é extinguida com NaHCOa aquoso saturado e extraída com CH2CI2 (2x). As camadas orgânicas são lavadas com salmoura, secas sobre MgSO4, filtradas e evaporadas. O resíduo é purificado através de cromatografia instantânea (CH2Ch-MeOH 49:1 a 19:1) para produzir 0 composto do título como um sólido amarelo- pálido. ES-MS: 205 (M + H)+; HPLC analítica: tret = 2,54 minutos (Grad 1).
Exemplo 149
3-Meti l-8-quInolIn-3-i1-1 -(4-[1,2,4]triazol-1 -IImetil-fen 11)-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000333] O composto do título é obtido tal como descrito no Exemplo 148 empregando ácido 3-quinolinaborônico. Composto do título: ES- MS: 484 (M+H)+; HPLC analítica: tret= 2,49 minutos (Grad 1).
Exemplo 150
1 -(4-lmidazol-1-Il metil-fenIl)-3-meti I -8-piridin-3-i 1-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona
[000334] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 1 iniciando com 4-imidazol-1-ilmetil- fenilamina (Exemplo 150a). Composto do título: ES-MS: 433 (M+H)+; HPLC analítica: tret= 1,96 minuto (Grad 1).
Exemplo 150a
4-lmidazol-1-ilmetil-fenilamina
[000335] O composto do título é obtido de uma maneira similar tal como descrito no Exemplo 147a/b iniciando com imidazol. Composto do título: ES-MS: 174 (M+H)+; HPLC analítica: tret= minutos (Grad 2).
Exemplo 151
1 -(4-lmidazol-1 -IImetil-fenIl)-3-meti I -8-quInolIn-3-iI-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona
[000336] O composto do título é obtido tal como descrito no Exemplo 150 empregando ácido 3-quinolinaborônico. Composto do título: ES- MS: 483 (M+H)+; HPLC analítica: tret= 2,33 minutos (Grad 1).
Exemplo 152
[000337] Os seguintes sais de ácidos 4-toluenossulfônico são preparados em uma relação estequiométrica de 1:1 seguindo condições de reação padrões em analogia aos ou de acordo com os métodos que são conhecidos na técnica: 152-1) sal de 2-metil-2-[4-(3-metil-2-oxo-8-piridin-4-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-2) sal de 2-metil-2-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-3) sal de 2-metil-2-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-4) sal de 2-metil-2-[4-(3-metil-2-oxo-8-quinolin-6-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-5) sal de 2-metil-2-[4-(3-metil-2-oxo-8-quinoxalin-6-il-2,3-di- hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-6) sal de 2-etil-2-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-butironitrila de ácido 4- toluenossulfônico; 152-7) sal de 2-etil-2-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-butironitrila de ácido 4- toluenossulfônico; 152-8) sal de 1 -[3-flúor-4-(2-oxo-pirrolidin-1 -il)-fenil]-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-9) sal de 1 -[3-flúor-4-(2-oxo-pirrolidin-1 -il)-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-10) sal de 3-metil-1 -[4-(2-oxo-pirrolidin-1 -il)-fenil]-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-11) sal de 3-metil-1 -[4-(2-oxo-pirrolidin-1 -il)-fenil]-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-12) sal de 1-{4-[bis-(2-metóxi-etil)-amino]-3-flúor-fenil}-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-13) sal de 1-{4-[bis-(2-metóxi-etil)-amino]-3-flúor-fenil}-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-14) sal de 1-{4-[bis-(2-metóxi-etil)-amino]-fenil}-3-metil-8-piridin- 3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-15) sal de 1-{4-[bis-(2-metóxi-etil)-amino]-fenil}-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-16) sal de 3-metil-1-naftalen-2-il-8-piridin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-17) sal de 3-metil-1-naftalen-2-il-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-18) sal de 1-(2-cloro-fenil)-3-metil-8-piridin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-19) sal de 1-(2-cloro-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-20) sal de 3-metil-8-piridin-3-il-1-o-tolil-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-21) sal de 3-metil-8-quinolin-3-il-1 -o-tolil-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-22) sal de 1-(2-etil-fenil)-3-metil-8-piridin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-23) sal de 1-(2-etil-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-24) sal de 3-metil-8-piridin-3-il-1-(2-trifluorometil-fenil)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-25) sal de 3-metil-8-quinolin-3-il-1-(2-trifluorometil-fenil)-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-26) sal de 1-(4-flúor-2-metil-fenil)-3-metil-8-quinolin-3-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-27) sal de 1-(4-flúor-2-metil-fenil)-3-metil-8-quinolin-3-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-28) sal de 1-(2-cloro-4-flúor-fenil)-3-metil-8-piridin-3-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-29) sal de 1-(2-cloro-4-flúor-fenil)-3-metil-8-quinolin-3-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-30) sal de 1-(3-cloro-fenil)-3-metil-8-piridin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-31) sal de 1-(3-cloro-fenil)-3-metil-8-quinolin-3-il-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-32) sal de 1-(4-metoximetil-fenil)-3-metil-8-quinolin-3-il-1,3-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-33) sal de 1-[2-cloro-4-(2-metóxi-etil)-fenil]-3-metil-8-quinolin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-34) sal de 1-[4-(2-metóxi-etil)-fenil]-3-metil-8-piridin-3-il-1 ,-di- hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-35) sal de 2-metil-2-[4-(3-metil-2-oxo-5-óxi-8-piridin-3-il-2,3-di- hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-36) sal de 2-metil-2-[4-(3-metil-2-oxo-5-óxi-8-quinolin-3-il-2,3-di- hidro-imidazo[4,5-c]quinolin-1 -il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-37) sal de 2-[4-(7-flúor-3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-2-metil-propionitrila de ácido 4- toluenossulfônico; 152-38) sal de 2-[4-(7-flúor-3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1 -il)-fenil]-2-metil-propionitrila de ácido 4- toluenossulfônico; 152-39) sal de N-metil-N-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-metanossulfonamida de ácido 4- toluenossulfônico; 152-40) sal de metil-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-amida de ácido etanossulfônico de ácido 4-toluenossulfônico; 152-41) sal de metil-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-amida de ácido etanossulfônico de ácido 4-toluenossulfônico; 152-42) sal de N-etil-N-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-metanossulfonamida de ácido 4- toluenossulfônico; 152-43) sal de N-etil-N-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-metanossulfonamida de ácido 4- toluenossulfônico; 152-44) sal de 2-[4-(3-etil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-2-metil-propionitrila de ácido 4- toluenossulfônico; 152-45) sal de 1-[3-flúor-4-(4-metanossulfonil-piperazin-1-il)-fenil]-3- metil-8-quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-46) sal de 1-[3-flúor-4-(4-metanossulfonil-piperazin-1-il)-fenil]-3- metil-8-piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-47) sal de 1-[3-cloro-4-(4-metil-piperazin-1-il)-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-48) sal de 1-[3-cloro-4-(4-metil-piperazin-1-il)-fenil]-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-49) sal de 1-(4-imidazol-1-il-2-metil-fenil)-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-50) sal de 3-metil-1 -(4-pirazol-1 -il-fenil)-8-piridin-3-iI-1,3-di-hidro- imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-51) sal de 1-(3-cloro-4-imidazol-1-il-fenil)-3-metil-8-piridin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-52) sal de 1-(3-cloro-4-imidazol-1-il-fenil)-3-metil-8-quinolin-3-il- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-53) sal de 2-metil-2-[4-(3-metil-8-quinolin-3-il-2-tioxo-2,3-di- hidro-imidazo[4,5-c]quinolin-1-il)-fenil]-propionitrila de ácido 4- toluenossulfônico; 152-54) sal de 2-metil-2-{4-[3-metil-8-(2-metil-piridin-4-il)-2-oxo-2,3- di-hidro-imidazo[4,5-c]quinolin-1 -il]-fenil}-propionitrila de ácido 4- toluenossulfônico; 152-55) sal de 1-[4-(3-metil-2-oxo-8-piridin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-ciclopropanocarbonitrila de ácido 4- toluenossulfônico; 152-56) sal de 1-[4-(3-metil-2-oxo-8-quinolin-3-il-2,3-di-hidro- imidazo[4,5-c]quinolin-1-il)-fenil]-ciclopropanocarbonitrila de ácido 4- toluenossulfônico; 152-57) sal de 1-{4-[8-(6-metóxi-piridin-3-il)-3-metil-2-oxo-2,3-di- hidro-imidazo[4,5-c]quinolin-1 -il]-fenil}-ciclopropanocarbonitrila de ácido 4-toluenossulfônico; 152-58) sal de 1-(3-cloro-4-piperazin-1-il-fenil)-3-metil-8-pirimidin-5- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-59) sal de 8-(6-metóxi-piridin-3-il)-3-metil-1-(4-[1,2,4]triazol-1-il- 3-trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-60) sal de 1-(3-cloro-4-[1,2,4]triazol-1-il-fenil)-3-metil-8-piridin-3- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-61) sal de 1-(3-cloro-4-[1,2,4]triazol-1-il-fenil)-3-metil-8-quinolin- 3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-62) sal de 1-(4-imidazol-1-il-3-trifluorometil-fenil)-3-metil-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-63) sal de 1-(4-imidazol-1-il-3-trifluorometil-fenil)-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-64) sal de 1-(4-imidazol-1-il-3-trifluorometil-fenil)-8-(6-metóxi- piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4- toluenossulfônico; 152-65) sal de 3-metil-8-quinolin-3-iI-1 -(4-[1,2,4]triazol-1 -iImetil-feniI)- 1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico; 152-66) sal de 1-(4-imidazol-1-ilmetil-fenil)-3-metil-8-quinolin-3-il-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido 4-toluenossulfônico.
Exemplo 153
[000338] Os seguintes sais de ácidos maleicos são preparados em uma relação estequiométrica de 1:1 seguindo condições de reação padrões em analogia aos ou de acordo com os métodos que são conhecidos na técnica. 153-1) sal de 2-metil-2-{4-[3-metil-2-oxo-8-(6-piperazin-1-il-piridin- 3-il)-2,3- di-hidro-imidazo[4,5-c]quinolin-1-il]-fenil}-propionitrila de ácido maleico; 153-2) sal de 1-(3-flúor-4-piperazin-1-il-fenil)-3-metil-8-quinolin-3-il- 1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-3) sal de 1-(3-flúor-4-piperazin-1-il-fenil)-3-metil-8-piridin-3-il- 1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-4) sal de 3-metil-1 -[4-(4-metil-piperazin-1 -il)-fenil]-8-quinolin- 3-ÍI-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-5) sal de 3-metil-1 -[4-(4-metil-piperazin-1 -il)-fenil]-8-piridin-3- il-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-6) sal de 3-metil-1 -[4-(4-metil-piperazin-1 -il)-3-trifluorometil- fenil]-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-7) sal de 3-metil-1-[4-(4-metil-piperazin-1-il)-3-trifluorometil- fenil]-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-8) sal de 1 -(3-cloro-4-piperazin-1 -il-fenil)-3-metil-8-quinolin-3- il-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-9) sal de 1 -(3-cloro-4-piperazin-1 -il-fenil)-3-metil-8-piridin-3-il- 1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-10) sal de 1 -(3-cloro-4-piperazin-1 -il-fenil)-8-(6-metóxi-piridin- 3-il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-11) sal de 1 -(3-cloro-4-piperazin-1 -il-fenil)-8-(5-metóxi-piridin-3- il)-3- metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-12) sal de 1-(3-cloro-4-piperazin-1-il-fenil)-3-metil-8-quinoxalin- δ-il-1,3- di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-13) sal de 3-metil-1 -(4-piperazin-1 -il-3-trifluorometil-fenil)-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-14) sal de 3-metil-1 -(4-piperazin-1 -il-3-trifluorometil-fenil)-8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-15) sal de 8-(6-metóxi-piridin-3-il)-3-metil-1 -(4-piperazin-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-16) sal de 8-(5-metóxi-piridin-3-il)-3-metil-1 -(4-piperazin-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-17) sal de 3-metil-1 -(4-piperazin-1 -il-3-trifluorometil-fenil)-8- quinoxalin-6- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-18) sal de 1 -[3-cloro-4-(4-etil-piperazin-1 -il)-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-19) sal de 1 -[3-cloro-4-(4-isopropil-piperazin-1 -il)-fenil]-3-metil-8- quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-20) sal de 1-[4-(c/s-3,5-dimetil-piperazin-1-il)-3-trifluorometil- fenil]-3- metil-8-piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-21) sal de 1-[4-(c/s-3,5-dimetil-piperazin-1-il)-3-trifluorometil- fenil]-3- metil-8-quinolin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-22) sal de 1 -[4-(4-etil-piperazin-1 -il)-3-trifluorometil-fenil]-3-metil- 8- piridin-3-il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-23) sal de 3-metil-8-(6-piperazin-1 -il-piridin-3-il)-1 -(3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-24) sal de 1-(3-cloro-4-piperazin-1-il-fenil)-3-metil-8-(2-metil- piridin-4- il)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-25) sal de 1-[3-cloro-4-(cis-3,5-dimetil-piperazin-1-il)-fenil]-8-(6- metóxi- piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-26) sal de 1-[3-cloro-4-(cis-3,5-dimetil-piperazin-1-il)-fenil]-8-(5- metóxi- piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-27) sal de 1 -[4-(cis-3,5-dimetil-piperazin-1 -il)-3-trifluorometil- fenil]-8-(6- metóxi-piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona de ácido maleico; 153-28) sal de 1 -[4-(cis-3,5-dimetil-piperazin-1 -il)-3-trifluorometil- fenil]-8-(5- metóxi-piridin-3-il)-3-metil-1,3-di-hidro-imidazo[4,5- c]quinolin-2-ona de ácido maleico; 153-29) sal de 8-(2-metóxi-pirimidin-5-il)-3-metiI-1 -(4-piperazin-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-30) sal de 3-metil-1 -(4-piperazin-1 -il-3-trifluorometil-fenil)-8- pirimidin-5- il-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-31) sal de 3-metil-8-(2-metil-piridin-4-il)-1 -(4-piperazin-1 -il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico; 153-32) sal de 8-(3,4-dimetóxi-fenil)-3-metil-1-(4-piperazin-1-il-3- trifluorometil-fenil)-1,3-di-hidro-imidazo[4,5-c]quinolin-2-ona de ácido maleico.
Exemplo 154: Cápsulas macias
[000339] 5000 cápsulas de gelatina macias, cada qual compreendendo como ingrediente ativo 0,05 g de um dos compostos de Fórmula I mencionados nos Exemplos precedentes, são preparadas como segue: Composição Ingrediente ativo 250 g Lauroglicol 2 litros Processo de preparação: O ingrediente ativo pulverizado é suspenso em Lauroglykol® (laurato de propileno glicol, Gattefossé S.A., Saint Priest, França) e triturado em um pulverizador por umidade para produzir um tamanho de partícula de cerca de 1 a 3 pm. Porções de 0,419 g da mistura são em seguida introduzidas em cápsulas de gelatina macias empregando-se uma máquina de enchimento de cápsula.