CAMPO DA INVENÇÃO
[0001] Esta invenção se refere de modo geral a enzimas usadas em composições de alimentos e rações; e em aspectos alternativos proporciona novas enzimas, polinucleotídeos codificando estas enzimas, e usos destes polinucleotídeos e polipeptídeos, e em aspectos alternativos proporciona polipeptídeos (por exemplo, enzimas, peptídeos, anticorpos) tendo uma atividade de glucanase, por exemplo, uma atividade de endoglucanase, por exemplo, catalisando hidrólise de ligações de endo- β-1,4- e/ou β-1,3- glucanase internas. Em um aspecto, a atividade de endoglucanase (por exemplo, atividade de endo-1,4-beta-D-glucan 4-glucano hidrolase) compreende hidrólise de ligações 1,4- e/ou β-1,3- beta-D-glicosídicas em celulose, derivados celulósicos (por exemplo, carbóxi metila celulose e hidróxi etil celulose), liquenina, ligações beta-1,4 em glucanos beta-1,3 mistos, tais como beta-D-glucanos ou xiloglucanos de cereais e outro material vegetal ou orgânico contendo partes celulósicas. Em um aspecto, os polipeptídeos da invenção têm uma atividade de glucanase, xilanase e/ou uma mananase.
ANTECEDENTES
[0002] Endoglucanases (por exemplo, endo-beta-1,4-glucanases, EC 3.2.1.4; endo-beta-1,3(1)-glucanases, EC 3.2.1.6; endo-beta-1,3- glucanases, EC 3.2.1.39) hidrolisam ligações β-1,4- e/ou β-1,3- glucosídicas internas em celulose e glucano para produzir glicose e oligômeros de glicose de menor peso molecular. Glucanos são polissacarídeos formados de D-glucopiranose ligada a 1,4-β- e/ou 1,3- glicosídeos. Endoglucanases são de considerável valor comercial, sendo usadas na indústria alimentícia, para cozimento e processamento de frutos e legumes, decomposição de resíduo agrícola, na fabricação de ração animal, por exemplo, uma ração de animal monogástrico, tal como uma ração de suíno ou aves domésticas (por exemplo, frango), na produção de polpa e papel, fabricação de têxteis e agentes de limpeza doméstica e industrial. Endoglucanases são produzidas por fungos e bactérias.
[0003] Beta-glucanos são os principais polissacarídeos não amiláceos dos cereais. O teor de glucano pode variar significativamente dependendo da variedade e das condições de crescimento. As propriedades fisicoquímicas deste polissacarídeo são tais que dão origem a soluções viscosas ou mesmo géis sob condições oxidativas. Além disso, glucanos têm alta capacidade de ligação de água. Todas estas características apresentam problemas para várias indústrias incluindo fermentação, cozimento, e nutrição animal. Em aplicações de fermentação, a presença de glucano resulta em problemas de filtrabilidade do mosto e formação de névoa. Em aplicações de cozimento (especialmente para biscoitos e bolachas), glucanos podem criar massas pegajosas que são difíceis de trabalhar à máquina e reduzir o tamanho do biscoito. Além disso, este carboidrato está implicado em rápida reidratação do produto assado resultando em perda da sensação de frescor e tempo de armazenamento reduzido. Para aplicações de rações de animais monogástricos com dietas de cereais, beta-glucano é um fator contribuinte para a viscosidade do conteúdo intestinal e deste modo afeta de modo adverso a digestibilidade da ração e a taxa de crescimento animal. Para animais ruminantes, estes beta-glucanos representam componentes substanciais da ingestão de fibras e a digestão mais completa de glucanos facilitaria maiores eficiências de conversão de ração. É desejável para ração animal que as endoglucanases sejam ativas no estômago do animal.
[0004] As endoglucanases também são importantes para a digestão de celulose, um glucano beta-1,4-ligado encontrado em todo material vegetal. A celulose é o polissacarídeo mais abundante na natureza. Enzimas comerciais que digerem celulose têm utilidade na indústria de polpa e papel, na fabricação de têxteis e em agentes de limpeza doméstica e industrial.
[0005] As publicações discutidas aqui, neste pedido de patente, são proporcionadas somente para sua divulgação antes da data de arquivamento do presente pedido. Nada aqui, neste pedido de patente, deve ser considerado como uma admissão de que a invenção não está intitulada a antedatar semelhante divulgação em virtude de invenção anterior.
SUMÁRIO DA INVENÇÃO
[0006] Em um aspecto, a invenção proporciona composições (por exemplo, rações, fármacos, suplementos dietéticos, e etc.) compreendendo os polipeptídeos (por exemplo, enzimas (por exemplo, glucanases), peptídeos, anticorpos) e/ou polinucleotídeos da invenção. Estas composições podem ser formuladas em uma variedade de formas, por exemplo, como líquidos, sprays, aerossóis, filmes, micelas, lipossomas, pós, alimentos, rações, aditivos, péletes, comprimidos, pílulas, géis, hidrogéis, implantes ou formas encapsuladas. Por exemplo, a invenção proporciona um produto enzimático de ração compreendendo uma enzima da invenção, por exemplo, para uso como um alimento ou ração de grão não-refinado monogástrico, em que os animais monogástricos incluem aves domésticas, suínos (porcos, varrões, suínos capados), carneiros, coelhos, aves, cavalos, animais domésticos monogástricos e seres humanos. Em um aspecto, dietas animais de ração compreendendo enzimas da invenção aumentarão o valor dietético do alimento ou ração compreendendo enzima. Em um aspecto, uma composição (por exemplo, rações, alimentos, fármacos, suplementos dietéticos, e etc.) da invenção pode compreender um, dois, três ou mais polinucleotídeos diferentes da invenção; e em um aspecto, uma composição da invenção pode compreender uma combinação de uma enzima da invenção com outro polipeptídeo (por exemplo, enzima, peptídeo) da invenção ou qualquer enzima conhecida.
[0007] Em um aspecto, a enzima da invenção é termotolerante e/ou termoestável; por exemplo, uma enzima da invenção pode reter pelo menos 75% de atividade residual (por exemplo, atividade de glucanase) depois de 2 minutos a 95°C; e em outro aspecto, retém 100% de atividade depois de aquecimento por 30 minutos a 95°C. Em um aspecto, uma enzima da invenção usada nestas composições compreende polipeptídeos recombinantes expressados, por exemplo, em sistemas de expressão de leveduras (por exemplo, Pichia spp., Saccharomyces spp.) ou bacterianos (por exemplo, Pseudomonas spp., Bacillus spp.), tais como sistemas de expressão de Pichia pastoris, Saccharomyces cerevisiae ou Pseudomonas fluorescens.
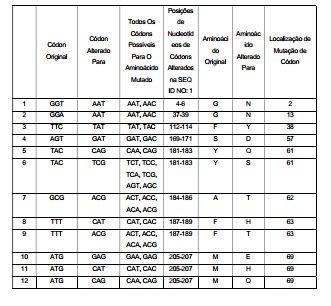
[0008] A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes compreendendo uma sequência de ácido nucleico tendo pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) com um ácido nucleico exemplar da invenção, por exemplo, SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22 e variações (modificações) da mesma conforme descrito aqui, neste pedido de patente, (vide, por exemplo, as Tabelas 1 e 2, abaixo), sobre uma região de pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200, 1250, 1300, 1350, 1400, 1450, 1500, 1550, 1600, 1650, 1700, 1750, 1800, 1850, 1900, 1950, 2000, 2050, 2100, 2200, 2250, 2300, 2350, 2400, 2450, 2500, ou mais resíduos, e a sequência compreende pelo menos uma, duas, três, quatro, cinco, seis, sete, oito, nove, dez, onze (11), doze (12), 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69 ou 70 ou mais ou todas as seguintes alterações com base na SEQ ID NO: 1:
[0009] os nucleotídeos nas posições 4 a 6 são AAT ou AAC,
[00010] os nucleotídeos nas posições 37 a 39 são AAT ou AAC,
[00011] os nucleotídeos nas posições 112 a 114 são TAT ou TAC,
[00012] os nucleotídeos nas posições 169 a 171 são GAT ou GAC,
[00013] os nucleotídeos nas posições 181 a 183 são CAA ou CAG,
[00014] os nucleotídeos nas posições 181 a 183 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00015] os nucleotídeos nas posições 184 a 186 são ACT, ACC, ACA ou ACG,
[00016] os nucleotídeos nas posições 187 a 189 são CAT ou CAC,
[00017] os nucleotídeos nas posições 187 a 189 são ACT, ACC, ACA ou ACG,
[00018] os nucleotídeos nas posições 205 a 207 são GAA ou GAG,
[00019] os nucleotídeos nas posições 205 a 207 são CAT ou CAC,
[00020] os nucleotídeos nas posições 205 a 207 são CAA ou CAG,
[00021] os nucleotídeos nas posições 205 a 207 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00022] os nucleotídeos nas posições 205 a 207 são TAT ou TAC,
[00023] os nucleotídeos nas posições 208 a 210 são CCA, CCC, CCG ou CCT,
[00024] os nucleotídeos nas posições 211 a 213 são GCT, GCC, GCA ou GCG,
[00025] os nucleotídeos nas posições 211 a 213 são GAA ou GAG,
[00026] os nucleotídeos nas posições 211 a 213 são CCA, CCC, CCG ou CCT,
[00027] os nucleotídeos nas posições 211 a 213 são CAA ou CAG,
[00028] os nucleotídeos nas posições 211 a 213 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00029] os nucleotídeos nas posições 211 a 213 são ACT, ACC, ACA ou ACG,
[00030] os nucleotídeos nas posições 220 a 222 são GAA ou GAG,
[00031] os nucleotídeos nas posições 220 a 222 são TTA, TTG, CTT, CTC, CTA ou CTG,
[00032] os nucleotídeos nas posições 220 a 222 são ATG,
[00033] os nucleotídeos nas posições 280 a 282 são CAA ou CAG,
[00034] os nucleotídeos nas posições 301 a 303 são TAT ou TAC,
[00035] os nucleotídeos nas posições 307 a 309 são TGT ou TGC,
[00036] os nucleotídeos nas posições 307 a 309 são CAA ou CAG,
[00037] os nucleotídeos nas posições 316 a 318 são GGT, GGC, GGA ou GGG,
[00038] os nucleotídeos nas posições 325 a 327 são TTA, TTG, CTT, CTC, CTA ou CTG,
[00039] os nucleotídeos nas posições 346 a 348 são GCT, GCC, GCA ou GCG,
[00040] os nucleotídeos nas posições 346 a 348 são CGT, CGC, CGA, CGG, AGA ou AGG,
[00041] os nucleotídeos nas posições 388 a 390 são TAT ou TAC,
[00042] os nucleotídeos nas posições 391 a 393 são TTA, TTG, CTT, CTC, CTA ou CTG,
[00043] os nucleotídeos nas posições 442 a 444 são CAT ou CAC,
[00044] os nucleotídeos nas posições 484 a 486 são CAA ou CAG,
[00045] os nucleotídeos nas posições 496 a 498 são GCT, GCC, GCA ou GCG,
[00046] os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG,
[00047] os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG,
[00048] os nucleotídeos nas posições 547 a 549 são GTT, GTC, GTA ou GTG,
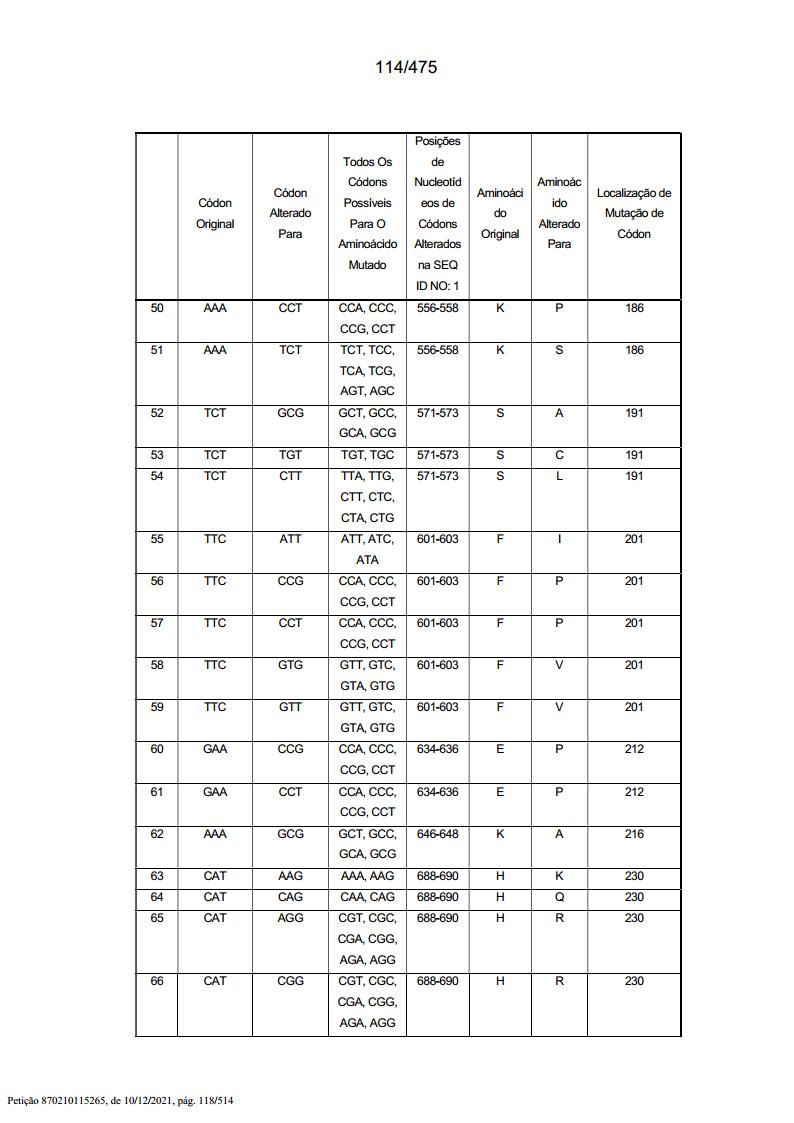
[00049] os nucleotídeos nas posições 556 a 558 são GCT, GCC, GCA ou GCG,
[00050] os nucleotídeos nas posições 556 a 558 são GAT ou GAC,
[00051] os nucleotídeos nas posições 556 a 558 são CCA, CCC, CCG ou CCT,
[00052] os nucleotídeos nas posições 556 a 558 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00053] os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG,
[00054] os nucleotídeos nas posições 571 a 573 são TGT ou TGC,
[00055] os nucleotídeos nas posições 571 a 573 são TTA, TTG, CTT, CTC, CTA ou CTG,
[00056] os nucleotídeos nas posições 601 a 603 são ATT, ATC ou ATA,
[00057] os nucleotídeos nas posições 601 a 603 são CCA, CCC, CCG ou CCT,
[00058] os nucleotídeos nas posições 601 a 603 são GTT, GTC, GTA ou GTG,
[00059] os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT,
[00060] os nucleotídeos nas posições 646 a 648 são GCT, GCC, GCA ou GCG,
[00061] os nucleotídeos nas posições 688 a 690 são AAA ou AAG,
[00062] os nucleotídeos nas posições 688 a 690 são CAA ou CAG,
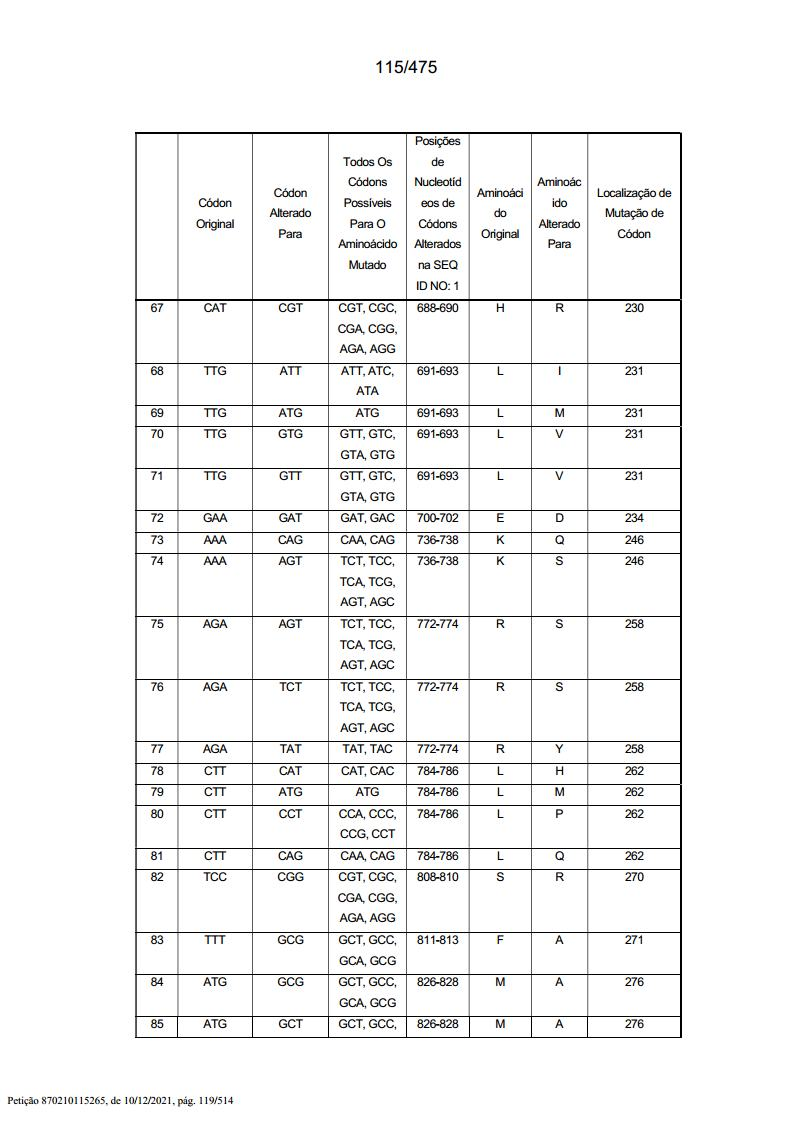
[00063] os nucleotídeos nas posições 688 a 690 são CGT, CGC, CGA, CGG, AGA ou AGG,
[00064] os nucleotídeos nas posições 691 a 693 são ATT, ATC ou ATA,
[00065] os nucleotídeos nas posições 691 a 693 são ATG,
[00066] os nucleotídeos nas posições 691 a 693 são GTT, GTC, GTA ou GTG,
[00067] os nucleotídeos nas posições 700 a 702 são GAT ou GAC,
[00068] os nucleotídeos nas posições 736 a 738 são CAA ou CAG,
[00069] os nucleotídeos nas posições 736 a 738 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00070] os nucleotídeos nas posições 772 a 774 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00071] os nucleotídeos nas posições 772 a 774 são TAT ou TAC,
[00072] os nucleotídeos nas posições 784 a 786 são CAT ou CAC,
[00073] os nucleotídeos nas posições 784 a 786 são ATG,
[00074] os nucleotídeos nas posições 784 a 786 são CCA, CCC,CCG ou CCT,
[00075] os nucleotídeos nas posições 784 a 786 são CAA ou CAG,
[00076] os nucleotídeos nas posições 808 a 810 são CGT, CGC, CGA, CGG, AGA ou AGG,
[00077] os nucleotídeos nas posições 811 a 813 são GCT, GCC, GCA ou GCG,
[00078] os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG,
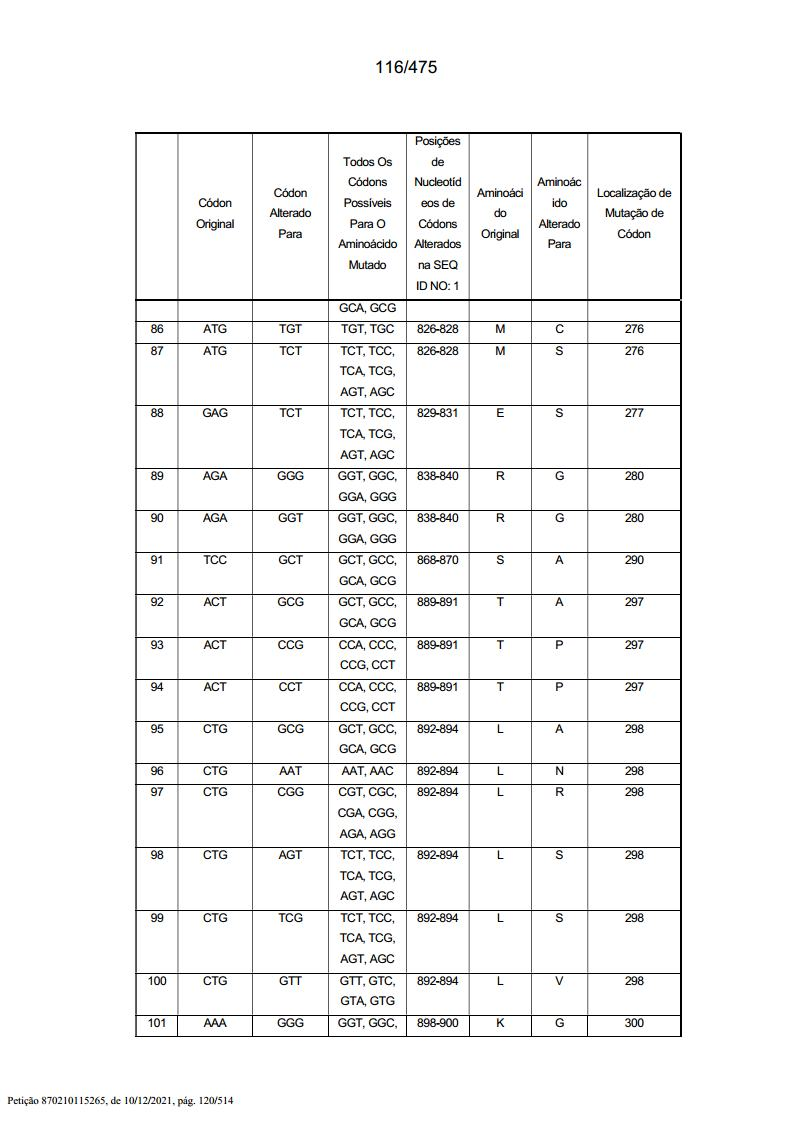
[00079] os nucleotídeos nas posições 826 a 828 são TGT ou TGC,
[00080] os nucleotídeos nas posições 826 a 828 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00081] os nucleotídeos nas posições 829 a 831 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00082] os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG,
[00083] os nucleotídeos nas posições 868 a 870 são GCT, GCC, GCA ou GCG,
[00084] os nucleotídeos nas posições 889 a 891 são GCT, GCC, GCA ou GCG,
[00085] os nucleotídeos nas posições 889 a 891 são CCA, CCC, CCG ou CCT,
[00086] os nucleotídeos nas posições 892 a 894 são GCT, GCC, GCA ou GCG,
[00087] os nucleotídeos nas posições 892 a 894 são AAT ou AAC,
[00088] os nucleotídeos nas posições 892 a 894 são CGT, CGC, CGA, CGG, AGA ou AGG,
[00089] os nucleotídeos nas posições 892 a 894 são TCT, TCC, TCA, TCG, AGT ou AGC,
[00090] os nucleotídeos nas posições 892 a 894 são GTT, GTC, GTA ou GTG,
[00091] os nucleotídeos nas posições 898 a 900 são GGT, GGC, GGA ou GGG,
[00092] os nucleotídeos nas posições 901 a 903 são CAA ou CAG,
[00093] os nucleotídeos nas posições 913 a 915 são CCA, CCC, CCG ou CCT,
[00094] os nucleotídeos nas posições 934 a 936 são ATT, ATC ou ATA, e/ou
[00095] os nucleotídeos nas posições 943 a 945 são ATT, ATC ou ATA.
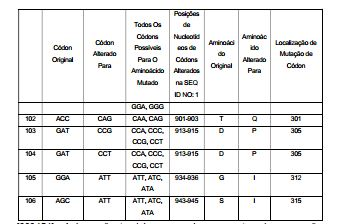
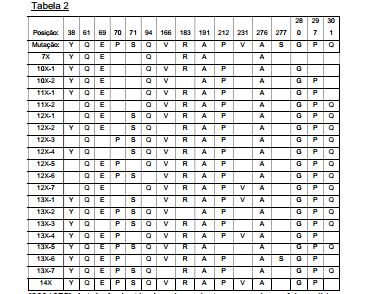
[00096] Todas estas sequências são sequências exemplares da invenção tendo alterações de resíduos específicas para a SEQ ID NO: 1 “parental”, resumidas (em parte) nas Tabelas 1 e 2, abaixo (a Tabela 2 está no Exemplo 5).
[00097] Em um aspecto, um ácido nucleico da invenção codifica pelo menos um polipeptídeo ou peptídeo tendo uma atividade de glucanase, por exemplo, uma atividade de endoglucanase, uma atividade de xilanase, ou uma atividade de mananase, ou um ácido nucleico da invenção codifica pelo menos um polipeptídeo ou peptídeo capaz de provocar uma reação imune, por exemplo, epitopos capazes de provocar uma reação imune humoral (de anticorpo) ou celular específica para um polipeptídeo exemplar da invenção. Em um aspecto, as identidades das sequências são determinadas por análise com um algoritmo de comparação de sequências ou por uma inspeção visual.
[00098] Em um aspecto, a invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes compreendendo uma modificação da sequência de ácido nucleico de SEQ ID NO: 1, em que a modificação compreende, ou alternativamente - consiste em, uma, duas, três, quatro, cinco, seis, sete, oito, nove, dez, onze (11), doze (12), 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69 ou 70 ou mais ou todas as seguintes alterações:
[00099] os nucleotídeos nas posições 4 a 6 são AAT ou AAC,
[000100] os nucleotídeos nas posições 37 a 39 são AAT ou AAC,
[000101] os nucleotídeos nas posições 112 a 114 são TAT ou TAC,
[000102] os nucleotídeos nas posições 169 a 171 são GAT ou GAC,
[000103] os nucleotídeos nas posições 181 a 183 são CAA ou CAG,
[000104] os nucleotídeos nas posições 181 a 183 são TCT, TCC,TCA, TCG, AGT ou AGC,
[000105] os nucleotídeos nas posições 184 a 186 são ACT, ACC, ACA ou ACG,
[000106] os nucleotídeos nas posições 187 a 189 são CAT ou CAC,
[000107] os nucleotídeos nas posições 187 a 189 são ACT, ACC, ACA ou ACG,
[000108] os nucleotídeos nas posições 205 a 207 são GAA ou GAG,
[000109] os nucleotídeos nas posições 205 a 207 são CAT ou CAC,
[000110] os nucleotídeos nas posições 205 a 207 são CAA ou CAG,
[000111] os nucleotídeos nas posições 205 a 207 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000112] os nucleotídeos nas posições 205 a 207 são TAT ou TAC,
[000113] os nucleotídeos nas posições 208 a 210 são CCA, CCC, CCG ou CCT,
[000114] os nucleotídeos nas posições 211 a 213 são GCT, GCC, GCA ou GCG,
[000115] os nucleotídeos nas posições 211 a 213 são GAA ou GAG,
[000116] os nucleotídeos nas posições 211 a 213 são CCA, CCC, CCG ou CCT,
[000117] os nucleotídeos nas posições 211 a 213 são CAA ou CAG,
[000118] os nucleotídeos nas posições 211 a 213 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000119] os nucleotídeos nas posições 211 a 213 são ACT, ACC, ACA ou ACG,
[000120] os nucleotídeos nas posições 220 a 222 são GAA ou GAG,
[000121] os nucleotídeos nas posições 220 a 222 são TTA, TTG, CTT, CTC, CTA ou CTG,
[000122] os nucleotídeos nas posições 220 a 222 são ATG,
[000123] os nucleotídeos nas posições 280 a 282 são CAA ou CAG,
[000124] os nucleotídeos nas posições 301 a 303 são TAT ou TAC,
[000125] os nucleotídeos nas posições 307 a 309 são TGT ou TGC,
[000126] os nucleotídeos nas posições 307 a 309 são CAA ou CAG,
[000127] os nucleotídeos nas posições 316 a 318 são GGT, GGC, GGA ou GGG,
[000128] os nucleotídeos nas posições 325 a 327 são TTA, TTG, CTT, CTC, CTA ou CTG,
[000129] os nucleotídeos nas posições 346 a 348 são GCT, GCC, GCA ou GCG,
[000130] os nucleotídeos nas posições 346 a 348 são CGT, CGC, CGA, CGG, AGA ou AGG,
[000131] os nucleotídeos nas posições 388 a 390 são TAT ou TAC,
[000132] os nucleotídeos nas posições 391 a 393 são TTA, TTG, CTT, CTC, CTA ou CTG,
[000133] os nucleotídeos nas posições 442 a 444 são CAT ou CAC,
[000134] os nucleotídeos nas posições 484 a 486 são CAA ou CAG,
[000135] os nucleotídeos nas posições 496 a 498 são GCT, GCC, GCA ou GCG,
[000136] os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG,
[000137] os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG,
[000138] os nucleotídeos nas posições 547 a 549 são GTT, GTC, GTA ou GTG,
[000139] os nucleotídeos nas posições 556 a 558 são GCT, GCC, GCA ou GCG,
[000140] os nucleotídeos nas posições 556 a 558 são GAT ou GAC,
[000141] os nucleotídeos nas posições 556 a 558 são CCA, CCC, CCG ou CCT,
[000142] os nucleotídeos nas posições 556 a 558 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000143] os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG,
[000144] os nucleotídeos nas posições 571 a 573 são TGT ou TGC,
[000145] os nucleotídeos nas posições 571 a 573 são TTA, TTG, CTT, CTC, CTA ou CTG,
[000146] os nucleotídeos nas posições 601 a 603 são ATT, ATC ou ATA,
[000147] os nucleotídeos nas posições 601 a 603 são CCA, CCC, CCG ou CCT,
[000148] os nucleotídeos nas posições 601 a 603 são GTT, GTC, GTA ou GTG,
[000149] os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT,
[000150] os nucleotídeos nas posições 646 a 648 são GCT, GCC, GCA ou GCG,
[000151] os nucleotídeos nas posições 688 a 690 são AAA ou AAG,
[000152] os nucleotídeos nas posições 688 a 690 são CAA ou CAG,
[000153] os nucleotídeos nas posições 688 a 690 são CGT, CGC, CGA, CGG, AGA ou AGG,
[000154] os nucleotídeos nas posições 691 a 693 são ATT, ATC ou ATA,
[000155] os nucleotídeos nas posições 691 a 693 são ATG,
[000156] os nucleotídeos nas posições 691 a 693 são GTT, GTC, GTA ou GTG,
[000157] os nucleotídeos nas posições 700 a 702 são GAT ou GAC,
[000158] os nucleotídeos nas posições 736 a 738 são CAA ou CAG,
[000159] os nucleotídeos nas posições 736 a 738 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000160] os nucleotídeos nas posições 772 a 774 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000161] os nucleotídeos nas posições 772 a 774 são TAT ou TAC,
[000162] os nucleotídeos nas posições 784 a 786 são CAT ou CAC,
[000163] os nucleotídeos nas posições 784 a 786 são ATG,
[000164] os nucleotídeos nas posições 784 a 786 são CCA, CCC,CCG ou CCT,
[000165] os nucleotídeos nas posições 784 a 786 são CAA ou CAG,
[000166] os nucleotídeos nas posições 808 a 810 são CGT, CGC, CGA, CGG, AGA ou AGG,
[000167] os nucleotídeos nas posições 811 a 813 são GCT, GCC, GCA ou GCG,
[000168] os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG,
[000169] os nucleotídeos nas posições 826 a 828 são TGT ou TGC,
[000170] os nucleotídeos nas posições 826 a 828 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000171] os nucleotídeos nas posições 829 a 831 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000172] os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG,
[000173] os nucleotídeos nas posições 868 a 870 são GCT, GCC, GCA ou GCG,
[000174] os nucleotídeos nas posições 889 a 891 são GCT, GCC, GCA ou GCG,
[000175] os nucleotídeos nas posições 889 a 891 são CCA, CCC, CCG ou CCT,
[000176] os nucleotídeos nas posições 892 a 894 são GCT, GCC, GCA ou GCG,
[000177] os nucleotídeos nas posições 892 a 894 são AAT ou AAC,
[000178] os nucleotídeos nas posições 892 a 894 são CGT, CGC, CGA, CGG, AGA ou AGG,
[000179] os nucleotídeos nas posições 892 a 894 são TCT, TCC, TCA, TCG, AGT ou AGC,
[000180] os nucleotídeos nas posições 892 a 894 são GTT, GTC, GTA ou GTG,
[000181] os nucleotídeos nas posições 898 a 900 são GGT, GGC, GGA ou GGG,
[000182] os nucleotídeos nas posições 901 a 903 são CAA ou CAG,
[000183] os nucleotídeos nas posições 913 a 915 são CCA, CCC, CCG ou CCT,
[000184] os nucleotídeos nas posições 934 a 936 são ATT, ATC ou ATA, e/ou
[000185] os nucleotídeos nas posições 943 a 945 são ATT, ATC ou ATA.
[000186] Todas estas sequências são sequências exemplares da invenção tendo alterações de resíduos específicas para a SEQ ID NO: 1 “parental”, resumidas (em parte) nas Tabelas 1 e 2, abaixo (a Tabela 2 está no Exemplo 5).
[000187] Ácidos nucleicos exemplares da invenção também incluem ácidos nucleicos isolados, sintéticos ou recombinantes codificando um polipeptídeo da invenção, por exemplo, um polipeptídeo tendo uma sequência conforme determinado na SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, e SEQ ID NO: 23, subsequências das mesmas e/ou variantes das mesmas, por exemplo, polipeptídeos codificados pelas sequências da invenção de ácidos nucleicos da invenção, incluindo as modificações das sequências de ácido nucleico de SEQ ID NO: 1, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e SEQ ID NO: 22, conforme descrito aqui, neste pedido de patente. Em um aspecto, o polipeptídeo tem uma atividade de glucanase, por exemplo, atividade de endoglucanase, por exemplo, catalisando hidrólise de ligações de endo- β-1,4- e/ou 1,3- glucanase internas, uma atividade de xilanase, e/ou uma atividade de mananase.
[000188] Em um aspecto, o algoritmo de comparação de sequências é um algoritmo BLAST versão 2.2.2 onde uma situação de filtragem é ajustada para blastall -p blastp -d "nr pataa" -F F, e todas as outras opções são ajustadas por definição, ou uma ou Versão FASTA 3.0t78, com parâmetros definidos.
[000189] Outro aspecto da invenção é um ácido nucleico isolado, sintético ou recombinante compreendendo, ou consistindo em, pelo menos 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200 ou mais bases consecutivas de uma sequência de ácido nucleico da invenção, sequências substancialmente idênticas a essa, e as sequências complementares a essas; e em um aspecto o ácido nucleico codifica uma proteína ou peptídeo tendo uma atividade de glucanase. Em um aspecto, a atividade de glucanase de um polipeptídeo ou peptídeo da invenção (o qual inclui uma proteína ou peptídeo codificado por um ácido nucleico da invenção) compreende uma atividade de endoglucanase, por exemplo, atividade de endo-1,4- e/ou 1,3-beta-D-glucan 4-glucano hidrolase. Em um aspecto, a atividade de endoglucanase compreende catalisar hidrólise de ligações 1,4-beta-D-glicosídicas. Em um aspecto, a atividade de glucanase, por exemplo, endoglucanase, compreende uma atividade de endo-1,4- e/ou 1,3-beta-endoglucanase ou atividade de endo-β-1,4-glucanase. Em um aspecto, a atividade de glucanase (por exemplo, atividade de endo-1,4-beta-D-glucan 4-glucano hidrolase) compreende hidrólise de ligações 1,4-beta-D-glicosídicas em celulose, derivados celulósicos (por exemplo, carbóxi metila celulose e hidróxi etil celulose) liquenina, ligações beta-1,4 em glucanos beta-1,3 mistos, tais como beta-D-glucanos de cereais e outro material vegetal contendo partes celulósicas.
[000190] Em um aspecto, a atividade de glucanase, xilanase, ou mananase compreende hidrolisar um glucano, manano, arabinoxilano ou xilano, ou outro polissacarídeo para produzir um polissacarídeo ou oligômero de menor peso molecular. Em um aspecto, o glucano compreende um beta-glucano, tal como um beta-glucano hidrossolúvel. O beta-glucano hidrossolúvel pode compreender uma massa ou um produto de pão.
[000191] Em um aspecto, a atividade de glucanase compreende hidrolisar polissacarídeos compreendendo D-glucopiranoses ligadas a 1,4-β-glicosideos. Em um aspecto, a atividade de glucanase compreende hidrolisar celulose. Em um aspecto, a atividade de glucanase compreende hidrolisar celulose em uma madeira ou polpa de papel ou um produto de papel.
[000192] Em um aspecto, a atividade de glucanase, por exemplo, endoglucanase, compreende catalisar hidrólise de glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos em uma bebida ou uma ração, por exemplo, uma ração animal, tal como uma ração de animal monogástrico, por exemplo, uma ração de suíno ou aves domésticas (por exemplo, galinha), ou um produto alimentício. A bebida, a ração ou o produto alimentício pode compreender uma ração animal à base de cereais, um mosto ou uma cerveja, um fruto ou um legume. Em um aspecto, a invenção proporciona um alimento, ração (por exemplo, uma ração animal, tal como uma ração de animal monogástrico, por exemplo, para suíno ou aves domésticas), um líquido, por exemplo, uma bebida (tal como um suco de frutas ou uma cerveja) ou um precursor de bebida (por exemplo, um mosto ), compreendendo um polipeptídeo da invenção. O alimento pode ser uma massa de pão ou um produto de pão. A bebida ou um precursor de bebida pode ser um suco de frutas, uma cerveja ou um mosto. Em um aspecto, a invenção proporciona métodos para a clarificação de um líquido, por exemplo, um suco, tal como um suco de frutas, ou uma cerveja, tratando o líquido com uma enzima da invenção.Em um aspecto, a invenção proporciona métodos de condicionamento de massa compreendendo contatar uma massa ou um produto de pão com pelo menos um polipeptídeo da invenção sob condições suficientes para condicionar a massa. Em um aspecto, a invenção proporciona métodos de produção de bebida compreendendo administração de pelo menos um polipeptídeo da invenção a uma bebida ou um precursor de bebida sob condições suficientes para reduzir a viscosidade da bebida.
[000193] Em um aspecto, a atividade de glucanase, por exemplo, endoglucanase, compreende catalisar hidrólise de glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos em uma célula, por exemplo, uma célula de planta ou uma célula microbiana.
[000194] Em um aspecto, o ácido nucleico isolado, sintético ou recombinante codifica um polipeptídeo tendo uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase que é termoestável. Por exemplo, um polipeptídeo da invenção, por exemplo, por exemplo, as enzimas variantes ou originadas da invenção, por exemplo, as variações específicas para SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, E SEQ ID NO: 23, conforme determinado nas Tabelas 1 e 2 (a Tabela 2 está no Exemplo 5), podem ser termoestáveis. O polipeptídeo termoestável de acordo com a invenção pode reter atividade de ligação e/ou enzimática, por exemplo, uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, sob condições compreendendo uma faixa de temperatura a partir de cerca de -100°C a cerca de -80°C, cerca de -80°C a cerca de -40°C, cerca de -40°C a cerca de -20°C, cerca de -20°C a cerca de 0°C, cerca de 0°C a cerca de 37°C, cerca de 0°C a cerca de 5°C, cerca de 5°C a cerca de 15°C, cerca de 15°C a cerca de 25°C, cerca de 25°C a cerca de 37°C, cerca de 37°C a cerca de 45°C, cerca de 45°C a cerca de 55°C, cerca de 55°C a cerca de 70°C, cerca de 70°C a cerca de 75°C, cerca de 75°C a cerca de 85°C, cerca de 85°C a cerca de 90°C, cerca de 90°C a cerca de 95°C, cerca de 95°C a cerca de 100°C, cerca de 100°C a cerca de 105°C, cerca de 105°C a cerca de 110°C, cerca de 110°C a cerca de 120°C, ou 95°C, 96°C, 97°C, 98°C, 99°C, 100°C, 101°C, 102°C, 103°C, 104°C, 105°C, 106°C, 107°C, 108°C, 109°C, 110°C, 111°C, 112°C, 113°C, 114°C, 115°C ou mais. Os polipeptídeos termoestáveis de acordo com a invenção podem reter atividade, por exemplo, uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, em temperaturas na faixa a partir de cerca de -100°C a cerca de -80°C, cerca de -80°C a cerca de -40°C, cerca de -40°C a cerca de -20°C, cerca de -20°C a cerca de 0°C, cerca de 0°C a cerca de 5°C, cerca de 5°C a cerca de 15°C, cerca de 15°C a cerca de 25°C, cerca de 25°C a cerca de 37°C, cerca de 37°C a cerca de 45°C, cerca de 45°C a cerca de 55°C, cerca de 55°C a cerca de 70°C, cerca de 70°C a cerca de 75°C, cerca de 75°C a cerca de 85°C, cerca de 85°C a cerca de 90°C, cerca de 90°C a cerca de 95°C, cerca de 95°C a cerca de 100°C, cerca de 100°C a cerca de 105°C, cerca de 105°C a cerca de 110°C, cerca de 110°C a cerca de 120°C, ou 95°C, 96°C, 97°C, 98°C, 99°C, 100°C, 101°C, 102°C, 103°C, 104°C, 105°C, 106°C, 107°C, 108°C, 109°C, 110°C, 111°C, 112°C, 113°C, 114°C, 115°C ou mais. Em algumas modalidades, os polipeptídeos termoestáveis de acordo com a invenção retêm atividade, por exemplo, uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, em uma temperatura nas faixas descritas acima, em cerca de pH 3,0, cerca de pH 3,5, cerca de pH 4,0, cerca de pH 4,5, cerca de pH 5,0, cerca de pH 5,5, cerca de pH 6,0, cerca de pH 6,5, cerca de pH 7,0, cerca de pH 7,5, cerca de pH 8,0, cerca de pH 8,5, cerca de pH 9,0, cerca de pH 9,5, cerca de pH 10,0, cerca de pH 10,5, cerca de pH 11,0, cerca de pH 11,5, cerca de pH 12,0 ou mais.
[000195] Em outro aspecto, o ácido nucleico isolado, sintético ou recombinante codifica um polipeptídeo tendo uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase que é termotolerante. Por exemplo, um polipeptídeo da invenção, por exemplo, as enzimas variantes ou originadas da invenção, por exemplo, as variações específicas para SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, E SEQ ID NO: 23, conforme determinado nas Tabelas 1 e 2 (a Tabela 2 está no Exemplo 5), podem ser termotolerantes ou termoativas. Os polipeptídeos termotolerantes de acordo com a invenção podem reter atividade de ligação e/ou enzimática, por exemplo, uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, depois de exposição a condições compreendendo uma temperatura na faixa a partir de cerca de -100°C a cerca de -80°C, cerca de -80°C a cerca de -40°C, cerca de -40°C a cerca de -20°C, cerca de -20°C a cerca de 0°C, cerca de 0°C a cerca de 5°C, cerca de 5°C a cerca de 15°C, cerca de 15°C a cerca de 25°C, cerca de 25°C a cerca de 37°C, cerca de 37°C a cerca de 45°C, cerca de 45°C a cerca de 55°C, cerca de 55°C a cerca de 70°C, cerca de 70°C a cerca de 75°C, cerca de 75°C a cerca de 85°C, cerca de 85°C a cerca de 90°C, cerca de 90°C a cerca de 95°C, cerca de 95°C a cerca de 100°C, cerca de 100°C a cerca de 105°C, cerca de 105°C a cerca de 110°C, cerca de 110°C a cerca de 120°C, ou 95°C, 96°C, 97°C, 98°C, 99°C, 100°C, 101°C, 102°C, 103°C, 104°C, 105°C, 106°C, 107°C, 108°C, 109°C, 110°C, 111°C, 112°C, 113°C, 114°C, 115°C ou mais. Os polipeptídeos termotolerantes de acordo com a invenção podem reter atividade, por exemplo, uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, depois de exposição a uma temperatura na faixa a partir de cerca de -100°C a cerca de -80°C, cerca de -80°C a cerca de -40°C, cerca de -40°C a cerca de -20°C, cerca de -20°C a cerca de 0°C, cerca de 0°C a cerca de 5°C, cerca de 5°C a cerca de 15°C, cerca de 15°C a cerca de 25°C, cerca de 25°C a cerca de 37°C, cerca de 37°C a cerca de 45°C, cerca de 45°C a cerca de 55°C, cerca de 55°C a cerca de 70°C, cerca de 70°C a cerca de 75°C, cerca de 75°C a cerca de 85°C, cerca de 85°C a cerca de 90°C, cerca de 90°C a cerca de 95°C, cerca de 95°C a cerca de 100°C, cerca de 100°C a cerca de 105°C, cerca de 105°C a cerca de 110°C, cerca de 110°C a cerca de 120°C, ou 95°C, 96°C, 97°C, 98°C, 99°C, 100°C, 101°C, 102°C, 103°C, 104°C, 105°C, 106°C, 107°C, 108°C, 109°C, 110°C, 111°C, 112°C, 113°C, 114°C, 115°C ou mais. Em algumas modalidades, os polipeptídeos termotolerantes de acordo com a invenção retêm atividade, por exemplo, uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, depois de exposição a uma temperatura nas faixas descritas acima, em cerca de pH 3,0, cerca de pH 3,5, cerca de pH 4,0, cerca de pH 4,5, cerca depH 5,0, cerca de pH 5,5, cerca de pH 6,0, cerca de pH 6,5, cerca de pH 7,0, cerca de pH 7,5, cerca de pH 8,0, cerca de pH 8,5, cerca de pH 9,0, cerca de pH 9,5, cerca de pH 10,0, cerca de pH 10,5, cerca de pH 11,0, cerca de pH 11,5, cerca de pH 12,0 ou mais. Em um aspecto, o polipeptídeo retem glucanase ou outra atividade depois de exposição a uma temperatura na faixa de mais de 90°C a cerca de 95°C em pH 4,5.
[000196] A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes compreendendo uma sequência que hibridiza sob condições estringentes a um ácido nucleico compreendendo uma sequência da invenção, por exemplo, a sequência de SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e SEQ ID NO: 22 ou fragmentos ou subsequências das mesmas; e em um aspecto esta sequência tem pelo menos uma, ou várias ou todas as modificações de sequências para SEQ ID NO: 1 (ou modificações equivalentes), conforme descrito aqui, neste pedido de patente. Em um aspecto, o ácido nucleico codifica um polipeptídeo tendo uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase. O ácido nucleico pode ter pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200 ou mais resíduos de extensão ou toda a extensão do gene ou transcripto. Em um aspecto, as condições estringentes incluem uma etapa de lavagem compreendendo uma lavagem em 0,2X SSC em uma temperatura de cerca de 65oC por cerca de 15 minutos.
[000197] A invenção proporciona uma sonda de ácido nucleico para identificação, isolamento, clonagem, amplificação ou sequenciamento de um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, em que a sonda compreende pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000 ou mais, bases consecutivas de uma sequência compreendendo uma sequência da invenção, ou fragmentos ou subsequências das mesmas (os quais incluem ambas as fitas, de senso e anti-senso, por exemplo, incluindo sequências totalmente complementares a SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, E SEQ ID NO: 22, e as modificações exemplares determinadas aqui, neste pedido de patente), em que a sonda identifica o ácido nucleico por ligação ou hibridização. A sonda pode compreender um oligonucleotídeo compreendendo entre cerca de 10 a 100 bases consecutivas de uma sequência de acordo com a invenção, ou fragmentos ou subsequências das mesmas, por exemplo, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 ou 100 bases ou mais, ou, qualquer extensão desejada no intervalo.
[000198] A invenção proporciona uma sonda de ácido nucleico para identificar um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, por exemplo, endoglucanase, uma xilanase, ou uma mananase, em que a sonda compreende, ou consiste em, um ácido nucleico compreendendo uma sequência pelo menos cerca de 10, 15, 20, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000 ou mais resíduos tendo pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) com um ácido nucleico da invenção, por exemplo, SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, E SEQ ID NO: 22, ou um ácido nucleico compreendendo uma modificação de sequência de SEQ ID NO: 1, conforme determinado aqui, neste pedido de patente, (por exemplo, SEQ ID NO: 3), em que as identidades das sequências são determinadas por análise com um algoritmo de comparação de sequências (por exemplo, BLAST ou FASTA) ou por inspeção visual. Outro aspecto da invenção é uma sonda de polinucleotídeo para isolamento ou identificação de glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, genes de celobio-hidrolase, mananase e/ou beta-glucosidase tendo uma sequência a qual é a mesma que, ou totalmente complementar a pelo menos uma sequência de ácido nucleico da invenção.
[000199] A invenção proporciona um par de iniciadores de amplificação para amplificar um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, em que o par de iniciadores é capaz de amplificar um ácido nucleico compreendendo uma sequência da invenção, ou fragmentos ou subsequências das mesmas. Um ou cada membro do par da sequência de iniciadores de amplificação podem compreender um oligonucleotídeo compreendendo pelo menos cerca de 10 a 50 ou mais bases consecutivas da sequência, ou cerca de 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 ou 35 ou mais bases consecutivas da sequência.
[000200] A invenção proporciona pares de iniciadores de amplificação, em que o par de iniciadores compreende um primeiro membro tendo uma sequência conforme determinado por cerca dos primeiros (os 5’) 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 ou 35 ou mais resíduos de um ácido nucleico da invenção, e um segundo membro tendo uma sequência conforme determinado por cerca dos primeiros (os 5’) 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 ou 35 ou mais resíduos da fita complementar do primeiro membro.
[000201] A invenção proporciona ácidos nucleicos codificando glucanase, por exemplo, codificando endoglucanase, codificando xilanase, ou codificando mananase gerados por amplificação, por exemplo, reação de cadeia polimerase (PCR), usando um par de iniciadores de amplificação da invenção. A invenção proporciona glucanases (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases geradas por amplificação, por exemplo, reação de cadeia polimerase (PCR), usando um par de iniciadores de amplificação da invenção. A invenção proporciona métodos para produzir glucanases (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases por amplificação, por exemplo, reação de cadeia polimerase (PCR), usando um par de iniciadores de amplificação da invenção. Em um aspecto, o par de iniciadores de amplificação amplifica um ácido nucleico de uma biblioteca, por exemplo, uma biblioteca genética, tal como uma biblioteca ambiental.
[000202] A invenção proporciona métodos para amplificar um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, por exemplo, endoglucanase, uma mananase, ou uma xilanase compreendendo amplificação de um ácido nucleico molde com um par de sequências de iniciadores de amplificação capaz de amplificar uma sequência de ácido nucleico da invenção, ou fragmentos ou subsequências das mesmas.
[000203] A invenção proporciona cassetes de expressão compreendendo um ácido nucleico da invenção ou uma subsequência do mesmo. Em um aspecto, o cassete de expressão pode compreender o ácido nucleico que é ligado operacionalmente a um promotor. Opcionalmente, o promotor pode ser um promotor fúngico, de levedura, viral, bacteriano, mamífero, de planta, sintético ou híbrido. O promotor pode ser um promotor constitutivo. Em outro aspecto, o promotor pode ser um promotor indutível. Em um aspecto, o promotor pode ser um promotor tecido-específico ou um promotor regulado ambientalmente ou um regulado pelo desenvolvimento. Em um aspecto, o cassete de expressão pode compreender adicionalmente um vetor de expressão de planta ou de vírus de planta.
[000204] A invenção proporciona veículos de clonagem compreendendo um cassete de expressão (por exemplo, um vetor) da invenção ou um ácido nucleico da invenção. O veículo de clonagem pode ser um vetor viral, um plasmídeo, um fago, um fagomídeo, um cosmídeo, um fosmídeo, um bacteriófago ou um cromossoma artificial. O vetor viral pode compreender um vetor de adenovírus, um vetor retroviral ou um vetor viral adeno-associado. O veículo de clonagem pode compreender um cromossoma artificial bacteriano (BAC), um plasmídeo, um vetor derivado de bacteriófago P1 (PAC), um cromossoma artificial de levedura (YAC), ou um cromossoma artificial de mamífero (MAC).
[000205] A invenção proporciona célula transformada compreendendo um ácido nucleico da invenção ou um cassete de expressão (por exemplo, um vetor) da invenção, ou um veículo de clonagem da invenção. Em um aspecto, a célula transformada pode ser uma célula bacteriana, uma célula de mamífero, uma célula fúngica, uma célula de levedura, uma célula de inseto ou uma célula de planta. Em um aspecto, a célula de planta pode ser de qualquer planta, por exemplo, plantas usadas para forragem e/ou ração para qualquer animal, incluindo ruminantes, ou como uma fonte de matéria- prima para produzir energia ou combustível. Plantas de particular interesse podem incluir plantas de safras e plantas de matéria-prima, por exemplo, milho, alfafa, girassol, Brassica, soja, algodão, açafrão, amendoim, sorgo, trigo, aveia, centeio, milheto, cevada, arroz, coníferas, gramíneas, por exemplo, switchgrass e Miscanthus, colheitas de leguminosas, por exemplo, ervilha, feijão e soja, tubérculos/raízes amiláceas, por exemplo, batata, batata-doce, mandioca, inhame, cana e beterraba açucareira e similares.
[000206] A invenção proporciona animais não-humanos transgênicos compreendendo um ácido nucleico da invenção ou um cassete de expressão (por exemplo, um vetor) da invenção. Em um aspecto, o animal é um camundongo, um rato, uma cabra, um coelho, um carneiro, um porco, uma vaca, ou qualquer mamífero.
[000207] A invenção proporciona plantas transgênicas compreendendo um ácido nucleico da invenção ou um cassete de expressão (por exemplo, um vetor) da invenção. A planta transgênica pode ser qualquer planta, mas em uma modalidade a planta seria usada para forragem e/ou ração para qualquer animal ou como uma matéria-prima para produzir energia ou combustível, tal como, milho, alfafa, girassol, Brassica, soja, algodão, açafrão, amendoim, sorgo, trigo, aveia, centeio, milheto, cevada, arroz, coníferas, gramíneas, por exemplo, switchgrass e Miscanthus, colheitas de leguminosas, por exemplo, ervilha, feijão e soja, tubérculos/raízes amiláceas, por exemplo, batata, batata-doce, mandioca, inhame, cana e beterraba açucareira e similares.
[000208] A invenção proporciona sementes transgênicas compreendendo um ácido nucleico da invenção ou um cassete de expressão (por exemplo, um vetor) da invenção. A semente transgênica pode ser de qualquer planta, mas em uma modalidade a planta seria usada para forragem e/ou ração para qualquer animal ou como uma matéria-prima para produzir energia ou combustível, tal como, milho, alfafa, girassol, Brassica, soja, algodão, açafrão, amendoim, sorgo, trigo, aveia, centeio, milheto, cevada, arroz, coníferas, gramíneas, por exemplo, switchgrass e Miscanthus, colheitas de leguminosas, por exemplo, ervilha, feijão e soja, tubérculos/raízes amiláceas, por exemplo, batata, batata-doce, mandioca, inhame, cana e beterraba açucareira e similares.
[000209] A invenção proporciona um oligonucleotídeo antissenso compreendendo uma sequência de ácido nucleico complementar a ou capaz de hibridizar sob condições estringentes a um ácido nucleico da invenção. A invenção proporciona métodos para inibir a translação da mensagem de uma glucanase, por exemplo, endoglucanase, uma mananase, ou uma xilanase em uma célula compreendendo administrar à célula ou expressar na célula um oligonucleotídeo antissenso compreendendo uma sequência de ácido nucleico complementar a ou capaz de hibridizar sob condições estringentes a um ácido nucleico da invenção. Em um aspecto, o oligonucleotídeo antissenso tem entre cerca de 10 a 50, cerca de 20 a 60, cerca de 30 a 70, cerca de 40 a 80, cerca de 60 a 100, ou cerca de 50 a 150 bases de extensão.
[000210] A invenção proporciona métodos para inibir a translação de mensagem de uma glucanase, por exemplo, endoglucanase, uma mananase, ou uma xilanase em uma célula compreendendo administrar à célula ou expressar na célula um oligonucleotídeo antissenso compreendendo uma sequência de ácido nucleico complementar a ou capaz de hibridizar sob condições estringentes a um ácido nucleico da invenção. A invenção proporciona moléculas de RNA inibitório de fita dupla (RNAi, ou RNA de interferência) (incluindo pequenos RNA interferentes, ou siRNAs, para inibir a transcrição, e microRNAs, ou miRNAs, para inibir a translação) compreendendo uma subsequência de uma sequência da invenção. Em um aspecto, o RNAi tem cerca de 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100 ou mais nucleotídeos dúplices de extensão. A invenção proporciona métodos para inibir a expressão de um polipeptídeo, enzima, proteína, peptídeo, por exemplo, proteína estrutural ou de ligação em uma célula compreendendo administrar à célula ou expressar na célula um RNA inibitório de fita dupla (iRNA, incluindo pequeno RNA interferente, ou siRNAs, para inibir transcrição, e microRNAs, ou miRNAs, para inibir translação), em que o RNA compreende uma subsequência de uma sequência da invenção.
[000211] A invenção proporciona polipeptídeos isolados, sintéticos ou recombinantes compreendendo uma sequência de aminoácidos tendo pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) com um polipeptídeo exemplar ou peptídeo da invenção sobre uma região de pelo menos cerca de 25, 50, 75, 100, 125, 150, 175, 200, 225, 250, 275, 300, 325, 350 ou mais resíduos, ou sobre toda a extensão do polipeptídeo, e as identidades das sequências são determinadas por análise com um algoritmo de comparação de sequências ou por uma inspeção visual. Sequências de polipeptídeos ou peptídeos exemplares da invenção incluem SEQ ID NO: 2, subsequências das mesmas e variantes das mesmas, em que em um aspecto sequências de polipeptídeos exemplares da invenção compreendem, ou alternativamente - consistem em, uma, duas, três, quatro, cinco, seis, sete, oito, nove, dez, onze (11), doze (12), 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69 ou 70 ou mais ou todas as seguintes alterações de resíduos aminoácidos para SEQ ID NO: 2:
[000212] a glicina na posição do aminoácido 2 é asparagina,
[000213] a glicina na posição do aminoácido 13 é asparagina,
[000214] a fenilalanina na posição do aminoácido 38 é tirosina,
[000215] a serina na posição do aminoácido 57 é ácido aspártico,
[000216] a tirosina na posição do aminoácido 61 é glutamina,
[000217] a tirosina na posição do aminoácido 61 é serina,
[000218] a alanina na posição do aminoácido 62 é treonina,
[000219] a fenilalanina na posição do aminoácido 63 é histidina,
[000220] a fenilalanina na posição do aminoácido 63 é treonina,
[000221] a metionina na posição do aminoácido 69 é ácido glutâmico,
[000222] a metionina na posição do aminoácido 69 é glutamina,
[000223] a metionina na posição do aminoácido 69 é histidina,
[000224] a metionina na posição do aminoácido 69 é serina,
[000225] a metionina na posição do aminoácido 69 é tirosina,
[000226] o ácido aspártico na posição do aminoácido 70 é prolina,
[000227] a arginina na posição do aminoácido 71 é alanina,
[000228] a arginina na posição do aminoácido 71 é ácido glutâmico,
[000229] a arginina na posição do aminoácido 71 é glutamina,
[000230] a arginina na posição do aminoácido 71 é prolina,
[000231] a arginina na posição do aminoácido 71 é serina,
[000232] a arginina na posição do aminoácido 71 é treonina,
[000233] a lisina na posição do aminoácido 74 é ácido glutâmico,
[000234] a lisina na posição do aminoácido 74 é leucina,
[000235] a lisina na posição do aminoácido 74 é metionina,
[000236] a isoleucina na posição do aminoácido 94 é glutamina,
[000237] a metionina na posição do aminoácido 101 é tirosina,
[000238] o ácido aspártico na posição do aminoácido 103 é cisteína,
[000239] o ácido aspártico na posição do aminoácido 103 é glutamina,
[000240] o ácido glutâmico na posição do aminoácido 106 é glicina,
[000241] o ácido glutâmico na posição do aminoácido 109 é leucina,
[000242] a lisina na posição do aminoácido 116 é alanina,
[000243] a lisina na posição do aminoácido 116 é arginina,
[000244] a fenilalanina na posição do aminoácido 130 é tirosina,
[000245] a fenilalanina na posição do aminoácido 131 é leucina,
[000246] o ácido glutâmico na posição do aminoácido 148 é histidina,
[000247] a lisina na posição do aminoácido 162 é glutamina,
[000248] a isoleucina na posição do aminoácido 166 é alanina,
[000249] a isoleucina na posição do aminoácido 166 é valina,
[000250] a serina na posição do aminoácido 183 é arginina,
[000251] a serina na posição do aminoácido 183 é valina,
[000252] a lisina na posição do aminoácido 186 é alanina,
[000253] a lisina na posição do aminoácido 186 é ácido aspártico,
[000254] a lisina na posição do aminoácido 186 é prolina,
[000255] a lisina na posição do aminoácido 186 é serina,
[000256] a serina na posição do aminoácido 191 é alanina,
[000257] a serina na posição do aminoácido 191 é cisteína,
[000258] a serina na posição do aminoácido 191 é leucina,
[000259] a fenilalanina na posição do aminoácido 201 é isoleucina,
[000260] a fenilalanina na posição do aminoácido 201 é prolina,
[000261] a fenilalanina na posição do aminoácido 201 é valina,
[000262] o ácido glutâmico na posição do aminoácido 212 é prolina,
[000263] a lisina na posição do aminoácido 216 é alanina,
[000264] a histidina na posição do aminoácido 230 é arginina,
[000265] a histidina na posição do aminoácido 230 é glutamina,
[000266] a histidina na posição do aminoácido 230 é lisina,
[000267] a leucina na posição do aminoácido 231 é isoleucina,
[000268] a leucina na posição do aminoácido 231 é metionina,
[000269] a leucina na posição do aminoácido 231 é valina,
[000270] o ácido glutâmico na posição do aminoácido 234 é ácido aspártico,
[000271] a lisina na posição do aminoácido 246 é glutamina,
[000272] a lisina na posição do aminoácido 246 é serina,
[000273] a arginina na posição do aminoácido 258 é serina,
[000274] a arginina na posição do aminoácido 258 é tirosina,
[000275] a leucina na posição do aminoácido 262 é glutamina,
[000276] a leucina na posição do aminoácido 262 é histidina,
[000277] a leucina na posição do aminoácido 262 é metionina,
[000278] a leucina na posição do aminoácido 262 é prolina,
[000279] a serina na posição do aminoácido 270 é arginina,
[000280] a fenilalanina na posição do aminoácido 271 é alanina,
[000281] a metionina na posição do aminoácido 276 é alanina,
[000282] a metionina na posição do aminoácido 276 é cisteína,
[000283] a metionina na posição do aminoácido 276 é serina,
[000284] o ácido glutâmico na posição do aminoácido 277 é serina,
[000285] a arginina na posição do aminoácido 280 é glicina,
[000286] a serina na posição do aminoácido 290 é alanina,
[000287] a treonina na posição do aminoácido 297 é alanina,
[000288] a treonina na posição do aminoácido 297 é prolina,
[000289] a leucina na posição do aminoácido 298 é alanina,
[000290] a leucina na posição do aminoácido 298 é arginina,
[000291] a leucina na posição do aminoácido 298 é asparagina,
[000292] a leucina na posição do aminoácido 298 é serina,
[000293] a leucina na posição do aminoácido 298 é valina,
[000294] a lisina na posição do aminoácido 300 é glicina,
[000295] a treonina na posição do aminoácido 301 é glutamina,
[000296] o ácido aspártico na posição do aminoácido 305 é prolina,
[000297] a glicina na posição do aminoácido 312 é isoleucina, e/ou
[000298] a serina na posição do aminoácido 315 é isoleucina.
[000299] Todas estas sequências são sequências exemplares de aminoácidos da invenção tendo alterações de resíduos específicas à “parental” SEQ ID NO: 2, resumida (em parte) nas Tabelas 1 e 2, abaixo. Polipeptídeos ou peptídeos típicos também incluem fragmentos de pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600 ou mais resíduos de extensão, ou sobre toda a extensão de uma enzima ou anticorpo. Sequências de polipeptídeos ou peptídeos exemplares da invenção incluem sequências codificadas por um ácido nucleico da invenção. Sequências de polipeptídeos ou peptídeos exemplares da invenção incluem polipeptídeos ou peptídeos especificamente ligados por um anticorpo da invenção, ou sequências capazes de provocar uma reação imune, por exemplo, epitopos capazes de provocar uma reação imune humoral (de anticorpo) ou celular específica para um polipeptídeo exemplar da invenção.
[000300] Em um aspecto, um polipeptídeo (por exemplo, uma enzima, anticorpo ou peptídeo) da invenção tem pelo menos uma atividade de glucanase, por exemplo, endoglucanase, uma mananase, ou uma xilanase. Em um aspecto, a atividade de endoglucanase compreende atividade de endo-1,4-beta-D-glucan 4-glucano hidrolase. Em um aspecto, a atividade de endoglucanase compreende catalisar hidrólise de ligações 1,4-beta-D-glicosídicas ou ligações 1,3-beta-D- glicosídicas. Em um aspecto, a atividade de endoglucanase compreende uma atividade de endo-1,4-beta-endoglucanase ou atividade de endo-β-1,4-glucanase, atividade de endo-1,3-beta- endoglucanase ou atividade de endo-β-1,3-glucanase. Em um aspecto, a atividade de glucanase (por exemplo, atividade de endo-1,4 e/ou 1,3-beta-D-glucan 4-glucano hidrolase) compreende hidrólise de ligações 1,4-beta-D-glicosídicas em celulose, derivados celulósicos (por exemplo, carbóxi metila celulose e hidróxi etil celulose) liquenina, ligações beta-1,4- e/ou 1,3- em glucanos beta-1,3 mistos, tais como beta-D-glucanos ou xiloglucanos de cereais e outro material vegetal contendo partes celulósicas.
[000301] Outro aspecto da invenção proporciona um polipeptídeo isolado, sintético ou recombinante ou peptídeo compreende, ou consiste em, pelo menos 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 ou 100 ou mais bases consecutivas de uma sequência de polipeptídeo ou peptídeo da invenção, sequências substancialmente idênticas a essa (incluindo as sequências típicas que são modificações de SEQ ID NO: 2, conforme descrito aqui, neste pedido de patente), e as sequências complementares a essas. O peptídeo pode ser, por exemplo, um fragmento imunogênico, um epitopo, um motivo (por exemplo, um sítio de ligação), uma sequência de sinal, uma sequência prepro ou um domínio catalítico (CD) ou sítio ativo.
[000302] A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes compreendendo uma sequência codificando um polipeptídeo (por exemplo, uma enzima, anticorpo ou peptídeo) da invenção, incluindo as sequências típicas da invenção, tendo uma atividade de glucanase, por exemplo, uma atividade de endoglucanase, uma atividade de mananase, ou uma atividade de xilanase com - ou sem - uma sequência de sinal (líder), em que o ácido nucleico compreende uma sequência da invenção. A sequência de sinal (líder) pode ser derivada de outra glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção, ou de outra glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase (não da invenção), ou uma não-glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, e etc., isto é, uma enzima heteróloga. A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes compreendendo uma sequência codificando um polipeptídeo tendo uma atividade de glucanase, por exemplo, uma endoglucanase, um (ou celulase), por exemplo, uma endoglucanase, uma mananase, uma xilanase, uma amilase, uma xantanase e/ou uma glicosidase, por exemplo, uma celobio-hidrolase, uma mananase e/ou uma betaglucosidase, em que a sequência não contém uma sequência de sinal (líder) e o ácido nucleico compreende uma sequência da invenção.
[000303] Em um aspecto, a atividade de glucanase, por exemplo, endoglucanase, compreende catalisar hidrólise de ligações 1,4-beta-D- glicosídicas ou ligações 1,3-beta-D-glicosídicas. Em um aspecto, a atividade de endoglucanase compreende uma atividade de endo-1,4- beta-endoglucanase. Em um aspecto, a atividade de endoglucanase compreende hidrolisar um glucano, um manano, um arabinoxilano ou um xilano para produzir um polissacarídeo ou oligômero de menor peso molecular. Em um aspecto, o glucano compreende um beta- glucano, tal como um beta-glucano hidrossolúvel. O beta-glucano hidrossolúvel pode compreender uma massa ou um produto de pão. Em um aspecto, a atividade de glucanase compreende hidrolisar polissacarídeos compreendendo D-glucopiranoses ligadas a 1,4-β- glicosídeos. Em um aspecto, a atividade de glucanase compreende hidrolisar celulose. Em um aspecto, a atividade de glucanase compreende hidrolisar celulose em uma madeira ou polpa de papel ou um produto de papel.
[000304] Em um aspecto, a atividade de glucanase, xilanase, ou mananase compreende catalisar hidrólise de um glucano, um manano, um arabinoxilano ou um xilano, ou outro carboidrato em uma ração (por exemplo, uma ração animal, tal como uma ração de animal monogástrico, incluindo suíno ou aves domésticas (por exemplo, frango) ração) ou um produto alimentício. A ração ou produto alimentício pode compreender uma ração animal à base de cereais, um mosto ou uma cerveja, um fruto ou um legume.
[000305] Em um aspecto, a atividade de glucanase, xilanase, ou mananase compreende catalisar hidrólise de um glucano, um manano, um arabinoxilano ou um xilano, ou outro carboidrato em uma célula, por exemplo, uma célula de planta, uma célula fúngica, ou uma célula microbiana (por exemplo, bacteriana).
[000306] Em um aspecto, o polipeptídeo isolado, sintético ou recombinante pode compreender o polipeptídeo da invenção que carece de toda ou parte de uma sequência de sinal (líder). Em um aspecto, o polipeptídeo isolado, sintético ou recombinante pode compreender, ou consistir de polipeptídeo da invenção compreendendo, ou consistindo em, uma sequência de sinal (líder) heteróloga, tal como uma sequência de sinal heteróloga de glucanase, ou mananase, xilanase ou não-glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, sequência de sinal (líder) de celobio- hidrolase, mananase e/ou beta-glucosidase.
[000307] Em um aspecto, a invenção proporciona proteínas quiméricas compreendendo um primeiro domínio compreendendo uma sequência de sinal da invenção e pelo menos um segundo domínio. A proteína pode ser uma proteína de fusão. O segundo domínio pode compreender uma enzima. A enzima pode ser uma glucanase, por exemplo, endoglucanase, uma mananase, ou uma xilanase.
[000308] A invenção proporciona polipeptídeos quiméricos compreendendo, ou consistindo em, pelo menos um primeiro domínio compreendendo peptídeo de sinal (SP), uma sequência prepro e/ou um domínio catalítico (CD) da invenção e pelo menos um segundo domínio compreendendo um polipeptídeo ou peptídeo heterólogo, em que o polipeptídeo ou peptídeo heterólogo não é naturalmente associado ao peptídeo de sinal (SP), a sequência prepro e/ ou o domínio catalítico (CD). Em um aspecto, o polipeptídeo ou peptídeo heterólogo não é uma glucanase, uma mananase, ou uma xilanase. O polipeptídeo ou peptídeo heterólogo pode ser terminal amino para, terminal carbóxi para ou sobre ambas as extremidades do peptídeo de sinal (SP), da sequência prepro e/ou do domínio catalítico (CD).
[000309] A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes codificando um polipeptídeo quimérico, em que o polipeptídeo quimérico compreende, ou consiste em, pelo menos um primeiro domínio compreendendo peptídeo de sinal (SP), um domínio prepro e/ou um domínio catalítico (CD) da invenção e pelo menos um segundo domínio compreendendo um polipeptídeo ou peptídeo heterólogo, em que o polipeptídeo ou peptídeo heterólogo não é naturalmente associado com o peptídeo de sinal (SP), o domínio prepro e/ ou o domínio catalítico (CD).
[000310] A invenção proporciona sequências de sinal (líder) isoladas, sintéticas ou recombinantes (por exemplo, peptídeos de sinal (líder)) consistindo em ou compreendendo uma sequência conforme determinado nos resíduos (terminal amino) 1 a 14, 1 a 15, 1 a 16, 1 a 17, 1 a 18, 1 a 19, 1 a 20, 1 a 21, 1 a 22, 1 a 23, 1 a 24, 1 a 25, 1 a 26, 1 a 27, 1 a 28, 1 a 29, 1 a 30, 1 a 31, 1 a 32, 1 a 33, 1 a 34, 1 a 35, 1 a 36, 1 a 37, 1 a 38, 1 a 40, 1 a 41, 1 a 42, 1 a 43 ou 1 a 44, de um polipeptídeo da invenção, por exemplo, um polipeptídeo exemplar da invenção, tal como SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, E SEQ ID NO: 23 e as modificações de sequências típicas das mesmas descritas aqui, neste pedido de patente.
[000311] Em um aspecto, a atividade de glucanase, por exemplo, endoglucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreende uma atividade específica em cerca de 37°C na faixa a partir de cerca de 1 a cerca de 1200 unidades por miligrama de proteína, ou cerca de 100 a cerca de 1000 unidades por miligrama de proteína. Em outro aspecto, a atividade de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase compreende uma atividade específica a partir de cerca de 100 a cerca de 1000 unidades por miligrama de proteína, ou, a partir de cerca de 500 a cerca de 750 unidades por miligrama de proteína. Alternativamente, a atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreende uma atividade específica a 37°C na faixa a partir de cerca de 1 a cerca de 750 unidades por miligrama de proteína, ou, a partir de cerca de 500 a cerca de 1200 unidades por miligrama de proteína. Em um aspecto, atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreende uma atividade específica a 37°C na faixa a partir de cerca de 1 a cerca de 500 unidades por miligrama de proteína, ou, a partir de cerca de 750 a cerca de 1000 unidades por miligrama de proteína. Em outro aspecto, atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreende uma atividade específica a 37°C na faixa a partir de cerca de 1 a cerca de 250 unidades por miligrama de proteína. Alternativamente, atividade de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase compreende uma atividade específica a 37°C na faixa a partir de cerca de 1 a cerca de 100 unidades por miligrama de proteína. Em outro aspecto, a termotolerância compreende retenção de pelo menos metade da atividade específica da glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase a 37°C depois de ser aquecida até uma temperatura elevada, tal como uma temperatura a partir de cerca de 0°C a cerca de 20°C, cerca de 20°C a cerca de 37°C, cerca de 37°C a cerca de 50°C, cerca de 50°C a cerca de 70°C, cerca de 70°C a cerca de 75°C, cerca de 75°C a cerca de 80°C, cerca de 80°C a cerca de 85°C, cerca de 85°C a cerca de 90°C, cerca de 90°C a cerca de 95°C, cerca de 95°C a cerca de 100°C, cerca de 100°C a cerca de 110°C, ou superior. Alternativamente, a termotolerância pode compreender retenção de atividade específica a 37°C na faixa a partir de cerca de 1 a cerca de 1200 unidades por miligrama de proteína, ou, a partir de cerca de 500 a cerca de 1000 unidades por miligrama de proteína, depois de ser aquecida até uma temperatura elevada. Em outro aspecto, a termotolerância pode compreender retenção de atividade específica a 37°C na faixa a partir de cerca de 1 a cerca de 500 unidades por miligrama de proteína depois de ser aquecida até uma temperatura elevada, conforme descrito acima.
[000312] A invenção proporciona o polipeptídeo isolado, sintético ou recombinante da invenção, em que o polipeptídeo compreende pelo menos um sítio de glicosilação. Em um aspecto, glicosilação pode ser uma glicosilação N-ligada e/ou uma glicosilação O-ligada. Em um aspecto, o polipeptídeo pode ser glicosilado depois de ser expressado em uma célula de levedura, por exemplo, uma P. pastoris ou uma S. pombe, ou em uma célula hospedeira de mamífero, de inseto, fúngica ou outra.
[000313] Em um aspecto, o polipeptídeo pode reter atividade de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase sob condições compreendendo cerca de pH 6,5, pH 6, pH 5,5, pH 5, pH 4,5, pH 4,0, pH 3,5, pH 3,0 ou pH menor (mais acídico). Em outro aspecto, o polipeptídeo pode reter uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase sob condições compreendendo cerca de pH 7, pH 7,5 pH 8,0, pH 8,5, pH 9, pH 9,5, pH 10, pH 10,5, pH 11,0, pH 11,5, pH 12, pH 12,5 ou pH maior (mais básico). Em um aspecto, o polipeptídeo pode reter uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase depois de exposição a condições compreendendo cerca de pH 6,5, pH 6, pH 5,5, pH 5, pH 4,5, pH 4,0, pH 3,5, pH 3,0 ou pH menor (mais acídico). Em outro aspecto, o polipeptídeo pode reter atividade de uma glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase depois de exposição a condições compreendendo cerca de pH 7, pH 7,5 pH 8,0, pH 8,5, pH 9, pH 9,5, pH 10, pH 10,5, pH 11,0, pH 11,5, pH 12, pH 12,5 ou pH maior (mais básico).
[000314] A invenção proporciona preparações de proteína compreendendo um polipeptídeo da invenção, em que a preparação de proteína compreende um líquido, um sólido ou um gel.
[000315] A invenção proporciona heterodímeros compreendendo um polipeptídeo da invenção e uma segunda proteína ou domínio. O segundo membro do heterodímero pode ser uma glicanase diferente, uma enzima diferente ou outra proteína. Em um aspecto, o segundo domínio pode ser um polipeptídeo e o heterodímero pode ser uma proteína de fusão. Em um aspecto, o segundo domínio pode ser um epitopo ou um rótulo. Em um aspecto, a invenção proporciona homomultímeros, incluindo, mas não limitados a, homodímeros, homotrímeros, homotetrâmeros, homopentâmeros, e homo-hexâmeros compreendendo um polipeptídeo (por exemplo, uma enzima, um peptídeo) da invenção.
[000316] A invenção proporciona polipeptídeos imobilizados tendo atividade de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase, em que o polipeptídeo compreende um polipeptídeo da invenção, um polipeptídeo codificado por um ácido nucleico da invenção, ou um polipeptídeo compreendendo um polipeptídeo da invenção e um segundo domínio. Em um aspecto, o polipeptídeo pode ser imobilizado sobre uma célula, um metal, uma resina, um polímero, uma cerâmica, um vidro, um microeletrodo, uma partícula grafítica, uma conta, um gel, uma lâmina, um arranjo ou um tubo capilar.
[000317] A invenção proporciona arranjos compreendendo um ácido nucleico imobilizado da invenção. A invenção proporciona arranjos compreendendo um anticorpo da invenção.
[000318] A invenção proporciona anticorpos isolados, sintéticos ou recombinantes que se ligam especificamente a um polipeptídeo da invenção ou a um polipeptídeo codificado por um ácido nucleico da invenção. O anticorpo pode ser um anticorpo monoclonal ou um anticorpo policlonal. A invenção proporciona hibridomas compreendendo um anticorpo da invenção, por exemplo, um anticorpo que se liga especificamente a um polipeptídeo da invenção ou a um polipeptídeo codificado por um ácido nucleico da invenção.
[000319] A invenção proporciona método para isolar ou identificar um polipeptídeo tendo atividade de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase compreendendo as etapas de: (a) proporcionar um anticorpo da invenção; (b) proporcionar uma amostra compreendendo polipeptídeos; e (c) contatar a amostra da etapa (b) com o anticorpo da etapa (a) sob condições em que o anticorpo pode ligar-se especificamente ao polipeptídeo, deste modo isolando ou identificando um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase.
[000320] A invenção proporciona métodos para produzir um anticorpo antiglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase compreendendo administrar a um animal não-humano um ácido nucleico da invenção ou um polipeptídeo da invenção ou subsequências dos mesmos em uma quantidade suficiente para gerar uma reação imune humoral, deste modo produzindo um anticorpo antiglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. A invenção proporciona métodos para produzir uma reação imune humoral ou celular antiglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreendendo administrar a um animal não-humano um ácido nucleico da invenção ou um polipeptídeo da invenção ou subsequências dos mesmos em uma quantidade suficiente para gerar uma reação imune.
[000321] A invenção proporciona métodos para produzir um polipeptídeo recombinante compreendendo as etapas de: (a) proporcionar um ácido nucleico da invenção ligado operavelmente a um promotor; e (b) expressar o ácido nucleico da etapa (a) sob condições que permitem expressão do polipeptídeo, deste modo produzindo um polipeptídeo recombinante. Em um aspecto, o método pode adicionalmente compreender transformar uma célula hospedeira com o ácido nucleico da etapa (a) seguido por expressão do ácido nucleico da etapa (a), deste modo produzindo um polipeptídeo recombinante em uma célula transformada.
[000322] A invenção proporciona métodos para identificar um polipeptídeo tendo atividade de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção; ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar substrato de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase ; e (c) contatar o polipeptídeo ou um fragmento ou variante do mesmo da etapa (a) com o substrato da etapa (b) e detectar uma redução na quantidade de substrato ou um aumento na quantidade de um produto da reação, em que uma redução na quantidade do substrato ou um aumento na quantidade do produto da reação detecta um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase.
[000323] A invenção proporciona métodos para identificar substrato de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção; ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar um substrato de teste; e (c) contatar o polipeptídeo da etapa (a) com o substrato de teste da etapa (b) e detectar uma redução na quantidade de substrato ou um aumento na quantidade de produto da reação, em que uma redução na quantidade do substrato ou um aumento na quantidade de um produto da reação identifica o substrato de teste como um substrato de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase.
[000324] A invenção proporciona métodos para determinar se um composto de teste se liga especificamente a um polipeptídeo compreendendo as seguintes etapas: (a) expressar um ácido nucleico ou um vetor compreendendo o ácido nucleico sob condições permissivas para translação do ácido nucleico a um polipeptídeo, em que o ácido nucleico compreende um ácido nucleico da invenção, ou, proporcionar um polipeptídeo da invenção; (b) proporcionar um composto de teste; (c) contatar o polipeptídeo com o composto de teste; e (d) determinar se o composto de teste da etapa (b) liga-se especificamente ao polipeptídeo.
[000325] A invenção proporciona métodos para identificar um modulador de uma atividade de glucanase, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar um composto de teste; (c) contatar o polipeptídeo da etapa (a) com o composto de teste da etapa (b) e medir uma atividade da glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase em que uma alteração na atividade da glucanase mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase medida na presença do composto de teste comparada com a atividade na ausência do composto de teste proporciona uma determinação de que o composto de teste modula a atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. Em um aspecto, a atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase pode ser medida proporcionando um substrato de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase e detectando uma redução na quantidade do substrato ou um aumento na quantidade de um produto da reação, ou, um aumento na quantidade do substrato ou uma redução na quantidade de um produto da reação. Uma redução na quantidade do substrato ou um aumento na quantidade do produto da reação com o composto de teste comparado com a quantidade de substrato ou produto da reação sem o composto de teste identifica o composto de teste como um ativador de atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Um aumento na quantidade do substrato ou uma redução na quantidade do produto da reação com o composto de teste comparado com a quantidade de substrato ou produto da reação sem o composto de teste identifica o composto de teste como um inibidor da atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta- glucosidase.
[000326] A invenção proporciona sistemas de computação compreendendo um processador e um dispositivo de armazenamento de dados em que o referido dispositivo de armazenamento de dados tem armazenada sobre o mesmo uma sequência de polipeptídeo ou uma sequência de ácido nucleico da invenção (por exemplo, um polipeptídeo codificado por um ácido nucleico da invenção). Em um aspecto, o sistema de computação pode compreender adicionalmente um algoritmo de comparação de sequências e um dispositivo de armazenamento de dados tendo pelo menos uma sequência de referência armazenada sobre o mesmo. Em outro aspecto, o algoritmo de comparação de sequências compreende um programa de computação que indica polimorfismos. Em um aspecto, o sistema de computação pode compreender adicionalmente um identificador que identifica uma ou mais características na referida sequência. A invenção proporciona meios legíveis nos computados tendo armazenada sobre os mesmos uma sequência de polipeptídeo ou uma sequência de ácido nucleico da invenção. A invenção proporciona métodos para identificar uma característica em uma sequência compreendendo as etapas de: (a) ler a sequência usando um programa de computação o qual identifica uma ou mais características em uma sequência, em que a sequência compreende uma sequência de polipeptídeo ou uma sequência de ácido nucleico da invenção; e (b) identificar uma ou mais características na sequência com o programa de computação. A invenção proporciona métodos para comparar uma primeira sequência com uma segunda sequência compreendendo as etapas de: (a) ler a primeira sequência e a segunda sequência através do uso de um programa de computação o qual compara sequências, em que a primeira sequência compreende uma sequência de polipeptídeo ou uma sequência de ácido nucleico da invenção; e (b) determinar diferenças entre a primeira sequência e a segunda sequência com o programa de computação. A etapa de determinar diferenças entre a primeira sequência e a segunda sequência pode compreender adicionalmente a etapa de identificar polimorfismos. Em um aspecto, o método pode compreender adicionalmente um identificador que identifica uma ou mais características em uma sequência. Em outro aspecto, o método pode compreender ler a primeira sequência usando um programa de computação e identificar uma ou mais características na sequência.
[000327] A invenção proporciona métodos para isolar ou recuperar um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase de uma amostra, tal como uma amostra ambiental, compreendendo as etapas de: (a) proporcionar um par de sequências de iniciadores de amplificação para amplificar um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, em que o par de iniciadores é capaz de amplificar um ácido nucleico da invenção; (b) isolar um ácido nucleico da amostra ou tratar a amostra de tal modo que o ácido nucleico na amostra seja acessível para hibridização para o par de iniciadores de amplificação; e, (c) combinar o ácido nucleico da etapa (b) com o par de iniciadores de amplificação da etapa (a) e amplificar ácido nucleico da amostra, deste modo isolando ou recuperando um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase de uma amostra. Um ou cada membro do par de sequências de iniciadores de amplificação pode compreender um oligonucleotídeo compreendendo pelo menos cerca de 10 a 50 bases consecutivas de uma sequência da invenção. Em um aspecto, o par de sequências de iniciadores de amplificação é um par de amplificação da invenção. Em uma modalidade da invenção, a amostra é uma amostra ambiental, por exemplo, compreendendo uma amostra de água, uma amostra de líquido, uma amostra de terra, uma amostra de ar ou uma amostra biológica. Em um aspecto, a amostra biológica pode ser derivada de uma célula bacteriana, uma célula de protozoário, uma célula de inseto, uma célula de levedura, uma célula de planta, uma célula fúngica ou uma célula de mamífero.
[000328] A invenção proporciona métodos para isolar ou recuperar um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase de uma amostra, tal como uma amostra ambiental, compreendendo as etapas de: (a) proporcionar uma sonda de polinucleotídeo compreendendo um ácido nucleico da invenção ou uma subsequência do mesmo; (b) isolar um ácido nucleico da amostra ou tratar a amostra de tal modo que o ácido nucleico na amostra esteja acessível para hibridização a uma sonda de polinucleotídeo da etapa (a); (c) combinar o ácido nucleico sintético isolado, ou a amostra tratada da etapa (b) com a sonda de polinucleotídeo da etapa (a); e (d) isolar um ácido nucleico que hibridiza especificamente com a sonda de polinucleotídeo da etapa (a), deste modo isolando ou recuperando um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase de uma amostra. Em uma modalidade da invenção, a amostra é uma amostra ambiental, por exemplo, compreendendo uma amostra de água, uma amostra de líquido, uma amostra de terra, uma amostra de ar ou uma amostra biológica. Em um aspecto, a amostra biológica pode ser derivada de uma célula bacteriana, uma célula de protozoário, uma célula de inseto, uma célula de levedura, uma célula de planta, uma célula fúngica ou uma célula de mamífero.
[000329] A invenção proporciona métodos para gerar uma variante de um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase compreendendo as etapas de: (a) proporcionar um ácido nucleico molde compreendendo um ácido nucleico da invenção; e (b) modificar, eliminar ou adicionar um ou mais nucleotídeos na sequência molde, ou uma combinação da mesma, para gerar uma variante do ácido nucleico molde. Em um aspecto, o método pode compreender adicionalmente expressar o ácido nucleico variante para gerar um polipeptídeo de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase variante. As modificações, adições ou eliminações podem ser introduzidas por um método compreendendo PCR propenso a erro, embaralhamento, mutagênese dirigida por oligonucleotídeo, PCR de montagem, mutagênese sexual por PCR, mutagênese in vivo, mutagênese de cassete, mutagênese de conjunto recursiva, mutagênese de conjunto exponencial, mutagênese sítio-específica, remontagem genética, mutagênese de saturação de sítio genético (GSSM), remontagem de ligação sintética (SLR) ou uma combinação dos mesmos. Em outro aspecto, as modificações, adições ou eliminações são introduzidas por um método compreendendo recombinação, recombinação de sequência recursiva, mutagênese de DNA modificado por fosfotioato, mutagênese molde contendo uracila, mutagênese de dúplices com espaço, mutagênese de reparo de combinação inadequada de ponto, mutagênese de cepa hospedeira reparo-deficiente, mutagênese química, mutagênese radiogênica, mutagênese de eliminação, mutagênese de restrição-seleção, mutagênese de restrição-purificação, síntese genética artificial, mutagênese de conjunto, criação de multímero de ácido nucleico quimérico e uma combinação dos mesmos.
[000330] Em um aspecto, o método pode ser repetido iterativamente até ser produzida uma glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase tendo uma atividade alterada ou diferente ou uma estabilidade alterada ou diferente de um polipeptídeo codificado pelo ácido nucleico molde. Em um aspecto, o polipeptídeo variante de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase é termotolerante, e retém alguma atividade depois de ser exposto a uma temperatura elevada. Em outro aspecto, o polipeptídeo variante de glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase tem glicosilação aumentada comparado com a glucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase codificada por um ácido nucleico molde. Alternativamente, o polipeptídeo variante tem atividade de uma glucanase, por exemplo, uma endoglucanase, um (ou celulase), por exemplo, uma endoglucanase, uma mananase, uma xilanase, uma amilase, uma xantanase e/ou uma glicosidase, por exemplo, uma celobio-hidrolase, uma mananase e/ou uma betaglucosidase sob uma temperatura elevada, em que a enzima codificada pelo ácido nucleico molde não é ativa sob a temperatura elevada. Em um aspecto, o método pode ser repetido iterativamente até ser produzida uma glucanase, por exemplo, uma endoglucanase, um (ou celulase), por exemplo, uma endoglucanase, uma mananase, uma xilanase, uma amilase, uma xantanase e/ou uma glicosidase, por exemplo, uma celobio-hidrolase, uma mananase e/ou uma betaglucosidase codificando sequência tendo um uso de códon alterado daquela do ácido nucleico molde. Em outro aspecto, o método pode ser repetido iterativamente até ser produzida uma glucanase, por exemplo, uma endoglucanase, um (ou celulase), por exemplo, uma endoglucanase, uma mananase, uma xilanase, uma amilase, uma xantanase e/ou uma glicosidase, por exemplo, uma celobio-hidrolase, uma mananase e/ou uma beta-glucosidase gene tendo nível maior ou menor de expressão de mensagem ou estabilidade daquela do ácido nucleico molde.
[000331] A invenção proporciona métodos para modificar códons em um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, por exemplo, uma endoglucanase, um (ou celulase), por exemplo, uma endoglucanase, uma mananase, uma xilanase, uma amilase, uma xantanase e/ou uma glicosidase, por exemplo, uma celobio-hidrolase, uma mananase e/ou uma beta-glucosidase para aumentar sua expressão em uma célula hospedeira, o método compreendendo as seguintes etapas: (a) proporcionar um ácido nucleico da invenção codificando um polipeptídeo tendo uma atividade de glucanase, por exemplo, uma endoglucanase, um (ou celulase), por exemplo, uma endoglucanase, uma mananase, uma xilanase, uma amilase, uma xantanase e/ou uma glicosidase, por exemplo, uma celobio-hidrolase, uma mananase e/ou uma beta-glucosidase; e, (b) identificar um códon não-preferêncial ou um menos preferêncial no ácido nucleico da etapa (a) e substituir este com um códon preferêncial ou neutralmente usado codificando o mesmo aminoácido que o códon substituído, em que um códon preferêncial é um códon super-representado em sequências codificantes em genes na célula hospedeira e um códon não-preferêncial ou menos preferêncial é um codon sub-representado em sequências codificantes em genes na célula hospedeira, deste modo modificando o ácido nucleico para aumentar sua expressão em uma célula hospedeira.
[000332] A invenção proporciona métodos para modificar códons em um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase; o método compreendendo as seguintes etapas: (a) proporcionar um ácido nucleico da invenção; e, (b) identificar um códon no ácido nucleico da etapa (a) e substituir este com um códon diferente codificando o mesmo aminoácido que o códon substituído, deste modo modificando códons em um ácido nucleico codificando uma glucanase, mananase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase.
[000333] A invenção proporciona métodos para modificar códons em um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase para aumentar sua expressão em uma célula hospedeira, o método compreendendo as seguintes etapas: (a) proporcionar um ácido nucleico da invenção codificando um polipeptídeo de glucanase, mananase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase; e, (b) identificar um códon não-preferêncial ou um menos preferêncial no ácido nucleico da etapa (a) e substituir este com um códon preferêncial ou usado neutralmente codificando o mesmo aminoácido que o códon substituído, em que um códon preferêncial é um códon super-representado em sequências codificantes em genes na célula hospedeira e um códon não- preferêncial ou menos preferêncial é um códon sub-representado em sequências codificantes em genes na célula hospedeira, deste modo modificando o ácido nucleico para aumentar sua expressão em uma célula hospedeira.
[000334] A invenção proporciona métodos para modificar um códon em um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, mananase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase para reduzir sua expressão em uma célula hospedeira, o método compreendendo as seguintes etapas: (a) proporcionar um ácido nucleico da invenção; e (b) identificar pelo menos um códon preferêncial no ácido nucleico da etapa (a) e substituir este com um códon não-preferêncial ou menos preferêncial codificando o mesmo aminoácido que o códon substituído, em que um códon preferêncial é um códon super-representado em sequências codificantes em genes em uma célula hospedeira e um códon não-preferêncial ou menos preferêncial é um códon sub-representado em sequências codificantes em genes na célula hospedeira, deste modo modificando o ácido nucleico para reduzir sua expressão em uma célula hospedeira. Em um aspecto, a célula hospedeira pode ser uma célula bacteriana, uma célula fúngica, uma célula de inseto, uma célula de levedura, uma célula de planta ou uma célula de mamífero.
[000335] A invenção proporciona métodos para produzir uma biblioteca de ácidos nucleicos codificando uma pluralidade de sítios ativos modificados de glucanase, mananase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta glucosidase (domínios catalíticos (CDs)) ou sítios de ligação de substrato, em que os sítios ativos modificados ou sítios de ligação de substrato são derivados de um primeiro ácido nucleico compreendendo uma sequência codificando um primeiro sítio ativo ou um primeiro sítio de ligação de substrato o método compreendendo as seguintes etapas: (a) proporcionar um primeiro ácido nucleico codificando um primeiro sítio ativo ou primeiro sítio de ligação de substrato, em que a primeira sequência de ácido nucleico compreende uma sequência que hibridiza sob condições estringentes a um ácido nucleico da invenção, e o ácido nucleico codifica uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase sítio ativo ou um sítio de ligação de substrato de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase; (b) proporcionar um conjunto de oligonucleotídeos mutagênicos que codificam variantes de aminoácidos que ocorrem naturalmente em uma pluralidade de códons alvo no primeiro ácido nucleico; e, (c) usando a série de oligonucleotídeos mutagênicos para gerar uma série de ácidos nucleicos variantes codificando sítio ativo ou codificando sítio de ligação de substrato codificando uma gama de variações de aminoácidos em cada códon de aminoácido que foi mutagenizado, deste modo produzindo uma biblioteca de ácidos nucleicos codificando uma pluralidade de sítios ativos ou sítios de ligação de substrato modificados de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. Em um aspecto, o método compreende mutagenizar o primeiro ácido nucleico da etapa (a) por um método compreendendo um sistema de evolução dirigida otimizada, mutagênese de saturação de sítio genético (GSSM), remontagem de ligação sintética (SLR), PCR propenso a erro, embaralhamento, mutagênese dirigida a oligonucleotídeo, PCR de montagem, mutagênese sexual por PCR, mutagênese in vivo, mutagênese de cassete, mutagênese de conjunto recursiva, mutagênese de conjunto exponencial, mutagênese sítio-específica, remontagem genética, remontagem de ligação sintética (SLR) e uma combinação dos mesmos. Em outro aspecto, o método compreende mutagenizar o primeiro ácido nucleico da etapa (a) ou variantes por um método compreendendo recombinação, recombinação de sequência recursiva, mutagênese de DNA modificado por fosfotioato, mutagênese molde contendo uracila, mutagênese de dúplices com espaço, mutagênese de reparo de combinação inadequada de ponto, mutagênese de cepa hospedeira reparo-deficiente, mutagênese química, mutagênese radiogênica, mutagênese de eliminação, mutagênese de restrição-seleção, mutagênese de restrição- purificação, síntese genética artificial, mutagênese de conjunto, criação de multímero de ácido nucleico quimérico e uma combinação dos mesmos.
[000336] A invenção proporciona métodos para fabricar uma molécula pequena compreendendo as seguintes etapas: (a) proporcionar uma pluralidade de enzimas biossintéticas capazes de sintetizar ou modificar uma molécula pequena, em que uma das enzimas compreende uma enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase codificada por um ácido nucleico da invenção; (b) proporcionar um substrato para pelo menos uma das enzimas da etapa (a); e (c) reagir o substrato da etapa (b) com as enzimas sob condições que facilitam uma pluralidade de reações biocatalíticas para gerar uma molécula pequena por meio de uma série de reações biocatalíticas. A invenção proporciona métodos para modificar uma molécula pequena compreendendo as seguintes etapas: (a) proporcionar uma enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, em que a enzima compreende um polipeptídeo da invenção, ou, um polipeptídeo codificado por um ácido nucleico da invenção, ou uma subsequência da mesma; (b) proporcionar uma molécula pequena; e (c) reagir a enzima da etapa (a) com a molécula pequena da etapa (b) sob condições que facilitam uma reação enzimática catalisada pela enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, deste modo modificando uma molécula pequena por uma reação enzimática de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Em um aspecto, o método pode compreender uma pluralidade de substratos de molécula pequena para a enzima da etapa (a), deste modo gerando uma biblioteca de moléculas pequenas modificadas produzidas por pelo menos uma reação enzimática catalisada pela enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Em um aspecto, o método pode compreender uma pluralidade de enzimas adicionais sob condições que facilitam uma pluralidade de reações biocatalíticas pelas enzimas para formar uma biblioteca de moléculas pequenas modificadas produzidas pela pluralidade de reações enzimáticas. Em outro aspecto, o método pode compreender adicionalmente a etapa de testar a biblioteca para determinar se uma molécula pequena modificada em particular que apresenta uma atividade desejada está presente dentro da biblioteca. A etapa de experimentação da biblioteca pode compreender adicionalmente as etapas de eliminar sistematicamente todas exceto uma das reações biocatalíticas usadas para produzir uma porção da pluralidade das moléculas pequenas modificadas dentro da biblioteca testando a porção da molécula pequena modificada para a presença ou ausência da molécula pequena modificada em particular com uma atividade desejada, e identificar pelo menos uma reação biocatalítica específica que produz a molécula pequena modificada em particular da atividade desejada.
[000337] A invenção proporciona métodos para determinar um fragmento funcional de uma enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase compreendendo as etapas de: (a) proporcionar uma enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, em que a enzima compreende um polipeptídeo da invenção, ou um polipeptídeo codificado por um ácido nucleico da invenção, ou uma subsequência da mesma; e (b) eliminar uma pluralidade de resíduos aminoácido da sequência da etapa (a) e testar a subsequência remanescente para uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, deste modo determinando um fragmento funcional de uma enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. Em um aspecto, a atividade de glucanase, mananase, ou xilanase é medida proporcionando um substrato de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase e detectando uma redução na quantidade do substrato ou um aumento na quantidade de um produto da reação.
[000338] A invenção proporciona métodos para engenharia celular completa de fenótipos novos ou modificados usando análise do fluxo metabólico em tempo real, o método compreendendo as seguintes etapas: (a) produzir uma célula modificada modificando a composição genética de uma célula, em que a composição genética é modificada por adição à célula de um ácido nucleico da invenção; (b) cultivar a célula modificada para gerar uma pluralidade de células modificadas; (c) medir pelo menos um parâmetro metabólico da célula monitorando a cultura celular da etapa (b) em tempo real; e, (d) analisar os dados da etapa (c) para determinar se o parâmetro medido difere de uma medição comparável em uma célula não modificada sob condições similares, deste modo identificando um fenótipo produzido na célula usando análise do fluxo metabólico em tempo real. Em um aspecto, a composição genética da célula pode ser modificada por um método compreendendo eliminação de uma sequência ou modificação de uma sequência na célula, ou, esvaziamento da expressão de um gene. Em um aspecto, o método pode compreender adicionalmente selecionar uma célula compreendendo um fenótipo recém-produzido. Em outro aspecto, o método pode compreender cultivar a célula selecionada, deste modo gerando uma nova cepa celular compreendendo um fenótipo recém-produzido.
[000339] A invenção proporciona métodos para aumentar a termotolerância ou a termoestabilidade de um polipeptídeo de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase, o método compreendendo glicosilar um polipeptídeo de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, em que o polipeptídeo compreende pelo menos 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250 ou mais aminoácidos contíguos de um polipeptídeo da invenção; ou um polipeptídeo codificado por uma sequência de ácido nucleico da invenção, deste modo aumentando a termotolerância ou a termoestabilidade do polipeptídeo de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. Em um aspecto, a atividade específica de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase pode ser termoestável ou termotolerante em uma temperatura na faixa a partir de acima de cerca de 37°C a cerca de 95°C, ou 0°C a cerca de 37°C.
[000340] A invenção proporciona métodos para superexpressar um polipeptídeo recombinante de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase em uma célula compreendendo expressar um vetor compreendendo um ácido nucleico compreendendo um ácido nucleico da invenção ou uma sequência de ácido nucleico da invenção, em que as identidades das sequências são determinadas por análise com um algoritmo de comparação de sequências ou por inspeção visual, em que superexpressão é efetuada por uso de um promotor de alta atividade, um vetor dicistrônico ou por amplificação genética do vetor.
[000341] A invenção proporciona métodos para produzir uma planta transgênica compreendendo as seguintes etapas: (a) introduzir uma sequência heteróloga de ácido nucleico na célula, em que a sequência nucléica heteróloga compreende uma sequência de ácido nucleico da invenção, deste modo produzindo uma célula da planta transformada; e (b) produzir uma planta transgênica a partir da célula transformada.
[000342] A invenção proporciona métodos para expressar uma sequência heteróloga de ácido nucleico em uma célula de planta compreendendo as seguintes etapas: (a) transformar a célula de planta com uma sequência heteróloga de ácido nucleico ligado operavelmente a um promotor, em que a sequência nucléica heteróloga compreende um ácido nucleico da invenção; (b) cultivar a planta sob condições em que a sequência de ácidos nucleicos heteróloga é expressada na célula da planta. A invenção proporciona métodos para expressar uma sequência heteróloga de ácido nucleico em uma célula de planta compreendendo as seguintes etapas: (a) transformar a célula da planta com uma sequência heteróloga de ácido nucleico ligada operavelmente a um promotor, em que a sequência nucléica heteróloga compreende uma sequência da invenção; (b) cultivar a planta sob condições em que a sequência de ácidos nucleicos heteróloga é expressada na célula da planta.
[000343] A invenção proporciona métodos para hidrolisar, dissolver ou romper uma composição compreendendo glucano compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar uma composição compreendendo um glucano; e (c) contatar o polipeptídeo da etapa (a) com a composição da etapa (b) sob condições em que a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase hidrolisa, dissolve ou rompe a composição compreendendo glucano. Em um aspecto, a composição compreende uma célula de planta, uma célula bacteriana, uma célula de levedura, uma célula de inseto, ou uma célula animal.
[000344] Portanto, a composição pode compreender qualquer planta ou parte de planta, qualquer alimento ou ração contendo glucano, manano, xiloglucano ou xilano, um produto de resíduo e similares. A invenção proporciona métodos para liquefazer ou remover uma composição compreendendo glucano compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar uma composição compreendendo um glucano; e (c) contatar o polipeptídeo da etapa (a) com a composição da etapa (b) sob condições em que a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase remove, amolece ou liquefaz a composição.
[000345] A invenção proporciona composições de detergente compreendendo um polipeptídeo da invenção, ou um polipeptídeo codificado por um ácido nucleico da invenção, em que o polipeptídeo tem uma atividade de glucanase, por exemplo, endoglucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. A glucanase pode ser uma glucanase não- tensoativa (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase ou uma glucanase tensoativa (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. A glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase pode ser formulada em uma composição líquida não-aquosa, um sólido fundido, uma forma granular, uma forma particulada, um comprimido prensado, uma forma de gel, uma pasta ou uma forma de pasta fluida. A invenção proporciona métodos para lavar um objeto compreendendo as seguintes etapas: (a) proporcionar uma composição compreendendo um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar um objeto; e (c) contatar o polipeptídeo da etapa (a) e o objeto da etapa (b) sob condições em que a composição pode lavar o objeto.
[000346] A invenção proporciona têxteis ou tecidos, incluindo, por exemplo, fios, compreendendo um polipeptídeo da invenção, ou um polipeptídeo codificado por um ácido nucleico da invenção. Em um aspecto, têxteis ou tecidos compreendem fibras contendo glucano. A invenção proporciona métodos para tratar um têxtila ou tecido (por exemplo, removendo uma mancha de uma composição) compreendendo as seguintes etapas: (a) proporcionar uma composição compreendendo um polipeptídeo da invenção tendo uma atividade de glucanase, por exemplo, endoglucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar um têxtila ou tecido compreendendo um glucano; e (c) contatar o polipeptídeo da etapa (a) e a composição da etapa (b) sob condições em que a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase pode tratar o têxtila ou tecido (por exemplo, remover a mancha). A invenção proporciona métodos para melhorar o acabamento de um tecido compreendendo as seguintes etapas: (a) proporcionar uma composição compreendendo um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, ou um polipeptídeo codificado por um ácido nucleico da invenção; (b) proporcionar um tecido; e (c) contatar o polipeptídeo da etapa (a) e o tecido da etapa (b) sob condições em que o polipeptídeo pode tratar o tecido deste modo melhorando o acabamento do tecido. Em um aspecto, o tecido é uma lã ou uma seda.
[000347] A invenção proporciona rações, incluindo rações animais para, por exemplo, animais monogástricos, tais como uma ração para suínos ou aves domésticas (por exemplo, frango), ou alimentos, compreendendo um polipeptídeo da invenção, ou um polipeptídeo codificado por um ácido nucleico da invenção. A invenção proporciona métodos para hidrolisar um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo em uma ração ou um alimento antes do consumo por um animal compreendendo as seguintes etapas: (a) obter um material de ração compreendendo uma glucanase por exemplo, endoglucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção, ou uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase codificada por um ácido nucleico da invenção; e (b) adicionar o polipeptídeo da etapa (a) ao material da ração ou de alimento em uma quantidade suficiente por um período de tempo suficiente para causar hidrólise de um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo e formação de um alimento ou ração tratados, deste modo hidrolisando um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo no alimento ou na ração antes do consumo pelo animal. Em um aspecto, a invenção proporciona métodos para hidrolisar um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo em uma ração ou um alimento depois do consumo por um animal compreendendo as seguintes etapas: (a) obter um material de ração compreendendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção, ou uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase codificada por um ácido nucleico da invenção; (b) adicionar o polipeptídeo da etapa (a) ao material da ração ou do alimento; e (c) administrar o material da ração ou do alimento ao animal, em que depois do consumo, a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta glucosidase causa hidrólise de um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo na ração ou no alimento no trato digestivo do animal. O alimento ou a ração (por exemplo, ração animal, inclusive para animais monogástricos tal como em ração para suínos ou aves domésticas (por exemplo, frango)) podem ser, por exemplo, um cereal, um grão, um milho e similares.
[000348] Em outro aspecto, a invenção proporciona métodos para reduzir a viscosidade de glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos em uma composição, por exemplo, em um alimento ou uma ração (por exemplo, uma ração animal, por exemplo, ração de animal monogástrico, tal como uma ração de aves domésticas (por exemplo, frango)), tratando a composição com uma glucanase da invenção, ou, incluindo uma glucanase da invenção na composição. O alimento ou a ração pode compreender cevada ou trigo, por exemplo, um alimento para ração para uma dieta de alto teor de cevada ou uma dieta de alto teor de trigo, como em uma dieta de um animal monogástrico, incluindo seu uso em uma dieta de aves domésticas (por exemplo, frango) ou suíno. Em um aspecto, a invenção proporciona métodos para minimizar gotejamentos a úmido alimentando um animal (por exemplo, uma ave, tal como quaisquer aves domésticas) com um alimento ou uma ração tratados por ou compreendendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção. Em um aspecto, a invenção proporciona métodos para aumentar a taxa de crescimento e/ou conversão de ração alimentando um animal (por exemplo, uma ave, tal como uma ave doméstica, por exemplo, um frango) com um alimento ou uma ração tratados por ou compreendendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção. Em um aspecto, a invenção proporciona métodos para reduzir excremento alimentando um animal (por exemplo, uma ave, tal como uma ave doméstica, por exemplo, um frango) um alimento ou uma ração tratados por ou compreendendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção. Alimentos ou rações da invenção incluem suplementos dietéticos e aditivos dietéticos, quer para animais ou seres humanos.
[000349] A invenção proporciona alimento, ração, uma adição dietética ou suplementos dietéticos e/ou suplementos nutricionais para um animal (por exemplo, uma ave comestível, tal como um frango), ou ser humano, compreendendo um polipeptídeo da invenção, por exemplo, um polipeptídeo codificado pelo ácido nucleico da invenção. Em um aspecto, o polipeptídeo no alimento, ração, adições ou suplementos dietéticos e/ou suplementos nutricionais pode ser glicosilado. O alimento, ração, adições ou suplementos dietéticos e/ou suplementos nutricionais podem compreender qualquer planta comestível, incluindo qualquer material vegetal usado para forragem e/ou ração para qualquer animal, incluindo ruminantes, tais como feno, milho (por exemplo, silagem), arroz, milheto, soja, trigo, trigo- sarraceno, cevada, alfafa, centeio, gramíneas anuais (incluindo sorgos de forragem, grama para ferro, capim de savana, gramíneas para pastagem e forragem (buffel grass), e etc.) e similares. O alimento, ração, uma adição dietética ou suplementos dietéticos e/ou suplementos nutricionais da invenção também podem ser parte de ou adicionados ao alimento, ração ou material de forragem, por exemplo, para um animal ruminante, incluindo cabras, carneiro, gado/vacas, bisão e lhamas e similares. Enzimas da invenção podem ser adicionadas a, misturadas em ou pulverizadas sobre o material de forragem, alimento ou ração, vide, por exemplo, a patente dos Estados Unidos No. 4.627.338; alternativamente o alimento, ração ou material de forragem desta invenção pode compreender material vegetal transgênico que expressam uma ou mais enzimas desta invenção.
[000350] A invenção proporciona matrizes de liberação de enzimas comestíveis compreendendo um polipeptídeo da invenção, por exemplo, um polipeptídeo codificado pelo ácido nucleico da invenção. Em um aspecto, a matriz de liberação compreende um pélete compreendendo uma enzima da invenção, por exemplo, um pélete compreendendo uma enzima termotolerante ou termoestável da invenção). Em um aspecto, o polipeptídeo pode ser glicosilado (o que em um aspecto pode tornar a enzima mais termotolerante ou termoestável). Em um aspecto, a atividade da glucanase por exemplo, endoglucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase é termotolerante. Em outro aspecto, a atividade da glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase é termoestável.
[000351] A invenção proporciona um alimento, uma ração (por exemplo, uma ração animal, por exemplo, ração de animal monogástrico, tal como ração de suíno ou de aves domésticas (por exemplo, frango) ou um suplemento nutricional compreendendo um polipeptídeo da invenção. A invenção proporciona métodos para utilizar uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase como um suplemento nutricional em uma dieta animal, o método compreendendo: preparar um suplemento nutricional contendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, enzima celobio-hidrolase, mananase e/ou beta-glucosidase compreendendo pelo menos 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250 ou mais aminoácidos contíguos de um polipeptídeo da invenção; e administrar o suplemento nutricional a um animal para aumentar a utilização de um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo contido em uma ração ou um alimento ingerido pelo animal. O animal pode ser um ser humano, um ruminante ou um animal monogástrico. Por exemplo, o animal pode ser qualquer ave doméstica ou ave, por exemplo, um frango; ou suíno, o qual inclui suínos capados, porcos e similares. A glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, enzima celobio-hidrolase, mananase e/ou beta-glucosidase pode ser preparada por expressão de um polinucleotídeo codificando a glucanase em um organismo tal como uma bactéria, uma levedura, uma planta, um inseto, um fungo ou um animal. Organismos exemplares para expressar polipeptídeos da invenção podem ser S. pombe, S. cerevisiae, Pichia sp., por exemplo, P. pastoris, E. coli, Streptomyces sp., Bacillus sp. e Lactobacillus sp.
[000352] A invenção proporciona matriz de liberação de enzima comestível compreendendo uma enzima glucanase recombinante termoestável (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase, por exemplo, um polipeptídeo da invenção. A invenção proporciona métodos para liberar uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou suplemento de glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta glucosidase a um animal (um ser humano, um ruminante, um animal monogástrico, uma ave, por exemplo, um frango), o método compreendendo: preparar uma matriz de liberação de enzima comestível sob a forma de péletes compreendendo um veículo comestível granulado e uma enzima glucanase (ou celulase) isolada, sintética ou recombinante termoestável, por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, em que os péletes prontamente dispersam a enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase contida nesse em meio aquoso, e administrar a matriz de liberação de enzima comestível ao animal. A enzima glucanase recombinante (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase pode compreender um polipeptídeo da invenção. O veículo comestível granulado pode compreender um veículo selecionado entre o grupo consistindo em uma semente de cereais, uma semente de cereais que é esgotada de óleo, um feno, uma alfafa, um capim-rabo-de-gato, uma casca de soja, uma farinha grossa de semente de girassol e um farelo de trigo. O veículo comestível pode compreender semente de cereais que é esgotada de óleo. A enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase pode ser glicosilada para proporcionar termoestabilidade em condições de peletização. A matriz de liberação pode ser formada por peletização de uma mistura compreendendo uma semente de cereais e uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. As condições de peletização podem incluir aplicação de vapor. As condições de peletização podem compreender aplicação de uma temperatura em excesso de cerca de 80°C por cerca de 5 minutos e a enzima retém uma atividade específica de pelo menos 350 a cerca de 900 unidades por miligrama de enzima.
[000353] A invenção proporciona métodos para melhorar a textura e o sabor de um produto lácteo compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase, ou uma glucanase codificada por um ácido nucleico da invenção; (b) proporcionar um produto lácteo; e (c) contatar o polipeptídeo da etapa (a) e o produto lácteo da etapa (b) sob condições em que a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase pode melhorar a textura ou o aroma do produto lácteo. Em um aspecto, o produto lácteo compreende um queijo ou um iogurte. A invenção proporciona produtos lácteos compreendendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção, ou é codificada por um ácido nucleico da invenção.
[000354] A invenção proporciona métodos para melhorar a extração de óleo de um material vegetal rico em óleo compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta- glucosidase, ou uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase codificada por um ácido nucleico da invenção; (b) proporcionar um material vegetal rico em óleo; e (c) contatar o polipeptídeo da etapa (a) e o material vegetal rico em óleo. Em um aspecto, o material vegetal rico em óleo compreende uma semente rica em óleo. O óleo pode ser um óleo de soja, um azeite de oliva, um óleo de colza (canola) ou um óleo de girassol e similares.
[000355] Em um aspecto, a invenção proporciona métodos usando uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção para produzir açúcares fermentáveis que podem ser convertidos em etanol combustível. Em um aspecto, a invenção proporciona combustíveis compreendendo um ou mais polipeptídeos da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, ou uma glucanase codificada por um ácido nucleico da invenção. Em um aspecto, uma enzima da invenção é usada para catalisar a hidrólise de celuloses e hemiceluloses. A degradação de celulose pode ser usada para a conversão de biomassa vegetal em combustíveis e produtos químicos. Vide, por exemplo, Kohlmann (1996) Adv. Space Res. 18:251-265; Perez (2002) Int Microbiol. 5:5363.
[000356] Em outro aspecto, material vegetal compreendendo as enzimas descritas aqui, neste pedido de patente, podem ser usadas em um processo industrial para produzir combustível ou energia. Enzimas expressadas em plantas podem ser adicionadas ao, misturadas no ou pulverizadas sobre o material da matéria-prima. Alternativamente, as enzimas podem ser expressadas diretamente no material da matéria-prima. Em uma modalidade, material vegetal expressando enzimas pode ser triturado, moído, aquecido ou semelhantes, de modo a romper a integridade física das células de plantas ou órgãos que contêm a enzima, deste modo liberando a enzima para entrar em contato com o substrato. Fontes opcionais - típicas -de material vegetal incluem, mas não estão limitada a, milho, alfafa, girassol, Brassica, soja, algodão, açafrão, amendoim, sorgo, trigo, aveia, centeio, milheto, cevada, arroz, coníferas, gramíneas, por exemplo, switchgrass e Miscanthus, safras de leguminosas, por exemplo, ervilha, feijão e soja, tubérculos/raízes amiláceas, por exemplo, batata, batata-doce, mandioca, inhame, cana e beterrabaaçucareira e similares.
[000357] A invenção proporciona métodos para preparar um suco de fruta ou legume, xarope, purê ou extrato compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, ou uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase codificada por um ácido nucleico da invenção; (b) proporcionar uma composição ou um líquido compreendendo um material de fruto ou legume; e (c) contatar o polipeptídeo da etapa (a) e a composição, deste modo preparando o suco de fruta ou legume, xarope, purê ou extrato.
[000358] A invenção proporciona papéis ou produtos de papel ou polpa de papel compreendendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção, ou um polipeptídeo codificado por um ácido nucleico da invenção. A invenção proporciona métodos para tratar um papel ou uma polpa de papel ou madeira compreendendo as seguintes etapas: (a) proporcionar um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, ou uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase codificada por um ácido nucleico da invenção; (b) proporcionar uma composição compreendendo um papel ou uma polpa de papel ou de madeira; e (c) contatar o polipeptídeo da etapa (a) e a composição da etapa (b) sob condições em que a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase pode tratar o papel ou polpa de papel ou de madeira. Em um aspecto, a composição farmacêutica age como um auxiliar digestivo ou um antimicrobiano (por exemplo, contra Salmonella). Em um aspecto, o tratamento é profilático. Em um aspecto, a invenção proporciona produtos para tratamento oral compreendendo um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, ou uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase codificada por um ácido nucleico da invenção. O produto para tratamento oral pode compreender uma pasta de dentes, um creme dental, um gel ou um pó para os dentes, um odôntico, um enxaguatório bucal, uma formulação de enxágue pré- ou pós- escovação, uma goma de mascar, uma pastilha ou uma bala. A invenção proporciona composições para limpeza de lentes de contato compreendendo um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase, ou uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase codificada por um ácido nucleico da invenção.
[000359] Em um aspecto, a invenção proporciona métodos para eliminar ou proteger animais contra um micro-organismo compreendendo um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo compreendendo administrar um polipeptídeo da invenção. O micro-organismo pode ser uma bactéria compreendendo um glucano, por exemplo, Salmonella.
[000360] Outro aspecto da invenção é um método para produzir um polipeptídeo da invenção. O método inclui introduzir um ácido nucleico codificando o polipeptídeo em uma célula hospedeira, em que o ácido nucleico é ligado operavelmente a um promotor e cultivar a célula hospedeira sob condições que permitem a expressão do ácido nucleico. Outro aspecto da invenção é um método para produzir um polipeptídeo tendo pelo menos 10 aminoácidos de uma sequência conforme determinado nas sequências de aminoácidos da invenção. O método inclui introduzir um ácido nucleico codificando o polipeptídeo em uma célula hospedeira, em que o ácido nucleico é ligado operavelmente a um promotor e cultivar a célula hospedeira sob condições que permitem expressão do ácido nucleico, deste modo produzindo o polipeptídeo.
[000361] Outro aspecto da invenção é um método para gerar uma variante incluindo obter um ácido nucleico tendo uma sequência da invenção, sequências substancialmente idênticas a essa, sequências complementares a uma sequência da invenção, fragmentos compreendendo pelo menos 30 nucleotídeos consecutivos das sequências precedentes e mudar um ou mais nucleotídeos na sequência para outro nucleotídeo, eliminar um ou mais nucleotídeos na sequência, ou adicionar um ou mais nucleotídeos à sequência.
[000362] Outro aspecto da invenção é um meio legível por computador tendo armazenado sobre o mesmo um sequência de ácido nucleico ou polipeptídeo da invenção. Outro aspecto da invenção é um sistema de computação incluindo um processador e um dispositivo de armazenamento de dados em que o dispositivo de armazenamento de dados tem armazenado sobre o mesmo um sequência de ácido nucleico ou polipeptídeo da invenção. Outro aspecto da invenção é um método para comparar uma primeira sequência com uma sequência de referência em que a primeira sequência é uma sequência de ácido nucleico ou polipeptídeo da invenção. O método inclui ler a primeira sequência e a sequência de referência através do uso de um programa de computação que compara sequências; e determinar diferenças entre a primeira sequência e a sequência de referência com o programa de computação. Outro aspecto da invenção é um método para identificar uma característica em um sequência de ácido nucleico ou polipeptídeo da invenção, incluindo ler a sequência através do uso de um programa de computação o qual identifica características em sequências; e identificar características na sequência com o programa de computação.
[000363] Ainda outro aspecto da invenção é um método para catalisar a decomposição de glicano ou um derivado do mesmo, compreendendo a etapa de contatar uma amostra contendo um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo ou um derivado da mesma com um polipeptídeo da invenção sob condições as quais facilitam a decomposição de um glucano.
[000364] Outro aspecto da invenção é um ensaio para identificar fragmentos ou variantes de um polipeptídeo da invenção, o qual retém a função enzimática (por exemplo, uma atividade de glucanase) de um polipeptídeo (por exemplo, enzima ou anticorpo) da invenção, incluindo sequências típicas da invenção. O ensaio inclui contatar um polipeptídeo da invenção com uma molécula de substrato sob condições as quais permitem que o polipeptídeo fragmento ou variante funcione e detectar ou uma redução no nível do substrato ou um aumento no nível do produto da reação específico da reação entre o polipeptídeo e o substrato deste modo identificando um fragmento ou uma variante de semelhantes sequências.
[000365] Em ainda outro aspecto, a invenção proporciona uma preparação de proteína compreendendo um polipeptídeo tendo uma sequência de aminoácidos da invenção em que a preparação de proteína é um líquido. Ainda outro aspecto da invenção proporciona uma preparação de proteína compreendendo um polipeptídeo tendo uma sequência de aminoácidos da invenção em que o polipeptídeo é um sólido.
[000366] Ainda outro aspecto da invenção proporciona um método para modificar moléculas pequenas, compreendendo a etapa de misturar pelo menos um polipeptídeo da invenção com pelo menos uma molécula pequena, para produzir pelo menos uma molécula pequena modificada através de pelo menos uma reação biocatalítica, onde o pelo menos um polipeptídeo tem atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase.
[000367] Outro aspecto da invenção é um vetor de clonagem de uma sequência que codifica um polipeptídeo da invenção tendo uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. Outro aspecto da invenção é uma célula hospedeira compreendendo uma sequência que codifica um polipeptídeo da invenção. Em ainda outro aspecto, a invenção proporciona um vetor de expressão capaz de replicação em uma célula hospedeira compreendendo um ácido nucleico da invenção ou um ácido nucleico codificando um polinucleotídeo da invenção.
[000368] Em outro aspecto, a invenção proporciona um método de condicionamento de massa de pão compreendendo contatar massa de pão com pelo menos um polipeptídeo da invenção sob condições suficientes para condicionar a massa de pão. Outro aspecto da invenção é um método de produção de bebida compreendendo administração de pelo menos um polipeptídeo da invenção sob condições suficientes para reduzir a viscosidade de cerveja não- fermentada, ou, aumentar a claridade (por exemplo, clarificação) da bebida.
[000369] As glucanases (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção são usadas para a decomposição dos glucanos, mananos, arabinoxilanos ou xilanos de alto peso molecular, ou outros polissacarídeos em ração animal (por exemplo, uma ração para um ser humano, um ruminante, um animal monogástrico, uma ave, por exemplo, um frango). Adicionar as enzimas da invenção estimula as taxas de crescimento melhorando a digestibilidade, o que também melhora a qualidade da ninhada do animal. A glucanase age através do trato gastrointestinal reduzindo a viscosidade intestinal e aumentando a difusão de enzimas pancreáticas. Adicionalmente, as enzimas da invenção podem ser usadas no tratamento das paredes de células do endosperma de grãos de ração e proteínas vegetais. Em um aspecto da invenção, as novas enzimas da invenção são administradas a um animal de modo a aumentar a utilização de um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo no alimento. Esta atividade das enzimas da invenção pode ser usada para decompor material insolúvel das paredes celulares, liberando nutrientes nas paredes celulares, os quais então se tornam disponíveis para o animal. Também muda hemicelulose para açúcares nutritivos de modo que nutrientes capturados anteriormente dentro das paredes celulares sejam liberados. Enzimas glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção podem produzir compostos que podem ser uma fonte nutritiva para a microflora ruminal.
[000370] Outro aspecto da invenção proporciona um método para utilizar glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase como um aditivo de alimento ou de ração ou um suplemento nutricional nas dietas de animais, compreendendo preparação de um suplemento nutricional contendo uma enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase recombinante da invenção, ou uma subsequência enzimaticamente ativa da mesma, por exemplo, uma subsequência compreendendo pelo menos trinta, 40, 50, 60, 70, 80, 90 ou 100 ou mais aminoácidos contíguos de uma sequência de aminoácidos da invenção, e administrar o aditivo de alimento ou de ração ou suplemento nutricional a um animal para aumentar a utilização de um glucano, um manano, um arabinoxilano ou um xilano, ou outro polissacarídeo contido em alimento ingerido pelo animal.
[000371] Em outro aspecto da invenção, é proporcionado um método para liberar um suplemento de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase para um animal, onde o método compreende preparar uma matriz de liberação de enzima comestível sob a forma de péletes compreendendo um veículo comestível granulado e uma enzima termoestável recombinante ou sintética glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, em que as partículas dispersam prontamente a enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase contida nesse em meio aquoso, e administrar a matriz de liberação de enzima comestível ao animal. O veículo comestível granulado pode compreender um veículo selecionado entre o grupo consistindo em semente de cereais que é esgotada de óleo, feno, alfafa, capim-rabo-de-gato, casca de soja, farinha grossa de semente de girassol e farelo de trigo. A enzima glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase pode ter uma sequência de aminoácidos da invenção.
[000372] A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes, em que o ácido nucleico codifica pelo menos um polipeptídeo tendo uma atividade de glucanase, ou codifica um polipeptídeo ou peptídeo capaz de produzir um anticorpo que ligase especificamente a um polipeptídeo tendo a sequência de SEQ ID NO: 2, e a sequência compreende as seguintes alterações com base na SEQ ID NO: 1:
[000373] (A) os nucleotídeos nas posições 112 a 114 são TAT ou TAC, os nucleotídeos nas posições 181 a 183 são CAA ou CAG, os nucleotídeos nas posições 205 a 207 são GAA ou GAG, os nucleotídeos nas posições 280 a 282 são CAA ou CAG, os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG, e os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG;
[000374] (B) os nucleotídeos nas posições 112 a 114 são TAT ou TAC, os nucleotídeos nas posições 181 a 183 são CAA ou CAG, os nucleotídeos nas posições 205 a 207 são GAA ou GAG, os nucleotídeos nas posições 280 a 282 são CAA ou CAG, os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG, os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT, os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG, e os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG;
[000375] (C) os nucleotídeos nas posições 112 a 114 são TAT ou TAC, os nucleotídeos nas posições 181 a 183 são CAA ou CAG, os nucleotídeos nas posições 205 a 207 são GAA ou GAG, os nucleotídeos nas posições 280 a 282 são CAA ou CAG, os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG, os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT, os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG, e os nucleotídeos nas posições 889 a 891 são CCA, CCC, CCG ou CCT;
[000376] (D) os nucleotídeos nas posições 181 a 183 são CAA ou CAG, os nucleotídeos nas posições 205 a 207 são GAA ou GAG, os nucleotídeos nas posições 280 a 282 são CAA ou CAG, os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG, os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT, os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG, os nucleotídeos nas posições 889 a 891 são CCA, CCC, CCG ou CCT, e os nucleotídeos nas posições 901 a 903 são CAA ou CAG;
[000377] (E) os nucleotídeos nas posições 181 a 183 são CAA ou CAG, os nucleotídeos nas posições 205 a 207 são GAA ou GAG, os nucleotídeos nas posições 211 a 213 são TCT, TCC, TCA, TCG, AGT ou AGC, os nucleotídeos nas posições 280 a 282 são CAA ou CAG, os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG, os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT, os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG, os nucleotídeos nas posições 889 a 891 são CCA, CCC, CCG ou CCT, e os nucleotídeos nas posições 901 a 903 são CAA ou CAG;
[000378] (F) os nucleotídeos nas posições 181 a 183 são CAA ou CAG, os nucleotídeos nas posições 205 a 207 são GAA ou GAG, os nucleotídeos nas posições 208 a 210 são CCA, CCC, CCG ou CCT, os nucleotídeos nas posições 211 a 213 são TCT, TCC, TCA, TCG, AGT ou AGC, os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG, os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT, os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG, os nucleotídeos nas posições 889 a 891 são CCA, CCC, CCG ou CCT, e os nucleotídeos nas posições 901 a 903 são CAA ou CAG;
[000379] (G) os nucleotídeos nas posições 112 a 114 são TAT ou TAC, os nucleotídeos nas posições 181 a 183 são CAA ou CAG, os nucleotídeos nas posições 205 a 207 são GAA ou GAG, os nucleotídeos nas posições 211 a 213 são TCT, TCC, TCA, TCG, AGT ou AGC, os nucleotídeos nas posições 496 a 498 são GTT, GTC, GTA ou GTG, os nucleotídeos nas posições 547 a 549 são CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos nas posições 571 a 573 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 634 a 636 são CCA, CCC, CCG ou CCT, os nucleotídeos nas posições 691 a 693 são ATT, ATC ou ATA, os nucleotídeos nas posições 826 a 828 são GCT, GCC, GCA ou GCG, os nucleotídeos nas posições 838 a 840 são GGT, GGC, GGA ou GGG, os nucleotídeos nas posições 889 a 891 são CCA, CCC, CCG ou CCT, e os nucleotídeos nas posições 901 a 903 são CAA ou CAG;
[000380] (H) os nucleotídeos no equivalente das posições 112 a 114 de SEQ ID NO: 1 são alterados para TAT ou TAC, os nucleotídeos no equivalente das posições 181 a 183 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 205 a 207 de SEQ ID NO: 1 são alterados para GAA ou GAG, os nucleotídeos no equivalente das posições 280 a 282 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 547 a 549 de SEQ ID NO: 1 são alterados para CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos no equivalente das posições 571 a 573 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, e os nucleotídeos no equivalente das posições 826 a 828 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG;
[000381] (I) os nucleotídeos no equivalente das posições 112 a 114 de SEQ ID NO: 1 são alterados para TAT ou TAC, os nucleotídeos no equivalente das posições 181 a 183 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 205 a 207 de SEQ ID NO: 1 são alterados para GAA ou GAG, os nucleotídeos no equivalente das posições 280 a 282 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 496 a 498 de SEQ ID NO: 1 são alterados para GTT, GTC, GTA ou GTG, os nucleotídeos no equivalente das posições 547 a 549 de SEQ ID NO: 1 são alterados para CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos no equivalente das posições 571 a 573 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 634 a 636 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, os nucleotídeos no equivalente das posições 826 a 828 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, e os nucleotídeos no equivalente das posições 838 a 840 de SEQ ID NO: 1 são alterados para GGT, GGC, GGA ou GGG;
[000382] (J) os nucleotídeos no equivalente das posições 112 a 114 de SEQ ID NO: 1 são alterados para TAT ou TAC, os nucleotídeos no equivalente das posições 181 a 183 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 205 a 207 de SEQ ID NO: 1 são alterados para GAA ou GAG, os nucleotídeos no equivalente das posições 280 a 282 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 496 a 498 de SEQ ID NO: 1 são alterados para GTT, GTC, GTA ou GTG, os nucleotídeos no equivalente das posições 547 a 549 de SEQ ID NO: 1 são alterados para CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos no equivalente das posições 571 a 573 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 634 a 636 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, os nucleotídeos no equivalente das posições 826 a 828 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 838 a 840 de SEQ ID NO: 1 são alterados para GGT, GGC, GGA ou GGG, e os nucleotídeos no equivalente das posições 889 a 891 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT;
[000383] (K) os nucleotídeos no equivalente das posições 181 a 183 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 205 a 207 de SEQ ID NO: 1 são alterados para GAA ou GAG, os nucleotídeos no equivalente das posições 280 a 282 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 496 a 498 de SEQ ID NO: 1 são alterados para GTT, GTC, GTA ou GTG, os nucleotídeos no equivalente das posições 547 a 549 de SEQ ID NO: 1 são alterados para CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos no equivalente das posições 571 a 573 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 634 a 636 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, os nucleotídeos no equivalente das posições 826 a 828 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 838 a 840 de SEQ ID NO: 1 são alterados para GGT, GGC, GGA ou GGG, os nucleotídeos no equivalente das posições 889 a 891 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, e os nucleotídeos no equivalente das posições 901 a 903 de SEQ ID NO: 1 são alterados para CAA ou CAG;
[000384] (L) os nucleotídeos no equivalente das posições 181 a 183 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 205 a 207 de SEQ ID NO: 1 são alterados para GAA ou GAG, os nucleotídeos no equivalente das posições 211 a 213 de SEQ ID NO: 1 são alterados para TCT, TCC, TCA, TCG, AGT ou AGC, os nucleotídeos no equivalente das posições 280 a 282 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 496 a 498 de SEQ ID NO: 1 são alterados para GTT, GTC, GTA ou GTG, os nucleotídeos no equivalente das posições 547 a 549 de SEQ ID NO: 1 são alterados para CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos no equivalente das posições 571 a 573 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 634 a 636 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, os nucleotídeos no equivalente das posições 826 a 828 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 838 a 840 de SEQ ID NO: 1 são alterados para GGT, GGC, GGA ou GGG, os nucleotídeos no equivalente das posições 889 a 891 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, e os nucleotídeos no equivalente das posições 901 a 903 de SEQ ID NO: 1 são alterados para CAA ou CAG;
[000385] (M) os nucleotídeos no equivalente das posições 181 a 183 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 205 a 207 de SEQ ID NO: 1 são alterados para GAA ou GAG, os nucleotídeos no equivalente das posições 208 a 210 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, os nucleotídeos no equivalente das posições 211 a 213 de SEQ ID NO: 1 são alterados para TCT, TCC, TCA, TCG, AGT ou AGC, os nucleotídeos no equivalente das posições 496 a 498 de SEQ ID NO: 1 são alterados para GTT, GTC, GTA ou GTG, os nucleotídeos no equivalente das posições 547 a 549 de SEQ ID NO: 1 são alterados para CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos no equivalente das posições 571 a 573 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 634 a 636 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, os nucleotídeos no equivalente das posições 826 a 828 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 838 a 840 de SEQ ID NO: 1 são alterados para GGT, GGC, GGA ou GGG, os nucleotídeos no equivalente das posições 889 a 891 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, e os nucleotídeos no equivalente das posições 901 a 903 de SEQ ID NO: 1 são alterados para CAA ou CAG; ou,
[000386] (N) os nucleotídeos no equivalente das posições 112 a 114 de SEQ ID NO: 1 são alterados para TAT ou TAC, os nucleotídeos no equivalente das posições 181 a 183 de SEQ ID NO: 1 são alterados para CAA ou CAG, os nucleotídeos no equivalente das posições 205 a 207 de SEQ ID NO: 1 são alterados para GAA ou GAG, os nucleotídeos no equivalente das posições 211 a 213 de SEQ ID NO: 1 são alterados para TCT, TCC, TCA, TCG, AGT ou AGC, os nucleotídeos no equivalente das posições 496 a 498 de SEQ ID NO: 1 são alterados para GTT, GTC, GTA ou GTG, os nucleotídeos no equivalente das posições 547 a 549 de SEQ ID NO: 1 são alterados para CGT, CGC, CGA, CGG, AGA ou AGG, os nucleotídeos no equivalente das posições 571 a 573 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 634 a 636 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, os nucleotídeos no equivalente das posições 691 a 693 de SEQ ID NO: 1 são alterados para ATT, ATC ou ATA, os nucleotídeos no equivalente das posições 826 a 828 de SEQ ID NO: 1 são alterados para GCT, GCC, GCA ou GCG, os nucleotídeos no equivalente das posições 838 a 840 de SEQ ID NO: 1 são alterados para GGT, GGC, GGA ou GGG, os nucleotídeos no equivalente das posições 889 a 891 de SEQ ID NO: 1 são alterados para CCA, CCC, CCG ou CCT, e os nucleotídeos no equivalente das posições 901 a 903 de SEQ ID NO: 1 são alterados para CAA ou CAG;
[000387] A invenção proporciona polipeptídeos isolados, sintéticos ou recombinantes tendo uma atividade de glucanase ou polipeptídeos ou peptídeos capazes de produzir um anticorpo que se liga especificamente a um polipeptídeo tendo a sequência de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, E SEQ ID NO: 23, e a sequência compreende as seguintes alterações com base na SEQ ID NO: 2:
[000388] (A) a fenilalanina na posição do aminoácido 38 é tirosina, a tirosina na posição do aminoácido 61 é glutamina, a metionina na posição do aminoácido 69 é ácido glutâmico, a isoleucina na posição do aminoácido 94 é glutamina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 191 é alanina, e a metionina na posição do aminoácido 276 é alanina;
[000389] (B) a fenilalanina na posição do aminoácido 38 é tirosina, a tirosina na posição do aminoácido 61 é glutamina, a metionina na posição do aminoácido 69 é ácido glutâmico, a isoleucina na posição do aminoácido 94 é glutamina, a isoleucina na posição do aminoácido 166 é valina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 191 é alanina, o ácido glutâmico na posição do aminoácido 212 é prolina, a metionina na posição do aminoácido 276 é alanina, e a arginina na posição do aminoácido 280 é glicina;
[000390] (C) a fenilalanina na posição do aminoácido 38 é tirosina, a tirosina na posição do aminoácido 61 é glutamina, a metionina na posição do aminoácido 69 é ácido glutâmico, a isoleucina na posição do aminoácido 94 é glutamina, a isoleucina na posição do aminoácido 166 é valina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 191 é alanina, o ácido glutâmico na posição do aminoácido 212 é prolina, a metionina na posição do aminoácido 276 é alanina, a arginina na posição do aminoácido 280 é glicina, e a treonina na posição do aminoácido 297 é prolina;
[000391] (D) a tirosina na posição do aminoácido 61 é glutamina, a metionina na posição do aminoácido 69 é ácido glutâmico, a isoleucina na posição do aminoácido 94 é glutamina, a isoleucina na posição do aminoácido 166 é valina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 191 é alanina, o ácido glutâmico na posição do aminoácido 212 é prolina, a metionina na posição do aminoácido 276 é alanina, a arginina na posição do aminoácido 280 é glicina, a treonina na posição do aminoácido 297 é prolina, e a treonina na posição do aminoácido 301 é glutamina;
[000392] (E) a tirosina na posição do aminoácido 61 é glutamina, a metionina na posição do aminoácido 69 é ácido glutâmico, a arginina na posição do aminoácido 71 é serina, a isoleucina na posição do aminoácido 94 é glutamina, a isoleucina na posição do aminoácido 166 é valina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 191 é alanina, o ácido glutâmico na posição do aminoácido 212 é prolina, a metionina na posição do aminoácido 276 é alanina, a arginina na posição do aminoácido 280 é glicina, a treonina na posição do aminoácido 297 é prolina, e a treonina na posição do aminoácido 301 é glutamina;
[000393] (F) a tirosina na posição do aminoácido 61 é glutamina, a metionina na posição do aminoácido 69 é ácido glutâmico, o ácido aspártico na posição do aminoácido 70 é prolina, a arginina na posição do aminoácido 71 é serina, a isoleucina na posição do aminoácido 166 é valina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 191 é alanina, o ácido glutâmico na posição do aminoácido 212 é prolina, a metionina na posição do aminoácido 276 é alanina, a arginina na posição do aminoácido 280 é glicina, a treonina na posição do aminoácido 297 é prolina, e a treonina na posição do aminoácido 301 é glutamina;
[000394] (G) a fenilalanina na posição do aminoácido 38 é tirosina, a tirosina na posição do aminoácido 61 é glutamina, a metionina na posição do aminoácido 69 é ácido glutâmico, a arginina na posição do aminoácido 71 é serina, a isoleucina na posição do aminoácido 166 é valina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 191 é alanina, o ácido glutâmico na posição do aminoácido 212 é prolina, a leucina na posição do aminoácido 231 é valina, a metionina na posição do aminoácido 276 é alanina, a arginina na posição do aminoácido 280 é glicina, a treonina na posição do aminoácido 297 é prolina, e a treonina na posição do aminoácido 301 é glutamina;
[000395] (H) o aminoácido no equivalente da fenilalanina na posição do aminoácido 38 de SEQ ID NO: 2 é alterado para uma tirosina, o aminoácido no equivalente da tirosina na posição do aminoácido 61 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da metionina na posição do aminoácido 69 de SEQ ID NO: 2 é alterado para um ácido glutâmico, o aminoácido no equivalente da isoleucina na posição do aminoácido 94 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da serina na posição do aminoácido 183 de SEQ ID NO: 2 é alterado para uma arginina, o aminoácido no equivalente da serina na posição do aminoácido 191 de SEQ ID NO: 2 é alterado para uma alanina, e o aminoácido no equivalente da metionina na posição do aminoácido 276 de SEQ ID NO: 2 é alterado para uma alanina;
[000396] (J) o aminoácido no equivalente da fenilalanina na posição do aminoácido 38 de SEQ ID NO: 2 é alterado para uma tirosina, o aminoácido no equivalente da tirosina na posição do aminoácido 61 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da metionina na posição do aminoácido 69 de SEQ ID NO: 2 é alterado para um ácido glutâmico, o aminoácido no equivalente da isoleucina na posição do aminoácido 94 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da isoleucina na posição do aminoácido 166 de SEQ ID NO: 2 é alterado para uma valina, o aminoácido no equivalente da serina na posição do aminoácido 183 de SEQ ID NO: 2 é alterado para uma arginina, o aminoácido no equivalente da serina na posição do aminoácido 191 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente do ácido glutâmico na posição do aminoácido 212 de SEQ ID NO: 2 é alterado para uma prolina, o aminoácido no equivalente da metionina na posição do aminoácido 276 de SEQ ID NO: 2 é alterado para uma alanina, e o aminoácido no equivalente da arginina na posição do aminoácido 280 de SEQ ID NO: 2 é alterado para uma glicina;
[000397] (K) o aminoácido no equivalente da fenilalanina na posição do aminoácido 38 de SEQ ID NO: 2 é alterado para uma tirosina, o aminoácido no equivalente da tirosina na posição do aminoácido 61 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da metionina na posição do aminoácido 69 de SEQ ID NO: 2 é alterado para um ácido glutâmico, o aminoácido no equivalente da isoleucina na posição do aminoácido 94 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da isoleucina na posição do aminoácido 166 de SEQ ID NO: 2 é alterado para uma valina, o aminoácido no equivalente da serina na posição do aminoácido 183 de SEQ ID NO: 2 é alterado para uma arginina, o aminoácido no equivalente da serina na posição do aminoácido 191 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente do ácido glutâmico na posição do aminoácido 212 de SEQ ID NO: 2 é alterado para uma prolina, o aminoácido no equivalente da metionina na posição do aminoácido 276 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente da arginina na posição do aminoácido 280 de SEQ ID NO: 2 é alterado para uma glicina, e o aminoácido no equivalente da treonina na posição do aminoácido 297 de SEQ ID NO: 2 é alterado para uma prolina;
[000398] (L) o aminoácido no equivalente da tirosina na posição do aminoácido 61 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da metionina na posição do aminoácido 69 de SEQ ID NO: 2 é alterado para um ácido glutâmico, o aminoácido no equivalente da isoleucina na posição do aminoácido 94 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da isoleucina na posição do aminoácido 166 de SEQ ID NO: 2 é alterado para uma valina, o aminoácido no equivalente da serina na posição do aminoácido 183 de SEQ ID NO: 2 é alterado para uma arginina, o aminoácido no equivalente da serina na posição do aminoácido 191 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente do ácido glutâmico na posição do aminoácido 212 de SEQ ID NO: 2 é alterado para uma prolina, o aminoácido no equivalente da metionina na posição do aminoácido 276 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente da arginina na posição do aminoácido 280 de SEQ ID NO: 2 é alterado para uma glicina, o aminoácido no equivalente da treonina na posição do aminoácido 297 de SEQ ID NO: 2 é alterado para uma prolina, e o aminoácido no equivalente da treonina na posição do aminoácido 301 de SEQ ID NO: 2 é alterado para uma glutamina;
[000399] (M) o aminoácido no equivalente da tirosina na posição do aminoácido 61 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da metionina na posição do aminoácido 69 de SEQ ID NO: 2 é alterado para um ácido glutâmico, o aminoácido no equivalente da arginina na posição do aminoácido 71 de SEQ ID NO: 2 é alterado para uma serina, o aminoácido no equivalente da isoleucina na posição do aminoácido 94 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da isoleucina na posição do aminoácido 166 de SEQ ID NO: 2 é alterado para uma valina, o aminoácido no equivalente da serina na posição do aminoácido 183 de SEQ ID NO: 2 é alterado para uma arginina, o aminoácido no equivalente da serina na posição do aminoácido 191 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente do ácido glutâmico na posição do aminoácido 212 de SEQ ID NO: 2 é alterado para uma prolina, o aminoácido no equivalente da metionina na posição do aminoácido 276 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente da arginina na posição do aminoácido 280 de SEQ ID NO: 2 é alterado para uma glicina, o aminoácido no equivalente da treonina na posição do aminoácido 297 de SEQ ID NO: 2 é alterado para uma prolina, e o aminoácido no equivalente da treonina na posição do aminoácido 301 de SEQ ID NO: 2 é alterado para uma glutamina;
[000400] (N) o aminoácido no equivalente da tirosina na posição do aminoácido 61 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da metionina na posição do aminoácido 69 de SEQ ID NO: 2 é alterado para um ácido glutâmico, o aminoácido no equivalente do ácido aspártico na posição do aminoácido 70 de SEQ ID NO: 2 é alterado para uma prolina, o aminoácido no equivalente da arginina na posição do aminoácido 71 de SEQ ID NO: 2 é alterado para uma serina, o aminoácido no equivalente da isoleucina na posição do aminoácido 166 de SEQ ID NO: 2 é alterado para uma valina, o aminoácido no equivalente da serina na posição do aminoácido 183 de SEQ ID NO: 2 é alterado para uma arginina, o aminoácido no equivalente da serina na posição do aminoácido 191 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente do ácido glutâmico na posição do aminoácido 212 de SEQ ID NO: 2 é alterado para uma prolina, o aminoácido no equivalente da metionina na posição do aminoácido 276 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente da arginina na posição do aminoácido 280 de SEQ ID NO: 2 é alterado para uma glicina, o aminoácido no equivalente da treonina na posição do aminoácido 297 de SEQ ID NO: 2 é alterado para uma prolina, e o aminoácido no equivalente da treonina na posição do aminoácido 301 de SEQ ID NO: 2 é alterado para uma glutamina;
[000401] (O) o aminoácido no equivalente da fenilalanina na posição do aminoácido 38 de SEQ ID NO: 2 é alterado para uma tirosina, o aminoácido no equivalente da tirosina na posição do aminoácido 61 de SEQ ID NO: 2 é alterado para uma glutamina, o aminoácido no equivalente da metionina na posição do aminoácido 69 de SEQ ID NO: 2 é alterado para um ácido glutâmico, o aminoácido no equivalente da arginina na posição do aminoácido 71 de SEQ ID NO: 2 é alterado para uma serina, o aminoácido no equivalente da isoleucina na posição do aminoácido 166 de SEQ ID NO: 2 é alterado para uma valina, o aminoácido no equivalente da serina na posição do aminoácido 183 de SEQ ID NO: 2 é alterado para uma arginina, o aminoácido no equivalente da serina na posição do aminoácido 191 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente do ácido glutâmico na posição do aminoácido 212 de SEQ ID NO: 2 é alterado para uma prolina, o aminoácido no equivalente da leucina na posição do aminoácido 231 de SEQ ID NO: 2 é alterado para uma valina, o aminoácido no equivalente da metionina na posição do aminoácido 276 de SEQ ID NO: 2 é alterado para uma alanina, o aminoácido no equivalente da arginina na posição do aminoácido 280 de SEQ ID NO: 2 é alterado para uma glicina, o aminoácido no equivalente da treonina na posição do aminoácido 297 de SEQ ID NO: 2 é alterado para uma prolina, e o aminoácido no equivalente da treonina na posição do aminoácido 301 de SEQ ID NO: 2 é alterado para uma glutamina.
[000402] A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes da invenção (incluindo os ácidos nucleicos codificando glucanase da invenção), em que resíduos nucleotídeo em um sítio de iniciação transcripcional críptica são modificados para eliminar a maior parte ou toda a produção de um transcripto truncado. Em um aspecto, as modificações de resíduos nucleotídeo no sítio de iniciação transcripcional críptica compreendem uma alteração em um sítio de ligação de ribossoma (RBS), por exemplo, as modificações de resíduos nucleotídeo no sítio de iniciação transcripcional críptica compreendem as seguintes modificações nos resíduos 77 a 106 de SEQ ID NO: 3: ATGAGGGCGACTGGGGAGTCGTGATAAAAG, ou equivalente.
[000403] A invenção proporciona polipeptídeos isolados, sintéticos ou recombinantes da invenção, em que o polipeptídeo adicionalmente compreende resíduos aminoácido adicionais entre a sequência de sinal (peptídeo líder) e a enzima; e em um aspecto, os resíduos aminoácido adicionais compreendem Glu-Ala, por exemplo, os resíduos aminoácido adicionais Glu-Ala são adicionados entre o resíduo XX e YY na SEQ ID NO: 2, por exemplo, os resíduos aminoácido adicionais Glu-Ala são adicionados entre o resíduo K-R de SEQ ID NO: 2 conforme ilustrado: MRFPSIFTAVLFAASSALAAPVNT TTEDETAQIPAEAVIGYSDLEGDFDVAVLPFSNSTNNGLLFINTTIASIAA KEEGVSLEKRGVDPFERNKILGRGINI (da SEQ ID NO: 2). Usando Enzimas de Degradação de Polímero em Processos de Perfuração e Industriais
[000404] A invenção proporciona composições para e métodos para usar enzimas de degradação de polímeros, tais como enzimas de degradação de polissacarídeos, em processos de perfuração de óleo, gás e relacionados e processos de lavagem e/ou fraturamento de poço de óleo e gás.
[000405] A invenção proporciona composições e métodos para usar enzimas de degradação de polímeros para modificar as propriedades reológicas de espessantes polissacarídicos (por exemplo, gomas guar), por exemplo, como enzimas para modificar polissacarídeos em géis e floculados, aglutinantes, lubrificantes, para servir como modificadores das propriedades de filmes, e têm uma função como ajustadores de parâmetros reológicos nestas composições.
[000406] Em um aspecto, enzimas de degradação de polímeros, por exemplo, enzimas de degradação de polissacarídeos (por exemplo, de degradação de amido), usadas para praticar esta invenção, incluindo qualquer amilase, glucanase, xantanase, glicosidase e/ou celulase, as quais incluem usar “coquetéis” de enzimas conforme descrito aqui, neste pedido de patente, e/ou outras enzimas. Em um aspecto, os polímeros degradados pelas composições (incluindo as misturas de enzimas) e métodos desta invenção incluem lignina, amido, celulose, derivados celulósicos (por exemplo, carboximetila celulose e hidroxietila celulose, goma guar, goma guar derivada, goma de alfarroba, beta- glucano e derivados de beta glucano, goma xantana, guar de hidroxialquila, guar de carboxialquila, ou polímeros de xantana ou derivados dos mesmos, tais como borato de guar, e/ou combinações dos mesmos.
[000407] Em uma modalidade, a invenção proporciona métodos compreendendo o uso de misturas (“coquetéis”) de enzimas compreendendo pelo menos uma, duas, três, quatro, cinco, seis, sete, oito, nove, dez, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 ou 25 ou mais ou todas as enzimas selecionadas entre o grupo consistindo em uma enzima de degradação de lignina, alfa amilase, beta amilase, glucoamilase, dextrinase, celulase, celobio-hidrolase, avicelase, carboximetilcelulase, beta-glucanase, glucosidase, xilanase, mananase, arabinofuranosidase, lacase, lignina peroxidase, pectinase, pectate liase, xantanase, xantana liase, xantana depolimerase, pululanase, liquenase, paquimanase, lipase, protease, proteinase, fitase, peptidase e catalase.
[000408] Por exemplo, em uma modalidade, métodos da invenção usando misturas (“coquetéis”) de enzimas são usados para degradar um guar, guar de hidroxialquila, guar de carboxialquila, goma guar, um pó de goma guar, ou uma camada lignificada de sementes de guar uma goma guar solidificada; e em um aspecto, o método compreende proporcionar uma mistura de enzimas de degradação de polímeros, em que pelo menos uma das enzimas é uma enzima de degradação de polímeros, e opcionalmente a enzima de degradação de polímeros é uma enzima de degradação de lignina, uma lignina peroxidase, uma enzima de degradação de polissacarídeos, uma enzima de degradação de proteína, uma amilase, uma xantanase, uma glucanase, uma protease, uma glicosidase e/ou uma celulase; e adicionar a mistura de enzimas de degradação de polímero à goma guar, ao pó de goma guar, à camada lignificada de sementes de guar ou à goma guar solidificada em uma quantidade suficiente para degradar a goma guar, o pó de goma guar, a camada lignificada de sementes de guar ou a goma guar solidificada.
[000409] Em outra modalidade, a invenção proporciona métodos para perfuração de poço de óleo e gás ou um método de lavagem e/ou fraturamento usando misturas (“coquetéis”) de enzimas; e em um aspecto, a mistura (“coquetel”) compreende enzimas de degradação de polímeros, e opcionalmente pelo menos uma enzima de degradação de polímeros é uma enzima de degradação de lignina, uma lignina peroxidase, uma enzima de degradação de polissacarídeos, uma enzima de degradação de proteína, uma amilase, uma xantanase, uma glucanase, uma protease, uma glicosidase e/ou uma celulase; e adicionar a mistura de enzimas de degradação de polímeros ao guar, ao guar de hidroxialquila, ao guar de carboxialquila, à goma guar, ao pó de goma guar, à camada lignificada de sementes de guar ou à goma guar solidificada em uma quantidade suficiente para degradar a goma guar, o pó de goma guar, a camada lignificada de sementes de guar ou a goma guar solidificada. Em um aspecto, os polímeros degradados compreendem lignina, amido, celulose, guar, guar de hidroxialquila, guar de carboxialquila, ou polímeros de xantana ou derivados dos mesmos, tais como borato de guar, e/ou combinações dos mesmos.
[000410] Em um aspecto, a composição e métodos da invenção são usados para degradar “torta de lama” (também conhecida como "torta de filtro") que acumula sobre uma parede do orifício do poço em um poço de óleo e/ou gás, produzindo enzimas de degradação de polímeros, tais como enzimas de degradação de polissacarídeos (por exemplo, amido) em fluidos de perfuração de poço de óleo e processos de lavagem e/ou fraturamento de poço de óleo e gás, e dando origem a sua ação por ajuste do pH. Em um aspecto, os polímeros degradados compreendem lignina, amido, celulose, guar ou xantana.
[000411] Em uma modalidade, a invenção proporciona a produção de uma enzima de degradação de polímeros (vide abaixo) no fluido de perfuração usado nas operações de perfuração de óleo e gás e/ou nos fluidos de lavagem e/ou fraturamento de poço de óleo e gás. Em um aspecto, a atividade da enzima de degradação de polímeros é disparada tratando os resíduos sólidos depositados na formação (torta de lama ou torta de filtro) com uma solução ácida.
[000412] Em modalidades alternativas, as vantagens de praticar as composições e os métodos da invenção podem ser: a) proporcionar melhor distribuição da uma ou mais enzimas dentro da torta de lama (também conhecida como "torta de filtro") que resultará em remoção da torta de lama mais uniforme e eficaz, b) simplificar as operações eliminando uma etapa de liberação de enzima separada (enzima é incluída na formulação do fluido de perfuração, e/ou nos fluidos para lavagem e/ou fraturamento de poço de óleo e gás), e c) eliminar a necessidade de sais de tamponamento uma vez que a enzima não é formulada com um fluido acídico.
[000413] Em modalidades alternativas, enzimas de degradação de polímeros, incluindo amilases, glucanases, xantanases, glicosidases, qualquer enzima de degradação de amido, qualquer celulase e/ou protease, por exemplo, conforme descrito aqui, neste pedido de patente, são adicionadas a um fluido de perfuração e/ou um fluido de lavagem e/ou fraturamento de poço de óleo e gás que é usado durante operações de perfuração de um poço de óleo e gás ou processos de lavagem e/ou fraturamento de poço de óleo e gás. Estes fluidos podem conter amido como um viscosificante e podem ser formulados em alcalinidade relativamente elevada (pH = 9 a 9,5). Devido à alcalinidade do fluido (nesta modalidade), uma enzima acídica-a- neutra permanecerá latente no fluido e na torta de lama ("torta de filtro") que é formada depois da perda de água do fluido sobre a superfície da formação. De modo a ativar a enzima, a torta de lama pode ser lavada com uma solução ácida. O ácido neutralizará a alcalinidade da torta de lama e proporcionará um ambiente acídico o qual disparará a atividade enzimática e a função hidrolítica em direção a amido ou outros polímeros. Nesta modalidade alternativa, a “lavagem ácida”’ é uma etapa necessária, e pode ser aplicada durante as operações de perfuração de poços e/ou as operações de limpeza de poços (incluindo processos de lavagem e/ou fraturamento de poço de óleo e gás) de modo a remover depósitos de carbonato de cálcio da formação. Uma vez ativada (por um ambiente ácido), a enzima degradará o amido ou outros polímeros, e removerá a torta de lama do orifício do poço.
[000414] Em uma operação, esta “lavagem” do orifício do poço é a etapa final na operação de perfuração, e/ou operação de lavagem e/ou fraturamento de poço de óleo e gás, e uma degradação completa da torta de lama ("torta de filtro") praticando as composições e os métodos da invenção possibilita produtividade ótima do poço.
[000415] Em um aspecto, uma enzima de degradação de polímeros usada para praticar esta invenção inclui qualquer amilase, xantanase, glicosidase, glucanase, protease e/ou celulase, as quais incluem usar misturas ou “coquetéis” destas e outras enzimas.
[000416] As composições e os métodos da invenção compreendem uso de ácidos nucleicos isolados, sintéticos ou recombinantes compreendendo uma sequência de ácido nucleico tendo pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) com um ácido nucleico exemplar usado para praticar a invenção, incluindo SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 14, SEQ ID NO: 16, SEQ ID NO: 18, SEQ ID NO: 20, e SEQ ID NO: 22, e as variantes exemplares de SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 14, SEQ ID NO: 16, SEQ ID NO: 18, SEQ ID NO: 20, e SEQ ID NO: 22, sobre uma região de pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200, 1250, 1300,1350, 1400, 1450, 1500, 1550, 1600, 1650, 1700, 1750, 1800, 1850,1900, 1950, 2000, 2050, 2100, 2200, 2250, 2300, 2350, 2400, 2450,2500, ou mais resíduos; onde estes ácidos nucleicos codificam pelo menos um polipeptídeo tendo uma atividade de amilase (em particular, o gênero baseado na exemplar SEQ ID NO: 14), e/ou uma atividade de glicosidase ou uma atividade de celulase, por exemplo, endoglucanase, celobio-hidrolase, xilanase, mananase e/ou betaglucosidase (em particular, o gênero baseado na exemplar SEQ ID NO: 1, as variantes descritas de SEQ ID NO: 1 (incluindo SEQ ID NO: 3), e/ou SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10 SEQ ID NO: 12, SEQ ID NO: 16 SEQ ID NO: 18, SEQ ID NO: 20, e SEQ ID NO: 22), e/ou uma atividade de xantanase. Em um aspecto, as identidades das sequências são determinadas por análise com um algoritmo de comparação de sequências ou por uma inspeção visual.
[000417] Os ácidos nucleicos usados para praticar as composições e os métodos da invenção podem codificar um polipeptídeo tendo a sequência de aminoácidos de SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23; e os ácidos nucleicos exemplares variantes de SEQ ID NO: 1, por exemplo, SEQ ID NO: 3, as variantes de aminoácidos exemplares de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 15, SEQ ID NO: 17, SEQ ID NO: 19, SEQ ID NO: 21, e SEQ ID NO: 23, respectivamente). Em um aspecto, estes polipeptídeos têm uma atividade de amilase (em particular, o gênero baseado nas exemplares SEQ ID NO: 14 e SEQ ID NO: 15), e/ou atividade de uma glicosidase ou uma celulase, por exemplo, atividade de endoglucanase, celobio- hidrolase, mananase e/ou beta-glucosidase (em particular, o gênero baseado naa exemplares SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 17 (codificada pela SEQ ID NO: 16), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), e/ou uma atividade de xantanase.
[000418] As composições e os métodos da invenção compreendem uso de polipeptídeos isolados, sintéticos ou recombinantes tendo uma atividade de amilase (em particular, o gênero baseado nas típicas SEQ ID NO: 14 e SEQ ID NO: 15), e/ou atividade de uma glicosidase ou uma celulase, por exemplo, atividade de endoglucanase, celobio- hidrolase, mananase e/ou beta-glucosidase (em particular, o gênero baseado nas exemplares SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 17 (codificada pela SEQ ID NO: 16), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), e/ou uma atividade de xantanase.
[000419] Em uma modalidade, um polipeptídeo usado para praticar esta invenção, quer sozinho ou com um “coquetel” da invenção, inclui amilases que podem catalisar a hidrólise de polissacarídeos compreendendo monômeros de glicose, tais como amido (um polímero de monômeros de glicose ligados por ligações 1,4-alfa ou 1,6- alfa). Em um aspecto, o polipeptídeo tem uma atividade de amilase, por exemplo, uma atividade de alfa amilase, atividade de endoamilase, ou uma atividade de glucoamilase; e o termo “amilase” conforme usado aqui, neste pedido de patente, também inclui atividade enzimática a qual catalisa a hidrólise de um polissacarídeo, por exemplo, um amido. Amilases usadas para praticar a invenção incluem polipeptídeos tendo uma atividade de α-amilase, uma atividade de β-amilase, uma atividade de glucoamilase, uma atividade de 1,4-α-D-glucano glucoidrolase, uma atividade de exoamilase, uma atividade de glucano α-maltotetra-hidrolase, uma atividade de maltase, uma atividade de isomaltase, uma atividade de glucano 1, 4, α-glucosidase, uma atividade de α-glucosidase, uma atividade de sucrase ou uma atividade de agarase (por exemplo, uma atividade de β-agarase). Por exemplo, uma amilase usada para a prática inclui polipeptídeos tendo atividade de α-amilase, incluindo a capacidade de hidrolisar ligações alfa-1,4-glucosídicas internas em amido para produzir de menor peso molecular maltodextrinas. Em um aspecto, a atividade de α-amilase inclui hidrolisar ligações alfa-1,4-glucosídicas internas em amido aleatoriamente. Uma amilase usada para a prática inclui polipeptídeos tendo atividade de glucoamilase, tais como a capacidade para hidrolisar polímeros de glicose ligados por ligações α-1,4- e α-1,6- glucosídicas. Em um aspecto, amilase usada para a prática inclui polipeptídeos tendo atividade de glucoamilase, hidrolisando ligações α- 1,4-glucosídicas internas para produzir maltodextrinas de menor peso molecular. Uma amilase usada para a prática inclui polipeptídeos tendo atividade de glucano 1,4-α-glucosidase, ou, 1,4-α-D-glucano glucohidrolase, denominada comumente glucoamilase mas também denominada amiloglucosidase e Y-amilase que, em um aspecto, libera β-D-glicose a partir de glucanos 1,4-α-, 1,6-α- e 1,3-α-ligados. Uma amilase usada para a prática inclui polipeptídeos tendo atividade de exoamilase.
[000420] As composições compreendendo enzimas da invenção podem compreender uma enzima de degradação de polissacarídeos conforme descrito aqui, neste pedido de patente, ou pode compreender uma mistura (um “coquetel” de) um, dois, três, quatro ou mais de quaisquer dos polipeptídeos de degradação de polissacarídeos descritos aqui, neste pedido de patente, incluindo os gêneros baseados na SEQ ID NO: 2, as variantes exemplares de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 15, SEQ ID NO: 17, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23. Uma composição usada para praticar a invenção pode compreender um, dois, três ou mais polipeptídeos descritos aqui, neste pedido de patente, incluindo os gêneros baseados na SEQ ID NO: 2, as variantes exemplares de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 15, SEQ ID NO: 17, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23, e qualquer combinação de outras enzimas, tais como triptofanases ou tirosina decarboxilases, lacases, catalases, lacases, outras celulases, endoglicosidases, endo-beta-1,4-lacases, amiloglucosidases, outras glucosidases, glicose isomerases, glicosiltransferases, lipases, fosfolipases, lipo-oxigenases, beta-lacases, endo-beta-1,3(4)-lacases, cutinases, peroxidases, amilases, xantanases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, arabinanases, hemicelulases, mananases, xilolacases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, proteases, peptidases, proteinases, poligalacturonases, ramnogalacturonases, galactanases, pectina liases, transglutaminases, pectina metilesterases, outras celobio- hidrolases e/ou transglutaminases.
[000421] A invenção proporciona métodos para modificar ou ajustar as propriedades reológicas de: um espessante polissacarídico; um espessante polissacarídico em um gel, um floculado, um aglutinante ou um lubrificante; ou, um polissacarídeo em um filme para modificar uma propriedade do filme, o método compreendendo
[000422] (I) proporcionar pelo menos uma enzima de degradação de polímero (“quebra de polímero”) compreendendo
[000423] (a) um polipeptídeo codificado por uma sequência de ácido nucleico tendo pelo menos 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%,69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%,81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%,93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais ou identidade de sequência completa com a SEQ ID NO: 1, a SEQ ID NO: 3, a SEQ ID NO: 6, a SEQ ID NO: 8, a SEQ ID NO: 10, a SEQ ID NO: 12, a SEQ ID NO: 18, a SEQ ID NO: 20, OU a SEQ ID NO: 22, e/ou as variantes exemplares de SEQ ID NO: 1, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 14, SEQ ID NO: 16, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22, sobre uma região de pelo menos cerca de 20, 30, 40, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150 ou mais resíduos, em que o ácido nucleico codifica pelo menos um polipeptídeo tendo uma atividade de degradação de polímero, ou uma amilase, xantanase, glucanase, protease e/ou uma glicosidase ou atividade de celulase, e opcionalmente as identidades das sequências são determinadas por análise com um algoritmo de comparação de sequências ou por uma inspeção visual; ou
[000424] (b) um polipeptídeo codificado por uma sequência de ácido nucleico que hibridiza sob condições estringentes a um ácido nucleico compreendendo a SEQ ID NO: 1, a SEQ ID NO: 3, a SEQ ID NO: 6, a SEQ ID NO: 8, a SEQ ID NO: 10, a SEQ ID NO: 12, a SEQ ID NO: 18, a SEQ ID NO: 20, e/ou a SEQ ID NO: 22, e/ou as variantes exemplares de SEQ ID NO: 1, em que o ácido nucleico codifica um polipeptídeo tendo uma atividade de degradação de polímero, ou atividade de uma amilase, xantanase, glucanase, protease e/ou uma glicosidase ou uma celulase, e as condições estringentes incluem uma etapa de lavagem compreendendo uma lavagem em 0,2X SSC em uma temperatura de cerca de 65oC por cerca de 15 minutos,
[000425] e opcionalmente o ácido nucleico tem pelo menos cerca de 20, 30, 40, 50, 60, 75, 100, 150, 200, 300, 400, 500, 600, 700, 800, 900, 1000 ou mais resíduos de extensão ou toda a extensão do gene ou transcripto;
[000426] (c) um polipeptídeo tendo uma sequência de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, OU SEQ ID NO: 23, as variantes exemplares de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 15, SEQ ID NO: 17, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23; ou
[000427] (d) um polipeptídeo isolado, sintético ou recombinante tendo uma atividade de degradação de polímero, ou atividade de uma amilase, xantanase, glucanase, protease e/ou uma glicosidase ou uma celulase e tendo uma sequência de aminoácidos tendo pelo menos 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou 100% de identidade de sequência com a SEQ ID NO: 2, a SEQ ID NO: 7, a SEQ ID NO: 9, a SEQ ID NO: 11, a SEQ ID NO: 13, a SEQ ID NO: 19, a SEQ ID NO: 21, OU a SEQ ID NO: 23, as variantes exemplares de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 15, SEQ ID NO: 17, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23, sobre uma região de pelo menos cerca de 20, 25, 30, 35, 40, 45, 50, 55, 60, 75, 100, 150, 200, 250, 300 ou mais resíduos,
[000428] em que opcionalmente as identidades das sequências são determinadas por análise com um algoritmo de comparação de sequências ou por uma inspeção visual, e opcionalmente o algoritmo de comparação de sequências é um algoritmo BLAST versão 2.2.2 onde uma situação de filtragem é ajustada para blastall -p blastp -d "nr pataa" -F F, e todas as outras opções são ajustadas para default.
[000429] (e) um polipeptídeo tendo uma sequência de aminoácidos de (a) a (d), e conservando atividade enzimática e compreendendo pelo menos uma substituição conservativa de resíduo de aminoácido,
[000430] em que opcionalmente substituição conservativa compreende substituição de um aminoácido alifático com outro aminoácido alifático; substituição de uma serina com uma treonina ou vice-versa; substituição de um resíduo acídico com outro resíduo acídico; substituição de um resíduo portando um grupo amida com outro resíduo portando um grupo amida; permuta de um resíduo básico com outro resíduo básico; ou, substituição de um resíduo aromático com outro resíduo aromático, ou uma combinação das mesmas,
[000431] e opcionalmente o resíduo alifático compreende Alanina, Valina, Leucina, Isoleucina ou um equivalente sintético dos mesmos; o resíduo acídico compreende Ácido aspártico, Ácido glutâmico ou um equivalente sintético dos mesmos; o resíduo compreendendo um grupo amida compreende Ácido aspártico, Ácido glutâmico ou um equivalente sintético dos mesmos; o resíduo básico compreende Lisina, Arginina ou um equivalente sintético dos mesmos; ou, o resíduo aromático compreende Fenilalanina, Tirosina ou um equivalente sintético dos mesmos; e
[000432] (II) adicionar a enzima ao espessante polissacarídico; o espessante polissacarídico em um gel, um floculado, um aglutinante ou um lubrificante; ou, o polissacarídeo em um filme, deste modo ajustando ou modificando as propriedades do gel, floculado, aglutinante, lubrificante ou filme.
[000433] Os detalhes de uma ou mais modalidades da invenção são determinados nos desenhos anexos e na descrição abaixo. Outras características, objetos, e vantagens da invenção serão evidentes a partir da descrição e dos desenhos, e das reivindicações.
[000434] Todas as publicações, patentes, pedidos de patente, sequências do GenBank e depósitos ATCC, citados aqui, neste pedido de patente, são por este expressamente incorporados por meio de referência para todos os fins.
BREVE DESCRIÇÃO DOS DESENHOS
[000435] Os desenhos seguintes são ilustrativos de aspectos da invenção e não pretendem limitar o escopo da invenção conforme englobado pelas reivindicações.
[000436] A figura 1 é um diagrama em bloco de um sistema de computação.
[000437] A figura 2 é um diagrama de fluxo ilustrando um aspecto de um processo para comparar uma nova sequência de nucleotídeos ou de proteína com um banco de dados de sequências de modo a determinar os níveis de homologia entre a nova sequência e as sequências no banco de dados.
[000438] A figura 3 é um diagrama de fluxo ilustrando um aspecto de um processo em um computador para determinar se duas sequências são homólogas.
[000439] A figura 4 é um diagrama de fluxo ilustrando um aspecto de um processo identificador 300 para detectar a presença de uma característica em uma sequência.
[000440] A figura 5 é uma tabela resumindo as atividades relativas de várias enzimas exemplares da invenção sob várias condições.
[000441] A figura 6 é uma ilustração em forma de gráfico de uma série de dados exemplares (“dados da amostra”) que é ilustrada como uma “curva-padrão”, conforme discutido no Exemplo 3.
[000442] A figura 7 ilustra os resultados de ensaios da atividade de glucanase mostrando o perfil da temperatura da glucanase exemplar da invenção codificada pela SEQ ID NO: 2, conforme discutido no Exemplo 4, abaixo.
[000443] A figura 8 ilustra os resultados das ensaios da atividade de glucanase mostrando a determinação da meia-vida da glucanase exemplar da invenção codificad pela SEQ ID NO: 2, conforme discutido no Exemplo 4, abaixo.
[000444] A figura 9 ilustra dados demonstrando a tolerância térmica de variantes exemplares da invenção, onde a atividade da SEQ ID NO: 2 “selvagem” parental purificada e 7X variantes foi medida e comparada, conforme discutido no Exemplo 5, abaixo.
[000445] A figura 10 ilustra dados demonstrando a tolerância térmica de variantes exemplares da invenção, onde a atividade da SEQ ID NO: 2 “selvagem” parental purificada e 7X variantes foi medida e comparada, conforme discutido no Exemplo 5, abaixo.
[000446] A figura 11 ilustra uma foto de um gel de dimensionamento de transcriptos gerados usando transcripto não-modificado “tipo selvagem (WT)” e modificado exemplar (variante) da invenção para demonstrar o efeito de um RBS e alteração do segundo sítio de iniciação sobre a expressão de transcripto de glucanase, conforme discutido no Exemplo 6, abaixo.
[000447] A figura 12 ilustra a termoestabilidade destas duas enzimas da invenção sobre uma gama de temperaturas de peletização, conforme discutido no Exemplo 8, abaixo.
[000448] A figura 13, dois códons foram inseridos entre o segundo (2o. códon) da sequência codificante de enzima (glucanase) SEQ ID NO: 2 e uma sequência de sinal de fator alha (sequência líder), conforme discutido no Exemplo 9, abaixo.
[000449] A figura 14A ilustra resultados do sequenciamento de N- terminal para as enzimas glucanase expressadas por Pichia da invenção designadas “12X-6” e “13X-1”; a figura 14A ilustra uma radiografia de um gel SDS-PAGE mostrando um dubleto de glucanase causado por processamento de sinal inconsistente; a figura 14B ilustra uma radiografia de um gel SDS-PAGE mostrando uma proteína conforme representado por uma banda de 37 kDa de gel SDS-PAGE, a qual foi excisada e sequenciada, conforme discutido no Exemplo 9, abaixo.
[000450] Símbolos de referência semelhantes nos vários desenhos indicam elementos semelhantes.
DESCRIÇÃO DETALHADA DA INVENÇÃO
[000451] A invenção proporciona polipeptídeos e polinucleotídeos codificando os mesmos e métodos para produzir e usar os mesmos, incluindo SEQ ID NO: 2, codificada, por exemplo, pela SEQ ID NO: 1, , SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), e as modificações específicas para SEQ ID NO: 1 e SEQ ID NO: 2 descritas aqui, neste pedido de patente. A atividade enzimática dos polipeptídeos da invenção engloba polipeptídeos tendo uma atividade de hidrolase, por exemplo, uma atividade de glucanase, por exemplo, polipeptídeos capazes de hidrolisar ligações glicosídicas presentes em um glucano, por exemplo, catalisando hidrólise de ligações β-1,4- glicosídicas internas. A atividade enzimática dos polipeptídeos e peptídeos da invenção (incluindo enzimas e anticorpos) engloba polipeptídeos tendo uma atividade de glucanase, uma xilanase, e/ou uma mananase. Os polipeptídeos e peptídeos (incluindo enzimas e anticorpos) podem ser usados para fabricar e/ou processar alimentos, rações (por exemplo, para um ser humano, um ruminante, um animal monogástrico, uma ave, por exemplo, um frango), bebidas, suplementos nutricionais, têxteis, detergentes e similares. Os polipeptídeos e peptídeos (incluindo enzimas e anticorpos) da invenção podem ser usados em composições farmacêuticas e auxiliares dietéticos. Glucanases (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção são úteis em processamento de alimentos, cozimento, rações animais ou alimentos, bebidas, detergentes, processos de processamento de polpa e papel.
Produzindo e Manipulando Ácidos Nucleicos
[000452] A invenção proporciona ácidos nucleicos isolados, recombinantes e sintéticos, incluindo os ácidos nucleicos exemplares da invenção, por exemplo, SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22 e sequências tendo as modificações específicas descritas aqui, neste pedido de patente, e sequências tendo uma identidade de sequência com um ácido nucleico exemplar; ácidos nucleicos codificando polipeptídeos da invenção, por exemplo, as sequências de aminoácidos típicas conforme determinado na SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23, e sequências tendo as modificações específicas descritas aqui, neste pedido de patente.
[000453] Ácidos nucleicos exemplares da invenção incluem os polipeptídeos que são variações de sequência da SEQ ID NO: 2, conforme determinado (resumido) na Tabela 1, abaixo (e na Tabela 2, vide o Exemplo 5). Nesta Tabela 1, “códon original” se refere ao códon como na sequência “parental” SEQ ID NO: 1, e “aminoácido original” se refere ao resíduo de aminoácido como na SEQ ID NO: 2 do polipeptídeo “parental”:
[000454] A invenção também proporciona cassetes de expressão tais como vetores de expressão, compreendendo ácidos nucleicos da invenção, os quais incluem polinucleotídeos os quais codificam os polipeptídeos da invenção. A invenção também inclui métodos para descobrir novas sequências de glucanase usando os ácidos nucleicos da invenção. A invenção também inclui métodos para inibir a expressão de genes de glucanase, transcriptos e polipeptídeos usando os ácidos nucleicos da invenção. Também são proporcionados métodos para modificar os ácidos nucleicos da invenção por, por exemplo, remontagem de ligação sintética, sistema de evolução dirigida otimizado e/ou mutagênese de saturação.
[000455] Os ácidos nucleicos da invenção podem ser fabricados, isolados e/ou manipulados, por exemplo, por clonagem e expressão de bibliotecas de cDNA, amplificação de mensagem ou DNA genômico por PCR, e similares. As expressões “ácido nucleico” ou “sequência de ácido nucleico” conforme usado aqui, neste pedido de patente, se referem a um oligonucleotídeo, nucleotídeo, polinucleotídeo, ou um fragmento de qualquer destes, a DNA ou RNA de origem genômica ou sintética o qual pode ser de fita única ou de fita dupla e pode representar uma fita de senso ou antissenso, a ácido nucleico peptídico (PNA), ou a qualquer material semelhante a DNA ou semelhante a RNA, de origem natural ou sintética. As expressões “ácido nucleico” ou “sequência de ácido nucleico” se referem a oligonucleotídeo, nucleotídeo, polinucleotídeo, ou um fragmento de qualquer destes, a DNA ou RNA (por exemplo, mRNA, rRNA, tRNA, iRNA) de origem genômica ou sintética o qual pode ser de fita única ou de fita dupla e pode representar uma fita de senso ou antissenso, a ácido nucleico peptídico (PNA), ou a qualquer material semelhante a DNA ou semelhante a RNA, de origem natural ou sintética, incluindo, por exemplo, iRNA, ribonucleoproteínas (por exemplo, por exemplo, iRNAs de fita dupla, por exemplo, iRNPs, siRNA ou miRNA). O termo engloba ácidos nucleicos, isto é, oligonucleotídeos, contendo análogos conhecidos de nucleotídeos naturais. O termo também engloba estruturas semelhantes a ácido nucleico com estruturas principais sintéticas, vide, por exemplo, Mata (1997) Toxicol. Appl. Pharmacol. 144:189-197; Strauss-Soukup (1997) Biochemistry 36:8692-8698; Samstag (1996) Antisense Nucleic Acid Drug Dev 6:153-156. “Oligonucleotídeo” inclui ou um polidesoxinucleotídeo de fita única ou de duas fitas de polidesoxinucleotídeo complementares as quais podem ser sintetizadas quimicamente. Os oligonucleotídeos sintéticos referidos não têm 5' fosfato e portanto não ligarão a outro oligonucleotídeo sem adicionar um fosfato com um ATP na presença de uma quinase. Um oligonucleotídeo sintético pode ligar a um fragmento que não tenha sido desfosforilado.
[000456] Uma “sequência codificante de” ou uma “sequência de nucleotídeos codificando” um polipeptídeo ou proteína em particular, é uma sequência de ácido nucleico a qual é transcrita e traduzida em um polipeptídeo ou proteína quando colocada sob o controle de sequências regulatórias apropriadas. O termo “gene” significa o segmento de DNA envolvido em produzir uma cadeia de polipeptídeo; inclui regiões precedendo e seguindo a região codificante (líder e "trailer") bem como, onde aplicável, sequências intervenientes (íntrons) entre segmentos codificantes individuais (éxons). “Ligado operavelmente" conforme usado aqui, neste pedido de patente, se refere a uma relação funcional entre dois ou mais segmentos de ácido nucleico (por exemplo, DNA). Tipicamente, se refere à relação funcional de sequência regulatória transcricional com uma sequência transcrita. Por exemplo, um promotor é ligado operavelmente a uma sequência codificante, tal como um ácido nucleico da invenção, se estimular ou modular a transcrição da sequência codificante em uma célula hospedeira apropriada ou outro sistema de expressão. Geralmente, sequências regulatórias transcricionais promotoras que são ligadas operavelmente a uma sequência transcrita são fisicamente contíguas à sequência transcrita, isto é, têm ação cis-. No entanto, algumas sequências regulatórias transcricionais, tais como reforçadores, não precisam ser fisicamente contíguas ou estar localizadas em íntima proximidade às sequências codificantes cuja transcrição reforçam.
[000457] Na prática dos métodos da invenção, genes homólogos podem ser modificados manipulando um ácido nucleico molde, conforme descrito aqui, neste pedido de patente. A invenção pode ser praticada em combinação com qualquer método ou protocolo ou dispositivo conhecido na técnica, os quais são descritos de modo geral na literatura científica e de patente.
[000458] Os ácidos nucleicos isolados podem compreender DNA, incluindo cDNA, DNA genômico e DNA sintético. O DNA pode ser de fita dupla ou de fita única e caso de fita única pode ser a fita codificante ou não- codificante (antissenso). Alternativamente, os ácidos nucleicos isolados podem compreender RNA. Os ácidos nucleicos isolados da invenção podem ser usados para preparar um dos polipeptídeos da invenção, ou fragmentos dos mesmos. As sequências codificantes destes ácidos nucleicos podem ser idênticas a uma das sequências codificantes de um dos ácidos nucleicos da invenção ou podem ser diferentes em consequência da redundância ou degeneração do código genético. O código genético é de conhecimento geral daqueles versados na técnica e pode ser obtido, por exemplo, à página 214 de B. Lewin, Genes VI, Oxford University Press, 1997.
[000459] O ácido nucleico isolado o qual codifica um dos polipeptídeos da invenção, mas não é limitado a: somente a sequência codificante de um ácido nucleico da invenção e sequências codificantes adicionais, tais como sequências líder ou sequências proproteína e sequências não-codificantes, tais como íntrons ou sequências não-codificantes 5’ e/ou 3’ da sequência codificante. Portanto, conforme usado aqui, neste pedido de patente, o termo “polinucleotídeo codificando um polipeptídeo” engloba um polinucleotídeo o qual inclui somente a sequência codificante para o polipeptídeo bem como um polinucleotídeo o qual inclui sequência codificante e/ou não-codificante adicional.
[000460] Alternativamente, as sequências de ácido nucleico da invenção podem ser mutagenizadas usando técnicas convencionais, tais como mutagênese sítio dirigida, ou outras técnicas familiares daqueles versados na técnica, para introduzir alterações inativas nos polinucleotídeos da invenção. Conforme usado aqui, neste pedido de patente, “alterações inativas” incluem, por exemplo, alterações as quais não alteram a sequência de aminoácidos codificada pelo polinucleotídeo. As alterações referidas podem ser desejáveis de modo a aumentar o nível do polipeptídeo produzido pelas células hospedeiras contendo um vetor codificando o polipeptídeo introduzindo códons ou pares de códons os quais ocorrem frequentemente no organismo hospedeiro.
[000461] A invenção também se refere a polinucleotídeos os quais têm alterações de nucleotídeos as quais resultam em substituições, adições, eliminações, fusões e truncações de aminoácidos nos polipeptídeos da invenção. As referidas alterações de nucleotídeos podem ser introduzidas usando técnicas tais como mutagênese sítio dirigida, mutagênese química aleatória, eliminação de exonuclease III e outras técnicas de DNA recombinante. Alternativamente, as referidas alterações de nucleotídeos podem ser variantes alélicas que ocorrem naturalmente as quais são isoladas identificando ácidos nucleicos os quais hibridizam especificamente a sondas da invenção, por exemplo, sequências compreendendo pelo menos 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, 150, 200, 300, 400, ou 500 bases consecutivas de uma das sequências da invenção (incluindo as sequências complementares às mesmas) sob condições de alta, moderada, ou baixa estringência conforme proporcionado aqui, neste pedido de patente.
Técnicas Gerais
[000462] Os ácidos nucleicos usados para praticar esta invenção, que RNA, iRNA (por exemplo, siRNA, miRNA), ácido nucleico antissenso, cDNA, DNA genômico, vetores, vírus ou híbridos dos mesmos, podem ser isolados a partir de uma variedade de fontes, produzidos geneticamente, amplificados, e/ou expressados/gerados de modo recombinante. Polipeptídeos recombinantes (por exemplo, glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases) produzidos a partir destes ácidos nucleicos podem ser individualmente isolados ou clonados e testados para uma atividade desejada. Pode ser usado qualquer sistema de expressão recombinante, incluindo sistemas de expressão de células bacterianas, mamíferas, de levedura, fúngicas, de insetos ou de plantas.
[000463] Alternativamente, estes ácidos nucleicos podem ser sintetizados in vitro por meio de técnicas de síntese química de conhecimento geral, conforme descrito, por exemplo, em Adams (1983) J. Am. Chem. Soc. 105:661; Belousov (1997) Nucleic Acids Res. 25:3440-3444; Frenkel (1995) Free Radic. Biol. Med. 19:373-380; Blommers (1994) Biochemistry 33:7886-7896; Narang (1979) Meth. Enzymol. 68:90; Brown (1979) Meth. Enzymol. 68:109; Beaucage (1981) Tetra. Lett. 22:1859; e na Patente dos Estados Unidos No. 4.458.066.
[000464] Técnicas para a manipulação de ácidos nucleicos, tais como, por exemplo, subclonagem, sondas de marcação (por exemplo, marcação de iniciadores aleatória usando polimerase de Klenow, translação de entalhe, amplificação), sequenciamento, hibridização e similares são descritas de modo geral na literatura científica e de patente, vide, por exemplo, Sambrook, ed., MOLECULAR CLONING: A LABORATORY MANUAL (2ND ED.), Vols. 1-3, Cold Spring Harbor Laboratory, (1989); CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, Ausubel, ed. John Wiley & Sons, Inc., New York (1997); LABORATORY TECHNIQUES IN BIOCHEMISTRY AND MOLECULAR BIOLOGY: HYBRIDIZATION WITH NUCLEIC ACID PROBES, Part I. Theory and Nucleic Acid Preparation, Tijssen, ed. Elsevier, N.Y. (1993).
[000465] Outros meios úteis para obter e manipular ácidos nucleicos usados para praticar os métodos da invenção são clonar a partir de amostras genômicas, e, caso desejado, triar e reclonar insertos isolados ou amplificados a partir de, por exemplo, clones genômicos ou clones de cDNA. Fontes de ácido nucleico usadas nos métodos da invenção incluem bibliotecas genômicas ou de cDNA contidas, por exemplo, em cromossomas artificiais de mamíferos (MACs), vide, por exemplo, as Patentes dos Estados Unidos Nos. 5.721.118; 6.025.155; cromossomas artificiais humanos, vide, por exemplo, Rosenfeld (1997) Nat. Genet. 15:333-335; cromossomas artificiais de levedura (YAC); cromossomas artificiais bacterianos (BAC); cromossomas artificiais P1, vide, por exemplo, Woon (1998) Genomics 50:306-316; vetores P1- derivados (PACs), vide, por exemplo, Kern (1997) Biotechniques 23:120-124; cosmídeos, vírus recombinantes, fagos ou plasmídeos.
[000466] Conforme usado aqui, neste pedido de patente, o termo “recombinante” significa que o ácido nucleico está adjacente a um ácido nucleico da “estrutura principal” ao qual não está adjacente em seu ambiente natural. Em alguns aspectos, para serem “enriquecidos” os ácidos nucleicos representam cerca de 1%, 2%, 3%, 4%, 5%, 6%, 10%, 11%, 12%, 13%, 14%, 15%, 20%, 30%, 45%, 50%, 60%, 70%, 80%, 90% ou mais do número de insertos de ácido nucleico em uma população de moléculas da estrutura principal de ácidos nucleicos, por exemplo, moléculas da estrutura principal recombinante. Moléculas da estrutura principal incluem ácidos nucleicos tais como vetores de expressão, ácidos nucleicos autorreplicantes, vírus, ácidos nucleicos integrantes e outros de ou ácidos nucleicos usados para manter ou manipular um inserto de ácido nucleico de interesse.
[000467] Em um aspecto, um ácido nucleico codificando um polipeptídeo da invenção é reunido em fase apropriada com uma sequência líder capaz de dirigir secreção do polipeptídeo traduzido ou fragmento do mesmo. A invenção proporciona proteínas de fusão e ácidos nucleicos codificando as mesmas. Um polipeptídeo da invenção pode ser fundido a um peptídeo ou polipeptídeo heterólogo, tal como peptídeos de identificação de N-terminal os quais conferem características desejadas, tais como aumento da estabilidade ou purificação simplificada. Peptídeos e polipeptídeos da invenção também podem ser sintetizados e expressados como proteínas de fusão com um ou mais domínios adicionais ligados aos mesmos para, por exemplo, produzir um peptídeo mais imunogênico, para mais prontamente isolar um peptídeo sntetizado de modo recombinante, para identificar e isolar anticorpos e célula B expressando anticorpos, e similares. Domínios facilitando detecção e purificação incluem, por exemplo, peptídeos quelantes de metais tais como traços de poli- histidina e módulos de histidina-triptofano que permitem purificação sobre metais imobilizados, domínios de proteína A que permitem purificação sobre imunoglobulina imobilizada, e o domínio utilizado no sistema de extensão FLAGS/purificação por afinidade (Immunex Corp, Seattle WA). A inclusão de algumas sequências ligantes cliváveis tais como Fator Xa ou enteroquinase (Invitrogen, San Diego CA) entre um domínio de purificação e o peptídeo ou polipeptídeo compreendendo motivo para facilitar purificação. Por exemplo, um vetor de expressão pode incluir uma sequência de ácido nucleico codificando epitopo ligado a seis resíduos histidina seguidos por uma tioredoxina e um sítio de clivagem de enteroquinase (vide por exemplo, Williams (1995) Biochemistry 34:1787-1797; Dobeli (1998) Protein Expr. Purif. 12:404414). Os resíduos histidina facilitam detecção e purificação enquanto o sítio de clivagem de enteroquinase proporciona um meio para purificar o epitopo a partir do restante da proteína de fusão. Tecnologia pertencente a vetores codificando proteínas de fusão e aplicação de proteínas de fusão são descritas de modo geral na literatura científica e de patente, vide, por exemplo, Kroll (1993) DNA Cell. Biol., 12:44153.
[000468] O termo “Mutagênese de Saturação” ou “Mutagênese de Saturação de Sítio Genético” ou “GSSM” inclui um método que usa iniciadores de oligonucleotídeos degenerados para introduzir mutações de ponto em um polinucleotídeo, conforme descrito em detalhes, abaixo. O termo “sistema de evolução dirigida otimizada” ou “evolução dirigida otimizada” inclui um método para remontar fragmentos de sequências de ácido nucleico relacionadas, por exemplo, genes relacionados, e explicado em detalhes, abaixo. O termo “remontagem de ligação sintética” ou “SLR” inclui um método para ligar fragmentos de oligonucleotídeos em um modo não- estocástico, e explicado em detalhes, abaixo.
Sequências de controle transcricionais e translacionais
[000469] A invenção proporciona sequências de ácido nucleico (por exemplo, DNA) da invenção ligadas operativamente a uma ou mais sequências controle de expressão (por exemplo, transcricional ou translacional), por exemplo, promotores ou reforçadores, para dirigir ou modular a síntese/expressão de RNA. A sequência de controle de expressão pode estar em um vetor de expressão. Promotores bacterianos típicos incluem lacI, lacZ, T3, T7, gpt, lambda PR, PL e trp. Promotores eucarióticos típicos incluem CMV imediato precoce, HSV timidina quinase, SV40 precoce e tardio, LTRs de retrovírus, e metalotioneína de camundongo I.
[000470] Conforme usado aqui, neste pedido de patente, o termo “promotor” inclui todas as sequências capazes de dirigir a transcrição de uma sequência codificante em uma célula. Deste modo, promotores usados nos construtos da invenção incluem elementos de controle transcricional de ação cis e sequências regulatórias que estão envolvidas em regular ou modular o timing e/ou a taxa de transcrição de um gene. Por exemplo, um promotor pode ser um elemento de controle transcricional de ação cis, incluindo um reforçador, um promotor, um terminador de transcrição, uma origem de replicação, uma sequência de integração cromossômica, regiões não-traduzidas 5' e 3’, ou uma sequência intrônica, os quais estão envolvidos em regulação transcricional. Estas sequências de ação cis tipicamente interagem com proteínas ou outras biomoléculas para realizar (ligar/desligar, regular, modular, e etc.) transcrição. Promotores “constitutivos” são aqueles que dirigem a expressão continuamente sob a maioria das condições ambientais e estados de desenvolvimento ou diferenciação celular. Promotores “indutíveis” ou “reguláveis” dirigem a expressão do ácido nucleico da invenção sob a influência de condições ambientais ou condições relativas ao desenvolvimento. Exemplos de condições ambientais que podem afetar transcrição por promotores indutíveis incluem condições anaeróbicas, temperatura elevada, estiagem, ou a presença de luz. Promotores-tecido- específicos são elementos de controle transcricional que são somente ativos em células ou tecidos ou órgãos particulares, por exemplo, em plantas ou animais. Regulação “tecido-específica” pode ser obtida por alguns fatores intrínsecos os quais asseguram que são expressados genes codificando proteínas específicas para um dado tecido. Sabe-se que os fatores referidos existem em mamíferos e plantas de modo a permitir que tecidos específicos se desenvolvam.
[000471] Promotores adequados para expressar um polipeptídeo em bactérias incluem os promotores de E. coli lac ou trp, o promotor lacI, o promotor lacZ, o promotor T3, o promotor T7, o promotor gpt, o promotor lâmbda PR, o promotor lâmbda PL, promotores de operons codificando enzimas glicolíticas tais como 3-fosfoglicerato quinase (PGK), e o promotor de fosfatase ácida. Promotores eucarióticos incluem o promotor precoce imediato CMV, o promotor de HSV timidina quinase, promotores de choque térmico, o promotor precoce e tardio SV40, LTRs de retrovírus, e o promotor de metalotioneína I de camundongo. Também podem ser usados outros promotores conhecidos por controlar a expressão de genes em células procarióticas ou eucarióticas ou seus vírus. Promotores adequados para expressar o polipeptídeo ou fragmento do mesmo em bactérias incluem os promotores de E. coli lac ou trp, o promotor lacI promotor, o promotor lacZ, o promotor T3, o promotor T7, o promotor gpt, o promotor lâmbda PR, o promotor lâmbda PL, promotores de operons codificando enzimas glicolíticas tais como 3-fosfoglicerato quinase (PGK) e o promotor de fosfatase ácida. Promotores fúngicos incluem o promotor do fator □ . Promotores eucarióticos incluem o promotor precoce imediato CMV, o promotor de HSV timidina quinase, promotores de choque térmico, o promotor precoce e tardio SV40, LTRs de retrovírus e o promotor de metalotioneína I de camundongo. Também pode ser usado qualquer promotor conhecido por controlar a expressão de genes em células procarióticas ou eucarióticas ou seus vírus.
Cassetes de Expressão em Plantas
[000472] A invenção proporciona cassetes de expressão que podem ser expressados de qualquer maneira em uma planta. A invenção também proporciona plantas ou sementes que expressam uma enzima da invenção de qualquer maneira.
[000473] O termo "planta" inclui plantas inteiras, partes de plantas (por exemplo, folhas, caules, flores, raízes, e etc.), protoplastos de plantas, sementes e células de plantas e progênie das mesmas. A classe de plantas as quais podem ser usadas no método da invenção é de modo geral tão ampla quanto a classe de plantas superiores suscetíveis a técnicas de transformação, incluindo angiospermas (plantas monocotiledôneas e dicotiledôneas), bem como gimnospermas. Inclui plantas de uma variedade de níveis de ploidia, incluindo poliplóide, diplóide, haplóide e estados hemizigóticos. Conforme usado aqui, neste pedido de patente, o termo “planta transgênica” inclui plantas ou células de plantas nas quais uma sequência heteróloga de ácido nucleico foi inserida, por exemplo, os ácidos nucleicos e vários construtos recombinantes (por exemplo, cassetes de expressão) da invenção.
Modificação de Sequências Codificantes e Sequências Adjacentes
[000474] A expressão transgênica em plantas de genes derivados de fontes heterólogas pode envolver a modificação destes genes para obter e otimizar sua expressão em plantas. Em particular, ORFs bacterianas as quais codificam enzimas separadas mas as quais são codificadas pelo mesmo transcripto no micróbio nativo são melhor expressadas em plantas sobre transcriptos separados. Para obter isto, cada ORF microbiana é isolada individualmente e clonada dentro de um cassete o qual proporciona uma sequência promotora vegetal na extremidade 5’ da ORF e um terminador transcricional vegetal na extremidade 3’ da ORF. A sequência de ORF isolada preferêncialmente inclui o códon ATG de inicialização e o códon STOP de terminação mas pode incluir sequência adicional além do códon ATG de inicialização e o códon STOP. Além disso, a ORF pode estar truncada, mas ainda reter a atividade requerida; para ORFs particularmente longas, versões truncadas as quais retèm atividade podem ser preferênciais para expressão em organismos transgênicos. Por “promotor vegetal” e “terminador transcricional vegetal” se pretende significar promotores e terminadores transcricionais os quais operam dentro de células de plantas. Isto inclui promotores e terminadores de transcrição os quais podem ser derivados de fontes não-vegetais tais como vírus (um exemplo é o Vírus do Mosaico da Couve-Flor).
[000475] Em alguns casos, não é necessária modificação para as sequências codificantes de ORF e sequência adjacente. É suficiente isolar um fragmento contendo a ORF de interesse e inserir a mesma a jusante de um promotor de planta. Por exemplo, Gaffney et. al. (Science 261: 754-756 (1993)) expressaram o gene de Pseudomonas nahG em plantas transgênicas sob o controle do promotor CaMV 35S e o terminador CaMV tml com successo sem modificação da sequência codificante e com nucleotídeos do gene de Pseudomonas a montante do ATG ainda anexado, e nucleotídeos a jusante do códon STOP ainda anexados a ORF nahG. Preferêncialmente sequência microbiana adjacente tão pequena deve ser deixada anexada a montante do ATG e a jusante do códon STOP. Na prática, a construção referida pode depender da disponibilidade de sítios de restrição.
[000476] Em outros casos, a expressão de genes derivados de fontes microbianas pode proporcionar problemas na expressão. Estes problemas foram bem caracterizados na técnica e são particularmente comuns com genes derivados de algumas fontes tais como Bacillus. Estes problemas podem se aplicar à sequência de nucleotídeos desta invenção e a modificação destes genes pode ser empreendida usando técnicas de conhecimento geral na técnica atualmente. Podem ser encontrados os problemas seguintes:
Uso de Códons
[000477] O uso de códons preferênciais em plantas difere do uso de códons preferênciais em alguns micro-organismos. A comparação do uso de códons dentro de uma ORF microbiana clonada para uso em genes de plantas (e em particular genes da planta-alvo) possibilitará uma identificação dos códons dentro da ORF os quais preferêncialmente devem ser alterados. Tipicamente evolução de planta tem tendido para uma forte preferência dos nucleotídeos C e G na posição da terceira base de monocotiledôneas, ao passo que dicotiledôneas frequentemente usam o nucleotídeo A ou T nesta posição. Modificando um gene para incorporar uso de uso de códons preferênciais para uma espécie transgênica alvo em particular, muitos dos problemas descritos abaixo para teor de GC/AT e junção ilegítima serão superados.
Teor de GC/AT
[000478] Os genes de plantas tipicamente têm um teor de GC de mais de 35%. Sequências de ORF as quais são ricas em nucleotídeos A e T podem causar graves problemas em plantas. Primeiramente, acredita-se que motivos de ATTTA causem desestabilização de mensages e sejam encontrados na extremidade 3’ de muitos mRNAs de vida curta. Em segundo lugar, acredita-se que a ocorrência de sinais de poliadenilação tais como AATAAA em posições inadequadas dentro da mensagem cause truncação prematura de transcrição. Além disso, monocotiledôneas podem reconhecer sequências ricas em AT como sítios de junção (vide abaixo).
Sequências Adjacentes à Metionina de Iniciação
[000479] As plantas diferem de micro-organismos em que suas mensagess não possuem um sítio de ligação de ribossoma definido. Ao contrário, acredita-se que ribossomas fixam-se à extremidade 5’ da mensagem e triam para o primeiro ATG disponível no qual inicia translação. Não obtante, acredita-se que haja uma preferência por alguns nucleotídeos adjacentes ao ATG e que a expressão de genes microbianos pode ser reforçada pela inclusão de um iniciador de translação de consenso eucariótico no ATG. Clontech (catálogo de 1993/1994, página 210, incorporado aqui, a este pedido de patente, por meio de referência) sugeriu uma sequência como um iniciador de translação de consenso para a expressão do gene uidA de E. coli em plantas. Além disso, Joshi (N.A.R. 15: 6643-6653 (1987), incorporado aqui, a este pedido de patente, por meio de referência) comparou muitas sequências de plantas adjacentes apo ATG e sugere outra sequência de consenso. Em situações onde são encontradas dificuldades na expressão de ORFs microbianas em plantas, inclusão de uma destas sequências no ATG de iniciação pode melhorar a translação. Em casos semelhantes, os três últimos nucleotídeos do consenso podem não ser apropriados para inclusão na sequência modificada devido a sua modificação do segundo resíduo AA. Sequências preferênciais adjacentes à metionina de iniciação podem diferir entre espécies de plantas diferentes. Um exame de 14 genes de milho localizados no banco de dados GenBank proporcionou os seguintes resultados:

[000480] Esta análise pode ser feita para a espécie de planta desejada na qual a sequência de nucleotídeos está sendo incorporada, e a sequência adjacente ao ATG modificado para incorporar os nucleotídeos preferênciais.
Remoção de Sítios de Junção Ilegítimos
[000481] Genes clonados de fontes não-vegetais e não-otimizados para expressão em plantas também podem conter motivos os quais podem ser reconhecidos em plantas como sítios de junção 5’ ou 3’, e ser clivados, deste modo gerando mensagens truncadas ou eliminadas. Estes sítios podem ser removidos usando as técnicas de conhecimento geral na técnica.
[000482] Técnicas para a modificação de sequências codificantes e sequências adjacentes são de conhecimento geral na técnica. Em casos onde a expressão inicial de uma ORF microbiana é baixa e é considerado apropriado fazer alterações para a sequência conforme descrito acima, então a construção de genes sintéticos pode ser realizada de acordo com métodos de conhecimento geral na técnica. Estes são descritos, por exemplo, nas divilgações de patentes publicadas EP 0 385 962 (para Monsanto), EP 0 359 472 (para Lubrizol) e WO 93/07278 (para Ciba-Geigy), todas as quais são incorporadas aqui, a este pedido de patente, por meio de referência. Na maioria dos casos é preferenciual testar a expressão de construções genéticas usando protocolos de testes transitórios (os quais são de conhecimento geral na técnica) antes de sua transferência para plantas transgênicas.
Promotores de Plantas
[000483] As composições da invenção podem conter sequências de ácido nucleico para transformação e expressão em uma planta de interesse. As sequências de ácido nucleico podem estar presentes em construtos de DNA ou cassetes de expressão. "Cassete de expressão " conforme usado aqui, neste pedido de patente, significa uma molécula de ácido nucleico capaz de dirigir a expressão de uma sequência de nucleotídeos em particular em uma célula hospedeira apropriada, compreendendo um promotor ligado operativamente à sequência de nucleotídeos de interesse, a qual é ligada operativamente a sinais de terminação. Tipicamente também compreende sequências requeridas para apropriada translação da sequência de nucleotídeos. A região codificante geralmente codifica uma proteína de interesse mas também pode codificar um RNA funcional de interesse, por exemplo, RNA antissenso ou um RNA não traduzido, na direção de senso ou anti-senso. O cassete de expressão compreendendo a sequência de nucleotídeos de interesse pode ser quimérico, significando que pelo menos um de seus componentes é heterólogo com respeito a pelo menos um de seus outros componentes. O cassete de expressão também pode ser um que esteja ocorrendo naturalmente mas tenha sido obtido em uma forma recombinante útila para expressão heteróloga. Tipicamente, no entanto, o cassete de expressão é heterólogo com respeito ao hospedeiro, isto é, a sequência de DNA particular do cassete de expressão não ocorre naturalmente na célula hospedeira e deve ser introduzida na célula hospedeira ou um ancestral da célula hospedeira por um evento de transformação. A expressão da sequência de nucleotídeos no cassete de expressão pode ser sob o controle de um promotor constitutivo ou de um promotor indutível que inicia transcrição somente quando a célula hospedeira é exposta a algum estímulo externo particular. Adicionalmente, o promotor também pode ser específico para um tecido ou órgão ou estágio de desenvolvimento em particular.
[000484] A presente invenção engloba a transformação de plantas com cassetes de expressão capazes de expressar polinucleotídeos. O cassete de expressão incluirá na direção de transcrição 5'-3', uma região de iniciação transcricional e translacional (isto é, um promotor) e um polinucleotídeo de interesse. O cassete de expressão pode compreender opcionalmente uma região de terminação transcricional e translacional (isto é, região de terminação) funcional em plantas. Em algumas modalidades, o cassete de expressão compreende um gene marcador selecionável para permitir seleção para transformantes estáveis. Construtos de expressão da invenção também podem compreender uma sequência líder e/ou uma sequência possibilitando expressão indutível do polinucleotídeo de interesse. Vide Guo et. al. (2003) Plant J. 34:383-92 e Chen et. al. (2003) Plant J. 36:731-40 para exemplos de sequências possibilitando expressão indutível.
[000485] As sequências regulatórias do construto de expressão são ligadas operavelmente ao polinucleotídeo de interesse. Por “ligadas operavelmente” se pretende uma ligação funcional entre um promotor e uma segunda sequência em que a sequência promotora inicia e medeia transcrição da sequência de DNA correspondendo a segunda sequência. Geralmente, ligadas operavelmente significa que as sequências de nucleotídeos estando ligadas são contíguas.
[000486] Qualquer promotor capaz de dirigir a expressão na planta de interesse pode ser usado na prática da invenção. O promotor pode ser nativo ou análogo ou estranho ou heterólogo ao hospedeira vegetal. Os termos "heterólogo" e "exógeno" quando usados aqui, neste pedido de patente, para se referir a uma sequência de ácido nucleico (por exemplo, uma sequência de DNA ou RNA) ou um gene, se referem a uma sequência que se origina de uma fonte estranha à célula hospedeira particular ou, caso da mesma fonte, é modificada de sua forma original. Portanto, um gene heterólogo em uma célula hospedeira inclui um gene que é endógeno à célula hospedeira particular mas foi modificado. Os termos também incluem múltiplas cópias que não ocorrem naturalmente de uma sequência de DNA que ocorre naturalmente. Portanto, os termos se referem a um segmento de DNA que é estranho ou heterólogo à célula, ou homólogo à célula mas em uma posição dentro do ácido nucleico da célula hospedeira no qual o elemento não é encontrado ordinariamente. Segmentos de DNA exógenos são expressados para produzir polipeptídeos exógenos.
[000487] Uma sequência de ácido nucleico "homóloga" (por exemplo, DNA) é uma sequência de ácido nucleico (por exemplo, DNA ou RNA) naturalmente associada a uma célula hospedeira na qual é introduzida.
[000488] A escolha de promotores a serem incluídos depende de vários fatores, incluindo, mas não limitados a, eficiência, selecionabilidade, indutibilidade, nível de expressão desejado, e expressão preferêncial em célula ou tecido. É uma questão de rotina para uma pessoa versada na técnica modular a expressão de uma sequência selecionando e posicionando adequadamente promotores e outras regiões regulatórias em relação à sequência.
[000489] Alguns promotores adequados iniciam transcrição somente, ou predominantemente, em alguns tipos celulares. Portanto, conforme usado aqui, neste pedido de patente, um promotor preferêncial de tipo celular ou tecido é um que dirige a expressão preferêncialmente no tecido alvo, mas também pode levar a alguma expressão em outros tipos celulares ou tecidos também. Métodos para identificar e caracterizar regiões promotoras em DNA genômico de planta incluem, por exemplo, os descritos nas seguintes referências: Jordano, et. al., Plant Cell, 1:855-866 (1989); Bustos, et. al., Plant Cell, 1:839-854 (1989); Green, et. al., EMBO J. 7, 4035-4044 (1988); Meier, et. al., Plant Cell, 3, 309-316 (1991); e Zhang, et. al., Plant Physiology 110: 1069-1079 (1996).
[000490] Vários genes e/ou promotores regulados por tecidos preferênciais têm sido reportados em plantas. Alguns genes tecido- preferênciais reportados incluem os genes codificando as proteínas de armazenamento de sementes (tais como napina, cruciferina, beta- conglicinina, e faseolina, prolaminas, glutelinas, globulinas, e zeínas) zeínas ou proteínas de corpo oleoso (tais como oleosina), ou genes envolvidos na biossíntese de ácidos graxos (incluindo proteína veículo de acila, estearoil-ACP dessaturase, e dessaturases de ácidos graxos (fad 2-1)), e outros genes expressados durante desenvolvimento de embriões (tais como Bce4, vide, por exemplo, EP 255378 e Kridl et. al., (1991) Seed Science Research, 1:209). Exemplos de promotores- tecido-específicos, os quais foram descritos, incluem a lecitina (Vodkin, Prog. Clin. Biol. Res., 138;87 (1983); Lindstrom et. al., (1990) Der. Genet., 11:160), deidrogenase de álcool de milho 1 (Dennis et. al., Nucleic Acids Res., 12:3983 (1984)), complexo de colheita leve de milho (vide, por exemplo, Simpson, (1986) Science, 233:34; Bansal (1992) Proc. Natl. Acad. Sci. USA 89:3654), proteína de choque térmico de milho (vide, por exemplo, Odell et. al., (1985) Nature, 313:810; carboxilase de pequena subunidade RuBP da ervilha (vide, por exemplo, Poulsen et. al., (1986) Mol. Gen. Genet., 205:193-200; Cashmore et. al., (1983) Gen. Eng. of Plants, Plenum Press, New York, 29-38); manopina sintase do plasmídeo Ti (vide, por exemplo, Langridge et. al., (1989) Proc. Natl. Acad. Sci. USA, 86:3219-3223), nopalina sintase do plasmídeo Ti (Langridge et. al., (1989) Proc. Natl. Acad. Sci. USA, 86:3219-3223), calcona isomerase da petúnia (vide, por exemplo, vanTunen (1988) EMBO J. 7:1257) ; proteína 1 rica em glicina do feijão (vide, por exemplo, Keller (1989) Genes Dev. 3:1639) ; CaMV 35s truncado (vide, por exemplo, Odell (1985) Nature 313:810) ; patatina da batata (vide, por exemplo, Wenzler (1989) Plant Mol. Biol. 13:347; célula das raízes (vide, por exemplo, Yamamoto (1990) Nucleic Acids Res. 18:7449) ; zeína do milho (vide, por exemplo, Reina (1990) Nucleic Acids Res. 18:6425; Lopes et. al. (1995) Mol. Gen. Genet. 247: 603-613; Kriz (1987) Mol. Gen. Genet. 207:90; Wandelt (1989) Nucleic Acids Res., 17:2354; Langridge (1983) Cell, 34:1015; Reina (1990) Nucleic Acids Res., 18:7449), promotor ADP-gpp (vide, por exemplo, a Patente dos Estados Unidos No. 7.102.057); globulina- 1 (vide, por exemplo, Belanger (1991) Genetics 129:863) ; α-globulina (Sunilkumar, et. al. (2002), Transgenic Res. 11 :347-359) ; D-tubulina ; cab (vide, por exemplo, Sullivan (1989) Mol. Gen. Genet., 215:431); PEPCase (vide por exemplo, Hudspeth & Grula, (1989) Plant Molec. Biol., 12:579-589); promotores associados a complexo genético R (Chandler et. al., (1989) Plant Cell, 1:1175); promotor de vicilina da ervilha (Czako et. al., (1992) Mol. Gen. Genet., 235:33; a Patente dos Estados Unidos No. 5.625.136); promotor GTL1 (Takaiwa et. al. (1991) Plant Mol. Biol. 16 (1), 49-58); promotores de calcona sintase (Franken et. al., (1991) EMBO J., 10:2605); promotor GY1 (Sims & Goldburg (1989) Nuc. Acid Res. 17(11) 4368) e similares; todas as quais são aqui, a este pedido de patente, incorporadas por meio de referência.
[000491] Uma classe de promotores-fruto preferênciais expressados em ou durante antétese através do desenvolvimento do fruto, pelo menos até o início do amadurecimento, é discutida na Patente U.S. 4.943.674, cuja descoberta é por este incorporada por meio de referência. O promotor para o gene da poligalacturonase está ativo no amadurecimento do fruto. O gene da poligalacturonase é descrito na Patente dos Estados Unidos No. 4.535.060, na Patente dos Estados Unidos No. 4.769.061, na Patente dos Estados Unidos No. 4.801.590, e na Patente dos Estados Unidos No. 5.107.065, cujas divulgações são incorporadas aqui, a este pedido de patente, por meio de referência.
[000492] Outros exemplos de promotores-tecido preferênciais incluem aqueles que dirigem a expressão em células de folhas depois de dano à folha (por exemplo, por mastigação por insetos), em tubérculos (por exemplo, promotor genético de patatina), e em células de fibras (um exemplo de uma proteína de células de fibras regulada pelo desenvolvimento é E6 (John & Crow (1992) PNAS 89:5769-5773). O gene E6 é mais ativo em fibra, embora baixos níveis de transcriptos sejam encontrados em folha, óvulo e flor.
[000493] Promotores ativos em tecido fotossintético de modo a orientar a transcrição em tecidos verdes tais como folhas e caules, são adequados quando orientam a expressão somente ou predominantemente em semelhantes tecidos. Alternativamente, o promotor pode conferir expressão constitutivamente por toda a planta, ou diferencialmente com respeito aos tecidos verdes, ou diferencialmente com respeito ao estágio de desenvolvimento do tecido verde no qual ocorre expressão, ou em resposta a estímulos externos.
[000494] Exemplos de tais promotores incluem os promotores de ribulose-1,5-bisfosfato carboxilase (RbcS) tais como o promotor RbcS do lariço oriental (Larix laricina), o promotor cab6 do pinheiro (Yamamoto et. al. (1994) Plant Cell Physiol. 35:773-778), o promotor genético Cab-1 do trigo (Fejes et. al. (1990) Plant Mol. Biol. 15:921932), o promotor CAB-1 do espinafre (Lubberstedt et. al. (1994) Plant Physiol. 104:997-1006), o promotor cab1R do arroz (Luan et. al. (1992) Plant Cell 4:971-981), o promotor de piruvato ortofosfato diquinase (PPDK) do milho (Matsuoka et. al. (1993) Proc Natl Acad Sci USA 90:9586-9590), o promotor Lhcb1*2 do tabaco (Cerdan et. al. (1997) Plant Mol. Biol. 33:245-255), o promotor SUC2 sucrose-H+ symporter da Arabidopsis thaliana (Truernit et. al. (1995) Planta 196:564-570), e promotores de proteínas da membrana tilacóide do espinafre (psaD, psaF, psaE, PC, FNR, atpC, atpD, cab, rbcS. Outros promotores que orientam a transcrição em caules, folhas e tecidos verdes são descritos na Publicação de Patente dos Estados Unidos No. 2007/0006346, aqui, a este pedido de patente, incorporada por meio de referência em sua totalidade.
[000495] A especificidade tecidual de alguns promotores "tecido preferênciais" pode não ser absoluta e pode ser testada por genes- repórter tais como Gus ou proteína fluorescente verde, proteína fluorescente ciano, proteína fluorescente amarela ou proteína fluorescente vermelha. Pode-se também obter expressão tecido preferêncial com expressão "imperfeita" por uma combinação de diferentes promotores-tecido preferênciais. Outros promotores-tecido preferênciais podem ser isolados por uma pessoa versada na técnica (vide a patente U.S. 5.589.379).
[000496] Em um aspecto, promotores de plantas os quais são induzíveis na exposição a hormônios vegetais, tais como auxinas, são usados para expressar os ácidos nucleicos da invenção. Por exemplo, a invenção pode usar o fragmento do promotor E1 de elementos de resposta à auxina (AuxREs) no soja (Glycine max L.) (Liu (1997) Plant Physiol. 115:397-407); o promotor GST6 de Arabidopsis responsivo à auxina (também responsivo ao ácido salicílico e ao peróxido de hidrogênio) (Chen (1996) Plant J. 10: 955-966); o promotor parC do tabaco induzível por auxina (Sakai (1996) 37:906-913); um elemento de resposta à biotina da planta (Streit (1997) Mol. Plant Microbe Interact. 10:933-937); e, o promotor responsivo ao ácido abscísico do hormônio do stress (Sheen (1996) Science 274:1900-1902).
[000497] Os ácidos nucleicos da invenção também podem ser ligados operavelmente a promotores de plantas os quais são induzíveis na exposição a reagentes químicos os quais podem ser aplicados à planta, tais como herbicidas ou antibiótico. Por exemplo, sistemas de expressão genética que são ativados na presença de um ligante químico, incluindo etanol, tais como podem ser encontrados na publicação de patente internacional No. WO 96/27673; na publicação de patente internacional No. WO 93/01294; na patente WO 94/03619; e na patente WO 02/061102, todas as quais são por este incorporadas por meio de referência. Pode ser usado o promotor In2-2 do milho, ativado por fitoprotetores de herbicida de benzenossulfonamida, (De Veylder (1997) Plant Cell Physiol. 38:568-577); a aplicação de diferentes safeners de herbicida induz padrões distintos de expressão genética, incluindo expressão na raiz, nas hidátodes, e no meristema apical do broto. Sequência codificante pode estar sob o controle de, por exemplo, um promotor induzível por tetraciclina, por exemplo, conforme descrito com plantas de tabaco transgênicas contendo o gene da arginina decarboxilase da Avena sativa L. (aveia) (Masgrau (1997) Plant J. 11:465-473); estrogênio, tal como, o receptor de ecdisona (patente WO 01/52620) ou, um elemento responsivo ao ácido salicílico (Stange (1997) Plant J. 11:1315-1324). Usando promotores induzidos quimicamente (por exemplo, por hormônio ou por pesticida), isto é, promotor responsivo a um produto químico o qual pode ser aplicado à planta transgênica no campo, a expressão de um polipeptídeo da invenção pode ser induzida em um estágio de desenvolvimento particular da planta.
[000498] Exemplos de alguns promotores constitutivos os quais têm sido descritos incluem actina do arroz 1 (Wang et. al. (1992) Mol. Cell. Biol., 12:3399; Patente dos Estados Unidos No. 5.641.876); outras isoformas de actina (McElroy et. al. (1990) Plant Cell 2: 163-171 e McElroy et. al. (1991) Mol. Gen. Genet. 231: 150-160); CaMV 35S (Odell et. al. (1985) Nature, 313:810); CaMV 19S (Lawton et. al. (1987) Plant Mol. Biol. 9:315-324; Patente dos Estados Unidos No. 5.639.949); nos (Ebert et. al. (1987) PNAS USA 84:5745-5749); Adh (Walker et. al. (1987) PNAS USA 84:6624-6628), sucrose sintase (Yang & Russell (1990) PNAS USA 87:4144-4148); e os promotores de ubiquitina (por exemplo, girassol - Binet et. al. (1991) Plant Science 79: 87-94; maize - Christensen et. al. (1989) Plant Molec. Biol. 12: 619632; e Arabidopsis - Callis et. al., J. Biol. Chem. (1990) 265:1248612493; e Norris et. al., Plant Mol. Biol. (1993) 21:895-906.
[000499] Uma variedade de terminadores transcricionais estão disponíveis para uso em cassetes de expressão. Estes são responsáveis pela terminação da transcrição além do transgene e correta poliadenilação de mRNA. A região de terminação pode ser nativa com a região de iniciação transcricional, pode ser nativa com a sequência de DNA de interesse ligada operavelmente, pode ser nativa com o hospedeiro da planta, ou pode ser derivada de outra fonte (isto é, estranha ou heteróloga ao promotor, à sequência de DNA de interesse, o hospedeiro da planta, ou qualquer combinação dos mesmos). Terminadores transcricionais apropriados são aqueles que são conhecidos por funcionar em plantas e incluem o terminador CAMV 35S, o terminador tml, o terminador de nopalina sintase e o terminador rbcs E9 de ervilha. Estes podem ser usados tanto em monocotiledôneas quanto em dicotiledôneas. Além disso, pode ser usado um terminador de transcrição nativo do gene.
[000500] Foi visto que numerosas sequências reforçam a expressão genética a partir de dentro da unidade transcricional e estas sequências podem ser usadsa em combinação com os genes desta invenção para aumentar sua expressão em plantas transgênicas. Por exemplo, foi demonstrado que várias sequências de íntrons reforçam a expressão, particularmente em células monocotiledôneas. Por exemplo, foi visto que os íntrons do gene Adhl de milho reforçam significativamente a expressão do gene selvagem sob seu promotor cognato quando introduzido em células de milho.Uma série de sequências líder não-traduzidas derivadas de vírus também são conhecidas por reforçar a expressão, e estas são particularmente eficazes em células dicotiledôneas. Especificamente, foi mostrado que sequências líder do Vírus do Mosaico do Tabaco (TMV, a " sequência W "), Vírus do Mosqueado Clorótico do Milho (MCMV), e do Vírus do Mosaico da Alfafa (AMV) são eficazes para reforçar a expressão (por exemplo, Gallie et. al. Nucl. Acids Res. 15: 8693-8711 (1987); Skuzeski et. al. Plant Molec. Biol. 15: 65-79 (1990)).
Direcionamento do Produto Genético Dentro da Célula
[000501] Qualquer mecanismo para direcionar produtos genéticos conhecidos em plantas podem ser usados para praticar esta invenção, e as sequências controlando o funcionamento destes mecanismos foram caracterizadas em algum detalhe. Sequências que foram caracterizadas como causando o direcionamento de produtos genéticos a outros compartimentos celulares também podem ser usads para praticar esta invenção. Sequências terminais amino responsáveis por direcionar uma proteína de interesse a qualquer compartimento celular, tal como, um vacúolo, mitocôndria, peroxissoma, estruturas protéicas, retículo endoplasmático, cloroplasto, grânulo de amido, amiloplasto, apoplasto ou parede celular de uma planta (por exemplo, Unger et. al. Plant Molec. Biol. 13: 411-418 (1989); Rogers et. al. (1985) Proc. Natl. Acad. Sci. USA 82: 6512-651; Patente dos Estados Unidos No. 7.102.057; patente internacional No. WO 2005/096704, todas as quais são por este incorporado por meio de referência), podem ser usadas para praticar esta invenção. Em um aspecto, a sequência de sinal é uma sequência de sinal N-terminal de waxy, uma sequência de sinal N-terminal de y- zeína, um domínio de ligação de amido, um domínio de ligação de amido de C-terminal, uma sequência de direcionamento de cloroplasto, a qual importa a proteína madura para o cloroplasto (Comai et. al. (1988) J. Biol. Chem. 263: 15104-15109; van den Broeck, et. al. (1985) Nature 313: 358-363; Patente dos Estados Unidos No. 5.639.949) ou uma sequência de sinal de secreção de células de aleurona (Koehler & Ho, Plant Cell 2: 769-783 (1990)). Adicionalmente, sequências de amino terminal em combinação com sequências de carbóxi terminal são responsáveis por direcionamento vacuolar de produtos genéticos (Shinshi et. al. (1990) Plant Molec. Biol. 14: 357-368) podem ser usadas para praticar esta invenção.
[000502] Em um aspecto, a sequência de sinal selecionada pode incluir o sítio de clivagem conhecido, e a fusão construída considera quaisquer aminoácidos depois do um ou mais sítios de clivagem, os quais são requeridos para clivagem. Em algumas modalidades, este requisito pode ser satisfeito pela adição de um pequeno número de aminoácidos entre o sítio de clivagem e o transgene ATG ou, alternativamente, substituição de alguns aminoácidos dentro da sequência do transgene. Estas técnicas de construção são de conhecimento geral na técnica e são igualmente aplicáveis a qualquer compartimento celular. Os mecanismos descritos acima para direcionamento celular podem ser utilizados não somente em combinação com seus promotores cognatos, mas também em combinação com promotores heterólogos de modo a realizar uma meta de direcionamento celular específica sob a regulação transcricional de um promotor que tem um padrão de expressão diferente daquele do promotor do qual o sinal de direcionamento deriva.
Vetores e veículos de clonagem
[000503] A invenção proporciona vetores, incluindo vetores de expressão e de clonagem, ou qualquer veículos de clonagem compreendendo ácidos nucleicos da invenção, por exemplo, sequências codificando as glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção. Vetores de expressão e veículos de clonagem da invenção podem compreender partículas virais, vírus recombinantes, baculovírus, fago, plasmídeos, fagemídeos, cosmídeos, fosmídeos, cromossomas artificiais bacterianos, DNA viral (por exemplo, varíola bovina, adenovírus, foul pox virus, pseudorabies e derivados de SV40), cromossomas artificiais à base de P1, plasmídeos de levedura, cromossomas artificiais de levedura, e quaisquer outros vetores específicos para hospedeiros de interesse específicos (tais como Pseudomonas, Bacillus, Aspergillus e levedura). Vetores da invenção podem incluir sequências de DNA cromossômico, não- cromossômico e sintéticos. Grandes números de vetores adequados são de conhecimento daqueles versados na técnica, e estão disponíveis comercialmente. Vetores exemplares incluem: bacterianos: vetores pQE (Qiagen), plasmídeos pBluescript, vetores pNH, (vetores lâmbda-ZAP (Stratagene); ptrc99a, pKK223-3, pDR540, pRIT2T (Pharmacia); Eucarióticos: pXT1, pSG5 (Stratagene), pSVK3, pBPV, pMSG, pSVLSV40 (Pharmacia). No entanto, qualquer outro plasmídeo ou outro vetor pode ser usado contanto que sejam replicáveis e viáveis no hospedeiro. Vetores de baixo número de cópias ou de alto número de cópias podem ser empregados com a presente invenção.
[000504] “Plasmídeos” podem estar disponíveis comercialmente, disponíveis publicamente em uma base não-restrita, ou podem ser construídos a partir de plasmídeos disponíveis de acordo com procedimentos publicados. Plasmídeos equivalentes aos descritos aqui, neste pedido de patente, são conhecidos na técnica e serão evidentes para o profissional ordinariamente versado. Os plasmídeos de partida aqui, neste pedido de patente, ou estão disponíveis comercialmente, disponíveis publicamente em uma base não-restrita, ou podem ser construídos a partir de plasmídeos disponíveis de acordo com procedimentos publicados. Além disso, plasmídeos equivalentes aos descritos aqui, neste pedido de patente, são conhecidos na técnica e serão evidentes para o técnico ordinariamente versado.
[000505] O vetor de expressão pode compreender um promotor, um sítio de ligação de ribossoma para iniciação de translação e um terminador de transcrição. O vetor também pode incluir sequências apropriadas para amplificar expressão. Vetores de expressão de mamíferos podem compreender uma origem de replicação, quaisquer sítios de ligação de ribossoma necessários, um sítio de poliadenilação, sítios doadores e aceitadores de junção, sequências de terminação transcricional, e sequências não-transcritas flanqueantes 5'. Em alguns aspectos, sequências de DNA derivadas dos sítios de junção SV40 e de poliadenilação podem ser usadas para proporcionar os elementos genéticos não-transcritos requeridos.
[000506] Em um aspecto, a invenção proporciona um "cassete de expressão" compreendendo uma sequência da invenção, por exemplo, um "cassete de expressão" pode compreender uma sequência de nucleotídeos o qual é capaz de afetar a expressão de um ácido nucleico, por exemplo, um gene estrutural (isto é, uma sequência codificante de proteína, tal como uma glucanase da invenção) em um hospedeiro compatível com as sequências referidas. Cassetes de expressão compreendem pelo menos um promotor ligado operavelmente com a sequência codificante de polipeptídeo; e, opcionalmente, com outras sequências, por exemplo, sinais de terminação de transcrição. Fatores adicionais necessários ou úteis para efetuar a expressão também podem ser usados, por exemplo, reforçadores. Portanto, cassetes de expressão também incluem plasmídeos, vetores de expressão, vírus recombinantes, qualquer forma de vetor de “DNA nu” recombinante, e similares. Um "vetor" compreende um ácido nucleico o qual pode infectar, transfectar, transduzir transitoriamente ou permanentemente uma célula. Será reconhecido que um vetor pode ser um ácido nucleico nu, ou um ácido nucleico em complexo com proteína ou lipídeo. O vetor opcionalmente compreende ácidos nucleicos e/ou proteínas, e/ou membranas virais ou bacterianos (por exemplo, uma membrana celular, um envelope lipídico viral, e etc.). Vetores incluem, mas não estão limitados a replicons (por exemplo, replicons de RNA, bacteriófagos) aos quais fragmentos de DNA podem ser fixados e se tornarem replicados. Vetores portanto incluem, mas não estão limitados a RNA, DNA ou RNA circular ou linear auto-replicante autônomo (por exemplo, plasmídeos, vírus, e similares, vide, por exemplo, a Patente dos Estados Unidos No. 5.217.879), e incluem tanto os plasmídeos de expressão quanto de não-expressão. Onde um micro-organismo recombinante ou cultura celular é descrito como hospedando um "vetor de expressão" isto inclui tanto DNA circular e linear extracromossômico quanto DNA que tenha sido incorporado em um ou mais cromossomas do hospedeiro. Onde um vetor está sendo mantido por uma célula hospedeira, o vetor pode ou ser estavelmente replicado pelas células durante mitose como uma estrutura autônoma, ou é incorporado dentro do genoma do hospedeiro.
[000507] Em um aspecto, a expressão vetores contêm um ou mais genes marcadores selecionáveis para permitir seleção de células hospedeiras contendo o vetor. Os marcadores selecionáveis referidos incluem genes codificando dihidrofolato redutase ou genes conferindo resistência à neomicina para cultura de células eucarióticas, genes conferindo resistência à tetraciclina ou ampicilina em E. coli, e o gene TRP1de S. cerevisiae. Regiões promotoras podem ser selecionadas de qualquer gene desejado usando vetores de cloranfenicol transferase (CAT) ou outros vetores com marcadores selecionáveis.
[000508] Vetores para expressar o polipeptídeo ou fragmento do mesmo em células eucarióticas também podem conter reforçadores para aumentar os níveis de expressão. Reforçadores são elementos de DNA de ação cis, geralmente a partir de cerca de 10 a cerca de 300 pb de extensão que agem sobre um promotor para aumentar sua transcrição. Exemplos incluem o reforçador SV40 sobre o lado tardio da origem de replicação pb 100 a 270, o reforçador do promotor precoce de cytomegalovirus, o reforçador de polioma sobre o lado tardio da origem de replicação, e os reforçadores de adenovírus.
[000509] Uma sequência de ácido nucleico pode ser inserida em um vetor por uma variedade de procedimentos. Em geral, a sequência é ligada à posição desejada no vetor seguindo a digestão do inserto e o vetor com endonucleases de restrição apropriadas. Alternativamente, extremidades cegas tanto no inserto quanto no vetor podem ser ligadas. Uma variedade de técnicas de clonagem são conhecidas na técnica, por exemplo, conforme descrito em Ausubel e Sambrook. Os referidos pocedimentos e outros são considerados estando dentro do escopo dos versados na técnica.
[000510] O vetor pode ser sob a forma de um plasmídeo, uma partícula viral, ou um fago. Outros vetores incluem sequências de DNA cromossômicos, não-cromossômicos e sintéticos, derivados de SV40; plasmídeos bacterianos, fago de DNA, baculovírus, plasmídeos de levedura, vetores derivado de combinações de plasmídeos e fago de DNA, DNA viral tal como varíola bovina, adenovírus, pox vírus aviário, e pseudorabies. Uma variedade de vetores de clonagem e expressão para uso com hospedeiros procarióticos e eucarióticos são descritas, por exemplo, por Sambrook.
[000511] Vetores bacterianos particulares os quais podem ser usados incluem os plasmídeos disponíveis comercialmente compreendendo elementos genéticos do vetor de clonagem de conhecimento geral pBR322 (ATCC 37017), pKK223-3 (Pharmacia Fine Chemicals, Uppsala, Sweden), GEM1 (Promega Biotec, Madison, WI, USA) pQE70, pQE60, pQE-9 (Qiagen), pD10, psiX174 pBluescript II KS, pNH8A, pNH16a, pNH18A, pNH46A (Stratagene), ptrc99a, pKK223-3, pKK233-3, DR540, pRIT5 (Pharmacia), pKK232-8 e pCM7. Vetores eucarióticos particulares incluem pSV2CAT, pOG44, pXT1, pSG (Stratagene) pSVK3, pBPV, pMSG, e pSVL (Pharmacia). No entanto, qualquer outro vetor pode ser usado contanto que seja replicável e viável na célula hospedeira.
[000512] Os ácidos nucleicos da invenção podem ser expressados em cassetes de expressão, vetores ou vírus e expressados transitoriamente ou estavelmente em células e sementes de plantas. Um sistema de expressão transitório exemplar usa sistemas de expressão epissomal, por exemplo, RNA viral do vírus do mosaico da couve-flor (CaMV) produzido no núcleo por transcrição de um minicromossoma epissomal contendo DNA superespiralado, vide, por exemplo, Covey (1990) Proc. Natl. Acad. Sci. USA 87:1633-1637. Alternativamente, sequências codificantes, isto é, todas ou subfragmentos de sequências da invenção podem ser inseridos no genoma de uma célula hospedeira vegetal se tornando uma parte integral do DNA cromossômico do hospedeiro. Transcriptos de senso ou antissenso podem ser expressados desta maneira. Um vetor compreendendo as sequências (por exemplo, promotores ou regiões codificantes) de ácidos nucleicos da invenção pode compreender um gene marcador que confere um fenótipo selecionável sobre uma célula de planta ou uma semente. Por exemplo, o marcador pode codificar resistência a biocida, particularmente resistência a antibiótico, tal como resistência à canamicina, G418, bleomicina, higromicina, ou resistência à herbicida, tal como resistência a clorossulfuron ou Basta.
[000513] Vetores de expressão capazes de expressar ácidos nucleicos e proteínas em plantas são de conhecimento geral na técnica, e podem incluir, por exemplo, vetores de Agrobacterium spp., vírus de batata X (vide, por exemplo, Angell (1997) EMBO J. 16:3675-3684), vírus do mosaico do tabaco (vide, por exemplo, Casper (1996) Gene 173:69-73), vírus da interrupção do crescimento do pé de tomate (vide, por exemplo, Hillman (1989) Virology 169:42-50), vírus da causticação do tabaco (vide, por exemplo, Dolja (1997) Virology 234:243-252), vírus do mosaico do bean golden (vide, por exemplo, Morinaga (1993) Microbiol Immunol. 37:471-476), vírus do mosaico da couve-flor (vide, por exemplo, Cecchini (1997) Mol. Plant Microbe Interact. 10:1094-1101), elemento transportável Ac/Ds do milho (vide, por exemplo, Rubin (1997) Mol. Cell. Biol. 17:6294-6302; Kunze (1996) Curr. Top. Microbiol. Immunol. 204:161-194), e o elemento transportável supressor-mutador (Spm) do milho (vide, por exemplo, Schlappi (1996) Plant Mol. Biol. 32:717-725); e derivados dos mesmos.
[000514] Em um aspecto, o vetor de expressão pode ter dois sistemas de replicação para permitir que seja mantido em dois organismos, por exemplo, em células de mamífero ou de inseto para expressão e em um hospedeiro procariótico para clonagem e amplificação. Além disso, para integrar vetores de expressão, o vetor de expressão pode conter pelo menos uma sequência homóloga ao genoma da célula hospedeira. Pode conter duas sequências homólogas as quais flanqueiam o construto de expressão. O vetor integrante pode ser dirigido para um lócus específico na célula hospedeira selecionando a sequência homóloga apropriada para inclusão no vetor. Construtos para integrar vetores são de conhecimento geral na técnica.
[000515] Vetores de expressão da invenção também podem incluir um gene marcador selecionável para permitir a seleção de cepas bacterianas que foram transformadas, por exemplo, genes os quais tornam as bactérias resistentes a fármacos tais como ampicilina, cloranfenicol, eritromicina, canamicina, neomicina e tetraciclina. Marcadores selecionáveis também podem incluir genes biossintéticos, tais como os nos caminhos biossintéticos de histidina, triptofano e leucina.
[000516] A sequência de DNA no vetor de expressão é ligada operativamente a uma ou mais sequências de controle de expressão apropriadas (promotor) para dirigir a síntese de RNA. Promotores bacterianos nomeados particulares incluem lacI, lacZ, T3, T7, gpt, lâmbda PR, PL e trp. Promotores eucarióticos incluem CMV imediato precoce, timidina quinase de HSV, SV40 precoce e tardio, LTRs de retrovírus e metalotioneína-I de camundongo. Seleção do vetor e promotor apropriados está bem dentro do nível de conhecimento regular da técnica. O vetor de expressão também contém um sítio de ligação de ribossoma para iniciação de translação e um terminador de transcrição. O vetor também pode incluir sequências apropriadas para amplificar a expressão. Regiões promotoras podem ser selecionadas entre qualquer gene desejado usando vetores de cloranfenicol transferase (CAT) ou outros vetores com marcadores selecionáveis. Além disso, os vetores de expressão em um aspecto contêm um ou mais genes marcadores selecionáveis para proporcionar um traço fenotípico para seleção de células hospedeiras transformadas tais como dihidrofolato redutase ou resistência à neomicina para cultura de células eucarióticas, ou tais como resistência à tetraciclina ou ampicilina em E. coli.
[000517] Vetores de expressão de mamíferos também podem compreender uma origem de replicação, quaisquer sítios de ligação de ribossoma necessários, um sítio de poliadenilação, sítios doadores e aceitadores de junção, sequências de terminação transcricional e sequências não transcritas 5' flanqueantes. Em alguns aspectos, sequências de DNA derivadas dos sítios de junção SV40 e de poliadenilação podem ser usadas para proporcionar os elementos genéticos não-transcritos requeridos.
[000518] Vetores para expressar o polipeptídeo ou fragmento do mesmo em células eucarióticas também podem conter reforçadores para aumentar os níveis de expressão. Reforçadores são elementos de DNA de ação cis, geralmente a partir de cerca de 10 a cerca de 300 pb de extensão que agem sobre um promotor para aumentar sua transcrição. Exemplos incluem o reforçador SV40 sobre o lado tardio da origem de replicação pb 100 a 270, o reforçador de promotor precoce de citomegalovírus, o reforçador de polioma sobre o lado tardio da origem de replicação e os reforçadores de adenovírus.
[000519] Além disso, os vetores de expressão tipicamente contêm um ou mais genes marcadores selecionáveis para permitir seleção de células hospedeiras contendo o vetor. Os referidos marcadores selecionáveis incluem genes codificando dihidrofolato redutase ou genes conferindo resistência à neomicina para cultura de células eucarióticas, genes conferindo resistência à tetraciclina ou ampicilina em E. coli e o gene TRP1 de S. cerevisiae.
[000520] Em alguns aspectos, o ácido nucleico codificando um dos polipeptídeos da invenção, ou fragmentos compreendendo pelo menos cerca de 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos é montado em fase apropriada com uma sequência líder capaz de dirigir a secreção do polipeptídeo traduzido ou fragmento do mesmo. Opcionalmente, o ácido nucleico pode codificar um polipeptídeo de fusão no qual um dos polipeptídeos da invenção, ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos é fundido a peptídeos ou polipeptídeos heterólogos, tais como peptídeos de identificação de N-terminal os quais conferem características desejadas, tais como aumento da estabilidade ou purificação simplificada.
[000521] A sequência de DNA apropriada pode ser inserida no vetor por uma variedade de procedimentos. Em geral, a sequência de DNA é ligada à posição desejada no vetor depois de digestão do inserto e do vetor com endonucleases de restrição apropriadas. Alternativamente, extremidades cegas tanto no inserto quanto no vetor podem ser ligadas. Uma variedade de técnicas de clonagem são divulgadas em Ausubel et al. Current Protocols in Molecular Biology, John Wiley 503 Sons, Inc. 1997 e Sambrook et al., Molecular Cloning: A Laboratory Manual 2nd Ed., Cold Spring Harbor Laboratory Press (1989. Os referidos pocedimentos e outros são considerados dentro do escopo dos versados na técnica.
[000522] O vetor pode ser, por exemplo, sob a forma de um plasmídeo, uma partícula viral, ou um fago. Outros vetores incluem sequências de DNA cromossômico, não-cromossômico e sintético, derivados de SV40; plasmídeos bacterianos, DNA de fago, baculovírus, plasmídeos de levedura, vetores derivados de combinações de plasmídeos e DNA de fago, DNA viral tal como varíola bovina, adenovírus, pox vírus aviário e pseudorabies. Uma variedade de vetores de clonagem e expressão para uso com hospedeiros procarióticos e eucarióticos são descritas por Sambrook, et al., Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor, N.Y., (1989).
Células hospedeiras e células transformadas
[000523] A invenção também proporciona uma célula transformada compreendendo uma sequência de ácido nucleico da invenção, por exemplo, uma sequência codificando uma glucanase da invenção, ou um vetor da invenção. A célula hospedeira pode ser qualquer das células hospedeiras familiares daqueles versados na técnica, incluindo células procarióticas, células eucarióticas, tais como células bacterianas, células fúngicas, células de levedura, células de mamífero, células de inseto, ou células de plantas. Células bacterianas típicas incluem qualquer espécie dentro dos gêneros Escherichia, Bacillus, Streptomyces, Salmonella, Pseudomonas e Staphylococcus, incluindo, por exemplo, Escherichia coli, Lactococcus lactis, Bacillus subtilis, Bacillus cereus, Salmonella typhimurium, Pseudomonas fluorescens. Células fúngicas típicas incluem qualquer espécie de Aspergillus. Células de levedura típicas incluem qualquer espécie de Pichia, Saccharomyces, Schizosaccharomyces, ou Schwanniomyces, incluindo Pichia pastoris, Saccharomyces cerevisiae, ou Schizosaccharomyces pombe. Células de inseto típicas incluem qualquer espécie de Spodoptera ou Drosophila, incluindo Drosophila S2 and Spodoptera Sf9. Células animais exemplares incluem CHO, COS ou melanoma de Bowes ou qualquer linhagem de células de camundongo ou humanas. A seleção de um hospedeiro apropriado está dentro das capacidades daqueles versados na técnica. Técnicas para transformar uma ampla variedade de espécies de plantas superiores são de conhecimento geral e estão descritas na literatura técnica e científica. Vide, por exemplo, Weising (1988) Ann. Rev. Genet. 22:421-477; e a Patente dos Estados Unidos No. 5.750.870.
[000524] O vetor pode ser introduzido nas células hospedeiras usando qualquer de uma variedade de técnicas, incluindo transformação, transfecção, transdução, infecção viral, pistolas genéticas, ou transferência genética mediada por Ti. Métodos particulares incluem transfecção de fosfato de cálcio, transfecção mediada por DEAE-Dextrano, lipofecção, ou eletroporação (Davis, L., Dibner, M., Battey, I., Basic Methods in Molecular Biology, (1986)).
[000525] Em um aspecto, os ácidos nucleicos ou vetores da invenção são introduzidos nas células para triagem, deste modo, os ácidos nucleicos penetram nas células em uma maneira adequada para expressão subsequente do ácido nucleico. O método de introdução é largamente ditado pelo tipo de célula-alvo. Métodos típicos incluem precipitação de CaPO4, fusão de lipossoma, lipofecção (por exemplo, LIPOFECTIN®), eletroporação, infecção viral, e etc. Os ácidos nucleicos candidatos podem integrar estavelmente no genoma da célula hospedeira (por exemplo, com introdução retroviral) ou pode existir quer transitoriamente ou estavelmente no citoplasma (isto é, através do uso de plasmídeos tradicionaos, utilizando sequências regulatórias de rotina, marcadores de seleção, e etc.). Como muitas varreduras farmaceuticamente importantes requerem alvos de células de mamíferos molde ou humanas, podem ser usados vetores retrovirais capazes de transfectar os alvos referidos.
[000526] Onde apropriado, as células hospedeiras produzidas podem ser cultivadas em meio nutriente convencional modificado conforme adequado para ativar promotores, selecionar transformantes ou amplificar os genes da invenção. Depois de transformação de uma cepa hospedeira adequada e crescimento da cepa hospedeira até uma densidade celular apropriada, o promotor selecionado pode ser induzido por meios apropriados (por exemplo, mudança de temperatura ou indução química) e as células podem ser cultivadas por um período adicional para permitir que as mesmas produzam o polipeptídeo desejado ou fragmento do mesmo.
[000527] As células podem ser colhidas por centrifugação, rompidas por meios físicos ou químicos, e o extrato bruto resultante é retido para purificação posterior. Células microbianas empregadas para expressão de proteínas podem ser rompidas por qualquer método conveniente, incluindo ciclagem de congelamento-descongelamento, sonicação, disrupção mecânica, ou uso de agentes de lise celular. Os referidos métodos são de conhecimento geral daqueles versados na técnica. O polipeptídeo expressado ou fragmento do mesmo pode ser recuperado e purificado a partir de culturas de células recombinantes por meio de métodos incluindo precipitação de etanol ou sulfato de amônio, extração de ácido, cromatografia de permuta de ânions ou cátions, cromatografia de fosfocelulose, cromatografia de interação hidrofóbica, cromatografia de afinidade, cromatografia de hidroxilapatita e cromatografia de lectina. Etapas de redobramento de proteína podem ser usadas, conforme necessário, para completar a configuração do polipeptídeo. Caso desejado, pode ser empregada cromatografia líquida de alto desempenho (HPLC) para etapas finais de purificação.
[000528] Os construtos em células hospedeiras podem ser usados em uma maneira convencional para produzir o produto genético codificado pela sequência recombinante. Dependendo do hospedeiro empregado em um procedimento de produção recombinante, os polipeptídeos produzidos pelas células hospedeiras contendo o vetor podem ser glicosilados ou podem ser não-glicosilados. Polipeptídeos da invenção podem ou não incluir também um resíduo de aminoácido metionina inicial.
[000529] Sistemas de translação livres de células também podem ser empregados para produzir um polipeptídeo da invenção. Sistemas de translação livres de células podem usar mRNAs transcritos de um construto de DNA compreendendo um promotor ligado operavelmente a um ácido nucleico codificando o polipeptídeo ou fragmento do mesmo. Em alguns aspectos, o construto de DNA pode ser linearizado antes de conduzir uma reação de transcrição in vitro. O mRNA transcrito é em seguida incubado com um extrato de translação livre de células apropriado, tal como um extrato de reticulócitos de coelho, para produzir o polipeptídeo desejado ou fragmento do mesmo.
[000530] Os vetores de expressão podem conter um ou mais genes marcadores selecionáveis para proporcionar um traço fenotípico para seleção de células hospedeiras transformadas tais como resistência a dihidrofolato redutase ou neomicina para cultura de células eucarióticas, ou tais como resistência à tetraciclina ou ampicilina em E. coli.
[000531] Células hospedeiras contendo os polinucleotídeos de interesse, por exemplo, ácidos nucleicos da invenção, podem ser cultivadas em meio nutriente convencional modificado conforme adequado para ativação de promotores, seleção de transformantes ou amplificação de genes. As condições de cultura, tais como temperatura, pH e similares, são as previamente usadas com a célula hospedeira selecionada para expressão e serão evidentes para o técnico ordinariamente versado. Os clones os quais são identificados como tendo a atividade enzimática especificada podem ser então sequenciados para identificar a sequência de polinucleotídeo codificando uma enzima tendo a atividade reforçada.
[000532] A invenção proporciona um método para superexpressar uma glucanase recombinante em uma célula compreendendo expressar um vetor compreendendo um ácido nucleico da invenção, por exemplo, um ácido nucleico exemplar da invenção, incluindo, por exemplo, SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, E SEQ ID NO: 22 e as modificações específicas para SEQ ID NO: 1 conforme descrito aqui, neste pedido de patente. A superexpressão pode ser efetuada por quaisquer meios, por exemplo, uso de um promotor de alta atividade, um vetor dicistrônico ou por amplificação genética do vetor.
[000533] Os ácidos nucleicos da invenção podem ser expressados, ou superexpressados, em qualquer sistema de expressão in vitro ou in vivo. Quaisquer sistemas de cultura celular podem ser empregados para expressar, ou superexpressar, proteína recombinante, incluindo culturas bacterianas, de inseto, de levedura, fúngicas ou de mamífero. A superexpressão pode ser efetuada por escolha apropriada de promotores, reforçadores, vetores (por exemplo, uso de vetores de replicon, vetores dicistrônicos (vide, por exemplo, Gurtu (1996) Biochem. Biophys. Res. Commun. 229:295-8), meios, sistemas de cultura e similares. Em um aspecto, amplificação de gene usando marcadores de seleção, por exemplo, glutamina sintetase (vide, por exemplo, Sanders (1987) Dev. Biol. Stand. 66:55-63), em sistemas celulares são usadas para superexpressar os polipeptídeos da invenção. Detalhes adicionais referentes a esta abordagem estão na literatura pública e/ou são de conhecimento do técnico versado, por exemplo, patente européia No. EP 0659215 (W0 9403612 A1) (Nevalainen et al.); Lapidot (1996) J. Biotechnol. Nov 51:259-64; Luthi (1990) Appl. Environ. Microbiol. Sep 56:2677-83 (1990); Sung (1993) Protein Expr. Purif. Jun 4:200-6 (1993).
[000534] A célula hospedeira pode ser qualquer das células hospedeiras familiar àqueles versados na técnica, incluindo células procarióticas, células eucarióticas, células de mamífero, células de inseto, células fúngicas, células de levedura e/ou células de plantas. Como exemplos representativos de hospedeiros apropriados, podem ser mencionadas: células bacterianas, tais como E. coli, Streptomyces, Bacillus subtilis, Bacillus cereus, Salmonella typhimurium e várias espécies dentro dos gêneros Pseudomonas, Streptomyces e Staphylococcus, células fúngicas, tais como Aspergillus, levedura tais como quaisquer espécies de Pichia, Saccharomyces, Schizosaccharomyces, Schwanniomyces, incluindo Pichia pastoris, Saccharomyces cerevisiae, ou Schizosaccharomyces pombe, células de inseto tais como Drosophila S2 e Spodoptera Sf9, células animais tais como CHO, COS ou melanoma de Bowes e adenovírus. A seleção de um hospedeiro apropriado está dentro das capacidades daqueles versados na técnica.
[000535] O vetor pode ser introduzido nas células hospedeiras usando qualquer uma de uma variedade de técnicas, incluindo transformação, transfecção, transdução, infecção viral, pistolas genéticas, ou transferência genética mediada por Ti. Métodos particulares incluem transfecção de fosfato de cálcio, transfecção mediada por DEAE-Dextrano, lipofecção, ou eletroporação (por exemplo, vide Davis, L., Dibner, M., Battey, I., Basic Methods in Molecular Biology, (1986)).
[000536] Onde apropriado, as células hospedeiras produzidas podem ser cultivadas em meio nutriente convencional modificado conforme adequado para ativar promotores, selecionar transformantes ou amplificar os genes da invenção. Depois de transformação de uma cepa hospedeira adequada e crescimento da cepa hospedeira até uma densidade celular apropriada, o promotor selecionado pode ser induzido por meios apropriados (por exemplo, mudança de temperatura ou indução química) e as células podem ser cultivadas por um período adicional para permitir que as produzam o polipeptídeo desejado ou fragmento do mesmo.
[000537] As células podem ser colhidas por centrifugação, rompidas por meios físicos ou químicos e o extrato bruto resultante é retido para purificação adicional. Células microbianas empregadas para expressão de proteínas podem ser rompidas por qualquer método conveniente, incluindo ciclos de congelamento-descongelamento, sonicação, disrupção mecânica, ou uso de agentes de lise celular. Os referidos métodos são de conhecimento geral daqueles versados na técnica. O polipeptídeo expressado ou fragmento do mesmo pode ser recuperado e purificado de culturas de células recombinantes por meio de métodos incluindo precipitação de etanol ou sulfato de amônio, extração de ácido, cromatografia de permuta de ânions ou cátions, cromatografia de fosfocelulose, cromatografia de interação hidrofóbica, cromatografia de afinidade, cromatografia de hidroxilapatita e cromatografia de lectina. Podem ser usadas etapas de redobramento de proteína, conforme necessário, ao completar a configuração do polipeptídeo. Caso desejado, pode ser empregada cromatografia de líquida de alto desempenho (HPLC) para etapas finais de purificação.
[000538] Vários sistemas de cultura de células de mamífero também podem ser empregados para expressar proteína recombinante. Exemplos de sistemas de expressão de mamífero incluem as linhagens COS-7 de fibroblastos de rim de macaco (descritas, por exemplo, por Gluzman (1981) Cell 23:175; e outras linhagens celulares capazes de expressar proteínas a partir de um vetor compatível, tais como as linhagens de células C127, 3T3, CHO, HeLa e BHK.
[000539] Os construtos em células hospedeiras podem ser usados em uma maneira convencional para produzir o produto genético codificado pela sequência recombinante. Dependendo do hospedeiro empregado em um procedimento de produção recombinante, os polipeptídeos produzidos por células hospedeiras contendo o vetor podem ser glicosilados ou podem ser não-glicosilados. Os polipeptídeos da invenção podem ou não incluir também um resíduo de aminoácido metionina inicial.
[000540] Alternativamente, os polipeptídeos e peptídeos da invenção podem ser produzidos sinteticamente por sintetizadores de peptídeos convencionais. Em outros aspectos, fragmentos ou porções dos polipeptídeos podem ser empregados para produzir o polipeptídeo de extensão total correspondente por síntese de peptídeo; portanto, os fragmentos podem ser empregados como intermediários para produzir os polipeptídeos de extensão total.
[000541] Sistemas de translação livres de células também podem ser empregados para produzir um dos polipeptídeos da invenção usando mRNAs transcritos a partir de um construto de DNA compreendendo um promotor ligado operavelmente a um ácido nucleico codificando o polipeptídeo ou fragmento do mesmo. Em alguns aspectos, o construto de DNA pode ser linearizado antes de conduzir uma reação de transcrição in vitro. O mRNA transcrito pode ser incubado com um extrato de translação livre de células apropriado, tal como um extrato de reticulócito de cfoelho, para produzir o polipeptídeo ou peptídeo desejado.
Amplificação de Ácidos Nucleicos
[000542] Ao praticar a invenção, ácidos nucleicos da invenção e ácidos nucleicos codificando as glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção, ou ácidos nucleicos modificados da invenção, podem ser reproduzidos por amplificação. Amplificação também pode ser usada para clonar ou modificar os ácidos nucleicos da invenção. Portanto, a invenção proporciona pares de sequências de iniciadores de amplificação para amplificar ácidos nucleicos da invenção. Uma pessoa versada na técnica pode projetar pares de sequências de iniciadores de amplificação para qualquer parte de ou toda a extensão destas sequências. Em um aspecto, a invenção proporciona um ácido nucleico amplificado por um par de iniciadores da invenção, por exemplo, um par de iniciadores conforme determinado por cerca dos primeiros (os 5’) ou cerca de 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 ou 35 ou mais resíduos de um ácido nucleico da invenção, e cerca dos primeiros (os 5’) ou cerca de 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 ou 35 ou mais resíduos da fita complementar.
[000543] A invenção proporciona um par de sequências de iniciadores de amplificação para amplificar um ácido nucleico codificando um polipeptídeo tendo uma atividade de glucanase, em que o par de iniciadores é capaz de amplificar um ácido nucleico compreendendo uma sequência da invenção, ou fragmentos ou subsequências das mesmas. Um ou cada membro do par de sequências de iniciadores de amplificação pode compreender um oligonucleotídeo compreendendo pelo menos cerca de 10 a 50 bases consecutivas da sequência, ou cerca de 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, ou 25 bases consecutivas da sequência. A invenção proporciona pares de iniciadores de amplificação, em que o par de iniciadores compreende um primeiro membro tendo uma sequência conforme determinado por cerca dos primeiros (os 5’) 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 ou 35 resíduos de um ácido nucleico da invenção, e um segundo membro tendo uma sequência conforme determinado por cerca dos primeiros (os 5’) 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 ou 35 resíduos da fita complementar do primeiro membro. A invenção proporciona glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases geradas por amplificação, por exemplo, reação de cadeia polimerase (PCR), usando um par de iniciadores de amplificação da invenção. A invenção proporciona métodos para produzir glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases por amplificação, por exemplo, reação de cadeia polimerase (PCR), usando um par de iniciadores de amplificação da invenção. Em um aspecto, o par de iniciadores de amplificação amplifica um ácido nucleico de uma biblioteca, por exemplo, uma biblioteca genética, tal como uma biblioteca ambiental.
[000544] Reações de amplificação também podem ser usadas para quantificar a quantidade de ácido nucleico em uma amostra (tal como a quantidade de mensagem em uma amostra celular), colocar rótulo no ácido nucleico (por exemplo, aplicá-lo a um arranjo ou a uma mancha), detectar o ácido nucleico, ou quantificar a quantidade de um ácido nucleico específico em uma amostra. Em um aspecto da invenção, são amplificadas mensagens isoladas de uma célula ou uma biblioteca de cDNA.
[000545] O técnico versado pode selecionar e projetar iniciadores de amplificação de oligonucleotídeos adequados. Métodos de amplificação também são de conhecimento geral na técnica, e incluem, por exemplo, reação de cadeia polimerase, PCR (vide, por exemplo, PCR PROTOCOLS, A GUIDE TO METHODS AND APPLICATIONS, ed. Innis, Academic Press, N.Y. (1990) e PCR STRATEGIES (1995), ed. Innis, Academic Press, Inc., N.Y., reação de cadeia ligase (LCR) (vide, por exemplo, Wu (1989) Genomics 4:560; Landegren (1988) Science 241:1077; Barringer (1990) Gene 89:117); amplificação de transcrição (vide, por exemplo, Kwoh (1989) Proc. Natl. Acad. Sci. USA 86:1173); e, replicação de sequência autossustentada (vide, por exemplo, Guatelli (1990) Proc. Natl. Acad. Sci. USA 87:1874); amplificação de Q Beta replicase (vide, por exemplo, Smith (1997) J. Clin. Microbiol. 35:1477-1491), ensaio de amplificação de Q-beta replicase automatizada (vide, por exemplo, Burg (1996) Mol. Cell. Probes 10:257-271) e outras técnicas mediadas por RNA polimerase (por exemplo, NASBA, Cangene, Mississauga, Ontario); vide também Berger (1987) Methods Enzymol. 152:307-316; Sambrook; Ausubel; Patentes dos Estados Unidos Nos. 4.683.195 e 4.683.202; Sooknanan (1995) Biotechnology 13:563-564.
Determinando o grau de identidade de sequência
[000546] A invenção proporciona ácidos nucleicos compreendendo sequências tendo pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) com um ácido nucleico exemplar da invenção, incluindo SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, E SEQ ID NO: 22, e as modificações de sequências para SEQ ID NO: 1 descritas aqui, neste pedido de patente, sobre uma região de pelo menos cerca de 10, 20, 30, 40, 50, 60, 70, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 1050, 1100, 1150, 1200, 1250, 1300, 1350, 1400, 1450, 1500, 1550 ou mais, resíduos. A invenção proporciona polipeptídeos compreendendo sequências tendo pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) com um polipeptídeo exemplar da invenção. A extensão da identidade de sequência (homologia) pode ser determinada usando qualquer programa de computação e parâmetros associados, incluindo os descritos aqui, neste pedido de patente, tais como BLAST 2.2.2. ou Versão FASTA 3.0t78, com os parâmetros definidos.
[000547] As sequências de ácido nucleico da invenção podem compreender pelo menos 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, 150, 200, 300, 400, ou 500 ou mais nucleotídeos consecutivos de uma sequência exemplar da invenção e sequências substancialmente idênticas a essa. Sequências homólogas e fragmentos de sequências de ácido nucleico da invenção podem se referir a uma sequência tendo pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) (homologia) com um ácido nucleico exemplar da invenção, por exemplo, SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22, e variações das mesmas conforme descrito aqui, neste pedido de patente, bem como SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e SEQ ID NO: 22, para estas sequências.
[000548] A expressão “substancialmente idênticas” no contexto de dois ácidos nucleicos ou polipeptídeos, se refere a duas ou mais sequências que têm, por exemplo, pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais de identidade de (sequência) nucleotídeos ou resíduos aminoácidos, quando comparadas e alimentadas para máxima correspondência, conforme medido usando um dos algoritmos de comparação de sequências conhecidos ou por inspeção visual. A identidade substancial pode existir sobre uma região de pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, 150, 200, 300, 400, ou 500 ou mais resíduos. Em alguns aspectos, as sequências são substancialmente idênticas sobre toda a extensão das regiões codificantes. Em um aspecto, uma sequência de aminoácidos “substancialmente idêntica” é uma sequência que difere de uma sequência de referência por uma ou mais substituições, eliminações, ou inserções de aminoácido conservativas ou não-conservativas, particularmente quando uma substituição semelhante ocorre em um sítio que não é o sítio ativo (domínios catalíticos (CDs)) da molécula e contanto que o polipeptídeo essencialmente retenha suas propriedades funcionais. Uma substituição de aminoácido conservativa, por exemplo, substitui um aminoácido por outro da mesma classe (por exemplo, substituição de um aminoácido hidrofóbico, tal como isoleucina, valina, leucina, ou metionina, por outro, ou substituição de um aminoácido polar por outr, tal como substituição de arginina por lisina, ácido glutâmico por ácido aspártico ou glutamina por asparagina). Um ou mais aminoácidos podem ser eliminados, por exemplo, de um polipeptídeo de glucanase, resultando em modificação da estrutura do polipeptídeo, sem alterar significativamente sua atividade biológica. Por exemplo, podem ser removidos aminoácidos de terminal amino ou carboxila que não são necessários para a atividade biológica de glucanase. Sequências de polipeptídeos modificados da invenção podem ser testadas para atividade biológica de glucanase por qualquer número de métodos, incluindo contatar a sequência de polipeptídeo modificado com um substrato de glucanase e determinar se o polipeptídeo modificado reduz a quantidade de substrato específico no ensaio ou aumenta os bioprodutos da reação enzimática de um polipeptídeo glucanase funcional com o substrato.
[000549] A identidade de sequência (homologia) pode ser determinada usando quaisquer dos programas de computação e parâmetros descritos aqui, neste pedido de patente, incluindo Versão FASTA 3.0t78 com os parâmetros definidos. Sequências homólogas também incluem sequências de RNA nas quais uridinas substituiem as timinas nas sequências de ácido nucleico da invenção. As sequências homólogas podem ser obtidas usando quaisquer dos procedimentos descritos aqui, neste pedido de patente, ou podem resultar da correção de um erro de sequenciamento. Será reconhecido que as sequências de ácido nucleico da invenção podem ser representadas no formato de caractere único tradicional (Vide a contracapa interna de Stryer, Lubert. Biochemistry, 3rd Ed., W. H Freeman & Co., New York.) ou em qualquer outro formato o qual registra a identidade dos nucleotídeos em uma sequência.
[000550] Conforme usado aqui, neste pedido de patente, os termos “computador,” “programa de computação” e “processador” são usados em seus contextos gerais mais amplos e incorporam todos os dispositivos semelhantes, conforme descrito em detalhes, abaixo. Uma “sequência codificante de” ou uma “sequência codifica” um polipeptídeo ou proteína em particular, é uma sequência de ácido nucleico a qual é transcrita e traduzida em um polipeptídeo ou proteína quando colocada sob o controle de sequências regulatórias apropriadas.
[000551] Vários programas de comparação de sequência identificados alhures nesta especificação de patente são particularmente contemplados para uso neste aspecto da invenção. Homologias de sequência de proteína e/ou ácido nucleico podem ser avaliadas usando qualquer um da variedade de algoritmos de comparação de sequências e programas conhecidos na técnica. Os algoritmos e programas referidos incluem, mas não estão de modo algum limitados a, TBLASTN, BLASTP, FASTA, TFASTA e CLUSTALW (Pearson and Lipman, Proc. Natl. Acad. Sci. USA 85(8):2444-2448, 1988; Altschul et al., J. Mol. Biol. 215(3):403-410, 1990; Thompson et al., Nucleic Acids Res. 22(2):4673-4680, 1994; Higgins et al., Methods Enzymol. 266:383-402, 1996; Altschul et al., J. Mol. Biol. 215(3):403-410, 1990; Altschul et al., Nature Genetics 3:266272, 1993).
[000552] A homologia ou identidade é frequentemente medida usando programa de análise de sequência (por exemplo, Sequence Analysis Software Package of the Genetics Computer Group, University of Wisconsin Biotechnology Center, 1710 University Avenue, Madison, WI 53705). O programa referido combina sequências similares atribuindo graus de homologia a várias eliminações, substituições e outras modificações. Os termos “homologia” e “identidade” no contexto de duas ou mais sequências de ácidos nucleicos ou polipeptídeo, se referem a duas ou mais sequências ou subsequências que são as mesmas ou têm uma percentagem especificada de resíduos aminoácido ou nucleotídeos que são os mesmos quando comparados e alinhados para máxima correspondência sobre uma janela de comparação ou região designada conforme medido usando qualquer número de algoritmos de comparação de sequências ou por alinhamento manual e inspeção visual.
[000553] Para comparação de sequências, uma sequência pode agir como uma sequência de referência, à qual as sequências de teste são comparadas. Ao usar um algoritmo de comparação de sequências, sequências de teste e de referência são introduzidas em um computador, coordenadas de subsequências são designadas, caso necessário e são designados parâmetros do programa de algoritmo de sequência. Podem ser usados parâmetros do programa default, ou podem ser designados parâmetros alternativos. O algoritmo de comparação de sequências em seguida calcula a percentagem de identidades de sequência para as sequências de teste em relação à sequência de referência, com base nos parâmetros do programa.
[000554] Uma “janela de comparação”, conforme usado aqui, neste pedido de patente, inclui referência a um segmento de qualquer uma da série de posições contíguas selecionadas entre o grupo consistindo em a partir de 20 até 600, geralmente cerca de 50 a cerca de 200, mais geralmente cerca de 100 a cerca de 150 no qual uma sequência pode ser comparada com uma sequência de referência do mesmo número de posições contíguas depois das duas sequências serem otimamente alinhadas. Métodos de alinhamento de sequência para comparação são de conhecimento geral na técnica. Alinhamento ótimo de sequências para comparação pode ser conduzido, por exemplo, pelo algoritmo de homologia local de Smith & Waterman, Adv. Appl. Math. 2:482, 1981, pelo algoritmo de alinhamento por homologia de Needleman & Wunsch, J. Mol. Biol 48:443, 1970, pelo método de estudo para similaridade de Person & Lipman, Proc. Nat'l. Acad. Sci. USA 85:2444, 1988, por implementações computerizadas destes algoritmos (ESPAÇO, BESTFIT, FASTA e TFASTA no Pacote de Programas Genéticos Wisconsin, Grupo Computador Genético, 575 Science Dr., Madison, WI), ou por alinhamento manual e inspeção visual. Outros algoritmos para determinar homologia ou identidade incluem, por exemplo, além de um programa BLAST (Ferramenta de Pesquisa de Alinhamento Local Básico no Centro Nacional para Informação Biológica, ALIGN, AMAS (Análise de Sequências Multiplamente Alinhadas, AMPS (Análise de Múltipla Sequência de Proteína, ASSET (Ferramenta de Avaliação Estatística de Segmento Alinhado, BANDS, BESTSCOR, BIOSCAN (Nodo de Análise Comparativa de Sequência Biológica, BLIMPS (Pesquisador Melhorado de Blocos), FASTA, Intervals & Points, BMB, CLUSTAL V, CLUSTAL W, CONSENSUS, LCONSENSUS, WCONSENSUS, algoritmo de Smith-Waterman, DARWIN, algoritmo Las Vegas, FNAT (Ferramenta de Alinhamento de Nucleotídeos Forçado, Framealign, Framesearch, DYNAMIC, FILTER, FSAP (Pacote de Análise de Sequência de Fristensky), ESPAÇO (Programa de Alinhamento Global), GENAL, GIBBS, GenQuest, ISSC (Comparação de Sequências Sensíveis), LALIGN (Alinhamento de Sequência Local), LCP (Programa de Conteúdo Local), MACAW (Banco de Construção e Análise de Alinhamento Múltiplo), MAP (Programa de Alinhamento Múltiplo), MBLKP, MBLKN, PIMA (Alinhamento Multissequência Padrão-Induzido, SAGA (Alinhamento de Sequência por Algoritmo Genético e WHAT-IF. Os programas de alinhamento referidos também podem ser usados para triar bancos de dados de genoma para identificar sequências de polinucleotídeos tendo substancialmente idênticas sequências. Uma série de bancos de dados de genoma estão disponíveis, por exemplo, uma porção substancial do genoma humano está disponível como parte do Projeto de Sequenciamento do Genoma Humano. Pelo menos vinte e um outros genomas já foram sequenciados, incluindo, por exemplo, M. genitalium (Fraser et al., 1995), M. jannaschii (Bult et al., 1996), H. influenzae (Fleischmann et al., 1995), E. coli (Blattner et al., 1997) e levedura (S. cerevisiae) (Mewes et al., 1997) e D. melanogaster (Adams et al., 2000). Também tem sido feito significativo progresso no sequenciamento dos genomas de organismo molde, tal como camundongo, C. elegans e Arabadopsis sp. Vários bancos de dados contendo informação genômica anotada com alguma informação funcional são mantidos por diferente organização e estão acessíveis através da internet.
[000555] Um exemplo de um algoritmo útila é algoritmos BLAST e BLAST 2.0, os quais são descritos em Altschul et al., Nuc. Acids Res. 25:3389-3402, 1977 e Altschul et al., J. Mol. Biol. 215: 403-410, 1990, respectivamente. Programa para realizar análises BLAST está disponível publicamente no National Center for Biotechnology Information. Este algoritmo envolve primeiro identificar pares de sequência de alto escore (HSPs) identificando palavras curtas de extensão W na sequência de dúvida ("query sequence"), a qual ou corresponde a ou satisfaz algum escore de limiar de valor positivo T quando alinhadas com uma palavra da mesma em uma sequência do banco de dados. T é referido como o limiar de escore de palavra da vizinhança (Altschul et al., supra). Estes hits de palavra da vizinhança inicial agem como sementes para iniciar pesquisas para descobrir HSPs mais longas contendo as mesmas. Os hits de palavras são estendidos em ambas as direções ao longo de cada sequência para até o escore de alinhamento cumulativo poder ser aumentado. Escores cumulativos são calculados usando, para sequências de nucleotídeos, os parâmetros M (escore de recompensa para um par de resíduos combinando; sempre >0). Para sequências de aminoácidos, uma matriz de escore é usada para calcular o escore cumulativo. A extensão dos hits de palavras em cada direção é parada quando: o escore do alinhamento cumulativo diminui pela quantidade X de seu valor obtido máximo; o escore cumulativo vai até zero ou abaixo, devido à acumulação de um ou mais alinhamentos de resíduo de escore negativo; ou a extremidade de qualquer sequência ser atingida. Os parâmetros do algoritmo BLAST W, T e X determinam a sensibilidade e a velocidade do alinhamento. O programa BLASTN (para sequências de nucleotídeos) usa por definição uma extensão de palavra (W) de 11, uma expectativa (E) de 10, M = 5, N = -4 e uma comparação de ambas as fitas. Para sequências de aminoácidos, o programa BLASTP usa por definição uma extensão de palavra de 3 e expectativas (E) de 10 e os alinhamentos (B) de 50 da matriz de escore BLOSUM62 (vide Henikoff & Henikoff, Proc. Natl. Acad. Sci. USA 89:10915, 1989), expectativa (E) de 10, M = 5, N = -4 e uma comparação de ambas as fitas.
[000556] O algoritmo BLAST também realiza uma análise estatística da similaridade entre duas sequências (vide, por exemplo, Karlin & Altschul, Proc. Natl. Acad. Sci. USA 90:5873, 1993). Uma medida da similaridade proporcionada pelo algoritmo BLAST é a menor soma de probabilidades (P(N)), a qual proporciona uma indicação da probabilidade pela qual uma combinação entre duas sequências de nucleotídeo ou aminoácidos ocorreria por acaso. Por exemplo, um ácido nucleico é considerado similar a uma sequência de referência se a menor soma de probabilidades em uma comparação do ácido nucleico de teste com o ácido nucleico de referência for menor do que cerca de 0,2, mais em um aspecto menor do que cerca de 0,01 e o mais em um aspecto menor do que cerca de 0,001.
[000557] Em um aspecto, homologias de sequências de proteína e ácido nucleico são avaliadas usando a Ferramenta de Pesquisa de Alinhamento Local Básico ("BLAST"). Em particular, cinco programas BLAST específicos são usados para realizar a seguinte tarefa: (1) BLASTP e BLAST3 comparam uma sequência de dúvida de aminoácidos contra um banco de dados de sequências de proteína; (2) BLASTN compara uma sequência de dúvida de nucleotídeos contra um banco de dados de sequências de nucleotídeos; (3) BLASTX compara os produtos de translação conceitual de seis estruturas de uma sequência de nucleotídeos de dúvida (ambas as fitas) contra um banco de dados de sequências de proteína; (4) TBLASTN compara uma sequência de proteína de dúvida contra um banco de dados de sequências de nucleotídeos traduzidas em todos as seis estruturas de leitura (ambas as fitas); e (5) TBLASTX compara as translações de seis estruturas de uma sequência de dúvida de nucleotídeos contra as translações de seis estruturas de um banco de dados de sequências de nucleotídeos.
[000558] Os programas BLAST identificam sequências homólogas identificando segmentos similares, os quais são referidos aqui, neste pedido de patente, como “pares de segmentos de alto escore,” entre uma sequência amino ou sequência de ácido nucleico de dúvida e uma sequência de teste a qual é em um aspecto obtida a partir de uma proteína ou sequência de ácido nucleico banco de dados. Pares de segmentos de alto escore são em um aspecto identificados (isto é, alinhados) por meio de uma matriz de escore, muitas das quais são conhecidas na técnica. Em um aspecto, a matriz de escore usada é a matriz BLOSUM62 (Gonnet et al., Science 256:1443-1445, 1992; Henikoff e Henikoff, Proteins 17:49-61, 1993). Menos em um aspecto, também podem ser usadas as matrizes PAM ou PAM250 (vide, por exemplo, Schwartz and Dayhoff, eds., 1978, Matrices for Detecting Distance Relationships: Atlas of Protein Sequence and Structure, Washington: National Biomedical Research Foundation). Programas BLAST são acessíveis na Biblioteca Nacional de Medicina dos Estados Unidos.
[000559] Os parâmetros usados com os algoritmos acima podem ser adaptados dependendo da extensão da sequência e do grau de homologia estudiado. Em alguns aspectos, os parâmetros podem ser os parâmetros definidos usados pelos algoritmos na ausência de instruções do usuário.
Sistemas de computação e produtos de programas de computação
[000560] Para determinar e identificar identidades de sequência, homologias estruturais, motivos e similares in silico, um sequência de ácido nucleico ou polipeptídeo da invenção pode ser armazenada, registrada, e manipulada sobre qualquer meio o qual pode ser lido e acessado por um computador.
[000561] Por conseguinte, a invenção proporciona computadores, sistemas de computação, meios legíveis por computador, produtos de programas de computação e similares registrados ou armazenados sobre os mesmos as sequências de ácido nucleico e de polipeptídeo da invenção. Conforme usado aqui, neste pedido de patente, as palavras “registrados” e “armazenados” se referem a um processo para armazenar informação em um meio de computação. Um técnico versado pode adotar prontamente quaisquer métodos conhecidos para registrar informação em um meio legível por computador para gerar fabricações compreendendo uma ou mais das sequências de ácido nucleico e/ou de polipeptídeo da invenção.
[000562] Os polipeptídeos da invenção compreendem sequências de aminoácidos da invenção, por exemplo, as sequências típicas da invenção, e sequências substancialmente idênticas a essa, e fragmentos das mesmas, incluindo fragmentos enzimaticamente ativos. Sequências de polipeptídeos substancialmente idênticas, ou homólogas, se referem a uma sequência de polipeptídeo tendo pelo menos 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%) com uma sequência exemplar da invenção.
[000563] Homologia (identidade de sequência) pode ser determinada usando quaisquer dos programas de computação e parâmetros descritos aqui, neste pedido de patente, incluindo Versão FASTA 3.0t78 com os parâmetros definidos ou com quaisquer parâmetros modificados. As sequências homólogas podem ser obtidas usando quaisquer dos procedimentos descritos aqui, neste pedido de patente, ou podem resultar da correção de um erro de sequenciamento. Os fragmentos de polipeptídeos compreendem pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 45, 50, 75, 100, 150, 200, 250, 300, 350, 400, 450, 500 ou mais aminoácidos consecutivos dos polipeptídeos da invenção. Será reconhecido que os códigos de polipeptídeos conforme determinado nas sequências de aminoácidos da invenção, podem ser representados no formato tradicional de caractere único ou no formato de três letras (Vide a contracapa interna de Stryer, Lubert. Biochemistry, 3rd Ed., W. H Freeman & Co., New York.) ou em qualquer outro formato o qual se refere à identidade dos polipeptídeos em uma sequência.
[000564] Uma sequência de ácido nucleico ou de polipeptídeo da invenção pode ser armazenada, registrada e manipulada sobre qualquer meio o qual pode ser lido e acessado por um computador. Conforme usado aqui, neste pedido de patente, as palavras “registrada” e “armazenada” se referem a um processo para armazenar informação sobre um meio de computação. Um técnico versado pode prontamente adotar quaisquer dos métodos presentemente conhecidos para registrar informação sobre um meio legível por computador para gerar fabricações compreendendo uma ou mais das sequências de ácido nucleico da invenção, uma ou mais das sequências de polipeptídeo da invenção. Outro aspecto da invenção é um meio legível por computador tendo registrado sobre o mesmo pelo menos 2, 5, 10, 15, ou 20 ou mais sequências de ácido nucleico da invenção.
[000565] Outro aspecto da invenção é um meio legível por computador tendo registrado sobre o mesmo uma ou mais das sequências de ácido nucleico da invenção. Outro aspecto da invenção é um meio legível por computador tendo registrado sobre o mesmo uma ou mais das sequências de polipeptídeo da invenção. Outro aspecto da invenção é um meio legível por computador tendo registrado sobre o mesmo pelo menos 2, 5, 10, 15, ou 20 ou mais das sequências conforme determinado acima.
[000566] Meios legíveis no computados incluem meios legíveis magneticamente, meios legíveis oticamente, meios legíveis eletronicamente e meios magnéticos/óticos. Por exemplo, os meios legíveis no computador podem ser um disco rígido, um disquete, uma fita magnética, CD-ROM, Disco Versátila Digital (DVD), Memória de acesso Randômico (RAM), ou Memória Soment Lida (ROM) bem como outros tipos de outros meios conhecidos daqueles versados na técnica.
[000567] Aspectos da invenção incluem sistemas (por exemplo, sistemas baseados na Internet), particularmente sistemas de computação os quais armazenam e manipulam a informação de sequência descrita aqui, neste pedido de patente. Um exemplo de um sistema de computação 100 é ilustrado em forma de diagrama em bloco na figura 1. Conforme usado aqui, neste pedido de patente, “um sistema de computação” se refere aos componentes de hardware, componentes de software e componentes de armazenamento de dados usados para analisar uma sequência de nucleotídeos de uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção. O sistema de computação 100 pode incluir um processador para processar, acessar e manipular os dados da sequência. O processador 105 pode ser qualquer tipo de conhecimento geral de unidade de processamento central, tal como, por exemplo, o Pentium III da Intel Corporation, ou processador similar da Sun, Motorola, Compaq, AMD ou International Business Machines.
[000568] O sistema de computação 100 pode ser um sistema de propósito geral que compreende o processador 105 e um ou mais componentes de armazenamento de dados internos 110 para armazenar dados e um ou mais dispositivos de recuperação de dados para recuperar os dados armazenados sobre os componentes de armazenamento de dados. Um técnico versado pode prontamente reconhecer que são adequados qualquer um dos sistemas de computação disponíveis atualmente.
[000569] Em um aspecto particular, o sistema de computação 100 inclui um processador 105 conectado a um barramento o qual é conectado a uma memória principal 115 (em um aspecto implementado como RAM) e um ou mais dispositivos internos de armazenamento de dados 110, tais como um hard drive e/ou outros meios legíveis no computados tendo dados registrados nos mesmos. Em alguns aspectos, o sistema de computação 100 inclui adicionalmente um ou mais dispositivos de recuperação de dados 118 para ler os dados armazenados sobre os dispositivos internos de armazenamento de dados 110.
[000570] O dispositivo de recuperação de dados 118 pode representar, por exemplo, um drive de disquete, um drive de CD, um drive de fita magnética, ou um modem capaz de conexão a um sistema de armazenamento de dados remoto (por exemplo, através da internet) e etc. Em alguns aspectos, o dispositivo interno de armazenamento de dados 110 é um meio legível por computador removível tal como um disquete, um CD, uma fita magnética, e etc. contendo controle lógico e/ou dados registrados sobre o mesmo. O sistema de computação 100 pode vantajosamente incluir ou ser programado por software apropriado para ler o controle lógico e/ou os dados do componente de armazenamento de dados uma vez inseridos no dispositivo de recuperação de dados.
[000571] O sistema de computação 100 inclui um display 120 o qual é usado para apresentar o resultado para um usuário do computador. Também deve ser observado que o sistema de computação 100 pode ser ligado a outros sistemas de computação 125a-c em uma rede ou rede de área ampla para proporcionar acesso centralizado ao de computação 100.
[000572] O software para acessar e processar as sequências de nucleotídeos de uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, (tais como ferramentas de pesquisa, ferramentas de comparação e ferramentas de modelagem e etc.) pode residir na memória principal 115 durante a execução.
[000573] Em alguns aspectos, o sistema de computação 100 pode compreender adicionalmente um algoritmo de comparação de sequências para comparar uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, armazenada sobre um meio legível por computador com uma ou mais sequências de nucleotídeo ou de polipeptídeo de referência armazenadas sobre um meio legível por computador. Um “algoritmo de comparação de sequências” se refere a um ou mais programas os quais são implementados (localmente ou remotamente) sobre o sistema de computação 100 para comparar uma sequência de nucleotídeos com outras sequências de nucleotídeos e/ou compostos armazenados dentro de um meio de armazenamento de dados. Por exemplo, o algoritmo de comparação de sequências pode comparar as sequências de nucleotídeos de uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, armazenada sobre um meio legível por computador com sequências de referência armazenadas sobre um meio legível por computador para identificar homologias ou motivos estruturais.
[000574] A figura 2 é um fluxograma ilustrando um aspecto de um processo 200 para comparar uma nova sequência de nucleotídeos ou de proteína com um banco de dados de sequências de modo a determinar os níveis de homologia entre a nova sequência e as sequências no banco de dados. O banco de dados de sequências pode ser um banco de dados privado armazenado dentro do sistema de computação 100, ou um banco de dados público tal como GENBANK que está disponível na Internet.
[000575] O processo 200 inicia em um estado de início 201 e em seguida se move para um estado 202 em que a nova sequência a ser comparada é armazenada em uma memória em um sistema de computação 100. Conforme discutido acima, a memória pode ser qualquer tipo de memória, incluindo RAM ou um dispositivo de armazenamento interno.
[000576] O processo 200 em seguida se move para um estado 204 em que um banco de dados de sequências é aberto para análise e comparação. O processo 200 em seguida se move para um estado 206 em que a primeira sequência armazenada no banco de dados é lida em uma memória no computador. Uma comparação é então realizada em um estado 210 para determinar se a primeira sequência é a mesma que a segunda sequência. É importante notar que esta etapa não é limitada a realizar uma comparação exata entre a nova sequência e a primeira sequência no banco de dados. Métodos de conhecimento geral são de conhecimento daqueles versados na técnica para comparar duas sequências de nucleotídeos ou proteína, mesmo se nãõ forem idênticas. Por exemplo, podem ser introduzidos gaps em uma sequência de modo a aumentar o nível de homologia entre as duas sequências testadas. Os parâmetros que controlam se gaps ou outras características são introduzidos em uma sequência durante comparação são normalmente introduzidos pelo usuário do sistema de computação.
[000577] Uma vez que uma comparação das duas sequências tenha sido realizada no estado 210, é feita uma determinação em um estado de decisão 210 se as duas sequências forem as mesmas. Logicamente, o termo “mesmas” não é limitado a sequências que são absolutamente idênticas. Sequências que estão dentro dos parâmetros de homologia introduzidos pelo usuário serão marcados como “mesmos” no processo 200.
[000578] Se for feita uma determinação de que as duas sequências são as mesmas, o processo 200 se move para um estado 214 em que o nome da sequência do banco de dados é apresentada ao usuário. Este estado notifica o usuário que a sequência com o nome apresentado satisfaz as restrições de homologia que foram introduzidas. Uma vez que o nome da sequência armazenada é apresentada ao usuário, o processo 200 se move para um estado de decisão 218 em que é feita uma determinação se existem mais sequências no banco de dados. Caso não existam mais sequências no banco de dados, então o processo 200 termina em um estado final 220. No entanto, se existirem mais sequências no banco de dados, então o processo 200 se move para um estado 224 em que um ponteiro é movido para a sequência seguinte no banco de dados de modo que pode ser comparado à nova sequência. Desta maneira, a nova sequência é alinhada e comparada com cada sequência no banco de dados.
[000579] Deve ser observado que se tiver sido feita uma determinação no estado de decisão 212 que as sequências não eram homólogas, então o processo 200 se moveria imediatamente para o estado de decisão 218 de modo a determinar se quaisquer outras sequências estavam disponíveis no banco de dados para comparação.
[000580] Por conseguinte, um aspecto da invenção é um sistema de computação compreendendo um processador, um dispositivo de armazenamento de dados tendo armazenada sobre o mesmo uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, um dispositivo de armazenamento de dados tendo armazenado de modo recuperável sobre o mesmo sequências de referência de nucleotídeos ou sequências de polipeptídeo a serem comparadas com uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção e um comparador de sequência para conduzir a comparação. O comparador de sequência pode indicar um nível de homologia entre as sequências comparadas ou motivos estruturais de identificação no ácido nucleico descrito acima codificam uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, ou pode identificar motivos estruturais em sequências as quais são comparadas a estes códigos de ácidos nucleicos e códigos de polipeptídeos. Em alguns aspectos, o dispositivo de armazenamento de dados pode ter armazenadas sobre o mesmo as sequências de pelo menos 2, 5, 10, 15, 20, 25, 30 ou 40 ou mais das sequências de ácido nucleico da invenção, ou as sequências de polipeptídeo da invenção.
[000581] Outro aspecto da invenção é um método para determinar o nível de homologia entre uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção e uma sequência de referência de nucleotídeos. O método incluindo ler o código de ácido nucleico ou o código de polipeptídeo e a sequência de nucleotídeos ou de polipeptídeo de referência através do uso de um programa de computação o qual determina níveis de homologia e determinar a homologia entre o código de ácido nucleico ou o código de polipeptídeo e a sequência de nucleotídeos ou de polipeptídeo de referência com o programa de computação. O programa de computação pode ser qualquer de uma série de programas de computação para determinar níveis de homologia, incluindo aqueles especificamente enumerados aqui, neste pedido de patente, (por exemplo, BLAST2N com os parâmetros definidos ou com quaisquer parâmetros modificados). O método pode ser implementado usando os sistemas de computação descritos acima. O método também pode ser realizado lendo pelo menos 2, 5, 10, 15, 20, 25, 30 ou 40 ou mais das sequências de ácido nucleico da invenção descritas acima, ou as sequências de polipeptídeo da invenção através do uso do programa de computação e determinar a homologia entre os códigos de ácido nucleico ou códigos de polipeptídeo e sequências de referência de nucleotídeos ou sequências de polipeptídeo.
[000582] A figura 3 é um fluxograma ilustrando um aspecto de um processo 250 em um computador para determinar se duas sequências são homólogas. O processo 250 se inicia em um estado de início 252 e em seguida se move para um estado 254 em que uma primeira sequência a ser comparada é armazenada em uma memória. A segunda sequência a ser comparada é então armazenada em uma memória em um estado 256. O processo 250 em seguida se move para um estado 260 em que o caractere na primeira sequência é lido e em seguida para um estado 262 em que o primeiro caractere da segunda sequência é lido. Deve ser entendido que se a sequência for uma sequência de nucleotídeos, então o caractere normalmente seria ou A, T, C, G ou U. Se a sequência for uma sequência de proteína, então está em um aspecto no código de aminoácido de letra única de modo que a primeira e a segunda sequências podem ser facilmente comparadas.
[000583] Uma determinação é então feita em um estado de decisão 264 se os dois caracteres são os mesmos. Se forem os mesmos, então o processo 250 se move para um estado 268 em que os caracteres seguintes na primeira e na segunda sequências são lidos. Uma determinação é então feita se os próximos caracteres são os mesmos. Se forem, então o processo 250 continua seu loop até dois caracteres não serem os mesmos. Se for feita uma determinação de que os dois caracteres seguintes não são os mesmos, o processo 250 se move para um estado de decisão 274 para determinar se há quaisquer caracteres mais ou sequência para ler.
[000584] Se não houver mais quaisquer caracteres para ler, então o processo 250 se move para um estado 276 em que o nível de homologia entre a primeira e a segunda sequências é apresentada ao usuário. O nível de homologia é determinado calculando a proporção de caracteres entre as sequências que foram os mesmos entre o número total de sequências na primeira sequência. Portanto, se cada caractere em uma primeira sequência de 100 nucleotídeos alinhou com cada caractere em uma segunda sequência, o nível de homologia seria de 100%.
[000585] Alternativamente, o programa de computação pode ser um programa de computação o qual compara as sequências de nucleotídeos de uma sequência de ácido nucleico conforme determinado na invenção, com uma ou mais sequências de referência de nucleotídeos de modo a determinar se o código do ácido nucleico da invenção, difere de uma sequência de referência de ácido nucleico em uma ou mais posições. Opcionalmente um programa semelhante registra a extensão e a identidade de nucleotídeos inseridos, eliminados ou substituídos com respeito ou à sequência do polinucleotídeo de referência ou a uma sequência de ácido nucleico da invenção. Em um aspecto, o programa de computação pode ser um programa o qual determina se uma sequência de ácido nucleico da invenção, contém um polimorfismo de único nucleotídeo (SNP) com respeito a uma sequência de referência de nucleotídeos.
[000586] Por conseguinte, outro aspecto da invenção é um método para determinar se uma sequência de ácido nucleico da invenção difere em um ou mais nucleotídeos de uma sequência de referência de nucleotídeos compreendendo as etapas de ler o código de ácido nucleico e a sequência de referência de nucleotídeos através do uso de um programa de computação o qual identifica diferenças entre sequências de ácido nucleico e identificar diferenças entre o código de ácido nucleico e a sequência de referência de nucleotídeos com o programa de computação. Em alguns aspectos, o programa de computação é um programa o qual identifica polimorfismos de único nucleotídeo. O método pode ser implementado pelos sistemas de computação descritos acima e o método ilustrado na figura 3. O método também pode ser realizado lendo pelo menos 2, 5, 10, 15, 20, 25, 30, ou 40 ou mais das sequências de ácido nucleico da invenção e as sequências de referência de nucleotídeos através do uso do programa de computação e identificando diferenças entre os códigos de ácido nucleico e as sequências de referência de nucleotídeos com o programa de computação.
[000587] Em outros aspectos, o sistema de computação pode compreender adicionalmente um identificador para identificar características dentro de uma sequência de ácido nucleico da invenção ou uma sequência de polipeptídeo da invenção.
[000588] Um “identificador” se refere a um ou mais programas os quais identificam algumas características dentro de uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção. Em um aspecto, o identificador pode compreender um programa o qual identifica uma estrutura de leitura aberta em uma sequência de ácido nucleico da invenção.
[000589] A figura 4 é um fluxograma ilustrando um aspecto de um processo identificador 300 para detectar a presença de uma característica em uma sequência. O processo 300 inicia em um estado de início 302 e em seguida move para um estado 304 em que uma primeira sequência que deve ser verificada para características é armazenada a uma memória 115 no sistema de computação 100. O processo 300 em seguida move para um estado 306 em que um banco de dados de características de sequências é aberto. Um banco de dados semelhante incluiria uma lista de atributos de cada característica com o nome da característica. Por exemplo, o nome de uma característica pode ser “Códon de Iniciação” e o atributo seria “ATG”. Outro exemplo seria o nome da característica “TAATAA Box” e o atributo da característica seria “TAATAA”. Um exemplo de um banco de dados semelhante é produzido pela University of Wisconsin Genetics Computer Group. Alternativamente, as características podem ser motivos de polipeptídeos estruturais tais como hélices alfa, folhas beta, ou motivos de polipeptídeos funcionais tais como domínios catalíticos enzimáticos (CDs), ou, sítios ativos, motivos de hélice-volta- hélice ou outros motivos conhecidos daqueles versados na técnica.
[000590] Uma vez que o banco de dados de características é aberto no estado 306, o processo 300 move para um estado 308 em que a primeira característica é lida do banco de dados. Uma comparação do atributo da primeira característica com a primeira sequência é então feita em um estado 310. Uma determinação é então feita em um estado de decisão 316 se o atributo da característica foi encontrado na primeira sequência. Se o atributo foi encontrado, então o processo 300 move para um estado 318 em que o nome da característica encontrada é apresentado ao usuário.
[000591] O processo 300 então move para um estado de decisão 320 em que uma determinação é feita se existirem mais características no banco de dados. Se não existirem mais características, então o processo 300 termina em um estado final 324. No entanto, se existirem mais características no banco de dados, então o processo 300 lê a característica da sequência seguinte em um estado 326 e continua o loop de volta ao estado 310 em que o atributo da característica seguinte é comparado com a primeira sequência. Deve ser observado, que se o atributo da característica não é encontrado na primeira sequência no estado de decisão 316, o processo 300 move diretamente para o estado de decisão 320 de modo a determinar se existem quaisquer características mais no banco de dados.
[000592] Por conseguinte, outro aspecto da invenção é um método para identificar uma característica dentro de uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, compreendendo ler o(s) código(s) de ácido nucleico ou o(s) código(s) de polipeptídeo através do uso de um programa de computação o qual identifica características do mesmo e identificando características dentro do(s) código(s) de ácido nucleico com o programa de computação. Em um aspecto, programa de computação compreende um programa de computação o qual identifica estruturas de leitura aberta. O método pode ser realizado lento uma única sequência ou pelo menos 2, 5, 10, 15, 20, 25, 30, ou 40 das sequências de ácido nucleico da invenção, ou as sequências de polipeptídeo da invenção, através do uso do programa de computação e identificando características dentro do(s) código(s) de ácido nucleico ou do(s) código(s) de polipeptídeo com o programa de computação.
[000593] Uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, pode ser armazenada e manipulada em uma variedade de programas processadores de dados em uma variedade de formatos. Por exemplo, uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção, pode ser armazenada como texto em um arquivo de processamento de palavras, tais como Microsoft WORD® ou WORDPERFECT® ou como um arquivo ASCII em uma variedade de programas de banco de dados familiares daqueles versados na técnica, tais como DB2®, SYBASE®, ou ORACLE®. Além disso, muitos programas de computação e bancos de dados podem ser usados como algoritmos de comparação de sequências, identificadores, ou fontes de sequências de referência de nucleotídeos ou sequências de polipeptídeo a serem comparadas com uma sequência de ácido nucleico da invenção, ou uma sequência de polipeptídeo da invenção. Não se pretende que a lista seguinte limite a invenção mas que proporcione orientação para programas e bancos de dados os quais são úteis com as sequências de ácido nucleico da invenção, ou as sequências de polipeptídeo da invenção.
[000594] Os programas e bancos de dados os quais podem ser usados incluem, mas não estão limitados a: MacPattern (EMBL), DiscoveryBase (Molecular Applications Group), GeneMine (Molecular Applications Group), Look (Molecular Applications Group), MacLook (Molecular Applications Group), BLAST e BLAST2 (NCBI), BLASTN e BLASTX (Altschul et al, J. Mol. Biol. 215: 403, 1990), FASTA (Pearson e Lipman, Proc. Natl. Acad. Sci. USA, 85: 2444, 1988), FASTDB (Brutlag et al. Comp. App. Biosci. 6:237-245, 1990), Catalyst (Molecular Simulations Inc.), Catalyst/SHAPE (Molecular Simulations Inc.), Cerius2.DBAccess (Molecular Simulations Inc.), HypoGen (Molecular Simulations Inc.), Insight II, (Molecular Simulations Inc.), Discover (Molecular Simulations Inc.), CHARMm (Molecular Simulations Inc.), Felix (Molecular Simulations Inc.), DelPhi, (Molecular Simulations Inc.), QuanteMM, (Molecular Simulations Inc.), Homology (Molecular Simulations Inc.), Modeler (Molecular Simulations Inc.), ISIS (Molecular Simulations Inc.), Quanta/Protein Design (Molecular Simulations Inc.), WebLab (Molecular Simulations Inc.), WebLab Diversity Explorer (Molecular Simulations Inc.), Gene Explorer (Molecular Simulations Inc.), SeqFold (Molecular Simulations Inc.), o banco de dados MDL Available Chemicals Directory, a base de dados MDL Drug Data Report, o banco de dados Comprehensive Medicinal Chemistry, banco de dados Derwents’s World Drug Index, o banco de dados BioByteMasterFile, o banco de dados Genbank e o banco de dados Genseqn. Muitos outros programas e bases de dados seriam evidentes para uma pessoa versada na técnica dada a presente descoberta.
[000595] Motivos os quais podem ser detectados usando os programas acima incluem sequências codificando zíperes de leucina, motivos de hélice-volta- hélice, sítios de glicosilação, sítios de ubiquitinação, alfa hélices e folhas beta, sequências de sinal codificando peptídeos de sinal as quais dirigem a secreção das proteínas codificadas, sequências implicadas em regulação de transcrição tais como homeoboxes, trechos acídicos, sítios ativos enzimáticos (domínios catalíticos (CDs)), sítios de ligação de substrato e sítios de clivagem enzimática.
Hibridização de ácidos nucleicos
[000596] A invenção proporciona ácidos nucleicos isolados, sintéticos ou recombinantes que hibridizam sob condições estringentes a uma sequência exemplar da invenção, por exemplo, SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22, ou uma modificação de SEQ ID NO: 1 conforme descrito aqui, neste pedido de patente, bem como SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e SEQ ID NO: 22. As condições estringentes podem ser condições altamente estringentes, condições estringentes médias e/ou condições estringentes baixas, incluindo as condições estringência elevada e reduzida descritas aqui, neste pedido de patente. Em um aspecto, é a estringência das condições de lavagem que determina as condições as quais determinam se um ácido nucleico está dentro do escopo da invenção, conforme discutido abaixo.
[000597] “Hibridização” se refere ao processo pelo qual uma fita de ácido nucleico une com uma fita complementar através de pareamento de bases. Reações de hibridização podem ser sensíveis e seletivas de modo que uma sequência de interesse em particular possa ser identificada mesmo em amostras nas quais está presente em baixas concentrações. Condições estringentes adequadas podem ser definidas, por exemplo, pelas concentrações de sal ou formamida nas soluções de pré-hibridização e hibridização, ou pela temperatura de hibridização e são de conhecimento geral na técnica. Em particular, a estringência pode ser aumentada reduzindo a concentração de sala, aumentando a concentração de formamida, ou aumentando a temperatura de hibridização. Em aspectos alternativos, ácidos nucleicos da invenção são definidos por sua capacidade para hibridizar sobre várias condições de estringência (por exemplo, alta, média, e baixa), conforme determinado aqui, neste pedido de patente.
[000598] Por exemplo, em um aspecto, hibridização sob condições de alta estringência ocorre em condições compreendendo cerca de 50% de formamida em cerca de 37°C a 42°C. Hibridização também pode ocorrer sob reduzida estringência em condições compreendendo cerca de 35% a 25% de formamida em cerca de 30°C a 35°C. Em um aspecto, hibridização ocorre sob alta estringência em condições compreendendo cerca de 42°C em 50% de formamida, 5X SSPE, 0,3% de SDS e 200 μg/ml de DNA de esperma de salmão cisalhado e desnaturado. Em um aspecto, hibridização ocorre sob condições de reduzida estringência conforme descrito acima, mas em 35% de formamida em uma temperatura reduzida de 35°C. A faixa de temperatura correspondente a um nível particular de estringência pode ser adicionalmente estreitada calculando a proporção de purina para pirimidina do ácido nucleico de interesse e ajustando a temperatura de acordo. Variações nas faixas e condições acima são de conhecimento geral na técnica.
[000599] Em aspectos alternativos, ácidos nucleicos da invenção conforme definido por sua capacidade para hibridizar sob condições estringentes pode ter entre cerca de cinco resíduos e toda a extensão do ácido nucleico da invenção; por exemplo, podem ter pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 55, 60, 65, 70, 75, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, ou mais, resíduos de extensão. Ácidos nucleicos mais curtos do que toda a extensão também estão incluídos. Estes ácidos nucleicos podem ser úteis como, por exemplo, sondas de hibridização, sondas de marcação, sondas de oligonucleotídeos de PCR, iRNA (siRNA ou miRNA, de fita única ou de fita dupla), sequências antissenso ou sequências codificando peptídeos de ligação de anticorpo (epitopos), motivos, sítios ativos (domínios catalíticos (CDs)) e similares.
[000600] Em um aspecto, ácidos nucleicos da invenção são definidos por sua capacidade para hibridizar sob alta estringência compreende condições de cerca de 50% de formamida em cerca de 37°C a 42°C. Em um aspecto, ácidos nucleicos da invenção são definidos por sua capacidade para hibridizar sob reduzida estringência compreendendo condições em cerca de 35% a 25% de formamida em cerca de 30°C a 35°C. Alternativamente, ácidos nucleicos da invenção são definidos por sua capacidade para hibridizar sob alta estringência compreendendo condições a 42°C em 50% de formamida, 5X SSPE, 0,3% de SDS, e um ácido nucleico de bloqueio de sequência repetitivo, tal como DNA de esperma de salmão ou cot-1 (por exemplo, 200 μg/ml de DNA de esperma de salmão cisalhado e desnaturado). Em um aspecto, ácidos nucleicos da invenção são definidos por sua capacidade para hibridizar sob condições de reduzida estringência compreendendo 35% de formamida em uma temperatura reduzida de 35°C.
[000601] Em reações de hibridização de ácido nucleico, as condições usadas para obter um nível particular de estringência variará, dependendo da natureza dos ácidos nucleicos sendo hibridizados. Por exemplo, a extensão, o grau de complementaridade, a composição da sequência de nucleotídeos (por exemplo, teor de GC v. AT) e tipo de ácido nucleico (por exemplo, RNA v. DNA) das regiões de hibridização dos ácidos nucleicos podem ser considerados ao selecionar as condições de hibridização. Uma consideração adicional é se um dos ácidos nucleicos é imobilizado, por exemplo, sobre um filtro.
[000602] Hibridização pode ser realizada sob condições de baixa estringência, moderada estringência ou alta estringência. Como um exemplo de hibridização de ácido nucleico, uma membrana de polímero contendo ácidos nucleicos desnaturados imobilizados é primeiro pré-hibridizada por 30 minutos a 45DC em uma solução consistindo em 0,9 M de NaCl, 50 mM de NaH2PO4, pH 7,0, 5,0 mM de Na2EDTA, 0,5% de SDS, 10X solução de Denhardt e 0,5 mg/ml de ácido polirriboadenílico. Aproximadamente 2 X 107 cpm (atividade específica de 4-9 X 108 cpm/ug) de sonda de oligonucleotídeo marcada da extremidade de 32P são então adicionados à solução. Depois de 12 a 16 horas de incubação, a membrana é lavada por 30 minutos em temperatura ambiente em 1X SET (150 mM de NaCl, 20 mM de cloridrato, pH 7,8, 1 mM de Na2EDTA) contendo 0,5% de SDS, seguida por uma lavagem de 30 minutos em 1X SET fresco a Tm- 10αC para a sonda de oligonucleotídeo. A membrana é então exposta a filme autorradiográfico para detecção de sinais de hibridização.
[000603] Todas as hibridizações precedentes são condições de alta estringência.
[000604] Depois da hibridização, um filtro pode ser lavado para remover qualquer sonda detectável ligada não-especificamente. A estringência usada para lavar os filtros também pode ser variada dependendo da natureza dos ácidos nucleicos sendo hibridizados, da extensão dos ácidos nucleicos sendo hibridizados, do grau de complementaridade, da composição da sequência de nucleotídeos (por exemplo, teor de GC v. AT) e do tipo de ácido nucleico (por exemplo, RNA v. DNA). Exemplos de lavagens de condições de estringência progressivamente maiores são como se segue: 2X SSC, 0,1% de SDS em temperatura ambiente por 15 minutos (baixa estringência); 0,1X SSC, 0,5% de SDS em temperatura ambiente por 30 minutos a 1 hora (moderada estringência); 0.1X SSC, 0,5% de SDS por 15 a 30 minutos em entre a temperatura de hibridização e 68oC (alta estringência); e 0,15M de NaCl por 15 minutos a 72oC (muito alta estringência). Uma lavagem de baixa estringência final pode ser conduzida em 0,1X SSC em temperatura ambiente. Os exemplos acima são simplesmente ilustrativos de uma série de condições que podem ser usadas para lavar filtros. Uma pessoa versada na técnica saberia que há numerosas receitas para lavagens de diferentes estringências. Alguns outros exemplos são dados abaixo. Ácidos nucleicos os quais foram hibridizados à sonda podem ser identificados por autoradiografia ou outras técnicas convencionais.
[000605] O procedimento acima pode ser modificado para identificar ácidos nucleicos tendo níveis decrescentes de homologia com a sequência de sonda. Por exemplo, para obter ácidos nucleicos de homologia decrescente com a sonda detectável, podem ser usadas condições menos estringentes. Por exemplo, a temperatura da hibridização pode ser reduzida em incrementos de 5oC a partir de 68oC até 42oC em um tampão de hibridização tendo uma concentração de Na+ de cerca de 1 M. Depois da hibridização, o filtro pode ser lavado com 2X SSC, 0,5% de SDS na temperatura de hibridização. Estas condições são consideradas como sendo condições “moderadas” acima de 50oC e condições “baixas” abaixo de 50oC. Um exemplo específico de condições de hibridização “moderadas” é quando a hibridização acima é conduzida a 55oC. Um exemplo específico de condições de “baixa estringência” é quando a hibridização acima é conduzida a 45oC.
[000606] Alternativamente, a hibridização pode ser realizada em tampões, tais como 6X SSC, contendo formamida em uma temperatura de 42oC. Neste caso, a concentração de formamida no tampão de hibridização pode ser reduzida em incrementos de 5% a partir de 50% até 0% para identificar clones tendo níveis decrescentes de homologia com a sonda. Depois da hibridização, o filtro pode ser lavado com 6X SSC, 0,5% de SDS a 50DC. Estas condições são consideradas como sendo condições “moderadas” acima de 25% de formamida e condições “baixas” abaixo de 25% de formamida. Um exemplo específico de condições de hibridização “moderadas” é quando a hibridização acima é conduzida a 30% de formamida. Um exemplo específico de condições de hibridização de “baixa estringência” é quando a hibridização acima é conduzida a 10% de formamida.
[000607] No entanto, a seleção de um formato de hibridização não é crucial - é a estringência das condições de lavagem que determina as condições as quais determinam se um ácido nucleico está dentro do escopo da invenção. Condições de lavagem usadas para identificar ácidos nucleicos dentro do escopo da invenção incluem, por exemplo: uma concentração salina de cerca de 0,02 molar em pH 7 e uma temperatura de pelo menos cerca de 50°C ou cerca de 55°C a cerca de 60°C; ou, uma concentração salina de cerca de 0,15 M de NaCl a 72°C por cerca de 15 minutos; ou, uma concentração salina de cerca de 0,2X SSC em uma temperatura de pelo menos cerca de 50°C ou cerca de 55°C a cerca de 60°C por cerca de 15 a cerca de 20 minutos; ou, o complexo de hibridização é lavado duas vezes com uma solução com uma concentração salina de cerca de 2X SSC contendo 0,1% de SDS em temperatura ambiente por 15 minutos e em seguida lavado duas vezes por 0,1X SSC contendo 0,1% de SDS a 68°C por 15 minutos; ou, condições equivalentes. Vide Sambrook, Tijssen e Ausubel para uma descripção de tampão de SSC e condições equivalentes.
[000608] Estes métodos podem ser usados para isolar ácidos nucleicos da invenção. Por exemplo, os métodos precedentes podem ser usados para isolar ácidos nucleicos tendo uma sequência com pelo menos cerca de 97%, pelo menos 95%, pelo menos 90%, pelo menos 85%, pelo menos 80%, pelo menos 75%, pelo menos 70%, pelo menos 65%, pelo menos 60%, pelo menos 55%, ou pelo menos 50% de homologia com uma sequência de ácido nucleico selecionada entre o grupo consistindo em uma das sequências da invenção, ou fragmentos compreendendo pelo menos cerca de 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, 150, 200, 300, 400, ou 500 bases consecutivas da mesma e as sequências complementares a essas. A homologia pode ser medida usando o algoritmo de alinhamento. Por exemplo, os polinucleotídeos homólogos podem ter uma sequência codificante a qual é uma variante alélica que ocorre naturalmente de uma das sequências codificantes descritas aqui, neste pedido de patente. As variantes alélicas referidas podem ter uma substituição, eliminação ou adição de um ou mais nucleotídeos quando comparadas com os ácidos nucleicos da invenção.
[000609] Adicionalmente, os procedimentos acima podem ser usados para isolar ácidos nucleicos os quais codificam polipeptídeos tendo pelo menos cerca de 99%, 95%, pelo menos 90%, pelo menos 85%, pelo menos 80%, pelo menos 75%, pelo menos 70%, pelo menos 65%, pelo menos 60%, pelo menos 55%, ou pelo menos 50% de homologia com um polipeptídeo da invenção, ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos do mesmo conforme determinado usando um algoritmo de alinhamento de sequência (por exemplo, tal como o algoritmo Versão FASTA 3.0t78 com os parâmetros definidos). Sondas de oligonucleotídeos e métodos para usar as mesmas
[000610] A invenção também proporciona sondas de ácido nucleico que podem ser usadas, por exemplo, para identificar ácidos nucleicos codificando um polipeptídeo com uma atividade de glucanase ou fragmentos do mesmo ou para identificar genes de glucanase. Em um aspecto, a sonda compreende pelo menos 10 bases consecutivas de um ácido nucleico da invenção. Alternativamente, uma sonda da invenção pode ter pelo menos cerca de 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120, 130, 150 ou cerca de 10 a 50, cerca de 20 a 60 cerca de 30 a 70, bases consecutivas de uma sequência conforme determinado em um ácido nucleico da invenção. As sondas identificam um ácido nucleico por ligação e/ou hibridização. As sondas podem ser usadas em arranjos da invenção, vide a discussão abaixo, incluindo, por exemplo, arranjos capilares. As sondas da invenção também podem ser usadas para isolar outros ácidos nucleicos ou polipeptídeos.
[000611] Os ácidos nucleicos isolados da invenção, as sequências complementares aos mesmos, ou um fragmento compreendendo pelo menos 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, 150, 200, 300, 400, ou 500 bases consecutivas de uma das sequências da invenção, ou as sequências complementares às mesmas também podem ser usados como sondas para determinar se uma amostra biológica, tal como uma amostra de terra, contém um organismo tendo uma sequência de ácido nucleico da invenção ou um organismo do qual o ácido nucleico foi obtido. Nos referidos procedimentos, uma amostra biológica potencialmente portando o organismo do qual o ácido nucleico foi isolado é obtida e ácidos nucleicos são obtidos da amostra. Os ácidos nucleicos são contactados com a sonda sob condições as quais permitem que a sonda hibridize especificamente a quaisquer sequências complementares das quais estão presentes na mesma.
[000612] Onde necessário, condições as quais permitem que a sonda hibridize especificamente a sequências complementares podem ser determinadas colocando a sonda em contato com sequências complementares de amostras conhecidas por conter a sequência complementar bem como sequências controle as quais não contêm a sequência complementar. Condições de hibridização, tais como a concentração de sal do tampão de hibridização, a concentração de formamida do tampão de hibridização, ou a temperatura de hibridização, pode ser variada para identificar condições as quais permitem que a sonda hibridize especificamente a ácidos nucleicos complementares.
[000613] Se a amostra contém o organismo do qual o ácido nucleico foi isolado, então é detectada hibridização específica da sonda. A hibridização pode ser detectada marcando a sonda com um agente detectável tal como um isótopo radioativo, um corante fluorescente ou uma enzima capaz de catalisar a formação de um produto detectável.
[000614] Muitos métodos para usar as sondas marcadas para detectar a presença de ácidos nucleicos complementares em uma amostra são familiares daqueles versados na técnica. Estes incluem Southern Blots, Northern Blots, procedimentos de hibridização de colônia e dot blots. Protocolos para cada um destes procedimentos são proporcionados em Ausubel et al. Current Protocols in Molecular Biology, John Wiley 503 Sons, Inc. (1997) e Sambrook et al., Molecular Cloning: A Laboratory Manual 2nd Ed., Cold Spring Harbor Laboratory Press (1989).
[000615] Alternativamente, mais de uma sonda (pelo menos uma a qual é capaz de hibridizar especificamente a quaisquer sequências complementares as quais estão presentes na amostra de ácido nucleico) pode ser usada em uma reação de amplificação para determinar se a amostra contém um organismo contendo uma sequência de ácido nucleico da invenção (por exemplo, um organismo a partir do qual o ácido nucleico foi isolado). As sondas podem compreender oligonucleotídeos. Em um aspecto, a reação de amplificação pode compreender uma reação de PCR. Protocolos de PCR são descritos em Ausubel and Sambrook, supra. Alternativamente, a amplificação pode compreender uma reação de cadeia ligase, 3SR, ou reação de deslocamento de fita. (Vide Barany, F., “The Ligase Chain Reaction in a PCR World”, PCR Methods and Applications 1:5-16, 1991; E. Fahy et al., “Self-sustained Sequence Replication (3SR): An Isothermal Transcription-based Amplification System Alternative to PCR”, PCR Methods and Applications 1:25-33, 1991; e Walker G.T. et al., “Strand Displacement Amplification-an Isothermal in vitro DNA Amplification Technique”, Nucleic Acid Research 20:1691-1696, 1992). Os referidos procedimentos, os ácidos nucleicos na amostra são contactados com as sondas, a reação de amplificação é realizada e qualquer produto da amplificação resultante é detectado. O produto da amplificação pode ser detectado realizando eletroforese por gel sobre os produtos da reação e corando o gel com um intercalador tal como brometo de etídio. Alternativamente, uma ou mais das sondas podem ser marcadas com um isótopo radioativo e a presença de um produto da amplificação radioativo pode ser detectada por autoradiografia depois de eletroforese por gel.
[000616] Sondas derivadas de sequências próximas às extremidades das sequências da invenção, também podem ser usadas em procedimentos de caminhadas cromossômicas para identificar clones contendo sequências genômicas localizadas adjacentes às sequências da invenção. Os referidos métodos permitem o isolamento de genes os quais codificam proteínas adicionais do organismo hospedeiro.
[000617] Os ácidos nucleicos isolados da invenção, as sequências complementares aos mesmos, ou um fragmento compreendendo pelo menos 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, 150, 200, 300, 400, ou 500 bases consecutivas de uma das sequências da invenção, ou as sequências complementares às mesmas podem ser usados como sondas para identificar e isolar ácidos nucleicos relacionados. Em alguns aspectos, os ácidos nucleicos relacionados podem ser cDNAs ou DNAs genômicos de organismos diferentes do organismo a partir do qual o ácido nucleico foi isolado. Por exemplo, os outros organismos podem ser organismos relacionados. Nos referidos procedimentos, uma amostra de ácido nucleico é contactada com a sonda sob condições as quais permitem que a sonda hibridize especificamente a sequências relacionadas. A hibridização da sonda a ácidos nucleicos do organismo relacionado é então detectada usando quaisquer dos métodos descritos acima.
[000618] Variando a estringência das condições de hibridização usadas para identificar ácidos nucleicos, tais como cDNAs ou DNAs genômicos, os quais hibridizam à sonda detectável, ácidos nucleicos tendo diferentes níveis de homologia com a sonda podem ser identificados e isolados. A estringência pode ser variada conduzindo a hibridização em temperaturas variáveis abaixo das temperaturas de fusão das sondas. A temperatura de fusão, Tm, é a temperatura (sob força iônica e pH definidos) na qual 50% da sequência alvo hibridiza a uma sonda perfeitamente complementar. Condições muitos estringentes são selecionadas para serem iguais a ou cerca de 5DC menores do que a Tm para uma sonda particular. A temperatura de fusão da sonda pode ser calculada usando as seguintes fórmulas:
[000619] Para sondas entre 14 e 70 nucleotídeos de extensão a temperatura de fusão (Tm) é calculada usando a fórmula: Tm = 81,5 + 16,6 (log [Na+]) + 0,41 (fração G+C) - (600/N) onde N é a extensão da sonda.Se a hibridização for realizada em uma solução contendo formamida, a temperatura de fusão pode ser calculada usando a equação: Tm = 81,5 + 16,6 (log [Na+]) + 0,41 (fração G+C) - (0,63% de formamida) - (600/N) onde N é a extensão da sonda.
[000620] Pré-hibridização pode ser realizada em 6X SSC, 5X reagente de Denhardt, 0,5% de SDS, 100 μg/ml de DNA de esperma de salmão fragmentado desnaturado ou 6X SSC, 5X reagente de Denhardt, 0,5% de SDS, 100 μg/ml de DNA de esperma de salmão fragmentado desnaturado, 50% de formamida. As fórmulas para soluções de SSC e de Denhardt estão listadas em Sambrook et al., supra.
[000621] A hibridização é conduzida adicionando a sonda detectável às soluções de pré-hibridização listadas acima. Onde a sonda compreende DNA de fita dupla, é desnaturada antes de adição à solução de hibridização. O filtro é contactado com a solução de hibridização por um período de tempo suficiente para permitir que a sonda hibridize a cDNAs ou DNAs genômicos contendo sequências complementares à mesma ou homólogas à mesma. Para sondas acima de 200 nucleotídeos de extensão, a hibridização pode ser realizada em cerca de 15 a 25°C abaixo da Tm. Para sondas mais curtas, tais como oligonucleotídeo sondas, a hibridização pode ser conduzida em cerca de 5°C a 10°C abaixo da Tm. Para hibridizações em 6X SSC, a hibridização pode ser conduzida em aproximadamente 68°C. Em um aspecto, para hibridizações em soluções compreendendo 50% de formamida, a hibridização é conduzida em aproximadamente 42°C.
Inibindo a Expressão de Enzimas (Glucanases)
[000622] A invenção proporciona ácidos nucleicos complementar a (por exemplo, sequências antissenso para) os ácidos nucleicos da invenção, por exemplo, ácidos nucleicos codificando endoglucanase, codificando mananase, ou codificando xilanase. Sequências antissenso são capazes de inibir o transporte, junção ou transcrição de genes codificando glucanase, codificando endoglucanase, codificando mananase, ou codificando xilanase. A inibição pode ser efetuada através do direcionamento do DNA genômico ou do RNA mensageiro. A transcrição ou função do ácido nucleico direcionado pode ser inibida, por exemplo, por hibridização e/ou clivagem. Uma série de inibidores particularmente útila proporcionada pela presente invenção inclui oligonucleotídeos os quais são capazes de ou ligar gene ou mensagem de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, em qualquer caso evitando ou inibindo a produção ou função de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. A associação pode ser através de hibridização sequência-específica. Outra classe útila de inibidores inclui oligonucleotídeos os quais causam inativação ou clivagem de mensagem de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. O oligonucleotídeo pode ter atividade enzimática a qual causa semelhante clivagem, tais como ribozimas. O oligonucleotídeo pode ser quimicamente modificado ou conjugado a uma enzima ou composição capaz de clivar o ácido nucleico complementar. Um grupo de muitos diferentes referidos oligonucleotídeos pode ser triado para os com a atividade desejada. Portanto, a invenção proporciona várias composições para a inibição da expressão de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase em um nível de ácido nucleico e/ou proteína, por exemplo, antissenso, iRNA (por exemplo, siRNA, miRNA) e ribozimas compreendendo sequências de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção e os anticorpos antiglucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção.
[000623] A inibição da expressão de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase pode ter uma variedade de aplicações industriais. Por exemplo, a inibição da expressão de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase pode retardar ou impedir a deterioração de alimento ou ração. Pode ocorrer deterioração quando polissacarídeos, por exemplo, polissacarídeos estruturais, são degradados enzimaticamente. Isto pode levar à deterioração, ou podridão, de frutos e legumes. Em um aspecto, uso de composições da invenção que inibem a expressão e/ou atividade de glucanases (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, por exemplo, anticorpos, oligonucleotídeos antissenso, ribozimas e RNAi, são usados para retardar ou evitar deterioração. Portanto, em um aspecto, a invenção proporciona métodos e composições compreendendo aplicação sobre uma planta ou produto vegetal (por exemplo, um cereal, um grão, um fruto, semente, raiz, folha, e etc.) de anticorpos, oligonucleotídeos antissenso, ribozimas e RNAi da invenção para retardar ou evitar deterioração. Estas composições também podem ser expressadas pela planta (por exemplo, uma planta transgênica) ou outro organismo (por exemplo, uma bactéria ou outro micro-organismo transformado com um gene de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção).
[000624] As composições da invenção para a inibição da expressão de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase (por exemplo, antissenso, iRNA (por exemplo, siRNA, miRNA), ribozimas, anticorpos) podem ser usadas como composições farmacêuticas, por exemplo, como agentes antipatógenos ou em outras terapias, por exemplo, como antimicrobianos para, por exemplo, Salmonella.
Oligonucleotídeos Antissenso
[000625] A invenção proporciona oligonucleotídeos antissenso capazes de ligar mensagem ou gene de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase o qual pode inibir um gene ou uma mensagem-alvo para, por exemplo, inibir atividade de um glucano, um manano, um arabinoxilano ou um xilano, hidrolase (por exemplo, catalisar hidrólise de ligações β-1,4-xilosidicas internas) direcionando mRNA. Estratégias para desenhar oligonucleotídeos antissenso são descritas de modo geral na literatura científica e de patente, e o técnico versado pode desenhar semelhantes oligonucleotídeos de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase usando os novos reagentes da invenção. Por exemplo, protocolos de caminhada genética/mapeamento de RNA para triar para oligonucleotídeos antissenso eficazes são de conhecimento geral na técnica, vide, por exemplo, Ho (2000) Methods Enzymol. 314:168183, descrevendo um ensaio de mapeamento de RNA, a qual se baseia em técnicas moleculares de rotina para proporcionar um método fácila e confiável para potente seleção de sequência antissenso. Vide também Smith (2000) Eur. J. Pharm. Sci. 11:191-198.
[000626] Ácidos nucleicos que ocorrem naturalmente são usados como oligonucleotídeos antissenso. Os oligonucleotídeos antissenso podem ser de qualquer extensão; por exemplo, em aspectos alternativos, os oligonucleotídeos antissenso são entre cerca de 5 a 100, cerca de 10 a 80, cerca de 15 a 60, cerca de 18 a 40. A extensão ótima pode ser determinada por triagem de rotina. Os oligonucleotídeos antissenso podem estar presentes em qualquer concentração. A concentração ótima pode ser determinada por triagem de rotina. São conhecidas uma ampla variedade de análogos de nucleotídeos e ácidos nucleicos sintéticos, que não ocorrem naturalmente os quais podem tratar este problema potencial. Por exemplo, podem ser usados ácidos nucleicos peptídicos (PNAs) contendo estruturas principais não-iônicas, tais como unidades de N- (2-aminoetila) glicina. Oligonucleotídeos antissenso tendo ligações fosforotioato também podem ser usados, conforme descrito na patente WO 97/03211; na patente WO 96/39154; Mata (1997) Toxicol Appl Pharmacol 144:189-197; Antisense Therapeutics, ed. Agrawal (Humana Press, Totowa, N.J., 1996). Oligonucleotídeos antissenso tendo análogos de estrutura principal de DNA sintético proporcionados pela invenção também podem incluir de fosforoditioato, metilfosfonato, fosforamidato, aquila fosfotriéster, sulfamato, 3'-tioacetal, metileno(metilimino), 3'-N-carbamato, e ácidos nucleicos de carbonato de morfolino, conforme descrito acima.
[000627] Metodologia de química combinatorial pode ser usada para criar vastos números de oligonucleotídeos que podem ser rapidamente triados para oligonucleotídeos específicos que têm afinidades de ligação apropriadas e especificidades para qualquer alvo, tais como as sequências senso e anti-senso de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção (vide, por exemplo, Gold (1995) J. of Biol. Chem. 270:13581-13584).
Ribozimas Inibitórias
[000628] A invenção proporciona ribozimas capazes de ligar mensagem ou genes de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Estas ribozimas podem inibir atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase por, por exemplo, direcionamento de mRNA. Estratégias para desenhar ribozimas e selecionar a sequência antissenso específica de glucanase, mananase, ou xilanase para direcionamento são bem descritas na literatura científica e de patente, e o técnico versado pode desenhar as referidas ribozimas usando os novos reagentes da invenção. Ribozimas agem ligando-se a um RNA alvo através da porção de ligação de RNA alvo de uma ribozima a qual é mantida em íntima proximidade com uma porção enzimática do RNA que cliva o RNA alvo. Deste modo, a ribozima reconhece e liga um RNA alvo através de pareamento de bases complementares, e uma vez ligada ao sítio correto, age enzimaticamente clivando e inativa o RNA alvo. A clivagem de um RNA alvo desta maneira destruirá sua capacidade para síntese direta de uma proteína codificada se a clivagem ocorrer na sequência codificante. Depois de uma ribozima ter ligado e clivado seu RNA alvo, pode ser liberada do RNA para ligar e clivar novos alvos repetidamente.
[000629] Em algumas circunstâncias, a natureza enzimática de uma ribozima pode ser vantajosa em relação a outras tecnologias, tais como tecnologia antissenso (onde uma molécula de ácido nucleico simplesmente liga-se a um ácido nucleico alvo para bloquear sua transcrição, translação ou associação com outra molécula) uma vez que a concentração eficaz de ribozima necessária para efetuar um tratamento terapêutico pode ser menor do que a de um oligonucleotídeo antissenso. Esta vantagem potencial reflete a capacidade da ribozima para agir enzimaticamente. Portanto, uma única molécula de ribozima é capaz de clivar muitas moléculas de RNA alvo. Além disso, uma ribozima pode ser um inibidor altamente específico, com a especificidade de inibição dependendo não somente do mecanismo de ligação de pareamento de bases, mas também do mecanismo pelo qual a molécula inibe a expressão do RNA ao qual se liga. Isto é, a inibição é causada por clivagem do RNA alvo e portanto a especificidade é definida como a proporção da taxa de clivagem do RNA alvo sobre a taxa de clivagem de RNA não-alvo. Este mecanismo de clivagem é dependente de fatores adicionais àqueles envolvidos em pareamento de bases. Portanto, a especificidade de ação de uma ribozima pode ser maior do que a de oligonucleotídeo antissenso ligando o mesmo sítio de RNA.
[000630] A ribozima da invenção, por exemplo, uma molécula de RNA de ribozima enzimática, pode ser formada em um motivo de cabeça do martelo, um motivo de grampo de cabelo, como um motivo do delta vírus da hepatite, um motivo do íntron grupo I e/ou um RNA semelhante a RNaseP em associação com uma sequência guia de RNA. Exemplos de motivos de cabeça do martelo são descritos por, por exemplo, Rossi (1992) Aids Research and Human Retroviruses 8:183; motivos de grampo de cabelo por Hampel (1989) Biochemistry 28:4929, e Hampel (1990) Nuc. Acids Res. 18:299; o motivo do delta vírus da hepatite por Perrotta (1992) Biochemistry 31:16; o motivo RNaseP por Guerrier-Takada (1983) Cell 35:849; e o íntron do grupo I por Cech, a Patente dos Estados Unidos No. 4.987.071. A enumeração destes motivos específicos não pretende ser limitante. Os versados na técnica reconhecerão que uma ribozima da invenção, por exemplo, uma molécula de RNA enzimático desta invenção, pode ter um sítio de ligação de substrato específico complementar a uma ou mais das regiões de RNA do gene-alvo. Uma ribozima da invenção pode ter uma sequência de nucleotídeos dentro ou circundando o sítio de ligação de substrato o qual confere uma atividade de clivagem de RNA à molécula.
Interferência de RNA (RNAi)
[000631] Em um aspecto, a invenção proporciona uma molécula inibitória de RNA, uma chamada molécula de “RNAi”, compreendendo uma sequência de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção. A molécula de RNAi compreende uma molécula de RNA de fita dupla (dsRNA). O RNAi pode inibir expressão de um gene de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Em um aspecto, o RNAi tem cerca de 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 ou mais nucleotídeos dúplices de extensão. Apesar da invenção não ser limitada por qualquer mecanismo de ação em particular, o RNAi pode penetrar em uma célula e causar a degradação de um RNA de fita única (ssRNA) de sequências similares ou idênticas, incluindo mRNAs endógenos. Quando uma célula é exposta a RNA de fita dupla (dsRNA), mRNA do gene homólogo é degradado seletivamente por um processo denominado interferência de RNA (RNAi). Um possível mecanismo básico por trás do RNAi é a ruptura de um RNA de fita dupla (dsRNA) combinando uma sequência genética específica em pequenos pedaços denominados RNA interferente, o qual dispara a degradação de mRNA que corresponde a sua sequência. Em um aspecto, os RNAi’s da invenção são usados em terapêutica de silenciamento genético, vide, por exemplo, Shuey (2002) Drug Discov. Today 7:1040-1046. Em um aspecto, a invenção proporciona métodos para degradar seletivamente RNA usando os RNAi’s da invenção. O processo pode ser praticado in vitro, ex vivo ou in vivo. Em um aspecto, as moléculas de RNAi da invenção podem ser usadas para gerar uma mutação de perda de função em uma célula, um órgão ou um animal. Métodos para preparar e usar moléculas de RNAi para degradar seletivamente RNA são de conhecimento geral na técnica, vide, por exemplo, a Patente dos Estados Unidos Nos. 6.506.559; 6.511.824; 6.515.109; 6.489.127.
Modificação de Ácidos Nucleicos
[000632] A invenção proporciona métodos para gerar variantes dos ácidos nucleicos da invenção, por exemplo, aqueles codificando uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. Estes métodos podem ser repetidos ou usados em várias combinações para gerar glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases tendo uma atividade alterada ou diferente ou uma estabilidade alterada ou diferente daquela de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase codificada pelo ácido nucleico molde. Estes métodos também podem ser repetidos ou usados em várias combinações, por exemplo, para gerar variações na expressão genética/de mensagem, translação de mensagem ou estabilidade de mensagem. Em outro aspecto, a composição genética de uma célula é alterada, por exemplo, por modificação de um gene homólogo ex vivo, seguido por sua reinserção na célula.
[000633] Em um aspecto, o termo “variante” se refere a polinucleotídeos ou polipeptídeos da invenção modificados em um ou mais pares de bases, códons, íntrons, éxons, ou resíduos aminoácido (respectivamente) ainda retêm a atividade biológica de uma glucanase da invenção. Variantes podem ser produzidas por qualquer número de meios incluem métodos tais como, por exemplo, PCR propenso a erro, embaralhamento, mutagênese dirigida por oligonucleotídeo, PCR de montagem, mutagênese sexual por PCR, mutagênese in vivo, mutagênese de cassete, mutagênese de conjunto recursiva, mutagênese de conjunto exponencial, mutagênese sítio-específica, remontagem genética, Mutagênese de Saturação de Sítio Genético (GSSM), remontagem de ligação sintética (SLR), e qualquer combinação dos mesmos.
[000634] Um ácido nucleico da invenção pode ser alterado por quaisquer meios. Por exemplo, métodos aleatórios ou estocásticos, ou, métodos não- estocásticos, ou de “evolução dirigida,”, vide, por exemplo, a Patente dos Estados Unidos No. 6.361.974. Métodos para mutação aleatória de genes são de conhecimento geral na técnica, vide, por exemplo, a Patente dos Estados Unidos No. 5.830.696. Por exemplo, mutágenos podem ser usados para mutar aleatoriamente um gene. Mutágenos incluem, por exemplo, luz ultravioleta ou irradiação gama, ou um mutágeno químico, por exemplo, mitomicina, ácido nitroso, psoralenos fotoativados, sozinhos ou em combinação, para induzir quebras de DNA suscetíveis a reparo por recombinação. Outros mutágenos químicos incluem, por exemplo, bissulfito de sódio, ácido nitroso, hidroxilamina, hidrazina ou ácido fórmico. Outros mutágenos são análogos de precursores de nucleotídeos, por exemplo, nitrosoguanidina, 5-bromouracila, 2-aminopurina, ou acridina. Estes agentes podem ser adicionados a uma reação de PCR ao invés do precursor de nucleotídeo deste modo mutando a sequência. Também podem ser usados agentes intercalantes tais como proflavina, acriflavina, quinacrina e similares.
[000635] Pode ser usada qualquer técnica de biologia molecular, por exemplo, mutagênese de PCR aleatória, vide, por exemplo, Rice (1992) Proc. Natl. Acad. Sci. USA 89:5467-5471; ou, mutagênese de cassete múltiplo combinatorial, vide, por exemplo, Crameri (1995) Biotechniques 18:194-196. Alternativamente, ácidos nucleicos, por exemplo, genes, podem ser remontados depois de fragmentação aleatória, ou “estocástica”, vide, por exemplo, as Patentes dos Estados Unidos Nos. 6.291.242; 6.287.862; 6.287.861; 5.955.358; 5.830.721; 5.824.514; 5.811.238; 5.605.793. Em aspectos alternativos,modificações, adições ou eliminações são introduzidas por PCR propenso a erro, embaralhamento, mutagênese dirigida por oligonucleotídeo, PCR de montagem, mutagênese sexual por PCR, mutagênese in vivo, mutagênese de cassete, mutagênese de conjunto recursiva, mutagênese de conjunto exponencial, mutagênese sítio- específica, remontagem genética, mutagênese de saturação de sítio genético (GSSM), remontagem de ligação sintética (SLR), recombinação, recombinação de sequência recursiva, mutagênese de DNA modificado por fosfotioato, mutagênese molde contendo uracila, mutagênese de dúplices com espaço, mutagênese de reparo de combinação inadequada de ponto, mutagênese de cepa hospedeira reparo-deficiente, mutagênese química, mutagênese radiogênica, mutagênese de eliminação, mutagênese de restrição-seleção, mutagênese de restrição-purificação, síntese genética artificial, mutagênese de conjunto, criação de multímero de ácido nucleico quimérico, e/ou uma combinação destes e outros métodos.
[000636] As seguintes publicações descrevem uma variedade de procedimentos e/ou métodos de recombinação recursiva os quais podem ser incorporados dos métodos da invenção: Stemmer (1999) "Molecular breeding of viruses for targeting and other clinical properties" Tumor Targeting 4:1-4; Ness (1999) Nature Biotechnology 17:893-896; Chang (1999) "Evolution of a cytokine using DNA family shuffling" Nature Biotechnology 17:793-797; Minshull (1999) "Protein evolution by molecular breeding" Current Opinion in Chemical Biology 3:284-290; Christians (1999) "Directed evolution of thymidine kinase for AZT phosphorilation using DNA family shuffling" Nature Biotechnology 17:259-264; Crameri (1998) "DNA shuffling of a family of genes from diverse species accelerates directed evolution" Nature 391:288-291; Crameri (1997) "Molecular evolution of an arsenate detoxification pathway by DNA shuffling," Nature Biotechnology 15:436-438; Zhang (1997) "Directed evolution of an effective fucosidase from a galactosidase by DNA shuffling and screening" Proc. Natl. Acad. Sci. USA 94:4504-4509; Patten et al. (1997) "Applications of DNA Shuffling to Pharmaceuticals and Vaccines" Current Opinion in Biotechnology 8:724-733; Crameri et al. (1996) "Construction and evolution of antibody-phage libraries by DNA shuffling" Nature Medicine 2:100-103; Gates et al. (1996) "Affinity selective isolation of ligands from peptide libraries through display on a lac repressor 'headpiece dimer'" Journal of Molecular Biology 255:373-386; Stemmer (1996) "Sexual PCR and Assembly PCR" In: The Encyclopedia of Molecular Biology. VCH Publishers, New York. pp.447-457; Crameri e Stemmer (1995) "Combinatorial multiple cassette mutagenesis creates all the permutations of mutant and wildtype cassettes" BioTechniques 18:194195; Stemmer et al. (1995) "Single-step assembly of a gene and entire plasmid form large numbers of oligodeoxyribonucleotides" Gene, 164:49-53; Stemmer (1995) "The Evolution of Molecular Computation" Science 270: 1510; Stemmer (1995) "Searching Sequence Space" Bio/Technology 13:549-553; Stemmer (1994) "Rapid evolution of a protein in vitro by DNA shuffling" Nature 370:389-391; e Stemmer (1994) "DNA shuffling by random fragmentation and reassembly: In vitro recombination for molecular evolution." Proc. Natl. Acad. Sci. USA 91:10747-10751.
[000637] Métodos mutacionais para gerar diversidade incluem, por exemplo, mutagênese sítio-dirigida (Ling et al. (1997) "Approaches to DNA mutagenesis: an overview" Anal Biochem. 254(2): 157-178; Dale et al. (1996) "Oligonucleotide-directed random mutagenesis using the phosphorothioate method" Methods Mol. Biol. 57:369-374; Smith (1985) "In vitro mutagenesis " Ann. Rev. Genet. 19:423-462; Botstein & Shortle (1985) "Strategies and applications of in vitro mutagenesis " Science 229:1193-1201; Carter (1986) "Site-directed mutagenesis " Biochem. J. 237:1-7; e Kunkel (1987) "The efficiency of oligonucleotide directed mutagenesis " em Nucleic Acids & Molecular Biology (Eckstein, F. e Lilley, D. M. J. eds., Springer Verlag, Berlin)); mutagênese usando moldes contendo uracila (Kunkel (1985) "Rapid and efficient site-specific mutagenesis without phenotypic selection" Proc. Natl. Acad. Sci. USA 82:488-492; Kunkel et al. (1987) "Rapid and efficient site-specific mutagenesis without phenotypic selection" Methods in Enzymol. 154, 367-382; e Bass et al. (1988) "Mutant Trp repressors with new DNA-binding specificities" Science 242:240-245); mutagênese dirigida a oligonucleotídeo (Methods in Enzymol. 100: 468-500 (1983); Methods in Enzymol. 154: 329-350 (1987); Zoller (1982) "Oligonucleotide-directed mutagenesis using M13-derived vectors: an efficient and general procedure for the production of point mutations in any DNA fragment" Nucleic Acids Res. 10:6487-6500; Zoller & Smith (1983) "Oligonucleotide-directed mutagenesis of DNA fragments cloned into M13 vectors" Methods in Enzymol. 100:468-500; e Zoller (1987) "Oligonucleotide-directed mutagenesis: a simple method using two oligonucleotide iniciadores and a single-stranded DNA template" Methods in Enzymol. 154:329-350); mutagênese de DNA modificada por fosforotioato (Taylor (1985) "The use of phosphorothioate-modified DNA in restriction enzyme reactions to prepare nicked DNA" Nucl. Acids Res. 13: 8749-8764; Taylor (1985) "The rapid generation of oligonucleotide-directed mutations at high frequency using phosphorothioate-modified DNA" Nucl. Acids Res. 13: 8765-8787 (1985); Nakamaye (1986) "Inhibition of restriction endonuclease Nci I cleavage by phosphorothioate groups and its application to oligonucleotide -directed mutagenesis" Nucl. Acids Res. 14: 9679-9698; Sayers (1988) "Y-T Exonucleases in phosphorothioate- based oligonucleotide-directed mutagenesis " Nucl. Acids Res. 16:791802; e Sayers et al. (1988) "Strand specific cleavage of phosphorothioate-containing DNA by reaction with restriction endonucleases in the presence of ethidium bromide" Nucl. Acids Res. 16: 803-814); mutagênese usando dúplices de DNA com espaço (Kramer et al. (1984) "The gapped dúplices DNA approach to oligonucleotide -directed mutation construction" Nucl. Acids Res. 12: 9441-9456; Kramer & Fritz (1987) Methods in Enzymol. "Oligonucleotide-directed construction of mutations via gapped dúplices DNA" 154:350-367; Kramer (1988) "Improved enzymatic in vitro reactions in the gapped dúplices DNA approach to oligonucleotide -directed construction of mutations " Nucl. Acids Res. 16: 7207; e Fritz (1988) "Oligonucleotide-directed construction of mutations: a gapped dúplices DNA procedure without enzyme reactions in vitro" Nucl. Acids Res. 16: 6987-6999).
[000638] Protocolos adicionais que podem ser usados para praticar os métodos da invenção, ou para preparar composições da invenção, incluem reparo de combinação inadequada de ponto (vide, por exemplo, Kramer (1984) Cell 38:879-887), mutagênese usando cepas hospedeiras reparo-deficientes (vide, por exemplo, Carter (1985) Nucl. Acids Res. 13: 4431-4443; Carter (1987) Methods in Enzymol. 154: 382-403), eliminação mutagênese (vide, por exemplo, Eghtedarzadeh (1986) Nucl. Acids Res. 14: 5115), restrição-seleção e restrição- seleção e restrição-purificação (vide, por exemplo, Wells (1986) Phil. Trans. R. Soc. Lond. A 317: 415-423), mutagênese por síntese genética total (vide, por exemplo, Nambiar (1984) Science 223: 12991301; Sakamar (1988) Nucl. Acids Res. 14: 6361-6372; Wells et al. (1985) Gene 34:315-323; Grundstrom (1985) Nucl. Acids Res. 13: 3305-3316), reparo de quebra de fita dupla (vide, por exemplo, Arnold (1993) Current Opinion in Biotechnology 4:450-455). Detalhes adicionais sobre muitos dos métodos acima podem ser encontrados em Methods in Enzymology Volume 154, o qual também descreve controles úteis para problemas incômodos com vários métodos de mutagênese.
[000639] Protocolos que podem ser usados para praticar a invenção são descritos, por exemplo, na Patente dos Estados Unidos No. 5.605.793 para Stemmer (25 de fevereiro de 1997), "Methods for In vitro Recombination;" na Patente dos Estados Unidos No. 5.811.238 para Stemmer et al. (22 de setembro de 1998) "Methods for Generating Polynucleotides having Desired Characteristics by Iterative Selection and Recombination;" na Patente dos Estados Unidos No. 5.830.721 para Stemmer et al. (3 de novembro de 1998), "DNA Mutagenesis by Random Fragmentation and Reassembly;" na Patente dos Estados Unidos No. 5.834.252 para Stemmer, et al. (10 de novembro de 1998) "End-Complementary Polymerase Reaction;" na Patente dos Estados Unidos No. 5.837.458 para Minshull, et al. (17 de novembro de 1998), "Methods and Compositions for Cellular and Metabolic Engineering;" na patente WO 95/22625, Stemmer and Crameri, "Mutagenesis by Random Fragmentation and Reassembly;" na patente WO 96/33207 por Stemmer e Lipschutz "End Complementary Polymerase Chain Reaction;" na patente WO 97/20078 por Stemmer e Crameri "Methods for Generating Polynucleotides having Desired Characteristics by Iterative Selection and Recombination;" na patente WO 97/35966 por Minshull e Stemmer, "Methods and Compositions for Cellular and Metabolic Engineering;" na patente WO 99/41402 por Punnonen et al. "Targeting of Genetic Vaccine Vectors;" na patente WO 99/41383 por Punnonen et al. "Antigen Library Immunization;" na patente WO 99/41369 por Punnonen et al. "Genetic Vaccine Vector Engineering;" na patente WO 99/41368 por Punnonen et al. "Optimization of Immunomodulatory Properties of Genetic Vaccines;" ma patente EP 752008 por Stemmer and Crameri, "DNA Mutagenesis by Random Fragmentation and Reassembly;" ma patente EP 0932670 por Stemmer "Evolving Cellular DNA Uptake by Recursive Sequence Recombination;" na patente WO 99/23107 por Stemmer et al., "Modification of Virus Tropism and Host Range by Viral Genome Shuffling;" na patente WO 99/21979 por Apt et al., "Human Papillomavirus Vectors;" na patente WO 98/31837 por del Cardayre et al. "Evolution of Whole Cells and Organisms by Recursive Sequence Recombination;" na patente WO 98/27230 por Patten e Stemmer, "Methods and Compositions for Polypeptide Engineering;" na patente WO 98/27230 por Stemmer et al., "Methods for Optimization of Gene Therapy by Recursive Sequence Shuffling and Selection," na patente WO 00/00632, "Methods for Generating Highly Diverse Libraries," na patente WO 00/09679, "Methods for Obtaining in vitro Recombined Polynucleotide Sequence Banks and Resulting Sequences," na patente WO 98/42832 por Arnold et al., "Recombination of Polynucleotide Sequences Using Random or Defined Iniciadores," na patente WO 99/29902 por Arnold et al., "Method for Creating Polynucleotide and Polypeptide Sequences," na patente WO 98/41653 por Vind, "An in vitro Method for Construction of a DNA Library," na patente WO 98/41622 por Borchert et al., "Method for Constructing a Library Using DNA Shuffling," e na patente WO 98/42727 por Pati e Zarling, "Sequence Alterations using Homologous Recombination."
[000640] Protocolos que podem ser usados para praticar a invenção (proporcionando detalhes referentes a vários métodos geradores de diversidade) são descritos, por exemplo, no pedido de patente dos Estados Unidos No. Serial (USSN) 09/407.800, "SHUFFLING OF CODON ALTERED GENES" por Patten et al. depositado em 28 de setembro de 1999; "EVOLUTION OF WHOLE CELLS AND ORGANISMS BY RECURSIVE SEQUENCE RECOMBINATION" por del Cardayre et al., Patente dos Estados Unidos No. 6.379.964; "OLIGONUCLEOTIDE MEDIATED NUCLEIC ACID RECOMBINATION" por Crameri et al., Patentes dos Estados Unidos Nos. 6.319.714; 6.368.861; 6.376.246; 6.423.542; 6.426.224 e publicação de patente No. PCT/US00/01203; "USE OF CODON- VARIED OLIGONUCLEOTIDE SYNTHESIS FOR SYNTHETIC SHUFFLING" por Welch et al., Patente dos Estados Unidos No. 6.436.675; "METHODS FOR MAKING CHARACTER STRINGS, POLYNUCLEOTIDES & POLYPEPTIDES HAVING DESIRED CHARACTERISTICS" por Selifonov et al., depositado em 18 de janeiro de 2000, (publicação de patente No. PCT/US00/01202) e, por exemplo, "METHODS FOR MAKING CHARACTER STRINGS, POLYNUCLEOTIDES & POLYPEPTIDES HAVING DESIRED CHARACTERISTICS" por Selifonov et al., depositado em 18 de julho de 2000 (pedido de patente dos Estados Unidos No. Serial 09/618.579); "METHODS OF POPULATING DATA STRUCTURES FOR USE IN EVOLUTIONARY SIMULATIONS" por Selifonov e Stemmer, depositado em 18 de janeiro de 2000 (publicação de patente No. PCT/US00/01138); e "SINGLE-STRANDED NUCLEIC ACID TEMPLATE-MEDIATED RECOMBINATION AND NUCLEIC ACID FRAGMENT ISOLATION" por Affholter, depositado em 6 de setembro de 2000 (pedido de patente dos Estados Unidos No. Serial 09/656.549); e Patentes dos Estados Unidos Nos. 6.177.263; 6.153.410.
[000641] Métodos não-estocásticos, ou “de evolução dirigida,” incluem, por exemplo, mutagênese de saturação de sítio genético (GSSM), remontagem de ligação sintética (SLR), ou uma combinação dos mesmos são usados para modificar os ácidos nucleicos da invenção para gerar glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases com propriedades novas ou alteradas (por exemplo, atividade sob condições altamente acídicas ou alcalinas, temperaturas altas ou baixas, e similares). Polipeptídeos codificados pelos ácidos nucleicos modificados podem ser triados para uma atividade antes de testar para atividade de glucano ou hidrólise de outro polissacarídeo ou outra. Pode ser usada qualquer modalidade ou protocolo de experimentação, por exemplo, usando uma plataforma de arranjo capilar. Vide, por exemplo, as Patentes dos Estados Unidos Nos. 6.361.974; 6.280.926; 5.939.250.
Mutagênese de saturação, ou, GSSM
[000642] A invenção também proporciona métodos para fabricar novas enzimas, ou modificando sequências da invenção, usando mutagênese de saturação de sítio genético, ou, GSSM, conforme descrito aqui, neste pedido de patente, e também nas Patentes dos Estados Unidos Nos. 6.171.820 e 6.579.258.
[000643] Em um aspecto, iniciadores de códons contendo uma sequência N,N,G/T degenerada são usados para introduzir mutações de ponto em um polinucleotídeo, por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase ou um anticorpo da invenção, de modo a gerar uma série de polipeptídeos da progênir nos quais uma ampla gama de substituições de aminoácido única é representada em cada posição de aminoácido, por exemplo, um resíduo de aminoácido em um sítio ativo enzimático (domínios catalíticos (CDs)) ou sítio de ligação de ligante alvo a ser modificado. Estes oligonucleotídeos podem compreender uma primeira sequência homóloga contígua, uma sequência N,N,G/T degenerada, e, opcionalmente, uma segunda sequência homóloga. Os produtos translacionais da progênie a jusante do uso de similares oligonucleotídeos incluem todas as alterações de aminoácidos possíveis em cada sítio de aminoácido ao longo do polipeptídeo, devido à degeneração da sequência N,N,G/T inclui códons para todos os 20 aminoácidos. Em um aspecto, um oligonucleotídeo degenerado semelhante (consistindo em, por exemplo, um cassete N,N,G/T degenerado) é usado para submeter cada códon original em um molde de polinucleotídeo parental para uma ampla gama de substituições de códons. Em outro aspecto, são usados pelo menos dois cassetes degenerados - que no mesmo oligonucleotídeo ou não, para submeter pelo menos dois códons originais em um molde de polinucleotídeo parental para uma ampla gama de substituições de códons. Por exemplo, mais de uma sequência N,N,G/T pode ser contida em um oligonucleotídeo para introduzir mutações de aminoácidos em mais de um sítio. Esta pluralidade de sequências N,N,G/T pode ser diretamente contígua, ou separada por uma ou mais sequências de nucleotídeos adicionais. Em outro aspecto, oligonucleotídeos úteis para introduzir adições e eliminações podem ser usados ou sozinhos ou e, combinação com os códons contendo uma sequência N,N,G/T, para introduzir qualquer combinação ou permutação de adições, eliminações, e/ou substituições de aminoácidos.
[000644] Em um aspecto, é feita mutagênese simultânea de duas ou mais posições de aminoácidos contíguos usando um oligonucleotídeo que contém tripletos N,N,G/T contíguos, isto é, uma sequência (N,N,G/T)n degenerada. Em outro aspecto, são usados cassetes degenerados tendo menos degeneração do que a sequência N,N,G/T. Por exemplo, pode ser desejável em alguns casos usar (por exemplo, em um oligonucleotídeo) uma sequência de tripleto degenerada consistindo em somente um N, onde o referido N pode estar na primeira, segunda ou terceira posição do tripleto. Quaisquer outras bases incluindo quaisquer combinações e permutações das mesmas podem ser usadas nas duas posições restantes do tripleto. Alternativamente, pode ser desejável em alguns casos usar (por exemplo, em um oligo) uma sequência de tripleto N,N,N degenerada.
[000645] Em um aspecto, uso de tripletos degenerados (por exemplo, tripletos N,N,G/T) permite a produção sistemática e fácila de uma ampla faixa de aminoácidos naturais possíveis (para um total de 20 aminoácidos) em toda e cada posição de aminoácido em um polipeptídeo (em aspectos alternativos, os métodos também incluem produção de menos do que todas as substituições possíveis por posição de resíduo de aminoácido, ou códon). Por exemplo, para um polipeptídeo de 100 aminoácidos, podem ser produzidas 2000 espécies distintas (isto é, 20 aminoácidos possíveis por posição X posições de 100 aminoácidos). Através do uso de um oligonucleotídeo ou série de oligonucleotídeos contendo um tripleto N,N,G/T degenerado, 32 sequências individuais podem codificar para todos os 20 aminoácidos naturais possíveis. Portanto, em um vaso de reação no qual uma sequência de polinucleotídeo parental é submetida a mutagênese de saturação usando pelo menos um oligonucleotídeo semelhante, são produzidos 32 polinucleotídeos de progênies distintas codificando 20 polipeptídeos distintos. Em contraste, o uso de um oligonucleotídeo não-degenerado em mutagênese sítio-dirigida leva a somente um produto de polipeptídeo da progênir por vaso da reação. Oligonucleotídeos não-degenerados podem ser usados opcionalmente em combinação com iniciadores degenerados divulgados; por exemplo, oligonucleotídeos não-degenerados podem ser usados para gerar mutações de pontos específicos em um polinucleotídeo da manipulação. Isto proporciona um meio para gerar mutações de pontos inativos específicos, mutações de pontos levando a alterações de aminoácidos correspondentes, e mutações de pontos que causam a produção de códons de interrupção e a expressão correspondente de fragmentos de polipeptídeos.
[000646] Em um aspecto, cada vaso de reação de mutagênese de saturação contém polinucleotídeos codificando pelo menos 20 moléculas de polipeptídeos da progênie (por exemplo, glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases) tais que todos os 20 aminoácidos naturais são representados na uma posição de aminoácido específica correspondente à posição de códon mutagenizado no polinucleotídeo parental (ouotros aspectos usam menos de todas as 20 combinações naturais). Os polipeptídeos de progênies degeneradas 32 vezes produzidos a partir de cada vaso de reação de mutagênese de saturação podem ser submetidos a amplificação clonal (por exemplo, clonados em um hospedeiro adequado, por exemplo, hospedeiro de E. coli, usando, por exemplo, um vetor de expressão) e submetidos a triagem de expressão. Quando um polipeptídeo de progênie individual é identificado por triagem por apresentar uma alteração favorável na propriedade (quando comparado com o polipeptídeo parental, tal como aumento da atividade de hidrólise de glucano sob condições alcalinas ou acídicas), pode ser sequenciado para identificar a substituição de aminoácido favorável correspondentemente contida no mesmo.
[000647] Em um aspecto, ao mutagenizar toda e cada posição de aminoácido em um polipeptídeo parental usando mutagênese de saturação conforme divulgado aqui, neste pedido de patente, alterações de aminoácidos favoráveis podem ser identificadas em mais de uma posição de aminoácido. Uma ou mais moléculas da nova progênie podem ser geradas que contêm uma combinação de todas ou parte destas substituições de aminoácidos favoráveis. Por exemplo, se 2 alterações de aminoácidos favoráveis específicas são identificadas em cada uma de 3 posições de aminoácidos em um polipeptídeo, as permutações incluem 3 possibilidades em cada posição (nenhuma alteração do aminoácido original, e cada uma de duas alterações favoráveis) e 3 posições. Portanto, há 3 x 3 x 3 ou total de 27 possibilidades, incluindo 7 que foram previamente examinadas - 6 mutações de ponto único (isto é, 2 em cada uma de três posições) e nenhuma alteração em qualquer posição.
[000648] Em ainda outro aspecto, mutagênese de saturação de sítio pode ser usada junto com embaralhamento, quimerização, recombinação e outros processos de mutagenização, junto com triagem. Esta invenção proporciona o uso de quaisquer processos de mutagenização, incluindo mutagênese de saturação, em uma maneira iterativa. Em uma exemplificação, o uso iterativo de quaisquer processos de mutagenização é usado em combinação com triagem.
[000649] A invenção também proporciona o uso de iniciadores de códons proprietários (contendo uma sequência N,N,N degenerada) para introduzir mutações de pontos em um polinucleotídeo, de modo a gerar uma série de polipeptídeos da progênie nos quais uma ampla faixa de substituições de aminoácido único é representada em cada posição de aminoácido (Mutagênese de Saturação de Sítio Genético (GSSM)). Os oligos usados consistem contiguamente em uma primeira sequência homóloga, uma sequência N,N,N degenerada e em um aspecto mas não necessariamente uma segunda sequência homóloga. Os produtos translacionais de progênies a jusante do uso dos referidos oligos incluem todas as alterações de aminoácido possíveis em cada sítio de aminoácido ao longo do polipeptídeo, devido à degeneração da sequência N,N,N inclui códons para todos os 20 aminoácidos.
[000650] Em um aspecto, um referido oligo degenerado (consistindo em um cassete N,N,N degenerado) é usado para submeter cada códon original em um molde de polinucleotídeo parental a uma ampla série de substituições de códons. Em outro aspecto, são usados pelo menos dois cassetes N,N,N degenerados - quer no mesmo oligo ou não, para submeter pelo menos dois códons originais em um molde de polinucleotídeo parental a uma ampla série de substituições de códons. Portanto, mais de uma sequência N,N,N pode ser contida em um oligo para introduzir mutações de aminoácidos em mais de um sítio. Esta pluralidade de sequências N,N,N pode ser diretamente contígua, ou separada por uma ou mais sequências de nucleotídeos adicionais. Em outro aspecto, oligos úteis para introduzir adições e eliminações podem ser usados ou sozinhos ou em combinação com os códons contendo uma sequência N,N,N, para introduzir qualquer combinação ou permutação de adições, eliminações e/ou substituições de aminoácidos.
[000651] Em um exemplo particular, é possível mutagenizar simultaneamente duas ou mais posições de aminoácidos contíguos usando um oligo que contém tripletos N,N,N contíguos, isto é, uma sequência (N,N,N)n degenerada.
[000652] Em outro aspecto, a presente invenção proporciona o uso de cassetes degenerados tendo menos degeneração do que a sequência N,N,N. Por exemplo, pode ser desejável em alguns casos usar (por exemplo, em um oligo) uma sequência de tripleto degenerada consistindo em somente um N, onde o N pode estar na primeira, segunda ou terceira posição do tripleto. Quaisquer outras bases incluindo quaisquer combinações e permutações das mesmas podem ser usadas nas duas posições restantes do tripleto. Alternativamente, pode ser desejável em alguns casos usar (por exemplo, em um oligo) uma sequência de tripleto N,N,N degenerada, N,N,G/T, ou uma sequência de tripleto N,N, G/C.
[000653] No entanto, é reconhecido que o uso de um tripleto degenerado (tal como sequência de tripleto N,N,G/T ou uma N,N, G/C) conforme divulgado na presente invenção é vantajoso por vários motivos. Em um aspecto, esta invenção proporciona um meio para sistematicamente e bastante facilmente gerar a substituição da ampla série de aminoácidos possíveis (para um total de 20 aminoácidos) em cada e toda posição de aminoácido em um polipeptídeo. Portanto, para um polipeptídeo de 100 aminoácidos, a invenção proporciona um modo para sistematicamente e bastante facilmente gerar 2000 espécies distintas (isto é, 20 aminoácidos possíveis por posição vezes 100 posições de aminoácido). É reconhecido que é proporcionado, através do uso de um oligo contendo uma sequência de tripleto degenerado N,N,G/T ou uma N,N, G/C, 32 sequências individuais que codificam 20 aminoácidos possíveis. Portanto, em um vaso de reação no qual uma sequência de polinucleotídeo parental é submetida à mutagênese de saturação usando um oligo semelhante, são gerados 32 polinucleotídeos de progênies distintas codificando 20 polipeptídeos distintos. Em contraste, o uso de um oligo não-degenerado em mutagênese sítio-dirigida leva a somente um produto de polipeptídeo da progênie por vaso de reação.
[000654] Esta invenção também proporciona o uso de oligos não- degenerados, os quais podem ser usados opcionalmente em combinação com iniciadores degenerados divulgados. É reconhecido que em algumas situações, é vantajoso usar oligos não-degenerados para gerar mutações de pontos específicos em um polinucleotídeo da manipulação. Isto proporciona um meio para gerar mutações de pontos inativos específicos, mutações de pontos levando a alterações de aminoácidos correspondentes e mutações de pontos que causam a produção de códons de interrupção e a expressão correspondente de fragmentos de polipeptídeos.
[000655] Portanto, em um aspecto desta invenção, cada vaso de reação de mutagênese de saturação contém polinucleotídeos codificando pelo menos 20 moléculas de polipeptídeos da progênie de tal modo que todos os 20 aminoácidos são representados na posição de um aminoácido específico correspondente à posição do códon mutagenizado no polinucleotídeo parental. Os polipeptídeos da progênie degenerada 32 vezes gerados a partir de cada vaso de reação de mutagênese de saturação podem ser submetidos a amplificação clonal (por exemplo, clonados em um hospedeiro de E. coli adequado usando um vetor de expressão) e submetidos a triagem de expressão. Quando um polipeptídeo de progênie individual é identificado por triagem para apresentar uma alteração favorável em propriedade (quando comparado com o polipeptídeo parental), pode ser sequenciado para identificar a substituição de aminoácido favorável correspondente contida no mesmo.
[000656] É reconhecido que ao mutagenizar toda e cada posição de aminoácido em um polipeptídeo parental usando mutagênese de saturação conforme divulgado aqui, neste pedido de patente, podem ser identificadas alterações de aminoácidos favoráveis em mais de uma posição de aminoácido. Uma ou mais moléculas da nova progênie podem ser geradas que contêm uma combinação de todas ou parte destas substituições de aminoácidos favoráveis. Por exemplo, se 2 alterações de aminoácidos favoráveis específicas são identificadas em cada uma de 3 posições de aminoácidos em um polipeptídeo, as permutações incluem 3 possibilidades em cada posição (nenhuma alteração do aminoácido original e cada uma de duas alterações favoráveis) e 3 posições. Portanto, há 3 x 3 x 3 ou total de 27 possibilidades, incluindo 7 que foram examinadas previamente - 6 mutações de pontos únicos (isto é, 2 em cada uma de três posições) e nenhuma alteração em qualquer posição.
[000657] Portanto, em um exemplo não-limitante, esta invenção proporciona o uso de mutagênese de saturação em combinação com processos de mutagenização adicionais, tais como processo onde dois ou mais polinucleotídeos relacionados são introduzidos em uma célula hospedeira adequada de tal modo que um polinucleotídeo híbrido é gerado por recombinação e reagrupamento redutivo.
[000658] Além de realizar mutagênese ao longo de toda a sequência de um gene, a presente invenção proporciona que a mutagênese pode ser usada para substituir cada uma de qualquer número de bases em um sequência de polinucleotídeo, em que o número de bases a serem mutagenizadas é em um aspecto cada inteiro de 15 a 100.000. Portanto, ao invés de mutagenizar cada posição ao longo de uma molécula, pode-se submeter todas ou um número distinto de bases (em um aspecto um subgrupo totalizando de 15 a 100.000) a mutagênese. Em um aspecto, um nucleotídeo separado é usado para mutagenizar cada posição ou grupo de posições ao longo de uma sequência de polinucleotídeo. Um grupo de 3 posições a serem mutagenizadas pode ser um códon. As mutações podem ser introduzidas usando um iniciador mutagênico, contendo um cassete heterólogo, também referido como um cassete mutagênico. Cassetes típicos podem ter de 1 a 500 bases. Cada posição de nucleotídeo nos referidos cassetes heterólogos pode ser N, A, C, G, T, A/C, A/G, A/T, C/G, C/T, G/T, C/G/T, A/G/T, A/C/T, A/C/G, ou E, onde E é qualquer base que não é A, C, G, ou T (E pode ser referido como um oligo designer).
[000659] Em um aspecto, mutagênese de saturação compreende mutagenizar uma série completa de cassetes mutagênicos (em que cada cassete tem em um aspecto cerca de 1 a 500 bases de extensão) na sequência de polinucleotídeo definida a ser mutagenizada (em que a sequência a ser mutagenizada tem em um aspecto a partir de cerca de 15 a 100.000 bases de extensão). Deste modo, um grupo de mutações (variando de 1 a 100 mutações) é introduzido em cada cassete a ser mutagenizado. Um grupo de mutações a serem introduzidas em um cassete pode ser diferente ou o mesmo de um segundo grupo de mutações a serem introduzidas em um segundo cassete durante a aplicação de uma rodada de mutagênese de saturação. Os referidos grupos são exemplificados por eliminações, adições, grupos de códons particulares e grupos de cassetes de nucleotídeos particulares.
[000660] Sequências definidas a serem mutagenizadas incluem um gene inteiro, caminho, cDNA, uma estrutura de leitura aberta inteira (ORF) e um promotor inteiro, reforçador, repressor/transativador, origem de replicação, íntron, operador, ou qualquer grupo de polinucleotídeo funcional. Geralmente, algumas “sequências definidas” para este fim pode ser qualquer polinucleotídeo que uma sequência de polinucleotídeo de 15 bases e sequências de polinucleotídeos de extensões entre 15 bases e 15.000 bases (esta invenção especificamente nomeia cada inteiro no intervalo). Considerações ao escolher grupos de códons incluem tipos de aminoácidos codificados por um cassete mutagênico degenerado.
[000661] Em um exemplo de um grupo de mutações que podem ser introduzidas em um cassete mutagênico, esta invenção especificamente proporciona substituições de códons degenerados (usando oligos degenerados) que codificam para 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 e 20 aminoácidos em cada posição e uma biblioteca de polipeptídeos codificados por estes. Remontagem de Ligação Sintética (SLR)
[000662] A invenção proporciona um sistema de modificação genética não-estocástica denominado “remontagem de ligação sintética,” ou simplesmente “SLR,” um “processo de evolução dirigida,” para gerar polipeptídeos, por exemplo, glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases ou anticorpos da invenção, com propriedades novas ou alteradas. SLR é um método para ligar fragmentos de oligonucleotídeos juntos não-estocasticamente. Este método difere de embaralhamento de oligonucleotídeo estocástico em que os blocos de construção de ácido nucleico não são embaralhados, concatenados ou quimerizados aleatoriamente, mas ao invés são reunidos não-estocasticamente. Vide, por exemplo, as Patentes dos Estados Unidos Nos. 6.773.900; 6.740.506; 6.713.282; 6.635.449; 6.605.449; 6.537.776.
[000663] Em um aspecto, SLR compreende as seguintes etapas: (a) proporcionar um polinucleotídeo molde, em que o polinucleotídeo molde compreende sequência codificando um gene homólogo; (b) proporcionar uma pluralidade de polinucleotídeos de blocos de construção, em que os polinucleotídeos de blocos de construção são designados para remontagem por permutação com o polinucleotídeo molde em uma sequência predeterminada, e um polinucleotídeo de bloco de construção compreende uma sequência que é uma variante do gene homólogo e uma sequência homóloga ao polinucleotídeo molde flanqueando a sequência variante; (c) combinar um polinucleotídeo de bloco de construção com um polinucleotídeo molde tal que o polinucleotídeo de bloco de construção remonta por permutação com o polinucleotídeo molde para gerar polinucleotídeos compreendendo variações de sequências genéticas homólogas.
[000664] SLR não depende da presença de altos níveis de homologia entre polinucleotídeos a serem rearranjados. Portanto, este método pode ser usado para gerar não-estocasticamente bibliotecas (ou séries) de moléculas de progênies consistindo em mais de 10100 quimeras diferentes. SLR pode ser usado para gerar bibliotecas consistindo em mais de 101000 quimeras de progênies diferentes. Portanto, aspectos da presente invenção incluem métodos não- estocásticos para produzir uma série de moléculas de ácido nucleico quimérico finalizadas passando um pente fino em uma ordem de montagem global que é escolhida por design. Este método inclui as etapas de gerar por design uma pluralidade de blocos de construção de ácidos nucleicos específicos tendo extremidades ligáveis úteis mutuamente compatíveis, e montar estes blocos de construção de ácidos nucleicos, de tal modo que é obtida uma ordem de montagem global designada.
[000665] As extremidades ligáveis mutuamente compatíveis dos blocos de construção de ácidos nucleicos a serem reunidos são consideradas como sendo “úteis” para este tipo de montagem ordenada se possibilitarem que os blocos de construção sejam acoplados em ordens predeterminadas. Portanto, a ordem de montagem global na qual os blocos de construção de ácido nucleico podem ser acoplados é especificada pelo design das extremidades ligáveis. Se mais de uma etapa de montagem for usada, então a ordem de montagem global na qual os blocos de construção de ácido nucleico podem ser acoplados também é especificada pela ordem sequencial da uma ou mais etapas de montagem. Em um aspecto, as peças de construção recozidas são tratadas com uma enzima, tal como uma ligase (por exemplo, T4 DNA ligase), para obter ligação covalente das peças de construção.
[000666] Em um aspecto, o design dos blocos de construção de oligonucleotídeo é obtido analisando uma série de moldes de sequências de ácidos nucleicos progenitores que servem como uma base para produzir uma série de progênies de polinucleotídeos quiméricos finalizados. Estes moldes de oligonucleotídeos parentais portanto servem como uma fonte de informação de sequência que ajuda no design dos blocos de construção de ácido nucleico que devem ser mutagenizados, por exemplo, quimerizados ou embaralhados. Em um aspecto deste método, as sequências de uma pluralidade de moldes de ácidos nucleicos parentais são alinhadas de modo a selecionar um ou mais pontos de demarcação. Os pontos de demarcação podem estar localizados em uma área de homologia, e consistem em um ou mais nucleotídeos. Estes pontos de demarcação são em um aspecto partilhados por pelo menos dois dos moldes progenitores. Os pontos de demarcação podem ser usados deste modo para delinear os limites de blocos de construção de oligonucleotídeo a serem gerados de modo a rearranjar os polinucleotídeos parentais. Os pontos de demarcação identificados e selecionados nas moléculas progenitoras servem como pontos de quimerização potenciais na montagem das moléculas da progênie quimérica final. Um ponto de demarcação pode ser uma área de homologia (consistindo em pelo menos uma base de nucleotídeo homóloga) partilhada por pelo menos duas sequências de polinucleotídeos parentais. Alternativamente, um ponto de demarcação pode ser uma área de homologia que é partilhada por pelo menos metade das sequências de polinucleotídeos parentais, ou, pode ser uma área de homologia que é partilhada por pelo menos dois terços das sequências de polinucleotídeos parentais. Ainda mais em um aspecto, um ponto de demarcação útila é uma área de homologia que é partilhada por pelo menos três quartos das sequências de polinucleotídeos parentais, ou, pode ser partilhada por quase todas as sequências de polinucleotídeos parentais. Em um aspecto, um ponto de demarcação é uma área de homologia que é partilhada por todas as sequências de polinucleotídeos parentais.
[000667] Em um aspecto, um processo de remontagem de ligação é realizado exaustivamente de modo a gerar uma biblioteca exaustiva de polinucleotídeos quiméricos da progênie. Em outras palavras, todas as combinações ordenadas possíveis dos blocos de construção de ácido nucleico são representadas na série de moléculas de ácidos nucleicos quiméricos finalizados. Ao mesmo tempo, em outro aspecto, a ordem de montagem (isto é, a ordem de montagem de cada bloco de construção na sequência 5’ para 3 de cada ácido nucleico quimérico finalizado) em cada combinação é por design (ou não-estocástico) conforme descrito acima. Devido à natureza não-estocástica desta invenção, a possibilidade de produtos colaterais indesejados é muito reduzida.
[000668] Em outro aspecto, o método de remontagem de ligação é realizado sistematicamente. Por exemplo, o método é realizado de modo a gerar uma biblioteca sistematicamente compartimentalizada de moléculas da progênie, com compartimentos que podem ser triados sistematicamente, por exemplo, um por um. Em outras palavras, esta invenção proporciona que, através do uso seletivo e criterioso de blocos de construção de ácido nucleico específicos, junto com o uso seletivo e criterioso de reações de montagem sequencialmente em etapas, pode ser obtido um design onde séries específicas de produtos da progênie são preparadas em cada um de vários vasos de reação. Isto permite que seja realizado um procedimento de exame sistemático e triagem. Portanto, estes métodos permitem que um número potencialmente muito grande de moléculas da progênie sejam examinados sistematicamente em grupos menores. Devido a esta capacidade para realizar quimerizações em uma maneira que é altamente flexível mas exaustiva e sistemática também, particularmente quando há um baixo nível de homologia entre as moléculas progenitoras, estes métodos provêm a geração de uma biblioteca (ou série) consistindo em um grande número de moléculas da progênie. Devido à natureza não-estocástica da remontagem de ligação da presente invenção, as moléculas da progênie produzidas em um aspecto compreendem uma biblioteca de moléculas de ácidos nucleicos quiméricos finalizados tendo uma ordem de montagem glogal que é escolhida por design. Os métodos de mutagênese de saturação e de evolução dirigida otimizada também podem ser usados para gerar diferentes espécies moleculares da progênie. É reconhecido que a invenção proporciona liberdade de escolha e controle com referência à seleção de pontos de demarcação, o tamanho e número dos blocos de construção de ácido nucleico, e o tamanho e design das ligações. É reconhecido, além disso, que o requisito para homologia intermolecular é altamente relaxado para a operabilidade desta invenção. De fato, pontos de demarcação podem mesmo ser escolhidos em áreas de pouca ou nenhuma homologia intermolecular. Por exemplo, devido ao balanço de códons, isto é, a degeneração de códons, substituições de nucleotídeos podem ser introduzidas em blocos de construção de ácido nucleico sem alterar o aminoácido originalmente codificado no molde progenitor correspondente. Alternativamente, um códon pode ser alterado de tal modo que a codificação para um aminoácido originalmente seja alterada. Esta invenção proporciona que similares substituições possam ser introduzidas no bloco de construção de ácido nucleico de modo a aumentar a incidência de pontos de demarcação homóloga intermolecular e deste modo permitir que seja obtido um maior número de ligações entre os blocos de construção, o qual por sua vez permite que seja gerado um número maior de moléculas quiméricas da progênie.
[000669] Em um aspecto, a presente invenção proporciona um método não-estocástico denominado remontagem genética sintética, que é um tanto relacionado com embaralhamento estocástico, excetuando que os blocos de construção de ácido nucleico não são embaralhados ou concatenados ou quimerizados aleatoriamente, mas ao invés são reunidos não-estocasticamente.
[000670] O método de remontagem genética sintética não depende da presença de um alto nível de homologia entre polinucleotídeos a serem embaralhados. A invenção pode ser usada para produzir não- estocasticamente bibliotecas (ou séries) de moléculas da progênie consistindo em mais de 10100 quimeras diferentes. Concebivelmente, a remontagem genética sintética pode mesmo ser usada para gerar bibliotecas consistindo em mais 101000 quimeras de progênies diferentes.
[000671] Portanto, em um aspecto, a invenção proporciona um método não-estocástico para produzir uma série de moléculas de ácido nucleico quiméricos finalizados tendo uma ordem de montagem global que é escolhido por design, cujo método consiste nas etapas de gerar por design uma pluralidade de blocos de construção de ácido nucleico específicos tendo extremidades ligáveis mutuamente compatíveis úteis e montando estes blocos de construção de ácido nucleico, de tal modo que seja obtida uma ordem de montagem global designada.
[000672] As extremidades ligáveis mutuamente compatíveis dos blocos de construção de ácido nucleico a serem reunidas são consideradas como sendo “úteis” para este tipo de montagem ordenada se permitirem que os blocos de construção sejam acoplados em ordens predeterminadas. Portanto, em um aspecto, a ordem de montagem global na qual os blocos de construção de ácido nucleico podem ser acoplados é especificada pelo design das extremidades ligáveis e, se mais de uma etapa de montagem tiver de ser usada, então a ordem de montagem global na qual os blocos de construção de ácido nucleico podem ser acoplados também é especificada pela ordem sequencial da uma ou mais etapas de montagem. Em um aspecto da invenção, as peças de construção recozidas são tratadas com uma enzima, tal como uma ligase (por exemplo, T4 DNA ligase) para obter ligação covalente das peças de construção.
[000673] Em um outro aspecto, o design dos blocos de construção de ácido nucleico é obtido por análise das sequências de uma série de moldes de ácidos nucleicos progenitores que servem como uma base para produzir uma série de progênies de moléculas de ácidos nucleicos quiméricos finalizados. Estes moldes de ácidos nucleicos progenitores portanto servem como uma fonte de informação de sequência que auxilia no design dos blocos de construção de ácido nucleico que devem ser mutagenizados, isto é, quimerizados ou embaralhados.
[000674] Em um exemplo, a invenção proporciona a quimerização de uma família de genes relacionados e sua família codificada de produtos relacionados. Em um exemplo particular, os produtos codificados são enzimas. As glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da presente invenção podem ser mutagenizadas de acordo com os métodos descritos aqui, neste pedido de patente.
[000675] Portanto de acordo com um aspecto da invenção, as sequências de uma pluralidade de moldes de ácidos nucleicos progenitores (por exemplo, polinucleotídeos da invenção) são alinhadas de modo a selecionar um ou mais pontos de demarcação, cujos pontos de demarcação podem estar localizados em uma área de homologia. Os pontos de demarcação podem ser usados para delinear os limites dos blocos de construção de ácido nucleico a serem gerados. Portanto, os pontos de demarcação identificados e selecionados nas moléculas progenitoras servem como pontos de quimerização potenciais na montagem das moléculas da progênie.
[000676] Um ponto de demarcação útila pode ser uma área de homologia (consistindo em pelo menos uma base de nucleotídeo homólogo) partilhada por pelo menos dois moldes progenitores, mas o ponto de demarcação pode ser uma área de homologia que é partilhada por pelo menos metade dos moldes progenitores, pelo menos dois terços dos moldes progenitores, pelo menos três quartos dos moldes progenitores e em um aspecto quase todos os moldes progenitores. Ainda mais em um aspecto ainda um ponto de demarcação útila é uma área de homologia que é partilhada por todos os moldes progenitores.
[000677] Em um aspecto, o processo de remontagem genética é realizado exaustivamente de modo a gerar uma biblioteca completa. Em outras palavras, todas as combinações ordenadas possíveis dos blocos de construção de ácido nucleico são representadas na série de moléculas de ácidos nucleicos quiméricos finalizados. Ao mesmo tempo, a ordem de montagem (isto é, a ordem de montagem de cada bloco de construção na sequência 5’ para 3’ de cada ácido nucleico quimérico finalizado) em cada combinação é por design (ou não- estocástica). Devido à natureza não-estocástica do método, a possibilidade de produtos colaterais indesejados é muito reduzida.
[000678] Em outro aspecto, o método proporciona que o processo de remontagem genética seja realizado sistematicamente, por exemplo, para gerar uma biblioteca sistematicamente compartimentalizada, com compartimentos que podem ser triados sistematicamente, por exemplo, um a um. Em outras palavras, a invenção proporciona que, através do uso seletivo e criterioso de blocos de construção de ácido nucleico específicos, junto com o uso seletivo e criterioso de reações de montagem sequencialmente em etapas, possa ser obtido um design experimental onde séries específicas de produtos da progênie são fabricados em cada um de vários vasos de reação. Isto permite que seja realizado um exame sistemático e procedimento de triagem. Portanto, permite que um número potentialmente muito grande de moléculas da progênie seja examinado sistematicamente em grupos menores.
[000679] Devido a sua capacidade para realizar quimerizações em uma maneira que é altamente flexível e exaustiva e sistemática também, particularmente quando há um baixo nível de homologia entre as moléculas progenitoras, a presente invenção proporciona a geração de uma biblioteca (ou série) consistindo em um grande número de moléculas da progênie. Devido à natureza não-estocástica da presente remontagem genética da invenção, as moléculas da progênie geradas em um aspecto compreendem uma biblioteca de moléculas de ácidos nucleicos quiméricos finalizados tendo uma ordem de montagem global que é escolhida por design. Em um aspecto particular, uma biblioteca gerada semelhante consiste em mais de 103 a mais de 101000 espécies moleculares de progênies diferentes.
[000680] Em um aspecto, uma série de moléculas de ácidos nucleicos quiméricos finalizados, produzida conforme descrito consiste em um polinucleotídeo codificando um polipeptídeo. De acordo com um aspecto, este polinucleotídeo é um gene, o qual pode ser um gene sintético. De acordo com outro aspecto, este polinucleotídeo é um caminho genético, o qual pode ser um caminho genético sintético. A invenção proporciona que um ou mais genes sintéticos gerados pela invenção podem ser incorporados em um caminho genético sintético, tal como caminho operável em um organismo eucariótico (incluindo uma planta).
[000681] Em outro exemplo, a natureza sintética da etapa na qual os blocos de construção são gerados permite o design e a introdução de nucleotídeos (por exemplo, um ou mais nucleotídeos, os quais podem ser, por exemplo, códons ou íntrons ou sequências regulatórias) que podem posteriormente ser opcionalmente removidos em um processo in vitro (por exemplo, por mutagênese) ou em um processo in vivo (por exemplo, utilizando a capacidade de junção genética de um organismo hospedeiro). É reconhecido que em muitos casos a introdução destes nucleotídeos também pode ser desejável por muitas outras razões além do benefício potencial de criar um ponto de demarcação útil.
[000682] Portanto, de acordo com outro aspecto, a invenção proporciona que um bloco de construção de ácido nucleico possa ser usado para introduzir um íntron. Portanto, a invenção proporciona que íntrons funcionais possam ser introduzidos em um gene sintético da invenção. A invenção também proporciona que íntrons funcionais possam ser introduzidos em um caminho genético sintético da invenção. Por conseguinte, a invenção proporciona a geração de um polinucleotídeo quimérico que é um gene sintético contendo um (ou mais) íntron(s) artificialmente introduzido(s).
[000683] Por conseguinte, a invenção também proporciona a geração de um polinucleotídeo quimérico que é um caminho genético sintético contendo um (ou mais) íntron(s) artificialmente introduzido(s). Em um aspecto, os íntrons artificialmente introduzidos são funcionais em uma ou mais células hospedeiras para união genética muito no modo em que íntrons que ocorrem naturalmente servem funcionalmente em união genética. A invenção proporciona um processo para produzir polinucleotídeos contendo íntrons sintéticos a serem introduzidos em organismos hospedeiros para recombinação e/ou união.
[000684] Um gene sintético produzido usando a invenção também pode servir como um substrato para recombinação com outro ácido nucleico. Do mesmo modo, um caminho genético sintético produzido usando a invenção também pode servir como um substrato para recombinação com outro ácido nucleico. Em um aspecto, a recombinação é facilitada por, ou ocorre em, áreas de homologia entre o gene contendo íntrons sintéticos e um ácido nucleico, o qual serve como um parceiro de recombinação. Em um aspecto, o parceiro de recombinação também pode ser um ácido nucleico gerado pela invenção, incluindo um gene sintético ou um caminho genético sintético. A recombinação pode ser facilitada por ou pode ocorrer em áreas de homologia que existem no um (ou mais) íntron(s) artificialmente introduzido(s) no gene sintético.
[000685] O método de remontagem genética sintética da invenção utiliza uma pluralidade de blocos de construção de ácido nucleico, cada um dos quais em um aspecto tem duas extremidades ligáveis. As duas extremidades ligáveis em cada bloco de construção de ácido nucleico pode ser duas extremidades cegas (isto é, cada uma tendo um ressalto de zero nucleotídeo), ou em um aspecto uma extremidade cega e um ressalto, ou mais em um aspecto ainda dois ressaltos.
[000686] Um ressalto útila para esta finalidade pode ser um ressalto 3’ ou um ressalto 5’. Portanto, um bloco de construção de ácido nucleico pode ter um ressalto 3’ ou alternativamente um ressalto 5’ ou alternativamente dois ressaltos 3’ ou alternativamente dois ressaltos 5’. A ordem global na qual os blocos de construção de ácido nucleico são montados para formar uma molécula de ácido nucleico quimérico finalizado é determinada por design propositadamente experimental e não é aleatória.
[000687] Em um aspecto, um bloco de construção de ácido nucleico é gerado por síntese química de dois ácidos nucleicos de fita única (também referidos como oligos de fita única) e contatando os mesmos de modo a permitir que eles anelem para formar um bloco de construção de ácido nucleico de fita dupla.
[000688] Um bloco de construção de ácido nucleico de fita dupla pode ser de tamanho variável. Os tamanhos destes blocos de construção podem ser pequenos ou grandes. Tamanhos típicos para bloco de construção variam de 1 par de bases (não incluindo quaisquer ressaltos) a 100.000 pares de bases (não incluindo quaisquer ressaltos). Outras faixas de tamanhos exemplares também são proporcionadas, as quais têm limites inferiores a partir de 1 pb até 10.000 pb (incluindo cada valor inteiro no intervalo) e limites superiores de a partir de 2 pb até 100. 000 pb (incluindo cada valor inteiro no intervalo).
[000689] Existem muitos métodos pelos quais pode ser gerado um bloco de construção de ácido nucleico de fita dupla que é útila para a invenção; e estes são conhecidos na técnica e podem ser prontamente realizados pelo técnico versado.
[000690] De acordo com um aspecto, um bloco de construção de ácido nucleico de fita dupla é gerado primeiro gerando dois ácidos nucleicos de fita única e permitindo que os mesmos anelem para formar um bloco de construção de ácido nucleico de fita dupla. As duas fitas de um bloco de construção de ácido nucleico de fita dupla podem ser complementares em cada nucleotídeo à parte de qualquer um que forme um ressalto; portanto não contendo combinações inadequadas, à parte de qualquer ou quaisquer ressaltos. De acordo com outro aspecto, as duas fitas de um bloco de construção de ácido nucleico de fita dupla são complementares em menos do que cada nucleotídeo à parte de qualquer um que forme um ressalto. Portanto, de acordo com estes aspectos, um bloco de construção de ácido nucleico de fita dupla pode ser usado para introduzir degeneração de códon. Em um aspecto, a degeneração de códon é introduzida usando a mutagênese de saturação de sítio descrita aqui, neste pedido de patente, usando um ou mais cassetes N,N,G/T ou alternativamente usando um ou mais cassetes N,N,N.
[000691] O método de recombinação in vivo da invenção pode ser realizado às cegas sobre um grupo de híbridos desconhecidos ou alelos de um polinucleotídeo ou sequência específicos. No entanto, não é necessário conhecer a sequência real de DNA ou RNA do polinucleotídeo específico.
[000692] A abordagem de usar recombinação dentro de uma população mista de genes pode ser útila para a geração de quaisquer proteínas úteis, por exemplo, interleucina I, anticorpos, tPA e hormônio do crecimento. Esta abordagem pode ser usada para gerar proteínas tendo especificidade ou atividade alterada. A abordagem também pode ser útila para a geração de sequências híbridas de ácido nucleico, por exemplo, regiões promotoras, íntrons, éxons, sequências de reforçador, regiões 31 não-traduzidas ou regiões 51 não-traduzidas de genes. Portanto esta abordagem pode ser usada para gerar genes tendo taxas de expressão aumentadas. Esta abordagem também pode ser útila no estudo de sequências de DNA repetitivas. Finalmente, esta abordagem pode ser útila para mutar ribozimas ou aptâmeros.
[000693] Em um aspecto, a invenção descrita aqui, neste pedido de patente, é dirigida ao uso de ciclos repetidos de reagrupamento redutivo, recombinação e seleção os quais possibilitam a evolução molecular dirigida de sequências lineares altamente complexas, tais como DNA, RNA ou proteínas através de recombinação.
Sistema de Evolução Dirigida Otimizada
[000694] A invenção proporciona um sistema de modificação genética não-estocástica denominado “sistema de evolução dirigida otimizada” para gerar polipeptídeos, por exemplo, glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases ou anticorpos da invenção, com propriedades novas ou alteradas. Evolução dirigida otimizada é dirigida ao uso de ciclos repetidos de reagrupamento redutivo, recombinação e seleção que possibilitam a evolução molecular dirigida de ácidos nucleicos através de recombinação. A evolução dirigida otimizada permite a geração de uma grande população de sequências quiméricas originadas, em que a população gerada é significativamente enriquecida para sequências que têm um número predeterminado de eventos de permutação genética entre cromossomas.
[000695] Um evento de permutação genética entre cromossomas é um ponto em uma sequência quimérica onde ocorre uma modificação na sequência de uma variante parental para outra variante parental. Um referido ponto é normalmente na junção de onde oligonucleotídeos de duas matrizes são ligados juntos para formar uma única sequência. Este método possibilita o cálculo das concentrações corretas de sequências de oligonucleotídeo de modo que a população quimérica final de sequências seja enriquecida para o número escolhido de eventos de permutação genética entre cromossomas. Isto proporciona mais controle sobre a escolha de variantes quiméricas tendo um número predeterminado de eventos de permutação genética entre cromossomas.
[000696] Além disso, este método proporciona um meio conveniente para explorar uma quantidade enorme do possível espaço de variantes de proteínas em comparação com outros sistemas. Previamente, caso se gere, por exemplo, 1013 moléculas quiméricas durante uma reação, seria extremamente difícila testar um tal alto número de variantes quiméricas para uma atividade particular. Além disso, uma porção significativa da população da progênie teria um número muito elevado de eventos de permutação genética entre cromossomas os quais resultaram em proteínas que tinham menos probabilidade de ter níveis aumentados de uma atividade particular. Usando estes métodos, a população de moléculas quiméricas pode ser enriquecida para as variantes que têm um número particular de eventos de permutação genética entre cromossomas. Portanto, embora ainda se possa gerar 1013 moléculas quiméricas durante uma reação, cada uma das moléculas escolhidas para análise posterior mais provavelmente tem, por exemplo, somente três eventos de permutação genética entre cromossomas. Como a população da progênie resultante pode ser desviada para ter um número predeterminado de eventos de permutação genética entre cromossomas, os limites sobre a variedade funcional entre as moléculas quiméricas são reduzidos. Isto proporciona um número mais exequível de variáveis ao calcular qual oligonucleotídeo dos polinucleotídeos parentais originais pode ser responsável por afetar um traço em particular.
[000697] Um método para criar uma sequência de polinucleotídeo da progênie quimérica é criar oligonucleotídeos correspondentes a fragmentos ou porções de cada sequência parental. Cada oligonucleotídeo em um aspecto inclui uma única região de sobreposição de modo que misturando os oligonucleotídeos juntos resulta em uma nova variante que tem cada fragmento de oligonucleotídeo montado na ordem correta. Alternativamente protocolos para praticar estes métodos da invenção podem ser encontrados nas Patentes dos Estados Unidos Nos. 6.773.900; 6.740.506; 6.713.282; 6.635.449; 6.605.449; 6.537.776; 6.361.974.
[000698] O número de oligonucleotídeos gerados para cada variante parental tem uma relação com o número total de permutações genéticas entre cromossomas resultantes na molécula quimérica que é essencialmente criada. Por exemplo, três sequências de nucleotídeos variantes parentais podem ser proporcionadas para serem submetidas a uma reação de ligação de modo a descobrir uma variante quimérica tendo, por exemplo, maior atividade em temperatura elevada. Como um exemplo, uma série de sequências de 50 oligonucleotídeos pode ser gerada correspondendo a cada uma das porções de cada variante parental. Por conseguinte, durante o processo de remontagem de ligação pode haver até 50 eventos de permutação genética entre cromossomas dentro de cada uma das sequências quiméricas. A probabilidade de que cada um dos polinucleotídeos quiméricos gerados venha a conter oligonucleotídeos de cada variante parental em ordem alternada é muito baixa. Se cada fragmento de oligonucleotídeo estiver presente na reação de ligação na mesma quantidade molar é provável que em algumas posições oligonucleotídeos do mesmo polinucleotídeo parental venham a ligar próximos um ao outro e portanto não resultem em um evento de permutação genética entre cromossomas. Se a concentração de cada oligonucleotídeo de cada matriz for mantida constante durante qualquer etapa de ligação neste exemplo, há uma chance de 1/3 (presumindo 3 matrizes) de que um oligonucleotídeo da mesma variante parental venha a ligar dentro da sequência quimérica e não produzir permutação genética entre cromossomas.
[000699] Por conseguinte, uma função de densidade de probabilidade (PDF) pode ser determinada para prever a população de eventos de permutação genética entre cromossomas que é provável de ocorrer durane cada etapa em uma reação de ligação dado um número determinado de variantes parentais, um número de oligonucleotídeos correspondente a cada variante, e as concentrações de cada variante durante cada etapa na reação de ligação. A estatística e a matemática por trás da determinação da PDF é descrita abaixo. Utilizando estes métodos, pode-se calcular uma referida função de densidade de probabilidade, e portanto enriquecer a população da progênie quimérica para um número predeterminado de eventos de permutação genética entre cromossomas resultantes de uma reação de ligação em particular. Além disso, um número-alvo de eventos de permutação genética entre cromossomas pode ser predeterminado, e o sistema então programado para calcular as quantidades de partida de cada oligonucleotídeo parental durante cada etapa na reação de ligação para resultar em uma função de densidade de probabilidade que centra sobre o número predeterminado de eventos de permutação genética entre cromossomas. Estes métodos são dirigidos ao uso de ciclos repetidos de reagrupamento redutivo, recombinação e seleção que permitem a evolução molecular dirigida de um ácido nucleico codificando um polipeptídeo através de recombinação. Este sistema permite a geração de uma grande população de sequências quiméricas originadas, em que a população gerada é significativamente enriquecida para sequências que têm um número predeterminado de eventos de permutação genética entre cromossomas. Um evento de permutação genética entre cromossomas é um ponto em uma sequência quimérica onde ocorre uma modificação na sequência de uma variante parental para outra variante parental. Um referido ponto é normalmente na junção de onde oligonucleotídeos de duas matrizes são ligados juntos para formar uma única sequência. O método permite o cálculo das concentrações corretas de sequências de oligonucleotídeo de modo que a população quimérica final de sequências seja enriquecida para o número escolhido de eventos de permutação genética entre cromossomas. Isto proporciona mais controle sobre a escolha de variantes quiméricas tendo um número predeterminado de eventos de permutação genética entre cromossomas.
[000700] Além disso, estes métodos proporcionam um meio conveniente para explorar uma enorme quantidade do espaço de variantes de proteínas possíveis em comparação com outros sistemas. Usando os métodos descritos aqui, neste pedido de patente, a população de moléculas quiméricas pode ser enriquecida para as variantes que têm um número particular de eventos de permutação genética entre cromossomas. Portanto, embora ainda se possa gerar 1013 moléculas quiméricas durante uma reação, cada uma das moléculas escolhidas para análise posterior mais provavelmente tem, por exemplo, somente três eventos de permutação genética entre cromossomas. Como a população da progênie resultante pode ser desviada para ter um número predeterminado de eventos de permutação genética entre cromossomas, os limites sobre a variedade funcional entre as moléculas quiméricas são reduzidos. Isto proporciona um número mais exequível de variáveis ao calcular qual oligonucleotídeo dos polinucleotídeos parentais originais podem ser responsáveis por afetar um traço em particular.
[000701] Em um aspecto, o método cria uma sequência de polinucleotídeo da progênie quimérica criando oligonucleotídeos correspondentes a fragmentos ou porções de cada sequência parental. Cada oligonucleotídeo em um aspecto inclui uma única região de sobreposição de modo que misturando os oligonucleotídeos juntos resulta em uma nova variante que tem cada fragmento de oligonucleotídeo montado na ordem correta. Vide também as Patentes dos Estados Unidos Nos. 6.537.776; 6.605.449.
Determinação de Eventos de Permutação Genética entre Cromossomas
[000702] Aspectos da invenção incluem um sistema e um software que recebem uma função de densidade de probabilidade (PDF) da permutação genética entre cromossomas desejada, o número de genes parentais a serem remontados, e o número de fragmentos na remontagem como entrada. A saída deste programa é um “PDF de fragmentos” que pode ser usado para determinar uma receita para produzir genes remontados, e o PDF da permutação genética entre cromossomas estimada destes genes. O processamento descrito aqui, neste pedido de patente, [e em um aspecto realizado em MATLAB® (The Mathworks, Natick, Massachusetts) uma linguagem de programação e ambiente de desenvolvimento para computação técnica.
Processos Iterativos
[000703] Ao praticar a invenção, estes processos podem ser repetidos iterativamente. Por exemplo, um ácido nucleico (ou, o ácido nucleico) responsável por um fenótipo alterado ou novo de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase é identificado, reisolado, novamente modificado, retestado para atividade. Este processo pode ser repetido iterativamente até ser produzido um fenótipo desejado. Por exemplo, um caminho bioquímico anabólico ou catabólico inteiro pode ser produzido em uma célula, incluindo, por exemplo, atividade de glucanase, mananase, ou xilanase.
[000704] Similarmente, se for determinado que um oligonucleotídeo particular não tem efeito de modo algum sobre o traço desejado (por exemplo, um fenótipo novo de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase), pode ser removido como uma variável sintetizando maiores oligonucleotídeos parentais que incluem a sequência a ser removida. Como a incorporação da sequência dentro de uma sequência maior evita quaisquer eventos de permutação genética entre cromossomas, não haverá mais qualquer variação desta sequência nos polinucleotídeos da progênie. Esta prática iterativa de determinar quais oligonucleotídeos são mais relacionados com o traço desejado, e quais são não relacionados, possibilita exploração mais eficaz de todas as variantes de proteínas possíveis que podem proporcionar um traço ou atividade particular.
Embaralhamento in vivo
[000705] Embaralhamento in vivo de moléculas é uso nos métodos da invenção que proporcionam variantes de polipeptídeos da invenção, por exemplo, anticorpos, glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases e similares. Embaralhamento in vivo pode ser realizado utilizando a propriedade natural das células para recombinar multímeros. Apesar da recombinação in vivo ter proporiconado a principal via natural para diversidade molecular, a recombinação genética permanece um processo relativamente complexo que envolve 1) o reconhecimento de homologias; 2) clivagem de fita, invasão de fita, e etapas metabólicas levando à produção de quiasma recombinante; e finalmente 3) a resolução do quiasma em moléculas recombinadas distintas. A formação do quiasma requer o reconhecimento de sequências homólogas.
[000706] Em outro aspecto, a invenção inclui um método para produzir um polinucleotídeo híbrido a partir de pelo menos um primeiro polinucleotídeo e um segundo polinucleotídeo. A invenção pode ser usada para produzir um polinucleotídeo híbrido introduzindo pelo menos um primeiro polinucleotídeo e um segundo polinucleotídeo os quais partilham pelo menos uma região de homologia de sequência parcial (por exemplo, SEQ ID NOS: 1, 3, 5, 7, 9, 11, 13, 15, 17, 19, 21, 23, 25, 27, 29, 31, 33, 35, 37, 39, 41, 43, 45 , 47, 49, 51, 53, 55, 57, 59, 61, 63, 65, 67, 69, 71, 73, 75, 77, 79, 81, 83, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105, 107, 109, 111, 113, 115, 117, 119, 121, 123, 125, 127, 129, 131, 133, 135, 137, 139, 141, 143, 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 191, 193, 195, 197, 199, 201, 203, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223, 225, 227, 229, 231, 233, 235, 237, 239, 241, 243, 245, 247, 249, 251, 253, 255, 257 e combinações das mesmas) em uma célula hospedeira adequada. As regiões de homologia de sequência parcial promovem processos os quais resultam em reorganização de sequência produzindo um polinucleotídeo híbrido. O termo “polinucleotídeo híbrido”, conforme usado aqui, neste pedido de patente, é qualquer sequência de nucleotídeos a qual resulta do método da presente invenção e contém sequência de pelo menos duas sequências de polinucleotídeos originais. Os referidos polinucleotídeos híbridos podem resultar em eventos de recombinação intermolecular os quais promovem integração de sequência entre moléculas de DNA. Além disso, os referidos polinucleotídeos híbridos podem resultar de processos de reagrupamento redutivo intramolecular os quais utilizam sequências repetidas para alterar uma sequência de nucleotídeos dentro de uma molécula de DNA.
[000707] Reagrupamento in vivo é focalizado em processos “intermoleculares” referidos coletivamente como “recombinação” a qual em bactérias, é geralmente vista como um fenômeno “RecA- dependente”. A invenção pode se basear em processos de recombinação de uma célula hospedeira para recombinar e reagrupar sequências, ou na capacidade das células para mediar processos redutivos para reduzir a complexidade de sequências quase-repetidas na célula por eliminação. Este processo de “reagrupamento redutivo” ocorre por um processo “intramolecular”, RecA-independente.
[000708] Portanto, em outro aspecto da invenção, novos polinucleotídeos podem ser gerados pelo processo de reagrupamento redutivo. O método envolve a geração de construtos contendo sequências consecutivas (sequências codificantes originais), sua inserção em um vetor apropriado e sua introdução subsequente em uma célula hospedeira apropriada. O reagrupamento das identidades moleculares individuais ocorre por processos combinatoriais entre as sequências consecutivas nas regiões de homologia possuindo construto, ou entre unidades quase-repetidas. O processo de reagrupamento recombina e/ou reduz a complexidade e a extensão das sequências repetidas e resulta na produção de novas espécies moleculares. Vários tratamentos podem ser aplicados para reforçar a taxa de reagrupamento. Estes podem incluir tratamento com luz ultravioleta, ou produtos químicos de dano de DNA e/ou o uso de linhagens de células hospedeiras apresentando níveis aumentados de “instabilidade genética”. Portanto o processo de reagrupamento pode envolver recombinação homóloga ou a propriedade natural de sequências quase-repetidas para dirigir sua própria evolução.
[000709] Sequências repetidas ou “quase-repetidas” têm um papel na instabilidade genética. Na presente invenção, “quase-repetições” são repetições que não estão restritas a sua estrutura da unidade original. Unidades quase-repetidas podem ser apresentadas como uma série de sequências em um construto; unidades consecutivas de sequências similares. Uma vez ligadas, as junções entre as sequências consecutivas se tornam essencialmente invisíveis e a natureza quase-repetitiva do construto resultante é agora contínua no nível molecular. O processo de eliminação que a célula realiza para reduzir a complexidade do construto resultante opera entre as sequências quase-repetidas. As unidades quase-repetidas proporcionam um repertório praticamente ilimitado de moldes nos quais podem ocorrer eventos de deslizamento. Os construtos contendo as quase-repetições portanto proporcionam de modo eficaz elasticidade molecular suficiente tal que podem ocorrer eventos de eliminação (e potencialmente inserção) virtualmente em qualquer parte dentro das unidades quase-repetitivas.
[000710] Quando as sequências quase-repetidas são todas ligadas na mesma orientação, por exemplo, cabeça à cauda ou vice-versa, a célula não pode distinguir unidades individuais. Consequentemente, o processo redutivo pode ocorrer por todas as sequências. Em contraste, quando, por exemplo, as unidades são apresentadas cabeça a cabeça, ao invés de cabeça à cauda, a inversão delineia os desfechos da unidade adjacente de modo que a formação de eliminação favorecerá a perda de unidades distintas. Portanto, é preferêncial com o presente método que as sequências estejam na mesma orientação. A orientação aleatória de sequências quase- repetidas resultará na perda da eficiência do reagrupamento, ao passo que a orientação consistente das sequências oferecerá a maior eficiência. No entanto, apesar de ter menos das sequências contíguas na mesma orientação reduz a eficiência, ainda pode proporcionar suficiente elasticidade para a recuperação eficaz de novas moléculas. Construtos podem ser fabricados com as sequências quase-repetidas na mesma orientação para permitir maior eficiência.
[000711] Sequências podem ser montadas em uma orientação cabeça a cauda usando qualquer um de uma variedade de métodos, incluindo os seguintes: a) Podem ser utilizados iniciadores que incluem uma cabeça poli-A e cauda poli-T os quais quando preparados de fita única proporcionariam orientação. Isto é, realizado tendo as primeiras poucas bases dos iniciadores preparadas a partir de RNA e portanto facilmente removida RNaseH. b) Podem ser utilizados iniciadores que incluem sítios de clivagem de única restrição. Seriam necessários múltiplos sítios, uma bateria de sequências únicas e etapas de síntese repetida e de ligação. c) A poucas bases internas do iniciador podem ser tioladas e uma exonuclease usada para produzir moléculas de cauda adequadas.
[000712] A recuperação das sequências reagrupadas se baseia na identificação de vetores de clonagem com um índice repetitivo reduzido (RI). As sequências codificantes reagrupadas podem ser então recuperadas por amplificação. Os produtos são reclonados e expressados. A recuperação de vetores de clonagem com RI reduzido podem ser afetados por: 1) O uso de vetores somente estavelmente mantidos quando o construto é de complexidade reduzida. 2) A recuperação física de vetores encurtados por procedimentos físicos. Neste caso, o vetor de clonagem seria recuperado usando procedimentos de isolamento de plasmídeos de rotina e fracionado por tamanho sobre ou um gel agarose, ou coluna com um corte de baixo peso molecular utilizando procedimentos de rotina. 3) A recuperação de vetores contendo genes interrompidos os quais podem ser selecionados quando diminui o tamanho do inserto. 4) O uso de técnicas de seleção direta com um vetor de expressão e a seleção apropriada.
[000713] Sequências codificantes (por exemplo, genes) de organismos relacionados podem demonstrar um alto grau de homologia e codificar produtos de proteínas bastante diversas. Estes tipos de sequências são particularmente úteis na presente invenção como quase-repetições. No entanto, apesar dos exemplos ilustrados abaixo demonstrarem o reagrupamento de sequências codificantes originais quase idênticas (quase-repetições), este processo não é limitado a referidas repetições quase idênticas.
[000714] O exemplo seguinte demonstra um método da invenção. São descritas sequências codificantes de ácido nucleico (quase- repetições) derivadas de três (3) espécies únicas. Cada sequência codifica uma proteína com uma série de propriedades distintas. Cada uma das sequências difere por um único ou uns poucos pares de bases em uma única posição na sequência. As sequências quase- repetidas são separadamente ou coletivamente amplificadas e ligadas em montagens aleatórias de tal modo que todas as permutações e combinações possíveis estejam disponíveis na população de moléculas ligadas. O número de unidades de quase-repetições pode ser controlado pelas condições da montagem. O número médio de unidades quase-repetidas em um construto é definido como o índice repetitivo (RI).
[000715] Uma vez formados, os construtos podem, ou não podem ser fracionados por tamanho sobre um gel agarose de acordo com protocolos publicados, inseridos em um vetor de clonagem e transfectados em uma célula hospedeira apropriada. As células são então propagadas e é realizado “reagrupamento redutivo”. A taxa do processo de reagrupamento redutivo pode ser estimulada pela introdução de dano de DNA caso desejado. Se a redução no RI for mediada por formação de eliminação entre sequências repetidas por um mecanismo “intramolecular”, ou mediada por eventos semelhantes à recombinação através de mecanismos “intermoleculares” é irrelevante. O resultado final é um reagrupamento das moléculas em todas as combinações possíveis.
[000716] Opcionalmente, o método compreende a etapa adicional de triar os membros da biblioteca do grupo embaralhado para identificar membros embaralhados de bibliotecas individuais tendo a capacidade de ligar ou de modo diverso interagir, ou catalisar uma reação particular (por exemplo, tal como domínio catalítico de uma enzima) com uma macromolécula predeterminada, tal como por exemplo, um receptor proteináceo, um oligossacarídeo, vírion, ou outro composto ou estrutura predeterminados.
[000717] Os polipeptídeos que são identificados a partir de referidas bibliotecas podem ser usados para fins terapêuticos, de diagnóstico, de pesquisa e relacionados (por exemplo, catalisadores, solutos para aumentar a osmolaridade de uma solução aquosa e similares) e/ou podem ser submetidos a um ou mais ciclos adicionais de embaralhamento e/ou seleção.
[000718] Em outro aspecto, é previsto que antes ou durante recombinação ou reagrupamento, polinucleotídeos gerados pelo método da invenção podem ser submetidos a agentes ou processos os quais promovem a introdução de mutações nos polinucleotídeos originais. A introdução de referidas mutações aumentaria a diversidade de polinucleotídeos híbridos resultantes e polipeptídeos codificados a partir dos mesmos. Os agentes ou processos os quais promovem mutagênese podem incluir, mas não estão limitados a: (+)-CC-1065, ou um análogo sintético tal como (+)-CC-1065-(N3-Adenina (Vide Sun and Hurley, (1992); um aduto 4'-flúor-4-aminobifenila N-acetilado ou desacetilado capaz de inibir a síntese de DNA (Vide, por exemplo, van de Poll et al. (1992)); ou um aduto 4-aminobifenila N-acetilado ou desacetilado capaz de inibir a síntese de DNA (Vide também, van de Poll et al. (1992), pp. 751-758); cromo trivalente, um sal de cromo trivalente, um aduto de DNA de hidrocarboneto aromático policíclico (PAH) capaz de inibir replicação de DNA, tal como 7-bromometil- benz[a]antraceno (“BMA”), tris(2,3-dibromopropil)fosfato (“Tris-PB”), 1,2-dibromo-3-cloropropano (“DBCP”), 2-bromoacroleína (2BA), benzo[a]pireno-7,8-di-hidrodiol-9-10-epóxido (“BPDE”), um sal de halogênio de platina(II), N-hidróxi-2-amino-3-metilimidazo[4,5-f]- quinolina (“N-hidróxi-IQ”) e N-hidróxi-2-amino-1-metil-6- fenilimidazo[4,5-f]-piridina (“N-hidróxi-PhIP”). Meios exemplares para tornar mais lenta ou interromper a amplificação por PCR consistem em luz UV (+)-CC-1065 e (+)-CC-1065-(N3-Adenina). Meios particularmente englobados são aductos de DNA ou polinucleotídeos compreendendo os aductos de DNA dos polinucleotídeos ou grupo de polinucleotídeos, os quais podem ser liberados ou removidos por um processo incluindo aquecimento da solução compreendendo os polinucleotídeos antes de processamento posterior.
[000719] Em outro aspecto, a invenção é dirigida a um método para produzir proteínas recombinantes tendo atividade biológica tratando uma amostra compreendendo polinucleotídeos molde de fita dupla codificando uma proteína selvagem sob condições de acordo com a invenção as quais proporcionam a produção de polinucleotídeos híbridos ou reagrupados.
Produzindo variantes de sequências
[000720] A invenção também proporciona métodos adicionais para fabricar variantes de sequências do ácido nucleico (por exemplo, sequências de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) da invenção, incluindo as sequências exemplares da invenção. A invenção também proporciona métodos adicionais para isolar glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases usando os ácidos nucleicos e polipeptídeos da invenção. Em sequência codificante (por exemplo, um gene, cDNA ou mensageiro) (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção, a qual pode ser alterada por quaisquer meios, incluindo, por exemplo, métodos aleatórios ou estocásticos, ou, não-estocásticos, ou métodos de “evolução dirigida,” conforme descrito acima.
[000721] As variantes isoladas podem ocorrer naturalmente. Variantes também podem ser criadas in vitro. Variantes podem ser criadas usando técnicas de engenharia genética tais como mutagênese sítio dirigida, mutagênese química aleatória, procedimentos de eliminação de Exonuclease III, e técnicas de clonagem de rotina. Alternativamente, referidas variantes, fragmentos, análogos, ou derivados podem ser criados usando procedimentos de síntese química ou de modificação. Outros métodos para produzir variantes também são familiares daqueles versados na técnica. Estes incluem procedimentos nos quais sequências de ácido nucleico obtidas de isolados naturais são modificadas para gerar ácidos nucleicos os quais codificam polipeptídeos tendo características as quais reforçam seu valor em aplicações industriais, agrícolas, de pesquisa e medicinais. Nos referidos procedimentos, um grande número de sequências variantes tendo uma ou mais diferenças de nucleotídeos com respeito à sequência obtida do isolado natural são geradas e caracterizadas. Estas diferenças de nucleotídeos podem resultar em alterações de aminoácido com respeito aos polipeptídeos codificados pelos ácidos nucleicos dos isolados naturais.
[000722] Por exemplo, variantes podem ser criadas usando PCR propenso a erro. Em PCR propenso a erro, é realizado PCR sob condições onde a fidelidade de cópia da DNA polimerase é baixa, de tal modo que uma alta taxa de mutações de pontos seja obtida ao longo de toda a extensão do produto de PCR. PCR propenso a erro é descrito, por exemplo, em Leung, D.W., et al., Technique, 1:11-15, 1989) e Caldwell, R. C. & Joyce G.F., PCR Methods Applic., 2:28-33, 1992. Em resumo, nos referidos procedimentos, ácidos nucleicos a serem mutagenizados são misturados com iniciadores de PCR, tampão de reação, MgCl2, MnCl2, Taq polimerase e uma concentração apropriada de dNTPs para obter uma alta taxa de mutação de ponto ao longo de toda a extensão do produto de PCR. Por exemplo, a reação pode ser realizada usando 20 fmols de ácido nucleico a ser mutagenizado, 30 pmols de cada iniciador de PCR, um tampão da reação compreendendo 50 mM de KCl, 10 mM de Tris HCl (pH 8,3) e 0,01% de gelatina, 7 mM de MgCl2, 0,5 mM de MnCl2, 5 unidades de Taq polimerase, 0,2 mM de dGTP, 0,2 mM de dATP, 1 mM de dCTP, e 1 mM de dTTP. PCR pode ser realizado por 30 ciclos de 94°C por 1 min, 45°C por 1 min, e 72°C por 1 min. No entanto, será reconhecido que estes parâmetros podem ser variados conforme apropriado. Os ácidos nucleicos mutagenizados são clonados em um vetor apropriado e as atividades dos polipeptídeos codificados pelos ácidos nucleicos mutagenizados são avaliadas.
[000723] Variantes também podem ser criadas usando mutagênese dirigida por oligonucleotídeos para gerar mutações sítio-específicas em qualquer DNA clonado de interesse. Mutagênese de oligonucleotídeos é descrita, por exemplo, em Reidhaar-Olson (1988) Science 241:53-57. Em resumo, os referidos procedimentos de uma pluralidade de oligonucleotídeos de fita dupla portando uma ou mais mutações a serem introduzidas no DNA clonado são sintetizadas e inseridas no DNA clonado a ser mutagenizado. Clones contendo o DNA mutagenizado são recuperados e as atividades dos polipeptídeos que codificam são avaliadas.
[000724] Outro método para gerar variantes é PCR de montagem. PCR de montagem envolve a montagem de um produto de PCR a partir de uma mistura de pequenos fragmentos de DNA. Um grande número de diferentes reações de PCR ocorrem em paralelo no mesmo frasco, com os produtos de uma reação preparando os produtos de outra reação. PCR de montagem é descrito, por exemplo, na Patente dos Estados Unidos No. 5.965.408.
[000725] Ainda outro método para gerar variantes é mutagênese sexual por PCR. Na mutagênese sexual por PCR, ocorre recombinação de homólogos forçada entre moléculas de DNA de sequência de DNA diferente mas altamente relacionada in vitro, em consequência de fragmentação aleatória da molécula de DNA com base em homologia de sequência, seguida por fixação da permutação genética entre cromossomas por extensão de iniciadores em uma reação de PCR. Mutagênese sexual por PCR é descrita, por exemplo, em Stemmer (1994) Proc. Natl. Acad. Sci. USA 91:10747-10751. Em resumo, os referidos procedimentos de uma pluralidade de ácidos nucleicos a serem recombinados são digeridos com DNase para gerar fragmentos tendo um tamanho médio de 50 a 200 nucleotídeos. Fragmentos do tamanho médio desejado são purificados e ressuspendidos em uma mistura de PCR. PCR é conduzido sob condições as quais facilitam recombinação entre os fragmentos de ácido nucleico. Por exemplo, PCR pode ser realizado ressuspendendo os fragmentos purificados em uma concentração de 10 a 30 ng/μl em uma solução de 0,2 mM de cada dNTP, 2,2 mM de MgCl2, 50 mM de KCL, 10 mM de Tris HCl, pH 9,0, e 0,1% Triton X-100. 2,5 unidades de Taq polimerase por 100:1 de mistura da reação é adicionado e é realizado PCR usando o seguinte regime: 94°C por 60 segundos, 94°C por 30 segundos, 50 a 55°C por 30 segundos, 72°C por 30 segundos (30 a 45 vezes) e 72°C por 5 minutos. No entanto, será reconhecido que estes parâmetros podem ser variados conforme apropriado. Em alguns aspectos, oligonucleotídeos podem ser incluídos nas reações de PCR. Em outros aspectos, o fragmento de Klenow da DNA polimerase I pode ser usado em uma primeira série de reações de PCR e Taq polimerase pode ser usada em uma série subsequente de reações de PCR. Sequências recombinantes são isoladas e as atividades dos polipeptídeos que codificam são avaliadas.
[000726] Variantes também podem ser criadas por mutagênese in vivo. Em alguns aspectos, mutações aleatórias em uma sequência de interesse são geradsa propagando a sequência de interesse em uma cepa bacteriana, tal como uma cepa de E. coli, a qual carrega mutações em um ou mais dos caminhos de reparo de DNA. As referidas cepas “mutadoras” têm uma maior taxa de mutações aleatórias do que as de uma matriz selvagem. Propagando o DNA em uma destas cepas eventualmente gerará mutações aleatórias dentro do DNA. Cepas mutadoras adequadas para uso para mutagênese in vivo são descritas na publicação de patente internacional PCT No. WO 91/16427, publicada em 31 de outubro de 1991, intitulada “Methods for Phenotype Creation from Multiple Gene Populations”.
[000727] Variantes também podem ser geradas usando mutagênese de cassete. Na mutagênese de cassete, uma pequena região de uma molécula de DNA de fita dupla é substituída com um “cassete” de oligonucleotídeo sintético que difere da sequência nativa. O oligonucleotídeo frequentemente contém sequência nativa completamente e/ou parcialmente randomizada.
[000728] Mutagênese de conjunto recursiva também pode ser usada para gerar variantes. Mutagênese de conjunto recursiva é um algoritmo para engenharia de proteína (mutagênese de proteína) desenvolvida para produzir populações diversas de mutantes fenotipicamente relacionados cujos membros diferem na sequência de aminoácidos. Este método usa um mecanismo de feedback para controlar rodadas sucessivas de mutagênese de cassete combinatorial. Mutagênese de conjunto recursiva é descrita em Arkin, A.P. and Youvan, D.C., PNAS, USA, 89:7811-7815, 1992.
[000729] Em alguns aspectos, variantes são criadas usando mutagênese de conjunto exponencial. Mutagênese de conjunto exponencial é um processo para gerar bibliotecas combinatoriais com uma alta percentagem de mutantes únicos e funcionais, em que grupos pequenos de resíduos são randomizados em paralelo para identificar, em cada posição alterada, aminoácidos os quais levam a proteínas funcionais. Mutagênese de conjunto exponencial é descrita em Delegrave, S. and Youvan, D.C., Biotechnology Research, 11:1548-1552, 1993. Mutagênese aleatória e sítio-dirigida são descritas em Arnold, F.H., Current Opinion in Biotechnology, 4:450455, 1993.
[000730] Em alguns aspectos, as variantes são criadas usando procedimentos de embaralhamento em que porções de uma pluralidade de ácidos nucleicos as quais codificam polipeptídeos distintos são fundidas juntas para criar sequências quiméricas de ácido nucleico as quais codificam polipeptídeos quiméricos conforme descrito na Patente dos Estados Unidos No. 5.965.408, depositada em 9 de julho de 1996, intitulada, “Method of DNA Reassembly by Interrupting Synthesis” e na Patente dos Estados Unidos No. 5.939.250, depositada em 22 de maio de 1996, intitulada, “Production of Enzymes Having Desired Activities by Mutagenesis”.
[000731] As variantes dos polipeptídeos da invenção podem ser variantes nas quais um ou mais dos resíduos aminoácidos dos polipeptídeos das sequências da invenção são substituídos com um resíduo de aminoácido conservado ou não-conservado (em um aspecto um resíduo de aminoácido conservado) e o resíduo de aminoácido substituído pode ser ou não um codificado pelo código genético.
[000732] A invenção proporciona modalidades alternativas dos polipeptídeos da invenção (e os ácidos nucleicos que codificam os mesmos) compreendendo pelo menos uma substituição de aminoácido conservadora, conforme discutido aqui, neste pedido de patente, (por exemplo, substituições de aminoácidos conservativas são aquelas que substituem um dado aminoácido em um polipeptídeo por outro aminoácido de características semelhantes). A invenção proporciona polipeptídeos (e os ácidos nucleicos que codificam os mesmos) em que qualquer um, alguns ou todos os resíduos aminoácidos são substituídos por outro aminoácido de características semelhantes, por exemplo, uma substituição de aminoácido conservadora.
[000733] Substituições conservadoras são aquelas que substituem um dado aminoácido em um polipeptídeo por outro aminoácido de características semelhantes. Substituições conservadoras da invenção podem compreender qualquer uma das seguintes substituições: um aminoácido alifático tal como Alanina, Valina, Leucina e Isoleucina com outro aminoácido alifático; substituição de uma Serina com uma Treonina ou vice-versa; substituição de um resíduo acídico tais como Ácido aspártico e Ácido glutâmico com outro resíduo acídico; substituição de um resíduo portando um grupo amida, tal como Asparagina e Glutamina, com outro resíduo portando um grupo amida; permuta de um resíduo básico tal como Lisina e Arginina com outro resíduo básico; e substituição de um resíduo aromático tal como Fenilalanina, Tirosina com outro resíduo aromático. Em aspectos alternativos, estas substituições conservativas também podem ser equivalentes sintéticos destes aminoácidos.
[000734] Em aspectos alternativos, variantes são aquelas nas quais um ou mais dos resíduos aminoácido de um polipeptídeo da invenção compreendem um grupo substituinte. Em aspectos alternativos, variantes compreendem polipeptídeos associados com outro composto, tal como um composto para aumentar a meia-vida do polipeptídeo (por exemplo, polietileno glicol). Variantes adicionais são aquelas nas quais aminoácidos adicionais são fundidos ao polipeptídeo, tais como uma sequência líder, uma sequência secretória, uma sequência de proproteína ou uma sequência o qual facilita purificação, enriquecimento, ou estabilização do polipeptídeo.
[000735] Em alguns aspectos, os fragmentos, derivados e análogos retêm a mesma atividade ou função biológica que os polipeptídeos da invenção. Em outros aspectos, o fragmento, derivado, ou análogo inclui uma proproteína, tal que o fragmento, derivado, ou análogo possa ser ativado por clivagem da porção de proproteína para produzir um polipeptídeo ativo.
Otimização de códons para obter altos níveis de expressão de proteína em células hospedeiras
[000736] A invenção proporciona métodos para modificar ácidos nucleicos codificando glucanase, mananase, ou xilanase para modificar o uso de códons. Em um aspecto, a invenção proporciona métodos para modificar códons em um ácido nucleico codificando uma glucanase para aumentar ou reduzir sua expressão em uma célula hospedeira. A invenção também proporciona ácidos nucleicos codificando uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta glucosidase modificada para aumentar sua expressão em uma célula hospedeira, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase modificada deste modo, e métodos para produzir a glucanase modificada (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. O método compreende identificar um códon “não-preferêncial” ou um “menos preferêncial” em ácido nucleico codificando glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase e substituindo um ou mais destes códons não- preferênciais ou menos preferênciais com um “códon preferêncial” codificando o mesmo aminoácido que o códon substituído e pelo menos um códon não- preferêncial ou menos preferêncial no ácido nucleico foi substituído por um códon preferêncial codificando o mesmo aminoácido. Um códon preferêncial é um códon super- representado em sequências codificantes em genes na célula hospedeira e um códon não- preferêncial ou menos preferêncial é um códon sub-representado em sequências codificantes em genes na célula hospedeira.
[000737] Células hospedeiras para expressar os ácidos nucleicos, cassetes de expressão e vetores da invenção incluem bactérias, levedura, fungos, células de plantas, células de inseto e células de mamífero. Portanto, a invenção proporciona métodos para otimizar uso de códons em todas estas células, ácidos nucleicos com códons- alterados e polipeptídeos fabricados pelos ácidos nucleicos com códons-alterados. Células hospedeiras típicas incluem bactérias Gram-negativas, tais como Escherichia coli; bactérias Gram-positivas, tais como Streptomyces, Lactobacillus gasseri, Lactococcus lactis, Lactococcus cremoris, Bacillus sp., Bacillus subtilis, Bacillus cereus. Células hospedeiras típicas também incluem organismos eucarióticos, por exemplo, várias leveduras, tais como Saccharomyces sp., incluindo Saccharomyces cerevisiae, Schizosaccharomyces pombe, Pichia pastoris, e Kluyveromyces lactis, Hansenula polymorpha, Aspergillus niger, e células e linhagens celulares de mamífero e células e linhagens celulares de inseto. Portanto, a invenção também inclui ácidos nucleicos e polipeptídeos otimizados para expressão nestes organismos e espécies, por exemplo, os ácidos nucleicos da invenção são códons-otimizados para expressão em uma célula hospedeira, por exemplo, Pichia sp., por exemplo, P. pastoris, Saccharomyces sp., ou Bacillus sp., Streptomyces sp., e similares.
[000738] Por exemplo, os códons de um ácido nucleico codificando um polipeptídeo da invenção, por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, ou uma enzima similar isolada de uma célula bacteriana, são modificados de tal modo que o ácido nucleico (codificando a enzima) seja otimamente expressado em uma célula bacteriana diferente das bactérias das quais a enzima (por exemplo, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase) foi derivada, uma levedura, alguns fungos, uma célula de planta, uma célula de inseto ou uma célula de mamífero. Métodos para otimizar códons são de conhecimento geral na técnica, vide, por exemplo, a Patente dos Estados Unidos No. 5.795.737; Baca (2000) Int. J. Parasitol. 30:113118; Hale (1998) Protein Expr. Purif. 12:185-188; Narum (2001) Infect. Immun. 69:7250-7253. Vide também Narum (2001) Infect. Immun. 69:7250-7253, descrevendo otimização de códons em sistemas de camundongo; Outchkourov (2002) Protein Expr. Purif. 24:18-24, descrevendo otimização de códons em levedura; Feng (2000) Biochemistry 39:15399-15409, descrevendo otimização de códons em E. coli; Humphreys (2000) Protein Expr. Purif. 20:252-264, descrevendo otimização de uso de códons que afeta a secreção em E. coli; Gao (2004) Biotechnol Prog. 20:443-448, descrevendo “UpGene”, uma aplicação de um algoritmo de otimização de códons de DNA baseado na web.
Animais transgênicos não-humanos
[000739] A invenção proporciona animais transgênicos não-humanos compreendendo um ácido nucleico, um polipeptídeo (por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase), um cassete de expressão ou vetor ou uma célula transfectada ou transformada da invenção. A invenção também proporciona métodos para produzir e usar estes animais transgênicos não-humanos.
[000740] Os animais transgênicos não-humanos podem ser, por exemplo, cabras, coelhos, ovelha, porcos, vacas, ratos e camundongos, compreendendo os ácidos nucleicos da invenção. Estes animais podem ser usados, por exemplo, como moldes in vivo para estudar a atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, ou, como moldes para triagem para agentes que alteram a atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase in vivo. As sequências codificantes para os polipeptídeos a serem expressados nos animais transgênicos não-humanos podem ser designados para serem constitutivos, ou, sob o controle de fatores regulatórios transcricionais tecido-específicos, desenvolvimento- específicos ou indutíveis. Animais transgênicos não-humanos podem ser designados e gerados usando qualquer método conhecido na técnica; vide, por exemplo, as Patentes dos Estados Unidos Nos. 6.211.428; 6.187.992; 6.156.952; 6.118.044; 6.111.166; 6.107.541; 5.959.171; 5.922.854; 5.892.070; 5.880.327; 5.891.698; 5.639.940; 5.573.933; 5.387.742; 5.087.571, descrevendo a fabricação e o uso de células transformadas e ovos e camundongos, ratos, coelhos, ovelha, porcos e cabras transgênicos. Vide também, por exemplo, Pollock (1999) J. Immunol. Methods 231:147-157, descrevendo a produção de proteínas recombinantes no leite de animais transgênicos da indústria de laticínios; Baguisi (1999) Nat. Biotechnol. 17:456-461, demonstrando a produção de cabras transgênicas. A Patente dos Estados Unidos No. 6.211.428 descreve fabricação e uso de mamíferos não-humanos transgênicos os quais expressam em seus cérebros um construto de ácido nucleico compreendendo uma sequência de DNA. A Patente dos Estados Unidos No. 5.387.742 descreve injetar sequências de DNA recombinantes clonadas ou sintéticas em ovos de camundongo fertilizados, implantando os ovos injetados em fêmeas pseudográvidas, e cultivar até o termo camundongos transgênicos cujas células expressam proteínas relacionadas com a patologia da doença de Alzheimer. A Patente dos Estados Unidos No. 6.187.992 descreve fabricação e uso de um camundongo transgênico cujo genoma compreende uma disrupção do gene codificando proteína precursora amilóide (APP).
[000741] “Animais de nocaute” também podem ser usados para praticar os métodos da invenção. Por exemplo, em um aspecto, os animais transgênicos ou modificados da invenção compreendem um “animal de nocaute,” por exemplo, um “camundongo de nocaute,” produzido para não expressar um gene endógeno, o qual é substituído com um gene expressando uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção, ou, uma proteína de fusão compreendendo uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção.
Plantas e Sementes Transgênicas
[000742] A invenção proporciona plantas e sementes transgênicas compreendendo um ácido nucleico, um polipeptídeo (por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase), um cassete de expressão ou vetor ou uma célula transfectada ou transformada da invenção. A invenção também proporciona produtos de plantas, por exemplo, óleos, sementes, folhas, extratos e similares, compreendendo um ácido nucleico e/ou um polipeptídeo (por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) da invenção. A planta transgênica pode ser dicotiledônea (um dicot) ou monocotiledônea (um monocot). A invenção proporciona plantas transgênicas com um sabor modificado, teor de sólidos e/ou textura, em que a modificação é gerada expressando pelo menos uma enzima da invenção quer constitutivamente ou seletivamente na planta transgênica (ou semente, ou fruto, e etc.), conforme descrito, por exemplo, no Pedido de Patente dos Estados Unidos No. 2006/0195940.
[000743] A invenção também proporciona métodos para produzir e usar estas plantas e sementes transgênicas. A planta transgênica ou célula de planta expressando um polipeptídeo da presente invenção pode ser construída de acordo com qualquer método conhecido na técnica. Vide, por exemplo, a Patente dos Estados Unidos No. 6.309.872.
[000744] Ácidos nucleicos e construtos de expressão da invenção podem ser introduzidos em uma célula de planta por quaisquer meios. O termo “introduzir” no contexto de um polinucleotídeo, por exemplo, um construto de nucleotídeo de interesse, pretende indicar apresentar à planta o polinucleotídeo de tal modo que o polinucleotídeo ganhe acesso ao interior de uma célula da planta. Onde mais de um polinucleotídeo deve ser introduzido, estes polinucleotídeos podem ser reunidos como parte de um único construto de nucleotídeo, ou como construtos de nucleotídeo separados, e podem estar localizados sobre os mesmos vetores de transformação ou sobre vetores de transformação diferentes. Por conseguinte, estes polinucleotídeos podem ser introduzidos na célula hospedeira de interesse em um único evento de transformação, em eventos de transformação separados, ou, por exemplo, em plantas, como parte de um protocolo de reprodução. Os métodos da invenção não dependem de um método particular para introduzir um ou mais polinucleotídeos em uma planta, somente que o um ou mais polinucleotídeos ganha acesso ao interior de pelo menos uma célula da planta. Métodos para introduzir polinucleotídeos em plantas são conhecidos na técnica incluindo, mas não limitados a, métodos de transformação transitória, métodos de transformação estável, e métodos mediados por vírus.
[000745] “Transformação transitória” no contexto de um polinucleotídeo pretende indicar que um polinucleotídeo é introduzido na planta e não integra no genoma da planta.
[000746] Por “introduzir estavelmente” ou “introduzido estavelmente” no contexto de um polinucleotídeo introduzido em uma planta se pretende que o polinucleotídeo introduzido seja estavelmente incorporado no genoma da planta, e deste modo a planta é estavelmente transformada com o polinucleotídeo.
[000747] “Transformação estável” ou “estavelmente transformado” pretende indicar que um polinucleotídeo, por exemplo, um construto de nucleotídeo descrito aqui, neste pedido de patente, introduzido em uma planta se integra no genoma da planta e é capaz de ser herdado pela progênie da mesma, mais particularmente, pela progênie de múltiplas gerações sucessivas. A introdução no genoma de uma planta desejada pode ser tal que a enzima é regulada por elementos controle transcricionais ou translacionais endógenos. Técnicas de transformação para tanto monocotiledôneas quanto dicotiledôneas são de conhecimento geral na técnica.
[000748] Os ácidos nucleicos da invenção podem ser usados para conferir traços desejados sobre essencialmente qualquer planta. Ácidos nucleicos da invenção podem ser usados para manipular caminhos metabólicos de uma planta de modo a otimizar ou alterar expressão de hospedeiros de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Podem alterar atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase em uma planta. Alternativamente, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção pode ser usada na produção de uma planta transgênica para produzir um composto não produzido naturalmente por aquela planta. Isto pode reduzir os custos de produção ou criar um novo produto. Em uma modalidade, a enzima da invenção pode ser expressada de tal modo que a enzima não entre em contato com seu substrato até ser desejado. Por exemplo, uma enzima da invenção pode ser direcionada e retida no retículo endoplasmático de uma célula de planta. Retenção da enzima, no retículo endoplasmático da célula, evitará que a enzima entrará em contato com seu substrato. A enzima e o substrato podem ser então trazidos em contato através de quaisquer meios capazes de romper a arquitetura subcelular, tal como, trituração, moagem, aquecimento, e similares. Vide, a patente WO 98/11235, a patente WO 2003/18766, e a patente WO 2005/096704, todas as quais são por este incorporadas por meio de referência.
[000749] Genes marcadores selecionáveis podem ser adicionados ao construto genético de modo a identificar células ou tecidos de plantas que tenham integrado o transgene com sucesso. Isto pode ser necessário porque obter incorporação e expressão de genes em células de plantas é um evento raro, ocorrendo somente em uma pequena percentagem dos tecidos ou células-alvo. Genes marcadores selecionáveis codificam proteínas que proporcionam resistência a agentes que são normalmente tóxicos às plantas, tais como antibióticos ou herbicidas. Somente células de plantas que têm integrado o gene marcador selecionável sobreviverão quando cultivadas sobre um meio contendo o antibiótico ou herbicida apropriado. Marcadores de seleção usados rotineiramente em transformação, e que podem ser usados para praticar esta invenção, incluem o gene nptll, o qual confere resistência à canamicina e antibióticos relacionados (Messing & Vierra. Gene 19: 259-268 (1982); Bevan et. al., Nature 304:184-187 (1983)), o gene bar, o qual confere resistência ao herbicida fosfinotricina (White et. al., Nucl. Acids Res 18: 1062 (1990), Spencer et. al. Theor. Appl. Genet 79: 625-631 (1990)), o gene hph, o qual confere resistência ao antibiótico higromicina (Blochinger & Diggelmann, Mol Cell Biol 4: 2929-2931), o gene dhfr, o qual confere resistência ao metatrexato (Bourouis et. al., EMBO J. 2(7): 1099-1104 (1983)), Gene EPSPS, o qual confere resistência ao glifosato (Patente dos Estados Unidos Nos. 4.940.935 e 5.188.642).
[000750] Alternativamente, material vegetal transgênico pode ser identificado através de um sistema de seleção positivo, tal como, o sistema utilizando o gene manose-6-fosfato isomerase, o qual proporciona a capacidade de metabolizar manose (Patente dos Estados unidos Nos. 5.767.378 e 5.994.629).
[000751] Em um aspecto, produzir plantas ou sementes transgênicas compreende incorporar sequências da invenção e, opcionalmente, genes marcadores em um construto de expressão alvo (por exemplo, um plasmídeo), junto com posicionamento das sequências de promotor e terminador. Isto pode envolver transferir o gene modificado para dentro da planta através de um método adequado. Uma ou mais das sequências da invenção podem ser combinadas com sequências que conferem resistência a inseto, doença, estiagem, aumento da produção, melhoram a qualidade nutricional do grão, aumentam a produção de etanol e similares.
[000752] Por exemplo, um construto pode ser introduzido diretamente dentro do DNA genômico da célula da planta usando técnicas tais como eletroporação e microinjeção de protoplastos de células da planta, ou os construtos podem ser introduzidos diretamente no tecido da planta usando métodos balísticos, tais como bombardeamento de partículas de DNA. Por exemplo, vide, por exemplo, Christou (1997) Plant Mol. Biol. 35:197-203; Pawlowski (1996) Mol. Biotechnol. 6:17-30; Klein (1987) Nature 327:70-73; Takumi (1997) Genes Genet. Syst. 72:63-69, discutindo o uso de bombardeamento de partículas para introduzir transgenes em trigo; e Adam (1997) supra, para uso de bombardeamento de partículas para introduzir YACs em células de plantas. Por exemplo, Rinehart (1997) supra, usou bombardeamento de partículas para gerar plantas de algodão transgênicas. Equipamento para acelerar partículas é descrito na Patente dos Estados Unidos No. 5.015.580; e, o instrumento de aceleração de partículas BioRad (Biolistics) PDS-2000 disponível comercialmente; vide também, John, Patente dos Estados Unidos No. 5.608.148; e Ellis, Patente dos Estados Unidos No. 5.681.730, descrevendo transformação de gimnospermas mediada por partículas.
[000753] Em um aspecto, protoplastos podem ser imobilizados e injetados com alguns ácidos nucleicos, por exemplo, um construto de expressão. Embora a regeneração da planta a partir dos protoplastos não seja fácila com cereais, a regeneração da planta é possível em legumes usando embriogênese somática de calo derivado de protoplastos. Tecidos organizados podem ser transformados com DNA nu usando técnica de pistola de genes, onde o DNA é revestido sobre microprojéteis de tungstênio, disparado 1/100o. o tamanho das células, os quais carregam o DNA profundo dentro de células e organelas. O tecido transformado é em seguida induzido a regenerar, geralmente por embriogênese somática. Esta técnica tem tido sucesso em várias espécies de cereais incluindo milho e arroz.
[000754] Ácidos nucleicos, por exemplo, construtos de expressão, também podem ser introduzidos em células de plantas usando vírus recombinantes. Células de plantas podem ser transformadas usando vetores virais, tais como, por exemplo, vetores derivados do vírus do mosaico do tabaco (Rouwendal (1997) Plant Mol. Biol. 33:989-999), vide Porta (1996) “Use of viral replicons for the expression of genes in plants”, Mol. Biotechnol. 5:209-221.
[000755] Alternativamente, ácidos nucleicos, por exemplo, um construto de expressão, podem ser combinados com regiões flanqueantes de T-DNA adequadas e introduzidos em um vetor hospedeiro de Agrobacterium tumefaciens convencional. As funções de virulência do hospedeiro de Agrobacterium tumefaciens orientarão a inserção do construto e do marcador adjacente dentro do DNA da célula de planta quando a célula é infectada pelas bactérias. Técnicas de transformação mediada por Agrobacterium tumefaciens, incluindo desarme e uso de vetores binários, são descritas de modo geral na literatura científica. Vide, por exemplo, Horsch (1984) Science 233:496-498; Fraley (1983) Proc. Natl. Acad. Sci. USA 80:4803 (1983); Gene Transfer to Plants, Potrykus, ed. (Springerlag, Berlin 1995). O DNA em uma célula de A. tumefaciens está contido no cromossoma bacteriano bem como em outra estrutura conhecida como um plasmídeo Ti (indutor de tumor). O plasmídeo Ti contém um trecho de DNA denominado T-DNA (~20 kb de extensão) que é transferido para a célula de planta no processo de infecção e uma série de genes vir (virulência) que dirigem o processo de infecção. A. tumefaciens pode infectar somente uma planta através de ferimentos: quando a raiz ou caule de uma planta é ferido emite alguns sinais químicos, em resposta aos quais, os genes vir de A. tumefaciens se tornam ativados e dirigem uma série de eventos necessários para a transferência do T- DNA a partir do plasmídeo Ti para o cromossoma da planta. O T-DNA então penetra na célula de planta através do ferimento. Uma especulação é que o T-DNA espera até o DNA da planta estar sendo replicado ou transcrito, então se insere dentro do DNA da planta exposta. De modo a usar A. tumefaciens como um vetor de transgene, a seção de T-DNA indutor de tumor tem de ser removida, ao mesmo tempo que retendo as regiões da borda do T-DNA e os genes vir. O transgene é então inserido entre as regiões da borda do T-DNA, onde é transferido para a célula da planta e se torna integrado nos cromossomas da planta.
[000756] A invenção proporciona a transformação de plantas monocotiledôneas usando os ácidos nucleicos da invenção, incluindo importantes cereais, vide Hiei (1997) Plant Mol. Biol. 35:205-218. Vide também, por exemplo, Horsch, Science (1984) 233:496; Fraley (1983) Proc. Natl. Acad. Sci USA 80:4803; Thykjaer (1997) supra; Park (1996) Plant Mol. Biol. 32:1135-1148, discutindo a integração de T-DNA em DNA genômico. Vide também D'Halluin, Patente dos Estados Unidos No. 5.712.135, descrevendo um processo para a integração estável de um DNA compreendendo um gene que é funcional em uma célula de um cereal, ou outra planta monocotiledônea.
[000757] Em um aspecto, a terceira etapa pode envolver seleção e regeneração de plantas inteiras capazes de transmitir o gene-alvo incorporado à generação seguinte. As técnicas de regeneração referidas se baseiam em manipulação de alguns fitormônios em um meio de crescimento de cultura de tecido, tipicamente se baseando em um marcador biocida e/ou herbicida que foi introduzido junto com as sequências de nucleotídeos desejadas. A regeneração de plantas a partir de protoplastos cultivados é descrita em Evans et al., Protoplasts Isolation and Culture, Handbook of Plant Cell Culture, pp. 124-176, MacMillilan Publishing Company, New York, 1983; e Binding, Regeneration of Plants, Plant Protoplasts, pp. 21-73, CRC Press, Boca Raton, 1985. Regeneração também pode ser obtida a partir de calo de plantas, explantes, órgãos, ou partes das mesmas. As técnicas de regeneração referidas são descritas de modo geral em Klee (1987) Ann. Rev. of Plant Phys. 38:467-486. Para obter plantas inteiras a partir de tecidos transgênicos tais como embriões imaturos, elas podem ser cultivadas sob condições ambientais controladas em uma série de meios contendo nutrientes e hormônios, um processo conhecido como cultura de tecido. Uma vez que as plantas inteiras são geradas e produzem semente, se inicia a avaliação da progênie.
[000758] Depois do cassete de expressão ser estavelmente incorporado em plantas transgênicas, pode ser introduzido em outras plantas por cruzamento sexual. Pode ser usada qualquer uma de uma série de técnicas de reprodução de rotina, dependendo da espécie a ser cruzada. Vide, por exemplo, Welsh J. R., Fundamentals of Plant Genetics and Breeding, John Wiley & Sons, NY (1981); Crop Breeding, Wood D. R. (Ed.) American Society of Agronomy Madison, Wis. (1983); Mayo O., The Theory of Plant Breeding, Second Edition, Clarendon Press, Oxford (1987); Singh, D. P., Breeding for Resistance to Diseases and Insect Pests, Springer-Verlag, NY (1986); e Wricke e Weber, Quantitative Genetics and Selection Plant Breeding, Walter de Gruyter and Co., Berlin (1986).
[000759] Como a expressão transgênica dos ácidos nucleicos da invenção leva a alterações fenotípicas, plantas compreendendo os ácidos nucleicos recombinantes da invenção podem ser cruzadas sexualmente com uma segunda planta para obter um produto final. Deste modo, a semente da invenção pode ser derivada de um cruzamento entre duas plantas transgênicas da invenção, ou um cruzamento entre uma planta da invenção e outra planta. Os efeitos desejados (por exemplo, expressão dos polipeptídeos da invenção para produzir uma planta na qual o comportamento de floração é alterado) podem ser reforçados quando ambas as plantas parentais expressam os polipeptídeos (por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) da invenção. Os efeitos desejados podem ser passados para gerações de plantas futuras por meios de propagação de rotina.
[000760] Qualquer planta pode ser usada para introdução do nucleotídeo de interesse, incluindo, mas não limitada a, milho ou milho (Zea mays), Brassica sp. (por exemplo, B. napus, B. rapa, B. juncea), particularmente as espécies Brassica úteis como fontes de óleo de semente, tais como canola, alfafa (Medicago sativa), arroz (Oryza sativa), centeio (Secale cereale), sorgo (Sorghum bicolor, Sorghum vulgare), milheto (por exemplo, pearl millet (Pennisetum glaucum), proso millet (Panicum miliaceum), foxtaila millet (Setaria italica), finger millet (Eleusine coracana)), girassol (Helianthus annuus), açafrão (Carthamus tinctorius), trigo (Triticum aestivum), soja (Glycine max), tabaco (Nicotiana tabacum), batata (Solanum tuberosum), amendoins (Arachis hypogaea), algodão (Gossypium barbadense, Gossypium hirsutum), batata-doce (Ipomoea batatus), mandioca (Manihot esculenta), café (Cofea spp.), coco (Cocos nucifera), abacaxi (Ananas comosus), árvores de cítricos (Citrus spp.), cacau (Theobroma cacao), chá (Camellia sinensis), banana (Musa spp.), abacate (Persea americana), figo (Ficus casica), goiaba (Psidium guajava), manga (Mangifera indica), oliva (Olea europaea), mamão papaia (Carica papaia), cajueiro (Anacardium occidentale), macadâmia (Macadamia integrifolia), amêndoa (Prunus amygdalus), beterrabas açucareiras (Beta vulgaris), cana-de-açúcar (Saccharum spp.), aveia, cevada, legumes, ornamentais, e coníferas.
[000761] Legumes podem incluir tomates (Lycopersicon esculentum), alface (por exemplo, Lactuca sativa), feijões verdes (Phaseolus vulgaris), feijões-de-lima (Phaseolus limensis), ervilhas (Lathyrus spp.), e membros do gênero Cucumis tais como pepino (C. sativus), cantalupo (C. cantalupensis), e melão almiscarado (C. melo). Ornamentais podem incluir azaléia (Rhododendron spp.), hortênsia (Macrophylla hydrangea), hibisco (Hibiscus rosasanensis), rosas (Rosa spp.), tulipas (Tulipa spp.), narcisos (Narcissus spp.), petúnias (Petunia hybrida), cravo (Dianthus caryophyllus), poinsétia (Euphorbia pulcherrima), cana (Cannaceae spp.) e crisântemo. Coníferas que podem ser empregadas, incluindo, por exemplo, pinheiros tais como espécie de pinheiro teda (Pinus taeda), slash pine (Pinus elliotii), ponderosa pine (Pinus ponderosa), lodgepole pine (Pinus contorta), e pinheiro de Monterey (Pinus radiata), Douglas-fir (Pseudotsuga menziesii); cicuta ocidental (Tsuga canadensis); Sitka spruce (Picea glauca); sequóia canadense (Sequoia sempervirens); abetos verdadeiros tais como silver fir (Abies amabilis) e abeto balsâmico (Abies balsamea); e cedros tais como cedro-vermelho ocidental (Thuja plicata) e cedro amarelo do Alasca (Chamaecyparis nootkatensis). Plantas leguminosas podem incluir, mas não estão limitadas a, feijões e ervilhas. Feijões podem incluir guar, alfarroba, feno-grego, soja, garden beans, feijão-de-corda, mungbean, feijão-de-lima, feijão fava, lentilhas, grão-de-bico, e etc. Legumes podem incluir, mas não estão limitados a, Arachis, por exemplo, amendoins, Vicia, por exemplo, ervilhaca de coroa, ervilhaca peluda, feijão azuki, mung bean, e grão- de-bico, Lupinus, por exemplo, tremoceiro, trifólio, Phaseolus, por exemplo, feijão comum e feijão-de-lima, Pisum, por exemplo, feijão branco, Melilotus, por exemplo, trevo, Medicago, por exemplo, alfafa, Lotus, por exemplo, trevo, lens, por exemplo, lentilha, e falso indigueiro. Forragem e gramíneas de turfa podem incluir alfafa, switchgrass (Panicum virgatum), Miscanthus, capim de pomar (orchard grass), erva-carneira, azevém perene, agróstea rasteira, e capim- panasco.
[000762] Plantas de particular interesse podem incluir plantas de colheitas e plantas usadas para produzir energia ou combustível, por exemplo, milho, alfafa, girassol, Brassica, soja, algodão, açafrão, amendoim, sorgo, trigo, aveia, centeio, milheto, cevada, arroz, coníferas, graíneas, por exemplo, switchgrass e Miscanthus, colheitas de legumes, por exemplo, ervilha, feijão e soja, tubérculos/raízes amiláceos, por exemplo, batata, batata-doce, mandioca, inhame, cana e beterraba açucareira e similares.
[000763] Em modalidades alternativas, os ácidos nucleicos da invenção são expressados em plantas as quais contêm células de fibra, incluindo, por exemplo, algodão, seda, algodoeiro (Kapok, Ceiba pentandra), salgueiro do deserto, creosote bush, winterfat, pau-de- balsa, rami, kenaf, cânhamo, roselle, juta, sisal abacá e linho. Em modalidades alternativas, as plantas transgênicas da invenção podem ser membros do gênero Gossypium, incluindo membros de qualquer espécie Gossypium, tal como G. arboreum;. G. herbaceum, G. barbadense, e G. hirsutum.
[000764] A invenção também proporciona plantas transgênicas a serem usadas para produzir grandes quantidades dos polipeptídeos (por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase ou anticorpo) da invenção. Por exemplo, vide Palmgren (1997) Trends Genet. 13:348; Chong (1997) Transgenic Res. 6:289-296 (produzindo proteína beta-caseína de leite humano em plantas de batatas transgênicas usando um promotor de manopina sintase bidirecional (mas1',2'), induzível por auxina, com métodos de transformação de disco de folha mediados por Agrobacterium tumefaciens).
[000765] Usando procedimentos conhecidos, uma pessoa versada pode fazer triagem de plantas da invenção detectando o aumento ou a redução de proteína ou mRNA de transgenes em plantas transgênicas. Os meios para detecção e quantificação de mRNAs ou proteínas são de conhecimento geral na técnica.
Polipeptídeos e peptídeos
[000766] Em um aspecto, a invenção proporciona polipeptídeos isolados, sintéticos ou recombinantes e peptídeos tendo uma identidade de sequência (por exemplo, pelo menos cerca de 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, ou mais, ou identidade de sequência completa (100%)) com uma sequência exemplar da invenção, por exemplo, proteínas tendo a sequência de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, E SEQ ID NO: 23, e as modificações específicas para SEQ ID NO: 2 conforme descrito aqui, neste pedido de patente. Sequências de polipeptídeos ou peptídeos exemplares da invenção incluem SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, E SEQ ID NO: 23, subsequências das mesmas e variantes das mesmas, em que em um aspecto sequências de polipeptídeos exemplares da invenção compreendem, ou alternativamente - consistem em, uma, duas, três, quatro, cinco, seis, sete, oito, nove, dez, onze (11), doze (12), 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69 ou 70 ou mais ou todas as seguintes alterações de resíduos aminoácidos para SEQ ID NO: 2: a glicina na posição do aminoácido 2 é asparagina, a glicina na posição do aminoácido 13 é asparagina, a fenilalanina na posição do aminoácido 38 é tirosina, a serina na posição do aminoácido 57 é ácido aspártico, a tirosina na posição do aminoácido 61 é glutamina, a tirosina na posição do aminoácido 61 é serina, a alanina na posição do aminoácido 62 é treonina, a fenilalanina na posição do aminoácido 63 é histidina, a fenilalanina na posição do aminoácido 63 é treonina, a metionina na posição do aminoácido 69 é ácido glutâmico, a metionina na posição do aminoácido 69 é glutamina, a metionina na posição do aminoácido 69 é histidina, a metionina na posição do aminoácido 69 é serina, a metionina na posição do aminoácido 69 é tirosina, o ácido aspártico na posição do aminoácido 70 é prolina, a arginina na posição do aminoácido 71 é alanina, a arginina na posição do aminoácido 71 é ácido glutâmico, a arginina na posição do aminoácido 71 é glutamina, a arginina na posição do aminoácido 71 é prolina, a arginina na posição do aminoácido 71 é serina, a arginina na posição do aminoácido 71 é treonina, a lisina na posição do aminoácido 74 é ácido glutâmico, a lisina na posição do aminoácido 74 é leucina, a lisina na posição do aminoácido 74 é metionina, a isoleucina na posição do aminoácido 94 é glutamina, a metionina na posição do aminoácido 101 é tirosina, o ácido aspártico na posição do aminoácido 103 é cisteína, o ácido aspártico na posição do aminoácido 103 é glutamina, o ácido glutâmico na posição do aminoácido 106 é glicina, o ácido glutâmico na posição do aminoácido 109 é leucina, a lisina na posição do aminoácido 116 é alanina, a lisina na posição do aminoácido 116 é arginina, a fenilalanina na posição do aminoácido 130 é tirosina, a fenilalanina na posição do aminoácido 131 é leucina, o ácido glutâmico na posição do aminoácido 148 é histidina, a lisina na posição do aminoácido 162 é glutamina, a isoleucina na posição do aminoácido 166 é alanina, a isoleucina na posição do aminoácido 166 é valina, a serina na posição do aminoácido 183 é arginina, a serina na posição do aminoácido 183 é valina, a lisina na posição do aminoácido 186 é alanina, a lisina na posição do aminoácido 186 é ácido aspártico, a lisina na posição do aminoácido 186 é prolina, a lisina na posição do aminoácido 186 é serina, a serina na posição do aminoácido 191 é alanina, a serina na posição do aminoácido 191 é cisteína, a serina na posição do aminoácido 191 é leucina, a fenilalanina na posição do aminoácido 201 é isoleucina, a fenilalanina na posição do aminoácido 201 é prolina, a fenilalanina na posição do aminoácido 201 é valina, o ácido glutâmico na posição do aminoácido 212 é prolina, a lisina na posição do aminoácido 216 é alanina, a histidina na posição do aminoácido 230 é arginina, a histidina na posição do aminoácido 230 é glutamina, a histidina na posição do aminoácido 230 é lisina, a leucina na posição do aminoácido 231 é isoleucina, a leucina na posição do aminoácido 231 é metionina, a leucina na posição do aminoácido 231 é valina, o ácido glutâmico na posição do aminoácido 234 é ácido aspártico, a lisina na posição do aminoácido 246 é glutamina, a lisina na posição do aminoácido 246 é serina, a arginina na posição do aminoácido 258 é serina, a arginina na posição do aminoácido 258 é tirosina, a leucina na posição do aminoácido 262 é glutamina, a leucina na posição do aminoácido 262 é histidina, a leucina na posição do aminoácido 262 é metionina, a leucina na posição do aminoácido 262 é prolina, a serina na posição do aminoácido 270 é arginina, a fenilalanina na posição do aminoácido 271 é alanina, a metionina na posição do aminoácido 276 é alanina, a metionina na posição do aminoácido 276 é cisteína, a metionina na posição do aminoácido 276 é serina, o ácido glutâmico na posição do aminoácido 277 é serina, a arginina na posição do aminoácido 280 é glicina, a serina na posição do aminoácido 290 é alanina, a treonina na posição do aminoácido 297 é alanina, a treonina na posição do aminoácido 297 é prolina, a leucina na posição do aminoácido 298 é alanina, a leucina na posição do aminoácido 298 é arginina, a leucina na posição do aminoácido 298 é asparagina, a leucina na posição do aminoácido 298 é serina, a leucina na posição do aminoácido 298 é valina, a lisina na posição do aminoácido 300 é glicina, a treonina na posição do aminoácido 301 é glutamina, o ácido aspártico na posição do aminoácido 305 é prolina, a glicina na posição do aminoácido 312 é isoleucina, e/ou a serina na posição do aminoácido 315 é isoleucina.
[000767] Todas estas sequências são sequências exemplares de aminoácidos da invenção tendo alterações de resíduos específicas para a SEQ ID NO: 2 “parental”, resumida (em parte) na Tabela 1, acima, e na Tabela 2, no Exemplo 5, abaixo.
[000768] Em um aspecto, o polipeptídeo tem uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase, por exemplo, pode hidrolisar uma ligação glicosídica em um polissacarídeo, por exemplo, um glucano. Em um aspecto, o polipeptídeo tem uma atividade de glucanase compreendendo catalisação de hidrólise de ligações 1,4- beta-D-glicosídicas ou ligações β-1,3-glicosidicas. Em um aspecto, a atividade de endoglucanase compreende uma atividade de endo-1,4- beta-endoglucanase. Em um aspecto, a atividade de endoglucanase compreende hidrolisar um glucano, um manano, um arabinoxilano ou um xilano, para produzir um glucano de menor peso molecular ou glucano-oligômero. Em um aspecto, o glucano compreende um beta- glucano, tal como um beta-glucano hidrossolúvel.
[000769] Enzimas codificadas pelos polinucleotídeos da invenção incluem, mas não estão limitadas a hidrolases tais como glucanases, por exemplo, endoglucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases. Em um aspecto, uma enzima da invenção também pode ter uma atividade de mananase, por exemplo, pode degradar (ou hidrolisar) mananos. Polissacarídeos contendo manano são um componente importante da fração de hemicelulose tanto em madeiras de lei quanto em madeiras brancas bem como no endosperma em muitas sementes de leguminosas e em algumas sementes maduras de plantas não-leguminosas. Em um aspecto, uma mananase da invenção hidrolisa ligações beta-1,4 em mananos, glucomananos, galactomananos e galactoglucomananos (mananos são polissacarídeos tendo uma estrutura principal composta de manose beta-1,4 ligada, glucomananos são polissacarídeos tendo uma estrutura principal de manose e glicose beta.-1,4 ligadas alternando mais ou menos regularmente). Ensaios para determinar atividade de mananase são de conhecimento geral na técnica, vide, por exemplo, os Pedidos de Patente dos Estados Unidos Nos: 20030215812; 20030119093; as Patentes dos Estados Unidos Nos. 5.661.021; 5.795.764; 6.376.445; 6.420.331. Ensaios para determinar atividade de xilanase são de conhecimento geral na técnica, vide, por exemplo, os Pedidos de Patente dos Estados Unidos Nos: 5.693.518; 5.885.819; 6.200.797; 6.586.209; 6.682.923.
[000770] “Aminoácido” ou “sequência de aminoácidos” conforme usado aqui, neste pedido de patente, se refere a uma sequência de oligopeptídeo, peptídeo, polipeptídeo, ou proteína, ou a um fragmento, porção, ou subunidade de quaisquer destas e a moléculas que ocorrem naturalmente ou sintéticas. “Aminoácido” ou “sequência de aminoácidos” se referem a uma sequência de oligopeptídeo, peptídeo, polipeptídeo, ou proteína, ou a um fragmento, porção, ou subunidade de quaisquer destas e a moléculas que ocorrem naturalmente ou sintéticas. O termo “polipeptídeo” conforme usado aqui, neste pedido de patente, se refere a aminoácidos unidos uns aos outros por ligações de peptídeos ou ligações de peptídeos modificados, isto é, isósteres de peptídeos e podem conter aminoácidos modificados diferentes dos 20 aminoácidos gene-codificados. Os polipeptídeos podem ser modificados ou por processos naturais, tais como processamento pós-translacional, ou por técnicas de modificação química as quais são de conhecimento geral na técnica. As modificações podem ocorrer em qualquer luga no polipeptídeo, incluindo a estrutura principal do peptídeo, as cadeias laterais de aminoácidos e os términos amino ou carboxila. Será reconhecido que o mesmo tipo de modificação pode estar presente no mesmo grau ou em graus variáveis em vários sítios em um dado polipeptídeo. Além disso um dado polipeptídeo pode ter muitos tipos de modificações. As modificações incluem acetilação, acilação, ADP-ribosilação, amidação, fixação covalente de flavina, fixação covalente de uma porção heme, fixação covalente de um nucleotídeo ou derivado nucleotídico, fixação covalente de um lipídeo ou derivado lipídico, fixação covalente de um fosfatidilinositol, ciclização de reticulação, formação de ligações dissulfeto, desmetilação, formação de reticulações covalentes, formação de cisteína, formação de piroglutamato, formilação, gama- carboxilação, glicosilação, formação de âncoras de GPI, hidroxilação, iodinação, metilação, miristoilação, oxidação, peguilação, processamento de glucano hidrolase, fosforilação, prenilação, racemização, selenoilação, sulfatação e adição de aminoácidos à proteína mediada por transferência-RNA tais como arginilação. (Vide Creighton, T.E., Proteins - Structure and Molecular Properties 2nd Ed., W.H. Freeman and Company, New York (1993); Posttranslational Covalent Modification of Proteins, B.C. Johnson, Ed., Academic Press, New York, pp. 1-12 (1983)). Os peptídeos e os polipeptídeos da invenção também incluem todas as formas “miméticas” e “peptidomiméticas”, conforme descrito em detalhes adicionais, abaixo.
[000771] “Fragmentos” conforme usado aqui, neste pedido de patente, são uma porção de uma proteína que ocorre naturalmente a qual pode existir em pelo menos duas conformações diferentes. Fragmentos podem ter a mesma ou substancialmente a mesma sequência de aminoácidos que a proteína que ocorre naturalmente. “Substancialmente a mesma” significa que uma sequência de aminoácidos é largamente, mas não inteiramente, a mesma, mas retém pelo menos uma atividade funcional da sequência à qual está relacionada, por exemplo, somente tem substituições de aminoácidos conservativas, conforme descrito aqui, neste pedido de patente. Fragmentos os quais têm diferentes estruturas tridimensionais como a proteína que ocorre naturalmente também são incluídos. Um exemplo disto é, uma molécula “pró-forma”, tal como uma proproteína de baixa atividade, que pode ser modificada por clivagem para produzir uma enzima matura com atividade significativamente maior.
[000772] Conforme usado aqui, neste pedido de patente, o termo “isolado” significa que o material é removido de seu ambiente original (por exemplo, o ambiente natural se estiver ocorrendo naturalmente). Por exemplo, um polinucleotídeo ou polipeptídeo que ocorre naturalmente presente em um animal vivo não é isolado, mas o mesmo polinucleotídeo ou polipeptídeo, separado de alguns ou de todos os materiais coexistentes no sistema natural, é isolado. Os referidos polinucleotídeos podem ser parte de um vetor e/ou os referidos polinucleotídeos ou polipeptídeos podem ser parte de uma composição e ainda serem isolados em que o vetor referido ou a composição referida não é parte de seu ambiente natural. Conforme usado aqui, neste pedido de patente, o termo “purificado” não requer pureza absoluta; ao invés, é pretendido como uma definição relativa. Ácidos nucleicos individuais obtidos de uma biblioteca têm sido convencionalmente purificados até homogeneidade eletroforética. As sequências obtidas a partir destes clones não podem ser obtidas diretamente quer da biblioteca quer de DNA humano total. Os ácidos nucleicos purificados da invenção foram purificados a partir do restante do DNA genômico no organismo por pelo menos 104 a 106 vezes. No entanto, o termo “purificado” também inclui ácidos nucleicos os quais foram purificados a partir do restante do DNA genômico ou de outras sequências em uma biblioteca ou outro ambiente por pelo menos uma ordem de magnitude, tipicamente duas ou três ordens e mais tipicamente quatro ou cinco ordens de magnitude.
[000773] Polipeptídeos ou proteínas “recombinantes” se referem a polipeptídeos ou a proteínas produzidas por meio de técnicas de DNA recombinante; isto é, produzidos a partir de células transformadas por um construto de DNA exógeno codificando o polipeptídeo ou a proteína desejados. Polipeptídeos ou proteína “sintéticos” são aqueles preparados por síntese química. Métodos de síntese química de peptídeo de fase sólida também podem ser usados para sintetizar o polipeptídeo ou fragmentos da invenção. O referido método é conhecido na técnica desde o início dos anos sessenta (Merrifield, R. B., J. Am. Chem. Soc., 85:2149-2154, 1963) (Vide também Stewart, J. M. and Young, J. D., Solid Phase Peptide Synthesis, 2nd Ed., Pierce Chemical Co., Rockford, Ill., pp. 11-12)) e tem sido empregado recentemente em kits de design e síntese de peptídeo laboratoriais disponíveis comercialmente (Cambridge Research Biochemicals). Kits laboratoriais disponíveis comercialmente têm utilizado geralmente os ensinamentos de H. M. Geysen et al, Proc. Natl. Acad. Sci., USA, 81:3998 (1984) e proporcionam a sintetização de peptídeos sobre as pontas de uma multitude de “hastes” ou “pinos” todos os quais são conectados a uma única lâmina. Quando é utilizado um sistema semelhante, uma lâmina de hastes ou pinos é invertida e inserida em uma segunda lâmina de cavidades ou reservatórios correspondentes, os quais contêm soluções para fixar ou ancorar um aminoácido apropriado às pontas dos pinos ou hastes. Repetindo uma etapa de processo semelhante, isto é, invertendo e inserindo as pontas das hastes e dos pinos em soluções apropriadas, aminoácidos são construídos em peptídeos desejados. Além disso, estão disponíveis uma série de sistemas de síntese de peptídeo FMOC disponíveis. Por exemplo, a montagem de um polipeptídeo ou fragmento pode ser realizada sobre um suporte sólido usando um sintetizador de peptídeo automático Applied Biosystems, Inc. Molde 431A. O referido equipamento proporciona pronto acesso aos peptídeos da invenção, quer por síntese direta ou por síntese de uma série de fragmentos que podem ser acoplados usando outras técnias conhecidas.
[000774] A invenção proporciona glucanases tendo uma novidade comum em que são primeiro derivadas de famílias de “glicosidase hidrolase” similares. As glicosidase hidrolases foram primeiro classificadas em famílias em 1991, vide, por exemplo, Henrissat (1991) Biochem,. J. 280:309-316. Desde então, as classificações têm sido continuamente atualizadas, vide, por exemplo, Henrissat (1993) Biochem. J. 293:781-788; Henrissat (1996) Biochem. J. 316:695-696; Henrissat (2000) Plant Physiology 124:1515-1519. Há aproximadamente 87 famílias de glicosidase hidrolases identificadas. As glucanases da invenção podem ser categorizadas como famílias, vide, por exemplo, Strohmeier (2004) Protein Sci. 13:3200-3213.
[000775] Os polipeptídeos da invenção incluem glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases em uma forma ativa ou inativa. Por exemplo, os polipeptídeos da invenção incluem proproteínas antes de “maturação” ou de processamento de sequências prepro, por exemplo, por uma enzima de processamento de proproteínas, tal como uma proproteína convertase para gerar uma proteína matura “ativa”. Os polipeptídeos da invenção incluem glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases inativa por outras razões, por exemplo, antes de “ativação” por um evento de processamento pós-translacional, por exemplo, ação de uma endo- ou exopeptidase ou proteinase, um evento de fosforilação, uma amidação, uma glicosilação ou uma sulfatação, um evento de dimerização, e similares. Os polipeptídeos da invenção incluem todas as formas ativas, incluindo subsequências ativas, por exemplo, domínios catalíticos ou sítios ativos, da glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidases. Métodos para identificar sequências de domínio "prepro" e sequências de sinal são de conhecimento geral na técnica, vide, por exemplo, Van de Ven (1993) Crit. Rev. Oncog. 4(2):115-136. Por exemplo, para identificar uma sequência prepro, a proteína é purificada do espaço extracelular e a sequência de proteína N-terminal é determinada e comparada com a forma não-processada.
[000776] Conforme observado acima, a invenção proporciona polipeptídeos isolados, sintéticos ou recombinantes e peptídeos tendo uma identidade de sequência com uma sequência exemplar da invenção, por exemplo, proteínas tendo a sequência de SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, E SEQ ID NO: 23, e as modificações específicas para SEQ ID NO: 2 conforme descrito aqui, neste pedido de patente, onde em vários aspectos a percentagem de identidade de sequência pode ser sobre toda a extensão do polipeptídeo, ou, a identidade pode ser sobre uma região de pelo menos cerca de 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700 ou mais resíduos. Polipeptídeos da invenção também podem ser mais curtos do que toda a extensão de polipeptídeos exemplares. Em aspectos alternativos, a invenção proporciona polipeptídeos (peptídeos, fragmentos) variando em tamanho entre cerca de 5 resíduos e toda a extensão de um polipeptídeo, por exemplo, uma enzima, tal como uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase; tamanhos exemplares sendo de cerca de 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 100, 125, 150, 175, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, ou mais resíduos, por exemplo, resíduos contíguos de uma glucanase exemplar (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção.
[000777] Peptídeos da invenção (por exemplo, uma subsequência de um polipeptídeo exemplar da invenção) podem ser úteis como, por exemplo, sondas de marcação, antígenos, epitopos, tolerágenos, motivos, sítios ativos de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase (por exemplo, “domínios catalíticos”), sequências de sinal e/ou domínios prepro. Polipeptídeos e peptídeos da invenção podem ser isolados de fontes naturais, ser sintéticos, ou ser polipeptídeos produzidos de modo recombinante. Peptídeos e proteínas podem ser expressados de modo recombinant in vitro ou in vivo. Os peptídeos e os polipeptídeos da invenção podem ser fabricados e isolados usando qualquer método conhecido na técnica. Polipeptídeo e peptídeos da invenção também podem ser sintetizados, no todo ou em parte, usando métodos químicos de conhecimento geral na técnica. Vide por exemplo, Caruthers (1980) Nucleic Acids Res. Symp. Ser. 215-223; Horn (1980) Nucleic Acids Res. Symp. Ser. 225-232; Banga, A.K., Therapeutic Peptides and Proteins, Formulation, Processing and Delivery Systems (1995) Technomic Publishing Co., Lancaster, PA. Por exemplo, a síntese de peptídeos pode ser realizada usando várias técnicas de fase sólida (vide por exemplo, Roberge (1995) Science 269:202; Merrifield (1997) Methods Enzymol. 289:3-13) e síntese automatizada pode ser obtida, por exemplo, usando o sintetizador de peptídeo ABI 431A (Perkin Elmer) de acordo com as instruções fornecidas pelo fabricante.
[000778] Os peptídeos e os polipeptídeos da invenção também podem ser glicosilados. A glicosilação pode ser adicionada pós- translacionalmente quer quimicamente quer por mecanismos biossintéticos celulares, em que o último incorpora o uso de motivos de glicosilação conhecidos, os quais podem ser nativos da sequência ou podem ser adicionados como um peptídeo ou adicionados na sequência de ácido nucleico codificante. A glicosilação pode ser ligada por O ou ligada por N.
[000779] Os peptídeos e os polipeptídeos da invenção, conforme definidos acima, incluem todas as formas “miméticas” e “peptidomiméticas”. Os termos “mimético” e “peptidomimético” se referem a um composto químico sintético o qual tem substancialmente as mesmas características estruturais e/ou funcionais dos polipeptídeos da invenção. O mimético pode ser ou inteiramente composto de análogos sintéticos, não-naturais de aminoácidos, ou, é uma molécula quimérica de aminoácidos de peptídeos parcialmente naturais e análogos parcialmente não-naturais de aminoácidos. O mimético também pode incorporar qualquer quantidade de substituições conservativas de aminoácidos naturais na medida que as referidas substituições também não alterem substancialmente a estrutura e/ou atividade do mimético. Como com polipeptídeos da invenção os quais são variantes conservativas, experimentação de rotina determinará se um mimético está dentro do escopo da invenção, isto é, que sua estrutura e/ou função não é substancialmente alterada. Deste modo, em um aspecto, uma composição mimética está dentro do escopo da invenção se tiver uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase.
[000780] Composições miméticas de polipeptídeos da invenção podem conter qualquer combinação de componentes estruturais não- naturais. Em aspecto alternativo, composições miméticas da invenção incluem um ou todos os três grupos estruturais seguintes: a) grupos de ligação de resíduo diferentes das ligações de ligação amida natural (“ligação de peptídeo”); b) resíduos não-naturais ao invés de resíduos aminoácido que ocorrem naturalmente; ou c) resíduos os quais induzem mimicria estrutural secundária, isto é, induzem ou estabilizam uma estrutura secundária, por exemplo, uma conformação de giro beta, giro gama, folha beta, hélice alfa, e similares. Por exemplo, um polipeptídeo da invenção pode ser caracterizado como um mimético quando todos ou alguns de seus resíduos são unidos por meios químicos diferentes de ligações de peptídeos naturais. Resíduos peptidomiméticos individuais podem ser unidos por ligações de peptídeos, outras ligações químicas ou meios de acoplamento, tais como, por exemplo, glutaraldeído, ésteres de N-hidroxissuccinimida, maleimidas bifuncionais, N,N’-diciclo-hexilcarbodi-imida (DCC) ou N,N’-di-isopropilcarbodi-imida (DIC). Grupos de licação que podem ser uma alternativa às ligações de ligação amida tradicional (“ligação de peptídeo”) incluem, por exemplo, cetometileno (por exemplo, - C(=O)-CH2- for -C(=O)-NH-), aminometileno (CH2-NH), etileno, olefina (CH=CH), éter (CH2-O), tioéter (CH2-S), tetrazol (CN4-), tiazol, retroamida, tioamida, ou éster (vide, por exemplo, Spatola (1983) em Chemistry and Biochemistry of Amino Acids, Peptides and Proteins, Vol. 7, pp 267-357, “Peptide Backbone Modifications”, Marcell Dekker, NY).
[000781] Um polipeptídeo da invenção também podem ser caracterizado como um mimético contendo todos ou alguns resíduos não-naturais ao invés de resíduos aminoácido que ocorrem naturalmente. Resíduos não-naturais são bem descritos na literatura científica e de patente; umas poucas composições não-naturais exemplares úteis como miméticos de resíduos aminoácido naturais e diretrizes são descritas abaixo. Miméticos de aminoácidos aromáticos podem ser gerados substituindo por, por exemplo, D- ou L- nafilalanina; D- ou L- fenilglicina; D- ou L-2 tieneilalanina; D- ou L-1, -2, 3-, ou 4- pireneilalanina; D- ou L-3 tieneilalanina; D- ou L-(2-piridinil)- alanina; D- ou L-(3-piridinil)-alanina; D- ou L-(2-pirazinil)-alanina; D- ou L-(4-isopropil)-fenilglicina; D-(trifluorometil)-fenilglicina; D- (trifluorometil)-fenilalanina; D-p-fluoro-fenilalanina; D- ou L-p- bifenilfenilalanina; D- ou L-p-metóxi-bifenilfenilalanina; D- ou L-2- indol(alquil)alaninas; e, D- ou L-alquilaminas, onde alquila pode ser substituída ou não-substituído metila, etila, propila, hexila, butila, pentila, isopropila, iso-butila, sec-isotila, iso-pentila, ou um aminoácido não-acídico. Anéis aromáticos de um aminoácido não-natural incluem, por exemplo, anéis aromáticos tiazolila, tiofenila, pirazolila, benzimidazolila, naftila, furanila, pirrolila, e piridil.
[000782] Miméticos de aminoácidos acídicos podem ser gerados por substituição por, por exemplo, aminoácidos não-carboxilato enquanto mantendo uma carga negativa; (fosfono)alanina; treonina sulfatada. Grupos laterais carboxila (por exemplo, aspartila ou glutamila) também podem ser modificados seletivamente por reação com carbodiimidas (R’-N-C-N-R’) tais como, por exemplo, 1-ciclohexil-3(2-morfolinil-(4- etila) carbodiimida ou 1-etil-3(4-azonia- 4,4- dimetolpentila) carbodiimida. Aspartila ou glutamila também podem ser convertidos para resíduos asparaginila e glutaminila por reação com íons amônio. Miméticos de aminoácidos básicos podem ser gerados por substituição com, por exemplo, (além de lisina e arginina) os aminoácidos ornitina, citrulina, ou ácido (guanidino)-acético, ou ácido (guanidino)alquil-acético, onde alquila é definido acima. Derivado nitrila (por exemplo, contendo a porção CN ao invés de COOH) podem ser substituídos por asparagina ou glutamina. Resíduos asparaginila e glutaminila podem ser desaminados para os resíduos aspartila ou glutamila correspondentes. Miméticos de resíduos arginina podem ser gerados reagindo arginila com, por exemplo, um ou mais reagentes convencionais, incluindo, por exemplo, fenilglioxal, 2,3-butanodiona, 1,2-ciclo-hexanodiona, ou ninidrina, em um aspecto sob condições alcalinas. Miméticos de resíduos tirosina podem ser gerados reagindo tirosila com, por exemplo, compostos de diazônio aromáticos ou tetranitrometano. N-acetilimidizol e tetranitrometano podem ser usados para formar espécies O-acetila tirosila e derivados 3-nitro, respectivamente. Miméticos de resíduos cisteína podem ser gerados reagindo resíduos cisteinila com, por exemplo, alfa-haloacetatos tais como ácido 2-cloroacético ou cloroacetamida e aminas correspondentes; para dar derivados carboximetila ou carboxiamidometil. Miméticos de resíduos cisteína também podem ser gerados reagindo resíduos cisteinila com, por exemplo, bromo- trifluoroacetona, ácido alfa-bromo-beta-(5-imidozoila) propiônico; fosfato de cloroacetila, N-alquilmaleimidas, dissulfeto de 3-nitro-2- piridila; 2-piridila dissulfeto de metila; p-cloromercuribenzoato; 2- cloromercúrio-4 nitrofenol; ou, cloro-7-nitrobenzo-oxa-1,3-diazol. Miméticos de lisina podem ser gerados (e resíduos de terminal amino podem ser alterados) reagindo lisinila com, por exemplo, anidridos de ácido succínico ou outros carboxílicos. Lisina e outros miméticos de resíduos contendo alfa-amino também podem ser gerados por reação com imidoésteres, tais como picolinimidato de metila, piridoxal fosfato, piridoxal, cloroboro-hidreto, ácido trinitro-benzenossulfônico, O- metilisoureia, 2,4, pentanodiona, e reações catalisadas por transamidase com glioxilato. Miméticos de metionina podem ser gerados por reação com, por exemplo, sulfóxido de metionina. Miméticos de prolina incluem, por exemplo, ácido pipecólico, ácido tiazolidina carboxílico, 3- ou 4- hidróxi prolina, deidroprolina, 3- ou 4- metilprolina, ou 3,3,-dimetilprolina. Miméticos de resíduos histidina podem ser gerados reagindo histidila com, por exemplo, dietilprocarbonato ou brometo de para-bromofenacila. Outros miméticos incluem, por exemplo, os gerados por hidroxilação de prolina e lisina; fosforilação dos grupos oxidrila de resíduos serila ou treonil; metilação dos grupos alfa-amino de lisina, arginina e histidina; acetilação da amina de N-terminal; metilação de resíduos amida da cadeia principal ou substituição com N-metila aminoácidos; ou amidação de grupos carboxila de C-terminal.
[000783] Um resíduo, por exemplo, um aminoácido, de um polipeptídeo da invenção também pode ser substituído por um aminoácido (ou resíduo peptidomimético) da quiralidade oposta. Deste modo, qualquer aminoácido que ocorre naturalmente na configuração- L (o qual também pode ser referido como o R ou S, dependendo da estrutura da entidade química) pode ser substituído com o aminoácido do mesmo tipo estrutural químico ou um peptidomimético, mas da quiralidade oposta, referido como o D- aminoácido, mas também pode ser referido como a forma R ou S.
[000784] A invenção também proporciona métodos para modificar os polipeptídeos da invenção por quaisquer processos naturais, tais como processamento pós-translacional (por exemplo, fosforilação, acilação, e etc), ou por técnicas de modificação química, e os polipeptídeos modificados resultantes. Podem ocorrer modificações em qualquer lugar no polipeptídeo, incluindo a estrutura principal do peptídeo, as cadeias laterais de aminoácido e os términos amino ou carboxila. Será reconhecido que o mesmo tipo de modificação pode estar presente no mesmo grau ou em graus variáveis em vários sítios em um dado polipeptídeo. Também um dado polipeptídeo pode ter muitos tipos de modificações. Modificações incluem acetilação, acilação, ribosilação de ADP, amidação, fixação covalente de flavina, fixação covalente de uma porção heme, fixação covalente de um nucleotídeo ou derivado de nucleotídeo, fixação covalente de um lipídeo ou derivado lipídico, fixação covalente de um fosfatidilinositol, ciclização por reticulação, formação de ligações dissulfeto, desmetilação, formação de reticulações covalentes, formação de cisteína, formação de piroglutamato, formilação, gama-carboxilação, glicosilação, formação de âncora GPI, hidroxilação, iodinação, metilação, miristoilação, oxidação, peguilação, processamento proteolítico, fosforilação, prenilação, racemização, selenoilação, sulfatação, e adição de aminoácidos mediada por RNA de transferência a proteína tal como arginilação. Vide, por exemplo, Creighton, T.E., Proteins - Structure and Molecular Properties 2nd Ed., W.H. Freeman and Company, New York (1993); Posttranslational Covalent Modification of Proteins, B.C. Johnson, Ed., Academic Press, New York, pp. 1-12 (1983).
[000785] Métodos de sintese química de peptídeo de fase sólida podem ser usados para sintetizar o polipeptídeo ou fragmentos da invenção. Os referidos métodos são conhecidos na técnica desde o início dos anos 1960 (Merrifield, R. B., J. Am. Chem. Soc., 85:21492154, 1963) (Vide também Stewart, J. M. and Young, J. D., Solid Phase Peptide Synthesis, 2nd Ed., Pierce Chemical Co., Rockford, Ill., pp. 11-12)) e foram empregados recentemente em kits de design e síntese de laboratório de peptídeo disponíveis comercialmente (Cambridge Research Biochemicals). Os kits laboratoriais disponíveis comercialmente têm utilizado geralmente os ensinamentos de H. M. Geysen et al, Proc. Natl. Acad. Sci., USA, 81:3998 (1984) e proporcionam a síntese de peptídeos sobre as pontas de uma multitude de “hastes” ou “pinos” todas as quais estão conectadas a uma única lâmina. Quando um referido sistema é utilizado, uma lâmina de hastes ou pinos é invertida e inserida em uma segunda lâmina de cavidades ou reservatórios correspondentes, os quais contêm soluções para fixar ou ancorar um aminoácido apropriado às pontas do pino ou da haste. Repetindo uma tal etapa do processo, isto é, invertendo e inserindo as pontas da haste e do pino em soluções apropriadas, aminoácidos são construídos em peptídeos desejados. Além disso, uma série de sistemas de síntese de peptídeo FMOC disponíveis estão disponíveis. Por exemplo, a montagem de um polipeptídeo ou fragmento pode ser realizada sobre um suporte sólido usando um sintetizador de peptídeo automático da Applied Biosystems, Inc. Model 431A®. O referido equipamento proporciona pronto acesso aos peptídeos da invenção, quer por síntese direta ou por síntese de uma série de fragmentos que pode ser acoplado usando outras técnicas conhecidas.
[000786] A invenção inclui glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção com e sem-sinal. O polipeptídeo compreendendo uma sequência de sinal da invenção pode ser uma glucanase da invenção ou outra glucanase ou outra enzima ou outro polipeptídeo.
[000787] A invenção inclui glucanases imobilizadas, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases, anticorpos antiglucanase, antimananase, ou antixilanase e fragmentos dos mesmos. A invenção proporciona métodos para inibir a atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, por exemplo, usando mutantes negativos dominantes ou anticorpos antiglucanase, antimananase, ou antixilanase da invenção. A invenção inclui heterocomplexos, por exemplo, proteínas de fusão, heterodímeros, e etc., compreendendo as glucanases da invenção.
[000788] Polipeptídeos da invenção podem ter uma atividade de glucanase, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases sobre várias condições, por exemplo, extremos em pH e/ou temperatura, agentes oxidantes, e similares. A invenção proporciona métodos levando a preparações alternativas de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase com diferentes eficiências e estabilidades catalíticas, por exemplo, para temperatura, agentes oxidantes e condições de lavagem variáveis. Em um aspecto, variantes de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase podem ser produzidas usando técnicas de mutagênese sítio-dirigida e/ou mutagênese aleatória. Em um aspecto, evolução dirigida pode ser usada para produzir uma grande variedade de variantes de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase com especificidades e estabilidade alternativas.
[000789] As proteínas da invenção também são úteis como reagentes de pesquisa para identificar moduladores de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, por exemplo, ativadores ou inibidores da atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. Em resumo, amostras de teste (compostos, caldos, extratos, e similares) são adicionadas a testes de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase para determinar sua capacidade para inibir clivagem de substrato. Inibidores identificados deste modo podem ser usados na indústria e pesquisa para reduzir ou evitar proteólise indejada. Inibidores de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase podem ser combinados para aumentar o espectro de atividade.
[000790] As enzimas da invenção também são úteis como reagentes de pesquisa para digerir proteínas ou em sequenciamento de proteínas. Por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase pode ser usada para decompor polipeptídeos em fragmentos menores para sequenciamento usando, por exemplo, um sequenciador automatizado.
[000791] A invenção também proporciona métodos para descobrir uma nova glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase usando os ácidos nucleicos, polipeptídeos e anticorpos da invenção. Em um aspecto, bibliotecas de fagemídeos são triadas para descoberta à base de expressão de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Em outro aspecto, bibliotecas de lâmbda fagos são triadas para descoberta à base de expressão de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. A triagem das bibliotecas de fagos ou fagemídeos podem permitir a detecção de clones tóxicos; acesso a substrato aprimorado; necessidade reduzida de produzir um hospedeiro, desviando do potencial para qualquer tendência resultante de excisão em massa da biblioteca; e, crescimento mais rápido em baixas densidades de clone. A triagem de bibliotecas de fagos ou fagemídeos pode ser em fase líquida ou em fase sólida. Em um aspecto, a invenção proporciona triagem em fase líquida. Isto dá uma maior flexibilidade em condições de teste; flexibilidade do substrato adicional; maior sensibilidade para clones fracos; e facilidade de automação em triagem de fase sólida.
[000792] A invenção proporciona métodos de triagem usando as proteínas e ácidos nucleicos da invenção e automação robótica para possibilitar a execução de muitos milhoares de reações biocatalíticas e ensaios de triagem em um curto período de tempo, por exemplo, pos dia, bem como assegurar um alto nível de acurácia e reprodutibilidade (vide discussão de arranjos, abaixo). Em consequência, uma biblioteca de compostos derivados pode ser produzida em uma questão de semanas. Para ensinamentos adicionais sobre modificação de moléculas, incluindo moléculas pequenas, vide a publicação de patente No. PCT/US94/09174.
[000793] Outro aspecto da invenção é um polipeptídeo isolado ou purificado compreendendo a sequência de um da invenção, ou fragmentos compreendendo pelo menos cerca de 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos da mesma. Conforme discutido acima, os polipeptídeos referidos podem ser obtidos inserindo um ácido nucleico codificando o polipeptídeo em um vetor de tal modo que a sequência codificante é ligada operavelmente a uma sequência capaz de dirigir a expressão do polipeptídeo codificado em uma célula hospedeira adequada. Por exemplo, o vetor de expressão pode compreender um promotor, um sítio de ligação de ribossoma para iniciação de translação e um terminador de transcrição. O vetor também pode incluir sequências apropriadas para amplificar a expressão.
[000794] Outro aspecto da invenção é polipeptídeos ou fragmentos dos mesmos os quais têm pelo menos cerca de 50%, pelo menos cerca de 55%, pelo menos cerca de 60%, pelo menos cerca de 65%, pelo menos cerca de 70%, pelo menos cerca de 75%, pelo menos cerca de 80%, pelo menos cerca de 85%, pelo menos cerca de 90%, pelo menos cerca de 95%, ou mais do que cerca de 95% de identidade de sequência (homologia) com um dos polipeptídeos da invenção, ou um fragmento compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 ou mais aminoácidos consecutivos dos mesmos. A identidade (homologia) de sequência pode ser determinada usando qualquer um dos programas descritos acima o qual alinhe os polipeptídeos ou fragmentos sendo comparados e determine a extensão da identidade ou similaridade de aminoácidos entre os mesmos. Será reconhecido que equivalência de aminoácidos, ou identidade, ou “homologia”, de sequência inclui substituições de aminoácido conservativas tais como as descritas acima.
[000795] Os polipeptídeos ou fragmentos tendo homologia com um dos polipeptídeos da invenção, ou um fragmento compreendendo pelo menos cerca de 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos podem ser obtidos isolando os ácidos nucleicos codificando os mesmos usando as técnicas descritas acima.
[000796] Alternativamente, os polipeptídeos ou fragmentos homólogos podem ser obtidos através de procedimentos de enriquecimento bioquímico ou de purificação. A sequência de polipeptídeos ou fragmentos potencialmente homólogos pode ser determinada por digestão por glucano hidrolase, eletroforese por gel e/ou microssequenciamento. A sequência do polipeptídeo ou fragmento homólogo prospectivo pode ser comparada com um dos polipeptídeos da invenção, ou um fragmento compreendendo pelo menos cerca de 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos usando qualquer um dos programas descritos acima.
[000797] Outro aspecto da invenção é um ensaio para identificar fragmentos ou variantes da invenção, os quais retêm a função enzimática dos polipeptídeos da invenção. Por exemplo, os fragmentos ou variantes dos polipeptídeos referidos, podem ser usados para catalisar reações bioquímicas, as quais indicam que o fragmento ou variante retém a atividade enzimática de um polipeptídeo da invenção.
[000798] O ensaio para determinar se fragmentos de variantes retêm a atividade enzimática dos polipeptídeos da invenção inclui as etapas de: contatar o polipeptídeo fragmento ou variante com uma molécula de substrato sob condições as quais permitem que o polipeptídeo fragmento ou variante funcione e detectar ou uma redução no nível de substrato ou um aumento no nível do produto da reação específico da reação entre o polipeptídeo e o substrato.
[000799] Os polipeptídeos da invenção ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos podem ser usados em uma variedade de aplicações. Por exemplo, os polipeptídeos ou fragmentos da mesma podem ser usados para catalisar reações bioquímicas. De acordo com um aspecto da invenção, é proporcionado um processo para utilizar os polipeptídeos da invenção ou polinucleotídeos codificando os polipeptídeos referidos para hidrolisar ligações glicosídicas. Os referidos procedimentos, uma substância contendo uma ligação glicosídica (por exemplo, um amido) é contactado com um dos polipeptídeos da invenção, ou sequências substancialmente idênticas a esses sob condições as quais facilitam a hidrólise da ligação glicosídica.
[000800] A presente invenção explora as propriedades catalíticas únicas de enzimas. Considerando que o uso de biocatalisadores (isto é, enzimas purificadas ou brutas, células não-vivas ou vivas) em transformações químicas normalmente requer a identificação de um biocatalisador em particular que reage com um composto de partida específico, a presente invenção usa biocatalisadores selecionados e condições de reação que são específicas para grupos funcionais que estão presentes em muitos compostos de partida, tais como moléculas pequenas. Cada biocatalisador é específico para um grupo funcional, ou vários grupos funcionais relacionados e pode reagir com muitos compostos de partida contendo este grupo funcional.
[000801] As reações biocatalíticas produzem uma população de derivados a partir de um único composto de partida. Estes derivados podem ser submetidos a outra rodada de reações biocatalíticas para produzir uma segunda população de compostos derivados. Milhares de variações da molécula pequena ou composto original podem ser produzidas com cada iteração de derivação biocatalítica.
[000802] As enzimas reagem em sítios específicos de um composto de partida sem afetar o resto da molécula, um processo o qual é muito difícila de obter usando métodos químicos tradicionais. Este alto grau de especificidade biocatalítica proporciona os meios para identificar um único composto ativo dentro da biblioteca. A biblioteca é caracterizada pela série de reações biocatalíticas usadas para a produzir, uma chamada "história biossintética ". A triagem da biblioteca para atividades biológicas e a investigação da história biossintética identifica a sequência de reação específica produzindo o composto ativo. A sequência da reação é repetida e a estrutura do composto sintetizado é determinada. Este modo de identificação, diferentemente de outras abordagens de síntese e triagem, não requer tecnologias de imobilização e os compostos podem ser sintetizados e testados livres em solução usando virtualmente qualquer tipo de ensaio de triagem. É importante notar que o alto grau de especificidade de reações de enzimas sobre grupos funcionais possibilita o "rastreamento" de reações enzimáticas específicas que compõem a biblioteca produzida biocataliticamente.
[000803] Muitas das etapas do procedimento são realizadas usando automação robótica possibilitando a execução de muitos milhares de reações biocatalíticas e ensaios de triagem por dia bem como assegurando um alto nível de precisão e reprodutibilidade. Em consequência, uma biblioteca de compostos derivados pode ser produzida em uma questão de semanas a qual levaria anos para produzir usando os métodos químicos correntes.
[000804] Em um aspecto particular, a invenção proporciona um método para modificar moléculas pequenas, compreendendo contatar um polipeptídeo codificado por um polinucleotídeo descrito aqui, neste pedido de patente, ou fragmentos enzimaticamente ativos do mesmo com uma molécula pequena para produzir uma molécula pequena modificada. Uma biblioteca de moléculas pequenas modificadas é testada para determinar se uma molécula pequena modificada está presente dentro da biblioteca a qual apresenta uma atividade desejada. Uma reação biocatalítica específica a qual produz a molécula pequena modificada de atividade desejada é identificada eliminando sistematicamente cada uma das reações biocatalíticas usadas para produzir uma porção da biblioteca e em seguida testando as moléculas pequenas produzidas na porção da biblioteca para a presença ou ausência da molécula pequena modificada com a atividade desejada. As reações biocatalíticas específicas as quais produzem a molécula pequena modificada de atividade desejada são opcionalmente repetidas. As reações biocatalíticas são conduzidas com um grupo de biocatalisadores que reagem com porções estruturais distintas encontradas dentro da estrutura de uma molécula pequena, cada biocatalisador é específico para uma porção estrutural ou um grupo de porções estruturais relacionadas; e cada biocatalisador reage com muitas moléculas pequenas diferentes as quais contêm a porção estrutural distinta.
Sequências de sinal, domínios prepro e catalíticos
[000805] A invenção proporciona sequências de sinal (por exemplo, signal peptídeos (SPs)), domínios prepro e domínios catalíticos (CDs) (por exemplo, sítios ativos) de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Uma "sequência de sinal" pode ser um sinal de secreção ou outro domínio que facilita secreção de um polipeptídeo da invenção pela célula hospedeira. Os SPs, domínios prepro e/ou CDs da invenção podem ser peptídeos isolados ou recombinantes ou podem ser parte de uma proteína de fusão, por exemplo, como um heteróloga domínio em uma proteína quimérica. A invenção proporciona ácidos nucleicos codificando estes domínios catalíticos (CDs), domínios prepro e sequências de sinal (líder) (SPs, por exemplo, um peptídeo tendo uma sequência compreendendo/ consistindo em resíduos de terminal amino de um polipeptídeo da invenção). Em um aspecto, a invenção proporciona uma sequência de sinal (líder) compreendendo um peptídeo compreendendo/ consistindo em uma sequência conforme determinado nos resíduos 1 a 15, 1 a 16, 1 a 17, 1 a 18, 1 a 19, 1 a 20, 1 a 21, 1 a 22, 1 a 23, 1 a 24, 1 a 25, 1 a 26, 1 a 27, 1 a 28, 1 a 28, 1 a 30, 1 a 31, 1 a 32, 1 a 33, 1 a 34, 1 a 35, 1 a 36, 1 a 37, 1 a 38, 1 a 39, 1 a 40, 1 a 41, 1 a 42, 1 a 43, 1 a 44 de um polipeptídeo da invenção.
[000806] A invenção também proporciona polipeptídeos quiméricos (e os ácidos nucleicos codificando os mesmos) compreendendo pelo menos duas enzimas da invenção ou subsequências das mesmas, por exemplo, sítios ativos, ou domínios catalíticos (CDs). Uma proteína quimérica da invenção (por exemplo, uma proteína de fusão, ou, outro heterodímero, por exemplo, dois domínios unidos por outros meios, por exemplo, um encadeador, ou, eletrostaticamente) pode compreender um polipeptídeo (por exemplo, sítio ativo ou domínio catalítico peptídeo) da invenção e outro polipeptídeo (por exemplo, sítio ativo ou domínio catalítico peptídeo) da invenção ou outro polipeptídeo. Por exemplo, uma proteína quimérica da invenção pode ter atividade de mananase e atividade de xilanase, mananase e glicanase, e etc. Em um aspecto a proteína quimérica da invenção compreende uma fusão de domínios, por exemplo, um único domínio pode apresentar glucanase/xilanase/mananase ou qualquer combinação de atividades (por exemplo, como uma proteína quimérica recombinante).
[000807] A invenção inclui polipeptídeos com ou sem uma sequência de sinal e/ou uma sequência prepro. A invenção inclui polipeptídeos com sequências heterólogas de sinal e/ou sequências prepro. A sequência prepro (incluindo uma sequência da invenção usada como um domínio prepro heterólogo) pode estar localizada sobre o terminal amino ou o terminal carbóxi da proteína. A invenção também inclui sequências de sinal isoladas ou recombinantes, sequências prepro e domínios catalíticos (por exemplo, “sítios ativos”) compreendendo sequências da invenção.
[000808] As sequências de sinal (SPs) e/ou prepro sequências de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção podem ser peptídeos isolados, ou, sequências unidas a outro polipeptídeo de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase ou uma não-glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, por exemplo, como uma proteína de fusão (quimérica). Em um aspecto, a invenção proporciona polipeptídeos compreendendo sequências de sinal de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção. Em um aspecto, polipeptídeos compreendendo sequências de sinal SPs e/ou prepro de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção compreendem sequências heterólogas a uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção (por exemplo, uma proteína de fusão compreendendo uma SP e/ou prepro da invenção e sequências de outra proteína glucanase ou uma não-glucanase). Em um aspecto, a invenção proporciona uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção com sequências heterólogas SPs e/ou prepro, por exemplo, sequências com uma sequência de sinal de levedura. Uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção pode compreender uma SP e/ou prepro heteróloga em um vetor, por exemplo, um vetor da série pPIC (Invitrogen, Carlsbad, CA).
[000809] Em um aspecto, sequências SPs e/ou prepro da invenção são identificadas seguindo a identificação de novos polipeptídeos de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. Os caminhos pelos quais proteínas são classificadas e transportadas para sua localização celular apropriada são frequentemente referidas como caminhos de direcionamento de proteínas. Um dos elementos mais importantes em todos estes sistemas de direcionamento é uma sequência de aminoácidos curta no término amino de um polipeptídeo recém sintetizado denominado a sequência de sinal. Esta sequência de sinal dirige uma proteína para sua localização apropriada na célula e é removida durante transporte ou quando a proteína atinge sua destinação final. A maioria das proteínas lisossômicas, de membrana, ou secretadas têm uma sequência de sinal de terminal amino que as marca para translocação para dentro do lúmen do retículo endoplasmático. Foram determinadas mais de 100 sequências de sinal paa proteínas neste grupo. As sequências de sinal podem variar de extensão de 13 a 36 resíduos aminoácido. Vários métodos de reconhecimento de sequências de sinal são conhecidos por aqaueles versados na técnica. Por exemplo, em um aspecto, novos peptídeos de sinal de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase são identificados por um referido método como SignalP. SignalP usa uma rede neural combinada a qual reconhece tanto peptídeos de sinal quanto seus sítios de clivagem. (Nielsen, et al., "Identification of prokaryotic and eukaryotic signal peptides and prediction of their cleavage sites." Protein Engineering, vol. 10, no. 1, p. 1-6 (1997).
[000810] Deve ser entendido que em alguns aspectos uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção pode não ter sequências SPs e/ou prepro, ou “domínios.” Em um aspecto, a invenção proporciona uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção carecendo de toda ou parte de uma SP e/ou um domínio prepro. Em um aspecto, a invenção proporciona uma sequência de ácido nucleico codificando uma sequência de sinal (SP) e/ou prepro de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase ligada operavelmente a uma sequência de ácido nucleico de uma glucanase diferente ou, opcionalmente, uma sequência de sinal (SPs) e/ou domínio prepro de uma proteína não-glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase pode ser desejada.
[000811] A invenção também proporciona polipeptídeos isolados ou recombinantes compreendendo sequências de sinal (SPs), domínio prepro e/ou domínios catalíticos (CDs) da invenção e sequências heterólogas. As sequências heterólogas são sequências não associadas naturalmente (por exemplo, a uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) com uma SP, domínio prepro e/ou CD. A sequência à qual a SP, domínio prepro e/ou CD não são naturalmente associadas pode estar sobre a extremidade de terminal amino da SP, do domínio prepro e/ou do CD, a extremidade de terminal carbóxi, e/ou sobre ambas as extremidades da SP e/ou CD. Em um aspecto, a invenção proporciona um polipeptídeo isolado ou recombinante compreendendo (ou consistindo em) um polipeptídeo compreendendo uma sequência de sinal (SP), domínio prepro e/ou domínio catalítico (CD) da invenção com a condição que não é associado com qualquer sequência à qual seja naturalmente associado (por exemplo, uma sequência de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase). Similarmente em um aspecto, a invenção proporciona ácidos nucleicos isolados ou recombinantes codificando estes polipeptídeos. Portanto, em um aspecto, o ácido nucleico isolado ou recombinante da invenção compreende sequência codificante para uma sequência de sinal (SP), domínio prepro e/ou domínio catalítico (CD) da invenção e uma sequência heteróloga (isto é, uma sequência não associada naturalmente com uma sequência de sinal (SP), domínio prepro e/ou domínio catalítico (CD) da invenção). A sequência heteróloga pode estar sobre a extremidade de terminal 3’, a extremidade de terminal 5’, e/ou sobre ambas as extremidades da sequência SP, de domínio prepro e/ou codificante CD.
Glucanase híbrida (quimérica), mananase, ou xilanase e bibliotecas de peptídeos
[000812] Em um aspecto, a invenção proporciona glucanases híbridas, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases e proteínas de fusão, incluindo bibliotecas de peptídeos, compreendendo sequências da invenção. As bibliotecas de peptídeos da invenção podem ser usadas para isolar moduladores peptídicos (por exemplo, ativadores ou inibidores) de alvos, tais como substratos de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, receptores, enzimas. As bibliotecas de peptídeos da invenção podem ser usadas para identificar parceiros de ligação formais de alvos, tais como ligantes, por exemplo, citocinas, hormônios e similares. Em um aspecto, a invenção proporciona proteínas quiméricas compreendendo uma sequência de sinal (SP), domínio prepro e/ou domínio catalítico (CD) da invenção ou uma combinação dos mesmos e uma sequência heteróloga (vide acima).
[000813] Em um aspecto, as proteínas de fusão da invenção (por exemplo, a porção peptídica) são estabilizadas conformacionalmente (em relação aos peptídeos lineares) para permitir uma maior afinidade de ligação para alvos. A invenção proporciona fusões de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção e outros peptídeos, incluindo peptídeos conhecidos e aleatórios. Podem ser fundidos em uma maneira tal que a estrutura de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase não é significativamente perturbada e o peptídeo é metabolicamente ou estruturalmente estabilizado conformacionalmente. Isto possibilita a criação de uma biblioteca de peptídeos que é facilmente monitorada tanto para sua presença dentro de células quanto sua quantidade.
[000814] Variantes de sequências de aminoácidos da invenção podem ser caracterizadas por uma natureza predeterminada da variação, uma característica que determina em seguida à parte de uma forma que ocorre naturalmente, por exemplo, uma variação alélica ou interespécies de uma sequência de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. Em um aspecto, as variantes da invenção apresentam a mesma atividade biológica qualitativa que o análogo que ocorre naturalmente. Alternativamente, as variantes podem ser selecionadas para terem características modificadas. Em um aspecto, apesar do sítio ou região para introduzir uma variação de sequência de aminoácidos ser predeterminado, a mutação per se não precisa ser predeterminada. Por exemplo, de modo a otimizar o desempenho de uma mutação em um dado sítio, mutagênese aleatória pode ser conduzida no códon ou região alvo e as variantes expressadas de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase triadas para a combinação ótima de atividade desejada. São de conhecimento geral técnicas para fazer mutações de substituição em sítios predeterminados em DNA tendo uma sequência conhecida, conforme discutido aqui, neste pedido de patente, por exemplo, mutagênese de iniciador M13 e mutagênese de PCR. Triagem dos mutantes pode ser feita usando, por exemplo, ensaios de hidrólise de glucano. Em aspectos alternativos, substituições de aminoácidos podem ser resíduos únicos; inserções podem ser da ordem de a partir de cerca de 1 a 20 aminoácidos, embora possam ser feitas inserções consideravelmente maiores. Eliminações podem variar a partir de cerca de 1 a cerca de 20, 30, 40, 50, 60, 70 resíduos ou mais. Para obter um derivado final com as propriedades ótimas, podem ser usadas substituições, eliminações, inserções ou qualquer combinação das mesmas. Geralmente, estas alterações são feitas sobre uns poucos aminoácidos para minimizar a alteração da molécula. No entanto, alterações maiores podem ser toleradas em algumas circunstâncias.
[000815] A invenção proporciona uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase onde a estrutura da estrutura principal do polipeptídeo, a estrutura secundária ou a terciária, por exemplo, uma estrutura alfa- helicoidal ou de folha beta, tenha sido modificada. Em um aspecto, a carga ou hidrofobicidade tenha sido modificada. Em um aspecto, o volume de uma cadeia lateral tenha sido modificada. Alterações substanciais na função ou identidade imunológica são feitas selecionando substituições que são menos conservadoras. Por exemplo, podem ser feitas substituições as quais mais significativamente afetam: a estrutura da estrutura principal do polipeptídeo na área da alteração, por exemplo, uma estrutura alfa- helicoidal ou uma estrutura folha beta; uma carga ou um sítio hidrofóbico da molécula, o qual pode estar em um sítio ativo; ou uma cadeia lateral. A invenção proporciona substituições no polipeptídeo da invenção onde (a) um resíduo hidrofílico, por exemplo, serila ou treonila, é substituído para (ou por) um resíduo hidrofóbico, por exemplo, leucila, isoleucila, fenilalanila, valila ou alanil; (b) uma cisteína ou prolina é substituída para (ou por) qualquer outro resíduo; (c) um resíduo tendo uma cadeia lateral eletropositiva, por exemplo, lisila, arginila, ou histidila, é substituído para (ou por) um resíduo eletronegativo, por exemplo, glutamila ou aspartil; ou (d) um resíduo tendo uma cadeia lateral volumosa, por exemplo, fenilalanina, é substituído para (ou por) um não tendo uma cadeia lateral, por exemplo, glicina. As variantes podem apresentar a mesma atividade biológica qualitativa (isto é, atividade de endoglucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase) embora variantes possam ser selecionadas para modificar as características da glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase conforme necessário.
[000816] Em um aspecto, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção compredem epitopos ou rótulos de purificação, sequências de sinal ou outras sequências de fusão, e etc. Em um aspecto, a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção pode ser fundida a um peptídeo aleatório para formar um polipeptídeo de fusão. Por "fundido" ou "ligado operavelmente" aqui, neste pedido de patente, se indica que o peptídeo aleatório e a glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase são ligados juntos, de uma tal maneira para minimizar a disrupção para a estabilidade da estrutura da glucanase, por exemplo, retém atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase. O polipeptídeo de fusão (ou fusão polinucleotídeo codificando o polipeptídeo de fusão) pode compreender componentes adicionais também, incluindo múltiplos peptídeos em múltiplas voltas.
[000817] Em um aspecto, os peptídeos e ácidos nucleicos codificando os mesmos são randomizados, quer totalmente randomizados ou são tendenciosos em sua randomização, por exemplo, em frequência de nucleotídeos/resíduos geralmente ou por posição. "Randomizados" significa que cada ácido nucleico e peptídeo consiste em nucleotídeos e aminoácidos essencialmente aleatórios, respectivamente. Em um aspecto, os ácidos nucleicos os quais dão origem aos peptídeos podem ser sintetizados quimicamente, e portanto podem incorporar qualquer nucleotídeo em qualquer posição. Portanto, quando os ácidos nucleicos são expressados para formar peptídeos, qualquer resíduo de aminoácido pode ser incorporado em qualquer posição. O processo sintético pode ser designado para gerar ácidos nucleicos randomizados, para permitir a formação de todas ou a maior partes das combinações possíveis por toda a extensão do ácido nucleico, portanto formando uma biblioteca de ácidos nucleicos randomizados. A biblioteca pode proporcionar uma população suficientemente estruturalmente diversa de produtos de expressão randomizados para afetar uma faixa probabilisticamente suficiente de respostas celulares para proporcionar uma ou mais células apresentando uma resposta desejada. Portanto, a invenção proporciona uma biblioteca de interação suficientemente grande de modo que pelo menos um de seus membros terá uma estrutura que lhe dá afinidade para alguma molécula, proteína, ou outro fator.
[000818] Endoglucanases são enzimas multidomínio que consistem opcionalmente em um peptídeo de sinal, um módulo de ligação de carboidrato, um domínio catalítico de glucanase, um encadeador e/ou outro domínio catalítico.
[000819] A invenção proporciona um meio para gerar polipeptídeos quiméricos os quais podem codificar polipeptídeos híbridos biologicamente ativos (por exemplo, glucanases híbridas, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases). Em um aspecto, o polinucleotídeos original codifica polipeptídeos biologicamente ativos. O método da invenção produz novos polipeptídeos híbridos utilizando processos celulares os quais integram a sequência dos polinucleotídeos originais de modo que o polinucleotídeo híbrido resultante codifica um polipeptídeo demonstrando atividades derivadas dos polipeptídeos biologicamente ativos originais. Por exemplo, os polinucleotídeos originais podem codificar uma enzima particular de diferentes micro-organismos. Uma enzima codificada por um primeiro polinucleotídeo de um organismo ou variante pode, por exemplo, funcionar efetivamente sob uma condição ambiental particular, por exemplo, alta salinidade. Uma enzima codificada por um segundo polinucleotídeo de um organismo ou variante diferente pode funcionar efetivamente sob uma condição ambiental diferente, tal como temperaturas extremamente elevadas. Um polinucleotídeo híbrido contendo sequências do primeiro e segundo polinucleotídeos originais pode codificar uma enzima a qual apresenta características de ambas as enzimas codificadas pelos polinucleotídeos originais. Portanto, a enzima codificada pelo polinucleotídeo híbrido pode funcionar de modo eficaz sob condições ambientais partilhadas por cada uma das enzimas codificadas pelos primeiro e segundo polinucleotídeos, por exemplo, alta salinidade e temperaturas extremas.
[000820] Um polipeptídeo híbrido resultante do método da invenção pode apresentar atividade enzimática especializada não apresentada nas enzimas originais. Por exemplo, depois de recombinação e/ou reagrupamento redutivo de polinucleotídeos codificando atividades de hidrolase, o polipeptídeo híbrido resultante codificado por um polinucleotídeo híbrido pode ser triado para atividades de hidrolase especializadas obtidas de cada uma das enzimas originais, isto é, o tipo de ligação sobre a qual a hidrolase age e a temperatura na qual a hidrolase funciona. Portanto, por exemplo, a hidrolase pode ser triada para discernir as funcionalidades químicas as quais distinguem a hidrolase híbrida das hidrolases originais, tais como: (a) amida (ligações peptídicas), isto é, endoglucanases; (b) ligações éster, isto é, esterases e lipases; (c) acetais, isto é, glicosidases e, por exemplo, a temperatura, o pH ou concentração salina na qual o polipeptídeo híbrido funciona.
[000821] Fontes dos polinucleotídeos originais podem ser isolados de organismos individuais (“isolados”), coleções de organismos que foram cultivados em meios definidos (“culturas de enriquecimento”), ou, organismos não cultivados (“amostras ambientais”). O uso de uma abordagem cultura-independente para derivar polinucleotídeos codificando novas bioatividades de amostras ambientais é mais preferêncial uma vez que permite acesso a recursos de biodiversidade não utilizados.
[000822] “Bibliotecas ambientais” são geradas a partir de amostras ambientais e representam os genomas coletivos de organismos que ocorrem naturalmente arquivados em vetores de clonagem que podem ser propagados em hospedeiros procarióticos adequados. Como o DNA clonado é inicialmente extraído diretamente de amostras ambientais, as bibliotecas não são limitadas à pequena fração de procariotas que podem ser cultivados em cultura pura. Adicionalmente, uma normalização do DNA ambiental presente nestas amostras pode permitir representação mais igual do DNA de todas as espécies presentes na amostra original. Isto pode aumentar dramaticamente a eficiência de descobrir genes interessantes de constituintes menores da amostra os quais podem ser sub-representados por várias ordens de magnitude comparados com a espécie dominante.
[000823] Por exemplo, bibliotecas genéticas geradas a partir de um ou mais micro-organismos não cultivados são triadas para uma atividade de interesse. Caminhos potenciais codificando moléculas bioativas de interesse são primeiro capturadas em células procarióticas sob a forma de bibliotecas de expressão genética. Polinucleotídeos codificando atividades de interesse são isolados de similares bibliotecas e introduzidos em uma célula hospedeira. A célula hospedeira é cultivada sob condições as quais promovem recombinação e/ou reagrupamento redutivo de biomoléculas potencialmente ativas com atividades novas ou reforçadas.
[000824] Adicionalmente, pode ser realizada subclonagem para isolar adicionalmente sequências de interesse. Na subclonagem, uma porção de DNA é amplificada, digerida, geralmente por enzimas de restrição, para cortar a sequência desejada, a sequência desejada é ligada em um vetor receptor e é amplificada. Em cada etapa na subclonagem, a porção é examinada para a atividade de interesse, de modo a assegurar que DNA que codifica a proteína estrutural não tenha sido excluído. O inserto pode ser purificado em qualquer etapa da subclonagem, por exemplo, por eletroforese por gel antes de ligação em um vetor ou onde células contendo o vetor receptor e células não contendo o vetor receptor são colocados sobre meio seletivo contendo, por exemplo, um antibiótico, o qual matará as células não contendo o vetor receptor. Métodos específicos de subclonagem de insertos de cDNA em vetores são de conhecimento geral na técnica (Sambrook et al., Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor Laboratory Press (1989)). Em outro aspecto, as enzimas da invenção são subclones. Os subclones referidos podem diferir do clone parental por, por exemplo, extensão, uma mutação, um rótulo ou um rótulo.
[000825] Em um aspecto, as sequências de sinal da invenção são identificadas depois de identificação de novos polipeptídeos de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. Os caminhos pelos quais proteínas são classificadas e transportadas para sua localização celular apropriada são frequentemente referidas como caminhos de direcionamento de proteínas. Um dos elementos mais importantes em todos estes sistemas de direcionamento é uma sequência de aminoácidos curta no término amino de um polipeptídeo recém sintetizado denominada a sequência de sinal. Esta sequência de sinal dirige uma proteína para sua localização apropriada na célula e é removida durante transporte ou quando a proteína atinge sua destinação final. A maioria das proteínas lisossômicas, de membrana, ou secretadas têm uma sequência de sinal de terminal amino que as marca para translocação para dentro do lúmen do retículo endoplasmático. Foram determinadas mais de 100 sequências de sinal para proteínas neste grupo. As sequências variam de extensão de 13 a 36 resíduos aminoácido. Vários métodos de reconhecimento de sequências de sinal são de conhecimento daqueles versados na técnica. Em um aspecto, os peptídeos são identificados por um referido método como SignalP. SignalP usa uma rede neural combinada a qual reconhece tanto peptídeos de sinal quanto seus sítios de clivagem. Vide, por exemplo, Nielsen (1997) “Identification of prokaryotic and eukaryotic signal peptides and prediction of their cleavage sites.” Protein Engineering, vol. 10, no. 1, p. 1-6. Deve ser entendido que algumas das glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta glucosidases da invenção podem ou não conter sequências de sinal. Pode ser desejável incluir uma sequência de ácido nucleico codificando uma sequência de sinal de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase ligada operavelmente a uma sequência de ácido nucleico de uma diferente glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase ou, opcionalmente, uma sequência de sinal de uma proteína não-glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase pode ser desejada.
[000826] Os micro-organismos a partir dos quais o polinucleotídeo pode ser preparado incluem micro-organismos procarióticos, tais como Eubacteria e Archaebacteria e micro-organismos eucarióticos menores tais como fungos, algumas algas e protozoários. Polinucleotídeos podem ser descobertos, isolados ou preparados a partir de amostras, tais como amostras ambientais, em cujo caso o ácido nucleico pode ser recuperado sem cultura de um organismo ou recuperado a partir de um ou mais organismos cultivados. Em um aspecto, os microorganismos referidos podem ser extremófilos, tais como hipertermófilos, psicrófilos, psicrotrofos, halófilos, barófilos e acidófilos. Podem ser usados polinucleotídeos codificando enzimas isoladas de micro-organismos extremofílicos. As enzimas referidas podem funcionar em temperaturas acima de 100oC em nascentes quentes terrestres e respiradouros térmicos de mares profundos, em temperaturas abaixo de 0oC em águas das regiões árticas, no ambiente salino saturado do Mar Morto, em valores de pH em torno de 0 em depósitos de hulha e nascentes ricas em enxofre geotérmicas, ou em valores de pH maiores do que 11 em lama de despejos. Por exemplo, várias esterases e lipases clonadas e expressadas a partir de organismos extremofílicos apresentam alta atividade através de uma ampla faixa de temperaturas e pHs.
[000827] Polinucleotídeos selecionados e isolados conforme descrito acima são introduzidos em uma célula hospedeira adequada. Uma célula hospedeira adequada é qualquer célula a qual é capaz de promover recombinação e/ou reagrupamento redutivo. Os polinucleotídeos selecionados em um aspecto já estão em um vetor o qual inclui sequências controle apropriadas. A célula hospedeira pode ser uma célula eucariótica maior, tal como uma célula de mamífero, ou uma célula eucariótica menor, tal como uma célula de levedura, ou em um aspecto, a célula hospedeira pode ser uma célula procariótica, tal como uma célula bacteriana. Introdução do construto na célula hospedeira pode ser efetuada por transfecção de fosfato de cálcio, transfecção mediada por DEAE-Dextrano, ou eletroporação (Davis et al., 1986).
[000828] Como exemplos representativos de hospedeiros apropriados, podem ser mencionados: células bacterianas, tais como E. coli, Streptomyces, Salmonella typhimurium; células fúngicas, tais como levedura; células de inseto tais como Drosophila S2 e Spodoptera Sf9; células animais tais como CHO, COS ou melanoma de Bowes; adenovírus; e células de plantas. A seleção de um hospedeiro apropriado é considerada como estando dentro do escopo dos versados na técnica a partir dos ensinamentos aqui, neste pedido de patente.
[000829] Com referências particulares a vários sistemas de cultura celular de mamíferos que podem ser empregados para expressar proteína recombinante, exemplos de sistemas de expressão de mamífero incluem as linhagens COS-7 de fibroblastos de rim de macaco, descritas em “SV40-transformed simian cells support the replication of early SV40 mutants” (Gluzman, 1981) e outras linhagens celulares capazes de expressar um vetor compatível, por exemplo, as linhagens celulares C127, 3T3, CHO, HeLa e BHK. Vetores de expressão de mamíferos compreenderão uma origem de replicação, um promotor adequado e reforçador e também quaisquer sítios de ligação de ribossoma necessários, sítio de poliadenilação, sítios doadores e aceitadores de junção, sequências de terminação transcricional e sequências não transcritas flanqueantes 5'. Sequências de DNA derivadas dos sítios de junção SV40 e de poliadenilação podem ser usadas para proporcionar os elementos genéticos não-transcritos requeridos.
[000830] Em outro aspecto, é previsto que o método da presente invenção pode ser usado para gerar novos polinucleotídeos codificando caminhos bioquímicos de um ou mais operons ou clusteres genéticos ou porções dos mesmos. Por exemplo, bactérias e muitos eucariotas têm um mecanismo coordenado para regular genes cujos produtos estão envolvidos em processos relacionados. Os genes são agrupados, em estruturas referidas como “clusteres genéticos,” sobre um único cromossoma e são transcritos juntos sob o controle de uma única sequência regulatória, incluindo um único promotor o qual inicia transcrição do cluster inteiro. Portanto, um cluster genético é um grupo de genes adjacentes que são ou idênticos ou relacionados, geralmente quanto a sua função. Um exemplo de um caminho bioquímico codificado pelos clusteres genéticos são policetídeos.
[000831] DNA do cluster genético pode ser isolado de diferentes organismos e ligado em vetores, particularmente vetores contendo sequências regulatórias de expressão as quais podem controlar e regular a produção de uma proteína detectável ou atividade de arranjo relacionada com proteína dos clusteres genéticos ligados. O uso de vetores os quais têm uma capacidade excepcionalmente grande para introdução de DNA exógeno é particularmente apropriado para uso com semelhantes clusteres genéticos e são descritos a título de exemplo aqui, neste pedido de patente, incluindo o fator f (ou fator de fertilidade) de E. coli. Este fator f de E. coli é um plasmídeo o qual afeta transferência em alta frequência de si próprio durante conjugação e é ideal para obter e propagar estavelmente grandes fragmentos de DNA, tais como clusteres genéticos de amostras microbianas mistas. Um aspecto é usar vetores de clonagem, referidos como "fosmídeos" ou vetores de cromossomas artificiais bacterianos (BAC). Estes são derivados do fator f de E. coli o qual é capaz de integrar estavelmente grandes segmentos de DNA genômico. Quando integrado com DNA de uma amostra ambiental não cultivada mista, isto torna possível obter grandes fragmentos genômicos sob a forma de uma “biblioteca de DNA ambiental” estável. Outro tipo de vetor para uso na presente invenção é um vetor de cosmídeo. Vetores de cosmídeo foram originalmente designados para clonar e propagar grandes segmentos de DNA genômico. Clonagem em vetores de cosmídeo é descrita em detalhes em Sambrook et al., Molecular Cloning: A Laboratory Manual, 2nd Ed., Cold Spring Harbor Laboratory Press (1989). Uma vez ligado em um vetor apropriado, dois ou mais vetores contendo diferentes clusteres genéticos de policetídeo sintase podem ser introduzidos em uma célula hospedeira adequada. Regiões de homologia de sequência parcial partilhada pelos clusteres genéticos promoverão processos os quais resultam em reorganização de sequência resultando em um cluster genético híbrido. O novo cluster genético híbrido pode ser então triado para atividades reforçadas não encontradas nos clusteres genéticos originais.
[000832] Portanto, em um um aspecto, a invenção se refere a um método para produzir um polipeptídeo híbrido biologicamente ativo e triar um polipeptídeo semelhante para atividade reforçada: 1) introduzindo pelo menos um primeiro polinucleotídeo em ligação operável e um segundo polinucleotídeo em ligação operável, os pelo menos primeiro polinucleotídeo e segundo polinucleotídeo partilhando pelo menos uma região de homologia de sequência parcial, em uma célula hospedeira adequada; 2) cultivando a célula hospedeira sob condições as quais promovem reorganização de sequência resultando em um polinucleotídeo híbrido em ligação operável; 3) expressando um polipeptídeo híbrido codificado pelo polinucleotídeo híbrido; 4) triando o polipeptídeo híbrido sob condições as quais promovem identificação de atividade biológica reforçada; e 5) isolando o um polinucleotídeo codificando o polipeptídeo híbrido. Métodos para triagem para várias atividades enzimáticas são de conhecimento daqueles versados na técnica e são discutidos do início ao fim da presente especificação. Os referidos métodos podem ser empregados ao isolar os polipeptídeos e polinucleotídeos da invenção.
Metodologias de Triagem e Dispositivos de Monitoramento “On-line”
[000833] Ao praticar os métodos da invenção, uma variedade de equipamentos e metodologias pode ser usada para em combinação com os polipeptídeos e ácidos nucleicos da invenção, por exemplo, para triar polipeptídeos para atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase (por exemplo, ensaios tais como hidrólise de caseína em zimogramas, a liberação de fluorescência de gelatina, ou a liberação de p-nitroanalida de vários substratos de peptídeos pequenos), para triar compostos como moduladores potenciais, por exemplo, ativadores ou inibidores, de uma atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, para anticorpos que ligam a um polipeptídeo da invenção, para ácidos nucleicos que hibridizam a um ácido nucleico da invenção, para triar células expressando um polipeptídeo da invenção e similares. Além dos formatos de arranjo descritos em detalhes abaixo para triar amostras, formatos alternativos também podem ser usadas para praticar os métodos da invenção. Os formatos referidos incluem, por exemplo, espectrômetros de massa, cromatógrafos, por exemplo, HPLC de alta produtividade e outras formas de cromatografia líquida, e formatos menores, tais como lâminas de 1536 cavidades, lâminas de 384 cavidades e assim por diante. Equipamento de triagem de alta produtividade pode ser adaptado e usado para praticar os métodos da invenção, vide, por exemplo, o Pedido de Patente dos Estados Unidos No. 20020001809.
Arranjos Capilares
[000834] Ácidos nucleicos ou polipeptídeos da invenção podem ser imobilizados a ou aplicados a um arranjo. Arranjos podem ser usados para triar para ou monitorar bibliotecas de composições (por exemplo, moléculas pequenas, anticorpos, ácidos nucleicos, e etc.) para sua capacidade para ligar a ou modular a atividade de um ácido nucleico ou um polipeptídeo da invenção. Arranjos de capilares, tais como a GIGAMATRIX®, Diversa Corporation, San Diego, CA; e arranjos descritos, por exemplo, no Pedido de Patente dos Estados Unidos No. 20020080350 A1; no Pedido de Patente Internacional No. WO 0231203 A; no Pedido de Patente Internacional No. WO 0244336 A, proporcionam um equipamento alternativo para encerrar e triar amostras. Em um aspecto, o arranjo de capilar inclui uma pluralidade de capilares formadas em um arranjo de capilares adjacentes, em que cada capilar compreende pelo menos uma parede definindo um lúmen para reter uma amostra. O lúmen pode ser cilíndrico, quadrado, hexagonal ou qualquer outra forma geométrica na medida que as paredes formam um lúmen para retenção de um líquido ou amostra. Os capilares do arranjo de capilares podem ser mantidos juntos em íntima proximidade para formar uma estrutura planar. Os capilares podem ser ligados juntos, sendo fundidos (por exemplo, onde os capilares são compostos de vidro), colados, ligados, ou grampeados lado a lado. Adicionalmente, o arranjo de capilares pode incluir material intersticial disposto entre capilares adjacentes no arranjo, deste modo formando um dispositivo planar sólido contendo uma pluralidade de furos de um lado a outro.
[000835] Um arranjo de capilares pode ser formada de qualquer número de capilares individuais, por exemplo, uma faixa de 100 a 4.000.000 capilares. Além disso, um arranjo de capilares tendo cerca de 100.000 ou mais capilares individuais pode ser formada no tamanho e formato de rotina de uma lâmina MICROTITER® para ajuste em equipamento de laboratório de rotina. Os lúmens são enchidos manualmente ou automaticamente usando ou ação capilar ou microinjeção usando uma agulha fina. Amostras de interesse podem ser subsequentemente removidas de capilares individuais para análise ou caracterização posterior. Por exemplo, uma sonda fina, semelhante a agulha é posicionada em communicação de fluidos com um capilar selecionado para ou adicionar ou retirar material do lúmen.
[000836] Em um ensaio de triagem de único pote, os componentes do ensaio são misturados produzindo uma solução de interesse, antes de inserção no arranjo de capilares. O lúmen é enchido por ação capilar quando pelo menos uma porção do arranjo é imersa em uma solução de interesse. Reações químicas ou biológicas e/ou atividade em cada capilar são monitoradas para eventos detectáveis. Um evento detectável é frequentemente referido como um “hit”, o qual pode ser usualmente distinguido de “não-hit” produzindo capilares por detecção ótica. Portanto, arranjos de capilares permitem detecção de “hits” massivamente paralela.
[000837] Em um ensaio de triagem multi-pote, um polipeptídeo ou ácido nucleico, por exemplo, um ligante, pode ser introduzido em um primeiro componente, o qual é introduzido em pelo menos uma porção de um capilar de um arranjo de capilares. Uma bolha de ar pode ser então introduzido no capilar atrás do primeiro componente. Um segundo componente pode ser então introduzida no capilar, em que o segundo componente é separado do primeiro componente pela bolha de ar. O primeiro e o segundo componentes podem ser então misturados aplicando pressão hidrostática em ambos os lados do arranjo de capilares para colapsar a bolha. O arranjo de capilares é então monitorado para um evento detectável resultante de reação ou não-reação dos dois componentes.
[000838] Em um ensaio de triagem de ligação, uma amostra de interesse pode ser introduzida como um primeiro líquido marcado com uma partícula detectável em um capilar de um arranjo de capilares, em que o lúmen do capilar é revestido com um material de ligação para ligar a partícula detectável ao lúmen. O primeiro líquido pode ser então removido do tubo capilar, em que a partícula detectável ligada é mantida dentro do capilar, e um segundo líquido pode ser introduzido no tubo capilar. O capilar é então monitorado para um evento detectável resultante de reação ou não-reação da partícula com o segundo líquido.
Arranjos, ou “Biochips”
[000839] Ácidos nucleicos ou polipeptídeos da invenção podem ser imobilizados ou aplicado a um arranjo. Arranjos podem ser usados para triar ou monitorar bibliotecas de composições (por exemplo, moléculas pequenas, anticorpos, ácidos nucleicos, e etc.) para sua capacidade para ligar a ou modular a atividade de um ácido nucleico ou um polipeptídeo da invenção. Por exemplo, em um aspecto da invenção, um parâmetro monitorado é expressão transcripta de um gene de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. Um ou mais, ou, todos os transcriptos de uma célula podem ser medidos por hibridização de uma amostra compreendendo transcriptos da célula, ou, ácidos nucleicos representativos de ou complementares a transcriptos de uma célula, por hibridização a ácidos nucleicos imobilizados sobre um arranjo, ou “biochip.” Usando um “arranjo” de ácidos nucleicos sobre um microchip, alguns ou todos os transcriptos de uma célula podem ser simultaneamente quantificados. Alternativamente, arranjos compreendendo ácido nucleico genômico também podem ser usadas para determinar o genótipo de uma cepa recém fabricada preparada pelos métodos da invenção. “Arranjos de polipeptídeos” também podem ser usadas para quantificar simultaneamente uma pluralidade de proteínas. A presente invenção pode ser praticada com qualquer “arranjo” conhecido, também referida como um “microarray” ou “arranjo de ácidos nucleicos” ou “arranjo de polipeptídeos” ou "arranjo de anticorpos" ou “biochip,” ou variação das mesmas. Arranjos são genericamente uma pluralidade de “pontos” ou “elementos alvo,” cada elemento alvo compreendendo uma quantidade definida de uma ou mais moléculas biológicas, por exemplo, oligonucleotídeos, imobilizados sobre uma área definida da superfície de um substrato para ligação específica a uma molécula da amostra, por exemplo, transcriptos de mRNA.
[000840] Os termos “arranjo” ou “microarray” ou “biochip” ou “chip” conforme usado aqui, neste pedido de patente, são uma pluralidade de elementos alvo, cada elemento alvo compreendendo uma quantidade definida de um ou mais polipeptídeos (incluindo anticorpos) ou ácidos nucleicos imobilizados sobre uma área definida da superfície de um substrato. Ao praticar os métodos da invenção, qualquer arranjo conhecido (incluindo “microarray” ou “biochip” ou “chip”) e/ou método para fabricar e usar arranjos podem ser incorporados no todo ou em parte, ou variações dos mesmos, conforme descrito, por exemplo, nas Patentes dos Estados Unidos Nos. 6.277.628; 6.277.489; 6.261.776; 6.258.606; 6.054.270; 6.048.695; 6.045.996; 6.022.963; 6.013.440; 5.965.452; 5.959.098; 5.856.174; 5.830.645; 5.770.456; 5.632.957; 5.556.752; 5.143.854; 5.807.522; 5.800.992; 5.744.305; 5.700.637; 5.556.752; 5.434.049; vide também, por exemplo, na patente WO 99/51773; na patente WO 99/09217; na patente WO 97/46313; na patente WO 96/17958; vide também, por exemplo, Johnston (1998) Curr. Biol. 8:R171-R174; Schummer (1997) Biotechniques 23:10871092; Kern (1997) Biotechniques 23:120-124; Solinas-Toldo (1997) Genes, Chromosomes & Cancer 20:399-407; Bowtell (1999) Nature Genetics Supp. 21:25-32. Vide também os pedidos de patente dos Estados Unidos publicados Nos. 20010018642; 20010019827; 20010016322; 20010014449; 20010014448; 20010012537;20010008765.
Anticorpos e métodos de triagem à base de anticorpos
[000841] A invenção proporciona anticorpos isolados, sintéticos ou recombinantes que ligam especificamente a uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção. Estes anticorpos podem ser usados para isolar, identificar ou quantificar uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção ou polipeptídeos relacionados. Estes anticorpos podem ser usados para isolar outros polipeptídeos dentro do escopo da invenção ou outras glucanases relacionadas, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases. Os anticorpos podem ser designados para ligar a um sítio ativo de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. Portanto, a invenção proporciona métodos para inibir glucanases, (ou celulases), por exemplo, endoglucanases, mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases usando os anticorpos da invenção (vide a discussão acima referente a aplicações para composições antiglucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção).
[000842] O termo “anticorpo” inclui um peptídeo ou polipeptídeo derivado de, modelado depois de ou substancialmente codificado por um gene de imunoglobulina ou genes de imunoglobulina, ou fragmentos dos mesmos, capaz de ligar especificamente um antígeno ou epitopo, vide, por exemplo, Fundamental Immunology, Third Edition, W.E. Paul, ed., Raven Press, N.Y. (1993); Wilson (1994) J. Immunol. Methods 175:267-273; Yarmush (1992) J. Biochem. Biophys. Methods 25:85-97. O termo anticorpo inclui porções de ligação de antígeno, isto é, “sítios de ligação de antígeno,” (por exemplo, fragmentos, subsequências, regiões determinantes de complementaridade (CDRs)) que retêm capacidade para ligar antígeno, incluindo (i) um fragmento Fab, um fragmento monovalente consistindo dos domínios VL, VH, CL e CH1; (ii) um fragmento F(ab')2, um fragmento bivalente compreendendo dois fragmentos Fab ligados por uma ponte dissulfeto na região de articulação; (iii) um fragmento Fd consistindo dos domínios VH e CH1; (iv) um fragmento Fv consistindo dos domínios VL e VH de um único braço de um anticorpo, (v) um fragmento dAb (Ward et al., (1989) Nature 341:544-546), o qual consiste em um domínio VH; e (vi) uma região determinante de complementaridade isolada (CDR). Anticorpos de cadeia única também são incluídos por meio de referência no termo "anticorpo."
[000843] A invenção proporciona fragmentos das enzimas da invenção, incluindo fragmentos imunogênicos de um polipeptídeo da invenção. A invenção proporciona composições compreendendo um polipeptídeo ou peptídeo da invenção e adjuvantes ou veículos e similares.
[000844] Os anticorpos podem ser usados em imunoprecipitação, mancha, colunas de imunoafinidade, e similares. Caso desejado, sequências de ácido nucleico codificando para antígenos específicos podem ser geradsa por imunização seguida por isolamento de polipeptídeo ou ácido nucleico, amplificação ou clonagem e imobilização de polipeptídeo sobre um arranjo da invenção. Alternativamente, os métodos da invenção podem ser usados para modificar a estrutura de um anticorpo produzido por uma célula a ser modificada, por exemplo, a afinidade de um anticorpo pode ser aumentada ou reduzida. Além disso, a capacidade para fabricar ou modificar anticorpos pode ser um fenótipo produzido em uma célula pelos métodos da invenção.
[000845] Métodos de imunização, produzindo e isolando anticorpos (policlonais e monoclonais) são conhecidos por aqueles versados na técnica e descritos na literatura científica e de patente, vide, por exemplo, Coligan, CURRENT PROTOCOLS IN IMMUNOLOGY, Wiley/Greene, NY (1991); Stites (eds.) BASIC AND CLINICAL IMMUNOLOGY (7th ed.) Lange Medical Publications, Los Altos, CA (“Stites”); Goding, MONOCLONAL ANTIBODIES: PRINCIPLES AND PRACTICE (2d ed.) Academic Press, New York, NY (1986); Kohler (1975) Nature 256:495; Harlow (1988) ANTIBODIES, A LABORATORY MANUAL, Cold Spring Harbor Publications, New York. Anticorpos também podem ser gerados in vitro, por exemplo, usando sítio de ligação de anticorpos recombinantes expressando bibliotecas de display de fago, além dos métodos tradicionais in vivo usando animais. Vide, por exemplo, Hoogenboom (1997) Trends Biotechnol. 15:62-70; Katz (1997) Annu. Rev. Biophys. Biomol. Struct. 26:27-45.
[000846] Os polipeptídeos da invenção ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos, também podem ser usados para gerar anticorpos os quais ligam especificamente aos polipeptídeos ou fragmentos. Os anticorpos resultantes podem ser usados em procedimentos de cromatografia por imunoafinidade para isolar ou purificar o polipeptídeo ou para determinar se o polipeptídeo está presente em uma amostra biológica. Os referidos procedimentos, uma preparação de proteína, tais como um extrato, ou uma amostra biológica é contactada com um anticorpo capaz de especificamente ligar a um dos polipeptídeos da invenção, ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos.
[000847] Em procedimentos de imunoafinidade, o anticorpo é fixado a um suporte sólido, tal como uma conta ou outra matriz de colunas. A preparação de proteína é colocada em contato com o anticorpo sob condições nas quais o anticorpo especificamente liga a um dos polipeptídeos da invenção, ou fragmentos dos mesmos. Depois de uma lavagem para remover proteínas ligadas não especificamente, os polipeptídeos ligados especificamente são elutriados.
[000848] A capacidade de proteínas em uma amostra biológica para ligar ao anticorpo pode ser determinada usando qualquer de uma variedade de procedimentos familiar daqueles versados na técnica. Por exemplo, a ligação pode ser determinada marcando o anticorpo com um rótulo detectável tal como um agente fluorescente, uma etiqueta enzimática, ou um radioisótopo. Alternativamente, a ligação do anticorpo à amostra pode ser detectada usando um anticorpo secundário tendo um rótulo detectável semelhante sobre o mesmo. Ensaios particulares incluem ensaios ELISA, ensaios sanduíche, radioimunoensaios e Western Blots.
[000849] Anticorpos policlonais gerados contra os polipeptídeos da invenção, ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos podem ser obtidos por injeção direta dos polipeptídeos em um animal ou administrando os polipeptídeos a um animal, por exemplo, um não humano. O anticorpo obtido deste modo ligará então o próprio polipeptídeo. Desta maneira, mesmo uma sequência codificando somente um fragmento do polipeptídeo pode ser usada para gerar anticorpos os quais podem ligar ao polipeptídeo nativo inteiro. Os anticorpos referidos podem ser então usados para isolar o polipeptídeo de células expressando este polipeptídeo.
[000850] Para preparação de anticorpos monoclonais, pode ser usada qualquer técnica a qual proporciona anticorpos produzidos por culturas de linhagens celulares contínuas. Exemplos incluem a técnica do hibridoma (Kohler and Milstein, Nature, 256:495-497, 1975), a técnica do trioma, a técnica do hibridoma de células B humanas (Kozbor et al., Immunology Today 4:72, 1983) e a técnica do EBV- hibridoma (Cole, et al., 1985, in Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, Inc., pp. 77-96).
[000851] Técnicas descritas para a produção de anticorpos de cadeia única (Patente dos Estados Unidos No. 4.946.778) podem ser adaptadas para produzir anticorpos de cadeia única para os polipeptídeos da invenção, ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos. Alternativamente, camundongos transgênicos podem ser usados para expressar anticorpos humanizados para estes polipeptídeos ou fragmentos dos mesmos.
[000852] Anticorpos gerados contra os polipeptídeos da invenção, ou fragmentos compreendendo pelo menos 5, 10, 15, 20, 25, 30, 35, 40, 50, 75, 100, ou 150 aminoácidos consecutivos dos mesmos podem ser usados em triagem para polipeptídeos similares de outros organismos e amostras. Em semelhantes técnicas, polipeptídeos do organismo são contactados com o anticorpo e são detectados os polipeptídeos os quais ligam especificamente o anticorpo. Quaisquer dos procedimentos descritos acima podem ser usados para detectar ligação de anticorpo. Um ensaio de triagem semelhante é descrito em “Methods for Measuring Celulase Activities”, Methods in Enzymology, Vol 160, pp. 87-116.
Kits
[000853] A invenção proporciona kits compreendendo as composições, por exemplo, ácidos nucleicos, cassetes de expressão, vetores, células, sementes ou plantas ou partes de plantas transgênicas, polipeptídeos (por exemplo, endoglucanases (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) e/ou anticorpos da invenção. Os kits também podem conter material instrucional ensinando as metodologias e usos industrial, agrícola, de pesquisa e medicinal da invenção, conforme descrito aqui, neste pedido de patente.
Engenharia celular completa e medição de parâmetros metabólicos
[000854] Os métodos da invenção proporcionam evolução celular completa, ou engenharia celular completa, de uma célula para desenvolver uma nova cepa celular tendo um novo fenótipo, por exemplo, uma atividade nova ou modificada de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase, modificando a composição genética da célula. A composição genética pode ser modificada por adição à célula de um ácido nucleico da invenção, por exemplo, uma sequência codificante para uma enzima da invenção. Vide, por exemplo, a patente WO0229032; e a patente WO0196551.
[000855] Para detectar o novo fenótipo, pelo menos um parâmetro metabólico de uma célula modificada é monitorado na célula em uma estrutura de tempo em “tempo real” ou “on-line”. Em um aspecto, uma pluralidade de células, tais como uma cultura celular, é monitorada em “tempo real” ou “on-line.” Em um aspecto, uma pluralidade de parâmetros metabólicos é monitorada em “tempo real” ou “on-line.” Parâmetros metabólicos podem ser monitorados usando uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção.
[000856] A análise do fluxo metabólico (MFA) se baseia em uma estrutura bioquímica conhecida. Uma matriz metabólica linearmente independente é construída com base na lei de conservação de massa e na hipótese de estado pseudo-estável (PSSH) sobre os metabólitos intracelulares. Ao praticar os métodos da invenção, são estabelecidas redes metabólicas, incluindo: • a identidade de todos os substratos do caminho, produtos e metabólitos intermediários • a identidade de todas as reações químicas interco- nvertendo os metabólitos do caminho, a estequiometria das reações do caminho, • a identidade de todas as enzimas catalisando as reações, a cinética da reação enzimática, • as interações regulatórias entre componentes do caminho, por exemplo, interações alostéricas, interações enzima-enzima e etc, • compartimentalização intracelular de enzimas ou qualquer outra organização supramolecular das enzimas, e, • a presença de qualquer concentração de gradientes de metabólitos, enzimas ou moléculas efetoras ou barreiras de difusão para seu movimento.
[000857] Uma vez que a rede metabólica para uma dada cepa é construída, a apresentação matemática por noção de matriz pode ser introduzida para estimar os fluxos intracelulares metabólicos se os dados de metaboloma on-line estiverem disponíveis. O fenótipo metabólico se baseia nas alterações de toda a rede metabólica dentro de uma célula. O fenótipo metabólico se baseia na alteração da utilização do caminho com respeito às condições ambientais, à regulação genética, ao estado de desenvolvimento e ao genótipo, e etc. Em um aspecto dos métodos da invenção, depois do cálculo de MFA on-line, o comportamento dinâmico das células, seu fenótipo e outras propriedades são analisados investigando a utilização do caminho. Por exemplo, se o suprimento de glicose for aumentado e o oxigênio reduzido durante a fermentação da levedura, a utilização de caminhos respiratórios será reduzida e/ou interrompida, e a utilização dos caminhos fermentativos dominarão. Controle do estado fisiológico de culturas celulares se tornará possível depois da análise do caminho. Os métodos da invenção podem ajudar a determinar como manipular a fermentação determinando como alterar o suprimento de substrato, a temperatura, o uso de indutores, e etc. para controlar o estado fisiológico das células para mover ao longo da direção desejável. Ao praticar os métodos da invenção, os resultados de MFA também podem ser comparados com dados de transcriptoma e proteoma para planejar experimentos e protocolos para engenharia metabólica ou embaralhamento genético, e etc.
[000858] Ao praticar os métodos da invenção, qualquer fenótipo modificado ou novo pode ser conferido e detectado, incluindo características novas ou aprimoradas na célula. Qualquer aspecto do metabolismo ou do crescimento pode ser monitorado.
Monitoramento da expressão de um transcripto de mRNA
[000859] Em um aspecto da invenção, o fenótipo produzido por engenharia compreende aumentar ou reduzir a expressão de um transcripto de mRNA (por exemplo, uma mensagem de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) ou gerando novos transcriptos (por exemplo, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase) em uma célula. Esta expressão aumentada ou reduzida pode ser traçada testante para a presença de uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção ou por ensaios da atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase. Transcriptos de mRNA, ou mensagens, também podem ser detectados e quantificados por qualquer método conhecido na técnica, incluindo, por exemplo, Northern blots, reações de amplificação quantitativa, hibridização o arranjos, e similares. Reações de amplificação quantitativa incluem, por exemplo, PCR quantitativo, incluindo, por exemplo, reação de cadeia polimerase de transcrição reversa quantitativa, ou RT-PCR; RT-PCR em tempo real quantitativa, ou “RT-PCR cinética em tempo real” (vide, por exemplo, Kreuzer (2001) Br. J. Haematol. 114:313-318; Xia (2001) Transplantation 72:907-914).
[000860] Em um aspecto da invenção, o fenótipo produzido por engenharia é gerado por esvaziamento da expressão de um gene homólogo. A sequência codificante do gene ou um ou mais elementos controle transcricionais pode ser eliminada por, por exemplo, promotores ou reforçadores. Portanto, a expressão de um transcripto pode ser completamente removida por ablação ou somente reduzida.
[000861] Em um aspecto da invenção, o fenótipo produzido por engenharia compreende aumentar a expressão de um gene homólogo. Isto pode ser efetuado por esvaziamento de um elemento controle negativo, incluindo um elemento regulatório transcricional agindo em cis- ou trans- , ou, mutagenizando um elemento controle positivo. Um ou mais, ou, todos os transcriptos de uma célula podem ser medidos por hibridização de uma amostra compreendendo transcriptos da célula, ou, ácidos nucleicos representativos de ou complementares a transcriptos de uma célula, por hibridização a ácidos nucleicos imobilizados sobre um arranjo.
Monitoramento da expressão de alguns polipeptídeos, peptídeos e aminoácidos
[000862] Em um aspecto da invenção, o fenótipo produzido compreende aumentar ou reduzir a expressão de um polipeptídeo (por exemplo, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) ou gerar novos polipeptídeos em uma célula. Esta expressão aumentada ou reduzida pode ser traçada determinando a quantidade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase presente ou por ensaios de atividade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase. Polipeptídeos, peptídeos e aminoácidos também podem ser detectados e quantificados por qualquer método conhecido na técnica, incluindo, por exemplo, ressonância magnética nuclear (NMR), espectrofotometria, radiografia (radiomarcação protéica), eletroforese, eletroforese capilar, cromatografia líquida de alto desempenho (HPLC), cromatografia de camada fina (TLC), cromatografia de hiperdifusão, vários métodos imunológicos, por exemplo, imunoprecipitação, imunodifusão, imunoeletroforese, radioimunoensaios (RIAs), ensaios de imunossorvente ligado a enzima (ELISAs), ensaios de imunofluorescente, eletroforese por gel (por exemplo, SDS-PAGE), mancha com anticorpos, classificador celular ativado por fluorescente (FACS), pirólise espectrometria de massa, Espectrometria Infravermelho de Transform de Fourier, espectrometria de Raman, GC-MS, e espectrometrias de massa de LC-Electropulverização e de cap-LC- tandem-electropulverização, e similares. Novas bioatividades também podem ser triadas usando métodos, ou variações dos mesmos, descritos na Patente dos Estados Unidos No. 6.057.103. Além disso, um ou mais, ou, todos os polipeptídeos de uma célula podem ser medidos usando um arranjo de proteína.
Aplicações Industriais, de Perfuração, de Energia, Agrícolas, de Pesquisa e Medicinais
[000863] A invenção proporciona muitas aplicações industriais, de perfuração, energia, agrícolas, de pesquisa e medicinais para os polipeptídeos, incluindo enzimas, peptídeos, anticorpos, e “coquetéis de enzimas” da invenção, incluindo por exemplo, os polipeptídeos da invenção tendo glucanase, mananase ou atividade de xilanase. Os polipeptídeos da invenção podem ser usados em processamento de alimentos (por exemplo, processamento de pão e massa de pão), fermentação, aditivos de banho, produção de álcool, síntese de peptídeos, enantiosseletividade, preparação de couro na indústria de couro, tratamento de resíduos e degradação animal, tratamento médico, degradação de biofilme, conversão de biomassa em etanol, biodefesa, agentes antimicrobianos e desinfetantes, cuidados pessoais e cosméticos, reagentes biotech, hidrólise, dissolução ou decomposição de uma composição compreendendo glucano, como auxiliares digestivos ou farmacêuticos, por exemplo, como agentes antiinflamatórios (antiflogísticos), e/ou na indústria de energia, de óleo ou gás. O método e composições (por exemplo, os “coquetéis de enzimas”) da invenção podem ser usados em qualquer processo de descoberta e/ou perfuração de óleo ou gás, ou qualquer processo de lavagem e/ou fraturamento de poço de óleo e gás.
[000864] Em uma modalidade, combinações de enzimas podem ser usadas. Uma mistura de enzimas ou um “coquetel de enzimas” pode incluir, mas não está limitada a, qualquer combinação de enzimas tais como xilanases, esterases, celulases, pectinases, pectate liases, amilases, decarboxilases, lacases, glucanases, proteases, peptidases, proteinases, amiloglucosidases, glicose isomerases, glucoamilases, beta-glucanases, endo-beta-1,3(4)-glucanases, hemicelulases, endoglicosidases, endo-beta.-1,4- glucanases, glicosiltransferases, fosfolipases, lipo-oxigenases, redutases, oxidases, fenoloxidases, ligninases, pululanases, arabinanases, outras mananases, xiloglucanases, pectina acetila esterases, ramnogalacturonano acetil esterases, poligalacturonases, ramnogalacturonases, galactanases, transglutaminases, pectina metilesterases, celobio-hidrolases e/ou transglutaminases. As enzimas glucanase, mananase ou xilanase da invenção podem ser combinadas umas com as outras ou com enzimas adicionais.
[000865] As enzimas glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção podem ser catalisadores altamente seletivos. Podem catalisar reações com excelentes estereo-, regio- e quimio- seletividades que não têm paralelo na química sintética convencional. Além disso, enzimas são exraordinariamente versáteis. As enzimas da invenção podem ser talhadas para funcionar em solventes orgânicos, operar em pHs extremos (por exemplo, pHs elevados e pHs baixos) temperaturas extremas (por exemplo, temperatura elevadas e baixas temperaturas), níveis de salinidade extrema (por exemplo, alta salinidade e baixa salinidade) e catalisar reações com compostos que são estruturalmente não relacionados com seus substratos fisiológicos naturais.
Composições de Detergentes
[000866] A invenção proporciona composições de detergentes compreendendo um ou mais polipeptídeos (por exemplo, endoglucanases (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) da invenção, e métodos para produzir e usar estas composições. A invenção incorpora todos os métodos para produzir e usar composições de detergentes, vide, por exemplo, as Patentes dos Estados Unidos Nos. 6.413.928; 6.399.561; 6.365.561; 6.380.147.
[000867] As composições de detergentes podem ser uma composição aquosa de uma e duas partes, uma composição líquida não-aquosa, um sólido fundido, uma forma granular, uma forma particulada, um comprimido comprimido, um gel e/ou uma pasta e uma forma de pasta semifluida. As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção também podem ser usadas como um produto aditivo de detergente em uma forma sólida ou uma forma líquida. Os produtos aditivos referidos são pretendidos para suplementar ou reforçar o desempenho de composições de detergentes convencionais e podem ser adicionados em qualquer estágio do processo de limpeza.
[000868] O teor de enzima ativa real depende do método de fabricação de uma composição detergente e não é crucial, presumindo que a solução detergente tenha a atividade desejada enzimática desejada. Em um aspecto, a quantidade de glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase presente na solução final varia a partir de cerca de 0,001 mg a 0,5 mg por grama da composição detergente. A enzima em particular escolhida para uso no processo e nos produtos desta invenção depende das condições de utilidade final, incluindo a forma física do produto, pH em uso, temperatura em uso, e tipos de solo a serem degradados ou alterados. A enzima pode ser escolhida para proporcionar ativiade ótima e estabilidade para qualquer série dada de condições de utilidade. Em um aspecto, as glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da presente invenção são ativas nas faixas de pH de a partir de cerca de 4 a cerca de 12 e na faixa de temperatura de a partir de cerca de 20oC a cerca de 95oC. Os detergentes da invenção podem compreender tensoativos catiônicos, não-iônicos semi-polares ou zviterônicos; ou, misturas dos mesmos.
[000869] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser formuladas em detergentes em pó e líquidos tendo pH entre 4,0 e 12,0 em níveis de cerca de 0,01 a cerca de 5% (em um aspecto 0,1% a 0,5%) em peso. Estas composições de detergentes também podem incluir outras enzimas tais como outras glucanases, mananases, ou xilanases, ou celulases, endoglicosidases, endo-beta.-1,4-glucanases, beta-glucanases, endo-beta-1,3(4)-glucanases, catalases, cutinases, peroxidases, lacases, lipases, amilases, glucoamilases, pectinases, redutases, oxidases, fenoloxidases, ligninases, pululanases, arabinanases, hemicelulases, mananases, xiloglucanases, pectina acetila esterases, ramnogalacturonano acetil esterases, poligalacturonases, ramnogalacturonases, galactanases, proteases, pectate liases, pectina metilesterases, celobio-hidrolases e/ou transglutaminases. Estas composições de detergentes também podem incluir reforçadores e estabilizantes. Estas composições de detergentes também podem incluir reforçadores e estabilizantes.
[000870] A adição de uma glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção a composições de limpeza convencionais não cria qualquer limitação de uso especial. Em outras palavras, qualquer temperatura e pH adequado para o detergente também é adequado para a composições da invenção na medida que a enzima seja ativa em ou tolerante ao pH e/ou à temperatura do uso pretendido. Além disso, uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção pode ser usada em uma composição de limpeza sem detergentes, novamente ou sozinha ou em combinação com reforçadores e estabilizantes.
[000871] A presente invenção proporciona composições de limpeza incluindo composições de detergente para limpar superfícies duras, composições de detergente para limpar tecidos, composições para lavar louças, composições para limpeza oral, composições para limpeza de dentadura, e soluções para limpeza de lentes de contato.
[000872] Em um aspecto, a invenção proporciona um método para lavar um objeto compreendendo contatar o objeto com um polipeptídeo da invenção sob condições suficientes para lavar. Uma glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase da invenção pode ser incluída como um aditivo de detergente. A composição de detergente da invenção pode ser formulada, por exemplo, como uma composição de detergente para lavar roupa manualmente ou à máquina compreendendo um polipeptídeo da invenção. Um aditivo para lavar roupa adequado para pré-tratamento de tecidos tingidos pode compreender um polipeptídeo da invenção. Uma composição de amaciante de tecido pode compreender uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase da invenção.
[000873] Alternativamente, uma glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta glucosidase da invenção pode ser formulada como uma composição de detergente para uso em operações de limpeza de superfícies duras domésticas gerais. Em aspectos alternativos, aditivos de detergente e composições de detergente da invenção podem compreender uma ou mais outras enzimas tais como outra glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase, ou, uma xilanase, uma lipase, uma cutinase, uma carboidrase, uma celulase, uma pectinase, uma arabinase, uma galactanase, uma oxidase, por exemplo, uma lactase, e/ou uma peroxidase (vide também, acima). As propriedades da uma ou mais enzimas da invenção são escolhidas para serem compatíveis com o detergente selecionado (isto é, pH ótimo, compatibilidade com outros ingredientes enzimáticos e não- enzimáticos, e etc.) e a uma ou mais enzimas estão presentes em quantidades eficazes. Em um aspecto, as enzimas da invenção são usadas para remover materiais malcheirosos de tecidos. Várias composições de detergente e métodos para fabricar as mesmas que podem ser usadas ao praticar a invenção são descritas, por exemplo, nas Patentes dos Estados Unidos Nos. 6.387.690; 6.333.301; 6.329.333; 6.326.341; 6.297.038; 6.309.871; 6.204.232; 6.197.070; 5.856.164.
[000874] Enzimas da invenção podem ser usadas em um agente detergente ou de limpeza compreendendo uma dispersão de partículas sólidas em um agente de dispersão, por exemplo, um polímero não-iônico tal como polietileno glicol ou polipropileno glicol, conforme descrito, por exemplo, no Pedido de Patente dos Estados Unidos No. 20060122089. Enzimas da invenção podem ser usadas em uma partícula solúvel em água e/ou dispersível em água, por exemplo, compreendendo um álcool polivinílico, conforme descrito por exemplo, no Pedido de Patente dos Estados Unidos No. 20050075261.
[000875] Enzimas da invenção podem ser usadas em um detergente, por exemplo, um detergente para lavar louças manualmente, eficaz na remoção de sujeiras de resíduos cozidos, assados, ou queimados conforme descrito, por exemplo, no Pedido de Patente dos Estados Unidos No. 20060281653.
[000876] Quando formuladas como composições adequadas para uso em um método de lavagem em máquina de lavar roupa, as enzimas da invenção podem compreender tanto um tensoativo quanto um composto reforçador. Podem compreender adicionalmente um ou mais componentes detergentes, por exemplo, compostos poliméricos orgânicos, agentes de alvejamento, enzimas adicionais, supressores de espuma de sabão, dispersantes, dispersantes de sabão de cal, agentes de suspensão e antirredeposição de mancha e inibidores de corrosão. As composições, para lavar roupa, da invenção também podem conter agentes amaciantes, como componentes detergentes adicionais. As composições referidas contendo carboidrase podem proporcionar limpeza de tecido, remoção de mancha, manutenção da brancura, amaciamento, aspecto da cor, inibição de transferência de corante e sanitização quando formuladas como composições de detergente para lavar roupa.
[000877] A densidade das composições de detergente para lavar roupa da invenção pode variar a partir de cerca de 200 a 1500 g/litro, ou cerca de 400 a 1200 g/litro, ou, cerca de 500 a 950 g/litro, ou, 600 a 800 g/litro, da composição; esta pode ser medida a cerca de 20oC.
[000878] A forma "compacta" das composições de detergente da invenção para lavar roupa é melhor refletida pela densidade e, em termos da composição, pela quantidade de sal de enchimento inorgânico. Sais de enchimento inorgânicos são ingredientes convencionais de composições de detergente em forma de pó. Em convencional composições de detergente, os sais de enchimento estão presentes em quantidades substanciais, tipicamente 17% a 35% em peso da composição total. Em um aspecto das composições compactas, o sal de enchimento está presente em quantidades não excedendo 15% da composição total, ou, não excedendo 10%, ou, não excedendo 5% em peso da composição. Os sais de enchimento inorgânicos pode ser selecionados entre os sais de metais de álcali e terrosos alcalinos de sulfatos e cloretos, por exemplo, sulfato de sódio.
[000879] As composições de detergente líquido da invenção também podem estar em uma "forma concentratada." Em um aspecto, as composições de detergente líquido podem conter uma quantidade menor de água, comparadas com detergentes líquidos convencionais. Em aspectos alternativos, o teor de água do detergente líquido concentrado é menos de 40%, ou, menos de 30%, ou, menos de 20% em peso da composição de detergente. Compostos detergentes da invenção podem compreender formulações conforme descrito na patente WO 97/01629.
[000880] Enzimas da invenção podem ser úteis para formular várias composições de limpeza. Uma série de compostos conhecidos são tensoativos adequados incluindo detergentes não-iônicos, aniônicos, catiônicos, ou zviteriônicos, podem ser usados, por exemplo, conforme divulgado nas Patentes dos Estados Unidos Nos. 4.404.128; 4.261.868; 5.204.015. Além disso, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas, por exemplo, em aplicações de sabão em barra ou líquido, formulações para tratamento de pratos, soluções ou produtos para limpeza de lentes de contato, hidrólise de peptídeo, tratamento de refugo, aplicações têxteis, como enzimas de clivagem por fusão na produção de proteína, e similares. Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem proporcionar desempenho reforçado em uma composição de detergente comparadas com outra glucanase detergente, isto é, o grupo enzimático pode aumentar a limpeza de algumas manchas sensíveis a enzima tais como grama ou sangue, conforme determinado por avaliação usual depois de um ciclo de lavagem de rotina. Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser formuladas em detergentes em pó e líquidos conhecidos tendo pH entre 6,5 e 12,0 em níveis de cerca de 0,01 a cerca de 5% (por exemplo, cerca de 0,1% a 0,5%) em peso. Estas composições de limpeza detergentes também podem incluir outras enzimas tais como glucanases, mananases, xilanases, amilases, celulases, lipases ou endoglicosidases conhecidas, bem como reforçadores e estabilizantes.
[000881] As composições de detergente da invenção, por exemplo, aquelas compreendendo glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção, também podem ser usadsa para limpar frutos, legumes e/ou compostos de lama e argila; vide, por exemplo, a Patente dos Estados Unidos No. 5.786.316.
[000882] Em um aspecto, a invenção proporciona composições de detergente tendo atividade de glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase (uma glucanase, (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção) para uso com frutos, legumes e/ou compostos lama e argila (vide, por exemplo, a Patente dos Estados Unidos No. 5.786.316).
Tratando fibras e têxteis
[000883] A invenção proporciona métodos para tratar fibras, têxteis, panos, fios, tecidos e similares, usando uma ou mais glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção. As enzimas da invenção podem ser usadas em quaisquer métodos de tratameno de têxteis, fios, panos, fibras ou tecidos, os quais são de conhecimento geral na técnica, vide, por exemplo, a Patente dos Estados Unidos No. 6.387.690; 6.261.828; 6.077.316; 6.024.766; 6.021.536; 6.017.751; 5.980.581; Publicação de Pedido de Patente dos Estados Unidos No. 20020142438 A1.
[000884] Por exemplo, as enzimas da invenção podem ser usadas em desengomação de fibras e/ou tecidos. Em um aspecto, a sensação e o aspecto de um tecido é aprimorado por um método compreendendo contatar o tecido com uma enzima da invenção em uma solução. Em um aspecto, o tecido é tratado com a solução sob pressão. Por exemplo, as enzimas da invenção podem ser usadas na remoção de manchas. Portanto, em outro aspecto, a invenção proporciona fibras, têxteis, panos, fios, tecidos e similares compreendendo um polipeptídeo da invenção.
[000885] Em um aspecto, as enzimas da invenção são aplicadas durante ou depois da tecedura de têxteis, ou durante o estágio de desengomação, ou durante uma ou mais etapas adicionais de processamento de tecido. Durante a tecedura de têxteis, os fios são expostos a considerável tensão mecânica. Antes de tecedura sobre teares mecânicos, os fios de urdidura são frequentemente revestidos com engomação com amido ou derivados de amido de modo a aumentar sua força de tração e a evitar ruptura. Depois dos têxteis terem sido tecidos, um tecido pode prosseguir para to um estágio de desengomação. Este pode ser seguido por uma ou mais etapas adicionais de processamento de tecido. Desengomação é o ato de remover “goma” de têxteis. Depois da tecedura, o revestimento de goma deve ser removido antes de processar adicionalmente o tecido de modo a assegurar um resultado homogêneo e à ensaio de lavagem.
[000886] As enzimas da invenção podem ser usadas para tratar qualquer material celulósico, incluindo fibras (por exemplo, fibras de algodão, cânhamo, fibra do linho ou linho), tecidos costurados e não costurados, por exemplo, malhas, tecelagens, brins, fios, e panos para toalhas, feitos de algodão, misturas de algodão ou celulósicas naturais ou artificiais (por exemplo, originárias de fibras de celulose compreendendo glucano tal como de polpa de madeira) ou misturas das mesmas. Exemplos de misturas são misturas de algodão ou raion/viscose com um ou mais material associado tal como lã, fibras sintéticas (por exemplo, fibras de poliamida, fibras acrílicas, fibras de poliéster, fibras de álcool polivinílico, fibras de cloreto polivinílico, fibras de cloreto de polivinilideno, fibras de poliuretano, fibras de poliuréia, fibras de aramida), e fibras contendo celulose (por exemplo, raion/viscose, rami, cânhamo, linho/fibra de linho, juta, fibras de acetato celulósico, lyocell).
[000887] As enzimas da invenção podem ser usadas para tratar tecidos ou qualquer material compreendendo glucano, mananano, xilano ou celulose, incluindo tecidos contendo algodão, como aditivos de detergentes, por exemplo, em composições aquosas. Para a fabricação de roupas, o tecido pode ser cortado e costurado em panos ou roupas. Estes podem ser acabados antes ou depois do tratamento. Em particular, para a fabricação de jeans de denim, foram desenvolvidos diferentes métodos de acabamento enzimático. O acabamento de roupas de denim normalmente é iniciado com uma etapa de desengomação enzimática, durante a qual as roupas são submetidas à ação de enzimas amilolíticas de modo a proporcionar maciez ao tecido e tornar o algodão mais acessível às etapas de acabamento enzimático subsequentes. A invenção proporciona métodos para tratar têxteis, por exemplo, acabamento de roupas de denim, desengomação enzimática e proporcionando maciez aos tecidos usando qualquer combinação de enzimas, tais como, mananases, xilanases, ou glucanases (por exemplo, endoglucanases) da invenção. Em um aspecto, as enzimas da invenção podem ser usadas em tratamentos para prevenir o acinzentamento de um têxtil.
[000888] Em um aspecto, algumas mananases, xilanases, e glucanases (por exemplo, endoglucanases) alcalinas e/ou termoestáveis da invenção são combinadas em um único banho de desengomação e biorremoção de óleo, graxa e sujidade que adere mecanicamente ao tecido. Entre vantagens de combinar desengomação e remoção de óleo, graxa e sujidade que adere mecanicamente ao tecido em uma etapa são redução do custo e menor impacto ambiental devido a economia de energia e de uso de água e menor produção de refugo. As condições de aplicação para desengomação e biorremoção de óleo, graxa e sujidade que adere mecanicamente ao tecido podem ser entre cerca de pH 8,5 a pH 10,0 e temperaturas a cerca de 40oC e acima. Podem ser usadas baixas dosagens de enzima (por exemplo, cerca de 5 g por uma tonelada de algodão) e curtos tempos de reação (por exemplo, cerca de 15 minutos) para obter desengomação e remoção de óleo, graxa e sujidade que adere mecanicamente ao tecido eficientes sem adição de cálcio.
[000889] As enzimas da invenção podem ser usadas no tratamento de tecidos contendo celulose para redução da aspereza, para clarificação da cor, ou para proporcionar uma variação localizada na cor de similares tecidos. Vide, por exemplo, a Patente dos Estados Unidos No. 6.423.524. Por exemplo, as enzimas da invenção podem ser usadas para reduzir a aspereza de tecidos contendo algodão, por exemplo, como um aditivo de detergente reduzindo a aspereza. As enzimas da invenção podem ser usadas no tratamento de tecidos para proporcionar um aspecto desgastado ("stonewashed") em um tecido colorido ao mesmo tempo que reduzindo a quantidade de redeposição de colorante sobre o tecido.
[000890] Os processos de tratamento de têxteis da invenção (usando as enzimas da invenção) podem ser usados em combinação com outros tratamentos de têxteis, por exemplo, e alvejamento. (Scouring) é a remoção de material não-celulósico da fibra de algodão, por exemplo, a cutícula (consistindo essencialmente em ceras) e parede celular primária (consistindo essencialmente em pectina, proteína e xiloglucano). Uma remoção de cera apropriada é necessária para obter uma alta umidificabilidade. Isto é, necerrário para o corante. A remoção das paredes celulares primárias pelos processos da invenção melhora a remoção de cera e assegura um corante mais uniforme. Tratar têxteis com os processos da invenção pode melhorar a brancura no processo de alvejamento. O principal produto químico usado em remoção de óleo, é sódio, hidróxido em altas concentrações e em temperaturas elevadas. Alvejamento compreende oxidação do têxtil. O alvejamento tipicamente envolve uso de peróxido de hidrogênio como o agente oxidante de modo ou a obter um tecido totalmente alvejado (branco) ou a assegurar um matiz limpo do corante.
[000891] A invenção também proporciona glucanases (por exemplo, endoglucanases ativa sob condições alcalinas), mananases, ou xilanases alcalinas. Estas têm aplicações amplas em processamento de têxteis, desengomação de fibras vegetais (por exemplo, fibras do floema da planta), tratamento de refugo, por exemplo, águas usadas pécticas, fabricação de papel, e fermentações de café e chá. Vide, por exemplo, Hoondal (2002) Applied Microbiology and Biotechnology 59:409-418.
[000892] Os processos de tratamento de têxteis da invenção também podem incluir o uso de qualquer combinação de outras enzimas (incluindo enzimas de degradação de carboidrato) tais como catalases, outras glucanases, celulases, lipases, endoglicosidases, endo-beta.- 1,4-glucanases, beta-glucanases, endo-beta-1,3(4)-glucanases, cutinases, peroxidases, lacases, amilases, glucoamilases, pectinases, redutases, oxidases, fenoloxidases, ligninases, pululanases, arabinanases, hemicelulases, outras mananases, xiloglucanases, outras xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, proteases, poligalacturonases, ramnogalacturonases, galactanases, pectate liases, pectina metilesterases, celobio- hidrolases e/ou transglutaminases. As enzimas da invenção podem ser usadas em combinação com outras enzimas de degradação de carboidrato, por exemplo, celulase, arabinanase, xiloglucanase, pectinase, xilanase, e similares, para a preparação de fibras ou para limpeza de fibras. Proteases também podem ser usadas em uma combinação de enzimas da invenção. Estas podem ser usadas em combinação com detergentes.
Tratando alimentos e processamento de alimentos
[000893] As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção têm numerosas aplicações na indústria de processamento de alimentos. Por exemplo, em um aspecto, as enzimas da invenção são usadas para melhorar a extração de óleo material vegetal rico em óleo, por exemplo, sementes ricas em óleo, por exemplo, óleo de soja de feijões-soja, azeite de oliva de azeitonas, óleo de colza de colza e/ou óleo de girassol de sementes de girassol.
[000894] As enzimas da invenção podem ser usadas para separação de componentes de materiais de células de plantas. Por exemplo, as enzimas da invenção podem ser usadas na separação de material rico em glucano (por exemplo, células de plantas) em componentes. Em um aspecto, as enzimas da invenção podem ser usadas para separar safras ricas em glucano ou ricas em óleo em valiosas frações de proteína e óleo e casca. O processo de separação pode ser realizado pelo uso de métodos conhecidos na técnica.
[000895] As enzimas da invenção podem ser usadas na preparação de sucos de frutas ou de legumes, xaropes, extratos e similares para aumentar a produção. As enzimas da invenção podem ser usadas no tratamento enzimático (por exemplo, materiais vegetais compreendendo hidrólise de glucano) de vários materiais derivados da parede de células de plantas ou materiais de refugo, por exemplo, de cereais, grãos, produção de vinho ou suco, ou resíduos agrícolas tais como cascas de legumes, cascas de feijão, polpa de beterraba, polpa de azeitona, polpa de batata, e similares. As enzimas da invenção podem ser usadas para modificar a consistência e o aspecto de frutos ou legumes processados. As enzimas da invenção podem ser usadas para tratar material vegetal para facilitar o processamento de material vegetal, incluindo alimentos, facilitar a purificação ou extração de componentes das plantas. As enzimas da invenção podem ser usadas para melhora o valor da ração, reduzir a capacidade de ligação de água, melhorar a degradabilidade em plantas aquáticas de refugo e/ou melhorar a conversão de material vegetal para ensilagem, e similares.
[000896] As enzimas da invenção também podem ser usadas na indústria de frutos e fermentação para limpeza e manutenção do equipamento.
[000897] As enzimas da invenção podem ser usadas em qualquer alimento ou ração (incluindo aditivos e suplementos nutricionais), ou em um processo para preparar ou preservar qualquer alimento ou ração; por exemplo, as enzimas da invenção podem ser usadas em processos para aumentar a viscosidade ou força de gel de produtos alimentícios, tais como geléia, geléia de laranja ou de outros frutos cítricos, gelatina, suco, massa, caldo, molho, e etc., conforme descrito, por exemplo, na Patente dos Estados Unidos No. 6.036.981. Os sabores em alimentos podem ser reforçados usando uma enzima desta invenção conforme descrito, por exemplo, no pedido de Patente dos Estados Unidos No. 20070020744. As enzimas da invenção podem ser usadas para controle de mofo e processos de vida de prateleira prolongada, por exemplo, para preparar qualquer alimento ou ração, tal como um produto à base de massa de pão comestível conforme descrito, por exemplo, no pedido de Patente dos Estados Unidos No. 20060286213.
[000898] Em um aspecto, enzimas, por exemplo, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção, são usadas em aplicações de cozimento, por exemplo, pães, cookies, crackers e similares, para hidrolisar glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos e reduzir a viscosidade. As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção também podem ser usadsa para criar massas de pão não- pegajosas que não são difíceis de trabalhar à máquina e para reduzir o tamanho do biscoito. O uso de enzimas da invenção para hidrolisar glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos, é usado para prevenir rápida reidratação do produto assado resultando em perda da sensação de frescor e reduzida vida de prateleira. Em um aspecto, enzimas da invenção são usadas como aditivos no processamento de massa de pão. Em um aspecto, enzimas da invenção da invenção são usadas em condicionamento de massa de pão, em que em um aspecto as enzimas possuem atividade elevada acima de uma faixa de temperatura de cerca de 25 a 35°C e em pH quase neutro (7,0 a 7,5). Em um aspecto, enzimas de condicionamento de massa de pão podem ser inativadas nas temperaturas extremas de cozimento 260°C (>500°F). As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção também podem ser usadas como beneficiadores de farinha, massa de pão e pão, vide, por exemplo, as Patentes dos Estados Unidos Nos. 5.108.765 e 5.306.633; portanto, a invenção proporciona farinhas, massas de pão e pães compreendendo uma enzima da invenção. As enzimas da invenção da invenção podem ser usadas no preparo de pães, por exemplo, pães de alto teor de fibras, conforme descrito por exemplo, no Pedido de Patente dos Estados Unidos No. 20070054024; em um aspecto, a invenção proporciona pães de alto teor de fibras compreendendo uma enzima desta invenção, ou um pão processado usando uma enzima desta invenção, e também, por exemplo, compreendendo carboximetilcelulose e pelo menos um outro tipo de material de fibras para melhorar a maciez do miolo do pão e proporcionar maciez prolongada no tempo.
[000899] Os processos de tratamento de alimentos da invenção também podem incluir o uso de qualquer combinação de outras enzimas tais como catalases, glucanases, celulases, endoglicosidases, endo-beta.-1,4-glucanases, amiloglucosidases, glicose isomerases, glicosiltransferases, lipases, fosfolipases, lipo- oxigenases, beta-glucanases, endo-beta-1,3(4)-glucanases, cutinases, peroxidases, lacases, amilases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, arabinanases, hemicelulases, mananases, xiloglucanases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, proteases, peptidases, proteinases, poligalacturonases, ramnogalacturonases, galactanases, pectate liases, transglutaminases, pectina metilesterases, celobio-hidrolases e/ou transglutaminases. Em algumas modalidades, incluindo uma enzima da invenção, estas misturas de enzimas compreendem “coquetéis de enzimas” da invenção.
Tratamento de papel ou polpa
[000900] As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção pode estar em tratamento de papel ou polpa ou destintagem de papel. Por exemplo, em um aspecto, a invenção proporciona um processo de tratamento de papel usando uma glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase da invenção. Portanto, a invenção também proporciona um papel, polpa, madeira, polpa de madeira, polpa Kraft, resíduo de paper ou de madeira e similares compreendendo uma enzima da invenção, ou, um produto ou sub-produto de papel não-madeira, tal como um papel de arroz. Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas na fabricação e/ou no processamento qualquer solução compreendendo celulose; vide, por exemplo, a Patente dos Estados Unidos No. 5.760.211.
[000901] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases também podem ser usadas em hidrólise de hemicelulose para a qual é seletiva, particularmente na presença de celulose; por exemplo, em processos descritos na Patente dos Estados Unidos No. 4.725.544. Enzimas da invenção podem ser usadas para processar retentado rico em celulase, usando enzimas adequadas para a hidrólise de celulose (vide a Patente dos Estados Unidos No. 4.725.544).
[000902] Em um aspecto, uma enzima da invenção, por exemplo, as exemplares SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23, codificadas, por exemplo, pela SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22, ou as variantes exemplares para estas sequências “parentais”, conforme determinado nas Tabelas 1 e 2, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), é aplicável tanto na redução da necessidade de um agente de alvejamento químico, tal como dióxido de cloro, e em ambientes altamente alcalinos e de temperatura elevada. Em um aspecto, uma enzima da invenção é uma glucanase alcalina termoestável a qual pode efetuar uma redução maior do que 25% na necessidade de dióxido de cloro de polpa kraft com uma perda de produção de polpa de menos de 0,5%. Em um aspecto, parâmetros de limite são pH 10, 65 a 85oC e tempo de tratamento de menos de 60 minutos em uma carga enzimática de menos de 0,001% em peso. Um grupo de endoglucanases pode ser testado para a capacidade para hidrolisar glucano marcado com corante em, por exemplo, pH 10 e a 60oC. As enzimas que dão resultado positivo no teste sob estas condições podem ser então avaliadas em, por exemplo, pH 10 e a 70oC. Alternativamente, enzimas podem ser testadas em pH 8 e pH 10 a 70oC. Na descoberta de endoglucanases desejáveis na indústria de polpa e papel, bibliotecas de temperatura elevada ou ambientes altamente alcalinos foram visadas. Especificamente, estas bibliotecas foram triadas para enzimas funcionando em pH alcalino e uma temperatura de aproximadamente 45oC. Em outro aspecto, as glucanases da invenção são úteis na indústria de polpa e papel na degradação de uma ligação de hemicelulose de lignina, de modo a liberar a lignina.
[000903] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas na indústria de papel e polpa conforme descrito, por exemplo, nas Patentes dos Estados Unidos Nos. 5.661.021; 6.387.690; 6.083.733; 6.140.095 e 6.346.407. Por exemplo, como na Patente dos Estados Unidos No. 6.140.095, uma enzima da invenção pode ser uma glucanase tolerante a álcali. Uma enzima da invenção, por exemplo, a SEQ ID NO: 2 exemplar, codificada, por exemplo, pela SEQ ID NO: 1, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), pode ser usada na indústria de papel e polpa onde a enzima é ativa na faixa de temperatura de 65oC a 75oC e em um pH de aproximadamente 10. Adicionalmente, uma enzima da invenção útila na indústria de papel e polpa reduziria a necessidade de produtos químicos alvejantes, tais como dióxido de cloro.
[000904] Enzimas da invenção, por exemplo, as variantes ou originadas enzimas da invenção, por exemplo, as variações específicas para SEQ ID NO: 2, conforme determinado nas Tabelas 1 e 2, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), podem ter atividade (por exemplo, atividade de ligação e/ou enzimática) que é termotolerante ou termoativa em acídicas ou básicas condições. Por exemplo, uma enzima da invenção, por exemplo, as enzimas típicas da invenção incluindo SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23, codificada, por exemplo, pela SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22, e as variações específicas para SEQ ID NO: 2, conforme determinado na Tabela 1, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), acima, podem ter atividade em pH ligeiramente acídico, por exemplo, entre cerca de pH 5,5 a pH 6,0, por exemplo, em uma faixa de temperatura de entre cerca de 40°C a 70°C. Em um aspecto, uma enzima da invenção, por exemplo, as exemplares SEQ ID NO: 2, SEQ ID NO: 7, SEQ ID NO: 9, SEQ ID NO: 11, SEQ ID NO: 13, SEQ ID NO: 19, SEQ ID NO: 21, e/ou SEQ ID NO: 23, codificadas, por exemplo, pelas SEQ ID NO: 1, SEQ ID NO: 3, SEQ ID NO: 6, SEQ ID NO: 8, SEQ ID NO: 10, SEQ ID NO: 12, SEQ ID NO: 18, SEQ ID NO: 20, e/ou SEQ ID NO: 22, tem uma atividade ótima entre cerca de 40°C a 75°C, e entre cerca de pH 5,5 a 6,0; é estável a 70°C por pelo menos 50 minutos, e é inativada a entre cerca de 96°C a 100°C. Em outro aspecto, enzimas da invenção, por exemplo, variantes de SEQ ID NO: 2, por exemplo, conforme determinado nas Tabelas 1 e 2, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), são termotolerantes e/ou termoestáveis; por exemplo, uma enzima da invenção, por exemplo, variantes de SEQ ID NO: 2, por exemplo, conforme determinado nas Tabelas 1 e 2, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), pode reter pelo menos 75% de atividade residual (por exemplo, atividade de glucanase) depois de 2 minutos a 95°C; e em outro aspecto, retém 100% de atividade depois de aquecimento por 30 minutos a 95°C. Em ainda outro aspecto, uma enzima da invenção, por exemplo, variantes de SEQ ID NO: 2, por exemplo, conforme determinado nas Tabelas 1 e 2, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), retém 100% de atividade depois de aquecimento por 30 minutos a 96°C, 97°C, 98°C ou 99°C. Em ainda outro aspecto, uma enzima da invenção, por exemplo, variantes de SEQ ID NO: 2, por exemplo, conforme determinado nas Tabelas 1 e 2, bem como SEQ ID NO: 7 (codificada pela SEQ ID NO: 6), SEQ ID NO: 9 (codificada pela SEQ ID NO: 8), SEQ ID NO: 11 (codificada pela SEQ ID NO: 10), SEQ ID NO: 13 (codificada pela SEQ ID NO: 12), SEQ ID NO: 19 (codificada pela SEQ ID NO: 18), SEQ ID NO: 21 (codificada pela SEQ ID NO: 20), e SEQ ID NO: 23 (codificada pela SEQ ID NO: 22), retém pelo menos 90% de atividade depois de aquecimento por 30 minutos a 100°C.
[000905] Adicionalmente, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser úteis em biobranqueamento e tratamento de polpas químicas, conforme descrito, por exemplo, na Patente dos Estados Unidos No. 5.202.249, biobranqueamento e tratamento de polpas de madeira ou ou papel, conforme descrito, por exemplo, nas Patentes dos Estados Unidos Nos. 5.179.021. 5.116.746. 5.407.827. 5.405.769. 5.395.765. 5.369.024. 5.457.045. 5.434.071. 5.498.534. 5.591.304. 5.645.686. 5.725.732. 5.759.840. 5.834.301. 5.871.730 e 6.057.438, na redução de lignina em madeira e modificando madeira, conforme descrito, por exemplo, nas Patentes dos Estados Unidos Nos. 5.486.468 e 5.770.012.
[000906] Em um aspecto, uma das glucanases (ou celulases), mananases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases ou outras enzimas da invenção é usada na indústria de papel e polpa ou sozinha ou junto com uma xilanase (por exemplo, uma xilanase da invenção). Em um aspecto, a enzima da invenção é usada em um processo de alvejamento para reforçar o brilho de polpas alvejadas, por exemplo, totalmente ou parcialmente de madeira branca. Usando uma enzima da invenção, a quantidade de cloro usada nos estágios de alvejamento pode ser reduzida. Em um aspecto, uma mananase da invenção é usada para aumentar a liberdade das polpas em processo de papel reciclado. Em um aspecto, uma das glucanases (ou celulases), mananases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção é usada sozinha ou em combinação com uma xilanase (por exemplo, uma xilanase da invenção) no tratamento de polpa lignocelulósica (por exemplo, totalmente ou parcialmente de madeira branca) para melhorar a alvejabilidade da mesma. Vide, por exemplo, a Patente dos Estados Unidos No. 5.795.764.
[000907] Os processos de polpa e papel da invenção também podem incluir o uso de qualquer combinação de outras enzimas tais como catalases, glucanases, celulases, endoglicosidases, endo-beta.-1,4- glucanases, amiloglucosidases, glicose isomerases, glicosiltransferases, lipases, fosfolipases, lipo-oxigenases, beta- glucanases, endo-beta-1,3(4)-glucanases, cutinases, peroxidases, lacases, amilases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, arabinanases, hemicelulases, mananases, xiloglucanases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, proteases, peptidases, proteinases, poligalacturonases, ramnogalacturonases, galactanases, pectate liases, transglutaminases, pectina metilesterases, celobio-hidrolases e/ou transglutaminases. Em algumas modalidades, incluindo uma enzima da invenção, estas misturas de enzimas compreendem “coquetéis de enzimas” da invenção.
Rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos
[000908] A invenção proporciona métodos para tratar rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos usando glucanases da invenção, para seres humanos e/ou animais (incluindo, por exemplo, mamíferos, aves, répteis, peixe e similares; incluindo ruminantes). A invenção proporciona rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos, compreendendo polipeptídeos da invenção, por exemplo, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção, incluindo os coquetéis de enzimas da invenção. A invenção proporciona rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos compreendendo enzimas e “coquetéis” da invenção conforme descrito, por exemplo, no Pedido de Patente dos Estados Unidos No. 20060193897.
[000909] Em um aspecto, tratar rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos usando glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção pode ajudar na disponibilidade de nutrientes, por exemplo, amido, proteína, e similares, na ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético. Ao decompor proteínas difíceis de digerir ou revelar amido (ou outros nutrientes) indiretamente ou diretamente, a enzima da invenção torns os nutrientes mais acessíveis a outras enzimas endógenas ou exógenas. A enzima da invenção também pode simplesmente causar a liberação de nutrientes e açúcares prontamente digeríveis e facilmente absorvidos. Em outro aspecto, as enzimas da invenção são usadas em rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos para reduzir a viscosidade de glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos, em um alimento, ração, gêneros alimentícios ou outro material comestível, por exemplo, em uma dieta de alto teor de cevada ou uma dieta de alto teor de trigo, tal como uma dieta para aves domésticas. Em um aspecto, isto pode minimizar gotejamentos a úmido.
[000910] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas como ou em rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos, incluindo uso em qualquer ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético conhecido na técnica, por exemplo, conforme determinado nas Patentes dos Estados Unidos Nos. 5.432.074, 5.429.828, 5.612.055, 5.720.971, 5.981.233, 5.948.667, 6.099.844, 6.132.727 e 6.132.716.
[000911] Quando adicionadas a rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos, as glucanases, xilanases e/ou uma mananases da invenção melhoram a decomposição in vivo do material das paredes de células vegetais parcialmente devido a uma redução da viscosidade intestinal (vide, por exemplo, Bedford et al., Proceedings of the 1st Symposium on Enzymes in Animal Nutrition, 1993, pp. 73-77), por meio do que é obtida uma melhor utilização dos nutrientes das plantas pelo animal. Portanto, ao usar enzimas (por exemplo, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases) da invenção em rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos é aumentada a taxa de crescimento e/ou a proporção de conversão da ração (isto é, o peso da ração ingerida relativo ao ganho de peso) do animal.
[000912] O aditivo de ração, aditivo alimentar, suplemento nutricional e/ou suplemento dietético da invenção pode ser um produto enzimático granulado o qual pode ser prontamente misturado com componentes de alimento ou ração. Alternativamente, rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos da invenção podem formar um componente de uma pré-mistura. O produto enzimático granulado da invenção pode ser revestido ou não revestido. O tamanho de partícula dos granulados enzimáticos pode ser compatível com o de componentes de ração e da pré-mistura. Isto proporciona um meio seguro e conveniente para incorporar enzimas em rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos. Alternativamente, as rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos da invenção podem ser uma composição líquida estabilizada. Esta pode ser uma pasta semifluida aquosa ou à base de óleo. Vide, por exemplo, a Patente dos Estados Unidos No. 6.245.546.
[000913] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da presente invenção, na modificação de rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos, podem processar as rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos ou in vitro (modificando componentes das rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos) ou in vivo. Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser adicionadas a ração, alimento, aditivo alimentar, aditivo de ração, composições de suplemento nutricional e/ou de suplemento dietético contendo altas quantidades de glucanos, por exemplo, ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético contendo material vegetal de cereais, grãos e similares. Quando adicionada à ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético a glucanase aumenta significativamente a decomposição in vivo de material contendo glucano, por exemplo, paredes celulares de plantas, por meio do quê uma melhor utilização dos nutrientes da planta pelo ser humano ou animal é obtida. Em um aspecto, a taxa de crescimento e/ou proporção de conversão de ração/alimento (isto é, o peso da ração/alimento ingerido em relação ao ganho de peso) do ser humano ou animal é melhorada. Por exemplo, uma proteína compreendendo glucano parcialmente ou indigestível é totalmente ou parcialmente degradada por glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção, por exemplo, em combinação com outra enzima, por exemplo, beta-galactosidase, para peptídeos e galactose e/ou galactooligômeros. Estes produtos de digestão enzimática são mais digestíveis pelo humano ou animal. Portanto, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem contribuir para a energia disponível da ração ou alimento. Além disso, contribuindo para a degradação de proteínas compreendendo glucano, uma glucanase da invenção pode melhorar a digestibilidade e a captação de constituintes de ração ou alimento de carboidrato e não-carboidrato tais como proteína, gordura e minerais.
[000914] Em outro aspecto, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser supridas expressando as enzimas diretamente em safras transgênicas de alimento e/ou ração (como, por exemplo, plantas transgênicas, sementes e similares), tais como grãos, cereais, milho, soja, semente de colza, tremoço e similares. Conforme discutido acima, a invenção proporciona plantas transgênicas, partes de plantas e células de plantas compreendendo uma sequência de ácido nucleico codificando um polipeptídeo da invenção. Em um aspecto, o ácido nucleico é expressada de tal modo que a enzima (por exemplo, glucanase) da invenção é produzida em quantidades recuperáveis. As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser recuperadas de qualquer planta ou parte de planta. Alternativamente, a planta ou parte de planta contendo o polipeptídeo recombinante pode ser usada deste modo para melhorar a qualidade de um alimento ou ração, por exemplo, melhorando o valor nutricional, a palatabilidade, e as propriedades reológicas, ou para destruir um fator antinutritivo.
[000915] Em um aspecto, a invenção proporciona métodos para remover oligossacarídeos de um alimento ou ração antes do consumo por um sujeito animal usando glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção. Neste processo é formado um alimento ou ração tendo um aumentado valor de energia metabolizável. Além de glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção, podem ser usadas galactosidases, celulases e combinações das mesmas. Em um aspecto, a enzima pode ser adicionada em uma quantidade igual a entre cerca de 0,001% e 1% em peso do material do alimento ou ração. Em um aspecto, o alimento ou ração é um cereal, um trigo, um grão, um material de soja (por exemplo, um grão desoja triturado). Vide, por exemplo, a Patente dos Estados Unidos No. 6.399.123.
[000916] Em outro aspecto, a invenção proporciona métodos para utilizar glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção como um suplemento nutricional ou suplemento dietético nas dietas de seres humanos ou animais preparando um suplemento nutricional ou dietético contendo uma enzima recombinante da invenção, e administrando o suplemento nutricional ou dietético a um ser humano ou animal para aumentar a utilização do glucano contido na alimento ou ração ingerida pelo ser humano ou animal.
[000917] Em um aspecto, as enzimas da invenção podem ser usadas para tratar/processar “DDGS”, ou grão secado em Destiladores com solúveis, o qual é subproduto de planta de etanol triturada a seco, por exemplo, para aplicações de alimento ou ração, por exemplo, para aves domésticas, bovinos, suínos e outros animais domésticos.
[000918] Em ainda outro aspecto, a invenção proporciona uma matriz de liberação de enzimas peletizadas comestíveis e método de uso para liberação de glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção a um ser humano ou animal, por exemplo, como um suplemento nutricional ou dietético. A matriz de liberação de enzimas prontamente libera uma enzima da invenção (por exemplo, uma glucanase), tal como uma enzima tendo uma sequência de aminoácidos da invenção, ou um fragmento enzimaticamente ativo da mesma (por exemplo, uma subsequência de pelo menos 30, 40, 50, 60, 70, 80, 90 ou 100 ou mais aminoácidos contíguos da mesma), em meio aquoso, tal como, por exemplo, o fluido digestivo de um ser humano ou animal.
[000919] A matriz de liberação de enzimas da invenção pode ser preparada a partir de um veículo comestível granulado selecionado entre componentes tais como semente de cereais que é esgotada de óleo, feno, alfafa, capim-rabo-de-gato, casca de soja, farinha grossa de semente de girassol, farelo de trigo, e similares, que prontamente dispersam a enzima recombinante aí contida em meio aquoso. No uso, a matriz de liberação de enzimas peletizadas comestíveis é administrada a um animal para liberação de glucanase ao ser humano ou animal. Substratos à base de grãos ou à base de grama adequados podem compreender ou ser derivados de qualquer grão ou grama comestível adequado, tal como trigo, trigo-sarraceno, milheto, centeio, milho, soja, arroz, sorgo, alfafa, cevada, uma grama anual e similares. Um substrato à base de grão exemplar é um substrato à base de milho. O substrato pode ser derivado de qualquer parte adequada do grão, mas é em um aspecto uma semente de cereais aprovada para uso em ração animal, tal como grão de milho que é obtido em um processo de moagem a úmido ou a seco. A semente de cereais em um aspecto compreende grão esgotado, o qual é semente de cereais do qual foi expelido óleo, tal como por prensagem ou extração de hexano ou outro solvente. Alternativamente, a semente de cereais é extraída por expelidor, isto é, o óleo foi removido por prensagem.
[000920] A matriz de liberação de enzimas da invenção pode ser sob a forma de partículas plurais distintas, péletes ou grânulos. Por "grânulos" se indica partículas que são comprimidas ou compactadas, tal como por uma peletização, extrusão, ou compactação similar para remover água da matriz. A compressão ou compactação referida das partículas também promove coesão intrapartícula das partículas. Por exemplo, os grânulos podem ser preparados por peletização do substrato à base de grão em um moinho de grãos. Os péletes preparados deste modo são triturados ou esmigalhados para um tamanho de grânulo adequado para uso como um adjuvante em alimento ou ração. A própria matriz pode ser usada como um diluente para liberação de enzimas em alimento ou ração.
[000921] Em um aspecto, a matriz de liberação de enzimas é sob a forma de grânulos tendo um tamanho de grânulo variando a partir de cerca de malha 4 a cerca de malha 400 (USS); mais em um aspecto, cerca de malha 8 a cerca de malha 80; e mais em um aspecto cerca de malha 14 a cerca de malha 20. Se a semente de cereais for esgotada através de extração de solvente, o uso de um agente de lubricidade tal como óleo de milho pode ser necessário no peletizador, mas um agente de lubricidade similar ordinariamente não é necessário se o grão for extraído por expelidor. Em outros aspectos da invenção, a matriz é preparada por outros processos de compactação ou compressão tais como, por exemplo, por extrusão do substrato à base de grão através de um molde e trituração do extrusado para um tamanho de grânulo adequado.
[000922] A matriz de liberação de enzimas pode incluir adicionalmente um componente polissacarídico como um agente de coesividade para reforçar a coesividade dos grânulos da matriz. Acredita-se que o agente de coesividade proporcione grupos oxidrila adicionais, os quais reforçam a ligação entre proteínas do grão dentro do grânulo da matriz. Adicionalmente se acredita que os grupos oxidrila adicionais funcionem reforçando a ligação de hidrogênio de proteínas a amido e a outras proteínas. O agente de coesividade pode estar presente em qualquer quantidade adequada para reforçar a coesividade dos grânulos da matriz de liberação de enzimas. Agentes de coesividade adequados incluem um ou mais de dextrinas, maltodextrinas, amidos, tais como amido de milho, farinhas finas, celulósicos, hemicelulósicos, e similares. Por exemplo, a percentagem de semente de cereais e agente de coesividade na matriz (não incluindo a enzima) é 78% de farinha grossa de germe de milho e 20% em peso de amido de milho.
[000923] Em uma modalidade, como a matriz de liberação de enzima da invenção é composta de materiais biodegradáveis, a matriz pode ser submetida a deterioração, tal como por emboloramento. Para prevenir ou inibir o emboloramento referido, a matriz pode incluir um inibidor de mofo, tal como um sal de propionato, o qual pode estar presente em qualquer quantidade suficiente para inibir o emboloramento da matriz de liberação de enzima, portanto proporcionando uma matriz de liberação em uma formulação estável que não requer refrigeração.
[000924] Em uma modalidade, a invenção proporciona uma enzima da invenção em uma matriz de liberação de enzimas da invenção, e métodos para usar a mesma; e em um aspecto, a enzima é uma glucanase, mananase ou xilanase termoestável conforme descrito aqui, neste pedido de patente, de modo a resistir a inativação da glucanase durante fabricação onde temperaturas elevadas e/ou vapor podem ser empregados para preparar a matriz de liberação de enzimas peletizadas. Durante digestão da ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético contendo a invenção matriz de liberação de enzimas, fluidos digestivos aquosos causarão liberação da enzima ativa. Outros tipos de enzimas termoestáveis e suplementos nutricionais que são termoestável também podem ser incorporados na matriz de liberação para liberação sob qualquer tipo de condições aquosas.
[000925] Um revestimento pode ser aplicado às partículas da matriz enzimática da invenção para muitos fins diferentes, tal como para adicionar um aroma ou suplemento nutricional à ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético, para retardar a liberação de suplementos e/ou enzimas em condições gástricas, e similares. Ou, o revestimento pode ser aplicado para atingir uma meta funcional, por exemplo, sempre que for desejável retardar a liberação da enzima das partículas da matriz ou controlar as condições sob as quais a enzima será liberada. A composição do material de revestimento pode ser tal que é seletivamente decomposto por um agente ao qual é suscetível (tal como calor, ácido ou base, enzimas ou outros produtos químicos). Alternativamente, dois ou mais revestimentos suscetíveis aos diferentes agentes de decomposição referidos podem ser aplicados consecutivamente às partículas da matriz.
[000926] A invenção também é dirigida a um processo para preparar uma matriz de liberação de enzimas. De acordo com a invenção, o processo compreende proporcionar partículas plurais distintas de um substrato à base de grão em um tamanho de partícula adequado para uso como uma matriz de liberação de enzimas, em que as partículas compreendem uma glucanase, xilanase e/ou uma mananase codificada por uma sequência de aminoácidos da invenção. Em um aspecto, o processo inclui compactar ou comprimir as partículas da matriz de liberação de enzimas em grânulos, o qual mais em um aspecto é realizado por peletização. O inibidor de mofo e agente de coesividade, quando usados, podem ser adicionados em qualquer momento adequado, e em um aspecto são misturados com o substrato à base de grão nas proporções desejadas antes de peletização do substrato à base de grão. O teor de umidade na ração de moinho de grãos em um aspecto está nas faixas determinadas acima com respeito ao teor de umidade no produto acabado, e em um aspecto é cerca de 14 a 15%. Em um aspecto, é adicionada umidade à matéria- prima sob a forma de uma preparação aquosa da enzima para trazer a matéria-prima para este teor de umidade. A temperatura no moinho de grãos em um aspecto é trazida a cerca de 82°C com vapor. O moinho de grãos pode ser operado sob quaisquer condições que confiram movimento suficiente à matéria-prima para proporcionar péletes. O próprio processo de peletização é um processo de custo eficaz para remover água da composição contendo enzima.
[000927] Em um aspecto, o moinho de péletes é operado com um molde de 3,175 x 10-3 m por 0,0508 m a 2668,24 kg/h (1/8 de polegada por 2 polegada a 100 lb./min). de pressão a 82°C para proporcionar péletes, os quais são então esmigalhados em um esmigalhador de moinho de péletes para proporcionar partículas plurais distintas tendo um tamanho de partícula capaz de passar através de uma tela de malha 8 mas sendo retida sobre uma tela de malha 20.
[000928] As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases termoestáveis da invenção podem ser usadas nos péletes da invenção. Podem ter temperaturas elevadas ótimas e elevada resistência térmica tais que pode ser obtida uma reação enzimática em uma temperatura não realizada até o momento. O gene codificando a glucanase de acordo com a presente invenção (por exemplo, conforme determinado em quaisquer das sequências da invenção) pode ser usado na preparação de glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases (por exemplo, usando tecnologia GSSM, conforme descrito aqui, neste pedido de patente) tendo características diferentes daquelas das glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção (em termos de pH ótimo, temperatura ótima, resistência ao calor, estabilidade a solventes, atividade específica, afinidade com substrato, capacidade de secreção, taxa de translação, controle de transcrição e similares). Além disso, um polinucleotídeo da invenção pode ser empregado para triagem de glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases variantes preparadas pelos métodos descritos aqui, neste pedido de patente, para determinar aquelas tendo uma atividade desejada, tal como termoestabilidade ou termotolerância aprimorada ou modificada. Por exemplo, a Patente dos Estados Unidos No. 5.830.732, descreve um ensaio de triagem para determinar termotolerância de uma glucanase.
[000929] Em um aspecto, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção em rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos são ativas no estômago de seres humanos ou animais. Portanto, em um aspecto, uma enzima da invenção, por exemplo, em uma ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético, tem uma atividade em cerca de 37 °C e em baixo pH para monogástricos (pH 2 a 4) e pH quase neutro para ruminantes (pH 6,5 a 7). A enzima da invenção tem resistência a enzimas intestinais, por exemplo, proteases, e estabilidade nas maiores temperaturas envolvidas em peletização de alimento e ração. Em um aspecto, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção são usadas em rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos, e podem ter uma alta atividade específica, por exemplo, atividade a 35 a 40°C e pH 2 a 4, meia-vida maior do que 30 minutos em SGF e uma meia-vida > 5 minutos a 85°C em estado formulado. Para ração para ruminantes, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção em rações, alimentos, aditivos alimentares, aditivos de ração, suplementos nutricionais e/ou suplementos dietéticos têm uma alta atividade específica, por exemplo, atividade a 35 a 40°C e pH 6,5 a 7,0, meia-vida maior do que 30 minutos em SRF e estabilidade como um pó seco concentrado.
[000930] A ração, alimento, aditivo alimentar, aditivo de ração, suplemento nutricional e/ou suplemento dietético produção processes da invenção pode incluir qualquer combinação de outras enzimas tais como catalases, outras glucanases, celulases, endoglicosidases, endo-beta.-1,4-glucanases, amiloglucosidases, glicose isomerases, glicosiltransferases, lipases, fosfolipases, lipo-oxigenases, beta- glucanases, endo-beta-1,3(4)-glucanases, cutinases, peroxidases, lacases, amilases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, fitases, arabinanases, hemicelulases, outras mananases, xiloglucanases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, poligalacturonases, ramnogalacturonases, galactanases, pectate liases, transglutaminases, pectina metilesterases, celobio- hidrolases e/ou transglutaminases. Em algumas modalidades, incluindo uma enzima da invenção, estas misturas de enzimas compreendem “coquetéis de enzimas” da invenção.
Tratamento de refugo
[000931] As glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas em uma variedade de outras aplicações industriais, por exemplo, em tratamento de refugo (além de, por exemplo, conversão de biomassa para combustíveis). Por exemplo, em um aspecto, a invenção proporciona um processo de digestão de refugo sólido usando glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção. Os métodos podem compreender reduzir a massa e o volume de refugo sólido substancialmente não tratado. Refugo sólido pode ser tratado com um processo digestivo enzimático na presença de uma solução enzimática (incluindo glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção) em uma temperatura controlada. Isto resulta em uma reação sem fermentação bacteriana apreciável de micro-organismos adicionados. O refugo sólido é convertido em um refugo liquefeito e qualquer refugo sólido residual. O refugo liquefeito resultante pode ser separado do qualquer refugo solidificado residual referido. Vide, por exemplo, a Patente dos Estados Unidos No. 5.709.796. Portanto, a invenção proporciona produtos de refugo, tais como refugo liquefeito ou qualquer refugo sólido residual compreendendo um polipeptídeo da invenção, por exemplo, uma enzima da invenção.
[000932] A invenção proporciona processos para tratar material de refugo derivado de áreas humanas, animais e/ou industriais usando uma enzima ou enzima coquetel desta invenção; e estes processos também podem ser usados para recuperar importantes elementos nutricionais e metais pesados tóxicos, conforme descrito por exemplo, no Pedido de Patente dos Estados Unidos No. 20060194299. Em um aspecto, a invenção proporciona um processo para liberar elementos nutricionais de plantas e utilizar metais tóxicos e recursos de energia de carbono presentes em semelhante refugo, compreendendo tratar o refugo com uma ou mais enzimas desta invenção.
[000933] Os processos de tratamento de refugo da invenção podem incluir o uso de qualquer combinação de outras enzimas tais como catalases, outras glucanases, celulases, endoglicosidases, endo-beta.- 1,4-glucanases, amiloglucosidases, glicose isomerases, glicosiltransferases, lipases, fosfolipases, lipo-oxigenases, beta- glucanases, endo-beta-1,3(4)-glucanases, cutinases, peroxidases, lacases, amilases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, fitases, arabinanases, hemicelulases, outras mananases, xiloglucanases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, proteases, peptidases, proteinases, poligalacturonases, ramnogalacturonases, galactanases, pectate liases, transglutaminases, pectina metilesterases, celobio-hidrolases e/ou transglutaminases. Em algumas modalidades, incluindo uma enzima da invenção, estas misturas de enzimas compreendem “coquetéis de enzimas” da invenção.
Produtos para tratamento oral
[000934] A invenção proporciona produto para tratamento oral compreendendo glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção. Produtos típicos para tratamento oral incluem pastas de dentes, cremes dentais, géis ou pós para os dentes, odônticos, enxaguatórios bucais, formulações de enxágue pré- ou pós-escovação, gomas de mascar, pastilhas, ou balas. Vide, por exemplo, a Patente dos Estados Unidos No. 6.264.925.
[000935] Os produtos orais da invenção podem incluir qualquer combinação de outras enzimas tais como proteases, peptidases, proteinases, glicose oxidases, peroxidases, glucanases, celulases, endoglicosidases, endo-beta-1,4-glucanases, amiloglucosidases, endo-beta-1,3(4)-glucanases, amiloglucosidases e glucosidases.
Fabrico de bebidas por fermentação e fermentação
[000936] A invenção proporciona métodos de fabricação (por exemplo, fermentação) de cerveja compreendendo glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases da invenção. Em um processo exemplar, matérias- primas contendo amido são desintegradas e processadas para formar um malte. Uma enzima da invenção é usada em qualquer ponto no processo de fermentação. Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas na indústria de cervejaria para a degradação de beta-glucanos. Em um aspecto, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção são usadas na indústria de cervejaria para a clarificação da bebida. Enzimas da invenção podem ser usadas na indústria de bebidas para melhorar a filtrabilidade do cerveja não-fermentada, conforme descrito, por exemplo, na Patente dos Estados Unidos No. 4.746.517.
[000937] Em um aspecto, glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas no processamento de malte da cevada. A matéria- prima principal da fermentação da cerveja é malte da cevada. Este pode ser um processo de três estágios. Primeiro, o grão da cevada pode ser macerado para aumentar o teor de água, por exemplo, para em torno de cerca de 40%. Segundo, o grão pode ser germinado por incubação a 15 a 25oC por 3 a 6 dias quando é estimulada síntese enzimática sob o controle de giberelinas. Em um aspecto, as enzimas da invenção são adicionadas neste estágio (ou em qualquer outro estágio) do processo.
[000938] Em um aspecto, enzimas da invenção são usadas em processos de brassagem de malte e de conversão. Nas indústrias de cervejaria e de fermentação, processos de brassagem de malte e de conversão são realizados em temperaturas que são baixas demais para promover degradação adequada de glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos hidrossolúveis. Estes polímeros formam substratos gomosos que podem causar aumento da viscosidade no brassagem de mosto, resultando em escoamento mais longo do malte moído, névoa residual e precipitados no produto de cerveja final devido a filtração ineficiente e baixa produção da extração. Por estas razões, as enzimas são adicionadas durante os processos de fermentação para decompor glucano β-1,4- e β-1,3- ligado, ou outros polissacarídeos.
[000939] Em um aspecto, as enzimas da invenção são usadas em operações de maltaria, por exemplo, glucanase é adicionada à água do processo, para encurtar os tempos de germinação e/ou para estimular conversão de cevada de baixa qualidade para maltes aceitáveis. Em um aspecto, as enzimas da invenção são usadas para preparar uma massa pastosa, por exemplo, são adicionadas para aumentar a filtrabilidade do mosto e/ou melhorar a lautering (separação do mosto da massa pastosa). Em um aspecto, as enzimas da invenção são usadas no fermentador e/ou tanque de sedimentação para, por exemplo, auxiliar no clareamento da névoa e/ou para melhorar a filtração. Em um aspecto, as enzimas da invenção são usadas em fermentação auxiliar, por exemplo, uma glucanase da invenção é adicionada para decompor glucanos, mananos, arabinoxilanos ou xilanos, ou outros polissacarídeos de cevada, trigo, e/ou outros cereais, incluindo glicanos em malte. Em um aspecto, as enzimas da invenção são usadas em fermentação de malte, por exemplo, uma glucanase da invenção é adicionada para modificar maltes pobres com alto teor de glucano.
[000940] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas em qualquer processo de produção de cerveja ou bebida alcólica, conforme descrito, por exemplo, in Patente dos Estados Unidos No. 5.762.991; 5.536.650; 5.405.624; 5.021.246; 4.788.066.
[000941] Os processos de fermentação da invenção podem incluir o uso de qualquer combinação de outras enzimas tais como outras xilanases, esterases, celulases, pectinases, pectate liases, amilases, decarboxilases, lacases, glucanases, proteases, peptidases, proteinases, amiloglucosidases, glicose isomerases, glucoamilases, beta-glucanases, endo-beta-1,3(4)-glucanases, hemicelulases, endoglicosidases, endo-beta.-1,4- glucanases, glicosiltransferases, fosfolipases, lipo-oxigenases, redutases, oxidases, fenoloxidases, ligninases, pululanases, arabinanases, outras mananases, xiloglucanases, pectina acetila esterases, ramnogalacturonano acetil esterases, poligalacturonases, ramnogalacturonases, galactanases, transglutaminases, pectina metilesterases, celobio-hidrolases e/ou transglutaminases. Em algumas modalidades, incluindo uma enzima da invenção, estas misturas de enzimas compreendem “coquetéis de enzimas” da invenção.
Aplicações medicinais e de pesquisa
[000942] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas como agentes antimicrobianos, por exemplo, composições farmacêuticas, devido a suas propriedades bacteriolíticas e propriedades antifúngicas. Enzimas da invenção podem ser usadas para melhorar, eliminar ou proteger animais contra infecções fúngicas, por levedura ou por bactérias, por exemplo, toxinas bacterianas ou esporos bacterianos, tais como salmonelas ou Bacillus, por exemplo, conforme descrito nos Pedidos de Patente Internacional PCT Nos. WO0049890 e WO9903497. Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas em um método de uso e composição de uma carbohidrase e/ou uma glucanase para a fabricação de um agente para os tratamentos e/ou a profilaxia de coccidiose. O agente fabricado pode estar sob a forma de um ração animal à base de cereais, vide, por exemplo, a Patente dos Estados Unidos No. 5.624.678.
[000943] Enzimas da invenção podem ser usadas em, e na fabricação de, um agente para o tratamento e/ou a profilaxia de infecção bacteriana em um animal, por exemplo, uma infecção causada por Salmonella, Campylobacter ou Clostridium perfringens, conforme descrito por exemplo, no Pedido de Patente dos Estados Unidos No. 20060083731; e em uma modalidade, as enzimas são adicionadas em uma ração, aditivo de ração ou suplemento nutricional. Conversão de biomassa e produção de bio combustíveis limpos
[000944] A invenção proporciona polipeptídeo, incluindo enzimas (glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção) e anticorpos, e métodos para a conversão de uma biomassa ou qualquer material lignocelulósico (por exemplo, qualquer composição compreendendo celulose, hemicelulose e lignina), para um combustível (por exemplo, bioetanol, biopropanol, biobutanol, biopropanol, biometanol, biodiesel), além de rações, alimentos e produtos químicos. Por exemplo, em um aspecto, uma enzima da invenção tem atividade de β-glucosidase para liberar D-glicose a partir de dímeros de celobiose. Em um aspecto, as enzimas têm atividade de exo- ou endo-beta-glucanase.
[000945] Portanto, as composições e métodos da invenção proporcionam alternativas ou auxiliares eficazes e sustentáveis ao uso de produtos à base de petróleo, por exemplo, como uma mistura de um biocombustíveis tais como biometanol, bioetanol, biopropanol, biobutanol, e similares, a diesel combustível, gasolina, querosene e similares. A invenção proporciona organismos expressando enzimas da invenção para participação em ciclos químicos envolvendo conversão de biomassa natural. Em um aspecto, enzimas e métodos para a conversão são usados em conjuntos de enzimas para a despolimerização eficiente de polissacarídeos, polímeros celulósicos e/ou hemicelulósicos para porções carbono metabolizáveis (por exemplo, fermentáveis). A invenção proporciona métodos para descoberta e implementação mais eficaz de enzimas para possibilitar estes importantes novos processos industriais de “conversão de biomassa” e de energias alternativas.
[000946] As composições e métodos da invenção podem ser usados para proporcionar alternativas ou auxiliares eficazes e sustentáveis ao uso de produtos à base de petróleo, por exemplo, como uma mistura de bioetanol, biopropanol, biobutanol, biopropanol, biometanol e/ou biodiesel e gasolina. A invenção proporciona organismos expressando enzimas da invenção para participação em ciclos químicos envolvendo conversão de biomassa natural. A invenção proporciona métodos para descoberta e implementação mais eficaz de enzimas para possibilitar estes importantes novos processos industriais de “conversão de biomassa” e de energias alternativas.
[000947] A invenção proporciona métodos, enzimas e misturas de enzimas ou “coquetéis” da invenção, para processar um material, por exemplo, um material de biomassa, compreendendo um celooligossacarídeo, um oligômero de arabinoxilano, uma lignina, uma lignocelulose, um xilano, um glucano, uma celulose e/ou um açúcar fermentável compreendendo contatar a composição com um polipeptídeo da invenção, ou um polipeptídeo codificado por um ácido nucleico da invenção, em que opcionalmente o material é derivado de uma colheita agrícola (por exemplo, trigo, cevada, batatas, switchgrass, madeira de choupo), é um subproduto de produção de um alimento ou uma ração, é um produto de resíduo lignocelulósico, ou é um resíduo vegetal ou um papel refugado ou produto de papel refugado, e opcionalmente o resíduo vegetal compreende caules, folhas, cascas, cascas secas, milho ou sabugos de milho, palha de milho, fibra de milho, feno, palha (por exemplo, palha de arroz ou palha de trigo), bagaço da cana-de-açúcar, polpa de beterraba, polpa de cítricos, e cascas de cítricos, madeira, aparas de madeira, lascas de madeira, polpa de madeira, refugo de polpa, resíduo de madeira, raspas de madeira e serragem, refugos e detritos de construção e/ou demolição (por exemplo, madeira, raspas de madeira e serragem), e opcionalmente o resíduo de papel compreende papel de fotocópia descartado ou usado, papel de impressora de computador, papel de caderno de apontamentos, papel de bloco de notas, papel para máquina de escrever, jornais, revistas, materiais de embalagem à base de cartão e papel, e materiais de papel reciclado. Além disso, podem ser usados refugos urbanos, por exemplo, a fração de papel de refugo sólido municipal, resíduo de madeira municipal, e refugo verde municipal, junto com outros materiais contendo açúcar, amido, e/ou celulose. Opcionalmente o processamento do material, por exemplo, o material de biomassa, produz um bioálcool, por exemplo, um bioetanol, biometanol, biobutanol ou biopropanol.
[000948] Alternativamente, o polipeptídeo da invenção pode ser expressada no material vegetal da biomassa ou na própria matéria- prima.
[000949] Os métodos da invenção também incluem tomar o material lignocelulósico convertido (processado por enzimas da invenção) e transformá-lo um combustível (por exemplo, um bioálcool, por exemplo, um bioetanol, biometanol, biobutanol ou biopropanol, ou biodiesel) por fermentação e/ou por síntese química. Em um aspecto, os açúcares produzidos são fermentados e/ou os produtos não- fermentáveis são gaseificados.
[000950] Os métodos da invenção também incluem converter algas, óleos vegetais não beneficiados, óleos vegetais de refugo, gorduras animais e graxas (por exemplo, sebo, banha, e graxa amarela), ou águas servidas, usando enzimas da invenção, e torná-las em um combustível (por exemplo, um bioálcool, por exemplo, um bioetanol, biometanol, biobutanol ou biopropanol, ou biodiesel) por fermentação e/ou por síntese química ou conversão.
[000951] As enzimas da invenção (incluindo, por exemplo, organismos, tais como micro-organismos, por exemplo, fungos, levedura ou bactérias, produzindo e em alguns aspectos secretando enzimas recombinantes da invenção) podem ser usadas em ou incluídas/integradas em qualquer estágio de qualquer processo de conversão de biomassa, por exemplo, em qualquer etapa, várias etapas, ou incluídas em todas as etapas, ou todos os métodos de processos de conversão de biomassa, ou todas estas alternativas de biocombustível: * Combustão direta: a combustão de material por calor direto e é a tecnologia de biomassa mais simples; pode ser muito econômica se uma fonte de biomassa estiver próxima. * Pirólise: é a degradação térmica de biomassa por calor na ausência de oxigênio. Em um aspecto, biomassa é aquecida até uma temperatura entre cerca de 800 e 1400 graus Fahrenheit, mas não é introduzido oxigênio para suportar combustão resultando na criação de gás, óleo combustível e carvão. * Gaseificação: biomassa pode ser usada para produzir metano através de calor ou digestão anaeróbica. Syngas, uma mistura de monóxido de carbono e hidrogênio, pode ser derivada de biomassa. * Gás de Aterro: é gerado pela decomposição (digestão anaeróbica) de lixo queimado em aterros. Quando o refugo orgânico se decompõe, produz gás consistindo em aproximadamente 50% de metano, o componente principal do gás natural. * Digestão anaeróbica: converte matéria orgânica em uma mistura de metano, o componente principal do gás natural, e dióxido de carbono. Em um aspecto, biomassa tal como águas usadas (esgoto), esterco, ou refugo de processamento de alimento, é misturado com água e introduzido em um tanque digestor sem ar. * Fermentação * Fermentação de Álcool: Álcool combustível é produzido convertendo massa celulósica e/ou amido para açúcar, fermentando o açúcar para álcool, em seguida separando a mistura de água e álcool por destilação. Matérias-primas tais como safras dedicadas (por exemplo, trigo, cevada, batatas, switchgrass, madeira de choupo), resíduos e refugos agrícolas (por exemplo, palha de arroz, palha de milho, palha de trigo, bagaço da cana-de-açúcar, cascas de arroz, fibra de milho, polpa de beterraba, polpa de cítricos, e cascas de cítricos), refugos de silvicultura (por exemplo, aparas de madeira de lei e de madeira branca, resíduos de madeira de lei e de madeira branca de operações de madeiramento, raspas de madeira, e serragem), refugos urbanos (por exemplo, fração de papel de refugo sólido municipal, resíduo de madeira municipal, refugo verde municipal), resíduos de madeira (por exemplo, refugo de serraria, refugo de moinho de polpa, refugo de construção, refugo de demolição, raspas de madeira, e serragem), e papel de refugo ou outros materiais contendo açúcar, amido, e/ou celulose podem ser convertidos para açúcares e em seguida para álcool por fermentação com levedura. Alternativamente, materiais contendo açúcares podem ser convertidos diretamente para álcool por fermentação. * Transesterificação: Uma reação típica para converter óleo em biodiesel é denominada transesterificação. O processo de transesterificação reage um álcool (como metanol) com os óleos triglicerídicos contidos em óleos vegetais, gorduras animais, ou graxas recicladas, formando ésteres alquílicos de ácidos graxos (biodiesel) e glicerina. A reação requer calor e um catalisador de base forte, tal como hidróxido de sódio ou hidróxido de potássio. * Biodiesel: Biodiesel é uma mistura de ésteres alquílicos de ácidos graxos preparada a partir de óleos vegetais, gorduras animais ou graxas recicladas. Biodiesel pode ser usado como um combustível para veículos em sua forma pura, ma geralmente é usado como um aditivo de diesel de petróleo para reduzir os níveis de particulados, monóxido de carbono, hidrocarbonetos e tóxicos para o ar de veículos equipados com motor a diesel. * Hidrólise: inclui hidrólise de um composto, por exemplo, uma biomassa, tal como um material lignocelulósico, catalisado usando uma enzima da presente invenção. * Cogeração: é a produção simultânea de mais de uma forma de energia usando um único combustível e instalação. Em um aspecto, cogeração de biomassa tem mais crescimento potencial do que a produção de biomassa somente porque a cogeração produz tanto calor quanto eletricidade.
[000952] Em um aspecto, os polipeptídeos da invenção têm atividade de hidrolase/celulolítica, por exemplo, atividade de glucanase, endoglucanase, mannase e/ou outra enzimática para produzir um combustível (por exemplo, um bioálcool, por exemplo, um bioetanol, biometanol, biobutanol ou biopropanol, ou biodiesel) a partir de um material orgânico, por exemplo, uma biomassa, tal como composições derivadas de plantas e animais, incluindo qualquer colheita agrícola ou outra matéria-prima renovável, um resíduo agrícola ou um refugo animal, os componentes orgânicos de refugos municipais e industriais, ou refugos ou detritos de construção ou demolição, ou micro-organismos tais como algas ou levedura.
[000953] Em um aspecto, polipeptídeos da invenção são usados em processos para converter biomassa lignocelulósica em um combustível (por exemplo, um bioálcool, por exemplo, um bioetanol, biometanol, biobutanol ou biopropanol, ou biodiesel), ou são usados de modo diverso em processos para hidrolisar ou digerir biomateriais de modo que possam ser usados como um combustível (por exemplo, um bioálcool, por exemplo, um bioetanol, biometanol, biobutanol ou biopropanol, ou biodiesel), ou para tornar mais fácila para a biomassa ser processada em um combustível.
[000954] Em um aspecto alternativo, polipeptídeos da invenção, incluindo a mistura de enzimas ou “coquetéis” da invenção, são usados em processos para um processo de transesterificação reagindo um álcool (como etanol, propanol, butanol, propanol, metanol) com um óleo triglicerídico contido em um óleo de legume, gordura animal ou graxas recicladas, formando ésteres alquíicos de ácidos graxos (biodiesel) e glicerina. Em um aspecto, biodiesel é fabricado a partir de óleo de soja ou óleos de cozimento reciclados. Gorduras animais, outros óleos vegetais, e outros óleos reciclados também podem ser usados para produzir biodiesel, dependendo de seus custos e disponibilidade. Em outro aspecto, misturas de todos os tipos de gorduras e óleos sã usadas para produzir um biodiesel combustível da invenção.
[000955] Enzimas da invenção, incluindo a mistura de enzimas ou “coquetéis” da invenção, também podem ser usadas no refino de glicerina. O subproduto de glicerina contém catalisador não-reagido e sabões que são neutralizados com um ácido. Água e álcool são removidos para produzir 50% a 80% de glicerina bruta. Os contaminantes restantes incluem gorduras e óleos não-reagidos, os quais podem ser processados usando os polipeptídeos da invenção. Em algumas grandes plantas de biodiesel da invenção, a glicerina pode ser adicionalmente purificada, por exemplo, até 99% ou maior pureza, para as indústrias farmacêutica e cosmética.
[000956] Combustíveis (incluindo bioálcoois tais como bioetanóis, biometanóis, biobutanóis ou biopropanóis, ou biodiesels) fabricados usando os polipeptídeos da invenção, incluindo a mistura de enzimas ou “coquetéis” da invenção, podem ser usados com combustíveis oxidados para melhorar as características da combustão. Adicionar oxigênio resulta em combustão mais completa, a qual reduz as emissões de monóxido de carbono. Isto é, outro benefício ambiental de substituir combustíveis de petróleo com biocombustíveis (por exemplo, um combustível da invenção). Um biocombustível fabricado usando as composições e/ou métodos desta invenção pode ser misturado com gasolina para formar uma mistura E10 (cerca de 5% a 10% de etanol e cerca de 90% a 95% de gasolina), mas pode ser usado em maiores concentrações tais como E85 ou em sua forma pura. Um biocombustível fabricado usando as composições e/ou métodos desta invenção pode ser misturado com diesel de petróleo para formar uma mistura B20 (20% de biodiesel e 80% de diesel de petróleo), embora outros níveis de misturas possan ser usados até B100 (biodiesel puro).
[000957] A invenção também proporciona processos para fabricar biocombustíveis (incluindo bioálcoois tais como bioetanóis, biometanóis, biobutanóis ou biopropanóis, ou biodiesels) a partir de composições compreendendo biomassa lignocelulósica. O material de biomassa de lignocelulose pode ser obtido a partir de colheitas agrícolas, como um subproduto de produção de alimento ou ração, ou como produtos de resíduos lignocelulósicos, tais como resíduos vegetais, papel de refugo ou refugos ou detritos de construção e/ou demolição. Exemplos de fontes de plantas ou resíduos vegetais adequados para tratamento com os polipeptídeos da invenção incluem cinza de algas, algas, grãos, sementes, caules, folhas, cascas, cascas secas, sabugos de milho, palha de milho, palha, gramíneas (por exemplo, Indian grass, tal como Sorghastrum nutans; ou, switchgrass, por exemplo, Panicum species, tal como Panicum virgatum), e similares, bem como madeira, lascas de madeira, polpa de madeira, e serragem. Exemplos de resíduo de papel adequado para tratamento com os polipeptídeos da invenção incluem papel de fotocópia de descarte, papel de impressora de computador, papel de caderno de apontamentos, papel de bloco de notas, papel para máquina de escrever, e similares, bem como jornais, revistas, papelão, e materiais de embalagem à base de papel. Exemplos de refugos e detritos de construção e demolição incluem madeira, pedaços de madeira, raspas de madeira e serragem.
[000958] Em uma modalidade, as enzimas, incluindo a mistura de enzimas ou “coquetéis” da invenção, e métodos da invenção podem ser usados em combinação com meios mais "tradicionais" de fabricar etanol, metanol, propanol, butanol, propanol e/ou diesel a partir de biomassa, por exemplo, como métodos compreendendo hidrolisar materiais lignocelulósicos submetendo material lignocelulósico seco em um reator a um catalisador consistindo em uma solução diluída de um ácido forte e um sal de metal; isto pode reduzir a energia de ativação, ou a temperatura, de hidrólise celulósica para obter maiores produções de açúcar; vide, por exemplo, as Patentes dos Estados Unidos Nos. 6.660.506 e 6.423.145.
[000959] Outro método exemplar que incorporou o uso de enzimas da invenção, incluindo a mistura de enzimas ou “coquetéis” da invenção, compreende hidrolisar material lignocelulósico contendo hemicelulose, celulose e lignina, ou qualquer outro polissacarídeo que pode ser hidrolisado por uma enzima desta invenção, submetendo o material a um primeiro estágio da etapa de hidrólise em um meio aquoso em uma temperatura e uma pressão escolhidas para realizar essencialmente emspolimerização de hemicelulose sem despolimerização importante de celulose para glicose. Esta etapa resulta em uma pasta semifluida na qual a fase aquosa líquida contém monossacarídeos dissolvidos resultantes de despolimerização de hemicelulose e uma fase sólida contendo celulose e lignina. Uma segundo estágio da etapa de hidrólise pode compreender condições tais que pelo menos uma porção importante da celulose é despolimerizada, semelhante etapa resultando em uma fase aquoas líquida contendo produtos de despolimerização de celulose dissolvidos/solúveis. Vide, por exemplo, a Patente dos Estados Unidos No. 5.536.325. Enzimas da invenção (incluindo as misturas da invenção, ou “coquetéis” de enzimas) podem ser adicionadas em qualquer estágio deste processo típico.
[000960] Outro método exemplar que incorporou o uso de enzimas da invenção, incluindo a mistura de enzimas ou “coquetéis” da invenção, compreende processar um material de biomassa contendo lignocelulose por um ou mais estágios de hidrólise ácida diluída com cerca de 0,4% a 2% de ácido forte; e tratar um componente lignocelulósico sólido não-reagido do material de biomassa hidrolisado com ácido por deslignificação alcalina para produzir precursores para termoplásticos biodegradáveis e derivados. Vide, por exemplo, a Patente dos Estados Unidos No. 6.409.841. Enzimas da invenção podem ser adicionadas em qualquer estágio deste processo típico.
[000961] Outro método exemplar que incorporou o uso de enzimas da invenção, incluindo a mistura de enzimas ou “coquetéis” da invenção, compreende prehidrolisar material lignocelulósico em um reator de pré-hidrólise; adicionar um líquido acídico ao material lignocelulósico sólido para fabricar uma mistura; aquecer a mistura até a temperatura da reação; manter a temperatura da reação por tempo suficiente para fracionar o material lignocelulósico em uma porção solubilizada contendo pelo menos cerca de 20% da lignina do material lignocelulósico e uma fração sólida contendo celulose; remover uma porção solubilizada da fração sólida enquanto em ou próximo à temperatura da reação em que a celulose na fração sólida é tornada mais suscetível a digestão enzimática; e recuperar uma porção solubilizada. Vide, por exemplo, a Patente dos Estados Unidos No. 5.705.369. Enzimas da invenção podem ser adicionadas em qualquer estágio deste processo típico.
[000962] A invenção proporciona métodos para fabricar composições de combustível para motores (por exemplo, para motores de ignição a centelhas) à base de hidrocarbonetos líquidos misturados com um álcool de grau combustível fabricado usando uma enzima ou um método da invenção. Em um aspecto, os combustíveis fabricados por uso de uma enzima da invenção compreendem, por exemplo, misturas de gás de carvão liquefeito e etanol ou de gás natural liquefeito e etanol. Em um aspecto, um co-solvente é 2-metiltetraidrofurano derivado de biomassa (MTHF). Vide, por exemplo, a Patente dos Estados Unidos No. 6.712.866.
[000963] Em um aspecto, métodos da invenção para a degradação enzimática de lignocelulose, por exemplo, para produção de biocombustíveis (incluindo bioálcoois tais como bioetanóis, biometanóis, biobutanóis ou biopropanóis, ou biodiesels) a partir de material lignocelulósico, também podem compreender uso de tratamento ultrassônico do material de biomassa; vide, por exemplo, a Patente dos Estados Unidos No. 6.333.181.
[000964] Em outro aspecto, métodos da invenção para produzir biocombustíveis (incluindo bioálcoois tais como bioetanóis, biometanóis, biobutanóis ou biopropanóis, ou biodiesels) a partir de um substrato celulósico compreendem proporcionar uma mistura da reação sob a forma de uma pasta semifluida compreendendo substrato celulósico, uma enzima desta invenção e um agente de fermentação (por exemplo, dentro de um vaso de reação, tal como um biorreator alimentado com sólidos semi-contínuos), e a mistura da reação é reagida sob condições suficientes para iniciar e manter uma reação de fermentação (conforme descrito, por exemplo, no Pedido de Patente dos Estados Unidos No. 20060014260). Em um aspecto, experimento ou cálculos teóricos podem determinar uma frequência de alimentação ótima. Em um aspecto, quantidades adicionais do substrato celulósico e a enzima são proporcionados no vaso de reação em um ou mais intervalos de acordo com a frequência de alimentação otimizada.
[000965] Um processo típico para fabricar biocombustíveis (incluindo bioálcoois tais como bioetanóis, biometanóis, biobutanóis ou biopropanóis, ou biodiesels) da invenção é descrito na Publicação do Pedido de Patente dos Estados Unidos Nos. 20050069998; 20020164730; e em um aspecto compreende estágios de trituração da biomassa lignocelulósica (por exemplo, até um tamanho de 15 a 30 mm), submeter o produto obtido a pré-tratamento por explosão de vapor (por exemplo, em uma temperatura de 190 a 230oC) por entre 1 e 10 minutos em um reator; coletar o material pré-tratado em um ciclone ou produdo de fabricação relacionado; e separar as frações líquida e sólida por filtração em um filtro à prensa, introduzindo a fração sólida em um depósito de fermentação e adicionando uma ou mais enzimas da invenção, por exemplo, uma celulase e/ou betaglucosidase enzima (por exemplo, dissolvida em tampão de citrato pH 4,8).
[000966] Outro processo típico para fabricar biocombustíveis (incluindo bioálcoois tais como bioetanóis, biometanóis, biobutanóis ou biopropanóis, ou biodiesels) da invenção compreendendo bioetanóis, biometanóis, biobutanóis ou biopropanóis usando enzimas da invenção compreende pretratar um material de partida compreendendo a matéria-prima lignocelulósica compreendendo pelo menos hemicelulose e celulose. Em um aspecto, O material de partida compreende batatas, soja (colza), cevada, centeio, milho, aveia, trigo, beterrabas ou cana-de-açúcar ou um componente ou refugo ou subproduto da produção de alimento ou ração. O material de partida (“matéria-prima”) é reagido em condições as quais rompem a estrutura da fibra da planta para realizar pelo menos uma hidrólise parcial da hemicelulose e celulose. Condições disruptivas podem compreender, por exemplo, submeter o material de partida a uma temperatura média de 180oC a 270oC e, pH 0,5 a 2,5 por um período de cerca de 5 segundos a 60 minutos; ou, temperatura de 220oC a 270oC, em pH 0,5 a 2,5 por um período de 5 segundos a 120 segundos, ou equivalente. Isto produz uma matéria-prima com aumentada acessibilidade para ser digerida por uma enzima, por exemplo, uma celulase enzima da invenção. Patente dos Estados Unidos No. 6.090.595.Condições típicas para usar as enzimas da invenção na hidrólise de material lignocelulósico incluem reações em temperaturas entre cerca de 30oC e 48oC, e/ou um pH entre cerca de 4,0 e 6,0. Outras condições típicas incluem uma temperatura entre cerca de 30oC e 60oC e um pH entre cerca de 4,0 e 8,0.
[000967] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas na conversão de biomassa em combustíveis, e na produção de etanol, por exemplo, conforme descrito nos Pedidos de Patente Internacional PCT Nos. WO0043496 e WO8100857. Glucanases (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas para produzir açúcares fermentáveis e biomassa contendo glucano que pode ser convertida em etanol combustível.
Aplicações Industriais, de Perfuração e de Energia
[000968] O método e composições (incluindo os “coquetéis de enzima” - vide abaixo) da invenção podem ser usados em qualquer processo de descoberta e/ou perfuração de óleo e gás, ou qualquer processo de lavagem e/ou fraturamento de poço de óleo e gás; por exemplo:
[000969] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas para modificar a viscosidade de qualquer material derivado de plantas, por exemplo, onde ser aplica à indústria de óleo e gás. Por exemplo, em um aspecto, as enzimas da invenção são usadas na indústria de óleo e gás onde goma guar e guar modificada são usadas em, por exemplo, fluidos de fraturamento e lamas de lubrificação de brocas. As enzimas da invenção podem ser usadas para limpar poços de óleo, por exemplo, para romper a alta viscosidade ou a estrutura de gel em fluido fratural depois do fraturamento. Em um aspecto, as enzimas da invenção usadas nestes aplicações têm uma alta termoestabilidade. Em um aspecto, as enzimas da invenção usadas nestes aplicações são resistentes às elevadas temperaturas no solo ou geradas por processos de perfuração. Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas para tratar lama de perfuração de brocas (por exemplo, lama usada).
[000970] As enzimas da invenção podem ser usadas em composições para prevenir dano da capacidade de fluxo para telas do orifício do poço e revestimentos chanfrados, incluindo seu uso com ou em revestimentos aplicados a telas do orifício do poço ou revestimentos chanfrados antes de inserção das telas ou revestimentos chanfrados em um orifício do poço, por exemplo, conforme descrito no Pedido de Patente dos Estados Unidos No. 20050065037.
Aumentando o fluxo de fluidos de produção de uma formação subterrânea
[000971] A invenção proporciona métodos usando uma ou mais enzimas ou coquetéis enzimáticos conforme descrito aqui, neste pedido de patente, em que o método aumenta o fluxo de fluidos de produção de uma formação subterrânea removendo fluidos prejudiciais viscosos, contendo amido, formados durante operações de produção; estes fluidos podem ser encontrados dentro da formação subterrânea a qual circunda um orifício do poço completado. Portanto, este método da invenção resulta em fluidos de produção sendo capazes de escoar do orifício do poço. Este método da invenção também trata o problema de fluidos prejudiciais reduzindo o fluxo de fluidos de produção de uma formação abaixo de taxas de fluxo esperadas. Em um aspecto, a invenção proporciona formular um tratamento enzimático (usando uma enzima da invenção) combinando juntos um fluido aquoso e um polipeptídeo da invenção; bombeando o tratamento enzimático para uma localização desejada dentro do orifício do poço; possibilitando que o tratamento enzimático degrade o fluido prejudicial viscoso, contendo amido, por meio do qual o fluido pode ser removido da formação subterrânea para a superfície do poço; e em que o tratamento enzimático é eficaz para atacar as ligações alfa glicosídicas no fluido contendo polissacarídeos.
[000972] Os processos de tratamento enzimático da formação subterrânea da invenção também podem incluir (além das enzimas desta invenção) o uso de qualquer combinação de outras enzimas tais como amilases, xantanases, glicosidases, celulases, triptofanases ou tirosina decarboxilases, lacases, catalases, lacases, outras celulases, endoglicosidases, endo-beta-1,4-lacases, amiloglucosidases, outras glucosidases, glicose isomerases, glicosiltransferases, lipases, fosfolipases, lipo-oxigenases, beta-lacases, endo-beta-1,3(4)-lacases, cutinases, peroxidases, outras amilases, xantanases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, arabinanases, hemicelulases, mananases, xilolacases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, proteases, peptidases, proteinases, poligalacturonases, ramnogalacturonases, galactanases, pectina liases, transglutaminases, pectina metilesterases, outras celobio- hidrolases e/ou transglutaminases.
Uso em operações de perfuração de poços e de mineração
[000973] A invenção também inclui métodos usando enzimas desta invenção (por exemplo, amilase, xantanase, glicosidase e/ou celulase, uma enzima de degradação de lignina, alfa amilase, beta amilase, glucoamilase, dextrinase, celulase, celobio-hidrolase, avicelase, carboximetilcelulase, beta-glucanase, glucosidase, xilanase, mananase, arabinofuranosidase, lacase, lignina peroxidase, pectinase, pectate liase, xantanase, xantana liase, xantana depolimerase, pululanase, liquenase, paquimanase, lipase, protease, proteinase, fitase, peptidase e/ou catalase enzimas) em operações de poços e de perfuração, por exemplo, operações de perfuração ou mineração de gás, óleo ou diversas, incluindo quaisquer processos de lavagem e/ou fraturamento de poço de óleo e gás. Por exemplo, em um aspecto, enzimas da invenção são usadas para aumentar o fluxo de fluidos de produção de uma formação subterrânea, por exemplo, um poço ou uma mina. Em um aspecto, as enzimas ou coquetéis de enzimas usados para praticar a invenção são usados para remover fluidos viscosos, contendo polissacarídeos (por exemplo, contendo amido) que podem ser prejudiciais, por exemplo, fluidos formados durante operações de produção. Estes fluidos contendo polissacarídeo (por exemplo, contendo amido) podem ser encontrados dentro de uma formação subterrânea a qual circunda um orifício do poço completado. Em um aspecto, enzimas ou coquetéis de enzimas da invenção são usados em um fluido de perfuração de poço de óleo para ajudar na retirada da lama de lubrificação de brocas.
[000974] Em um aspecto, o método compreende possibilitar que fluidos de produção (compreendendo enzimas ou coquetéis de enzimas da invenção) escoem do orifício do poço ou de uma mina. Os métodos podem compreender reduzir o fluxo de fluidos de produção da formação abaixo de taxas de fluxo esperadas e formular um tratamento enzimático misturando juntos um fluido aquoso e um polipeptídeo da invenção. Os métodos podem compreender bombear o tratamento enzimático para uma localização desejada dentro do orifício do poço ou outro poço de mina perfurado e possibilitar que o tratamento enzimático degrade o fluido prejudicial viscoso, contendo polissacarídeo. Os métodos podem compreender remover o fluido da formação subterrânea para a superfície do poço ou poço de mina. Em um aspecto, o tratamento enzimático é eficaz para atacar as ligações alfa glicosídicas no fluido contendo polissacarídeo. Em um aspecto, enzimas ou coquetéis de enzimas da invenção são usados em perfuração de minas, perfuração de poços (por exemplo, perfuração de poços de gás ou óleo), e similares para retirar a lama de lubrificação de brocas, por exemplo, enquanto perfurando o poço (orifício do poço ou poço de mina).
[000975] As enzimas ou coquetéis de enzimas da invenção podem ser usados em qualquer operação de perfuração de poço, poço de mina ou mina, muitos dos quais são de conhecimento geral na técnica. Por exemplo, a invenção proporciona métodos para introduzir enzimas ou coquetéis de enzimas da invenção, os quais em um aspecto também podem compreender um produto químico de produção de campo de óleo ou gás, em uma formação de rocha compreendendo óleo e/ou gás, o qual compreende passar uma microemulsão compreendendo a enzima (e, em um aspecto, o produto químico) para dentro de um poço de produção e em seguida para dentro da formação. Em um aspecto, um poço de produção é submetido a um tratamento de "encerramento" por meio do qual uma composição aquosa compreendendo uma enzima da invenção é injetada no poço de produção sob pressão e "comprimida" dentro da formação e aí mantida. Vide, por exemplo, a Patente dos Estados Unidos No. 6.581.687.
[000976] Em um aspecto, enzimas ou coquetéis de enzimas da invenção que são usados nestas operações de perfuração ou mineração de gás, óleo ou diversas, ou incluindo quaisquer processos de lavagem e/ou fraturamento de poço de óleo e gás, são ativos em elevado ou baixo pH e/ou temperaturas elevadas ou baixas, por exemplo, enzimas de degradação de polímeros ou de degradação de polissacarídeos (“quebrador de polímero”) desta invenção, os quais incluem usar “coquetéis” destas e outras enzimas tais como amilase, xantanase, glicosidase e/ou celulase enzimas, ou uma enzima de degradação de lignina, alfa amilase, beta amilase, glucoamilase, dextrinase, celulase, celobio-hidrolase, avicelase, carboximetilcelulase, beta-glucanase, glucosidase, xilanase, mananase,arabinofuranosidase, lacase, lignina peroxidase, pectinase, pectate liase, xantanase, xantana liase, xantana depolimerase, pululanase, liquenase, paquimanase, lipase, protease, proteinase, fitase, peptidase e catalase, os quais incluem usar “coquetéis” destas e outras enzimas, são usados nestes processos e são ativos sob condições compreendendo cerca de pH 6,5, pH 6, pH 5,5, pH 5, pH 4,5, pH 4,0, pH 3,5, pH 3,0 ou menos (mais acídico), ou, sob condições compreendendo cerca de pH 7, pH 7,5 pH 8,0, pH 8,5, pH 9, pH 9,5, pH 10, pH 10,5, pH 11,0, pH 11,5, pH 12, pH 12,5 ou mais (mais básico). Em um aspecto, enzimas ou coquetéis de enzimas da invenção usados nestes processos são ativos sob condições compreendendo uma faixa de temperatura de qualquer ponto entre cerca de -100°C a cerca de -80°C, cerca de -80°C a cerca de -40°C, cerca de -40°C a cerca de -20°C, cerca de -20°C a cerca de 0°C, cerca de 0°C a cerca de 37°C, cerca de 0°C a cerca de 5°C, cerca de 5°C a cerca de 15°C, cerca de 15°C a cerca de 25°C, cerca de 25°C a cerca de 37°C, cerca de 37°C a cerca de 45°C, cerca de 45°C a cerca de 55°C, cerca de 55°C a cerca de 70°C, cerca de 70°C a cerca de 75°C, cerca de 75°C a cerca de 85°C, cerca de 85°C a cerca de 90°C, cerca de 90°C a cerca de 95°C, cerca de 95°C a cerca de 100°C, cerca de 100°C a cerca de 105°C, cerca de 105°C a cerca de 110°C, cerca de 110°C a cerca de 120°C, ou 95°C, 96°C, 97°C, 98°C, 99°C, 100°C, 101°C, 102°C, 103°C, 104°C, 105°C, 106°C, 107°C, 108°C, 109°C, 110°C, 111°C, 112°C, 113°C, 114°C, 115°C, 120°C ou mais.
Uso de enzimas livres e imobilizadas em operações hidráulicas de fraturamento e de perfuração:
[000977] A invenção proporciona composições e métodos compreendendo a inclusão de enzimas de fragmentação de polímeros (de degradação de polímeros), por exemplo, de degradação de polissacarídeos, em uma forma livre ou em uma forma imobilizada, por exemplo, em uma forma imobilizada como sobre um revestimento, por exemplo, de uma partícula, por exemplo, de um grão de areia ou um material cerâmico tal como uma bauxita sinterizada.
[000978] Em um aspecto, as composições e métodos compreendendo a inclusão de enzimas de fragmentação de polímeros (de degradação de polímeros), por exemplo, de degradação de polissacarídeos, em ou sobre uma resina ou material similar que reveste partículas, por exemplo, grãos de areia ou um material cerâmico tal como uma bauxita sinterizada; estas partículas (por exemplo, grãos de areia) podem ser usadas como o "proppant" em um fluido de fraturamento hidráulico. Em um aspecto, um "proppant" usado para praticar esta invenção é algumas partículas modeladas misturadas com um fluido de fraturamento para manter as fraturas abertas depois de um tratamento de fraturamento hidráulica. Além de grãos de areia que ocorrem naturalmente, também podem ser usados "proppants" sintéticos ou produzidos especialmente, tais como areia revestida com resina ou materiais cerâmicos de alta potência como bauxita sinterizada. Materiais "proppants" podem ser classificados por tamanho e esfericidade para proporcionar um conduto eficiente para produção de fluido a partir do reservatório para o orifício do poço. Depois da sedimentação da areia nas fissuras e fraturas do poço, as enzimas ligadas a resina podem se difundir e trabalhar sobre o polímero concentrado e intacto que é frequentemente depositado sobre a superfície de formação no completamento das operações de fraturamento. Portanto, este aspecto da invenção pode efetivamente remover um polissacarídeo, um xantana ou um guar, por exemplo, uma torta de filtro de guar, de poços de óleo e gás fraturados, e/ou pode reforçar a permeabilidade da zona fraturada.
[000979] Em uma modalidade, durante as operações de fraturamento hidráulica, grandes volumes de água, areia, produtos químicos auxiliares (incluindo enzimas e as misturas de enzimas desta invenção) e um polímero à base de polissacarídeo (por exemplo, um guar e/ou seus derivados) são misturados e injetados sob pressão nas cavidades de óleo e/ou gás para 'fraturar' a formação circunjacente e reforçar o fluxo de gás ou óleo no orifício do poço. Enzimas e misturas de enzimas conforme descrito aqui, neste pedido de patente, podem ser usadsa para hidrolisar estes polímeros de polissacarídeos e reduzir a viscosidade do fluido (usado nas operações de fraturamento hidráulica) para melhor penetração na formação e fluxo de volta mais eficaz ao fim da operação.
[000980] Em uma modalidade, as composições e métodos desta invenção são usados em hidrólise enzimática de polímeros básicos (por exemplo, polímeros à base de polissacarídeos, tais como guar, xantana e/ou seus derivados); a prática desta invenção pode resolver o problema onde a hidrólise enzimática destes polímeros básicos pode ser incompleta deixando algum polímero "intacto" no fluido usado nas operações de fraturamento hidráulica. À medida que o teor de água do fluido é perdido para a formação o fluido se torna mais concentrado e os polímeros intactos formam uma torta de filtro espessa; esta torta de filtro obstrui os poros da formação e reduz o fluxo de óleo ou gás para dentro do orifício do poço - em uma modalidade, as composições e métodos desta invenção são usados para fragmentar estas obstruções da torta de filtro.
[000981] Fluidos de fraturamento contêm grandes quantidades de areia, referida comumente como o "proppant". À medida que o fluido é bombeado para dentro do poço, o proppant sedimenta dentro das fissuras e fraturas e impede que as mesmas fechem. Isto ajuda a reforçar a porosidade e a permeabilidade da formação para melhor fluxo de gás/óleo. Os grãos de areia são frequentemente revestidos com diferentes resinas industriais para aumentar sua potência mecânica e evitar que os mesmos sejam triturados sob pressão da formação. Deste modo, em uma modalidade, a invenção proporciona composições e métodos usando enzimas de degradação de polímeros (“quebra de polímero”) livres ou imobilizadas em torno, em ou sobre o material de revestimento da areia. Em um aspecto, isto é, feito por captura da enzima na resina ou por imobilização sobre a superfície de resvestimento. Portanto, neste aspecto, uma ou mais enzimas usadas para praticar esta invenção podem permanecer em contato com a torta de filtro deste modo proporcionando hidrólise contínua do polímero concentrado, removendo a torta das fraturas, e reforçando a permeabilidade da formação fraturada.
[000982] Em um aspecto, a invenção proporciona métodos usando estas enzimas descritas em operações de perfuração, por exemplo, uma operação de perfuração típica, onde um poço é criado por perfuração de um poço de 13 a 76 cm (5 a 30 polegadas) de diâmetro dentro da terra com uma torre de óleo, a qual gira uma broca. Depois do poço ser perfurado, um tubo de aço (tubo de aço) ligeiramente menor do que o poço é disposto dentro do poço, e fixado com cimento. O tubo de aço proporciona integridade estrutural ao orifício do poço recém perfurado além de isolar zonas de alta pressão potencialmente perigosas umas das outras e da superfície.
[000983] Com estas zonas isoladas seguramente e a formação protegida pelo tubo de aço, o poço pode ser perfurado mais fundo (em formações potencialmente mais instáveis e violentas) com uma broca menor, e também revestida com um tubo de aço de tamanho menor. Alguns poços podem ter 2 a 5 séries de tamanhos de furos subsequentemente menores perfurados um dentro do outro, cada um cimentado com tubo de aço.
[000984] Para perfurar o poço, a broca, auxiliada por torque giratório e pelo peso compressivo de comandos de perfuração acima desta, dissolve a terra. Fluido de perfuração, ou "lama ", compreendendo a inclusão de enzimas de fragmentação de polímeros (de degradação de polímeros), por exemplo, de degradação de polissacarídeos, e misturas de enzimas desta invenção, em uma forma livre ou em uma forma imobilizada, é bombeado para dentro do cano da perfuratriz. O fluido sai na broca e ajuda a fragmentar a rocha, mantendo pressão na parte superior da broca, bem como limpando, resfriando e lubrificando a broca.
[000985] Os "cortes " da rocha gerados são varridos pelo fluido de perfuração à medida que este circula de volta para a superfície fora do cano da perfuratriz. Fluido compreendendo enzimas de fragmentação de polímeros (de degradação de polímeros), por exemplo, de degradação de polissacarídeos, e misturas de enzimas desta invenção, em uma forma livre ou em uma forma imobilizada, pode ser adicionado neste estágio, também.
[000986] Os fluidos então vão sobre agitadores os quais agitam os cortes sobre telas permitindo que fluido bom retorne para dentro das minas. Fluido compreendendo enzimas de fragmentação de polímeros (de degradação de polímeros), por exemplo, de degradação de polissacarídeos, e misturas de enzimas desta invenção, em uma forma livre ou em uma forma imobilizada, podem ser adicionados neste estágio, também.
[000987] Estes processos da invenção podem ser facilitados por adição de enzimas de fragmentação de polímeros (de degradação de polímeros), por exemplo, de degradação de polissacarídeos, e misturas de enzimas desta invenção, em uma forma livre ou em uma forma imobilizada. A torre de perfuração pode conter todo o equipamento necessário para circular o fluido de perfuração, erguer e girar o cano, controlar pressões poço abaixo, remover cortes do fluido de perfuração, e gerar energia onsite para estas operações.
[000988] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser praticadas com qualquer lama de lubrificação de brocas ou fluido de perfuração (algumas pessoas preferem reservar o termo "fluido de perfuração" para "lamas” mais sofisticadas e bem definidas), ou qualquer fluido usado em operações para perfurar furos de sondagem dentro da terra. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser praticados ao perfurar poços de óleo e/ou gás natural e na exploração de torres de perfuração, incluindo uso com poços mais simples.
[000989] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com qualquer operação de poço ou de perfuração, por exemplo, onde qualquer lama é usada, incluindo uso de quaisquer dos três esquemas de classificação principais de lama, onde “lama” é usada amplamente e é separada em 3 categorias com base no componente principal que compõe a lama: (1) “Lama à Base de Água” (WBM, Water Based Mud), a qual pode ser subdividida em lamas dispersadas e não- dispersadas; (2) “Não Aquosa” ou mais comumente “Lama à Base de Óleo” (OBM, Oila Based Mud), incluindo óleos sintéticos (SBM); e/ou (3) Lama Gaseosa ou Pneumática.
[000990] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com qualquer operação de poços ou de perfuração, por exemplo, também podem ser usados em ou com: • poços de produção quando são perfurados essencialmente para produzir óleo ou gás, uma vez que a estrutura de produção e as características são estabelecidas, • poços de avaliação ("appraisal") quando são usados para avaliar características (tais como taxa de fluxo) de uma acumulação de hidrocarboneto comprovada, • poços de exploração quando são perfurados puramente para fina exploratórios (para obter informação) em uma nova área, • poços pioneiros ("wildcat") quando um poço é perfurado, com base em um grande elemento de esperança, em uma área de fronteira onde muito pouco se sabe sobre a subsuperfície.
[000991] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados juntos com qualquer operação de poço ou de perfuração, por exemplo, também podem ser usados em combinação com métodos, equipamento e/ou operações de perfuração conforme descrito, por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070089910, Hewson, et al., descrevendo, por exemplo, métodos para formar um orifício de poço subterrâneo suportado, e usa, por exemplo, um motor de lama de deslocamento positivo.
[000992] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com métodos, equipamento e/ou operações de perfuração conforme descrito, por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070084638, Bohnsack; C., et al., descrevendo, por exemplo, um sistema para facilitar o fluxo de sólidos sedimentados com fluido de perfuração de um recipiente, o sistema incluindo equipamento de bocal de pressão com pelo menos um bocal do qual é escoável fluido sob pressão, equipamento de rotação equipado com motor para rotar seletivamente o equipamento de bocal de pressão de modo que pelo menos um bocal seja movível dentro do recipiente à medida que o fluido seja bombeado através de pelo menos um bocal para dentro do recipiente; e, em um aspecto, equipamento de translação para mover o equipamento de bocal de pressão com respeito ao container à medida que o fluido sob pressão é bombeado para o pelo menos um bocal giratório. Tanques de lama e fossos de lama também são descritos, e as enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com quaisquer destes fluidos, e/ou em quaisquer tanques de lama e fossos de lama usados nestes tipos de operações.
[000993] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com métodos, equipamento e/ou operações de perfuração conforme descrito, por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070081157, Csutak; S., et al., descrevendo, por exemplo, equipamento para estimar uma propriedade de um fluido poço abaixo compreendendo uma fonte de luz ultravioleta (UV) para induzir luz dentro do fluido em um comprimento de onda que produz luz dispersa de Raman em comprimentos de onda que são mais curtos do que comprimentos de onda de substancial fluorescência refletida a partir do fluido em resposta à luz induzida; um detector que detecta um espectro da luz dispersa de Raman e proporciona sinais em resposta ao espectro detectado; e um processador que processa os sinais para proporcionar uma estimativa de uma propriedade do fluido. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com quaisquer destes fluidos, e/ou em operações para estimar contaminação do filtrado em um fluido da formação. Por exemplo, estes métodos incluem detectar dispersões de Raman em uma pluralidade de comprimentos de onda de pelo menos um componente presente em uma lama à base de óleo que não está presente naturalmente na formação, e enzimas, misturas de enzimas, e métodos da invenção podem ser usados para ajudar na precisão desta detecção.
[000994] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com métodos, equipamento e/ou operações de perfuração conforme descrito, por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070075706, Chen, S. , et al., descrevendo, por exemplo, métodos para avaliar uma formação terrosa compreendendo fazer medições com uma ferramenta poço abaixo em um furo de sondagem na formação terrosa; medir um fator de Qualidade de uma antena da ferramenta poço abaixo em profundidades onde são feitas as medições; e usando o Q medido e uma resistividade de uma lama no furo de sondagem e uma resistividade da formação, e/ou um indicador do tamanho do furo de sondagem (BSI), para estimar o outro da resistividade da formação e BSI, incluindo medir a resistividade da lama no furo de sondagem. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com quaisquer destes fluidos, e/ou em operações para avaliar uma formação terrosa.
[000995] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com métodos, equipamento e/ou operações de perfuração conforme descrito, por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070068675, Barry, M., et al, descrevendo, por exemplo, métodos para perfurar e completar um poço enchido com cascalho, compreendendo perfuração de um orifício do poço com um fluido de perfuração, condicionar o fluido de perfuração, dirigindo as ferramentas de montagem de enchimento com cascalho para o fundo no orifício do poço com o fluido de perfuração condicionado, e enchendo com cascalho um intervalo do orifício do poço com um fluido de completamento. O fluido de completamento pode ser o mesmo que o fluido de perfuração. Este método pode ser combinado com tecnologia de peneira de areia de caminho alternado para assegurar distribuição apropriada do enchimento com cascalho. Os fluidos apropriados para perfuração, enchimento com cascalho e instalação de peneiras de areia são essenciais para o sucesso do completamento do poço. São necessários cuidadoso planejamento, preparação do poço e execução do completamento para aumentar a produtividade e a longevidade do completamento. Geralmente, tem sido usado um mínimo de três fluidos para perfurar e completar poços enchidos com cascalho. O primeiro fluido é um fluido de perfuração carregado com sólidos usado para perfurar o intervalo do completamento. O segundo fluido é um fluido de completamento livres de sólidos usado para deslocar o fluido de perfuração carregado com sólidos e para dirigir o equipamento de exclusão de areia e as ferramentas de enchimento com cascalho em um ambiente geralmente livre de sólidos. O terceiro fluido é um fluido de veículo para o cascalho durante o enchimento com cascalho do intervalo do completamento. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com quaisquer destes fluidos (incluindo fluidos de perfuração carregados com sólidos, fluidos de completamento livres de sólidos e/ou fluidos de veículo), e/ou em operações para perfuração e completamento de um poço enchido com cascalho.
[000996] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com métodos, equipamento e/ou operações de perfuração conforme descrito, por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070066491, Bicerano; J., et al., uso de partículas na construção, perfuração, completamento e/ou estimulação de fratura de poços de óleo e gás natural; por exemplo, como uma monocamada parcial proppant, um pacote proppant, um componente integral de um completamento de enchimento com cascalho, um rolamento de esferas, um lubrificante sólido, um constituinte de lama de lubrificação de brocas, e/ou um aditivo de cimento, incluindo uso de partículas de polímero termocuradas para uso em aplicações requerendo partículas leves possuindo alta rigidez, resistência, resistência à temperatura, e/ou resistência a ambientes agressivos. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com quaisquer destes enchimentos com cascalho, rolamentos de esferas, lubrificantes sólidos, constituintes de lamas de lubrificação de brocas, aditivos de cimento e/ou as partículas de polímeros termocuradas descritas. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com nanoenchimentos e/ou nanocompostos, incluindo morfologias de nanocompostos heterogêneos.
[000997] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com métodos, equipamento e/ou operações de perfuração conforme descrito, por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070039735, Robertson; B., et al., descrevendo, por exemplo, métodos de vedação de uma zona permeável dentro de uma formação subterrânea, compreendendo: preparar uma composição de obstrução compreendendo óleo, argila, cloreto de magnésio, e pó de óxido de magnésio; e contatar a composição de obstrução com água dentro da formação subterrânea de tal modo que a composição de obstrução forme uma massa vedante, deste modo substancialmente vedando uma zona permeável dentro da formação subterrânea.
[000998] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em, misturados com e/ou praticados junto com lamas de lubrificação de brocas de densidades variáveis compreendendo materiais particulados compressíveis, por exemplo, conforme descrito na Publicação do Pedido de Patente dos Estados Unidos No. 20070027036, Polizzotti; R., et al. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com, por exemplo, lamas de lubrificação de brocas compreendendo um material particulado compressível na lama de lubrificação de brocas, em que a densidade da lama de lubrificação de brocas se altera devido a uma mudança do volume do material particulado compressível em resposta a alterações na pressão ou na temperatura e em que o material particulado compressível é configurado para manter a densidade da lama de lubrificação de brocas entre um gradiente de pressão de poro e um gradiente de fratura com base na mudança de volume do material particulado compressível em resposta a alterações na pressão em determinadas profundidades.
[000999] As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados para modificar a viscosidade da lama de lubrificação de brocas sozinhos ou em combinação com os materiais compressíveis descritos (vide Polizzotti; R., et al.), por exemplo, para por a viscosidade do fluido dentro de requisitos de bombeabilidade, e/ou para ajustar o gradiente de pressão de poro e o gradiente de fratura. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados para efetuar uma mudança do volume na lama de lubrificação de brocas, por exemplo, onde a reologia da lama de lubrificação de brocas é configurada para atingir uma desejada reologia da lama de lubrificação de brocas composta.
[0001000] Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção são usados para alterar as propriedades da lama de lubrificação de brocas para proporcionar um composto desejado um ponto de gel de lama, por exemplo, um ponto de gel de lama que pode suspender cortes de rochas em uma coroa anular de um orifício do poço durante operações de perfuração; e/ou alterar a viscosidade da lama de lubrificação de brocas em combinação com, ou sozinho (sem), objetos ocos compressíveis (vide Polizzotti; R., et al.) para alterar os requisitos de bombeabilidade.
[0001001] Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção são usados para alterar as propriedades de fluidos de poços compreendendo lamas de lubrificação de brocas, fluidos de limpeza de poços, fluidos de exame minucioso, fluidos espacejadores, fluidos de enchimento com cascalho, fluidos acidificantes e/ou fluidos de fraturamento. Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção são usados para facilitar a perfuração, o completamento e/ou a estimulação de uma formação subterrânea usando um fluido de densidade variável, e para modificar o fluido de densidade variável.
[0001002] Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção são usados em métodos de perfuração, completamento e/ou estimulação de formações subterrâneas usando um fluido de densidade variável, por exemplo, modificando e/ou “ajustando” a densidade do fluido; por exemplo, um método (vide Polizzotti; R., et al.) compreendendo as etapas de: introduzir um fluido tendo uma densidade que varia em função da pressão dentro da formação subterrânea, onde o fluido compreende um fluido de base e uma porção de partículas elásticas; e perfurar, completar e/ou estimular uma formação subterrânea usando o fluido de densidade variável (o qual pode compreender as enzimas, misturas de enzimas da invenção, ou ter sido modificado pelos métodos da invenção).
[0001003] Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção são usados com os métodos e composições conforme descrito na Patente dos Estados Unidos No. 4.099.583, descrevendo, por exemplo, um sistema de perfuração de gradiente duplo, onde um fluido mais leve é injetado dentro da coroa anular de retorno da lama (tipicamente no tubo de subida) ou outro caminho para reduzir a densidade da lama do ponto de injeção para cima, e as enzimas, as misturas de enzimas, e os métodos da invenção podem modificar e/ou “ajustar” a densidade deste fluido.
[0001004] Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção são usados com os métodos e composições conforme descrito na Patente dos Estados Unidos No. 6.530.437 e na Patente dos Estados Unidos No. 6.588.501, descrevendo um método de perfuração multi-gradiente e um equipamento para redução da pressão hidrostática em tubos de subida submarinos; e a Patente dos Estados Unidos No. 6.422.326, a Patente dos Estados Unidos No. 6.156.708, as Patentes dos Estados Unidos Nos. 5.910.467 e 5.881.826, descrevendo a adição de vários afrons de fluidos para formulações de lama de lubrificação de brocas.
[0001005] Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção são usados com os métodos e composições conforme descrito na Patente dos Estados Unidos No. 6.497.289, descrevendo o uso de revestimentos expansíveis sólidos, por exemplo, como sistemas tubulares que são operados dentro de um poço e expandidos.
[0001006] Em modalidades alternativas, as enzimas, as misturas de enzimas, e os métodos da invenção são usados para adequar a densidade das lamas de lubrificação de brocas com a profundidade de modo que peso da lama eficaz permaneça entre a pressão do poro e o gradiente de fratura em todas as profundidades. A variação requerida na densidade da lama pode ser obtida alterando as propriedades dos fluidos com as enzimas, as misturas de enzimas, e os métodos da invenção para modificar/alterar o volume e a densidade, para efetura uma alteração em resposta à pressão. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados com quaisquer componentes particulados, por exemplo, várias formas, tais como esferas, cubos, pirâmides, esferóides oblatos ou prolatos, cilindros, almofadas e/ou outras formas ou estruturas. As enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados com quaisquer componentes particulados, por exemplo, objetos ocos compressíveis os quais são preenchidos com gás pressurizado, ou materiais sólidos compressíveis ou objetos conforme descrito em Polizzotti; R., et al., supra.
[0001007] Em aspectos alternativos, as enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em ou com qualquer operação de poço ou de perfuração, por exemplo, incluindo perfuração direcional, algumas vezes conhecida como perfuração inclinda, para perfurar poços não-verticais; inclusive usados em quaisquer dos três grupos principais de perfuração direcional; Perfuração Direcional de Campo de Óleo (Oilfield Directional Drilling), Perfuração Direcional de Instalação de Utilidade [Utility Installation Directional Drilling, conhecida comumente como Perfuração Direcional Horizontal (H.D.D./Horizontal Directional Drilling/sondagem Direcional)); e/ou perfuração direcional dentro de costura (metano em Leito de Carvão).
[0001008] Em um aspecto, as enzimas, as misturas de enzimas, e os métodos da invenção podem ser usados em combinação com perfilagem do poço, uma técnica usada na indústria de óleo e gás para registrar propriedades das rochas e dos fluidos para descobrir zonas de hidrocarbonetos nas formações geológicas dentro da crosta terrestre. A perfilagem pode ser realizada para medir o efeito de praticar os métodos desta invenção, por exemplo, bombeando fluidos compreendendo as enzimas ou misturas de enzimas desta invenção dentro de um poço. Um procedimento de perfilagem pode consistir de baixar uma 'ferramenta de perfilagem' sobre a extremidade de um cabo de aço (wireline) dentro de um poço de óleo (ou poço) para medir as propriedades das rochas e dos fluidos da formação. Uma interpretação destas medições é então feita para localizar e quantificar zonas de profundidades potenciais contendo óleo e gás (hidrocarbonetos). As ferramentas de perfilagem desenvolvidas durante os anos medem as propriedades elétricas, acústicas, radioativas, eletromagnéticas, e outras das rochas e seus fluidos contidos. A perfilagem é geralmente realizada à medida que as ferramentas de perfilagem são retiradas do poço. Estes dados são registrados em um registro impresso denominado um 'Well Log' e são normalmente transmitidos digitalmente para localizações de escritórios. A perfilagem do poço é realizada em vários intervalos durante a perfuração do poço e quando a profundidade total é perfurada, a qual pode variar em profundidades de 300 m a 8000 m (1000 pés a 25.000 pés) ou mais.
[0001009] Além dos métodos, enzimas ou misturas de enzimas descritos aqui, neste pedido de patente, os métodos, as lamas enzimáticas ou outros fluidos de perfuração usados para praticar esta invenção podem compreender (uso de) uma lama de lubrificação de brocas à base de água que pode compreender uma argila de bentonita (gel), e em alguns aspectos, também compreendendo aditivos tais como sulfato de bário (barita), carbonato de cálcio (giz) ou hematita. Vários espessantes também podem ser usados para influenciar a viscosidade do fluido, por exemplo, lignossulfonatos, goma xantana, goma guar, glicol, carboximetilcelulose, celulose polianiônica (PAC), ou amido. As enzimas ou misturas de enzimas descritas aqui, neste pedido de patente, usadas para praticar esta invenção podem ser usadas para modificar as propriedades de (por exemplo, a viscosidad de) os fluidos, por exemplo, para modificar as propriedades de lignossulfonatos, goma xantana, goma guar, glicol, carboximetilcelulose, celulose polianiônica (PAC), ou amido.
[0001010] Os métodos, as enzimas ou as misturas de enzimas descritas aqui, neste pedido de patente, usados para praticar esta invenção podem ser usados para modificar as propriedades de defloculantes, os quais são usados para reduzir a viscosidade de lamas à base de argila; polieletrólitos aniônicos, por exemplo, acrilatos, polifosfatos, lignossulfonatos (Lig) ou derivados de ácido tânico tais como Quebracho (lama vermelha foi o nome para uma mistura à base de Quebracho, denominada de acordo com a cor dos sais de ácido tânico vermelho; era comumente usada dos anos quarenta aos anos cinquenta, então se tornou obsoleta quando se tornaram disponíveis lignossulfatos).
[0001011] Os métodos, as enzimas ou as misturas de enzimas descritas aqui, neste pedido de patente, usados para praticar esta invenção podem ser usados em (por exemplo, adicionados a) injetores de água para injeta água em uma formação, quer para manter a pressão do reservatório ou simplesmente para descarte da água produzida com um hidrocarboneto (por exemplo, porque mesmo depois de tratamento, seria oleosa demais e solução salina demais para ser considerada limpa para descarregar, por exemplo, descarregar ao mar ou em uma fonte de água fresca no caso de poços terrestres). Portanto, os métodos e composições (por exemplo, misturas de enzimas, enzimas imobilizadas) desta invenção são usados com injeção de água como um elemento de tratamento de reservatórios e descarte da água produzida.
[0001012] Os métodos, as enzimas ou as misturas de enzimas descritas aqui, neste pedido de patente, usados para praticar esta invenção podem ser usados em (por exemplo, adicionados a) produtores aquíferos, por exemplo, como em produzindo intencionalmente água de reservatório para re-injeção (por exemplo, em um orifício do poço) para controlar a pressão; isto é, na prática mover água de reservatório de onde não é tão útila, para onde é mais útil. Estes poços geralmente somente serão usados se a água produzida pelo produtor de óleo ou gás for insuficiente para os fins de tratamento do reservatório. Portanto, em um aspecto, os métodos e composições (por exemplo, misturas de enzimas, enzimas imobilizadas) desta invenção são usados com água produzida aquífera e/ou água do mar.
Modificando as propriedades de Lignossulfonatos, ou ligninas sulfonadas
[0001013] Os métodos, as enzimas ou as misturas de enzimas descritos aqui, neste pedido de patente, usados para praticar esta invenção podem ser usados para modificar as propriedades de lignossulfonatos ou lignina sulfonada em qualquer processo. Por exemplo, os métodos, as enzimas ou as misturas de enzimas descritos aqui, neste pedido de patente, usados para praticar esta invenção podem ser usados para modificar as propriedades de quaisquer polímeros de polieletrólitos aniônicos hidrossolúveis, incluindo ligninas sulfonadas e subprodutos de ligninas de um sulfito ácido e/ou um proceso de sulfito para produção de polpa de madeira, incluindo “black liquor”.
[0001014] Os métodos, as enzimas ou as misturas de enzimas descritos aqui, neste pedido de patente, usados para praticar esta invenção podem ser usados para modificar as propriedades de lignossulfonatos usados como defloculantes em lama de lubrificação de brocas usadas em perfuração de óleo (onde substituiu Quebracho). Em modalidades alternativas, os métodos, as enzimas ou as misturas de enzimas descritos aqui, neste pedido de patente, usados para praticar esta invenção podem ser usados para modificar os lignossulfonatos usados na indústria de cimento como um defloculante de pasta semifluida de mistura bruta; usados em o como um plastificante e/ou usados como estabilizantes de emulsões.
Espessamento, suspensão e estabilização de sistemas aquosos
[0001015] A invenção proporciona métodos para usar polissacarídeos em processos comerciais-industriais para espessar, suspender ou estabilizar sistemas aquosos. Por exemplo, em um aspecto, os métodos da invenção são usados para modificar ou “ajustar as propriedades de” polímeros de polissacarídeos e tensoativos em pasta de impressão. Em um aspecto, os métodos da invenção são usados para modificar ou “ajustar as propriedades de” polímeros de polissacarídeos e tensoativos para produzir géis e agir como floculados, aglutinantes, lubrificantes, para servir como modificadores de propriedades de filmes.
[0001016] Em um aspecto, as composições e métodos da invenção são usados para modificar ou “ajustar as propriedades de” polímeros de polissacarídeos e tensoativos que agem como ajustadores de parâmetros reológicos em, por exemplo, floculados, aglutinantes, lubrificantes, filmes e/ou géis.
[0001017] Em um aspecto, as composições e métodos da invenção são usados para modificar ou “ajustar as propriedades de” polímeros de polissacarídeos e tensoativos que agem como floculados, aglutinantes, lubrificantes e/ou tensoativos em dispersantes, agentes umectantes, emulsificantes e agentes antiespumação. Em um aspecto, os métodos da invenção são usados para modificar ou “ajustar as propriedades de” polímeros de polissacarídeos e tensoativos que modificam a propriedade de alguns espessantes polissacarídicos tais como uma goma guar, com níveis de substituição diferentes e diferentes produtores usados em diferentes concentrações e temperaturas.
Outras aplicações industriais, medicinais, agrícolas, de pesquisa
[0001018] Glucanases, (ou celulases), mananases, xilanases,amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas em uma ampla variedade de aplicações industriais, de pesquisa, agrícolas e medicinais, incluindo e além das descritas aqui, neste pedido de patente, para detergentes, tratamento de têxteis ou fibras, tratamento de ou preparo de alimento, ração animal e bebidas, tratamento de resíduos, produtos para tratamento oral, aplicações medicinais e de pesquisa, aplicações de conversão de biomassa, aplicações de perfuração para, por exemplo, óleo e gás, e similares.
[0001019] Em um aspecto, as composições e métodos da invenção são usadas para modificar polímeros polissacarídicos para uso como anti-escalantes e dispersantes, onde os polímeros modificados são úteis em composições usadas em sistemas aquosos, por exemplo, em formulações de detergente, tratamento de água, dispersantes e aplicações do campo petrolífero e como aglutinantes de fibra de vidro, conforme descrito por exemplo, na Publicação do Pedido de Patente dos Estados Unidos No. 20070015678, Rodrigues; K, et al. Em um aspecto, as composições e métodos da invenção são usados juntos com reforçadores, tensoativos, enzimas, solventes, hidrótropos, enchimentos, alvejante, perfumes e/ou colorantes em sistemas aquosos, por exemplo, em formulações de detergente, tratamento de água, dispersantes e aplicações do campo petrolífero e como aglutinantes de fibra de vidro.Em um aspecto, as composições e métodos da invenção são usados para modificar polímeros polissacarídicos para uso em sistemas aquosos tais como água de caldeira ou sistemas de produção de vapor, sistemas de refrigeração de água, sistemas de purificação de gás, sistemas de moinho de polpa e papel, sistemas de dessalinização, tecido, sistemas de limpeza de louça e de superfícies duras e sistemas poço abaixo encontrados durante a produção de poços de gás, de óleo, e geotérmicos.
[0001020] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas em uma série de outras aplicações. Por exemplo, um uso alternativo compreende usar as composições (por exemplo, sondas e anticorpos) e métodos de triagem da invenção, para identificar e/ou isolar novas glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases; estas são divulgações por triagem das bibliotecas existentes (por exemplo, bibliotecas de DNA) e bibliotecas construídas a partir de diversas fontes ambientais, incluindo de localizações mesofílicas e moderadamente termofílicas bem como de fontes alvo incluindo flora digestiva, micro-organismos no oceano, refugo animal, bactérias do solo e habitats altamente alcalinos. Estratégias de biotrap e de enriquecimento primário usando substratos compreendendo glucano e/ou frações de polissacarídeos não-solúveis de material de ração animal também são úteis; vide, por exemplo, a Patente dos Estados Unidos No. 7.018.793; a Patente dos Estados Unidos No. 6.790.605; a Patente dos Estados Unidos No. 6.361.974; e a Patente dos Estados Unidos No. 5.939.250.
[0001021] Glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases da invenção podem ser usadas em combinação com outras enzimas envolvidas em digestão de celulose como celobio-hidrolases e beta-glucosidases, vide discussão de “coquetéis” de enzimas da invenção, conforme descrito aqui, neste pedido de patente.
[0001022] Enzimas da invenção podem ser usadas para melhorar a qualidade e a quantidade da produção de proteína do leite em vacas leiteiras (vide, por exemplo, Kung, L., et al, J. Dairy Science, 2000 Jan 83:115-122), aumentando a quantidade de sacarídeos solúveis no estômago e intestino delgado de porcos (vide, por exemplo, van der Meulen, J. et al, Arch. Tierernahr, 2001 54:101-115), aumentando a eficiência da produção de ovos tardia e as produções de ovos em galinhas (vide, por exemplo, Jaroni, D., et al, Poult. Sci., 1999 June 78:841-847).
[0001023] Usos adicionais para glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção incluem: uso na produção de fibra dietética hidrossolúvel (vide, por exemplo, a Patente dos Estados Unidos No. 5.622.738); melhorando a filtrabilidade, a separação e a produção de amido (vide, por exemplo, as Patentes dos Estados Unidos Nos. 4.960.705 e 5.023.176); em uma composição enzimática para promover a secreção de leite da criação e melhorar a qualidade do leite (vide, por exemplo, a Patente dos Estados Unidos No. 4.144.354); na redução da viscosidade de material vegetal (vide, por exemplo, a Patente dos Estados Unidos No. 5.874.274).
[0001024] Vários usos de glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou beta-glucosidases da invenção incluem a transformação de um micróbio que produz etanol (vide, por exemplo, a Patente WO 99/46362), na produção de taninos enológicos e composição enzimática (vide, por exemplo, a Patente WO 0164830), no estímulo das defesas naturais das plantas (vide, por exemplo, a Patente WO 0130161), na produção de açúcares de substratos hemicelulósicos (vide, por exemplo, a Patente WO 9203541), na limpeza de frutos, legumes, verduras, solos contendo lama ou argila (vide, por exemplo, a Patente WO 9613568), na limpeza de membranas de filtração de cerveja (vide, por exemplo, a Patente WO 9623579), em um método para matar ou inibir células microbianas (vide, por exemplo, a Patente WO 9732480) e na determinação das características de águas do processo de alvejamento de polpa de madeira usando as proporções de duas medições de absorção UV e comparando os espectros (vide, por exemplo, a Patente WO 9840721).
[0001025] Enzimas da invenção podem ser usadas em sistemas de purificação do ar e/ou da água, por exemplo, em meios e sistemas de filtro de ar ou água, conforme descrito por exemplo, no Pedido de Patente dos Estados Unidos No. 20060117958, descrevendo sistemas de purificação do ar tendo uma força de tração a seco, uma força de tração a úmido em associação com resistência à água e repelência à água e apresentando propriedades de meios bactericidas/esterilizantes ou antimicrobianos usando uma reação enzimática (tal como uma enzima desta invenção).
[0001026] Dois formatos de triagem (à base de atividade e à base de sequência) são usados na descoberta de novas glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio-hidrolases, mananases e/ou betaglucosidases. A abordagem à base de atividade é triagem direta para atividade de glucanase em lâminas ágar usando um substrato tal como AZO-beta glucano de cevada (Megazyme). Alternativamente pode ser usada uma abordagem à base de sequência, a qual se baseia em bioinformática e biologia molecular para desenhar sondas para hibridização e "biopanning". Vide, por exemplo, as Patentes dos Estados Unidos Nos. 6.054.267, 6.030.779, 6.368.798, e 6.344.328. Os hits da triagem são purificados, sequenciados, caracterizados (por exemplo, determinação da especificidade, temperatura e pH ótimos), analisados usando bioinformática, subclonados e expressados para caracterização bioquímica básica. Estes métodos podem ser usados em triagem para glucanases, (ou celulases), mananases, xilanases, amilases, xantanases e/ou glicosidases, por exemplo, celobio- hidrolases, mananases e/ou beta-glucosidases úteis em uma miríade de aplicações, incluindo condicionamento de massa de pão e como enzimas aditivas de ração animal.
[0001027] Na caracterização de enzimas obtidas da triagem, pode ser avaliada a utilidade típica em aplicações de processamento e cozimento de massa de pão. A caracterização pode incluir, por exemplo, medição da especificidade do substrato (glucano, CMC, BBG), estabilidade da temperatura e do pH e atividade específica. Uma enzima comercial pode ser usada como um benchmark. Em um aspecto, as enzimas da invenção têm atividade significativa em pH > 7 e 25oC a 35oC, são inativas sobre glucano insolúvel, são estáveis e ativas em 50 a 67% de sucrose.
[0001028] Em outro aspecto, a utilidade como aditivos de ração pode ser avaliada a partir da caracterização de enzimas candidatas. A caracterização pode incluir, por exemplo, medição da especificidade do substrato (glucano, CMC, BβG), estabilidade de temperatura e pH, atividade específica e estabilidade gástrica. Em um aspecto a ração é designa para um animal monogástrico e em outro aspecto a ração é designada para um animal ruminantee. Em um aspecto, as enzimas da invenção têm atividade significativa em pH 2 a 4 e 35 a 40oC, uma meia-vida maior do que 30 minutos em fluido gástrico, meia-vida da formulação (em tampão ou células) maior do que 5 minutos a 85oC e são usadsa como um aditivo de ração de animal monogástrico. Em outro aspecto, as enzimas da invenção têm uma ou mais das seguintes características: atividade significativa em pH 6,5 a 7,0 e 35 a 40oC, uma meia-vida maior do que 30 minutos no fluido do rume, estabilidade da formulação tão estável quanto pó seco e são usadas como um aditivo de ração para animal ruminante.
[0001029] Enzimas são reativas para uma ampla gama de substratos naturais e não naturais, portanto permitindo a modificação de virtualmente qualquer composto de chumbo orgânico. Além disso, diferentemente de catalisadores químicos tradicionais, enzimas são altamente enantio- e regio-seletivas. O alto grau de especificidade de grupos funcionais exibido pelas enzimas permite que se acompanhe o curso de cada reação em uma sequência sintética levando a um novo composto ativo. Enzimas também são capazes de catalisar muitas reações diversas não relacionadas com sua função fisiológica na natureza. Por exemplo, peroxidases catalisam a oxidação de fenóis por peróxido de hidrogênio. Peroxidases também podem catalisar reações de hidroxilação que não são relacionadas com a função nativa da enzima. Outros exemplos são glucanases as quais catalisam a decomposição de polipeptídeos. Em solução orgânica algumas glucanases também podem acilar açúcares, uma função não relacionada com a função nativa destas enzimas.
[0001030] A presente invenção explora as propriedades catalíticas únicas de enzimas. Considerando que o uso de biocatalisadores (isto é, enzimas purificadas ou brutas, células não-vivas ou vivas) em transformações químicas normalmente requer a identificação de um biocatalisador particular que reage com um composto de partida específico, a presente invenção usa biocatalisadores selecionados e condições de reação que são específicas para grupos funcionais que estão presentes em muitos compostos de partida. Cada biocatalisador é específico para um grupo funcional, ou vários grupos funcionais relacionados e pode reagir com muitos compostos de partida contendo este grupo funcional. As reações biocatalíticas produzem uma população de derivados de um único composto de partida. Estes derivados podem ser submetidos a outra rodada de reações biocatalíticas para produzir uma segunda população de compostos derivados. Milhares de variações do composto original podem ser produzidos com cada iteração de derivação biocatalítica.
[0001031] Enzimas reagem em sítios específicos de um composto de partida sem afetar o resto da molécula, um processo o qual é muito difícila de obter usando métodos químicos tradicionais. Este alto grau de especificidade biocatalítica proporciona os meios para identificar um único composto ativo dentro da biblioteca. A biblioteca é caracterizada pela série de reações biocatalíticas usadas para produzir esta, uma chamada "história biossintética". Triagem da biblioteca para atividades biológicas e a investigação da história biossintética identifica a sequência da reação específica produzindo o composto ativo. A sequência da reação é repetida e a estrutura do composto sintetizado é determinado. Este modo de identificação, diferentemente de outras abordagens de síntese e triagem, não requer tecnologias de imobilização e os compostos podem ser sintetizados e testados livres em solução usando virtualmente qualquer tipo de ensaio de triagem. É importante notar que o alto grau de especificidade de reações enzimáticas sobre grupos funcionais permitem a "investigação" de reações enzimáticas específicas que compõem a biblioteca produzida biocataliticamente.
[0001032] Muitas das etapas dos procedimentos são realizadas usando automação robótica possibilitando a execução de muitos milhares de reações biocatalíticas e ensaios de triagem por dia bem como assegurando um alto nível de precisão e reprodutibilidade. Em consequência, uma biblioteca de compostos derivados pode ser produzida em uma questão de semanas a qual levaria anos para produzir usando os métodos químicos atuais. (Para ensinamentos adicionais sobre modificação de moléculas, incluindo moléculas pequenas, vide a publicação de patente No. PCT/US94/09174).
Coquetéis ou misturas de enzimas
[0001033] Em modalidades alternativas, qualquer composição, método, produto ou processo da invenção pode incluir qualquer combinação de uma ou qualquer outra uma ou mais enzimas, quer uma mistura de uma variedade de enzimas desta invenção, ou uma mistura com outras enzimas da mesma classe ou de classe diferente: os chamados “coquetéis de enzimas” desta invenção. Estas misturas de enzimas, ou coquetéis, podem compreender, por exemplo, outras glucanases, outras mananases, outras xilanases, qualquer hidrolase (por exemplo, proteases, esterases, e etc.), catalases, glucanases, celulases, endoglicosidases, endo-beta.-1,4-glucanases, amiloglucosidases, glicose isomerases, glicosiltransferases, lipases, esterase, fosfolipases, lipo-oxigenases, beta-glucanases, endo-beta- 1,3(4)-glucanases, cutinases, peroxidases, lacases, amilases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, fitases, arabinanases, hemicelulases, mananases, xiloglucanases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, poligalacturonases, ramnogalacturonases, galactanases, pectate liases, transglutaminases, pectina metilesterases, celobio-hidrolases e/ou transglutaminases - qualquer combinação das mesmas.
[0001034] Por exemplo, conforme observado acima, “coquetéis de enzimas” desta invenção podem ser usados em processos de perfuração de óleo ou gás, por exemplo, processos de tratamento enzimático da formação subterrânea, compreendendo o uso de qualquer combinação de pelo menos uma enzima desta invenção e qualquer outra uma ou mais enzimas, tais como amilases, xantanases, glicosidases, celulases, triptofanases ou tirosina decarboxilases, lacases, catalases, lacases, outras celulases, endoglicosidases, endo- beta-1,4-lacases, amiloglucosidases, outras glucosidases, glicose isomerases, glicosiltransferases, lipases, fosfolipases, lipo-oxigenases, beta-lacases, endo-beta-1,3(4)-lacases, cutinases, peroxidases, outras amilases, xantanases, glucoamilases, pectinases, redutases, oxidases, decarboxilases, fenoloxidases, ligninases, pululanases, arabinanases, hemicelulases, mananases, xilolacases, xilanases, pectina acetila esterases, ramnogalacturonano acetil esterases, proteases, peptidases, proteinases, poligalacturonases, ramnogalacturonases, galactanases, pectina liases, transglutaminases, pectina metilesterases, outras celobio-hidrolases e/ou transglutaminases.
[0001035] A invenção será adicionalmente descrita com referência aos seguintes exemplos; no entanto, deve ser entendido que a invenção não está limitada a semelhantes exemplos.
EXEMPLOS
EXEMPLO 1: DESCOBERTA ENZIMÁTICA DE ENDOGLICOSIDASE À BASE DE LÂMINA: TRIAGEM DE EXPRESSÃO
[0001036] O exemplo seguinte demonstra o isolamento de e a confirmação da atividade enzimática de enzimas típicas e ácidos nucleicos da invenção. Estes ensaios também podem ser usados para determinar se um polipeptídeo tem a atividade da enzima requerida (por exemplo, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou beta-glucosidase) para estar dentro do escopo da invenção
[0001037] Determinação do título da Biblioteca Lambda: Adicionar 1,0 μL de estoque da biblioteca amplificado Lambda Zap Express para 600 μL de células de E. coli MRF (OD600=1.0). Diluir estoque de MRF com 10 mM de MgS04. Incubar a mistura a 37°C por 15 minutos, em seguida transferir a suspensão para 5 a 6 mL de NZY top ágar a 50°C e misturar gentilmente. Imediatamente verter a solução de ágar sobre grande lâmina de meio NZY (150 mm) e permitir que o top ágar solidifique completamente (aproximadamente 30 minutos). Inverter a lâmina. Incubar a lâmina a 39°C por 8 a 12 horas. (O número de lâminas é aproximado. Título de fagos determinado para dar 50.000 pfu/ lâmina. Diluir uma alíquota de fago Library com tampão SM caso necessário.)
[0001038] Triagem de substrato: Adicionar Lambda Zap Express (50.000 pfu) da biblioteca amplificada a 600 μL de células de E. coli MRF (OD600 = 1,0) e incubar a 37oC por 15 minutos. Enquanto a suspensão de fago/célula está incubando, adicionar 1,0 mL do substrato marcado com corante do polissacarídeo desejado (geralmente 1 a 2% em peso/ vol) para 5,0 mL de NZY top ágar a 50oC e misturar completamente. (Solução mantida a 50°C até necessário.) Transferir a suspensão celular para solução de substrato/top ágar e misturar gentilmente. Imediatamente verter a solução sobre grande lâmina de meio NZY (150 mm). Permitir que o top ágar solidifique completamente (aproximadamente 30 minutos), em seguida inverter a lâmina. Incubar a lâmina a 39°C por 8 a 12 horas. Observar a lâmina para zonas de clareamento (halos) em torno das placas. Placas de núcleo com halos fora do ágar e transferir para um microtubo estéril. (Uma ponta de pipeta de 200 μL de orifício grande funciona bem para remover (retirar a parte central) a rolha de ágar contendo a placa desejada.) Ressuspender fago em 500 μL de tampão SM. Adicionar 20 μL de clorofórmio para inibir qualquer crescimento celular adicional.
[0001039] Isolamento de clones puros: Adicionar 5 μL de suspensão de fago ressuspendida a 500μL de células de E. coli MRF (OD600 = 1,0). Incubar a 37oC por 15 minutos. Enquanto a suspensão de fago/célula está incubando, adicionar 600μL do substrato marcado com corante do polissacarídeo desejado (geralmente 1 a 2% em peso/ vol) para 3,0 mL de NZY top ágar a 50oC e misturar completamente. (Solução mantida a 50°C até necessário.) Transferir a suspensão celular para solução de substrato/top ágar e misturar gentilmente. Imediatamente verter a solução sobre pequena lâmina de meio NZY (90 mm) e permitir que o top ágar solidifique completamente (aproximadamente 30 minutos), em seguida inverter a lâmina. Incubar a lâmina a 39°C por 8 a 12 horas. A lâmina observada para uma zona de clareamento (halo) em torno de uma única placa (clone puro). (Se não puder ser isolada uma única placa, ajustar o título e relaminar a suspensão de fago.) Os fagos são ressuspendidos em 500 μL de tampão SM e 20 μL de Clorofórmio é adicionaro para inibir qualquer crescimento celular adicional.
[0001040] Excisão de clone puro: Deixar que suspensão de fago puro incube em temperatura ambiente por 2 a 3 horas ou de um dia para o outro a 4°C. Adicionar 100 μL de suspensão de fago puro a 200 μL de células de E. coli MRF (OD600 = 1,0). Adicionar 1,0 μL de fago auxiliar ExAssist (>1 x 106 pfu/mL; Stratagene). Incubar a suspensão a 37°C por 15 minutos. Adicionar 3,0 mL de 2 x meio YT à suspensão celular. Incubar a 37°C por 2 a 2,5 horas enquanto agitando. Transferir o tubo para 70°C por 20 minutos. Transferir 50 a 100 μL de suspensão de fagemídeo para um microtubo contendo 200 μL de células de E. coli Exp 505 (OD600 = 1,0). Incubar a suspensão a 37°C por 45 minutos. Laminar 100 μL de suspensão celular sobre meio LBkan 50 (meio LB com Canamicina 50 μg/mL). Incubar a lâmina a 37°C por 8 a 12 horas. Observar a lâmina para colônias. Quaisquer colônias que crescem contêm o fagemídeo puro. Selecionar uma colônia e cultivar uma pequena cultura líquida (3 a 10 mL) por 8 a 12 horas. O meio de cultura é LB kan 50 líquido.
[0001041] Verificação da atividade: Transferir 1,0 mL de cultura líquida para um microtubo estéril. Centrifugar a 13200 rpm (16000 g’s) por 1 minuto. Descartar o sobrenadante e adicionar 200 μL de tampão de fosfato pH 6,2. Sonicar por 5 a 10 segundos sobre gelo usando uma microponta. Adicionar 200 μL de substrato apropriado, misturar gentilmente e incubar a 37°C por 1,5 a 2 horas. Também deve ser operado um controle negativo que contém somente tampão e substrato. Adicionar 1,0 mL de etanol absoluto (ensaio 200) à suspensão e misturado. Centrifugar a 13200 rpm por 10 minutos. Observe supernatant for color. A quantidade da mancha pode variar, mas qualquer tubo com mais mancha do que controle é considerado positivo para atividade. Um espectrofotômetro pode ser usado para esta etapa caso seja desejado ou necessário. (Para beta glucano de cevada Azo, Megazyme, ler a 590 nm).
[0001042] RFLP de clones puros das mesmas Bibliotecas: Transferir 1,0 mL de cultura líquida para um microtubo estéril. Centrifugar a 13200 rpm (16000 g’s) por 1 minuto. Seguir o protocolo do QIAprep spin mini kit (Qiagen) para isolamento de plasmídeo e usar 40 μL de água benta como o tampão de elutriação. Transferir 10 μL de DNA de plasmídeo para um microtubo estéril. Adicionar 1,5 μL de Tampão 3 (New England Biolabs), 1,5 μL de 100X solução BSA (New England Biolabs) e 2,0 μL de água benta. A isto adicionar 1,0 μL de Not 1 e 1,0 μL de endonucleases de restrição Pst 1 (New England Biolabs). Incubar por 1,5 horas a 37°C. Adicionar 3,0 μL de 6X tampão de carga (Invitrogen). Passar 15 μL de amostra digerida sobre um agarose gel a 1,0% por 1 a 1,5 horas a 120 volts. Visualizar o gel com um imager de gel. Realizar a análise de sequência sobre todos os clones com um padrão de digestão diferente.
[0001043] A figura 5 é uma tabela contendo caracterização da enzima “parental” exemplar da invenção SEQ ID NO: 2, incluindo resumir as atividades relativas de várias enzimas exemplares da invenção sob várias condições, por exemplo, variando o pH e a temperatura, conforme discutido acima.
EXEMPLO 2: ENSAIOS DE ATIVIDADE
[0001044] O exemplo seguinte demonstra a atividade enzimática de enzimas exemplares da invenção. Estas ensaios também podem ser usadas para determinar se um polipeptídeo tem a enzima requerida (por exemplo, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, atividade de celobio-hidrolase, mananase e/ou betaglucosidase) para estar dentro do escopo da invenção.
[0001045] Foi demonstrado que os polipeptídeos da invenção têm atividade de glucanase, conforme descrito abaixo. A atividade específica foi determinada sobre β-glucano de cevada (BBG) ou carboximetilcelulose (CMC) usando o ensaio do açúcar redutor BCA. 1 unidade (U) de atividade de glucanase = 1 Dmol/min-1 de equivalentes redutores de glicose liberados a 37°C, pH 5,3.
[0001046] Foi demonstrado que polipeptídeos típicos da invenção têm atividade de endoglucanase alcalina/celulase, com vários ótimos de pH e temperatura. A atividade pode ser determinada usando um ensaio da atividade de celulase (um ensaio de extremidades redutoras de BCA), conforme descrito em detalhes no Exemplo 3, abaixo.
EXEMPLO 3: Ensaio da atividade de celulase: ensaio de extremidades redutoras de BCA
[0001047] O exemplo seguinte descreve um ensaio, um ensaio de atividade de celulase (um ensaio de extremidades redutoras de BCA) que pode ser usada para determinar se um polipeptídeo tem a atividade da enzima requerida (por exemplo, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio-hidrolase, mananase e/ou betaglucosidase), por exemplo, uma atividade de endoglucanase alcalina/celulase (vide o Exemplo 2, acima) para estar dentro do escopo da invenção.
[0001048] Este ensaio foi designada para medir a quantidade de extremidades redutoras produzidas durante a degradação enzimática de carboximetilcelulose (CMC) em um formato de 96 cavidades de múltipla amostra de alta produtividade. Materiais: Soluções de substrato: 1% de CMC
[0001049] Dissolver 1 gm de CMC em 100 ml de tampão a 50 mM de Britton-Robinson em pH ~4, aquecer a solução de CMC em banho de água em ebulição, ao mesmo tempo que misturando, por 20 a 40 minutos até dissolver (a solução ainda aparecerá ligeiramente leitosa, porém translúcida). Ajustar para pH desejado com 1 M de NaOH ou HCl. Solução A: 64 mg/ml de monoidrato de carbonato de sódio 24 mg/ml de bicarbonato de sódio 1,95 mg/ml de BCA (sal dissódico de 4,4’-dicarboxi-2,2’- biquinolina (Sigma Chemical cat no. D-8284) Adicionar acima a dH2O,
[0001050] Pode ser necessário dissolver o BCA por aquecimento, não aquecer mais de ~80 C. Solução B: 1,24 mg/ml de pentaidrato de sulfato cúprico 1,26 mg/ml de L-serina Adicionar acima a dH2O Reagente de trabalho:
[0001051] 1:1 das soluções A e B, preparar mistura de reagentes de trabalho fresca a cada dia (geralmente somente preparar suficiente para cada teste), preparar Soluções A e B frescas a cada semana. Solução de estoque de glicose: 10 mM de Glicose em dH2O. filtro de 0,2 um, armazenar a 4C. Padrões de glicose:
[0001052] Diluir o estoque de Glicose a 10 mM em 1% de CMC em pH desejado; para uma concentração final de 0, 100, 200, 300, 400, e 500 uM. Uma vez que a curva é determinada adicionando 10 ul dos padrões ao reagente de trabalho resulta até 0 a 0,005 umol de glicose/ cavidade. A curva-padrão precisa ser gerada para cada pontos de tempo das lâmina da amostra, uma vez que o ciclo de aquecimento pode afetar a quantidade de sinal observado.
Métodos:
Estrutura:
[0001053] Aliquotar 1 ml de solução de substrato (1% de CMC) em lâmina de cavidade profunda (caso usando Temp ambiente) ou tubos Acme em bloco quente, equilibrar até temperatura desejada (~5 min) em bloco de calor ou banho de água aquecida.
[0001054] Enquanto a solução está equilibrando, preparar 10 ml do reagente de trabalho e aliquotar 100 ul em lâmina de PCR de 96 cavidades. Depositar a lâmina sobre gelo.
Reação/Amostragem:
[0001055] Depois da equilibração da temperatura estar completa, adicionar solução de enzima à solução de substrato. Misturar imediatamente pipetando para cima e para baixo. Imediatamente aliquotar 10 ul em lâmina de PCR (isto é, t = 0, ponto de tempo zero). Aliquotar 10 ul em lâmina de PCR em cada ponto de tempo desejado (por exemplo, 0, 2, 5, 10,15, 20, 30 minutos).
[0001056] Salvar a última linha sobre a lâmina para adição de 10 ul de padrões de glicose (isto é, as cavidades somente devem ter 100 ul do reagente de trabalho nas mesmas) .
Desenvolvimento da Cor do ensaio:
[0001057] Quando todos os pontos de tempo são coletados e são adicionados padrões, covrir a lâmina e aquecer até 100 °C por 10 min usando máquina de PCR. Resfriar a lâmina sobre gelo por 5 a 10 min (ou ajustar a máquina de PCR para 1°C por 10 min).
[0001058] Adicionar 100 ul de H2O às cavidades. Misturar. Aliquotar 100 ul de mistura em lâmina de 96 cavidades de fundo liso claro e ler a absorvência a 560 nm.
Curva-padrão gerada:
[0001059] Plotar a A560 vs. umol de glicose das cavidades contendo os padrões de glicose. Usar regressão linear para calcular a inclinação (Sstd).
Gerar o gráfico da inclinação da reação:
[0001060] Plotar A560 vs. os pontos de tempo. Zerar cada um dos pontos de tempo das amostras contra seu própria T = 0 (isto é, subtrair o valor de absorvência T = 0 da amostra de todos os outros pontos de tempo da mesma amostra).
[0001061] Gerar a inclinação (Srxn) para cada grupo de pontos de tempo das amostras (A560/ tempo).
Determinação da Atividade:
[0001062] Dividir Srxn pelo Sstd, e multiplicar por 100 (uma vez que o umol de produto detectado é a quantidade de extremidades redutoras no 10 ul usado no ensaio, não a quantidade total gerada na reação enzimática de 1 ml).
Determinação da Atividade Específica:
[0001063] Dividir a Atividade (em unidades de umol/min) pelo total de mg de proteína adicionado na reação de 1 ml. Determinar a concentração de proteína por ensaio de Bradford ou similar.
[0001064] Dividir a concentração de proteína por quaisquer diluições usadas.
[0001065] Multiplicar pelo volume (e, ml) usado na reação.Todos os pontos devem ser feitos em duplicata com triplicata sendo melhor.
[0001066] A seguinte planilha determina uma série de dados exemplar (“dados da amostra”) que é ilustrada em forma de gráfico como uma “curva-padrão” na figura 6. DADOS DA AMOSTRA data mg/ml Diln. ul/rxn 0 min 5 min 8 min 12 min 24 min 36 min 45 min Enz x 06/09 20 500 20 0,1252 0,1654 0,1889 0,2315 0,3386 0,4036 0,4695 Inclinação da curva-padrão: 88,375 A560/umol de glicose Inclinação da reação: 0,0076 A560/min Atividade (inclinação da reação/inclinação padrão): 8,70061E-05 umol/min Atividade verdadeira/1ml rxn (=Atividade x 100): 0,0087 umol/min Atividade Específica: 10,87 umol/min,mg
Exemplo 4: Ensaios da Atividade Enzimática
[0001067] O exemplo seguinte descreve ensaios de atividade enzimática exemplar, e proporciona dados demonstrando/confirmando a atividade enzimática de enzimas exemplares da invenção. Estas ensaios também podem ser usadas para determinar se um polipeptídeo tem a atividade enzimática requerida (por exemplo, glucanase (ou celulase), por exemplo, endoglucanase, mananase, xilanase, amilase, xantanase e/ou glicosidase, por exemplo, celobio- hidrolase, mananase e/ou beta-glucosidase) está dentro do escopo da invenção. Por exemplo, enzimas da invenção podem catalisar a hidrólise de glucano, e/ou galactomanano de cevada e/ou aveia (polissacarídeos consistindo em uma estrutura principal de manose com grupos laterais de galactose; um exemplo mais específico de um substrato compreende uma estrutura principal de beta-D- manopiranose (1-4)-ligada com pontos de ramificação de suas 6- posições ligadas a alfa-D-galactose, isto é, alfa-D-galactopiranose 1-6- ligada; por exemplo, conforme visto em goma guar, tara, alfarroba ou goma de alfarroba, ou feno-grego (Trigonella foenum-graecum)). Em outro aspecto, enzimas são testadas para determinar se estão dentro do escopo da invenção usando um substrato de glucanase (muitos dos quais são de conhecimento geral na técnica), por exemplo, composições compreendendo galactomanano e/ou glucano de cevada e/ou aveia.
Atividade específica da glucanase codificada pela SEQ ID NO: 2
[0001068] A atividade específica da enzima exemplar da invenção tendo uma sequência conforme determinado na SEQ ID NO: 2 “parental” (codificada, por exemplo, pela SEQ ID NO: 1) foi demonstrada usando o seguinte protocolo:
[0001069] A glucanase codificada pela SEQ ID NO: 2 “parental” foi purificada até a homogeneidade usando cromatografia de permuta iônica. As atividades específicas foram determinadsa sobre 1% de substrato em 50 mM de tampão de acetato de sódio pH 5,3, a 37°C usando o ensaio do açúcar redutor BCA. 1 unidade (U) de atividade de glucanase = 1 ímol/min-1 de equivalentes redutores de glicose liberados a 37oC, pH 5,3. o Beta Glucano de Cevada (BBG): 30 U/mg o Beta Glucano de Aveia (OBG): 38 U/mg o Carboximetilcelulose (CMC): 40 U/mg o Galactomanano de Alfarroba: 0,3 U/mg
Perfil da temperatura da glucanase codificada pela SEQ ID NO: 2
[0001070] O perfil da temperatura foi determinada sobre três substratos separados (BBG, OBG e CMC). A glucanase codificada pela SEQ ID NO: 2 “parental” teve a maior atividade em maiores temperaturas. A atividade específica da glucanase codificada pela SEQ ID NO: 2 sobre BBG e CMC a 80°C é 10X melhor do que a atividade vista a 37°C. Na presença de manano, a glucanase codificada pela SEQ ID NO: 2 apresentou a maior atividade a 100°C, conforme ilustrado na figura 7.
[0001071] O perfil da temperatura foi determinado incubando a SEQ ID NO: 2 (codificada pela SEQ ID NO: 1) na presença de substrato (CMC, BBG ou Manano). As velocidades iniciais foram determinadas usando ensaio do açúcar redutor BCA e tampão de acetato de sódio pH 5,3. As velocidades iniciais foram normalizadas e plotadas como% de atividade, conforme ilustrado na figura 7.
Determinação da meia-vida da glucanase codificada pela SEQ ID NO: 2
[0001072] A meia-vida da glucanase codificada pela SEQ ID NO: 2 “parental” foi determinada a 85°C e 90°C. A glucanase codificada pela SEQ ID NO: 2 foi testada com calor por vários momentos a 85 e 90 graus e a atividade residual foi medida a 37°C. A glucanase codificada pela SEQ ID NO: 2 reteve mais de 60% de sua atividade depois de 10 minutos de incubação a 85°C. A 90°C, não houve atividade residual restante depois de 2 minutos, conforme ilustrado na figura 8.
[0001073] Conforme ilustrado na figura 8, a meia-vida da SEQ ID NO: 2 (codificada pela SEQ ID NO: 1) foi determinada testando com calor a enzima por 30 seg, 1 min, 2 min, 3 min, 4 min, 5 min, e 10 min nas temperaturas indicadas (85°C e 90°C) e monitorando a atividade sob condições de rotina usando o açúcar redutor BCA.
Exemplo 5: Ensaios de Atividade Enzimática
[0001074] O exemplo seguinte descreve enzimas típicas da invenção, variantes da SEQ ID NO: 2 “parental” ou “selvagem”, e dados demonstrando sua atividade. A invenção proporciona sequências tendo alterações de resíduos específicas para a SEQ ID NO: 2 “parental” (ou “selvagem”) (codificada, por exemplo, pela SEQ ID NO: 1), conforme resumido (em parte) na Tabela 1, acima, Tabela 2, abaixo, e:
[0001075] A tolerância térmica de variantes exemplares foi medida usando enzima purificada comparada com a SEQ ID NO: 2 parental “selvagem”, e um subgrupo das variantes enzimáticas da Tabela 2 (as chamadas “variantes 7X”), conforme ilustrado na figura 9 e na figura 10; onde os dados ilustrados na mesma demonstram a tolerância témica dos polipeptídeos exemplares testados (variantes da SEQ ID NO: 2 “parental” ou “selvagem”) em 96°C a 100°C. Nestas figuras, a enzima purificada foi aquecida por 30 minutos na temperatura indicada nas figuras, e a atividdade residual (termotolerante) foi medida a 37°C. Aquecendo as temperaturas entre 84°C e 95°C ativa as variantes “termotolerantes” (variantes da SEQ ID NO: 2 “parental” ou “selvagem”) ligeiramente, resultando em ter uma atividade residual (termotolerante) de mais do que o nível de atividade inicial (isto é, mais de 100%) (possivelmente devido a se dobrar acentuadamente mediante esfriamento). Deste modo, a atividade residual foi normalizada até 100%. A figura 9 ilustra um sumário gráfico dos dados destes estudos de tolerância témica para as enzimas da invenção identificadas como “10X-1”, “12X-1”, “13X-1”, “12X-6”, “11X-1”, “11X-2” e “7X”, além do tipo selvagem; e a figura 10 é um “close-up” de parte da figura 9.
[0001076] Portanto, em um aspecto, enzimas da invenção são termotolerantes e/ou termoestáveis; por exemplo, uma enzima da invenção pode reter pelo menos 75% de atividade residual (por exemplo, atividade de glucanase) depois de 2 minutos a 95°C; e em outro aspecto, retém 100% de atividade depois de aquecer por 30 minutos a 95°C. Em ainda outro aspecto, uma enzima da invenção retém 100% de atividade depois de aquecer por 30 minutos a 96°C, 97°C, 98°C ou 99°C. Em ainda outro aspecto, uma enzima da invenção retém pelo menos 90% de atividade depois de aquecer por 30 minutos a 100°C.
[0001077] Em um aspecto, estas enzimas da invenção são usadas em um produto enzimático de ração, por exemplo, uma ração ou alimento de grãos não-refinados para monogástricos, em que os animais monogástricos incluem suíno (porcos, suínos capados), carneiro, coelhos, aves, cavalos, animais domésticos e humanos.
Exemplo 6: Projetando sítios de iniciação alternativos
[0001078] A invenção também proporciona sequências codificantes de glucanase que são variantes do ácido nucleico exemplar SEQ ID NO: 1, codificando a SEQ ID NO: 2 “parental”, que são especificamente modificadas para remover, ou ao invés alterar, um segundo sítio de iniciação translacional dentro da SEQ ID NO: 1. Este segundo sítio de iniciação translacional causa produção de uma versão truncada indesejada da proteína em hospedeiros não-nativos (não-nativos no contexto que o hospedeiro usado para expressar a proteína não é o organismo do qual a enzima foi derivada inicialmente). Quando a enzima de SEQ ID NO: 2 exemplar é expressada a partir de seu organismo nativo, Thermotoga maritima MSB8, esta proteína truncada não é produzida. No entanto, quando um ácido nucleico tendo este segundo sítio de iniciação translacional (críptico) de SEQ ID NO: 1 é colocado em um hospedeiro não-nativo, o segundo sítio de iniciação translacional é reconhecido, causando produção de uma proteína truncada.
[0001079] Para romper esta translação indesejada (de uma proteína truncada em um hospedeiro não-nativo), a SEQ ID NO: 1 (codificando SEQ ID NO: 2) foi alterada. Em particular, o sítio de ligação ribossômica potencial (RBS), e o códon do segundo (2o- ) sítio de iniciação no resíduo de aminoácido (aa) 32 foram alterados conforme mostrado abaixo. Especificamente, o resíduo de nucleotídeo 84 de SEQ ID NO: 1 foi alterado de A para C e o resíduo de nucleotídeo 96 de SEQ ID NO: 1 foi alterado de G para C (a sequência modificada resultante é mostrada na SEQ ID NO: 3). As alterações de nucleotídeo não causaram quaisquer alterações de aminoácido no polipeptídeo codificado pela SEQ ID NO: 1 alterada.
[0001080] Esta alteração ilustrada no sítio de ligação de ribossoma (RBS) e no segundo sítio de iniciação foram feitas para assegurar que a proteína truncada ná é produzida em um hospedeiro “não-nativo”.
[0001081] A figura 11 ilustra uma foto de uma fotomicrografia de um gel SDS-PAGE para proteínas de engomação geradas em um hospedeiro de Pseudomonas fluorescens não-nativo usando transcriptos “selvagens (WT) (ou, proteína de SEQ ID NO: 2)” não- modificados e modificados (a variante que foi ilustrada, acima) para demonstrar o efeito desta alteração do RBS e do segundo sítio de iniciação sobre a expressão de transcripto de glucanase. O gel ilustrado na figura 11 mostra proteína produzida no “gene”não induzido e inalterado, ou sequência codificante (alameda 2), gene induzido e inalterado (alamedas 3 a 5, mesmo gene feito em triplicata), gene não induzido e alterado (alameda 6) e gene induzido e alterado (alamedas 7 a 9). Conforme ilustrado por estes dados, as alterações dobraram a quantidade de atividade. Na figura 11, cada alameda é carregada com 5 μl de lisado celular total com 10 OD600/ml. Glucanase traduzida do primeiro códon de partida (ATG) é indicada por uma seta preta (à esquerda da alegação 9); a proteína truncada traduzida do segundo códon de partida (GTG) é indicada pela seta interna, mais longa (término interno na linha 5). Na figura 11:
[0001082] A Alameda 1: são os marcadores de proteína MW; a Alameda 2 é SEQ ID NO: 2 (não induzida) = 0,22 U/OD600; a Alameda 3 é SEQ ID NO: 2, amostra 1 = 1,82 U/OD600; a Alameda 4 é SEQ ID NO: 2, amostra 2 = 2,00 U/OD600; a Alameda 5 é SEQ ID NO: 2, amostra 3 = 1,93 U/OD600; a Alameda 6 é SEQ ID NO: 3 (não induzida) = 0,20 U/OD600; a Alameda 7 é SEQ ID NO: 3 amostra 1 = 3,79 U/OD600; a Alameda 8 é SEQ ID NO: 3 amostra 3 = 3,60 U/OD600; a Alameda 9 é SEQ ID NO: 3 amostra 3 = 4,03 U/OD600.
[0001083] Apesar destes dados demonstrarem que estas modificações das sequências de ácido nucleico tratam o problema do sítio de iniciação transcripcional críptica no hospedeiro de expressão exemplar de Pseudomonas fluorescens, estas modificações ou modificações equivalentes para eliminar um ou mais sítios de iniciação crípticos podem ser usados em qualquer hospedeiro, por exemplo, em qualquer hospedeiro de expressão procariótica. Em outras palavras, qualquer que seja a célula hospedeira usada para expressar uma enzima da invenção, problemas de sítios de iniciação transcripcional críptica podem ser prontamente identificados e eliminados com modificações de sequências, cujas técnicas são conhecidas na técnica, e podem ser análogas às técnicas determinadas neste exemplo. Em aspectos alternativos, a célula hospedeira é uma célula bacteriana, uma célula de mamífero, uma célula fúngica, uma célula de levedura, uma célula de inseto ou uma célula de planta, por exemplo, a célula bacteriana pode ser qualquer espécie dentro dos gêneros Escherichia, Bacillus, Streptomyces, Salmonella, Pseudomonas ou Staphylococcus, ou Escherichia coli, Lactococcus lactis, Bacillus subtilis, Bacillus cereus, Salmonella typhimurium ou Pseudomonas fluorescens.
Exemplo 7: Dietas de alimento ou ração compreendendo enzima
[0001084] A invenção também proporciona alimentos ou rações (os quais incluem suplementos para ambos) compreendendo enzimas da invenção, incluindo as variantes enzimáticas de SEQ ID NO: 2, por exemplo, conforme descrito nas Tabelas 1 ou 2, acima. Em um aspecto, alimentar animais com dietas compreendendo enzimas da invenção aumentará o valor dietético do alimento ou ração compreendendo enzima. Em um aspecto, alimentar animais com dietas compreendendo enzimas da invenção reduzirá a viscosidade do fluido intestinal e a taxa de passagem de ração no animal (a qual pode ser testada/confirmada conforme descrito, por exemplo, em Sieo (2005) Poult. Sci. May; 84(5):734-741. A adição de uma enzima da invenção (sozinha, ou junto com outra enzima, por exemplo, uma xilanase e/ou uma beta-glucanase conhecida ou fitase) à dieta de um animal pode aumentar o tamanho das vilosidades intestinais e a proporção da profundidade da altura das vilosidades para cripta, aumentar a concentração de ácidos biliares conjugados no conteúdo do intestino delgado, melhorar a digestibilidade dos nutrientes e o desempenho animal (por exemplo, aves domésticas, frango) (provavelmente melhorando a capacidade de absorção do intestino delgado através de aumento da superfície das vilosidades e da concentração intestinal de ácidos biliares conjugados; vide, por exemplo, Mathlouthi (2002) J. Animal Sci. Nov; 80(11):2773-2779). Em alguns aspectos, os alimentos ou rações compreendendo enzimas da invenção são introduzidas em animais em dietas especiais, por exemplo, aves domésticas alimentadas com dietas à base de centeio; centeio na ração pode conferir desempenho à ave para grelhar e aumentar a viscosidade da digesta e a incidência de distúrbios das pernas -- a administração de alimentos ou rações compreendendo enzimas da invenção pode reduzir a magnitude deste problema; vide, por exemplo, Lazaro (2004) Poult. Sci. Feb; 83 (2): 152-160.
[0001085] Em um aspecto, uma ração ou alimento (ou fármaco, suplemento dietético, e etc.) da invenção pode compreender um, dois, três ou mais polinucleotídeos diferentes da invenção; ou em um aspecto, uma ração ou alimento da invenção pode compreender uma combinação de uma enzima da invenção com outro polipeptídeo (por exemplo, enzima, peptídeo) da invenção ou qualquer enzima conhecida. O alimento ou ração pode estar sob a forma de um comprimido, um geltab, uma pílula, um implante, um pélete, uma pré- mistura seca, um sólido, pó ou um suplemento dietético líquido, e similares.
[0001086] O valor de uma enzima particular da invenção em uma dieta pode ser testado usando qualquer sistema de alimento ou ração, por exemplo, alimentando um animal, por exemplo, um animal monogástrico, uma dieta limitante de energia, tal como algums dietas de milho e soja, com e sem suplementação por uma enzima da invenção.
[0001087] Por exemplo, um estudo exemplar pode ser projetado para determinar se há qualquer vantagem em dietas processadas em temperatura elevada (90oC na face do molde) de duas variantes da invenção (isto é, variantes de sequências da SEQ ID NO: 2 “parental”), comparadas com a SEQ ID NO: 2 “parental”, ou “selvagem”, quando introduzidas em dietas de milho e soja limitante de energia.
[0001088] Um sistema de teste exemplar compreende o uso de aves domésticas, por exemplo, galinhas, tais como galinhas para grelhar (por exemplo, cepa Cobb X Cobb, um híbrido comercial Commercial Hybrid, origem incubadora de Cobb-Vantress, Cleveland, GA); e:
[0001089] Animais que parecem estar em má condição serão removidos antes do início do estudo. Caso no início permaneçam insuficientes para satisfazer o número requerido para o estudo, então será ordenado um lote fresco de animais. Um funcionário adequado examinará os animais para o estado de saúde do início ao fim do experimento.
[0001090] Os animais serão atribuídos a seus grupos de tratamento usando uma técnica de randomização reconhecida. Os animais somente serão identificados antes do início da administração do artigo de teste caso sejam requeridos dados individuais dos animais, caso contrário somente serão etiquetadas as gaiolas onde os animais são mantidos.
Enzimas típicas
[0001091] Qualquer enzima da invenção, incluindo quaisquer das variantes enzimáticas de SEQ ID NO: 2 da invenção, por exemplo, conforme descrito nas Tabelas 1 ou 2, acima pode ser usada sozinha ou em combinação em um alimento ou ração da invenção. Deste modo, sistemas e protocolos de teste exemplares podem usar quaisquer das enzimas da invenção sozinha ou em combinação com outra enzima da invenção, ou uma enzima conhecida. Em um aspecto, alimentar animais com dietas compreendendo enzimas da invenção aumentará o valor dietético do alimento ou ração compreendendo enzima.
[0001092] Para as variantes “13-1X” e “7X” da glucanase SEQ ID NO: 2, vide a Tabela 2 e a discussão acima. O termo “DNS U/kg” significa “unidades de DNS por quilograma de ração”. DNS = ácido 3,5- dinitrossalicílico, um reagente usado para a quantificação das extremidades redutoras livres liberadas por ação de glucanase sobre polissacarídeos. DNS indica que o método do ensaio de DNS foi usada para determinar atividade de glucanase.
[0001093] Todas as aves serão tratadas humanamente. Somente métodos aprovados pela Associação Médica Veterinária Americana (American Veterinary Medical Association) serão usados para eutanizar as aves. Todas as aves serão enterradas em uma cova de descarte no local e não penetrarão na cadeia alimentar.
[0001094] Todos os animais serão examinados diariamente por pessoal convenientemente qualificado e qualquer variação no aspecto ou comportamento será registrada. Se qualquer animal estiver em má condição será observado mais frequentemente. Caso considerado improváveis se sobreviver, ou de estarem sofrendo dor ou angústia, serão apartados e necropsiados. Todas as mortalidades também serão necropsiadas em uma tentativa de estabelecer a causa da morte ou angústia. Em todos os casos, os animais devem ser pesados e a data da morte registrada. Se forem observados efeitos adversos do tratamento durante o estudo, os animais de cada grupo de tratamento afetado são necropsiados e os tecidos avaliados para histopatologia.Medições
[0001095] Todo o mat erial de teste e animais alimentados com o material de teste devem ser descartados de maneira a evitar que ou penetrem em outra ração animal e/ou na cadeia de alimentação humana.
[0001096] *NOTA, para as duas amostras de 400 g pré e pós peletização, compor cada uma de 3 amostras de 200 g retiradas separadas as quais são misturadas e em seguida reduzidas para 400 g. Coletas de diferentes partes do misturador para as amostras de malte moído, e no início, no ponto central e no fim da fabricação das amostras peletizadas e etiquetar de acordo. Amostras pós pélete a serem tomadas pós cooler e algumas descrição do processo de esfriamento a ser proporcionado ao contrator, amostras de malte moído pré-pélete a serem tomadas de diferentes pontos do misturador. Amostras peletizadas acima NÃO devem ser confundidas com teste de temperatura.
[0001097] Para as variantes “13-1X” e “7X” da glucanase SEQ ID NO: 2, vide a Tabela 2 e a discussão acima.
Exemplo 8: Métodos para Produzir Péletes de Alimento ou Ração da Invenção
[0001098] A invenção também proporciona péletes de alimento ou ração (os quais em um aspecto podem ser considerados “suplementos de alimento ou ração) compreendendo uma ou mais enzimas da invenção, e métodos para fabricar e usar os mesmos. A invenção também proporciona péletes compreendendo enzimas da invenção, incluindo as variantes enzimáticas de SEQ ID NO: 2, por exemplo, conforme descrito nas Tabelas 1 ou 2, acima, para uso como alimentos ou rações. Este exemplo descreve um método exemplar para fabricar péletes de alimento ou ração da invenção.
[0001099] Este estudo é planejado para gerar uma curva robusta de termo-tolerância para enzimas glucanase das rações da invenção peletizadas a 70oC, 83oC, 86oC, 89oC, 92oC, ou 95oC. As enzimas foram dosadas em um nível (250 U/kg) em cada temperatura para desenvolver uma curva da atividade com base no novo método de teste em ração desta invenção. Uma segunda glucanase foi peletizada em duas temperaturas (70oC e 95oC) e comparada com o produto principal. Além disso, QUANTUM XT™ PHYTASE (ou, “QPXT”) (Syngenta Biotechnology Inc., Research Triangle Park, NC) foi suplementado na ração em branco por duas rodadas para ser usado como um marcador interno.
Materiais e Métodos
Formulação da dieta
[0001100] As dietas serão formuladas para serem uma dieta para ave para grelhar comercial típica (à base de milho/farinha grossa de soja/farinha grossa de carne e osso). Haverá somente uma dieta basal usada e três dietas experimentais: (1) uma dieta controle consistindo em nenhuma enzima glucanase adicionada (mas QUANTUM XT™ PHYTASE (Syngenta Biotechnology Inc., Research Triangle Park, NC) adicionado a 200 g/mt); (2) a dieta controle com a glucanase SEQ ID NO: 2 a 250 U/kg de ração; e, (3) controle com 7X Glucanase (vide a Tabela 2, Exemplo 5, acima) a 250 U/kg de ração.Apresentação/aditivos da dieta
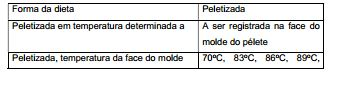

Peletização da dieta e amostragem Procedimentos de peletização - • Inicialmente um misturador de 1-mt foi limpo e inspecionado antes do início do teste. Ração suficiente foi misturada com base na quantidade de ração requerida para uma operação contínua para obter os 6 aumentos de temperatura alvo (em estado estacionário) dentro de cada operação. • Todos os ingredientes secos foram adicionados ao misturador na ordem da formulação da dieta (para dietas de glucanase foi adicionado dentro do misturador substituindo pequena quantidade de milho) e o misturador foi operado por 2 a 3 minutos, em seguida o óleo foi adicionado, e misturado os 1 a 2 minutos finais. O tempo de operação total foi 3 a 4 minutos de extensão. • Antes da operação de pélete duas amostras compostas de malte moído foram removidas do misturador para cada operação de teste (cada amostra de aproximadamente 500 g cada). • A ração foi peletizada iniciando na menor temperatura e uma vez que a temperatura alvo é atingida em um estado estacionário foram colhidas amostras de ração. Aproximadamente 5 x 500 g amostras foroam colhidas no meio da operação pós-molde e estas foram resfriadas antes do ensacamento final e identificadas (etiquetadas). • Depois das amostras de ração serem colhidas e soprado ar quente através das amostras para reduzir os níveis de umidade em seguida foram resfriadas até a temperatura ambiente em uma câmara de esfriamento. • Os sacos das amostras foram etiquetados para operação (replicata), temperatura e nível enzimático. Houve operações de três replicata para cada dieta de teste individual. Houve 5 amostras de ração para cada temperatura (6) dentro de uma dieta com 3 replicatas (operação) dando um total de 90 amostras de ração peletizada por dieta de teste; mas houve 3 amostras de malte moído compostas para cada dieta de teste. • Sacos das amostras como se segue: • Sacos das amostras: no. da operação/enzima/temperatu- ra/amostra. • Onde: o no. da operação é 1-3, a dose é em branco, SEQ ID NO: 2 ou 7X (a variante de SEQ ID NO: 2, vide a tabela 2 e discussão acima), a temperatura é 70, 83, 86, 89, 92, ou 95 e amostra de 1-5. Por exemplo, a rótulo 1/SEQ ID NO: 2/92/ 1 descreve a amostra tomada durante a primeira operação da SEQ ID NO: 2 a 92DC e foi a primeira amostra coletada que passa.Design Experimental:


[0001101] * Com as temperaturas de peletização, precisa ser mantida pelo menos uma diferença de 3°C entre os valores, sem alteração na passagem (tempo de retenção) durante a operação.
[0001102] ** Um lote de ração foi misturado e usado para toda a operação dentro de uma dieta de teste nas 6 temperaturas com amostras coletadas e resfriadas uma vez que a temperatura foi atingida e estável. Uma série de 5 amostras foi coletada para cada temperatura dentro de uma operação dando um total de 30 amostras de ração por operação. Um total global de amostras de ração peletizada foi 210 amostras, não incluindo amostras de malte moído. Medições e esquema de eventos
[0001103] Caso não capaz de completar todas as operações de pélete no primeior dia elas foram completadas na manhã do segundo dia. A etapa crítica é não alterar o tempo de retenção no condicionador (acelerá-lo) quando atingir as altas temperaturas de pélete.Toda a ração foi descartada enterrando em aterro.
Resultados
[0001104] Resultados de estudos que confirmam a termoestabilidade de enzimas da invenção depois de peletização são ilustrados na figura 12, onde “selvagem” (ou WT), isto é, SEQ ID NO: 2, e a variante designada “a variante 7X”, a qual tem é uma sequência variação de SEQ ID NO: 2 consistindo das alterações de resíduos aminoácidos: 38Y, 61Q, 69E, 94Q, 183R, 191A, e 276A (vide a Tabela 2, e discussão, acima). Os dados na figura 12 ilustram a termoestabilidade destas duas enzimas da invenção por uma faixa de temperaturas de peletização a partir de cerca de 70oC a cerca de 100oC durante três operações; os dados comparam a percentagem (%) de atividade do resíduo da enzima na temperatura de teste comparada com sua atividade a 70oC comparada com a “temperatura de peletização”.
Exemplo 9: Enzimas da Invenção Modificadas para Evitar “N-Términos Imperfeitos”
[0001105] A invenção também proporciona sequências codificando enzima, e os ácidos nucleicos codificando as mesmas, em que as sequências são modificadas de tal modo que é gerada uma melhor sequência de reconhecimento para clivagem de protease de sequência de sinal.
[0001106] Por exemplo, conforme ilustrado na figura 13, dois códons foram inseridos entre o segundo (2o. códon) da enzima (glucanase) codificando sequência (isto é, sem o início ATG) (da SEQ ID NO: 1) e a sequência de sinal de fator alfa (sequência líder). Estes dois códons adicionais codificam para os resíduos aminoácidos ácido glutâmico (Glu) e alanina (Ala). A adição destes dois códons adicionais produz uma melhor sequência de reconhecimento para a protease que cliva a proteína entre a sequência de sinal e a glucanase. Ocorre clivagem sobre o lado N-terminal da sequência Glu-Ala e deste modo o N- término da proteína madura começa com Glu-Ala. Sem estes aminoácidos adicionais houve processamento incompleto de proteína nascente, resultando na produção de uma proteína heterogênea, tendo um chamado “N-término imperfeito”. A adição da sequência Glu- Ala (ou “EA”) produz uma proteína homogênea com um término amino (N-término) “limpo” (ou, não “imperfeito”, ou heterogêneo). Tudo isso foi verificado por sequenciamento de N-terminal. A figura 13 ilustra Sequenciamento N-terminal de Doublet de SEQ ID NO: 2.
[0001107] A figura 14 ilustra resultados do sequenciamento de N- terminal para as enzimas glucanase expressadas por Pichia da invenção designadas “12X-6” e “13X-1”, as quais são variantes de SEQ ID NO: 2, vide a Tabela 2, e discussão acima. A figura 14A ilustra uma radiografia de um gel SDS-PAGE apresentando um doublet de glucanase causado por processamento de sinal inconsistente; a figura 14B ilustra uma radiografia de um gel SDS-PAGE apresentando uma banda de 37 kDa; a qual foi excisada e sequenciada, conforme mostrado na figura. Estes dados ilustram que a inserção da sequência Glu-Ala, conforme descrito acima (para EAGVDPFERN) resulta em um término amino “limpo”.
[0001108] Apesar destes dados demonstrarem que o acréscimo de resíduos aminoácido adicionais entre a sequência líder (sinal) e a sequência enzimática trata o problema de “extremidades imperfeitas” na enzima glucanase recombinante expressada no hospedeiro de expressão Pichia exemplar, estas modificações ou modificações equivalentes podem ser usadas para expressão em qualquer hospedeiro, por exemplo, em qualquer hospedeiro de expressão procariótico ou eucariótico, por exemplo, e célula hospedeira bacteriana. Em aspectos alternativos, a célula é uma célula bacteriana, uma célula de mamífero, uma célula fúngica, uma célula de levedura, uma célula de inseto ou uma célula de planta, por exemplo, a célula bacteriana pode ser qualquer espécie dentro dos gêneros Escherichia, Bacillus, Streptomyces, Salmonella, Pseudomonas ou Staphylococcus, ou Escherichia coli, Lactococcus lactis, Bacillus subtilis, Bacillus cereus, Salmonella typhimurium ou Pseudomonas fluorescens.
Exemplo 10: Enzimas da Invenção Expressadas em Plantas e Sementes Transgênicas
[0001109] Uma modalidade da invenção proporciona plantas transgênicas (ou célula de planta derivada das mesmas) e sementes compreendendo sequências codificando enzimas desta invenção. Conforme discutido acima, a planta transgênica (ou célula de planta) ou semente pode ser produzida para constitutivamente, indutivelmente, ou em um maneira tecido- preferêncial expressar uma enzima desta invenção, por exemplo, por seleção do apropriado promotor ou outro regulador transcricional, conforme discutido acima. Opcionalmente, a enzima pode ser dirigida para um compartimento subcelular específico. Em um aspecto, a planta ou semente transgênica desta invenção é modificada para expressar uma enzima termotolerante “planta-optimizada”, por exemplo, como em uma planta exemplar da invenção, a planta transgênica expressa uma endoglucanase diretamente em uma célula ou semente, por exemplo, diretamente em uma semente de milho, por exemplo, para um alimento ou ração, tal como uma ração de animal monogástrico ou para uso em um processo industrial requerendo a decomposição de celulose. Este exemplo descreve expressão direta de uma enzima em uma semente de milho (milho); em particular, descreve endoglucanase termotolerante expressada diretamente em uma semente de milho (milho) para utilização aprimorada da ração ou para uso em um processo industrial requerendo a decomposição de celulose. A liberação de uma enzima expressada em uma planta pode ser usada como uma fonte de enzima purificada ou não purificada, expressada na própria matéria-prima para uso em processos industriais requerendo a decomposição de celulose ou usada como um componente da ração.
[0001110] A expressão específica em semente de milho de endoglucanases termotolerante otimizada para códon vegetal possibilita liberação desta enzima diretamente na colheita que é a fonte de um dos componentes básicos da ração animal (milho dietético). A expressão em milho também proporciona uma produção de baixo custo, em larga escala, e flexível desta - ou qualquer outra enzima - desta invenção. A enzima pode ser armazenada como semente seca ou em uma forma triturada para adição direta à ração sozinha ou em combinação com outras enzimas da ração e ingredientes da ração.
[0001111] Alternativamente, a expressão preferêncial de semente de milho de endoglucanases termotolerantes códon-otimizadas de plantas pode permitir a liberação da enzima na matéria-prima da biomassa para hidrólise da celulose em açúcares fermentáveis. Os açúcares fermentáveis têm muitos usos incluindo fermentação dos açúcares em álcool para energia ou combustível. As enzimas expressadas pela planta podem ser adicionadas à matéria-prima ou mesmo expressadas em matéria-prima usada para produzir açúcares fermentáveis. Uma enzima expressada pela planta pode ser dirigida para uma localização subcelular para evitar acesso ao substrato e deste modo degradação prematura do substrato. A enzima e o substrato podem ser então trazidos juntos por qualquer método necessário para decompor a organização subcelular, tal como, moagem, trituração, aquecimento e similares. A adição de um líquido pode aumentar a degradação do substrato. Deste modo, semente de milho triturada ou moída pode ser adicionada a qualquer matéria-prima antes ou durante hidrólise da matéria-prima.
[0001112] Uma segunda característica importante é a capacidade das enzimas para suportar as condições adstringentes (alta temperatura e vapor) do processo de peletização da ração. Portanto, em uma modalidade, o correto direcionamento subcelular da enzima para o retículo endoplasmático (ER) par obter alto nível de expressão sem impactar negativamente o desenvolvimento das sementes também é crucial (Vide a patente WO 2005/096704). Para obter esta modalidade, podem ser usadas sequências genéticas sintéticas e vetores de expressão semente-específicos, e similares sequências são descritas neste exemplo.
[0001113] Estoques de glicerol foram preparados para cada clone, 7X (SEQ ID NO: 7, codificada pela SEQ ID NO: 6), 12X-1 (SEQ ID NO: 13, codificada pela SEQ ID NO: 12), 12X-6 (SEQ ID NO: 9, codificada pela SEQ ID NO: 8), e 13X-1 (SEQ ID NO: 11, codificada pela SEQ ID NO: 10). DNA foi preparado para cada clone e sequenciado.
[0001114] Genes otimizados para milho foram designados para variantes de glucanase 7X (SEQ ID NO: 7, codificada pela SEQ ID NO: 6), 12X-6 (SEQ ID NO: 9, codificada pela SEQ ID NO: 8), E 13X-1 (SEQ ID NO: 11, codificada pela SEQ ID NO: 10) usando o programa de retro translação em Vector NTI 9.0 (Invitrogen, Carlsbad, CA). Genes sintéticos foram sintetizados por Entelechon GmbH (Alemanha). Sequência adicional foi adicionada à extremidade 5’ e 3’ de cada variante. Estas sequências incluíram um sítio de clonagem BamHI, sequência de Kozak, sequência de sinal de gaa zeína na extremidade 5’, uma sequência de retenção SEKDEL ER (Munro and Pelham (1987) Cell, 48:899-907), e um sítio de clonagem SacI na extremidade 3’. Um sítio de restrição BamHI interno foi removido de cada um dos genes otimizados para milho mutando a sequência de DNA para arginina (R69) de AGG para AGA próximo à extremidade 5’ do gene (AGGATCCcgat ... DAGAATCCcgat).
[0001115] As sequências variantes de otimizadas para milho finais foram traduzidas e alinhadas à sequência traduzida para cada uma das sequências microbianas. Foi visto que as sequências proteína- deduzidas codificadas pelas sequências otimizadas para milho combinam 100% com a sequência proteína-deduzida codificada pelas sequências microbianas. A correlação da sequência de DNA e proteína entre cada uma das variantes de glucanase otimizadas para milho e sua variante de glucanase selvagem é mostrada abaixo.
[0001116] Cada uma das variantes de glucanase otimizadas para milho foi clonada após o promotor de Glutelina de arroz (prGTL, Takaiwa et. al. (1991) Plant Mol. Biol. 16 (1), 49-58) e o promotor de gama zeína de milho (prGzein, patente WO 2005/096704) para expressão no endosperma da semente de milho. O terminador usado para todos os construtos foi o terminador 35S (patente WO 2005/096704). Conforme descrito acima, sequências adicionais foram adicionadas para direcionamento da proteína para o ER do endosperma. Cada gene foi excisado do vetor de clonagem Entelechon original, pMBL, como um fragmentoBamHI -SacI (1039 pb). Para construção dos construtos do promotor de Glutelina de arroz, o fragmento de 1039 pb foi clonado em pSM323 nos sítios BamHI- SacI. Para os construtos do promotor de Gama zeína, os fragmentos de 1039 pb foram clonados em pSH231. Fragmentos de promoter-GOI foram cortados de cada um dos vetores de clonatem como um fragmento HindIII-KpnI e subclonados no agro vetor, pNOV2117 (um vetor binário, vide Negrotto et al (2000) Plant Cell Reports 19:798803). As sequências de DNA de todos os Agro vetores foi confirmada por análise de sequência. Os vetores pode ser descritos como se segue:
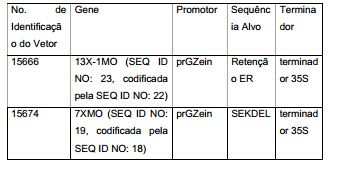

[0001117] Os construtos 15660 e 15671 foram transformados em Agrobacterium cepa LBA4404 de acordo com Negrotto et al.,(2000) Plant Cell Rep 19: 798-803. Agrobacterium strain LBA4404 (pSB1) contendo o plasmídeo de transformação vegetal foi cultivado sobre YEP (extrato de levedura (5 g/L), peptona (10 g/L), NaCl (5 g/L),15 g/l de ágar, pH 6,8) meio sólido por 2 a 4 dias a 28oC. Aproximadamente 0,8 X 109 Agrobacterium foram suspendidos em meio de infecção LS suplementado com 100 μM de As. Bactérias foram pré-induzidas neste meio por 30 a 60 minutos.
[0001118] A transformação de embriões de milho imaturos foi realizada conforme descrito de modo geral em Negrotto et al.,(2000) Plant Cell Rep 19: 798-803. Em resumo, embriões imaturos de milho produzidos por endogamia JHAX707 foram excisados de espigas de 8 a 12 dias de idade em LS-inf líquido + 100 μM de As. Os embriões foram enxaguados uma vez com meio de infecção fresco. A solução de Agrobacterium foi em seguida adicionada e os embriões foram turbilhonados por 30 segundos e deixados para assentar com as bactérias por 5 minutos. Os embriões foram em seguida transferidos com o lado do escutelo para cima para meio LSAs e cultivados no escuro por dois a três dias. Em seguida, entre 20 e 25 embriões por placa de petri foram transferidos para meio LSDc suplementado com cefotaxima (250 mg/l) e nitrato de prata (1,6 mg/l) e cultivados no escuro por 28oC por 10 dias.
[0001119] Embriões imaturos produzindo calo embriogênico foram transferidos para meio LSD1M0.5S. As culturas foram selecionadas neste meio por 6 semanas com uma etapa de subcultura em 3 semanas. Os calos sobreviventes foram transferidos para meio Reg1 suplementado com mannose. Depois de cultivo na luz (regime de 16 horas de luz/ 8 horas de escuridão), os tecidos verdes foram então transferidos para meio Reg2 sem reguladores do crescimento e incubados por 1 a 2 semanas. As mudas são transferidas para caixas Magenta GA-7 (Magenta Corp, Chicago Ill.) contendo meio Reg3 e cultivadas na luz. Depois de 2 a 3 semanas, as plantas foram testadas para a presença do genes PMI e outros genes de interesse por PCR. Plantas positivas do ensaio de PCR foram transferidas para a estufa e cultivadas para produzir semente.
[0001120] De modo a testar para atividade de glucanase, foi realizado o seguinte teste.
[0001121] Reagentes usados no Teste:
[0001122] Tampão de extração é tamponado em pH 5,30 e contém 100 mM de acetato de sódio, 100 mM de NaCl, 1 mg/ml de Gelatina, 1 mM de EDTA, 0,02% de Tween-20 e 0,02% de NaN3
[0001123] Reagente DNS Um litro de reagente DNS contém 5,0 g de ácido 3,5-dinitrossalicílico, 150 g tetraidrato de tartarato de sódio potássio e 0,36 mol de hidróxido de sódio.
[0001124] Solução de substrato é em pH 5,3 e contém 0,7% (em peso/ vol) de beta-glucano de aveia, 100 mM de acetato de sódio pH 5,3 e 0,02% (em peso/ vol) azida de sódio.
Moagem e Extração:
[0001125] Uma grupo de 16 sementes transgênicas foi triturado usando o moinho de esferas Kleco Molde 8200 8 canister. 100 mg da farinha triturada foi em seguida extraído em 10 ml de tampão de extração agitando em temperatura ambiente por 30 minutos. A mistura foi em seguida centrifugada e o sobrenadante foi removido.
Ensaio de enzima extraída
[0001126] O sobrenadante foi diluído a 1:50 no tampão de extração. Dez microlitros do extrato diluído foi adicionado a 50 microlitros de 0,7% de substrato de beta-glucano de aveia e incubado a 80°C por uma hora. Também é possível incubar a mistura em temperaturas menores, tais como, 70°C. Cinquenta microlitros de reagente DNS foi imediatamente adicionado e aquecido a 95°C por dez minutos. Amostras para momentos de 0 min foram preparadas misturando 50 microlitros de reagente DNS com 50 microlitros de solução de substrato e 10 microlitros de extrato. Padrões foram preparados misturando 10 microlitros de concentrações conhecidas de glicose (dissolvida em tampão de extração) com 50 microlitros de solução de substrato e 50 microlitros de reagente DNS. Os padrões, e as amostras dos momentos de 0 e 60 min são então incubados 10 min a 95°C e em seguida resfriados até a temperatura ambiente. Isto foi seguido por leitura da absorvência da amostra a A540. A quantidade de extremidades redutoras produzidas (em micromoles) foi determinada por comparação das leitura da absorvência das amostra com as dos padrões.
[0001127] Uma unidade de atividade é a quantidade de enzima que produz um micromol de extremidade redutora por minuto. A composição enzimática da semente é reportada como unidades de enzima/g de farinha.
[0001128] Foi analisado um total de 306 amostras de sementes transgênicas. Para eventos contendo o construto 15660, 164 amostras foram analisadas para atividade de glucanase. Para eventos contendo o construto 15671, 142 amostras foram analisadas para atividade de glucanase. O evento de maior expressão contendo o construto 15660 teve um nível de atividade de 3527 U/g (+/- 49 U/g) ao passo que o evento de maior expressão contendo o construto 15671 teve um nível de atividade de 2794 U/g (+/- 80U/g).
Exemplo 11: Atividade de Glucanase Em Ensaios de Ração
[0001129] Reagentes usados no ensaio:
[0001130] Tampão de extração é tamponada a pH 5,30 e contém 100 mM de acetato de sódio, 100 mM de NaCl, 1 mg/ml de Gelatina, 1 mM de EDTA, 0,02% de Tween-20 e 0,02% de NaN3.
[0001131] Reagente DNS Um litro de reagente DNS contém 5,0 g de ácido 3,5-dinitrossalicílico, 150 g de tetraidrato de tartarato de potássio de sódio e 0,36 mol de hidróxido de sódio.
[0001132] Solução de substrato está em pH 5,3 e contém 0,7% (em peso/ vol) de beta-glucano de aveia, 100 mM de acetato de sódio pH 5,3 e 0,02% (em peso/ vol) de azida de sódio.
[0001133] Etapas de Moagem e Extração Amostras de ração foram moídas por passagem através de um moinho de martelo de martelos de laboratório (Perten 3100) equipado com uma tela de 0,8 mm. A enzima foi extraída da ração agitando a mesma em tampão de extração. A extração foi realizada a 60°C com 10 g de tampão/1 g de ração moída. Temperatura elevada pode aumentar a eficiência da extração.
Ensaio de enzima extraída
[0001134] A enzima foi testada a 70°C com a atividade sendo monitorada medindo o aumento nas extremidades redutoras de 0 a 60 minutos. Amostras para 0 pontos de tempo foram preparadsa misturando 50 microlitros de reagente DNS com 50 microlitros de solução de substrato e 10 microlitros de extrato. Amostras para momentos de 60 min foram preparadas misturando 50 microlitros de solução de substrato e 10 microlitros de extrato, incubando por 60 min a 70°C em seguida adicionando 50 microlitros de reagente DNS. Padrões foram preparados misturando 10 microlitros de concentrações conhecidas de glicose (dissolvida em tampão de extração) com 50 microlitros de solução de substrato e 50 microlitros de reagente DNS. Os padrões, amostras dos momentos de 0 e 60 min foram em seguida incubadas 10 min a 95°C em seguida resfriada até a temperatura ambiente. Isto foi seguido lendo a absorvência da amostra a A540. A quantidade de extremidades redutoras produzidas (em micromoles) é determinada por comparação das leituras da absorvência das amostras com a dos padrões.
[0001135] Uma unidade de atividade é a quantidade de enzima que produz um micromol de extremidade redutora por minuto. A composição enzimática da ração é reportada como unidades de enzima/kg de ração.
Exemplo 12: Desempenho de frangos para grelhar quando alimentados com uma dieta contendo enzimas
[0001136] Foi adicionada enzima a uma dieta de milho/soja limitante de energia antes de processamento em uma temperatura elevada (90°C na face do molde). O desempenho dos frangos em dietas limitantes de energia contendo enzimas foi comparado com dietas limitantes de energia sem enzima (dieta controle negativo) e em dietas que não são limitantes de energia (dieta controle positivo). As enzimas foram expressadas e produzidas em Pichia..
[0001137] Pintos machos Cobb x Cobb de um dia de idade foram alimentados por 28 dias. Os frangos foram alimentados com uma dieta iniciadora para os dias 1 a 18 e uma dieta cultivadora para os dias 18 a 28. São usados oito tratamentos com 6 replicatas por tratamento e 6 aves por replicata. Os tratamentos e as dietas são resumidas nas tabelas abaixo.
[0001138] As tabelas abaixo apresentam o desempenho dos frangos nos vários tratamentos. FCR significa proporção de conversão da ração, por exemplo, kg de ração por kg de ganho de peso corporal. Amostras de ração de cada tratamento foram coletadas e analisadsa para atividade enzimática. A atividade enzimática foi detectada em ou acima do nível esperado exceto pela dieta do dia 0 ao dia 18 para o tratamento 3.
[0001139] Conforme visto abaixo nas Tabelas abaixo, aves alimentadas com uma dieta com energia suficiente (controle positivo) tiveram melhor ganho do que as alimentadas com o controle negativo; uma diferença de 70 g de peso é economicamente significativa. As enzimas geralmente aumentaram o ganho das aves, em algumas doses próximo ao nível do controle positivo. A proporção de conversão da ração corrigida (FCRc) não foi tão "clear-cut". Neste experimento a SEQ ID NO: 7 (codificada, por exemplo, pela SEQ ID NO: 6) e a SEQ ID NO: 9 (codificada, por exemplo, pela SEQ ID NO: 8) tiveram cada uma pelo menos uma dose que deu uma FCR significativamente melhor (menor) do que o controle negativo. A SEQ ID NO: 11 (codificada, por exemplo, pela SEQ ID NO: 10), no entanto foi similar ao controle negativo sobre a FCR.Tabela: Desempenho de 0 a 28 dias
[0001140] A recuperação da SEQ ID NO: 7, codificada, por exemplo, pela SEQ ID NO: 6 glucanase de péletes foi determinada medindo a atividade extraída de ração de malte moído peletizada em várias temperaturas. Os resultados são apresentados na figura 15. As dietas foram formuladas como uma dieta de ave para grelhar comercial típica (à base de milho/farinha grossa de soja/farinha grossa de osso e carne). Uma dieta basal foi preparada e é conforme indicado e suplementada com SEQ ID NO: 7, codificada, por exemplo, pela SEQ ID NO: 6 a 250 U/kg. Três amostras de malte moído foram preparadas para cada rodada de peletização. Durante as rodadas de peletização a temperatura foi aumentada em incrementos de 70 oC a 95 oC. O moinho foi monitorado cuidadosamente para assegurar que a retenção das amostras não aumentou com a temperatura. Foram coletadas amostras (500 g cada) de malte moído e péletes em cada temperatura e analisadas para atividade de glucanase de acordo com o protocolo do Exemplo 11.
[0001141] As Rodada 1 e 2 não apresentaram perda na atividade de glucanase quando peletizadas a 95°C. No entanto, a Rodada 3 apresentou cerca de 30% de perda de atividade enzimática quando peletizada a 95oC. A enzima pode perder atividade em solução com temperaturas acima de 95oC, caindo de 86% de atividade a 95°C para cerca de 8% de atividade a 97 oC. Portanto, a variabilidade na temperatura de peletização pode explicar a variabilidade na recuperação da SEQ ID NO: 7, codificada, por exemplo, pela SEQ ID NO: 6 da terceira rodada de peletização.
[0001142] Exemplo 14: Análise estatística de cinco experimentos de alimentação de enzimas glucanase.
[0001143] A glucanase "selvagem" e 3 das variantes (SEQ ID NO: 11 (codificada, por exemplo, pela SEQ ID NO: 10), SEQ ID NO: 9 (codificada, por exemplo, pela SEQ ID NO: 8) e SEQ ID NO: 7 (codificada, por exemplo, pela SEQ ID NO: 6)) foram testadas para eficácia na melhora do desempenho de frangos para grelhar alimentados com dietas as quais são marginalmente deficientes em energia mas suficientes em aminoácidos. Um resultado positivo seria visto como uma variante retornando desempenho que foi melhor do que o controle negativo.
[0001144] Foi estabelecida uma série de 5 experimentos planejados de modo idêntico, por meio dos quais as aves foram alimentadas com uma dieta de soja e milho de rotina Agri-stats como um controle positivo, e um controle negativo o qual foi idêntico em todos os aspectos com a exceção de que o nível de energia da ração foi reduzido por 80 a 90 kcals/kg (dependendo do experimento). Os experimentos duraram quer de 0 a 28 dias (3 experimentos) ou de 0 a 35 dias (2 experimentos) de idade. (Vide o Exemplo xy para detalhes do design experimental de um experimento típico).
Holo-análise de todos os dados de variantes
[0001145] Uma holo- análise de todos os dados combinados foi rezlizada para determinar uma medida do efeito das enzimas sobre o desempenho das aves. As análises foram realizadas sobre a FCR (proporção de conversão de ração), sobre o ganho de peso e sobre a recuperação de enzima da ração. • N = 78 testes no total (onde um teste = um tratamento em um ensaio onde uma enzima está presente) • Molde de FCR - nenhum efeito significativo de enzima ou dose • Molde de ganho - efeitos significativos de enzima e dose. • A recuperação de enzima da ração foi melhor com as variantes (SEQ ID NO: 7 (codificada, por exemplo, pela SEQ ID NO: 6), SEQ ID NO: 11 (codificada, por exemplo, pela SEQ ID NO: 10) e SEQ ID NO: 9 (codificada, por exemplo, pela SEQ ID NO: 8)) do que a enzima selvagem.
[0001146] O efeito da presença de enzima sobre o ganho foi modelado usando regressão em etapas usando os seguintes termos: Intercept, Log Dose de enzima, % de Milho, Regime de luz (horas por dia), Ganho controle negativo, Ganho controle positivo e Log dose de enzima). Os parâmetros estimados são dados abaixo. Estimativas de Parâmetros
[0001147] Todas as quatro enzimas tiveram um efeito da dose sobre o ganho. Os maiores efeitos da dose foram associados com a SEQ ID NO: 7 (codificada, por exemplo, pela SEQ ID NO: 6) e SEQ ID NO: 9 (codificada, por exemplo, pela SEQ ID NO: 8).
[0001148] As tabelas abaixo analisam a excelência do ajuste global (P<0,0001) e para vários parâmetros. Combinando os dados das enzimas houve um efeito significativo da dose enzimática (P<0,05) Sumário do Ajuste
[0001149] Apesar da invenção ter sido descrita em detalhes com referência a alguns aspectos típicos da mesma, será entendido que modificações e variações estão dentro do espírito e do escopo da qual é descrita e reivindicada.