BRPI1008745A2 - pró-fármacos de inibidores esteroidais de cyp17/antiandrogênios - Google Patents
pró-fármacos de inibidores esteroidais de cyp17/antiandrogênios Download PDFInfo
- Publication number
- BRPI1008745A2 BRPI1008745A2 BRPI1008745A BRPI1008745A BRPI1008745A2 BR PI1008745 A2 BRPI1008745 A2 BR PI1008745A2 BR PI1008745 A BRPI1008745 A BR PI1008745A BR PI1008745 A BRPI1008745 A BR PI1008745A BR PI1008745 A2 BRPI1008745 A2 BR PI1008745A2
- Authority
- BR
- Brazil
- Prior art keywords
- alkyl
- compound
- cancer
- group
- fact
- Prior art date
Links
- 230000002280 anti-androgenic effect Effects 0.000 title claims abstract description 9
- 239000000051 antiandrogen Substances 0.000 title claims abstract description 9
- 229940002612 prodrug Drugs 0.000 title abstract description 36
- 239000000651 prodrug Substances 0.000 title abstract description 36
- 239000003112 inhibitor Substances 0.000 title abstract description 12
- 150000003431 steroids Chemical class 0.000 title description 10
- 101150051357 CYP17A1 gene Proteins 0.000 title 1
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 40
- 201000011510 cancer Diseases 0.000 claims abstract description 34
- 238000000034 method Methods 0.000 claims abstract description 31
- 239000003098 androgen Substances 0.000 claims abstract description 22
- 206010060862 Prostate cancer Diseases 0.000 claims abstract description 17
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 17
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims abstract description 16
- 201000010099 disease Diseases 0.000 claims abstract description 14
- 238000011282 treatment Methods 0.000 claims abstract description 14
- 210000002307 prostate Anatomy 0.000 claims abstract description 8
- 206010006187 Breast cancer Diseases 0.000 claims abstract description 6
- 208000026310 Breast neoplasm Diseases 0.000 claims abstract description 6
- 229940124766 Cyp17 inhibitor Drugs 0.000 claims abstract description 6
- 206010020718 hyperplasia Diseases 0.000 claims abstract description 4
- 150000001875 compounds Chemical class 0.000 claims description 102
- 239000000203 mixture Substances 0.000 claims description 47
- 125000003118 aryl group Chemical group 0.000 claims description 37
- -1 bentimidazol Chemical compound 0.000 claims description 30
- 239000002253 acid Substances 0.000 claims description 29
- 125000000217 alkyl group Chemical group 0.000 claims description 29
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 27
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 23
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 claims description 22
- 125000002877 alkyl aryl group Chemical group 0.000 claims description 22
- 125000001072 heteroaryl group Chemical group 0.000 claims description 20
- 230000004962 physiological condition Effects 0.000 claims description 17
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 claims description 12
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 claims description 12
- 239000003795 chemical substances by application Substances 0.000 claims description 12
- 150000003839 salts Chemical class 0.000 claims description 11
- 229910052736 halogen Inorganic materials 0.000 claims description 10
- 239000008194 pharmaceutical composition Substances 0.000 claims description 10
- 208000008385 Urogenital Neoplasms Diseases 0.000 claims description 9
- 125000004432 carbon atom Chemical group C* 0.000 claims description 9
- 150000002367 halogens Chemical class 0.000 claims description 9
- 125000000623 heterocyclic group Chemical group 0.000 claims description 9
- 208000025609 Urogenital disease Diseases 0.000 claims description 8
- 229910052799 carbon Inorganic materials 0.000 claims description 8
- 239000003085 diluting agent Substances 0.000 claims description 8
- 125000004183 alkoxy alkyl group Chemical group 0.000 claims description 7
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 claims description 7
- 239000012964 benzotriazole Substances 0.000 claims description 7
- PBMFSQRYOILNGV-UHFFFAOYSA-N pyridazine Chemical compound C1=CC=NN=C1 PBMFSQRYOILNGV-UHFFFAOYSA-N 0.000 claims description 7
- 125000001453 quaternary ammonium group Chemical group 0.000 claims description 7
- 208000037964 urogenital cancer Diseases 0.000 claims description 7
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 claims description 6
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical compound OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 claims description 6
- 229940030486 androgens Drugs 0.000 claims description 6
- 125000004122 cyclic group Chemical group 0.000 claims description 6
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 claims description 5
- 125000003545 alkoxy group Chemical group 0.000 claims description 5
- 125000003282 alkyl amino group Chemical group 0.000 claims description 5
- 230000000694 effects Effects 0.000 claims description 5
- 239000011737 fluorine Substances 0.000 claims description 5
- 229910052731 fluorine Inorganic materials 0.000 claims description 5
- 229910052757 nitrogen Inorganic materials 0.000 claims description 5
- 239000006187 pill Substances 0.000 claims description 5
- GIIGHSIIKVOWKZ-UHFFFAOYSA-N 2h-triazolo[4,5-d]pyrimidine Chemical compound N1=CN=CC2=NNN=C21 GIIGHSIIKVOWKZ-UHFFFAOYSA-N 0.000 claims description 4
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 claims description 4
- 230000001548 androgenic effect Effects 0.000 claims description 4
- 239000002775 capsule Substances 0.000 claims description 4
- 238000002512 chemotherapy Methods 0.000 claims description 4
- 229910052739 hydrogen Inorganic materials 0.000 claims description 4
- 238000009169 immunotherapy Methods 0.000 claims description 4
- 238000004519 manufacturing process Methods 0.000 claims description 4
- 239000006186 oral dosage form Substances 0.000 claims description 4
- 238000001959 radiotherapy Methods 0.000 claims description 4
- 238000001356 surgical procedure Methods 0.000 claims description 4
- 239000000556 agonist Substances 0.000 claims description 3
- 239000011230 binding agent Substances 0.000 claims description 3
- 229940011871 estrogen Drugs 0.000 claims description 3
- 239000000262 estrogen Substances 0.000 claims description 3
- 238000001794 hormone therapy Methods 0.000 claims description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 claims description 2
- 206010004446 Benign prostatic hyperplasia Diseases 0.000 claims description 2
- 108700012941 GNRH1 Proteins 0.000 claims description 2
- 239000000579 Gonadotropin-Releasing Hormone Substances 0.000 claims description 2
- 230000009471 action Effects 0.000 claims description 2
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 2
- BDHFUVZGWQCTTF-UHFFFAOYSA-N sulfonic acid Chemical compound OS(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-N 0.000 claims 2
- LYUQWQRTDLVQGA-UHFFFAOYSA-N 3-phenylpropylamine Chemical compound NCCCC1=CC=CC=C1 LYUQWQRTDLVQGA-UHFFFAOYSA-N 0.000 claims 1
- 241000272478 Aquila Species 0.000 claims 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical class S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 claims 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 claims 1
- 239000002246 antineoplastic agent Substances 0.000 claims 1
- 229940044683 chemotherapy drug Drugs 0.000 claims 1
- 230000002611 ovarian Effects 0.000 claims 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 claims 1
- ODHXBMXNKOYIBV-UHFFFAOYSA-O triphenylazanium Chemical compound C1=CC=CC=C1[NH+](C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-O 0.000 claims 1
- 239000003814 drug Substances 0.000 abstract description 15
- 230000003389 potentiating effect Effects 0.000 abstract description 15
- 229940079593 drug Drugs 0.000 abstract description 13
- 241000282414 Homo sapiens Species 0.000 abstract description 8
- 230000015572 biosynthetic process Effects 0.000 abstract description 8
- 238000003786 synthesis reaction Methods 0.000 abstract description 7
- 230000003637 steroidlike Effects 0.000 abstract description 4
- 102000004190 Enzymes Human genes 0.000 abstract description 3
- 108090000790 Enzymes Proteins 0.000 abstract description 3
- 239000005557 antagonist Substances 0.000 abstract description 3
- 102000005962 receptors Human genes 0.000 abstract description 3
- 108020003175 receptors Proteins 0.000 abstract description 3
- 238000011275 oncology therapy Methods 0.000 abstract 1
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 39
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 19
- 229940125898 compound 5 Drugs 0.000 description 18
- 239000000243 solution Substances 0.000 description 18
- 150000002148 esters Chemical class 0.000 description 15
- 239000012267 brine Substances 0.000 description 13
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 description 10
- 229960000853 abiraterone Drugs 0.000 description 10
- 239000007787 solid Substances 0.000 description 10
- 230000037396 body weight Effects 0.000 description 9
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 9
- 239000007909 solid dosage form Substances 0.000 description 9
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- GZOSMCIZMLWJML-VJLLXTKPSA-N abiraterone Chemical compound C([C@H]1[C@H]2[C@@H]([C@]3(CC[C@H](O)CC3=CC2)C)CC[C@@]11C)C=C1C1=CC=CN=C1 GZOSMCIZMLWJML-VJLLXTKPSA-N 0.000 description 8
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 7
- 235000019439 ethyl acetate Nutrition 0.000 description 7
- 239000003981 vehicle Substances 0.000 description 7
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 5
- OJRUSAPKCPIVBY-KQYNXXCUSA-N C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N Chemical compound C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N OJRUSAPKCPIVBY-KQYNXXCUSA-N 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 102000001854 Steroid 17-alpha-Hydroxylase Human genes 0.000 description 5
- 108010015330 Steroid 17-alpha-Hydroxylase Proteins 0.000 description 5
- 239000000443 aerosol Substances 0.000 description 5
- XUYJLQHKOGNDPB-UHFFFAOYSA-N carboxymethyl phosphonic acid Natural products OC(=O)CP(O)(O)=O XUYJLQHKOGNDPB-UHFFFAOYSA-N 0.000 description 5
- 229940125758 compound 15 Drugs 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 5
- 239000000546 pharmaceutical excipient Substances 0.000 description 5
- 238000004007 reversed phase HPLC Methods 0.000 description 5
- 239000000741 silica gel Substances 0.000 description 5
- 229910002027 silica gel Inorganic materials 0.000 description 5
- 238000006467 substitution reaction Methods 0.000 description 5
- 239000000725 suspension Substances 0.000 description 5
- 210000001550 testis Anatomy 0.000 description 5
- 229960003604 testosterone Drugs 0.000 description 5
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 4
- 125000003342 alkenyl group Chemical group 0.000 description 4
- 239000000460 chlorine Substances 0.000 description 4
- 238000003818 flash chromatography Methods 0.000 description 4
- 230000012010 growth Effects 0.000 description 4
- 229940088597 hormone Drugs 0.000 description 4
- 239000005556 hormone Substances 0.000 description 4
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical class CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 4
- 239000012044 organic layer Substances 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 3
- NSPMIYGKQJPBQR-UHFFFAOYSA-N 4H-1,2,4-triazole Chemical compound C=1N=CNN=1 NSPMIYGKQJPBQR-UHFFFAOYSA-N 0.000 description 3
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 3
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 3
- QMMFVYPAHWMCMS-UHFFFAOYSA-N Dimethyl sulfide Chemical compound CSC QMMFVYPAHWMCMS-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 206010033128 Ovarian cancer Diseases 0.000 description 3
- 206010061535 Ovarian neoplasm Diseases 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 210000004100 adrenal gland Anatomy 0.000 description 3
- 125000006294 amino alkylene group Chemical group 0.000 description 3
- 229940030495 antiandrogen sex hormone and modulator of the genital system Drugs 0.000 description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 3
- 229910052794 bromium Inorganic materials 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 229910052801 chlorine Inorganic materials 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 239000002361 compost Substances 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 230000029142 excretion Effects 0.000 description 3
- 229960002074 flutamide Drugs 0.000 description 3
- MKXKFYHWDHIYRV-UHFFFAOYSA-N flutamide Chemical compound CC(C)C(=O)NC1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 MKXKFYHWDHIYRV-UHFFFAOYSA-N 0.000 description 3
- 239000012634 fragment Substances 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 230000007062 hydrolysis Effects 0.000 description 3
- 238000006460 hydrolysis reaction Methods 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 230000002085 persistent effect Effects 0.000 description 3
- 239000002953 phosphate buffered saline Substances 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- 239000006188 syrup Substances 0.000 description 3
- 235000020357 syrup Nutrition 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 2
- ADFXKUOMJKEIND-UHFFFAOYSA-N 1,3-dicyclohexylurea Chemical compound C1CCCCC1NC(=O)NC1CCCCC1 ADFXKUOMJKEIND-UHFFFAOYSA-N 0.000 description 2
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
- NVKAWKQGWWIWPM-ABEVXSGRSA-N 17-β-hydroxy-5-α-Androstan-3-one Chemical compound C1C(=O)CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CC[C@H]21 NVKAWKQGWWIWPM-ABEVXSGRSA-N 0.000 description 2
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Chemical compound C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 2
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- 241000220479 Acacia Species 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 2
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 2
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 2
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 2
- LSDPWZHWYPCBBB-UHFFFAOYSA-N Methanethiol Chemical compound SC LSDPWZHWYPCBBB-UHFFFAOYSA-N 0.000 description 2
- 208000002193 Pain Diseases 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- YBCVMFKXIKNREZ-UHFFFAOYSA-N acoh acetic acid Chemical compound CC(O)=O.CC(O)=O YBCVMFKXIKNREZ-UHFFFAOYSA-N 0.000 description 2
- 150000004703 alkoxides Chemical class 0.000 description 2
- 102000001307 androgen receptors Human genes 0.000 description 2
- 108010080146 androgen receptors Proteins 0.000 description 2
- 230000000259 anti-tumor effect Effects 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 210000000481 breast Anatomy 0.000 description 2
- 239000004067 bulking agent Substances 0.000 description 2
- 150000001720 carbohydrates Chemical class 0.000 description 2
- 235000014633 carbohydrates Nutrition 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 229940126543 compound 14 Drugs 0.000 description 2
- 229940125782 compound 2 Drugs 0.000 description 2
- 229960004397 cyclophosphamide Drugs 0.000 description 2
- YSEKNCXYRGKTBJ-UHFFFAOYSA-N dimethyl 2-hydroxybutanedioate Chemical compound COC(=O)CC(O)C(=O)OC YSEKNCXYRGKTBJ-UHFFFAOYSA-N 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 229960002949 fluorouracil Drugs 0.000 description 2
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical compound OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 230000003054 hormonal effect Effects 0.000 description 2
- 238000001361 intraarterial administration Methods 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 125000005647 linker group Chemical group 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000004060 metabolic process Effects 0.000 description 2
- 229960000485 methotrexate Drugs 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 238000011474 orchiectomy Methods 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 239000012071 phase Substances 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 201000005825 prostate adenocarcinoma Diseases 0.000 description 2
- 208000023958 prostate neoplasm Diseases 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- JMSVCTWVEWCHDZ-UHFFFAOYSA-N syringic acid Chemical compound COC1=CC(C(O)=O)=CC(OC)=C1O JMSVCTWVEWCHDZ-UHFFFAOYSA-N 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 230000004797 therapeutic response Effects 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 230000000699 topical effect Effects 0.000 description 2
- 150000003852 triazoles Chemical class 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- VUDZSIYXZUYWSC-DBRKOABJSA-N (4r)-1-[(2r,4r,5r)-3,3-difluoro-4-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-4-hydroxy-1,3-diazinan-2-one Chemical compound FC1(F)[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)N[C@H](O)CC1 VUDZSIYXZUYWSC-DBRKOABJSA-N 0.000 description 1
- MDHIWBNJNHUBJL-VMXHOPILSA-N (8s,9s,10r,13r,14s)-10,13-dimethyl-2,3,4,7,8,9,11,12,14,15-decahydro-1h-cyclopenta[a]phenanthrene Chemical compound C1CCC[C@]2(C)[C@H]3CC[C@](C)(C=CC4)[C@@H]4[C@@H]3CC=C21 MDHIWBNJNHUBJL-VMXHOPILSA-N 0.000 description 1
- 125000001607 1,2,3-triazol-1-yl group Chemical group [*]N1N=NC([H])=C1[H] 0.000 description 1
- LVEYOSJUKRVCCF-UHFFFAOYSA-N 1,3-Bis(diphenylphosphino)propane Substances C=1C=CC=CC=1P(C=1C=CC=CC=1)CCCP(C=1C=CC=CC=1)C1=CC=CC=C1 LVEYOSJUKRVCCF-UHFFFAOYSA-N 0.000 description 1
- PAMIQIKDUOTOBW-UHFFFAOYSA-N 1-methylpiperidine Chemical compound CN1CCCCC1 PAMIQIKDUOTOBW-UHFFFAOYSA-N 0.000 description 1
- VKIGAWAEXPTIOL-UHFFFAOYSA-N 2-hydroxyhexanenitrile Chemical compound CCCCC(O)C#N VKIGAWAEXPTIOL-UHFFFAOYSA-N 0.000 description 1
- XIDUQFVTIOZRKM-UHFFFAOYSA-N 2-methylsulfanylethyl thiohypofluorite Chemical compound CSCCSF XIDUQFVTIOZRKM-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 208000004998 Abdominal Pain Diseases 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical group N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 1
- 102100022704 Amyloid-beta precursor protein Human genes 0.000 description 1
- 241000837181 Andina Species 0.000 description 1
- KWIUHFFTVRNATP-UHFFFAOYSA-N Betaine Natural products C[N+](C)(C)CC([O-])=O KWIUHFFTVRNATP-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical class OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- 108010037003 Buserelin Proteins 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- DLGOEMSEDOSKAD-UHFFFAOYSA-N Carmustine Chemical compound ClCCNC(=O)N(N=O)CCCl DLGOEMSEDOSKAD-UHFFFAOYSA-N 0.000 description 1
- 208000005443 Circulating Neoplastic Cells Diseases 0.000 description 1
- 208000002881 Colic Diseases 0.000 description 1
- 206010011224 Cough Diseases 0.000 description 1
- 102000002004 Cytochrome P-450 Enzyme System Human genes 0.000 description 1
- 108010015742 Cytochrome P-450 Enzyme System Proteins 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- FMGSKLZLMKYGDP-UHFFFAOYSA-N Dehydroepiandrosterone Natural products C1C(O)CCC2(C)C3CCC(C)(C(CC4)=O)C4C3CC=C21 FMGSKLZLMKYGDP-UHFFFAOYSA-N 0.000 description 1
- 239000004338 Dichlorodifluoromethane Substances 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 241000975394 Evechinus chloroticus Species 0.000 description 1
- 241000276457 Gadidae Species 0.000 description 1
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 206010061178 Genital haemorrhage Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- NMJREATYWWNIKX-UHFFFAOYSA-N GnRH Chemical compound C1CCC(C(=O)NCC(N)=O)N1C(=O)C(CC(C)C)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)CNC(=O)C(NC(=O)C(CO)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C(CC=1NC=NC=1)NC(=O)C1NC(=O)CC1)CC1=CC=C(O)C=C1 NMJREATYWWNIKX-UHFFFAOYSA-N 0.000 description 1
- 108010069236 Goserelin Proteins 0.000 description 1
- BLCLNMBMMGCOAS-URPVMXJPSA-N Goserelin Chemical compound C([C@@H](C(=O)N[C@H](COC(C)(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NNC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 BLCLNMBMMGCOAS-URPVMXJPSA-N 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 241001326189 Gyrodactylus prostae Species 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- 101000823051 Homo sapiens Amyloid-beta precursor protein Proteins 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 108010000817 Leuprolide Proteins 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 208000008771 Lymphadenopathy Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 208000007101 Muscle Cramp Diseases 0.000 description 1
- LKJPYSCBVHEWIU-UHFFFAOYSA-N N-[4-cyano-3-(trifluoromethyl)phenyl]-3-[(4-fluorophenyl)sulfonyl]-2-hydroxy-2-methylpropanamide Chemical compound C=1C=C(C#N)C(C(F)(F)F)=CC=1NC(=O)C(O)(C)CS(=O)(=O)C1=CC=C(F)C=C1 LKJPYSCBVHEWIU-UHFFFAOYSA-N 0.000 description 1
- HTLZVHNRZJPSMI-UHFFFAOYSA-N N-ethylpiperidine Chemical compound CCN1CCCCC1 HTLZVHNRZJPSMI-UHFFFAOYSA-N 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 102000004316 Oxidoreductases Human genes 0.000 description 1
- 108090000854 Oxidoreductases Proteins 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000009328 Perro Species 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-N Propionic acid Chemical class CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 1
- 208000004403 Prostatic Hyperplasia Diseases 0.000 description 1
- 206010051482 Prostatomegaly Diseases 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 206010040829 Skin discolouration Diseases 0.000 description 1
- 244000061456 Solanum tuberosum Species 0.000 description 1
- 235000002595 Solanum tuberosum Nutrition 0.000 description 1
- 101000857870 Squalus acanthias Gonadoliberin Proteins 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 208000025865 Ulcer Diseases 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 238000010317 ablation therapy Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 150000001336 alkenes Chemical group 0.000 description 1
- 125000005157 alkyl carboxy group Chemical group 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- ROBVIMPUHSLWNV-UHFFFAOYSA-N aminoglutethimide Chemical compound C=1C=C(N)C=CC=1C1(CC)CCC(=O)NC1=O ROBVIMPUHSLWNV-UHFFFAOYSA-N 0.000 description 1
- 229960003437 aminoglutethimide Drugs 0.000 description 1
- DZHSAHHDTRWUTF-SIQRNXPUSA-N amyloid-beta polypeptide 42 Chemical compound C([C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O)[C@@H](C)CC)C(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 DZHSAHHDTRWUTF-SIQRNXPUSA-N 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 229960003473 androstanolone Drugs 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 239000013059 antihormonal agent Substances 0.000 description 1
- 230000004596 appetite loss Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000000305 astragalus gummifer gum Substances 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- VSRXQHXAPYXROS-UHFFFAOYSA-N azanide;cyclobutane-1,1-dicarboxylic acid;platinum(2+) Chemical compound [NH2-].[NH2-].[Pt+2].OC(=O)C1(C(O)=O)CCC1 VSRXQHXAPYXROS-UHFFFAOYSA-N 0.000 description 1
- 125000003828 azulenyl group Chemical group 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 229960003237 betaine Drugs 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- OYVAGSVQBOHSSS-WXFSZRTFSA-O bleomycin Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](OC1C(C(O)C(O)C(CO)O1)OC1C(C(OC(N)=O)C(O)C(CO)O1)O)C=1NC=NC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-WXFSZRTFSA-O 0.000 description 1
- 150000001649 bromium compounds Chemical class 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- CUWODFFVMXJOKD-UVLQAERKSA-N buserelin Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](COC(C)(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 CUWODFFVMXJOKD-UVLQAERKSA-N 0.000 description 1
- 229960002719 buserelin Drugs 0.000 description 1
- 239000003560 cancer drug Substances 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- OKTJSMMVPCPJKN-YPZZEJLDSA-N carbon-10 atom Chemical class [10C] OKTJSMMVPCPJKN-YPZZEJLDSA-N 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 229960004562 carboplatin Drugs 0.000 description 1
- 125000004181 carboxyalkyl group Chemical group 0.000 description 1
- 229960005243 carmustine Drugs 0.000 description 1
- 229940097647 casodex Drugs 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 150000005829 chemical entities Chemical class 0.000 description 1
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 1
- 229960004630 chlorambucil Drugs 0.000 description 1
- 150000001805 chlorine compounds Chemical class 0.000 description 1
- WORJEOGGNQDSOE-UHFFFAOYSA-N chloroform;methanol Chemical compound OC.ClC(Cl)Cl WORJEOGGNQDSOE-UHFFFAOYSA-N 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 235000008504 concentrate Nutrition 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- FMGSKLZLMKYGDP-USOAJAOKSA-N dehydroepiandrosterone Chemical compound C1[C@@H](O)CC[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC=C21 FMGSKLZLMKYGDP-USOAJAOKSA-N 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- PXBRQCKWGAHEHS-UHFFFAOYSA-N dichlorodifluoromethane Chemical compound FC(F)(Cl)Cl PXBRQCKWGAHEHS-UHFFFAOYSA-N 0.000 description 1
- 235000019404 dichlorodifluoromethane Nutrition 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N dimethylmethane Natural products CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 229940000406 drug candidate Drugs 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- WBJINCZRORDGAQ-UHFFFAOYSA-N ethyl formate Chemical compound CCOC=O WBJINCZRORDGAQ-UHFFFAOYSA-N 0.000 description 1
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 150000004675 formic acid derivatives Chemical class 0.000 description 1
- ZZUFCTLCJUWOSV-UHFFFAOYSA-N furosemide Chemical compound C1=C(Cl)C(S(=O)(=O)N)=CC(C(O)=O)=C1NCC1=CC=CO1 ZZUFCTLCJUWOSV-UHFFFAOYSA-N 0.000 description 1
- 229940074391 gallic acid Drugs 0.000 description 1
- 235000004515 gallic acid Nutrition 0.000 description 1
- 229910052733 gallium Inorganic materials 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- 210000004907 gland Anatomy 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229960002913 goserelin Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- 231100000304 hepatotoxicity Toxicity 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 239000005457 ice water Substances 0.000 description 1
- 229960001101 ifosfamide Drugs 0.000 description 1
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 150000004694 iodide salts Chemical class 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 1
- 229960004338 leuprorelin Drugs 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 230000007056 liver toxicity Effects 0.000 description 1
- 235000021266 loss of appetite Nutrition 0.000 description 1
- 208000019017 loss of appetite Diseases 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- KBPHJBAIARWVSC-RGZFRNHPSA-N lutein Chemical compound C([C@H](O)CC=1C)C(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\[C@H]1C(C)=C[C@H](O)CC1(C)C KBPHJBAIARWVSC-RGZFRNHPSA-N 0.000 description 1
- 235000012680 lutein Nutrition 0.000 description 1
- 229960005375 lutein Drugs 0.000 description 1
- ORAKUVXRZWMARG-WZLJTJAWSA-N lutein Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2C(=CC(O)CC2(C)C)C ORAKUVXRZWMARG-WZLJTJAWSA-N 0.000 description 1
- 239000001656 lutein Substances 0.000 description 1
- 208000018555 lymphatic system disease Diseases 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 238000009115 maintenance therapy Methods 0.000 description 1
- 150000004701 malic acid derivatives Chemical class 0.000 description 1
- 239000000845 maltitol Substances 0.000 description 1
- 235000010449 maltitol Nutrition 0.000 description 1
- VQHSOMBJVWLPSR-WUJBLJFYSA-N maltitol Chemical compound OC[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O VQHSOMBJVWLPSR-WUJBLJFYSA-N 0.000 description 1
- 229940035436 maltitol Drugs 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 125000005358 mercaptoalkyl group Chemical group 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M methanesulfonate group Chemical class CS(=O)(=O)[O-] AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N methanol Substances OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 238000002493 microarray Methods 0.000 description 1
- 230000027939 micturition Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- SMBBZHGTZJNSRQ-UHFFFAOYSA-N n'-(6,6-dichlorohexyl)methanediimine Chemical compound ClC(Cl)CCCCCN=C=N SMBBZHGTZJNSRQ-UHFFFAOYSA-N 0.000 description 1
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 1
- PHVXTQIROLEEDB-UHFFFAOYSA-N n-[2-(2-chlorophenyl)ethyl]-4-[[3-(2-methylphenyl)piperidin-1-yl]methyl]-n-pyrrolidin-3-ylbenzamide Chemical compound CC1=CC=CC=C1C1CN(CC=2C=CC(=CC=2)C(=O)N(CCC=2C(=CC=CC=2)Cl)C2CNCC2)CCC1 PHVXTQIROLEEDB-UHFFFAOYSA-N 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 229960002653 nilutamide Drugs 0.000 description 1
- XWXYUMMDTVBTOU-UHFFFAOYSA-N nilutamide Chemical compound O=C1C(C)(C)NC(=O)N1C1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 XWXYUMMDTVBTOU-UHFFFAOYSA-N 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- BSCHIACBONPEOB-UHFFFAOYSA-N oxolane;hydrate Chemical compound O.C1CCOC1 BSCHIACBONPEOB-UHFFFAOYSA-N 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 235000015927 pasta Nutrition 0.000 description 1
- 210000004197 pelvis Anatomy 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 150000003009 phosphonic acids Chemical class 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 1
- 125000005498 phthalate group Chemical class 0.000 description 1
- SIOXPEMLGUPBBT-UHFFFAOYSA-N picolinic acid Chemical class OC(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-N 0.000 description 1
- 230000036470 plasma concentration Effects 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 230000023603 positive regulation of transcription initiation, DNA-dependent Effects 0.000 description 1
- BDAWXSQJJCIFIK-UHFFFAOYSA-N potassium methoxide Chemical compound [K+].[O-]C BDAWXSQJJCIFIK-UHFFFAOYSA-N 0.000 description 1
- 230000036515 potency Effects 0.000 description 1
- 229960002847 prasterone Drugs 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 239000003380 propellant Substances 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 201000001514 prostate carcinoma Diseases 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 239000003488 releasing hormone Substances 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 238000011808 rodent model Methods 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 230000037370 skin discoloration Effects 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000011272 standard treatment Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 150000003890 succinate salts Chemical class 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- YIBXWXOYFGZLRU-UHFFFAOYSA-N syringic aldehyde Natural products CC12CCC(C3(CCC(=O)C(C)(C)C3CC=3)C)C=3C1(C)CCC2C1COC(C)(C)C(O)C(O)C1 YIBXWXOYFGZLRU-UHFFFAOYSA-N 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 125000001981 tert-butyldimethylsilyl group Chemical group [H]C([H])([H])[Si]([H])(C([H])([H])[H])[*]C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- VLLMWSRANPNYQX-UHFFFAOYSA-N thiadiazole Chemical compound C1=CSN=N1.C1=CSN=N1 VLLMWSRANPNYQX-UHFFFAOYSA-N 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 230000001256 tonic effect Effects 0.000 description 1
- KBPHJBAIARWVSC-XQIHNALSSA-N trans-lutein Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CC(O)CC1(C)C)C=CC=C(/C)C=CC2C(=CC(O)CC2(C)C)C KBPHJBAIARWVSC-XQIHNALSSA-N 0.000 description 1
- 125000005208 trialkylammonium group Chemical group 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 230000002485 urinary effect Effects 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 230000004584 weight gain Effects 0.000 description 1
- 235000019786 weight gain Nutrition 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 230000037303 wrinkles Effects 0.000 description 1
- FJHBOVDFOQMZRV-XQIHNALSSA-N xanthophyll Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CC(O)CC1(C)C)C=CC=C(/C)C=CC2C=C(C)C(O)CC2(C)C FJHBOVDFOQMZRV-XQIHNALSSA-N 0.000 description 1
- 229920001221 xylan Polymers 0.000 description 1
- 150000004823 xylans Chemical class 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J43/00—Normal steroids having a nitrogen-containing hetero ring spiro-condensed or not condensed with the cyclopenta(a)hydrophenanthrene skeleton
- C07J43/003—Normal steroids having a nitrogen-containing hetero ring spiro-condensed or not condensed with the cyclopenta(a)hydrophenanthrene skeleton not condensed
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/675—Phosphorus compounds having nitrogen as a ring hetero atom, e.g. pyridoxal phosphate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N5/00—Radiation therapy
- A61N5/10—X-ray therapy; Gamma-ray therapy; Particle-irradiation therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/24—Drugs for disorders of the endocrine system of the sex hormones
- A61P5/28—Antiandrogens
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Epidemiology (AREA)
- Biomedical Technology (AREA)
- Urology & Nephrology (AREA)
- Endocrinology (AREA)
- Pathology (AREA)
- Radiology & Medical Imaging (AREA)
- Reproductive Health (AREA)
- Diabetes (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Steroid Compounds (AREA)
Abstract
pró-fármacos de antiandrogênios/inibidores de cyp17 esteroidal pró-fármacos de esteróides c-17-heterocíclicos fornecendo biodisponibilidade oral melhorada e farmacocinética são descri tos. os fármacos são inibidores da enzima humana cyp 17, assim como antagonistas potentes de ambos os receptores do tipo selvagem e mutante de andrógeno (ar) , e são úteis para o tratamento de câncer urogenital e/ ou relacionadas a andrógeno, as doenças e/ ou condições, tais como câncer de próstata humana, câncer de mama, e hiperplasia de próstata. a divulgação descreve métodos de síntese e usando a pró- fármacos na terapia do câncer.
Description
PRÓ-FÁRMACOS DE INIBIDORES ENTEROIDAIS DE
CYP 17 /ANTIANDROGÊNIOE
REFERÊNCIA CRUZADA
Este pedido reivindica o beneficia do Pedido C.S.
Provisório N 61/150.031, depositado em 5 de fevereiro de 2009, e que 0 aqui ina.orpo.rado por referência em sua totalidade
CAMPO DA INVENÇÃO
Flat a invenção fornece novos px-ó-fãrmacos de inibidores 10 esteroidais de CYP17 para o tratamento de cânceres, doenças e/ou condições urogenitaís e/ou relacionados aos androgênios, incluindo câncer de próstata resistente à castração, à sintase dessas novas entidades químicas e aos métodos de utilização das mesmas no tratamento de cânceres, 15 doenças e/ou. condições urogeni.tais e/ou relacionados aos andregênios,
FUNDAMENTOS DA INVENÇÃO
O câncer de próstata (PCA; é a malignidade e causa relacionada à idade mais comum de morte por câncer em todo 20 o mundo. Com exceção do câncer do pulmão, o PCA. é a forma •de câncer mais comum, nos homens., e a segunda causa principal de marte nos homens dos Estados Unidos. Nos Estados Unidos em 2008, foi estimada que 186,320 novos casos de câncer de próstata, seriam dia.gnosticados e cerca 25 de 28.66 0 .homens morreríam dessa, doença, com homens ar.roamericanos e homens jamaicanos com ascendência africana tendo as maiores taxas de incidência deste no mundo {American Cancer Society* Cancer Facts and Figures' 2008;.
C>s androgênios tcâm um papel importante no desenvolvimento < cresc?lmento e progressão de PCA (McConnell, J.D., Urol, Clin. A-orth Am. , 1991, 18χ 1-W, com os dole androgênios mars importantes nessa questão sendo a testosterona, das quais .90% são sintetizados nos 5 testículos, e o restante (10%) sendo sintetizado pelas glândulas adrenals, e o androgênio mais potente, diidrotestosterona (DHT) ,. no qual a testosterona s convertida pela enzima estareide, So-redutase, que está localizada primarlamente na próstata (Eruchovsky, N, e 10 cols., J. Βίοι. Chem., 1.968, 243. 2,012-2,021}.
Huggins e coda, introduziram a privação de androgênio como uma terapia para o PCA avançado e metastátioc em 1941 (Huggins, C. e cols., Arch. Curq. , 1941, 43, 209-212), e, desde então, foi demonstrado que a terapia de ablação de 15 androgênic produz as respostas mais beneficias em vários quadros em pacientes com PCA (Denmeade, S.R. e cola,, fature Rev, Cancer, 200.2, 2; 339-3 56) . A orquidectomia (cirúrgica ou médica com um agonists de GnRH) permanece ii opção da tratamento-padrão para a maioria dos pacientes com 20 câncer de próstata, reduzindo ou eliminando a produção de androgenic· pelos testículos, mas não afetando a sintase de androgenic nas glândulas adrenals. Vários estudos relataram que uma terapia combinada de orquidectomia com antiandrogênios para inibir a ação de androgênios adrs.ua.is 25 prolonga significativamente a sobrevida de pacientas com rCA (Crawford, E,D. e cola., Nw ã'ng.1 > <7. IfecL, 1989, 321, 4 33-424 ,· Crawford, E.D. e cols, , J. Cro.7.. , 1932, 147; 41.7A;
e Denis, L·,, Próstata, 19.94, 5 (Supl<), 17s-22s).
Em um artigo recente por Mohler e colaboradores 30 (Mohler, J.L, e cols. , Clin. Cancer Res.,- 2004, 10, 44044 8}, foi demonstrado claramente que testosterona e diidrotestosterona ocorrera em tecidos de PC?A recorrente em níveia suficientes para ativar receptores de androgenic. Além disso, ceando definição de perfil baseado em 5 microarranjo de modelos isogânicos de xenoenxerto de PCA, Sawyer e colaboradores (Chen, C.D.. e cds., &Tat. Med.,. 2004, 10, 33-39) verificaram que ® aumente modesto no mRNA de receptor de androgânio era a única alteração associada consistentemente ac desenvolvimento de resistência à terapia com antiandrogênio. Compos tos potentes e específicos que inibem a síntese de androgênio nos testículos, adrenais e em outros tecidos podem, portanto, ser mais eficazes para o tratamento de PCA. (N;jar, V.C.O, e Brodie, A.M.R., Current Pharm. Design, 1999, 5: 163-180 .
IS Nos testículos e glândulas adrenals, a última etapa na biossíntese de testosterone envolve duas reações cruciais que ocorrem seqüencialmente, ambas as reações sendo catalisadas por uma única enzima, a citocromo P450 monooxigenase 17a-hidroxilase/ry. 20 -liass (CYP17) (Hall, 20 P.F,, J, Steroid Bíochenn Zíolec. BioL, 1991, 40, 527-532).
Cetoconasol, um agente antifúngico que também inibe enzimas
P450, também é urn inibidor de CVP17 modesto, e foi usado clinicamente para o tratamento de PCA (Trachtenberg, J. e cole., <Z. Tirol. 1993, 130, 152-153}. Foi relatado que a 25 posologia cuidadosa do tratamento pode produzir respostas prolongadas am padentes com câncer de próstata de outro modo resistente à castração (Moscato, >3. J. e uds. , Proc.
Am. Assoo. Cancer Pas. ,· 1994, 13: 22 (Resumo)) , Além disso, verificou-se que o cetoconasol retém atividade em pacientes 30 com PCA avançado com progressão, apesar da retirada da flutamida (Small, E.J, s t'ols. , J, rtrol., 1997, 157, 1.204··
1.207}, e embora o fârmacc agora tenha sido retirado do uso por causa de toxicidade hepâtica e de outros efeitos colatera is, os resu.ltados do cetoccnazol sugerem que inibidores de CYP17 mais potentes e seletivos poderíam foxmecer agentes úteis para o tratamento dessa doença, até mesmo em estágios avançados, s em alguns pacientes que podem parecer ser refratârios aos hormônios.
Foram relatados diversos inibidores esteroidais e não esteroldais de CYP17 potentes, alguns dos quais demonstraram ser inibidores potentes da nroduçâo de testostarena am modelos em roedores (Njar e Brodie, op. cít,}. Racentemente, Jarman e colaboradores descreveram o impacto hormonal de seu Inibidos.·' de CYP17 mais potente, abiraterona, em pacientes com câncer de próstata (O'Donnell, A, e cais.. Br. J. Câncer, 2 904, 9ü: 2.3172.325}. Alguns inibidores de CFP17 potentes também demonstraram inibir So-redutase e/ou ser antiandrogênios potentes com atividade antitumoral potente em modelos animais (N'jar a Brodie, op. cit,, e Long, B.J, e
Cancer Res, , 2000, 00,. s.s3Q - §. 640) .
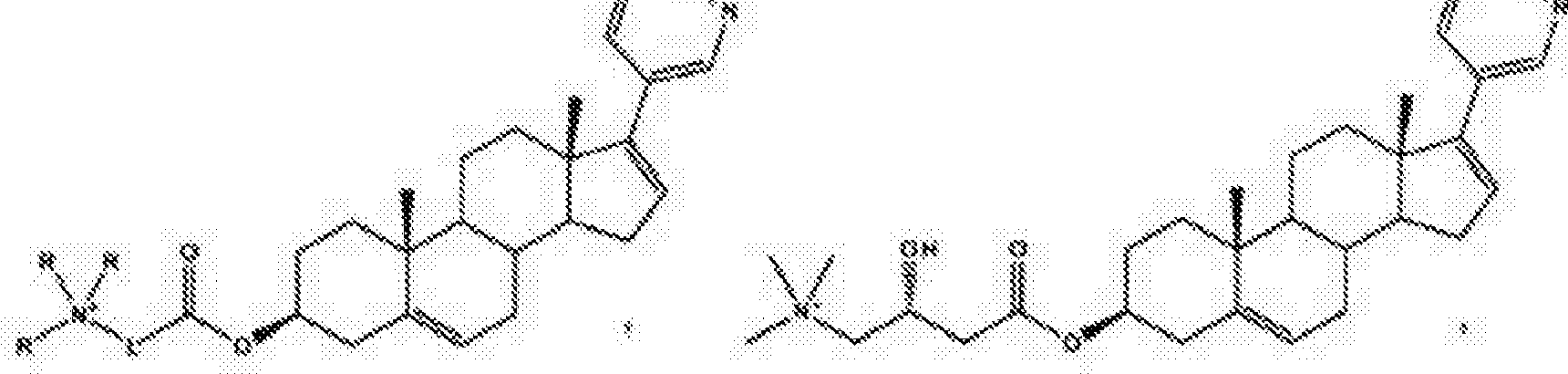
Além da ahir*aterona e das publicações relacionadas de Barrie e Jarman, Njar e ools. revelaram uma séria de inibidores de CYP17/antiandrogêxiics potentes, os 17benzoaaóis, 17-pirimidinoasôis e 17-diatinas, no Pedido de Patente internacional Publicado WO 2006/0$>3$93 (''‘University of Mari land} . Esses compostos são inibidores potentes da snsi.ma. CYPl humana, além de antagonistas potentes de receptores de androgênio (AP.) tanto do tipo selvagem quanto mutante. Inibidores de CYP17 particularmente potentes incluíam 3-β-hidròxi -17 - (IH-benziraidazol -1 -11)andrcsua 5,16-dieno (Composto 5) , 17- (IH-henzimidazol · 1 -11) androsta 4,16 -dleno- 3 -ona (Composto 6) e 3 -β- hidtôxi-17 -(5'pirimidil)andxosta-5,16~diena (Composto 15), com valores de IGj3 de 300, 915 e 500 rdí, respectivamente.
Composto 5 Composto 0 Composto 15
Os Compostos 5, 6 e 15 foram eficazes na competição com a ligação de H-RlSSl ímetiltrienolona, um androgênio sintético estável) tanto ao LNOaP AR mutante quanto ac AR 15 do tipo selvagem,, com uma eficiência de ligação 2,2 a 5 vazes maior para o ultimo. Os Compostos 5 e 5 também demonstraram ser antagonistas puros de AR potentes, com estudos de crescimento celular demonstrando que os Compostos 5 e 5 inibem o crescimento de células de câncer <í\í de próstaua i.Di,.a(·' e LaLCã estxmuladas por CHT com valores de IC5:J na faixa micromolar baixa (ou seja, < 10 μΜ) , Suas potências inibidoras eram comparáveis com aquela de casodex, mas acentuadamente superiores à da flutamida.
A farmacocinética dos Compostos 5 e 6 em camundongos 15 ueraonstrou que, após a administração s< c. da 50 mg/kq de Compostos 5 s δ, ocorreram níveis plasmáticos de pico de 16,82 e 5.15 ng/mlt respectivamente, apôs 30 a 60 minutos, ambos os compostos foram depurados rapidamente do plasma isie.i.as-vidas· terminais de 44,17 e 39,93 minutos.
respectívamentS;, e nenhum era detestável era 8 horas. 0
S / 49
Composto 5 sra rapidamente convertido em um metabolite, temporariamente .identificada cama 17 ~(lH-benzimidazol-1i 1) andras t a ·· 3 - ona .
Quando testado in vivo, o Composto 5 provou ser muito eficaz na inibição do crescimento de xenoenxerto de tumor de próstata humano a.ndrogênia-dependent.s LA.PC4, enquanto o Composto é provou ser ineficaz. A administração do Composto (50 mg/kg, duas vezes a.o dia) resultou em uma redução de $3,8% (P ~ 0,00055} no volume tumoral final médio, comparado com controles, e ele também foi sign!ficativamente mais eficaz do que a castração. Este foi o primeiro exemplo de um agents anti hormonal (um inibidor da síntese de androgênio (inibidor de CYPI7)/antiandrogênio? que ê significativamente mais eficaz do que a castração na supressão de crescimento de tumor de próstata androgênio-dependente. À. Xus dessas propriedades anticâncer impressionantes, o Composto 5 e análogos podem ser usados para o tratamento de câncer de próstata hunvano, bem como de câncer de mama, câncer ovariano e outras câneerss urogenitais ou outras condições ou doenças relacionadas aos androgênios.
Além. da. eficácia de um composto, a biodisponibilidade oral também é frequentemente uma consideração importante para o desenvolvimento de moléculas como agentes 25 terapêuticos. As propriedades físicas calculadas do Composto 5, par exemplo, satisfazem tanto a regra de eina-o de Lipinski (Lipinski, C.A., d. Aharmaool. Toxicol, rtóthads 2000. 44. (1), 235-49) quanto ã regra proposta recentemente por xfeber e cols. (Veber, D.F. s cods., d.
0 Afed. Che.m. 200 2, 45, (12; , 2,615-23) para previsão de uma probabi1idade aumentada de biodisponibilidade oral elevada ou f árwaco- .2i k& para novos candidatos a iárinacos, como apresentado para o Composto 5 na Tabela 1. Esses dados sugerem que o composto deve ser oralmente biodisponivel e, dessa forma, usi forte candidato a fármaco.
Tabela 1; Propriedades moleculares do Composto 5 (VN/124~1 com base aos critérios de Lipinski e de Verber
£.^KKK~^.SS.^SHSS-~.W.SSSWSSSSSSSSSSSSSSSSSSSSSSSSS-.W»W»W.W»V»V»V.W^ ..........................................W---W-^WW?SNNN^SSSSSSSSSSSSSSV.VrtVrtSS^^.„„,^.....^...........................^..w
A. Critério de Lipinski i Limita i W/124-1 | Resultados
| Doadores | de. ligação de i i L ú s i 1 i Aprovado |
| hic | teagènio i I j |
| A C tç ** ti. í Τ'ν? & | de ligação de 1 1 i |
| íl 10 i 2 i Aprovado hidrogênio j j.|
| χί¥·\<ί | molecular [ < 500 i 385,2515 | Aprovado |
CLogP ί <5 | 5,822 I Reprovad<
B, Critério da Verber li
.......................................................................................ί............................................j ......... i......................................
Número de ligações ; ;i l s 10 i 1 i Aprovado grraveis s ,í
Área de superfície I il
I 5 .14.0« A2 i 38,05° A2 ί Aprovado polar j ij
| doao.o.ir^^ & s j í | |
| aceptares | de ligação de i <12 1 3 j Aprovado |
hidrogênio | ||
No entanto, alguns estudos iniciais indicaram que o Composto 5 possui biodisponibilida.de oral baixa {aproximadamente 10%) em ratos. Com base na regra de
| Lipinski, | o Composto 5 possui um valor de cLogP maior (ou |
| se. j a, > 5) | , o que podería ser a principal razão para o |
| achado de | baixa õiodisponibilidade oral, como é típico de |
muitos -esterdides. Como as administrações orais da íãrmacos sâo geralmente preferidas, é importante encontrar formas de aumentar a biodisponihilidade oral de esteróides exemplificados pelo Composto Sf bem cornu de out res compostos apresentados em WO 2006/093992¾.
Adicionalmente, modificações da estrutura de um composto, de tal modo que a meia-vida sêrica seja estendida e C«x seja retardada, são desejadas, em função dos melhox'es regimes de dosagem e da liberação consistente do fármaco ao alvo em uma única dosagem.
Fundamentes adicionais da invenção estão contidos nas Patentes U.S. 5.604<213 (Barrie e cais.); 5.994,335 (Brodie e cois.H 6.200.5)65 (Brodie e ools.); a 6.444.683 (Brodie e cole,}.
Todas as referências aqui citadas são incorporadas por referência em sua totalidade.
SWÃRIG DA INVENÇÃO
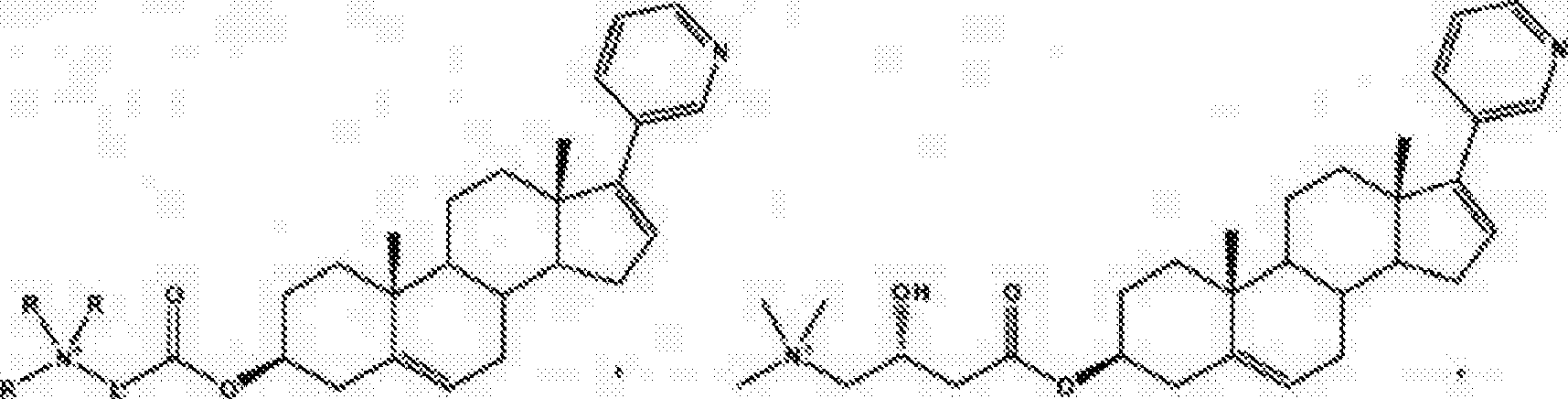
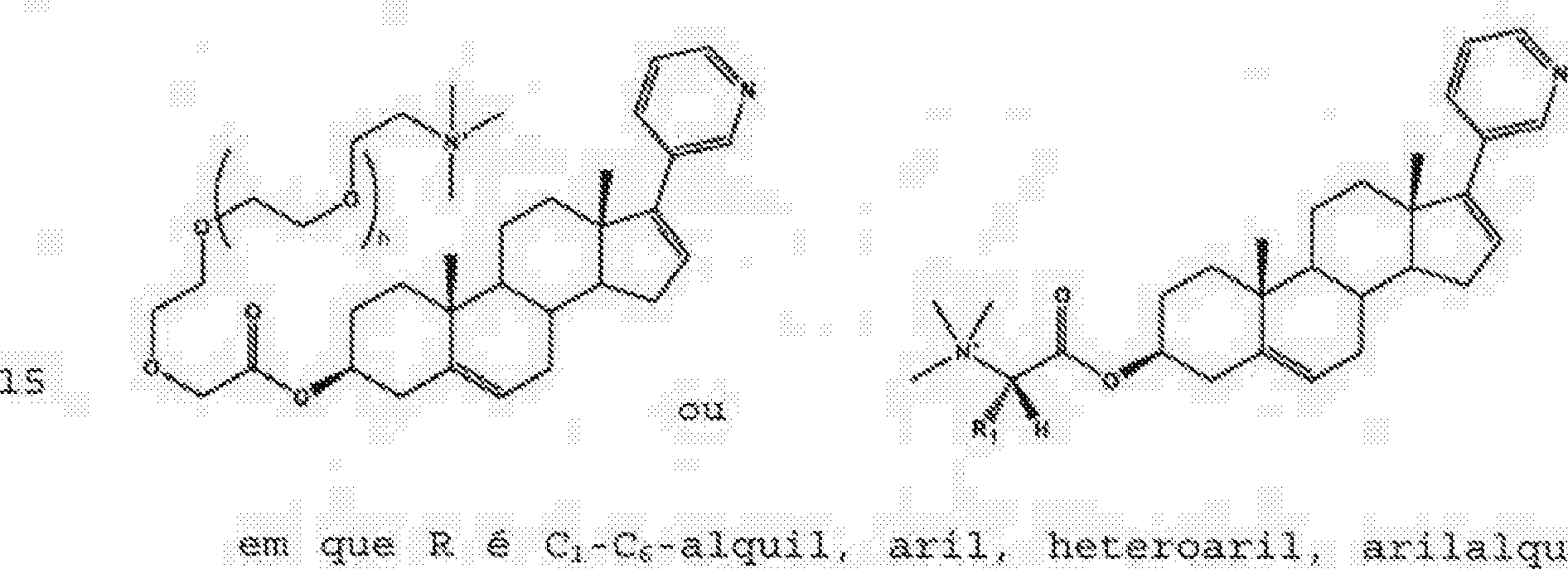
Em algumas modalidadesf a invenção contempla um composto de Fórmula I:
Formula X $s que;
a estrutura do anel .ABC ê opcionalmente substituída independeu temente em cada posição e em que substituirxtes de hidrogênio em átomos de carbono adjacentes da estrutura do anel ABC são opcionalmante removidos e substituídos por uma ligação-· pi entre os átomos de carbono adjacentes;
Y é S~L-C(~O)Q-; e
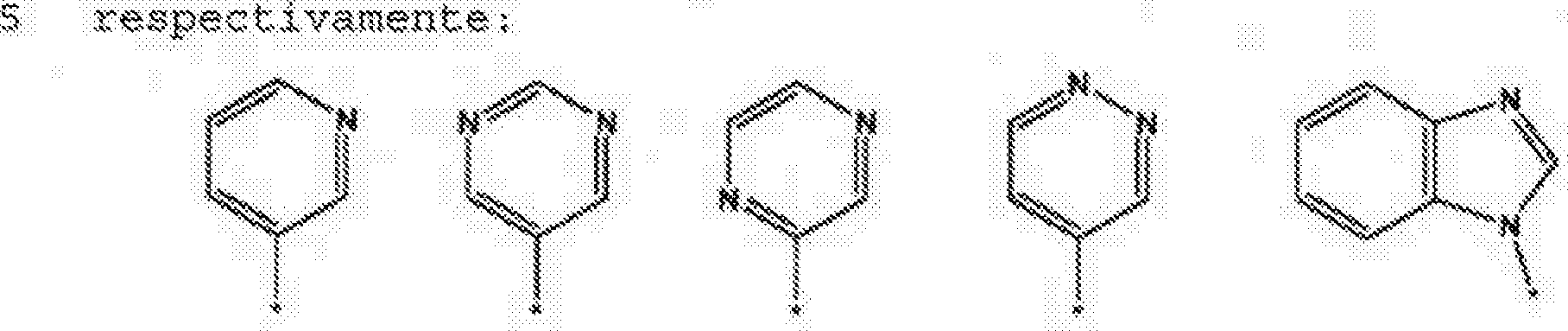
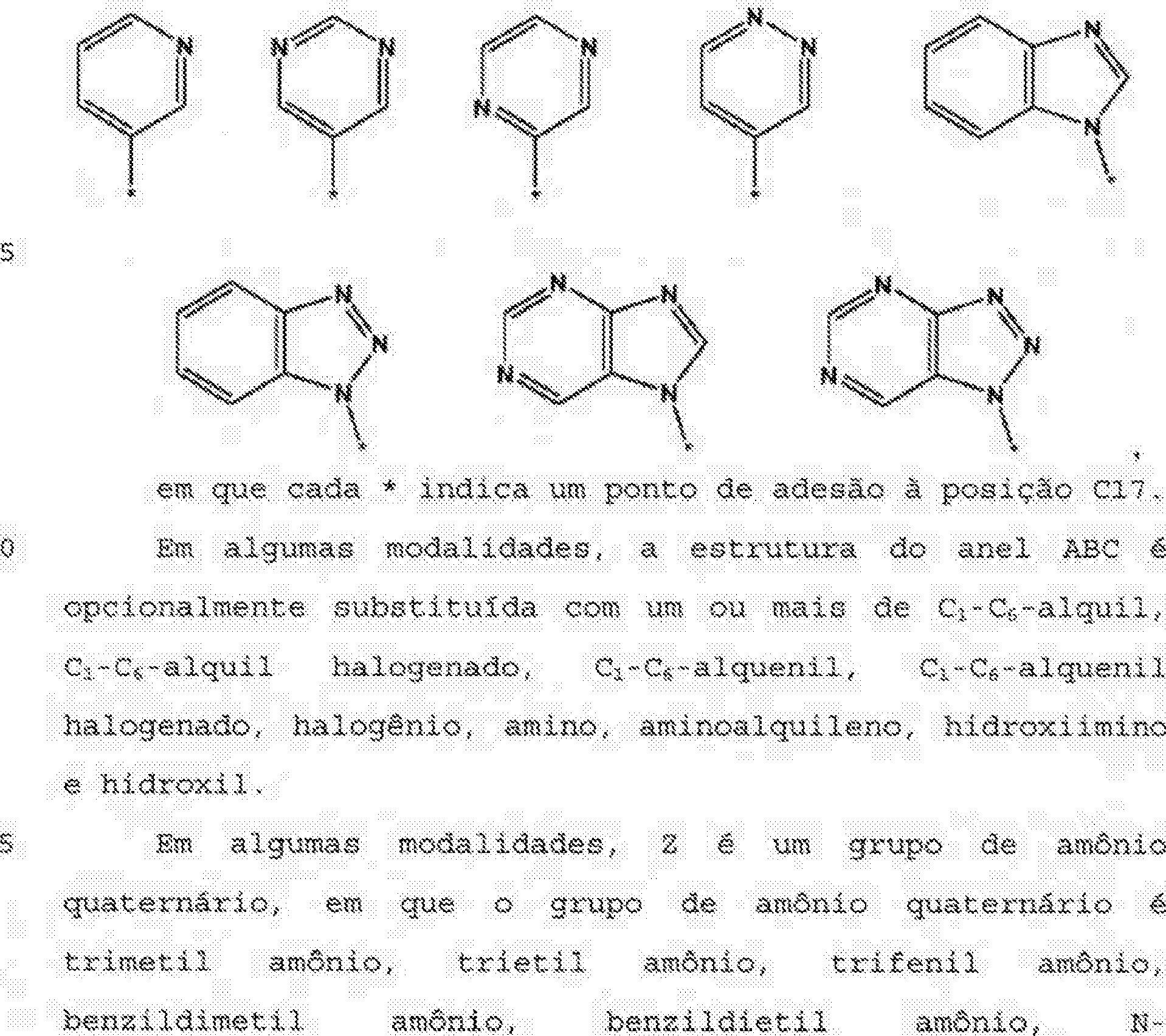
X é um heterociclo opcionalmsnte substituído que ê um grupo piridina, pirasína, pirimidiua, piridaeina, bensimídasol,. benzotria^ol, pírimidinoimidazol dl; pirimidinotriazol, em que o grupo benzimidazol, bensotriaso.!, pirimidinoimidaKOl ou pirimidinotriawl está 5 ligado à posição C17 por meio de um átomo de nitrogênio etn um anel de 5 membros do heterociolo, e o grupo piridina, pir&zina, pirimidina ou piridazina está ligado à posição C17 por meio de um átomo de carbono do heterociclo;
L é Cj~Cj2~alquíX, flúor-^q-Q-alcfuil, aril.
arílalquil, alquílaril, alcoxialquil, políalcoxialquil ou heteroaril , qualquer um deles sendo opcíonalmente cíclico, ou, junto oom 3, forma um anel, em que L é opcíonalmente substituído com um ou mais de alquíl, arílalquil, a 1 qu 1 lari I, al.qui 1 hs t eroar 11, halogênio, hidróxi .1, aIcóxi e
IS mere apt ano,· o
2. é um grupo can carga que está carregado sob condições fisiológicas normais, em que o grupo com carga é um ácido sulfõnico; um ácido fosfônico,- um tluoralcanol; ou um grupo hidróxi1 ácido,
OU........... ......
X e um grupo piridina opcíonalmente substituído;
L é Cj. Ci?-alquil, f lúor-C^ ··€$·· alquíl, aril, arílalquil, alquíl aril., alcoxíalquil, polialcoxialqu.il ou heteroaril, qualquer um deles sendo opcíonalmente cíclico, 25 ©u, junto com 2, forma um anel, em que L ê opcional meu te substituído com um ou mais de alquil, arílalquil, al qu 1.1 ar i 1, al qu i 1 he t eroar 11, ha logênio, hi drox 11, a 1 cõx 1, aIquilamino e mercaptano; e
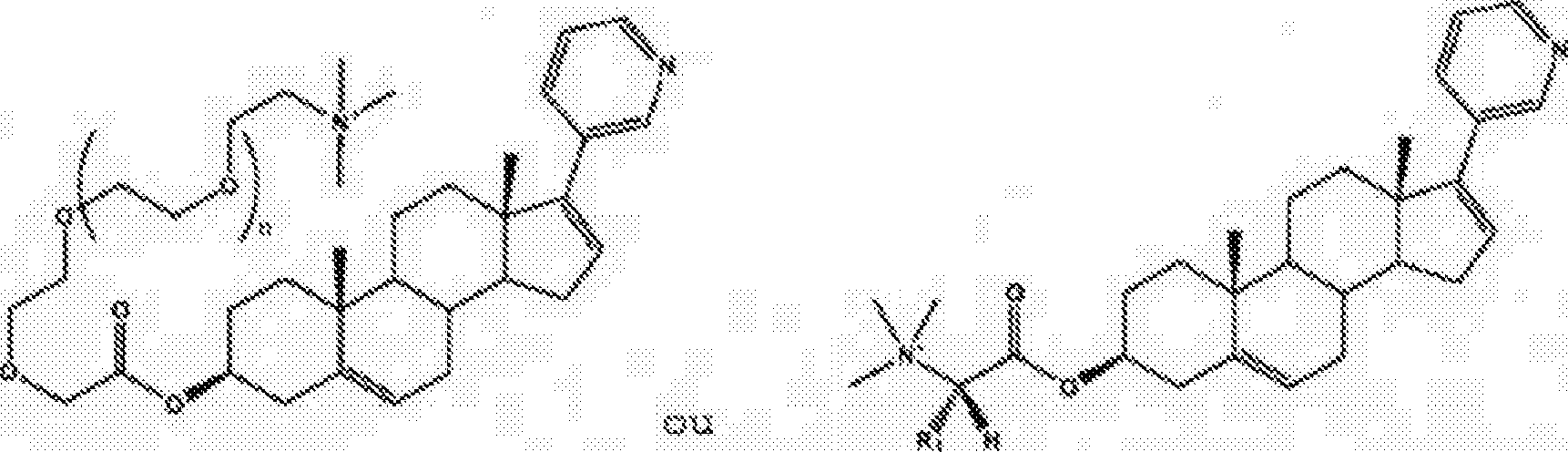
Z e um grupo com carga que está carregado sob íondiçces fisiológicas normais, em que o grupo com carga é
10/49 um grupo do amônio quaternária da formulai (R^N*)', em que cada grupo R é independentemente Ct-CÇ-alquíl ramificada, Cs.-£·,·-alquil de cadeia linear, aril, alquilaríl, aralquil, hetercar.il, au dois ou mais grupes R em conjunto formam, um anel; um ácido sulfônico; um ácido fosf.ôni.uo,- um f luoralcano.1; ou um grupo hidróxi.1 ácido, ou um sal f armaceuti.uamente aceitável das cea .
Em algumas modalidades, a invenção contempla uma composição farmacêutica que compreende uma quantidade terapeuticamente eficaz de um ou mais compostos da invenção e um ou mais exclpie-ites, agentes de volume, aglutinastes, agentes de fluxo, agentes de liberação, veículos ou díluentes farmaceuticamente aceitáveis.
Em algumas modalidades, a invenção contempla um método de tratamento de um câncer ou usaa doença urogenital em um indivíduo que o necessita ou deseja, o método compreendendo a administração ao indivíduo de uma quantidade terapeuticamente eficaz de um composto da invenção.
Em algumas modalidades, a invenção contempla, um método de tratamento da um câncer ou uma doença urogenital em um indivíduo que o necessita ou deseja, o método compreendendo a administração ao indivíduo d.e uma quantidade terapeuticamente eficaz de um composto da invenção, em combinação com uma terapia hormonal, uma. quimioterapia, uma radioterapia, uma imunoterapia ou cirurgia,
DESCRIÇÃO DBTALHADA DA INVENÇÃO
Como aqui usados, os seguintes termos possuem as seguintes definições, a menos que especificado de forma di ferente,
Alquíl é um grupo C=-C\3-linear, CX~CÍ2~ ramificado ou
C.s C-:·· οI c 11 co, ope lona 1 ment e subs t i tuí da independeutemence em cada posição con> um ou mais da hidroxil, raetóxi, etdxi, sulfidrila, sistilmercapto, e ti 1 me rca.pt. o,. flúor, cloro, bromo, í ode., a r ί 1 ê he teroa r 1.1..
Aril é um sistema aromático mono- ou policfclico. Exemplos não limitantes de aril incluem fenil, naftil, indeni 1, fluorenil, fenantrenil e azulenil. Aril ê opcionalmente substituído Índependentemente em cada posição com um ou mais de hidroxil, metóxi, etõxí, sulfidrila, metilmercapto, etilmercapto, flúor, cloro, bromo, iodo, cxo e heteroar.il. Em algumas modalidades, grupos aril contêm de cinca a dez átomos no anel,
Heteroaril é um sistema aromático mano- ou polí cíclica que compreende pelo menos um anel aromático com pelo manos um heteroátcmo no anel, em que o heteraátomo é nitrogênio, oxigênio au enxofre. Heteroar.il ê opcionalmente substituído índependentemente em cada posição com hidrox.il, metóxi, etóxi, sulf idrila, metilmercapto, et lime rear-to. flúor,, cloro, bromo, iodo, oxo e aril. Exemplos não limitantes de grupas heteroaril incluem fura.no, tiafeno, pirrol, pirrazol, imida&ol, oxasal, isoxazol, tiazol, isatiasol, triazol, tiadíazol, oxadiasol, pir.id.ina, pirimidina, pirsuna, pir idazina, tries ina, indol, oarbazol, bensofurano, benzotíofeno, benzotiasol, indasol, quinolina, isoquinoiina, ciuolina e ftalasina. Em algumas modalidades, grupos heteroaril contêm de cinco a dose átomos .no anel.
Alquilaril é um grupo alquil que está distalmsnte anexado por mero oe um grupo aril, por exemplo, tolil.
Ararquil. é um grupo aril que estã distalmente anexado por meio de um grupo alquil, por exemplo, benzil.
Polialcoxil ê poli (propileno glicol) ου poli (etileno glicol) , em que cs monômeros estão repetidos 2-100 vezes, em que esses grupos políalcoxí podem ser definidos pela gema precisa de unidades de repetição (por exemplo,. 35··40) , pelo pico visado de distribuição de envelope nas unidades de repetição (por exemplo, '114 de PEG5000) .. ou por uma seleção cruento ã soluhilídade ou propriedades físicas, e em que esses grupos são opcionalmente cobertos·'·' por um grupo slqui.l (MPEGSOOO para metóxi~PE(350G0) ou um grupo ar.il, por IO exemplo, fenll (polialcoxilar.il) A nuraeraçao do núcleo de esterõide aqui usada ê:
Numeração do núcleo de esterci.de
A presente invenção contempla o uso de pró-fármacos (versões modificadas ou precursores de ura composto parente, projetados para aprimorar as propriedades de liberação e serem convertidos no composto parente no corpo de uma forma consistente, previsível), para aumentar a hiod.ispon.ibil idade oral e f ax'macocinét.i.ca. de agentes terapêuticos eficates. A invenção fornece pró-fármacos de C ··· 17 he t er o c í c 1 os este r o i dai is, e mé t odo s de síntese e utilização dos mesmos para tratar cânceres, doenças e condições urogen.itais e/ou relacionados aos androgenioe,
Em algumas modalidades, um prõ-fármaco da invenção compreende um grupo de pro-fárraaco no carbono 3 na anel A* do composto. Era alqumas modalidades, o cfmoo de oró-fármaco compreende uma ligação éster. Em algumas modal id & de s, o grupo do pró-fármaco está anexado ao anel A pela ligação éster. Em algumas modalidades, o grupe de pró-fármaco compreende um grupo com carga. Um grupo com carga é um.
grupo que esta carregado sob condições fisiológica© normais. Exemplos não limitantes de um grupo com carga incluem grupos de trialquilamónio, grupos da amônio quaternário, ácidos sulfónicos, ácidos fosfônicos, fluoralcanóis; ou grupes hidróxi1 ácidos. Em alguma© 10 modalidades, um grupo hidroxil ácido é tornado ácido pelo efeito de ressonância e/ou indutivo de um grupo· removedor
| de elétrons | próximo, En | mod a .1 i da d e s | um grupo | |
| h idroxi1 ac i | do é tornado | ácido pel | o efeito da | res aonância |
| e / o u i ri d u b i v< | ·.> de um grupo | removeder | de elétrons próximo, em |
que o grupo hidróxiI ácido é mais ácido do que um grupo hidróxi1 análogo desprovido do grupo removedor de elétrons próximo, ?Em algumas modalidades, o grupo hidróxi 1 ácido é mais ácido d© que água. Em algumas modalidades, o grupo hidróxi1 ácido é fenólico. Em algumas modalidades, o grupo hidróxi1 ácido possui uma carga negativa substancial em água. Em algumas modalidades, o grupo hidrox.il. ácido existe suh.s tanc ialmente como um alcóxíd© em água. Em algumas modalidades,, o grupo hidroxil ácido possui uma carga negativa substancial em fluidos fisiológicos. Em algumas .xdauu no grupo hld-roxxl áumu* possua uma carga negativa substancial sob condições fisiológicas normais. Em algumas modalidades, o grupo hidroxil ácido existe substancialmente como um alcóxido sob condições fisiológicas normais. Em algumas modalidades, condições fisiológicas normais são condições inerentes em um organi s me : vivo:.
Em algumas modalidades, o grupo com carga. está conectado â ligação éster por um grupo de ligação.
algumas modalidades, o grupo de ligação ê C:.-Cx2-alquil, f lúor-Cl-Cs-alquil., aril,, ari.lalquil, alquilar.il, a1coxiaIqui1, polialcoxialquil cu heteroar.il. Em algumas modal idades, o grupo de ligação é cio lice. Em algumas modalidades, o grupo de ligação, junto com o grupo com carga, forma um anel. Em algumas modalidades, o grupo de 10 ligação é opcionalmente substituído com nm ou ’.meia de alquil, aril, heteroaril , aralquil, alquilaril, ha.logdn.io, hidroxil, alcôxi, alquilamino e mercaptano.
.Em algumas modalidades, o grupo de pro-farmsco é uma espécie de amônio quaternário.. por exemplo, bstaina, 15 carnítina e. oocamídoprapilbetalna (CAPB) . Em algumas modalidades, o grupo de prd·· fârmaao é um ox 1. carbon i .1 alqu 11 f os £ onat o; um ox icarbon 11 alqu 1 Isulfonato ;ou um carboxilato fenõlico, por exemplo, ácido siríngico ou .ácido gá.lico, ou um sal farmaceuticamente aceitável de 20 qualquer composta desse tipo. A invenção também contempla análogos sintéticos desses compostos. Em algumas modalidades, o análogo sintética possuí biodisponibilidade aumentada. Em algumas modalidades, o análogo sintético possui farmacocinética aprimorada. Em algumas modalidades, 25 o grupo de pró~fá.rmaco se fragmenta in vivo para fornecer um f ármaco:.
Em algumas modalidades, um pró-fármaco se fragmenta sob um canjunto de condições fisiológicas. Em algumas modalidades, o conjunto de condições fisiológicas que 30 fragmenta um prô~£ámaco é geral. Em algumas modalidades, o conjunto de condições fisiolôgicas que fragmenta um. prófârmaco ê específico para a identidade do prõ-fármaco. Em algumas modalidades, o conjunto de condições fisiológicas
| compreende | pH, Em algumas | moda1i da de s, o | conjunto de |
| condições f | isiológicas compre | sende temperatura. | Em algumas |
| moda 1 .idades | , o conjunto | de condições | t ÍS.l 01 Òg LCàS |
| compreende i | uetabolismo, Em al | gumas modalidades | , o conjunto |
| de condiçõe.· | » tisaológícas ooms | preende hidrõlise | , Em algumas |
| moda1 idades | , o conjunto | de condições | f i sio16gi cas |
compreende catâlise, Em algumas modalidades, o conjunto de condições fisiológicas compreende atividade ensimática. Em algumas modalidades, o conjunto de condições fisiológicas compreende oxidação ou redução.
Em algumas modalidades, a substituição opcional para a estrutura do a.nel ABC inclui um ou mais de: Ci-Q-alquil; C;-Cs~alquil halogenado, C}.-C\;-alquenil; CU C^-alqueni?·. halogenado; halogênio; amino; amínoalquíleno; hidróxiimino; e hidróxi.. Em algumas modalidades, um grupo alqueníl está ligado à estrutura, do anel ABC por um carbono sp::‘ do grupo alqueníl. Em algumas modalidades, um grupo alqueníl está ligado à estrutura do anel ABC por um carbono aps do grupo alqueníl. Em algumas modalidades, substituintes de hidrogênio em átomos de carbono adjacentes da estrutura do anel ABC são removidos e substituídos por uma ligação-pi entre os átomos de carbono adjacentes.
Em. algumas modalidades, as funcionalidades píridina, pírazina, pirimidína, pirldazina > benzimídazol. benzotriazol, pirimídinoímidazol ou. pirimidinotxiazol anexadas ao anel D são opcionalmente substituídas oom um ou mais de halogênio, amino, aminoalquileno, hidróxi,· -SH, -s15/4 9
CL-alquil, C; -0$-alquiI e C;.-C^-alquil halogenado.
Em algumas modal idades., os grupos piridina, pirazina, pirimidina, pirIdas ina, benz inti dazoI, Benzo triazol, pii'imidinoimidasol e pirimidinotriazol são,
Prõ-fãrmauos Pró-fármacos do Composto 5 de abiraterona
A habilidade do Composto 5 a da abiraterona para inibir CYP17 e esterõíde 5o-redutases, a ligação e transativagão de receptores de andxogênio, a os efeitos antiproliferatives contra duas linhagens de cé.lnlas de câncer de próstata humano, LNCai? e LAFC-4, foxam estudados e relatados em WO 2006/093.993 e em Potter e cole?. (Potter, G.A. e col a. , J. Med. Cham,, 1995,. 38,. 2.463--2.47,1}. WO 30 2006/093993 também relatou a avaliaçao da farmacocinêtica dos Compost os 5 e β do Esquema 1 em camundongos e as atividades anti tumorais in vivo contra carcinoma de próstata humano LAPC-4 em camundongos. Essas referências são incorporadas por referência es sua totalidade..
Em uma modalidade, o prô-fármaco desta invenção inclui um grupo de pró-fármaco farmaceuticamente aceitável. Em algumas modalidades, c grupo de pró-fármaco está anexado ao fármaco por meio de isaa ou mais ligações que são lábeis sob condições fisiológicas normais.. Em algumas modalidades, o 1.0 grupo de pro-fármaco fornece biodisponibi lidada oral e f amacocinêtica aprimoradas am relação ac- fármaco. Em algumas modalidades, o grupo de pró-fármaco ê incorporado na posição Y de um composto d.s Fórmula I.
Em algumas modalidades, o composto de Fórmula I é;
em que R!' ê H, alquil, aIquilar11, mercaptoalquil, hidróxiaIqui1, arilaIqui1, alquilamino, aminoaiqui1, alquiIcarboxí1, carboxialquil, alquilamido, amidoalguíl, ou. outro grupo derivado de aminoácidos naturais ou não naturais; R ê independantemente, em nada ocorrência, Ct-Clalquil, hidroxialquii, fenil, piridil, benzil ou alcoxialquil, em que cada grupo R pode ou não estar imide a outro grupo R para formar um anel; e n ê da 1-SQ, ou um estereoisomero ou sal farmaceuticamente aceitável destes. Em algumas modalidades, um valor para n é selecionado quanta as propriedades farmacocinéticas aprimoradas.
Em algumas modalidades, o composto de fórmula X ΰ;
Em algumas modalidades, a substituição do grupo de pró-fármaco é modificada para ajustar a p.Ka do pró-fârmaco.
Em. algumas modalidades, a substituição do grupo de pró fármaco é modificada para ajustar a pK.a do prô-fármaco de tal forma que o pró-.fármaco exista em um estado carregado no ponto de adscrção, distribuição, metabolismo e/ou excreção desejado.
Sm. algumas modalidades, o composto de Formula I e:
Em algomas snodalidades> a substituição do grupo da pró-fármaco ê modificada para ajustar a pKa do prõ~fármaco. Em algumas modal idades, a. substituição do grupo de pró fármaco é modificada para ajustar a pKa dc- prá-fármacc- de tal forma que o prô-fármaco exista em um estado- carregado no porto da adsorçao, distribuição., metabolismo e/ou excreção dese jado
Em algumas modalidades,, o composto de Fórmula I é:
em que n é de 0 a tO. Em algumas modalidades, um valor de n é escolhido de tal forma que a pKa do fluoralcanol esteja destro da faixa fisiológica.
Em algumas modalidades,, o composto de Form's la X é:
em que n ê de Q a so. Em algumas modalidades, um valor da n ê escolhido de tal. forma que a pKa do fluoralcanol esteja dentro da faixa fisiológica.
.Algumas modalidades contemplam sais farmaceuticamente aceitáveis d.a invenção. Sais farmaceuticamente aceitáveis dos compostos da invenção são gerados. por exemplo,· por tratamento dos compostos da invenção com um ácido, um hemiácido ou um sal para gerar' a forma de sal correspondente. Exemplos não limitastes de sais farmaceuticamente aceitáveis incluem cloretos, brometos, i ode tos. f os f st t os, sul fatos .< carbona tos, bi ca rbonatos , formates, acetates, propionates, benzoatos, picolinatos, tumaratos, malsatos, malatos, succinatos, metanossulfonatos, toluenessulfonates, mesicilencssulfonatos, trifluarmetanossulf.ona.tos; tetrafluorboratos, cetrafenilboratos e hexafluorfosfatos.
Preparação de camposto exemplar
A p.repat“a.ção de IV-benzoasõis e 17-diazinas ê aqui, descrita, com esses métodos sendo aplicáveis, de forma análoga, a outros análogos aqui descritos.
O intermediário crucial na síntese do 17-benzazol, .space tõxi 17 - c 1 oro-16“ form! 1 -androsta - 5, .16 » d 1 ano (2) , foi obtido pelo procedimento da rotina como descrito prevίamente CNjar , V.C.O. e cols. , Hioorq, ATed. Chem,
Lett., 199$, 6, 2.777-2.782, e Nfjar, V.C.O. e cols., J.
Med. Ch&n;. , 1998, 41, 903-.4:12j . O tratamento do Composto 2 com benzimidazol na presença da K^CCh em DMF a aproximadamente 8C°C gerou o sp-acetóxi-17-IH-benzimidazol 5 {3) desejado em rendimento quase quantitativo. O Composto 3 foi gentílmente deformilado oom paládio sobre carvão ativado 10% em N-metilpírzulidinona. para gerar o Composto 4 em 9 3%· de rendimento, do qual a hidrôlise gerou o hidróxi-17 -benzimidazol (.5) necessário:
A oxidaçâc de Cppenauer modificada do Composto 5 gerou o análogo άΜ-οχο correspondente {$) ,
A reação do Composto 2 com benzotriasol na presença de Κ;.;Ο'.Χ em DMF a aproximadamente 8 0*C gerou o 3p-açetóxi-17benzo-líí-1,2,3-triazol (7b) desejada cm excelente, rendimento, junto com a regioisômero 2H«l,2,S-triazol (7a) aproximadamente 1% de rendimento. Essas dois regioisômeros foram facilmente separados por cromatografia
| em coluna | instantânea | ΐ <' C; | em silica gel, | e foram | |
| facilmente | ident ifi cados | por set | , i. X. 't Λ-.Α'1 C, Λ.Ϊ· 4- | jsetros | RÍ4M |
| de prõt.on. | Destes, os | quatro | prótons aromá tic | OS O.O: | 2H·· |
1,2,3-triazol (7a) simétrico apareceram como dois pazes de dupletos em Õ 7,43, 7,45. 7,88 e 7,90, enquanto os quatro protons aromáticos do 11Γ-1,2, .l-trlazol (7b) assimétrico apareceram como multiple to em δ 7,46 (2H) e duple tos em δ 7,57 (IH) e 8/15 (IH) , respectivamente, .Além disso, o 1.0 próton 16-CHQ no Composto 7a foi eignificativamente mudado doarofield para Ò 10,66 comparado com aquele no Composta 7 b em Ô 9,59. A des form ilação do Composto 7b com geração ,in a X tu de Rh (1,3 - bis (di feni 1 f osf i no} propane) /Cl ’ cata 1 i nadar [Rh(dppp)/ClΊ em xilanos em refluxo gerou o Composto 8; e 15 a hidróliss do grupo 3p~acetôxi gerou o 3p~hidróxi-17 (benzo- 1H~ 1, 2,3-triazol -l-il) androsta-5,16dieno ·: 9; -alvo em 90% de rendimento.
Ά sintese das 17-diadnas, 17-diarina (14; a 17pxrimidxna {15} ,. começou a partir da dehidroepiandrosterona {Composto 11} facilmente disponível, que foi convertida na
17-hidrazana (12) correspondente per tratamento com hidrato de hidraaina e sulfato de hidraxina, corso descrito previamente per? Potter e cols. (Potter, G.A. a cols.., Org. Prep. Proc. Tor., 1957, 29, 123-1280}. 0 tratamento do
Composts 12 com iodo na presença. de 1,1,.3,3tetrametilguan Idina, gerou o vin.il 17~iodeto (.13) em excelente rendimento. As reações de acoplamento crurado cut.ax2 sadaS’ pox .palauiu (uhosux,. x... e coxs. , u. Orq·.., ú.nem.w , 1995, 60, 5.89.9--5.904) do Composto 13 com (2txibut lies ta.nil) pi ra Kina ou (5-tributiiestanil} pirimidina procederam para gerar 3p-hidróxi- 17 ~ {2~piraK.il) -androsta15 5, lO-dieno (14, 15%} e 3p-hidrôx.i-i7-(5-pirimidil)a.ndrosta-5,16-dieno (15, 10%), respectivamente.
χ$; J.·?.
Ά identidade dos Compostos 14 e 15-alvo fox facilmente confirmada por seus espectros RNM de próton; os três prótons não equivalentes da porção de 17-pxrazina no Composto 14 que? aparecem como três singletos em δ 8,35, 8,4 8 e 8,7ô, enquanto os três prótons da porção de 17 pirimidina no Composto 15 que aparecem como dole singleton em δ 8,73 (2K) e δ 9,ô7 (IK). Além disso, os grupos de 17diasina dos Compostos 14 e 15 exibem diferentes influências sobre as mudanças químicas dos prótons 16 olefínieos correspondentes com relação àqueles do ά*’·· 17 iode to 13 precursor: o 16 ~H no Composto 14 que aparece como um síngleto em δ 6,7?, sendo significatívamente desprotegido, comparado com o 16-14 no Composto 13 (δ 6,14); e o 16-H no Composto 15 que aparece em δ 6,11, similar ao Composto 13. O Composto 15 foi. relatado previamente por Haidar e caís. (Haidar, S. e cols., Ara,*?. Pharm. Medi Chem. . 2001, 3 34, 373-374) e suas atividades biológicas a farmacológicas também furam descritas (Haidar, S. e coisu, J. steroid Bíochem. Molec. BioK, 2003, 84, S5S-562}.
A abiraterona pode ser preparada como descrito na literatura (Fetter, U.A. e cols,, o. Med, £hem. , op. cífc.).
A síntese dos pró-fãrmacos revelados ê aqui ilustrada, com a compreensão de que os exemplos foxuiecidos podem ser aplicados a todos os compostos contemplados pela presente revelação.
A presente invenção também fornece composições farmacêuticas qua compreendem um veículo farmaceuticamente aceitável e um ou mais dos compostos aqui revelados, veículos farmaceutioamente aceitáveis adequados incluem, por exemplo, veículos, adjuvantes, excipíentes e diluentes,
A presente invenção também fornece métodos de tratamento de câxxceres, doenças e/ou condições urogenitais e/ou relacionados aos androgênios que incluem, sem limitação, câncer de mama, câncer de próstata (por exemplo, adenocarcinoma prostãtíco), outros cânoeres urogenitaís, niperpsasxa oa próstata ÍHPH; e/ou outras ooenças e/ou condições relacionadas aos androgênios, por administração a um indivíduo que os necessita ou deseja de uma. quantidade terapeuticamente eficaz de um composto da presente invenção. Q tratamento pode se.r profílático íque se refere a qualquer grau de inibição do surgimento de um distúrbio celular,, incluindo a inibição completa, por exemplo, em um indivíduo que supostamente exibirá um breve o distúrbio celular} ou terapêutico (que se refere a qualquer grau de inibição ou qualquer grau da efeitos .benéficos sobre o distúrbio ou condição no indivíduo, por exemplo, um ser humano) (por exemplo., inibição do crescimento ou metâstase de um tumor ou células tumorais circulantes). A terapia de manutenção, na qual a. supressão continuada de sintomas ou da progressão de doença e obtida por administração continuada dc composto, também e contemplada ροχ- estas invenção. Exemplos de doenças da próstata que podem ser u.ratadas incluem, por exemplo, hiperplasia prostática (BPH) e câncer de próstata (por exemplo, adenocarcinoma pros tático) ,.
Exemplos não limitantes de sintomas de câncer incluem; tumores, tosse persistente, saliva sanguinelenta, alterações nos hábitos intestinais, tezes ssngui.nolentas, anemia, caroços, incluindo caroços da mama ou do testículo, secreções corpóreas, alterações nos hábitos urinários, dor ou queimaçao na micção, aumento da próstata, urina sanguinolenta, glândulas edemacíadas, vai rugas , manchas, sangramento genital, ganho ou perda de peso involuntária, ooce.t.ra persistente, descoloração cutânea persistente, úlceras que não cicatrizam, dores de cabeça, dor ou
25/49 desconforto, por exemplo, nas costas ou pelve, cólicas, por exemplo, cólicas abdominais, fraqueza e perda de apetite.
Os métodos de administração de um composto da presente
| invenção a | ura indivíduo | , por exemplo, um | mamífero, | por |
| exemplo, um | rato, coelho, | cão ou ser humano, | sao connect | dos- |
| na técnica. | Embora mais | de uma via possa s | - e r u u a da ρ | ar a |
| administrar | uma compos.i | ç ao em part1cuIar, | uma via | em |
particular pode fornecer um resultado mais imediato e mais eficaz do que outra via.
Em algumas modalidades, uma composição farmacêutica e formulada para administração oral, Era algumas modalidades, a composição compreende uma. suspensão de um composto era um veículo adequado. Exemplos não 1iraitantas de veículos para administração oral incluem solução salina tamponada com fosfato (PBS) , dextrose era água (DSW) , carboximet.i.1 celulose 1% (CMC) e ura xarope. Em -algumas modalidades, urna composição é formulada para estabilizar a consistência de uma dose ao longo de um período de armazenamento e administração. Em algumas modalidades, a composição compreende uma solução. Em algumas modalidades, uma solução compreende uma quantidade eficaz de um ou mais compostos dissolvida era um diluante. Exemplos não limitantes de diluentes incluem água, solução salina s tampões. Em algumas modalidades, a composição compreende uma forma de dosagem sólida. Era algumas modalidades, a forma de dosagem sólida compreende uma cápsula, uraa drágea, ura losango, um sachê ou um comprimido. Em algumas modalidades, a forma de dosagem sólida é uma forma, de dosagem preenchida com um liquida. Em algumas modalidades, a forma de dosagem sólida é uraa forma de dosages1, preenchida com um solido. Era algumas modalidades, a forma de dosagem solida é um comprimido, cápsula ou drâgea preenchida com um solido. Em algumas modalidades, a forma de dosagem preenchida com um solido é
| uma forma | de dosag» | tm preen< | :’hida com um pó. E | ím algumas | |
| 5 | mod a 11. da.de s | , a fcjn | ta de d | osagem. sólida oomp | reende um |
| composto n | & forma | de part | levies, sólidos ou | grânulos | |
| mi cronica do | s. jsm | algemas | modalidades, a. | c omposxçao | |
| compreende | uma emuls | :áo. Sm a | Igumas moda1idades, | a emursao |
compreende um. composto da invenção caracterizada par à 0 px'opxaeda-Q.ee censoaLivas.
Em algumas modalidades, a forma de dosagem sólida compreende um ou mais de lactose, sorbitol, maltitol,
| manitol, | amido | de milho,. | amido de | batata, < | cjelulos: | |
| microeri | stalina, | h idroxiprop | i 1 c e 1 u 1 o s e, | acacia, g< | ilat ina | |
| 15 | dióxido | de silíc | :ia coloidal | , croscarmel | ose sódioa, | talco |
estearato de magnésio, esteãrico ácido, excipientes corantes,· diluent es, agentes de tamponament o, agentes umidif icantes , conservantes, agentes f lavorizantes, veículos e aglntinantes farmaceuticamente aceitáveis. Em algumas modalidades, a forma de dosagem sólida compreende um ou mais materiel is gue facilitam a fabricação., processamento ou estabilidade dst forma de dosagem sólida. Em algumas modalidades, um losango compreende um agente flavor leant e. Exemplos não límitantes de excipientes úteis na presente invenção incluem sacaxose, goma acácia, goma tragacanto, uma pastilha, uma base inerte, uma gelatina, glicerina, uma emulsão da sacarose, uma emulsão de acácia e um gel. Em algumas modalidades, uma forma de dosagem sólida é .revestida. Em algumas modalidades, o revestimento aumenta a absorção do composto no trato gastrintestinal. Exemplos âa/O não límitantas de revestimentos incluem acetato ftaiato de celulose {CAP), acetato ftaiato de polívinil (CVAP). e revestimentos modificados destes.
Em algumas modalidades, a composição é formulada como um aerossol. Em algumas modalidades, o aerossol ê administrado por meio de inalação. Em algumas modalidades., o aerossol compreende um ou mais propelentes.. Exemplos não limitantes de propelentss incluem diclorodifluormetano, hi.drof.luoxcarbo.no (por exemplo, hfc 134a e/ou 22?) e nitrogênio.
Em algumas modalidades, um composto ê administrado por uma via que é oral, parenteral, enteral, intraperitoneal,. topical, transdérmica, oftâIraica, nasal, local, não oral, aerossol, spray, inalação, subcutânea,. intravenosa, intramuscular, hucal, sublingual, ratal, vaginal, intraarterial ou incratecal. Em algumas modalidades, uma dose e administrada por uma via que é oral, parenteral, enteral, intraperitoneal, topical, transdéxniica., oftâlmica, nasal > local, não oral, aerossol, spray, inalação, subcutânea., intravenosa, intramuscular,. bucal, sublingual, ratal, vaginal, intra-arterial ou intratecal, Em algumas modalidades, o composto é administrado como uma suspensão em PBS, D5W ou um xarope ã base de carboidrato.
Em algumas modalidades, a dose ê administrada como uma suspensão em PEE, P5W ou um xarope â base de carboídrato.
Em algumas modalidades,, uma dose administrada a um indivíduo ê uma dose eficaz, Era algumas modalidades, a dose eficaz fornece uma resposta terapêutica no indivíduo dentro de um intervalo de tempo terapeuticamente útil. Era algumas modalidades, a dose e ficas compreende uma quaint idade terapeut icamente of leas de um composta. Etn algumas modal idades, a quantidade terapeuti earner, te eficaz fornece uma resposta terapêutica no indivíduo dentro de um intervalo de tempo terapeuticements útil. O nível de dose e a frequência de dosagem específicos são influenclados por diversos fatores·,. incluindo a atividade, estabilidade metabolica> biodisponib.il idade, taxa de excreção, meia-vida biológica. e modo e tempo d.e administração do composto; a idade, peso corporal, condição de saúde, sexo, dieta e caracteristícas físicas e de saude do xndavíduo; e a gravidade do câncer ou de outra doença ou condição.
Qualquer quantidade eficaz do composto pode ser administrada. Em algumas modalidades, uma dose compreende uma quantidade eficaz de um composto. Em algumas modalidades, uma dose ê administrada uma vez ao dia. Em algumas modalidades, uma dose é administrada mais de uma vez ao dia. Em algumas modalidades, uma dose é maior do que cerca de 1 mg/dia. Em algumas modalidades, uma dose é maior do que cerca de 5 mg/dia. Em algumas modalidades, uma dose é maior do que cerca de 10 mg/dia. Em algumas modalidades, uma dose é maior do que cerca de 25 mg/dia. Em algumas modalidades, uma dose é maior do que cerca de 50 mg/dia. Em algumas modalidades, uma dosa ã maior do que cerca de 100 mg/día. Em algumas modalIdades, uma dose ê menor do que. cerca de 5,000 mg/día. Em algumas modalidades, uma dose é menor do que cerca de 4.000 mg/dia. Em algumas modalidades, uma dose ã menor do que cerca de 3,000 mg/dia. Em algumas modalidades, uma dose é menor do que cerca de 2.500 mg/dia. Em algumas modalidades,, uma dosa ê menor do que cerca de 2.000 mg/dia. Em algumas modalidades, uma dosa é menor do que cerca de 1.500 mg/dia, Em algumas modalidades, uma dose ã menor do que cerca de 1.000 mg/dia, Em algumas modalidades, uma dose è menor do que cerca de 500 mg/dia. Em algumas modalidades, uma dose ê de cerca de 500 mg a cerca de 1.200 mg por dia. Em algumas modalidades, uma dase é de. cerca de 500 mg a cerca de l.SOO mg par dia. Em algumas modalidades, uma dose e de cerca de 1 mg a cerca de 5.000 mg por dia. Em algumas modal idades, uma dose é de cerca de 5 mg a cerca de 4.000 mg por dia. Em algumas modal idades, uma. dosa s de cerca de 10 mg a cerca de 3,000 mg por dia. Em algumas modalidades< uma dose é de cerca de 25 mg a cerca de 2,000 mg por dia. Em algumas modalidades, uma dose é de cerca da 50 mg a cerca da 2.500 mg per dia. Em algumas modalidades, uma dose s da cerca, de 10G mg a cerca de 2,000 mg por dia. Em algumas modalidades, uma dose é de cerca de 100 mg a cerca de 1.000 mg por dia. Em. algumas modalidades, uma dose ê de cerca, de 100 mg a cerca de 555 mg .por dia,.
Em uma modalidade, uma dose é de cerca de 0,01 a cerca da 100 mg/kg da massa corporal do indivíduo per dia. Em algumas medalidades, uma dose é de cerca de 0,05 a cerca de 50 mg/kg de massa corporal do indivíduo por dia. Em algumas modalidades, uma dose ê de cerca de 0,1 a cerca de 40 mg/kg de massa corporal do indivíduo por dia. Em algumas modalidades, uma dosa é de cerca de 0,25 a cerca de 30 mg/kg de massa corporal do indivíduo por dia. Em algumas modalidades, uma dose ê de cerca de 0,5 a cerca de 20 mg/kg de massa corporal da indivíduo por dia. Em algumas modalidades, uma dose é de cerca de 0,75 a cerca de 15 mg/kg de massa corporal do indivíduo por dia. Em algumas modalidades, wa dose ê de cerca de 1 a cerca de 10 mg/kg de massas corporal do indivíduo por dia. Em algumas modalidades, uma dose é de cerca de 2 a cerca de 5 mg/kg de massa corporal dc indivíduo por dia..
Em algumas modalidades. uma composição possuí uma concentração de mais do que cerca de 0,01% do composto por massa. Em algumas modalidades, uma composição possui uma concentração de mais do que cerca de 0,025% do composto por massa.. Em algumas modalidades, uma composição possui uma 10 concentração de mais do que cerca de 0,05% do composto post massa. Em algumas modalidades, uma composição possui uma concentração de mais do que cerca de 0,075% do composto por massa. Em algumas modalidades, uma composição possui uma concentração de mais do que cerca de 0,1¾ do composto por 15 massa. Em algumas modalidades, uma composição possui uma concentração menor do que cerca de 25% do composto por massa. Em algumas modalidades, uma composição possui uma concentração menor do que cerca de 20% do composto por massa. Em algumas modalidades, uma composição possui uma 20 concentração menor do que cerca de 15% do composto por massa. Em algumas modalidades, uma composição possui, uma concentração menor do que cerca de 10% do composto por massa. Em algumas modalidades, uma composição possuí, uma concentração menor do que cerca, de 7,5% do composto per 25 massa. Em algumas modalidades, uma composição possuí, uma concentração menor do que cerca de S% do composto per massa. Em algumas modalidades, uma composição possui uma concentração menor do que cerca de 3% do composto por massa. Em algumas modalidades, uma composição possui uma 3G concentração de cerca de 0,01% a cerca de 25% dc- composto por massa, Em algumas modalidades< uma composição possui uma concentração de cerca de 0,025% a cerca de 20% do composto por massa. Era algumas modalidades, uma composição possui uma concentração de cerca de 0,05% a cerca de 15% do
| compos | to | por massa. Em | algumas moda1idades, | uma | composição |
| possui. | rm | ia coneent.rsçao | de cerca de 0,03% a | cerc | :a da 5% do |
| compos | to | por massa. Em | a 1 gumas moda 1 ida.de s, | uma | campos1ção |
| possui | uu | '>& C OI) C £1 l X'& ç <á.o | da cerca de ü, w a | cerc | a de 3% do |
| campos | to | pOX'· 2»·ςΙ <. ·&£)) | arguraas mooali.danes, | uma | composição |
possui uma concentração de cerca, de 10% a cerca de 80% do composta per massa.
Em algumas modalidades, um composto da invenção é administrado isoladamente. Em algumas modalidades, um compostu é administrado com um ou mais outros ingredientes, por exemplo,. ura excipiente, veículo ou diluente farmaceuticamente aceitável. Era. algumas modalidades, um composto é usado em combinação com outros tratamentos contra o câncer. Em algumas modalidades, os compostas desta invenção são usados como urna parta -da ou era combinação com tratamentos contra u câncer conhecidos, per exemplo, terapia hormonal, quimioterapiat radioterapia, imunoterapia e/ou cirurgia. Em uma modalidade, um ou mala compostos são usados em combinação com um ou mais agentes adicionais. Em algumas modalidades, o agente adicional é um tãrmaca. Em algumas modalidades, o agente adicional ã um hormônio. Exemplos não limitantes de fãrmaccs e/ou hormônios para uso em combinação com os prô-fãrmacos desta invenção incluem antiandrogênios como, por exemplo, flutamida e nilutamida; outro inibidor de CYP17, por exemplo, abiraterona; agouistas do hormônio de liberação de hormônio lutein!zante, pur exemplo, leuprolida, goserelina e buserelina; e fãrmaoos que evitam que as glândulas adrenals produzam androgânios, por exemplo, cetocouasol e aminoglutetimida; e estrogênios. Exemplos não limitantes de fãrmacos contra o câncer incluem ciclofosfamida, metotrexato, 5-fluoruracil (5-FU) , dox.orrubioina, carboplatina, carmustína, clorambucil, cisplatina, ciclofosfamida, dacarbasína, ifosfamida, mecloretamina, me 1 fa lan, procarba zi na, bleomic ina, doxor rubi e ina, Idarruni c 1 na mi toxa n t rona , c 1 crude sox iadenos Ina., oitarabina, fludarahina, 6-marcaptopuxina, metotrexato, 6-ticguanina, psutostatina, etoposide, gemcitabina, cremes de esteróides, corticosteróides, prednisona e dexametasona.
Os compostos desta invenção podem ser administrados a um indivíduo em qualquer momento, como determinado pelo médico responsável pelo tratamento. Em algumas moda1idades, c composto ê administrado durante um ou mais de Estagio II, Estágio III e Estágio IV do câncer. Em algumas modalidades, c composto ê administrado durante um estágio avançado de uma doença ou condição urogenital e/ou relacionada aos androgênius.
As modalidades da revelação são fornecidas com o objetivo áe ilustração, e não de limitação.
Em algumas modalidades, a invenção fornece composto de Fórmula: I::
Formula, em qua:
a estretura do anel ABC é opcionaimente substituída independentsmsnte era cada posição e era que substituintes de 5 hidrogênio era átomos da carbono adjacentes da estrutura do anel ABC são opcionaimente removidos e substituídos por uma Ügação-pi entre os átomos de carbono adjacentes;
í* & '·£ ** C- à ::i0) O··*· j <5
X é um heterociclo opcionaimente substituído que ê ura grupo pxridina, pirasína, pirimidina, piridazina, benzimidazol, benzotriazol, pirimidínoimidazol ou pirimidinotriazo.1., era que o grupo beuzimidazol, benzotriazol , pirimídinoimidasol ou pirimidinotriazol está ligado ã posição Cl7 por meio de um átomo de nitrogênio em 15 um anel de 5 membros do heterociclo, e o grupo piridina, pirazina, pirimidina ou piridazina está ligado ã posição Cl7 por meio de um átomo da carbono do hetercciclo;
L é Q-alqu.il > flúor-C?-Cg-alquil, aril., arilalquil, alquilaril, alcoxialqui1, pdiaIcoxialquil ou 20 heteroaril, qualquer ura deles sendo opcionaimente cíclico, ou, junto com 2, forma um anal., em que L é opcionaimente substituído com um ou mais de alquil, arílalqull, alquí la.ril, alquilhetercaril, halogênio,. hidroxil, alcõxi e meroapta.no; e
0 1 e um grupo com carga que está, car .regado sob condições fisiológicas normais, em que o grupo com carga é um grupo de amônio quaternário da fórmula (R.Wj, em que cada grupo R é independentemente Cj·· C?~alquil ramificado, C.-C-;-alquil de cadeia linear,, aril, alquilaril, aralquil, hôteroanl, gu dois ou. mais gruoos R era conjunto formam um anel; um ácido sulfônico; uui ácido tos fônico; ® fluoralcanol; ou um grupo hidróxi1 ácido, ou um sal farmaceuticamente aceitável destes.
: £>/ À-í.
X é um grupo piridina opcionalmente substituído;
L é Ci«Cs3»alquil, fllôor^Ca-Cç-alquil, aril, a ri lal qu 11, al gu i lar i 1, al coxia Iqui 1, po 1 ia looxi a Iqui 1 ou heteroaríl, qualquer um deles sendo opcionalmente cíclico, ou, junto com 1, forma um anel, nm que L é opcionalmente substituído com um ou mais de alquil, arilalquil, aIquilari1, alquilhe teroar i1, halogênio, hidr oxi 1, a1côxi, alquilamíno s mercaptano; e.
z é um grupo com carga que está carregado sob condições fisiológicas normais, em que o grupo com carga é um grupo de amônia quaternário da fórmula , em que cada grupo R é independentemente. Ci~C?-alquil ramificado, C; Cvalquil de cadeia linear, aril, alquilar11, aralqu.il, heteroaril, ou dois ou mais grupos R em conjunto formam um anel; um ácido sulfônico; nm ácido fosfônico; um fluoralcanol; ou um grupo hidróxi1 ácido, ou um sal farmaceuticamente aceitável dastes.
Hm algumas modalidades, X é opcionalmente substituída cam um ou mais de halogênio, amina, aminoalquileno, hidróxi, -SH, ~S-Cj.-Cs~alquil, C-.-Cç-alquil e Ct-Q -alquil halogenaòc
Em algumas modalidades, os grupos piridina, pirarina, pirimidina, piridazina, bensimidazol, benzotriazol, pir imidinoimidazol. e pirimidinotriazol são, resoe cti vamente;
metilpiperidínio, N-etilpiperidínio ou tribensil amônio.
Em algumas modalidades, E é um ácido sulfônico, e L é Cί · Sí; -alquil...
Em algumas modalidades, E é um ácido fosfônico, e L é C;.--0,:--alquil *
Em algumas modalidades, o compos to é ·;
Επ': algumas modalidades, o composto é:
em que R õ Q-C^-alquíl, aril, heteroaril, arilalquil u alquilaril; R? é C5-C^-alquil, aril, aralquil, alquilaril u alquilheteroari1; e n ê de 1 a 4$.
Em algumas modalidades, a invenção fornece uma omposição farmacêutica que compreende uma quantidade erapeuticamente eficaz de um ou mais compostos da invenção um ou mais excipientes, agentes de volume, aglutina.nt.es, gentes de fluxo, agentes de liberação, veicules ou di1uentes farnceuticamente aceítáveis.
Em algumas modalidades, a composição é uma forma de dosagem oral.
Em algumas modalidades, a. forma de dosagem oral é um comprimido,. uma drágea, uma cápsula au uma suspensão líquida.
Em algumas; modalidades, a quantidade do composto é menor do que cerca de ι.ΰΰΟ mg, Em algumas modalidades, a quantidade do composto ê menor do que cerca de 2.000 mg.
Em algumas modalidades, a quantidade do composto é de cerca de 100 mg a cerca de SOO mg. Em algumas modalidades, a quant idade do composto é de cerca de 500 mg a. cerca de 1.600 mg.
Em algumas modalidades, o composto é:
em que R ê -Q-aIquil, aril, heteroari 1, arílalquil ou alquilaril; e R?' é CR -Cl -alquíl, ar.il, aralquil, alquilaril ou alquilheteroaril; n n é de I. a 45.
Em algumas modalidades, a invenção fornece um método de tratamento de um câncer ou uma doença urogenital em um indivíduo que o necessita ou deseja, o método compreendendo a administração ao indivíduo de uma quantidade terapeuticamente eficaz de um composto da invenção.
Em algumas modalidades, o câncer ê um câncer urogenital e/ou relacionado aos androgénios.
Em algumas modalidades, o câncer ou doença urogenital 0 câncer da próstata., câncer- de mama., câncer ovariano, outro câncer urogenital ou hiperplasía da próstata.
Em algumas modal idades., o método ainda compreende a administração ao indivíduo de uma quantidade terapeuticamente eficaz da um ou mais de um antiandrogênio, um inibidor de CY?17, um agonista de hormônio de liberação de hormônio luteinizante, um. fármaco para prevenção da produção de androgen xo., um estrogânio e um fármaco qu imlote r ãpíco,
Em algumas modalidades, a quantidade e menor do que cerca de 1,000 mg. Em algumas modalidades, a quantidade é menor do que cerca de 1.000 mg.
Em algumas modalidades, a quantidade é de cerca de 100 a cerca de 500 mg. Em algumas modalidades, a quantidade é de cerca, de 500 a cerca, de 1.500 mg.
Em algumas modalidades, o composto é-.
em que R á C\-C«~alquil, aril, heteroaril, arilalqu.il ou alquilar.il; e R: é d-CValqull, aril, ara Iqui 1, aIquilaril ou alquilheteroaril; e n ê de 1 a 49,
Em algumas modalidades, a invenção fornece um método de tratamento de um câncer ou uma doença urogenital em um indivíduo que o necessita ou deseja, o método compreendendo a administração ao indivíduo de uma quantidade terapeuticamante eficaz de um composto da invenção, em combinação com uma terapia hormonal, uma quimioterapia, uma radioterapia, uma imunoterapis. ou cirurgia.
Em algumas modalidades, o câncer compreende um câncer urogenital e/ou relacionado aos androgênios.
Em algumas modalidades, o câ.ncer ou doença urogenital é câncer de próstata, câncer de mama, câncer ovariano, outro câncer urogenital ou hiperplasia da próstata.
Em algumas modalidades, a quantidade é menor do que cerca de 1,003 mg. Em algumas modalidades, a quantidade ê menor do que cerca de 2,000 mg.
41/4 9
Em algumas moda1idades, a quantidade é de cerca de 1 a cex'ca de 500 mg. Em algumas modali a quantidade de cerca de 500 a cerca de 1.500 mg.
Em algumas modalidades, c composto é;
ou alquilaril; e R' é C<~Cs~alquil., aril. aralqui alquilaril ou alquiihetercaril; e n é de 1 a 4 9..
EXEMRLOE
Exempla 1
Ester de betaina de ahirat arena
Uma solução de ácido bromoacética (3,0 mmol, 417 mg) em diclorametanc (10 ml 5 é agitada enquanto diciclohexilcarbadiimida (3,0 mmol, 519 mg), dimetilaminopiridina (0,5 mmol, 51 mg), seguidos por uma solução da ahiraterona (2,9 mmol, 1,08 g) em diclorometano (3 ml), são adicionados. A mistura resultante é agitada em temperatura ambienta por quatro horas.. A mistura é filtrada para remover dic.iclohax.il uréia precipitada, e derramada em acetato de etila. As camadas orgânicas são lavadas (HC1 .1
NaHCCu saturado 3%)f secas (salmoura, MgSCg) e concentradas, com purificação por aromatografia em coluna gerando o alfa-halo éster puro.
O bromoéster preparado acima (1,5 mmol, 743 mg) é dissolvido em acetona (10 ml), a trie ti lamina (2,5 mmol, 153 mg, 350 p.l) é adicionada. A mistura é agitada ate que seja demonstrado que o material, esterôide de partida foi exaurido por TLC. A mistura de reação é concentrada in vacuo,, e o resíduo é purificada par HPLC de fase reversa para gerar trietilamõnio acetato de abiraterana ouro.
3 /4 9
Altemativamente, o bromoéster preparado acima (1,8
| mmol, | '-’43 mg) é dissolvido em acetona (10 ml) , a |
| trimeti' | Lamina {2,5 mmol, 14 8 mg, 232 ui) ê adicionada. A |
| mistura | é agitada até que seja demonstrado que o material. |
| de esta | rói de de partida foi exaurido por TLC, e depois |
| concent? | rado in vacuo, e o resíduo é purificado por HPLC de |
fase reversa para gerar trimstilamonio acetato ab i raterena pure.
Exemplo 2
| Ester de caxnifciua de ahlrafcs.rona ô <»< o &w ,AX xz.q W* 1; | » ''^5?si g i | X^ X^ X^ ^z^x^x^ | |
| s solução de R~dimetiImalato (10 mmol, 1,62 g) em | |
| THF (40 | ml) ã resfriada a ~7S°C e agitada enquanto complexo |
| no-dimetilsulfeto (9,5 mmol, 4,75 m.l de uma solução | |
| de 2,0 | ã) em TWF é adicionado. Permite-se que a mistura se |
| aqueça | até a temperatura ambiente e ela ê agitada durante |
aquecimento no refluxo ate que a exaustão do diester de
| par ti da | seja indicada por TbC. A misturai de reação é |
| extinta | por adição lenta de THF-ãgua (itl, 10 ml), e a. |
| mistura | resultante é cuidadosamente derramada em uma. |
| solução | de hidróxido de sódio (5 M, 10 ml), e agitada, de um |
| dia par | a o outro. A mistura de reação é concentrada in |
| vácuo, í | s o resíduo ê recolhido em acetato de atila (50 ml). |
A camada orgânica é lavada (1 N, KC1, NaHCO. aquoso saturado 5%) , seca (salmoura, MgSOU e concentrada .in
| vaouo, | com c· resíduo sendo destilado in vacuo para gerar |
netil R-3 , 4-diidroxibntirato purificado, c-u o resíduo pode tr usado díratamente na etapa seguinte.
Uma solução de metil R-3,4~diídroxibutiraco (6 mmol, 804 mg) em DMF seca. (12 ml) s agitada sc temperatura ambiente enquanto terc-foutildimetilsilil cloreto (13,2 mmol, 996 mg) e imidazol (16 mmol, 545 mg) são adicionados alternativamente em porções. A. mistura resultante ê agitada em temperatura ambiente por três horas, e ê derramada em uma mistura de acetato de etila <100 ml) e água. A fase aguosa é separada e extraída com acetato de etila (50 ml), e os orgânicos combinados são secos (salmoura, MgSCa) .· filtrados e concentrados in vacuo para gerar o bis-sililoxi éster bruto. A. destilação in vacuo iscando um forno de
Kugelrohr gera metil
R3,4cis(terebut iIdimet11s i1iox1) but irato puro.
Q és ter protegido preparado acima (5 mmol..
1,81 g) n iissolvido em THF;água (4·. 1, 20 ml).
hidróxido de lí tio (3.0 mmol, 239 mg) e uma solução de em água í.4 mr.; 1 adicionada. A mistura de reação é. agitada até que o estar esteja exaurido, como indicado por TLC, e derramada em água, antes de o pH ser ajustado até <5 com HC1. A mistura é extraída com acetato de etila (3 x 50 ml) e os orgânicos combinadas são secos (salmoura, MgSCb) e concentrados in vacuo para gerar o ácido bruto, que é purificado por HPLC de fase reversa ou eromatografia em coluna para gerar o ácido R -.3,4 -bis (terc-butíIdimetiisililoxi} butirico ca se j.au,o,.
O ácido protegido é usado na preparação de um pró fãrmaco de abiraterona.
GTs &a solução de ácido R-3,4-bis (terobutildimetiisililoxi)butirico (1,0 mmol, 340 mmol) .. abiraterona. {1..0 mmol, 374 mg; em diclorometano (10 ml} é tratada com EDC-HC.I {1,0 mmol, 192 mg) a I3MAP (0,1 mmol, 12 mg). A mistura resultante e agitada em temperatura ambiente por três horas, e depois derramada em HC1 1. K. A fase aquosa ê separada, lavada com diclorometano (3 x 20 ml), e cs orgânicos combinados são lavados (3 x SO ml de HCI 1 N,
1 x 50 ml de NaHCO;, 5% aquoso) , secos {salmoura, EgSO^S e concentrados, com o resíduo sendo purificado por
| crema | tografia | em coluna ir | istantânea (s | , 111ca, e1u1ção | xlA5, |
| EtÜAc | /hexanos) | para gerar o | bis-dst ar prt | ;tegido dosej ado. | |
| 2 .bis-si | ill éster pr< | o usqxd.o t u, 5 | mmol, 3 58 mgj | é | |
| 25 disso | Lvido em | THE (5 ml) e | de TEAR (1,Q M | em | |
| 1,1 ml) | é adicionada. | A solução | á agitada por 2 | ||
| horas | e é d. | erramada em ã | .gua (10 ml) . | A fase aguosa |
extraída cosí EtOAc (3 x 20 ml) e os orgânicos combinados são secos {salmoura, MgSO<.) e concentrados in vacuo, com ο resíduo sendo purificado por cromatografia em coluna
5 / 4 9 instantânea (silica, eluição de EtOAc/hexanes) para gerar o diidrôxi éster desejada,
Uma solução do R-3, á-diídroxibutiril éster de abiratnrcna (0,5 mmol, 238 mg) em píridina ê tratada com 5 toltienossulfonzl cloreto (0,5 mmol, '22 mg,! e agitada por 24 horas a. 4*0, A mistura é derramada em água gelada (20 ml) e extraída cot diclorometano (3 x 50 ml). Os orgânicos combinados são lavados (3 x KC1. 1 N, 1 x NaHCCt 5%) , secos (salmoura,. MgSO^) e concentrados .in vácuo (<20*O, com o 10 resídua saudo usado dlretamente na etapa seguinte,
O éster de toluenossulfonato bruto da etapa precedente é dissolvido em toluene (50 mlj e agitado, enquanto trimetilamina (0,8 ramal, 4 7 mg, 74 pl) e adicionada, A mistura resultante, é aquecida por três horas, ou até que a 15 exaustão do éster de tol.ue.n,ossulf onato seja indicada par análise por HPLC ou TLC. .5 mistura resultante, ê filtrada e os sólidos lavados cora tolseno, O A--3hid.r6xi4·' trimetilamô.nicbutirato éster de abi rater ona e purificado por maio de HPLC de fase reversa,
2:0. Exemplo 3
Éster d® ácido gálico de sbiraterona.
Uma solução de abíraterona (2 mraal, 747 mg) , ácido
3,4,5- tris [ (terc-butil-dimetilsilil) oxij hensõico (2 mmol,
1,026’ g) e 4-dimetilarainopiridina (1,0 mmol, 122 mg) era diclorometano (10 ml'> é. acitada encuanto dicialemexilcuarbcxiiimida. (2..0 mmol, 412 mg) ê. adicionada. A suspensão resultante é agitada por três horas., o depois filtrada para remover diciclohexiluréia precipitada. O filtrado ê lavado com KC1 1 K (2 x 50 ml) , e as camadas de 5 ácido são extraídas com diclorometano (1 x 100 ml? . Os orgânicos combinados são secos (salmoura, I4g$O.j e concentrados in vacuo para geras um sólido. O sólido é purificado per cromatografia em coluna instantânea (silica gel , CHCl3~MeOK) para gerar o tris-silil és ter protegido lü puro.
O éster preparado acima é dissolvido em THF (8 ml) e TB.eP é adicionado como uma solução em THE (1 M, 8 ml, 6 mmol) .. e a solução resultante é agitada por duas horas em temperatura ambiente. A mistura e derramada ao cloreto de 15 ?sódio aquoso saturado pala. metade e extraída com diclorometano (2 x 100 ml; . Os orgânicos combinados são lavados (1 x HC1 1 Η, 1 x água) , secos (salmoura, MgSO.;} e concentrados in vacuo para, gerar o éster gãlico bruto,, que é purificado por cromatografia em coluna instantânea 20 (silica gel, CHCl^MeOH) para gerar o material puro desejado.
Exemplo 4 tster de ácido fosfonoacético de abiraterona.
Uma mistura de ácido fosfonoacético (2 mmol, 200 mg}.
abiraterona (^46 mg, 2 mmol) e 4-dimetilaminopiridina (2,5 eq, 305 mg} em diclorometano (15 ml’} ê agitada enquanto EDC-HC1 (384 mg, 2,0 mmol) e adicionado. A mistura resultante ê agitada por oito horas em temperatura ambiente. A mistura é derramada em HC1 1 N (100 ml) e e extraída com diclorometano (2 x 100 ml). As camadas orgânicas são combinadas, secas (salmoura, ?4gSCq) e concentradas. Q residua é purificado por HPLC de fase reversa para gerar o. éster de ácido fosfonoacético de abiraterona desejado.
Exemplo 5
Ester de ácido gálioo do Composto 5
| Uma solução do Composto 5 (2 mmol, 77'? mo) , | ácido |
| 3,4,5-tris((terc-butil-dimet ilsilí1}oxi]benzóico (2 | mmol, |
1,025 g) . 4 dime t i 1 aminopir ídina (1,0 mmol, 122 mg ) em diclorometano (10 ml) ê agitada enquanto diciclahexilcarbodiimida (2,0 mmol, 412 mg) é adicionada> A suspensão resultante é agitada por três .horas, e depois filtrada, para remover diciclohexiluréia precipitada. O filtrado é lavado oom HC1 1 N (2 x SO ml) , e as camadas de ácido são extraídas com diclorometano (1 x 100 ml) . Os orgânicos combinados são secos (salmoura, MgSOJ e concentrados in vacuo para gerar um sólido. 0 sólido é purificado por crornatografia em coluna instantânea (silica gel, CHC1S-MeOM) para gerar o tris-silil êster protegido puro, o éster preparado acima e dissolvido em ΤΗΈ* (8 ml} e TBAF é adicionado como uma solução em THE ί 1 M, 6 ml, 6 mmol), e a solução resultante ê agitada por duas horas em temperatura ambiexxte. A mistura é derramada em cloreto de sódio aquosa saturado pela metade e extraída com d.iclorcmetano (2 x 100 ml) . Os orgânicos combinados são lavados (1 x. HC1 1 N, 1 x ãgua) , secos (salmoura, MgSO*) e concentradas in vacuo para obter o éster gâlico bruto, que s purificado por cromatografia em coluna instantânea {silica gel, CHdj-MeOH) para gerar o material pu.ro üesej ado.
Exemplo 6
Ester de ácido fosfonoacético do Composto 5
Uma mistura de ácida fosfonaacético (2 mmol, 2 80 mg) , Composto 5 {76 mg,. 2 mmol) e 4-dimatilamínupirídi.na (2,S eq, 305 mg) e.m d.iclorametana (15 ml} é agitada enquanto EDC-HCl {384 mg_, .2,0 mmol) é adicionado, A mistura resultante é agitada por oito horas e® temperatura ambiente. A mistura e derramada em HC1 I N (100 ml) e é extraída cam diclorometana (2 x 100 ml), As camadas orgânicas são combinadas, secas (salmoura, MgSOJ e concentradas. O resíduo â purificado por HPLC de fase reversa, para gerar o éster de ácida fosfanoacética do
Composto 5 deseiado.
Claims (2)
1.500 mg.
15 . Composi ção farmacêutica.
acordo com reivindicação 10, caracterisada pelo fato de que o composto e: ...................
ou alquílaril; e R* é h, C5.-Cs alquil, aril, aralquil, aigu3.axi 1 ou aiquxliietexoarxi; e n e de 1 a 49.
16 < Método de tratamento de um câncex ou uma doença urogenital em usi indivíduo que o necessita ou deseja, o método caracterizado por compreender a administração ao indivíduo de uma quantidade terapeuticamente eficaz de um Composto, da reivindicação 1.
17, Método, de acordo com a xe.lv indicação 1.6, caracterizado pelo fato de que o câncer é um câncer urogenital e/ou x'elacionado aos androgênios >
18, Método, de acordo com a reivindicação 16, caracterizado pelo fato de que o câncer ou doença
caracterizado ainda por compreender a administração ao indivíduo de. uma quantidade, terapeuticamente eficaz de um ou mais de um antiandrogênio, um inibidor de CYP17, um r
agonists do hormônio de liberação de hormônio luteinisante, um filrmauo para prevenção da produção de androgenic, um estrogênío e um fármaco quimioterâpico,
20. Método, acordo com a reivindicação
16, fate de que a quantidade e manor do qua cerca de 2.000 mg.
Fé todo, da acordo com a reivindicação
16, oaracterizadc pelo fa to de que a quantidade é de cerca da
EGO a eerca da 1,500 me;.
12. Fãtodo, de acordo com reivindicação 16, caracterizadc pelo fa to de que o composto e:
em que R é C?.-C^-alquil, aril , heteroaril, ou alquílaril; e M é H( Cj-Cs-alquil, aril, era iquil.
alquil.aril ou alquilheteroaril; e n é de 1 a 49.
20. Método da tratamento de um câncer ou uma doença.
urogenital em um indivíduo que o necessita era deseja, método caracterizado por compreender a administração so indivíduo de uma quantidade terapeuticamente of loas de uni r
Composto, da reivindicação 1, em combinação com uma terapia hormonal, uma quimioterapia, uma radioterapia, uma imunaterapia ou cirurgia.
24. Método, de acordo oom a reivindicação 23,
5 caracterizado pelo fato de que o câncer compreende um câncer urogenital e/ou relacionado aos androgénios.
25. Método, de acorda com a reivindicação 23, caracterizada pelo fato de que o câncer au doença, urogenital ê câncer de próstata, câncer de mama, câncer
10 ovariano, outra câncer urogenital, ou hiperplasia da próstata..
26. Método, de acorda com a reivindicação 23, c ara o t e r i z ado pelo fato de que a quantidade é menor do que cerca de 2.000 mg.
15 27. Método, de acordo com. a reivindicação 23, paio fato de que a quant idade é de cerca de 300 a osrca de I..500 mg.
1 é um grupo com carga que está carregado sob condições fisiológicas normais, em que o grupo com carga a um grupo de amônio quaternário da fórmula {R;N:5'( em que ô cada grupo R é independentemente Ci-Ο?-alquil ramificado, Ci~C>-alqull de cadela linear, aril, alquilaril, aralquíl, heteroaríl, ou dois ou mais grupos R em conjunto formam um anel; um ácido sulfônico; um ácido fosfônico; um flucraicanal; ou um grupa hidrcxil ácido, < ou um sal farmaceuticamente aceitável destes.
2. Composta, de acordo oom a reivindicação 1, caractari zado pelo fato de que X ê opcionalmente substituído com um ou mais de halogênio, amino, ami noa Iqui 1 ano, h idrôxi, EK, S - C; ·· Ce - al qu i 1, C;i - C,; - alqui 1 0 e C:i Ce-alquil ha lege nado.
3 fã
3. Composto, de acordo coo a reivindicação 2, caracterizado pelo fato de que os grupos pis'idi na, pirazína, pirimidina. piridazína, benzimidazol, benzotriazol, pirimidinoímidazol e pirimidínotriazol são., respectivamente:
em que cada * indica ura ponto de adesão à posição C17,
4. Composto, de acordo com a reivindicação 3, caracterizado pelo fato de que a estrutura do anel ABC e opcionalmente substituída cora ura ou mais de Cj-Cg-alquil, Ct - Ug ~ axgnxl harog enado, cc C§ ··· alquem.1, Cx ·· Cg a Áqueta r ha logenado, ha 1 ogãnio. arai no, arainoal qui leno, h idrox i irai no e hidrox.il.
5. Composto., de acordo com a reivindicação 4. cara c te rí z ado pelo fato de que 2 ê um grupo de amônio quaternário,- em que o grupo de amônío quaternário ê tríraeti.l amdnio, tríetil araônio, trifeníl amônio, benziidimetil araônio, benzildietil amônio, smetilpiperidínio, ?í~etilpiperidí.nio ou tribenzil amônío>
6, Composto, de acordo cora a reivindicação4, caracterizado pelo fato de que 2 é utn ácido sul fônico eI, é
Ci-Q-alquil,
7, Composto, de acordo com a. reivindicaçãoí,
ou
R:· é H, Cj.-Cs -alquil, aril, aralquil, alquilaxil au alquilheteroaril; e n é de I a 4Sb
10, Composição farmacêutica ££baoterirada compreender uma quantidade terapeuticamente eficaz de um ou mais compostas da reivindicação 1 e um on raai s axe ip .1 a n t e s , agentes de volume, aglutinant.es, agentes de liberação. veiculas ou diluent.es aceitáveis.
11. Composição farmacêutica, de reivindicação 10, caracterizada de fluxo, agentes
f. a rma c e u t i c a m s n t e a eordo fato de qua composição ê uma forma de dosagem oral.
12. Composição farmacêutica, de acordo com reivindicação 11 caracterizada pelo fato de que a .forma de dosagem oral é um comprimido, uma drágea ou uma cápsula.
13. Composição farmacêutica,. de acordo com
10, caracterizada pelo fato de que quantidade do composto ê menor do que cerca de 2.000 mg .1.4. Composição farmacêutica.. de. acorda com reivindi cação
10.. ££Y.^.Çf£ti.saâa pelo fato de que quant idade da composto é de cerca de 500 mg a cerca de
1. Composto caracterizado pode ter a Fórmula
em que:
a estrutura do anel ABC é opcionalmente substituída independentemente em cada posição e em que substítuintes de hidrogênio em átomos de carbono adjacentes da estrutura do anel ABC são opcionalmente removidos e substituídos por uma ligação-pi entre .os átomos de carbono adjacentes;
¥ ê 2-L-C(»O)O-; e além disso,
X ã um heterociclo opcionalmente substituído que é um grupo piridina., pirazina, pirimidina, piridazina, bentimidazol, benzotriazols pirim.idin.oimidazcl ou pirimidinotriasol, em que o grupo benzimidazol, benzotriazol, pírimidínoimídazol ou pirimidinotriazol está ligado à posição Cl'? por meio de um átomo de nitrogênio em um anel de 5 membros do heterociclo, e o grupo piridina. pirazina, pirimidina ou piridazina esta ligado à posição Cl7 por meio de um átomo de carbono do heterociclo;
L é C.\~C;:S-alquil, flúorCg-a.1 quil, aril, aril&Iqull, alquilaril, alcoxialquil, po.l.ialccxia.lquil ou heteroaríl. qualquer um deles sendo opcionalmente cíclico, ou, junto com Z, forma um anel, em que L é opcionalmente substituído can um ou mais da alquil, arilalqui .1, a Iquil ar .11 , alquí lhe teroari .1, ha logênio, hi dr ox il, a loóxi a mercapt-ano,* e
2 é um grupo com carga que está, carregado sob
5 condições fisiológicas normals, em que o grupo com carga é um ácido sulfônloo.; um ácido fosfônlco; um fluoraloanol; on um grupo hidróxi1 ácido, ou
X é um qruoo oiridina opcionalmente substituído;
0 L t C:.-Cis-alguil, f lúo r-C2-Ce-al quil, axil, arilalquil, alquilaríl, alcoxialquil, polialcoxialqui1 ou heteroaril, qualquer um deles sendo opcionalmente cíclico, ou, junto com 2, forma um anel, em que L é opcionalmente substituído com um ou mais de alquil, arilalquil,
5 alquilaril, alquilheteroarí1, halogênio, hidróxi 1, aleóxi, alquilamino e mercaptans·; e
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15003109P | 2009-02-05 | 2009-02-05 | |
| PCT/US2010/023391 WO2010091306A1 (en) | 2009-02-05 | 2010-02-05 | Novel prodrugs of steroidal cyp17 inhibitors/antiandrogens |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| BRPI1008745A2 true BRPI1008745A2 (pt) | 2019-09-17 |
Family
ID=42115803
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI1008745A BRPI1008745A2 (pt) | 2009-02-05 | 2010-02-05 | pró-fármacos de inibidores esteroidais de cyp17/antiandrogênios |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US20110312916A1 (pt) |
| EP (2) | EP2393827B1 (pt) |
| JP (2) | JP2012516900A (pt) |
| CN (1) | CN102686600A (pt) |
| AU (1) | AU2010210422A1 (pt) |
| BR (1) | BRPI1008745A2 (pt) |
| CA (1) | CA2761389A1 (pt) |
| ES (1) | ES2552087T3 (pt) |
| WO (1) | WO2010091306A1 (pt) |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100047338A1 (en) | 2008-03-14 | 2010-02-25 | Angela Brodie | Novel C-17-Heteroaryl Steroidal CYP17 Inhibitors/Antiandrogens, In Vitro Biological Activities, Pharmacokinetics and Antitumor Activity |
| US8785423B2 (en) * | 2008-04-14 | 2014-07-22 | University Of Maryland, Baltimore | Compositions and methods of inducing endoplasmic reticulum stress response for the treatment of cell proliferative diseases |
| AU2010210422A1 (en) | 2009-02-05 | 2011-08-18 | Tokai Pharmaceuticals, Inc. | Novel prodrugs of steroidal CYP17 inhibitors/antiandrogens |
| JP2014523445A (ja) * | 2011-07-18 | 2014-09-11 | トーカイ ファーマシューティカルズ,インク. | 前立腺癌を処置するための新規な組成物及び方法 |
| DE102011083725A1 (de) | 2011-09-29 | 2013-04-04 | Bayer Pharma AG | Estra-1,3,5(10),16-tetraen-3-carboxamid-Derivate, Verfahren zu ihrer Herstellung, pharmazeutische Präparate die diese enthalten, sowie deren Verwendung zur Herstellung von Arzneimitteln |
| CA2856646C (en) * | 2011-11-30 | 2020-01-14 | Astrazeneca Ab | Combination treatment of cancer |
| US20150005265A1 (en) * | 2011-12-22 | 2015-01-01 | Susan Stewart | Methods and compositions for combination therapy using p13k/mtor inhibitores |
| EP2938625B1 (en) | 2012-12-31 | 2018-02-21 | Hetero Research Foundation | Process for the preparation of abiraterone acetate |
| CA2898573A1 (en) * | 2013-01-18 | 2014-07-24 | Cortendo Ab (Publ) | Abiraterone and analogs thereof for the treatment of diseases associated with cortisol overproduction |
| MA38349A1 (fr) | 2013-02-21 | 2017-02-28 | Bayer Pharma AG | Œstra-1,3,5(10),16-tétraéno-3-carboxamide pour inhiber la 17-bêta-hydroxystéroïde déshydrogénase (akr1c3) |
| KR20150127720A (ko) | 2013-03-14 | 2015-11-17 | 유니버시티 오브 매릴랜드, 발티모어 | 안드로겐 수용체 하향 조절제 및 그의 용도 |
| EP2991644B1 (en) | 2013-04-04 | 2020-03-25 | University of Maryland, Baltimore | Nonsteroidal and steroidal compounds with potent androgen receptor down-regulation and anti prostate cancer activity |
| WO2015023710A1 (en) | 2013-08-12 | 2015-02-19 | Tokai Pharmaceuticals, Inc. | Biomarkers for treatment of neoplastic disorders using androgen-targeted therapies |
| CN104017045B (zh) * | 2014-06-23 | 2016-01-13 | 广州艾格生物科技有限公司 | 甾体cyp17抑制剂的新型药物前体及其应用、制备方法 |
| CN105646637B (zh) * | 2014-11-28 | 2018-12-14 | 四川海思科制药有限公司 | 一种阿比特龙衍生物及其制备方法和医药用途 |
| CN107188922B (zh) * | 2016-03-14 | 2019-12-20 | 四川海思科制药有限公司 | 一种阿比特龙衍生物的盐及其制备方法和医药用途 |
| CN107188921A (zh) * | 2016-03-15 | 2017-09-22 | 四川海思科制药有限公司 | 阿比特龙衍生物的制备方法及其新固态形式和用途 |
| CN107365343A (zh) * | 2016-05-12 | 2017-11-21 | 四川海思科制药有限公司 | 一种苯并咪唑雄甾衍生物及其制备方法和医药用途 |
| WO2017208132A1 (en) * | 2016-06-01 | 2017-12-07 | Industriale Chimica S.R.L. | Process for the preparation of galeterone |
| ITUA20164043A1 (it) * | 2016-06-01 | 2017-12-01 | Ind Chimica Srl | Processo per la preparazione di 3β-idrossi-17-(1H-benzimidazol-1-il)androsta-5,16-diene |
| CN106220705A (zh) * | 2016-07-25 | 2016-12-14 | 厦门市瑞思医药科技有限公司 | 一种2’‑(n,n,n‑三甲基氯化铵基)乙酸阿比特龙酯的合成方法 |
| CN109846826A (zh) * | 2019-01-25 | 2019-06-07 | 湖南华腾制药有限公司 | 醋酸阿比特龙柔性脂质体及其制备方法 |
| CN114026106B (zh) | 2019-03-06 | 2025-01-21 | 普洛拉治疗公司 | 阿比特龙前药 |
| WO2021100019A1 (en) | 2019-11-22 | 2021-05-27 | Suven Life Sciences Limited | Prodrugs of abiraterone |
| WO2022122042A1 (zh) * | 2020-12-12 | 2022-06-16 | 上海喀露蓝科技有限公司 | 阿比特龙衍生物及其制备方法 |
| WO2022174134A1 (en) | 2021-02-15 | 2022-08-18 | Propella Therapeutics, Inc. | Abiraterone prodrugs |
| CN116917009A (zh) | 2021-02-19 | 2023-10-20 | 美国迈胜医疗系统有限公司 | 用于粒子治疗系统的机架 |
| CN113061154B (zh) * | 2021-03-25 | 2022-07-08 | 天津海润家和创新医药研究有限责任公司 | 新型注射用阿比特龙衍生物的制备方法和用途 |
Family Cites Families (183)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2664423A (en) | 1952-03-12 | 1953-12-29 | Searle & Co | 4-(cyclopentanopolyhydrophenanthr-17-yl) imidazoles and derivatives thereof |
| US3060174A (en) * | 1960-01-14 | 1962-10-23 | Ciba Geigy Corp | Esters of the androstane series and process for their manufacture |
| GB972672A (en) * | 1960-01-14 | 1964-10-14 | Ciba Ltd | Pharmaceutical preparations containing compounds of the androstane series |
| US3313809A (en) | 1965-03-05 | 1967-04-11 | Sterling Drug Inc | Steroido[21, 20-d]isoxazoles |
| US3317520A (en) | 1965-03-05 | 1967-05-02 | Sterling Drug Inc | Steroido[20, 21-c]pyrazoles and intermediates |
| DE1493169A1 (de) * | 1965-09-03 | 1969-06-04 | Schering Ag | Verfahren zur Herstellung von 5 beta-Bisnorcholanderivaten |
| US3480621A (en) | 1967-01-17 | 1969-11-25 | Phytogen Prod Inc | Steroid ketal |
| CH621803A5 (pt) | 1974-08-08 | 1981-02-27 | Siphar Sa | |
| JPS563000Y2 (pt) | 1976-07-27 | 1981-01-23 | ||
| JPS563000A (en) * | 1979-06-20 | 1981-01-13 | Green Cross Corp:The | Water-soluble cholesterol derivative |
| US4316885A (en) | 1980-08-25 | 1982-02-23 | Ayerst, Mckenna And Harrison, Inc. | Acyl derivatives of rapamycin |
| US4469689A (en) * | 1983-03-30 | 1984-09-04 | The Upjohn Company | Sulfonate containing ester prodrugs of corticosteroids |
| US4650803A (en) | 1985-12-06 | 1987-03-17 | University Of Kansas | Prodrugs of rapamycin |
| US5232917A (en) | 1987-08-25 | 1993-08-03 | University Of Southern California | Methods, compositions, and compounds for allosteric modulation of the GABA receptor by members of the androstane and pregnane series |
| IT1216687B (it) | 1988-04-01 | 1990-03-08 | Boehringer Biochemia Srl | Complessi di platino (ii), loro preparazione e impiego come antitumorali. |
| US5028726A (en) | 1990-02-07 | 1991-07-02 | The University Of Vermont And State Agricultural College | Platinum amine sulfoxide complexes |
| US5683867A (en) | 1990-06-11 | 1997-11-04 | Nexstar Pharmaceuticals, Inc. | Systematic evolution of ligands by exponential enrichment: blended SELEX |
| US5637459A (en) | 1990-06-11 | 1997-06-10 | Nexstar Pharmaceuticals, Inc. | Systematic evolution of ligands by exponential enrichment: chimeric selex |
| US6011020A (en) | 1990-06-11 | 2000-01-04 | Nexstar Pharmaceuticals, Inc. | Nucleic acid ligand complexes |
| US5707796A (en) | 1990-06-11 | 1998-01-13 | Nexstar Pharmaceuticals, Inc. | Method for selecting nucleic acids on the basis of structure |
| US5496938A (en) | 1990-06-11 | 1996-03-05 | Nexstar Pharmaceuticals, Inc. | Nucleic acid ligands to HIV-RT and HIV-1 rev |
| US5660985A (en) | 1990-06-11 | 1997-08-26 | Nexstar Pharmaceuticals, Inc. | High affinity nucleic acid ligands containing modified nucleotides |
| US5567588A (en) | 1990-06-11 | 1996-10-22 | University Research Corporation | Systematic evolution of ligands by exponential enrichment: Solution SELEX |
| CA2084987C (en) | 1990-06-11 | 2007-02-13 | Gilead Sciences, Inc. | Nucleic acid ligands |
| US5270163A (en) | 1990-06-11 | 1993-12-14 | University Research Corporation | Methods for identifying nucleic acid ligands |
| US5300294A (en) | 1990-06-27 | 1994-04-05 | Smithkline Beecham Corporation | Method of treating prostatic adenocarcinoma |
| US5385936A (en) | 1990-07-12 | 1995-01-31 | The United States Of America As Represented By The Secretary Of The Department Of The Health And Human Services | Gossypol acetic acid for the treatment of cancer |
| US5023264A (en) | 1990-07-16 | 1991-06-11 | American Home Products Corporation | Rapamycin oximes |
| NZ239142A (en) | 1990-08-01 | 1994-05-26 | Merrell Dow Pharma | 4-amino-delta-4-steroids; preparatory processes and pharmaceutical compositions |
| US5023263A (en) | 1990-08-09 | 1991-06-11 | American Home Products Corporation | 42-oxorapamycin |
| US5221670A (en) | 1990-09-19 | 1993-06-22 | American Home Products Corporation | Rapamycin esters |
| PT98990A (pt) | 1990-09-19 | 1992-08-31 | American Home Prod | Processo para a preparacao de esteres de acidos carboxilicos de rapamicina |
| US5233036A (en) | 1990-10-16 | 1993-08-03 | American Home Products Corporation | Rapamycin alkoxyesters |
| US5120842A (en) | 1991-04-01 | 1992-06-09 | American Home Products Corporation | Silyl ethers of rapamycin |
| US5100883A (en) | 1991-04-08 | 1992-03-31 | American Home Products Corporation | Fluorinated esters of rapamycin |
| EP0580860B2 (en) | 1991-04-16 | 2004-12-15 | Nippon Shinyaku Company, Limited | Method of manufacturing solid dispersion |
| US5118678A (en) | 1991-04-17 | 1992-06-02 | American Home Products Corporation | Carbamates of rapamycin |
| US5118677A (en) | 1991-05-20 | 1992-06-02 | American Home Products Corporation | Amide esters of rapamycin |
| US5162333A (en) | 1991-09-11 | 1992-11-10 | American Home Products Corporation | Aminodiesters of rapamycin |
| US5151413A (en) | 1991-11-06 | 1992-09-29 | American Home Products Corporation | Rapamycin acetals as immunosuppressant and antifungal agents |
| GB9125660D0 (en) | 1991-12-03 | 1992-01-29 | Smithkline Beecham Plc | Novel compound |
| US5264427A (en) | 1992-01-29 | 1993-11-23 | Research Corporation Technologies, Inc. | 20-substituted pregnene derivatives and their use as androgen synthesis inhibitors |
| US5177203A (en) | 1992-03-05 | 1993-01-05 | American Home Products Corporation | Rapamycin 42-sulfonates and 42-(N-carboalkoxy) sulfamates useful as immunosuppressive agents |
| CZ287434B6 (en) | 1992-03-31 | 2000-11-15 | British Tech Group | Use of steroids, substituted in position 17, steroids functioning as carcinostatics and pharmaceutical preparation containing thereof |
| US5604213A (en) | 1992-03-31 | 1997-02-18 | British Technology Group Limited | 17-substituted steroids useful in cancer treatment |
| US5237064A (en) | 1992-05-20 | 1993-08-17 | Merck & Co., Inc. | Process for producing 7β-substituted-aza-5αandrostan-3-ones |
| US5620986A (en) | 1992-05-20 | 1997-04-15 | Merck & Co., Inc. | 17 urea, thiourea, thiocarbamyl and carbamyl4-azasteroid 5-reductase inhibitors useful in the prevention and treatment of hyperandrogenic disorders |
| ZA935112B (en) | 1992-07-17 | 1994-02-08 | Smithkline Beecham Corp | Rapamycin derivatives |
| ZA935111B (en) | 1992-07-17 | 1994-02-04 | Smithkline Beecham Corp | Rapamycin derivatives |
| US5256790A (en) | 1992-08-13 | 1993-10-26 | American Home Products Corporation | 27-hydroxyrapamycin and derivatives thereof |
| DE4232681C2 (de) | 1992-09-29 | 1994-11-24 | Sigma Tau Ind Farmaceuti | 17-Phenyl- und 17-Furyl-14beta,5alpha-androstan- und androsten- Derivate, Verfahren zu deren Herstellung und diese enthaltende pharmazeutische Zusammensetzung |
| GB9221220D0 (en) | 1992-10-09 | 1992-11-25 | Sandoz Ag | Organic componds |
| US5489680A (en) | 1992-10-13 | 1996-02-06 | American Home Products Corporation | Carbamates of rapamycin |
| US5480988A (en) | 1992-10-13 | 1996-01-02 | American Home Products Corporation | Carbamates of rapamycin |
| US5411967A (en) | 1992-10-13 | 1995-05-02 | American Home Products Corporation | Carbamates of rapamycin |
| US5434260A (en) | 1992-10-13 | 1995-07-18 | American Home Products Corporation | Carbamates of rapamycin |
| US5302584A (en) | 1992-10-13 | 1994-04-12 | American Home Products Corporation | Carbamates of rapamycin |
| US5480989A (en) | 1992-10-13 | 1996-01-02 | American Home Products Corporation | Carbamates of rapamycin |
| US5262423A (en) | 1992-10-29 | 1993-11-16 | American Home Products Corporation | Rapamycin arylcarbonyl and alkoxycarbonyl carbamates as immunosuppressive and antifungal agents |
| US5258389A (en) | 1992-11-09 | 1993-11-02 | Merck & Co., Inc. | O-aryl, O-alkyl, O-alkenyl and O-alkynylrapamycin derivatives |
| US5260300A (en) | 1992-11-19 | 1993-11-09 | American Home Products Corporation | Rapamycin carbonate esters as immuno-suppressant agents |
| US5504091A (en) | 1993-04-23 | 1996-04-02 | American Home Products Corporation | Biotin esters of rapamycin |
| US5665553A (en) | 1993-04-30 | 1997-09-09 | Pacific Northwest Research Foundation | Methods for determining and modulating cellular redox potential and genotoxic states |
| US5373014A (en) | 1993-10-08 | 1994-12-13 | American Home Products Corporation | Rapamycin oximes |
| US5378836A (en) | 1993-10-08 | 1995-01-03 | American Home Products Corporation | Rapamycin oximes and hydrazones |
| US5391730A (en) | 1993-10-08 | 1995-02-21 | American Home Products Corporation | Phosphorylcarbamates of rapamycin and oxime derivatives thereof |
| EP0729471A1 (en) | 1993-11-19 | 1996-09-04 | Abbott Laboratories | Semisynthetic analogs of rapamycin (macrolides) being immunomodulators |
| US5385909A (en) | 1993-11-22 | 1995-01-31 | American Home Products Corporation | Heterocyclic esters of rapamycin |
| US5385910A (en) | 1993-11-22 | 1995-01-31 | American Home Products Corporation | Gem-distributed esters of rapamycin |
| US5385908A (en) | 1993-11-22 | 1995-01-31 | American Home Products Corporation | Hindered esters of rapamycin |
| NZ277498A (en) | 1993-12-17 | 1998-03-25 | Novartis Ag | Rapamycin derivatives |
| US5637310A (en) | 1993-12-20 | 1997-06-10 | Smithkline Beecham Corporation | Method of treating prostatic adenocarcinoma |
| US5389639A (en) | 1993-12-29 | 1995-02-14 | American Home Products Company | Amino alkanoic esters of rapamycin |
| TW385308B (en) | 1994-03-04 | 2000-03-21 | Merck & Co Inc | Prodrugs of morpholine tachykinin receptor antagonists |
| US5362718A (en) | 1994-04-18 | 1994-11-08 | American Home Products Corporation | Rapamycin hydroxyesters |
| US5463048A (en) | 1994-06-14 | 1995-10-31 | American Home Products Corporation | Rapamycin amidino carbamates |
| US5491231A (en) | 1994-11-28 | 1996-02-13 | American Home Products Corporation | Hindered N-oxide esters of rapamycin |
| US5563145A (en) | 1994-12-07 | 1996-10-08 | American Home Products Corporation | Rapamycin 42-oximes and hydroxylamines |
| KR100400620B1 (ko) | 1995-06-09 | 2004-02-18 | 노파르티스 아게 | 라파마이신유도체 |
| WO1997014418A1 (en) | 1995-10-19 | 1997-04-24 | Merck & Co., Inc. | 16-substituted-6-aza-steroid 5-alpha-reductase inhibitors |
| US5780462A (en) | 1995-12-27 | 1998-07-14 | American Home Products Corporation | Water soluble rapamycin esters |
| US6258823B1 (en) | 1996-07-12 | 2001-07-10 | Ariad Pharmaceuticals, Inc. | Materials and method for treating or preventing pathogenic fungal infection |
| US6368598B1 (en) | 1996-09-16 | 2002-04-09 | Jcrt Radiation Oncology Support Services, Inc. | Drug complex for treatment of metastatic prostate cancer |
| US5994334A (en) | 1997-02-05 | 1999-11-30 | University Of Maryland | Androgen synthesis inhibitors |
| DE69837903T2 (de) | 1997-08-11 | 2008-02-14 | Pfizer Products Inc., Groton | Feste pharmazeutische Dispersionen mit erhöhter Bioverfügbarkeit |
| US5994335A (en) | 1997-10-17 | 1999-11-30 | The University Of Maryland, Baltimore | 17-azolyl steroids useful as androgen synthesis inhibitors |
| US20030059471A1 (en) | 1997-12-15 | 2003-03-27 | Compton Bruce Jon | Oral delivery formulation |
| WO1999052931A1 (fr) | 1998-04-10 | 1999-10-21 | Mitsubishi Chemical Corporation | Dispersion solide contenant un derive d'acide sialique |
| US6465445B1 (en) | 1998-06-11 | 2002-10-15 | Endorecherche, Inc. | Medical uses of a selective estrogen receptor modulator in combination with sex steroid precursors |
| EP1027885B1 (en) | 1999-02-09 | 2008-07-09 | Pfizer Products Inc. | Basic drug compositions with enhanced bioavailability |
| ES2219388T3 (es) | 1999-08-24 | 2004-12-01 | Ariad Gene Therapeutics, Inc. | 28-epi-rapalogos. |
| ES2299434T3 (es) | 1999-09-17 | 2008-06-01 | ABBOTT GMBH & CO. KG | Inhibidores de kinasa utilizados como agentes terapeuticos. |
| CA2669753C (en) | 1999-09-30 | 2012-06-26 | Hollis-Eden Pharmaceuticals, Inc. | Therapeutic treatment of androgen receptor driven conditions |
| BR0016555A (pt) | 1999-12-23 | 2002-09-17 | Pfizer Prod Inc | Composições farmacêuticas que proporcionam concentrações acrescidas de droga |
| UA80393C2 (uk) | 2000-12-07 | 2007-09-25 | Алтана Фарма Аг | Фармацевтична композиція, яка містить інгібітор фде 4, диспергований в матриці |
| US6960584B2 (en) | 2001-04-10 | 2005-11-01 | Merck & Co., Inc. | Inhibitors of Akt activity |
| WO2002083139A1 (en) | 2001-04-10 | 2002-10-24 | Merck & Co., Inc. | Inhibitors of akt activity |
| EP1269994A3 (en) | 2001-06-22 | 2003-02-12 | Pfizer Products Inc. | Pharmaceutical compositions comprising drug and concentration-enhancing polymers |
| US20030054053A1 (en) | 2001-09-20 | 2003-03-20 | Charles Young | Methods and compositions for inhibiting the proliferation of prostate cancer cells |
| CA2463505C (en) | 2001-10-12 | 2011-07-12 | Johns Hopkins University | Low-calcemic oxime analogs of 1.alpha.,25-dihydroxy vitamin d3 |
| SE0103424D0 (sv) | 2001-10-15 | 2001-10-15 | Astrazeneca Ab | Pharmaceutical formulation |
| US20070015713A1 (en) | 2005-07-14 | 2007-01-18 | Voyager Pharmaceutical Corporation | Methods for treating prostate cancer |
| MXPA04007433A (es) | 2002-02-01 | 2004-10-11 | Pfizer Prod Inc | Procedimiento para preparar dispersiones solidas amorfas homogeneas de farmaco secadas por pulverizacion utilizando un dispositivo de secado por pulverizacion modificado. |
| PL371593A1 (en) | 2002-02-01 | 2005-06-27 | Pfizer Products Inc. | Method for making homogeneous spray-dried solid amorphous drug dispersions using pressure nozzles |
| CA2480800C (en) | 2002-04-08 | 2008-09-23 | Mark T. Bilodeau | Inhibitors of akt activity |
| EP1496906A4 (en) | 2002-04-08 | 2006-05-03 | Merck & Co Inc | HEMMER OF ACT ACTIVITY |
| AU2003249474A1 (en) | 2002-08-12 | 2004-02-25 | Pfizer Products Inc. | Pharmaceutical compositions of semi-ordered drugs and polymers |
| AU2003270087B2 (en) | 2002-09-03 | 2009-04-23 | Georgetown University | Akt inhibitors, pharmaceutical compositions, and uses thereof |
| US6933312B2 (en) | 2002-10-07 | 2005-08-23 | Agouron Pharmaceuticals, Inc. | Pyrazole derivatives |
| CA2501365C (en) | 2002-10-30 | 2011-05-31 | Merck & Co., Inc. | Inhibitors of akt activity |
| TW200500360A (en) | 2003-03-01 | 2005-01-01 | Astrazeneca Ab | Hydroxymethyl compounds |
| AU2004233828B2 (en) | 2003-04-24 | 2009-05-28 | Merck Sharp & Dohme Corp. | Inhibitors of Akt activity |
| CN1809351A (zh) | 2003-04-24 | 2006-07-26 | 麦克公司 | Akt活性抑制剂 |
| ATE446752T1 (de) | 2003-04-24 | 2009-11-15 | Merck & Co Inc | Hemmer der akt aktivität |
| JP4673300B2 (ja) | 2003-04-24 | 2011-04-20 | メルク・シャープ・エンド・ドーム・コーポレイション | Akt活性の阻害剤 |
| US7439268B2 (en) * | 2003-07-18 | 2008-10-21 | Idexx Laboratories | Compositions containing prodrugs of florfenicol and methods of use |
| PL1660115T3 (pl) | 2003-07-29 | 2011-11-30 | Dompe Spa | Farmaceutyczna kombinacja G-CSF i PLGF użyteczna wobec komórek macierzystych krwi |
| WO2005018562A2 (en) | 2003-08-22 | 2005-03-03 | University Of Virginia Patent Foundation | Blockade of mtor to prevent a hormonal adaptive response |
| US7605120B2 (en) | 2003-10-22 | 2009-10-20 | Amgen Inc. | Antagonists of the brandykinin B1 receptor |
| CA2546192C (en) | 2003-11-17 | 2010-04-06 | Pfizer Products Inc. | Pyrrolopyrimidine compounds useful in treatment of cancer |
| EP1720855A4 (en) | 2004-03-02 | 2008-12-17 | Smithkline Beecham Corp | HEMMER OF ACT ACTIVITY |
| US20050239751A1 (en) * | 2004-03-26 | 2005-10-27 | Rigel Pharmaceuticals, Inc. | Heterocyclic anti-viral compounds comprising metabolizable moieties and their uses |
| WO2005098446A2 (en) | 2004-03-31 | 2005-10-20 | The Johns Hopkins University | Biomarkers for ovarian cancer |
| CA2562399A1 (en) | 2004-04-08 | 2005-10-20 | Topotarget A/S | Diphenyl - indol-2-on compounds and their use in the treatment of cancer |
| DE602005026509D1 (de) | 2004-04-09 | 2011-04-07 | Merck Sharp & Dohme | Hemmer der akt aktivität |
| WO2005100356A1 (en) | 2004-04-09 | 2005-10-27 | Merck & Co., Inc. | Inhibitors of akt activity |
| US7604947B2 (en) | 2004-06-09 | 2009-10-20 | Cornell Research Foundation, Inc. | Detection and modulation of cancer stem cells |
| US20060013873A1 (en) | 2004-07-16 | 2006-01-19 | Chih-Chiang Yang | Bioadhesive dosage form of steroids |
| EP1784175A4 (en) | 2004-08-23 | 2009-07-22 | Merck & Co Inc | INHIBITORS OF ACT ACTIVITY |
| CA2582347C (en) | 2004-09-30 | 2014-09-23 | Janssen Pharmaceutica N.V. | Novel benzimidazole derivatives useful as selective androgen receptor modulators (sarms) |
| EP1850843A4 (en) | 2005-02-14 | 2012-02-15 | Merck Sharp & Dohme | INHIBITORS OF ACT ACTIVITY |
| EA019560B1 (ru) | 2005-03-02 | 2014-04-30 | Юнивесити Оф Мэриленд, Балтимор | Способ лечения простаты (варианты) |
| US20100047338A1 (en) | 2008-03-14 | 2010-02-25 | Angela Brodie | Novel C-17-Heteroaryl Steroidal CYP17 Inhibitors/Antiandrogens, In Vitro Biological Activities, Pharmacokinetics and Antitumor Activity |
| AU2006235314B2 (en) | 2005-04-12 | 2011-01-20 | Merck Sharp & Dohme Corp. | Inhibitors of Akt activity |
| DK1898903T3 (da) | 2005-06-10 | 2013-07-01 | Merck Sharp & Dohme | Inhibitorer af Akt-aktivitet |
| AU2006292212A1 (en) | 2005-09-19 | 2007-03-29 | The Johns Hopkins University | Biomarker for prostate cancer |
| AU2006316605B2 (en) | 2005-11-17 | 2012-04-26 | Osi Pharmaceuticals, Inc. | Fused bicyclic mTOR inhibitors |
| AR057960A1 (es) | 2005-12-02 | 2007-12-26 | Osi Pharm Inc | Inhibidores de proteina quinasa biciclicos |
| TW200738725A (en) | 2006-01-25 | 2007-10-16 | Osi Pharm Inc | Unsaturated mTOR inhibitors |
| US7943732B2 (en) | 2006-06-05 | 2011-05-17 | Intrexon Corporation | AKT ligands and polynucleotides encoding AKT ligands |
| CA2656618C (en) | 2006-07-06 | 2014-08-26 | Array Biopharma Inc. | Cyclopenta [d] pyrimidines as akt protein kinase inhibitors |
| US20080051380A1 (en) | 2006-08-25 | 2008-02-28 | Auerbach Alan H | Methods and compositions for treating cancer |
| JP2010502640A (ja) | 2006-08-30 | 2010-01-28 | ノバルティス アクチエンゲゼルシャフト | mTORシグナル伝達を調節する組成物および方法 |
| CA2700573C (en) | 2006-09-26 | 2016-11-22 | Cedars-Sinai Medical Center | Cancer stem cell antigen vaccines and methods |
| WO2008047201A2 (en) | 2006-10-17 | 2008-04-24 | Pfizer Products Inc. | Solid dispersion comprising a poorly water soluble drug |
| AR064010A1 (es) | 2006-12-06 | 2009-03-04 | Merck & Co Inc | Inhibidores de la actividad de la akt |
| WO2008070823A2 (en) | 2006-12-07 | 2008-06-12 | University Of South Florida | Substrate-mimetic akt inhibitor |
| US7960435B2 (en) | 2006-12-15 | 2011-06-14 | University Of Maryland, Baltimore | Anti-cancer agents and androgen inhibition activity compound |
| US7807393B2 (en) | 2007-01-29 | 2010-10-05 | Northwestern University | Biomarkers for prostate cancer |
| UY30892A1 (es) | 2007-02-07 | 2008-09-02 | Smithkline Beckman Corp | Inhibidores de la actividad akt |
| KR20150002886A (ko) | 2007-03-07 | 2015-01-07 | 아브락시스 바이오사이언스, 엘엘씨 | 항암제로서 라파마이신 및 알부민을 포함하는 나노입자 |
| WO2008154382A1 (en) | 2007-06-06 | 2008-12-18 | University Of Maryland, Baltimore | Hdac inhibitors and hormone targeted drugs for the treatment of cancer |
| WO2008154402A2 (en) | 2007-06-06 | 2008-12-18 | University Of Maryland, Baltimore | Hdac inhibitors and hormone targeted drugs for the treatment of cancer |
| US20090012045A1 (en) | 2007-06-26 | 2009-01-08 | Rigel Pharmaceuticals, Inc. | Methods of Treating Cell Proliferative Disorders |
| WO2009005690A2 (en) | 2007-06-29 | 2009-01-08 | Gilead Sciences, Inc. | Antiviral compounds |
| US8324221B2 (en) | 2008-01-09 | 2012-12-04 | Array Biopharma Inc. | Pyrimidyl cyclopentanes as Akt protein kinase inhibitors |
| GB2470873A (en) | 2008-03-12 | 2010-12-08 | Univ Maryland | Androgen receptor inactivation contributes to antitumor efficacy of CYP17 inhibitors in prostrate cancer |
| US20110118219A1 (en) | 2008-03-25 | 2011-05-19 | University Of Maryland, Baltimore | Novel prodrugs of c-17-heteroaryl steroidal cyp17 inhibitors/antiandrogens: synthesis, in vitro biological activities, pharmacokinetics and antitumor activity |
| US8785423B2 (en) | 2008-04-14 | 2014-07-22 | University Of Maryland, Baltimore | Compositions and methods of inducing endoplasmic reticulum stress response for the treatment of cell proliferative diseases |
| ES2836128T3 (es) | 2008-04-16 | 2021-06-24 | Univ Johns Hopkins | Método para determinar variantes del receptor de andrógenos en cáncer de próstata |
| EP2311842A3 (en) | 2008-06-24 | 2011-07-13 | Takeda Pharmaceutical Company Limited | PI3K/M TOR inhibitors |
| WO2010089763A2 (en) | 2008-06-30 | 2010-08-12 | Reliance Life Sciences Pvt. Ltd. | Poly(n-vinyl caprolactam-co-acrylamide) microparticles for controlled release applications |
| US20110224223A1 (en) | 2008-07-08 | 2011-09-15 | The Regents Of The University Of California, A California Corporation | MTOR Modulators and Uses Thereof |
| US20110313229A1 (en) | 2008-07-24 | 2011-12-22 | Kiminobu Sugaya | Therapy Targeting Cancer Stem Cells |
| JP5616892B2 (ja) | 2008-09-12 | 2014-10-29 | ダコ・デンマーク・エー/エス | 前立腺癌バイオマーカー |
| US8133724B2 (en) | 2008-09-17 | 2012-03-13 | University Of Maryland, Baltimore | Human androgen receptor alternative splice variants as biomarkers and therapeutic targets |
| US8841422B2 (en) | 2008-09-17 | 2014-09-23 | University Of Maryland, Baltimore | Human androgen receptor alternative splice variants |
| BRPI0921802A8 (pt) | 2008-10-31 | 2018-03-13 | Novartis Ag | uso de um inibidor de fosfatidilinositol-3-cinase (pi3k) e um inibidor de mtor,bem como composição e combinação farmacêuticas os compreendendo. |
| CN101607985B (zh) | 2008-12-24 | 2013-03-27 | 中国科学院生物物理研究所 | 抗人cea的单克隆抗体,包含其的组合物,及其用途 |
| US8791095B2 (en) | 2009-02-05 | 2014-07-29 | Tokai Pharmaceuticals, Inc. | Steroidal CYP17 inhibitors/antiandrogens |
| GB2514957A (en) | 2009-02-05 | 2014-12-10 | Tokai Pharmaceuticals Inc | Combination of a 17 alpha-hydroxylase/c17, 20-lyase inhibitor with an additional therapeutic agent |
| AU2010210422A1 (en) | 2009-02-05 | 2011-08-18 | Tokai Pharmaceuticals, Inc. | Novel prodrugs of steroidal CYP17 inhibitors/antiandrogens |
| US8168652B2 (en) | 2009-03-12 | 2012-05-01 | Merck Sharp & Dohme Corp. | Inhibitors of AKT activity |
| US9724664B2 (en) | 2009-03-27 | 2017-08-08 | Bend Research, Inc. | Spray-drying process |
| AU2010279398A1 (en) | 2009-08-07 | 2012-03-08 | Tokai Pharmaceuticals, Inc. | Treatment of prostate cancer |
| EP2499151A4 (en) | 2009-11-13 | 2013-03-20 | Tokai Pharmaceuticals Inc | MAMMALIAN STEROID METABOLITES |
| CA2791244A1 (en) | 2010-03-08 | 2011-09-15 | Regents Of The University Of Minnesota | Androgen receptor isoforms and methods |
| US8703712B2 (en) | 2010-03-18 | 2014-04-22 | The Uab Research Foundation | Targeting cancer stem cells with DR5 agonists |
| US20120028972A1 (en) | 2010-07-30 | 2012-02-02 | Lilly Wong | Biomarker assays for detecting or measuring inhibition of tor kinase activity |
| US9594086B2 (en) | 2011-03-22 | 2017-03-14 | The Johns Hopkins University | Biomarkers for aggressive prostate cancer |
| JP2014523445A (ja) | 2011-07-18 | 2014-09-11 | トーカイ ファーマシューティカルズ,インク. | 前立腺癌を処置するための新規な組成物及び方法 |
| CA2856646C (en) | 2011-11-30 | 2020-01-14 | Astrazeneca Ab | Combination treatment of cancer |
| US20150005265A1 (en) | 2011-12-22 | 2015-01-01 | Susan Stewart | Methods and compositions for combination therapy using p13k/mtor inhibitores |
-
2010
- 2010-02-05 AU AU2010210422A patent/AU2010210422A1/en not_active Abandoned
- 2010-02-05 WO PCT/US2010/023391 patent/WO2010091306A1/en not_active Ceased
- 2010-02-05 JP JP2011549296A patent/JP2012516900A/ja active Pending
- 2010-02-05 BR BRPI1008745A patent/BRPI1008745A2/pt not_active IP Right Cessation
- 2010-02-05 EP EP10704283.0A patent/EP2393827B1/en not_active Not-in-force
- 2010-02-05 CN CN2010800071882A patent/CN102686600A/zh active Pending
- 2010-02-05 US US13/146,004 patent/US20110312916A1/en not_active Abandoned
- 2010-02-05 ES ES10704283.0T patent/ES2552087T3/es active Active
- 2010-02-05 EP EP15188218.0A patent/EP3023433A1/en not_active Withdrawn
- 2010-02-05 CA CA2761389A patent/CA2761389A1/en not_active Abandoned
-
2014
- 2014-07-10 US US14/328,378 patent/US9359395B2/en not_active Expired - Fee Related
-
2015
- 2015-08-12 JP JP2015159619A patent/JP2016034946A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CA2761389A1 (en) | 2010-08-12 |
| WO2010091306A1 (en) | 2010-08-12 |
| US20140371181A1 (en) | 2014-12-18 |
| CN102686600A (zh) | 2012-09-19 |
| JP2016034946A (ja) | 2016-03-17 |
| ES2552087T3 (es) | 2015-11-25 |
| US9359395B2 (en) | 2016-06-07 |
| US20110312916A1 (en) | 2011-12-22 |
| EP2393827A1 (en) | 2011-12-14 |
| AU2010210422A1 (en) | 2011-08-18 |
| JP2012516900A (ja) | 2012-07-26 |
| AU2010210422A8 (en) | 2011-08-25 |
| EP3023433A1 (en) | 2016-05-25 |
| EP2393827B1 (en) | 2015-10-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI1008745A2 (pt) | pró-fármacos de inibidores esteroidais de cyp17/antiandrogênios | |
| ES2353413T3 (es) | 3-beta-hidroxi-17-(1h-bencimidazol-1-il)androsta-5,16-dieno para uso en el tratamiento de una enfermedad de la próstata. | |
| US9018198B2 (en) | Prodrugs of C-17-heteroaryl steroidal CYP17 inhibitors/antiandrogens: synthesis, in vitro biological activities, pharmacokinetics and antitumor activity | |
| CN102532235B (zh) | 蟾毒配基衍生物及其制备方法、包含该衍生物的组合物、及其用途 | |
| US8791095B2 (en) | Steroidal CYP17 inhibitors/antiandrogens | |
| US10098896B2 (en) | C-17-heteroaryl steroidal CYP17 inhibitors/antiandrogens, in vitro biological activities, pharmacokinetics and antitumor activity | |
| CN104017045B (zh) | 甾体cyp17抑制剂的新型药物前体及其应用、制备方法 | |
| JP7371933B2 (ja) | がんを処置する方法 | |
| JPH08333370A (ja) | 水に可溶な新規フルオロエチルカンプトテシン誘導体、及びその製造方法 | |
| JP2022538602A (ja) | Akr1c3阻害剤およびその医学的使用 | |
| CN120904168A (zh) | 第四代egfr抑制剂、及其制备方法和在药学上的应用 | |
| HK40041158A (en) | Methods of treating cancer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B08K | Patent lapsed as no evidence of payment of the annual fee has been furnished to inpi [chapter 8.11 patent gazette] |
Free format text: EM VIRTUDE DO ARQUIVAMENTO PUBLICADO NA RPI 2542 DE 24-09-2019 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDO O ARQUIVAMENTO DO PEDIDO DE PATENTE, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |
|
| B350 | Update of information on the portal [chapter 15.35 patent gazette] |