ES2862073T3 - Grupo auxiliar asimétrico - Google Patents
Grupo auxiliar asimétrico Download PDFInfo
- Publication number
- ES2862073T3 ES2862073T3 ES13817386T ES13817386T ES2862073T3 ES 2862073 T3 ES2862073 T3 ES 2862073T3 ES 13817386 T ES13817386 T ES 13817386T ES 13817386 T ES13817386 T ES 13817386T ES 2862073 T3 ES2862073 T3 ES 2862073T3
- Authority
- ES
- Spain
- Prior art keywords
- group
- formula
- aryl
- alkyl
- hydrogen atom
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 *C(*)C(C1NCCC1)O Chemical compound *C(*)C(C1NCCC1)O 0.000 description 4
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6581—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus and nitrogen atoms with or without oxygen or sulfur atoms, as ring hetero atoms
- C07F9/6584—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus and nitrogen atoms with or without oxygen or sulfur atoms, as ring hetero atoms having one phosphorus atom as ring hetero atom
- C07F9/65842—Cyclic amide derivatives of acids of phosphorus, in which one nitrogen atom belongs to the ring
- C07F9/65844—Cyclic amide derivatives of acids of phosphorus, in which one nitrogen atom belongs to the ring the phosphorus atom being part of a five-membered ring which may be condensed with another ring system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B53/00—Asymmetric syntheses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/04—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D207/08—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hydrocarbon radicals, substituted by hetero atoms, attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D473/00—Heterocyclic compounds containing purine ring systems
- C07D473/02—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6
- C07D473/18—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 one oxygen and one nitrogen atom, e.g. guanine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D473/00—Heterocyclic compounds containing purine ring systems
- C07D473/26—Heterocyclic compounds containing purine ring systems with an oxygen, sulphur, or nitrogen atom directly attached in position 2 or 6, but not in both
- C07D473/32—Nitrogen atom
- C07D473/34—Nitrogen atom attached in position 6, e.g. adenine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/10—Compounds having one or more C—Si linkages containing nitrogen having a Si-N linkage
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H1/00—Processes for the preparation of sugar derivatives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
- C07H19/067—Pyrimidine radicals with ribosyl as the saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
- C07H19/073—Pyrimidine radicals with 2-deoxyribosyl as the saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
- C07H19/10—Pyrimidine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/06—Pyrimidine radicals
- C07H19/10—Pyrimidine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
- C07H19/11—Pyrimidine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids containing cyclic phosphate
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/16—Purine radicals
- C07H19/20—Purine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
- C07H19/207—Purine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids the phosphoric or polyphosphoric acids being esterified by a further hydroxylic compound, e.g. flavine adenine dinucleotide or nicotinamide-adenine dinucleotide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H19/00—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof
- C07H19/02—Compounds containing a hetero ring sharing one ring hetero atom with a saccharide radical; Nucleosides; Mononucleotides; Anhydro-derivatives thereof sharing nitrogen
- C07H19/04—Heterocyclic radicals containing only nitrogen atoms as ring hetero atom
- C07H19/16—Purine radicals
- C07H19/20—Purine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids
- C07H19/213—Purine radicals with the saccharide radical esterified by phosphoric or polyphosphoric acids containing cyclic phosphate
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H21/00—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids
- C07H21/04—Compounds containing two or more mononucleotide units having separate phosphate or polyphosphate groups linked by saccharide radicals of nucleoside groups, e.g. nucleic acids with deoxyribosyl as saccharide radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H23/00—Compounds containing boron, silicon or a metal, e.g. chelates or vitamin B12
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/07—Optical isomers
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Engineering & Computer Science (AREA)
- Saccharide Compounds (AREA)
- Pyrrole Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
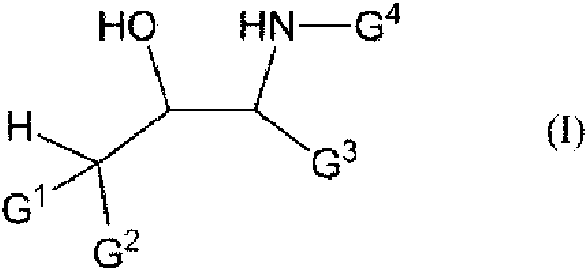
Un reactivo quiral o una sal del mismo, teniendo el reactivo quiral la siguiente fórmula química (I), **(Ver fórmula)** en donde G1 es un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo de fórmula (II), (III) o (V), G2 es un grupo nitro, un grupo ciano, o un grupo de fórmula (II), (III) o (V), o tanto G1 como G2 se toman juntos para formar un grupo de fórmula (IV), **(Ver fórmula)** en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3, **(Ver fórmula)** en donde G31 a G33 son independientemente grupo alquilo C1-4, grupo alcoxi C1-4, grupo arilo C6-14, grupo aralquilo C7-14, grupo alquil C1-4 arilo C6-14, grupo alcoxi C1-4 arilo C6-14 o grupo aril C6-14 alquilo C1-4, en donde G41 a G46 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3, **(Ver fórmula)** en donde G51 a G53 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano, un grupo alquilo C1-3 o alquil C1-3oxi y G3 y G4 se toman juntos para formar un anillo que contiene heteroátomos que tiene de 3 a 16 átomos de carbono.
Description
DESCRIPCIÓN
Grupo auxiliar asimétrico
[CAMPO DE LA INVENCIÓN]
La presente invención está dirigida a un reactivo quiral que se utiliza para sintetizar derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados.
[ANTECEDENTES DE LA INVENCIÓN]
El documento JP 2005-89441 A describe un método para producir un derivado de nucleótidos, denominado método de oxazafosfolidina. Sin embargo, el rendimiento aislado de los monómeros es bajo y el método requiere agentes de terminación de cadena especiales que no están disponibles comercialmente. Además, los monómeros obtenidos son químicamente inestables. Además, los rendimientos aislados de derivados de oligonucleótidos no son altos. Se cree que el bajo rendimiento de derivados de oligonucleótidos es provocado por las reacciones de degradación bajo las etapas de desprotección.
El documento WO2010/064146 describe un método para producir un derivado de nucleótidos. El método allí descrito requiere agentes de terminación de cadena especiales que no están disponibles comercialmente. Además, los rendimientos aislados de derivados de oligonucleótidos no son altos. Se cree que el bajo rendimiento es provocado por las reacciones de degradación bajo las etapas de desprotección. Esta tendencia se vuelve muy evidente cuando la longitud de los derivados de oligonucleótidos se vuelve grande.
El documento WO2012 / 039448 describe un grupo auxiliar asimétrico que se utiliza para producir derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados. El documento WO2005/014609 describe un método para producir un análogo de nucleótido modificado con un átomo de fósforo estereorregular.
[Lista de Citas]
[Bibliografía de Patentes]
[Bibliografía de Patente 1] documento JP 2005-89441 A
[Bibliografía de Patente 2 ] documento WO2010/064146 A
[Bibliografía de Patente 3 ] documento WO2012/039448 A
[SUMARIO DE LA INVENCIÓN]
El primer aspecto de la invención se refiere a un reactivo quiral o una sal del mismo. El reactivo quiral tiene la siguiente fórmula química (I).
En la fórmula (I), G1 es un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo de fórmula (II), (III) o (V), G2 es un grupo nitro, un grupo ciano, o un grupo de fórmula (II), (III) o (V), o tanto G1 como G2 se toman juntos para formar un grupo de fórmula (IV).
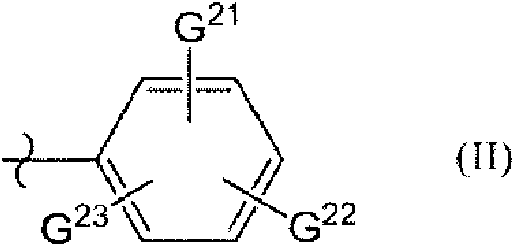
En la fórmula (II), G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C 1-3.
G31
- j l —g j ----q 32 ( m )
¿33
En la fórmula (III), G31 a G33 son independientemente grupo alquilo C1-4, grupo arilo C6-14, grupo alcoxi C1-4, grupo aralquilo C7-14, grupo alquil C1-4 arilo C6-14, grupo alcoxi C1-4 arilo C6-14 o grupo aril C6-14 alquilo C1-4.
En la fórmula (IV), G41 a G46 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3.
En la fórmula (V), G51 a G53 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano, un grupo alquilo C1-3 o alquil C1-3oxi.
G3 y G4 se toman juntos para formar un anillo que contiene heteroátomos que tiene de 3 a 16 átomos de carbono, junto con el resto Nh en la fórmula (I).
Una realización preferida es que el reactivo quiral tiene la siguiente fórmula química (I').
En la fórmula (I'), G1 y G2 son los mismos que arriba.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y cada uno de G1 y G2 es un grupo de fórmula (II), en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y cada uno de G1 y G2 es un grupo de fórmula (II) y cada uno de G21 a G23 es un átomo de hidrógeno.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (II) y G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (II) y cada uno de G21 a G22 es un átomo de hidrógeno y G23 es un grupo nitro.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), y G31 a G33 son independientemente un grupo alquilo C1-4, un grupo arilo C6-14, un grupo aralquilo C7-14, un grupo alquil C1-4 arilo C6-14, un grupo alcoxi C1-4 arilo C6-14 o un grupo aril C6-14 alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), y G31 a G33 son independientemente un grupo alquilo C1-4, un grupo arilo C6, un grupo aralquilo C7-10, un grupo alquil C1-4 arilo C6, un grupo alcoxi C1-4 arilo C6 o un grupo aril C6 alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (IiI) y G31 a G33 son independientemente un grupo alquilo C1-4 o un grupo arilo C6. Ejemplos de grupo alquilo C1-4 son grupo metilo, grupo etilo, grupo n-propilo, grupo /so-propilo, grupo n-butilo y grupo ferc.—butilo.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (III) y G31 a G33 son independientemente un grupo alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (III) y G31 a G33 son un grupo arilo C6 y G32 es grupo alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 y G2, tomados juntos para formar un grupo de fórmula (IV), y G41 a G46 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y cada uno de G 1 y G2, tomados juntos para formar un grupo de fórmula (IV), en donde cada uno de G41 a G46 es un átomo de hidrógeno.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I1) y G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (V). Además, cada uno de G51 a G53 es independientemente un átomo de hidrógeno, un grupo nitro, un grupo metilo o un grupo metoxi. Una realización más preferida es aquella en la que G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (V), en donde cada uno de G51 a G53 es un átomo de hidrógeno y G53 es un grupo 4-metilo.
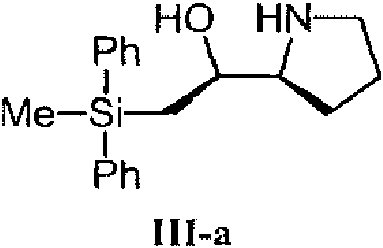
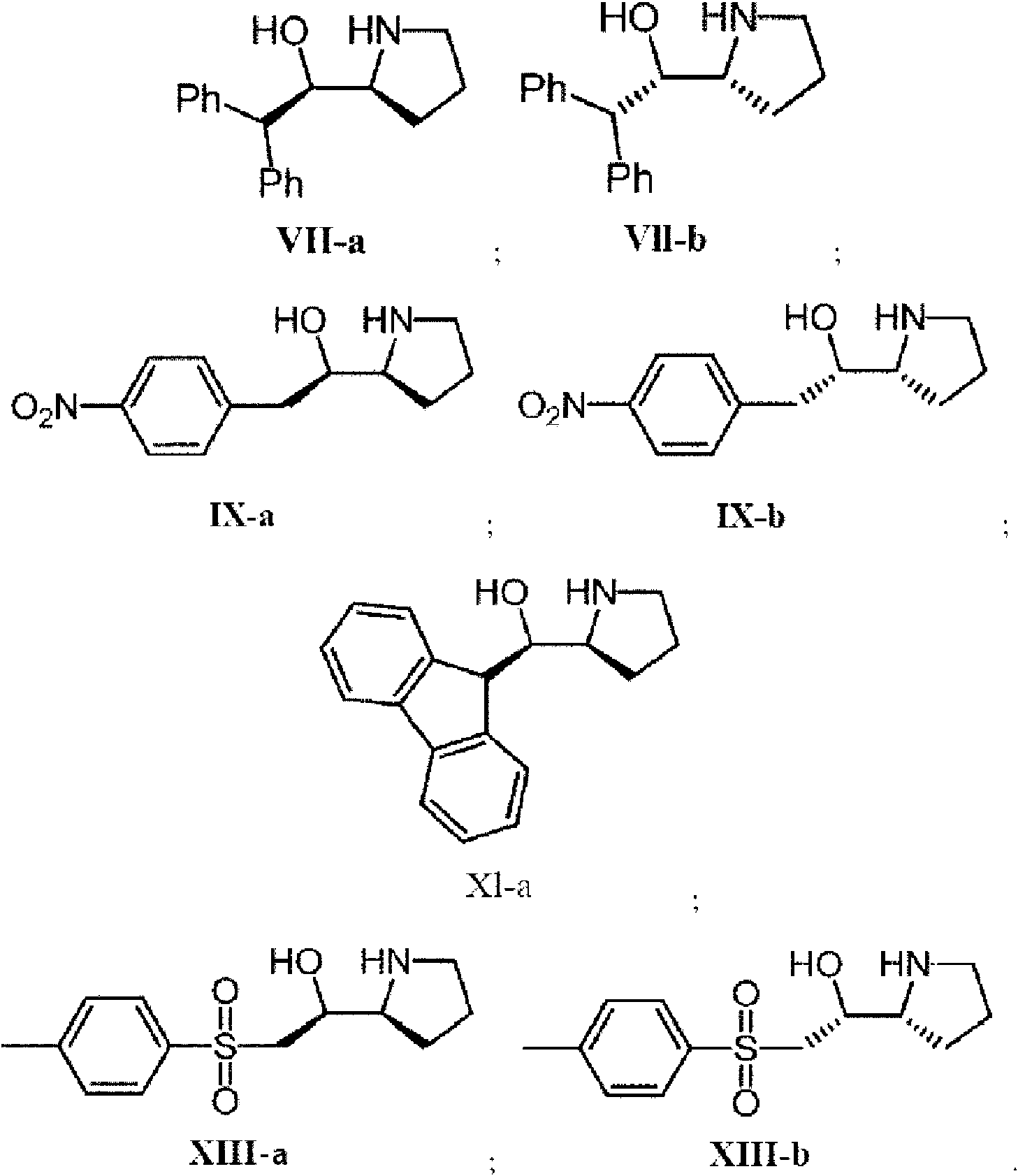
Una realización preferida es aquella en la que el reactivo quiral se selecciona de IlI-a, IlI-b, V-a, VlI-a, VlI-b, IX-a, IX-b, XI-a, XIII-a y XIII-b:
(S)-2-(metildifenilsilil)-1 -((S)-pirrolidin-2-il)etanol (III-a)
(R) -2-(metildifenilsilil)-1-((R)-1-pirrolidin-2-il)etanol (III-b)
(S) -2-(trimetilsilil)-1-((S)-1-pirrolidin-2-il)etanol (V-a)
difenil-1-((S)-pirrolidin-2-il)etanol (VII-a)
difenil-1-((R)-pirrolidin-2-il)etanol (VII-b) -nitrofenil)-1-((S)-pirrolidin-2-il)etanol (IX-a) -nitrofenil)-1-((R)-pirrolidin-2-il)etanol (IX-b)
(S) -2-tosil-1-((S)-pirrolidin-2-il)etanol (XIII-a)
(R)-2-tosil)-1-((R)-pirrolidin-2-il)etanol (XIII-b)
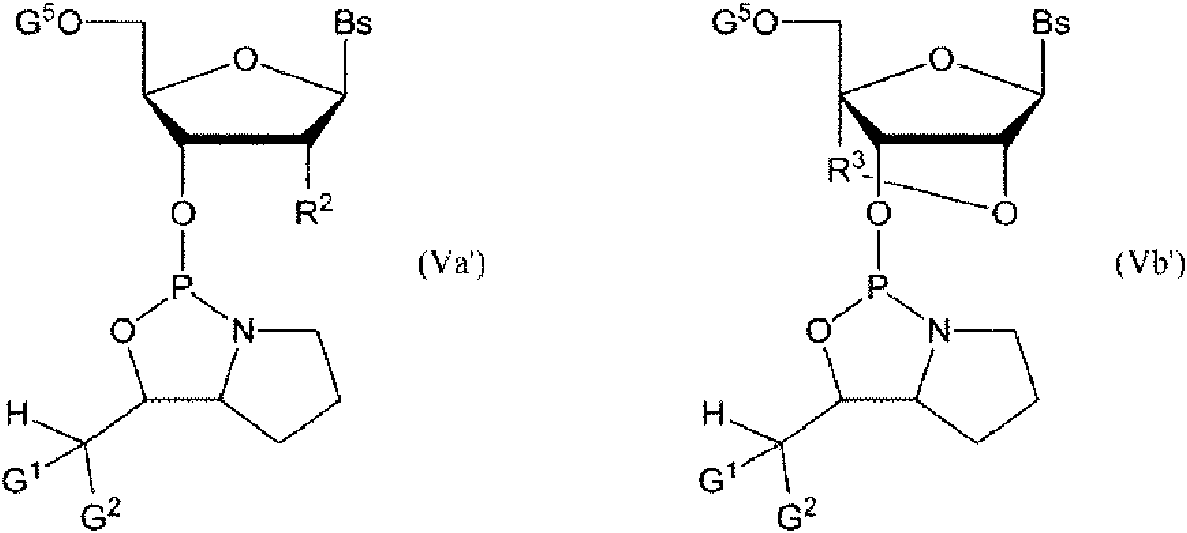
El segundo aspecto de la invención se refiere a un derivado de nucleósido 3’-fosforamidita que está representado por la fórmula (Va) o (Vb) según se define en la reivindicación 5.
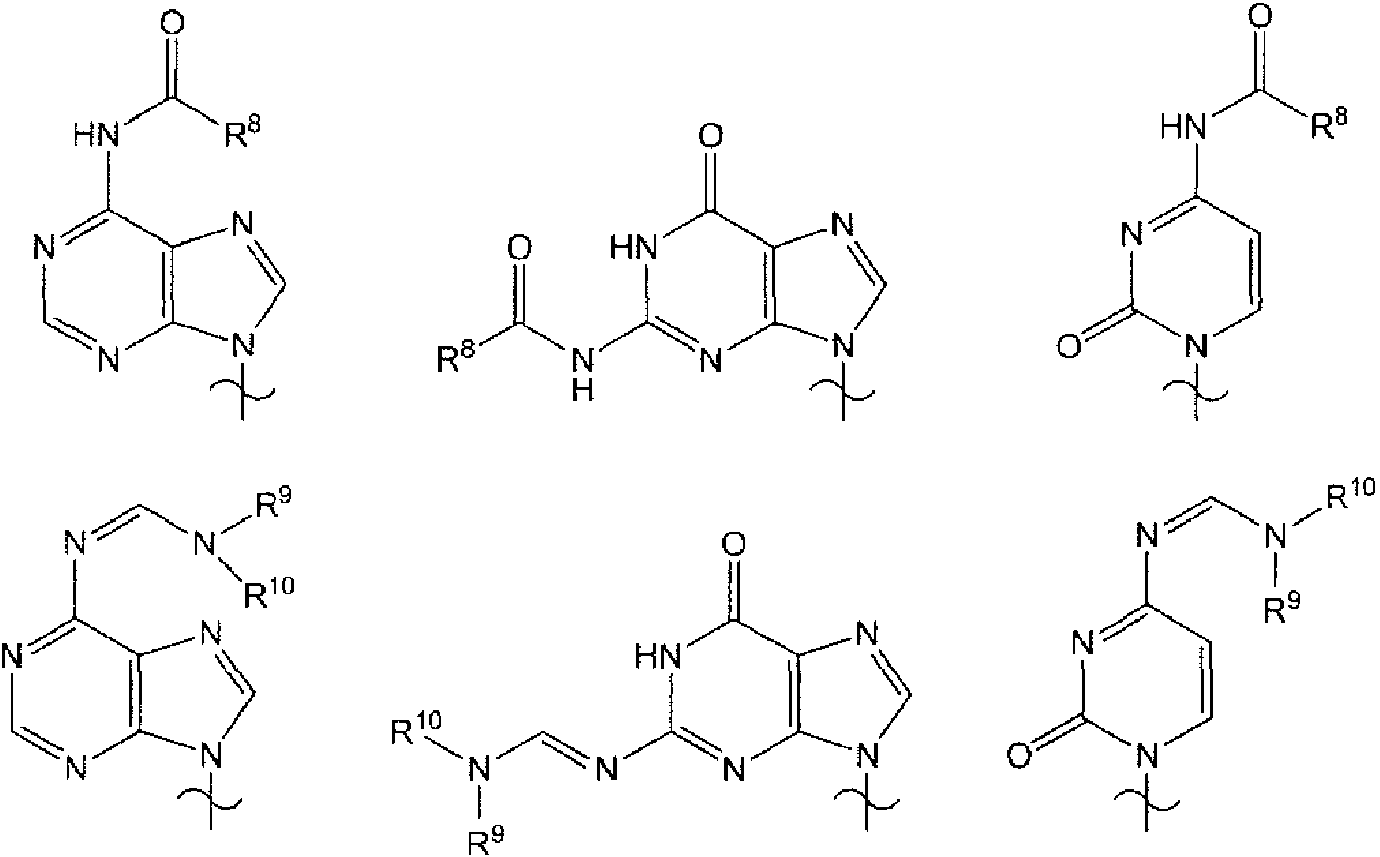
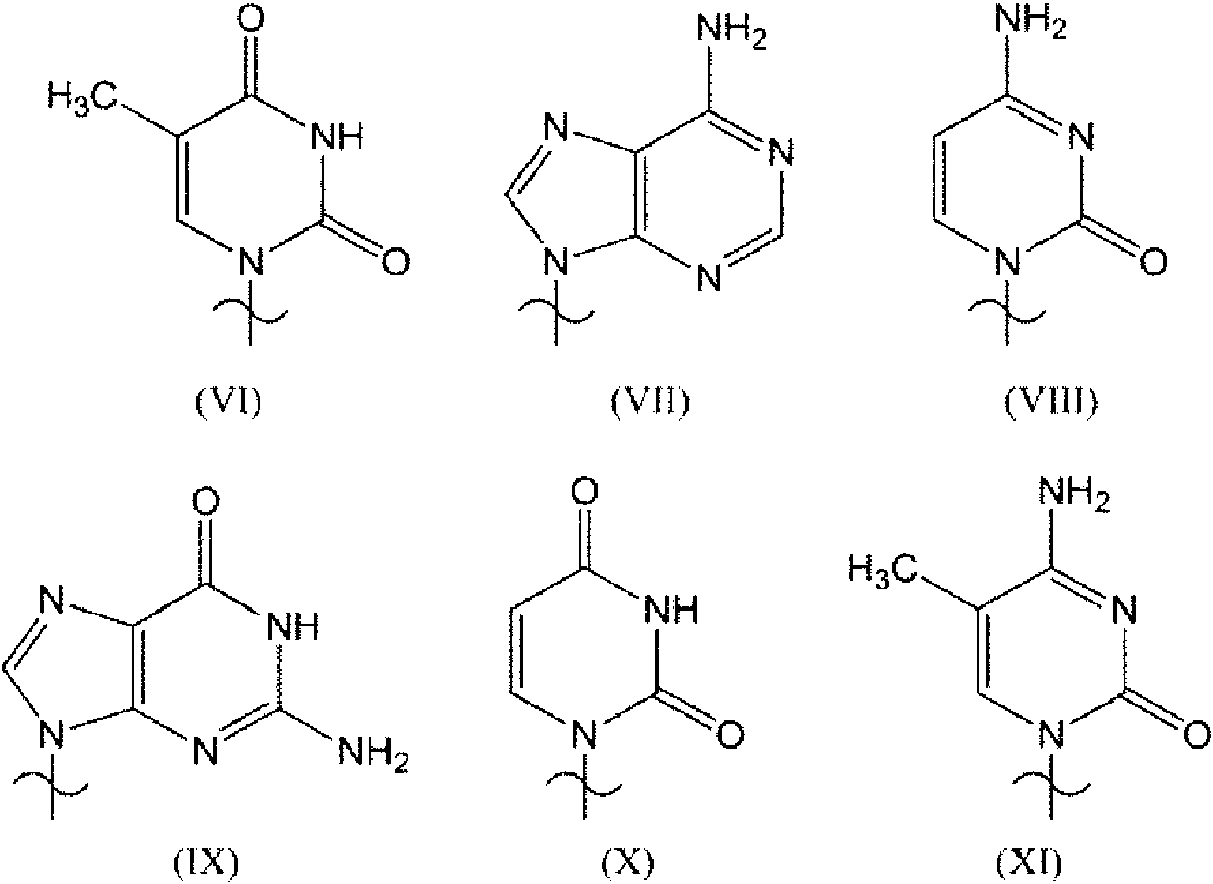
En la fórmula (Va) y (Vb), G1 a G4 son iguales que arriba, G5 es un grupo protector del grupo hidroxilo y Bs es un grupo seleccionado de los grupos representados por la siguiente fórmula (VI) a ( XI) o derivados de los mismos.
Ejemplos de B son una adenina, una timina, una citosina, una guanina, un uracilo, una 5-metilcitosina o un derivado de los mismos.
R2 es hidrógeno, -OH, -SH, -NRdRd, -N3 , halógeno, alquilo, alquenilo, alquinilo, alquil-Y1-, alquenil-Y1-, alquinil-Y1-, aril-Y1-, heteroaril-Y1-, -ORb o -SRb, en donde Rb es un resto de bloqueo.
Y1 es O, NRd, S o Se.
Rd es es independientemente hidrógeno, alquilo, alquenilo, alquinilo, arilo, acilo, sililo sustituido, carbamato, -P(O)(Re)2 o -HP(O)(Re).
Re es independientemente hidrógeno, alquilo, arilo, alquenilo, alquinilo, alquil-Y2-, alquenil-Y2-, alquinil-Y2-, aril-Y2- o heteroaril-Y2- o un catión que es Na+, Li+ o K+.
Y2 es O, NRd o S.
R3 es un grupo representado por -CH2-, -(CH2)2-, -CH2NH- o -CH2N(CH3)-.
Ejemplos de G5 son tritilo, 4-monometoxitritilo, 4,4'-dimetoxitritilo, 4,4',4"-trimetoxitritilo, 9-fenilxantin-9-ilo (pixilo) y 9-(p-metoxifenil)xantin-9-ilo (MOX).
Una realización preferida del segundo aspecto es aquella en la que el derivado de nucleósido 3'-fosforamidita está representado por la fórmula Va1 o Vb1.
El tercer aspecto de la invención se refiere a un método para la síntesis de un derivado de oligonucleótido modificado con un átomo de fósforo estereocontrolado según se define en la reivindicación 8.
La primera etapa es una etapa de hacer reaccionar una molécula que comprende un resto H-fosfonato aquiral, el primer reactivo de activación y un reactivo quiral o una sal del mismo para formar un monómero. El reactivo quiral tiene la fórmula química (I) o (I') y el monómero puede estar representado por las fórmulas (Va), (Vb), (Va') o (Vb'). El monómero reacciona con el segundo reactivo activador y un nucleósido para formar un compuesto intermedio condensado. La siguiente etapa es una etapa de convertir el compuesto intermedio condensado en el ácido nucleico que comprende un resto X-fosfonato quiral.
Basado en el presente método, es posible utilizar materiales estables y disponibles comercialmente como materiales de partida. Es posible producir derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados utilizando un material de partida aquiral.
Como se muestra en un ejemplo de trabajo, el método de la presente invención no provoca degradaciones bajo las etapas de desprotección. Además, el método no requiere agentes de terminación de cadena especiales para producir derivados de oligonucleótidos modificados con átomos de fósforo.
El cuarto aspecto de la invención se refiere a un método para la síntesis de derivados de oligonucleótidos modificados con un átomo de fósforo estereocontrolados utilizando un monómero quiral según se define en la reivindicación 11.
La primera etapa es hacer reaccionar un derivado de nucleósido 3'-fosforamidita que está representado por la fórmula (Va), (Vb), (Va') o (Vb') con el segundo reactivo activador y un nucleósido para formar un compuesto intermedio condensado. La segunda etapa es convertir el compuesto intermedio condensado en el ácido nucleico que comprende un resto X-fosfonato quiral.
[BREVE DESCRIPCIÓN DE LOS DIBUJOS]
[Fig. 1]
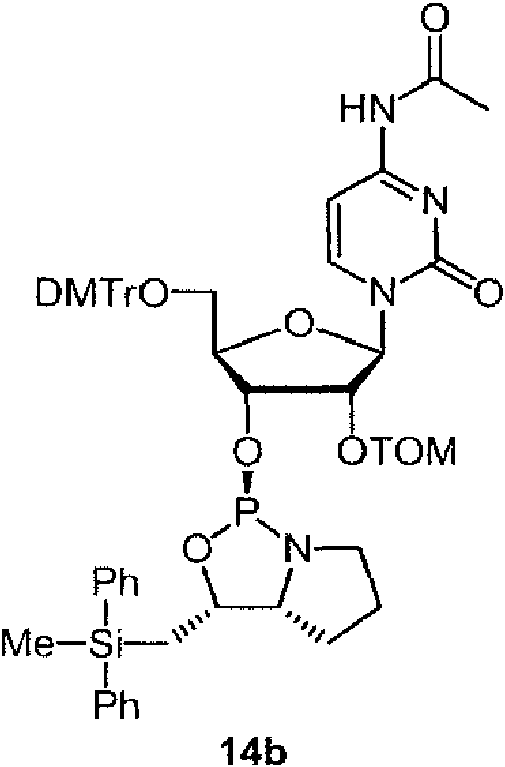
La Figura 1 es el perfil de UPLC en la producción de un derivado de oligonucleótido utilizando el monómero de 4b.
[Fig. 2]
La Figura 2 es el perfil de UPLC en la producción de un derivado de oligonucleótido utilizando el monómero de 25.
[MEJOR MODO PARA LLEVAR A CABO LA INVENCIÓN]
La expresión "ácido nucleico" incluye poli- u oligo-ribonucleótidos (ARN) y poli- u oligo-desoxirribonucleótidos (ADN); ARN 0 ADN derivado de /V-glicósidos o C-glicósidos de nucleobases y/o nucleobases modificadas; ácidos nucleicos derivados de azúcares y/o azúcares modificados; y ácidos nucleicos derivados de puentes de fosfato y/o puentes de átomos de fósforo modificados. La expresión abarca ácidos nucleicos que contienen cualesquiera combinaciones de nucleobases, nucleobases modificadas, azúcares, azúcares modificados, puentes de fosfato o puentes de átomos de fósforo modificados. Ejemplos incluyen, pero no se limitan a ácidos nucleicos que contienen restos ribosa, los ácidos nucleicos que contienen restos desoxirribosa, ácidos nucleicos que contienen restos ribosa y desoxirribosa, ácidos nucleicos que contienen restos ribosa y ribosa modificados. El prefijo poli- se refiere a un ácido nucleico que contiene aproximadamente 1 a aproximadamente 10.000 unidades de monómero nucleotídico y en donde el prefijo oligo- se refiere a un ácido nucleico que contiene aproximadamente 1 a aproximadamente 200 unidades de monómeros nucleotídicos.
El término "nucleobase" se refiere a las partes de ácidos nucleicos que están implicadas en el enlace de hidrógeno que une una cadena de ácido nucleico a otra cadena complementaria de una manera específica para la secuencia. Las nucleobases que se producen de forma natural más comunes son adenina (A), guanina (G), uracilo (U), citosina (C), 5-metilcitosina y timina (T).
La expresión "nucleobase modificada" se refiere a un resto que puede reemplazar una nucleobase. La nucleobase modificada imita la disposición espacial, las propiedades electrónicas o alguna otra propiedad fisico-química de la nucleobase y conserva la propiedad del enlace de hidrógeno que une una cadena de ácido nucleico a otra de una manera específica para la secuencia. Una nucleobase modificada puede emparejarse con las cinco bases que se producen de forma natural (uracilo, timina, adenina, citosina o guanina) sin afectar sustancialmente el comportamiento de fusión, el reconocimiento por enzimas intracelulares o la actividad del dúplex de oligonucleótidos.
El término "nucleósido" se refiere a un resto en el que una nucleobase o una nucleobase modificada está unida covalentemente a un azúcar o azúcar modificado.
El término "azúcar" se refiere a un monosacárido en forma cerrada y/o abierta. Los azúcares incluyen, pero no se limitan a restos de ribosa, desoxirribosa, pentofuranosa, pentopiranosa y hexopiranosa.
La expresión "azúcar modificado" se refiere a un resto que puede reemplazar un azúcar. El azúcar modificado imita la disposición espacial, las propiedades electrónicas o alguna otra propiedad fisico-química de un azúcar.
El término "nucleótido" se refiere a un resto en el que una nucleobase o una nucleobase modificada está enlazada covalentemente a un azúcar o azúcar modificado, y el azúcar o azúcar modificado está enlazado covalentemente a un grupo fosfato o un resto de átomo de fósforo modificado.
La expresión "reactivo quiral" se refiere a un compuesto que es quiral o puro en cuanto a los enantiómeros y se puede utilizar para la inducción asimétrica en la síntesis de ácidos nucleicos.
La expresión "ligando quiral" o "auxiliar quiral" se refiere a un resto que es quiral o puro en cuanto a los enantiómeros y controla el resultado estereoquímico de una reacción.
En una reacción de condensación, la expresión "reactivo activador" se refiere a un reactivo que activa un sitio menos reactivo y lo hace más susceptible al ataque por parte de un nucleófilo.
La expresión "resto de bloqueo" se refiere a un grupo que enmascara transitoriamente la reactividad de un grupo funcional. El grupo funcional se puede desenmascarar posteriormente mediante la eliminación del resto de bloqueo.
Las expresiones "agentes boronantes", "electrófilos de azufre", "electrófilos de selenio" se refieren a compuestos que son útiles en la etapa de modificación utilizada para introducir grupos BH3, S y Se, respectivamente, para la modificación en el átomo de fósforo.
El término "resto" se refiere a un segmento específico o grupo funcional de una molécula. A menudo, los restos químicos son entidades químicas reconocidas embebidas en o adjuntas a una molécula
La expresión "soporte sólido" se refiere a cualquier soporte que permita la producción en masa sintética de ácidos nucleicos y pueda reutilizarse según sea necesario. Tal como se utiliza en esta memoria, la expresión se refiere a un polímero que es insoluble en el medio empleado en las etapas de reacción realizadas para sintetizar ácidos nucleicos, y se derivatiza para comprender grupos reactivos.
La expresión "resto de enlace" se refiere a cualquier resto colocado opcionalmente entre el nucleósido terminal y el soporte sólido o entre el nucleósido terminal y otro nucleósido, nucleótido o ácido nucleico.
Tal como se utiliza en esta memoria, "tratamiento" o "tratar" o "paliar" o "mejorar" se utilizan indistintamente en esta memoria. Estos términos se refieren a un enfoque para obtener resultados beneficiosos o deseados que incluyen, pero no se limitan a un beneficio terapéutico y/o un beneficio profiláctico. Por beneficio terapéutico se entiende la erradicación o la mejora del trastorno subyacente que se está tratando. Además, se logra un beneficio terapéutico con la erradicación o mejora de uno o más de los síntomas fisiológicos asociados con el trastorno subyacente, de manera que se observa una mejora en el paciente, a pesar de que el paciente todavía puede estar afectado por el trastorno subyacente. Para obtener un beneficio profiláctico, las composiciones se pueden administrar a un paciente con riesgo de desarrollar una enfermedad particular, o a un paciente que declara uno o más de los síntomas fisiológicos de una enfermedad, incluso aunque no se haya realizado un diagnóstico de esta enfermedad.
Un "efecto terapéutico", tal como se utiliza ese término en esta memoria, abarca un beneficio terapéutico y/o un beneficio profiláctico tal como se describe arriba. Un efecto profiláctico incluye retrasar o eliminar la aparición de una enfermedad o afección, retrasar o eliminar la aparición de síntomas de una enfermedad o afección, ralentizar, detener 0 revertir la progresión de una enfermedad o afección, o cualquier combinación de los mismos.
Un grupo "alquilo" se refiere a un grupo hidrocarbonado alifático. El resto alquilo puede ser un grupo alquilo saturado (lo que significa que no contiene unidad de insaturación alguna, p. ej., dobles enlaces carbono-carbono o triples enlaces carbono-carbono) o el resto alquilo puede ser un grupo alquilo insaturado (lo que significa que contiene al menos una unidad de insaturación). El resto alquilo, ya sea saturado o insaturado, puede ser ramificado, de cadena lineal o puede incluir una porción cíclica. El punto de unión de un alquilo es en un átomo de carbono que no forma parte de un anillo. El resto "alquilo" puede tener de 1 a 10 átomos de carbono (siempre que aparezca en esta memoria, un intervalo numérico tal como "1 a 10" se refiere a cada uno de los números enteros en el intervalo dado; p. ej., "1 a 10 átomos de carbono" significa que el grupo alquilo puede consistir en 1 átomo de carbono, 2 átomos de carbono, 3 átomos de carbono, etc., hasta 10 átomos de carbono inclusive, aunque la presente definición también cubre la aparición del término "alquilo" en que no se designa un intervalo numérico). Alquilo incluye grupos alquilo tanto de cadena lineal como ramificada. El grupo alquilo de los compuestos descritos en esta memoria se puede designar como "alquilo C1-C6" o designaciones similares. Solo a modo de ejemplo, "alquilo C1-C6" indica que hay uno, dos, tres, cuatro, cinco o seis átomos de carbono en la cadena de alquilo, es decir, la cadena de alquilo se selecciona del grupo que consiste en metilo, etilo, propilo,/so-propilo, n-butilo, /so-butilo, sec.-butilo y terc.-butilo. Grupos alquilo típicos incluyen, pero no se limitan de modo alguno a metilo, etilo, propilo, isopropilo, butilo, isobutilo, butilo terciario, pentilo, hexilo, alilo, ciclopropilmetilo, ciclobutilmetilo, ciclopentilmetilo, ciclohexilmetilo y similares. En un aspecto, un alquilo es un alquilo C1-C6.
Grupo alquilo C1-3 significa grupo alquilo lineal o ramificado que tiene de 1 a 3 átomos de carbono. Ejemplos de grupos alquilo C1-3 son metilo, etilo, propilo e isopropilo. Grupo alquilo C1-4 significa grupo alquilo lineal o ramificado que tiene de 1 a 4 átomos de carbono. Ejemplos de grupos alquilo C1-4 son metilo, etilo, propilo, isopropilo, butilo, isobutilo y terc.-butilo.
Tal como se utiliza en esta memoria, el término "arilo" se refiere a un anillo aromático, en el que cada uno de los átomos que forman el anillo es un átomo de carbono. Los anillos de arilo están formados por cinco, seis, siete, ocho, nueve o más de nueve átomos de carbono. Los grupos arilo están sustituidos o no sustituidos. En un aspecto, un arilo es un fenilo o un naftalenilo. Dependiendo de la estructura, un grupo arilo puede ser un monorradical o dirradical (es decir, un grupo arileno). En un aspecto, un arilo es un arilo C6-C10.
Grupo alquilo C6-14 significa grupo arilo que tiene de 6 a 14 átomos de carbono. Los ejemplos de grupo arilo C6-14 son fenilo, bifenilo, naftilo, antracilo, indanilo, ftalimidilo, naftimidilo, fenantridinilo y tetrahidronaftilo.
El término "aralquilo" se refiere a un grupo alquilo sustituido con un grupo arilo. Grupos aralquilo adecuados incluyen bencilo, picolilo y similares, todos los cuales pueden estar opcionalmente sustituidos.
Un "resto acilo" se refiere a un grupo alquilo(C = O), arilo(C = O) o aralquilo(C = O). Un resto acilo puede tener un resto intermedio (Y) que es oxi, amino, tio o seleno entre el carbonilo y el grupo hidrocarbonado. Por ejemplo, un grupo acilo puede ser alquil-Y-(C=O), aril-Y-(C=O) o aralquil-Y-(C=O).
Los grupos "alquenilo" son grupos hidrocarbonados de cadena lineal, de cadena ramificada y cíclicos que contienen al menos un doble enlace carbono-carbono. Los grupos alquenilo pueden estar sustituidos.
Los grupos "alquinilo" son grupos hidrocarbonados de cadena lineal, de cadena ramificada y cíclicos que contienen al menos un triple enlace carbono-carbono. Los grupos alquinilo pueden estar sustituidos.
Un grupo "alcoxi" se refiere a un grupo alquilo enlazado a oxígeno, es decir, un grupo (alquil)-O-, en que alquilo es como se define en esta memoria. Ejemplos incluyen grupos metoxi (-OCH3) o etoxi (-OCH2CH3).
Un grupo "alqueniloxi" se refiere a un grupo alquenilo enlazado a oxígeno, es decir, un grupo (alquenil)-O-, en que alquenilo es como se define en esta memoria.
Un grupo "alquiniloxi" se refiere a un grupo alquinilo enlazado a oxígeno, es decir, un grupo (alquinil)-O-, en que alquinilo es como se define en esta memoria.
Un grupo "ariloxi" se refiere a un grupo alquilo enlazado a oxígeno, es decir, un grupo (aril)-O-, en que el arilo es como se define en esta memoria. Un ejemplo incluye el grupo fenoxi (-OC6H5).
El término "alquilseleno" se refiere a un grupo alquilo que tiene un grupo seleno sustituido fijado al mismo, es decir, grupo (alquil) -Se-, en donde alquilo se define en esta memoria.
El término "alquenilseleno" se refiere a un grupo alquenilo que tiene un grupo seleno sustituido fijado al mismo, es decir, grupo (alquenil) -Se-, en donde alquenilo se define en esta memoria.
El término "alquinilseleno" se refiere a un grupo alquinilo que tiene un grupo seleno sustituido fijado al mismo, es decir, grupo (alquinil) -Se-, en donde alquinilo se define en esta memoria.
El término "alquiltio" se refiere a un grupo alquilo fijado a un átomo de azufre de puente, es decir, un grupo (alquil) -S-, en donde alquilo se define en esta memoria. Por ejemplo, un alquiltio es un metiltio y similares.
El término "alqueniltio" se refiere a un grupo alquenilo fijado a un átomo de azufre de puente, es decir, un grupo (alquenil) -S-, en donde alquenilo se define en esta memoria.
El término "alquiniltio" se refiere a un grupo alquinilo fijado a un átomo de azufre de puente, es decir, un grupo (alquinil) -S-, en donde alquinilo se define en esta memoria.
El término "alquilamino" se refiere a un grupo amino sustituido con al menos un grupo alquilo, es decir,. -NH(alquilo) o -N (alquilo)2 , en donde alquilo se define en esta memoria.
El término "alquenilamino" se refiere a un grupo amino sustituido con al menos un grupo alquenilo, es decir, -NH(alquenilo) o -N (alquenilo)2 , en donde alquenilo se define en esta memoria.
El término "alquinilamino" se refiere a un grupo amino sustituido con al menos un grupo alquinilo, es decir,. -NH(alquinilo) o -N (alquinilo)2 , en donde alquinilo se define en esta memoria.
El término "halógeno" pretende incluir flúor, cloro, bromo y yodo.
Un "grupo fluorescente" se refiere a una molécula que, cuando se excita con luz que tiene una longitud de onda seleccionada, emite luz de una longitud de onda diferente. Grupos fluorescentes incluyen, pero no se limitan a grupos
indol, fluoresceína, tetrametilrodamina, rojo Texas, BODIPY, ácido 5-[(2-aminoetil)amino]naftalen-1-sulfónico (EDANS), cumarina y amarillo Lucifer.
Un "ion amonio" es un catión poliatómico cargado positivamente de fórmula química NH4+.
Un "ion alquilamonio" es un ion amonio que tiene al menos uno de sus átomos de hidrógeno reemplazado por un grupo alquilo, en donde alquilo se define en esta memoria. Ejemplos incluyen ion trietilamonio, ion N,N-diisopropiletilamonio.
Un "ion iminio" tiene la estructura general R2C=NR2+. Los grupos R se refieren a grupos alquilo, alquenilo, alquinilo, arilo tal como se definen en esta memoria. Un "ion iminio heteroaromático" se refiere a un ion iminio, en donde el nitrógeno y sus grupos R fijados forman un anillo heteroaromático. Un "ion iminio heterocíclico" se refiere a un ion iminio, en donde el nitrógeno y sus grupos R fijados forman un anillo heterocíclico.
Los términos "amino" o "amina" se refieren a un grupo radical -N(Rh)2 , en donde cada uno de los Rh es independientemente hidrógeno, alquilo, fluoroalquilo, carbociclilo, carbociclilalquilo, arilo, aralquilo, heterociclilo, heterociclilalquilo, heteroarilo o heteroarilalquilo, a menos que se indique lo contrario específicamente en la memoria descriptiva. Cuando un grupo -N(Rh)2 tiene dos Rh distintos de hidrógeno, pueden combinarse con el átomo de nitrógeno para formar un anillo de 4, 5, 6 o 7 miembros. Por ejemplo, se pretende que -N(Rh)2 incluya, pero no se limite a 1 -pirrolidinilo y 4-morfolinilo. Cualquiera o más del hidrógeno, alquilo, fluoroalquilo, carbociclilo, carbociclilalquilo, arilo, aralquilo, heterociclilo, heterociclilalquilo, heteroarilo o heteroarilalquilo están opcionalmente sustituidos con uno o más sustituyentes que son independientemente alquilo, heteroalquilo, alquenilo, alquinilo, cicloalquilo, heterocicloalquilo, arilo, arilalquilo, heteroarilo, heteroarilalquilo, hidroxi, halo, ciano, trifluorometilo, trifluorometoxi, nitro, trimetilsililo, -ORi, -SRi, -OC(O)Ri, -N(Ri)2 , -C(O)Ri, -C(O)ORi, -OC(O)N(Ri)2 , -C(O)N(Ri)2 , -N(Ri)C(O)OR, -N(Ri)C(O)Ri, - N(Ri)C(O)N(Ri)2 , N(Ri)C(NRi)N(Ri)2 , -N(Ri)S(O)tRi (en que t es 1 o 2), -S(O) o -S(O)tN(Ri)2 (en que t es 1 o 2), en que cada uno de los Ri es independientemente hidrógeno, alquilo, fluoroalquilo, carbociclilo, carbociclilalquilo, arilo, aralquilo, heterociclilo, heterociclilalquilo, heteroarilo o heteroarilalquilo.
"Carbamato", tal como se utiliza en esta memoria, se refiere a un resto unido a un grupo amino que tiene la fórmula -C(O)OR, en que R es alquilo, fluoroalquilo, carbociclilo, carbociclilalquilo, arilo, aralquilo, heterociclilo, heterociclilalquilo, heteroarilo o heteroarilalquilo. Ejemplos incluyen, pero no se limitan a un grupo Boc (ferc.-butil-OC(O)-), CBz (bencil-OC(O)-), Teoc (Me3SiCH2CH2OC(O)-), aloc (alil-OC(O)-) o Fmoc (9-fluorenilmetil-OC(O)-).
"Sililo sustituido", tal como se utiliza en esta memoria, se refiere a un resto que tiene la fórmula R3Si-. Ejemplos incluyen, pero no se limitan a, el grupo TBDMS (ferc.-butildimetilsililo), TBDPS (ferc.-butildifenilsililo) o TMS (trimetilsililo).
El término "tiol" se refiere a grupos -SH e incluye grupos tiol sustituidos, es decir, grupos -SRJ, en donde RJ son, cada uno independientemente, un grupo alquilo, cicloalquilo, alquenilo, alquinilo, arilaralquilo, heterociclilo o heterociclilalquilo sustituido o no sustituido tal como se define en esta memoria.
El primer aspecto de la invención se refiere a un reactivo quiral o una sal del mismo tal como se define en la reivindicación 1. El reactivo quiral tiene la siguiente fórmula química (I). La expresión "reactivo quiral" es una composición química que se utiliza para producir derivados de nucleótidos u oligonucleótidos modificados con átomos de fósforo estereocontrolados. El reactivo quiral reacciona con un nucleótido para formar un compuesto intermedio quiral.
En la fórmula (I), G1 es un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo de fórmula (II), (III) o (V), G2 es un grupo nitro, un grupo ciano, o un grupo de fórmula (II), (III) o (V), o tanto G1 como G2 se toman juntos para formar un grupo de fórmula (IV).
En la fórmula (II), G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3. Ejemplos preferidos de G21 a G23 son un átomo de hidrógeno.
En la fórmula (III), G31 a G33 son independientemente grupo alquilo C1-4, grupo arilo C6-14, grupo alcoxi C1-4, grupo aralquilo C7-14, grupo alquil C1-4 arilo Ca-14, grupo alcoxi C1-4 arilo C6-14 o grupo aril C6-14 alquilo C1-4. Ejemplos de un grupo alquil C1-4 arilo Ca-14 son un grupo metilfenilo y un grupo etilfenilo. Ejemplos de un grupo alcoxi C1-4 arilo Ca-14 son un grupo metoxifenilo y un grupo etoxifenilo. Ejemplos de un grupo alquil Ca-14 arilo C1-4 son un grupo bencilo y un grupo feniletilo. Ejemplos preferidos de G31 a G33 son independientemente un grupo metilo y un grupo fenilo.
En la fórmula (IV), G41 a G4a son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3. Ejemplos preferidos de G41 a G4a son un átomo de hidrógeno.
En la fórmula (V), G51 a G53 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano, un grupo alquilo C1-3 o alquil C1-3oxi.
G3 y G4 se toman juntos para formar un anillo que contiene heteroátomos que tiene de 3 a 16 átomos de carbono. Ejemplos preferidos de G3 y G4 se toman juntos para formar un anillo que contiene heteroátomos que tiene de 3 a 16 átomos de carbono, con el resto NH en la fórmula (I).
Una realización preferida es que el reactivo quiral tiene la siguiente fórmula química (I').
En la fórmula (I'), G1 y G2 son los mismos que arriba.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y cada uno de G1 y G2 es un grupo de fórmula (II), en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y cada uno de G1 y G2 es un grupo de fórmula (II) y cada uno de G21 a G23 es un átomo de hidrógeno.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (II) y G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (II) y cada uno de G21 y G22 es un átomo de hidrógeno y G23 es un grupo nitro (-NO2).
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), y G31 a G33 son independientemente un grupo alquilo C1-4, un grupo arilo Ca-14, un grupo aralquilo C7-14, un grupo alquil C1-4 arilo Ca-14, un grupo alcoxi C1-4 arilo Ca-14 o un grupo aril Ca-14 alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), y G31 a G33 son independientemente un grupo alquilo C1-4, un grupo arilo Ca, un grupo aralquilo C7-10, un grupo alquil C1-4 arilo Ca, un grupo alcoxi C1-4 arilo Ca o un grupo aril Ca alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (III) y G31 a G33 son independientemente un grupo alquilo C1-4 o un grupo arilo Ca (un grupo fenilo). Ejemplos de grupo alquilo C1-4 son grupo metilo, grupo etilo, grupo n-propilo, grupo /so-propilo, grupo n-butilo y grupo ferc.—butilo.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (III) y G31 a G33 son independientemente un grupo alquilo C1-4.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (III) y G31 y G33 son un grupo arilo Ca (un grupo fenilo) y G32 es grupo alquilo C1-2.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 y G2, tomados juntos para formar un grupo de fórmula (IV), y G41 a G4a son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y cada uno de G1 y G2, tomados juntos para formar un grupo de fórmula (IV), en donde cada uno de G41 a G4a es un átomo de hidrógeno.
Una realización preferida es aquella en la que el reactivo quiral tiene la fórmula química (I') y G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (V). Además, cada uno de G51 a G53 es independientemente un átomo de hidrógeno, un grupo nitro, un grupo metilo o un grupo metoxi. Una realización más preferida es aquella en la que G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (V), en donde cada uno de G51 a G53 es un átomo de hidrógeno y G53 es un grupo 4-metilo.
Una realización preferida es aquella en la que el reactivo quiral se selecciona de uno de IlI-a, IlI-b, V-a, VlI-a, VlI-b, IX-a, IX-b, XI-a, XIII-a y XIII-b:
(S)-2-(metildifenilsilil)-1-((S)-pirrolidin-2-il)etanol (III-a)
(R) -2-(metildifenilsilil)-1-((R)-1-pirrolidin-2-il)etanol (III-b)
(S) -2-(trimetilsilil)-1-((S)-1-pirrolidin-2-il)etanol (V-a)
(R) -2,2-difenil-1-((S)-pirrolidin-2-il)etanol (VII-a)
(S) -2,2-difenil-1-((R)-pirrolidin-2-il)etanol (VII-b)
(R) -2-(4-nitrofenil)-1 -((S)-pirrolidin-2-il)etanol (IX-a)
(S) -2-(4-nitrofenil)-1 -((R)-pirrolidin-2-il)etanol (IX-b)
(R) -(9H-fluoren-9-il)((S)-pirrolidin-2-il)metanol (XI-a)
(S) -2-tosil-1-((S)-pirrolidin-2-il)etanol (XIII-a)
(R)-2-tosil)-1-((R)-pirrolidin-2-il)etanol (XIII-b)
El reactivo quiral reacciona con un ácido nucleico o ácido nucleico modificado para ser un grupo auxiliar asimétrico. Un derivado de nucleósido 3'-fosforamidita, que es un compuesto intermedio de la fabricación de un derivado de oligonucleótido modificado con átomo de fósforo estereocontrolado, se obtiene mediante la reacción de un reactivo quiral con un ácido nucleico o ácido nucleico modificado.
El segundo aspecto de la invención se refiere a un derivado de nucleósido 3'-fosforamidita que está representado por la fórmula (Va) o (Vb) según se define en la reivindicación 5. Los compuestos de fórmula (Va) y (Vb) se conocen como
monómeros que se utilizan en la síntesis de derivados de oligonucleótidos. Estos compuestos también se conocen como monómeros de oxazafosfolidina. Los restos de azúcar de los compuestos representados por la fórmula (Vb) se conocen como BNA y LNA (cuando R3 es un grupo metileno).
En las fórmulas (Va) y (Vb), G1 a G4 son iguales que arriba, G5 es un grupo protector del grupo hidroxilo y Bs es un grupo seleccionado de los grupos representados por las fórmulas (VI) a ( XI) o derivados de los mismos.
Ejemplos de Bs son una adenina, una timina, una citosina, una guanina, un uracilo, una 5-metilcitosina o un derivado de los mismos.
R2 es hidrógeno, -OH, -SH, -NRdRd, -N3 , halógeno, alquilo, alquenilo, alquinilo, alquil-Y1-, alquenil-Y1-, alquinil-Y1-, aril-Y1-, heteroaril-Y1-, -ORb o -SRb, en donde Rb es un resto de bloqueo.
Y1 es O, NRd, S o Se.
Rd es es independientemente hidrógeno, alquilo, alquenilo, alquinilo, arilo, acilo, sililo sustituido, carbamato, -P(O)(Re )2 o -HP(O)(Re).
Re es independientemente hidrógeno, alquilo, arilo, alquenilo, alquinilo, alquil-Y2-, alquenil-Y2-, alquinil-Y2-, aril-Y2- o heteroaril-Y2- o un catión que es Na+, Li+ o K+.
Y2 es O, NRd o S.
Ejemplos preferidos de alquilo son el grupo alquilo C1-10, ejemplos preferidos de alquenilo son alquenilo C2-10, ejemplos preferidos de alquinilo son alquinilo C2-10, ejemplos preferidos de arilo son arilo C6-14 y ejemplos preferidos de heteroarilo son heteroarilo C6-14.
R3 es un grupo representado por -CH2-, -(CH2)2-, -CH2NH- o -CH2N(CH3)-.
Ejemplos de G5 son tritilo, 4-monometoxitritilo, 4,4'-dimetoxitritilo, 4,4',4"-trimetoxitritilo, 9-fenilxantin-9-ilo (pixilo) y 9-(p-metoxifenil)xantin-9-ilo (MOX).
Los Bs son una adenina, una timina, una citosina, una guanina o un derivado de los mismos. Los Bs son una nucleobase o una nucleobase modificada. Los ejemplos de los derivados son los descritos en el documento JP 2005 89441 A y se representan como sigue.
En la fórmula anterior, cada uno de R8 a R10 es independientemente alquilo C1-10, arilo C6-C10, aralquilo C6-C10 o aril C6-C10oxialquilo. Ejemplos preferidos de R8 son metilo, isopropilo, fenilo, bencilo y fenoximetilo. Ejemplos preferidos de R9 y R10 son grupos alquilo C1-4.
Una realización preferida del segundo aspecto es aquella en la que el derivado de nucleósido 3'-fosforamidita está representado por la fórmula (Va') o (Vb').
En la fórmula (Va') y (Vb'), G1, G2, G5, Bs, R2 y R3 son iguales que arriba. El derivado de nucleósido 3'-fosforamidita es un monómero quiral que se utiliza para producir nucleótidos modificados con átomos de fósforo estereocontrolados y derivados de oligonucleótidos.
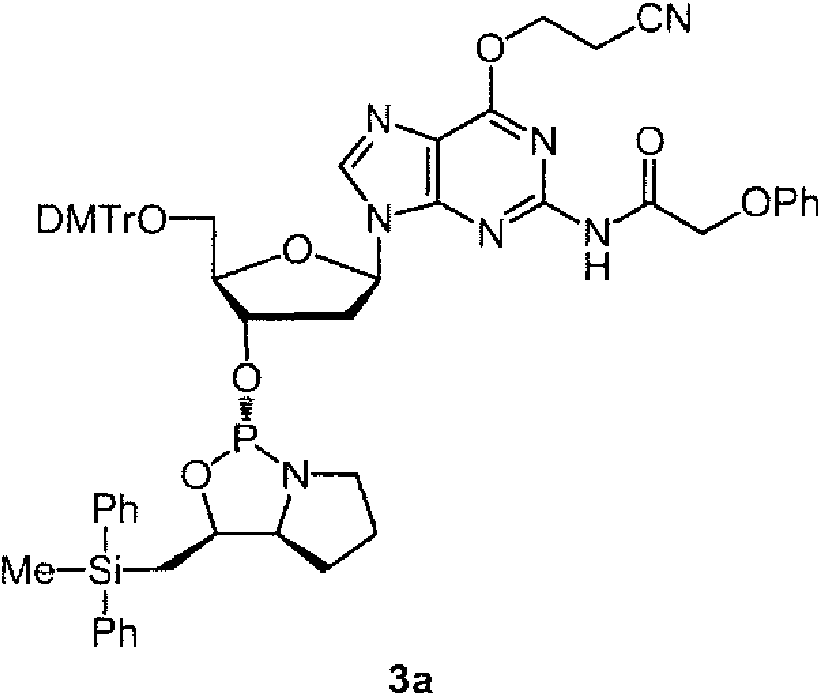
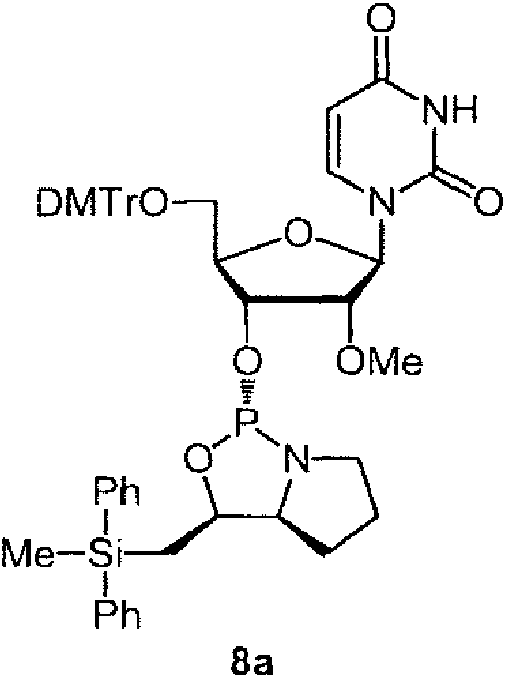
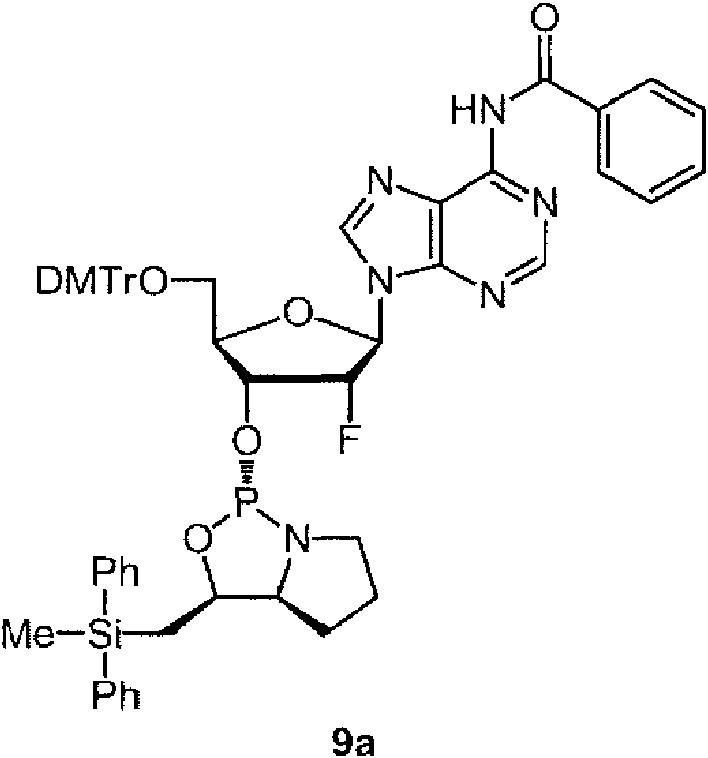
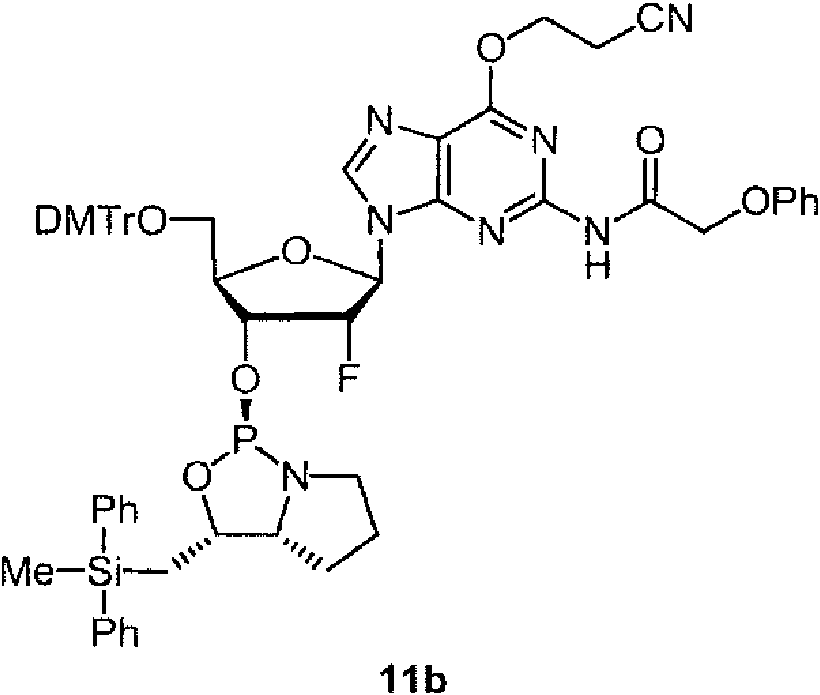
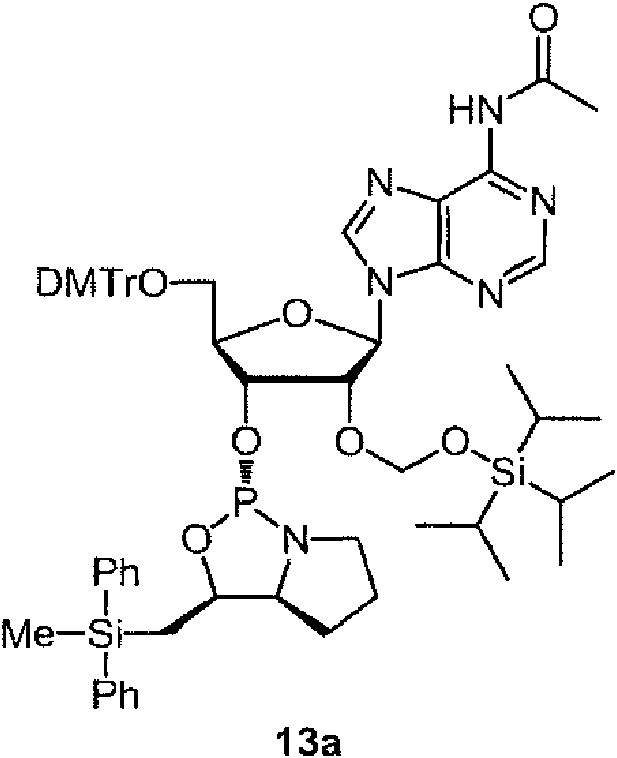
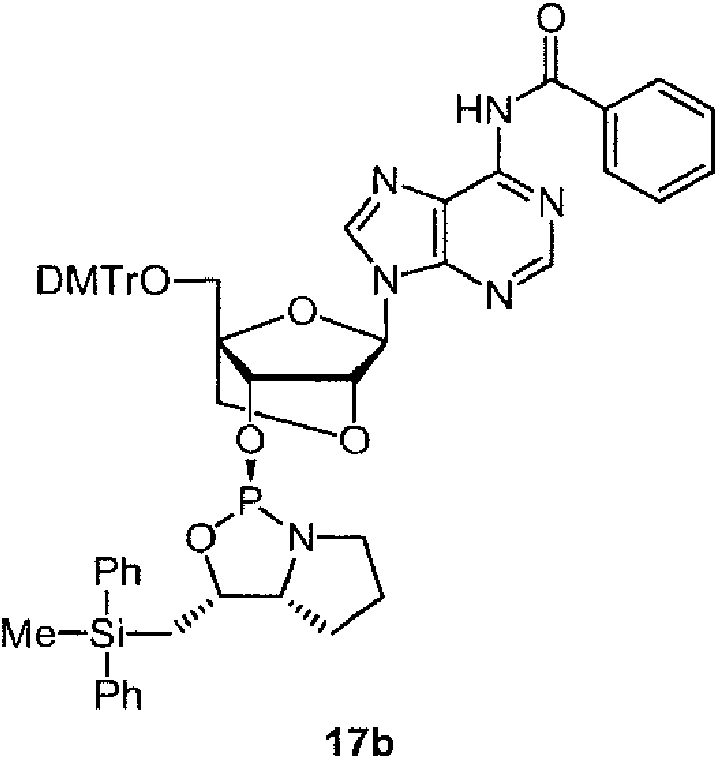
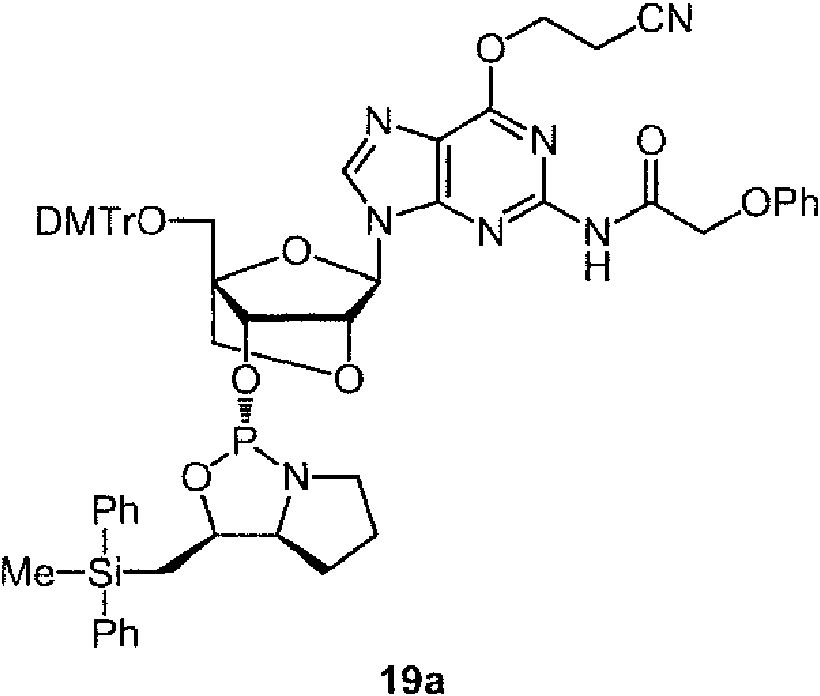
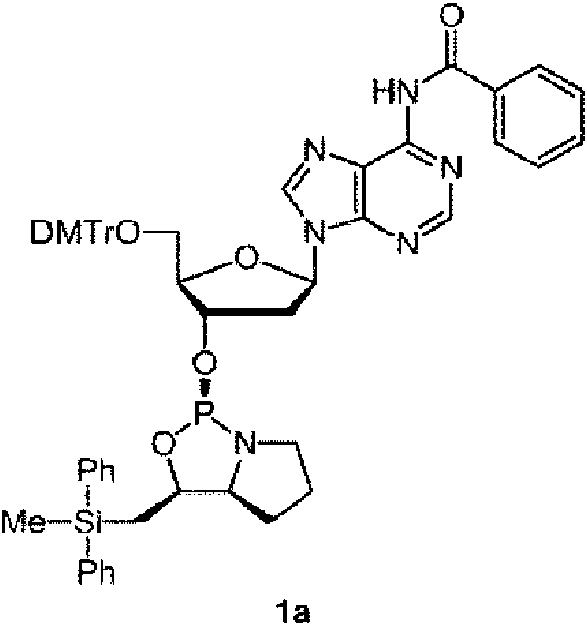
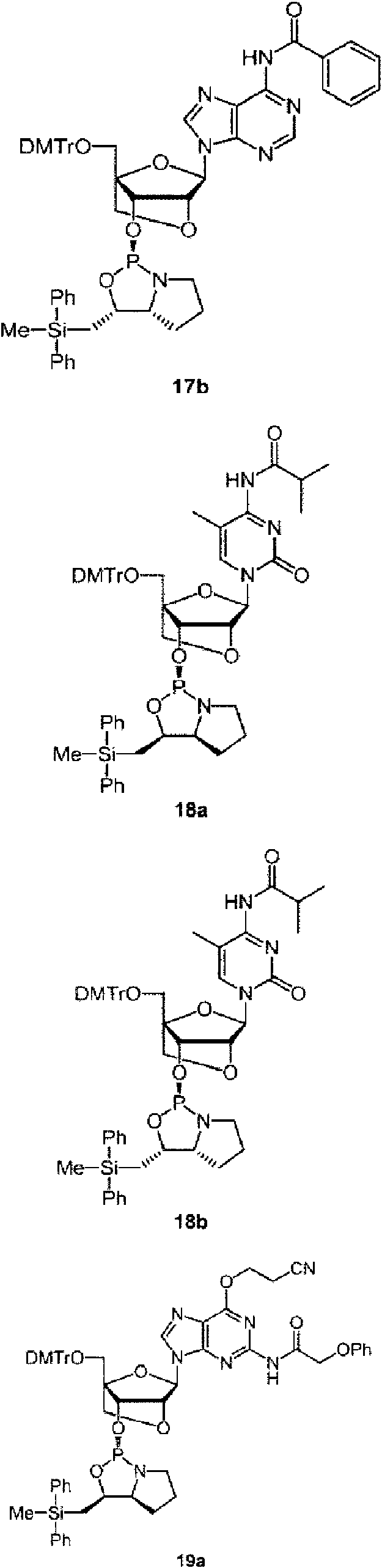
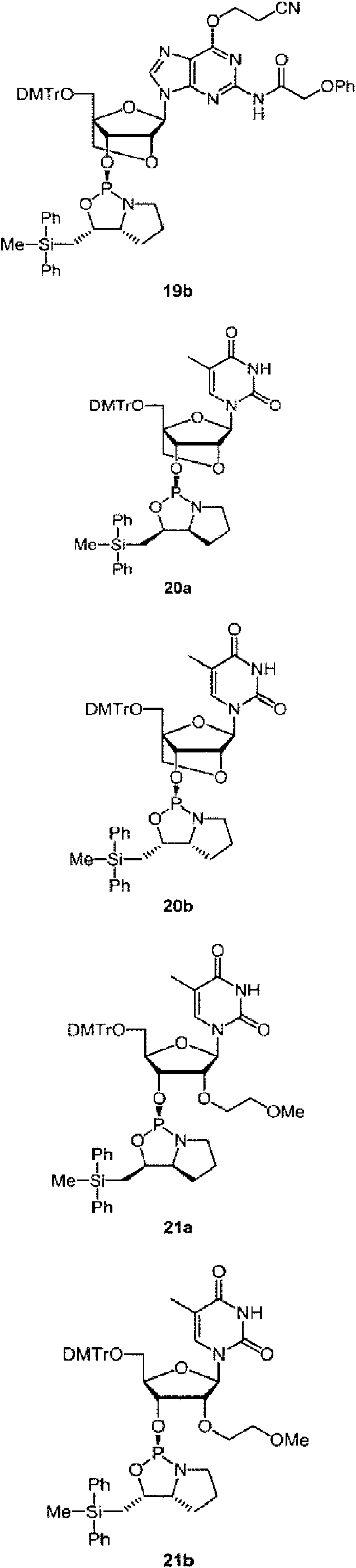
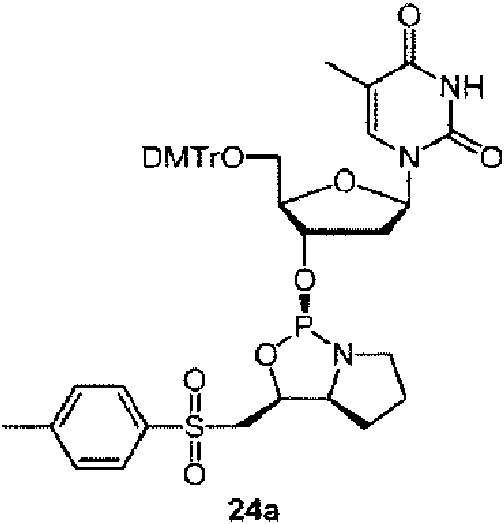
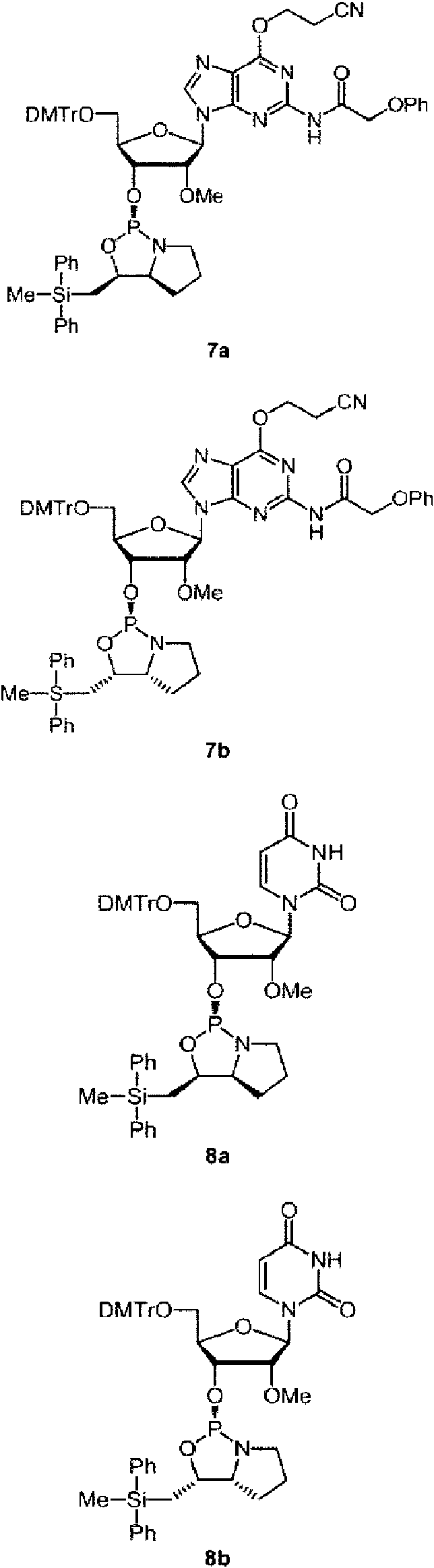
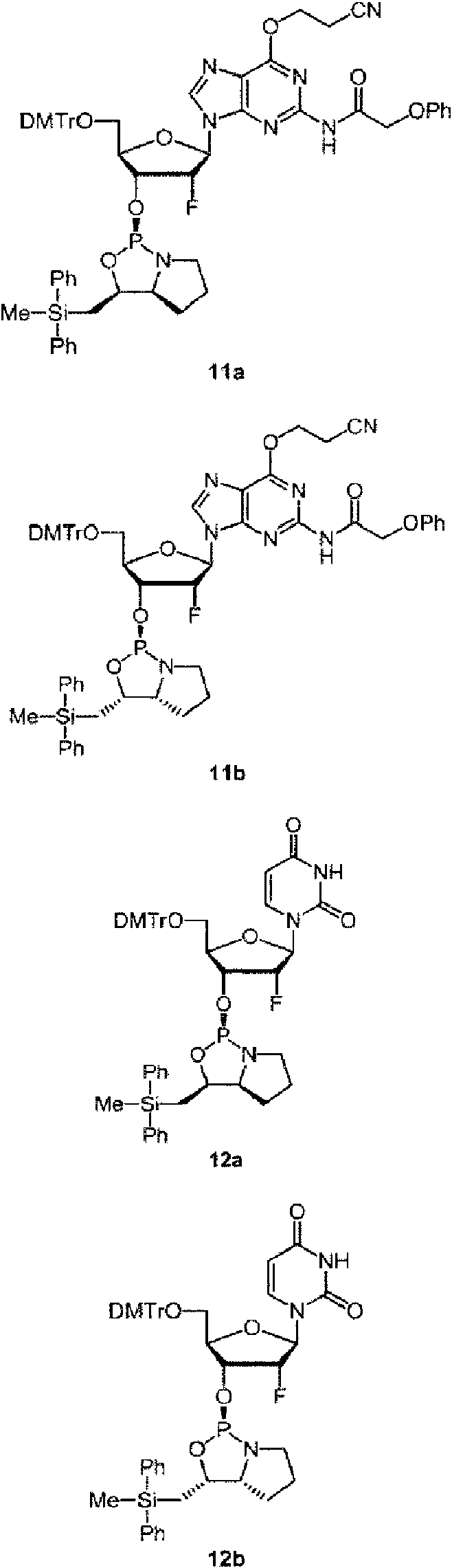
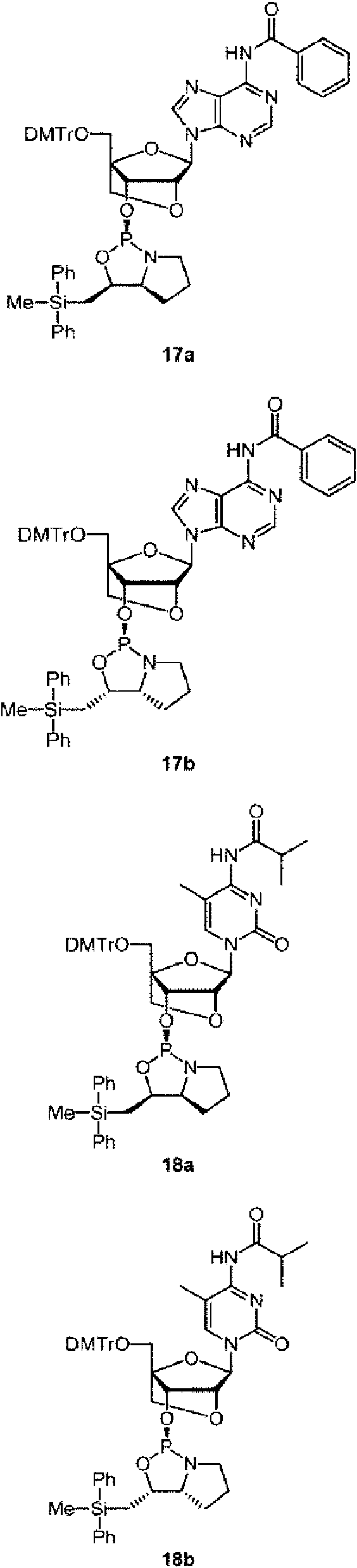
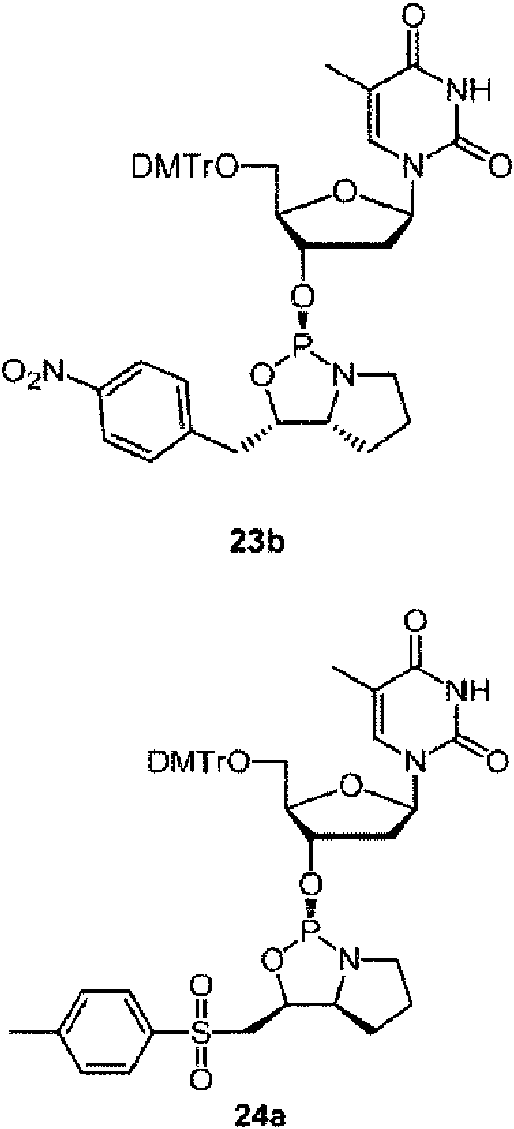
Ejemplos preferidos de los derivados de nucleósido 3'-fosforamidita están representados por la fórmula 1a, 1b, 2a, 2b, 3a, 3b, 4a, 4b, 5a, 5b, 6a, 6b, 7a, 7b, 8a, 8b, 9a, 9b, 10a, 10b, 11a, 11b 12a, 12b, 13a, 13b, 14a, 14b, 15a, 15b, 16a, 16b, 17a, 17b, 18a, 18b, 19a, 19b, 20a, 20b, 21a, 21b, 22a, 22b, 23a, 23b, o 24a. Estas fórmulas se describen en la sección Experimental.
DMTr representa un grupo 4,4'-dimetoxitritilo y TOM representa un grupo triisopropilsiloximetilo.
Los ejemplos de utilizar el derivado de nucleósido 3'-fosforamidito se describen, p. ej., en el documento JP 2005 89441 A. Repitiendo las etapas de condensación y desprotección, es posible alargar la cadena de derivados de oligonucleótidos como se describe allí.
La fórmula de un derivado de oligonucleótido de este tipo se muestra en la fórmula (X).
En la fórmula (X), X representa sulfuro (= S), alquilo C1-3, alcoxi C1-3, alquil Ci-3tio, arilo C6-C10, aralquilo C6-C10 o aril C6-Cioox¡alqu¡lo. Preferiblemente, X representa sulfuro (= S). "n" es un número entero que representa de 1 a 150, de 1 a 100, de 1 a 50 o de 1 a 30. "n" puede ser preferiblemente de 2 a 100, preferiblemente de 10 a 100, preferiblemente de 10 a 50 y más preferiblemente de 15 a 30.
El tercer aspecto de la invención se refiere a un método para la síntesis de un derivado de oligonucleótido modificado con un átomo de fósforo estereocontrolado según se define en la reivindicación 8. La primera etapa es una etapa de hacer reaccionar una molécula que comprende un resto H-fosfonato aquiral, el primer reactivo de activación y un reactivo quiral o una sal del mismo para formar un monómero. El reactivo quiral tiene la fórmula química (I) o (I') y el monómero puede estar representado por las fórmulas (Va), (Vb), (Va') o (Vb'). El monómero reacciona con el segundo reactivo activador y un nucleósido para formar un compuesto intermedio condensado. La siguiente etapa es una etapa de convertir el compuesto intermedio condensado en el ácido nucleico que comprende un resto X-fosfonato quiral. El método se basa básicamente en la divulgación del documento WO 2010/064146. Es decir, los etapas fundamentales se describen como ruta A y ruta B en el mismo. En el método se utiliza el reactivo quiral de la presente invención.
El primer esquema se refiere a la síntesis de Oligos Quirales.
Se trata un resto de H-fosfonato aquiral con el primer reactivo de activación para formar el primer compuesto intermedio. En una realización, el primer reactivo activador se añade a la mezcla de reacción durante la etapa de condensación. El uso del primer reactivo de activación depende de las condiciones de reacción tales como los disolventes que se utilizan para la reacción. Ejemplos del primer reactivo activador son fosgeno, cloroformiato de triclorometilo, carbonato de bis(triclorometilo) (BTC), cloruro de oxalilo, Ph3PCl2, (PhO)3PCl2, cloruro N,W-bis(2-oxo-3-oxazolidinil)fosfínico (BopCl), hexafluorofosfato de 1,3-dimetil-2-(3-nitro-1,2,4-triazol-1-il)-2-pirrolidin-1-il-1,3,2-diazafosfolidinio (MNTP) o hexafluorofosfato de 3-nitro-1,2,4-triazol-1-il-tris(pirrolidin-1-il)fosfonio (PyNTP).
El ejemplo de resto de H-fosfonato aquiral es un compuesto mostrado en el Esquema anterior. DBU representa 1,8-diazabiciclo[5.4.0]undec-7-eno. H+DBU puede ser, por ejemplo, ion amonio, ion alquilamonio, ion iminio heteroaromático o ion iminio heterocíclico, cualquiera de los cuales es primario, secundario, terciario o cuaternario, o un ion metálico monovalente.
Reacción con Reactivo Quiral
Después de la primera etapa de activación, el resto de H-fosfonato aquiral activado reacciona con un reactivo quiral, que está representado por la fórmula (I) o (I'), para formar un compuesto intermedio quiral de fórmula (Va), (Vb), (Va') o (Vb').
Etapa de Condensación Estereoespecífica
Un compuesto intermedio quiral de Fórmula Va ((Vb), (Va') o (Vb')) se trata con el segundo reactivo activador y un nucleósido para formar un compuesto intermedio condensado. El nucleósido puede solidificarse. Ejemplos del segundo reactivo activador son 4,5-dicianoimidazol (DCI), 4,5-dicloroimidazol, triflato de 1-fenilimidazolio (PhIMT), triflato de bencimidazolio (BIT), benzotriazol, 3-nitro-1,2,4-triazol ( NT), tetrazol, 5-etiltiotetrazol (ETT), 5-benciltiotetrazol (BTT), 5-(4-nitrofenil)tetrazol, triflato de N-cianometilpirrolidinio (CMPT), triflato de N-cianometilpiperidinio, triflato de N-cianometildimetilamonio. Un compuesto intermedio quiral de fórmula Va ((Vb), (Va') o (Vb')) se puede aislar como un monómero. Habitualmente, el compuesto intermedio quiral de Va ((Vb), (Va') o (Vb')) no se aísla y se somete a una reacción en el mismo recipiente con un nucleósido o nucleósido modificado para proporcionar un compuesto de fosfito quiral, un compuesto intermedio condensado. En otras realizaciones, cuando el método se realiza mediante síntesis en fase sólida, el soporte sólido que comprende el compuesto se separa por filtración de productos secundarios, impurezas y/o reactivos.
Etapa de rematado
Si el ácido nucleico final es más grande que un dímero, el resto -OH que no ha reaccionado se remata con un grupo bloqueante y el auxiliar quiral en el compuesto también se puede rematar con un grupo bloqueante para formar un compuesto intermedio condensado rematado. Si el ácido nucleico final es un dímero, entonces no es necesario la etapa de rematado.
Etapa de Modificación
El compuesto se modifica por reacción con un electrófilo. El compuesto intermedio condensado rematado se puede ejecutar en la etapa de modificación. En algunas realizaciones del método, la etapa de modificación se realiza utilizando un electrófilo de azufre, un electrófilo de selenio o un agente boronante. Los ejemplos preferidos de etapas de modificación son las etapas de oxidación y sulfuración.
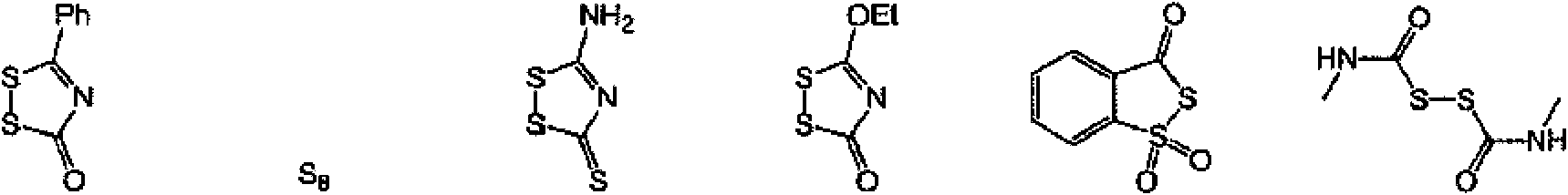
En algunas realizaciones del método, el electrófilo de azufre es un compuesto que tiene una de las siguientes fórmulas:
S8 (Fórmula B), Z1-S-S-Z2 o Z1-S-V-Z2.
Z1 y Z2 son independientemente alquilo, aminoalquilo, cicloalquilo, heterocíclico, cicloalquilalquilo, heterocicloalquilo, arilo, heteroarilo, alquiloxi, ariloxi, heteroariloxi, acilo, amida, imida o tiocarbonilo, o Z1 y Z2 se toman juntos para formar un anillo alicíclico o heterocíclico de 3 a 8 miembros, que puede estar sustituido o no sustituido; V es SO2 , O o NRf; y Rf es hidrógeno, alquilo, alquenilo, alquinilo o arilo.
En algunas realizaciones del método, el electrófilo de azufre es un compuesto de la siguiente Fórmula A, B, C, D, E o F:
Fórmula A Fórmula B Fórmula C Fórmula D Fórmula E Fórmula F
En algunas realizaciones del método, el electrófilo de selenio es un compuesto que tiene una de las siguientes fórmulas:
Se (Fórmula G), Z3-Se-Se-Z4 o Z3-Se-V-Z4
Z3 y Z4 son independientemente alquilo, aminoalquilo, cicloalquilo, heterocíclico, cicloalquilalquilo, heterocicloalquilo, arilo, heteroarilo, alquiloxi, ariloxi, heteroariloxi, acilo, amida, imida o tiocarbonilo, o Z3 y Z4 se toman juntos para formar
un anillo alicíclico o heterocíclico de 3 a 8 miembros, que puede estar sustituido o no sustituido; V es SO2 , O o NRf; y Rf es hidrógeno, alquilo, alquenilo, alquinilo o arilo.
En algunas realizaciones del método, el electrófilo de selenio es un compuesto de Fórmula G, H, I, J, K o L.
En algunas realizaciones del método, el agente boronante es borano-W,W-diisopropiletilamina (BH3 DIPEA), boranopiridina (BH3 Py), borano-2-cloropiridina (BH3 CPy), borano-anilina (BH3 An), borano-tetrahidrofurano (BH3 THF), o borano-sulfuro de dimetilo (BH3 Me2S).
En algunas realizaciones del método, el etapa de modificación es la etapa de oxidación. La etapa de oxidación se describe, p. ej., en los documentos JP 2010-265304 A y WO2010/064146.
Ciclo de Alargamiento de Cadena y Etapa de Desprotección
El compuesto intermedio condensado rematado se desbloquea para eliminar el grupo de bloqueo en el extremo 5' de la cadena de ácido nucleico en crecimiento para proporcionar un compuesto. Opcionalmente, se permite que el compuesto vuelva a entrar en el ciclo de alargamiento de la cadena para formar un compuesto intermedio condensado, un compuesto intermedio condensado rematado, un compuesto intermedio condensado rematado modificado y un compuesto intermedio rematado modificado 5'-desprotegido. Después de al menos una ronda de ciclo de alargamiento de la cadena, el compuesto intermedio rematado modificado 5'-desprotegido se desbloquea adicionalmente mediante la eliminación del ligando auxiliar quiral y otros grupos protectores, p. ej., nucleobase, nucleobase modificada, azúcar y grupos protectores de azúcar modificado, para proporcionar un ácido nucleico. En otras realizaciones, el nucleósido que comprende un resto 5'-OH es un compuesto intermedio de un ciclo de alargamiento de cadena anterior tal como se describe en esta memoria. En aún otras realizaciones, el nucleósido que comprende un resto 5'-OH es un compuesto intermedio obtenido a partir de otro método de síntesis de ácido nucleico conocido. En realizaciones en las que se utiliza un soporte sólido, el ácido nucleico modificado con átomo de fósforo se escinde luego del soporte sólido. En determinadas realizaciones, los ácidos nucleicos se dejan unidos al soporte sólido con fines de purificación y luego se escinden del soporte sólido después de la purificación.
Basado en el presente método, es posible utilizar materiales estables y disponibles comercialmente como materiales de partida. Es posible producir derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados utilizando un material de partida aquiral.
Como se muestra en un ejemplo de trabajo, el método de la presente invención no provoca degradaciones bajo las etapas de desprotección. Además, el método no requiere agentes de terminación de cadena especiales para producir derivados de oligonucleótidos modificados con átomos de fósforo.
El cuarto aspecto de la invención se refiere a un método para la síntesis de derivados de oligonucleótidos modificados con un átomo de fósforo estereocontrolados utilizando un monómero quiral según se define en la reivindicación 11. La primera etapa es hacer reaccionar un derivado de nucleósido 3'-fosforamidita que está representado por la fórmula (Va), (Vb), (Va') o (Vb') con el segundo reactivo activador y un nucleósido para formar un compuesto intermedio condensado. La segunda etapa es convertir el compuesto intermedio condensado en el ácido nucleico que comprende un resto X-fosfonato quiral.
El segundo Esquema se refiere a la síntesis de Oligos Quirales utilizando un monómero de Fórmula Va ((Vb), (Va') o (Vb')). El segundo Esquema basado en el método descrito en el documento JP 2005-89441 A.
Las condiciones detalladas del esquema anterior son similares a las del primer esquema. El material de partida de fórmula Va (Vb), especialmente de fórmula Va' (o Vb'), es químicamente estable. Como se muestra en un ejemplo de trabajo, el método de la presente invención no provoca degradaciones bajo las etapas de desprotección. Además, el método no requiere agentes de terminación de cadena especiales para producir derivados de oligonucleótidos modificados con átomos de fósforo.
El mecanismo para la eliminación de auxiliares se muestra como sigue:
En el esquema anterior, Nu representa Nucleófilo. Se cree que el mecanismo anterior es diferente del mecanismo previo para la eliminación de auxiliares.
[EJEMPLOS]
Abreviaturas
ac: acetilo
bz: benzoilo
CSO: (1 S)-(+)-(10-alcanforsulfonil)oxaziridina
DBU: 1,8-diazabiciclo[5.4.0]undec-7-eno
DCA: ácido dicloroacético
DCM: diclorometano, CH2Cl2
DMTr: 4,4-dimetoxitritilo
Tr: tritilo, trifenilmetilo
Melm: W-metilimidazol
NIS: W-yodosuccinimida
pac: fenoxiacetilo
Ph: fenilo
PhIMT: triflato de W-fenilimidazolio
POS: 3-fenil-1,2,4-ditiazolin-5-ona
TBS: ferc.-butildimetilsililo
TBDPS: ferc.-butildifenilsililo
TOM: triisopropiisiloximetilo
TFA: ácido trifluoroacético
[Ejemplo 1]
(S)-1-tritilpirrolidin-2-carbaldehído (I-a).
Compuesto I-a se sintetizó a partir de L-prolina de acuerdo con el procedimiento descrito en la bibliografía (Guga, P. Curr. Top. Med.Chem. 2007, 7, 695-713.).
[Ejemplo 2]
(R-1-tritilpirrolidin-2-carbaldehído (I-b).
Compuesto I-b se sintetizó a partir de D-prolina de una manera similar al compuesto I-a.
[Ejemplo 3]
(S)-2-(metildifenilsilil)-1-((S)-1-tritilpirrolidin-2-il)etanol (II-a).
A una solución de cloruro de metildifenilsililmetil magnesio en THF, preparada a partir de clorometildifenilmetilsilano (4,02 g, 16,3 mmol) y magnesio (402 mg, 16,3 mmol) en THF (14 mL) se añadió solución de I-a (2,79 g, 8,14 mmol) en THF (30 mL). con enfriamiento con hielo. Después de agitar durante 1,5 h con enfriamiento con hielo, la mezcla se calentó a temperatura ambiente y se continuó agitando durante 30 min. Se añadió NH4Cl acuoso saturado (100 mL) a la mezcla de reacción a 0 grados C y se realizó la extracción con dietil éter (100 mL) tres veces. El extracto combinado se secó sobre Na2SO4, se filtró y se concentró a presión reducida. El residuo se cromatografió sobre gel de sílice, proporcionando II-a en forma de una espuma incolora (3,91 g, 87%).
1H RMN (300 MHz, CDCla) 67,48-7,08 (25H, m), 4,33-4,23 (1H, m), 3,16-2,89 (3H, m), 2,84 (1H, s a), 1,70-1,54 (1H, m), 1,35 (1H, dd, J = 14,7, 6,3Hz), 1,10 (1H, dd, J = 14,7, 8,1Hz), 1,18-1,05 (1H, m), 1,04-0,90 (1H, m), 0,34 (3H, s), -0,17- -0,36 (1H, m).
[Ejemplo 4]
(S)-2-(metildifenilsilil)-1-((S)-pirrolidin-2-il)etanol (III-a).
II-a (3,91 g, 7,06 mmol) se disolvió en DCA al 3% en DCM (70 mL) y se agitó durante 10 min a temperatura ambiente. A la mezcla se añadió NaOH 1 M (200 mL) y la extracción se realizó con DCM (100 mL) tres veces. El extracto
combinado se secó sobre Na2SÜ4, se filtró y se concentró a presión reducida. El residuo se cromatografió sobre gel de sílice, proporcionando IlI-a en forma de un aceite amarillo (1,99 g, 90%).
1H RMN (300 MHz, CDCls) ó 7,57-7,52 (5H, m), 7,38-7,33 (5H, m), 3,77 (1H, ddd, J = 8,9, 5,4, 3,5Hz), 3,01 (1H, dt, J = 7,4, 3,6Hz), 2,97-2,79 (2H, m), 2,27 (2H, s a), 1,76-1,53 (4H, m), 1,38 (1H, dd, J = 15,0, 9,0Hz), 1,24 (1H, dd, J = 15,0, 5,4Hz), 0,65 (3H, s); 13C RMN (100,4 MHz, CDCb) ó 137,4, 137,1, 134,6, 134,5, 129,1, 127,8, 69,5, 64,1, 47,0, 25,8, 24,0, 19,6, -3,4. MALDI TOF-MS m/z Calculado para Ci9H26NOSi [M+H]+ 312,18, encontrado 312,06.
[Ejemplo 5]
(R)-2-(metildifenilsilil)-1-((R)-1-tritilpirrolidin-2-il)etanol (ll-b).
Compuesto II-bse obtuvo utilizando I-b en lugar de I-a de una manera similar al compuesto II-a.
1H RMN (300 MHz, CDCla) ó 7,48-7,12 (25H, m), 4,33-4,24 (1H, m), 3,16-2,89 (3H, m), 2,86 (1H, s a), 1,69-1,52 (1H, m), 1,35 (1H, dd, J = 14,4, 6,0Hz), 1,10 (1H, dd, J = 14,4, 8,4Hz), 1,18-1,05 (1H, m), 1,03-0,89 (1H, m), 0,33 (3H, s), -0,19- -0,39 (1H, m); 13C RMN (75,5 MHz, CDCb) ó 144,5, 137,5, 136,8, 134,6, 134,3, 129,8, 129,0, 127,8, 127,7, 127,4, 126,1, 77,9, 71,7, 65,1, 53,5, 25,0, 24,8, 19,6, -4,0. MALDI TOF-MS m/z Calculado para Ca8H4oNOSi [M+H]+ 554,29, encontrado 554,09.
[Ejemplo 6]
(R)-2-(metildifenilsilil)-1-((R)-1-pirrolidin-2-il)etanol (III-b).
Compuesto III-bse obtuvo utilizando II-b en lugar de II-a de una manera similar al compuesto III-a.
1H RMN (300 MHz, CDCb) ó 7,58-7,52 (5H, m), 7,38-7,33 (5H, m), 3,78 (1H, ddd, J = 9,0, 5,1, 3,6Hz), 3,00 (1H, dt, J = 7,4, 3,3Hz), 2,97-2,78 (2H, m), 2,19 (2H, s a), 1,76-1,53 (4H, m), 1,38 (1H, dd, J = 14,6, 9,0Hz), 1,24 (1H, dd, J = 14,6, 5,1Hz), 0,66 (3H, s); 13C RMN (75,5 MHz, CDCla) ó 137,5, 137,1, 134,5, 134,4, 129,0, 127,7, 69,2, 64,2, 46,9, 25,8, 24,0, 19,7, -3,4. MALDI TOF-MS m/z Calculado para C19H26NOSi [M+H]+ 312,18, encontrado 312,09.
[Ejemplo 7]
(S)-2-(trimetillsilil)-1-((S)-1-tritilpirrolidin-2-il)etanol (IV-a).
Compuesto IV-ase obtuvo utilizando "clorometiltrimetilsilano" en lugar de "clorometildifenilmetilsilano" de una manera similar al compuesto II-a.
1H RMN (300 MHz, CDCb) ó 7,58-7,51 (5H, m), 7,31-7,14 (10H, m), 4,13 (1H, dt, J = 7,5, 3,0Hz), 3,39-3,31 (1H, m), 3,20-2,99 (2H, m), 2,84 (1H, s), 1,74-1,57 (1H, m), 1,29-1,10 (2H, m), 0,74 (1H, dd, J = 14,4, 7,2Hz), 0,46 (1H, dd, J = 14,4, 7,2Hz), -0,15 (9H, s). MALDI TOF-MS m/z Calculado para C28H36NOSi [M+H]+ 430,26, encontrado 430,09.
[Ejemplo 8]
(S)-2-(trimetilsilil)-1-((S)-1-pirrolidin-2-il)etanol (IV-a).
Compuesto V-ase obtuvo utilizando IV-a en lugar de Il-a de una manera similar al compuesto IlI-a.
1H RMN (300 MHz, CDCls) 63,76 (1H, ddd, J = 8,8, 5,7, 3,3Hz), 3,08 (1H, dt, J = 7,8, 3,3Hz), 3,02-2,87 (2H, m), 2,48 (2H, s a), 1,81-1,58 (4H, m), 0,83 (1H, dd, J = 14,7, 8,7Hz), 0,68 (1H, dd, J = 14,7, 6,0Hz), 0,05 (9H, s); 13C RMN (75,5 MHz, CDCla) 669,6, 64,3, 46,9, 25,8, 23,9, 22,0, -0,8. MALDI TOF-MS m/z Calculado para C s^N O S i [M+H]+ 188,15, encontrado 188,00.
[Ejemplo 9]
(R)-2,2-difenil-1-((S)-1-tritilpirrolidin-2-il)etanol (VI-a).
A una solución de difenilmetano (6,7 mL, 40 mmol) en THF anhidro (36 mL) se añadió gota a gota n-BuLi (solución 1,67 M de Hexano, 24 mL, 40 mmol) a temperatura ambiente y se agitó durante 1 h. A la mezcla se añadió lentamente I-a (3,41 g, 10 mmol), que se secó mediante co-evaporaciones repetidas con tolueno, en THF anhidro (40 mL) a 0 grados C y se continuó agitando durante 45 min. Luego se añadieron una solución acuosa saturada de NH4Cl (100 mL) y Et2O (100 mL), se separó la capa orgánica y la capa acuosa se extrajo con Et2O (2 x 100 mL). La capa orgánica se combinó, se secó sobre Na2SO4, se filtró y se concentró a presión reducida. El residuo se purificó mediante cromatografía en gel de sílice para proporcionar VI-a (1,41 g, 28%) en forma de una espuma blanca.
1H RMN (300 MHz, CDCla) 67,45-7,01 (23H, m), 6,67-6,61 (2H, m), 4,80 (1H, d, J = 10,8Hz), 3,63 (1H, d, J = 10,8Hz), 3,36-3,27 (1H, m), 3,23-3,09 (1H, m), 3,02-2,89 (1H, m), 2,66 (1H, s), 1,90-1,75 (1H, m), 1,32-1,04 (2H, m), 0- -0,18 (1H, m).
[Ejemplo 10]
(R)-2,2-difenil-1-((S)-pirrolidin-2-il)etanol (VII-a).
Compuesto VII-ase obtuvo utilizando VI-a en lugar de II-a de una manera similar al compuesto III-a.
1H RMN (300 MHz, CDCla) 67,44-7,38 (2H, m), 7,33-7,14 (8H, m), 4,46 (1H, dd, J = 9,9, 3,3Hz), 3,91 (1H, d, J = 9,9Hz), 3,02-2,88 (2H, m), 2,81-2,69 (1H, m), 2,52 (2H, s a), 1,88-1,56 (4H, m); 13C RMN (75,5 MHz, CDCb) 6142,3, 142,0, 128,6, 128,5, 128,4, 128,2, 126,5, 126,4, 73,5, 60,1,55,8, 46,6, 25,8, 23,4. MALDI TOF-MS m/z Calculado para C18H22NO [M+H]+ 268,17, encontrado 268,06.
[Ejemplo 11]
(S)-2,2-difenil-1-((R)-1-tritilpirrolidin-2-il)etanol (VI-b).
Compuesto Vl-bse obtuvo utilizando I-b en lugar de I-a de una manera similar al compuesto Vl-a.
1H RMN (300 MHz, CDCls) 67,44-7,37 (6H, m), 7,30-7,01 (17H, m), 6,66-6,61 (2H, m), 4,80 (1H, d, J = 10,8Hz), 3,63 (1H, d, J = 10,8Hz), 3,36-3,28 (1H, m), 3,22-3,09 (1H, m), 3,01-2,89 (1H, m), 2,66 (1H, s), 1,90-1,75 (1H, m), 1,29 1,04 (2H, m), 0,00-0,19 (1H, m); 13C RMN (75,5 MHz, CDCla) 6144,2, 142,9, 141,6, 130,0, 128,5, 128,4, 127,9, 127,8, 127,4, 126,4, 126,2, 77,9, 75,9, 61,9, 55,4, 53,4, 24,7, 24,5. MALDI TOF-MS m/z Calculado para Ca7Ha6NO [M+H]+ 510,28, encontrado 510,11.
[Ejemplo 12]
(S)-2,2-difenil-1-((R)-pirrolidin-2-il)etanol (Vll-b).
Compuesto VII-bse obtuvo utilizando VI-b en lugar de VI-a de una manera similar al compuesto VII-a.
1H RMN (300 MHz, CDCls) 67,45-7,14 (10H, m), 4,45 (1H, dd, J = 9,9, 3,3Hz), 3,91 (1H, d, J = 9,9Hz), 3,00-2,89 (2H, m), 2,82-2,71 (1H, m), 2,40 (2H, s a), 1,87-1,55 (4H, m); 13C RMN (75,5 MHz, CDCls) 6 142,3, 142,0, 128,5, 128,3, 128,1, 126,3, 126,2, 73,4, 60,1, 55,9, 46,5, 25,8, 23,5. MALDI TOF-MS m/z Calculado para C18H22NO [M+H]+ 268,17, encontrado 268,03.
[Ejemplo 13]
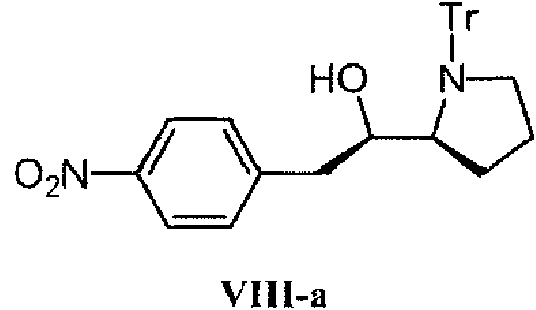
(R)-2-(4-nitrofenil)-1-((S)-1-tritilpirrolidin-2-il)etanol (VIII-a).
Compuesto VIII-ase obtuvo utilizando "cloruro de 4-nitrobencilo" en lugar de "difenilmetano" de una manera similar al compuesto VI-a.
1H RMN (300 MHz, CDCls) 68,09-8,03 (2H, m), 7,49-7,43 (6H, m), 7,28-7,09 (11H, m), 4,23 (1H, ddd, J = 8,3, 5,6, 3,0Hz), 3,43-3,33 (1H, m), 3,23-3,11 (1H, m), 3,07-2,96 (1H, m), 2,83 (1H, s a), 2,74 (1H, dd, J = 13,8, 8,4Hz), 2,49 (1H, dd, J = 13,8, 5,1Hz), 1,83-1,67 (1H, m), 1,41-1,17 (2H, m), 0,27-0,08 (1H, m); 13C RMN (75,5 MHz, CDCta) 6 147,3, 146,3, 144,3, 129,8, 129,6, 127,5, 126,3, 123,4, 77,9, 74,8, 63,5, 53,2, 39,5, 25,0, 24,9. MALDI TOF-MS m/z Calculado para C31H31N2O3 [M+H]+ 479,23, encontrado 479,08.
[Ejemplo 14]
(R)-2-(4-nitrofenil)-1-((S)-pirrolidin-2-il)etanol (IX-a).
Compuesto IX-ase obtuvo utilizando VIII-a en lugar de VI-a de una manera similar al compuesto VII-a.
1H RMN (300 MHz, CDCta) 68,15 (2H, d, J = 8,7Hz), 7,42 (2H, d, J = 8,7Hz), 3,86-3,79 (1H, m), 3,16-3,07 (1H, m), 2,99-2,68 (6H, m), 1,84-1,68 (4H, m); 13C RMN (75,5 MHz, CDCb) 6147,4, 146,2, 129,9, 123,2, 72,4, 62,0, 46,6, 40,4, 25,7, 24,4. MALDI TOF-MS m/z Calculado para C12H1/N2O3 [M+H]+ 237,12, encontrado 237,01.
[Ejemplo 15]
(S)-2-(4-nitrofenil)-1 -((R)-1-tritilpirrolidin-2-il)etanol (VIII-b).
Compuesto VlII-bse obtuvo utilizando I-b en lugar de I-a de una manera similar al compuesto VlII-a.
1H RMN (300 MHz, CDCls) 68,09-8,04 (2H, m), 7,49-7,43 (6H, m), 7,28-7,09 (11H, m), 4,22 (1H, ddd, J = 8,4, 5,6, 3,0Hz), 3,43-3,33 (1H, m), 3,24-3,10 (1H, m), 3,08-2,94 (1H, m), 2,81 (1H, s a), 2,75 (1H, dd, J = 14,0, 8,1Hz), 2,49 (1H, dd, J = 14,0, 5,1Hz), 1,81-1,67 (1H, m), 1,40-1,16 (2H, m), 0,26-0,09 (1H, m); 13C RMN (75,5 MHz, CDCla) 6 147,3, 144,3, 129,8, 129,6, 129,4, 126,3, 123,5, 77,9, 74,8, 63,5, 53,2, 39,5, 25,0, 24,9. MALDI TOF-MS m/z Calculado para C31H31N2O3 [M+H]+ 479,23, encontrado 479,08.
[Ejemplo 16]
(S)-2-(4-nitrofenil)-1-((R)-pirrolidin-2-il)etanol (IX-b).
Compuesto IX-bse obtuvo utilizando VIII-b en lugar de VIII-a de una manera similar al compuesto IX-a.
1H RMN (300 MHz, CDCla) 68,19-8,13 (2H, m), 7,45-7,39 (2H, m), 3,83 (1H, ddd, J = 7,7, 5,4, 3,9Hz), 3,14 (1H, dt, J = 7,7, 3,9Hz), 3,01-2,87 (2H, m), 2,83 (1H, d, J = 3,3Hz), 2,81 (1H, s), 2,62 (2H, s a), 1,79-1,72 (4H, m); 13C RMN (75,5 MHz, CDCl3) 6 147,3, 146,5, 130,0, 123,5, 72,7, 61,7, 46,7, 40,1, 25,8, 24,2. MALDI TOF-MS m/z Calculado para C12H17N2O3 [M+H]+ 237,12, encontrado 237,02.
[Ejemplo 17]
(R)-(9H-fluoren-9-il)((S)-1-tritilpirrolidin-2-il)metanol (X-a).
Compuesto X-ase obtuvo utilizando "fluoreno" en lugar de "difenilmetano" de una manera similar al compuesto VI-a.
1H RMN (300 MHz, CDCls) 67,70 (1H, d, J = 7,5Hz), 7,66 (1H, d, J = 7,8Hz), 7,55 (2H, d, J = 7,5Hz), 7,44-7,09 (18H, m), 6,87-6,62 (1H, m), 4,55-4,48 (1H, m), 4,06 (1H, d, J = 7,5Hz), 3,43-3,34 (1H, m), 3,18-3,06 (1H, m), 2,98-2,88 (1H, m), 2,85 (1H, s a), 1,42-1,24 (1H, m), 1,18-1,04 (1H, m), 0,53-0,39 (1H, m), -0,02- -0,20 (1H, m); MALDI TOF-MS m/z Calculado para C37H34NO [M+H]+ 508,26, encontrado 508,12.
[Ejemplo 18]
(R)-9H-fluoren-9-(S)-pirrolidin-2-il)metanol (XI-a).
Compuesto Xl-ase obtuvo utilizando X-a en lugar de Il-a de una manera similar al compuesto IlI-a.
1H RMN (300 MHz, CDCb) 67,76 (2H, d, J = 7,5Hz), 7,68 (2H, t, J = 8,0Hz), 7,43-7,35 (2H, m), 7,34-7,25 (2H, m), 4,28 (1H, d, J = 6,3Hz), 4,03 (1H, dd, J = 6,5, 4,2Hz), 3,19-3,11 (1H, m), 2,97-2,88 (1H, m), 2,86-2,76 (1H, m), 2,02 (2H, s a), 1,77-1,53 (3H, m), 1,38-1,23 (1H, m); MALDI TOF-MS m/z Calculado para C18H20NO [M+H]+ 266,15, encontrado 266,04.
[Ejemplo 19]
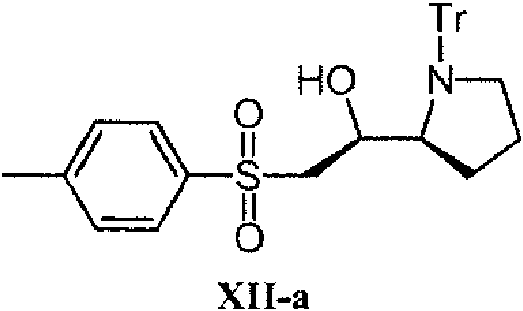
(S)-2-tosil-1-((S)-1-tritilpirrolidin-2-il)etanol (Xll-a).
Compuesto Xll-ase obtuvo utilizando"clorometil p-tolil sulfona" en lugar de "clorometildifenilmetilsilano" de una manera similar al compuesto ll-a.
1H RMN (600 MHz, CDCla) 67,66 (2H, d, J = 8,4Hz), 7,48-7,44 (6H, m), 7,35 (2H, d, J = 7,2Hz), 7,21-7,13 (9H, m), 4,39-4,36 (1H, m), 3,33 (1H, s), 3,24-3,20 (1H, m), 3,19-3,10 (2H, m), 2,98-2,92 (2H, m), 2,49 (3H, s), 1,55-1,49 (1H, m), 1,33-1,26 (1H, m), 1,12-1,04 (1H, m), 0,22-0,14 (1H, m); 13C RMN (150,9 MHz, CDCb) 6144,6, 144,5, 136,3, 129,9, 129,5, 128,1, 127,5, 126,2, 78,0, 69,1, 63,9, 60,2, 52,6, 25,5, 24,7, 21,7.
[Ejemplo 20]
(S)-2-tosil-1-((S)-pirrolidin-2-il)etanol (Xlll-a).
Compuesto Xlll-ase obtuvo utilizando Xll-a en lugar de ll-a de una manera similar al compuesto lll-a.
1H RMN (600 MHz, CDCla) 67,82 (2H, d, J = 8,4Hz), 7,37 (2H, d, J = 8,4Hz), 4,01 (1H, ddd, J = 12,0, 5,1, 3,0Hz), 3,32 (1H, dd, J = 14,4, 3,0Hz), 3,25 (1H, dd, J = 14,4, 9,0Hz), 3,16 (1H, dt, J = 7,8, 5,1Hz), 2,90-2,82 (2H, m), 2,46 (3H, s), 2,04 (2H, s a), 1,78-1,63 (3H, m), 1,62-1,55 (1H, m); 13C RMN (150,9 MHz, CDCb) 6144,5, 136,7, 129,7, 127,7, 67,4, 61,8, 60,1, 46,7, 25,7, 21,4. MALDI TOF-MS m/z Calculado para C13H20NO3S [M+H]+ 270,12, encontrado 270,04.
[Ejemplo 2]
(R)-2-tosil-1-((R)-1-tritilpirrolidin-2-il)etanol (Xll-b).
Compuesto Xll-bse obtuvo utilizando l-b en lugar de I-a de una manera similar al compuesto Xll-a.
1H RMN (600 MHz, CDCb) 67,66 (2H, d, J = 8,4Hz), 7,47-7,44 (6H, m), 7,35 (2H, d, J = 7,8Hz), 7,21-7,13 (9H, m), 4,37 (1H, dt, J = 8,6, 2,4Hz), 3,33 (1H, s), 3,23-3,20 (1H, m), 3,19-3,12 (2H, m), 2,98-2,92 (2H, m), 2,49 (3H, s), 1,56 1,49 (1H, m), 1,32-1,26 (1H, m), 1,11-1,03 (1H, m), 0,23-0,15 (1H, m); 13C RMN (150,9 MHz, CDCb) 6144,6, 144,5, 136,3, 129,9, 129,6, 128,1, 127,6, 126,2, 78,0, 69,1, 63,9, 60,2, 52,6, 25,5, 24,7, 21,7.
[Ejemplo 21]
(R)-2-tosil-1-((R)-pirrolidin-2-il)etanol (Xlll-b).
Compuesto XlII-bse obtuvo utilizando XlI-b en lugar de XlI-a de una manera similar al compuesto XlII-a.
1H RMN (600 MHz, CDCls) 67,82 (2H, d, J = 8,4Hz), 7,37 (2H, d, J = 8,4Hz), 4,01 (1H, ddd, J = 9,0, 5,1, 3,0Hz), 3,32 (1H, dd, J = 14,4, 3,0Hz), 3,25 (1H, dd, J = 14,4, 9,0Hz), 3,17 (1H, dt, J = 7,2, 5,1Hz), 2,89-2,83 (2H, m), 2,46 (3H, s), 2,04 (2H, s a), 1,79-1,64 (3H, m), 1,62-1,55 (1H, m); 13C RMN (150,9 MHz, CDCla) 6144,8, 136,6, 129,8, 127,9, 67,7, 61,8, 60,1,46,8, 25,9, 25,8, 21,6. MALDI TOF-MS m/z Calculado para C13H20NO3S [M+H]+ 270,12, encontrado 270,05.
[Ejemplo 22]
Monómero de oxazafosfolidina 3a.
3a (560 mg, 1,80 mmol) se secó mediante co-evaporaciones repetidas con tolueno seco y se disolvió en dietil éter seco (0,90 mL) bajo argón.. Se añadió W-metilmorfolina (400 pL, 3,60 mmol) a la solución y la solución resultante se añadió gota a gota a una solución de PCl3 (160 pL, 1,80 mmol) en dietil éter seco (0,90 mL) a 0 grados C bajo argón con agitación. Después, la mezcla se dejó calentar a temperatura ambiente y se agitó durante 30 min. El hidrocloruro de W-metilmorfolina resultante se eliminó mediante filtración bajo nitrógeno, y el filtrado se concentró a sequedad a presión reducida para proporcionar el derivado de 2-cloro-1,3,2-oxazafosfolidina bruto. Los materiales brutos se disolvieron en THF recién destilado (3,6 mL) para preparar soluciones 0,5 M, que se utilizaron para sintetizar los nucleósidos 3'-0-oxazafosfolidinas sin purificación adicional
5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina (636 mg, 0,84 mmol) se secó mediante co-evaporaciones repetidas con tolueno seco y se disolvió en THF recién destilado (2,5 mL) bajo argón. Se añadió Et3N (0,58 mL, 4,2 mmol) y la mezcla se enfrió a -78 grados C. Una solución 0,5 M del correspondiente derivado de 2-cloro-1,3,2-oxazafosfolidina bruto en THF recién destilado (3,6 mL, 1,80 mmol) se añadió gota a gota mediante una jeringa y la mezcla se agitó durante 15 min a temperatura ambiente. Luego se añadieron una solución acuosa saturada de NaHCO3 (70 mL) y CHCb (70 mL) y la capa orgánica se separó y se lavó con soluciones acuosas saturadas de NaHCO3 (2 x 70 mL). Las capas acuosas combinadas se volvieron a extraer con CHCb (70 mL). Las capas orgánicas se combinaron, se secaron sobre Na2SO4, se filtraron y se concentraron a presión reducida. El residuo se purificó mediante cromatografía en gel de sílice para proporcionar 3a (829 mg, 90%) en forma de una espuma blanca.
1H RMN (300 MHz, CDCla) 68,77 (1H, s a), 7,99 (1H, s), 7,54-6,98 (24H, m), 6,81-6,73 (4H, m), 6,35 (1H, dd, J = 8,0, 6,3Hz), 4,89-4,73 (4H, m), 4,68 (2H, s a), 4,05-3,98 (1H, m), 3,75 (6H, s), 3,62-3,46 (1H, m), 3,41-3,20 (3H, m), 3,18 3,04 (1H, m), 3,08 (2H, t, J = 6,6Hz), 2,58-2,36 (2H, m), 1,94-1,59 (2H, m), 1,56 (1H, dd, J = 15,0, 8,7Hz), 1,43 (1H, dd, J = 15,0, 5,7Hz), 1,33-1,16 (2H, m), 0,62 (3H, s); 31P RMN (121,5 MHz, CDCb) 6153,5 (1P, s).
[Ejemplo 23]
Monómero de oxazafosfolidina 3b.
Compuesto 3bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 68,80 (1H, s a), 7,96 (1H, s), 7,54-6,96 (24H, m), 6,79-6,71 (4H, m), 6,19 (1H, t, J = 6,6Hz), 4,90-4,73 (4H, m), 4,66 (2H, s a), 4,16-4,08 (1H, m), 3,76 (6H, s), 3,60-3,36 (2H, m), 3,29 (1H, d, J = 3,9Hz), 3,27-3,12 (2H, m), 3,09 (2H, t, J = 6,6Hz), 2,59-2,46 (1H, m), 2,07-1,97 (1H, m), 1,94-1,41 (5H, m), 1,36-1,18 (1H, m), 0,65 (3H, s); 31P RMN (121,5 MHz, CDCla) 6157,1 (1P, s).
[Ejemplo 24]
Monómero de oxazafosfolidina 1a.
Compuesto 1a se obtuvo utilizando "5'-0-(DMTr)-6-W-(benzoil)adenosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (600 MHz, CDCta) 68,71 (1H, s), 8,12 (1H, s), 8,04 (2H, d, J = 7,8Hz), 7,62-7,15 (23H, m), 6,80-6,75 (4H, m), 6,37 (1H, dd, J = 7,8, 6,0Hz), 4,94-4,88 (1H, m), 4,80 (1H, ddd, J = 12,0, 6,0, 5,4Hz), 4,07-4,04 (1H, m), 3,76 (6H, s), 3,58-3,49 (1H, m), 3,41-3,34 (1H, m), 3,33 (1H, dd, J = 10,8, 4,8Hz), 3,25 (1H, dd, J = 10,8, 4,8Hz), 3,13-3,06 (1H, m), 2,66-2,58 (1H, m), 2,40-2,35 (1H, m), 1,91-1,84 (1H, m), 1,73-1,66 (1H, m), 1,56 (1H, dd, J = 15,0, 9,0Hz), 1,44 (1H, dd, J = 15,0, 5,4Hz), 1,47-1,41 (1H, m), 1,30-1,23 (1H, m), 0,63 (3H, s); 31P RMN (243,0 MHz, CDCta) 6151,8 (1P, s).
[Ejemplo 25]
Monómero de oxazafosfolidina 1b.
Compuesto 1bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 1a.
1H RMN (300 MHz, CDCls) 69,06 (1H, s a), 8,76 (1H, s), 8,12 (1H, s), 8,07-7,99 (2H, m), 7,64-7,14 (22H, m), 6,83 6,75 (4H, m), 6,25 (1H, t, J = 6,6Hz), 4,86-4,75 (2H, m), 4,20-4,15 (1H, m), 3,77 (6H, s), 3,61-3,38 (2H, m), 3,36 (1H, dd, J = 10,2, 4,2Hz), 3,27 (1H, dd, J = 10,2, 4,2Hz), 3,27-3,13 (1H, m), 2,71-2,59 (1H, m), 2,12-2,01 (1H, m), 1,94-1,42 (5H, m), 1,36-1,20 (1H, m), 0,67 (3H, s); 31P RMN (121,5 MHz, CDCla) 6157,3 (1P, s).
[Ejemplo 26]
Monómero de oxazafosfolidina 2a.
Compuesto 2a se obtuvo utilizando "5'-0-(DMTr)-4-W-(isobutinil)citidina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 68,33 (1H, s a), 8,17 (1H, d, J = 7,5Hz), 7,52-7,22 (19H, m), 7,07 (1H, d, J = 7,5Hz), 6,88 6,81 (4H, m), 6,20 (1H, t, J = 6,2Hz), 4,81-4,64 (2H, m), 3,93-3,87 (1H, m), 3,79 (6H, s), 3,59-3,43 (1H, m), 3,39-3,29 (3H, m), 3,16-3,02 (1H, m), 2,69-2,52 (2H, m), 2,12-2,00 (1H, m), 1,91-1,50 (3H, m), 1,47-1,32 (2H, m), 1,27-1,16 (7H, m), 0,60 (3H, s); 31P RMN (121,5 MHz, CDCls) 6154,8 (1P, s).
[Ejemplo 27]
Monómero de oxazafosfolidina 2b.
Compuesto 2bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 2a.
1H RMN (300 MHz, CDCls) 68,33 (1H, d, J = 7,5Hz), 8,23 (1H, s a), 7,57-7,22 (19H, m), 7,12 (1H, d, J = 7,5Hz), 6,88 6,81 (4H, m), 6,15 (1H, dd, J = 6,6, 4,2Hz), 4,82-4,63 (2H, m), 4,03-3,97 (1H, m), 3,80 (6H, s), 3,55-3,26 (4H, m), 3,19 3,05 (1H, m), 2,59 (1H, quintuplete, J = 6,9Hz), 2,39-2,27 (1H, m), 2,21-2,10 (1H, m), 1,90-1,56 (3H, m), 1,50-1,32 (2H, m), 1,26-1,17 (7H, m), 0,66 (3H, s); 31P RMN (121,5 MHz, CDCla) 6157,2 (1P, s).
[Ejemplo 28]
Monómero de oxazafosfolidina 4a.
Compuesto 4a se obtuvo utilizando "5'-0-(DMTr)timidina" en lugar de "5'-O-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 67,58-7,23 (21H, m), 6,86-6,79 (4H, m), 6,35 (1H, dd, J = 8,1, 5,7Hz), 4,79-4,67 (2H, m), 3,83-3,78 (1H, m), 3,78 (6H, s), 3,59-3,43 (1H, m), 3,34 (1H, dd, J = 10,5, 2,4Hz), 3,35-3,24 (1H, m), 3,20 (1H, dd, J = 10,5, 2,4Hz), 3,16-3,02 (1H, m), 2,36-2,26 (1H, m), 2,15-2,02 (1H, m), 1,92-1,77 (1H, m), 1,74-1,59 (1H, m), 1,52 (1H, dd, J = 14,7, 9,0Hz), 1,40 (3H, s), 1,45-1,15 (3H, m), 0,60 (3H, s); 31P RMN (121,5 MHz, CDCta) 6153,7 (1P, s).
[Ejemplo 29]
Monómero de oxazafosfolidina 4b.
Compuesto 4bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 4a.
1H RMN (300 MHz, CDCls) 68,46 (1H, s a), 7,59-7,20 (20H, m), 6,86-6,79 (4H, m), 6,26 (1H, t, J = 6,8Hz), 4,78-4,65 (2H, m), 4,01-3,95 (1H, m), 3,78 (6H, s), 3,55-3,40 (1H, m), 3,42 (1H, dd, J = 10,5, 2,7Hz), 3,40-3,28 (1H, m), 3,22 (1H, dd, J = 10,5, 3,0Hz), 3,19-3,06 (1H, m), 2,16-1,95 (2H, m), 1,90-1,54 (3H, m), 1,49-1,35 (1H, m), 1,43 (3H, s), 1,34 1,17 (2H, m), 0,67 (3H, s); 31P RMN (121,5 MHz, CDCla) 6156,2 (1P, s).
[Ejemplo 30]
Monómero de oxazafosfolidina 5a.
Compuesto 5a se obtuvo utilizando "5'-0-(DMTr)-2'-0-metil-6-W-(benzoil)adenosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 68,66 (1H, s), 8,13 (1H, s), 8,03 (2H, d, J = 7,2Hz), 7,64-7,16 (23H, m), 6,79 (4H, d, J = 8,7Hz), 6,08 (1H, d, J = 6,3Hz), 4,91-4,81 (1H, m), 4,77-4,69 (1H, m), 4,64-4,57 (1H, m), 4,15-4,10 (1H, m), 3,76 (6H, s), 3,60-3,23 (4H, m), 3,35 (3H, s), 3,14-3,00 (1H, m), 1,90-1,19 (6H, m), 0,62 (3H, s); 31P RMN (121,5 MHz, CDCta) 6 155,8 (1P, s).
[Ejemplo 31]
Monómero de oxazafosfolidina 5b.
Compuesto 5bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 5a.
1H RMN (300 MHz, CDCls) 69,12 (1H, s a), 8,73 (1H, s), 8,24 (1H, s), 8,07-8,01 (2H, m), 7,62-7,17 (22H, m), 6,83 6,77 (4H, m), 6,12 (1H, d, J = 4,8Hz), 4,84-4,73 (2H, m), 4,43 (1H, t, J = 4,8Hz), 4,25-4,19 (1H, m), 3,77 (6H, s), 3,55 3,20 (4H, m), 3,28 (3H, s), 3,16-3,03 (1H, m), 1,90-1,17 (6H, m), 0,65 (3H, s); 31P RMN (121,5 MHz, CDCla) 6 155,0 (1P, s).
[Ejemplo 32]
Monómero de oxazafosfolidina 6a.
Compuesto 6a se obtuvo utilizando "5'-0-(DMTr)-2'-0-metil-4-W-(isobutill)citidina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 68,49 (1H, d, J = 7,2Hz), 7,58-7,20 (19H, m), 6,96 (1H, d, J =7,2Hz), 6,90-6,82 (4H, m), 5,98 (1H, s), 4,84 (1H, dd, J = 13,1, 7,5Hz), 4,59 (1H, dt, J = 8,3, 4,5Hz), 4,19-4,13 (1H, m), 3,79 (6H, s), 3,78-3,72 (1H, m), 3,63-3,40 (3H, m), 3,55 (3H, s), 3,36-3,24 (1H, m), 3,09-2,95 (1H, m), 2,59 (1H, septuplete, J = 6,9Hz), 1,85 1,53 (5H, m), 1,48-1,37 (1H, m), 1,24-1,17 (6H, m), 0,59 (3H, s); 31P RMN (121,5 MHz, CDCb) 6155,2 (1P, s).
[Ejemplo 33]
Monómero de oxazafosfolidina 6b.
Compuesto 6bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 6a.
1H RMN (300 MHz, CDCls) 68,62 (1H, d, J = 7,5Hz), 7,57-7,23 (19H, m), 7,02 (1H, d, J =7,5Hz), 6,89-6,81 (4H, m), 5,92 (1H, s), 4,90 (1H, dt, J = 9,0, 5,7Hz), 4,61 (1H, dt, J = 8,7, 4,8Hz), 4,25-4,17 (1H, m), 3,81 (6H, s), 3,67 (1H, d, J = 4,5Hz), 3,62-3,25 (4H, m), 3,38 (3H, s), 3,16-3,02 (1H, m), 2,58 (1H, septuplete, J = 6,9Hz), 1,87-1,40 (6H, m), 1,26 1,14 (6H, m), 0,64 (3H, s); 31P RMN (121,5 MHz, CDCla) 6158,2 (1P, s).
[Ejemplo 34]
Monómero de oxazafosfolidina 7a.
Compuesto 7a se obtuvo utilizando "5'-0-(DMTr)-2'-0-metil-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 68,67 (1H, s a), 8,01 (1H, s), 7,56-7,16 (24H, m), 6,83-6,74 (4H, m), 6,08 (1H, d, J = 6,9Hz), 4,85-4,76 (1H, m), 4,84 (2H, t, J = 6,6Hz), 4,65-4,56 (1H, m), 4,59 (2H, s a), 4,48 (1H, dd, J = 6,6, 5,1Hz), 4,09-4,05 (1H, m), 3,75 (6H, s), 3,60-3,42 (2H, m), 3,40-3,26 (2H, m), 3,35 (3H, s), 3,18-3,05 (1H, m), 3,08 (2H, t, J = 6,6Hz), 1,89-1,49 (3H, m), 1,48-1,16 (3H, m), 0,59 (3H, s); 31P RMN (121,5 MHz, CDCls) 6156,9 (1P, s).
[Ejemplo 35]
Monómero de oxazafosfolidina 7b.
Compuesto 7bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 7a.
1H RMN (300 MHz, CDCls) 68,74 (1H, s a), 8,09 (1H, s), 7,56-6,94 (24H, m), 6,84-6,71 (4H, m), 6,09 (1H, d, J = 4,8Hz), 4,83-4,70 (2H, m), 4,83 (2H, t, J = 6,6Hz), 4,63 (2H, s a), 4,35 (1H, t, J = 5,0Hz), 4,23-4,16 (1H, m), 3,75 (6H, s), 3,58 3,19 (4H, m), 3,32 (3H, s), 3,16-3,04 (1H, m), 3,07 (2H, t, J = 6,6Hz), 1,90-1,55 (3H, m), 1,48-1,15 (3H, m), 0,64 (3H, s); 31P RMN (121,5 MHz, CDCla) 6154,6 (1P, s).
[Ejemplo 36]
Monómero de oxazafosfolidina 8a.
Compuesto 8a se obtuvo utilizando "5'-0-(DMTr)-2-0-(metil)uridina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 67,91 (1H, d, J = 7,8Hz), 7,58-7,20 (19H, m), 6,88-6,80 (4H, m), 5,96 (1H, d, J = 3,3Hz), 5,19 (1H, d, J = 7,8Hz), 4,88-4,78 (1H, m), 4,66-4,57 (1H, m), 4,03-3,95 (1H, m), 3,90-3,74 (1H, m), 3,78 (6H, s), 3,77 3,71 (1H, m), 3,58-3,29 (2H, m), 3,45 (3H, s), 3,13-2,82 (2H, m), 1,88-1,53 (3H, m), 1,49-1,16 (3H, m), 0,60 (3H, s); 31P RMN (121,5 MHz, CDCls) 6155,3 (1P, s).
[Ejemplo 37]
Monómero de oxazafosfolidina 8b.
Compuesto 8bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 8a.
1H RMN (300 MHz, CDCls) 68,10 (1H, d, J = 8,4Hz), 7,58-7,20 (19H, m), 6,87-6,79 (4H, m), 5,89 (1H, d, J = 1,5Hz), 5,21 (1H, d, J = 8,4Hz), 4,92-4,82 (1H, m), 4,73-4,63 (1H, m), 4,15-4,08 (1H, m), 3,89-3,73 (1H, m), 3,78 (6H, s), 3,66 3,62 (1H, m), 3,57-3,27 (2H, m), 3,30 (3H, s), 3,17-2,82 (2H, m), 1,89-1,55 (3H, m), 1,55-1,40 (1H, m), 1,35-1,15 (2H, m), 0,66 (3H, s); 31P RMN (121,5 MHz, CDCla) 6157,5 (1P, s).
[Ejemplo 38]
Monómero de oxazafosfolidina 9a.
Compuesto 9a se obtuvo utilizando "5'-0-(DMTr)-2’-desoxi-2’-fluoro-6-W-(benzoil)adenosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacet¡l)-6-0-(c¡anoet¡l)guanos¡na" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCta) 68,64 (1H, s), 8,14 (1H, s), 8,06-8,01 (2H, m), 7,63-7,07 (23H, m), 6,78-6,70 (4H, m), 6,12 (1H, dd, J = 18,0, 2,4Hz), 5,24-5,01 (2H, m), 4,94-4,84 (1H, m), 4,17-4,06 (1H, m), 3,73 (6H, s), 3,55-3,40 (3H, m), 3,30-3,22 (1H, m), 3,03-2,88 (1H, m), 1,92-1,19 (6H, m), 0,62 (3H, s); 31P RMN (121,5 MHz, CDCta) 6150,5 (1P, d, J = 7,7Hz).
[Ejemplo 39]
Monómero de oxazafosfolidina 9b.
Compuesto 9bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 9a.
1H RMN (300 MHz, CDCls) 69,07 (1H, s a), 8,80 (1H, s), 8,24 (1H, s), 8,08-8,01 (2H, m), 7,66-7,15 (22H, m), 6,81 6,75 (4H, m), 6,14 (1H, dd, J = 18,0, 1,8Hz), 5,16-4,91 (3H, m), 4,28-4,21 (1H, m), 3,76 (6H, s), 3,57-3,11 (5H, m), 1,82-1,16 (6H, m), 0,65 (3H, s); 31P RMN (121,5 MHz, CDCla) 6157,8 (1P, d, J = 5,6Hz).
[Ejemplo 40]
Monómero de oxazafosfolidina 10a.
Compuesto 10a se obtuvo utilizando "5'-0-(DMTr)-2’-desoxi-2’-fluoro-4-W-(isobutiril)citidina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 68,66 (1H, s a), 8,41 (1H, d, J = 7,5Hz), 7,55-7,20 (19H, m), 7,01 (1H, d, J = 7,5Hz), 6,89 6,81 (4H, m), 6,06 (1H, d, J = 15,9Hz), 4,85 (1H, dd, J = 51,4, 3,9Hz), 4,84 (1H, dd, J = 12,9, 7,5Hz), 4,77-4,59 (1H, m), 4,15-4,08 (1H, m), 3,79 (6H, s), 3,63-3,29 (4H, m), 3,10-2,96 (1H, m), 2,65 (1H, septuplete, J = 6,9Hz), 1,85-1,53 (3H, m), 1,48-1,17 (3H, m), 1,21 (3H, d, J = 4,8Hz), 1,19 (3H, d, J = 4,8Hz), 0,59 (3H, s); 31P RMN (121,5 MHz, CDCb) 6 155,5 (1P, d, J = 6,6Hz).
[Ejemplo 41]
Monómero de oxazafosfolidina 10b.
Compuesto 10bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 10a.
1H RMN (300 MHz, CDCls) 68,53 (1H, d, J = 7,5Hz), 7,57-7,23 (20H, m), 7,10 (1H, d, J = 7,5Hz), 6,89-6,81 (4H, m), 6,10 (1H, d, J = 15,9Hz), 5,00-4,92 (1H, m), 4,84 (1H, dd, J = 51,5, 3,3Hz), 4,75-4,58 (1H, m), 4,24 (1H, d, J = 9,3Hz), 3,81 (6H, s), 3,65-3,39 (3H, m), 3,32-3,06 (2H, m), 2,59 (1H, septuplete, J = 6,9Hz), 1,88-1,53 (4H, m), 1,49-1,34 (2H, m), 1,27-1,18 (6H, m), 0,65 (3H, s); 31P RMN (121,5 MHz, CDCla) 6159,0 (1P, d, J = 4,4).
[Ejemplo 42]
Monómero de oxazafosfolidina 11a.
Compuesto 11a se obtuvo utilizando"5'-0-(DMTr)-2'-desoxi-2'-fluoro-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 68,74 (1H, s a), 8,03 (1H, s), 7,55-6,94 (24H, m), 6,80-6,69 (4H, m), 6,21 (1H, dd, J = 14,9, 3,6Hz), 5,34 (1H, dt, J = 52,3, 3,6Hz), 5,01-4,75 (2H, m), 4,84 (1H, t, J = 6,6Hz), 4,62 (2H, s a), 4,15-4,07 (1H, m), 3,73 (6H, s), 3,59-3,29 (4H, m), 3,15-3,00 (1H, m), 3,07 (2H, t, J = 6,6Hz), 1,90-1,49 (3H, m), 1,47-1,12 (3H, m), 0,58 (3H, s); 31P RMN (121,5 MHz, CDCla) 6155,6 (1P, d, J = 10,9Hz).
[Ejemplo 43]
Monómero de oxazafosfolidina 11b.
Compuesto 11bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 11a.
1H RMN (300 MHz, CDCls) 6 8,81 (1H, s a), 8,06 (1H, s), 7,55-6,95 (24H, m), 6,77-6,69 (4H, m), 6,06 (1H, d, J = 17,1Hz), 5,24-5,08 (1H, m), 5,04-4,80 (2H, m), 4,87 (1H, t, J = 6,6Hz), 4,62 (2H, s a), 4,25-4,19 (1H, m), 3,73 (6H, s), 3,58-3,02 (5H, m), 3,10 (2H, t, J = 6,6Hz), 1,90-1,56 (3H, m), 1,50-1,15 (3H, m), 0,63 (3H, s); 31P RMN (121,5 MHz, CDCla) 6158,0 (1P, d, J = 4,4Hz).
[Ejemplo 44]
Monómero de oxazafosfolidina 12a.
Compuesto 12a se obtuvo utilizando "5'-0-(DMTr)-2'-desoxi-2'-fluorouridina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 67,85 (1H, d, J = 8,1Hz), 7,58-7,20 (19H, m), 6,87-6,79 (4H, m), 5,98 (1H, d, J = 16,5Hz), 5,23 (1H, d, J = 8,1 Hz), 4,86-4,61 (3H, m), 3,99 (1H, d, J = 6,9Hz), 3,76 (6H, d, J = 3,0Hz), 3,56-3,34 (4H, m), 3,10 2,96 (1H, m), 1,88-1,74 (1H, m), 1,72-1,52 (2H, m), 1,48-1,16 (3H, m), 0,61 (3H, s); 31P RMN (121,5 MHz, CDCb) 6 154,3 (1P, d, J = 8,9Hz).
[Ejemplo 45]
Monómero de oxazafosfolidina 12b.
Compuesto 12bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 12a.
1H RMN (300 MHz, CDCls) 68,01 (1H, d, J = 8,4Hz), 7,58-7,20 (19H, m), 6,87-6,79 (4H, m), 6,03 (1H, d, J = 16,2Hz), 5,29 (1H, d, J = 8,4Hz), 4,96 (1H, dd, J = 13,1, 7,5Hz), 4,80-4,54 (2H, m), 4,15 (1H, d, J = 9,0Hz), 3,78 (6H, s), 3,61 3,39 (3H, m), 3,37-3,25 (1H, m), 3,23-3,09 (1H, m), 1,91-1,56 (3H, m), 1,51-1,13 (3H, m), 0,66 (3H, s); 31P RMN (121,5 MHz, CDCla) 6158,9 (1P, d, J = 4,4Hz).
[Ejemplo 46]
Monómero de oxazafosfolidina 13a.
Compuesto 13a se obtuvo utilizando "5'-0-(DMTr)-2'-0-TOM-6-W-(acetil)adenosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 68,82 (1H, s a), 8,49 (1H, s), 8,10 (1H, s), 7,58-7,17 (19H, m), 6,83-6,73 (4H, m), 6,11 (1H, d, J = 6,6Hz), 5,15 (1H, dd, J = 6,6, 5,4Hz), 4,98-4,77 (4H, m), 4,18-4,11 (1H, m), 3,76 (6H, s), 3,59-3,25 (4H, m), 3,16 3,02 (1H, m), 2,62 (3H, s), 1,91-1,53 (3H, m), 1,49-1,18 (3H, m), 0,96-0,80 (3H, m), 0,90 (18H, s), 0,62 (3H, s); 31P RMN (121,5 MHz, CDCla) 6156,7 (1P, s).
[Ejemplo 47]
Monómero de oxazafosfolidina 13b.
Compuesto 13bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 13a.
1H RMN (300 MHz, CDCls) 68,56 (1H, s a), 8,55 (1H, s), 8,13 (1H, s), 7,57-7,17 (19H, m), 6,82-6,73 (4H, m), 6,16 (1H, d, J = 5,7Hz), 5,06 (1H, t, J = 5,6Hz), 4,93 (1H, d, J = 5,1Hz), 4,83 (1H, d, J = 5,1Hz), 4,81-4,69 (2H, m), 4,27-4,19 (1H, m), 3,76 (6H, s), 3,55-3,40 (2H, m), 3,33-3,16 (2H, m), 3,12-2,97 (1H, m), 2,63 (3H, s), 1,88-1,52 (3H, m), 1,45-1,16 (3H, m), 0,91-0,79 (3H, m), 0,86 (18H, s), 0,64 (3H, s); 31P RMN (121,5 MHz, CDCla) 6154,8 (1P, s).
[Ejemplo 48]
Monómero de oxazafosfolidina 14a.
Compuesto 14a se obtuvo utilizando "5'-0-(DMTr)-2'-0-TOM-4-W-(acetil)citidina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 610,04 (1H, s a), 8,30 (1H, d, J = 7,5Hz), 7,51-7,21 (19H, m), 6,99 (1H, d, J = 7,5Hz), 6,89 6,81 (4H, m), 6,12 (1H, d, J = 3,3Hz), 5,07 (1H, d, J = 4,8Hz), 5,05 (1H, d, J = 4,8Hz), 4,84-4,75 (1H, m), 4,62-4,52 (1H, m), 4,31-4,25 (1H, m), 4,08-4,01 (1H, m), 3,78 (6H, d, J = 3,0Hz), 3,55-3,23 (4H, m), 3,10-2,96 (1H, m), 2,24 (3H, s), 1,84-1,49 (3H, m), 1,46-0,96 (24H, m), 0,58 (3H, s); 31P RMN (121,5 MHz, CDCls) 6156,5 (1P, s).
[Ejemplo 49]
Monómero de oxazafosfolidina 14b.
Compuesto 14bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 14a.
1H RMN (300 MHz, CDCla) 610,19 (1H, s a), 8,46 (1H, d, J = 7,5Hz), 7,54-7,23 (19H, m), 7,01 (1H, d, J = 7,5Hz), 6,88 6,79 (4H, m), 6,19 (1H, d, J = 1,8Hz), 5,11 (1H, d, J = 4,8Hz), 5,07 (1H, d, J = 4,8Hz), 4,81-4,71 (1H, m), 4,60-4,51 (1H, m), 4,26-4,18 (2H, m), 3,79 (6H, s), 3,63-3,55 (1H, m), 3,48-3,28 (2H, m), 3,21-2,94 (2H, m), 2,26 (3H, s), 1,81 1,49 (3H, m), 1,43-0,96 (24H, m), 0,62 (3H, s); 31P RMN (121,5 MHz, CDCla) 6156,4 (1P, s).
[Ejemplo 50]
Monómero de oxazafosfolidina 15a.
Compuesto 15a se obtuvo utilizando "5'-0-(DMTr)-2'-0-TOM-2-W-(acetil)guanosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 67,70 (1H, s), 7,63-7,13 (21H, m), 6,84-6,76 (4H, m), 5,77 (1H, d, J = 8,4Hz), 5,41-5,33 (1H, m), 4,90 (2H, s), 4,78-4,68 (2H, m), 3,86 (1H, s a), 3,75 (3H, s), 3,74 (3H, s), 3,56-3,41 (2H, m), 3,32-2,90 (3H, m), 1,92-1,10 (9H, m), 0,97-0,87 (21H, m), 0,52 (3H, s); 31P RMN (121,5 MHz, CDCta) 6158,1 (1P, s).
[Ejemplo 51]
Monómero de oxazafosfolidina 15b.
Compuesto 15bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 15a.
1H RMN (300 MHz, CDCls) 67,77 (1H, s), 7,56-7,15 (21H, m), 6,82-6,75 (4H, m), 5,86 (1H, d, J = 7,5Hz), 5,26-5,17 (1H, m), 4,95 (1H, d, J =5,4Hz), 4,85 (1H, d, J =5,4Hz), 4,78-4,71 (1H, m), 4,59-4,49 (1H, m), 4,10-4,05 (1H, m), 3,74 (6H, s), 3,52-3,37 (2H, m), 3,30-3,18 (1H, m), 3,11-2,85 (2H, m), 1,85-1,15 (9H, m), 0,93-0,84 (21H, m), 0,62 (3H, s); 31P RMN (121,5 MHz, CDCla) 6152,3 (1P, s).
[Ejemplo 52]
Monómero de oxazafosfolidina 16a.
Compuesto 16a se obtuvo utilizando "5'-0-(DMTr)-2'-0-TOM-uridina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 67,76 (1H, d, J = 8,1Hz), 7,55-7,18 (20H, m), 6,88-6,80 (4H, m), 6,11 (1H, d, J = 6,0Hz), 5,32 (1H, d, J = 8,1Hz), 4,99 (1H, d, J = 5,1Hz), 4,93 (1H, d, J = 5,1Hz), 4,84-4,75 (1H, m), 4,54-4,46 (1H, m), 4,38 (1H, t, J = 5,7Hz), 3,87-3,83 (1H, m), 3,78 (3H, s), 3,77 (3H, s), 3,56-3,42 (1H, m), 3,39-3,28 (1H, m), 3,36 (1H, dd, J = 11,0, 2,7Hz), 3,25 (1H, dd, J = 11,0, 2,7Hz), 3,16-3,03 (1H, m), 1,88-1,12 (6H, m), 1,08-0,97 (21H, m), 0,59 (3H, s); 31P RMN (121,5 MHz, CDCb) 6156,6 (1P, s).
[Ejemplo 53]
Monómero de oxazafosfolidina 16b.
Compuesto 16bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 16a.
1H RMN (600 MHz, CDCls) 67,87 (1H, d, J = 7,8Hz), 7,52-7,48 (4H, m), 7,38-7,21 (16H, m), 6,83-6,79 (4H, m), 6,14 (1H, d, J = 4,8Hz), 5,33 (1H, d, J = 7,8Hz), 4,99 (1H, d, J = 5,4Hz), 4,89 (1H, d, J = 5,4Hz), 4,67 (1H, dd, J = 13,8, 7,2Hz), 4,52 (1H, dt, J = 10,4, 4,8Hz), 4,31 (1H, t, J = 4,8Hz), 4,06-4,03 (1H, m), 3,78 (3H, s), 3,77 (3H, s), 3,47 (1H, dd, J = 10,4, 2,4Hz), 3,47-3,39 (1H, m), 3,22-3,17 (2H, m), 3,00 (1H, ddd, J = 19,5, 10,4, 4,8Hz), 1,82-1,74 (1H, m), 1,68-1,58 (1H, m), 1,56 (1H, dd, J = 14,4, 8,4Hz), 1,38 (1H, dd, J = 14,4, 7,2Hz), 1,31-1,25 (1H, m), 1,26-1,17 (1H, m), 1,08-0,98 (21H, m), 0,63 (3H, s); 31P RMN (243,0 MHz, CDCla) 6154,3 (1P, s).
[Ejemplo 54]
Monómero de oxazafosfolidina 17a.
Compuesto 17a se obtuvo utilizando "5'-0-(DMTr)-2'-0,4'-C-metileno-6-W-(benzoil)adenosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 69,10 (1H, s a), 8,76 (1H, s), 8,32 (1H, s), 8,04 (2H, d, J = 7,2Hz), 7,64-7,18 (22H, m), 6,84 (4H, d, J = 8,7Hz), 6,10 (1H, s), 4,76 (1H, d J = 6,9Hz), 4,58 (1H, s), 4,61-4,51 (1H, m), 3,91 (1H, d, J = 7,8Hz), 3,77 (1H, d, J = 7,8Hz), 3,75 (6H, s), 3,50 (1H, s), 3,47-3,33 (1H, m), 3,31-3,19 (1H, m), 3,03-2,88 (1H, m), 1,84-1,09 (6H, m), 0,51 (3H, s); 31P RMN (121,5 MHz, CDCla) 6152,9 (1P, s).
[Ejemplo 55]
Monómero de oxazafosfolidina 17b.
Compuesto 17bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 17a.
1H RMN (300 MHz, CDCb) 68,81 (1H, s), 8,30 (1H, s), 8,07-8,00 (2H, m), 7,64-7,17 (22H, m), 6,86-6,79 (4H, m), 6,12 (1H, s), 4,81-4,72 (1H, m), 4,62 (1H, d J = 7,2Hz), 4,57 (1H, s), 3,94 (1H, d, J = 7,8Hz), 3,89 (1H, d, J = 7,8Hz), 3,77 (6H, s), 3,48 (2H, s), 3,46-3,32 (1H, m), 3,24-3,13 (1H, m), 3,10-2,97 (1H, m), 1,84-1,49 (3H, m), 1,42-1,09 (3H, m), 0,58 (3H, s); 31P RMN (121,5 MHz, CDCla) 6157,3 (1P, s).
[Ejemplo 56]
Monómero de oxazafosfolidina 18a.
Compuesto 18a se obtuvo utilizando "5'-0-(DMT r)-2'-0,4'-C-metileno-4-W-(isobutiril)-5-metilcitidina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacet¡l)-6-0-(c¡anoet¡l)guanos¡na" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 67,88 (1H, s a), 7,58-7,18 (20H, m), 6,88-6,80 (4H, m), 5,65 (1H, s), 4,69-4,60 (1H, m), 4,52 (1H, d, J = 6,6Hz), 4,49 (1H, s), 3,81-3,74 (1H, m), 3,75 (3H, s), 3,73 (3H, s), 3,64 (1H, d, J = 8,1Hz), 3,56 (1H, d, J = 11,1Hz), 3,53 (1H, d, J = 8,1Hz), 3,46 (1H, d, J = 11,1Hz), 3,56-3,40 (1H, m), 3,32-3,20 (1H, m), 3,14-3,00 (1H, m), 1,85-1,12 (6H, m), 1,60 (3H, s), 1,19 (6H, d, J = 6,9Hz), 0,55 (3H, s); 31P RMN (121,5 MHz, CDCb) 6155,9 (1P, s).
[Ejemplo 57]
Monómero de oxazafosfolidina 18b.
Compuesto 18bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 18a.
1H RMN (300 MHz, CDCls) 67,86 (1H, s a), 7,56-7,19 (20H, m), 6,88-6,79 (4H, m), 5,69 (1H, s), 4,86-4,76 (1H, m), 4,46 (1H, s), 4,45 (1H, d, J = 7,5Hz), 3,80-3,75 (1H, m), 3,79 (6H, s), 3,74 (1H, d, J = 8,1Hz), 3,69 (1H, d, J = 8,1Hz), 3,51 (1H, d, J = 11,1Hz), 3,44-3,30 (1H, m), 3,39 (1H, d, J = 11,1Hz), 3,29-3,17 (1H, m), 3,11-2,97 (1H, m), 1,86-1,52 (3H, m), 1,64 (3H, s), 1,45-1,10 (3H, m), 1,21 (6H, d, J = 6,6Hz), 0,62 (3H, s); 31P RMN (121,5 MHz, CDCla) 6158,2 (1P, s).
[Ejemplo 58]
Monómero de oxazafosfolidina 19a.
Compuesto 19a se obtuvo utilizando "5'-0-(DMTr)-2'-0,4'-C-metileno-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 68,71 (1H, s a), 8,16 (1H, s), 7,50-7,17 (21H, m), 7,09-7,01 (3H, m), 6,86-6,79 (4H, m), 6,03 (1H, s), 4,84 (2H, t, J = 6,6Hz), 4,72 (2H, s), 4,68 (1H, d, J = 7,2Hz), 4,55-4,46 (1H, m), 4,50 (1H, s), 3,90 (1H, d, J = 7,8Hz), 3,77 (1H, d, J = 7,8Hz), 3,75 (6H, s), 3,51 (1H, d, J = 10,8Hz), 3,47 (1H, d, J = 10,8Hz), 3,45-3,21 (2H, m), 3,08 (2H, t, J =6,6Hz), 3,03-2,89 (1H, m), 1,80-1,08 (6H, m), 0,47 (3H, s); 31P RMN (121,5 MHz, CDCb) 6 153,2 (1P, s).
[Ejemplo 59]
Monómero de oxazafosfolidina 19b.
Compuesto 19bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 19a.
1H RMN (300 MHz, CDCls) 68,86 (1H, s a), 8,13 (1H, s), 7,55-7,17 (21H, m), 7,08-6,98 (3H, m), 6,95-6,78 (4H, m), 6,01 (1H, s), 4,86 (2H, t, J = 6,6Hz), 4,82-4,73 (1H, m), 4,70 (2H, s), 4,64 (1H, d, J = 7,5Hz), 4,49 (1H, s), 3,94 (1H, d, J = 7,8Hz), 3,89 (1H, d, J = 7,8Hz), 3,77 (6H, s), 3,46 (2H, s), 3,45-3,30 (1H, m), 3,24-3,12 (1H, m), 3,09 (2H, t, J =6,6Hz), 3,09-2,96 (1H, m), 1,81-1,50 (3H, m), 1,41-1,06 (3H, m), 0,58 (3H, s); 31P RMN (121,5 MHz, CDCla) 6157,4 (1P, s).
[Ejemplo 60]
Monómero de oxazafosfolidina 20a.
Compuesto 20a se obtuvo utilizando "5'-0-(DMTr)-2'-0,4'-C-metileno-5-metiluridina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCls) 67,71 (1H, d, J = 0,9Hz), 7,50-7,17 (20H, m), 6,87-6,80 (4H, m), 5,61 (1H, s), 4,69-4,60 (1H, m), 4,55 (1H, d, J = 6,9Hz), 4,41 (1H, s), 3,74 (3H, s), 3,73 (3H, s), 3,64 (1H, d, J = 7,8Hz), 3,55 (1H, d, J = 7,8Hz), 3,53 (1H, d, J = 10,8Hz), 3,46 (1H, d, J = 10,8Hz), 3,56-3,42 (1H, m), 3,35-3,24 (1H, m), 3,13-3,00 (1H, m), 1,85-1,45 (3H, m), 1,55 (3H, d, J = 0,9Hz), 1,41-1,12 (3H, m), 0,56 (3H, s); 31P RMN (121,5 MHz, CDCta) 6155,1 (1P, s).
[Ejemplo 61]
Monómero de oxazafosfolidina 20b.
Compuesto 20bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 20a.
1H RMN (300 MHz, CDCla) 67,69 (1H, s), 7,56-7,19 (20H, m), 6,88-6,79 (4H, m), 5,66 (1H, s), 4,87-4,77 (1H, m), 4,47 (1H, d, J = 7,8Hz), 4,40 (1H, s), 3,78 (6H, s), 3,74 (1H, d, J = 7,8Hz), 3,68 (1H, d, J = 7,8Hz), 3,50 (1H, d, J = 10,8Hz), 3.46- 3,32 (1H, m), 3,39 (1H, d, J = 10,8Hz), 3,30-3,19 (1H, m), 3,12-2,98 (1H, m), 1,85-1,56 (3H, m), 1,59 (3H, s), 1.46- 1,12 (3H, m), 0,63 (3H, s); 31P RMN (121,5 MHz, CDCla) 6158,1 (1P, s).
[Ejemplo 62]
Monómero de oxazafosfolidina 21a.
Compuesto 21a se obtuvo utilizando "5'-0-(DMTr)-2'-0-metoxietil-5-metiluridina" en lugar de "5'-0-(DMTr)-2-W-(fenoxiacetil)-6-0-(cianoetil)guanosina" de una manera similar al compuesto 3a.
1H RMN (300 MHz, CDCla) 67,62-7,18 (21H, m), 6,84 (4H, d, J = 8,7Hz), 6,07 (1H, d, J = 5,7Hz), 4,86-4,76 (1H, m), 4,63-4,54 (1H, m), 4,20 (1H, t, J = 5,4Hz), 3,95-3,89 (1H, m), 3,78 (6H, s), 3,78-3,71 (2H, m), 3,60-3,48 (2H, m), 3,44 3,02 (5H, m), 3,31 (3H, s), 1,88-1,15 (6H, m), 1,35 (3H, s), 0,58 (3H, s); 31P RMN (121,5 MHz, CDCls) 6156,3 (1P, s).
[Ejemplo 63]
Monómero de oxazafosfolidina 21b.
Compuesto 21bse obtuvo utilizando IlI-b en lugar de IlI-a de una manera similar al compuesto 21a.
1H RMN (300 MHz, CDCls) 67,71 (1H, d, J = 1,2Hz), 7,55-7,22 (20H, m), 6,86-6,78 (4H, m), 5,99 (1H, d, J = 3,9Hz), 4,78-4,62 (2H, m), 4,13-4,08 (1H, m), 4,07-4,02 (1H, m), 3,77 (6H, s), 3,77-3,70 (1H, m), 3,65-3,56 (1H, m), 3,52-3,36 (4H, m), 3,33-3,14 (2H, m), 3,29 (3H, s), 3,08-2,94 (1H, m), 1,86-1,72 (1H, m), 1,71-1,55 (2H, m), 1,30 (3H, d, J = 1,2Hz), 1,47-1,16 (3H, m) 0,64 (3H, s); 31P RMN (121,5 MHz, CDCla) 6155,6 (1P, s).
[Ejemplo 64]
Monómero de oxazafosfolidina 22a.
Compuesto 22ase obtuvo utilizando VII-a en lugar de III-a de una manera similar al compuesto 4a.
1H RMN (300 MHz, CDCls) 67,57 (1H, d, J = 0,9Hz), 7,37-6,94 (20H, m), 6,87-6,78 (4H, m), 6,48 (1H, dd, J = 8,6, 5,7Hz), 5,42 (1H, dd, J = 11,0, 5,1Hz), 4,81-4,71 (1H, m), 4,02 (1H, d, J = 11,0Hz), 3,83 (1H, d, J = 2,1Hz), 3,79 (6H, s), 3,61-3,41 (2H, m), 3,24-3,09 (1H, m), 3,16 (1H, dd, J = 10,8, 2,4Hz), 3,02 (1H, dd, J = 10,8, 2,4Hz), 2,54-2,44 (1H, m), 2,34-2,22 (1H, m), 1,94-1,79 (1H, m), 1,74-1,56 (1H, m), 1,38 (3H, s), 1,38-1,28 (2H, m); 31P RMN (121,5 MHz, CDCta) 6160,9 (1P, s).
[Ejemplo 65]
Monómero de oxazafosfolidina 22b.
Compuesto 22bse obtuvo utilizando VlI-b en lugar de VlI-a de una manera similar al compuesto 22a.
1H RMN (300 MHz, CDCla) 67,57 (1H, d, J = 1,5Hz), 7,43-7,11 (20H, m), 6,85-6,78 (4H, m), 6,48 (1H, dd, J = 7,5, 5,7Hz), 5,58 (1H, dd, J = 11,4, 5,1Hz), 4,82-4,73 (1H, m), 4,17-4,02 (2H, m), 3,78 (6H, s), 3,56-3,40 (3H, m), 3,32 (1H, dd, J = 10,7, 2,4Hz), 3,22-3,07 (1H, m), 2,26-2,04 (2H, m), 1,95-1,81 (1H, m), 1,74-1,56 (1H, m), 1,40 (3H, d, J = 1,5Hz), 1,44-1,34 (2H, m); 31P RMN (121,5 MHz, CDCla) 6162,2 (1P, s).
[Ejemplo 66]
Monómero de oxazafosfolidina 23a.
Compuesto 23ase obtuvo utilizando IX-a en lugar de III-a de una manera similar al compuesto 4a.
1H RMN (300 MHz, CDCla) 69,22 (1H, s a), 8,05-7,99 (2H, m), 7,52 (1H, d, J = 1,2Hz), 7,41-7,19 (11H, m), 6,87-6,79 (4H, m), 6,37 (1H, dd, J = 8,4, 5,7Hz), 4,88-4,75 (2H, m), 3,86-3,80 (1H, m), 3,79 (6H, s), 3,64-3,49 (2H, m), 3,27-3,12 (3H, m), 2,97 (2H, d, J = 6,6Hz), 2,51-2,41 (1H, m), 2,33-2,20 (1H, m), 2,03-1,75 (2H, m), 1,72-1,59 (1H, m), 1,46-1,36 (1H, m), 1,40 (3H, s); 31P RMN (121,5 MHz, CDCls) 6157,5 (1P, s).
[Ejemplo 67]
Monómero de oxazafosfolidina 23b.
Compuesto 23bse obtuvo utilizando IX-b en lugar de IX-a de una manera similar al compuesto 23a.
1H RMN (300 MHz, CDCls) 68,67 (1H, s a), 8,18-8,11 (2H, m), 7,57 (1H, d, J = 1,2Hz), 7,47-7,22 (11H, m), 6,86-6,79 (4H, m), 6,29 (1H, t, J = 6,6Hz), 4,87 (1H, dt, J = 7,5, 5,7Hz), 4,80-4,72 (1H, m), 4,11-4,05 (1H, m), 3,79 (6H, s), 3,67 3,47 (2H, m), 3,43 (1H, dd, J = 10,8, 2,7Hz), 3,27 (1H, dd, J = 10,8, 2,4Hz), 3,25-3,13 (1H, m), 3,07-2,99 (2H, m), 2,19 2,12 (2H, m), 2,03-1,62 (3H, m), 1,46-1,30 (1H, m), 1,41 (3H, s); 31P RMN (121,5 MHz, CDCla) 6158,1 (1P, s).
[Ejemplo 68]
Monómero de oxazafosfolidina 24a.
Compuesto 24ase obtuvo utilizando XIII-a en lugar de III-a de una manera similar al compuesto 4a.
1H RMN (600 MHz, CDCla) 67,76 (2H, d, J = 9,0Hz), 7,62 (1H, d, J = 1,2Hz), 7,40 (2H, d, J = 7,2Hz), 7,32-7,23 (10H, m), 6,85 (4H, d, J = 8,4Hz), 6,41 (1H, dd, J = 8,4, 5,4Hz), 4,94 (1H, dd, J = 12,3, 5,4Hz), 4,84-4,79 (1H, m), 4,03-4,01 (1H, m), 3,79 (6H, s), 3,59-3,53 (1H, m), 3,52-3,44 (2H, m), 3,41 (1H, dd, J = 14,7, 7,2Hz), 3,37-3,30 (2H, m), 3,13 (1H, ddd, J = 19,3, 10,3, 4,1Hz), 2,50-2,44 (1H, m), 2,39 (3H, s), 2,35-2,29 (1H, m), 1,91-1,72 (2H, m), 1,64-1,59 (1H, m), 1,40 (3H, s), 1,12-1,05 (1H, m); 31P RMN (243,0 MHz, CDCta) 6154,2 (1P, s).
Procedim iento general para la síntesis de olíaos guirales:
La síntesis automatizada en fase sólida de oligos quirales se realizó de acuerdo con los ciclos mostrados en la Tabla 1. Después de la síntesis, la resina se trató con una solución acuosa de NH3 al 25% (1 mL) durante 12 ha 55 grados C. La mezcla se enfrió a temperatura ambiente y la resina se eliminó mediante filtración con membrana. El filtrado se concentró a sequedad a presión reducida. El residuo se disolvió en H2O (3 mL) y se analizó mediante RP-UPLC-MS con un gradiente lineal de acetonitrilo (0-50%/30 min) en tampón de acetato de trietilamonio 0,1 M (pH 7,0) a 50 grados C a un caudal de 0,3 mL/min.
Tabla. 1
etapa operación reactivos y disolvente volumen espera
1 destritilación 3% DCA/DCM 1,6 mL 20 s
2 acoplamiento monómero 0,1 M/MeCN 1 M 0,5 mL 5 min
3 rematado Ac2O/THF-piridina 16% /THF 0,5 mL 30 s
4 oxidación / urización CSO/MeCN 0,5 M o MeCN 0,1 M 0,5 mL 90 s
[Ejemplo Comparativo 1]
El Compuesto 25, anterior, que representa un monómero convencional, se utilizó para producir oligos. La Figura 2 muestra una tabla de productos obtenidos mediante el Ejemplo Comparativo 1.
Análisis
Los monómeros de los ejemplos de trabajo fueron químicamente estables. El rendimiento aislado de los monómeros fue superior al 80%, superior al del método convencional.
Los autores de la invención sintetizaron derivados de oligonucleótidos utilizando los reactivos quirales de los ejemplos de trabajo anteriores basados en el segundo procedimiento general y los monómeros de los ejemplos de trabajo anteriores basados en el primer procedimiento general. Como se muestra en la Figura 2, el monómero convencional provoca productos de desprotección incompletos, productos secundarios y secuencias de fallo. Por otro lado, el método de la invención provoca pocos productos de desprotección incompletos y pocos productos secundarios, aunque provoca secuencias de fallo como se muestra en la Figura 1. Es obvio que el método de la invención puede disminuir los productos de desprotección incompletos. y productos secundarios. Fue fácil aislar los derivados de oligonucleótidos diana, porque la presente invención puede reducir los productos indeseables.
Claims (21)
1. Un reactivo quiral o una sal del mismo, teniendo el reactivo quiral la siguiente fórmula química (I),
en donde G1 es un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo de fórmula (II), (III) o (V), G2 es un grupo nitro, un grupo ciano, o un grupo de fórmula (II), (III) o (V), o tanto G1 como G2 se toman juntos para formar un grupo de fórmula (IV),
en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3,
G31
-¿ -S i— G32 (Mí)
G33
en donde G31 a G33 son independientemente grupo alquilo C1-4, grupo alcoxi C1-4, grupo arilo C6-14, grupo aralquilo C7-14, grupo alquil C1-4 arilo C6-14, grupo alcoxi C1-4 arilo C6-14 o grupo aril C6-14 alquilo C1-4,
en donde G41 a G46 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3,
en donde G51 a G53 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano, un grupo alquilo C1-3 o alquil C1-3oxi y
G3 y G4 se toman juntos para formar un anillo que contiene heteroátomos que tiene de 3 a 16 átomos de carbono.
3. El reactivo quiral o una sal del mismo de acuerdo con la reivindicación 2,
en donde cada uno de G1 y G2 es un grupo de fórmula (II), en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3; o
en donde cada uno de G1 y G2 es un grupo de fórmula (II), en donde cada uno de G21 a G23 es un átomo de hidrógeno; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (II), en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (II), en donde cada uno de G21 y G22 es un átomo de hidrógeno y G23 es un grupo nitro; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), y G31 a G33 son independientemente un grupo alquilo C1-4, un grupo arilo C6-14, un grupo aralquilo C7-14, un grupo alquil C1-4 arilo C6-14, un grupo alcoxi C1-4 arilo C6-14 o un grupo aril C6-14 alquilo C1-4; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), y G31 a G33 son independientemente un grupo alquilo C1-4, un grupo arilo C6, un grupo aralquilo C7-10, un grupo alquil C1-4 arilo C6, un grupo alcoxi C1-4 arilo C6 o un grupo aril C6 alquilo C1-4; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), en donde G31 a G33 son independientemente un grupo alquilo C1-4 o un grupo arilo C6; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), en donde G31 a G33 son independientemente un grupo alquilo C1-4; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (III), en donde G31 y G33 son un grupo arilo C6 y G32 es un grupo alquilo C1-4; o
en donde G1 y G2 se toman juntos para formar un grupo de fórmula (IV), en donde G41 a G46 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3; o
en donde G1 y G2 se toman juntos para formar un grupo de fórmula (IV), en donde cada uno de G41 a G46 es un átomo de hidrógeno; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (V), en donde G51 a G53 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo metilo o un grupo metoxi; o
en donde G1 es un átomo de hidrógeno y G2 es un grupo de fórmula (V), en donde cada uno de G51 y G53 es un átomo de hidrógeno y G53 es un grupo 4-metilo.
5. Un derivado de nucleósido 3'-fosforamidita que está representado por la fórmula (Va) o (Vb),
en donde G1 es un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo de fórmula (II), (III) o (V), G2 es un grupo nitro, un grupo ciano o un grupo de fórmula (II), (III) o (V), o tanto G1 como G2 se toman juntos para formar un grupo de fórmula (IV),
en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3,
en donde G31 a G33 son independientemente grupo alquilo C1-4, grupo alcoxi C1-4, grupo arilo C6-14, grupo aralquilo C7-14, grupo alquil C1-4 arilo C6-14, grupo alcoxi C1-4 arilo C6-14 o grupo aril C6-14 alquilo C1-4,
en donde G41 a G46 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3,
en donde G51 a G53 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano, un grupo alquilo C1-3 o un grupo alquil C1-3oxi,
G3 y G4 se toman juntos para formar un anillo que contiene heteroátomos que tiene de 3 a 16 átomos de carbono, G5 es un grupo protector de un grupo hidroxilo,
R2 es hidrógeno, -OH, -SH, -NRdRd, -N3 , halógeno, alquilo, alquenilo, alquinilo, alquil-Y1-, alquenil-Y1-, alquinil-Y1-, aril-Y1-, heteroaril-Y1-, -ORb o -SRb, en donde Rb es un resto de bloqueo,
Y1 es O, NRd, S o Se,
Rd es independientemente hidrógeno, alquilo, alquenilo, alquinilo, arilo, acilo, sililo sustituido, carbamato, -P(O)(Re)2 o -HP(O)(Re),
Re es independientemente hidrógeno, alquilo, arilo, alquenilo, alquinilo, alquil-Y2-, alquenil-Y2-, alquinil-Y2-, aril-Y2- o heteroaril-Y2- o un catión que es Na+, Li+ o K+,
Y2 es O, S o NRd, en donde Rd es independientemente hidrógeno, alquilo, alquenilo, alquinilo, arilo, acilo, sililo sustituido o carbamato,
R3 es un grupo representado por -CH2-, -(CH2)2-, -CH2NH- o -CH2N(CH3)-, y
Bs es un grupo seleccionado de los grupos representados por las siguientes fórmulas (VI) a (XI) o derivados de las mismas.
7. El derivado de nucleósido 3'-fosforamidita de acuerdo con la reivindicación 5, en donde el derivado de nucleósido 3'-fosforamidita está representado por la fórmula 1a, 1b, 2a, 2b, 3a, 3b, 4a, 4b, 5a, 5b, 6a, 6b, 7a, 7b, 8a, 8b, 9a, 9b, 10a, 10b, 11a, 11 b,12a, 12b, 13a, 13b, 14a, 14b, 15a, 15b, 16a, 16b, 17a, 17b, 18a, 18b, 19a, 19b, 20a, 20b, 21a, 21b, 22a, 22b, 23a, 23b o 24a,
en donde DMTr representa un grupo 4,4'-dimetoxitritilo y TOM representa un grupo triisopropiisiloximetilo.
8. Un método para la síntesis de derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados, que comprende las etapas de:
hacer reaccionar una molécula que comprende un resto H-fosfonato aquiral, un reactivo quiral o una sal del mismo para formar un monómero de un derivado de nucleósido 3'-fosforamidita,
hacer reaccionar el monómero y un nucleósido para formar un compuesto intermedio condensado; y
convertir el compuesto intermedio condensado en el ácido nucleico que comprende un resto X-fosfonato quiral, en donde el reactivo quiral tiene la siguiente fórmula química (I),
en donde G1 es un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo de fórmula (II), (III) o (V), G2 es un grupo nitro, un átomo de halógeno, un grupo ciano, o un grupo de fórmula (Il), (III) o (V), o tanto G1 como G2 se toman juntos para formar un grupo de fórmula (IV),
en donde G21 a G23 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3,
G31
r^-Sí— G32 (ni)
l
G33
en donde G31 a G33 son independientemente grupo alquilo C1-4 o grupo arilo Ca-14, grupo alcoxi C1-4, grupo arilo Ca-14, grupo aralquilo C7-14, grupo alquil C1-4 arilo Ca-14, grupo alcoxi C1-4 arilo Ca-14 o grupo aril Ca-14 alquilo C1-4,
en donde G41 a G46 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano o un grupo alquilo C1-3,
en donde G51 a G53 son independientemente un átomo de hidrógeno, un grupo nitro, un átomo de halógeno, un grupo ciano, un grupo alquilo C1-3 o alquil C1-3oxi y
G3 y G4 se toman juntos para formar un anillo que contiene heteroátomos que tiene de 3 a 16 átomos de carbono.
11. Un método para la síntesis de derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados, que comprende las etapas de:
hacer reaccionar un derivado de nucleósido 3'-fosforamidita que está representado por la fórmula (Va) o (Vb) de acuerdo con la reivindicación 5, con un reactivo de activación y un nucleósido para formar un compuesto intermedio condensado; y convertir el compuesto intermedio condensado en el ácido nucleico que comprende un resto X-fosfonato quiral.
13. El método para la síntesis de derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados de acuerdo con la reivindicación 11, en el que el derivado de nucleósido 3'-fosforamidita está representado por la fórmula 1a, 1b, 2a, 2b, 3a, 3b, 4a, 4b, 5a, 5b, 6a, 6b, 7a, 7b, 8a, 8b, 9a, 9b, 10a, 10b, 11a, 11b, 12a, 12b, 13a, 13b, 14a, 14b, 15a, 15b, 16a, 16b, 17a, 17b, 18a, 18b, 19a, 19b, 20a, 20b, 21a, 21b, 22a, 22b, 23a, 23b o 24a,
en donde DMTr representa un grupo 4,4'-dimetoxitritilo y TOM representa un grupo triisopropiisiloximetilo.
14. El reactivo quiral o una sal del mismo de acuerdo con la reivindicación 2, en donde G1 es un átomo de hidrógeno, G2 es un grupo de fórmula (III), en donde G31 y G33 son un grupo arilo C6 y G32 es un grupo alquilo C1-4.
15. El reactivo quiral o una sal del mismo de acuerdo con la reivindicación 14, en donde G32 es metilo.
17. El derivado de nucleósido 3'-fosforamidita de la reivindicación 6, en donde:
G1 es hidrógeno, G2 es un grupo de fórmula (III):
en donde G31 a G33 son independientemente grupo alquilo C1-4, grupo alcoxi C1-4, grupo arilo C6-14, grupo aralquilo C7-14, grupo alquil C1-4 arilo C6-14, grupo alcoxi C1-4 arilo C6-14 o grupo aril C6-14 alquilo C1-4.
18. El derivado de nucleósido 3'-fosforamidita de la reivindicación 17, en donde G31 y G33 son grupos arilo C6 y G32 es un grupo alquilo C1-4,
R2 es hidrógeno, -OH, halógeno u -ORb, en donde Rb es un resto de bloqueo, y
Bs es un grupo seleccionado de los grupos representados por las siguientes fórmulas (VI) a (XI) o derivados de las mismas,
en donde un derivado se selecciona de:
en donde cada uno de R8 a R10 es independientemente alquilo C1-10, arilo C6-C10, aralquilo C6-C10 o aril C6-Ciooxialquilo.
19. El derivado de nucleósido 3'-fosforamidita de la reivindicación 6, 17 o 18, en donde G31 y G33 son fenilo y G32 es metilo.
20. El método para la síntesis de un derivado de oligonucleótidos modificados con átomos de fósforo estereocontrolados de acuerdo con la reivindicación 8, en el que el el reactivo quiral es un reactivo quiral de acuerdo con una cualquiera de las reivindicaciones 14-16.
21. El método para la síntesis de derivados de oligonucleótidos modificados con átomos de fósforo estereocontrolados de acuerdo con la reivindicación 11, en el que el derivado de nucleósido 3'-fosforamidita es un derivado de nucleósido 3'-fosforamidito de acuerdo con una cualquiera de las reivindicaciones 17-19.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261671652P | 2012-07-13 | 2012-07-13 | |
| PCT/JP2013/004303 WO2014010250A1 (en) | 2012-07-13 | 2013-07-12 | Asymmetric auxiliary group |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2862073T3 true ES2862073T3 (es) | 2021-10-06 |
Family
ID=49915731
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13817386T Active ES2862073T3 (es) | 2012-07-13 | 2013-07-12 | Grupo auxiliar asimétrico |
Country Status (15)
| Country | Link |
|---|---|
| US (5) | US9598458B2 (es) |
| EP (2) | EP3812370A1 (es) |
| JP (5) | JP6268157B2 (es) |
| KR (1) | KR101850319B1 (es) |
| CN (2) | CN104684893B (es) |
| AU (5) | AU2013288048A1 (es) |
| BR (1) | BR112015000784A8 (es) |
| CA (1) | CA2879023C (es) |
| DK (1) | DK2872485T3 (es) |
| ES (1) | ES2862073T3 (es) |
| PL (1) | PL2872485T3 (es) |
| PT (1) | PT2872485T (es) |
| RU (1) | RU2693381C2 (es) |
| SG (1) | SG11201500239VA (es) |
| WO (1) | WO2014010250A1 (es) |
Families Citing this family (97)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2572826C2 (ru) | 2008-12-02 | 2016-01-20 | Чиралджен, Лтд. | Способ синтеза модифицированных по атому фосфора нуклеиновых кислот |
| SG10201403841QA (en) | 2009-07-06 | 2014-09-26 | Ontorii Inc | Novel nucleic acid prodrugs and methods of use thereof |
| JP5868324B2 (ja) | 2010-09-24 | 2016-02-24 | 株式会社Wave Life Sciences Japan | 不斉補助基 |
| CN107365339A (zh) | 2011-07-19 | 2017-11-21 | 波涛生命科学有限公司 | 合成官能化核酸的方法 |
| RU2693381C2 (ru) * | 2012-07-13 | 2019-07-02 | Уэйв Лайф Сайенсес Лтд. | Асимметричная вспомогательная группа |
| EP2872147B1 (en) | 2012-07-13 | 2022-12-21 | Wave Life Sciences Ltd. | Method for making chiral oligonucleotides |
| WO2014010718A1 (ja) | 2012-07-13 | 2014-01-16 | 株式会社新日本科学 | キラル核酸アジュバント |
| EP3095459A4 (en) | 2014-01-15 | 2017-08-23 | Shin Nippon Biomedical Laboratories, Ltd. | Chiral nucleic acid adjuvant having antitumor effect and antitumor agent |
| JPWO2015108047A1 (ja) | 2014-01-15 | 2017-03-23 | 株式会社新日本科学 | 免疫誘導活性を有するキラル核酸アジュバンド及び免疫誘導活性剤 |
| JPWO2015108046A1 (ja) | 2014-01-15 | 2017-03-23 | 株式会社新日本科学 | 抗アレルギー作用を有するキラル核酸アジュバンド及び抗アレルギー剤 |
| CA2936712A1 (en) | 2014-01-16 | 2015-07-23 | Meena | Chiral design |
| RU2708237C2 (ru) | 2014-08-22 | 2019-12-05 | Общество с ограниченной ответственностью "НооГен" | Модифицированные олигонуклеотиды и способ их получения |
| CN107208092B (zh) | 2014-12-16 | 2021-09-10 | 罗氏创新中心哥本哈根有限公司 | 手性毒性筛选方法 |
| WO2016097212A1 (en) | 2014-12-17 | 2016-06-23 | Proqr Therapeutics Ii B.V. | Targeted rna editing |
| CR20180107A (es) | 2015-07-22 | 2018-04-03 | Wave Life Sciences Ltd | Composiciones de oligonucleótidos y métodos de los mismos |
| JP7511326B2 (ja) | 2015-10-09 | 2024-07-05 | ウェイブ ライフ サイエンシズ リミテッド | オリゴヌクレオチド組成物およびその方法 |
| CA3015823A1 (en) * | 2016-03-13 | 2017-09-21 | Wave Life Sciences Ltd. | Compositions and methods for phosphoramidite and oligonucleotide synthesis |
| CN114717235A (zh) | 2016-03-14 | 2022-07-08 | 豪夫迈·罗氏有限公司 | 用于减少pd-l1表达的寡核苷酸 |
| WO2017157672A1 (en) | 2016-03-18 | 2017-09-21 | Roche Innovation Center Copenhagen A/S | Acyl-protected l-lna-guanosine monomers |
| BR112018071477A2 (pt) | 2016-04-18 | 2019-02-19 | Sarepta Therapeutics, Inc. | oligômeros antisenso e métodos de utilização dos mesmos para tratamento de doenças associadas com o gene da alfa-glicosidase ácida |
| MX2018013157A (es) | 2016-04-29 | 2019-05-23 | Sarepta Therapeutics Inc | Analogos de oligonucleotidos dirigidos a lmna humana. |
| MA45270A (fr) | 2016-05-04 | 2017-11-09 | Wave Life Sciences Ltd | Compositions d'oligonucléotides et procédés associés |
| CN109311925B (zh) * | 2016-05-12 | 2022-06-03 | 罗氏创新中心哥本哈根有限公司 | 立体限定的氧杂氮杂磷杂环戊烷亚磷酰胺单体与核苷或寡核苷酸的增强的偶联 |
| EP3458464A1 (en) | 2016-05-18 | 2019-03-27 | ETH Zurich | Stereoselective synthesis of phosphorothioate oligoribonucleotides |
| EP3463386A4 (en) | 2016-06-03 | 2020-03-04 | Wave Life Sciences Ltd. | OLIGONUCLEOTIDES, COMPOSITIONS AND ASSOCIATED METHODS |
| WO2017220751A1 (en) | 2016-06-22 | 2017-12-28 | Proqr Therapeutics Ii B.V. | Single-stranded rna-editing oligonucleotides |
| TW201811807A (zh) | 2016-06-30 | 2018-04-01 | 美商薩羅塔治療公司 | 用於肌肉萎縮症之外顯子跳躍寡聚物 |
| EP4252845A3 (en) | 2016-07-05 | 2024-05-22 | BioMarin Technologies B.V. | Pre-mrna splice switching or modulating oligonucleotides comprising bicyclic scaffold moieties, with improved characteristics for the treatment of genetic disorders |
| AU2017312116A1 (en) | 2016-08-17 | 2019-03-07 | Solstice Biologics, Ltd. | Polynucleotide constructs |
| KR102501980B1 (ko) | 2016-09-01 | 2023-02-20 | 프로큐알 테라퓨틱스 Ⅱ 비.브이. | 화학적으로 변형된 단일 가닥 rna-편집 올리고뉴클레오타이드 |
| MA46905A (fr) * | 2016-11-23 | 2019-10-02 | Wave Life Sciences Ltd | Compositions et procédés de synthèse de phosphoramidites et d'oligonucléotides |
| LT3554553T (lt) | 2016-12-19 | 2022-08-25 | Sarepta Therapeutics, Inc. | Egzoną šalinantys oligomero konjugatai nuo raumenų distrofojos |
| PL3554554T3 (pl) | 2016-12-19 | 2022-12-19 | Sarepta Therapeutics, Inc. | Koniugaty oligomerów z pominięciem egzonu w dystrofii mięśniowej |
| RS63621B1 (sr) | 2016-12-19 | 2022-10-31 | Sarepta Therapeutics Inc | Oligomerni konjugati za preskakanje egzona za mišićnu distrofiju |
| KR102873477B1 (ko) * | 2016-12-28 | 2025-10-20 | 엘지디스플레이 주식회사 | 표시 장치용 기판과 그를 포함하는 표시 장치 |
| EP3610022A1 (en) | 2017-04-14 | 2020-02-19 | Tollnine, Inc. | Immunomodulating polynucleotides, antibody conjugates thereof, and methods of their use |
| EP3630199A4 (en) | 2017-06-02 | 2021-11-10 | Wave Life Sciences Ltd. | OLIGONUCLEOTIDE COMPOSITIONS AND METHODS FOR THEIR USE |
| CA3065523A1 (en) | 2017-06-02 | 2018-12-06 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods of use thereof |
| WO2018237194A1 (en) * | 2017-06-21 | 2018-12-27 | Wave Life Sciences Ltd. | Compounds, compositions and methods for synthesis |
| CN110831951B (zh) * | 2017-06-28 | 2023-10-27 | 罗氏创新中心哥本哈根有限公司 | 多重偶联和氧化方法 |
| US11597744B2 (en) | 2017-06-30 | 2023-03-07 | Sirius Therapeutics, Inc. | Chiral phosphoramidite auxiliaries and methods of their use |
| CA3072076A1 (en) | 2017-08-08 | 2019-02-14 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| KR20200052369A (ko) | 2017-09-18 | 2020-05-14 | 웨이브 라이프 사이언시스 리미티드 | 올리고뉴클레오티드 제조 기술 |
| EA201991450A1 (ru) | 2017-09-22 | 2019-12-30 | Сарепта Терапьютикс, Инк. | Конъюгаты олигомеров для пропуска экзона при мышечной дистрофии |
| US20210145852A1 (en) | 2017-09-28 | 2021-05-20 | Sarepta Therapeutics, Inc. | Combination Therapies for Treating Muscular Dystrophy |
| US20200254002A1 (en) | 2017-09-28 | 2020-08-13 | Sarepta Therapeutics, Inc. | Combination therapies for treating muscular dystrophy |
| JP2020536060A (ja) | 2017-09-28 | 2020-12-10 | サレプタ セラピューティクス, インコーポレイテッド | 筋ジストロフィーを処置するための併用療法 |
| WO2019075357A1 (en) | 2017-10-12 | 2019-04-18 | Wave Life Sciences Ltd. | OLIGONUCLEOTIDE COMPOSITIONS AND RELATED METHODS |
| JP7394753B2 (ja) | 2017-10-18 | 2023-12-08 | サレプタ セラピューティクス, インコーポレイテッド | アンチセンスオリゴマー化合物 |
| JPWO2019187691A1 (ja) | 2018-03-26 | 2021-03-25 | 株式会社カネカ | コラゲナーゼ活性を有するポリペプチド及びその製造方法 |
| AU2019252680B2 (en) * | 2018-04-12 | 2025-11-06 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods of use thereof |
| JP7427608B2 (ja) | 2018-05-11 | 2024-02-05 | ウェイブ ライフ サイエンシズ リミテッド | オリゴヌクレオチド組成物及びその使用方法 |
| GB201808146D0 (en) | 2018-05-18 | 2018-07-11 | Proqr Therapeutics Ii Bv | Stereospecific Linkages in RNA Editing Oligonucleotides |
| US10765760B2 (en) | 2018-05-29 | 2020-09-08 | Sarepta Therapeutics, Inc. | Exon skipping oligomer conjugates for muscular dystrophy |
| EP3806868A4 (en) | 2018-06-13 | 2022-06-22 | Sarepta Therapeutics, Inc. | EXON SKIPPING OLIGOMERS FOR MUSCULAR DYSTROPHY |
| TW202449155A (zh) | 2018-07-27 | 2024-12-16 | 美商薩羅塔治療公司 | 用於肌肉萎縮症之外顯子跳躍寡聚物 |
| MX2021004822A (es) | 2018-11-02 | 2021-07-06 | Biomarin Tech Bv | Oligonucleotidos antisentido biespecificos para la omision del exon de la distrofina. |
| CN113412330A (zh) | 2018-12-13 | 2021-09-17 | 萨勒普塔医疗公司 | 用于肌营养不良的外显子跳跃寡聚物缀合物 |
| JP2022525541A (ja) * | 2019-03-20 | 2022-05-17 | ウェイブ ライフ サイエンシズ リミテッド | オリゴヌクレオチド調製に有用な技術 |
| CN113631564B (zh) | 2019-03-28 | 2025-02-25 | 味之素株式会社 | 具有硫代磷酸酯化部位的寡核苷酸的制造方法 |
| CN113661168A (zh) * | 2019-04-16 | 2021-11-16 | 罗氏创新中心哥本哈根有限公司 | 用于制备核苷酸p(v)单体的新方法 |
| EP3955966A1 (en) | 2019-04-18 | 2022-02-23 | Sarepta Therapeutics, Inc. | Compositions for treating muscular dystrophy |
| CN115885042A (zh) | 2020-05-22 | 2023-03-31 | 波涛生命科学有限公司 | 双链寡核苷酸组合物及其相关方法 |
| WO2023285700A1 (en) | 2021-07-16 | 2023-01-19 | Academisch Ziekenhuis Leiden H.O.D.N. Lumc | Oligonucleotide for inhibiting quaking activity |
| CA3233242A1 (en) | 2021-09-30 | 2023-04-06 | Sarepta Therapeutics, Inc. | Antisense oligonucleotides having one or more abasic units |
| CN118660876A (zh) * | 2022-02-11 | 2024-09-17 | 波涛生命科学有限公司 | 手性化合物的立体选择性技术 |
| US20250154504A1 (en) | 2022-02-14 | 2025-05-15 | Proqr Therapeutics Ii B.V. | Guide oligonucleotides for nucleic acid editing in the treatment of hypercholesterolemia |
| CA3252028A1 (en) | 2022-05-06 | 2023-11-09 | Academisch Ziekenhuis Leiden H.O.D.N. Lumc | OLIGONUCLEOTIDE |
| WO2024013360A1 (en) | 2022-07-15 | 2024-01-18 | Proqr Therapeutics Ii B.V. | Chemically modified oligonucleotides for adar-mediated rna editing |
| WO2024013361A1 (en) | 2022-07-15 | 2024-01-18 | Proqr Therapeutics Ii B.V. | Oligonucleotides for adar-mediated rna editing and use thereof |
| AU2023312939A1 (en) | 2022-07-25 | 2025-03-06 | Katholieke Universiteit Leuven | Antisense oligonucleotides for treating a disease or condition associated with an abnormal processing of app |
| WO2024064237A2 (en) | 2022-09-21 | 2024-03-28 | Sarepta Therapeutics, Inc. | Dmd antisense oligonucleotide-mediated exon skipping efficiency |
| GB202215614D0 (en) | 2022-10-21 | 2022-12-07 | Proqr Therapeutics Ii Bv | Heteroduplex rna editing oligonucleotide complexes |
| TW202435897A (zh) | 2022-11-24 | 2024-09-16 | 荷蘭商Proqr治療上市公司Ii | 用於治療遺傳性hfe血色沉著病之反義寡核苷酸 |
| GB202218090D0 (en) | 2022-12-01 | 2023-01-18 | Proqr Therapeutics Ii Bv | Antisense oligonucleotides for the treatment of aldehyde dehydrogenase 2 deficiency |
| CA3276262A1 (en) | 2022-12-09 | 2024-06-13 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of cardiovascular disease |
| GB202300865D0 (en) | 2023-01-20 | 2023-03-08 | Proqr Therapeutics Ii Bv | Delivery of oligonucleotides |
| EP4669753A1 (en) | 2023-02-20 | 2025-12-31 | ProQR Therapeutics II B.V. | Antisense oligonucleotides for the treatment of atherosclerotic cardiovascular disease |
| WO2024206175A1 (en) | 2023-03-24 | 2024-10-03 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of neurological disorders |
| GB202304363D0 (en) | 2023-03-24 | 2023-05-10 | Proqr Therapeutics Ii Bv | Chemically modified antisense oligonucleotides for use in RNA editing |
| EP4688143A1 (en) | 2023-03-27 | 2026-02-11 | ProQR Therapeutics II B.V. | Antisense oligonucleotides for the treatment of liver disease |
| TW202442246A (zh) | 2023-04-27 | 2024-11-01 | 美商薩羅塔治療公司 | 用於治療慢性腎病之反義寡聚物 |
| WO2024256620A1 (en) | 2023-06-16 | 2024-12-19 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of neurodegenerative disease |
| AU2024287308A1 (en) | 2023-07-13 | 2025-12-18 | Korro Bio, Inc. | Rna-editing oligonucleotides and uses thereof |
| WO2025051946A1 (en) | 2023-09-07 | 2025-03-13 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of metabolic disorders |
| WO2025085810A2 (en) | 2023-10-18 | 2025-04-24 | Sarepta Therapeutics, Inc. | Antisense oligomers for treatment of centronuclear myopathies |
| AU2024369609A1 (en) | 2023-10-31 | 2025-12-11 | Korro Bio, Inc. | Oligonucleotides comprising phosphoramidate internucleotide linkages |
| WO2025104239A1 (en) | 2023-11-16 | 2025-05-22 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of classic galactosemia |
| WO2025128799A1 (en) | 2023-12-12 | 2025-06-19 | Korro Bio, Inc. | Double-stranded rna-editing oligonucleotides and uses thereof |
| WO2025132708A1 (en) | 2023-12-20 | 2025-06-26 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of huntington's disease |
| GB202404661D0 (en) | 2024-04-02 | 2024-05-15 | Proqr Therapeutics Ii Bv | Antisense oligoncleotides for the treatment of liver disease |
| WO2025224230A1 (en) | 2024-04-25 | 2025-10-30 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of fatty liver disease |
| GB202410081D0 (en) | 2024-07-11 | 2024-08-28 | Proqr Therapeutics Ii Bv | Antisense oligonucleotides for the treatment of cardiovascular disease |
| WO2026022136A1 (en) | 2024-07-23 | 2026-01-29 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of metabolic disorders |
| WO2026050243A1 (en) | 2024-08-26 | 2026-03-05 | Korro Bio, Inc. | Galnac conjugated oligonucleotides for rna editing |
| WO2026057769A1 (en) | 2024-09-12 | 2026-03-19 | Vico Therapeutics B.V. | New dosing regimen for huntington treatment |
| WO2026060374A2 (en) | 2024-09-16 | 2026-03-19 | Proqr Therapeutics Ii B.V. | Antisense oligonucleotides for the treatment of neurological disorders |
Family Cites Families (727)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2878264A (en) | 1959-03-17 | Substituted amino alcohols | ||
| DE1144279B (de) | 1957-09-26 | 1963-02-28 | Robins Co Inc A H | Verfahren zur Herstellung von 3-Aryl-3-hydroxypyrrolidinen und deren Salzen |
| US3135766A (en) | 1961-10-03 | 1964-06-02 | Mead Johnson & Co | 3-substituted-3-pyrrolidinols |
| US3484473A (en) | 1967-05-12 | 1969-12-16 | Buckman Labor Inc | Methylene bisesters of thiolsulfonic acids |
| DE1934150A1 (de) | 1968-07-10 | 1970-01-15 | Pennwalt Corp | Neue 1-Alkanoyloxy-1,2,4,5-tetrahydro-3H,3-benzazepine |
| US3687808A (en) | 1969-08-14 | 1972-08-29 | Univ Leland Stanford Junior | Synthetic polynucleotides |
| US3745162A (en) | 1970-08-31 | 1973-07-10 | Robins Co Inc A H | 1,2,3,4-tetrahydroisoquinoline-2-(thio)-carboxamides |
| GB1448437A (en) | 1973-02-24 | 1976-09-08 | Beecham Group Ltd | Diphenylpropylamines |
| US4022791A (en) | 1975-06-03 | 1977-05-10 | Pfizer Inc. | 2-Aminomethyl-3,4-dihydronaphthalenes |
| GB1504424A (en) | 1975-08-09 | 1978-03-22 | Beecham Group Ltd | Isoquinoline-derived aminoethers |
| BR7807288A (pt) | 1977-11-08 | 1979-06-12 | Genentech Inc | Processo para sintese de polinucleotidos |
| DD133885B1 (de) | 1978-01-04 | 1981-02-25 | Hans Lehmann | Mittel zur bekaempfung von phytopathogenen bakterien und pilzen |
| US5132418A (en) | 1980-02-29 | 1992-07-21 | University Patents, Inc. | Process for preparing polynucleotides |
| US4500707A (en) | 1980-02-29 | 1985-02-19 | University Patents, Inc. | Nucleosides useful in the preparation of polynucleotides |
| US4458066A (en) | 1980-02-29 | 1984-07-03 | University Patents, Inc. | Process for preparing polynucleotides |
| US4668777A (en) | 1981-03-27 | 1987-05-26 | University Patents, Inc. | Phosphoramidite nucleoside compounds |
| US4973679A (en) | 1981-03-27 | 1990-11-27 | University Patents, Inc. | Process for oligonucleo tide synthesis using phosphormidite intermediates |
| US4415732A (en) | 1981-03-27 | 1983-11-15 | University Patents, Inc. | Phosphoramidite compounds and processes |
| US4542142A (en) | 1982-11-22 | 1985-09-17 | Roussel Uclaf | Insecticidal cyclopropane carboxylic acid derivatives with 3-unsaturated-side chain |
| DE3329892A1 (de) | 1983-08-18 | 1985-03-07 | Köster, Hubert, Prof. Dr., 2000 Hamburg | Verfahren zur herstellung von oligonucleotiden |
| US5118800A (en) | 1983-12-20 | 1992-06-02 | California Institute Of Technology | Oligonucleotides possessing a primary amino group in the terminal nucleotide |
| US5643889A (en) | 1984-07-11 | 1997-07-01 | Temple University-Of The Commonwealth System Of Pennsylvania | Cholesterol conjugates of 2'5'-oligoadenylate derivatives and antiviral uses thereof |
| FR2567892B1 (fr) | 1984-07-19 | 1989-02-17 | Centre Nat Rech Scient | Nouveaux oligonucleotides, leur procede de preparation et leurs applications comme mediateurs dans le developpement des effets des interferons |
| US5367066A (en) | 1984-10-16 | 1994-11-22 | Chiron Corporation | Oligonucleotides with selectably cleavable and/or abasic sites |
| FR2575751B1 (fr) | 1985-01-08 | 1987-04-03 | Pasteur Institut | Nouveaux nucleosides de derives de l'adenosine, leur preparation et leurs applications biologiques |
| FR2576898B1 (fr) | 1985-02-01 | 1988-01-08 | Lafon Labor | Derives de 3-phenyl-tetrahydropyridine, procede de preparation et utilisation en therapeutique |
| US4659774A (en) | 1985-11-01 | 1987-04-21 | American Hoechst Corporation | Support for solid-phase oligonucleotide synthesis |
| US4666777A (en) | 1985-12-23 | 1987-05-19 | The Dow Chemical Company | Structured latex core-shell polymer particles suitable for use in the preparation of composite sheets |
| US4735949A (en) | 1986-02-18 | 1988-04-05 | Warner-Lambert Company | Disubstituted-7-pyrrolidinonaphthyridine antibacterial agents |
| US4840956A (en) | 1986-02-18 | 1989-06-20 | Warner-Lambert Company | Novel disubstituted-7-pyrrolidinoquinoline antibacterial agents |
| IL83663A0 (en) | 1986-10-27 | 1988-01-31 | Robins Co Inc A H | Preparation of 3-pyrrolidinols |
| ATE113059T1 (de) | 1987-06-24 | 1994-11-15 | Florey Howard Inst | Nukleosid-derivate. |
| DE3884517T2 (de) | 1987-07-30 | 1994-02-10 | Kupat Holim Health Insurance | Biologisch aktive Carbonsäureester. |
| US4923901A (en) | 1987-09-04 | 1990-05-08 | Millipore Corporation | Membranes with bound oligonucleotides and peptides |
| US5175273A (en) | 1988-07-01 | 1992-12-29 | Genentech, Inc. | Nucleic acid intercalating agents |
| US4945158A (en) | 1988-08-12 | 1990-07-31 | American Cyanamid Company | Antidiabetic phosphonates |
| US4943629A (en) | 1988-08-12 | 1990-07-24 | American Cyanamid Company | Antidiabetic alpha-substituted phosphonates |
| US5047524A (en) | 1988-12-21 | 1991-09-10 | Applied Biosystems, Inc. | Automated system for polynucleotide synthesis and purification |
| US5262530A (en) | 1988-12-21 | 1993-11-16 | Applied Biosystems, Inc. | Automated system for polynucleotide synthesis and purification |
| US5141813A (en) | 1989-08-28 | 1992-08-25 | Clontech Laboratories, Inc. | Multifunctional controlled pore glass reagent for solid phase oligonucleotide synthesis |
| US5134066A (en) | 1989-08-29 | 1992-07-28 | Monsanto Company | Improved probes using nucleosides containing 3-dezauracil analogs |
| CA2029273A1 (en) | 1989-12-04 | 1991-06-05 | Christine L. Brakel | Modified nucleotide compounds |
| US5130302A (en) | 1989-12-20 | 1992-07-14 | Boron Bilogicals, Inc. | Boronated nucleoside, nucleotide and oligonucleotide compounds, compositions and methods for using same |
| EP0507863A4 (en) | 1989-12-28 | 1993-07-07 | Virginia Commonwealth University | Sigma receptor ligands and the use thereof |
| US5459255A (en) | 1990-01-11 | 1995-10-17 | Isis Pharmaceuticals, Inc. | N-2 substituted purines |
| US5212295A (en) | 1990-01-11 | 1993-05-18 | Isis Pharmaceuticals | Monomers for preparation of oligonucleotides having chiral phosphorus linkages |
| US5457191A (en) | 1990-01-11 | 1995-10-10 | Isis Pharmaceuticals, Inc. | 3-deazapurines |
| US5620963A (en) | 1991-10-15 | 1997-04-15 | Isis Pharmaceuticals, Inc. | Oligonucleotides for modulating protein kinase C having phosphorothioate linkages of high chiral purity |
| US5587470A (en) | 1990-01-11 | 1996-12-24 | Isis Pharmaceuticals, Inc. | 3-deazapurines |
| US7101993B1 (en) | 1990-01-11 | 2006-09-05 | Isis Pharmaceuticals, Inc. | Oligonucleotides containing 2′-O-modified purines |
| US5587361A (en) | 1991-10-15 | 1996-12-24 | Isis Pharmaceuticals, Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| US5635488A (en) | 1991-10-15 | 1997-06-03 | Isis Pharmaceuticals, Inc. | Compounds having phosphorodithioate linkages of high chiral purity |
| US5681941A (en) | 1990-01-11 | 1997-10-28 | Isis Pharmaceuticals, Inc. | Substituted purines and oligonucleotide cross-linking |
| AU651569B2 (en) | 1990-01-11 | 1994-07-28 | Isis Pharmaceuticals, Inc. | Compositions and methods for detecting and modulating RNA activity and gene expression |
| US5506212A (en) | 1990-01-11 | 1996-04-09 | Isis Pharmaceuticals, Inc. | Oligonucleotides with substantially chirally pure phosphorothioate linkages |
| US6339066B1 (en) | 1990-01-11 | 2002-01-15 | Isis Pharmaceuticals, Inc. | Antisense oligonucleotides which have phosphorothioate linkages of high chiral purity and which modulate βI, βII, γ, δ, Ε, ζ and η isoforms of human protein kinase C |
| US5646265A (en) | 1990-01-11 | 1997-07-08 | Isis Pharmceuticals, Inc. | Process for the preparation of 2'-O-alkyl purine phosphoramidites |
| US5852188A (en) | 1990-01-11 | 1998-12-22 | Isis Pharmaceuticals, Inc. | Oligonucleotides having chiral phosphorus linkages |
| US5914396A (en) | 1990-01-11 | 1999-06-22 | Isis Pharmaceuticals, Inc. | 2'-O-modified nucleosides and phosphoramidites |
| US5151510A (en) | 1990-04-20 | 1992-09-29 | Applied Biosystems, Inc. | Method of synethesizing sulfurized oligonucleotide analogs |
| US5292875A (en) | 1990-04-20 | 1994-03-08 | Lynx Therapeutics, Inc. | Method of synthesizing sulfurized oligonucleotide analogs |
| HUT63568A (en) | 1990-05-23 | 1993-09-28 | Isis Pharmaceuticals Inc | Composition and process for controlling the activity of rna by modifying the rna 5' cap structure |
| US5783682A (en) | 1990-07-27 | 1998-07-21 | Isis Pharmaceuticals, Inc. | Oligonucleotide mimics having nitrogen-containing linkages |
| US5998603A (en) | 1994-09-29 | 1999-12-07 | Isis Pharmaceuticals, Inc. | 4'-desmethyl nucleoside analogs, and oligomers thereof |
| US5138045A (en) | 1990-07-27 | 1992-08-11 | Isis Pharmaceuticals | Polyamine conjugated oligonucleotides |
| US6087482A (en) | 1990-07-27 | 2000-07-11 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5489677A (en) | 1990-07-27 | 1996-02-06 | Isis Pharmaceuticals, Inc. | Oligonucleoside linkages containing adjacent oxygen and nitrogen atoms |
| US5223618A (en) | 1990-08-13 | 1993-06-29 | Isis Pharmaceuticals, Inc. | 4'-desmethyl nucleoside analog compounds |
| US5677437A (en) | 1990-07-27 | 1997-10-14 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5834607A (en) | 1990-07-27 | 1998-11-10 | Isis Pharmaceuticals, Inc. | Amines and methods of making and using the same |
| JPH0874B2 (ja) | 1990-07-27 | 1996-01-10 | アイシス・ファーマシューティカルス・インコーポレーテッド | 遺伝子発現を検出および変調するヌクレアーゼ耐性、ピリミジン修飾オリゴヌクレオチド |
| US5610289A (en) | 1990-07-27 | 1997-03-11 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogues |
| US5608046A (en) | 1990-07-27 | 1997-03-04 | Isis Pharmaceuticals, Inc. | Conjugated 4'-desmethyl nucleoside analog compounds |
| US5688941A (en) | 1990-07-27 | 1997-11-18 | Isis Pharmaceuticals, Inc. | Methods of making conjugated 4' desmethyl nucleoside analog compounds |
| US5386023A (en) | 1990-07-27 | 1995-01-31 | Isis Pharmaceuticals | Backbone modified oligonucleotide analogs and preparation thereof through reductive coupling |
| US6121433A (en) | 1990-07-27 | 2000-09-19 | Isis Pharmaceuticals, Inc. | Oligomeric compounds having nitrogen-containing linkages |
| US5378825A (en) | 1990-07-27 | 1995-01-03 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs |
| US5541307A (en) | 1990-07-27 | 1996-07-30 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs and solid phase synthesis thereof |
| US5792844A (en) | 1990-07-27 | 1998-08-11 | Isis Pharmaceuticals, Inc. | Oligonucleoside linkages containing adjacent nitrogen atoms |
| US5618704A (en) | 1990-07-27 | 1997-04-08 | Isis Pharmacueticals, Inc. | Backbone-modified oligonucleotide analogs and preparation thereof through radical coupling |
| WO1994022886A1 (en) | 1993-03-30 | 1994-10-13 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5602240A (en) | 1990-07-27 | 1997-02-11 | Ciba Geigy Ag. | Backbone modified oligonucleotide analogs |
| US5623070A (en) | 1990-07-27 | 1997-04-22 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5432272A (en) | 1990-10-09 | 1995-07-11 | Benner; Steven A. | Method for incorporating into a DNA or RNA oligonucleotide using nucleotides bearing heterocyclic bases |
| US5512668A (en) | 1991-03-06 | 1996-04-30 | Polish Academy Of Sciences | Solid phase oligonucleotide synthesis using phospholane intermediates |
| US7015315B1 (en) | 1991-12-24 | 2006-03-21 | Isis Pharmaceuticals, Inc. | Gapped oligonucleotides |
| US20020183502A1 (en) | 1991-05-21 | 2002-12-05 | Mesmaeker Alain De | Backbone-modified oligonucleotide analogs and methods for using same |
| US6414112B1 (en) | 1991-05-24 | 2002-07-02 | Ole Buchardt | Peptide nucleic acids having 2,6-diaminopurine nucleobases |
| AU659649B2 (en) | 1991-06-10 | 1995-05-25 | Lucky Limited | Hepatitis C diagnostics and vaccines |
| US5646267A (en) | 1991-08-05 | 1997-07-08 | Polish Academy Of Sciences | Method of making oligonucleotides and oligonucleotide analogs using phospholanes and enantiomerically resolved phospholane analogues |
| US5359052A (en) | 1991-08-05 | 1994-10-25 | Polish Academy Of Sciences | Chalcophospholanes useful in the synthesis of oligonucleoside phosphorothioates, phosphorodithioates and related selenates |
| US7119184B2 (en) | 1991-08-12 | 2006-10-10 | Isis Pharmaceuticals, Inc. | Oligonucleotides having A-DNA form and B-DNA form conformational geometry |
| US6369209B1 (en) | 1999-05-03 | 2002-04-09 | Isis Pharmaceuticals, Inc. | Oligonucleotides having A-DNA form and B-DNA form conformational geometry |
| US5661134A (en) | 1991-10-15 | 1997-08-26 | Isis Pharmaceuticals, Inc. | Oligonucleotides for modulating Ha-ras or Ki-ras having phosphorothioate linkages of high chiral purity |
| US5576302A (en) | 1991-10-15 | 1996-11-19 | Isis Pharmaceuticals, Inc. | Oligonucleotides for modulating hepatitis C virus having phosphorothioate linkages of high chiral purity |
| US5599797A (en) | 1991-10-15 | 1997-02-04 | Isis Pharmaceuticals, Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| US5654284A (en) | 1991-10-15 | 1997-08-05 | Isis Pharmaceuticals, Inc. | Oligonucleotides for modulating RAF kinase having phosphorothioate linkages of high chiral purity |
| ATE221127T1 (de) | 1991-10-15 | 2002-08-15 | Isis Pharmaceuticals Inc | Über chirale phosphoratome gebundene oligonukleotide |
| US5607923A (en) | 1991-10-15 | 1997-03-04 | Isis Pharmaceuticals, Inc. | Oligonucleotides for modulating cytomegalovirus having phosphorothioate linkages of high chiral purity |
| ES2103918T3 (es) | 1991-10-17 | 1997-10-01 | Ciba Geigy Ag | Nucleosidos biciclicos, oligonucleotidos, procedimiento para su obtencion y productos intermedios. |
| US5594121A (en) | 1991-11-07 | 1997-01-14 | Gilead Sciences, Inc. | Enhanced triple-helix and double-helix formation with oligomers containing modified purines |
| US6235887B1 (en) | 1991-11-26 | 2001-05-22 | Isis Pharmaceuticals, Inc. | Enhanced triple-helix and double-helix formation directed by oligonucleotides containing modified pyrimidines |
| US5484908A (en) | 1991-11-26 | 1996-01-16 | Gilead Sciences, Inc. | Oligonucleotides containing 5-propynyl pyrimidines |
| US5359044A (en) | 1991-12-13 | 1994-10-25 | Isis Pharmaceuticals | Cyclobutyl oligonucleotide surrogates |
| DK1695979T3 (da) | 1991-12-24 | 2011-10-10 | Isis Pharmaceuticals Inc | Gappede modificerede oligonukleotider |
| GB9213601D0 (en) | 1992-06-26 | 1992-08-12 | Mastico Robert A | Protein based delivery system |
| US7067497B2 (en) | 1992-09-29 | 2006-06-27 | Isis Pharmaceuticals, Inc. | Modulation of telomere length by oligonucleotides having a G-core sequence |
| US6444656B1 (en) | 1992-12-23 | 2002-09-03 | Biochem Pharma, Inc. | Antiviral phosphonate nucleotides |
| US6005107A (en) | 1992-12-23 | 1999-12-21 | Biochem Pharma, Inc. | Antiviral compounds |
| NZ262254A (en) | 1993-01-25 | 1997-10-24 | Hybridon Inc | Oligonucleotide analogue containing a ribonucleotide alkylphosphon(ate or thioate), gene repression |
| CA2159632A1 (en) | 1993-03-31 | 1994-10-13 | Ashis Kumar Saha | Novel 5'-substituted nucleosides and oligomers produced therefrom |
| AU6551094A (en) | 1993-03-31 | 1994-10-24 | Sterling Winthrop Inc. | Bifunctional nucleosides, oligomers thereof, and methods of making and using the same |
| US5955591A (en) | 1993-05-12 | 1999-09-21 | Imbach; Jean-Louis | Phosphotriester oligonucleotides, amidites and method of preparation |
| US6015886A (en) | 1993-05-24 | 2000-01-18 | Chemgenes Corporation | Oligonucleotide phosphate esters |
| EP0628394B1 (en) | 1993-06-10 | 1998-08-26 | Idemitsu Petrochemical Co. Ltd. | Injection molding die |
| US5502177A (en) | 1993-09-17 | 1996-03-26 | Gilead Sciences, Inc. | Pyrimidine derivatives for labeled binding partners |
| US5643989A (en) | 1993-10-29 | 1997-07-01 | Azdel, Inc. | Fiber reinforced functionalized polyolefin composites |
| US5457187A (en) | 1993-12-08 | 1995-10-10 | Board Of Regents University Of Nebraska | Oligonucleotides containing 5-fluorouracil |
| DE4435728A1 (de) | 1994-01-19 | 1995-07-20 | Boehringer Mannheim Gmbh | Biotinsilan-Verbindungen und diese Verbindungen enthaltende Bindematrix |
| US6117679A (en) | 1994-02-17 | 2000-09-12 | Maxygen, Inc. | Methods for generating polynucleotides having desired characteristics by iterative selection and recombination |
| AU1806795A (en) | 1994-02-22 | 1995-09-04 | Novo Nordisk A/S | A method of preparing a variant of a lipolytic enzyme |
| US5596091A (en) | 1994-03-18 | 1997-01-21 | The Regents Of The University Of California | Antisense oligonucleotides comprising 5-aminoalkyl pyrimidine nucleotides |
| HUT75368A (en) | 1994-05-11 | 1997-05-28 | Novo Nordisk As | An enzyme with endo-1,3(4)-beta-glucanase activity |
| US5525711A (en) | 1994-05-18 | 1996-06-11 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Pteridine nucleotide analogs as fluorescent DNA probes |
| HRP950288A2 (en) | 1994-05-31 | 1997-08-31 | Bayer Ag | Oxalylamino-benzofuran- and benzothienyl-derivatives |
| EP0685475B1 (en) | 1994-05-31 | 1999-01-13 | Bayer Ag | Amino-benzofuryl-and thienyl-derivatives |
| PT772619E (pt) | 1994-07-15 | 2006-10-31 | Univ Iowa Res Found | Oligonucleotidos imunomoduladores |
| US6207646B1 (en) | 1994-07-15 | 2001-03-27 | University Of Iowa Research Foundation | Immunostimulatory nucleic acid molecules |
| US6239116B1 (en) | 1994-07-15 | 2001-05-29 | University Of Iowa Research Foundation | Immunostimulatory nucleic acid molecules |
| AU3675195A (en) | 1994-09-07 | 1996-03-27 | Hybridon, Inc. | Oligonucleotide prodrugs |
| US5681940A (en) * | 1994-11-02 | 1997-10-28 | Icn Pharmaceuticals | Sugar modified nucleosides and oligonucleotides |
| CA2208528A1 (en) | 1994-12-22 | 1996-06-27 | Hybridon, Inc. | Synthesis of stereospecific oligonucleotide phosphorothioates |
| GB9501465D0 (en) | 1995-01-25 | 1995-03-15 | King S College London | Nucleoside phosphorothioate derivatives,synthesis and use thereof |
| US6222025B1 (en) | 1995-03-06 | 2001-04-24 | Isis Pharmaceuticals, Inc. | Process for the synthesis of 2′-O-substituted pyrimidines and oligomeric compounds therefrom |
| US6166197A (en) | 1995-03-06 | 2000-12-26 | Isis Pharmaceuticals, Inc. | Oligomeric compounds having pyrimidine nucleotide (S) with 2'and 5 substitutions |
| EP0739983B1 (en) | 1995-04-27 | 2009-12-30 | Takara Bio Inc. | Gene encoding lacto-n-biosidase |
| US6004813A (en) | 1995-05-11 | 1999-12-21 | Applied Research Systems Ars Holding N.V. | Il-6 activity inhibitor |
| AU5855296A (en) | 1995-05-19 | 1996-11-29 | Glycomed Incorporated | Collection of activated glycoside compounds and their biolog ical use |
| AU5869696A (en) | 1995-05-23 | 1996-12-11 | Hybridon, Inc. | Novel synthons for stereoselective oligonucleotide synthesis |
| AU5871196A (en) | 1995-05-23 | 1996-12-24 | Hybridon, Inc. | Methods and compounds for the synthesis of oligonucleotides and the oligonucleotides thereby produced |
| CA2223103A1 (en) | 1995-06-06 | 1996-12-12 | Isis Pharmaceuticals Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| US5932450A (en) | 1995-06-07 | 1999-08-03 | Gen-Probe Incorporated | Enzymatic synthesis of oligonucleotides using digestible templates |
| US5824503A (en) | 1995-06-29 | 1998-10-20 | Takara Shuzo Co, Ltd. | Gene encoding endoglycoceramidase activator |
| DE69635849T2 (de) | 1995-06-29 | 2006-10-19 | Takara Bio Inc., Otsu | Für Endoglycoceramidase kodierendes Gen |
| US6017700A (en) | 1995-08-04 | 2000-01-25 | Bayer Corporation | Cationic oligonucleotides, and related methods of synthesis and use |
| US5936080A (en) | 1996-05-24 | 1999-08-10 | Genta Incorporated | Compositions and methods for the synthesis of organophosphorus derivatives |
| WO1997009443A1 (en) | 1995-09-05 | 1997-03-13 | Michigan State University | PROCESS FOR THE ISOLATION AND PURIFICATION OF TAXOL AND TAXANES FROM TAXUS spp |
| US6476216B1 (en) | 1995-10-20 | 2002-11-05 | Mcgill University | Preparation of phosphorothioate oligomers |
| US6160109A (en) | 1995-10-20 | 2000-12-12 | Isis Pharmaceuticals, Inc. | Preparation of phosphorothioate and boranophosphate oligomers |
| US5734041A (en) | 1995-10-20 | 1998-03-31 | Mcgill University | Preparation of chiral phosphorothioate oligomers |
| US7018793B1 (en) | 1995-12-07 | 2006-03-28 | Diversa Corporation | Combinatorial screening of mixed populations of organisms |
| US6214805B1 (en) | 1996-02-15 | 2001-04-10 | The United States Of America As Represented By The Department Of Health And Human Services | RNase L activators and antisense oligonucleotides effective to treat RSV infections |
| CA2246503A1 (en) | 1996-02-15 | 1997-08-21 | National Institutes Of Health | Rnase l activators and antisense oligonucleotides effective to treat rsv infections |
| GB9604669D0 (en) | 1996-03-05 | 1996-05-01 | Ciba Geigy Ag | Chemical compounds |
| US5824669A (en) | 1996-03-22 | 1998-10-20 | Nitromed, Inc. | Nitrosated and nitrosylated compounds and compositions and their use for treating respiratory disorders |
| AU3025597A (en) | 1996-05-10 | 1997-12-05 | Novo Nordisk A/S | Method of providing novel dna sequences |
| US5856465A (en) | 1996-05-24 | 1999-01-05 | Polska Akademia Nauk Centrum Badan Molekularnych I Makromolekularnych | Compositions and methods for the synthesis of chirally pure organophosphorus nucleoside derivatives |
| US5898031A (en) | 1996-06-06 | 1999-04-27 | Isis Pharmaceuticals, Inc. | Oligoribonucleotides for cleaving RNA |
| WO2005121370A2 (en) | 2004-06-03 | 2005-12-22 | Isis Pharmaceuticals, Inc. | Oligomeric compounds that facilitate risc loading |
| DE19622783A1 (de) | 1996-06-07 | 1997-12-11 | Hoechst Ag | Isolierung der Biosynthesegene für Pseudo-Oligosaccharide aus Streptomyces glaucescens GLA.O und ihre Verwendung |
| ATE339514T1 (de) | 1996-07-16 | 2006-10-15 | Gen Probe Inc | Verfahren zum nachweis und amplifikation von nukleinsäuresequenzen unter verbrauch von modifizierten oligonukleotiden mit erhöhter zielschmelztemperatur (tm) |
| CA2261566A1 (en) | 1996-07-24 | 1998-01-29 | Buchardt, Dorte | Peptide nucleic acids having enhanced binding affinity, sequence specificity and solubility |
| WO1998007734A1 (en) | 1996-08-21 | 1998-02-26 | Hybridon, Inc. | Oligonucleotide prodrugs |
| US6056973A (en) | 1996-10-11 | 2000-05-02 | Sequus Pharmaceuticals, Inc. | Therapeutic liposome composition and method of preparation |
| GB9621522D0 (en) | 1996-10-16 | 1996-12-04 | Biocompatibles Ltd | Synthesis of phosphorus compounds |
| US6639062B2 (en) | 1997-02-14 | 2003-10-28 | Isis Pharmaceuticals, Inc. | Aminooxy-modified nucleosidic compounds and oligomeric compounds prepared therefrom |
| US6172209B1 (en) | 1997-02-14 | 2001-01-09 | Isis Pharmaceuticals Inc. | Aminooxy-modified oligonucleotides and methods for making same |
| US6369237B1 (en) | 1997-03-07 | 2002-04-09 | President And Fellows Of Harvard College | DNA glycosylase inhibitors, and uses related thereto |
| US6015887A (en) | 1997-04-11 | 2000-01-18 | Isis Pharmaceuticals, Inc. | Chiral peptide nucleic acids and methods for preparing same |
| US6468983B2 (en) | 1997-04-21 | 2002-10-22 | The Cleveland Clinic Foundation | RNase L activators and antisense oligonucleotides effective to treat telomerase-expressing malignancies |
| PL184612B1 (pl) | 1997-04-25 | 2002-11-29 | Pan | Sposób wytwarzania modyfikowanych P chiralnych analogów nukleotydów |
| JP2001501975A (ja) | 1997-05-28 | 2001-02-13 | ペーター・エー・ニールセン | 亢進した細胞取り込みを有する結合ペプチド核酸 |
| AR013142A1 (es) | 1997-06-27 | 2000-12-13 | Procter & Gamble | Compuesto de pro-fragancia con acetales ciclicos composicion detergente para lavado de ropa, composicion suavizante de telas y articulo de fabricacionpara proporcionar beneficios de apariencia a las telas, que lo comprenden |
| WO1999005160A2 (en) | 1997-07-25 | 1999-02-04 | Hybridon, Inc. | Oligonuclotides having 3' terminal stereospecific phosphorothioates |
| US6767739B2 (en) | 2001-07-30 | 2004-07-27 | Isis Pharmaceuticals Inc. | Antisense modulation of microsomal triglyceride transfer protein expression |
| US6383808B1 (en) | 2000-09-11 | 2002-05-07 | Isis Pharmaceuticals, Inc. | Antisense inhibition of clusterin expression |
| GB9717158D0 (en) | 1997-08-13 | 1997-10-22 | King S College London | Solution synthesis of oligonucleotides and their phosphorothioate analogues |
| US6750344B1 (en) | 1997-09-05 | 2004-06-15 | Isis Pharmaceuticals, Inc. | Amine compounds and combinatorial libraries comprising same |
| US6794499B2 (en) | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| DE19741715A1 (de) | 1997-09-22 | 1999-03-25 | Hoechst Ag | Pentopyranosyl-Nucleosid, seine Herstellung und Verwendung |
| US6232463B1 (en) | 1997-10-09 | 2001-05-15 | Isis Pharmaceuticals, Inc. | Substituted purines and oligonucleotide cross-linking |
| US6617438B1 (en) | 1997-11-05 | 2003-09-09 | Sirna Therapeutics, Inc. | Oligoribonucleotides with enzymatic activity |
| US6528640B1 (en) | 1997-11-05 | 2003-03-04 | Ribozyme Pharmaceuticals, Incorporated | Synthetic ribonucleic acids with RNAse activity |
| US6080543A (en) | 1997-12-08 | 2000-06-27 | E. & J. Gallo Winery | Detection of fungal pathogens |
| US6582936B1 (en) | 1997-12-12 | 2003-06-24 | The Regents Of The University Of California | Methods for making nucleic acids |
| US6248519B1 (en) | 1998-03-11 | 2001-06-19 | E & J Gallo Winery | Detection of fermentation-related microorganisms |
| US7045610B2 (en) | 1998-04-03 | 2006-05-16 | Epoch Biosciences, Inc. | Modified oligonucleotides for mismatch discrimination |
| CA2328602A1 (en) | 1998-05-06 | 1999-11-11 | University Of Iowa Research Foundation | Methods for the prevention and treatment of parasitic infections and related diseases using cpg oligonucleotides |
| EP1674574A1 (en) | 1998-05-14 | 2006-06-28 | Coley Pharmaceutical GmbH | Methods for Regulating Hematopoiesis using CpG-Oligonucleotides |
| US6867294B1 (en) | 1998-07-14 | 2005-03-15 | Isis Pharmaceuticals, Inc. | Gapped oligomers having site specific chiral phosphorothioate internucleoside linkages |
| US6242589B1 (en) | 1998-07-14 | 2001-06-05 | Isis Pharmaceuticals, Inc. | Phosphorothioate oligonucleotides having modified internucleoside linkages |
| WO2000006588A1 (en) | 1998-07-27 | 2000-02-10 | University Of Iowa Research Foundation | STEREOISOMERS OF CpG OLIGONUCLEOTIDES AND RELATED METHODS |
| DK1104306T3 (da) | 1998-08-10 | 2006-05-22 | Antigenics Inc | Præparater af CpG- og saponinadjuvanser og fremgangsmåder til anvendelse deraf |
| WO2000023444A1 (en) | 1998-10-21 | 2000-04-27 | Abbott Laboratories | 5,7-disubstituted-4-aminopyrido[2,3-d]pyrimidine compounds |
| US6995259B1 (en) | 1998-10-23 | 2006-02-07 | Sirna Therapeutics, Inc. | Method for the chemical synthesis of oligonucleotides |
| WO2000031110A1 (en) | 1998-11-25 | 2000-06-02 | Isis Pharmaceuticals, Inc. | Identification of disease predictive nucleic acids |
| US6451524B1 (en) | 1998-11-25 | 2002-09-17 | Isis Pharmaceuticals, Inc. | Identification of disease predictive nucleic acids |
| EP1141335B1 (en) | 1998-12-21 | 2009-08-05 | Genencor International, Inc. | Chemically modified enzymes with multiple charged variants |
| AU1853600A (en) | 1999-01-06 | 2000-07-24 | Choong-Chin Liew | Method for the detection of gene transcripts in blood and uses thereof |
| US6265172B1 (en) | 1999-02-08 | 2001-07-24 | University Of Kentucky | Diagnostic test and therapy for manganese superoxide dismutate (mNsod) associated diseases |
| US6121437A (en) | 1999-03-16 | 2000-09-19 | Isis Pharmaceuticals, Inc. | Phosphate and thiophosphate protecting groups |
| US6506594B1 (en) | 1999-03-19 | 2003-01-14 | Cornell Res Foundation Inc | Detection of nucleic acid sequence differences using the ligase detection reaction with addressable arrays |
| GB9907245D0 (en) | 1999-03-29 | 1999-05-26 | Goldsborough Andrew | Cleavage of nucleic acids from solid supports |
| JP3072345B1 (ja) | 1999-03-31 | 2000-07-31 | 農林水産省家畜衛生試験場長 | 豚丹毒菌の組換えサブユニットワクチン |
| US5998148A (en) | 1999-04-08 | 1999-12-07 | Isis Pharmaceuticals Inc. | Antisense modulation of microtubule-associated protein 4 expression |
| US6977245B2 (en) | 1999-04-12 | 2005-12-20 | The United States Of America As Represented By The Department Of Health And Human Services | Oligodeoxynucleotide and its use to induce an immune response |
| US6300069B1 (en) | 1999-05-03 | 2001-10-09 | Qiagen Gmbh | Generation and amplification of nucleic acids from ribonucleic acids |
| US6656730B1 (en) | 1999-06-15 | 2003-12-02 | Isis Pharmaceuticals, Inc. | Oligonucleotides conjugated to protein-binding drugs |
| US6271004B1 (en) | 1999-06-25 | 2001-08-07 | Display Systems Biotech A/S | Method for improved reverse transcription at high temperatures |
| US6066500A (en) | 1999-06-25 | 2000-05-23 | Isis Pharmaceuticals Inc. | Antisense modulation of Beta catenin expression |
| US6414135B1 (en) | 1999-07-07 | 2002-07-02 | Isis Pharmaceuticals, Inc. | C3′-methylene hydrogen phosphonate monomers and related compounds |
| US20030092647A1 (en) | 2001-08-08 | 2003-05-15 | Crooke Rosanne M. | Antisense modulation of cholesteryl ester transfer protein expression |
| US6147200A (en) | 1999-08-19 | 2000-11-14 | Isis Pharmaceuticals, Inc. | 2'-O-acetamido modified monomers and oligomers |
| US7264932B2 (en) | 1999-09-24 | 2007-09-04 | Applera Corporation | Nuclease inhibitor cocktail |
| ES2248126T3 (es) | 1999-09-25 | 2006-03-16 | University Of Iowa Research Foundation | Acidos nucleicos inmunoestimuladores. |
| EP1220684B2 (en) | 1999-09-27 | 2010-07-14 | Coley Pharmaceutical Group, Inc. | Methods related to immunostimulatory nucleic acid-induced interferon |
| US6949520B1 (en) | 1999-09-27 | 2005-09-27 | Coley Pharmaceutical Group, Inc. | Methods related to immunostimulatory nucleic acid-induced interferon |
| US20020082227A1 (en) | 1999-09-30 | 2002-06-27 | Scott Henry | Use of oligonucleotides for inhibition of complement activation |
| AU7863200A (en) | 1999-10-06 | 2001-05-10 | Quark Biotech, Inc. | Method for enrichment of natural antisense messenger rna |
| GB9924285D0 (en) | 1999-10-14 | 1999-12-15 | Avecia Ltd | Process |
| US20010055761A1 (en) | 1999-10-29 | 2001-12-27 | Agilent Technologies | Small scale dna synthesis using polymeric solid support with functionalized regions |
| FR2800750B1 (fr) | 1999-11-05 | 2003-01-31 | Centre Nat Rech Scient | Proteines membranaires ctl (choline transporter like) impliquees dans le transport de la choline |
| AU1656601A (en) | 1999-11-12 | 2001-06-12 | Isis Pharmaceuticals, Inc. | Gapped oligomers having site specific chiral phosphorothioate internucleoside linkages |
| US6322985B1 (en) | 1999-12-27 | 2001-11-27 | Technion Research And Development Foundation Ltd. | Abundant, well distributed and hyperpolymorphic simple sequence repeats in prokaryote genomes and use of same for prokaryote classification and typing |
| WO2001050117A1 (en) | 1999-12-30 | 2001-07-12 | Cabot Corporation | Sensors with improved properties |
| WO2001050349A1 (en) | 1999-12-30 | 2001-07-12 | Rutgers, The State University Of New Jersey | Electronic document customization and transformation utilizing user feedback |
| US6649750B1 (en) | 2000-01-05 | 2003-11-18 | Isis Pharmaceuticals, Inc. | Process for the preparation of oligonucleotide compounds |
| US6159697A (en) | 2000-01-19 | 2000-12-12 | Isis Pharmaceuticals, Inc. | Antisense modulation of Smad7 expression |
| US7585847B2 (en) | 2000-02-03 | 2009-09-08 | Coley Pharmaceutical Group, Inc. | Immunostimulatory nucleic acids for the treatment of asthma and allergy |
| US6495677B1 (en) | 2000-02-15 | 2002-12-17 | Kanda S. Ramasamy | Nucleoside compounds |
| GB0004889D0 (en) | 2000-03-01 | 2000-04-19 | Avecia Ltd | Synthesis of oligonucleotides |
| US6936432B2 (en) | 2000-03-01 | 2005-08-30 | Message Pharmaceuticals | Bacterial RNase P proteins and their use in identifying antibacterial compounds |
| US6649172B2 (en) | 2000-03-17 | 2003-11-18 | Corixa Corporation | Amphipathic aldehydes and their uses as adjuvants and immunoeffectors |
| DE10019756A1 (de) | 2000-04-20 | 2001-10-25 | Bayer Ag | Verfahren zur Herstellung von superabsorbierenden Polymeren aus Polyacrylnitrilen |
| WO2001081303A1 (en) | 2000-04-20 | 2001-11-01 | F. Hoffmann-La Roche Ag | Pyrrolidine and piperidine derivatives and their use for the treament of neurodegenerative disorders |
| WO2001085751A1 (en) | 2000-05-09 | 2001-11-15 | Reliable Biopharmaceutical, Inc. | Polymeric compounds useful as prodrugs |
| US6492171B2 (en) | 2000-05-16 | 2002-12-10 | Isis Pharmaceuticals, Inc. | Antisense modulation of TERT expression |
| US6815542B2 (en) | 2000-06-16 | 2004-11-09 | Ribapharm, Inc. | Nucleoside compounds and uses thereof |
| JP3074398U (ja) | 2000-06-27 | 2001-01-12 | ドンウー キヨン ジュシクヘサ | 自動車内装形オゾン発生装置 |
| WO2002012263A1 (en) | 2000-08-03 | 2002-02-14 | Roche Diagnostics Gmbh | Nucleic acid binding compounds containing pyrazolo[3,4-d]pyrimidine analogues of purin-2,6-diamine and their uses |
| US6725412B1 (en) | 2000-08-15 | 2004-04-20 | Dolby Laboratories Licensing Corporation | Low latency data encoder |
| US6809195B1 (en) | 2000-08-16 | 2004-10-26 | Isis Pharmaceuticals, Inc. | Process for the preparation of oligonucleotides |
| US6559279B1 (en) | 2000-09-08 | 2003-05-06 | Isis Pharmaceuticals, Inc. | Process for preparing peptide derivatized oligomeric compounds |
| AU2001291096A1 (en) | 2000-09-15 | 2002-03-26 | Coley Pharmaceutical Gmbh | Process for high throughput screening of CpG-based immuno-agonist/antagonist |
| EP1191097A1 (en) | 2000-09-21 | 2002-03-27 | Leids Universitair Medisch Centrum | Induction of exon skipping in eukaryotic cells |
| GB0024752D0 (en) | 2000-10-10 | 2000-11-22 | Univ Belfast | Oxidative halogenation of aromatic compounds |
| JP2004511527A (ja) | 2000-10-18 | 2004-04-15 | グラクソスミスクライン バイオロジカルズ ソシエテ アノニム | ワクチン |
| US6372492B1 (en) | 2000-10-30 | 2002-04-16 | Isis Pharmaceuticals, Inc. | Antisense modulation of talin expression |
| US6682889B1 (en) | 2000-11-08 | 2004-01-27 | Becton, Dickinson And Company | Amplification and detection of organisms of the Chlamydiaceae family |
| NL1016978C2 (nl) | 2000-12-22 | 2002-06-25 | Robert Jan Colenbrander | Inrichting en werkwijze voor het verpakken en bereiden van voedsel en werkwijze voor het vervaardigen van een dergelijke inrichting. |
| IL156641A0 (en) | 2001-01-22 | 2004-01-04 | Merck & Co Inc | Nucleoside derivatives as inhibitors of rna-dependent rna viral polymerase |
| ATE501251T1 (de) | 2001-01-25 | 2011-03-15 | Evolva Ltd | Zellbibliothek |
| US8008459B2 (en) | 2001-01-25 | 2011-08-30 | Evolva Sa | Concatemers of differentially expressed multiple genes |
| CA2429397C (en) | 2001-01-26 | 2014-06-03 | Commonwealth Scientific And Industrial Research Organisation | Methods and means for producing efficient silencing construct using recombinational cloning |
| US20050277133A1 (en) | 2001-05-18 | 2005-12-15 | Sirna Therapeutics, Inc. | RNA interference mediated treatment of polyglutamine (polyQ) repeat expansion diseases using short interfering nucleic acid (siNA) |
| WO2002097134A2 (en) | 2001-05-25 | 2002-12-05 | Isis Pharmaceuticals, Inc. | Modified peptide nucleic acid |
| GB0113523D0 (en) | 2001-06-04 | 2001-07-25 | Torotrak Dev Ltd | An Hydraulic control circuit for a continuosly variable transmission |
| US20030069410A1 (en) | 2001-06-14 | 2003-04-10 | Isis Pharmaceuticals, Inc. | Methods for preparing oligonucleotides having chiral phosphorothioate linkages |
| US20050019915A1 (en) | 2001-06-21 | 2005-01-27 | Bennett C. Frank | Antisense modulation of superoxide dismutase 1, soluble expression |
| AU2002322358B2 (en) | 2001-06-29 | 2009-06-18 | Novartis Vaccines And Diagnostics, Inc. | HCV E1E2 vaccine compositions |
| CA2452458A1 (en) | 2001-07-03 | 2003-01-16 | Isis Pharmaceuticals, Inc. | Nuclease resistant chimeric oligonucleotides |
| US7205399B1 (en) | 2001-07-06 | 2007-04-17 | Sirna Therapeutics, Inc. | Methods and reagents for oligonucleotide synthesis |
| US6440739B1 (en) | 2001-07-17 | 2002-08-27 | Isis Pharmaceuticals, Inc. | Antisense modulation of glioma-associated oncogene-2 expression |
| US7425545B2 (en) | 2001-07-25 | 2008-09-16 | Isis Pharmaceuticals, Inc. | Modulation of C-reactive protein expression |
| US7888324B2 (en) | 2001-08-01 | 2011-02-15 | Genzyme Corporation | Antisense modulation of apolipoprotein B expression |
| US6455308B1 (en) | 2001-08-01 | 2002-09-24 | Isis Pharmaceuticals, Inc. | Antisense modulation of serum amyloid A4 expression |
| US7407943B2 (en) | 2001-08-01 | 2008-08-05 | Isis Pharmaceuticals, Inc. | Antisense modulation of apolipoprotein B expression |
| US7259150B2 (en) | 2001-08-07 | 2007-08-21 | Isis Pharmaceuticals, Inc. | Modulation of apolipoprotein (a) expression |
| US7227014B2 (en) | 2001-08-07 | 2007-06-05 | Isis Pharmaceuticals, Inc. | Antisense modulation of apolipoprotein (a) expression |
| US7354909B2 (en) | 2001-08-14 | 2008-04-08 | The United States Of America As Represented By Secretary Of The Department Of Health And Human Services | Method for rapid generation of mature dendritic cells |
| EP1418877A2 (en) | 2001-08-24 | 2004-05-19 | Massachusetts Institute Of Technology | Reagents that facilitate the purification of compounds synthesized on a solid support |
| US7049122B2 (en) | 2001-09-21 | 2006-05-23 | Academia Sinica | Mutant-type lipases and applications thereof |
| US6933288B2 (en) | 2002-02-04 | 2005-08-23 | Isis Pharmaceuticals, Inc. | Pyranosyl cytosines: pharmaceutical formulations and methods |
| JP4348044B2 (ja) | 2002-02-12 | 2009-10-21 | 株式会社キラルジェン | 立体規則性の高いジヌクレオシドホスホロチオエートの製造法 |
| US20040149587A1 (en) | 2002-02-15 | 2004-08-05 | George Hradil | Electroplating solution containing organic acid complexing agent |
| US20030159938A1 (en) | 2002-02-15 | 2003-08-28 | George Hradil | Electroplating solution containing organic acid complexing agent |
| US20050096284A1 (en) | 2002-02-20 | 2005-05-05 | Sirna Therapeutics, Inc. | RNA interference mediated treatment of polyglutamine (polyQ) repeat expansion diseases using short interfering nucleic acid (siNA) |
| US8232383B2 (en) | 2002-02-20 | 2012-07-31 | Sirna Therapeutics, Inc. | RNA interference mediated inhibition of gene expression using chemically modified short interfering nucleic acid (siNA) |
| WO2003073989A2 (en) | 2002-02-28 | 2003-09-12 | Biota, Inc. | Nucleoside 5'-monophosphate mimics and their prodrugs |
| RU2004128943A (ru) | 2002-02-28 | 2005-04-20 | Байота, Инк. (Us) | Средства, имитирующие нуклеотиды, и их пролекарственные формы |
| US7288376B2 (en) | 2002-03-22 | 2007-10-30 | Council Of Scientific And Industrial Research | Method of detection of SP-A2 gene variants useful for prediction of predisposition to aspergillosis |
| US20040102394A1 (en) | 2002-11-23 | 2004-05-27 | Isis Pharmaceuticals Inc. | Modulation of huntingtin interacting protein 2 expression |
| US7247621B2 (en) | 2002-04-30 | 2007-07-24 | Valeant Research & Development | Antiviral phosphonate compounds and methods therefor |
| WO2003097662A1 (en) | 2002-05-15 | 2003-11-27 | Isis Pharmaceuticals, Inc. | Antisense modulation of apolipoprotein b expression |
| AU2003237249A1 (en) | 2002-05-24 | 2003-12-12 | Isis Pharmaceuticals, Inc. | Oligonucleotides having modified nucleoside units |
| US20040014108A1 (en) | 2002-05-24 | 2004-01-22 | Eldrup Anne B. | Oligonucleotides having modified nucleoside units |
| US7507808B2 (en) | 2002-12-12 | 2009-03-24 | Isis Pharmaceuticals, Inc. | Modulation of endothelial lipase expression |
| WO2003106477A1 (en) | 2002-06-01 | 2003-12-24 | Isis Pharmaceuticals, Inc. | Oligomeric compounds that include carbocyclic nucleosides and their use in gene modulation |
| AU2003242742B2 (en) | 2002-06-20 | 2009-04-30 | Cytos Biotechnology Ag | Packaged virus-like particles for use as adjuvants: method of preparation and use |
| WO2004003228A1 (en) | 2002-07-01 | 2004-01-08 | Unisearch Limited | Genotyping method |
| CA2489174C (en) | 2002-07-10 | 2013-02-05 | Thomas Tuschl | Rna-interference by single-stranded rna molecules |
| US20040023905A1 (en) | 2002-07-31 | 2004-02-05 | Isis Pharmaceuticals Inc. | Antisense modulation of LAR expression |
| US20050042646A1 (en) | 2002-08-05 | 2005-02-24 | Davidson Beverly L. | RNA interference suppresion of neurodegenerative diseases and methods of use thereof |
| US20080274989A1 (en) | 2002-08-05 | 2008-11-06 | University Of Iowa Research Foundation | Rna Interference Suppression of Neurodegenerative Diseases and Methods of Use Thereof |
| US20050255086A1 (en) | 2002-08-05 | 2005-11-17 | Davidson Beverly L | Nucleic acid silencing of Huntington's Disease gene |
| AU2003261449A1 (en) | 2002-08-07 | 2004-02-25 | Compositions for rna interference and methods of use thereof | |
| WO2004014312A2 (en) | 2002-08-08 | 2004-02-19 | Sirna Therapeutics, Inc. | Small-mer compositions and methods of use |
| AR040996A1 (es) | 2002-08-19 | 2005-04-27 | Coley Pharm Group Inc | Acidos nucleicos inmunoestimuladores |
| US7414116B2 (en) | 2002-08-23 | 2008-08-19 | Illumina Cambridge Limited | Labelled nucleotides |
| EP2330194A3 (en) | 2002-09-13 | 2011-10-12 | Replicor, Inc. | Non-sequence complementary antiviral oligonucleotides |
| US7030230B2 (en) | 2002-10-25 | 2006-04-18 | Isis Pharmaceuticals, Inc. | Process of purifying phosphoramidites |
| KR20050089799A (ko) | 2002-10-29 | 2005-09-08 | 콜리 파마슈티칼 그룹, 리미티드 | C형 간염 바이러스 감염의 치료에 있어 CpG올리고뉴클레오티드의 용도 |
| AU2003291721A1 (en) | 2002-11-05 | 2004-06-03 | Isis Pharmaceuticals, Inc. | Phosphorous-linked oligomeric compounds and their use in gene modulation |
| AU2003291755A1 (en) | 2002-11-05 | 2004-06-07 | Isis Pharmaceuticals, Inc. | Oligomers comprising modified bases for binding cytosine and uracil or thymine and their use |
| CA2504694C (en) | 2002-11-05 | 2013-10-01 | Isis Pharmaceuticals, Inc. | Polycyclic sugar surrogate-containing oligomeric compounds and compositions for use in gene modulation |
| WO2004044141A2 (en) | 2002-11-05 | 2004-05-27 | Isis Pharmaceuticals, Inc. | Conjugated oligomeric compounds and their use in gene modulation |
| US7381527B2 (en) | 2002-11-06 | 2008-06-03 | Council Of Scientific And Industrial Research | Method of detection of SP-A2 gene variants |
| US7511131B2 (en) | 2002-11-13 | 2009-03-31 | Genzyme Corporation | Antisense modulation of apolipoprotein B expression |
| EP2336318B1 (en) | 2002-11-13 | 2013-04-24 | Genzyme Corporation | Antisense modulation of apolipoprotein b expression |
| DK2284266T3 (da) | 2002-11-14 | 2014-01-13 | Thermo Fisher Scient Biosciences Inc | sIRNA-MOLEKYLE MOD TP53 |
| EP2216407B1 (en) | 2003-03-07 | 2016-01-13 | Alnylam Pharmaceuticals, Inc. | Therapeutic compositions |
| WO2004080466A1 (en) | 2003-03-07 | 2004-09-23 | Ribapharm Inc. | Cytidine analogs and methods of use |
| AU2003225410A1 (en) | 2003-03-21 | 2004-10-11 | Academisch Ziekenhuis Leiden | Modulation of exon recognition in pre-mrna by interfering with the secondary rna structure |
| GB0306657D0 (en) | 2003-03-24 | 2003-04-30 | Avecia Ltd | Process and compounds |
| AU2004223736B2 (en) | 2003-03-26 | 2010-05-27 | Cytos Biotechnology Ag | Melan-A peptide analogue-virus-like-particle conjugates |
| US7537767B2 (en) | 2003-03-26 | 2009-05-26 | Cytis Biotechnology Ag | Melan-A- carrier conjugates |
| ITRM20030149A1 (it) | 2003-04-02 | 2004-10-03 | Giuliani Spa | Oligonucleotidi (odn) antisenso per smad7 e loro usi in campo medico |
| US7598227B2 (en) | 2003-04-16 | 2009-10-06 | Isis Pharmaceuticals Inc. | Modulation of apolipoprotein C-III expression |
| KR20060061930A (ko) | 2003-04-25 | 2006-06-08 | 길리애드 사이언시즈, 인코포레이티드 | 항암성 포스포네이트 유사체 |
| US7407965B2 (en) | 2003-04-25 | 2008-08-05 | Gilead Sciences, Inc. | Phosphonate analogs for treating metabolic diseases |
| EA014685B1 (ru) | 2003-04-25 | 2010-12-30 | Джилид Сайэнс, Инк. | Фосфонатсодержащие антивирусные соединения (варианты) и фармацевтическая композиция на их основе |
| WO2005002626A2 (en) | 2003-04-25 | 2005-01-13 | Gilead Sciences, Inc. | Therapeutic phosphonate compounds |
| US7470724B2 (en) | 2003-04-25 | 2008-12-30 | Gilead Sciences, Inc. | Phosphonate compounds having immuno-modulatory activity |
| US7452901B2 (en) | 2003-04-25 | 2008-11-18 | Gilead Sciences, Inc. | Anti-cancer phosphonate analogs |
| US7432261B2 (en) | 2003-04-25 | 2008-10-07 | Gilead Sciences, Inc. | Anti-inflammatory phosphonate compounds |
| US20090247488A1 (en) | 2003-04-25 | 2009-10-01 | Carina Cannizzaro | Anti-inflammatory phosphonate compounds |
| US20050261237A1 (en) | 2003-04-25 | 2005-11-24 | Boojamra Constantine G | Nucleoside phosphonate analogs |
| CN101410120A (zh) | 2003-04-25 | 2009-04-15 | 吉里德科学公司 | 抗炎的膦酸酯化合物 |
| WO2004096233A2 (en) | 2003-04-25 | 2004-11-11 | Gilead Sciences, Inc. | Nucleoside phosphonate conjugates |
| US7045306B2 (en) | 2003-04-28 | 2006-05-16 | The General Hospital Corporation | Method for identifying compounds in vitro that modulate the dysregulation of transcription of transcription mediated by mutant huntingtin protein |
| US7214491B2 (en) | 2003-05-07 | 2007-05-08 | E. I. Du Pont De Nemours And Company | Δ-12 desaturase gene suitable for altering levels of polyunsaturated fatty acids in oleaginous yeasts |
| JP4179562B2 (ja) | 2003-05-14 | 2008-11-12 | 独立行政法人科学技術振興機構 | ハンチンチン遺伝子の発現抑制 |
| JP4579911B2 (ja) | 2003-06-03 | 2010-11-10 | アイシス・ファーマシューティカルズ・インコーポレイテッド | スルビビン発現の調節 |
| AU2004257149A1 (en) | 2003-06-20 | 2005-01-27 | Coley Pharmaceutical Gmbh | Small molecule toll-like receptor (TLR) antagonists |
| US7683036B2 (en) | 2003-07-31 | 2010-03-23 | Regulus Therapeutics Inc. | Oligomeric compounds and compositions for use in modulation of small non-coding RNAs |
| JP2005089441A (ja) * | 2003-08-08 | 2005-04-07 | Toudai Tlo Ltd | 立体規則性の高いリン原子修飾ヌクレオチド類縁体の製造法 |
| JP2011088935A (ja) | 2003-08-08 | 2011-05-06 | Chiralgen Ltd | リン原子修飾ヌクレオチド類縁体の製造のための光学活性ヌクレオシド3’−ホスホロアミダイト |
| US7825235B2 (en) | 2003-08-18 | 2010-11-02 | Isis Pharmaceuticals, Inc. | Modulation of diacylglycerol acyltransferase 2 expression |
| MXPA06001974A (es) | 2003-08-21 | 2006-05-31 | Univ Griffith | Nuevos oxidos de sulfenamida. |
| BRPI0413684A (pt) | 2003-08-21 | 2006-10-24 | Univ Griffith | compostos, composição farmacêutica e respectivos métodos de preparação, de tratamento de infecção microbiana e de extermìnio de microrganismo e usos |
| JP2007504152A (ja) | 2003-08-27 | 2007-03-01 | ビオタ, インコーポレイテッド | 治療剤としての新規三環ヌクレオシドまたはヌクレオチド |
| US7427672B2 (en) | 2003-08-28 | 2008-09-23 | Takeshi Imanishi | Artificial nucleic acids of n-o bond crosslinkage type |
| WO2005028494A1 (ja) | 2003-09-02 | 2005-03-31 | Takeshi Wada | 5'-ホスフィチル化モノマーおよびh-ホスホネートオリゴヌクレオチド誘導体の製造方法 |
| WO2005023828A1 (ja) | 2003-09-02 | 2005-03-17 | Takeshi Wada | リボヌクレオチド又はリボヌクレオチド誘導体の製造方法 |
| US20050053981A1 (en) | 2003-09-09 | 2005-03-10 | Swayze Eric E. | Gapped oligomeric compounds having linked bicyclic sugar moieties at the termini |
| US20050074801A1 (en) | 2003-09-09 | 2005-04-07 | Monia Brett P. | Chimeric oligomeric compounds comprising alternating regions of northern and southern conformational geometry |
| JP4690324B2 (ja) | 2003-09-09 | 2011-06-01 | ジェロン・コーポレーション | テロメラーゼ阻害のための改変オリゴヌクレオチド |
| WO2008005562A2 (en) | 2006-07-07 | 2008-01-10 | University Of Massachusetts | Rna silencing compositions and methods for the treatment of huntington's disease |
| WO2005027980A1 (en) | 2003-09-12 | 2005-03-31 | University Of Massachusetts | Rna interference for the treatment of gain-of-function disorders |
| US8680063B2 (en) | 2003-09-12 | 2014-03-25 | University Of Massachusetts | RNA interference for the treatment of gain-of-function disorders |
| GB0323968D0 (en) | 2003-10-13 | 2003-11-19 | Glaxosmithkline Biolog Sa | Immunogenic compositions |
| BRPI0416079A (pt) | 2003-10-30 | 2007-01-02 | Coley Pharm Gmbh | análogos de oligonucleotìdeos de classe c com uma potência imunoestimuladora aumentada |
| WO2005042716A2 (en) | 2003-10-31 | 2005-05-12 | President And Fellows Of Harvard College | Nucleic acid binding oligonucleotides |
| US7846436B2 (en) | 2003-11-28 | 2010-12-07 | Chemgenes Corporation | Oligonucleotides and related compounds |
| AU2003300239A1 (en) | 2003-12-29 | 2005-07-21 | Galapagos Genomics N.V. | Modulators of bone homeostasis identified in a high-throughput screen |
| WO2005070859A1 (ja) | 2004-01-27 | 2005-08-04 | Takeshi Wada | フルオラス担体およびそれを用いたオリゴヌクレオチド誘導体の製造方法 |
| US20050176045A1 (en) | 2004-02-06 | 2005-08-11 | Dharmacon, Inc. | SNP discriminatory siRNA |
| WO2005076744A2 (en) | 2004-02-18 | 2005-08-25 | Frutarom Ltd. | Method for the preparation of peptide-oligonucleotide conjugates |
| JP3976742B2 (ja) | 2004-02-27 | 2007-09-19 | 江守商事株式会社 | インターフェロンアルファを誘導する免疫刺激オリゴヌクレオチド |
| WO2005085272A1 (ja) | 2004-03-05 | 2005-09-15 | Takeshi Wada | ボラノホスフェートモノマーおよびそれを用いたオリゴヌクレオチド誘導体の製造方法 |
| JP4865544B2 (ja) * | 2004-03-25 | 2012-02-01 | 株式会社キラルジェン | 立体規則性の高いリボヌクレオチド類縁体及びデオキシリボヌクレオチド類縁体の製造法 |
| JP2007531794A (ja) | 2004-04-05 | 2007-11-08 | アルニラム ファーマスーティカルズ インコーポレイテッド | オリゴヌクレオチドの合成および精製に使用する方法および反応試薬 |
| US20050244869A1 (en) | 2004-04-05 | 2005-11-03 | Brown-Driver Vickie L | Modulation of transthyretin expression |
| TWI350168B (en) | 2004-05-07 | 2011-10-11 | Incyte Corp | Amido compounds and their use as pharmaceuticals |
| EP1753881A2 (en) | 2004-05-27 | 2007-02-21 | The Government of the United States of America as represented by The Secretary of the Department of Health and Human Services | Differential expression of molecules associated with acute stroke |
| US7759318B1 (en) | 2004-05-28 | 2010-07-20 | Isis Pharmaceuticals, Inc. | Identification of novel pathways, genes and promoter motifs regulating adipogenesis |
| EP2500430B1 (en) | 2004-06-28 | 2017-03-08 | The University Of Western Australia | Antisense oligonucleotides for inducing exon skipping and methods of use thereof |
| ES2550824T3 (es) | 2004-08-10 | 2015-11-12 | Genzyme Corporation | Oligonucleótidos para su uso en la modulación de lipoproteínas y en los niveles de colesterol en humanos |
| ATE556085T1 (de) | 2004-08-26 | 2012-05-15 | Nippon Shinyaku Co Ltd | Phosphoramiditverbindung und verfahren zur herstellung von oligo-rna |
| JP2008512097A (ja) | 2004-09-07 | 2008-04-24 | アーケミックス コーポレイション | アプタマー医薬品化学 |
| US7884086B2 (en) | 2004-09-08 | 2011-02-08 | Isis Pharmaceuticals, Inc. | Conjugates for use in hepatocyte free uptake assays |
| WO2006031461A2 (en) | 2004-09-09 | 2006-03-23 | Isis Pharmaceuticals, Inc. | Pyrrolidinyl groups for attaching conjugates to oligomeric compounds |
| JP2008513507A (ja) | 2004-09-17 | 2008-05-01 | アイシス ファーマシューティカルズ インコーポレイティッド | 増強されたアンチセンスオリゴヌクレオチド |
| US20090036355A1 (en) | 2004-10-13 | 2009-02-05 | Sanjay Bhanot | Antisense Modulation of PTP1B Expression |
| US9120774B2 (en) | 2004-11-03 | 2015-09-01 | University Of Kansas | Novobiocin analogues having modified sugar moieties |
| US8212011B2 (en) | 2004-11-03 | 2012-07-03 | University Of Kansas | Novobiocin analogues |
| US8212012B2 (en) | 2004-11-03 | 2012-07-03 | University Of Kansas | Novobiocin analogues having modified sugar moieties |
| WO2006050501A2 (en) | 2004-11-03 | 2006-05-11 | University Of Kansas | Novobiocin analogues as anticancer agents |
| US7622451B2 (en) | 2004-11-03 | 2009-11-24 | University Of Kansas | Novobiocin analogues as neuroprotective agents and in the treatment of autoimmune disorders |
| KR100721928B1 (ko) | 2004-11-05 | 2007-05-28 | 주식회사 바이오씨에스 | CpG 올리고데옥시뉴클레오티드를 함유하는 피부질환의치료 또는 예방용 약학적 조성물 |
| EP1657307A1 (en) | 2004-11-16 | 2006-05-17 | Immunotech S.A. | Oligonucleotides that induce the secretion of GM-CSF |
| JP4981681B2 (ja) | 2004-12-09 | 2012-07-25 | アルナイラム ファーマシューティカルズ, インコーポレイテッド | 哺乳類における免疫応答誘導組成物および方法、ならびに短鎖干渉rnaなどのオリゴヌクレオチド剤に対する免疫応答の回避方法 |
| US9809824B2 (en) | 2004-12-13 | 2017-11-07 | The United States Of America, Represented By The Secretary, Department Of Health And Human Services | CpG oligonucleotide prodrugs, compositions thereof and associated therapeutic methods |
| WO2006066260A2 (en) | 2004-12-17 | 2006-06-22 | Thiosense, Inc. | Compositions of and methods for producing phosphorus-chiral monomers and oligomers |
| US20070099851A1 (en) | 2004-12-30 | 2007-05-03 | Linn Gregory S | Stable analogues of ribose-1-phosphate and methods for treating diabetes and other metabolic disorders |
| US20060183763A1 (en) | 2004-12-31 | 2006-08-17 | Pfizer Inc | Novel pyrrolidyl derivatives of heteroaromatic compounds |
| EP1841777B1 (en) | 2005-01-28 | 2015-09-30 | Kwon, Hyung-Joo | Oligonucleotides derived from mycobacterium for stimulating immune function, treating immune-related diseases, atopic dermatitis and/or protecting normal immune cell |
| WO2006091915A2 (en) | 2005-02-24 | 2006-08-31 | Coley Pharmaceutical Group, Inc. | Immunostimulatory oligonucleotides |
| US8222257B2 (en) | 2005-04-01 | 2012-07-17 | The Regents Of The University Of California | Phosphono-pent-2-en-1-yl nucleosides and analogs |
| ATE418992T1 (de) | 2005-05-05 | 2009-01-15 | Antisense Pharma Gmbh | Verwendung von tgf-beta2 antisense oligonukleotiden |
| US7902352B2 (en) | 2005-05-06 | 2011-03-08 | Medtronic, Inc. | Isolated nucleic acid duplex for reducing huntington gene expression |
| US20060257912A1 (en) | 2005-05-06 | 2006-11-16 | Medtronic, Inc. | Methods and sequences to suppress primate huntington gene expression |
| PT3308788T (pt) | 2005-06-23 | 2019-01-30 | Cold Spring Harbor Laboratory | Composições e métodos para a modulação do splicing de smn2 |
| US9133517B2 (en) | 2005-06-28 | 2015-09-15 | Medtronics, Inc. | Methods and sequences to preferentially suppress expression of mutated huntingtin |
| WO2007002904A2 (en) | 2005-06-28 | 2007-01-04 | Medtronic, Inc. | Methods and sequences to preferentially suppress expression of mutated huntingtin |
| WO2007005941A2 (en) | 2005-07-05 | 2007-01-11 | President And Fellows Of Harvard College | Liver targeted conjugates |
| JP4984634B2 (ja) | 2005-07-21 | 2012-07-25 | ソニー株式会社 | 物理情報取得方法および物理情報取得装置 |
| CN101272773A (zh) | 2005-07-28 | 2008-09-24 | Id-菲什技术公司 | 改善细胞对杂质粒子渗透性的方法 |
| AU2006284855B2 (en) | 2005-08-29 | 2011-10-13 | Regulus Therapeutics Inc. | Methods for use in modulating miR-122a |
| US8501703B2 (en) | 2005-08-30 | 2013-08-06 | Isis Pharmaceuticals, Inc. | Chimeric oligomeric compounds for modulation of splicing |
| US7700567B2 (en) | 2005-09-29 | 2010-04-20 | Supergen, Inc. | Oligonucleotide analogues incorporating 5-aza-cytosine therein |
| US20070077993A1 (en) | 2005-09-30 | 2007-04-05 | Midgley Timothy M | Method and apparatus for collecting user game play data and crediting users in a gaming environment |
| EP2341059A1 (en) | 2005-10-12 | 2011-07-06 | Idera Pharmaceuticals, Inc. | Immune regulatory oligonucleotide (IRO) compounds to modulate toll-like receptor based immune response |
| US9308252B2 (en) | 2005-10-27 | 2016-04-12 | Cook Biotech, Inc. | Extracellular matrix materials as vaccine adjuvants for diseases associated with infectious pathogens or toxins |
| US8883969B2 (en) | 2005-10-28 | 2014-11-11 | Tosoh Corporation | Method for production of carotenoid-synthesizing microorganism and method for production of carotenoid |
| WO2007051045A2 (en) | 2005-10-28 | 2007-05-03 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibiting expression of huntingtin gene |
| JP2009515896A (ja) | 2005-11-11 | 2009-04-16 | ファイザー・インク | 免疫調節性オリゴデオキシヌクレオチドを使用する併用療法 |
| WO2007064291A1 (en) | 2005-11-30 | 2007-06-07 | Jyoti Chattopadhyaya | Method and compounds for rna synthesis |
| AU2006320374B2 (en) | 2005-12-02 | 2012-08-30 | Isis Pharmaceuticals, Inc. | Antibacterial 4,5-substituted aminoglycoside analogs having multiple substituents |
| US8076303B2 (en) | 2005-12-13 | 2011-12-13 | Spring Bank Pharmaceuticals, Inc. | Nucleotide and oligonucleotide prodrugs |
| PT1979356E (pt) | 2005-12-21 | 2013-11-21 | Pfizer Prod Inc | Carbonilaminopirrolopirazolos, inibidores potentes de cinase |
| PL2161038T3 (pl) | 2006-01-26 | 2014-06-30 | Ionis Pharmaceuticals Inc | Kompozycje i ich zastosowanie ukierunkowane na huntingtynę |
| KR101304071B1 (ko) | 2006-01-27 | 2013-09-06 | 아이시스 파마수티컬즈 인코포레이티드 | 6-변형된 바이시클릭 핵산 유사체 |
| JP5473336B2 (ja) | 2006-02-15 | 2014-04-16 | アディウタイド・ファーマスーティカルズ・ゲーエムベーハー | オリゴヌクレオチドの処方に関する組成物および方法 |
| US7759470B2 (en) | 2006-02-20 | 2010-07-20 | Roche Diagnostics Operations, Inc. | Labeling reagent |
| US8383660B2 (en) | 2006-03-10 | 2013-02-26 | Pfizer Inc. | Dibenzyl amine compounds and derivatives |
| US9040674B2 (en) | 2006-03-31 | 2015-05-26 | Applied Biosystems, Llc | Reagents useful for synthesizing rhodamine-labeled oligonucleotides |
| US8088582B2 (en) | 2006-04-06 | 2012-01-03 | Ibis Biosciences, Inc. | Compositions for the use in identification of fungi |
| RU2439065C2 (ru) | 2006-04-20 | 2012-01-10 | Ф.Хоффманн-Ля Рош Аг | Производные диазепана в качестве модуляторов хемокиновых рецепторов |
| US8206923B2 (en) | 2006-04-24 | 2012-06-26 | Elvira Garza Gonzalez | Method for detection and multiple, simultaneous quantification of pathogens by means of real-time polymerase chain reaction |
| EP2018436A2 (en) | 2006-04-25 | 2009-01-28 | Immune Disease Institute Inc. | Targeted delivery to leukocytes using non-protein carriers |
| GB0608838D0 (en) | 2006-05-04 | 2006-06-14 | Novartis Ag | Organic compounds |
| WO2007143317A2 (en) | 2006-05-05 | 2007-12-13 | Isis Pharmaceuticals, Inc | Compounds and methods for modulating expression of crp |
| EP2023936A4 (en) | 2006-05-05 | 2010-11-24 | Isis Pharmaceuticals Inc | COMPOSITIONS AND THEIR USES ASSOCIATED WITH THE ALPHA PTPR RECEPTOR |
| US20090012120A1 (en) | 2006-05-10 | 2009-01-08 | Board Of Trustees Of Michigan State University | Synthesis of N-heterocycles, beta-amino acids, and allyl amines via aza-payne mediated reaction of ylides and hydroxy aziridines |
| US7666854B2 (en) | 2006-05-11 | 2010-02-23 | Isis Pharmaceuticals, Inc. | Bis-modified bicyclic nucleic acid analogs |
| WO2007134181A2 (en) | 2006-05-11 | 2007-11-22 | Isis Pharmaceuticals, Inc. | 5'-modified bicyclic nucleic acid analogs |
| KR101065760B1 (ko) | 2006-05-31 | 2011-09-19 | 오사카 유니버시티 | 면역자극 올리고뉴클레오티드 및 그 의약 용도 |
| US8097596B2 (en) | 2006-06-30 | 2012-01-17 | Lakewood-Amedex, Inc. | Compositions and methods for the treatment of muscle wasting |
| CN101506368B (zh) | 2006-07-12 | 2017-02-08 | 加利福尼亚大学董事会 | 通过可逆的磷酸三酯电荷中和保护基转导运输核酸 |
| WO2008011453A2 (en) | 2006-07-20 | 2008-01-24 | Amgen Inc. | SUBSTITUTED AZOLE AROMATIC HETEROCYCLES AS INHIBITORS OF LLβ-HSD-1 |
| GB0614947D0 (en) | 2006-07-27 | 2006-09-06 | Isis Innovation | Epitope reduction therapy |
| AU2007281082A1 (en) | 2006-08-04 | 2008-02-07 | Isis Pharmaceuticals, Inc. | Compositions and methods for the modulation of JNK proteins |
| AT504194B1 (de) | 2006-09-07 | 2008-07-15 | Oesterr Rotes Kreuz | Bakteriennachweis |
| US8138330B2 (en) | 2006-09-11 | 2012-03-20 | Sigma-Aldrich Co. Llc | Process for the synthesis of oligonucleotides |
| CN101517082B (zh) | 2006-09-27 | 2014-01-22 | 科勒制药有限责任公司 | 具有增强的免疫刺激活性的含疏水性T类似物的CpG寡聚核苷酸类似物 |
| EP3916095A1 (en) | 2006-10-18 | 2021-12-01 | Ionis Pharmaceuticals, Inc. | Antisense compounds |
| CN101589047A (zh) | 2006-10-23 | 2009-11-25 | Irm责任有限公司 | 组织蛋白酶类抑制剂 |
| KR20090058584A (ko) | 2006-10-26 | 2009-06-09 | 콜리 파마슈티칼 게엠베하 | 올리고리보뉴클레오티드 및 그의 용도 |
| FR2908414B1 (fr) | 2006-11-13 | 2012-01-20 | Centre Nat Rech Scient | Immobilisation de proteines membranaires sur un support par l'intermediaire d'une molecule amphiphile |
| CA2669917A1 (en) | 2006-11-17 | 2008-05-22 | Dawn M. George | Aminopyrrolidines as chemokine receptor antagonists |
| US8093222B2 (en) | 2006-11-27 | 2012-01-10 | Isis Pharmaceuticals, Inc. | Methods for treating hypercholesterolemia |
| EP2453016A1 (en) | 2006-11-27 | 2012-05-16 | Isis Pharmaceuticals, Inc. | Methods for treating hypercholesterolemia |
| CA2671883A1 (en) | 2006-12-12 | 2008-06-19 | Idera Pharmaceuticals, Inc. | Synthetic agonists of tlr9 |
| UY30892A1 (es) | 2007-02-07 | 2008-09-02 | Smithkline Beckman Corp | Inhibidores de la actividad akt |
| EP2125852B1 (en) | 2007-02-15 | 2016-04-06 | Ionis Pharmaceuticals, Inc. | 5'-substituted-2'-f modified nucleosides and oligomeric compounds prepared therefrom |
| BRPI0809320A2 (pt) | 2007-03-24 | 2014-09-23 | Genzyme Corp | Método |
| US7960353B2 (en) | 2007-05-10 | 2011-06-14 | University Of Kansas | Novobiocin analogues as neuroprotective agents and in the treatment of autoimmune disorders |
| HRP20150759T1 (hr) | 2007-05-11 | 2015-08-14 | Adynxx, Inc. | Ekspresija gena i bolovi |
| CA2688008A1 (en) | 2007-05-24 | 2008-11-27 | Kyorin Pharmaceutical Co., Ltd. | Mutilin derivative having heterocyclic aromatic ring carboxylic acid structure in substituent at 14-position |
| GB0710186D0 (en) | 2007-05-29 | 2007-07-04 | Texas Instr Denmark | PWM loop with minimum allasing error property |
| ES2388590T3 (es) | 2007-05-30 | 2012-10-16 | Isis Pharmaceuticals, Inc. | Análogos de ácidos nucleicos bicíclicos con puente aminometileno N-sustituido. |
| EP2155671B8 (en) | 2007-06-05 | 2018-02-21 | Integrative Research Laboratories Sweden AB | Disubstituted phenylpyrrolidines as modulators of cortical catecholaminergic neurotransmission |
| WO2008154401A2 (en) | 2007-06-08 | 2008-12-18 | Isis Pharmaceuticals, Inc. | Carbocyclic bicyclic nucleic acid analogs |
| WO2008151833A2 (en) | 2007-06-13 | 2008-12-18 | Hochschule Mannheim | Compounds for the modulation of huntingtin aggregation, methods and means for identifying such compounds |
| ATE462787T1 (de) | 2007-06-18 | 2010-04-15 | Commissariat Energie Atomique | Reversibles sirna-silencing eines mutierten und endogenen huntington-wildtypgens und dessen anwendung zur behandlung von morbus huntington |
| GB0712494D0 (en) | 2007-06-27 | 2007-08-08 | Isis Innovation | Substrate reduction therapy |
| ATE538127T1 (de) | 2007-07-05 | 2012-01-15 | Isis Pharmaceuticals Inc | 6-disubstituierte bicyclische nukleinsäureanaloga |
| EP2348112B1 (en) | 2007-07-09 | 2018-11-28 | Idera Pharmaceuticals, Inc. | Stabilized immune modulatory RNA (SIMRA) compounds |
| TWI413530B (zh) | 2007-07-20 | 2013-11-01 | Kao Corp | 有機聚矽氧 |
| AU2008281281A1 (en) | 2007-07-31 | 2009-02-05 | University Of Saskatchewan | Genetic variation in Pro-Melanin-Concentrating Hormone gene affects carcass traits in cattle |
| US7812003B2 (en) | 2007-08-02 | 2010-10-12 | Safe Stephen H | Antisense microRNA and uses therefor |
| AU2008286735A1 (en) | 2007-08-15 | 2009-02-19 | Idera Pharmaceuticals, Inc. | Toll like receptor modulators |
| BRPI0817527A2 (pt) | 2007-10-01 | 2017-05-02 | Isis Pharmaceuticals Inc | modulação antissenso da expressão do receptor de fator de crescimento de fibroblasto humano 4 |
| KR100886139B1 (ko) | 2007-11-13 | 2009-02-27 | 주식회사 삼천리제약 | 올리고뉴클레오타이드의 제조방법 |
| AR069869A1 (es) | 2007-12-21 | 2010-02-24 | Exelixis Inc | Derivados de benzofuro[3,2-d]pirimidinas inhibidores de proteinquinasas,composiciones farmaceuticas que los comprenden y usos de los mismos en el tratamiento del cancer. |
| TWI340765B (en) | 2007-12-26 | 2011-04-21 | Ind Tech Res Inst | Oligonucleotide sequences and dna chip for identifying filamentous microorganisms and the identification method thereof |
| US20100309376A1 (en) | 2008-01-15 | 2010-12-09 | Yungchun Lei | Multimedia Presenting System, Multimedia Processing Apparatus Thereof, and Method for Presenting Video and Audio Signals |
| WO2009089659A1 (en) | 2008-01-18 | 2009-07-23 | Shanghai Targetdrug Co., Ltd. | Pyrollidine-based compounds |
| CA2711587A1 (en) | 2008-02-04 | 2009-08-13 | Galapagos Nv | Target sequences and methods to identify the same, useful in treatment of neurodegenerative diseases |
| JP2009190983A (ja) | 2008-02-12 | 2009-08-27 | Tokyo Institute Of Technology | オリゴヌクレオチド誘導体 |
| US8426378B2 (en) | 2008-03-21 | 2013-04-23 | Isis Pharmaceuticals, Inc. | Oligomeric compounds comprising tricyclic nucelosides and methods for their use |
| WO2009120878A2 (en) | 2008-03-26 | 2009-10-01 | Alnylam Pharmaceuticals, Inc. | Non-natural ribonucleotides, and methods of use thereof |
| WO2009146123A2 (en) | 2008-04-03 | 2009-12-03 | Spring Bank | Compositions and methods for treating viral infections |
| DE112009001327A5 (de) | 2008-04-04 | 2011-03-31 | Universität Hamburg | Verfahren zur stereoselektiven Synthese von Phosphor-Verbindungen |
| US9290534B2 (en) | 2008-04-04 | 2016-03-22 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds having at least one neutrally linked terminal bicyclic nucleoside |
| WO2009135322A1 (en) | 2008-05-09 | 2009-11-12 | The Universtity Of British Columbia | Methods and compositions for the treatment of huntington's disease |
| US8679750B2 (en) | 2008-05-09 | 2014-03-25 | The University Of British Columbia | Methods and compositions for the treatment of Huntington'S disease |
| US8815817B2 (en) | 2008-05-15 | 2014-08-26 | Dynavax Technologies Corporation | Long term disease modification using immunostimulatory oligonucleotides |
| WO2009143387A2 (en) | 2008-05-22 | 2009-11-26 | Isis Pharmaceuticals, Inc. | Modulation of smrt expression |
| US8541388B2 (en) | 2008-05-22 | 2013-09-24 | Isis Pharmaceuticals, Inc. | Methods for modulating expression of RBP4 |
| WO2009143391A2 (en) | 2008-05-22 | 2009-11-26 | Isis Pharmaceuticals, Inc | Methods for modulation expression of creb |
| WO2009148605A2 (en) | 2008-06-04 | 2009-12-10 | Isis Pharmaceuticals, Inc. | Methods for treating hypercholesterolemia |
| CN102143746A (zh) * | 2008-07-03 | 2011-08-03 | 埃克塞利希斯股份有限公司 | Cdk 调节剂 |
| US8410070B2 (en) | 2008-09-12 | 2013-04-02 | University Of Louisville Research Foundation, Inc. | Compositions and methods for treating cancer, inhibiting proliferation, and inducing cell death |
| WO2010030858A1 (en) | 2008-09-15 | 2010-03-18 | Enanta Pharmaceuticals, Inc. | 4'-allene-substituted nucleoside derivatives |
| WO2010033133A1 (en) * | 2008-09-22 | 2010-03-25 | Daymen Photo Marketing Lp | Suitcase with integrated pull-out carrier |
| WO2010039543A2 (en) | 2008-09-23 | 2010-04-08 | Traversa Therapeutics, Inc. | Self delivering bio-labile phosphate protected pro-oligos for oligonucleotide based therapeutics and mediating rna interference |
| US8604192B2 (en) | 2008-09-24 | 2013-12-10 | Isis Pharmaceuticals, Inc. | Cyclohexenyl nucleic acids analogs |
| WO2010036698A1 (en) | 2008-09-24 | 2010-04-01 | Isis Pharmaceuticals, Inc. | Substituted alpha-l-bicyclic nucleosides |
| AU2009302385B2 (en) | 2008-10-07 | 2015-12-03 | President And Fellows Of Harvard College | Telomerase inhibitors and methods of use thereof |
| CA2962219C (en) | 2008-10-22 | 2020-08-25 | Quark Pharmaceuticals, Inc. | Methods for treating eye disorders |
| WO2010048549A2 (en) | 2008-10-24 | 2010-04-29 | Isis Pharmaceuticals, Inc. | 5' and 2' bis-substituted nucleosides and oligomeric compounds prepared therefrom |
| EP2447274B1 (en) | 2008-10-24 | 2017-10-04 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds and methods |
| RU2572826C2 (ru) | 2008-12-02 | 2016-01-20 | Чиралджен, Лтд. | Способ синтеза модифицированных по атому фосфора нуклеиновых кислот |
| CN102307889A (zh) | 2008-12-23 | 2012-01-04 | 集润德斯股份公司 | 硫化剂及其用于寡核苷酸合成的用途 |
| WO2010080953A1 (en) | 2009-01-08 | 2010-07-15 | Isis Pharmaceuticals, Inc. | Transgenic murine model of human lipoprotein metabolism, hypercholesterolemia and cardiovascular disease |
| KR20100087540A (ko) | 2009-01-28 | 2010-08-05 | 삼성전자주식회사 | 잉크젯 기록용 잉크 조성물 |
| US20120264806A1 (en) | 2009-02-06 | 2012-10-18 | Bennett C Frank | Oligomeric compounds and excipients |
| MX2011008383A (es) | 2009-02-10 | 2011-09-06 | Idera Pharmaceuticals Inc | Agonistas basados en acido ribonucleico sintetico de receptor 7 tipo toll. |
| JP5766617B2 (ja) | 2009-02-20 | 2015-08-19 | ユニバーシティ・オブ・カンザス | 修飾された糖部分を有するノボビオシン類似体 |
| CA2753975C (en) | 2009-03-02 | 2017-09-26 | Alnylam Pharmaceuticals, Inc. | Nucleic acid chemical modifications |
| EP2408796B1 (en) | 2009-03-16 | 2020-04-22 | Ionis Pharmaceuticals, Inc. | Targeting Apolipoprotein B for the reduction of Apolipoprotein C-III |
| EP2415777B1 (en) | 2009-03-31 | 2015-07-29 | Takeda Pharmaceutical Company Limited | Process for producing nucleoside |
| US8987222B2 (en) | 2009-04-08 | 2015-03-24 | University Of Massachusetts | Single nucleotide polymorphism (SNP) targeting therapies for the treatment of huntington'S disease |
| CA2759098A1 (en) | 2009-04-14 | 2010-10-21 | Smith Holdings, Llc | Methods and compositions for the treatment of medical conditions involving cellular programming |
| US9260493B2 (en) | 2009-05-07 | 2016-02-16 | The Regents Of The University Of California | Transducible delivery of nucleic acids using modified dsRNA binding domains |
| EP2438079A4 (en) | 2009-06-01 | 2013-05-22 | Univ California | NUCLEIC ACID DELIVERY COMPOSITIONS AND METHOD OF USE THEREOF |
| SI2437753T1 (sl) | 2009-06-05 | 2016-12-30 | Infectious Disease Research Institute | Sintetični glukopiranozil-lipidni adjuvansi in cepivni sestavki, ki jih vsebujejo |
| PT3449926T (pt) | 2009-06-17 | 2019-11-12 | Cold Spring Harbor Laboratory | Composições e métodos de modulação de excisões de smn2 em um sujeito |
| JP5670097B2 (ja) | 2009-06-19 | 2015-02-18 | 花王株式会社 | 二層分離型毛髪化粧料 |
| JPWO2010150789A1 (ja) | 2009-06-23 | 2012-12-10 | 武田薬品工業株式会社 | 核酸の合成法 |
| SG10201403841QA (en) | 2009-07-06 | 2014-09-26 | Ontorii Inc | Novel nucleic acid prodrugs and methods of use thereof |
| US8329024B2 (en) | 2009-07-06 | 2012-12-11 | Ada Technologies, Inc. | Electrochemical device and method for long-term measurement of hypohalites |
| US8927513B2 (en) | 2009-07-07 | 2015-01-06 | Alnylam Pharmaceuticals, Inc. | 5′ phosphate mimics |
| WO2011005942A2 (en) | 2009-07-08 | 2011-01-13 | Idera Pharmaceuticals, Inc. | Oligonucleotide-based compounds as inhibitors of toll-like receptors |
| EP2458005A1 (en) | 2009-07-23 | 2012-05-30 | Galaxy Pharma Inc. | Fgf21 cis-element binding substance |
| WO2011015572A1 (en) | 2009-08-03 | 2011-02-10 | Galapagos Nv | Molecular targets and compounds, and methods to identify the same, useful in the treatment of neurodegenerative diseases |
| WO2011015573A1 (en) | 2009-08-03 | 2011-02-10 | Galapagos Nv | Molecular targets and compounds, and methods to identify the same, useful in the treatment of neurodegenerative diseases |
| UA107360C2 (en) | 2009-08-05 | 2014-12-25 | Biogen Idec Inc | Bicyclic aryl sphingosine 1-phosphate analogs |
| WO2011017521A2 (en) | 2009-08-06 | 2011-02-10 | Isis Pharmaceuticals, Inc. | Bicyclic cyclohexose nucleic acid analogs |
| US8927553B2 (en) | 2009-08-10 | 2015-01-06 | Daljit Singh Dhanoa | Deuterium-enriched alkyl sulfonamides and uses thereof |
| US8906873B2 (en) | 2009-09-11 | 2014-12-09 | Isis Pharmaceuticals, Inc. | Modulation of huntingtin expression |
| EP2479182B8 (en) | 2009-09-16 | 2016-07-13 | Wave Life Sciences Japan, Inc. | Novel protecting group for synthesizing rna and derivative thereof |
| EP2480667A4 (en) | 2009-09-25 | 2013-07-03 | Isis Pharmaceuticals Inc | MODULATION OF TTC39 EXPRESSION FOR HDL INCREASE |
| PE20121077A1 (es) | 2009-10-15 | 2012-08-10 | Pfizer | Compuestos de pirrolo[2,3-d]pirimidina |
| TWI475051B (zh) | 2009-11-18 | 2015-03-01 | 花王股份有限公司 | Organic polysiloxane |
| JP5809408B2 (ja) | 2009-11-25 | 2015-11-10 | 花王株式会社 | 毛髪化粧料 |
| US8735417B2 (en) | 2009-12-17 | 2014-05-27 | Merck Sharp & Dohme Corp. | Aminopyrimidines as Syk inhibitors |
| US8647742B2 (en) | 2009-12-28 | 2014-02-11 | Achira Labs Pvt. Ltd. | Diagnostic gel composition, method for making a diagnostic gel composition |
| EP3421040A1 (en) | 2010-01-08 | 2019-01-02 | Ionis Pharmaceuticals, Inc. | Modulation of angiopoietin-like 3 expression |
| US8750507B2 (en) | 2010-01-25 | 2014-06-10 | Cisco Technology, Inc. | Dynamic group creation for managed key servers |
| JP6006120B2 (ja) | 2010-02-08 | 2016-10-12 | アイオーニス ファーマシューティカルズ, インコーポレーテッドIonis Pharmaceuticals,Inc. | 対立遺伝子多様体の選択的低減 |
| JP6018506B2 (ja) | 2010-02-08 | 2016-11-02 | アイオーニス ファーマシューティカルズ, インコーポレーテッドIonis Pharmaceuticals,Inc. | 対立遺伝子多様体の選択的低減 |
| JP5922587B2 (ja) | 2010-02-10 | 2016-05-24 | グラクソスミスクライン エルエルシー | 6−アミノ−2−{[(1s)−1−メチルブチル]オキシ}−9−[5−(1−ピペリジニル)ペンチル]−7,9−ジヒドロ−8h−プリン−8−オンマレイン酸塩 |
| WO2011108682A1 (ja) | 2010-03-05 | 2011-09-09 | 国立大学法人 東京大学 | リボヌクレオシドホスホロチオエートの製造方法 |
| WO2011127175A1 (en) | 2010-04-06 | 2011-10-13 | Isis Pharmaceuticals, Inc. | Modulation of cd130 (gp130) expression |
| CA2795750A1 (en) | 2010-04-07 | 2011-10-13 | Isis Pharmaceuticals, Inc. | Modulation of cetp expression |
| WO2011133871A2 (en) | 2010-04-22 | 2011-10-27 | Alnylam Pharmaceuticals, Inc. | 5'-end derivatives |
| CN103154014B (zh) | 2010-04-28 | 2015-03-25 | Isis制药公司 | 修饰核苷、其类似物以及由它们制备的寡聚化合物 |
| US9127033B2 (en) | 2010-04-28 | 2015-09-08 | Isis Pharmaceuticals, Inc. | 5′ modified nucleosides and oligomeric compounds prepared therefrom |
| WO2011139911A2 (en) | 2010-04-29 | 2011-11-10 | Isis Pharmaceuticals, Inc. | Lipid formulated single stranded rna |
| US8906607B2 (en) | 2010-04-30 | 2014-12-09 | Cellectis | Method for modulating double-strand break-induced homologous recombination |
| GB201008902D0 (en) | 2010-05-27 | 2010-07-14 | Imp Innovations Ltd | Membrane enhanced polymer sythesis |
| ES2908978T3 (es) | 2010-08-31 | 2022-05-04 | Sirna Therapeutics Inc | Nuevas entidades químicas simples y métodos para la administración de oligonucleótidos |
| JP5868324B2 (ja) | 2010-09-24 | 2016-02-24 | 株式会社Wave Life Sciences Japan | 不斉補助基 |
| JP5996431B2 (ja) | 2010-09-30 | 2016-09-21 | Lsipファンド運営合同会社 | 優性変異遺伝子発現抑制剤 |
| KR101381048B1 (ko) | 2010-10-20 | 2014-04-14 | 씨제이제일제당 (주) | O-포스포세린 생산 균주 및 이로부터 생산된 o-포스포세린으로부터 l-시스테인 또는 이의 유도체의 생산방법 |
| WO2012058210A1 (en) | 2010-10-29 | 2012-05-03 | Merck Sharp & Dohme Corp. | RNA INTERFERENCE MEDIATED INHIBITION OF GENE EXPRESSION USING SHORT INTERFERING NUCLEIC ACIDS (siNA) |
| US9328346B2 (en) | 2010-11-12 | 2016-05-03 | The General Hospital Corporation | Polycomb-associated non-coding RNAs |
| EP2647644B1 (en) | 2010-11-30 | 2020-09-09 | Wave Life Sciences Japan, Inc. | 2'-o-modified rna |
| US20140050778A1 (en) | 2010-12-28 | 2014-02-20 | University Of Rochester | Nucleic acid binding compounds, methods of making, and use thereof |
| EP2673361B1 (en) | 2011-02-08 | 2016-04-13 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleotides and uses thereof |
| WO2012109667A1 (en) | 2011-02-12 | 2012-08-16 | University Of Iowa Research Foundation | Therapeutic compounds |
| WO2012151324A1 (en) | 2011-05-02 | 2012-11-08 | Isis Pharmaceuticals, Inc. | Antisense compounds targeting genes associated with usher syndrome |
| FR2975600B1 (fr) | 2011-05-24 | 2013-07-05 | Assist Publ Hopitaux De Paris | Agents pour le traitement de tumeurs |
| RU2014106024A (ru) | 2011-07-19 | 2015-08-27 | Юниверсити Оф Айдахо | Варианты осуществления зонда и способы направленного действия на нуклеиновые кислоты |
| CN107365339A (zh) | 2011-07-19 | 2017-11-21 | 波涛生命科学有限公司 | 合成官能化核酸的方法 |
| EP2742136B1 (en) | 2011-08-11 | 2017-09-27 | Ionis Pharmaceuticals, Inc. | Gapped oligomeric compounds comprising 5'-modified deoxyribonucleosides in the gap and uses thereof |
| EP2751269B1 (en) | 2011-08-29 | 2016-03-23 | Ionis Pharmaceuticals, Inc. | Methods and compounds useful in conditions related to repeat expansion |
| US20140080896A1 (en) | 2011-08-30 | 2014-03-20 | The Regents Of The University Of California | Identification of small molecules that facilitate therapeutic exon skipping |
| DK2751284T3 (en) | 2011-08-31 | 2017-03-27 | Univ Manchester | PROCEDURE FOR DIAGNOSTICING A NEURODEGENERATIVE DISEASE |
| WO2013036833A1 (en) | 2011-09-09 | 2013-03-14 | Mayo Foundation For Medical Education And Research | Detecting frontotemporal dementia and amyotrophic lateral sclerosis |
| ES2832531T3 (es) | 2011-11-30 | 2021-06-10 | Sarepta Therapeutics Inc | Oligonucleótidos para el tratamiento de enfermedades por expansión de repeticiones |
| WO2013090457A2 (en) | 2011-12-12 | 2013-06-20 | Oncoimmunin Inc. | In vivo delivery of oligonucleotides |
| CN112386605A (zh) | 2011-12-16 | 2021-02-23 | 国立大学法人东京医科齿科大学 | 嵌合的双链核酸 |
| JP6619140B2 (ja) | 2011-12-20 | 2019-12-11 | サウジ アラムコ テクノロジーズ カンパニー | ポリマー合成方法 |
| CN102675386B (zh) | 2011-12-24 | 2014-07-02 | 河南科技大学 | 一种龙胆苦苷分离提纯方法 |
| US8957042B2 (en) | 2012-03-07 | 2015-02-17 | The Texas A&M University System | Cancer treatment targeting non-coding RNA overexpression |
| EP2834258B1 (en) | 2012-03-13 | 2017-01-04 | Gilead Sciences, Inc. | 2'- substituted carba-nucleoside analogs for antiviral treatment |
| KR20130114435A (ko) | 2012-04-09 | 2013-10-17 | 삼성전자주식회사 | 다수의 전극을 갖는 생분자 검출 장치 |
| PT2841578T (pt) | 2012-04-23 | 2017-08-10 | Biomarin Tech Bv | Resumo |
| EP2852603B1 (en) | 2012-05-22 | 2021-05-12 | Idenix Pharmaceuticals LLC | D-amino acid compounds for liver disease |
| WO2013179412A1 (ja) | 2012-05-30 | 2013-12-05 | 北海道システム・サイエンス株式会社 | 高分散性液相支持体を用いたオリゴヌクレオチド合成法 |
| EP2872147B1 (en) | 2012-07-13 | 2022-12-21 | Wave Life Sciences Ltd. | Method for making chiral oligonucleotides |
| WO2014010718A1 (ja) | 2012-07-13 | 2014-01-16 | 株式会社新日本科学 | キラル核酸アジュバント |
| RU2693381C2 (ru) | 2012-07-13 | 2019-07-02 | Уэйв Лайф Сайенсес Лтд. | Асимметричная вспомогательная группа |
| WO2014025805A1 (en) | 2012-08-06 | 2014-02-13 | Alnylam Pharmaceuticals, Inc. | Carbohydrate conjugated rna agents and process for their preparation |
| KR102237882B1 (ko) | 2012-08-15 | 2021-04-07 | 아이오니스 파마수티컬즈, 인코포레이티드 | 변형된 캡핑 프로토콜을 이용하는 올리고머 화합물 제조 방법 |
| US20150275208A1 (en) | 2012-10-12 | 2015-10-01 | Isis Pharmaceuticals, Inc. | Selective antisense compounds and uses thereof |
| WO2014062736A1 (en) | 2012-10-15 | 2014-04-24 | Isis Pharmaceuticals, Inc. | Methods for monitoring c9orf72 expression |
| DK2906696T4 (da) | 2012-10-15 | 2023-02-27 | Ionis Pharmaceuticals Inc | Fremgangsmåder til modulering af c9orf72-ekspression |
| RU2730677C2 (ru) | 2012-10-15 | 2020-08-24 | Ионис Фармасьютикалз, Инк. | Соединение для модуляции экспрессии гена c9orf72 и его применение |
| MX2015005500A (es) | 2012-10-29 | 2016-02-09 | Cocrystal Pharma Inc | Nucleotidos de pirimidina y sus profarmacos de monofosfato para el tratamiento de infecciones virales y cancer. |
| EP2725029A1 (en) | 2012-10-29 | 2014-04-30 | Laboratoire Biodim | New antibacterial compounds and biological applications thereof |
| JP6358955B2 (ja) | 2012-10-31 | 2018-07-18 | 武田薬品工業株式会社 | 新規修飾核酸 |
| HK1214297A1 (zh) | 2012-11-15 | 2016-07-22 | Roche Innovation Center Copenhagen A/S | 寡核苷酸缀合物 |
| MX2015006289A (es) | 2012-11-26 | 2015-12-03 | Roche Innovation Ct Copenhagen As | Composiciones y metodos para la modulacion de la expresion del receptor del factor de crecimiento de fibroblastos tipo 3 (fgfr3). |
| WO2014099941A1 (en) | 2012-12-19 | 2014-06-26 | Idenix Pharmaceuticals, Inc. | 4'-fluoro nucleosides for the treatment of hcv |
| WO2014118272A1 (en) | 2013-01-30 | 2014-08-07 | Santaris Pharma A/S | Antimir-122 oligonucleotide carbohydrate conjugates |
| RU2018108405A (ru) | 2013-01-30 | 2019-02-26 | Ф. Хоффманн-Ля Рош Аг | Конъюгаты углевода и lna-олигонуклеотида |
| ES2817050T3 (es) | 2013-02-04 | 2021-04-06 | Ionis Pharmaceuticals Inc | Compuestos antisentido selectivos y usos de los mismos |
| DK2958998T3 (en) | 2013-02-22 | 2018-04-16 | Sirna Therapeutics Inc | SHORT INTERFERATING NUCLEIC ACID (SINA) MOLECULES CONTAINING A 2'-INTERNUCLEOSIDE BOND |
| CA2901983A1 (en) | 2013-03-01 | 2014-09-04 | National University Corporation Tokyo Medical And Dental University | Chimeric single-stranded antisense polynucleotides and double-stranded antisense agent |
| EA201500984A1 (ru) | 2013-03-28 | 2016-04-29 | Зингента Партисипейшнс Аг | Способы контроля устойчивых к неоникотиноидам вредителей |
| JP2016520536A (ja) | 2013-03-28 | 2016-07-14 | シンジェンタ パーティシペーションズ アーゲー | ネオニコチノイド抵抗性有害生物の防除方法 |
| DK2991656T3 (da) | 2013-05-01 | 2020-03-23 | Ionis Pharmaceuticals Inc | Sammensætninger og fremgangsmåder til modulering af apolipoprotein c-iii-ekspression |
| JP2016520310A (ja) | 2013-05-24 | 2016-07-14 | ロシュ・イノベーション・センター・コペンハーゲン・アクティーゼルスカブRoche Innovation Center Copenhagen A/S | B細胞cll/リンパ腫11a(bcl11a)のオリゴヌクレオチドモデュレーター及びその使用 |
| CN105228999B (zh) | 2013-05-24 | 2021-03-02 | 味之素株式会社 | 吗啉代寡核苷酸的制备方法 |
| CN105264073A (zh) | 2013-05-30 | 2016-01-20 | 国立大学法人东京医科齿科大学 | 用于递送治疗性寡核苷酸的双链剂 |
| JP6604544B2 (ja) | 2013-06-16 | 2019-11-13 | 国立大学法人 東京医科歯科大学 | エクソンスキッピング効果を有する二本鎖アンチセンス核酸 |
| AU2014284152B2 (en) | 2013-06-21 | 2020-01-23 | Ionis Pharmaceuticals, Inc. | Compositions and methods for modulation of target nucleic acids |
| MX391977B (es) | 2013-06-27 | 2025-03-21 | Roche Innovation Ct Copenhagen As | Oligómeros antisentido y conjugados con diana en la proteína-convertasa subtilisina/kexina tipo 9(pcsk9). |
| TWI657819B (zh) | 2013-07-19 | 2019-05-01 | 美商Ionis製藥公司 | 用於調節τ蛋白表現之組合物 |
| CA2919268C (en) | 2013-07-25 | 2023-09-05 | Exicure, Inc. | Spherical nucleic acid-based constructs as immunostimulatory agents for prophylactic and therapeutic use |
| US10435430B2 (en) | 2013-07-31 | 2019-10-08 | Ionis Pharmaceuticals, Inc. | Methods and compounds useful in conditions related to repeat expansion |
| BR112016004352A2 (pt) | 2013-09-06 | 2017-09-12 | Syngenta Participations Ag | compostos inseticidas |
| EP3052511A4 (en) | 2013-10-02 | 2017-05-31 | Moderna Therapeutics, Inc. | Polynucleotide molecules and uses thereof |
| BR112016007255A2 (pt) | 2013-10-03 | 2017-09-12 | Moderna Therapeutics Inc | polinucleotídeos que codificam receptor de lipoproteína de baixa densidade |
| US9988627B2 (en) | 2013-10-04 | 2018-06-05 | Novartis Ag | Formats for organic compounds for use in RNA interference |
| SG11201602597YA (en) | 2013-10-11 | 2016-05-30 | Ionis Pharmaceuticals Inc | Compositions for modulating c9orf72 expression |
| EP3058068B1 (en) | 2013-10-14 | 2019-04-24 | Ionis Pharmaceuticals, Inc. | Compositions for modulating expression of c9orf72 antisense transcript |
| CA2926341A1 (en) | 2013-10-14 | 2015-04-23 | Ionis Pharmaceuticals, Inc. | Methods for modulating expression of c9orf72 antisense transcript |
| WO2015070212A1 (en) | 2013-11-11 | 2015-05-14 | Sangamo Biosciences, Inc. | Methods and compositions for treating huntington's disease |
| CA2928349A1 (en) | 2013-11-14 | 2015-05-21 | Roche Innovation Center Copenhagen A/S | Apob antisense conjugate compounds |
| US20150167017A1 (en) | 2013-12-13 | 2015-06-18 | Moderna Therapeutics, Inc. | Alternative nucleic acid molecules and uses thereof |
| JPWO2015108046A1 (ja) | 2014-01-15 | 2017-03-23 | 株式会社新日本科学 | 抗アレルギー作用を有するキラル核酸アジュバンド及び抗アレルギー剤 |
| JPWO2015108047A1 (ja) | 2014-01-15 | 2017-03-23 | 株式会社新日本科学 | 免疫誘導活性を有するキラル核酸アジュバンド及び免疫誘導活性剤 |
| EP3095459A4 (en) | 2014-01-15 | 2017-08-23 | Shin Nippon Biomedical Laboratories, Ltd. | Chiral nucleic acid adjuvant having antitumor effect and antitumor agent |
| CA2936712A1 (en) | 2014-01-16 | 2015-07-23 | Meena | Chiral design |
| EP3119797B1 (en) | 2014-03-18 | 2020-12-23 | University of Massachusetts | Raav-based compositions and methods for treating amyotrophic lateral sclerosis |
| EP3137476B1 (en) | 2014-04-28 | 2019-10-09 | Ionis Pharmaceuticals, Inc. | Linkage modified oligomeric compounds |
| JP2017521045A (ja) | 2014-05-01 | 2017-08-03 | アイオーニス ファーマシューティカルズ, インコーポレーテッドIonis Pharmaceuticals,Inc. | アンジオポエチン様因子3発現を調節するための組成物及び方法 |
| EP3139966B1 (en) | 2014-05-08 | 2020-11-18 | Sangamo Therapeutics, Inc. | Compositions for use in treating huntington's disease |
| WO2015179525A1 (en) | 2014-05-20 | 2015-11-26 | University Of Iowa Research Foundation | Huntington's disease therapeutic compounds |
| US20160017327A1 (en) | 2014-07-11 | 2016-01-21 | The Johns Hopkins University | Phosphorodiamidate morpholino oligomers (pmos) and their use in suppression of mutant huntingtin expression and attenuation of neurotoxicity |
| EP3169693B1 (en) | 2014-07-16 | 2022-03-09 | ModernaTX, Inc. | Chimeric polynucleotides |
| EP2982758A1 (en) | 2014-08-04 | 2016-02-10 | Centre Hospitalier Universitaire Vaudois (CHUV) | Genome editing for the treatment of huntington's disease |
| CA2956554C (en) | 2014-08-07 | 2022-03-01 | Takeda Pharmaceutical Company Limited | Preparation of cationic lipid compounds and their salts as nucleic acid carriers |
| WO2016024205A1 (en) | 2014-08-15 | 2016-02-18 | Pfizer Inc. | Oligomers targeting hexanucleotide repeat expansion in human c9orf72 gene |
| WO2016027168A2 (en) | 2014-08-20 | 2016-02-25 | Lifesplice Pharma Llc | Splice modulating oligonucleotides and methods of use thereof |
| WO2016037191A1 (en) | 2014-09-05 | 2016-03-10 | Health Research, Inc. | Use of huntingtin-derived plasmids and peptides for active immunization as a huntington's disease (hd) therapeutic |
| EP3221329A1 (en) | 2014-11-19 | 2017-09-27 | Roche Innovation Center Copenhagen A/S | Lna gapmer oligonucleotides comprising chiral phosphorothioate linkages |
| CN107208092B (zh) | 2014-12-16 | 2021-09-10 | 罗氏创新中心哥本哈根有限公司 | 手性毒性筛选方法 |
| EP3237618B1 (en) | 2014-12-24 | 2019-05-22 | uniQure IP B.V. | Rnai induced huntingtin gene suppression |
| US9688707B2 (en) | 2014-12-30 | 2017-06-27 | Ionis Pharmaceuticals, Inc. | Bicyclic morpholino compounds and oligomeric compounds prepared therefrom |
| WO2016112132A1 (en) | 2015-01-06 | 2016-07-14 | Ionis Pharmaceuticals, Inc. | Compositions for modulating expression of c9orf72 antisense transcript |
| WO2016127002A1 (en) | 2015-02-04 | 2016-08-11 | Bristol-Myers Squibb Company | Lna oligonucleotides with alternating flanks |
| EP3254104B1 (en) | 2015-02-04 | 2021-08-25 | Bristol-Myers Squibb Company | Methods of selecting therapeutic molecules |
| AU2016215155A1 (en) | 2015-02-04 | 2017-08-17 | F. Hoffmann-La Roche Ag | Tau antisense oligomers and uses thereof |
| MX2017010369A (es) | 2015-02-10 | 2017-12-14 | Genzyme Corp | Arni variante. |
| JP2018510621A (ja) | 2015-02-13 | 2018-04-19 | アルナイラム ファーマシューティカルズ, インコーポレイテッドAlnylam Pharmaceuticals, Inc. | パタチン様ホスホリパーゼドメイン含有3(PNPLA3)iRNA組成物およびその使用方法 |
| WO2016138017A1 (en) | 2015-02-23 | 2016-09-01 | Ionis Pharmaceuticals, Inc. | Compounds and methods for increasing antisense activity |
| EP3265098B1 (en) | 2015-03-03 | 2025-03-26 | Ionis Pharmaceuticals, Inc. | Compositions for modulating mecp2 expression |
| WO2016145142A1 (en) | 2015-03-10 | 2016-09-15 | Emory University | Nucleotide and nucleoside therapeutics compositions and uses related thereto |
| WO2016154096A1 (en) | 2015-03-20 | 2016-09-29 | Ionis Pharmaceuticals, Inc. | Modulation of smggds expression |
| CA2980337A1 (en) | 2015-04-03 | 2016-10-06 | University Of Massachusetts | Oligonucleotide compounds for targeting huntingtin mrna |
| US10851371B2 (en) | 2015-04-10 | 2020-12-01 | Ionis Pharmaceuticals, Inc. | Modulation of SMN expression |
| MX366128B (es) | 2015-04-16 | 2019-06-28 | Ionis Pharmaceuticals Inc | Composiciones para modular la expresion de c90rf72. |
| WO2016167780A1 (en) | 2015-04-16 | 2016-10-20 | Ionis Pharmaceuticals, Inc. | Compositions for modulating expression of c9orf72 antisense transcript |
| WO2016209862A1 (en) | 2015-06-23 | 2016-12-29 | Alnylam Pharmaceuticals, Inc. | Glucokinase (gck) irna compositions and methods of use thereof |
| EP4545544A3 (en) | 2015-06-29 | 2025-10-08 | Ionis Pharmaceuticals, Inc. | Modified crispr rna and modified single crispr rna and uses thereof |
| EP3320094B1 (en) | 2015-07-10 | 2022-04-13 | Ionis Pharmaceuticals, Inc. | Modulators of diacyglycerol acyltransferase 2 (dgat2) |
| WO2017011286A1 (en) | 2015-07-10 | 2017-01-19 | Alnylam Pharmaceuticals, Inc. | Insulin-like growth factor binding protein, acid labile subunit (igfals) and insulin-like growth factor 1 (igf-1) irna compositions and methods of use thereof |
| AU2016295168B2 (en) | 2015-07-17 | 2021-08-19 | Alnylam Pharmaceuticals, Inc. | Multi-targeted single entity conjugates |
| CR20180107A (es) | 2015-07-22 | 2018-04-03 | Wave Life Sciences Ltd | Composiciones de oligonucleótidos y métodos de los mismos |
| US20180216114A1 (en) | 2015-07-27 | 2018-08-02 | Alnylam Pharmaceuticals, Inc. | Xanthine dehydrogenase (xdh) irna compositions and methods of use thereof |
| DK3329002T3 (da) | 2015-07-31 | 2021-01-11 | Alnylam Pharmaceuticals Inc | Transthyretin (ttr)-irna-sammensætninger og fremgangsmåder til anvendelse deraf til behandling eller forebyggelse af ttr-forbundne sygdomme |
| EP3341479B1 (en) | 2015-08-24 | 2019-12-18 | Roche Innovation Center Copenhagen A/S | Lna-g process |
| KR102793532B1 (ko) | 2015-08-25 | 2025-04-14 | 알닐람 파마슈티칼스 인코포레이티드 | 전구단백질 컨버타제 서브틸리신 켁신 (pcsk9) 유전자-관련 장애를 치료하기 위한 방법 및 조성물 |
| EP4393495A3 (en) | 2015-09-02 | 2024-09-25 | Alnylam Pharmaceuticals, Inc. | Programmed cell death 1 ligand 1 (pd-l1) irna compositions and methods of use thereof |
| US20180273573A1 (en) | 2015-10-01 | 2018-09-27 | Memorial Sloan-Kettering Cancer Center | Inhibitors of menaquinone biosynthesis |
| US10874686B2 (en) | 2015-10-01 | 2020-12-29 | Memorial Sloan-Kettering Cancer Center | Anthranilyl-adenosinemonosulfamate analogs and uses thereof |
| WO2017055423A1 (en) | 2015-10-02 | 2017-04-06 | Roche Innovation Center Copenhagen A/S | Oligonucleotide conjugation process |
| JP7511326B2 (ja) | 2015-10-09 | 2024-07-05 | ウェイブ ライフ サイエンシズ リミテッド | オリゴヌクレオチド組成物およびその方法 |
| WO2017068087A1 (en) | 2015-10-22 | 2017-04-27 | Roche Innovation Center Copenhagen A/S | Oligonucleotide detection method |
| WO2017067970A1 (en) | 2015-10-22 | 2017-04-27 | Roche Innovation Center Copenhagen A/S | In vitro toxicity screening assay |
| WO2017079291A1 (en) | 2015-11-02 | 2017-05-11 | Ionis Pharmaceuticals, Inc. | Compounds and methods for modulating c90rf72 |
| EP3374498A1 (en) | 2015-11-12 | 2018-09-19 | H. Hoffnabb-La Roche Ag | Standardized neuronal cell assays from primate species |
| CA3015823A1 (en) | 2016-03-13 | 2017-09-21 | Wave Life Sciences Ltd. | Compositions and methods for phosphoramidite and oligonucleotide synthesis |
| CN114717235A (zh) | 2016-03-14 | 2022-07-08 | 豪夫迈·罗氏有限公司 | 用于减少pd-l1表达的寡核苷酸 |
| WO2017157672A1 (en) | 2016-03-18 | 2017-09-21 | Roche Innovation Center Copenhagen A/S | Acyl-protected l-lna-guanosine monomers |
| WO2017165489A1 (en) | 2016-03-23 | 2017-09-28 | Emory University | Antiviral agents for treating zika and dengue virus infections |
| ES2933435T3 (es) | 2016-04-13 | 2023-02-08 | Ionis Pharmaceuticals Inc | Métodos para reducir la expresión de C9ORF72 |
| EP3442983A1 (en) | 2016-04-14 | 2019-02-20 | H. Hoffnabb-La Roche Ag | TRITYL-MONO-Ga1NAc COMPOUNDS AND THEIR USE |
| MA45270A (fr) | 2016-05-04 | 2017-11-09 | Wave Life Sciences Ltd | Compositions d'oligonucléotides et procédés associés |
| JP2019516679A (ja) | 2016-05-04 | 2019-06-20 | ウェイブ ライフ サイエンシズ リミテッドWave Life Sciences Ltd. | 生物活性剤に関する方法および組成物 |
| CN109311925B (zh) | 2016-05-12 | 2022-06-03 | 罗氏创新中心哥本哈根有限公司 | 立体限定的氧杂氮杂磷杂环戊烷亚磷酰胺单体与核苷或寡核苷酸的增强的偶联 |
| CA3023621C (en) | 2016-05-13 | 2021-07-27 | F. Hoffmann-La Roche Ag | Protein-based sample collection matrices and devices |
| EP3458464A1 (en) | 2016-05-18 | 2019-03-27 | ETH Zurich | Stereoselective synthesis of phosphorothioate oligoribonucleotides |
| EP3463386A4 (en) | 2016-06-03 | 2020-03-04 | Wave Life Sciences Ltd. | OLIGONUCLEOTIDES, COMPOSITIONS AND ASSOCIATED METHODS |
| EP4212176A1 (en) | 2016-06-20 | 2023-07-19 | Genahead Bio, Inc. | Antibody-drug conjugate |
| WO2018022473A1 (en) | 2016-07-25 | 2018-02-01 | Wave Life Sciences Ltd. | Phasing |
| MA46905A (fr) | 2016-11-23 | 2019-10-02 | Wave Life Sciences Ltd | Compositions et procédés de synthèse de phosphoramidites et d'oligonucléotides |
| JP2020522265A (ja) | 2017-06-02 | 2020-07-30 | ウェイブ ライフ サイエンシズ リミテッドWave Life Sciences Ltd. | オリゴヌクレオチド組成物及びその使用方法 |
| CA3065523A1 (en) | 2017-06-02 | 2018-12-06 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods of use thereof |
| EP3630199A4 (en) | 2017-06-02 | 2021-11-10 | Wave Life Sciences Ltd. | OLIGONUCLEOTIDE COMPOSITIONS AND METHODS FOR THEIR USE |
| WO2018237194A1 (en) | 2017-06-21 | 2018-12-27 | Wave Life Sciences Ltd. | Compounds, compositions and methods for synthesis |
| CA3072076A1 (en) | 2017-08-08 | 2019-02-14 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| KR20200052369A (ko) | 2017-09-18 | 2020-05-14 | 웨이브 라이프 사이언시스 리미티드 | 올리고뉴클레오티드 제조 기술 |
| WO2019075357A1 (en) | 2017-10-12 | 2019-04-18 | Wave Life Sciences Ltd. | OLIGONUCLEOTIDE COMPOSITIONS AND RELATED METHODS |
| AU2019252680B2 (en) | 2018-04-12 | 2025-11-06 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods of use thereof |
| JP7427608B2 (ja) | 2018-05-11 | 2024-02-05 | ウェイブ ライフ サイエンシズ リミテッド | オリゴヌクレオチド組成物及びその使用方法 |
| WO2020118246A1 (en) | 2018-12-06 | 2020-06-11 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| KR20210121199A (ko) | 2019-02-01 | 2021-10-07 | 웨이브 라이프 사이언시스 리미티드 | 올리고뉴클레오티드 조성물 및 이의 방법 |
| JP2022525541A (ja) | 2019-03-20 | 2022-05-17 | ウェイブ ライフ サイエンシズ リミテッド | オリゴヌクレオチド調製に有用な技術 |
| JPWO2020196662A1 (es) | 2019-03-25 | 2020-10-01 | ||
| CA3137741A1 (en) | 2019-04-25 | 2020-10-29 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods of use thereof |
| BR112021021203A2 (pt) | 2019-04-25 | 2022-01-04 | Wave Life Sciences Ltd | Oligonucleotídeo; composição de oligonucleotídeo quiralmente controlada; composição farmacêutica; método para prevenir, tratar ou melhorar uma afecção, distúrbio ou doença relacionada a ush2a e/ou prevenir, atrasar o início, desenvolvimento e/ou progresso, e/ou tratar uma afecção, distúrbio ou doença relacionada a ush2a em um indivíduo suscetível à mesma ou que sofre da mesma; método para aumentar o nível de salto de um éxon prejudicial em uma transcrição de gene ush2a ou seu produto de gene em uma célula; método para prevenir, atrasar o início ou progressão de, tratar ou melhorar uma afecção, distúrbio ou doença relacionada a ush2a em um indivíduo suscetível à mesma ou que sofre da mesma; método para saltar um éxon prejudicial 13 em um alelo de ush2a em um indivíduo; método para produzir ou aumentar o nível de um éxon de proteína ush2a com salto 13 em um sistema; e composto, oligonucleotídeo, composição ou método |
| US20220145300A1 (en) | 2019-05-09 | 2022-05-12 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods of use thereof |
| CN114585370A (zh) | 2019-10-06 | 2022-06-03 | 波涛生命科学有限公司 | 寡核苷酸组合物及其使用方法 |
| US20230220384A1 (en) | 2019-10-06 | 2023-07-13 | Prashant Monian | Oligonucleotide compositions and methods of use thereof |
| US20230295619A1 (en) | 2020-03-01 | 2023-09-21 | Abbie Madeline Maguire | Oligonucleotide compositions and methods thereof |
| WO2021237223A1 (en) | 2020-05-22 | 2021-11-25 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| CN115885042A (zh) | 2020-05-22 | 2023-03-31 | 波涛生命科学有限公司 | 双链寡核苷酸组合物及其相关方法 |
| EP4200616A1 (en) | 2020-08-24 | 2023-06-28 | Wave Life Sciences Ltd. | Immunoassays for detecting wild type huntingtin protein and methods of treatment employing such immunoassays |
| WO2022046667A1 (en) | 2020-08-24 | 2022-03-03 | Wave Life Sciences Ltd. | Cells and non-human animals engineered to express adar1 and uses thereof |
| EP4217363A4 (en) | 2020-09-24 | 2024-09-25 | Mayo Foundation for Medical Education and Research | Screening platforms |
| CN116507724A (zh) | 2020-11-08 | 2023-07-28 | 波涛生命科学有限公司 | 寡核苷酸组合物及其方法 |
| MX2023005326A (es) | 2020-11-08 | 2023-07-31 | Wave Life Sciences Ltd | Composiciones de oligonucleótidos y métodos de las mismas. |
| US20250135036A1 (en) | 2021-09-26 | 2025-05-01 | Wave Life Sciences Ltd. | Compositions for editing mecp2 transcripts and methods thereof |
| IL311625A (en) | 2021-09-26 | 2024-05-01 | Wave Life Sciences Ltd | Oligonucleotide compositions and methods thereof |
| WO2023075766A1 (en) | 2021-10-27 | 2023-05-04 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods of use thereof |
| EP4422645A4 (en) | 2021-10-27 | 2025-12-03 | Wave Life Sciences Ltd | OLIGONUCLEOTID COMPOSITIONS AND THEIR METHODS OF USE |
| CN118660876A (zh) | 2022-02-11 | 2024-09-17 | 波涛生命科学有限公司 | 手性化合物的立体选择性技术 |
| CA3244794A1 (en) | 2022-03-02 | 2023-09-07 | Wave Life Sciences Ltd. | OLIGONUCLEOTID COMPOSITIONS AND ASSOCIATED PROCESSES ENABLING EXON SKIPPING |
| AU2023253657A1 (en) | 2022-04-15 | 2024-11-14 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods relating thereto |
| CN119452084A (zh) | 2022-05-12 | 2025-02-14 | 波涛生命科学有限公司 | 寡核苷酸组合物及其方法 |
| KR20250051686A (ko) | 2022-08-11 | 2025-04-17 | 웨이브 라이프 사이언시스 리미티드 | 올리고뉴클레오티드 조성물 및 이의 방법 |
| WO2025030155A1 (en) | 2023-08-03 | 2025-02-06 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| WO2025072879A1 (en) | 2023-09-28 | 2025-04-03 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| WO2025072881A2 (en) | 2023-09-28 | 2025-04-03 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| WO2025072886A1 (en) | 2023-09-28 | 2025-04-03 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| WO2025072862A1 (en) | 2023-09-28 | 2025-04-03 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| WO2025072685A1 (en) | 2023-09-28 | 2025-04-03 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| WO2025072883A2 (en) | 2023-09-28 | 2025-04-03 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
| WO2025151895A1 (en) | 2024-01-12 | 2025-07-17 | Wave Life Sciences Ltd. | Oligonucleotide compositions and methods thereof |
-
2013
- 2013-07-12 RU RU2015100197A patent/RU2693381C2/ru not_active Application Discontinuation
- 2013-07-12 KR KR1020157004038A patent/KR101850319B1/ko active Active
- 2013-07-12 US US14/414,604 patent/US9598458B2/en active Active
- 2013-07-12 DK DK13817386.9T patent/DK2872485T3/da active
- 2013-07-12 CN CN201380037512.9A patent/CN104684893B/zh active Active
- 2013-07-12 BR BR112015000784A patent/BR112015000784A8/pt not_active Application Discontinuation
- 2013-07-12 SG SG11201500239VA patent/SG11201500239VA/en unknown
- 2013-07-12 AU AU2013288048A patent/AU2013288048A1/en not_active Abandoned
- 2013-07-12 EP EP20214250.1A patent/EP3812370A1/en active Pending
- 2013-07-12 PL PL13817386T patent/PL2872485T3/pl unknown
- 2013-07-12 CN CN201610835862.5A patent/CN107011400B/zh active Active
- 2013-07-12 CA CA2879023A patent/CA2879023C/en active Active
- 2013-07-12 PT PT138173869T patent/PT2872485T/pt unknown
- 2013-07-12 WO PCT/JP2013/004303 patent/WO2014010250A1/en not_active Ceased
- 2013-07-12 EP EP13817386.9A patent/EP2872485B1/en active Active
- 2013-07-12 ES ES13817386T patent/ES2862073T3/es active Active
- 2013-07-12 JP JP2015500697A patent/JP6268157B2/ja active Active
-
2016
- 2016-07-08 AU AU2016204770A patent/AU2016204770B2/en active Active
- 2016-10-14 US US15/294,602 patent/US10167309B2/en active Active
-
2017
- 2017-10-30 JP JP2017209854A patent/JP6608413B2/ja active Active
-
2018
- 2018-04-26 AU AU2018202884A patent/AU2018202884B2/en active Active
- 2018-11-06 US US16/182,302 patent/US10696711B2/en active Active
-
2019
- 2019-08-21 JP JP2019150815A patent/JP7030749B2/ja active Active
-
2020
- 2020-05-19 US US16/878,461 patent/US11136346B2/en active Active
- 2020-08-10 AU AU2020213420A patent/AU2020213420B2/en active Active
-
2021
- 2021-09-02 US US17/465,238 patent/US12583883B2/en active Active
-
2022
- 2022-02-22 JP JP2022026049A patent/JP7390417B2/ja active Active
-
2023
- 2023-03-20 AU AU2023201700A patent/AU2023201700A1/en active Pending
- 2023-11-17 JP JP2023196280A patent/JP2024023334A/ja active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2862073T3 (es) | Grupo auxiliar asimétrico | |
| ES2586683T3 (es) | Grupo protector novedoso para sintetizar ARN y derivados del mismo | |
| EP2921499A1 (en) | Method for liquid-phase synthesis of nucleic acid | |
| HK40051606A (en) | Asymmetric auxiliary group | |
| JP7433684B1 (ja) | 疑似固相保護基、それを用いたヌクレオシド保護体又はオリゴヌクレオチド保護体、オリゴアミダイト前駆体の製造方法 | |
| HK1242331B (zh) | 不对称辅助基团 | |
| HK1242331A1 (en) | Asymmetric auxiliary group | |
| EP4308580A1 (en) | Chiral synthons for the synthesis of chiral phosphorothioates | |
| TW202409277A (zh) | 用於製備反義寡核苷酸之結晶單體及其製備方法及用途 |