ES2909612T3 - Compuestos de aminotiazol y uso de los mismos - Google Patents
Compuestos de aminotiazol y uso de los mismos Download PDFInfo
- Publication number
- ES2909612T3 ES2909612T3 ES17747997T ES17747997T ES2909612T3 ES 2909612 T3 ES2909612 T3 ES 2909612T3 ES 17747997 T ES17747997 T ES 17747997T ES 17747997 T ES17747997 T ES 17747997T ES 2909612 T3 ES2909612 T3 ES 2909612T3
- Authority
- ES
- Spain
- Prior art keywords
- cancer
- alkyl
- atom bonded
- cycloalkyl
- halo
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Thiazole And Isothizaole Compounds (AREA)
Abstract
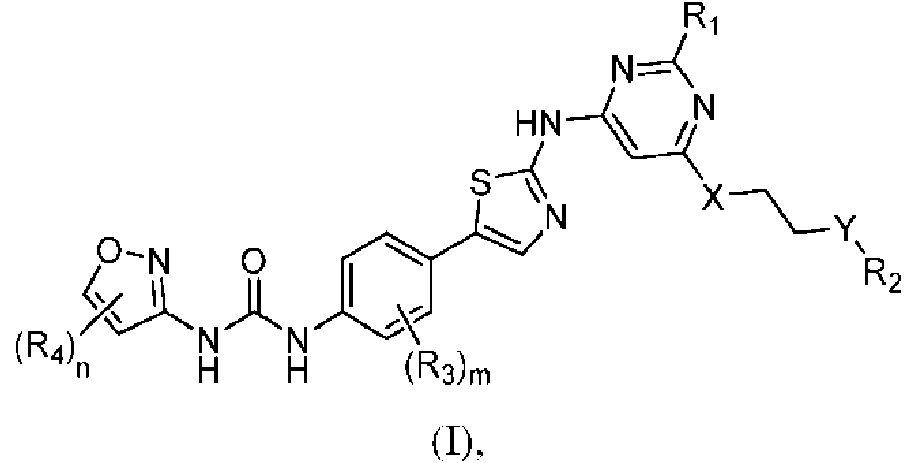
Un compuesto de fórmula (I): **(Ver fórmula)** en donde R1 es H; X es O o NRa, siendo Ra H o alquilo C1-6; Y es CRbRc o NRd, en el que cada uno de Rb y Rc, independientemente, es H, halo, alquilo C1-6, alcoxilo C1-6, o amino, y Rd es H o alquilo C1-6; o Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es heterocicloalquilo C3-10, o Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es heterocicloalquilo C3-10; R2 es -CH2CH2Re o NRfRg, en el que Re es H, halo, alquilo C1-6, u ORh, siendo cada uno de Rf y Rg, independientemente, alquilo C1-6 o cicloalquilo C3-8 y siendo Rh H o alquilo C1-6, o siendo Rh, junto con Rd, el átomo de oxígeno unido a Rh, y el átomo de nitrógeno unido a Rd, heterocicloalquilo C3-10; cada uno de R3 y R4, independientemente, es H, halo, nitro, ciano, amino, alquilo C1-6, alcoxilo C1-6, cicloalquilo C3-10, heterocicloalquilo C3-10, arilo o heteroarilo; m es 1, 2, 3 ó 4; y n es 1 ó 2.
Description
DESCRIPCIÓN
Compuestos de aminotiazol y uso de los mismos
Antecedentes
Las proteínas quinasas son importantes en las rutas de señalización celular que regulan diversas funciones celulares, incluidas la diferenciación, la proliferación, la migración y la apoptosis. La desregulación de las proteínas quinasas está implicada en el cáncer y en un número de otras enfermedades.
Los compuestos heterocíclicos se han estudiado ampliamente como potentes inhibidores de la proteína quinasa. Entre varias clases de compuestos heterocíclicos, los aminotiazoles aparecen como un motivo estructural recurrente en muchos compuestos biológicamente activos.
Como candidatos a fármacos, los aminotiazoles presentan varios desafíos. En primer lugar, por lo general carecen de una adecuada exposición in vivo para ejercer la eficacia deseable en estudios preclínicos o clínicos. Además, al ser inhibidores promiscuos de proteína quinasa, los aminotiazoles poseen poca selectividad de quinasa. Además, a menudo causan la muerte de animales en los estudios de toxicidad, lo que plantea problemas de seguridad.
La solicitud de patente de EE.UU. 2012/225880 describe ciertos compuestos de pirazol y compuestos de tiazol que pueden usarse para inhibir la actividad de FLT3, VEGFR y aurora quinasa.
Existe la necesidad de desarrollar nuevos aminotiazoles que inhiban eficazmente ciertas proteína quinasas, ejerzan suficiente eficacia in vivo en el tratamiento de enfermedades diana y demostrar perfiles de seguridad deseables.
Resumen
La presente invención se basa en descubrimientos inesperados de que ciertos compuestos de aminotiazol inhiben eficazmente múltiples proteína quinasas, ejercen una alta eficacia in vivo contra el cáncer, y muestran una gran seguridad.
La presente invención se define en las reivindicaciones adjuntas. Las realizaciones y los ejemplos que no caen dentro de estas reivindicaciones son solo para fines ilustrativos.
En un aspecto, esta invención se refiere a compuestos de aminotiazol de Fórmula (I):
en donde R1 es H; X es O o NRa, siendo Ra H o alquilo C1-6; Y es CRbRc o NRd, en donde cada uno de Rb y Rc, independientemente, es H, halo, alquilo C1-6, alcoxilo C1-6, o amino, y Rd es H o alquilo C1-6; o Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es heterocicloalquilo C3-10, o Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es heterocicloalquilo C3-10; R2 es -CH2CH2Re o NRfRg, en donde Re es H, halo, alquilo C1-6, u ORh, siendo cada uno de Rf y Rg, independientemente, alquilo C1-6 o cicloalquilo C3-8 y siendo Rh H o alquilo C1-6, o siendo Rh, junto con Rd, el átomo de oxígeno unido a Rh, y el átomo de nitrógeno unido a Rd, heterocicloalquilo C3-10; cada uno de R3 y R4, independientemente, es H, halo, nitro, ciano, amino, alquilo C1-6, alcoxilo C1-6, cicloalquilo C3-10, heterocicloalquilo C3-10, arilo o heteroarilo; m es 1,2, 3 ó 4; y n es 1 ó 2.
El término "alquilo" en el presente documento se refiere a un resto de hidrocarburo saturado, lineal o ramificado, tal como -CH3 o -C3H7 ramificado. El término "cicloalquilo" se refiere a un resto de hidrocarburo no aromático, monocíclico, bicíclico, tricíclico o tetracíclico, tal como ciclohexilo, ciclohexen-3-ilo o adamantilo. El término "alcoxilo" se refiere a un radical -O-alquilo. Los ejemplos de alcoxilo incluyen, pero no se limitan a, metoxi, etoxi, n-propoxi, isopropoxi, n-butoxi, iso-butoxi, sec-butoxi y terc-butoxi. El término "tioalquilo" se refiere a un radical -S-alquilo. Los ejemplos de tioalquilo incluyen, pero no se limitan a, metiltiol, etiltiol y benciltiol. El término "heterocicloalquilo" se refiere a un resto no aromático, monocíclico, bicíclico, tricíclico o tetracíclico que tiene uno o más heteroátomos en el anillo (p.ej., N, O o S). Los ejemplos de heterocicloalquilo incluyen, pero no se limitan a, 4-morfolinilo, 1 -piperazinilo, 4-tetrahidropiranilo y 4-piranilo. El término "arilo" se refiere a un resto de hidrocarburo que tiene uno o más anillos aromáticos. Los ejemplos de restos arilo incluyen fenilo (Ph), fenileno, naftilo, naftileno, pirenilo, antrilo y fenantrilo. El término "heteroarilo" se refiere a un resto que tiene uno o más anillos aromáticos que contienen al menos un heteroátomo (p.ej., N, O o S). Los ejemplos de restos heteroarilo incluyen furilo, furileno, fluorenilo, pirrolilo, tienilo, oxazolilo, imidazolilo, tiazolilo,
piridilo, pirimidinilo, quinazolinilo, quinolilo, isoquinolilo e indolilo.
Los alquilo, tioalquilo, alcoxilo, cicloalquilo, heterocicloalquilo, arilo y heteroarilo mencionados en el presente documento incluyen restos tanto sustituidos como no sustituidos, a menos que se especifique lo contrario. Los posibles sustituyentes en cicloalquilo, heterocicloalquilo, arilo y heteroarilo incluyen alquilo C1-10, alquenilo C2-10, alquinilo C2-10, cicloalquilo C3-20, cicloalquenilo C3-20, heterocicloalquilo C1-20, heterocicloalquenilo C1-20, alcoxi C1-10, arilo, ariloxi, heteroarilo, heteroariloxi, amino, alquilamino C1-10, dialquilamino C1-20, arilamino, diarilamino, hidroxilo, halógeno, tio, alquiltio C1-10, ariltio, alquilsulfonilo C1-10, arilsulfonilo, acilamino, aminoacilo, aminotioacilo, amidino, guanidina, ureido, ciano, nitro, acilo, tioacilo, aciloxi, carboxilo y éster carboxílico. Por otro lado, los posibles sustituyentes en el alquilo incluyen todos los sustituyentes mencionados anteriormente excepto alquilo C1-10, alquenilo C2-10 y alquinilo C2-10. El cicloalquilo, heterocicloalquilo, arilo y heteroarilo también se pueden fusionar entre sí.
Los compuestos de aminotiazol descritos anteriormente incluyen los propios compuestos, así como sus sales y solvatos, si procede. Se puede formar una sal, por ejemplo, entre un anión y un grupo cargado positivamente (por ejemplo, amino) en un compuesto de aminotiazol. Los aniones adecuados incluyen cloruro, bromuro, yoduro, sulfato, nitrato, fosfato, citrato, metanosulfonato, trifluoroacetato, acetato, malato, tosilato, tartrato, fumurato, glutamato, glucuronato, lactato, glutarato y maleato. Asimismo, también se puede formar una sal entre un catión y un grupo cargado negativamente (p.ej., carboxilato) en un compuesto de aminotiazol. Los cationes adecuados incluyen ion de sodio, ion de potasio, ion de magnesio, ion de calcio y un catión de amonio tal como ion de tetrametilamonio. Los compuestos de aminotiazol también incluyen aquellas sales que contienen átomos de nitrógeno cuaternario. Un solvato se refiere a un complejo formado entre un compuesto de aminotiazol activo y un disolvente farmacéuticamente aceptable. Los ejemplos de un disolvente farmacéuticamente aceptable incluyen agua, etanol, isopropanol, acetato de etilo, ácido acético y etanolamina.
Se describe adicionalmente un método para inhibir una proteína quinasa. El método incluye poner en contacto la proteína quinasa con una cantidad eficaz de uno o más de los compuestos de aminotiazol descritos anteriormente.
También se describe un método para tratar el cáncer asociado con una proteína quinasa. El método incluye administrar a un sujeto que lo necesite una cantidad eficaz de uno o más de los compuestos de aminotiazol de fórmula (I) descritos anteriormente.
La proteína quinasa puede ser de tipo salvaje o mutante. Los ejemplos de la proteína quinasa incluyen tirosina quinasa 3 similar a FMS (FLT3), tirosina quinasa 4 similar a FMS (FLT4), aurora quinasa (Au RK) A, AURK B, receptor del factor de crecimiento endotelial vascular (VEGFR), receptor del factor de crecimiento derivado de plaquetas (PDGFR) A, PDGFR B, c-Src (SRC), tirosina-proteína quinasa Lyn (LYN) A, LYN B, tirosina quinasa de reorganizado durante la transfección (RET), receptor del factor estimulante de colonias 1 (CSF1R), proteína tirosina quinasa específica de linfocitos (LCK), homólogo del oncogén viral del sarcoma felino de Gardner-Rasheed (v-fgr) (FGR), receptor de dominio de discoidina 1 (DDR1), receptor de dominio de inserción de quinasa (KDR), quinasa del receptor de tropomiosina (TRK) A, TRK B, quinasa de linfocitos B (BLK), tirosina-proteína quinasa Yes (YES1), homólogo 1 del oncogén viral de la leucemia murina de Abelson (ABL1), tirosina-proteína quinasa Kit (KIT), proteína quinasa 1 activada por mitógeno de doble especificidad (MEK1), quinasa 4 asociada al receptor de interleucina-1 (IRAK4), tirosinaproteína quinasa Tek (TEK), RET V804L, RET Y791 F, FLT3 D835Y, PDGFR AV 561 D y ABL1 T315I.
Los ejemplos del cáncer incluyen leucemia mieloide aguda, cloroma, leucemia mielógena crónica, leucemia linfoblástica aguda, leucemia linfocítica crónica, enfermedad de Hodgkin, linfoma no de Hodgkin, linfoma de células B, mieloma múltiple, macroglobulinemia de Waldenstrom, síndrome mielodisplásico, cáncer de páncreas, cáncer de vejiga, cáncer colorrectal, cáncer de mama, cáncer del tracto genital masculino, cáncer renal, cáncer hepatocelular, cáncer de pulmón, cáncer de ovario, cáncer de cuello uterino, cáncer de útero, enfermedad trofoblástica gestacional, cáncer gástrico, cáncer de las vías biliares, cáncer de vesícula biliar, cáncer de intestino delgado, cáncer de esófago, cáncer de orofaringe, cáncer de hipofaringe, cáncer de ojo, cáncer de nervio, cáncer de cabeza y cuello, melanoma, plasmocitoma, neoplasia de glándula endocrina, cáncer neuroendocrino, tumor cerebral, cáncer de hueso y sarcoma.
Además, dentro del alcance de esta invención se encuentra una composición farmacéutica que contiene uno o más de los compuestos de aminotiazol de fórmula (I) descritos anteriormente. La composición farmacéutica puede usarse para tratar el cáncer.
Por lo tanto, se describe el uso de uno o más de los compuestos de aminotiazol de fórmula (I) descritos anteriormente para la fabricación de un medicamento para tratar el cáncer.
El término "tratar" o "tratamiento" se refiere a la administración de uno o más de los compuestos de aminotiazol a un sujeto que tiene una enfermedad descrita anteriormente, es decir, cáncer, un síntoma de dicha enfermedad o una predisposición hacia dicha enfermedad, con el propósito de conferir un efecto terapéutico, p.ej., para curar, aliviar, alterar, afectar, mejorar o prevenir la enfermedad descrita anteriormente, el síntoma de la misma o la predisposición hacia ella. "Una cantidad eficaz" se refiere a la cantidad de un compuesto activo que se requiere para conferir el efecto terapéutico. Las dosis eficaces variarán, como reconocen los expertos en la técnica, dependiendo de los tipos de enfermedad tratada, la ruta de administración, el uso de excipientes y la posibilidad de uso conjunto con otro tratamiento terapéutico.
Según la invención, una composición que tiene uno o más de los compuestos de aminotiazol descritos anteriormente puede administrarse por vía parenteral, oral, nasal, rectal, tópica o bucal. El término "parenteral", como se usa en el presente documento, se refiere a inyección subcutánea, intracutánea, intravenosa, intraperitoneal, intramuscular, intraarticular, intraarterial, intrasinovial, intraesternal, intratecal, intralesional o intracraneal, así como a cualquier técnica de infusión adecuada.
Una composición inyectable estéril puede ser una solución o suspensión en un diluyente o disolvente no tóxico aceptable por vía parenteral, tal como una solución en 1,3-butanodiol. Entre los vehículos y disolventes aceptables que se pueden emplear están el manitol, el agua, la solución de Ringer y la solución isotónica de cloruro de sodio. Además, los aceites fijos se emplean convencionalmente como disolvente o medio de suspensión (p.ej., monoglicéridos o diglicéridos sintéticos). Los ácidos grasos, como el ácido oleico y sus derivados glicéridos, son útiles en la preparación de inyectables, al igual que los aceites naturales farmacéuticamente aceptables, como el aceite de oliva y el aceite de ricino, especialmente en sus versiones polioxietiladas. Estas soluciones o suspensiones de aceite también pueden contener un diluyente o dispersante de alcohol de cadena larga, carboximetilcelulosa o agentes dispersantes similares. Otros tensioactivos comúnmente usados tales como Tweens y Spans u otros agentes emulsionantes similares o potenciadores de la biodisponibilidad que se usan comúnmente en la fabricación de formas de dosificación sólidas, líquidas u otras farmacéuticamente aceptables también se pueden usar para el propósito de la formulación.
Una composición para administración oral puede ser cualquier forma de dosificación oralmente aceptable, incluidas cápsulas, comprimidos, emulsiones y suspensiones, dispersiones y disoluciones acuosas. En el caso de los comprimidos, los vehículos comúnmente utilizados incluyen lactosa y almidón de maíz. También se suelen añadir agentes lubricantes, como el estearato de magnesio. Para la administración oral en forma de cápsula, los diluyentes útiles incluyen lactosa y almidón de maíz seco. Cuando las suspensiones o emulsiones acuosas se administran por vía oral, el ingrediente activo puede suspenderse o disolverse en una fase oleosa combinada con agentes emulsionantes o de suspensión. Si se desea, se pueden añadir ciertos agentes edulcorantes, saborizantes o colorantes.
Una composición de inhalación o aerosol nasal se puede preparar según técnicas bien conocidas en la técnica de la formulación farmacéutica. Por ejemplo, dicha composición se puede preparar como una solución en solución salina, empleando alcohol bencílico u otros conservantes adecuados, promotores de absorción para mejorar la biodisponibilidad, fluorocarbonos y/u otros agentes solubilizantes o dispersantes conocidos en la técnica.
Una composición que tiene uno o más de los compuestos de aminotiazol descritos anteriormente también se puede administrar en forma de supositorios para administración rectal.
El vehículo en la composición farmacéutica debe ser "aceptable" en el sentido de que sea compatible con el ingrediente activo de la composición (y preferiblemente, capaz de estabilizar el ingrediente activo) y no perjudicial para el sujeto a tratar. Se pueden utilizar uno o más agentes solubilizantes como excipientes farmacéuticos para la administración de un compuesto activo de 1,5-difenil-penta-1,4-dien-3-ona. Los ejemplos de otros vehículos incluyen óxido de silicio coloidal, estearato de magnesio, celulosa, lauril sulfato de sodio y D&C Amarillo núm. 10.
Los detalles de una o más realizaciones de la invención se exponen en la descripción siguiente.
Descripción detallada
Se describen compuestos de aminotiazol de fórmula (I):
Con referencia a esta fórmula, los compuestos de aminotiazol de la invención son aquellos en los que R1 es H; X es O o NRa, siendo Ra H o alquilo C1-6; Y es CRbRc o NRd, en donde cada uno de Rb y Rc, independientemente, es H, halo, alquilo C1-6, alcoxilo C1-6, o amino, y Rd es H o alquilo C1-6; o Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es heterocicloalquilo C3-10, o Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es heterocicloalquilo C3-10; R2 es -CH2CH2Re o NRfRg, en el que Re es H, halo, alquilo C1-6, u ORh, siendo cada uno de Rf y Rg, independientemente, alquilo C1-6 o cicloalquilo C3-8 y siendo Rh H o alquilo C1-6, o siendo Rh, junto con Rd, el átomo de oxígeno unido a Rh, y el átomo de nitrógeno unido a Rd, heterocicloalquilo C3-10; cada uno de R3 y R4, independientemente, es H, halo, nitro, ciano, amino, alquilo C1-6, alcoxilo C1-6, cicloalquilo C3-10, heterocicloalquilo C3-10, arilo o heteroarilo; m es 1, 2, 3 ó 4; y n es 1 ó 2.
En una realización, los compuestos de aminotiazol descritos anteriormente son compuestos de fórmula (II):
en donde R1, R2, R3, R4, X e Y se definen como los descritos en la Fórmula (I) anterior.
En un subgrupo, los compuestos de Fórmula (II) tienen R1 como H y X como O. Preferiblemente, Y es NRd y R2 es -CH2CH2Re, en el que Re es ORh, siendo Rh, junto con Rd, el átomo de oxígeno unido a Rh, y el átomo de nitrógeno unido a Rd, heterocicloalquilo C3-10; R3 es H, halo o alquilo C1-6; y R4 es alquilo C1-6 o cicloalquilo C3-10. Un compuesto ejemplar es
En otro subgrupo, los compuestos de Fórmula (II) tienen R1 como H y X como NRa, siendo Ra H o alquilo C1-6. En particular, algunos compuestos en este subgrupo tienen Y como CRbRc, en donde Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es heterocicloalquilo C3-10 y Rc es H, halo, alquilo C1-6, alcoxilo C1-6 o amino; R2 como NRfRg, siendo cada uno de Rf y Rg, independientemente, alquilo C1-6 o cicloalquilo C3-8; R3 como H, halo, alquilo C1-6, o cicloalquilo C3-10; y R4 como alquilo C1-6 o cicloalquilo C3-10. Preferiblemente, Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es pirrolidinilo o piperidinilo. Otros compuestos en este subgrupo tienen Y como NRd, en donde Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es heterocicloalquilo C3-10; R2 como -CH2CH2Re, en donde Re es H, halo, alquilo C1-6, u ORh, siendo Rh H o alquilo C1-6; R3 como H, halo, alquilo C1-6, o cicloalquilo C3-10; y R4 como alquilo C1-6 o cicloalquilo C3-10. Preferiblemente, Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es piperazinilo. Los ejemplos de este grupo de compuestos incluyen
También dentro de esta invención hay una composición farmacéutica que contiene uno o más de los compuestos de aminotiazol de fórmula (I) para tratar el cáncer.
Se describe adicionalmente un método para tratar el cáncer, el método que incluye administrar a un sujeto que lo necesite una cantidad eficaz de un compuesto de Fórmula (I).
Las transformaciones químicas sintéticas y las metodologías de grupos protectores (protección y desprotección) utilizadas para sintetizar los compuestos de fórmula (I) son bien conocidas en la técnica. Véase, por ejemplo, R. Larock, Comprehensive Organic Transformations (2a ed., VCH Publishers 1999); P. G. M. Wuts y T. W. Greene, Greene’s Protective Groups in Organic Synthesis (4.a ed., John Wiley and Sons 2007); L. Fieser y M. Fieser, Fieser and Fieser's Reagents for Organic Synthesis (John Wiley and Sons 1994); L. Paquette, ed., Encyclopaedia of Reagents for Organic Synthesis (2.a ed., John Wiley and Sons 2009); y G. J. Yu et al., J. Med. Chem. 2008, 51,6044-6054.
Los compuestos de Fórmula (I) así preparados pueden seleccionarse inicialmente usando ensayos bioquímicos, p.ej., el ensayo de quinasa descrito en el Ejemplo 7 posterior, por su potencia para inhibir las proteínas quinasas. Se pueden evaluar posteriormente utilizando ensayos in vivo, p.ej., un ensayo de modelo animal de xenoinjerto, para determinar su actividad en la supresión del crecimiento tumoral en un mamífero. Los compuestos seleccionados pueden probarse adicionalmente para verificar su eficacia en el tratamiento del cáncer. Por ejemplo, se puede administrar un compuesto a un animal (p.ej., un ratón) que tiene cáncer y luego se evalúa su efecto terapéutico. En base a los resultados, se pueden investigar y determinar los rangos de dosificación y las rutas de administración apropiados.
Los siguientes ejemplos específicos deben interpretarse como meramente ilustrativos.
En los ejemplos siguientes se muestran las estructuras de los compuestos ejemplares de Fórmula (I) y cómo se prepararon. Los datos analíticos para los compuestos así preparados también se describen en los Ejemplos 1-6 y los procedimientos para ensayar estos compuestos se describen en los ejemplos que siguen.
Ejemplo de referencia 1: Síntesis del Compuesto 1
El compuesto 1 se preparó según los métodos sintéticos descritos en Chen et al., European Journal of Medicinal Chemistry, 2015, 100, 151-161.
Todos los productos químicos y solventes se compraron a proveedores comerciales y se usaron tal como se recibieron. Todas las reacciones se llevaron a cabo bajo una atmósfera de nitrógeno seco. Las reacciones se monitorizaron mediante TLC utilizando placas con respaldo de vidrio de gel de sílice Merck 60 F254 (5 x 10 cm); y las zonas se detectaron visualmente bajo irradiación ultravioleta (254 nm) o por pulverización con reactivo de ácido fosfomolíbdico (Aldrich) seguido de calentamiento a 80°C. La cromatografía en columna ultrarrápida se realizó con gel de sílice Merck Kieselgel 60, No. 9385, malla 230-400 ASTM como fase estacionaria. los espectros de resonancia magnética nuclear de protones (1H) se midieron en un espectrómetro Varian Mercury-300 o Varian Mercury-400. Los desplazamientos químicos se registraron en partes por millón (ppm) en la escala delta (5) en relación con la resonancia del pico del disolvente. Se usaron las siguientes abreviaturas para describir el acoplamiento: s = singlete; d = doblete; t = triplete; q = cuarteto; quin = quinteto; br = ancho; y m = multiplete. Los datos de LCMS se midieron en un sistema Agilent MSD-1100 ESI-MS/MS, Agilent 1200 series LC/MSD VL y Waters Acquity UPLC-ESI-MS/MS.
1 -(5-Etilisoxazol-3-il)-3-(4-(2-((6-(4-(2-hidroxietil)piperazin-1 -il)-2-metilpirimidin-4-il)amino)tiazol-5-il)fenil)urea (sal de HCl)
1H RMN (400 MHz, DMSO-d6): 5 10,87 (s, 1H), 9,79 (s, 1H), 9,74 (s, 1H), 7,75 (s, 1H), 7,51 (q, J = 8,8 Hz, 4H), 6,54 (s, 1H), 6,34 (s, 1H), 5,55 (br s, 1H), 4,37 (d, J = 4,0 Hz, 2H), 3,78 (t, J = 4,8 Hz, 2H), 3,61 (d, J = 12,0 Hz, 2H), 3,48 (t, J = 12,8 Hz, 2H), 3,19-3,12 (m, 4H), 2,69 (q, J = 8,0 Hz, 2H), 2,47 (s, 3H), 1,19 (t, J = 6,0 Hz, 3H); MS (ES+) m/z calc. para C26H31N9O3S: 549,23; encontrado: 550,3 (M+H+).
En cada uno de los Ejemplos 2-20 posteriores, el compuesto se sintetizó de la misma manera que se describe en el Ejemplo 1. Solo se muestran la estructura del compuesto y los datos analíticos.
Ejemplo 2
1 -(5-Etilisoxazol-3-il)-3-(4-(2-((6-(4-etilpiperazin-1 -il)pirimidin-4-il)amino)tiazol-5-il)fenil)urea (sal de HCl)
1H RMN (400 MHz, DMSO-d6): 5 11,14 (s, 1H), 9,78 (s, 1H), 9,62 (s, 1H), 8,48 (s, 1H), 7,74 (s, 1H), 7,50 (q, J = 8,8 Hz, 4H), 6,55 (s, 1H), 6,38 (s, 1H), 4,34 (d, J = 14,0 Hz, 2H), 3,55 (d, J = 11,6 Hz, 2H), 3,44-3,38 (m, 2H), 3,14-3,08 (m, 2H), 3,00 (q, J = 9,6 Hz, 2H), 2,69 (q, J = 7,6 Hz, 2H), 1,26 (t, J = 7,6 Hz, 3H), 1,19 (t, J = 7,6 Hz, 3H); MS (ES+) m/z calc. para C25H29N9O2S: 519,22; encontrado: 520,2 (M+H+).
Ejemplo 3
1 -(5-Etilisoxazol-3-il)-3-(4-(2-((6-(2-morfolinoetoxi)pirimidin-4-il)amino)tiazol-5-il)fenil)urea (sal de HCl)
1H RMN (400 MHz, DMSO-d6): 5 11,08 (s, 1H), 9,75 (s, 1H), 9,56 (s, 1H), 8,62 (s, 1H), 7,73 (s, 1H), 7,50 (q, J = 8,8 Hz, 4H), 6,54 (s, 1H), 6,50 (s, 1H), 4,71 (s, 2H), 3,95 (d, J = 11,6 Hz, 2H), 3,79 (t, J = 12,4 Hz, 2H), 3,56 (s, 2H), 3,47 (d, j = 12,4 Hz, 2H), 3,15 (d, J = 10,0 Hz, 2H), 2,69 (q, J = 7,6 Hz, 2H), 1,19 (t, J = 7,6 Hz, 3H); MS (ES+) m/z calc. para C25H28N8O4S: 536,20; encontrado: 537,2 (M+H+).
Ejemplo 4
1 -(5-Etilisoxazol-3-il)-3-(4-(2-((6-(4-(2-hidroxietil)piperazin-1 -il)pirimidin-4-il)amino)tiazol-5-il)fenil)urea (sal de HCl) 1
1H RMN (300 MHz, DMSO-d6): 510,69 (s, 1H), 9,75 (s, 1H), 9,57 (s, 1H), 8,48 (s, 1H), 7,73 (s, 1H), 7,52 (s, 4H), 6,56 (s, 1H), 6,39 (s, 1H), 5,27 (br s, 1H), 4,34 (d, J = 12,9 Hz, 2H), 3,80 (s, 2H), 3,62 (d, J = 11,4 Hz, 2H), 3,44 (t, J = 11,7 Hz, 2H), 3,22-312 (m, 4H), 2,71 (q, J = 7,2 Hz, 2H), 1,21 (t, J = 7,2 Hz, 3H); MS (ES+) m/z calc. para C25H29N9O3S: 535,21; encontrado: 536,2 (M+H+).
Ejemplo 5
1 -(5-Etilisoxazol-3-il)-3-(4-(2-((6-(4-(2-fluoroetil)piperazin-1 -il)pirimidin-4-il)amino)tiazol-5-il)fenil)urea (sal de HCl)
1H RMN (400 MHz, DMSO-d6): 5 11,56 (s, 1H), 9,78 (s, 1H), 9,62 (s, 1H), 8,48 (s, 1H), 7,74 (s, 1H), 7,52 (q, J = 8,8 Hz, 4H), 6,56 (s, 1H), 6,39 (s, 1H), 4,99 (t, J = 3,6 Hz, 1H), 4,88 (t, J = 3,6 Hz, 1H), 4,38 (d, J = 10,4 Hz, 2H), 3,59 (s, 2H), 3,44 (d, J = 12,0 Hz, 4H), 3,19 (s, 2H), 2,71 (q, J = 7,2 Hz, 2H), 1,21 (t, J = 7,6 Hz, 3H); MS (ES+) m/z calc. para C25H28FN9O2S: 537,21; encontrado: 538,2 (M+H+).
Ejemplo de referencia 6
1 -(5-Etilisoxazol-3-il)-3-(4-(2-((6-(4-(2-fluoroetil)piperazin-1 -il)-2-metilpirimidin-4-il)amino)tiazol-5-il)fenil)urea (sal de HCl)
1H RMN (300 MHz, DMSO-d6): 511,56 (s, 1H), 9,76 (s, 1H), 9,63 (s, 1H), 7,75 (s, 1H), 7,52 (t, J = 13,2 Hz, 4H), 6,55 (s, 1H), 6,30 (s, 1H), 5,01 (s, 1H), 4,85 (s, 1H), 4,39 (s, 2H), 3,75-3,30 (m, 6 H), 3,19 (s, 2H), 2,50 (s, 3H), 2,71 (q, J = 7,2 Hz, 2H), 1,21 (t, J = 7,5 Hz, 3H); MS (ES+) m/z calc. para C26H30FN9O2S: 551,22; encontrado: 552,2 (M+H+). Ejemplo 7: Inhibición de la Proteína Quinasa
Los datos de inhibición de la quinasa se obtuvieron de Servicio de Perfiles Bioquímicos de Quinasas SelectScreen®. Más específicamente, los compuestos de prueba se seleccionaron en 160 nL de una solución de DMSO al 1% en el pocillo de una placa de 384 pocillos; las mezclas de quinasa/anticuerpo (8 pL) se diluyeron a una concentración de trabajo de 2 veces en un tampón de quinasa apropiado (3,84 pL) y se preparó un trazador marcado con AlexaFluor® 4 veces (4 pL) en el tampón de quinasa; la incubación de las soluciones de prueba se realizó a temperatura ambiente durante 60 minutos; y se registró y analizó la lectura en un lector de placas de fluorescencia.
Tabla 1. Datos de inhibición de quinasa
* El número entre paréntesis indica un valor de IC50.
Se observó que ciertos compuestos de Fórmula (I), por ejemplo, Compuestos 2, y 3, inhibían inesperadamente múltiples proteínas quinasas con concentraciones inhibitorias máximas medias o valores IC50 inferiores a 100 nM.
Los resultados indican que los compuestos de fórmula (I) ejercen una gran actividad en la inhibición de múltiples proteínas quinasas.
Ejemplo 8: Actividad celular in vitro
AC220 es un inhibidor de FLT3 de molécula pequeña en ensayos clínicos, que ejerce una alta potencia contra el mutante de duplicación en tándem interno de FLT3 (FLT3-ITD). Las mutaciones clínicamente relevantes que confieren resistencia a AC220 se han restringido a residuos en el dominio de la quinasa FLT3, por ejemplo, ITD-D835Y, ITD-D835V, ITD-D835F, ITD-F691L e ITD-F691I.
Se realizó un estudio para evaluar la potencia de los compuestos de Fórmula (I) en la inhibición del crecimiento de líneas celulares que contenían estos mutantes, en comparación con el compuesto AC220, como sigue.
Las cinco líneas celulares 32D leucémicas se adquirieron de la Colección americana de cultivos tipo (ATCC, Manassas, VA, EE.UU.). Las líneas celulares 32D de pro-linfocitos B murinos se transfectaron de forma estable con vectores de expresión que codificaban FLT3 humano que contenía una mutación ITD (células 32D-ITD), mutaciones ITD y D835Y (células 32D-ITD/D835Y), ITD y D835V (células 32D-ITD/D835V), ITD y D835F (células 32D-ITD/D835F) e ITD y F691L (células 32D-ITD/F691L), que conducen a la activación constitutiva de las proteínas de señalización corriente abajo de FLT3. La viabilidad celular se evaluó con el ensayo MTS descrito en PLoS One, 2014, 9, e97116. Se sembraron células 32D-ITD/D835Y, 32D-ITD/D835V, 32D-ITD/D835F, 32D-ITD/F691L y 32D-ITD/F6911 en placas de 96 pocillos a 1 x 104 células/ml (100 pl por pocillo) para incubación de 24 h. Los compuestos de prueba (en varias concentraciones en dimetilsulfóxido (DMSO) se agregaron posteriormente al medio de cultivo para una incubación de 72 h. La viabilidad celular se determinó mediante el ensayo MTS (Promega, Madison, WI, EE.UU.).
Los resultados que se muestran en la Tabla 2 a continuación se obtuvieron del estudio de compuestos de prueba para inhibir el crecimiento de líneas celulares que contienen mutantes ITD.
Tabla 2. Actividad de compuestos frente a células 32D que expresan mutantes de FLT3-ITD resistentes a AC220
Se observó que los compuestos 1,2, y 4 todos exhibieron inesperadamente efectos inhibidores del crecimiento celular mucho mayores que los ejercidos por AC220 contra todos los mutantes ITD-D835Y, ITD-D835V, ITD-D835F, ITD-F691L e ITD-F691I. Más específicamente, todos los compuestos 1, 2, y 4 ejercieron inesperadamente altos efectos inhibidores del crecimiento celular con valores de GI50 inferiores a 6 nM contra mutantes ITD-D835Y, ITD-D835V e ITD-D835F, en comparación con los valores de GI50 de 19-103 nM ejercidos por AC220; y el compuesto 4 ejerció inesperadamente altos efectos inhibidores del crecimiento celular con valores de GI50 inferiores a 20 nM contra mutantes ITD-F691L e ITD-F6911, en comparación con los valores de GI50 superiores a 100 nM ejercidos por AC220.
Los datos comparativos indican que los compuestos de Fórmula (I) ejercen inesperadamente una alta potencia celular y superan a un compuesto clínico en la inhibición de ciertos mutantes de proteína quinasa.
Ejemplo 9: Biodisponibilidad Oral (% de F) de compuestos de Fórmula (I)
Se realizó un estudio para evaluar las exposiciones in vivo de compuestos de fórmula (I) cuando se administran oralmente como sigue.
Se obtuvieron ratones macho ICR que pesaban 25-35 g cada uno de BioLASCO (Taiwan Co., Ltd, Ilan, Taiwán). Los estudios en animales se realizaron de acuerdo con los procedimientos institucionales de cuidado de animales y aprobados por el comité de los Institutos Nacionales de Investigación en Salud (NHRI, por sus siglas en inglés). Una dosis única de 2,0 mg/kg de cada uno de los compuestos 2, 3, 5, y 6 se administró por vía intravenosa (IV) a un total de 33 ratones macho. Se administró una dosis única de 10 mg/kg de cada uno de estos cuatro compuestos por vía oral (PO) a un total de 27 ratones macho. Cada ratón recibió 100 mL de la solución de dosificación IV por inyección intravenosa en la vena de la cola y 200 mL de la solución de dosificación PO por sonda oral. Los animales que recibieron la dosis IV no estuvieron en ayunas y los que recibieron la dosis PO estuvieron en ayunas durante la noche antes de la dosificación. A los 0 (inmediatamente antes de la dosificación), 2 (solo IV), 5 (solo IV), 15 y 30 min y a las 1, 2, 4, 6, 8, 16 y 24 h después de la dosificación, se extrajo sangre (-500 ml) de grupos de 3 ratones en cada punto de tiempo por punción cardiovascular y se almacenó en hielo (0-4°C). Como anticoagulante se utilizó ácido etilendiaminotetraacético (EDTA). El plasma se separó de la sangre por centrifugación (3000 rpm durante 15 minutos a 4°C en una centrífuga Beckman Modelo Allegra 6R) y se almacenó en un congelador (-20°C). Se obtuvo plasma de control de ratones que no recibieron compuesto para usar en la construcción de la curva estándar y para la preparación de muestras de control de calidad (QC). Todas las muestras se analizaron para el compuesto original por LC-MS/MS.
La biodisponibilidad oral, presentada como porcentaje (% de F), se calculó dividiendo el valor promedio del área bajo la curva (AUC) de un compuesto después de la dosificación PO por el valor promedio del AUC del compuesto después de la dosificación IV luego de la normalización de la dosis. Los valores de AUC y % de F se muestran en la Tabla 3 posterior.
Tabla 3. Perfiles farmacocinéticos de compuestos de fórmula (I) en ratones
Se observó que los cuatro Compuestos, es decir, 2, 3, 5, y 6, inesperadamente ejercieron altas exposiciones como se indica por los valores IV AUC y PO AUC. También, los compuestos 2, 3, 5, y 6 exhibieron inesperadamente una alta biodisponibilidad oral con valores de % de F de 38, 96, 67 y 89, respectivamente.
Los resultados descritos en la Tabla 3 anterior indican que los compuestos de Fórmula (I) exhiben inesperadamente una alta exposición in vivo cuando se administran por vía oral.
Ejemplo 10: Eficacia en modelos de ratones con xenoinjerto
Se realizó un estudio para evaluar la eficacia in vivo de los compuestos de fórmula (I), es decir, inhibición del crecimiento tumoral (TGI), como sigue.
Se adquirieron ratones desnudos machos (Nu-fox1nu) de 8 semanas de edad de BioLASCO (Taipei, Taiwán, R.O.C.). Se inocularon células tumorales Colo205 humanas colorrectales, pancreáticas Mia-PaCa 2 o células de leucemia MOLM-13, 32D-ITD/D835Y por vía subcutánea a 1 x 106 células cada uno en los ratones desnudos. Todas las células cancerosas humanas se detectaron como libres de Micoplasma spp antes de que fueran inyectados en animales. Las células tumorales crecen como tumores de xenoinjerto y el tamaño del tumor alcanzó aproximadamente 200~250 mm3 en los ratones desnudos listos para los tratamientos de dosis. Los compuestos de prueba se disolvieron en 2-hidroxipropil-p-ciclodextrina al 20% individualmente para administraciones por sonda oral a los ratones desnudos. Los
ratones portadores de tumores se trataron con compuestos de prueba en varias dosis, 5 veces a la semana durante 2 semanas. Los tamaños de los tumores se midieron con un calibrador electrónico y se calcularon con la fórmula: tamaño del tumor = largo x ancho2/2. El tamaño del tumor y el peso corporal del animal se midieron dos veces por semana antes y después de la inoculación de células tumorales durante todo el período de observación. Los usos de animales y los procedimientos experimentales de los mismos fueron aprobados por el Comité Institucional de Cuidado y Uso de Animales (IACUC) de los Institutos Nacionales de Investigación en Salud.
Tabla 4. Eficacia in vivo de compuestos de fórmula (I) frente a xenoinjertos del modelo colo205 en ratones desnudos
Como se muestra en la Tabla 4 anterior, en el modelo de xenoinjerto colo205 en ratones desnudos, todos los compuestos de prueba, es decir, los compuestos 1 (PO; 50 mg/kg), 2 (PO; 50 mg/kg), 3 (PO; 100 mg/kg), 4 (PO; 150 mg/kg), y 6 (PO; 25 mg/kg), ejercieron inesperadamente un TGI elevado con un valor del 80% en el día 18.
Tabla 5. Eficacia antitumoral in vivo de los compuestos de fórmula (I) frente al xenoinjerto modelo tumoral Mia-paca2
Como se muestra en la Tabla 5 anterior, en el modelo de tumor de xenoinjerto Mia-paca2, ambos compuestos 5 y 6, administrados por vía oral a 25 mg/kg, inesperadamente ejercieron un TGI alto con valores respectivos de 65% y 68% en el día 18.
Tabla 6. Eficacia in vivo de los compuestos de fórmula (I) frente a xenoinjertos del modelo MOLM-13 en ratones desnudos
•Tamaño inicial del tumor ~250 mm3. En el día 18, el tamaño del tumor de control llegó a >2000 mm3 y los ratones fueron sacrificados.
Como se muestra en la Tabla 6 anterior, en el modelo de xenoinjerto MOLM-13 en ratones desnudos, ambos compuestos 2 (PO; 25 y 50 mg/kg) y 4 (PO; 150 mg/kg) inesperadamente ejercieron un TGI y regresión del tumor altos en el día 25.
Tabla 7. Eficacia in vivo de compuestos de fórmula (I) frente a xenoinjertos del modelo FLT3-ITD-D835Y en ratones desnudos
Como se muestra en la Tabla 7 anterior, en el modelo de xenoinjerto FLT3-ITD-D835Y en ratones desnudos, ambos compuestos 2 (PO; 25 mg/kg) y 5 (PO; 25 mg/kg) ejercieron inesperadamente una alta regresión tumoral con un valor de > 20% en el día 12.
Estos resultados indican que los compuestos de Fórmula (I), cuando se administran por vía oral, ejercen inesperadamente una alta eficacia antitumoral en modelos animales de xenoinjerto.
Ejemplo 11: Estudios de toxicidad en ratones
Se realizó un estudio para evaluar la toxicidad in vivo de los compuestos de fórmula (I) como sigue.
Los compuestos de fórmula (I) se ensayaron en animales para determinar su eficacia in vivo siguiendo el procedimiento descrito en el ejemplo 10. Se administró por vía oral a ratones desnudos nu/nu atímicos de nueve semanas de edad una dosis diaria de 25, 50, 100 o 150 mg/kg los días 1 -5 y 8-12. Se observaron los signos clínicos de los ratones y se les midió el peso corporal durante el período de observación de 14 días posterior al tratamiento.
Tabla 8. Estudio de toxicidad in vivo de compuestos de Fórmula (I) en xenoinjertos colo205 de ratones desnudos
Como se muestra en la Tabla 8 anterior, los xenoinjertos colo205 en ratones desnudos se toleraron bien. Los compuestos 1, 2, 3, 4, y 6, que se administraron por vía oral (50, 50, 100, 150 y 25 mg/kg) una vez al día. No se observó mortalidad durante el estudio.
Tabla 9. Estudio de toxicidad in vivo de compuestos de fórmula (I) en xenoinjertos de ratones desnudos Mia-paca2
Como se muestra en la Tabla 9 anterior, los xenoinjertos de ratones desnudos Mia-paca2 se toleraron bien. Los compuestos 5 y 6, que se administraron por vía oral (25 mg/kg) una vez al día. Nuevamente, no se observó mortalidad durante este estudio.
Tabla 10. Estudio de toxicidad in vivo de compuestos de fórmula (I) en xenoinjertos de ratones desnudos MOLM-13
Como se muestra en la Tabla 10 anterior, los xenoinjertos MOLM-13 en ratones desnudos se toleraron bien. Los compuestos 2 y 4, que se administraron por vía oral (25 y 50, 50 o 150 mg/kg) una vez al día. Tampoco se observó mortalidad durante este estudio.
Tabla 11. Estudio de toxicidad in vivo de compuestos de Fórmula (I) en xenoinjertos FLT3-ITD-D835Y de ratones desnudos
Como se muestra en la Tabla 11 anterior, los xenoinjertos FLT3-ITD-D835Y en ratones desnudos se toleraron bien. Los compuestos 2 y 5, que se administraron por vía oral (25 mg/kg) una vez al día. No se observó mortalidad durante este estudio.
Estos resultados descritos anteriormente demuestran que los compuestos de Fórmula (I) exhiben inesperadamente perfiles de seguridad deseables.
Claims (13)
1. Un compuesto de fórmula (I):
en donde
R1 es H;
X es O o NRa, siendo Ra H o alquilo C1-6;
Y es CRbRc o NRd, en el que cada uno de Rb y Rc, independientemente, es H, halo, alquilo C1-6, alcoxilo C1-6, o amino, y Rd es H o alquilo C1-6; o Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es heterocicloalquilo C3-10, o Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es heterocicloalquilo C3-10;
R2 es -CH2CH2Re o NRfRg, en el que Re es H, halo, alquilo C1-6, u ORh, siendo cada uno de Rf y Rg, independientemente, alquilo C1-6 o cicloalquilo C3-8 y siendo Rh H o alquilo C1-6, o siendo Rh, junto con Rd, el átomo de oxígeno unido a Rh, y el átomo de nitrógeno unido a Rd, heterocicloalquilo C3-10;
cada uno de R3 y R4, independientemente, es H, halo, nitro, ciano, amino, alquilo C1-6, alcoxilo C1-6, cicloalquilo C3-10, heterocicloalquilo C3-10, arilo o heteroarilo;
m es 1, 2, 3 ó 4; y
n es 1 ó 2.
3. El compuesto según la reivindicación 2, en donde Y es NRd y R2 es -CH2CH2Re, en donde Re es ORh, siendo Rh, junto con Rd, el átomo de oxígeno unido a Rh, y el átomo de nitrógeno unido a Rd, heterocicloalquilo C3-10; R3 es H, halo o alquilo C1-6; y R4 es alquilo C1-6 o cicloalquilo C3-10.
6. El compuesto según la reivindicación 5, en donde
Y es CRbRc, en el que Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es heterocicloalquilo C3-10 y Rc es H, halo, alquilo C1-6, alcoxilo C1-6 o amino;
R2 es NRfRg, siendo cada uno de Rf y Rg, independientemente, alquilo C1-6 o cicloalquilo C3-8;
R3 es H, halo, alquilo C1-6, o cicloalquilo C3-10; y
R4 es alquilo C1-6 o cicloalquilo C3-10.
7. El compuesto según la reivindicación 6, en donde Rb, junto con Ra, el átomo de carbono unido a Rb, y el átomo de nitrógeno unido a Ra, es pirrolidinilo o piperidinilo.
8. El compuesto según la reivindicación 5, en donde
Y es NRd, en donde Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es heterocicloalquilo C3-10; R2 es -CH2CH2Re, en el que Re es H, halo, alquilo C1-6, u ORh, siendo Rh H o alquilo C1-6;
R3 es H, halo, alquilo C1-6, o cicloalquilo C3-10; y
R4 es alquilo C1-6 o cicloalquilo C3-10.
9. El compuesto según la reivindicación 8, en donde Rd, junto con Ra y los átomos de nitrógeno unidos a Rd y Ra, es piperazinilo.
11. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable y un compuesto como se define en cualquiera de las reivindicaciones 1 a 10.
12. Un compuesto como se define según cualquiera de las reivindicaciones 1 a 10, para usar en el tratamiento de un
cáncer asociado con una proteína quinasa.
13. El compuesto para el uso según la reivindicación 12, en donde el cáncer es leucemia mieloide aguda, cloroma, leucemia mielógena crónica, leucemia linfoblástica aguda, leucemia linfocítica crónica, enfermedad de Hodgkin, linfoma no de Hodgkin, linfoma de células B, mieloma múltiple, macroglobulinemia de Waldenstrom, síndrome mielodisplásico, cáncer de páncreas, cáncer de vejiga, cáncer colorrectal, cáncer de mama, cáncer del tracto genital masculino, cáncer renal, cáncer hepatocelular, cáncer de pulmón, cáncer de ovario, cáncer de cuello uterino, cáncer de útero, enfermedad trofoblástica gestacional, cáncer gástrico, cáncer de las vías biliares, cáncer de la vesícula biliar, cáncer del intestino delgado, cáncer de esófago, cáncer de orofaringe, cáncer de hipofaringe, cáncer de ojo, cáncer de nervio, cáncer de cabeza y cuello, melanoma, plasmocitoma, neoplasia de glándula endocrina, cáncer neuroendocrino, tumor cerebral, cáncer de hueso o sarcoma.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662291667P | 2016-02-05 | 2016-02-05 | |
| PCT/US2017/015765 WO2017136315A1 (en) | 2016-02-05 | 2017-01-31 | Aminothiazole compounds and use thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2909612T3 true ES2909612T3 (es) | 2022-05-09 |
Family
ID=59496120
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17747997T Active ES2909612T3 (es) | 2016-02-05 | 2017-01-31 | Compuestos de aminotiazol y uso de los mismos |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US10047078B2 (es) |
| EP (1) | EP3411035B1 (es) |
| JP (1) | JP6883049B2 (es) |
| KR (1) | KR102449712B1 (es) |
| CN (1) | CN109069504B (es) |
| ES (1) | ES2909612T3 (es) |
| TW (1) | TWI620748B (es) |
| WO (1) | WO2017136315A1 (es) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR112012029405B1 (pt) | 2010-05-20 | 2021-01-05 | Array Biopharma Inc. | compostos macrocíclicos como inibidores de trk quinase, composição farmacêutica, uso de um composto de fórmula i ou um sal farmaceuticamente aceitável do mesmo, processo para a preparação de um composto |
| EP3322706B1 (en) | 2015-07-16 | 2020-11-11 | Array Biopharma, Inc. | Substituted pyrazolo[1,5-a]pyridine compounds as ret kinase inhibitors |
| JOP20190077A1 (ar) | 2016-10-10 | 2019-04-09 | Array Biopharma Inc | مركبات بيرازولو [1، 5-a]بيريدين بها استبدال كمثبطات كيناز ret |
| TWI704148B (zh) | 2016-10-10 | 2020-09-11 | 美商亞雷生物製藥股份有限公司 | 作為ret激酶抑制劑之經取代吡唑并[1,5-a]吡啶化合物 |
| WO2018136663A1 (en) | 2017-01-18 | 2018-07-26 | Array Biopharma, Inc. | Ret inhibitors |
| CN110267960B (zh) | 2017-01-18 | 2022-04-26 | 阿雷生物药品公司 | 作为RET激酶抑制剂的取代的吡唑并[1,5-a]吡嗪化合物 |
| JOP20190213A1 (ar) | 2017-03-16 | 2019-09-16 | Array Biopharma Inc | مركبات حلقية ضخمة كمثبطات لكيناز ros1 |
| TWI876442B (zh) | 2017-10-10 | 2025-03-11 | 美商絡速藥業公司 | 6-(2-羥基-2-甲基丙氧基)-4-(6-(6-((6-甲氧基吡啶-3-基)甲基)-3,6-二氮雜雙環[3.1.1]庚-3-基)吡啶-3-基)吡唑并[1,5-a]吡啶-3-甲腈之調配物 |
| TWI791053B (zh) | 2017-10-10 | 2023-02-01 | 美商亞雷生物製藥股份有限公司 | 6-(2-羥基-2-甲基丙氧基)-4-(6-(6-((6-甲氧基吡啶-3-基)甲基)-3,6-二氮雜雙環[3.1.1]庚-3-基)吡啶-3-基)吡唑并[1,5-a]吡啶-3-甲腈之結晶形式及其醫藥組合物 |
| CA3087578C (en) | 2018-01-18 | 2023-08-08 | Array Biopharma Inc. | Substituted pyrazolo[3,4-d]pyrimidine compounds as ret kinase inhibitors |
| CA3087354C (en) | 2018-01-18 | 2023-01-03 | Array Biopharma Inc. | Substituted pyrrolo[2,3-d]pyrimidines compounds as ret kinase inhibitors |
| CA3087972C (en) | 2018-01-18 | 2023-01-10 | Array Biopharma Inc. | Substituted pyrazolyl[4,3-c]pyridinecompounds as ret kinase inhibitors |
| CN112469414A (zh) | 2018-05-25 | 2021-03-09 | 昂科库博疗法有限责任公司 | 作为新型候选抗癌药物的高效力tacc3抑制剂 |
| ES2922314T3 (es) | 2018-09-10 | 2022-09-13 | Array Biopharma Inc | Compuestos heterocíclicos condensados como inhibidores de cinasa RET |
| CN117460724A (zh) * | 2021-04-12 | 2024-01-26 | A2A制药有限公司 | 用于治疗癌症的组合物和方法 |
| IL315800A (en) | 2022-03-24 | 2024-11-01 | A2A Pharmaceuticals Inc | Preparations and methods for the treatment of cancer |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1169038B9 (en) * | 1999-04-15 | 2013-07-10 | Bristol-Myers Squibb Company | Cyclic protein tyrosine kinase inhibitors |
| PT1347971E (pt) * | 2000-12-21 | 2006-06-30 | Bristol Myers Squibb Co | Inibidores tiazolilicos de tirosina-cinases da familia tec |
| WO2004041164A2 (en) * | 2002-10-30 | 2004-05-21 | Merck & Co., Inc. | Kinase inhibitors |
| US20090105250A1 (en) * | 2005-01-26 | 2009-04-23 | Irm Llc | Compounds and compositions as protein kinase inhibitors |
| EA019289B1 (ru) | 2008-04-21 | 2014-02-28 | Тайджен Байотекнолоджи Ко., Лтд. | Производные аминопиридина, аминопиримидина и амино-1,3,5-триазина |
| WO2010046780A2 (en) | 2008-10-22 | 2010-04-29 | Institut Pasteur Korea | Anti viral compounds |
| MX346042B (es) | 2010-08-10 | 2017-03-03 | Astellas Pharma Inc | Compuesto heterociclico. |
| US9255072B2 (en) * | 2011-03-04 | 2016-02-09 | National Health Rsearch Institutes | Pyrazole compounds and thiazole compounds as protein kinases inhibitors |
| PH12014500682A1 (en) | 2011-09-27 | 2014-05-12 | Novartis Ag | 3-pyrimidin-4-yl-oxazolidin-2-ones as inhibitors of mutant idh |
| WO2013143466A1 (zh) * | 2012-03-27 | 2013-10-03 | 广东东阳光药业有限公司 | 作为欧若拉激酶抑制剂的取代嘧啶衍生物 |
-
2017
- 2017-01-26 TW TW106103165A patent/TWI620748B/zh active
- 2017-01-30 US US15/419,183 patent/US10047078B2/en active Active
- 2017-01-31 EP EP17747997.9A patent/EP3411035B1/en active Active
- 2017-01-31 ES ES17747997T patent/ES2909612T3/es active Active
- 2017-01-31 CN CN201780010118.4A patent/CN109069504B/zh active Active
- 2017-01-31 KR KR1020187024997A patent/KR102449712B1/ko active Active
- 2017-01-31 WO PCT/US2017/015765 patent/WO2017136315A1/en not_active Ceased
- 2017-01-31 JP JP2018560435A patent/JP6883049B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2017136315A1 (en) | 2017-08-10 |
| CN109069504A (zh) | 2018-12-21 |
| TW201728583A (zh) | 2017-08-16 |
| KR102449712B1 (ko) | 2022-09-30 |
| KR20180132618A (ko) | 2018-12-12 |
| US20170226100A1 (en) | 2017-08-10 |
| EP3411035A4 (en) | 2019-08-14 |
| CN109069504B (zh) | 2022-06-28 |
| EP3411035B1 (en) | 2022-03-02 |
| JP6883049B2 (ja) | 2021-06-02 |
| US10047078B2 (en) | 2018-08-14 |
| TWI620748B (zh) | 2018-04-11 |
| EP3411035A1 (en) | 2018-12-12 |
| HK1258689A1 (zh) | 2019-11-15 |
| JP2019511564A (ja) | 2019-04-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2909612T3 (es) | Compuestos de aminotiazol y uso de los mismos | |
| ES2981592T3 (es) | Derivados de 6-(4-amino-3-metil-2-oxa-8-azaespiro[4.5]decan-8-il)-3-(2,3-diclorofenil)-2-metilpirimidin-4(3H)-ona y compuestos relacionados como inhibidores de PTPN11 (SHP2) para tratar el cáncer | |
| JP7058345B2 (ja) | Bcl-2阻害剤及びMDM2阻害剤の組合せ製品並びに疾患の予防及び/又治療におけるその使用 | |
| ES2732026T3 (es) | Sal de adición de ácido de un compuesto inhibidor de Trk | |
| KR20180017013A (ko) | K-Ras 조절제 | |
| BRPI0616202A2 (pt) | formas de dosagem e uso de um inibidor da tirosina quinase | |
| ES2949616T3 (es) | Compuestos de aminotiazol como inhibidores de proteína cinasa | |
| TW202019409A (zh) | Bcl-2抑制劑與利妥昔單抗和/或苯達莫司汀或bcl-2抑制劑與chop聯合用藥的協同抗腫瘤作用 | |
| WO2014204856A1 (en) | Fatty acid anticancer derivatives and their uses | |
| AU2006236812A1 (en) | Combinations, methods and compositions for treating cancer | |
| BRPI0613644A2 (pt) | moduladores de tieno pirimidina e tieno pirimidina cinase | |
| ES2685974T3 (es) | Derivados de cefalosporina para tratar el cáncer | |
| CN113543784A (zh) | 用于治疗或预防癌症的喹啉衍生物 | |
| AU2017295858A1 (en) | Treatment of cancer | |
| US20220048863A1 (en) | Dna2 inhibitors for cancer treatment | |
| HK1258689B (en) | Aminothiazole compounds and use thereof | |
| JP2024526918A (ja) | 癌の処置におけるbakアクティベーター、医薬組成物および使用 | |
| KR20240128955A (ko) | 암 치료제로서의 강력하고 선택적인 smarca2 분해 키메라 분자 | |
| EA045568B1 (ru) | Солевые и кристаллические формы 4-амино-5-(6-(4-метилпиперазин-1-ил)-1н-бензо[d]имидазол-2-ил)тиено[2,3-в]пиридин-6(7н)-она | |
| BR112019026577B1 (pt) | Compostos aminotiazol, composição farmacêutica e uso como inibidores de proteína quinase e no tratamento de câncer | |
| HK1233924B (en) | Derivatives of cephalosporin for treating cancer | |
| HK1233924A1 (en) | Derivatives of cephalosporin for treating cancer |