BRPI0314325B1 - Derivados de aza-bicicloalquila, seu uso, seu processo de preparação e composição farmacêutica que os compreende - Google Patents
Derivados de aza-bicicloalquila, seu uso, seu processo de preparação e composição farmacêutica que os compreende Download PDFInfo
- Publication number
- BRPI0314325B1 BRPI0314325B1 BRPI0314325-2A BR0314325A BRPI0314325B1 BR PI0314325 B1 BRPI0314325 B1 BR PI0314325B1 BR 0314325 A BR0314325 A BR 0314325A BR PI0314325 B1 BRPI0314325 B1 BR PI0314325B1
- Authority
- BR
- Brazil
- Prior art keywords
- aza
- phenyl
- octane
- yloxy
- pyridin
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/439—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom the ring forming part of a bridged ring system, e.g. quinuclidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/444—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring heteroatom, e.g. amrinone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/04—Drugs for disorders of the muscular or neuromuscular system for myasthenia gravis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/30—Drugs for disorders of the nervous system for treating abuse or dependence
- A61P25/34—Tobacco-abuse
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
- A61P33/06—Antimalarials
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D453/00—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids
- C07D453/02—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids containing not further condensed quinuclidine ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/08—Bridged systems
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Neurosurgery (AREA)
- Epidemiology (AREA)
- Pain & Pain Management (AREA)
- Psychiatry (AREA)
- Tropical Medicine & Parasitology (AREA)
- Psychology (AREA)
- Physical Education & Sports Medicine (AREA)
- Virology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Addiction (AREA)
- Vascular Medicine (AREA)
- Hospice & Palliative Care (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- AIDS & HIV (AREA)
- Oncology (AREA)
- Rheumatology (AREA)
- Anesthesiology (AREA)
- Urology & Nephrology (AREA)
- Communicable Diseases (AREA)
- Molecular Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
"éteres aza-bicicloalquílicos e seu uso como agonistas de alfa7-nachr". a presente invenção refere-se a derivados de 1-azabicicloalquila de fórmula i, em que x é ch~ 2~ ou uma ligação simples; y é um grupo de fórmula e em que r tem os significados como definido no relatório descritivo cujos compostos são agonistas de receptores de acetilcolina alfa 7 nicotínicos (nachr); a processos para sua produção, seu uso como produtos farmacêuticos e a composições farmacêuticas compreendendo os mesmos.
Description
(54) Título: DERIVADOS DE AZA-BICICLOALQUILA, SEU USO, SEU PROCESSO DE PREPARAÇÃO E COMPOSIÇÃO FARMACÊUTICA QUE OS COMPREENDE (51) Int.CI.: C07D 453/02; A61K 31/439; A61P 25/28; C07D 487/08 (30) Prioridade Unionista: 04/09/2002 GB 02 20581.3 (73) Titular(es): NOVARTIS AG (72) Inventor(es): DOMINIK FEUERBACH; KONSTANZE HURTH; TIMOTHY JOHN RITCHIE
Relatório Descritivo da Patente de Invenção para DERIVADOS DE AZA-BICICLOALQUILA, SEU USO, SEU PROCESSO DE PREPARAÇÃO E COMPOSIÇÃO FARMACÊUTICA QUE OS COMPREENDE.
A presente invenção refere-se a novos derivados de 1-azabicicloalquíla, a processos para sua produção, seu uso como produtos farmacêuticos e a composições farmacêuticas compreendendo os mesmos.
Mais particularmente, a presente invenção proporciona, em um primeiro aspecto, um composto de fórmula I
em que
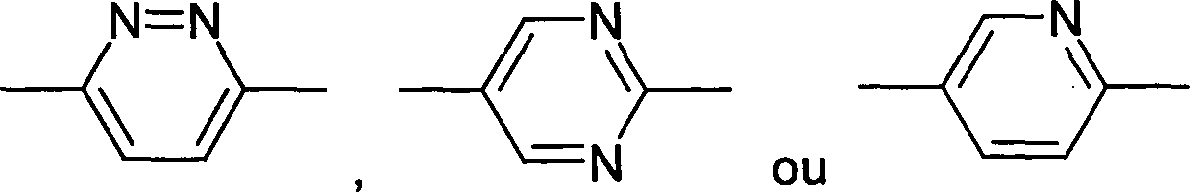
X é CH2 ou uma ligação simples Y é um grupo de fórmula
N=N
R é uma C5-C10 arila substituída ou não substituída ou hetero-CsC10 arila substituída ou não substituída, N(R1)(R4), ou N(R2)(CKR3R4);
cada um de R1, R2 e R3é de modo independente H, C1-C4 alquila, ou CF3;
R4 é uma C5-C-10 arila substituída ou não substituída ou heteroC5-C-10 arila substituída ou não substituída;
em forma de sal de adição ácido ou base livre.
C5-C10 arila e hetero-C5-C10 arila conforme usados neste relatório significam especialmente resíduos parciaimente ou totalmente insaturados, por exemplo, aromáticos, opcionalmente substituídos por um ou mais substituintes, preferencialmente até três substituintes, selecionados entre halogênio, por exemplo, F, Cl, Br, I; CN; C1-C4 alquila, tal como metila, etila ou propila, C2-C4 alquenila, tal como vinila, C2-C4 alquinila, cujos radicais podem ser eles mesmos não substituídos ou substituídos por halogênio, por exemplo, difluorometila ou trifluorometila; C1-C4 alcóxi, cujo radical pode ser ele mesmo não substituído ou substituído por halogênio, por exemplo, trifluorometóxi; formila, acetila; C-1-C3 alcoxicarbonila; N,N-di-(Ci-C3 alquila) carbamoíla; fenila, fenóxi; ou cujos substituintes podem ser condensados, por exemplo, para um benzo[1,3]dioxol ou 2,3-dihidrobenzo[1,4]dioxina e/ou para um anel heterocíclico adicional. Hetero-Cs-C-io arila é um sistema heterocíclico aromático compreendendo um, dois ou três heteroátomos selecionados entre N, O, S, por exemplo, um resíduo heterocíclico aromático de 5 ou 7 membros opcionalmente condensado, por exemplo, para 1 ou 2 anéis fenila e/ou para um anel heterocíclico adicional. Exemplos de resíduos C5-C10 arila ou hetero-Cs-C-io arila, conforme mencionados acima incluem fenila, naftila, tetrahidronaftila tal como tetralinila, indanila, tienila, benzotienila, furanila, benzofuranila e isobenzofuranila.
Preferencialmente, C5-C10 arila e hetero-Cs-Cio arila, conforme usados neste relatório, significam resíduos parcialmente ou totalmente insaturados, por exemplo, aromáticos, opcionalmente substituídos por um ou mais substituintes, preferencialmente até três substituintes, selecionados entre halogênio, por exemplo, F, Cl, Br, I; CN; C1-C4 alquila, tal como metila, etila ou propila, cujo radical pode ser ele mesmo não substituído ou substituído por halogênio, por exemplo, difluorometila ou trifluorometila; C1C4 alcóxi, cujo radical pode ser ele mesmo não substituído ou substituído por halogênio, por exemplo, trifluorometóxi; ou cujos substituintes podem ser condensados, por exemplo, para um benzo[1,3]dioxol ou 2,3-dihidrobenzo[1,4]dioxina e/ou para um anel heterocíclico adicional. Hetero-Cs-Cio arila é um sistema heterocíclico aromático compreendendo um, dois ou três heteroátomos selecionados entre N, O, S, por exemplo, um resíduo heterocíclico aromático de 5 ou 7 membros opcionalmente condensado, por exemplo, para 1 ou 2 anéis fenila e/ou para um anel heterocíclico adicional. Exemplos de resíduos C5-C10 arila ou hetero-C5-C10 arila, conforme mencionados acima, incluem fenila, naftila, indanila, tetralinila, tienila, - benzotienila, furanila, benzofuranila e isobenzofuranila.
Sais de adição de ácido são, especialmente, sais farmaceu3 ticamente aceitáveis de compostos de fórmula I. Para fins de isolamento ou purificação, também é possível usar sais farmaceuticamente inaceitáveis, por exemplo, picratos ou percloratos. Para fins terapêuticos, somente são empregados sais farmaceuticamente aceitáveis ou compostos livres (onde aplicável, sob a forma de preparações farmacêuticas), e estes são portanto preferidos.
Por conta do átomo ou átomos de carbono assimétricos presentes nos compostos de fórmula I e seus sais, os compostos podem existir em forma oticamente ativa ou em forma de misturas de isômeros óticos, por exemplo, sob a forma de misturas racêmicas. Todos os isômeros óticos e suas misturas, inclusive as misturas racêmicas, são parte da presente invenção.
Na fórmula I são preferidos os seguintes significados, de modo independente, coletivamente ou em qualquer combinação ou subcombinação, caso aplicável:
(d) R é 1-isobenzofuranila ou fenila substituída ou não substituída, por exemplo, monossubstituída por um cloro ou flúor na posição 2, 3 ou 4, CF3 na posição 2 ou 3, metóxi na posição 2; trifluorometóxi na posição 3; benzo[1,3]-dioxol; 2,3-dihidrobenzo[1,4]-dioxina; ciano; ou dissubstituído, por exemplo, por um flúor na posição 2 e 5, 3 e 5, ou cloro na posição 2 e flúor na posição 6.
São preferidos os derivados de aza-bicicloalquila de fórmula I em que
X é CH2 ou uma ligação simples;
Y é um grupo de fórmula
e
R é fenila, naftila, tetraidronaftila, indariila, tienila, benzotienila, furanila, benzofuranila e isobenzofuranila, os quais, em cada caso, podem ser não substituídos ou mono-, di- ou trissubstituídos por halogênio, ciano, formila, acetila, C1-C3 alcoxicarbonila, N,N-di-(CrC3 alquila) carbamoíla, fenila, fenóxi, metilendióxi, etilendióxi; ou C1-C4 alquila, C2-C4 alquenila, C2C4 alquinila ou C1-C4 alcóxi, cujos radicais podem ser eles mesmos não substituídos ou mono-, di- ou trissubstituídos por halogênio.
Mais preferidos são aqueles, derivados de aza-bicicloalquila de fórmula I em que
X é CH2 ou uma ligação simples;
Y é um grupo de fórmula
e
Ré (a) fenila, a qual é não substituída ou mono-, di- ou trissubstituída por halogênio, ciano, metilendióxi,
C1-C4 alquila, a qual é não substituída ou mono-, di- ou trissubstituída por halogênio, ou
C1-C4 alcóxi, 0 qual é não substituído ou mono-, di- ou trissubstituído por halogênio, (b) naftila, indanila, tetralinila ou (c) furanila, benzofuranila, isobenzofuranila, benzotienila ou tienila, em forma de sal de adição de ácido ou base livre.
Ainda mais preferidos são os derivados de aza-bicicloalquila de fórmula I em que
X é CH2 ou uma ligação simples; Y é um grupo de fórmula
e
Ré (a) fenila a qual é não substituída ou mono-, di- ou tri-substituída por halogênio, ciano, metilendióxi,
C1-C4 alquila, a qual é não substituída ou mono-, di- ou trissubstituída por halogênio, ou
C1-C4 alcóxi, o qual é não substituído ou mono-, di- ou trissubstituído por halogênio, (b) naftila, ou (c) furanila, benzofuranila, isobenzofuranila, ou tienila, em forma de sal de adição de ácido ou base livre.
Além do precedente, a presente invenção também proporciona um processo para a produção de um composto de fórmula I, cujo processo compreende a etapa de reagir um composto de fórmula II z-Y-R (II);
em que Y e R são como definidos acima e z é um grupo de partida, por exemplo, F, Cl, Br, I ou OSO2CF3l com um composto de fórmula III
em que X é conforme definido acima para um composto de fórmula I, e recuperar o composto de fórmula I obtido desta forma, em forma de sal de adição de ácido ou base livre.
A reação pode ser realizada de acordo com procedimentos de rotina, por exemplo, conforme ilustrado nos Exemplos.
Compostos de fórmula II são conhecidos ou podem ser preparados a partir de compostos conhecidos correspondentes, por exemplo, conforme descrito nos Exemplos, por exemplo, em analogia a Coates WJ, McKillop A (1992) Synthesis 334-342. Os compostos de fórmula III são conhecidos.
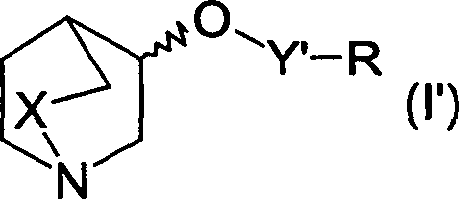
Alternativamente, os compostos de fórmula I’
em que
X e R são como definidos acima e Y’ é
N-a
N
Λ
ou
-N podem ser produzidos por um processo compreendendo a etapa de reagir um composto de fórmula IV
Y'-z (IV);
em que Y’, z e X são como definidos acima, com um composto de fórmula V
OH
R-B
OH (V) em que R é conforme definido acima para um composto de fórmula I, e recuperar o composto de fórmula I’ obtido deste modo, em forma de sal de adição de ácido ou base livre.
Compostos de fórmula IV são conhecidos ou podem ser preparados a partir de compostos conhecidos correspondentes, por exemplo, conforme descrito no Exemplo 17, por exemplo, reagindo compostos de fórmula III com compostos de fórmula ΙΓ;
e z é conforme descrito acima.
Compostos de fórmula V (por exemplo, ácidos fenilborônicos não substituídos ou substituídos) são conhecidos ou podem ser preparados a partir de compostos conhecidos correspondentes. Por exemplo, um composto de fórmula VI,
R-Br (VI) em que R tem o significado conforme proporcionado para um composto de fórmula I, podem ser reagidos com um trialquila borato em um solvente inerte, tal como benzeno, tolueno, tetrahidrofurano, ou misturas dos mesmos, por meio da adição de butila lítio, a uma temperatura dentre cerca de -78°C e -25°C, por exemplo, cerca de -40°C, por um período de cerca de 1 hora a 6 horas, fornecendo um composto de fórmula V.
A elaboração das misturas da reação de acordo com os processos acima e a purificação dos compostos obtidos deste modo podem ser realizadas de acordo com procedimentos conhecidos.
Sais de adição de ácido podem ser produzidos a partir das bases livres, de maneira conhecida, e vice versa. Sais de adição de ácido adequados para uso de acordo com a presente invenção incluem, por exemplo, o cloridrato e o formato.
Compostos de fórmula I em forma oticamente pura podem ser obtidos a partir dos racematos correspondentes, de acordo com procedimentos de conhecimento geral, por exemplo, HPLG com matriz quiral.
Alternativamente, podem ser usados materiais de partida oticamente puros.
Misturas estereoisoméricas, por exemplo, misturas de diastereômeros, podem ser separadas em seus isômeros correspondentes em uma maneira conhecida per se por meio de métodos de separação adequados. Misturas diastereoméricas, por exemplo, podem ser separadas em seus diastereômeros individuais por meio de cristalização fracionada, cromatografia, distribuição de solvente, e procedimentos similares. Esta separação pode ocorrer ou no nível de um composto de partida ou em um próprio composto de fórmula I. Enantiômeros podem ser separados através da formação de sais diastereoméricos, por exemplo, por formação de sal com um ácido quiral enantiomericamente puro, ou por meio de cromatografia, por exemplo, por HPLC, usando substratos cromatográficos com ligantes quirais.
Nas etapas adicionais do processo, realizadas conforme desejado, grupos funcionais dos compostos de partida, os quais não deveríam tomar parte na reação, podem estar presentes sob forma não protegida ou podem ser protegidos, por exemplo, por um ou mais dos grupos protetores mencionados abaixo. Os grupos protetores são, em seguida, total ou parcialmente removidos, de acordo com um dos métodos descritos aí.
Os grupos protetores podem já estar presentes em precursores e devem proteger os grupos funcionais em questão contra reações secundárias indesejadas. É uma característica dos grupos protetores que eles se combinem prontamente, isto é, sem reações secundárias indesejadas, para remoção, tipicamente por solvólise, redução, fotólise ou também por atividade enzimática, por exemplo, sob condições análogas para condições fisiológicas, e que eles não estejam presentes nos produtos finais. O versado na técnica sabe, ou pode determinar facilmente, quais grupos protetores são adequados com as reações mencionadas anteriormente neste relatório e nas partes que se seguem.
A proteção de semelhantes grupos funcionais por grupos protetores, os próprios grupos protetores, e suas reações de remoção, são descritos, por exemplo, em trabalhos de referência de rotina, tais como J. F. W. McOmie, Protective Groups in Organic Chemistry, Plenum Press, London and New York 1973, em T. W. Greene, Protective Groups in Organic Synthesis, Wiley, New York 1981, em The Peptides; Volunrie 3 (editores: E. Gross and J. Meienhofer), Academic Press, London and New York 1981, em Methoden der organischen Chemie, Houben Weyl, 4th edition, Volume 15/1, Georg Thieme Verlag, Stuttgata 1974, em H.-D. Jakubke and H. Jescheit, Aminosáuren, Peptide, Proteine, Verlag Chemie, Weinheim, Deerfield Beach, and Basel 1982, e em Jochen Lehmann, Chemie der Kohlenhydrate: Monosaccharide und Derivate, Georg Thieme Verlag, Stuttgart 1974.
Todas as etapas do processo descritas aqui podem ser realizadas sob condições de reação conhecidas, preferencialmente sob as especificamente mencionadas, na ausência de ou geralmente na presença de solventes ou diluentes, preferencialmente tais como são inertes aos reagentes usados e capazes de dissolver estes, na ausência de ou na presença de catalisadores, agentes de condensação ou agentes neutralizantes, por exemplo, agentes de troca iônica, tipicamente agentes de troca catiônica, por exemplo, sob a forma de H+ , dependendo do tipo de reação e/ou reagentes, em temperatura reduzida, normal, ou elevada, por exemplo, na faixa de -100°C a cerca de 190°C, preferencialmente de cerca de -80°C a cerca de 150°C, por exemplo, a -80 até -60°C, a temperatura ambiente, a - 20 até 40°C, ou no ponto de ebulição do solvente usado, sob pressão atmosférica ou dentro de um vaso fechado, quando apropriado sob pressão, e/ou em uma atmosfera inerte, por exemplo, sob argônio ou nitrogênio.
Os compostos da invenção e seus sais de adição de ácido farmaceuticamente aceitáveis, nas partes que se seguem referidos como agentes da invenção, apresentam valiosas propriedades farmacológicas quando testadas in vitro e em animais, e portanto são úteis como fármacos.
Em particular, os agentes da invenção são agonistas de receptores de acetilcolina a7 nicotínico (nAChR).
Em ensaios funcionais, os agentes da invenção apresentam alta afinidade ao a7 nAChR, conforme demonstrado nos testes seguintes:
a) Um ensaio funcional para afinidade ao a7 nAChR é realizado com uma linhagem de células de pituitária de rato estavelmente expressando o a7 nAChR. Como uma leitura, se usa o influxo de cálcio na estimulação do receptor. Neste ensaio, os agentes da invenção apresentam valores de pEC50 de cerca de 5 a cerca de 8.
b) Para avaliar a atividade dos agentes da invenção sobre o nAChR α4β2 neuronal humano, um ensaio funcional semelhante é realizado, usando uma linhagem de células epiteliais humanas estável expressando o subtipo humano α4β2. Neste ensaio, os agentes da invenção apresentam seletividade para os subtipos a.7 nAChR.
c) Para avaliar a atividade dos compostos da invenção sobre o subtipo gangliônico” e o tipo muscular de receptor nicotínico, ensaios funcionais similares, conforme descrito em a), são realizados com uma linhagem de células epiteliais humanas estavelmente expressando o subtipo gangliônico humano, ou uma linhagem de células endogenamente expressando o tipo muscular humano de receptores nicotínicos. Nestes ensaios, os agentes da invenção apresentam pouca ou nenhuma atividade sobre o tipo gangliônico e muscular de subtipos de receptores nicotínicos.
No modelo de camundongos apresentando déficit na passagem de controle sensorial (camundongos DBA/2), descrito por S. Leonard et al. no Schizophrenia Bulletin 22, 431-445 (1996), os agentes da invenção induzem importante passagem de controle sensorial em concentrações de cerca de 10 a cerca de 40 μΜ.
Os agentes da invenção são portanto úteis para a prevenção e o tratamento de distúrbios psicóticos, tais como esquizofrenia, mania, depressão e ansiedade, e para a prevenção e o tratamento de distúrbios neurodegenerativos, tais como demência senila, mal de Alzheimer e outros distúrbios de diminuição intelectual, tais como distúrbios de hiperatividade por déficit de atenção (ADHD); mal de Parkinson, coréia de Huntington, esclerose lateral amiotrófica, esclerose múltipla, epilepsia, convulsões, síndrome de Tourette, TOC (transtorno obsessivo compulsivo), dor neuropática, pós-operatória e inflamatória, dor de membro fantasma, cognição, cessação do fumo, défícits e disfunção da memória, déficit de aprendizado, distúrbios de pânico, narcolepsia, nocicepção, demência por AIDS, demência senila, autismo, discinesia tardia, fobia social, pseudodemência. A utilidade de agonistas a7 nAChR em neurodegeneração está documentada na literatura, por exemplo, em Wang et al., J. biok Chem. 275, 5626-5632 (2000).
Para as indicações acima a dosagem apropriada dos agentes da invenção, logicamente, variará, dependendo, por exemplo, do hospedeiro, do modo de administração e da natureza e da gravidade da condição que estiver sendo tratada, bem como da potência relativa do agente em particular da invenção empregado. Por exemplo, a quantidade de agente ativo necessária pode ser determinada com base em técnicas conhecidas ”in vitro e in vivo, determinando por quanto tempo uma concentração de agente ativo em particular permanece no plasma sangüíneo em um nível aceitável para um efeito terapêutico. Em geral, são indicados para serem obtidos resultados satisfatórios em animais em dosagens diárias de a partir de cerca de 0,01 a cerca de 20,0 mg/kg por via oral. Em seres humanos, uma dosagem diária indicada está na faixa de cerca de 0,7 a cerca de 1400 mg/dia por via oral, por exemplo, de cerca de 50 a 200 mg (homem de 70 kg), convenientemente administrada uma vez ou em doses divididas até 4 x por dia, ou em forma de liberação gradual. Formas de dosagem oral, por consegüinte, compreendem adequadamente de cerca de 1,75 ou 2,0 a cerca de 700 ou 1400 mg de um agente da invenção misturado com um diluente ou veículo apropriado para o mesmo, farmaceuticamente aceitável.
Exemplos para composições compreendendo um agente da invenção incluem, por exemplo, uma dispersão sólida, uma solução aquosa, por exemplo, contendo um agente solubilizante, uma microemulsão e uma suspensão de, por exemplo, um sal de cloridrato de um composto de fórmula
I na faixa de 0,1 a 1%, por exemplo, 0,5%.< A composição pode ser tamponada para um pH na faixa de, por exemplo, 3,5 a 9,5, por exemplo, para pH 4,5, por um tampão adequado.
Os agentes da invenção também são úteis como produtos químicos de pesquisa.
Para uso de acordo com a invenção, o agente da invenção pode ser administrado como agente ativo único ou em combinação com outros agentes ativos empregados comumente para o tratamento dos distúrbios mencionados neste relatório, em qualquer maneira usual, por exemplo, por via oral, por exemplo, sob a forma de comprimidos ou cápsulas, ou por via parenteral, por exemplo, sob a forma de suspensões ou soluções para injeção.
As composições farmacêuticas para administração separada dos parceiros da combinação e para a administração em uma combinação fixa, isto é, uma única composição galênica compreendendo no mínimo dois parceiros da combinação, de acordo com a invenção, podem ser preparadas em uma maneira conhecida per se e são as adequadas para administração enteral, tal como oral ou retal, e parenteral a mamíferos, inclusive o homem, compreendendo uma quantidade terapeuticamente eficaz de no mínimo um parceiro da combinação farmacologicamente ativo sozinho ou em combinação com um ou mais veículos farmaceuticamente aceitáveis, especialmente adequados para uso enteral ou parenteral.
Composições farmacêuticas contêm, por exemplo, de cerca de 0,1% a cerca de 99,9%, preferencialmente de cerca de 20% a cerca de 60%, dos ingredientes ativos. Preparações farmacêuticas para a terapia de combinação para administração enteral ou parenteral são, por exemplo, aquelas em formas de unidade de dosagem, tais como comprimidos revestidos com açúcar, comprimidos, cápsulas ou supositórios, e, além disso, ampolas. Caso não indicado de outro modo, estas são preparadas em uma maneira conhecida per se, por exemplo, por meio de processos convencionais de misturação, granulação, revestimento com açúcar, dissolução ou liofilização. Será reconhecido que o teor unitário de um parceiro da combinação contido em uma dose individual de cada forma de dosagem não precisa constituir ele mesmo uma quantidade eficaz contanto que possa ser atingida a quantidade eficaz, necessária por meio da administração de uma pluralidade de unidades de dosagens.
Em particular, uma quantidade terapeuticamente eficaz de cada um dos parceiros da combinação pode ser administrada simultaneamente ou seqüencialmente e em qualquer ordem, e os componentes podem ser administrados separadamente ou como uma combinação fixa. Por exemplo, o método de retardo da progressão ou tratamento de uma doença proliferativa de acordo com a invenção pode compreender (i) administração do parceiro da combinação (a) em forma livre ou de sal farmaceuticamente aceitável e (ii) administração de um parceiro da combinação (b) em forma livre ou de sal farmaceuticamente aceitável, simultaneamente ou seqüencialmente em qualquer ordem, em quantidades conjuntamente terapeuticamente eficazes, preferencialmente em quantidades sinergicamente eficazes, por exemplo, em dosagens diárias correspondentes às quantidades descritas neste relatório. Os parceiros individuais da combinação podem ser administrados separadamente em diferentes momentos durante o curso da terapia ou simultaneamente em formas de combinação dividida ou única. Além disso, o termo administrar também engloba o uso de uma pró-droga de um parceiro da combinação que converte in vivo para o parceiro da combinação como tal. A presente invenção, portanto, deve ser entendida como englobando todos os regimes referidos de tratamento simultâneo ou alternado e o termo administrar deve ser interpretado de acordo.
A dosagem eficaz de cada um dos parceiros da combinação empregados pode variar dependendo do composto ou composição farmacêutica em particular empregados, o modo de administração, a condição sendo tratada, a gravidade da condição sendo tratada. Portanto, o regime de dosagem é selecionado de acordo com uma variedade de fatores, inclusive a via de administração e a função renal e hepática do paciente. Um médico, clínico ou veterinário, normal, podem prontamente determinar e prescrever a quantidade eficaz dos ingredientes ativos únicos requeridos para prevenir, neutralizar ou deter o progresso da condição. A ótima precisão para atingir a concentração dos ingredientes ativos dentro da faixa que produz eficácia sem toxicidade requer um regime com base na cinética da disponibilidade dos ingredientes ativos para os sítios alvo.
De acordo com o precedente, a presente invenção também proporciona:
(1) Um agente da invenção para uso como um agonista de receptor alfa-7, por exemplo, para uso em qualquer uma das indicações em particular determinadas anteriormente neste relatório.
(2) Uma composição farmacêutica compreendendo um agente da invenção como ingrediente ativo junto com um diluente ou veículo para o mesmo farmaceuticamente aceitável.
(2’) Uma composição farmacêutica para o tratamento ou a prevenção de uma doença ou condição na qual a ativação do receptor alfa-7 desempenha uma função, ou está implicada, compreendendo um agente da invenção e um veículo.
(3) Um método para o tratamento de qualquer indicação particular determinada anteriormente neste relatório em um paciente que necessite do mesmo, o qual compreende administrar uma quantidade eficaz de um agente da invenção.
(3’) Um método para tratar ou prevenir uma doença ou condição na qual a ativação do receptor alfa-7 desempenha uma função, ou está implicada, compreendendo administrar a um mamífero que necessite do mesmo uma quantidade terapeuticamente eficaz de um agente da invenção.
(4) O uso de um agente da invenção para a fabricação de um medicamento para o tratamento ou a prevenção de uma doença ou condição na qual a ativação do receptor alfa-7 desempenha uma função, ou está implicada.
(5) Um método conforme definido acima compreendendo coadministração, por exemplo, concomitantemente ou em seqüência, de uma quantidade terapeuticamente eficaz de um agonista de alfa-7, por exemplo, um agente da invenção e uma segunda substância de droga, a referida segunda substância de droga sendo, por exemplo, para uso em qualquer uma das indicações em particular determinadas anteriormente neste relatório.
(6) Uma combinação compreendendo uma quantidade terapeuticamente eficaz de um agonista de alfa-7, por exemplo, um agente da invenção e uma segunda substância de droga, a referida segunda substância de droga sendo por exemplo, para uso em qualquer uma das indicações em particular determinadas anteriormente neste relatório.
Os Exemplos seguintes ilustram a invenção.
Abreviações usadas nos Exemplos:
AcOEt acetato de etila aq. aquosa
DEAD dietilazodicarboxilato
DMF dimetilaformamida
EtOH etanol
FC cromatografia flash h hora
HV alto vácuo
MeOH MeOH
RP-HPLC cromatografia líquida de alto desempenho de fase reversa ta temperatura ambiente rac. racemato soln. solução
TFA ácido trifluoroacético
THF tetrahidrofurano
Exemplo 1: Preparação de (rac.)-3-[6-(4-fluorofenil)-piridazin-3-ilóxi]-1aza-biciclo[2.2.2]octano
Uma solução de (rac.)-3-quinuclidinol (0,007 mol) em THF seco sob nitrogênio, é tratada com hidreto de sódio (60% em óleo mineral ; 1,1 equiv.). Depois de uma hora à temperatura ambiente, uma solução de 3cloro-6-(4-flúor-fenil)piridazina (1,0 equiv.) em THF (30 ml) é adicionada, e a mistura da reação é aquecida até o refluxo durante 6 horas. Depois de resfriar até a temperatura ambiente, a THF é evaporada e o resíduo é dissolvido em acetato de etila (100 ml) e em seguida lavado com água (3 χ 20 ml), seguida por solução de cloreto de sódio (20 ml). O acetato de etila é seco sobre sulfato de magnésio anídrico, filtrado e evaporado até a secagem, e o óleo residual purificado por cromatografia de coluna de sílicagel (eluente: acetato de etil-metanol-trietilamina (50:10:2)) para proporcionar (rac.)-3-[6-(4-fluorofenil)-piridazin-3-ilóxi]-1 -aza-biciclo[2.2.2]octano como um sólido incolor. 1H-RMN (400 MHz, CDCI3): δ = 8,00 (m, 2H), 7,75 (d, 1H), 7,17 (m, 2H), 7,1 (d, 1H), 5,35 (m, 1H), 3,5 (m, 1H), 2,99-2,83 (m, 5H), 2,32 (m, 1H), 1,98 (m, 1H), 1,76-1,68 (m, 2H), 1,46 (m, 1H).
Os compostos seguintes de fórmula I, em que Y é
N=N podem ser preparados em analogia ao Exemplo 1:
| + X + 2 | 268 | 268 | 282,2 | 316,2 | 316,2 | 312,4 | 350,5 | 300,2 | 316,2 | 300,2 | 300,2 | 350,2 | 350,3 | 350,2 | 321,38 |
| ponto de fusão °C (sal) | ------, 143-145 (nenhum sal) | 145-147 (nenhum sal) | I 128-130 (nenhum sal) | 175-177 (nenhum sal) | 98-100 (nenhum sal) | 125-128 (nenhum sal) | 172-175 (nenhum sal) | 110-113 (nenhum sal) | 85-87 (nenhum sal) | 146-149 (nenhum sal) | 118-121 (nenhum sal) | 173-175 (nenhum sal) | 112-115 (nenhum sal) | 127-130 (nenhum sal) | 193-195° (nenhum sal) |
| -23,5° (0,1% MeOH) | -26,5° (0,1% MeOH) | -32,5° (0,5% MeOH) | +29,0° (0,1% MeOH) | X O <u í o o m cd ? | V/N | +28 (0,1% MeOH) | +23,5° (0,1% MeOH) | +29,5° (0,1% MeOH) | +39,5° (0,1% MeOH) | I +31,5° (0,1% MeOH) | +29,5° (0,1% MeOH) | +23,0° (0,1% MeOH) | +31,0° (0,1% MeOH) | +29,0 (0,1% MeOH) | |
| HPLC ta (min) | 5,7 | id | 5,2 J | 6,2 ! | 6,2 | 5,5 | o | 5,6 | 5,7 | 5,7 | 5,5 | |- 7,3 | 6*9 | co l< | 6,8 |
| o: | fenila | fenila | fenila | 4-cloro-fenila | 3-cloro-fenila | 2-metóxi-fenila | 4-trifluorometil-fenila | 2-flúor-fenila | 2-cloro-fenila | 4-flúor-fenila | 3-flúor-fenila | 3,4-dicloro-fenila | 3-trifluorometil-fenila | 3,5-dicloro-fenila | 1-isobenzofuranila |
| X | ligação | ligação | CN δ | CN X o | CN X o | CN X o | CN X o | CN X o | CN X o | CN X o | CM X o | CM X o | CN X o | CN X o | CN X o |
| èstereo- quím. | (3R.4S) | (3S,4R) | w | g | g | rac. | g | g | g | g | g | g | g | g | g |
| X LJJ | CM | CO | ^tf | IO | CO | b- | oo | <35 | o | T· | CM | co | 'tf | IO | co |
Exemplo 17: Preparação de (rac,)-3-(5-fenil-pirimidin-2-ilóxi)-1-azabiciclo[2.2.2]octano
5-Bromo-2-hidróxi-pirimidina (400 mg, 2,29 mmoles), (rac.)-3quinuclidinol (432 mg, 3,36 mmoles) e trifenilafosfina (890 mg, 3,40 mmoles) são dissolvidos em THF (25 ml). Depois de agitar durante 10' a -10°C, uma solução de DEAD (522 μΙ, 3,36 mmoles) em THF (20 ml) é adicionada, gota a gota. A mistura da reação é deixada aquecer até a temperatura ambiente e é agitada durante 16 horas, à temperatura ambiente. A mistura da reação é evaporada para dar um semi-sólido laranja (2,50 g), o qual é triturado com AcOEt e filtrado para dar (rac.)-3-(5-bromo-pirimidin-2-ilóxi)-1-aza-biciclo[2.2.2]-octano, como um sólido branco. O filtrado é purificado por FC (gel de sílica, eluentes: AcOEt/MeOH a 9:1, em seguida AcOEt/MeOH/NEt3 a 70:27:3). (rac.)-3-(5-Bromo-pirimidin-2-ilóxi)-1-aza-biciclo[2.2.2]octano (150 mg, 0,53 mmol), ácido fenilborônico (66 mg, 0,54 mmol) e tetracis(trifenilfosfina)paládio são dissolvidos em tolueno:EtOH a 9:1 (15 ml). Na2CO3 (225 mg, 2,12 mmoles) é dissolvido em água (1,5 ml) e adicionado à mistura da reação, a qual é aquecida a 90°C durante 20 horas. Depois de resfriar até a temperatura ambiente, é filtrada sobre celite; a camada de tolueno é separada e lavada com salmoura. As camadas aquosas são reextraídas com AcOEt, os extratos orgânicos combinados são secos sobre MgSO4, filtrados, e o filtrado é evaporado para dar uma goma amarela clara (195 mg), que é purificada por FC (gel de sílica, eluentes: AcOEt/MeOH a 9:1, em seguida AcOEt/MeOH/NEt3 a 70:27:3) para dar um sólido branco, o qual ainda contém material de partida. É feita uma segunda purificação por RP-HPLC (coluna Phenomenex RP18, gradiente 0,08% HCOOH aq. /CH3CN a 95:5 -> CH3CN, em 20') para dar (rac)-3-(5-fenil-pirimidin-2-ilóxi)-1-azabiciclo[2.2.2]octano como seu sal de formato; HPLC ta (min): 5,4; ponto de fusão °C: 108-114; M+H+ 282,2.
Exemplo 18: Preparação de (R)-3-(5-fenil-pirimidin-2-ilóxi)-1-azabiciclo[2.2.2]octano
5-Bromo-2-cloro-pirimidina (400 mg, 2,03 mmoles), ácido fenilborônico (253 mg, 2,07 mmoles) e tetracis(trifenilfosfina)paládio (118 mg, 0,102 mmol) são dissolvidos em tolueno/EtOH a 9:1 (50 ml). Na2CO3 (861 mg, 8,12 mmoles) é dissolvido em água (4 ml) e adicionado à mistura da reação. A mistura é agitada a 90°C durante 19 horas, resfriada até a temperatura ambiente e filtrada sobre celite. A camada de tolueno é separada e lavada com salmoura. As camadas aquosas são reextraídas com AcOEt; os extratos orgânicos combinados são secos sobre MgSO4 e filtrados. O filtrado é evaporado para dar um sólido amarelo (503 mg), o qual é purificado por FC (sílica-gel, eluentes ciclohexano e AcOEt/ciclohexano a 1:9), para dar 2-cloro-5-fenil-pirimidina.
(R)-3-quinuclidinol (478 mg, 3,76 mmoles) é adicionado a uma suspensão de NaH (164 mg de uma dispersão a 60% em óleo mineral, 4,09 mmoles) em DMF (10 ml). A mistura é agitada durante uma hora, à temperatura ambiente. 2-Cloro-5-fenil-pirimidina (177 mg, 0,93 mmol) é adicionado e a mistura é aquecida durante 3,5 horas a 90°C. A mistura da reação é diluída com tolueno e lavada com solução aquosa 1M de NaOH e salmoura. As camadas aquosas são reextraídas com tolueno (3x). Os extratos orgânicos combinados são secos sobre MgSO4 e filtrados. O filtrado é evaporado para dar um sólido amarelo (310 mg), o qual é purificado por FC (sílica-gel, eluentes: AcOEt, em seguida AcOEt/MeOH/NEt3 a 80.18:2). Uma segunda purificação é feita por RP-HPLC (coluna Phenomenex RP18, gradiente HCOOH aq. a 0,08% -» HCOOH aq. a 0,08% /CH3CN a 80:20, em 10', -> CH3CN, em 15'), para dar (R)-3-(5-fenil-pirimidin-2-ilóxi)-1-azabiciclo[2.2.2]-octano como seu sal de formato, HPLC ta (min): 5,4; ponto de fusão °C: 108-110; [o]D te +8,6 (1,03, MeOH), M+H+ 282,2.
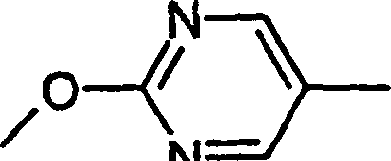
Os compostos seguintes de fórmula I, em que -O-Y- é
, podem ser preparados em analogia ao Exemplo 17 ou
| + X + 2 | 282,2 | 300,2 | 316,2 | 350,1 | 350,1 | 350,1 | 307,2 | 350,2 | 326,2 | 300,2 | 418,2 | 316,2 | 316,2 | 288,1 | 332,2 | 316,2 | 322,2 | 00 00 CM | 332,2 |
| ponto de fusão °C (sal) | 126-129 (nenhum sal) | 87-93 (nenhum sal) | 163-165 (nenhum sal) | 182-184 (nenhum sal) | N/A (oila) (sal de HCI) | 183-184 (nenhum sal) | 189 (nenhum sal) | 158-159 (nenhum sal) | nd (nenhum sal) | nd (nenhum sal) | nd (nenhum sal) | nd (nenhum sal) | 160-163 (nenhum sal) | nd (nenhum sal) | nd (nenhum sal) | 170-173 (nenhum sal) | 183-186 (nenhum sal) | 167-174 (nenhum sal) | 170-190 (nenhum sal) |
| <0 Q 2 | -31,0° (0,95% MeOH) | V/N | V/N | V/N | V/N | V/N | V/N | V/N | V/N | Ό CZ | V/N | +29,6° (0,50% EtOH) | TO c | TO c | TO c | V/N | +33,8° (0,97% MeOH) | +26,2° (0,99% MeOH) | +27,0° (0,1% MeOH) |
| HPLC ta (min) | CO iri | <31 1X1 | CO co | o CO | CO co' | co | IO co | UI co | <31 Ul | γ- ιο | CD K | co | co | CM_ Ul | co co | Ul CO | <31 co | CO_ 1X1 | o Γ- |
| Dí | fenila | 2-flúor-fenila | 3-cloro-fenila | 3,4-dicloro-fenila | 2,4-dicloro-fenila | 3,5-dicloro-fenila | 3-ciano-fenila | 3-trifluorometil-fenila | benzoM ,3]dioxol-5-ila | 2-flúor-fenila | 3,5-bis-trifluorometil-fenila | 2-cloro-fenila | 3-cloro-fenila | tiofen-2-ila | naftalen-1-ila | 4-cloro-fenila | benzofuran-2-ila | tiofen-3-ila | naftalen-2-ila |
| X | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o | CM X o |
| estereo- quím. | g | rac. | rac. | rac. | rac. | rac. | rac. | rac. | rac. | g | rac. | g | g | g | g | rac. | g | g | g |
| X ' LU | Oi | o CM | CM | CM CM | cO CM | CM | ui CM | CD CM | h- CM | co CM | σι CM | o co | CO | CM CO | co co | co | Ul co | co co | CO |
| + X | CM | 0Μ | CM | C0 | CM | ΟΜ | ΟΜ | ΟΜ | ΟΜ | ΟΜ | CM | CM | CM | O | CM | co | |||||
| ο | 00 | CM | ο | Ο | ΟΜ | 0Μ | C0 | O | Ο | CO | (Ο | CD | Ο | Tf | Tf | o | O | o | o | ||
| ΙΟ | χ— | V— | ΙΩ | Ο | r- | r- | χ— | ΙΩ | ΙΩ | <3 | σ> | C3 | 0Ο | V“ | T— | T | CO | o | co | ||
| <> | C0 | ΟΟ | οο | 00 | C0 | 0Μ | 04 | οο | CO | C0 | ΟΜ | ΟΜ | ΟΜ | CO | CO | CO | CO | CO | co | co | |
| φ w | X** | χ**«· | X-*» | X-*· | X—* | X-*» | X*x | x^»· | X**» | ||||||||||||
| φ | φ | φ | φ | φ | φ | Φ | Φ | Φ | Φ | Φ | |||||||||||
| (Ζ) | ω | ω | C? | σ> | ω | CA | w | V) | V) | V) | CA | ||||||||||
| Ο Ο | ζ-. | Ε 3 | Ε 3 | ζ-. | Ζ-. | Ε 3 | φ V) | ε 3 | um | um | um | um | E 3 | E 3 | E 3 | ι sal) | |||||
| ο | Φ | ΧΣ | χζ | ω | C0 | ιυ | φ | φ | Φ | ΧΖ | Ε | JZ | χζ | .C. | x: | ΧΞ | £ | x: | X= | ||
| ICTJ | V) | C | C | Φ | C0 | (/> | Φ | C/5 | £/) | C | 3 | C | C | C | c | C | C | c | c | ||
| ω £ | Ε | ne | φ Γ | Ε | Ε | Ε | Ε | Ε | E | ne | ΧΖ C | ne | φ C | ne | ne | ne | eu | ne | Φ c: | E | |
| 3 | 3 | 3 | 3 | 3 | 3 | 3 | (ne | z | |||||||||||||
| φ Ό | JC. C φ | 36 | 00 CO | 3nh | snh | 3nh | enh | enh | enh | 107 | 40 | 64 | οο | 32 | 45 | 56 | CO | 30 | enf | ||
| 2 C | C | ν- 1 ΙΟ | 1 Ο | C | CZ | C | C | c | ΟΜ ι 0- | τγ C3 | τ- ι <3 | οό | 1 ΙΌ | 1 O | 1 ΙΌ | T“ 1 | 1 | có | c | ||
| ο | Ό | C0 | οο | σ | σ | σ | Ό | Ό | σ | οο | ΙΩ | 00 | ΙΩ | 00 | CO | ΙΩ | CM | Ό | |||
| Ω. | C | C | C | C | C | C | c | τ— | 00 | V— | T“ | T“ | ·* | T“ | 2 | ||||||
| χ | X | χ>—S | x**s | Z—x | >»*X | ||||||||||||||||
| ο | o | X | X | X | X | X | X | X | |||||||||||||
| X | φ | φ | ο | ο | ο | o | o | o | O | ||||||||||||
| Ο | φ | φ | φ | Φ | Φ | Φ | φ | ||||||||||||||
| φ | |||||||||||||||||||||
| c£ ΙΩ | ΙΩ | ||||||||||||||||||||
| ÒS | ΟΜ | CM | ΟΜ | Tf | ΙΩ | Tf | 00 | o | CM | ||||||||||||
| ΙΩ | ΙΩ | ΙΩ | ΙΩ | ΙΩ | ΙΩ | ΙΩ | ΙΩ | to | ΙΩ | ||||||||||||
| Ο | Ο | O | Ο | Ο | Ο | O | O | o | O | ||||||||||||
| 'X*** | **-χ | ***··* | ***** | '*·-** | |||||||||||||||||
| Ο | 0 | o | ο | Ο | ο | o | o | o | O | ||||||||||||
| <ο | 6- | r- | <3 | τ— | <Ο | ΙΩ | CM | CO | to | CO | |||||||||||
| “ω | 00 | < | Tf | <3 | ΟΟ | 00 | ΙΩ | O | o | (3 | |||||||||||
| σ | C0 | το | Τ3 | Τ7 | Τ3 | CM | V | τ> | TJ | οο | CM | CM | CO | CO | 00 | CM | Ό | ||||
| C | + | 2 | £Ζ | C | C | C | + | + | C | C | + | + | + | + | + | + | + | ||||
| Φ | |||||||||||||||||||||
| Μ—» · | |||||||||||||||||||||
| Ο | |||||||||||||||||||||
| _ι | C | ||||||||||||||||||||
| 0. | Ε | <3 | co_ | Tf | TJ | Τ3 | σ | CM_ | τ—_ | C0_ | ΙΩ | Tf | Tf | Ν-_ | ΙΩ | o_ | 00_ | to_ | IO_ | Tf | IO_ |
| X | ο | 00 | οο | C | C | £Ζ | οο | Tf | ΙΩ | οο | Tf | οο | Tf | Tf | Tf | Tf | có | co | co | co’ | |
| 15 | 15 σ | (Π | Φ | 15 | Φ | 15 | |||||||||||||||
| _ro | 15 | xi-fenila | 15 | 15 | 15 | C 2 | 2 | Έ 2 | Έ 2 | 15 | c 2 | c 2 | c 2 | ||||||||
| loro-fen | úor-feni | loro-fen | fenila | 15 | 15 | úor-feni | loro-fen | φ Ε 2 | φ | 2-metó: | 4-metil- | 5-metil- | ietil-fen | -4-metil | 4-metil- | -5-metil | |||||
| Ο | Μ= | ο | ο | lí | 00 | ΟΜ | O | Ο | <0 | Ο | lÍ | LÍ | &L | t | o | LÍ | o | ||||
| X | 3-di | 3-di | φ Ε | Ώ ι CO | Ο >3 Η— | ran- | ran- | Ώ 1 ΙΩ | •σ 1 IO | •trifli | õ | -tolil | Έ | flúo | flúo | •flúo | 4-di | •clor | O -3 M— | L— O o | |
| CM | CM | 0Μ | cm | οό | 3 | 2 | CM | ομ’ | ΟΜ | ό | Ε | Ω. | ΙΩ | OM | CM | CO | CM | CM | CM | ||
| 04 | 04 | ΟΙ | ΟΙ | 04 | οι | 04 | 04 | ΟΙ | 04 | 04 | 04 | 04 | ΟΙ | 04 | OI | 04 | 04 | ;ão única | Oí | ||
| X | X | X | X | X | X | X | X | X | X | X | X | X | X | X | X | X | X | (ü | X | ||
| X | ο | ο | ο | ο | ο | ο | ο | o | ο | ο | ο | ο | ο | ο | o | o | o | o | .σ | o | |
| tereo- | Ε | ο | |||||||||||||||||||
| ω | 3 | cc | α: | φ | ο: | ο: | ο: | cc | o: | cc | ο: | ο; | ο: | CC | CC | CC | CC | o: | CC | CC | CC |
| φ | σ | ||||||||||||||||||||
| X | 00 | Ο) | ο | CM | οο | Tf | ΙΩ | CO | ο- | οο | <3 | σ | CM | 00 | Tf | to | CD | I-- | |||
| ΙΌ | C0 | οο | Tf | Tf | Tf | Tf | Tf | Tf | Tf | Tf | Tf | Tf | ΙΩ | to | to | to | ΙΩ | to | to | ΙΩ |
Exemplo 58: Preparação de (R)-3-(6-p-Tolil-piridin-3-ilóxi)-1-azabiciclo[2.2.2]octano
Bromo (18,0 ml, 353,7 mmoles) é lentamente adicionado a uma solução de 2-amino-5-cloropiridina (15,0 g, 116,7 mmoles) em HBr aq. a 47% (75,0 ml), a -10°C. Uma solução aquosa de NaNO2 (28,1 g, 407,3 mmoles) é lentamente adicionada. A mistura é agitada durante uma hora a -10 para -5°C, em seguida, durante uma hora, a 5°C. A mistura é neutralizada com solução aquosa 5M de NaOH, mantendo a temperatura abaixo de 25°C. O precipitado é filtrado e recristalizado a partir de pentano, para dar 2-bromo-5-cloropiridina.
2-Bromo-5-cloropiridina (5,0 g, 26,0 mmoles), ácido p-tolilborônico (4,0 g, 29,4 mmoles) e tetracis(trifenilafosfina)paládio (1,44 g, 1,2 mmol) são dissolvidos em tolueno:EtOH, a 9:1 (1375 ml). Uma solução aquosa 2M de Na2CO3 (62,5 ml) é adicionada à mistura da reação. A mistura é agitada a 90°C durante 24 horas, resfriada até a temperatura ambiente e filtrada sobre celite. A camada de tolueno é separada e lavada com salmoura. As camadas aquosas são extraídas com AcOEt. Os extratos orgânicos combinados são secos sobre MgSO4 e filtrados. O filtrado é evaporado para dar um sólido marrom, o qual é purificado por FC (sílica-gel, eluente: tolueno) para dar 5-cloro-2-p-tolil-piridina.
(R)-3-Quinuclidinol (2,97 g, 23,4 mmoles) é adicionado a uma suspensão de NaH (0,96 g de uma dispersão a 60% em óleo mineral, 22,8 mmoles) em DMF (90 ml). A mistura é agitada durante uma hora, à temperatura ambiente. 5-Cloro-2-p-tolil-piridina (4,00 g, 19,6 mmoles) é adicionada e a mistura é aquecida durante 135 horas, a 135°C. A mistura da reação é diluída com tolueno e lavada com solução aquosa 1M de NaOH e salmoura. As camadas aquosas são reextraídas com tolueno (3x). Os extratos orgânicos combinados são secos sobre MgSO4 e filtrados. O filtrado é evaporado para dar um óleo marrom, o qual é purificado por FC (sílica-gel, eluentes: AcOEt, em seguida AcOEt/MeOH/NEt3 a 87:10:3) e recristalizado a partir de CH3CN para dar (R)-3-(6-p-tolil-piridin-3-ilóxi)-1 -azabiciclo[2.2.2]octano; ponto de fusão °C: 110-112; [a]ota = +21,2° (0,50,
MeOH), M+H+ 295,2.
Os compostos seguintes de fórmula I, em que -O-Y-R é
VA
ou
R ou podem ser preparados em analogia ao Exemplo 58:
Condições da HPLC:
para os Exemplos 1-21, 27-29, 32, 33, 35-38, 41-46, 48-53: Coluna Phenomenex Luna ou Kingsorb C18, 30x4,6 mm, 3 μΜ. Gradiente (A {H2O+ 0,08% HCOOH} B CH3CN): 0 a 5min: A:B a 100:0 para 80:20, 5 a 10 min: 80:20 para 0:100, fluxo 3,0 ml/min.
para os Exemplos 22-26: Coluna Waters Xterra MS C18, 50x2,1 mm, 2,5 μΜ. Gradiente (A:{H2O+0,02%TFA}, B:{CH3CN+0,02%TFA}): 0 a 2 min: A:B 90:10 para 5:95; 2 a 4 min: 5:95, 4 a 5,5 min 5:95 para 10:90, 5,5 a 6 min: 10:90 para 90:10, 6 a 7 min: 90:10, fluxo 0,35 ml/min.
para os Exemplos 30, 31, 34, 39, 40, 47, 54-74: Coluna Waters Xterra MS C18, 150x2,1 mm, 3,5 μΜ. Gradiente (A:{H20+0,02%TFA},
B:{CH3CN+0,02%TFA}): 0 a 3 min: A:B 90:10 para 10:90; 3 a 8 min: 10:90, 8 a 9 min: 10:90 para 90:10, 9 a 15 min: 90:10, fluxo 0,35 ml/min.
Exemplo 75: Preparação de R-3-(6-(2-flúor-4-metil-fenil)piridazin-3-ilóxi)-1-aza-biciclo[2.2.2]octano
Uma solução de (R)-(-)-3-quinuclidinol (0,742g, 5,84 mmoles) em DMF seco (5 ml) é adicionado lentamente a uma suspensão de hidreto de sódio (60% em óleo mineral, 0,234 g, 5,84 mmoles) em DMF (5 ml) e agitado a 50°C, durante duas horas. A mistura da reação é resfriada para a temperatura ambiente e uma solução de 3-cloro-6-(2-flúor-4-metil-fenil)piridazina (1,05g, 4,49 mmoles) em DMF (10 ml) é adicionada. A mistura da reação resultante é agitada durante 24 horas, resfriada bruscamente pela adição de H2O e evaporada em alto vácuo, para dar um resíduo laranja. Ao resíduo é adicionada H2O (100 ml) e extraído com EtOAc (3 x 50 ml).Os extratos orgânicos são combinados, lavados com H2O (100 ml), secos sobre MgSCU (anídrico) e evaporados sob pressão reduzida, para dar um sólido amarelo, 0 qual é purificado por cromatografia, proporcionando o produto do título, HPLC ta (min): 4,7; ponto de fusão °C: 128-130; [a]D ta = +37° (0,1%, MeOH).
Etapa 75.1: Preparação de ácido 2-flúor-4-metilabenzeno borônico
A uma mistura de tolueno (160 ml) e THF (40 ml) são adicionados trrisopropila borato (13,56 ml, 58,42 mmoles) e 3-fIúor-427 bromotolueno (10,0 g, 48,69 mmoles). A mistura é resfriada até -40°C e nButillítio (2,5M em hexano) (23,4 ml, 58,42 mmoles) é lentamente adicionado durante uma hora e a mistura é agitada durante uma hora adicional, enquanto a temperatura é mantida a -40°C. O banho de acetona/gelo seco é removido e a mistura da reação é deixada aquecer para -20°C, antes de uma solução 2,5 M de HCI (20 ml) ser adicionada. Quando a mistura atingiu a temperatura ambiente, a camada aquosa é extraída com EtOAc(3 x 50 ml), os extratos orgânicos são combinados, secos sobre MgSO4 (anídrico) e evaporados sob pressão reduzida, para dar um sólido amarelo, o qual é recristalizado de acetonitrila, proporcionando o produto do título.
Etapa 75.2: Preparação de 3-Cloro-6-(2-flúor-4-metil-fenil)- piridazina
A uma solução de 3,6-dicloropiridazina (2,0g, 13,42 mmoles) em 1,4-dioxana (20ml) são adicionados Pd2(dba)3 (0,21 g, 0,2 mmol), P(*Bu)3 (0,122 g, 0,6 mmol) em 1,4-dioxana (1 ml), KF (2,57 g, 44,3 mmoles) e ácido
2-flúor-4-metilbenzenoborônico (etapa 31,1, 2,68 g, 17,45 mmoles). A mistura resultante é aquecida a 120°C durante 48 horas. A mistura da reação é filtrada através de celite e a almofada lavada com EtOAc. O filtrado é lavado com H2O, seco sobre MgSO4 (anídrico) e evaporado sob pressão reduzida, para dar um sólido marrom, o qual é purificado por cromatografia, proporcionando 0 produto do título.
Os compostos seguintes de fórmula I em que Y é
N=N podem ser preparados em analogia ao Exemplo 75:
| + X + 2 | 328,3 | 310,2 | 368,2 | 326,2 | 312,2 | 330,3 | 348,3 , | 312,2 | 324,29 | |
| Ο | ||||||||||
| «co | ||||||||||
| 03 | ||||||||||
| 3 | ||||||||||
| Μ- | ||||||||||
| Φ | ||||||||||
| “Ο | ο | o | o | CM | xf | o | IO | co | co | |
| «o | xf | CO | xt | CM | to | to | co | |||
| Ο | ν~ | t— | T— | T— | V | T-* | V | T— | V— | |
| C | 00 | 00 | 00 | O | CM | 00 | co | Xf | xf | |
| ο | Ο | ο | xf | 00 | 00 | Xf | M— | IO | to | co |
| Ω. | Ο | 5^· | M— | *“ | ||||||
| X | X | X | X | X | X | X | X | X | ||
| Ο | O | O | o | o | o | o | O | O | ||
| Φ | φ | Φ | Φ | Φ | φ | Φ | Φ | φ | ||
| S | ||||||||||
| =£ | SÊ | sS | £ | â? | ||||||
| τ— | to | V | T™ | T” | T“ | T- | T“ | |||
| ο | o | o | o | o | o | o | o | o | ||
| 'x·—'* | >—** | >—«** | S— | |||||||
| (Q | ο | o | 0 | 0 | o | O | o | o | O | |
| ο | (Ο | to | N- | 03 | CD | co | CO | co | ||
| ' η’ | 00 | CM | CO | xf | CO | CM | CM | IO | to | |
| κ°, | + | + | + | + | + | + | + | + | + | |
| C0 | ||||||||||
| 4-» | ||||||||||
| Ο | ||||||||||
| _ι | C | |||||||||
| 0_ | £ | ΙΟ | h- | <33 | CD | co | xf | CO | oo | N. |
| X | ιη | to | co | to | to | xf | Xf | to | to | |
| ro | ||||||||||
| c | ||||||||||
| C0 | £ | w c | ||||||||
| feni | etil- | nila | ||||||||
| d | E | C0 | £ | |||||||
| Ο | p | X •o | CO | |||||||
| >3 0= | O | c Φ | ro | X -o | ro | c | ||||
| CM | 5-trifli | *£— | c | Φ | Φ | c | £ | |||
| Φ | Φ Έ | o CM X | £ X | E | E 2 | £ X | '5. o | |||
| Ε | Φ | d. | o | •o | d. | O | •o | kí | ||
| ,5-di | ¢-. Φ | flúo | o 1 Tt | met | •flúo | diflt | Φ E | isop | ||
| QÍ | xr | xf | CM | co | co | CM | Xf | xf | xf | |
| CM | CM | CM | CM | CM | CM | CM | CM | CM | ||
| X | X | X | X | X | X | X | X | X | ||
| X | ο | o | o | o | o | o | o | o | o | |
| ό | ||||||||||
| φ | ||||||||||
| κ_ φ | Ε | |||||||||
| 03 | 3 | Σ' | Σ' | Σ' | Σ | Σ | Σ | Σ | Σ | Σ |
| φ | σ | *** | ' ' | —' | ||||||
| X | - | co | r- | 00 | 03 | o | — | CM | CO | xf |
| LLI | r- | r- | N- | 1^- | co | co | 00 | oo | 00 |
Exemplo 85:
Os compostos seguintes de fórmula I em que Y é podem ser preparados em analogia ao Exemplo 75: ,
| Ex. | estereo-quím. | X | R |
| 85a | (R) | ch2 | 3,4-dimetil-fenila |
| 85b | (R) | ch2 | 4-metil-fenila |
| 85c | (R) | ch2 | 3-metil-fenila |
| 85d | (R) | ch2 | 2,5-diflúor-4-metil-fenila |
| 85e | (R) | ch2 | 2-flúor-5-metil-fenila |
| 85f | (R) | ch2 | 3-trifluorometóxi-fenila |
| 85g | (3R, 4S) | ligação | 2-flúor-4-metil-fenila |
| 85h | (3S.4R) | ligação | 2-flúor-4-metil-fenila |
| 85i | (R) | ch2 | 2,5-diflúor-fenila |
| 85j | (R) | ch2 | 4-n-propil-fenila |
| 85k | (R) | ch2 | 2-cloro-4-metil-fenila |
| 85I | (R) | ch2 | indan-5-ila |
| 85m | (R) | ch2 | 2-tíenila |
| 85n | (R) | ch2 | 6-tetralinila |
| 85o | (R) | ch2 | 2-naftila |
| 85p | (R) | ch2 | 2-benzotienila |
| 85q | (R) | ch2 | 3-tienila |
| 85r | (R) | ch2 | 1 -naftila |
Exemplo 86: Cápsulas Moles
5000 cápsulas de gelatina mole, cada uma compreendendo, como ingrediente ativo, 0,05 g de um dos compostos de fórmula I mencionados nos Exemplos precedentes, são preparadas como se segue: Composição
Ingrediente ativo 250 g
Lauroglicol 2 litros
Processo de preparação: O ingrediente ativo pulverizado é — suspenso em Lauroglykol® (Ia ura to de propileno glicol, Gattefossé S.A.,
Saint Priest, França) e moído em um pulverizador a úmido, para produzir uma medida de pataícula de cerca de 1 a 3 pm. Porções de 0,419 g da mistura são em seguida introduzidas em cápsulas de gelatina mole, usando uma máquina de preenchimento de cápsulas.
Claims (14)
- REIVINDICAÇÕES1. Derivado de aza-bicicloaiquila, caracterizado pelo fato de que apresenta a fórmula i:em queX é CH2 ou uma ligação simples; Y é um grupo de fórmula eR é fenila, naftila, tetraidronaftila, indanila, tienila, benzotienila, furanila, benzofuranila e isobenzofuranila, o qual em cada caso, pode ser não substituído ou mono-, di- ou trissubstituído com halogênio, ciano, formila, acetila, C1-C3 alcoxicarbonila, N,N-di-(C1-C3 alquila) carbamoíla, fenila, fenóxi, metilendióxi, etilendióxi; ouC1-C4 alquila, C2-C4 alquenila, C2-C4 alquinila ou Ci-C4 alcóxi, cujos radicais podem ser eles mesmos não substituídos ou mono-, di- ou trissubstituídos com halogênio;na forma de sal de adição de ácido ou base livre.
- 2. Derivado de aza-bicicloalquila de fórmula I de acordo com a reivindicação 1, caracterizado pelo fato de queX e Y são como definidos na reivindicação 1; eRé (a) fenila que é não substituído ou mono-, di- ou trissubstituído com halogênio, ciano, metilendióxi;Ci-C4 alquila que é não substituída ou mono-, di- ou trissubstituída com halogênio; ouC-i-C4 alcóxi que é não substituído ou mono-, di- ou trissubstituído com halogênio, (b) naftiia, indanila, tetralinila ou (c) furanila, benzoíuranila, isobenzofuranila, benzotienila ou tienila, na forma de sal de adição de ácido ou base livre.
- 3. Derivado de aza-bicicloalquila de fórmula I de acordo com a reivindicação 1, caracterizado pelo fato de queX e Y são como definidos na reivindicação 1; eRé (a) fenila que é não substituída ou mono-, di- ou trissubstituída com halogênio, ciano, metiíendióxi,C1-C4alquila, que é não substituída ou mono-, di- ou trissubstituída com halogênio, ouC-i-C4alcóxi, que é não substituído ou mono-, di- ou trissubstituído com halogênio, (b) naftiia, ou (c) furanila, benzofuranila, isobenzofuranila, ou tieniia, na forma de sal de adição de ácido ou base livre.
- 4. Derivado de aza-bicicloaiquila de fórmula í de acordo com a reivindicação 1, caracterizado pelo fato de que é selecionado do grupo consistindo em;(R)-3-(6-p-tolil-piridin-3-ilóxi)-1-aza-biciclo[2.2.2]octano (rac.)-3-(5-fenil-piridin-2-ilóxi)-1-aza-biciclo[2.2.2]octano (R)-3-(5-fenil-piridin-2-ilóxi)-1-aza-biciclo[2.2.2]octano (R)-3-(6-feniI-piridin-3-ílóxi)-1-aza-bicicio[2.2.2]octano (R)-3-(6-(3-trifluorometil-fenil)-piridin-3-iióxi)-1-azabiciclo[2.2.2]octano (R)-3-(6-(2-cloro-fenil)-piridin-3-ilóxi)-1-aza-bicicio[2.2.2]octano (R)-3-(6-tiofen-2-il)-piridin-3-ilóxi)-1-aza-biciclo[2.2.2]octano (R)-3-(6-o-toii!)-piridin-3-ilóxi)-1-aza-biciclo[2.2.2]octano (R)-3-(6-m-tolil)-piridin-3-iióxi)-1-aza-bicicio[2.2.2]octano (R)-3-(6-(2,3-dimetil-feni!)-piridin-3-ilóxi)-1-azabicicio[2.2.2]octano (R)-3-(6-(4-etil-fenil)-pirídin-3-ilóxi)-1-aza-bicido[2.2.2]octano (R)-3-(6-(3,4-dimetil-fenil)-piridin-3-ilóxi)-1-azabiciclo[2.2.2]octano (R)-3-(6-(2-cloro-4-metil-fenil)-piridin-3-ilóxi)-1-azabiciclo[2.2.2]octano (R)-3-(6-p-tolil-pí rid in-3-ilóxi)-1 -aza-biciclo[2.2.1 ]heptano (R)-3-(6-(1-naftilil)-piridin-3-ilóxi)-1-aza-biciclo[2.2.2]octano (R)-3-(6-(2-naftil)-piridin-3-ilóxi)-1-aza-biciclo[2.2.2]octano, e (R)-3-(6-(2-cloro-5-metil-fenil)-piridin-3-ilóxi)-1 -azabiciclo[2.2.2]octano, na forma de sal de adição de ácido ou base livre.
- 5. Derivado de aza-bícicloalquila de fórmula I de acordo com a reivindicação 1, caracterizado pelo fato de que é selecionado do grupo consistindo em:(R)-3-(6-p-tolil-piridin-3-ilóxi)~1-aza-biciclo[2.2.2]octano, (R)-3-(6-fenil-piridin-3-i!óxi)-1-aza-bicicio[2.2.2]octano, (R)-3-(6-(4-etil-fenil)-piridÍn-3-ilóxi)-1-aza-biciclo[2.2.2]octano, e (R)-3-(6-(3,4-dimetil-fenil)-piridin-3-ílóxi)-1 -azabiciclo[2.2.2]octano, na forma de sal de adição de ácido ou base livre.
- 6. Derivado de aza-bícicloalquila de fórmula I de acordo com a reivindicação 1, caracterizado pelo fato de que é (R)-3-(6-p-tolil-piridín-3-ilóxi)-1aza-biciclo[2.2.2]octano na forma de sal de adição de ácido ou base livre.
- 7. Derivado de aza-bicicloalquila de fórmula I de acordo com a reivindicação 1, caracterizado pelo fato de que é (R)-3-(6-fenil-piridin-3-ilóxi)1-aza-biciclo[2.2.2]octano na forma de sal de adição de ácido ou base livre.
- 8. Derivado de aza-bicicloalquila de fórmula I de acordo com a reivindicação 1, caracterizado pelo fato de que é (R)-3-(6-(4-etil-fenil)-piridin-3-ilóxi)1-aza-biciclo[2.2.2]octano na forma de sal de adição de ácido ou base livre.
- 9. Derivado de aza-bicicloalquila de fórmula I de acordo com a reivindicação 1, caracterizado pelo fato de que é (R)-3-(6-(3,4-dimetil-feníl)piridin-3-ilóxi)-1-aza-biciclo[2.2.2]octano na forma de sal de adição de ácido ou base livre.
- 10. Processo para a preparação de um derivado de azabicicloalquila de fórmula I, como definido na reivindicação 1, ou um sal do mesmo, caracterizado pelo fato de que compreende a etapa de reagir um composto de fórmula II z-Y-R (II) em que Y e R são como definidos na reivindicação 1 e z é um grupo de partida, com um composto de fórmula III em que X é como definido na reivindicação 1, e recuperar o composto de fórmula I obtido deste modo na forma de sal de adição de ácido ou base livre.
- 11. Derivado de aza-bicicloalquila de acordo com qualquer uma das reivindicações 1 a 9, na forma de base livre ou sal de adição de ácido farmaceuticamente aceitável, caracterizado pelo fato de ser para uso como um fármaco.
- 12. Derivado de aza-bicicloalquila de acordo com qualquer uma das reivindicações 1 a 9, na forma de base livre ou sal de adição de ácido farmaceuticamente aceitável, caracterizado pelo fato de ser para uso na prevenção e no tratamento de distúrbios psicóticos e neurodegenerativos.
- 13. Composição farmacêutica, caracterizada pelo fato de que compreende um derivado de aza-bicicloalquila, como definido em qualquer uma das reivindicações 1 a 9, na forma de base livre ou sal de adição de ácido farmaceuticamente aceitável, em associação com um veículo ou diluente farmacêutico.
- 14. Uso de um derivado de aza-bicicloalquila, como definido em qualquer uma das reivindicações 1 a 9, na forma de base livre ou sal de adição de ácido farmaceuticamente aceitável, caracterizado pelo fato de ser para a fabricação de um medicamento para a prevenção e o tratamento de distúrbios psicóticos e neurodegenerativos.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB0220581.3 | 2002-09-04 | ||
| GB0220581A GB0220581D0 (en) | 2002-09-04 | 2002-09-04 | Organic Compound |
| PCT/EP2003/009772 WO2004022556A1 (en) | 2002-09-04 | 2003-09-03 | Aza-bicycloalkyl ethers and their use as alpha7-nachr agonist |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BR0314325A BR0314325A (pt) | 2005-07-05 |
| BRPI0314325B1 true BRPI0314325B1 (pt) | 2018-04-17 |
| BRPI0314325B8 BRPI0314325B8 (pt) | 2021-07-27 |
Family
ID=9943515
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0314325A BRPI0314325B8 (pt) | 2002-09-04 | 2003-09-03 | derivados de aza-bicicloalquila, seu uso, seu processo de preparação e composição farmacêutica que os compreende |
| BR122014026685-5A BR122014026685B1 (pt) | 2002-09-04 | 2003-09-03 | Derivados de aza-bicicloalquila, seu uso, seu processo de preparação e composição farmacêutica que os compreende |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR122014026685-5A BR122014026685B1 (pt) | 2002-09-04 | 2003-09-03 | Derivados de aza-bicicloalquila, seu uso, seu processo de preparação e composição farmacêutica que os compreende |
Country Status (25)
| Country | Link |
|---|---|
| US (8) | US20060167002A1 (pt) |
| EP (3) | EP2308876A1 (pt) |
| JP (2) | JP4348422B2 (pt) |
| KR (2) | KR20070058027A (pt) |
| CN (1) | CN1325493C (pt) |
| AT (1) | ATE448225T1 (pt) |
| AU (1) | AU2003260486C1 (pt) |
| BR (2) | BRPI0314325B8 (pt) |
| CA (1) | CA2495685C (pt) |
| CY (1) | CY1109765T1 (pt) |
| DE (1) | DE60330015D1 (pt) |
| DK (1) | DK1537104T3 (pt) |
| EC (1) | ECSP055621A (pt) |
| ES (1) | ES2336099T3 (pt) |
| GB (1) | GB0220581D0 (pt) |
| IL (2) | IL166918A (pt) |
| MX (1) | MXPA05002546A (pt) |
| NO (1) | NO331556B1 (pt) |
| NZ (1) | NZ538534A (pt) |
| PL (1) | PL209425B1 (pt) |
| PT (1) | PT1537104E (pt) |
| RU (1) | RU2352569C2 (pt) |
| SI (1) | SI1537104T1 (pt) |
| WO (1) | WO2004022556A1 (pt) |
| ZA (1) | ZA200500816B (pt) |
Families Citing this family (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6262265A (ja) * | 1985-09-13 | 1987-03-18 | Hitachi Ltd | 復水器自動検査補修システム |
| DE10164139A1 (de) | 2001-12-27 | 2003-07-10 | Bayer Ag | 2-Heteroarylcarbonsäureamide |
| GB0220581D0 (en) | 2002-09-04 | 2002-10-09 | Novartis Ag | Organic Compound |
| DE602004031124D1 (de) | 2003-08-13 | 2011-03-03 | Neurosearch As | Neue chinuklidinderivative und deren pharmazeutische verwendung |
| US20050137398A1 (en) * | 2003-12-22 | 2005-06-23 | Jianguo Ji | 3-Quinuclidinyl heteroatom bridged biaryl derivatives |
| US7241773B2 (en) | 2003-12-22 | 2007-07-10 | Abbott Laboratories | 3-quinuclidinyl heteroatom bridged biaryl derivatives |
| US20050137203A1 (en) * | 2003-12-22 | 2005-06-23 | Jianguo Ji | 3-quinuclidinyl amino-substituted biaryl derivatives |
| EP1824848A1 (en) * | 2004-12-10 | 2007-08-29 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US20050245531A1 (en) * | 2003-12-22 | 2005-11-03 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US7309699B2 (en) | 2003-12-22 | 2007-12-18 | Abbott Laboratories | 3-Quinuclidinyl amino-substituted biaryl derivatives |
| US7655657B2 (en) | 2003-12-22 | 2010-02-02 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US7160876B2 (en) | 2003-12-22 | 2007-01-09 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US20050137217A1 (en) * | 2003-12-22 | 2005-06-23 | Jianguo Ji | Spirocyclic quinuclidinic ether derivatives |
| PE20060437A1 (es) | 2004-06-18 | 2006-06-08 | Novartis Ag | COMPUESTOS AZA-BICICLONONANOS COMO LIGANDOS COLINERGICOS DE nAChR |
| GB0415746D0 (en) * | 2004-07-14 | 2004-08-18 | Novartis Ag | Organic compounds |
| AU2005286648A1 (en) | 2004-09-20 | 2006-03-30 | Xenon Pharmaceuticals Inc. | Heterocyclic derivatives and their use as stearoyl-CoA desaturase inhibitors |
| CA2580857A1 (en) | 2004-09-20 | 2006-09-28 | Xenon Pharmaceuticals Inc. | Heterocyclic derivatives and their use as stearoyl-coa desaturase inhibitors |
| US7829712B2 (en) * | 2004-09-20 | 2010-11-09 | Xenon Pharmaceuticals Inc. | Pyridazine derivatives for inhibiting human stearoyl-CoA-desaturase |
| GB0424564D0 (en) * | 2004-11-05 | 2004-12-08 | Novartis Ag | Organic compounds |
| AU2006343359A1 (en) | 2005-06-03 | 2007-11-15 | Xenon Pharmaceuticals Inc. | Aminothiazole derivatives as human stearoyl-coa desaturase inhibitors |
| GB0521508D0 (en) * | 2005-10-21 | 2005-11-30 | Novartis Ag | Organic compounds |
| GB0525672D0 (en) | 2005-12-16 | 2006-01-25 | Novartis Ag | Organic compounds |
| GB0525673D0 (en) * | 2005-12-16 | 2006-01-25 | Novartis Ag | Organic compounds |
| JP2009526777A (ja) | 2006-02-14 | 2009-07-23 | ノイロサーチ アクティーゼルスカブ | ニコチン性アセチルコリン受容体作用薬としての3,9−ジアザビシクロ(3.3.1)ノナ−3−イル−アリールメタノン誘導体 |
| US20100227869A1 (en) * | 2006-02-16 | 2010-09-09 | Dan Peters | Enantiopure quinuclidinyloxy pyridazines and their use as nicotinic acetylcholine receptor ligands |
| ES2528797T3 (es) | 2006-08-21 | 2015-02-12 | Genentech, Inc. | Compuestos de aza-benzotiofenilo y métodos de uso |
| RU2476220C2 (ru) * | 2007-08-02 | 2013-02-27 | Таргасепт, Инк. | (2s,3r)-n-(2-((3-пиридинил)метил)-1-азабицикло[2.2.2]окт-3-ил)бензофуран-2-карбоксамид, новые солевые формы и способы их применения |
| US8383657B2 (en) | 2007-12-21 | 2013-02-26 | Abbott Laboratories | Thiazolylidine urea and amide derivatives and methods of use thereof |
| MX2010014565A (es) | 2008-07-01 | 2011-03-04 | Genentech Inc | Isoindolona y metodos de uso. |
| RU2509078C2 (ru) | 2008-07-01 | 2014-03-10 | Дженентек, Инк. | Бициклические гетероциклы в качестве ингибиторов киназы мек |
| KR20180011888A (ko) | 2008-11-19 | 2018-02-02 | 포럼 파마슈티칼즈 인크. | (r)-7-클로로-n-(퀴누클리딘-3-일)벤조[b]티오펜-2-카르복사미드 및 그 약학적으로 허용가능한 염을 이용한 인지 장애의 치료 |
| PE20120324A1 (es) * | 2009-05-11 | 2012-04-17 | Envivo Pharmaceuticals Inc | Combinacion que comprende (r)-7-cloro-n-(quinuclidin-3-il)benzo[b]tiofeno-2-carboxamida y donezepilo como moduladora de trastornos cognitivos |
| CN102573842A (zh) * | 2009-07-23 | 2012-07-11 | 诺瓦提斯公司 | 氮杂双环烷基衍生物或吡咯烷-2-酮衍生物的用途 |
| JO3250B1 (ar) | 2009-09-22 | 2018-09-16 | Novartis Ag | إستعمال منشطات مستقبل نيكوتينيك أسيتيل كولين ألفا 7 |
| EP2488520B1 (en) | 2009-10-13 | 2015-09-02 | Merck Sharp & Dohme B.V. | Condensed azine-derivatives for the treatment of diseases related to the acetylcholine receptor |
| AR081402A1 (es) | 2010-05-17 | 2012-08-29 | Envivo Pharmaceuticals Inc | Una forma cristalina de clorhidrato de (r)-7-cloro-n-(quinuclidin-3-il) benzo(b)tiofeno-2-carboxamida monohidrato |
| KR20140003580A (ko) * | 2011-01-27 | 2014-01-09 | 노파르티스 아게 | 니코틴성 아세틸콜린 수용체 알파 7 활성화제의 용도 |
| WO2012127393A1 (en) | 2011-03-18 | 2012-09-27 | Novartis Ag | COMBINATIONS OF ALPHA 7 NICOTINIC ACETYLCHOLINE RECEPTOR ACTIVATORS AND mGluR5 ANTAGONISTS FOR USE IN DOPAMINE INDUCED DYSKINESIA IN PARKINSON'S DISEASE |
| TWI589576B (zh) | 2011-07-15 | 2017-07-01 | 諾華公司 | 氮雜-雙環二芳基醚之鹽類及製造彼等或其前驅物之方法 |
| JP6162705B2 (ja) * | 2011-10-20 | 2017-07-12 | ノバルティス アーゲー | アルファ7ニコチン性アセチルコリン受容体活性化剤による処置に対する応答性を予測するバイオマーカー |
| CA2872005A1 (en) | 2012-05-08 | 2013-11-14 | Forum Pharmaceuticals, Inc. | Methods of maintaining, treating or improving cognitive function |
| KR102043309B1 (ko) * | 2012-12-11 | 2019-11-11 | 노파르티스 아게 | 알파 7 니코틴성 아세틸콜린 수용체 활성화제 치료에 대한 반응성의 예측 바이오마커 |
| EP2742940B1 (en) * | 2012-12-13 | 2017-07-26 | IP Gesellschaft für Management mbH | Fumarate salt of (R)-3-(6-(4-methylphenyl)-pyridin-3-yloxy)-l-aza-bicyclo-[2.2.2]octane for adminstration once daily, twice daily or thrice daily |
| BR112015016992A8 (pt) * | 2013-01-15 | 2018-01-23 | Novartis Ag | uso de agonistas do receptor alfa 7 nicotínico de acetilcolina |
| EP2945633B1 (en) * | 2013-01-15 | 2021-06-30 | Novartis AG | Use of alpha 7 nicotinic acetylcholine receptor agonists |
| US20150313884A1 (en) | 2013-01-15 | 2015-11-05 | Novartis Ag | Use of alpha 7 nicotinic acetylcholine receptor agonists |
| CN105263492B (zh) * | 2013-01-15 | 2018-04-10 | 诺华有限公司 | α7烟碱型乙酰胆碱受体激动剂在治疗发作性睡病中的应用 |
| GB201301626D0 (en) | 2013-01-30 | 2013-03-13 | Dignity Sciences Ltd | Composition comprising 15-OHEPA and methods of using the same |
| UY38687A (es) | 2019-05-17 | 2023-05-15 | Novartis Ag | Inhibidores del inflamasoma nlrp3, composiciones, combinaciones de los mismos y métodos para su uso |
| US20210315851A1 (en) | 2020-04-03 | 2021-10-14 | Afimmune Limited | Compositions comprising 15-hepe and methods of treating or preventing hematologic disorders, and/or related diseases |
| CN116761604A (zh) * | 2020-11-25 | 2023-09-15 | 万达制药公司 | 用α-7烟碱型乙酰胆碱受体激动剂治疗当众讲话焦虑 |
| CA3199760A1 (en) * | 2020-11-25 | 2022-06-02 | Vanda Pharmaceuticals Inc. | Treatment of public speaking anxiety with an alpha-7 nicotinic acetylcholine receptor agonist |
| KR20250005196A (ko) * | 2022-05-05 | 2025-01-09 | 필립모리스 프로덕츠 에스.에이. | 니코틴 아세틸콜린 수용체 리간드 |
| UY40374A (es) | 2022-08-03 | 2024-02-15 | Novartis Ag | Inhibidores de inflamasoma nlrp3 |
| WO2025188847A1 (en) * | 2024-03-07 | 2025-09-12 | The Texas A&M University System | Method for treating epilepsy |
Family Cites Families (95)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB809574A (en) | 1956-01-26 | 1959-02-25 | Gasaccumulator Svenska Ab | Improvements in or relating to electrical signal light systems |
| US3539573A (en) | 1967-03-22 | 1970-11-10 | Jean Schmutz | 11-basic substituted dibenzodiazepines and dibenzothiazepines |
| BE759371A (fr) | 1969-11-24 | 1971-05-24 | Bristol Myers Co | Azaspirodecanediones heterocycliques et procedes pour leur preparation |
| DE2139107A1 (de) | 1971-08-04 | 1973-02-15 | Merck Patent Gmbh | Heterocyclisch substituierte adenosinverbindungen |
| ZA848275B (en) | 1983-12-28 | 1985-08-28 | Degussa | New piridine-2-ethers or pyridine-2-thioethers having a nitrogen-containing cycloaliphatic ring |
| US4605652A (en) | 1985-02-04 | 1986-08-12 | A. H. Robins Company, Inc. | Method of enhancing memory or correcting memory deficiency with arylamido (and arylthioamido)-azabicycloalkanes |
| ES2053451T3 (es) | 1986-01-07 | 1994-08-01 | Beecham Group Plc | Un procedimiento para la preparacion de un compuesto que tiene propiedades farmacologicas utiles. |
| KR880007433A (ko) | 1986-12-22 | 1988-08-27 | 메리 앤 터커 | 3-아릴옥시-3-치환된 프로판아민 |
| EP0287356B1 (en) | 1987-04-15 | 1996-01-24 | Beecham Group Plc | Bridgehead substituted azabicyclic derivatives |
| GB8718445D0 (en) | 1987-08-04 | 1987-09-09 | Wyeth John & Brother Ltd | Pyridyl-ethers |
| CA1307790C (en) | 1987-08-04 | 1992-09-22 | Ian Anthony Cliffe | Ethers |
| US5006528A (en) | 1988-10-31 | 1991-04-09 | Otsuka Pharmaceutical Co., Ltd. | Carbostyril derivatives |
| DE3839385A1 (de) | 1988-11-22 | 1990-05-23 | Boehringer Ingelheim Kg | Neue quinuclidine, ihre herstellung als arzneimittel und verfahren zu ihrer herstellung |
| GB8829079D0 (en) | 1988-12-13 | 1989-01-25 | Beecham Group Plc | Novel compounds |
| CA2002182C (en) | 1989-11-03 | 2000-06-13 | Richard J. Wurtman | Compositions for treating the premenstrual or late luteal phase syndrome and methods for their use |
| DE4116582A1 (de) | 1990-05-19 | 1991-11-21 | Boehringer Ingelheim Kg | Bicyclische 1-aza-cycloalkane |
| YU84791A (sh) | 1990-05-19 | 1994-06-10 | Boehringer Ingelheim Kg. | Biciklicni 1-aza-cikloalkalni |
| US5589477A (en) | 1990-08-31 | 1996-12-31 | Nippon Shinyaku Company, Limited | Pyrimidine derivatives and drugs |
| JP3087763B2 (ja) | 1990-11-30 | 2000-09-11 | 三井化学株式会社 | 新規な複素環式化合物およびそれを含有する医薬組成物 |
| US5260303A (en) | 1991-03-07 | 1993-11-09 | G. D. Searle & Co. | Imidazopyridines as serotonergic 5-HT3 antagonists |
| US5385912A (en) | 1991-03-08 | 1995-01-31 | Rhone-Poulenc Rorer Pharmaceuticals Inc. | Multicyclic tertiary amine polyaromatic squalene synthase inhibitors |
| CA2105655A1 (en) | 1991-03-08 | 1992-09-09 | Kent Neuenschwander | Multicyclic tertiary amine polyaromatic squalene synthetase inhibitors |
| AU657552B2 (en) * | 1991-05-31 | 1995-03-16 | Pfizer Inc. | Quinuclidine as substance P antagonists |
| JPH05310732A (ja) | 1992-03-12 | 1993-11-22 | Mitsubishi Kasei Corp | シンノリン−3−カルボン酸誘導体 |
| JPH06508377A (ja) | 1992-04-10 | 1994-09-22 | ゼネカ リミテッド | ヘテロ環式化合物 |
| IL107184A (en) | 1992-10-09 | 1997-08-14 | Abbott Lab | Heterocyclic ether compounds that enhance cognitive function |
| AU7394394A (en) | 1992-10-13 | 1995-12-05 | Rhone-Poulenc Rorer Pharmaceuticals Inc. | 3-hydroxyquinuclidin-3-ylphenylquinolines as squalene synthase inhibitors |
| JPH06293768A (ja) | 1993-02-12 | 1994-10-21 | Sankyo Co Ltd | イソオキサゾールオキシ誘導体 |
| WO1994018201A1 (fr) | 1993-02-12 | 1994-08-18 | Sankyo Company, Limited | Derive d'isoxazoleoxy |
| JP3235913B2 (ja) | 1993-07-30 | 2001-12-04 | エーザイ株式会社 | アミノ安息香酸誘導体 |
| US5998404A (en) | 1994-10-24 | 1999-12-07 | Eli Lilly And Company | Heterocyclic compounds and their use |
| JPH11512443A (ja) | 1995-09-22 | 1999-10-26 | ノボ ノルディスク アクティーゼルスカブ | 新規な置換アザ環式またはアザ二環式化合物 |
| SE9600683D0 (sv) | 1996-02-23 | 1996-02-23 | Astra Ab | Azabicyclic esters of carbamic acids useful in therapy |
| JP2002500652A (ja) | 1997-05-30 | 2002-01-08 | ニューロサーアチ・アクティーゼルスカブ | スピロ−キヌクリジン誘導体、その製造方法及びその使用方法 |
| AR013184A1 (es) | 1997-07-18 | 2000-12-13 | Astrazeneca Ab | Aminas heterociclicas espiroazobiciclicas, composicion farmaceutica, uso de dichas aminas para preparar medicamentos y metodo de tratamiento o profilaxis |
| US6953855B2 (en) | 1998-12-11 | 2005-10-11 | Targacept, Inc. | 3-substituted-2(arylalkyl)-1-azabicycloalkanes and methods of use thereof |
| US6432975B1 (en) | 1998-12-11 | 2002-08-13 | Targacept, Inc. | Pharmaceutical compositions and methods for use |
| SE9900100D0 (sv) | 1999-01-15 | 1999-01-15 | Astra Ab | New compounds |
| ES2313900T3 (es) | 1999-07-28 | 2009-03-16 | The Board Of Trustees Of The Leland Stanford Junior University | Nicotina en angiogenesis y vasculogenesis terapeutica. |
| SE9903760D0 (sv) | 1999-10-18 | 1999-10-18 | Astra Ab | New compounds |
| SE9904176D0 (sv) | 1999-11-18 | 1999-11-18 | Astra Ab | New use |
| SE0000540D0 (sv) * | 2000-02-18 | 2000-02-18 | Astrazeneca Ab | New compounds |
| WO2001066546A1 (en) | 2000-03-09 | 2001-09-13 | Mitsubishi Pharma Corporation | Spiro compounds, process for preparing the same and use thereof as drugs |
| GB0010955D0 (en) | 2000-05-05 | 2000-06-28 | Novartis Ag | Organic compounds |
| JP4616971B2 (ja) | 2000-07-18 | 2011-01-19 | 田辺三菱製薬株式会社 | 1−アザビシクロアルカン化合物およびその医薬用途 |
| US6479510B2 (en) | 2000-08-18 | 2002-11-12 | Pharmacia & Upjohn Company | Quinuclidine-substituted aryl compounds for treatment of disease |
| US6599916B2 (en) | 2000-08-21 | 2003-07-29 | Pharmacia & Upjohn Company | Quinuclidine-substituted heteroaryl moieties for treatment of disease |
| GB0021885D0 (en) | 2000-09-06 | 2000-10-18 | Fujisawa Pharmaceutical Co | New use |
| PE20021019A1 (es) | 2001-04-19 | 2002-11-13 | Upjohn Co | Grupos azabiciclicos sustituidos |
| AR036040A1 (es) | 2001-06-12 | 2004-08-04 | Upjohn Co | Compuestos de heteroarilo multiciclicos sustituidos con quinuclidinas y composiciones farmaceuticas que los contienen |
| BR0213760A (pt) | 2001-10-26 | 2004-10-19 | Upjohn Co | Composto, composição farmacêutica, uso do composto e método para tratamento de doença ou condição |
| DE10156719A1 (de) | 2001-11-19 | 2003-05-28 | Bayer Ag | Heteroarylcarbonsäureamide |
| DE10162375A1 (de) | 2001-12-19 | 2003-07-10 | Bayer Ag | Bicyclische N-Aryl-amide |
| CA2475773A1 (en) | 2002-02-20 | 2003-09-04 | Pharmacia & Upjohn Company | Azabicyclic compounds with alfa7 nicotinic acetylcholine receptor activity |
| DE10211415A1 (de) | 2002-03-15 | 2003-09-25 | Bayer Ag | Bicyclische N-Biarylamide |
| DE10211416A1 (de) | 2002-03-15 | 2003-09-25 | Bayer Ag | Essig- und Propionsäureamide |
| DE10234424A1 (de) | 2002-07-29 | 2004-02-12 | Bayer Ag | Benzothiophen-, Benzofuran- und Indolharnstoffe |
| AU2003250322B2 (en) * | 2002-08-14 | 2010-01-21 | Neurosearch A/S | Novel quinuclidine derivatives and their use |
| GB0220581D0 (en) * | 2002-09-04 | 2002-10-09 | Novartis Ag | Organic Compound |
| MXPA05003317A (es) | 2002-09-25 | 2005-07-05 | Memory Pharm Corp | Indazoles, benzotiazoles y benzoisotiazoles asi como preparacion y usos de los mismos. |
| WO2004039321A2 (en) | 2002-10-29 | 2004-05-13 | Miicro, Inc. | Combinative nicotinic/d1 agonism therapy for the treatment of alzheimer’s disease |
| WO2004039366A1 (en) | 2002-11-01 | 2004-05-13 | Pharmacia & Upjohn Company Llc | Nicotinic acetylcholine agonists in the treatment of glaucoma and retinal neuropathy |
| WO2004039815A2 (en) | 2002-11-01 | 2004-05-13 | Pharmacia & Upjohn Company Llc | Compounds having both alpha7 nachr agonist and 5ht antagonist activity for treatment of cns diseases |
| DK1562945T3 (da) | 2002-11-11 | 2007-03-05 | Neurosearch As | Hidtil ukendte diazebicykliske biarylderivater |
| KR20050085535A (ko) | 2002-12-11 | 2005-08-29 | 파마시아 앤드 업존 캄파니 엘엘씨 | 알파 7 니코틴성 아세틸콜린 수용체 아고니스트와 다른화합물의 조합물을 사용한 질환의 치료 방법 |
| WO2004064836A2 (en) | 2003-01-22 | 2004-08-05 | Pharmacia & Upjohn Company Llc | Treatment of diseases with alpha-7 nach receptor full agonists |
| WO2005013910A2 (en) | 2003-08-07 | 2005-02-17 | University Of South Florida | Cholinergic modulation of microglial activation via alpha-7 nicotinic receptors |
| JP4226981B2 (ja) | 2003-09-24 | 2009-02-18 | 三井金属鉱業株式会社 | プリント配線板の製造方法及びその製造方法で得られたプリント配線板 |
| US20050137203A1 (en) | 2003-12-22 | 2005-06-23 | Jianguo Ji | 3-quinuclidinyl amino-substituted biaryl derivatives |
| US20050137398A1 (en) | 2003-12-22 | 2005-06-23 | Jianguo Ji | 3-Quinuclidinyl heteroatom bridged biaryl derivatives |
| EP1824848A1 (en) | 2004-12-10 | 2007-08-29 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US20050137204A1 (en) | 2003-12-22 | 2005-06-23 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US20070060588A1 (en) | 2003-12-22 | 2007-03-15 | Jianguo Ji | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US7655657B2 (en) | 2003-12-22 | 2010-02-02 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US20050245531A1 (en) | 2003-12-22 | 2005-11-03 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| US7241773B2 (en) | 2003-12-22 | 2007-07-10 | Abbott Laboratories | 3-quinuclidinyl heteroatom bridged biaryl derivatives |
| US7160876B2 (en) | 2003-12-22 | 2007-01-09 | Abbott Laboratories | Fused bicycloheterocycle substituted quinuclidine derivatives |
| WO2005063296A2 (en) | 2003-12-23 | 2005-07-14 | Pfizer Products Inc. | Therapeutic combination for cognition enhancement and psychotic disorders |
| US7875624B2 (en) | 2004-02-20 | 2011-01-25 | Novartis Vaccines And Diagnostics, Inc. | Modulating and measuring cellular adhesion |
| KR20070030196A (ko) | 2004-04-13 | 2007-03-15 | 이카겐, 인코포레이티드 | 칼륨 이온 채널 조절제로서의 폴리시클릭 피리딘 |
| JP2007538046A (ja) | 2004-05-19 | 2007-12-27 | ノイロサーチ アクティーゼルスカブ | 新規なアザビシクロアリール誘導体 |
| PE20060437A1 (es) | 2004-06-18 | 2006-06-08 | Novartis Ag | COMPUESTOS AZA-BICICLONONANOS COMO LIGANDOS COLINERGICOS DE nAChR |
| GB0415746D0 (en) | 2004-07-14 | 2004-08-18 | Novartis Ag | Organic compounds |
| EP1802616B1 (en) | 2004-10-15 | 2011-01-12 | NeuroSearch A/S | Novel azabicyclic aryl derivatives and their medical use |
| GB0424564D0 (en) | 2004-11-05 | 2004-12-08 | Novartis Ag | Organic compounds |
| ATE481407T1 (de) | 2005-02-16 | 2010-10-15 | Neurosearch As | Neue diazabicyclische arylderivate und medizinische verwendung dafür |
| EP1863485A2 (en) | 2005-03-18 | 2007-12-12 | Abbott Laboratories | Alpha7 neuronal nicotinic receptor ligand and antipsychotic compositions |
| WO2006113650A1 (en) | 2005-04-18 | 2006-10-26 | Khan Saeed R | Design and synthesis of novel tubulin polymerization inhibitors: bonzoylphenyluria (bpu) sulfur analogs |
| FR2884822B1 (fr) | 2005-04-22 | 2007-06-29 | Aventis Pharma Sa | Derives de triazines, leur preparation et leur application en therapeutique |
| GB0508314D0 (en) | 2005-04-25 | 2005-06-01 | Novartis Ag | Organic compounds |
| MX2007016180A (es) | 2005-06-14 | 2008-03-07 | Schering Corp | Inhibidores de aspartil proteasas. |
| GB0521508D0 (en) | 2005-10-21 | 2005-11-30 | Novartis Ag | Organic compounds |
| GB0525672D0 (en) | 2005-12-16 | 2006-01-25 | Novartis Ag | Organic compounds |
| GB0525673D0 (en) | 2005-12-16 | 2006-01-25 | Novartis Ag | Organic compounds |
| TW200813067A (en) | 2006-05-17 | 2008-03-16 | Astrazeneca Ab | Nicotinic acetylcholine receptor ligands |
-
2002
- 2002-09-04 GB GB0220581A patent/GB0220581D0/en not_active Ceased
-
2003
- 2003-09-03 AT AT03793791T patent/ATE448225T1/de active
- 2003-09-03 NZ NZ538534A patent/NZ538534A/en not_active IP Right Cessation
- 2003-09-03 JP JP2004533455A patent/JP4348422B2/ja not_active Expired - Lifetime
- 2003-09-03 MX MXPA05002546A patent/MXPA05002546A/es active IP Right Grant
- 2003-09-03 US US10/526,759 patent/US20060167002A1/en not_active Abandoned
- 2003-09-03 PL PL374013A patent/PL209425B1/pl unknown
- 2003-09-03 EP EP20100184187 patent/EP2308876A1/en not_active Withdrawn
- 2003-09-03 BR BRPI0314325A patent/BRPI0314325B8/pt not_active IP Right Cessation
- 2003-09-03 AU AU2003260486A patent/AU2003260486C1/en not_active Expired
- 2003-09-03 CN CNB038207303A patent/CN1325493C/zh not_active Expired - Lifetime
- 2003-09-03 KR KR1020077011698A patent/KR20070058027A/ko not_active Ceased
- 2003-09-03 EP EP20030793791 patent/EP1537104B1/en not_active Expired - Lifetime
- 2003-09-03 EP EP20090164576 patent/EP2100893A1/en not_active Withdrawn
- 2003-09-03 RU RU2005109913A patent/RU2352569C2/ru active
- 2003-09-03 BR BR122014026685-5A patent/BR122014026685B1/pt not_active IP Right Cessation
- 2003-09-03 CA CA 2495685 patent/CA2495685C/en not_active Expired - Lifetime
- 2003-09-03 DK DK03793791T patent/DK1537104T3/da active
- 2003-09-03 SI SI200331746T patent/SI1537104T1/sl unknown
- 2003-09-03 PT PT03793791T patent/PT1537104E/pt unknown
- 2003-09-03 ES ES03793791T patent/ES2336099T3/es not_active Expired - Lifetime
- 2003-09-03 DE DE60330015T patent/DE60330015D1/de not_active Expired - Lifetime
- 2003-09-03 WO PCT/EP2003/009772 patent/WO2004022556A1/en not_active Ceased
- 2003-09-03 KR KR20057003665A patent/KR100808324B1/ko not_active Expired - Lifetime
-
2005
- 2005-01-27 ZA ZA200500816A patent/ZA200500816B/xx unknown
- 2005-02-15 IL IL16691805A patent/IL166918A/en active IP Right Grant
- 2005-02-22 EC ECSP055621 patent/ECSP055621A/es unknown
- 2005-04-01 NO NO20051626A patent/NO331556B1/no not_active IP Right Cessation
-
2007
- 2007-06-26 US US11/823,312 patent/US7579362B2/en not_active Expired - Lifetime
-
2008
- 2008-10-31 US US12/262,896 patent/US8236803B2/en not_active Expired - Fee Related
-
2009
- 2009-02-19 JP JP2009036918A patent/JP5124714B2/ja not_active Expired - Fee Related
-
2010
- 2010-02-10 CY CY101100129T patent/CY1109765T1/el unknown
-
2012
- 2012-05-02 US US13/462,187 patent/US9012451B2/en not_active Expired - Lifetime
-
2013
- 2013-02-28 IL IL225002A patent/IL225002A/en active IP Right Grant
-
2015
- 2015-03-10 US US14/643,275 patent/US9567343B2/en not_active Expired - Fee Related
-
2017
- 2017-01-04 US US15/398,427 patent/US9849117B2/en not_active Expired - Fee Related
- 2017-11-21 US US15/819,535 patent/US20180078536A1/en not_active Abandoned
-
2018
- 2018-11-15 US US16/191,693 patent/US20190083474A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0314325B1 (pt) | Derivados de aza-bicicloalquila, seu uso, seu processo de preparação e composição farmacêutica que os compreende | |
| RU2402551C2 (ru) | 3-(ГЕТЕРОАРИЛОКСИ)-2-АЛКИЛ-1-АЗАБИЦИКЛОАЛКИЛЬНЫЕ ПРОИЗВОДНЫЕ, КАК ЛИГАНДЫ АЛЬФА-7-nAChR (НИКОТИНОВЫХ АЦЕТИЛХОЛИНОВЫХ РЕЦЕПТОРОВ), ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | |
| KR101343654B1 (ko) | 1-아자-비시클로〔3.3.1〕노난 | |
| AU2006303453B2 (en) | Novel 1-aza bicycloalkyl derivatives for the treatment of psychotic and neurodegenerative disorders | |
| TW202003496A (zh) | 一種新穎磷酸肌醇3 - 激酶抑制劑及其製備方法和用途 | |
| HK1077822B (en) | Aza-bicycloalkyl ethers and their use as alpha7-nachr agonist | |
| HK1078868B (en) | Aza-bicycloalkyl ethers and their use as alpha7-nachr agonists |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07F | Notification of approval that there is no relation to art. 229 of lpi (pipeline patents) [chapter 7.6 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] | ||
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 03/09/2003, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 22A ANUIDADE. |
|
| B24J | Lapse because of non-payment of annual fees (definitively: art 78 iv lpi, resolution 113/2013 art. 12) |
Free format text: EM VIRTUDE DA EXTINCAO PUBLICADA NA RPI 2846 DE 22-07-2025 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDA A EXTINCAO DA PATENTE E SEUS CERTIFICADOS, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |