Relatório de Técnica Relacionada
[0001] lnterleucina-6 (IL-6) é uma citocina pleiotrópica produzida por células imunes e não imunes que desempenham um papel crucial na regulação da resposta imune, reações de fase aguda, e hemato- poiese. Ela liga-se ao IL-6R de ligação de membrana celular e solúvel (cadeia a) formando um complexo binário e este complexo é capaz de interagir com gp130 de ligação de membrana celular (cadeia β), induz formação de complexo de sinalização compreendendo dois de cada de IL-6, IL-6R, egp130.
[0002] Anticorpos para hlL-6R são descritos na patentes US 5.670.373, 5.795.965, 5.817.790, 6.410.691, e EP 409 607B1. Métodos terapêuticos são descritos na patentes US 5.888.510 e 6.723.319.
Breve Sumário da Invenção
[0003] Em um primeiro aspecto, a invenção fornece anticorpos humanos, preferivelmente anticorpos humanos recombinantes, que especificamente ligam-se ao receptor de interleucina-6 humana (hlL- 6R). Estes anticorpos são caracterizados por ligação ao hlL-6R com alta afinidade e cinéticos de dissociação lenta e pela capacidade de neutralizar a atividade de IL-6. Os anticorpos podem ser de tamanho natural (por exemplo, um anticorpo IgGI ou lgG4) ou podem compreender apenas uma porção de ligação ao antígeno (por exemplo, um fragmento Fab, F(ab')2 ou scFv), e podem ser modificados para executar a funcionalidade, por exemplo, para eliminar as funções efetoras residuais (Reddy e outro. (2000) J. Immunol. 164:1925-1933). Em uma modalidade preferida, a invenção fornece um anticorpo ou fragmento de ligação ao antígeno deste, que se liga ao receptor de IL-6 humano (SEQ ID NO: 1) com um KD de cerca de 500 pM ou menos, como medido por ressonância de plasmon de superfície. Em uma modalidade mais específica, o anticorpo ou fragmento de ligação ao antígeno tem um KD de menos do que 300 pM, ou menos do que 200 pM, ou ainda menos do que 100 pM. Em várias modalidades, o anticorpo ou fragmento de ligação ao antígeno deste bloqueia a atividade de hlL-6 com um IC50 de 250 pM ou menos, como medido por bioensaio de luciferase. Em modalidades mais específicas, o anticorpo ou fragmento de ligação ao antígeno deste exibe um IC50 de 150 pM ou menos.
[0004] Em aspectos relacionados, o anticorpo ou fragmento de ligação ao antígeno da invenção liga-se ao hIL- 6R com uma afinidade de pelo menos 2 vezes maior do que ele liga-se ao IL-6R de macaco. Em modalidades mais preferidas, 0 anticorpo ou fragmento de ligação ao antígeno liga-se à proteína de hlL-6R (SEQ ID NO: 1) com uma afinidade que é até cerca de 3 vezes maior relativa a sua ligação ao IL-6R de macaco (Domínio extracelular fascicular de Macaca mostrado em SEQ ID NO: 251).
[0005] Em uma modalidade, 0 anticorpo ou porção de ligação ao antígeno do anticorpo da invenção compreende uma região variável de cadeia pesada (HCVR) selecionada do grupo consistindo em SEQ ID NO: 3, 227, 19, 231, 35, 51, 67, 83, 99, 115, 131, 147, 239, 241, 163, 179, 235, 195 e 211, ou sequência substancialmente similar desta. Em uma modalidade mais específica, o anticorpo ou fragmento de ligação ao antígeno deste também compreende uma região variável de cadeia leve (LCVR) selecionada do grupo consistindo em SEQ ID NO: 11, 229, 27, 233, 43, 59, 75, 91, 107, 123, 139, 155, 171, 187, 237, 203 e 219, ou uma sequência substancialmente similar destas. Em modalidades específicas, o anticorpo ou fragmento de ligação ao antígeno deste compreende pares de HCVR/LCVR selecionados do grupo consistindo em SEQ ID NO: 3/11 ; 227/229; 19/27; 231/233; 35/43; 51/59; 67/75; 83/91 ; 99/107; 115/123; 131/139; 147/155; 239/155; 241/155; 163/171 ; 179/187; 235/237; 195/203; e 211/219, ou sequências substancialmente similares destas.
[0006] Em um segundo aspecto, a invenção fornece moléculas de ácido nucléico isoladas que codificam um anticorpo ou fragmento de ligação ao antígeno de um anticorpo da invenção. Em uma modalidade, a molécula de ácido nucléico da invenção codifica um anticorpo ou fragmento deste compreendendo um HCVR como descrito acima. Em modalidades específicas, a molécula de ácido nucléico que codifica o HCVR é selecionada do grupo consistindo em SEQ ID NO: 2, 226, 18, 230, 34, 50, 66, 82, 98, 114, 130, 146, 238, 240, 162, 178, 234, 194 e 210, ou uma sequência substancialmente idêntica destas. Em um aspecto relacionado, a invenção fornece uma molécula de ácido nucléico isolada que codifica um LCVR como descrito acima. Em modalidades específicas, a molécula de ácido nucléico que codifica o LCVR é uma sequência de nucleotídeo selecionada do grupo consistindo em SEQ ID NO: 10, 228, 26, 232, 42, 58, 74, 90, 106, 122, ou uma sequência substanci- 138, 154, 170, 186, 236, 202 e 218, almente idêntica destas.
[0007] Em um terceiro aspecto, anticorpo ou fragmento de ligação ao antígeno,'compreendendo minio de região de determinação complementar 3 (CDR3) pesada e um domínio de CDR3 de cadeia leve, CDR3 de cadeia pesada comnrppnn^ do f. ∞mpreende uma sequencia de aminoáririn da formu a X1 - X2 x3 X4 vs ^minoacido X» XI. vi. ’X5"Xδ' X7 - X8 - X9 - X10 - X11 - X12 - X’3 A - X s- X16 - X17 - X18 V19 /or~ A - A - LvsX3-ri 4 (SEQ ID NO: 247) em que Xi = Ala X2 - Lys’ X - Gly, x4 = Arg, X5 = Asn Y6 A a’ A ~ 9 Asp’X = Ser ou Ala, X7 = Phe, X8 = Asp; OU ou ou a invenção caracteriza um 1 um de cadeia θm que o domínio de X9 = He, Xio = Pro ausente, X1. = Tyr ou ausente, X’8 = G,y ou ou ausente, X" = Phe ou ausente, X12 - Va| ausente, Xu = Tyr ou ausente, X1. = Tvr ausente, X17 = Met ou ausente, X18 = Asp ou ausente, e X19 = Vai ou ausenteje o domínio de CDR3 de cadeia leVe sequência de aminoácido da fórmula X1 - x2 - x3 Urηa X9 (SEQ ID NO: 250) em que X1 = Gin, X2 = Gin ' X8 Asn ou Tyr, X5 = Ser, X6 = Phe, X7 = Pro X8 - p. °” H'S’ X3 = Ala, X4 -
[0008] Em uma modalidade mais específica fragmento de ligação ao antígeno também compreend ° um domínio de CDR1 de cadeia pesada θ uma sequência de aminoácido da fórmula X1 - x2- x3 C°,rnpreenden<fo - Xs(SEQ ID NO: 245) em que X’ = Gly ou Arg, X2 - pX' 'X<*'X? = Phe, X5 = Asp, X6 = Asp, X7 = Tyr, e X8 = Ala; ** = Thr'X4 um domínio de CDR2 de cadeia pesada co uma sequência de aminoácido da fórmula X1 - X2- x3 °yipreendendo - X8 (SEQ ID NO: 246) em que X’ = lie ou Vai, X2 = S ' * Asn, X5 = Ser, X8 = Gly, X7 = Ser, e X8 = He; = Trp’X4 = um domínio de CDR1 de cadeia leve compreendendo uma sequencia de aminoácido da fórmula X1 - X2 - X3 - x4 X5 e 7 (SEQ ID NO: 248), em que X1 = Gin, X2 = Glv X3 - uΩ Ser, eX8 = Trp;e * X'He, X4 = Ser, X8 = um domínio de CDR2 de cadeia leve compreendendo uma sequência de aminoácido da fórmula X1 - X2 - *3 IPX k A (otQ ID NO: 249) em que X1 = Gly ou Ala, X2 = Ala, e X3 = Ser.
[0009] Em um quarto aspecto, a invenção caracteriza um anticorpo ou fragmento de ligação ao antígeno, compreendendo: um domínio de CDR3 de cadeia pesada selecionado do grupo consistindo em SEQ ID NO: 25, 153, 9, 185, 41, 57, 73, 89, 105 121, 137, 169, 201 e 217; e um domínio de CDR3 de cadeia leve selecionado do grupo consistindo em SEQ ID NO: 33, 161, 17, 193, 49, 65, 81, 97, 113, 129 145, 177, 209 e 225.
[00010] Em uma modalidade mais específica, o anticorpo ou fragmento de ligação ao antígeno também compreende: um domínio de CDR1 de cadeia pesada selecionado do grupo consistindo em SEQ ID NO: 21, 149, 5, 181, 37, 53, 69, 85, 101, 117, 133, 165, 197, e 213; um domínio de CDR2 de cadeia pesada selecionado do grupo consistindo em SEQ ID NO: 23, 151, 7, 183, 39, 55, 71, 87, 103, 119, 135, 167, 199 e 215; um domínio de CDR1 de cadeia leve selecionado do grupo consistindo em SEQ ID NO: 29, 157, 13, 189, 45, 61, 77, 93, 109, 125, 141, 173, 205 e 221; e um domínio de CDR2 de cadeia leve selecionado do grupo consistindo em SEQ ID NO: 31, 159, 15, 191,47, 63, 79, 95, 111, 127, 143, 175, 207 e 223.**
[00011] Em modalidades específicas, o antígeno ou fragmento de ligação ao antígeno compreende sequências de CDR de cadeia pesada SEQ ID NO: 21, 23, 25 e sequências de CDR de cadeia leve SEQ ID NO: 29, 31, 33; sequências de CDR de cadeia pesada SEQ ID NO: 149, 151, 153 e sequências de CDR de cadeia leve SEQ ID NO: 157, 159, 161; sequências de CDR de cadeia pesada SEQ ID NO: 5, 7, 9 e cadeia leve SEQ ID NO: 13, 15, 17; e sequências de CDR de cadeia pesada SEQ ID NO: 181, 183, 185 e sequências de CDR de cadeia leve SEQ ID NO: 189, 191, 193.
[00012] Em um quinto aspecto, a invenção caracteriza moléculas de ácido nucléico isoladas que codificam um anticorpo ou fragmentos de ligação ao antígeno da invenção, em que o anticorpo ou fragmento deste compreende um domínio de CDR3 de cadeia pesada codificado por uma sequência de nucleotídeo selecionada do grupo consistindo em SEQ ID NO: 24, 152, 8, 184, 40, 56, 72, 88, 104, 120, 136, 168, 200 e 216; e um domínio de CDR3 de cadeia leve codificado por uma sequência de nucleotídeo selecionada do grupo consistindo em SEQ ID NO: 32, 160, 16, 192, 48, 64, 80, 96, 1 12, 128, 144, 176, 208 e 224; bem como sequências de ácido nucléico substancialmente idênticas destas.
[00013] Em uma modalidade mais específica, moléculas de ácido nucléico isoladas são fornecidas codificando um anticorpo ou fragmento de ligação ao antígeno da invenção, em que o anticorpo ou fragmento deste compreende uma CDR1 de cadeia pesada codificada por uma sequência de nucleotídeo selecionada do grupo consistindo em SEQ ID NO: 20, 148, 4, 180, 36, 52, 68, 84, 100, 116, 132, 164, 196 e 212; um domínio de CDR2 de cadeia pesada codificado por uma sequência de nucleotídeo selecionada do grupo consisntindo em SEQ ID NO: 22, 150, 6, 182, 38, 54, 70, 86, 102, 118, 134, 166, 198 e 214; um domínio de CDR1 de cadeia leve codificado por uma sequência de nucleotídeo selecionada do grupo consistindo em SEQ ID NO: 28, 156, 12, 188, 44, 60, 76, 92, 108, 124, 140, 172, 204 e 220; e um domínio de CDR2 de cadeia leve codificado por uma sequência de nucleotídeo selecionada do grupo consistindo em SEQ ID NO: 30, 158, 14, 190, 30, 46, 62, 78, 94, 110, 126, 142, 174, 206 e 222; bem como sequências de ácido nucléico substancialmente idênticas destas.
[00014] A invenção abrange anticorpos anti-hlL-6R ou fragmentos de ligação ao antígeno destes tendo um padrão de glicosilação modificado. Em algumas aplicações, modificação para remover sítios de glicosilação indesejáveis pode ser útil, ou um anticorpo com falta de uma porção fucose sobre uma cadeia de oligossacarídeo, por exemplo, para aumentar a citotoxicidade celular dependente de anticorpo (ADCC) (veja Shield e outro. (2002) JBC 277:26733). Em outras aplicações, modificação de uma galactosilação pode ser feita a fim de modificar a citotoxicidade dependente de complemento (CDC).
[00015] Em outros aspectos, a invenção fornece vetores de expressão recombinantes transportando umas moléculas de ácido nucléico da invenção, e células hospedeiras nas quais tais vetores foram introduzidos, como são métodos de preparar os anticorpos ou fragmentos de ligação ao antígeno da invenção obtidos por cultura das células hospedeiras da invenção. A célula hospedeira pode ser uma célula procariótica ou eucariótica, preferivelmente a célula hospedeira é uma célula de E. coli ou uma célula de mamífero, tal como uma célula CHO.
[00016] Em um outro aspecto, a invenção caracteriza uma composição farmacêutica compreendendo um anticorpo humano ou fragmento de ligação ao antígeno de um anticorpo que especificamente liga-se ao hlL-6R e um veículo farmaceuticamente aceitável.
[00017] Em outros aspectos, a invenção caracteriza métodos para inibir atividade de IL-6 humana utilizando um anticorpo, ou porção de ligação ao antígeno deste, da invenção. Em uma modalidade, a invenção abrange um método terapêutico compreendendo administrar um anticorpo da invenção, ou um fragmento deste, a um indivíduo humano sofrendo de um distúrbio que é tratado ou melhorado por inibição da atividade de IL-6. O distúrbio pode ser, por exemplo, artrite, incluindo artrite reumatóide crônica; doenças inflamatórias do intestino, incluindo doença de Crohn e colite ulcerativa; lúpus eritematoso sistêmico; e doenças inflamatórias.
[00018] Em outros aspectos, a invenção fornece o uso de um anticorpo ou fragmento de ligação ao antígeno de um anticorpo como definido acima na fabricação de um medicamento para uso para atenuar ou inibir um distúrbio ou doença mediada por IL-6 em um ser humano. Em um aspecto relacionado, a invenção fornece um anticorpo ou fragmento de ligação ao antígeno de um anticorpo como definido acima para uso na atenuação ou inibição de um distúrbio ou doença mediada por IL-6 em um humano.
[00019] Outros objetivos e vantagens tornar-se-ão evidentes a partir de uma revisão da seguinte descrição detalhada.
DESCRIÇÃO DETALHADA
[00020] Antes dos presentes métodos serem descritos, deve ser entendido que esta invenção não é limitada aos métodos particulares e condições experimentais descritas, visto que tais métodos e condições podem variar. Deve ser também entendido que a terminologia utilizada aqui é para o propósito de descrever modalidades particulares apenas, e não é pretendida ser limitante, uma vez que o escopo da presente invenção será limitado apenas pelas reivindicações anexas.
[00021] A menos que definido de outra maneira, todos os termos técnicos e científicos utilizados aqui têm o mesmo significado como comumente entendido por alguém versado na técnica a qual esta invenção pertence. Embora quaisquer métodos e materiais similares ou equivalentes àqueles descritos aqui possam ser utilizados na prática ou teste da presente invenção, os métodos e materiais preferidos são agora descritos.
[00022] O termo "IL6R humano" (hlL-6R), como utilizado aqui, é pretendido referir-se a um receptor de citocina humano que especificamente liga-se à interleucina-6 (IL-6). O domínio extracelular de hlL-6R é mostrado em SEQ ID NO: 1.
[00023] O termo "anticorpo", como utilizado aqui, é pretendido referir-se às moléculas de imunoglobulina compreendendo quatro cadeias de polipeptídeo, duas cadeias pesadas (H) e duas cadeias leves (L) interconectadas por pontes de dissulfeto. Cada cadeia pesada compreende uma região variável de cadeia pesada (abreviada aqui como HCVR ou VH) e uma região constante de cadeia pesada. A região constante de cadeia pesada compreende três domínios, CH1, CH2 e CH3. Cada cadeia leve compreende uma região variável de cadeia leve (abreviada aqui como LCVR ou VL) e uma região constante de cadeia leve. A região constante de cadeia leve é compreendida de um domínio (CL1). As regiões VH e VL podem ser também subdivididas em regiões de hipervariabilidade, denominadas regiões de determinação complementares (CDR), entremeadas com regiões que são mais conservadas, denominadas regiões de estrutura (FR). Cada VH e VL é composta de três CDRs e quatro FRs, dispostas do terminal amino ao terminal carbóxi na seguinte ordem: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4.
[00024] O termo "porção de ligação ao antígeno" de um anticorpo (ou simplesmente "porção de anticorpo" ou "fragmento de anticorpo"), como utilizado aqui, refere-se a um ou mais fragmentos de um anticorpo que mantêm a capacidade de especificamente ligar-se a um antígeno (por exemplo, hlL-6R). Foi mostrado que a função de ligação ao antígeno de um anticorpo pode ser realizada por fragmentos de um anticorpo de tamanho natural. Exemplos de fragmentos de ligação abrangidos dentro do termo "porção de ligação ao antígeno" de um anticorpo incluem (i) um fragmento Fab, um fragmento monovalente consistindo nos domínios de VL, VH, CL1 e CH1; (ii) um fragmento F(ab')2, um fragmento bivalente compreendendo dois fragmentos Fab ligados por uma ponte de dissulfeto na região de dobradiça; (iii) um fragmento Fd consistindo nos domínios de VH e CH1; (iv) um fragmento Fv consistindo nos domínios de VL e VH de um único braço de um anticorpo, (v) um fragmento dAb (Ward e outro. (1989) Nature 241 :544-546), que consiste em um domínio de VH; e (vi) uma região de determinação complementar isolada (CDR). Além disso, embora os dois domínios do fragmento Fv, VL e VH, sejam codificados por genes separados, eles podem ser unidos, utilizando métodos recombinantes, por um ligante sintético que permite eles serem feitos como uma única cadeia contígua na qual as regiões VL e VH pareiam-se para formar moléculas monovalentes (conhecidas como Fv de cadeia única (scFv); veja por exemplo, Bird e outro. (1988) Science 242:423-426, e Huston e outro. (1988) Proc. Natl. Acad. Sei. USA 85:5879-5883). Tais anticorpos de cadeia única são também pretendidos ser abrangidos dentro do termo "porção de ligação ao antígeno" de um anticorpo. Outras formas de anticorpos de cadeia única, tais como diacorpos, são também abrangidas (veja por exemplo, Holliger e outro. (1993) Proc. Natl. Acad Sei. USA 90:6444-6448).
[00025] Um anticorpo de "neutralização" ou "bloqueio", como utilizado aqui, é pretendido referir-se a um anticorpo cuja ligação ao hlL-6R resulta na inibição da atividade biológica de hlL-6. Esta inibição da atividade biológica de hlL-6 pode ser estimada medindo-se um ou mais indicadores de atividade biológica de hlL-6 conhecidos na técnica, tais como ativação celular induzida por hlL-6 e ligação de hlL- 6 ao hlL-6R (veja exemplos abaixo).
[00026] Uma "CDR" ou região de determinação complementar é uma região de hipervariabilidade entremeada dentro de regiões que são mais conservadas, denominadas "regiões de estrutura"(FR). Em modalidades diferentes do anticorpo anti-hlL-6R ou fragmento da invenção, as FRs podem ser idênticas às sequências de linha germinativa humanas ou podem ser naturalmente ou artificialmente modificadas. Um grupo de CDRs pode ser definido como uma sequência de consenso de ammoáado; por exemplo, em uma modalidade, o anticorpo anti-hIL 6R OU fragmento de ligação ao antígeno da invenção pode ser descrito como compreendendo um domínio de CDR3 de cadeia pesada compreen dendo uma sequencia de aminoácido da fórmula X’ - X2 - X3 « X3- X7 - Xa - X9 - X10 - X11 - X’2 - X13. X« - x«. xrs x„ £ ’ * ’ ‘D NO: 247) em que X3 = Aia, X2 = Lys, Xa = Gly, Xa = Arg, X- Asp.Í = Ser ou Ala, x7 - DHA VR . "" Pπθj = Asp" Xθ *- ou ausente yi2 _ v ■ ’ ' ^e, X10 = Pro ou ausente, X11 = Phe ’ A ~ va|ou ausente yi3 -r ausente, X18 - Tw * = Tyr ou ausθnte> X14 = Tyr ou - Tyr ou ausente, X1θ - m ausente, X18 - AOr, ~ ~ θ y ou ausθntθ> X = Met ou " Asp ou ausente, e X19 - \/^i + CDR3 de cari^o । ~ Va ou ausente; e umdomínio de cadeia leve compreenda fórmula X' - X2 - X3 - X< - ys vβ ° sequênCia de amin°ácido da X1 = Gin X2 <AI X - x8 - X9 (SEQ ID NO: 250) em que A um, x = Gin ou His, X3 = Ala y4 - A T VS O X7 = Prn yβ r. o ’X - Asn ou Tyr, X5 = Ser, X6 = Phe, A Pro, X = pro e X9 = Thr. [ t r J °. term° reSSOnância de plasmon de superfície", como aQui, refere-se a um fenômeno ótico que leva em conta a de interações em tempo real por detecção de alterações em concentrações de proteína dentro de uma matriz de biossensor, por exemplo utilizando o sistema BIAcore® (Pharmacia Biosensor AB).
[00028] o termo epítopo" é um determinante antigênico que interage com um sítio de ligação de antígeno específico na região variável de uma molécula de anticorpo conhecida como um parátopo. Um único antígeno pode ter mais do que um epítopo. Epítopos podem ser conformacionais ou lineares. Um epítopo conformational é produzido espacialmente por aminoácidos justapostos de diferentes segmentos da cadeia de polipeptídeo linear. Um epítopo linear é um produzido por resíduos de aminoácido adjacentes em uma cadeia de polipeptídeo. Em certas circunstâncias, um epítopo pode incluir porções de sacarídeos, grupos fosforila, ou grupos sufonila sobre o antígeno.
[00029] O termo "identidade substancial" ou "substancialmente idêntico", quando referindo-se a um ácido nucléico ou fragmento deste, indica que, quando idealmente alinhado com deleções ou inserções de nucleotídeo apropriadas com outro ácido nucléico (ou seu filamento complementar), existe identidade de sequência de nucleotídeo em pelo menos cerca de 95%, e mais preferivelmente pelo menos cerca de 96%, 97%, 98% ou 99% das bases de nucleotídeo, como medido por qualquer algoritmo bem conhecido de identidade de sequência, tal como FASTA, BLAST ou Gap, como descrito abaixo.
[00030] Como aplicado para polipeptídeos, o termo "similaridade substancial" ou "substancialmente similar" significa que duas sequências de peptídeo, quando idealmente alinhadas, tais como pelos programas GAP ou BESTFIT utilizando pesos de intervalo padrão, compartilham pelo menos 95% de identidade de sequência, ainda mais preferivelmente pelo menos 98% ou 99% de identidade de sequência. Preferivelmente, posições de resíduo que não são idênticas diferem-se por substituições de aminoácido conservatives. Uma "substituição de aminoácido conservative"é uma em que um resíduo de aminoácido é substituído por outro resíduo de aminoácido tendo uma cadeia lateral (grupo R) com propriedades químicas similares (por exemplo, carga ou hidrofobicidade). Em geral, a substituição de aminoácido conservative substancialmente não alterará as propriedades funcionais de uma proteína. Em casos onde duas ou mais sequências de aminoácido diferem-se uma da outra por substituições conservatives, a porcentagem de identidade de sequência ou grau de similaridade pode ser ajustado para cima para corrigir quanto à natureza conservativa da substituição. Métodos para executar este ajuste são bem conhecidos por aqueles versados na técnica. Veja, por exemplo, Pearson (1994) Methods Mol. Biol. 24: 307-331. Exemplos de grupos de aminoácidos que têm cadeias laterais com propriedades químicas similares incluem 1) cadeias laterais alifáticas: glicina, alanina, valina, leucina e isoleucina; 2) cadeias laterais de hidroxila alifática: serina e treonina; 3) cadeias laterais contendo amida: asparagina e glutamina; 4) cadeias laterais aromáticas: fenilalanina, tirosina, e triptofano; 5) cadeias laterais básicas: lisina, arginina, e histidina; 6) cadeias laterais acídicas: aspartato e glutamato, e 7) cadeias laterais contendo enxofre são cisteína e metionina. Grupos de substituição de aminoácidos conservativa preferidos são: valina-leucina-isoleucina, fenilalanina-tirosina, lisina-arginina, alanina-valina, glutamato-aspartato, e asparagina-glutamina. Alternativamente, uma substituição conservativa é qualquer alteração tendo um valor positivo na matriz de probabilidade log PAM250 descrita em Gonnet e outro. (1992) Science 256: 1443 45. Uma substituição "moderadamente conservativa" é qualquer alteração tendo um valor não negativo na matriz de probabilidade log PAM250.
[00031] Similaridade de sequência para polipeptídeos, que é também referida como identidade de sequência, é tipicamente medida utilizando software de análise de sequência. Software de análise de proteína compara sequências similares utilizando medidas de similaridade designadas a várias substituições, deleções e outras modificações, incluindo substituições de aminoácido conservativas. Por exemplo, software GCG contém programas tais como Gap e Bestfit que podem ser utilizados com parâmetros padrões para determinar a homologia de sequência ou identidade de sequência entre polipeptídeos intimamente relacionados, tais como polipeptídeos homólogos de diferentes espécies de organismos ou entre uma proteína de tipo selvagem e uma muteína desta. Veja, por exemplo, GCG Versão 6.1. Sequências de polipeptídeo também podem ser comparadas utilizando FASTA utilizando parâmetros padrão ou recomendados, um programa em GCG Versão 6.1. FASTA (por exemplo, FASTA2 e FASTA3) fornece alinhamentos e porcentagem de identidade de sequência das regiões da melhor sobreposição entre as sequências de dúvida e pesquisa (Pearson (2000) supra). Outro algoritmo preferido quando compara-se uma sequência da invenção a uma base de dados contendo um grande número de sequências de diferentes organismos é o programa de computador BLAST, especialmente blastp ou tblastn, utilizando parâmetros padrão. Veja, por exemplo, Altschul e outro. (1990) J. Mol. Biol. 215: 403 410 e Altschul e outro. (1997) Nucleic Acids Res. 25:3389 402.
Preparação de Anticorpos Humanos
[00032] Métodos para gerar anticorpos humanos incluem, por exemplo, Veloclmmune® (Regeneron Pharmaceuticals), tecnologia XenoMouse® (Green e outro. (1994) Nature Genetics 7:13-21 ; Abgenix), o método de "minilocos", e exibição de fago (e veja, por exemplo, US 5.545.807, US 6.787.637). A tecnologia Veloclmmune® (US 6.596.541) abrange um método de gerar um anticorpo totalmente humano de especificidade elevada para um antígeno selecionado. Esta tecnologia envolve geração de um camundongo transgênico tendo um genoma compreendendo regiões variáveis de cadeias leve e pesada humanas operavelmente ligadas aos locos de região constante de camundongo endógenos de modo que o camundongo produza um anticorpo compreendendo uma região variável humana e uma região constante de camundongo em resposta à estimulação antigênica. O DNA que codifica as regiões variáveis das cadeias leve e pesada do anticorpo é isolado e operavelmente ligado ao DNA que codifica as regiões constantes de cadeias leve e pesada humanas. O DNA é em seguida expresso em uma célula capaz de expressar o anticorpo totalmente humano. Em modalidade específica, a célula é uma célula CHO.
[00033] Anticorpos podem ser terapeuticamente úteis no bloqueio de uma interação de ligando-receptor ou inibição de interação de componente de receptor, em vez de morte de células através de fixação de complemento (citotoxicidade dependente de complemento) (CDC) e participação de citotoxicidade mediada por célula dependente de anticorpo (ADCC). A região constante de um anticorpo é importante na capacidade de um anticorpo fixar-se ao complemento e mediar citotoxicidade dependente de célula. Desse modo, o isotipo de um anticorpo pode ser selecionado com base no caso de ser desejável para o anticorpo mediar a citotoxicidade.
[00034] Imunoglobulinas humanas podem existir em duas formas que são associadas com heterogeneidade de dobradiça. Em uma forma, uma molécula de imunoglobulina compreende uma construção de quatro cadeias estável de aproximadamente 150-160 kDa em que os dímeros são mantidos juntos por uma ligação de dissulfeto de cadeia pesada entre as cadeias. Em uma segunda forma, os dímeros não são ligados por meio de pontes de dissulfeto entre as cadeias e uma molécula de cerca de 75-80 kDa é formada composta de cadeias leve e pesada covalentemente acopladas (meio anticorpo). Estas formas foram extremamente difícies de separar, mesmo após purificação de afinidade. A frequência de aparecimento da segunda forma em vários isotipos de IgG intactos é devido a, porém não limitada a, diferenças estruturais associadas com o isotipo de região de dobradiça do anticorpo. De fato, uma única substituição de aminoácido na região de dobradiça da dobradiça de lgG4 humana pode significantemente reduzir o aparecimento da segunda forma (Angal e outro. (1993) Molecular Imunology 30:105) para níveis tipicamente observados utilizando uma dobradiça de lgG1 humana. A presente invenção abrange anticorpos tendo uma ou mais mutações na região de dobradiça, CH2 ou CH3 que pode ser desejável, por exemplo, na produção, para melhorar a produção da forma de anticorpo desejada.
[00035] Anticorpos da invenção são preferivelmente preparados com o uso de tecnologia Veloclmmune®. Um camundongo transgênico em que as regiões variáveis de cadeias leve e pesada de imunoglobulina endógena são substituídas com as regiões variáveis humanas correspondentes é desafiado com o antígeno de interesse, e células linfáticas (tais como células B) são recuperadas dos camundongos que expressam anticorpos. As células linfáticas podem ser fundidas com uma linhagem de célula de mieloma para preparar linhagens de célula de hibridoma imortais, e tais linhagens de célula de hibridoma são avaliadas e selecionadas para identificar linhagens de célula de hibridoma que produzem anticorpos específicos ao antígeno de interesse. DNA que codifica as regiões variáveis da cadeia pesada e cadeia leve pode ser isolado e ligado às regiões constantes isotípicas desejáveis da cadeia pesada e cadeia leve. Uma tal proteína de anticorpo pode ser produzida em uma célula, tal como uma célula CHO. Alternativamente, o DNA que codifica os anticorpos quiméricos específicos ao antígeno ou os domínios variáveis das cadeias leve e pesada pode ser isolado diretamente de linfócitos específicos ao antígeno.
[00036] Em uma modalidade, o camundongo transgênico compreende até 18 genes de cadeia pesada variável humana funcional e 12 genes de cadeia leve kapa variável humana funcional. Em outra modalidade, o camundongo transgênico compreende até 39 genes de cadeia pesada variável humana e 30 genes de cadeia leve kapa variável humana. Em ainda outra modalidade, o camundongo transgênico compreende até 80 genes de cadeia pesada variável humana e 40 genes de cadeia leve kapa variável humana.
[00037] Em geral, os anticorpos da presente invenção possuem afinidades muito elevadas, tipicamente possuindo KDS de cerca de 10-9 até cerca de 10'12 M, quando medido por ligação ao antígeno imobilizado em fase sólida ou em fase de solução.
[00038] Inicialmente, anticorpos quiméricos de alta afinidade são isolados tendo uma região variável humana e uma região constante de camundongo. Como descrito abaixo, os anticorpos são caracterizados e selecionados quanto às características desejáveis, incluindo afinidade de ligação ao hlL-6R, capacidade de bloquear hlL-6, e/ou seletividade para a proteína humana. As regiões constantes de camundongo são substituídas com uma região constante humana desejada para gerar o anticorpo totalmente humano da invenção, por exemplo lgG1 ou lgG4 modificada ou tipo selvagem (por exemplo, SEQ ID NO: 242, 243, 244). Enquanto a região constante selecionada pode variar de acordo com o uso específico, características de especificidade alvo e ligação ao antígeno de alta afinidade residem na região variável.
Mapeamento de Epítopo e Tecnologias Relacionadas
[00039] Para avaliar os anticorpos que se ligam a um epítopo particular, um ensaio de interbloqueio de rotina tal como aquele descrito em Antibodies: A Laboratory Manual 1988 Cold Spring Harbor Laboratory, Harlow e Lane, eds., pode ser realizado. Outros métodos incluem análise de mutantes de varredura de alanina, manchas de peptídeo (Reineke (2004) Methods Mol Biol 248:443-63), ou clivagem de peptídeo como descrito nos exemplos abaixo. Além disso, métodos tais como excisão de epítopo, extração de epítopo e modificação química de antígenos podem ser empregados (Tomer (2000) Protein Science: 9: 487-496).
[00040] Perfil de Modificação Assistida (MAP), também conhecido como Perfil de Anticorpo com Base em Estrutura de Antígeno (ASAP) é um método que categoriza grandes números de anticorpos monoclonais (mAbs) direcionados contra o mesmo antígeno de acordo com as similaridades do perfil de ligação de cada anticorpo às superfícies de antígeno quimicamente ou enzimaticamente modificado (Publicação de Pedido de Patente dos Estados Unidos N- 2004/0101920). Cada categoria pode refletir um único epítopo distintamente diferente de ou parcialmente sobrepondo-se com um epítopo representado por outra categoria. Esta tecnologia permite filtração rápida de anticorpos geneticamente idênticos, de modo que a caracterização possa ser focalizada em anticorpos geneticamente distintos. Quando aplicado à avaliação de hibridoma, MAP pode facilitar a identificação de clones de hibridoma raros com características desejadas. MAP pode ser utilizado para classificar os anticorpos de hlL-6R da invenção em grupos de diferentes epitopos de ligação de anticorpos.
[00041] Agentes úteis para alteração da estrutura do antígeno imobilizado são enzimas, tais como, por exemplo enzimas proteolíticas e agentes químicos. A proteína de antígeno pode ser imobilizada em superfícies de chipbiossensor ou contas de poliestireno. As últimas podem ser processadas com, por exemplo, um ensaio tal como um ensaio de detecção multiplex Luminex® (Luminex Corp., TX). Por causa da capacidade de Luminex® conduzir análise multiplex com até 100 tipos diferentes de contas, Luminex® fornece superfícies de antígeno quase não limitadas com várias modificações, resultando em resolução melhorada no perfil de epítopo de anticorpo sobre um ensaio de biossensor.
Administração e Formulações Terapêuticas
[00042] A administração de entidades terapêuticas de acordo com a invenção será administrada com adequados veículos, excipientes, e outros agentes que são incorporados em formulações para fornecer transferência, distribuição, tolerância melhoradas, e similares. Uma multidão de formulações apropriadas pode ser encontrada no formulário conhecido por todos os químicos farmacêuticos: Remington's Pharmaceutical Sciences (15a ed, Mack Publishing Company, Easton, Pa., 1975), particularmente Capítulo 87 por Blaug, Seymour, nesse particular. Estas formulações incluem, por exemplo, pós, pastas, unguentos, geléias, ceras, óleos, lipídeos, vesículas contendo lipídeo (catiônico ou aniônico) (tais como Lipofectin®), conjugados de DNA, pastas de absorção anidrosas, emulsões óleo em água e água em óleo, emulsões carbowax (polietileno glicóis de vários pesos molécula- res), géis semi-sólidos, e misturas semi-sólidas contendo carbowax. Qualquer uma das misturas precedentes pode ser apropriada em tratamentos e terapias de acordo com a presente invenção, contanto que o ingrediente ativo na formulação não seja inativado pela formulação e a formulação seja fisiologicamete compatível e tolerável com a rotina de administração. Veja também Powell e outro. PDA (1998) J Pharm Sei Technol. 52:238-311 e as citações a esse respeito para informação adicional relacionada aos excipientes e veículos bem conhecidos por químicos farmacêuticos.
Exemplos
[00043] Os seguintes exemplos são apresentados a fim de prover aqueles versados na técnica com uma descrição completa e descrição de como preparar e usar os métodos e composições da invenção, e não são pretendidos limitar o escopo do qual os inventores consideram como sua invenção. Esforços foram feitos para assegurar exatidão com respeito aos números utilizados (por exemplo, quantidades, temperatura etc.), porém algumas divergências e erros experimentais devem ser considerados. A menos que indicado de outra maneira, partes são partes por peso, peso molecular é peso molecular médio, temperatura é em graus centígrados, e pressão é em ou próxima a atmosférica.
Exemplo 1
<HEAD>> Geração de Anticorpos humanos para Receptor de IL-6 Humana
[00044] Imunização de roedores pode ser feita por quaisquer métodos conhecidos na técnica (veja, por exemplo, Harlow e Lane (1988) supra; Malik e Lillehoj, Antibody techniques: Academic Press, 1994, CA). Em uma modalidade preferida, antígeno de hlL-6R é administrado diretamente aos camundongos que compreendem locos de DNA codificando tanto região variável de cadeia pesada de lg humana quanto região variável de cadeia leve capa (Veloclmmune®, Regeneron Pharmaceuticals, Inc.; US 6,596,541), com um adjuvante para estimular a resposta imune. Um tal adjuvante inclui adjuvante de Freund completo e incompleto, sistema adjuvante MPL+TDM (Sigma), ou RIBI (dipeptideos de muramila) (veja O'Hagan, Vaccine Adjuvant, por Human Press, 2000, NJ). Um tal adjuvante pode prevenir dispersão rápida de polipeptídeo por sequestro do antígeno em um depósito local, e pode conter fatores que podem estimular a resposta imune do hospedeiro. Em uma modalidade, hlL-6R é administrado indiretamente como DNA plasmídeo que contém gene de hlL-6R e expressa hlL-6R utilizando a maquinaria de expressão de proteína celular hospedeira para produzir polipeptídeo de antígeno in vivo. Em ambos os métodos, o esquema de imunização requer diversas administrações espaçadas por algumas semanas. A resposta imune de anticorpo é monitorada por imunoensaio específico ao antígeno padrão. Quando os animais alcançaram sua resposta imune máxima, as células B de expressão de anticorpo foram colhidas e fundidas com células de mieloma de camundongo para preservar sua viabilidade, formando células de hibridoma. Para selecionar anticorpos monoclonais funcionalmente desejáveis, meios condicionados das células de hibridoma ou células transfectadas foram avaliados quanto à especificidade, afinidade de ligação ao antígeno, e potência no bloqueio de ligação de hlL-6 ao hlL- 6R (descrito abaixo).
Exemplo 2
Anticorpos anti-hlL6R gerados por meio de isolamento direto de esplenócitos
[00045] DNA que codifica domínios de VH e VL pode ser isolado diretamente de uma única célula B positiva de antígeno. Resumidamente, o camundongo transgênico imunizado por hlL-6Ra foi terminado e esplenócitos foram colhidos. Células sanguíneas vermelhas foram removidas por lise seguida por peletização dos esplenócitos colhidos. Esplenócitos ressuspensos foram primeiro incubados com um coquetel de IgG humana, FITC-anti-mFc, e biotina-IL6Ra durante 1 hora. As células manchadas foram lavadas duas vezes com PBS, em seguida manchadas com um ∞quetel de IgG de rato e humana, APC-anti-mlgM, e SA-PE durante uma hora. As células manchadas foram lavadas uma vez com PBS e foram analisadas por citometria de fluxo em um MoFIo (Cytomation). Cada IgG positiva, IgM negativa, e célula B positiva de antígeno foi classificada e semeada em uma cavidade separada em uma placa de 96 cavidades. RT-PCR de genes de anticorpo destas células B foi realizada de acordo com um método descrito por Wang e outro. (2000) (J Imunol Methods 244:217-225). Resumidamente, cDNAs para cada célula B única foram sintetizados por meio de RT-PCR. Cada produto de RT resultante foi em seguida dividido e transferido em duas cavidades correspondentes em duas placas de 96 cavidades. Um grupo dos produtos de RT resultantes foi primeiro amplificado por PCR utilizando um iniciador degenerado 5' específico para sequência líder de região variável de cadeia pesada humana de IgG e um iniciador 3' específico para região constante de cadeia pesada de camundongo, para formar um amplicon. O amplicon foi em seguida amplificado novamente por PCR utilizando um grupo de iniciador degenerado 5' específico para estrutura 1 de sequência de região variável de cadeia pesada humana de IgG e um iniciador 3'nestedespecífico para região constante de cadeia pesada de camundongo. O outro grupo dos produtos de RT resultantes foi primeiro amplificado por PCR utilizando um iniciador degenerado 5' específico para sequência líder de região variável de cadeia leve capa humana e um iniciador 3' específico para região constante de cadeia leve kapa de camundongo para formar um amplicon. O amplicon foi em seguida amplificado novamente por PCR utilizando um grupo de iniciador degenerado 5' específico para estrutura 1 de sequência de região variável de cadeia leve kapa humana e um iniciador 3'nestedespecífico para região constante de cadeia leve kapa de camundongo. Os produtos de PCR de cadeia pesada e cadeia leve foram clonados em vetores de anticorpo linearizados por Sap I contendo região constante de cadeia pesada de lgG1 e região constante de cadeia leve kapa, respectivamente. O plasmídeo de cadeia pesada tem um sítio Iox2272 e um sítio Iox511 flanqueando os cassetes de expressão de cadeia pesada. Além disso, imediatamente a jusante do Iox2272 no plasmídeo de cadeia pesada existe um gene de resistência à higromicina que carece de um promotor e um ATG de iniciação. O gene de resistência à higromicina é também transcricionalmente ligado a um gene eGFP a jusante por meio de uma sequência IRES. O plasmídeo de cadeia leve tem um sítio loxP e sítio Iox2272 flanqueando o cassete de expressão de cadeia leve. Além disso, o plasmídeo de cadeia leve tem um promotor SV40 imediatamente antes de um ATG no sítio Iox2272, de modo que sob integração em uma célula hospedeira apropriada o promotor SV40 próximo ao Iox2272 e ATG de iniciação do plasmídeo de cadeia leve seja trazido adjacente ao gene de resistência à higromicina no plasmídeo de cadeia pesada na estrutura de leitura apropriada para permitir transcrição e translação dos genes de resistência à higromicina e eGFP. Plasmídeos recombinantes purificados tendo uma sequência de região variável de cadeia pesada e plasmídeos tendo uma sequência de região variável de cadeia leve da mesma célula B foram em seguida combinados e transfectados, juntamente com um plasmídeo que expressa a Cre recombinase, em uma linhagem de célula hospedeira CHO modificada. A linhagem de célula hospedeira CHO modificada contém, de 5' a 3', um sítio loxP, um eCFP, um sítio Iox2272, DsRed, e um sítio Iox511 em um locos transcricionalmente ativo. Consequentemente, a célula CHO hospedeira pode ser isolada por citometria de fluxo como uma célula positiva azul, positiva vermelha, e negativa verde. Quando plasmídeos recombinantes expressando genes de cadeia pesada e cadeia leve são transfectados juntamente com um plasmídeo expressando a Cre recombinase, recombinação específica de sítio mediada pela Cre recombinase resulta na integração dos plasmídeos de anticorpo no locos cromossômico contendo os sítios lox e substituição dos genes eCFP e DsRed. Recombinantes podem em seguida ser isolados como células negativa azul, negativa vermelha, e positiva verde por citometria de fluxo. Consequentemente, células CHO transfectadas com plasmídeos recombinantes tendo uma sequência de região variável de cadeia pesada e plasmídeos tendo uma sequência de região variável de cadeia leve da mesma célula B foram classificados por citometria de fluxo, e recombinantes apropriados que mostram os fenótipos negativo azul, negativo vermelho, e positivo verde foram isolados, e linhagens de célula CHO expressando anticorpo recombinante estável foram estabelecidas de clones isolados.
Exemplo 3
Determinação de Afinidade de Ligação ao Antígeno
[00046] O KD da ligação de antígeno aos anticorpos selecionados descritos acima foi determinado por cinéticos de superfície em um ensaio de ressonância de plasmon de superfície de biossensor em tempo real (BIAcore®). Mais especificamente, a afinidade dos anticorpos ao IL-6R humano foi medida utilizando um BIAcore® 2000 ou BIAcore® 3000. O anticorpo foi capturado em uma superfície de IgG anti-camundongo e exposto a várias concentrações de proteína de hlL- 6R recombinante em forma monomérica ou dimérica. Análise cinética utilizando software BIAevaluation® foi realizada para obter as constantes de taxas de associação e dissociação.
[00047] Afinidades de ligação dos anticorpos ao hlL-6R foram também medidas para meios condicionados de hibridoma ou proteínas purificadas por imunoensaio de competição com base em placa. As proteínas de anticorpo foram purificadas utilizando cromatografia de afinidade de Proteína G de meio de condicionamento de célula de hibridoma que foi depauperado de IgG bovina (Invitrogen). Para o ELISA de competição, resumidamente, quantidades constantes de anticorpo em diferentes níveis foram pré-misturadas com diluições seriais de proteína de antígeno, hlL-6R-hFc, variando de 0 a 10 pg/ml, e incubadas durante duas horas em temperatura ambiente para alcançar equilíbrio de pseudo-ligação entre o anticorpo e antígeno. Estas soluções foram em seguida transferidas para placas pré- revestidas de hlL-6R-hFc de 96 cavidades para permitir o anticorpo livre nas misturas ligar-se à hlL-6R-hFc revestida na placa. As placas foram tipicamente revestidas com 1 a 2 pg/ml de proteína hlL-6R-hFc em solução PBS durante a noite a 4°C seguido por bloqueio não específico de BSA. Após lavagem do excesso de anticorpo em solução, anticorpos ligados à placa foram detectados com um reagente de anticorpo policlonal IgG ou IgA anticamundongo de cabra conjugado a HRP e desenvolvidos utilizando substratos colori métricos ou de quimioluminescência. A dependência dos sinais nas concentrações de antígeno em solução foi analisada com uma análise de ajuste de 4 parâmetros utilizando softwarePrism® (Graph Pad) e relatada como IC50. Imunoensaio de competição foi também realizado utilizando instrumento Kinexa® de fase de solução em estado equilibrado (Sapidyne Inc.).
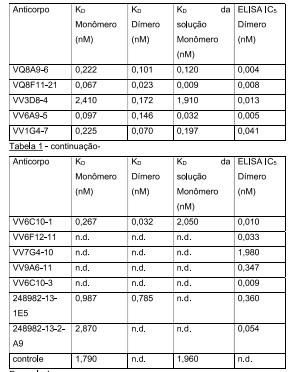
[00048] Os resultados são mostrados na Tabela 1 (controle: anticorpo monoclonal humanizado ao IL-6R humano (Patente dos Estados Unidos N2 5.817.790 SEQ ID NO: 69 e 71). Anticorpo (sequências de aminoácido de HCVR e LCVR): VQ8A9-6 (3, 11); VQ8F11-21 (19, 27); W7G4-1 (35, 43); W7G4-10 (51, 59); W6C10-1 (67, 75); W6C10-3 (83, 91); W6C10-4 (99, 107); W6F12-11 (115, 123); W9A6-11 (131, 139); W6A9-5 (147, 155), W3D8-4 (163, 171); W1G4-7 (179, 187); 248982- 13-1-E5 (195, 203); 248982-13-2-A9 (211, 219). KD de monômero e dímero determinado por BIAcore®; KD da solução por Kinexa®; IC50 por ensaios ELISA (n.d. = não determinado). Tabela 1 - Afinidade de Ligação ao Antígeno
[00049] Atividades de bloqueio de hlL-6 dos anticorpos anti-hlL- 6R da invenção foram avaliadas por imunoensaios de bloqueio de hlL-6, bioensaios de crescimento de célula dependente de hlL-6 in vitro, e ressonância de plasmon de superfície (BIAcore®). O imuno- ensaio foi utilizado para avaliar a capacidade do anticorpo testado bloquear ligação de hlL-6 ao hlL-6R, e o bioensaio in vitrofoi utilizado para determinar a potência dos anticorpos na neutralização de transdução de sinal celular mediado por hlL-6R.
[00050] Para o imunoensaio, proteína recombinante de hlL-6 foi revestida em uma placa de 96 cavidades em tampão PBS durante a noite a 4°C. Esta placa foi utilizada para capturar hlL-6R-hFc livre de soluções de amostra de anticorpo, e a quantidade de hlL-6R-hFc capturada foi quantificada de acordo com a curva padrão. As soluções de amostra foram compostas de uma quantidade constante de proteína recombinante de hlL-6R-hFc (100 pM) e quantidades variantes de anticorpo, em meio de condição de hibridoma cru ou como proteína de anticorpo purificado, variando de 0 a cerca de 50 nM em diluições seriais. As misturas de anticorpo-antígeno foram incubadas em temperatura ambiente durante ~2 horas para permitir ligação anticorpo-antígeno para alcançar o equilíbrio. As soluções de amostra equilibradas foram em seguida transferidas para as placas revestidas por hlL-6 para medida de hlL-6R-hFc livre. Após 1 hora de ligação, a placa foi lavada e hlL-6R-hFc ligada foi detectada utilizando anticorpos policlonais anti-hFc de cabra conjugados a HRP (Jackson Immuno Research), e desenvolvida utilizando substrato TMB (BD Pharmigen). IC50S foram determinadas como a quantidade de anticorpo requerida para reduzir 50% de IL-6R-hFc detectável por ligando hlL-6 ligado à placa. Os resultados são mostrados na primeira coluna da Tabela 2.
[00051] Adicionalmente, a capacidade do anticorpo teste bloquear ligação de hlL-6 ao receptor hlL-6R foi determinada utilizando ressonância de plasmon de superfície. Moléculas de hIL- 6R-hFc de antígeno purificadas foram capturadas por anticorpos policlonais de IgG anti-humanos de cabra imobilizados em superfície de CM-5 através de acoplamento de amina em uma densidade de 250 RU. Solução de hlL-6 (0,25 ml, 50 nM) foi injetada sobre a superfície do receptor e hlL-6 ligada registrada (primeiro injeção de IL-6). hlL-6 ligada foi em seguida removida com um pulso de 3 M de MgCh seguindo por tampão de condicionamento. Anticorpo anti- hlL6R em meio condicionado de hibridoma foi injetado sobre a superfície do receptor capturado seguido por segunda injeção de hlL-6. A porcentagem de redução em ligação de hL-6 resultando de complexo anticorpo e receptor pré-formado foi utilizada como um escore para definir bloqueadores de hlL-6 de não bloqueadores (segunda coluna, Tabela 2). Tabela 2 - Neutralização de Ligação de hlL-6
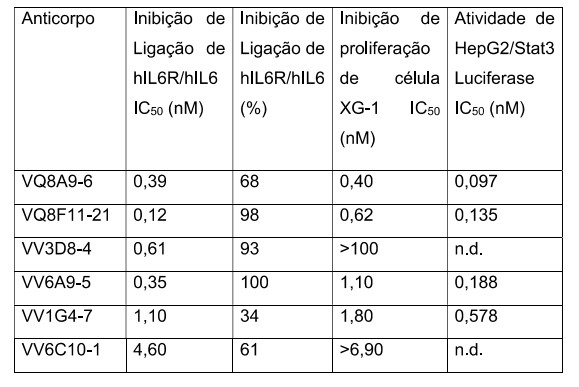
Tabela 2 - continuação-
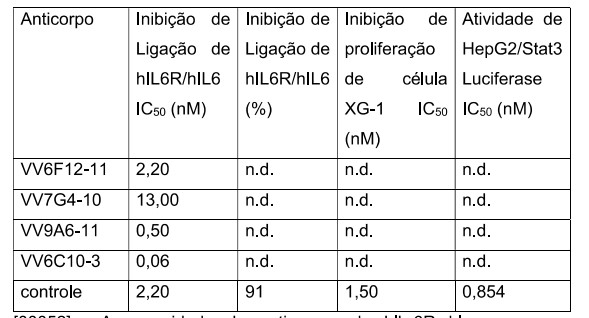
[00052] A capacidade de anticorpos de hlL-6R bloquearem a atividade de hlL-6 in vitrofoi medida na linhagem XG-1 de mieloma dependente de hlL-6. Células XG-1 mantidas em meio contendo hlL-6 foram lavadas duas vezes com meios livres de hlL-6 e cultivadas durante 24 horas em meio livre de hlL-6 para depauperar hlL-6 residual. As células privadas de alimento foram em seguida centrifugadas e ressuspensas no meio em 4 x 105 células por ml e semeadas 20.000 células por cavidade em uma placa de cultura de tecido de 96 cavidades. As proteínas de anticorpo purificadas foram serialmente diluídas em meio e adicionadas às células semeadas em concentrações variando de 0 a 50 nM. Subsequentemente, hlL-6 recombinante foi adicionada às cavidades para uma concentração final de 8 pM. As células foram deixadas desenvolver durante ~72 horas a 37°C em uma incubadora de CO2 a 5% umidificada. No final do período de desenvolvimento, as células vivas foram medidas utilizando kit CCK-8 (Dojindo, Japan). IC50S foram determinadas como descrito acima, e relatadas na terceira coluna da Tabela 2.
[00053] A capacidade de anticorpos de hlL-6R bloquearem a atividade de hlL-6 foi também medida in vitrona linhagem de célula de hepatoma humano sensível a hlL-6, HepG2. Células HepG2 foram transfectadas com um plasmídeo repórter contendo um elemento de resposta a STAT3 (Transdutor de Sinal e Ativador de Transcrição 3) ligado a um gene de luciferase. As células transfectadas foram tripsini- zadas, centrifugadas e ressuspensas no meio em aproximadamente 2,5 x 105 células por ml e semeadas em 20.000 células por cavidade em uma placa de cultura de tecido de 96 cavidades. As proteínas de anticorpo purificadas foram serialmente diluídas em meio e adicionadas às células semeadas em concentrações variando de 0 a 100 nM. Subsequentemente, hlL-6 recombinante foi adicionada às cavidades para uma concentração final de 50 pM. A resposta foi medida após incubação das células durante 6 horas a 37°C em uma incubadora de CO2 a 5% humidificada. Atividade de luciferase foi medida com 0 sistema de ensaio de luciferase Steady-GIo® (Promega). IC50S foram determinadas como descrito acima, e relatadas na quarta coluna da Tabela 2.
Exemplo 5.
Diversidade de Epítopo de Ligação
[00054] Um imunoensaio de competição de ligação de anticorpo foi realizado utilizando como um controle anticorpo humanizado para IL-6R humana. Resumidamente, uma placa imunoabsorvente de 96 cavidades foi revestida com 20 ng por cavidade de proteína recombinante de hlL-6R durante a noite a 4°C. Após bloquear ligação não-específica com BSA, os sítios de ligação de hlL-6R em uma metade da placa foram saturados com ligação do anticorpo de controle pela adição de 500 ng do controle por cavidade, e à outra metade da placa foi adicionado apenas o tampão de ligação. Após três horas de ligação em temperatura ambiente, os anticorpos purificados atingiram o máximo de uma concentração final de 50 ng/ml com e sem o anticorpo de controle preexistente na cavidade. Após uma hora de ligação adicional, o anticorpo livre foi desgastado pela água e um anticorpo ligador à placa foi detectado com IgG ou IgA anti- camundongo de cabra conjugado a HRP, anticorpo policlonal e a placa foi desenvolvida utilizando substratos de HRP cromáticos e a absorvên- cia em 450 nm foi registrada. Deduções de percentage da ligação dos anticorpos anti-hll_6R pela presence do anticorpo de controle são listadas na Tabela 3 abaixo. Um experimento similar foi conduzido utilizando tecnologia de ressonância de plasmon de superfície (Tabela 3). Ambos os métodos geraram Resultados consistentes. Anticorpos VQ8F11, W3D8, W6A9, W6C10-1 ligaram epítopos sobrepondo com o anticorpo de controle; enquanto que os anticorpos VQ8A9, W1 G4, W6F12, W7G4, W9A6, e W6C10-3 pareceram ligar-se a epítopos distintos quando a ligação de antígeno não foi bloqueada pelo anticorpo de controle. Competição parcial pode resultar de impedimento estérico da primeira ligação de anticorpo, mesmo que os epítopos não possam ser sobrepostos. Tabela 3 - Competição de Ligação de Antígeno com Anticorpo Controle

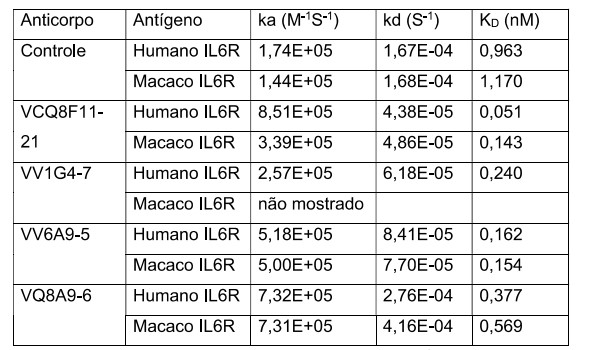
[00055] Quatro anticorpos foram testados quanto a inter-reativi- dade para IL-6R de proteína recombinante de macaco utilizando tecnologia BIAcore®. Resumidamente, um chipbiossensor sobre o qual anticorpo policlonal de Fc anti-camundongo de cabra foi imobilizado foi utilizado para apresentar anticorpos monoclonais anti-hlL-6R em uma densidade de cerca de 75 RU. Proteína IL-6R humana recombinante ou monomérica de macaco (Macaca fasci- culahs, domínio extracelular; SEQ ID NO: 251), em uma faixa de concentração entre 1,25 - 40 nM, foi injetada sobre a superfície do anticorpo. A ligação do receptor ao anticorpo e a dissociação do complexo de ligação foram monitoradas em tempo real. Tanto a constant da taxa de associação (ka) quanto a constante da taxa dissociada (kd) foram obtidas, e KD calculada (Tabela 4). Tabela 4 - Comparação de Afinidade de Ligação ao IL-6R Humano e de Macaco
[00056] Entre os quatro anticorpos testados, VQ8F11, W6A9, e VQ8A9 reagiram fortemente ao receptor de macaco com valores Ko que diferiram em até cerca de 1,5 a cerca de 3 vezes de ligação de receptor humano, respectivamente. W1G4, que não foi bloqueado pelo anticorpo de controle (Tabela 3), não mostrou nenhuma ligação ao receptor de macaco a despeito de forte ligação ao receptor humano com KD de 241 pM.
Exemplo 7.
Efeito de Região Constante sobre a Afinidade de Ligação
[00057] A afinidade de ligação ao hlL-6R monomérico de quatro anticorpos tendo IgG de camundongo, IgG humano ou lgG4 humano (tipo selvagem e modificado) foram determinado utilizando BIAcore® como descrito acima exceto uma superfície de anticorpo policlonal de Fc anti-humano de cabra foi utilizada para capturar anticorpos de hlgG. hlL-6R monomérica foi injetada em concentrações de 12,5, 6,25, 3,12, e 1,56 nM. A capacidade dos anticorpos para neutralizar a transdução de sinal de HepG2/STAT3 dependente de hlL-6 foi também determinada em um ensaio de luciferase (ICso)- IC50S para isótipos de IgG diferentes foram similares, sugerindo nenhum efeito de isótipo sobre a afinidade de anticorpo para antígeno. Tabela 5 - Comparação de Isótipos de IgG