JP2012017331A - アンジオポエチン様4タンパク質のインヒビター、組み合わせ、およびそれらの使用 - Google Patents
アンジオポエチン様4タンパク質のインヒビター、組み合わせ、およびそれらの使用 Download PDFInfo
- Publication number
- JP2012017331A JP2012017331A JP2011175420A JP2011175420A JP2012017331A JP 2012017331 A JP2012017331 A JP 2012017331A JP 2011175420 A JP2011175420 A JP 2011175420A JP 2011175420 A JP2011175420 A JP 2011175420A JP 2012017331 A JP2012017331 A JP 2012017331A
- Authority
- JP
- Japan
- Prior art keywords
- angptl4
- antibody
- cells
- antibodies
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/10—Drugs for disorders of the urinary system of the bladder
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/06—Antiabortive agents; Labour repressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/08—Drugs for genital or sexual disorders; Contraceptives for gonadal disorders or for enhancing fertility, e.g. inducers of ovulation or of spermatogenesis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/14—Drugs for disorders of the endocrine system of the thyroid hormones, e.g. T3, T4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/08—Vasodilators for multiple indications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/14—Vasoprotectives; Antihaemorrhoidals; Drugs for varicose therapy; Capillary stabilisers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2839—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the integrin superfamily
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Cardiology (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Heart & Thoracic Surgery (AREA)
- Reproductive Health (AREA)
- Dermatology (AREA)
- Urology & Nephrology (AREA)
- Endocrinology (AREA)
- Ophthalmology & Optometry (AREA)
- Epidemiology (AREA)
- Gynecology & Obstetrics (AREA)
- Oncology (AREA)
- Vascular Medicine (AREA)
- Diabetes (AREA)
- Rheumatology (AREA)
- Physical Education & Sports Medicine (AREA)
- Hematology (AREA)
- Pregnancy & Childbirth (AREA)
- Obesity (AREA)
- Zoology (AREA)
- Orthopedic Medicine & Surgery (AREA)
Abstract
【解決手段】ANGPTL4アンタゴニストと他の治療薬(例えば、抗癌薬)との組み合わせ、癌に感受性を示すかまたは癌と診断された哺乳動物、あるいは腫瘍成長が再発したかまたは癌細胞増殖が再発した哺乳動物の治療におけるその使用方法も提供する。また、ANGPTL4のインヒビターと血管形成のインヒビターとの組み合わせ、ならびに癌成長および/または血管形成に関与する障害を阻害するためのこのような組み合わせの使用方法を提供する。
【選択図】なし
Description
本出願は、第119条(e)項の下、2004年7月20日出願の米国特許仮出願番号60/589,782号(その全体が本明細書中で参考として援用される)の優先権を主張する。
本発明は、一般に、ヒトの疾患および病的状態(癌など)の治療に関する。本発明は、アンジオポエチン様4タンパク質(ANGPTL4)のインヒビター、ANGPTL4のインヒビターと他の治療薬との組み合わせ、ならびに疾患または病的状態の診断および治療のためのこのような組成物の使用方法に関する。
癌は米国における主な死亡原因である。癌の治療のために種々の療法が使用されている。例えば、癌組織または死滅した組織を除去するために外科的方法が使用されている。充実性腫瘍の萎縮によって作用する放射線療法および急速に分化する細胞を死滅させる化学療法が癌治療として使用されている。
本発明は、アンジオポエチン様4タンパク質(ANGPTL4)のインヒビターならびに疾患および病的状態を治療する(例えば、腫瘍成長または癌細胞増殖を遮断するかまたは減少させるか、腫瘍成長の再発を遮断するかまたは減少させるなど)ためのこのようなインヒビターの使用方法に関する。本発明は、ANGPTL4のインヒビターと抗癌薬との組み合わせおよび腫瘍成長を阻害するためのこのような組み合わせの使用方法を提供する。本発明はまた、ANGPTL4のインヒビターと血管形成のインヒビターとの組み合わせならびに癌成長および/または血管形成に関与する障害(例えば、新生物障害(例えば、腫瘍成長)および非新生物障害)を阻害するためのこのような組み合わせの使用方法を提供する。
例えば、本発明は以下の項目を提供する。
(項目1)
腫瘍成長または癌細胞の増殖を遮断するかまたは減少させる方法であって、
a)有効量の抗癌薬を該腫瘍または該癌細胞に投与する工程と、
b)有効量のアンジオポエチン様4タンパク質(ANGPTL4)アンタゴニストを該腫瘍または該癌細胞に投与する工程と、
を包含し、
有効量の組み合わせによって該腫瘍成長または該癌細胞の増殖が遮断されるかまたは減少する、方法。
(項目2)
前記抗癌薬が抗血管形成薬を含む、項目1に記載の方法。
(項目3)
前記抗血管形成薬がVEGFアンタゴニストである、項目2に記載の方法。
(項目4)
前記VEGFアンタゴニストが抗VEGF抗体である、項目3に記載の方法。
(項目5)
前記抗VEGF抗体がヒト化A4.6.1である、項目4に記載の方法。
(項目6)
前記ANGPTL4アンタゴニストが抗ANGPTL4抗体である、項目1に記載の方法。
(項目7)
前記抗ANGPTL4抗体がANGPTL4(184〜406)に結合する、項目6に記載の方法。
(項目8)
前記ANGPTL4アンタゴニストが抗αVβ5抗体である、項目1に記載の方法。
(項目9)
前記抗体がヒト化抗体である、項目4、項目6、または項目8に記載の方法。
(項目10)
前記ANGPTL4アンタゴニストがSiRNA分子を含む、項目1に記載の方法。
(項目11)
前記SiRNA分子がANGPTL4−SiRNA分子である、項目10に記載の方法。
(項目12)
前記ANGPTL4−SiRNA分子が、ANGPTL4をコードする核酸のDNA配列をターゲティングし、前記DNA配列が、少なくともGTGGCCAAGCCTGCCCGAAGA(配列番号3)を含む、項目11に記載の方法。
(項目13)
前記腫瘍または前記癌細胞に第3の抗癌薬を投与する工程をさらに包含する、項目1に記載の方法。
(項目14)
前記第3の抗癌薬が化学療法薬である、項目13に記載の方法。
(項目15)
前記第3の抗癌薬が別の血管形成インヒビターである、項目13に記載の方法。
(項目16)
前記投与工程(a)および(b)を連続的に行う、項目1に記載の方法。
(項目17)
前記投与工程(a)および(b)を同時に行う、項目1に記載の方法。
(項目18)
前記投与工程(a)および(b)を連続的にも同時にも行う、項目1に記載の方法。
(項目19)
前記投与工程を任意の順序で行う、項目1に記載の方法。
(項目20)
前記腫瘍または前記癌細胞が被験体中に存在する、項目1に記載の方法。
(項目21)
前記被験体がヒトである、項目20に記載の方法。
(項目22)
前記被験体が腫瘍成長または癌細胞の増殖を再発している、項目20に記載の方法。
(項目23)
被験体における腫瘍成長または癌細胞の増殖を遮断するかまたは減少させる方法であって、
有効量の抗血管形成薬および有効量のアンジオポエチン様4タンパク質(ANGPTL4)アンタゴニストを含む組み合わせ組成物を該被験体に投与する工程をさらに含み、有効量の組み合わせによって該腫瘍成長または該癌細胞の増殖が遮断されるかまたは減少する、方法。
(項目24)
さらなる薬剤を投与する工程をさらに含み、該さらなる薬剤が抗癌薬である、項目23に記載の方法。
(項目25)
被験体における腫瘍成長の再発または癌細胞増殖の再発を遮断するかまたは減少させる方法であって、
有効量のアンジオポエチン様4(ANGPTL4)アンタゴニストを被験体に投与する工程を含み、該被験体が抗癌薬での癌治療を受けていたかまたは同時に受けており、有効量の前記ANGPTL4アンタゴニストの投与により、前記腫瘍成長の再発または癌細胞増殖の再発が遮断されるかまたは減少する、方法。
(項目26)
前記抗癌薬が1つまたは複数の化学療法薬である、項目25に記載の方法。
(項目27)
前記抗癌薬が抗血管形成薬を含む、項目25に記載の方法。
(項目28)
前記抗血管形成薬が抗VEGFインヒビターを含む、項目27に記載の方法。
(項目29)
前記抗VEGFインヒビターが抗VEGF抗体である、項目28に記載の方法。
(項目30)
前記抗VEGF抗体がヒト化A4.6.1である、項目29に記載の方法。
(項目31)
前記ANGPTL4アンタゴニストが抗ANGPTL4抗体である、項目25に記載の方法。
(項目32)
前記ANGPTL4アンタゴニストが抗αVβ5抗体である、項目25に記載の方法。
(項目33)
前記抗体がヒト化抗体である、項目29、項目31、または項目32に記載の方法。
(項目34)
前記ANGPTL4アンタゴニストがSiRNA分子を含む、項目25に記載の方法。
(項目35)
前記SiRNA分子がANGPTL4−SiRNA分子である、項目34に記載の方法。
(項目36)
前記ANGPTL4−SiRNA分子が、ANGPTL4をコードする核酸のDNA配列をターゲティングし、前記DNA配列が、少なくともGTGGCCAAGCCTGCCCGAAGA(配列番号3)を含む、項目35に記載の方法。
(項目37)
さらなる薬剤を投与する工程をさらに含み、該さらなる薬剤が抗癌薬である、項目25に記載の方法。
(項目38)
腫瘍成長または癌細胞の増殖を遮断するかまたは減少させる方法であって、
有効量のアンジオポエチン様4(ANGPTL4)アンタゴニストを該腫瘍または該癌細胞に投与する工程を含み、該抗ANGPTL4アンタゴニストがANGPTL4(184〜406)に結合する抗体であり、該有効量によって該腫瘍成長または該癌細胞の増殖が遮断されるかまたは減少する、方法。
(項目39)
ANGPTL4(184〜406)に結合する抗体およびVEGFアンタゴニストを含む組成物。
(項目40)
ANGPTL4−SiRNA分子を含む組成物であって、該ANGPTL4−SiRNA分子が、ANGPTL4をコードする核酸のDNA配列をターゲティングし、該DNA配列が、少なくともGTGGCCAAGCCTGCCCGAAGA(配列番号3)を含む、組成物。
(項目41)
第1の量の抗血管形成薬、第2の量のアンジオポエチン様4(ANGPTL4)薬、および薬学的に受容可能なキャリア、賦形剤または希釈剤、ならびに容器を含むキット。
(項目42)
第1の単位投薬形態の一定量の抗血管形成薬および薬学的に受容可能なキャリア、賦形剤、または希釈剤;第2の単位投薬形態の一定量のアンジオポエチン様4(ANGPTL4)アンタゴニストおよび薬学的に受容可能なキャリア、賦形剤、または希釈剤;ならびに容器を含むキット。
定義
本発明を詳細に説明する前に、本発明は特定の組成物または生物系に制限されず、勿論、変化し得ると理解すべきである。本明細書中で使用した専門用語は特定の実施形態を説明することのみを目的とし、本発明を制限することを意図しないことも理解すべきである。本明細書および添付の特許請求の範囲で使用されるように、単数形「a」、「an」、および「the」には、明らかに別の内容を示さない限り、複数形が含まれる。したがって、例えば、「分子」には、任意選択的に、2つまたはそれを超えるこのような分子の組み合わせなどが含まれる。他で定義しない限り、全ての科学用語および技術用語は、関連分野で一般的に使用されているものと同一の意味を有すると理解される。本発明の目的のために、以下の用語を以下のように定義する。
100×分数X/Y
(式中、Xは、配列アラインメントプログラムALIGN−2によって、このプログラムのAおよびBのアラインメントにおいて完全な一致とスコアリングされたアミノ酸残基数であり、Yは、B中の総アミノ酸残基数である)。アミノ酸配列Aの長さはアミノ酸配列Bの長さと等しくなく、Bに対するAのアミノ酸同一率はAに対するBのアミノ酸同一率と等しくないと認識される。
(1)非極性:Ala(A)、Val(V)、Leu(L)、Ile(I)、Pro(P)、Phe(F)、Trp(W)、Met(M)
(2)非電荷極性:Gly(G)、Ser(S)、Thr(T)、Cys(C)、Tyr(Y)、Asn(N)、Gln(Q)
(3)酸性:Asp(D)、Glu(E)
(4)塩基性:Lys(K)、Arg(R)、His(H)
あるいは、天然に存在する残基を、以下のように共通の側鎖の性質に基づいて分類することができる。
(1)疎水性:ノルロイシン、Met、Ala、Val、Leu、Ile;
(2)中性疎水性:Cys、Ser、Thr、Asn、Gln;
(3)酸性:Asp、Glu;
(4)塩基性:His、Lys、Arg;
(5)鎖の配向に影響を与える残基:Gly、Pro;
(6)芳香族:Trp、Tyr、Phe
14:826(1996);Lonberg and Huszar,Intern.Rev.Immunol.13:65−93(1995)に記載されている。あるいは、ヒト抗体を、標的抗原に対して指向する抗体を産生するヒトBリンパ球(このようなBリンパ球を、個体から回収するか、インビトロで免疫化することができる)の不死化によって調製することができる。例えば、Cole et al.,Monoclonal Antibodies and Cancer Therapy,Alan R.Liss,p.77(1985);Boerner et al.,J.Immunol.,147(1):86−95(1991);および米国特許第5,750,373号を参照のこと。
of Proteins of Immunological Interest,5th Ed. Public Health Service,National Institutes of Health,Bethesda,MD.(1991)))および/または「超可変ループ」由来の残基(例えば、軽鎖可変ドメイン中の残基26〜32(L1)、50〜52(L2)、および91〜96(L3)、ならびに重鎖可変ドメイン中の26〜32(H1)、53〜55(H2)、および96〜101(H3)(Chothia and Lesk,J.Mol.Biol.196:901−917(1987)))を含む。「フレームワーク領域」または「FR」残基は、本明細書中で定義された超可変領域残基以外の可変ドメイン残基である。
ために使用する。好ましいFcRは、未変性配列のヒトFcRである。さらに、好ましいFcRは、IgG抗体に結合する(γ受容体)FcRであり、FcγRI、FcγRII、およびFcγRIIIサブクラスの受容体(これらの受容体の対立遺伝子改変体および選択的スプライシング形態が含まれる)が含まれる。FcγRII受容体には、主にその細胞質ドメインが異なる類似のアミノ酸配列を有するFcγRIIA(「活性化受容体」)およびFcγRIIB(「阻害受容体」)が含まれる。活性化受容体FcγRIIAは、その細胞質ドメイン中に免疫受容体チロシン活性化モチーフ(ITAM)を含む。阻害受容体FcγRIIIBは、その細胞質ドメイン中に、免疫受容体チロシン阻害モチーフ(ITIM)を含む(Daeron,Annu.Rev.Immunol.15:203
−234(1997)に概説)。FcRは、Ravetch and Kinet,Annu.Rev.Immunol 9:457−92(1991);Capel et al.,Immunomethods 4:25−34(1994);およびde Haas et al.,J.Lab.Clin.Med.126:330−41(1995)に概説されている。他のFcR(将来的に同定されるFcRが含まれる)は、本明細書中の用語「FcR」に含まれる。この用語には、母方のIgGの胎児への輸送を担う新生児受容体(neonatal receptor)(FcRn)も含まれる(Guyer et al.,J.Immunol.117:587(1976);およびKim et
al.,J.Immunol.24:249(1994))。
Spring Harbor Laboratory,Ed Harlow and David Lane(1988)などに記載の日常的な交差遮断(cross−blocking)アッセイを行うことができる。
疾患;ニューロン、神経膠細胞、星状細胞、視床下部、および他の腺、マクロファージ、
上皮、間質、および胞胚腔の障害;ならびに不適当な、異常な、過剰のおよび/または病
理学的な血管新生および/または血管透過性を生じる炎症性障害、血管形成障害、および免疫障害、血管障害が含まれる。
Murakami et al.(WB Saunders:Philadelphia,1995)(特に、p.13)に見出すことができる。
Society Transactions,14,pp.375−382,615th Meeting Belfast(1986)およびStella et al.,“Prodrugs:A Chemical Approach to Targeted Drug Delivery,” Directed Drug Delivery,Borchardt et al.,(ed.),pp.247−267,Humana Press(1985)を参照のこと。本発明のプロドラッグには、より活性な細胞傷害性遊離薬に変換することができるリン酸塩含有プロドラッグ、チオホスフェート含有プロドラッグ、硫酸塩含有プロドラッグ、ペプチド含有プロドラッグ、D−アミノ酸修飾プロドラッグ、グリコシル化プロドラッグ、βラクタム含有プロドラッグ、任意選択的に置換されたフェノキシアセトアミド含有プロドラッグまたは任意選択的に置換されたフェニルアセトアミド含有プロドラッグ、5−フルオロシトシンプロドラッグおよび他の5−フルオロウリジンプロドラッグが含まれるが、これらに限定されない。本発明で使用するためにプロドラッグ形態に誘導体化することができる細胞傷害薬の例には、上記の化学療法薬が含まれるが、これらに限定されない。
アンジオポエチン様4タンパク質(ANGPTL4)は、分泌タンパク質であり、アンジオポエチンファミリーのメンバーである。これは、肝臓フィブリノーゲン/アンジオポエチン関連タンパク質(HFARP)(Kim et al.,Biochem.J.346:603−610(2000))、PGAR(PPARγアンジオポエチン関連タンパク質)(Yoon,et al.,Mol.Cell Biol.,20:5343−5349(2000))、絶食誘発性脂肪因子(FIAF)(Kerten et al.,J.Biol.Chem.,275:28488−28493(2000));アンジオポエチン関連タンパク質(ARP−4);NL2(米国特許第6,348,350号;同第6,372,491号;および同第6,455,496を参照のこと);およびAng6としても公知である。
Biol.Chem.,279(33):34411−34420(2004)も参照のこと。ANGPTL4を、タンパク質分解的にプロセシングすることもできる。例えば、Ge et al.,J.Biol.Chem.,279(3):2038−2045(2004);およびMandard et al.,J.of Biol.Chem.,279(33):34411−34420(2004)も参照のこと。本明細書中に記載するように、ANGPTL4のR162GおよびR164E置換により、SDSゲル上で野生型(または未変性)タンパク質よりも高い分子量に泳動する変異ANGPTL4が得られる(図3、パネルBを参照のこと)。
ANGPTL4のモジュレーターは、ANGPTL4活性を調整する分子(例えば、アゴニストおよびアンタゴニスト)である。用語「アゴニスト」を、未変性のANGPTL4受容体(例えば、αVβ5インテグリン)を介してシグナルを伝達する能力を有する場合、ANGPTL4のペプチドアナログおよび非ペプチドアナログならびにこのようなANGPTL4分子に特異的に結合する抗体をいうために使用する。ANGPTL4受容体(例えば、αVβ5)の生物学的役割の文脈で、用語「アゴニスト」を定義する。特定の実施形態では、アゴニストは、上記に定義するように、未変性のANGPTL4の生物活性(細胞の増殖、移動、および/もしくは接着、ならびに/または脂質ホメオスタシス(homestasis)の調整など)を有する。
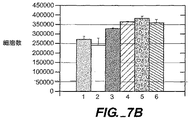
ANGPTL4は、癌標的に関与する。ANGPTL4は、いくつかの腫瘍細胞で発現される場合、インビトロおよびインビボでの腫瘍細胞増殖を引き起こす(例えば、図4、図5、図7、ならびに図8のパネルAおよびパネルBを参照のこと)。ANGPTL4が抗血管形成因子(例えば、抗VEGF抗体)で治療された腫瘍で発現した場合、腫瘍は成長能力を維持することができる(例えば、図8のパネルCを参照のこと)。ANGPTL4はまた、腫瘍細胞を移動させる(例えば、図9を参照のこと)。これは、腎癌で上方制御されることも示されている。例えば、代理人整理番号P5032R1;WO 02/07941;およびLe Jan et al.,American Journal of Pathology,162(5):1521−1528(2003)を参照のこと。さらに、ANGPTL4は血管形成促進因子(proangiogenic factor)であり(例えば、S.Le Jan et al.,Am.J.Pathol.,162(5):1521−1528(2003)を参照のこと)、癌療法の標的である。VEGFのように(Shweiki et al.,Proc.Natl.Acad.Sci,USA 92:768−772(1995)、ANGPTL4発現は、低酸素状態に応答して増加する。例えば、Le Jan et al.,American Journal of Pathology,162(5):1521−1528(2003)を参照のこと。
al.,“Biological Action of Leptin as an Angiogenic Factor” Science 281:1683−1686;(1998);Rupnick et al.,“Adipose tissue mass can be regulated through the vasculature” Proc.Nat.Acad.Sci.USA,99(16):10730−10735(2002);およびFukumura et al.,“Paracrine Regulation of Angiogenesis and Adipocyte Differentiation During In Vivo Adipogenesis.” Circ.Res.93:e88−e97(2003)を参照のこと。
disease)(膵炎、区画症候群、熱傷、腸疾患)、子宮筋腫、早産、慢性炎症(IBD(クローン病および潰瘍性大腸炎)など)、腎臓の同種移植片拒絶、炎症性腸疾患、ネフローゼ症候群、望ましくないか異常な組織塊の成長(非癌性)、肥満、脂肪組織塊の成長、血友病性関節、肥厚性瘢痕、発毛の抑制、オスラー−ウェーバー症候群、化膿性肉芽腫水晶体後線維増殖症、強皮症、トラコーマ、血管接着、滑膜炎、皮膚炎、子癇前症、腹水、心膜滲出液(心膜炎に関連する)、および胸膜滲出液が含まれるが、これらに限定されない。
上に示すように、本発明は、ANGPTL4アンタゴニストを別の治療薬と共に投与する併用療法を提供する。例えば、ANGPTL4アンタゴニストを、抗癌治療薬または抗新血管形成治療薬と組み合わせて使用して、種々の新生物容態または非新生物容態を治療する。一実施形態では、新生物容態または非新生物容態を、異常または望ましくない血管形成に関連する病理学的障害を特徴とする。ANGPTL4アンタゴニストを、同一組成物中または個別の組成物としてこれらの目的に有効な別の薬剤と連続的または組み合わせて投与することができる。あるいはまたはさらに、ANGPTL4の複数のインヒビターを投与することができる。
特定の態様では、本発明は、有効量のANGPTL4のアンタゴニストおよび/または血管形成インヒビターおよび1つまたは複数の化学療法薬を癌に感受性を示すか癌と診断された患者に投与することによる、腫瘍成長または癌細胞の増殖を遮断するかまたは減少させる方法を提供する。種々の化学療法薬を、本発明の併用治療方法で使用することができる。意図される化学療法薬の例示的且つ非限定的なリストを、本明細書中の「定義」に示す。
本発明はまた、腫瘍成長の再発または癌細胞増殖の再発を阻害または防止する方法および組成物を提供する。例えば、図8のパネルCは、腫瘍がANGPTL4も発現する場合に抗VEGF抗体(AVASTIN)で治療される腫瘍が治療を回避する能力(例えば、1つの再発型)を概略的に示す。
本発明の抗体には、抗ANGPTL4抗体および抗ANGPTL4フラグメント抗体、抗血管形成薬または血管形成インヒビターである抗体、抗癌薬である抗体、ANGPTL4受容体に対する抗体(例えば、抗αVβ5抗体)、または本明細書中に記載の他の抗体が含まれる。例示的な抗体には、例えば、ポリクローナル抗体、モノクローナル抗体、ヒト化抗体、フラグメント抗体、多重特異性抗体、ヘテロ抱合抗体、多価抗体、エフェクター機能抗体などが含まれる。
本発明の抗体は、ポリクローナル抗体を含み得る。ポリクローナル抗体の調製方法は、当業者に公知である。例えば、本発明の抗体に対するポリクローナル抗体を、関連抗原およびアジュバントの1回または複数回の皮下(sc)注射または腹腔内(ip)注射によって動物内に惹起する。二官能性剤または誘導体化剤(derivatizing agent)(例えば、マレイミドベンゾイルスルホスクシンイミドエステル(システイン残基を介して抱合)、N−ヒドロキシスクシンイミド(リジン残基を介する)、グルタルアルデヒド、無水コハク酸、SOCl2、またはR1N=C=NR(式中、RおよびR1は異なるアルキル基である))を使用して、免疫化すべき種で免疫原性を示すタンパク質(例えば、キーホールリンペットヘモシアニン、血清アルブミン、ウシサイログロブリン、またはダイズトリプシンインヒビター)に関連抗原を抱合するのに有用であり得る。
本明細書中に記載の抗原に対するモノクローナル抗体を、Kohler et al.,Nature,256:495(1975)に最初に記載されたハイブリドーマ法を使用して作製することができるか、組換えDNA法(米国特許第4,816,567号)によって作製することができる。
Practice,pp.59−103(Academic Press,1986))によって増殖させることができる。この目的に適切な培養培地には、例えば、D−MEM培地またはRPMI−1640培地が含まれる。さらに、ハイブリドーマ細胞を、動物内で腹水腫瘍としてインビボで増殖させることができる。
本発明の抗体は、ヒト化抗体またはヒト抗体を含み得る。ヒト化抗体は、これに移入された非ヒト供給源由来の1つまたは複数のアミノ酸残基を有する。しばしば、これらの非ヒトアミノ酸残基を、「導入(import)」残基といい、典型的には、「導入」可変領域から取り出される。本質的にWinter and co−workers(Jones et al.,Nature,321:522−525(1986);Riechmann et al.,Nature,332:323−327(1988);Verhoeyen et al.,Science,239:1534−1536(1988))の方法にしたがって、げっ歯類CDRまたはCDR配列へのヒト抗体の対応する配列の置換によってヒト化することができる。したがって、このような「ヒト化」抗体は、実質的にインタクト未満のヒト可変ドメインが非ヒト種由来の対応する配列に置換されたキメラ抗体(米国特許第4,816,567号)である。実際には、ヒト化抗体は、典型的には、いくつかのCDR残基およびおそらくいくつかのFR残基がげっ歯類抗体中の類似の部位由来の残基に置換されているヒト抗体である。
抗体フラグメントも本発明に含まれる。抗体フラグメント産生のための種々の技術が開発されている。伝統的には、これらのフラグメントは、インタクトな抗体のタンパク質分解性消化に由来していた(Morimoto et al.,Journal of Biochemical and Biophysical Methods 24:107−117(1992)およびBrennan et al.,Science,229:81(1985))を参照のこと)。しかし、現在、これらのフラグメントを、組換え宿主細胞によって直接産生することができる。例えば、抗体フラグメントを、上記で考察の抗体ファージライブラリーから単離することができる。あるいは、Fab’−SHフラグメントを、大腸菌から直接回収し、化学的にカップリングしてF(ab’)2フラグメントを形成することができる(Carter et al.,Bio/Technology 10:163−167(1992))。別のアプローチにしたがって、F(ab’)2フラグメントを、組換え宿主細胞培養物から直接単離することができる。抗体フラグメントの他の産生技術は、当業者に明らかである。他の実施形態では、最適な抗体は、一本鎖Fvフラグメント(scFv)である。WO 93/16185;米国特許第5,571,894号および米国特許第5,587,458号を参照のこと。FvおよびsFvは、定常領域を欠くインタクトな組み合わせ部位を有する唯一の種である。したがって、これらは、インビボでの非特異的結合の減少に適切である。sFv融合タンパク質を構築して、sFvのアミノ末端およびカルボキシ末端のいずれかにエフェクタータンパク質の融合物を得ることができる。Antibody Engineering,ed.Borrebaeck,supraを参照のこと。抗体フラグメントは、例えば、米国特許第5,641,870号に記載の「線状抗体」でもあり得る。このような線状抗体フラグメントは、単一特異性または二重特異性であり得る。
本発明の抗体には、例えば、少なくとも2つの異なる抗原に対する結合特異性を有する多重特異性抗体も含まれる。このような分子は、通常、2つの抗原のみに結合する一方で(すなわち、二重特異性抗体、BsAb)、本明細書中で使用される場合、三重特異性抗体などのさらなる特異性を有する抗体がこの表現に含まれる。BsAbの例には、腫瘍細胞抗原に指向する1つのアームおよび細胞傷害性誘発分子に指向する他のアームを有するBsAb(抗FcγRI/抗CD15、抗p185HER2/FcγRIII(CD16)、抗CD3/抗悪性B細胞(1D10)、抗CD3/抗p185HER2、抗CD3/抗p97、抗CD3/抗腎細胞癌、抗CD3/抗OVCAR−3、抗CD3/L−D1(抗結腸癌)、抗CD3/抗メラニン細胞刺激ホルモンアナログ、抗EGF受容体/抗CD3、抗CD3/抗CAMA1、抗CD3/抗CD19、抗CD3/MoV18、抗神経細胞接着分子(NCAM)/抗CD3、抗葉酸結合タンパク質(FBP)/抗CD3、抗膵臓癌(pan carcinoma)関連抗原(AMOC−31)/抗CD3など);腫瘍抗原に特異的に結合する1つのアームおよび毒素に結合する1つのアームを有するBsAb(抗サポリン/抗Id−1、抗CD22/抗サポリン、抗CD7/抗サポリン、抗CD38/抗サポリン、抗CEA/抗リシンA鎖、抗インターフェロン−α(IFN−α)/抗ハイブリドーマイディオタイプ、抗CEA/抗ビンカアルカロイドなど);変換酵素活性化プロドラッグのBsAb(抗CD30/抗アルカリホスファターゼ(リン酸マイトマイシンプロドラッグのマイトマイシンアルコールへの変換を触媒する)など);繊維素溶解薬として使用することができるBsAb(抗フィブリン/抗組織プラスミノゲンアクチベーター(tPA)、抗フィブリン/抗ウロキナーゼ型プラスミノゲンアクチベーター(uPA)など);免疫複合体を細胞表面受容体にターゲティングするためのBsAb(抗低密度リポタンパク質(LDL)/抗Fc受容体(例えば、FcγRI、FcγRII、またはFcγRIII)など);感染症の治療で使用されるBsAb(抗CD3/抗単純ヘルペスウイルス(HSV)、抗T細胞受容体:CD3複合体/抗インフルエンザ、抗FcγR/抗HIVなど);インビトロまたはインビボでの腫瘍検出のためのBsAb(抗CEA/抗EOTUBE、抗CEA/抗DPTA、抗p185HER2/抗ハプテンなど);ワクチンアジュバンとしてのBsAb;ならびに診断ツールとしてのBsAb(抗ウサギIgG/抗フェリチン、抗西洋ワサビペルオキシダーゼ(HRP)/抗ホルモン、抗ソマトスタチン/抗物質P、抗HRP/抗FITC、抗CEA/抗β−ガラクトシダーゼなど)が含まれる。三重特異性抗体の例には、抗CD3/抗CD4/抗CD37、抗CD3/抗CD5/抗CD37、および抗CD3/抗CD8/抗CD37が含まれる。全長抗体または抗体フラグメント(例えば、F(ab’)2二重特異性抗体)として二重特異性抗体を調製することができる。
二重特異性抗体には、架橋または「ヘテロ複合体(heteroconjugate)」抗体が含まれ、本発明の抗体である。例えば、ヘテロ複合体中の抗体の一方をアビジンにカップリングし、他方をビオチンにカップリングすることができる。このような抗体は、例えば、免疫系細胞の望ましくない細胞へのターゲティング(米国特許第4,676,980号)およびHIV感染症の治療(WO 91/00360、WO 92/200373、欧州特許第03089号)が提案されている。ヘテロ複合体抗体を、任意の従来の架橋法を使用して作製することができる。適切な架橋剤は当該分野で周知であり、多数の架橋技術と共に米国特許第4,676,980号に開示されている。
本発明の抗体には、多価抗体が含まれる。多価抗体を、抗体が結合する抗原を発現する細胞によって2価抗体よりも迅速に内在化(および/または異化)することができる。本発明の抗体は、3つまたはそれを超える抗原結合部位を有し、抗体のポリペプチド鎖をコードする核酸の組換え発現によって容易に産生することができる(IgMクラス以外の)多価抗体(例えば、4価抗体)であり得る。多価抗体は、二量体化ドメインおよび3つまたはそれを超える抗原結合部位を含み得る。好ましい二量体化ドメインは、Fc領域またはヒンジ領域を含む(またはこれらからなる)。このシナリオでは、抗体は、Fc領域およびFc領域のアミノ末端側に3つまたはそれを超える抗原結合部位を含む。本明細書中の好ましい多価抗体は、3〜約8個の抗原結合部位を含むが(またはこれらからなる)、4つが好ましい。多価抗体は、少なくとも1つのポリペプチド鎖(および好ましくは2つのポリペプチド鎖)を含み、ポリペプチド鎖は2つまたはそれを超える可変ドメインを含む。例えば、ポリペプチド鎖は、VD1−(X1)n−VD2−(X2)n−Fc(式中、VD1は第1の可変ドメインであり、VD2は第2の可変ドメインであり、FcはFc領域の1つのポリペプチド鎖であり、X1およびX2はアミノ酸またはポリペプチドを示し、nは0または1である)を含み得る。例えば、ポリペプチド鎖は、VH−CH1−可動性リンカー−VH−CH1−Fc領域鎖またはVH−CH1−VH−CH1−Fc領域鎖を含み得る。本明細書中の多価抗体は、好ましくは、少なくとも2つ(好ましくは4つ)の軽鎖可変ドメインポリペプチドをさらに含む。本明細書中の多価抗体は、例えば、約2〜約8個の軽鎖可変ドメインポリペプチドを含み得る。本明細書中で意図される軽鎖可変ドメインポリペプチドは、軽鎖可変ドメインを含み、任意選択的に、CLドメインをさらに含む。
例えば、癌治療における抗体の有効性を増強するために、エフェクター機能に関して本発明の抗体を修飾することが望ましいかもしれない。例えば、システイン残基をFc領域に移入し、それにより、この領域中の鎖間ジスルフィド結合を形成することができる。このようにして生成されたホモ二量体抗体は、内在化能力が改良され、そして/または補体媒介性細胞死滅および抗体依存性細胞傷害性(ADCC)を増加させることができる。Caron et al.,J.Exp Med.176:1191−1195(1992)およびShopes,B.J.Immunol.148:2918−2922(1992)を参照のこと。抗腫瘍活性が増強されたホモ二量体を、Wolff et al.,Cancer Research 53:2560−2565(1993)に記載のように、ヘテロ二官能性架橋剤を使用して調製することもできる。あるいは、二重Fc領域を有し、それにより、補体溶解およびADCC能力を増強することができるように抗体を操作することができる。Stevenson et al.,Anti−Cancer Drug Design 3:219−230(1989)を参照のこと。抗体の血清半減期を増加させるために、例えば、米国特許第5,739,277号に記載されているように、抗体(特に、抗体フラグメント)にサルベージ(salvage)受容体結合エピトープを組み込むことができる。本明細書中で使用される、用語「サルベージ受容体結合エピトープ」は、IgG分子のインビボ血清半減期の増加を担うIgG分子(例えば、IgG1、IgG2、IgG3、またはIgG4)のFc領域のエピトープをいう。
本発明はまた、治療薬、毒素(例えば、細菌、真菌、植物、または動物を起源とする酵素活性毒素またはそのフラグメント)、または放射性同位体(すなわち、放射性複合体(radioconjugate))などの細胞傷害薬に抱合した本明細書中に記載の抗体を含む免疫複合体に関する。放射性複合体抗体の産生のために、種々の放射性核種を利用可能である。例には、212Bi、131I、131In、90Y、および186Reが含まれるが、これらに限定されない。
238:1098(1987)に記載のように調製することができる。炭素−14標識1−イソチオシアナトベンジル−3−メチルジエチレントリアミン五酢酸(MX−DTPA)は、抗体への放射性ヌクレオチドの抱合のための例示的キレート剤である。WO 94/11026を参照のこと。リンカーは、細胞中の細胞傷害薬の放出を容易にする「切断リンカー」であり得る。例えば、酸不安定性リンカー、ペプチダーゼ感受性リンカー、感光リンカー、ジメチルリンカー、またはジスルフィド含有リンカー(Chari et
al.,Cancer Research 52:127−131(1992);米国特許第5,208,020号)を使用することができる。
本発明は、1つまたは複数のマイタンシノイド分子に抱合した本発明の抗体を提供する。マイタンシノイドは、チューブリン重合の阻害によって作用する有糸分裂(mitototic)インヒビターである。マイタンシンは、東アフリカの低木マイテナス・セラタ(Maytenus serrata)から最初に単離された(米国特許第3,896,111号)。その後、一定の微生物がマイタンシノイド(マイタンシノール(maytansinol)およびC−3マイタンシノールエステルなど)も産生することが発見された(米国特許第4,151,042号)。合成マイタンシノールならびにその誘導体およびアナログは、例えば、米国特許第4,137,230号;同第4,248,870号;同第4,256,746号;同第4,260,608号;同第4,265,814号;同第4,294,757号;同第4,307,016号;同第4,308,268号;同第4,308,269号;同第4,309,428号;同第4,313,946号;同第4,315,929号;同第4,317,821号;同第4,322,348号;同第4,331,598号;同第4,361,650号;同第4,364,866号;同第4,424,219号;同第4,450,254号;同第4,362,663号;および同第4,371,533号に開示されている。
別の目的の免疫複合体は、1つまたは複数のカリケアマイシン分子と抱合した本発明の抗体を含む。抗生物質のカリケアマイシンファミリーは、ピコモル以下の濃度で二本鎖DNAを破壊することができる。カリケアマイシンファミリーの複合体の調製については、米国特許第5,712,374号、同第5,714,586号、同第5,739,116号、同第5,767,285号、同第5,770,701号、同第5,770,710号、同第5,773,001号、同第5,877,296号(全てAmerican Cyanamid Company)を参照のこと。使用することができるカリケアマイシンの構造アナログには、γ1 I、α2 I、α3 I、N−アセチル−γ1 I、PSAG、およびθI 1(Hinman et al.,Cancer Research 53:3336−3342(1993),Lode et al.,Cancer Research 58:2925−2928(1998)および上記のAmerican Cyanamidの米国特許)が含まれるが、これらに限定されない。抗体を抱合することができる別の抗腫瘍薬は、葉酸拮抗薬であるQFAである。カリケアマイシンおよびQFAは共に細胞内作用部位を有し、原形質膜を容易に通過しない。したがって、抗体媒介性内在化によるこれらの薬剤の細胞取り込みにより、その細胞傷害作用が非常に増強される。
他の抗体修飾が本明細書中で意図される。例えば、抗体を、種々の非タンパク質性ポリマー(例えば、ポリエチレングリコール、ポリプロピレングリコール、ポリオキシアルキレン、またはポリエチレングリコールとポリプロピレングリコールとのコポリマー)のうちの1つと結合することができる。抗体を、例えば、コアセルベーション技術または界面重合によって調製されたマイクロカプセル(例えば、それぞれ、ヒドロキシメチルセルロースまたはゼラチンマイクロカプセル、およびポリ−(メチルメタクリレート)マイクロカプセル)、コロイド状薬物送達系(例えば、リポソーム、アルブミンミクロスフェア、マイクロエマルジョン、ナノ粒子、およびナノカプセル)、またはマクロエマルジョン中に捕捉することができる。このような技術は、Remington’s Pharmaceutical Sciences,16th edition,Oslo,A.,Ed.,(1980)に開示されている。
本発明のポリペプチドを、リポソーム中に処方することができる。例えば、本発明の抗体を、免疫リポソームとして処方することができる。抗体を含むリポソームを、Epstein et al.,Proc.Natl.Acad.Sci.USA,82:3688(1985);Hwang et al.,Proc.Natl Acad.Sci.USA,77:4030(1980);および米国特許第4,485,045号および同第4,544,545号などに記載の当該分野で公知の方法によって調製する。循環時間が造抗されたリポソームは、米国特許第5,013,556号に開示されている。一般に、リポソームの処方および使用は、当業者に公知である。
本発明の抗体には種々の用途がある。例えば、抗ANGPTL4抗体を、ANGPTL4の診断アッセイ(例えば、癌検出(例えば、腎癌検出)のための特定の細胞、組織、または血清におけるその発現の検出など)で使用することができる。一実施形態では、ANGPTL4抗体を、本明細書中に提供した方法を使用した治療のための患者集団(例えば、ANGPTL4を発現する患者、ANGPTL4が上昇した患者、ANGPTL4レベルに感受性を示す癌患者)の選択のために使用する。当該分野で公知の種々の診断アッセイ技術(競合結合アッセイ、直接または間接的サンドイッチアッセイ、および均一相または不均一相において行った免疫沈降アッセイなど)を使用することができる(Zola,Monoclonal Antibodies:A Manual of Techniques,CRC Press,Inc.(1987)pp.147−158)。診断アッセイで使用する抗体を、検出可能な部分で標識することができる。検出可能な部分は、直接または間接的に検出可能なシグナルを生じることができるはずである。例えば、検出可能な部分は、放射性同位体(3H、14C、32P、35S、または125Iなど)、蛍光化合物、化学発光化合物(フルオレセインイソチオシアネート、ローダミン、またはルシフェリンなど)、または酵素(アルカリホスファターゼ、β−ガラクトシダーゼ、または西洋ワサビペルオキシダーゼなど)であり得る。当該分野で公知の検出可能部分に抗体を抱合する任意の方法(Hunter et al.,Nature,144:945(1962);David et al.,Biochemistry,13:1014(1974);Pain et al.,J.Immunol.Meth.,40:219(1981);およびNygren,J.Histochem.And Cytochem.,30:407(1982)に記載の方法が含まれる)を使用することができる。
本発明のポリペプチド(例えば、ポリペプチドアンタゴニストフラグメント、融合分子(例えば、免疫融合分子)、本発明の抗体)の共有結合修飾は、本発明の範囲内に含まれる。適切な場合、ポリペプチドの化学合成または酵素切断もしくは化学的切断によってこれを行うことができる。ターゲティングされたポリペプチドのアミノ酸残基と選択された側鎖、N末端残基、もしくはC末端残基と反応することができる有機誘導体化剤との反応または修飾アミノ酸もしくは非天然アミノ酸の成長中のポリペプチド鎖への組み込みによって、他のポリペプチドの共有結合修飾型を分子に移入する(例えば、Ellman et al.,Meth.Enzym.202:301−336(1991);Noren
et al.,Science 244:182(1989);ならびに米国特許出願公開番号20030108885号および同第20030082575号)。
本発明のポリペプチドを、容易に入手可能な技術および材料を使用した組換えによって産生することができる。
本発明のポリペプチドを、組換えによって直接産生することができるだけでなく、異種ポリペプチド(典型的には、成熟タンパク質またはポリペプチドのN末端に特異的切断部位を有するシグナル配列または他の配列である)との融合ポリペプチドとして産生することもできる。選択された異種シグナル配列は、典型的には、宿主細胞によって認識およびプロセシングされた(すなわち、シグナルペプチドによって切断された)配列である。未変性のポリペプチドシグナル配列を認識およびプロセシングしない原核宿主細胞については、シグナル配列を、例えば、アルカリホスファターゼ、ペニシリナーゼ、lpp、または熱安定性エンテロトキシンIIリーダーの群から選択される原核生物シグナル配列に置換する。酵母分泌のために、未変性シグナル配列を、例えば、酵母インベルターゼリーダー、α因子リーダー(サッカロミセス属およびクリベロミセス属のα因子リーダーが含まれる)、酸ホスファターゼリーダー、カンジタ・アルビカンスのグルコアミラーゼリーダー、またはWO 90/13646に記載のシグナルに置換することができる。哺乳動物細胞発現では、哺乳動物シグナル配列およびウイルス分泌リーダー(例えば、単純ヘルペスgDシグナル)が利用可能である。
発現ベクターおよびクローニングベクターは共に、1つまたは複数の選択された宿主細胞中でベクターが複製することができる核酸配列を含む。一般に、クローニングベクターでは、この配列は、宿主染色体DNAと無関係にベクターが複製することができる配列であり、複製起点または自己複製配列が含まれる。このような配列は、種々の細菌、酵母、およびウイルスで周知である。プラスミドpBR322由来の複製起点は、ほとんどのグラム陰性細菌に適切であり、2μプラスミドの複製起点は酵母に適切であり、種々のウイルスの複製起点(SV40、ポリオーマ、アデノウイルス、VSV、またはBPV)は哺乳動物細胞におけるクローニングベクターに有用である。一般に、複製起点成分は、哺乳動物発現ベクターに必要ない(初期プロモーターを含むので、典型的にはSV40の複製起点のみを使用することができる)。
発現ベクターおよびクローニングベクターは、選択マーカーとも呼ばれる選択遺伝子を含み得る。典型的な選択遺伝子は、抗生物質または他の毒素(例えば、アンピシリン、ネオマイシン、メトトレキセート、またはテトラサイクリン)に対する耐性を付与するか、(b)栄養要求性欠損を補足するか、(c)天然培地から利用できない重要な栄養素を供給するタンパク質をコードする(例えば、バチルス属のD−アラニンラセマーゼをコードする遺伝子)。
selection)の例は、薬物ネオマイシン、ミコフェノール酸、およびハイグロマイシンを使用する。
発現ベクターおよびクローニングベクターは、通常、宿主生物によって認識され、本発明のポリペプチドをコードする核酸に作動可能に連結されたプロモーターを含む。原核生物宿主と共に使用するのに適切なプロモーターには、phoAプロモーター、β−ラクタマーゼおよびラクトースプロモーター系、アルカリホスファターゼ、トリプトファン(trp)プロモーター系、ならびにtacプロモーターなどのハイブリッドプロモーターが含まれる。しかし、他の公知の細菌プロモーターも適切である。細菌系で使用されるプロモーターは、本発明のポリペプチドをコードするDNAに作動可能に連結されたシャイン−ダルカルノ(S.D.)配列も含む。
高等真核生物による本発明のポリペプチドをコードするDNAの転写を、しばしば、ベクターへのエンハンサー配列の挿入によって増加させる。現在、哺乳動物遺伝子由来の多数のエンハンサー配列が公知である(グロビン、エラスターゼ、アルブミン、α−フェトプロテイン、およびインスリン)。典型的には、真核生物細胞ウイルス由来のエンハンサーを使用する。例には、複製起点の後期側(bp100〜270)のSV40エンハンサー、サイトメガロウイルス初期プロモーターエンハンサー、複製起点の後期側のポリオーマエンハンサー、およびアデノウイルスエンハンサーが含まれる。真核生物プロモーターの活性化エレメントの増強については、Yaniv,Nature 297:17−18(1982)も参照のこと。エンハンサーを、ベクター中のポリペプチドコード配列の5’位または3’位にスプライシングすることができるが、典型的には、プロモーターから5’位に配置する。
真核生物宿主細胞(酵母、真菌、昆虫、植物、動物、ヒト、または他の多細胞生物由来の有核細胞)で使用される発現ベクターは、転写終結およびmRNAの安定化に必要な配列も含む。このような配列は、真核生物またはウイルスのDNAまたはcDNAの一般に5’、時折3’の非翻訳領域から利用可能である。これらの領域は、本発明のポリペプチドをコードするmRNAの非翻訳部分にポリアデニル化部位として転写されるヌクレオチドセグメントを含む。1つの有用な転写終結成分は、ウシ成長ホルモンポリアデニル化領域である。WO 94/11026およびこれに開示されている発現ベクターを参照のこと。
本明細書中のベクターにおける本発明のポリペプチドをコードするDNAをクローニングまたは発現する適切な宿主細胞は、上記の原核細胞、酵母細胞、または高等真核細胞である。この目的に適切な原核生物には、グラム陰性またはグラム陽性生物などの真正細菌(例えば、腸内細菌科(大腸菌属(例えば、大腸菌、エンテロバクター、エルウィニア、クレブシエラ、プロテウス、サルモネラ(例えば、ネズミチフス菌)、セラチア(例えば、セラチア・マルセスカンス)、および赤痢菌など)、ならびに桿菌(枯草菌、バチルス・リケニホルミス(例えば、1989年4月12日公開のDD 266,710に開示のバチルス・リケニホルミス41P)など)、シュードモナス(緑膿菌など)および放線菌類)が含まれる。典型的には、大腸菌クローニング宿主は、大腸菌294(ATCC 31,446)であるにもかかわらず、大腸菌B株、大腸菌X1776株(ATCC 31,537)、および大腸菌W3110株(ATCC 27,325)などの他の株も適切である。これらの例は、制限ではなく、むしろ例示である。
本発明のポリペプチドを産生するのに使用される宿主細胞を、種々の培地中で培養することができる。Ham’s F10(Sigma)、最少必須培地((MEM)(Sigma)、RPMI−1640(Sigma)、およびダルベッコ改変イーグル培地((DMEM)Sigma)などの市販されている培地が宿主細胞の培養に適切である。さらに、Ham et al.,Meth.Enz.58:44(1979),Barnes et al.,Anal.Biochem.102:255(1980)、米国特許第4,767,704号;同第4,657,866号;同第4,927,762号;同第4,560,655号;または同第5,122,469号;WO 90/03430;WO 87/00195;または米国特許再発行30,985号に記載の任意の培地を、宿主細胞の培養培地として使用することができる。これらの培地のいずれかに、必要に応じて、ホルモンおよび/または他の成長因子(インスリン、トランスフェリン、または上皮成長因子など)、塩(塩化ナトリウム、カルシウム、マグネシウム、およびリン酸塩など)、緩衝液(HEPESなど)、ヌクレオチド(アデノシンおよびチミジンなど)、抗生物質(ゲンタマイシン(商標)薬など)、微量元素(通常、μモル範囲の最終濃度で存在する無機化合物と定義する)、およびグルコースまたは等価なエネルギー源を補足することができる。任意の他の必要な栄養補助剤を、当業者に公知の適切な濃度で含めることもできる。培養条件(温度およびpHなど)は、発現のために選択した宿主細胞で以前に使用した条件であり、当業者に明らかである。
組換え技術を使用する場合、本発明のポリペプチド(例えば、ANGPTL4)、本発明の抗体(例えば、抗ANGPTL4抗体、抗αVβ5抗体、または抗血管形成分子抗体)を、細胞内に産生するか、細胞膜周辺腔中に産生するか、培地に直接分泌させることができる。本発明のポリペプチドを、培養培地または宿主細胞溶解物から回収することができる。膜に結合している場合、適切な界面活性剤溶液(例えば、Triton−X 100)を使用するか、酵素切断によって膜から放出させることができる。本発明のポリペプチド発現で使用される細胞を、種々の物理的手段または化学的手段(凍結融解サイクル、超音波処理、機械的破壊、または細胞溶解剤など)によって破壊することができる。
保存のための凍結乾燥処方物または水溶液の形態の本発明のポリペプチド、本発明の分子、およびその組み合わせの治療処方物ならびに本発明にしたがって使用される本明細書中に記載の治療処方物を、所望の精製度のポリペプチドと任意選択的な薬学的に受容可能なキャリア、賦形剤、または安定剤(Remington’s Pharmaceutical Sciences 16th edition,Osol,A.Ed.[1980])との混合によって調製する。受容可能なキャリア、賦形剤、または安定剤は、使用される投薬量および濃度でレシピエントに無毒であり、緩衝液(リン酸緩衝液、クエン酸緩衝液、および他の有機酸の緩衝液など);抗酸化剤(アスコルビン酸およびメチオニンが含まれる);防腐剤(オクタデシルジメチルベンジルアンモニウムクロリド;塩化ヘキサメトニウム;塩化ベンザルコニウム、塩化ベンゼトニウム;フェノール、ブチル、またはベンジルアルコール;アルキルパラベン(メチルパラベンまたはプロピルパラベンなど);カテコール;レゾルシノール;シクロヘキサノール;3−ペンタノール;およびm−クレゾールなど);低分子量(約10残基未満)ポリペプチド;タンパク質(血清アルブミン、ゼラチン、または免疫グロブリンなど);親水性ポリマー(ポリビニルピロリドンなど);アミノ酸(グリシン、グルタミン、アスパラギン、ヒスチジン、アルギニン、またはリジンなど);モノサッカリド、ジサッカリド、および他の炭水化物(グルコース、マンノース、またはデキストリンが含まれる);キレート剤(EDTAなど);糖(スクロース、マンニトール、トレハロース、またはソルビトールなど);塩形成対イオン(ナトリウムなど);金属複合体(例えば、Zn−タンパク質複合体);および/または非イオン性界面活性剤(TWEEN(商標)、PLURONICS(商標)、またはポリエチレングリコール(PEG)など)が含まれる。
公知の方法(ボーラスとしての静脈内投与、長期間にわたる連続的注入、筋肉内投与、腹腔内投与、脳脊髄内(intracerobrospinal)投与、皮下投与、関節内投与、髄液嚢内投与、鞘内、経口投与、局所投与、または吸入経路、および/または皮下投与など)にしたがって、本発明の分子を、ヒト患者に投与する。
本発明の治療有効性を、新生物障害または非新生物障害の評価で一般的に使用されている種々の終点によって測定することができる。例えば、癌治療を、例えば、腫瘍の緩解、腫瘍重量、またはサイズの縮小、無増悪期間、生存期間、無増悪生存率、全奏功率、奏功期間、および生活の質によって評価することができる。本明細書中に記載の抗血管形成薬が腫瘍血管系をターゲティングし、必ずしも新生物細胞自体ではないので、抗血管形成薬は固有の抗癌薬クラスを示し、それにより、薬物に対する臨床反応を固有に測定および定義する必要があり得る。例えば、二次元分析における50%を超える腫瘍の縮小は、応答を宣言するための標準的なカットオフである。しかし、本発明のインヒビターは、原発性腫瘍を縮小させることなく転移の拡大を阻害することができるか、単純に腫瘍静止効果(tumouristatic effect)を発揮することができる。したがって、治療法の有効性を決定するアプローチ(例えば、血管形成の血漿マーカーまたは尿マーカーの測定および放射線画像化による応答の測定が含まれる)を使用することができる。
本発明の別の実施形態では、上記の障害の治療に有用な材料を含む製品を提供する。製品は、容器、ラベル、および添付文書を含む。適切な容器には、例えば、ボトル、バイアル、シリンジなどが含まれる。容器を、ガラスまたはプラスチックなどの種々の材料から形成することができる。容器は、容態治療に有効な組成物を保持し、滅菌アクセスポートを有し得る(例えば、容器は、皮下注射針で突き刺すことができるストッパーを有する静脈注射用溶液バッグまたはバイアルであり得る)。組成物中の少なくとも1つの活性成分は、ANGPTL4モジュレーターである。容器上または容器に封入したラベルは、最適な容態の治療のために組成物を使用することを示す。製品は、さらに、薬学的に受容可能な緩衝液(リン酸緩衝化生理食塩水など)、リンゲル液、およびデキストロース溶液を含む第2の容器を含み得る。製品は、さらに、商業的および使用者の観点から望ましい他の材料(さらなる活性成分、他の緩衝液、希釈剤、フィルター、ニードル、およびシリンジが含まれる)を含む。
以下の材料を、American Type Culture Collection,10801 University Boulevard,Manassas,VA.20110−2209,USA(ATCC)に寄託した。
アデノウイルスベクターの生成および形質導入。アデノウイルス構築物を、本質的に製造者が説明するように、Stratagene(LaJolla,CA)のAd−easyベクター構築キットのポリリンカー部位へのNot1−Not1 cDNAインサートのクローン化によって構築した。例えば、Hesser et al.,Blood,104(1):149−158(2004)を参照のこと。
ースラインまで洗浄し、50mMクエン酸ナトリウム(pH3.0)で溶離した。この体積を、Amicon−15 10,000MWCO(Millipore#UFC901024)で濃縮した。最終工程は、1mM HCl/SuperQ水への透析および0.2μmの濾過であった。4〜20%のトリス/グリシン(Invitrogen#EC6028box)SDSpageゲル+/−10mM DTTを使用して、純度を決定した。正確なタンパク質を、質量分析またはエドマンN末端配列決定によって同定した。
ムを、PBSでベースラインまで洗浄した。次いで、4カラム体積の0.5M TMAC/PBS(pH7.5)洗浄工程を行い、その後、ベースラインまでPBS洗浄を行った。溶離工程は、50mMクエン酸ナトリウム(pH3.0)バンプ(bump)であった。この体積を、Amicon−15 10,000MWCO(Millipore#UFC901024)で濃縮した。最終工程は、1mM HCl/SuperQ水への透析および0.2μmの濾過であった。4〜20%のトリス/グリシン(Invitrogen#EC6028box)SDSpageゲル+/−10mM DTTを使用して、純度を決定する。正確なタンパク質を、質量分析またはエドマンN末端配列決定によって同定した。当該分野で公知の標準的技術を使用して、組換えタンパク質を作製することもできる。
ANGPTL4は、抗血管形成薬(例えば、抗VEGF)(AVASTIN(登録商標)(Genentech,South San Francisco)など)で処置した腫瘍における腫瘍細胞増殖を刺激した。図8のパネルCを参照のこと。ヒトA673横紋筋肉腫細胞(HTB 1598)を、以前に記載のように培養した(Kim et al.,Nature 362:841−844(1993);およびGerber et al.,Cancer Research,60:6253−6258(2000))。5×106個のA673細胞を含む0.1mlのMatrigelを、ベージュヌードマウス(Harlan Sprague Dawley)の背側の側腹部に皮下注射して異種移植片を確立させた。アデノウイルス構築物を、7日毎に(1、7、14、21、28日目に)1×108プラーク形成単位(PFU)で腫瘍内に(IT)注射した。アデノウイルス構築物は、アデノウイルス−ANGPTL4構築物(Ad−Angptl4)、コントロールとしてのアデノウイルス−LacZ構築物(Ad−LacZ)、またはアデノウイルス−ANGPTL3構築物(Ad−Angptl3)であった。マウスにAvastin(登録商標)(Genentech)を、5mg/kgの用量で1週間に2回腹腔内を処置した。28ゲージの針および0.5mlのツベルクリンシリンジを使用して、腫瘍塊の側面および底面に直接注射した。2日毎に腫瘍サイズを測定し、楕円体積の式(π/6×L×W×H(式中、L=長さ、W=幅、H=高さ);Tomayko & Reynolds,Cancer Chemother.Pharmacol.,24:148−154(1989))を使用して腫瘍体積を計算した。図8のパネルCに示すように、腫瘍サイズは、AVASTIN(登録商標)治療と組み合わせたAd−LacZまたはAd−Angptl3構築物を含む細胞を注射したマウスと比較して、AVASTIN(登録商標)で処置したにもかかわらず、A673細胞およびアデノウイルス−ANGPTL4構築物(Ad−Angptl4)を注射したマウスで増加した。
抗ANGPTL4抗体がANGPTL4の生物活性(例えば、腫瘍細胞の増殖)を阻害する能力を試験した。1×104腫瘍細胞(例えば、HeLa−S3、Caki、U87MG、293、A673、HM7、およびCalu6)/ウェルを、10%FCSを含む培地中の12ウェルプレートにプレートした。細胞を、5%CO2加湿インキュベーター中にて37℃で一晩インキュベートした。培地を、5%FCSと交換し(10%FCSを含むCalu6細胞以外)、1、2.5、5、または10μg/mlの抗hANGPTL4抗体または抗Dscrをウェルに添加するか、抗体を添加しなかった。プレートを、37℃の5%CO2加湿インキュベーター中に入れた。抗hANGPTL4抗体の添加から2または3日後に細胞を計数した。抗ANGPTL4抗体は、HeLa−S3、Caki
U87MG、293、A673、およびCalu 6の細胞成長を阻害したが、HM7細胞は阻害されなかった。図10のパネルAおよびBを参照のこと。
ポリクローナル抗体およびモノクローナル抗体の産生技術は、当該分野で公知であり、本明細書中に記載されている。使用することができる抗原(または免疫原)には、本発明の精製タンパク質、タンパク質フラグメント、このようなタンパク質を含む融合タンパク質、ならびに細胞表面上に組換えタンパク質および/またはタンパク質フラグメントを発現する細胞が含まれる。当業者は、過度に実験することなく、抗原を選択することができる。
本明細書中に記載の抗体を、当該分野で公知の種々の技術(例えば、ELISA)によって同定することができる。例えば、プレートを、目的のポリペプチド(例えば、ANGPTL4またはそのフラグメント)でコーティングし、このポリペプチド(例えば、ANGPTL4)に対して生成された抗体とインキュベートした(例えば、米国特許第6,348,350号、同第6,372,491号、および同第6,455,496号の説明を参照のこと)。結合した抗体を、種々の方法によって検出することができる。
アンジオポエチンは、そのフィブリノーゲン(FBN)様ドメインを介した内皮細胞特異性チロシンキナーゼ受容体Tie2への結合によって血管形成を調節する分泌性因子である。分泌性リガンドファミリー中に存在するコイルドコイルドメインは、リガンドオリゴマー形成に必要であることが見出された(例えば、Procopio et al.,J.Biol.Chem.,274:30196−201(1999)を参照のこと)。
MgCl2、100mM NaCl)中で調製し、30分間インキュベートした。サンプルをプレートに添加し(100μl/ウェル、上記でインキュベートした量)、穏やかに震盪しながら室温で2時間インキュベートした。プレートを緩衝液で洗浄し、100μl/ウェル抗Flag−西洋ワサビペルオキシダーゼ(HRP)(100ng/ml)(Jackson,#109−036−098)を含むアッセイ緩衝液(PBS(pH7.
4)、0.5%BSA、0.05%Tween20)を添加し、穏やかに震盪しながら室温で1時間インキュベートした。プレートを洗浄した。100μl/ウェルのテトラメチルベンジジン(TMB)(Moss,Inc.)を添加し、室温で良好に発色するまでプレート中でインキュベートした。100μl/ウェルの停止液(1M H3PO4)を添加して、反応を停止させた。プレートを、630nmで読み取った。mANGPTL4、IgG−hANGPTL4−N末端、およびIgG−hANGPTL4−C末端はαVβ5コーティングプレートに結合したが、IgG−hANGPTL4−C末端がプレートにわずかにより結合した。図13のパネルAを参照のこと。
Claims (1)
- 明細書に記載の発明。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US58978204P | 2004-07-20 | 2004-07-20 | |
| US60/589,782 | 2004-07-20 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007522697A Division JP4947717B2 (ja) | 2004-07-20 | 2005-07-19 | アンジオポエチン様4タンパク質のインヒビター、組み合わせ、およびそれらの使用 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2012017331A true JP2012017331A (ja) | 2012-01-26 |
Family
ID=35787710
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007522697A Expired - Fee Related JP4947717B2 (ja) | 2004-07-20 | 2005-07-19 | アンジオポエチン様4タンパク質のインヒビター、組み合わせ、およびそれらの使用 |
| JP2011175420A Withdrawn JP2012017331A (ja) | 2004-07-20 | 2011-08-10 | アンジオポエチン様4タンパク質のインヒビター、組み合わせ、およびそれらの使用 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007522697A Expired - Fee Related JP4947717B2 (ja) | 2004-07-20 | 2005-07-19 | アンジオポエチン様4タンパク質のインヒビター、組み合わせ、およびそれらの使用 |
Country Status (23)
| Country | Link |
|---|---|
| US (2) | US7740846B2 (ja) |
| EP (3) | EP2361931B1 (ja) |
| JP (2) | JP4947717B2 (ja) |
| KR (1) | KR101254815B1 (ja) |
| CN (2) | CN101044164A (ja) |
| AT (1) | ATE456579T1 (ja) |
| AU (2) | AU2005269716B2 (ja) |
| BR (1) | BRPI0513534A (ja) |
| CA (1) | CA2574758A1 (ja) |
| CY (1) | CY1109931T1 (ja) |
| DE (1) | DE602005019167D1 (ja) |
| DK (1) | DK1771474T3 (ja) |
| ES (1) | ES2339789T3 (ja) |
| IL (1) | IL180725A0 (ja) |
| MX (1) | MX2007000784A (ja) |
| NO (1) | NO20070951L (ja) |
| NZ (1) | NZ552956A (ja) |
| PL (1) | PL1771474T3 (ja) |
| PT (1) | PT1771474E (ja) |
| RU (1) | RU2392966C2 (ja) |
| SI (1) | SI1771474T1 (ja) |
| WO (1) | WO2006014729A2 (ja) |
| ZA (1) | ZA200701183B (ja) |
Families Citing this family (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6582959B2 (en) * | 1991-03-29 | 2003-06-24 | Genentech, Inc. | Antibodies to vascular endothelial cell growth factor |
| US20050123925A1 (en) | 2002-11-15 | 2005-06-09 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| WO2005007819A2 (en) | 2003-07-09 | 2005-01-27 | Wisconsin Alumni Research Foundation | Charge-dynamic polymers and delivery of anionic compounds |
| WO2006014678A2 (en) | 2004-07-20 | 2006-02-09 | Genentech, Inc. | Compositions and methods of using angiopoietin-like 4 protein |
| ES2339789T3 (es) | 2004-07-20 | 2010-05-25 | Genentech, Inc. | Inhibidores de proteina 4 de tipo angiopoyetina, combinaciones y su utilizacion. |
| US8604185B2 (en) | 2004-07-20 | 2013-12-10 | Genentech, Inc. | Inhibitors of angiopoietin-like 4 protein, combinations, and their use |
| BRPI0606432A2 (pt) | 2005-01-07 | 2009-06-30 | Lexicon Pharmaceuticals Inc | anticorpos monoclonais contra angptl4 |
| US8734851B2 (en) * | 2005-04-29 | 2014-05-27 | Wisconsin Alumni Research Foundation | Localized delivery of nucleic acid by polyelectrolyte assemblies |
| ES2643469T3 (es) | 2006-04-07 | 2017-11-23 | Aerpio Therapeutics, Inc. | Anticuerpos que se unen a la proteína tirosina fosfatasa beta humana (HPTP-beta) y usos de los mismos |
| US7622593B2 (en) | 2006-06-27 | 2009-11-24 | The Procter & Gamble Company | Human protein tyrosine phosphatase inhibitors and methods of use |
| KR100962301B1 (ko) | 2006-11-03 | 2010-06-11 | 재단법인서울대학교산학협력재단 | 자궁경부암을 위한 치료용 조성물 |
| HUE029445T2 (en) * | 2006-12-19 | 2017-02-28 | Genentech Inc | VEGF-specific antagonists for adjuvant and neoadjuvant therapy and treatment of early-stage tumors |
| US8834918B2 (en) * | 2007-01-22 | 2014-09-16 | Wisconsin Alumni Research Foundation | Modified multilayered film |
| EP2178531A4 (en) * | 2007-07-02 | 2012-01-11 | Yu Ming | METHODS AND COMPOSITIONS, TARGETS FOR COMBINED CANCER TREATMENTS |
| US20090105375A1 (en) * | 2007-10-09 | 2009-04-23 | Lynn David M | Ultrathin Multilayered Films for Controlled Release of Anionic Reagents |
| US8126437B1 (en) | 2008-01-24 | 2012-02-28 | Invent Again | Ubiquitous voice messaging |
| US8324333B2 (en) | 2008-06-05 | 2012-12-04 | Wisconsin Alumni Research Foundation | Anionic charge-dynamic polymers for release of cationic agents |
| CN102625714B (zh) * | 2008-07-16 | 2015-08-19 | 贝勒研究院 | 基于将最大化的gag和nef靶向树突细胞的hiv疫苗 |
| HUE032693T2 (en) | 2008-11-22 | 2017-10-30 | Hoffmann La Roche | Use of anti-vegf antibody in combination with chemotherapy for treating breast cancer |
| EP3556367A1 (en) | 2009-07-06 | 2019-10-23 | Aerpio Therapeutics, Inc. | Benzosulfonamide derivatives, compositions thereof, and their use in the treatment of cancer or metastasis |
| US20120207770A1 (en) * | 2009-10-14 | 2012-08-16 | Nanyang Technological University | Antiproliferative agent |
| EP3421040A1 (en) | 2010-01-08 | 2019-01-02 | Ionis Pharmaceuticals, Inc. | Modulation of angiopoietin-like 3 expression |
| US9139629B2 (en) | 2010-06-05 | 2015-09-22 | The Uab Research Foundation | Methods for treatment of nephrotic syndrome and related conditions |
| US9475850B2 (en) | 2010-06-05 | 2016-10-25 | The Uab Research Foundation | Methods for treatment of nephrotic syndrome and related conditions |
| ES2649340T3 (es) * | 2010-07-12 | 2018-01-11 | Threshold Pharmaceuticals, Inc. | Administración de fármacos activados por hipoxia y agentes antiangiogénicos para el tratamiento del cáncer |
| WO2012088254A1 (en) | 2010-12-22 | 2012-06-28 | Genentech, Inc. | Autophagy inducer and inhibitor combination therapy for the treatment of neoplasms |
| RU2665952C2 (ru) | 2011-07-22 | 2018-09-05 | Пасилекс Фармасьютикалз Инк. | Синтетическая летальность и лечение рака |
| WO2013022406A1 (en) * | 2011-08-08 | 2013-02-14 | Nanyang Technological University | Angiopoietin-like 4 and its use in modulating cell leakiness |
| CA2850830A1 (en) | 2011-10-13 | 2013-04-18 | Aerpio Therapeutics, Inc. | Methods for treating vascular leak syndrome and cancer |
| SG10201610869TA (en) | 2012-06-26 | 2017-02-27 | Del Mar Pharmaceuticals | Methods for treating tyrosine-kinase-inhibitor-resistant malignancies in patients with genetic polymorphisms or ahi1 dysregulations or mutations employing dianhydrogalactitol, diacetyldianhydrogalacti |
| SG11201408340SA (en) * | 2012-08-14 | 2015-01-29 | Univ Nanyang Tech | Angiopoietin-like 4 antibody and a method of its use in cancer treatment |
| US9259435B2 (en) | 2012-08-31 | 2016-02-16 | W. L. Gore & Associates, Inc. | Reactive oxidative species generating materials and methods of use |
| EP3858350A1 (en) * | 2012-10-30 | 2021-08-04 | Pacylex Pharmaceuticals Inc. | Synthetic lethality and the treatment of cancer |
| KR101407730B1 (ko) * | 2012-11-23 | 2014-06-12 | 인하대학교 산학협력단 | 안지오포이에틴-4 단백질을 유효성분으로 포함하는 발기부전의 예방 또는 치료용 조성물 |
| GB201301313D0 (en) * | 2013-01-25 | 2013-03-06 | Univ Singapore | Respiratory Tract Infections |
| US20150050277A1 (en) | 2013-03-15 | 2015-02-19 | Aerpio Therapeutics Inc. | Compositions and methods for treating ocular diseases |
| KR20160061911A (ko) | 2013-04-08 | 2016-06-01 | 데니스 엠. 브라운 | 최적하 투여된 화학 화합물의 치료 효과 |
| DK2991656T3 (da) | 2013-05-01 | 2020-03-23 | Ionis Pharmaceuticals Inc | Sammensætninger og fremgangsmåder til modulering af apolipoprotein c-iii-ekspression |
| KR102198082B1 (ko) | 2013-12-24 | 2021-01-05 | 아이오니스 파마수티컬즈, 인코포레이티드 | 안지오포이에틴-유사 3 발현의 조절 |
| CN106456614A (zh) | 2014-03-14 | 2017-02-22 | 爱尔皮奥治疗有限公司 | HPTP‑β抑制剂 |
| JP2017521045A (ja) * | 2014-05-01 | 2017-08-03 | アイオーニス ファーマシューティカルズ, インコーポレーテッドIonis Pharmaceuticals,Inc. | アンジオポエチン様因子3発現を調節するための組成物及び方法 |
| EP3194437B1 (en) | 2014-08-07 | 2021-01-20 | Novartis AG | Angiopoietin-like 4 (angptl4) antibodies and methods of use |
| BR112017002173B1 (pt) * | 2014-08-07 | 2023-11-21 | Novartis Ag | Anticorpo isolado anti-angptl4, ou fragmento de ligação ao antígeno do mesmo, seu uso, e composição farmacêutica |
| US11788145B2 (en) | 2015-07-17 | 2023-10-17 | Pacylex Pharmaceuticals Inc. | Epigeneiic silencing of NMT2 |
| MX387804B (es) | 2015-09-23 | 2025-03-19 | Aerpio Therapeutics Inc | Metodos para tratar presion intraocular con activadores de tie-2 |
| CN106596979B (zh) * | 2017-02-28 | 2018-10-09 | 汉氏联合(天津)干细胞研究院有限公司 | 一种用于帕金森综合症检测的试剂盒及其检测方法 |
| US12024708B2 (en) * | 2018-11-13 | 2024-07-02 | Lipigon Pharmaceuticals Ab | ANGPTL4 oligonucleotides influencing the regulation of the fatty acid metabolism |
| WO2020223209A1 (en) | 2019-04-29 | 2020-11-05 | Aerpio Pharmaceuticals, Inc. | Tie-2 activators targeting the schlemm's canal |
| JP2023514000A (ja) * | 2019-12-09 | 2023-04-05 | エンピリコ インク. | アンジオポエチン様4(angptl4)関連疾患の処置のためのオリゴヌクレオチド |
| CN112611877B (zh) * | 2020-12-31 | 2022-09-16 | 四川大学华西医院 | 一款利用angptl4预测急性呼吸窘迫综合征患病及预后的试剂盒 |
| US20240279663A1 (en) * | 2021-06-07 | 2024-08-22 | Empirico Inc. | Treatment of angptl4 related diseases |
| CN113797355B (zh) * | 2021-10-14 | 2023-07-21 | 四川大学华西医院 | 具有滑膜炎症抑制功能的纳米材料的制备方法及应用 |
| WO2025040097A1 (zh) * | 2023-08-22 | 2025-02-27 | 成都先衍生物技术有限公司 | 一种靶向ANGPTL4的siRNA及其缀合物和用途 |
| CN119405811A (zh) * | 2024-11-13 | 2025-02-11 | 杭州师范大学 | 禁食诱导因子Angptl4蛋白作为分子靶点在治疗或预防压力性脱发中的应用 |
Family Cites Families (151)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3773919A (en) | 1969-10-23 | 1973-11-20 | Du Pont | Polylactide-drug mixtures |
| US3896111A (en) | 1973-02-20 | 1975-07-22 | Research Corp | Ansa macrolides |
| US4179337A (en) | 1973-07-20 | 1979-12-18 | Davis Frank F | Non-immunogenic polypeptides |
| US4151042A (en) | 1977-03-31 | 1979-04-24 | Takeda Chemical Industries, Ltd. | Method for producing maytansinol and its derivatives |
| US4137230A (en) | 1977-11-14 | 1979-01-30 | Takeda Chemical Industries, Ltd. | Method for the production of maytansinoids |
| USRE30985E (en) | 1978-01-01 | 1982-06-29 | Serum-free cell culture media | |
| FR2413974A1 (fr) | 1978-01-06 | 1979-08-03 | David Bernard | Sechoir pour feuilles imprimees par serigraphie |
| US4265814A (en) | 1978-03-24 | 1981-05-05 | Takeda Chemical Industries | Matansinol 3-n-hexadecanoate |
| US4307016A (en) | 1978-03-24 | 1981-12-22 | Takeda Chemical Industries, Ltd. | Demethyl maytansinoids |
| JPS5562090A (en) | 1978-10-27 | 1980-05-10 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| JPS55164687A (en) | 1979-06-11 | 1980-12-22 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| US4256746A (en) | 1978-11-14 | 1981-03-17 | Takeda Chemical Industries | Dechloromaytansinoids, their pharmaceutical compositions and method of use |
| JPS5566585A (en) | 1978-11-14 | 1980-05-20 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| JPS55102583A (en) | 1979-01-31 | 1980-08-05 | Takeda Chem Ind Ltd | 20-acyloxy-20-demethylmaytansinoid compound |
| JPS55162791A (en) | 1979-06-05 | 1980-12-18 | Takeda Chem Ind Ltd | Antibiotic c-15003pnd and its preparation |
| JPS55164685A (en) | 1979-06-08 | 1980-12-22 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| JPS55164686A (en) | 1979-06-11 | 1980-12-22 | Takeda Chem Ind Ltd | Novel maytansinoid compound and its preparation |
| JPS6023084B2 (ja) | 1979-07-11 | 1985-06-05 | 味の素株式会社 | 代用血液 |
| US4309428A (en) | 1979-07-30 | 1982-01-05 | Takeda Chemical Industries, Ltd. | Maytansinoids |
| JPS5645483A (en) | 1979-09-19 | 1981-04-25 | Takeda Chem Ind Ltd | C-15003phm and its preparation |
| EP0028683A1 (en) | 1979-09-21 | 1981-05-20 | Takeda Chemical Industries, Ltd. | Antibiotic C-15003 PHO and production thereof |
| JPS5645485A (en) | 1979-09-21 | 1981-04-25 | Takeda Chem Ind Ltd | Production of c-15003pnd |
| WO1982001188A1 (en) | 1980-10-08 | 1982-04-15 | Takeda Chemical Industries Ltd | 4,5-deoxymaytansinoide compounds and process for preparing same |
| US4450254A (en) | 1980-11-03 | 1984-05-22 | Standard Oil Company | Impact improvement of high nitrile resins |
| US4419446A (en) | 1980-12-31 | 1983-12-06 | The United States Of America As Represented By The Department Of Health And Human Services | Recombinant DNA process utilizing a papilloma virus DNA as a vector |
| US4315929A (en) | 1981-01-27 | 1982-02-16 | The United States Of America As Represented By The Secretary Of Agriculture | Method of controlling the European corn borer with trewiasine |
| US4313946A (en) | 1981-01-27 | 1982-02-02 | The United States Of America As Represented By The Secretary Of Agriculture | Chemotherapeutically active maytansinoids from Trewia nudiflora |
| JPS57192389A (en) | 1981-05-20 | 1982-11-26 | Takeda Chem Ind Ltd | Novel maytansinoid |
| US4485045A (en) | 1981-07-06 | 1984-11-27 | Research Corporation | Synthetic phosphatidyl cholines useful in forming liposomes |
| NZ201705A (en) | 1981-08-31 | 1986-03-14 | Genentech Inc | Recombinant dna method for production of hepatitis b surface antigen in yeast |
| NZ201918A (en) | 1981-09-18 | 1987-04-30 | Genentech Inc | N-terminal methionyl analogues of bovine growth hormone |
| US4640835A (en) | 1981-10-30 | 1987-02-03 | Nippon Chemiphar Company, Ltd. | Plasminogen activator derivatives |
| US4601978A (en) | 1982-11-24 | 1986-07-22 | The Regents Of The University Of California | Mammalian metallothionein promoter system |
| US4560655A (en) | 1982-12-16 | 1985-12-24 | Immunex Corporation | Serum-free cell culture medium and process for making same |
| US4657866A (en) | 1982-12-21 | 1987-04-14 | Sudhir Kumar | Serum-free, synthetic, completely chemically defined tissue culture media |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| DD266710A3 (de) | 1983-06-06 | 1989-04-12 | Ve Forschungszentrum Biotechnologie | Verfahren zur biotechnischen Herstellung van alkalischer Phosphatase |
| US4544545A (en) | 1983-06-20 | 1985-10-01 | Trustees University Of Massachusetts | Liposomes containing modified cholesterol for organ targeting |
| US4767704A (en) | 1983-10-07 | 1988-08-30 | Columbia University In The City Of New York | Protein-free culture medium |
| US4496689A (en) | 1983-12-27 | 1985-01-29 | Miles Laboratories, Inc. | Covalently attached complex of alpha-1-proteinase inhibitor with a water soluble polymer |
| US4965199A (en) | 1984-04-20 | 1990-10-23 | Genentech, Inc. | Preparation of functional human factor VIII in mammalian cells using methotrexate based selection |
| US4879231A (en) | 1984-10-30 | 1989-11-07 | Phillips Petroleum Company | Transformation of yeasts of the genus pichia |
| EP0206448B1 (en) | 1985-06-19 | 1990-11-14 | Ajinomoto Co., Inc. | Hemoglobin combined with a poly(alkylene oxide) |
| GB8516415D0 (en) | 1985-06-28 | 1985-07-31 | Celltech Ltd | Culture of animal cells |
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| JPS63502716A (ja) | 1986-03-07 | 1988-10-13 | マサチューセッツ・インステチュート・オブ・テクノロジー | 糖タンパク安定性の強化方法 |
| US4927762A (en) | 1986-04-01 | 1990-05-22 | Cell Enterprises, Inc. | Cell culture medium with antioxidant |
| GB8610600D0 (en) | 1986-04-30 | 1986-06-04 | Novo Industri As | Transformation of trichoderma |
| US4791192A (en) | 1986-06-26 | 1988-12-13 | Takeda Chemical Industries, Ltd. | Chemically modified protein with polyethyleneglycol |
| US5567610A (en) | 1986-09-04 | 1996-10-22 | Bioinvent International Ab | Method of producing human monoclonal antibodies and kit therefor |
| IL85035A0 (en) | 1987-01-08 | 1988-06-30 | Int Genetic Eng | Polynucleotide molecule,a chimeric antibody with specificity for human b cell surface antigen,a process for the preparation and methods utilizing the same |
| US5770701A (en) | 1987-10-30 | 1998-06-23 | American Cyanamid Company | Process for preparing targeted forms of methyltrithio antitumor agents |
| US5606040A (en) | 1987-10-30 | 1997-02-25 | American Cyanamid Company | Antitumor and antibacterial substituted disulfide derivatives prepared from compounds possessing a methyl-trithio group |
| US5053394A (en) | 1988-09-21 | 1991-10-01 | American Cyanamid Company | Targeted forms of methyltrithio antitumor agents |
| WO1990003430A1 (en) | 1988-09-23 | 1990-04-05 | Cetus Corporation | Cell culture medium for enhanced cell growth, culture longevity and product expression |
| GB8823869D0 (en) | 1988-10-12 | 1988-11-16 | Medical Res Council | Production of antibodies |
| US5750373A (en) | 1990-12-03 | 1998-05-12 | Genentech, Inc. | Enrichment method for variant proteins having altered binding properties, M13 phagemids, and growth hormone variants |
| FR2646437B1 (fr) | 1989-04-28 | 1991-08-30 | Transgene Sa | Nouvelles sequences d'adn, leur application en tant que sequence codant pour un peptide signal pour la secretion de proteines matures par des levures recombinantes, cassettes d'expression, levures transformees et procede de preparation de proteines correspondant |
| EP0402226A1 (en) | 1989-06-06 | 1990-12-12 | Institut National De La Recherche Agronomique | Transformation vectors for yeast yarrowia |
| DE3920358A1 (de) | 1989-06-22 | 1991-01-17 | Behringwerke Ag | Bispezifische und oligospezifische, mono- und oligovalente antikoerperkonstrukte, ihre herstellung und verwendung |
| AU641673B2 (en) | 1989-06-29 | 1993-09-30 | Medarex, Inc. | Bispecific reagents for aids therapy |
| US5013556A (en) | 1989-10-20 | 1991-05-07 | Liposome Technology, Inc. | Liposomes with enhanced circulation time |
| CA2026147C (en) | 1989-10-25 | 2006-02-07 | Ravi J. Chari | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5229275A (en) | 1990-04-26 | 1993-07-20 | Akzo N.V. | In-vitro method for producing antigen-specific human monoclonal antibodies |
| US5545806A (en) | 1990-08-29 | 1996-08-13 | Genpharm International, Inc. | Ransgenic non-human animals for producing heterologous antibodies |
| DE69133476T2 (de) | 1990-08-29 | 2006-01-05 | GenPharm International, Inc., Palo Alto | Transgene Mäuse fähig zur Produktion heterologer Antikörper |
| US5661016A (en) | 1990-08-29 | 1997-08-26 | Genpharm International Inc. | Transgenic non-human animals capable of producing heterologous antibodies of various isotypes |
| US5633425A (en) | 1990-08-29 | 1997-05-27 | Genpharm International, Inc. | Transgenic non-human animals capable of producing heterologous antibodies |
| US5625126A (en) | 1990-08-29 | 1997-04-29 | Genpharm International, Inc. | Transgenic non-human animals for producing heterologous antibodies |
| US5122469A (en) | 1990-10-03 | 1992-06-16 | Genentech, Inc. | Method for culturing Chinese hamster ovary cells to improve production of recombinant proteins |
| US5571894A (en) | 1991-02-05 | 1996-11-05 | Ciba-Geigy Corporation | Recombinant antibodies specific for a growth factor receptor |
| US6582959B2 (en) | 1991-03-29 | 2003-06-24 | Genentech, Inc. | Antibodies to vascular endothelial cell growth factor |
| US20030206899A1 (en) | 1991-03-29 | 2003-11-06 | Genentech, Inc. | Vascular endothelial cell growth factor antagonists |
| WO1992020373A1 (en) | 1991-05-14 | 1992-11-26 | Repligen Corporation | Heteroconjugate antibodies for treatment of hiv infection |
| ES2206447T3 (es) | 1991-06-14 | 2004-05-16 | Genentech, Inc. | Anticuerpo humanizado para heregulina. |
| US5565332A (en) | 1991-09-23 | 1996-10-15 | Medical Research Council | Production of chimeric antibodies - a combinatorial approach |
| FI941572A7 (fi) | 1991-10-07 | 1994-05-27 | Oncologix Inc | Anti-erbB-2-monoklonaalisten vasta-aineiden yhdistelmä ja käyttömenete lmä |
| WO1993008829A1 (en) | 1991-11-04 | 1993-05-13 | The Regents Of The University Of California | Compositions that mediate killing of hiv-infected cells |
| JPH07501451A (ja) | 1991-11-25 | 1995-02-16 | エンゾン・インコーポレイテッド | 多価抗原結合タンパク質 |
| EP0625200B1 (en) | 1992-02-06 | 2005-05-11 | Chiron Corporation | Biosynthetic binding protein for cancer marker |
| US5573905A (en) | 1992-03-30 | 1996-11-12 | The Scripps Research Institute | Encoded combinatorial chemical libraries |
| ZA932522B (en) | 1992-04-10 | 1993-12-20 | Res Dev Foundation | Immunotoxins directed against c-erbB-2(HER/neu) related surface antigens |
| WO1994004690A1 (en) | 1992-08-17 | 1994-03-03 | Genentech, Inc. | Bispecific immunoadhesins |
| RU2170589C2 (ru) * | 1992-10-28 | 2001-07-20 | Генентек Инк. | Композиция для ингибирования ангиогенеза, моноклональное антитело, полипептид, способ ингибирования роста опухоли (варианты) |
| CZ291047B6 (cs) | 1992-10-28 | 2002-12-11 | Genentech, Inc. | Farmaceutický prostředek obsahující antagonisty faktoru růstu vaskulárních endoteliálních buněk |
| PL174494B1 (pl) | 1992-11-13 | 1998-08-31 | Idec Pharma Corp | Kompozycja farmaceutyczna do leczenia chłoniaka z limfocytów B i sposób wytwarzania kompozycji farmaceutycznej do leczenia chłoniaka z limfocytów B |
| US5641756A (en) | 1993-07-27 | 1997-06-24 | Hybridon, Inc. | Modified VEGF oligonucleotides |
| US5643755A (en) | 1994-10-07 | 1997-07-01 | Regeneron Pharmaceuticals Inc. | Nucleic acid encoding tie-2 ligand |
| US5753230A (en) * | 1994-03-18 | 1998-05-19 | The Scripps Research Institute | Methods and compositions useful for inhibition of angiogenesis |
| US5773001A (en) | 1994-06-03 | 1998-06-30 | American Cyanamid Company | Conjugates of methyltrithio antitumor agents and intermediates for their synthesis |
| US5650490A (en) | 1994-10-07 | 1997-07-22 | Regeneron Pharmaceuticals, Inc. | Tie-2 ligand 2 |
| US5814464A (en) | 1994-10-07 | 1998-09-29 | Regeneron Pharma | Nucleic acids encoding TIE-2 ligand-2 |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| IL117645A (en) | 1995-03-30 | 2005-08-31 | Genentech Inc | Vascular endothelial cell growth factor antagonists for use as medicaments in the treatment of age-related macular degeneration |
| US5641870A (en) | 1995-04-20 | 1997-06-24 | Genentech, Inc. | Low pH hydrophobic interaction chromatography for antibody purification |
| US5739277A (en) | 1995-04-14 | 1998-04-14 | Genentech Inc. | Altered polypeptides with increased half-life |
| US5714586A (en) | 1995-06-07 | 1998-02-03 | American Cyanamid Company | Methods for the preparation of monomeric calicheamicin derivative/carrier conjugates |
| US5712374A (en) | 1995-06-07 | 1998-01-27 | American Cyanamid Company | Method for the preparation of substantiallly monomeric calicheamicin derivative/carrier conjugates |
| WO1999066041A1 (en) | 1998-06-16 | 1999-12-23 | Human Genome Sciences, Inc. | 94 human secreted proteins |
| US20020137890A1 (en) | 1997-03-31 | 2002-09-26 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| KR100856995B1 (ko) | 1997-04-07 | 2008-09-04 | 제넨테크, 인크. | 인간화 항체 및 인간화 항체의 제조 방법 |
| WO1998045331A2 (en) | 1997-04-07 | 1998-10-15 | Genentech, Inc. | Anti-vegf antibodies |
| US20020032315A1 (en) | 1997-08-06 | 2002-03-14 | Manuel Baca | Anti-vegf antibodies |
| US6884879B1 (en) | 1997-04-07 | 2005-04-26 | Genentech, Inc. | Anti-VEGF antibodies |
| US6348350B1 (en) | 1997-09-19 | 2002-02-19 | Genentech, Inc. | Ligand homologues |
| US20030207375A1 (en) | 1997-10-24 | 2003-11-06 | Genentech, Inc. | Secreted and transmembrane polypeptides and nucleic acids encoding the same |
| WO1999032515A2 (en) | 1997-12-19 | 1999-07-01 | Zymogenetics, Inc. | Angiopoietin homolog, dna encoding it, and method of making it |
| EP1058737A4 (en) | 1998-03-02 | 2003-01-02 | Millennium Pharm Inc | NOVEL FDRG PROTEIN AND NUCLEIC ACID MOLECULES AND USE OF SUCH MOLECULES |
| AU4643699A (en) | 1998-06-24 | 2000-01-10 | Compugen Ltd. | Angiopoietin-like growth factor sequences |
| DE59914547D1 (de) | 1998-07-15 | 2007-12-20 | Max Planck Gesellschaft | Polyelektrolythüllen auf biologischen templaten |
| US6375447B1 (en) | 1998-09-29 | 2002-04-23 | Cq Inc. | Apparatus for dewatering and pelletizing particulate fuel |
| WO2001053455A2 (en) | 1999-12-23 | 2001-07-26 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| JP2000308488A (ja) | 1999-02-23 | 2000-11-07 | Herikkusu Kenkyusho:Kk | 血管新生に関連するタンパク質および該タンパク質をコードする遺伝子 |
| AU3391200A (en) | 1999-03-04 | 2000-09-21 | Corixa Corporation | Compositions and methods for breast cancer therapy and diagnosis |
| EP1175439A4 (en) | 1999-04-09 | 2002-10-09 | Human Genome Sciences Inc | 49 HUMANE SECRETIED PROTEINS |
| EP1655368B1 (en) | 1999-04-16 | 2009-01-07 | Genentech, Inc. | Vascular endothelial cell growth factor variants and uses thereof |
| US6703020B1 (en) | 1999-04-28 | 2004-03-09 | Board Of Regents, The University Of Texas System | Antibody conjugate methods for selectively inhibiting VEGF |
| AU5979300A (en) | 1999-07-02 | 2001-01-22 | Bayer Aktiengesellschaft | Angiopoietin-6 and uses thereof |
| CA2379152A1 (en) | 1999-07-16 | 2001-01-25 | Hyseq, Inc. | Novel angiopoietin materials and methods |
| US20030207348A1 (en) | 1999-07-20 | 2003-11-06 | Shimkets Richard A. | Polypeptides and polynucleotides encoding same |
| AU6229100A (en) | 1999-07-20 | 2001-02-05 | Curagen Corporation | Polypeptides and polynucleotides encoding same |
| EP1285084A1 (en) | 2000-01-25 | 2003-02-26 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| AU2001243142A1 (en) | 2000-02-03 | 2001-08-14 | Hyseq, Inc. | Novel nucleic acids and polypeptides |
| WO2002081628A2 (en) * | 2001-04-05 | 2002-10-17 | Ribozyme Pharmaceuticals, Incorporated | Modulation of gene expression associated with inflammation proliferation and neurite outgrowth, using nucleic acid based technologies |
| CN1315451A (zh) | 2000-03-29 | 2001-10-03 | 上海博德基因开发有限公司 | 一种新的多肽——人血管形成素类似因子45和编码这种多肽的多核苷酸 |
| AU2001249929A1 (en) | 2000-04-07 | 2001-10-23 | Dana-Farber Cancer Institute Inc. | Fdrg proteins and nucleic acid molecules and uses therefor |
| EP1292335B1 (en) | 2000-06-23 | 2007-05-30 | Bayer Schering Pharma Aktiengesellschaft | Combinations and compositions which interfere with vegf/vegf and angiopoietin/tie receptor function and their use (ii) |
| US6673545B2 (en) | 2000-07-28 | 2004-01-06 | Incyte Corporation | Prostate cancer markers |
| CN1170850C (zh) * | 2000-09-19 | 2004-10-13 | 上海市肿瘤研究所 | 人血管生成素样蛋白和编码序列及其用途 |
| US20030120056A1 (en) | 2000-10-16 | 2003-06-26 | Audrey Goddard | TIE ligand homologues |
| EP1460900A4 (en) | 2001-03-27 | 2004-11-03 | Human Genome Sciences Inc | SEPARATE HUMAN PROTEINS |
| US7667004B2 (en) * | 2001-04-17 | 2010-02-23 | Abmaxis, Inc. | Humanized antibodies against vascular endothelial growth factor |
| DK2128246T3 (da) | 2001-04-19 | 2014-05-12 | Univ California | Fremgangsmåder og sammensætninger til fremstilling af ortogonale tRNA-aminoacyl-tRNA-syntetasepar. |
| US20030170891A1 (en) * | 2001-06-06 | 2003-09-11 | Mcswiggen James A. | RNA interference mediated inhibition of epidermal growth factor receptor gene expression using short interfering nucleic acid (siNA) |
| WO2002101039A1 (fr) | 2001-06-08 | 2002-12-19 | Sankyo Company, Limited | Procede de test de medicament destine a traiter ou a prevenir des maladies telles que l'hyperlipemie |
| WO2003010205A1 (en) | 2001-07-26 | 2003-02-06 | Duke University Medical Center | Genes induced by hypoxia |
| CA2459219A1 (en) | 2001-09-17 | 2003-03-27 | Protein Design Labs, Inc. | Methods of diagnosis of cancer compositions and methods of screening for modulators of cancer |
| US20050123925A1 (en) | 2002-11-15 | 2005-06-09 | Genentech, Inc. | Compositions and methods for the diagnosis and treatment of tumor |
| WO2003040330A2 (en) | 2001-11-05 | 2003-05-15 | Curagen Corporation | Therapeutic polypeptides, nucleic acids encoding same, and methods of use |
| US20040038230A1 (en) | 2001-11-05 | 2004-02-26 | Alsobrook John P. | Therapeutic polypeptides, nucleic acids encoding same, and methods of use |
| CN101905024A (zh) | 2001-11-16 | 2010-12-08 | 杰南技术公司 | 含有血管生成素-样蛋白质3angptl3的组合物及其使用方法 |
| WO2003048185A2 (en) | 2001-11-30 | 2003-06-12 | Genvec, Inc. | Angiopioetin related factors |
| EP1997829A1 (en) | 2001-12-21 | 2008-12-03 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| WO2005044853A2 (en) | 2003-11-01 | 2005-05-19 | Genentech, Inc. | Anti-vegf antibodies |
| US20050106667A1 (en) | 2003-08-01 | 2005-05-19 | Genentech, Inc | Binding polypeptides with restricted diversity sequences |
| US20050239706A1 (en) | 2003-10-31 | 2005-10-27 | Washington University In St. Louis | Modulation of fiaf and the gastrointestinal microbiota as a means to control energy storage in a subject |
| CA2499791A1 (en) | 2004-03-30 | 2005-09-30 | F. Hoffmann-La Roche Ag | Angptl4/fiaf as marker for ppardelta modulation |
| ES2339789T3 (es) | 2004-07-20 | 2010-05-25 | Genentech, Inc. | Inhibidores de proteina 4 de tipo angiopoyetina, combinaciones y su utilizacion. |
| WO2006014678A2 (en) | 2004-07-20 | 2006-02-09 | Genentech, Inc. | Compositions and methods of using angiopoietin-like 4 protein |
| BRPI0606432A2 (pt) | 2005-01-07 | 2009-06-30 | Lexicon Pharmaceuticals Inc | anticorpos monoclonais contra angptl4 |
-
2005
- 2005-07-19 ES ES05790352T patent/ES2339789T3/es not_active Expired - Lifetime
- 2005-07-19 AT AT05790352T patent/ATE456579T1/de active
- 2005-07-19 BR BRPI0513534-6A patent/BRPI0513534A/pt not_active Application Discontinuation
- 2005-07-19 EP EP10010294.6A patent/EP2361931B1/en not_active Expired - Lifetime
- 2005-07-19 SI SI200530979T patent/SI1771474T1/sl unknown
- 2005-07-19 JP JP2007522697A patent/JP4947717B2/ja not_active Expired - Fee Related
- 2005-07-19 DE DE602005019167T patent/DE602005019167D1/de not_active Expired - Lifetime
- 2005-07-19 WO PCT/US2005/025734 patent/WO2006014729A2/en not_active Ceased
- 2005-07-19 US US11/185,215 patent/US7740846B2/en not_active Expired - Lifetime
- 2005-07-19 CN CNA2005800316893A patent/CN101044164A/zh active Pending
- 2005-07-19 PL PL05790352T patent/PL1771474T3/pl unknown
- 2005-07-19 DK DK05790352.8T patent/DK1771474T3/da active
- 2005-07-19 CN CN2012100589479A patent/CN102641503A/zh active Pending
- 2005-07-19 EP EP05790352A patent/EP1771474B1/en not_active Revoked
- 2005-07-19 KR KR1020077003872A patent/KR101254815B1/ko not_active Expired - Fee Related
- 2005-07-19 EP EP09013335A patent/EP2172482A1/en not_active Withdrawn
- 2005-07-19 AU AU2005269716A patent/AU2005269716B2/en not_active Expired
- 2005-07-19 PT PT05790352T patent/PT1771474E/pt unknown
- 2005-07-19 RU RU2007106076/14A patent/RU2392966C2/ru active
- 2005-07-19 CA CA002574758A patent/CA2574758A1/en not_active Abandoned
- 2005-07-19 NZ NZ552956A patent/NZ552956A/en not_active IP Right Cessation
- 2005-07-19 ZA ZA200701183A patent/ZA200701183B/en unknown
- 2005-07-19 MX MX2007000784A patent/MX2007000784A/es active IP Right Grant
-
2006
- 2006-09-28 US US11/540,884 patent/US20070026002A1/en not_active Abandoned
-
2007
- 2007-01-16 IL IL180725A patent/IL180725A0/en unknown
- 2007-02-19 NO NO20070951A patent/NO20070951L/no not_active Application Discontinuation
-
2010
- 2010-03-30 CY CY20101100299T patent/CY1109931T1/el unknown
-
2011
- 2011-03-30 AU AU2011201436A patent/AU2011201436A1/en not_active Withdrawn
- 2011-08-10 JP JP2011175420A patent/JP2012017331A/ja not_active Withdrawn
Non-Patent Citations (2)
| Title |
|---|
| JPN5007012188; Mesiano,S. et al.: 'Role of Vascular Endotherial Growth Factor in Ovarian Cancer; Inhibition of Ascites Formation by Imm' Am. J. Pathol. Vol.153,No.4, 199810, P.1249-1256 * |
| JPN5007012189; Ito,Y. et al.: 'Inhibition of Angiogenesis and Vascular Leakiness by Angiopoietin-Related Protein 4' Cancer Res. Vol.63,No.20, 20031015, P.6651-6657 * |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4947717B2 (ja) | アンジオポエチン様4タンパク質のインヒビター、組み合わせ、およびそれらの使用 | |
| JP5615709B2 (ja) | 脈管形成の阻害 | |
| US20100129356A1 (en) | Compositions and methods for modulating vascular development | |
| US20100119526A1 (en) | DLL4 Signaling Inhibitors and Uses Thereof | |
| JP2009531463A (ja) | 腫瘍の診断と治療 | |
| BRPI0706935A2 (pt) | anticorpos anti-efrina b2 isolado, vetor, célula hospedeira, método de elaboração de anticorpo anti-efrina b2, método de elaboração de imunoconjugado anti-efrina b2, método de detecção de efrina b2, método de diagnóstico de disfunção, composição, método de inibição da angiogênese e uso de anticorpo anti-efrina b2 | |
| US8604185B2 (en) | Inhibitors of angiopoietin-like 4 protein, combinations, and their use | |
| HK1161273A (en) | Inhibitors of angiopoietin-like 4 protein, combinations, and their use | |
| HK1143378A (en) | Inhibitors of angiopoietin-like 4 protein, combinations, and their use | |
| HK1108897A (en) | Inhibitors of angiopoietin-like 4 protein, combinations, and their use | |
| HK1131628A (en) | Diagnostics and treatments for tumors | |
| HK1122505A (en) | Treatment with anti-vegf antibodies |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120731 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130111 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130410 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130415 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130510 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130515 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130610 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130613 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20130710 |